JP2005298736A - 硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 - Google Patents
硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 Download PDFInfo
- Publication number
- JP2005298736A JP2005298736A JP2004119379A JP2004119379A JP2005298736A JP 2005298736 A JP2005298736 A JP 2005298736A JP 2004119379 A JP2004119379 A JP 2004119379A JP 2004119379 A JP2004119379 A JP 2004119379A JP 2005298736 A JP2005298736 A JP 2005298736A
- Authority
- JP
- Japan
- Prior art keywords
- sulfur
- compound
- group
- mmol
- dithiol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Landscapes
- Polymers With Sulfur, Phosphorus Or Metals In The Main Chain (AREA)
- Polyesters Or Polycarbonates (AREA)
- Polyurethanes Or Polyureas (AREA)
Abstract
【課題】高屈折率、高アッベ数で、透明性、耐熱性に優れたジチオール化合物とジエン化合物との反応生成物、その製造方法および該硫黄含有化合物の少なくとも一種を構成成分の一つとする、光学材料の提供。
【解決手段】下記一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物とを反応させて、アッベ数(νd)40以上の硫黄含有化合物とする。HS−G1−SH(II)、G2”(III)(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
【選択図】なし
【解決手段】下記一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物とを反応させて、アッベ数(νd)40以上の硫黄含有化合物とする。HS−G1−SH(II)、G2”(III)(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
【選択図】なし
Description
本発明は、ジチオール化合物を構成成分の一つとし、高屈折率、高アッベ数で、透明性に優れ、かつ耐熱性等に優れた含硫黄重合体を与える硫黄含有化合物、その製造方法および該硫黄含有化合物の少なくとも一種を構成成分の一つとする、前記の好ましい性質を有する含硫黄重合体および該含硫黄重合体を含有する光学材料に関する。
従来、脂環式スルフィドである1,4−ジチアン環を有するポリチオール化合物および該ポリチオール化合物と、一分子内に二つ以上のビニル基を有する化合物、一分子内に二つ以上のイソ(チオ)シアネート基を有する化合物および一分子内に一つ以上のビニル基と一つ以上のイソ(チオ)シアネート基を有する化合物のうちの少なくとも一種とを反応させた重合体、該重合体を使用する光学材料が知られている(たとえば、特許文献1および非特許文献1参照)。しかしながら、上記ポリチオール化合物を原料とする光学材料は、屈折率は高いものの、アッベ数、耐熱性等の点で必ずしも充分といえるものではない。
本発明は、上記事情に鑑みてなされたもので、高屈折率、高アッベ数で、透明性に優れ、かつ耐熱性等に優れた含硫黄重合体を与える、ジチオール化合物とジエン化合物との反応生成物である硫黄含有化合物、その製造方法および該硫黄含有化合物の少なくとも一種を構成成分の一つとする、前記の好ましい性質を有する含硫黄重合体および該重合体を含有する光学材料を提供することを目的とする。
本発明者は、上記課題を解決するために鋭意研究を重ねた結果、特定のジチオール化合物と特定のジエン化合物との反応生成物であって、該ジチオール化合物の残基に由来する構造単位と該ジエン化合物の残基に由来する構造単位とからなる繰り返し単位を有する硫黄含有化合物が、含硫黄重合体の原料として前記目的に適合しうること、そして該硫黄含有化合物の少なくとも一種を構成成分の一つとする含硫黄重合体および該含硫黄重合体を含有する光学材料が、高屈折率、高アッベ数で、透明性に優れ、かつ耐熱性等に優れた材料になることを見出し、この知見に基づいて本発明を完成した。
本発明は以下から構成される。
(1)下記一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物との反応生成物であって、該ジチオール化合物の残基に由来する構造単位と該ジエン化合物の残基に由来する構造単位とからなる繰り返し単位を有する、アッベ数(νd)40以上の硫黄含有化合物。
HS−G1−SH (II)
G2” (III)
(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
(2)一般式(II)で表されるジチオール化合物が、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(3)一般式(II)で表されるジチオール化合物が、シクロヘキサン基を有するC6〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(4)一般式(II)で表されるジチオール化合物が、ノルボルナン基を有するC7〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(5)一般式(II)で表されるジチオール化合物が、アダマンタン基を有するC10〜C35の、脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(6)一般式(II)で表されるジチオール化合物が、HSCH2CH2SH、HSCH2CH2CH2SH、HSCH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2CH2SH、HSCH2CH2OCH2CH2SHおよびHSCH2CH2SCH2CH2SHの中から選ばれる少なくとも一種である上記(1)に記載の硫黄含有化合物。
(7)一般式(II)で表されるジチオール化合物が、下記のジチオール化合物の中から選ばれる少なくとも一種である上記(1)に記載の硫黄含有化合物。
(1)下記一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物との反応生成物であって、該ジチオール化合物の残基に由来する構造単位と該ジエン化合物の残基に由来する構造単位とからなる繰り返し単位を有する、アッベ数(νd)40以上の硫黄含有化合物。
HS−G1−SH (II)
G2” (III)
(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
(2)一般式(II)で表されるジチオール化合物が、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(3)一般式(II)で表されるジチオール化合物が、シクロヘキサン基を有するC6〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(4)一般式(II)で表されるジチオール化合物が、ノルボルナン基を有するC7〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(5)一般式(II)で表されるジチオール化合物が、アダマンタン基を有するC10〜C35の、脂環式炭化水素基であるG1を有するジチオール化合物である上記(1)に記載の硫黄含有化合物。
(6)一般式(II)で表されるジチオール化合物が、HSCH2CH2SH、HSCH2CH2CH2SH、HSCH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2CH2SH、HSCH2CH2OCH2CH2SHおよびHSCH2CH2SCH2CH2SHの中から選ばれる少なくとも一種である上記(1)に記載の硫黄含有化合物。
(7)一般式(II)で表されるジチオール化合物が、下記のジチオール化合物の中から選ばれる少なくとも一種である上記(1)に記載の硫黄含有化合物。
(8)繰り返し単位中のジチオール化合物の残基に由来する構造単位とジエン化合物の残基に由来する構造単位とのモル比が、1:0.5〜0.5:1である上記(1)〜(7)のいずれかに記載の硫黄含有化合物。
(9)G2”が、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、メタクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アリル基を有する脂肪族もしくは脂環式炭化水素化合物;および酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、ビニル基を有する脂肪族もしくは脂環式炭化水素化合物;の中から選ばれる少なくとも一つである上記(1)〜(8)のいずれかに記載の硫黄含有化合物。
(10)G2”が、ノルボルナジエン化合物、エチリデンノルボルネン、ビニルノルボルネン、ジシクロペンタジエン化合物もしくはトリシクロペンタジエン化合物の中から選ばれる少なくとも一つである上記(1)〜(9)のいずれかに記載の硫黄含有化合物。
(11)G2”が、下記に示されるジエン化合物の中から選ばれる少なくとも一種である上記(1)〜(10)のいずれかに記載の硫黄含有化合物。
(10)G2”が、ノルボルナジエン化合物、エチリデンノルボルネン、ビニルノルボルネン、ジシクロペンタジエン化合物もしくはトリシクロペンタジエン化合物の中から選ばれる少なくとも一つである上記(1)〜(9)のいずれかに記載の硫黄含有化合物。
(11)G2”が、下記に示されるジエン化合物の中から選ばれる少なくとも一種である上記(1)〜(10)のいずれかに記載の硫黄含有化合物。
(12)一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物との反応生成物が、下記一般式(I)で表される構造のチオコオリゴマーである上記(1)〜(11)のいずれかに記載の硫黄含有化合物。
X−(S−G1−S−G2)n−S―G1−S−X’ (I)
(式中、XおよびX’はそれぞれ独立に−Hまたは−G2’を表す。G1は、硫黄および/または酸素原子を含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2とG2’はG2”由来の反応基であり、G2はG2”の炭素―炭素二重結合が二つ反応したものであり、G2’はG2”の炭素―炭素二重結合が一つ反応したものであり、G2”は炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち、少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である。nは1〜200の整数である)。
(13)nが1〜20の整数である上記(12)に記載の硫黄含有化合物。
(14)一般式(II)で表されるジチオール化合物を含有する上記(1)〜(13)のいずれかに記載の硫黄含有化合物。
X−(S−G1−S−G2)n−S―G1−S−X’ (I)
(式中、XおよびX’はそれぞれ独立に−Hまたは−G2’を表す。G1は、硫黄および/または酸素原子を含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2とG2’はG2”由来の反応基であり、G2はG2”の炭素―炭素二重結合が二つ反応したものであり、G2’はG2”の炭素―炭素二重結合が一つ反応したものであり、G2”は炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち、少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である。nは1〜200の整数である)。
(13)nが1〜20の整数である上記(12)に記載の硫黄含有化合物。
(14)一般式(II)で表されるジチオール化合物を含有する上記(1)〜(13)のいずれかに記載の硫黄含有化合物。
(15)一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物とを反応させることを特徴とする上記(1)〜(14)のいずれかに記載の硫黄含有化合物の製造方法。
(16)ジチオール化合物とジエン化合物とのモル比が1:0.5〜0.5:1である上記(15)に記載の硫黄含有化合物の製造方法。
(16)ジチオール化合物とジエン化合物とのモル比が1:0.5〜0.5:1である上記(15)に記載の硫黄含有化合物の製造方法。
(17)上記(1)〜(14)のいずれかに記載の硫黄含有化合物の中から選ばれる少なくとも一種を構成成分とする含硫黄重合体。
(18)上記(1)〜(14)のいずれかに記載の硫黄含有化合物の中から選ばれる少なくとも一種と、ポリイソシアナート化合物、ポリイソチオシアナート化合物およびイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物との重合生成物である上記(17)に記載の含硫黄重合体。
(19)上記(1)〜(14)のいずれかに記載の硫黄含有化合物の中から選ばれる少なくとも一種と、二価フェノールまたは末端にこれら硫黄含有化合物と反応する官能基を有するポリカーボネートオリゴマーとを反応させて得られるポリチオカーボネートである上記(17)に記載の含硫黄重合体。
(20)上記(17)〜(19)のいずれかに記載の含硫黄重合体を含有する光学材料。
(18)上記(1)〜(14)のいずれかに記載の硫黄含有化合物の中から選ばれる少なくとも一種と、ポリイソシアナート化合物、ポリイソチオシアナート化合物およびイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物との重合生成物である上記(17)に記載の含硫黄重合体。
(19)上記(1)〜(14)のいずれかに記載の硫黄含有化合物の中から選ばれる少なくとも一種と、二価フェノールまたは末端にこれら硫黄含有化合物と反応する官能基を有するポリカーボネートオリゴマーとを反応させて得られるポリチオカーボネートである上記(17)に記載の含硫黄重合体。
(20)上記(17)〜(19)のいずれかに記載の含硫黄重合体を含有する光学材料。
本発明によれば、高屈折率、高アッベ数で、透明性に優れ、かつ耐熱性等に優れた含硫黄重合体を与える、ジチオール化合物とジエン化合物との反応生成物である硫黄含有化合物、その製造方法および該硫黄含有化合物の少なくとも一種を構成成分の一つとする、高屈折率、高アッベ数で、透明性に優れ、かつ耐熱性等に優れた含硫黄重合体および該重合体を含有する光学材料を提供することができる。該硫黄含有化合物は、前記含硫黄重合体用原料の外、ポリカーボネート樹脂用原料、ポリウレタン樹脂用原料、エポキシ硬化剤、接着剤、塗料硬化剤、合成樹脂の加硫剤、メタクリレート樹脂、アクリレート樹脂、エポキシ樹脂の中間体等の多種多様な用途で使われている原料として有用である。また、該含硫黄重合体は、特に高屈折率・高アッベ数を有する眼鏡レンズ、視力矯正用眼鏡レンズ、カメラレンズ、ピックアップレンズなどに代表されるプラスチック光学レンズ、情報記録用光ディスク基板、液晶セル用プラスチック基板、プリズム、光ファイバー、光導波路などの各種光学部品に好適に使用することができる。
以下、本発明を詳細に説明する。
本発明の硫黄含有化合物は、例えば、下記スキーム(A)に示したように、ジチオール化合物(II)とジエン化合物(III)とを反応させることにより得られる。該ジチオールと該ジエンは、それぞれ1種ずつとは限らず、それぞれ1種以上用いても良い。
HS−G1−SH + G2”→ X−(S−G1−S−G2)n−S−G1−S−X’ (A)
(II) (III) (I)
(式中、XおよびX’はそれぞれ独立に−Hまたは−G2’を表す。G1は、硫黄および/または酸素原子を含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2とG2’はG2”由来の反応基であり、G2はG2”の炭素―炭素二重結合が二つ反応したものであり、G2’はG2”の炭素―炭素二重結合が一つ反応したものであり、G2”は炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち、少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である。nは1〜200の整数である)。
本発明の硫黄含有化合物は、例えば、下記スキーム(A)に示したように、ジチオール化合物(II)とジエン化合物(III)とを反応させることにより得られる。該ジチオールと該ジエンは、それぞれ1種ずつとは限らず、それぞれ1種以上用いても良い。
HS−G1−SH + G2”→ X−(S−G1−S−G2)n−S−G1−S−X’ (A)
(II) (III) (I)
(式中、XおよびX’はそれぞれ独立に−Hまたは−G2’を表す。G1は、硫黄および/または酸素原子を含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2とG2’はG2”由来の反応基であり、G2はG2”の炭素―炭素二重結合が二つ反応したものであり、G2’はG2”の炭素―炭素二重結合が一つ反応したものであり、G2”は炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち、少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である。nは1〜200の整数である)。
該反応は、ジチオール(II)とジエン(III)を混合するだけで進行することもあるが、用いるジエン(III)の種類によって、加熱、光照射、触媒が必要である。加熱する場合、温度としては、0℃から200℃が好ましい。用いる触媒としては、重合させるジエン(III)の反応基の種類にもよるが、アミン類(例えば、エチルアミン、アミノエタノール、トリエチルアミン、トリブチルアミン、N,N-ジエチルアミノエタノール、トリエタノールアミン、ピリジン、モルホリン、イミダゾール、アニリン、エチレンジアミンなど);アゾ系ラジカル開始剤(例えば、2,2’−アゾビスイソブチロニトリル(AIBN)、2,2’−アゾビス (2,4−ジメチルバレロニトリル)(ADVN)、2,2’−アゾビス (2−メチルプロピオン酸メチル)、2,2’−アゾビス(2−メチルブチロニトリル)(AMBN)、2,2’−アゾビス(2,4’−ジメチル-4-メトキシバレロニトリル)(V−70)、4,4’-アゾビス(4−シアノペンタン酸)(ACVA);過酸化物系ラジカル開始剤(例えば、ラウロイルパーオキシド、ベンゾイルパーオキシド、ビス(4−tert−ブチルシクロヘキシル)パーオキシジカーボネート、tert−ブチルパーオキシ−2−エチルヘキサノエート、メチルエチルケトンパーオキシド、過酸化水素水、空気、酸素、オゾン);ホスフィン類(例えば、トリメチルホスフィン、トリエチルホスフィン、トリプロピルホスフィン、トリブリルホスフィン、トリフェニルホスフィン);ルイス酸(例えば、塩化アルミ、塩化亜鉛、塩化鉄、塩化チタン、ジメチル錫ジクロリド、ジメチル錫オキシド、テトラクロロ錫、モノブチル錫トリクロリド、ジブチル錫ジクロリド、トリブチル錫クロリド、テトラブチル錫、ジブチル錫オキシド、ジブチル錫ジウラート、ジブチル錫ジラウレート、ジブチル錫オクタノエート、ステアリン酸錫、テトライソプロポキシチタン、テトラブトキシチタン、トリエチルボラン、9−ボラビシクロ[3.3.1]ノナン(9-BBN)、三フッ化ホウ素);が挙げられる。
反応溶媒は、用いても用いなくても良いが、用いる場合は、炭化水素類(例えば、ペンタン、ヘキサン、シクロヘキサン、ヘプタン、オクタン、ノナン、デカン);芳香族類(例えば、ベンゼン、トルエン、キシレン、クロロベンゼン);ハロゲン化炭化水素類(例えば、クロロホルム,ジクロロメタン、ジクロロエタン,四塩化炭素);ケトン類(例えば、アセトン,メチルエチルケトン、イソプロピルケトン、イソホロン);エステル類(例えば、酢酸エチル、酢酸メチル);エーテル類(例えば、ジエチルエーテル,tert―ブチルメチルエーテル、モノグライム、テトラヒドロフラン、ジオキサン);水;アルコール類(例えば、メタノール,エタノール、プロパノール、イソプロパノール、ブタノール、エチレングリコール、ジエチレングリコール、トリエチレングリコール);および非プロトン性極性溶媒(例えば、アセトニトリル、ジメチルスルホキシド,N,N−ジメチルホルムアミド、N−メチルピロリドン)等;が挙げられる。
反応温度は、用いるジチオールやジエンの種類、ジチオールとジエンとの反応モル比、反応溶媒の種類や使用量、用いる触媒の種類や使用量によって異なり、一概に定まらない。実際には、例えば、触媒に塩基を用い、無溶媒の場合は、ジチオールとジエンの混合物が溶解し、攪拌できる温度が好ましく、室温から150℃が好ましい。また、触媒に塩基を用い、かつ溶媒を用いるときは、溶媒の室温から溶媒の還流温度が好ましい。触媒にラジカル開始剤を用い、無溶媒の場合、ジチオールとジエンの混合物が溶解し、攪拌できる温度や、ラジカル開始剤の10時間半減期の温度付近で反応させることが好ましい。触媒にラジカル開始剤および溶媒を用いる場合、室温から溶媒の還流する温度や用いるラジカル開始剤の10時間半減期の温度付近が好ましい。反応に光照射をするときは、0℃から溶媒の沸点までが好ましい。
生成したオリゴマーは、2量体、3量体、4量体、それ以上の多量体の少なくとも1種類を含有し、未反応の原料を含んでも良いオリゴマーおよびオリゴマー混合物である。通常、反応生成物には、未反応の原料および数種類のオリゴマーが含まれている。
本発明において、無溶媒で反応を行った場合、そのまま光学材料用の重合体原料に用いることがでる。また、溶媒を用いて反応を行った場合、反応後溶媒を留去させ、光学材料の重合体原料として用いることもできる。また、樹脂の製造時に用いる溶媒を用いて反応させた場合は、そのまま重合体原料として用いることができる。必要に応じて、オリゴマーを単離精製または、必要なオリゴマー成分を取り出し、重合体原料に用いても良い。
生成したオリゴマーは、2量体、3量体、4量体、それ以上の多量体の少なくとも1種類を含有し、未反応の原料を含んでも良いオリゴマーおよびオリゴマー混合物である。通常、反応生成物には、未反応の原料および数種類のオリゴマーが含まれている。
本発明において、無溶媒で反応を行った場合、そのまま光学材料用の重合体原料に用いることがでる。また、溶媒を用いて反応を行った場合、反応後溶媒を留去させ、光学材料の重合体原料として用いることもできる。また、樹脂の製造時に用いる溶媒を用いて反応させた場合は、そのまま重合体原料として用いることができる。必要に応じて、オリゴマーを単離精製または、必要なオリゴマー成分を取り出し、重合体原料に用いても良い。
本発明においては、ジチオール化合物として、下記一般式(II)で表されるものが用いられる。
HS−G1−SH (II)
(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である)。
前記一般式(II)で表されるジチオール化合物の好ましいものとしては、G1が脂肪族基または脂環式炭化水素基であるものが挙げられる。G1が脂肪族基であるジチオール化合物の具体例としては、HSCH2CH2SH、HSCH2CH2CH2SH、HSCH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2CH2SH、HSCH2CH2OCH2CH2SHおよびHSCH2CH2SCH2CH2SHなどを好ましく挙げることができる。G1が脂環式炭化水素基である場合には、シクロヘキサン基を有するC6〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるジチオール化合物;ノルボルナン基を有するC7〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるジチオール化合物;アダマンタン基を有するC10〜C35の、脂環式炭化水素基であるジチオール化合物;等を挙げることができる。これらの中で下記化5に示されるジチオール化合物が好ましく挙げられる。本発明ではこれらのジチオール化合物は一種を単独で用いてもよく、二種以上を組み合わせて用いても良い。
HS−G1−SH (II)
(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である)。
前記一般式(II)で表されるジチオール化合物の好ましいものとしては、G1が脂肪族基または脂環式炭化水素基であるものが挙げられる。G1が脂肪族基であるジチオール化合物の具体例としては、HSCH2CH2SH、HSCH2CH2CH2SH、HSCH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2CH2SH、HSCH2CH2OCH2CH2SHおよびHSCH2CH2SCH2CH2SHなどを好ましく挙げることができる。G1が脂環式炭化水素基である場合には、シクロヘキサン基を有するC6〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるジチオール化合物;ノルボルナン基を有するC7〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるジチオール化合物;アダマンタン基を有するC10〜C35の、脂環式炭化水素基であるジチオール化合物;等を挙げることができる。これらの中で下記化5に示されるジチオール化合物が好ましく挙げられる。本発明ではこれらのジチオール化合物は一種を単独で用いてもよく、二種以上を組み合わせて用いても良い。
本発明においては、ジエン化合物として、下記一般式(III)で表されるものが用いられる。
G2” (III)
(G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
このG2”で表されるジエン化合物としては、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良いアクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、メタクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アリル基を有する脂肪族もしくは脂環式炭化水素化合物;および酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、ビニル基を有する脂肪族もしくは脂環式炭化水素化合物;の中から選ばれる少なくとも一つのジエン化合物を好ましく挙げることができ、具体的には、下記化6に示されるジエン化合物の中から選ばれる少なくとも一種を例示することができる。また、UA−NDP、UA−160TM,UA−122P(以上、新中村化学工業株式会社製)、BY16−152D、BY16−152B(以上、東レダウコーニング・シリコーン株式会社製)などを用いることができる。
G2” (III)
(G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。
このG2”で表されるジエン化合物としては、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良いアクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、メタクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アリル基を有する脂肪族もしくは脂環式炭化水素化合物;および酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、ビニル基を有する脂肪族もしくは脂環式炭化水素化合物;の中から選ばれる少なくとも一つのジエン化合物を好ましく挙げることができ、具体的には、下記化6に示されるジエン化合物の中から選ばれる少なくとも一種を例示することができる。また、UA−NDP、UA−160TM,UA−122P(以上、新中村化学工業株式会社製)、BY16−152D、BY16−152B(以上、東レダウコーニング・シリコーン株式会社製)などを用いることができる。
上記一般式(II)で表されるジチオール化合物は、例えば下記スキーム(B)
Cl−G1−Cl → HS−G1−SH (B)
(IV) (II)
(式中、G1は上記と同様である。)
で示されるように、ハロゲン化物(IV)にメルカプト化剤を反応させることにより合成することができる。上記スキーム(B)による代表的な合成方法としては、例えば、以下の(1)〜(5)の方法が挙げられる。
(1)ハロゲン化物(IV)とチオ尿素とを反応させてイソチウロニウム塩を合成し、このイソチウロニウム塩を加水分解することにより、ジチオール化合物を合成する方法。
(2)ハロゲン化物(IV)と、水硫化アルカリ金属塩とを反応させることにより、ジチオール化合物を合成する方法。
(3)ハロゲン化物(IV)とO−アルキルジチオ炭酸アルカリ金属塩とを反応させて、O−アルキルジチオ炭酸エステルを合成し、このO−アルキルジチオ炭酸エステルをアルカリ金属塩で加水分解することにより、ジチオール化合物を合成する方法。
(4)ハロゲン化物(IV)とチオ硫酸ナトリウムと反応させてブンテ(Bunte)塩を合成し、このブンテ塩を酸で加水分解することにより、ジチオール化合物を合成する方法。
(5)ハロゲン化物(IV)とチオカルボン酸アルカリ金属塩とを反応させてチオカルボン酸エステルを合成し、このチオカルボン酸エステルを塩基で加水分解することにより、ジチオール化合物を合成する方法。
Cl−G1−Cl → HS−G1−SH (B)
(IV) (II)
(式中、G1は上記と同様である。)
で示されるように、ハロゲン化物(IV)にメルカプト化剤を反応させることにより合成することができる。上記スキーム(B)による代表的な合成方法としては、例えば、以下の(1)〜(5)の方法が挙げられる。
(1)ハロゲン化物(IV)とチオ尿素とを反応させてイソチウロニウム塩を合成し、このイソチウロニウム塩を加水分解することにより、ジチオール化合物を合成する方法。
(2)ハロゲン化物(IV)と、水硫化アルカリ金属塩とを反応させることにより、ジチオール化合物を合成する方法。
(3)ハロゲン化物(IV)とO−アルキルジチオ炭酸アルカリ金属塩とを反応させて、O−アルキルジチオ炭酸エステルを合成し、このO−アルキルジチオ炭酸エステルをアルカリ金属塩で加水分解することにより、ジチオール化合物を合成する方法。
(4)ハロゲン化物(IV)とチオ硫酸ナトリウムと反応させてブンテ(Bunte)塩を合成し、このブンテ塩を酸で加水分解することにより、ジチオール化合物を合成する方法。
(5)ハロゲン化物(IV)とチオカルボン酸アルカリ金属塩とを反応させてチオカルボン酸エステルを合成し、このチオカルボン酸エステルを塩基で加水分解することにより、ジチオール化合物を合成する方法。
上記一般式(II)で表されるジチオール化合物は、例えば下記スキームC
HO−G1−OH → HS−G1−SH (C)
(V) (II)
に示されるように、ヒドロキシ化合物(V)にメルカプト化剤を反応させることによっても合成することができる。上記スキーム(C)による代表的な合成方法としては、例えば、ヒドロキシ化合物(V)を臭酸または塩酸の存在下、チオ尿素と反応させてイソチウロニウム塩とした後、加水分解することにより、ジチオール化合物を合成する方法が挙げられる。
HO−G1−OH → HS−G1−SH (C)
(V) (II)
に示されるように、ヒドロキシ化合物(V)にメルカプト化剤を反応させることによっても合成することができる。上記スキーム(C)による代表的な合成方法としては、例えば、ヒドロキシ化合物(V)を臭酸または塩酸の存在下、チオ尿素と反応させてイソチウロニウム塩とした後、加水分解することにより、ジチオール化合物を合成する方法が挙げられる。
脂環式ジチオール化合物は、例えば、スキームDに示されるように、対応する脂環式ジエン化合物(VI)にメルカプト化剤を反応させ、アルカリ金属塩で加水分解することにより合成することができる。下記スキーム(D)に示されるように、対応する脂環式ジエン化合物(VI)にチオ酢酸を反応させ、アセチルチオ化合物とした後、アルカリ金属塩で加水分解することにより、ジチオール化合物を得ることができる。
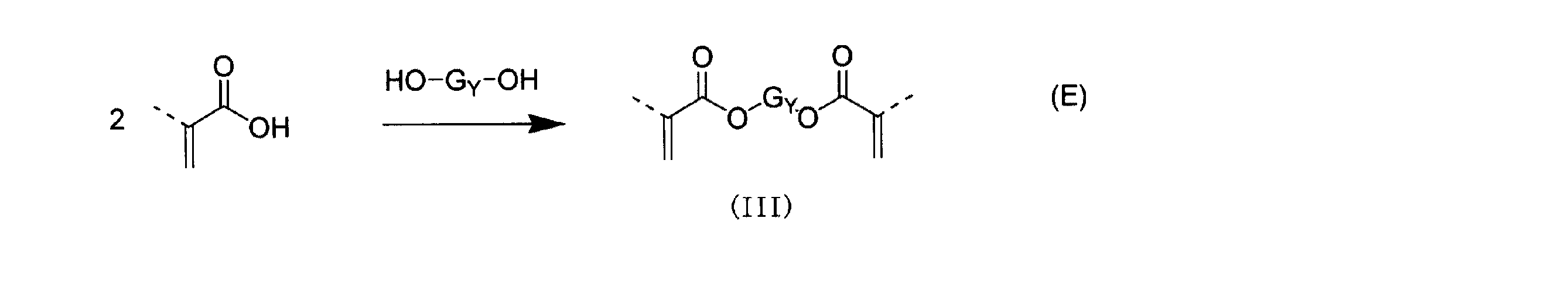
本発明で用いる一般式(III)で示されるジエン化合物のうち、炭素−炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも1つの原子を含んでも良い、アクリレート基または、メタクリレート基を有する脂肪族もしくは脂環式炭化水素化合物は、例えば、下記スキーム(E)に示されるように、(メタ)アクリル酸と対応するジオール(HO−GY−OH)を加熱下、反応させることにより得られる。例えば、(メタ)アクリル酸とジオール(HO−GY−OH)をトルエン溶媒中、p−トルエンスルホン酸または、メタンスルホン酸を用い、生成する水をディーンシュタークトラップ等で系外に留去することによりジ(メタ)アクリレート(III)を得ることができる。
また、スキーム(F)に示されるように、(メタ)アクリル酸クロリドと対応するジオール(HO−GY−OH)を塩基存在下、反応させることにより得られる。例えば、(メタ)アクリル酸クロリドとジオール(HO−GY−OH)をトルエン溶媒中トリエチルアミンを触媒に用い、ジ(メタ)アクリレート(III)を得ることができる。
本発明の含硫黄重合体としては、本発明の硫黄含有化合物を原料とする重合体であれば特に限定されないが、好ましくは、本発明の硫黄含有化合物の中から選ばれる少なくとも一種と、ポリイソシアナート化合物、ポリイソチオシアナート化合物およびイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物との重合生成物および二価フェノールまたは末端にこれら硫黄含有化合物と反応する官能基を有するポリカーボネートオリゴマーとを反応させて得られるポリチオカーボネートなどを挙げることができる。
前記硫黄含有化合物の中から選ばれる少なくとも一種と、ポリイソシアナート化合物、ポリイソチオシアナート化合物およびイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物との重合生成物において、ポリイソシアナート化合物、ポリイソチオシアナート化合物、及びイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物と、硫黄含有化合物との使用割合は、[(NCO+NCS)/SH](官能基)がモル比で、通常0.5〜3.0、好ましくは0.5〜1.5となる量である。
該重合生成物は、通常、注型重合により得られる。具体的には、ポリイソシアナート化合物、ポリイソチオシアナート化合物、及びイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物と、硫黄含有化合物とを混合し、この混合液を必要に応じて適当な方法で脱泡を行なった後、モールド中に注入し、通常、低温から高温に徐々に昇温しながら重合させることにより、得られる。
重合温度および重合時間は、モノマーの組成、添加剤の種類、使用量によっても異なるが、一般的には20℃程度から開始し、120℃程度まで8〜24時間程度かけて昇温する。この際、重合後の離型性を容易にするため、モールドに公知の離型処理を施しても差し支えない。また、目的に応じて、公知の成形法におけると同様に、内部離型剤、鎖延長剤、架橋剤、光安定剤、紫外線吸収剤、酸化防止剤、油溶染料、充填剤などの種々の物質を添加しても良い。さらに、所望の反応速度に調整するために、ポリウレタンの製造において用いられる公知の反応触媒を適宜に添加することもできる。
重合温度および重合時間は、モノマーの組成、添加剤の種類、使用量によっても異なるが、一般的には20℃程度から開始し、120℃程度まで8〜24時間程度かけて昇温する。この際、重合後の離型性を容易にするため、モールドに公知の離型処理を施しても差し支えない。また、目的に応じて、公知の成形法におけると同様に、内部離型剤、鎖延長剤、架橋剤、光安定剤、紫外線吸収剤、酸化防止剤、油溶染料、充填剤などの種々の物質を添加しても良い。さらに、所望の反応速度に調整するために、ポリウレタンの製造において用いられる公知の反応触媒を適宜に添加することもできる。
該重合生成物は、チオカルバミン酸S−アルキルエステル系樹脂及び/またはジチオウレタン系樹脂を主材とするものであり、イソシアナート基とメルカプト基によるチオカルバミン酸S−アルキルエステル結合及び/またはイソチオシアナート基とメルカプト基によるジチオウレタン結合を主体とするものである。含硫黄重合体の使用目的によっては、これらの結合以外にアロハネート結合、ウレア結合、チオウレア結合、ビウレット結合等を含有しても差し支えない。例えば、チオカルバミン酸S−アルキルエステル結合に、さらにイソシアナート基を反応させたり、ジチオウレタン結合にさらにイソチオシアナート基を反応させて架橋密度を増大させることなどが挙げられ、これらは好ましい結果を与える場合が多い。この場合には反応温度を100℃以上とし、イソシアナート成分及び/またはイソチオシアナート成分を多く使用する。あるいはまた、アミン等を一部併用し、ウレア結合、ビウレット結合を利用することもできる。このようにイソシアナート化合物またはイソチオシアナート化合物と反応するメルカプト化合物以外のものを使用する場合には、特に着色の点に留意する必要がある。
ポリチオカーボネートは、上述したように、硫黄含有化合物と、二価フェノールまたは末端に硫黄含有化合物と反応する官能基を有するポリカーボネートオリゴマーとの反応により得られるものである。ポリカーボネートオリゴマーとしては、例えば塩化メチレン等の溶媒中において、公知の酸受容体の存在下、二価フェノールとホスゲン等のカーボネート前駆体との反応により、あるいは溶媒の存在下または不存在下、二価フェノールと炭酸エステル化合物等のカーボネート前駆体とのエステル交換反応などによって製造されたものを用いることができる。
二価フェノールとしては、2,2−ビス(4−ヒドロキシフェニル)プロパン(ビスフェノールA),ビス(4−ヒドロキシフェニル)メタン,1,1−ビス(4−ヒドロキシフェニル)エタン,1,2−ビス(4−ヒドロキシフェニル)エタン等のビス(4−ヒドロキシフェニル)アルカン、1,1−ビス(4−ヒドロキシフェニル)シクロヘキサン,1,1−ビス(4−ヒドロキシフェニル)シクロデカン等のビス(4−ヒドロキシフェニル)シクロアルカン、4,4’−ジヒドロキシジフェニル、ビス(4−ヒドロキシフェニル)オキシド、ビス(4−ヒドロキシフェニル)スルフィド、ビス(4−ヒドロキシフェニル)スルホン、ビス(4−ヒドロキシフェニル)スルホキシド、ビス(4−ヒドロキシフェニル)エーテル、ビス(4−ヒドロキシフェニル)ケトンなどが挙げられる。
硫黄含有化合物と上記ポリカーボネートオリゴマーとの反応における反応温度および反応時間は、モノマーの組成、添加剤の種類、使用量によっても異なるが、一般的には、0〜40℃で数分〜数日間、好ましくは10〜30℃で10分〜5時間程度である。必要に応じて、分子調節剤、触媒及び酸化防止剤などを添加しても良い。
上記ポリチオカーボネートにおいて、共重合組成は、1〜100質量%であることが好ましい。
二価フェノールとしては、2,2−ビス(4−ヒドロキシフェニル)プロパン(ビスフェノールA),ビス(4−ヒドロキシフェニル)メタン,1,1−ビス(4−ヒドロキシフェニル)エタン,1,2−ビス(4−ヒドロキシフェニル)エタン等のビス(4−ヒドロキシフェニル)アルカン、1,1−ビス(4−ヒドロキシフェニル)シクロヘキサン,1,1−ビス(4−ヒドロキシフェニル)シクロデカン等のビス(4−ヒドロキシフェニル)シクロアルカン、4,4’−ジヒドロキシジフェニル、ビス(4−ヒドロキシフェニル)オキシド、ビス(4−ヒドロキシフェニル)スルフィド、ビス(4−ヒドロキシフェニル)スルホン、ビス(4−ヒドロキシフェニル)スルホキシド、ビス(4−ヒドロキシフェニル)エーテル、ビス(4−ヒドロキシフェニル)ケトンなどが挙げられる。
硫黄含有化合物と上記ポリカーボネートオリゴマーとの反応における反応温度および反応時間は、モノマーの組成、添加剤の種類、使用量によっても異なるが、一般的には、0〜40℃で数分〜数日間、好ましくは10〜30℃で10分〜5時間程度である。必要に応じて、分子調節剤、触媒及び酸化防止剤などを添加しても良い。
上記ポリチオカーボネートにおいて、共重合組成は、1〜100質量%であることが好ましい。
本発明の含硫黄重合体は、各種添加剤を加えた含硫黄重合体組成物とすることができる。添加剤としては、離型剤、熱安定剤、紫外線吸収剤、ブルーインク剤などが挙げられる。
本発明の含硫黄重合体や上記含硫黄重合体組成物は、モノマー取り扱い時の硫黄臭による不快感や、後加工時の硫黄臭による不快感が無く、物性的には極めて低分散、高屈折率、耐熱性に優れ、かつ無色透明であり、軽量で、耐候性、耐衝撃性等に優れた特徴を有しており、眼鏡レンズ、カメラレンズ等の光学素子材料やグレージング材料、塗料、接着剤の材料として好適である。本発明の含硫黄重合体や含硫黄重合体組成物を素材とするレンズは、必要に応じ、反射防止、高硬度付与、耐摩耗性向上、耐薬品性向上、防曇性付与、あるいはファッション性付与等の改良を行うため、表面研磨、帯電防止処理、ハードコート処理、無反射コート処理、染色処理、調光処理等の物理的あるいは化学処理を施すことができる。
本発明の含硫黄重合体や上記含硫黄重合体組成物は、モノマー取り扱い時の硫黄臭による不快感や、後加工時の硫黄臭による不快感が無く、物性的には極めて低分散、高屈折率、耐熱性に優れ、かつ無色透明であり、軽量で、耐候性、耐衝撃性等に優れた特徴を有しており、眼鏡レンズ、カメラレンズ等の光学素子材料やグレージング材料、塗料、接着剤の材料として好適である。本発明の含硫黄重合体や含硫黄重合体組成物を素材とするレンズは、必要に応じ、反射防止、高硬度付与、耐摩耗性向上、耐薬品性向上、防曇性付与、あるいはファッション性付与等の改良を行うため、表面研磨、帯電防止処理、ハードコート処理、無反射コート処理、染色処理、調光処理等の物理的あるいは化学処理を施すことができる。
次に、本発明を実施例によりさらに詳細に説明するが、本発明はこれらの例によってなんら限定されるものではない。
<屈折率およびアッベ数の測定方法>
屈折率およびアッベ数は、アッベ屈折率計(アタゴ社製)を用いて20℃にて測定した。試料が樹脂の場合、縦×横×厚み=20mm×8mm×3mmの試験片を作製し、中間液として硫黄−ヨウ化メチレン溶液を用いて測定した。試料が常温で固体粉末である場合、外挿法により屈折率を求め、この屈折率からアッベ数を求める。
<屈折率およびアッベ数の測定方法>
屈折率およびアッベ数は、アッベ屈折率計(アタゴ社製)を用いて20℃にて測定した。試料が樹脂の場合、縦×横×厚み=20mm×8mm×3mmの試験片を作製し、中間液として硫黄−ヨウ化メチレン溶液を用いて測定した。試料が常温で固体粉末である場合、外挿法により屈折率を求め、この屈折率からアッベ数を求める。
実施例1
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とノルボルナジエン化合物0.80g(8.64ミリモル)の混合物を70℃で5時間攪拌し、無色透明の粘性液体を得た。
得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
実施例2
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とジアリルエーテル0.85g(8.64ミリモル)の混合物を70℃にて5時間、90℃にて5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
実施例3
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とエチリデン-2-ノルボルネン1.04g(8.64ミリモル)の混合物を70℃にて5時間、90℃で5時間、120℃で5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、47であった。
実施例4
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)と5-ビニル-2-ノルボルネン1.04g(8.64ミリモル)の混合物を70℃にて5時間、90℃で5時間、120℃で5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
実施例5
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)8.94g(34.6ミリモル)とエチレングリコールジアクリレート2.94g(17.3ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、49であった。
実施例6
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)8.95g(34.6ミリモル)とジアリルアジペート3.91g(17.3ミリモル)の混合物を70℃にて5時間攪拌し、AIBN0.057g(0.35ミリモル)を加えて、70℃にて5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、53であった。
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とノルボルナジエン化合物0.80g(8.64ミリモル)の混合物を70℃で5時間攪拌し、無色透明の粘性液体を得た。
得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
実施例2
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とジアリルエーテル0.85g(8.64ミリモル)の混合物を70℃にて5時間、90℃にて5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
実施例3
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とエチリデン-2-ノルボルネン1.04g(8.64ミリモル)の混合物を70℃にて5時間、90℃で5時間、120℃で5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、47であった。
実施例4
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)と5-ビニル-2-ノルボルネン1.04g(8.64ミリモル)の混合物を70℃にて5時間、90℃で5時間、120℃で5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
実施例5
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)8.94g(34.6ミリモル)とエチレングリコールジアクリレート2.94g(17.3ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、49であった。
実施例6
メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)8.95g(34.6ミリモル)とジアリルアジペート3.91g(17.3ミリモル)の混合物を70℃にて5時間攪拌し、AIBN0.057g(0.35ミリモル)を加えて、70℃にて5時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、53であった。
実施例7
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とノルボルナジエン化合物1.59g(17.3ミリモル)の混合物を70℃にて7時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.60、アッベ数(νd)は、48であった。
実施例8
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とエチレングリコールジアクリレート2.94g(17.3ミリモル)、トリエチルアミン0.06g(0.6ミリモル)の混合物を70℃にて8時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例9
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジアリルエーテル1.70g(17.3ミリモル)の混合物を90℃にて8時間攪拌し、さらに2,2‘−アゾビスイソブチロニトリル(AIBN)0.06g(0.35ミリモル)を加え、90℃にて4時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、51であった。
実施例10
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジアリルアジペート3.91g(17.3ミリモル)の混合物を90℃にて8時間攪拌し、さらにAIBN0.06g(0.35ミリモル)を加え、90℃にて2時間、110℃にて2時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.59、アッベ数(νd)は、49であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とノルボルナジエン化合物1.59g(17.3ミリモル)の混合物を70℃にて7時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.60、アッベ数(νd)は、48であった。
実施例8
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とエチレングリコールジアクリレート2.94g(17.3ミリモル)、トリエチルアミン0.06g(0.6ミリモル)の混合物を70℃にて8時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例9
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジアリルエーテル1.70g(17.3ミリモル)の混合物を90℃にて8時間攪拌し、さらに2,2‘−アゾビスイソブチロニトリル(AIBN)0.06g(0.35ミリモル)を加え、90℃にて4時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、51であった。
実施例10
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジアリルアジペート3.91g(17.3ミリモル)の混合物を90℃にて8時間攪拌し、さらにAIBN0.06g(0.35ミリモル)を加え、90℃にて2時間、110℃にて2時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.59、アッベ数(νd)は、49であった。
実施例11
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とエチレングリコールジアクリレート4.41g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例12
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とノルボルナジエン化合物2.39g(25.9ミリモル)の混合物を70℃にて9時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.59、アッベ数(νd)は、46であった。
実施例13
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)と1,4-ブタンジオールジアクリレート5.14g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、49であった。
実施例14
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)と1,6-ヘキサンジオールジアクリレート5.86g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、49であった。
実施例15
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とジエチレングリコールジアクリレート5.55g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、51であった。
実施例16
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)と1,9-ノナンジオールジアクリレート4.64g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、52であった。
実施例17
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)トリプロピレングリコールジアクリレート5.19g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.53、アッベ数(νd)は、52であった。
実施例18
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)テトラエチレングリコールジアクリレート5.22g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、52であった。
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とエチレングリコールジアクリレート4.41g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例12
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とノルボルナジエン化合物2.39g(25.9ミリモル)の混合物を70℃にて9時間攪拌し、薄い黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.59、アッベ数(νd)は、46であった。
実施例13
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)と1,4-ブタンジオールジアクリレート5.14g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、49であった。
実施例14
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)と1,6-ヘキサンジオールジアクリレート5.86g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、49であった。
実施例15
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とジエチレングリコールジアクリレート5.55g(25.9ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、51であった。
実施例16
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)と1,9-ノナンジオールジアクリレート4.64g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、52であった。
実施例17
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)トリプロピレングリコールジアクリレート5.19g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.53、アッベ数(νd)は、52であった。
実施例18
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)テトラエチレングリコールジアクリレート5.22g(17.3ミリモル)、トリエチルアミン0.03g(0.3ミリモル)の混合物を70℃にて9時間攪拌し、更にトリエチルアミン0.10g(1.0ミリモル)を加え、70℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.54、アッベ数(νd)は、52であった。
実施例19
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,4-ブタンジオールジアクリレート3.43g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例20
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,6-ヘキサンジオールジアクリレート3.91g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて16時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、50であった。
実施例21
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジエチレングリコールジアクリレート3.70g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例22
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,9-ノナンジオールジアクリレート4.64g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例23
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とトリプロピレングリコールジアクリレート5.19g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、52であった。
実施例24
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とテトラエチレングリコールジアクリレート5.22g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、50であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,4-ブタンジオールジアクリレート3.43g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例20
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,6-ヘキサンジオールジアクリレート3.91g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて16時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、50であった。
実施例21
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とジエチレングリコールジアクリレート3.70g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて8時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例22
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)と1,9-ノナンジオールジアクリレート4.64g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例23
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とトリプロピレングリコールジアクリレート5.19g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、52であった。
実施例24
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.91g(25.9ミリモル)とテトラエチレングリコールジアクリレート5.22g(17.3ミリモル)、トリエチルアミン0.15g(1.5ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、50であった。
実施例25
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とエチレングリコールジアクリレート1.47g(8.64ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を90℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、52であった。
実施例26
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とエチレングリコールジアクリレート1.47g(8.64ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例27
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)2.63g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、50であった。
また、該淡黄色の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量1972であり、チャートの面積比から
モノマー :22.2%
ダイマー :20.1%
トリマー :16.5%
テトラマー :11.0%
ペンタマー以上 :28.3%
の重合度のオリゴマー混合物であった。
実施例28
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)5.26g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、50であった。
実施例29
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)2.63g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、53であった。
実施例30
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.90g(25.9ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)5.26g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、50であった。
また、淡黄色の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量3240であり、チャートの面積比から、
モノマー :10.2%
ダイマー :15.6%
トリマー :16.3%
テトラマー :12.0%
ペンタマー以上 :43.5%
の重合度のオリゴマー混合物であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とエチレングリコールジアクリレート1.47g(8.64ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を90℃にて9時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、52であった。
実施例26
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とエチレングリコールジアクリレート1.47g(8.64ミリモル)、トリエチルアミン0.05g(0.5ミリモル)の混合物を70℃にて9時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例27
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)2.63g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、50であった。
また、該淡黄色の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量1972であり、チャートの面積比から
モノマー :22.2%
ダイマー :20.1%
トリマー :16.5%
テトラマー :11.0%
ペンタマー以上 :28.3%
の重合度のオリゴマー混合物であった。
実施例28
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)5.26g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.57、アッベ数(νd)は、50であった。
実施例29
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)2.63g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、53であった。
実施例30
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)6.90g(25.9ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)5.26g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、50であった。
また、淡黄色の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量3240であり、チャートの面積比から、
モノマー :10.2%
ダイマー :15.6%
トリマー :16.3%
テトラマー :12.0%
ペンタマー以上 :43.5%
の重合度のオリゴマー混合物であった。
実施例31
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とエチレングリコールジメタクリレート(異性体混合物)1.71g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて3時間攪拌し、更にAIBN0.07g(0.4ミリモル)を加え、70℃にて4時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、47であった。
実施例32
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とエチレングリコールジメタクリレート(異性体混合物)1.71g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を90℃にて3時間攪拌し、更にAIBN0.07g(0.4ミリモル)を加え、90℃にて4時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、50であった。
実施例33
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.37g(20.2ミリモル)とエチレングリコールジアクリレート1.96g(11.5ミリモル)、トリエチルアミン0.06g(0.6ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例34
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.99g(22.5ミリモル)とエチレングリコールジアクリレート2.35g(13.8ミリモル)、トリエチルアミン0.14g(1.4ミリモル)の混合物を90℃にて20時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例35
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とネオペンチルグリコールジアクリレート(異性体混合物)1.83g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて14時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、48であった。
実施例36
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とネオペンチルグリコールジアクリレート(異性体混合物)5.50g(25.9ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて14時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
実施例37
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とトリシクロデカンジメタノールジメタクリレート(異性体混合物)2.87g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、更にAIBN0.03g(0.2ミリモル)を加え、80℃にて20時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、49であった。
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とエチレングリコールジメタクリレート(異性体混合物)1.71g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて3時間攪拌し、更にAIBN0.07g(0.4ミリモル)を加え、70℃にて4時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、47であった。
実施例32
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)とエチレングリコールジメタクリレート(異性体混合物)1.71g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を90℃にて3時間攪拌し、更にAIBN0.07g(0.4ミリモル)を加え、90℃にて4時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、50であった。
実施例33
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.37g(20.2ミリモル)とエチレングリコールジアクリレート1.96g(11.5ミリモル)、トリエチルアミン0.06g(0.6ミリモル)の混合物を90℃にて15時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例34
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.99g(22.5ミリモル)とエチレングリコールジアクリレート2.35g(13.8ミリモル)、トリエチルアミン0.14g(1.4ミリモル)の混合物を90℃にて20時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.58、アッベ数(νd)は、51であった。
実施例35
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とネオペンチルグリコールジアクリレート(異性体混合物)1.83g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて14時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、48であった。
実施例36
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)6.92g(34.6ミリモル)とネオペンチルグリコールジアクリレート(異性体混合物)5.50g(25.9ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて14時間攪拌し、無色透明の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
実施例37
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)3.46g(17.3ミリモル)とトリシクロデカンジメタノールジメタクリレート(異性体混合物)2.87g(8.64ミリモル)、トリエチルアミン0.09g(0.9ミリモル)の混合物を70℃にて10時間攪拌し、更にAIBN0.03g(0.2ミリモル)を加え、80℃にて20時間攪拌し、淡黄色の粘性液体を得た。得られた粘性液体の屈折率(nd)は、1.56、アッベ数(νd)は、49であった。
実施例38
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)とトリシクロデカンジメタノールジメタクリレート(異性体混合物)(新中村化学工業株式会社製)5.74g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)のジクロロメタン20mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、室温にて10時間攪拌した。更に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、室温にて16時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
ジメルカプト-オクタヒドロ-メタノ-インデン(異性体混合物)5.19g(25.9ミリモル)とトリシクロデカンジメタノールジメタクリレート(異性体混合物)(新中村化学工業株式会社製)5.74g(17.3ミリモル)、トリエチルアミン0.09g(0.9ミリモル)のジクロロメタン20mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、室温にて10時間攪拌した。更に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、室温にて16時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.56、アッベ数(νd)は、51であった。
実施例39
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.30g(19.9ミリモル)とネオペンチルグリコールジアクリレート(新中村化学工業株式会社製)2.38g(11.2ミリモル)、トリエチルアミン0.11g(1.1ミリモル)を90℃にて10時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.30g(19.9ミリモル)とネオペンチルグリコールジアクリレート(新中村化学工業株式会社製)2.38g(11.2ミリモル)、トリエチルアミン0.11g(1.1ミリモル)を90℃にて10時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例40
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.76g(21.6ミリモル)とネオペンチルグリコールジアクリレート(新中村化学工業株式会社製)2.75g(13.0ミリモル)、トリエチルアミン0.13g(1.3ミリモル)を90℃にて10時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)5.76g(21.6ミリモル)とネオペンチルグリコールジアクリレート(新中村化学工業株式会社製)2.75g(13.0ミリモル)、トリエチルアミン0.13g(1.3ミリモル)を90℃にて10時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例41
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)28.8g(108.0ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)(新中村化学工業株式会社製)19.7g(64.8ミリモル)、トリエチルアミン0.66g(6.48ミリモル)を90℃にて15時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.58、アッベ数(νd)は、48であった。
また、この無色透明の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量2904であり、
チャートの面積比から
モノマー :14.9%
ダイマー :18.1%
トリマー :16.3%
テトラマー :11.6%
ペンタマー以上 :36.8%
の重合度のオリゴマー混合物であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)28.8g(108.0ミリモル)とトリシクロデカンジメタノールジアクリレート(異性体混合物)(新中村化学工業株式会社製)19.7g(64.8ミリモル)、トリエチルアミン0.66g(6.48ミリモル)を90℃にて15時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.58、アッベ数(νd)は、48であった。
また、この無色透明の粘性液体は、ガスクロマトグラフィー法(GPC)による分析(東ソーカラム:TSK−8+G3000H8+G2000H8、検出器:RI検出器、温度:24℃、移動相:テトラヒドロフラン、流速:1.4ml/分、濃度2mg/ml)の結果、標準ポリスチレン換算で重量平均分子量2904であり、
チャートの面積比から
モノマー :14.9%
ダイマー :18.1%
トリマー :16.3%
テトラマー :11.6%
ペンタマー以上 :36.8%
の重合度のオリゴマー混合物であった。
実施例42
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)、トリシクロデカンジメタノールジアクリレート2.37g(7.78ミリモル)、UA−160TM(新中村化学工業株式会社製)1.38g(0.86ミリモル)とトリエチルアミン0.09g(0.86ミリモル)を90℃にて15時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.56、アッベ数(νd)は、48であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)、トリシクロデカンジメタノールジアクリレート2.37g(7.78ミリモル)、UA−160TM(新中村化学工業株式会社製)1.38g(0.86ミリモル)とトリエチルアミン0.09g(0.86ミリモル)を90℃にて15時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.56、アッベ数(νd)は、48であった。
実施例43
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)、トリシクロデカンジメタノールジアクリレート2.37g(7.78ミリモル)、UA−122P(新中村化学工業株式会社製)0.75gとトリエチルアミン0.09g(0.86ミリモル)を90℃にて9時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)4.60g(17.3ミリモル)、トリシクロデカンジメタノールジアクリレート2.37g(7.78ミリモル)、UA−122P(新中村化学工業株式会社製)0.75gとトリエチルアミン0.09g(0.86ミリモル)を90℃にて9時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。
該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、49であった。
実施例44
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)とBY16−152D(東レ・ダウコーニング・シリコーン株式会社製)2.84g(7.34ミリモル)のジクロロメタン10mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、40℃にて5時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、薄黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.54、アッベ数(νd)は、51であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)とBY16−152D(東レ・ダウコーニング・シリコーン株式会社製)2.84g(7.34ミリモル)のジクロロメタン10mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、40℃にて5時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、薄黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.54、アッベ数(νd)は、51であった。
実施例45
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、トリシクロデカンジメタノールジアクリレート2.12g(6.97ミリモル)とBY16−152B(東レ・ダウコーニング・シリコーン株式会社製)0.95g(0.37ミリモル)のジクロロメタン10mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、40℃にて5時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、薄黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、トリシクロデカンジメタノールジアクリレート2.12g(6.97ミリモル)とBY16−152B(東レ・ダウコーニング・シリコーン株式会社製)0.95g(0.37ミリモル)のジクロロメタン10mlの混合物に2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)0.06g(0.2ミリモル)を加え、40℃にて5時間攪拌した。反応終了後、減圧下ジクロロメタンを留去し、薄黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.55、アッベ数(νd)は、50であった。
実施例46
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、トリシクロデカンジメタノールジアクリレート1.79g(5.87ミリモル)、UA−NDP(新中村化学工業株式会社製)0.75gとトリエチルアミン0.07g(0.73ミリモル)を90℃にて18時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、トリシクロデカンジメタノールジアクリレート1.79g(5.87ミリモル)、UA−NDP(新中村化学工業株式会社製)0.75gとトリエチルアミン0.07g(0.73ミリモル)を90℃にて18時間攪拌し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.57、アッベ数(νd)は、48であった。
実施例47
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、ジアリルエーテル0.72g(7.34ミリモル)の塩化メチレン10mlの混合溶液に、加熱還流下、2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)(V−70)0.02g(0.07ミリモル)を加え、加熱還流下、7時間攪拌した。塩化メチレンを留去し、黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.58、アッベ数(νd)は、47であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、ジアリルエーテル0.72g(7.34ミリモル)の塩化メチレン10mlの混合溶液に、加熱還流下、2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)(V−70)0.02g(0.07ミリモル)を加え、加熱還流下、7時間攪拌した。塩化メチレンを留去し、黄色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.58、アッベ数(νd)は、47であった。
実施例48
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、ビニルメタクリレート0.82g(7.34ミリモル)の塩化メチレン10mlの混合溶液に、加熱還流下、2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)(V−70)0.02g(0.07ミリモル)を加え、加熱還流下、6時間攪拌した。塩化メチレンを留去し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.59、アッベ数(νd)は、46であった。
ジメルカプト−ドデカヒドロ−ジメタノ−シクロペンタ[b]ナフタレン(異性体混合物)3.91g(14.7ミリモル)、ビニルメタクリレート0.82g(7.34ミリモル)の塩化メチレン10mlの混合溶液に、加熱還流下、2,2′−アゾビス(4−メトキシ−2,4−ジメチルバレロニトリル)(V−70)0.02g(0.07ミリモル)を加え、加熱還流下、6時間攪拌した。塩化メチレンを留去し、無色透明の粘性液体のオリゴマー混合物を得た。該オリゴマー混合物の屈折率(nd)は、1.59、アッベ数(νd)は、46であった。
実施例49
実施例1で得られた、メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とノルボルナジエン化合物0.80g(8.64ミリモル)とを反応させて得られた無色透明の粘性液体5.27gと、m−キシリレンジイソシアナート1.63g(8.64ミリモル)と、ジブチル錫ジクロリド0.05gと、ジオクチル燐酸0.05gとを混合し、均一溶液とした後、室温にて減圧下脱泡した後、離型処理を施したガラスモールドとガスケットよりなるモールド型に注入した。次いで、40〜120℃まで徐々に昇温しながら20時間かけて加熱硬化させた。重合終了後、徐々に冷却し、含硫黄重合体をモールドより取り出した。得られた含硫黄重合体の屈折率(nd)は1.59、アッベ数(νd)は42であった。
実施例1で得られた、メルカプトプロポキシ−メルカプト−オクタヒドロ−メタノ−インデン(異性体混合物)4.47g(17.3ミリモル)とノルボルナジエン化合物0.80g(8.64ミリモル)とを反応させて得られた無色透明の粘性液体5.27gと、m−キシリレンジイソシアナート1.63g(8.64ミリモル)と、ジブチル錫ジクロリド0.05gと、ジオクチル燐酸0.05gとを混合し、均一溶液とした後、室温にて減圧下脱泡した後、離型処理を施したガラスモールドとガスケットよりなるモールド型に注入した。次いで、40〜120℃まで徐々に昇温しながら20時間かけて加熱硬化させた。重合終了後、徐々に冷却し、含硫黄重合体をモールドより取り出した。得られた含硫黄重合体の屈折率(nd)は1.59、アッベ数(νd)は42であった。
Claims (20)
- 下記一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物との反応生成物であって、該ジチオール化合物の残基に由来する構造単位と該ジエン化合物の残基に由来する構造単位とからなる繰り返し単位を有する、アッベ数(νd)40以上の硫黄含有化合物。
HS−G1−SH (II)
G2” (III)
(G1は、硫黄および/または酸素原子含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2”は、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である)。 - 一般式(II)で表されるジチオール化合物が、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有する請求項1に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物が、シクロヘキサン基を有するC6〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有する請求項1に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物が、ノルボルナン基を有するC7〜C35の、硫黄および/または酸素原子を含んでも良い脂環式炭化水素基であるG1を有する請求項1に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物が、アダマンタン基を有するC10〜C35の、脂環式炭化水素基であるG1を有する請求項1に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物が、HSCH2CH2SH、HSCH2CH2CH2SH、HSCH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2SH、HSCH2CH2CH2CH2CH2CH2SH、HSCH2CH2OCH2CH2SHおよびHSCH2CH2SCH2CH2SHの中から選ばれる少なくとも一種である請求項1に記載の硫黄含有化合物。
- 繰り返し単位中のジチオール化合物の残基に由来する構造単位とジエン化合物の残基に由来する構造単位とのモル比が、1:0.5〜0.5:1である請求項1〜7のいずれか1項に記載の硫黄含有化合物。
- G2”が、炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、メタクリレート基を有する脂肪族もしくは脂環式炭化水素化合物;酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、アリル基を有する脂肪族もしくは脂環式炭化水素化合物;および酸素、窒素、硫黄または珪素のうち少なくとも一つの原子を含んでも良い、ビニル基を有する脂肪族もしくは脂環式炭化水素化合物;の中から選ばれる少なくとも一種である請求項1〜8のいずれか1項に記載の硫黄含有化合物。
- G2”が、ノルボルナジエン化合物、エチリデンノルボルネン、ビニルノルボルネン、ジシクロペンタジエン化合物もしくはトリシクロペンタジエン化合物の中から選ばれる少なくとも一種である請求項1〜9のいずれか1項に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物との反応生成物が、下記一般式(I)で表される構造のチオコオリゴマーである請求項1〜11のいずれか1項に記載の硫黄含有化合物
X−(S−G1−S−G2)n−S―G1−S−X’ (I)
(式中、XおよびX’はそれぞれ独立に−Hまたは−G2’を表す。G1は、硫黄および/または酸素原子を含んでも良い脂肪族もしくは脂環式炭化水素基、置換されても良い芳香族基または縮合多環式芳香族基である。G2とG2’はG2”由来の反応基であり、G2はG2”の炭素―炭素二重結合が二つ反応したものであり、G2’はG2”の炭素―炭素二重結合が一つ反応したものであり、G2”は炭素―炭素二重結合を二つ以上有し、酸素、窒素、硫黄または珪素のうち、少なくとも一つの原子を含んでも良い脂肪族もしくは脂環式炭化水素化合物、置換されても良い芳香族もしくは縮合多環式芳香族炭化水素化合物である。nは1〜200の整数である)。 - nが1〜20の整数である請求項12に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物を含有する請求項1〜13のいずれか1項に記載の硫黄含有化合物。
- 一般式(II)で表されるジチオール化合物と一般式(III)で表されるジエン化合物とを反応させることを特徴とする請求項1〜14のいずれか1項に記載の硫黄含有化合物の製造方法。
- ジチオール化合物とジエン化合物とのモル比が1:0.5〜0.5:1である請求項15に記載の硫黄含有化合物の製造方法。
- 請求項1〜14のいずれか1項に記載の硫黄含有化合物の中から選ばれる少なくとも一種を構成成分とする含硫黄重合体。
- 請求項1〜14のいずれか1項に記載の硫黄含有化合物の中から選ばれる少なくとも一種と、ポリイソシアナート化合物、ポリイソチオシアナート化合物およびイソシアナート基を有するイソチオシアナート化合物から選ばれる少なくとも一種の化合物との重合生成物である請求項17に記載の含硫黄重合体。
- 請求項1〜14のいずれか1項に記載の硫黄含有化合物の中から選ばれる少なくとも一種と、二価フェノールまたは末端にこれら硫黄含有化合物と反応する官能基を有するポリカーボネートオリゴマーとを反応させて得られるポリチオカーボネートである請求項17に記載の含硫黄重合体。
- 請求項17〜19のいずれか1項に記載の含硫黄重合体を含有する光学材料。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004119379A JP2005298736A (ja) | 2004-04-14 | 2004-04-14 | 硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 |
| CNA2005800123640A CN1946769A (zh) | 2004-04-14 | 2005-04-14 | 含硫化合物、其制造方法以及含硫聚合物和光学材料 |
| PCT/JP2005/007212 WO2005100443A1 (ja) | 2004-04-14 | 2005-04-14 | 硫黄含有化合物、その製造方法及び含硫黄重合体並びに光学材料 |
| US11/578,374 US20080146759A1 (en) | 2004-04-14 | 2005-04-15 | Sulfur-Containing Compound, Method for Producing Same, Sulfur-Containing Polymer, and Optical Material |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004119379A JP2005298736A (ja) | 2004-04-14 | 2004-04-14 | 硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005298736A true JP2005298736A (ja) | 2005-10-27 |
Family
ID=35330667
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004119379A Withdrawn JP2005298736A (ja) | 2004-04-14 | 2004-04-14 | 硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP2005298736A (ja) |
| CN (1) | CN1946769A (ja) |
Cited By (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006070279A (ja) * | 2005-11-01 | 2006-03-16 | Gika Oyo Kagi Kofun Yugenkoshi | 高光学性能の樹脂組成物 |
| JP2008231409A (ja) * | 2007-02-19 | 2008-10-02 | Mitsubishi Rayon Co Ltd | 硬化性組成物及びその硬化物 |
| JP2009513790A (ja) * | 2005-10-27 | 2009-04-02 | ピーアールシー−デソト インターナショナル,インコーポレイティド | ジメルカプタン末端ポリチオエーテルポリマー、ならびにその合成方法および使用方法 |
| JP2009520058A (ja) * | 2005-12-16 | 2009-05-21 | ピーピージー インダストリーズ オハイオ, インコーポレイテッド | 硫黄含有オリゴマーおよびそれから調製された高指数ポリウレタン |
| JP2009524725A (ja) * | 2006-02-22 | 2009-07-02 | ピーピージー インダストリーズ オハイオ インコーポレーテツド | 高衝撃ポリ(ウレタンウレア)ポリスルフィド |
| JP2009209277A (ja) * | 2008-03-05 | 2009-09-17 | Jsr Corp | 高アッベ数を有する高屈折率材料 |
| JP2010084122A (ja) * | 2008-09-05 | 2010-04-15 | Jsr Corp | 高アッベ数及び優れた耐熱性を有する高屈折率材料 |
| JP2010254880A (ja) * | 2009-04-28 | 2010-11-11 | Jsr Corp | 架橋重合体 |
| JP2011032360A (ja) * | 2009-07-31 | 2011-02-17 | Kureha Corp | フッ素樹脂および反射防止材料 |
| JP2014084326A (ja) * | 2012-10-19 | 2014-05-12 | Mitsubishi Gas Chemical Co Inc | 耐熱・耐候性樹脂組成物 |
| JP2015025092A (ja) * | 2013-07-29 | 2015-02-05 | 旭化成イーマテリアルズ株式会社 | 硬化性組成物 |
| JP2017508860A (ja) * | 2014-03-07 | 2017-03-30 | ピーアールシー−デソト インターナショナル,インコーポレイティド | ホスフィン触媒マイケル付加硬化性硫黄含有ポリマー組成物 |
| JP2018511559A (ja) * | 2015-01-29 | 2018-04-26 | シェブロン フィリップス ケミカル カンパニー エルピー | メルカプタン化ビニルノルボルネン組成物及びその作製方法 |
| WO2020262659A1 (ja) * | 2019-06-28 | 2020-12-30 | ホヤ レンズ タイランド リミテッド | 光学材料用重合性組成物、光学材料および光学材料の製造方法 |
| CN117003765A (zh) * | 2023-07-24 | 2023-11-07 | 深圳大学 | 降冰片二烯含硫化合物及制备方法、降冰片二烯光学材料 |
| WO2024202415A1 (ja) * | 2023-03-29 | 2024-10-03 | 株式会社ニコン | ポリスルフィド樹脂、前駆体、ポリスルフィド樹脂の製造方法、光学素子、光学系、赤外線カメラ用レンズ、光学装置 |
| CN118909254A (zh) * | 2024-08-21 | 2024-11-08 | 广东省大湾区华南理工大学聚集诱导发光高等研究院 | 一种有机光学材料用组合物和有机光学玻璃 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5444251B2 (ja) * | 2008-12-08 | 2014-03-19 | 三井化学株式会社 | 光学材料用重合性組成物、光学材料および光学材料の製造方法 |
| CN109651612A (zh) * | 2018-12-13 | 2019-04-19 | 江南大学 | 一种含硫高折射率光学树脂的制备方法 |
| CN113480722B (zh) * | 2021-08-06 | 2022-11-22 | 中国科学院过程工程研究所 | 一种聚碳酸酯及其制备方法和应用 |
| CN115232585B (zh) * | 2022-06-24 | 2023-11-24 | 同济大学 | 一种耐湿热水解的单组分环氧树脂组合物及其制备方法和应用 |
| CN120192464B (zh) * | 2025-05-27 | 2025-07-29 | 成都传视科技有限公司 | 一种高透复合材料的加工工艺、高透复合材料及其应用 |
-
2004
- 2004-04-14 JP JP2004119379A patent/JP2005298736A/ja not_active Withdrawn
-
2005
- 2005-04-14 CN CNA2005800123640A patent/CN1946769A/zh active Pending
Cited By (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009513790A (ja) * | 2005-10-27 | 2009-04-02 | ピーアールシー−デソト インターナショナル,インコーポレイティド | ジメルカプタン末端ポリチオエーテルポリマー、ならびにその合成方法および使用方法 |
| JP2006070279A (ja) * | 2005-11-01 | 2006-03-16 | Gika Oyo Kagi Kofun Yugenkoshi | 高光学性能の樹脂組成物 |
| JP2009520058A (ja) * | 2005-12-16 | 2009-05-21 | ピーピージー インダストリーズ オハイオ, インコーポレイテッド | 硫黄含有オリゴマーおよびそれから調製された高指数ポリウレタン |
| JP2009524725A (ja) * | 2006-02-22 | 2009-07-02 | ピーピージー インダストリーズ オハイオ インコーポレーテツド | 高衝撃ポリ(ウレタンウレア)ポリスルフィド |
| JP2008231409A (ja) * | 2007-02-19 | 2008-10-02 | Mitsubishi Rayon Co Ltd | 硬化性組成物及びその硬化物 |
| JP2009209277A (ja) * | 2008-03-05 | 2009-09-17 | Jsr Corp | 高アッベ数を有する高屈折率材料 |
| JP2010084122A (ja) * | 2008-09-05 | 2010-04-15 | Jsr Corp | 高アッベ数及び優れた耐熱性を有する高屈折率材料 |
| JP2010254880A (ja) * | 2009-04-28 | 2010-11-11 | Jsr Corp | 架橋重合体 |
| JP2011032360A (ja) * | 2009-07-31 | 2011-02-17 | Kureha Corp | フッ素樹脂および反射防止材料 |
| JP2014084326A (ja) * | 2012-10-19 | 2014-05-12 | Mitsubishi Gas Chemical Co Inc | 耐熱・耐候性樹脂組成物 |
| JP2015025092A (ja) * | 2013-07-29 | 2015-02-05 | 旭化成イーマテリアルズ株式会社 | 硬化性組成物 |
| JP2017508860A (ja) * | 2014-03-07 | 2017-03-30 | ピーアールシー−デソト インターナショナル,インコーポレイティド | ホスフィン触媒マイケル付加硬化性硫黄含有ポリマー組成物 |
| JP2018511559A (ja) * | 2015-01-29 | 2018-04-26 | シェブロン フィリップス ケミカル カンパニー エルピー | メルカプタン化ビニルノルボルネン組成物及びその作製方法 |
| WO2020262659A1 (ja) * | 2019-06-28 | 2020-12-30 | ホヤ レンズ タイランド リミテッド | 光学材料用重合性組成物、光学材料および光学材料の製造方法 |
| WO2024202415A1 (ja) * | 2023-03-29 | 2024-10-03 | 株式会社ニコン | ポリスルフィド樹脂、前駆体、ポリスルフィド樹脂の製造方法、光学素子、光学系、赤外線カメラ用レンズ、光学装置 |
| CN117003765A (zh) * | 2023-07-24 | 2023-11-07 | 深圳大学 | 降冰片二烯含硫化合物及制备方法、降冰片二烯光学材料 |
| CN118909254A (zh) * | 2024-08-21 | 2024-11-08 | 广东省大湾区华南理工大学聚集诱导发光高等研究院 | 一种有机光学材料用组合物和有机光学玻璃 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1946769A (zh) | 2007-04-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2005298736A (ja) | 硫黄含有化合物、その製造方法および含硫黄重合体並びに光学材料 | |
| JP6557315B2 (ja) | ポリウレタン、ポリウレタン(ウレア)、硫黄含有ポリウレタンおよび硫黄含有ポリウレタン(ウレア)ならびに調製方法 | |
| EP1456264A1 (en) | High refractive index and high impact resistant polythiourethane/urea material, method of manufacturing same and its use in the optical field | |
| AU2002363596A1 (en) | High refractive index and high impact resistant polythiourethane/urea material, method of manufacturing same and its use in the optical field | |
| EP3486272B1 (en) | Aromatic polythiol compound for optical material | |
| JPH065323B2 (ja) | ポリチオール化合物を用いて得られた光学材料及び光学製品 | |
| US5484872A (en) | Cyclic sulfide compound, polymerizable compositions for optical products and optical products formed thereof | |
| AU2002301988B2 (en) | Thiol compound, method for producing the same and optical product comprising the same | |
| WO2005100443A1 (ja) | 硫黄含有化合物、その製造方法及び含硫黄重合体並びに光学材料 | |
| EP0972772B1 (en) | Polyisocyanate compounds, process for producing the same and optical materials using the same | |
| JP2813535B2 (ja) | 光学材料及びその製造方法 | |
| CN1414987A (zh) | 光学树脂组合物 | |
| JPH1067736A (ja) | チオール化合物、含硫o−(メタ)アクリレート化合物およびその用途 | |
| JP2002348349A (ja) | 光学材料用重合体の製造方法 | |
| EP0976728B1 (en) | Polyisocyanate compound, process for the production thereof and optical resin material comprising the same | |
| JPH11100428A (ja) | 光学材料用組成物並びにプラスチックレンズおよびその製造方法 | |
| JP2001174601A (ja) | 光学製品 | |
| JPH09132563A (ja) | 含硫(メタ)アクリレート化合物およびその用途 | |
| JPH06256459A (ja) | 光学材料用重合体及びその製造方法 | |
| JP2002020433A (ja) | 単量体組成物及びその硬化物 | |
| JP3174762B2 (ja) | 光学製品 | |
| JP3029603B2 (ja) | 光学製品 | |
| EP0976727B1 (en) | Polyisocyanate compound, process for producing the same and optical resin materials using the same | |
| JPH10330450A (ja) | 硬化性組成物およびそれからなる光学材料 | |
| JP5986446B2 (ja) | (メタ)アクリレート化合物、これを用いた重合性組成物および樹脂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061221 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20091109 |