ES2922132T3 - Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae - Google Patents
Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae Download PDFInfo
- Publication number
- ES2922132T3 ES2922132T3 ES18177128T ES18177128T ES2922132T3 ES 2922132 T3 ES2922132 T3 ES 2922132T3 ES 18177128 T ES18177128 T ES 18177128T ES 18177128 T ES18177128 T ES 18177128T ES 2922132 T3 ES2922132 T3 ES 2922132T3
- Authority
- ES
- Spain
- Prior art keywords
- less
- protein
- ratio
- polysaccharide
- serotype
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229920001282 polysaccharide Polymers 0.000 title claims abstract description 302
- 239000005017 polysaccharide Substances 0.000 title claims abstract description 302
- 150000004676 glycans Chemical class 0.000 title claims abstract description 297
- 241000193998 Streptococcus pneumoniae Species 0.000 title claims abstract description 27
- 229940031000 streptococcus pneumoniae Drugs 0.000 title claims abstract description 27
- 238000004519 manufacturing process Methods 0.000 title claims description 12
- 238000000746 purification Methods 0.000 title description 103
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 190
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 190
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 97
- 238000000034 method Methods 0.000 claims abstract description 79
- 230000020477 pH reduction Effects 0.000 claims abstract description 55
- 239000013592 cell lysate Substances 0.000 claims abstract description 39
- 238000001914 filtration Methods 0.000 claims abstract description 35
- 238000013060 ultrafiltration and diafiltration Methods 0.000 claims abstract description 29
- 230000008569 process Effects 0.000 claims abstract description 28
- 239000006166 lysate Substances 0.000 claims abstract description 21
- 108020004707 nucleic acids Proteins 0.000 claims description 95
- 150000007523 nucleic acids Chemical class 0.000 claims description 95
- 102000039446 nucleic acids Human genes 0.000 claims description 95
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 24
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 12
- 239000002244 precipitate Substances 0.000 claims description 12
- 229940124733 pneumococcal vaccine Drugs 0.000 claims description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 4
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 2
- 229910017604 nitric acid Inorganic materials 0.000 claims description 2
- 230000000670 limiting effect Effects 0.000 abstract description 3
- 238000010979 pH adjustment Methods 0.000 abstract description 2
- 239000000243 solution Substances 0.000 description 88
- 210000004027 cell Anatomy 0.000 description 47
- 239000012465 retentate Substances 0.000 description 47
- 239000003795 chemical substances by application Substances 0.000 description 40
- KXGVEGMKQFWNSR-LLQZFEROSA-N deoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 KXGVEGMKQFWNSR-LLQZFEROSA-N 0.000 description 38
- 238000011026 diafiltration Methods 0.000 description 38
- 230000002101 lytic effect Effects 0.000 description 38
- 235000010633 broth Nutrition 0.000 description 35
- 229940009976 deoxycholate Drugs 0.000 description 29
- 238000005119 centrifugation Methods 0.000 description 27
- 239000012535 impurity Substances 0.000 description 27
- 238000001179 sorption measurement Methods 0.000 description 26
- 238000000855 fermentation Methods 0.000 description 22
- 230000004151 fermentation Effects 0.000 description 22
- 241001465754 Metazoa Species 0.000 description 20
- 230000001580 bacterial effect Effects 0.000 description 17
- 239000003599 detergent Substances 0.000 description 16
- 229910052799 carbon Inorganic materials 0.000 description 15
- BACYUWVYYTXETD-UHFFFAOYSA-N N-Lauroylsarcosine Chemical compound CCCCCCCCCCCC(=O)N(C)CC(O)=O BACYUWVYYTXETD-UHFFFAOYSA-N 0.000 description 14
- 239000012528 membrane Substances 0.000 description 11
- 230000009467 reduction Effects 0.000 description 9
- 239000002023 wood Substances 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 8
- 230000008859 change Effects 0.000 description 8
- 229960003964 deoxycholic acid Drugs 0.000 description 8
- 229910052500 inorganic mineral Inorganic materials 0.000 description 8
- 101150082581 lytA gene Proteins 0.000 description 8
- 239000002609 medium Substances 0.000 description 8
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 8
- 239000011550 stock solution Substances 0.000 description 8
- -1 tert-octylphenoxy Chemical group 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 230000009089 cytolysis Effects 0.000 description 7
- 239000011707 mineral Substances 0.000 description 7
- 229960005486 vaccine Drugs 0.000 description 7
- 239000002253 acid Substances 0.000 description 6
- 230000006037 cell lysis Effects 0.000 description 6
- 150000001875 compounds Chemical class 0.000 description 6
- 238000004128 high performance liquid chromatography Methods 0.000 description 6
- 230000002934 lysing effect Effects 0.000 description 6
- 238000001542 size-exclusion chromatography Methods 0.000 description 6
- 238000001228 spectrum Methods 0.000 description 6
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 238000004042 decolorization Methods 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 238000004062 sedimentation Methods 0.000 description 5
- ADWNFGORSPBALY-UHFFFAOYSA-M sodium;2-[dodecyl(methyl)amino]acetate Chemical compound [Na+].CCCCCCCCCCCCN(C)CC([O-])=O ADWNFGORSPBALY-UHFFFAOYSA-M 0.000 description 5
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 230000001413 cellular effect Effects 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 239000012064 sodium phosphate buffer Substances 0.000 description 4
- 238000000108 ultra-filtration Methods 0.000 description 4
- 108010060123 Conjugate Vaccines Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical group CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 3
- 229920004890 Triton X-100 Polymers 0.000 description 3
- 238000013019 agitation Methods 0.000 description 3
- 210000002421 cell wall Anatomy 0.000 description 3
- RUDATBOHQWOJDD-BSWAIDMHSA-N chenodeoxycholic acid Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 RUDATBOHQWOJDD-BSWAIDMHSA-N 0.000 description 3
- 229960001231 choline Drugs 0.000 description 3
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 229940031670 conjugate vaccine Drugs 0.000 description 3
- 238000011068 loading method Methods 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000000569 multi-angle light scattering Methods 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 230000007935 neutral effect Effects 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000003998 size exclusion chromatography high performance liquid chromatography Methods 0.000 description 3
- 238000011146 sterile filtration Methods 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- KVGOXGQSTGQXDD-UHFFFAOYSA-N 1-decane-sulfonic-acid Chemical compound CCCCCCCCCCS(O)(=O)=O KVGOXGQSTGQXDD-UHFFFAOYSA-N 0.000 description 2
- QPRDKAJJYCDOFV-UHFFFAOYSA-N CCCCCCCCCCCCOC(=O)CCNCCC(O)=O Chemical compound CCCCCCCCCCCCOC(=O)CCNCCC(O)=O QPRDKAJJYCDOFV-UHFFFAOYSA-N 0.000 description 2
- 108010035713 Glycodeoxycholic Acid Proteins 0.000 description 2
- 206010018910 Haemolysis Diseases 0.000 description 2
- 238000003231 Lowry assay Methods 0.000 description 2
- 238000009013 Lowry's assay Methods 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 239000006161 blood agar Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 210000004899 c-terminal region Anatomy 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 230000008618 cell wall macromolecule catabolic process Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229940009025 chenodeoxycholate Drugs 0.000 description 2
- 229940099352 cholate Drugs 0.000 description 2
- BHQCQFFYRZLCQQ-OELDTZBJSA-N cholic acid Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 BHQCQFFYRZLCQQ-OELDTZBJSA-N 0.000 description 2
- 239000012141 concentrate Substances 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- 238000005187 foaming Methods 0.000 description 2
- WVULKSPCQVQLCU-BUXLTGKBSA-N glycodeoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 WVULKSPCQVQLCU-BUXLTGKBSA-N 0.000 description 2
- 230000008588 hemolysis Effects 0.000 description 2
- DGABKXLVXPYZII-SIBKNCMHSA-M hyodeoxycholate Chemical compound C([C@H]1[C@@H](O)C2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC([O-])=O)C)[C@@]2(C)CC1 DGABKXLVXPYZII-SIBKNCMHSA-M 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 229920000831 ionic polymer Polymers 0.000 description 2
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 229940031999 pneumococcal conjugate vaccine Drugs 0.000 description 2
- 238000011045 prefiltration Methods 0.000 description 2
- 230000006920 protein precipitation Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 238000009938 salting Methods 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 229910000162 sodium phosphate Inorganic materials 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000002798 spectrophotometry method Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- BHTRKEVKTKCXOH-BJLOMENOSA-N taurochenodeoxycholic acid Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCS(O)(=O)=O)C)[C@@]2(C)CC1 BHTRKEVKTKCXOH-BJLOMENOSA-N 0.000 description 2
- AWDRATDZQPNJFN-VAYUFCLWSA-N taurodeoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCS(O)(=O)=O)C)[C@@]2(C)[C@@H](O)C1 AWDRATDZQPNJFN-VAYUFCLWSA-N 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 2
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 1
- RUDATBOHQWOJDD-UHFFFAOYSA-N (3beta,5beta,7alpha)-3,7-Dihydroxycholan-24-oic acid Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)CC2 RUDATBOHQWOJDD-UHFFFAOYSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000283725 Bos Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 208000035109 Pneumococcal Infections Diseases 0.000 description 1
- 238000010306 acid treatment Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 238000012443 analytical study Methods 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- 239000003833 bile salt Substances 0.000 description 1
- 229940093761 bile salts Drugs 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000022534 cell killing Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229960001091 chenodeoxycholic acid Drugs 0.000 description 1
- 238000005352 clarification Methods 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- KXGVEGMKQFWNSR-UHFFFAOYSA-N deoxycholic acid Natural products C1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)C(O)C2 KXGVEGMKQFWNSR-UHFFFAOYSA-N 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 239000012538 diafiltration buffer Substances 0.000 description 1
- 239000012471 diafiltration solution Substances 0.000 description 1
- 238000011038 discontinuous diafiltration by volume reduction Methods 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000011143 downstream manufacturing Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000007392 microtiter assay Methods 0.000 description 1
- 235000006180 nutrition needs Nutrition 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000012466 permeate Substances 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 238000009522 phase III clinical trial Methods 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 150000004728 pyruvic acid derivatives Chemical class 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229930182490 saponin Natural products 0.000 description 1
- 150000007949 saponins Chemical class 0.000 description 1
- 235000017709 saponins Nutrition 0.000 description 1
- 238000009738 saturating Methods 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 230000001018 virulence Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/09—Lactobacillales, e.g. aerococcus, enterococcus, lactobacillus, lactococcus, streptococcus
- A61K39/092—Streptococcus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/646—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the entire peptide or protein drug conjugate elicits an immune response, e.g. conjugate vaccines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
- C07H1/06—Separation; Purification
- C07H1/08—Separation; Purification from natural products
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/0003—General processes for their isolation or fractionation, e.g. purification or extraction from biomass
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/04—Polysaccharides, i.e. compounds containing more than five saccharide radicals attached to each other by glycosidic bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6087—Polysaccharides; Lipopolysaccharides [LPS]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
Abstract
Se describe un proceso acortado para producir una solución que contiene polisacáridos capsulares sustancialmente purificados a partir de un caldo de lisado de Streptococcus pneumoniae celular. Ultrafilterización y diafilteración de un lisado aclarado de S. pneumoniae seguido de un ajuste de pH a menos de 4.5, preferiblemente aproximadamente 3.5, precipitó al menos el 98% de la proteína en la solución sin afectar seriamente el rendimiento del polisacárido. Además, después de la ultrafiltración y la diafiltración y la acidificación a un pH de menos de 4.5, la filtración usando carbono activado precipitó al menos el 90% de la proteína restante sin afectar seriamente el rendimiento de polisacáridos. Ejemplar, no limitante s. Los serotipos de pneumoniae que se pueden purificar utilizando el proceso acortado de la invención son 1, 4, 5, 6a, 6b, 7f, 9v, 14, 18c, 19a, 19f y 23f. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae
Campo de la invención
La presente invención se refiere a procedimientos para retirar el exceso de proteína soluble y otras impurezas de lisados celulares de serotipos de Streptococcus pneumoniae (S. pneumoniae) usados en la producción de polisacáridos purificados de neumococos.
Antecedentes de la invención
Streptococcus pneumoniae son cocos gram-positivos con forma de lanceta que se observan habitualmente en parejas (diplococos), pero también en cadenas cortas o como células individuales. Crecen fácilmente en placas de agar con sangre con colonias brillantes y presentan alfa hemolisis salvo que crezcan de forma anaeróbica donde muestran beta hemolisis. Son sensibles a las sales biliares que pueden descomponer la pared celular con la presencia de la propia enzima de las células, autolisina. El organismo es un anaerobio aerotolerante y es exigente porque tiene necesidades nutritivas complejas.
Las células de la mayoría de los serotipos de neumococos tienen una cápsula que es un polisacárido de recubrimiento que rodea cada célula. Esta cápsula es un determinante de virulencia en seres humanos porque impide la fagocitosis evitando que los anticuerpos ataquen a las células bacterianas. Actualmente existen 90 serotipos capsulares identificados, con 23 serotipos responsables de aproximadamente el 90 % de enfermedades invasivas. Como vacuna, el polisacárido puede conferir un grado razonable de inmunidad contra S. pneumoniae en individuos con sistemas inmunitarios desarrollados o no alterados. Sin embargo, cuando el polisacárido se conjuga con una proteína de alto peso molecular tal como CRM197 y se formula en una vacuna que contiene conjugados de múltiples serotipos, dichas vacunas de conjugado permiten una respuesta inmunitaria en lactantes y en ancianos que son los que están en mayor riesgo de infecciones por neumococos.
El polisacárido capsular para cada serotipo de S. pneumoniae utilizado para productos de vacuna se produce cultivando el organismo en medio líquido. La población del organismo a menudo se aumenta en escala desde un vial de siembra hasta frascos de siembra y se pasa a través de uno o más fermentadores de siembra de volumen creciente hasta que se alcanzan los volúmenes de fermentación a escala de producción. El final del ciclo de crecimiento puede determinarse por uno de varios medios, punto en el cual las células se lisan a través de la adición de un detergente u otro reactivo que ayude en la descomposición de la pared celular y libere autolisina que causa la lisis celular cuando las células alcanzan la fase estacionaria. El caldo después se recoge para procesamiento corriente abajo (purificación). Los contaminantes principales son proteínas celulares, ácidos nucleicos, polisacárido-C y componentes del medio.
Para la mayoría de los serotipos para la vacuna 7-valente de conjugado de neumococos (7vPnC) actualmente comercializada (Prevnar®), así como la vacuna 13-valente de conjugado de neumococos (13vPnC) recientemente desarrollada, el procedimiento actual de purificación requiere dieciséis etapas que incluyen muchas operaciones caras, muy laboriosas y exigen mucha tecnología, tal como cromatografía y múltiples separaciones en membrana. Los intentos previos de mejorar los procedimientos de purificación para polisacáridos de S. pneumoniae han incluido, por ejemplo, manipulación del pH durante la fermentación y la recuperación (véase la publicación de solicitud de patente de Estados Unidos Pub. Núm. 2006/0228381) y la precipitación con disolventes y detergentes. Sin embargo, la retirada de impurezas en estos procedimientos aún se extiende sobre muchas etapas muy laboriosas y costosas. El nivel de proteínas es la especificación más problemática de cumplir debido a las propiedades físicas y químicas de las proteínas solubles. El documento US5623057 desvela un procedimiento de purificación del polisacárido neumocócico preparado por medio de la hidrolización parcial de una preparación cruda hasta un punto final predeterminado. El documento EP1762245 desvela la eliminación de polisacáridos no ligados de vacunas de polisacáridos-proteínas conjugadas mediante el uso del procedimiento de ultrafiltración en el que la solución de diafiltración contiene niveles saturantes de sulfato de amonio. El documento EP0002404 desvela un procedimiento de purificación de polisacáridos neumocócicos que comprende una precipitación de alcohol en dos etapas. El documento WO82/01995 desvela un procedimiento de purificación de polisacáridos neumocócicos que comprende el tratamiento con fenol. El documento US2006228381 desvela un procedimiento de purificación de polisacáridos neumocócicos que utiliza la reducción del pH tras la lisis celular.
Por tanto, existe una necesidad de un procedimiento de purificación simplificado para reducir los niveles de proteína soluble en lisados de S. pneumoniae y eliminar las ineficacias del actual procedimiento de purificación de producción de polisacáridos capsulares sustancialmente purificados adecuados para su incorporación en vacunas de conjugado de neumococos.
Sumario de la divulgación
La presente divulgación se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados a partir de un lisado celular de Streptococcus pneumoniae. Este procedimiento comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen un serotipo seleccionado de Streptococcus pneumoniae;
(b) lisar las células bacterianas en la etapa (a) con un agente lítico, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido;
(e) disminuir el pH del retenido de la etapa (d) hasta menos de 4,5 para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido;
(f) mantener la solución acidificada de retenido formada en la etapa (e) durante un tiempo suficiente para permitir la sedimentación del precipitado, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) filtrar la solución aclarada de polisacárido de la etapa (f) a través de un filtro de carbono activado;
(h) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (g), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(i) filtrar la solución concentrada de polisacárido purificado producida por la etapa (h) usando un filtro estéril;
mediante lo cual se producen polisacáridos capsulares sustancialmente purificados en forma de una solución. Los serotipos no limitantes ejemplares de S. pneumoniae seleccionados para esta realización de la invención son 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19a , 19F, y 23f . En una realización particular, el pH de la etapa (e) se disminuye hasta aproximadamente 3,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 5,5 a aproximadamente 7,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 7,0 a aproximadamente 7,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH hasta aproximadamente 7,4. En otra realización más, la etapa (e) retira al menos el 98 % de las proteínas del retenido de la etapa (d). En otra realización, la etapa (g) retira al menos el 90 % de las proteínas de la solución aclarada de polisacárido de la etapa (f). En otra realización, el filtro de carbono activado de la etapa (g) comprende carbono activado con ácido fosfórico basado en madera. En otra realización, la etapa (f) comprende mantener la solución acidificada de retino formada en la etapa (e) durante al menos 2 horas. En otra realización más, el agente lítico de la etapa (b) es desoxicolato sódico (DOC). En otra realización, el agente lítico de la etapa (b) es un agente lítico de origen no animal. En otra realización más, el agente lítico de la etapa (b) es el agente lítico de origen no animal N-lauril sarcosina sódica (NLS).
El polisacárido capsular sustancialmente purificado producido por un procedimiento de la invención a partir de un lisado celular de Streptococcus pneumoniae puede usarse en la fabricación de una vacuna de neumococos, preferentemente una vacuna de neumococos que contiene polisacárido conjugado con un vehículo proteico.
La presente divulgación también se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados a partir de un lisado celular de Streptococcus pneumoniae que comprende el serotipo 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F o 23F. Este procedimiento comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen Streptococcus pneumoniae serotipo 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F o 23F;
(b) lisar las células bacterianas en la etapa (a) con un agente lítico, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) a temperatura ambiente a pH neutro en medio sin sal para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido sin sal;
(e) disminuir el pH del retenido sin sal de la etapa (d) hasta menos de 4,5 para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido;
(f) mantener la solución acidificada de retenido formada en la etapa (e) durante al menos 2 horas a temperatura ambiente para permitir la sedimentación del precipitado, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) filtrar la solución aclarada de polisacárido de la etapa (f) a través de un filtro de carbono activado;
(h) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (g), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(i) filtrar la solución concentrada de polisacárido purificado producida por la etapa (h) usando un filtro estéril;
mediante lo cual se producen polisacáridos capsulares sustancialmente purificados que comprenden el serotipo 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F o 23F en forma de una solución. En una realización particular, el pH de la etapa (e) se disminuye hasta aproximadamente 3,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 5,5 a aproximadamente 7,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 7,0 a aproximadamente 7,5. En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH hasta aproximadamente 7,4. En otra realización más, la etapa (e) retira al menos el 98 % de las proteínas del retenido sin sal de la etapa (d). En otra realización, la etapa (g) retira al menos el
90 % de las proteínas de la solución aclarada de polisacárido de la etapa (f). En otra realización, el filtro de carbono activado de la etapa (g) comprende carbono activado con ácido fosfórico basado en madera. En otra realización más, el agente lítico de la etapa (b) es desoxicolato sódico (DOC). En otra realización, el agente lítico de la etapa (b) es un agente lítico de origen no animal.
En otra realización más, el agente lítico de la etapa (b) es el agente lítico de origen no animal N-lauril sarcosina sódica (NLS).
La presente invención también se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados a partir de un lisado celular de Streptococcus pneumoniae que comprende el serotipo 19A. Este procedimiento comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen Streptococcus pneumoniae serotipo 19A;
(b) lisar las células bacterianas en la etapa (a) con un agente lítico, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) a aproximadamente 4 °C a un pH de aproximadamente 6 en tampón fosfato sódico para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido;
(e) disminuir el pH del retenido de la etapa (d) hasta menos de 4,5 para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido;
(f) mantener la solución acidificada de retenido formada en la etapa (e) durante al menos 2 horas a aproximadamente 4 °C para permitir la sedimentación del precipitado, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) ajustar el pH de la solución aclarada de polisacárido de la etapa (f) hasta aproximadamente 6, produciendo de ese modo una solución aclarada de polisacárido de pH ajustado;
(h) filtrar la solución aclarada de polisacárido de pH ajustado de la etapa (g) a través de un filtro de carbono activado;
(i) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (h), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(j) filtrar la solución concentrada de polisacárido purificado producida por la etapa (i) usando un filtro estéril;
mediante lo cual se producen polisacáridos capsulares sustancialmente purificados que comprenden el serotipo 19A en forma de una solución. En una realización particular, el pH de la etapa (e) se disminuye hasta aproximadamente 3,5. En otra realización, la diafiltración de la etapa (i) comprende un ajuste de pH entre aproximadamente 5,5 hasta aproximadamente 7,5. En otra realización, la diafiltración de la etapa (i) comprende un ajuste de pH entre aproximadamente 7,0 hasta aproximadamente 7,5. En otra realización, la diafiltración de la etapa (i) comprende un ajuste de pH hasta aproximadamente 7,4. En otra realización más, la etapa (e) retira al menos el 98 % de las proteínas del retenido de la etapa (d). En otra realización, la etapa (h) retira al menos el 90 % de las proteínas de la solución aclarada de polisacárido de pH ajustado de la etapa (g). En otra realización, el filtro de carbono activado de la etapa (h) comprende carbono activado con ácido fosfórico basado en madera. En otra realización, el tampón fosfato sódico de la etapa (d) es fosfato sódico 25 mM. En otra realización más, el agente lítico de la etapa (b) es desoxicolato sódico (DOC). En otra realización, el agente lítico de la etapa (b) es un agente lítico de origen no animal. En otra realización más, el agente lítico de la etapa (b) es el agente lítico de origen no animal N-lauril sarcosina sódica (NLS).
Breve descripción de los dibujos
La Figura 1 muestra el rendimiento promedio de polisacárido en el procedimiento (PS), la relación proteína/PS y la relación ácido nucleico (NA)/PS para el serotipo 5 usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 2 muestra los espectros de NMR para PS de serotipo 4 del actual procedimiento de purificación (A) en comparación con el PS de serotipo 4 del procedimiento acortado de purificación (B). No se observaron diferencias significativas entre los dos espectros. El segundo pico de la derecha en ambos espectros era piruvato, y la altura del pico del grupo piruvato era comparable en ambos espectros.
La Figura 3 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 4 usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 4 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 19A usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 5 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 7F usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
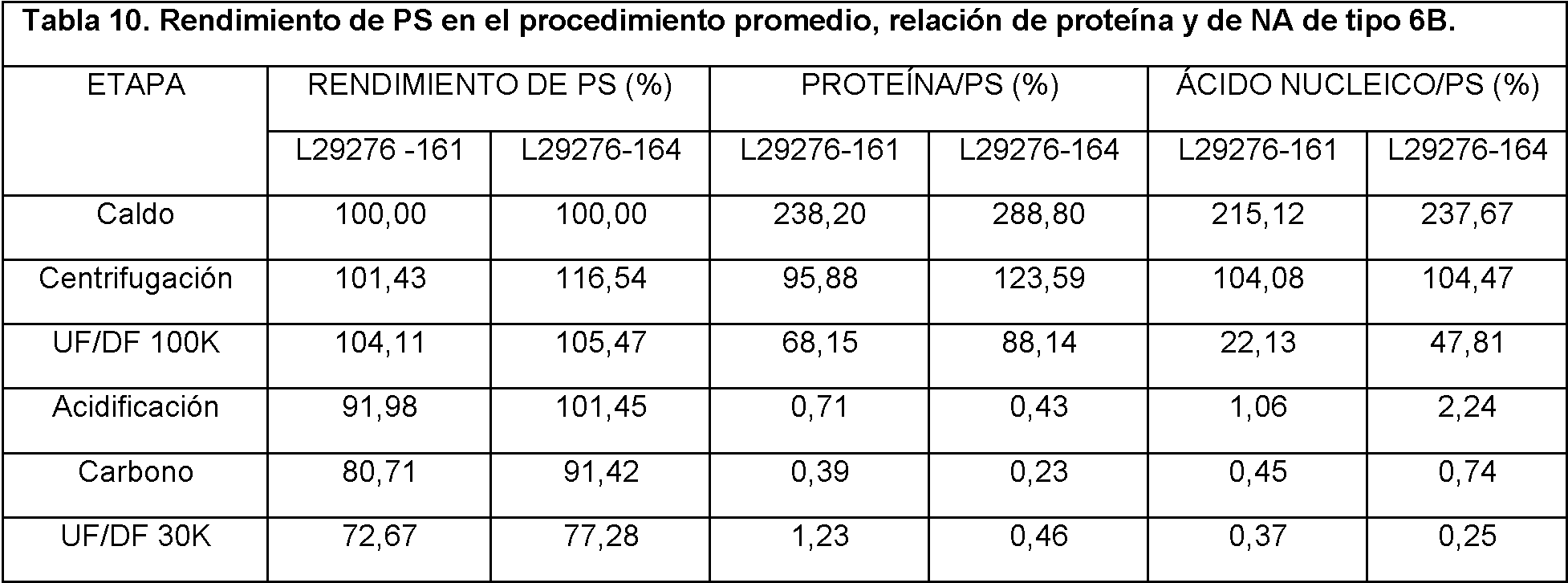
La Figura 6 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación
de NA/PS para el serotipo 6B usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 7 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 6B mediante el uso del procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 8 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 1 usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
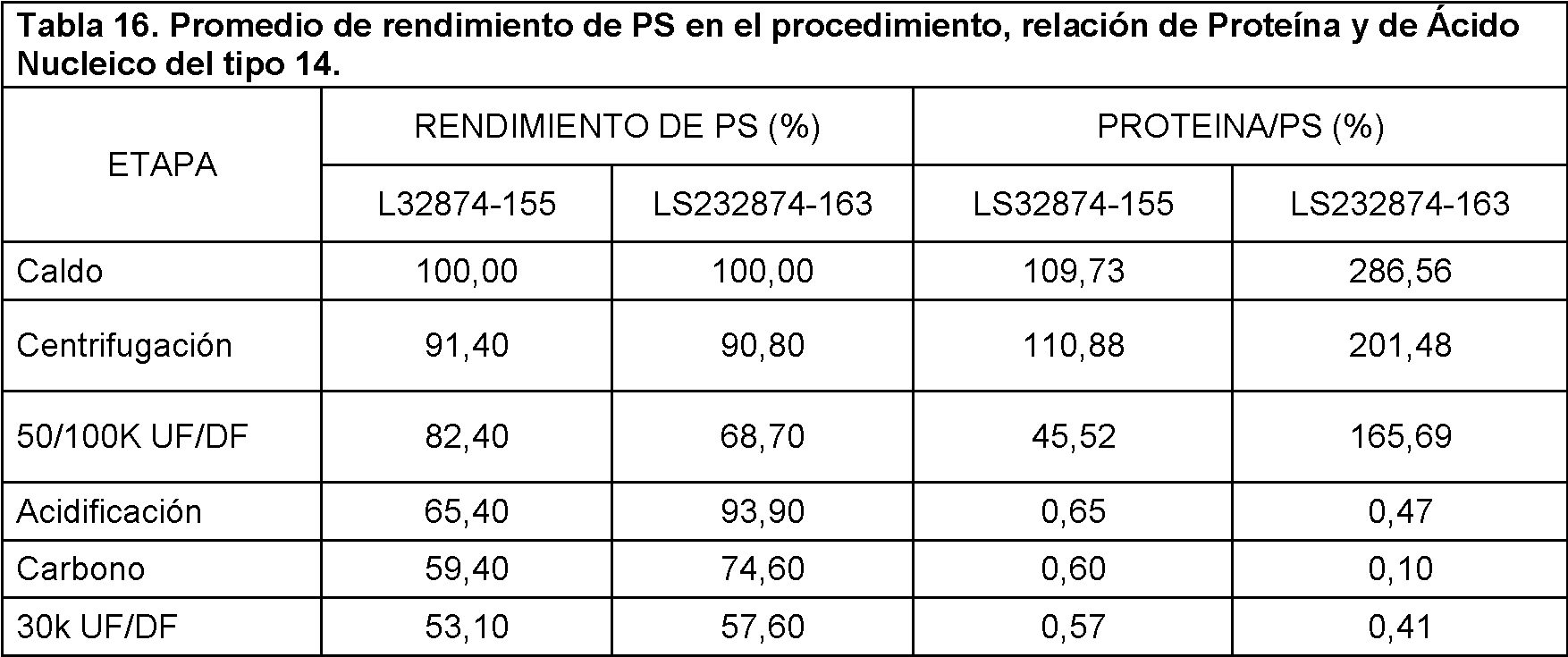
La Figura 9 muestra el rendimiento promedio de PS en el procedimiento, la relación de proteína/PS y la relación de NA/PS para el serotipo 14 usando el procedimiento acortado de purificación de la invención. Los resultados se muestran para cada etapa de purificación.
La Figura 10 muestra una comparación de los rendimientos de PS en el procedimiento para los serotipos 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, y 19F purificados usando el procedimiento acortado de purificación de la invención. La Figura 11 muestra una comparación de las relaciones de proteína/PS para los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, y 19F purificados usando el procedimiento acortado de purificación de la invención. Los resultados se comparan para cada etapa de purificación.
La Figura 12 muestra una comparación de las relaciones de NA/PS para los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, y 19F purificados usando el procedimiento acortado de purificación de la invención. Los resultados se comparan para cada etapa de purificación.
La Figura 13 muestra la eficacia de retirada de proteínas que se puede atribuir a la etapa de acidificación del procedimiento acortado de purificación de la invención. La diferencia en la concentración de proteínas (SDS-PAGE) antes y después de la acidificación se representa frente a la concentración inicial de proteínas antes de la acidificación para lotes de los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, y 19F. La diferencia de concentración de proteínas dividida por la concentración inicial de proteínas reflejaba la tasa de retirada de proteínas por la etapa de acidificación.
La Figura 14 muestra la eficacia de retirada de proteínas que se puede atribuir a la etapa de adsorción en carbono del procedimiento acortado de purificación de la invención. La cantidad de proteínas retirada (adsorbida sobre carbono) se representó frente a las cantidades iniciales de carga de proteínas para lotes de los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, y 19F. La cantidad de proteínas retiradas dividida por las cantidades iniciales de carga de proteínas reflejaba la tasa de retirada de proteínas por la etapa de adsorción en carbono.
Descripción detallada de la invención
La presente invención se refiere a un procedimiento acortado de purificación para reducir los niveles de proteínas solubles en lisados celulares de Streptococcus pneumoniae de producción de polisacáridos capsulares sustancialmente purificados adecuados para su incorporación en vacunas de conjugado de neumococos. Para la mayoría de los serotipos para la vacuna 7-valente de conjugado de neumococos (7vPnC) actualmente comercializada (Prevnar®), así como la vacuna 13-valente de conjugado de neumococos (13vPnC) recién desarrollada, el actual procedimiento de purificación de polisacáridos requiere hasta dieciséis etapas. Estas etapas implican muchas operaciones caras, muy laboriosas y exigen mucha tecnología, tal como cromatografía y múltiples separaciones en membrana. El procedimiento de la presente invención elimina hasta ocho de estas etapas consiguiendo al mismo tiempo la misma purificación y elimina la necesidad de cromatografía. Por tanto, la presente invención se refiere a un procedimiento más eficaz de purificación que es menos caro, consume menos tiempo e implica menos etapas.
El procedimiento acortado de purificación de la presente invención se refiere al descubrimiento de que la ultrafiltración y la diafiltración de un caldo de lisado celular aclarado de S. pneumoniae, seguido por acidificación del caldo de lisado concentrado con un ácido orgánico o uno mineral hasta un pH de 4,5, preferentemente aproximadamente 3,5, precipita al menos el 98 % de las proteínas en la solución sin afectar de forma grave al rendimiento de polisacáridos. Ultrafiltrando y diafiltrando el caldo de fermentación lisado y aclarado antes de la acidificación hasta un pH de menos de 4,5, preferentemente aproximadamente 3,5, se eliminan los efectos de "salado" de las proteínas y se aumenta la fracción de proteínas que está "desalada". "Salación" se refiere a solubilidad aumentada de las proteínas mientras que "desalado" se refiere a precipitación de las proteínas en solución según alcanzan sus puntos isoeléctricos. La etapa de ultrafiltración y de diafiltración también evita la formación de espuma observada cuando el caldo tratado con carbonato sódico experimenta acidificación incluso hasta un pH de 5,0 (véase la publicación de solicitud de patente de Estados Unidos Núm. 2006/0228381). Por tanto, la ultrafiltración y la diafiltración del caldo de lisado aclarado hace posible usar cualquier agente de titulación de pH de bajo peso molecular tal como carbonato sódico durante la fermentación del serotipo de S. pneumoniae y evita la formación de espuma del caldo de lisado aclarado cuando se acidifica hasta un pH de menos de 4,5.
"Caldo de lisado aclarado" se refiere a un caldo de lisado que ha experimentado centrifugación o filtración para retirar los desechos celulares.
"Diafiltrar", "diafiltración", "DF" y términos similares se refieren a, por ejemplo, usar membranas semipermeables con propiedades físicas y químicas apropiadas para retirar moléculas pequeñas de una solución.
"Ultrafiltrar", "ultrafiltración", "UF" y términos similares se refieren a, por ejemplo, usar membranas semipermeables
con propiedades físicas y químicas apropiadas para discriminar entre moléculas en una solución y moléculas de tipo concentrado en un volumen más pequeño de solución.
Dentro de los procedimientos de la presente invención, la ultrafiltración y la diafiltración típicamente comprenden filtración de "flujo transversal" o de "flujo tangencial" a fin de evitar la obstrucción de las membranas de filtración. En la filtración de "flujo transversal", la solución a filtrar se pasa a través de la superficie de la membrana. Los materiales que pasan a través de la membrana se mencionan como permeado. Los materiales que no pasan a través de la membrana se mencionan como retenido. El retenido se recicla hasta un depósito de alimentación para volver a filtrarse.
Como se usa en la presente memoria, se usa un ácido orgánico o uno mineral para disminuir el pH del caldo de lisado ultrafiltrado y diafiltrado siempre que se consiga un pH de menos 4,5, particularmente aproximadamente 3,5. Por consiguiente, pueden usarse ácidos tanto orgánicos como minerales dentro de los procedimientos de la invención. Como se usa en el presente documento, la expresión "ácido mineral" se refiere a un ácido derivado de mineral inorgánico por reacción química en oposición a los ácidos orgánicos. Los ejemplos no limitantes, ejemplares de ácidos minerales que pueden usarse dentro de los procedimientos de la presente invención incluyen ácido clorhídrico, ácido nítrico, ácido fosfórico y ácido sulfúrico. En realizaciones particulares, el pH del caldo de lisado concentrado se disminuye hasta menos de 4,4, 4,3, 4,2, 4,1, 4,0, 3,9, 3,8, 3,7, 3,6, 3,5, 3,4, 3,3, 3,2, 3,1 o 3,0. En otras realizaciones, el pH del caldo de lisado concentrado se disminuye hasta aproximadamente 4,4, aproximadamente 4,3, aproximadamente 4,2, aproximadamente 4,1, aproximadamente 4,0, aproximadamente 3,9, aproximadamente 3,8, aproximadamente 3,7, aproximadamente 3,6, aproximadamente 3,5, aproximadamente 3,4, aproximadamente 3,3, aproximadamente 3,2, aproximadamente 3,1, aproximadamente 3,0, aproximadamente 2,9, aproximadamente 2,8, aproximadamente 2,7, aproximadamente 2,6, aproximadamente 2,5, aproximadamente 2,4, aproximadamente 2,3, aproximadamente 2,2, aproximadamente 2,1 o aproximadamente 2,0.
El procedimiento acortado de purificación de la presente invención también se refiere al descubrimiento en que, en combinación con las etapas de concentración y bajo pH descritas anteriormente, la filtración mediante el uso de carbono activado precipita al menos el 90 % de las proteínas restantes sin afectar de forma grave al rendimiento de polisacáridos. En realizaciones particulares, la filtración con carbono usando carbono derivado de serrín u otros productos de la madera y activado con ácido fosfórico se descubrió que es más eficaz en reducir o retirar las impurezas de proteínas que carbonos usados dentro de los actuales procedimientos de filtración con carbono.
Por consiguiente, la presente invención se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados de un lisado celular de Streptococcus pneumoniae que comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen un serotipo seleccionado de Streptococcus pneumoniae;
(b) lisar las células bacterianas en la etapa (a) con un agente lítico, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido;
(e) disminuir el pH del retenido de la etapa (d) hasta menos de 4,5, particularmente aproximadamente 3,5, para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido;
(f) mantener la solución acidificada de retenido formada en la etapa (e) durante un tiempo suficiente para permitir la sedimentación del precipitado, particularmente durante al menos 2 horas con o sin agitación, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) filtrar la solución aclarada de polisacárido de la etapa (f) a través de un filtro de carbono activado, particularmente un filtro de carbono activado que comprende carbono activado por ácido fosfórico basado en madera;
(h) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (g), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(i) filtrar la solución concentrada de polisacárido purificado producida por la etapa (h) usando un filtro estéril; mediante lo cual se producen polisacáridos capsulares sustancialmente purificados en forma de una solución. La filtración a esterilidad de la etapa (i) es útil para retirar las bacterias y partículas de la solución concentrada de polisacárido purificado. Los serotipos no limitantes ejemplares de S. pneumoniae seleccionados para esta realización de la invención son 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, y 23F. En una realización particular, la etapa (e) retira al menos el 98 % de las proteínas del retenido de la etapa (d). En otra realización, la etapa (g) retira al menos el 90 % de las proteínas de la solución aclarada de polisacárido de la etapa (f). En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 5,5 a aproximadamente 7,5. Para una estabilidad mejorada del polisacárido capsular sustancialmente purificado durante almacenamiento a largo plazo, sin embargo, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 7,0 hasta aproximadamente 7,5, y más particularmente hasta aproximadamente 7,4.
Como se usa en la presente memoria, la expresión "lisado que contiene polisacárido capsular sustancialmente purificado" o "solución que contiene polisacáridos capsulares sustancialmente purificados" se refieren a un lisado celular o solución de Streptococcus pneumoniae a partir de la cual se han retirado las proteínas de forma que la relación porcentual de proteína a polisacárido (proteína/PS) sea de menos del 10 %, menos del 9 %, menos del 8 %, menos del 7 %, menos del 6 %, menos del 5 %, menos del 4 %, menos del 3 %, menos del 2 % o menos del 1 % y la relación porcentual de ácido nucleico a polisacárido (NA/PS) sea menos del 5 %, menos del 4 %, menos del 3 %, menos del 2 % o menos del 1 %. En realizaciones particulares, las relaciones porcentuales de proteína/PS y NA/PS para lisados o soluciones que contienen polisacárido capsular sustancialmente purificado que comprenden serotipos específicos son las siguientes: para el serotipo 1 la relación de proteína/PS es de menos del 2 % y la relación de nA/PS es menor del 2 %, para el serotipo 4 la relación de proteína/PS es menor del 3 % y la relación de NA/PS es menor del 2 %, para el serotipo 5 la relación de proteína/PS es menor o igual al 7,5 % y la relación de NA/PS es menor o igual 2 %, para el serotipo 6A la relación de proteína/PS es menor del 2 % y la relación de NA/PS es menor del 2 %, para el serotipo 6B la relación de proteína/PS es menor del 4 % y la relación de NA/PS es menor del 1 %, para el serotipo 7F la relación de proteína/PS es menor del 5 % y la relación de NA/PS es menor del 2 %, para el serotipo 9V la relación de proteína/PS es menor del 2 % y la relación de NA/PS es menor del 1 %, para el serotipo 14 la relación de proteína/PS es menor del 3 % y la relación de NA/PS es menor del 2 %, para el serotipo 18C la relación de proteína/PS es menor del 2 % y la relación de NA/PS es menor del 2 %, para el serotipo 19A la relación de proteína/PS es menor del 2 % y la relación de NA/PS es menor del 2 %, para el serotipo 19F la relación de proteína/PS es menor del 3 % y la relación de NA/PS es menor del 2 %, y para el serotipo 23F la relación de proteína/PS es menor del 2 % y la relación de NA/PS es menor del 2 %. Los procedimientos para la cuantificación de concentraciones de proteína, polisacárido y ácido nucleico en el lisado celular o solución son bien conocidos en la técnica e incluyen, por ejemplo, análisis SDS-PAGE (electroforesis en gel de poliacrilamida con dodecil sulfato sódico), HPLC (cromatografía de líquida de alto rendimiento) y SEC (cromatografía por exclusión de tamaño), ensayos de Lowry modificados, espectrofotometría, SEC-MALLS (cromatografía por exclusión de tamaño/dispersión de luz láser de múltiple ángulo), y NMR (resonancia magnética nuclear).
Dentro de los procedimientos de la presente invención, las células bacterianas se pueden lisar mediante el uso de cualquier agente lítico. Un "agente lítico" es cualquier agente que ayuda en la descomposición de la pared celular y libera la autolisina que causa lisis celular incluyendo, por ejemplo, detergentes. Como se usa en el presente documento, el término "detergente" se refiere a cualquier detergente aniónico o catiónico capaz de inducir la lisis de células bacterianas. Ejemplos representativos de dichos detergentes para su uso dentro de los procedimientos de la presente invención incluyen desoxicolato sódico (DOC), N-lauril sarcosina (NLS), ácido quenodesoxicólico de sodio y saponinas.
En una realización de la presente invención, el agente lítico usado para lisar las células bacterianas es DOC. DOC es la sal sódica del ácido biliar ácido desoxicólico, que se obtiene habitualmente de fuentes biológicas tales como vacas o bueyes. DOC activa la proteína LytA, que es una autolisina que está implicada en el crecimiento de la pared celular y en la división en Streptococcus pneumoniae. La proteína LytA tiene dominios de unión a colina en su parte C-terminal, y se sabe que mutaciones del gen lytA producen mutantes LytA que son resistentes a lisis con DOC.
Aunque no existen evidencias de que el uso de DOC durante la purificación de polisacáridos de Streptococcus pneumoniae posea un riesgo para la salud, el uso de dichos reactivos biológicamente derivados podría generar preocupaciones reguladoras potenciales. Por consiguiente, en una realización de la presente invención, el agente lítico usado para lisar las células bacterianas es un agente lítico de origen no animal. Los agentes líticos de origen no animal para su uso dentro de los procedimientos de la presente invención incluyen agentes de fuentes no animales con modos de acción similares a los de DOC (es decir, que afectan a la función LytA y provocan la lisis de células de Streptococcus pneumoniae). Dichos agentes líticos de origen no animal incluyen, aunque sin limitación, análogos de DOC, tensioactivos, detergentes y análogos estructurales de colina, y pueden determinarse usando procedimientos como se describe en la sección experimental en el presente documento a continuación. En una realización, el agente lítico no derivado de animales se selecciona del grupo que consiste en ácido decanesulfónico, tert-octilfenoxi poli(oxietileno)etanoles (porejemplo, Igepal® CA-630, CAS núm.: 9002-93-1, disponible en Sigma Aldrich, St), condensados de óxido de etileno de octilfenol (por ejemplo, Triton® X-100, disponible en Sigma Aldrich, St. Louis, MO), N-lauril sarcosina sódica (NLS), iminodipropionato de laurilo, dodecil sulfato de sodio, quenodesoxicolato, hiodeoxicolato, glicodeoxicolato, taurodeoxicolato, taurochenodesoxicolato y colato. En otra realización, el agente lítico de origen no animal es NLS.
La presente invención también se refiere a modificaciones específicas de serotipo al procedimiento descrito anteriormente. Por ejemplo, como el polisacárido de serotipo 19A es inestable y su peso molecular cambia durante la purificación, se descubrió que modificaciones al procedimiento descrito eran útiles para estabilizar el polisacárido 19A. Estas modificaciones incluían realizar la etapa de ultrafiltración y de diafiltración antes de la acidificación a aproximadamente 4 °C a un pH de aproximadamente 6 en tampón fosfato sódico, mantener la solución acidificada de retenido durante al menos 2 horas a aproximadamente 4 °C para permitir la sedimentación del precipitado y ajustar el pH de la solución aclarada de polisacárido hasta 6 antes de la etapa de filtración con carbono activado. En contraste, se descubrió que para los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F y 23F, se perdía menos polisacárido y se conseguía mayor retirada de proteínas cuando la etapa de ultrafiltración y de diafiltración antes de la acidificación se llevaba a cabo en medios sin sal tales como agua, y esta etapa se podía llevar a cabo a temperatura ambiente a pH neutro.
Por consiguiente, la presente invención también se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados de un lisado celular de Streptococcus pneumoniae que comprende el serotipo 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F o 23F, que comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen Streptococcus pneumoniae serotipo 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19F o 23F;
(b) lisar las células bacterianas en la etapa (a) con un detergente, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) a temperatura ambiente a pH neutro en medio sin sal para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido sin sal;
(e) disminuir el pH del retenido sin sal de la etapa (d) hasta menos de 4,5, particularmente aproximadamente 3,5, para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido;
(f) mantener la solución acidificada de retenido formada en la etapa (e) durante al menos 2 horas a temperatura ambiente con o sin agitación para permitir la sedimentación del precipitado, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) filtrar la solución aclarada de polisacárido de la etapa (f) a través de un filtro de carbono activado, particularmente un filtro de carbono activado que comprende carbono activado por ácido fosfórico basado en madera;
(h) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (g), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(i) filtrar la solución concentrada de polisacárido purificado producida por la etapa (h) usando un filtro estéril;
mediante lo cual se producen polisacáridos capsulares sustancialmente purificados que comprenden el serotipo 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19f o 23F en forma de una solución. En una realización particular, la etapa (e) retira al menos el 98 % de las proteínas del retenido sin sal de la etapa (d). En otra realización, la etapa (g) retira al menos el 90 % de las proteínas de la solución aclarada de polisacárido de la etapa (f). En otra realización, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 5,5 a aproximadamente 7,5. Para una estabilidad mejorada del polisacárido capsular sustancialmente purificado durante almacenamiento a largo plazo, sin embargo, la diafiltración de la etapa (h) comprende un ajuste de pH entre aproximadamente 7,0 hasta aproximadamente 7,5, y más particularmente hasta aproximadamente 7,4.
La presente divulgación también se refiere a un procedimiento de producción de polisacáridos capsulares sustancialmente purificados a partir de un lisado celular de Streptococcus pneumoniae que comprende el serotipo 19A, que comprende las etapas de:
(a) proporcionar un caldo de fermentación que comprende células bacterianas que producen Streptococcus pneumoniae serotipo 19A;
(b) lisar las células bacterianas en la etapa (a) con un detergente, produciendo de ese modo un lisado celular que comprende desechos celulares, proteínas solubles, ácidos nucleicos y polisacáridos;
(c) aclarar el lisado celular de la etapa (b) usando centrifugación o filtración para retirar los desechos celulares, produciendo de ese modo un lisado celular aclarado;
(d) ultrafiltrar y diafiltrar el lisado celular aclarado de la etapa (c) a aproximadamente 4 °C a un pH de aproximadamente 6 en tampón fosfato sódico, fosfato sódico 25 mM, para retirar las impurezas de bajo peso molecular y aumentar la concentración de polisacárido, produciendo de ese modo un retenido;
(e) disminuir el pH del retenido de la etapa (d) hasta menos de 4,5, particularmente aproximadamente 3,5, para precipitar las proteínas y los ácidos nucleicos, para de este modo formar una solución acidificada de retenido; (f) mantener la solución acidificada de retenido formada en la etapa (e) durante al menos 2 horas a aproximadamente 4 °C con o sin agitación para permitir la sedimentación del precipitado, seguido por filtración o centrifugación de la solución acidificada de retenido, produciendo de ese modo una solución aclarada de polisacárido;
(g) ajustar el pH de la solución aclarada de polisacárido de la etapa (f) hasta aproximadamente 6, produciendo de ese modo una solución aclarada de polisacárido de pH ajustado;
(h) filtrar la solución aclarada de polisacárido de pH ajustado de la etapa (g) a través de un filtro de carbono activado, particularmente un filtro de carbono activo que comprende carbono activado con ácido fosfórico basado en madera;
(i) ultrafiltrar y diafiltrar la solución filtrada producida por la etapa (h), produciendo de ese modo una solución concentrada de polisacárido purificado; y
(j) filtrar la solución concentrada de polisacárido purificado producida por la etapa (i) usando un filtro estéril;
mediante lo cual se producen polisacáridos capsulares sustancialmente purificados que comprenden el serotipo 19A en forma de una solución. En una realización particular, la etapa (e) retira al menos el 98 % de las proteínas del retenido de la etapa (d). En otra realización, la etapa (h) retira al menos el 90 % de las proteínas de la solución aclarada de polisacárido de pH ajustado de la etapa (g). En otra realización, la diafiltración de la etapa (i) comprende
un ajuste de pH entre aproximadamente 5,5 hasta aproximadamente 7,5. Para una estabilidad mejorada del polisacárido 19A sustancialmente purificado durante almacenamiento a largo plazo, sin embargo, la diafiltración de la etapa (i) comprende un ajuste de pH entre aproximadamente 7,0 hasta aproximadamente 7,5, y más particularmente hasta aproximadamente 7,4.
Los siguientes ejemplos se ofrecen a modo de ilustración y no a modo limitación.
Parte experimental
Los siguientes Ejemplos presentan resultados para los serotipos de polisacáridos de S. pneumoniae 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A y 19F purificados a escala de 10 l mediante el uso del procedimiento mejorado de la presente invención, y los resultados se comparan con aquellos del actual procedimiento de purificación.
Ejemplo 1. Procedimiento acortado de purificación para los serotipos de polisacáridos de S. pneumoniae 1, 4, 5, 6A, 6B, 7F, 14 y 19A.
Se obtuvieron caldos de fermentación de S. pneumoniae lisados con desoxicolato sódico (DOC) en dos días después de su recolección o se almacenaron a 4 °C y se procesaron en la siguiente semana. Como se describe a continuación, el presente procedimiento de purificación incluía los siguientes cambios en comparación con el procedimiento existente de purificación: 1) la etapa de acidificación se movió desde el inicio hasta después de la primera etapa de ultrafiltración/diafiltración (UF/DF), y el pH se ajustó hasta 7,5 en lugar de 5; 2) el tampón de diafiltración se cambió de fosfato 0,025 M a agua desionizada (DI); 3) la adsorción en carbono se cambió a 2 discos de carbono CUNO R32SP (CUNO Inc., Wayne, NJ) mediante el uso de carbono activado con ácido fosfórico basado en madera, y el tiempo de adsorción se prologó de 4 a 12 rotaciones (cada rotación era de 22 minutos); y 4) el pH se ajustó hasta 7,4 durante la última etapa de diafiltración 30 K cuando se diafiltraba aproximadamente 5 veces. Se aplicó el mismo procedimiento de purificación para los serotipos 1, 4, 5, 6A, 6B o 7f . Para el serotipo 19A, las etapas se modificaron adicionalmente y la purificación se realizó en una habitación refrigerada, como se describe a continuación.
Etapas de purificación
Todas las etapas se realizaron a temperatura ambiente excepto para el tipo 19A, en cuyo caso el procedimiento se llevó a cabo a 4 °C en una habitación refrigerada.
Aclaración del lisado: El propósito de esta etapa fue retirar los desechos celulares y aclarar el caldo. Esto se consiguió por centrifugación o filtración. El caldo se centrifugó a 10.000 g durante 30 minutos o hasta que el caldo estaba transparente a 20 °C (4 °C para el tipo 19A), o se filtró con un Millipore Prefilter (Millipore Corp., Billerica, MA) con la adición de auxiliares de filtro Celpure® (Advanced Minerals, Santa Bárbara, CA). El lisado aclarado se recogió para procesamiento adicional y se desecharon los sedimentos.
Primera UF/DF (Ultrafiltración/Diafiltración): Esta etapa proporcionó reducción del volumen e intercambio de tampón y también retiró las impurezas de bajo peso molecular. El lisado aclarado se concentró hasta aproximadamente 1/8 del volumen original. La diafiltración se realizó usando aproximadamente 10 volúmenes de agua DI (pH 6, fosfato 25 mM para 19A).
Acidificación: Se retiró más del 98 % de las proteínas en esta etapa. Mientras se agitaba, se añadió cuidadosamente ácido fosfórico concentrado al retenido. El pH del retenido se ajustó hasta un valor diana de pH 3,5. El retenido acidificado se agitó durante media hora y se curó a temperatura ambiente para curarlo durante una noche (2 horas a 4 °C para 19A), provocando la precipitación de las proteínas y de los ácidos nucleicos.
Aclarado del retenido acidificado: Esta era la etapa de aclarado para retirar los precipitados después de la acidificación. La suspensión de solución acidificada se centrifugó en un rotor a 10.000 rpm (17.000 de fuerza centrífuga relativa o RCF) durante 1 hora a 20 °C (excepto para 6B, en cuyo caso la centrifugación fue de 6 horas a 37 °C). El sobrenadante se recogió y se desechó el sedimento. También se puede usar diafiltración en profundidad con un Millipore Prefilter (Millipore Corp., Billerica, MA) con la adición de auxiliares de filtro Celpure® (Advanced Minerals, Santa Bárbara, CA) para esta etapa.
Adsorción en carbono: En la mayoría de los casos, había un ligero color amarillo tras la centrifugación del retentado 100K acidificado. La eliminación del color se logró por medio de la adsorción de carbono mediante el uso de carbón activado con ácido fosfórico a base de madera. Esta etapa también retiró las proteínas residuales que permanecían después de la acidificación. La solución aclarada de polisacárido se hizo circular de nuevo a través del filtro de carbono durante 5-6 horas o durante una noche (para 19A, el pH se ajustó hasta 6 antes de la adsorción en carbono).
UF/DF 30 K final: Esta fue otra etapa de concentración e intercambio de tampón para concentrar la solución hasta una concentración final de polisacárido (PS) de > 2 g/l, que se diafiltró en agua desionizada (DI). Se concentró la solución de PS filtrada en carbono. Después, el concentrado se diafiltró 10X con agua DI. El pH se ajustó hasta 7,4 durante la diafiltración.
Filtración final a esterilidad con 0,2 um: La solución final de PS se filtró a esterilidad con un filtro de 0,22 |jm o unidad desechable estéril de filtración y se almacenó en un refrigerador a 4 °C.
Procedimientos analíticos
La cuantificación de concentraciones de proteína, PS y ácido nucleico se realizaron mediante el uso de procedimientos que son bien conocidos en la técnica, que incluyen análisis de SDS-PAGE (electroforesis en gel de poliacrilamida con dodecil sulfato sódico), HPLC (cromatografía líquida de alto rendimiento) y SEC (cromatografía por exclusión de tamaño), ensayos de Lowry modificados, espectrofotometría, SEC-MALLS (cromatografía por exclusión de tamaño/dispersión de luz láser de múltiples ángulos) y NMR (resonancia magnética nuclear).
Resultados y análisis
Lotes de purificación acortada de tipo 5: La comparación del rendimiento final de PS, el peso molecular de PS y los niveles de impurezas principales de tres lotes de purificación usando el procedimiento acortado y aquellos que se usan el procedimiento actual para el tipo 5 se muestran en la Tabla 1. Todos los casos de partida eran lotes de fermentación de alta densidad celular lisados con DOC, que tenían una mayor concentración de polisacárido (~ 0,5 g/l) que el caldo convencional de fermentación con SOP (~ 0,3 g/l). Se usó una membrana de 30 K o de 50 K para la primera etapa de UF/DF. Los niveles de impurezas se calcularon y usando relaciones de impureza/PS. Se usó el mismo enfoque para todos los demás serotipos descritos en el presente documento.
Como muestran los datos de la Tabla 1, las relaciones de proteína de los tres lotes mediante el uso del procedimiento acortado de purificación cumplían la especificación de < 7,5 %, y también eran comparables con los del procedimiento actual. Las relaciones de ácido nucleico (NA), así como de polisacárido-C (C-PS), también estaban muy por debajo de las especificaciones de < 2,0 % y de < 35 %, respectivamente y eran comparables con los del procedimiento actual. Los resultados del rendimiento final de PS y los niveles de impurezas de los tres lotes mostrados en la Tabla 1 demuestran la reproducibilidad y robustez del procedimiento acortado.
Hubo alguna preocupación acerca de si los polisacáridos se podían hidrolizar a un pH inferior de 3,5. El cambio del tiempo de retención de PS durante el procedimiento de purificación, por lo tanto, se controló y se midió el peso molecular del PS purificado final. No se observaron cambios significativos en el tiempo de retención de PS de serotipo 5 a partir del cromatograma de HPLC. Tampoco hubo diferencias significativas en los pesos moleculares para el PS purificado por el procedimiento acortado y el del procedimiento actual (284 kg/mol) basándose en la medición MALLS. Por tanto, se concluyó que el peso molecular del PS purificado no se veía afectado de forma adversa por el procedimiento acortado de purificación.
El rendimiento de polisacárido en el procedimiento, la relación de proteína/polisacárido y la relación de ácido nucleico/polisacárido en cada una de las etapas del procesamiento para los tres lotes del procedimiento acortado se resumen en la Tabla 2.
Siempre existe una pérdida de producto durante cada etapa de cualquier procedimiento de purificación. Para estos tres lotes del procedimiento acortado, la pérdida de PS sucedía principalmente en la primera etapa de UF/DF y en la etapa de acidificación. La pérdida de PS en la primera etapa de UF/DF se debía a la adsorción de PS o complejo de PS/proteína a la superficie de la membrana. Esta pérdida se minimizó aclarando el lado de retenido de la membrana con agua DI después de la diafiltración y combinando el aclarado con el retenido original. La pérdida de PS en la etapa de acidificación podía deberse a dos razones: adsorción física de PS a los sólidos de precipitación y unión del polisacárido a la proteína con co-precipitación durante la acidificación. Esta segunda posibilidad se investigó adicionalmente y los resultados mostraron evidencias de unión de PS/proteína.
La Figura 1 muestra la reducción de la relación de proteína/PS en cada etapa de purificación. Aunque la etapa de purificación retiraba un pequeño porcentaje de proteínas, la mayoría de las proteínas se retiraba en la etapa de acidificación. Solamente se detectó una cantidad traza de proteína después de tratamiento a pH 3,5 incluso para el lote de mayor potencia de proteínas.
Similar a la relación de proteína/PS, la relación de ácido nucleico/PS mostró variabilidad de niveles de impurezas entre los lotes. La etapa de UF/DF 30/50 K retiraba una cantidad significativa de ácido nucleico en comparación con la retirada de proteínas en la misma etapa de procesamiento. Sin el deseo de limitarse a teoría alguna, esto se puede deber al tamaño molecular de los ácidos nucleicos que es más pequeño que el de las proteínas, lo que los hace relativamente más fáciles de retirar por medio de la etapa de UF/DF 30/50 K. La primera etapa de centrifugación y acidificación también eliminó una cantidad considerable de ácido nucleico.
La Tabla 2 muestra que la etapa de adsorción con carbono activado también reduce el nivel de proteína/PS y de NA/PS. La reducción del porcentaje no era tan significativa como en las dos primeras etapas, pero esta etapa era importante para retirar el color de la solución y aseguraba que el nivel de impurezas cumplía la especificación.
Lotes de purificación acortada de tipo 4. Se muestra un sumario de tres lotes de purificación acortada para el tipo 4 en la Tabla 3. Los caldos de alimentación para los tres lotes estaban lisados con DOC.
El rendimiento de PS de tipo 4 también estaba entre el 50 y el 60 %. La relación de proteína/PS y la relación de ácido nucleico/PS estaban dentro de sus especificaciones. La relación de C-PS también estaba dentro de la especificación. El peso molecular de los tres lotes estaba cercano a ~ 300 kg/mol. El PS de serotipo 4 purificado por el actual procedimiento de purificación usando el caldo similar de fermentación también dio un peso molecular inferior de 285 kg/mol. La comparación de los cromatogramas de HPLC del PS del caldo de fermentación y la solución purificada final mostró que no había diferencias en el tiempo de retención de PS. Esto sugirió que la diferencia en el peso molecular no estaba causada por el cambio del procedimiento, sino en su lugar se debía a la naturaleza intrínseca del procedimiento de fermentación.
El PS de Tipo 4 contiene un grupo piruvato en la molécula modificada, y este piruvato era importante para la conjugación para su uso en una vacuna de conjugado de neumococos. Para asegurar que la cantidad de piruvato no estaba afectada de forma adversa por el tratamiento ácido, se realizó análisis de r Mn . La Figura 2 muestra los espectros de RMN para PS de tipo 4 convencional y los del lote L29276-47. No se observaron diferencias significativas entre los dos espectros. El segundo pico de la derecha en ambos espectros era piruvato, y la altura del pico del grupo piruvato era comparable en ambos espectros. Las relaciones de piruvato para los tres lotes del procedimiento acortado fueron de 0,8 mol/mol, y cumplían la especificación de > 0,7 mol/mol.
El rendimiento de PS en el procedimiento, la relación de proteína/PS y de NA/PS para los tres lotes de tipo 4 se resumen en la Tabla 4. La pérdida de PS sucedía principalmente en la primera centrifugación, las etapas de acidificación y adsorción en carbono activado, con un promedio del 10 %, del 8 % y del 20 % respectivamente. El rendimiento global de PS era cercano al de tipo 5, aproximadamente el 55 %.
La Figura 3 muestra el cambio promedio en el rendimiento de PS, la relación de proteína/PS y de NA/PS en cada una de las etapas de purificación para los tres lotes de la Tabla 4. La retirada de proteínas sucedía principalmente en la etapa de acidificación como se esperaba. La primera centrifugación y las etapas de UF/DF también retiraban colectivamente una cierta cantidad de proteínas, pero la reducción de proteínas era menor que en la etapa de acidificación.
Similar al tipo 5, la mayor parte de la reducción de la relación de ácido nucleico/PS tenía lugar en las etapas UF/DF 50/100 K, en la primera centrifugación y en la acidificación, y la reducción de NA en la primera etapa de UF/DF era más significativa que para proteínas. De nuevo, como se muestra en la Figura 3, la etapa de carbono activado retiraba una cierta cantidad de proteínas y NA y llevaba los niveles de impurezas por debajo de las especificaciones. También se retiraba el color de la solución.
Lotes de purificación acortada de tipo 19A: El polisacárido de tipo 19A es inestable y el peso molecular cambia durante la purificación. El procedimiento acortado de purificación se modificó ligeramente para estabilizar el polisacárido 19A. Estas modificaciones se resumen del siguiente modo: 1) las etapas de purificación se realizaron principalmente a 4 °C en la habitación refrigerada; 2) la primera diafiltración 100 K se refrigeró usando tampón fosfato 25 mM (4 °C) con un pH de 6 en lugar de usar agua a temperatura ambiente; 3) el tiempo de mantenimiento de acidificación se redujo desde una noche a 2 horas; y 4) después de aclarar el retenido 100 K acidificado, el pH se ajustó hasta 6 y se realizó adsorción en carbono activado a pH 6 en lugar de a 3,5.
Los resultados de dos lotes 19A purificados por el procedimiento acortado de purificación se muestran en la Tabla 5.
Los rendimientos de PS de los dos lotes de purificación acortada fueron del 62 y 76%, respectivamente. La relación final de proteína/PS, la relación de ácido nucleico y la relación de C-PS cumplieron todas sus especificaciones respectivas. Los pesos moleculares finales de los polisacáridos de los dos lotes fueron de 525 kg/mol y de 488 kg/mol, respectivamente, y estaban cercanos a los de PS de 19A usado en ensayos clínicos en fase III (486 kg/mol). La relación de proteína/PS para los dos lotes cumplía ambos la especificación de < 2 %. La relación tanto de NA como de C-PS de los dos lotes estaba dentro de sus especificaciones.
El rendimiento de PS, la reducción de proteína y NA en cada una de las etapas de purificación se muestra en la Tabla 6 y en la Figura 4. Los resultados mostraron la pérdida de PS en cada una de las etapas de purificación excepto en la primera etapa de centrifugación. Como los serotipos 5 y 4, la retirada de proteínas y NA tuvo lugar principalmente en las tres primeras etapas, y había apenas proteína y NA detectables después de la acidificación. Aunque la etapa de adsorción en carbono activado no retiraba una cantidad significativa de proteínas y NA, posiblemente debido a la muy baja concentración de proteínas y NA después de la acidificación, la etapa aún era necesaria para la eliminación del color.
Lotes de purificación acortada de tipo 7F: El tipo 7F es un polisacárido no iónico, que típicamente requiere cambio en las etapas durante la purificación mediante el uso del procedimiento existente en comparación con los serotipos descritos anteriormente. Sin embargo, el procedimiento acortado de purificación de la presente invención se aplicó satisfactoriamente al serotipo 7F sin la necesidad de desviación del procedimiento. Se purificaron dos lotes de caldo de tipo 7F usando el procedimiento acortado. Uno fue un caldo de fermentación convencional (L29276-107) y uno fue un caldo de alta densidad celular (L29276-157). Los resultados de los dos lotes se resumen en la Tabla 7.
El rendimiento de PS de tipo 7F era realmente mayor que en los otros serotipos, posiblemente debido a menor unión del polímero no iónico a las moléculas proteicas cargadas. Las relaciones finales de proteína, de NA y de C-PS están todas dentro de sus especificaciones. El peso molecular del tipo 7F era comparable al de los lotes convencionales y aunque el peso molecular de 7F era bastante alto, la solución de PS no era muy viscosa debido al volumen excluido más pequeño del polímero no iónico.
El rendimiento de PS, la relación de proteína y de NA del tipo 7F en cada una de las etapas de purificación se muestran en la Tabla 8 y se representó el promedio de los dos lotes en la Figura 5.
Hubo alguna pérdida de PS de tipo 7F en cada etapa de purificación. Globalmente, la pérdida de PS fue menor que la de los serotipos 5 y 4. La reducción de la relación de proteína y de NA fue principalmente por las etapas de primera centrifugación, de UF/DF 100 K y de acidificación. Similar a otros serotipos, la UF/DF 100 K fue más eficaz
en retirar NA que en proteínas. Aunque la etapa de adsorción en carbono activado no retiraba una cantidad significativa de proteínas y de NA debido a niveles muy bajos de impurezas después de la acidificación, la etapa aún era necesaria para la eliminación del color.
Lotes de purificación acortada de tipo 6B: Se purificaron dos lotes de 6B usando el procedimiento acortado de purificación. Se descubrió que el aclarado del retenido 100 K acidificado tardaba más tiempo que los otros serotipos (6 horas en lugar de 1 hora). Excepto por esta diferencia, el procedimiento de purificación fue similar al de los serotipos. Los resultados de los dos lotes se resumen en la Tabla 9.
Todos los niveles de impurezas (proteínas, NA y C-PS) estaban dentro de sus especificaciones. El rendimiento de PS fue relativamente alto, y también la relación de proteína de NA en comparación con los otros serotipos.
El rendimiento de PS en el procedimiento, las relaciones de proteína y de NA en cada una de las etapas de purificación se muestran en la Tabla 10 y en la Figura 6.
Similar a 19A, la pérdida de PS sucedía en cada una de las etapas de purificación excepto en la primera etapa de centrifugación, en que hubo un ligero aumento de PS. La retirada de proteínas y de NA se consiguió principalmente por la primera centrifugación, por la primera UF/DF 100 K y por la etapa de acidificación. Sin embargo, también hubo alguna reducción de la relación de proteína y de NA en la etapa de adsorción en carbono.
Lotes de purificación acortada de tipo 6A: Se purificaron dos lotes de tipo 6A usando el procedimiento acortado de purificación. El rendimiento de PS, los niveles de impurezas y el peso molecular de las soluciones finales se resumen en la Tabla 11.
Los rendimientos finales de PS de los dos lotes 6A fueron ambos > 70 %, que eran los más altos entre los serotipos procesados mediante el uso del procedimiento acortado. Las relaciones de proteína, de NA y de C-PS estaban todas dentro de las especificaciones.
La Tabla 12 y la Figura 7 muestran el cambio en el rendimiento de PS en el procedimiento, la relación de proteína y de NA en cada una de las etapas de purificación. Apenas hubo pérdida de PS en las etapas de primera centrifugación y 100K UF/DF. En las etapas de acidificación y adsorción con carbón activado se produjo una pérdida de PS de entre el 10 y el 15%, que se aproxima a la de los demás serotipos. La reducción principal de la relación de proteína y de NA era por la primera centrifugación, por UF/DF 100 K y por acidificación. Después de la acidificación, ambas relaciones de proteína y de NA ya estaban por debajo de sus especificaciones. Para las proteínas, la acidificación era la etapa más eficaz, mientras que para NA, la UF/DF 100 K reducía la mayor cantidad de la relación de NA/PS. Aunque la etapa de adsorción en carbono activado no retiraba una cantidad significativa de proteínas y de NA debido a niveles muy bajos de impurezas después de la acidificación, la etapa aún era necesaria para la eliminación del color.
Lotes de purificación acortada de tipo 1: Se resumen dos lotes de tipo 1 purificados por el procedimiento acortado en la Tabla 13. El lote L29276-170 se purificó a partir de caldo de fermentación de alta densidad celular y L29276-173 era de caldo de fermentación convencional.
Los rendimientos de PS para ambos lotes fueron de aproximadamente el 50 %, y los niveles de impurezas para proteínas, para NA y para C-PS estuvieron todos dentro de sus especificaciones.
El rendimiento de PS en el procedimiento, las relaciones de proteína y de NA después de cada una de las etapas de purificación se muestran en la Tabla 14 y en la Figura 8. Las tendencias fueron similares a otros serotipos modificados. La pérdida de PS sucedía principalmente en las etapas de acidificación y adsorción en carbono activado, y la mayoría de la retirada de proteínas y de NA sucedía en las tres primeras etapas. Se retiraba más NA en la etapa de UF/DF 100 K que proteínas. Aunque la etapa de adsorción en carbono activado no retiraba una cantidad significativa de proteínas y de NA debido a niveles muy bajos de impurezas después de la acidificación, la etapa aún era necesaria para la eliminación del color.
Lotes de purificación acortada de tipo 14: Se purificaron dos lotes de serotipo 14 usando el procedimiento acortado de purificación sin desviaciones del procedimiento. El rendimiento final de PS y los niveles de impurezas se resumen en la Tabla 15.
Similar al serotipo 7F, el serotipo 14 es un polisacárido no iónico, y su procedimiento actual de purificación es ligeramente diferente de los otros serotipos. Sin embargo, el procedimiento acortado de purificación de la presente invención se aplicó satisfactoriamente al serotipo 14 sin la necesidad de dichas etapas adicionales. Los rendimientos de PS de los dos lotes del procedimiento acortado de purificación fueron del 50-60 %, y las relaciones de proteína y de NA estuvieron dentro de sus especificaciones. Los pesos moleculares del PS purificado también cumplían la especificación.
El rendimiento de PS en el procedimiento, las relaciones de proteínas y de NA se resumen en la Tabla 16 y en la Figura 9. Se observaron tendencias similares de pérdida de PS, retirada de proteínas y de NA que para los otros serotipos ensayados descritos anteriormente.
Ejemplo 2. Comparación de diferentes serotipos (serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A y 19F).
A fin de comparar la purificación de los diferentes serotipos mediante el uso del procedimiento acortado de purificación de la presente invención, se representó la retirada de PS de todos los serotipos descritos en el Ejemplo 1 más los serotipos 9V, 18C y 19F en un gráfico en la Figura 10. La mayoría de los serotipos seguía una tendencia similar con pérdida de PS en cada una de las etapas de purificación. Hubo un aumento en el rendimiento de PS para el tipo 6B en la primera etapa de centrifugación y del tipo 14 en la etapa de acidificación. El porcentaje de pérdida de PS varió de un serotipo a otro. El tipo 5 parecía perder la mayoría de PS en la etapa de acidificación y el tipo 14 en la etapa de adsorción en carbono activado.
Las relaciones de proteína/PS para cada etapa de purificación para cada uno de los serotipos se muestran en la Figura 11. La figura muestra que había una diferencia en las relaciones iniciales de proteína/PS para los diferentes serotipos, teniendo los tipos 1, 4, 5, 9V, 19F y 18C las mayores relaciones iniciales de proteína/PS. Aunque las relaciones de proteína/PS eran mucho mayores para los tipos 1, 4, 5, 9V, 19F y 18C en comparación con los otros serotipos incluso después de la primera etapa de UF/DF, la etapa de acidificación reducía enormemente la relación de proteína/PS y no quedaba mucha más proteína después de esta etapa.
Como se muestra en la Figura 2, las relaciones de NA/PS también variaban de un serotipo a otro. Los tipos 1 y 5 tenían la mayor relación de NA/PS, seguido por los tipos 18C y 4. La primera etapa de centrifugación y de UF/DF retiraba una cantidad significativa de NA de estos serotipos y el tipo 1 parecía ser el más eficaz. Había muy poco NA después de la etapa de acidificación.
Ejemplo 3. Análisis de eficacia de la etapa de acidificación y de adsorción en carbono activado (serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A y 19F).
Para la purificación de polisacáridos PnC, la impureza más significativa y difícil de retirar son las proteínas. Para entender mejor la eficacia de retirada de impurezas del procedimiento acortado, se analizaron dos de las etapas principales de purificación, la acidificación y la adsorción en carbono activado, para la retirada de proteínas. Para la etapa de acidificación, la diferencia en la concentración de proteínas (SDS-PAGE) antes y después de la acidificación se representó frente a la concentración inicial de proteínas antes de la acidificación para los serotipos 1, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A y 19F usando el procedimiento acortado de purificación de la invención (Figura 13).
Debido a los cambios relativamente pequeños en el volumen de solución antes y después de la etapa de acidificación, la diferencia en la concentración de proteínas dividida por la concentración inicial de proteínas reflejaba la tasa de retirada de proteínas por la etapa de acidificación. La Figura 13 muestra la pendiente del ajuste lineal de la diferencia en la concentración de proteínas con respecto a la concentración inicial de proteínas (por ensayo de SDS-PAGE). Se observó una muy buena relación lineal entre el cambio de concentración de proteínas y la concentración inicial, con el R2 cercano a 1. La pendiente era de 0.9876, que corresponde a una retirada de proteínas del 98,76 % (asumiendo un cambio insignificante de volumen de solución). Por lo tanto, para todos los serotipos estudiados, la etapa de acidificación era muy eficaz y, de promedio, retiraba más del 98 % de las proteínas.
Similar a la etapa de acidificación, también se evaluó la eficacia de la etapa de adsorción en carbono activado al representar la cantidad de proteínas retirada (adsorbida en carbono) con respecto a la carga inicial de proteínas (Figura 14). Se observó una buena relación lineal entre las proteínas retiradas y la carga inicial de proteínas, aunque el R2 (0,9723) no era tan alto como para la etapa de acidificación. Como la pendiente de este ajuste lineal corresponde a la tasa de retirada de proteínas, la etapa de adsorción en carbono activado producía una retirada de proteínas del 93,87 %.
En base a un análisis de las etapas de acidificación y de adsorción en carbono activado, después de las dos etapas quedaba solamente aproximadamente un 0,1 % de proteínas en la solución.
Conclusiones para los Ejemplos 1-3
Se desarrolló un procedimiento acortado de purificación para remplazar el actual procedimiento de purificación para polisacáridos capsulares de S. pneumoniae. El procedimiento acortado de purificación se aplicaba directamente a los serotipos 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C y 19f y para 19A con una ligera desviación. El procedimiento se realizó a escala de 10 l usando caldos de fermentación lisados con DOC. Los niveles de impurezas, incluyendo las relaciones de proteína/PS, de NA/PS y de C-PS/PS, cumplían, todos, sus respectivas especificaciones. Los rendimientos de PS eran por encima del 50 % y comprables a los del actual procedimiento de purificación. El rendimiento de PS en el procedimiento, las relaciones de proteína/PS y de NA/PS se representaron para comparar el comportamiento de diferentes serotipos. Se descubrió que los serotipos 1,5, 9V, 19F y 18C eran los más difíciles de purificar basándose en las relaciones de proteína/PS antes y después de la etapa de Uf/DF 100 K.
El análisis de etapas mostró que las etapas de acidificación y de adsorción en carbono activado retiraban más del 98 % y del 90 % de las proteínas, respectivamente (medido por SDS-PAGE).
Ejemplo 4. Sustitución de agentes líticos de origen no animal por desoxicolato sódico en la producción de polisacáridos
El presente ejemplo investigó si agentes líticos de origen no animal se podrían usar como sustituto para desoxicolato sódico (DOC) dentro del procedimiento descrito anteriormente para la producción de polisacáridos capsulares sustancialmente purificados de Streptococcus pneumoniae. Como se describe anteriormente, DOC activa la proteína LytA, que es una autolisina que está implicada en el crecimiento de la pared celular y en la división en Streptococcus pneumoniae. La proteína LytA tiene dominios de unión a colina en su parte C-terminal, y se sabe que mutaciones del gen lytA producen mutantes LytA que son resistentes a lisis con DOC.
Se desarrolló un rápido ensayo en placa de microtitulación para identificar compuestos que causan lisis celular por un mecanismo similar al de DOC. Se identificaron varias alternativas de origen no animal a DOC que son igual de eficaces que DOC en la eliminación de células de Streptococcus pneumoniae y en la liberación de polisacárido. Después del procesamiento usando condiciones convencionales, el tamaño y la pureza de los polisacáridos producidos con los compuestos de origen no animal eran idénticos a los producidos con DOC.
Procedimientos
Lisis celular: Los compuestos a ensayar se añadieron al caldo de fermentación a una concentración final del 0,1 al 0,01 % (v/v) y se permitió que la solución se incubara a 37 °C durante una hora. La solución después se almacenó a 2-8 °C durante una noche. La siguiente mañana la solución se centrifugó para retirar todos los desechos celulares. Se analizó el caldo sin células por SEC-HPLC para determinar la concentración de polisacárido liberado. La lisis podía realizarse a cualquier temperatura entre 2-37 °C, preferentemente a un intervalo de pH de 6,0-7,5. La concentración del detergente era típicamente entre el 0,05-0,2 % dependiendo del detergente particular.
Ensayo de microtitulación: Se ideó un rápido ensayo en placa de microtitulación para examinar la lisis dependiente de lytA de neumococos por diferentes detergentes o tensioactivos. Se usaron dos pares de cepas isogénicas de S. pneumoniae en el ensayo; un miembro de cada par era de tipo silvestre para el gen lytA mientras que la otra cepa portaba una deleción en el gen lytA. Por tanto, si la lisis era dependiente de una función lytA activa, ese detergente no lisaría las cepas mutantes. Las cuatro cepas, R6X, R6X AlytA, D39 y D39 AlytA, se cultivaron en medio HySoy hasta aproximadamente fase semi-log (DO600 ~0,2-0,8; DO600 = densidad óptica a 600 nm). Las células después se centrifugaron y se resuspendieron los sedimentos celulares en medio HySoy. A cada pocillo de la placa de microtitulación, se le añadieron 100 pl de suspensión celular, junto con 10 pl de soluciones madre de detergente o agua como control. Después de aproximadamente 15 minutos a 36 °C, se midió la DO600 de las muestras con un espectrofotómetro Spectramax® (Molecular Devices, Sunnyvale, CA). Se observaron los siguientes resultados para las células recién preparadas o las congeladas y descongeladas: células de tipo silvestre expuestas a DOC, dodecil sulfato sódico, Triton® X-100 y N-lauril sarcosina todas tenían valores de DO comparables al blanco de medio, que indicaba que había sucedido lisis. Por otro lado, las células AlytA no se lisaban en presencia de estos detergentes, lo que indica que la función LytA es necesaria para que estos detergentes lisen las células.
Aislamiento de PS usado para estudios analíticos comparativos: Se hicieron crecer cultivos en medio Hy-Soy en biorreactores de 10 l. El pH se controló a aproximadamente 7,0 usando NaOH o Na2CO3. Al final del cultivo (indicado por ausencia de aumento adicional en la densidad óptica), los cultivos se trataron con DOC al 0,12 % o con NLS al 0,1 %. Los cultivos se incubaron durante 12-16 horas. La eficacia de eliminación celular se confirmó sembrando una muestra de caldo tratado en placas de agar con sangre-TSA. El polisacárido se purificó del lisado aclarado usando procedimientos convencionales (como se describe anteriormente). El polisacárido purificado se examinó usando una diversidad de técnicas analíticas convencionales apropiadas para determinar la pureza e identidad del material. El contenido de PS del lisado se determinó mediante el uso de SEC-HPLC acoplada a un detector del índice de refracción (RI).
Selección de agentes líticos de origen no animal usando los serotipos 1 y 6B
Se cultivaron por separados los serotipos 1 y 6B de S. pneumoniae en medios basados en Hy-Soy. Los cultivos se recogieron por separado y se distribuyeron por separado en tubos. Los compuestos de origen no animal a seleccionar para la actividad lítica comparable con DOC se prepararon como soluciones madre (en disolventes adecuados) y se añadieron a los cultivos. Después de incubación durante una noche, los tubos se centrifugaron y se determinó el contenido de PS de los lisados para cada serotipo por SEC-HPLC y se compararon con DOC.
Selección de agentes líticos de origen no animal usando mutantes lytA
Se cultivaron pares isogénicos de cepas que contenían la mutación lytA en un medio basado en Hy-Soy. Las células se recogieron y se distribuyeron en pocillos en una placa de microtitulación. El compuesto de ensayo se añadió y se incubó el cultivo. Después de 15 minutos a 36 °C, se determinó la densidad óptica (DO600) de cada pocillo mediante el uso de un lector de placa SpectraMax® (Molecular Devices, Sunnyvale, CA) (véanse las Tablas 17 y 18, que resumen los resultados de dos ensayos diferentes para compuestos ejemplares).
En base a los estudios de selección descritos anteriormente, se identificaron las siguientes alternativas de agente lítico de origen no animal a DOC: ácido decanosulfónico, Igepal® CA-630 (terc-octilfenoxi poli(oxietileno)etanol; CAS núm.: 9002-93-1; disponible en Sigma Aldrich, St. Louis, MO), N-lauril sarcosina sódica (NLS), iminodipropionato de laurilo, dodecil sulfato sódico, Triton® X-100, quenodesoxicolato, hiodesoxicolato, glicodesoxicolato, taurodesoxicolato, tauroquenodesoxicolato y colato.
Comparación de PS lisado con DOC a PS lisado con NLS
Se purificaron los serotipos 1, 4, 5, 6A, 6B y 7F de polisacáridos de S. pneumoniae a la escala de 10 l como se describe anteriormente en los Ejemplos 1 y 2 mediante el uso del procedimiento mejorado de la presente invención. Sin embargo, en un grupo se usó NLS (0,1 %) como agente lítico mientras que en otro grupo se usó DOC (0,12 %) como agente lítico.
Se midieron el rendimiento de PS, las relaciones de proteína/PS, las relaciones de NA/PS y el peso molecular de PS como se describe anteriormente, y los resultados se resumen en la Tabla 19. Estos resultados mostraron que el uso de NLS como agente lítico en los procedimientos de purificación de la invención producía rendimientos relativamente altos de PS con niveles relativamente bajos de proteínas y de ácido nucleicos. De hecho, para la mayoría de los serotipos ensayados, el uso de NLS como agente lítico producía mayores rendimientos de PS en comparación con el uso de DOC.
Todas las publicaciones y solicitudes de patentes mencionadas en la memoria descriptiva son indicativas del nivel de los expertos en la técnica a la que pertenece la presente invención.
Aunque la invención anterior se ha descrito en algún detalle a modo de ilustración y ejemplo con propósitos de claridad de comprensión, será obvio que se pueden poner en práctica ciertos cambios y modificaciones dentro del alcance de las reivindicaciones adjuntas.
Claims (12)
1. Un procedimiento de purificación de un polisacárido capsular de S. pneumoniae que comprende la ultrafiltración y la diafiltración de un caldo lisado celular clarificado de S. pneumoniae, seguido de la acidificación del caldo lisado concentrado hasta un pH inferior a 4,5.
2. El procedimiento de la reivindicación 1, en el que el pH del caldo de lisado concentrado se disminuye hasta menos de 4,4, 4,3, 4,2, 4,1, 4,0, 3,9, 3,8, 3,7, 3,6, 3,5, 3,4, 3,3, 3,2, 3,1 o 3,0.
3. El procedimiento de la reivindicación 1, en el que el pH del caldo de lisado concentrado se disminuye hasta aproximadamente 4,4, aproximadamente 4,3, aproximadamente 4,2, aproximadamente 4,1, aproximadamente 4.0, aproximadamente 3,9, aproximadamente 3,8, aproximadamente 3,7, aproximadamente 3,6, aproximadamente 3,5, aproximadamente 3,4, aproximadamente 3,3, aproximadamente 3,2, aproximadamente 3.1, aproximadamente 3,0, aproximadamente 2,9, aproximadamente 2,8, aproximadamente 2,7, aproximadamente 2,6, aproximadamente 2,5, aproximadamente 2,4, aproximadamente 2,3, aproximadamente 2.2, aproximadamente 2,1 o aproximadamente 2,0.
4. El procedimiento de cualquiera de las reivindicaciones 1 a 3, en el que la acidificación se consigue mediante el uso de ácido clorhídrico, ácido nítrico, ácido fosfórico o ácido sulfúrico.
5. El procedimiento de una cualquiera de las reivindicaciones 1 a 4, en el que el proceso precipita al menos el 98 % de las proteínas de la solución.
6. El procedimiento de cualquiera de las reivindicaciones 1 a 5, en el que la etapa de acidificación va seguida de una filtración con carbón activado.
7. El procedimiento de la reivindicación 6, en el que dicho procedimiento precipita al menos el 90% de la proteína restante.
8. El procedimiento de cualquiera de las reivindicaciones 1 a 7, en el que dicho S. pneumoniae se selecciona entre los serotipos 1,4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F y 23F.
9. Una solución que contiene polisacáridos capsulares sustancialmente purificados obtenidos por medio del procedimiento de cualquiera de las reivindicaciones 1 a 8 en el que la relación porcentual de proteína a polisacárido (proteína/PS) sea de menos del 10 %, menos del 9 %, menos del 8 %, menos del 7 %, menos del 6 %, menos del 5 %, menos del 4 %, menos del 3 %, menos del 2 % o menos del 1 % y la relación porcentual de ácido nucleico a polisacárido (NA/PS) sea menos del 5 %, menos del 4 %, menos del 3 %, menos del 2 % o menos del 1 %.
10. La solución de la reivindicación 11, en la que:
- el polisacárido capsular es del serotipo 1 y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 4 y la relación proteína/PS es inferior al 3% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 5 y la relación proteína/PS es inferior o igual al 7,5% y la relación NA/Ps es inferior o igual al 2%;
- el polisacárido capsular es del serotipo 6A y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 6B y la relación proteína/PS es inferior al 4% y la relación NA/PS es inferior al 1%;
- el polisacárido capsular es del serotipo 7F y la relación proteína/PS es inferior al 5% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 9V y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 1%;
- el polisacárido capsular es del serotipo 14 y la relación proteína/PS es inferior al 3% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 18C y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 19A y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 2%;
- el polisacárido capsular es del serotipo 19F y la relación proteína/PS es inferior al 3% y la relación NA/PS es inferior al 2%; o
- el polisacárido capsular es del serotipo 23F y la relación proteína/PS es inferior al 2% y la relación NA/PS es inferior al 2%.
11. Un procedimiento de fabricación de una vacuna de neumococos, que comprende producir polisacáridos capsulares purificados a partir de un lisado celular de Streptococcus pneumoniae por un procedimiento
reivindicado en una cualquiera de las reivindicaciones 1 a 8 y mediante el uso de dichos polisacáridos capsulares purificados en la fabricación de una vacuna de neumococos.
12. El procedimiento de la reivindicación 11, en el que la vacuna de neumococos contiene polisacárido conjugado con un vehículo proteico.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US89661607P | 2007-03-23 | 2007-03-23 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2922132T3 true ES2922132T3 (es) | 2022-09-08 |
Family
ID=39712482
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES11194173.8T Active ES2677353T3 (es) | 2007-03-23 | 2008-03-20 | Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae |
| ES18177128T Active ES2922132T3 (es) | 2007-03-23 | 2008-03-20 | Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae |
| ES08732592.4T Active ES2614249T3 (es) | 2007-03-23 | 2008-03-20 | Procedimiento abreviada de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES11194173.8T Active ES2677353T3 (es) | 2007-03-23 | 2008-03-20 | Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES08732592.4T Active ES2614249T3 (es) | 2007-03-23 | 2008-03-20 | Procedimiento abreviada de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae |
Country Status (30)
| Country | Link |
|---|---|
| US (3) | US8652480B2 (es) |
| EP (3) | EP2436700B8 (es) |
| JP (5) | JP5688902B2 (es) |
| KR (2) | KR101500771B1 (es) |
| CN (1) | CN101663327B (es) |
| AU (1) | AU2008231041B2 (es) |
| BR (1) | BRPI0809212B8 (es) |
| CA (1) | CA2681570C (es) |
| CL (2) | CL2008000831A1 (es) |
| CO (1) | CO6251324A2 (es) |
| CR (1) | CR11041A (es) |
| DK (3) | DK2436700T5 (es) |
| EC (1) | ECSP099652A (es) |
| ES (3) | ES2677353T3 (es) |
| GT (1) | GT200900249A (es) |
| HK (1) | HK1141815A1 (es) |
| HN (1) | HN2009001965A (es) |
| HU (3) | HUE031567T2 (es) |
| IL (1) | IL201106A (es) |
| MX (1) | MX2009010221A (es) |
| MY (1) | MY150927A (es) |
| NI (1) | NI200900172A (es) |
| NZ (1) | NZ580134A (es) |
| PL (3) | PL2129693T3 (es) |
| PT (3) | PT2129693T (es) |
| RU (1) | RU2516340C2 (es) |
| SI (3) | SI2436700T1 (es) |
| UA (1) | UA99278C2 (es) |
| WO (1) | WO2008118752A2 (es) |
| ZA (1) | ZA200906625B (es) |
Families Citing this family (83)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101663327B (zh) * | 2007-03-23 | 2014-05-07 | 惠氏公司 | 产生肺炎链球菌(streptococcus pneumoniae)荚膜多糖的缩短的纯化方法 |
| GB0818453D0 (en) * | 2008-10-08 | 2008-11-12 | Novartis Ag | Fermentation processes for cultivating streptococci and purification processes for obtaining cps therefrom |
| ES2586308T3 (es) | 2008-10-27 | 2016-10-13 | Glaxosmithkline Biologicals Sa | Procedimiento de purificación de un hidrato de carbono de Streptococcus del grupo A |
| BRPI0923165A8 (pt) * | 2008-12-18 | 2017-09-12 | Wyeth Llc | método para a produção de uma solução contendo polissacarídeos capsulares de streptococcus pneumoniae isolados de alto peso molecular, bem como solução contendo os referidos polissacarídeos |
| BRPI0922981A8 (pt) * | 2008-12-18 | 2019-11-26 | Wyeth Llc | método para o controle do peso molecular polissacarídeo para o sorotipo 19a de streptococcus pneumoniae |
| EP2424562B1 (en) | 2009-04-30 | 2015-10-07 | Coley Pharmaceutical Group, Inc. | Pneumococcal vaccine and uses thereof |
| PL2445522T3 (pl) | 2009-06-22 | 2018-01-31 | Wyeth Llc | Kompozycje immunogenne antygenów Staphylococcus aureus |
| AU2010301043B2 (en) | 2009-06-22 | 2014-01-09 | Wyeth Llc | Compositions and methods for preparing Staphylococcus aureus serotype 5 and 8 capsular polysaccharide conjugate immunogenic compositions |
| TW201136603A (en) * | 2010-02-09 | 2011-11-01 | Merck Sharp & Amp Dohme Corp | 15-valent pneumococcal polysaccharide-protein conjugate vaccine composition |
| US8841104B2 (en) | 2010-04-21 | 2014-09-23 | Nanomr, Inc. | Methods for isolating a target analyte from a heterogeneous sample |
| US9476812B2 (en) | 2010-04-21 | 2016-10-25 | Dna Electronics, Inc. | Methods for isolating a target analyte from a heterogeneous sample |
| US20110262989A1 (en) | 2010-04-21 | 2011-10-27 | Nanomr, Inc. | Isolating a target analyte from a body fluid |
| WO2011145108A2 (en) * | 2010-05-15 | 2011-11-24 | Serum Institute Of India Ltd. | Purification of capsular polysaccharides |
| JP5944480B2 (ja) * | 2011-03-22 | 2016-07-05 | セルム・インスティテュート・オブ・インディア・ピーブイティー.・リミテッド | 多糖を調製するための新規な方法 |
| CN102660602B (zh) * | 2012-04-17 | 2015-03-25 | 江苏康泰生物医学技术有限公司 | 快速纯化细菌荚膜多糖的方法 |
| CN102660603B (zh) * | 2012-04-17 | 2015-03-25 | 江苏康泰生物医学技术有限公司 | 一种快速纯化细菌荚膜多糖的方法 |
| CN102660601B (zh) * | 2012-04-17 | 2015-10-28 | 江苏康泰生物医学技术有限公司 | 快速纯化细菌荚膜多糖的方法 |
| US9650411B2 (en) * | 2012-08-07 | 2017-05-16 | Kyowa Hakko Kirin Co., Ltd. | Method of purifying protein |
| ES2651415T3 (es) * | 2012-09-07 | 2018-01-26 | Sk Chemicals Co., Ltd. | Método de producción de un polisacárido capsular que tiene un serotipo neumocócico |
| CN104582718B (zh) | 2012-10-03 | 2017-10-24 | 诺华股份有限公司 | 免疫原性组合物 |
| US9599610B2 (en) | 2012-12-19 | 2017-03-21 | Dnae Group Holdings Limited | Target capture system |
| US9551704B2 (en) | 2012-12-19 | 2017-01-24 | Dna Electronics, Inc. | Target detection |
| US10000557B2 (en) | 2012-12-19 | 2018-06-19 | Dnae Group Holdings Limited | Methods for raising antibodies |
| US9995742B2 (en) | 2012-12-19 | 2018-06-12 | Dnae Group Holdings Limited | Sample entry |
| US9434940B2 (en) | 2012-12-19 | 2016-09-06 | Dna Electronics, Inc. | Methods for universal target capture |
| US9804069B2 (en) | 2012-12-19 | 2017-10-31 | Dnae Group Holdings Limited | Methods for degrading nucleic acid |
| CN105339388B (zh) | 2013-07-12 | 2021-06-15 | Emd密理博公司 | 确定利用活性炭从包含靶蛋白的样品去除病毒的方法 |
| US11708411B2 (en) | 2013-12-20 | 2023-07-25 | Wake Forest University Health Sciences | Methods and compositions for increasing protective antibody levels induced by pneumococcal polysaccharide vaccines |
| EP3583947B1 (en) | 2014-01-21 | 2023-10-11 | Pfizer Inc. | Streptococcus pneumoniae capsular polysaccharides and conjugates thereof |
| US11160855B2 (en) | 2014-01-21 | 2021-11-02 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| NZ755769A (en) | 2014-01-21 | 2023-06-30 | Pfizer | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| CA2937184A1 (en) | 2014-01-21 | 2015-07-30 | Pfizer Inc. | Streptococcus pneumoniae capsular polysaccharides and conjugates thereof |
| US9107906B1 (en) | 2014-10-28 | 2015-08-18 | Adma Biologics, Inc. | Compositions and methods for the treatment of immunodeficiency |
| HRP20230416T1 (hr) | 2015-01-15 | 2023-07-07 | Pfizer Inc. | Imunogeni pripravci, namijenjeni upotrebi u cjepivima protiv pneumokoka |
| TWI718144B (zh) | 2015-05-04 | 2021-02-11 | 美商輝瑞股份有限公司 | B型鏈球菌多醣-蛋白質軛合物、製造軛合物之方法、含軛合物之免疫原性組成物、及其用途 |
| JPWO2016204265A1 (ja) * | 2015-06-18 | 2018-06-14 | 一般財団法人阪大微生物病研究会 | 肺炎球菌補体依存性殺菌能測定方法 |
| EP3325008A1 (en) | 2015-07-21 | 2018-05-30 | Pfizer Inc | Immunogenic compositions comprising conjugated capsular saccharide antigens, kits comprising the same and uses thereof |
| CN105131139B (zh) * | 2015-07-31 | 2018-02-13 | 兰州生物制品研究所有限责任公司 | 一种肺炎链球菌荚膜多糖的纯化方法 |
| WO2017085586A1 (en) | 2015-11-20 | 2017-05-26 | Pfizer Inc. | Immunogenic compositions for use in pneumococcal vaccines |
| CN109862908B (zh) | 2016-08-05 | 2023-05-02 | 圣诺菲·帕斯图尔公司 | 多价肺炎球菌多糖-蛋白质缀合物组合物 |
| MX2019001341A (es) | 2016-08-05 | 2019-07-04 | Sanofi Pasteur Inc | Composicion de conjugado de polisacarido neumococico multivalente-proteina. |
| US10751402B2 (en) | 2016-11-09 | 2020-08-25 | Pfizer Inc. | Immunogenic compositions and uses thereof |
| US11951165B2 (en) | 2016-12-30 | 2024-04-09 | Vaxcyte, Inc. | Conjugated vaccine carrier proteins |
| MX2019007910A (es) | 2016-12-30 | 2019-12-05 | Sutrovax Inc | Conjugados de polipeptido-antigeno con aminoacidos no naturales. |
| CA3050622A1 (en) | 2017-01-20 | 2018-07-26 | Pfizer Inc. | Immunogenic compositions for use in pneumococcal vaccines |
| CN110225764A (zh) | 2017-01-31 | 2019-09-10 | 默沙东公司 | 制备多糖-蛋白缀合物的方法 |
| WO2018144438A1 (en) | 2017-01-31 | 2018-08-09 | Merck Sharp & Dohme Corp. | Methods for production of capsular polysaccharide protein conjugates from streptococcus pneumoniae serotype 19f |
| AU2018225099A1 (en) | 2017-02-24 | 2019-07-25 | Merck Sharp & Dohme Llc | Enhancing immunogenicity of Streptococcus pneumoniae polysaccharide-protein conjugates |
| US10259865B2 (en) | 2017-03-15 | 2019-04-16 | Adma Biologics, Inc. | Anti-pneumococcal hyperimmune globulin for the treatment and prevention of pneumococcal infection |
| BR112019026192B1 (pt) | 2017-06-10 | 2022-05-10 | Inventprise, Llc | Vacinas de conjugado multivalente com polissacarídeos de conjugado bivalente ou multivalente que fornecem imunogenicidade e avidez melhoradas |
| US10729763B2 (en) | 2017-06-10 | 2020-08-04 | Inventprise, Llc | Mixtures of polysaccharide-protein pegylated compounds |
| KR102472936B1 (ko) * | 2017-07-05 | 2022-11-30 | 인벤트프라이즈 엘엘씨 | 용해 효소, 접선방향 유동 여과, 및 다중모드 크로마토그래피를 이용한, 백신 제조를 위한 다당류 정제 |
| US10702596B2 (en) | 2017-07-05 | 2020-07-07 | Inventprise, Llc | Polysaccharide purification for vaccine production using lytic enzymes, tangential flow filtration, and multimode chromatography |
| US11395849B2 (en) | 2017-09-07 | 2022-07-26 | Merck Sharp & Dohme Llc | Pneumococcal polysaccharides and their use in immunogenic polysaccharide-carrier protein conjugates |
| KR20200051004A (ko) | 2017-09-07 | 2020-05-12 | 머크 샤프 앤드 돔 코포레이션 | 폐렴구균 폴리사카라이드 및 면역원성 폴리사카라이드-담체 단백질 접합체에서의 그의 용도 |
| BR112020004502A8 (pt) | 2017-09-07 | 2022-11-01 | Merck Sharp & Dohme | Polissacarídeos pneumocócicos e uso dos mesmos em conjugados imunogênicos polissacarídeo-proteína carreadora |
| CN107936128B (zh) * | 2017-11-22 | 2020-07-03 | 成都欧林生物科技股份有限公司 | 一种简便有效的细菌疫苗纯化方法 |
| SG11202005255PA (en) | 2017-12-06 | 2020-07-29 | Merck Sharp & Dohme | Compositions comprising streptococcus pneumoniae polysaccharide-protein conjugates and methods of use thereof |
| JP7397000B2 (ja) | 2018-04-30 | 2023-12-12 | メルク・シャープ・アンド・ドーム・エルエルシー | 凍結乾燥変異ジフテリア毒素のジメチルスルホキシド中均一溶液を提供する方法 |
| WO2020010000A1 (en) | 2018-07-04 | 2020-01-09 | Sutrovax, Inc. | Improved methods for the preparation of immunogenic conjugates |
| WO2020009993A1 (en) | 2018-07-04 | 2020-01-09 | Sutrovax, Inc. | Improvements in immunogenic conjugates |
| WO2020010016A1 (en) | 2018-07-04 | 2020-01-09 | Sutrovax, Inc. | Self-adjuvanted immunogenic conjugates |
| CA3106291A1 (en) * | 2018-07-19 | 2020-01-23 | Glaxosmithkline Biologicals Sa | Processes for preparing dried polysaccharides |
| EP3893926A1 (en) | 2018-12-12 | 2021-10-20 | Pfizer Inc. | Immunogenic multiple hetero-antigen polysaccharide-protein conjugates and uses thereof |
| JP7275277B2 (ja) | 2018-12-19 | 2023-05-17 | メルク・シャープ・アンド・ドーム・エルエルシー | ストレプトコッカス・ニューモニエ多糖-タンパク質コンジュゲートを含む組成物およびその使用方法 |
| JP7239509B6 (ja) | 2019-02-22 | 2023-03-28 | ファイザー・インク | 細菌多糖類を精製するための方法 |
| US20220184199A1 (en) | 2019-04-10 | 2022-06-16 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens, kits comprising the same and uses thereof |
| US20220265803A1 (en) | 2019-07-31 | 2022-08-25 | Sanofi Pasteur Inc. | Multivalent pneumococcal polysaccharide-protein conjugate compositions and methods of using the same |
| US20210070890A1 (en) * | 2019-09-06 | 2021-03-11 | Serum Institute Of India Private Limited | Method for obtaining purified bacterial polysaccharides |
| IL295713A (en) * | 2020-02-21 | 2022-10-01 | Pfizer | Isolation of saccharides |
| US20230321212A1 (en) | 2020-08-26 | 2023-10-12 | Pfizer Inc. | Group b streptococcus polysaccharide-protein conjugates, methods for producing conjugates, immunogenic compositions comprising conjugates, and uses thereof |
| GB202016165D0 (en) | 2020-10-12 | 2020-11-25 | Optivalent Ltd | Vaccine |
| WO2022084852A1 (en) | 2020-10-22 | 2022-04-28 | Pfizer Inc. | Methods for purifying bacterial polysaccharides |
| CA3200602A1 (en) | 2020-11-04 | 2022-05-12 | Pfizer Inc. | Immunogenic compositions for use in pneumococcal vaccines |
| JP2023549736A (ja) | 2020-11-10 | 2023-11-29 | ファイザー・インク | コンジュゲートさせた莢膜糖抗原を含む免疫原性組成物およびその使用 |
| TW202245835A (zh) | 2021-02-04 | 2022-12-01 | 美商默沙東有限責任公司 | 用於肺炎球菌結合物疫苗之奈米乳化液佐劑組合物 |
| WO2022234416A1 (en) | 2021-05-03 | 2022-11-10 | Pfizer Inc. | Vaccination against pneumoccocal and covid-19 infections |
| EP4333879A1 (en) | 2021-05-03 | 2024-03-13 | Pfizer Inc. | Vaccination against bacterial and betacoronavirus infections |
| AU2022281543A1 (en) | 2021-05-28 | 2023-11-23 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| TW202306969A (zh) | 2021-05-28 | 2023-02-16 | 美商輝瑞大藥廠 | 包含結合之莢膜醣抗原的免疫原組合物及其用途 |
| WO2023135515A1 (en) | 2022-01-13 | 2023-07-20 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| GB2614916A (en) | 2022-01-25 | 2023-07-26 | Optivalent Ltd | Intradermal vaccine complement |
| WO2023161817A1 (en) | 2022-02-25 | 2023-08-31 | Pfizer Inc. | Methods for incorporating azido groups in bacterial capsular polysaccharides |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0002004B1 (en) | 1977-11-07 | 1982-03-24 | Ciba-Geigy Ag | Process for the manufacture of fluorinated cationic compounds and their use as surfactants |
| CA1115210A (en) * | 1977-11-28 | 1981-12-29 | Dennis J. Carlo | Pneumococcal vaccine |
| US4221906A (en) * | 1979-03-19 | 1980-09-09 | American Cyanamid Company | Stabilization of pneumococcal polysaccharides |
| US4242501A (en) * | 1979-08-08 | 1980-12-30 | American Cyanamid Company | Purification of pneumococcal capsular polysaccharides |
| FR2495939B1 (fr) * | 1980-12-11 | 1985-10-11 | Merieux Inst | Procede de purification de polyosides de streptococcus pneumoniae et vaccin a base de polyosides ainsi purifies |
| US4686102A (en) * | 1984-04-12 | 1987-08-11 | American Cyanamid Company | Multivalent pneumococcal vaccine and preparation thereof |
| JPS6170994A (ja) * | 1984-09-14 | 1986-04-11 | Daikin Ind Ltd | 環状(1→2)−β−D−グルカンの製法 |
| IT1187753B (it) * | 1985-07-05 | 1987-12-23 | Sclavo Spa | Coniugati glicoproteici ad attivita' immunogenica trivalente |
| CA2059692C (en) * | 1991-01-28 | 2004-11-16 | Peter J. Kniskern | Pneumoccoccal polysaccharide conjugate vaccine |
| US5714354A (en) * | 1995-06-06 | 1998-02-03 | American Home Products Corporation | Alcohol-free pneumococcal polysaccharide purification process |
| RU2087156C1 (ru) * | 1995-06-22 | 1997-08-20 | Леонид Николаевич Падюков | Вакцина против пневмококковой инфекции |
| AU754256C (en) * | 1997-12-23 | 2004-05-20 | Pfizer Ireland Pharmaceuticals | Procedures for the extraction and isolation of bacterial capsular polysaccharides for use as vaccines or linked to proteins as conjugate vaccines |
| US6146902A (en) * | 1998-12-29 | 2000-11-14 | Aventis Pasteur, Inc. | Purification of polysaccharide-protein conjugate vaccines by ultrafiltration with ammonium sulfate solutions |
| GB0108079D0 (en) * | 2001-03-30 | 2001-05-23 | Microbial Technics Ltd | Protein |
| GB0115176D0 (en) * | 2001-06-20 | 2001-08-15 | Chiron Spa | Capular polysaccharide solubilisation and combination vaccines |
| BRPI0607026B1 (pt) * | 2005-04-08 | 2022-02-15 | Wyeth | Processos para redução do teor de proteína e preservação do teor de polissacarídeo capsular em um caldo de lisado celular de streptococcus pneumoniae complexo antes da purificação |
| US7709001B2 (en) * | 2005-04-08 | 2010-05-04 | Wyeth Llc | Multivalent pneumococcal polysaccharide-protein conjugate composition |
| EP2425851A1 (en) * | 2005-04-08 | 2012-03-07 | Wyeth LLC | Multivalent Pneumococcal Polysaccharide-Protein Conjugate Composition |
| CN101663327B (zh) * | 2007-03-23 | 2014-05-07 | 惠氏公司 | 产生肺炎链球菌(streptococcus pneumoniae)荚膜多糖的缩短的纯化方法 |
-
2008
- 2008-03-20 CN CN200880012946.2A patent/CN101663327B/zh active Active
- 2008-03-20 PL PL08732592T patent/PL2129693T3/pl unknown
- 2008-03-20 HU HUE08732592A patent/HUE031567T2/hu unknown
- 2008-03-20 DK DK11194173.8T patent/DK2436700T5/en active
- 2008-03-20 AU AU2008231041A patent/AU2008231041B2/en active Active
- 2008-03-20 PT PT87325924T patent/PT2129693T/pt unknown
- 2008-03-20 KR KR1020097021976A patent/KR101500771B1/ko active IP Right Grant
- 2008-03-20 US US12/052,525 patent/US8652480B2/en active Active
- 2008-03-20 HU HUE18177128A patent/HUE059085T2/hu unknown
- 2008-03-20 MX MX2009010221A patent/MX2009010221A/es active IP Right Grant
- 2008-03-20 EP EP11194173.8A patent/EP2436700B8/en active Active
- 2008-03-20 EP EP18177128.8A patent/EP3406635B1/en active Active
- 2008-03-20 NZ NZ580134A patent/NZ580134A/en unknown
- 2008-03-20 SI SI200831984T patent/SI2436700T1/sl unknown
- 2008-03-20 CA CA2681570A patent/CA2681570C/en active Active
- 2008-03-20 ES ES11194173.8T patent/ES2677353T3/es active Active
- 2008-03-20 PL PL18177128.8T patent/PL3406635T3/pl unknown
- 2008-03-20 PT PT181771288T patent/PT3406635T/pt unknown
- 2008-03-20 UA UAA200909741A patent/UA99278C2/ru unknown
- 2008-03-20 CL CL200800831A patent/CL2008000831A1/es unknown
- 2008-03-20 JP JP2009554744A patent/JP5688902B2/ja active Active
- 2008-03-20 HU HUE11194173A patent/HUE039169T2/hu unknown
- 2008-03-20 BR BRPI0809212A patent/BRPI0809212B8/pt active IP Right Grant
- 2008-03-20 EP EP08732592.4A patent/EP2129693B1/en active Active
- 2008-03-20 SI SI200831741A patent/SI2129693T1/sl unknown
- 2008-03-20 WO PCT/US2008/057688 patent/WO2008118752A2/en active Application Filing
- 2008-03-20 RU RU2009135485/10A patent/RU2516340C2/ru active
- 2008-03-20 KR KR1020157002150A patent/KR20150021127A/ko not_active Application Discontinuation
- 2008-03-20 ES ES18177128T patent/ES2922132T3/es active Active
- 2008-03-20 SI SI200832196T patent/SI3406635T1/sl unknown
- 2008-03-20 DK DK08732592.4T patent/DK2129693T3/en active
- 2008-03-20 PL PL11194173T patent/PL2436700T3/pl unknown
- 2008-03-20 DK DK18177128.8T patent/DK3406635T3/da active
- 2008-03-20 PT PT111941738T patent/PT2436700T/pt unknown
- 2008-03-20 MY MYPI20093908 patent/MY150927A/en unknown
- 2008-03-20 ES ES08732592.4T patent/ES2614249T3/es active Active
-
2009
- 2009-09-17 HN HN2009001965A patent/HN2009001965A/es unknown
- 2009-09-21 NI NI200900172A patent/NI200900172A/es unknown
- 2009-09-21 GT GT200900249A patent/GT200900249A/es unknown
- 2009-09-22 IL IL201106A patent/IL201106A/en active IP Right Grant
- 2009-09-22 ZA ZA200906625A patent/ZA200906625B/xx unknown
- 2009-09-23 EC EC2009009652A patent/ECSP099652A/es unknown
- 2009-09-23 CR CR11041A patent/CR11041A/es unknown
- 2009-10-20 CO CO09117278A patent/CO6251324A2/es active IP Right Grant
-
2010
- 2010-09-02 HK HK10108299.9A patent/HK1141815A1/xx unknown
-
2014
- 2014-01-24 US US14/163,863 patent/US8999697B2/en active Active
-
2015
- 2015-01-27 JP JP2015013167A patent/JP2015143225A/ja not_active Withdrawn
- 2015-02-27 US US14/633,141 patent/US9675681B2/en active Active
-
2017
- 2017-03-23 JP JP2017056848A patent/JP6825950B2/ja active Active
- 2017-08-08 CL CL2017002029A patent/CL2017002029A1/es unknown
-
2018
- 2018-11-06 JP JP2018208647A patent/JP2019048844A/ja not_active Withdrawn
-
2020
- 2020-01-31 JP JP2020014532A patent/JP6872649B2/ja active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2922132T3 (es) | Procedimiento abreviado de purificación para la producción de polisacáridos capsulares de Streptococcus pneumoniae | |
| JP2010521972A5 (es) | ||
| RU2524436C2 (ru) | Способ получения жидкой фракции, содержащей изолированные высокомолекулярные капсульные полисахариды streptococcus pneumoniae, и жидкая фракция, полученная таким способом | |
| ES2651415T3 (es) | Método de producción de un polisacárido capsular que tiene un serotipo neumocócico | |
| KR20160127028A (ko) | 다당류를 정제하는 신규한 다운스트림 방법 | |
| CN111295450A (zh) | 使用裂解酶、切向流过滤和多模式色谱法的用于疫苗生产的多糖纯化 | |
| WO2024062494A1 (en) | Method for the purification of capsular polysaccharides | |
| BR102015002980A2 (pt) | processo para purificar polissacarídeo bacteriano |