BRPI0809583B1 - Polipeptídeo fgf-21 modificado, composição compreendendo o mesmo, método para produzir o referido polipetídeo fgf-21 e célula compreendendo um polinucleotídeo - Google Patents
Polipeptídeo fgf-21 modificado, composição compreendendo o mesmo, método para produzir o referido polipetídeo fgf-21 e célula compreendendo um polinucleotídeo Download PDFInfo
- Publication number
- BRPI0809583B1 BRPI0809583B1 BRPI0809583-3A BRPI0809583A BRPI0809583B1 BR PI0809583 B1 BRPI0809583 B1 BR PI0809583B1 BR PI0809583 A BRPI0809583 A BR PI0809583A BR PI0809583 B1 BRPI0809583 B1 BR PI0809583B1
- Authority
- BR
- Brazil
- Prior art keywords
- fgf
- polypeptide
- amino acid
- seq
- group
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/50—Fibroblast growth factor [FGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1825—Fibroblast growth factor [FGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K19/00—Hybrid peptides, i.e. peptides covalently bound to nucleic acids, or non-covalently bound protein-protein complexes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/70—Vectors or expression systems specially adapted for E. coli
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Communicable Diseases (AREA)
- Rheumatology (AREA)
- Cardiology (AREA)
Abstract
POLIPEPTÍDEOS FGF-21 MODIFICADOS E SEUS USOS" .. Polipeptídeos FGF-21 modificados e usos dos mesmos são providos .
Description
[001]Este pedido reivindica prioridade a e benefícios do Pedido de Patente Seriado Provisório dos EUA No. 60/921.297, depositada em 30 de Março de 2007 e Pedido de Patente Seriado Provisório No. 60/988.060, depositado em 14 de Novem-bro de 2007, as especificações e revelações dos mesmos são aqui incorporadas em sua totalidade.
[002]Esta invenção relaciona-se a polipeptídeos FGF-21 opcionalmente mo-dificados com pelo menos um aminoácido não naturalmente codificado.
[003]Fatores de crescimento de fibroblastos são polipeptídeos grandes am-plamente expressos em tecidos de desenvolvimento e adultos (Baird et al, Cancer Cells, 3:239-243, 1991) e desempenham papéis cruciais em múltiplas funções fisio-lógicas incluindo angiogênese, mitogênese, formação de padrão, diferenciação celu-lar, regulação metabólica e reparo de injúria tecidual (McKeehan e tal, Prog. Nucleic Acid Res. Mol. Biol. 59:135-176, 1998; Burgess, W.H. et al, Annu. Rev. Biochem. 58:575-606 (1989). Os fatores de crescimento de fibroblastos protótipos (FGFs), FGF-1 e FGF-2, foram originalmente isolados a partir do cérebro e pituitária como mitógenos para fibroblastos. FGF-3 foi identificado como um alvo comum para ativa-ção por vírus de tumor mamário de camundongo (Disckson et al, Ann. N.Y. Acad. Sci.638:18-26 (1991); FGF-4 a FGF-6 foram identificados como produtos oncogenes (Yoshida et al, Ann. NY Acad. Sci. 638:27-37 (1991); Goldfarb et al, Ann. NY Acad. Sci. 638:38-52 (1991); Coulier et al, Ann. NY Acad. Sci. 638:53-61 (1991). FGF-10 foi identificado a partir de pulmão de rato por reação de polimerase em cadeia baseado em homologia (PCR) (Yamasaki et al, J. Biol. Chem. 271:15918-15921 (1996)). FGF-11 a FGF-14 (fatores homólogos FGF (FHFs) 1 a 4) foram identificados a partir de retina humana por uma combinação de uma sequência de cDNA aleatória, pes-quisas em bases de dados e PCR baseado em homologia (Swallwood et al, Proc. Natl. Acad. Sci. EUA 93:9850-9857 (1996)). FGF-15 foi identificado como um alvo na cascata de uma oncoprotéina homeodomínio quimérico (McWhirter et al, Deve-lopment 124:3221-3232 (1997)). FGF-16, FGF-17, e FGF-18 foram identificadas a partir de coração e embriões de rato por PCR baseado em homologia, respectiva-mente (Miyake et al, Biochem. Biophys. Res. Commun. 243:148-152 (1998); Hoshi- kawa et al, Biochem. Biophys. Res. Commun. 244:187-191 (1998); Ohbayashi et al, J. Biol. Chem. 273:18161-18164 (1998)). FGF-19 foi identificado a partir de cérebro fetal humano por pesquisa em banco de dados (Nishimura et al, Biochim. Biophys. Acta 1444:148-151 (1999)). Eles têm um núcleo resíduo de ~120 aminoácidos con-servados com ~30 a 60% de identidade de aminoácidos.
[004]Modelos animais, super expressão, e análise de mutações de ocorrên-cia natural implicam fatores de crescimento de fibroblasto e seus receptores em uma ampla variedade de doenças (por exemplo, Willie et al, Current Biology, (1995) 5:500-507; Pugh-Humpreys et al, In: The Cytokine Handbook, A. Thomson ed, 2a edição, Academic Press, Harcourt Brace & co. Publicadores, Londres, pp 525-566) sugerindo que a regulação da atividade pode ser utilizada para tratamento. Por exemplo, inibição do fator de crescimento de fibroblasto 2 pelo composto Suramina previne a neovascularização e crescimento de tumor em camundongos (Pesenti et al, British Journal of Cancer, 66:367-372). Fatores de crescimento de fibroblasto também em angiogênese (Lyons, M.K. et al, Brain Res. (1991) 558:315-320), cicatri- zação de ferida (Uhl, E. et al, Br. J. Surg. (1993) 80:977-980, 1993), astrogliose, proliferação e diferenciação de células da glia (Biagini, G. et al, Neurochem. Int. (1994) 25:17-24), vasodilatação cerebral (Tanaka, R. et al, Stroke (1995) 26:2154-2159), e processos neutróficos/neuromodulatórios.
[005]Fator de crescimento de fibroblasto também tem múltiplos efeitos posi-tivos incluindo fluxo de sangue e proteção da toxicidade de cálcio para melhorar o resultado na isquemia cerebral (Mattson, M.P. et al, Semin. Neurosci. (1993) 5:295- 307; Doetrocj. W.D. et al, J. Neurotrauma (1996) 13:309-316). Tratamento com FGF básico promove neoangiogênese no miocárdio isquêmico (Schumacher et al, Circu-lation (1998) 97:645-650). FGF básico aumenta a recuperação funcional e promove o desenvolvimento neuronal seguindo de infarto cerebral focal (Kawamata et al, Proc. Natl. Acad. Sci. (1997) 94 (15):8179-84). De acordo com a literatura publicada, a família FGF consiste em pelo menos vinte e dois membros (Reuss et al, Cell Tissue Res. 313-139-157 (2003)).
[006]Fator de crescimento do fibroblasto 21 (FGF-21) tem sido reportado ser preferencialmente expresso no fígado (Nishimura et al, Biochimica et Biophysica Ac-ta, 1492:203-206 (2000); WO 01/36640; e WO 01/18172, que são aqui incorporados por referência) e descrito como um tratamento para doença vascular isquêmica, ci- catrização de ferida, e doenças associadas com perda de células ou funções pulmo-nares, brônquicas ou alvéolos e numerosos outros distúrbios. FGF-21 é expresso primariamente no fígado, rim e tecido muscular (ver Exemplo 2 do Pedido de Patente dos EUA No. 20040259780 que é aqui incorporado por referência em sua totalidade). O gene FGF-21 é composto de 3 éxons e é localizado no cromossomo 19. Ao contrário dos outros FGFs, FGF-21 não tem efeitos proliferativos e tumorgênicos (Genome Biol. 2001; 2(3): REVIEWS 3005).
[007]Publicação do Pedido de Patente No. 20010012628, que incorporada por referência em sua totalidade, descreve um nucleotídeo e sequência de proteína para FGF-21 humano (ver SEQ ID NO:1 e 2, respectivamente do Publicação do Pe-dido de Patente No. 20010012628). SEQ ID NO:2 na publicação acima mencionada, referida aos aminoácidos sbgFGF-19, é tem 209 aminoácidos no comprimento e contém uma sequência de 28 aminoácidos líderes no N-terminal. A sequência FGF- 21 humana apresentada como SEQ ID NO:3 aqui é a mesma sequência como SEQ ID NO:2 do Pedido de Patente dos EUA No. 20010012628. Esta sequência tem um polimorfismo de nucleotídeo único (PNU) com prolina (P) na posição 174, de agora em diante referida como a “forma P” do aminoácido 209 de FGF-21”.
[008]Patente dos EUA No. 6.716.626, que é aqui incorporada por referência em sua totalidade, discute FGF-21 humana e proteínas homólogas em outros mamíferos, particularmente camundongos e ratos. Camundongos FGF mostraram que a SEQ ID NO:1 da Patente dos EUA No. 6.716.626 foi altamente expressa em fígado e expressa no testículo e timo, e foi sugerido que FGF-21 pode desempenhar um papel no desenvolvimento de e recuperação de doença hepática e/ou distúrbios da função testicular ou funções de células derivadas a partir do timo. SEQ ID NO:4 da Patente dos EUA No. 6.716.626 é aminoácido 209 no comprimento e contém uma sequência líder de 28 aminoácidos na sequência N-terminal. A sequência FGF-21 humana apresentada como SEQ ID NO:6 aqui é a mesma sequência como SEQ ID NO:4 da Patente dos EUA No. 6.716.626. Esta sequência tem um polimorfismo de nucleotídeo único (PNU) com leucina (L) na posição 174, de agora em diante referida como “forma L do aminoácido 209 do FGF-21”.
[009]Pedido de Patente dos EUA No. 20040259780, que é aqui incorporado por referência em sua totalidade, discute o FGF-21 humano e apresenta a sequência que tem 208 aminoácidos no comprimento (SEQ ID NO:2 do Pedido de Patente dos EUA No. 20040259780) e contém uma sequência líder de 27 aminoácidos no N- terminal. A sequência do FGF-21 humano apresentada como SEQ ID NO:7 aqui é a mesma sequência como SEQ ID NO:2 da Publicação de Patente dos EUA No. 20040259780. A sequência tem um polimorfismo de nucleotídeo único (PNU) com leucina (L) na posição 173, aqui em diante referido como a “forma L do aminoácido 208 de FGF-21”.
[0010]FGF-21 tem sido mostrado estimular captação de glicose em adipóci- tos 3T3-L1 de camundongos em presença e ausência de insulina, e diminuir dos ní-veis de glicose sanguínea, triglicerídeos, e glucagon na alimentação e no jejum em camundongos ob/ob e db/db e ratos ZDF de 8 semanas de idade em uma forma do- se-dependente, então, provendo, a base para o uso de FGF-21 como uma terapia para tratar diabetes e obesidade (WO 03/11213, que é aqui incorporado por referên-cia e Kharitonenkon et al, J. Clin. Invest., 2005 Junho; 115(6): 1627-35). Kharitonen- kov et al J. Clin. Invest. 2005 Junho; 115 (6):1627-35 também mostrou que camun- dongos transgênicos expressando FGF-21 humano são hipoglicêmicos, sensíveis a insulina, e resistente a obesidade induzida pela dieta. Kharitonenkov et al. Endocri-nology (em impressão) também mostra que FGF-21 diminui a glicose, triglicerídeo, insulina, e glucagon em macacos Rhesus diabéticos.
[0011]Em adição, FGF-21 tem sido mostrada ser efetiva em reduzir a morta-lidade e morbidade de pacientes criticamente doentes (WO 03/059270, que é aqui incorporada por referência). FGF-21 tem sido descrito no Pedido de Patente dos EUA 2005501176631, que é aqui incorporada por referência, para afetar o estado metabólico geral e pode ter efeitos colaterais e reações negativas que podem ocorrer durante a resposta do estresse do corpo para sepse bem como síndrome da resposta inflamatória sistêmica (SRIS) resultando de causas patológicas não infecciosas. Então, FGF-21 pode ser utilizada para reduzir a mortalidade e morbidade que ocorre em pacientes criticamente doentes. Pacientes criticamente doentes incluem aqueles pacientes que são fisiologicamente instáveis requerendo cuidados contínuo, coordenados por médicos, enfermagem, e respiratórios. Este tipo de cuidado neces-sita ter atenção particular para detalhes a fim de prover constante sobrevivência e titulação de terapia. Pacientes criticamente doentes incluem aqueles pacientes que estão em risco para descompensação fisiológica e então requerem monitoramento constante tal que o time de cuidado intensivo pode prover intervenção imediata para prevenir ocorrências adversas. Pacientes criticamente doentes têm necessidades especiais para monitorar o suporte de vida que deve ser provido por um time que pode prover cuidado de titulação contínuo.
[0012]Polipeptídeos PEGilados FGF-21 são descritos em WO 2005/091944, que é aqui incorporado por referência. O polipeptídeo FGF-21 descrito em WO 2005/091944 é um polipeptídeo de 181 aminoácidos. A sequência FGF-21 humana madura, selvagem ou nativa indicada como SEQ ID NO:1 da WO 2005/091944 falta uma sequência líder. Este FGF-21 humano é altamente idêntico ao FGF-21 de ca-mundongo (~79% de identidade de aminoácido) e FGF-21 de rato (~80% de identi-dade de aminoácido). A sequência FGF-21 humana apresentada como SEQ ID NO:5 aqui é a mesma sequência como SEQ ID NO:1 da WO 05/091944. Esta se-quência tem um polimorfismo de nucleotídeo único (PNU) com leucina (L) na posi-ção 146. Um versado na técnica pode facilmente usar sequências polipeptídicas FGF-21 mamíferas alternativas ou análogos, muteínas, ou derivados que têm homo- logia suficiente às sequências FGF-21 para os usos aqui descritos.
[0013]A sequência FGF-21 humana apresentada como SEQ ID NO:1 aqui tem um polimorfismo de nucleotídeo único (PNU) com prolina (P) na posição 146. Uma versão com marcador His no N-terminal da SEQ ID NO:1 é mostrada como SEQ ID NO:2 aqui.
[0014]WO 2005/091944 descreve a ligação covalente de uma ou mais molé-culas de PEG à resíduos particulares de um composto FGF-21. O composto resul-tante foi um biologicamente ativo, composto FGF-21 PEGilado com uma meia vida de eliminação estendida e depuração reduzida quando comparado ao FGF-21 nativo. As moléculas PEG foram covalentemente ligadas a resíduos de cisteína ou lisina. Substituições foram feitas em várias posições com cisteína para permitir a ligação de pelo menos uma molécula PEG. PEGilação em um ou mais resíduos lisian (56, 59, 69, e 122) foi descrita.
[0015]Compostos FGF-21 PEGilados podem ser úteis no tratamento de pa-cientes com distúrbios, incluindo, mas não limitados a diabetes do tipo 2, obesidade, resistência a insulina, hiperinsulinemia, intolerância a glicose, hiperglicemia, e sín- drome metabólica. Pode ser particularmente vantajoso ter compostos FGF-21 PEGi- lados que pode aumentar a eficácia por permitir por um tempo maior a meia vida de circulação e que pode requerer doses menores, aumentado ambos, a conveniência para um paciente em necessidade de tal terapia e a possibilidade de uma adesão do paciente com requerimento de doses. Síndrome metabólica pode ser definida como um grupo de pelo menos três dos seguintes sinais: gordura abdominal - na maioria homens, uma cintura de 101,6 cm (40 polegadas) ou mais; açúcar alto no sangue - pelo menos 110 miligramas por decilitro (mg/dL) após alimentação; triglicerídeo alto - pelo menos 150 mg/dL na corrente sanguínea; HDL baixo - menos que 40 mg/dL; e, pressão sanguínea de 130/85 da mais alta.
[0016]Ligação covalente do polímero hidrofílico poli(etileno glicol), abreviado PEG, é um método de aumentar a solubilidade em água, biodisponibilidade, aumen-to da meia vida sérica, aumento da meia vida terapêutica, modulação da imunogeni- cidade, modulação da atividade biológica, ou extensão do tempo de circulação de muitas moléculas biologicamente ativas, incluindo proteínas, peptídeos, e particu-larmente moléculas hidrofóbicas. PEG tem sido utilizado extensivamente em farma-cêuticos, implantes artificiais, e em outras aplicações onde a biocompatibilidade, au-sência de toxicidade, e ausência de imunogenicidade é de importância. A fim de ma-ximizar as propriedades desejadas de PEG, o peso molecular total e estado de hi-dratação do polímero ou polímeros PEG ligados à molécula biologicamente ativo deve ser suficientemente alto para impedir as características vantajosas tipicamente associadas com ligação de polímero PEG, tal como solubilidade em água aumentada e meia vida de circulação, enquanto não impacta adversamente a bioatividade da molécula parente.
[0017]Derivados PEG são frequentemente ligadas as moléculas biologica-mente ativas através de funcionalidades químicas reativas, tais como resíduos lisina, cisteína e histidina, a N-terminal e frações carboidratos. Tem havido pesquisa na formulação de um composto FGF-21 terapêutico, mas tem sido problemático por muitas razões, uma das quais é porque proteínas e outras moléculas sempre têm um número limitado de sítios reativos disponíveis para ligação a polímero. Sempre, os sítios mais desejáveis para modificação através de ligação a polímero desempenham um papel significante na ligação ao receptor, e são necessários para retenção da atividade biológica da molécula. Como um resultado, ligação indiscriminada de cadeias de polímeros a tais sítios reativos em uma molécula biologicamente ativa sempre leva a uma redução significante ou mesmo perda total da atividade biológica da molécula modificada de polímero. R. Clark et al (1996), J. Biol. Chem., 271:21969-21977. Para formar conjugados tendo suficiente peso molecular de polímero para prejudicar as vantagens desejadas a uma molécula alvo, abordagens an- tecedentes da técnica têm tipicamente envolvido ligação aleatória de numerosos braços do polímero à molécula, assim aumentando o risco de uma redução ou mes-mos perda total na bioatividade da molécula parente.
[0018]Sítios reativos que formam o loci para ligação de derivados PEG à proteínas são ditados pela estrutura da proteína. Proteínas, incluindo enzimas, são compostas de várias sequências de alfa-aminoácidos, que têm a estrutura geral H2N--CHN--COOH. A fração alfa-amino (H2N--) de um aminoácido se junta à fração carboxila (--COOH) de um aminoácido adjacente para formar ligações amida, que podem ser representadas como -(NH--CHR--CO)n--, onde o sobrescrito “n” pode ser igual a centenas ou milhares. O fragmento representado por R pode conter sítios reativos para atividade biológica e para ligação de derivados PEG.
[0019]Por exemplo, no caso do aminoácido lisina, existe uma fração --NH2 na posição epsilon bem como na posição alfa. A --NH2 epsilon é livre para reagir sobre condições de pH básico. Muito da técnica no campo da derivatização de prote-ína com PEG tem sido direcionada para desenvolvimento de derivados PEG para ligação a fração --NH2 epsilon dos resíduos lisina nas proteínas. “Polyethylene Gly-col and Derivatives for Advanced PEGylation”, Nektar Molecular Engineering Cata-log, 2003, pp. 1-17. Esses derivados PEG todos têm a limitação comum, entretanto, eles não podem ser instalados seletivamente entre os sempre numerosos resíduos lisina presentes nas superfícies de proteínas. Esta pode ser uma limitação significan- te em exemplos onde um resíduo lisina é importante para a atividade de proteína, existindo em um sítio ativo de enzima, por exemplo, ou em casos onde o resíduo lisina desempenha um papel em mediar a interação da proteína com outras molécu-las biológicas, como no caso de sítios de ligação de receptor.
[0020]Uma segunda e igualmente importante complicação de métodos exis-tentes para PEGilação de proteína é que o derivados PEG podem experimentar rea-ções colaterais não desejadas com outros resíduos que aqueles desejados. Histidina contém uma fração reativa imino, representada estruturalmente como --N(H)--, mas muitas espécies quimicamente reativas que reagem com --NH2 epsilon podem tam- bém reagir com --N(H)--. Similarmente, a cadeia lateral do aminoácido cisteína produz um grupo sulfidrila livre, estruturalmente representado como -SH. Em algumas modalidades, os PEG derivados direcionados ao grupo NH2-epsilon da lisina tam-bém reage com cisteína, histidina ou outros resíduos. Isto pode criar complexo, mis-turas heterogêneas de moléculas bioativas derivadas de PEG e riscos de destruir a atividade da molécula bioativa sendo alvos. Pode ser desejável desenvolver deriva-dos PEG que permitam um grupo funcional químico ser introduzido em um sítio úni-co dentro da proteína que pode então permite o acoplamento seletivo de um ou mais polímeros PEG para a molécula bioativa em sítios específicos na superfície da prote-ína que são ambos bem definidos e preditíveis.
[0021]Em adição aos resíduos lisina, esforços consideráveis na técnica têm sido direcionados para o desenvolvimento de reagentes PEG ativados que tem como alvo outras cadeias aminoácidos, incluindo cisteína, histidina e N-terminal. Ver, por exemplo, Pat. EUA No. 6.610.281 que é aqui incorporada por referência, e “Polyethylene Glycol and Derivatives for Advanced PEGylation”, Nektar Molecular Engineering Catalog, 2003, pp. 1-17. Um resíduo cisteína pode ser introduzido em sítio-seletivo na estrutura de proteínas utilizando mutagênese sítio-direcionada e ou-tras técnicas conhecidas no meio, e a fração sulfidrila livre resultante pode ser reagi-da com derivados PEG que produzem grupos funcionais reativos a tiol. Esta aborda-gem é complicada, entretanto, nela a introdução de um grupo sulfidrila livre pode complicar a expressão, envelopamento e estabilidade da proteína resultante. Então, pode ser desejável ter um meio de introduzir um grupo químico funcional no FGF-21 que permite o acoplamento seletivo de um ou mais polímeros PEG à proteína en-quanto simultaneamente sendo compatível com (isto é, não reagindo em reações colaterais não desejadas com) sulfidrilas e outros grupos funcionais químicos tipica-mente encontrados em proteínas.
[0022]Como pode ser visto a partir de amostras da técnica, muitos desses derivados que têm sido desenvolvidos para ligação às cadeias laterais de proteínas, em particular, a fração --NH2 na cadeia aminoácido lisina e a fração -SH na cadeia lateral cisteína, tem problemática provada em sua síntese e uso. Algumas formas de ligações instáveis com a proteína que são sujeitas à hidrólises e assim decompõem, degradam, ou são de outra forma instáveis em ambientes aquosos, tal como na cor-rente sanguíneo. Alguma forma de ligações mais estáveis, mas são sujeitos a hidró-lises antes da ligação ser formada, que significa que o grupo reativo no derivado PEG pode ser inativado antes da proteína pode ser ligada. Alguns são de alguma forma tóxicos e são dessa forma menos adequados para uso in vivo. Alguns são muito lentos para reagir para serem praticamente úteis. Alguns resultados em uma perda de atividade de proteína por ligação a sítios responsáveis para a atividade da proteína. Alguns não são específicos nos sítios aos quais eles serão ligados, que podem também resultar em uma perda de atividade desejável e em uma ausência de reprodutibilidade de resultados. A fim de superar os desafios associados com modificações de proteínas com frações poli(etileno glicol), derivados PEG têm sido desenvolvidos que são mais estáveis (por exemplo, Patente dos EUA 6.602.498, que é aqui incorporada por referência) ou que reage seletivamente com frações tiol em moléculas e superfícies (por exemplo, Patente dos EUA 6.610.281, que é aqui incorporado por referência). Existe claramente uma necessidade na técnica para derivados PEG que são quimicamente inertes no ambiente fisiológico até chamado sob a reação seletivamente para formar ligações químicas estáveis.
[0023]Recentemente, uma tecnologia inteiramente nova nas ciências protei-cas tem sido relatada, que promete superar muitas limitações associadas com modi-ficações sítio-específicas de proteínas. Especificamente, novos componentes têm sido adicionados à maquinaria biossintética de proteína do procarioto Escherichia coli (E. coli) (por exemplo, L. Wang. et al (2001). Science 292:498-500) e o eucarioto Saccharomyces cerevisae (S. cerevisae) (por exemplo, H. Chin. et al, Science 301:964-7 (2003)), que tem permitido a incorporação de aminoácidos não genetica-mente codificados à proteínas in vivo. Um número de novos aminoácidos com novas propriedades químicas, físicas ou biológicas, incluindo marcadores com fotoafinida- de e aminoácidos fotoisomerizáveis, aminoácidos com ligação foto-cruzada (ver, por exemplo, Chin, J.W., et al (2002) Proc. Natl. Acad. Sci. EUA 99:11020-11024; e, Chin, J.W. et al (2002) J. Am. Chem. Soc. 124:9026-9027), ceto aminoácidos, ami- noácidos contendo átomo pesado, e aminoácidos glicosilados têm eficientemente incorporados e com alta fidelidade nas proteínas em E. coli e em levedura em res-postas ao códon âmbar, TAG, utilizando esta metodologia. Ver, por exemplo, J.W. Chin et al (2002), Journal of the American Chemical Society 124:9026-9027; J.W. Chin, & P.G. Schultz, (2002), ChemBioChem 3(11):1135-1137; J. W. Chin et al (2002), PNAS United Stated of America 99:11020-11024; e, L. Wang, & P.G. Schultz, (2002), Chem, Comm., 1:1-11. Todas as referências são incorporadas por referência em sua totalidade. Esses estudos têm demonstrado que é possível ser seletivamente e rotineiramente introduzidos grupos funcionais químicos, tal como grupos cetonas, grupos alquino e frações azida, que não são encontrados em proteínas, que são quimicamente inertes a todos os grupos funcionais encontrados nos 20 aminoácidos geneticamente codificados, comuns e que podem ser utilizados para reagir eficientemente e seletivamente para formar ligações covalentemente estáveis.
[0024]A habilidade de incorporar aminoácidos não geneticamente codificados em proteínas permite a introdução de grupos químicos funcionais que podem prover alternativas valiosas para os grupos funcionais de ocorrência natural, tais como o NH2-epsilon de lisona, a sulfidrila-SH de cisteína, o grupo imino de histidina etc. Certos grupos funcionais químicos são conhecidos serem inertes para os grupos funcionais nos 20 aminoácidos geneticamente codificados, comuns mas reagem de forma limpa e eficientemente para formar ligações estáveis. Grupos azida e acetileno, por exemplo, são conhecidos na técnica por suportarem a reação de cicloadição de Huisgen [3+2] em condições aquosas em presença de uma quantidade catalítica de cobre. Ver, por exemplo, Tornoe et al (2002) J. Org. Chem. 67:3057-3064; e, Rostovtsev et al, (2002) Angew. Chem. Int. Ed. 41:2596-2599. Por introdução de uma fração azida em uma estrutura protéica, por exemplo, uma é capaz de incorporar um grupo funcional que é quimicamente inerte a aminas, sulfidrilas, ácidos car- boxílicos, grupo hidroxilas encontrados em proteínas, mas que também reagem fa- cilmente e eficientemente com uma fração acetileno para formar um produto de ci- cloadição. Importantemente, na ausência da fração acetileno, a azida permanece quimicamente inerte e não reativa em presença de outras cadeias laterais de proteína e sobre condições fisiológicas.
[0025]A presente invenção é direcionada, entre outras coisas, para proble-mas associados com a atividade e produção de polipeptídeos FGF-21, e também se direciona a produção de um polipeptídeo FGF-21 com propriedades biológicas ou farmacológicas aumentadas, tal como meia vida terapêutica aumentada.
[0026]Esta invenção provê polipeptídeos FGF-21 compreendendo um ou mais aminoácidos codificados não naturalmente.
[0027]Em algumas modalidades, o polipeptídeo FGF-21 compreende uma ou mais modificações pós-traducionais. Em algumas modalidades, o polipeptídeo FGF-21 está ligado a um ligante, polímero, ou molécula biologicamente ativa. Em algumas modalidades, o polipeptídeo FGF-21 está ligado a um polímero bifuncional, ligante bifuncional, ou pelo menos um polipeptídeo FGF-21 adicional.
[0028]Em algumas modalidades, o aminoácido não codificado naturalmente está ligado a um polímero solúvel em água. Em algumas modalidades, o polímero solúvel em água compreende uma fração poli(etileno glicol). Em algumas modalida-des, o aminoácido não naturalmente codificado está ligado ao polímero solúvel em água com um ligante ou está ligado ao polímero solúvel em água. Em algumas mo-dalidades, o aminoácido não naturalmente codificado está ligado ao polímero solúvel em água com um ligante ou é ligado ao polímero solúvel em água. Em algumas mo-dalidades, a molécula de poli(etileno glicol) é um polímero bifuncional. Em algumas modalidades, o polímero bifuncional está ligado a um segundo polipeptídeo. Em al-gumas modalidades, o segundo polipeptídeo é um polipeptídeo FGF-21.
[0029]Em algumas modalidades, o polipeptídeo FGF-21 compreende pelo menos dois aminoácidos ligados a um polímero solúvel em água compreendendo uma fração poli(etileno glicol). Em algumas modalidades, pelo menos um aminoáci- do é um aminoácido não naturalmente codificado.
[0030]Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em um ou mais das seguintes posições em FGF-21: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais posições a partir da posição 1 (isto é, no N-terminal) através do C-terminal na SEQ ID NOs: 34-36. Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorpora-dos em uma ou mais das seguintes posições em FGF-21: 10, 52, 117, 126, 131, 162, 87, 77, 83, 72, 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou aminoácidos corres-pondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoáci- dos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 10, 52, 77, 117, 126, 131, 162 (SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 87, 77, 83, 72 (SEQ ID NO:1 ou aminoácidos cor-respondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais amino- ácidos não naturalmente codificados são incorporados em uma ou mais das seguin-tes posições em FGF-21: 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturais são incorporados na sequência líder ou sinal da SEQ ID NOs: 3, 4, 6, 7, ou outra sequência FGF-21. Em algumas modalidades, as sequên-cias líder podem ser escolhidas a partir da SEQ ID NOs: 39, 40, 41, 42, 43 ou 44. Em algumas modalidades, secreção de construções de FGF-21 são clonadas em pVK7ara (Nde/Eco) com uma sequência líder escolhida a partir das SEQ ID NOs: 39, 40, 41, 42, 43 ou 44.
[0031]Em algumas modalidades, o aminoácido de ocorrência não natural em um ou mais dessas posições está ligado a um polímero solúvel em água, incluindo, mas não limitado às posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, no carbóxi terminal da proteína) (SEQ ID NO:1 ou os aminoácidos cor-respondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais posições a partir da posição 1 (isto é, no N- terminal) até o C-terminal nas SEQ ID NOs: 34-36 é ligado a um polímero solúvel em água. Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água, incluindo mas não limitado às posições: 10, 52, 117, 126, 131, 162, 87, 77, 83, 72, 69, 79, 91, 96, 108 e 110 (SEQ ID NO: 1 ou os aminoácidos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições estão ligados a um polímero solúvel em água, incluindo, mas não limitado às posições: 10, 52, 77, 117, 126, 131, 162 (SEQ ID NO:1 ou nos aminoáci- dos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, o aminoáci- do de ocorrência não natural em uma ou mais dessas posições está ligado a um po-límero solúvel em água: 87, 77, 83, 72 (SEQ ID NO: 1 ou aminoácidos correspon-dentes das SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero: 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou os correspondentes aminoácidos das SEQ ID NOs: 2-7). Em algumas modalidades, o um ou mais aminoácidos de ocorrência não natural é a sequência líder ou sinal das SEQ ID NOs: 3, 4, 6, 7, 39, 40, 41, 42, 43, 44 ou outra sequência FGF-21 está ligada a um polímero solúvel em água. Em algumas modalidades, um ou mais aminoácidos de ocorrência não natural na sequência líder ou sinal das SEQ ID NOs: 3, 4, 6, 7 ou outra sequência FGF-21 está ligada a um polímero solúvel em água.
[0032]Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que modula afinidade do polipeptídeo FGF-21 para um receptor do polipeptídeo FGF-21 ou parceiro ligador, incluindo, mas não limitado a uma proteína, polipeptídeo, pequena molécula, ou ácido nucléico. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou dele- ção que aumenta a estabilidade do polipeptídeo FGF-21 quando comparado com a estabilidade do correspondente FGF-21 sem a substituição, adição ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que modula a imunogenicidade do polipeptídeo FGF-21 quando compa-rado com a imunogenicidade do correspondente FGF-21 sem a substituição, adição ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que modula a meia vida sérica ou tempo de circula-ção do polipeptídeo FGF-21 quando comparado com a meia vida sérica ou tempo de circulação do correspondente FGF-21 sem a substituição, adição ou deleção.
[0033]Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que aumenta a solubilidade aquosa do polipeptídeo FGF-21 quando comparado a solubilidade aquosa do FGF-21 correspondente sem a substituição, adição, ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 sem a substituição, adição ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que aumenta a solubilida-de do polipeptídeo FGF-21 produzido em uma célula hospedeira quando comparado à solubilidade do FGF-21 correspondente sem a substituição, adição ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que aumenta a expressão do polipeptídeo FGF-21 em uma célula hos-pedeira ou aumenta a síntese in vitro quando comparado à expressão ou síntese do FGF-21 correspondente sem a substituição, adição ou deleção. O polipeptídeo FGF- 21 compreendendo esta substituição retém atividade agonista e retém ou melhora os níveis de expressão em uma célula hospedeira. Em algumas modalidades, o poli- peptídeo FGF-21 compreende uma substituição, adição ou deleção que aumenta a resistência a protease do polipeptídeo FGF-21 quando comparado a resistência a protease do FGF-21 correspondente sem a substituição, adição ou deleção. Patente dos EUA No. 6.716.626 indicou que os sítios potenciais que podem ser substituídos para alterar a clivagem de protease incluem, mas não são limitados a, um sítio mo- nobásico dentro de 2 resíduos de uma prolina. Em algumas modalidades, o polipep- tídeo FGF-21 compreende uma substituição, adição ou deleção que modula a ativi-dade de transdução de sinal do receptor FGF-21 quando comparado com a atividade do receptor sob a interação com o correspondente polipeptídeo FGF-21 sem a substituição, adição ou deleção. Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição ou deleção que modula sua ligação a outra molécula tal como um receptor quando comparado a ligação do polipeptídeo FGF-21 correspondente sem a substituição, adição ou deleção.
[0034]Em algumas modalidades, o polipeptídeo FGF-21 compreende uma substituição, adição, ou deleção que aumenta a compatibilidade do polipeptídeo FGF-21 com conservantes farmacêuticos (por exemplo, m-cresol, fenol, benzil álcool) quando comparado a compatibilidade do FGF-21 correspondente sem a substi- tuição, adição ou deleção. Esta compatibilidade aumentada pode permitir a prepara-ção de uma formulação farmacêutica conservada que mantém as propriedades fisi- co-químicas e atividade biológica da proteína durante o armazenamento. WO 2005/091944, que é aqui incorporado por referência em sua totalidade, discute os seguintes exemplos de muteínas FGF-21 com estabilidade farmacêutica aumentada: a substituição com uma carga e/ou polar mas aminoácido não carregado para um dos seguintes: glicina 42, glutamina 54, arginina 77, alanina 81, leucina 86, fenilala- nina 88, lisina 122, histidina 125, arginina 126, prolina 130, arginina 131, leucina 139, alanina 145, leucina 146, isoleucina 152, alanina 154, glutamina 156, glicina 161, serina 163, glicina 170, ou serina 172 de SEQ ID NO:1 de WO 05/091944. Um polipeptídeo FGF-21 da presente invenção pode incluir uma ou mais dessas substi-tuições, adições ou deleções. Em algumas modalidades, um ou mais aminoácidos não naturais são substituídos em uma ou mais das seguintes posições: glicina 42, glutamina 54, arginina 77, alanina 86, fenilalanina 88, lisina 122, histidina 125, argi- nina 126, prolina 130, arginina 131, leucina 139, alanina 145, prolina/leucina 146, isoleucina 152, alanina 154, glutamina 156, glicina 161, serina 163, glicina 170, seri-na 172 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturais são substituídos em uma ou mais das seguintes posições: glutamato 91, arginina 131, glutamina 108, arginina 77, arginina 72, histidina 87, leucina 86, arginina 126, glutamato 110, tirosi- na 83, prolina 146, arginina 135, arginina 96, arginina 36 (SEQ ID NO: 1 ou aminoá- cidos correspondentes nas SEQ ID NOs: 2-7).
[0035]WO 05/091944 descreve muteínas adicionais do FGF-21 com estabili-dade farmacêutica aumentada. Tais muteínas incluem a substituição de uma cisteína por dois ou mais dos seguintes em FGF-21 (ver SEQ ID NO: 1 de WO 05/091944): arginina 19, tirosina 20, leucina 21, tirosina 22, treonina 23, aspartato 24, aspartato 25, alanina 26, glutamina 27, glutamina 28, alanina 31, leucina 33, isoleucina 35, leucina 37, valina 41, glicina 42, glicina 43, glutamato 50, glutamina 54, leucina 58, valina 62, leucina 66, glicina 67, lisina 69, arginina 72, fenilalanina 73, glutamina 76, arginina 77, aspartato 79, glicina 80, alanina 81, leucina 82, glicina 84, serina 85, prolina 90, alanina 92, serina 94, fenilalanina 95, leucina 100, aspartato 102, tirosina 104, tirosina 107, serina 109, glutamato 110, prolina 115, histidina 117, leucina 118, prolina 119, asparagina 121, lisina 122, serina 123, prolina 124, histidina 125, argini- na 126, aspartato 127, alanina 129, prolina 130, glicina 132, alanina 134, arginina 135, leucina 137, prolina 138, ou leucina 139. Polipeptídeos FGF-21 da presente invenção podem incluir uma ou mais dessas substituições na posição corresponden-te e/ou podem incluir uma ou mais de outras substituições, adições ou deleções. Em algumas modalidades, um ou mais aminoácidos não naturais são substituídos em uma ou mais das seguintes posições: arginina 19, tirosina 20, leucina 21, tirosina 22, treonina 23, aspartato 24, aspartato 25, alanina 26, glutamina 27, glutamina 28, ala- nina 31, leucina 33, isoleucina 35, leucina 37, valina 41, glicina 42, glicina 43, gluta- mato 50, glutamina 54, leucina 58, valina 62, leucina 66, glicina 67, lisina 69, argini- na 72, fenilalanina 73, glutamina 76, arginina 77, aspartato 79, glicina 80, alanina 81, leucina 82, glicina 84, serina 85, prolina 90, alanina 92, serina 94, fenilalanina 95, leucina 100, aspartato 102, tirosina 104, tirosina 107, serina 109, glutamato 110, prolina 115, histidina 117, leucina 118, prolina 119, asparagina 121, lisina 122, serina 123, prolina 124, histidina 125, arginina 126, aspartato 127, alanina 129, prolina 130, glicina 132, alanina 134, arginina 135, leucina 137, prolina 138, ou leucina 139 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[0036]WO 05/091944 ainda descreve muteínas específicas do FGF-21 com ligações dissulfeto construídas (aminoácidos substituídos com cisteína), em adição ao de ocorrência natural em Cys75-Cus93, são como segue: Gln76Cys-Ser109Cys, Cys75-Ser85Cys, Cys75-Ala92Cys, Phe73Cys-Cys93, Ser123Cys-His125Cys, Asp102Cys-Tyr104Cys, Asp127Cys-Gly132Cys, Ser94Cys-Glu110Cys, Pro115Cys- His117Cys, Asn121Cys-Asp127Cys, Leu100Cys-Asp102Cys, Phe95Cys-Tyr107Cys, Arg19CysPro138Cys, Tyr20Cys-Leu139Cys, Tyr22Cys-Leu137Cys, Arg77Cys- Asp79Cys, Pro90Cys-Ala92Cys, Glu50Cys-Lys69Cys, Thr23Cys-Asp25Cys, Ala31Cys-Gly43Cys, Gln28Cys-Gly43Cys, Thr23Cys-Gln28Cys, Val31Cys- Leu82Cys, Leu58Cys-Val62Cys, Gln54Cys-Leu66Cys, Ile35Cys-Gly67Cys, Gly67Cys-Arg72Cys, Ile35Cys-Gly84Cys, Arg72Cys-Gly84Cys ou Arg77Cys- Ala81Cys, onde o número é baseado na SEQ ID NO:1 da WO 05/091944. Muteínas adicionais com ligações dissulfeto construídas são Tyr22Cys-Leu139Cys; Asp24Cys- Arg135Cys; Leu118Cys-Gly132Cys; His117Cys-Pro130Cys; His117CysAla129Cys; Leu82Cys-Pro119Cys; Gly80Cys-Ala129Cys; Gly43Cys-Pro124Cys; Gly42Cys- Arg126Cys; Gly42Cys-Pro124Cys; Gln28Cys-Pro124Cys; Gln27Cys-Ser123Cys; Ala26Cys-Lys122Cys; ou Asp25Cys-Lys122Cys, onde o número é baseado na SEQ ID NO:1 da WO 05/091944. Muteínas adicionais com ligações dissulfeto construídas são Leu118Cys-Ala134Cys; Leu21Cys-Leu33Cys; Ala26Cys-Lys122Cys; Leu21Cys- Leu33Cys/Leu118Cys-Ala134Cys, onde o número é baseado na SEQ ID NO:1 da WO 05/091944. Polipeptídeos FGF-21 da presente invenção podem incluir uma ou mais dessas substituições na(s) posição(s) correspondente(s) no polipeptídeo e/ou podem incluir uma ou mais outras substituições, adições ou deleções. Polipeptídeos FGF-21 da presente invenção podem incluir uma ou mais dessas substituições na(s) posição(s) correspondente(s) no polipeptídeo (SEQ ID NO:1 ou os aminoácidos cor-respondentes nas SEQ ID NOs:2-7). Em algumas modalidades, polipeptídeos FGF- 21 da presente invenção podem incluir uma ou mais dessas substituições nas posi-ções correspondentes a partir de antes da posição 1 (isto é, N-terminal) até o C- terminal nas SEQ ID NOs: 34-36.
[0037]WO 05/091944 descreve muteinas adicionais do FGF-21 que foram PEGiladas. Essas muteínas tiveram uma das seguintes substituições: D25C, D38C, L58C, K59C, P60C, K69C, D79C, H87C, E91C, E101C, D102C, L114C, L116C, K122C, R126C, R126C, P130C, P133C, P140C. Polipeptídeos FGF-21 da presente invenção podem incluir uma ou mais dessas substituições na posição corresponden-te no polipeptídeo e/ou podem incluir uma ou mais outras substituições, adições ou deleções. Em algumas modalidades, um ou mais aminoácidos não naturais são substituídos em uma ou mais das seguintes posições: 25, 38, 58, 59, 60, 69, 79, 87, 91, 101, 102, 114, 116, 122, 126, 130, 133, 140 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, polipeptídeos FGF-21 da presente invenção podem incluir uma ou mais dessas substituições nas posições correspondentes a partir de antes da posição 1 (isto é, no N-terminal) até o C-terminal nas SEQ ID NOs: 34-36.
[0038]WO 05/091944 descreve substituições cisteínas nas seguintes posi-ções: 19, 21, 26, 28, 29, 30, 36, 39, 42, 50, 56, 61, 64, 65, 68, 70, 71, 77, 81, 85, 86, 90, 92, 94, 98, 107, 108, 112, 113, 123 e 124. WO 05/091944 indica substituições cisteína nas seguintes posições: 24, 27, 37, 40, 44, 46, 49, 57, 88, 89, 106, 110, 111, 115, 120 e 139. WO 05/091944 também descreve substituições cisteína nas seguintes posições: 18, 45, 47, 48, 78, 83, 99, 103, 125, 128, 131, 132 e 138. Wo 05/091944 também descreve substituições cisteínas nas seguintes posições: 25, 38, 58, 59, 60, 69, 79, 87, 91, 101, 102, 114, 116, 122, 130, 133, e 140.
[0039]Em algumas modalidades, uma ou mais ligações construídas são cri-ada com um ou mais aminoácidos não naturais. A ligação intramolecular pode ser criada de muitas formas, incluindo mas não limitado a uma reação entre dois amino- ácidos na proteína sobre condições adequadas (um ou ambos aminoácidos podem ser um aminoácido não natural); uma reação com dois aminoácidos, cada um dos quais pode ser naturalmente codificado ou não naturalmente codificado, com um ligante, polímero, ou outra molécula sobre condições adequadas etc.
[0040]Em algumas modalidades, uma ou mais substituições aminoácidos no polipeptídeo FGF-21 podem ser com um ou mais aminoácidos de ocorrência natural ou não natural. Em algumas modalidades as substituições aminoácidos no polipeptí- deo FGF-21 podem ser aminoácidos de ocorrência natural ou não natural, provido que pelo menos uma substituição é com um aminoácido não naturalmente codifica-do. Em algumas modalidades, uma ou mais substituições aminoácidos do polipeptí- deo FGF-21 pode ser com um ou mais aminoácidos de ocorrência natural, e adicio-nalmente pelo menos uma substituição é com um aminoácido não naturalmente co-dificado.
[0041]Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo carbonila, um grupo acetila, um grupo aminoóxi, um grupo hidrazina, um grupo hidrazida, um grupo semi-carbazinda, um grupo azida, um grupo alquino.
[0042]Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo carbonila. Em algumas modalidades, o aminoácido não natu-ralmente codificado tem a estrutura:
[0043]Em que n é 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída; R2 é H, uma alquila, arila, alquila substituída, e arila substituída; e R3 é H, um aminoácido, um polipeptídeo, ou um grupo de modificação de amino-terminal, e R4 é H, um aminoácido, um polipeptídeo, ou um grupo de modificação carboxi- terminal.
[0044]Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo aminoóxi. Em algumas modalidades, o aminoácido não natu-ralmente codificado compreende um grupo hidrazida. Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo hidrazina. Em algu-mas modalidades, os resíduos aminoácidos não naturalmente codificados compre-endem um grupo semi-carbazida.
[0045]Em algumas modalidades, o resíduo aminoácido não naturalmente codificado compreende um grupo azida. Em algumas modalidades, o aminoácido não naturalmente codificado tem a estrutura:
[0046]Em que n é 0-10; R1 é uma alquila, arila, alquila substituída, arila substituída ou não presente; X é O, N, S ou não presente; m é 0-10; R2 é H, um aminoácido, um polipeptídeo, um grupo de modificação amino-terminal, e R3 é H, um aminoácido, um polipeptídeo, ou um grupo de modificação carboxi-terminal.
[0047]Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo alquino. Em algumas modalidades, o aminoácido não natu-ralmente codificado tem a estrutura:
[0048]Em que n é 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída; X é O, N, S ou não presente; m é 0-10l R2 é H, um aminoácido, um poli- peptídeo, ou um grupo de modificação amino-terminal, e R3 é H, um aminoácido, um polipeptídeo, ou um grupo de modificação carboxi-terminal.
[0049]Em algumas modalidades, o polipeptídeo é um agonista polipeptídeo FGF-21, agonista parcial, antagonista, antagonista parcial, ou agonista inverso. Em algumas modalidades, o agonista polipeptídeo FGF-21, agonista parcial, antagonista, antagonista parcial, ou agonista inverso compreende um aminoácido não natu-ralmente codificado ligado a um polímero solúvel em água. Em algumas modalida-des, o polímero solúvel em água compreende uma fração poli(etileno glicol). Em al-gumas modalidades, o agonista polipeptídeo FGF-21, agonista parcial, antagonista, antagonista parcial, ou agonista inverso compreende um aminoácido não natural-mente codificado e uma ou mais modificação pós-traducional, ligante, polímero, ou molécula biologicamente ativa.
[0050]A invenção presente também provê ácidos nucléicos isolados com-preendendo um polinucleotídeo que hibridiza sobre condições severas para a SEQ ID NO: 8-14. A presente invenção também provê ácidos nucléicos isolados compre-endendo um polinucleotídeo que hibridiza sobre condições severas para a SEQ ID NO: 8-14 em que o polinucleotídeo compreende pelo menos um códon seletor. A presente invenção também provê ácidos nucléicos isolados compreendendo um po- linucleotídeo que codifica os polinucleotídeos mostrados como SEQ ID NOs: 1-7. A presente invenção também provê ácidos nucléicos isolados compreendendo um po- linucleotídeo que codifica os polinucleotídeos mostrados como SEQ ID NOs; 1-7 com um ou mais aminoácidos não naturalmente codificados. É facilmente aparente àqueles versados na técnica que um número de diferentes polinucleotídeos pode codificar qualquer polipeptídeo da presente invenção.
[0051]Em algumas modalidades, o códon seletor é selecionado a partir do grupo consistindo em um códon âmbar, códon ocre, códon opala, um códon único, um códon raro, um códon de cinco bases, e um códon de quatro bases.
[0052]A presente invenção também provê métodos de fazer um polipeptídeo FGF-21 ligado a um polímero solúvel em água. Em algumas modalidades, o método compreende por em contato um polipeptídeo FGF-21 compreendendo um aminoáci- do não naturalmente codificado com um polímero solúvel em água compreendendo uma fração que reage com um aminoácido não naturalmente codificado. Em algu-mas modalidades, o aminoácido não naturalmente codificado incorporado no poli- peptídeo FGF-21 é reativo para um polímero solúvel em água que é de outra forma não reativo para qualquer dos 20 aminoácidos comuns.
[0053]Em algumas modalidades, o polipeptídeo FGF-21 ligado ao polímero solúvel em água é feito reagir com um polipeptídeo FGF-21 compreendendo um aminoácido contendo carbonila com uma molécula poli(etileno glicol) compreenden-do um grupo aminoóxi, hidrazina, hidrazida ou semi-carbazida. Em algumas modali-dades, o grupo aminoóxi, hidrazina, hidrazida ou semi-carbazida está ligado a molé-cula poli(etileno glicol) atrações de uma ligação amida.
[0054]Em algumas modalidades, o polipeptídeo FGF-21 ligado ao polímero solúvel em água é feito por reação de uma molécula poli(etileno glicol) compreen-dendo um grupo carbonila com um polipeptídeo compreendendo um aminoácido não naturalmente codificado que compreende um grupo aminoóxi, hidrazina, hidrazida ou semi-carbazida.
[0055]Em algumas modalidades, o polipeptídeo FGF-21 ligado ao polímero solúvel em água é feito por reação de um polipeptídeo FGF-21 compreendendo um aminoácido contendo alquino com uma molécula poli(etileno glicol) compreendendo uma fração azida. Em algumas modalidades, o grupo azida ou alquino está ligado a molécula poli(etileno glicol) através de uma ligação amida.
[0056]Em algumas modalidades, o polipeptídeo FGF-21 ligado ao polímero solúvel em água com uma molécula poli(etileno glicol) compreendendo uma fração alquino. Em algumas modalidades, o grupo azida ou alquino é ligado a molécula po- li(etileno glicol) através de uma ligação amida.
[0057]Em algumas modalidades, a molécula poli(etileno glicol) tem um peso molecular de entre cerca de 0,1 kDa e cerca de 100 kDa. Em algumas modalidades, a molécula poli(etileno glicol) tem um peso molecular entre 0,1 kDa e 50 kDa.
[0058]Em algumas modalidades, a molécula poli(etileno glicol) é um polímero ramificado. Em algumas modalidades, cada ramificação do polímero ramificado poli(etileno glicol) tem um peso molecular de entre cerca de 1 kDa e cerca de 100 kDa, ou entre 1 kDa e 50 kDa.
[0059]Em algumas modalidades, o polímero solúvel em água ligado ao poli- peptídeo FGF-21 compreende uma fração polialquileno glicol. Em algumas modali-dades, o resíduo aminoácido não naturalmente codificado incorporado no polipeptí- deo FGF-21 compreende um grupo carbonila, um grupo aminoóxi, um grupo hidrazi- da, um hidrazina, um semi-carbazida, um grupo azida, um grupo alquino. Em algu-mas modalidades, o resíduo aminoácido não naturalmente codificado incorporado no polipeptídeo FGF-21 compreende uma fração carbonila e o polímero solúvel em água compreende uma fração aminoóxi, hidrazida, hidrazina, ou semi-carbaxida. Em algumas modalidades, o resíduo aminoácido não naturalmente codificado incorpora-do no polipeptídeo FGF-21 compreende uma fração alquino e o polímero solúvel em água compreende uma fração azida. Em algumas modalidades, o resíduo aminoáci- do não naturalmente codificado incorporado no polipeptídeo FGF-21 compreende uma fração azida e o polímero solúvel em água compreende uma fração alquino.
[0060]A presente invenção também provê composições compreendendo um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado e um veículo farmaceuticamente aceitável. Em algumas modalidades, o aminoácido não naturalmente codificado está ligado a um polímero solúvel em água.
[0061]A presente invenção também provê células compreendendo um poli- nucleotídeo codificando o polipeptídeo FGF-21 compreendendo um códon seletor. Em algumas modalidades, as células compreendem uma RNA sintetase ortogonal e/ou tRNA ortogonal para substituir um aminoácido não naturalmente codificado no polipeptídeo FGF-21.
[0062]A presente invenção também provê métodos de fazer um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado. Em algumas modalidades, os métodos compreendem cultivo de células compreendendo um poli- nucleotídeo ou polinucleotídeos codificando um polipeptídeo FGF-21, um RNA sinte- tase ortogonal e/ou tRNA ortogonal sob condições para permitir expressão do poli- peptídeo FGF-21; e purificando o polipeptídeo FGF-21 a partir de células e/ou meio de cultura.
[0063]A presente invenção também provê métodos de aumentar a meia-vida terapêutica, meia-vida sérica ou tempo de circulação dos polipeptídeos FGF-21. A presente invenção provê métodos de modulação da imunogenicidade dos polipeptí- deos FGF-21. Em algumas modalidades, os métodos compreendem substituir um aminoácido não naturalmente codificado por qualquer um ou mais aminoácidos em polipeptídeos FGF-21 de ocorrência natural e/ou ligações dos polipeptídeos FGF-21 a um ligante, um polímero, um polímero solúvel em água, ou uma molécula biologi-camente ativa.
[0064]A presente invenção também provê métodos de tratar um paciente em necessidade de tal tratamento com uma quantidade efetiva de uma molécula FGF- 21 da presente invenção. Em algumas modalidades, os métodos compreendem ad-ministração ao paciente de uma quantidade terapeuticamente efetiva de uma com-posição farmacêutica compreendendo um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado e um veículo farmaceuticamente aceitável. Em algumas modalidades, o aminoácido não naturalmente codificado está ligado a um polímero solúvel em água.
[0065]A presente invenção também provê polipeptídeos FGF-21 compreen-dendo uma sequência mostrada na SEQ ID NO:1-7 ou qualquer sequência polipep- tídica FGF-21, exceto que pelo menos um aminoácido é substituído por um aminoá- cido não naturalmente codificado. A presente invenção também provê polipeptídeos FGF-21 compreendendo uma sequência mostrada como SEQ ID NO:1, 2, 4 e 5. Em algumas modalidades, o aminoácido não naturalmente codificado é ligado a um po-límero solúvel em água. Em algumas modalidades, o polímero solúvel em água compreende uma fração poli(etileno glicol). Em algumas modalidades, o aminoácido não naturalmente codificado compreende um grupo carbonila, um grupo aminoóxi, um grupo hidrazida, um grupo hidrazina, um grupo semi-carbazida, um grupo azida, ou um grupo alquino.
[0066]A presente invenção também provê composições farmacêuticas com-preendendo um veículo farmaceuticamente aceitável e um polipeptídeo FGF-21 compreendendo a sequência mostrada na SEQ ID NO:1-7 ou qualquer outra se-quência polipeptídeo FGF-21, em que pelo menos um aminoácido é substituído por um aminoácido não naturalmente codificado. A presente invenção também provê composições farmacêuticas compreendendo um veículo farmaceuticamente aceitá-vel e um polipeptídeo FGF-21 compreendendo a sequência mostrada na SEQ ID NO: 1-7. Em algumas modalidades, o aminoácido não naturalmente codificado com-preende uma fração sacarídea. Em algumas modalidades, o polímero solúvel em água está ligado ao polipeptídeo através de uma fração sacarídeo. Em algumas mo-dalidades, um ligante, polímero, ou molécula biologicamente ativa está ligado ao po- lipeptídeo FGF-21 através de uma fração sacarídea.
[0067]A presente invenção também provê um polipeptídeo FGF-21 compre-endendo um polímero solúvel em água ligado por uma ligação covalente ao polipep- tídeo FGF-21 em um aminoácido único. Em algumas modalidades, o polímero solú-vel em água compreende uma fração poli(etileno glicol). Em algumas modalidades, o aminoácido covalentemente ligado ao polímero solúvel em água é um aminoácido não naturalmente codificado presente no polipeptídeo.
[0068]A presente invenção provê um polipeptídeo FGF-21 compreendendo pelo menos um ligante, polímero, ou molécula biologicamente ativa, em que o referi-do ligante, polímero, ou molécula biologicamente ativa é ligado ao polipeptídeo atra-vés de um grupo funcional de um aminoácido não naturalmente codificado ribosso- malmente incorporado no polipeptídeo. Em algumas modalidades, o polipeptídeo é monoPEGilado. A presente invenção também provê um polipeptídeo FGF-21 com-preendendo um ligante, polímero, ou molécula biologicamente ativa que é ligada a um ou mais aminoácidos não naturalmente codificados em que o aminoácido não naturalmente codificado é ribossomalmente incorporado no polipeptídeo nos sítios pré-selecionados.
[0069]Incluído dentro do objetivo desta invenção é a sequência líder ou sinal FGF-21 juntos a uma região de codificação FGF-21, bem como uma sequência sinal heteróloga junto a uma região de codificação FGF-21. A sequência líder ou sinal he- teróloga selecionada deve ser um que é reconhecida e processada, por exemplo, pelo sistema de secreção da célula hospedeira para secretar e possivelmente clivada por um sinal de peptidase, pela célula hospedeira. Sequência líder da presente invenção pode ser escolhida a partir das seguintes: as três sequências líderes a par-tir de SEQ ID NO:3 e SEQ ID NO:6 (posições de aminoácidos 1-28), as duas leuci- nas líderes a partir de SEQ ID NO:4 e SEQ ID NO:7 (posições de aminoácidos 1-27), o marcador His a partir da SEQ ID NO:2 (posições de aminoácidos 1-10), SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44. Um método de tratar uma condição ou distúrbio com o FGF-21 da presente invenção é significado para implicar o tratamento com FGF-21 com ou sem um pep- tídeo sinal ou líder.
[0070]A presente invenção também provê métodos de induzir um aumento na captação de glicose em células adipócitos, o referido método compreendendo administração de FGF-21 às referidas células em uma quantidade efetiva para indu-zir um aumento a captação de glicose. O referido aumento na captação de glicose pode causar um aumento no gasto de energia por a utilização de glicose mais rápida ou mais eficiente.
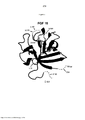
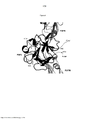
[0071]Em outra modalidade, conjunção do polipeptídeo FGF-21 compreen-dendo um ou mais aminoácidos de ocorrência não natural para outra molécula, incluindo, mas não limitado a PEG, provê FGF-21 substancialmente purificado devido a reação química única utilizada para conjugação do aminoácido não natural. Conjugação de FGF-21 compreendendo um ou mais aminoácidos não naturalmente codificados a outra molécula, tal como PEG, pode ser feita com outras técnicas de purificação antes ou seguindo o passo de conjugação para prover FGF-21 substancialmente puro. BREVE DESCRIÇÃO DOS DESENHOS Figura 1 - Mutações âmbar em FGF-21 e sítios correspondentes em FGF-19 são mostrados. Figura 2 - A estrutura do FGF-19 humano é mostrada. Figura 3 - Mutações âmbar em FGF-21 e sítios correspondentes em FGF-2 são mostrados. Figura 4 - A estrutura do FGF-19 humano é mostrada. 'Figura 5 - Expressão de His N-terminal marcado com FGF-21 e supressão em 7 sítios âmbar são mostrados. Figura 6 - Amostras de sobrenadante BPER a partir da expressão do His N- terminal marcado com FGF-21 e supressão nos 7 sítios âmbar são mostrados. Figura 7a - Valores de EC50 calculados no SigmaPlot para diluições seria-das de variantes de FGF21 PEG-391 30K, PEG-477 30K, PEG-R131 30K, PEG- Q108 30K, HIS-FGF21 (selvagem marcado com His). Figura 7b - uma tabela mostrando a média de vezes de perda de atividade para cada um das variantes FGF21 pegilados listados. Figura 8 - Uma análise SDS-PAGE de FGF-21 não marcado com His ex-presso em E. coli. Figura 9 - (A) Análise de SDS-PAGE de frações de eluição de FGF-21- Y83pAF. (B) Cromatograma de eluição Q HP de FGF-21-Y83pAF não marcado. (C) Análise SDS-PAGE de grupo de eluição FGF-21-Y832pAFQ HP. Figura 10 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 11 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 12 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 13 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 14 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 15 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 16 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 17 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 18 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 19 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 20 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 21 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 22 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 23 - Dados a partir do Exemplo 28, propriedades farmacocinéticas dos compostos FGF-21 em ratos. Figura 24 - mapa do vetor pVK10-FGF21. Figura 25 - sequência do vetor pVK10-FGF21. Figura 26a - Perfis de tempo/concentração sérica de três doses de N-6His WT FGF21 em ratos. Ratos foram dados com uma administração de artigo teste subcutaneamente. N=4 animais por grupo. Símbolos indicam médias de concentra-ções séricas, barras de erros indicam erro padrão. Figura 26b - Perfis de tempo/concentração sérica de três doses de N-6His WT FGF21 dosados ou subcutaneamente ou intravenosamente a 0,25 mg/kg. Ratos foram dados com uma administração única de artigo teste subcutaneamente. N=4 animais por grupo. Símbolos indicam médias de concentrações séricas, barras de erros indicam erro padrão. Biodisponibilidade total é ~87%. Figura 27a - Relação dose para a concentração sérica do artigo teste em Cmax. Valores Cmax são relatados como observação não teórica. N=4 animais por grupo de tratamento. O valor da regressão linear é 0,59 com uma inclinação de 348,5 ± 91,22. Figura 27b - Relação dose para concentração sérica AUC. Valores AUC são relatados como observado, calculados para infinito. N=4 animais por grupo de trata-mento. O valor da regressão linear é 0,75 com uma inclinação de 1079±194,1. Figura 28a - Perfis de tempo/concentração sérica de três doses de PP WT FGF21 em ratos. Ratos foram dados uma administração única de artigo teste subcu- taneamente. N=4 animais por grupo. Símbolos indicam meios de medir concentra-ções séricas, barras de erro indicam erro padrão. Figura 28b - Perfis tempo/concentração sérica de PP WT FGF21 doseado ou subcutaneamente ou intravenosamente a 0,25 mg/kg. Ratos foram dados uma administração única de artigo teste subcutaneamente. N-4 animais por grupo. Sím-bolos indicam médias de medidas de concentrações séricas, barras de erro indicam erro padrão. A biodisponibilidade total é ~65%. Figura 29a - Relação dose para a concentração sérica do artigo teste em Cmax. Valores de Cmax são relatados como observado não teórico. N=4 animais por grupo de tratamento. O valor da regressão linear é 0,92 com uma inclinação de 454,2±42,42. Figura 29b - Relação dose para a meia vida terminal do artigo teste. N=4 animais por grupo de tratamento. O valor de regressão linear pode não ser calculado devido a uma saturação aparente de depuração acima de 0,125 mg/kg. Figura 29c - Relação dose para a concentração sérica AUC. Valores AUC são relatados como observado, calculados para infinito. N=4 animais por grupo de tratamento. O valor de regressão linear é 0,93 com uma inclinação de 1585 ± 137,1. Figura 30a - Comparação da meia vida terminal calculada para compostos PP versus N6-His WT FGF21 doseados a 0,5 mg/kg subcutaneamente em ratos. O valor de p calculado utilizando um test-t de duas caudas é 0,7715. N=3-4 animais por grupo. Figura 30b - Comparação dos valores de Cmaz para compostos PP versus N6-His WT FGF21 doseados a 0,5 mg/kg subcutaneamente em ratos. O valor de p calculado utilizando um test-t de duas caudas é 0,7652. N=3-4 animais por grupo. Figura 30c - Comparação de AUCinf para compostos PP versus N6-His WT FGF21 doseados a 0,5 mg/kg subcutaneamente em ratos. O valor de p calculado utilizando um test-t de duas caudas é 0,4372. Figura 31a - Perfis PK de dez isômeros FGF21 marcados com N6-His PEGi- lados. Figura 31b - Perfis de absorção para isômeros FGF21 PEGilados após 0,25 mg/kg de injeção subcutânea. Figura 31c - Perfis de eliminação para isômeros FGF21 PEGilados após 0,25 mg/kg de injeção subcutânea. Figura 32 - Comparação farmacocinética de 20 e 30 kDa de PEGilação. Figura 33 - Curvas de tempo/concentração plasmática para ratos doseados intravenosamente ou subcutaneamente com 0,25 mg/kg de 20KPEG-pAF91(N6- His)FGF21. Uma dose única foi administrada a cada animal. N=4 animais por grupo. Símbolos indicam meios de medir concentrações plasmáticas, barras indicam desvio padrão. Biodisponibilidade total é ~30%. Figura 34 - Dois géis mostrando a secreção de FGF21 em E. coli e mostrando os líderes utilizados que OmpA, MalE, e StII trabalharam bem, como demonstrado pela liberação periplasmática da fração solúvel no segundo gel.
[0072]É para ser entendido que esta invenção não é limitada a metodologia particular, protocolos, linhagens celulares, construções, e reagentes descritos aqui e tal como podem variar. É também para ser entendido que a terminologia utilizada aqui é para o propósito de descrever modalidades particulares somente, e não é tencionado limitar o objetivo da presente invenção, que será limitado somente pelas reivindicações em apêndice.
[0073]Como aqui utilizado nas reivindicações em apêndice, as formas singu-lares “um”, e “o” incluem referência no plural a menos que o contexto claramente indica de outra forma. Então, por exemplo, referência a um “polipeptídeo FGF-21” ou “FGF-21” é uma referência a uma ou mais de tais proteínas e incluem equivalentes dos mesmos conhecidos pelos versados na técnica, e semelhantes.
[0074]A menos que definido de outra forma, todos os termos técnicos e cien-tíficos aqui utilizados têm o mesmo significado como comumente entendido a um versado na técnica a qual esta invenção pertence. Embora qualquer método, dispo-sitivo, e material similar ou equivalente aos versados na técnica podem ser utilizados na prática ou teste da invenção, os métodos preferidos, dispositivos e materiais são agora descritos.
[0075]Todas as publicações e patentes mencionadas aqui são aqui incorpo-radas por referência para o propósito de descrever e revelar, por exemplo, as cons-truções e metodologias que são descritas nas publicações, que podem ser utilizadas em conexão com a invenção presentemente descrita. As publicações aqui discutidas são providas somente para sua revelação anterior para os dados apresentados o presente pedido. As publicações discutidas aqui são providas somente para sua re-velação antes da data apresentada do presente pedido. Nada aqui é para ser cons- truído como uma admissão que os inventores não são intitulados para antedata tal revelação por virtude da invenção antecedente ou por qualquer outra razão.
[0076]O termo “substancialmente purificado” refere-se a um polipeptídeo FGF-21 que pode ser substancialmente ou essencialmente livre de componentes que normalmente acompanham ou interagem com a proteína como encontrado em seu ambiente de ocorrência natural, isto é, uma célula nativa, ou célula hospedeira no caso de polipeptídeo FGF-21 recombinantemente produzido. Polipeptídeo FGF- 21 que pode ser substancialmente livre de material celular inclui preparações de pro-teína tendo menos que cerca de 30%, menos que 25%, menos que cerca de 20%, menos que cerca de 15%, menos que cerca de 10%, menos que cerca de 5%, menos que cerca de 4%, menos que cerca de 3%, menos que cerca de 2%, ou menos que cerca de 1 % (por peso seco) de contaminação da proteína. Quando o polipep- tídeo FGF-21 ou variante do mesmo é recombinantemente produzido pelas células hospedeiras, a proteína pode estar presente em cerca de 30%, cerca de 25%, cerca de 20%, cerca de 15%, cerca de 10%, cerca de 5%, cerca de 4%, cerca de 3%, cerca de 2%, ou cerca de 1% ou menos do peso seco das células. Quando o polipeptí- deo FGF-21 ou variante do mesmo é recombinantemente produzido pelas células hospedeiras, a proteína pode estar presente no meio de cultura em cerca de 5 g/L, cerca de 4 g/L, cerca de 3 g/L, cerca de 2 g/L, cerca de 1 g/L, cerca de 750 mg/L, cerca de 500 mg/mL, cerca de 250 mg/L, cerca de 100 mg/L, cerca de 50 mg/L, cerca de 10 mg/L, ou cerca de 1 mg/L ou menos de peso seco das células. Então, poli- peptídeo FGF-21 “substancialmente purificado” como produzido pelos métodos da presente invenção podem ter um nível de pureza de pelo menos cerca de 30%, pelo menos cerca de 35%, pelo menos cerca de 40%, pelo menos cerca de 45%, pelo menos cerca de 50%, pelo menos cerca de 55%, pelo menos cerca de 60%, pelo menos cerca de 65%, pelo menos cerca de 70%, especificamente, um nível de pureza de pelo menos cerca de 75%, 80%, 85% e mais especificamente, um nível de pureza de pelo menos cerca de 90%, um nível de pureza de pelo menos cerca de 95%, um nível de pureza de pelo menos cerca de 99%, ou maior como determinado pelos métodos apropriados tal como análise SDS/PAGE, RP-HPLC, SEC, e eletrofo-rese de capilaridade.
[0077]Uma “célula hospedeira recombinante” ou “células hospedeira” refere- se a uma célula que inclui um polinucleotídeo exógeno, sem levar em consideração o método utilizado para inserção, por exemplo, captação direta, transdução, f- emparelhamento, ou outros métodos conhecidos na técnica para criar células hos-pedeiras recombinantes. O polinucleotídeo exógeno pode ser mantido como um vetor não integrado, por exemplo, um plasmídeo, ou alternativamente, pode ser integrado no genoma hospedeiro.
[0078]Como aqui utilizado, o termo “meio” ou “meios” incluem qualquer meio de cultura, solução, sólido, semi-sólido, ou suporte rígido que pode suportar ou con-ter qualquer célula hospedeira, incluindo células hospedeiras, células hospedeiras de levedura, células hospedeiras de inseto, células hospedeiras de planta, células hospedeiras eucarióticas, células hospedeiras de mamíferos, células CHO, células hospedeiras procarióticas, E. coli, ou células hospedeiras Pseudomonas, e conteú-dos celulares. Então, o termo pode compreender meio em que a célula hospedeira tenha sido crescida, por exemplo, meio em que o polipeptídeo FGF-21 tenha sido secretado, incluindo meio ou antes ou depois do passo de proliferação. O termo também compreende tampões ou reagentes que contêm lisados de célula hospedei-ra, tal como no caso de onde o polipeptídeo FGF-21 é produzido intracelularmente e as células hospedeiras ou rompidas para liberar o polipeptídeo FGF-21.
[0079]“Agente redutor”, como aqui utilizado com respeito para re- envelopamento de proteína, é definido como qualquer composto ou material que mantém grupos sulfidrila no estado reduzido e reduz ligações dissulfeto intra- ou in- termoleculares. Agentes redutores adequados incluem, mas não são limitados a, ditiotreitol (DTT), 2-mercaptoetanol, ditioeritritol, cisteína, cisteamina (2- aminoetanotiol), e glutationa reduzida. É facilmente aparente aos versados na técni-ca que uma ampla variedade de agentes redutores são adequados para uso nos métodos e composições da presente invenção.
[0080]“Agente oxidante”, como aqui utilizado respeita o re-envelopamento da proteína, é definido como qualquer composto ou material que é capaz de remover um elétron a partir de um composto sendo oxidado. Agentes oxidantes adequados incluem, mas não são limitados a, glutationa oxidada, cistina, cistamina, ditiotreitol oxidado, eritreitol oxidado, e oxigênio. É facilmente aparente aos versados na técnica que uma grande variedade de agentes oxidantes são adequados para uso nos métodos da presente invenção.
[0081]O termo “agentes anti-diabético” deve significar qualquer droga que é útil no tratamento, prevenção, ou de outra forma redução da severidade de qualquer distúrbio do metabolismo da glicose, ou qualquer complicação do mesmo, incluindo qualquer das condições, doença, ou complicações descritas aqui. Agentes anti- diabéticos incluem insulina, tiazolidinodionas, sulfoniluréias, derivados ácido benzói- cos, inibidores alfa-glicosidase, ou semelhantes. Outras categorias gerais de agentes anti-diabéticos que podem ser parte de uma composição sujeita inclui (como termos definidos sendo nas marcas de cotação): “drogas artigos” reconhecidas na Farmacopéia dos Estados Unidos oficial ou Formulário Nacional oficial (ou qualquer suplemento do mesmo); “droga nova” e “droga animal nova” aprovada pelo FDA dos EUA são aqueles termos utilizados no Título 21 do Código dos Estados Unidos; qualquer droga que requer aprovação de uma entidade governamental, nos EUA ou fora dos EUA (“droga aprovada”); qualquer droga que seja necessária para obter aprovação regulatória de forma a cumprir com 21 U.S.C § 355 (a) (droga regulatória aprovada”); qualquer agente que é ou foi sujeito a uma aplicação de droga humana sob 21 U.S.C. § 379 (g) (“droga humana”). (Todas as referências para código estatu-tário para esta definição refere-se a tal código como o da data de apresentação ori-ginal deste pedido). Outros agentes anti-diabéticos são aqui revelados, e são conhe-cidos pelos versados na técnica. É preferido que as composições anti-diabéticas in-ventivas, como aqui utilizado, são capazes de reduzir níveis de HbA1c por pelo me-nos uma mudança de 10% a partir da linha base, e é mais particularmente preferido que as composições anti-diabéticas inventivas, como aqui utilizado, são capazes de reduzir níveis de HbA1c por pelo menos uma mudança de 50% a partir da linha base. Agentes anti-diabéticos incluem potenciadores de insulina, tais como incluindo, mas não limitados a, pequenas moléculas potenciadoras, Taurina, Ácido Alfa- Lipóico, um extrato de Mulberry, Crômio, Glutamina, Enicostemma littorale Blume, Scoparia dulcis, um extrato de Tarragon, Andrographis paniculata, Isomalt, Trealose ou D-Manose que pode ainda potenciar a secreção ou atividade de insulina.
[0082]“Agente desnaturante” ou “desnaturante”, como aqui utilizado, é defi-nido como qualquer composto ou material que pode causar um desenvelopamento reversível de uma proteína. A força de um agente desnaturante ou desnaturante de-terminará ambos pelas propriedades e a concentração do agente desnaturante ou desnaturante particular. Agentes desnaturante ou desnaturantes adequados podem ser caotrópicos, detergentes, solventes orgânicos, solventes miscíveis em água, fos- folipídeos, ou uma combinação de dois ou mais de tais agentes. Caotrópicos ade-quados incluem, mas não são limitados a, uréia, guanidina, e tiocianato de sódio. Detergentes úteis podem incluir, mas não são limitados a, detergentes fortes tais como sulfato de dodecila de sódio, ou éteres polioxietileno (por exemplo, detergentes Tween ou Triton), Sarkosil, detergentes não iônicos leves (por exemplo, digitoni- na), detergentes catiônicos leves tal como N-2,3-(Dioleióxi)-propil-N,N,N- trimetulamônio, detergentes iônicos leves (por exemplo, colato de sódio ou deoxico- lato de sódio) ou detergentes anfóteros incluindo, mas não limitados a, sulfobetaínas (Anfótero), sulfato de 3-(3-clolamidopropil)dimetilamônio-1-propano (CHAPS), e sulfonato de 3-(3-clolamidopropil)dimetilamônio-2-hidróxi-1-propano (CHAPSO). Solventes orgânicos, miscíveis em água tais como acetonitrila, alcanoóis inferiores (es-pecialmente alcanol C2-C4 tais como etanol ou isopropanol), ou alcandióis inferiores (especialmente alcandióis C2-C4 tal como etileno-glicol) podem ser utilizados como desnaturastes. Fosfolipídeos úteis na presente invenção podem ser fosfolipídeos de ocorrência natural tais como fosfatidiletanolamina, fosfatidilcolina, fosfatidilserina, e fosfatidilinositol ou derivados fosfolipídeos sintéticos ou variantes de tais diexanoil- fosfatidilcolina ou dieptanoilfosfatidilcolina.
[0083]“Re-envelopamento”, como aqui utilizado descreve qualquer processo, reação ou método que transforma ligação dissulfeto contendo polipeptídeos a partir de um estado envelopado impropriamente ou não envelopado para uma conforma-ção nativa ou envelopada apropriadamente com respeito às ligações dissulfetos.
[0084]“Co-envelopamento”, como aqui utilizado, refere-se especificamente ao processo de re-envelopamento, reações ou método que empregam pelo menos dois polipeptídeos que interagem com cada outro e resultam na transformação dos polipeptídeos não envelopados ou impropriamente envelopados para polipeptídeos nativos, ou propriamente envelopados.
[0085]Como aqui utilizado, “polipeptídeo FGF-21”, “fator de crescimento de fibroblasto 21” ou “FGF-21” e formas não hifenizadas dos mesmos devem incluir aqueles polipeptídeos e proteínas que têm pelo menos uma atividade biológica de um fato de crescimento de fibroblasto 21, bem como análogos FGF-21, isoformas FGF-21,FGF-21 miméticos, fragmentos FGF-21, proteínas FGF-21 híbridas, proteínas de fusão, oligômeros e multímeros, homólogos, variantes de padrão de glicosila- ção, variantes, variantes de splice (de corte), e muteínas dos mesmos, sem levar em consideração que a atividade biológica dos mesmos, a ainda sem levar em conside-ração o método de síntese ou fabricação do mesmo incluindo, mas não limitado a, recombinantes (se produzido a partir de cDNA, DNA genômico, síntese de DNA ou outra forma de ácido nucléico), in vitro, in vivo, por microinjeção de moléculas de ácido nucléico, transgênico, e métodos ativados por gene. O termo “polipeptídeo FGF-21” e “FGF-21” compreende polipeptídeos FGF-21 compreendendo uma ou mais substituições, adições ou deleções aminoácidos.
[0086]Substituições em uma ampla variedade de posições aminoácidos em FGF-21 de ocorrência natural têm sido descritas. Substituições incluindo, mas não limitadas àquelas que modulam a estabilidade farmacêutica, atividade agonista au-mentada, resistência de protease aumentada, conversão do polipeptídeo em um an-tagonista, etc, e são compreendidos pelo termo “polipeptídeo FGF-21” ou “FGF-21”.
[0087]Para sequências de FGF-21 que faltam uma sequência líder, ver SEQ ID NO:1, SEQ ID NO:2 e SEQ ID NO:5 aqui. Para sequências de FGF-21 com uma sequência líder, ver SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:6 e SEQ ID NO:7, aqui. Em algumas modalidades, polipeptídeos FGF-21 da invenção são substancialmente idênticos as SEQ ID NOs: 1-7 ou qualquer outra sequência de um polipeptí- deo FGF-21. Polimorfismos múltiplos de FGF-21 têm sido identificados. Leucina ou prolina têm sido descritos na mesma posição na Publicação de Patente dos EUA No. 20010012628 e Patente dos EUA No. 6.716.626. Sequências líder ou sinal N- terminal que diferem por 1 aminoácido (leucina) são mostradas na Patente dos EUA No. 6.716.626 e Publicação de Patente dos EUA No. 200402559780. Moléculas de ácido nucléico FGF-21 e polipeptídeos FGF-21 incluindo mutantes e métodos para expressar e purificar polipeptídeos FGF-21 são bem conhecidos e incluem, mas não são limitados àquelas reveladas na Patente dos EUA No. 6.716.626; Publicação da Patente dos EUA Nos. 2005/0176631, 2005/0037457, 2004/0185494, 2004/0259780, 2002/0164713. E 2001/0012628; WO 01/36640’WO 03/011213; WO 03/059270; WO 04/110472; WO 05/061712; WO 05/072769; WO 05/091944; WO 05/113606; WO 06/028595; WO 06/028714; WO 06/051247; WO 06/065582; WO 06/078463, que são incorporados por referência em sua totalidade aqui.
[0088]O termo “polipeptídeo FGF-21” também inclui os sais farmaceutica- mente aceitáveis e pró-drogas, e pró-drogas dos sais, polimorfos, hidratos, solvatos, fragmentos biologicamente ativos, variantes biologicamente ativos e estereoisôme- ros do FGF-21 de ocorrência natural bem como variantes agonista, miméticos e an-tagonistas do FGF-21 de ocorrência natural e fusões de polipeptídeos dos mesmos. Fusões compreendendo aminoácidos adicionais no amino terminal, carboxi-terminal, ou ambos, são compreendidos pelo termo “polipeptídeos FGF-21”. Fusões exempla-res incluem, mas não são limitados a, por exemplo, metionila FGF-21 em que uma metionina está ligada ao N-terminal do FGF-21 resultante a partir da expressão re- combinante da forma madura do FGF-21 faltando o peptídeo líder ou sinal ou porção do mesmo (uma metionina é ligada ao N-terminal do FGF-21 resultante a partir da expressão recombinante), fusões para o propósito de purificação (incluindo, mas não limitados a, poli-histidina ou epítopos de afinidade), fusões com albumina sérica li-gando peptídeos e fusões com proteínas séricas tal como albumina sérica. Patente dos EUA No. 5.750.373 que é aqui incorporado por referência, descreve um método para selecionar proteínas novas tal como hormônio de crescimento e variantes de fragmento de anticorpo tendo propriedades de ligação alteradas para suas respecti-vas moléculas receptoras. O método compreende fusão de um gene codificando uma proteína de interesse para o domínio carboxi-terminal do gene III da proteína de revestimento do fago filamentoso M13. Moléculas quiméricas compreendendo FGF- 21 e uma ou mais outra moléculas, incluindo, mas não limitados a, fator de cresci-mento de queratinócito (FCQ) pode ser gerado (Reich-Slotky, R. et al, J. Biol. Chem. 270:29813-29818 (1995)). A molécula quimérica pode conter regiões específicas ou fragmentos de uma ou ambas as moléculas FGF-21 e FCQ. Qualquer de tais frag-mentos pode ser preparado a partir de proteínas por métodos bioquímicos padrões, ou expressão de um polinucleotídeo codificando o fragmento. FGF-21, ou um frag-mento do mesmo, pode ser produzido como uma proteína de fusão compreendendo albumina sérica humana (ASH) ou uma porção da mesma. Tal construção de fusão é adequada para aumentar a expressão do FGF-21, ou fragmento do mesmo, em uma célula eucariótica. Porções ASH exemplares incluem o polipeptídeo N-terminal (aminoácidos 1-369, 1-419, e comprimentos intermediários começando com aminoá- cido 1), como revelado na Pat. EUA No. 5.766.883, e Publicação PCT WO 97/24445, que é incorporado por referência aqui. Outros polipeptídeos quiméricos podem incluir uma proteína ASH com FGF-21, ou fragmentos dos mesmos, ligados a cada uma das terminações C-terminal e N-terminal da ASH. Tal ASH constrói são reveladas na Patente dos EUA No. 5.876.969, que é incorporado aqui por referência. Expressão em célula mamífera do FGF-21 é descrita em WO 2005/091944 que é aqui incorpo-rado por referência.
[0089]Várias referências revelam modificação de polipeptídeos por conjuga-ção de polímero ou glicosilação. O termo “polipeptídeo FGF-21” inclui polipeptídeos conjugados a um polímero tal com PEG e pode ser compreendido de uma ou mais derivatizações adicionais de cisteína, lisina, ou outros resíduos. Em adição, o poli- peptídeo FGF-21 pode compreender um ligante ou polímero, em que o aminoácido ao qual o ligante ou polímero é conjugado pode ser um aminoácido não natural de acordo com a presente invenção, ou pode ser conjugada a um aminoácido natural-mente codificado utilizando técnicas conhecidas na técnica tal como acoplamento a lisina ou cisteína.
[0090]Conjugação de polímero de FGF-21 e outros polímeros têm sido re-portados. Ver, por exemplo, WO 2005/091944 que é aqui incorporada por referência. Pat. dos EUA No. 4.904.584 revela polipeptídeos com lisina PEGilada depletada, em que pelo menos resíduo lisina tem sido deletado ou substituído com qualquer outro resíduo aminoácido. WO 99/67291 revela um processo para conjugar uma proteína com PEG, em que pelo menos um resíduo aminoácido na proteína é deletado e a proteína está em contato com PEG sob condições suficientes para alcançar a conju-gação à superfamília de hormônio de crescimento, em que um resíduo cisteína tem sido substituído com um resíduo aminoácido não essencial localizado em uma regi-ão especificada do polipeptídeo. WO 00/26354 revela um método de produção de um variante polipeptídeo glicosilado com alergenicidade reduzida, que é comparada a um polipeptídeo parente correspondente compreendendo pelo menos um sítio de glicosilação adicional. Pat. dos EUA No. 5.218.092, que é aqui incorporado por refe-rência, revela modificação de fator estimulante de colônia de granulócito (G-CSF) e outros polipeptídeos de força a introduzir pelo menos uma cadeia de carboidrato adicional como comparado ao polipeptídeo nativo.
[0091]O termo “polipeptídeo FGF-21” também inclui FGF-21 glicosilado, tal como, mas não limitado a polipeptídeos glicosilados em qualquer posição aminoáci- do, formas glicosiladas N-ligadas ou O-ligadas do polipeptídeos. Variantes contendo mudanças únicas de nucleotídeos são também consideradas como variantes biolo-gicamente ativas do polipeptídeo FGF-21. Em adição, variantes splice (de corte) são também incluídos. O termo “polipeptídeo FGF-21” também inclui polipeptídeo FGF- 21, heterodímeros, homodímeros, heteromultímeros, ou homomultímeros de qual- quer um ou mais dos polipeptídeos FGF-21 ou qualquer outro polipeptídeo, proteína, carboidrato, polímero, pequena molécula, ligante, ligante, ou outra molécula biologi-camente ativa de qualquer tipo, ligados por meios químicos ou expressos como uma proteína de fusão, bem como análogos polipeptídeos contendo, por exemplo, dele- ções específicas ou outras modificações ainda mantendo a atividade biológica.
[0092]Todas as referências das posições aminoácidos em FGF-21 descritas aqui são baseadas na posição an SEQ ID NO:1, a menos que de outra forma especi-ficada (isto é, quando é colocado que a comparação é baseada na SEQ ID NO:2, 3, 4, 5, 6, 7 ou outra sequência FGF-21). Por exemplo, o aminoácido na posição 77 da SEQ ID NO:1, é uma arginina e a arginina correspondente é localizada na SEQ ID NO:2 na posição 87. Aqueles versados na técnica apreciarão que posições aminoá- cidos correspondendo às posições na SEQ ID NO:1 podem ser facilmente identifica-das em qualquer outra molécula FGF-21 tal como SEQ ID NO:2, 3, 4, 5, 6, e 7. Àqueles versados na técnica apreciarão que posições aminoácidos correspondendo a posições na SEQ ID NO: 1, 2, 3, 4, 5, 6, 7 ou qualquer outra sequência FGF-21 pode ser facilmente identificado em qualquer outra molécula FGF-21 tal como fusões FGF-21, variantes, fragmentos etc. Por exemplo, programas de alinhamento de se-quência tal como BLAST pode ser utilizado para alinhar e identificar uma posição particular em uma proteína que corresponde com uma posição na SEQ ID NO: 1, 2, 3, 4, 5, 6, 7 ou outra sequência FGF-21. Substituições, deleções ou adições de ami- noácidos descritos aqui em referência a SEQ ID NO: 1, 2, 3, 4, 5, 6, 7 ou outra se-quência FGF-21 são tencionadas também se referem a substituições, deleções ou adições nas posições correspondentes nas fusões FGF-21, variantes, fragmentos etc, aqui descritos ou conhecidos na técnica e são expressamente compreendidos pela presente invenção.
[0093]O termo “polipeptídeo FGF-21” ou “FGF-21” compreende polipeptí- deos FGF-21 compreendendo uma ou mais substituições, adições ou deleções ami- noácidos. Polipeptídeos FGF-21 da presente invenção podem ser compreendidos de modificações com um ou mais aminoácidos naturais em conjunção com uma ou mais modificações de aminoácidos não naturais. Substituições exemplares em uma ampla variedade de posições aminoácidos em polipeptídeos FGF-21 de ocorrência natural têm sido descritas, incluindo uma ou mais das atividades biológicas do poli- peptídeo FGF-21, tal como, mas não limitado ao aumento da atividade agonista, aumento da solubilidade do polipeptídeo, diminuição da susceptibilidade da pro-tease, conversão do polipeptídeo em um antagonista, etc, e são compreendidos pelo termo “polipeptídeo FGF-21”. Em algumas modalidades, o antagonista FGF-21 com-preende um aminoácido não naturalmente codificado ligado a um polímero solúvel em água que está presente em uma região ligadora do receptor da molécula FGF- 21.
[0094]Em algumas modalidades, os polipeptídeos FGF-21 ainda compreen-dem uma adição, substituição ou deleção que modula a atividade biológica do poli- peptídeo FGF-21. Por exemplo, as adições, substituições ou deleções podem modu-lar uma ou mais propriedades ou atividades do FGF-21. Por exemplo, as adições, substituições ou deleções podem modular a afinidade para o receptor do polipeptí- deo FGF-21, modular a meia vida circulante, modular a meia vida terapêutica, modu-lar a estabilidade do polipeptídeo, modular a clivagem por proteases, modular a dose, modular a liberação ou bio-disponibilidade, facilitar a purificação, ou melhorar ou alterar uma via particular de administração. Similarmente, polipeptídeos FGF-21 po-dem compreender sequências de clivagem de protease, grupos reativos, domínios de ligação de anticorpo (incluindo, mas não limitado a, FLAG ou poli-His), grupos reativos, domínios de ligação de anticorpo (incluindo, mas não limitado a FLAG ou poli-His) ou outras sequências baseadas em afinidade (incluindo, mas não limitado a, FLAG, poli-His, GST etc) ou moléculas ligadas (incluindo, mas não limitadas a biotina) que melhoram a detecção (incluindo, mas não limitado a GFP), purificação ou outros traços do polipeptídeo.
[0095]O termo “polipeptídeo FGF-21” também compreende homodímeros, heterodímeros, homomultímeros, e heteromultímeros que são ligados, incluindo, mas não limitados àqueles ligados diretamente através de cadeias laterais aminoá- cidos não naturalmente codificados, ou as mesmas ou diferentes cadeias laterais de aminoácidos não naturalmente codificados, para cadeias laterais de aminoácidos naturalmente codificados, ou indiretamente através de um ligante. Ligantes exempla-res incluindo, mas não limitados a, pequenos compostos orgânicos, polímeros solú-veis em água de uma variedade de comprimentos tais como poli(etileno glicol) ou polidextran, ou polipeptídeos de vários comprimentos.
[0096]Um “aminoácido não naturalmente codificado” refere-se a um aminoá- cido que não é um dos 20 aminoácidos comuns ou pirrolisina ou selenocisteína. Ou-tros termos que podem ser utilizados sinonimamente com o termo “aminoácido não naturalmente codificado” são “aminoácidos não naturais”, “aminoácido não natural”, “aminoácido de ocorrência não natural”, e variações de versões hifenadas e não hi- fenadas dos mesmos. O termo “aminoácido não naturalmente codificado” também inclui, mas não é limitado a aminoácidos que ocorrem por modificação (por exemplo, modificações pós-traducionais) de um aminoácido naturalmente codificado (incluin-do, mas não limitado aos 20 aminoácidos comuns ou pirrolisina e selenocisteína), mas não são por eles mesmos naturalmente incorporados em uma cadeia de poli- peptídeo crescente pelo complexo de tradução. Exemplos de tais aminoácidos ocor-rência não natural incluem, mas não são limitados a, N-acetilglicosaminil-L-serina, N- acetilglicosaminil-L-treonina, e O-fosfotirosina.
[0097]Um “grupo de modificação amino terminal” refere-se a qualquer molé-cula que pode ser ligada ao amino-terminal de um polipeptídeo. Similarmente, um “grupo de modificação carboxi-terminal” refere-se a qualquer molécula que pode ser ligada ao carboxi-terminal de um polipeptídeo. Grupos de modificação terminal inclu-em, mas não são limitados a vários polímeros solúveis em água, peptídeos ou prote-ínas tais como albumina sérica, ou outras frações que aumentam a meia vida sérica dos peptídeos.
[0098]Os termos “grupo funcional”, “fração ativa”, “grupo de ativação”, “grupo de saída”, “sítio reativo”, “grupo quimicamente reativo” e “fração quimicamente reati-va” são utilizados na técnica e aqui para referir a porções distintas, definidas ou uni dades de uma molécula. Os termos são de alguma forma sinônima nas técnicas químicas e são aqui utilizadas para indicar as porções das moléculas que desempe-nham alguma função ou atividade e são reativos com outras moléculas.
[0099]O termo “ligação” ou “ligante” é aqui utilizado para referir a grupos ou ligações que normalmente são formadas como o resultado de uma reação química e tipicamente são ligações covalentes. Ligações hidroliticamente estáveis significam que as ligações são substancialmente estáveis em água e não reagem em valores úteis de pH, incluindo, mas não limitados a, sob condições fisiológicas por um perío-do de tempo estendido, talvez mesmo indefinidamente. Ligações hidroliticamente instáveis ou degradáveis significam que as ligações são degradáveis em água ou em soluções aquosas, incluindo, por exemplo, sangue. Ligações enzimaticamente instáveis ou degradáveis significam que a ligação pode ser degradada por uma ou mais enzimas. Como entendido na técnica, PEG e polímeros relacionados podem incluir ligações degradáveis na estrutura do polímero ou no grupo ligante entre a es-trutura do polímero e um ou mais grupos terminais funcionais da molécula do polí-mero. Por exemplo, ligações éster formadas pela reação de ácidos carboxílicos PEG ou ácidos carboxílicos PEG com grupos álcool em um agente biologicamente ativo geralmente hidrolizado sob condições fisiológicas para liberação do agente. Outras ligações hidroliticamente degradáveis incluem, mas não são limitadas a ligações carbonato; ligações imina resultadas a partir da reação de uma amina e um aldeído; ligações éster fosfato formadas por reação de álcool com um grupo fosfato; ligações hidrazona que são produto de reação de uma hidrazida e um aldeído; ligações acetal que são o produto de reação de um aldeído e um álcool; ligações ortoéster que são o produto de reação de um formato e um álcool; ligações peptídicas formadas por um grupo amina, incluindo, mas não limitadas a uma terminação de um polímero tal como PEG, e um grupo carboxila de um peptídeo; e ligações oligonucleotídicas formadas por um grupo fosforamidita, incluindo, mas não limitados a uma terminação de um polímero, e um grupo 5’-hidroxila de um oligonucleotídeo.
[00100]O termo “molécula biologicamente ativa”, “fração biologicamente ati- va” ou “agente biologicamente ativo” quando aqui utilizado significa qualquer substância que pode afetar qualquer propriedade física ou bioquímica de um sistema biológico, via, molécula, ou interação relacionada a um organismo, incluindo, mas não limitada a, vírus, bactéria, bacteriófago, transposon, príon, insetos, fungos, plantas, animais, e humanos. Em particular, como aqui utilizado, moléculas biologicamente ativas incluem, mas não são limitados a, qualquer substância tencionada para diagnóstico, cura, alívio, tratamento, ou prevenção de doença em humanos ou outros animais, ou de outra forma aumento do bem estar físico ou mental de humanos ou animais. Exemplos biologicamente ativos de moléculas ativas incluem, mas não são limitados a peptídeos, proteínas, enzimas, pequenas moléculas de drogas, vacinas, imunógenos, drogas duras, drogas leves, carboidratos, átomos inorgânicos, corantes, lipídeos, nucleosídeos, radioisótopos, oligonucleotídeos, toxóides, toxinas, células procarióticas e eucarióticas, vírus, polissacarídeos, ácidos nucléicos e porções dos mesmos obtidos ou derivados de vírus, bactérias, insetos, animais ou qualquer outra célula ou tipo celular, lipossoma, micropartículas e micelas. Classes de agen-tes biologicamente ativos que são adequados para uso com a invenção incluem, mas não são limitadas a drogas, pró-drogas, radioisótopos, agentes de imagem, polímeros, antibióticos, fungicidas, agentes anti-virais, agentes antiinflamatórios, agentes anti-tumor, agentes cardiovasculares, agentes anti-ansiedade, hormônios, fatores de crescimento, agentes esteroidais, toxinas microbialmente derivadas, e semelhantes.
[00101]Um “polímero bifuncional” refere-se a um polímero compreendendo dois grupos funcionais discretos que são capazes de reagir especificamente com outras frações (incluindo, mas não limitados a grupos laterais aminoácidos) para formar ligações covalentes ou não covalentes. Um ligante bifuncional tendo um gru-po funcional reativo com um grupo de um componente particular biologicamente ati-vo, e outro grupo reativo com um grupo em um segundo componente biológico, pode ser utilizado para formar um conjugado que inclui o primeiro componente biologica-mente ativo, o ligante bifuncional e o segundo componente biologicamente ativo. Muitos procedimentos e moléculas ligantes para ligação de vários compostos para peptídeos são conhecidos. Ver, por exemplo, Publicação de Patente Européia No. 188.256; Patente dos EUA Nos. 4.671.958, 4.659.839, 4.414.148, 4.699.784; 4.680.338 e 4.569.789 que são aqui incorporadas por referência. Um “polímero mul- ti-funcional” refere-se a um polímero compreendendo dois ou mais grupos funcionais discretos que são capazes de reagir especificamente com outras frações (incluindo, mas não limitada a grupos laterais de aminoácidos) para formar ligações covalentes ou não covalentes. Um polímero bi-funcional ou polímero multi-funcional pode ter qualquer comprimento desejado ou peso molecular, e pode ser selecionado para prover um espaço ou conformação particular desejada entre uma ou mais moléculas ligadas ao FGF-21 e seu receptor ou FGF-21.
[00102]Onde grupos substituintes são especificados pelas fórmulas químicas convencionais, escritas a partir da esquerda para direita, eles igualmente compreendem os substituintes quimicamente idênticos que podem resultar a partir de escrever a estrutura da direita para a esquerda, por exemplo, a estrutura -CH2O- é equivalente a estrutura -OCH2-.
[00103]Os termos “substituintes” inclue, mas não é limitado a “substituintes não interferentes”. “Substituintes não interferentes” são aqueles grupos que produ-zem compostos estáveis. Substituintes não interferentes adequados ou radicais in-cluem, mas não são limitados a halo, alquilaC1-C10, alquenilaC2-C10, alquinilaC2-C10, alcóxiC1-C10, aralquilaC1-C12, alcarilaC1-C12, cicloalquilaC3-C12, cicloaquenilaC3-C12, fenila, fenila substituída, toluoila, xilenila, bifenila, alcoxialquilaC2-C12, alcoxiarilaC2- C12, ariloxialquilaC7-C12, oxiarilaC7-C12, alquilsulfinilaC1-C6, alquilsulfonilaC1-C10, -- (CH2)m -O—(alquilaCi-Cio) em que m é de 1 a 8, arila, arila substituída, alcóxi substituído, fluoralquila, radical heterocíclico, radical heterocíclico substituído, nitroalquila, --NO2, --CN, --NRC(O)—(alquilaC1-C10), --C(O)—(alquilaC1-C10), alquilaC2-C10 tioal- quila, --C(O)O-(alquilaC1-C10), --OH, --SO2, =S, --COOH, --NR2, carbonila, --C(O)— (alquilaC1-C10)-CF3, --C(O)-CF3, --C(O)NR2, --(arilaC1-C10)-S—(arilaC6-C10), --C(O)— (arilaC1-C10), --(CH2)m -O—(--(CH2)m—O—(alquilaC1-C10) em que cada m é de 1 a 8, --C(O)NR2, --C(S)NR2, --C(S)NR2, --SO2NR2, --NRC(O)NR2, --NRC(S)NR2, sais dos mesmos, e semelhantes. Cada R como aqui utilizado é H, alquila ou alquila substitu-ída, arila, o arila substituída, aralquila ou alcarila. O termo “halogênio” inclui flúor, cloro, iodo e bromo.
[00104]O termo “alquila”, por ele mesmo ou como parte de outro substituinte, significa, a menos que de outra forma atestado, uma cadeia simples ou ramificada, ou radical hidrocarboneto cíclico, ou combinação dos mesmos, que podem ser com-pletamente saturados, mono- ou poliinsaturados e podem incluir radicais di- e multi-valentes, tendo o número de átomos de carbono desenhados (isto é, C1-C10 signifi-ca um a dez carbonos). Exemplos de radicais hidrocarbonetos saturados incluem, mas não são limitados a, grupo tais como metila, etila, n-propila, isopropila, n-butila, isobutila, sec-butila, cicloexila, (cicloexila)metila, ciclopropilmetila, homólogos e isô- meros de, por exemplo, n-pentila, n-hexila, n-heptila, n-octila, e semelhantes. Um grupo alquila insaturado é um tendo uma ou mais ligações duplas ou ligações triplas. Exemplos de grupos alquilas insaturados inclue, mas não são limitados a vinil, 2- propenila, crotil, 2-isopentenila, 2-(butadienila), 2,4-pentadienila, 3-(1,4-pentadienila), etinil, 1- e 3-propinila, 3-butinila, e homólogos e isômeros mais altos. O termo “alquila”, a menos que de outra forma notado, é também significado incluir aqueles derivados de alquila definida em mais detalhes abaixo, tal como “heteroalquila”. Grupos alquila que são limitados a grupos hidrocarbonos são nomeados “homoalquila”.
[00105]O termo “alquileno” por ele mesmo ou como parte de outros meios substituintes significam um radical divalente derivado a partir de um alcano, como exemplificado, mas não limitado, pelas estruturas -CH2CH2- e -CH2CH2CH2CH2-, e ainda inclui aqueles grupos descritos abaixo como “heteroalquileno”. Tipicamente, um grupo alquila (ou alquileno) terá de 1 a 24 átomos de carbono, com aqueles gru-pos tendo 10 ou menos átomos de carbono sendo uma modalidade particular dos métodos e composições aqui descritas. Uma “alquila inferior” ou “alquileno inferior” é uma cadeia alquila mais curta ou grupo alquileno, geralmente tendo oito ou menos átomos de carbono.
[00106]Os termos “alcóxi”, “alquilamino” e “alquitio” (ou tioalcóxi) são utiliza-dos no senso convencional, e referem-se àqueles grupos alquila ligados ao resíduo da molécula através de um átomo de oxigênio, um grupo amino, ou um átomo de enxofre, respectivamente.
[00107]O termo “heteroalquila”, por ele mesmo ou em combinação com outro termo, significa, a menos que de outra forma atestado, uma cadeia simples ou rami-ficada estável, ou radical hidrocarboneto cíclico, ou combinações dos mesmos, con-sistindo do número de átomos de carbono e pelo menos um heteroátomo seleciona-do a partir do grupo consistindo de O, N, Si e S, e em que o nitrogênio e átomos de enxofre podem opcionalmente ser oxidados e o heteroátomos nitrogênio pode opci-onalmente ser quaternizado. O(s) heteroátomo(s) O, N e S e Si podem ser colocados em qualquer posição interior do grupo heteroalquila ou na posição em que o grupo alquila é ligado ao resíduo da molécula. Exemplos incluem, mas não são limitados a, -CH2-CH2-O-CH3, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)-CH3, -CH2-S- CH2-CH3, -CH2-CH2-S(O)-CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-O-CH3, -Si(CH3)3, - CH2-CH=N-OCH3, e -CH=CH-N(CH3)-CH3. Até dois heteroátomos podem ser con-secutivos, tal como, por exemplo, -CH2-NH-OCH3 e -CH2-O-Si(CH3)3.
[00108]Similarmente, o termo “heteroalquileno” pode ele mesmo ou como parte de outro substituinte significa um radical divalente derivado a partir de hetero- alquila, como exemplificado, mas não limitado por, -CH2-CH2-S-CH2-CH2- e -CH2-S- CH2-CH2-NH-CH2-. Para grupos heteroalquileno, os mesmos ou diferentes heteroá- tomos podem também ocupar uma ou ambas as cadeias de terminação (incluindo, mas não limitados, alquilenóxi, alquilenodióxi, alquilenoamino, alquilenodiamino, aminoóxialquileno e semelhantes). Ainda adicional, para grupos ligantes alquileno e heteroalquileno, nenhuma orientação do grupo ligante é implicado pela direção em que a fórmula do grupo ligante é escrita. Por exemplo, a fórmula -C(O)2R‘- representa ambas -C(O)2R’- e R’C(O)2-.
[00109]Os termos “cicloalquila” e “heterocicloalquila” por eles mesmos ou em combinação com outros termos, representam, a mesmo que de outra forma atesta- do, versões cíclicas de “alquila” e “heteroalquila”, respectivamente. Então, uma ci- cloalquila ou heterocicloalquila incluem ligações de anéia saturados, parcialmente insaturados e completamente insaturados. Adicionalmente, para heteroacicloalquila, um heteroátomo pode ocupar a posição em que o heterociclo é ligado ao resíduo da molécula. Exemplos de cicloalquila incluem, mas não são limitados a, ciclopentila, cicloexila, 1-cicloexenila, 3-cicloexenila, cicloeptila e semelhantes. Exemplos de he- terocicloalquila incluem, mas não são limitados a, 1,(1,2,5,6-tetraidropiridil), 1- piperidinila, 2-piperidinila, 3-piperidinila, 4-morfolinila, 3-morfolinila, tetraidrofuran-2-il, tetraidrofuran-3-il, tetraidrotien-2-il, tetraidrotien-3-il, 1-piperazinil, 2-piperazinila, e semelhantes. Adicionalmente, o termo compreende estruturas de anéis bicíclicos e tricíclicos. Similarmente, o termo “heterocicloalquileno” por ele mesmo ou como parte de outro substituinte significa um radical divalente derivado a partir de heterocicloal- quila, e o termo “cicloalquileno” por ele mesmo ou como parte de outro substituinte significa um radical divalente derivado a partir de cicloalquila.
[00110]Como aqui utilizado, o termo “polímero solúvel em água” refere-se a qualquer polímero que é solúvel em solventes aquosos. Ligações de polímero solú-veis em água para polipeptídeos FGF-21 podem resultar em mudanças incluindo, mas não limitados a, meia vida séria aumentada ou modulada, ou meia vida terapêu-tica aumentada ou modulada relativa a uma forma não modificada, imunogenicidade modulada, características de associação física moduladas tais como agregação e formação de multímeros, ligação do receptor alterada, ligação alterada a um ou mais parceiros de ligação, e dimerização ou multimerização do receptor alterada. O polí-mero solúvel em água ou pode não ter sua própria atividade biológica, e pode ser utilizado como um ligante para ligar o FGF-21 a outras substâncias, incluindo, mas não limitados a um ou mais polipeptídeos FGF-21, ou uma ou mais moléculas biolo-gicamente ativas. Polímeros adequados incluem, mas não são limitados a polietileno glicol, polietileno glicol propionaldeído, monoalcóxoC1-C10 ou derivados arilóxi dos mesmos (descrito na Patente dos EUA No. 5.252.714 que é aqui incorporado por referência), monometóxi-polietileno glicol, polivinil pirrolidona, polivinil álcool, ácidos poliaminos, anidreto diviniléter maléico, N-(2-hidroxipropil)-metacrilamida, dextrano, derivados dextrano incluindo dextran sulfato, polipropileno glicol, copolímero óxido polipropileno/óxido etileno, poliol polioxietilado, heparina, fragmentos de heparina, polissacarídeos, oligossacarídeos, glicanos, celulose e derivados de celulose, inclu-indo mas não limitados a metilcelulose e carboximetil celulose, amido ou derivados de amido, polipeptídeos, polialquileno glicol e derivados dos mesmos, copolímeros de polialquileno glicóis e derivados dos mesmos, polivinil etil éteres, e alfa-beta- poli[(2-hidroxietil)-DL-aspartamida, e semelhantes, ou misturas dos mesmos. Exemplos de tais polímeros solúveis em água incluem, mas não são limitados a polietilano glicol e albumina sérica.
[00111]Como aqui utilizado, o termo “polialquileno glicol” ou “poli(alqueno glicol)” referem-se a polietileno glicol (poli(etileno glicol)), polipropileno glicol, polibuti- leno glicol, e derivados dos mesmos. O termo “polialquileno glicol” compreende ambos, polímeros lineares e ramificados e pesos moleculares médios de entre 0,1 kDa e 100 kDa. Outras modalidades exemplares são listadas, por exemplo, em catálogos de suprimentos comerciais, tais como catálogo da Shearwater Corporation “Polietile- no glicol e Derivados para Aplicações Biomédicas” (2001).
[00112]O termo “arila” significa, a menos que de outra forma atestado, um substituinte poliinsaturado, aromático, hidrocarboneto, que pode ser um anel único ou anéis múltiplos (incluindo, mas não limitado a partir de 1 a 3 anéis) que são fundi-dos juntos ou ligados covalentemente. O termo “heteroarila” refere-se a grupos arila (ou anéis) que contêm a partir de um a quatro heteroátomos selecionados a partir de N, O, e S, em que os átomos de nitrogênio e enxofre são opcionalmente oxidados, e o(s) átomo(s) de nitrogênio(s) é(são) opcionalmente quaternizados. Um grupo hete- roarila pode ser ligado ao resíduo da molécula através de um heteroátomo. Exemplos não limitantes de arila e grupos heteroarilas incluem fenila, 1-naftila, 2-naftila, 4- bifenila, 1-pirrolil, 2-pirrolil, 3-pirrolil, 3-pirazolil, 2-imidazolil, 4-imidazolil, pirazinila, 2- oxazolil, 4-oxazolil, 2-fenil-4-oxazolil, 5-oxazolil, 3-isoxazolil, 4-isoxazolil, 5-isoxazolil, 2-tiazolil, 4-tiazolil, 5-tiazolil, 2-furila, 3-furila, 2-tienila, 3-tienil, 3-piridila, 3-piridila, 4- piridila, 2-pirimidila, 4-pirimidila, 5-benzotiazolil, purinila, 2-benzimidazolil, 5-indolil, 1- isoquinolil, 5-isoquinolil, 2-quinoxalinila, 5-quinozalinila, 3-quinolila, e 6-quinolila. Substituintes para cada um dos sistemas de anel arila e heteroarila são selecionados a partir do grupo de substituintes aceitáveis descritos abaixo.
[00113]Para brevidade, o termo “arila” quando utilizado em combinação com outros termos (incluindo, mas não limitados a arilóxi, ariltióxi, arilalquila) inclui am-bos, anéis arila e heteroarila como definido acima. Então, o termo “arilalquila” signifi-ca incluir aqueles radicais em que um grupo arila é ligado a um grupo alquila (inclu-indo mas não limitado a, benzila, fenetila, piridilmetila e semelhantes) incluindo grupo aqueles grupo alquila em que um átomos de carbono (incluindo, mas não limitado a um grupo metileno) tem sido substituído por, por exemplo, um átomo de oxigênio (incluindo mas não limitado a fenoximetila, 2-piridiloximetila, 3-(1-naftilóxi)propil, e semelhantes).
[00114]Cada um dos termos acima (incluindo, mas não limitado a “alquila”, “heteroalquila”, “arila” e “heteroarila”) significam incluir ambas, formas substituídas e não substituídas do radical indicado. Substituintes exemplares para cada tipo de ra-dical são providos abaixo.
[00115]Substituintes para radicais alquila e heteroalquila (incluindo aqueles grupos sempre referidos como alquileno, alquenila, heteroalquileno, heteroalquenila, alquinila, cicloalquila, heterocicloalquila, cicloalquenila, e heterocicloalquenila) podem ser um ou mais de uma variedade de grupos selecionados a partir de, mas não limitados a: -OR’, =O. =NR’, =N-OR’, -NR’R’’, -SR’, -halogênio, -SiR’R’’R’’’, - OC(O)R’, -C(O)R’, -CO2R’, -CONR’R’’, -OC(O)NR’R”, -NR’’C(O)R’, -NR’- C(O)NR’’R’’, -NR’’C(O)2R’, -NR-C(NR’R’’R’’’)=NR’’’’, -NR-C(NR’R’’)=NR’’’, -S(O)R’, - S(O)2R’, -S(O)2NR’R’’, -NRSO2R’, -CN e -NO2 em um número variando de zero a (2m’+1), onde m’ é o número total de átomos de carbono em tal um radical. R’, R’’, R’’’cada independentemente refere-se a hidrogênio, heteroalquila substituída ou não substituída, arila substituída ou não substituída, incluindo mas não limitado a arila substituída com 1-3 halogênio, alquila substituída ou não substituída, grupo alcóxi ou tialcóxi, ou grupo arilaquila. Quando um composto da invenção inclui mais que um grupo R, por exemplo, cada um dos grupos R é independentemente selecionado como são cada R’, R’’, R’’’ e R’’’’ quando mais que um dos grupos está presente. Quando R’ e R’’ são ligados ao mesmo átomos de nitrogênio, eles podem ser com-binados com os átomos de nitrogênio para formar um anel de 5-, 6- ou 7-membros. Por exemplo, -NR’R’’ significa incluir, mas não limitado a, 1-pirrilidinil e 4-morfolinil. A partir da discussão acima de substituintes, um versado na técnica entenderá que o termo “alquila” significa incluir grupo incluindo átomos de carbono ligados a grupos outros que grupos de hidrogênio, tais como haloalquila (incluindo mas não limitados a -CF3 e -CH2CF3) e acila (incluindo mas não limitado a -C(O)CH3, -C(O)CF3, - C(O)CH2OCH3, e semelhantes).
[00116]Similar aos substituintes descritos para o radical alquila, substituintes para grupo arila e heteroarila são variados e são selecionados a partir de, mas não são limitados a: halogênio, -OR’, =O, +NR’, =N-OR’, -SR’, -halogênio, -SiR’R’’R’’’, - OC(O)R’, -C(O)R’, -CO2R’, -CONR’R’’, -OC(O)NR’R’’, -NRÇ(O)R’, -NR’-C(O)NR’’R’’’, -NR’’C(O)2R’, -NR-C(NR’R’’R’’’)=NR’’’’, -NR-C(NR’R’’)=NR’’’, -S(O)R’, -S(O)2R’, - S(O)2NR’R’’, -NRSO2R’, -CN e -NO2, -R’, -N3, -CH(Ph)2, fluoralcóxi(Ci-C4), e fluoral- quila(C1-C4), em um número varinado a partir de zero para o número total de valências abertas no sistema de anel aromático; e onde R’, R’’, R’’’ e R’’’’ são independentemente selecionados a partir de hidrogênio, alquila, heteoalquila, arila e heteroarila. Quando um composto da invenção inclui mais que um grupo R, por exemplo, cada um dos grupos R é independentemente selecionado como cada grupos R’, R’’, R’’’ e R’’’’ quando mais que um desses grupos está presente.
[00117]Como aqui utilizado, o termo “meia vida séria modulada” significa a mudança positiva ou negativa na meia-vida circulante de um FGF-2i modificado re-lativo a sua forma não modificada. Meia vida sérica é medida por coleta de amostras de sangue em vários pontos de tempo após a administração de FGF-2i, e determi-nação da concentração desta molécula em cada amostra. Correlação da concentra-ção sérica com o tempo permite o cálculo da meia vida sérica. Meia vida sérica au- mentada desejavelmente tem pelo menos duas vezes, mas um aumento menor pode ser útil, por exemplo, onde ele permita um regime de dosagem satisfatório ou evitar um efeito tóxico. Em algumas modalidades, o aumento é pelo menos cerca de três vezes, pelo menos cerca de cinco vezes, ou pelo menos cerca de dez vezes.
[00118]O termo “meia vida terapêutica modulada” como aqui utilizado signifi-ca a mudança positiva ou negativa na meia vida da quantidade terapeuticamente efetiva do FGF-21, relativa à sua forma não modificada. Meia vida terapêutica é me-dida por medida das propriedades farmacocinéticas e/ou farmacodinâmicas da mo-lécula em vários pontos de tempo após a administração. Meia vida terapêutica au-mentada desejada permite um regime de dose benéfico particular, uma dose total benéfica particular, ou evita um efeito indesejado. Em algumas modalidades, a meia vida terapêutica aumentada resulta a partir da potência aumentada, ligação aumen-tada ou diminuída da molécula modificada ao seu alvo, quebra aumentada ou dimi-nuída da molécula por enzimas tal como proteases, ou um aumento ou diminuição em outro parâmetro ou mecanismo de ação da molécula não modificada ou um au-mento ou diminuição na depuração mediada por receptor da molécula.
[00119]O termo “isolado”, quando aplicado a um ácido nucléico ou proteína, denota que o ácido nucléico ou proteína é livre de pelo menos algum dos componen-tes celulares com os quais ele é associado no estado natural, ou que o ácido nucléi- co ou proteína tenha sido concentrada em um nível maior que a concentração de sua produção in vivo ou in vitro. Isto pode ser em um estado homogêneo. Substân-cias isoladas podem ser ou em um estado seco ou semi-seco, ou em solução, inclu-indo, mas não limitado a uma solução aquosa. Pode ser um componente de uma composição farmacêutica que compreende veículos farmaceuticamente aceitáveis adicionais e/ou excipientes. Pureza e homogeneidade são tipicamente determinados utilizando técnicas de química analítica tais como eletroforese de gel de poliacrilami- da ou cromatografia líquida de alto desempenho. Uma proteína que é predominan-temente presente em uma preparação é substancialmente purificada. Em particular, um gene isolado é separado a partir de estruturas de leitura abertas que flanquea o gene e codificam uma proteína outra que o gene de interesse. O termo “purificado” denota que um ácido nucléico ou proteína dá aumento a substancialmente uma banda em um gel eletroforético. Particularmente, isto pode significar que o ácido nu- cléico ou proteína é pelo menos 85% pura, pelo menos 90% pura, pelo menos 95% pura, pelo menos 99% ou mais pura.
[00120]O termo “ácido nucléico” refere-se a deoxiribonucleotídeos, deoxiri- bonucleosídeos, ribonucleosídeos, ou ribonucleotídeos e polímeros dos mesmos em ou na forma de fita simples ou dupla. A menos que especificamente limitado, o termo compreende ácidos nucléicos contendo análogos conhecidos de nucleotídeos natu-rais que têm propriedades de ligação similares como o ácido nucléico de referência e são metabolizados em uma forma similar para nucleotídeos de ocorrência natural. A menos que especificamente limitado de outra forma, o termo também se refere a análogos oligonucleotídeos incluindo PNA (ácido peptidonucléico), análogos de DNA utilizados em tecnologia anti-senso (fosforotioatos, fosforoamidatos e semelhantes). A menos que de outra forma indicado, uma sequência de ácido nucléico particular também compreende implicitamente variantes modificadas conservativamente das mesmas (incluindo, mas não limitados a substituições de códon degenerado) e sequências complementares bem como a explicidade da sequência indicada. Especificamente, substituições do códon degenarado podem ser alcançadas por sequências geradas em que a terceira posição de um ou mais códons selecionados (ou todos) ser substituídos com resíduos de bases misturadas e/ou deoxiinosina (Batzer et al, Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al, J. Biol. Chem. 260:2605-2608 (1985); Rossolini et al, Mol. Cell. Probes 8:91-98 (1994)).
[00121]Os termos “polipeptídeo”, “peptídeo” e “protéina” são utilizados aqui de modo passível de mudança para referir a um polímero de resíduos aminoácidos. Isto é, uma descrição direcionada a um polipeptídeo aplica igualmente a uma descrição de um peptídeo e uma descrição de uma proteína, e vice-versa. Os termos aplicam a polímeros amináoácidos de ocorrência natural bem como polímeros aminoá- cidos em que um ou mais resíduos aminoácidos estão em um aminoácido codificado não-naturalmente. Como aqui utilizado, os termos compreendem cadeias aminoáci- dos de qualquer comprimento, incluindo proteínas de comprimento inteiro, em que os resíduos aminoácidos estão ligados por ligações peptídicas covalentes.
[00122]O termo “aminoácido” refere-se a aminoácidos de ocorrência natural ou de ocorrência não natural, bem como análogos de aminoácido e aminoácidos miméticos que funcionam e uma forma similar aos aminoácidos de ocorrência natu-ral. Aminoácidos naturalmente codificados são só 20 aminoácidos comuns (alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutâmico, glicina, histidina, isoleucina, leucina, lisina, metionina, fenilalalanina, prolina, serina, treoni- na, triptofano, tirosina e valina)e pirrolisina e selenocisteína. Análogos aminoácidos referem-se a compostos que têm a mesma estrutura química como um aminoácido de ocorrência natural, isto é, um carbono α que está ligado a um hidrogênio, grupo carboxila, um grupo amino, e um grupo R, tais como homoserina, norleucina, sulfó- xido de metionina, metionina metil sulfônio. Tais análogos têm grupo R modificados (tal como, norleucina) ou estruturas de peptídeo modificadas, mas retém a mesma estrutura química básica como um aminoácido de ocorrência natural. Referência a um aminoácido inclui, por exemplo, L-aminoácidos proteogênicos de ocorrência na-tural; D-aminoácidos, aminoácidos quimicamente modificados tal como variantes aminoácidos e derivados; aminoácidos não proteogênicos de ocorrência natural tais como β-alanina, ornitina etc; e compostos quimicamente sintetizados tendo proprie-dades conhecidas na técnica para ser característica de aminoácidos. Exemplos de aminoácidos de ocorrência não natural incluem, mas não são limitados a α-metil aminoácidos (por exemplo, α-metil alanina), D-aminoácidos, aminoácidos do tipo histidina (por exemplo, 2-amino-histidina, β-hidr0xi-histidina, homohistidina, α- fluormetil-histidina e α-metil-histidina), aminoácidos tendo um extra metileno na ca-deia lateral (“homo” aminoácidos), e aminoácidos em que um grupo funcional do áci-do carboxílico na cadeia lateral é substituído com um grupo de ácido sulfônico (por exemplo, ácido cistéico).
[00123]Aminoácidos podem ser referidos aqui por ou suas três letras símbo- los comumente conhecidas ou por símbolos de uma letra recomendada pela Comissão de Nomenclatura Bioquímica IUPAC-IUB. Nucleotídeos, por sua vez, podem ser referidos por seus códons de letra única comumente aceitos.
[00124]“Variantes conservativamente modificados” aplicam a ambas, se-quências aminoácidos e ácido nucléico. Com respeito a sequências de ácido nucléi- co particulares, “variantes conservativamente modificados” referem-se àqueles áci-dos nucleicos que codificam sequências aminoácidos idênticas ou essencialmente idênticas, ou onde o ácido nucléico não codifica uma sequência de aminoácido, para sequências essencialmente idênticas. Por causa da degeneração do código genético, um grande número de ácidos nucléicos funcionalmente idênticos codifica qualquer dada proteína. Por exemplo, os códons GCA, GCC, GCG e GCU todos codificam o aminoácido alanina. Então, em cada posição onde uma alanina é especificada por um códon, o códon pode ser alterado para qualquer os códons correspondentes descritos sem alterar o polipeptídeo codificado. Tais variações de ácido nucléico são “variações silenciosas”, que são uma espécie de variações conservativamente modificadas. Cada sequência de ácido nucléico aqui que codifica um polipeptídeo também descreve cada variação silenciosa possível do ácido nucléico. Um versado na técnica reconhecerá que cada códon em um ácido nucléico (exceto AUG, que é ordinariamente o único códon para metionina, e TGG, que é ordinariamente somente o códon para triptofano). Pode ser modificado para produzir uma molécula de funcionalidade idêntica. Consequentemente, cada variação silenciosa de um ácido nu- cléico que codifica um polipeptídeo está implícito em cada sequência descrita.
[00125]Como as sequências aminoácidos, um versado na técnica reconhe-cerá que substituições individuais, deleções ou adições a um ácido nucléico, peptí- deo, polipeptídeo, ou sequência de proteína que alteram, adicionam ou deletam um aminoácido único ou uma pequena porcentagem de aminoácidos na sequência codificada é um “variante conservativamente modificado” onde a alteração resulta na deleção de um aminoácido, adição de um aminoácido, ou substituição de um amino- ácido com um aminoácido quimicamente similar. Tabelas de substituição conservada provêm aminoácidos funcionalmente similares são conhecidos pelos versados na técnica. Tais variantes conservativamente modificados estão em adição e não exclu-em variantes polimórficas, homólogos interespécies e alelos da invenção.
[00126]Tabelas de substituições conservadas provêm aminoácidos funcio-nalmente similares são conhecidas pelos versados na técnica. Os oito grupos se-guintes contêm cada aminoácidos que são substituições conservadas para um outro: 1)Alanina (A), Glicina (G); 2) Ácido aspártico (D), ácido glutâmico (E); 3) Asparagina (N), Glutamina (Q); 4) Arginina (R), Lisina (K); 5) Isoleucina (I), Leucina (L), Metionina (M), Valina (V); 6) Fenilalanina (F), Tirosina (Y), Triptofano (W); 7) Serina (S), Treonina (T); e 8) Cisteína (C), Metionina (M) (ver, por exemplo, Creighton, Proteins: Structures and Molecular Properties (W H Freeman & Co; 2a edição (Dezembro 1993).
[00127]Os termos “idênticos” ou porcentagem de “identidade”, no contexto de dois ou mais ácidos nucléicos ou sequências polipeptídeos, refere-se a duas ou mais sequências ou subsequências que são as mesmas. Sequências são “substan-cialmente idênticas” se elas têm uma porcentagem de resíduos aminoácidos ou nu- cleotídeos que são os mesmos (isto é, cerca de 60% de identidade, cerca de 65%, cerca de 70%, cerca de 75%, cerca de 80%, cerca de 85%, cerca de 90%, ou cerca de 95% de identidade ao longo de uma região especificada), quando comparado e alinhado para correspondência máxima ao longo de uma janela de comparação, ou região designada como medida utilizando um dos seguintes algoritmos de compara-ção de sequência (ou outros algoritmos disponíveis para pessoas versadas na técni-ca) ou por alinhamento manual e inspeção visual. Esta definição também se refere ao complemento da sequência teste. A identidade pode existir ao longo de uma re-gião que é pelo menos cerca de 50 aminoácidos ou nucleotídeos de comprimento, ou por uma região que é 75-100 aminoácidos ou nucleotídeos em comprimento, ou, onde não especificado, atravessa a sequência inteira de um polinucleotídeo ou poli- peptídeo. Um polinucleotídeo codificando um polipeptídeo da presente invenção, incluindo homólogo a partir de espécies outras que humana, podem ser obtidas por um processo compreendendo os passos de seleção em uma biblioteca sob condi-ções de hibridização severas com um padrão marcado tendo uma sequência poloi- nucleotídica da invenção ou um fragmento do mesmo, e isolando um cDNA de com-primento inteiro e clones genômicos contendo a referida sequência polinucleotídica. Tais técnicas de hibridização são bem conhecidas pelo versado na técnica.
[00128]Para comparação de sequência, tipicamente uma sequência atua como uma sequência de referência, para qual sequências testes são comparadas. Quando utilizando um algoritmo de comparação, sequências teste e de referência são colocadas em um computador, coordenadas subsequentes são desenhadas, se necessário, e parâmetros do programa de sequência algoritma são desenhados. Fa-lha de parâmetros de programa pode ser utilizados, ou parâmetros alternativos po-dem ser designados. A sequência de comparação algoritma então calcula as porcen-tagens de identidades de sequência para sequências testes relativas à sequência de referência, baseadas em programas parâmetros.
[00129]Uma “janela de comparação”, como aqui utilizada, inclui referência a um segmento de qualquer um do número de posições contíguas selecionadas a par-tir do grupo consistindo a partir de 20 a 600, usualmente cerca de 50 a 200, mais usualmente cerca de 100 a cerca de 150 em cuja sequência pode ser comparada a uma sequência de referência no mesmo número de posições contíguas após as su-as sequências estarem otimamente alinhadas. Métodos de alinhamento de sequên-cias para comparação são conhecidos pelos versados na técnica. Alinhamento ópti-mo de sequências para comparação podem ser conduzidos, incluindo, mas não limi-tados a, pelo algoritmo de homologia local de Smith e Waterman (1970) Adv. Appl. Math. 2:482c, pelo algoritmo de alinhamento de homologia de Needleman e Wunsch (1970) J. Mol. Biol. 48:443, pela pesquisa para método de similaridade de Pearson e Lipman (1988) Proc. Natl. Acad.Sci. EUA 85:2444, por implementações computado-rizadas desses algoritmos (GAP, BESTFIT, FASTA, e TFASTA no Pacote de Pro- grema da Wisconsin Genetics, Genetics Computer Group, 575 Science Dr., Madison, WI), ou por alinhamento manual e inspeção visual (ver, por exemplo, Ausubel et al, Current Protocols in Molecular Biology (1995 suplemento)).
[00130]Um exemplo de um algoritmo que é adequado para determinar a porcentagem de identidade de sequência e similaridade de sequência são os algo-ritmos BLAST e BLAST 2.0, que são descritos em Altschul et al (1997) Nuc. Acids. Res. 25:3389-3402, e Altschul et al (1990) j. Mol. Biol. 215:403-410, respectivamente. Programa para fazer análises BLAST é publicamente disponível através do Centro Nacional de Informação Biotecnológica disponível na World Wide Web em ncbi.nlm.nig.gov. O programa BLASTN (para sequências de nucleotídeo) usa como falhas um comprimento de palavra (W) de 11, uma expectativa (E) ou 10, M=5, N=4 e uma comparação de ambas as fitas. Para sequências aminoácidos, o programa BLASTP usa como falha um comprimento de palavra de 3, e expectativa (E) de 10, e a matriz de ganho BLOSUM62 (ver Henikoff e Henikoff (1992) Proc. Natl. Acad. Sci. EUA 89:10915) alinhamentos (B) de 50, expectativa (E) de 10, M=5, N=4, e uma comparação de ambas as fitas. O algoritmo BLAST é tipicamente feito com o filtro de “baixa complexidade” desligado.
[00131]O algoritmo BLAST também faz uma análise estatística de similari-dade entre duas sequências (ver, por exemplo, Karlin e Altschul (1993) Proc. Natl. Acad. Sci. EUA 90:5873-5787). Uma medida da similaridade provida pelo algoritmo BLAST a probabilidade da menor soma (P(N)), que provê uma indicação da probabi-lidade pela qual um encontro entre duas sequências nucleotídicas ou aminoácidos deve ocorrer pela chance. Por exemplo, um ácido nucléico é considerado similar a uma sequência de referência se a probabilidade da menor soma em uma compara-ção de ácido nucléico teste para o ácido nucléico de referência é menor que cerca de 0,2, ou menos que cerca de 0,01, ou menor que cerca de 0,001.
[00132]A frase “seletivamente ( ou especificamente) hibridiza a “ refere-se à ligação, duplexação ou hibridização de uma molécula somente a uma sequência nu- cleotídica particular sob condições de hibridização severas quando esta sequência está presente em uma mistura complexa (incluindo, mas não limitada a, DNA ou RNA celular total ou biblioteca).
[00133]A frase “condições de hibridização severas” referem-se à hibridiza- ção de sequências de DNA, RNA e PNA, ou outros ácidos nucléicos mimetizadores, ou combinações dos mesmos sob condições de baixa força iônica e alta temperatura como é conhecido na técnica. Tipicamente, sob condições severas um padrão hibri- dizará a seu alvo subsequente em uma mistura complexa de ácido nucléico (incluin-do, mas não limitado ao DNA ou RNA celular total ou biblioteca) mas não hibridiza a outras sequências na mistura complexa. Condições severas são dependentes de sequências e serão diferentes em circunstâncias diferentes. Sequências mais longas hibridizam especificamente em temperaturas mais altas. Um guia extenso para a hibridização de ácidos nucléicos é entrado em Tijssen, Laboratory Techniques in Biochemistry and Molecular Biology - Hybridization with Nucleic Probes. “Overview if principles of hybridization and the strategy of nucleic acid assays”(1993). Geralmente, condições severas são selecionadas para cerca de 5-10oC menores que o ponto de fusão térmico (Tm) para a sequência específica em um pH de força iônica definido. A Tm é a temperatura (sob força iônica definida, pH, e concentração nucléica) em que 50% dos padrões complementares ao alvo hibridizam à sequência alvo em equilíbrio (como as sequências alvo estão presentes em excesso, uma Tm, 50% de padrões são ocupadas em equilíbrio). Condições severas podem ser aquelas em que a concentração salina é menor que cerca de 1,0 M de íon sódio tipicamente cerca de 0,01 a 1,0 M de concentração de íon sódio (ou outros sais) em pH 7.0 para 8.3 e a temperatura é pelo menos cerca de 30oC para padrões curtos (incluindo mas não limitados a, 10 a 50 nucleotídeos) e pelo menos cerca de 60oC para padrões longos (incluindo mas não limitados a, maiores que 50 nucleotídeos). Condições severas podem também ser alcançadas com a adição de agentes desestabilizantes tal como formamida. Para hibridização seletiva ou específica, um sinal positivo pode ser pelo menos duas vezes antecedentes, opcionalmente 10 vezes de hibridização antece-dente. Condições de hibridização severas exemplares podem ser como segue: 50% de formamida, 5X SSC, e 1% de SDS, incubando a 42oC, ou 5X SSC, 1% SDS, in-cubando a 65oC, com lavagem em 0m2X SSC, e 0,1% SDS a 65oC, Tais lavagens podem ser feitas por 5, 15, 30, 60, 120 ou mais minutos.
[00134]Como aqui utilizado, o termo “eucarioto” refere-se a organismos per-tencendo ao domínio filogenético Eucarya tal como animais (incluindo, mas não limi-tado a mamíferos, insetos, répteis, pássaros etc), ciliados, plantas (incluindo, mas não limitados a monocotiledôneas, dicotiledôneas, algas etc), fungos, leveduras, fla-gelados, microesporídeos, protistas etc.
[00135]Como aqui utilizado, o termo “não eucarioto” refere-se a organismos não eucariotos. Por exemplo, um organismo não eucarioto pode pertencer ao domí-nio filogenético Eubacteria (incluindo mas não limitado a, Escherichia coli, Thermus thermophilus, Bacillus stearothermophilus, Pseudomonas fluorescens, Pseudomonas aeruginosa, Pseudomonas putida etc), ou o domínio filogenético Archaea (incluindo mas não limitado a Methanococcus jannarchii, Methanobacterium thermoautotrophi- cum, Halobacterium tais como Haloferax volcanii e espécies de Halobacterium NRC- 1, Archaeoglobus fulgidus, Pyrococcus furiosus, Pyrococcus horikoshii, Aeuropyrum pernix etc). O termo “paciente” como aqui utilizado, refere-se a um animal, em algumas modalidades um mamífero, e em outras modalidades, um humano, que é objeto de tratamento, observação ou experimento. Um animal pode ser um animal de companhia (por exemplo, cachorros, gatos e semelhantes), animais de fazenda (por exemplo, vacas, ovelhas, porcos, cavalos e semelhantes) ou um animal de laboratório (por exemplo, ratos, camundongos, cobaias e semelhantes).
[00136]O termo “quantidade efetiva” como aqui utilizado refere-se àquela quantidade de polipeptídeo aminoácido não natural modificado sendo administrado que aliviará em alguma extensão um ou mais sintomas da doença, condição ou dis-túrbio sendo tratada. Composições contendo o polipeptídeo aminoácido não natural modificado descrito aqui pode ser administrado para tratamentos profiláticos, aumen- tadores e/ou terapêuticos.
[00137]Os termos “aumento” ou “aumentando” significam um aumento ou prolongamento ou da potência ou duração de um efeito desejado. Então, em relação ao efeito aumentado dos agentes terapêuticos, o termo “aumentado” refere-se à ha-bilidade de aumentar ou prolongar, ou a potência ou duração, o efeito ou outros agentes terapêuticos em um sistema. Uma “quantidade efetiva para aumento” como aqui utilizada, refere-se a uma quantidade adequada para aumentar o efeito de outro agente terapêutico em um sistema desejado. Quando utilizado em um paciente, quantidades efetivas para este uso dependerão da severidade e curso da doença, distúrbio ou condição, terapia prévia, o estado de saúde do paciente e resposta a drogas, e o julgamento do médico que está tratando.
[00138]O termo “modificado”, como aqui utilizado refere-se a qualquer mu-dança feita a um dado polipeptídeo, tais mudanças no comprimento do polipeptídeo, a sequência de aminoácido, estrutura química, modificação co-traducional, ou modi-ficação pós-traducional de um polipeptídeo. O termo forma “(modificada)” significa que os polipeptídeos sendo discutidos são opcionalmente modificados, isto é, os polipeptídeos sob discussão podem ser modificados ou não modificados.
[00139]O termo “pós-traducionalmente modificado” refere-se a qualquer mo-dificação e um aminoácido natural ou não natural que ocorre a tal aminoácido após ele ter sido incorporado em uma cadeia polipeptídica. O termo compreende, por meio de exemplo, somente modificações co-traducionais in vivo, modificações co- traducionais in vitro (tal como em um sistema de tradução livre de célula), modifica-ções pós-traducionais in vivo, e modificações pós-traducionais in vitro.
[00140]Em aplicações profiláticas, composições contendo o polipeptídeo FGF-21 são administradas a um paciente susceptível a ou de forma em risco de uma doença, distúrbio ou condição particular. Tal quantidade é definida ser uma “quanti-dade profilaticamente efetiva”. Neste uso, as quantidades precisas também depen-dem do estado do paciente de saúde, peso e semelhantes. É bem considerado compreendido dentro da técnica para uma pessoa determinar tais quantidades profi- laticamente eficazes através de experimentação rotineira (por exemplo, um ensaio clínico de aumento de dose).
[00141]O termo “protegido” se refere à presença de um “grupo protetor” ou porção que evite a reação do grupo funcional quimicamente reativo sob certas con-dições reacionais. O grupo protetor irá variar dependendo do tipo de grupo quimica-mente reativo sendo protegido. Por exemplo, se o grupo quimicamente reativo for uma amina ou hidrazida, o grupo protetor pode ser selecionado do grupo de terc- butoxicarbonil (t-Boc) e 9-fluorenilmetoxicarbonil (Fmoc). Se o grupo quimicamente reativo for um tiol, o grupo protetor pode ser ortopiridilsulfeto. Se o grupo quimica-mente reativo for um ácido carboxílico, tal como ácido butanóico ou propiônico, ou um grupo hidroxila, o grupo protetor pode ser benzil ou um grupo alquil, tal como metil, etil ou terc-butil. Outros grupos protetores conhecidos na técnica também po-dem ser usados em ou com os métodos e composições aqui descritos, incluindo grupos foto instáveis tais como Nvoc e MeNvoc. Outros grupos protetores conhecidos na técnica também podem ser usados em ou com os métodos e composições aqui descritos.
[00143]Outros grupos protetores estão descritos em Greene e Wuts, Protec- tive Groups in Organic Synthesis, 3a Ed., John Wiley & Sons, Nova Iorque, NY, 1999, o qual é aqui incorporado por referência na sua totalidade.
[00144]Em aplicações terapêuticas, as composições contendo polipeptídeo de aminoácidos não-natural modificado são administradas a um paciente que já so-fre de uma doença, condição ou distúrbio em uma quantidade suficiente para curar ou pelo menos interromper parcialmente os sintomas da doença, distúrbio ou condi-ção. Tal quantidade é definida como sendo uma “quantidade terapeuticamente efi-caz” e irá depender da gravidade e curso da doença, distúrbio ou condição, terapia anterior, o status de saúde do paciente e resposta aos fármacos, e do julgamento do clínico geral do tratamento. É considerado como estando bem dentro da técnica o fato de uma pessoa determinar tais quantidades terapeuticamente eficazes por ex-perimentação rotineira (por exemplo, um ensaio clínico de aumento de dose).
[00145]O termo “tratando” é usado para se referir a tratamentos ou profiláticos e/ou terapêuticos.
[00146]Polipeptídeos de aminoácidos artificialmente codificados aqui apre-sentados podem incluir compostos isotopicamente marcados com um ou mais átomo substituídos por um átomo com uma massa atômica ou número de massa diferente da massa atômica ou número de massa geralmente encontrado na natureza. Exem-plos de isótopos que podem ser incorporados nos presentes compostos incluem isó-topos de hidrogênio, carbono, nitrogênio, oxigênio, flúor e cloro, tais como 2H, 3H, 13C, 14C, 15N, 18O, 17O, 35S, 18F, 36Cl, respectivamente. Certos compostos isotopica- mente marcados aqui descritos, por exemplo, aqueles nos quais os isótopos radioa-tivos tais como 3H e 14C são incorporados, podem ser úteis em ensaios de distribui-ção tecidual de fármaco e/ou substrato. Certos compostos isotopicamente marcados aqui descritos, por exemplo, aqueles nos quais isótopos radioativos tais como 3H e 14C são incorporados, podem ser úteis em ensaios de distribuição de fármaco e/ou substrato. Além disso, a substituição com isótopos tal como deutério, isto é, 2H, pode proporcionar certas vantagens terapêuticas resultantes de maior estabilidade meta-bólica, por exemplo, meia vida in vivo aumentada ou necessidade de dosagem redu- zida.
[00147]Todos os isômeros incluindo, porém sem se limitar aos diastereoisô- meros, enantiômeros e misturas suas são considerados como parte das composições aqui descritas. Em outras ou adicionais modalidades, os polipeptídeos de ami- noácidos artificialmente codificados são metabolizados na administração a um orga-nismo necessitado para produzir um metabólito que é, então usado para produzir um efeito desejado, incluindo um efeito terapêutico desejado. Em outras ou adicionais modalidades, são metabólitos ativos de polipeptídeos de aminoácidos artificialmente codificados.
[00148]Em algumas situações, polipeptídeo de aminoácidos artificialmente codificados podem existir como tautômeros. Além disso, os polipeptídeos de amino- ácidos artificialmente codificados aqui descritos podem existir nas formas solvatadas e não-solvatada com solventes farmaceuticamente aceitáveis, tais como água, eta- nol e semelhantes. As formas solvatadas também são consideradas como sendo aqui reveladas. As pessoas normalmente versadas na técnica irão reconhecer que alguns dos compostos daqui podem existir em várias formas tautoméricas. Todas as tais formas tautoméricas são consideradas como parte das composições aqui descri-tas.
[00149]A não ser que seja indicado de outra forma, métodos convencionais de espectroscopia de massa, RMN, HPLC, química de proteína, bioquímica, técnicas de DNA recombinantes e farmacologia dentro da habilidade da técnica são empre-gadas.
[00150]Moléculas FGF-21 compreendendo pelo menos um aminoácido artifi-cial são fornecidas na invenção. Em certas modalidades da invenção, o polipeptídeo FGF-21 com pelo menos um aminoácido artificial inclui pelo menos uma modificação pós-tradução. Em uma modalidade, essa pelo menos uma modificação pós-tradução compreende a ligação de uma molécula incluindo, porém sem se limitar, a um mar- cador, um corante, um polímero, um polímero hidrossolúvel, um derivado de polieti- lenoglicol, um fotorreticulador, um radionuclídeo, um composto citotóxico, um fárma- co, um marcador de afinidade, um marcador de fotoafinidade, um composto reativo, uma resina, uma segunda proteína ou polipeptídeo ou análogo de polipeptídeo, um anticorpo ou fragmento de anticorpo, um quelante de metal, um cofator, um ácido graxo, um carboidrato, um polinucleotídeo, um DNA, um RNA, um polinucleotídeo anti-sentido, um sacarídeo, um dendrímero hidrossolúvel, uma ciclodextrina, um áci-do ribonucléico inibitório, um biomaterial, uma nanopartícula, um marcador de rota-ção, um fluoróforo, uma porção contendo metal, uma porção radioativa, um grupo funcional novo, um grupo que interaja covalentemente ou não-covalentemente com outras moléculas, uma porção fotoaprisionada, uma porção excitável por radiação actínica, uma porção fotoisomerizável, biotina, um derivado da biotina, um análogo da biotina, uma porção incorporando um átomo pesado, um grupo quimicamente clivável, um grupo fotoclivável, uma cadeia lateral alongada, um açúcar ligado a car-bono, um agente redox ativo, um aminotioácido, uma porção tóxica, uma porção iso- topicamente marcada, uma sonda biofísica, um grupo fosforescente, um grupo qui- miluminescente, um grupo elétron denso, um grupo magnético, um grupo intercala- dor, um cromóforo, um agente de transferência de energia, um agente biologicamen-te ativo, um marcador detectável, uma molécula pequena, um ponto de quantum, um nanotransmissor, um radionuclídeo, um radiotransmissor, um agente de captura de nêutrons ou qualquer combinação dos grupos acima ou qualquer outro composto ou substância desejável compreendendo um segundo grupo reativo para pelo menos um aminoácido artificial compreendendo um primeiro grupo reativo utilizando a me-todologia química que é conhecida por uma pessoa normalmente versada na técnica para ser adequado para os grupos reativos particulares. Por exemplo, o primeiro grupo reativo é uma porção alquinil (incluindo, porém sem se limitar, ao aminoácido p-propargiloxifenilalanina artificial, onde o grupo propargil também é algumas vezes referido como uma porção acetileno) e o segundo grupo reativo é uma porção azido, e metodologias químicas de cicloadição [3+2] são utilizadas. Em outro exemplo, o primeiro grupo reativo é a porção azido (incluindo, porém sem se limitar, ao aminoá- cido artificial p-azido-L-fenilalanina) e o segundo grupo reativo sendo a porção al- quinil. Em certas modalidades do polipeptídeo FGF-21 modificado da presente in-venção, pelo menos um aminoácido artificial (incluindo, porém sem se limitar, ao aminoácido artificial contendo um grupo ceto funcional) compreendendo pelo menos uma modificação pós-tradução, é usado onde pelo menos uma modificação pós- tradução compreende uma porção sacarídica. Em certas modalidades, a modificação pós-tradução é feita in vivo em uma célula eucariótica ou em uma célula não- eucariótica. Um ligante, polímero, polímero hidrossolúvel ou outra molécula pode ligar a molécula ao polipeptídeo. A molécula pode ser ligada diretamente ao polipep- tídeo.
[00151]Em certas modalidades, a proteína inclui pelo menos uma modifica-ção pós-tradução que é feita in vivo por uma célula hospedeira, onde a modificação pós-tradução não é normalmente feita por outro tipo de célula hospedeira. Em certas modalidades, a proteína inclui pelo menos uma modificação pós-tradução que é feita in vivo por uma célula eucariótica, onde a modificação pós-tradução não é normal-mente feita por uma célula não-eucariótica. Exemplos de modificações pós-tradução incluem, porém não estão limitadas, à glicosilação, acetilação, acilação, modificação lipídica, palmitoilação, adição de palmitato, fosforilação, modificação de ligação com glicolipídeo e semelhantes. Em uma modalidade, a modificação pós-tradução com-preende a ligação de um oligossacarídeo a uma asparagina por uma ligação Glc- NAc-asparagina (incluindo, porém sem se limitar, a onde o oligossacarídeo compre-ende (GlcNAc-Man)2-Man-GlcNAc-GlcNAc, e semelhantes). Em outra modalidade, a modificação pós-tradução compreende a ligação de um oligossacarídeo (incluindo, porém sem se limitar, a Gal-GalNAc, Gal-GlcNAc, etc.) e uma serina ou treonina por uma ligação GalNAc-serina, uma GalNAc-treonina, uma Glc-NAc-serina ou uma GlcNAc-treonina. Em certas modalidades, uma proteína ou polipeptídeo da invenção pode compreender uma sequência de localização ou secreção, um marcador de epí- topo, um marcador FLAG, um marcador de poliistidina, uma fusão GST e/ou seme- lhantes. Exemplos de sequências de sinal de secreção incluem, porém não estão limitados, a uma sequência de sinal de secreção procariótica, uma sequência de si-nal de secreção eucariótica, uma sequência de sinal de secreção eucariótica 5’- otimizada para expressão bacteriana, uma sequência de sinal de secreção nova, uma sequência de sinal de secreção de pectato liase, uma sequência de sinal de secreção Omp A e uma sequência de sinal de secreção de fago. Exemplos de se-quências de sinal de secreção incluem, porém não estão limitadas, a STII (procarió- tica), Fd GIII e M13 (fago), Bg12 (levedura) e a sequência de sinal bla derivada de um transposon. Qualquer sequência como esta pode ser modificada para fornecer um resultado desejado com o polipeptídeo incluindo, porém sem se limitar, à substituição de uma sequência de sinal com uma sequência de sinal diferente, substituindo uma sequência líder com uma sequência líder diferente, etc.
[00152]A proteína ou polipeptídeo de interesse pode conter pelo menos um, pelo menos dois, pelo menos três, pelo menos quatro, pelo menos cinco, pelo menos seis pelo menos sete, pelo menos oito, pelo menos nove ou dez ou mais amino- ácidos não-naturais. O aminoácido não-natural pode ser igual ou diferente, por exemplo, pode haver 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ou mais sítios diferentes na proteína que compreendem 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ou mais aminoácido não-naturais dife-rentes. Em certas modalidades, pelo menos um, porém menos do que todos os ami- noácidos particulares presentes em uma versão natural da proteína é substituído com um aminoácido artificial.
[00153]A presente invenção fornece métodos e composições à base de FGF-21 compreendendo pelo menos um aminoácido codificado não-naturalmente. A introdução de pelo menos um aminoácido codificado não-naturalmente em FGF-21 pode permitir a aplicação de química de conjugação que envolve reações químicas específicas incluindo, porém sem se limitar, a um ou mais aminoácidos codificados artificialmente enquanto não reagem com os 20 aminoácidos que ocorrem de forma comum. Em algumas modalidades, FGF-21 compreendendo o aminoácido artificial codificado é ligado a um polímero solúvel em água, tal como polietilenoglicol (PEG), através da cadeia lateral do aminoácido codificado não-naturalmente. Esta invenção proporciona um método altamente eficiente para a modificação seletiva de proteínas com derivados PEG, o qual envolve a incorporação seletiva de aminoácidos não- geneticamente codificados incluindo, porém sem se limitar, àqueles aminoácidos contendo grupos funcionais ou substituintes não encontrados nos 20 aminoácidos naturalmente incorporados, incluindo porém sem se limitar a uma porção cetona, azida ou acetileno, em proteínas em resposta a um códon seletor e a subsequente modificação daqueles aminoácidos com um derivado PEG adequadamente reativo. Uma vez incorporadas, as cadeias laterais de aminoácidos podem ser então modifi-cadas pelo uso e metodologias químicas conhecidas pelas pessoas versadas na técnica como sendo adequadas para os grupos funcionais particulares ou substituin- tes presentes no aminoácido artificialmente codificado. Metodologias químicas co-nhecidas de uma ampla variedade são adequadas para uso na presente invenção para incorporar um polímero solúvel em água na proteína. Tais metodologias inclu-em, porém não estão limitadas, à reação de cicloadição de Huisgen [3+2] (ver, por exemplo, Padwa, A. em Comprehensive Organic Synthesis, Vol. 4, (1991) Ed. Trost, B. M., Pergamon, Oxford, p. 1069- 1109; e, Huisgen, R. em 1,3-Dipolar Cvcloaddition Chemistry, (1984) Ed. Padwa, A., Wiley, Nova Iorque, p. 1-176) incluindo, porém sem se limitar, com derivados acetileno ou azida, respectivamente.
[00154]Devido ao fato do método de cicloadição de Huisgen [3+2] envolver a cicloadição ao invés da reação de substituição nucleofílica, as proteínas podem ser modificadas com seletividade extremamente alta. A reação pode ser efetuada em temperatura ambiente em condições aquosas com excelente regiosseletividade (1,4 > 1,5) pela adição de quantidades catalíticas de sais de Cu(I) à mistura reacional. Ver, por exemplo, Tornoe, et al., (2002) J. Org. Chem. 67:3057-3064; e Rostovtsev, et al., (2002) Angew. Chem. Int. Ed. 41:2596-2599; e WO 03/101972. Uma molécula que pode ser adicionada a uma proteína da invenção através da cicloadição de [3+2] inclui virtualmente qualquer molécula com um grupo funcional adequado ou substi- tuinte incluindo, porém sem se limitar, a um derivado azido o acetileno. Essas molé- culas podem ser adicionadas a um aminoácido artificial com um grupo acetileno in-cluindo, porém sem se limitar, a p-propargiloxifenilalanina, ou grupo azido incluindo, porém sem se limitar, a p-azidofenilalanina, respectivamente.
[00155]O anel e cinco membros que resulta da cicloadição de Huisgen [3+2] não é geralmente reversível em ambientes redutores e é estável contra a hidrólise por períodos prolongados em ambientes aquosos. Consequentemente, as características físicas e químicas de uma ampla variedade de substâncias podem ser modificadas sob condições aquosas exigidas com os derivados PEG ativos da presente invenção. De modo ainda mais importante, devido ao fato das porções azida e acetileno serem específicas entre si (e não reagirem, por exemplo, com qualquer um dos 20 aminoácidos geneticamente codificados comuns), as proteínas podem ser modifi-cadas em um ou mais sítios específicos com seletividade extremamente alta.
[00156]A invenção também fornece derivados hidrossolúveis e hidrolitica- mente estáveis dos derivados PEG e polímeros hidrofílicos relacionados com uma ou mais porções acetileno ou azida. Os derivados poliméricos PEG que contém porções acetileno são altamente seletivos para o acoplamento com porções azida que tenham sido introduzidas seletivamente em proteínas em resposta a um códon sele- tor. Semelhantemente, derivados poliméricos PEG que contêm porções azida são altamente seletivos para o acoplamento com porções acetileno que tenham sido in-troduzidas seletivamente em proteínas em resposta a um códon seletor.
[00157]Mais especificamente, as porções azida compreendem, porém não estão limitadas, a alquilazidas, arilazidas e derivados dessas azidas, os derivados de alquil e arilazidas podem incluir outros substituintes, contanto que a reatividade es-pecífica para o acetileno seja mantida. As porções acetileno compreendem alquil e arilacetilenos e derivados de cada uma. Os derivados do alquil e arilacetilenos po-dem incluir outros substituintes contanto que a reatividade específica para azida seja mantida.
[00158]A presente invenção fornece conjugados de substâncias com uma ampla variedade de grupos funcionais, substituintes ou porções, com outras subs- tâncias incluindo, porém sem se limitar, a um marcador; um corante; um polímero; um polímero hidrossolúvel; um derivado de polietilenoglicol; um fotorreticulador; um radionuclídeo; um composto citotóxico; um fármaco; um marcador de afinidade; um marcador de fotoafinidade; um composto reativo; uma resina; uma segunda proteína ou polipeptídeo ou análogo de polipeptídeo; um anticorpo ou fragmento de anticorpo; um quelante de metal; um cofator; um ácido graxo; um carboidrato; um polinucleotí- deo; um DNA; um RNA; um polinucleotídeo anti-sentido; um sacarídeo; um dendrí- mero hidrossolúvel; uma ciclodextrina; um ácido ribonucléico inibitório; um biomate-rial; uma nanopartícula; um marcador de rotação; um fluoróforo; uma porção conten-do metal; uma porção radioativa; um grupo funcional novo; um grupo que interaja covalentemente ou não-covalentemente com outras moléculas; uma porção fotoapri- sionada; uma porção excitável por radiação actínica; uma porção fotoisomerizável; biotina; um derivado da biotina; um análogo da biotina; uma porção incorporando um átomo pesado; um grupo quimicamente clivável; um grupo fotoclivável; uma cadeia lateral alongada; um açúcar ligado a carbono; um agente redox ativo; um aminotioá- cido; uma porção tóxica; uma porção isotopicamente marcada; uma sonda biofísica; um grupo fosforescente; um grupo quimiluminescente; um grupo elétron denso; um grupo magnético; um grupo intercalador; um cromóforo; um agente de transferência de energia; um agente biologicamente ativo; um marcador detectável; uma molécula pequena; um ponto de quantum; um nanotransmissor; um radionuclídeo; um radio- transmissor; um agente de captura de nêutrons ou qualquer combinação dos grupos acima ou qualquer outro composto ou substância desejável. A presente invenção também inclui conjugados de substâncias com porções azida ou acetileno co deriva-dos poliméricos PEG com as porções acetileno ou azida correspondentes. Por exemplo, um polímero PEG contendo uma porção azida pode ser acoplado a uma molécula biologicamente ativa em uma posição na proteína que contenha um ami- noácido que não seja codificado geneticamente com uma funcionalidade acetileno. A ligação pela qual o PEG e a molécula biologicamente ativa são acoplados inclui, porém não está limitada, ao produto de cicloadição de Huisgen [3+2].
[00159]É bem estabelecido na técnica que PEG pode ser usado para modifi-car as superfícies dos biomateriais (ver, por exemplo, a Patente Americana 6.610.281; Mehvar, R., J. Pharm Sci, 3(1):125-136 (2000) as quais são incorporadas por referência aqui). A invenção também inclui biomateriais compreendendo uma superfície com um ou mais sítio de azida ou acetileno reativos e um ou mais dos po-límeros contendo azida ou acetileno da invenção acoplados com a superfície através da ligação de cicloadição [3+2] de Huisgen. Biomateriais e outras substâncias tam-bém podem ser acopladas com os derivados poliméricos azida ou acetileno ativados através de uma ligação diferente da ligação azida ou acetileno, tal como através de uma ligação compreendendo uma porção ácido carboxílico, amina, álcool ou tiol para deixar a porção azida ou acetileno disponível para reações subsequentes.
[00160]A invenção inclui um método de síntese dos polímeros contendo azi- da e acetileno da invenção. No caso do derivado PEG contendo azida, a azida pode se ligar diretamente a um átomo de carbono do polímero. Alternativamente, o deri-vado PEG contendo azida pode ser preparado pela ligação de um agente de ligação que tenha a porção azida em um terminal em relação a um polímero ativado con-vencional, de modo que o polímero resultante tenha a porção azida em sua parte terminal. No caso do derivado PEG contendo acetileno, o acetileno pode ser ligado diretamente a um átomo de carbono do polímero. Alternativamente, o derivado PEG contendo acetileno pode ser preparado pela ligação de um agente de ligação que tenha a porção acetileno em um terminal em um polímero ativado convencional de modo que o polímero resultante tenha a porção acetileno em sua extremidade.
[00161]Mais especificamente, no caso do derivado PEG contendo azida, um polímero hidrossolúvel com pelo menos uma porção hidroxila ativa sofre uma reação para produzir um polímero substituído com uma porção mais reativa, tal como um grupo de saída mesilato, tresilato, tosilato ou halogênio nisso. A preparação e uso dos derivados PEG contendo haletos de ácido de sulfonila, átomos de halogênio e outros grupos de saída são conhecidos pelas pessoas normalmente versadas na técnica. O polímero substituído resultante a seguir sofre uma reação para substituir para a porção mais reativa uma porção azida na extremidade do polímero. Alternati-vamente, um polímero hidrossolúvel com pelo menos uma porção nucleofílica ou eletrofílica ativa sobre uma reação com um agente de ligação que tem uma porção azida em uma extremidade, de modo que uma ligação covalente é formada ente o polímero PEG e o agente de ligação e a porção azida é posicionada na extremidade do polímero. Porções nucleofílicas e eletrofílicas, incluindo aminas, tióis, hidrazidas, hidrazinas, alcoóis, carboxilatos, aldeídos, cetonas, tioésteres e semelhantes são conhecidas pelas pessoas normalmente versadas na técnica.
[00162]Mais especificamente, no caso do derivado PEG contendo acetileno, um polímero solúvel em água com pelo menos uma porção hidroxila sofre uma rea-ção para deslocar um halogênio ou outro grupo de saída ativado de um precursor que contém uma porção acetileno. Alternativamente, um polímero solúvel em água com pelo menos uma porção nucleofílica ou eletrofílica ativa sofre uma reação com um agente de ligação que tem um acetileno em uma extremidade de modo que uma ligação covalente é formada entre o polímero PEG e o agente de ligação e a porção acetileno são posicionados na extremidade do polímero. O uso de porções de halo- gênio, grupo de saída ativado, porções nucleofílicas e eletrofílicas no contexto da síntese orgânica e a preparação e uso dos derivados PEG é bem estabelecido para os profissionais da técnica.
[00163]A invenção também fornece um método para a modificação seletiva de proteínas para adicionar outras substâncias à proteína modificada incluindo, po-rém sem se limitar, aos polímeros solúveis em água tais como PEG e derivados PEG contendo uma porção azida ou acetileno. Os derivados PEG contendo azida e acetileno podem ser usados para modificar as propriedades das superfícies e molé-culas onde a biocompatibilidade, estabilidade, solubilidade e falta de imunogenicida- de são importantes, enquanto ao mesmo tempo fornecem um meio mais seletivo de ligar os derivados PEG às proteínas que foram anteriormente conhecidas na técnica. II.Fatores de Crescimento de Fibroblasto
[00164]Por causa de suas potentes atividades para promover o crescimento, proliferação, sobrevivência e diferenciação de uma ampla variedade de células e tipos celulares, FGFs continuam a ser procurados como agentes terapêuticos para uma variedade de diferentes indicações, incluindo cicatrização de feridas, tais como condições músculo-esqueléticas, por exemplo, fraturas ósseas, reparo de ligamento e tecido, tendinite, bursite, etc; condições de pele, por exemplo, queimaduras, cortes, lacerações, chagas de cama, úlceras de lenta cicatrização, etc; proteção tecidu- al, reparo e indução de angiogênese durante enfarte do miocárdio e isquemia, no tratamento de condições neurológicas, por exemplo, doença neurodegenerativa e apoplexia, no tratamento de doenças oculares, incluindo degeneração macular, e semelhantes.
[00165]AS proteínas do fator de crescimento de fibroblasto (FGF) identifica-das até o momento pertencem a uma família de moléculas de sinalização que regu-lam o crescimento e diferenciação de vários tipos celulares. A significância das pro-teínas FGF para a fisiologia e patologia humana se refere em parte aos seus papéis chave na embriogênese, no desenvolvimento de vasos sanguíneos e no crescimen-to, e no crescimento ósseo. Experimentos in vitro demonstraram que um papel para o FGF na regulação do crescimento celular e divisão de células endoteliais, células do músculo liso vasculares, fibroblastos e miócitos cardíacos e esqueléticos. Outros membros da família FGF e de seus papéis biológicos são descritos em Crossley et al., Development 121: 439-451 (1995); Ohuchi et al., Development 124: 2235-2244 (1997); Gemel et al., Genomics 35: 253-257 (1996); e Ghosh et al., Cell Growth and Differentiation 7:1425- 1434 (1996).
[00166]As proteínas FGF também são significativas para a saúde humana e doença devido a um papel no crescimento de células cancerígenas. Por exemplo, FGF-8 foi identificado como um fator de crescimento indutor de andrógeno em célu-las do câncer de próstata e mama. Tanaka et al., FEBS Lett. 363:226-230 (1995) e P.N.A.S. 89:8928-8932 (1992)).
[00167]O papel de FGF no desenvolvimento normal está sendo desvendado em parte através dos estudos dos receptores de FGF. Wilke, T. et al., Dev. Dynam. 210:41-52 (1997) descobriram que os transcritos FGFR1, FGFR2 e FGFR3 foram localizados em regiões específicas da cabeça durante o desenvolvimento embrioná-rio em galinhas. O padrão de expressão correlacionado com as áreas afetadas por modificações FGFR humanas na síndrome de Crouzon, uma condição de formação óssea intramembranosa anormal. Belluardo, N. et al., Jour. Comp. Neur. 379:226246 (1997) estudou a localização dos RNAms de FGFR 1, 2 e 3 no cérebro de rato, e encontraram especificidade celular em várias regiões cerebrais. Além disso, os RNAms FGFR1 e FGFR2 foram expressos em células reativas astrogliais depois da lesão cerebral, suportando um papel de certos FGFs na doença e injúria cerebral. Ozawa, K. et al., Mol. Brain Res. 41:279-288 (1996) reportou que a expressão de FGF1 e FGF-5 aumentou depois do nascimento, enquanto os genes FGF3, FGF-6, FGF-7 e FGF-8 mostraram uma expressão mais elevada nos estágios embrionários posteriores do que os estágios pós-natal. Um cofator, Klotho beta (Klb), pode também estar envolvido com a transdução de sinal do FGF-21 e seu receptor. Klb foi reportado por aumentar a capacidade de FGFR1 e FGFR4 de se ligar ao FGF21. Klb é uma proteína transmembranar de passagem única e embora o papel da forma transmembranar total seja desconhecido, foi demonstrado em relação ao FGF23 que Klotho aumentou a ligação de FGF23 e aumentou a fosforilação do receptor FGF enquanto que Klotho beta mostrou aumentar a ligação de FGF-21 (H. Kurosu, Y. Ogawa, M. Miyoshi, M. Yamamoto, A. Nandi, K. P. Rosenblatt, M. G. Baum, S. Schi- avi, M.-C. Hu, O. W. Moe, M. Kuro-o, Regulation of fibroblast growth factor-23 signa-ling by Klotho. J. Biol. Chem. 281, 6120-6123 (2006) aqui incorporado por referência).
[00168]Katoh et al. (International Journal of Oncology (2006) 29:163-168) descrevem a família FGF e a análise filogenética dos membros da família. Katoh et al. também discutem a rede da via de sinalização no trato gastrintestinal.
[00169]Plotnikov et al. (Cell (1999) 98:641-650) descrevem a estrutura crista-lina de FGF2 com o receptor FGF 1 (FGFR1) e o dímero simétrico de duas dobras que é formado ente dois desses complexos. Plotnikov et al. fornece um modelo para a dimerização do receptor e indução da dimerização por FGF e heparina.
[00170]Membros adicionais da família FGF são propensos a serem desco-bertos no futuro. Novos membros da família FGF podem ser identificados através de análise estrutural secundária e terciária auxiliada por computador das sequências de proteína previstas, e por técnicas de seleção projetadas para identificar moléculas que se ligam a um alvo particular.
[00171]Deste modo, a descrição da família FGF é fornecida para fins ilustra-tivos e somente a título de exemplo e não Omo limitante do escopo dos métodos, composições, estratégias e técnicas aqui descritas. Além disso, referência à FGF-21 neste pedido é tencionada a usar o termo genérico como um exemplo de qualquer membro da família FGF. Deste modo, se entende que as modificações e químicas aqui descritas com referência aos polipeptídeos ou proteína FGF-21 podem ser igualmente aplicadas a qualquer membro da família FGF, incluindo aqueles especifi-camente aqui listados. III.Métodos de Ácido Nucleico Recombinante Gerais para uso com a Inven-ção
[00172]Em várias modalidades da presente invenção, ácidos nucleicos codi-ficando um polipeptídeo FGF-21 de interesse serão isolados, clonados e geralmente alterados usando métodos recombinantes. Tais modalidades são usadas incluindo, porém sem se limitar, à expressão de proteínas ou durante a geração de variantes, derivados, cassetes de expressão ou outras sequências derivadas de um polipeptí- deo FGF-21. Em algumas modalidades, as sequências codificando os polipeptídeos da invenção são operativamente ligadas a um promotor heterólogo.
[00173]Uma sequência de nucleotídeo codificando um polipeptídeo FGF-21 compreendendo um aminoácido codificado não-naturalmente pode ser sintetizada com base na sequência de aminoácidos do polipeptídeo de origem incluindo, porém sem se limitar, a ter a sequência de aminoácidos mostrada nas SEQ ID Nos: 1 a 7 e a seguir alterar a sequência de nucleotídeos de modo a efetuar a introdução (isto é, incorporação ou substituição) ou remoção (isto é, eliminação ou substituição) do(s) resíduo(s) de aminoácido relevante(s). A sequência de nucleotídeos pode ser con-venientemente modificada por mutagênese direcionada a sítio de acordo com méto-dos convencionais. Alternativamente, a sequência de nucleotídeos pode ser prepa-rada por síntese química incluindo, porém sem se limitar, ao uso de um sintetizador de oligonucleotídeos, em que os oligonucleotídeos são modelados baseando-se na sequência de aminoácido do polipeptídeo desejado, e preferivelmente selecionando aqueles códons que são favorecidos na célula hospedeira na qual o polipeptídeo recombinante será produzido. Por exemplo, vários pequenos oligonucleotídeos que codificam porções do polipeptídeo desejado podem ser sintetizados e montados por PCR, ligação ou reação em cadeia de ligação. Ver, por exemplo, Barany, et al, Proc. Natl. Acad. Sci 88: 189-193 (1991); Patente Americana No. 6.521.427, os quais são incorporados aqui por referência.
[00174]Esta invenção utiliza técnicas rotineiras no campo da genética re- combinante. Textos básicos revelando os métodos gerais de uso nesta invenção incluem Sambrook et al., Molecular Cloning, A Laboratory Manual (3a Ed. 2001); Kri- egler, Gene Transfer and Expression: A Laboratory Manual (1990); e Current Proto-cols in Molecular Biology (Ausubel et al, eds., 1994)).
[00175]Textos gerais os quais descrevem técnicas de biologia molecular in-cluem Berger e Kimmel, Guide to Molecular Cloning Techniques, Methods in Enzvmology volume 152 Academic Press, Inc., São Diego, CA (Berger); Sambrook et al., Molecular Cloning - A Laboratory Manual (2a Ed.), Vol. 1-3, Cold Spring Harbor Laboratory, Cold Spring Harbor, Nova Iorque, 1989 ("Sambrook") e Current Protocols in Molecular Biology, F. M. Ausubel et al., eds., Current Protocols, a um empreendi-mento em conjunto entre Greene Publishing Associates, Inc. e John Wiley & Sons, Inc., (adicionado em 1999) (“Ausubel”)). Estes textos descrevem mutagênese, o uso de vetores, promotores e muitos outros tópicos relevantes relacionados com, e inclu-indo, porém sem se limitar, à geração dos genes ou polinucleotídeos que incluem códons seletores para a produção de proteínas que incluem aminoácido não- naturais, RNAts ortogonais, sintetases ortogonais e seus pares.
[00176]Vários tipos de mutagêneses são usadas na invenção para vários propósitos incluindo, porém sem se limitar, à produção de novas sintetases ou RNAts, à mutação de moléculas de RNAt, à mutação de polinucleotídeos que codifi-cam sintetases, à produção de bibliotecas de RNAts, à produção de bibliotecas de sintetases, à produção de códons seletores, à inserção de códons seletores que co-dificam aminoácido não-naturais em uma proteína ou polipeptídeo de interesse. Elas incluem, porém não estão limitadas, à mutagênese de ponto aleatório direcionada a sítio, recombinação homóloga, embaralhamento de DNA ou outros métodos de mu- tagênese recorrentes, construção quimérica, mutagênese usando moldes contendo uracila, mutagênese direcionada a oligonucleotídeo, mutagênese de DNA modifica-do por fosforotioato, mutagênese usando DNA duplex intervalado ou semelhantes, mutagênese mediada por PCT ou qualquer combinação desses. Métodos adequados adicionais incluem reparo de mau emparelhamento pontual, mutagênese usando cepas hospedeiras deficientes de reparo, restrição-seleção e restrição- purificação, mutagênese por eliminação, mutagênese por síntese de gene total, reparo de quebra de dupla fita e semelhantes. Mutagêneses incluindo, porém sem se limitar, ao envolvimento de constructos quiméricos, também são incluídas na presente invenção. Em uma modalidade, a mutagênese pode ser orientada por informações conhecidas da molécula de ocorrência natural ou molécula de ocorrência natural alterada ou modificada incluindo, porém sem se limitar, às sequências, comparações de sequência, propriedades físicas, estrutura secundária, terciária ou quaternária, estrutura cristalina ou semelhantes.
[00177]Os textos e exemplos aqui encontrados descrevem esses procedi-mentos. Informações adicionais são encontradas nas seguintes publicações e refe-rências citadas em: Ling et al., Approaches to DNA mutagenesis: an overview, Anal Biochem. 254(2): 157-178 (1997); Dale et al., Oligonucleotide-directed random mu-tagenesis using the phosphor othioate method, Methods Mol. Biol. 57:369-374 (1996); Smith, In vitro mutagenesis, Ann. Rev. Genet. 19:423-462 (1985); Botstein & Shortle, Strategies and applications of in vitro mutagenesis, Science 229:1193-1201 (1985); Carter, Site-directed mutagenesis, Biochem. J. 237:1-7 (1986); Kunkel, The efficiency of oligonucleotide directed mutagenesis, in Nucleic Acids & Molecular Biology (Eckstein, F. and Lilley, D.M.J, eds., Springer Verlag, Berlin) (1987); Kunkel, Rapid and efficient site-specific mutagenesis without phenotypic selection, Proc. Natl. Acad. Sci. USA 82:488-492 (1985); Kunkel et al., Rapid and efficient site-specific mutagenesis without phenotypic selection, Methods in Enzymol. 154, 367-382 (1987); Bass et al., Mutant Trp repressors with new DNA-binding specificities, Science 242:240-245 (1988); Zoller & Smith, Oligonucleotide-directed mutagenesis using M13-derived vectors: an efficient and general procedure for the production of point mutations in any DNA fragment, Nucleic Acids Res. 10:6487-6500 (1982); Zoller & Smith, Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors, Methods in Enzymol. 100: 468-500 (1983); Zoller & Smith, Oligonucleotide- directed mutagenesis: a simple method using two oligonucleotide primers and a single-stranded DNA template, Methods in Enzymol. 154:329-350 (1987); Taylor et al., The use of phosphorothioate-modified DNA in restriction enzyme reactions to prepare nicked DNA, Nucl. Acids Res. 13: 8749-8764 (1985); Taylor et al., The rapid generation of oligonucleotide-directed mutations at high frequency using phos- phorothioate-modified DNA, Nucl. Acids Res. 13: 8765-8785 (1985); Nakamaye & Eckstein, Inhibition of restriction endonuclease Nci I cleavage by phosphorothioate groups and its application to oligonucleotide-directed mutagenesis, Nucl. Acids Res. 14: 9679-9698 (1986); Sayers et al., 5'-3' Exonucleases in phosphorothioate-based oligonucleotide-directed mutagenesis, Nucl. Acids Res. 16:791-802 (1988); Sayers et al., Strand specific cleavage of phosphor othioate-containing DNA by reaction with restriction endonucleases in the presence ofethidium bromide, (1988) Nucl. Acids Res. 16: 803-814; Kramer et al., The gapped duplex DNA approach to oligonucleo- tide-directed mutation construction, Nucl. Acids Res. 12: 9441-9456 (1984); Kramer & Fritz Oligonucleotide-directed construction of mutations via gapped duplex DNA, Methods in Enzymol. 154:350-367 (1987); Kramer et al., Improved enzymatic in vitro reactions in the gapped duplex DNA approach to oligonucleotide-directed construc tion of mutations, Nucl. Acids Res. 16: 7207 (1988); Fritz et al., Oligonucleotide- directed construction of mutations: a gapped duplex DNA procedure without enzy-matic reactions in vitro, Nucl. Acids Res. 16: 6987-6999 (1988); Kramer et al., Differ-ent base/base mismatches are corrected with different efficiencies by the methyl- directed DNA mismatch-repair system of E. coli, Cell 38:879-887 (1984); Carter et al., Improved oligonucleotide site-directed mutagenesis using M13 vectors, Nucl. Acids Res. 13: 4431-4443 (1985); Carter, Improved oligonucleotide-directed mutagenesis using M13 vectors, Methods in Enzymol. 154: 382-403 (1987); Eghtedarzadeh & Henikoff, Use of oligonucleotides to generate large deletions, Nucl. Acids Res. 14: 5115 (1986); Wells et al., Importance of hydrogen-bond formation in stabilizing the transition state of subtilisin, Phil. Trans. R. Soc. Lond. A 317: 415- 423 (1986); Nam- biar et al., Total synthesis and cloning of a gene coding for the ribonuclease S pro-tein, Science 223: 1299-1301 (1984); Sakmar e Khorana, Total synthesis and ex-pression of a gene for the alpha-subunit of bovine rod outer segment guanine nucleotide-binding protein (transducin), Nucl. Acids Res. 14: 6361-6372 (1988); Wells et al., Cassette mutagenesis: an efficient method for generation of multiple mutations at defined sites, Gene 34:315-323 (1985); Grundstrom et al., Oligonucleotide-directed mutagenesis by micros vale ‘shot-gun’ gene synthesis, Nucl. Acids Res. 13: 33053316 (1985); Mandecki, Oligonucleotide-directed double- strand break repair in plasmids of Escherichia coli: a method for site-specific mutagenesis, Proc. Natl. Acad. Sci. USA. 83:7177-7181 (1986); Arnold, Protein engineering for unusual environments, Current Opinion in Biotechnology 4:450-455 (1993); Sieber, et al., Nature Biotechnology, 19:456-460 (2001); W. P. C. Stemmer, Nature 370, 389-91 (1994); e, I. A. Lorimer, I. Pastan, Nucleic Acids Res. 23, 3067-8 (1995). Detalhes adicionais de muitos dos métodos acima podem ser encontrados em Methods in Enzymology, volume 154, os quais também descrevem controles úteis para problemas de diagnóstico com vários métodos de mutagênese.
[00178]Oligonucleotídeos, por exemplo, para uso na mutagênese da presen-te invenção, por exemplo, para modificar bibliotecas de sintetases ou alterar RNAts, são tipicamente sintetizados quimicamente de acordo com a método do triéster de fosforoamidita em fase sólida descrito por Beaucage e Caruthers, Tetrahedron Letts. 22(20): 1859-1862, (1981), por exemplo, usando um sintetizador automático, con-forme descrito em Needham-VanDevanter et al., Nucleic Acids Res., 12:6159-6168 (1984).
[00179]A invenção também se refere às células hospedeiras eucarióticas, células hospedeiras não-eucarióticas e organismos para a incorporação in vivo de um aminoácido natural através dos pares RNAt/RS ortogonais. Células hospedeiras são geralmente projetadas (incluindo, porém sem se limitar, a células transformadas, transduzidas ou transfectadas) com os polinucleotídeos da invenção ou constructos os quais incluem um polinucleotídeo da invenção incluindo, porém sem se limitar, a um vetor da invenção, o qual pode ser, por exemplo, um vetor de clonagem ou um vetor de expressão. Por exemplo, as regiões codificadoras para o RNAt ortogonal, o RNAt sintetase ortogonal e a proteína a ser derivada são operativamente ligadas aos elementos de controle de expressão gênica que são funcionais na célula hospedeira desejada. O vetor pode estar, por exemplo, na forma de um plasmídeo, um cosmí- deo, um fago, uma bactéria, um vírus, um polinucleotídeo nu ou um polinucleotídeo conjugado. Os vetores são introduzidos nas células e/ou microrganismo por métodos padrões incluindo eletroporação (Fromm et al., Proc. Natl. Acad. Sci. USA 82, 5824 (1985)), infecção por vetores virais, penetração balística de alta velocidade por pe-quenas partículas com o ácido nucleico, ou na matriz de pérolas ou partículas pe-quenas, ou na superfície (Klein et al., Nature 327, 70-73 (1987)), e/ou semelhantes.
[00180]As células hospedeiras projetadas podem ser cultivadas em meio nu-triente convencional modificado conforme apropriado para tais atividades como, por exemplo, passos de varredura, ativação de promotores ou seleção de transforman- tes. Essas células podem ser opcionalmente cultivadas em organismos transgêni- cos. Outras referências úteis incluindo, porém sem se limitar, ao isolamento e cultura celular (por exemplo, para isolamento de ácido nucleico subsequente) incluem Freshney (1994) Culture of Animal Cells, a Manual of Basic Technique, terceira edi- ção, Wiley-Liss, Nova Iorque e as referências ali citadas; Payne et al. (1992) Plant Cell and Tissue Culture in Liquid Systems John Wiley & Sons, Inc. Nova Iorque, NY; Gamborg e Phillips (eds.) (1995) Plant Cell, Tissue and Organ Culture; Fundamental Methods Springer Lab Manual, Springer-Verlag (Berlin Heidelberg Nova Iorque) e Atlas e Parks (eds.) The Handbook of Microbiological Media (1993) CRC Press, Boca Raton, FL.
[00181]Vários métodos bem conhecidos de introdução de ácidos nucleicos alvos em células são disponíveis, qualquer um dos quais podendo ser usado na in-venção. Esses incluem: fusão das células receptoras com protoplastos bacteriano contendo o DNA, eletroporação, bombardeamento com projétil e infecção com veto-res virais (discutidos adicionalmente abaixo), etc. Células bacterianas podem ser usadas para amplificar a quantidade de plasmídeo contendo constructos de DNA desta invenção. As bactérias crescem até a fase log e os plasmídeos na bactéria podem ser isolados por vários métodos conhecidos na técnica (ver, por exemplo, Sambrook). Além disso, kits são comercialmente disponíveis para a purificação de plasmídeos de bactérias (ver, por exemplo, EasyPrep™, FlexiPrep™, ambos de Pharmacia Biotech; StrataClean™ de Stratagene; e, QIAprep™ de Qiagen). Os plasmídeos isolados e purificados são então adicionalmente manipulados para pro-duzir outros plasmídeos, usados para transfectar células ou incorporados em vetores relacionados para infectar organismos. Vetores típicos contêm terminadores de transcrição e tradução, sequências de iniciação de transcrição e tradução e promoto-res úteis para a regulação da expressão do ácido nucleico alvo particular. Os vetores compreendem opcionalmente cassetes de expressão genéricos contendo pelo me-nos uma sequência terminadora independente, sequências que permitam a replica- ção do cassete nos eucariotos ou procariotos, ou ambos (incluindo, porém sem se limitar, aos vetores de transferência) e marcadores de seleção para sistemas tanto procarióticos quanto eucarióticos. Vetores são adequados para a replicação e inte-gração em procariotos, eucariotos ou ambos. Ver Gillam & Smith, Gene 8:81 (1979); Roberts, et al, Nature. 328:731 (1987); Schneider, E., et al, Protein Expr. Purif. 6(l):10-14 (1995); Ausubel, Sambrook, Berger (todos acima). Um catálogo de bacté-rias e bacteriófagos úteis para clonagem é fornecido, por exemplo, por ATCC, por exemplo, The ATCC Catalogue of Bacteria and Bacteriophage (1992) Gherna et al. (eds) publicado por ATCC. Procedimentos básicos adicionais para o sequenciamen- to, clonagem e ouros aspectos de biologia molecular e subjacentes às considerações teóricas são também encontrados em Watson et al. (1992) Recombinant DNA Second Edition Scientific American Books, NY. Além disso, essencialmente qualquer ácido nucleico (e virtualmente qualquer ácido nucleico marcado, quer seja padrão ou não-padrão) pode ser solicitado sob encomenda ou de modo usual de qualquer uma dentre uma variedade de fontes comerciais, tais como a Midland Certified Reagent Company (Midland, TX disponível na Rede Mundial de Computadores em mcrc.com), The Great American Gene Company (Ramona, CA disponível na Rede Mundial de Computadores em genco.com), ExpressGen Inc. (Chicago, IL disponível na Rede Mundial de Computadores em expressgen.com), Operon Technologies Inc. (Alameda, CA) e muitas outras. CÓDONS SELETORES
[00182]Códons seletores da invenção expandem a estrutura do códon gené-tica da maquinaria biossintética da proteína. Por exemplo, um códon seletor inclui, porém não está limitado, a um códon de três bases único, um códon sem sentido, tal como um códon de parada incluindo, porém sem se limitar, a um códon âmbar (UAG), um códon ocre ou um códon opala (UGA), um códon artificial, um códon com quatro ou mais bases, um códon raro ou semelhantes. É prontamente aparente para as pessoas normalmente versadas na técnica que existe uma ampla variação na quantidade de códons seletores que podem ser introduzidos em um gene ou polinu- cleotídeo desejado incluindo, porém sem se limitar, a um ou mais, dois ou mais, três ou mais, 4, 5, 6, 7, 8, 9, 10 ou mais em um único polinucleotídeo codificando pelo menos uma porção do polipeptídeo FGF-21.
[00183]Em uma modalidade, os métodos envolvem o uso de um códon sele- tor que é um códon de parada para a incorporação de um ou mais dos aminoácidos não-naturais in vivo. Por exemplo, um O-RNAt é produzido o qual reconhece o có- don de parada incluindo, porém sem se limitar, a UAG, e é aminoacilado por um O- RS com um aminoácido artificial desejado. Este O-RNAt não é reconhecido pelas aminoacil-RNAt sintetases do hospedeiro que ocorrem naturalmente. Mutagênese direcionada a sítio convencional pode ser usada para introduzir o códon de parada incluindo, porém sem se limitar, ao TAG, no sítio de interesse em um polipeptídeo de interesse. Ver, por exemplo, Sayers, J.R., et al. (1988), 5’-3’ Exonucleases in phos- phorothioate-based oligonucleotide-directed mutagenesis. Nucleic Acids Res, 16:791-802. Quando o O-RS, O-RNAt e o ácido nucleico que codifica o polipeptídeo de interesse são combinados in vivo, o aminoácido artificial é incorporado em res-posta ao códon UAG para produzir um polipeptídeo contendo o aminoácido artificial na posição especificada.
[00184]A incorporação de aminoácido não-natural in vivo pode ser feita sem perturbação significativa da célula hospedeira eucariótica. Por exemplo, devido ao fato da eficiência de supressão para o códon UAG depender da competição entre o O-RNAt incluindo, porém sem se limitar, ao RNAt supressor âmbar, e um fator de liberação eucariótico (incluindo, porém sem se limitar, ao eRF) (o qual se liga a um códon de parada e inicia a liberação do peptídeo de crescimento do ribossomo), a eficiência da supressão pode ser modulada por, incluindo, porém sem se limitar, ao aumento do nível de expressão de O-RNAt, e/ou o RNAt supressor.
[00185]Aminoácido não-naturais também pode ser codificados com códons raros. Por exemplo, quando a concentração de arginina em uma reação de síntese de proteína in vitro é reduzida, o códon de arginina rara, AGG, demonstrou ser efici-ente para inserção de Ala por um RNAt sintético acilado com alanina. Ver, por exemplo, Ma et al, Biochemistry, 32:7939 (1993). Neste caso, o RNAt sintético com-pete com p RNAtArg de ocorrência natural, o qual existe como uma espécie secun-dária em Escherichia coli. Alguns organismos não usam todos os códons triplete. Um códon AGA não-atribuído em Micococcus luteus foi utilizado para inserção dos ami- noácidos em um extrato de transcrição/tradução in vitro. Ver, por exemplo, Kowal e Oliver, Nucl. Acid. Res., 25: 4685 (1997). Componentes da presente invenção podem ser gerados para usar esses códons raros in vivo.
[00186]Códons seletores também compreendem códons prolongados inclu-indo, porém sem se limitar, a quatro ou mais códons de base, tais como quatro, cinco, seis ou mais códons de base. Exemplos de códons com quatro bases incluem, porém não estão limitados, a AGGA, CUAG, UAGA, CCCU e semelhantes. Exemplos de códons com cinco bases incluem, porém não estão limitados, a AGGAC, CCCCU, CCCUC, CUAGA, CUACU, UAGGC e semelhantes. Uma característica da invenção inclui o uso de códons prolongados baseando-se na supressão de frameshift. Códons de quatro ou mais bases podem inserir incluindo, porém sem se limitar, a um ou mais aminoácido não-naturais múltiplos na mesma proteína. Por exemplo, na presença de O-RNAts modificados incluindo, porém sem se limitar, a RNAts su-pressores de frameshift especiais, com alças de anti-códons, por exemplo, com alças de anti-códon com pelo menos 8 a 10 nt, o códon com quatro ou mais bases está pronto como um único aminoácido. Em outras modalidades, as alças anti-códon podem codificar, incluindo, porém sem se limitar, a um códon com quatro bases, pelo menos um códon com cinco bases ou pelo menos um códon com seis bases ou mais. Uma vez que existem 256 códons com quatro bases possíveis, vários aminoá- cidos não-naturais podem ser codificados na mesma célula usando um códon com quatro ou mais bases. Ver Anderson et al., (2002) Exploring the Limits of Codon and Anticodon Size, Chemistry and Biology, 9:237-244; Magliery, (2001) Expanding the Genetic Code: Selection of Efficient Suppressors of Four-base Codons and Identifi-cation of "Shifty" Four-base Codons with a Library Approach in Escherichia coli, J. Mol. Biol. 307: 755-769.
[00187]Por exemplo, códons com quatro bases foram usados para incorporar aminoácidos não-naturais em proteínas usando métodos biossintéticos in vitro. Ver, por exemplo, Ma et al., (1993) Biochemistry. 32:7939; e Hohsaka et al., (1999) J. Am. Chem. Soc, 121:34. CGGG e AGGU foram usados para incorporar simultaneamente 2-naftilalanina e um derivado NBD da lisina em estreptavidina in vitro com dois RNAts supressores de frameshift quimicamente acilados. Ver, por exemplo, Hohsaka et al., (1999) J. Am. Chem. Soc, 121 :12194. Em um estudo in vivo, Moore et al. examinaram a capacidade de derivados RNAtLeu com anticódons NCUA su-primirem códons UAGN (N pode ser U, A, G ou C) e descobriram que o quadruplete UAGA pode ser decodificado por uma RNAtLeu com um anticódon UCUA com uma eficiência de 13 a 26% com pouca decodificação na estrutura 0 ou -1. Ver Moore et al., (2000) J. Mol. Biol., 298:195. Em uma modalidade, códons prolongados com base em códons raros ou em códons sem sentido podem ser usados na presente in-venção, os quais podem reduzir a leitura sem sentido e a supressão de frameshift em outros sítios indesejados.
[00188]Para um dado sistema, um códon seletor também pode incluir um três códons de bases naturais, onde o sistema endógeno não usa (ou raramente usa) o códon de base natural. Por exemplo, este inclui um sistema que está faltando um RNAt que reconhece o códon com três bases natural e/ou um sistema onde o códon com três bases é um códon raro.
[00189]Códons seletores opcionalmente incluem pares de bases artificiais. Estes pares de bases artificiais ainda expandem o alfabeto genético existente. Um par de bases extra aumenta a quantidade de códons triplete de 64 para 125. Propri-edades do terceiro par de bases incluem o pareamento de bases estável e eficaz, a incorporação enzimática eficiente no DNA com alta fidelidade por uma polimerase, e o prolongamento do iniciador continuado eficiente depois da síntese do par de bases artificial nascente. Descrições dos pares de bases artificiais, as quais podem ser adaptadas para os métodos e composições incluem, por exemplo, Hirao, et al., (2002) An unnatural base pair for incorporating amino acid analogues into protein, Nature Biotechnology, 20:177-182. Ver também, Wu, Y., et al., (2002) J. Am. Chem. Soc. 124: 14626-14630. Outras publicações relevantes estão listadas abaixo.
[00190]Para o uso in vivo, o nucleosídeo artificial é permeável à membrana e é fosforilado para formar o trifosfato correspondente. Além disso, a informação gené-tica aumentada é estável e não destruída por enzimas celulares. Esforços anteriores de Brenner e outros tiraram vantagem dos padrões de ligação de hidrogênio que são diferentes daqueles nos pares canônicos Watson-Crick, o exemplo mais notável sendo o par ISO-C:ISO-G. Ver, por exemplo, Switzer et al., (1989) J. Am. Chem. Soc, 111 :8322; e Piccirilli et al., (1990) Nature, 343:33; Kool, (2000) Curr. Opin. Chem. Biol., 4:602. Essas bases geralmente desemparelham em algum grau com as bases naturais e não podem ser enzimaticamente replicadas. Kool e colaboradores demonstraram que interação de empacotamento hidrofóbica entre as bases pode substituir a ligação de hidrogênio para guiar a formação do par de bases. Ver Kool, (2000) Curr. Opin. Chem. Biol., 4:602; e Guckian e Kool, (1998) Angew. Chem. Int. Ed. Engl, 36, 2825. Em um esforço para desenvolver um par de bases artificial que satisfaça todos os requisitos acima, Schultz, Rosemberg e colaboradores sintetiza-ram sistematicamente e estudaram várias bases hidrofóbicas artificiais. Um auto-par PICS:PICS foi considerado como sendo mais estável do que os pares de bases na-turais, e pode ser eficientemente incorporado no DNA pelo fragmento Klenow da DNA polimerase I de Escherichia coli (KF). Ver, por exemplo, McMinn et al., (1999) J. Am. Chem. Soc 121 :11585-6; e Ogawa et al., (2000) J. Am. Chem. Soc, 122:3274. Um auto-par 3MN:3MN pode ser sintetizado por KF com eficiência e seletividade suficientes para a função biológica. Ver, por exemplo, Ogawa et al., (2000) J. Am. Chem. Soc., 122: 8803. Entretanto, ambas as bases atuam como um termi- nador de cadeia para replicação posterior. Uma DNA polimerase mutante foi recentemente desenvolvida que pode ser usada para replicar o auto par PICS. Além disso, um auto par 7AI pode ser replicado. Ver, por exemplo, Tae et al., (2001) J. Am. Chem. Soc, 123:7439. Um novo par de metalobase, Dipic:Py, também foi desenvolvido, o qual forma um par estável na ligação ao Cu(II). Ver Meggers et al., (2000) J. Am. Chem. Soc. 122:10714. Devido ao fato dos códons prolongados e códons artificiais serem intrinsecamente ortogonais aos códons naturais, os métodos da invenção podem tirar vantagem desta propriedade para gerar RNAts ortogonais para eles.
[00191]Um sistema de passagem secundária de tradução pode também ser usado para incorporar um aminoácido artificial em um polipeptídeo desejado. Em um sistema de passagem secundária de tradução, uma sequência grande é incorporada em um gene, porém não é traduzida em proteína. A sequência contém uma estrutura que serve como uma sugestão para induzir o ribossomo a saltar pela sequência e reiniciar a tradução à jusante da inserção.
[00192]Em certas modalidades, a proteína ou polipeptídeo de interesse (ou porção sua) nos métodos e/ou composições da invenção é codificada por um ácido nucleico. Tipicamente, o ácido nucleico compreende pelo menos um códon seletor, pelo menos dois códons seletores, pelo menos três códons seletores, pelo menos quatro códons seletores, pelo menos cinco códons seletores, pelo menos seis có- dons seletores, pelo menos sete códons seletores, pelo menos oito códons seleto- res, pelo menos nove códons seletores, dez ou mais códons seletores.
[00193]Genes codificados para as proteínas ou polipeptídeos de interesse podem ser modificados usando métodos conhecidos por uma pessoa versada na técnica e aqui descritos para incluir, por exemplo, um ou mais códons seletores para a incorporação de um aminoácido artificial. Por exemplo, um ácido nucleico para uma proteína de interesse é modificado para incluir um ou mais códons seletores, sustentando a incorporação de um ou mais aminoácido não-naturais. A invenção inclui qualquer tal variante incluindo, porém sem se limitar, aos mutantes, versões de qualquer proteína, por exemplo, incluindo pelo menos um aminoácido artificial. Se-melhantemente, a invenção também inclui ácidos nucleicos correspondentes, isto é, um ácido nucleico com um ou mais códons seletores que codifica um ou mais ami- noácido não-naturais.
[00194]Moléculas de ácido nucleico codificando uma proteína de interesse, tal como o polipeptídeo FGF-21 pode ser prontamente modificado para introduzir uma cistina em qualquer posição desejada do polipeptídeo. A cisteína é amplamente usada para introduzir moléculas reativas, polímeros hidrossolúveis, proteínas ou uma ampla variedade de outras moléculas em uma proteína de interesse. Métodos adequados para a incorporação da cisteína em uma posição desejada de um poli- peptídeo são conhecidos por uma pessoa normalmente versada na técnica, tais co mo aqueles descritos na Patente Americana No. 6.608.183, o qual é incorporado aqui por referência, e técnicas de mutagênese padrões. IV.Aminoácidos Codificados Artificialmente
[00195]Uma variedade muito ampla de aminoácidos codificados artificial-mente é adequada para o uso na presente invenção. Qualquer variedade de amino- ácidos codificados artificialmente pode ser introduzida em um polipeptídeo FGF-21. Em geral, os aminoácidos codificados artificialmente introduzidos são substancial-mente quimicamente inertes para os 20 aminoácidos comuns geneticamente codifi-cados (isto é, alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, áci-do glutâmico, glicina, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina e valina). Em algumas modalidades, os ami- noácidos codificados artificialmente incluem grupos funcionais de cadeias laterais que reagem eficientemente e seletivamente com grupos funcionais não encontrados nos 20 aminoácidos comuns (incluindo, porém sem se limitar, aos grupos azido, ce- tona, aldeído e aminóxi) para formar conjugados estáveis. Por exemplo, um polipep- tídeo FGF-21 que inclui um aminoácido de ocorrência não-natural contendo um grupo funcional azido pode reagir com um polímero (incluindo, porém sem se limitar, a (poli)etilenoglicol, ou alternativamente, um segundo polipeptídeo contendo uma porção alquino para formar um conjugado estável resultando para a reação seletiva da azida e os grupos alquino funcionais para formar um produto de cicloadição de Huisgen [3+2].
[00197]Um aminoácido codificado não-naturalmente é tipicamente qualquer estrutura com a fórmula listada acima, em que o grupo R é qualquer substituinte diferente daquele usado nos vinte aminoácidos naturais, e pode ser adequado para uso na presente invenção. Devido ao fato dos aminoácidos codificados artificialmente da invenção diferirem tipicamente dos aminoácidos naturais somente na estrutura da cadeia lateral, os aminoácidos codificados artificialmente formam ligações amida com outros aminoácidos incluindo, porém sem se limitar, a um codificado naturalmente ou artificialmente, da mesma forma na qual eles são formados em polipeptí- deos de ocorrência natural. Entretanto, os aminoácidos não-naturalmente codificados têm grupos de cadeias laterais que os distinguem dos aminoácidos naturais. Por exemplo, R compreende opcionalmente um grupo alquil, aril, acil, ceto, azido, hidro- xila, hidrazina, ciano, halo, hidrazida, alquenil, alquinil, éter,tiol, seleno, sulfonil, borato, boronato, fosfo, fosfono, fosfina, heterocíclico, enona, imina, aldeído, éster, tioá- cido, hidroxilamina, amino ou semelhante ou qualquer combinação desses. Outros aminoácidos de ocorrência natural de interesse que podem ser adequados para o uso na presente invenção incluem, porém não estão limitados, aos aminoácidos compreendendo um reticulador fotoativável, aminoácidos marcados por rotação, aminoácidos fluorescentes, aminoácidos de ligação a metal, aminoácidos contendo metais, aminoácidos radioativos, aminoácidos com novos grupo funcionais, aminoá- cidos que interagem covalentemente ou não-covalentemente com outras moléculas, fotoaprisionadas e/ou aminoácidos fotoisomerizáveis, aminoácidos compreendendo biotina ou um análogo de biotina, aminoácidos glicosilados tal como uma serina substituída com açúcar, outros aminoácidos modificados com carboidrato, aminoáci- dos contendo ceto, aminoácidos compreendendo polietilenoglicol ou poliéter, amino- ácidos substituídos com átomos pesados, aminoácidos quimicamente cliváveis e/ou fotocliváveis, aminoácidos com cadeias laterais alongadas em comparação com aminoácidos naturais, porém sem se limitar, aos poliéteres de hidrocarbonetos de cadeia longa incluindo, porém sem se limitar, a mais do que cerca de 5 ou mais do que cerca de 10 carbonos, aminoácidos contendo açúcar ligado ao carbono, amino- ácidos com atividade redox, aminoácidos contendo aminotioácido e aminoácidos compreendendo uma ou mais porções tóxicas.
[00198]Aminoácidos artificialmente codificados exemplares que podem ser adequados para uso na presente invenção e que são úteis para as reações com po-límeros hidrossolúveis incluem, porém não estão limitados, àqueles com grupos rea-tivos carbonil, aminóxi, hidrazina, hidrazida, semicarbazida, azida e alquino. Em al-gumas modalidades, aminoácidos artificialmente codificados compreendem uma porção sacarídica. Exemplos de tais aminoácidos incluem N-acetil-L-glicosaminil-L- serina, N- acetil-L-galactosaminil-L-serina, N-acetil-L-glicosaminil-L-treonina, N- acetil-L- glicosaminil-L-asparagina e O-manosaminil-L-serina. Exemplos de tais ami- noácidos também incluem exemplos onde a ligação com N ou O de ocorrência natu-ral entre o aminoácido e o sacarídeo é substituída por uma ligação covalente não encontrada comumente na natureza - incluindo, porém sem se limitar, a um alque- no, oxima, tioéter, uma amida e semelhantes. Exemplos de tais aminoácidos também incluem sacarídeos que não são comumente encontrados nas proteínas de ocorrência natural, tais como 2-desoxiglicose, 2-desoxigalactose e semelhantes.
[00199]Muitos dos aminoácidos artificialmente codificados aqui fornecidos são comercialmente disponíveis, por exemplo, de Sigma-Aldrich (St. Louis, MO, EUA), Novabiochem (uma divisão de EMD Biosciences, Darmstadt, Alemanha), ou Peptech (Burlington, MA, EUA). Aqueles que não são comercialmente disponíveis são opcionalmente sintetizados conforme aqui fornecido ou usando métodos padrão conhecidos pelas pessoas normalmente versadas na técnica. Para técnicas de sín-tese orgânica ver, por exemplo, Organic Chemistry de Fessendon e Fessendon, (1982, Segunda Edição, Willard Grant Press, Boston Mass.); Advanced Organic Chemistry por March (Terceira Edição, 1985, Wiley and Sons, Nova Iorque); e Ad-vanced Organic Chemistry por Carey e Sundberg (Terceira Edição, Partes A e B, 1990, Plenum Press, Nova Iorque). Ver também as Patentes Americanas Nos. 7.045.337 e 7.083.970, as quais são aqui incorporadas por referência. Além dos aminoácido não-naturais que contêm novas cadeias laterais, aminoácido não- naturais que podem ser adequados para uso na presente invenção também com- preendem opcionalmente estruturas de suporte modificadas incluindo, porém sem se limitar, às estruturas ilustradas pelas Fórmulas II e III: em que Z tipicamente compreende OH, NH2, SH, NH-R', ou S-R'; X e Y, os quais podem ser iguais ou diferentes, tipicamente compreendem S ou O, e R e R’; os quais são opcionalmente iguais ou diferentes, são tipicamente selecionados da mesma lista de constituintes para o grupo R descrito acima para os aminoácido não- naturais de Fórmula I, assim como hidrogênio. Por exemplo, aminoácidos não- naturais da invenção opcionalmente compreendem substituições no grupo amino ou carboxil conforme ilustrado pelas Fórmulas II e III. Aminoácidos não-naturais desse tipo incluem, porém não estão limitados, aos a-hidroxiácidos a-tioácidos, a- aminotiocarboxilatos incluindo, porém sem se limitar, a com cadeias laterais corres-pondendo aos vinte aminoácidos naturais comuns ou às cadeias laterais artificiais. Além disso, substituintes no carbono a incluem, porém não estão limitados, aos aminoácidos L, D o a-a-dissubstituídos tais como D-glutamato, D-alanina, D-metil-O- tirosina, ácido aminobutírico e semelhante. Outras alternativas estruturais incluem aminoácidos cíclicos, tais como análogos da prolina, assim como análogos do anel prolina com 3, 4, 6, 7, 8 ou 9 membros, β e y-aminoácidos, tal como β-alanina substi-tuída e ácido y-aminobutírico.
[00200]Muitos aminoácidos não-naturais são à base de aminoácidos natu-rais, tais como tirosina, glutamina, fenilalanina e semelhantes, e são adequados para uso na presente invenção. Análogos de tirosina incluem, porém não estão limitados, às tirosinas para-substituídas, tirosinas orto-substituídas e tirosinas meta- substituídas,onde a tirosina substituída compreende, incluindo porém sem se limitar, a um grupo ceto (incluindo, porém sem se limitar, a um grupo acetil), um grupo ben-zoil, um grupo amino, uma hidrazina, hidroxiamina, um grupo tiol, um grupo carbóxi, um grupo isopropil,um grupo metil, uma cadeia linear ou hidrocarboneto ramificado de C6 a C20, um hidrocarboneto saturado ou insaturado, um grupo O-metil, um grupo poliéter, um grupo nitro, um grupo alquinil ou semelhante. Além disso, uma variedade de anéis aril substituídos também é contemplada. Análogos de glutamina que podem ser adequados para uso na presente invenção incluem, porém não estão limitados, a derivados a-hidróxi, derivados y-substituídos, derivados cíclicos e deriva-dos de glutamina substituída com amida. Análogos de fenilalaina exemplares que podem ser adequados para uso na presente invenção incluem, porém não estão li-mitados, às fenilalaninas para-substituídas, fenilalaninas orto-substituídas e fenilala- ninas meta-substituídas, onde o substituinte compreende, incluindo, porém sem se limitar, a um grupo hidróxi, um grupo metóxi, alil, aldeído, azido, iodo, bromo, ceto (incluindo, porém sem se limitar, a um grupo acetil), benzoil, alquinil ou semelhante. Exemplos específicos de aminoácido não-naturais que podem ser adequados para uso na presente invenção incluem, porém não estão limitados, a p-acetil-L- fenilalanina, O-metil-L-tirosina, L-3-(2-naftil)alanina, 3-metilfenilalanina e O-4-alil-L- tirosina, 4-propil-L-tirosina, tri-O-acetil-GlcNAcβ-serina, L-dopa, fenilalanina fluorada, isopropil-L-fenilalanina, p-azido-L-fenilalanina, p-acil-L-fenilalanina, p-benzoil-L- fenilalanina, L-fosfosserina, fosfonosserina, fosfonotirosina, p-iodofenilalanina, p- bromofenilalanina, p-amino-L-fenilalanina, isopropil-L-fenilalanina, p- proprgiloxifenilalanina e semelhantes. Exemplos de estruturas de uma variedade de aminoácido não-naturais que podem ser adequados para uso na presente invenção são fornecidos, por exemplo, em WO 2002/085923, intitulado “In vivo incorporation of unnatural amino acids.” Ver também Kiick et al., (2002) Incorporation of azides into recombinant proteins for chemoselective modification by the Staudinger ligation, PNAS 99:19-24, o qual é aqui incorporado por referência, para outros análogos de metionina. O Pedido Internacional No. PCT/US06/47822, intitulado “Compositions Containing, Methods Involving, and Uses of Non-natural Amino Acids and Polypepti-des”, o qual é aqui incorporado por referência, descreve a alquilação redutiva de porções aminoaromáticas incluindo, porém sem se limitar, a p-aminofenilalanina em aminação redutiva.
[00201]Em uma modalidade, composições de um polipeptídeo FGF-21 que incluem um aminoácido artificial (tal como p-(propargilóxi)-fenilalanina) são forneci-das. Várias composições compreendendo p-(propargilóxi)-fenilalanina e, incluindo, porém sem se limitar, às proteínas e/ou células, também são fornecidas. Em um as-pecto, uma composição que inclui o aminoácido p-(propargilóxi)-fenilalanina artificial também inclui um RNAt ortogonal. O aminoácido artificial pode estar ligado (incluin-do, porém sem se limitar, a ligação covalente) ao RNAt ortogonal, incluindo, porém sem se limitar, a estar covalentemente ligado ao RNAt ortogonal por meio de uma ligação aminoacil, covalentemente ligado a um 3’OH ou 2’OH de um açúcar ribose terminal do RNAt ortogonal, etc.
[00202]As porções químicas através de aminoácido não-naturais que podem ser incorporadas nas proteínas oferecem uma variedade de vantagens e manipula-ções da proteína. Por exemplo, a única reatividade de um grupo ceto funcional per-mite a modificação seletiva das proteínas com qualquer uma de uma variedade de reagentes contendo hidrazina ou hidroxilamina in vitro e in vivo. Um aminoácido arti-ficial com átomo pesado, por exemplo, pode ser útil para dispor em fases os dados da estrutura de raio-X. A introdução sítio-específica dos átomos pesados usando aminoácidos não-naturais proporciona seletividade e flexibilidade na escolha das posições para os átomos pesados. Aminoácidos não-naturais fotorreativos (incluin-do, porém sem se limitar, aos aminoácidos com cadeias laterais de benzofenona e arilazidas (incluindo, porém sem se limitar a fenilazida)), por exemplo, permitem a fotorreticulação in vivo e in vitro de proteína. Exemplos de aminoácido não-naturais fotorreativos incluem, porém não estão limitados, ao p-azidofenilalanina, e p- benzoilfenilalanina. A proteína com os aminoácidos não-naturais fotorreativos pode ser então reticulada por excitação do controle temporal fornecedor de grupos fotor- reativos. Em um exemplo, o grupo metil de um aminoácido artificial pode ser substi-tuído com um isotopicamente marcado incluindo, porém sem se limitar, ao grupo metil, como uma sonda de estrutural local e dinâmica, incluindo, porém sem se limi-tar, ao uso de ressonância magnética nuclear e espectroscopia vibracional. Grupos alquinil ou azido funcionais, por exemplo, permitem a modificação seletiva das prote-ínas com moléculas através de uma reação de cicloadição [3+2].
[00203]Um aminoácido artificial incorporado em um polipeptídeo na parte aminoterminal pode ser composto de um grupo R que é qualquer substituinte dife-rente daquele usado nos vinte aminoácidos naturais e um segundo grupo reativo diferente do grupo NH2 normalmente presente em a-aminoácidos (ver Fórmula I). Um aminoácido artificial similar pode ser incorporado no carboxil terminal com um segundo grupo reativo diferente do grupo COOH normalmente presente nos a- aminoácidos (ver Fórmula I).
[00204]Os aminoácidos não-naturais da invenção podem ser selecionados ou projetados para fornecer características adicionais indisponíveis nos vinte amino- ácidos naturais. Por exemplo, aminoácido natural pode ser opcionalmente projetado ou selecionado para modificar as propriedades biológicas de uma proteína, por exemplo, na qual eles estão incorporados. Por exemplo, as propriedades a seguir podem ser opcionalmente modificadas por inclusão de um aminoácido artificial em uma proteína; toxicidade, biodistribuição, solubilidade, estabilidade, por exemplo, térmica, hidrolítica, oxidativa, resistência à degradação enzimática e semelhantes, facilidade de purificação e processamento, propriedades estruturais, propriedades espectroscópicas, propriedades químicas e/ou fotoquímicas, atividade catalítica, po-tencial redox, meia-vida, capacidade de reagir com outras moléculas, por exemplo, covalentemente ou não-covalentemente, e semelhantes. ESTRUTURA E SÍNTESE DOS AMINOÁCIDO NÃO-NATURAIS: GRUPOS CARBONIL, TIPO CARBONIL, CARBONIL OCULTOS, CARBONIL PROTEGIDOS E GRUPOS HIDROXILAMINA
[00205]Em algumas modalidades, a presente invenção fornece FGF-21 liga- do a um polímero solúvel em água, por exemplo, um PEG, por uma ligação oxima.
[00206]Muitos tipos de aminoácidos codificados artificialmente são adequa-dos para a formação de ligações oxima. Estas incluem, porém não estão limitadas, aos aminoácidos codificados artificialmente contendo um grupo carbonil, dicarbonil ou hidroxilamina. Tais aminoácidos são descritos nas Publicações de Patentes Ame-ricanas Nos. 2006/0194256, 2006/0217532 e 2006/0217289 e WO 2006/069246 inti-tulado “Compositions containing, methods involving, and uses of non-natural amino acids and polypeptides,” os quais são aqui incorporados por referência na sua totali-dade. Aminoácidos artificialmente codificados também são descritos na Patente Americana No. 7.083.970 e na Patente Americana No. 7.045.337, os quais são aqui incorporados por referência na sua totalidade.
[00207]Algumas modalidades da invenção utilizam polipeptídeos FGF-21 que são substituídos em uma ou em mais posições com um aminoácido para- acetilfenilalanina. As sínteses de p-acetil-(+/-)-fenilalanina e m-acetil-(+/-)-fenilalanina são descritas em Zhang, Z., et al., Biochemistry 42: 6735-6746 (2003), incorporadas por referência. Outros aminoácidos contendo carbonil ou dicarbonil podem ser semelhantemente preparados por uma pessoa normalmente versada na técnica. Além disso, sínteses exemplares não-limitativas do aminoácido artificial que estão aqui incluídas estão apresentadas nas FIGS. 4, 24 - 34 e 36 - 39 da Patente Americana No. 7.083.970, a qual é aqui incorporada por referência na sua totalidade.
[00208]Aminoácidos com um grupo reativo eletrofílico permitem uma varie-dade de reações para ligar moléculas através de reações de adição nucleofílica entre si. Tais grupos reativos eletrofílicos incluem um grupo carbonil (incluindo um grupo ceto e um grupo dicarbonil), um grupo tipo carbonil (o qual tem reatividade similar a um grupo carbonil (incluindo um grupo ceto e um grupo dicarboil) e é estrutural-mente semelhante a um grupo carbonil), um grupo carbonil oculto (o qual pode ser prontamente convertido em um grupo carbonil (incluindo um grupo ceto e um grupo dicarbonil) ou um grupo carbonil protegido (o qual tem reatividade similar a um grupo carbonil (incluindo um grupo ceto e um grupo dicarbonil) na desproteção). Tais ami- noácidos incluem aminoácidos com a estrutura da Fórmula (IV): em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquileno inferior, al- quenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno inferior substituído, arileno, arileno substituído, hetroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; B é opcional, e quando presente é um ligante selecionado do grupo consis-tindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR' -( alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')-( alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R' )-( alquileno ou alquileno substituído)-, - N(R')CO-( alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N- N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é alquil, alquil substituído, cicloalquil ou cicloalquil substituído; cada R” é independentemente H, alquil, alquil substituído ou um grupo protetor, ou quando mais de um grupo R” está presente, dois R” opcionalmente formam um heterocicloalquil; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo. cada um de R3 e R4 é independentemente H, halogênio, alquil inferior ou al- quil inferior substituído, ou R3 e R4 ou dois grupos R3 opcionalmente formam um ci- cloalquil ou heterocicloalquil; ou os grupos -A-B-J-R juntamente formam um cicloalquil ou heterocicloalquil bicíclico ou tricíclico compreendendo pelo menos um grupo carbonil, incluindo um grupo dicarbonil, grupo carbonil protegido, incluindo um grupo dicarbonil protegido, ou um grupo carbonil oculto, incluindo um grupo dicarbonil oculto; ou o grupo -J-R forma junto um cicloalquil ou heterocicloalquil monocíclico ou bicíclico compreendendo pelo menos um grupo carbonil, incluindo um grupo di- carbonil, um grupo carbonil protegido, incluindo um grupo dicarbonil protegido, ou um grupo carbonil oculto, incluindo um grupo dicarbonil oculto; com a condição de que quando A é fenileno e cada R3 é H, B está presente; e que quando A é -(CH2)4- e cada R3 é H, B não é -NHC(O)(CH2CH2)-; e que quan-do A e B estão ausentes e cada R3 é H, R não é metil.
[00209]Além disso, com a estrutura de fórmula (V) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, arileno, arileno substituído, hetroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; B é opcional, e quando presente é um ligante selecionado do grupo consis-tindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR' -(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, -N(R')CO-(alquileno ou alquileno substituído)-, -N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; com a condição de que quando A é fenileno, B está presente; e que quando A é -(CH2)4-, B não é -NHC(O)(CH2CH2)-; e que quando A e B estão ausentes, R não é metil. Além disso, aminoácidos com a estrutura da Fórmula (VI) são incluídos: em que: B é um ligante selecionado do grupo consistindo de alquileno inferior, alqui- leno inferior substituído, alquenileno inferior, alquenileno inferior substituído, hetero- alquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, -C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'- (alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')-(alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO- (alquileno ou alquileno substituído)-, - N(R')C(O)O-, -S(O)kN(R')-, -N(R')C(O)N(R')-, - N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, -C(R')=N-, -C(R')=N- N(R')-, -C(R')=N- N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; cada Ra é independentemente selecionado do grupo consistindo de H, halo- gênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, -C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído.
[00210]Além disso, os seguintes aminoácidos são incluídos: em que tais compostos são grupos aminoprotegidos, carboxil protegidos ou sais seus. Além disso, qualquer um dos aminoácidos não-naturais podem ser incorporados em um polipeptídeo de aminoácido artificial.
[00211]Além disso, os seguintes aminoácidos com a estrutura da Fórmula em que B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; cada Ra é independentemente selecionado do grupo consistindo de H, halo- gênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, -C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído; e n é de 0 a 8; com a condição de que quando A é -(CH2>, B não é -NHC(O)(CH2CH2)-.
[00212]Além disso, os seguintes aminoácidos são incluídos: e ’ em que tais compostos são opcionalmente amino protegidos, opcionalmente carbóxi protegidos, opcionalmente amino protegidos e carboxil protegidos, ou um sal seu. Além disso, esses aminoácidos não- naturais e qualquer um dos aminoácidos não-naturais a seguir podem ser incorporados em um polipeptídeo de aminoácidos artificial.
[00213]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (VIII) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalcano inferior, heterocicloalcano inferior substituído, arileno, arileno substituído, hetroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N- N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo.
[00214]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (IX) são incluídos: B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; em que cada Ra é independentemente selecionado do grupo consistindo de H, halogênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, - C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído.
[00215]Além disso, os seguintes aminoácidos são incluídos: em que tais compostos são opcionalmente amino protegidos, opcionalmente carbóxi protegidos, opcionalmente amino protegidos e carbóxi protegidos, ou um sal seu. Além disso, esses aminoácidos não-naturais e qualquer um dos aminoácidos não-naturais a seguir podem ser incorporados em um polipeptídeo de aminoácidos artificial.
[00216]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (X) são incluídos: em que B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, heteroalquileno inferior, heteroalquileno inferior subs-tituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, - C(O)-, -C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquile- no substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, - CON(R')-(alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou al- quileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; cada Ra é independentemente selecionado do grupo consistindo de H, halo- gênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, -C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído.
[00217]Além disso, os compostos a seguir são incluídos: e ’ em que tais compostos são opcionalmente amino protegidos, opcionalmente carbóxi protegidos, opcionalmente amino protegidos e carbóxi protegidos, ou um sal seu. Além disso, esses aminoácidos não-naturais e qualquer um dos ami- noácidos não-naturais a seguir podem ser incorporados em um polipeptídeo de ami- noácidos artificial.
[00218]Além das estruturas monocarbonílicas, os aminoácidos não-naturais descritos aqui podem incluir grupos tais como grupos dicarbonil, tipo dicarbonil, di- carbonil oculto e dicarbonil protegido.
[00219]Por exemplo, os seguintes aminoácidos com a estrutura da Fórmula (XI) são incluídos: em que A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, hetero- alquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substi-tuído, arileno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R é independentemente H, alquil ou alquil substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo.
[00220]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XII) são incluídos: B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alqueni- leno inferior substituído, heteroalquileno inferior, heteroalquileno inferior substituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, -C(O)-, - C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquileno substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, -CON(R')- (alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou alquileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R’ é independentemente H, alquil ou alquil substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; em que cada Ra é independentemente selecionado do grupo consistindo de H, halogênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, - C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído.
[00221]Além disso, os seguintes aminoácidos são incluídos: e em que tais compostos são opcionalmente amino protegidos, opcionalmente carbóxi protegidos, opcionalmente amino protegidos e carbóxi protegidos, ou um sal seu. Além disso, esses aminoáci- dos não-naturais e qualquer um dos aminoácidos não-naturais a seguir podem ser incorporados em um polipeptídeo de aminoácidos artificial.
[00222]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XIII) são incluídos: em que B é opcional, e quando presente é um ligante selecionado do grupo consistindo de alquileno inferior, alquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, heteroalquileno inferior, heteroalquileno inferior subs-tituído, -O-, -O-(alquileno ou alquileno substituído)-, -S-, -S-(alquileno ou alquileno substituído)-, -S(O)k-, onde k é 1, 2 ou 3, -S(O)k(alquileno ou alquileno substituído)-, - C(O)-, -C(O)-(alquileno ou alquileno substituído)-, -C(S)-, -C(S)-(alquileno ou alquile- no substituído)-, -N(R')-, -NR'-(alquileno ou alquileno substituído)-, -C(O)N(R')-, - CON(R')-(alquileno ou alquileno substituído)-, -CSN(R')-, -CSN(R')-(alquileno ou al- quileno substituído)-, - N(R')CO-(alquileno ou alquileno substituído)-, - N(R')C(O)O-, - S(O)kN(R')-, -N(R')C(O)N(R')-, -N(R')C(S)N(R')-, -N(R')S(O)kN(R')-, -N(R')-N=, - C(R')=N-, -C(R')=N-N(R')-, -C(R')=N-N=, -C(R')2-N=N- e -C(R')2-N(R')-N(R')-, onde cada R’ é independentemente H, alquil ou alquil substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; em que cada Ra é independentemente selecionado do grupo consistindo de H, halogênio, alquil, alquil substituído, -N(R')2, -C(O)k' onde k é 1, 2 ou 3, - C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído; e n é de 0 a 8.
[00223]Além disso, os seguintes aminoácidos são incluídos: em que tais compostos são opcionalmente amino protegidos, opcionalmente carbóxi protegidos, opcionalmente amino protegidos e carbóxi protegidos, ou um sal seu. Além disso, esses aminoácidos não- naturais e qualquer um dos aminoácidos não-naturais a seguir podem ser incorporados em um polipeptídeo de aminoácidos artificial.
[00224]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XIV) são incluídos:em que: em que A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, hetero- alquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substi-tuído, arileno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; X1 é C, S ou S(O); e L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno substituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou ci- cloalquil substituído.
[00225]Além disso, os compostos a seguir com a estrutura de Fórmula (XIV- A) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, hetero- alquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substi-tuído, arileno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno subs-tituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído.
[00226]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XIV-B) são incluídos: em que A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, hetero- alquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substi-tuído, arileno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno subs-tituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído.
[00227]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (XV) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substituído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, hetero- alquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substi-tuído, arileno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarileno substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; X1 é C, S ou S(O); e n é 0, 1, 2, 3, 4 ou 5; e cada R8 e R9 em cada grupo CR8R9 é independentemente selecionado do grupo consistindo de H, alcóxi, alquila- mina, halogênio, alquil, aril ou qualquer um dentre R8 e R9 juntos formam =O ou um cicloalquil, ou qualquer um aos grupos R8 adjacentes pode formar um cicloalquil.
[00228]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XV-A) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; n é 0, 1, 2, 3, 4 ou 5; e cada R8 e R9 em cada grupo CR8R9 é independentemente selecionado do grupo consistindo de H, alcóxi, alquilamina, halogênio, alquil, aril ou qualquer um dentre R8 e R9 juntos formam =O ou um cicloalquil, ou qualquer um aos grupos R8 adjacentes pode formar um cicloalquil.
[00229]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (XV-B) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; R é H, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; n é 0, 1, 2, 3, 4 ou 5; e cada R8 e R9 em cada grupo CR8R9 é independentemente selecionado do grupo consistindo de H, alcóxi, alquilamina, halogênio, alquil, aril ou qualquer um dentre R8 e R9 juntos formam =O ou um cicloalquil, ou qualquer um aos grupos R8 adjacentes pode formar um cicloalquil.
[00230]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (XVI) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; X1 é C, S ou S(O); e L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno substituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou ci- cloalquil substituído.
[00231]Além disso, os seguintes aminoácidos com a estrutura da Fórmula (XVI-A) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno subs-tituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído.
[00232]Além disso, os seguintes aminoácidos com a estrutura de Fórmula (XVI-B) são incluídos: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; R é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo; L é alquileno, alquileno substituído, N(R’)(alquileno) ou N(R’)(alquileno subs-tituído), onde R’ é H, alquil, alquil substituído, cicloalquil ou cicloalquil substituído.
[00233]Além disso, aminoácidos com a estrutura de Fórmula (XVII) são in-cluídos: em que: em que: A é opcional, e quando presente é alquileno inferior, alquileno inferior substi-tuído, cicloalquileno inferior, cicloalquileno inferior substituído, alquenileno inferior, alquenileno inferior substituído, alquinileno, heteroalquileno inferior, heteroalquileno substituído, heterocicloalquileno inferior, heterocicloalquileno inferior substituído, ari- leno, arileno substituído, heteroarileno, heteroarileno substituído, alcarileno, alcarile- no substituído, aralquileno ou aralquileno substituído; onde (a) indica ligação ao grupo A e (b) indica ligação aos respectivos grupos carbonil, R3 e R4 são independentemente escolhidos de H, halogênio, alquil, al- quil substituído, cicloalquil ou cicloalquil substituído, ou R3e R4 ou dois grupos R3 ou dois grupos R4 opcionalmente formam um cicloalquil ou um heterocicloalquil; R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; T3 é uma ligação, C(R)(R), O ou S, e R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo.
[00234]Além disso, aminoácido com a estrutura de Fórmula (XVIII) são inclu-ídos: em que: onde (a) indica ligação ao grupo A e (b) indica ligação aos respectivos grupos car- bonil, R3e R4 são independentemente escolhidos de H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído, ou R3 e R4 ou dois grupos R3 ou dois grupos R4 opcionalmente formam um cicloalquil ou um heterocicloalquil; R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; T3 é uma ligação, C(R)(R), O ou S, e R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído; R1 é opcional, e quando presente, é H, um grupo amino protetor, resina, aminoácido, polipeptídeo ou polinucleotídeo; e R2 é opcional, e quando presente, é OH, um grupo protetor éster, resina, aminoácido, polipeptídeo ou polinucleotídeo. cada Ra é independentemente selecionado do grupo consistindo de H, halo- gênio, alquil, alquil substituído, -N(R')2, -C(O)kR' onde k é 1, 2 ou 3, -C(O)N(R')2, -OR' e -S(O)kR', onde cada R’ é independentemente H, alquil ou alquil substituído.
[00235]Além disso, aminoácidos com a estrutura de Fórmula (XIX) são inclu- ídos: em que: R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituí- do; e T3 é O ou S.
[00236]Além disso, aminoácidos com a estrutura da Fórmula (XX) são inclu- ídos: em que: R é H, halogênio, alquil, alquil substituído, cicloalquil ou cicloalquil substituído.
[00238]Em algumas modalidades, um polipeptídeo compreendendo um ami- noácido artificial é quimicamente modificado para gerar um grupo funcional carbonil ou dicarbonil reativo. Por exemplo, uma funcionalidade aldeído útil para reações de conjugação pode ser gerada a partir de uma funcionalidade com grupos amino e hi- droxil adjacentes. Onde a molécula biologicamente ativa é um polipeptídeo, por exemplo, uma serina ou treonina N-terminal (a qual pode estar normalmente presente ou pode ser exposta por digestão química ou enzimática), pode ser usada para gerar uma funcionalidade aldeído sob condições de clivagem oxidativa branda usando periodato. Ver Gaertner, et. al., Bioconjug. Chem. 3: 262-268 (1992); Geoghegan, K. & Stroh, J., Bioconjug. Chem. 3:138-146 (1992); Gaertner et al., J. Biol. Chem. 269:7224-7230 (1994). Entretanto, métodos conhecido na técnica são restritos ao aminoácido e ao N-terminal do peptídeo ou proteína.
[00239]Na presente invenção, uma hidroxila adjacente com aminoácido artificial e grupo amino pode ser incorporada no polipeptídeo como uma funcionalidade aldeído “oculta”. Por exemplo, 5-hidroxilisina possui um grupo hidroxila adjacente à amina épsilon. As condições reacionais para gerar o aldeído tipicamente envolvem a adição de excesso molar de metaperiodato de sódio sob condições brandas para evitar a oxidação em outros sítios no polipeptídeo. O pH da reação de oxidação é tipicamente de cerca de 7,0. Uma reação típica envolve a adição de excesso molar de cerca de 1,5 de metaperiodato de sódio a uma solução tamponada do polipeptí- deo, seguido por incubação por cerca de 10 minutos no escuro. Ver, por exemplo, Patente Americana No 6.423.685.
[00240]A funcionalidade carbonil ou dicarboil pode reagir seletivamente com um reagente contendo hidroxilamina sob condições brandas em solução aquosa para formar a ligação oxima correspondente que é estável sob condições fisiológicas. Ver, por exemplo, Jencks, W. P., J. Am. Chem. Soc. 81, 475-481 (1959); Shao, J. and Tarn, J. P., J. Am. Chem. Soc. 117:3893-3899 (1995). Além disso, a reatividade singular do grupo carbonil ou dicarbonil permite a modificação seletiva na presença de outras cadeias laterais de aminoácidos. Ver, por exemplo, Cornish, V. W., et al., J. Am. Chem. Soc. 118:8150-8151 (1996); Geoghegan, K. F. & Stroh, J. G., Biocon- jug. Chem. 3:138-146 (1992); Mahal, L. K., et al., Science 276:1125-1128 (1997).
[00241]Estrutura e Síntese dos Aminoácido não-naturais: Aminoácidos Con-tendo Hidroxilamina
[00242]O Pedido Provisório Americano No. 60/638.418 é incorporado por re-ferência na sua totalidade. Deste modo, as descobertas fornecidas na Seção V (inti-tulada “Aminoácidos não-naturais”, Parte B (intitulada “Estrutura e Síntese de Ami- noácido não-naturais: Aminoácidos Contendo Hidroxilamina”), no Pedido de Patente Provisória Americana No. 60/638.418, aplicado plenamente aos métodos, composições (incluindo fórmulas I-XXXV), técnicas e estratégias para fazer, purificar, caracterizar e usar aminoácidos não-naturais, polipeptídeos de aminoácidos não-naturais e polipeptídeos de aminoácidos não-naturais modificados descrito aqui até a mesma extensão que se tais descobertas fossem totalmente apresentadas aqui. As Publicações de Patentes Americanas Nos. 2006/0194256, 2006/0217532 e 2006/0217289 e WO 2006/069246 intituladas "Compositions containing, methods involving, and uses of non-natural amino acids and polypeptides," também são incorporadas aqui por referência nas suas totalidades. SÍNTESE QUÍMICA DOS AMINOÁCIDOS NÃO-NATURAIS
[00243]Muitos dos aminoácidos não-naturais adequados para uso na presente invenção são comercialmente disponíveis, por exemplo, de Sigma (EUA) ou Aldrich (Milwaukee, WI, EUA). Aqueles que não são comercialmente disponíveis são opcionalmente sintetizados conforme aqui fornecidos ou conforme fornecidos em várias publicações ou usando métodos padrões conhecidos pelas pessoas normalmente versadas na técnica. Para técnicas de síntese orgânica, ver, por exemplo, Organic Chemistry por Fessendon e Fessendon, (1982, Segunda Edição, Willard Grant Press, Boston Mass.); Advanced Organic Chemistry por March (Terceira Edição, 1985, Wiley and Sons, Nova Iorque); e Advanced Organic Chemistry por Carey e Sundberg (Terceira Edição, Partes A e B, 1990, Plenum Press, Nova Iorque). Outras publicações descrevendo a síntese de aminoácidos não-naturais inclui, por exemplo, WO 2002/085923 intitulado "In vivo incorporation of Unnatural Amino Acids;” Matsoukas et al., (1995) J. Med. Chem., 38, 4660-4669; King, F.E. & Kidd, D.A.A. (1949) A New Synthesis ofGlutamine and of Y-Dipeptides of Glutamic Acid from Phthylated Intermediates. J. Chem. Soc, 3315-3319; Friedman, O. M. & Chat- terrji, R. (1959) Synthesis of Derivatives of Glutamine as Model Substrates for AntiTumor Agents. J. Am. Chem. Soc. 81, 3750-3752; Craig, J.C. et al. (1988) Absolute Configuration of the Enantiomers of 7-Chloro-4 [[4-(diethylamino)-l- methylbutyl]amino]quinoline (Chloroquine). J. Org. Chem. 53, 1167-1170; Azoulay, M., Vilmont, M. & Frappier, F. (1991) Glutamine analogues as Potential Antimalarials, Eur. J. Med. Chem. 26, 201-5; Koskinen, A.M.P. & Rapoport, H. (1989) Synthesis of 4-Substituted Prolines as Conformationally Constrained Amino Acid Analogues. J. Org. Chem. 54, 1859- 1866; Christie, B.D. & Rapoport, H. (1985) Synthesis of Optically Pure Pipecolates from L- Asparagine. Application to the Total Synthesis of (+)- Apovincamine through Amino Acid Decarbonylation and Iminium Ion Cyclization. J. Org. Chem. 50:1239-1246; Barton et al., (1987) Synthesis of Novel alpha-AminoAcids and Derivatives Using Radical Chemistry: Synthesis of L- and D-alpha-Amino- Adipic Acids, L-alpha-aminopimelic Acid and Appropriate Unsaturated Derivatives. Tetrahedron 43:4297-4308; e, Subasinghe et al., (1992) Quisqualic acid analogues: synthesis of beta-heterocyclic 2-aminopropanoic acid derivatives and their activity at a novel quisqualate-sensitized site. J. Med. Chem. 35:4602-7. Ver também a Publicação de Patente Americana No. US 2004/0198637 intitulada "Protein Arrays," a qual é aqui incorporada por referência. A. Grupo Reativos Carbonil
[00244]Aminoácidos com um grupo reativo carbonil permitem uma variedade de reações para ligar moléculas (incluindo, porém sem se limitar, a PEG, ou outras moléculas solúveis em água) através de reações de adição nucleofílica ou conden-sação aldólica, dentre outras.
[00245]Aminoácidos contendo carbonil exemplares podem ser representados da seguinte maneira: em que n é 0 - 10; Ri é um alquil, aril, alquil substituído, ou aril substituído; R2 é H, alquil, aril, alquil substituído e aril substituído; e R3 é H, um aminoácido, um polipeptídeo ou um grupo de modificação amino terminal, e R4 é H, um aminoácido, um polipeptídeo ou um grupo de modificação carbóxi terminal. Em algumas modalidades, n é 1, R1 é fenil e R2 é um alquil simples (isto é, metil, etil ou propil) e a porção cetona é posicionada na posição para em relação à cadeia lateral alquílica. Em algumas modalidades, n é 1, R1 é fenil e R2 é alquil simples (isto é, metil, etil ou pro- pil) e a porção cetona é posicionada na posição meta em relação à cadeia alquílica lateral.
[00246]A síntese de p-acetil-(+/-)-fenilalanina e m-acetil-(+/-)-fenilalanina é descrita em Zhang, Z., et al., Biochemistry 42: 6735-6746 (2003), o qual é aqui in-corporado por referência. Outros aminoácidos contendo carbonil podem ser seme-lhantemente preparados por uma pessoa normalmente versada na técnica.
[00247]Em algumas modalidades, um polipeptídeo compreendendo um ami- noácido não-naturalmente codificado é quimicamente modificado para gerar um grupo funcional carbonil reativo. Por exemplo, uma funcionalidade aldeído útil para reações de conjugação pode ser gerada a partir de uma funcionalidade com grupos amino e hidroxila adjacentes. Onde a molécula biologicamente ativa é um polipeptí- deo, por exemplo, uma serina ou treonina N-terminal (a qual pode ser normalmente presente ou pode ser exposta através de uma digestão química ou enzimática) pode ser usada para gerar uma funcionalidade aldeído sob as condições de clivagem oxi- dativas leves usando periodato. Ver, por exemplo, Gaertner, et al, Bioconjug. Chem. 3:262-268 (1992); Geoghegan, K. & Stroh, J., Bioconjug. Chem. 3:138-146 (1992); Gaertner et al, J. Biol. Chem. 269:7224-7230 (1994). Entretanto, métodos conhecidos na técnica são restritos para aminoácido no N-terminal do peptídeo ou proteína.
[00248]Na presente invenção, um aminoácido não naturalmente codificado produzindo hidroxila e grupos amino podem ser incorporados no polipeptídeo como uma funcionalidade aldeído “mascarado”. Condições de reação para gerar o aldeído tipicamente envolve adição de excesso molar de metaperiodato de sódio sob condições leves para evitar oxidação em outros sítios dentro do polipeptídeo. O pH da reação de oxidação é tipicamente cerca de 7.0. Uma reação típica envolve a adição de cerca de 1,5 molar do excedido de meta periodato de sódio a uma solução tem- ponada do polipeptídeo, seguido pela incubação por cerca de 10 minutos no escuro. Ver, por exemplo, Patente dos Estados Unidos No. 6.423.685, que é aqui incorporado por referência.
[00249]A funcionalidade carbonila pode ser reagida seletivamente com um reagente contendo hidrazina, hidrazida, hidroxilamina, ou semi-carbazida sob condi-ções leves na solução aquosa para formar as correspondentes ligações hidrazona, oxima, ou semi-carbazona, respetivamente, que são estáveis sob condições fisiológicas. Ver, por exemplo, Jencks, W.P., J. Am. Chem. Soc. 81, 475-481 (1959); Shao, J. e Tam, J.P., J. Am. Chem. Soc. 117:3893-3899 (1995). Além disso, a única reati- vidade do grupo carbonila permite a modificação seletiva em presença de outras cadeias laterais aminoácidos. Ver, por exemplo, Cornish, V.W. et al, J. Am. Chem. Soc. 118:8150-8151 (1996); Geoghegan, K.F. & Strih, J.G., Bioconjug. Chem. 3:138-146 (1992); Mahal, L.K., et al, Science 276:1125-1128 (1997). B. Grupo reativos hidrazina, hidrazida ou semi-carbazida
[00250]Aminoácidos não naturalmente codificados contendo um grupo nu- cleofílico, tais como hidrazina, hidrazida ou semi-carbazida, permite a reação com uma variedade de grupo eletrofílico para formar conjugados (incluindo, mas não limitado a, com PEG ou outros polímeros solúveis em água).
[00251]Aminoácidos contendo hidrazina, hidrazida ou semi-carbazida exem-plares podem ser representados como segue:
[00252]Em que n é 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída ou não presente; X, é O, N, ou S ou não presente; R2 é H, um aminoáci- do, um polipeptídeo, ou um grupo de modificação amino terminal, e R3 é H, um ami- noácido, um polipeptídeo, ou um grupo de modificação carbóxi terminal.
[00253]Em algumas modalidades, n é 4, R1 não está presente, e X é N. Em algumas modalidades, n é 2, R1 não está presente, e X não está presente. Em algumas modalidades, n é 1, R1 é fenila, X é O, e o átomos de oxigênio está posicionado em para o grupo alifático no anel arila.
[00254]Aminoácidos contendo hidrazida, hidrazina e semi-carbazida são disponíveis a partir de fontes comerciais. Por exemplo, L-glutamato-y-hidrazida está disponível a partir de Sigma Chemical (St. Loius, MO). Outros aminoácidos não co-mercialmente disponíveis podem ser preparados por um versado na técnica. Ver, por exemplo, Pat. dos EUA No. 6.281.211, que é aqui incorporado por referência.
[00255]Polipeptídeos contendo aminoácidos não naturalmente codificados que produzem funcionalidades hidrazida, hidrazina ou semi-carbazida podem ser reagidos eficientemente e seletividade com uma variedade de moléculas que contêm aldeídos ou outros grupos funcionais com reatividade química similar. Ver, por exemplo Shao, J. e Tam, J., J. Am. Chem. Soc. 117:3893-3899 (1995). A reatividade única de grupos hidrazida, hidrazina e semi-carbazida fazem eles significantemente mais reativos para aldeídos, cetonas e outros grupos eletrofílicos como comparado aos grupos nucleofílicos presentes nos 20 aminoácidos comuns (incluindo, mas não limitado ao grupo hidroxila de serina ou treonina ou grupo aminos de lisina e N- terminal). C. Aminoácidos contendo aminoóxi.
[00256]Aminoácidos não naturalmente codificados contendo um grupo ami- noóxi (também chamado uma hidroxilamina) permitiu para reação com uma varieda- de de grupos eletrofílicos para formar conjugados (incluindo, mas não limitados a, com PEG ou outros polímeros solúveis em água). Como hidrazinas, hidrazidas e semi-carbazidas, a nucleofilicidade aumentada do grupo aminoóxi permite sua reação eficientemente e seletivamente com uma variedade de moléculas que contêm aldeídos ou outros grupos funcionais com reatividade química similar. Ver, por exemplo, Shao, J. e Tam, J., J. Am. Chem. Soc. 117:3893-3899 (1995); H. Hang e C. Bertozzi, Acc. Chem. Res. 34:727-736 (2001). Enquanto o resultado de reação com um grupo hidrazina é a hidrazona correspondente, entretanto, uma oxima resulta geralmente a partir da reação de um grupo aminoóxi com um grupo contendo carbonila tal como cetona.
[00257]Aminoácidos exemplares contendo grupos aminoóxi podem ser re-presentados como segue:em que n é 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída ou não presente; X é O, N, S ou não presente; m é 0-10; Y=C(O) ou não presente; R2 ;e H, um aminoácido, um polipeptídeo, ou um grupo de modificação aminoterminal, e R3 é H, um aminoácido, um polipeptídeo, ou um grupo de modificação carboxi-terminal. Em algumas modalidades, n é 1, R1 é fenila, X é O, m é 1, e Y está presente. Em algumas modalidades, n é 2, R1 e X não são presentes, m é 0, e Y não está presente.
[00258]Aminoácidos contendo aminoóxi podem ser preparados a partir de precursores aminoácidos facilmente disponíveis (homoserina, serina e treonina). Ver, por exemplo, M. Carrasco e R. Brown, J. Org. Chem. 68:8853-8858 (2003). Certos aminoácidos contendo aminoóxi, tal como ácido L-2-amino-4-(aminoóxi)butírico, tem sido isolado a partir de fontes naturais (Rosenthal, G., Life Sci. 60:1635-1641 (1997). Outros aminoácidos contendo aminoóxi podem ser preparados por um versado na técnica. D. Grupos reativos azida e alquino
[00259]A reatividade única dos grupos funcionais azida e alquino os fazem extremamente úteis para a modificação seletiva de polipeptídeos e outras moléculas biológicas. Azidas orgânicas, particularmente azidas alifáticas, e alquinos são geral-mente estáveis para condições químicas reativas. Em particular, ambos, grupos azi- da e alquino funcionais são inertes para as cadeias laterais (isto é, grupos R) dos 20 aminoácidos comuns encontrados em polipeptídeos de ocorrência natural. Quando trazido em proximidade, entretanto, a natureza “carregada de fonte” da azida e grupo alquino é revelada e eles reagem seletivamente e eficientemente através da reação de cicloadição [3+2] Huisgen para gerar o trizol correspondente. Ver, por exemplo, Chin J. et al, Science 301:964-7 (2003); Wang, Q., et al, J.Am. Chem. Soc. 125, 3192-3193 (2003); Chin, J. W., et al, J. Am. Chem. Soc. 124:9026-9027 (2002).
[00260]Por que a reação de cicloadição de Huisgen envolve uma reação de cicloadição seletiva (ver, por exemplo, Padwa, A., em COMPREHENSIVE ORGANIC SYNTHESIS< Vol. 4 (ed. Trost, B. M., 1991), p. 1069-1109; Huisgen, R. em 1,3DIPOLAR CYCLOADDITION CHEMISTRY (ed. Padwa, A. 1984), p. 1-176) ao invém de uma substituição nucleofílica, a incorporação de aminoácidos não naturalmente codificados produzindo azida e cadeias laterais contendo alquino permitem os poli- peptídeos resultantes serem modificados seletivamente na posição do aminoácido não naturalmente codificado. Reação de cicloadição envolvendo azida ou polipeptí- deo FGF-21 contendo alquino pode ser realizada em temperatura ambiente sob condições aquosas pela adição de Cu(II) (incluindo mas não limitado a, na forma de uma quantidade catalítica de CuSO4) em presença de um agente redutor para reduzir Cu(II) a Cu(I), no local, em quantidade catalítica. Ver, por exemplo, Wang, Q. et al, J.Am. Chem. Soc. 125, 3192-3193 (2003(; Tornoe, C.W., et al, J. Org. Chem. 67:3057-3064 (2002); Rostovtsev, et al, Angew. Chem. Int. Ed. 41:2596-2599 (2002). Agentes redutores exemplares incluem, incluindo, mas não limitados a, ascorbato, cobre metálico, quinina, hidroquinona, vitamina K, glutationa, cisteína, Fe2+, Co2+, e um potencial elétrico aplicado.
[00261]Em alguns casos, onde uma reação de cicloadição [3+2] Huisgen en- tre uma azida e um alquino é desejada, o polipeptídeo FGF-21 compreende um ami- noácido não naturalmente codificado compreendendo uma fração alquino e o polímero solúvel em água para ser ligada ao aminoácido compreende uma fração azida. Alternativamente, a reação conversa (isto é, com a fração azida no aminoácido e a fração alquino presente no polímero solúvel em água) pode também ser feita.
[00262]O grupo funcional azida pode também ser reagido seletivamente com um polímero solúvel em água contendo um éster arila e apropriadamente funcionali- zada com uma fração fosfina arila para gerar uma ligação amida. O grupo fosfino arila reduz a azida no local e a amida resultante então reage eficientemente com uma ligação éster proximal para gerar a amida correspondente. Ver, por exemplo, E. Saxon e C. Bertozzi, Science 287, 2007-2010 (2000). O aminoácido contendo azida pode ser ou uma alquil azida (incluindo, mas não limitado a, ácido 2-amino-6-azido- 1-hexanóico)ou um aril azida (p-azido-fenilalanina).
[00263]Polímeros solúveis em água exemplares contendo um aril éster e uma fração fosfina pode ser representada como segue: Em que X pode ser O, N, S ou não presente, Ph é fenil, W é um polímero so-lúvel em água e R pode ser H, alquila, arila, alquila substituída e grupos arila substi-tuída. Grupos R exemplares incluem mas não são limitados a -CH2, -C(CH3)3, -OR’, -NR’R’’, -SR’, -halogênio, -C(O)R’, -CONR’R”, -S(O)2R’, -S(O)2NR’R’’, -CN e -NO2. R’, R’’, R’’’e R’’’’ cada independentemente refere-se a hidrogênio, heteroalquila substituída ou não substituída, arila substituída ou não substituída, incluindo, mas não limitado a arila substituída com 1-3 halogênios, alquila substituída ou não substituída, grupos alcóxi ou tioalcóxi, ou grupos arilalquila. Quando um composto da invenção inclui mais que um grupo R, por exemplo, cada um dos grupos R é independentemente selecionado como são cada grupo R’, R’’, R’’’, e R’’’’ quando mais que um desse grupos está presente. Quando R’ e R’’ são ligados ao mesmo átomo de nitro gênio, eles podem ser combinados com o átomo de nitrogênio para formar um anel de 5-, 6- ou 7-membros. Por exemplo, -NR’R’’ significa incluir, mas não limitado a, 1- pirrolidinil e 4-morfolinil. A partir da discussão acima de substituintes, um versado na técnica entenderá que o termo “alquila” significa incluir grupos incluindo átomos de carbono ligados aos grupos outros que grupos hidrogênio, tais como haloalquila (in-cluindo mas não limitados a, -CF3 e -CH2CF3) e acila (incluindo mas não limitado a, - C(O)CH3, -C(O)CF3, -C(O)CH2OCH3, e semelhantes).
[00264]O grupo funcional azida pode também ser reagido seletivamente com um polímero solúvel em água contendo um tioéster e apropriadamente funcionaliza- do com uma fração aril fosfina para gerar uma ligação amida. O grupo aril fosfina reduz a azida no local e a amida resultante então reage eficientemente com a ligação tioéster para gerar a amida correspondente. Polímeros solúveis em água exemplares contendo um tioéster e uma fração fosfina pode ser representada como segue: Em que n é 1-10; X pode ser O, N, S ou não presente, Ph é fenil, e W é um polímero solúvel em água.
[00265]Aminoácidos contendo alquino exemplares podem ser representados como segue: em que n e 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída ou não presente; X é O, N, S ou não presente; m é 0-10, R2 é H, um aminoácido, um polipeptídeo, ou grupo de modificação de amino-terminal, e R2 é H, um aminoá- cido, um polipeptídeo, ou um grupo de modificação carboxi-terminal. Em algumas modalidades, n é 1, R1 é fenila, X não está presente, m é 0 e a fração acetileno é posicionada na posição para relativa a cadeia lateral alquila. Em algumas modalidades, n é 1, R1 é fenila, X é O, m é 1 e o grupo propargilóxi é posicionado na posição para relativa a cadeia lateral alquila (isto é, O-propargil-tirosina). Em algumas modalidades, n é 1, R1 e X não são presentes e m é 0 (isto é, proparilglicina).
[00266]Aminoácidos contendo alquino são comercialmente disponíveis. Por exemplo, propargilglicina é comercialmente disponível a partir de Peptech (Burlington, MA). Alternativamente, aminoácidos contendo alquino podem ser preparados de acordo com os métodos padrões. Por exemplo, p-propargiloxifenilalanina pode ser sintetizada, por exemplo, como descrito em Deiters, A., et al, J. Am. Chem. Soc. 125:11782-11783 (2003), e 4-alquinil-L-fenilalanina pode ser sintetizada com odes- crito em Kayser, B., et al, Tetrahedron 53(7):2475-2484 (1997). Outros aminoácidos contendo alquino podem ser preparados por um versado na técnica.
[00267]Aminoácidos contendo azida exemplares podem ser representados como segue: em que n e 0-10; R1 é uma alquila, arila, alquila substituída, ou arila substituída ou não presente; X é O, N, S ou não presente; m é 0-10, R2 é H, um aminoácido, um polipeptídeo, ou grupo de modificação de amino-terminal, e R3 é H, um aminoá- cido, um polipeptídeo, ou um grupo de modificação carboxi-terminal. Em algumas modalidades, n é 1, R1 é fenila, X não está presente, m é 0 e a fração azida é posi-cionada na posição para relativa a cadeia lateral alquila. Em algumas modalidades, n é 0-4, e R1 e X não estão presentes, e m=0. Em algumas modalidades, n é 1, R1 é fenila, X é O, m é 2 e a fração β-azidoet0xi é posicionado na posição para relativa a cadeia lateral alquila.
[00268]Aminoácidos contendo azida são disponíveis a partir de fontes co-merciais. Por exemplo, 4-azidofenilalanina pode ser obtida a partir de Chem-Impex International, Inc. (Wood Dale, IL). Para aqueles aminoácidos contendo azida que não são comercialmente disponíveis, o grupo azida pode ser preparado relativamente facilmente utilizando métodos padrões conhecidos pelos versados na técnica, incluindo mas não limitados, através da substituição de um grupo de saída adequado (incluindo, mas não limitado a, haleto, mesilato, tosilato) ou através da abertura de uma lactona protegida adequada. Ver, por exemplo, Advanced Organic Chemistry by March (Terceira Edição, 1985, Wiley e Sons, Nova Iorque). E. Grupos reativos aminotiol
[00269]A única reativa de grupos funcionais aminotiol beta-substituídos os fazem extremamente úteis para a modificação seletiva de polipeptídeos e outras mo-léculas que contêm grupos aldeídos através da formação doa tiazolidina. Ver, por exemplo, J. Shao e J. Tam., J. Am. Chem. Soc. 1995, 117 (14) 3893-3899. Em algumas modalidades, aminoácidos aminotiol beta-substituídos podem ser incorporados em polipeptídeos FGF-21 e então reagidos com polímeros solúveis em água compreendendo uma funcionalidade aldeído. Em algumas modalidades, um polímero solúvel em água, conjugado a droga ou outro carga útil pode ser acoplado a um polipeptídeo FGF-21 compreendendo um aminoácido aminotiol beta-substituído através da formação de tiazolidina. F. Grupos reativos adicionais
[00270]Grupos reativos adicionais e aminoácidos não naturalmente codificados que podem ser incorporados em polipeptídeos FGF-21 da invenção são descritos nos seguintes pedidos de patentes que são todos incorporados por referência em sua totalidade aqui: Pedido de Patente dos EUA No. 2006/0194256, Pedido de Patente dos EUA No. 2006/0217532, Pedido de Patente dos EUA No. 2006/0217289, Patente Provisória dos EUA No. 60/755.338; Patente Provisória dos EUA No. 60/755.711; Patente Provisória dos EUA No. 60/755.018; Pedido de Patente Internacional No. PCT/US06/49397; WO 2006/069246; Patente Provisória dos EUA No. 60/743.041; Patente Provisória dos EUA No. 60/743.040; Pedido de Patente Internacional No. PCT/US06/47822; Patente Provisória dos EUA No. 60/882.819; Patente Provisória dos EUA No. 60/882.500; e Patente Provisória dos EUA No. 60/870.584. CAPTAÇÃO CELULAR DE AMINOÁCIDOS NÃO NATURAIS
[00271]Captação de aminoácido não natural pode uma célula é um assunto que é tipicamente considerada quando designando e selecionado aminoácidos não naturais, incluindo, mas não limitados, para incorporado em uma proteína. Por exemplo, a densidade de alta carga de a-aminoácidos sugere que esses compostos são improváveis para ser permeáveis. Aminoácidos naturais são tomados na célula eucariótica através de uma coleção de sistemas de transporte baseados em proteína. Uma seleção rápida pode ser feita que acesse aminoácidos não naturais, se qualquer, são captados pelas células. Ver, por exemplo, os ensaios de toxicidade, por exemplo, Pedido de Patente dos EUA No. US2004/0198637 intitulado “Protein Arrays” que é incorporado aqui por referência; e Liu, D.R. & Schultz, P.G. (1999) Progress for the evolution of an organism with an expanded genetic code. PNAD Estados Unidos 96:4780-4785. Embora a captação é facilmente analisada com vários ensaios, uma alternativa para aminoácidos não naturais designados que são fáceis para vias de captação celular é para prover vias biossintéticas para criar aminoáci- dos in vivo. BIOSSÍNTESE DE AMINOÁCIDOS NÃO NATURAIS
[00272]Muitas vias biossintéticas já existem nas células para a produção de aminoácidos e outros compostos. Enquanto um método biossintético para um ami- noácido não natural particular pode não existir em natureza, incluindo, mas não limi-tado a, em uma célula, a invenção provê tais métodos. Por exemplo, vias biossíntese para aminoácidos não naturais são opcionalmente gerados na célula hospedeira por adição de novas enzimas ou modificação de vias de célula hospedeira existentes. Novas enzimas adicionais são opcionalmente enzimas de ocorrência natural ou en-zimas artificialmente envolvidas. Por exemplo, a biossíntese de p-aminofenilalanina (como apresentado em um exemplo em WO 2002/085923 intitulado “In vivo incorpo-ration of unnatural amino acids”) se baseia na adição de uma combinação de enzimas conhecidas a partir de outros organismos. Os genes para essas enzimas po- dem ser introduzidos em uma célula eucariótica por transformação da célula com um plasmídeo compreendendo os genes. Os genes, quando expressos na célula, provêm uma via enzimática para sintetizar o composto desejado. Exemplos dos tipos de enzimas que são opcionalmente adicionados são providos nos exemplos abaixo. Sequências de enzimas adicionais que são encontradas, por exemplo, no Genbank. Enzimas artificialmente envolvidas são também opcionalmente adicionadas em uma célula da mesma maneira. Desta maneira, a maquinaria celular e fontes de uma célula são manipuladas para produzir aminoácidos não naturais.
[00273]Uma variedade de métodos é disponível para produzir novas enzimas para uso em vias biossintéticas ou para evolução de vias existentes. Por exemplo, recombinação recursiva, incluindo, mas não limitados a, como desenvolvido por Maxygen, Inc. (disponível na World Wide Web em maxygen.com), é opcionalmente utilizado para desenvolver novas enzimas e vias. Ver, por exemplo, Stemmer (1994), Rapid evolution of a protein in vitro by DNA shuffling, Nature 370(4):389-391l e, Stemmer (1994), DNA shuffling by random fragmentation and reassembly. In vitro recombination for molecular evolution, Proc. Natl. Acad. Sci. EUA. 91:10747-10751. Similarmente DesignPath®, desenvolvido por Genercor (disponível na World Wide Web em genercor.com) é opcionalmente utilizado para construção de via metabólica, incluindo, mas não limitado a, construção de uma via para criar O-metil-L-tirosina em uma célula. Esta tecnologia reconstrói vias existentes em organismos hospedeiros utilizando uma combinação de novos genes, incluindo, mas não limitado àqueles identificados através de genômica funcional, e evolução molecular e desenho. Diversa Corporationm (disponível na World Wide Web em diversa.com) também provê tecnologia para rápida seleção de bibliotecas de genes e vias de gene, incluindo, mas não limitado a, criar novas vias.
[00274]Tipicamente, o aminoácido não natural produzido com uma via bio- síntética construída da invenção é produzida em uma concentração suficiente para biosíntese de proteína eficiente incluindo, mas não limitado a uma quantidade celular natural mas não para tal grau como afetar a concentração de outros aminoácidos ou exaustão de fontes celulares. Concentrações típicas produzidas in vivo desta forma são cerca de 10 mM a cerca de 0,05 mM. Uma vez uma célula é transformada com um plasmídeo compreendendo os genes utilizados para produzir enzimas desejadas para a via específica e um aminoácido não natural é gerada, seleções in vivo são opcionalmente utilizadas para ainda otimizar a produção de aminoácido não natural para ambas, síntese de proteína ribossomal e crescimento celular. POLIPEPTÍDEOS COM AMINOÁCIDOS NÃO NATURAIS
[00275]A incorporação de um aminoácido não natural pode ser feita para uma variedade de propósitos, incluindo mas não limitados a, mudanças nas terminações na estrutura da proteína e/ou função, mudança do tamanho, acidez, nucleofili- cidade, ligação a hidrogênio, hidrofobicidade, acessibilidade de sítios alvos de proteases, alvos para uma fração (incluindo mas não limitados a, para uma rede de proteína), adicionando uma molécula biologicamente ativa, ligando um polímero, ligando um radioisótopo, modulando a meia vida sérica, modulando a penetração tissular (por exemplo, tumores), modulando transporte ativo, modulando tecido, especificidade ou distribuição celular ou em órgão, modulação da imunogenicidade, modulação da resistência a protease, etc. Proteínas que incluem um aminoácido não natural podem ter propriedades catalíticas ou biofísicas aumentadas ou mesmo inteiramente novas. Por exemplo, as seguintes propriedades são opcionalmente modificadas por inclusão de um aminoácido não natural em uma proteína: toxicidade, biodistribuição, propriedades estruturais, propriedades espectroscópicas, propriedades químicas e/ou fotoquímicas, habilidade catalítica, meia-vida (incluindo mas não limitado a, meia-vida sérica), habilidade de reagir com outras moléculas, incluindo mas não limitada a, covalentemente ou não covalentemente, e semelhantes. As composições incluindo proteínas que incluem pelo menos um aminoácido não natural são úteis para, incluindo mas não limitadas a novas terapêuticas, diagnósticos, enzimas catalíticas, enzimas industriais, proteínas de ligação (incluindo mas não limitadas a, anticorpos), e incluindo mas não limitadas a, estudo de estrutura e função de proteína. Ver, por exemplo, Dougherty, (2000) Unnatural Amino Acids as Probes of Protein Structure and Function, Current Opinion in Chemical Biology, 4:645-652.
[00276]Em um aspecto da invenção, uma composição inclui pelo menos uma proteína com pelo menos um, incluindo, mas não limitado a, pelo menos dois, pelo menos três, pelo menos quatro, pelo menos cinco, pelo menos seis, pelo menos sete, pelo menos oito, pelo menos nove ou pelo menos dez ou mais aminoácidos não naturais. Os aminoácidos não naturais podem ser os mesmos ou diferentes, incluindo, mas não limitados a, podem ser 1, 2, 3, 4, 5, 6, 7, 8, 9 ou 10 ou mais sítios diferentes na proteína que compreendem 1, 2, 3, 4, 5, 6, 7, 8, 9 ou 10 ou mais ami- noácidos não naturais diferentes. Em outro aspecto, uma composição inclui uma proteína com pelo menos um, mas menos que todos, de um aminoácido particular presente na proteína é substituído com um aminoácido não natural. Para uma dada proteína com mais que um aminoácido não natural, os aminoácidos não naturais podem ser idênticos ou diferentes (incluindo, mas não limitados, a proteína pode incluir dois ou mais tipos diferentes de aminoácidos não naturais, ou podem incluir dois ou mais aminoácidos não naturais). Para uma dada proteína com mais que dois aminoácidos não naturais, os aminoácidos não naturais podem ser os mesmos, diferentes ou uma combinação de um aminoácido não natural múltiplo do mesmo tipo com pelo menos um aminoácido não natural diferente.
[00277]Proteínas ou polipeptídeos de interesse com pelo menos um amino- ácido não natural são uma característica da invenção. A invenção também inclui po- lipeptídeos ou proteínas com pelo menos um aminoácido não natural produzido utili-zando as composições e métodos da invenção. Um excipiente (incluindo, mas não limitado a, um excipiente farmaceuticamente aceitável) pode também estar presente com a proteína.
[00278]Por produção de proteínas ou polipeptídeos de interesse com pelo menos um aminoácido não natural em células eucarióticas, proteínas ou polipeptí- deos tipicamente incluirão modificações pós-traducionais eucarióticas. Em certas modalidades, uma proteína inclui pelo menos um aminoácido não natural e pelo menos uma modificação pós-traducional que é feita in vivo por uma célula eucariótica, onde a modificação pós-traducional não é feita por uma célula procariota. Por exemplo, a modificação pós-traducional inclui, incluindo, mas não limitada a acetilação, acilação, modificação lipídica, palmitoilação, adição de palmitato, fosforilação, modificação de ligação de glicolipídeo, glicosilação, e semelhantes. Em um aspecto, a modificação pós-traducional inclui ligação de um oligossacarídeo (incluindo, mas não limitado a, (GlcNAc-Man)2-Man-GlcNAc-GlcNAc)) a uma asparagina por uma ligação Glc-Nac-asparagina. Ver Tabela 1 que lista algum exemplos de oligossacarídeos N- ligados de proteínas eucarióticas (resíduos adicionais podem também estar presentes, que não são mostrados). Em outro aspecto, a modificação pós-traducional inclui ligação de um oligossacarídeo (incluindo, mas não limitado a, Gal-GalNAc, Gal- GlcNAc, etc) a uma serina ou treonina por uma ligação GalNAc-serina ou GalNAc- treonina, ou uma ligação GlcNAc-serina ou uma GlcNAc-treonina. TABELA 1: EXEMPLOS DE OLIGOSSACARÍDEOS ATRAVÉS DA LIGAÇÃO GlcNAc
[00279]Em ainda outro aspecto, a modificação pós-traducional inclui proces-samento proteolítico de precursores (incluindo mas não limitado a, precursor calcito- nina, precursor peptídico relacionado ao gene da calcitonina, hormônio pré- proparatireóide, pré-proinsulina, pró-insulina, pré-proopiomelanocortina, pró- opiomeanocortina e semelhantes), reunião em uma proteína multi-subunidade ou reunião macromolecular, tradução para outro sítio na célula (incluindo mas não limitado a, organelas, tais como retículo endoplasmático, aparato de Golgi, núcleo, li- sossoma, peroxisoma, mitocôndria, cloroplasto, vacúolos etc, ou através da via se- cretória). Em certas modalidades, a proteína compreende uma secreção ou sequência localizadora, um epítopo marcador, um marcador FLAG, um marcador poli- histidina, uma fusão GST, ou semelhantes.
[00280]Uma vantagem de um aminoácido é que ele está presente em frações adicionais químicas que podem ser utilizadas para adicionar moléculas adicionais. Essas modificações podem ser feitas in vivo em uma célula eucariótica ou não eucariótica, ou in vitro. Então, em certas modalidades, a modificação pós-traducional é através do aminoácido não natural. Por exemplo, a modificação pós-traducional pode ser através de uma reação nucleofílica-eletrofílica. Mais reações correntemente utilizadas para a modificação seletiva de proteínas envolve formação de ligação co-valente entre parceiros de reação nucleofílicos e eletrofílicos, incluindo, mas não li-mitados a reação de α-halocetonas com cadeias laterais de histidina ou cisteína. Se-letividade nesses casos é determinada pelo número e acessibilidade de resíduos nucleofílicos na proteína. Em proteínas da invenção, outras reações mais seletivas podem ser utilizadas tal como a reação de um ceto-aminoácido não natural com hi- drazidas ou compostos aminoóxido, in vitro e in vivo. Ver, por exemplo, Cornish, et al (1996) J. Am. Chem. Soc., 188:8150-8151; Mahal et al (1997) Science, 276:11251128; Wang, et al (2001) Science 292:498-500: Chin, et al, (2002) J. Am Chem. Soc. 124:9026-9027; Chin, et al (2002) Proc. Natl. Acad. Sci. 99:11020-11024; Wang, et al (2003) Proc. Natl. Acad. Sci. 100:56-61; Zhang, et al (2003) Biochemistry 42:67356746; e, Chin, et al, (2003) Science, 301:964-7, todas as quais são aqui incorporadas por referência. Isto permite a marcação seletiva de virtualmente qualquer proteína com um hospedeiro de reagentes incluindo fluoróforos, agentes de ligação cruza- da, derivados sacarídeos e moléculas citotóxicas. Ver também, Patente dos EUA No. 6.927.042 intitulada “Glycoprotein synthesis”, que é aqui incorporada por referência. Modificações pós-traducionais, incluindo, mas não limitado a, através de aminoáci- dos azida, podem também ser feitas através da ligação Staudinger (incluindo, mas não limitada a, com reagentes triarilfosfino). Ver, por exemplo, Kiick et al (2002) Incorporation of azides into recombinant proteins for chemoselective modification by the Staudinger ligation, PNAS, 99:19-24.
[00281]Esta invenção prove outro método altamente eficiente para a modifi-cação seletiva de proteínas, que envolvem a incorporação genética de aminoácidos não naturais, incluindo, mas não limitados a, contendo uma fração azida ou alquinila em proteínas em resposta a um códon seletor. Essas cadeias laterais aminoácidos podem então ser modificadas por, incluindo, mas não limitadas a, uma reação de cicloadição [3+2] de Huisgen (ver, por exemplo, Padwa, A. Em Comprehensive Organic Synthesis, vol. 4 (1991) Ed. Trost. B.M. Pergamon, Oxford, p. 1069-1109; e Huisgen, R. em 1,3-Dipolar Cycloaddition Chemistry (1984) Ed. Padwa, A., Wiley, Nova Iorque, p.1-176) com, incluindo, mas não limitado a, derivados alquinila ou azi- da, respectivamente. Porque este método envolve uma cicloadição ao invés de uma substituição nucleofílica, proteínas podem ser modificadas com extremamente alta seletividade. Esta reação pode ser realizada em temperatura ambiente em condições aquosas com excelente regioseletividade (1,4>1,5) pela adição de quantidades catalíticas de sais de Cu(I) à mistura reacional. Ver, por exemplo, Tornoe et al, (2002), J. Org. Chem. 67:3057-3064; e, Rostovtsev, et al (2002) Angew. Chem. Int. Ed. 41:2596-2599. Outro método que pode ser utilizado é a troca de ligante em um composto biarsênico com um motivo tetracisteína, ver, por exemplo, Griffin, et al (1998) Science, 281:269-272.
[00282]Uma molécula que pode ser adicionada a uma proteína da invenção através de uma cicloadição [3+2] inclui virtualmente qualquer molécula com um deri-vado azida ou alquinila. Moléculas incluem, mas não são limitadas a, corantes, fluo- róforos, agentes de ligação cruzada, derivados sacarídeos, polímeros (incluindo mas não limitados a, derivados de polietileno glicol), ligantes foto-cruzados, compostos citotóxicos, marcadores de afinidade, derivados de biotina, resinas, esferas, uma segunda proteína ou polipeptídeo (ou mais), polinucleotídeo(s) (incluindo mas não limitados a DNA, RNA etc), quelantes de metais, co-fatores, ácidos graxos, carboidratos, e semelhantes. Essas moléculas podem ser adicionadas a um aminoácido não natural com um grupo alquinila, incluindo, mas não limitado a p- propargiloxifenilalanina, ou grupo azido, incluindo, mas não limitado a p-azido- fenilalanina, respectivamente. V. Geração in vivo de polipeptídeo FGF-21 compreendendo aminoácidos não naturalmente codificados
[00283]Os polipeptídeos FGF-21 da invenção podem ser gerados in vivo uti-lizando tRNA e tRNA sintetases modificados para adicionar a ou aminoácidos substi-tutos que são codificados em sistemas de ocorrência não natural.
[00284]Métodos para gerar tRNAs e tRNA sintetases que usam aminoácidos que não são codificados em sistemas de ocorrência não natural são descritos em, por exemplo, Patente dos EUA Nos. 7.045.337 e 7.083.970 que são incorporados aqui por referência. Esses métodos envolvem geração de uma maquinaria de tradução que funciona independentemente das sintetases e tRNAs endógenas para o sistema de tradução (e são assim algumas vezes referidos como “ortogonal”). Tipicamente, o sistema de tradução compreende um tRNA ortogonal (O-tRNA) e uma ami- noacil tRNA sintetase ortogonal (O-RS). Tipicamente, o O-RS preferencialmente aminoacila o O-tRNA com pelo menos um aminoácido de ocorrência não natural no sistema de tradução e o O-tRNA com pelo menos um aminoácido de ocorrência não natural no sistema de tradução e o O-tRNA reconhece pelo menos um códon seletor que não é reconhecido por outros tRNAs no sistema. O sistema de tradução então insere o aminoácido não naturalmente codificado em uma proteína produzida no sistema, em resposta a um códon seletor codificado, assim “substituindo” um aminoáci- do na posição no polipeptídeo codificado.
[00285]Uma ampla variedade de tRNAs ortogonais e aminoacil tRNA sinte- tases têm sido descrito na técnica para inserir aminoácidos sintéticos particulares em polipeptídeos, e são geralmente adequados para uso na presente invenção. Por exemplo, ceto-específico O-tRNA/aminoacil-tRNA sintetase são descritos em Wang, L. et al, Proc. Natl. Acad. Sci. EUA 100:56-61 (2003) e Zhang, Z., et al, Biochem. 42(22):6735-6746 (2003). O-RS exemplar, ou porções dos mesmo, são codificados por sequências polinucleotídicas e incluem sequências aminoácidos reveladas na Patente dos EUA Nos. 7.045.337 e 7.083.970, cada uma incorporada aqui por referência. Moléculas O-tRNA correspondente para uso com os O-RSs são também descritos na Patente dos EUA Nos. 7.045.337 e 7.083.970 que são aqui incorporados por referência. Exemplos adicionais de pares O-tRNA/aminoacil-tRNA são descritas em WO 2005/007870, WO 2005/007624; e WO 2005/019415.
[00286]Um exemplo de sistema O-tRNA/aminoacil-tRNA azida-específico é descrito em Chin, J.W., et al, J. Am. Chem. Soc. 124:9026-9027 (2002). Sequências O-RS exemplares para p-azido-L-Phe incluem, mas não são limitados a, sequências nucleotídicas SEQ ID NOs: 14-16 e 29-32 e sequências aminoácidos SE Q ID NOs: 46-48 e 61-64 como revelado na Patente nos EUA No. 7.083.970 que é aqui incorporado por referência. Sequências O-tRNA exemplares adequadas para uso na presente invenção incluem, mas não são limitadas a, sequências nucleotídicas SEQ ID NOs: 1-3 como revelado na Patente dos EUA No. 7.083.970) que é aqui incorporada por referência. Outros exemplos de pares O-tRNA/aminoacil-tRNA sintetase específicos para aminoácidos não naturalmente codificados particulares são descritos na Patente dos EUA No. 7.045.337 que é aqui incorporado por referência. O-RS e O- tRNA que incorpora ambos, aminoácidos contendo ceto- e azida em S. cerevisiae são descritos em Chin, J.W., et al, Science 301:964-967 (2003).
[00287]Vários outros pares ortogonais têm sido relatados. Glutaminil (ver, por exemplo, Liu, D.R., e Schultz, P.G. (1999) Proc. Natl. Acad. Sci. EUA. 96:47804785), aspartil (ver, por exemplo, Pastrnak, M. et al (2000) Helv. Chim. Acta 83:2277-2286), e tirosil (ver, por exemplo, Ohno, S., et al, (1998) J. Biochem. (Tokyo, Japão) 124:1065-1068; e, Kowal, A.K., et al (2001)Proc. Natl. Acad. Sci. EUA 98:2268-2273) sistemas derivados a partir de tRNA de S. cerevisae sintetases têm sido descritas para a potencial incorporação de aminoácidos não naturais em E. coli. Sistemas derivados a partir de glutaminil de E. coli (ver, por exemplo, Kowal, A.K., et al (2001) Proc. Natl. Acad. Sci. EUA 98:2268-2273) e tirosil (ver, por exemplo, Edwards, H., e Schimmel, P. (1990) Mol. Cell. Biol. 10:1633-1641) sintetases têm sido descritas para uso em S. cerevisiae. O sistema E. coli tem sido utilizado para incorporação de 3-iodo-L-tirosina in vivo, em células mamíferas. Ver, Sakamoto, K., et al, (2002) Nucleic Acids Res. 30:4692-4699.
[00288]Uso de O-tRNA/aminoacil-tRNA sintetases envolve seleção de um códon específico que codifica o aminoácido não naturalmente codificado. Enquanto qualquer códon pode ser utilizado, é geralmente desejável selecionar um códon que é raramente ou nunca utilizado na célula em que a O-tRNA/aminoacil-tRNA sintetase é expressa. Por exemplo, códons exemplares incluem códon não sendo tal como códon de parada (âmbar, ocre e opala), quatro ou mais bases códons e outros três códons base que são raros ou não utilizados.
[00289]Códon(s) seletor(es) específico(s) podem ser introduzidos em posições apropriadas na sequência codificante do polinucleotídeo FGF-21 utilizando métodos de mutagênese conhecidos na técnica (incluindo, mas não limitado a, mutagê- nese sítio-específica, mutagênese cassete, mutagênese de restrição de seleção etc).
[00290]Métodos para gerar componentes da maquinaria biossintética de pro-teína, tal como O-RSs, O-tRNAs e pares O-tRNA/O-RS que podem ser utilizados para incorporar um aminoácido não naturalmente codificado são descritos em Wang, L. et al, Science 292:498-500 (2001); Chin, J. W., et al, J. Am. Chem. Soc. 124:90269027 (2002); Zhang, Z., et al, Biochemistry 42: 6735-6746 (2003). Métodos e composições para a incorporação in vivo de aminoácidos não naturalmente codificados são descritos na Patente dos EUA No. 7.045.337, que é aqui incorporada por referência. Métodos para selecionar um par tRNA ortogonal/tRNA sintetase para uso no sistema de tradução in vivo de um organismo são também descritos na Patente dos EUA Nos. 7.045.337 e 7.083.970 que são aqui incorporados por referência. Pedido PCT No. WO04/035743 intitulado “site Specific Incorporation of Keto Amino Acids into Proteins”, que é aqui incorporado por referência em sua totalidade, descreve pares RS ortogonal e tRNA para a incorporação de ceto-aminoácidos. Pedido PCT No. WO04/094593 intitulado “Expanding the Eukaryotic Genetic Code”, que é aqui incorporado por referência em sua totalidade, descreve pares RS ortogonal e tRNA para a incorporação de aminoácidos não naturalmente codificiados em células hospedeiras eucarióticas.
[00291]Métodos para produção de pelo menos uma aminoacil-tRNA sinte- tase ortogonal (O-RS) recombinante compreende: (a) geração de uma biblioteca de (opcionalmente mutante) RSs derivados a partir de pelo menos uma aminoacil-tRNA sintetase (RS) a partir de um primeiro organismo, incluindo mas não limitado a, or-ganismo procariótico, tais como Methanococcus jannaschii, Methanobacterium ther- moautotrophicum, Halobacterium, Escherichia coli, A. Fulgidus, P. Furiosus, P. Hori- koshii, A. Pernix, T. Thermophilus, ou semelhantes, ou um organismo eucarioto; (b) seleção (e/ou avaliação) da biblioteca de RSs (opcionalmente RSs mutante) para membros que aminoacilam um tRNA ortogonal (O-tRNA) em presença de um ami- noácido não naturalmente codificado e um aminoácido natural, assim provendo um grupo de RSs ativos (opcionalmente mutante); e/ou, (c) seleção (opcionalmente através de seleção negativa) do grupo para RSs ativa (incluindo, mas não limitada a RSs mutante) que preferivelmente aminoacila o O-tRNA em ausência do aminoácido não naturalmente codificado, assim provendo pelo menos um O-RS recombinante; em que pelo menos um O-RS recombinante preferivelmente aminoacila o O-tRNA com o aminoácido não naturalmente codificado.
[00292]Em uma modalidade, o RS é um RS inativo. O RS inativo pode ser gerado por mutação de um RS ativo. Por exemplo, o RS inativo pode ser gerado por mutação pelo menos cerca de 1, pelo menos cerca de 2, pelo menos cerca de 3, pelo menos cerca de 4, pelo menos cerca de 5, pelo menos cerca de 6, ou pelo menos cerca de 10 ou mais aminoácidos para diferentes aminoácidos, incluindo, mas não limitados a alanina.
[00293]Bibliotecas de RSs mutantes podem ser geradas utilizando várias técnicas conhecidas na arte, incluindo, mas não limitadas pelo desenho racional na estrutura RS de proteína tri-dimensional, ou mutagênese de nucleotídeos RS em uma técnica de desenho aleatória ou racional. Por exemplo, o mutante RSs pode ser gerado por mutações sítio-específicas, mutações aleatórias, mutações de recombi- nação de geração de diversidade, construções quiméricas, desenho racional e por outros métodos descritos aqui ou conhecidos na técnica.
[00294]Em uma modalidade, seleção (e/ou avaliação) da biblioteca de RSs (opcionalmente RSs mutantes) para membros que são ativos, incluindo mas não limitados a, que aminoacilam um tRNA ortogonal (O-tRNA) em presença de um ami- noácido não naturalmente codificado e um aminoácido natural, inclui: introdução de um marcador de seleção ou análise positiva, incluindo mas não limitada a um gene de resistência a antibiótico, ou semelhantes, e a biblioteca de (opcionalmente mutante) RSs em uma pluralidade de células, em que o marcador de seleção e/ou avaliação positiva compreende pelo menos um códon seletor incluindo, mas não limitado a, códon âmbar, ocre, ou opala; crescimento de uma pluralidade de células em presença de um agente de seleção; identificação de células que sobrevivem (ou mostram uma resposta específica) em presença da seleção e/ou avaliação do agente por supressão de pelo menos um códon seletor no marcador de seleção ou avaliação positiva, assim provendo um subgrupo de células positivamente selecionadas que contêm o grupo de RSs ativos (opcionalmente mutantes). Opcionalmente, a concentração do agente de seleção e/ou avaliação pode ser variada.
[00295]Em um aspecto, o marcador de seleção positiva é um gene cloram- fenicol acetiltransferase (CAT) e o códon seletor é um códon de parada âmbar no gene CAT. Opcionalmente, o marcador de seleção positiva é um gene de β- lactamase e o códon seletor é um códon de parada âmbar no gene da β-lactamase. Em outro aspecto, o marcador de seleção positiva compreende um marcador fluorescente ou luminescente ou um marcador de seleção baseado em afinidade (incluindo, mas não limitado a um marcador de superfície celular).
[00296]Em uma modalidade, grupo de seleção ou avaliação negativa para RSs ativos (opcionalmente mutantes) que preferivelmente aminoacilam o O-tRNA em ausência de aminoácidos não naturalmente codificados incluem: introdução de um marcador de seleção ou avaliação negativa com o grupo de RSs ativos (opcionalmente mutantes) a partir da seleção ou avaliação positiva em uma pluralidade de células de um segundo organismo, em que o marcador de seleção ou avaliação negativa compreende pelo menos um códon seletor (incluindo mas não limitado a um gene de resistência a antibiótico, incluindo, mas não limitado a um gene cloranfeni- col acetiltransferase (CAT); e identificando células que sobrevivem ou mostram uma resposta de seleção específica em um primeiro meio suplementado com o aminoáci- do não naturalmente codificado e um agente de seleção ou avaliação, mas falha em sobreviver ou mostrar a resposta específica em um segundo meio não suplementado com aminoácido não naturalmente codificado e o agente de seleção ou avaliação, assim provendo células de sobrevivência ou células selecionadas com pelo menos um O-RS recombinante. Por exemplo, protocolo de identificação CAT opcionalmente atua como uma seleção positiva e/ou seleção negativa na determinação de O-RS recombinantes apropriados. Por exemplo, um grupo de clones é opcionalmente re-plicado em placas de crescimento contendo CAT (que compreende pelo menos um códon seletor) ou com ou sem um ou mais aminoácidos não naturalmente codificados. Colônias crescendo exclusivamente nas placas contendo aminoácidos não na-turalmente codificados são então selecionados como contendo O-RS recombinante. Em um aspecto, a concentração do agente de seleção (e/ou avaliação) é variada. Em alguns aspectos o primeiro e segundo organismos são diferentes. Então, o primeiro e/ou segundo organismo opcionalmente compreende: um procarioto, um euca- rioto, um mamífero, uma Escherichia cole, um fungo, uma levedura, uma archeabac- téria , uma eubactéria, uma planta, um inseto, um protista etc. Em outras modalidades, o marcador de seleção compreende um marcador de seleção de fluorescência ou luminescência ou um marcador de seleção baseado em afinidade.
[00297]Em outra modalidade, seleção ou avaliação (incluindo mas não limi- tado a, seleção negativa) o grupo para RSs ativos (opcionalmente mutantes) incluem: isolamento do grupo de RSs mutantes ativos a partir do passo de seleção positiva (b); introdução de um marcador de seleção ou avaliação negativo, em que o marcador de seleção ou avaliação negativa compreende pelo menos um códon seletor (incluindo mas não limitados a gene de marcador tóxico, incluindo mas não limitado a, gene da ribonucleoase barnase, compreendendo pelo menos um códon seletor), e o grupo do RSs ativo (opcionalmente mutante) em uma pluralidade de células de um segundo organismo; e identificados células que sobrevivem ou mostram uma resposta de seleção específica em um primeiro meio não suplementado com o aminoá- cido não naturalmente codificado, mas falha em sobreviver ou demonstrar uma resposta de seleção específica em um segundo meio suplementado com o aminoácido não naturalmente codificado, assim provendo células sobreviventes ou selecionadas com pelo menos um O-RS recombinante, em que pelo menos um O-RS recombinan- tes é específico para o aminoácido não naturalmente codificado. Em um aspecto, pelo menos um códon seletor compreende cerca de dois ou mais códons seletores. Tais modalidades opcionalmente podem incluir em que pelo menos um códon sele- tor compreende dois ou mais códons seletores, e em que o primeiro e segundo organismo são diferentes (incluindo, mas não limitado a, cada organismo é opcionalmente, incluindo mas não limitado a, um procarioto, um eucarioto, um mamífero, uma Escherichia coli, um fungo, uma levedura, uma archeabactéria, uma planta, um inseto, um protista, etc). Também, alguns aspectos incluem em que o marcador de seleção negativa compreende um gene ribonuclease barnase (que compreende pelo menos um códon seletor). Outros aspecto incluem em que o marcador de seleção opcionalmente compreende um marcador de seleção fluorescente ou luminescente ou um marcador de seleção baseado em afinidade. Nas modalidades aqui, as seleções e/ou avaliações opcionalmente incluem variação da severidade de seleção e/ou avaliação.
[00298]Em uma modalidade, os métodos para produzir pelo menos uma aminoacil-tRNA sintetase ortogonal (O-RS) recombinante pode ainda compreender: (d) isolar pelo menos uma O-RS recombinante; (e) gerar um segundo grupo de O- RS (opcionalmente mutado) derivado a partir de pelo menos uma O-RS recombinan- te; e, (f) passos de repetição (b) e (c) até uma O-RS mutada ser obtida que compreenda uma habilidade de preferencialmente aminoacilar a O-tRNA. Opcionalmente, passos (d)-(f) são repetidos, incluindo, mas não limitados a, pelo menos cerca de suas vezes. Em um aspecto, o segundo grupo de O-RS derivado a partir de pelo menos um O-RS recombinante pode ser gerado por mutagênese, incluindo, mas não limitado a, mutagênese aleatória, mutagênese sítio-específica, recombinação ou um combinação das mesmas.
[00299]A severidade dos passos de seleção/avaliação, incluindo, mas não limitado ao passo de seleção/avaliação positiva (b), o passo de seleção/avaliação negativo (c) ou ambos, passos de seleção/avaliação positiva e negativa (b) e (c), nos métodos acima descritos, opcionalmente incluem variação na severidade de sele- ção/avaliação. Em outra modalidade, o passo de seleção/avaliação positiva (b), o passo de seleção/avaliação negativa (c) ou ambos os passos de seleção/avaliação positiva e negativa (b) e (c) compreendem uso de um repórter, em que o repórter é detectado por seleção de célula ativada por fluorescência (FACS) ou em que o repórter é detectado por luminescência. Opcionalmente, o repórter é revelado em uma superfície celular, revelado em um fago ou semelhante, e selecionado baseado sob a afinidade ou atividade catalítica envolvendo o aminoácido não naturalmente codificado ou um análogo. Em uma modalidade, a sintetase mutada é revelada em uma superfície celular, em um fago revelado ou semelhante.
[00300]Métodos para produzir um tRNA ortogonal recombinante (O-tRNA) incluem: (a) geração de uma biblioteca de tRNAs mutantes derivada a partir de pelo menos um tRNA, incluindo, mas não limitado a um supressor de tRNA, a partir de um primeiro organismo; (b) seleção (incluindo, mas não limitado a seleção negativa) ou seleção da biblioteca para (opcionalmente mutante) tRNAs que são aminoacila- dos por aminoacil-tRNA sintetase (RS) a partir de um segundo organismo em ausência de um RS a partir do primeiro organismo, assim provendo um grupo de tRNAs (opcionalmente mutante); e, (c) selecionando ou avaliando o grupo de tRNAs (opcionalmente mutantes) para membros que são aminoacilados por um RS ortogonal introduzido (O-RS), assim provendo pelo menos um O-tRNA recombinante; em que pelo menos um O-tRNA recombinante reconhece um códon seletor e não é eficientemente reconhecido pelo RS a partir do segundo organismo e é preferivelmente aminoacilado por O-RS. Em algumas modalidades, pelo menos um tRNA é um tRNA supressor e/ou compreende um único códon de três bases de bases naturais e/ou não naturais, ou é um códon não senso, um códon raro, ou um códon de parada opala. Em uma modalidade, o O-tRNA recombinante possui um melhoramento de ortogonalidade. Será apreciado que em algumas modalidades, O-tRNA é opcionalmente importado em um primeiro organismo a partir de um segundo organismo sem a necessidade para modificação. Em várias modalidades, os primeiro e segundo organismos são ou os mesmos ou diferentes e são opcionalmente escolhidos a partir de, incluindo, mas não limitados a, procariotos (incluindo, mas não limitados a, Me- thanococcus jannaschii, Methanobacterium thermoautotrophicum, Escherichia coli, Halobacterium etc), eucariotos, mamíferos, fungos, leveduras, archeabactéria, eubactéria, plantas, inspetor, protistas etc. Adicionalmente, o tRNA recombinante é opcionalmente aminoacilado por um aminoácido não naturalmente codificado, em que o aminoácido não naturalmente codificado é biosintetizado in vivo ou naturalmente ou através de manipulação genética. O aminoácido não naturalmente codificado é opcionalmente adicionado a um meio de crescimento por pelo menos o primeiro ou segundo organismo.
[00301]Em um aspecto, seleção (incluindo, mas não limitado a, seleção ne-gativa) ou seleção de biblioteca para (opcionalmente mutante) tRNAs que são ami- noacilados por uma aminoacil-tRNA sintetase (passo (b)) incluem: introdução de um gene marcador tóxico, em que o gene marcador tóxico compreende pelo menos um dos códons seletores (ou um gene que leva a produção de uma agente tóxico ou estático ou um gene essencial para o organismo em que tal gene marcador compreende pelo menos um códon seletor) e a biblioteca de (opcionalmente mutante) tRNAs em uma pluralidade de células a partir do segundo organismo; e, seleção de células sobreviventes, em que as células sobreviventes contêm o grupo de (opcio-nalmente mutante) tRNAs compreendendo pelo menos um tRNA ortogonal ou tRNA não funcional. Por exemplo, células sobreviventes podem ser selecionadas por uso de uma comparação da proporção do ensaio de densidade celular.
[00302]Em um aspecto, o gene marcador tóxico inclui dois ou mais códons seletores. Em uma modalidade dos métodos, o gene marcador tóxico é um gene ribonuclease barnase, onde o gene ribonuclease barnase compreende pelo menos um códon âmbar. Opcionalmente, o gene ribonuclease barnase pode incluir dois ou mais códons âmbar.
[00303]Em uma modalidade, seleção ou avaliação do grupo de (opcionalmente mutante) tRNAs para membros que são aminoacilados por um RS ortogonal (O-RS) introduzido pode incluir: introdução de um gene marcador de seleção ou avaliação positiva, em que o gene marcador positivo compreende um gene de resistência a droga (incluindo, mas não limitado a gene da β-lactamase, compreendendo pelo menos um dos códons seletores, tal como pelo menos um códon de parada âmbar) ou um gene essencial para o organismo, ou um gene que leva a detoxifica- ção de um agente tóxico, junto com o O-RS, e o grupo de (opcionalmente mutante) tRNA em um pluralidade de células a partir do segundo organismo; e, identificando a sobrevivência ou crescimento de células selecionadas em presença de um agente seletor ou avaliador, incluindo mas não limitado a, um antibiótico, assim provendo um grupo de células possuindo pelo menos um tRNA recombinante, onde pelo menos um tRNA recombinante é aminoacilado pelo O-RS e insere um aminoácido em um produto de tradução codificado pelo gene marcador positivo, em resposta a pelo menos um códon seletor. Em outra modalidade, a concentração do agente seletor e/ou avaliador é variada.
[00304]Métodos para gerar pares O-tRNA/O-RS específicos são providos. Métodos incluem: (a) gerar uma biblioteca de tRNAs mutantes derivada a partir de pelo menos um tRNA a partir de um primeiro organismo; (b) selecionar ou avaliar negativamente a biblioteca para (opcionalmente mutante) tRNAs que são aminoaci- lados por uma aminoacil-tRNA sintetase (RS) a partir de um segundo organismo em ausência de uma RS a partir do primeiro organismo, assim provendo um grupo de (opcionalmente mutante) tRNAs; (c) selecionando ou avaliando o grupo de (opcio-nalmente mutante) tRNAs para membros que são aminoacilados por um RS ortogonal (O-RS) introduzido, assim provendo pelo menos um O-tRNA recombinante. Pelo menos um O-tRNA recombinante reconhece um códon seletor e não é eficientemente reconhecido pela RS a partir do segundo organismo e é preferivelmente aminoaci- lado pelo O-RS. O método também inclui (d) gerar uma biblioteca de (opcionalmente mutante) RSs derivada a partir de pelo menos uma aminoacil-tRNA sintetase (RS) a partir de um terceiro organismo; (e) selecionando ou avaliando a biblioteca de RSs mutantes para membros que preferivelmente aminoacilam pelo menos um O-tRNA recombinante em presença de um aminoácido não naturalmente codificado e um aminoácido natural, assim provendo um grupo de RSs ativos (opcionalmente mutante); e, (f) negativamente selecionando ou avaliando o grupo para RSs ativo (opcionalmente mutante) que preferencialmente aminoacila pelo menos um O-tRNA re- combinante em ausência do aminoácido não naturalmente codificado, assim provendo pelo menos um par O-tRNA/O-RS específico, em que pelo menos um par O- tRNA/O-RS específico compreende pelo menos um O-RS recombinante que é específico para o aminoácido não naturalmente codificado e pelo menos um O-tRNA re- combinante. Pares O-tRNA/O-RS específicos produzidos pelos métodos são incluídos. Por exemplo, o par O-tRNA/O-RS específico pode incluir, incluindo, mas não limitado a um par mutRNATYr-mutTyrRS, tal como um par mutRNATyr-SS12TyrRS, um par mutRNALeu-mutLeuRS, um par mutRNAThr-mutThrRS, um par mutRNAGlu- mutGluRS, ou semelhantes. Adicionalmente, tais métodos incluem em que o primeiro e terceiro organismo são os mesmos (incluindo, mas não limitados a, Methano- coccus jannaschii).
[00305]Métodos para seleção de um par tRNA ortogonal-tRNA sintetase para uso em um sistema de tradução in vivo de um segundo organismo são também incluídos na presente invenção. Os métodos incluem: introdução de um gene marcador, um tRNA e uma aminoacil-tRNA sintetase (RS) isolada ou derivada a partir de um primeiro organismo em um primeiro grupo de células a partir de um segundo organismo; introduzindo o gene marcador e o tRNA em um grupo celular duplicado a partir de um segundo organismo; e, selecionado para células sobreviventes no primeiro grupo que falham em sobreviver em um grupo de células duplicadas ou selecionando para células mostrando uma resposta de seleção específica que falha para dar tal resposta no grupo celular duplicado, em que o primeiro grupo e o grupo celular duplicado são crescidos em presença de uma agente de seleção ou de avaliação, em que as células sobreviventes ou selecionadas compreendem o par tRNA ortogo- nal-tRNA sintetase para uso no sistema de tradução in vivo do segundo organismo. Em uma modalidade, comparando e selecionando ou avaliando inclui um ensaio de complementação in vivo. A concentração do agente de seleção ou avaliação pode ser variada.
[00306]Os organismos da presente invenção compreendem uma variedade de organismos e uma variedade de combinações. Por exemplo, o primeiro e segundo organismos dos métodos da presente invenção podem ser os mesmos ou diferentes. Em uma modalidade, os organismos são opcionalmente um organismo pro- carioto, incluindo, mas não limitado a Methanococcus jannaschii, Methanobacterium thermoautotrophicum, Halobacterium, Escherichia coli, A. fulgidus, P. furiosus, P. horikoshii, A. pernix, T. thermophilus, ou semelhantes. Alternativamente, os organismos opcionalmente compreendem um organismo eucarioto, incluindo mas não limitado a plantas (incluindo mas não limitado a plantas complexas tais como mono- cotiledôneas ou dicotiledôneas), algas, protistas, fungos (incluindo mas não limitados a levedura etc), animais (incluindo mas não limitados a mamíferos, insetos, artrópodes, etc) ou semelhantes. Em outra modalidade, o segundo organismo é um organismo procarioto, incluindo, mas não limitado a, Methanococcus jannaschii, Metha- nobacterium thermoautotrophicum, Halobacterium, Escherichia coli, A. fulgidus, P. furiosus, P. horikoshii, A. pernix, T. Thermophilus ou semelhantes. Alternativamente, o segundo organismo pode ser um organismo eucarioto, incluindo, mas não limitado a uma levedura, uma célula animal, uma célula de planta, um fungo, uma célula mamífera, ou semelhantes. Em várias modalidades o primeiro e segundo organismos são diferentes. VI. Localização de aminoácidos não ocorrência não natural em polipeptídeos FGF-21
[00307]A presente invenção contempla incorporação de um ou mais amino- ácidos de ocorrência não natural em polipeptídeos FGF-21. Um ou mais aminoáci- dos de ocorrência não natural podem ser incorporados em uma posição particular que não impede a atividade do polipeptídeo. Isto pode ser alcançado por fazer substituições “conservadas”, incluindo, mas não limitado a, substituição de aminoácidos hidrofóbicos com aminoácidos hidrofóbicos, aminoácidos grandes por aminoácidos grandes, aminoácidos hidrofílicos por aminoácidos hidrofílicos e/ou inserindo o ami- noácido de ocorrência não natural em um local que não é requerido para atividade.
[00308]Uma variedade de abordagens bioquímicas e estruturais pode ser empregada para selecionar os sítios desejados para substituição com um aminoáci- do não codificado naturalmente dentro do polipeptídeo FGF-21. É facilmente aparente para os versados na técnica que qualquer posição da cadeia polipeptídica é adequada para seleção para incorporar um aminoácido não naturalmente codificado, e seleção pode ser baseada no desenho racional ou pode seleção aleatória para qualquer ou nenhum propósito particular desejado. Seleção de sítios desejados pode ser para produzir uma molécula FGF-21 tendo qualquer propriedade ou atividade desejada, incluindo mas não limitado a agonistas, super-agonistas, agonistas inversos, antagonistas, moduladores de ligação a receptor, moduladores de atividade do receptor, formação de dímeros ou multímeros, nenhuma mudança na atividade ou propriedade comparada a molécula nativa, ou manipulação de qualquer propriedade física ou química do polipeptídeo tal como solubilidade, agregação, ou estabilidade. Por exemplo, localizações no polipeptídeo requeridas para atividade biológica de polipeptídeos FGF-21 podem ser identificadas utilizando análise de mutação pontu- al, mapeamento de alanina, saturação de mutagênese e seleção para atividade bio-lógica, ou métodos de mapeamento homólogo na técnica. Resíduos que são críticos para bioatividade de FGF-21, resíduos que são envolvidos com a estabilidade far-macêutica, epítopos de anticorpos, ou resíduos ligantes de receptor ou heparina podem ser mutados. Patente dos EUA No. 5.580.723; 6.013.478; 6.428.954; e 6.451.561, que são aqui incorporadas por referência, métodos descritos para análise sistemática da estrutura e função de polipeptídeos tal como FGF-21 por identificação de domínios ativos que influenciam a atividade do polipeptídeo com uma substância alvo. Resíduos outros que aqueles identificados como críticos para a atividade biológica por mapeamento de mutagênese de alanina ou homóloga podem ser bons candidatos para substituição com um aminoácido não naturalmente codificado dependendo da atividade desejada procurada para o polipeptídeo. Alternativamente, os sítios identificados como críticos para atividade biológica podem também ser bons candidatos para substituição com um aminoácido não naturalmente codificado, novamente dependendo da atividade desejada procurada para o polipeptídeo. Outra alternativa pode ser simplesmente fazer substituições seriadas em cada posição na cadeia polipeptídica com um aminoácido não naturalmente codificado e observar o efeito nas atividades do polipeptídeo. É facilmente aparente para os versados na técnica que qualquer meio, técnica, ou método para selecionar uma posição para substituição com um aminoácido não natural em qualquer polipeptídeo é adequada para uso na presente invenção.
[00309]Muitos dados já têm sido coletados utilizando os métodos apresentados neste pedido e sítios potenciais e benéficos de mutação têm sido encontrados e testados com sucesso, como descrito nos exemplos providos nesta especificação. Informação adicional descoberta em relação a estrutura e atividade de mutantes, mesmo aqueles que incluem alguns detalhes em relação a formulação e/ou teste que não tenha sido especificamente descrito nos exemplos, dos polipeptídeos FGF- 21 que contêm deleções podem também ser examinados para determinar regiões da proteína que são provavelmente ser tolerantes de substituição com um aminoácido não naturalmente codificado. Em uma forma similar, digestão de protease e anticorpos monoclonais pode ser utilizada para identificar regiões de FGF-21 que são res-ponsáveis para ligação do receptor FGF-21. Uma vez os resíduos que são prova-velmente para serem intolerantes para substituição com aminoácidos não naturalmente codificados tenham sido eliminados, o impacto das substituições propostas em cada uma das posições remanescentes pode ser examinado. Modelos podem ser gerados a partir de estruturas cristaus tri-dimensionais de outros membros da família FGF e receptores FGF. Banco de Dados de Proteína (BDP, disponível na World Wide Web em rcsb.org) é um banco de dados centralizado contendo dados estruturais tri-dimensionais de grandes moléculas de proteínas e ácidos nucléicos. Modelos podem ser feitos investigando a estrutura secundária e terciária de polipep- tídeos, se dados tri-dimensionais não são disponíveis. Então, aqueles versados na técnica podem facilmente identificar posições aminoácidos que podem ser substituídas com aminoácidos não naturalmente codificados.
[00310]Em algumas modalidades, os polipeptídeos FGF-21 da invenção compreendem um ou mais aminoácidos de ocorrência não natural em uma região da proteína que não rompe a estrutura do polipeptídeo.
[00311]Resíduos exemplares de incorporação de um aminoácido não natu-ralmente codificado podem ser aqueles que são excluídos a partir de potenciais regiões de ligação de receptor, podem ser completamente ou parcialmente expostas a solvente, têm mínimas ou nenhuma interação de ligação de hidrogênio com resíduos vizinhos, podem ser minimamente expostos para resíduos reativos ao redor, podem ter uma ou mais das faces expostas, podem ser um sítio ou sítios que são justapostos a um segundo FGF-21, ou outra molécula ou fragmento do mesmo, podem estar em regiões que são altamente flexíveis, ou estruturalmente rígidas, como predito pela estrutura tri-dimensional secundária, terciária ou quaternária do FGF-21, ligado ou não ligado a seu receptor, ou acoplado ou não acoplado a outra molécula biologicamente ativa, ou pode modular a conformação do FGF-21 por si mesmo ou um dí- mero ou multímero compreendendo um ou mais FGF-21, por alterar a flexibilidade ou rigidez da estrutura completa como desejado.
[00312]A família de proteínas FGF tem uma estrutura comum β-trevo ou β- folha como identificado por cristalografia (Harmer et al, Biochemistry 43:629-640 (2004)). Um versado na técnica reconhece que tais análises de FGF-21 permitem a determinação de quais resíduos aminoácidos são expostos a superfície comparada a resíduos aminoácidos que são enterrados dentro da estrutura terciária da proteína. Assim, é uma modalidade da presente invenção substituir um aminoácido não naturalmente codificado por um aminoácido que é um resíduo exposto na superfície.
[00313]Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em qualquer posição em FGF-21: 1-181 a partir da SEQ ID NO:1 ou aminoácidos correspondentes na SEQ ID NOs:2-7. Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições no FGF-21: antes da posição 1 (isto é, no N-terminal), , 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais posições em FGF-21: 10, 52, 117, 126, 131, 162, 87, 77, 83, 72, 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 10, 52, 77, 117, 126, 131, e 162 (SEQ ID NO:1 ou aminoácidos correspon-dentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 87, 77, 83, 72 (SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7).
[00314]Em uma modalidade, o aminoácido de ocorrência não natural está na posição 91 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na po-sição 131 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 108 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 77 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 72 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 87 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 86 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 126 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 110 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 83 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na po- sição 146 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 135 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 96 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7). Em uma modalidade, o aminoácido de ocorrência não natural está na posição 36 em FGF-21(SEQ ID NO:1 ou aminoácidos correspondentes das SEQ ID NOs: 2-7).
[00315]Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e outro aminoácido de ocorrência não natural em uma das seguintes posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e outro aminoácido de ocorrência não natural em uma das seguintes posições: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96 e 36 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e na posição 131 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e na posição 77 (SEQ ID NO: 1 ou os aminoácidos cor- respondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e na posição 108 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 131 e na posição 108 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 131 e na posição 77 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 131 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 108 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 77 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 72 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 87 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 86 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado. Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 126 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 110 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 83 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00316]Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e um ou mais outros aminoácidos de ocorrência não natural em uma ou mais das seguintes posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os ami- noácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 91 e um ou mais outros ami- noácidos de ocorrência não natural em uma ou mais das seguintes posições: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96 e 36 (SEQ ID NO: 1 ou os aminoáci- dos correspondentes nas SEQ ID NOs: 2-7).
[00317]Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 131 e um outro aminoácido de ocorrência não natural em uma ou mais das seguintes posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 131 e um outro aminoácido de ocorrência não natural em uma ou mais das seguintes posições: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96 e 36 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00318]Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 108 e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 108 e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96 e 36 (SEQ ID NO: 1 ou os ami- noácidos correspondentes nas SEQ ID NOs: 2-7).
[00319]Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 77 e um outro aminoácido de ocorrência não natural em uma ou mais das seguintes posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, tem um aminoácido de ocorrência não natural está na posição 77 e outro aminoácido de ocorrência não natural em uma ou mais das seguintes posições: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96 e 36 (SEQ ID NO: 1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00320]Um exame na estrutura cristal do FGF-21 ou membro(s) da família FGF-21 e sua interação com o receptor FGF pode indicar que certos resíduos ami- noácidos têm cadeias laterais que são complementarmente ou parcialmente acessíveis ao solvente. A cadeia lateral de um aminoácido não naturalmente codificado nessas posições pode apontar a partir da superfície protéica e fora no solvente. Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água, incluindo mas não limitado às posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocor- rência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água, incluindo mas não limitado às posições: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em duas ou mais dessas posi-ções está ligado a um polímero solúvel em água, incluindo mas não limitado às posi-ções: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na ter-minação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água, incluindo mas não limitado às posições: 10, 52, 117, 126, 131, 162, 87, 77, 83, 72, 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água: 10, 52, 77, 117, 126, 131, 162 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água: 87, 77, 83, 72 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água: 69, 79, 91, 96, 108 e 110 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27). Em algumas modalidades, o aminoácido de ocorrência não natural em uma ou mais dessas posições está ligado a um polímero solúvel em água: 91, 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, onde um aminoácido de ocorrência não natural ocorre no aminoácido 91 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) o aminoácido de ocorrência não natural está ligado a um polímero solúvel em água.
[00321]Em outra modalidade, existe um aminoácido de ocorrência não natural em 91 ligado a um polímero solúvel em água e um outro aminoácido de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural está ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 91 e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os ami- noácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 91 ligado a um polímero solúvel em ágia e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 91 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural que são ligados a um polímero solúvel em água: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 91 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoáci- dos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um ami- noácido de ocorrência não natural em 91 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 131, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00322]Em outra modalidade, existe um aminoácido de ocorrência não natural em 131 ligado a um polímero solúvel em água e um outro aminoácido de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 131 e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os amino- ácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 131 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural em das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspon-dentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocor-rência não natural em 131 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 131 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 108, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00323]Em outra modalidade, existe um aminoácido de ocorrência não natural em 108 ligado a um polímero solúvel em água e um outro aminoácido de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra mo-dalidade, existe um aminoácido de ocorrência não natural em 108 e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 131, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os amino- ácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 108 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 108 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural que são ligados a um polímero solúvel em água: 91, 131, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 108 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoáci- dos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um ami- noácido de ocorrência não natural em 108 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 131, 77, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00324]Em outra modalidade, existe um aminoácido de ocorrência não natural em 77 ligado a um polímero solúvel em água e um outro aminoácido de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 77 e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 131, 108, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os ami- noácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 77 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural em uma das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 77 ligado a um polímero solúvel em água e um ou mais outros aminoácidos de ocorrência não natural que são ligados a um polímero solúvel em água: 91, 131, 108, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um aminoácido de ocorrência não natural em 77 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: antes da posição 1 (isto é, no N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182 (isto é, na terminação carbóxi da proteína) (SEQ ID NO:1 ou os aminoáci- dos correspondentes nas SEQ ID NOs: 2-7). Em outra modalidade, existe um ami- noácido de ocorrência não natural em 77 ligado a um polímero solúvel em água e dois ou mais outros aminoácidos de ocorrência não natural em duas ou mais das seguintes posições e esses aminoácidos de ocorrência não natural são ligados a um polímero solúvel em água: 91, 131, 108, 72, 87, 86, 126, 110, 83, 146, 135, 96, e 36 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7).
[00325]Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 91 e posição 131 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) e uma ou mais dessas posições estão ligadas a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 91 e posição 77 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) e uma ou mais dessas posições estão ligadas a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 91 e posição 108 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) e uma ou mais dessas posições estão ligadas a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 131 e posição 108 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) e uma ou mais dessas posições estão liga- das a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 131 e posição 77 (SEQ ID NO:1 ou os aminoáci- dos correspondentes nas SEQ ID NOs: 2-7) e uma ou mais dessas posições estão ligadas a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 91 (SEQ ID NO:1 ou os aminoácidos corres-pondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 131 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 108 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 77 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 72 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoáci- do de ocorrência não natural na posição 87 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 86 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 126 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 110 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 2-7) ligado a um polímero solúvel em água. Em outra modalidade, existe um aminoácido de ocorrência não natural na posição 83 (SEQ ID NO:1 ou os aminoácidos correspondentes nas SEQ ID NOs: 27) ligado a um polímero solúvel em água.
[00326]Uma ampla variedade de aminoácidos não naturalmente codificados pode ser substituída por, ou incorporado em, uma dada posição em um polipeptídeo FGF-21. Em geral, um aminoácido não naturalmente codificado particular é selecionado para incorporação baseada em um exame da estrutura cristal tri-dimensional de um polipeptídeo FGF-21 ou outro membro da família FGF com seu receptor, uma preferência para substituições conservadas (isto é, aminoácidos não naturalmente codificados baseados em arila, tais como p-acetilfenilalanina ou O-propargiltirosona substituindo por Phe, Tyr ou Trp), e conjugação química específica que um deseja introduz no polipeptídeo FGF-21 (por exemplo, a introdução de 4-azidofenilalanina se um quer o efeito da cicloadição [3+2] Huisgen com um polímero solúvel em água produzindo uma fração alquino ou uma formação de ligação amida com um polímero solúvel em água que produz um éster arila que, por sua vez, incorpora uma fração fosfina).
[00327]Em uma modalidade, o método ainda inclui incorporação na proteína de aminoácido não natural, onde o aminoácido não natural compreende um primeiro grupo reativo; e em colocando em contado a proteína com uma molécula (incluindo mas não limitado a um marcador, um corante, um polímero, um polímero solúvel em água, um derivado de polietileno glicol, um ligante foto-cruzado, um radioisótopo, um composto citotóxico, uma droga, um marcador de afinidade, um marcador de foto- afinidade, um composto reativo, uma resina, uma segunda proteína ou polipeptídeo ou análogo de polipeptídeo, um anticorpo ou fragmento de anticorpo, um quelante metal, um co-fator, um ácido graxo, um polinucleotídeo, um DNA, um RNA, um poli- nucleotídeo anti-senso, um sacarídeo, um dendrímero solúvel em água, uma ciclo- dextrina, um ácido ribonucléico inibitório, um biomaterial, uma nanopartícula, um marcador de rotação, um fluoróforo, uma fração contendo metal, uma fração radioativa, um novo grupo funcional, um grupo que covalentemente ou não covalentemen- te interage com outras moléculas, uma fração foto-ligada, uma fração actínica de radiação excitável, uma fração foto-isomerizável, biotina, um derivado de biotina, um análogo de biotina, uma fração de incorporação de um átomo pesado, um grupo quimicamente clivável, um grupo foto-clivável, uma cadeia lateral alongada, um açú- car ligado a carbono, um agente redox-ativo, um amino tioácido, uma fração tóxica, uma fração isotipicamente marcada, um padrão biofísico, um grupo fosforescente, um grupo quimioluminescente, um grupo eletro denso, um agente biologicamente ativo, um marcador detectável, uma molécula pequena, um ponto quântico, um na- notransmissor, um radionucleotídeo, um radiotransmissor, um agente de captura de nêutron, ou qualquer combinação acima, ou qualquer outro composto ou substância desejável) que compreende um segundo grupo reativo. O primeiro grupo reativo reage com o segundo grupo reativo para ligar à molécula ao aminoácido não natural através de uma cicloadição [3+2]. Em uma modalidade, o primeiro grupo reativo é uma fração alquinila ou azida e o segundo grupo reativo é uma fração azida ou al- quinila. Por exemplo, o primeiro grupo reativo é uma fração alquinila (incluindo, mas não limitada a um aminoácido p-propargiloxifenilalanina não natural) e o segundo grupo reativo é a fração azida. Em outro exemplo, o primeiro grupo reativo é a fração azida (incluindo, mas não limitado ao aminoácido p-azido-L-fenilalanina não natural) e o segundo grupo reativo é a fração alquinila.
[00328]Em alguns casos, a(s) substituição(s) de aminoácido(s) não natural-mente codificado(s) será(ão) combinada(s) com outras adições, substituições ou de- leções dentro do polipeptídeo FGF-21 para afetar outros traços biológicos do poli- peptídeo FGF-21. Em alguns casos, as outras adições, substituições ou deleções podem aumentar a estabilidade (incluindo, mas não limitada a, resistência a degra-dação proteolítica) do polipeptídeo FGF-21 ou aumentar a afinidade do polipeptídeo FGF-21 para seu receptor. Em alguns casos, as outras adições, substituições ou deleções podem aumentar a estabilidade farmacêutica do polipeptídeo FGF-21. Em alguns casos, as outras adições, substituições ou deleções podem aumentar a solu-bilidade (incluindo, mas não limitado a quando expresso em E. coli ou outras células hospedeiras) do polipeptídeo FGF-21. Em algumas modalidades adições, substituições ou deleções podem aumentar a solubilidade do polipeptídeo seguindo expressão em E. coli ou outras células hospedeiras recombinantes. Em algumas modalidades são selecionadas para substituição com um aminoácido naturalmente ou não naturalmente codificado em adição ao outro sítio para incorporação de um aminoáci- do não natural que resulta no aumento da solubilidade do polipeptídeo seguindo a expressão em E. coli ou outras células hospedeiras recombinantes. Em algumas modalidades, os polipeptídeos FGF-21 compreendem outra adição, substituição ou deleção que modula a afinidade para o receptor do polipeptídeo FGF-21, ligação de proteínas, ou ligante associado, modula o sinal de transdução após a ligação ao re-ceptor FGF-21, modula a meia vida de circulação, modula a liberação ou biodisponi- bilidade, facilita a purificação, ou melhora ou altera uma via particular de administração. Em algumas modalidades, os polipeptídeos FGF-21 compreendem uma adição, substituição ou deleção que aumenta a afinidade da variante FGF-21 para seu receptor. Similarmente, polipeptídeos FGF-21 podem compreender sequências de clivagem química ou enzimática, sequência de clivagem de protease, grupos reativos, domínios ligadores de anticorpos (incluindo, mas não limitado a FLAG ou poli-His) ou outras sequências baseadas em afinidade (incluindo, mas não limitado a FLAG, poli- His, GST, etc) ou moléculas ligadas (incluindo, mas não limitadas a biotina) que aumentam a detecção (incluindo, mas não limitado a GFP), purificação, transporte através de tecido ou membranas celulares, liberação de pró-droga ou ativação, redução do tamanho de FGF-21, ou outros traços do polipeptídeo.
[00329]Em algumas modalidades, a substituição de um aminoácido não na-turalmente codificado gera um antagonista FGF-21. Em algumas modalidades, um aminoácido não naturalmente codificado é substituído ou adicionado em uma região envolvida com a ligação do receptor. Em algumas modalidades, um aminoácido não naturalmente codificado é substituído ou adicionado em uma região envolvida com ligação de heparina. Em algumas modalidades, antagonistas de FGF-21 compreendem pelo menos uma substituição que causa FGF-21 para atuar como um antagonista. Em algumas modalidades, o antagonista FGF-21 compreende um aminoácido não naturalmente codificado ligado a um polímero solúvel em água que está presente em uma região de ligação ao receptor da molécula FGF-21.
[00330]Em alguns casos, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ou mais aminoácidos são substituídos com um ou mais aminoácidos não naturalmente codificados. Em alguns casos, o polipeptídeo FGF-21 ainda inclui 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ou mais substi-tuições de um ou mais aminoácidos não naturalmente codificados para aminoácidos de ocorrência natural. Por exemplo, em algumas modalidades, um ou mais resíduos em FGF-21 são substituídos com um ou mais aminoácidos não naturalmente codificados. Em alguns casos, o um ou mais resíduos não naturalmente codificados são ligados a um ou mais PEGs lineares ou ramificados de peso molecular mais baixo, assim, aumentado a afinidade de ligação e comparável meia vida sérica relativa às espécies ligadas a um PEG único de peso molecular mais alto.
[00331]Em algumas modalidades, até dois dos seguintes resíduos de FGF- 21 são substituídos com um ou mais aminoácidos não naturalmente codificados. VII. Expressão em Não-eucariotos e Eucariotos
[00332]Para obter alto nível de expressão de um polipeptídeo FGF-21 clo- nado, um típico polinucleotídeo subclone codificando um polipeptídeo FGF-21 da invenção em um vetor de expressão que contém um promotor forte para direcionar a transcrição, um terminador de transcrição/tradução, e se para um ácido nucléico codificando uma proteína, um sítio ligador de ribossomo para iniciação da tradução. Promotores bacterianos adequados são conhecidos pelos versados na técnica e descritos, por exemplo, em Sambrook et al e Ausubel et al.
[00333]Sistemas de expressão bacteriano para expressão de polipeptídeos FGF-21 da invenção são disponíveis em, incluindo mas não limitados a, E. coli, Bacillus sp. Pseudomonas fluorescens, Pseudomonas aeruginosa, Pseudomonas putida, e Salmonella (Palva et al, gene 22:229-235 (1983); Mosbach et al, Nature 302:543545 (1983)). Kits para tais sistemas de expressão são comercialmente disponíveis. Sistemas de expressão eucariotos para células mamíferas, levedura, e células de inseto são conhecidos pelos versados na técnica e são também comercialmente disponíveis. Em casos onde tRNAs ortogonais e aminoacil tRNA sintetases (descrito acima) são utilizados para expressar os polipeptídeos FGF-21 da invenção, células hospedeiras para expressão são selecionadas baseadas em sua habilidade para usar os componentes ortogonais. Células hospedeiras exemplares incluem bactérias Gram-positivas (incluindo, mas não limitadas a B.brevis, B. Subtilis, ou Strep- tomyces) e bactérias Gram-negativas (E. coli, Pseudomonas fluorescens, Pseudomonas aeruginosa, Pseudomona putida), bem como levedura e outras células euca- riotas.
[00334]Uma célula hospedeira eucariota ou célula hospedeira não eucariota da presente invenção provê a habilidade de sintetizar proteínas que compreendem aminoácidos não naturais em grandes quantidades úteis. Em um aspecto, a compo-sição opcionalmente inclui, incluindo mas não limitado a pelo menos 10 microgra- mas, pelo menos 50 microgramas, pelo menos 75 microgramas, pelo menos 100 microgramas, pelo menos 200 microgramas, pelo menos 250 microgramas, pelo menos 500 microgramas, pelo menos 1 miligrama, pelo menos 10 miligramas, pelo menos 100 miligramas, pelo menos um grama, ou mais da proteína que compreende um aminoácido não natural, ou uma quantidade que pode ser alcançada com métodos de produção de proteína in vivo (detalhes na produção e purificação de proteína recombinante são providas aqui). Em outro aspecto, a proteína está opcionalmente presente na composição em uma concentração de, incluindo mas não limitado a, pelo menos 10 microgramas de proteína por litro, pelo menos 50 microgramas de proteína por litro, pelo menos 75 microgramas de proteína por litro, pelo menos 100 microgramas de proteína por litro, pelo menos 200 microgramas de proteína por litro, pelo menos 250 microgramas de proteína por litro, pelo menos 500 microgramas de proteína por litro, pelo menos 1 miligrama de proteína por litro, pelo menos 10 miligramas de proteína por litro ou mais, em, incluindo mas não limitado a, um lisado celular, um tampão, uma tampão farmacêutico, ou outra suspensão líquida (incluindo mas não limitado a, em um volume de, incluindo mas não limitado a qualquer um entre 1 nL a cerca de 100 L ou mais). A produção de grandes quantidades (incluindo, mas não limitado a maiores que, que tipicamente possível com outros métodos, incluindo mas não limitado a tradução in vitro) de uma proteína em uma célula euca- riota incluindo pelo menos um aminoácido não natural que é a característica da in- venção.
[00335]Uma célula hospedeira eucariota ou célula hospedeira não eucariota da presente invenção provê a habilidade de biosintetizar proteínas que compreendem aminoácidos não naturais em grandes quantidades úteis. Por exemplo, proteínas compreendendo um aminoácido não natural podem ser produzidas em uma concentração de, incluindo mas não limitada a pelo menos 10 μg/litro, pelo menos 50 μg/litro, pelo menos 75 μg/litro, pelo menos 100 μg/litro, pelo menos 200 μg/litro, pelo menos 250 μg/litro, ou pelo menos 500 μg/litro, pelo menos 1 mg/litro, pelo me-nos 2 mg/litro, pelo menos 3 mg/litro, pelo menos 4 mg/litro, pelo menos 5 mg/litro, pelo menos 6 mg/litro, pelo menos 7 mg/litro, pelo menos 8 mg/litro, pelo menos 9 mg/litro, pelo menos 10 mg/litro, pelo menos 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900 mg/litro, 1 g/litro, 5 g/litro, 10 g/litro ou mais da proteína em um extrato celular, lisado celular, meio de cultura, um tampão, e/ou semelhantes. I.Sistemas de Expressão, Cultura e Isolamento
[00336]Polipeptídeos FGF-21 podem ser expressos em qualquer número de sistemas de expressão adequados incluindo, por exemplo, levedura, células de inseto, células mamíferas, e bactérias. Uma descrição de sistemas de expressão exemplares é provida abaixo.
[00337]Levedura. Como aqui utilizado, o termo “levedura” inclui qualquer das várias leveduras capazes de expressar um gene codificando um polipeptídeo FGF- 21. Tais leveduras incluem, mas não são limitadas a leveduras ascosporogenous (Endomycetales), leveduras basidiosporogenous e leveduras pertencendo ao grupo de Fungos imperfeitos (Blastomycetes). As leveduras ascosporogenous são divididas em duas famílias, Spermophthraceae e Saccharomycetaceae. A última é compreendida de quatro famílias, Schizosaccharomycoideae (por exemplo, gênero Schi- zosaccharomyces), Nadsonioideae, Lipomycoideae e Saccharomycoideae (por exempo, gênero Pichia, Kluyveromyces e Saccharomyces). As leveduras basidios- porogenous incluem o gênero Leucosporidium, Rhodosporidium, Sporidiobolus, Filo- basidium, e Filobasidiella. Leveduras pertencendo ao grupo de Fungos imperfeitos (Blastomycetes) são divididas em duas famílias, Sporobolomycetaceae (por exemplo, gênero Sporobolomyces e Bullera) e Cryptococcaceae (por exemplo, gênero Candida).
[00338]De particular interesse para uso com a presente invenção são espécies dentro do gênero Pichia, Kluyveromyces, Saccharomyces, Schizosaccha- romyces, Hansenula, Torulopsis, e Candida, incluindo, mas não limitado a P. Pastoris, P. Guillerimondii, S. cerevisiar, S. carlsbergensis, S. diastaticus, S. douglasii, S. kluyveri, S. norbensis, S. oviformis, K. lactis, K. fragilis, C. albicans, C. maltosa, e H. polymorpha.
[00339]A seleção de levedura adequada para expressão de polipeptídeos FGF-21 está dentro das habilidades de um versado na técnica. Na seleção de hospedeiros de levedura para expressão, hospedeiros adequados podem incluir aqueles mostrados para ter, por exemplo, boa capacidade de secreção, baixa atividade pro- teolítica, boa capacidade de secreção, boa produção de proteína solúvel, e robustez geral. Leveduras são geralmente disponíveis a partir de uma variedade de fontes incluindo, mas não limitadas ao Centro de Estoque Genético de Levedura, Departamento de Biofísica e Física Médica, Universidade da Califórnia (Berkeley, CA), e a Coleção de Cultura do Tipo Americada (“ATCC”) (Manassas, VA).
[00340]O termo “levedura hospedeira” ou “célula levedura hospedeira” inclui levedura que pode ser, ou tem sido, utilizada como um recipiente para vetores re- combinantes ou outros de transferência de DNA. O termo incluir a progênie da célula levedura hospedeira original que tenha recebido os vetores recombinantes ou outros DNA de transferência. É entendido que a progênie de uma célula parental única pode não necessariamente ser completamente idêntica em morfologia ou em genômica ou DNA total complementar para o parente original, devido a mutação acidental ou deliberada. Progênie da célula parental que é suficientemente similar ao parental a ser CARACTERIZADO pela propriedade relevante tal como a presença de uma sequência nucleotídica codificando um polipeptídeo FGF-21, é incluída na progênie pela definição.
[00341]Vetores de expressão e transformação, incluindo replicons extra- cromossomais ou vetores integrantes, têm sido desenvolvidos para transformação em muitas leveduras hospedeiras. Por exemplo, vetores de expressão têm sido de-senvolvidos para S. cerevisiae (Sikorsi et al, GENETICS (1989) 122:19; Ito et al, J. BACTERIOL. (1983) 153:163; Hinnen et al, PROC. NATL. ACAD. SCI. EUA (1978) 75:1929); C. Albicans (Kurtz, et al, MOL. CELL. BIOL. (1986) 6:142); C. maltose (Kunze et al, J. BASIC MICROBIOL. (1985) 25:141); H. polymorpha (Gleeson et al, J. GEN. MICROBIOL. (1986) 132:3459; Roggenkamp et al, MOL. GENETICS AND GENOMICS (1986) 202:302); K. fragilis (Das et al, J. BACTERIOL. (1984) 158:1165); K. lactis (De Louvencourt et al, J. BACTERIOL. (1983) 154:737; Van den Berg et al, BIOTECHNOLOGY (NI) (199) 8:135); P. guillerimondii (Kunze et al, J. BASIC MICROBIOL. (1985) 25:141); P. pastoris (Patente dos EUA Nos. 5.324.639, 4.929.555; e 4.837.148; Cregg et al, MOL. CELL. BIOL. (1985) 5:3376); Schizosac- charomyces pombe (Beach et al, NATURE (1982) 300:706); e Y. lipolytica; A. nidu- lans (Ballance et al, BIOCHEM. BIOPHYS. RES. COMMUN. (1983) 112:284-89; Til- burn et al, GENE (1983) 26:205-221; e Yelton et al, PROC. NATL. ACAD. SCI. EUA (1984) 81:1470-74); A. niger (Kelly e Hynes, EMBO J. (1985) 4:475-479); T. reesia (EP 0 244 234); e fungos filamentosos tais como, por exemplo, Neurospora, Penicil- lium, Tolypoclacladium (WO 91/00357), cada um aqui incorporado por referência.
[00342]Sequências controle para leveduras vetores são conhecidas pelos versados na técnica e incluem, mas não são limitadas a regiões promotoras a partir de genes tais como álcool deiidrogenase (ADH) (EP 0 284 044); enolase; glucoqui- nase; glicose-6-fosfato isomerase; gliceraldeído-3-fosfato-deiidrogenase (GAP ou GAPDH); hexoquinase; fosfofrutoquinase; 3-fosfoglucerato mutase; e piruvato quinse (PyK) (EP 0 329 203). O gene PH05 da levedura, codificando fosfatase ácida, também pode prover sequências promotoras úteis (Miyanohara et al, PROC. NATL. ACAD. SCI. EUA (1983) 80:1). Outras sequências promotoras adequadas para uso com leveduras hospedeiras podem incluir os promotores para 3-fosfoglicerato qui- nase (Hitzeman et al, J. BIOL. CHEM. (1980) 255:12073); e outras enzimas glicolíti- cas, tais como piruvato decarboxilase, triosefosfato isomerase, e fosfoglicose isomerase (Holland et al, BIOCHEMISTRY (1978) 17:4900; Hess et al, J. ADV. ENZYME REG. (1969) 7:149). Promotores de levedura induzíveis tendo a vantagem adicional de transcrição controlada por condições de crescimento podem incluir as regiões promotoras para álcool deidrogenase 2; isocitocrommo C; fosfatase ácida; meta- lotioneína; gliceraldeído-3-fosfato deidrogenase; enzimas degradativas associadas com metabolismo de nitrogênio; e enzimas responsáveis para uso de maltose e galactose. Vetores e promotores adequados para uso em expressão em levedura são ainda descritos na EP 0 073 657.
[00343]Aumentadores de levedura podem ser utilizados com promotores de levedura. Em adição, promotores sintéticos podem também funcionar como promotores de levedura. Por exemplo, sequências de ativação supra-correntes (UAS) de um promotor podem ser unidos com a região de ativação de transcrição de outro promotor de levedura, criando um promotor híbrido sintético. Exemplos de tais promotores híbridos incluem a sequência regulatória ADH ligada a região de ativação de trans-crição GAP. Ber, Patente dos EUA Nos. 4.880.734 e 4.876.197, que são aqui incor-poradas por referência. Outros exemplos de promotores híbridos incluem promotores que consistem em sequências regulatórias dos genes ADH2, GAL4, GAL10 ou PHO5, combinados com região de ativação transcricional de um gene da enzima glicolítica tais como GAP e PyK. Ver, EP 0 164 556. Além disso, um promotor de levedura pode incluir promotores de ocorrência natural de origem não levedura que têm habilidade de se ligar a RNA polimerase de levedura e iniciar a transcrição.
[00344]Outros elementos controle que podem compreender parte dos vetores de expressão de levedura incluem terminadores, por exemplo, a partir GAPDH ou os genes enolase (Holland et al, J. BIOL. CHEM. (1981) 256:1385). Em adição, a origem da replicação a partir de 2 μ do plasmídeo de origem é adequada para levedura. Um gene de seleção adequado para uso em leveduras é o presente gene trp1 no plasmídeo da levedura. Ver, Tschumper et al, GENE (1980) 10:157; Kingsman et al, GENE (1979) 7:141. O gene trp1 provê um marcador de seleção para uma cepa mutante de levedura faltando a habilidade de crescimento no triptofano. Similarmente, cepas de levedura deficientes em Leu2 (ATCC 20, 622, ou 38.626) são comple-mentadas por plasmídeos conhecidos produzindo o gene Leu2.
[00345]Métodos de introdução de DNA exógeno em leveduras hospedeiras são conhecidos pelos versados na técnica, e tipicamente incluem, mas não são limitados a ou a transformação de esferoplastos ou se células leveduras hospedeiras intactas com cátions álcalis. Por exemplo, transformação de levedura pode ser realizada de acordo com o método descrito em Hsiao et al, PROC. NATL. ACAD. SCI. EUA (1979) 76:3829 e Van Solingen et al, J. BACT. (1977) 130:946. Entretanto, outros métodos para introdução de DNA em células tais como injeção nuclear, eletro- poração, ou fusão de protoplasto podem também ser utilizados como descrito geralmente em SAMBROOK et al, MOLECULAR CLONING: A LAB. MANUAL (2001). Células leveduras hospedeiras podem então ser cultivadas utilizando técnicas padrões conhecidas pelos versados na técnica.
[00346]Outros métodos para expressão de proteínas homólogas em células leveduras hospedeiras são conhecidos pelos versados na técnica. Ver, geralmente, Pedido de Patente dos EUA No. 20020055169, Patente dos EUA Nos. 6.361.969, 6.312.923; 6.183.985; 6.083.723; 6.017.731; 5.674.706; 5.629.203; 5.602.034; e 5.089.398; Patente Re-examiada dos EUA Nos. RE37.343 e RE35.749; Pedidos de Patente Publicados PCT WO 99/07862; WO 98/37208; e WO 98/26080; Pedidos de Patente Européia EP 0 946 736; EP 0 732 403; EP 0 480 480; WO 90/10277; EP 0 340 986; EP 0 329 203; EP 0 324 274; e EP 0 164 556. Ver também Gellissen et al, ANTONIE VAN LEEUWENHOEK (1992) 62(1-2):79-93; Romanos et al, YEAST (1992) 8(6):423-488; Goeddel, METHODS IN ENZYMOLOGY (1990) 185-3-7, cada uma dos quais é aqui incorporada por referência.
[00347]As cepas de leveduras hospedeiras podem ser crescidas em fermen- tadores durante o estágio de amplificação utilizando métodos de alimentação em banhos de fermentação conhecidos pelos versados na técnica. Os métodos de fer- mentação podem ser adaptados para contar para diferenças em uma via de utilização de carbono da levedura hospedeira particular ou modo de controle de expressão. Por exemplo, fermentação de uma levedura hospedeira Saccharomyces pode requerer uma alimentação única de glicose, fonte de nitrogênio complexa (por exemplo, hidrolisados de caseína), e suplementação com múltiplas vitaminas. Em contraste, levedura metilotrófica P. Pastoris pode requerer glicerol, metanol, e traços de alimento mineral, mas somente sais de amônio simples (nitrogênio) para ótimo crescimento e expressão. Ver, por exemplo, Patente dos EUA No. 5.324.639; Elliott et al, J. PROTEIN CHEM. (1990) 9:95; e Fieschko et al, BIOTECH, BIOENG. (1987) 29:1113, aqui incorporada por referência.
[00348]Tais métodos de fermentação, entretanto, podem ter certas caracte-rísticas comuns independentes da cepa de levedura hospedeira empregada. Por exemplo, um nutriente limitante de crescimento, tipicamente carbono, pode ser adi-cionado ao fermentador durante a fase de amplificação para permitir crescimento máximo. Em adição, métodos de fermentação geralmente empregam um meio de fermentação desenhado para conter quantidades adequadas de carbono, nitrogênio, sais básicos, fósforo, e outros nutrientes menores (vitaminas, traços de minerais e sais, etc). Exemplos de meios de fermentação para uso com Pichia são descritos na Patente dos EUA Nos. 5.324.639 e 5.231.187, que são aqui incorporados por referência. WO 2005/091944 que é aqui incorporada por referência descreve a expressão do FGF-21 em levedura.
[00349]Células de Inseto Infectadas com Baculovírus. O termo “inseto hos-pedeiro” ou “célula hospedeira de inseto” refere-se a um inseto que pode estar, ou tenha sido utilizado como um recipiente para vetores recombinantes ou outra trans-ferência de DNA. O termo inclui a progênie da célula hospedeira do inseto original que tenha sido transfectado. É entendido que a progênie de uma célula parental única pode não necessariamente ser completamente idêntica em morfologia ou em ge- nômica ou DNA complementar total ao parental original, devido a mutação acidental ou deliberada. Progênie da célula parental que é suficientemente similar ao parental para ser caracterizada pela propriedade relevante, tal como a presença de sequência nucleotídica codificando um polipeptídeo FGF-21, são incluídas em progênie ten-cionada por esta definição.
[00350]A seleção de células de inseto adequadas para expressão de poli- peptídeos FGF-21 é conhecida pelos versados na técnica. Várias espécies de inseto são bem descritas na técnica e são comercialmente disponíveis incluindo Aedes ae- gypti, Bombyx mori, Drosophila melanogaster, Spodoptera frugiperda e Trichoplusia ni. Na seleção de insetor hospedeiros para expressão, hospedeiros adequados podem incluir aqueles mostrados ter, entre outros, boa capacidade de secreção, baixa atividade proteolítica, e robustez geral. Insetos são geralmente disponíveis a partir de uma variedade de fontes, incluindo, mas não limitadas ao Centro de Estoque Genético de Inseto, Departamento de Biofísica e Física Médica, Universidade da Califórnia (Berkeley, CA); e a Coleção de Cultura Tipo Americana (“ATCC”) (Manassas, VA).
[00351]Geralmente, os componentes de um sistema de expressão de inseto infectado com baculovírus incluem um vetor de transferência, usualmente um plas- mídeo bacteriano, que contém ambos, um fragmento do genoma do baculovírus, e um sítio de restrição conveniente para inserção do gene heterólogo a ser expresso; um baculovírus selvagem com sequências homólogas ao fragmento baculovírus- específico no vetor de transferência (este permite a recombinação homóloga do gene heterólogo no genoma do baculovírus); e células de hospedeiras de insetos apropriadas e meio de crescimento. Os materiais, métodos e técnicas utilizadas na construção dos vetores, células transfectadas, placas coletadas, células crescendo em cultura, e semelhantes são conhecidos na técnica e manuais estão disponíveis descrevendo essas técnicas.
[00352]Após inserir o gene heterólogo no vetor de transferência, o vetor e o genoma viral selvagem são transfectados em uma célula hospedeira de inseto onde o vetor e o genoma viral se recombinam. O pacote vírus recombinante é expresso e placas recombinantes são identificadas e purificadas. Materiais e métodos para sis- temas de expressão baculovírus/célula de inseto são comercialmente disponíveis na forma de kit a partir de, por exemplo, Invitrogen Corp. (Carlsbac, CA). Essas técnicas são geralmente conhecidas pelos versados na técnica e completamente descritas em SUMMERS E SMITH, TEXAS AGRICULTURAL EXPERIMENT STATION BULLETIN No. 1555 (1987), aqui incorporada por referência. Ver também, RICHARDSON, 39 METHODS IN MOLECULAR BIOLOGY: BACULOVIRUS EXPRESSION PROTOCOLS (1995); AUSUBEL et al, CURRENT PROTOCOLS IN MOLECULAR BIOLOGY 16.9-16.11 (1994); KING e POSSEE, THE BACULOVIRUS SYSTEM: A LABORATORY GUIDE (1992); e O’REILLY et al, BACULOVIRUS EXPRESSION VECTORS: A LABORATORY MANUAL (1992).
[00353]De fato, a produção de várias proteínas heterólogas utilizando sistemas de expressão baculovírus/célula de inseto são conhecidos pelos versados na técnica. Ver, por exemplo, Patente dos EUA Nos. 6.368.825; 6.342.216; 6.338.846; 6.261.805; 6.245.528; 6.225.060; 6.183.987; 6.168.932; 6.126.944; 6.096.304; 6.013.433; 5.965.393; 5.939.285; 5.891.676; 5.871.986; 5.861.279; 5.858.368; 5.843.733; 5.762.939; 5.753.220; 5.605.827; 5.583.023; 5.571.709; 5.516.657; 5.290.686; WO 02/06305; WO 01/90390; WO 01/27301; WO 01/05956; WO 00/55345; WO 00/20032; WO 99/51721; WO 99/45130; WO 99/31257; WO 99/10515; WO 99/09193; WO 97/26332; WO 96/29400; WO 96/25496; WO 96/06161; WO 95/20672; WO 93/03171; WO 92/16619; WO 92/02628; WO 92/01801; WO 89/01037; WO 88/07082; que são aqui incorporadas por referência.
[00354]Vetores que são úteis nos sistemas de expressão baculovírus/célula de inseto são conhecidos na técnica e incluem, por exemplo, expressão no inseto e vetores de transferência derivados a partir do baculovírus vírus poliedrose nuclear Autographacalifornica (AcNPV), que é independente de auxílio, vetor de expressão viral. Vetores de expressão viral derivados a partir do sistema usualmente usam o forte promotor do gene poliedrina viral para dirigir a expressão dos genes heterólo- gos. Ver, geralmente, O’Reilly et al, BACULOVIRUS EXPRESSION VECTORS: A LABORATORY MANUAL (1992).
[00355]Antes de inserir o gene estranho no genoma do baculovírus, os com-ponentes acima descritos, compreendendo um promotor, líder (se desejado), sequência codificadora de interesse, e sequência de terminação de transcrição, são tipicamente unidos em uma construção transplacemente intermediária (vetor de transferência). Construções transplacementes intermediárias são sempre mantidas em um replicon, tal como um elemento cromossomal extra (por exemplo, plasmí- deos) capazes de manutenção estável em um hospedeiro, tal como bactéria. O replicon terá um sistema de replicação, então permitindo ser mantido em um hospedeiro adequado para clonar e amplificar. Mais especificamente, o plasmídeo pode conter o sinal poliedrina poliadenilação (Miller, ANN. REV. MICROBIOL. (1988) 42:177) e um gene de resistência a ampicilina (amp) procarioto e origem de replicação para seleção e propagação em E. coli.
[00356]Um vetor de transferência comumente usado para introduzir genes externos no AcNPV é pAc373. Muitos outros vetores, conhecidos pelos versados na técnica, têm também sido desenhados incluindo, por exemplo, pVL985, que altera o códon inicial poliedrina a partir de ATG e ATT, e que introduz um sítio de clonagem BamHI de 32 pares de base abaixo da cascata de ATT. Ver, Luckon e Summers, VIROLOGY 170:31 (1989). Outros vetores disponíveis comercialmente incluem, por exemplo, PblueBac4.5/V5-His; pBlueBacHis2; pMelBac; pBlueBac4.5 (Invitrogen Corp. Carlsbad, CA).
[00357]Após a inserção do gene heterólogo, o vetor de transferência e ge- noma baculoviral selvagem são co-transfectados em uma célula hospedeira de inseto. Métodos para introduzir DNA heterólogo em um sítio desejado no vírus baculoví- rus são conhecidos na técnica. Ver, SUMMERS e SMITH, TEXAS AGRICULTURAL EXPERIMENT STATION BULLETIN No. 1555 (1987); Smith et al, MOL. CELL. BIOL. (1983) 3:2156; Luckow e Summers, VIROLOGY (1989) 170:31. Por exemplo, a inserção pode ser em um gene tal como o gene poliedrina, por recombinação de dupla ligação cruzada homóloga; inserção pode também estar em um sítio de restrição de enzima construído no gene baculovírus desejado. Ver, Miller et al, BIOESSAYS (1989) 11(4):91.
[00358]Transfecção pode ser realizada por eletroporação. Ver, TROTTER e WOOD, 39 METHODS IN MOLECULAR BIOLOGY (1995); Mann e King, J. GEN. VIROL. (1989) 70:3501. Alternativamente, lipossomos podem ser utilizados para transfectar as células de insetos com vetor de expressão recombinante e o baculoví- rus. Ver, por exemplo, Liebman et al, BIOTECHNIQUES (1999) 26(1):36; Graves et al, BIOCHEMISTRY (1998) 37:6050; Nomura et al, J. BIOL. CHEM. (1998) 273 (22):13570; Schmidt et al, PROTEIN EXPRESSION AND PURIFICATION (1998) 12:323; Siffert et al, NATURE GENETICS (1998) 18:45; TILKINS et al, CELL BIOLOGY: A LABORATORY HANDBOOK 145-154 (1998); Cai et al. PROTEIN EXPRESSION AND PURIFICATION (1997) 10:263; Dolphin et al, NATURE GENETICS (1997) 17:491; Kost et al, GENE (1997) 190:139; Jakobsson et al, J. BIOL. CHEM. (1996) 271:22203; Rowles et al, J. BIOL. CHEM. (1996) 271(37):22376; Reverey et al, J. BIOL. CHEM. (1996) 271(39):23607-10; Stanley et al, J. BIOL. CHEM. (1995) 270:4121; Sisk et al, J. VIROL. (1994) 68(2):766; e Peng et al, BIOTECHNIQUES (1993) 14(2):274. Lipossomos comercialmente disponíveis incluem, por exemplo, Cellfectin® e Lipofectin® (Invitrogen, Corp. Carlsbad, CA). Em adição, transfecção com fosfato de cálcio pode ser utilizada. Ver, TROTTER e WOOD, 39 METHODS IN MOLECULAR BIOLOGY (1995); Kitts, NAR (1990) 18(19):5667; e Mann e King, J. GEN. VIROL. (1989) 70:3501.
[00359]Vetores de expressão baculovírus usualmente contêm um promotor baculovírus. Um promotor baculovírus e qualquer sequência de DNA capaz de se ligar a uma RNA polimerase de baculovírus e iniciar a cascata de transcrição (3’) de uma sequência codificante (por exemplo, gene estrutural) em RNAm. Um promotor terá uma região de iniciação de transcrição que é usualmente colocada próxima a terminação 5’ da sequência codificante. Esta região de iniciação de transcrição tipicamente inclui um sítio de ligação de RNA polimerase e um sítio de iniciação de transcrição. Um promotor baculovírus pode também ter um segundo domínio chamado um aumentador, que, se presente, é usualmente distal ao gene estrutural. Além disso, expressão pode ser ou regulada ou constitutiva.
[00360]Genes estruturais, abundantemente transcritos em tempos tardios no ciclo de infecção, provêm particularmente sequências promotoras úteis. Exemplos incluem sequências derivadas a partir do gene codificando a proteína viral poliedron (FRIESEN et al, The Regulation of Baculovirus Gene Expression in THE MOLECULAR BIOLOGY OF BACULOVIRUSES (1986); EP 0, 127 839 e 0 155 476) e o gene codificando a proteína p10 (Vlak et al, J. GEN. VIROL. (1988) 69:765).
[00361]O vetor de expressão de baculovírus recém-formado é empacotado em um baculovírus recombinante infeccioso e subsequentemente crescimento de placas podem ser purificados por técnicas conhecidas pelos versados na técnica. Ver, Miller et al, BIOESSAYS (1989) 11(4):91; SUMMERS AND SMITH, TEXAS AGRICULTURAL EXPERIMENT STATION BULLETIN No. 1555 (1987).
[00362]Vetores de expressão de baculovírus recombinante têm sido desen-volvidos para infecção em várias células de inseto. Por exemplo, baculovírus recom- binantes têm sido desenvolvidos para, por exemplo, Aedes aegypti (ATCC No. CCL- 125), Bombyx mori (ATCC No. CRL-8910). Drosophila melanogaster (ATCC No. 1963), Spodoptera frugiperda, e Trichoplusia ni. Ver, Wright, NATURE (1986) 321:718; Carbonell et al, J. VIROL. (1985) 56:153; Smith et al, MOL. CELL. BIOL. (1983) 3:2156. Ver, geralmente, Fraser et al, IN VITRO CELL. DEV. BIOL. (1989) 25:225. Mais especificamente, as linhagens celulares utilizadas para sistemas de vetor de expressão de baculovírus comumente incluem, mas não são limitados a, Sf9 (Spodoptera frugiperda) (ATCC No. CRL-1711), Sf21 (Spodoptera frugiperda) (Invitrogen Corp., Cat. No. 11497-013) (Carlsbad, CA)). Tri-368 (Trichopulsia ni), e High-Five® BTI-TN-5BI-4 (Trichopulsia ni).
[00363]Células e meios de cultura são comercialmente disponíveis para ambas, expressão direta e fusão de polipeptídeos heterólogos em um baculoví- rus/expressão, e uma tecnologia de cultura celular é geralmente conhecida pelos versados na técnica.
[00364]E. coli, espécies de Pseudomonas, e outros Procariotos. Técnicas de expressão bacteriana são conhecidas pelos versados na técnica. Uma ampla variedade de vetores está disponível para uso em hospedeiros bacterianos. Os vetores podem ser vetores de cópias únicas ou baixas e altas multi-cópias. Vetores podem servir para clonagem e/ou expressão. Em visão da ampla literatura que concerne vetores, disponibilidade comercial de muitos vetores, e mesmo manuais descrevendo vetores e seus mapas de restrição e características, nenhuma discussão extensa é requerida aqui. Como é bem conhecido, os vetores normalmente envolvem marcadores permitindo a seleção, cujos marcadores podem prover resistência a agente citóxico, prototrofia ou imunidade. Frequentemente, uma pluralidade de marcadores está presente, que provê para diferentes características.
[00365]Um promotor bacteriano é qualquer sequência de DNA capaz de se ligar a RNA polimerase bacteriana e iniciar a cascada de transcrição (3) de uma sequência codificante (por exemplo, gene estrutural) em RNAm. Um promotor terá uma região de iniciação de transcrição que é usualmente colocada próxima a terminação 5’ da sequência codificante. Esta região de iniciação de transcrição tipicamente inclui um sítio de ligação de RNA polimerase e um sítio de iniciação de transcrição. Um promotor bacteriano pode também ter um segundo domínio chamado um operador, que pode sobrepor um sítio de ligação da RNA polimerase em que a síntese de RNA começa. O operador permite transcrição negativa regulada (induzível), como uma proteína repressora de gene pode ligar o operador e assim inibir a transcrição de um gene específico. Expressão constitutiva pode ocorrer em ausência de elementos re- gulatórios negativos, tal como operador. Em adição, regulação positiva pode ser alcançada por uma sequência ligante de proteína ativadora, que, se presente é usualmente próxima (5’) a sequência ligante de RNA polimerase. Um exemplo de uma proteína ativadora do gene é a proteína ativadora de catabólito (CAP), que ajuda a iniciar a transcrição do lac operon em Escherichia coli (E. coli) [Raibaud et al, ANNU. REV. GENET. (1984) 18:173]. Expressão regulada pode assim ser ou positiva ou negativa, assim, ou aumentando ou reduzindo a transcrição.
[00366]Sequências codificando enzimas da via metabólica provêm sequên- cias promotoras particularmente úteis. Exemplos incluem sequências promotoras derivadas a partir de enzimas metabolizadoras de açúcar, tais como galactose, lactose (lac) {Chang et al, NATURE (1977) 198:1056}, e maltose. Exemplos adicionais incluem sequências promotoras derivadas a partir de enzimas biossintéticas tais como triptofano (trp) [Goeddel et al, NUC. ACIDS. RES. (1980) 8:4057; Yelverton et al, NUCL, ACIDS RES. (1981) 9:731; Pat. dos EUA No. 4.738.921; Ped. EP Nos. 036 776 e 121 775, que são aqui incorporados por referência]. O sistema promotor de β- galactosidase (bla) [Weissmann (1981) “the cloning of interferon and other mistakes” Em Interferon 3 (Ed. I. Gresser)], bacteriófago lambda PL [Shimatake et al, NATURE (1981) 292:128] e T5 [Pat. EUA No. 4.689.406, que são aqui incorporadas por referência] sistemas promotores também provêm sequências promotoras úteis. Métodos preferidos da presente invenção utilizam fortes promotores, tal como o promotor T7 para induzir polipeptídeos FGF-21 em altos níveis. Exemplos de tais vetores são conhecidos pelos versados na técnica e incluem as sérias pET29 a partir de Novagen, e os vetores pPOP descritos em WO99/05297, que é aqui incorporado por referência. Tais sistemas de expressão produzem altos níveis de polipeptídeos FGF-21 no hospedeiro sem comprometer a viabilidade da célula hospedeira ou parâmetros de crescimento. pWT19 (Novagen) é outro vetor conhecido na técnica.
[00367]Em adição, promotores sintéticos que não ocorrem na natureza também funcionam, com promotores bacterianos. Por exemplo, sequências ativadoras de transcrição de um promotor bacteriano ou bacteriófago podem ser unidos com as sequências operon de outro promotor bacteriano ou bacteriófago, criando um promotor híbrido sintético [Pat. dos EUA No. 4.551.433, que é aqui incorporado por referência]. Por exemplo, o tac promotor é um promotor trp-lac híbrido compreendendo de ambos, promotor trp e sequências operon que é regulada pelo repressor lac [Amann et al, GENE (1983) 25:167; de Boer, et al, PROC. NATL. ACAD. SCI. (1983) 80:21]. Além disso, um promotor bacteriano pode incluir promotores de ocorrência natural de origen não bacteriana que tem a habilidade de se ligar a RNA polimerase e iniciar a transcrição. Um promotor de ocorrência natural de origem não bacteriana pode também ser acoplado com uma RNA polimerase compatível para produzir altos níveis de expressão de alguns genes em procariotos. O sistema bacteriófago T7 RNA polimerase/promotor é um exemplo de um sistema promotor acoplado [Studier et al, J. MOL. BIOL. (1986) 189;113; Tabor et al, Proc. Natl. Acad. Sci. (1985) 82:1074]. Em adição, um promotor híbrido pode também ser compreendido de um promotor bacteriófago e uma região operadora E. coli (EP Pub. 267 851).
[00368]Em adição a uma sequência promotora funcionando, um sítio de ligação ao ribossomo eficiente é também útil para a expressão de genes externos em procariotos. Em E. coli, o sítio de ligação de ribossomo é chamado sequência Shine- Dalgarno (SD) e inclui um códon de iniciação (ATG) e uma sequência de 3-9 nucleo- tídeos no comprimento localizado 3-11 nucleotídeos acima do códon de iniciação (Shine et al, NATURE (1975) 254:34]. A sequência SD é pensada promover a ligação de RNAm ao ribossomo pelo pareamento de bases entre a sequência SD e a terminação 3’ da E. coli 16S rRNA [Steitz et al, “Genetic signals and nucleotide sequences in messenger RNA”, In Biological Regulation and Development: Gene Expression (Ed. R.F. Goldberger, 1979)]. Para expressar genes eucariotos e genes procariotos com sítio de ligação ao ribossomo fraco [Sambrook et al. “Expression of cloned genes in Escherichia coli”, Molecular Cloning; A Laboratory Manual, 1989].
[00369]O termo “hospedeiro bacteriano” ou “célula bacteriana hospedeira” refere-se a uma bactéria que pode ser, ou tem sido, utilizada como um recipiente para vetores de recombinação ou outra transferência de DNA. O termo inclui a pro- gênie da célula bacteriana hospedeira original que tem sido transfectada. É entendido que a progênie de uma célula parental única pode não necessariamente estar completamente idêntica na morfologia ou na genômica ou DNA total complementar ao parental original, devido a mutação acidental ou deliberada. Progênie da célula parental que é suficientemente similar ao parental para ser caracterizada por propriedade relevante tal como a presença de uma sequência nucleotídica codificando um polipeptídeo FGF-21, são incluídas na progênie tencionada por esta definição.
[00370]A seleção de bactéria hospedeira adequada para expressão de poli- peptídeos FGF-21 é conhecida pelos versados na técnica. Na seleção dos hospedeiros bacterianos para expressão, hospedeiros adequados podem incluir aqueles que mostraram ter, entre outros, boa capacidade de formação de inclusão corporal, baixa atividade proteolítica, e robustez geral. Hospedeiros bacterianos são geralmente dis-poníveis a partir de uma variedade de fontes incluindo, mas não limitada pelo Centro de Estoque Genético de Bactéria, Departamento de Biofísica e Física Médica, Universidade da Califórnia (Berkeley, CA) e a Coleção de Cultura do Tipo Americana (“ATCC”) (Manassas, VA). Fermentação industrial/farmacêutica geralmente usa bactérias derivadas de cepas K (por exemplo W3110) ou a partir de bactérias derivadas a partir de cepas B (por exemplo, BL21). Essas cepas são particularmente úteis porque seus parâmetros de crescimento são extremamente bem conhecidos e robustos. Em adição, essas cepas são não patogênicas, que é de importância comercial pela segurança e razões ambientais. Outros exemplos de hospedeiro E. coli adequados incluem, mas não limitados a, cepas de BL21, DH10B, ou derivados dos mesmo. Em outra modalidade dos métodos da presente invenção, o hospedeiro E. coli é uma cepa de protease mínima incluindo, mas não limitada a, OMP- e LON-. A cepa hospedeira pode ser uma espécie de Pseudomonas, incluindo mas não limitada a, Pseudomonas fluorescens, Pseudomonas aeruginosa, e Pseudomonas putida. Pseudomonas fluorescens biovar 1, designada cepa MB101, é conhecida ser útil para produção recombinante e está disponível para processos de produção terapêutica. Exemplos de um sistema de expressão de Pseudomonas incluem o sistema disponível a partir da The Dow Chemical Company como uma cepa hospedeira (Midland, MI disponível na World Wide Wed em dow.com).
[00371]Uma vez uma cepa de células hospedeiras recombinantes tem sido estabelecida (isto é, a expressão da construção tem sido introduzida em uma célula hospedeira e células hospedeiras com a apropriada expressão da construção são isoladas), a cepa da célula hospedeira recombinante é cultivada sobre condições apropriadas para produção dos polipeptídeos FGF-21. Será aparente a um versado na técnica, o método de cultivo de uma cepa de célula hospedeira recombinante de- penderá da natureza da expressão da construção utilizada e a identidade da célula hospedeira. Cepas hospedeiras recombinantes são normalmente cultivadas usando método que são conhecidos pelos versados na técnica. Células hospedeiras recom- binantes são tipicamente cultivadas em meio líquido contendo fontes assimiláveis de carbono, nitrogênio, e sais inorgânicos e, opcionalmente, contendo vitaminas, ami- noácidos, fatores de crescimento, e outros suplementos proteináceos da cultura co-nhecidos pelos versados na técnica. Meios líquidos para cultura de células hospedeiras podem opcionalmente conter antibióticos ou anti-fúngicos para prevenir o crescimento de microrganismos não desejáveis e/ou compostos incluindo, mas não limitado a antibióticos para selecionar células hospedeiras contendo o vetor de expressão.
[00372]Células hospedeiras recombinantes podem ser cultivadas no formato de banho ou formato contínuo, com ou coleta de célula (no caso onde o polipeptídeo FGF-21 acumula intracelularmente) ou coletando o sobrenadante da cultura no formato de banho ou contínuo. Para produção nas células hospedeiras procarióticas, cultura em banho e coleta celular é preferida.
[00373]Os polipeptídeos FGF-21 da presente invenção são normalmente pu-rificados após a expressão em sistemas recombinantes. O polipeptídeo FGF-21 pode ser purificado a partir de células hospedeiras ou meio de cultura por uma variedade de métodos conhecidos na técnica. Polipeptídeos FGF-21 produzidos nas células hospedeiras bacterianas pode ser pobremente solúveis ou insolúveis (na forma de corpos de inclusão). Em uma modalidade da presente invenção, substituições aminoácidos pode facilmente ser feitas no polipeptídeo FGF-21 que são selecionados para o propósito de aumentar a solubilidade da proteína recombinantemente produzida usando os métodos revelados aqui, bem como aqueles conhecidos na técnica. No caso de proteína insolúvel, a proteína pode ser coletada a partir de lisa- dos de células hospedeiras por centrifugação e pode ainda ser seguidas por homogeneização de células. No caso de proteína pobremente solúvel, compostos, incluindo, mas não limitados a polietileno imina (PEI) podem ser adicionados para induzir a precipitação de proteína parcialmente solúvel. A proteína precipitada pode então ser convenientemente coletada por centrifugação. Células hospedeiras recombinan- tes podem ser rompidas ou homogeneizadas para liberar os corpos de inclusão de dentro das células utilizando uma variedade de métodos conhecidos pelos versados na técnica. Rompimento de célula hospedeira ou homogeneização pode ser feita usando técnicas bem conhecidas incluindo, mas não limitadas a, rompimento enzi- mático celular, sonicação, homogeneização dounce, ou rompimento de liberação por alta pressão. Em uma modalidade do método da presente invenção, a técnica de liberação de alta pressão é utilizada para romper as células hospedeiras E. coli para liberar os corpos de inclusão dos polipeptídeos FGF-21. Quando manuseando corpos de inclusão de polipeptídeo FGF-21, pode ser vantajoso minimizar o tempo de homogeneização em repetições a fim de maximizar a produção de corpos de inclusão sem a perda devida a fatores tais como solubilização, estresse mecânico ou pro- teólise.
[00374]Polipeptídeo FGF-21 insolúvel ou precipitado pode ser então ser so- lubilizado usando qualquer de um número de agentes de solubilização adequado conhecido na técnica. O polipeptídeo FGF-21 pode ser solubilizado com uréia ou cloridrato de guanidina. O volume do polipeptídeo FGF-21 solubilizado pode ser mi-nimizado de forma que grandes lotes podem ser produzidos utilizando tamanhos de lotes convenientemente maleáveis. Este fator pode ser significante em um ambiente comercial em grande escala onde o hospedeiro recombinante pode ser crescido em recipientes que são milhares de litros em volume. Em adição, quando o polipeptídeo FGF-21 fabricado em grande escala comercial, em particular para uso farmacêutico humano, evitar o uso de químicos adversos que podem danificar a maquinaria e o recipiente, ou o produto protéico propriamente dito, deve ser evitado, se possível. Tem sido mostrado no método da presente invenção que o agente desnaturante mais leve, uréia, pode ser utilizado para solubilizar os corpos de inclusão do polipep- tídeo FGF-21 no lugar do agente desnaturante mais danoso, cloridrato de guanidina. O uso de uréia significantemente reduz o risco de dano para o equipamento sem mancha de aço utilizando na fabricação e processo de purificação do polipeptídeo FGF-21 enquanto eficientemente solubilizando os corpos de inclusão do polipeptí- deo FGF-21.
[00375]No caso de proteína FGF-21 solúvel, o FGF-21 pode ser secretado no espaço periplasmático ou no meio de cultura. Por exemplo, FGF-21 foi secretado no espaço periplasmático de células W3110-B2 por uso de plasmídeos codificando construções incluindo oito sequências líderes diferentes, incluindo aquelas listadas na SEQ ID NOs: 39-44, e transformando essas em células W31110-B2, as células foram então crescidas a 37oC até OD alcançar cerca de 0,8, em cujo ponto a expressão foi induzida com arabinosa 0,01%. Cinco horas após as amostras liberadas no ambiente periplasmático foram pré-preparados a partir de culturas e corridas em géis (Figura 33) mostrando a expressão geral (lisado total) e secreções periplasmáti- cas (fração solúvel).
[00376]Em adição, FGF-21 solúvel pode estar presente no citoplasma das células hospedeiras. Pode ser desejado concentrar o FGF-21 solúvel antes dos passos de purificação serem feitos. Técnicas padrões conhecidas pelos versados na técnica podem ser utilizadas para concentrar o FGF-21 solúvel a partir, por exemplo, lisados celulares ou meio de cultura. Em adição, técnicas padrões conhecidas pelos versados na técnica pode ser utilizadas para romper as células hospedeiras e liberar o FGF-21 solúvel a partir do citoplasma ou espaço periplasmático das células hospedeiras.
[00377]Quando o polipeptídeo FGF-21 é produzido como uma proteína de fusão, a sequência de fusão pode ser removida. Remoção de uma sequência de fusão pode ser realizada por clivagem enzimática ou química. Remoção enzimática de sequências de fusão pode ser realizadas utilizando métodos conhecidos pelos ver-sados na técnica. A escolha da enzima par remoção da sequência de fusão determinará a identidade da fusão, e as condições de reação serão especificadas pela escolha da enzima como será aparente para um versado na técnica. Clivagem química pode ser realizada usando reagentes conhecidos pelos versados na técnica, incluin- do, mas não limitados a, brometo de cianogênio, protease TEV, e outros reagentes. O polipeptídeo FGF-21 clivado pode ser purificado a partir da sequência de fusão clivada pelos métodos conhecidos pelos versados na técnica. Tais métodos serão determinados pela identidade e propriedades da sequência de fusão e polipeptídeo FGF-21, como será aparente a um versado na técnica. Métodos para purificação podem incluir, mas não são limitados a cromatografia de exclusão de tamanho, cro- matografia de interação hidrofóbica, cromatografia de troca iônica ou diálise ou qualquer combinação dos mesmos.
[00378]O polipeptídeo FGF-21 pode também ser purificado para remover DNA a partir da solução protéica. DNA pode ser removido por qualquer método conhecido na técnica, tais como precipitação ou cromatografia de troca iônica, mas pode ser removido por precipitação com uma gente de precipitação de ácido nucléi- co, tal como, mas não limitado a sulfato de protamina. O polipeptídeo FGF-21 pode ser separado a partir do DNA precipitado usando padrões bem conhecidos nos métodos, incluindo, mas não limitado a centrifugação ou filtração. Remoção de moléculas de ácido nucléico hospedeiro é um fator importante em um ambiente onde o poli- peptídeo FGF-21 é para ser usado para tratar humanos e os métodos da presente invenção reduzem o DNA celular do hospedeiro a níveis farmaceuticamente aceitáveis.
[00379]Métodos para fermentação em pequena escala ou larga escala pode também ser usada na expressão de proteína, incluindo, mas não limitado a fermen- tadores, frascos agitadores, bioreatores de cama fluidizada, bioreatores de fibra vazia, sistemas de cultura de garrafa rolante, e sistemas de bioreatores de tanque agitado. Cada um desses métodos pode ser feito em um lote, lote alimentado ou processo de modo contínuo.
[00380]Polipeptídeos FGF-21 humanos da invenção pode geralmente ser recuperados usando métodos padrões na técnica. Por exemplo, meio de cultura ou lisado celular pode ser centrifugados ou filtrados para remover restos celulares. O sobrenadante pode ser concentrado ou diluído a um volume desejado ou diafiltrado em um tampão adequado para condicionar a preparação para uma purificação adici-onal. Purificação adicional do polipeptídeo FGF-21 da presente invenção inclui sepa-ração de formas deaminadas e unidas ao variante polipeptídeo FGF-21 a partir da forma intacta.
[00381]Qualquer dos seguintes procedimentos exemplares pode ser empre-gados para purificação dos polipeptídeos da invenção: cromatografia de afinidade; cromatografia de troca aniônica ou catiônica (usando, incluindo mas não limitada a, DEAE SEFAROSE); cromatografia em sílica; cromatografia líquida de alto desempenho (HPLC); HPLC de fase reversa; filtração em gel (usando, incluindo mas não limitado a, SEPHADEX G-75); cromatografia de interação hidrofóbica; cromatografia de exclusão por tamanho; cromatografia metal-quelado; ultrafiltração/diafiltração; precipitação por etanol; precipitação pode sulfato de amônio; cromatofoco; cromatografia de substituição; procedimentos eletroforéticos (incluindo mas não limitados a preparação de foco isoelétrico), solubilidade diferencial (incluindo mas não limitado a precipitação por sulfato de amônio), SDS-PAGE, ou extração.
[00382]Proteínas da presente invenção, incluindo mas não limitadas a prote-ínas compreendendo aminoácidos não naturais, peptídeos compreendendo aminoá- cidos não naturais, anticorpos para proteínas compreendendo aminoácidos não na-turais, parceiros ligadores para proteínas compreendendo aminoácidos não naturais, etc, podem ser purificados, ou parcialmente ou substancialmente para homogeneidade, de acordo com procedimentos padrões conhecidos para e utilizados pelos versados na técnica. Consequentemente, polipeptídeos da invenção podem ser recuperados e purificados por qualquer de um número de métodos conhecidos pelos versados na técnica, incluindo mas não limitados a sulfato de amônio ou precipitação de etanol, extração ácido ou base, cromatografia em coluna, cromatografia de coluna de afinidade, cromatografia de troca aniônica ou catiônica, cromatografia fosfoce- lulose, cromatografia de interação hidrofóbica, cromatografia de hidroxilapatite, cro- matografia lectina, gel de eletroforese e semelhantes. Passos de re-envelopamento de proteína podem ser utilizados, como desejado, em fazer o envelopamento de pro- teínas maduras corretamente. Cromatografia líquida de alto desempenho (HPLC), cromatografia de afinidade ou outros métodos adequados podem ser empregados nos passos de purificação final onde alta pureza é desejada. Em uma modalidade, anticorpos foram feitos contra aminoácidos não naturais (ou proteínas ou peptídeos compreendendo aminoácidos não naturais) são utilizados como reagentes de purifi-cação, incluindo, mas não limitados a purificação baseada por afinidade de proteínas ou peptídeos compreendendo um ou mais aminoácidos não naturais. Uma vez puri-ficada, parcialmente ou para homogeneidade, como desejado, os polipeptídeos são opcionalmente utilizados para uma ampla variedade de utilidades, incluindo, mas não limitados a componentes de ensaios, terapêutica, profilaxia, diagnóstico, reagentes de pesquisa, e/ou imunógenos para produção de anticorpo. Anticorpos gerados contra polipeptídeos da presente invenção podem ser obtidos por administração dos polipeptídeos ou fragmentos produzindo epítopos, ou células a um animal, pre-ferivelmente um animal não humano, usando protocolos de rotina. Também, camun-dongos transgênicos, ou outros organismos, incluindo outros mamíferos, podem ser utilizados para expressar anticorpos humanizados. Os anticorpos descritos acima podem ser empregados para isolar ou para identificar clones expressando o polipep- tídeo ou para purificar os polipeptídeos. Anticorpos contra polipeptídeos da presente invenção podem também ser empregados para tratar doenças.
[00383]Polipeptídeos e polinucleotídeos da presente invenção podem também ser utilizados como vacinas. Consequentemente, em um aspecto adicional, a presente invenção relaciona-se a um método para induzir uma resposta imunológica em um mamífero que compreende inoculação em um mamífero com um polipeptídeo da presente invenção, adequada para produzir anticorpo e/ou resposta imune a célula T, incluindo, por exemplo, células T produtoras de citocina ou células T citotóxicas, para proteger o referido animal a partir de doença, se esta doença já estabilizada dentro do indivíduo ou não. Uma resposta imunológica em um mamífero pode também ser induzida por um método compreendido de distribuição de um polipeptídeo da presente invenção através de um vetor direcionado para expressão do polinu- cleotídeo e codificando o polipeptídeo in vivo a fim de induzir tal resposta imunológi- ca para produzir anticorpo para proteger o referido animal a partir de doenças da invenção. Uma via de administração do vetor é por acelerar nas células desejadas como um revestimento nas partículas ou outra forma. Tal vetor de ácido nucléico pode compreender, DNA, RNA, um ácido nucléico modificado, ou um DNA/RNA híbrido. Para uso como uma vacina, um polipeptídeo o um vetor de ácido nucléico serão normalmente providos como uma formulação de vacina (composição). A formulação pode ainda compreender um veículo adequado. Desde que um polipeptídeo pode ser quebrado no estômago, pode ser administrado parenteralmente (por exemplo, injeção subcutânea, intramuscular, intravenosa ou intra-dérmica). Formulações adequadas para administração parenterais incluem injeção de soluções estéreis aquosas e não aquosas que podem conter antioxidantes, tampões, bacteriostá- ticos e solutos que rendem a formulações isotônica com o sangue do recipiente; e suspensões estéreis aquosas e não aquosas que podem incluir agentes de suspensão ou agentes espessantes. A formulação de vacina pode também incluir sistemas adjuvantes para aumentar a imunogenicidade da formulação que são conhecidos pelos versados na técnica. A dose dependerá da atividade específica dependerá da atividade específica da vacina e pode ser facilmente determinada pela experimentação de rotina.
[00384]Em adição a outras referências notadas aqui, uma variedade de mé-todos de purificação/envelopamento de proteína são conhecidos pelos versados na técnica, incluindo, mas não limitados àquelas reveladas em R. Scopes, Protein Puri-fication, Springer-Verlag, N.I. (1982); Deutscher, Methods in Enzymology Vol. 182: Guide to Protein Purification, Academic Press, Inc. N.I. (1990); Sandana (1997) Bi-oseparation of Proteins, Academic Press, Inc.: Bollag et al (1996) Protein Methods, 2a edição Wiley-Liss; Walker (1996) The Protein Protocols Handbook, Humana Pre- es, NJ, Harris e Angal (1990) Protein Purification Application: A Practical Approach IRL, Press at Oxford, Oxford, Inglaterra; Harris e Angal Protein Purification Methods: A Practical Approach IRL, Press at Oxford, Oxford, Inglaterra; Scopes, (1993) Protein Purification: Principles and Practice 3a Edição, Springer Verlag, NI; Janson e Ryden (1998) Protein Purification: Principles, High Resolution Methods and Applications, Segunda Edição, Wiley-VCH, NI; e Walker (1998), Protein Protocols on CD-ROM, Humana Press, NJ; e as referências citadas aqui.
[00385]Uma vantagem de produzir uma proteína ou polipeptídeo de interesse com um aminoácido não natural em uma célula hospedeira eucariota ou célula hospedeira não eucariota é que tipicamente as proteínas ou polipeptídeos serão en- velopadas em suas conformações nativas. Entretanto, em certas modalidades da invenção, os versados na técnica reconhecerão que após síntese, expressão e/ou purificação, proteínas ou peptídeos podem possuir uma confirmação diferente das conformações desejadas dos polipeptídeos relevantes. Em um aspecto da invenção, a proteína ou polipeptídeo expresso é opcionalmente desnaturado e então recapturado. Isto é alcançado utilizando método conhecidos na técnica, incluindo mas não limitados a, por adição de uma chaperonina da proteína ou polipeptídeo de interesse, por solubilização das proteínas em um agente caotrópico tal como HCl guanidi- na, usando dissulfeto isomerase protéica etc.
[00386]Em geral, é ocasionalmente desejável desnaturar e reduzir polipeptí- deos expressos e então causar re-envelopamento dos polipeptídeos na conformação preferida. Por exemplo, guanidina, uréia, DTT, DTE, e/ou chaperonina podem ser adicionados a um produção de tradução de interesse. Métodos de redução, des-naturação ou renaturação de proteínas são conhecidos pelos versados na técnica (ver, as referências acima, e Debinski et al (1993) J. Biol. Chem. 268: 14065-14070; Kreitman e Pastan (1993) Bioconjug. Chem. 4;581-585; e Buchner et al (1992) Anal. Biochem. 205:263-270). Debinski et al, por exemplo, descreve a desnaturação e redução da inclusão de corpos protéicos em guanidina-DTE. As proteínas podem ser re-envelopadas em um tampão redox contendo, incluindo, mas não limitado a, gluta- tiona oxidada e L-arginina. Reagentes re-envelopantes podem ser passados em fluxo ou de outra forma movidos em contato com um ou mais polipeptídeos ou outro produto de expressão, ou vice-versa.
[00387]No caso de produção procariota de polipeptídeo FGF-21, o polipeptí- deo FGF-21 então produzido pode ser envelopada incorretamente e então faltar ou ter a atividade biológica reduzida. A bioatividade da proteína pode ser restaurada por “re-envelopamento”. Em geral, polipeptídeo FGF-21 envelopada incorretamente é re- envelopado por solubilização (onde o polipeptídeo FGF-21 é também insolúvel), densenvelopando e reduzindo a cadeia polipeptídica usando, por exemplo, um ou mais agentes caotrópicos (por exemplo, uréia e/ou guanidina) e um agente redutor capaz de reduzir pontes de dissulfeto (por exemplo, ditiotreito, DTT ou 2- mercaptoetanol, 2-ME). Em uma concentração moderada caotrópica, um agente oxidante é então adicionado (por exemplo, oxigênio, cistina ou cistamina), que permite a reformação de pontes dissulfeto. Polipeptídeo FGF-21 podem ser re-envelopado usando métodos padrões conhecido na técnica, tais como aqueles descritos na Pat. dos EUA Nos. 4.511.502, 4.511.503 e 4.512.922 que são aqui incorporadas por referência. O polipeptídeo FGF-21 pode também ser co-envelopado com outras proteínas para formar heterodímeros ou heteromultímeros.
[00388]Após re-envelopamento, o FGF-21 pode ser ainda purificado. Purifi-cação de FGF-21 pode ser realizada usando uma variedade de técnicas conhecidas pelos versados na técnica, incluindo cromatografia de interação hidrofóbica, croma- tografia de exclusão de tamanho, cromatografia de troca iônica, cromatografia líquida de alto desempenho de fase reversa, cromatografia de afinidade e semelhantes ou qualquer combinação das mesmas. Purificação adicional pode também incluir um passo de secagem ou precipitação da proteína purificada.
[00389]Após a purificação, FGF-21 pode ser trocado em diferentes tampões e/ou concentrado pr qualquer de uma variedade de métodos conhecidos na técnica, incluindo, mas não limitado por diafiltração e diálise. FGF-21 que é provido como uma proteína única pode ser sujeito a agregação e precipitação.
[00390]O FGF-21 purificado pode ser pelo menos 90% puro (como medido por cromatografia líquida de alto desempenho de fase reversa, RP-HPLC, ou gel eletroforese de docecil sulfato de sódio - poliacrilamida, SDS-PAGE) ou pelo menos 95% puro, ou pelo menos 98% puro, ou pelo menos 99% ou mais puro. Em relação ao valor numérico exato da pureza do FGF-21, o FGF-21 é suficientemente puro par auso como um produto farmacêutico ou para ainda processamento, tal como conjugação com um polímero solúvel em água com PEG.
[00391]Certas moléculas FGF-21 podem ser utilizadas como agentes tera-pêuticos em ausência de outros ingredientes ativos ou proteínas (outros que excipi- entes, veículos, e estabilizadores, albumina sérica e semelhantes), ou eles podem ser complexados com outras proteínas ou um polímero.
[00392]Métodos Gerais de Purificação. Qualquer um de uma variedade de passos de isolamento pode ser feitos no lisado celular, extrato, meio de cultura, corpos de inclusão, espaço periplasmático das células hospedeiras, citoplasma das células hospedeiras, ou outro material, compreendendo o polipeptídeo FGF-21 ou qualquer mistura de polipeptídeo FGF-21 resultando de qualquer passo de isolamento, mas não limitado a cromatografia de afinidade, cromatografia de troca iônica, cromatografia de interação hidrofóbica, cromatografia em gel filtração, cromatografia líquida de alto desempenho (“HPLC”), HPLC de fase reversa (“RP-HPLC”), adsorção de leito expandido, ou qualquer combinação e/ou repetição dos mesmos e em qualquer ordem apropriada.
[00393]Equipamento e outros materiais necessários usados no desempenho das técnicas descritas aqui são comercialmente disponíveis. Bombas, coletores de fração, monitores, gravadores, e sistemas inteiros são disponíveis de, por exemplos, Applied Biosystems (Foster City, CA), Bio-Rad Laboratories, Inc. (Hercules, CA) e Amercham Biosciences, Inc. (Piscataway, NJ). Materiais cromatográficos incluindo, mas não limitados a, materiais de matriz de troca, meios, e tampões são também disponíveis a partir de tais companhias.
[00394] Equilíbrio, e outros passos no processo da coluna de cromatografia descritos aqui tais como lavagem e eluição, podem ser mais facilmente realizados usando equipamento especializado como uma bomba. Bombas comercialmente dis-poníveis incluem, mas não são limitadas a HILOAD® Bomba P-50, Bomba Peristálti- ca P-1, Bomba P-901, e Boma P-903 (Amersham, Biosciences, Piscataway, NJ).
[00395]Exemplos de coletores de fração incluem Coletor de Fração RediFrac, Coletores de Fração FRAC-100 e FRAC-200, e Coletor de Fração SUPERFRAC® (Amersham Biosciences, Piscataway, NJ). Misturadores são também disponíveis para formar pH e gradiente de concentração linear. Misturadores comercialmente disponíveis incluem Misturador de Gradiente GM-1 e Misturadores Em-Linha (Amersham Biosciences, Piscataway, NJ).
[00396]O processo cromatográfico pode ser monitorado usando qualquer monitor comercialmente disponível. Tais monitores podem ser usados para coletar informação tipo UV, pH, e condutividade. Exemplos de detectores incluem Monitor UV-1, UNICORD® S II, Monitor UV-M II, Monitor UV-900, Monitor UPC-900, Monitor pH/C-900, e Monitor de Condutividade (Amersham Biosciences, Piscataway, NJ). De fato, sistemas inteiros são comercialmente disponíveis incluindo os vários sistemas AKTA® a partir da Amersham Biosciences (Piscataway, NJ).
[00397]Em uma modalidade da presente invenção, por exemplo, o polipeptí- deo FGF-1 pode ser reduzido e desnaturado por primeiro desnaturar o polipeptídeo FGF-21 purificado resultante em uréia, seguido por diluição em tampão TRIS contendo um agente redutor (tal como DTT) em um pH adequado. Em outra modalidade, o polipeptídeo FGF-21 é desnaturado em uréia em uma concentração variando de entre cerca de 2 M a cerca de 9 M, seguido por diluição em tampão TRIS em um pH variando de cerca de 5.0 a cerca de 8.0. A mistura re-envelopada desta modalidade pode então ser incubada. Em uma modalidade, a mistura re-envelopada é incubada em temperatura ambiente por quatro a vinte e quatro horas. A mistura de polipeptídeo FGF-21 reduzida ou desnaturada pode então ser ainda isolada ou puri- dicada.
[00398]Como aqui atestado, o pH da primeira mistura de polipeptídeo FGF- 21 pode ser ajustado antes de fazer qualquer passo subsequente de isolamento. Em adição, a primeira mistura de polipeptídeo FGF-21 ou qualquer mistura subsequente da mesma pode ser concentrada usando técnicas conhecidas na arte. Além disso, o tampão de eluição compreendendo a primeira mistura de polipeptídeo FGF-21 ou qualquer mistura subsequente da mesma pode ser trocada por um tampão adequado para o próximo passo de isolamento usando técnicas conhecidas pelos versados na técnica.
[00399]Cromatografia de Troca Iônica. Em uma modalidade, e como um passo adicional opcional, cromatografia de troca iônica pode ser feita na primeira mistura do polipeptídeo FGF-21. Ver, geralmente, ION EXCHANGE CHROMATOGRAPHY: PRINCIPLES AND METHODS (Cat. No. 18-1114-21, Amer- sham Biosciences (Piscataway, NJ)). Colunas de troca iônica comercialmente disponíveis incluem Colunas HITRAP®, HIPREP® e HILOAD® (Amersham Biosciences (Piscataway, NJ)). Tais colunas usam trocadores aniônicos fortes tais como Q SEPHAROSE® de Fluxo Rápido, Q SEPHAROSE® de Alto Desempenho, e Q SEPHAROSE® XL; trocadores catiônicos fortes tais como SP SEPHAROSE® de Alto Desempenho, SP SEPHAROSE® de Fluxo Rápido, e SP SEPHAROSE® XL; trocadores aniônicos fracos tal como DEAE SEPHAROSE® de Fluxo Rápido; e trocadores catiônicos fracos tal como CM SEPHAROSE® de Fluxo Rápido (Amersham Biosciences (Piscataway, NJ)). Cromatografia em coluna de troca aniônica ou catiô- nica pode ser feita no polipeptídeo FGF-21 em qualquer estágio do processo de purificação para isolar o polipeptídeo FGF-21 substancialmente purificado. O passo de cromatografia de troca catiônica pode ser feito usando qualquer matriz de troca ca- tiônica adequada. Matrizes de troca catiônica úteis incluem, mas não são limitados a materiais fibrosos, porosos, não porosos, microgranulares, com microesferas, ou matriz de troca catiônica de ligação cruzada. Tais materiais de matriz de troca catiô- nica incluem, mas não é limitada a celulose, agarose, dextran, poliacrilato, pilivinil, poliestireno, sílica, poliéter, ou compostos de qualquer dos antecendentes.
[00400]A matriz de troca catiônica pode ser qualquer trocador de cátion ade-quado incluindo trocadores catiônicos fortes e fracos. Trocadores catiônicos fortes podem permanecer ionizados ao longo de uma ampla variação de pH e então, pode ser capaz de se ligar a FGF-21 por uma ampla variedade de pH. Trocadores catiôni- cos fracos, entretanto, podem perder a ionização em função do pH. Por exemplo, um trocador catiônico fraco pode perder a carga quando o pH cai abaixo de cerca de pH 4 ou pH 5. Trocadores catiônicos fortes adequados incluem, mas não limitados a, grupo funcionais carregados tais como sulfonilpropila (SP), metil sulfonato (S), ou sulfoetila (SE). A matriz trocadora de cátion pode ser uma trocadora de cátion forte, preferivelmente tendo um FGF-21 ligante em pH variando de cerca de 2,5 a cerca de 6,0. Alternativamente, o trocador catiônico forte pode ter um FGF-21 ligando em pH variando de cerca de pH 2.5 a cerca de pH 5.5. A matriz trocadora catiônica pode ser uma trocadora catiônica forte tendo um FGF-21 de ligação em pH de cerca de 3.0. Alternativamente, a matriz de troca iônica pode ser um trocador catiônico forte, preferivelmente tendo um FGF-21 ligando a pH variando de cerca de 6.0 a cerca de 8.0. A matriz de troca catiônica pode ser um trocador catiônico forte preferivelmente tendo um FGF-21 de ligação pH de cerca 8.0 a cerca de 12.5. Alternativamente, o trocador catiônico forte pode ter um FGF-21 ligando a pH variando de cerca de pH 8.0 a cerca de pH 12.0.
[00401]Antes de carregar o FGF-21, a matriz de troca catiônica pode ser equilibrada, por exemplo, usando vários volumes na coluna de um dilunete, ácido fraco, por exemplo, quatro volumes de coluna de 20 mM de ácido acético, pH 3. Seguindo equilíbrio, o FGF-21 pode ser adicionado a coluna pode ser lavada de uma a várias vezes, antes a eluição de FGF-21 substancialmente purificado, também usando uma solução ácida fraca tal como uma solução de ácido acético fraco ou ácido fosfórico. Por exemplo, aproximadamente 2-4 volumes de coluna de 20 mM de ácido acético, pH 3, podem ser usados para lavar a coluna. Lavagens adicionais usando, por exemplo, 2-4 volumes de coluna de 0,05 M de acetato de sódio, pH 5.5, ou 0,05 M de acetato de sódio misturado com 0,1 M de cloreto de sódio, pH 5.5, pode também ser usado. Alternativamente, usando métodos conhecidos na técnica, a matriz de troca catiônica pode ser equilibrada usando vários volumes de coluna de um dilu- ente, base fraca.
[00402]Alternativamente, FGF-21 substancialmente purificado pode ser eluí- do por contato com a matriz trocadora catiônica com um tampão tendo um pH sufici-entemente baixo ou força iônica para substituir o FGF-21 da matriz. O pH do tampão de eluição pode variar de cerca de pH 2.5 a cerca de pH 6.0. Mais especificamente, o pH do tampão de eluição pode variar de cerca de pH 2.5 a cerca de pH 5.5, cerca de pH 2.5 a cerca de pH 5.0. O tampão de eluição pode ter um pH de cerca de 3.0. Em adição, a quantidade de tampão de eluição pode variar amplamente geralmente estará na variação de cerca de 2 a cerca de 10 volumes de coluna.
[00403]Seguindo a adsorção do polipeptídeo FGF-21 da matriz trocadora ca- tiônica, polipeptídeo FGF-21 substancialmente purificado pode ser eluído por contato da matriz com um tampão tendo um pH suficientemente alto ou força iônica para substituir o polipeptídeo FGF-21 a partir da matriz. Tampões adequados para uso em eluição em alto pH de polipeptídeo FGF-21 substancialmente purificado pode incluir, mas não limitado a citrato, fosfato, formato, acetato, HEPES, e tampões MES variando em concentração de pelo menos cerca de 5 mM a pelo menos cerca de 100 mM.
[00404]Cromatografia em fase-reversa. RP-HPLC pode ser feita para purificar proteínas seguindo protocolos adequados que são conhecidos pelos versados na técnica. Ver, por exemplo, Pearson et al, ANAL. BIOCHEM. (1982) 124:217-230 (1982); Rivier et al, J. CHROM. (1983) 268:11-119; Kunitani et al, J. CHROM. (1986) 359:391-402. RP-HPLC pode ser feita em polipeptídeo FGF-21 para isolar substancialmente polipeptídeo FGF-21 purificado. Assim, resinas derivadas de sílica com funcionalidades alquila com uma ampla variedade de comprimentos, incluindo mas não limitado a, pelo menos cerca de C3 a pelo menos cerca de C30, pelo menos cerca de C3 a pelo menos cerca de C20, ou pelo menos cerca de C3 a pelo menos cerca de C18, resinas podem ser usadas. Alternativamente, uma resina polimérica pode ser usada. Por exemplo, resina TosoHaas Amberchrome CG1000sd pode ser usada, que é uma resina de polímero estireno. Ciano ou resinas poliméricas com uma ampla variedade de comprimentos de cadeia alquila podem também ser usadas. Além disso, a coluna RP-HPLC pode ser lavada com um solvente tal como eta- nol. A coluna Source RP é outro exemplo de uma coluna RP-HPLC.
[00405]Um tampão de eluição adequado contendo um agente pareador iôni- co e um modificador orgânico tal como metanol, isopropanol, tetraidrofurano, aceto- nitrila ou etanol, pode ser usado para eluir o polipeptídeo FGF-21 a partir da coluna RP-HPLC. Os agentes pareadores iônicos mais comumente usados incluem, mas não são limitados a ácido acético, ácido fórmico, ácido perclórico, ácido fosfórico, ácido trifluoracético, ácido heptafluorbutírico, trietilamina, tetrametilamônio, tetrabuti- lamônio, e acetato de trietilamônio. Eluição pode ser feita usando um ou mais gradientes ou condições isocráticas, com condições de gradientes preferidas para reduzir o tempo de separação e diminuir a largura do pico. Outro método envolve o uso de dois gradientes com diferentes variações de concentração dos solventes. Exemplos de tampões de eluição adequados para uso em que podem incluir, mas não são limitados a acetato de amônio e soluções de acetonitrila.
[00406]Técnicas de Purificação de Cromatografia de Interação Hidrofóbica: Cromatografia de interação hidrofóbica (HIC) pode ser feita no polipeptídeo FGF-21. Ver geralmente, HYDROPHOBIC INTERACTION CHROMAOGRAFY HANDBOOK: PRINCIPLES AND METHODS (Cat. No. 18-1020-90, Amersham Biosciences (Pisca-taway, NJ) que é aqui incorporado por referência. Matrizes HIC adequadas podem incluir, mas não são limitadas, a matrizes substituídas com alquila ou arila, tais como matrizes substituídas com butila, hexila, octila, ou fenila incluindo matrizes de agarose, agarose de ligação cruzada, sefarose, celulose, sílica, dextran, poliestireno, po- li(metacrialto), e resinas de modo de mistura, incluindo mas não limitadas a resina polietilenoamina ou uma matriz poli(metacrilato) substituída com butila ou fenila. Fontes comercialmente disponíveis para cromatografia de coluna de interação hidro- fóciba incluem, mas não são limitadas a, colunas HITRAP®, HIPREP® e HILOAD® (Amersham Biosciences, Piscataway, NJ).
[00407]Resumidamente, antes do carregamento, a coluna HIC pode ser equilibrada usando tampões padrões conhecida pelos versados na técnica, tais como solução de ácido acético/cloreto de sódio ou HEPES contendo sulfato de amô- nio. Sulfato de amônio pode ser usado como um tampão para carregamento da coluna HIC. Após o carregamento do polipeptídeo FGF-21, a coluna pode então ser lavada usando tampões padrões e condições para remover materiais não desejados, mas retendo o polipeptídeo FGF-21 na coluna HIC. O polipeptídeo FGF-21 pode elu- ir com cerca de 3 a cerca de 10 volumes de coluna de um tampão padrão, tal como tampão HEPES contendo EDTA e concentração de sulfato de amônio mais baixa que o tampão de equilíbrio, ou um tampão ácido acético/cloreto de sódio, entre outros. Um gradiente de sal linear diminuindo usando, por exemplo, um gradiente de fosfato de potássio, pode também ser usado para eluir as moléculas de FGF-21. O eluente pode então ser concentrado, por exemplo, por filtração tais como diafiltração ou ultrafiltração. Diafiltração pode ser utilizada para remover o sal usado para eluir o polipeptídeo FGF-21.
[00408]Outras Técnicas de Purificação. Ainda outro passo de isolamento, por exemplo, gel filtração (GEL FILTRATION: PRINCIPLES AND METHODS (Cat. No. 18-1022-18, Amersham Biosciences (Piscataway, NJ)) que é aqui incorporado por referência, cromatografia em hidroxiapatita (matrizes adequadas incluem, mas não são limitadas a HA-Ultrogel, Alta Resolução, (Calbiochem), CHT Hidroxiapatita Cerâmica (BioRad), Bio-Gel HTP Hidroxiapatita (BioRad), HPLC, adsorção em leito expandido, ultrafiltração, diafiltração, liofilização, e semelhantes, pode ser feitos na primeira mistura de polipeptídeo FGF-21 ou qualquer mistura subsequente do mesmo, para remover qualquer excesso de sais e para substituir o tampão com um tampão adequado para o próximo passo de isolamento ou mesmo formulação do produto droga final.
[00409]Para produção do polipeptídeo FGF-21, incluindo polipeptídeo FGF- 21 substancialmente purificado, pode ser monitoado cada passo descrito aqui usando técnicas conhecidas pelos versados na técnica. Tais técnicas podem também ser usadas para acessar a produção de polipeptídeo FGF-21 substancialmente purificado seguindo o último passo de isolamento. Por exemplo, a produção do polipeptídeo FGF-21 pode ser monitorado usando qualquer coluna cromatografia líquida de alta pressão de fase reversa, tendo uma variedade de comprimentos de cadeia alquila tais como RP-HPLC ciano, C18RP-HPLC; bem como HPLC de troca catiônica e HPLC de gel filtração.
[00410]Em modalidades específicas da presente invenção, a produção de FGF-21 após cada passo de purificação pode ser pelo menos cerca de 30%, menos cerca de 35%, menos cerca de 40%, menos cerca de 45%, menos cerca de 50%, menos cerca de 55%, menos cerca de 60%, menos cerca de 65%, menos cerca de 70%, menos cerca de 75%, menos cerca de 80%, menos cerca de 85%, menos cerca de 90%, menos cerca de 91%, menos cerca de 92%, menos cerca de 93%, menos cerca de 94%, menos cerca de 95%, menos cerca de 96%, menos cerca de 97%, menos cerca de 98%, menos cerca de 99%, menos cerca de 99,9%, menos cerca de 99,99%, do FGF-21 no material de partida para cada passo de purificação.
[00411]Pureza pode ser determinada usando técnicas padrões, tais como SDS-PAGE, ou por medida do polipeptídeo FGF-21 usando ensaios de Western blot e ELISA. Por exemplo, anticorpos policlonais podem ser gerados contra proteínas isoladas a partir do controle negativo de fermentação de levedura e a recuperação da troca de catiônica. Os anticorpos podem também ser usados para provar a presença de contaminação de proteínas da célula hospedeira.
[00412]RP-HPLC material Vydac C4 (Vydac) consiste em partículas de sílica gel, as superfícies das quais carreiam cadeias C4-alquila. A separação do polipeptí- deo FGF-21 a partir de impurezas proteináceas é baseada em diferenças na força de interações hidrofóbicas. Eluição feita com um gradiente de acetonitrila em ácido trifluoracético diluído. HPLC preparativa é feita usando uma coluna sem mancha de aço (enchida com 2,8 a 3,2 litros de Vydac C4 sílica gel). O eluato Hidroxiapatita Ultragel é acidificado ou adição de ácido trifluoracético e carregado na coluna Vydac C4. Para lavagem e eluição um gradiente de acetonitrila em ácido trifluoracético diluído é usado. Frações são coletadas e imediatamente neutralizadas com tampão fosfato. As frações de polipeptídeo FGF-21 que estão dentro dos limites IPC são agrupadas.
[00413]Material DEAE Sepharose (Pharmacia) consiste em grupo dietilami- noetila (DEAE) que são covalentemente ligados a superfície de esferas de Sepharose. A ligação do polipeptídeo FGF-21 aos grupos DEAE é mediada por interações iônicas. Acetonitrila e ácido trifluoracético passa através da coluna sem ser retida. Após essas substâncias terem sido lavadas, traços de impurezas são removidos por lavagem da coluna com tampão acetato em um pH abaixo. Então a coluna é lavada com tampão fosfato neutro e polipeptídeo FGF-21 é eluído com um tampão com for- çao iônica aumentada. A coluna é empacotada com DEAE Sepharose de fluxo rápido. O volume da coluna é ajustado para assegurar um carregamento de polipeptídeo FGF-21 na variação de 1-10 mg de polipeptídeo FGF-21/mL de gel. A coluna é lavada com água e tampão de equilíbrio (fosfato de sódio/potássio). As frações agrupadas do eluato da HPLC são carregadas e a coluna é lavada com tampão de equillí- brio. Então a coluna é lavada com tampão de lavagem (tampão acetato de sódio) seguido por lavagem com tampão de equilíbrio. Subsequentemente, polipeptídeo FGF-21 é eluído a partir da coluna com tampão de eluição (cloreto de sódio, fosfato de sódio/potássio) e coletado em uma fração única de acordo com um perfil máximo de eluição. O eluato da coluna DEAE Sepharose é ajustado para a condutividade especificada. A droga resultante é esterilizada por filtração em garrafas de Teflon e estocadas a -70oC.
[00414]Método adicionais que podem ser empregados inclui, mas não são limitados a passos de remoção de endotoxinas. Endotoxinas são lipopolissacarídeos (LPSs) que são localizados externamente na membrana de células hospedeiras Gram-negativas, tal como, por exemplo, Escherichia coli. Métodos para redução dos níveis de endotoxina são conhecidos pelo versado na técnica e inclui, mas não limitado a técnicas de purificação usando suportes de sílica, pó de vidro ou hidroxiapati- ta, fase-reversa, afinidade, exclusão por tamanho, cromatografia de troca aniônica, cromatografia de interação hidrofóbica, uma combinação desses métodos e seme-lhantes. Modificações ou métodos adicionais podem ser requeridos para remover contaminantes tais como proteínas co-migratórias a partir do polipeptídeo de interes- se. Métodos para medir níveis de endotoxina são conhecidos por um versado na técnica e incluem, mas não limitados a ensaio de Lisado de Limulis Amebócito (LAL). O ensaio Endosafe®-PTS é um sistema colorimétrico, de tubo único que utiliza cartuchos pré-carregados com reagente LAL, substrato cromogênico, e endotoxina padrão controle junto com um espectrofotômetro portátil. Métodos alternativos incluem, mas não são limitados a método LAL Cinético que é turbidimétrico e usa um formato de placa de 96 poços.
[00415]Uma ampla variedade de métodos e procedimentos podem ser usados para avaliar a produção e pureza de uma proteína FGF-21 compreendendo um ou mais aminoácidos não naturalmente codificados, incluindo mas não limitados a ensaio de Bradfors, SDS-PAGE, SDS-PAGE corado com prata, SDS-PAGE corado com Coomassie, espectrometria de massa (incluindo mas não limitado a MALDI- TOF) e outros métodos para caracterização de proteínas conhecidos pelo versado na técnica.
[00416]Métodos adicionais incluem, mas não são limitados a; SDS-PAGE acoplado com métodos de corar proteínas, imunoblotting, matriz assistida com es- pectrometria de massa ionizante/dessorção a laer (MALDI-MS), cromatografia líqui- da/espectrometria de massa, foco isoelétrico, troca aniônica analítica, cromatofoco, e docroismo circular. VIII. Expressão em Sistemas Alternados
[00417]Várias estratégias têm sido empregadas para introduzir aminoácidos não naturais em proteínas em células hospedeiras não recombinantes, células hospedeiras mutageneizadas, ou em sistemas livre de células. Esses sistemas são também adequados para uso em fazer os polipeptídeos FGF-21 da presente invenção. Derivatização de aminoácidos com cadeias laterais ácidas tais como Lys, Cys e Tyr resultou na conversão de lisina em N2-acetil-lisina. Síntese química também provê um método direto para incorporar aminoácidos não naturais. Com o recente desen-volvimento da ligação enzimática e a ligação química nativa dos fragmentos peptídi- cos, é possível fazer proteínas maiores. Ver, por exemplo, P.E. Dawson e S.B.H. Kent, Annu. Rev. Biochem. 69:923 (2000). Ligação química de peptídeo e ligação química nativa é descritas na Patente dos EUA No. 6.184.344, Pedido de Patente dos EUA No. 2004/0138412, Pedido de Patente dos EUA No. 2003/0208046, WO 02/098901, e WO 03/042235, que são aqui incorporadas por referência. Um método biosssintético in vitro geral em que um tRNA supressor quimicamente acilado com o aminoácido não natural desejado é adicionado a um extrato in vitro capaz de suportar a biossíntese de proteína, tem sido usado para incorporação sítio-específica de mais de 100 aminoácidos não naturais em uma variedade de proteínas de virtualmente qualquer tamanho. Ver, por exemplo, V.W. Cornish, D. Mende; e P.G. Schultz, Angew Chem. Int. Ed. Engl., 1995, 34:621 (1995); c.J. Noren, S.J. Anthony- Cahill, M.C. Griffith, P.g. Schultz, A general methos for site-specific incorporation of unnatural amino acids into proteins, Science 244:182-188 (1989); e, J.D. bain, C.G. Glabe, T.A. Dix, A.R. Chamberlin, E.S. Diala, Biosynthetic site-specific incorporation of a non-natural amino acid into a polypeptide, J. Am. Chem. Soc. 111:8013-8014 (1989). Uma ampla variedade de grupos funcionais tem sido introduzida em proteínas para estudos de estabilidade de proteína, envelopamento de proteínas, mecanismo enzimático, e transdução de sinal.
[00418]Um método in vivo, denominado incorporação de pressão seletiva, foi desenvolvido para explorar a promiscuidade de sintetases selvagens. Ver, por exemplo, N. Budisa, C. Minks, S. Alefelder, W. Wenger, F.M. Dong, L. Moroder e R. Huber, FASEB J., 13:41 (1999). Uma cepa auxotrófica, em que a via metabólica relevante suprindo a célula com aminoácido natural particular é mudada é crescida em meio mínimo contendo concentrações limitadas do aminoácido natural, enquanto transcrição do gene alvo é reprimida. No início da fase de crescimento estacionária, o aminoácido natural é depletado e substituído com um aminoácido não natural análogo. Indução de expressão de proteína recombinante resulta no acúmulo de uma proteína contendo o análogo não natural. Por exemplo, usando esta estratégia, o m e p-fluorfenilalanna têm sido incorporados em proteínas, e exibe duas características básicas no espectro UV que podem ser facilmente identificadas, ver, por exemplo, C. Minks, R. Huber, L. Moroder e N. Budisa, Anal. Biochem., 284:29 (2000); trilfuorme- tionina tem sido usada para substituir metionina em bacteriófago T4 lisozima para estudar sua interação com ligantes quitooligosacarídeos por 19F RMN, ver, por exemplo, H. Duewel, E. Daub, V. Robinson e J.F. Honek, Biochemistry, 36:3404 (1997); e trifluorleucina tem sido incorporada no lugar de leucina, resultando em aumento térmico e estabilidade química de uma proteína leucina-adesiva. Ver, por exemplo, Y. Tang, G. Ghirlanda, W.A. Petka, T. Nakajima, W.F. DeGrado e D.A. Tirrell, Angew Chem Int Ed. Engl. 40:1494 (2001). Além disso, selenometionina e telu- rometionina são incorporadas em várias proteínas recombinantes para facilitar a solução de fases na cristalografia de raio X. Ver, por exemplo, W.A. Hendrickson, J.R. Horton e D.M. Lemaster, EMBO J. 9:1665 (1990); J.O. Boles, K. Lewinski, M. Kunkle, J.D. Odom, B. Dunlap, L. Lebioda e M. Hatada, Nat. Struct. Biol., 1:283 (1994); N. Budisa, B. Steipe, P. Demange, C. Echerskorn, J. Kellermann e R. Huber, Eur. J. Biochem., 230:788 (1995); e N. Budisa, W. Karnbrock, S. Steinbacher, A.Humm, L. Prade, T. Neuefeind, L. Moroder e R. Huber, J. Mol. Biol. 270:616 (1997). Análogos de metionina com funcionalidades alqueno ou alquino têm também sido eficientemente incorporados, permitindo a modificação adicional de protéinas por meios químicos. Ver, por exemplo, J.C. van Hest e D.A. Tirrell, FEBS Lett. 428:68 (1998); J.C. van Hest, K.L. Kiick e D.A. Tirrell, J. Am. Chem. Soc. 122:1282 (2000); e K.L. Kiick e D.A. Tirrell, Tetrahedron, 56:9487 (2000); Patente dos EUA No. 6.586.207; Pedido de Patente dos EUA 2002/0042097, que são aqui incorporados por referência.
[00419]O sucesso deste método depende do reconhecimento dos aminoáci- dos não naturais análogos por aminoacil-tRNA sintetase, que, em geral, requer alta seletividade para garantir a fidelidade da tradução da proteína. Uma via de expandir o objetivo deste método é relaxar a especificidade do substrato da aminoacil-tRNA sintetase, que tem dido alcançado em um número limitado de casos. Por exemplo, substituição de Ala294 por Gly em Escherichia colie fenilalanil-tRNA sintetase (PheRS) aumenta o tamanho do bolsa de ligação do substrato, e resulta em acilação de tRNAPhe por (p-Cl-Phe). Ver, M. Ibba, P. Kast e H. Hennecke, Biochemistry, 33:7107 (1994). Uma cepa de Escherichia coli contendo este mutante PheRS permite a incorporação de p-Cl-fenilalanina ou p-Br-fenilalanina no lugar da fenilalanina. Ver, por exemplo, M. Ibba e D.A. Tirrell, FEBS Lett., 467:37 (2000). Similarmente, um ponto de mutação Phe130Ser perto do sítio de ligação aminoácido de Escherichia coli tirosil-tRNA sintetase foi mostrado permitir azatirosina ser incorporada mais eficientemente que tirosina. Ver, F. Hamano-Takaku, T. Iwama, S. Saito-Yano, K. Takaku, Y. Monden, M. Kitabatake, D. Soll e S. Nishimura, J. Biol. Chem. 275:40324 (2000).
[00420]Outra estratégia para incorporar aminoácidos não naturais em proteínas in vivo é modificar sintetases que têm mecanismos revisores. Essa sintetases não podem discriminar e assim ativar aminoácidos que são estruturalmente similares aos aminoácidos naturais cognatos. Este erro é corrigido em um sítio separado, que deacila o aminoácido carregado erroneamente a partir do tRNA para manter a fidelidade da tradução da proteína. Se a atividade revisora da sintetase é inabilitada, análogos estruturais que são ativadas erroneamente podem escapar da função de adição e ser incorporados. Esta abordagem tem sido demonstrada recentemente com a valil-tRNA sintetase (ValRS). Ver, V. Doring, H. D. Mootz, L. A. Nangle, T.L. Hendrickson, V. de Crecy-Lagard, P. Schimmel e P. Marliere, Science, 292:501 (2001). ValRS pode aminoacilar erroneamente tRNAVal com Cys, Thro ou aminobutirato (Abu); esses aminoácidos não cognatos são subsequentemente hidrolizados por domínio de edição. Após mutagênese aleatória do cromossomo de Escherichia coli, uma cepa mutante de Escherichia coli foi selecionada que tenha uma mutação no sítio de edição de ValRS. Este ValRS com defeito de edição incorretamente carrega tRNA Val com Cys. Porque Abu estericamente lembra Cys (grupo -SH de Cys é substituído com -CH3 em Abu), o mutante ValRS também incorpora Abu nas proteínas quando esta cepa mutante Escherichia coli é crescida em presença de Abu. Análise de espectrometria de massa mostra que cerca de 24% de valinas são substituídas por Abu em cada posição valina na proteína nativa.
[00421]Síntese de fase sólida e métodos semi-sintéticos têm também permi- tido a síntese de um número de protéinas contendo aminoácidos novos. Por exemplo, ver as seguintes publicações e referências citadas nas mesmas, que são como segue: Crick, F.H.C., Barrett, L. Brenner, S. Watts-Tobin, R. General nature of the genetic code for proteins. Nature, 192:1227-1232 (1961); Hofmann, K., Bohn, H. Studies on polypeptídes. XXXVI. The effect of pyrazole-imidazole replacements on the S-protein activating potency of an S-peptide fragment. J. Am. Chem. 88(24):5914-5919 (1966): Kaiser, E.T. Synthetic approaches to biologically active peptides and proteins including enzymes, Acc. Chem. Res., 22:47-54 (1989); Na- katsuka, T., Sasaki, T., Kaiser, E.T., Peptide segment coupling catalyzed by the semisynthetic enzyme thiosubtilisin, J. Am. Chem. Soc. 109:3808-3810 (1987); Schnolzer, M., Kent. S.B.H. Constructing proteins by dovetailing unprotected synthetic peptides: backbone-engineered HIV protease, Science, 256(5054):221-225 (1992); Chaiken, I.M. Semisynthetic peptides and proteins CRC Crit. Rev. Biochem. 11(3):255-301 (1981); Offord, R.E. Protein engineering by chemical means? Protein Eng. 1(3):151-157 (1987); e Jackson, D.Y., Burnier, J., Quan, C., Stanley, M., Tom, J., Wells, J.A. A Designed Peptide Ligase for Total Synthesis of Ribonuclease A with Unnatural Catalytic Residues, Science, 266(5183):243 (1994).
[00422]Modificação química tem sido usada para introduzir uma variedade de cadeias laterais não naturais, incluindo co-fatores, marcadores de rotação, e oli- gonucleotídeos em proteínas in vitro. Ver, por exemplo, Corey, D.R., Schultz, P.G., Generation of a hybrid sequence-specific single-stranded deoxyribonuclease, Science, 238(4832):1401-1403 (1987);Kaiser, E.T., Lawrence, D.S. Rokita, S.E., The chemical mutation of enzyme active sites, Science, 226(4674):505-511 (1984); Neet, K.E., Nanci, A., Koshland, D.E. Properties of thiol-subtilisin, J. Biol. Chem. 243(24)6392-6401 (1968); Polgar, L. e M.L. Bender. A new enzyme containing a synthetically formed active site. Thiol-subtilisin. J. Am. Chem. Soc. 88:3153-3154 (1966); e Pollack, S.J., Nakayama, G., Schultz, P.G., Introduction of nucleophiles and spectroscopic probes into aantibody combining sites, Science, 242(4881):1038-1040 (1988).
[00423]Alternativamente, métodos biossintéticos que empregam aminoacil- tRNAs quimicamente modificados têm sido incorporados em vários padrões biofísicos em proteínas sintetizadas in vitro. Ver a seguintes publicações e referências citadas dentro: Brunner, J. New Photolabeling and crosslinking methods, Annu. Rev. Biochem. 62:483-514 (1993); e, Krieg, U.C., Walter, P., Hohnson, A.E. Photocrosslinking of the signal sequence of nascent preprolactin of the 54-kilodalton polypeptide of the signal recognition particle, Proc. Natl. Acad. Sci. 83(22):8604-0608 (1986).
[00424]Previamente, tem sido mostrado que aminoácidos não naturais podem ser incorporados sítio-especificamente em proteínas in vitro pela adição de supressores de tRNA quimicamente aminoacilados para reações de síntese de proteína programas com um gene contendo uma mutação não senso âmbar desejada. Usando estas abordagens, um pode substituir um número de vinte aminoácidos comuns com homólogos estruturais próximos, por exemplo, fluorfenilalanina para feni- lalanina, usando cepas auxotrópicas para um aminoácido particular. Ver, por exemplo, Noren, C.J.m Anthony-Cahill, Griffith, M.C., Schultz, P.G., A general method for site-specific incorporation of unnatural amino acids into proteins, Science, 244:182188 (1989); M.W. Nowak, et al, Science, 268:439-42 (1995); Bain, J.D., Glabe, C.G., Dix. T.A., Chamberlin, A.R., Diala, E.S. Biosynthetic site-specific Incorporation of a non-natural amino acid into a polypeptide, J. Am. Chem. Soc., 111:8013-8014 (1989); N. Budisa et al, FASEB J. 13:41-51 (1999); Ellman, J.A., Mendel, D., Anthony-Cahill, S., Noren, C.J., Schultz, P.G. Biosybthetic methos for introducing unnatural amino acids site-specifically into proteins, Methods in Enz., vol. 202, 301-336 (1992); e, Mendel, D., Cornish, V.W. & Schultz, P.G. Site-Directed Mutagenesis with an Expanded Genetic Code, Annu. Rev. Biophys, Biomol. Struct. 24, 435-62 (1995).
[00425]Por exemplo, um tRNA supressor foi preparado de forma a reconhecer um códon de parada UAG e foi quimicamente aminoacilado com um aminoácido não natural. Mutagênese sítio-direcionada convencional foi usada para introduzir o códon de parada TAG, no sítio de interesse no gene da proteína. Ver, por exemplo, Sayers, J.R., Schmidt, W. Eckstein, F., 5’-3’ Exonucleases in phosphorothioate- based oligonucleotide-directed mutagenesis, Nucleic Acids Res, 16(3):791-802 (1988). Quando o tRNA supressor acilado e o gene mutante foram combinados em um sistema transcrição/tradução in vitro, o aminoácido não natural foi incorporado em resposta ao códon UAG que deu uma proteína contendo aquele aminoácido na posição especificada. Experimentos usando [3H]-Phe e experimentos com a-hidróxi ácidos demonstraram que somente o aminoácido desejado é incorporado na posição especificada pelo códon UAG e que este aminoácido não é incorporado em qualquer outro sítio na proteína. Ver, por exemplo, Noren, et al, acima; Kobayaschi, et al (2003) Nature Structural Biology 10(6):425-432; e Ellman, J.A., Mendel, D., Schultz, P.G. Site-specific incorporation of novel backbone structures into proteins, Sciences, 255(5041):197-200 (1992).
[00426]Um tRNA pode ser aminoacilado com um aminoácido desejado por qualquer método ou técnica, incluindo, mas não limitado a aminoacilação química ou enzimática.
[00427]Aminoacilação pode ser realizada por aminoacil tRNA sintetases ou por moléculas enzimáticas, incluindo, mas não limitado a ribozimas. O termo “ribozi- ma” é passível de mudança com “RNA catalitico”. Cech e colaboradores (Cech, 1987, Science, 236:1532-1539; McCorkle et al, 1987, Concepts Biochem. 64:221226) demonstraram a presença de RNAs de ocorrência natural que pode atuar como catalisador (ribozima). Entretanto, embora esses RNAs catalisadores naturais têm somente sido mostrados agir em substratos de ácido ribonucléico para clivagem e splicing, o desenvolvimento recente da evolução artificial de ribozimas tem expandido o repertório de catálise para várias reações químicas. Estudos têm identificado moléculas de RNA que pode catalisar ligações aminoacil-RNA em sua própria (2’)3- terminal (Illangakekare et al, 1995, Science 267:643-647), e uma molécula RNA que pode transferir um aminoácido a partir da molécula de RNA a outra (Lohse et al, 1996, Nature, 31:442-444).
[00428]Publicação do Pedido de Patente dos EUA 2003/0228593, que é aqui incorporada por referência, descreve métodos para construir ribozimas e seu uso em aminoacilação de tRNAs com naturalmente codificados e aminoácidos não natural-mente codificados. Formas de substrato imunobilizado de moléculas enzimáticas que podem aminoacilar tRNAs, incluindo, mas não limitado a, ribozimas, pode permitir purificação por afinidade eficiente de produtos aminoacilados. Exemplos de susb- tratos adequados incluem agarose, sepharose e esferas magnéticas. A produção e uso da forma de substrato imobilizado de ribozima para aminoacilação é descrita em Chemistry and Biology, 2003, 10:1077-1084 e Publicação do Pedido de Patente dos EUA 2003/0228593, que são aqui incorporados por referência.
[00429]Métodos de aminoacilação química incluem, mas não são limitados àqueles introduzidos por Hecht e colaboradores (Hecht, S.M. Acc. Chem. Res. 1992, 25, 545; Heckler, T., G.; Roesser, J.R.; Xu, C.; Chang, P.; Hecht, S.M. Biochemistry 1988, 27, 7254; Hecht, S.M.; Alford, B.L.; Kuroda, Y.; Kitano, S. J. Biol. Chem. 1978, 253, 4517) e por Schultz, Chamberlin, Dougherty e outros (Cornish, V.W.; Mendel, D.; Schultz, P.G. Angew Chem. Int. Ed. Engl. 1995, 34, 621; Robertson, S.A.; Ellman, J.A.; Schultz, P.G. J. Am. Chem. Soc. 1991, 113, 2722; Noren, C.J.; Anthony-Cahill, S.J.; Griffith, M.C.; Schultz, P.G. Science 1989, 24, 182; Bain, J.D.; Glabe, S.G.; Dix, T.A.; Chamberlin, A.R. J. Am. Chem. Soc. 1989, 111, 8013; Bain, J.D. et al, Nature, 1992, 356, 537; Gallivan, J.P.; Lester, H.A.; Dougherty, D.A. Chem. Biol. 1997, 4, 740: Turcatti, et al, J. Biol. Chem. 1996, 271, 1991; Nowak, M.W. et al, Science, 1995, 268, 439; Saks, M.E. et al, J. Biol. Chem. 1996, 271, 23169; Hohsaka, T. et al J. Am. Chem. Soc. 1999, 121, 24), que são aqui incorporados por referência, para evitar o uso de sintetases na aminoacilação. Tais métodos ou outros métodos de aminoacilação química podem ser usados para aminoacilar moléculas tRNA.
[00430]Métodos para gerar RNA catalítico podem envolver a geração de grupos separados de sequências de ribozimas aleatórias, fazendo a evolução direcionada dos grupos, selecionando os grupos para atividade de aminoacilação desejada, e selecionada sequências para essas ribozimas exibindo a atividade a aminoaci- lação desejada.
[00431]Ribozimas podem compreender motivos e/ou regiões que facilitam a atividade de acilação, tal como um motivo GGU e uma região rica em U. Por exemplo, tem sido relatado que regiões ricas em U podem facilitar o reconhecimento de um substrato aminoácido, e um motivo GGU pode formar um par de base com o terminal 3’de um tRNA. Em combinação, o Ggu e o motivo e região rica em U facilita o reconhecimento simultâneo de ambos, aminoácido e tRNA simultaneamente, e assim facilita a aminoacilação do 3’terminal do tRNA.
[00432]Ribozimas podem ser geradas por seleção in vitro usando um r24mini conjugado parcialmente aleatório com tRNAAsmCCCG, seguido por construção sistemática de uma sequência consenso encontrada nos clones ativos. Uma ribozi- ma exemplar obtida por este método é denomiado “Fx3 ribozima” e é descrita em Pub. Ped. Pat. dos EUA No. 2003/0228593, o conteúdo da qual é aqui incorporado por referência, age como um catalisador versátil para a síntese de vários aminoacil- tRNA carregado com aminoácidos não naturais cognatos.
[00433]Imobilização em um substrato pode ser usada para permitir a purificação de afinidade eficiente dos tRNAs aminoacilados. Exemplos de substratos adequados incluem, mas não são limitados a agarose, sepharose, e esferas magnéticas. Ribozimas podem ser imobilizada em resinas por tomar vantagem da estrutura química do RNA, tal como 3’-cis-diol na ribose de RNA pode ser oxidada com perio- dato para produzir o dialdeído correspondente para facilitar a imobilização do RNA na resina. Vários tipos de resinas podem ser usados incluindo as resinas hidrazida acessíveis em que a aminação redutiva faz a interação entre a resina e a ribozima uma ligação irreversível. Síntese de aminoacil-tRNAs pode ser significantemente facilitada por esta técnica de aminoacilação em coluna. Kourouklis et al, Methods 2005; 36:239-4 descreve um sistema de aminoacilação baseada em coluna.
[00434]Isolamento dos tRNAs aminoacilados pode ser realizados em uma variedade de formas. Um método adequado é para eluir os tRNAs aminoacilados a partir de uma coluna com um tampão tal como solução de acetato de sódio com 10 mM de EDTA, um tampão contendo 50 mM N-(2-hidroxietil)piperazina-N’-(ácido 3- propanossulfônico), 12,5 mM KCl, pH 7.0, 10 mM EDTA, ou simplesmente um EDTA tamponado com água (pH 7.0).
[00435]Os tRNAs aminoacilados podem ser adicionados para reações de tradução a fim de incorporar o aminoácido com que o tRNA foi aminoacilado em uma posição de escolha em um polipeptídeo feito por reação de tradução. Exemplos de sistemas de tradução em que os tRNAs aminoacilados da presente invenção pode ser usados incluem, mas não são limitados a lisados celulares. Lisados celulares provêm componentes reacionais necessários para tradução in vitro de um polipeptí- deo a partir de uma entrada de mRNA. Exemplos de tais componentes de reação incluem, mas não são limitados de proteínas ribossomais, rRNA, aminoácidos, tRNAs, GTP, ATP, iniciação de tradução e fatores de alongamento e fatores adicionais associados com tradução. Adicionalmente, sistemas de tradução podem ser lotes de traduções ou tradução compartimentalizada. Sistemas de tradução em lotes combinam componentes da reação em um compartimento único enquanto sistemas de tradução compartimentalizada separam os componentes da reação de tradução a partir de produtos de reação que podem inibir a eficiência de tradução. Tais sistemas de tradução estão comercialmente disponíveis.
[00436]Ainda, um sistema transcrição/tradução acoplado pode ser usado. Sistemas de transcrição/tradução acoplados permitem para ambos, transcrição de uma entrada de DNA em um mRNA correspondente, que é por sua vez traduzida por componentes de reação. Um exemplo de uma transcrição/tradução acoplada comer-cialmente disponível no Sistema de Tradução Rápida (RTS, Roche Inc). O sistema inclui uma mistura contendo lisado de E. coli para prover componentes traducionais tais como ribossomos e fatores de tradução. Adicionalmente, uma RNA polimerase é incluída para a transcrição da entrada de DNA em um modelo de mRNA para uso na tradução. RTS pode ser compartimentalizado dos componentes de reação por via de uma membrana interposta entre os compartimentos de reação, incluindo um compar-timento de suprimento/perda e um compartimento de transcrição/tradução.
[00437]Aminoacilação de tRNA pode ser feita por outros reagentes, incluin- do, mas não limitados a transferases, polimerases, anticorpos catalíticos, proteínas multi-funcionais, e semelhantes.
[00438]Stephan em Scientist 10 de Outubro de 2005; páginas 30-33 descrevem métodos adicionais para incorporar aminoácidos não naturalmente codificados em proteínas. Lu et al em Mol. Cell. 2001 Out; 8(4):759-69 descreve um método em que uma proteína é quimicamente ligada a um peptídeo sintético contendo aminoá- cidos não naturais (ligação de proteína expressa).
[00439]Técnicas de microinjeção têm também sido usadas para incorporar aminoácidos não naturais em proteínas. Ver, por exemplo, M.W. Nowak, P.C. Kearney, J.R. sampson, M.E. Saks, C.G. Labarca, S.K. Silverman, W.G. Chong, J. Thorson, J.N. Abelson, N. Davidson, P.G. Schultz, D.A. Dougherty e H.A. Lester, Science, 268:439 (1995); e D.A. Dougherty, Curr. Opin. Chem. Biol. 4:645 (2000). Um oó- cito Xenopus foi co-injetado com espécies de RNA feitas em in vitro: um mRNA codificando a proteína alvo com um códon parador UAG na posição aminoácido de interesse e esse tRNA supressor âmbar aminoacilado com o aminoácido não natural desejado. A maquinaria traducional do oócito então insere o aminoácido não natural na posição especificada por UAG. Este método tem permitido estudos estrutura- função in vivo de proteínas integrais de membrana, que são geralmente não permitem sistemas de expressão in vitro. Exemplos incluem a incorporação de um amino- ácido fluorescente no receptor de taquicinina neuroquinina-2 para medir distâncias por transferência de energia de ressonância flurorescente, ver, por exemplo, G. Tur- catti, K. Nemeth, M.D. Edgerton, U. Meseth, F. Talabot, M. Peitsch, J. Knowles, H. Vogel e a. Chollet, J. Biol. Chem., 271:19991 (1996); a incorporação de aminoácidos biotinilados para identificar resíduos expostos na superfície em canais de íon, ver, por exemplo, J.P. Galliven, H.A. Lester e D.A. Dougherty, Chem. Biol. 4: 739 (1997); o uso de análogos tirosina presa para monitorar mudanças conformacionais em um canal iônico em tempo real, por exemplo, J.C. Miller, S.K. Silverman, P.M. England, D.A. Dougherty e H.A. Lester, Neuron, 20:619 (1998); e, o uso de aminoácido alfa hidróxi para mudar as estruturas de canal iônico para permitir seus mecanismos li- gantes. Ver, por exemplo, P.M. England, Y. Zhang. D.A. Dougherty e H.A. Lester, Cell, 96:89 (1999); e T. Lu, A.U. Ting, J. Mainland, L.Y. Jan. P.G. Schultz e J. Yang, Nat. Neurosci., 4:239 (2001).
[00440]A habilidade de incorporar aminoácidos não naturais diretamente em proteínas in vivo oferece uma ampla variedade de vantagens incluindo mas não limi-tados a altas produções de protéinas mutantes, facilidade técnica, o potencial de estudar as proteínas mutantes em células ou possivelmente em organismos vivos e o uso dessas proteínas mutantes em tratamento terapêuticos e usos diagnósticos. A habilidade de incluir aminoácidos não naturais com vários tamanhos, acidez, nucleo- filicidade, hidrofobicidade, e outras propriedades em proteínas pode grandemente expandir nossa habilidade de racionalmente e sistematicamente manipular as estru-turas de proteínas, ambas, a função padrão protéica e criar novas proteínas ou or-ganismos com propriedades novas.
[00441]Em uma tentativa de incorporar sítio-especificamente para-F-Phe, um par tRNAPheCUA supressor âmber/fenilalanil-tRNA sintetase de levedura foi utilizada em uma cepa de Escherichia coli Phe auxotrófica, p-F-Phe resistente. Ver, por exemplo, R. Furter, Protein Sci. 7:419 (1998).
[00442]Pode também ser possível para obter expressão de um polinucleotí- deo FGF-21 da presente invenção usando um sistema de tradução livre de célula (in vitro). Sistemas de tradução podem ser celulares ou livres de células, e podem ser procariotos ou eucariotos. Sistemas de tradução celulares incluem, mas não são limitados a preparações de células inteiras tais como células permeabilizadas ou culturas de células em que uma sequência de ácido nucléico desejada pode ser transcrita para RNAm e o RNAm traduzido. Sistemas de tradução livre de célula são comercialmente disponíveis e muitos tipos diferentes e sistemas são bem conhecidos. Exemplos de sistemas livres de células incluem, mas não são limitados a lisados procariotos tal como lisados de Escherichia coli, e lisados eucariotos como extratos de germem de trigo, lisados de célula de inseto, lisados de reticulócito de coelho, lisados de oócito de coelho e lisados de célula humana. Extratos ou lisados eucario- tos podem ser preferidos quando a proteína resultante é glicosilada, fosforilada ou de outra forma modificada porque muitas dessas modificações são somente possíveis em sistemas eucariotos. Alguns desses extratos e lisados são comercialmente disponíveis (Promega; Madison, Wis; Stratagene; La Jolla; Calif; Amersham; Arlington Heights; III.; GINCO/BRL; Grand Island; NI). Extratos membranosos, tais como extratos pancreáticos caninos contendo membranas microssomais, são também disponíveis que são úteis para tradução de proteínas secretórias. Nesses sistemas, que podem incluir ou RNAm como um padrão (tradução in vitro) ou DNA como um padrão (tradução e transcrição in vitro combinadas), a síntese in vitro é direcionada pelos ribossomos. Esforços consideráveis têm sido aplicados para o desenvolvimento de sistemas de expressão de proteína livre de célula. Ver, por exemplo, Kin, D.M. e J.R. Swartz, Biotechnology and Bioengineering, 74:309-316 (2001)(; Kim, D.M. e J.R. Swartz, Biotechnology Letters, 22, 1537-1542 (2000); Kim; D.M. e J.R. Swartz, Biotechnology Progress, 16, 385-390 (2000); Kim, D.M., e J.R. Swartz, Biotechnology and Bioengineering, 66, 180-188 (1999); e Parnaik, R. e J.R. Swartz, Biotecni- ques 24, 862-868 (1998); Patente dos EUA No. 6.337.191; Publicação de Patente dos EUA No. 2002/0081660; WO 00/55353; WO 90/05785, que são aqui incorporados por referência. Outra abordagem que pode ser aplicada a expressão de polipep- tídeo FGF-21 compreendendo um aminoácido não naturalmente codificado inclui a técnica de fusão RNAm-peptideo. Ver, por exemplo, R. Roberts e J. Szostak, Proc. Natl. Acad. Sci. (EUA) 94:12297-12302 (1997); A. Frankel et al, Chemistry & Biology 10:1043-1050 (2003). Nesta abordagem, um padrão mRNA ligado a puromicina é traduzido em peptídeo no ribossomo. Se uma ou mais moléculas tRNA tem sido modificada, aminoácidos não naturais podem ser incorporados em peptídeo também. Após o último códon de RNAm ter sido lido, puromicina captura o C-terminal do pep- tídeo. Se o conjugado mRNA-peptídeo resultante é encontrado para ter propriedades interessantes em um ensaio in vitro, sua identidade pode ser facilmente revelada a partir da sequência mRNA. Desta forma, um pode selecionar bibliotecas de poli- peptídeos FGF-21 compreendendo um ou mais aminoácidos não naturalmente codi- ficados para identificar polipeptídeos tendo propriedades desejadas. Mais recentemente, traduções ribossomais com componentes purificados têm sido relatados permitir a síntese de peptídeos substituídos com aminoácidos não naturalmente codificados. Ver, por exemplo, A. Foster et al, Proc. Natl. Acad. Sci (EUA) 100:6353 (2003).
[00443]Sistemas de tradução reconstituídos podem também ser usados. Misturas de fatores de tradução purificados têm também sido usados com sucesso para traduzir mRNA em proteína bem como combinações de lisados ou lisados su-plementados com fatores de tradução purificados tais como fator de iniciação 1 (IF- 1), IF-2, IF-3 (α ou β), fator de alongamento T (EF-Tu) ou fatores de terminação. Sistemas livres de células podem também ser sistemas de transcrição/tradução acoplados em que DNA é introduzido ao sistema, transcrito em mRNA e mRNA traduzido como descrito em Current Protocols in Molecular Biology (F.M. Ausubel et al, editores, Wiley Interscience, 1993), que é aqui especificamente incorporado por referência. RNA transcrito em sistema de transcrição eucarioto pode ser na forma de RNA heteronuclear (hnRNA) ou terminação 5’caps (7-metil guanosina) e terminação 3’poli A de mRNA de causa madura, que pode ser uma vantagem em certos sistemas de tradução. Por exemplo, mRNAs recobertos são traduzidos com alta eficiência no sistema reticulado lisado. IX. Polímeros Macromoleculares acoplados a polipeptídeos FGF-21
[00444]Várias modificações nos polipeptídeos aminoácidos não naturais descritos aqui podem ser efetuadas usando as composições, métodos, técnicas e estratégias descritas aqui. Essas modificações incluem a incorporação de funcionali-dade adicional no componente aminoácido não natural do polipeptídeo, incluindo mas não limitado a um marcador, um corante, um polímero, um polímero solúvel em água, um derivado de polietileno glicol, um ligante foto-cruzado, um radioisótopo, um composto citóxico, uma droga, um marcado de afinidade, um marcador de foto- afinidade, um composto reativo, um resina, uma segunda proteína o polipeptídeo ou polipeptídeo análogo, um anticorpo ou fragmento de anticorpo, um metal quelante, um cofator, um ácido graxo, um carboidrato, um polinucleotídeo, um DNA, um RNA, um polinucleotídeo anti-senso, um sacarídeo, um dendrímero solúvel em água, uma ciclodextrina, um ácido ribonucléico inibitório, um biomaterial, uma nanopartícula, um marcador de rotação, um fluoróforo, uma fração contendo metal, uma fração radioativa, um grupo funcional novo, um grupo que interage covalentemente ou não cova- lentemente com outras moléculas; uma fração foto-ligada, uma fração excitável de radiação actínica, uma fração foto-isomerizável, biotina, um derivado de biotina, um análogo de biotina, uma fração incorporada a um átomo pesado, um grupo quimica-mente clivável, um grupo foto-clivável, um cadeia lateral alongada, um açúcar ligado a carbono, um agente redox ativo, um aminotioácido, uma fração tóxica, uma fração isotopicamente marcada, um padrão biofísico, um grupo fosforescente, um grupo quimioluminescente, um grupo eletro-denso, um grupo magnético, um grupo interca- lante, um cromóforo, um agente de transferência de energia, um agente biologicamente ativo, um macador detectável, uma molécula pequena, um ponto quântico, um nanotransmissor, um radionucleotídeo, um radiotransmissor, um agente de captura de nêutron, ou qualquer combinação dos acimas, ou qualquer composto ou substância desejável.
[00445]Como uma ilustração, exemplos não limitante das composições, mé-todos, técnicas e estratégias aqui descritos, a seguinte descrição focará em adicionar polímeros macromoleculares ao polipeptídeo aminoácido não natural com o en-tendimento que as composições, métodos, técnicas, e estratégias descritas aqui são também aplicáveis (com modificações apropriadas, se necessário e para as quais um versado na técnica pode fazer com as revelações aqui) para adicionar outras funcionalidades, incluindo, mas não limitadas àquelas listadas acima.
[00446]Uma ampla variedade de polímeros macromoleculares e outras mo-léculas podem estar ligadas a polipeptídeos FGF-21 da presente invenção para modular as propriedades biológicas do polipeptídeo FGF-21, e/ou provêm novas propriedades biológicas para a molécula FGF-21. Esses polímeros macromoleculares podem ser ligados ao polipeptídeo FGF-21 através de um aminoácido naturalmente codificado, através de um aminoácido não naturalmente codificado, ou qualquer substituinte de um aminoácido natural ou não natural, ou qualquer substituinte ou grupo funcional adicionado a um aminoácido natural ou não natural. O peso molecular do polímero pode ser de uma ampla variedade, incluindo, mas não limitado a, entre cerca de 100 Da e cerca de 100.000 Da ou mais. O peso molecular do polímero pode estar entre cerca de 100 Da e cerca de 100.000 Da, incluindo mas não limitado a 100.000 Da, 95.000 Da, 90.000 Da, 85.000 Da, 80.000 Da, 75.000 Da, 70.000 Da, 65.000 Da, 60.000 Da, 55.000 Da, 50.000 Da, 45.000 Da, 40.000 Da, 35.000 Da, 30.000 Da, 25.000 Da, 20.000 Da, 15.000 Da, 10.000 Da, 9.000 Da, 8.000 Da, 7.000 Da, 6.000 Da, 5.000 Da, 4.000 Da, 3.000 Da, 2.000 Da, 1.000 Da, 900 Da, 800 Da, 700 Da, 600 Da, 500 Da, 400 Da, 300 Da, 200 Da e 100 Da. Em algumas modalidades, o peso molecular do polímero está entre cerca de 100 da e cerca de 50.000 Da. Em algumas modalidades, o peso molecular do polímero está entre cerca de 100 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular do polímero está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular do polímero está entre cerca de 5.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular do polímero está entre cera de 10.000 Da e cerca de 40.000 Da.
[00447]A presente invenção provê substancialmente preparações homogêneas de conjugados polímero:proteína. “Substancialmente homogêneo” como aqui utilizado significa que moléculas com conjugados polímero:proteína são observadas serem mais que metade da proteína total. O conjugado polímero:proteína tem uma atividade biológica e as presentes preparações polipeptídicas FGF-21 PEGiladas “substancialmente homogêneas” providas aqui são aquelas que são homogêneas o suficiente para revelarem as vantagens de uma preparação homogênea, por exemplo, fácil aplicação clínica em predictabilidade de várias farmacocinéticas.
[00448]Um pode também escolher preparar uma mistura de moléculas con-jugadas polímero:proteína, e a vantagem provida aqui é que um pode selecionar a proporção de conjugado monopolímero:proteína para incluir na mistura. Então, se desejado, um pode preparar uma mistura de várias proteínas com vários números de frações poliméricas ligadas (isto é, di-, tri-, tetra-, etc) e combinar os referidos conjugados com conjugado monopolímero:proteína usando os métodos da presente invenção, e têm uma mistura com uma proporção pré-determinada de conjugados monopolímeros:proteína.
[00449]O polímero selecionado pode ser solúvel em água de forma que a proteína a qual ele está ligado não precipita em ambiente aquoso, tal como um am-biente fisiológico. O polímero pode ser ramificado ou não ramificado. Para uso tera-pêutico da do produto final da preparação, o polímero será farmaceuticamente aceitável.
[00450]Exemplos de polímeros incluem mas não são limitados a éteres poli- alquila e análodos alcóxi-recobertos dos mesmos (por exemplo, polioxietileno glicol, polioxietileno/propileno glicol, e análogos recobertos metóxi ou etóxi dos mesmos, especialmente polioxietileno glicol, o último é também conhecido como polietilenogli- col ou PEG); polivinilpirrolidonas; éteres polivinilalquila; polioxazolinas; polialquil oxazolinas e poliidroxialquil oxazolinas; poliacrilamidas; polialquilacrilamiads e polii- droxialquil acrilamidas (por exemplo, poliidroxipropilmetacrilamida e derivados dos mesmos0; poliidroxialquil acrilatos; ácidos polisiálicos e análogos dos mesmos; se-quências peptídicas hidrofílicas; polissacarídeos e seus derivados, incluindo dextran e derivados de dextran, por exemplo, carboximetildextran, dextran sulfato, aminodextran, celular e seus derivados, por exemplo, carboximetil celulose, hidroxialquil celuloses, quitina e seus derivados, por exemplo, quitosana, succinil quitosana, carboi- metilquitina, carboximetilquitosana, ácido hialurônico e seus derivados; amidos, algi- natos, sulfato de condroitina, albumina, pululan e carboximetil puluan, poliaminoáci- dos e derivados dos mesmos, por exemplo, ácidos poliglutâmicos, polisinas, ácidos poliaspárticos, poliaspartamidas, copolímeros de anidreto maléico tais como, copo- límero de anidreto estireno maléico, copolímero de anidreto maléico de étre divinile- til, polivinil álcool, copolímeros dos mesmo, terpolímeros dos mesmo, misturas dos mesmo, e derivados dos antecedentes.
[00451]A prorporção das moléculas de polietileno glicol para moléculas de proteínas variarão, como também suas concentrações na mistura de reação. Em geral, a proporção ótima (em termos de eficiência de reação em que existe um excesso mínimo de proteína ou polímero não reagido) pode ser determinada pelo peso molecular do polietileno glicol selecionado e no número de grupos reativos disponíveis. Como relacionado ao peso molecular, tipicamente o peso molecular mais alto do polímero, o menor número de moléculas de polímero que podem ser ligar a proteína. Similarmente, a ramificação do polímero pode ser levada em consideração quando otimizando esses parâmetros. Geralmente, quanto mais alto o peso molecular (ou mais ramificações), mais alta a proporção polímero:proteína.
[00452]Como aqui utilizado, e quando contemplando os conjugados PEG:polipeptídeo FGF-21, o termo “quantidade terapeuticamente efetiva” refere-se a uma quantidade que dá o benefício desejado a um paciente. A quantidade variará de um indivíduo a outro e dependerá de um número de fatores, incluindo a condição geral física do paciente e fundamentando a causa da condição a ser tratada. A quantidade de polipeptídeo FGF-21 usada para terapia dá uma taxa aceitável de mudança e mantém a resposta desejada em um nível benéfico. Uma quantidade terapeuti- camente efetiva das presentes composições pode ser facilmente acertada pelo versado na técnica usando materiais e procedimentos publicamente disponíveis.
[00453]O polímero solúvel em água pode ser qualquer forma estrutural inclu-indo, mas não limitado a linear, dividida ou ramificado. Tipicamente, o polímero solúvel em água é um poli(alquileno glicol), tai como poli(etileno glicol) (PEG), mas outros polímeros solúveis em água podem também ser empregados. Por meio de exemplo, PEG é utilizado para descrever certas modalidades desta invenção.
[00454]PEG é um polímero solúvel em água bem conhecido que é comerci-almente disponível ou pode ser preparado por polimerização por abertura de anel de etileno glicol, de acordo com os métodos conhecidos pelos versados na técnica (Sandler e Karo, Polymer Synthesis, Academic Press, Nova Iorque, vol.3 páginas 138-161). O termo “PEG” é usado amplamente para compreender qualquer molécula de polietileno glicol, sem relação com tamanho ou modificação em uma terminação do PEG, e pode ser representado como oligado ao polipeptídeo FGF-21 pela fórmula: onde n é 2 a 10.000 e X é H ou uma modificação terminal, incluindo, mas não limitado a alquilaC1-4, um grupo protetor ou um grupo terminal funcional.
[00455]Em alguns casos, um PEG utilizado na invenção terminada em uma terminação com hidróxi ou metóxi, isto é, X é H ou CH3 (“metóxi PEG”). Alternativa-mente, o PEG pode terminar com um grupo reativo, assim formando um polímero bifuncional. Grupos reativos típicos podem incluir aqueles grupos reativos que são comumente utilizados para reagir com grupo funcionais encontrados em 20 aminoá- cidos comuns (incluindo mas não limitado a grupo maleimida, carbonatos ativados (incluindo mas não limitados a éster p-nitrofenil) e aldeídos) bem como grupos funci-onais que são inertes aos 20 aminoácidos comuns mas que reagem especificamente com grupos funcionais complementares presentes em aminoácidos não naturalmente codificados (incluindo mas não limitados a grupos azida, grupo alquino). É notado que outra terminação do PEG, que é mostrada na fórmula acima pelo Y, se ligará ou diretamente ou indiretamente a um polipeptídeo FGF-21 através de um aminoácido de ocorrência natural ou não natural. Por exemplo, Y pode ser uma ligação amida, carbamato ou uréia para um grupo amina (incluindo, mas não limitado a amina epsilon da lisina ou N-terminal) do polipeptídeo. Alternativamente, Y pode ser uma ligação maleimida a um grupo tiol (incluindo, mas não limitado a grupo tiol de cisteína). Alternativamente, Y pode ser um ligado a um resíduo não comumente acessível através de 20 aminoácidos comuns. Por exemplo, um grupo azida no PEG pode ser reagido com um grupo alquino no polipeptídeo FGF-21 para formar um produto de cicloadição [3+2] Huisgen. Alternativamente, um grupo alquino no PEG pode ser reagido com um grupo azida presente em um aminoácido não naturalmente codificado para formar um produto similar. Em algumas modalidades, um nucleófilo forte (incluindo mas não limitado a hidrazina, hidrazida, hidroxilamina, semicarbazida) pode ser reagido com um grupo aldeído ou cetona presente em um aminoácido não natural-mente codificado para formar uma hidrazona, oxima ou semi-carbazona, como apli-cável, que em alguns casos pode ser ainda reduzido pelo tratamento com um agente redutor apropriado. Alternativamente, o nucleófilo forte pode ser incorporado no poli- peptídeo FGF-21 através de um aminoácido não naturalmente codificado e usado para reagir preferivelmente com um grupo cetona ou aldeído presente no polímero solúvel em água.
[00456]Qualquer massa molecular para um PEG pode ser utilizada como praticamente desejado, incluindo, mas não limitado a cerca de 100 Daltons (Da) e cerca de 100.000 Da ou mais como desejado (incluindo mas não limitado a, algumas vezes, 0,1-50 kDa ou 10-40 kDA). O peso molecular do PEG pode estar em uma ampla variação, mas não limitado a, entre cerca de 100 Da e cerca de 100.000 Da ou mais. PEG pode estar entre cerca de 100 Da e cerca de 100.000 Da ou mais. PEG pode estar entre cerca de 100 Da e cerca de 100.000 Da, incluindo mas não limitado a 100.000 Da, 95.000 Da, 90.000 Da, 85.000 Da, 80.000 Da, 75.000 Da, 70.000 Da, 65.000 Da, 60.000 Da, 55.000 Da, 50.000 Da, 45.000 Da, 40.000 Da, 35.000 Da, 30.000 Da, 25.000 Da, 20.000 Da, 15.000 Da, 10.000 Da, 9.000 Da, 8.000 Da, 7.000 Da, 6.000 Da, 5.000 Da, 4.000 Da, 3.000 Da, 2.000 Da, 1.000 Da, 900 Da, 800 Da, 700 Da, 600 Da, 500 Da, 400 Da, 300 Da, 200 Da e 100 Da. Em algumas modalidades, PEG está entre cerca de 100 da e cerca de 50.000 Da. Em algumas modalidades, o peso molecular do polímero está entre cerca de 100 Da e cerca de 40.000 Da. Em algumas modalidades, PEG está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, PEG está entre cerca de 5.000 Da e cerca de 40.000 Da. Em algumas modalidades, PEG está entre cera de 10.000 Da e cerca de 40.000 Da. PEGs de cadeias ramificadas, incluindo mas não limitados , moléculas PEG com cada cadeia tendo um PM variando de 1-100 kDA (incluindo mas não limitado a, 1-50 kDA ou 5-20 kDA) pode também ser usado. O peso molecular de cada cadeia do PEG de cadeia ramificada pode ser, incluindo, mas não limitado a, entre 1.000 Da e cerca de 100.000 Da ou mais. O peso molecular de cada cadeia do PEG de cadeia ramificada pode estar entre 1.00 Da e cerca de 100.000 Da, incluindo mas não limitado a, 100.000 Da, 95.000 Da, 90.000 Da, 85.000 Da, 80.000 Da, 75.000 Da, 70.000 Da, 65.000 Da, 60.000 Da, 55.000 Da, 50.000 Da, 45.000 Da, 40.000 Da, 35.000 Da, 30.000 Da, 25.000 Da, 20.000 Da, 15.000 Da, 10.000 Da, 9.000 Da, 8.000 Da, 7.000 Da, 6.000 Da, 5.000 Da, 4.000 Da, 3.000 Da, 2.000 Da, 1.000 Da. Em algumas modalidades, o peso molecular de cadeia de PEG de cadeia ramificada está entre cerca de 1.000 Da e cerca de 50.000 Da. Em algumas modalidades, o peso molecular do PEG de cadeia ramificada está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de cada PEG de cadeia ramificada está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, PEG está entre cerca de 5.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de cada cadeia do PEG de cadeia ramificada está entre cera de 5.000 Da e cerca de 20.000 Da. Uma ampla variedade de moléculas PEG são descritas em, incluindo mas não limitado a, catálogo Shearwater Polymers, Inc., catálogo Nektar Therapeutics, aqui incorporados por referência.
[00457]Geralmente, pelo menos um terminal da molécula PEG está disponível para reação com o aminoácido não naturalmente codificado. Por exemplo, derivados PEG produzindo frações alquino e azida para reação com cadeias laterais aminoácidos podem ser utilizadas para ligar Peg a aminoácidos não naturalmente codificados como aqui descrito. Se os aminoácidos não naturalmente codificados compreendem uma azida, então o PEG tipicamente conterá ou uma fração alquino para efetuar a formação do produto da cicloadição [3+2] ou uma espécie PEG ativada (isto é, éster, carbonato), contendo um grupo fosfino para efetuar a formação da ligação amida. Alternativamente, se o aminoácido não naturalmente codificado compreende um alquino, então o PEG tipicamente conterá uma fração azida para efetuar a formação do produto da cicloadição Huisgen [3+2]. Se um aminoácido não naturalmente codificado compreende um grupo carbonila, o PEG tipicamente compreenderá um potente nucleófilo (incluindo, mas não limitado a uma funcionalidade hidra- zida, hidrazina, hidroxilamina ou semi-carbazida) a fim de efetuar a formação de li- gações hidrazona, oxima e semi-carbazona, respectivamente. Em outras alternativas, um reverso da orientação dos grupos reativos descritos acima pode ser utilizados, isto é, uma fração azida no aminoácido não naturalmente codificado pode ser reagido com um PEG derivado contendo um alquino.
[00458]Em algumas modalidades, o variante polipeptídeo FGF-21 com um derivado PEG contém uma funcionalidade química que é reativa com uma funciona-lidade química presente na cadeia lateral do aminoácido não naturalmente codificado.
[00459]A invenção provê em algumas modalidades derivados polímero con-tendo azida e acetileno compreendendo uma estrutura polímero solúvel em água tendo um peso molecular médio a partir de cerca de 800 Da a cerca de 100.000 Da. A estrutura do polímero solúvel em água pode ser poli(etileno glicol). Entretanto, deve ser entendido que uma ampla variedade de polímeros solúveis em água incluindo mas não limitado a poli(etileno)glicol e outros polímeros relacionados, incluindo po- li(dextran) e poli(propileno glicol), são também adequados para uso na prática da invenção e que o uso do termo PEG ou poli(etileno glicol) é tencionado compreender e inclui todas tais moléculas. O termo PEG inclui, mas não é limitado a poli(etileno) glicol em qualquer de suas formas, incluindo PEG bifuncional, PEG multi-armado, PEG derivatizado, PEG dividido, PEG ramificado, PEG pendente (isto é, Peg ou polímeros relacionados tendo um ou mais grupos funcionais pendentes a uma estrutura polímero), ou PEG com ligações degradáveis dos mesmos.
[00460]PEG é tipicamente claro, incolor, inodoro, solúvel em água, estável ao calor, inerte a muitos agentes químicos, não hidroliza ou deteriora, e é geralmente não tóxico. Poli(etileno glicol) é considerado ser biocompatível, que é para dizer que PEG é capaz de coexistir com tecidos vivos ou organismo vivos sem causar dano. Mais especificamente, Peg é substancialmente não imunogênico, que é para dizer que PEG não tende a produzir uma resposta imune no corpo. Quando ligado a uma molécula tendo alguma função desejável no corpo, tal como um agente biologicamente ativo, o PEG tende a mascarar o agente pode reduzir ou eliminar qualquer resposta imune assim um organismo pode tolerar a presença do agente. PEG conju-gado tende a não produzir uma resposta imune substancial ou causar coagulação ou outros efeitos não desejáveis. PEG tendo a fórmula --CH2CH2O--(CH2CH2O)n -- CH2CH2--, onde n é a partir de 3 a cerca de 4000, tipicamente de cerca de 20 a cerca de 2000, é adequado para uso na presente invenção. PEG tendo um peso molecular de cerca de 800 Da a cerca de 100.000 Da são em algumas modalidades da presente invenção particularmente úteis como a estrutura do polímero. O peso molecular do PEG pode ser uma ampla variação, incluindo, mas não limitado a, entre cerca de 100 Da e cerca de 100.000 Da ou mais. O peso molecular de PEG pode ser entre cerca de 100 Da e cerca de 100.000 Da, incluindo mas não limitado a, 100.000 Da, 95.000 Da, 90.000 Da, 85.000 Da, 80.000 Da, 75.000 Da, 70.000 Da, 65.000 Da, 60.000 Da, 55.000 Da, 50.000 Da, 45.000 Da, 40.000 Da, 35.000 Da, 30.000 Da, 25.000 Da, 20.000 Da, 15.000 Da, 10.000 Da, 9.000 Da, 8.000 Da, 7.000 Da, 6.000 Da, 5.000 Da, 4.000 Da, 3.000 Da, 2.000 Da, 1.000 Da, 900 Da, 800 Da, 700 Da, 600 Da, 500 Da, 400 Da, 300 Da, 200 Da, e 100 Da. Em algumas modalidades, o peso molecular do PEG está entre cerca de 100 Da e cerca de 50.000 Da. Em algumas modalidades, o peso molecular de PEG está entre cerca de 100 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de PEG está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de PEG está entre cerca de 5.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de Peg está entre cerca de 10.000 Da e cerca de 40.000 Da.
[00461]A estrutura do polímero pode ser linear ou ramificada. Estruturas do polímero ramificado são geralmente conhecidas na técnica. Tipicamente, um polímero ramificado tem uma fração núcleo ramificado central e uma pluralidade de cadeias polímero lineares ligadas ao núcleo ramificado central. PEG é comumente usado nas formas ramificadas que podem ser preparadas por adição de óxido de etileno para vários polióis, tais como glicerol, oligômeros glicerol, pentaeritritol e sorbitol. A fração ramificada central pode também ser derivada a partir de vários aminoácidos, tal como lisina. O poli(etileno glicol) ramificado pode ser representado ne forma geral co mo R(-PEG-OH)m em que R é derivado a partir de uma fração núcleo, tais como glicerol, oligômeros glicerol, ou pentaeritritol, e m representa o número de braços. Moléculas PEG multi-braços, tais como aquelas descritas na Pat. dos EUA Nos. 5.932.462; 5.643.575; 5.229.490; 4.289.872; Ped. de Pat. dos EUA 2003/0143596; WO 96/21469; e WO 93/21259, cada uma das quais é aqui incorporada em sua totalidade, pode também ser usada como estrutura do polímero.
[00462]PEG ramificado pode também ser na forma de um PEG dividido re-presentado por PEG(-- YCHZ2)n, onde Y é um grupo ligante e Z é um grupo terminal ativado ligado a CH por uma cadeia de átomos de comprimento definido.
[00463]Ainda outra forma ramificada, o PEG pendente, tem grupo reativos, tal como carboxila, junto com a estrutura Peg ao invés de na terminação de cadeias PEG.
[00464]Em adição dessas formas de PEG, o polímero pode também ser pre-parado com ligações fracas ou degradáveis na estrutura. Por exemplo, PEG pode ser preparado com ligações ésteres na estrutura polímero que são sujeitas a hidrólise. Como mostrado abaixo, esta hidrólise resulta em clivagem do polímero em fragmentos de peso molecular inferior:
[00465]É entendido que os versados na técnica que o termo poli(etileno gli- col) ou PEG representa ou inclui todas as formas conhecidas na técnica incluindo, mas não limitado àqueles revelados aqui.
[00466]Muitos outros polímeros são também adequados para uso na presente invenção. Em algumas modalidades, estruturas polímeros que são solúveis em água, com a partir de 2 a cerca de 300 terminações, são particularmente úteis na invenção. Exemplos de polímeros adequados incluem, mas não são limitados a, outro poli(alquileno glicol), tal como poli(propileno glicol) (“PPG”), copolímeros dos mesmos (incluindo mas não limitados a copolímeros de etileno glicol e propileno gli- col), terpolímeros dos mesmo, misturas dos mesmos, e semelhantes. Embora o peso molecular de cada cadeia da estrutura do polímero pode variar, é tipicamente em uma variação de cerca de 800 Da a cerca de 100.00 Da, sempre a partir de 6.000 Da a cerca de 80.000 Da. O peso molecular de cada cadeia da estrutura do polímero pode estar entre cerca de 100 Da e cerca de 100.000 Da, incluindo mas não limitado a 100.000 Da, incluindo mas não limitado a, 100.000 Da, 95.000 Da, 90.000 Da, 85.000 Da, 80.000 Da, 75.000 Da, 70.000 Da, 65.000 Da, 60.000 Da, 55.000 Da, 50.000 Da, 45.000 Da, 40.000 Da, 35.000 Da, 30.000 Da, 25.000 Da, 20.000 Da, 15.000 Da, 10.000 Da, 9.000 Da, 8.000 Da, 7.000 Da, 6.000 Da, 5.000 Da, 4.000 Da, 3.000 Da, 2.000 Da, 1.000 Da, 900 Da, 800 Da, 700 Da, 600 Da, 500 Da, 400 Da, 300 Da, 200 Da, e 100 Da. Em algumas modalidades, o peso molecular de cada cadeia da estrutura do polímero está entre cerca de 100 Da e cerca de 50.000 Da. Em algumas modalidades, o peso molecular de cada cadeia da estrutura do polímero está entre cerca de 100 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de cada cadeia da estrutura do polímero está entre cerca de 1.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de cada cadeia da estrutura do polímero está entre cerca de 5.000 Da e cerca de 40.000 Da. Em algumas modalidades, o peso molecular de cada cadeia da estrutura do polímero está entre cerca de 10.000 Da e cerca de 40.000 Da.
[00467]Aqueles versados na técnica reconhecerão que a lista acima para substancialmente estrutura solúveis em água é por nenhum meio exaustivo e é me-ramente ilustrativa, e todos os materiais poliméricos tendo as qualidades descritas acima são contemplados como sendo adequados para uso na presente invenção.
[00468]Em algumas modalidades da presente invenção os derivados de po-límeros são “multi-funcionais”, significando que e estrutura do polímero tem pelo menos duas terminações, e possivelmente como muitos com cerca de 300 terminações, funcionalizados ou ativados com um grupo funcional. Derivados de polímeros multi-funcionais incluem, mas não são limitados a, polímeros lineares tendo duas termina-ções, cada terminação sendo ligada a um grupo funcional que pode ser o mesmo ou diferente.
[00469]Em uma modalidade, o derivado do polímero tem a estrutura:Em que: N=N=N é uma fração azida; B é uma fração ligante, que pode estar presente ou ausente; POLI é um polímero não antigênico solúvel em água; A é uma fração ligante, que pode estar presente ou ausente e que pode ser a mesma como B ou diferente; e X é um segundo grupo funcional.
[00470]Exemplos de uma fração ligante para A e B incluem, mas não são li-mitados a um grupo alquila multiplamente funcionalizado contendo até 18, e pode conter entre 1-10 átomos de carbono. Um heteroátomo tais como nitrogênio, oxigênio ou enxofre podem ser incluídos com uma cadeia alquila. A cadeia alquila pode também ser ramificada em um heteroátomo. Outros exemplos de uma fração ligante para A e B incluem, mas não são limitados a uma multiplicidade do grupo arila funci- onalizada, contendo até 10 e pode conter de 5-6 átomos de carbono. O grupo arila pode ser substituído com um ou mais átomos de carbono, nitrogênio, oxigênio ou enxofre. Outros exemplos de grupos ligantes adequados incluem aqueles grupos ligantes descritos na Pat. dos EUA Nos. 5.932.462; 5.643.575; e Publicação do Ped. de Pat. dos EUA 2003/0143596, cada um dos quais é aqui incorporado por referência. Aqueles versados na técnica reconhecerão que a lista acima para ligações de frações não é por meio exaustiva e é meramente ilustrativa, e que todas as frações tendo as qualidades descritas acima são contempladas para serem adequada para uso na presente invenção.
[00471]Exemplos de grupos funcionais adequados para uso como X incluem, mas não são limitados a hidroxila, hidroxila protegida, alcoxila, éster ativo, tais como N-hidroxisuccinimidil ésteres e 1-benzotriazolil ésteres, carbonato ativo, tais como N-hidroxisuccinimidil carbonatos e 1-benzotriazolil carbonatos, acetal, aldeído, hidratos aldeídos, alquenila, acrilato, metacrilato, acrilamida, sulfona ativa, amina, aminoóxi, amina protegida, hidrazida, hidrazida protegida, tiol protegido, ácido car- boxílico, ácido carboxílico protegido, isocianato, isotiocianato, maleimida, vinilsulfo- na, ditiopiridina, vinilpiridina, iodoacetamida, epóxido, glioxais, dionas, mesilatos, tosilatos, tresilato, alqueno, cetona, e azida. Como é entendido pelos versados na técnica, a fração X selecionada deve ser compatível com o grupo azida de forma que a reação com o grupo azida não ocorre. Os derivados de polímero contendo azida podem ser homobifuncionais, significando que o segundo grupo funcional (isto é, X) é também uma fração azida, ou heterobifuncional, significando que o segundo grupo funcional é um grupo funcional diferente.
[00472]O termo “protegido” refere-se a presença de um grupo ou fração pro-tetora que previne a reação do grupo funcional quimicamente reativo sob certas condições de reação. O grupo protetor variará dependendo do tipo do grupo quimi-camente reativo sendo protegido. Por exemplo, se o grupo quimicamente reativo é uma amina ou uma hidrazida, o grupo protetor pode ser selecionado a partir do grupo de terc-butiloxicarbonila (t-Boc) e 9-fluorfenilmetoxicarbonila (Fmoc). Se o grupo quimicamente reativo é um tiol, o grupo protetor pode ser ortopiridildissulfeto. Se o grupo quimicamente reativo é um ácido carboxílico, tais ácidos butanóicos ou pro- piônico, ou um grupo hidroxila, o grupo protetor pode ser grupo benzila ou alquila tais como metila, etila, ou terc-butila. Outros grupos protetores conhecidos na técnica podem também ser usados na presente invenção.
[00473]Exemplos específicos de grupos funcionais terminais na literatura in-cluem, mas não são limitados a, carbonato de N-succinimidila (ver, por exemplo, Pat. dos EUA Nos. 5.281.698, 5.468.478), amina (ver, por exemplo, Buckmann et al, Ma- kromol. Chem. 182:1379 (1981), Zalipsky et al. Eur. Polym. J. 19:1177 (1983)), hi- drazida (Ver, por exemplo, Andresz et al, Makromol. Chem 179:301 (1978)), propionato de succinimidila e butanoato de succinimidila (ver, por exemplo, Olson et al, em Poli(etileno glicol) Chemistry & Biological Apllications, pp 170-181, Harris & Zalipsky Eds., ACS, Washington, D.C., 1997; ver, também Pat. dos EUA No. 5.672.662), suc- cinato de succinimidila (ver, por exemplo, Abuchowski et al, Cancer Biochem. Biophys. 7:175 (1984) e Joppich et al, Makromol. Chem. 180:1381 (1979), succinimidil éster (ver, por exemplo, Pat. dos EUA No. 4.670.417), carbonato de benotriazol (ver, por exemplo, Pat. dos EUA No. 5.650.234), glicidil éter (ver, por exemplo, Pitha et al. Eur. J. Biochem. 94:11 (1979), Elling, et al, Biotech. Appl. Biochem. 13:354 (1991), aldeído (ver, por exemplo, Harris et al, J. Polym. Sci. Chem. Ed 22:341 (1984), Pat. Dos EUA No. 5.824.784, Pat. dos EUA No. 5.252.714), maleimida (ver, por exemplo, Goodson et al, Biotechnology (NI) 8:343 (1990), Romani et al, em Chemistry of Peptides and Proteins 2:29 (1984)), e Kogan, Synthetic Comm. 22:2417 (1992)), otopiri- dil-dissulfeto (ver, por exemplo, Woghiren, et al, Bioconj. Chem. 4:314 (1993)), acrilol (ver, por exemplo, Sawhney et al, Macromolecules, 26:581 (1993)), vinilsulfona (ver, por exemplo, Pat. dos EUA No. 5.900.461). Todas as referências e patentes acima são incorporadas aqui por referência.
[00474]Em certas modalidades da presente invenção, os derivados de polímeros da invenção compreendem uma estrutura do polímero tendo a estrutura: Em que: X é um grupo funcional como descrito acima; e n é cerca de 20 a cerca de 4000.
[00475]Em outra modalidade, os derivados polímeros da invenção compre- Em que: W é uma fração ligante alifática ou aromática compreendendo entre 1-10 átomos de carbono; n é cerca de 20 a cerca de 4000; e X é um grupo funcional como descrito acima. M está entre 1 e 10.
[00476]Os derivados PEG contendo azida da invenção podem ser preparados por uma variedade de métodos conhecidos na técnica e/ou aqui revelados. Em um método, mostrado abaixo, uma estrutura de polímero solúvel em água tendo um peso molecular médio de cerca de 800 Da a cerca de 100.00 Da, a estrutura do po- límero tendo uma primeira ligação terminal a um primeiro grupo funcional e uma se-gunda ligação terminal a um grupo de saída adequado, é reagido com um ânion azi- da (que pode ser pareado com qualquer de um número de contra-íons adequados, incluindo sódio, potássio, terc-butilamônio e semelhantes). O grupo de saída passa por substituição e é substituída pela fração azida, fornecendo o polímero PEG contendo azida desejado.
[00477]Como mostrado, uma estrutura de polímero adequada para uso na presente invenção tem uma fórmula X-PEG-L, em que PEG é poli(etileno glicol) e X é um grupo funcional que não reage com grupos azida e L é um grupo de saída adequado. Exemplos de grupos funcionais adequados incluem, mas não são limitados a hidroxila, hidroxila protegida, acetal, alquenila, amina, aminoóxi, amina protegida, hidrazida protegida, tiol protegido, ácido carboxílico, ácido carboxílico protegido, maleimida, ditiopiridina, e vinilpiridina e cetona. Exemplos de grupos de saída adequados incluem, mas não são limitados a cloreto, brometo, iodeto, mesilato, tre- silato e tosilato.
[00478]Em outro método para preparação dos derivados de polímero contendo azida da presente invenção, um agente ligador produzindo uma funcionalidade azida é contactado com uma estrutura polímero solúvel em água tendo um peso molecular médio de cerca de 800 Da a cerca de 100.000 Da, em que o agente ligador produz uma funcionalidade química que reagirá seletivamente com uma funcionalidade química no polímero PEG, para formar um produto derivado do polímero contendo azida em que a azida é separada a partir da estrutura polímero por um grupo ligante.
[00479]Um esquema de reação exemplar é mostrado abaixo:Em que: PEG é poli(etileno glicol) e X é um grupo revestimento tal como alcóxi ou um grupo funcional como descrito acima; e M é um grupo funcional que não é reativo com a funcionalidade azida, mas que reagirá eficientemente e seletivamente como grupo funcional N.
[00480]Exemplos de grupos funcionais adequados incluem, mas não são li-mitados a, M sendo um ácido carboxílico, carbonato ou éster ativo se N é uma amina; M sendo uma cetona se N é uma hidrazida ou fração aminoóxi; M sendo um grupo de saída se N é um nucleófilo.
[00481]Purificação do produto bruto pode ser realizada por métodos conhecidos incluindo, mas não são limitada, precipitação do produto seguido por cromato- grafia, se necessário.
[00482]Um exemplo mais específico é mostrado abaixo no caso do PEG di-amina, em que uma das aminas é protegido por uma fração do grupo protetor tal como terc-butil-Boc e a diamina PEG mono-protegida resultante é reagida com uma fração ligante que produz a funcionalidade azida:
[00483]Nestes exemplos, o grupo amina pode ser acoplado ao grupo ácido carboxílico usando uma variedade de agentes ativadoras tais como cloreto de tionila ou reagentes carbodiimida e N-hidroxisuccinimida ou N-hidroxibenzotriazol para criar uma ligação amida entre o derivado PEG monoamina e a fração ligante produzindo azida. Após a formação bem sucedida da ligação amida, o derivado contendo N-terc- butil-Boc-protegido resultante pode ser usado diretamente para modificar moléculas bioativas ou ele pode ser ainda elaborada para instalar outros grupos funcionais. Por exemplo, o grupo N-t-Boc pode ser hidrolizado por tratamento com ácido forte para gerar um omega-amino-PEG-azida. A amina resultante pode ser utilizada como um gancho para instalar outra funcionalidade útil tais como grupos maleimida, dissulfe- tos ativados, ésteres ativados e semelhantes para criação de reagentes heterobifun- cionais valiosos.
[00484]Derivados heterobifuncionais são particularmente úteis quando eles são desejados para ligar diferentes moléculas a cada terminação do polímero. Por exemplo, o PEG omega-N-amino-N-azido pode permitir a ligação de uma molécula tendo um grupo eletrofílico ativado, tais como aldeído, cetona, éster ativado, carbo- nato ativado e semelhantes, para uma terminação do PEG e uma molécula tendo um grupo acetileno a outras terminações do PEG.
[00485]Em outra modalidade da invenção, o derivado de polímero tem a es-trutura: X-A-POLI-B-C C-R Em que: R pode ser ou H ou um grupo alquila, alqueno, alcóxi, ou arila ou arila substituída; B é uma fração ligante, que pode estar presente ou ausente; POLI é um polímero não antigênico solúvel em água; A é uma fração ligante, que pode estar presente ou ausente e que pode ser o mesmo como B ou diferente; e X é um segundo grupo funcional.
[00486]Exemplos de uma fração ligante para A e B incluem, mas são não são limitados a, um grupo alquila multiplamente-funcionalizada contendo até 18, e podem conter entre 1-10 átomos de carbono. Um heteroátomo tais como nitrogênio, oxigênio ou enxofre pode estar incluído com uma cadeia alquila. A cadeia alquila pode também ser ramificada em um heteroátomo. Outros exemplos de uma fração ligante para A e B incluem, mas não são limitados a um grupo arila funcionalizado, contendo até 10 e pode conter 5-6 átomos de carbono. O grupo arila pode ser substituído com um ou mais átomos de carbono, nitrogênio, oxigênio ou enxofre. Outros exemplos de grupos ligantes adequados incluem aqueles grupos ligantes descritos na Pat. dos EUA Nos. 5.932.462 e 5.643.575 e Pub. Do Ped. de Pat. dos EUA 2003/0143596, cada uma das quais é aqui incorporada por referência. Aqueles versados na técnica reconhecerão que a lista antecedente para frações ligantes não é por meio exaustivo e é tencionado ser meramente ilustrativo, e que uma ampla variedade de frações ligantes tendo as qualidades descritas acima são contempladas ser úteis na presente invenção.
[00487]Exemplos de grupos funcionais adequados para uso como X incluem hidroxila, hidroxila protegida, alcoxila, éster ativo, tais como N-hidroxisuccinimidil és- ter e 1-benzotriazolil éster, carbonato ativo, tais como N-hidroxisuccinimidil carbonato e 1-benzotriazol carbonato, acetal, aldeído, aldeído hidrato, alquenila, acrilato, metacrilato, acrilamida, sulfona ativa, amina, amionoóxi, amina protegida, hidrazida, hidrazida protegida, tiol protegido, ácido carboxílico, ácido carboxílico protegido, iso- cianato, isotiocianato, maleimida, vinilsulfona, ditiopiridina, vinilpiridina, iodoacetami- da, epóxido, glioxais, dionas, mesilatos, tosilatos, e tresilato, alqueno, cetona e acetileno. Como pode ser entendido, a fração X selecionada deve ser compatível com o grupo acetileno de forma que a reação com o grupo acetileno não ocorre. Os derivados de polímero contendo acetileno podem ser homobifuncionais, significando que o segundo grupo funcional (isto é, X) é também uma fração acetileno, ou heterobifun- cional, significando que o segundo grupo funcional é um grupo funcional diferente.
[00488]Em outra modalidade da presente invenção, os derivados polímeros compreendem uma estrutura polímero tendo a estrutura: Em que: X é um grupo funcional como descrito acima; n é cerca 20 a cerca de 4000; e m está entre 1 e 10.
[00489]Exemplos específicos de cada um dos polímeros PEG heterobifunci- onais são conhecidos abaixo.
[00490]Os derivados PEG contendo acetileno da invenção podem ser prepa-rados usando métodos conhecidos pelos versados na técnica e/ou revelados aqui. Em um método, uma estrutura polímero solúvel em água tendo um peso molecular médio a partir de cerca de 800 Da a cerca de 100.000 Da, a estrutura polímero tendo um primeiro terminal ligado a um primeiro grupo funcional e um segundo terminal ligado a um grupo nucleofílico adequado, é reagido com um composto que produz ambos, uma funcionalidade acetileno e um grupo de saída que é adequado para reação com o grupo nucleofílico no PEG. Quando o polímero PEG produzindo a fração nucleofílica e a molécula produzindo o grupo de saída são combinados, o grupo de saída passar por uma substituição nucleofílica e é substituído pela fração nucleofí- lica, fornecendo o polímero contendo o acetileno desejado.
[00491]Como mostrado, uma estrutura de polímero preferida para uso na reação tem a fórmula X-PEG-Nu, em que PEG é poli(etileno glicol), Nu é uma fração nucleofílica e X é um grupo funcional que não reage com Nu, l ou a funcionalidade acetileno.
[00492]Exemplos de Nu incluem, mas não são limitados a grupos amina, alcóxi, arilóxi, sulfidrila, imino, carboxilato, hidrazida, aminóxi que podem reagir primariamente através de um mecanismo do tipo SN2. Exemplos adicionais de grupos Nu incluem aqueles grupos funcionais que podem reagir primariamente através de uma reação de adição nucleofílica. Exemplos de grupos L incluem cloreto, brometo, iodeto, mesilato, tresilato, e tosilato e outros grupos esperados a passar por substituição nucleofílica bem como cetonas, aldeídos, tioesteres, olefinas, grupos carbonilas não saturadas alfa-beta, carbonatos e outros grupos eletrofílicos esperados passar por adição por nucleófilos.
[00493]Em outra modalidade da presente invenção, A é um ligante alifático de entre 1-10 átomos de carbono ou um anel arila substituída de entre 6-14 átomos de carbono. X é um grupo funcional que não reage com grupo azida e L é um grupo de saída adequado.
[00494]Em outro método para preparação dos derivados do polímero contendo acetileno da invenção, um polímero PEG tendo um peso molecular médio de cerca de 800 Da a cerca de 100.00 Da, produzindo ou um grupo funcional protegido ou um agente de revestimento em um terminal e um grupo de saída adequado em outras terminações conectadas por um ânion acetileno.
[00495]Um esquema de reação exemplar é mostrado abaixo: Em que: PEG é poli(etileno glicol) e X é um grupo re revestimento tal como alcóxi ou um grupo funcional como descrito acima; e R’ é ou grupo alquila, alcóxi, arila, ou arilóxi ou um grupo alquila substituída, alcoxila, arila ou arilóxi.
[00496]No exemplo acima, o grupo de saída L deve ser suficientemente reativo ao passar por substituição do tipo SN2 quando em contato com uma concentração suficiente do ânion acetileno. As condições de reação requeridas para realizar a substituição SN2 dos grupos de saída por ânions acetileno são conhecidos pelos versados na técnica.
[00497]Purificação do produto bruto pode usualmente ser realizada pelos métodos conhecidos na técnica incluindo, mas não são limitados a precipitação do produto seguido por cromatografia, se necessário.
[00498]Polímeros solúveis em água podem ser ligados a polipeptídeos FGF- 21 da invenção. Os polímeros solúveis em água podem ser ligados através de um aminoácido não naturalmente codificados incorporados no polipeptídeo FGF-21 ou qualquer grupo funcional ou substituinte de um aminoácido não naturalmente ou na-turalmente codificado, ou qualquer grupo funcional ou substituinte adicionado a um aminoácido não naturalmente ou naturalmente codificado. Alternativamente, os po-límeros solúveis em água são ligados a um polipeptídeo FGF-21 incorporando um aminoácido não naturalmente codificado através de um aminoácido de ocorrência não natural (incluindo, mas não limitado a, grupo cisteína, lisina ou amina do resíduo N-terminal). Em alguns casos, os polipeptídeo FGF-21 da invenção compreendem 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 aminoácidos não naturais, em que um ou mais aminoácidos não naturalmente codificados são ligados a polímeros solúveis em água (incluindo, mas não limitados a PEG e/ou oligossacarídeos). Em alguns casos, os polipeptídeos FGF-21 da invenção ainda compreendem 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ou mais aminoá- cidos naturalmente codificados ligados a polímeros solúveis em água. Em alguns casos, os polipeptídeos FGF-21 da invenção compreendem um ou mais aminoáci- dos não naturalmente codificados ligados a polímeros solúveis em água e um ou mais aminoácidos de ocorrência natural ligados a polímeros solúveis em água. Em algumas modalidades, os polímeros solúveis em água usados na presente invenção aumentam a meia vida sérica do polipeptídeo FGF-21 relativo a forma não conjugada.
[00499]O número de polímeros solúveis de água ligados a um polipeptídeo FGF-21 (isto é, a extensão de PEGilação ou glicosilação) da presente invenção pode ser ajustado para prover uma característica farmacológica, farmacocinética ou far- macodinâmico (incluindo, mas não limitado a aumentado ou diminuído) alterado tal como meia vida in vivo. Em algumas modalidades, a meia vida do FGF-21 é aumentada pelo menos cerca de 10, 20, 30, 40, 50, 60, 70, 80, 90 porcento, 2-vezes, 5- vezes, 6-vezes, 7-vezes, 8-vezes, 9-vezes, 10-vezes, 11-vezes, 12-vezes, 13-vezes, 14-vezes, 15-vezes, 16-vezes, 17-vezes, 18-vezes, 19-vezes, 20-vezes, 25-vezes, 30-vezes, 35-vezes, 40-vezes, 50-vezes, ou pelo menos cerca de 100-vezes ao longo de um polipeptídeo não modificado.
[00500]Derivados PEG contendo um grupo nucleofílico forte (isto é, hidrazi- da, hidrazina, hidroxilamina ou semi-carbazida).
[00501]Em uma modalidade da presente invenção, um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado contendo carbonila é modificado com um derivado PEG que contém uma fração hidrazina, hidroxilamina, hidrazida ou semi-carbazida terminal que está ligado diretamente a estrutura PEG.
[00502]Em algumas modalidades, oderivado PEG hidroxilamina-terminal terá a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 1001.000 (isto é, peso molecular médio está entre 5-40 kDa).
[00503]Em algumas modalidades, o derivado PEG contendo hidrazina ou hi- drazida terá a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100- 1.000 e X é opcionalmente um grupo carbonila (C=O) que pode estar presente ou ausente.
[00504]Em algumas modalidades, o derivado PEG contendo semi-carbazida terá a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100- 1.000.
[00505]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre-endendo um aminoácido contendo carbonila é modificado com um derivado PEG que contém uma fração hidroxilamina, hidrazida, hidrazina ou semi-carbanazida terminal que está ligada a estrutura PEG por meio de uma ligação amida.
[00506]Em algumas modalidades, os derivados PEG hidroxilamina-terminal têm a estrutura: onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 1001.000 (isto é, peso molecular médio está entre 5-40 kDa).
[00507]Em algumas modalidades, os derivados PEG contendo hidrazina ou hidrazida têm a estrutura: onde R é uma alquila simples (metila, etila, propila etc), m é 2-10, n é 1001.000 e X é opcionalmente um grupo carbonila (C=O) que pode estar presente ou ausente.
[00508]Em algumas modalidades, derivados PEG contendo semi-carbazida têm a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100- 1.000.
[00509]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre- endendo um aminoácido contendo carbonila é modificado com um derivado PEG ramificado que contém uma fração hidrazina, hidroxilamina, hidrazina ou semi- carbazida terminal, com cada cadeia do PEG ramificado tendo um PM variando a partir de 10-40 kDa e, pode ser a partir de 5-20 kDa.
[00510]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre-endendo um aminoácido não naturalmente codificado é modificado com um derivado PEG tendo uma estrutura ramificada. Por exemplo, em algumas modalidades, o de-rivado PEG terminal hidrazina ou hidrazida terá a seguinte estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100-1.000, e X é opcionalmente um grupo carbonila (C=O) que pode estar presente ou ausente.
[00511]Em algumas modalidades, os derivados PEG contendo um grupo semi-carbazida terão a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), X é opcionalmente NH, O, S, C(O) ou não presente, m é 2-10 e n é 100-1.000.
[00512]Em algumas modalidades, derivados PEG contendo um grupo hidroxilamina terão a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), X é opcionalmente NH, O, S, C(O) ou não presente, m é 2-10 e n é 100-1.000.
[00513]O grau e sítios em que o(s) polímero(s) solúvel(s) em água é(são) li-gados ao polipeptídeo FGF-21 pode modular a ligação do polipeptídeo FGF-21 para o receptor polipeptídico FGF-21. Em algumas modalidades, as ligações são arranja-das tal que o polipeptídeo FGF-21 se liga ao receptor de polipeptídeo FGF-21 com um Kd de cerca de 400 nM ou menor, com um Kd de 150 nM ou menor, e em alguns casos com um Kd de 100 nM ou menos, como medido por um ensaio de ligação em equilíbrio, tal como descrito em Spencer et al, J. Biol. Chem. 263:7862-7867 (1988) para FGF-21.
[00514]Métodos e química para ativação de polímeros bem como para con-jugação de peptídeos são descritos na literatura e são conhecidos na técnica. Méto-dos comumente usados para ativação de polímeros incluem, mas não são limitados a ativação de grupos funcionais com brometo de cianogênio, periodato, glutaraldeí- do, biopóxidos, epicloroidrina, divinilsulfona, carbodiimida, haletos sulfonila, tricloro- triazina etc (ver, R.F. Taylor (1991), PROTEIN IMMOBILISATION FUNDAMENTAL AND APPLICATIONS, Marcel Dekker, N.I.; S.S. Wong (1992), CHEMISTRY OF PROTEIN CONJUGATION AND CROSSLINKING, CRC Press, Boca Raton; G.T. Hermanson et al (1993), IMMOBILIZED AFFINITY LIGAND TECHNIQUES, Academic Press, N.I.; Dunn, R.L. et al, Eds. POLYMERIC DRUGS AND DRUG DELIVERY SYSTEMS, ACS Symposium Series Vol. 469, American Chemical Society, Washing-ton, D.C. 1991).
[00515]Várias revises e monografias na funcionalização e conjugação de PEG são disponíveis. Ver, por exemplo, Harris, Macromol. Chem. Phys. C25:325- 373 (1985); Scouten, Methods in Enzymology 135:30-65 (1987); Wong et al, Enzyme Microb. Technol. 14: 866-874 (1992); Delgado et al, Critical Reviews in Therapeutic Drug Carrier Systems 9:249-304 (1992); Zalipsky, Bioconjugate Chem. 6:150-165 (1995).
[00516]Métodos para ativação de polímeros podem também ser encontrados em WO 94/17039, Pat. dos EUA No. 5.324.844, WO 94/ 18247, WO 94/04193, Pat. dos EUA No. 5.219.564, Pat. dos EUA No. 5.122. 614, WO 90/13540, Pat. dos EUA No. 5.281.698, e WO 93/15189, e para conjugação entre polímeros ativados e enzi-mas incluindo, mas não limitados a Fator de Coagulação VIII (WO 94/15625), hemo-globina (WO 94/09027), molécula carreadora de oxigênio (Pat. dos EUA No. 4.412.989), ribonuclease e superóxido dismutase (Veronese et al, App. Biochem. Biotech. 11:141-52 (1985)). Todas as referências e patentes citadas aqui.
[00517]PEGilação (isto é, adição de qualquer polímero solúvel em água) de polipeptídeos FGF-21 contendo um aminoácido não naturalmente codificado, tal co mo p-azido-L-fenilalanina, é realizada por qualquer método conveniente. Por exem-plo, polipeptídeo FGF-21 é PEGilado com um derivado mPEG terminado com alqui- no. Brevemente, um excesso de sólido mPEG (5000)-O-CH2-C CH é adicionado, com agitação, a uma solução aquosa de p-azido-L-Phe-contendo polipeptídeo FGF- 21 em temperatura ambiente. Tipicamente a solução aquosa é tamponada com um tampão tendo um pKa perto do pH em que a reação é para ser realizada (geralmente cerca de pH 4-10). Exemplos de tampões adequados para PEGilação em pH 7.5, por exemplo, incluem, mas não são limitados a HEPES, fosfato, borato, TRIS-HCl, EPPS, e TES. O pH é continuamente monitorado e ajustado se necessário. A reação é tipicamente permitida continuar por entre cerca de 1-48 horas.
[00518]Os produtos de reação são subsequentemente sujeitos a cromato- grafia de interação hidrofóbica para separar os variantes do polipeptídeo FGF-21 PEGilado a partir de mPEG(5000)-O-CH2-C CH livre e qualquer complexo de alto peso molecular do polipeptídeo FGF-21 PEGilado que pode formar quando PEG não bloqueado é ativado em ambas as terminações da molécula, assim ligando cruza-damente moléculas variantes de polipeptídeo FGF-21. As condições durante a cro- matografia de interação hidrofóbica é tal que mPEG(5000)-O-CH2-C CH livre flui através da coluna, enquanto qualquer complexo variante de polipeptídeo FGF-21 PEGilado elui após as formas desejadas, que contém uma molécula variante de po- lipeptídeo FGF-21 conjugado a um ou mais grupos PEG. Condições adequadas va-riam dependendo dos tamanhos relativos dos complexos ligados cruzadamente ver-sus o conjugado desejado e são facilmente determinados pelos versados na técnica. O eluente contendo os conjugados desejados é concentrado pode ultrafiltração e dessalinizado por diafiltração.
[00519]Se necessário, o polipeptídeo FGF-21 PEGilado obtido a partir de cromatografia hidrofóbica pode ser purificada ainda por um ou mais procedimentos conhecidos pelos versados na técnica incluindo, mas não limitados a, cromatografia de afinidade, cromatografia aniônica ou catiônica (usando, incluindo mas não limita-do a DEAE SEPHAROSE); cromatografia em sílica; HPLC de fase reversa; gel filtra- ção (usando, incluindo mas não limitado a SEPHADEX G-75); interação de interação hidrofóbica; cromatografia de exclusão por tamanho, cromatografia de quelação por metal, ultrafiltração/diafiltração, precipitação por etanol; precipitação por sulfato de amônio; cromatofoco; cromatografia de substituição; procedimentos eletroforéticos (incluindo mas não limitado a foco isoelétrico preparativo), solubilidade diferencial (incluindo mas não limitado a precipitação por sulfato de amônio) ou extração. Peso molecular aparente pode ser estimado por GPC por comparação a padrões de proteínas globulares (Preneta, AZ em PROTEIN PURIFICATION METHODS, A PRACTICAL APPROACH (Harris & Angal, Eds.) IRL Press 1989, 293-306). A pureza do conjugado FGF-21-PEG pode ser acessada por degradação proteolítica (incluindo, mas não limitada a clivagem de tripsina) seguido por análise de espectrometria de massa. Pepinsky RB, et al, J. Pharmacol. & Exp. Ther. 297(3):1059-66 (2001).
[00520]Um polímero solúvel em água ligado a um aminoácido de um poli- peptídeo FGF-21 da invenção pode ser ainda derivado ou substituído sem limitação. Derivados PEG contendo azida
[00521]Em outra modalidade da invenção, um polipeptídeo FGF-21 é modifi-cado com um derivado PEG que contém uma fração azida que reagirá com uma fra-ção alquino presente na cadeia lateral do aminoácido não naturalmente codificado. Em geral, os derivados PEG terão um peso molecular médio variando de 1-100 kDa e, em algumas modalidades, a partir de 10-40 kDa.
[00522]Em algumas modalidades, o derivado PEG com azida terminal terá a estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100-1.000 (isto é, peso molecular médio está entre 5-40 kDa).
[00523]Em outra modalidade, o derivado PEG terminado em azida terá a es-trutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10, p é 2-10 e n é 100-1.000 (isto é, peso molecular médio está entre 5-40 kDa).
[00524]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre-endendo um aminoácido contendo alquino é modificado com um derivado PEG ramificado que contém uma fração terminal azida, que cada cadeia do PEG ramificado tendo um PM variando de 10-40 kDa e pode ser a partir de 5-20 kDa. Por exemplo, em algumas modalidades, o derivado PEG terminado com azida terá a seguinte estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10, p é 2-10, e n é 100-1.000, e X é opcionalmente um O, N, S ou grupo carbonila (C=O), em cada caso que pode estar presente ou ausente. Derivados PEG contendo alquino
[00525]Em outra modalidade da invenção, um polipeptídeo FGF-21 é modifi-cado com um derivado PEG que contém uma fração alquino que reagirá com uma fração azida presente na cadeia lateral do aminoácido não naturalmente codificado.
[00526]Em algumas modalidades, o derivado PEG terminado em alquino terá a seguinte estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10 e n é 100-1.000 (isto é, peso molecular médio está entre 5-40 kDa).
[00527]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre-endendo um aminoácido não naturalmente codificado contendo alquino é modificado com um derivado PEG que contém um terminal azida ou fração terminal alquino que está ligado a estrutura PEG por meio de uma ligação amida.
[00528]Em algumas modalidades, o derivado PEG terminado em alquino terá a seguinte estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10, p é 2-10 e n é 100-1.000.
[00529]Em outra modalidade da invenção, um polipeptídeo FGF-21 compre-endendo um aminoácido contendo azida é modificado com um derivado PEG ramifi-cado que contém uma fração alquino terminal, com cada cadeia do PEG ramificado tendo um PM variando de 10-40 kDa e pode ser de 5-20 kDa. Por exemplo, em al-gumas modalidades, o derivado PEG terminado em alquino terá a seguinte estrutura: Onde R é uma alquila simples (metila, etila, propila etc), m é 2-10, p é 2-10, e n é 100-1.000, e X é opcionalmente um grupo O, N, S ou carbonila (C=O), ou não presente. Derivados PEG contendo fosfino
[00530]Em outra modalidade da invenção, um polipeptídeo FGF-21 é modifi-cado com um derivado PEG que contém um grupo funcional ativado (incluindo, mas não limitado a éster, carbonato) ainda compreendendo um grupo aril fosfino que re-agirá com uma fração azida presente na cadeia lateral do aminoácido não natural-mente codificado. Em geral, os derivados PEG terá um peso molecular médio variando de 1-100 kDa e, em algumas modalidades a partir de 10-40 kDa.
[00531]Em algumas modalidades, o derivado PEG terá a estrutura: Em que n é 1-10; X pode ser O, N, S ou não presente, Ph é fenila, e W é um polímero solúvel em água.
[00533]Em que X pode ser O, N, S ou não presente, Ph é fenila, W é um po-límero solúvel em água e R pode ser grupos H, alquila, arila, alquila substituída e arila substituída. Grupos R exemplares incluem mas não são limitados a -CH2, - C(CH3)3, -OR’, -NR’R’’, -SR’, -halogênio, -C(O)R’, -CONR’R’’, -S(O)2R’, - S(O)2NR’R’’, -CN e -NO2. R’, R’’, R’’’ e R’’’’ cada um independentemente refere-se a hidrogênio, heteroalquila substituído ou não substituído, arila substituída ou não substituída, incluindo, mas não limitada a arila substituída com 1-3 halogênios, alquila substituída ou não substituída, grupos alcóxi ou tioalcóxi, ou grupos arilalquila. Quando um composto da invenção inclui mais que um grupo R, por exemplo, cada um dos grupos R é independentemente selecionado como são cada grupo R’, R’’, R’’’ e R’’’’ quando mais que um desses grupo está presente. Quando R’ e R’’ são ligados ao mesmo átomo de nitrogênio, eles podem ser combinados com o átomo de nitrogênio para formar um anel 5-, 6- ou 7-membros. Por exemplo, -NR’R’’ é tencionado incluir, mas não limitado a, 1-pirrolidinil e 4-morofolinil. A partir da discussão acima de substituintes, um versado na técnica entenderá que o termo “alquila” tenciona incluir grupos incluindo átomos de carbono ligados a grupos outros que grupos hidrogênio, tais como haloalquila (incluindo mas não limitado a -CF3 e -CH2CF3) uma acila (incluindo mas não limitado a, -C(O)CH3, -C(O)CF3, -C(O)CH2OCH3, e semelhantes). Outros derivados PEG e técnicas de PEGilação geral
[00534]Outras moléculas PEG exemplares que podem estar ligadas a poli- peptídeos FGF-21, bem como métodos PEGilação incluem, mas não são limitados àquelas descritas em, por exemplo, Publicação de Patente dos EUA No. 2004/0001838; 2002/0052009; 2003/0162949; 2004/0013637; 2003/0228274; 2003/0220447, 2003/0158333; 2003/0143596; 2003/0114647; 2003/0105275; 2003/0105224; 2003/0023023; 2002/0156047; 2002/0099133; 2002/0086939; 2002/0082345; 2002/0072573; 2002/0052430; 2002/0040076; 2002/0037949; 2002/0002250; 2001/0056171; 2001/0044526; 2001/0021763; Patente dos EUA No. 6.646.110; 5.824.778; 5.476.653; 5.219.564; 5.629.384; 5.736.625; 4.902.502; 5.281.698; 5.122.614; 5.473.034; 5.516.673; 5.382.657; 6.552.167; 6.610.281; 6.515.100; 6.461.603; 6.436.386; 6.214.966; 5.990.237; 5.900.461; 5.739.208; 5.672.662; 5.446.090; 5.808.096; 5.612.460; 5.324.844; 5.252.714; 6.420.339; 6.201.072; 6.451.346; 6.306.821; 5.559.213; 5.747.646; 5.834.594; 5.849.860; 5.980.948; 6.004.573; 6.129.912; WO 97/32607, EP 229.108, EP 402.378, WO 92/16555, WO 94/04193, WO 94/14758, WO 94/17039, WO 94/18247, WO 94/28024, WO 95/00162, WO 95/11924, WO95/13090, WO 95/33490, WO96/00080, WO97/18832, WO98/41562, WO98/48837, WO99/21134, WO99/32139, WO99/31140, WO96/40791, WO98/32466, WO95/06058, EP 439 508, WO97/03106, WO96/21469, WO95/13312, EP 921 131, WO 98/05363, EP 809 996, WO 96/41813, WO96/07670, EP 605 963, EP 510 356, EP 400 472, EP 183 503 e EP 154 316, que são aqui incorporados por referência. Qualquer das moléculas PEG descritas aqui podem ser usadas em qualquer forma, incluindo, mas não limitado a cadeia única, cadeia ramificada, cadeia multi-braço, única funcional, bi-funcional, multi-funcional ou qualquer combinação dos mesmo.
[00535]Polímero adicional e derivados PEG são descritos nos seguintes pe-didos de patente que são todos aqui incorporados por referência em sua totalidade: Publicação de Patente dos EUA No. 2006/194256, Publicação de Patente dos EUA No. 2006/0217532, Publicação de Patente dos EUA No. 2006/0217289, Patente Provisória dos EUA No. 60/755.338, Patente Provisória dos EUA No.60/755.711; Patente Provisória dos EUA No.60/755.018; Publicação de Patente Internacional No. PCT/US06/49397; WO2006/069246; Patente Provisória dos EUA No. 60/743.041; Patente Provisória dos EUA No. 60/743.040; Pedido de Patente Internacional No. PCT/US06/47822; Patente Provisória dos EUA No. 60/882.819; Patente Provisória dos EUA No. 60/882.500; e Patente Provisória dos EUA No. 60/870.594. Aumentando a afinidade para albumina sérica
[00536]Várias moléculas podem ser também fusionadas aos polipeptídeos FGF-21 da invenção pra modular a meia vida dos polipeptídeos FGF-21 no soro. Em algumas modalidades, moléculas são ligadas ou fusionadas a polipeptídeos FGF-21 da invenção para aumentar a afinidade para albumina sérica endógena em um ani-mal.
[00537]Por exemplo, em alguns casos, uma fusão recombinante de um poli- peptídeo FGF-21 e uma sequência de ligação de albumina é feita. Sequências de ligação a albumina exemplares incluem, mas não são limitadas a, domínio de ligação a albumina a partir da proteína G estreptocócica (ver, por exemplo, Makrides et al, J. Pharmaol. Exp. Ther. 277:534-542 (1996) e Sjolander et al, J. Immunol. Methods 201:115-123 (1997)), ou peptídeos ligantes a albumina como aquelas descritas em, por exemplo, Dennis et al, J. Biol. Chem. 277:35035-35043 (2002).
[00538]Em outras modalidades, os polipeptídeos FGF-21 da presente inven-ção são acilados com ácidos graxos. Em alguns casos, os ácidos graxos promovem a ligação a albumina sérica. Ver, por exemplo, Kurtzhals et al, Biochem. J. 312:725731 (1995).
[00539]Em outras modalidades, os polipeptídeos FGF-21 da invenção são fusionadas diretamente com albumina sérica (incluindo, mas não limitados a albumi-na sérica humana). Aqueles versados na técnica reconhecerão que uma ampla vari-edade de outras moléculas podem também estar ligados a FGF-21 na presente in-venção para modular a ligação sérica da albumina ou outros componentes séricos. X. Glicosilação de Polipeptídeos FGF-21
[00540]A invenção inclui polipeptídeos FGF-21 incorporado um ou mais ami- noácidos não naturalmente codificados produzindo resíduos sacarídeos. Os resíduos sacarídeos podem ser ou naturais (incluindo, mas não limitados a N- acetilglucosamina) ou não naturais (incluindo, mas não limitados a 3-fluorgalactose). Os sacarídeos podem estar ligados a aminoácidos não naturalmente codificados ou por uma ligação glicosídica ligada a N ou O (incluindo, mas não limitado a N- acetilgalactose-L-serina) ou uma ligação não natural (incluindo mas não limitado a uma oxima ou o correspondente glicosídeo ligado a C ou s).
[00541]As frações sacarídeas (incluindo, mas não limitadas a glicosil) podem ser adicionadas a polipeptídeos FGF-21 ou in vivo ou in vitro. Em algumas modali- dades da invenção, um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado contendo carbonila é modificado com um derivado sacarí- deo com um grupo aminoóxi para gerar o correspondente polipeptídeo glicosilado ligado através de uma ligação oxima. Uma vez ligado ao aminoácido não natural-mente codificado, o sacarídeo pode ainda elaborado por tratamento com glicosil- transferases e outras enzimas para gerar um oligossacarídeo ligado ao polipeptídeo FGF-21. Ver, por exemplo, H. Liu et al, J. Am. Chem. Soc. 125:1702-1703 (2003).
[00542]Em algumas modalidades da invenção, um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado contendo carbonila é diretamente modificado com um glicano com estrutura definida preparada como um derivado aminoóxi. Um versado na técnica reconhecerá que outras funcionalidades, incluindo azida, alquino, hidrazida, hidrazina, e semi-carbazida, podem ser usados para ligar o sacarídeo a um aminoácido não naturalmente codificado.
[00543]Em algumas modalidades da invenção, um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado contendo alquinila po-de então ser modificado por, incluindo, mas não limitado a uma reação de cicloadi- ção [3+2] de Huisgen com, incluindo mas não limitado a derivadas alquinila ou azida, respectivamente. Este método permite a modificação de proteínas com seletividade altamente alta. XI. Dímeros e Multímeros FGF-21
[00544]A presente invenção também provê para combinações FGF-21 e análogos FGF-21 tais como homodímeros, heterodímeos, homomultímeros, ou hete- romultímeros (isto é, trímeros, tetrâmeros, etc) onde FGF-21 contendo um ou mais aminoácidos não naturalmente codificados estão ligados a outro FGF-21 ou variante de FGF-21 dos mesmos ou qualquer outro polipeptídeo que não é FGF-21 ou variante FGF-21 do mesmo, ou diretamente a estrutura do polipeptídeo ou através de um ligante. Devido a seu peso molecular aumentado comparado a monômeros, o díme- ro ou multímero FGF-21 conjugado pode exibir novas ou desejadas propriedades, incluindo, mas não limitado a diferenças farmacológicas, farmacocinéticas, farmaco- dinâmicas, meia vida terapêutica modulada, ou media vida plasmática modulada re-lativa a FGF-21 monomérico. Em algumas modalidades, dímeros FGF-21 da invenção modularão a transdução de sinal do receptor FGF-21. Em outras modalidades, os dímeros ou multímeros FGF-21 da presente invenção atuarão como um antagonista, agonista ou modulador do receptor FGF-21.
[00545]Em algumas modalidades, uma ou mais moléculas FGF-21 presentes em um dímero ou multímero contendo FGF-21 compreendem um aminoácido não naturalmente codificado ligado a um polímero solúvel em água.
[00546]Em algumas modalidades, os polipeptídeos FGF-21 são ligados dire-tamente, incluindo, mas não limitados a, através de uma ligação Asn-Lys amida ou ligação dissulfeto Cys-Cys. Em algumas modalidades, os polipeptídeos FGF-21, e/ou a molécula não FGF-21 ligada, compreenderão aminoácidos não naturalmente codificados diferentes para facilitar a dimerização, incluindo mas não limitado a um alquino em um aminoácido não naturalmente codificado de um primeiro polipeptídeo FGF-21 e uma azida em um segundo aminoácido não naturalmente codificado de uma segunda molécula serão conjugado através de cicloadição [3+2] de Huisgen. Alternativamente, FGF-21, e/ou a molécula não FGF-21 ligada compreendendo um aminoácido não naturalmente codificado contendo cetona pode ser conjugado a um segundo polipeptídeo compreendendo um aminoácido não naturalmente codificado contendo hidroxilamina e os polipeptídeos são reagidos através da formação da cor-respondente oxima.
[00547]Alternativamente, os dois polipeptídeos FGF-21, e/ou a molécula não FGF-21 ligada, são ligados através de um ligante. Qualquer ligante hetero- ou homo- bifuncional podem ser usados para ligar duas moléculas, e/ou as moléculas não FGF-21 ligadas, que pode ter a mesma ou diferente sequência primária. Em alguns casos, o ligante usado para unir o FGF-21, e/ou as moléculas não FGF-21 ligadas junto podem ser um reagente PEG bifuncional. O ligante pode ter uma grande variedade de peso molecular ou comprimento molecular. Ligantes de peso molecular maior ou menor podem ser usados para prover uma relação especial desejada ou conformação entre FGF-21 e a entidade ligada ou entre FGF-21 e seu receptor, ou entre a entidade ligada e seu parceiro ligador, se qualquer. Ligantes tendo compri-mento molecular mais longo ou mais curto podem também ser usados para prover um espaço desejado ou flexibilidade entre FGF-21 e a entidade ligada, ou entre a entidade ligada e seu parceiro ligante, se qualquer.
[00548]Em algumas modalidades, a invenção provê ligantes bifuncionais so-lúveis em água que têm uma estrutura pesada que inclua: a) uma azida, um alquino, uma hidrazina, uma hidrazida, uma hidroxilamina, ou uma fração contendo carbonila em pelo menos uma primeira terminação de uma estrutura de polímero; e b) pelo menos um segundo grupo funcional em uma segunda terminação da estrutura do polímero. O segundo grupo funcional pode ser o mesmo ou diferente como o primeiro grupo funcional. O segundo grupo funcional, em algumas modalidades, não é reativo com o primeiro grupo funcional. A invenção provê, em algumas modalidades, compostos solúveis em água que compreendem pelo menos um braço da estrutura molecular ramificada. Por exemplo, a estrutura molecular ramificada pode ser den- drítica.
[00549]Em algumas modalidades, a invenção provê multímeros compreen-dendo um ou mais polipeptídeos FGF-21, formados por reações com polímeros ati-vados solúveis em água que têm a estrutura: Em que n é a partir de 5 a 3.000, m é 2-10, X pode ser uma azida, um alqui- no, uma hidrazina, uma hidrazida, um grupo aminoóxi, uma hidroxilamina, uma aceti-la, ou fração contendo carbonila, e R é um grupo revestimento, um grupo funcional, um grupo de saída que pode o mesmo ou diferente como X. R pode ser, por exemplo, um grupo funcional selecionado a partir do grupo consistindo de hidroxila, hidro- xila protegida, alcoxila, N-hidroxisuccinimidila éster, 1-benzotriazol éster, acetal, aldeído, hidratos aldeído, alquenila, acrilato, metacrilato, acrilamida, sulfona ativa, amina, aminoóxi, amina protegida, hidrazida, hidrazida protegida, tiol protegido, ácido carboxílico, ácido carboxílico protegido, isocianato, isotiocianato, maleimida, vi- nilsulfona, ditiopiridina, vinilpiridina, iodoacetamida, apóxido, glioxais, dionas, mesila- tos, tosilatos, e tresilato, alqueno e cetona. XII. Medida da Atividade do Polipeptídeo FGF-21 e Afinidade do Polipeptí- deo FGF-21 para o Receptor do Polipeptídeo FGF-21
[00550]FGF-21 tem sido mostrado estimular a captação de glicose e aumentar a sensibilidade de insulina em adipócitos 3T3-L1, um modelo in vitro usado para estudo de metabolismo de tecido adiposo como mostrado no Exemplo 3 na Publicação da Patente dos EUA No. 20040259780 que é aqui incorporada por referência em sua totalidade. Uma característica do diabetes do Tipo 2 é a deficiência de captação de glicose em vários tipos de tecidos incluindo tecido adiposo. Então, FGF-21 é útil para tratar diabetes Tipo 2 pode diminuir os níveis de glicose sanguíneo. Além disso, FGF-21 é útil para tratar obesidade por aumentar a energia dispensada por uso de glicose mais rápido e mais eficiente. Adicionalmente, FGF-21 tem sido mostrado estimular captação de glicose em adipócitos 3T3-L1 em uma forma independente de insulina, indicando que ele é útil para tratar diabetes do Tipo 1 também. Ver, Publicação de Patente dos EUA No. 20040259780. FGF-21 é mostrado estimular captação de glicose em adipócitos 3T3-L1 em uma forma dependente de concentração em uma concentração sub-ótima de insulina (5 nM) e em ausência de insulina na Publicação de Patente dos EUA No. 20040259780.
[00551]Captação de glicose em adipócitos 3t3-L1 pode ser verificada usando o seguinte método. Células 3T3-L1 são obtidas a partir da Coleção de Cultura do Tipo Americana (ATCC, Rockville, Md.). Células são cultivadas em meio de cultura (MC) contendo soro fetal bovino enriquecido com 10% de ferro em meio Eagle modificado da Dulbecco. Para diferenciação de adipócito padrão, 2 dias após as células alcançaram confluência (referido como dia 0), células são expostas ao meio de dife-renciação (MD) contendo 10% de soro fetal bovino, 10 μg/mL de insulina, 1 μM de dexametasona, e 0,5 μM de isobutilmetilxantina, por 48 horas. Células então são mantidas no meio de pós-diferenciação contendo 10% de soro fetal bovino, e 10 μg/mL de insulina. Potência in vitro pode ser medida com o ensaio de captação de glicose que é conhecido pelos versados na técnica. Potência in vitro pode ser definida como a medida da captação de glicose de um composto FGF-21 em um ensaio baseado em célula e é medido para a potência biológica do composto FGF. Pode ser expresso como RC50 que é a concentração efetiva do composto que resulta em 50% da atividade em um experimento dose-resposta único.
[00552]Ensaio de Transporte de Glicose - Dependente de Insulina - captação de Hexose, como ensaiado pelo acúmulo de 0,1 mM de 2-deóxi-D-[14C]glicose, é medido como segue: adipócitos 3T3-L1 em placas de 12 poços são lavados duas vezes com tampão KRP (136 mM de NaCl, 4,7 mM de KCl, 10 mM de NaPO4, 0,9 mM de CaCl2, 0,9 mM de MgSO4, pH 7.4) aquecido para 37oC e contendo 0,2% d eBSA, incubado em meio Leibovitz’s L-15 contendo 0,2% de BSA por 2 horas a 37oC em temperatura ambiente, lavadas duas vezes novamente com KRP contendo, 0,2% de tampão BSA, e incubado em KRP, 0,2% de tampão BSA em ausência (somente Me2SO) ou presença de wortmanina por 30 minutos a 37oC em temperatura ambiente. Insulina é então adicionada a uma concentração final de 100 nM por 15 minutos, e a captação de 2-deóxi-D-[14C]glicose é medida por pelo menos 4 minutos. Captação não específica, medida em presença de 10 μM de citocalasina B, é subtraída a partir de todos os valores. Concentrações de proteína são determinadas com o ensaio de ácido bicinconínico Pierce. Captação é medida rotineiramente em triplicata ou quadruplicata para cada experimento. O efeito do pré-tratamento agudo e crônico de adipócitos 3T3-L1 com FGF-21 em presença de insulina pode ser inves-tigado.
[00553]Ensaio de Transporte de Glicose - Independente de Insulina - fi- broblasto 3T3-L1 são plaqueados em placas de 96 poços e diferenciados em células de gordura (adipócitos) por 2 semanas. Após a diferenciação eles são coletados em meio livre de soro e tratados com FGF-21 por 24 horas. Sob tratamento, células são lavadas duas vezes com tampão KRBH, contendo 0,1% de BSA. Captação de glicose é feita em presença de glicose marcada (sem insulina) em tampão KPBH. FGF- 21 tem sido mostrado estimular a captação de glicose em adipócitos 3T3-L1 em uma forma dependente de concentração em uma concentração sub-ótima de insulina (5 nM) e em ausência de insulina (ver, Publicação de Patente dos EUA No. 2004259780). Adicionalmente, polipeptídeos FGF-21 da presente invenção podem ser mostrados para induzir captação de glicose em um modelo de tecido ex vivo.
[00554]O modelo de transporte de glicose ex vivo, o ensaio de transporte de glicose é descrito como segue: Soluções Estoque de Tampão de Krebs-Hnseleit - Estoque 1 : NaCl (1,16 M); KCl (0,046 M); KH2PO4 (0,0116 M); NaHCO3 (0,0253 M). Estoque 2: CaCl2 (0,025 M); MgSO4 (2H2O) (0,0116 M). BSA: Uso Fração ICN Cohn V, BSA livre de ácido graxo diretamente sem dialisar. Preparação dos Meios: Adicionar 50 mL de estoque de Krebs 1 a 395 mL de dH2O e gás com 95% de P2/5% de CO2 por 1 hora. Adicionar 50 mL de estoque 2 e trazer para 500 mL com dH2O. Adicionar 500 mg de BSA livre de ácido graxo CN. Meios de pré-incubação e incubação: 32 mM de Manitol, 8 mM de Glicose. Meio de Lavagem: 40 mM de Mani- tol, 2 mM de Piruvato. Meios de Transporte: 39 mM de Manitol, 1 mM de 2-DG; 32 mM de Manitol, 8 mM de 3-O-MG. Solução de Insulina: (Insulina Porcina [Lilly] 100.000.000 μU/mL) em uma concentração final de 2000 μU/mL ou 13,3 nM. Preparação dos Meios de Marcação Radioativa: atividades específicas usadas: 2DG=1,5 mCi/mL; 3-O-MG=437 μCi/mL; ou, Manitol=8 μCi/m. Ratos são anestesiados com 0,1 cc de Nembutal por 100 g de peso corpóreo. Tecido muscular é retirado e lavado em 0,9% de solução salina e então colocado em meio de pré-incubação (2 mL) a 29oC por 1 hora. O tecido muscular é transferido para o meio de incubação (2 mL, mesmo com pré-incubação exceto incluindo insulina ou composto teste) e incubado por 30 minutos (depende das condições experimentais). O tecido muscular é então transferido para meio de lavagem (2 mL) por 10 minutos a 29oC, então transferido para meio de marcação (1,5 mL) por 10 min (3-O-MG) ou 20 min (2DG). O tecido muscular é cortado, pesado e colocado em tubos de polipropileno em gelo seco. 1 mL de KOH 1 N é adicionado aos tubos que são então colocados em um banho de água 70oC por 10-15 minutos, agitando os tubos a cada poucos minutos. Os tubos são arrefecidos em gelo e 1 mL de HCl 1 N é adicionado, então misturado bem. 200 μL de sobrenandante é então colocado em frascos de cintilação duplicados e conta-dos em um contador de cintilação comparados a padrões radioativos conhecidos.
[00555]Para contração, os músculos são primeiro incubados por 1 hora em meio de pré-incubação/incubação. Após 1 hora, um músculo de cada par (um par por rato) é fixo para o aparato de estimulação e outro músculo é transferido para um novo frasco de meio de incubação. O músculo contraído é estimulado por 200 mseg com correntes de 70 Hz com cada impulso em uma corrente sendo 0,1 mseg. As correntes são distribuídas a 1/seg am 10-15 V por 2x10 minutos com 1 minutos de repouso entre elas. No fim do período de estimulação, o músculo é removido a partir do aparato de estimulação, e colocado em meio de lavagem por 10 minutos, seguido pelo meio de marcação como ressaltado acima.
[00556]O receptor FGF-21 pode ser preparado usando técnicas e métodos que são conhecidos por um versado na técnica. Atividade do polipeptídeo FGF-21 pode ser determinada usando ensaios padrões ou conhecidos in vitro ou in vivo. Para um polipeptídeo FGF-21 não-PEGilado ou PEGilado compreendendo um aminoá- cido não natural, a afinidade do FGF-21 para seu receptor pode ser medida pelo uso de um biosensor BIAcore® (Pharmacia).
[00557]Apesar de tais métodos serem usados para criar os polipeptídeos FGF-21, os polipeptídeos FGF-21 são sujeitos a ensaios para atividade biológica. Em geral, o teste para atividade biológica pode prover análise para o resultado desejado, tal como aumento ou diminuição na atividade biológica (como comparado ao FGF-21 modificado), atividade biológica diferente (como comparado com o FGF-21 modificado), análise de afinidade do receptor ou parceiro ligante, mudanças confor- macionais ou estruturais do FGF-21 por si só ou seu receptor (como comparado ao FGF-21 modificado), ou análise da meia vida sérica.
[00558]A compilacão acima de referências para metodologias de ensaios não é exaustiva, e aqueles versados na técnica reconhecerão outros ensaios úteis para testes para o resultado final desejado. XIII. Medida da Potência, Meia Vida Funcional In vivo, e Parâmetros Farma- cocinéticos
[00559]Um importante aspecto da invenção é meia vida biológica prolongada que é obtida pela construção de polipeptídeo FGF-21 com ou sem conjugação do polipeptídeo a uma fração polímera solúvel em água. A rápida diminuição pós- administração das concentrações séricas do polipeptídeo FGF-21 tem feito importante a avaliação de suas respostas biológicas para tratamento com polipeptídeo FGF- 21 conjugado e não conjugado e variantes dos mesmos. O polipeptídeo FGF-21 conjugado e não conjugado da presente invenção pode ter meia vida sérica prolon-gada também após a administração através, por exemplo, de administração subcu-tânea ou i.v., tornando impossível sua dosagem por, por exemplo, métodos de ELISA ou por ensaio de seleção primária. Kits ELISA ou RIA a partir de fontes comerciais podem ser usados. Medidas de meia vida biológica in vivo são realizadas como aqui descrito.
[00560]A potência e meia vida funcional in vivo de um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado pode ser determinada de acordo com protocolos conhecidos pelos versados na técnica.
[00561]Parâmetros farmacocinéticos para um polipeptídeo FGF-21 compre-endendo um aminoácido não naturalmente codificado pode ser avaliado em ratos machos Sprague-Dawley normais (n=5 animais por grupo de tratamento). Animais receberão ou uma dose única de 25 μg/rato iv ou 50 μg/rato s.c., e aproximadamente 5-7 amostras de sangue serão tomadas de acordo com um curso temporal pré- definido, geralmente cobrindo cerca de 6 horas para um polipeptídeo FGF-21 com-preendendo um aminoácido não naturalmente codificado não conjugado a um polí-mero solúvel em água e cerca de 4 dias para um polipeptídeo FGF-21 compreendendo um aminoácido não naturalmente codificado e conjugado com um polímero solúvel em água Dados farmacocinéticos para FGF-21 sem um aminoácido não naturalmente codificado pode ser comparado diretamente aos dados obtidos para os polipeptídeos FGF-21 compreendendo um aminoácido não naturalmente codificado.
[00562]Parâmetros farmacocinéticos podem também ser avaliados em um primata, por exemplo, macacos cinomolgos. Tipicamente, uma injeção única é admi-nistrada ou subcutaneamente ou intravenosamente, e níveis de FGF-21 séricos são monitorados ao longo do tempo.
[00563]A atividade específica dos polipeptídeos FGF-21 em acordo com esta invenção pode ser determinada por vários ensaios conhecidos na técnica. A atividade biológica das muteínas do polipeptídeo FGF-21, ou fragmentos dos mesmos, obtidos e purificados em acordo com esta invenção podem ser testados por métodos descritos ou referenciados aqui ou conhecidos pelos versados na técnica.
[00564]Polipeptídeos da presente invenção podem ser usados para tratar mamíferos sofrendo de Diabetes Mellitus não dependente de insulina (DMNDI: Tipo 2), diabetes dependente de insulina (Tipo 1), bem como obesidade, depuração de glicose inadequada, hiperglicemia, hiperinsulinemia e semelhantes. FGF-21 é efetivo em modelos animais de diabetes e obesidade, como mostrado na Publicação de Pa-tente dos EUA No. 20040159780, que é aqui incorporada por referência em sua tota-lidade. Como perfis metabólicos diferem entre vários modelos animais de obesidade e diabetes, análise de múltiplos modelos tem sido feita para separar os efeitos de hiperinsulimenia, hiperglicemina e obesidade. Os camundongos diabéticos (db/db) e obesos (ob/ob) são caracterizados pela obesidade massiva, hiperfagia, hiperglicemi- na variável, resistência a insulina, hiperinsulinemia e termogênese impedida (Cole-man, Diabetes 31:1, 1982; E. Shafrir, em Diabetes Mellitus; H. Rifkin e D. Porte, Jr. Eds. (Elsevier Science Publishing Co., Inc., Nova Iorque, ed. 4, 1990), pp. 299340). Entretanto, diabetes e muito mais severa em modelo db/db (Coleman, Diabetes 31;1. 1982; E. Shafrir, em Diabetes Mellitus; H. Rifkin e D. Porte, Jr. Ed.s (Elsevier Science Publishing Co., Inc. Nova Iorque, ed. 4, 1990) pp. 299-340). Ratos Zucker (fa/fa) são severamente obesos, hiperinsulinêmicos, e resistentes a insulina (Coleman, Diabetes 31;1. 1982; E. Shafrir, em Diabetes Mellitus; H. Rifkin e D. Porte, Jr. Ed.s (Elsevier Science Publishing Co., Inc. Nova Iorque, ed. 4, 1990), e a mutação fa/fa pode ser a equivalente em rato da mutação db murina (Friedman, et al, Cell 69:217220, 1992; Truett et al, Proc. Natl. Acad. Sci. EUA 88:7806, 1991), Camundongos Tubby (tub/tub) são caracterizados por obesidade, resistência a insulina moderada e hiperinsulinemia sem hiperglicemia significante (Coleman et al, J. Heredity 81:424, 1990).
[00565]O modelo de glutamato monosódico (MSG) para obesidade induzida quimicamente (Olney, Science 164:719 1969; Cameron et al, Cli. Exp. Pharmacol. Physiol. 5:41, 1978), em que a obesidade é menos severa que os modelos genéticos e desenvolve se hiperfagia, hiperinsulinemia e resistência a insulina, pode também ser examinado. Finalmente, o modelo estreptozotocina (STZ) para diabetes induzida quimicamente pode ser testado para examinar os efeitos da hiperglicemia em au-sência de obesidade. Animais tratados com STZ são deficientes em insulina e seve-ramente hiperglicêmicos (Coleman, Diabetes 31;1. 1982; E. Shafrir, em Diabetes Mellitus; H. Rifkin e D. Porte, Jr. Ed.s (Elsevier Science Publishing Co., Inc. Nova Iorque, ed. 4, 1990) pp. 299-340).
[00566]Polipeptídeos FGF-21 da invenção podem ser avaliados em um mo-delo de choque séptico in vivo em camundongos ob/ob. Ver, Publicação de Patente dos EUA No. 20050176631, que é aqui incorporado por referência em sua totalidade. XIV. Administração e Composições Farmacêuticas
[00567]Os polipeptídeos ou proteínas da invenção (incluindo, mas não limi-tados a FGF-21, sintetases, proteínas compreendendo um ou mais aminoácidos não naturais etc) são opcionalmente empregados para usos terapêuticos, incluindo, mas não limitados a, em combinação com um veículo farmaceuticamente adequado. Tais composições, por exemplo, compreendem uma quantidade terapeuticamente efetiva do composto, e um veículo ou excipiente farmaceuticamente aceitável. Tais veículos ou excipientes incluem, mas não são limitados a solução salina, salina tamponada, dextrose, água, glicerol, etanol, e/ou combinações dos mesmos. A formulação é feita para adequar o modo de administração. Em geral, métodos de administração de pro-teínas são conhecidos pelos versados na técnica e podem ser aplicados para admi-nistração de polipeptídeos da invenção.
[00568]Composições terapêuticas compreendendo um ou mais polipeptí- deos da invenção são opcionalmente testados em um ou mais modelos animais in vitro e/ou in vivo apropriados de doença, para confirmar a eficácia, metabolismo tissular, e estimar doses, de acordo com os métodos conhecidos pelos versados na técnica. Em particular, doses podem ser inicialmente determinadas por atividade, estabilidade ou outras medidas adequadas de aminoácidos não naturais e naturais homólogos (incluindo mas não limitado a comparação de um polipeptídeo FGF-21 modificado para incluir um ou mais aminoácidos não naturais a um aminoácido natural do polipeptídeo FGF-21), isto é, em um ensaio relevante.
[00569]Administração é por qualquer das vias normalmente usadas para in-troduzir uma molécula em contato final com células sanguíneas ou tissulares. Os aminoácidos não naturais dos polipeptídeos da invenção são administrados em qualquer maneira, opcionalmente com um ou mais veículos farmaceuticamente acei-táveis. Métodos adequados de administração de tais polipeptídeos no contexto da presente invenção a um paciente são disponíveis, e, embora mais que uma via pode ser usada para administrar uma composição particular, uma via particular pode sempre prover uma ação ou reação mais imediata e mais efetiva que outra via.
[00570]Veículos farmaceuticamente aceitáveis são determinados em parte pela composição particular sendo administrada, bem como pelo método particular usado para administrar a composição. Consequentemente, existe uma ampla varie-dade de formulações adequadas para composições farmacêuticas da presente in-venção.
[00571]Polipeptídeos FGF-21 da invenção podem ser administrados por qualquer via convencional adequada para proteínas ou peptídeos, incluindo, mas não limitados a parenteral, por exemplo, injeções incluindo, mas não limitado a sub- cutaneamente ou intravenosamente ou qualquer outra forma de injeções ou infusões. Composições polipeptídicas podem ser administradas por um número de vias incluindo, mas não limitadas a meios oral, intravenosa, intraperitoneal, intramuscular, transdérmica, subcutânea, tópica, sublingual ou retal. Composições compreendendo polipeptídeos aminoácidos não naturais, modificados ou não modificados, podem também ser administrados através de lipossomos. Tais vias de administração e for-mulações apropriadas são geralmente conhecidas pelos versados na técnica. O po- lipeptídeo FGF-21, pode ser usado sozinho ou em combinação com outros compo-nentes adequados tal como um veículo farmacêutico. O polipeptídeo FGF-21 pode ser usado em combinação com outros agentes, incluindo, mas não limitados a um agente anti-diabético oral.
[00572]O termo “agente anti-diabético” deve significar qualquer droga que é útil no tratamento, prevenindo, ou de outra forma reduzindo a severidade de qualquer distúrbio de metabolismo de glicose, ou qualquer complicação do mesmo, incluindo qualquer das condições, doença, ou complicações descritas aqui. Agentes anti- diabéticos incluem insulina, tiazolidinodionas, sulfoniluréias, derivados do ácido ben- zóico, inibidores de alfa-glucosidase ou semelhantes. Outra categorias gerais de agentes anti-diabéticos que podem ser parte de uma composição do paciente inclui (com termos definidos sendo mas marcas citadas): “drogas artigos” reconhecidas na Farmacopéia dos Estados Unidos oficial ou Formulário Nacional oficial (ou qualquer suplemento do mesmo); “nova droga” e “nova droga animal” aprovada pelo FDA dos EUA como aqueles termos são usados no Título 21 do Código dos Estados Unidos; qualquer droga que requeira aprovação de uma entidade governamental, nos EUA ou fora (“droga aprovada”); qualquer droga que é necessária para obter aprovação regulatória de forma a cumprir com 21 U.S.C.sctn.355(a) (“droga regulatória aprova-da”); qualquer agente que é ou foi sujeito a uma aplicação de droga humana sob 21 U.S.C. sctn.379 (g) (“droga humana”). (Todas as referências do código estatutário para esta definição referem-se a tal código como os dados de preenchimento originais deste pedido). Outros agentes anti-diabéticos são aqui revelados, e são conhecidos por aqueles versados na técnica. Drogas correntes ou agentes anti-diabéticos usados para controlar a diabetes do Tipo 2 que são bem conhecidos na técnica incluem um número de categorias: as biguanidas, tiazolidinodionas, as sulfoniluréias, derivados do ácido benzóico e inibidores da glucosidase. Essas drogas usualmente têm modos distintos de ação. As biguanidas, por exemplo, metformina, são acreditadas prevenir a gliconeogênese hepática excessiva. As tiazolidinodionas são acreditadas agirem por aumento da taxa de diposição de glicose periférica. As sulfonilu- réias, por exemplo, tolbutamida e gliburida, e derivados do ácido benzóico, por exemplo, repaglinida, diminuem a glicose plasmática por estimular a secreção de insulina. Os inibidores da alfa-glicosidase competitivamente inibem a alfa- glicosidase, que metaboliza carboidratos, assim atrasando a absorção de carboidrato e atenuando a hiperglicemia pós-prandial. Em adição, existem um número de terapias propostas para tratamento de diabetes que não têm sido aprovadas para uso humano.
[00573]Drogas correntes ou agentes anti-diabéticos para controle da diabetes e suas síndromes precurssoras, tais como resistência a insulina, que são bem conhecidas na técnica incluem cinco classes de compostos: as biguanidas, por exemplo, metformina; tiazolidinodionas; as sulfoniluréias, por exemplo, tolbutamida e gliburida; derivados do ácido benzóico, por exemplo, repaglinida; e inibidores da glu-cosidase. Em adição a esses agentes, um número de outras terapias podem ser usado em combinação com os polipeptídeos FGF-21 da presente invenção para melhorar o controle da glicose, incluindo, mas não limitado a inibidores DPP-4. Certos agentes anti-diabéticos têm sido aprovados para uso humano. Os compostos líderes DPP-4 testados em testes clínicos incluem Vildagliptin (Galvus) (LAF237), Sitagliptin (Januvia), Saxagliptina e Alogliptina. Januvia (Sitagliptina) foi aprovado para trata-mento de diabetes do tipo 2 nos Estados Unidos em 17 de Outubro de 2006, para uso como monoterapia, ou combinação de terapia, com ou metformina ou uma tiazo- lidinodiona. Administração da primeira geração do composto Novartis 1-[[2-(5- cianopiridin-2-il)amino]etil]amino]acetil]-2-ciano-(S)-pirrolidina (NVP DPP728) por um período de 4 semanas para 93 pacientes com diabetes do Tipo 2 (significa HbA1c de 7,4%) reduziu níveis de glicose plasmática, insulina, e HbA1c por um período de es-tudo de 4 semanas. Ver, Inhibition of Dipeptidyl Peptidase IV Improves Metabolic Control Over a 4-week Study Period in Type 2 Diabetes. Diabetes Care. 2002, Maio, 25(5):869-875. Pacientes recebendo metformina têm também sido notado existir adi-tivo de benefícios de diminuir a glicose seguindo instituição de terapia GLP-1. Ver, Additive glucose-lowering effects of glucagon-like peptide-1 and metformin in type 2 diabetes. Diabetes Care. 2001 Abril; 24(4):720-5. Em um estudo de 10 pacientes masculinos não diabéticos obesos, administração de metformina foi associada com níveis aumentados de circulação de GLP-1 seguindo carregamento de glicose oral, e em experimentos usando um grupo de plasma humano, metformina (0,1-0,5 mi- crog/mL) inibiu significantemente a degradação de GLP-1 (7-36)amida após uma incubação de 30 minutos a 37 graus de C, em presença ou ausência de DPP-4. Os autores deste estudo aumentaram a possibilidade que metformina pode inibir a que-bra enzimática de GLP-1 ambos, in vitro e in vivo. 'Ver Effect of metformin on gluca-gon-like peptide 1 (GLP-1) and leptin levels in obese nondiabetic subjects. Diabetes Care. 2001 Mar; 24(3):489-94. Análise da relação entre DPP-1, e degradação de GLP-1 usando análises bioquímicas in vitro. Demuth e colaboradores não encontraram efeito de metformina na degradação mediada por DPP-4 de GLP-1 usando uma variedade de fontes de DPP-4 humano. Ver Metformin Effects on Dipeptidylpepti- dase IV Degradation of Glucagon-like Peptide-1. Biochem Biophys Res Commun 2002 Março 15:291(5):1302-8.
[00574]Entre biguanidas úteis como agentes terapêuticos diabéticos, met- formina tem provado particularmente ser bem sucedida. Metformina (N,N- dimetilimidocarbonimidicdiamida; 1,1-dimetilbiguanida; N,N-dimetilbiguanida; N.N- dimetildiguanida; N’-dimetilguanilguanidina) e uma gente anti-diabético que atua por reduzir a produção de glicose pelo fígado e por diminuir a absorção intestinal de gli-cose. É também acreditado melhorar a sensibilidade a insulina de tecidos em qual-quer lugar no corpo (aumenta a captação e utilização de glicose periférica). Metfor- mina melhora a tolerância a glicose na tolerância a glicose impedida (IGT) em paci-entes e pacientes diabéticos do Tipo 2, diminuindo ambas, a glicose pré- e pós- prandial. Metformina é geralmente não efetiva em ausência de insulina. Baiiley, Dia-betes Care 15:755-72 (1992).
[00575]A eficácia de metformina tem sido mostrada em vários testes. Em um estudo de diabéticos do Tipo 2 moderadamente obesos, níveis de HbA1c aumentou de 8,6% a 7,1% após 29 semanas de terapia de metformina sozinha ou em combinação com sulfoniluréia. DeFronzo et al, New Engl. J. Med. 333:541-49 (1995). Met- formina também tem um efeito favorável em lipídios séricos, diminuindo a média de jejum de triglicerídeos séricos, colesterol total, e níveis de colesterol LDL e não mostrando efeitos adversos em outros níveis lipídicos. Em outro teste, metformina melhorou o controle glicêmico em pacientes DMNDI em uma forma dose-dependente. Após 14 semanas, metformina 500 e 2000 mg diárias reduziram HbA1c por 0,9% e 2,0% respectivamente. Garber et al, Am. J. Med. 102:491-97 (1997). Metformina pode também ter um efeito terapêutico benéfico em não diabéticos resistentes a insulina. Um estudo indicou que tratamento de mulheres não diabéticas obesas hipertensas com metformina diminuiu a pressão sanguínea, jejum e fibrinogênio insulina no plasma estimulado por glicose. Giugliano et al, Diabetes Care 16:1387-90 (1993).
[00576]Metformina é comumente administrada como metformina HCl. Esta bem como todas as outras formas de metformina é contemplada para uso com poli- peptídeos FGF-21 da presente invenção. Geralmente, um regime de dose fixo é in-dividualizado para o controle da hiperglicemia em diabetes com metformina HCl ou qualquer outro agente farmacológico. Individualização de dose é feita na base de ambas, efetividade e tolerância, enquanto geralmente não excede a dose diária má-xima recomendada de 2550 mg.
[00577]Tiazolidinodionas contempladas para uso na prática da presente in-venção incluem troglitazona e semelhantes. Tais compostos são bem conhecidos, por exemplo, como descrito na Pat. dos EUA Nos. 5.223.522, 5.132.317, 5.120.754, 5.0061.717, 4.897.405, 4.873.255, 4.687.777, 4.572.912, 4.287.200 e 5.002.953; e Current Pharmaceutical Design 2:85-101 (1996). Troglitazona é um agente anti- hiperglicêmico oral que aumenta o transporte de glicose possivelmente por ativação do receptor ativado por proliferador peroxisoma-y (PPARy). Por tal ativação, troglita- zona pode aumentar a expressão de transportadores de glicose GLUT4, resultando em captação de glicose estimulada por insulina aumentada. Troglitazona pode tam-bém atenuar gliconeogênese e/ou ativação de glicólise.
[00578]HbA1c é um teste sanguíneo que mede a quantidade de glicosilado que é geralmente maior quando um paciente tem períodos experimentador de au-mento da glicose sanguínea. O teste provê uma estimativa de pelo menos 2-3 meses de controle de diabetes para um paciente. Controle glicêmico resultando de terapia com troglitazona reduz Hb1Ac por aproximadamente 1 a 2%. Mimura et al, Diabetes Med. 11:685-91 (1994); Kumar et al, Diabetologia 39:701-09 (1996). Efeitos podem não ocorrer por umas poucas semanas após o início da terapia. Troglitazona pode também diminuir os requerimentos de insulina. Em um teste de pacientes com DMNDI e usando insulina exógena, média de HbA1c caiu cerca de 0,8% e 1,4% para doses de 200 e 600 mg de troglitazona, respectivamente. Requerimentos de insulina foram reduzidos por até 29%, Schwartz et al, New. Engl. J. Med. 338:861-66 (1998). Em outro estudo de diabéticos DMNDI usando 400 e 600 mg de troglitazona, níveis de glicose em jejum e pós-pradial foram diminuídos, e clamp hiperinsulinêmico euglicêmico indicou que disposição de glicose foi aproximadamente 45% acima dos níveis de pré-tratamento. Maggs et al, Ann. Intern. Med. 128:176-85 (1998).
[00579]Em um estudo, 400 mg de troglitazona aumentou as taxas de dispo-sição de glicose em pacientes obesos com ou tolerância a glicose impedida ou nor-mal. Nolan et al, New Eng. J. Med. 331:1188-93 (1994). Em outro estudo de mulheres com TGI e uma história de diabetes gestacional, 600 mg de troglitazona aumentou a homeostase da insulina, incluindo melhora na sensibilidade de insulina e diminuição das concentrações de insulina circulante, mas tolerância de glicose foi não mudada. Berkowitz et al, Diabetes 45:172-79 (1996). Tiazolidinodionas podem ser com populações em risco para DMNDI, tais como mulheres com POCS ou GDM, para prevenir ou atrasar o início da DMNID. Pat. dos EUA No. 5.874.454. Quantidades efetivas de troglitazona, quando usadas sozinhas, variando a partir de cerca de 10 mg até cerca de 800 mg por dose diária e uma variação comensurada é contemplada para uso na presente invenção. Em adição a seu uso com metformina, trogli- tazona pode ser usada em combinação com insulina e um agente sulfoniluréia. Ver, por exemplo, Pat. dos EUA No. 5.859.037.
[00580]Sulfoniluréias geralmente operam por diminuição de glicose plasmá- tica por aumento da liberação de insulina a partir do pâncreas. Especificamente, sul- foniluréias atuem bloqueando os canais de potássio sensíveis a ATP. A sulfoniluréia glimepirida podem também aumentar a sensibilidade da insulina por estimular a translocação de transportadores GLUT4. Sulfoniluréias são tipicamente prescritos quando HbA1c é cerca de 8%. Ver, também Pat. dos EUA Nos. 5.258.185, 4.873.080.
[00581]As sulfoniluréias são uma classe de compostos que são bem conhe-cidos na técnica, por exemplo, como descrito na Pat. dos EUA Nos. 3.454.635, 3.669.966, 2.968.158, 3.501.495, 3.708.486, 3.668.215, 3.654.357, e 3.097.242. Sul- foniluréias exemplares contempladas para uso em certas modalidades da presente invenção (com doses típicas diárias indicadas em parênteses) incluem acetoexamida (na variação de cerca de 250 até cerca de 1500 mg), clorpropamida (na variação de cerca de 100 até cerca de 500 mg), tolazimida (na variação de cerca 100 até cerca 1000 mg), tolbutamida (na variação de cerca 500 até cerca 3000 mg), gliclazida (na variação de cerca 80 até cerca 320 mg), glipizida (na variação de cerca 5 até cerca 40 mg), glipizida GITS (na variação de cerca 5 até cerca 20 mg), gliburida (na variação de cerca 1 até cerca 20 mg), gliburida micronizada (na variação de cerca 0,75 até cerca 12 mg), glimeperida (na variação de cerca 1 até cerca 8 mg), AG-EE 623 ZW, e semelhantes. Glimepirida é o primeiro agente anti-diabético nesta classe a ser aprovado para uso com insulina, e pode ter menos risco de hipoglicemia associada com seu uso.
[00582]Uma variedade de inibidores da alfa-glicosidase pode ser usada com a presente invenção para tratar e/ou prevenir diabetes. Tais inibidores competitivamente inibem a alfa-glicosidase, que metaboliza carboidratos, assim atrasando absorção de carboidrato e atenuando a hiperglicemia pós-prandial. Clissod et al, Drugs 35:214-23 (1988). A diminuição na glicose pode ser mostrada através da diminuição dos níveis de HbA1c. Inibidores da alfa-glucisodase exemplares contemplados para uso na prática da presente invenção incluem acarbose, miglitol e semelhantes. Doses efetivas de ambos, acarbose e miglitol estão na variação de cercde 25 até 300 mg diários.
[00583]Inibidores alfa-glucosidase podem ser usados com polipeptídeos da presente invenção em combinação com sulfoniluréias. Inibidores da alfa-glucosidase em combinação com sulfoniluréias sozinhas tem mostrado diminuir os níveis de HbA1c geralmente, de cerca de 0,5 a 1,0%. Em adição, inibidores de alfa- glucosidase têm sido mostrado ser efetivos em reduzir o aumento pós-pradial na glicose sanguínea. Lefevre et al, Drugs 44:29-38 (1992).
[00584]Uma variedade de derivados do ácido benzóico podem ser usados com polipeptídeos da presente invenção para tratar e/ou prevenir diabetes. Esses agentes, também conhecidos como meglitinidas, são agentes hipoglicêmicos Não sulfoniluréia tendo capacidade secretória de insulina. Por exemplo, repaglinida parece ligar a canais de potássio sensíveis a ATP ou células beta-pancreáticas e assim aumentam a secreção de insulina. Derivados do ácido benzóico exemplares contemplados para uso na prática da presente invenção incluem repaglinida e semelhantes. Para repaglinida, a dose diária efetiva pode ser na variação de cerca de 0,5 mg até cerca de 16 mg, e o agente pode ser tomado antes de cada refeição.
[00585]Um número de agentes estão presentemente sob investigação como potencial anti-diabéticos em humanos. Qualquer de tais agentes pode ser usada com polipeptídeos da presente invenção para tratamento e/ou prevenção de distúrbios metabólicos, e em particular de diabetes, se eles se tornam disponíveis para uso terapêutico.
[00586]Outra categoria de agentes anti-diabéticos que é inibidora de carniti- na palmotoil-transferase I (CPT-I), tal como etomoxir, que em uma modalidade adici-onal da invenção pode ser usado com os polipeptídeos FGF-21 modificados para modular a glicose sanguínea. Etomoxir inibe irreversivelmente carnitina palmitoil- transferase I, que é necessária para oxidação de ácido graxo. Tal inibição pode re- duzir a hiperglicemia de jejum, porque produtos de oxidação de ácido graxo estimulam gliconeogênese hepática. Etomoxir pode melhorar a sensibilidade de insulina em diabetes do Tipo 2. Hubinger et al, Hormone Metab. Res. 24:115-18 (1992).
[00587]Outros agentes anti-diabéticos conhecidos incluem preparações de insulina (por exemplo, preparações de insulina animal extraída de pâncreas de boi e porco; preparações de insulina humana geneticamente sintetizada usando Escheri-chia coli, levedura; insulina com zinco; insulina protamina com zinco; fragmento ou derivado de insulina (por exemplo, INS-1), preparação oral de insulina), sensibiliza- dores de insulina (por exemplo, pioglitazona ou um sal do mesmo (preferivelmente cloridrato), rosiglitazona ou um sal do mesmo (preferivelmente maleato), Netoglita- zona, Rivoglitazona (CS-011), FK-614, o composto descrito em WO01/38325, Tesa- glitazar (AZ-242), Ragaglitazar (N,N-622), Muraglitazar (BMS-298585), Edaglitazona (BM-13-1258), Metaglidasen (MBX-102), Naveglitazar (LY-519818), MX-6054, LY- 510929, AMG-131 (T-131), THR-0921), inibidores da α-glucosidase (por exemplo, voglibose, acarbose, miglitol, emiglitato etc), biguanidas (por exemplo, fenformina, metformina, buformina ou sais dos mesmos (por exemplo, cloridrato, fumarato, suc- cinato)), secretagoges de insulina [sulfoniluréia (por exemplo, tolbutaminda, gliben- clamida, gliclazida, clorpropamida, tolazamida, acetoexamida, glicopiramida, glimepi- rida, glipizida, glubuzol), repaglinida, nateglinida, mitiglinida ou hidrato de sal de cál-cio dos mesmos], inibidores da dipeptidil peptidase IV (por exemplo, Vidagliptin (LAF237), P32/98, Sitagliptin (MK-431), P93/01, PT-100, Saxagliptin (BMS-477118), T-6666, TS-021), beta.3 agonistas (por exemplo, AJ-9677), agonistas GPR40, poli- peptídeos do tipo glucagon (I) (glp I), (glp2), ou outros hormônios peptídeos diabeto- gênicos, agonistas do receptor GLP-1 [por exemplo, GLP-1, agente GLP-1MR, N,N- 2211, AC-2993 (exendin-4), BIM-51077, Aib(8,35)hGLP-1 (7,37)NH.sub.2, CJC- [131], agonistas amilina (por exemplo, pramlintida), inibidores da fosfotirosina fosfa- tase (por exemplo, vanadato de sódio), inibidores gliconeogênese (por exemplo, inibidores da glicogênio fosforilase, inibidores da glicose-6-fosfatase, antagonista do glucagon), inibidores SGLUT (co-transportador de sódio-glicose) (por exemplo, T- 1095), inibidores da 11.beta-hidroxiesteróide deidrogenase (por exemplo, BVT- 3498), adiponectina ou agonistas dos mesmos, inibidores IKK (por exemplo, AS_2868), drogas que aumentam a resistência a leptina, agonistas do receptor de somatostatina (compostos descritos em WO01/25228, WO03/42204, WO98/44921, WO98/45285, WO99/2273.5 etc), atividores da glucoquinase (por exemplo, R.sup.o- 28-1675), GIP (peptídeo insulinotrópico dependente de glicose) e semelhantes podem ser mencionados.
[00588]O polipeptídeo FGF-21 compreendendo um aminoácido não natural, sozinho ou em combinação com outros componentes adequados, pode também ser feito em formulações aerossóis (isto é, eles podem ser “nebulizados”) para serem administradas através de inalação. Formulações aerossóis podem ser colocadas em propulsores pressurizados aceitáveis, tais como diclorodifluormetano, propano, ni-trogênio e semelhantes.
[00589]Formulações adequadas para administração parenteral, tais como, por exemplo, por vias intraarticular (nas juntas), intravenosa, intramuscular, intra- dérmica, intraperitoneal, e subcutânea, incluem soluções de injeção estéril isotônica aquosa e não aquosa, que podem conter antioxidantes, tampões, bacteriostáticos e solutos que rendem a formulação isotônica com o sangue do recipiente tencionado, e suspensões estéreis aquosas e não aquosas que podem incluir agentes suspenso- res, solubilizadores, agentes espessantes, estabilizadores, e conservantes. As for-mulações de FGF-21 podem ser apresentadas em dose única ou recipientes selados multi-doses, tais como ampolas e frascos.
[00590]Administração parenteral e administração intravenosa são métodos preferidos de administração. Em particular, as vias de administração já em uso para terapêuticos homólogos de aminoácidos naturais (incluindo mas não limitados a aqueles usados para EPO, GH, G-CSF, GM-GSF, IFNs, interleucinas, anticorpos, FGFs, e/ou qualquer proteína farmaceuticamente distribuída), junto com formulações no uso corrente, prove vias preferidas de administração e formulação para os poli- peptídeos da invenção.
[00591]A dose administrada a um paciente, no contexto da presente invenção, é suficiente ter uma resposta terapêutica benéfica no paciente ao longo do tempo, ou outra atividade apropriada, dependendo da aplicação. A dose é determinada pela eficácia do vetor particular, ou formulação, e a atividade, estabilidade ou meia vida sérica do aminoácido não natural com polipeptídeo empregado e a condição do paciente, bem como o peso do corpo ou área de superfície do paciente a ser tratado. O tamanho da dose é também determinado pela existência, natureza e extensão de qualquer efeito adverso que acompanha a administração de um vetor particular, for-mulação ou semelhantes em um paciente particular.
[00592]Determinando a quantidade efetiva do vetor ou formulação a ser ad-ministrada no tratamento ou profilaxia da doença (incluindo mas não limitada a cân-ceres, doenças inerentes, diabetes, AIDS, ou semelhantes), o médico avalia os níveis plasmáticos circulantes, toxidez da formulação, progressão da doença, e/ou onde relevante, a produção de anticorpos para aminoácido não-natural de polipeptídeo.
[00593]A dose administrada, por exemplo, a um paciente de 70 quilogramas, é tipicamente na variação equivalente a doses de proteínas terapêuticas correntemente usadas, ajustadas para a atividade alterada ou meia vida sérica da composição relevante. Os vetores ou formulações farmacêuticas desta invenção podem su-plementar as condições de tratamento por qualquer terapia convencional conhecida, incluindo a administração do anticorpo, administração de vacina, administração de agentes citotóxicos, aminoácido natural de polipeptídeos, ácidos nucléicos, nucleotí- deos análogos, modificadores da resposta biológica e semelhantes.
[00594]Para administração, formulações da presente invenção são adminis-tradas em uma taxa determinada por DL-50 ou DE-50 da formulação relevante, e/ou observação de qualquer efeito colateral dos aminoácidos não naturais de polipeptí- deos em várias concentrações, incluindo, mas não limitados a, como aplicado para a massa e saúde geral do paciente. Administração pode ser realizada através d doses únicas ou divididas.
[00595]Se um paciente passando por infusão de uma formulação desenvol- ve febre, calafrios, ou dores musculares, ele/ela recebe a dose apropriada de aspirina, ibuprofeno, acetaminofeno, ou outra droga controlando dor/febre. Pacientes que reagem a experiência para infusão tais como febre, dores musculares e calafrios são pré-medicados 30 minutos antes das infusões futuras com ou aspirina, acetaminofe- no, ou incluindo, mas não limitados a difenidramina. Meperidina é usada para cala-frios mais severas e dores musculares que não respondem rapidamente a antipiréticos e anti-histamínicos. Infusão celular é diminuída ou descontinuada dependendo da severidade da reação.
[00596]Polipeptídeos FGF-21 humanos da invenção podem ser administrados diretamente a um paciente mamífero. Administração é por qualquer via normalmente usada para introduzir polipeptídeo FGF-21 a um paciente. As composições polipeptídicas FGF-21 de acordo com as modalidades da presente invenção incluem aquelas para oral, retal, tópica, inalação (incluindo mas não limitado a, através de um aerosol), bucal (incluindo mas não limitado, sub-lingual), vaginal, parenteral (in-cluindo mas não limitado a, subcutâneo, intramuscular, intradérmico, intraarticular, intrapleural, intraperitoneal, intracerebral, intraarterial ou intravenosa), tópica (isto é, ambas superfícies da pele e mucosa, incluindo superfícies das vias aéreas) e admi-nistração transdérmica, embora a via mais adequado em qualquer dado caso de-penderá da natureza e severidade da condição sendo tratada. Administração pode ser ou local ou sistêmica. As formulações de compostos podem ser apresentadas em recipientes selados de dose única ou doses múltiplas, tais como ampolas ou frascos. Polipeptídeos FGF-21 da invenção podem ser preparados em uma mistura em uma forma injetável de dose única (incluindo, mas não limitado a solução, suspensão ou emulsão) com um veículo farmaceuticamente aceitável. Polipeptídeos FGF-21 da invenção podem também ser administrados por infusão contínua (usando, incluindo, mas não limitado a, mini-bombas tal como bombas osmóticas), bolo único ou formulações depósito de liberação lenta.
[00597]Formulações adequadas para administração incluem soluções aquo-sas e não aquosas, soluções estéreis isotônicas, que podem conter antioxidantes, tampões, bacteristáticos, e solutos que rendem a formulação isotônica, e suspensões estéreis aquosas e não aquosas que podem incluir agentes de suspensão, so- lubilizadores, agentes espessantes, estabilizadores, e conservantes. Soluções e suspensões podem ser preparadas a partir de pós estéreis, grânulos, e comprimidos do tipo previamente descrito.
[00598]Congelamento-secagem é uma técnica comumente empregada para apresentar proteínas que servem para remover água a partir da preparação de proteína de interesse. Congelamento-secagem, ou liofilização, é um processo pelo qual o material a ser seco é primeiro congelado e então o gelo ou solvente congelado é removido pela sublimação em um ambiente a vácuo. Um excipiente pode ser incluído em formulações pré-liofilizadas para aumentar a estabilidade durante o processo de congelamento-secagem e/ou para melhorar a estabilidade do produto liofilizado sob estoque. Pikal, M. Biopharm. 3(9)26-30 (199) e Arakawa et al. Pharm. Res. 8(30:285-291 (1991).
[00599]A pulverização e secagem de farmacêuticos são também conhecidas pelos versados na técnica. Por exemplo, ver, Broadhead, J. et al., “The Spray Drying of Pharmaceuticals:, em Drug Dev. Ind. Pharm., 18(11 & 12), 1169-1206 (1992). Em adição a pequenas moléculas farmacêuticas, uma variedade de materiais biológicos tem sido congelado e secos e essas incluem, enzimas, soros, plasma, microrganismos e leveduras. Pulverização e secagem é uma técnica útil porque ela pode converter uma preparação líquida farmacêutica em um pó fino, sempoeria ou pó aglomerado em um processo de um passo. A técnica básica compreende os seguintes quatro passos: a) atomização da solução de alimentação em um pulverizador; b) contato pulverizador-ar; c) secagem do pulverizador; e d) separação do produto seco a partir do ar seco. Patente dos EUA Nos. 6.235.710 e 6.001.800, que são aqui incorporados por referência, descrevem a preparação de eritropoietina recombinante por pulverização e secagem.
[00600]As composições farmacêuticas e formulações da invenção podem compreendem um veículo, excipiente ou estabilizador farmaceuticamente aceitável. Veículos farmaceuticamente aceitáveis são determinados em parte pela composição particular sendo administrada, bem como pelo método particular usado para admi-nistrar a composição. Consequentemente existe uma variedade ampla de formulações adequadas de composições farmacêuticas (incluindo veículos opcionais farma- ceuticamente aceitáveis) da presente invenção (ver, por exemplo, Remington’s Pharmaceutical Sciences, 17a ed. 1985)).
[00601]Veículos adequados incluem mas não são limitados a tampões con-tendo succinato, fosfato, borato, HEPES, citrato, histidina, imidazol, acetato, bicar-bonato, e outros ácidos orgânicos; antioxidantes incluindo mas não limitados a ácido ascórbico; polipeptídeos de baixo peso molecular incluindo mas não limitados àqueles de menos que 10 resíduos; proteínas, incluindo mas não limitados a albumina sérica, gelatina, ou imunoglobulinas; polímeros hidrofílicos incluindo mas não limitado a polivinilpirrolidona; aminoácidos incluindo mas não limitados a glicina, glutama- to, asparagina, arginina, histidina ou derivados histidina, metionina, glutamato, ou lisina; monossacarídeos, dissacarídeos, e outros carboidratos, incluindo mas não limitados a trealose, sacarose, glicose, manose, ou dextrinas; agentes quelantes incluindo mas não limitados a, EDTA e edentato disódico; íons metais divalentes incluindo mas não limitados a zinco, cobalto, ou cobre; álcool açúcar incluindo mas não limitado a manitol ou sorbitol; contra-íons formando sal mas não limitado a sódio e cloreto de sódio; e/ou tensoativos não iônicos incluindo mas não limitados a Tween® (incluindo, mas não limitado a, Tween 80 (polisorbato 80) e Tween 20 (polisorbato 20). Pluronics® e outros ácidos pulrônicos, incluindo, mas não limitados a outros ácidos plurônicos, incluindo, mas não limitados a ácido plurônico F68 (poloxâmero 188), ou PEG. Tensoativos adequados incluem, por exemplo, mas não limitado a poliéteres baseados sob poli(óxido etileno)-poli(óxido propileno)-poli(óxido etileno), isto é, (PEO-PPO-PEO), ou poli(óxido propileno)-poli(óxido etileno)-poli(óxido propi- leno), isto é, (PPO-PEO-PPO), ou uma combinação dos mesmos. PEO-PPO-PEO e PPO-PEO-PPO são comercialmente disponíveis sob as marcas registradas Pluro- nics®, R-Pluronics®, Tetronics® e R-Tetronics® (BASF Wyandotte Corp., Wyandot te, Mich) e são ainda descritos na Pat. dos EUA No. 4.820.352 aqui incorporadas em sua totalidade por referência. Outros polímeros bloqueadores etileno/polipropileno podem ser tensoativos adequados. Um tensoativo ou uma combinação de tensoati- vos podem ser usados para estabilizar FGF-21 Pegilado contra um ou mais estresses incluindo, mas não limitados para estresse que resultam a partir de agitação. Alguns dos acima podem ser referidos como “agentes de enchimento”. Alguns podem também ser referidos como “modificadores de tonicidade”. Conservantes anti- microbianos podem também ser aplicados para estabilidade de produto e efetividade de antimicrobiano; conservantes adequados incluem, mas não são limitados a, álcool benzílico, cloreto de benzalcônio, metacresol, metil/propil parabeno, cresol, e fe- nol, ou uma combinação dos mesmos.
[00602]Polipeptídeos FGF-21 da invenção, incluindo aqueles ligados a polí-meros solúveis em água, tal como PEG, pode também ser administrado por ou como parte de sistemas de liberação adequada. Composições de liberação adequadas incluem, incluindo mas não limitada a, matrizes de polímero semi-permeável na forma de artigos moldados, incluindo mas não limitados a, filmes, ou microcápsulas. Matrizes de liberação adequadas incluem a partir de materiais biocompatíveis tais como poli(2-hidroxietilmetacrilato) (Langer et al, J. Biomed. Mater. Res. 15:267-277) (1981); Langer, Chem. Tech. 12:98-105 (1982), vinil acetato de etileno (Langer et al, acima) ou ácido poli-D-(-)-3-hidroxibutírico (EP 133.988), polilactídeos (ácido poliláti- co) (Patente dos EUA No. 3.773.919; EP 58.481), poliglicolídeo (polímero de ácido glicólico), polilactídeo co-glicolídeo (copolímeros de ácido lático e ácido glicolítico) polianidretos, copolímeros de ácido L-glutâmico e gama-etil-L-glutamato (Sidman et al, Biopolymers, 22, 547-556 (1983), poli(orto)ésteres, polipeptídeos, ácido hialurôni- co, colágeno, sulfato de condroitina, ácidos carboxílicos, ácidos graxos, fosfolipí- deos, polissacarídeos, ácidos nucléicos, ácidos poliamino, aminoácidos tais como fenilalanina, tirosona, isoleucina, polinucleotídeos, polivinil propileno, polivinilpirroli- dina e silicone. Composições de liberação controlada também incluem um composto contido em lipossoma. Lipossomas contendo o composto são preparados pelos mé- todos conhecidos por si: DE 3.218.121; Eppstein et al, Proc. Natl. Acad. Sci. EUA, 82: 3688-3692 (1985); Hwang et al, Proc. Natl. Acad. Sci. EUA, 77: 4030-4034 (1980); EP 52.322; EP 36.676; Patente dos EUA No. 4.619.794; EP 143.949; Patente dos EUA No. 5.021.234; Pedido de Pat. Japonesa 83-118008; Pat. dos EUA Nos. 4.485.045 e 44.544.545; e EP 102.324. Todas as referências e patentes citadas são aqui incorporadas por referência.
[00603]Polipeptídeos FGF-21 contidos em lipossomas podem ser preparados pelos métodos descritos em, por exemplo, DE 3.218.121; Eppstein et al, Proc. Natl. Acad. Sci. EUA, 82: 3688-3692 (1985); Hwang et al, Proc. Natl. Acad. Sci. EUA, 77: 4030-4034 (1980); EP 52.322; EP 36.676; Patente dos EUA No. 4.619.794; EP 143.949; Patente dos EUA No. 5.021.234; Pedido de Pat. Japonesa 83-118008; Pat. dos EUA Nos. 4.485.045 e 44.544.545; e EP 102.324. Composição e tamanho de lipossomas são bem conhecidos ou capazes de ser facilmente determinado empiri-camente por um versado na técnica. Alguns exemplos de lipossomas como descritos em, por exemplo, Park JW, et al, Proc. Natl. Acad. Sci. EUA 92:1327-1331 (1995); Lasic D e Papahadjopoulos D (eds): MEDICAL APPLICATIONS OF LIPOSOMES (1998); Drummond DC, et al, Liposomal drug delivery systems for cancer therapy, em Teicher B (ed): CANCER DRUG DISCOVERY AND DEVELOPMENT (2002); Park JW, et al, Clin. Cancer Res. 8:1172-1181 (2002); Nielsen, UB, et al, Biochem. Biophys. Acta 1591 (1-3):109-118 (2002); Mamot C, et al, Cncer Res. 63:3154-3161 (2003). Todas referências e patentes citadas são aqui incorporados em referência.
[00604]Essa dose administrada a um paciente no contexto da presente in-venção deve ser suficiente para causar uma resposta benéfica no paciente ao longo do tempo. Geralmente, a quantidade farmaceuticamente efetiva total do polipeptídeo FGF-21 da presente invenção administrada parenteralmente por dose na variação de cerca de 0,01 μg/kg/dia a cerca de 100 μg/kg, ou cerca de 0,05 mg/kg a cerca de 1 mg/kg, do peso do corpo do paciente, embora este é sujeito para discrição terapêutica. A frequência de dose é também sujeita a discrição terapêutica, e pode ser mais frequente ou menos frequente que o produto do polipeptídeo FGF-21 comerci- almente disponível aprovado para uso em humanos. Geralmente, um polipeptídeo FGF-21 PEGilado da invenção pode ser administrado por qualquer das vias de ad-ministração descrita acima.
[00605]Em algumas modalidades, polipeptídeos FGF-21 modificados da presente invenção modulam o efeito de um agente anti-diabético. Em outra modali-dade da presente invenção, polipeptídeos FGF-21 modificado podem ser co- administrados com um agente anti-diabético. Em outra modalidade da presente in-venção, polipeptídeos FGF-21 modificados podem ser administrados antes do trata-mento com agente anti-diabético. Em outra modalidade da presente invenção, poli- peptídeos FGF-21 modificados podem ser administrados seguindo o tratamento com um agente anti-diabético. Em outra modalidade da presente invenção, polipeptídeos FGF-21 modificados são co-administrados com metformina. Em outra modalidade da presente invenção, tratamento terapêutico com polipeptídeos FGF-21 da invenção e metformina aumenta a habilidade de metformina para modular glicose plasmática, em presença ou ausência de insulina. Em terapia de combinação, metformina tem sido usada com sulfoniluréia, inibidores de alfa-glucosidase, troglitazeon, e insulina. Metformina combinada com uma sulfoniluréia aumenta a sensibilidade a insulina e podem diminuir a glicose plasmática. Alternativamente, metformina com repaglinida podem ser mais efetivas que glipizida, e pelo menos tão efetiva como gliburida, em manter o controle glicêmico ao longo de muitos meses. Metformina com troglitazona melhora o controle da glicose em excesso do agente sozinho. Inzucchi et al, New Eng. J. Med. 338:867-72 (1998). Em algumas modalidades, os polipeptídeos FGF-21 da presente invenção são co-administrados com Klotho beta. Em algumas modalidades, os polipeptídeos FGF-21 da presente invenção são co-administrados com Klotho beta que inclui um ou mais aminoácidos não naturalmente codificados. Em algumas modalidades, os polipeptídeos FGF-21 da presente invenção são co- administrados com Klotho beta e um agente anti-diabético. Em algumas modalidades, os polipeptídeos FGF-21 da presente invenção são co-administrados com um agente anti-diabético. Em algumas modalidades, polipeptídeos FGF-21 da presente invenção são utilizadas em combinação com um ou mais dos seguintes: Taurina, Ácido Alfa Lipóico, um extrado de Mulberry, Crômio, Glutamina, Enicostemma littora- le Blume, Scoparia dulcis, um extrato de Tarragon e Andrographis paniculata. Em algumas modalidades, polipeptídeos FGF-21 da presente invenção são utilizadas em combinação com um ou mais dos seguintes: preparações de insulina (por exemplo, extratos de preparações de insulina animal a partir de pâncreas de boi e porco; pre-parações de insulina humana geneticamente usando Escherichia coli, levedura; in-sulina com zinco; protamina insulina com zinco; fragmento ou derivados de insulina (por exemplo, INS-1), preparação de insulina oral), sensibilizadores de insulina (por exemplo, pioglitazina ou um sal do mesmo (preferivelmente cloridrato), rosiglitazina ou um sal do mesmo (preferivelmente maleato), Netoglitazona, Rivoglitazina (CS- 011), FK-614, o composto descrito em WO01/38325, Tesaglitazar (AZ-242), Ragagli- tazar (N,N-622), Muraglitazar (BMS-298585), Edaglitazona (BM-13-1258), Metagli- dasen (MBX-102), Naveglitazar (LY-519818), MX-6054, LY-510929, AMG-131 (T- 131), THR-0921), inibidores da α-glucosidase (por exemplo, voglibose, acarbose, miglitol, emiglitato etc), biguanidas (por exemplo, fenformina, metformina, buformina ou um sal dos mesmos (por exemplo, cloridrato, fumarato, succinato)), secretagoges de insulina [sulfonuliréia (por exemplo, tolbutamida, glibenclamida, gliclazida, clor- propamida, tolazamida, acetoexamida, glicopiramida, glimepirida, glipizida, glibuzol), repaglinida, nateglinida, mitiglinida ou hidrato de sal de cálcio dos mesmos], inibidores da dipeptidil peptidase IV (por exemplo, Vidagliptin (LAF237), P32/98, Sitagliptin (MK-431), P93/01, PT-100, Saxagliptin (BMS-477118), T-6666, TS-021), beta.3 ago- nistas (por exemplo, AJ-9677), agonistas GPR40, polipeptídeos do tipo glucagon (I) (glp I), (glp2), ou outros hormônios peptídeos diabetogênicos, agonistas do receptor GLP-1 [por exemplo, GLP-1, agente GLP-1MR, N,N-2211, AC-2993 (exendin-4), BIM-51077, Aib(8,35)hGLP-1 (7,37)NH.sub.2, CJC-[131], agonistas amilina (por exemplo, pramlintida), inibidores da fosfotirosina fosfatase (por exemplo, vanadato de sódio), inibidores gliconeogênese (por exemplo, inibidores da glicogênio fosforila- se, inibidores da glicose-6-fosfatase, antagonista do glucagon), inibidores SGLUT (co-transportador de sódio-glicose) (por exemplo, T-1095), inibidores da 11.beta- hidroxiesteróide deidrogenase (por exemplo, BVT-3498), adiponectina ou agonistas dos mesmos, inibidores IKK (por exemplo, AS-2868), drogas que aumentam a resis-tência a leptina, agonistas do receptor de somatostatina (compostos descritos em WO01/25228, WO03/42204, WO98/44921, WO98/45285, WO99/2273.5 etc), ativido- res da glucoquinase (por exemplo, R.sup.o-28-1675), GIP (peptídeo insulinotrópico dependente de glicose).
[00606]Em algumas modalidades, polipeptídeos da presente invenção são utilizadas em combinação com potenciadores de insulina tais como, incluindo, mas não limitado a, Taurina, Ácido Alfa Lipóico, um extrado de Mulberry, Crômio, Gluta- mina, Enicostemma littorale Blume, Scoparia dulcis, um extrato de Tarragon e An- drographis paniculata. Em outra modalidade, a presente invenção pode compreender um ou mais de Isomalt, Trealose ou D-Manose para ainda potenciar a secreção ou atividade de insulina. Em uma modalidade adicional, o potenciador de insulina e polipeptídeos da presente invenção são usado em adição a outro agente anti- diabético.
[00607]Uma forma em que a eficácia terapêutica dos polipeptídeos e terapias combinadas incluindo os polipeptídeos da presente invenção pode ser determinado é através da redução nos níveis de HbA1c do paciente. Em uma modalidade, polipeptídeos da presente invenção diminui os níveis de HbA1c por pelo menos 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 25%, 30%, 35%, 40%, 45%, 50% ou pelo menos 50% de mudança a partir dos níveis HbA1c dois meses antes da terapia começar com polipeptídeos FGF-21 modificados, a partir de três meses antes do início da terapia com polipeptí- deos FGF-21, ou por mudanças de porcentagem a partir da linha de base. Em outra modalidade, polipeptídeos da presente invenção administrados a um paciente também sendo tratados com um agente anti-diabético modula a habilidade do agente anti-diabético para diminuir a glicose sanguínea. Em outra modalidade, polipeptídeos da presente invenção administrados a um paciente também sendo tratados com um agente anti-diabético níveis inferiores de HbA1c por pelo menos 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 25%, 30%, 35%, 40%, 45%, 50% ou pelo menos 50% de mudança a partir dos níveis HbA1c dois meses antes da terapia começar com polipeptídeos FGF-21 modificados, a partir de três meses antes do início da terapia com polipeptídeos FGF-21, ou por mudanças de porcentagem a partir da linha de base.
[00608]Em outra modalidade, polipeptídeos FGF-21 modificados da presente invenção modulam a habilidade de Troglitazona diminuir requerimentos de insulina. Em outra modalidade, modalidade adicional, polipeptídeos FGF-21 modificados da presente invenção quando administrados a um paciente sendo tratados com Trogli- tazona ainda diminuem os requerimentos de insulina do referido paciente. Troglita- zona usada em combinação com a presente invenção pode ser usada para atrasar ou prevenir diabetes do Tipo 2 em certas modalidades da presente invenção.
[00609]Em uma modalidade da presente invenção, polipeptídeos FGF-21 modificados são co-administrados com uma sulfoniluréia. Em outra modalidade da presente invenção, polipeptídeos FGF-21 modificados são administrados antes do tratamento com sulfoniluréia. Em outra modalidade da presente invenção, polipeptí- deos FGF-21 são administrados após o tratamento com uma sulfoniluréia. Em algu-mas modalidades da presente invenção, tratamento com uma dose terapêutica de polipeptídicos FGF-21 modicados modulam glicose sérica. Em outra modalidade, polipeptídeos FGF-21 da presente invenção são administrados com Klotho beta que modula os efeitos dos polipeptídeos na glicose sanguínea. Em outra modalidade, polipeptídeos FGF-21 da presente invenção são administrados com Klotho beta que diminui a glicose sanguínea mais que o uso dos polipeptídeos FGF-21 modificados sozinhos. Em outra modalidade, essas mudanças são medidas usando testes HbA1c. Em outra modalidade, polipeptídeos FGF-21 da presente invenção e Klotho beta são administrados e um paciente sendo tratados com um agente anti-diabético que diminui glicose sanguínea mais que uso de agente anti-diabético sozinho. XV. Usos Terapêuticos de Polipeptídeos FGF-21 da Invenção
[00610]Os polipeptídeos FGF-21 da invenção são úteis para tratar uma ampla variedade de distúrbios.
[00611]Polipeptídeos FGF-21 da invenção podem ser usados para tratar mamíferos sofrendo de Diabetes Mellitus não dependente de insulina (DMNDI: Tipo 2), diabetes dependente de insulina (Tipo 1), bem como obesidade, depuração de glicose inadequada, hiperglicemia, hiperinsulinemia, e qualquer outra doença ou condição que pode ser mediada por FGF-21. Intolerância a glicose pode ser definida como uma sensibilidade excepcional a glicose. Hiperglicemia é definida como um excesso de açúcar (glicose) no sangue. Hiperinsulinemia é definida como um nível mais alto que o normal de insulina no sangue. Resistência a insulina é definida como um estado em que uma quantidade normal de insulina produz uma resposta biológica subnormal. Obesidade, em termos de paciente humano, pode ser definida como peso corporal de 20% acima do peso corporal ideal para uma dada população (R.H. Williams, Livro Texto de Endocrinologia, 1974, p. 904-916).
[00612]Diabetes mellitus é caracterizada em dois amplos grupos baseados em manifestações clínicas, denominados, a forma não dependente de insulina ou forma inicial na maturidade, também conhecida como tipo 2; e a dependente de insulina ou forma de início na juventude, também conhecido com o tipo 1. clinicamente, a maioria do tipo 2, diabéticos de início na maturidade são obesos, com manifestações de sintomas clínicos da doença usualmente aparecendo em uma idade acima dos 40. em contraste, tipo 1, pacientes de início na juventude não são estão além do peso relativo a sua idade e altura, com rápido início da doença em uma idade precoce, sempre antes dos 30, embora a diabetes do tipo 1 pode ocorrer em qualquer idade.
[00613]diabetes mellitus e um distúrbio metabólico em humanos com uma prevalência de aproximadamente m porcento na população geral, com um quarto desses sendo o tipo 1 (foster, d.w., harrison’s principles if internal medicine, cap. 114, pp. 661-678, 10a ed., mcgraw-hill, nova iorque). A doença manifesta sozinha como uma série de anormalidades metabólicas induzidas por hormônio que eventu- almente levam a complicações sérias, de longo termo e debilitantes, envolvendo vá-rios sistemas de órgãos incluindo olhos, rins, nervos e vasos sanguíneos. patologi-camente, a doença é caracterizada por lesões de base em membranas, demonstrável sob microscopia eletrônica.
[00614]Diabetes mellitus não dependente de insulina (DMNDI: Tipo 2) é uma doença debilitante caracterizada por altos níveis de glicose, insulina e corticosterói- des circulante no sangue. A incidência de diabetes do Tipo 2 é alta e aumentado e está se tornando uma causa líder de mortalidade, morbidade e gasto em cuidado da saúde através do mundo (Amos et al, Diabetic Med. 14:S1-85, 1997).
[00615]As causas da diabetes do Tipo 2 não são bem entendidos. Diabetes do Tipo 2 é caracterizada pelo excesso de produção de glicose em despeito da viabilidade de insulina, e níveis circulantes de glicose permanecem excessivamente altos como um resultado da depuração de glicose inadequada. É pensado que ambas, resistência de tecidos alvos à ação de insulina e diminuição da secreção de insulina (“falência de célula β”) ocorrem. Tecidos responsivos a insulina principais para homeostase de glicose são fígado, em que insulina estimula a síntese de glicogênio e inibe a gliconeogênese; músculo, em que insulina estimula síntese de glicogênio e inibe a gliconeogênese; músculo, em que a insulina estimula captação de glicose e glicogênio estimula a captação de glicose e inibe a lipólise. Então, como uma conse-quência da condição diabética, existem elevados níveis de glicose no sangue, e pro-longado alto açúcar sanguíneo é indicativo de uma condição que causará vaso san-guíneo e dano nervoso.
[00616]Correntemente, existem várias abordagens farmacológicas para o tratamento da diabetes do Tipo 2 (Scheen et al, Diabetes Care, 22(9):1568-1577, 1999). Eles atuam através de diferentes formas de ação: 1) sulfoniluréias essencial-mente estimulam a secreção de insulina; 2) biguanidas (metformina) atuam promo-vendo a utilização de glicose, reduzindo a produção de glicose hepática e diminuindo a saída de glicose intestinal; 3) inibidores da α-glucosidase (acarbose, miglitol) diminui a digestão de carboidrato e consequentemente a absorção intestinal e reduz a hiperglicemia pós-prandial; 4) tiazol-idinadionas (triglitazona) aumenta a ação de insulina, então, promovendo a utilização de glicose nos tecidos periféricos; e 5) insu-lina estimula utilização de glicose tecidual e inibe a saída da glicose hepática. As abordagens farmacológicas mencionadas podem ser usadas individualmente ou em combinação de terapia. Entretanto, cada abordagem tem suas limitações e efeitos adversos.
[00617]Obesidade é uma doença crônica que é altamente prevalente na so-ciedade moderna e está associada não somente com um estigma social, mas também com amplitude de vida diminuída e numerosos problemas médicos, incluindo desenvolvimento de psicológico adverso, distúrbios dermatológicos, tais como, in-fecções, variconse venosa, tolerância a exercício, diabetes mellitus, resistência a insulina, hipertensão, hipercolesterolemia, e doença coronária cardíaca. Rissanen et al, British Medical Journal, 301:835-837 (1990).
[00618]Terapias existentes para obesidade incluem dietas padrões e exercí-cios, dietas de muito baixas calorias, terapia comportamental, farmacoterapia envol-vendo supressores de apetite, drogas termogênicas, inibidores de absorção de co-mida, dispositivos mecânicos tais como conexão de maxilar, cintura de cordas e ba-lões, cirurgia. Jung e Chong, Clinical Endocrinology, 35:11-20 (1991); Bray, Am. J. Clin. Nutr. 55:528S-544S (1992).
[00619]Considerando a alta prevalência de obesidade em nossa sociedade e as sérias consequências associadas a mesma, qualquer droga terapêutica potenci-almente útil na redução de peso de pessoas obesas podem ter um profundo efeito benéfico em sua saúde. Existe uma necessidade na técnica para uma droga que reduzirá o peso corporal total de pacientes obesos para seu peso ideal sem efeitos adversos significante e que ajudarão o paciente obeso a manter o nível de redução de peso.
[00620]É assim desejável prover um regime de tratamento que é útil em re-tornar o peso corpóreo de pacientes obesos ao normal, peso corpóreo ideal. É ainda desejável prover uma terapia para obesidade que resulte em manutenção do peso corpóreo diminuído por um período de tempo estendido.
[00621]Obesidade é altamente correlacionada com resistência a insulina e diabetes em animais experimentais e humanos. De fato, a obesidade e resistência a insulina, a última é geralmente acompanhada por hiperinsulinemia ou hiperglicemia, ou ambos, são marcadores da diabetes do Tipo 2. Em adição, diabetes do Tipo 2 é associada com um risco dobrado ou quadruplicado de doença arterial coronária. Apesar das décadas de pesquisa nesses sérios problemas de saúde, a etiologia da obesidade e resistência a insulina é desconhecida.
[00622]Diabéticos do Tipo 1 caracteristicamente mostram muito baixa ou imensurável insulina plasmática com elevado glucagon. A despeito da exata etiologia, a maioria dos pacientes do Tipo 1 tem anticorpos circulantes direcionados contra suas células pancreáticas incluindo anticorpos para insulina, às células citoplasmáti- cas da ilhota de Langerhans e à enzima ácido glutâmico descarboxilase. Uma resposta imune especificamente direcionada contra células beta (células produtoras de insulina) leva a diabetes do Tipo 1. Esta especificidade é suportada pela figura clínica acima, desde que células beta secreta, insulina enquanto células alfa secretam glucagon.
[00623]Regimes terapêuticos correntes para diabetes do Tipo 1 incluem mo-dificações na dieta a fim de minimizar a hiperglicemia resultante da ausência de in-sulina natural, que por sua vez, é o resultado de células beta danificadas. Dieta é também modificada com respeito a administração de insulina para conter os efeitos hipoglicêmicos do hormônio. Qualquer que seja a forma de tratamento, administração parenteral de insulina é requerida para todos os diabéticos do Tipo 1, daí o termo diabetes “insulino-dependente”.
[00624]Então, existe uma necessidade para uma terapia efetiva de diabetes do Tipo 2 que tem poucos efeitos adversos que as abordagens farmacêuticas dispo-níveis. Além disso, uma terapia alternativa efetiva para insulina pode ser útil para o tratamento do diabetes do Tipo 1. A presente invenção provê uma terapia farmaco-lógica que estimula a captação de glicose e aumenta a sensibilidade à insulina nos tecido periféricos e tem menor efeitos adversos que os regimes de tratamento cor-rentes para o diabetes Tipo 2. Em adição, a presente invenção provê um tratamento alternativo para diabetes do Tipo 1. Além disso, a presente invenção é útil para tratar a obesidade por aumento do gasto de energia por utilização mais rápida e mais eficiente da glicose.
[00625]A presente invenção provê um método para tratar um mamífero exi-bindo um ou mais de diabetes Tipo 1, diabetes Tipo 2, obesidade, resistência a insu-lina, hiperinsulinemia, intolerância a glicose, ou hiperglicemina, compreendendo ad-ministração ao referido mamífero em necessidade de tal tratamento uma quantidade terapeuticamente efetiva do polipeptídeo FGF-21 da invenção.
[00626]O método de tratar pode ser suficiente para alcançar no referido mamífero pelo menos uma das seguintes modificações: redução do estoques de gordura do corpo, diminuição na resistência a insulina, redução de hiperinsulinemia, aumento na tolerância a glicose, e redução de hiperglicemia.
[00627]Em outro aspecto, a presente invenção relaciona-se a um método de tratar um animal doméstico incluindo, mas não limitado a gado, porcos, ovelhas, ca-valos, e semelhantes compreendendo a administração de uma quantidade efetiva do FGF-21 ou variante do mesmo, a fim de reduzir os estoques de gordura corpórea. A redução dos estoques de gordura corpórea em um longo termo, ou em base perma-nente em animais domésticos pode obviamente ser de considerável benefício eco-nômico ao homem, particularmente desde que os animais suprem a principal porção da dieta do homem; e o animal gordo pode terminar como depósitos novos de gordura no homem.
[00628]Fatore de crescimento de fibroblasto 21 (FGF-21) pode ser usado para reduzir a morbidade e mortalidade associada com pacientes criticamente doentes. Ver Publicação da Patente dos EUA No. 20050176631 que é aqui incorporada por referência em sua totalidade. Pacientes criticamente doentes requerem cuidado in-tensivo por um período de tempo extenso tendo um alto risco de morte e substancial mortalidade. Uma causa comum para admissão de pacientes em unidades de cuida- do intensivo (UCIs) é a síndrome de resposta inflamatória sistêmica (SRISs) associada com insultos infecciosos (sepse) bem como causas patológicas não infecciosas tais como pancreatite, isquemia, trauma múltiplo e injúria tissular, choque hemorrágico, e injúria de órgão mediada por imunidade. A presente invenção também compreende um método de redução da mortalidade e morbidade em pacientes criticamente doentes sofrendo de síndrome de resposta inflamatória sistêmica (SRIS) associada com insultos infecciosos, bem como causas patológicas não infecciosas que com-preendem administração a pacientes criticamente doentes de uma quantidade tera- peuticamente efetiva de FGF-21. Exemplos de condições que envolvem SRIS incluem sepse, pancreatite, isquemia, trauma múltiplo e injúria tissular, choque hemorrágico, injúria de órgão mediada por imunidade, síndrome de estresse respiratório agudo (SERA), choque, falência renal, e síndrome da disfunção múltipla dos órgãos (SDMO). A presente invenção também compreende um método para reduzir a mortalidade e morbidade em pacientes criticamente doentes sofrendo de estresse respiratório.
[00629]Uma complicação frequente de SRIS é o desenvolvimento de disfun-ção sistêmica do órgão incluindo síndrome de estresse respiratório agudo (SERA), choque, falência renal, e síndrome da disfunção múltipla dos órgãos (SDMO), todas as quais amplificam o risco de um final adverso. Enquanto muitos especialistas acreditam que alguns tipos de suporte nutricional sejam benéficos para pacientes criticamente doentes para ajudar a restaurar a estabilidade metabólica, os benefícios e especificidade de tal suporte permanecem controverso devido a ausência de testes clínicos aleatórios bem controlados.
[00630]Porque a hiperglicemia e resistência a insulina são comuns em paci-entes criticamente doentes dados o suporte nutricional, alguns UCIs administram insulina para tratar hiperglicemia excessiva na alimentação de pacientes criticamente doentes. De fato, estudos recentes documentam o uso de insulina exógena para manter a glicose sanguínea em um nível não muito mais alto que 110 mg por decilitro reduz a morbidade e mortalidade entre pacientes criticamente doentes na unida de de cuidado intensivo cirúrgico, a despeito se eles tiveram uma história de diabetes (Van der Bergue, et al, N. Engl. J. Med., 345(19):1359, 2001).
[00631]A presente invenção compreende um método para reduzir a mortali-dade e morbidade nesses pacientes criticamente doentes através da administração do FGF-21. Os pacientes criticamente doentes compreendidos pela presente invenção geralmente experimentam um estado hipermetabólico instável. Este estado metabólico instável é devido a mudanças no metabolismo do substrato que pode levar a deficiências relativas em alguns nutrientes. Geralmente existe uma oxidação aumen-tada de ambos, gordura e músculo.
[00632]Os pacientes criticamente doentes em que a administração do FGF- 21 pode reduzir o risco de mortalidade e morbidade são preferivelmente pacientes que experimentam síndrome de resposta inflamatória sistêmica ou estresse respiratório. Uma redução na morbidade significa redução da possibilidade que um paciente criticamente doente desenvolverá doenças adicionais, condições, ou sintomas ou redução da severidade de doenças adicionais, condições ou sintomas. Por exemplo, redução da morbidade por corresponder a uma diminuição na incidência de bacte-remia ou sepse ou complicações associadas com falência múltipla dos órgãos.
[00633]Síndrome de resposta inflamatória sistêmica (SRIS) descreve um processo inflamatório associado com um grande número de condições clínicas e inclui, mas não é limitado, a mais que uma das seguintes manifestações clínicas: (1) uma temperatura corporal maior que 38oC ou menor que 36oC; (2) uma taxa cardíaca maior que 90 batimentos por minuto; (3) taquipnéia, manifestada por uma taxa respiratória maior que 20 respirações pode minuto, ou hiperventilação, como indicado por um PaCo2 de menos que 32 m Hg; e (4) uma alteração da contagem de células brancas sanguíneas, tais como, uma contagem maior que 12000/cu mm, uma contagem de menos que 4000/ cu mm, ou a presença de mais que 10% de neutrófi- los imaturos. Essas mudanças fisiológicas devem representar uma alteração aguda a partir da linha base na ausência de outras causas conhecidas para tais anormali-dades, tais como quimioterapia, neutropenia induzida, e leucopenia.
[00634]Sepse é definida como um SRIS aumentado a partir de infecção. Causas patogênicas não infecciosas de SRIS podem incluir pancreatite, isquemia, trauma múltiplo e injúria tissular, incluindo, mas não limitado a injúrias de esmaga-mento ou queimaduras severas, choque hemorrágico, injúria de órgão mediada por imunidade, e administração exógena de tais mediadores pontuais do processo in-flamatório como fator de necrose tumoral e outras citocinas.
[00635]Choque séptico e disfunção em múltiplos órgãos são os principais contribuidores para a morbidade e mortalidade no ambiente UCI. Sepse é associada com e mediada pela ativação de um número de mecanismos de defesa do hospedeiro incluindo a rede de citocinas, leucócitos, e cascata de complemento, e sistemas de coagulação/fibrinólise incluindo o endotélio. Coagulação intravascular disseminada (CID) e outros graus de consumo de coagulopatia associada com deposição de fibrina dentro da microvasculatura de vários órgãos, são manifestações de sepse/choque séptico. Os efeitos em cascata da resposta de defesa do hospedeiro em órgãos alvos é uma importante mediadora no desenvolvimento de síndrome de disfunção de múltiplos órgãos (SDMO) e contribui para o pobre prognóstico de pacientes com sepse, sepse severa e sepse complicada por choque.
[00636]Estresse respiratório denota uma condição em que pacientes têm di-ficuldade de respirar devido a algum tipo de disfunção pulmonar. Sempre esses pa-cientes exibem graus variados de hipoxemia que podem ou não podem ser refratários para tratamento com oxigênio suplementar. Estresse respiratório pode ocorrer em pacientes com função pulmonar impedida devido a injúria direta no pulmão ou pode ocorrer devido a injúria indireta no pulmão tal como no ambiente de um processo sistêmico. Em adição, a presença de distúrbios pré-disponentes múltiplos substancialmente aumentam o risco, como faz a presença de fatores secundários tais como abuso crônico de álcool, doença crônica pulmonar, e baixo pH sérico.
[00637]Algumas causas de injúria pulmonar direta incluem pneumonia, aspi-ração de conteúdos gástricos, contusão pulmonar, gordura embólica, quase- afogamento, injúria de inalação, alta altitude e edema de reperfusão pulmonar após transplante pulmonar ou embolectomia pulmonar. Algumas causas de injúria indireta pulmonar incluem sepse, trauma severo com choque e múltiplas transfusões; bypass cardiopulmonar, overdose de droga, pancreatite aguda, e transfusões de produtos sanguíneos.
[00638]Uma classe de distúrbios pulmonares que causam estresse respiratório são associados com a síndrome conhecida como Cor Pulmonale. Esses distúrbios são associados com hipoxemia crônica resultando em aumento da pressão dentro da circulação pulmonar chamada hipertensão pulmonar. O resultado da hipertensão pulmonar aumenta o trabalho de carregamento do ventrículo direito, então levando ao seu alargamento ou hipertrofia. Cor Pulmonale geralmente apresente como falência cardíaca direita definida por um aumento sustentado na pressão ventricular direita e evidência clínica de retorno venoso reduzido no coração direito.
[00639]Doenças pulmonares crônicas obstrutivas (DPCOs) que incluem en- fisema e bronquite crônica também causam estresse respiratório e são caracterizadas pela obstrução do fluxo de ar. DPCOs são a quarta causa líder de morte e reivindica mais de 100.000 vidas anualmente.
[00640]Síndrome do estresse respiratório agudo (SERA) é geralmente pro-gressiva e caracterizada por estágios distintos. A síndrome é geralmente manifestada pelo rápido início da falência respiratória em um paciente com um fator de risco para a condição. Hipoxemia arterial que refratária ao tratamento com oxigênio suplementar é um aspecto característico. Deve ter enchimento alveolar, consolidação, e atelectase ocorrendo nas zonas dependentes do pulmão; entretanto, áreas não dependentes podem ter inflamação substancial. A síndrome pode progredir para al- veolite fibrosante com hipoxemia persistente, aumento do espaço morte alveolar, e uma diminuição adicional na submissão pulmonar. Hipertensão pulmonar que resulta a partir do dano na cama de capilares pulmonares podem também se desenvolver.
[00641]A severidade da injúria pulmonar clínica varia. Ambos, pacientes com hipoxemia menos severa como definido pela proporção da pressão parcial do oxigênio arterial para a fração do oxigênio inspirado como 300 ou menos e pacientes com hipoxemia mais severa como definida por uma proporção de 200 ou menos são compreendidos pela presente invenção. Geralmente, pacientes com uma proporção de 300 ou menos são classificados como tendo uma injúria pulmonar aguda e paci-entes tendo uma proporção de 200 ou menos são classificados como tendo síndro- me do estresse agudo respiratório.
[00642]A fase aguda da injúria pulmonar aguda é caracterizada por um influ-xo de fluído de edema rico em proteína nos espaços aéreos como uma consequência da permabilidade vascular aumentada da barreia alveolar-capilar. A perda da integridade epitelial em que a permeabilidade está alterada pode causar hemorragia alveolar, rompimento do transporte normal de fluídos que afeta a remoção de edema fluído a partir do espaço alveolar, redução da produção e retroalimentação de tenso- ativo, leva ao choque séptico em pacientes com pneumonia bacteriana, e causa fi-brose. Sepse é associada com risco mais alto mais progressão de injúria aguda pulmonar.
[00643]Em condições tal como sepse, onde hipermetabolismo ocorre, existe uma quebra acelerada de proteína, ambas, para sustentar gliconeogênese e para liberar os aminoácidos requeridos para aumentar a síntese protéica. Hiperglicemina pode estar presente em altas concentrações de triglicerídeos e outros lipídeos no soro podem estar presentes.
[00644]Para pacientes com função respiratória comprometida, hipermetabo- lismo pode afetar a proporção da produção de dióxido de carbono para consumo de oxigênio. Isto é conhecido como o quociente respiratório (R/Q) e em indivíduos nor-mais está entre cerca de 0,85 e cerca de 0,90. Excesso de gordura no metabolismo tem uma tendência a diminuir o R/Q enquanto o metabolismo de glicose aumenta o R/Q. Pacientes com estresse respiratório sempre têm dificuldade de eliminação de dióxido de carbono e então têm quocientes respiratórios anormalmente altos.
[00645]Pacientes criticamente doentes compreendidos pela presente inven-ção também geralmente experimentais uma resposta particular de estresse caracte-rizado por uma diminuição transiente da maioria dos produtos celulares e a super- regulação de proteínas do choque térmico. Além disso, esta resposta ao estresse envolve a ativação de hormônios tais como glucagon, hormônios do crescimento, e citocinas pró- e antiinflamatórias. Enquanto esta resposta ao estresse parece ter uma função protetora, a resposta cria instabilidade metabólica adicional nesses pacientes criticamente doentes. Por exemplo, ativação desses hormônios específicos causa elevação na glicose sérica que resulta em hiperglicemia. Em adição, danos ao coração e outros órgãos podem ser exacerbados por estímulo adrenérgico. Ainda, pode ter mudanças na tireóide que podem ter efeitos significantes na atividade me-tabólica.
[00646]Quantidade média de FGF-21 pode variar e em particular devem ser baseadas em recomendações e prescrição de um médico qualificado. A quantidade extada de FGF-21 é uma questão de preferência sujeita a fatores tais como exato tipo de condição a ser tratada, a condição do paciente a ser tratado, bem como outros ingredientes na composição. A invenção também provê para administração de uma quantidade terapeuticamente efetiva de outro agente ativo. A quantidade a ser dada pode ser facilmente determinada por um versado na técnica baseada na terapia com FGF-21.
[00647]Composições farmacêuticas da invenção podem ser fabricadas em uma forma convencional. EXEMPLOS
[00648]Os exemplos seguintes são oferecidos para ilustrar, mas não para limitar a reivindicação de invenção. Exemplo 1
[00649]Este exemplo descreve um de vários conjuntos de critérios potenciais para a seleção da região de incorporação de aminoácidos não naturalmente codifi-cados no FGF-21.
[00650]Figura 1 mostra a homologia sequencial entre FGF-21 (Proteína acesso número BC018404) e FGF-19 (Proteína acesso número BAA75500) como determinado usando o vetor NTI (Invitrogen; Carlsbad, CA). Os aminoácidos marca- dos com um asterisco são similares entre as duas moléculas. Os aminoácidos que estão sublinhados são idênticos entre os dois polipeptídeos. Sete diferentes polipep- tídeos de FGF-21 foram gerados substituindo um aminoácido codificado naturalmente por um aminoácido codificado não-naturalmente. Cada polipeptídeo tem um dos aminoácidos marcados com um retângulo na Figura 1 substituídos por para- acetilfenilalanina. Os polipeptídeos gerados não apresentam a sequência líder mos-trada nas Figuras 1 e 3 e foram marcados no N terminal com 6 resíduos de histidina. SEQ ID NO.: 1 é uma sequência de 181 aminoácidos de FGF-21 humano (forma P) sem a sequência guia. SEQ ID NO.: 2 é a sequência de FGF-21 humano (forma P) sem a sequência guia e com a marca de His no N terminal. Cada um dos aminoáci- dos gerados tem uma substituição do aminoácido codificado não-naturalmente nas seguintes posições 10, 52, 77, 117,126, 131 e 162 da SEQ ID NO: 1.
[00651]Figura 2 mostra a estrutura do FGF-19 humano que foi obtido de um Banco de Dados de Proteína (PDB) (Bernstein et al. J. Mol. Biol. 1997, 112, pp535) (1PWA) e foi classificado usando o softwear PyMOL (DeLano Scientific; Palo Alto, CA). Os aminoácidos correspondentes a V34, L79, G104, S144, K155, L160, e S196 de FGF-19 foram substituídos com para-acetilfenilalanina no polipeptídeo FGF-21 da invenção. A linha tracejada indica regiões que não foram modificadas na estrutura original.
[00652]Figura 3 mostra a homologia sequencial entre FGF-21 (proteína acesso número BC018404) e FGF-2 (proteína acesso número BAA75500) como de-terminado usando o vetor NTI (Invitrogen; Carlsbad, CA). Os aminoácidos marcados com asterisco são similares entre as duas moléculas. Os aminoácidos que estão sublinhados são idênticos entre os dois polipeptídeos. Os sete aminoácidos mostrados na Figura 1como regiões para substituição estão também marcados por retângulos na Figura 3.
[00653]Figura 4 mostra a estrutura de FGF-2 humano que foi obtida do PDB (1CVS) e foi classificada usando o softwear PyMOL (DeLano Scientific; Palo Alto, CA). As estruturas cinza são receptores FGF 1 humanos (FGFR1) e a preta é FGF2 humano. Plotnikov, NA et al Cell 1999, 3 de Setembro; 98 (5): 641-50 descreve a estrutura cristalina de FGF2 ligado ao receptor FGF. Os aminoácidos correspondentes a F21, K62, K86, V125, K134, T139 de FGF-2 foram substituídos com para- acetilfenilalanina no polipeptídeo FGF-21 da invenção. A linha tracejada indica regi-ões que não foram modificadas na estrutura original.
[00654]Outro conjunto de critérios para a seleção de regiões preferenciais de incorporação de aminoácidos não naturalmente codificados é o seguinte. Dez estru-turas cristalinas do banco de dados de proteína foram usadas como modelo para estrutura de FGF-21: 1PWA (FGF-19 humano); 1IJT ( FGF-4 humano); 1NUN (com-plexo FGF10- receptor FGF 2b humano); 1G82 (dímero FGF-9 humano com receptor FGF e heparina); 1IHK (FGF-9 humano); 1BAR (FGF-1 bovino); 1QQK (FGF-7 de rato); 1K5U (FGF-1 humano); 1FQ9 (FGF-2 humano com receptor FGF1 e hepari- na); e 2FDB (FGF-8 humano com receptor FGF 2c). As coordenadas para estas estruturas estão disponíveis no banco de dados de proteína (PDB) (Bernstein et al. J. Mol. Biol. 1997, 112, pp535). Uma comparação das estruturas cristalinas indicou que elas foram todas muito similares na estrutura do núcleo. No entanto, as porções N e C- terminais demonstraram ser altamente divergentes entre estas moléculas de FGF, e, portanto, a terminação não pode ser modelada. A modelagem identificou dois resíduos, Y22 e Y104, que foram altamente conservados e foram envolvidos com ligação ao receptor. Duas potenciais regiões ligadoras à heparina foram também identificadas envolvendo R36 e E37. As posições de aminoácidos identificadas para a ligação com o receptor e com resíduos de heparina correspondem a SEQ ID NO:1.
[00655]Como resultado, resíduos foram identificados em 1) não interfeririam com a ligação ao receptor FGF ou heparina, 2) não estariam presentes no interior da proteína, e 3) não estariam em regiões que fossem fracamente consistentes entre as estruturas cristalinas. Em algumas modalidades, um ou mais aminoácidos não natu-ralmente codificados são incorporados, mas não limitados, um ou mais das seguintes posições de FGF-21: 87, 77, 83, 72 de SEQ ID NO:1 ou os aminoácidos corres- pondentes em SEQ ID NOs:2-7). Em algumas modalidades, um ou mais aminoáci- dos codificados naturais são incorporados, mas não limitados, um ou mais das seguintes posições de FGF-21: 69, 79, 91, 96, 108 e 110 da SEQ ID NO:1 ou os ami- noácidos correspondentes na SEQ ID NOs:2-7).
[00656]Os seguintes critérios foram usados para avaliar cada posição de FGF-21 para a introdução de um aminoácido codificado não-naturalmente: o resíduo (a) não deve interferir na ligação ao receptor FGF-21 baseado na análise estrutural, b) não deve ser afetado por alanina ou mapeamento de mutagênese homólogo (c) deve ser exposto na superfície e exibir mínimas interações de van der Walls ou pontes de hidrogênio com resíduos vizinhos, (d) deve ser ou deletado ou variável nas variantes de FGF-21, (e) resultaria em mudanças conservativas em substituições por um aminoácido codificado não-naturalmente e (f) deve ser encontrado tanto em regiões altamente flexíveis ou regiões rígidas estruturalmente.
[00657]Estruturas cristalinas adicionais ou diferentes de membros da família FGF como as estruturas de FGF-23 e/ou FGF-19 também podem ser usadas para selecionar regiões de incorporação de um ou mais aminoácidos não naturalmente codificados no FGF-21. Por exemplo, a estrutura cristalina de FGF-19 humano (PDB ID 2P23) e/ou estrutura cristalina de FGF-19 (PDB ID 2P23) e/ou FGF-23 humana (PDB ID 2P39) pode prover informações adicionais para selecionar regiões para in-corporação de aminoácidos não naturalmente codificados no FGF-21. Tais regiões podem estar em diferentes locais da proteína, incluindo, mas não limitando, o N- e C-terminal, regiões de ligação ao receptor e à heparina. Além disso, outros cálculos podem ser feitos na molécula de FGF-21, utilizando o programa Cx (Pintar et al. (2002) Bioinformatics, 18, pp 980) para avaliar a extensão da protusão de cada átomo protéico.
[00658]Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF- 21: antes da posição 1 (na posição N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 27). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 10, 52, 117, 126, 131, 162, 87, 77, 83, 72, 69, 79, 91, 96, 108, e 110 (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 10, 52, 77, 117, 126, 131, e 162 (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 87, 77, 83, 72 (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7). Em algumas modalidades, um ou mais aminoácidos não naturalmente codificados são incorporados em uma ou mais das seguintes posições em FGF-21: 69, 79, 91, 96, 180, e 110 (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7). Exemplo 2
[00659]Este exemplo contém detalhes da clonagem e expressão de um poli- peptídeo FGF-21 incluindo um aminoácido codificado não-naturalmente em E. coli. Este exemplo também descreve um método para avaliar a atividade biológica de polipeptídeos FGF-21 modificados.
[00660]Métodos para clonagem de FGF-21 são conhecidos como aqueles versados na técnica. Sequências de polipeptídeos e polinucleotídeos para FGF-21 e clonagem de FGF-21 em células hospedeiras estão detalhados na U.S. Patent No. 6,716,626; U.S. Patent Publication Nos. 2005/0176631, 2005/0037457, 2004/0185494, 2004/0259780, 2002/0164713, e 2001/0012628; WO01/36640; WO 03/011213; WO 03/059270; WO 04/110472; WO 05/061712; WO 05/072769; WO 05/091944; WO 05/113606; WO 06/028595; WO 06/028714; WO 06/050247; WO 06/065582; WO 06/078463, que estão incorporadas aqui por referências na íntegra.
[00661]cDNA codificando a forma P de FGF-21 sem a sequência líder é mostrado como SEQ ID NO:8. Este polipeptídeo é mostrado como SEQ ID NO:1.
[00662]cDNA codificando a forma P marcada com His de FGF-21 sem a se-quência líder é mostrado como SEQ ID NO:9. Este polipeptídeo é mostrado como SEQ ID NO:2.
[00663]cDNA codificando a forma P de FGF-21 com a sequência líder con-tendo 3 leucinas juntas é mostrado como SEQ ID NO:10. Este polipeptídeo é mostrado como SEQ ID NO:3.
[00664]cDNA codificando a forma P de FGF-21 com a sequência líder con-tendo 2 leucinas juntas é mostrado como SEQ ID NO:11. Este polipeptídeo é mostrado como SEQ ID NO:4.
[00665]cDNA codificando a forma L de FGF-21 sem a sequência líder é mostrado como SEQ ID NO:12. Este polipeptídeo é mostrado como SEQ ID NO:5.
[00666]cDNA codificando a forma L de FGF-21 com a sequência líder con-tendo 3 leucinas juntas é mostrado como SEQ ID NO:13. Este polipeptídeo é mostrado como SEQ ID NO:6.
[00667]cDNA codificando a forma L de FGF-21 com a sequência líder con-tendo 2 leucinas juntas é mostrado como SEQ ID NO:14. Este polipeptídeo é mostrado como SEQ ID NO:7.
[00668]Um sistema de translação introduzido que compreende um tRNA or-togonal (O-tRNA) e um aminoacil tRNA sintetase ortogonal (O-RS) é usado para ex-pressar FGF-21 contendo um aminoácido codificado não-naturalmente. A O-RS aminoacila preferencialmente o O-tRNA com um aminoácido codificado não- naturalmente. Por sua vez, o sistema de translação insere o aminoácido codificado não-naturalmente no FGF-21, em resposta ao códon seletor codificado. O-RS e se-quências de O-tRNA adequadas estão descritas na WO 2006/068802 intitulada “Composições de Aminoacil-tRNA sintetase e seus usos” (E9; SEQ ID NO 15) e WO 2007/021297 intitulada “Composições de tRNA e seus usos” (F13; SEQ ID NO:16), que estão incorporadas aqui por referências na íntegra. Tabela 2: Sequências de O-RS e O-tRNA.
[00669]A transformação de E. coli com plasmídeos contendo o gene de FGF-21 modificado e o par ortogonal aminoacil tRNA sintetase/ tRNA (específicos para o aminoácido codificado não-naturalmente desejado) permitem a incorporação região-específica de aminoácido codificado não-naturalmente no polipeptídeo FGF- 21.
[00670]FGF-21 selvagem maduro dói amplificado por PCR de uma reação de síntese de cDNA derivado de poliA+mRNA de fígado humano saudável (Biochain) usando protocolos padrões e clonados em pET30 (Ncol-BamHI). Seguindo confirmação de sequência, FGF-21 incluindo uma sequência HHHHHHSGG no N- terminal foi subclonado em um vetor de supressão contendo tirosil tRNA Tir/CUA supressor âmbar de Methanococcus jannaschii (Mj tRNA Tir/CUA ) sob controle constitutivo de um promotor sintético derivado de uma sequência promotora de lipoproteína de E coli (Miller, J.H., Gene, 1986), assim como a tirosil-tRNA-sintetase (Mj TirRS) sob controle do promotor GlnRS de E coli. Expressão de FGF-21 foi sob controle do promotor T7. Mutações âmbar foram introduzidas usando protocolos de mutação de mudança rápida padrões (Stratagene; La Jolla; Califórnia). Todas as construções foram sequencialmente verificadas. Supressão com para-acetil-fenilalalanina (pAcf)
[00671]Plasmídeos (pVK3-HisFGF21) foram transformados em cepa W3110 B2 de E coli na qual a expressão de T7 polimerase estava sob controle de um pro-motor arabinose- induzível. Culturas bacterianas de uma noite foram diluídas na pro-porção de 1:100 em balões de agitação contendo meio de cultura 2X YT e crescidas a 37°C até uma densidade ótica em 600nm de ~0,8. Expressão de proteína foi induzida pela adição final de arabinose (0,2% final), e para-acetil-fenilalanina (pAcf) para uma concentração final de 4mM. Culturas foram incubadas a 37°C por 4 horas. Células foram centrifugadas e resuspensas em tampão de lise B-PER (Pierce) 100ul/OD/mL + 10ug/mL DNAse e incubadas a 37°C por 30 minutos. Material celular foi removido por centrifugação e o sobrenadante removido. O sedimento foi ressus- penso na mesma quantidade de tampão SDS-PAGE para captação de proteína. Métodos de purificação de FGF-21 são conhecidos como aqueles versados na técnica e são confirmados por SDS-PAGE, por análise de Western Blot, ou espectroscopia de massa com captura de íon em eletropulverização-ionização e similares.
[00672]Expressão de FGF-21 marcado com HIs no N-terminal e supressão na região âmbar 7 é mostrada como Figura 5. O polipeptídeo FGF-21 está marcado com uma seta. Figura 5 mostra as amostras B-PER dos sedimentos—coluna 1: mar-cador; coluna 2: pré-indução de VK3-FGF21, sobrenadante; coluna 3: pré-indução de VK3-FGF21, sedimento; coluna 4: VK3-FGF21 0,2% arabinose, sobrenadante; coluna 5: VK3-FGF21 0,2% arabinose, sedimento; coluna 6: VK3-FGF21-pAcf-L10, 0,2% arabinose; coluna 7: VK3-FGF21-pAcf-L52, 0,2% arabinose; coluna 8: VK3- FGF21-pAcf-R77, 0,2% arabinose; coluna 9: VK3-FGF21-pAcf-H117, 0,2% arabinose; coluna 10: VK3-FGF21-pAcf-R126, 0,2% arabinose; coluna 11: VK3-FGF21- pAcf-R131, 0,2% arabinose; coluna 12: VK3-FGF21-pAcf-S162, 0,2% arabinose. Os números de posição indicados para a substituição do aminoácido são baseados no SEQ ID NO:1.
[00673]Figura 6 mostra as amostras B-PER dos sobrenadantes—coluna 1: pré-indução de VK3-FGF21, sobrenadante; coluna 2: pré-indução de VK3-FGF21, sedimento; coluna 3: marcador; coluna 4: VK3-FGF21 0,2% arabinose, sobrenadan- te; coluna 5: VK3-FGF21 0,2% arabinose, sedimento; coluna 6: VK3-FGF21-pAcf- L10, 0,2% arabinose; coluna 7: VK3-FGF21-pAcf-L52, 0,2% arabinose; coluna 8: VK3-FGF21-pAcf-R77, 0,2% arabinose; coluna 9: VK3-FGF21-pAcf-H117, 0,2% arabinose; coluna 10: VK3-FGF21-pAcf-R126, 0,2% arabinose; coluna 11: VK3-FGF21- pAcf-R131, 0,2% arabinose; coluna 12: VK3-FGF21-pAcf-S162, 0,2% arabinose. Os números de posição indicados para a substituição do aminoácido são baseados no SEQ ID NO:1.
[00674]Proteínas mutantes FGF-21 marcadas com His podem ser purificadas usando métodos conhecidos como aqueles versados na técnica. A resina pré- ligada de quelação de níquel (Invitrogen, Carlsbad, CA) pode ser usada via procedimento padrão de purificação de proteínas marcadas por His fornecido pelo fabricante.
[00675]pVK10 (Figures 24) foi desenvolvido para o uso com a proteína FGF- 21 não marcada, com uma sequência dada na Figura 25. Este foi o vetor usado para fazer os mutantes R36am e Y83am e há resultados adicionais de sua proteína mu-tante FGF-21 não marcada com HIs e suas purificações posteriores nos exemplos e mostradas pelas figuras. Diferenciação de 3T3-L1 para adipócitos e ensaio de captação de glicose
[00676]Para avaliar a atividade biológicas de polipeptídeos FGF-21, o ensaio seguinte pode ser realizado. Fibroblastos murinos 3T3-L1 (ATCC#CL-173) são se-dimentados em placas de 10 cm com DMEM contendo 10% de soro fecal bovino. As células foram mantidas a uma densidade não maior que 70% de expansão. Antes de começar a diferenciação a adipócitos, as células foram levadas a 100% de confluên-cia, o meio teve que ser trocado a cada 2 dias. As células foram contadas e sedi-mentadas a 25000 células por poço em placas de 96 poços ( células podem ser pla- queadas em placa Cytostar-T de 96 poços) e incubadas por mais 48 horas. Diferen-ciação é induzida pela adição do meio seguinte depois da remoção do meio de cultura anterior: DMEM suplementado com 10% de soro fetal bovino, 1μM dexametasona (DBX), 0,5 mM 3-isobutil-1-metilxantina (IBMX), e 5μg/mL insulina. Uma maneira alternativa de induzir diferenciação é tratar as células com 1μM Rosiglitazona e in-cubar por 6 dias antes de trocar o meio para DMEM/10% soro fetal bovino, já que esta é uma maneira rápida de induzir a diferenciação de fibroblastos 3T3-L1 a adi- pócitos. Uma terceira possibilidade é combinar os dois processos para diminuir o tempo de diferenciação.
[00677]Depois de adicionar meio contendo DBX/IBMX/insulina às células, as células são incubadas por 48 horas. O meio é trocado por DMEM/10% soro fetal bo- vino/5 μg/mL insulina, e as células são incubadas por 48 horas. Depois o meio é tro-cado por DMEM/10% soro fetal bovino e o meio é substituído com meio fresco a cada 2 dias. As células diferenciarão entre 7-14 dias. Células diferenciadas acumulam gotículas lipídicas. As células podem ser coradas com Óleo vermelho O. Uma vez que 95% dos adipócitos contêm gotículas lipídicas, as células podem ser usadas para o ensaio de captação de glicose.
[00678]3T3-L1 diferenciadas são tratadas com FGF-21 (1μg/mL) em meio DMEM suplementado com 0,1% BSA livre de ácidos graxos por 18 horas para depri- var de nutrientes as células. As células são então lavadas três vezes com tampão HEPES Ciclo de Krebs (KRK= 0,118M NaCl, 5mM KCl, 2,54 mM CaCl2, 1,19 mM KH2PO4, e 20mM HEPES) suplementado com 0,1% BSA livre de ácidos graxos. A mistura para marcação é preparada pela adição de 4μCi, 0,1mM de 2-desoxiD-[1- 3H]-glicose ao tampão KRK/ BSA livre de ácido graxo. As células foram adicionadas e incubadas por 1 hora a 37°C. A reação é parada lavando as células duas vezes com PBS gelado contendo citocalasina B. A placa é lavada para eliminar qualquer resíduo do tampão. Líquido de cintilação é adicionado a cada poço e amostras são contadas em um TopCounter.
[00679]Uma maneira alternativa para medir a captação de glicose é marcar as células 3T3-L1 diferenciadas com um substrato não radioativo como 2-NBDG e ler com um fluorímetro de placa. Um procedimento indireto para a medida da captação de glicose é medir a expressão de GLUT1 ou GLUT4 na superfície de membrana celular. GLUT1 e GLUT4 são transportadores de glicose que são translocados para superfície de membrana celular de vesículas internas sob estimulação de insulina ou FGF-21. Um método de Elisa em células vivas pode ser desenvolvido. Exemplo 3
[00680]Este exemplo detalha a introdução de aminoácido contendo carbonila e a reação subsequente com PEG contendo aminoóxi.
[00681]Este exemplo demonstra um método para a geração de polipeptí- deos FGF-21 que incorporam um aminoácido codificado não-naturalmente contendo cetona que é subsequentemente reagido com PEG contendo aminoóxi de aproxima-damente 5000 peso molecular. Cada um dos resíduos antes da posição 1 (na posição N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7) é substituído separadamente com um aminoácido não naturalmente codificado com a seguinte estrutura:
[00682]As sequências utilizadas para incorporação em regiões específicas de p-acetil-fenilalanina em FGF-21 estão na SEQ ID NO:1 (FGF-21), e SEQ ID NO:16 ou 17 (muttRNA, M jannaschii mtRNA tir/CUA), e 15, 29, 30, ou 31 (TiRS L W1, 5 ou 6) descritos no exemplo 2 acima.
[00683]Uma vez modificado, a variação do polipeptídeo FGF-21 contendo o aminoácido que contém carbonila é reagido com o derivado de PEG contendo ami- noóxi de forma:
[00684]R-PEG(N)-O-(CH2)n-O-NH2, onde R é metila, n é 3 e N é de aproxi-madamente 5000 peso molecular. O FGF-21 contendo p-acetilfenilalanina purificado dissolvido em 10mg/mL em 25 mL MES (Sigma Chemical, St. Louis, MO) pH 6,0, 25 mM HEPES (Sigma Chemical, St. Louis, MO) pH 4,5, é reagido com um excesso de 10-100 vezes de PEG contendo aminoóxi, e então agitado por 10-16 horas 'a tem-peratura ambiente (Jencks, W. J. AM. Chem. Soc. 1959, 81, pp475). O FGF-21 PE- Gilado é então diluído em tampão apropriado para purificação imediata e análise. Exemplo 4
[00685]Conjugação com PEG consistindo em um grupo hidroxiamina ligado ao PEG via uma ligação amida.
[00686]Um reagente de PEG tendo a estrutura seguinte é ligado a um ami- noácido codificado não-naturalmente contendo cetona usando o procedimento des-crito no exemplo 3:
[00687]R-PEG(N)-O-(CH2)2-NH-C(O)(CH2)n -O-NH2, onde R= metila, n=4, e N= é aproximadamente 20000 peso molecular. A reação, purificação, e condições de análise são como descritos no Exemplo 3. Exemplo 5
[00688]Este exemplo detalha a introdução de dois aminoácidos não natural-mente codificados distintos em polipeptídeo FGF-21.
[00689]Este exemplo demonstra um método para a geração de polipeptí- deos FGF-21 que incorporam aminoácido codificado não-naturalmente contendo cetona funcional em duas posições entre os resíduos seguintes: antes da posição 1 (na posição N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7). O polipeptídeo FGF-21 é preparado como descrito nos Exemplos 1 e 2, exceto naquele em que o códon seletor é introduzido em duas regiões distintas dentro do ácido nucleico. Exemplo 6
[00690]Este exemplo detalha a conjugação de polipeptídeo FGF-21 a PEG contendo hidrazida e redução in situ subsequente.
[00691]Um polipeptídeo FGF-21 incorporando um aminoácido contendo car-bonila é preparado de acordo com o procedimento descrito nos Exemplos 2 e 3. Uma vez modificado, um PEG contendo hidrazida tendo a seguinte estrutura é conjugado ao polipeptídeo FGF-21:
[00692]R-PEG(N)-O-(CH2)2-NH-C(O)(CH2)n -X-NH-NH2, onde R= metila, n=2, e N= é 10000 peso molecular e X é um grupo carbonila (C=O). O FGF-21 contendo p-acetilfenilalanina purificado é dissolvido de 0,1-10 mg/mL em 25 mM MES (Sigma Chemical, St. Louis, MO) pH 7,0, ou em 10 mM acetato de sódio (Sigma Chemical, St. Louis, MO) pH 4,5, é reagido com excesso de 1-100 vezes de PEG contendo hidrazida, e a hidrazona correspondente é reduzida in situ pela adição de 1M NaCNBH3 solução mãe (Sigma Chemical, St. Louis, MO), dissolvido em H2O, para uma concentração final de 10-50 mM. Reações são conduzidas no escuro a 4°C para RT por 18-48 horas. Reações são paradas pela adição de 1M Tris (Sigma Chemical, St. Louis, MO) a pH próximo de 7,6 a uma concentração de Tris final de 50 mM ou diluída em tampão apropriado para purificação imediata. Exemplo 7
[00693]Este exemplo detalha a introdução de um aminoácido contendo al- quino no polipeptídeo FGF-21 e derivatização com m-PEG-azida.
[00694]Os resíduos seguintes: antes da posição 1 (na posição N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7), são cada um substituídos pelo seguinte ami- noácido não naturalmente codificado:
[00695]As sequências utilizadas para incorporação em regiões específicas de p-propargil-tirosina em FGF-21 estão na SEQ ID NO:1 (FGF-21), SEQ ID NO:16 ou 17 (muttRNA, M jannaschii mtRNA tir/CUA), e 22, 23 ou 24 descritos no exemplo 2 acima. O polipeptídeo FGF-21 contendo propargil-tirosina é expresso em E. coli e purificado usando as condições descritas no Exemplo 3.
[00696]O FGF-21 contendo propargil-tirosina purificado dissolvido de 0,1-10 mg/mL em tampão PB (100 mM fosfato de sódio, 0,015M NaCl, pH=8) e um excesso de 10-1000 vezes de PEG contendo azida é adicionado à mistura reacional. Depois a mistura é incubada (incluindo, mas não limitada a, próximo 4 horas a temperatura ambiente ou 37°C, ou durante a noite a 4°C), H2O é adicionada e a mistura é filtrada por uma membrana de diálise. A amostra pode ser analisada para a adição, incluindo, mas não limitada a, por procedimentos similares descritos no exemplo 3.
[00697]Neste exemplo, o PEG terá a seguinte estrutura: R-PEG(N)-O-(CH2)2-NH-C(O)(CH2)n -N3 , onde R é metila, n é 4 e N é 10000 peso molecular. Exemplo 8
[00698]Este exemplo detalha a substituição de um aminoácido grande e hi- drofóbico no polipeptídeo FGF-21com propargil-tirosina.
[00699]Um resíduo de Phe, Trp ou Tyr presentes em uma das regiões de FGF-21: antes da posição 1 (na posição N-terminal), 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7) é substituída com o seguinte aminoácido codificado não-naturalmente como descrito no Exemplo 7:
[00700]Uma vez modificado, um PEG é ligado ao polipeptídeo FGF-21 vari-ante compreendendo o aminoácido contendo alquino. O PEG terá a seguinte estru-tura:
[00701]Me-PEG(N)-O-(CH2)2-N3 e o procedimento de ligação seguirá aquele do Exemplo 7. Isto gerará uma variante de polipeptídeo FGF-21 contendo um ami- noácido codificante não-natural que é quase isostérico ao de ocorrência natural. Aminoácidos grandes e hidrofóbicos e que é modificado com um derivado de PEG em uma região distinta dentro do polipeptídeo. Exemplo 9
[00702]Este exemplo detalha a geração de um homodímero de polipeptídeo FGF-21, heterodímero, homomultímero, ou heteromultímero separados por um ou mais ligantes de PEG.
[00703]O polipeptídeo variante FGF-21 contendo alquino produzido no Exemplo 7 é reagido com um derivado de PEG bifuncional de forma:
[00704]N3-(CH2)n -C(O)-NH-(CH2)2 -O-PEG(N)-O-(CH2)2-NH-C(O)-(CH2)n - N3, onde n é 4 e o PEG tem um peso molecular médio de aproximadamente 5000, para gerar o polipeptídeo FGF-21 homodímero onde duas moléculas de FGF-21 são fisicamente separadas por PEG. De uma maneira análoga, um polipeptídeo FGF-21 pode ser ligado a um ou mais outros polipeptídeos para formar heterodímeros, ho- momultímeros, ou heteromultímeros. Ligação, purificação, e análise serão realizadas como nos Exemplos 7 e 3. Exemplo 10
[00705]Este exemplo detalha a ligação de um alvo sacarídeo ao polipeptídeo FGF-21.
[00706]Um resíduo seguinte é substituído com pelo aminoácido codificado não -natural abaixo: antes da posição 1 (na posição N-terminal), 1,2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66 ,67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 151, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176 ,177, 178, 179, 180, 181, 182 (na terminação carboxil da proteína) (SEQ ID NO:1 ou os aminoácidos correspondentes na SEQ ID NOs: 2-7) como descrito no Exemplo 3.
[00707]Uma vez modificado, o polipeptídeo FGF-21 variante compreendendo o aminoácido contendo carbonila é reagido com um análogo aminoóxi β-ligado de N-acetilglicosamina (GlcNAc). O polipeptídeo FGF-21 variante (10mg/mL) e o saca- rídeo aminoóxi (21mM) são misturados em tampão aquoso 100mM sódio acatato (pH 5,5) e incubado a 37°C por 7 a 26 horas. Um segundo sacarídeo é ligado ou primeiro enzimaticamente pela incubação do polipeptídeo FGF-21 sacarídeo- conjugado (5mg/mL) com UDP-galactose (16mM) e β-1,4-galactosiltransferase (0,4 unidades/mL) em 150 mM tampão HEPES (pH 7,4) por 48 horas a temperatura am-biente ( Schanbacher et al. J. Biol. Chem. 1970,0245, 5057-5061). Exemplo 11
[00708]Este exemplo detalha a geração de um antagonista polipeptídeo FGF-21 PEGilado.
[00709]Um resíduo, incluindo, mas não limitado a, aquele envolvido na liga-ção ao receptor FGF-21 é substituído pelo seguinte aminoácido codificado não- naturalmente como descrito no Exemplo 3.
[00710]Uma vez modificado, o polipeptídeo FGF-21 variante compreendendo o aminoácido contendo carbonila será reagido com um derivado de PEG contendo aminoóxi de forma:
[00711]R-PEG(N)-O-(CH2)n-O-NH2 , onde R é metila, n é 4 e N é 20000 peso molecular para gerar um polipeptídeo FGF-21 antagonista contendo um aminoácido codificado não -natural que é modificado com um derivado de PEG em uma única região dentro do polipeptídeo. Ligação, purificação, e análise são realizadas como no Exemplo 3. Exemplo 12
[00712]Geração de um homodímero de polipeptídeo FGF-21, heterodímero, homomultímero, ou heteromultímero onde as moléculas FGF-21 estão ligadas dire-tamente.
[00713]Um polipeptídeo FGF-21 variante compreendendo o aminoácido con-tendo alquila pode ser ligado diretamente a outro polipeptídeo FGF-21 variante com-preendendo o aminoácido contendo azida. De uma maneira análoga, um polipeptí- deo FGF-21 pode ser ligado a um ou mais polipeptídeos para formar heterodímeros, homomultímeros, ou heteromultímeros. Ligação, purificação , e análise são realizadas como nos Exemplos 3, 6 e 7. Exemplo 13
[00714]O polialquileno glicol (P-OH) é reagido com o haleto alquila (A) para formar o éter (B). Nestes compostos, n é um inteiro de 1 a 9 e R’ pode ser uma cadeia reta ou ramificada, C1 saturado ou insaturado, a grupos C20 alquila ou hetero- alquila. R’ pode também ser um C3 a C7 alquila cíclica ou heteroalquila cíclica satu-rada ou insaturada, um grupo arila ou heteroarila substituído ou não substituído, ou um grupo alcarila (a alquila é um C1 a C20 alquila saturada ou insaturada) ou hete- roalcarila. Tipicamente, PEG-OH é polietileno glicol (PEG) ou monometoxi polietileno glicol (mPEG) tendo um peso molecular de 800 a 40000 Daltons (Da). Exemplo 14
[00715]mPEG-OH com um peso molecular de 20000 Da (mPEG-OH 20kDa; 2,0g, 0,1 mmol, Sunbio) foi tratado com NaH (12mg, 0,5 mmol) em THF (35 mL). Uma solução de propargil bromida, dissolvida em xileno em uma solução de 80% de peso (0,56mL, 5mmol, 50 equiv., Aldrich), e uma quantidade catalítica de KI foram então adicionados à solução e a mistura resultante foi aquecida com refluxo por 2 horas. Água (1mL) foi então adicionada e o solvente foi removido sob vácuo. Para o resíduo, foi adicionado CH2Cl2 (25mL) e a camada orgânica foi separada, seca com Na2SO4 anidro, e o volume foi reduzido a aproximadamente 2mL. Esta solução de CH2Cl2 foi adicionada a éter dietila (150 mL) gota a gota. O precipitado resultante foi coletado, lavado com várias porções de éter dietila frio, e seco para gerar propargil- O-PEG. Exemplo 15
[00716]O mPEG-OH com um peso molecular de 20000 Da (mPEG-OH 20kDa; 2,0g, 0,1 mmol, Sunbio) foi tratado com NaH (12mg, 0,5 mmol) em THF (35 mL). Cinquenta equivalentes de 5-bromo-1-pentino (0,53mL, 5mmol, Aldrich) e uma quantidade catalítica de KI foram então adicionadas à mistura. A mistura resultante foi aquecida com refluxo por 16 horas. Água (1mL) foi então adicionada e o solvente foi removido sob vácuo. Para o resíduo, foi adicionado CH2Cl2 (25mL) e a camada orgânica foi separada, secada com Na2SO4 anidro, e o volume foi reduzido a apro-ximadamente 2mL. Esta solução de CH2Cl2 foi adicionada a éter dietila (150 mL) gota a gota. O precipitado resultante foi coletado, lavado com várias porções de éter dietila frio, e seco para gerar o alquino correspondente. 5-cloro-1-pentino pode ser usado em uma reação similar. Exemplo 16
[00717]Para uma solução de 3-hidroxibenzilalcool (2,4g, 20mmol) em THF (50mL) e água (2,5mL) foi primeiro adicionado hidróxido de sódio em pó (1,5g, 37,5 mmol) e então uma solução de brometo de propargila, dissolvida em xileno em uma solução de 80% de peso (3,36 mL, 30mmol). A mistura reacional foi aquecida em refluxo por 6 horas. Para a mistura foi adicionado ácido cítrico 10% (2,5mL) e o sol-vente foi removido sob vácuo. O resíduo foi extraído com acetato de etila (3 x 15mL) e as camadas orgânicas combinadas foram lavadas com solução de NaCl saturado (10mL). Seco com MgSO4 e concentrado para gerar o 3-propargiloxibenzil álcool.
[00718]Cloreto de metanosulfonil (2,5 g, 15,7 mmol) e trietilamina (2,8mL, 20 mmol) foram adicionados à solução do composto 3 (2,0g, 15,7mmol) em CH2Cl2 a 0°C e a reação foi colocada em geladeira por 16 horas. Um trabalho usual proporci- onou o mesilato como um óleo amarelo pálido. Este óleo (2,4g, 9,2 mmol) foi dissolvido em THF (20mL) e LiBr (2,0g, 23,0 mmol) foi adicionado. A mistura reacional foi aquecida em refluxo por 1 hora e foi então resfriada a temperatura ambiente. Para a mistura, foi adicionada água (2,5mL) e o solvente foi removido sob vácuo. O resíduo foi extraído com acetato de etila (3 x 15mL) e as camadas orgânicas combinadas foram lavadas com solução saturada de NaCl (10mL), seca com Na2SO4 anidro, e concentrada para gerar o brometo desejado.
[00719]m-PEG-OH 20kDa (1,0g, 0,05mmol, Sunbio) foi dissolvido em THF (20mL) e a solução foi resfriada em banho de gelo. NaH (6mg, 0,25mmol) foi adicio-nado com agitação vigorosa durante um período de vários minutos seguido pela adi-ção do brometo obtido acima (2,55g, 11,4mmol) e uma quantidade catalítica de KI. O banho de resfriamento foi removido e a mistura resultante foi aquecida em refluxo por 12 horas. Água (1,0mL) foi adicionada à mistura e o solvente foi removido sob vácuo. Ao resíduo foi adicionado CH2Cl2 (25mL) e a camada orgânica foi separada, seca com Na2SO4 anidro, e o volume foi reduzido a aproximadamente 2mL. Adição gota a gota a uma solução de éter (150mL) resultou em um precipitado branco, o qual foi coletado para a produção do derivado de PEG. Exemplo 17
[00720] Os polímeros de polietileno glicol contendo alquina terminais podem também ser obtidos ligando polímero de polietileno glicol contendo um grupo funcio-nal termina a uma molécula reativa contendo a funcionalidade alquina como mostra-do acima. N é entre 1 e 10. R’ pode ser H ou um grupo alquila pequeno de C1 a C4. Exemplo 18
[00721]Ácido 4-pentinoico (2,943g, 3,0mmol) foi dissolvido em CH2Cl2 (25mL). N-hidroxisuccinimida (3,80g, 3,3mmol) e DCC (4,66g, 3,0mmol) foram adio- cinados e a solução foi agitada durante a noite a temperatura ambiente. O éster NHS 7 cru resultante foi usado na seguinte reação sem purificação adicional.
[00722]m-PEG-NH2 com um peso molecular de 5000 Da (m-PEG-NH2 , 1g, Sunbio) foi dissolvido em THF (50mL) e a mistura foi resfriada a 4°C. Éster 7 NHS (400mg, 0,4mmol) foi adicionado com aos poucos com agitação vigorosa. A mistura foi deixada agitando por 3 horas durante aquecimento a temperatura ambiente. Água (2mL) foi então adicionada e o solvente foi removido sob vácuo. Ao resíduo foi adici-onado CH2Cl2 (50mL) e a camada orgânica foi separada, seca com Na2SO4 anidro, e o volume foi reduzido a aproximadamente 2mL. Esta solução de CH2Cl2 foi adicionada a éter (150mL) gota a gota. O precipitado resultante foi coletado e seco a vácuo. Exemplo 19
[00723]Este exemplo representa a preparação de éster de metanosulfonila de polipolietileno glicol, que pode também ser referidos como o metanosulfonato ou mesilato de polietileno glicol. O tosilato correspondente e os halogenetos podem ser preparados por procedimentos similares.
[00724]O mPEG-OH (peso molecular = 3400, 25g, 10mmol) em 150mL de tolueno foi azeotropicamente destilado por 2 horas sob nitrogênio e a solução foi res-friada a temperatura ambiente. 40 mL de CH2Cl2 seco e 2,1 mL de trietilamina seca (15mmol) foram adicionados à solução. A solução foi resfriada em um banho de gelo e 1,2 mL de cloreto de metanosulfonila destilado (15mmol) foi adicionado gota a gota. A solução foi agitada a temperatura ambiente sob nitrogênio durante a noite, e a reação foi extinta pela adição de 2 mL de etanol absoluto. A mistura foi evaporada sob vácuo para remover solvente, principalmente aqueles além de tolueno, filtrada, concentrada sob vácuo, e então precipitada em 100 mL de éter dietílico. O filtrado foi lavado com várias porções de éter dietílico frio e seco sob vácuo para gerar o mesi- lato.
[00725]O mesilato (20g, 8mmol) foi dissolvido em 75 mL de THF e a solução foi resfriada a 4°C. À solução resfriada foi adicionada azida de sódio (1,56g, 24mmol). A reação foi aquecida em refluxo sob nitrogênio por 2 horas. Os solventes foram então evaporados e o resíduo diluído com CH2Cl2 (50mL). A fração orgânica foi lavada com solução de NaCl e seca com MgSO4 anidro. O volume foi reduzido a 20mL e o produto foi precipitado pela adição de 150mL de éter frio seco. Exemplo 20
[00726]Álcool 4-azido benzila pode ser produzido usando o método descrito em U.S. Patent 5,998,595, que é incorporado aqui pela referência. Cloreto de meta- nosulfonila (2,5g, 15,7mmol) e trietanolamina (2,8 mL, 20mmol) foram adicionados a uma solução de álcool 4-azido benzila (1,75 g, 11,0 mmol) em CH2Cl2 a 0°C e a reação foi deixada na geladeira por 16 horas. Um trabalho usual proporcionou o mesila- to como um óleo amarelo pálido. Este óleo (9,2 mmol) foi dissolvido em THF (20mL) e LiBr (2,0g, 23,0 mmol) foi adicionado. A mistura reacional foi aquecida em refluxo por 1 hora e foi então resfriada a temperatura ambiente. Para a mistura, foi adicionada água (2,5mL) e o solvente foi removido sob vácuo. O resíduo foi extraído com acetato de etila (3 x 15mL) e as camadas orgânicas combinadas foram lavadas com solução saturada de NaCl (10mL), seca com Na2SO4 anidro, e concentrada para gerar o brometo desejado.
[00727]m-PEG-OH 20kDa (2,0g, 0,1 mmol, Sunbio) foi tratado com NaH (12 mg, 0,5 mmol) em TFH (35 mL) e o brometo (3,32 g, 15 mmol) foi adicionado à mistura junto com uma quantidade catalítica de KI. A mistura resultante foi aquecida em refluxo por 12 horas. Água (1,0 mL) foi adicionada à mistura e o solvente foi removido sob vácuo. Ao resíduo foi adicionado CH2Cl2 (25 mL) e a camada orgânica foi separada, seca com Na2SO4 anidro, e o volume foi reduzido a aproximadamente 2mL. Adição gota a gota em uma solução de éter (150mL) resultou em um precipitado, o qual foi coletado para gerar mPEG-O-CH2-C6H4-N3. Exemplo 21
[00728]NH2-PEG-O-CH2CH2CO2H (PESO MOLECULAR 3400Da, 2,0 g) foi dissolvido em uma solução aquosa saturada de NaHCO3 (10 mL) e a solução foi resfriada a 0°C. Propionato de 3-azido-1-N-hidroxisuccinimida (5 equiv.) foi adicio-nado com a agitação vigorosa. Depois de 3 horas, 20 mL de H2O foi adicionado e a mistura foi agitada por mais 45 minutos a temperatura ambiente. O pH estava ajustado a 3 com 0,5 N de H2SO4 e NaCl foi adicionado para a concentração de aproxi-madamente 15 % em peso. A mistura reacional foi extraída com CH2Cl2 (100 mL x 3), seca com Na2SO4 e concentrada. Depois de precipitação com éter etílico frio, o produto foi coletado por filtração e seco sob vácuo para gerar o derivado PEG Ome- ga-carboxil-azida. Exemplo 22
[00729]À uma solução de acetilada de lítio (4 equiv.), preparada como co-nhecida na técnica e resfriada a -78°C em THF, é adicionado gota a gota uma solução de mPEG-OMs dissolvido em THF com agitação vigorosa. Depois de 3 horas, a reação é deixada para aquecer a temperatura ambiente e extinta com a adição de 1 mL de butanol. 20 mL de H2O é então adicionados e a mistura foi agitada por mais 45 minutos a temperatura ambiente. O pH foi ajustado a 3 com 0,5 N de H2SO4 e NaCl foi adicionado para a concentração de aproximadamente 15 % em peso. A mistura reacional foi extraída com CH2Cl2 (100 mL x 3), seca com Na2SO4 e concentrada. Depois de precipitação com éter etílico frio, o produto foi coletado por filtração e seco sob vácuo para gerar o 1-(but-3-inilóxi)-metoxipolietileno glicol (mPEG). Exemplo 23
[00730]Aminoácidos contendo azida e acetileno podem ser incorporados em sítios seletivamente em proteínas usando os métodos descritos em L. Wang, et al (2001) Science 292:498-500, J.W. Chin et al, Science 301:964-7 (2003)), J.W. Chin, et al (2002), Journal of the American Chemical Society 124:9026-9027 (2002), PNAS Estados Unidos da América 99:11020-11024: e, L. Wang, & P.G. Schultz, (2002) Chem Comm. 1:1-11. Uma vez os aminoácidos foram incorporados, a reação de ci- cloadição é realizada com 0,01 mM de proteína em tampão fosfato (PB), pH 8, em presença de 2 mM de derivado PEG, 1 mM de CuSO4, e ~1 mg de fio de Cu por 4 horas a 37oC. Exemplo 24
[00731]Este exemplo descreve a síntese de p-Acetil-D,L-fenilalanina (pAF) e derivados m-PEG-hidroxilamina.
[00732]A pAF racêmica é sintetizada usando o procedimento previamente descrito em Zhang, Z., Smith, B.A.C., Wang, L., Brock, A., Cho, C. & Schultz, P.G., Biochemistry, (2003) 42, 6735-6746.
[00733]Para sintetizar o derivado m-PEG-hidroxilamina, os seguintes proce-dimentos são completados. A uma solução de ácido (N-t-Boc-aminoóxi) acético (0,382 g, 2,0 mmol) e 1,3-diisopropilcarbodiimida (0,16 mL, 1,0 mmol) em diclorome- tano (DCM, 70 mL), que é agitado em temperatura ambiente (TA) por 1 hora, metóxi- polietileno glicol amina (m-PEG-NH2, 7,5 g, 0,25 mmol, Mt 30 K, de Bio Vectra) e Diisopropiletilamina (0,1 mL, 0,5 mmol) é adicionada. A reação é agitada em TA por 48 horas, e então é concentrada por cerca de 100 mL. A mistura é adicionada gota a gota para esfriar o éter (800 mL). O produto t-Boc-protegido precipitou e coletado por filtração, lavado por éter 3x100 mL. É ainda purificado por re-dissolução em DCM (100 mL) e precipitando em éter (800 mL) duas vezes. O produto é seco a vácuo produzindo 7,2 g (96%), confirmado por RMN e teste de Nihydrin.
[00734]O deBoc do produto protegido (7,0 g) obtido acima é realizado em 50% de TFA/DCM (40 mL) a 0oC por 1 hora e então a TA por 1,5 hora. Após a remoção a maioria do TFA a vácuo, o sal TFA do derivado hidroxilamina é convertido ao sal HCl por adição de HCl 4N em dioxano (1 mL) ao resíduo. O precipitado é dissolvido em DCM (50 mL) e re-precipitado em éter (800 mL). O produto final (6,8 g, 97%) é coletado por filtração, lavado com éter 3x 100 mL, seco a vácuo, estocado sob nitrogênio. Outro PEG (5K, 20K) derivados hidroxilamina são sintetizados usan- do os mesmos procedimentos. Exemplo 25 Análise de fosforilação de ERK1/2 induzida por FGF-21 WT e análogos PEG 30K:
[00735]Klotho beta humano estavelmente transfectada plaqueadas em 293 com a 100.000 células/poço (DMEM+10% SFB) em uma placa revestida poli-Lys. No dia seguinte, células estão 100% confluentes, meio é aspirado e substituído com um meio fresco e incubadas por uma noite. Após 24 horas, células são estimuladas com os análogos FGF-21 PEG 30K apropriados usando como FGF-21 WT padrão. Cada composto individual é preparado por diluição dos mesmo em PBS/BSA 1%. Células são tratados em triplicada por 10 min. Por 37oC no incubador. Após 10 minutos de incubação, o meio é cuidadosamente aspirado a partir de cada poço e 40 μL de tampão de lise de sinalização celular 1x gelado contendo inibidores pro- tease/fosfatase (coquetel PI, Na3VN4 e PMSF) são adicionados a cada poço para produzir lisados celulares. Placas de 96 poços no gelo por 20 minutos e então centri-fugadas a 4000 rpm por 10 minutos. Lisados celulares são congeladas a -80oC. Após, cada amostra é congelada e 10 μL de lisados celulares é adicionado a placa tratada com MSD revestida com anticorpo capturando ambas, as formas não fosfori- ladas e fosforiladas de ERK1/2. Incubação com anticorpo primário ocorre por 2 horas, então a placa é lavada várias vezes com tampão específico seguido pela adição do anticorpo secundário. Após 1 hora de incubação da placa é lavada novamente várias vezes. Tampão para leitura é adicionado a cada poço. Placa é transferida para máquina de leitura MSD. A curva que é produzida é baseada nas unidades de leitura ERK1/2 anti-fosforilado e EC50 é calculada usando Sigma Plot. A perda da atividade é calculada por divisão da EC50 do composto específico PEGilado 30 K com EC50 do WT. Exemplo 26: Protocolo de Ensaio de Fosforilação da ERK1/2 Celular (pERK) e Análise MSD
[00736]Células βKlotho-4 foram mantidas em DMEM+10% SFB + P/S + 0,5 mg/mL de Geneticina. Quando as células alcançaram 50-90% de confluência, elas foram tripsinizadas, e plaqueadas 100.000 células/poço em placas de 96 poços re-vestidas com poli-D-lys em DMEM+10% SFB + P/S.
[00737]O dia seguinte quando as células foram ~100% confluente, eles foram avaliados para garantir que o meio estava ainda vermelho, então o meio foi aspirado, 200 μL/poço de diluições seriadas de variantes FGF-21 (em PBS+1% de BSA) foram pipetados em placas de 96 poços. A placa de 96 poços foi então colocada em 37oC, incubador 5% de CO2 para exatamente 9 minutos. Os tratamentos FGF-21 foram então completamente aspirados, e 40 μL/poço de Tampão de Lise de Sinalização Celular 1x + Coquetel Inibidor de Protease Sigma 1x + Ortovanadato de Sódio 2 mM + PMSF 1 mM + Inibidor de Fosfatase MSD I 1x + Inibidor Fosfatase MSD II 1x + Coquetel Inibidor de Protease MDS 1x + PMSF MSD 2 mM foi adicionado. A placa foi colocada no gelo, e deixada por 25 minutos, enquanto, cada poço pipetado para cima e para baixo com pipetador P20 para mistura os lisados. Após misturar os poços, colocar o recipiente com gelo e placa em agitador 4C pelo tempo restante. Após 25 minutos, a placa foi centrifugada a 4000 rpm, 10 minutos, a 4C. Transferir os sobrenadantes para uma placa de 96 poços de fundo redondo em gelo. Análise MDS
[00738]Este ensaio foi feito usando o Ensaio MULTI-SPOT Meso Scale Dis-covery, Sistema de lisado de célula total, Kit Fosfo (T/Y 202/204; 185/187)/Total - Ensaio ERK1/2.
[00739]Todos os reagentes MDS foram descongelados em temperatura am-biente e todos os tampões necessários foram feitos pelas instruções do kit. Para cada poço, 150 μL de Bloqueador A foi adicionado a uma placa fosfoERK-Erktotal Duplex e ela foi permitida bloquear por 1 hora em temperatura ambiente em uma agitador. A placa foi então lavada 4x com 160 μL/poço de Tampão de Lavagem 1x. 16 μL/poço de Tampão de Lise + protease e inibidores de fosfatase (feito mais cedo para estimulação das células) foram adicionados e 10 μL/poço foram transferidos a partir do sobrenadante lisado gelado da placa para os poços da placa MSD (volume total então se torna 26 μL/poço). A placa MSD incubada por 3 horas em temperatura ambiente em um agitador, a placa foi então lavada 4x com 160 μL/poço de tampão de lavagem 1x. 25 μL/poço de anticorpo de detecção (diluído 50x em tampão de diluição de anticorpo) foram adicionados e colocados para incubar por 1 hora em temperatura ambiente em um agitador. A placa foi novamente lavada 4x com 160 μL/poço de tampão de lavagem 1x e 150 μL/poço de Tampão Vermelho T 1x foi adicionado após o qual a placa foi imediatamente lida em máquina MSD Sector Imager 2400. Quantificação BCA
[00740]O Kit de Ensaio de Proteína Pierce BCA foi utilizado. Padrão BSA foi diluída em placa de 96 poços a partir de uma concentração máxima de 2 mg/mL, com 2x diluições abaixo das colunas em Tampão de Lise de Sinalização Celular 1x (último grupo de poços foram tampões, não BSA). 25 μL/poço de padrões BSA foram pipetados em duplicatas para duas placas de 96 poços de MaxiSorp. Diluições 3x de lisados foram feitas em Tampão de Lise de Sinalização Célula 1x e 25 μL/poço foram adicionados a placas MaxiSorp. O reagente de trabalho foi feito como pela folha de instrução do Kit Pierce, onde 200 μL foram pipetados em cada poço em placas MaxiSorp. As placas incubadas em temperatura ambiente e foram lidas a À=562 em leitor de placa. Análise dos Dados
[00741]As concentrações foram calculadas para todos os lisados com o Kit BCA. Quando lisados são todos similares em concentração, então não foram norma-lizados para análise MSD. Para análise MSD, pontos médios de replicatas, cálculo do desvio padrão, e valores de CV. Uso de SigmaPlot para calcular os valores de EC50 para diluições seriadas de variantes FGF-21, e uso de Fold Above WT EC50 como critérios de escalonamento para as variantes. Resultados podem ser vistos na Figura 7a e 7b deste pedido. Exemplo 27: Processo de Cascata de FGF-21 Não-marcado Preparo da Solubilização do Corpo de Inclusão
[00742]Pasta celular foi ressuspensa por mistura a um sólido final de 10% em Tampão de Corpo de Inclusão (CI) I a 4oC (50 mM de Tris, pH 8.0; 100 mM de NaCl; 1 mM de EDTA; 1% de Triton X-100; 4oC0. Células foram lisadas por passagem de material ressuspenso através de um microfluidizador em um total de duas vezes, então elas foram centrifugadas (10.000 g; 15 min.; 4oC) e o sobrenadante foi decantado. O concentrado CI foi lavado por ressuspensão em um volume adicional de Tampão CI I (50 mM de Tris pH 8.0; 100 mM de NaCl; 1 mM de EDTA; 1% de Triton X-100; 4oC) e o material ressuspenso foi passado através do microfluidizador em um total de duas vezes, então ele foi centrifugado (10.000 g; 15 min; 4oC) e o sobrenadante decantado. O concentrado CI foi ressuspenso em um volume de Tam-pão CI II (50 mM de Tris pH 8.0; 100 mM de NaCl; 1 mM de EDTA; 4oC), então ele foi centrifugado (10.000 g; 15 min; 4oC) e o sobrenadante decantado. O concentrado CI foi então ressuspenso em % volume de tampão II (50 mM de Tris pH 8.0; 100 mM de NaCl; 1 mM de EDTA; 4oC). Ci foi aliquotado em recipientes apropriados, então ele foi centrifugado (10.000 g; 15 min; 4oC) e o sobrenadante foi decantado. Corpos de inclusão foram solubilizados (este é o ponto em que eles podem, de outra forma, ser estocados a -80oC até uso adicional). Solubilização do Corpo de Inclusão
[00743]Corpos de inclusão foram solubilizados para uma concentração final entre 10-15 mg/mL em tampão de solubilização (20 mM Tris, pH 8.0; 8M Uréia; 10 mM β-ME) e o solubilizado CI incubado em temperatura ambiente sob mistura constante por 1 hora. Material insolúvel foi removido por filtração (0,45 μm filtro PES) e a concentração da proteína foi ajustada (nem sempre necessário) por diluição com tampão de solubilização adicional (quando a concentração da proteína é alta). Re-envelopamento
[00744]Re-envelopamento por diluição a uma concentração final de proteína de 0,5 mg/mL em 20 mM de Tris, pH 8.0; 4oC. O re-envelopamento foi permitido por 18 a 24 horas a 4oC. Purificação
[00745]Reação de re-envelopamento filtrado através de um filtro 0,45 μM PES. Material carregado em uma coluna HP Q (GE Heathcare) equilibrada em Tam-pão A (20 mM Tris, pH 7.5). FGF-21 eluído com um gradiente linear por 20 CV a 100% de tampão B (20 mM Tris, pH 7.5; 250 mM de NaCl). FGF-21 monomérico foi agrupado. Pegilação e Purificação
[00746]O grupo tomado de Q HP e tampão trocado para 20 mM Tris, pH 8.0; 2 M uréia; 1 mM de EDTA. pH caiu para 4.0 com 50% de ácido acético glacial. Amostra concentrada caiu para 4,0±1,0 mg/mL. 12:1 molar de PEG em excesso foi adicionado e uma concentração final de ácido hidrazida 1%, pH 4.0 para a amostra. Incubar a 28oC por 48-72 horas. Adicionar um final de 50 mM de Tris base para reação PEG e diluir 10 vezes com água RO. Ter certeza que a condutividade é <1mS/cm e pH está entre 8.0-9.0. Material carregado em uma coluna Source 30Q (GE Healthcare) equilibrada em Tampão A (20 mM Tris, pH 8.0). PEG-FGF-21 elui com um gradiente linear por 20CV a 100% B (20 mM Tris, pH 8.0; 100 mM de NaCl). Grupo PEG-FGF-21 e troca de tampão em 20 mM Tris, pH 7.4; 150 mM NaCl. Concentrar o material PEG entre 1-2 mg/mL e esterilizar por filtração usando filtro 0,22 μm PES. Estocar a 4oC. Para estocagem prolongada, congelar rapidamente a -80oC. Exemplo 28 Propriedades farmacocinéticas dos compostos FGF-21 em ratos
[00747]Este protocolo foi usado a fim de prover dados (encontrados nas Fi-guras 11-23) nas propriedades farmacocinéticas de compostos FGF-21 Nativos ou modificados com peg produzidos por tecnologia pertencente a ambrix em ratos ca-racterizados. As farmacocinéticas de artigos testes foram avaliadas por ELISA espe-cífico para FGF-21 humano a partir de amostras séricas obtidas em pontos de tempos específicos após a dose da droga. Teste dos artigos: 1 .Composto Ambrix PEG-R77 FGF-21 será usado em 0,25 mg/mL diluído em PBS 1x. 2 .Composto Ambrix PEG-Y104 FGF-21 será usado em 0,25 mg/mL diluído em PBS 1x. 3 .Composto Ambrix PEG-R126 FGF-21 será usado em 0,25 mg/mL diluído em PBS 1x. Qualidade do Artigo Teste/ Formulação: Concentrações Estoques: 1,0 mg/mL PEG-R77 FGF-21 1,16 mg/mL PEG-Y104 FGF-21 1,08 mg/mL PEG-R126 FGF-21 Animais:
[00748]Doze (12) ratos machos Sprague-Dawley (SD) pesando aproxima-damente 250-275 gramas no início do estudo terão catéteres cirurgicamente colocados na veia jugular antes de chegar a Ambrx. Animais foram recebidos a partir de CRL em boas condições e serão aclimatados ao local do estudo por pelo menos 3 dias antes do início do estudo. Ratos serão pesados no dia da administração do artigo teste. Animais serão mantidos em condições padrões, livres de patógeno com comida e água a vontade. Grupos de Animais: Todos os compostos serão administrados subcutanea- mente Grupo 1 (n=4): PEG-R77 injeção SC (0,25 mg/kg). Grupo 2 (n=4): PEG-Y104 injeção SC (0,25 mg/kg). Grupo 3 (n=4): PEG-R126 injeção SC (0,25 mg/kg).
[00749]Animais são pesados antes da administração do artigo teste. Com-postos são formulados de forma a serem administrados em 1X PM em μL. Adminis-tração subcutânea de artigo teste é injetado na região escapular dorsal. Animais re-ceberão uma injeção única do artigo teste (tempo =0). Em pontos de tempo específicos (ver abaixo). Sangue total será coletado a partir de animais, coletado em tubos de coleta de microtainer SST. Soro será permitido goagular por 30 minutos antes da centrifugação. Soro será transferido para tubos titulados de polipropileno, selados com microstrips, e estocados a -80oC até análise por ELISA para determinar concen-trações séricas do FGF-21. Coleta de Dados/Ponto Final:
[00750]Cada animal será usado para um completo curso temporal da FC. Aproximadamente 0,25 mL de sangue total será retirado dos catéteres da veia jugular. Imediatamente após a coleta de sangue, os catéteres serão fluídos com 0,1 mL de salina. Os seguintes pontos de tempo de coleta para animais recebendo o material artigo teste são requeridos baseados no perfil famacocinético antecipado dos artigos testes: Pré-sangramento, 1, 2, 4, 8, 24, 48, 56, 72 e 96 horas pós-dose. Terminação: Todos os animais serão eutanasiados seguindo o término do estudo. Resultados: Resultados são dados na tabela abaixo e nas figuras acompanhando este pedido. Propriedades FC de Isômero PEG FGF-21 - IV Propriedades FC Isômero PEG FGF-21 - SC
Tmax aumentado de compostos PEGilados T1/2 aumentado de compostos PEGilados AUC aumentado de compostos PEGilados Atributos FC dependentes do sítio de PEGilação Exemplos 29 Estudos in vivo de FGF-21 PEGilado
[00751]PEG-FGF-21, FGF-21 não modificado e solução tampão são admi-nistrados a camundongos e ratos. Os resultados mostrarão atividade superior e meia vida prolongada de FGF-21 Pegilado da presente invenção comparado a FGF-21 não modificado. Similarmente, FGF-21 modificado, FGF-21 não modificado, e solução tampão são administrados a camundongos e ratos. Análise Farmacocinética
[00752]WO 2005/091944 descreve estudos farmacocinéticos que podem ser feitos com compostos FGD-21 da presente invenção. Um polipeptídeo FGF-21 da invenção é administrado por vias intravenosas ou subcutâneas a camundongos. Os animais são sangrados antes e em pontos de tempo após a dose. Plasma é coletado a partir de cada amostra e analisado por radioimunoensaio. Meia vida de eliminação pode ser calculada e comparada entre polipeptídeos FGF-21 compreendendo um aminoácido não naturalmente codificado e FGF-21 selvagem ou várias formas de polipeptídeos FGF-21 da invenção. Similarmente, polipeptídeos FGF-21 da invenção podem ser administrados em macacos cinomolgos. Os animais são sangrados antes e em pontos de tempo após a dose. Plama é coletado a partir de cada amostra e analisado por radioimunoensaio.
[00753]Polipeptídeos da invenção podem ser administrados a ratos machos ZDF (ratos obesos, diabéticos; 8 semanas de idade no início do estudo, Charles River - GMI). Ratos são alimentados com ração Purina 5008 a vontade. Os seguintes grupos teste são feitos: Salina; Insulina 4U/dia; FGF-21, 500 μg/dia Aguda (grupo de dose aguda é dosado uma vez e sangrado em T=0, 2, 4, 8 e 24 horas após a dose); FGF-21, 100 μg/dia; FGF-21, 250 μg/dia; FGF-21, 500 μg/dia; FGF-21 (uma vez/dia) 500 μg/dia; salina não gordurosa; Insulina não gordurosa 4U/dia; FGF-21 não gorduroso 500 μg/dia. Grupos Lean representam ratos ZDF não gorduroso, não diabéticos.
[00754]Compostos são injetados s.c. (Duas vezes ao dia.), exceto pelo se-gundo grupo 500 μg/dia que recebe uma injeção por dia para duração do estudo (7 dias). Ratos controle são injetados com veículo (PBS; 0,1 mL). Seguindo 7 dias de dose, os animais são sujeitos a um teste de tolerância de glicose oral. Sangue para glicose e triglicerídeos é coletado por sangramento por corte da cauda sem anestésico. Polipeptídeos FGF-21 podem reduzir os níveis de glicose plasmática em uma forma dose-dependente. Também ratos magros podem não se tornar hipoglicêmicos após a exposição dos polipeptídeos FGF-21 da invenção quando comparados a ratos dosados com insulina. Modelo de Obesidade ob/ob
[00755]O modelo de camundongo ob/oc é um modelo animal para hipergli- cemina, resistência a insulina e obesidade. Os níveis de glicose plasmática após tratamento com polipeptídeo FGF-21 comparado aos grupos veículo e controle insu-lina podem ser medidos em camundongos ob/ob. Neste modelo de obesidade, os grupos testes de camundongos machos ob/ob (7 dias de idade) são injetados com veículo sozinho (PBS), insulina (4U/dia), ou polipeptídeo FGF-21 (5 μg/dia e 25 μg/dia), subcutaneamente (0,1 mL, duas vezes ao dia) por sete dias. Sangue é cole-tado por sangramento do corte da cauda nos dias 1, 3 e 7, uma hora antes da primeira injeção do composto, e níveis de glicose plasmática são medidos usando um protocolo padrão. Polipeptídeos FGF-21 da invenção estimulam a captação de glico- se se eles reduzem os níveis de glicose plasmática quando comparados ao grupo controle veículo. Níveis de triglicerídeos podem ser comparados após o tratamento com polipeptídeos FGF-21 da invenção comparado a outras moléculas. O polipeptí- deo pode ser administrado a camundongos através de doses múltiplas, infusão contínua, ou dose única etc. Exemplo 30
[00756]Avaliação Farmacocinética de análogos FGF-21: As propriedades farmacocinéticas de análogos PEG30K-pAF(N6-His)FGF21 com sítios variando de conjugação PEG foram avaliados em rato. Outros parâmetros estudados foram PM PEG, bem como dose de composto administrada. A porcentagem de biodisponibili- dade para uns poucos variantes PEG30K-pAF(N6-His)FGF21foi determinada.
[00757]Animais: Toda experimentação com animal foi conduzida sob proto-colos aprovados pelo Comitê de Uso e Cuidado de Animal Instituicional. Ratos Spra-gue-Dawley machos (175-300 g) foram obtidos a partir de Laboratórios Charles River. Ratos foram colocados individualmente em gaiolas em salas com ciclo 120h luz/escuro e aclimatado ao vivário Ambrx por pelo menos 3 dias antes da experimen-tação. Animais tiveram acesso provido a ração de roedor 5001 Purina certificada e água a vontade.
[00758]Dose e Coleta de Soro: Catéteres foram cirurgicamente instalados na veia jugular para coleta de sangue por CRL antes do envio. Seguindo a colocação do catéter com sucesso, animais foram separados para grupos de tratamento antes da dose. Uma dose única de composto foi administrada intravenosamente ou subcu- taneamente em um volume de dose de 1 mL/kg. Concentrações de dose do composto foram derivadas pela diluição em PBS usando a concentração estoque como de-terminado no certificado de Liberação. Amostras de sangue foram coletadas em vários pontos de tempo através do catéter colocado e colocadas em tubos de micro- centrífuga SST. Soro foi coletado após a centrifugação, e estocado a -80oC até análise.
[00759]Análise Farmacocinética: O ensaio para a quantificação de PEG- FGF-21 em soro de rato Sprague-Dawley foi desenvolvido em Ambrx Inc., La Jolla, CA. Poços de microplaca são revestidos com anticorpo policlonal IgG de cabra anti- FGF-21 humano. Amostras Padrões (PD) e Controle de qualidade (CQ), ambas, feitas por injeção de análogo PEG-FGF-21 em 100% de soro de rato Sprague Sawley, e estudo de amostras são colocadas em poços após o pré-tratamento 1:100 com tampão Bloqueador I. O FGF-21 nos PDs, CQs e amostras de estudo é capturado por Pab imobilizado. Materiais não ligados são removidos por lavagem dos poços. Pab IgG biotinilado de cabra anti-FGF-21 humano (RnD Systems, clone BAF2539) é adicionado aos poços seguido por um passo de lavagem e a adição de estreptavidi- na-peroxidase rábano silvestre (SA-HRP; RnD Systems, Catálogo #DY998) para detecção do PEG-FGF-21 capturado. Após o passo de lavagem, solução de substrato tetrametilbenzidina (TMB, Kirkegaard Perry Laboratories) é adicionado aos poços. TMB reage com o peróxido em presença de HRP e produz um sinal colorimétrico proporcional a quantidade de PEG-FGF-21 análogo ligado pelo reagente de captura no passo inicial. O desenvolvimento de cor é parado pela adição de ácido sulfúrico 2N e a intensidade da cor (densidade ótica, DO) é medida a 450 nm. A conversão de unidades DO para as amostras do estudo e os CQs para concentração é alcançado através de um programa de computador mediado pela comparação a uma curva pa-drão na mesma placa, que é regresso de acordo com um modelo de regressão de logística de parâmetro 5 usando pacote de redução de dados SOFTmax Pro v5. Re-sultados são relatados em unidades de concentração ng/mL.
[00760]Concentrações podem também ser medidas por um ensaio de san-duíche de duplo anticorpo ou outros métodos conhecidos pelos versados na técnica. Concentrações foram calculadas usando uma curva padrão geradas a partir de um composto de dose correspondente. Parâmetros farmacocinéticos foram estimados usando o programa de modelamento WinNonlin (Pharsight, versão 4.1). Análise não comportamental para dados de animal individual com integração trapezóide line- ar/corte-baixo foi usada, e dados de concentração foi uniformemente pesado.
[00761]Conclusões: As propriedades farmacocinéticas de N6-His FGF21 WT foi alinhadas com aquele relatado por Kharitonenkov et al, 2005 e foi comparável a proteína FGF21 WT não marcada.
[00762]Os perfis farmacocinéticos de isômeros PEG30K-pAF(N6-His)FGF21 foram significantemente aumentados pela adição de uma molécula PEG 30kDa como comparado a resultados obtidos a partir de FGF21 (não PEGilado) WT.
[00763]Os compostos PEGilados exibiram marcadamente diferentes perfis FC quando dosados em 0,25 mg/kg nível subcutaneamente. H87 e L86 tendem a ter FC inferior atribuído como comparado a outros isômeros. Ainda, compostos R131 e Q108 PEG30 diferencialmente geraram propriedades FC superiores. Mais especificamente, esses compostos tiveram AUC, Cmax e meia vida terminal aumentados. Uma análise estrutura-atividade mais profunda pode revelar explicações estruturais para várias propriedades FC de cada isômero.
[00764]Comparação do peso molecular PEG mostrou PEG30K-pAF91(N6- His)FGF21 tem uma persistência levemente maior na circulação que PEG20K- pAF91(N6-His)FGF21. Entretanto, como o isômero 20 kDa tem um valor Cmax maior, o AUCinf total para os dois compostos foi comparável. Biodisponibilidade para a isoforma de 20 kDa foi levemente melhor que a variante 30 kDa em 30% versus 20%, respectivamente. Tabela 3: Valores do parâmetro farmacocinético para compostos dosados em 0,25 mg/kg subcutaneamente em rato.
[00765]Concentração sérica versus curva de tempo foram avaliados por aná-lise não comportamental (Pharsight, versão 4.1). N=3-4 ratos por composto. ND: não feito; NE: não avaliado.
[00766]Tmax: tempo para alcançar Cmax; Cmax: concentração máxima; t1/2 terminal: meia vida terminal; AUCúltimo: área sob a curva de concentração-tempo para a última amostra de plasma/ponto de tempo; AUCinf: área sob a curva concentração-tempo extrapolada para infinidade; MRT: tempo médio de residência; Cl/f: depuração de plasma total aparente; Vz/f: volume aparente de distribuição durante fase terminal. Tabela 4. Valores de parâmetro farmacocinético para PEG20K-pAF91(N6- hHis)FGF21 dosado 0,25 mg/kg subcutaneamente em rato.
[00767]Curvas de concentração versus tempo foram avaliados por análise não comportamental (Pharsight, versão 4.1). ND: não feito; NE: pode não ser avaliado. Tmax: tempo para alcançar Cmax; Cmax: concentração máxima; Terminal1/2: meia vida terminal; AUCfinal: área sob a curva de concentração-tempo para a última amostra de plasma/ponto de tempo; AUCinf: área sobre a curva concentração-tempo extrapolada para infinidade; MRT: média do tempo de resistência; Cl/f: depuração do plasma total aparente; Vz/f: volume aparente de distribuição durante a fase terminal. Exemplo 31 Teste Clínico Humano de Segurança e/ou Eficácia do FGF-21 PEGilado compreendendo um Aminoácido Não Naturalmente codificado
[00768]Objetivo: Para observar a segurança e farmacocinética de FGF-21 humano recombinante PEGilado subcutaneamente administrado compreendendo um aminoácido não naturalmente codificado.
[00769]Pacientes: dezoito voluntários saudáveis variando entre 20-40 anos de idade e peso entre 60-90 kg são inscritos neste estudo. Os pacientes não terão valores de laboratório clinicamente anormais significantes para hematologia ou química do soro, e um estudo toxicológico de urina negativo, estudo de HIV, e antígeno de superfície de hepatite B. Eles não devem ter qualquer evidência do seguinte: hi-pertensão; uma história de qualquer doença hematológica primária; história de do-ença hepática, cardiovascular, gastrointestinal, genitourinário, metabólica, doença neurológica significante; uma história de anemia ou distúrbio de epilepsia; uma sen-sibilidade a produtos bacterianos ou derivados de mamíferos conhecidos, PEG, ou albumina sérica humana; consumo habitual ou pesado de bebidas contendo cafeína; participação em qualquer outro teste clínico ou tiveram sangue transfundido ou doado dentro de 30 dias da entrada do estudo; tiveram exposição a FGF-21 dentro de três meses da entrada do estudo; tiveram uma doença dentro de sete dias da entrada do estudo; e têm anormalidades significantes no exame pré-estudo físico ou nas avaliações laboratoriais clínicas dentro de 14 dias da entrada de estudo. Todos os pacientes são avaliados para segurança e todas as coletas de sangue para análise de farmacocinética são coletadas como esquematizado. Todos os estudos são feitos com aprovação do comitê ético institucional e consenso do paciente.
[00770]Desenho do Estudo: Esta será a Fase I, centro único, marcação aberta, aleatório, estudo de ligação cruzada de dois períodos em voluntários de machos saudáveis. Dezoito pacientes são aleatoriamente distribuídos a um de dois grupos de sequência de tratamento (nove pacientes/grupo). FGF-21 é administrado ao longo de dois períodos de doses separadas como uma injeção bolus s.c. na coxa superior usando doses equivalentes do FGF-21 PEGilado compreendendo um ami- noácido não naturalmente codificado e o produto comercialmente disponível escolhido. A dose e frequência de administração do produto comercialmente disponível é como instruída na bula da embalagem. Dose adicional, frequência de dose, ou outro parâmetro como desejado, usando os produtos comercialmente disponíveis podem ser adicionados ao estudo por inclusão de grupos adicionais de pacientes. Cada período de dosagem é separado por um período de descanso de 14 dias. Pacientes são confinados ao centro de estudo pelo menos 12 horas antes a e 72 horas seguindo a dose para cada um dos dois períodos de dosagem, mas não entre os períodos de dosagem. Grupos adicionais de pacientes podem ser adicionados se existem doses adicionais, frequência, ou outro parâmetro a ser testado para o FGF-21 PEGilado também. A formulação experimental do FGF-21 é o FGF-21 PEGilado compreendendo um aminoácido não naturalmente codificado.
[00771]Amostra de sangue: sangue seriado é coletado por punção direta na veia antes e após administração do FGF-21. Amostras de sangue venoso (5 mL) para determinação das concentrações de FGF-21 sérico são obtidas em cerca de 30, 20 e 10 minutos antes da dose (3 amostras iniciais) e em aproximadamente os seguintes tempos após a dosagem: 30 minutos e em 1, 2, 5, 8, 12, 15, 18, 24, 30, 36, 48, 60 e 72 horas. Cada amostra de soro é dividida em duas alíquotas. Todas as amostras de soro são estocadas a -20oC. Amostras de soro são enviadas no gelo seco. Testes de laboratório clínico em jejum (hematologia, química do soro, e urináli- se) são feitos imediatamente antes a dose inicial no dia 1, a manhã do dia 4, imediatamente antes da dose no dia 16, e na manhã do dia 19. Métodos Bioanalíticos. Um kit ELISA é usado para a determinação das con-centrações de FGF-21 séricas.
[00772] Determinações de Segurança. Sinais vitais são gravados imediata-mente antes de cada dosagem (Dias 1 e 16), e nas 6, 24, 48 e 72 horas após cada dose. Determinações de segurança são baseadas na incidência e tipo de eventos adversos e mudanças nos testes clínicos de laboratórios a partir do basal. Em adição, mudanças a partir do pré-estudo em medidas de sinais vitais, incluindo pressão sanguínea, e resultados de exame físico são avaliados.
[00773]Análise de Dados. Valores de concentração sérica pós-dose são cor-rigidos para concentrações de FGF-21 basais na pré-dose por subtração de cada um dos valores pós-dose da média da concentração do FGF-21 basal determinado a partir da média dos níveis de FGF-21 a partir de três amostras coletadas em 30, 20 e 10 minutos antes da dosagem. Concentrações FGF-21 séricas na pré-dosagem não são incluídas no cálculo do valor médio se elas estão abaixo do nível de quantificação do ensaio. Parâmetros farmacocinéticos são determinados a partir dos dados de concentração sérica para as concentrações de FGF-21 basais. Parâmetros farmaco- cinéticos são calculados por métodos independentes de modelo em um sistema computacional Digital Equipament Corporation VAX 8600 usando a última versão do programa BIOAVL. Os seguintes parâmetros farmacocinéticos são determinados: pico de concentração sérica (Cmax); tempo do pico de concentração sérica (tmax); área sob a curva concentração-tempo (AUC) a partir do tempo zero para o último tempo de amostra de sangue (AUC0-72) calculado com o uso de regras trapezóides lineares; e meia vida de eliminação terminal (t1/2), computados a partir da taxa de eliminação constante. A taxa de eliminação constante é estimada por regressão linear de pontos de dados consecutivos na região linear terminal do gráfico de con-centração-tempo log-linear. A média, desvio padrão (DP), e coeficiente de variação (CV) dos parâmetros farmacocinéticos são calculados para cada tratamento. A pro-porção das médias dos parâmetros (formulação conservada/formulação não conser-vada) é calculada.
[00774]Resultados de Segurança. A incidência de eventos adversos é igualmente distribuída através dos grupos de tratamento. Existem mudanças clini-camente significantes a partir dos testes laboratoriais basais ou pré-estudo clínico ou pressões sanguíneas, e nenhuma mudança notável a partir do pré-estudo em resul-tados de exame físico e medidas de sinais vitais. Os perfis de segurança para os dois grupos de tratamento devem parecer similares.
[00775]Resultados Farmacocinéticos: Médias dos perfis de concentração- tempo FGF-21 sérico (não corrigidos para níveis de FGF-21 basais) em todos os 18 pacientes após receber FGF-21 PEGilados compreendendo um aminoácido não na-turalmente codificado em cada ponto de tempo medido. Todos os pacientes devem ter concentrações de FGF-32 basais de pré-dose dentro da variação fisiológica normal. Parâmetros farmacocinéticos são determinados a partir dos dados séricos corrigidos para média da concentração do FGF-21 basal na pré-dose e Cmax e tmax são determinados. O tmax médio para comparador(es) clínico(s) escolhido(s) é(são) significantemente mais curtos que o tmax para FGF-21 PEGilado compreendendo o aminoácido não naturalmente codificado. Os valores de meia vida terminais são sig-nificativamente mais curtos para comparador(es) pré-clínicos testados comparados com a meia vida terminal para o FGF-21 PEGilado compreendendo um aminoácido não naturalmente codificado.
[00776]Embora o presente estudo seja conduzido em pacientes masculinos saudáveis, características de absorção similar e perfis de segurança podem ser an-tecipados em outras populações de paciente; tais pacientes masculinos ou femininos com câncer ou falência renal crônica, pacientes com falência renal pediátrica, paci-entes em programas de pré-depósito autólogo, ou pacientes com cirurgia eletiva agendada.
[00777]Em conclusão, doses únicas subcutaneamente administradas de FGF-21 PEGilado compreendendo aminoácido não naturalmente codificado serão seguras e bem toleradas por pacientes masculinos saudáveis. Baseado em uma in-cidência comparativa de eventos adversos, valores de laboratório clínico, sinais vitais, e resultados de exame físico, os perfis de segurança das formas comercialmente disponíveis de FGF-21 e FGF-21 PEGilado compreendendo aminoácido não natu-ralmente codificado serão equivalentes. O FGF-21 PEGilado compreendendo ami- noácido não naturalmente codificado potencialmente provê grande utilidade clínica para pacientes e provedores de assistência a saúde.
[00778]É entendido que os exemplos e modalidades descritos aqui são para propósitos ilustrativos somente e que várias modificações ou mudanças na luz dos mesmos sugerirão aos versados na técnica e serão incluídos dentro do espírito e alcance deste pedido e objetivo das reivindicações em anexo. Todas as publicações, patentes , pedidos de patentes, e/ou outros documentos citados neste pedido incor-porados em sua totalidade para todos os propósitos para a mesma extensão como se cada publicação individual, patente, pedido de patente, e/ou outro documento fossem individualmente indicados a ser incorporados por referência para todos os propósitos. TABELA 5: Sequências Citadas.
Claims (41)
1. Polipeptídeo FGF-21 CARACTERIZADO pelo fato de que contém um aminoácido codificado não-naturalmente, em que: (a) o polipeptídeo FGF-21 tem a sequência de aminoácidos consistindo na SEQ ID NO:1, SEQ ID NO:1 fundida a uma metionina N-terminal, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:5 fundida a uma metionina Nterminal, SEQ ID NO:6 ou SEQ ID NO:7; em que a referida sequência de aminoácidos é substituída com o referido aminoácido codificado não-naturalmente localizado nos resíduos 72, 77, 86, 108, 110, 131 ou 146 da SEQ ID NO:1 ou na posição do aminoácido correspondente na SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6 ou SEQ ID NO:7; (b) o aminoácido codificado não-naturalmente tem a estrutura: em que o grupo R é qualquer substituinte diferente da cadeia lateral encontrada em alanina, arginina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutâmico, glicina, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina, valina, pirrolisina, ou selenocisteína; (c) o polipeptídeo FGF-21 mantém a atividade biológica dos polipeptídeos FGF-21 humanos; (d) o aminoácido codificado não-naturalmente está ligado a um ligante, polímero, ou molécula biologicamente ativa; e (e) o polipeptídeo FGF-21 tem uma meia vida in vivo pelo menos duas vezes maior do que o polipeptídeo FGF-21 humano na SEQ ID NO:1.
2. Polipeptídeo FGF-21, de acordo com a reinvindicação 1, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente é um derivado de fenilalanina.
3. Polipeptídeo FGF-21, de acordo com a reinvindicação 1 ou 2, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente compreende um primeiro grupo funcional e o ligante, polímero ou molécula biologicamente ativa compreende um segundo grupo funcional, em que o primeiro grupo funcional e o segundo grupo funcional não são idênticos e cada um compreende um grupo carbonil, um grupo aminoóxi, um grupo hidrazida, um grupo hidrazina, um grupo semicarbazida, um grupo azida, ou um grupo alcino.
4. Polipeptídeo FGF-21, de acordo com a reinvindicação 3, CARACTERIZADO pelo fato de que o primeiro grupo funcional no aminoácido codificado não-naturalmente é uma fração carbonil e o segundo grupo funcional no ligante, polímero ou molécula biologicamente ativa é uma fração aminoóxi e a ligação covalente resultante criada pela reação do primeiro e do segundo grupos funcionais é uma ligação oxima.
5. Polipeptídeo FGF-21, de acordo com a reinvindicação 3, CARACTERIZADO pelo fato de que o primeiro grupo funcional no aminoácido codificado não-naturalmente é uma fração azida e o segundo grupo funcional no ligante, polímero ou molécula biologicamente ativa é uma fração alcino.
6. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 5, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente está ligado a um polímero.
7. Polipeptídeo FGF-21, de acordo com a reivindicação 6, CARACTERIZADO pelo fato de que o polímero compreende poli(etilenoglicol).
8. Polipeptídeo FGF-21, de acordo com a reivindicação 7, CARACTERIZADO pelo fato de que o poli(etilenoglicol) tem um peso molecular médio de entre 0,1 kDa e 100 kDa.
9. Polipeptídeo FGF-21, de acordo com a reivindicação 7, CARACTERIZADO pelo fato de que o poli(etilenoglicol) tem um peso molecular médio de 30 kDa.
10. Polipeptídeo FGF-21, de acordo com a reivindicação 6, CARACTERIZADO pelo fato de que o polímero é um oligossacarídeo.
11. Polipeptídeo FGF-21, de acordo com qualquer uma das reinvindicações 1 a 10, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem uma meia vida in vivo de pelo menos cinco vezes maior do que o polipeptídeo FGF-21 humano na SEQ ID NO:1.
12. Polipeptídeo FGF-21, de acordo com qualquer uma das reinvindicações 1 a 11, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem uma meia-vida in vivo de 10 vezes a 40 vezes maior do que o polipeptídeo FGF-21 humano na SEQ ID NO:1.
13. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 12, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente está em uma posição correspondente ao resíduo 108 da SEQ ID NO:1.
14. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 3, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente é selecionado a partir de uma fenilalanina para-substituída, orto-substituída ou metasubstituída compreendendo um grupo carbonil, um grupo aminoóxi, um grupo hidrazida, um grupo hidrazina, um grupo semicarbazida, um grupo azida ou um grupo alcino.
15. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 14, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente é para-acetil-L-fenilalanina.
16. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 15, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem a sequência de aminoácidos consistindo na SEQ ID NO: 1 ou SEQ ID NO:1 fundida a uma metionina N-terminal.
17. Polipeptídeo FGF-21, de acordo com a reivindicação 16, CARACTERIZADO pelo fato de que (a) o polipeptídeo FGF-21 tem a sequência de aminoácidos consistindo na SEQ ID NO: 1 fundida a uma metionina N-terminal contendo para-acetil-L-fenilalanina no resíduo 108 da SEQ ID NO:1, (b) a referida para-acetil-L-fenilalanina está ligada a um polímero, e (c) o referido polímero compreende poli(etilenoglicol) tendo um peso molecular médio de 30 kDa.
18. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 15, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem a sequência de aminoácidos da SEQ ID NO: 1 e contém a referida substituição de um aminoácido com um aminoácido codificado não-naturalmente.
19. Polipeptídeo FGF-21, de acordo com a reinvindicação 1, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem a sequência de aminoácidos da SEQ ID NO: 1 contendo a referida substituição de um aminoácido como referido aminoácido codificado não-naturalmente, em que: (a) o referido aminoácido codificado não-naturalmente está no resíduo 108 da SEQ ID NO: 1; (b) o referido aminoácido codificado não-naturalmente compreende para-acetil-fenilalanina ligada a um polímero compreendendo um poli(etilenoglicol), em que o referido poli(etilenoglicol) tem um peso molecular médio de 30 kDa; e (c) o referido aminoácido codificado não-naturalmente está ligado ao referido polímero através de uma ligação oxima.
20. Polipeptídeo FGF-21, de acordo com a reinvindicação 19, CARACTERIZADO pelo fato de que o referido polímero compreende um grupo aminoóxi, e o referido aminoácido codificado não-naturalmente está ligado ao referido polímero através da referida ligação oxima formada por uma reação da referida paraacetil-fenilalanina com o referido grupo aminoóxi.
21. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 1 a 15, CARACTERIZADO pelo fato de que o referido polipeptídeo FGF-21 tem a sequência de aminoácidos SEQ ID NO:1 fundida a uma metionina N-terminal e contendo a referida substituição de um aminoácido com um aminoácido codificado não-naturalmente.
22. Polipeptídeo FGF-21, de acordo com a reinvindicação 1, CARACTERIZADO pelo fato de que o polipeptídeo FGF-21 tem a sequência de aminoácidos consistindo na SEQ ID NO: 1 fundida a uma metionina N-terminal, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 fundida a uma metionina Nterminal, SEQ ID NO: 6 ou SEQ ID NO: 7; em que a referida sequência de aminoácidos contém a referida substituição de um aminoácido com o aminoácido codificado não naturalmente na posição 108 da SEQ ID NO: 1 ou a posição de aminoácido correspondente na SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 ou SEQ ID NO: 7.
23. Polipeptídeo FGF-21, de acordo com a reinvindicação 22, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente é um derivado de fenilalanina ou é para-acetil-L-fenilalanina.
24. Polipeptídeo FGF-21, de acordo com a reivindicação 22 ou 23, CARACTERIZADO pelo fato de que o aminoácido codificado não-naturalmente compreende um primeiro grupo funcional e o ligante, polímero ou molécula biologicamente ativa compreende um segundo grupo funcional, em que o primeiro grupo funcional e o segundo grupo funcional não são idênticos e cada um compreende um grupo carbonil, um grupo aminoóxi, um grupo hidrazida, um grupo hidrazina, um grupo semicarbazida, um grupo azida, ou um grupo alcino.
25. Polipeptídeo FGF-21, de acordo com a reinvindicação 24, CARACTERIZADO pelo fato de que o primeiro grupo funcional no aminoácido codificado não-naturalmente é uma fração carbonil e o segundo grupo funcional no ligante, polímero ou molécula biologicamente ativa é uma fração aminoóxi, e a ligação covalente resultante criada pela reação do primeiro e segundo grupos funcionais é uma ligação oxima.
26. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 22 a 25, CARACTERIZADO pelo fato de que o polímero compreende um poli(etilenoglicol).
27. Polipeptídeo FGF-21, de acordo com a reivindicação 26, CARACTERIZADO pelo fato de que o referido poli(etilenoglicol) tem um peso molecular médio de entre 0,1 kDa e 100 kDa.
28. Polipeptídeo FGF-21, de acordo com a reivindicação 27, CARACTERIZADO pelo fato de que o referido poli(etilenoglicol) tem um peso molecular médio de 30 kDa.
29. Polipeptídeo FGF-21, de acordo com a reinvindicação 1, CARACTERIZADO pelo fato de que o referido polipeptídeo FGF-21 tem a sequência de aminoácidos que consiste na SEQ ID NO: 1 fundido a uma metionina N-terminal, exceto que um aminoácido no polipeptídeo FGF-21 é substituído pelo referido aminoácido codificado não-naturalmente na posição 108 da SEQ ID NO: 1; (b) o referido aminoácido codificado não-naturalmente compreende para-acetil-Lfenilalanina ligada ao referido polímero, em que o referido polímero compreende um poli(etilenoglicol), em que o referido poli(etilenoglicol) tem um peso molecular médio de 30 kDa; e (c) a referida para-acetil-L-fenilalanina está ligada ao referido polímero através de uma ligação oxima.
30. Polipeptídeo FGF-21, de acordo com a reinvindicação 1, CARACTERIZADO pelo fato de que o referido polipeptídeo FGF-21 tem a sequência de aminoácidos que consiste na SEQ ID NO: 1 fundida a uma metionina N-terminal, exceto que um aminoácido no polipeptídeo FGF-21 é substituído pelo referido aminoácido codificado não-naturalmente na posição 108 da SEQ ID NO: 1; (b) o referido aminoácido codificado não-naturalmente compreende para-acetil-Lfenilalanina ligada a um poli(etilenoglicol), em que o referido poli(etilenoglicol) tem um peso molecular médio de 30 kDa; e (c) a referida para-acetil-L-fenilalanina está ligada ao referido polímero através de uma ligação oxima.
31. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 26 a 30, CARACTERIZADO pelo fato de que o referido polipeptídeo FGF-21 tem uma meia vida in vivo pelo menos duas vezes maior do que o polipeptídeo FGF-21 humano da SEQ ID NO:1.
32. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 26 a 31, CARACTERIZADO pelo fato de que o referido poli(etilenoglicol) compreende um monometoxi-polietilenoglicol.
33. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 26 a 31, CARACTERIZADO pelo fato de que o referido poli(etilenoglicol) compreende um polietilenoglicol linear.
34. Polipeptídeo FGF-21, de acordo com qualquer uma das reivindicações 26 a 31, CARACTERIZADO pelo fato de que o referido poli(etilenoglicol) compreende um monometoxi-polietilenoglicol linear.
35. Método para produzir o polipeptídeo FGF-21, como definido na reivindicação 1, CARACTERIZADO pelo fato de que compreende contatar um polipeptídeo FGF-21 isolado tendo a sequência de aminoácidos que consiste na SEQ ID NO: 1, SEQ ID NO: 1 fundida a uma metionina N-terminal, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 5 fundida a uma metionina Nterminal, SEQ ID NO: 6 ou SEQ ID NO: 7 que contém uma substituição de um aminoácido com o referido aminoácido codificado não-naturalmente em uma posição correspondente ao resíduo 72, 77, 86, 108, 110, 131 ou 146 da SEQ ID NO:1 ou a posição de aminoácido correspondente na SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6 ou SEQ ID NO:7 com um ligante, polímero ou molécula biologicamente ativa compreendendo uma fração que reage com o aminoácido codificado não-naturalmente.
36. Composição CARACTERIZADA pelo fato de que compreende o polipeptídeo FGF-21, como definido em qualquer uma das reivindicações 1 a 34, e um veículo farmaceuticamente aceitável.
37. Método, de acordo com a reivindicação 35, CARACTERIZADO pelo fato de que compreende sintetizar ribossomalmente o referido polipeptídeo FGF-21 e contatar o referido polipeptídeo FGF-21 com um ligante, polímero, ou molécula biologicamente ativa que reage com o aminoácido codificado não-naturalmente para fornecer o polipeptídeo FGF-21 como definido em qualquer uma das reivindicações 1 a 34.
38. Método para produzir o polipeptídeo FGF-21, de acordo com a reivindicação 37, CARACTERIZADO pelo fato de que o ligante, polímero, ou molécula biologicamente ativa compreende uma fração de alcino, aminoóxi, azida, hidrazina, hidrazida ou semicarbazida.
39. Método para produzir o polipeptídeo FGF-21, de acordo com a reivindicação 38, CARACTERIZADO pelo fato de que a fração de alcino, aminoóxi, azida, hidrazina, hidrazida, ou semicarbazida está ligada ao ligante, polímero, ou molécula biologicamente ativa através de uma ligação amida.
40. Célula CARACTERIZADA pelo fato de que compreende um polinucleotídeo compreendendo pelo menos um códon seletor que quando expresso na presença de uma sintetase tRNA ortogonal, um tRNA ortogonal, ou ambos sob condições que permitam a expressão de um polipeptídeo resulte no polipeptídeo FGF- 21, como definido em qualquer uma das reivindicações 1 a 34, em que a célula compreende uma sintetase tRNA ortogonal ou um tRNA ortogonal, em que a referida célula compreende uma célula procariótica, uma célula bacteriana ou uma célula de levedura.
41. Célula, de acordo com a reivindicação 40, CARACTERIZADA pelo fato de que a referida célula bacteriana compreende uma célula de Escherichia coli.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US92129707P | 2007-03-30 | 2007-03-30 | |
| US60/921.297 | 2007-03-30 | ||
| US98806007P | 2007-11-14 | 2007-11-14 | |
| US60/988.060 | 2007-11-14 | ||
| PCT/US2008/057563 WO2008121563A2 (en) | 2007-03-30 | 2008-03-19 | Modified fgf-21 polypeptides and their uses |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0809583A2 BRPI0809583A2 (pt) | 2019-09-03 |
| BRPI0809583B1 true BRPI0809583B1 (pt) | 2022-02-22 |
Family
ID=39808850
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0809583-3A BRPI0809583B1 (pt) | 2007-03-30 | 2008-03-19 | Polipeptídeo fgf-21 modificado, composição compreendendo o mesmo, método para produzir o referido polipetídeo fgf-21 e célula compreendendo um polinucleotídeo |
Country Status (18)
| Country | Link |
|---|---|
| US (8) | US8012931B2 (pt) |
| EP (1) | EP2068909B1 (pt) |
| JP (4) | JP2010523084A (pt) |
| KR (4) | KR101476472B1 (pt) |
| CN (2) | CN107501407B (pt) |
| AT (1) | ATE554785T1 (pt) |
| AU (1) | AU2008232937B2 (pt) |
| BR (1) | BRPI0809583B1 (pt) |
| CA (1) | CA2682147C (pt) |
| CY (1) | CY1113188T1 (pt) |
| DK (1) | DK2068909T3 (pt) |
| ES (1) | ES2385114T3 (pt) |
| HR (1) | HRP20120522T1 (pt) |
| IL (2) | IL200749B (pt) |
| MX (1) | MX2009010531A (pt) |
| PL (1) | PL2068909T3 (pt) |
| PT (1) | PT2068909E (pt) |
| WO (1) | WO2008121563A2 (pt) |
Families Citing this family (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7459540B1 (en) | 1999-09-07 | 2008-12-02 | Amgen Inc. | Fibroblast growth factor-like polypeptides |
| US8981061B2 (en) | 2001-03-20 | 2015-03-17 | Novo Nordisk A/S | Receptor TREM (triggering receptor expressed on myeloid cells) and uses thereof |
| DE10163106A1 (de) * | 2001-12-24 | 2003-07-10 | Univ Hannover | Medizinische Implantate, Prothesen, Protheseteile, medizinische Instrumente, Geräte und Hilfsmittel aus einem halogenid-modifizierten Magnesiumwerkstoff |
| GB0426146D0 (en) | 2004-11-29 | 2004-12-29 | Bioxell Spa | Therapeutic peptides and method |
| PL2068909T3 (pl) * | 2007-03-30 | 2012-09-28 | Ambrx Inc | Modyfikowane polipeptydy fgf-21 i ich zastosowanie |
| JP2010535781A (ja) * | 2007-08-03 | 2010-11-25 | イーライ リリー アンド カンパニー | 肥満に対する処置 |
| US8946148B2 (en) | 2007-11-20 | 2015-02-03 | Ambrx, Inc. | Modified insulin polypeptides and their uses |
| EA024751B8 (ru) | 2008-06-04 | 2020-01-31 | Амген Инк. | Мутанты fgf21 и их применение |
| AU2013211503C1 (en) * | 2008-10-10 | 2016-09-29 | Amgen Inc. | FGF21 mutants and uses thereof |
| EP2358749B1 (en) * | 2008-10-10 | 2018-07-18 | Amgen, Inc | Fgf21 mutants and uses thereof |
| WO2010065439A1 (en) * | 2008-12-05 | 2010-06-10 | Eli Lilly And Company | Variants of fibroblast growth factor 21 |
| ES2692495T3 (es) * | 2009-01-23 | 2018-12-03 | Novo Nordisk A/S | Derivados del FGF21 con aglutinante de albúmina A-B-C-D-E- y sus usos |
| WO2010096394A2 (en) | 2009-02-17 | 2010-08-26 | Redwood Biosciences, Inc. | Aldehyde-tagged protein-based drug carriers and methods of use |
| SMT202400036T1 (it) * | 2009-05-05 | 2024-03-13 | Amgen Inc | Mutanti fgf21 e loro utilizzi |
| US20120052069A1 (en) | 2009-05-05 | 2012-03-01 | Amgen Inc | Fgf21 mutants and uses thereof |
| AU2010262927A1 (en) | 2009-06-17 | 2012-01-19 | Amgen Inc. | Chimeric FGF19 polypeptides and uses thereof |
| CN101993485B (zh) | 2009-08-20 | 2013-04-17 | 重庆富进生物医药有限公司 | 促胰岛素分泌肽类似物同源二聚体及其用途 |
| CA2779088A1 (en) | 2009-11-16 | 2011-05-19 | Mellitech | [1,5]-diazocin derivatives |
| MX2012006397A (es) * | 2009-12-02 | 2012-11-30 | Amgen Inc | PROTEINAS DE ENLACE QUE ENLAZAN A FGFR1C HUMANO, ß-KLOTHO HUMANA Y TANTO FGFR1C HUMANO COMO ß-KLOTHO HUMANA. |
| UA109888C2 (uk) | 2009-12-07 | 2015-10-26 | ІЗОЛЬОВАНЕ АНТИТІЛО АБО ЙОГО ФРАГМЕНТ, ЩО ЗВ'ЯЗУЄТЬСЯ З β-КЛОТО, РЕЦЕПТОРАМИ FGF І ЇХНІМИ КОМПЛЕКСАМИ | |
| EP2359843A1 (en) * | 2010-01-21 | 2011-08-24 | Sanofi | Pharmaceutical composition for treating a metabolic syndrome |
| US9517264B2 (en) | 2010-04-15 | 2016-12-13 | Amgen Inc. | Human FGF receptor and β-Klotho binding proteins |
| CA2796459C (en) | 2010-04-16 | 2016-05-24 | Salk Institute For Biological Studies | Methods for treating metabolic disorders using fgf-1 |
| JP2013533227A (ja) | 2010-06-08 | 2013-08-22 | ノヴォ ノルディスク アー/エス | Fgf21類似体および誘導体 |
| CN103415300B (zh) | 2010-07-20 | 2018-02-23 | 诺沃—诺迪斯克有限公司 | N‑末端修饰的fgf21化合物 |
| EP3572091B1 (en) | 2010-08-17 | 2023-12-13 | Ambrx, Inc. | Modified relaxin polypeptides and their uses |
| US9567386B2 (en) | 2010-08-17 | 2017-02-14 | Ambrx, Inc. | Therapeutic uses of modified relaxin polypeptides |
| CN101935346B (zh) * | 2010-08-24 | 2012-08-08 | 哈尔滨博翱生物医药技术开发有限公司 | 突变的人源成纤维生长因子及在治疗内分泌疾病中的用途 |
| BR112013011172A2 (pt) * | 2010-11-05 | 2017-06-06 | Covx Tech Ireland Ltd | compostos antidiabéticos |
| US9023791B2 (en) * | 2010-11-19 | 2015-05-05 | Novartis Ag | Fibroblast growth factor 21 mutations |
| US9540438B2 (en) | 2011-01-14 | 2017-01-10 | Redwood Bioscience, Inc. | Aldehyde-tagged immunoglobulin polypeptides and methods of use thereof |
| JP2014512814A (ja) * | 2011-04-08 | 2014-05-29 | アンセム・バイオサイエンシズ・プライベート・リミテッド | 大腸菌での異種タンパク質生成のための新規発現および分泌ベクター系 |
| WO2012140650A2 (en) * | 2011-04-12 | 2012-10-18 | Hepacore Ltd. | Conjugates of carboxy polysaccharides with fibroblast growth factors and variants thereof |
| US8754044B2 (en) | 2011-05-03 | 2014-06-17 | Northwestern University | Neuroprotection by hepatic cells and hepatocyte secretory factors |
| TWI527590B (zh) * | 2011-06-17 | 2016-04-01 | 艾瑞斯貿易公司 | Fgf-18之凍乾調配物 |
| PL2726511T3 (pl) | 2011-07-01 | 2019-12-31 | Ngm Biopharmaceuticals, Inc. | Kompozycje, zastosowania i sposoby leczenia zaburzeń oraz chorób metabolicznych |
| EP2548570A1 (en) | 2011-07-19 | 2013-01-23 | Sanofi | Pharmaceutical composition for treating a metabolic syndrome |
| CA2845357A1 (en) * | 2011-08-31 | 2013-03-07 | Amgen Inc. | Method of treating or ameliorating type 1 diabetes using fgf21 |
| UY34347A (es) | 2011-09-26 | 2013-04-30 | Novartis Ag | Proteínas de función dual para tratar trastornos metabólicos |
| AR087973A1 (es) | 2011-10-04 | 2014-04-30 | Lilly Co Eli | Variantes del factor 21 del crecimiento de fibroblastos |
| HUE043171T2 (hu) | 2011-10-07 | 2019-08-28 | Takeda Pharmaceuticals Co | Neurodegeneratív betegségek kezelésére hasznos 1-arilkarbonil-4-oxi-piperidinvegyületek |
| CA2859969A1 (en) | 2011-12-22 | 2013-06-27 | Pfizer Inc. | Processes for purifying a sample of h38c2 antibody or variant thereof |
| LT2814842T (lt) | 2012-02-15 | 2018-11-12 | Novo Nordisk A/S | Antikūnai, kurie suriša peptidoglikaną atpažįstantį baltymą 1 |
| LT2814844T (lt) | 2012-02-15 | 2017-10-25 | Novo Nordisk A/S | Antikūnai, kurie jungiasi ir blokuoja ekspresuotą ant mieloidinių ląstelių inicijuojantį receptorių 1 (trem-1) |
| US9550830B2 (en) | 2012-02-15 | 2017-01-24 | Novo Nordisk A/S | Antibodies that bind and block triggering receptor expressed on myeloid cells-1 (TREM-1) |
| US9475856B2 (en) | 2012-03-02 | 2016-10-25 | New York University | Chimeric FGF21 proteins with enhanced binding affinity for β-klotho for the treatment of type II diabetes, obesity, and related metabolic disorders |
| HK1202800A1 (en) * | 2012-05-15 | 2015-10-09 | Eli Lilly And Company | Therapeutic uses of fibroblast growth factor 21 proteins |
| US9474785B2 (en) | 2012-06-07 | 2016-10-25 | New York University | Chimeric fibroblast growth factor 19 proteins and methods of use |
| US9657075B2 (en) | 2012-06-07 | 2017-05-23 | New York University | Chimeric fibroblast growth factor 23 proteins and methods of use |
| US9464126B2 (en) | 2012-06-07 | 2016-10-11 | New York University | Chimeric fibroblast growth factor 21 proteins and methods of use |
| KR20150006059A (ko) | 2012-06-11 | 2015-01-15 | 일라이 릴리 앤드 캄파니 | 섬유모세포 성장 인자 21 변이체 |
| TWI513705B (zh) * | 2012-06-11 | 2015-12-21 | Lilly Co Eli | 纖維母細胞生長因子21蛋白質 |
| US8955588B2 (en) * | 2012-09-10 | 2015-02-17 | Halliburton Energy Services, Inc. | Electron-poor orthoester for generating acid in a well fluid |
| EP3798228A1 (en) | 2012-11-28 | 2021-03-31 | NGM Biopharmaceuticals, Inc. | Compositions and methods for treatment of metabolic disorders and diseases |
| US9290557B2 (en) | 2012-11-28 | 2016-03-22 | Ngm Biopharmaceuticals, Inc. | Compositions comprising variants and fusions of FGF19 polypeptides |
| SG11201504815QA (en) | 2012-12-27 | 2015-07-30 | Ngm Biopharmaceuticals Inc | Methods for modulating bile acid homeostasis and treatment of bile acid disorders and diseases |
| US9273107B2 (en) | 2012-12-27 | 2016-03-01 | Ngm Biopharmaceuticals, Inc. | Uses and methods for modulating bile acid homeostasis and treatment of bile acid disorders and diseases |
| WO2014130659A1 (en) | 2013-02-22 | 2014-08-28 | New York University | Chimeric fibroblast growth factor 23 proteins and methods of use |
| US20160235810A1 (en) | 2013-10-18 | 2016-08-18 | Novartis Ag | Methods of treating diabetes and related disorders |
| CA2928135A1 (en) | 2013-10-21 | 2015-04-30 | Salk Institute For Biological Studies | Mutated fibroblast growth factor (fgf) 1 and methods of use |
| WO2015061331A1 (en) | 2013-10-21 | 2015-04-30 | Salk Institute For Biological Studies | Chimeric fibroblast growth factor (fgf) 2/fgf1 peptides and methods of use |
| NZ718962A (en) | 2013-10-28 | 2019-12-20 | Ngm Biopharmaceuticals Inc | Cancer models and associated methods |
| AU2015209131B2 (en) | 2014-01-24 | 2020-06-25 | Ngm Biopharmaceuticals, Inc. | Binding proteins and methods of use thereof |
| WO2015138278A1 (en) | 2014-03-11 | 2015-09-17 | Novartis Ag | Methods of treating metabolic disorders associated with lipodystrophies and defects in insulin production or signaling |
| WO2015183890A2 (en) | 2014-05-28 | 2015-12-03 | Ngm Biopharmaceuticals, Inc. | Methods and compositions for the treatment of metabolic disorders and diseases |
| EP3155005A4 (en) | 2014-06-16 | 2018-07-11 | NGM Biopharmaceuticals, Inc. | Methods and uses for modulating bile acid homeostasis and treatment of bile acid disorders and diseases |
| CN106536559B (zh) | 2014-07-17 | 2021-04-27 | 诺和诺德股份有限公司 | 定点诱变trem-1抗体以降低黏度 |
| CN114129709A (zh) | 2014-10-23 | 2022-03-04 | 恩格姆生物制药公司 | 包含肽变异体的药物组合物及其使用方法 |
| CN107108710B (zh) * | 2014-10-24 | 2022-02-15 | 百时美施贵宝公司 | 修饰的fgf-21多肽及其用途 |
| US10434144B2 (en) | 2014-11-07 | 2019-10-08 | Ngm Biopharmaceuticals, Inc. | Methods for treatment of bile acid-related disorders and prediction of clinical sensitivity to treatment of bile acid-related disorders |
| HUE044783T2 (hu) | 2014-12-23 | 2019-11-28 | Novo Nordisk As | FGF21 származékok és alkalmazásaik |
| KR20160088656A (ko) | 2015-01-16 | 2016-07-26 | 주식회사유한양행 | 지속형 fgf21 융합 단백질 및 이를 포함하는 약학적 조성물 |
| US10676723B2 (en) | 2015-05-11 | 2020-06-09 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| CN105018482B (zh) * | 2015-07-21 | 2017-10-24 | 吉林大学 | 一种杂合tRNA及其在制备谷胱甘肽过氧化物酶中的应用 |
| WO2017019957A2 (en) | 2015-07-29 | 2017-02-02 | Ngm Biopharmaceuticals, Inc. | Binding proteins and methods of use thereof |
| AU2016344134A1 (en) | 2015-10-30 | 2018-05-31 | Salk Institute For Biological Studies | Treatment of steroid-induced hyperglycemia with fibroblast growth factor (FGF) 1 analogs |
| CA3003616C (en) | 2015-11-09 | 2020-07-28 | Ngm Biopharmaceuticals, Inc. | Methods for treatment of bile acid-related disorders |
| HUE052634T2 (hu) * | 2015-11-23 | 2021-05-28 | Bristol Myers Squibb Co | Adalékrendszerek felhasználásra protein pegilálásban |
| TW201731867A (zh) | 2015-12-02 | 2017-09-16 | 賽諾菲公司 | Fgf21變異體 |
| CN109071634A (zh) | 2016-04-26 | 2018-12-21 | R.P.谢勒技术有限责任公司 | 抗体偶联物及其制备和使用方法 |
| CN106279437B (zh) | 2016-08-19 | 2017-10-31 | 安源医药科技(上海)有限公司 | 高糖基化人凝血因子viii融合蛋白及其制备方法与用途 |
| CN107759694B (zh) | 2016-08-19 | 2023-01-13 | 安源医药科技(上海)有限公司 | 双特异性抗体及其制备方法与用途 |
| US11123438B2 (en) | 2016-08-19 | 2021-09-21 | Ampsource Biopharma Shanghai Inc. | Linker peptide for constructing fusion protein |
| CN109689079A (zh) * | 2016-08-22 | 2019-04-26 | 伊兰科美国公司 | 牛成纤维细胞生长因子21和乳畜中的酮病 |
| CA3034399A1 (en) | 2016-08-26 | 2018-03-01 | Ngm Biopharmaceuticals, Inc. | Methods of treating fibroblast growth factor 19-mediated cancers and tumors |
| US11129906B1 (en) | 2016-12-07 | 2021-09-28 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| PE20191716A1 (es) | 2017-02-08 | 2019-12-05 | Bristol Myers Squibb Co | Polipeptidos de relaxina modificada que comprenden un mejorador farmacocinetico y sus usos |
| IL306098A (en) | 2017-05-24 | 2023-11-01 | Univ Barcelona Autonoma | Viral expression vectors containing the coding sequence for FIBROBLAST GROWTH FACTOR 21 (FGF21) |
| CA3074380C (en) * | 2017-09-04 | 2023-01-03 | 89Bio Ltd. | Mutant fgf-21 peptide conjugates and uses thereof |
| CN111050786A (zh) | 2017-09-08 | 2020-04-21 | 百时美施贵宝公司 | 用于治疗非酒精性脂肪性肝炎(nash)的方法的修饰的成纤维细胞生长因子21(fgf-21) |
| WO2019119673A1 (zh) | 2017-12-19 | 2019-06-27 | 北京吉源生物科技有限公司 | 一种双基因修饰的干细胞及其用途 |
| IL275499B2 (en) | 2017-12-22 | 2024-03-01 | Novartis Ag | Methods of treating metabolic disorders with fgf21 variants |
| TWI790370B (zh) | 2018-04-02 | 2023-01-21 | 美商必治妥美雅史谷比公司 | 抗trem-1抗體及其用途 |
| US12226451B2 (en) | 2018-07-03 | 2025-02-18 | Bristol-Myers Squibb Company | FGF-21 formulations |
| JP2022506649A (ja) | 2018-11-05 | 2022-01-17 | ブリストル-マイヤーズ スクイブ カンパニー | Peg化タンパク質の精製方法 |
| CN111195234B (zh) * | 2018-11-16 | 2022-08-26 | 鲁南制药集团股份有限公司 | 一种重组FGF21-Fc融合蛋白冻干粉制剂 |
| JP7495420B2 (ja) | 2019-02-20 | 2024-06-04 | ノヴォ ノルディスク アー/エス | アミノアシル-tRNA合成酵素およびこの使用 |
| US11427623B1 (en) | 2019-05-28 | 2022-08-30 | 89Bio Ltd. | Methods of treatment using mutant FGF-21 peptide conjugates |
| US11542309B2 (en) | 2019-07-31 | 2023-01-03 | Salk Institute For Biological Studies | Fibroblast growth factor 1 (FGF1) mutant proteins that selectively activate FGFR1B to reduce blood glucose |
| WO2021142143A1 (en) | 2020-01-08 | 2021-07-15 | Bristol-Myers Squibb Company | Fgf-21 conjugate formulations |
| CN115322794B (zh) | 2020-01-11 | 2025-09-19 | 北京质肽生物医药科技有限公司 | Glp-1和fgf21的融合蛋白的缀合物 |
| WO2021152396A1 (en) * | 2020-01-31 | 2021-08-05 | 89Bio Ltd. | Methods for promoting weight loss |
| US11981718B2 (en) | 2020-05-27 | 2024-05-14 | Ampsource Biopharma Shanghai Inc. | Dual-function protein for lipid and blood glucose regulation |
| EP4192495A1 (en) | 2020-08-07 | 2023-06-14 | Bristol-Myers Squibb Company | Fgf21 combined with ccr2/5 antagonists for the treatment of fibrosis |
| WO2022115597A1 (en) | 2020-11-25 | 2022-06-02 | Bristol-Myers Squibb Company | Methods of treating liver diseases |
| CA3224743A1 (en) | 2021-07-14 | 2023-01-19 | Beijing Ql Biopharmaceutical Co., Ltd. | Fusion polypeptides for metabolic disorders |
| US12036284B2 (en) | 2022-06-24 | 2024-07-16 | 89Bio, Inc. | Compositions and methods of treatment for severe hypertriglyceridemia |
| KR20250075578A (ko) * | 2022-08-24 | 2025-05-28 | 89바이오 인코포레이티드 | 돌연변이 fgf-21 펩타이드 접합체를 사용한 nash의 치료 방법 |
| EP4631972A1 (en) | 2022-11-18 | 2025-10-15 | Nanjing Novoacine Biotechnology Co., Ltd. | Site-specific coupled pegylated interleukin-2 mutant with receptor affinity preference and use thereof |
| EP4700044A1 (en) * | 2023-03-31 | 2026-02-25 | Shanghai Duomirui Biotechnology., Ltd. | Protein analogue and use thereof |
Family Cites Families (308)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2968158A (en) * | 1955-08-08 | 1961-01-17 | Upjohn Co | New benzene sulfonyl ureas; composition and process for lowering blood sugar therewith |
| US3097242A (en) * | 1960-06-29 | 1963-07-09 | Olin Mathieson | Hydrindene sulfonylureas |
| US3454635A (en) * | 1965-07-27 | 1969-07-08 | Hoechst Ag | Benzenesulfonyl-ureas and process for their manufacture |
| NL132376C (pt) * | 1966-02-10 | |||
| US3668215A (en) * | 1967-11-25 | 1972-06-06 | Bayer Ag | Aryl-sulphonyl-semicarbazides containing heterocyclic acylamino groups |
| CH505073A (de) * | 1968-04-26 | 1971-03-31 | Hoffmann La Roche | Verfahren zur Herstellung von Sulfonylharnstoffderivaten |
| NL138933B (nl) * | 1969-03-26 | 1973-05-15 | Erba Carlo Spa | Werkwijze voor het bereiden van benzeensulfonylureumderivaten met bloedsuikerspiegelverlagende werking. |
| US3708486A (en) * | 1969-04-17 | 1973-01-02 | Boehringer Sohn Ingelheim | 2-(p-(n'-cycloalkyl-carbamido-n-sulfonyl)-phenethyl)-1,2,3,4-tetrahydro-1,3-dioxo-4,4-dimethyl-isoquinolines and alkali metal salts thereof |
| US3773919A (en) * | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| US4263428A (en) | 1978-03-24 | 1981-04-21 | The Regents Of The University Of California | Bis-anthracycline nucleic acid function inhibitors and improved method for administering the same |
| JPS5522636A (en) * | 1978-08-04 | 1980-02-18 | Takeda Chem Ind Ltd | Thiazoliding derivative |
| US4289872A (en) * | 1979-04-06 | 1981-09-15 | Allied Corporation | Macromolecular highly branched homogeneous compound based on lysine units |
| ZA811368B (en) | 1980-03-24 | 1982-04-28 | Genentech Inc | Bacterial polypedtide expression employing tryptophan promoter-operator |
| EP0052322B1 (de) | 1980-11-10 | 1985-03-27 | Gersonde, Klaus, Prof. Dr. | Verfahren zur Herstellung von Lipid-Vesikeln durch Ultraschallbehandlung, Anwendung des Verfahrens und Vorrichtung zur Durchführung des Verfahrens |
| IE52535B1 (en) | 1981-02-16 | 1987-12-09 | Ici Plc | Continuous release pharmaceutical compositions |
| FR2504010B1 (fr) * | 1981-04-15 | 1985-10-25 | Sanofi Sa | Medicaments anticancereux contenant la chaine a de la ricine associee a un anticorps antimelanome et procede pour leur preparation |
| US4551433A (en) * | 1981-05-18 | 1985-11-05 | Genentech, Inc. | Microbial hybrid promoters |
| JPS57206622A (en) * | 1981-06-10 | 1982-12-18 | Ajinomoto Co Inc | Blood substitute |
| US4485045A (en) * | 1981-07-06 | 1984-11-27 | Research Corporation | Synthetic phosphatidyl cholines useful in forming liposomes |
| NZ201705A (en) | 1981-08-31 | 1986-03-14 | Genentech Inc | Recombinant dna method for production of hepatitis b surface antigen in yeast |
| DE3374837D1 (en) * | 1982-02-17 | 1988-01-21 | Ciba Geigy Ag | Lipids in the aqueous phase |
| US4671958A (en) * | 1982-03-09 | 1987-06-09 | Cytogen Corporation | Antibody conjugates for the delivery of compounds to target sites |
| US4452747A (en) | 1982-03-22 | 1984-06-05 | Klaus Gersonde | Method of and arrangement for producing lipid vesicles |
| DE3218121A1 (de) | 1982-05-14 | 1983-11-17 | Leskovar, Peter, Dr.-Ing., 8000 München | Arzneimittel zur tumorbehandlung |
| EP0102324A3 (de) | 1982-07-29 | 1984-11-07 | Ciba-Geigy Ag | Lipide und Tenside in wässriger Phase |
| US4511502A (en) * | 1982-12-22 | 1985-04-16 | Genentech, Inc. | Purification and activity assurance of precipitated heterologous proteins |
| US4511503A (en) * | 1982-12-22 | 1985-04-16 | Genentech, Inc. | Purification and activity assurance of precipitated heterologous proteins |
| US4512922A (en) * | 1982-12-22 | 1985-04-23 | Genentech, Inc. | Purification and activity assurance of precipitated heterologous proteins |
| US4820352A (en) | 1983-01-10 | 1989-04-11 | Bausch & Lomb Incorporated | Cleaning and conditioning solutions for contact lenses and methods of use |
| US5089398A (en) * | 1983-02-22 | 1992-02-18 | Chiron Corporation | Enhanced yeast transcription employing hybrid GAPDH promoter region constructs |
| CA1341116C (en) | 1983-02-22 | 2000-10-17 | Rae Lyn Burke | Yeast expression systems with vectors having gapdh or pyk promoters and synthesis or foreign protein |
| US4876197A (en) * | 1983-02-22 | 1989-10-24 | Chiron Corporation | Eukaryotic regulatable transcription |
| JPS59166086A (ja) | 1983-03-09 | 1984-09-19 | Teruhiko Beppu | 新規な発現型プラスミドとそれらを用いて仔牛プロキモシン遺伝子を大腸菌内で発現させる方法 |
| US4859600A (en) * | 1983-04-25 | 1989-08-22 | Genentech, Inc. | Recombinant procaryotic cell containing correctly processed human growth hormone |
| US4755465A (en) * | 1983-04-25 | 1988-07-05 | Genentech, Inc. | Secretion of correctly processed human growth hormone in E. coli and Pseudomonas |
| EP0127839B1 (en) | 1983-05-27 | 1992-07-15 | THE TEXAS A&M UNIVERSITY SYSTEM | Method for producing a recombinant baculovirus expression vector |
| DE3320583A1 (de) * | 1983-06-08 | 1984-12-13 | Dr. Karl Thomae Gmbh, 7950 Biberach | Neue galenische zubereitungsformen von oralen antidiabetika und verfahren zu ihrer herstellung |
| US4544545A (en) * | 1983-06-20 | 1985-10-01 | Trustees University Of Massachusetts | Liposomes containing modified cholesterol for organ targeting |
| JPS607934A (ja) | 1983-06-29 | 1985-01-16 | Dai Ichi Seiyaku Co Ltd | リポソ−ムの製造方法 |
| HUT35524A (en) | 1983-08-02 | 1985-07-29 | Hoechst Ag | Process for preparing pharmaceutical compositions containing regulatory /regulative/ peptides providing for the retarded release of the active substance |
| US4689406A (en) * | 1983-08-10 | 1987-08-25 | Amgen | Enhancement of microbial expression of polypeptides |
| JPS6051189A (ja) * | 1983-08-30 | 1985-03-22 | Sankyo Co Ltd | チアゾリジン誘導体およびその製造法 |
| ATE159858T1 (de) * | 1983-09-26 | 1997-11-15 | Ehrenfeld Udo | Mittel und erzeugnis für die diagnose und therapie von tumoren sowie zur behandlung von schwächen der zelligen und humoralen immunabwehr |
| DE3474511D1 (en) | 1983-11-01 | 1988-11-17 | Terumo Corp | Pharmaceutical composition containing urokinase |
| ZA848495B (en) | 1984-01-31 | 1985-09-25 | Idaho Res Found | Production of polypeptides in insect cells |
| EP0154316B1 (en) | 1984-03-06 | 1989-09-13 | Takeda Chemical Industries, Ltd. | Chemically modified lymphokine and production thereof |
| DE3587759T2 (de) | 1984-05-11 | 1994-07-07 | Chiron Corp., Emeryville, Calif. | Erhöhte Hefetranskription unter Verwendung einer Hybridkonstruktion der Promotorregion. |
| US4880734A (en) * | 1984-05-11 | 1989-11-14 | Chiron Corporation | Eukaryotic regulatable transcription |
| US4542225A (en) * | 1984-08-29 | 1985-09-17 | Dana-Farber Cancer Institute, Inc. | Acid-cleavable compound |
| US4738921A (en) * | 1984-09-27 | 1988-04-19 | Eli Lilly And Company | Derivative of the tryptophan operon for expression of fused gene products |
| US4659839A (en) * | 1984-10-10 | 1987-04-21 | Mallinckrodt, Inc. | Coupling agents for radiolabeled antibody fragments |
| US4837148A (en) * | 1984-10-30 | 1989-06-06 | Phillips Petroleum Company | Autonomous replication sequences for yeast strains of the genus pichia |
| GB8430252D0 (en) | 1984-11-30 | 1985-01-09 | Beecham Group Plc | Compounds |
| EP0188256B1 (en) | 1985-01-14 | 1991-08-21 | NeoRx | Metal radionuclide labeled proteins for diagnosis and therapy |
| AR240698A1 (es) * | 1985-01-19 | 1990-09-28 | Takeda Chemical Industries Ltd | Procedimiento para preparar compuestos de 5-(4-(2-(5-etil-2-piridil)-etoxi)benzil)-2,4-tiazolidindiona y sus sales |
| EP0206448B1 (en) * | 1985-06-19 | 1990-11-14 | Ajinomoto Co., Inc. | Hemoglobin combined with a poly(alkylene oxide) |
| DE3676670D1 (de) | 1985-06-26 | 1991-02-07 | Cetus Corp | Solubilisierung von proteinen fuer pharmazeutische zusammensetzungen mittels polymerkonjugierung. |
| US4680338A (en) * | 1985-10-17 | 1987-07-14 | Immunomedics, Inc. | Bifunctional linker |
| US4699784A (en) * | 1986-02-25 | 1987-10-13 | Center For Molecular Medicine & Immunology | Tumoricidal methotrexate-antibody conjugate |
| GB8610600D0 (en) | 1986-04-30 | 1986-06-04 | Novo Industri As | Transformation of trichoderma |
| US5614492A (en) | 1986-05-05 | 1997-03-25 | The General Hospital Corporation | Insulinotropic hormone GLP-1 (7-36) and uses thereof |
| JPS63123383A (ja) | 1986-11-11 | 1988-05-27 | Mitsubishi Kasei Corp | ハイブリツドプロモ−タ−、発現調節dna配列および発現ベクタ− |
| US5186933A (en) | 1986-12-30 | 1993-02-16 | Baylor College Of Medicine | Synthesis and immunogenicity of rotavirus genes using a baculovirus expression system |
| US4873255A (en) * | 1987-02-04 | 1989-10-10 | Sankyo Company Limited | Thiazolidinone derivatives, their preparation and their use |
| WO1988007082A1 (en) | 1987-03-16 | 1988-09-22 | American Biogenetic Sciences, Inc. | Recombinant baculovirus occlusion bodies in vaccines and biological insecticides |
| DE3888561T2 (de) | 1987-03-23 | 1994-09-01 | Zymogenetics Inc | Hohe Proteinsyntheserate in Hefe. |
| US5229490A (en) * | 1987-05-06 | 1993-07-20 | The Rockefeller University | Multiple antigen peptide system |
| WO1989001037A1 (en) | 1987-07-24 | 1989-02-09 | Cetus Corporation | Production of ricin toxins in a baculovirus-insect cell expression system |
| CA1317244C (en) | 1987-07-24 | 1993-05-04 | Ernest Seigo Kawasaki | Production of biologically active forms of csf using a baculovirus (acnpv)-insect cell expression system |
| US5080891A (en) * | 1987-08-03 | 1992-01-14 | Ddi Pharmaceuticals, Inc. | Conjugates of superoxide dismutase coupled to high molecular weight polyalkylene glycols |
| EP0842925A1 (en) * | 1987-09-04 | 1998-05-20 | Beecham Group Plc | Substituted thiazolidinedione derivatives |
| US4929555A (en) * | 1987-10-19 | 1990-05-29 | Phillips Petroleum Company | Pichia transformation |
| US4904584A (en) * | 1987-12-23 | 1990-02-27 | Genetics Institute, Inc. | Site-specific homogeneous modification of polypeptides |
| CA1340772C (en) | 1987-12-30 | 1999-09-28 | Patricia Tekamp-Olson | Expression and secretion of heterologous protiens in yeast employing truncated alpha-factor leader sequences |
| US4847325A (en) | 1988-01-20 | 1989-07-11 | Cetus Corporation | Conjugation of polymer to colony stimulating factor-1 |
| US5223522A (en) * | 1988-03-08 | 1993-06-29 | Pfizer Inc. | Thiazolidinedione hypoglycemic agents |
| US5120754A (en) * | 1988-03-08 | 1992-06-09 | Pfizer Inc. | Thiazolidinedione hypoglycemic agents |
| US5061717A (en) * | 1988-03-08 | 1991-10-29 | Pfizer Inc. | Thiazolidinedione hypoglycemic agents |
| CA1324969C (en) | 1988-05-06 | 1993-12-07 | Jeffrey R. Shuster | High level expression of proteins in yeast |
| US5674706A (en) * | 1988-05-06 | 1997-10-07 | Chiron Corporation | High level expression of proteins in yeast |
| FR2631974B1 (fr) * | 1988-05-31 | 1992-12-11 | Agronomique Inst Nat Rech | Baculovirus modifie, son procede de preparation et son application en tant que vecteur d'expression de genes |
| WO1990001556A1 (en) | 1988-08-05 | 1990-02-22 | Mount Sinai School Of Medicine Of The City University Of New York | In vivo infection of live insects with a recombinant baculovirus |
| GB8819453D0 (en) | 1988-08-16 | 1988-09-21 | Roy P | Production of bluetongue virus non-structural proteins using baculovirus expression vector |
| NZ230425A (en) | 1988-09-02 | 1992-07-28 | Molecular Eng Ass | Production of paramyxovirus fusion (f) protein using recombinant baculovirus expression vector |
| US5218092A (en) | 1988-09-29 | 1993-06-08 | Kyowa Hakko Kogyo Co., Ltd. | Modified granulocyte-colony stimulating factor polypeptide with added carbohydrate chains |
| GB8824591D0 (en) | 1988-10-20 | 1988-11-23 | Royal Free Hosp School Med | Fractionation process |
| CA2345497A1 (en) | 1988-10-28 | 1990-04-28 | Genentech, Inc. | Growth hormone variants and method for forming growth hormone variants |
| US6780613B1 (en) | 1988-10-28 | 2004-08-24 | Genentech, Inc. | Growth hormone variants |
| JPH04504651A (ja) | 1988-11-18 | 1992-08-20 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 自然に存在しないアミノ酸をタンパク質に部位特異的に導入する方法 |
| JP2989002B2 (ja) | 1988-12-22 | 1999-12-13 | キリン―アムジエン・インコーポレーテツド | 化学修飾顆粒球コロニー刺激因子 |
| US4902502A (en) * | 1989-01-23 | 1990-02-20 | Cetus Corporation | Preparation of a polymer/interleukin-2 conjugate |
| AU5187190A (en) | 1989-02-23 | 1990-09-26 | University Of Ottawa | Improved baculovirus expression system capable of producing foreign gene proteins at high levels |
| WO1990010277A1 (en) | 1989-02-24 | 1990-09-07 | Cell Analysis Systems, Inc. | Method and apparatus for determining a proliferation index of a cell sample |
| US5122614A (en) | 1989-04-19 | 1992-06-16 | Enzon, Inc. | Active carbonates of polyalkylene oxides for modification of polypeptides |
| US5324844A (en) * | 1989-04-19 | 1994-06-28 | Enzon, Inc. | Active carbonates of polyalkylene oxides for modification of polypeptides |
| WO1990013540A1 (en) | 1989-04-19 | 1990-11-15 | Enzon, Inc. | Active carbonates of polyalkylene oxides for modification of polypeptides |
| US4897405A (en) * | 1989-04-21 | 1990-01-30 | American Home Products Corporation | Novel naphthalenylalkyl-3H-1,2,3,5-oxathiadiazole 2-oxides useful as antihyperglycemic agents |
| US5766883A (en) * | 1989-04-29 | 1998-06-16 | Delta Biotechnology Limited | Polypeptides |
| CA2033070A1 (en) | 1989-05-17 | 1990-11-18 | Lois K. Miller | Baculovirus expression vectors |
| ES2085297T3 (es) | 1989-05-27 | 1996-06-01 | Sumitomo Pharma | Procedimiento para preparar derivados de poli(etilenglicol) y proteina modificada. |
| FR2649120B1 (fr) | 1989-06-30 | 1994-01-28 | Cayla | Nouvelle souche et ses mutants de champignons filamenteux, procede de production de proteines recombinantes a l'aide de ladite souche et souches et proteines obtenues selon ce procede |
| US5258185A (en) * | 1989-08-23 | 1993-11-02 | Bauer Kurt H | Highly active, rapidly absorbable formulations of glibenclamide, processes for the production thereof and their use |
| GB8919434D0 (en) * | 1989-08-25 | 1989-10-11 | Beecham Group Plc | Novel compounds |
| US5162601A (en) * | 1989-11-22 | 1992-11-10 | The Upjohn Company | Plant potyvirus expression vector with a gene for protease |
| US5312808A (en) | 1989-11-22 | 1994-05-17 | Enzon, Inc. | Fractionation of polyalkylene oxide-conjugated hemoglobin solutions |
| US5219564A (en) * | 1990-07-06 | 1993-06-15 | Enzon, Inc. | Poly(alkylene oxide) amino acid copolymers and drug carriers and charged copolymers based thereon |
| FR2664905B1 (fr) | 1990-07-18 | 1994-08-12 | Agronomique Inst Nat Rech | Baculovirus modifie, son procede d'obtention, et vecteurs d'expression obtenus a partir dudit baculovirus. |
| WO1992001800A1 (en) * | 1990-07-20 | 1992-02-06 | Chiron Corporation | Method for integrative transformation of yeast using dispersed repetitive elements |
| EP0541721A4 (en) | 1990-08-02 | 1993-12-29 | Chiron Corporation | Expression of human cmv glycoprotein-h using the baculovirus-insect cell expression system |
| CA2090969C (en) * | 1990-09-04 | 2001-08-21 | Russell Arthur Brierley | Production of insulin-like growth factor-1 in methylotrophic yeast cells |
| CA2073511A1 (en) * | 1990-11-14 | 1992-05-29 | Matthew R. Callstrom | Conjugates of poly(vinylsaccharide) with proteins for the stabilization of proteins |
| US5252714A (en) * | 1990-11-28 | 1993-10-12 | The University Of Alabama In Huntsville | Preparation and use of polyethylene glycol propionaldehyde |
| DE69129154T2 (de) * | 1990-12-03 | 1998-08-20 | Genentech, Inc., South San Francisco, Calif. | Verfahren zur anreicherung von proteinvarianten mit geänderten bindungseigenschaften |
| US5231178A (en) * | 1991-01-16 | 1993-07-27 | The Salk Institute Biotechnology/Industrial Associates, Inc. | Method for the purification of intact, correctly-folded insulin-like growth factor-1 |
| JPH06506217A (ja) | 1991-03-18 | 1994-07-14 | エンゾン,インコーポレーテッド | ポリペプチドまたはグリコポリペプチドとポリマーとのヒドラジン含有結合体 |
| AU1651992A (en) | 1991-03-19 | 1992-10-21 | United States of America, as represented by the Secretary, U.S. Department of Commerce, The | Expression of influenza nucleoprotein antigens in baculovirus |
| US5595732A (en) | 1991-03-25 | 1997-01-21 | Hoffmann-La Roche Inc. | Polyethylene-protein conjugates |
| US6013433A (en) | 1991-04-26 | 2000-01-11 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Baculovirus expression vectors and recombinant antigens for detecting type-specific antibodies to herpes simplex virus |
| US5281698A (en) * | 1991-07-23 | 1994-01-25 | Cetus Oncology Corporation | Preparation of an activated polymer ester for protein conjugation |
| US5290686A (en) | 1991-07-31 | 1994-03-01 | The United States Of America As Represented By The Department Of Health And Human Services | Expression of influenza a M2 protein in baculovirus |
| IT1260468B (it) | 1992-01-29 | 1996-04-09 | Metodo per mantenere l'attivita' di enzimi proteolitici modificati con polietilenglicole | |
| FR2686899B1 (fr) | 1992-01-31 | 1995-09-01 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides biologiquement actifs, leur preparation et compositions pharmaceutiques les contenant. |
| DE69312700T2 (de) | 1992-04-14 | 1998-02-19 | Cornell Res Foundation Inc | Makromoleküle auf basis von dendritischen polymeren und verfahren zur herstellung |
| US5516657A (en) * | 1992-05-11 | 1996-05-14 | Cambridge Biotech Corporation | Baculovirus vectors for expression of secretory and membrane-bound proteins |
| ZA933926B (en) * | 1992-06-17 | 1994-01-03 | Amgen Inc | Polyoxymethylene-oxyethylene copolymers in conjuction with blomolecules |
| WO1994004193A1 (en) | 1992-08-21 | 1994-03-03 | Enzon, Inc. | Novel attachment of polyalkylene oxides to bio-effecting substances |
| US5382657A (en) * | 1992-08-26 | 1995-01-17 | Hoffmann-La Roche Inc. | Peg-interferon conjugates |
| NZ250375A (en) | 1992-12-09 | 1995-07-26 | Ortho Pharma Corp | Peg hydrazone and peg oxime linkage forming reagents and protein derivatives |
| US5298643A (en) | 1992-12-22 | 1994-03-29 | Enzon, Inc. | Aryl imidate activated polyalkylene oxides |
| AU6029594A (en) | 1993-01-15 | 1994-08-15 | Enzon, Inc. | Factor viii - polymeric conjugates |
| US5349001A (en) | 1993-01-19 | 1994-09-20 | Enzon, Inc. | Cyclic imide thione activated polyalkylene oxides |
| US5321095A (en) | 1993-02-02 | 1994-06-14 | Enzon, Inc. | Azlactone activated polyalkylene oxides |
| US5532142A (en) * | 1993-02-12 | 1996-07-02 | Board Of Regents, The University Of Texas System | Method of isolation and purification of fusion polypeptides |
| IL104734A0 (en) * | 1993-02-15 | 1993-06-10 | Univ Bar Ilan | Bioactive conjugates of cellulose with amino compounds |
| AU7097094A (en) | 1993-06-01 | 1994-12-20 | Enzon, Inc. | Carbohydrate-modified polymer conjugates with erythropoietic activity |
| AU7113594A (en) | 1993-06-21 | 1995-01-17 | Enzon, Inc. | Site specific synthesis of conjugated peptides |
| GB9317618D0 (en) | 1993-08-24 | 1993-10-06 | Royal Free Hosp School Med | Polymer modifications |
| US5762939A (en) | 1993-09-13 | 1998-06-09 | Mg-Pmc, Llc | Method for producing influenza hemagglutinin multivalent vaccines using baculovirus |
| US5874454A (en) | 1993-09-15 | 1999-02-23 | Warner-Lambert Company | Use of thiazolidinedione derivatives in the treatment of polycystic ovary syndrome, gestational diabetes and disease states at risk for progressing to noninsulin-dependent diabetes mellitus |
| US5643575A (en) | 1993-10-27 | 1997-07-01 | Enzon, Inc. | Non-antigenic branched polymer conjugates |
| US5919455A (en) | 1993-10-27 | 1999-07-06 | Enzon, Inc. | Non-antigenic branched polymer conjugates |
| US5491076A (en) * | 1993-11-01 | 1996-02-13 | The Texas A&M University System | Expression of foreign genes using a replicating polyprotein producing virus vector |
| US5605792A (en) * | 1993-11-04 | 1997-02-25 | The Ohio State University Research Foundation | Infectious bursal disease virus VP2 fusion protein expressed by baculovirus, use as diagnostic |
| HUT75533A (en) | 1993-11-10 | 1997-05-28 | Schering Corp | Improved interferon polymer conjugates |
| US5951974A (en) | 1993-11-10 | 1999-09-14 | Enzon, Inc. | Interferon polymer conjugates |
| US5446090A (en) * | 1993-11-12 | 1995-08-29 | Shearwater Polymers, Inc. | Isolatable, water soluble, and hydrolytically stable active sulfones of poly(ethylene glycol) and related polymers for modification of surfaces and molecules |
| FR2715664B1 (fr) | 1994-01-31 | 1996-04-12 | Proteine Performance Sa | Baculovirus recombinant et son utilisation pour la production d'anticorps monoclonaux. |
| JP3090586B2 (ja) * | 1994-03-15 | 2000-09-25 | 片倉工業株式会社 | システインプロテアーゼ遺伝子欠損バキュロウイルスおよびその製造法並びにこれを利用する有用タンパク質の製造法 |
| US5473034A (en) * | 1994-03-18 | 1995-12-05 | Hyogo Prefectural Government | Method for producing protein-synthetic polymer conjugate and said conjugate produced thereby |
| US5629384A (en) * | 1994-05-17 | 1997-05-13 | Consiglio Nazionale Delle Ricerche | Polymers of N-acryloylmorpholine activated at one end and conjugates with bioactive materials and surfaces |
| US5686110A (en) | 1994-06-02 | 1997-11-11 | Enzon, Inc. | Water soluble complex of an alkyl or olefinic end capped polyalkylene oxide and a water insoluble substance |
| US5730990A (en) | 1994-06-24 | 1998-03-24 | Enzon, Inc. | Non-antigenic amine derived polymers and polymer conjugates |
| US6403375B1 (en) | 1994-08-24 | 2002-06-11 | Boyce Thompson Institute For Plant Research, Inc. | Establishment of Trichoplusia ni cell lines in serum-free medium for recombinant protein and baculovirus production |
| US5650234A (en) * | 1994-09-09 | 1997-07-22 | Surface Engineering Technologies, Division Of Innerdyne, Inc. | Electrophilic polyethylene oxides for the modification of polysaccharides, polypeptides (proteins) and surfaces |
| US5871986A (en) | 1994-09-23 | 1999-02-16 | The General Hospital Corporation | Use of a baculovirus to express and exogenous gene in a mammalian cell |
| US5824784A (en) | 1994-10-12 | 1998-10-20 | Amgen Inc. | N-terminally chemically modified protein compositions and methods |
| EP0788375A2 (en) | 1994-11-09 | 1997-08-13 | Robin Ewart Offord | Functionalized polymers for site-specific attachment |
| US5738846A (en) | 1994-11-10 | 1998-04-14 | Enzon, Inc. | Interferon polymer conjugates and process for preparing the same |
| IL116085A (en) | 1994-12-16 | 1999-12-31 | Ortho Pharma Corp | Spray dried erythropoietin |
| US6852502B1 (en) | 1995-06-06 | 2005-02-08 | Bioveris Corporation | Electrochemiluminescent enzyme biosensors |
| US5932462A (en) | 1995-01-10 | 1999-08-03 | Shearwater Polymers, Inc. | Multiarmed, monofunctional, polymer for coupling to molecules and surfaces |
| EP0842275A1 (en) | 1995-02-17 | 1998-05-20 | Instituut Voor Dierhouderij En Diergezondheid (Id-Dlo) | PRODUCTION OF BIOLOGICALLY ACTIVE RECOMBINANT BOVINE FOLLICLE STIMULATING HORMONE (REC bFSH) IN THE BACULOVIRUS EXPRESSION SYSTEM |
| FR2732035B1 (fr) | 1995-03-23 | 1997-05-30 | Agronomique Inst Nat Rech | Procede de regulation de l'expression d'un gene dans un baculovirus, par un site de fixation d'un recepteur de l'acide retinoique, et vecteur pour la mise en oeuvre du dit procede |
| US6184344B1 (en) | 1995-05-04 | 2001-02-06 | The Scripps Research Institute | Synthesis of proteins by native chemical ligation |
| NZ308772A (en) | 1995-05-17 | 1999-04-29 | Du Pont | Recombinant baculovirus insecticides |
| AU5893696A (en) | 1995-06-07 | 1996-12-30 | Novo Nordisk A/S | Modification of polypeptides |
| WO1996040662A2 (en) * | 1995-06-07 | 1996-12-19 | Cellpro, Incorporated | Aminooxy-containing linker compounds and their application in conjugates |
| US5672662A (en) * | 1995-07-07 | 1997-09-30 | Shearwater Polymers, Inc. | Poly(ethylene glycol) and related polymers monosubstituted with propionic or butanoic acids and functional derivatives thereof for biotechnical applications |
| GB9526733D0 (en) | 1995-12-30 | 1996-02-28 | Delta Biotechnology Ltd | Fusion proteins |
| AU1690697A (en) | 1996-01-17 | 1997-08-11 | Schering Corporation | Baculovirus expression system for human interleukin 5 receptor and method of screening for interleukin antagonists |
| US5861279A (en) | 1996-01-17 | 1999-01-19 | Schering Corporation | Baculovirus expression system for human interleukin 5 receptor and method of screening for interleukin 5 antagonists |
| US5747639A (en) | 1996-03-06 | 1998-05-05 | Amgen Boulder Inc. | Use of hydrophobic interaction chromatography to purify polyethylene glycols |
| TW517067B (en) | 1996-05-31 | 2003-01-11 | Hoffmann La Roche | Interferon conjugates |
| AU3908597A (en) | 1996-08-02 | 1998-02-25 | Ortho-Mcneil Pharmaceutical, Inc. | Polypeptides having a single covalently bound n-terminal water-soluble polymer |
| US5980948A (en) | 1996-08-16 | 1999-11-09 | Osteotech, Inc. | Polyetherester copolymers as drug delivery matrices |
| US6214966B1 (en) | 1996-09-26 | 2001-04-10 | Shearwater Corporation | Soluble, degradable poly(ethylene glycol) derivatives for controllable release of bound molecules into solution |
| WO1998025963A1 (en) | 1996-12-13 | 1998-06-18 | Chiron Corporation | Analysis and separation of platelet-derived growth factor proteins |
| AU5773798A (en) | 1997-01-29 | 1998-08-18 | Polymasc Pharmaceuticals Plc | Pegylation process |
| GB9703406D0 (en) | 1997-02-19 | 1997-04-09 | Chiron Spa | Expression of heterologous proteins |
| US5859037A (en) | 1997-02-19 | 1999-01-12 | Warner-Lambert Company | Sulfonylurea-glitazone combinations for diabetes |
| US6057338A (en) | 1997-04-04 | 2000-05-02 | Merck & Co., Inc. | Somatostatin agonists |
| US6025372A (en) | 1997-04-04 | 2000-02-15 | Merck & Co., Inc. | Somatostatin agonists |
| JP2002505574A (ja) | 1997-04-30 | 2002-02-19 | エンゾン,インコーポレイテッド | ポリアルキレンオキシド修飾された単鎖ポリペプチド |
| US5990237A (en) | 1997-05-21 | 1999-11-23 | Shearwater Polymers, Inc. | Poly(ethylene glycol) aldehyde hydrates and related polymers and applications in modifying amines |
| US6583267B2 (en) | 1997-06-06 | 2003-06-24 | Kyowa Hakko Kogyo Co., Ltd. | Chemically modified polypeptides |
| US5965393A (en) | 1997-07-01 | 1999-10-12 | National Institute Of Immunology | Method for enhancing foreign gene expression in baculovirus expression vector system |
| IL133974A0 (en) | 1997-07-14 | 2001-04-30 | Bolder Biotechnology Inc | Derivatives of growth hormone and related proteins |
| GB9715660D0 (en) | 1997-07-25 | 1997-10-01 | Zeneca Ltd | Proteins |
| EP1003889A1 (en) | 1997-08-05 | 2000-05-31 | Chiron Corporation | NOVEL $i(PICHIA PASTORIS) GENE SEQUENCES AND METHODS FOR THEIR USE |
| DE19735593C2 (de) | 1997-08-15 | 1999-08-26 | Hepavec Ag Fuer Gentherapie | Hüllprotein-modifizierter Baculovirus-Vektor für die Gentherapie |
| US6090584A (en) | 1997-08-21 | 2000-07-18 | University Technologies International Inc. | Baculovirus artificial chromosomes and methods of use |
| US5989868A (en) | 1997-09-12 | 1999-11-23 | The Board Of Regents Of The University Of Oklahoma | Fusion protein systems designed to increase soluble cytoplasmic expression of heterologous proteins in esherichia coli |
| DK1015576T3 (da) | 1997-09-16 | 2005-08-29 | Egea Biosciences Llc | Fremgangsmåde til fuldstændig kemisk syntese og aggregering af gener og genomer |
| AU752037B2 (en) | 1997-09-26 | 2002-09-05 | Uab Research Foundation | Reduced antigenic cells and uses therefor |
| US6201072B1 (en) | 1997-10-03 | 2001-03-13 | Macromed, Inc. | Biodegradable low molecular weight triblock poly(lactide-co- glycolide) polyethylene glycol copolymers having reverse thermal gelation properties |
| US6004573A (en) | 1997-10-03 | 1999-12-21 | Macromed, Inc. | Biodegradable low molecular weight triblock poly(lactide-co-glycolide) polyethylene glycol copolymers having reverse thermal gelation properties |
| AU1285499A (en) | 1997-10-30 | 1999-05-24 | Merck & Co., Inc. | Somatostatin agonists |
| DE19748489A1 (de) | 1997-11-03 | 1999-05-06 | Roche Diagnostics Gmbh | Polyethylenglykol-derivatisierte Biomoleküle und deren Verwendung in heterogenen Nachweisverfahren |
| US6448369B1 (en) | 1997-11-06 | 2002-09-10 | Shearwater Corporation | Heterobifunctional poly(ethylene glycol) derivatives and methods for their preparation |
| EP0924298A1 (en) | 1997-12-18 | 1999-06-23 | Stichting Instituut voor Dierhouderij en Diergezondheid (ID-DLO) | Protein expression in baculovirus vector expression systems |
| US5981709A (en) | 1997-12-19 | 1999-11-09 | Enzon, Inc. | α-interferon-polymer-conjugates having enhanced biological activity and methods of preparing the same |
| US5985263A (en) | 1997-12-19 | 1999-11-16 | Enzon, Inc. | Substantially pure histidine-linked protein polymer conjugates |
| US6225060B1 (en) | 1998-03-04 | 2001-05-01 | Onyx Pharmaceuticals, Inc. | Baculovirus expression system and method for high throughput expression of genetic material |
| ATE279430T1 (de) | 1998-03-05 | 2004-10-15 | Chiron Corp | Verfahren zur verbesserung der serum halbwertszeit von biologisch aktiven molekülen |
| ATE268609T1 (de) | 1998-03-12 | 2004-06-15 | Nektar Therapeutics Al Corp | Polyethylenglycolderivate mit benachbarten reaktiven gruppen |
| KR100264953B1 (ko) | 1998-04-03 | 2001-03-02 | 박현우 | 재조합 베큘로바이러스, 이의 제조방법 및 이를 포함하는 미생물 살충제 |
| US6451986B1 (en) | 1998-06-22 | 2002-09-17 | Immunex Corporation | Site specific protein modification |
| US6168932B1 (en) | 1998-07-13 | 2001-01-02 | Parker Hughes Institute | Recombinant DTctGMCSF fusion toxin in a baculovirus expression vector system |
| US6245528B1 (en) | 1998-07-28 | 2001-06-12 | Academia Sinica | Latent baculovirus expression system |
| US6368825B1 (en) | 1998-08-10 | 2002-04-09 | Academia Sinica | Baculovirus containing minimal CMV promoter |
| DE69936322T2 (de) | 1998-08-28 | 2008-02-21 | Amylin Pharmaceuticals, Inc., San Diego | Polyamideketten von genauer Länge und deren Konjugate mit Proteinen |
| WO2000020032A1 (en) | 1998-10-06 | 2000-04-13 | Trustees Of Dartmouth College | RECOMBINANT CAT ALLERGEN, Fel dI, EXPRESSED IN BACULOVIRUS FOR DIAGNOSIS AND TREATMENT OF CAT ALLERGY |
| US6420339B1 (en) | 1998-10-14 | 2002-07-16 | Amgen Inc. | Site-directed dual pegylation of proteins for improved bioactivity and biocompatibility |
| WO2000026354A1 (en) | 1998-10-30 | 2000-05-11 | Novozymes A/S | Glycosylated proteins having reduced allergenicity |
| US6451346B1 (en) | 1998-12-23 | 2002-09-17 | Amgen Inc | Biodegradable pH/thermosensitive hydrogels for sustained delivery of biologically active agents |
| US6281211B1 (en) | 1999-02-04 | 2001-08-28 | Euro-Celtique S.A. | Substituted semicarbazides and the use thereof |
| US6994986B2 (en) | 1999-03-17 | 2006-02-07 | The Board Of Trustees Of The Leland Stanford University | In vitro synthesis of polypeptides by optimizing amino acid metabolism |
| EP1177311B1 (en) | 1999-03-17 | 2014-11-12 | The Board Of Trustees Of The Leland Stanford Junior University | In vitro macromolecule biosynthesis methods using exogenous amino acids and a novel atp regeneration system |
| US6342216B1 (en) | 1999-03-17 | 2002-01-29 | The Board Of Regents, The University Of Texas System | Therapy of cancer by insect cells containing recombinant baculovirus encoding genes |
| US6337191B1 (en) | 1999-03-22 | 2002-01-08 | The Board Of Trustees Of The Leland Stanford Junior University | Vitro protein synthesis using glycolytic intermediates as an energy source |
| JP2002542349A (ja) | 1999-04-16 | 2002-12-10 | ダブリューエム・マーシュ・ライス・ユニバーシティー | ポリ(プロピレンフマラート)−ジアクリレートマクロマーで交差結合された生体分解性のポリ(プロピレンフマラート)ネットワーク |
| US6261805B1 (en) | 1999-07-15 | 2001-07-17 | Boyce Thompson Institute For Plant Research, Inc. | Sialyiation of N-linked glycoproteins in the baculovirus expression vector system |
| US7459540B1 (en) | 1999-09-07 | 2008-12-02 | Amgen Inc. | Fibroblast growth factor-like polypeptides |
| US7408047B1 (en) * | 1999-09-07 | 2008-08-05 | Amgen Inc. | Fibroblast growth factor-like polypeptides |
| WO2001025228A1 (en) | 1999-10-07 | 2001-04-12 | Tadeka Chemical Industries, Ltd. | Amine derivatives |
| US6485937B1 (en) | 1999-10-15 | 2002-11-26 | The Rockefeller University | System for rapid generation of recombinant baculovirus-based expression vectors for silkworm larvae |
| WO2001032678A1 (en) | 1999-11-05 | 2001-05-10 | Smithkline Beecham Corporation | sbgFGF-19a |
| PL356487A1 (en) | 1999-11-10 | 2004-06-28 | Takeda Chemical Industries, Ltd. | 5-membered n-heterocyclic compounds with hypoglycemic and hypolipidemic activity |
| EP2163626A1 (en) * | 1999-11-18 | 2010-03-17 | Novartis Vaccines and Diagnostics, Inc. | Human FGF-21 gene and gene expression products |
| US6716626B1 (en) | 1999-11-18 | 2004-04-06 | Chiron Corporation | Human FGF-21 nucleic acids |
| US6348558B1 (en) | 1999-12-10 | 2002-02-19 | Shearwater Corporation | Hydrolytically degradable polymers and hydrogels made therefrom |
| US6376604B2 (en) | 1999-12-22 | 2002-04-23 | Shearwater Corporation | Method for the preparation of 1-benzotriazolylcarbonate esters of poly(ethylene glycol) |
| MXPA02006216A (es) | 1999-12-22 | 2004-02-26 | Nektar Therapeutics Al Corp | Derivados estericamente impedidos de polimeros solubles en agua. |
| US6413507B1 (en) | 1999-12-23 | 2002-07-02 | Shearwater Corporation | Hydrolytically degradable carbamate derivatives of poly (ethylene glycol) |
| US6646110B2 (en) | 2000-01-10 | 2003-11-11 | Maxygen Holdings Ltd. | G-CSF polypeptides and conjugates |
| WO2001062827A2 (en) | 2000-02-22 | 2001-08-30 | Shearwater Corporation | N-maleimidyl polymer derivatives |
| AU2001257577A1 (en) | 2000-02-28 | 2001-09-03 | Shearwater Corporation | Water-soluble polymer conjugates of artelinic acid |
| WO2001068854A2 (en) * | 2000-03-13 | 2001-09-20 | Amgen, Inc. | Fibroblast growth factor-like molecules and uses thereof |
| GB0012997D0 (en) | 2000-05-26 | 2000-07-19 | Eurogene Limited | Gene delivery |
| US6586207B2 (en) | 2000-05-26 | 2003-07-01 | California Institute Of Technology | Overexpression of aminoacyl-tRNA synthetases for efficient production of engineered proteins containing amino acid analogues |
| JP2002030098A (ja) | 2000-07-17 | 2002-01-29 | Institute Of Immunology Co Ltd | バキュロウィルスの発芽ウイルスからウイルスエンベロープを回収する方法 |
| AU2001273385B2 (en) | 2000-09-08 | 2005-04-07 | Gryphon Therapeutics, Inc. | Polymer-modified synthetic proteins |
| US7118737B2 (en) * | 2000-09-08 | 2006-10-10 | Amylin Pharmaceuticals, Inc. | Polymer-modified synthetic proteins |
| US6436386B1 (en) | 2000-11-14 | 2002-08-20 | Shearwater Corporation | Hydroxyapatite-targeting poly (ethylene glycol) and related polymers |
| TW593427B (en) | 2000-12-18 | 2004-06-21 | Nektar Therapeutics Al Corp | Synthesis of high molecular weight non-peptidic polymer derivatives |
| TWI246524B (en) | 2001-01-19 | 2006-01-01 | Shearwater Corp | Multi-arm block copolymers as drug delivery vehicles |
| DK2322631T3 (en) | 2001-04-19 | 2015-01-12 | Scripps Research Inst | Methods and compositions for the production of orthogonal tRNA-aminoacyl-tRNA syntetasepar |
| GB0113657D0 (en) | 2001-06-05 | 2001-07-25 | Geneprot Inc | Improved native chemical ligation with three or more components |
| US20040259780A1 (en) | 2001-07-30 | 2004-12-23 | Glasebrook Andrew Lawrence | Method for treating diabetes and obesity |
| US20040138412A1 (en) | 2001-09-07 | 2004-07-15 | Paolo Botti | Extended native chemical ligation |
| US6908963B2 (en) | 2001-10-09 | 2005-06-21 | Nektar Therapeutics Al, Corporation | Thioester polymer derivatives and method of modifying the N-terminus of a polypeptide therewith |
| EP2305312B1 (en) * | 2001-10-10 | 2015-03-04 | ratiopharm GmbH | Remodelling and glycoconjugation of follicle-stimulating hormone (FSH) |
| WO2003042204A1 (en) | 2001-10-19 | 2003-05-22 | Takeda Chemical Industries, Ltd. | Amine derivative |
| EP1446438A2 (en) | 2001-11-07 | 2004-08-18 | Nektar Therapeutics Al, Corporation | Branched polymers and their conjugates |
| EP1456225A2 (en) | 2001-11-14 | 2004-09-15 | Geneprot, Inc. | Extended native chemical ligation of three or more peptide fragments |
| US6716821B2 (en) | 2001-12-21 | 2004-04-06 | Immunogen Inc. | Cytotoxic agents bearing a reactive polyethylene glycol moiety, cytotoxic conjugates comprising polyethylene glycol linking groups, and methods of making and using the same |
| AU2003201810A1 (en) | 2002-01-15 | 2003-07-30 | Eli Lilly And Company | Method for reducing morbidity and mortality in critically ill patients |
| DE60328587D1 (de) | 2002-02-15 | 2009-09-10 | Univ New York State Res Found | RIBOZYME MIT BREITER tRNA-AMINOACYLIERUNGSWIRKUNG |
| ES2566761T3 (es) | 2002-05-30 | 2016-04-15 | The Scripps Research Institute | Ligación de azidas y acetilenos catalizada por cobre |
| CA2500653A1 (en) | 2002-10-16 | 2004-04-29 | The Scripps Research Institute | Glycoprotein synthesis |
| US7432092B2 (en) | 2002-10-16 | 2008-10-07 | The Scripps Research Institute | Site specific incorporation of keto amino acids into proteins |
| EP1583816A4 (en) | 2002-12-22 | 2007-06-13 | Scripps Research Inst | PROTEIN ARRAYS |
| CN100522988C (zh) * | 2003-04-09 | 2009-08-05 | 诺和诺德公司 | 糖peg化方法及由该方法生产的蛋白质/肽 |
| KR101171397B1 (ko) | 2003-04-17 | 2012-08-07 | 더 스크립스 리서치 인스티튜트 | 진핵 유전자 코드의 확장 |
| CN1802167A (zh) | 2003-06-12 | 2006-07-12 | 伊莱利利公司 | 融合蛋白质 |
| ES2301099T3 (es) | 2003-07-07 | 2008-06-16 | The Scripps Research Institute | Composiciones de parejas ortogonales lisil-arnt y aminoacil-arnt sintetasa y usos de las mismas. |
| WO2005007870A2 (en) | 2003-07-07 | 2005-01-27 | The Scripps Research Institute | COMPOSITIONS OF ORTHOGONAL LEUCYL-tRNA AND AMINOACYL-tRNA SYNTHETASE PAIRS AND USES THEREOF |
| EP1658366A4 (en) | 2003-07-07 | 2006-08-09 | Scripps Research Inst | COMPOSITIONS OF ORTHOGONAL GLUTAMYL-TRNA AND AMINOACYL-TRNA-SYNTHETASEPAARES AND THEIR USES |
| ES2737837T3 (es) | 2003-10-09 | 2020-01-16 | Ambrx Inc | Derivados poliméricos |
| AU2004303783A1 (en) | 2003-12-10 | 2005-07-07 | Eli Lilly And Company | Muteins of fibroblast growth factor 21 |
| EP1727559A1 (en) | 2004-01-26 | 2006-12-06 | Eli Lilly And Company | Use of fgf-21 and a thiazolidinedione for treating type 2 diabetes |
| US7896406B2 (en) | 2004-01-30 | 2011-03-01 | Certainteed Corporation | Hose connector |
| US8778880B2 (en) | 2004-02-02 | 2014-07-15 | Ambrx, Inc. | Human growth hormone modified at position 35 |
| CN101001866A (zh) * | 2004-02-02 | 2007-07-18 | Ambrx公司 | 经修饰的人类干扰素多肽和其用途 |
| JP2007531715A (ja) * | 2004-03-17 | 2007-11-08 | イーライ リリー アンド カンパニー | グリコール結合fgf−21化合物 |
| DK1751184T3 (da) * | 2004-05-13 | 2009-11-23 | Lilly Co Eli | FGF-21 fusionsproteiner |
| MX2007002616A (es) * | 2004-09-02 | 2007-05-16 | Lilly Co Eli | Muteinas de factor de crecimiento de fibroblasto 21. |
| WO2006028714A1 (en) | 2004-09-02 | 2006-03-16 | Eli Lilly And Company | Muteins of fibroblast growth factor 21 |
| EP1814573B1 (en) | 2004-10-29 | 2016-03-09 | ratiopharm GmbH | Remodeling and glycopegylation of fibroblast growth factor (fgf) |
| US7655627B2 (en) * | 2004-12-14 | 2010-02-02 | Eli Lilly And Company | Muteins of fibroblast growth factor 21 |
| WO2006071840A2 (en) | 2004-12-22 | 2006-07-06 | Ambrx, Inc. | Formulations of human growth hormone comprising a non-naturally encoded amino acid |
| WO2006068802A2 (en) | 2004-12-22 | 2006-06-29 | Ambrx, Inc. | COMPOSITIONS OF AMINOACYL-tRNA SYNTHETASE AND USES THEREOF |
| MX2007007590A (es) | 2004-12-22 | 2007-12-10 | Ambrx Inc | Composiciones que contienen, metodos que involucran y usos de aminoacidos no naturales y polipeptidos. |
| US20080261875A1 (en) | 2005-01-21 | 2008-10-23 | Eli Lilly And Company | Method For Treating Cardiovascular Disease |
| MX2007015106A (es) * | 2005-06-03 | 2008-02-15 | Ambrx Inc | Incorporacion de aminoacidos codificadores de manera no natural en proteinas. |
| WO2007021297A1 (en) | 2005-08-18 | 2007-02-22 | Ambrx, Inc. | COMPOSITIONS OF tRNA AND USES THEREOF |
| US7855279B2 (en) | 2005-09-27 | 2010-12-21 | Amunix Operating, Inc. | Unstructured recombinant polymers and uses thereof |
| US7846445B2 (en) | 2005-09-27 | 2010-12-07 | Amunix Operating, Inc. | Methods for production of unstructured recombinant polymers and uses thereof |
| ES2529065T3 (es) | 2005-12-14 | 2015-02-16 | Ambrx, Inc. | Composiciones que contienen, procedimientos que implican y usos de aminoácidos no naturales y polipéptidos |
| CA2632832A1 (en) | 2005-12-30 | 2007-07-12 | Ambrx, Inc. | Compositions containing, methods involving, and uses of non-natural amino acids and polypeptides |
| US20100098630A1 (en) | 2006-12-28 | 2010-04-22 | Ambrx, Inc. | Phenazine and Quinoxaline Substituted Amino Acids and Polypeptides |
| PL2068909T3 (pl) | 2007-03-30 | 2012-09-28 | Ambrx Inc | Modyfikowane polipeptydy fgf-21 i ich zastosowanie |
| HRP20110368T1 (hr) | 2007-06-21 | 2011-06-30 | Technische Universitt Mnchen | Biološki aktivni proteini s povećanom stabilnošću in vivo i/ili in vitro |
| EA024751B8 (ru) | 2008-06-04 | 2020-01-31 | Амген Инк. | Мутанты fgf21 и их применение |
| EP2358749B1 (en) | 2008-10-10 | 2018-07-18 | Amgen, Inc | Fgf21 mutants and uses thereof |
| ES2692495T3 (es) | 2009-01-23 | 2018-12-03 | Novo Nordisk A/S | Derivados del FGF21 con aglutinante de albúmina A-B-C-D-E- y sus usos |
| US20120052069A1 (en) | 2009-05-05 | 2012-03-01 | Amgen Inc | Fgf21 mutants and uses thereof |
| US20120172298A1 (en) | 2009-06-11 | 2012-07-05 | Novo Nordisk A/S | Glp-1 and fgf21 combinations for treatment of diabetes type 2 |
| TW201138808A (en) | 2010-05-03 | 2011-11-16 | Bristol Myers Squibb Co | Serum albumin binding molecules |
| JP2013533227A (ja) | 2010-06-08 | 2013-08-22 | ノヴォ ノルディスク アー/エス | Fgf21類似体および誘導体 |
| US9023791B2 (en) | 2010-11-19 | 2015-05-05 | Novartis Ag | Fibroblast growth factor 21 mutations |
| JP2014516049A (ja) | 2011-05-25 | 2014-07-07 | アミリン・ファーマシューティカルズ,リミテッド・ライアビリティ・カンパニー | アミリンペプチドおよび誘導体ならびにそれらの使用 |
| UY34346A (es) | 2011-09-26 | 2013-04-30 | Novartis Ag | Proteínas de fusión para tratar trastornos metabólicos |
| AR087973A1 (es) | 2011-10-04 | 2014-04-30 | Lilly Co Eli | Variantes del factor 21 del crecimiento de fibroblastos |
| TWI513705B (zh) | 2012-06-11 | 2015-12-21 | Lilly Co Eli | 纖維母細胞生長因子21蛋白質 |
| AU2013311777B2 (en) | 2012-09-07 | 2018-02-01 | Sanofi | Fusion proteins for treating a metabolic syndrome |
| CN103923207B (zh) | 2014-04-08 | 2016-03-09 | 东北农业大学 | 一种fgf-21突变体蛋白的制备及其在治疗非酒精性脂肪肝中的应用 |
| CN107108710B (zh) | 2014-10-24 | 2022-02-15 | 百时美施贵宝公司 | 修饰的fgf-21多肽及其用途 |
-
2008
- 2008-03-19 PL PL08732507T patent/PL2068909T3/pl unknown
- 2008-03-19 MX MX2009010531A patent/MX2009010531A/es active IP Right Grant
- 2008-03-19 DK DK08732507.2T patent/DK2068909T3/da active
- 2008-03-19 EP EP08732507A patent/EP2068909B1/en active Active
- 2008-03-19 JP JP2010501093A patent/JP2010523084A/ja active Pending
- 2008-03-19 KR KR1020097022588A patent/KR101476472B1/ko active Active
- 2008-03-19 CA CA2682147A patent/CA2682147C/en active Active
- 2008-03-19 CN CN201710585053.8A patent/CN107501407B/zh not_active Expired - Fee Related
- 2008-03-19 KR KR1020167027888A patent/KR20160121601A/ko not_active Ceased
- 2008-03-19 AU AU2008232937A patent/AU2008232937B2/en not_active Ceased
- 2008-03-19 AT AT08732507T patent/ATE554785T1/de active
- 2008-03-19 PT PT08732507T patent/PT2068909E/pt unknown
- 2008-03-19 WO PCT/US2008/057563 patent/WO2008121563A2/en not_active Ceased
- 2008-03-19 BR BRPI0809583-3A patent/BRPI0809583B1/pt not_active IP Right Cessation
- 2008-03-19 HR HRP20120522AT patent/HRP20120522T1/hr unknown
- 2008-03-19 KR KR1020137034998A patent/KR20140012199A/ko not_active Ceased
- 2008-03-19 KR KR1020157014075A patent/KR101808787B1/ko active Active
- 2008-03-19 US US12/051,830 patent/US8012931B2/en active Active
- 2008-03-19 ES ES08732507T patent/ES2385114T3/es active Active
- 2008-03-19 CN CN201410360138.2A patent/CN104163864B/zh not_active Expired - Fee Related
-
2009
- 2009-09-06 IL IL200749A patent/IL200749B/en active IP Right Grant
-
2011
- 2011-03-18 US US13/051,953 patent/US8383365B2/en active Active
-
2012
- 2012-07-20 CY CY20121100645T patent/CY1113188T1/el unknown
-
2013
- 2013-01-02 US US13/732,522 patent/US9079971B2/en active Active
-
2014
- 2014-10-24 JP JP2014217739A patent/JP6158158B2/ja not_active Expired - Fee Related
-
2015
- 2015-04-07 US US14/680,543 patent/US9517273B2/en active Active
-
2016
- 2016-10-13 US US15/292,700 patent/US9975936B2/en active Active
-
2017
- 2017-06-07 JP JP2017112750A patent/JP2017212986A/ja active Pending
-
2018
- 2018-04-13 US US15/953,091 patent/US10377805B2/en active Active
- 2018-04-16 IL IL258724A patent/IL258724B/en active IP Right Grant
-
2019
- 2019-06-17 US US16/443,226 patent/US10961291B2/en active Active
- 2019-10-03 JP JP2019182614A patent/JP2020018314A/ja active Pending
-
2021
- 2021-02-02 US US17/165,351 patent/US11993637B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11993637B2 (en) | Modified FGF-21 polypeptides with non-naturally encoded amino acids | |
| US20110015345A1 (en) | Modified FGF-23 Polypeptides and Their Uses | |
| CN101663046B (zh) | 经修饰fgf‑21多肽和其用途 | |
| AU2012268895B2 (en) | Modified FGF-21 polypeptides and their uses | |
| HK1248715B (en) | Modified fgf-21 polypeptides and their uses | |
| HK1134239B (en) | Modified fgf-21 polypeptides and their uses | |
| HK1204331B (en) | Modified fgf-21 polypeptides and their uses |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 19/03/2008, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 18A ANUIDADE. |