RU2352583C2 - ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ Fc-ОБЛАСТЬ ИММУНОГЛОБУЛИНА В КАЧЕСТВЕ НОСИТЕЛЯ - Google Patents
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ Fc-ОБЛАСТЬ ИММУНОГЛОБУЛИНА В КАЧЕСТВЕ НОСИТЕЛЯ Download PDFInfo
- Publication number
- RU2352583C2 RU2352583C2 RU2005120239/13A RU2005120239A RU2352583C2 RU 2352583 C2 RU2352583 C2 RU 2352583C2 RU 2005120239/13 A RU2005120239/13 A RU 2005120239/13A RU 2005120239 A RU2005120239 A RU 2005120239A RU 2352583 C2 RU2352583 C2 RU 2352583C2
- Authority
- RU
- Russia
- Prior art keywords
- peg
- fragment
- immunoglobulin
- protein
- factor
- Prior art date
Links
- 108060003951 Immunoglobulin Proteins 0.000 title claims abstract description 64
- 102000018358 immunoglobulin Human genes 0.000 title claims abstract description 64
- 239000008194 pharmaceutical composition Substances 0.000 title description 13
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 claims abstract description 149
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 claims abstract description 149
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 81
- 102000004196 processed proteins & peptides Human genes 0.000 claims abstract description 56
- 229920001184 polypeptide Polymers 0.000 claims abstract description 52
- 238000000034 method Methods 0.000 claims abstract description 50
- 238000001727 in vivo Methods 0.000 claims abstract description 32
- 230000009471 action Effects 0.000 claims abstract description 14
- 108090000623 proteins and genes Proteins 0.000 claims description 182
- 102000004169 proteins and genes Human genes 0.000 claims description 176
- 235000018102 proteins Nutrition 0.000 claims description 173
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 claims description 43
- 238000009739 binding Methods 0.000 claims description 35
- 102000002265 Human Growth Hormone Human genes 0.000 claims description 34
- 108010000521 Human Growth Hormone Proteins 0.000 claims description 34
- 108010047761 Interferon-alpha Proteins 0.000 claims description 33
- 102000006992 Interferon-alpha Human genes 0.000 claims description 33
- 102000003951 Erythropoietin Human genes 0.000 claims description 32
- 108090000394 Erythropoietin Proteins 0.000 claims description 32
- 239000000854 Human Growth Hormone Substances 0.000 claims description 32
- 229940105423 erythropoietin Drugs 0.000 claims description 32
- 230000027455 binding Effects 0.000 claims description 31
- 210000004027 cell Anatomy 0.000 claims description 31
- 230000001965 increasing effect Effects 0.000 claims description 27
- 108010088751 Albumins Proteins 0.000 claims description 21
- 102000009027 Albumins Human genes 0.000 claims description 21
- 239000012634 fragment Substances 0.000 claims description 21
- 239000003102 growth factor Substances 0.000 claims description 11
- 102100022641 Coagulation factor IX Human genes 0.000 claims description 10
- 108010076282 Factor IX Proteins 0.000 claims description 10
- 229960004222 factor ix Drugs 0.000 claims description 10
- -1 antibodies Substances 0.000 claims description 9
- 239000000427 antigen Substances 0.000 claims description 9
- 102000036639 antigens Human genes 0.000 claims description 9
- 108091007433 antigens Proteins 0.000 claims description 9
- 102000014150 Interferons Human genes 0.000 claims description 8
- 108010050904 Interferons Proteins 0.000 claims description 8
- 102000004190 Enzymes Human genes 0.000 claims description 7
- 108090000790 Enzymes Proteins 0.000 claims description 7
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 7
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 7
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 7
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 7
- 229940088598 enzyme Drugs 0.000 claims description 7
- 102000005962 receptors Human genes 0.000 claims description 7
- 108020003175 receptors Proteins 0.000 claims description 7
- 230000004913 activation Effects 0.000 claims description 5
- 230000001939 inductive effect Effects 0.000 claims description 5
- 108010071942 Colony-Stimulating Factors Proteins 0.000 claims description 4
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 claims description 4
- 102000015696 Interleukins Human genes 0.000 claims description 4
- 108010063738 Interleukins Proteins 0.000 claims description 4
- 102000013275 Somatomedins Human genes 0.000 claims description 4
- 230000008468 bone growth Effects 0.000 claims description 4
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 4
- 210000002540 macrophage Anatomy 0.000 claims description 4
- 102000003886 Glycoproteins Human genes 0.000 claims description 3
- 108090000288 Glycoproteins Proteins 0.000 claims description 3
- 102000001617 Interferon Receptors Human genes 0.000 claims description 3
- 108010054267 Interferon Receptors Proteins 0.000 claims description 3
- 229940088597 hormone Drugs 0.000 claims description 3
- 239000005556 hormone Substances 0.000 claims description 3
- 229940047124 interferons Drugs 0.000 claims description 3
- 229960004854 viral vaccine Drugs 0.000 claims description 3
- DDYAPMZTJAYBOF-ZMYDTDHYSA-N (3S)-4-[[(2S)-1-[[(2S)-1-[[(2S)-5-amino-1-[[(2S)-1-[[(2S)-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S,3R)-1-[[(2S)-6-amino-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S)-1-[[(2S)-4-amino-1-[[(2S)-4-amino-1-[[(2S,3S)-1-[[(1S)-1-carboxyethyl]amino]-3-methyl-1-oxopentan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-5-carbamimidamido-1-oxopentan-2-yl]amino]-1-oxohexan-2-yl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-1,4-dioxobutan-2-yl]amino]-4-methylsulfanyl-1-oxobutan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1,5-dioxopentan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-6-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S,3R)-2-[[2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-amino-3-(1H-imidazol-4-yl)propanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]acetyl]amino]-3-hydroxybutanoyl]amino]-3-phenylpropanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-3-hydroxypropanoyl]amino]hexanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-methylpentanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]amino]-5-oxopentanoyl]amino]-4-oxobutanoic acid Chemical class [H]N[C@@H](CC1=CNC=N1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O DDYAPMZTJAYBOF-ZMYDTDHYSA-N 0.000 claims description 2
- HFDKKNHCYWNNNQ-YOGANYHLSA-N 75976-10-2 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@@H](NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](C)N)C(C)C)[C@@H](C)O)C1=CC=C(O)C=C1 HFDKKNHCYWNNNQ-YOGANYHLSA-N 0.000 claims description 2
- 102400000068 Angiostatin Human genes 0.000 claims description 2
- 108010079709 Angiostatins Proteins 0.000 claims description 2
- 108010064733 Angiotensins Proteins 0.000 claims description 2
- 102000015427 Angiotensins Human genes 0.000 claims description 2
- 101710081722 Antitrypsin Proteins 0.000 claims description 2
- 102100029470 Apolipoprotein E Human genes 0.000 claims description 2
- 101710095339 Apolipoprotein E Proteins 0.000 claims description 2
- 102100033367 Appetite-regulating hormone Human genes 0.000 claims description 2
- 102000002723 Atrial Natriuretic Factor Human genes 0.000 claims description 2
- 101800001288 Atrial natriuretic factor Proteins 0.000 claims description 2
- 101000645291 Bos taurus Metalloproteinase inhibitor 2 Proteins 0.000 claims description 2
- 108010074051 C-Reactive Protein Proteins 0.000 claims description 2
- 102100032752 C-reactive protein Human genes 0.000 claims description 2
- 108060001064 Calcitonin Proteins 0.000 claims description 2
- 101800001982 Cholecystokinin Proteins 0.000 claims description 2
- 102100025841 Cholecystokinin Human genes 0.000 claims description 2
- 102100023804 Coagulation factor VII Human genes 0.000 claims description 2
- 229940122097 Collagenase inhibitor Drugs 0.000 claims description 2
- 102000004127 Cytokines Human genes 0.000 claims description 2
- 108090000695 Cytokines Proteins 0.000 claims description 2
- 102000009024 Epidermal Growth Factor Human genes 0.000 claims description 2
- 101800003838 Epidermal growth factor Proteins 0.000 claims description 2
- 108010023321 Factor VII Proteins 0.000 claims description 2
- 108010054218 Factor VIII Proteins 0.000 claims description 2
- 102000001690 Factor VIII Human genes 0.000 claims description 2
- 108010054265 Factor VIIa Proteins 0.000 claims description 2
- 108010073385 Fibrin Proteins 0.000 claims description 2
- 102000009123 Fibrin Human genes 0.000 claims description 2
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 claims description 2
- 102000012673 Follicle Stimulating Hormone Human genes 0.000 claims description 2
- 108010079345 Follicle Stimulating Hormone Proteins 0.000 claims description 2
- 108091006027 G proteins Proteins 0.000 claims description 2
- 102000030782 GTP binding Human genes 0.000 claims description 2
- 108091000058 GTP-Binding Proteins 0.000 claims description 2
- 108060003199 Glucagon Proteins 0.000 claims description 2
- 102400000321 Glucagon Human genes 0.000 claims description 2
- 108010088406 Glucagon-Like Peptides Proteins 0.000 claims description 2
- 239000000095 Growth Hormone-Releasing Hormone Substances 0.000 claims description 2
- 102000007625 Hirudins Human genes 0.000 claims description 2
- 108010007267 Hirudins Proteins 0.000 claims description 2
- 101000987586 Homo sapiens Eosinophil peroxidase Proteins 0.000 claims description 2
- 101000920686 Homo sapiens Erythropoietin Proteins 0.000 claims description 2
- 101000669513 Homo sapiens Metalloproteinase inhibitor 1 Proteins 0.000 claims description 2
- 206010020751 Hypersensitivity Diseases 0.000 claims description 2
- 102000004877 Insulin Human genes 0.000 claims description 2
- 108090001061 Insulin Proteins 0.000 claims description 2
- 102000004407 Lactalbumin Human genes 0.000 claims description 2
- 108090000942 Lactalbumin Proteins 0.000 claims description 2
- 102000016267 Leptin Human genes 0.000 claims description 2
- 108010092277 Leptin Proteins 0.000 claims description 2
- 102000009151 Luteinizing Hormone Human genes 0.000 claims description 2
- 108010073521 Luteinizing Hormone Proteins 0.000 claims description 2
- 108090000542 Lymphotoxin-alpha Proteins 0.000 claims description 2
- 102000004083 Lymphotoxin-alpha Human genes 0.000 claims description 2
- 102100039364 Metalloproteinase inhibitor 1 Human genes 0.000 claims description 2
- 206010028851 Necrosis Diseases 0.000 claims description 2
- 206010028980 Neoplasm Diseases 0.000 claims description 2
- 102000018886 Pancreatic Polypeptide Human genes 0.000 claims description 2
- 102000003982 Parathyroid hormone Human genes 0.000 claims description 2
- 108090000445 Parathyroid hormone Proteins 0.000 claims description 2
- 101800004937 Protein C Proteins 0.000 claims description 2
- 102000017975 Protein C Human genes 0.000 claims description 2
- 102000003743 Relaxin Human genes 0.000 claims description 2
- 108090000103 Relaxin Proteins 0.000 claims description 2
- 101800001700 Saposin-D Proteins 0.000 claims description 2
- 102100037505 Secretin Human genes 0.000 claims description 2
- 108010086019 Secretin Proteins 0.000 claims description 2
- 101710142969 Somatoliberin Proteins 0.000 claims description 2
- 102100022831 Somatoliberin Human genes 0.000 claims description 2
- 108010023197 Streptokinase Proteins 0.000 claims description 2
- 102000019197 Superoxide Dismutase Human genes 0.000 claims description 2
- 108010012715 Superoxide dismutase Proteins 0.000 claims description 2
- 101000983124 Sus scrofa Pancreatic prohormone precursor Proteins 0.000 claims description 2
- 102000000479 TCF Transcription Factors Human genes 0.000 claims description 2
- 108010016283 TCF Transcription Factors Proteins 0.000 claims description 2
- 108010079274 Thrombomodulin Proteins 0.000 claims description 2
- 102100026966 Thrombomodulin Human genes 0.000 claims description 2
- 102100030951 Tissue factor pathway inhibitor Human genes 0.000 claims description 2
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 claims description 2
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 claims description 2
- 230000003213 activating effect Effects 0.000 claims description 2
- 208000026935 allergic disease Diseases 0.000 claims description 2
- 230000007815 allergy Effects 0.000 claims description 2
- 230000001475 anti-trypsic effect Effects 0.000 claims description 2
- FZCSTZYAHCUGEM-UHFFFAOYSA-N aspergillomarasmine B Natural products OC(=O)CNC(C(O)=O)CNC(C(O)=O)CC(O)=O FZCSTZYAHCUGEM-UHFFFAOYSA-N 0.000 claims description 2
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 2
- 108091008324 binding proteins Proteins 0.000 claims description 2
- 230000015572 biosynthetic process Effects 0.000 claims description 2
- 229960004015 calcitonin Drugs 0.000 claims description 2
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 claims description 2
- 229950008486 carperitide Drugs 0.000 claims description 2
- NSQLIUXCMFBZME-MPVJKSABSA-N carperitide Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)=O)[C@@H](C)CC)C1=CC=CC=C1 NSQLIUXCMFBZME-MPVJKSABSA-N 0.000 claims description 2
- 210000000845 cartilage Anatomy 0.000 claims description 2
- DDPFHDCZUJFNAT-PZPWKVFESA-N chembl2104402 Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CCCCCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 DDPFHDCZUJFNAT-PZPWKVFESA-N 0.000 claims description 2
- 229940107137 cholecystokinin Drugs 0.000 claims description 2
- 239000002442 collagenase inhibitor Substances 0.000 claims description 2
- 210000002808 connective tissue Anatomy 0.000 claims description 2
- 102000026898 cytokine binding proteins Human genes 0.000 claims description 2
- 108091008470 cytokine binding proteins Proteins 0.000 claims description 2
- 108700032313 elcatonin Proteins 0.000 claims description 2
- 229960000756 elcatonin Drugs 0.000 claims description 2
- 229940116977 epidermal growth factor Drugs 0.000 claims description 2
- 230000008472 epithelial growth Effects 0.000 claims description 2
- 229940012413 factor vii Drugs 0.000 claims description 2
- 229940012414 factor viia Drugs 0.000 claims description 2
- 229960000301 factor viii Drugs 0.000 claims description 2
- 229950003499 fibrin Drugs 0.000 claims description 2
- 229940028334 follicle stimulating hormone Drugs 0.000 claims description 2
- 108010077689 gamma-aminobutyryl-2-methyltryptophyl-2-methyltryptophyl-2-methyltryptophyl-lysinamide Proteins 0.000 claims description 2
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 claims description 2
- 229960004666 glucagon Drugs 0.000 claims description 2
- 229940006607 hirudin Drugs 0.000 claims description 2
- WQPDUTSPKFMPDP-OUMQNGNKSA-N hirudin Chemical compound C([C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC(OS(O)(=O)=O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@@H]2CSSC[C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(=O)N[C@H](C(NCC(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N2)=O)CSSC1)C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)C(C)C)[C@@H](C)O)CSSC1)C(C)C)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 WQPDUTSPKFMPDP-OUMQNGNKSA-N 0.000 claims description 2
- 102000044890 human EPO Human genes 0.000 claims description 2
- 229940051026 immunotoxin Drugs 0.000 claims description 2
- 230000002637 immunotoxin Effects 0.000 claims description 2
- 231100000608 immunotoxin Toxicity 0.000 claims description 2
- 239000002596 immunotoxin Substances 0.000 claims description 2
- 229940125396 insulin Drugs 0.000 claims description 2
- 102000002467 interleukin receptors Human genes 0.000 claims description 2
- 108010093036 interleukin receptors Proteins 0.000 claims description 2
- 229940047122 interleukins Drugs 0.000 claims description 2
- 229940039781 leptin Drugs 0.000 claims description 2
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 claims description 2
- 239000003446 ligand Substances 0.000 claims description 2
- 108010013555 lipoprotein-associated coagulation inhibitor Proteins 0.000 claims description 2
- 229940040129 luteinizing hormone Drugs 0.000 claims description 2
- 230000006510 metastatic growth Effects 0.000 claims description 2
- 230000017074 necrotic cell death Effects 0.000 claims description 2
- 210000000944 nerve tissue Anatomy 0.000 claims description 2
- 239000000199 parathyroid hormone Substances 0.000 claims description 2
- 229960001319 parathyroid hormone Drugs 0.000 claims description 2
- 230000001737 promoting effect Effects 0.000 claims description 2
- 229960000856 protein c Drugs 0.000 claims description 2
- 239000002464 receptor antagonist Substances 0.000 claims description 2
- 229940044551 receptor antagonist Drugs 0.000 claims description 2
- 239000002461 renin inhibitor Substances 0.000 claims description 2
- 229940086526 renin-inhibitors Drugs 0.000 claims description 2
- 229960002101 secretin Drugs 0.000 claims description 2
- OWMZNFCDEHGFEP-NFBCVYDUSA-N secretin human Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(N)=O)[C@@H](C)O)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)C1=CC=CC=C1 OWMZNFCDEHGFEP-NFBCVYDUSA-N 0.000 claims description 2
- IZTQOLKUZKXIRV-YRVFCXMDSA-N sincalide Chemical compound C([C@@H](C(=O)N[C@@H](CCSC)C(=O)NCC(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](N)CC(O)=O)C1=CC=C(OS(O)(=O)=O)C=C1 IZTQOLKUZKXIRV-YRVFCXMDSA-N 0.000 claims description 2
- 229960005202 streptokinase Drugs 0.000 claims description 2
- 239000002753 trypsin inhibitor Substances 0.000 claims description 2
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 claims description 2
- 229960005356 urokinase Drugs 0.000 claims description 2
- 235000021241 α-lactalbumin Nutrition 0.000 claims description 2
- 102000007644 Colony-Stimulating Factors Human genes 0.000 claims 2
- 108010039209 Blood Coagulation Factors Proteins 0.000 claims 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 claims 1
- 102000055006 Calcitonin Human genes 0.000 claims 1
- 102400000739 Corticotropin Human genes 0.000 claims 1
- 101800000414 Corticotropin Proteins 0.000 claims 1
- 108010071289 Factor XIII Proteins 0.000 claims 1
- 108090001053 Gastrin releasing peptide Proteins 0.000 claims 1
- 102000004862 Gastrin releasing peptide Human genes 0.000 claims 1
- 102000005755 Intercellular Signaling Peptides and Proteins Human genes 0.000 claims 1
- 108010070716 Intercellular Signaling Peptides and Proteins Proteins 0.000 claims 1
- 101710172711 Structural protein Proteins 0.000 claims 1
- 102000003790 Thrombin receptors Human genes 0.000 claims 1
- 108090000166 Thrombin receptors Proteins 0.000 claims 1
- 102000040945 Transcription factor Human genes 0.000 claims 1
- 108091023040 Transcription factor Proteins 0.000 claims 1
- 102000023732 binding proteins Human genes 0.000 claims 1
- 230000033228 biological regulation Effects 0.000 claims 1
- 239000003114 blood coagulation factor Substances 0.000 claims 1
- 229940019700 blood coagulation factors Drugs 0.000 claims 1
- 229940047120 colony stimulating factors Drugs 0.000 claims 1
- IDLFZVILOHSSID-OVLDLUHVSA-N corticotropin Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)NC(=O)[C@@H](N)CO)C1=CC=C(O)C=C1 IDLFZVILOHSSID-OVLDLUHVSA-N 0.000 claims 1
- 229960000258 corticotropin Drugs 0.000 claims 1
- 229940012444 factor xiii Drugs 0.000 claims 1
- PUBCCFNQJQKCNC-XKNFJVFFSA-N gastrin-releasingpeptide Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC(N)=O)NC(=O)CNC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)CNC(=O)[C@H](C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)C(C)C)[C@@H](C)O)C(C)C)[C@@H](C)O)C(C)C)C1=CNC=N1 PUBCCFNQJQKCNC-XKNFJVFFSA-N 0.000 claims 1
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 claims 1
- 230000033885 plasminogen activation Effects 0.000 claims 1
- 239000003488 releasing hormone Substances 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 84
- 239000003814 drug Substances 0.000 abstract description 82
- 210000002966 serum Anatomy 0.000 abstract description 54
- 238000002360 preparation method Methods 0.000 abstract description 30
- 239000000126 substance Substances 0.000 abstract description 16
- 230000001766 physiological effect Effects 0.000 abstract description 12
- 238000004519 manufacturing process Methods 0.000 abstract description 9
- 230000028993 immune response Effects 0.000 abstract description 8
- 230000002035 prolonged effect Effects 0.000 abstract description 4
- 230000003416 augmentation Effects 0.000 abstract 2
- 230000006698 induction Effects 0.000 abstract 1
- 239000000562 conjugate Substances 0.000 description 236
- 229920001223 polyethylene glycol Polymers 0.000 description 186
- 239000002202 Polyethylene glycol Substances 0.000 description 103
- 229940079593 drug Drugs 0.000 description 81
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 50
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 34
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 34
- 238000006243 chemical reaction Methods 0.000 description 34
- 239000011541 reaction mixture Substances 0.000 description 25
- 239000011780 sodium chloride Substances 0.000 description 25
- 239000000203 mixture Substances 0.000 description 22
- 239000000872 buffer Substances 0.000 description 19
- 239000008363 phosphate buffer Substances 0.000 description 19
- 239000000243 solution Substances 0.000 description 17
- 239000012505 Superdex™ Substances 0.000 description 16
- 238000003756 stirring Methods 0.000 description 16
- 239000006227 byproduct Substances 0.000 description 15
- 230000007423 decrease Effects 0.000 description 15
- 239000012064 sodium phosphate buffer Substances 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 239000000539 dimer Substances 0.000 description 14
- 238000000746 purification Methods 0.000 description 14
- 238000001542 size-exclusion chromatography Methods 0.000 description 14
- 241000588724 Escherichia coli Species 0.000 description 13
- 229920000642 polymer Polymers 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 11
- 239000003937 drug carrier Substances 0.000 description 11
- 125000000539 amino acid group Chemical group 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 10
- 108020001507 fusion proteins Proteins 0.000 description 10
- 102000037865 fusion proteins Human genes 0.000 description 10
- 230000003834 intracellular effect Effects 0.000 description 10
- 238000012360 testing method Methods 0.000 description 10
- 241001415846 Procellariidae Species 0.000 description 9
- 241000700159 Rattus Species 0.000 description 9
- 125000003275 alpha amino acid group Chemical group 0.000 description 9
- 230000004071 biological effect Effects 0.000 description 9
- 239000003638 chemical reducing agent Substances 0.000 description 9
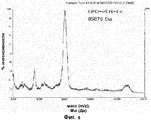
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 9
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 8
- 235000001014 amino acid Nutrition 0.000 description 8
- 239000000178 monomer Substances 0.000 description 8
- 230000009257 reactivity Effects 0.000 description 8
- 230000006798 recombination Effects 0.000 description 8
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical group SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 7
- 239000012535 impurity Substances 0.000 description 7
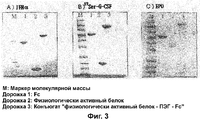
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 7
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 6
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- 150000001413 amino acids Chemical class 0.000 description 6
- 239000012298 atmosphere Substances 0.000 description 6
- 230000004540 complement-dependent cytotoxicity Effects 0.000 description 6
- 239000013604 expression vector Substances 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- 230000003287 optical effect Effects 0.000 description 6
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 5
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 5
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 5
- 125000003412 L-alanyl group Chemical group [H]N([H])[C@@](C([H])([H])[H])(C(=O)[*])[H] 0.000 description 5
- 239000008351 acetate buffer Substances 0.000 description 5
- 230000000295 complement effect Effects 0.000 description 5
- 238000012217 deletion Methods 0.000 description 5
- 230000037430 deletion Effects 0.000 description 5
- 239000012091 fetal bovine serum Substances 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 229940079322 interferon Drugs 0.000 description 5
- 244000005700 microbiome Species 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 239000002773 nucleotide Substances 0.000 description 5
- 125000003729 nucleotide group Chemical group 0.000 description 5
- 239000013612 plasmid Substances 0.000 description 5
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 5
- 210000001995 reticulocyte Anatomy 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 4
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 4
- 150000001299 aldehydes Chemical group 0.000 description 4
- 125000003277 amino group Chemical group 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 239000000969 carrier Substances 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 230000021615 conjugation Effects 0.000 description 4
- 238000001962 electrophoresis Methods 0.000 description 4
- 239000012149 elution buffer Substances 0.000 description 4
- 230000013595 glycosylation Effects 0.000 description 4
- 238000006206 glycosylation reaction Methods 0.000 description 4
- 229940072221 immunoglobulins Drugs 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 238000004949 mass spectrometry Methods 0.000 description 4
- 230000035790 physiological processes and functions Effects 0.000 description 4
- 239000008057 potassium phosphate buffer Substances 0.000 description 4
- 238000010188 recombinant method Methods 0.000 description 4
- 230000003248 secreting effect Effects 0.000 description 4
- 239000001632 sodium acetate Substances 0.000 description 4
- 235000017281 sodium acetate Nutrition 0.000 description 4
- 239000007974 sodium acetate buffer Substances 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 241000283690 Bos taurus Species 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 108090000467 Interferon-beta Proteins 0.000 description 3
- 102000003996 Interferon-beta Human genes 0.000 description 3
- 125000000570 L-alpha-aspartyl group Chemical group [H]OC(=O)C([H])([H])[C@]([H])(N([H])[H])C(*)=O 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- 108090000526 Papain Proteins 0.000 description 3
- 108091005804 Peptidases Proteins 0.000 description 3
- 102000035195 Peptidases Human genes 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 241000711975 Vesicular stomatitis virus Species 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 238000005349 anion exchange Methods 0.000 description 3
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 210000004899 c-terminal region Anatomy 0.000 description 3
- 238000005277 cation exchange chromatography Methods 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 238000003776 cleavage reaction Methods 0.000 description 3
- 210000004748 cultured cell Anatomy 0.000 description 3
- 230000003013 cytotoxicity Effects 0.000 description 3
- 231100000135 cytotoxicity Toxicity 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 239000012636 effector Substances 0.000 description 3
- 239000000147 enterotoxin Substances 0.000 description 3
- 238000000855 fermentation Methods 0.000 description 3
- 230000004151 fermentation Effects 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 230000002209 hydrophobic effect Effects 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 239000003076 neurotropic agent Substances 0.000 description 3
- 208000004235 neutropenia Diseases 0.000 description 3
- 238000011580 nude mouse model Methods 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 230000007017 scission Effects 0.000 description 3
- 239000012128 staining reagent Substances 0.000 description 3
- 239000010421 standard material Substances 0.000 description 3
- 238000013268 sustained release Methods 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- AASBXERNXVFUEJ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) propanoate Chemical compound CCC(=O)ON1C(=O)CCC1=O AASBXERNXVFUEJ-UHFFFAOYSA-N 0.000 description 2
- CJVXHUAPYZJGDW-ILXRZTDVSA-N (2s)-1-[3-[2-[3-[[(1s,2r)-1-carboxy-2-hydroxypropyl]amino]propoxy]ethoxy]propyl]pyrrolidine-2-carboxylic acid Chemical compound C[C@@H](O)[C@@H](C(O)=O)NCCCOCCOCCCN1CCC[C@H]1C(O)=O CJVXHUAPYZJGDW-ILXRZTDVSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 102000004506 Blood Proteins Human genes 0.000 description 2
- 108010017384 Blood Proteins Proteins 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 241000700198 Cavia Species 0.000 description 2
- 102000014447 Complement C1q Human genes 0.000 description 2
- 108010078043 Complement C1q Proteins 0.000 description 2
- 241000699800 Cricetinae Species 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 101710146739 Enterotoxin Proteins 0.000 description 2
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 2
- 108010029961 Filgrastim Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 2
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 2
- 108091006905 Human Serum Albumin Proteins 0.000 description 2
- 102000008100 Human Serum Albumin Human genes 0.000 description 2
- 102100040018 Interferon alpha-2 Human genes 0.000 description 2
- 108010079944 Interferon-alpha2b Proteins 0.000 description 2
- 108010074328 Interferon-gamma Proteins 0.000 description 2
- 102000008070 Interferon-gamma Human genes 0.000 description 2
- 102000010787 Interleukin-4 Receptors Human genes 0.000 description 2
- 108010038486 Interleukin-4 Receptors Proteins 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 2
- 125000003440 L-leucyl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])C(C([H])([H])[H])([H])C([H])([H])[H] 0.000 description 2
- 125000002842 L-seryl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])O[H] 0.000 description 2
- 125000000769 L-threonyl group Chemical group [H]N([H])[C@]([H])(C(=O)[*])[C@](O[H])(C([H])([H])[H])[H] 0.000 description 2
- 102100033342 Lysosomal acid glucosylceramidase Human genes 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 229930012538 Paclitaxel Natural products 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 102000000447 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Human genes 0.000 description 2
- 108010055817 Peptide-N4-(N-acetyl-beta-glucosaminyl) Asparagine Amidase Proteins 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 239000012980 RPMI-1640 medium Substances 0.000 description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 2
- 241000282887 Suidae Species 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 108090000190 Thrombin Proteins 0.000 description 2
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 238000007259 addition reaction Methods 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 210000000601 blood cell Anatomy 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 238000005341 cation exchange Methods 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 239000013592 cell lysate Substances 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 2
- 230000024203 complement activation Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000022811 deglycosylation Effects 0.000 description 2
- 238000011033 desalting Methods 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 108700003933 eflapegrastim Proteins 0.000 description 2
- 229950007926 eflapegrastim Drugs 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 231100000655 enterotoxin Toxicity 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 238000006911 enzymatic reaction Methods 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 229960004177 filgrastim Drugs 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 102000035122 glycosylated proteins Human genes 0.000 description 2
- 108091005608 glycosylated proteins Proteins 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 2
- 239000000411 inducer Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- VJMRKWPMFQGIPI-UHFFFAOYSA-N n-(2-hydroxyethyl)-5-(hydroxymethyl)-3-methyl-1-[2-[[3-(trifluoromethyl)phenyl]methyl]-1-benzothiophen-7-yl]pyrazole-4-carboxamide Chemical compound OCC1=C(C(=O)NCCO)C(C)=NN1C1=CC=CC2=C1SC(CC=1C=C(C=CC=1)C(F)(F)F)=C2 VJMRKWPMFQGIPI-UHFFFAOYSA-N 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 229940071846 neulasta Drugs 0.000 description 2
- PGSADBUBUOPOJS-UHFFFAOYSA-N neutral red Chemical compound Cl.C1=C(C)C(N)=CC2=NC3=CC(N(C)C)=CC=C3N=C21 PGSADBUBUOPOJS-UHFFFAOYSA-N 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 229960001592 paclitaxel Drugs 0.000 description 2
- 229940055729 papain Drugs 0.000 description 2
- 235000019834 papain Nutrition 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 108010044644 pegfilgrastim Proteins 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 239000000825 pharmaceutical preparation Substances 0.000 description 2
- 229920000747 poly(lactic acid) Polymers 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 2
- 239000011535 reaction buffer Substances 0.000 description 2
- 238000003757 reverse transcription PCR Methods 0.000 description 2
- 238000004007 reversed phase HPLC Methods 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 229960004072 thrombin Drugs 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 1
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 description 1
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 description 1
- 150000003923 2,5-pyrrolediones Chemical class 0.000 description 1
- JVJUWEFOGFCHKR-UHFFFAOYSA-N 2-(diethylamino)ethyl 1-(3,4-dimethylphenyl)cyclopentane-1-carboxylate;hydrochloride Chemical compound Cl.C=1C=C(C)C(C)=CC=1C1(C(=O)OCCN(CC)CC)CCCC1 JVJUWEFOGFCHKR-UHFFFAOYSA-N 0.000 description 1
- VHVPQPYKVGDNFY-DFMJLFEVSA-N 2-[(2r)-butan-2-yl]-4-[4-[4-[4-[[(2r,4s)-2-(2,4-dichlorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N([C@H](C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@@H]3O[C@](CN4N=CN=C4)(OC3)C=3C(=CC(Cl)=CC=3)Cl)=CC=2)C=C1 VHVPQPYKVGDNFY-DFMJLFEVSA-N 0.000 description 1
- BIGBDMFRWJRLGJ-UHFFFAOYSA-N 3-benzyl-1,5-didiazoniopenta-1,4-diene-2,4-diolate Chemical compound [N-]=[N+]=CC(=O)C(C(=O)C=[N+]=[N-])CC1=CC=CC=C1 BIGBDMFRWJRLGJ-UHFFFAOYSA-N 0.000 description 1
- NLPWSMKACWGINL-UHFFFAOYSA-N 4-azido-2-hydroxybenzoic acid Chemical class OC(=O)C1=CC=C(N=[N+]=[N-])C=C1O NLPWSMKACWGINL-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 101710126783 Acetyl-hydrolase Proteins 0.000 description 1
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- APKFDSVGJQXUKY-KKGHZKTASA-N Amphotericin-B Natural products O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1C=CC=CC=CC=CC=CC=CC=C[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-KKGHZKTASA-N 0.000 description 1
- 102000009840 Angiopoietins Human genes 0.000 description 1
- 108010009906 Angiopoietins Proteins 0.000 description 1
- 102000007536 B-Cell Activation Factor Receptor Human genes 0.000 description 1
- 108010046304 B-Cell Activation Factor Receptor Proteins 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N Butyraldehyde Chemical group CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 1
- 108010053652 Butyrylcholinesterase Proteins 0.000 description 1
- 102400000113 Calcitonin Human genes 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- PTHCMJGKKRQCBF-UHFFFAOYSA-N Cellulose, microcrystalline Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC)C(CO)O1 PTHCMJGKKRQCBF-UHFFFAOYSA-N 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 102000012286 Chitinases Human genes 0.000 description 1
- 108010022172 Chitinases Proteins 0.000 description 1
- 102100032404 Cholinesterase Human genes 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 102000016917 Complement C1 Human genes 0.000 description 1
- 108010028774 Complement C1 Proteins 0.000 description 1
- 108010022152 Corticotropin-Releasing Hormone Proteins 0.000 description 1
- 102000012289 Corticotropin-Releasing Hormone Human genes 0.000 description 1
- 239000000055 Corticotropin-Releasing Hormone Substances 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 108010019673 Darbepoetin alfa Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- IIUZTXTZRGLYTI-UHFFFAOYSA-N Dihydrogriseofulvin Natural products COC1CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 IIUZTXTZRGLYTI-UHFFFAOYSA-N 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 102100021977 Ectonucleotide pyrophosphatase/phosphodiesterase family member 2 Human genes 0.000 description 1
- 108050004000 Ectonucleotide pyrophosphatase/phosphodiesterase family member 2 Proteins 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 108010075944 Erythropoietin Receptors Proteins 0.000 description 1
- 102100036509 Erythropoietin receptor Human genes 0.000 description 1
- 241001198387 Escherichia coli BL21(DE3) Species 0.000 description 1
- 108091006020 Fc-tagged proteins Proteins 0.000 description 1
- 108010008177 Fd immunoglobulins Proteins 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- 101710198884 GATA-type zinc finger protein 1 Proteins 0.000 description 1
- 102400000921 Gastrin Human genes 0.000 description 1
- 108010052343 Gastrins Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 1
- 108010017544 Glucosylceramidase Proteins 0.000 description 1
- 102000008214 Glutamate decarboxylase Human genes 0.000 description 1
- 108091022930 Glutamate decarboxylase Proteins 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- UXWOXTQWVMFRSE-UHFFFAOYSA-N Griseoviridin Natural products O=C1OC(C)CC=C(C(NCC=CC=CC(O)CC(O)C2)=O)SCC1NC(=O)C1=COC2=N1 UXWOXTQWVMFRSE-UHFFFAOYSA-N 0.000 description 1
- 102100039939 Growth/differentiation factor 8 Human genes 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 101000746367 Homo sapiens Granulocyte colony-stimulating factor Proteins 0.000 description 1
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- 101150084658 INA gene Proteins 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 102100029199 Iduronate 2-sulfatase Human genes 0.000 description 1
- 101710096421 Iduronate 2-sulfatase Proteins 0.000 description 1
- 102000004627 Iduronidase Human genes 0.000 description 1
- 108010003381 Iduronidase Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000000589 Interleukin-1 Human genes 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 102000019223 Interleukin-1 receptor Human genes 0.000 description 1
- 108050006617 Interleukin-1 receptor Proteins 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000010786 Interleukin-5 Receptors Human genes 0.000 description 1
- 108010038484 Interleukin-5 Receptors Proteins 0.000 description 1
- 102000010782 Interleukin-7 Receptors Human genes 0.000 description 1
- 108010038498 Interleukin-7 Receptors Proteins 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- 125000001176 L-lysyl group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C([H])([H])C([H])([H])C([H])([H])C(N([H])[H])([H])[H] 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 125000003580 L-valyl group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(C([H])([H])[H])(C([H])([H])[H])[H] 0.000 description 1
- 108010063045 Lactoferrin Proteins 0.000 description 1
- 102000010445 Lactoferrin Human genes 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 1
- 102000004882 Lipase Human genes 0.000 description 1
- 108090001060 Lipase Proteins 0.000 description 1
- 239000004367 Lipase Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 102400000569 Myeloperoxidase Human genes 0.000 description 1
- 108090000235 Myeloperoxidases Proteins 0.000 description 1
- 108010056852 Myostatin Proteins 0.000 description 1
- 108020001621 Natriuretic Peptide Proteins 0.000 description 1
- 102000004571 Natriuretic peptide Human genes 0.000 description 1
- DDUHZTYCFQRHIY-UHFFFAOYSA-N Negwer: 6874 Natural products COC1=CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-UHFFFAOYSA-N 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 102000015336 Nerve Growth Factor Human genes 0.000 description 1
- 108010063605 Netrins Proteins 0.000 description 1
- 102000010803 Netrins Human genes 0.000 description 1
- 206010029719 Nonspecific reaction Diseases 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 102100040918 Pro-glucagon Human genes 0.000 description 1
- 239000012614 Q-Sepharose Substances 0.000 description 1
- 238000010802 RNA extraction kit Methods 0.000 description 1
- 230000006819 RNA synthesis Effects 0.000 description 1
- 239000012979 RPMI medium Substances 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 206010070834 Sensitisation Diseases 0.000 description 1
- 229920005654 Sephadex Polymers 0.000 description 1
- 239000012507 Sephadex™ Substances 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- WKDDRNSBRWANNC-UHFFFAOYSA-N Thienamycin Natural products C1C(SCCN)=C(C(O)=O)N2C(=O)C(C(O)C)C21 WKDDRNSBRWANNC-UHFFFAOYSA-N 0.000 description 1
- 102000011923 Thyrotropin Human genes 0.000 description 1
- 108010061174 Thyrotropin Proteins 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 108010092464 Urate Oxidase Proteins 0.000 description 1
- 108091008605 VEGF receptors Proteins 0.000 description 1
- 238000005411 Van der Waals force Methods 0.000 description 1
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 229960004150 aciclovir Drugs 0.000 description 1
- MKUXAQIIEYXACX-UHFFFAOYSA-N aciclovir Chemical compound N1C(N)=NC(=O)C2=C1N(COCCO)C=N2 MKUXAQIIEYXACX-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 108010080374 albuferon Proteins 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 102000005840 alpha-Galactosidase Human genes 0.000 description 1
- 108010030291 alpha-Galactosidase Proteins 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 229920000469 amphiphilic block copolymer Polymers 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229960003942 amphotericin b Drugs 0.000 description 1
- 239000003708 ampul Substances 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000002421 anti-septic effect Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 229940064004 antiseptic throat preparations Drugs 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 150000008209 arabinosides Chemical class 0.000 description 1
- 229940115115 aranesp Drugs 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 229920000249 biocompatible polymer Polymers 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000008436 biogenesis Effects 0.000 description 1
- 239000012888 bovine serum Substances 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 230000005907 cancer growth Effects 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 190000008236 carboplatin Chemical compound 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 229960005361 cefaclor Drugs 0.000 description 1
- QYIYFLOTGYLRGG-GPCCPHFNSA-N cefaclor Chemical compound C1([C@H](C(=O)N[C@@H]2C(N3C(=C(Cl)CS[C@@H]32)C(O)=O)=O)N)=CC=CC=C1 QYIYFLOTGYLRGG-GPCCPHFNSA-N 0.000 description 1
- 229960004261 cefotaxime Drugs 0.000 description 1
- GPRBEKHLDVQUJE-VINNURBNSA-N cefotaxime Chemical compound N([C@@H]1C(N2C(=C(COC(C)=O)CS[C@@H]21)C(O)=O)=O)C(=O)/C(=N/OC)C1=CSC(N)=N1 GPRBEKHLDVQUJE-VINNURBNSA-N 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- AOXOCDRNSPFDPE-UKEONUMOSA-N chembl413654 Chemical compound C([C@H](C(=O)NCC(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](C)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)CNC(=O)[C@@H](N)CCC(O)=O)C1=CC=C(O)C=C1 AOXOCDRNSPFDPE-UKEONUMOSA-N 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 230000001886 ciliary effect Effects 0.000 description 1
- 229960003405 ciprofloxacin Drugs 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 229960002626 clarithromycin Drugs 0.000 description 1
- AGOYDEPGAOXOCK-KCBOHYOISA-N clarithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@](C)([C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)OC)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 AGOYDEPGAOXOCK-KCBOHYOISA-N 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 230000001268 conjugating effect Effects 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 210000000172 cytosol Anatomy 0.000 description 1
- 238000002784 cytotoxicity assay Methods 0.000 description 1
- 231100000263 cytotoxicity test Toxicity 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 239000003405 delayed action preparation Substances 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 229960001259 diclofenac Drugs 0.000 description 1
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 229960003722 doxycycline Drugs 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 108010002601 epoetin beta Proteins 0.000 description 1
- 239000006167 equilibration buffer Substances 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 229960003276 erythromycin Drugs 0.000 description 1
- 239000002389 essential drug Substances 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 230000006126 farnesylation Effects 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- RFHAOTPXVQNOHP-UHFFFAOYSA-N fluconazole Chemical compound C1=NC=NN1CC(C=1C(=CC(F)=CC=1)F)(O)CN1C=NC=N1 RFHAOTPXVQNOHP-UHFFFAOYSA-N 0.000 description 1
- 229960004884 fluconazole Drugs 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 201000003444 follicular lymphoma Diseases 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000002518 glial effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 239000011544 gradient gel Substances 0.000 description 1
- DDUHZTYCFQRHIY-RBHXEPJQSA-N griseofulvin Chemical compound COC1=CC(=O)C[C@@H](C)[C@@]11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-RBHXEPJQSA-N 0.000 description 1
- 229960002867 griseofulvin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000007954 hypoxia Effects 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 150000002463 imidates Chemical class 0.000 description 1
- 108010039650 imiglucerase Proteins 0.000 description 1
- 229960002127 imiglucerase Drugs 0.000 description 1
- 229960002182 imipenem Drugs 0.000 description 1
- ZSKVGTPCRGIANV-ZXFLCMHBSA-N imipenem Chemical compound C1C(SCC\N=C\N)=C(C(O)=O)N2C(=O)[C@H]([C@H](O)C)[C@H]21 ZSKVGTPCRGIANV-ZXFLCMHBSA-N 0.000 description 1
- 229940127121 immunoconjugate Drugs 0.000 description 1
- 229940027941 immunoglobulin g Drugs 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 210000003000 inclusion body Anatomy 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 238000009776 industrial production Methods 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 229960001388 interferon-beta Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 229960004130 itraconazole Drugs 0.000 description 1
- 229960004125 ketoconazole Drugs 0.000 description 1
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 1
- 229960000991 ketoprofen Drugs 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- CSSYQJWUGATIHM-IKGCZBKSSA-N l-phenylalanyl-l-lysyl-l-cysteinyl-l-arginyl-l-arginyl-l-tryptophyl-l-glutaminyl-l-tryptophyl-l-arginyl-l-methionyl-l-lysyl-l-lysyl-l-leucylglycyl-l-alanyl-l-prolyl-l-seryl-l-isoleucyl-l-threonyl-l-cysteinyl-l-valyl-l-arginyl-l-arginyl-l-alanyl-l-phenylal Chemical compound C([C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CS)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)C1=CC=CC=C1 CSSYQJWUGATIHM-IKGCZBKSSA-N 0.000 description 1
- 229940078795 lactoferrin Drugs 0.000 description 1
- 235000021242 lactoferrin Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 229960003376 levofloxacin Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 235000019421 lipase Nutrition 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000000845 maltitol Substances 0.000 description 1
- VQHSOMBJVWLPSR-WUJBLJFYSA-N maltitol Chemical compound OC[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O VQHSOMBJVWLPSR-WUJBLJFYSA-N 0.000 description 1
- 235000010449 maltitol Nutrition 0.000 description 1
- 229940035436 maltitol Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 230000011987 methylation Effects 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 229960004023 minocycline Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 102000035118 modified proteins Human genes 0.000 description 1
- 108091005573 modified proteins Proteins 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000000066 myeloid cell Anatomy 0.000 description 1
- OHDXDNUPVVYWOV-UHFFFAOYSA-N n-methyl-1-(2-naphthalen-1-ylsulfanylphenyl)methanamine Chemical compound CNCC1=CC=CC=C1SC1=CC=CC2=CC=CC=C12 OHDXDNUPVVYWOV-UHFFFAOYSA-N 0.000 description 1
- 239000000692 natriuretic peptide Substances 0.000 description 1
- 230000017095 negative regulation of cell growth Effects 0.000 description 1
- 229940053128 nerve growth factor Drugs 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 229960001699 ofloxacin Drugs 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 229960002702 piroxicam Drugs 0.000 description 1
- QYSPLQLAKJAUJT-UHFFFAOYSA-N piroxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 QYSPLQLAKJAUJT-UHFFFAOYSA-N 0.000 description 1
- 230000010118 platelet activation Effects 0.000 description 1
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920001289 polyvinyl ether Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 239000001990 protein-drug conjugate Substances 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 230000008313 sensitization Effects 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 238000006277 sulfonation reaction Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- GUVRBAGPIYLISA-UHFFFAOYSA-N tantalum atom Chemical group [Ta] GUVRBAGPIYLISA-UHFFFAOYSA-N 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000008467 tissue growth Effects 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 235000012431 wafers Nutrition 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 230000004584 weight gain Effects 0.000 description 1
- 235000019786 weight gain Nutrition 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6813—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin the drug being a peptidic cytokine, e.g. an interleukin or interferon
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/06—Drugs for disorders of the endocrine system of the anterior pituitary hormones, e.g. TSH, ACTH, FSH, LH, PRL, GH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/10—Drugs for disorders of the endocrine system of the posterior pituitary hormones, e.g. oxytocin, ADH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/505—Erythropoietin [EPO]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/53—Colony-stimulating factor [CSF]
- C07K14/535—Granulocyte CSF; Granulocyte-macrophage CSF
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/555—Interferons [IFN]
- C07K14/56—IFN-alpha
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/61—Growth hormone [GH], i.e. somatotropin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K19/00—Hybrid peptides, i.e. peptides covalently bound to nucleic acids, or non-covalently bound protein-protein complexes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/734—Complement-dependent cytotoxicity [CDC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Diabetes (AREA)
- Endocrinology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Child & Adolescent Psychology (AREA)
- Reproductive Health (AREA)
- Emergency Medicine (AREA)
- Inorganic Chemistry (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Настоящее изобретение относится к области биотехнологии и иммунологии. Описан способ увеличения продолжительности действия физиологически активного полипептида in vivo. Способ основан на том, что физиологически активный полипептид конъюгируют с Fc-фрагментом иммуноглобулина посредством полиэтиленгликоля. Использование изобретения, по сравнению с нативным физиологически активным полипептидом, обеспечивает повышенную физиологическую активность in vivo конструкции и/или увеличение времени полужизни в сыворотке физиологически активного полипептида с минимальным риском индуцирования нежелательных иммунных ответов. Это может найти применение при изготовлении различных полипептидных лекарственных препаратов пролонгированного действия. 10 з.п. ф-лы, 10 табл., 18 ил.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к новому использованию Fc-фрагмента иммуноглобулина. Более конкретно, настоящее изобретение относится к фармацевтической композиции, содержащей Fc-фрагмент иммуноглобулина в качестве носителя, и к способу увеличения продолжительности in vivo действия лекарственного средства, связанного с Fc-фрагментом иммуноглобулина.
Предшествующий уровень техники
Ранее многими фармакологами и химиками были предприняты попытки химического изменения и/или модификации in vivo активности природных физиологически активных молекул. Эти попытки были направлены, главным образом, на усиление in vivo активности или увеличение времени действия физиологически активных молекул, а также на снижение токсичности, устранение или уменьшение побочных эффектов или на модификацию специфической физиологической активности физиологически активных веществ. Если физиологически активное вещество является химически модифицированным, то в большинстве случаев оно теряет некоторую или большую часть своей физиологической активности. Однако в некоторых случаях такая модификация может приводить к увеличению или изменению физиологической активности. В этой связи многие исследования были направлены на химическую модификацию, с помощью которой можно было бы достичь нужной физиологической активности, а большинство таких исследований было направлено на ковалентное связывание физиологически активного вещества (лекарственного средства) с физиологически приемлемым носителем.
Так, например, в публикации Международной патентной заявки № WO 01/93911 описан полимер, имеющий множество кислотных групп в качестве носителя лекарственного средства. В публикации Международной патентной заявки № WO 03/00778 описаны содержащие анионогенную группу амфифильные блоксополимеры, которые, при их использовании в качестве носителя для катионогенного лекарственного средства, повышают стабильность такого лекарственного средства. В Европейском патенте № 0681481 описан метод улучшения свойств основных лекарственных средств с использованием циклодекстрина и кислот в качестве носителей. С другой стороны, гидрофобные лекарственные средства обладают низкой стабильностью in vivo, что обусловлено, главным образом, их низкой степенью растворимости в воде. В публикации Международной патентной заявки № WO 04/064731 сообщалось, что для улучшения растворимости гидрофобных лекарственных средств в воде в качестве носителя использовали липид. Однако до настоящего времени не появлялось каких-либо сообщений об использовании Fc-фрагмента иммуноглобулина в качестве носителя лекарственного средства.
Обычно, поскольку полипептиды имеют тенденцию к относительно быстрому разложению, что обусловлено их низкой стабильностью, расщеплением протеолитическими ферментами в крови и свободным прохождением через почки или печень, то белковые лекарственные препараты, содержащие такие полипептиды в качестве фармацевтически эффективных компонентов, должны часто вводиться пациентам для поддержания нужного уровня их концентраций и титров в крови. Однако частое введение белковых лекарственных препаратов, особенно путем инъекции, вызывает боли у пациентов. Для решения этой проблемы было предпринято множество попыток повысить стабильность белковых лекарственных средств в сыворотке и добиться поддержания высоких уровней лекарственных средств в крови в течение длительного периода времени и таким образом максимизировать фармацевтическую эффективность указанных лекарственных средств. Поэтому возникла необходимость в получении фармацевтических композиций с пролонгированной активностью, которые обеспечивали бы высокую стабильность белковых лекарственных средств и поддержание их титров на достаточно высоких уровнях, не вызывая при этом нежелательных иммунных ответов у пациентов.
Для стабилизации белков и предотвращения их преждевременного ферментативного расщепления и выведения почками обычно, в целях химической модификации поверхности белкового лекарственного средства, используют полимер, обладающий высокой растворимостью, такой как полиэтиленгликоль (далее называемый просто "ПЭГ"). ПЭГ, благодаря своему связыванию со специфическими или различными областями белка-мишени, стабилизирует белок и предотвращает его гидролиз, не вызывая при этом каких-либо серьезных побочных эффектов (Sada et al., J. Fermentation Bioengineering 71:137-139, 1991). Однако это присоединение ПЭГ, несмотря на его способность повышать стабильность белка, связано с такими проблемами, как значительное снижение титров физиологически "активных" белков. Кроме того, с увеличением молекулярной массы ПЭГ уменьшается выход белка, что обусловлено снижением реакционной способности белков.
Недавно были предложены конъюгаты "полимер-белковое лекарственное средство". Так, например, как описано в патенте США № 5738846, для повышения активности белкового лекарственного средства конъюгат может быть получен путем присоединения идентичных белковых лекарственных средств к обоим концам ПЭГ. Кроме того, как описано в публикации Международной патентной заявки WO 92/16221, к обоим концам ПЭГ могут быть присоединены два различных белковых лекарственных средства с получением конъюгата, обладающего двумя различными активностями. Однако вышеуказанные методы оказались не очень эффективными для сохранения уровня активности белковых лекарственных средств.
С другой стороны, в работе Kinstler и др. сообщалось, что гибридный белок, полученный путем связывания гранулоцитарного колониестимулирующего фактора (ГКСФ) с человеческим альбумином, обладал более высокой стабильностью (Kinstler et al., Pharmaceutical Research 12(12):1883-1888, 1995). Однако в этой публикации указывалось, что поскольку модифицированное лекарственное средство, имеющее структуру "ГКСФ-ПЭГ-альбумин", обнаруживало примерно только четырехкратное увеличение времени его пребывания в организме и лишь небольшое увеличение времени полужизни в сыворотке, по сравнению с нативным ГКСФ, то промышленное производство такого лекарственного средства в качестве эффективного белкового препарата пролонгированного действия не является целесообразным.
Альтернативный методом повышения in vivo стабильности физиологически активных белков предусматривает присоединение гена физиологически активного белка к гену, кодирующему белок, обладающий высокой стабильностью в сыворотке, посредством генетической рекомбинации, и культивирование клеток, трансфецированных таким рекомбинантным геном, с получением гибридного (слитого) белка. Так, например, гибридный белок может быть получен путем конъюгирования альбумина, белка, который, как известно, является наиболее эффективным для повышения стабильности белка, или его фрагмента с представляющим интерес физиологически активным белком посредством генетической рекомбинации (публикация Международной патентной заявки № WO 93/15199 и WO 93/15200, публикация Европейской патентной заявки № 413622). Время полужизни гибридного белка интерферона-альфа и альбумина, полученного компанией Human Genome Science Company и поставляемого под торговым знаком AlbuferonTM, было увеличено с 5 часов до 93 часов у обезьян, однако проблема заключалась в том, что такое увеличение времени полужизни приводило к снижению активности in vivo до менее чем 5% по сравнению с немодифицированным интерфероном-альфа (Osborn et al., J. Phar. Exp. Ther. 303(2):540-548, 2002).
Для присоединения белкового лекарственного средства к Fc-фрагменту иммуноглобулина была использована техника рекомбинантных ДНК. Так, например, интерферон (публикация выложенной корейской патентной заявки № 2003-9464) и рецептор интерлейкина-4, рецептор интерлейкина-7 или рецептор эритропоэтина (ЕРО) (Корейский патент, регистрационный номер № 249572) были предварительно экспрессированы у млекопитающих в форме гибрида с Fc-фрагментом иммуноглобулина. В публикации Международной патентной заявки № WO 01/03737 описан гибридный белок, содержащий цитокин или фактор роста, связанные с Fc-фрагментом иммуноглобулина посредством пептидной связи. Кроме того, в патенте США № 5116964 описаны белки, присоединенные к амино-концу или к карбокси-концу Fc-фрагмента иммуноглобулина посредством генетической рекомбинации. В патенте США № 5349053 описан гибридный белок, содержащий IL-2, присоединенный к Fc-фрагменту иммуноглобулина посредством пептидной связи. Другими примерами Fc-гибридных белков, полученных посредством генетической рекомбинации, являются гибридный белок интерферона-бета или его производного и Fc-фрагмента иммуноглобулина (публикация Международной патентной заявки № WO 00/23472) и гибридный белок рецептора IL-5 и Fc-фрагмента иммуноглобулина (патент США № 5712121), гибридный белок интерферона-альфа и Fc-фрагмента иммуноглобулина G4 (патент США № 5723125) и гибрид белка CD4 и Fc-фрагмента иммуноглобулина G2 (патент США № 6451313).
Известны также методы, предусматривающие модификацию аминокислотных остатков Fc-фрагмента иммуноглобулина. Так, например, в патенте США № 5605690 описан гибридный белок TNFR-Fc IgG1, который был получен путем генетической рекомбинации с использованием Fc-фрагмента IgG1, имеющего аминокислотные альтерации в комплемент-связывающей области или в области связывания с рецептором. Кроме того, другие методы получения гибридного белка с использованием Fc-фрагмента иммуноглобулина, модифицированного посредством генетической рекомбинации, описаны в патентах США №№ 6277375, 6410008 и 6444792.
Кроме того, описанные Fc-гибридные белки, продуцированные посредством генетической рекомбинации, имеют следующие недостатки: такой гибридный белок присутствует только в специфической области Fc-фрагмента иммуноглобулина, которая расположена у амино- или у карбокси-конца; продуцируются лишь гомодимерные, а не мономерные формы этого белка; и такой гибрид может находиться только между гликозилированными белками или между агликозилированными белками, и невозможно получить такой гибридный белок, который состоял бы из гликозилированного белка и агликозилированного белка. Кроме того, новая аминокислотная последовательность, созданная путем слияния, может индуцировать иммунные ответы, а линкерная область может оказаться восприимчивой к протеолитическому расщеплению.
Для решения этих проблем авторами настоящей заявки было проведено исследование, в результате которого было установлено, что при введении лекарственного средства в форме гибрида с Fc-фрагментом IgG такое лекарственное средство имеет повышенную стабильность in vivo при минимальном снижении in vivo активности.
Раскрытие изобретения
Учитывая вышеизложенное, задачей настоящего изобретения является получение фармацевтической композиции, содержащей Fc-фрагмент иммуноглобулина в качестве носителя.
Другой задачей настоящего изобретения является разработка способа увеличения продолжительности действия in vivo лекарственного средства путем включения в него Fc-фрагмента иммуноглобулина в качестве носителя.
Краткое описание чертежей
Вышеуказанные и другие задачи, а также отличительные признаки и другие преимущества настоящего изобретения будут более понятны из нижеследующего подробного описания, сопровождаемого графическим материалом, где:
на фиг.1 представлены результаты хроматографии Fc-фрагмента иммуноглобулина, полученного путем расщепления иммуноглобулина папаином;
на фиг.2 представлены результаты электрофореза в ДСН-ПААГ очищенного Fc-фрагмента иммуноглобулина (М: маркер молекулярной массы, дорожка 1: IgG; дорожка 2: Fc);
на фиг.3 представлены результаты электрофореза в ДСН-ПААГ для конъюгатов: (А) IFNα-ПЭГ-Fc, (В) 17Ser-КГСФ-ПЭГ-Fc и (С) ЕРО-ПЭГ-Fc, которые были продуцированы путем реакции связывания (М: маркер молекулярной массы, дорожка 1: Fc, дорожка 2: физиологически активный белок, дорожка 3: конъюгат физиологически активный белок-ПЭГ-Fc);
на фиг.4 представлены результаты эксклюзионной хроматографии конъюгата IFNα-ПЭГ-Fc, очищенного после реакции связывания;
на фиг.5 представлены результаты масс-спектрометрии MALDI-TOF конъюгата ЕРО-ПЭГ-Fc;
на фиг.6а и 6b представлены результаты масс-спектрометрии MALDI-TOF и ДСН-ПААГ-анализа соответственно нативного Fc-фрагмента иммуноглобулина и дегликозилированного Fc-фрагмента иммуноглобулина (DG Fc);
на фиг. 7 представлены результаты масс-спектрометрии MALDI-TOF конъюгата IFNα-ПЭГ-Fc и конъюгата IFNα-ПЭГ-DG-Fc;
на фиг. 8а-8с представлены результаты обращенно-фазовой ВЭЖХ конъюгатов IFNα-ПЭГ-Fc, IFNα-ПЭГ-DG-Fc и IFNα-ПЭГ-производное Fc-фрагмента рекомбинантного AG;
на фиг.9 представлен график, иллюстрирующий результаты фармакокинетического анализа нативного IFNα, комплекса IFNα-40К ПЭГ, конъюгата IFNα-ПЭГ-альбумина и конъюгата IFNα-ПЭГ-Fc;
на фиг.10 представлен график, иллюстрирующий результаты фармакокинетического анализа нативного ЕРО, в высокой степени гликозилированного ЕРО, конъюгата ЕРО-ПЭГ-Fc и конъюгата ЕРО-ПЭГ-AG-Fc;
на фиг.11 представлен график, иллюстрирующий результаты фармакокинетического анализа конъюгатов IFNα-ПЭГ-Fc, IFNα-ПЭГ-DG-Fc и IFNα-ПЭГ-производное рекомбинантного AG-Fc;
на фиг.12 представлен график, иллюстрирующий результаты фармакокинетического анализа Fab', комплекса Fab'-S-40K-ПЭГ, конъюгата Fab'-N-ПЭГ-N-Fc и конъюгата Fab'-S-ПЭГ-N-Fc;
на фиг.13 представлен график, иллюстрирующий in vivo-активности Fab', комплекса Fab'-S-40K-ПЭГ, конъюгата Fab'-N-ПЭГ-N-Fc и конъюгата Fab'-S-ПЭГ-N-Fc;
на фиг.14 представлен график, иллюстрирующий результаты сравнения аффинности связывания человеческих иммуноглобулинов подкласса IgG с комплементом C1q;
на фиг.15 представлен график, иллюстрирующий результаты сравнения аффинности связывания гликозилированного Fc, ферментативно дегликозилированного (DG) Fc и конъюгата интерферон-ПЭГ-носитель, где носителем является неглигозилированный (AG) Fc, продуцируемый E.coli, с комплементом C1q.
Осуществление изобретения
В одном из своих аспектов настоящее изобретение относится к фармацевтической композиции, содержащей Fc-фрагмент иммуноглобулина в качестве носителя.
Используемый здесь термин "носитель" означает вещество, связанное с лекарственным средством, которое обычно повышает, снижает или нейтрализует физиологическую активность лекарственного средства путем его связывания с указанным лекарственным средством. Однако в целях осуществления настоящего изобретения носитель используется для минимизации снижения физиологической активности представляющего интерес лекарственного средства, связанного с указанным носителем, и для увеличения in vivo стабильности этого лекарственного средства.
Настоящее изобретение отличается тем, что для достижения его задач в настоящем изобретении в качестве носителя используется Fc-фрагмент иммуноглобулина.
Fc-фрагмент иммуноглобулина является безопасным для использования в качестве носителя лекарственного средства, поскольку он представляет собой биологически разлагаемый полипептид, который подвергается метаболизму в организме. Кроме того, Fc-фрагмент иммуноглобулина имеет относительно низкую молекулярную массу по сравнению с целыми молекулами иммуноглобулина, что делает его предпочтительным с точки зрения получения, очистки и выхода конъюгата. Кроме того, поскольку Fc-фрагмент иммуноглобулина не содержит Fab-фрагмента, аминокислотная последовательность которого отличается от аминокислотных последовательностей антител других подклассов и который поэтому является в высокой степени негомогенным, то этот Fc-фрагмент может значительно повышать степень гомогенности веществ и является менее антигенным.
Используемый здесь термин "Fc-фрагмент иммуноглобулина" означает белок, который содержит константную область 2 тяжелой цепи (СН2) и константную область 3 тяжелой цепи (СН3) иммуноглобулина и не содержит вариабельных областей тяжелой и легкой цепей, константной области 1 тяжелой цепи (СН1) и константной области 1 легкой цепи (СL1) иммуноглобулина. Кроме того, он может содержать шарнирную область в константной области тяжелой цепи. Fc-фрагмент иммуноглобулина по настоящему изобретению может также содержать часть константной области 1 тяжелой цепи (СН1) или всю эту область и/или часть константной области 1 легкой цепи (СL1) или всю эту область, за исключением вариабельных областей тяжелой и легкой цепей. Кроме того, в том случае, если Fc-фрагмент иммуноглобулина обладает физиологической функцией, в основном, аналогичной физиологической функции нативного белка, или лучшей физиологической функцией, чем нативный белок, то таким Fc-фрагментом IgG может быть фрагмент, имеющий делецию в относительно длинной части аминокислотной последовательности СН2 и/или СН3. То есть Fc-фрагмент иммуноглобулина по настоящему изобретению может содержать (1) домен СН1, домен СН2, домен СН3 и домен СН4, (2) домен СН1 и домен СН2, (3) домен СН1 и домен СН3, (4) домен СН2 и домен СН3, (5) комбинацию одного или нескольких доменов и шарнирной области иммуноглобулина (или части такой шарнирной области) и (6) димер каждого из этих доменов константных областей тяжелой цепи и константной области легкой цепи.
Fc-фрагмент иммуноглобулина по настоящему изобретению включает нативную аминокислотную последовательность и производные этой последовательности (мутанты). Производной аминокислотной последовательностью является последовательность, отличающаяся от нативной аминокислотной последовательности тем, что она включает делецию, инсерцию, не-консервативную или консервативную замену одного или нескольких аминокислотных остатков или их комбинации. Так, например, в Fc IgG аминокислотные остатки в положениях 214-238, 297-299, 318-322 или 327-331, которые, как известно, играют важную роль в связывании, могут быть использованы в качестве подходящей мишени для модификации. Кроме того, могут быть использованы и другие различные производные, включая производные, в которых либо делетирована область, способная образовывать дисульфидную связь, либо элиминированы некоторые аминокислотные остатки, которые обычно присутствуют у N-конца нативной Fc-формы, либо добавлен метиониновый остаток. Кроме того, для ингибирования эффекторных функций может быть осуществлена делеция в комплемент-связывающем сайте, таком как C1q-связывающий сайт и ADCC-сайт. Методы получения таких производных последовательностей Fc-фрагмента иммуноглобулина описаны в публикациях Международных патентных заявок №№ WO 97/34631 и WO 96/32478.
Аминокислотные замены в белках и пептидах, которые, в основном, не влияют на активность таких белков или пептидов, известны специалистам (H. Neurath, R.L. Hill, The Proteins, Academic Press, New York, 1979). Наиболее часто встречающимися заменами являются Ala/Ser, Val/Ile, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Thr/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/Ile, Leu/Val, Ala/Glu и Asp/Gly и наоборот.
Кроме того, Fc-фрагмент, если это необходимо, может быть модифицирован путем фосфорилирования, сульфирования, акрилирования, гликозилирования, метилирования, фарнезилирования, ацетилирования, амидирования и т.п.
Вышеупомянутыми производными Fc являются производные, которые обладают биологической активностью, идентичной активности Fc-фрагмента настоящего изобретения, или обладают повышенной структурной устойчивостью, например, к нагреванию, к изменению рН или т.п.
Кроме того, эти Fc-фрагменты могут быть получены из нативных форм, выделенных у человека и других животных, включая коров, коз, свиней, мышей, кроликов, хомячков, крыс и морских свинок, либо они могут быть их рекомбинантами или производными, полученными из трансформированных клеток животных или микроорганизмов. В соответствии с настоящим изобретением они могут быть получены из нативного иммуноглобулина путем выделения целых иммуноглобулинов из организма человека или животного и их обработки протеолитическим ферментом. Папаин гидролизует нативный иммуноглобулин на Fab- и Fc-фрагменты, а обработка пепсином приводит к продуцированию pF'c- и F(ab')2-фрагментов. Эти фрагменты могут быть подвергнуты, например, эксклюзионной хроматографии для выделения Fc или pF'c.
Человеческим Fc-фрагментом предпочтительно является рекомбинантный Fc-фрагмент иммуноглобулина, полученный из микроорганизма.
Кроме того, Fc-фрагмент иммуноглобулина по настоящему изобретению может присутствовать в форме, имеющей обычно присущее ей число сахарных цепей, или в форме, имеющей повышенное число сахарных цепей по сравнению с нативной формой или пониженное число сахарных цепей по сравнению с нативной формой, либо он может присутствовать в дегликозилированной форме. Увеличение, уменьшение или удаление сахарных цепей Fc-фрагмента иммуноглобулина может быть достигнуто методами, известными специалистам, такими как химический метод, ферментативный метод и метод генной инженерии с использованием микроорганизма. Удаление сахарных цепей из Fc-фрагмента приводит к резкому снижению аффинности связывания с C1q-частью первого компонента комплемента С1, а также к снижению или к потере антитело-зависимой клеточно-опосредованной цитотоксичности (ADCC) или комплемент-зависимой цитотоксичности (CDC), не индуцируя при этом нежелательных иммунных ответов in vivo. В этой связи следует отметить, что Fc-фрагмент иммуноглобулина в дегликозилированной или негликозилированной форме может оказаться более подходящим для использования в настоящем изобретении в качестве носителя лекарственного средства.
Используемый здесь термин "дегликозилирование" означает ферментативное удаление сахарных групп из Fc-фрагмента, а термин "агликозилирование" означает, что Fc-фрагмент был продуцирован в негликозилированной форме прокариотом, предпочтительно E.coli.
С другой стороны, Fc-фрагмент иммуноглобулина может происходить от человека или от других животных, включая коров, коз, свиней, мышей, кроликов, хомячков, крыс и морских свинок, а предпочтительно от человека. Кроме того, Fc-фрагментом иммуноглобулина может быть Fc-фрагмент, происходящий от IgG, IgA, IgD, IgE и IgM или полученный из их комбинаций или гибридов. Предпочтительно, если этот Fc-фрагмент происходит от иммуноглобулинов IgG или IgM, которые среди прочих белков присутствуют в наибольшем количестве в крови человека, а наиболее предпочтительно, если он происходит от IgG, который, как известно, увеличивает время полужизни связывающихся с лигандом белков.
С другой стороны, используемый здесь термин "комбинация" означает, что полипептиды, кодирующие одноцепочечные Fc-области иммуноглобулина того же самого происхождения, присоединены к одноцепочечному полипептиду другого происхождения и образуют димер или мультимер. То есть димер или мультимер могут быть образованы из двух или более фрагментов, выбранных из группы, состоящей из Fc-фрагментов IgG1, IgG2, IgG3 и IgG4.
Используемый здесь термин "гибрид" означает, что последовательности, кодирующие два или более Fc-фрагментов иммуноглобулина различного происхождения, присутствуют в одноцепочечном Fc-фрагменте иммуноглобулина. В настоящем изобретении могут быть использованы различные типы гибридов. То есть гибриды доменов могут состоять из одного-четырех доменов, выбранных из группы, состоящей из СН1, СН2, СН3 и СН4 Fc-фрагментов IgG1, IgG2, IgG3 и IgG4, и могут включать шарнирную область.
С другой стороны, IgG подразделяется на подклассы IgG1, IgG2, IgG3 и IgG4, и настоящее изобретение включает их комбинации и гибриды. Предпочтительными являются подклассы IgG2 и IgG4, а наиболее предпочтительным является Fc-фрагмент IgG4, который редко обладает эффекторными функциями, такими как CDC (комплемент-зависимая цитотоксичность) (см. фиг.14 и 15).
Таким образом, в качестве носителя лекарственного средства по настоящему изобретению наиболее предпочтительным Fc-фрагментом иммуноглобулина является негликозилированный Fc-фрагмент, происходящий от человеческого IgG4. Человеческий Fc-фрагмент является более предпочтительным, чем Fc-фрагмент, происходящий от другого источника, который может действовать в организме человека как антиген и вызывать нежелательные иммунные ответы, такие как вырабатывание нового антитела против антигена.
Fc-фрагмент иммуноглобулина по настоящему изобретению, полученный, как описано выше, действует как носитель лекарственного средства и образует конъюгат с этим лекарственным средством.
Используемый здесь термин "конъюгат лекарственного средства" или "конъюгат" означает, что одно или несколько лекарственных средств связаны с одним или несколькими Fc-фрагментами иммуноглобулина.
Используемый здесь термин "лекарственное средство" означает вещество, обладающее терапевтической активностью при его введении человеку или животному, и примерами такого лекарственного средства являются, но не ограничиваются ими, полипептиды, соединения, экстракты и нуклеиновые кислоты. При этом предпочтительным является полипептидное лекарственное средство.
Используемые здесь термины "физиологически активный полипептид", "физиологически активный белок", "активный полипептид", "полипептидное лекарственное средство" и "белковое лекарственное средство" являются взаимозаменяемыми и отличаются тем, что, присутствуя в физиологически активной форме, они обладают различными физиологическими функциями in vivo.
Полипептидное лекарственное средство имеет тот недостаток, что оно неспособно поддерживать физиологическое действие в течение длительного периода времени, что обусловлено присущим ему свойством легко денатурироваться или разлагаться под действием протеолитических ферментов, присутствующих в организме. Однако, если полипептидное лекарственное средство присоединяют к Fc-фрагменту иммуноглобулина по настоящему изобретению с образованием конъюгата, то такое лекарственное средство обладает повышенной структурной стабильностью и увеличенным временем полужизни до разложения. Кроме того, полипептид, конъюгированный с Fc-фрагментом, гораздо меньше подвержен снижению физиологической активности, чем другие известные полипептидные лекарственные препараты. Поэтому, по сравнению с биологической доступностью in vivo стандартных полипептидных лекарственных средств, конъюгат по настоящему изобретению, состоящий из полипептида и Fc-фрагмента иммуноглобулина, отличается тем, что он обладает значительно лучшей биологической доступностью in vivo. Это также наглядно проиллюстрировано в описании вариантов осуществления изобретения. То есть при связывании с Fc-фрагментом иммуноглобулина по настоящему изобретению лекарственные средства на основе IFNα, ГКСФ, чГР и других белков обнаруживают примерно 2-6-кратное увеличение биологической доступности in vivo по сравнению с их стандартными формами, конъюгированными с одним ПЭГ или с ПЭГ и альбумином (таблицы 8, 9 и 10).
С другой стороны, конъюгат белка и Fc-фрагмента иммуноглобулина по настоящему изобретению отличается тем, что он не является гибридом, полученным стандартным рекомбинантным методом. В рекомбинантном методе гибридную форму Fc-фрагмента иммуноглобулина и активного полипептида, используемого в качестве лекарственного средства, получают так, чтобы указанный полипептид был присоединен к N-концу или С-концу Fc-фрагмента, в результате чего он экспрессируется и подвергается укладке как один полипептид, продуцируемый из нуклеотидной последовательности, кодирующей его гибридную форму.
Это приводит к резкому снижению активности полученного гибридного белка, поскольку активность белка как физиологически функционального вещества определяется конформацией этого белка. Таким образом, при присоединении полипептидного лекарственного средства к Fc-фрагменту рекомбинантным методом не наблюдается какого-либо влияния на биологическую доступность in vivo, даже если этот гибридный белок имеет повышенную структурную стабильность. Кроме того, поскольку такой гибридный белок часто имеет неправильную укладку, а поэтому экспрессируется в виде телец включения, то такой метод присоединения, применяемый для продуцирования белка и его выделения, является экономически невыгодным. Кроме того, если активная форма полипептида является гликозилированной, то такой полипептид должен экспрессироваться в эукариотических клетках. В этом случае Fc также является гликозилированным, и такое гликозилирование может индуцировать нежелательные иммунные ответы in vivo.
Таким образом, лишь применение настоящего изобретения позволяет получить конъюгат глигозилированного активного полипептида и агликозилированного Fc-фрагмента иммуноглобулина и позволяет решить все вышеуказанные проблемы, включая увеличение выхода белка, поскольку два компонента этого комплекса получают отдельно и выделяют с использованием самых эффективных систем.
Неограничивающими примерами белковых лекарственных средств, способных образовывать конъюгаты с Fc-фрагментом иммуноглобулина по настоящему изобретению, являются человеческий гормон роста, рилизинг-фактор гормона роста, пептид, высвобождающий гормон роста, интерфероны и рецепторы интерферона (например, интерферон-α, -β и -γ, водорастворимый рецептор интерферона 1 и т.п.), гранулоцитарный колониестимулирующий фактор (Г-КСФ), гранулоцитарный-макрофагальный колониестимулирующий фактор (ГМ-КСФ), глюкагон-подобные пептиды (например, GLP-1 и т.п.), рецептор, связанный с G-белком, интерлейкины (например, интерлейкин-1,
-2, -3, -4, -5, -6, -7, -8, -9, -10, -11, -12, -13, -14, -15, -16, -17, -18, -19, -20, -21, -22, -23, -24, -25, -26, -27, -28, -29, -30 и т.п.) и рецепторы интерлейкинов (например, рецептор IL-1, рецептор IL-4 и т.п.), ферменты (например, глюкоцереброзидаза, идуронат-2-сульфатаза, альфа-галактозидаза-А, агалсидаза-альфа и -бета, альфа-L-идуронидаза, бутирилхолинэстераза, хитиназа, глутамат-декарбоксилаза, имиглюцераза, липаза, уриказа, ацетилгидролаза фактора активации тромбоцитов, нейтральная эндопептидаза, миелопероксидаза и т.п.), интерлейкин- и цитокин-связывающие белки (например, IL-18bp, TNF-связывающий белок и т.п.), фактор активации макрофагов, пептид макрофага, В-клеточный фактор, Т-клеточный фактор, белок А, ингибитор аллергии, гликопротеины некроза клеток, иммунотоксин, лимфотоксин, фактор некроза опухоли, супрессоры опухолей, метастатический фактор роста, антитрипсин альфа-1, альбумин, альфа-лактальбумин, аполипопротеин-Е, эритропоэтин, высокогликозилированный эритропоэтин, ангиопоэтины, гемоглобин, тромбин, пептид, активирующий рецептор тромбина, тромбомодулин, фактор VII, фактор VIIa, фактор VIII, фактор IX, фактор XIII, фактор активации плазминогена, фибрин-связывающий пептид, урокиназа, стрептокиназа, гирудин, белок С, С-реактивный белок, ингибитор ренина, ингибитор коллагеназы, супероксиддисмутаза, лептин, тромбоцитарный фактор роста, эпителиальный фактор роста, эпидермальный фактор роста, ангиостатин, ангиотензин, фактор роста костей, белок, стимулирующий рост костей, кальцитонин, инсулин, атриопептин, фактор, индуцирующий образование хряща, элкатонин, фактор активации соединительной ткани, ингибитор пути тканевого фактора, фолликулостимулирующий гормон, лютеинизирующий гормон, фактор высвобождения лютеинизирующего гормона, факторы роста нервной ткани (например, фактор роста нервной ткани, цилиарный нейротропный фактор, фактор-1 аксогенеза, натрийуретический пептид головного мозга, глиальный нейротропный фактор, нетрин, ингибитор нейтрофилов, нейротропный фактор, нейтурин и т.п.), паратиреоидный гормон, релаксин, секретин, соматомедин, инсулиноподобный фактор роста, адренокортикоидный гормон, глюкагон, холецистокинин, панкреатический полипептид, пептид высвобождения гастрина, рилизинг-фактор кортикотропина, тиреоид-стимулирующий гормон, аутотаксин, лактоферрин, миостатин, рецепторы (например, TNFR(Р75), TNFR(Р55), рецептор IL-1, рецептор VEGF, рецептор фактора активации В-клеток и т.п.), антагонисты рецепторов (например, IL-1-Ra и т.п.), антигены клеточной поверхности (например, CD 2, 3, 4, 5, 7, 11а, 11b, 18, 19, 20, 23, 25, 33, 38, 40, 45, 69 и т.п.), антигены вирусных вакцин, моноклональные антитела, поликлональные антитела, фрагменты антител (например, оцFv, Fab, Fab', F(ab')2 и Fd) и вакцинные антигены, происходящие от вирусов. Фрагментом антитела могут быть фрагменты Fab, Fab', F(ab')2, Fd или оцFv, способные связываться со специфическим антигеном, а предпочтительно фрагмент Fab'. Fab-фрагменты содержат вариабельный домен (VL) и константный домен (СL) легкой цепи и вариабельный домен (VН) и первый константный домен (СН1) тяжелой цепи. Fab'-фрагменты отличаются от Fab-фрагментов тем, что они содержат несколько дополнительных аминокислотных остатков, включая один или несколько цистеиновых остатков шарнирной области со стороны карбокси-конца СН1-домена. Fd-фрагменты содержат только VН- и СН1-домены, а F(ab')2-фрагменты продуцируются в виде пары Fab'-фрагментов, образуемых либо посредством дисульфидной связи, либо посредством химической реакции. оцFv-фрагменты (одноцепочечные Fv-фрагменты) содержат домены VL и VН, которые связаны друг с другом посредством пептидного линкера, а поэтому присутствуют в одной полипептидной цепи.
В частности, предпочтительными физиологически активными полипептидами являются полипептиды, требующие частого введения в организм пациента для лечения или предупреждения заболеваний, и такими полипептидами являются человеческий гормон роста, интерфероны (интерферон-α, -β и -γ,), гранулоцитарный колониестимулирующий фактор, эритропоэтин (ЕРО) и фрагменты антител. Кроме того, в объем физиологически активных пептидов по настоящему изобретению входят некоторые производные, при условии, что, по сравнению с нативными формами физиологически активных полипептидов, они имеют, в основном, аналогичные или улучшенные функции, структуры, активность или стабильность. Наиболее предпочтительным полипептидным лекарственным средством по настоящему изобретению является интерферон-альфа.
Помимо полипептидных лекарственных средств, в объем настоящего изобретения входят также и другие лекарственные средства. Неограничивающими примерами таких лекарственных средств являются антибиотики, выбранные из производных и смесей тетрациклина, миноциклина, доксициклина, офлоксацина, левофлоксацина, ципрофлоксацина, кларитромицина, эритромицина, цефаклора, цефотаксима, имипенема, пенициллина, гентамицина, стрептомицина, ванкомицина и т.п.; противораковые средства, выбранные из производных и смесей метотрексата, карбоплатина, таксола, цисплатина, 5-фторурацила, доксорубицина, этопозида, паклитаксела, камтотецина, арабинозида цитозина и т.п.; противовоспалительные средства, выбранные из производных и смесей индометацина, ибупрофена, кетопрофена, пироксикама, пробипрофена, диклофенака и т.п.; антивирусные средства, выбранные из производных и смесей ацикловира и робавина, и антибактериальные средства, выбранные из производных и смесей кетоконазола, итраконазола, флуконазола, амфотерицина В и гризеофульвина.
С другой стороны, Fc-фрагмент иммуноглобулина по настоящему изобретению способен образовывать конъюгат, связанный с лекарственным средством посредством линкера.
Таким линкером являются пептидный и не-пептидный линкеры. При этом предпочтительным является не-пептидный линкер, а более предпочтительным является не-пептидный полимер.
Используемый здесь термин "пептидный линкер" означает аминокислоты, а предпочтительно 1-20 аминокислот, которые линейно связаны друг с другом пептидной связью и могут присутствовать в гликозилированной форме. Для задач настоящего изобретения предпочтительно, чтобы они имели агликозилированную форму. Таким пептидным линкером предпочтительно является пептид, имеющий повторяющееся звено из аминокислот Gly и Ser, которые являются иммунологически не активными для Т-клеток.
Используемый здесь термин "не-пептидный полимер" означает биологически совместимый полимер, включающий два или более повторяющихся звена, связанных друг с другом ковалентной связью, за исключением пептидной связи. Примерами не-пептидного полимера являются полиэтиленгликоль, полипропиленгликоль, сополимеры этиленгликоля и пропиленгликоля, полиоксиэтилированные полиолы, поливиниловый спирт, полисахариды, декстран, поливиниловый эфир, биологически разлагаемые полимеры, такие как PLA (поли(молочная кислота)) и PLGA (сополимер молочной и гликолевой кислоты), липидные полимеры, хитины и гиалуроновая кислота. Наиболее предпочтительным является полиэтиленгликоль (ПЭГ).
Конъюгаты по настоящему изобретению "Fc-фрагмент иммуноглобулина - лекарственное средство" или "Fc-фрагмент иммуноглобулина - линкер-лекарственное средство" получают в различных молярных отношениях. То есть число Fc-фрагментов иммуноглобулина и/или линкера, связанного с одним полипептидым лекарственным средством, не имеет ограничений. Однако предпочтительно, чтобы в конъюгате лекарственного средства по настоящему изобретению лекарственное средство и Fc-фрагмент иммуноглобулина были конъюгированы друг с другом в молярном отношении 1:1-10:1, а предпочтительно 1:1-2:1.
Кроме того, связью между Fc-фрагментом иммуноглобулина по настоящему изобретению, определенным линкером и определенным лекарственным средством могут быть все ковалентные связи, за исключением пептидной связи, образуемой в том случае, когда Fc-фрагмент и полипептидное лекарственное средство экспрессируются в виде гибридного белка посредством генетической рекомбинации, и нековалентные связи всех типов, такие как водородные связи, связи, образуемые при ионных взаимодействиях, под действием ван-дер-ваальсовых сил и при гидрофобных взаимодействиях. Однако, с точки зрения физиологической активности лекарственного средства, предпочтительными связями являются ковалентные связи.
Кроме того, Fc-фрагмент иммуноглобулина по настоящему изобретению, определенный линкер и определенное лекарственное средство могут быть связаны друг с другом в определенном сайте лекарственного средства. С другой стороны, Fc-фрагмент иммуноглобулина по настоящему изобретению и полипептидное лекарственное средство могут быть связаны друг с другом у N-конца или у С-конца, а предпочтительно посредством свободной группы, а ковалентная связь между Fc-фрагментом иммуноглобулина и лекарственным средством легко образуется, в частности, у амино-конца Fc и у аминогруппы лизинового остатка, аминогруппы гистидинового остатка или свободного цистеинового остатка.
С другой стороны, присоединение Fc-фрагмента иммуноглобулина по настоящему изобретению, определенного линкера и определенного лекарственного средства может быть осуществлено в определенном направлении. То есть такой линкер может быть связан с N-концом, с С-концом или со свободной группой Fc-фрагмента иммуноглобулина, и он может быть также связан с N-концом, с С-концом или со свободной группой белкового лекарственного средства. Если указанным линкером является пептидный линкер, то такая связь может находится в определенном сайте связывания.
Кроме того, конъюгат по настоящему изобретению может быть получен с использованием любого числа связывающих агентов, известных специалистам. Неограничивающими примерами связывающих агентов являются 1,1-бис-(диазоацетил)-2-фенилэтан, глутаральдегид, N-гидроксисукцинимидоэфиры, такие как сложные эфиры 4-азидосалициловой кислоты, имидоэфиры, включая дисукцинимидиловые эфиры, такие как 3,3'-дитиобис(сукцинимидилпропионат), и бифункциональные малеимиды, такие как бис-N-малеимидо-1,8-октан.
С другой стороны, фармацевтическая композиция по настоящему изобретению, содержащая Fc-фрагмент иммуноглобулина в качестве носителя, может быть введена различными способами.
Используемый здесь термин "введение" означает введение предварительно определенного количества вещества пациенту конкретным подходящим способом. Конъюгат по настоящему изобретению может быть введен любым известным способом при условии, что он обеспечивает его доставку в нужную ткань. Примерами таких способов введения являются, но не ограничиваются ими, внутрибрюшинный, внутривенный, внутримышечный, подкожный, внутрикожный, пероральный, местный, интраназальный, интрапульмональный и ректальный способы введения. Однако, поскольку при пероральном введении пептиды подвергаются гидролизу, то активные ингредиенты, входящие в состав композиции для перорального введения, должны иметь покрытие, или они должны быть защищены от их разложения в желудке. Композиция по настоящему изобретению может быть предпочтительно введена в форме инъекции. Кроме того, фармацевтическая композиция по настоящему изобретению может быть введена с использованием определенных устройств, способных доставлять активные ингредиенты в клетки-мишени.
Фармацевтическая композиция, содержащая конъюгат по настоящему изобретению, может включать фармацевтически приемлемый носитель. Для перорального введения фармацевтически приемлемый носитель может включать связующие вещества, замасливатели, дезинтеграторы, наполнители, солюбилизаторы, диспергирующие агенты, стабилизаторы, суспендирующие агенты, красители и ароматизаторы. Для инъецируемых препаратов фармацевтически приемлемый носитель может включать забуферивающие агенты, консерванты, анальгетики, солюбилизаторы, изотонические агенты и стабилизаторы. Для препаратов местного применения фармацевтически приемлемый носитель может включать основания, наполнители, замасливатели и консерванты. Фармацевтические композиции по настоящему изобретению могут быть приготовлены в виде различных лекарственных форм с использованием вышеуказанных фармацевтически приемлемых носителей. Так, например, для перорального введения фармацевтическая композиция может быть приготовлена в виде таблеток, пастилок, капсул, эликсиров, суспензий, сиропов или облаток. Для инъецируемых препаратов фармацевтическая композиция может быть приготовлена в виде разовой лекарственной формы, такой как флакон, содержащий лекарственные средства для многократного приема, или ампула для введения одной дозы. Фармацевтическая композиция может быть приготовлена в виде растворов, суспензий, таблеток, капсул и препаратов пролонгированного действия.
С другой стороны, примерами носителей, наполнителей и разбавителей, подходящих для приготовления фармацевтических препаратов, являются лактоза, декстроза, сахароза, сорбит, маннит, ксилит, эритритол, мальтит, крахмал, аравийская камедь, альгинат, желатин, фосфат кальция, силикат кальция, целлюлоза, метилцеллюлоза, микрокристаллическая целлюлоза, поливинилпирролидон, вода, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральные масла. Кроме того, фармацевтические препараты могут включать наполнители, антикоагулянты, замасливатели, увлажнители, отдушки, эмульгаторы и антисептики.
В основном, доза лекарственного средства в комбинации с Fc-фрагментом по настоящему изобретению, используемым в качестве носителя, может быть определена в зависимости от нескольких факторов, включая тип заболевания, подвергаемого лечению, способ введения, возраст, пол и вес пациента, тяжесть заболевания пациента, а также тип лекарственного средства, используемого в качестве активного компонента. Поскольку фармацевтическая композиция по настоящему изобретению имеет очень длительное время действия in vivo, то его преимущество заключается в том, что оно не требует частого введения фармацевтических лекарственных средств.
В другом своем аспекте настоящее изобретение относится к способу увеличения продолжительности действия лекарственного средства in vivo путем включения в это лекарственное средство Fc-фрагмента иммуноглобулина.
В одном из вариантов осуществления изобретения конъюгат "физиологически активный полипептид-ПЭГ-Fc-фрагмент иммуноглобулина" обладает гораздо большей стабильностью, чем комплекс "полипептид-ПЭГ" или конъюгат "полипептид-ПЭГ-альбумин". Фармакокинетический анализ выявил, что при связывании с 40 кДа-ПЭГ (комплекс IFNα-40 К-ПЭГ) время полужизни IFNα в сыворотке примерно в 20 раз выше, чем у нативного IFNα, а в конъюгате IFNα-ПЭГ-альбумин это время полужизни примерно в 10 раз выше, чем у нативного IFNα. В отличие от этого, конъюгат IFNα-ПЭГ-Fc по настоящему изобретению дает увеличение времени полужизни примерно в 50 раз (см. таблицу 3). Кроме того, тот же самый результат наблюдался и с использованием других нужных белков, таких как человеческий гормон роста (чГР), гранулоцитарный колониестимулирующий фактор (ГКСФ) и его производное (17S-ГКСФ) и эритропоэтин (ЕРО). Белковые конъюгаты настоящего изобретения, каждый из которых включает нужный белок, связанный с ПЭГ-Fc, дает примерно 10-кратное увеличение среднего времени пребывания в сыворотке (MRT) и времени полужизни в сыворотке по сравнению с нативными формами белков или формами, конъюгированными с ПЭГ или с ПЭГ-альбумином (см. таблицы 4-7).
Кроме того, при связывании комплекса ПЭГ-Fc с группой SH возле С-конца Fab' или N-конца Fab' полученный конъюгат Fab'-ПЭГ-Fc обнаруживал в 2 или 3 раза большее время полужизни в сыворотке, чем комплекс 40К-ПЭГ-Fab' (см. фиг.12).
Кроме того, если белковые конъюгаты были получены с использованием дегликозилированного Fc иммуноглобулина (DG Fc), из которого были удалены сахарные группы, и производных рекомбинантного агликозилированного Fc иммуноглобулина (AG Fc), то их время полужизни в плазме и in vitro активность были такими же, как и у белковых конъюгатов, полученных с использованием нативного Fc (см. таблицу 3 и фиг.8 и 11).
Поэтому, поскольку белковые конъюгаты по настоящему изобретению, полученные путем конъюгирования различных физиологически активных полипептидов, включая человеческий гормон роста, интерферон, эритропоэтин, колониестимулирующий фактор или его производные и производные антител, имеют более длительное время полужизни в сыворотке и среднее время пребывания в сыворотке (MRT), то они могут быть использованы для изготовления композиций различных физиологически активных полипептидов пролонгированного действия.
Для лучшего понимания настоящего изобретения ниже описаны примеры, которые приводятся лишь в иллюстративных целях, и не рассматриваются как ограничение объема настоящего изобретения.
Пример 1: Получение I конъюгата "IFNα-ПЭГ-Fc-фрагмент иммуноглобулина"
<Стадия 1> Получение Fc-фрагмента иммуноглобулина с использованием иммуноглобулина
Fc-фрагмент иммуноглобулина получали следующим образом. 200 мг 150 кДа-иммуноглобулина G (IgG) (Green Cross, Korea), растворенного в 10 мМ фосфатного буфера, обрабатывали 2 мг протеолитического фермента папаина (Sigma) при 37°С в течение 2 часов при мягком помешивании. После ферментативной реакции регенерированный таким образом Fc-фрагмент иммуноглобулина подвергали хроматографии для последовательной очистки на колонке с Superdex, на колонке с белком А и на катионообменной колонке. Более конкретно, реакционный раствор загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатным буфером (PBS, рН 7,3), и колонку элюировали тем же самым буфером при скорости потока 1 мл/мин. Непрореагировавшие молекулы иммуноглобулина (IgG) и F(ab')2, которые имели относительно высокую молекулярную массу, сравнимую с молекулярной массой Fc-фрагмента иммуноглобулина, удаляли благодаря их способности элюироваться раньше, чем Fc-фрагмент Ig. Fab-фрагменты, имеющие молекулярную массу, аналогичную молекулярной массе Fc-фрагмента Ig, удаляли колоночной хроматографией на белке А (фиг.1). Полученные фракции, содержащие Fc-фрагмент Ig, элюированный из колонки с Superdex 200, загружали при скорости потока 5 мл/мин на колонку с белком А (Pharmacia), уравновешенную 20 мМ фосфатным буфером (рН 7,0), и эту колонку промывали тем же самым буфером для удаления белков, не связанных с колонкой. Затем колонку с белком А элюировали 100 мМ натрийцитратного буфера (рН 3,0) и получали Fc-фрагмент иммуноглобулина с высокой степенью чистоты. И наконец, Fc-фракции, собранные из колонки с белком А, очищали на катионообменной колонке (polyCAT, PolyLC, Company), где указанную колонку, загруженную Fc-фракциями, элюировали линейным градиентом 0,15-0,4М NaCl в 10 мМ ацетатного буфера (рН 4,5), в результате чего получали Fc-фракции с высокой степенью чистоты. Fc-фракции с высокой степенью чистоты анализировали с помощью электрофореза в 12% ПААГ с ДСН (дорожка 2 на фиг.2).
<Стадия 2> Получение комплекса IFNα-ПЭГ
3,4 кДа-полиэтиленгликоль, имеющий альдегидную реакционноспособную группу по обоим концам, ALD-ПЭГ-ALD (Shearwater), смешивали с человеческим интерфероном альфа-2b (hIFNα-2b, молекулярная масса (MW): 20 кДа), растворенным в 100 мМ фосфатного буфера в количестве 5 мг/мл в молярном отношении IFNα:ПЭГ, равном 1:1, 1:2,5, 1:5, 1:10 и 1:20. К этой смеси добавляли восстановитель, а именно цианоборогидрид натрия (NaCNBH3, Sigma), в конечной концентрации 20 мМ и проводили реакцию при 4°С в течение 3 часов при мягком помешивании, в результате чего происходило присоединение ПЭГ к амино-концу интерферона-альфа. Для получения комплекса ПЭГ и интерферона-альфа (1:1) реакционную смесь подвергали эксклюзионной хроматографии на колонке с Superdex® (Pharmacia). Комплекс IFNα-ПЭГ элюировали с колонки с использованием 10 мМ калийфосфатного буфера (рН 6,0) в качестве элюирующего буфера, и интерферон-альфа, не связанный с ПЭГ, непрореагировавший ПЭГ и димерные побочные продукты, в которых ПЭГ был связан с двумя молекулами интерферона-альфа, удаляли. Очищенный комплекс IFNα-ПЭГ концентрировали до 5 мг/мл. Во время проведения этого эксперимента было обнаружено, что оптимальное молярное отношение IFNα к ПЭГ в данной реакции, при котором обеспечивается самая высокая реактивность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляло 1:2,5-1:5.
<Стадия 3> Получение конъюгата IFNα-ПЭГ-Fc
Для присоединения комплекса IFNα-ПЭГ, очищенного в стадии 2, к N-концу Fc-фрагмента иммуноглобулина Fc-фрагмент иммуноглобулина (примерно 53 кДа), полученный в стадии 1, растворяли в 10 мМ фосфатного буфера и смешивали с комплексом IFNα-ПЭГ в молярном отношении "комплекс IFNα-ПЭГ:Fc-фрагмент", равном 1:1, 1:2, 1:4 и 1:8. После доведения концентрации фосфатного буфера в реакционном растворе до 100 мМ к реакционному раствору добавляли восстановитель, NaCNBH3, в конечной концентрации 20 мМ и смесь оставляли на 20 часов для реакции при 4°С и при мягком помешивании. Во время проведения этого эксперимента было обнаружено, что в данной реакции оптимальное молярное отношение "комплекс IFNα-ПЭГ-Fc-фрагмент", при котором обеспечивается самая высокая реактивность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляло 1:2.
<Стадия 4> Выделение и очистка конъюгата IFNα-ПЭГ-Fc
После проведения реакции в стадии 3 реакционную смесь подвергали эксклюзионной хроматографии на Superdex для удаления непрореагировавших веществ и побочных продуктов и для очистки продуцируемого белкового конъюгата IFNα-ПЭГ-Fc. После концентрирования реакционной смеси и ее загрузки на колонку с Superdex, через эту колонку пропускали 10 мМ фосфатный буфер (рН 7,3) при скорости потока 2,5 мл/мин для удаления несвязанного Fc и непрореагировавших веществ, а затем колонку элюировали и собирали фракции белкового конъюгата IFNα-ПЭГ-Fc. Поскольку собранные фракции белкового конъюгата IFNα-ПЭГ-Fc содержали небольшое количество примесей, непрореагировавших Fc и димеров интерферона-альфа, то такие примеси удаляли с помощью катионообменной хроматографии. Фракции белкового конъюгата IFNα-ПЭГ-Fc загружали на колонку PolyCAT LP (PolyLC), уравновешенную 10 мМ ацетата натрия (рН 4,5), и эту колонку элюировали линейным градиентом 0-0,5М NaCl в 10 мМ натрийацетатного буфера (рН 4,5) с использованием 1М NaCl. И наконец, белковый конъюгат IFNα-ПЭГ-Fc очищали на анионообменной колонке. Фракции белкового конъюгата IFNα-ПЭГ-Fc загружали на колонку PolyWAX LP (PolyLC), уравновешенную 10 мМ Трис-HCl (рН 7,5), а затем колонку элюировали линейным градиентом 0-0,3М NaCl в 10 мМ Трис-HCl (рН 7,5) с использованием 1М NaCl, в результате чего выделяли белковый конъюгат IFNα-ПЭГ-Fc с высокой степенью чистоты.
Пример 2: Получение II белкового конъюгата IFNα-ПЭГ-Fc
<Стадия 1> Получение комплекса Fc-ПЭГ
3,4 кДа-полиэтиленгликоль, имеющий альдегидную реакционноспособную группу на обоих концах, ALD-ПЭГ-ALD (Shearwater), смешивали с Fc-фрагментом иммуноглобулина, полученным в стадии 1 Примера 1, в молярных отношениях Fc:ПЭГ, равных 1:1, 1:2,5, 1:5, 1:10 и 1:20, где Fc-фрагмент Ig растворен в 100 мМ фосфатного буфера в количестве 15 мг/мл. К этой смеси добавляли восстановитель, NaCNBH3 (Sigma), в конечной концентрации 20 мМ и проводили реакцию при 4°С в течение 3 часов при мягком помешивании. Для получения комплекса ПЭГ и Fc (1:1) реакционную смесь подвергали эксклюзионной хроматографии на колонке с Superdex® (Pharmacia). Комплекс Fc-ПЭГ элюировали с колонки с использованием 10 мМ калийфосфатного буфера (рН 6,0) в качестве элюирующего буфера и Fc-фрагмент иммуноглобулина, не связанный с ПЭГ, а также непрореагировавший ПЭГ и димерные побочные продукты, в которых ПЭГ был связан с двумя молекулами интерферона-альфа, удаляли. Очищенный комплекс Fc-ПЭГ концентрировали примерно до 15 мг/мл. Во время проведения этого эксперимента было обнаружено, что оптимальное молярное отношение Fc к ПЭГ в данной реакции, при котором обеспечивается самая высокая реактивность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляло 1:3 - 1:10.
<Стадия 2> Получение и очистка конъюгата "комплекс Fc-ПЭГ-интерферон-альфа"
Для присоединения комплекса Fc-ПЭГ, очищенного в стадии 1, к N-концу IFNα этот комплекс Fc-ПЭГ смешивали с IFNα растворенным в 10 мМ фосфатного буфера в молярном отношении "комплекс Fc-ПЭГ:IFNα", равном 1:1, 1:1,5, 1:3 и 1:6. После доведения концентрации фосфатного буфера в реакционном растворе до 100 мМ к реакционному раствору добавляли восстановитель, NaCNBH3, в конечной концентрации 20 мМ, и смесь оставляли на 20 часов при 4°С и при мягком помешивании для прохождения реакции. После завершения реакции непрореагировавшие вещества и побочные продукты удаляли методом очистки, описанным в стадии 4 примера 1, в результате чего выделяли белковый конъюгат Fc-ПЭГ-IFNα с высокой степенью очистки.
Пример 3: Получение конъюгата чГР-ПЭГ-Fc
Получали конъюгат чГР-ПЭГ-Fc, который очищали методом, описанным в Примере 1, за исключением того, что в качестве лекарственного средства вместо интерферона-альфа использовали человеческий гормон роста (чГР, мол.масса: 22 кДа), а молярное отношение чГР:ПЭГ составляло 1:5.
Пример 4: Получение конъюгата ГКСФ-ПЭГ-Fc
Получали конъюгат ГКСФ-ПЭГ-Fc, который очищали методом, описанным в Примере 1, за исключением того, что в качестве лекарственного средства вместо интерферона-альфа использовали человеческий гранулоцитарный колониестимулирующий фактор (ГКСФ), а молярное отношение ГКСФ:ПЭГ составляло 1:5.
Кроме того, белковый конъюгат 17S-ГКСФ-ПЭГ-Fc получали и очищали методом, описанным выше, с использованием производного ГКСФ, 17S-ГКСФ, в котором семнадцатый аминокислотный остаток нативного ГКСФ был заменен серином.
Пример 5: Получение конъюгата EPO-ПЭГ-Fc
Конъюгат ЕРО-ПЭГ-Fc получали и очищали методом, описанным в Примере 1, за исключением того, что в качестве лекарственного средства вместо интерферона-альфа использовали человеческий эритропоэтин (ЕРО), а молярное отношение ЕРО:ПЭГ составляло 1:5.
Пример 6: Получение белкового конъюгата с использованием ПЭГ, имеющего другую реакционноспособную группу
Белковый конъюгат IFNα-ПЭГ-Fc получали с использованием ПЭГ, имеющего сукцинимидилпропионатную (SPA) реакционноспособную группу по обоим концам, в соответствии с нижеследующей процедурой. 3,4 кДа-полиэтиленгликоль, SPA-ПЭГ-SPA (Shearwater), смешивали с 10 мг интерферона-альфа, растворенного в 100 мМ фосфатного буфера в молярных отношениях IFNα:ПЭГ, равных 1:1, 1:2,5, 1:5, 1:10 и 1:20. Затем смесь подвергали реакции при комнатной температуре при мягком помешивании в течение 2 ч. Для получения комплекса ПЭГ и интерферона-альфа (1:1) (комплекса IFNα-ПЭГ), где ПЭГ был селективно присоединен к аминогруппе лизинового остатка интерферона-альфа, реакционную смесь подвергали эксклюзионной хроматографии на Superdex. Комплекс IFNα-ПЭГ элюировали с колонки с использованием 10 мМ калийфосфатного буфера (рН 6,0) в качестве элюирующего буфера, а затем интерферон-альфа, не связанный с ПЭГ, непрореагировавший ПЭГ и димерные побочные продукты, в которых две молекулы интерферона-альфа были присоединены по обоим концам ПЭГ, удаляли. Для связывания комплекса IFNα-ПЭГ с аминогруппой лизинового остатка Fc-фрагмента иммуноглобулина очищенный комплекс IFNα-ПЭГ концентрировали примерно до 5 мг/мл, после чего получали конъюгат IFNα-ПЭГ-Fc, который очищали методами, описанными в стадиях 3 и 4 примера 1. В результате проведения этого эксперимента было обнаружено, что оптимальное молярное отношение IFNα:ПЭГ в данной реакции, при котором обеспечивается самая высокая реакционная способность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляло 1:2,5-1:5.
Кроме того, получали другой конъюгат IFNα-ПЭГ-Fc методами, описанными выше, с использованием ПЭГ, имеющего N-гидроксисукцинимидильную (NHS) реакционноспособную группу на обоих концах, NHS-ПЭГ-NHS (Shearwater), или ПЭГ, имеющего бутилальдегидную реакционноспособную группу на обоих концах, BUA-ПЭГ-BUA (Shearwater).
Пример 7: Получение белкового конъюгата с использованием ПЭГ, имеющего другую молекулярную массу
Комплекс IFNα-10кДа ПЭГ получали с использованием 10 кДа-полиэтиленгликоля, имеющего альдегидную реакционноспособную группу по обоим концам, ALD-ПЭГ-ALD (Shearwater). Этот комплекс получали и очищали методом, используемым в стадии 2 примера 1. В результате проведения этого эксперимента было обнаружено, что оптимальное молярное отношение IFNα:10 кДа-ПЭГ в данной реакции, при котором обеспечивается самая высокая реактивность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляло 1:2,5-1:5. Очищенный комплекс IFNα-10 кДа-ПЭГ концентрировали примерно до 5 мг/мл и с использованием этого концентрата получали конъюгат IFNα-10кДа ПЭГ-Fc, который очищали методами, описанными в стадиях 3 и 4 примера 1.
Пример 8: Получение конъюгата Fab'-S-ПЭГ-N-Fc (с группой -SH)
<Стадия 1> Экспрессия и очистка Fab'
Трансформант E.coli, BL21/poDHLF (регистрационный номер: КССМ-10511), экспрессирующий Fab'-фрагмент против фактора некроза опухоли-альфа, культивировали, перемешивая, в 100 мл среды LB в течение ночи, а затем инокулировали в 5-литровый ферментер (Marubishi) и культивировали при 30°С и при 500 об/мин при скорости воздушного потока 20 об.% в минуту. В целях компенсации недостатка питательных элементов для роста бактерий в процессе ферментации в культуры добавляли глюкозу и дрожжевые экстракты в зависимости от состояния сбраживания бактерий. После того как культуры достигали величины OD600, равной 80-100, в эти культуры добавляли индуктор, IPTG, для индуцирования экспрессии белка. Затем культуры выращивали в течение 40-45 часов до тех пор, пока значение OD при 600 нм не увеличивалось до 120-140. Полученную таким образом сбраживаемую жидкость центрифугировали при 20000g в течение 30 минут. Затем супернатант собирали и осадок отбрасывали.
Супернатант подвергали описанной ниже трехстадийной колоночной хроматографии для очистки Fab'-фрагмента против фактора некроза опухоли-альфа. Этот супернатант загружали на колонку HiTrap с белком G (5 мл, Pharmacia), уравновешенную 20 мМ фосфатным буфером (рН 7,0), и колонку элюировали 100 мМ глицином (рН 3,0). Затем собранные Fab'-фракции загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатным буфером (PBS, рН 7,3), и эту колонку элюировали тем же самым буфером. И наконец, вторые Fab'-фракции загружали на колонку polyCAT 21 × 250 (PolyLC) и эту колонку элюировали линейным градиентом NaCl 0,15-0,4М в 10 мМ ацетатном буфере (рН 4,5) с получением фракций Fab'-фрагмента против фактора некроза опухоли-альфа с высокой степенью чистоты.
<Стадия 2> Получение и очистка комплекса Fc-ПЭГ
Для присоединения линкера ПЭГ к N-концу Fc-фрагмента иммуноглобулина Fc-фрагмент иммуноглобулина, полученный методом, описанным в стадии 1 примера 1, растворяли в 100 мМ фосфатного буфера (рН 6,0) при концентрации 5 мг/мл и смешивали с NHS-ПЭГ-MAL (3,4 кДа, Shearwater) в молярном отношении Fc:ПЭГ, равном 1:10, а затем инкубировали при 4°С в течение 12 часов при мягком помешивании.
После завершения реакции реакционный буфер заменяли 20 мМ натрийфосфатным буфером (рН 6,0) для удаления несвязанного NHS-ПЭГ-MAL. Затем реакционную смесь загружали на колонку polyCAT (PolyLC). Эту колонку элюировали линейным градиентом 0,15-0,5М NaCl в 20 мМ натрийфосфатного буфера (рН 6,0). В процессе элюирования комплекс "Fc-фрагмент иммуноглобулина - ПЭГ" элюировался раньше, чем непрореагировавший Fc-фрагмент иммуноглобулина, а непрореагировавший Fc Ig элюировался позже, что позволяло удалять непрореагировавшие молекулы Fc Ig.
<Стадия 3> Получение и очистка конъюгата Fab'-S-ПЭГ-N-Fc (с группой -SH)
Для связывания комплекса "Fc-фрагмент иммуноглобулина - ПЭГ" с цистеиновой группой Fab' этот Fab', очищенный в стадии 1, растворяли в 100 мМ натрийфосфатного буфера (рН 7,3) при концентрации 2 мг/мл и смешивали с комплексом "Fc-фрагмент иммуноглобулина-ПЭГ, полученным выше в стадии 2, в молярном отношении Fab':комплекс, равном 1:5. Реакционную смесь концентрировали до конечной концентрации белка 50 мг/мл и инкубировали при 4°С в течение 24 часов при мягком помешивании.
После завершения реакции реакционную смесь загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатного буфера (рН 7,3), и колонку элюировали тем же самым буфером при скорости потока 1 мл/мин. Связанный конъюгат Fab'-S-ПЭГ-N-Fc элюировался относительно рано, что обусловлено его высокой молекулярной массой, а непрореагировавший комплекс "Fc-фррагмент иммуноглобулина-ПЭГ" и Fab' элюировались позже, что позволяло удалять непрореагировавшие молекулы. Для полного удаления непрореагировавшего комплекса "Fc иммуноглобулина-ПЭГ" собранные фракции конъюгата Fab'-S-ПЭГ-N-Fc снова загружали на колонку polyCAT, 21 × 250 (PolyLC) и эту колонку элюировали линейным градиентом NaCl 0,15-0,5М в 20 мМ натрийфосфатного буфера (рН 6,0), в результате чего получали чистый конъюгат Fab'-S-ПЭГ-N-Fc, содержащий комплекс Fc-ПЭГ, связанный с группой -SH возле С-конца Fab'.
Пример 9: Получение конъюгата Fab'-N-ПЭГ-N-Fc (с N-концом)
<Стадия 1> Получение и очистка комплекса Fab'-ПЭГ (с N-концом)
40 мг Fab', очищенного в стадии 1 примера 8, растворяли в 100 мМ натрийфосфатного буфера (рН 6,0) при концентрации 5 мг/мл, и смешивали с бутил-ALD-ПЭГ-бутил-ALD (3,4 кДа, Nektar) в молярном отношении Fab':ПЭГ, равном 1:5. К реакционной смеси добавляли восстановитель, NaCNBH3, при конечной концентрации 20 мМ, а затем смесь подвергали реакции при 4°С в течение 2 часов при мягком помешивании.
После завершения реакции реакционный буфер заменяли 20 мМ натрийфосфатным буфером (рН 6,0). Затем реакционную смесь загружали на колонку polyCAT (PolyLC). Эту колонку элюировали линейным градиентом NaCl 0,15-0,4М в 20 мМ ацетатном буфере (рН 4,5). В процессе элюирования с колонки комплекс Fab'-ПЭГ, содержащий линкер ПЭГ, связанный с N-концом Fab', элюировался раньше, чем непрореагировавший Fab', а непрореагировавший Fab' элюировался позже, что позволяло удалять непрореагировавшие молекулы Fab'.
<Стадия 2> Получение и очистка конъюгата Fab'-N-ПЭГ-N-Fc
Для связывания комплекса Fab'-ПЭГ, очищенного в вышеописанной стадии 1, с N-концом Fc иммуноглобулина комплекс Fab'-ПЭГ растворяли в 100 мМ натрийфосфатного буфера (рН 6,0) при концентрации 10 мг/мл и смешивали с Fc-фрагментом иммуноглобулина, растворенным в том же самом буфере в молярном отношении "комплекс Fab'-ПЭГ:Fc", равном 1:5. После концентрирования реакционной смеси до конечной концентрации белка 50 мг/мл к реакционной смеси добавляли восстановитель, NaCNBH3, при конечной концентрации 20 мМ, а затем реакционную смесь подвергали реакции при 4°С в течение 24 часов при мягком помешивании.
После завершения реакции реакционную смесь загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатного буфера (рН 7,3), и колонку элюировали тем же самым буфером при скорости потока 1 мл/мин. Связанный конъюгат Fab'-N-ПЭГ-N-Fc элюировался относительно рано, что обусловлено его высокой молекулярной массой, а непрореагировавший Fc-фррагмент иммуноглобулина и комплекс Fab'-ПЭГ элюировался позже, что позволяло удалять непрореагировавшие молекулы. Для полного удаления непрореагировавших молекул Fc иммуноглобулина собранные фракции конъюгата Fab'-N-ПЭГ-N-Fc снова загружали на колонку polyCAT 21 × 250 (PolyLC) и эту колонку элюировали линейным градиентом NaCl 0,15-0,5М в 20 мМ натрийфосфатном буфере (рН 6,0), в результате чего получали чистый конъюгат Fab'-N-ПЭГ-N-Fc, содержащий комплекс "Fc иммуноглобулина-ПЭГ", связанный с N-концом Fab'.
Пример 10: Получение и очистка дегликозилированного Fc иммуноглобулина
200 мг Fc иммуноглобулина, полученного методом, описанным в примере 1, растворяли в 100 мМ фосфатного буфера (рН 7,5) при концентрации 2 мг/мл и смешивали с 300 ед./мг дегликозилазы, PNGазы F (NEB). Реакционную смесь оставляли на 24 часа при 37°С для прохождения реакции при мягком помешивании. Затем, для очистки дегликозилированного Fc-фрагмента иммуноглобулина, реакционную смесь загружали на колонку с SP сефарозой FF (Pharmacia) и колонку элюировали линейным градиентом NaCl 0,1-0,6 М в 10 мМ ацетатном буфере (рН 4,5) с использованием 1М NaCl. Нативный Fc иммуноглобулина элюировался раньше, а дегликозилированный Fc иммуноглобулина (DG Fc) элюировался позже.
Пример 11: Получение конъюгата IFNα-ПЭГ-DG Fc
Для связывания дегликозилированного Fc иммуноглобулина, полученного, как описано в примере 10, с комплексом IFNα-ПЭГ, очищенным в стадии 2 примера 1, комплекс IFNα-ПЭГ смешивали с DG Fc, растворенным в 10 мМ фосфатного буфера в молярном отношении комплекс IFNα-ПЭГ:DG Fc, равном 1:1, 1:2, 1:4 и 1:8. После доведения концентрации фосфатного буфера реакционного раствора до 100 мМ к реакционному раствору добавляли восстановитель, NaCNBH3, при конечной концентрации 20 мМ, а затем смесь подвергали реакции при 4°С в течение 2 часов при мягком помешивании. При проведении этого эксперимента было обнаружено, что оптимальное молярное отношение комплекса IFNα-ПЭГ к DG Fc в реакционной смеси, при котором обеспечивалась самая высокая реактивность и продуцировалось наименьшее количество побочных продуктов, таких как димеры, составляет 1:2.
После завершения реакции реакционную смесь подвергали эксклюзионной хроматографии на колонке с Superdex (Pharmacia) для удаления непрореагировавших веществ и побочных продуктов и для очистки белкового конъюгата IFNα-ПЭГ-DG Fc. После загрузки реакционной смеси на колонку через эту колонку пропускали фосфатный буфер (рН 7,3) при скорости потока 2,5 мл/мин для удаления несвязанного DG Fc и непрореагировавших веществ и колонку элюировали для сбора фракций белкового конъюгата IFNα-ПЭГ-DG Fc. Поскольку собранные фракции белкового конъюгата IFNα-ПЭГ-DG Fc содержали небольшое количество примесей непрореагировавшего DG Fc и комплекса IFNα-ПЭГ, то эти примеси удаляли с помощью катионообменной хроматографии. Фракции белкового конъюгата IFNα-ПЭГ-DG Fc загружали на колонку polyCAT LP (PolyLC), уравновешенную 10 мМ ацетата натрия (рН 4,5), и эту колонку элюировали линейным градиентом 0-0,6М NaCl в 10 мМ натрийацетатного буфера (рН 4,5) с использованием 1М NaCl. И наконец, белковый конъюгат IFNα-ПЭГ-DG Fc очищали на анионообменной колонке. Фракции белкового конъюгата IFNα-ПЭГ-Fc загружали на колонку PolyWAX LP (PolyLC), уравновешенную 10 мМ Трис-HCl (рН 7,5), а затем колонку элюировали линейным градиентом 0-0,3М NaCl в 10 мМ Трис-HCl (рН 7,5) с использованием 1М NaCl и выделяли белковый конъюгат IFNα-ПЭГ-DG Fc с высокой степенью чистоты.
Пример 12: Получение и очистка рекомбинантного производного агликозилированного Fc иммуноглобулина
<Получение экспрессирующего вектора производного 1 Fc IgG4>
Для создания константных областей тяжелой цепи человеческого иммуноглобулина IgG4 получали первое производное (дельта-Cys IgG4), имеющее делецию в девять аминокислот на амино-конце нативной шарнирной области, и второе производное (мономер IgG4), в котором отсутствовала шарнирная область в результате делеции всех двенадцати аминокислот шарнирной области. В качестве экспрессирующего вектора, содержащего секреторную последовательность E.coli, использовали плазмиду pT14S1SH-4T20V22Q (патент Кореи № 38061), полученную авторами настоящего изобретения еще до подачи настоящей заявки.
Для получения константных областей тяжелой цепи человеческого иммуноглобулина IgG4 в соответствии с нижеследующей процедурой проводили ОТ-ПЦР с использованием РНК, выделенной из клеток крови человека, в качестве матрицы. Сначала всю РНК выделяли примерно из 6 мл крови с использованием набора для выделения РНК крови Qiamp (Qiagen) и гены амплифицировали с использованием полноразмерной РНК в качестве матрицы и с использованием набора для одностадийной ОТ-ПЦР (Qiagen). В этой ПЦР использовали пару синтезированных праймеров, представленных в SEQ ID NO:1 и 2, и другую пару синтезированных праймеров, представленных в SEQ ID NO:2 и 3. SEQ ID NO:1 представляет собой нуклеотидную последовательность из 12 аминокислотных остатков шарнирной области IgG4, начиная с 10-го остатка, серина, и ниже. SEQ ID NO:3 имеет нуклеотидную последовательность, кодирующую домен СН2, содержащий аланин в качестве первого аминокислотного остатка. SEQ ID NO:2 имеет BamHI-сайт распознавания, содержащий стоп-кодон.
Для клонирования каждого фрагмента константной области амплифицированного IgG4 в экспрессирующий вектор, содержащий производное секреторной последовательности E.coli, использовали плазмиду pT14S1SH-4T20V22Q (патент Кореи № 38061), полученную авторами настоящего изобретения еще до подачи настоящей заявки. Этот экспрессирующий вектор содержит производное секреторной последовательности термостабильного энтеротоксина, имеющее нуклеотидную последовательность, представленную в SEQ ID NO:4. Для облегчения клонирования StuI-сайт распознавания встраивали в конец производного секреторной последовательности плазмиды pT14S1SH-4T20V22Q термостабильного энтеротоксина E.coli посредством сайт-направленного мутагенеза с использованием пары праймеров, представленных в SEQ ID NO:5 и 6, в целях индуцирования мутагенеза для введения StuI-сайта в нуклеотидную последовательность, кодирующую последний аминокислотный остаток секреторной последовательности. При секвенировании ДНК было установлено, что встраивание StuI-сайта было успешным. Полученную плазмиду pT14S1SH-4T20V22Q, содержащую StuI-сайт, обозначали "pmSTII". Эту плазмиду pmSTII обрабатывали ферментами StuI и BamHI и подвергали электрофорезу в агарозном геле, в результате чего получали очищенный большой фрагмент (4,7 т.п.н.), который содержал производное секреторной последовательности термостабильного энтеротоксина E.coli. Затем амплифицированные генные фрагменты гидролизовали ферментом BamHI и лигировали с линеаризованным экспрессирующим вектором, в результате чего получали pSTIIdCG4Fc и pSTIIG4Mo.
Конечные экспрессирующие векторы отдельно трансформировали в BL21(DE3) E.coli, и полученные трансформанты были обозначены "BL21/pSTIIdCG4Fc (НМ10932)" и "BL21/pSTIIG4Mo
(НМ10933)" и депонированы в Корейском центре культур микроорганизмов (КССМ) 15 сентября 2004 под регистрационными номерами КССМ-10597 и КССМ-10598 соответственно. Затем, когда культуры достигали OD600=80, в эти культуры добавляли индуктор IPTG для индуцирования экспрессии белка. После этого культуры культивировали в течение 40-45 часов до тех пор, пока значение OD при 600 нм не достигало 100-120. Клетки E.coli, собранные из сбраживаемых жидкостей, разрушали, и полученные клеточные лизаты подвергали двухстадийной колоночной хроматографии для очистки производных константных областей рекомбинантного иммуноглобулина, присутствующих в цитозоле E.coli.
5 мл-аффинную колонку с белком-А (Pharmacia) уравновешивали PBS и клеточные лизаты загружали на колонку при скорости потока 5 мл/мин. Несвязанные белки отмывали PBS, а связанные белки элюировали 100 мМ цитратом (рН 3,0). Собранные фракции обессоливали на обессоливающей колонке HiPrep 26/10 (Pharmacia) с использованием 10 мМ трис-буфера (рН 8,0). Затем осуществляли вторую анионообменную колоночную хроматографию на 50 мл-колонке с Q Нр 26/10 (Pharmacia). Первичные очищенные Fc-фракции рекомбинантного агликозилированного иммуноглобулина загружали на колонку с Q-сефарозой НР 26/10 и колонку элюировали линейным градиентом 0-0,2 М NaCl в 10 мМ трис-буфере (рН 8,0), в результате чего получали производное Fc рекомбинантного агликозилированного иммуноглобулина (AG Fc) с высокой степенью чистоты, дельта-Cys IgG4 и мономерную фракцию IgG4 с высокой степенью чистоты.
Пример 13: Получение конъюгата комплекса IFNα-ПЭГ и производного рекомбинантного AG Fc
В соответствии с методами, описанными в примерах 1 и 11, комплекс IFNα-ПЭГ присоединяли к N-концу дельта-Cys IgG4 в качестве производного AG Fc, полученного, как описано в примере 12. После реакции присоединения непрореагировавшие вещества и побочные продукты удаляли из реакционной смеси и полученный таким образом белковый конъюгат IFNα-ПЭГ-AG Fc (I) сначала очищали на 50 мл-колонке с Q НР 26/10 (Pharmacia), а затем очищали с помощью аналитической жидкостной хроматографии высокого давления на колонке polyCAT LP 21,5 × 250 (PolyLC), в результате чего получали конъюгат с высокой степенью очистки. Реакционный раствор для связывания обессоливали на обессоливающей колонке HiPrep 26/10 (Pharmacia) с использованием 10 мМ трис-буфера (8,0). Затем реакционный раствор загружали на 20 мл-колонку с Q НР 26/10 (Pharmacia) при скорости потока 8 мл/мин и эту колонку элюировали линейным градиентом 0-0,2М NaCl с получением нужных фракций. Собранные фракции снова загружали на колонку polyCAT 21,5 × 250, уравновешенную 10 мл ацетатным буфером (рН 5,2), при скорости потока 15 мл/мин и эту колонку элюировали линейным градиентом 0,1-0,3М NaCl и получали фракции с высокой степенью чистоты. В соответствии с методом, описанным выше, получали другой белковый конъюгат IFNα-ПЭГ-AG Fc (II) с использованием другого производного AG Fc, полученного, как описано в примере 12, мономера IgG4.
Пример 14: Получение конъюгата "ЕРО-ПЭГ-производное рекомбинантного AG Fc"
Методом, описанным в примере 13, получали конъюгат "ЕРО-ПЭГ-производное рекомбинантного AG Fc" путем присоединения производного AG Fc, дельта-Cys IgG4, к комплексу ЕРО-ПЭГ.
Сравнительный пример 1: Получение комплекса IFNα-40К ПЭГ
5 мг интерферона-альфа растворяли в 100 мМ фосфатного буфера до конечного объема 5 мл и смешивали с активированным 40 кДа-метокси-ПЭГ-альдегидом (Shearwater) в молярном отношении IFNα:40 кДа-ПЭГ, равном 1:4. К этой смеси добавляли восстановитель, NaCNBH3, при конечной концентрации 20 мМ и смесь оставляли для прохождения реакции на 18 часов при 4°С и при мягком помешивании. Для инактивации ПЭГ, который не реагирует с IFNα, к реакционной смеси добавляли этаноламин при конечной концентрации 50 мМ.
Колонку с сефадексом G-25 (Pharmacia) использовали для удаления непрореагировавшего ПЭГ и этот буфер заменяли другим буфером. Сначала эту колонку уравновешивали двумя колоночными объемами (КО) 10 мМ Трис-HCl-буфера (рН 7,5), а затем в нее загружали реакционную смесь. Скорость потока детектировали путем измерения оптической плотности при 260 нм на УФ-спектрофотометре. При элюировании колонки тем же самым буфером интерферон-альфа, модифицированный путем присоединения ПЭГ с более высокой молекулярной массой к его N-концу, элюировался раньше, а непрореагировавший ПЭГ элюировался позже, что позволяло выделять только IFNα-40К ПЭГ.
Описанную ниже хроматографию проводили для дополнительной очистки комплекса IFNα-40К ПЭГ из собранных фракций. 3 мл-колонку PolyWAX LP (PolyLC) уравновешивали 10 мМ Трис-HCl (pH 7,5). Собранные фракции, содержащие комплекс IFNα-40К ПЭГ, загружали на колонку при скорости потока 1 мл/мин и эту колонку промывали 15 мл уравновешивающего буфера. Затем колонку элюировали линейным градиентом NaCl 0-100% с использованием 30 мл 1М NaCl, в результате чего осуществляли последовательное элюирование интерферона-альфа, конъюгированного с три-, ди- и моно-ПЭГ. Для последующей очистки моно-ПЭГ-конъюгированного интерферона-альфа собранные фракции, содержащие моно-ПЭГ-конъюгированный интерферон-альфа, подвергали эксклюзионной хроматографии. Фракции концентрировали и загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатного буфера (рН 7,0), и эту колонку элюировали тем же самым буфером при скорости потока 1 мл/мин. Молекулы три- и ди-ПЭГ-конъюгированного интерферона-альфа удаляли исходя из их способности элюироваться раньше, чем моно-ПЭГ-конъюгированный интерферон-альфа, в результате чего выделяли моно-ПЭГ-конъюгированный интерферон-альфа с высокой степенью чистоты.
В соответствии с методом, описанным выше, 40 кДа-ПЭГ конъюгировали с N-концом человеческого гормона роста, гранулоцитарного колониестимулирующего фактора (ГКСФ) и производного ГКСФ, в результате чего получали комплексы чГР-40К ПЭГ, ГКСФ-40К ПЭГ и производное 40К ПЭГ-17S-ГКСФ.
Сравнительный пример 2: Получение конъюгата "IFNα-ПЭГ-альбумин"
Для присоединения комплекса IFNα-ПЭГ, очищенного в стадии 2 примера 1, к N-концу альбумина комплекс IFNα-ПЭГ смешивали с альбумином человеческой сыворотки (HSA, примерно 67 кДа, Green Cross), растворенным в 10 мМ фосфатного буфера в молярном отношении "комплекс IFNα-ПЭГ:альбумин", равном 1:1, 1:2, 1:4 и 1:8. После доведения концентрации фосфатного буфера реакционного раствора до 100 мМ к реакционному раствору добавляли восстановитель, NaCNBH3, при конечной концентрации 20 мМ и смесь оставляли на 20 часов для реакции при 4°С и при мягком помешивании. При проведении этого эксперимента было обнаружено, что оптимальное молярное отношение комплекса IFNα-ПЭГ к альбумину в реакционной смеси, при котором обеспечивается наибольшая реактивность и продуцируется наименьшее количество побочных продуктов, таких как димеры, составляет 1:2.
После завершения реакции присоединения реакционную смесь подвергали эксклюзионной хроматографии на колонке с Superdex® (Pharmacia) для удаления непрореагировавших веществ и побочных продуктов и для очистки продуцированного белкового конъюгата IFNα-ПЭГ-альбумин. После концентрирования реакционной смеси и ее загрузки на колонку через эту колонку пропускали 10 мМ натрийацетатный буфер при скорости потока 2,5 мл/мин для удаления несвязанного альбумина и непрореагировавших веществ, а затем колонку элюировали для очистки только белкового конъюгата IFNα-ПЭГ-альбумин. Поскольку собранные фракции белкового конъюгата IFNα-ПЭГ-альбумин содержали небольшое количество примесей, непрореагировавшего альбумина и димеров интерферона-альфа, то эти примеси удаляли с помощью катионообменной хроматографии. Фракции белкового конъюгата IFNα-ПЭГ-альбумин загружали на колонку SP5PW (Waters), уравновешенную 10 мМ ацетата натрия (рН 4,5), и эту колонку элюировали линейным градиентом 0-0,5М NaCl в 10 мМ натрийацетатного буфера (рН 4,5) с использованием 1М NaCl, в результате чего выделяли белковый конъюгат "IFNα-ПЭГ-альбумин" с высокой степенью очистки.
Методом, описанным выше, альбумин конъюгировали с человеческим гормоном роста, ГКСФ, и с производным ГКСФ, в результате чего получали конъюгаты чГР-ПЭГ-альбумин, ГКСФ-ПЭГ-альбумин и 17S-ГКСФ-ПЭГ-альбумин.
Сравнительный пример 3: Получение комплекса Fab'-S-40К ПЭГ
Свободный цистеиновый остаток Fab'-фрагмента, очищенного в стадии 1 примера 8, активировали путем инкубирования в активирующем буфере (20 мМ ацетат натрия (рН 4,0), 0,2 мМ (DTT) в течение 1 часа. Затем буфер заменяли ПЭГ-модифицирующим буфером, 50 мМ фосфатом калия (рН 6,5), добавляли малеимид-ПЭГ (Mw: 40 кДа, Shearwater) в молярном отношении Fab':40 кДа ПЭГ = 1:10 и проводили реакцию при 4°С в течение 24 часов при мягком помешивании.
После завершения реакции реакционный раствор загружали на колонку с Superdex 200 (Pharmacia), уравновешенную 10 мМ натрийфосфатным буфером (рН 7,3), и эту колонку элюировали тем же самым буфером при скорости потока 1 мл/мин. Fab', конъюгированный с 40 кДа ПЭГ (Fab'-40К ПЭГ), элюировался относительно рано, что обусловлено его высокой молекулярной массой, а непрореагировавший Fab' элюировался позже, что позволяло удалять непрореагировавший Fab'. Для полного удаления непрореагировашего Fab' собранные фракции комплекса Fab'-40К ПЭГ снова загружали на колонку polyCAT, 21 × 250 (PolyLC) и эту колонку элюировали линейным градиентом 0,15-0,5М NaCl в 20 мМ натрийфосфатного буфера (рН 4,5), в результате чего получали чистый комплекс Fab'-S-40К ПЭГ, содержащий 40-кДа ПЭГ, присоединенный к группе -SH фрагмента Fab'.
Экспериментальный пример 1: Идентификация и количественный анализ белковых конъюгатов
<1-1> Идентификация белковых конъюгатов
Белковые конъюгаты, полученные, как описано в предыдущих примерах, анализировали с помощью электрофореза в нередуцирующем ПААГ с ДСН с использованием 4-20% градиентного геля и 12% геля и ELISA (R&D System).
Результаты ДСН-ПААГ-анализа, проиллюстрированные на фиг.3, показали, что реакция связывания физиологически активного полипептида, не-пептидного полимера, ПЭГ и Fc-фрагмента иммуноглобулина приводила к успешному продуцированию конъюгата IFNα-ПЭГ-Fc (А), конъюгата 17Ser-КГСФ-ПЭГ-Fc (В) и конъюгата ЕРО-ПЭГ-Fc (С).
Кроме того, DG Fc, полученный, как описано в примере 10, анализировали с помощью электрофореза в нередуцирующем 12% ПААГ с ДСН. Как показано на фиг.6b, полоса DG Fc детектировалась в положении, которое соответствовало молекулярной массе нативного Fc, не содержащего сахарных групп.
<1-2> Количественный анализ белковых конъюгатов
Белковые конъюгаты, полученные, как описано в предыдущих примерах, количественно оценивали с помощью эксклюзионной хроматографии на колонке HiLoad 26/60 с Superdex 75 (Pharmacia) с использованием 10 мМ калийфосфатного буфера (рН 6,0) в качестве элюирующего буфера, где площадь пика каждого белкового конъюгата сравнивали с площадью пика контрольной группы. Стандарты в предварительно определенном количестве, а именно IFNα, чГР, КГСФ, 17Ser-КГСФ, ЕРО и Fc, отдельно подвергали эксклюзионной хроматографии и определяли переводной коэффициент между концентрацией и пиком. Каждый белковый конъюгат в предварительно определенном количестве снова подвергали эксклюзионной хроматографии. Затем путем вычитания площади пика, соответствующего Fc-фрагменту иммуноглобулина, из полученной площади пика определяли количество физиологически активного белка, присутствующего в каждом белковом конъюгате. На фиг.4 представлен результат эксклюзионной хроматографии очищенного конъюгата IFNα-ПЭГ-Fc, где наблюдался один пик. Этот результат показал, что очищенный белковый конъюгат не содержит мультимерных примесей, таких как димер, тример или мономеры с большим числом звеньев.
После количественной оценки физиологически активного полипептида, конъюгированного с Fc, с использованием антитела против физиологически активного полипептида, было выявлено, что это антитело препятствует связыванию с этим полипептидом, на что указывало получение значения более низкого, чем фактивческое значение, вычисленное с помощью хроматографии. В случае ELISA-анализа конъюгата IFNα-ПЭГ-Fc этот анализ давал значение, составляющее примерно 30% от фактического значения.
<1-3> Оценка чистоты и массы белковых конъюгатов
Белковые конъюгаты, полученные, как описано в предыдущих примерах, подвергали эксклюзионной хроматографии и измеряли оптическую плотность при 280 нм. Результаты показали, что конъюгаты IFNα-ПЭГ-Fc, чГР-ПЭГ-Fc, ГКСФ-ПЭГ-Fc и 17Ser-КГСФ-ПЭГ-Fc обнаруживали один пик при времени удерживания вещества с молекулярной массой 70-80 кДа.
С другой стороны, проводили обращенно-фазовую ВЭЖХ для определения чистоты белковых конъюгатов, полученных, как описано в примерах 1, 11 и 13, а именно "IFNα-ПЭГ-Fc", "IFNα-ПЭГ-DG Fc" и "IFNα-ПЭГ-производное рекомбинантного AG Fc". При этом использовали обращенно-фазовую колонку (колонка 259 VHP54, Vydac). Эту колонку элюировали 40-100% градиентом ацетонитрила с 0,5% TFA и чистоту анализировали путем измерения оптической плотности при 280 нм. Результаты, проиллюстрированные на фиг.8, показали, что образцы не содержали несвязанный интерферон или Fc-фрагмент иммуноглобулина, и было обнаружено, что все белковые конъюгаты IFNα-ПЭГ-Fc (А), IFNα-ПЭГ-DG Fc (В) и IFNα-ПЭГ-производное рекомбинантного AG Fc (С) имели чистоту, превышающую 96%.
Для определения точных молекулярных масс очищенных белковых конъюгатов массу каждого конъюгата анализировали на высокоэффективном масс-спекторофотометре MALDI-TOF (Voyager De-STR, Apllied Biosystems). В качестве матрикса использовали синаповую кислоту. 0,5 мкл каждого тест-образца наносили на предметное стекло и сушили воздухом, а затем снова смешивали с равным объемом матриксного раствора, сушили воздухом и вводили в источник ионов. Детекцию осуществляли с использованием линейного анализатора TOF, работающего в позитивном режиме. Ионы подвергали ускорению с использованием щелевого источника для вылета частиц с запаздыванием вылета (DE), где время запаздывания вылета частиц составляло от 750 нсек до 1500 нсек при общем напряжении ускорения примерно 2,5 кВ.
Молекулярные массы, наблюдаемые при масс-спектрометирии MALDI-TOF для белковых конъюгатов Fc, полученных, как описано в примерах, представлены ниже в таблице 1. На фиг.5 представлены результаты масс-спекторметрии MALDI-TOF для конъюгата ЕРО-ПЭГ-Fc, а на фиг.7 представлены результаты масс-спекторметрии MALDI-TOF для конъюгатов IFNα-ПЭГ-Fc и IFNα-ПЭГ-DG Fc. В результате было обнаружено, что белковый конъюгат ЕРО-ПЭГ-Fc имеет чистоту более чем 95% и молекулярную массу, очень близкую к теоретической Mw. Кроме того, было обнаружено, что ЕРО связывался с Fc-фрагментом иммуноглобулина в отношении 1:1.
| Таблица 1 | ||
| Теоретическая Mw (кДа) | Измеренная Mw (кДа) | |
| IFNα-ПЭГ-Fc (E.1) | 75,4 | 75,9 |
| чГР-ПЭГ-Fc (E.3) | 78,4 | 78,6 |
| ГКСФ-ПЭГ-Fc (E.4) | 75,3 | 75,9 |
| Производное 17S-ГКСФ-ПЭГ-Fc (E.4) | 75,0 | 75,9 |
| EPO-ПЭГ-Fc (E.5) | 91,4 | 91,0 |
Кроме того, в результате оценки с помощью масс-спектрометрии MALDI-TOF молекулярных масс Fc и DG Fc, полученных, как описано в примере 10, было установлено, что DG Fc имеет молекулярную массу 50 кДа, которая примерно на 3 кДа меньше массы нативного Fc (фиг.6а). Поскольку Mw 3 кДа соответствует теоретическому размеру сахарных групп, то эти результаты продемонстрировали, что сахарные группы были полностью удалены.
В нижеследующей таблице 2 представлены результаты масс-спектрометрии MALDI-TOF конъюгата IFNα-ПЭГ-DG Fc, полученного, как описано в примере 11, и конъюгатов IFNα-ПЭГ-производное рекомбинантного AG Fc (I и II), полученных, как описано в примере 13. Было установлено, что конъюгат IFNα-ПЭГ-DG Fc был на 3 кДа меньше, чем конъюгат IFNα-ПЭГ-Fc, а конъюгат IFNα-ПЭГ-производное рекомбинантного AG Fc (I) был примерно на 3-4 кДа меньше, чем указанный конъюгат IFNα-ПЭГ-Fc, имеющий массу 75,9 кДа. Конъюгат "IFNα-ПЭГ-производное рекомбинантного AG Fc" (II), связанный с Fc-мономером, имел молекулярную массу, которая была меньше на 24,5 кДа, то есть на величину, соответствующую молекулярной массе мономера Fc.
| Таблица 2 | ||
| Теоретическая Mw (кДа) | Измеренная Mw (кДа) | |
| IFNα-ПЭГ-DG Fc (Е.11) | 72,8 | 73,0 |
| IFNα-ПЭГ-производное рекомбинантного AG Fc (I)(Е.13) | 72,3 | 72,2 |
| IFNα-ПЭГ-производное рекомбинантного AG Fc (II)(Е.13) | 46,8 | 46,6 |
Экспериментальный пример 2: Фармакокинетический анализ
Нативные формы физиологически активных белков (контролей) и белковые конъюгаты, полученные, как описано выше в примерах и в сравнительных примерах, комплексы -40К ПЭГ, конъюгаты - ПЭГ-альбумин, конъюгаты - ПЭГ-Fc, конъюгаты - ПЭГ-DG Fc и конъюгаты - ПЭГ-производное рекомбинантного AG Fc оценивали на их стабильность в сыворотке и на фармакокинетические параметры у крыс SD (пять крыс на группу). Контроль, а также комплексы -40К ПЭГ, конъюгаты -ПЭГ-альбумин, конъюгаты -ПЭГ-Fc, конъюгаты -ПЭГ-DG Fc и конъюгаты -ПЭГ-производное рекомбинантного AG Fc (тест-группы) отдельно подкожно инъецировали крысам в дозе 100 мкг/кг. После подкожной инъекции через 0,5, 1, 2, 4, 6, 12, 24, 30, 48, 72 и 96 часов брали пробы крови у животных контрольных групп, и через 1, 6, 12, 24, 30, 48, 72, 96, 120, 240 и 288 часов брали пробы крови у животных тест-групп. Пробы крови собирали в пробирки с антикоагулянтом, гепарином, и центрифугировали в течение 5 минут в высокоскоростной микроцентрифуге Эппендорфа для удаления клеток крови. Уровни белка в сыворотке измеряли с помощью ELISA с использованием антител, специфичных к физиологически активным белкам.
Результаты фармакокинетических анализов нативных форм IFNα, чГР, КГСФ и ЕРО и их -40К ПЭГ-комплексов, их -ПЭГ-альбумин-конъюгатов, -ПЭГ-Fc-конъюгатов и -ПЭГ-DG Fc-конъюгатов представлены ниже в таблицах 3-7. В нижеследующих таблицах Тmax означает время, необходимое для достижения максимальной концентрации лекарственного средства в сыворотке, Т1/2 означает время полужизни лекарственного средства в сыворотке, а MRT (среднее время пребывания) означает среднее время пребывания молекулы лекарственного средства в организме.
| Таблица 4 | |||||||||||
| Фармакокинетические данные человеческого фактора роста | |||||||||||
| Нативный чГР | чГР-40К ПЭГ (С.Е.1) | чГР-ПЭГ-альбумин (С.Е.2) | чГР-ПЭГ-Fc (E.3) | ||||||||
| Tmax (ч) | 1,0 | 12 | 12 | 12 | |||||||
| T1/2 (ч) | 1,1 | 7,7 | 5,9 | 11,8 | |||||||
| MRT (ч) | 2,1 | 18,2 | 13,0 | 18,8 | |||||||
| Таблица 5 | |||||||||||
| Фармакокинетические данные ГКСФ | |||||||||||
| Нативный ГКСФ | ГКСФ-40К ПЭГ (С.Е.1) | ГКСФ-ПЭГ-альбумин (С.Е.2) | ГКСФ-ПЭГ-Fc (E.4) | ||||||||
| Tmax (ч) | 2,0 | 12 | 12 | 12 | |||||||
| T1/2 (ч) | 2,8 | 4,8 | 5,2 | 6,9 | |||||||
| MRT (ч) | 5,2 | 24,5 | 25,0 | 32,6 | |||||||
| Таблица 6 | |||||||||||
| Фармакокинетические данные производного 17S-ГКСФ | |||||||||||
| Производное нативного 17S-ГКСФ | 17S-ГКСФ-40К ПЭГ (С.Е.1) | 17S-ГКСФ-ПЭГ-альбумин (С.Е.2) | 17S-ГКСФ-ПЭГ-Fc (E.4) | ||||||||
| Tmax (ч) | 2,0 | 24 | 24 | 24 | |||||||
| T1/2 (ч) | 2,9 | 4,3 | 6,4 | 7,0 | |||||||
| MRT (ч) | 5,8 | 24,4 | 25,1 | 33,2 | |||||||
| Таблица 7 | |||||||||||
| Фармакокинетические данные ЕРО | |||||||||||
| Нативный ЕРО | В высокой степени гликозилированный ЕРО | ЕРО-ПЭГ-Fc (Е.5) | ЕРО-ПЭГ-производное рекомбинантного AG Fc (E.13) | ||||||||
| Tmax (ч) | 6,0 | 12 | 30 | 48 | |||||||
| T1/2 (ч) | 9,4 | 18,4 | 61,5 | 87,9 | |||||||
| MRT (ч) | 21,7 | 26,8 | 117,6 | 141,6 | |||||||
Как видно из полученных результатов, представленных в таблице 3, и на графике фармакокинетических данных, представленном на фиг.9, белковый конъюгат IFNα-ПЭГ-Fc имеет время полужизни в сыворотке 90,4 часа, и это время примерно в 50 раз выше, чем у нативного IFNα, и примерно в 2,5 раза выше, чем у комплекса IFNα-40К ПЭГ, имеющего время полужизни 35,8 часов и полученного, как описано в сравнительном примере 1. Кроме того, было обнаружено, что время полужизни в сыворотке белкового конъюгата IFNα-ПЭГ-Fc настоящего изобретения значительно превышает время полужизни в сыворотке конъюгата IFNα-ПЭГ-альбумин, которое составляет 17,1 часа.
С другой стороны, как показано в таблице 3 и на фиг.11, время полужизни конъюгата IFNα-ПЭГ-DG Fc в сыворотке составляет 71,0 часа, т.е. почти аналогично времени полужизни конъюгата IFNα-ПЭГ-Fc, что указывает на то, что дегликозилирование Fc не оказывает значительного влияния на in vivo стабильность конъюгата IFNα-ПЭГ-DG Fc. Кроме того, было обнаружено, что конъюгат, полученный с использованием производного рекомбинантного AG Fc, продуцированного рекомбинантным методом, обладает таким же эффектом, как и DG Fc, происходящий от нативной формы. Однако время полужизни в сыворотке комплекса, связанного с мономером Fc, было наполовину меньше, чем у комплекса, связанного с нормальным димером Fc.
Как показано в таблице 4, человеческий гормон роста, конъюгированный с Fc-фрагментом IgG настоящего изобретения, имел более длительное время полужизни в сыворотке. То есть, по сравнению с нативной формой (1,1 ч), комплекс чГР-40К ПЭГ и конъюгат чГР-ПЭГ-альбумин имели несколько более длительное время полужизни, составляющее 7,7 ч и 5,9 ч соответственно, а белковый конъюгат чГР-ПЭГ-Fc настоящего изобретения имел значительно более длительное время полужизни в сыворотке, которое составляло 11,8 ч.
Фармакокинетические данные для ГКСФ и его производных, представленные в таблице 5 и 6, показали, что конъюгаты ГКСФ-ПЭГ-Fc и 17S-ГКСФ-ПЭГ-Fc обнаруживают гораздо большее время полужизни в сыворотке, чем комплекс -40К ПЭГ- и конъюгат -ПЭГ-альбумин. Было установлено, что Fc-фрагмент иммуноглобулина, присутствующий в сыворотке, способствовал увеличению продолжительности действия физиологически активных белков в нативных формах, а также в форме их производных, имеющих модификации в некоторых аминокислотных остатках, на уровне, аналогичном уровню нативных форм. Исходя из этих результатов, совершенно очевидно, что способ настоящего изобретения будет столь же эффективен и в отношении других белков и их производных.
Как показано в таблице 7 и на фиг.10, конъюгирование нативного гликозилированного ЕРО с Fc-фрагментом также приводит к увеличению времени полужизни в сыворотке. То есть ЕРО, в своей нативной форме, имеет время полужизни в сыворотке 9,4 часа, а при высокой степени гликозилирования, способствующего увеличению его стабильности в сыворотке, он имел более длительное время полужизни в сыворотке, составляющее 18,4 часа. Конъюгат ЕРО-ПЭГ-Fc, содержащий ЕРО, присоединенный к Fc-фрагменту иммуноглобулина по настоящему изобретению, обнаруживал значительное увеличение времени полужизни в сыворотке, а именно до 61,5 часов. Кроме того, при конъюгировании с рекомбинантным агликозилированным (AG) Fc-производным, происходящим от E.coli, время полужизни ЕРО увеличивалось до 87,9 часов, что указывало на то, что агликозилирование Fc-фрагмента позволяет получить белковый конъюгат, не оказывающий нежелательного влияния на стабильность данного белка в сыворотке, т.е. этот Fc-фрагмент не обладал функциями антитела.
Исходя из вышеуказанных результатов, совершенно очевидно, что белковые конъюгаты настоящего изобретения, полученные путем ковалентного присоединения Fc-фрагмента иммуноглобулина посредством не-пептидного полимера, дают увеличение времени полужизни в сыворотке в несколько раз или в несколько десятков раз по сравнению со временем полужизни их нативных форм. Кроме того, если Fc иммуноглобулина был агликозилирован путем продуцирования в E.coli или дегликозилирован путем обработки ферментом, то указанное увеличение времени полужизни в сыворотке его белкового конъюгата поддерживалось на аналогичном уровне.
Более конкретно, по сравнению с белками, модифицированными 40 кДа-ПЭГ, который, среди других молекул ПЭГ, обеспечивал наиболее продолжительное действие этих белков в сыворотке, эти конъюгаты белка с Fc иммуноглобулина обнаруживали самую высокую стабильность в сыворотке. Кроме того, по сравнению с белковыми конъюгатами, которые, вместо Fc иммуноглобулина, имели присоединенный к ним альбумин, белковые конъюгаты настоящего изобретения обладали исключительно высокой стабильностью в сыворотке, что указывало на то, что белковые конъюгаты настоящего изобретения могут быть с успехом использованы для получения белковых лекарственных средств с пролонгированным действием. Эти результаты показали, что конъюгаты настоящего изобретения, по сравнению со стандартными белками, конъюгированными с ПЭГ или альбумином, дают превосходный эффект в отношении стабильности в сыворотке и MRT для белков широкого спектра, включая производные колониестимулирующего фактора, образованные точковой мутацией, что указывает на то, что такая стабильность и продолжительность действия белковых конъюгатов настоящего изобретения может быть достигнута и для других физиологически активных полипептидов.
С другой стороны, после получения белкового конъюгата IFNα-10К-ПЭГ-Fc (пример 7) с использованием не-пептидного полимера, 10 кДа-ПЭГ, этот конъюгат был проанализирован на время его полужизни в сыворотке методом, описанным выше, и полученные результаты показали, что его время полужизни в сыворотке составляло 48,8 часов, и это время было значительно короче, чем время полужизни (79,7 часов) белкового конъюгата, полученного с использованием 3,4 кДа-ПЭГ.
Кроме того, время полужизни белковых конъюгатов в сыворотке снижается с увеличением молекулярной массы не-пептидного полимера ПЭГ. Эти данные указывают на то, что самым главным фактором, способствующим увеличению стабильности в сыворотке и продолжительности действия белковых конъюгатов в сыворотке, является конъюгированный Fc-фрагмент иммуноглобулина, а не не-пептидный полимер.
Даже если реакционноспособную группу ПЭГ заменить на другую реакционноспособную группу, не являющуюся альдегидной группой, то белковые конъюгаты с таким ПЭГ будут давать такие же эффекты в отношении кажущейся молекулярной массы и времени полужизни в сыворотке, как и конъюгаты, полученные с использованием ПЭГ, имеющего альдегидную реакционноспособную группу.
Экспериментальный пример 3: Фармакокинетический анализ II
Для определения времени полужизни в сыворотке конъюгатов Fab'-S-ПЭГ-N-Fc и Fab'-N-ПЭГ-N-Fc, полученных, как описано в примерах 8 и 9, и комплекса Fab'-S-40К ПЭГ, полученного, как описано в сравнительном примере 3, проводили фармакокинетический анализ лекарственных средств, полученных на основе указанных конъюгатов и указанного комплекса, методом, описанным в экспериментальном примере 2 с использованием Fab' в качестве контроля. Результаты представлены на фиг.12.
Как показано на фиг.12, конъюгаты Fab'-S-ПЭГ-N-Fc и Fab'-N-ПЭГ-N-Fc обнаруживали более длительное время полужизни в сыворотке, которое было в два или в три раза больше, чем время полужизни Fab' или комплекса Fab'-S-40К ПЭГ.
Экспериментальный пример 4: Оценка внутриклеточной активности белковых конъюгатов
<4-1> Сравнение внутриклеточных активностей конъюгатов белка IFNα
Для сравнения внутриклеточной активности конъюгатов белка IFNα конъюгаты: IFNα-ПЭГ-Fc (пример 1), IFNα-ПЭГ-DG Fc (пример 11), IFNα-ПЭГ-производное рекомбинантного AG Fc (пример 13), IFNα-40К ПЭГ (сравнительный пример 1) и IFNα-ПЭГ-альбумин (сравнительный пример 2) оценивали на противовирусную активность в биоанализе клеточных культур с использованием клеток коровьих почек Madin Darby (MDBK) (АТСС CCL-22), инфицированных вирусом везикулярного стоматита. В качестве стандартного материала использовали не-ПЭГилированный интерферон альфа-2b, поставляемый Национальным институтом по биологическим стандартам и контролю (NIBSC).
Клетки MDBK культивировали в среде МЕМ (минимальная поддерживающая среда, JBI), в которую были добавлены 10% FBS и 1% пенициллин/стрептомицин, при 37°С в атмосфере 5% СО2. Анализируемые образцы и стандартный материал разводили культуральной средой в предварительно определенных концентрациях и 100 мкл-аликвоты этих разведений вносили в каждую лунку 96-луночного планшета. Культивированные клетки отделяли, добавляли в планшет, содержащий образцы в объеме 100 мкл, и культивировали примерно в течение 1 часа при 37°С в атмосфере 5% СО2. Затем в каждую лунку планшета добавляли 50 мкл вируса везикулярного стоматита (VSV) при 5-7 × 103 б.о.е., после чего клетки культивировали примерно в течение 16-20 часов при 37°С в атмосфере 5% СО2. Лунку, которая не содержала образца или стандартного материала, а содержала лишь один вирус, использовали в качестве негативного контроля, а лунку, которая содержала только клетки, использовали в качестве позитивного контроля.
После удаления культуральной среды в планшет добавляли 100 мкл раствора нейтрального красного для окрашивания жизнеспособных клеток, а затем инкубировали в течение 2 часов при 37°С в атмосфере 5% СО2. После удаления супернатантов в каждую лунку планшета добавляли 100 мкл смеси 1:1 100% этанола и 1% уксусной кислоты. После тщательного перемешивания для растворения всех кристаллов нейтрального красного, элюированного из окрашенных клеток, измеряли оптическую плотность при 540 нм. Негативный контроль использовали в качестве "пустышки", и вычисляли величины ED50 (дозы, вызывающие 50% ингибирование клеточного роста), принимая клеточный рост позитивного контроля за 100%.
| Таблица 8 | |||
| Конц. (нг/мл) | Удельная активность (МЕ/мг) | Относительная активность (%) для нативного IFNα | |
| Нативный IFNα | 100 | 4,24Е+08 | 100 |
| IFNα-40К ПЭГ | 100 | 2,04Е+07 | 4,8 |
| IFNα-ПЭГ-альбумин | 100 | 2,21Е+07 | 5,2 |
| IFNα-ПЭГ-Fc | 100 | 1,19Е+08 | 28,1 |
| IFNα-ПЭГ-DG Fc | 100 | 1,09Е+08 | 25,7 |
| IFNα-ПЭГ-производное рекомбинантного AG Fc | 100 | 9,58Е+07 | 22,6 |
Как показано в таблице 8, IFNα-40К ПЭГ давал уменьшение активности до 4,8% по отношению к активности нативного IFNα. В частности, по мере увеличения размера ПЭГ-части стабильность белкового конъюгата в сыворотке увеличивалась, а его активность постепенно снижалась. Сообщалось, что интерферон-альфа при его модификации 12 кДа-ПЭГ имеет in vitro активность 25%, а при его модификации 40 кДа-ПЭГ его активность составляет 7% (Р. Bailon et al., Bioconjugate Chem. 12: 195-202, 2001). Таким образом, поскольку при увеличении молекулярной массы ПЭГ-части время полужизни белкового конъюгата увеличивается, а его биологическая активность резко снижается, то необходимо было получить такой белковый конъюгат, который имел бы более продолжительное время полужизни в сыворотке и более высокую активность. Кроме того, конъюгат IFNα-ПЭГ-альбумин имел слабую активность, которая составляла примерно 5,2% от активности нативного IFNα. В противоположность этому, конъюгаты IFNα-ПЭГ-Fc и IFNα-ПЭГ-DG Fc настоящего изобретения обнаруживали значительно более высокую относительную активность, которая составляла 28,1% и 25,7% по отношению к активности нативного IFNα. Кроме того, конъюгирование IFNα с производным рекомбинантного AG Fc приводило к аналогичному увеличению активности. Исходя из этих результатов, имеются все основания предполагать, что интерферон-альфа, конъюгированный с Fc-фрагментом иммуноглобулина, имеет значительно более длительное время полужизни в сыворотке и обладает значительно более высокой фармацевтической эффективностью in vivo.
<4-2> Сравнение внутриклеточных активностей конъюгатов белка человеческого гормона роста
Для сравнения внутриклеточной активности конъюгатов белка человеческого гормона роста проводили сравнительную оценку внутриклеточной активности конъюгатов чГР-ПЭГ-Fc, чГР-40К-ПЭГ и чГР-ПЭГ-альбумин.
Внутриклеточные активности конъюгатов чГР измеряли с помощью in vitro анализа с использованием клеточной линии нодулярной лимфомы крыс, Nb2 (Европейская коллекция клеточных культур (ЕСАСС) #97041101), в которой наблюдался зависящий от человеческого гормона роста митогенез.
Клетки Nb2 культивировали в среде Фишера, в которую были добавлены 10% FBS (фетальной бычьей сыворотки), 0,075% NaCO3, 0,05 мМ 2-меркаптоэтанола и 2 мМ глутамина, после чего их 24 часа культивировали в той же самой среде, но не содержащей 10% FBS. Затем культивированные клетки подсчитывали и в каждую лунку 96-луночного планшета добавляли примерно 2 × 104-аликвоты клеток. Затем конъюгат чГР-ПЭГ-Fc, конъюгат чГР-40К ПЭГ, конъюгат чГР-ПЭГ-альбумин (стандартные конъюгаты, поставляемые Национальным институтом по биологическим стандартам и контролю (NIBSC)), используемые в качестве контроля, и нативный человеческий гормон роста (НМ-чГР) разводили и добавляли в каждую лунку при различных концентрациях с последующим инкубированием в течение 48 часов при 37°С в атмосфере 5% СО2. После этого, для измерения пролиферативной активности клеток путем определения числа клеток в каждой лунке, в каждую лунку добавляли 25 мкл 1х водного раствора реагента 96 для определения клеточного титра (Promega) и клетки снова культивировали в течение 4 часов. Затем измеряли оптическую плотность при 490 нм и подсчитывали титр для каждого образца. Результаты представлены ниже в таблице 9.
| Таблица 9 | |||
| Конц. (нг/мл) | Удельная активность (МЕ/мг) | Относительная активность (%) для нативного НМ-чГР | |
| Нативный чГР | 100 | 2,71Е+06 | 100 |
| чГР (стандарт от NIBSC) | 100 | 2,58Е+06 | 95,2 |
| чГР-40К ПЭГ | 100 | 0,206Е+06 | 7,6 |
| чГР-ПЭГ-альбумин | 100 | 0,141Е+06 | 5,2 |
| чГР-ПЭГ-Fc | 100 | 0,76Е+06 | 28,1 |
| Удельная активность*=1/ED50х106 (ED50: количество белка, необходимого для стимуляции 50%-го роста от максимального роста клеток. | |||
Как показано в таблице 9, в случае человеческого гормона роста конъюгирование с 40-кДа ПЭГ (чГР-40К ПЭГ) также приводило к снижению активности примерно до 7,6% по отношению к активности нативной формы, а конъюгат чГР-ПЭГ-альбумин обнаруживал низкую in vitro активность, которая составляла примерно 5,2% от активности нативного чГР. Однако конъюгат чГР-ПЭГ-Fc настоящего изобретения обнаруживал увеличение относительной активности до более чем 28% по отношению к активности нативного чГР. Исходя из этих результатов, имеются все основания предполагать, что человеческий гормон роста, конъюгированный с Fc-фрагментом иммуноглобулина, имеет значительно более длительное время полужизни в сыворотке и обладает значительно более высокой фармацевтической эффективностью in vivo. Кроме того, очевидно, что повышенная активность белковых конъюгатов Fc иммуноглобулина по настоящему изобретению обусловлена увеличением их стабильности в сыворотке и сохранением аффинности связывания с рецепторами благодаря присутствию Fc иммуноглобулина или наличию пространства, образованного не-пептидным полимером. Поэтому можно предположить, что такими эффектами также обладают белковые конъюгаты Fc-фрагмента иммуноглобулина, связанного с другими физиологически активными белками.
<4-3> Сравнение внутриклеточных активностей конъюгатов белка ГКСФ
Для сравнения внутриклеточных активностей белковых конъюгатов с производным ГКСФ проводили сравнение внутриклеточной активности нативного ГКСФ (Filgrastim, Jell Pharm. Co., Ltd.), 17Ser-ГКСФ-производного, 20К ПЭГ-ГКСФ (Neulasta), 40К ПЭГ-17Ser-ГКСФ, 17Ser-ГКСФ-ПЭГ-альбумин и 17S-ГКСФ-ПЭГ-Fc.
Сначала человеческую миелоидную клеточную линию HL-60 (АТСС CCL-240, пациентка с промиелоцитарным лейкозом/36-летняя женщина индоевропейской расы) культивировали в среде RPMI 1640, в которую было добавлено 10% FBS. Культивированные клетки суспендировали при плотности примерно 2,2 × 105 клеток/мл и добавляли ДМСО (диметилсульфоксид со степенью чистоты, пригодной для культивирования, Sigma) при конечной концентрации 1,25% (об./об.). Затем 90 мкл клеточной суспензии высевали в каждую лунку 96-луночного планшета (Corning/96-луночный планшет с выпариванием при низкой температуре), после чего планшет оставляли до достижения плотности примерно 2 × 104 клеток на лунку и культивировали в инкубаторе при 37°С в атмосфере 5% СО2 в течение примерно 72 часов.
Каждый образец, в котором концентрация белка была определена с использованием набора для ELISA ГКСФ (R&D systems), разводили средой RPMI 1640 до идентичной концентрация 10 мкг/мл, а затем проводили двукратное разведение средой RPMI девятнадцать раз. Эти серийные двукратные разведения отдельно добавляли в каждую лунку, содержащую клетки HL-60 в объеме 10 мкл, так, чтобы концентрация каждого образца изначально составляла 1 мкг/мл. Затем клетки культивировали в инкубаторе при 37°С в течение 72 часов.
Пролиферацию клеток HL-60 анализировали с использованием реагента 96 для определения клеточного титра (Cell Titer 96TM (Cat. NO G4100, Promega), и увеличивающееся число клеток определяли путем измерения оптической плотности при 670 нМ.
| Таблица 10 | ||
| ED50 (МЕ/мг) | Относительная активность (%) для нативного ГКСФ | |
| Нативный ГКСФ | 0,30 | 100 |
| 17Ser-ГКСФ | 0,26 | 115 |
| ГКСФ-20К ПЭГ (Neulasta) | 1,20 | 25 |
| 17Ser-ГКСФ-40К ПЭГ | 10,0 | <10,0 |
| 17Ser-ГКСФ-ПЭГ-альбумин | 1,30 | 23,0 |
| 17Ser-ГКСФ-ПЭГ-Fc | 0,58 | 51,7 |
Как показано в таблице 10, белковые конъюгаты Fc имммуноглобулина и производного ГКСФ, имеющие аминокислотную замену, 17Ser-ГКСФ, также обнаруживали такие же эффекты, как и нативные белковые ГКСФ-конъюгаты. Ранее уже сообщалось, что 17Ser-ГКСФ-ПЭГ имел относительно более длительное время полужизни в сыворотке, но более низкую активность по сравнению с не-ПЭГилированным 17Ser-ГКСФ (публикация выложенной корейской патентной заявки № 2004-82268). Более конкретно, по мере увеличения размера ПЭГ-части стабильность белкового конъюгата в сыворотке увеличивалась, а его активность постепенно снижалась. 17Ser-ГКСФ-40К ПЭГ обнаруживал очень низкую активность, которая составляла примерно менее 10% от активности нативной формы. Таким образом, поскольку при увеличении молекулярной массы ПЭГ-части время полужизни белкового конъюгата в сыворотке увеличивается, а его биологическая активность резко снижается, то необходимо получить такой белковый конъюгат, который имел бы более длительное время полужизни в сыворотке и более высокую активность. Конъюгат 17Ser-ГКСФ-ПЭГ-альбумин также обнаруживал слабую активность, которая составляла примерно 23% от активности нативного ГКСФ. В противоположность этому, конъюгат 17Ser-ГКСФ-ПЭГ-Fc обладал значительно более высокой относительной активностью, которая составляла более чем 51% от активности нативного ГКСФ. Исходя из этих результатов, имеются все основания предполагать, что 17Ser-ГКСФ, конъюгированный с Fc-фрагментом иммуноглобулина, имеет значительно более длительное время полужизни в сыворотке и обладает значительно более высокой фармацевтической эффективностью in vivo.
<4-4> Анализ на нейтрализацию цитотоксичности Fab'-конъюгатов
Анализ на активность in vitro проводили с использованием конъюгатов Fab'-S-ПЭГ-N-Fc и Fab'-N-ПЭГ-N-Fc, полученных, как описано в примерах 8 и 9, и комплекса Fab'-S-40К ПЭГ, полученного, как описано в сравнительном примере 3. В процессе анализа на цитотоксичность, проводимого путем измерения TNFα-опосредованной цитотоксичности, оценивали Fab'- конъюгаты для того, чтобы определить, нейтрализуют ли указанные конъюгаты TNFα-индуцированный апоптоз в клеточной линии мышиных фибробластов, L929 (АТСС CRL-2148).
Конъюгаты Fab'-S-ПЭГ-N-Fc и Fab'-N-ПЭГ-N-Fc и комплекс Fab'-S-40К ПЭГ подвергали серийному двукратному разведению и в лунки 96-луночного планшета добавляли 100 мкл-аликвоты. rhTNF-α (R&D Systems) и актиномицин D (Sigma), используемый в качестве ингибитора синтеза РНК при конечных концентрациях 10 нг/мл и 1 мкг/мл соответственно, добавляли в каждую лунку, а затем инкубировали в течение 30 минут в инкубаторе при 37°С в 5% СО2 и переносили в микропланшет для анализа. В каждую лунку добавляли клетки L929 при плотности 5 × 104 клеток/50 мкл среды и культивировали в течение 24 часов в инкубаторе при 37°С в 5% СО2. После удаления культуральной среды в каждую лунку добавляли 50 мкл МТТ (Sigma), растворенного в PBS при концентрации 5 мг/мл, и клетки культивировали примерно в течение 4 часов в инкубаторе при 37°С в 5% СО2. Затем в каждую лунку добавляли 150 мкл ДМСО и определяли степень нейтрализации цитотоксичности путем измерения оптической плотности при 540 нм. В качестве контроля использовали Fab', очищенный в стадии 1 примера 8.
Как показано на фиг.13, все белковые конъюгаты, используемые в этом тесте, имели такой же титр, как и Fab'. Эти результаты показали, что если белковый конъюгат получали путем присоединения Fc иммуноглобулина к свободному цистеиновому остатку у N-конца или у С-конца Fab' посредством ПЭГ, то Fab' имел значительно более длительное время полужизни в сыворотке и обладал высокой активностью in vivo.
<4-5> Анализ на комплемент-зависимую цитотоксичность (CDC)
Для того, чтобы определить, связываются ли производные, полученные, как описано в примерах, и белки, соответствующие константным областям иммуноглобулинов, которые были экспрессированы в трансформантах E.coli или очищены, с человеческим C1q, проводили твердофазный иммуноферментный анализ (ELISA) в соответствии с нижеописанной процедурой. В качестве тест-групп были использованы константные области иммуноглобулина, полученные с использованием трансформантов НМ10932 и НМ10927 и депонированные в Корейском центре культур микроорганизмов (КССМ) 15 сентября 2004 под регистрационными номерами КССМ-10597 и КССМ-10598, и производные, полученные, как описано в предыдущих примерах. В качестве стандартов были использованы гликозилированный иммуноглобулин (IVIG-глобулин S, Green Cross PBM) и несколько коммерчески доступных антител, применяемых в качестве терапевтических антител. Тестируемые и стандартные образцы приготавливали в 10 мМ карбонатного буфера (рН 9,6) при концентрации 1 мкг/мл. Образцы разделяли на аликвоты и вносили в 96-луночный планшет (Nunc) в количестве 200 нг на лунку и планшет оставляли на ночь при 4°С для сенсибилизации. Затем каждую лунку три раза промывали PBS-T (137 мМ NaCl, 2 мМ KCl, 10 мМ Na2HPO4, 2 мМ КН2РО4, 0,05% твина-20), блокировали 250 мкл блокирующего буфера (1% альбумина бычьей сыворотки в PBS-T) при комнатной температуре в течение ночи, после чего снова три раза промывали тем же самым PBS-T. Стандартные и тестируемые образцы разводили PBS-T до предварительно определенной концентрации и добавляли в сенсибилизированные антителами лунки и планшет инкубировали при комнатной температуре в течение 1 часа, а затем три раза промывали PBS-T. После этого в планшет добавляли 2 мкг/мл Clq (R&D Systems) и этот планшет оставляли для реакции на 2 часа при комнатной температуре, а затем шесть раз промывали PBS-T. Затем в каждую лунку добавляли 200 мкл, при 1:1000-разведении, конъюгата "человеческая пероксидаза-антитело против человеческого Clq" (Biogenesis, USA) в блокирующем буфере и оставляли для реакции на 1 час при комнатной температуре. После трехкратной промывки каждой лунки PBS-T равные объемы окрашивающих реагентов А и В смешивали (окрашивающий реагент А: стабилизированная пероксидаза; и окрашивающий реагент В: стабилизированный хромоген; DY 999, R&D Systems), а затем в каждую лунку добавляли 200 мкл смеси и смесь инкубировали в течение 30 минут. После этого в каждую лунку добавляли 50 мкл раствора 2М серной кислоты для завершения реакции. Планшет считывали с использованием микропланшет-ридера (Molecular Device). Оптическую плотность стандартных и тестируемых образцов измеряли при 450 нм, и полученные результаты были систематизированы на фиг.14 и 15 соответственно.
При сравнивании подклассов иммуноглобулина на предмет активности их Fc-фрагментов по отношению к комплементу самая высокая аффинность связывания с C1q наблюдалась для человеческого иммуноглобулина IgG1 (Fitzgerald), более низкая - в IgG2 (Fitzgerald), а еще более низкая - в IgG4 (Fitzgerald), что указывало на различие в активностях этих подклассов по отношению к комплементу. IVIG, используемый в этом тесте и представляющий собой пул подклассов IgG, обладал почти такой же аффинностью связывания с C1q, как и очищенный IgG1, поскольку IVIG, в основном, состоит из IgG1. По сравнению с этими стандартами, с точки зрения изменения аффинности связывания с C1q при агликозилировании, активность Fc IgG1, обладающего наиболее сильной активностью по отношению к комплементу, заметно снижалась. Fc IgG4, который, как известно, не индуцирует активацию комплемента, в очень редких случаях обладал аффинностью связывания с C1q, что указывает на то, что Fc IgG4 может быть использован как превосходный рекомбинантный носитель, не обладающий активностью по отношению к комплементу (фиг.14).
Для того, чтобы определить, сохраняет ли данный носитель присущее ему отсутствие аффинности связывания с C1q даже после его конъюгирования с физиологически активным пептидом, были получены конъюгаты IFN-альфа-Fc с использованием гликозилированного Fc, ферментативно дегликозилированного Fc и агликозилированного рекомбинантного Fc в качестве носителей для IFN-альфа, и эти конъюгаты оценивали на их аффинность связывания с C1q. Гликозилированный конъюгат IFN-альфа с присоединенным к нему Fc (IFNα-ПЭГ-Fc: гликозилированный IgG1Fc) сохранял высокую аффинность связывания с C1q. В противоположность этому, если интерферон-альфа присоединен к Fc, который был дегликозилирован с использованием PNGазы F и других ферментов, то полученный конъюгат (IFNα-ПЭГ-DGFc: дегликозилированный IgG1Fc) обнаруживал значительно более низкую аффинность связывания с C1q, которая была аналогична аффинности происходящего от E.coli конъюгата агликозилированного Fc. Кроме того, в случае, когда IgG1-часть конъюгата агликозилированного IgG1 с Fc, присоединенным к интерферону-альфа (IFNα-ПЭГ-AGFcG1: агликозилированный IgG1Fc), заменяли на IgC4-часть, то полученный конъюгат интерферона (IFNα-ПЭГ-FcG4, производное 1: агликозилированный IgG4Fc) обнаруживал полную потерю своей аффиности связывания с C1q. Если IgGl-Fc-часть заменяли на мономер Fc IgG4, то полученный конъюгат (IFNa-ПЭГ-FcG4, производное 2: агликозилированный IgG4Fc) также обнаруживал полную потерю своей аффинности связывания с C1q. Эти результаты показали, что такие формы Fc-фрагмента IgG4 могут быть использованы в качестве превосходных носителей, у которых отсутствуют эффекторные функции, присущие фрагментам антител (фиг.15).
Экспериментальный пример 5: Измерение относительной активности ЕРО-ПЭГ-Fc
<5-1> Измерение относительной активности BRP-EPO относительно ЕРО-ПЭГ-Fc
Биологическую активность конъюгата ЕРО-ПЭГ-Fc измеряли способом, описанным в европейской фармакопеи (ЕР). Мышам с моделью гипоксии, BDF-1, вводили ЕРО-ПЭГ-Fc в 3 различных концентрациях, а затем измеряли повышение количества ретикулоцитов в крови для оценки относительной активности ЕРО-ПЭГ-Fc относительно BRP-EPO.
Биологическая активность конъюгата ЕРО-ПЭГ-Fc составила 6580000 Ед/мг по концентрации ЕРО. Также биологическая активность составляла 248000 Ед/мг по концентрации всего белка. Таким образом, биологическая активность ЕРО-ПЭГ-Fc была значительно выше, чем активность ЕРО (>100000 Ед/мг).
<5-2>Тест PD in vivo
Измеряли изменение концентрации ретикулоцитов после однократного введения конъюгата ЕРО-ПЭГ-Fc крысам SD. Крысам RD вводили одинаковое количество природного ЕРО (Recormon, Roche) и в качестве контроля высокогликозилированный ЕРО (Aranesp, Amgen) соответственно и вводили ЕРО-ПЭГ-Fc в том же количестве, что нативный ЕРО и высокогликозилированный ЕРО, и 1/10 указанного количества ЕРО-ПЭГ-Fc. Результаты показаны на фиг.16.
В результате у группы, которой вводили ЕРО-ПЭГ-Fc в количестве 1/10 нативного ЕРО и высокогликозилированный ЕРО, отмечали сходное повышение концентрации ретикулоцитов с концентрацией группы, которой вводили природный ЕРО и высокогликозилированный ЕРО. Кроме того, у группы, которой вводили ЕРО-ПЭГ-Fc в том же количестве, что и природный ЕРО и высокогликозилированный ЕРО, отмечали аналогичное повышение концентрации ретикулоцитов, но время возращения к нормальной концетрации ретикулоцитов было в 10 раз длиннее, чем у природного ЕРО и высокогликозилированного ЕРО. Следовательно, эти результаты указывают, что ЕРО-ПЭГ-Fc в 10 раз сильнее, чем природный ЕРО и высокогликозилированный ЕРО.
Экспериментальный пример 6: Тест на повышение массы
Измеряли биологическую активность конъюгата hGH-ПЭГ-Fc. Крысам с удаленным гипофизом вводили природный hGH-ПЭГ-Fc и затем измеряли повышение веса.
Конкретно, ежедневно вводили 300 мкг/кг rhGH в течение 12 суток (общее введенное количество: 3600 мкг/кг) в качестве контроля. Также вводили 600 мкг/кг hGH-ПЭГ-Fс два раза в течение 12 суток (общее введенное количество: 1200 мкг/кг) и 300 мкг/кг hGH-ПЭГ-Fc четыре раза в течение 12 суток (общее введенное количество: 1200 мкг/кг). Результаты показаны на фиг.17.
В результате в группе, которой вводили hGH-PEG-Fc в количестве 1/3 природного hGH 1 раз в течение 6 дней, отмечали сходное изменение веса, как в группе, которой вводили природный hGH. Кроме того, у группы, которой вводили hGH-PEG-Fc в количестве 1/3 природного hGH 2 раза в течение 6 дней, отмечали большее повышение массы, чем в группе, получавшей природный hGH. Следовательно, эти результаты указывают, что биологическая активность hGH-PEG-Fc в 6-раз выше активности природного.
Экспериментальный пример 7: Конъюгат IFN альфа-2а (НМ10660А) с повышенной продолжительностью действия
В этом эксперименте измеряли in vivo активность конъюгата IFN альфа-2а (IFN-PEG-Fc) с повышенной продолжительностью действия. Клетки SK-OV-3 (раковые клетки яичника человека) трансплантировали мышам nude. Мышам nude вводили 30 мкг/кг нативного IFN альфа-2а, 5 дней/неделя в течение 4 недель. Другим мышам nude вводили 30 или 150 мкг/кг IFN-PEG-Fc (НМ10660А) один раз в неделю в течение 4 недель. Измеряли способность ингибировать рост раковых клеток.
Как показано на фиг.18, активность конъюгата IFN-PEG-Fc по настоящему изобретению выше физиологической активности природного IFN.
Экспериментальный пример 8: Конъюгат G-CSF (HM10460A) с повышенной продолжительностью действия
В этом эксперименте измеряли in vivo активность конъюгата G-CSF (G-CSF-PEG-Fc) с повышенной продолжительностью действия. Модель нейтропении получали путем введения противоопухолевого средства СРА у мышей CD-1. Через 2 дня после введения СРА мышам с моделью нейтропении однократно вводили 200 мкг/кг G-CSF-PEG-Fc (НМ10460А). В сравнительном эксперименте другим мышам с моделью нейтропении вводили 50 мкг/кг/день филграстим (природный G-CSF) в течение 4 последовательных дней. Затем измеряли повышение ANC в каждой группе.
Как показано на фиг.19, конъюгат G-CSF-PEG-Fc по настоящему изобретению имел гораздо большую активность по сравнению с физиологической активностью природного G-CSF.
Промышленное применение
Как описано выше, белковый конъюгат по настоящему изобретению значительно увеличивает время полужизни в плазме полипептидных лекарственных средств до уровней, превышающих время полужизни любых стандартных модифицированных белков. С другой стороны, использование белковых конъюгатов позволяет устранить большинство значительных недостатков, присущих стандартным композициям пролонгированного действия, путем снижения титров лекарственных средств и, тем самым, увеличения их времени пребывания в кровотоке и увеличения in vivo активности этих белковых конъюгатов по сравнению с альбумином, который, как ранее считалось, является наиболее эффективным. Кроме того, при использовании белковых конъюгатов риск индуцирования иммунных ответов отсутствует. Благодаря этим преимуществам указанные белковые конъюгат могут быть использованы для изготовления белковых лекарственных препаратов пролонгированного действия. В соответствии с настоящим изобретением белковые лекарственные препараты пролонгированного действия способны ослаблять боли у пациентов, возникающих при частых инъекциях, а также поддерживать соответствующие концентрации активных полипептидов в сыворотке в течение длительного периода времени и, тем самым, обеспечивать стабильную фармацевтическую эффективность.
Кроме того, описанный способ получения белковых конъюгатов позволяет решить проблемы, связанные с продуцированием гибридных белков путем генетических манипуляций, включая трудности, связанные с получением экспрессионных систем и гликозилированием в различных нативных формах; с риском индуцирования иммунного ответа; с ограниченной ориентацией белкового гибрида и с низкими выходами, обусловленными неспецифическими реакциями, а также проблемы, связанные с химическим синтезом, такие как токсичность химических соединений, используемых в качестве связующих агентов, а поэтому указанный способ получения белковых лекарственных средств с более длительным временем полужизни в сыворотке и с высокой активностью является экономически выгодным.
Claims (11)
1. Способ увеличения продолжительности действия физиологически активного полипептида in vivo, отличающийся тем, что физиологически активный полипептид конъюгируют с Fc-фрагментом иммуноглобулина посредством PEG.
2. Способ по п.1, где указанный Fc-фрагмент иммуноглобулина является агликозилированным.
3. Способ по п.1, где указанный Fc-фрагмент иммуноглобулина состоит из 1-4 доменов, выбранных из группы, состоящей из доменов СH1, СH2, СH3 и СH4.
4. Способ по п.3, где указанный Fc-фрагмент иммуноглобулина дополнительно содержит шарнирную область.
5. Способ по п.1, где указанный Fc-фрагмент иммуноглобулина выбран из группы, состоящей из Fc-фрагментов IgG, IgA, IgD, IgE, IgM, их комбинаций и гибридов.
6. Способ по п.5, где указанный Fc-фрагмент иммуноглобулина выбран из группы, состоящей из Fc-фрагментов IgGI, IgG2, IgG3, IgG4, их комбинаций и гибридов.
7. Способ по п.6, где указанным Fc-фрагментом иммуноглобулина является Fc-фрагмент IgG4.
8. Способ по п.7, где указанным Fc-фрагментом иммуноглобулина является Fc-фрагмент агликозилированного IgG4 человека.
9. Способ по п.1, где указанный физиологически активный полипептид выбран из группы, состоящей из гормонов, цитокинов, ферментов, антител, факторов роста, факторов регуляции транскрипции, факторов свертывания крови, из вирусных вакцинных антигенов, структурных белков, белков-лигандов и рецепторов.
10. Способ по п.9, где указанный физиологически активный полипептид выбран из группы, состоящей из гормона роста человека, рилизинг-фактора гормона роста, пептида, высвобождающего гормон роста, интерферонов, рецепторов интерферона, колониестимулирующих факторов, глюкагоноподобных пептидов, рецептора, связанного с G-белком, интерлейкинов, рецепторов интерлейкинов, ферментов, интерлейкинсвязывающих белков, цитокинсвязывающих белков, фактора активации макрофагов, пептида макрофага, В-клеточного фактора, Т-клеточного фактора, белка А, ингибитора аллергии, гликопротеинов некроза клеток, иммунотоксина, лимфотоксина, фактора некроза опухоли, супрессоров опухолей, метастатического фактора роста, антитрипсина альфа-1, альбумина, альфа-лактальбумина, аполипопротеина-Е, эритропоэтина, высокогликозилированного эритропоэтина, ангиопоэтинов, гемоглобина, тромбина, пептида, активирующего рецептор тромбина, тромбомодулина, фактора VII, фактора VIIa, фактора VIII, фактора IX, фактора XIII, фактора активации плазминогена, фибринсвязывающего пептида, урокиназы, стрептокиназы, гирудина, белка С, С-реактивного белка, ингибитора ренина, ингибитора коллагеназы, супероксиддисмутазы, лептина, тромбоцитарного фактора роста, эпителиального фактора роста, эпидермального фактора роста, ангиостатина, ангиотензина, фактора роста костей, белка, стимулирующего рост костей, кальцитонина, инсулина, атриопептина, фактора, индуцирующего образование хряща, элкатонина, фактора активации соединительной ткани, ингибитора пути тканевого фактора, фолликуло-стимулирующего гормона, лютеинизирующего гормона, рилизинг-фактора лютеинизирующего гормона, факторов роста нервной ткани, паратиреоидного гормона, релаксина, секретина, соматомедина, инсулиноподобного фактора роста, адренокортикоидного гормона, глюкагона, холецистокинина, панкреатического полипептида, пептида, высвобождающего гастрин, рилизинг-фактора кортикотропина, тиреоидстимулирующего гормона, аутотаксина, лактоферрина, миостатина, рецепторов, антагонистов рецепторов, антигенов клеточной поверхности, вирусных вакцинных антигенов, моноклональных антител, поликлональных антител и фрагментов антител.
11. Способ по п.10, где указанный физиологически активный полипептид выбран из группы, состоящей из гормона роста человека, колониестимулирующего фактора, интерферона-альфа, эритропоэтина человека и Fab'-фрагмента антитела.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20030080299 | 2003-11-13 | ||
| KR10-2003-0080299 | 2003-11-13 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005120239A RU2005120239A (ru) | 2006-04-20 |
| RU2352583C2 true RU2352583C2 (ru) | 2009-04-20 |
Family
ID=36589418
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005120239/13A RU2352583C2 (ru) | 2003-11-13 | 2004-11-13 | ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ Fc-ОБЛАСТЬ ИММУНОГЛОБУЛИНА В КАЧЕСТВЕ НОСИТЕЛЯ |
| RU2005120240/13A RU2356909C2 (ru) | 2003-11-13 | 2004-11-13 | Белковый комплекс, полученный с использованием фрагмента иммуноглобулина, и способ получения такого комплекса |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005120240/13A RU2356909C2 (ru) | 2003-11-13 | 2004-11-13 | Белковый комплекс, полученный с использованием фрагмента иммуноглобулина, и способ получения такого комплекса |
Country Status (17)
| Country | Link |
|---|---|
| US (13) | US8846874B2 (ru) |
| EP (6) | EP1682584B1 (ru) |
| JP (7) | JP2007531513A (ru) |
| KR (5) | KR100775343B1 (ru) |
| CN (4) | CN1723219B (ru) |
| AT (3) | ATE555133T1 (ru) |
| AU (2) | AU2004282984B2 (ru) |
| BR (2) | BRPI0406605B8 (ru) |
| CA (2) | CA2512657C (ru) |
| DK (3) | DK1682583T3 (ru) |
| ES (6) | ES2426169T3 (ru) |
| HK (2) | HK1149570A1 (ru) |
| MX (2) | MXPA05007210A (ru) |
| PL (2) | PL2239273T3 (ru) |
| PT (3) | PT2256134E (ru) |
| RU (2) | RU2352583C2 (ru) |
| WO (4) | WO2005047334A1 (ru) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2483081C2 (ru) * | 2008-07-23 | 2013-05-27 | Ханми Сайенс Ко.,Лтд.,Kr | Полипептидный комплекс, содержащий непептидильный полимер, обладающий тремя функциональными концами |
| RU2503688C2 (ru) * | 2009-04-22 | 2014-01-10 | Алтеоген, Инк | Слитый белок или пептид с увеличенным временем полужизни in vivo, поддерживаемый за счет замедленного высвобождения in vivo, и способ увеличения времени полужизни in vivo с его применением |
| RU2589697C2 (ru) * | 2009-12-18 | 2016-07-10 | Экзодос Лайф Сайенсиз Лимитед Партнершип | Способы получения стабильных жидких лекарственных препаратов и их композиции |
| US9862779B2 (en) | 2012-09-14 | 2018-01-09 | Hoffmann-La Roche Inc. | Method for the production and selection of molecules comprising at least two different entities and uses thereof |
| US10106612B2 (en) | 2012-06-27 | 2018-10-23 | Hoffmann-La Roche Inc. | Method for selection and production of tailor-made highly selective and multi-specific targeting entities containing at least two different binding entities and uses thereof |
| RU2711485C2 (ru) * | 2014-04-11 | 2020-01-17 | МЕДИММЬЮН, ЭлЭлСи | Конъюгированные соединения, содержащие сконструированные с цистеином антитела |
| RU2766200C1 (ru) * | 2015-10-01 | 2022-02-09 | Хит Байолоджикс, Инк. | Композиции и способы для соединения внеклеточных доменов типа i и типа ii в качестве гетерологичных химерных белков |
| US11421022B2 (en) | 2012-06-27 | 2022-08-23 | Hoffmann-La Roche Inc. | Method for making antibody Fc-region conjugates comprising at least one binding entity that specifically binds to a target and uses thereof |
| US11618790B2 (en) | 2010-12-23 | 2023-04-04 | Hoffmann-La Roche Inc. | Polypeptide-polynucleotide-complex and its use in targeted effector moiety delivery |
| RU2805873C2 (ru) * | 2019-07-18 | 2023-10-24 | Ханми Фарм. Ко., Лтд. | Новый способ получения длительно действующего конъюгата лекарственного средства посредством получения промежуточного соединения |
Families Citing this family (253)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7157555B1 (en) * | 1997-08-08 | 2007-01-02 | Amylin Pharmaceuticals, Inc. | Exendin agonist compounds |
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| US7829084B2 (en) * | 2001-01-17 | 2010-11-09 | Trubion Pharmaceuticals, Inc. | Binding constructs and methods for use thereof |
| SI1581649T1 (sl) | 2002-12-20 | 2011-09-30 | Amgen Inc | Vezna sredstva, ki zavirajo miostatin |
| ES2333598T5 (es) | 2003-05-06 | 2013-09-04 | Biogen Idec Hemophilia Inc | Proteinas quimericas del factor de coagulacion fc para tratar la hemofilia. |
| TWI353991B (en) | 2003-05-06 | 2011-12-11 | Syntonix Pharmaceuticals Inc | Immunoglobulin chimeric monomer-dimer hybrids |
| US7850970B2 (en) | 2003-08-26 | 2010-12-14 | The Regents Of The University Of Colorado | Inhibitors of serine protease activity and their use in methods and compositions for treatment of bacterial infections |
| US8263084B2 (en) * | 2003-11-13 | 2012-09-11 | Hanmi Science Co., Ltd | Pharmaceutical composition for treating obesity-related disease comprising insulinotropic peptide conjugate |
| KR101135244B1 (ko) * | 2007-11-29 | 2012-04-24 | 한미사이언스 주식회사 | 인슐린 분비 펩타이드 결합체를 포함하는 비만 관련질환 치료용 조성물 |
| WO2005047334A1 (en) * | 2003-11-13 | 2005-05-26 | Hanmi Pharmaceutical. Co., Ltd. | Igg fc fragment for a drug carrier and method for the preparation thereof |
| US8110665B2 (en) | 2003-11-13 | 2012-02-07 | Hanmi Holdings Co., Ltd. | Pharmaceutical composition comprising an immunoglobulin FC region as a carrier |
| EP1759001B1 (en) | 2004-04-21 | 2011-04-13 | Enobia Pharma Inc. | Bone delivery conjugates and method of using same to target proteins to bone |
| US20070081984A1 (en) | 2005-10-11 | 2007-04-12 | Shunji Tomatsu | Compositions and methods for treating hypophosphatasia |
| US8143380B2 (en) * | 2004-07-08 | 2012-03-27 | Amgen Inc. | Therapeutic peptides |
| KR100594607B1 (ko) * | 2004-11-03 | 2006-06-30 | 재단법인서울대학교산학협력재단 | 신규한 경구투여용 재조합 인간 성장호르몬 분비미생물제제 및 그 제조방법 |
| US20090087478A1 (en) * | 2004-12-27 | 2009-04-02 | Progenics Pharmaceuticals (Nevada), Inc. | Orally Deliverable and Anti-Toxin Antibodies and Methods for Making and Using Them |
| CA2597346A1 (en) * | 2005-02-14 | 2006-08-17 | Apollo Life Sciences Limited | A molecule and chimeric molecules thereof |
| KR100754667B1 (ko) * | 2005-04-08 | 2007-09-03 | 한미약품 주식회사 | 비펩타이드성 중합체로 개질된 면역글로불린 Fc 단편 및이를 포함하는 약제학적 조성물 |
| US7833979B2 (en) | 2005-04-22 | 2010-11-16 | Amgen Inc. | Toxin peptide therapeutic agents |
| SI1912675T1 (sl) * | 2005-07-25 | 2014-07-31 | Emergent Product Development Seattle, Llc | zmanjšanje števila celic B z uporabo molekul, ki se specifično vežejo na CD37 in CD20 |
| US8008453B2 (en) * | 2005-08-12 | 2011-08-30 | Amgen Inc. | Modified Fc molecules |
| KR100824505B1 (ko) * | 2005-08-16 | 2008-04-22 | 한미약품 주식회사 | 개시 메티오닌 잔기가 제거된 면역글로불린 Fc 영역의대량 생산방법 |
| EP1928910B1 (en) * | 2005-08-16 | 2014-01-15 | Hanmi Science Co., Ltd. | A method for the mass production of immunoglobulin fc region with deleted initial methionine residues |
| CN101534865A (zh) * | 2005-10-19 | 2009-09-16 | Ibc药品公司 | 生物活性装配体的制备方法及其用途 |
| JP2009512443A (ja) * | 2005-10-20 | 2009-03-26 | ザ スクリップス リサーチ インスチチュート | 免疫染色及び免疫標的化のためのFc標識化 |
| AR056142A1 (es) * | 2005-10-21 | 2007-09-19 | Amgen Inc | Metodos para generar el anticuerpo igg monovalente |
| US8067562B2 (en) | 2005-11-01 | 2011-11-29 | Amgen Inc. | Isolated nucleic acid molecule comprising the amino acid sequence of SEQ ID NO:1 |
| WO2007059782A1 (en) | 2005-11-28 | 2007-05-31 | Genmab A/S | Recombinant monovalent antibodies and methods for production thereof |
| US20070149458A1 (en) * | 2005-12-06 | 2007-06-28 | Amgen Inc. | Uses of myostatin antagonists |
| CN101002945B (zh) | 2006-01-20 | 2012-09-05 | 清华大学 | 一种用于肿瘤治疗的新型复合物 |
| CN100475270C (zh) | 2006-01-20 | 2009-04-08 | 清华大学 | 一种治疗肿瘤的药物及其应用 |
| CA2654317A1 (en) * | 2006-06-12 | 2007-12-21 | Trubion Pharmaceuticals, Inc. | Single-chain multivalent binding proteins with effector function |
| PL2061803T5 (pl) | 2006-08-28 | 2023-03-27 | Ares Trading S.A. | Proces oczyszczania białek zawierających fc |
| US20140147441A1 (en) * | 2006-09-12 | 2014-05-29 | The General Hospital Corporation | Compositions containing alpha-1-antitrypsin and methods for use |
| US7820623B2 (en) | 2006-10-25 | 2010-10-26 | Amgen Inc. | Conjugated toxin peptide therapeutic agents |
| US20080181903A1 (en) * | 2006-12-21 | 2008-07-31 | Pdl Biopharma, Inc. | Conjugate of natriuretic peptide and antibody constant region |
| JP2008169195A (ja) | 2007-01-05 | 2008-07-24 | Hanmi Pharmaceutical Co Ltd | キャリア物質を用いたインスリン分泌ペプチド薬物結合体 |
| CN101219219B (zh) * | 2007-01-10 | 2013-02-13 | 北京普罗吉生物科技发展有限公司 | 包含血管抑素或其片段的复合物、其制备方法及应用 |
| US20080238882A1 (en) * | 2007-02-21 | 2008-10-02 | Ramesh Sivarajan | Symmetric touch screen system with carbon nanotube-based transparent conductive electrode pairs |
| US8501678B2 (en) | 2007-03-06 | 2013-08-06 | Atara Biotherapeutics, Inc. | Variant activin receptor polypeptides and uses thereof |
| TWI454479B (zh) | 2007-03-06 | 2014-10-01 | Amgen Inc | 變異之活動素受體多肽及其用途 |
| CA2687141C (en) | 2007-05-22 | 2014-04-01 | Amgen Inc. | Compositions and methods for producing bioactive fusion proteins |
| EP3173484B1 (en) * | 2007-05-30 | 2018-09-26 | Postech Academy-Industry- Foundation | Immunoglobulin fusion proteins |
| AU2008255350B2 (en) | 2007-05-31 | 2014-07-10 | Genmab A/S | Transgenic animals producing monovalent human antibodies and antibodies obtainable from these animals |
| CN101835802B (zh) | 2007-06-01 | 2014-04-09 | 马里兰大学巴尔的摩分校 | 免疫球蛋白恒定区Fc受体结合剂 |
| EP2162464A1 (en) * | 2007-06-06 | 2010-03-17 | Boehringer Ingelheim International GmbH | Natriuretic fusion proteins |
| AU2008266952A1 (en) * | 2007-06-12 | 2008-12-24 | Trubion Pharmaceuticals, Inc. | Anti-CD20 therapeutic compositions and methods |
| AU2008287195A1 (en) * | 2007-07-06 | 2009-02-19 | Emergent Product Development Seattle, Llc | Binding peptides having a C-terminally disposed specific binding domain |
| US8492347B2 (en) * | 2007-10-17 | 2013-07-23 | The Regents Of The University Of California | Peptide for induction of immune tolerance as treatment for systemic lupus erythematosus |
| EP2214700A4 (en) * | 2007-11-02 | 2012-08-22 | Janssen Biotech Inc | HALF-SYNTHETIC GLP-1 PEPTIDE FUSION CONSTRUCTS, METHOD AND USES |
| PT2132228E (pt) * | 2008-04-11 | 2011-10-11 | Emergent Product Dev Seattle | Imunoterapia de cd37 e sua combinação com um quimioterápico bifuncional |
| RU2457856C2 (ru) * | 2008-08-05 | 2012-08-10 | Виктор Владимирович Чалов | Композиция, обладающая противовирусным и антимикробным действием, для перорального применения |
| MX339137B (es) * | 2008-08-07 | 2016-05-13 | Ipsen Pharma Sas | Analogos de polipeptidos insulinotropicos dependientes de glucosa (gip) modificados en n terminal. |
| US9072703B2 (en) | 2008-08-07 | 2015-07-07 | Ipsen Pharma S.A.S. | Glucose-dependent insulinotropic polypeptide analogues |
| EP2987805A3 (en) * | 2008-08-07 | 2016-04-13 | Ipsen Pharma S.A.S. | Analogues of glucose-dependent insulinotropic polypeptide |
| WO2010033216A1 (en) * | 2008-09-19 | 2010-03-25 | Nektar Therapeutics | Polymer conjugates of nesiritide peptides |
| WO2010033240A2 (en) | 2008-09-19 | 2010-03-25 | Nektar Therapeutics | Carbohydrate-based drug delivery polymers and conjugates thereof |
| EP2344527A4 (en) * | 2008-10-31 | 2012-04-04 | Amgen Inc | MATERIALS AND METHODS FOR STEM CELL MOBILIZATION THROUGH A MULTIPLE PEGYLATED GRANULOCYTE COLONY STIMULATING FACTOR |
| LT2370463T (lt) | 2008-11-26 | 2016-12-12 | Amgen Inc. | Stabilizuotas aktivino iib receptoriaus variantas |
| WO2010065578A2 (en) * | 2008-12-04 | 2010-06-10 | Leukosight Inc. | POLYPEPTIDES COMPRISING Fc FRAGMENTS OF IMMUNOGLOBULIN G (IgG) AND METHODS OF USING THE SAME |
| US20100158893A1 (en) * | 2008-12-19 | 2010-06-24 | Baxter International Inc. | Systems and methods for obtaining immunoglobulin from blood |
| KR20100084996A (ko) * | 2009-01-19 | 2010-07-28 | 한미홀딩스 주식회사 | 면역글로불린 단편을 이용한 생리활성 단백질 또는 펩타이드의 생산 방법 |
| WO2010096394A2 (en) | 2009-02-17 | 2010-08-26 | Redwood Biosciences, Inc. | Aldehyde-tagged protein-based drug carriers and methods of use |
| CN102333872B (zh) | 2009-02-25 | 2014-07-09 | 默沙东公司 | 在糖工程化的酵母巴斯德毕赤酵母中对半乳糖同化途径的代谢工程化 |
| JP5739865B2 (ja) * | 2009-03-24 | 2015-06-24 | バイエル・ヘルスケア・エルエルシー | 第viii因子変異体および使用の方法 |
| US20120219538A1 (en) * | 2009-11-02 | 2012-08-30 | Therapeomic Ag | Stabilized protein formulations and use thereof |
| US8765432B2 (en) | 2009-12-18 | 2014-07-01 | Oligasis, Llc | Targeted drug phosphorylcholine polymer conjugates |
| CN107412737A (zh) * | 2010-01-19 | 2017-12-01 | 韩美科学株式会社 | 长效g‑csf缀合物的液体制剂 |
| US8829163B2 (en) * | 2010-01-19 | 2014-09-09 | Hanmi Science Co., Ltd | Liquid formulations for long-acting erythropoietin conjugate |
| WO2011093470A1 (ja) * | 2010-01-28 | 2011-08-04 | 協和発酵キリン株式会社 | Bone morphogenetic protein receptor 1B(BMPR1B)細胞外ドメイン又はその変異体を含む蛋白質を含有する骨疾患治療用医薬組成物 |
| US8715963B2 (en) | 2010-02-24 | 2014-05-06 | Merck Sharp & Dohme Corp. | Method for increasing N-glycosylation site occupancy on therapeutic glycoproteins produced in Pichia pastoris |
| CA2789738C (en) * | 2010-03-08 | 2021-03-09 | Ge Healthcare Bio-Sciences Ab | Immunoglobulin g fc region binding polypeptide |
| AR081066A1 (es) * | 2010-04-02 | 2012-06-06 | Hanmi Holdings Co Ltd | Conjugado de insulina donde se usa un fragmento de inmunoglobulina |
| AR080993A1 (es) * | 2010-04-02 | 2012-05-30 | Hanmi Holdings Co Ltd | Formulacion de accion prolongada de interferon beta donde se usa un fragmento de inmunoglobulina |
| US9981017B2 (en) | 2010-04-02 | 2018-05-29 | Hanmi Science Co., Ltd. | Insulin conjugate using an immunoglobulin fragment |
| AR081755A1 (es) * | 2010-04-02 | 2012-10-17 | Hanmi Holdings Co Ltd | Formulacion de accion prolongada de la hormona estimuladora de los foliculos donde se usa un fragmento de inmunoglobulina, metodo de preparacion y metodo para tratar a un sujeto que sufre un trastorno reproductivo |
| CA2797865A1 (en) | 2010-04-30 | 2011-11-03 | Alexion Pharma International Sarl | Methods, compositions, and kits for the treatment of matrix mineralization disorders |
| CA2800173C (en) | 2010-05-21 | 2019-05-14 | Ulrik Nielsen | Bi-specific fusion proteins |
| KR101330868B1 (ko) * | 2010-06-08 | 2013-11-18 | 한미사이언스 주식회사 | 면역글로불린 단편을 이용한 인슐린 유도체 약물 결합체 |
| KR20120002129A (ko) * | 2010-06-30 | 2012-01-05 | 한미홀딩스 주식회사 | 면역글로불린 단편을 이용한 제7인자(Factor Ⅶa)약물 결합체 |
| KR101337797B1 (ko) * | 2010-07-14 | 2013-12-06 | 한미사이언스 주식회사 | 지속형 인간 성장 호르몬 결합체 액상 제제 |
| KR101382593B1 (ko) * | 2010-07-21 | 2014-04-10 | 한미사이언스 주식회사 | 신규한 지속형 글루카곤 결합체 및 이를 포함하는 비만 예방 및 치료용 약학적 조성물 |
| AU2011282579B2 (en) | 2010-07-28 | 2014-10-23 | Gliknik Inc. | Fusion proteins of natural human protein fragments to create orderly multimerized immunoglobulin Fc compositions |
| KR101333958B1 (ko) * | 2010-10-20 | 2013-11-27 | 주식회사 한독 | 인간 인터루킨-1 수용체 길항제-하이브리드 Fc 융합단백질 |
| WO2012053828A2 (ko) * | 2010-10-20 | 2012-04-26 | 주식회사 한독약품 | 인간 인터루킨-1 수용체 길항제-하이브리드 Fc 융합단백질 |
| KR101303388B1 (ko) * | 2010-10-26 | 2013-09-03 | 한미사이언스 주식회사 | 지속형 인터페론 알파 결합체의 액상 제제 |
| EP2465536A1 (en) | 2010-12-14 | 2012-06-20 | CSL Behring AG | CD89 activation in therapy |
| CA2823066A1 (en) | 2010-12-27 | 2012-07-05 | Alexion Pharma International Sarl | Compositions comprising natriuretic peptides and methods of use thereof |
| JP6162606B2 (ja) | 2011-01-14 | 2017-07-12 | レッドウッド バイオサイエンス, インコーポレイテッド | アルデヒド−タグ付き免疫グロブリンポリペプチド及びその使用方法 |
| CN102309765B (zh) * | 2011-02-28 | 2013-10-16 | 北京韩美药品有限公司 | 包含免疫球蛋白Fc片段作为载体的长效抗凝多肽及其制备方法 |
| EP2694092B1 (en) | 2011-04-08 | 2017-01-04 | Amgen Inc. | Method of treating or ameliorating metabolic disorders using growth differentiation factor 15 (gdf-15) |
| UA113626C2 (xx) * | 2011-06-02 | 2017-02-27 | Композиція для лікування діабету, що містить кон'югат інсуліну тривалої дії та кон'югат інсулінотропного пептиду тривалої дії | |
| CN102807619B (zh) * | 2011-06-03 | 2016-08-03 | 北京韩美药品有限公司 | 含有免疫球蛋白Fc片段和粒细胞-巨噬细胞集落刺激因子的复合物及其药物组合物 |
| EP3434687B1 (en) | 2011-06-10 | 2021-03-10 | Hanmi Science Co., Ltd. | Novel oxyntomodulin derivatives and pharmaceutical composition for treating obesity comprising the same |
| CN109306015B (zh) * | 2011-06-17 | 2022-04-26 | 韩美科学株式会社 | 包括泌酸调节肽和免疫球蛋白片段的结合物以及其应用 |
| EP2723370A4 (en) * | 2011-06-24 | 2015-06-03 | Univ Colorado Regents | COMPOSITIONS, PROCESS AND USE OF ALPHA-1-ANTITRYPHIN FUSION MOLECULES |
| IL312872A (en) * | 2011-06-28 | 2024-07-01 | Inhibrx Inc | Methods for purifying fusion proteins containing serphin |
| US10400029B2 (en) | 2011-06-28 | 2019-09-03 | Inhibrx, Lp | Serpin fusion polypeptides and methods of use thereof |
| MX356433B (es) * | 2011-06-28 | 2018-05-29 | Inhibrx Lp | Polipéptidos de fusión con domino de proteína ácida del suero, y métodos de uso de los mismos. |
| WO2013036032A1 (en) | 2011-09-05 | 2013-03-14 | Hanmi Science Co., Ltd. | A pharmaceutical composition for treating cancer, comprising interferon alpha conjugate |
| UY34347A (es) | 2011-09-26 | 2013-04-30 | Novartis Ag | Proteínas de función dual para tratar trastornos metabólicos |
| JP6108630B2 (ja) * | 2011-10-06 | 2017-04-05 | ハンミ サイエンス カンパニー リミテッドHanmi Science Co.,Ltd. | 血液凝固因子VII及びVIIa誘導体、それらを含む結合体及び複合体、並びにそれらの使用 |
| JP6158090B2 (ja) * | 2011-10-31 | 2017-07-05 | ダニエル・ジェイ・カポン | 非ペプチドヒンジ部含有フレキシブル抗体様分子 |
| KR20130049671A (ko) * | 2011-11-04 | 2013-05-14 | 한미사이언스 주식회사 | 생리활성 폴리펩타이드 결합체 제조 방법 |
| AU2012364736A1 (en) | 2011-12-19 | 2014-07-24 | Amgen Inc. | Variant activin receptor polypeptides, alone or in combination with chemotherapy, and uses thereof |
| CN103172745A (zh) * | 2011-12-21 | 2013-06-26 | 北京韩美药品有限公司 | 包含免疫球蛋白Fc片段的长效人内皮抑素 |
| KR102041412B1 (ko) * | 2011-12-30 | 2019-11-11 | 한미사이언스 주식회사 | 면역글로불린 Fc 단편 유도체 |
| KR101895047B1 (ko) | 2011-12-30 | 2018-09-06 | 한미사이언스 주식회사 | 면역글로불린 단편을 이용한 위치 특이적 글루카곤 유사 펩타이드-2 약물 결합체 |
| CA2862979A1 (en) | 2012-01-09 | 2013-07-18 | The Scripps Research Institute | Humanized antibodies with ultralong cdr3s |
| US10774132B2 (en) | 2012-01-09 | 2020-09-15 | The Scripps Research Instittue | Ultralong complementarity determining regions and uses thereof |
| KR20140137347A (ko) | 2012-01-10 | 2014-12-02 | 더 리젠츠 오브 더 유니버시티 오브 콜로라도, 어 바디 코포레이트 | 알파-1 안티트립신 융합 분자용 조성물, 방법 및 용도 |
| WO2013113008A1 (en) | 2012-01-26 | 2013-08-01 | Amgen Inc. | Growth differentiation factor 15 (gdf-15) polypeptides |
| AR090281A1 (es) | 2012-03-08 | 2014-10-29 | Hanmi Science Co Ltd | Proceso mejorado para la preparacion de un complejo polipeptidico fisiologicamente activo |
| EP2636681A1 (en) | 2012-03-09 | 2013-09-11 | CSL Behring AG | Process for enriching IgA |
| EP2636684A1 (en) | 2012-03-09 | 2013-09-11 | CSL Behring AG | Prevention of infection |
| AU2013201393B2 (en) | 2012-03-09 | 2015-08-27 | Csl Behring Ag | Compositions |
| US10064951B2 (en) * | 2012-03-30 | 2018-09-04 | Hanmi Science Co., Ltd. | Liquid formulation of highly concentrated long-acting human growth hormone conjugate |
| US9809641B2 (en) * | 2012-04-23 | 2017-11-07 | Nrl Pharma, Inc. | Lactoferrin fusion protein and method for preparation thereof |
| US10052366B2 (en) | 2012-05-21 | 2018-08-21 | Alexion Pharmaceuticsl, Inc. | Compositions comprising alkaline phosphatase and/or natriuretic peptide and methods of use thereof |
| DK2859017T3 (da) | 2012-06-08 | 2019-05-13 | Sutro Biopharma Inc | Antistoffer omfattrende stedsspecifikke ikke-naturlige aminosyrerester, fremgangsmåder til fremstilling heraf og fremgangsmåder til anvendelse heraf |
| US9732161B2 (en) | 2012-06-26 | 2017-08-15 | Sutro Biopharma, Inc. | Modified Fc proteins comprising site-specific non-natural amino acid residues, conjugates of the same, methods of their preparation and methods of their use |
| KR101968344B1 (ko) | 2012-07-25 | 2019-04-12 | 한미약품 주식회사 | 옥신토모듈린 유도체를 포함하는 고지혈증 치료용 조성물 |
| AR094821A1 (es) | 2012-07-25 | 2015-09-02 | Hanmi Pharm Ind Co Ltd | Formulación líquida de un conjugado de péptido insulinotrópico de acción prolongada |
| AR091902A1 (es) | 2012-07-25 | 2015-03-11 | Hanmi Pharm Ind Co Ltd | Formulacion liquida de un conjugado de insulina de accion prolongada |
| US10441665B2 (en) | 2012-07-25 | 2019-10-15 | Hanmi Pharm. Co., Ltd. | Liquid formulation of long acting insulinotropic peptide conjugate |
| AR092862A1 (es) | 2012-07-25 | 2015-05-06 | Hanmi Pharm Ind Co Ltd | Formulacion liquida de insulina de accion prolongada y un peptido insulinotropico y metodo de preparacion |
| US9683044B2 (en) | 2012-08-20 | 2017-06-20 | Gliknik Inc. | Molecules with antigen binding and polyvalent FC gamma receptor binding activity |
| ES2728864T3 (es) | 2012-08-31 | 2019-10-29 | Sutro Biopharma Inc | Aminoácidos modificados que comprenden un grupo azido |
| US9561275B2 (en) | 2012-09-14 | 2017-02-07 | The Johns Hopkins University | Compositions and methods for rendering tumor cells susceptible to CD8+ T cell-mediated killing |
| CA2890324C (en) | 2012-11-06 | 2021-02-23 | Hanmi Pharm. Co., Ltd. | Liquid formulation of protein conjugate comprising the oxyntomodulin and an immunoglobulin fragment |
| KR101993393B1 (ko) * | 2012-11-06 | 2019-10-01 | 한미약품 주식회사 | 옥신토모듈린 유도체를 포함하는 당뇨병 또는 비만성 당뇨병 치료용 조성물 |
| EP2943512A4 (en) * | 2013-01-11 | 2016-06-01 | California Inst Biomedical Res | FUSION BOVINE ANTIBODIES |
| CN103217489B (zh) * | 2013-01-15 | 2016-03-09 | 珠海市丽珠单抗生物技术有限公司 | 一种测定蛋白纯化工艺过程中样品的糖基化和末端修饰情况的方法 |
| KR102073748B1 (ko) * | 2013-01-31 | 2020-02-05 | 한미약품 주식회사 | 재조합 효모 형질전환체 및 이를 이용하여 면역글로불린 단편을 생산하는 방법 |
| EP3985024A1 (en) | 2013-02-01 | 2022-04-20 | Atara Biotherapeutics, Inc. | Anti-activin-a compounds for the treatment of ovarian cancer |
| CA2900814A1 (en) | 2013-02-22 | 2014-08-28 | Zoetis Services Llc | In ovo administration of growth factors for improving poultry performance |
| KR102136336B1 (ko) * | 2013-03-05 | 2020-07-22 | 한미약품 주식회사 | 생리활성 폴리펩타이드 결합체의 고수율 생산을 위한 개선된 제조 방법 |
| TW201513880A (zh) | 2013-03-11 | 2015-04-16 | Novo Nordisk As | 生長激素化合物 |
| US20140271641A1 (en) * | 2013-03-14 | 2014-09-18 | University Of Guelph | Thrombospondin-1 polypeptides and methods of using same |
| DK3460054T3 (da) | 2013-03-15 | 2021-01-18 | Atyr Pharma Inc | Histidyl-tRNA-syntetase-Fc-konjugater |
| TWI683666B (zh) | 2013-03-15 | 2020-02-01 | 美商百歐維拉提夫治療公司 | 因子ix多肽調配物 |
| KR101895634B1 (ko) * | 2013-05-31 | 2018-09-05 | 한미약품 주식회사 | 변이된 힌지 영역을 포함하는 IgG4 Fc 단편 |
| ES2658039T3 (es) | 2013-07-10 | 2018-03-08 | Sutro Biopharma, Inc. | Anticuerpos que comprenden múltiples residuos de aminoácidos no naturales sitio-específicos, métodos para su preparación y métodos de uso |
| AR096891A1 (es) * | 2013-07-12 | 2016-02-03 | Hanmi Pharm Ind Co Ltd | Conjugado de monómero polipéptido biológicamente activo y conjugado de fragmento fc de inmunoglobulina, que muestra aclaramiento mediado por receptor reducido, y el método para la preparación del mismo |
| AR096890A1 (es) * | 2013-07-12 | 2016-02-03 | Hanmi Pharm Ind Co Ltd | Conjugando fc de inmunoglobulina, que mantiene la afinidad de unión del fragmento fc de la inmunoglobulina a fcrn |
| WO2015010100A2 (en) | 2013-07-18 | 2015-01-22 | Fabrus, Inc. | Humanized antibodies with ultralong complementarity determining regions |
| MA38873B1 (fr) | 2013-07-31 | 2018-11-30 | Amgen Inc | Constructions contenant le facteur 15 de différentiation de croissance (gdf-15) |
| US20150093399A1 (en) | 2013-08-28 | 2015-04-02 | Bioasis Technologies, Inc. | Cns-targeted conjugates having modified fc regions and methods of use thereof |
| SI3041513T1 (sl) | 2013-09-08 | 2020-11-30 | Kodiak Sciences Inc. | Zwitterionski polimerni konjugati faktorja VIII |
| EP3043810B1 (en) | 2013-09-09 | 2019-10-23 | CanImGuide Therapeutics AB | Immune system modulators |
| MX2016003705A (es) | 2013-09-27 | 2016-05-16 | Hanmi Pharm Ind Co Ltd | Formulacion de un conjugado de hormona del crecimiento humana de accion prolongada. |
| WO2015047890A1 (en) * | 2013-09-30 | 2015-04-02 | 3M Innovative Properties Company | Fibers and wipes with epoxidized fatty ester disposed thereon, and methods |
| WO2015070210A1 (en) | 2013-11-11 | 2015-05-14 | Wake Forest University Health Sciences | Epha3 and multi-valent targeting of tumors |
| PE20161153A1 (es) | 2014-01-20 | 2016-10-27 | Hanmi Pharm Ind Co Ltd | Insulina de accion prolongada y uso de la misma |
| WO2015112597A1 (en) * | 2014-01-21 | 2015-07-30 | Belmont Biosciences, Inc. | Variants of igg fc with limited amine groups that retain functional properties |
| ES2897935T3 (es) * | 2014-03-31 | 2022-03-03 | Hanmi Pharm Ind Co Ltd | Método para mejorar la solubilidad de proteína y péptido mediante el uso del enlace a un fragmento Fc de inmunoglobulina |
| AU2015254818A1 (en) * | 2014-04-28 | 2016-11-17 | The National Institute for Biotechnology in the Negev Ltd. | Variants of DR3 and use thereof |
| KR20150133576A (ko) * | 2014-05-20 | 2015-11-30 | 삼성전자주식회사 | 화학적 개질된 표적화 단백질 및 그의 이용 |
| AR100639A1 (es) | 2014-05-29 | 2016-10-19 | Hanmi Pharm Ind Co Ltd | Composición para tratar diabetes que comprende conjugados de análogos de insulina de acción prolongada y conjugados de péptidos insulinotrópicos de acción prolongada |
| AR100695A1 (es) | 2014-05-30 | 2016-10-26 | Hanmi Pharm Ind Co Ltd | Composición para el tratamiento de diabetes mellitus que comprende insulina y un agonista dual glp-1 / glucagón |
| AU2015279316B2 (en) | 2014-06-27 | 2021-03-04 | Innate Pharma | Multispecific NKp46 binding proteins |
| WO2015197598A2 (en) * | 2014-06-27 | 2015-12-30 | Innate Pharma | Multispecific antigen binding proteins |
| US9840553B2 (en) | 2014-06-28 | 2017-12-12 | Kodiak Sciences Inc. | Dual PDGF/VEGF antagonists |
| US10822596B2 (en) | 2014-07-11 | 2020-11-03 | Alexion Pharmaceuticals, Inc. | Compositions and methods for treating craniosynostosis |
| CN106536540A (zh) | 2014-07-24 | 2017-03-22 | 基因泰克公司 | 将试剂缀合至含有至少一个三硫键的蛋白质中的巯基部分的方法 |
| TWI772252B (zh) | 2014-09-16 | 2022-08-01 | 南韓商韓美藥品股份有限公司 | 長效glp-1/高血糖素受體雙促效劑治療非酒精性脂肝疾病之用途 |
| US9616114B1 (en) | 2014-09-18 | 2017-04-11 | David Gordon Bermudes | Modified bacteria having improved pharmacokinetics and tumor colonization enhancing antitumor activity |
| KR20210013299A (ko) | 2014-10-17 | 2021-02-03 | 코디악 사이언시스 인코포레이티드 | 부티릴콜린에스테라제 양성이온성 중합체 컨쥬게이트 |
| MX2017007392A (es) | 2014-12-05 | 2019-01-24 | Alexion Pharma Inc | Tratamiento de convulsiones con fosfatasa alcalina recombinante. |
| KR102418477B1 (ko) | 2014-12-30 | 2022-07-08 | 한미약품 주식회사 | 글루카곤 유도체 |
| US11135271B2 (en) | 2014-12-30 | 2021-10-05 | Hanmi Pharm. Co., Ltd. | Glucagon derivatives with improved stability |
| JP6868561B2 (ja) | 2015-01-28 | 2021-05-12 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | アルカリホスファターゼ欠損を有する被験者を治療する方法 |
| WO2016144650A1 (en) | 2015-03-06 | 2016-09-15 | Canimguide Therapeutics Ab | Immune system modulators and compositions |
| KR20170141215A (ko) | 2015-04-06 | 2017-12-22 | 악셀레론 파마 인코포레이티드 | 싱글-암 유형 i과 유형 ii 수용체 융합 단백질들 및 이들의 용도 |
| RU2733492C2 (ru) * | 2015-04-22 | 2020-10-02 | Байоджен Ма Инк. | Новые гибридные ActRIIB белки-ловушки лигандов для лечения заболеваний, связанных с мышечной атрофией |
| JP2018518945A (ja) * | 2015-04-29 | 2018-07-19 | メディオラヌム・ファルマチェウティチ・ソチエタ・ペル・アツィオーニ | 可溶性キメラインターロイキン−10受容体およびその療法使用 |
| CN107743494B (zh) | 2015-06-02 | 2022-04-29 | 诺和诺德股份有限公司 | 具有极性重组延伸体的胰岛素 |
| BR112017026713A2 (pt) * | 2015-06-12 | 2018-08-28 | Ubi Pharma Inc | proteínas de fusão de imunoglobulina e usos das mesmas |
| US11820807B2 (en) * | 2015-06-12 | 2023-11-21 | Ubi Pharma Inc | Immunoglobulin fusion proteins and uses thereof |
| JP6971153B2 (ja) | 2015-06-23 | 2021-11-24 | イナート・ファルマ・ソシエテ・アノニムInnate Pharma Pharma S.A. | 多重特異的nkエンゲイジャータンパク質 |
| EP3322437B1 (en) | 2015-06-30 | 2024-01-17 | Hanmi Pharm. Co., Ltd. | Glucagon derivative and a composition comprising a long acting conjugate of the same |
| ES2978112T3 (es) | 2015-07-24 | 2024-09-05 | Hanmi Pharmaceutical Co Ltd | Método de preparación de un conjugado polipeptídico fisiológicamente activo |
| AU2016308624B2 (en) | 2015-08-17 | 2022-06-23 | Alexion Pharmaceuticals, Inc. | Manufacturing of alkaline phosphatases |
| UY36870A (es) | 2015-08-28 | 2017-03-31 | Hanmi Pharm Ind Co Ltd | Análogos de insulina novedosos |
| EP3352760A4 (en) | 2015-09-21 | 2019-03-06 | Aptevo Research and Development LLC | CD3 BINDING POLYPEPTIDES |
| KR102231217B1 (ko) * | 2015-09-24 | 2021-03-24 | 한미약품 주식회사 | 면역글로불린 단편의 특정 위치를 연결 부위로 이용한 단백질 결합체 |
| TW201718629A (zh) * | 2015-09-25 | 2017-06-01 | 韓美藥品股份有限公司 | 包含多個生理多肽及免疫球蛋白Fc區之蛋白質接合物 |
| JP6868617B2 (ja) | 2015-09-28 | 2021-05-12 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 低ホスファターゼ血症の組織非特異的アルカリホスファターゼ(tnsalp)酵素補充療法に有効な投薬計画の特定 |
| MA43348A (fr) | 2015-10-01 | 2018-08-08 | Novo Nordisk As | Conjugués de protéines |
| CN115960249A (zh) | 2015-10-02 | 2023-04-14 | 银溪制药股份有限公司 | 用于组织修复的双特异性治疗性蛋白质 |
| US20170095577A1 (en) * | 2015-10-06 | 2017-04-06 | Washington University | Noninvasive imaging of focal atherosclerotic lesions using fluorescence molecular tomography |
| EP3368062A4 (en) | 2015-10-30 | 2019-07-03 | Alexion Pharmaceuticals, Inc. | METHODS OF TREATING CRANIOSYNOSTOSIS IN A PATIENT |
| CN108430511B (zh) * | 2015-12-21 | 2021-06-04 | 合肥立方制药股份有限公司 | 一种药物设计方法和获得的药物及其应用 |
| IL290457B1 (en) | 2015-12-30 | 2024-10-01 | Kodiak Sciences Inc | Antibodies and their conjugates |
| KR20170079409A (ko) * | 2015-12-30 | 2017-07-10 | 한미약품 주식회사 | 지속형 인간 성장 호르몬 결합체의 신규 액상 제제 |
| BR112018013525A2 (pt) | 2015-12-31 | 2018-12-04 | Hanmi Pharm. Co., Ltd. | conjugado de longa atuação de agonista de receptor de glucagon/glp-1/gip triplo e composição farmacêutica |
| WO2017132617A1 (en) | 2016-01-27 | 2017-08-03 | Sutro Biopharma, Inc. | Anti-cd74 antibody conjugates, compositions comprising anti-cd74 antibody conjugates and methods of using anti-cd74 antibody conjugates |
| AR107483A1 (es) * | 2016-01-29 | 2018-05-02 | Hanmi Pharm Ind Co Ltd | Conjugado de enzimas terapéuticas |
| US11065306B2 (en) | 2016-03-08 | 2021-07-20 | Alexion Pharmaceuticals, Inc. | Methods for treating hypophosphatasia in children |
| EP3436020A4 (en) | 2016-04-01 | 2019-12-25 | Alexion Pharmaceuticals, Inc. | METHOD FOR TREATING HYPOPHOSPHATASIE IN TEENS AND ADULTS |
| EP3436052A4 (en) | 2016-04-01 | 2019-10-09 | Alexion Pharmaceuticals, Inc. | TREATMENT OF MUSCLE WEAKNESS USING ALKALINE PHOSPHATASES |
| WO2017189432A1 (en) | 2016-04-26 | 2017-11-02 | R.P. Scherer Technologies, Llc | Antibody conjugates and methods of making and using the same |
| JP7020403B2 (ja) | 2016-05-02 | 2022-02-16 | 味の素株式会社 | アジド基含有Fcタンパク質 |
| CN106008722B (zh) * | 2016-05-13 | 2019-10-15 | 未名生物医药有限公司 | 一种重组β-hNGF-Fc融合蛋白、制备方法及用途 |
| US10988744B2 (en) | 2016-06-06 | 2021-04-27 | Alexion Pharmaceuticals, Inc. | Method of producing alkaline phosphatase |
| CA3026420A1 (en) | 2016-06-07 | 2017-12-14 | Gliknik Inc. | Cysteine-optimized stradomers |
| SG11201811697SA (en) | 2016-06-29 | 2019-01-30 | Hanmi Pharmaceutical Co Ltd | Glucagon derivative, conjugate thereof, composition comprising same and therapeutic use thereof |
| US11116821B2 (en) | 2016-08-18 | 2021-09-14 | Alexion Pharmaceuticals, Inc. | Methods for treating tracheobronchomalacia |
| JOP20190019A1 (ar) * | 2016-08-30 | 2019-02-12 | Genexine Inc | تركيبة صيدلانية لعلاج نقص في هرمون نمو يحتوي على بروتين اندماجي لهرمون نمو بشري (hGH) |
| BR112019005637A2 (pt) | 2016-09-23 | 2019-07-30 | Hanmi Pharm Ind Co Ltd | análogos da insulina com afinidade reduzida para o receptor de insulina e seu uso |
| US20200078470A1 (en) * | 2016-12-05 | 2020-03-12 | Hanmi Pharm. Co., Ltd. | Conjugate with attenuated immune response |
| US11129906B1 (en) | 2016-12-07 | 2021-09-28 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| US11180535B1 (en) | 2016-12-07 | 2021-11-23 | David Gordon Bermudes | Saccharide binding, tumor penetration, and cytotoxic antitumor chimeric peptides from therapeutic bacteria |
| AU2017371179B2 (en) | 2016-12-09 | 2022-07-14 | Gliknik Inc. | Manufacturing optimization of GL-2045, a multimerizing stradomer |
| KR102645064B1 (ko) * | 2017-02-03 | 2024-03-08 | 한미약품 주식회사 | 지속성이 증가된 생리활성 물질의 결합체 및 이의 용도 |
| EP3585409A4 (en) | 2017-02-27 | 2020-12-02 | Shattuck Labs, Inc. | CHEMERICAL PROTEINS BASED ON CSF1R |
| AU2018223821B2 (en) | 2017-02-27 | 2022-05-19 | Shattuck Labs, Inc. | TIGIT- and LIGHT-based chimeric proteins |
| CA3054899A1 (en) | 2017-03-23 | 2018-09-27 | Hanmi Pharm. Co., Ltd. | Insulin analog complex with reduced affinity for insulin receptor and use thereof |
| EP3600383A4 (en) | 2017-03-31 | 2020-10-28 | Alexion Pharmaceuticals, Inc. | METHODS FOR TREATMENT OF HYPOPHOSPHATASIA (HPP) IN ADULTS AND ADOLESCENTS |
| JP2020513019A (ja) * | 2017-04-05 | 2020-04-30 | ノヴォ ノルディスク アー/エス | オリゴマー伸長インスリン−Fcコンジュゲート |
| US11767520B2 (en) | 2017-04-20 | 2023-09-26 | Atyr Pharma, Inc. | Compositions and methods for treating lung inflammation |
| CN110770251A (zh) * | 2017-04-20 | 2020-02-07 | 诺和诺德股份有限公司 | 纯化白蛋白融合蛋白的方法 |
| CN109206522B (zh) * | 2017-07-07 | 2021-11-09 | 北京三有利和泽生物科技有限公司 | 一种长效抗凝血融合蛋白及其应用 |
| KR20190038456A (ko) * | 2017-09-29 | 2019-04-08 | 한미약품 주식회사 | 효력이 향상된 지속성 단백질 결합체 |
| JP6566324B2 (ja) * | 2017-09-29 | 2019-08-28 | サイデン化学株式会社 | 粘着シート |
| CA3076369A1 (en) | 2017-10-02 | 2019-04-11 | Denali Therapeutics Inc. | Fusion proteins comprising enzyme replacement therapy enzymes |
| KR102167827B1 (ko) * | 2017-12-20 | 2020-10-20 | 주식회사 알테오젠 | 신규한 성장 호르몬 수용체 길항제 및 이의 융합 단백질 |
| CN108218998A (zh) * | 2017-12-31 | 2018-06-29 | 武汉班科生物技术股份有限公司 | 一种突变型人源IgG的Fc片段及其制备方法与应用 |
| KR101974305B1 (ko) * | 2018-02-14 | 2019-04-30 | 한미사이언스 주식회사 | 생리활성 폴리펩타이드 결합체 제조 방법 |
| MX2020009152A (es) | 2018-03-02 | 2020-11-09 | Kodiak Sciences Inc | Anticuerpos de il-6 y constructos de fusion y conjugados de los mismos. |
| JP7328243B2 (ja) * | 2018-03-26 | 2023-08-16 | リジェネロン・ファーマシューティカルズ・インコーポレイテッド | 治療薬を試験するためのヒト化げっ歯類 |
| KR102209108B1 (ko) | 2018-03-27 | 2021-01-28 | 국립암센터 | Oct4 기능 저해용 펩티드를 포함하는 줄기세포성 억제용 조성물 |
| EP3773684A1 (en) | 2018-03-30 | 2021-02-17 | Alexion Pharmaceuticals, Inc. | Manufacturing of glycoproteins |
| CN111954537A (zh) | 2018-04-09 | 2020-11-17 | 美国安进公司 | 生长分化因子15融合蛋白 |
| US10780121B2 (en) | 2018-08-29 | 2020-09-22 | Shattuck Labs, Inc. | FLT3L-based chimeric proteins |
| EP3978518A4 (en) * | 2019-04-23 | 2022-11-02 | Lg Chem, Ltd. | FUSION POLYPEPTIDE COMPRISING FC REGION OF IMMUNOGLOBULIN AND GDF15 |
| US11267858B2 (en) * | 2019-05-31 | 2022-03-08 | Spectrum Pharmaceuticals, Inc. | Methods of treatment using G-CSF protein complex |
| CN112142850A (zh) * | 2019-06-27 | 2020-12-29 | 深圳市卫光生物制品股份有限公司 | 人神经生长因子-乳铁蛋白重组蛋白及用途 |
| CA3157509A1 (en) | 2019-10-10 | 2021-04-15 | Kodiak Sciences Inc. | Methods of treating an eye disorder |
| CN110669134A (zh) * | 2019-10-15 | 2020-01-10 | 广东菲鹏生物有限公司 | IgM-FC片段、IgM-FC抗体及制备方法和应用 |
| AU2020400805B2 (en) * | 2019-12-11 | 2024-03-28 | Lg Chem, Ltd. | Fusion polypeptide comprising GDF15 and polypeptide region capable of O-glycosylation |
| CN111153996B (zh) * | 2020-01-10 | 2021-12-14 | 苏州睿瀛生物技术有限公司 | G蛋白偶联受体的抗体及其制备方法和g蛋白偶联受体试剂盒 |
| CN111505291B (zh) * | 2020-04-14 | 2023-04-25 | 山东省千佛山医院 | 一种排除巨酶分子对血清酶浓度检测带来干扰的方法 |
| BR112022023738A2 (pt) | 2020-05-22 | 2023-01-31 | Hanmi Pharm Ind Co Ltd | Formulação líquida |
| CN112098639B (zh) * | 2020-09-21 | 2024-01-02 | 天津医科大学 | 以氧化石墨烯为载体的二抗的合成及应用 |
| EP4291224A1 (en) | 2021-02-12 | 2023-12-20 | Alexion Pharmaceuticals, Inc. | Alkaline phosphatase polypeptides and methods of use thereof |
| WO2023147489A2 (en) * | 2022-01-28 | 2023-08-03 | argenx BV | Anti-musk antibodies for use in treating neuromuscular disorders |
| IL315251A (en) * | 2022-03-03 | 2024-10-01 | The Trustees Of The Univ Of Pennsylvania | Viral vectors encoding parathyroid hormone fusions and their uses for the treatment of hypoparathyroidism |
| CN114588315A (zh) * | 2022-03-14 | 2022-06-07 | 东莞市人民医院 | 抗炎蛋白涂层的制备方法、生物工程功能材料及其应用 |
| WO2024123675A2 (en) * | 2022-12-05 | 2024-06-13 | Alexion Pharmaceuticals, Inc. | Taci-fc fusion proteins for multifunctional inhibition of baff, april, and neonatal fc receptor |
| WO2024148240A1 (en) | 2023-01-06 | 2024-07-11 | Lassen Therapeutics 1, Inc. | ANTI-IL-11Rα ANTIBODIES FOR TREATING THYROID EYE DISEASE |
| WO2024148241A1 (en) | 2023-01-06 | 2024-07-11 | Lassen Therapeutics 1, Inc. | Anti-il-18bp antibodies |
| WO2024148243A1 (en) | 2023-01-06 | 2024-07-11 | Lassen Therapeutics 1, Inc. | Anti-il-18bp antibodies |
Family Cites Families (120)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4399216A (en) | 1980-02-25 | 1983-08-16 | The Trustees Of Columbia University | Processes for inserting DNA into eucaryotic cells and for producing proteinaceous materials |
| GB8504099D0 (en) * | 1985-02-18 | 1985-03-20 | Wellcome Found | Physiologically active substances |
| JPS62153300A (ja) * | 1985-12-26 | 1987-07-08 | Teijin Ltd | ヒト免疫グロブリンGFc領域蛋白質およびその製造方法 |
| JPH0728746B2 (ja) | 1986-02-28 | 1995-04-05 | 理化学研究所 | 新規プラスミド、微生物細胞及びヒト免疫グロブリンG Fc領域蛋白質の製造法 |
| US5643758A (en) * | 1987-03-10 | 1997-07-01 | New England Biolabs, Inc. | Production and purification of a protein fused to a binding protein |
| JPS63245691A (ja) | 1987-03-31 | 1988-10-12 | Teijin Ltd | ヒト免疫グロブリンGFc領域蛋白質およびその製造方法 |
| JPS63290899A (ja) | 1987-05-22 | 1988-11-28 | Takeda Chem Ind Ltd | ヒトIgEFc蛋白質のフラグメントおよびその製造法 |
| US6710169B2 (en) * | 1987-10-02 | 2004-03-23 | Genentech, Inc. | Adheson variants |
| DE3889546T2 (de) | 1987-12-21 | 1994-09-08 | Univ Toledo | Transformation von keimenden pflanzensamen mit hilfe von agrobacterium. |
| US6018026A (en) | 1988-01-22 | 2000-01-25 | Zymogenetics, Inc. | Biologically active dimerized and multimerized polypeptide fusions |
| US5567584A (en) | 1988-01-22 | 1996-10-22 | Zymogenetics, Inc. | Methods of using biologically active dimerized polypeptide fusions to detect PDGF |
| US6004781A (en) | 1988-01-22 | 1999-12-21 | The General Hospital Corporation | Nucleic acid encoding Ig-CD4 fusion proteins |
| GB8824869D0 (en) | 1988-10-24 | 1988-11-30 | Stevenson G T | Synthetic antibody |
| US5225538A (en) | 1989-02-23 | 1993-07-06 | Genentech, Inc. | Lymphocyte homing receptor/immunoglobulin fusion proteins |
| US6406697B1 (en) | 1989-02-23 | 2002-06-18 | Genentech, Inc. | Hybrid immunoglobulins |
| US5116964A (en) | 1989-02-23 | 1992-05-26 | Genentech, Inc. | Hybrid immunoglobulins |
| US6307025B1 (en) | 1989-04-28 | 2001-10-23 | Biogen, Inc. | VCAM fusion proteins and DNA coding therefor |
| FR2650598B1 (fr) | 1989-08-03 | 1994-06-03 | Rhone Poulenc Sante | Derives de l'albumine a fonction therapeutique |
| US6541610B1 (en) | 1989-09-05 | 2003-04-01 | Immunex Corporation | Fusion proteins comprising tumor necrosis factor receptor |
| US5605690A (en) | 1989-09-05 | 1997-02-25 | Immunex Corporation | Methods of lowering active TNF-α levels in mammals using tumor necrosis factor receptor |
| GB9009106D0 (en) | 1990-04-23 | 1990-06-20 | 3I Res Expl Ltd | Processes and intermediates for synthetic antibody derivatives |
| US5349053A (en) | 1990-06-01 | 1994-09-20 | Protein Design Labs, Inc. | Chimeric ligand/immunoglobulin molecules and their uses |
| US7253264B1 (en) * | 1990-06-28 | 2007-08-07 | Sanofi-Arentideutschland GmbH | Immunoglobulin fusion proteins, their production and use |
| ES2120949T4 (es) | 1990-06-28 | 2011-12-29 | Sanofi-Aventis Deutschland Gmbh 50% | Proteinas de fusión con porciones de inmunoglobulinas, su preparación y empleo. |
| US5650150A (en) | 1990-11-09 | 1997-07-22 | Gillies; Stephen D. | Recombinant antibody cytokine fusion proteins |
| US5191066A (en) | 1990-12-07 | 1993-03-02 | Abbott Laboratories | Site-specific conjugation of immunoglobulins and detectable labels |
| JP3670276B2 (ja) | 1991-02-08 | 2005-07-13 | プロゲニクス・ファーマスーティカルズ、インコーポレイテッド | CD4― ガンマ・2キメラ及びCD4 ― IgG2・キメラ |
| GEP20033082B (en) | 1991-03-15 | 2003-10-27 | Amgen Inc | Pegylation of Polypeptides |
| CA2585487A1 (fr) * | 1991-04-17 | 1992-10-29 | Medarex Inc. | Polypeptides hydrosolubles ayant une haute affinite pour les interferons .alpha. et .beta. |
| EP0533006A1 (en) | 1991-09-18 | 1993-03-24 | F.Hoffmann-La Roche & Co. Aktiengesellschaft | Chimaeric interleukin 5-receptor/immunoglobulin polypeptides |
| US20020037558A1 (en) | 1991-10-23 | 2002-03-28 | Kin-Ming Lo | E.coli produced immunoglobulin constructs |
| FR2686901A1 (fr) | 1992-01-31 | 1993-08-06 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides antithrombotiques, leur preparation et compositions pharmaceutiques les contenant. |
| FR2686899B1 (fr) | 1992-01-31 | 1995-09-01 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides biologiquement actifs, leur preparation et compositions pharmaceutiques les contenant. |
| GB9206422D0 (en) * | 1992-03-24 | 1992-05-06 | Bolt Sarah L | Antibody preparation |
| US5447851B1 (en) | 1992-04-02 | 1999-07-06 | Univ Texas System Board Of | Dna encoding a chimeric polypeptide comprising the extracellular domain of tnf receptor fused to igg vectors and host cells |
| JPH0640945A (ja) | 1992-07-23 | 1994-02-15 | Kureha Chem Ind Co Ltd | Fcフラグメント結合抗腫瘍剤 |
| JPH08503125A (ja) * | 1992-08-07 | 1996-04-09 | プロジェニクス・ファーマスーティカルス・インコーポレーテッド | 非ペプチジル成分と複合化されたCD4−ガンマ2およびCD4−IgG2免疫複合体、並びにその使用 |
| IT1263831B (it) | 1993-01-29 | 1996-09-04 | Paolo Chiesi | Complessi di inclusione multicomponente ad elevata solubilita' costituiti da un farmaco di tipo basico, un acido ed una ciclodestrina |
| US6482919B2 (en) | 1993-02-01 | 2002-11-19 | Bristol-Myers Squibb Company | Expression vectors encoding bispecific fusion proteins and methods of producing biologically active bispecific fusion proteins in a mammalian cell |
| US5470952A (en) | 1993-10-20 | 1995-11-28 | Regeneron Pharmaceuticals, Inc. | CNTF and IL-6 antagonists |
| US5738846A (en) | 1994-11-10 | 1998-04-14 | Enzon, Inc. | Interferon polymer conjugates and process for preparing the same |
| US6410008B1 (en) * | 1994-12-12 | 2002-06-25 | Beth Israel Hospital Association | Chimeric IL-10 proteins and uses thereof |
| US6030613A (en) * | 1995-01-17 | 2000-02-29 | The Brigham And Women's Hospital, Inc. | Receptor specific transepithelial transport of therapeutics |
| WO1996028475A1 (fr) | 1995-03-10 | 1996-09-19 | Nakamura, Toshikazu | Facteur de croissance des hepatocytes modifie a l'aide de polyethylene glycol |
| US6096871A (en) | 1995-04-14 | 2000-08-01 | Genentech, Inc. | Polypeptides altered to contain an epitope from the Fc region of an IgG molecule for increased half-life |
| GB9511935D0 (en) | 1995-06-13 | 1995-08-09 | Smithkline Beecham Plc | Novel compound |
| HUP9900017A3 (en) * | 1995-09-21 | 2001-08-28 | Andaris Ltd Ruddington | Transcytosis vehicles and enhancers for drug delivery |
| US6936439B2 (en) | 1995-11-22 | 2005-08-30 | Amgen Inc. | OB fusion protein compositions and methods |
| US6620413B1 (en) | 1995-12-27 | 2003-09-16 | Genentech, Inc. | OB protein-polymer chimeras |
| US5723125A (en) | 1995-12-28 | 1998-03-03 | Tanox Biosystems, Inc. | Hybrid with interferon-alpha and an immunoglobulin Fc linked through a non-immunogenic peptide |
| US6750334B1 (en) | 1996-02-02 | 2004-06-15 | Repligen Corporation | CTLA4-immunoglobulin fusion proteins having modified effector functions and uses therefor |
| EP0904107B1 (en) | 1996-03-18 | 2004-10-20 | Board Of Regents, The University Of Texas System | Immunoglobin-like domains with increased half lives |
| KR19980038061A (ko) | 1996-11-23 | 1998-08-05 | 유우준 | 음식물 쓰레기 수분분리 처리장치 |
| US7122636B1 (en) * | 1997-02-21 | 2006-10-17 | Genentech, Inc. | Antibody fragment-polymer conjugates and uses of same |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| MY118835A (en) * | 1997-04-18 | 2005-01-31 | Ipsen Pharma Biotech | Sustained release compositions and the process for their preparation |
| US5990237A (en) * | 1997-05-21 | 1999-11-23 | Shearwater Polymers, Inc. | Poly(ethylene glycol) aldehyde hydrates and related polymers and applications in modifying amines |
| AU8182298A (en) | 1997-07-10 | 1999-02-08 | Beth Israel Deaconess Medical Center | Recombinant erythropoietin / immunoglobulin fusion proteins |
| US6165476A (en) | 1997-07-10 | 2000-12-26 | Beth Israel Deaconess Medical Center | Fusion proteins with an immunoglobulin hinge region linker |
| US6451986B1 (en) * | 1998-06-22 | 2002-09-17 | Immunex Corporation | Site specific protein modification |
| US6703381B1 (en) * | 1998-08-14 | 2004-03-09 | Nobex Corporation | Methods for delivery therapeutic compounds across the blood-brain barrier |
| KR100316347B1 (ko) | 1998-09-15 | 2002-08-27 | 한미약품(주) | 대장균엔테로톡신ⅱ신호펩티드의변형체와인체성장호르몬의융합단백질을발현하는재조합미생물및그를이용한인체성장호르몬의제조방법 |
| IL142350A0 (en) * | 1998-10-16 | 2002-03-10 | Biogen Inc | Interferon-beta fusion proteins and pharmaceutical compositions containing the same |
| US6660843B1 (en) | 1998-10-23 | 2003-12-09 | Amgen Inc. | Modified peptides as therapeutic agents |
| CA2356401A1 (en) * | 1999-01-07 | 2000-07-13 | Lexigen Pharmaceuticals, Corp. | Expression and export of anti-obesity proteins as fc fusion proteins |
| US6737056B1 (en) * | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| AU3224700A (en) | 1999-02-08 | 2000-08-25 | Chiron Corporation | Fibroblast growth factor receptor-immunoglobulin fusion |
| US20040266673A1 (en) * | 2002-07-31 | 2004-12-30 | Peter Bakis | Long lasting natriuretic peptide derivatives |
| CA2372400C (en) | 1999-05-19 | 2010-04-27 | Lexigen Pharmaceuticals Corp. | Expression and export of interferon-alpha proteins as fc fusion proteins |
| US6833349B2 (en) * | 1999-06-08 | 2004-12-21 | Regeneron Pharmaceuticals, Inc. | Methods of treating inflammatory skin diseases |
| EP1194451A1 (en) | 1999-07-02 | 2002-04-10 | Genentech, Inc. | Fusion peptides comprising a peptide ligand domain and a multimerization domain |
| JO2291B1 (en) | 1999-07-02 | 2005-09-12 | اف . هوفمان لاروش ايه جي | Erythropoietin derivatives |
| EP1200124B1 (en) | 1999-07-13 | 2008-09-10 | Bolder Biotechnology, Inc. | Erythropoietin-immunoglobulin fusion proteins |
| KR100360594B1 (ko) | 2000-01-19 | 2002-11-13 | 한미약품공업 주식회사 | 인간 인터페론 알파의 발현 분비벡터 및 이를 이용한인터페론 알파의 생산 방법 |
| MXPA02010324A (es) | 2000-04-21 | 2003-04-25 | Amgen Inc | Derivados de peptidos apo-ai/aii. |
| US6756480B2 (en) * | 2000-04-27 | 2004-06-29 | Amgen Inc. | Modulators of receptors for parathyroid hormone and parathyroid hormone-related protein |
| US20020168367A1 (en) * | 2000-04-28 | 2002-11-14 | Planet Biotechnology Incorporated | Novel immunoadhesins for treating and preventing viral and bacterial diseases |
| US6677136B2 (en) | 2000-05-03 | 2004-01-13 | Amgen Inc. | Glucagon antagonists |
| DE10021731B4 (de) | 2000-05-04 | 2005-12-08 | Aventis Pharma Deutschland Gmbh | Cyclipostine, Verfahren zu ihrer Herstellung und pharmazeutische Zubereitung derselben |
| US6417237B1 (en) | 2000-06-08 | 2002-07-09 | The Board Of Trustees Of The University Of Illinois | Macromolecular drug complexes and compositions containing the same |
| KR20080085082A (ko) * | 2000-12-07 | 2008-09-22 | 일라이 릴리 앤드 캄파니 | Glp-1 융합 단백질 |
| DE60117601T2 (de) | 2000-12-14 | 2006-11-16 | Genentech Inc., San Francisco | Bakterielle wirtstämme |
| US6979556B2 (en) | 2000-12-14 | 2005-12-27 | Genentech, Inc. | Separate-cistron contructs for secretion of aglycosylated antibodies from prokaryotes |
| US7829084B2 (en) | 2001-01-17 | 2010-11-09 | Trubion Pharmaceuticals, Inc. | Binding constructs and methods for use thereof |
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| EP1392826A2 (en) | 2001-01-18 | 2004-03-03 | MERCK PATENT GmbH | Bifunctional fusion proteins with glucocerebrosidase activity |
| WO2002066514A2 (en) * | 2001-02-19 | 2002-08-29 | Merck Patent Gmbh | Artificial fusion proteins with reduced immunogenicity |
| KR100566911B1 (ko) | 2001-06-25 | 2006-04-03 | 주식회사 삼양사 | 약물 전달체용 음이온기-함유 양친성 블록 공중합체 및 그의 양이온성 약물과의 복합체 |
| WO2003002144A1 (en) | 2001-06-26 | 2003-01-09 | Imclone Systems Incorporated | Bispecific antibodies that bind to vegf receptors |
| US20030026764A1 (en) | 2001-07-31 | 2003-02-06 | Immunomedics, Inc. | Polymeric delivery systems |
| US6900292B2 (en) * | 2001-08-17 | 2005-05-31 | Lee-Hwei K. Sun | Fc fusion proteins of human erythropoietin with increased biological activities |
| US6797493B2 (en) * | 2001-10-01 | 2004-09-28 | Lee-Hwei K. Sun | Fc fusion proteins of human granulocyte colony-stimulating factor with increased biological activities |
| US7125843B2 (en) * | 2001-10-19 | 2006-10-24 | Neose Technologies, Inc. | Glycoconjugates including more than one peptide |
| US7138370B2 (en) | 2001-10-11 | 2006-11-21 | Amgen Inc. | Specific binding agents of human angiopoietin-2 |
| KR100811138B1 (ko) | 2001-11-13 | 2008-03-07 | 오리온피디피주식회사 | 저온소성세라믹기판을 이용한 다층회로기판의 제조방법과 이에 의해 제조된 다층회로기판 |
| US20030211078A1 (en) * | 2001-12-07 | 2003-11-13 | Heavner George A. | Pseudo-antibody constructs |
| US20040110226A1 (en) * | 2002-03-01 | 2004-06-10 | Xencor | Antibody optimization |
| EP1572936A2 (en) | 2002-03-05 | 2005-09-14 | Eli Lilly And Company | Heterologous g-csf fusion proteins |
| EP1487992A4 (en) | 2002-03-15 | 2007-10-31 | Brigham & Womens Hospital | CENTRAL AIRWAY DELIVERY FOR SYSTEMIC DRUG DELIVERY |
| US20030191056A1 (en) * | 2002-04-04 | 2003-10-09 | Kenneth Walker | Use of transthyretin peptide/protein fusions to increase the serum half-life of pharmacologically active peptides/proteins |
| WO2004024889A2 (en) * | 2002-09-16 | 2004-03-25 | Elusys Therapeutics, Inc. | Production of bispecific molecules using polyethylene glycol linkers |
| EP1578447A4 (en) * | 2002-10-31 | 2009-06-03 | Genentech Inc | METHODS AND COMPOSITIONS THAT CAN INCREASE ANTIBODY PRODUCTION |
| SI1581649T1 (sl) | 2002-12-20 | 2011-09-30 | Amgen Inc | Vezna sredstva, ki zavirajo miostatin |
| WO2004064731A2 (en) | 2003-01-14 | 2004-08-05 | University Of Washington | Lipid-drug formulations and methods for targeted delivery of lipid-drug complexes to lymlplhoid tissues |
| US20050176108A1 (en) * | 2003-03-13 | 2005-08-11 | Young-Min Kim | Physiologically active polypeptide conjugate having prolonged in vivo half-life |
| KR20040083268A (ko) | 2003-03-21 | 2004-10-01 | 한미약품 주식회사 | 안정성이 증가된 인간 과립구 콜로니 자극인자 융합체 및이의 제조방법 |
| ES2333598T5 (es) | 2003-05-06 | 2013-09-04 | Biogen Idec Hemophilia Inc | Proteinas quimericas del factor de coagulacion fc para tratar la hemofilia. |
| TWI353991B (en) * | 2003-05-06 | 2011-12-11 | Syntonix Pharmaceuticals Inc | Immunoglobulin chimeric monomer-dimer hybrids |
| WO2004108885A2 (en) | 2003-05-06 | 2004-12-16 | Syntonix Pharmaceuticals, Inc. | Fc chimeric proteins with anti-hiv drugs |
| CA2527878A1 (en) * | 2003-05-30 | 2005-01-27 | Alexion Pharmaceuticals, Inc. | Antibodies and fusion proteins that include engineered constant regions |
| WO2005047334A1 (en) | 2003-11-13 | 2005-05-26 | Hanmi Pharmaceutical. Co., Ltd. | Igg fc fragment for a drug carrier and method for the preparation thereof |
| BRPI0507174A (pt) | 2004-01-28 | 2008-04-01 | Syntonix Pharmaceuticals Inc | proteìnas de fusão hormÈnio-fc (fsh-fc) heterodiméricas estimuladoras de folìculo para o tratamento da infertilidade |
| AU2005289594B2 (en) * | 2004-09-27 | 2012-02-02 | Centocor, Inc. | Srage mimetibody, compositions, methods and uses |
| KR100594607B1 (ko) | 2004-11-03 | 2006-06-30 | 재단법인서울대학교산학협력재단 | 신규한 경구투여용 재조합 인간 성장호르몬 분비미생물제제 및 그 제조방법 |
| KR100754667B1 (ko) * | 2005-04-08 | 2007-09-03 | 한미약품 주식회사 | 비펩타이드성 중합체로 개질된 면역글로불린 Fc 단편 및이를 포함하는 약제학적 조성물 |
| JP2010106019A (ja) | 2008-10-02 | 2010-05-13 | Kanazawa Univ | リマプロストを含有してなる癌化学療法に起因する末梢神経障害予防、治療および/または症状軽減剤 |
| AR081755A1 (es) * | 2010-04-02 | 2012-10-17 | Hanmi Holdings Co Ltd | Formulacion de accion prolongada de la hormona estimuladora de los foliculos donde se usa un fragmento de inmunoglobulina, metodo de preparacion y metodo para tratar a un sujeto que sufre un trastorno reproductivo |
| AR081066A1 (es) * | 2010-04-02 | 2012-06-06 | Hanmi Holdings Co Ltd | Conjugado de insulina donde se usa un fragmento de inmunoglobulina |
| AR080993A1 (es) * | 2010-04-02 | 2012-05-30 | Hanmi Holdings Co Ltd | Formulacion de accion prolongada de interferon beta donde se usa un fragmento de inmunoglobulina |
| KR20120002129A (ko) * | 2010-06-30 | 2012-01-05 | 한미홀딩스 주식회사 | 면역글로불린 단편을 이용한 제7인자(Factor Ⅶa)약물 결합체 |
-
2004
- 2004-11-13 WO PCT/KR2004/002942 patent/WO2005047334A1/en active Application Filing
- 2004-11-13 JP JP2006539396A patent/JP2007531513A/ja active Pending
- 2004-11-13 CN CN2004800017702A patent/CN1723219B/zh active Active
- 2004-11-13 ES ES04800092T patent/ES2426169T3/es active Active
- 2004-11-13 JP JP2006539399A patent/JP5216216B2/ja active Active
- 2004-11-13 ES ES04800090T patent/ES2372495T3/es active Active
- 2004-11-13 WO PCT/KR2004/002944 patent/WO2005047336A1/en active Application Filing
- 2004-11-13 EP EP04800092.1A patent/EP1682584B1/en active Active
- 2004-11-13 PT PT100091297T patent/PT2256134E/pt unknown
- 2004-11-13 CA CA2512657A patent/CA2512657C/en active Active
- 2004-11-13 WO PCT/KR2004/002945 patent/WO2005047337A1/en active Application Filing
- 2004-11-13 US US10/535,341 patent/US8846874B2/en active Active
- 2004-11-13 AU AU2004282984A patent/AU2004282984B2/en active Active
- 2004-11-13 BR BRPI0406605A patent/BRPI0406605B8/pt active IP Right Grant
- 2004-11-13 KR KR1020040092781A patent/KR100775343B1/ko active Protection Beyond IP Right Term
- 2004-11-13 US US10/535,231 patent/US7736653B2/en active Active
- 2004-11-13 KR KR1020040092782A patent/KR100725315B1/ko active Protection Beyond IP Right Term
- 2004-11-13 KR KR1020040092780A patent/KR20050047030A/ko not_active Application Discontinuation
- 2004-11-13 AT AT04800089T patent/ATE555133T1/de active
- 2004-11-13 MX MXPA05007210A patent/MXPA05007210A/es active IP Right Grant
- 2004-11-13 CN CN201810616347.7A patent/CN108743967B/zh active Active
- 2004-11-13 AT AT04800091T patent/ATE540980T1/de active
- 2004-11-13 CN CNA2004800017755A patent/CN1723220A/zh active Pending
- 2004-11-13 ES ES04800091T patent/ES2378167T3/es active Active
- 2004-11-13 EP EP04800091A patent/EP1682583B1/en active Active
- 2004-11-13 ES ES04800089T patent/ES2383300T3/es active Active
- 2004-11-13 WO PCT/KR2004/002943 patent/WO2005047335A1/en active Application Filing
- 2004-11-13 PT PT100063262T patent/PT2239273E/pt unknown
- 2004-11-13 AU AU2004282985A patent/AU2004282985B8/en active Active
- 2004-11-13 RU RU2005120239/13A patent/RU2352583C2/ru active
- 2004-11-13 US US10/535,312 patent/US8029789B2/en active Active
- 2004-11-13 AT AT04800090T patent/ATE522548T1/de not_active IP Right Cessation
- 2004-11-13 ES ES10006326.2T patent/ES2438098T3/es active Active
- 2004-11-13 CN CN201210190634.9A patent/CN103212084B/zh active Active
- 2004-11-13 EP EP04800090A patent/EP1682582B1/en active Active
- 2004-11-13 DK DK04800091.3T patent/DK1682583T3/da active
- 2004-11-13 US US10/535,232 patent/US7737260B2/en active Active
- 2004-11-13 MX MXPA05007211A patent/MXPA05007211A/es active IP Right Grant
- 2004-11-13 JP JP2006539398A patent/JP4870569B2/ja active Active
- 2004-11-13 PL PL10006326T patent/PL2239273T3/pl unknown
- 2004-11-13 EP EP10006326.2A patent/EP2239273B1/en active Active
- 2004-11-13 EP EP04800089A patent/EP1682581B1/en active Active
- 2004-11-13 JP JP2006539397A patent/JP4762904B2/ja active Active
- 2004-11-13 PT PT04800091T patent/PT1682583E/pt unknown
- 2004-11-13 CA CA2512933A patent/CA2512933C/en not_active Expired - Fee Related
- 2004-11-13 PL PL10009129T patent/PL2256134T3/pl unknown
- 2004-11-13 RU RU2005120240/13A patent/RU2356909C2/ru active
- 2004-11-13 ES ES10009129.7T patent/ES2454666T3/es active Active
- 2004-11-13 EP EP10009129.7A patent/EP2256134B1/en active Active
- 2004-11-13 DK DK10009129.7T patent/DK2256134T3/en active
- 2004-11-13 KR KR1020040092783A patent/KR100725314B1/ko active IP Right Grant
- 2004-11-13 DK DK10006326.2T patent/DK2239273T3/da active
- 2004-11-13 BR BR0406606-5A patent/BRPI0406606A/pt not_active Application Discontinuation
-
2006
- 2006-04-24 KR KR1020060036697A patent/KR20060054252A/ko active Search and Examination
-
2007
- 2007-05-03 US US11/744,162 patent/US20080085862A1/en not_active Abandoned
- 2007-05-10 US US11/747,153 patent/US20080124347A1/en not_active Abandoned
-
2010
- 2010-04-09 US US12/757,635 patent/US20100255014A1/en not_active Abandoned
-
2011
- 2011-04-13 HK HK11103711.9A patent/HK1149570A1/xx unknown
- 2011-04-15 US US13/087,593 patent/US8822650B2/en active Active
- 2011-05-06 HK HK11104515.5A patent/HK1150612A1/xx unknown
- 2011-09-15 JP JP2011202199A patent/JP5425150B2/ja not_active Expired - Fee Related
- 2011-09-26 JP JP2011209594A patent/JP2011256211A/ja not_active Abandoned
-
2012
- 2012-07-26 JP JP2012166208A patent/JP2012224635A/ja not_active Withdrawn
-
2013
- 2013-03-12 US US13/796,135 patent/US10071166B2/en active Active
-
2014
- 2014-07-09 US US14/327,064 patent/US10272159B2/en active Active
- 2014-07-09 US US14/327,120 patent/US9750820B2/en active Active
-
2018
- 2018-07-20 US US16/041,263 patent/US20180326083A1/en active Pending
-
2019
- 2019-03-12 US US16/351,338 patent/US11058776B2/en active Active
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2483081C2 (ru) * | 2008-07-23 | 2013-05-27 | Ханми Сайенс Ко.,Лтд.,Kr | Полипептидный комплекс, содержащий непептидильный полимер, обладающий тремя функциональными концами |
| RU2503688C2 (ru) * | 2009-04-22 | 2014-01-10 | Алтеоген, Инк | Слитый белок или пептид с увеличенным временем полужизни in vivo, поддерживаемый за счет замедленного высвобождения in vivo, и способ увеличения времени полужизни in vivo с его применением |
| RU2589697C2 (ru) * | 2009-12-18 | 2016-07-10 | Экзодос Лайф Сайенсиз Лимитед Партнершип | Способы получения стабильных жидких лекарственных препаратов и их композиции |
| US9629920B2 (en) | 2009-12-18 | 2017-04-25 | Exodos Life Sciences Limited Partnership | Methods and compositions for stable liquid drug formulations |
| US11618790B2 (en) | 2010-12-23 | 2023-04-04 | Hoffmann-La Roche Inc. | Polypeptide-polynucleotide-complex and its use in targeted effector moiety delivery |
| US10106612B2 (en) | 2012-06-27 | 2018-10-23 | Hoffmann-La Roche Inc. | Method for selection and production of tailor-made highly selective and multi-specific targeting entities containing at least two different binding entities and uses thereof |
| US11407836B2 (en) | 2012-06-27 | 2022-08-09 | Hoffmann-La Roche Inc. | Method for selection and production of tailor-made highly selective and multi-specific targeting entities containing at least two different binding entities and uses thereof |
| US11421022B2 (en) | 2012-06-27 | 2022-08-23 | Hoffmann-La Roche Inc. | Method for making antibody Fc-region conjugates comprising at least one binding entity that specifically binds to a target and uses thereof |
| US9862779B2 (en) | 2012-09-14 | 2018-01-09 | Hoffmann-La Roche Inc. | Method for the production and selection of molecules comprising at least two different entities and uses thereof |
| RU2711485C2 (ru) * | 2014-04-11 | 2020-01-17 | МЕДИММЬЮН, ЭлЭлСи | Конъюгированные соединения, содержащие сконструированные с цистеином антитела |
| RU2766200C1 (ru) * | 2015-10-01 | 2022-02-09 | Хит Байолоджикс, Инк. | Композиции и способы для соединения внеклеточных доменов типа i и типа ii в качестве гетерологичных химерных белков |
| RU2805873C2 (ru) * | 2019-07-18 | 2023-10-24 | Ханми Фарм. Ко., Лтд. | Новый способ получения длительно действующего конъюгата лекарственного средства посредством получения промежуточного соединения |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2352583C2 (ru) | ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ Fc-ОБЛАСТЬ ИММУНОГЛОБУЛИНА В КАЧЕСТВЕ НОСИТЕЛЯ | |
| US8110665B2 (en) | Pharmaceutical composition comprising an immunoglobulin FC region as a carrier |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20110413 |
|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20121106 |