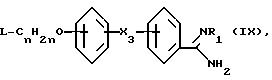RU2159228C2 - Производные замещенного бензамидина - Google Patents
Производные замещенного бензамидина Download PDFInfo
- Publication number
- RU2159228C2 RU2159228C2 RU97102043/04A RU97102043A RU2159228C2 RU 2159228 C2 RU2159228 C2 RU 2159228C2 RU 97102043/04 A RU97102043/04 A RU 97102043/04A RU 97102043 A RU97102043 A RU 97102043A RU 2159228 C2 RU2159228 C2 RU 2159228C2
- Authority
- RU
- Russia
- Prior art keywords
- carbon atoms
- alkyl
- formula
- group
- methyl
- Prior art date
Links
- 0 CC(*)(C=C1)C=C1OC Chemical compound CC(*)(C=C1)C=C1OC 0.000 description 1
- GYVGXEWAOAAJEU-UHFFFAOYSA-N Cc(cc1)ccc1N(C)C Chemical compound Cc(cc1)ccc1N(C)C GYVGXEWAOAAJEU-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/62—Compounds containing any of the groups, X being a hetero atom, Y being any atom, e.g. N-acylcarbamates
- C07C271/64—Y being a hydrogen or a carbon atom, e.g. benzoylcarbamates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C259/00—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups
- C07C259/12—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. N-hydroxyamidines
- C07C259/18—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups with replacement of the other oxygen atom of the carboxyl group by nitrogen atoms, e.g. N-hydroxyamidines having carbon atoms of hydroxamidine groups bound to carbon atoms of six-membered aromatic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/08—Bronchodilators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Abstract
Предложены производные замещенного бензамидина общей формулы I, где А представляет собой -O-CmH2m-X1-группу или группу формулы IV; m = 2-6; Х1 - группа формулы III, Х3 - группа -О-CnH2n-; X2 - группа -CnH2n-О-; n = 1 или 2; R1 - ОН, COR7 или COOR7; R2 - (С1 - С6)-алкил, -CR5R6-арил или водород (если А - остаток формулы IV или если Х1 - остаток формулы III), (С1 - С6)-алкокси (если А - -ОСmH2mХ1-группа и Х1 - группа формулы III); R3 - водород, (С1 - С6)-алкил, (С1 - С6)-алкокси (при условии, что R2 - -CR5R6-арил или если Х1 - группа формулы III); R4 - Н или (С1 - С6)-алкил; R5 и R6 - (С1 - С4)-алкил; R7 - (С1 - С6)-алкил, (С5 - С7)-циклоалкил, арил, гетероарил с атомом азота в качестве гетероатома, обладающие антагонистическим действием на рецепторы лейкотриена В4, при условии, что если А - группа -OCmH2mX1-; m = 2, 3 или 4, Х1 - группа формулы III; R2 - H или (С1 - С6)-алкил; R3 - Н, (С1 - С6)-алкил, (С1 - С6)-алкокси; R4 - водород или (С1 - С6)-алкил, то R1 не означает ОН. 9 з.п. ф-лы.
Description
Изобретение относится к производным замещенного амидина, обладающим биологической активностью, в частности к новым производным замещенного бензамидина, обладающим биологической активностью, в частности антагонистическим действием на рецепторы лейкотриена B4.
Известны производные замещенного бензамидина, обладающие антагонистическим действием на рецепторы лейкотриена B4 (см. заявку WO 93/16036, кл. C 07 C 257/18, A 61 K 31/35, 19.08.1993).
Задачей изобретения является расширение арсенала производных замещенного бензамидина, обладающих антагонистическим действием на рецепторы лейкотриена B4.
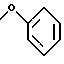
Поставленная задача решается предлагаемыми производными замещенного бензамидина общей формулы I
где A представляет собой 1) группу формулы
-O-CmH2m-X1- (II)
где m означает 2-6, а
X1 означает группу формулы
или 2) группу формулы
где X2 означает группу -CnH2n-O-, где n означает 1 или 2;
X3 означает группу -O-CnH2n-;
R1 означает гидроксил, COR7, COOR7;
R2 означает алкил с 1-6 атомами, -CR5R6-арил, или водород (если A означает остаток формулы IV или если X1 означает остаток формулы III), а также алкоксил с 1-6 атомами углерода (если A означает группу формулы II, m имеет вышеуказанное значение и X1 означает группу формулы III);
R3 означает водород, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода (при условии, что R2 означает -CR5R6-арил или если X1 означает группу формулы III);
R4 означает водород или алкил с 1-6 атомами углерода;
R5 и R6 означают алкил с 1-4 атомами углерода;
R7 означает алкил с 1-6 атомами углерода, циклоалкил с 5-7 атомами углерода, арил, гетероарил с атомом азота в качестве гетероатома, аралкил;
при условии, что если
A означает группу -O-CmH2m-X1-, где m = 2, 3 или 4,
X1 означает группу формулы
R2 означает водород, алкил с 1-6 атомами углерода;
R3 означает водород, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода;
R4 означает водород, алкил с 1-6 атомами углерода,
то R1 не означает гидроксил.
где A представляет собой 1) группу формулы
-O-CmH2m-X1- (II)
где m означает 2-6, а
X1 означает группу формулы
или 2) группу формулы
где X2 означает группу -CnH2n-O-, где n означает 1 или 2;
X3 означает группу -O-CnH2n-;
R1 означает гидроксил, COR7, COOR7;
R2 означает алкил с 1-6 атомами, -CR5R6-арил, или водород (если A означает остаток формулы IV или если X1 означает остаток формулы III), а также алкоксил с 1-6 атомами углерода (если A означает группу формулы II, m имеет вышеуказанное значение и X1 означает группу формулы III);
R3 означает водород, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода (при условии, что R2 означает -CR5R6-арил или если X1 означает группу формулы III);
R4 означает водород или алкил с 1-6 атомами углерода;
R5 и R6 означают алкил с 1-4 атомами углерода;
R7 означает алкил с 1-6 атомами углерода, циклоалкил с 5-7 атомами углерода, арил, гетероарил с атомом азота в качестве гетероатома, аралкил;
при условии, что если
A означает группу -O-CmH2m-X1-, где m = 2, 3 или 4,
X1 означает группу формулы
R2 означает водород, алкил с 1-6 атомами углерода;
R3 означает водород, алкил с 1-6 атомами углерода, алкоксил с 1-6 атомами углерода;
R4 означает водород, алкил с 1-6 атомами углерода,
то R1 не означает гидроксил.
Вышеупомянутый арил предпочтительно означает фенил, замещенный гидроксидом, а гетероарил - пиридил, пиридазинил, пиримидил или пиразинил.
В первую группу предпочтительных производных замещенного бензамидина вышеприведенной общей формулы I входят соединения, у которых
A, m, n, X2, X3 и R1 имеют указанное значение,
X1 означает группу формулы III;
R2 означает алкил с 1-6 атомами углерода, -CR5R6-арил или алкоксил с 1-6 атомами углерода (если X1 означает группу формулы III);
R3 означает водород, алкил с 1-6 атомами углерода или алкоксил с 1-6 атомами углерода (если R2 означает -CR5R6-арил);
R4 означает водород;
R5 и R6 означают алкил с 1-3 атомами углерода.
A, m, n, X2, X3 и R1 имеют указанное значение,
X1 означает группу формулы III;
R2 означает алкил с 1-6 атомами углерода, -CR5R6-арил или алкоксил с 1-6 атомами углерода (если X1 означает группу формулы III);
R3 означает водород, алкил с 1-6 атомами углерода или алкоксил с 1-6 атомами углерода (если R2 означает -CR5R6-арил);
R4 означает водород;
R5 и R6 означают алкил с 1-3 атомами углерода.
Во вторую группу предпочтительных производных замещенного бензамидина вышеприведенной общей формулы I входят соединения, у которых
X1 означает группу формулы III;
R1 означает группу COOR7;
R2 означает алкил с 1-6 атомами углерода или -CR5R6-арил;
R3 означает водород, алкил с 1-6 атомами углерода или алкоксил с 1-6 атомами углерода (если R2 означает -CR5R6-арил);
R4 означает водород;
R5, R6 означают алкил с 1-3 атомами углерода;
R7 означает алкил с 1-6 атомами углерода, аралкил или циклоалкил с 5-7 атомами углерода.
X1 означает группу формулы III;
R1 означает группу COOR7;
R2 означает алкил с 1-6 атомами углерода или -CR5R6-арил;
R3 означает водород, алкил с 1-6 атомами углерода или алкоксил с 1-6 атомами углерода (если R2 означает -CR5R6-арил);
R4 означает водород;
R5, R6 означают алкил с 1-3 атомами углерода;
R7 означает алкил с 1-6 атомами углерода, аралкил или циклоалкил с 5-7 атомами углерода.
В частности, предпочитаются производные замещенного бензамидина вышеприведенной общей формулы I, выбранные из группы, включающей (метоксикарбонил-имино-{ 4'-[2-(2-пропилфенокси)-этокси] -бифенил-4- ил}метил)-амин, (бензилоксикарбонил-имино-{4'-[2-(2-пропилфенокси)-этокси]-бифенил-4- ил} метил)-амин, [гидрокси-имино-(4-{3-[4-(1-метил-1-фенилэтил)- феноксиметил] -бензилокси}фенил)-метил]-амин, (этоксикарбонил-имино-(4-{3-[4-(1-метил-1-фенилэтил)-феноксиметил] - бензилокси}фенил)-метил]-амин, [3'-пиридилкарбонил-имино-(4-{ 3-[4-(1- метил-1-фенилэтил)-феноксиметил] -бензилокси} фенил)-метил] -амин и (этоксикарбонил-имино-(4-{3-[4-(1-метил-(4'-гидрокси)фенилэтил)- феноксиметил]-бензилокси}фенил)-метил]амин.
Новые соединения могут содержать один или несколько хиральных центров. Поэтому изобретение относится также к рацематам, чистым энантиомерам или обогащенным энантиомерами формам, в случае необходимости в виде пар диастереомеров. Изобретение также охватывает возможные таутомеры (с остатком -C(NH)-NHR1).
Новые соединения можно получать по известным способам, например нижеследующим.
1. Взаимодействие амидина формулы
где A, R2, R3 и R4 имеют вышеуказанное значение, с соединением формулы
L-R'1 (VI)
где R'1 имеет то же самое значение, что и R1, за исключением гидроксила, а L означает нуклеофильную удаляемую группу, как например атом галогена (например хлор, бром) или ацилоксил.
где A, R2, R3 и R4 имеют вышеуказанное значение, с соединением формулы
L-R'1 (VI)
где R'1 имеет то же самое значение, что и R1, за исключением гидроксила, а L означает нуклеофильную удаляемую группу, как например атом галогена (например хлор, бром) или ацилоксил.
Реакцию целесообразно осуществляют в среде растворителя, такого как, например, тетрагидрофуран, хлористый метилен, хлороформ или диметилформамид, предпочтительно в присутствии основания, такого как, например, карбонат натрия, карбонат калия или натровый щелок, или в присутствии третичного органического основания, такого как, например, триэтиламин, N-этил-диизопропиламин, N-метилморфолин или пиридин, которые могут одновременно служить в качестве растворителя, при температурах между -30 и +100oC, предпочтительно, однако, при температурах между -10 и +80oC.
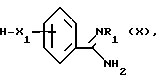
2. Взаимодействие соединений формулы
где R2, R3 и R4 имеют вышеуказанное значение,
с производным бензамидина формулы
или
где L, m, n, X1, X3 и R1 имеют вышеуказанное значение.
где R2, R3 и R4 имеют вышеуказанное значение,
с производным бензамидина формулы
или
где L, m, n, X1, X3 и R1 имеют вышеуказанное значение.
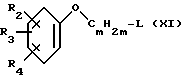
3. Взаимодействие соединений формулы
где X1, R1 и R2 имеют вышеуказанное значение,
с соединением формулы
или
где L, m, n, R2, R3, R4, R8, R9 и X2 имеют вышеуказанное значение.
где X1, R1 и R2 имеют вышеуказанное значение,
с соединением формулы
или
где L, m, n, R2, R3, R4, R8, R9 и X2 имеют вышеуказанное значение.
Способы 2 и 3 целесообразно осуществляют в среде апротонных растворителей, таких как, например, диметилсульфоксид, диметилформамид, ацетонитрил, или спиртов, таких как, например, метанол, этанол, изопропанол, с добавкой основных веществ, таких как, например, карбонаты металла, гидроксиды металла, гидриды металла, при температурах между около 0 и 140oC или же при температуре кипения реакционной смеси.
4. Для получения соединений формулы I, где R1 означает гидроксил:
взаимодействие нитрилов формулы
где A, R2, R3 и R4 имеют вышеуказанное значение,
с гидроксиламином.
взаимодействие нитрилов формулы
где A, R2, R3 и R4 имеют вышеуказанное значение,
с гидроксиламином.
Способ 4 целесообразно осуществляют при нагревании в спирте, таком как, например, метанол, этанол или пропанол, или в среде апротонного растворителя, такого как, например, диметилсульфоксид, диметилформамид или ацетонитрил, в случае необходимости в смеси с водой. Гидроксиламин применяют, например, в виде гидрохлорида или метансульфоната с добавкой пригодного основания, например карбоната натрия.
Исходные вещества можно синтезировать по стандартным методам.
Новые соединения формулы I отличаются многочисленными возможностями терапевтического применения. Следует подчеркнуть такие возможности применения, в случае которых определенную роль играют антагонистическое действие на рецепторы лейкотриена B4. В частности, необходимо назвать следующие области применения: артрит, астма, хронические обструктивные заболевания легких, например хронический бронхит, псориаз, язвенный колит, индуцированная нестероидными противовоспалительными средствами гастропатия или энтеропатия, болезнь Альцгеймера, шок, повреждения, связанные с реперфузией/ишемии, атеросклероз, рассеянный склероз.
Кроме того, новыми соединениями можно лечить болезни или состояния, при которых проход клеток из крови через васкулярный эндотелий в ткань имеет определенное значение (например в случае метастазирования), или болезни и состояния, при которых комбинация лейкотриена B4 или другой молекулы (например 12-оксиэйкозатетраеновой кислоты) с рецептором лейкотриена B4 имеет влияние на клеточную пролиферацию (например хроническая миелоцитическая лейкемия).
Новые соединения можно также применять в комбинации с другими активными началами, например такими, которые применяются в случае тех же самых показаний, или, например, с антиаллергическими средствами, секретолитическими средствами, β2-адренергическими средствами, стероидами для ингаляции, противогистаминными средствами и/или антагонистами фактора активации тромбоцитов. Введение может осуществляться местно, орально, трансдермально, через нос, парентерально или путем ингаляции.
Новые соединения отличаются хорошей переносимостью и благоприятной биологической доступностью.
Терапевтическая или профилактическая доза зависит - кроме от степени действия отдельных соединений и веса тела пациента - от состояния и серьезности болезни. В случае орального применения доза составляет от 10 до 500 мг, предпочтительно от 20 до 250 мг. В случае ингаляции пациенту дают около от 0,5 до 25, предпочтительно около от 2 до 20 мг активного начала. Растворы для ингаляции в общем содержат около от 0,5 до 5% активного начала. Новые соединения можно давать в качестве стандартных препаратов, таких как, например, таблетки, драже, капсулы, облатки, порошки, грануляты, растворы, эмульсии, сиропы, аэрозоли для ингаляции, мази, суппозитории. В качестве примеров стандартных препаратов можно привести следующие конкретные примеры.
1. Таблетки
Состав, вес.ч.:
Активное начало согласно изобретению - 20
Стеариновая кислота - 6
Виноградный сахар - 474
Ингредиенты стандартным образом перерабатывают в таблетки весом 500 мг. При желании можно повышать или уменьшать содержание активного начала и соответственно повышать или уменьшать количество виноградного сахара.
Состав, вес.ч.:
Активное начало согласно изобретению - 20
Стеариновая кислота - 6
Виноградный сахар - 474
Ингредиенты стандартным образом перерабатывают в таблетки весом 500 мг. При желании можно повышать или уменьшать содержание активного начала и соответственно повышать или уменьшать количество виноградного сахара.
2. Суппозитории
Состав, вес.ч.:
Активное начало согласно изобретению - 100
Порошковая лактоза - 45
Какао-масло - 1555
Ингредиенты стандартным образом перерабатывают в суппозитории весом 1,7 г.
Состав, вес.ч.:
Активное начало согласно изобретению - 100
Порошковая лактоза - 45
Какао-масло - 1555
Ингредиенты стандартным образом перерабатывают в суппозитории весом 1,7 г.
3. Порошок для ингаляции
Порошковое активное начало (соединение формулы I) с размером частиц около 0,5 - 7 мкм) подают в количестве 5 мг, в случае необходимости с добавкой порошковой лактозы, в твердые желатиновые капсулы. Порошок ингалируют с помощью любого стандартного ингалятора.
Порошковое активное начало (соединение формулы I) с размером частиц около 0,5 - 7 мкм) подают в количестве 5 мг, в случае необходимости с добавкой порошковой лактозы, в твердые желатиновые капсулы. Порошок ингалируют с помощью любого стандартного ингалятора.
Производные бензамидина согласно изобретению проявляют лучшую переносимость по сравнению с производными бензамидина по вышеприведенному ближайшему аналогу, например с соединением формулы
о чем свидетельствуют результаты опыта, в котором ежедневно в течение 5 дней крысам орально давали соединение примера 2 данной заявки и вышеуказанное известное соединение в дозах 30, 100 и 300 мг/кг. Каждый день животных исследовали на наличие симптомов и в последний день определяли действие на желудочно-кишечный тракт. При этом было установлено, что при даче известного соединения в дозе 300 мг/кг умерло одно из десяти животных, а восемь животных должны были умерщвляться из-за наличия синдромов одышки. При последующей аутопсии в легких были обнаружены кровотечения. Даже при даче известного соединения в дозе 100 мг/кг умерло два животных.
о чем свидетельствуют результаты опыта, в котором ежедневно в течение 5 дней крысам орально давали соединение примера 2 данной заявки и вышеуказанное известное соединение в дозах 30, 100 и 300 мг/кг. Каждый день животных исследовали на наличие симптомов и в последний день определяли действие на желудочно-кишечный тракт. При этом было установлено, что при даче известного соединения в дозе 300 мг/кг умерло одно из десяти животных, а восемь животных должны были умерщвляться из-за наличия синдромов одышки. При последующей аутопсии в легких были обнаружены кровотечения. Даже при даче известного соединения в дозе 100 мг/кг умерло два животных.
В отличие от известного соединения соединение примера 2 данной заявки переносилось животными без проблем, т.е. состояние подопытных животных ничем не отличалось от тех подопытных животных, которым давали только носитель (без добавки активного вещества).
Нижеприведенные примеры поясняют получение новых соединений.
Пример 1. (Метоксикарбонил-имино-{4'-[2-(2-пропилфенокси)- этокси]-бифенил-4-ил}-метил)-амин
3,8 г амидинового соединения вышеуказанной формулы, где R = NH (которое можно получать по стандартным способам, описанным, например, в вышеуказанном ближайшем аналоге), суспендируют в 200 мл хлороформа. К смеси добавляют 1,6 мл триэтиламина и при комнатной температуре прикапывают 0,8 мл сложного метилового эфира хлормуравьиной кислоты. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Выход соединения вышеприведенной формулы, где R = NCOOCH3: 3,7 г.
3,8 г амидинового соединения вышеуказанной формулы, где R = NH (которое можно получать по стандартным способам, описанным, например, в вышеуказанном ближайшем аналоге), суспендируют в 200 мл хлороформа. К смеси добавляют 1,6 мл триэтиламина и при комнатной температуре прикапывают 0,8 мл сложного метилового эфира хлормуравьиной кислоты. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Выход соединения вышеприведенной формулы, где R = NCOOCH3: 3,7 г.
Т.п.: 170-176oC.
Пример 2. (Бензилоксикарбонил-имино-{4'-[2-(2-пропилфенокси)- этокси]-бифенил-4-ил}-метил)-амин
2,6 г амидинового соединения вышеуказанной формулы, где R = NH, подают в 200 мл хлороформа. К смеси добавляют 1,3 мл триэтиламина и при комнатной температуре прикапывают 1 мл сложного бензилового эфира хлормуравьиной кислоты. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Продукт перекристаллизуют из этанола. Выход соединения вышеприведенной формулы, где R = NCOOCH2Ph: 2,2 г.
2,6 г амидинового соединения вышеуказанной формулы, где R = NH, подают в 200 мл хлороформа. К смеси добавляют 1,3 мл триэтиламина и при комнатной температуре прикапывают 1 мл сложного бензилового эфира хлормуравьиной кислоты. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Продукт перекристаллизуют из этанола. Выход соединения вышеприведенной формулы, где R = NCOOCH2Ph: 2,2 г.
Т.п.: 128-131oC.
Соответственно полученные соединения с другими остатками R:
R = NCOOC2H5; Т.п.: 120-123oC
R = NCOO-н-C3H7; Т.п.: 113-114oC
R = NCOO-изо-C3H7: Т.п.: 110-117oC
R = NCOO-н-C4H9: Т.п.: 135-138oC
R = NCOO-изо-C4H9; Т.п.: 103oC
R = NCOO-трет-C4H9: Т.п.: 129-132oC
R = NCOO-н-C6H13: Т.п.: 117-121oC
Пример 3. 3,5 г амидинового соединения вышеуказанной формулы, где R = NH, подают в 150 мл хлороформа. К смеси добавляют 2 мл триэтиламина и при комнатной температуре прикапывают 1 мл ди-трет-бутилдикарбоната. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Продукт перекристаллизуют из 20 мл этанола. Выход соединения вышеприведенной формулы, где R = NCOO-трет-бутил: 3 г.
R = NCOOC2H5; Т.п.: 120-123oC
R = NCOO-н-C3H7; Т.п.: 113-114oC
R = NCOO-изо-C3H7: Т.п.: 110-117oC
R = NCOO-н-C4H9: Т.п.: 135-138oC
R = NCOO-изо-C4H9; Т.п.: 103oC
R = NCOO-трет-C4H9: Т.п.: 129-132oC
R = NCOO-н-C6H13: Т.п.: 117-121oC
Пример 3. 3,5 г амидинового соединения вышеуказанной формулы, где R = NH, подают в 150 мл хлороформа. К смеси добавляют 2 мл триэтиламина и при комнатной температуре прикапывают 1 мл ди-трет-бутилдикарбоната. После растворения компонентов перемешивают в течение 3 часов, три раза экстрагируют водой, упаривают, остаток перемешивают с диэтиловым эфиром и отсасывают. Продукт перекристаллизуют из 20 мл этанола. Выход соединения вышеприведенной формулы, где R = NCOO-трет-бутил: 3 г.
Т.п.: 129-132oC.
Пример 4. а) [Гидрокси-имино-(4-{3-[4-(1-метил-1-фенилэтил)- феноксиметил]-бензилокси}фенил)-метил]-амин
5,25 г полученного по стандартным приемам нитрила вышеуказанной формулы, где R = CN, подают в 60 мл этанола и кипятят. В течение 30 минут к смеси прикапывают раствор 2,7 г карбоната натрия и 3,4 г гидроксиламина в виде гидрохлорида в 10 мл воды. Затем кипятят с обратным холодильником в течение 5 часов. После охлаждения смесь сгущают, остаток подают в 50 мл воды и три раза экстрагируют этилацетатом, взятым в количестве по 40 мл. Органические фазы сушат над сульфатом магния, фильтруют и сгущают. Кристаллы подают в 20 мл ацетона и подкисляют эфирной соляной кислотой. После недолгого растворения образуется 5,3 г гидрохлорида амидоксима вышеприведенной формулы, где R = C(NOH)-NH2.
5,25 г полученного по стандартным приемам нитрила вышеуказанной формулы, где R = CN, подают в 60 мл этанола и кипятят. В течение 30 минут к смеси прикапывают раствор 2,7 г карбоната натрия и 3,4 г гидроксиламина в виде гидрохлорида в 10 мл воды. Затем кипятят с обратным холодильником в течение 5 часов. После охлаждения смесь сгущают, остаток подают в 50 мл воды и три раза экстрагируют этилацетатом, взятым в количестве по 40 мл. Органические фазы сушат над сульфатом магния, фильтруют и сгущают. Кристаллы подают в 20 мл ацетона и подкисляют эфирной соляной кислотой. После недолгого растворения образуется 5,3 г гидрохлорида амидоксима вышеприведенной формулы, где R = C(NOH)-NH2.
Т.п.: 180-181oC.
б) [Имино-(4-{3-[4-(1-метил-1-фенилэтил)-феноксиметил]- бензилокси}фенил)-метил]-амин
5,1 г амидоксима вышеуказанной формулы, где R = NOH, растворяют в 120 мл метанола и гидрируют в присутствии 10 г увлажненного метанолом никеля Ренея при атмосферном давлении и комнатной температуре в течение 2 часов. Никель отсасывают и раствор фильтруют над кизельгуром. Фильтрат подкисляют этанольной соляной кислотой, раствор сгущают и перекристаллизуют из этанола. Выход составляет 3,3 г амидинового соединения вышеприведенной формулы, где R = NH.
5,1 г амидоксима вышеуказанной формулы, где R = NOH, растворяют в 120 мл метанола и гидрируют в присутствии 10 г увлажненного метанолом никеля Ренея при атмосферном давлении и комнатной температуре в течение 2 часов. Никель отсасывают и раствор фильтруют над кизельгуром. Фильтрат подкисляют этанольной соляной кислотой, раствор сгущают и перекристаллизуют из этанола. Выход составляет 3,3 г амидинового соединения вышеприведенной формулы, где R = NH.
Т.п.: 160oC.
в) [Этоксикарбонил-имино-(4-{ 3-[4-(1-метил-1-фенилэтил)- феноксиметил] -бензилокси}фенил)-метил]-амин
2,44 г полученного на стадии б) амидинового соединения вышеуказанной формулы, где R = NH, подают в 150 мл дихлорметана. К смеси добавляют 0,6 г сложного этилового эфира хлормуравьиной кислоты, после чего при комнатной температуре в течение 15 минут прикапывают 52,5 мл 0,2 н. натрового щелока. Получаемый раствор перемешивают при комнатной температуре в течение 2 часов. Потом органическую фазу отделяют, экстрагируют 100 мл воды и сушат над сульфатом натрия. Раствор сгущают и остаток перекристаллизуют из 10 мл этанола. Получают 2,1 г целевого соединения, где R = NCOOC2H5.
2,44 г полученного на стадии б) амидинового соединения вышеуказанной формулы, где R = NH, подают в 150 мл дихлорметана. К смеси добавляют 0,6 г сложного этилового эфира хлормуравьиной кислоты, после чего при комнатной температуре в течение 15 минут прикапывают 52,5 мл 0,2 н. натрового щелока. Получаемый раствор перемешивают при комнатной температуре в течение 2 часов. Потом органическую фазу отделяют, экстрагируют 100 мл воды и сушат над сульфатом натрия. Раствор сгущают и остаток перекристаллизуют из 10 мл этанола. Получают 2,1 г целевого соединения, где R = NCOOC2H5.
Т.п.: 99oC.
Аналогичным образом можно получать, например, следующие соединения указанной в примере 4 б) формулы:
R = NCOO-(-)-ментил; Т.п.: 113oC
R = NCO-C6H5; Т.п.: 101-103oC
Пример 5. [3'-пиридилкарбонил-имино-(4-{3-[4-(1-метил-1-фенилэтил)- феноксиметил]-бензилокси}фенил)-метил]-амин
5,0 г амидинового соединения вышеуказанной формулы, где R = NH (см. пример 4 б)), подают в 250 мл дихлорметана. В течение 10 минут при комнатной температуре прикапывают раствор 3,9 г хлорида никотиновой кислоты в виде гидрохлорида и 16,3 мл триэтиламина в 50 мл дихлорметана. Спустя 15 часов при комнатной температуре два раза экстрагируют водой, взятой в количестве по 300 мл. Органическую фазу сушат над сульфатом натрия, фильтруют и фильтрат сгущают. Остаток очищают путем хроматографии низкого давления на силикагеле марки 60 с применением в качестве элюента этилацетата. Продукт растворяют в 50 мл ацетона, подкисляют этанольной соляной кислотой и после добавления диэтилового эфира осаждают в виде гидрохлорида. Выход составляет 2,0 г производного никотиноила вышеуказанной формулы, где R = N-CO-3-пиридил, с т.п. 172oC.
R = NCOO-(-)-ментил; Т.п.: 113oC
R = NCO-C6H5; Т.п.: 101-103oC
Пример 5. [3'-пиридилкарбонил-имино-(4-{3-[4-(1-метил-1-фенилэтил)- феноксиметил]-бензилокси}фенил)-метил]-амин
5,0 г амидинового соединения вышеуказанной формулы, где R = NH (см. пример 4 б)), подают в 250 мл дихлорметана. В течение 10 минут при комнатной температуре прикапывают раствор 3,9 г хлорида никотиновой кислоты в виде гидрохлорида и 16,3 мл триэтиламина в 50 мл дихлорметана. Спустя 15 часов при комнатной температуре два раза экстрагируют водой, взятой в количестве по 300 мл. Органическую фазу сушат над сульфатом натрия, фильтруют и фильтрат сгущают. Остаток очищают путем хроматографии низкого давления на силикагеле марки 60 с применением в качестве элюента этилацетата. Продукт растворяют в 50 мл ацетона, подкисляют этанольной соляной кислотой и после добавления диэтилового эфира осаждают в виде гидрохлорида. Выход составляет 2,0 г производного никотиноила вышеуказанной формулы, где R = N-CO-3-пиридил, с т.п. 172oC.
Claims (10)
1. Производные замещенного бензамидина общей формулы (I)
где A представляет собой:
1) группу формулы II
-O-CmH2m-X1-
где m = 2 - 6; X1 - группа формулы
или 2) группу формулы
где X2 - группа -CnH2n-O-, где n = 1 или 2; X3 - группа -O-CnH2n-;
R1 - гидроксил, COR7, COOR7;
R2 - алкил с 1 - 6 атомами, -CR5R6-арил или водород (если A - остаток формулы (IV) или если X1 - остаток формулы (III)), а также алкоксил с 1 - 6 атомами углерода (если A - группа формулы (II), m имеет указанное значение и X1 - группа формулы (III));
R3 - водород, алкил с 1 - 6 атомами углерода, алкоксил с 1 - 6 атомами углерода (при условии, что R2 - -CR5R6-арил или если X1 - группа формулы (III));
R4 - водород или алкил с 1 - 6 атомами углерода;
R5 и R6 - алкил с 1 - 4 атомами углерода;
R7 - алкил с 1 - 6 атомами углерода, циклоалкил с 5 - 7 атомами углерода, арил, гетероарил с атомом азота в качестве гетероатома, аралкил;
при условии, что если A - группа -O-CmH2m-X1-, где m = 2, 3 или 4, X1 - группа формулы
R2 - водород, алкил с 1 - 6 атомами углерода; R3 - водород, алкил с 1 - 6 атомами углерода, алкоксил с 1 - 6 атомами углерода; R4 - водород, алкил с 1 - 6 атомами углерода, то R1 не означает гидроксил.
где A представляет собой:
1) группу формулы II
-O-CmH2m-X1-
где m = 2 - 6; X1 - группа формулы
или 2) группу формулы
где X2 - группа -CnH2n-O-, где n = 1 или 2; X3 - группа -O-CnH2n-;
R1 - гидроксил, COR7, COOR7;
R2 - алкил с 1 - 6 атомами, -CR5R6-арил или водород (если A - остаток формулы (IV) или если X1 - остаток формулы (III)), а также алкоксил с 1 - 6 атомами углерода (если A - группа формулы (II), m имеет указанное значение и X1 - группа формулы (III));
R3 - водород, алкил с 1 - 6 атомами углерода, алкоксил с 1 - 6 атомами углерода (при условии, что R2 - -CR5R6-арил или если X1 - группа формулы (III));
R4 - водород или алкил с 1 - 6 атомами углерода;
R5 и R6 - алкил с 1 - 4 атомами углерода;
R7 - алкил с 1 - 6 атомами углерода, циклоалкил с 5 - 7 атомами углерода, арил, гетероарил с атомом азота в качестве гетероатома, аралкил;
при условии, что если A - группа -O-CmH2m-X1-, где m = 2, 3 или 4, X1 - группа формулы
R2 - водород, алкил с 1 - 6 атомами углерода; R3 - водород, алкил с 1 - 6 атомами углерода, алкоксил с 1 - 6 атомами углерода; R4 - водород, алкил с 1 - 6 атомами углерода, то R1 не означает гидроксил.
2. Производные замещенного бензамидина по п.1 общей формулы (I), где арил означает фенил или фенил, замещенный гидроксилом, гетероарил означает пиридил, пиридазинил, пиримидил или пиразинил.
3. Производные замещенного бензамидина по п.1 или 2 общей формулы (I), где A, m, n, X2, X3 и R1 имеют указанные значения, X1 - группа формулы (III); R2 - алкил с 1 - 6 атомами углерода, -CR5R6-арил или алкоксил с 1 - 6 атомами углерода (если X1 - группа формулы (III)); R3 - водород, алкил с 1 - 6 атомами углерода или алкоксил с 1 - 6 атомами углерода (если R2 - -CR5R6-арил); R4 - водород; R5 и R6 - алкил с 1 - 3 атомами углерода.
4. Производные замещенного бензамидина по п.1 или 2 общей формулы (I), где X1 - группа формулы (III); R1 - группа COOR7; R2 - алкил с 1 - 6 атомами углерода или -CR5R6-арил; R3 - водород, алкил с 1 - 6 атомами углерода или алкоксил с 1 - 6 атомами углерода (если R2 - -CR5R6-арил); R4 - водород; R5 и R6 - алкил с 1 - 3 атомами углерода; R7 - алкил с 1 - 6 атомами углерода, аралкил или циклоалкил с 5 - 7 атомами углерода.
5. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой (метоксикарбонил-имино-{4'-[2-(2-пропилфенокси)-этокси] -бифенил-4-ил}метил)-амин.
6. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой (бензилоксикарбонил-имино-{4'-[2-(2-пропилфенокси)-этокси]-бифенил-4-ил}метил)-амин.
7. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой [гидрокси-имино-(4-{3-[4-(1-метил-1-фенилэтил)-феноксиметил]-бензилокси}фенил)-метил]-амин.
8. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой (этоксикарбонил-имино-(4-{3-[4-(1-метил-1-фенилэтил)-феноксиметил]-бензилокси}фенил)-метил]-амин.
9. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой [3'-пиридилкарбонил-имино-(4-{3-[4-(1-метил-1-фенилэтил)-феноксиметил]-бензилокси}фенил)-метил]-амин.
10. Производное замещенного бензамидина общей формулы (I) по п.1, представляющее собой (этоксикарбонил-имино-(4-{ 3-[4-(1-метил-(4'-гидрокси)фенилэтил)-феноксиметил]-бензилокси}фенил)-метил)амин.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DEP4424713.3 | 1994-07-13 | ||
| DE4424713A DE4424713A1 (de) | 1994-07-13 | 1994-07-13 | Substituierte Benzamidine, ihre Herstellung und Verwendung als Arnzneistoffe |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU97102043A RU97102043A (ru) | 1999-02-27 |
| RU2159228C2 true RU2159228C2 (ru) | 2000-11-20 |
Family
ID=6523047
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU97102043/04A RU2159228C2 (ru) | 1994-07-13 | 1995-06-03 | Производные замещенного бензамидина |
Country Status (37)
| Country | Link |
|---|---|
| US (1) | US5731332A (ru) |
| EP (1) | EP0770059B1 (ru) |
| JP (1) | JP2931410B2 (ru) |
| KR (1) | KR100421580B1 (ru) |
| CN (1) | CN1083830C (ru) |
| AT (1) | ATE178590T1 (ru) |
| AU (1) | AU700585B2 (ru) |
| BG (1) | BG62090B1 (ru) |
| BR (1) | BR9508374A (ru) |
| CA (1) | CA2194885C (ru) |
| CO (1) | CO4410184A1 (ru) |
| CZ (1) | CZ289376B6 (ru) |
| DE (2) | DE4424713A1 (ru) |
| DK (1) | DK0770059T3 (ru) |
| EE (1) | EE03311B1 (ru) |
| ES (1) | ES2131830T3 (ru) |
| FI (1) | FI970094A (ru) |
| GR (1) | GR3030043T3 (ru) |
| HK (1) | HK1011966A1 (ru) |
| HR (1) | HRP950365B1 (ru) |
| HU (1) | HU224823B1 (ru) |
| IL (1) | IL114571A (ru) |
| MX (1) | MX9700273A (ru) |
| MY (1) | MY117090A (ru) |
| NO (1) | NO307373B1 (ru) |
| NZ (1) | NZ287883A (ru) |
| PE (1) | PE32496A1 (ru) |
| PL (1) | PL179595B1 (ru) |
| RO (1) | RO118653B1 (ru) |
| RU (1) | RU2159228C2 (ru) |
| SA (1) | SA95160355B1 (ru) |
| SK (1) | SK281744B6 (ru) |
| TW (1) | TW555738B (ru) |
| UA (1) | UA45351C2 (ru) |
| WO (1) | WO1996002497A1 (ru) |
| YU (1) | YU48934B (ru) |
| ZA (1) | ZA955780B (ru) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6191169B1 (en) | 1992-08-28 | 2001-02-20 | City Of Hope | Human leukocyte 12-lipoxygenase and its role in the pathogenesis of disease states |
| US6486181B1 (en) | 1992-08-28 | 2002-11-26 | City Of Hope | Human leukocutye 12-lipoxygenase and its role in the pathogenesis of disease states |
| DK0813525T3 (da) * | 1995-03-10 | 2004-02-16 | Berlex Lab | Benzamidinderivater, deres fremstilling og anvendelse som antikoagulanter |
| WO1996036347A1 (en) * | 1995-05-17 | 1996-11-21 | Eli Lilly And Company | Use of leukotriene antagonists for alzheimer's disease |
| DE19636689A1 (de) * | 1996-09-10 | 1998-03-12 | Boehringer Ingelheim Kg | Neue Benzamidinderivate |
| DE19718334A1 (de) * | 1997-04-30 | 1998-11-05 | Boehringer Ingelheim Pharma | Neue Benzylaminderivate und Phenylethylaminderivate, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| TW513402B (en) * | 1997-05-30 | 2002-12-11 | Daiichi Seiyaku Co | Process for preparing 3-(7-amidino-2-naphthyl)-2-phenylpropionic acid derivatives |
| EP1023064A1 (en) * | 1997-10-15 | 2000-08-02 | City Of Hope | 12(s)-hete receptor blockers |
| ID24720A (id) | 1997-12-12 | 2000-08-03 | Novartis Ag | Senyawa amidino tersubstitusi dalam perawatan penyakit gangguan paru-paru kronis |
| DE19834713A1 (de) * | 1998-07-31 | 2000-02-03 | Boehringer Ingelheim Pharma | Neue Phenylethylaminderivate, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| US6291531B1 (en) * | 1999-10-07 | 2001-09-18 | Boehringer Ingelheim Pharma Kg | LTB4 antagonist, processes for the preparation thereof and its use as a pharmaceutical composition |
| DE10000907A1 (de) * | 2000-01-12 | 2001-07-19 | Boehringer Ingelheim Pharma | Verfahren zur Herstellung von Aryl-iminomethyl-carbaminsäureestern |
| US6417382B2 (en) * | 2000-01-12 | 2002-07-09 | Boehringer Ingelheim Pharma Kg | Process for preparing aryl-iminomethyl-carbamino acid esters |
| US6528491B2 (en) * | 2000-10-24 | 2003-03-04 | Boehringer Ingelheim Pharma Kg | Pyranoside derivatives |
| CA2433451A1 (en) | 2001-01-16 | 2002-07-18 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Use of an ltb4 antagonist for the treatment and/or prevention of diseases caused by increased expression of mucin genes |
| US20030119901A1 (en) * | 2001-07-14 | 2003-06-26 | Boehringer Ingelheim Pharma Kg | Pharmaceutical formulation containing an LTB4 antagonist |
| IL159493A0 (en) * | 2001-07-14 | 2004-06-01 | Boehringer Ingeiheim Pharma Gm | Pharmaceutical formulation containing an ltb4 antagonist |
| IL160208A0 (en) * | 2001-08-31 | 2004-07-25 | Neurochem Int Ltd | Amidine derivatives for treating amyloidosis |
| RS20050390A (en) * | 2002-11-26 | 2008-04-04 | Boehringer Ingelheim Pharma Gmbh. & Co.Kg., | Pharmaceutical composition comprising a ltb4 antagonist and a cox-2 inhibitor or a combined cox 1/2 inhibitor |
| DE10350528A1 (de) * | 2003-10-29 | 2005-06-09 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Arzneimittelformulierung, enthaltend einen LTB4-Antagonisten, sowie Verfahren zu deren Herstellung und deren Verwendung |
| US7262223B2 (en) * | 2004-01-23 | 2007-08-28 | Neurochem (International) Limited | Amidine derivatives for treating amyloidosis |
| CN103012200B (zh) * | 2011-09-20 | 2014-12-17 | 北京大学 | 具有β-分泌酶抑制功能的化合物及其制备方法与应用 |
| WO2018207950A1 (ja) | 2017-05-12 | 2018-11-15 | 横山 茂之 | クラスa gpcr結合性化合物改変体 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0518818A3 (en) * | 1991-06-11 | 1993-04-28 | Ciba-Geigy Ag | Arylethers, their manufacture and use as medicament |
| ATE125791T1 (de) * | 1991-06-11 | 1995-08-15 | Ciba Geigy Ag | Amidino-verbindungen, ihre herstellung und verwendung als arzneimittel. |
| US5451700A (en) * | 1991-06-11 | 1995-09-19 | Ciba-Geigy Corporation | Amidino compounds, their manufacture and methods of treatment |
| DK0902013T3 (da) * | 1992-02-05 | 2002-03-25 | Boehringer Ingelheim Pharma | Hidtil ukendte amidinderivater, deres fremstilling og anvendelse som lægemidler med LTB4-antagonistisk virkning |
| US5455274A (en) * | 1992-12-09 | 1995-10-03 | Ciba-Geigy Corporation | Hydroxyamidine derivatives |
-
1994
- 1994-07-13 DE DE4424713A patent/DE4424713A1/de not_active Withdrawn
-
1995
- 1995-06-03 ES ES95921824T patent/ES2131830T3/es not_active Expired - Lifetime
- 1995-06-03 NZ NZ287883A patent/NZ287883A/xx not_active IP Right Cessation
- 1995-06-03 JP JP8504618A patent/JP2931410B2/ja not_active Expired - Lifetime
- 1995-06-03 KR KR1019970700124A patent/KR100421580B1/ko not_active IP Right Cessation
- 1995-06-03 UA UA97020598A patent/UA45351C2/uk unknown
- 1995-06-03 DE DE59505600T patent/DE59505600D1/de not_active Expired - Lifetime
- 1995-06-03 HU HU9700059A patent/HU224823B1/hu not_active IP Right Cessation
- 1995-06-03 PL PL95318115A patent/PL179595B1/pl not_active IP Right Cessation
- 1995-06-03 DK DK95921824T patent/DK0770059T3/da active
- 1995-06-03 RU RU97102043/04A patent/RU2159228C2/ru not_active IP Right Cessation
- 1995-06-03 MX MX9700273A patent/MX9700273A/es not_active IP Right Cessation
- 1995-06-03 BR BR9508374A patent/BR9508374A/pt not_active IP Right Cessation
- 1995-06-03 WO PCT/EP1995/002112 patent/WO1996002497A1/de active IP Right Grant
- 1995-06-03 RO RO97-00018A patent/RO118653B1/ro unknown
- 1995-06-03 AU AU26742/95A patent/AU700585B2/en not_active Ceased
- 1995-06-03 CN CN95194048A patent/CN1083830C/zh not_active Expired - Fee Related
- 1995-06-03 AT AT95921824T patent/ATE178590T1/de active
- 1995-06-03 CZ CZ199766A patent/CZ289376B6/cs not_active IP Right Cessation
- 1995-06-03 CA CA002194885A patent/CA2194885C/en not_active Expired - Fee Related
- 1995-06-03 EP EP95921824A patent/EP0770059B1/de not_active Expired - Lifetime
- 1995-06-03 EE EE9700066A patent/EE03311B1/xx not_active IP Right Cessation
- 1995-06-03 SK SK19-97A patent/SK281744B6/sk not_active IP Right Cessation
- 1995-06-03 US US08/765,692 patent/US5731332A/en not_active Expired - Lifetime
- 1995-06-28 HR HRP4424713.3A patent/HRP950365B1/xx not_active IP Right Cessation
- 1995-07-04 TW TW084106873A patent/TW555738B/zh active
- 1995-07-06 YU YU45295A patent/YU48934B/sh unknown
- 1995-07-11 PE PE1995273519A patent/PE32496A1/es not_active Application Discontinuation
- 1995-07-12 CO CO95030618A patent/CO4410184A1/es unknown
- 1995-07-12 IL IL11457195A patent/IL114571A/xx not_active IP Right Cessation
- 1995-07-12 ZA ZA955780A patent/ZA955780B/xx unknown
- 1995-07-13 MY MYPI95001982A patent/MY117090A/en unknown
- 1995-11-01 SA SA95160355A patent/SA95160355B1/ar unknown
-
1997
- 1997-01-04 BG BG101105A patent/BG62090B1/bg unknown
- 1997-01-10 NO NO970122A patent/NO307373B1/no unknown
- 1997-01-10 FI FI970094A patent/FI970094A/fi not_active Application Discontinuation
-
1998
- 1998-12-14 HK HK98113328A patent/HK1011966A1/xx not_active IP Right Cessation
-
1999
- 1999-04-23 GR GR990401120T patent/GR3030043T3/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2159228C2 (ru) | Производные замещенного бензамидина | |
| KR0142417B1 (ko) | 3급알킬작용성화된피레라진유도체 | |
| JP3054677B2 (ja) | 第三級アルキル官能基化ピペラジン誘導体 | |
| JP4617292B2 (ja) | アリールアルキルカルバメート誘導体の製造およびそれらの治療用途 | |
| JP2000515133A (ja) | 血糖降下性および脂質低下性の化合物 | |
| JPH10182583A (ja) | 新規ヒドロキサム酸誘導体 | |
| US5686496A (en) | Chemical compound, the preparation thereof and its use in pharmaceutical compositions | |
| KR100300566B1 (ko) | 피리미디논유도체와그의제조방법및용도 | |
| WO1997032863A1 (fr) | Derives de thiazolidine-2,4-dione | |
| EP0164247B1 (en) | Dihydropyridines | |
| JP2018538355A (ja) | ベンズアミド誘導体 | |
| US20060135785A1 (en) | Alpha-phenyl acetanilide derivatives having an acat inhibiting activity and the therapeutic application thereof | |
| JP7312745B2 (ja) | アゼチジン誘導体及びそのプロドラッグ | |
| US20040087604A1 (en) | Hetero-tricyclic compounds having substituted amino groups | |
| EP0055145B1 (en) | 4-(aminomethyl)cyclohexane-1-carboxylic acid derivatives | |
| US6046218A (en) | Pyridine derivative and medicament containing the same as an effective ingredient | |
| KR820000508B1 (ko) | 페닐에탄올 아민 유도체의 제조방법 | |
| EP0971916A1 (fr) | Derives de n-(arginyl)benzenesulfonamide et leur utilisation comme agents antithrombotiques | |
| JPS603391B2 (ja) | 新規ピリミジン化合物の製法 | |
| CA2077238A1 (en) | N-phenyl-n'-alkyl-n'-pyridylmethyl- bis-diamino-5-methylene-1,3-dioxane- 4,6-dione inhibitors of acyl-coa: cholesterol-acyl transferase | |
| JPH0772168B2 (ja) | グアニジノ安息香酸エステル誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20090604 |