KR101238525B1 - Cetp 저해제로서의 신규 벤질아민 유도체 - Google Patents
Cetp 저해제로서의 신규 벤질아민 유도체 Download PDFInfo
- Publication number
- KR101238525B1 KR101238525B1 KR1020077017632A KR20077017632A KR101238525B1 KR 101238525 B1 KR101238525 B1 KR 101238525B1 KR 1020077017632 A KR1020077017632 A KR 1020077017632A KR 20077017632 A KR20077017632 A KR 20077017632A KR 101238525 B1 KR101238525 B1 KR 101238525B1
- Authority
- KR
- South Korea
- Prior art keywords
- carbon atoms
- alkyl
- independently selected
- cycloalkyl
- formula
- Prior art date
Links
- 150000003939 benzylamines Chemical class 0.000 title abstract description 46
- 239000003354 cholesterol ester transfer protein inhibitor Substances 0.000 title description 4
- -1 benzylamine compound Chemical class 0.000 claims abstract description 264
- 238000000034 method Methods 0.000 claims abstract description 100
- 125000004432 carbon atom Chemical group C* 0.000 claims description 550
- 125000000217 alkyl group Chemical group 0.000 claims description 330
- 125000005842 heteroatom Chemical group 0.000 claims description 326
- 150000001875 compounds Chemical class 0.000 claims description 285
- 125000000623 heterocyclic group Chemical group 0.000 claims description 210
- 125000001072 heteroaryl group Chemical group 0.000 claims description 203
- 229910005965 SO 2 Inorganic materials 0.000 claims description 187
- 125000001424 substituent group Chemical group 0.000 claims description 187
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 177
- 150000003839 salts Chemical class 0.000 claims description 151
- 125000003118 aryl group Chemical group 0.000 claims description 144
- 125000001188 haloalkyl group Chemical group 0.000 claims description 136
- 239000001257 hydrogen Substances 0.000 claims description 122
- 229910052739 hydrogen Inorganic materials 0.000 claims description 122
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 109
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 70
- 229910052757 nitrogen Inorganic materials 0.000 claims description 50
- 125000003545 alkoxy group Chemical group 0.000 claims description 49
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 45
- 229910052736 halogen Inorganic materials 0.000 claims description 45
- 150000002367 halogens Chemical class 0.000 claims description 45
- 229910052717 sulfur Inorganic materials 0.000 claims description 42
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 41
- 125000002950 monocyclic group Chemical group 0.000 claims description 29
- 125000002619 bicyclic group Chemical group 0.000 claims description 26
- 125000004122 cyclic group Chemical group 0.000 claims description 26
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 25
- 125000003831 tetrazolyl group Chemical group 0.000 claims description 24
- 125000002971 oxazolyl group Chemical group 0.000 claims description 22
- 125000004076 pyridyl group Chemical group 0.000 claims description 22
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 21
- 125000000842 isoxazolyl group Chemical group 0.000 claims description 20
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 20
- 125000000335 thiazolyl group Chemical group 0.000 claims description 20
- 125000004438 haloalkoxy group Chemical group 0.000 claims description 19
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 17
- 125000004429 atom Chemical group 0.000 claims description 13
- 125000001781 1,3,4-oxadiazolyl group Chemical group 0.000 claims description 12
- 125000004104 aryloxy group Chemical group 0.000 claims description 12
- 150000004820 halides Chemical class 0.000 claims description 12
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 11
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims description 9
- 229910052799 carbon Inorganic materials 0.000 claims description 6
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 claims description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 4
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 4
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 2
- 229910052760 oxygen Inorganic materials 0.000 claims 40
- 239000000203 mixture Substances 0.000 abstract description 214
- WGQKYBSKWIADBV-UHFFFAOYSA-N aminomethyl benzene Natural products NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 abstract description 62
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 30
- 201000010099 disease Diseases 0.000 abstract description 27
- 108010061846 Cholesterol Ester Transfer Proteins Proteins 0.000 abstract description 21
- 102000012336 Cholesterol Ester Transfer Proteins Human genes 0.000 abstract description 21
- 208000024891 symptom Diseases 0.000 abstract description 17
- 239000000126 substance Substances 0.000 abstract description 12
- 102000004895 Lipoproteins Human genes 0.000 abstract description 7
- 108090001030 Lipoproteins Proteins 0.000 abstract description 7
- 230000008604 lipoprotein metabolism Effects 0.000 abstract description 5
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 139
- 235000002639 sodium chloride Nutrition 0.000 description 137
- 230000015572 biosynthetic process Effects 0.000 description 88
- 238000003786 synthesis reaction Methods 0.000 description 88
- 238000006243 chemical reaction Methods 0.000 description 81
- 239000000651 prodrug Substances 0.000 description 69
- 229940002612 prodrug Drugs 0.000 description 69
- 239000002904 solvent Substances 0.000 description 67
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 63
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 57
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 53
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 53
- 238000002360 preparation method Methods 0.000 description 50
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 48
- 235000019439 ethyl acetate Nutrition 0.000 description 47
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 44
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 43
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 41
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 40
- 239000000243 solution Substances 0.000 description 38
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 37
- 125000004939 6-pyridyl group Chemical group N1=CC=CC=C1* 0.000 description 36
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 36
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 35
- 239000007788 liquid Substances 0.000 description 35
- 238000003756 stirring Methods 0.000 description 32
- 239000002585 base Substances 0.000 description 31
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 27
- 108010010234 HDL Lipoproteins Proteins 0.000 description 26
- 102000015779 HDL Lipoproteins Human genes 0.000 description 26
- 239000012044 organic layer Substances 0.000 description 26
- 239000011541 reaction mixture Substances 0.000 description 26
- 229910052938 sodium sulfate Inorganic materials 0.000 description 26
- 235000011152 sodium sulphate Nutrition 0.000 description 26
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 26
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 24
- 239000007787 solid Substances 0.000 description 24
- 238000011282 treatment Methods 0.000 description 23
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 22
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol group Chemical group [C@@H]1(CC[C@H]2[C@@H]3CC=C4C[C@@H](O)CC[C@]4(C)[C@H]3CC[C@]12C)[C@H](C)CCCC(C)C HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 22
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 21
- 239000000741 silica gel Substances 0.000 description 21
- 229910002027 silica gel Inorganic materials 0.000 description 21
- 239000008194 pharmaceutical composition Substances 0.000 description 20
- 229910000027 potassium carbonate Inorganic materials 0.000 description 20
- 235000011181 potassium carbonates Nutrition 0.000 description 20
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 19
- NKUQXCMUVWBWBU-UHFFFAOYSA-N n-(cyclobutylmethyl)ethanamine Chemical compound CCNCC1CCC1 NKUQXCMUVWBWBU-UHFFFAOYSA-N 0.000 description 19
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 19
- 239000000047 product Substances 0.000 description 19
- 230000035484 reaction time Effects 0.000 description 19
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 18
- 239000012267 brine Substances 0.000 description 17
- 230000000694 effects Effects 0.000 description 17
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 17
- 239000003112 inhibitor Substances 0.000 description 16
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 15
- 229960000583 acetic acid Drugs 0.000 description 15
- 239000003921 oil Substances 0.000 description 15
- 108010007622 LDL Lipoproteins Proteins 0.000 description 14
- 102000007330 LDL Lipoproteins Human genes 0.000 description 14
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 14
- 150000001412 amines Chemical class 0.000 description 14
- 239000003153 chemical reaction reagent Substances 0.000 description 14
- 239000003795 chemical substances by application Substances 0.000 description 14
- 238000004440 column chromatography Methods 0.000 description 13
- 238000002844 melting Methods 0.000 description 13
- 230000008018 melting Effects 0.000 description 13
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 12
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 12
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 12
- 239000003638 chemical reducing agent Substances 0.000 description 12
- NWIOJXJADHKWLZ-UHFFFAOYSA-N n-(cyclopentylmethyl)ethanamine Chemical compound CCNCC1CCCC1 NWIOJXJADHKWLZ-UHFFFAOYSA-N 0.000 description 12
- 239000003208 petroleum Substances 0.000 description 12
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 12
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 12
- 230000037396 body weight Effects 0.000 description 11
- 239000003814 drug Substances 0.000 description 11
- 150000002148 esters Chemical class 0.000 description 11
- 239000012299 nitrogen atmosphere Substances 0.000 description 11
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 11
- 201000001320 Atherosclerosis Diseases 0.000 description 10
- 208000024172 Cardiovascular disease Diseases 0.000 description 10
- 239000002246 antineoplastic agent Substances 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 10
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 10
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 9
- 108010078791 Carrier Proteins Proteins 0.000 description 9
- 102000014914 Carrier Proteins Human genes 0.000 description 9
- 108010023302 HDL Cholesterol Proteins 0.000 description 9
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 9
- 239000002253 acid Substances 0.000 description 9
- 125000002252 acyl group Chemical group 0.000 description 9
- 239000002671 adjuvant Substances 0.000 description 9
- 235000012000 cholesterol Nutrition 0.000 description 9
- 230000002265 prevention Effects 0.000 description 9
- 239000007858 starting material Substances 0.000 description 9
- 101100132433 Arabidopsis thaliana VIII-1 gene Proteins 0.000 description 8
- 206010020772 Hypertension Diseases 0.000 description 8
- 241000124008 Mammalia Species 0.000 description 8
- 238000005481 NMR spectroscopy Methods 0.000 description 8
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 8
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 8
- 150000001298 alcohols Chemical class 0.000 description 8
- 230000003110 anti-inflammatory effect Effects 0.000 description 8
- 239000003085 diluting agent Substances 0.000 description 8
- 239000000284 extract Substances 0.000 description 8
- 239000012280 lithium aluminium hydride Substances 0.000 description 8
- 208000010125 myocardial infarction Diseases 0.000 description 8
- 239000000546 pharmaceutical excipient Substances 0.000 description 8
- 239000003755 preservative agent Substances 0.000 description 8
- 230000000069 prophylactic effect Effects 0.000 description 8
- 230000009467 reduction Effects 0.000 description 8
- 238000006722 reduction reaction Methods 0.000 description 8
- 238000006268 reductive amination reaction Methods 0.000 description 8
- 239000012312 sodium hydride Substances 0.000 description 8
- 229910000104 sodium hydride Inorganic materials 0.000 description 8
- 238000006467 substitution reaction Methods 0.000 description 8
- GROJIEMGBWEVOY-UHFFFAOYSA-N 6-chloro-1,3-dimethylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound ClC1=C(C=O)C=C2C(C)=NN(C)C2=N1 GROJIEMGBWEVOY-UHFFFAOYSA-N 0.000 description 7
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 description 7
- 125000003342 alkenyl group Chemical group 0.000 description 7
- 125000004103 aminoalkyl group Chemical group 0.000 description 7
- MNFORVFSTILPAW-UHFFFAOYSA-N azetidin-2-one Chemical compound O=C1CCN1 MNFORVFSTILPAW-UHFFFAOYSA-N 0.000 description 7
- 229940127089 cytotoxic agent Drugs 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 230000002335 preservative effect Effects 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 7
- 235000011121 sodium hydroxide Nutrition 0.000 description 7
- 239000012453 solvate Substances 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- 238000002560 therapeutic procedure Methods 0.000 description 7
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 101100156282 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) vib-1 gene Proteins 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 239000000654 additive Substances 0.000 description 6
- 230000000996 additive effect Effects 0.000 description 6
- 125000000304 alkynyl group Chemical group 0.000 description 6
- 150000001408 amides Chemical class 0.000 description 6
- 239000002775 capsule Substances 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 238000004587 chromatography analysis Methods 0.000 description 6
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 6
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 6
- 125000004663 dialkyl amino group Chemical group 0.000 description 6
- 239000002552 dosage form Substances 0.000 description 6
- 238000001704 evaporation Methods 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 239000011734 sodium Substances 0.000 description 6
- 229910000029 sodium carbonate Inorganic materials 0.000 description 6
- 235000017550 sodium carbonate Nutrition 0.000 description 6
- 239000003826 tablet Substances 0.000 description 6
- JRMUNVKIHCOMHV-UHFFFAOYSA-M tetrabutylammonium bromide Chemical compound [Br-].CCCC[N+](CCCC)(CCCC)CCCC JRMUNVKIHCOMHV-UHFFFAOYSA-M 0.000 description 6
- 230000001225 therapeutic effect Effects 0.000 description 6
- 229940086542 triethylamine Drugs 0.000 description 6
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 5
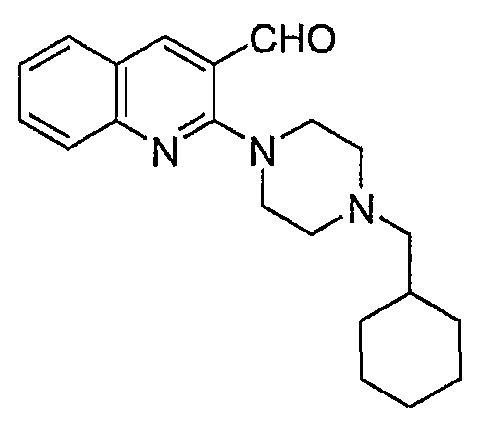
- LRPGNFROBDUREU-UHFFFAOYSA-N 1-(cyclohexylmethyl)piperazine Chemical compound C1CNCCN1CC1CCCCC1 LRPGNFROBDUREU-UHFFFAOYSA-N 0.000 description 5
- ZAHWCHOEOKIPLN-UHFFFAOYSA-N 1-cyclopropyl-n-(cyclopropylmethyl)methanamine Chemical compound C1CC1CNCC1CC1 ZAHWCHOEOKIPLN-UHFFFAOYSA-N 0.000 description 5
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 5
- 108010028554 LDL Cholesterol Proteins 0.000 description 5
- 229920002472 Starch Polymers 0.000 description 5
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 5
- 239000000556 agonist Substances 0.000 description 5
- 239000011230 binding agent Substances 0.000 description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- 239000000460 chlorine Substances 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- ATDGTVJJHBUTRL-UHFFFAOYSA-N cyanogen bromide Chemical compound BrC#N ATDGTVJJHBUTRL-UHFFFAOYSA-N 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- 239000002158 endotoxin Substances 0.000 description 5
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 229940096701 plain lipid modifying drug hmg coa reductase inhibitors Drugs 0.000 description 5
- 125000003367 polycyclic group Chemical group 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- 239000008107 starch Substances 0.000 description 5
- 235000019698 starch Nutrition 0.000 description 5
- 239000003039 volatile agent Substances 0.000 description 5
- QFMZQPDHXULLKC-UHFFFAOYSA-N 1,2-bis(diphenylphosphino)ethane Chemical compound C=1C=CC=CC=1P(C=1C=CC=CC=1)CCP(C=1C=CC=CC=1)C1=CC=CC=C1 QFMZQPDHXULLKC-UHFFFAOYSA-N 0.000 description 4
- FVSYLLUZSRCXEH-UHFFFAOYSA-N 2-[1-[(4-aminophenyl)methyl]indol-3-yl]-2-oxo-n-pyridin-4-ylacetamide Chemical compound C1=CC(N)=CC=C1CN1C2=CC=CC=C2C(C(=O)C(=O)NC=2C=CN=CC=2)=C1 FVSYLLUZSRCXEH-UHFFFAOYSA-N 0.000 description 4
- 125000004938 5-pyridyl group Chemical group N1=CC=CC(=C1)* 0.000 description 4
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 4
- 206010002383 Angina Pectoris Diseases 0.000 description 4
- 102000007527 Autoreceptors Human genes 0.000 description 4
- 108010071131 Autoreceptors Proteins 0.000 description 4
- 208000032928 Dyslipidaemia Diseases 0.000 description 4
- 102000010726 Glycine Plasma Membrane Transport Proteins Human genes 0.000 description 4
- 108010063380 Glycine Plasma Membrane Transport Proteins Proteins 0.000 description 4
- 208000000563 Hyperlipoproteinemia Type II Diseases 0.000 description 4
- 206010021024 Hypolipidaemia Diseases 0.000 description 4
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 4
- 208000017170 Lipid metabolism disease Diseases 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- FZERHIULMFGESH-UHFFFAOYSA-N N-phenylacetamide Chemical compound CC(=O)NC1=CC=CC=C1 FZERHIULMFGESH-UHFFFAOYSA-N 0.000 description 4
- 208000018262 Peripheral vascular disease Diseases 0.000 description 4
- 206010063837 Reperfusion injury Diseases 0.000 description 4
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 4
- 208000006011 Stroke Diseases 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 150000001299 aldehydes Chemical class 0.000 description 4
- 125000001931 aliphatic group Chemical group 0.000 description 4
- 125000004414 alkyl thio group Chemical group 0.000 description 4
- 125000003277 amino group Chemical group 0.000 description 4
- 230000001430 anti-depressive effect Effects 0.000 description 4
- 239000000935 antidepressant agent Substances 0.000 description 4
- 229940005513 antidepressants Drugs 0.000 description 4
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 4
- 150000001721 carbon Chemical group 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 238000001816 cooling Methods 0.000 description 4
- 208000029078 coronary artery disease Diseases 0.000 description 4
- ZOOSILUVXHVRJE-UHFFFAOYSA-N cyclopropanecarbonyl chloride Chemical compound ClC(=O)C1CC1 ZOOSILUVXHVRJE-UHFFFAOYSA-N 0.000 description 4
- 201000009101 diabetic angiopathy Diseases 0.000 description 4
- 239000003937 drug carrier Substances 0.000 description 4
- 238000010828 elution Methods 0.000 description 4
- 201000001386 familial hypercholesterolemia Diseases 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 229960003692 gamma aminobutyric acid Drugs 0.000 description 4
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical compound NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 description 4
- 125000004994 halo alkoxy alkyl group Chemical group 0.000 description 4
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 125000001183 hydrocarbyl group Chemical group 0.000 description 4
- 150000002431 hydrogen Chemical class 0.000 description 4
- 208000029498 hypoalphalipoproteinemia Diseases 0.000 description 4
- 238000007912 intraperitoneal administration Methods 0.000 description 4
- 208000028867 ischemia Diseases 0.000 description 4
- 239000000314 lubricant Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000012074 organic phase Substances 0.000 description 4
- 239000012071 phase Substances 0.000 description 4
- 235000011118 potassium hydroxide Nutrition 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 208000037803 restenosis Diseases 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 238000010898 silica gel chromatography Methods 0.000 description 4
- 239000001632 sodium acetate Substances 0.000 description 4
- 235000017281 sodium acetate Nutrition 0.000 description 4
- 238000010189 synthetic method Methods 0.000 description 4
- CXNIUSPIQKWYAI-UHFFFAOYSA-N xantphos Chemical compound C=12OC3=C(P(C=4C=CC=CC=4)C=4C=CC=CC=4)C=CC=C3C(C)(C)C2=CC=CC=1P(C=1C=CC=CC=1)C1=CC=CC=C1 CXNIUSPIQKWYAI-UHFFFAOYSA-N 0.000 description 4
- AJGBQAAXUVSBCH-UHFFFAOYSA-N (3,4,5-trifluorophenyl)methanamine Chemical compound NCC1=CC(F)=C(F)C(F)=C1 AJGBQAAXUVSBCH-UHFFFAOYSA-N 0.000 description 3
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 3
- GPWNWKWQOLEVEQ-UHFFFAOYSA-N 2,4-diaminopyrimidine-5-carbaldehyde Chemical compound NC1=NC=C(C=O)C(N)=N1 GPWNWKWQOLEVEQ-UHFFFAOYSA-N 0.000 description 3
- ZFDGMMZLXSFNFU-UHFFFAOYSA-N 2,5-dimethylpyrazol-3-amine Chemical compound CC=1C=C(N)N(C)N=1 ZFDGMMZLXSFNFU-UHFFFAOYSA-N 0.000 description 3
- SDKQWXCBSNMYBN-UHFFFAOYSA-N 2-chloroquinoline-3-carbaldehyde Chemical compound C1=CC=C2C=C(C=O)C(Cl)=NC2=C1 SDKQWXCBSNMYBN-UHFFFAOYSA-N 0.000 description 3
- DLISRKZBEGZMEV-UHFFFAOYSA-N 6-[cyclopentylmethyl(ethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound N=1C=2N(C)N=C(C)C=2C=C(C=O)C=1N(CC)CC1CCCC1 DLISRKZBEGZMEV-UHFFFAOYSA-N 0.000 description 3
- XJHIGWNRBZZZAB-UHFFFAOYSA-N 6-chloro-1-methylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound O=CC1=C(Cl)N=C2N(C)N=CC2=C1 XJHIGWNRBZZZAB-UHFFFAOYSA-N 0.000 description 3
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 208000035150 Hypercholesterolemia Diseases 0.000 description 3
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- 108010062497 VLDL Lipoproteins Proteins 0.000 description 3
- DHVHORCFFOSRBP-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenyl]methanamine Chemical compound NCC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 DHVHORCFFOSRBP-UHFFFAOYSA-N 0.000 description 3
- 150000001241 acetals Chemical class 0.000 description 3
- 150000001336 alkenes Chemical class 0.000 description 3
- 125000004450 alkenylene group Chemical group 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 150000001450 anions Chemical class 0.000 description 3
- 230000000879 anti-atherosclerotic effect Effects 0.000 description 3
- 239000002220 antihypertensive agent Substances 0.000 description 3
- 229940030600 antihypertensive agent Drugs 0.000 description 3
- 230000003143 atherosclerotic effect Effects 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- MUALRAIOVNYAIW-UHFFFAOYSA-N binap Chemical compound C1=CC=CC=C1P(C=1C(=C2C=CC=CC2=CC=1)C=1C2=CC=CC=C2C=CC=1P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MUALRAIOVNYAIW-UHFFFAOYSA-N 0.000 description 3
- 230000004071 biological effect Effects 0.000 description 3
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 3
- 229910000024 caesium carbonate Inorganic materials 0.000 description 3
- 239000004202 carbamide Substances 0.000 description 3
- 150000001735 carboxylic acids Chemical class 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- YMGUBTXCNDTFJI-UHFFFAOYSA-N cyclopropanecarboxylic acid Chemical compound OC(=O)C1CC1 YMGUBTXCNDTFJI-UHFFFAOYSA-N 0.000 description 3
- 239000002254 cytotoxic agent Substances 0.000 description 3
- 231100000599 cytotoxic agent Toxicity 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 239000007884 disintegrant Substances 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 230000008020 evaporation Effects 0.000 description 3
- 239000006260 foam Substances 0.000 description 3
- 238000005755 formation reaction Methods 0.000 description 3
- 239000008103 glucose Substances 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 125000005638 hydrazono group Chemical group 0.000 description 3
- 230000007062 hydrolysis Effects 0.000 description 3
- 238000006460 hydrolysis reaction Methods 0.000 description 3
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 3
- 208000006575 hypertriglyceridemia Diseases 0.000 description 3
- 239000003018 immunosuppressive agent Substances 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 229920006008 lipopolysaccharide Polymers 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 125000005905 mesyloxy group Chemical group 0.000 description 3
- 229920000609 methyl cellulose Polymers 0.000 description 3
- XMJHPCRAQCTCFT-UHFFFAOYSA-N methyl chloroformate Chemical compound COC(Cl)=O XMJHPCRAQCTCFT-UHFFFAOYSA-N 0.000 description 3
- 239000001923 methylcellulose Substances 0.000 description 3
- 235000010981 methylcellulose Nutrition 0.000 description 3
- UHFLNWZBNRVHGM-UHFFFAOYSA-N n-(cyclopropylmethyl)ethanamine Chemical compound CCNCC1CC1 UHFLNWZBNRVHGM-UHFFFAOYSA-N 0.000 description 3
- LGLVAAGLXHQHJJ-UHFFFAOYSA-N n-ethylcyclopentene-1-carboxamide Chemical compound CCNC(=O)C1=CCCC1 LGLVAAGLXHQHJJ-UHFFFAOYSA-N 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- 239000006072 paste Substances 0.000 description 3
- 239000002798 polar solvent Substances 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- NTTOTNSKUYCDAV-UHFFFAOYSA-N potassium hydride Chemical compound [KH] NTTOTNSKUYCDAV-UHFFFAOYSA-N 0.000 description 3
- 229910000105 potassium hydride Inorganic materials 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 239000012268 protein inhibitor Substances 0.000 description 3
- 229940121649 protein inhibitor Drugs 0.000 description 3
- QJZUKDFHGGYHMC-UHFFFAOYSA-N pyridine-3-carbaldehyde Chemical compound O=CC1=CC=CN=C1 QJZUKDFHGGYHMC-UHFFFAOYSA-N 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 229940124530 sulfonamide Drugs 0.000 description 3
- 150000003456 sulfonamides Chemical class 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 230000032258 transport Effects 0.000 description 3
- ICIJWOWQUHHETJ-UHFFFAOYSA-N (3,5-dichlorophenyl)methanamine Chemical compound NCC1=CC(Cl)=CC(Cl)=C1 ICIJWOWQUHHETJ-UHFFFAOYSA-N 0.000 description 2
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 2
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 2
- JPRPJUMQRZTTED-UHFFFAOYSA-N 1,3-dioxolanyl Chemical group [CH]1OCCO1 JPRPJUMQRZTTED-UHFFFAOYSA-N 0.000 description 2
- 125000005940 1,4-dioxanyl group Chemical group 0.000 description 2
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 2
- AMFYRKOUWBAGHV-UHFFFAOYSA-N 1h-pyrazolo[4,3-b]pyridine Chemical compound C1=CN=C2C=NNC2=C1 AMFYRKOUWBAGHV-UHFFFAOYSA-N 0.000 description 2
- KYZDVSZQNPZLPM-UHFFFAOYSA-N 2-[cyclopentylmethyl(ethyl)amino]quinoline-3-carbaldehyde Chemical compound N=1C2=CC=CC=C2C=C(C=O)C=1N(CC)CC1CCCC1 KYZDVSZQNPZLPM-UHFFFAOYSA-N 0.000 description 2
- LSBDFXRDZJMBSC-UHFFFAOYSA-N 2-phenylacetamide Chemical class NC(=O)CC1=CC=CC=C1 LSBDFXRDZJMBSC-UHFFFAOYSA-N 0.000 description 2
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 2
- ATJZELDNCZHTIK-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methylamino]methyl]-n-(cyclopentylmethyl)-n-ethylquinolin-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CNCC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=1N(CC)CC1CCCC1 ATJZELDNCZHTIK-UHFFFAOYSA-N 0.000 description 2
- SVEGALQCHKKLJT-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,1-diethyl-N-methylpyrazolo[3,4-b]pyridin-6-amine Chemical compound FC(C=1C=C(CN(C=2N=NN(N2)C)CC=2C=C3C(=NC2N(C)CC)N(N=C3)CC)C=C(C1)C(F)(F)F)(F)F SVEGALQCHKKLJT-UHFFFAOYSA-N 0.000 description 2
- SABJTGRHCWIEEB-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,1-diethyl-N-methylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CCN(C)c1nc2n(CC)ccc2cc1CN(Cc1cc(cc(c1)C(F)(F)F)C(F)(F)F)c1nnn(C)n1 SABJTGRHCWIEEB-UHFFFAOYSA-N 0.000 description 2
- VZQWOWIWMZYDBS-UHFFFAOYSA-N 6-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,3-diethyl-N-methylimidazo[4,5-b]pyridin-5-amine Chemical compound FC(C=1C=C(CN(C=2N=NN(N2)C)CC=2C=C3C(=NC2N(C)CC)N(C=N3)CC)C=C(C1)C(F)(F)F)(F)F VZQWOWIWMZYDBS-UHFFFAOYSA-N 0.000 description 2
- ZHTPNUSQKLHJRI-UHFFFAOYSA-N 6-[cyclobutylmethyl(ethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound N=1C=2N(C)N=C(C)C=2C=C(C=O)C=1N(CC)CC1CCC1 ZHTPNUSQKLHJRI-UHFFFAOYSA-N 0.000 description 2
- 241000220479 Acacia Species 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- 241000416162 Astragalus gummifer Species 0.000 description 2
- GUBGYTABKSRVRQ-DCSYEGIMSA-N Beta-Lactose Chemical compound OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-DCSYEGIMSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- XZMCDFZZKTWFGF-UHFFFAOYSA-N Cyanamide Chemical compound NC#N XZMCDFZZKTWFGF-UHFFFAOYSA-N 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 206010012689 Diabetic retinopathy Diseases 0.000 description 2
- 208000013600 Diabetic vascular disease Diseases 0.000 description 2
- 208000010228 Erectile Dysfunction Diseases 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- 102100031545 Microsomal triglyceride transfer protein large subunit Human genes 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 229940127473 Prostaglandin Receptor Agonists Drugs 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 229940124639 Selective inhibitor Drugs 0.000 description 2
- BCKXLBQYZLBQEK-KVVVOXFISA-M Sodium oleate Chemical compound [Na+].CCCCCCCC\C=C/CCCCCCCC([O-])=O BCKXLBQYZLBQEK-KVVVOXFISA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 2
- 229920001615 Tragacanth Polymers 0.000 description 2
- 102000004357 Transferases Human genes 0.000 description 2
- 108090000992 Transferases Proteins 0.000 description 2
- 108091008605 VEGF receptors Proteins 0.000 description 2
- 240000008042 Zea mays Species 0.000 description 2
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 2
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 2
- 230000000895 acaricidal effect Effects 0.000 description 2
- 239000000642 acaricide Substances 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 229960001413 acetanilide Drugs 0.000 description 2
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 2
- 239000012346 acetyl chloride Substances 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000010933 acylation Effects 0.000 description 2
- 238000005917 acylation reaction Methods 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 235000010419 agar Nutrition 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001345 alkine derivatives Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 150000001350 alkyl halides Chemical class 0.000 description 2
- 230000029936 alkylation Effects 0.000 description 2
- 238000005804 alkylation reaction Methods 0.000 description 2
- 238000005576 amination reaction Methods 0.000 description 2
- 235000019270 ammonium chloride Nutrition 0.000 description 2
- 230000001708 anti-dyslipidemic effect Effects 0.000 description 2
- 239000002260 anti-inflammatory agent Substances 0.000 description 2
- 229940121363 anti-inflammatory agent Drugs 0.000 description 2
- 239000000883 anti-obesity agent Substances 0.000 description 2
- 239000003472 antidiabetic agent Substances 0.000 description 2
- 239000003435 antirheumatic agent Substances 0.000 description 2
- 239000003443 antiviral agent Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 125000004069 aziridinyl group Chemical group 0.000 description 2
- 239000000440 bentonite Substances 0.000 description 2
- 229910000278 bentonite Inorganic materials 0.000 description 2
- 235000012216 bentonite Nutrition 0.000 description 2
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 2
- 230000036772 blood pressure Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 229940105329 carboxymethylcellulose Drugs 0.000 description 2
- 239000002327 cardiovascular agent Substances 0.000 description 2
- 229940125692 cardiovascular agent Drugs 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 230000001906 cholesterol absorption Effects 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000011260 co-administration Methods 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 235000005822 corn Nutrition 0.000 description 2
- NZNMSOFKMUBTKW-UHFFFAOYSA-N cyclohexanecarboxylic acid Chemical compound OC(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-N 0.000 description 2
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- JBDSSBMEKXHSJF-UHFFFAOYSA-N cyclopentanecarboxylic acid Chemical compound OC(=O)C1CCCC1 JBDSSBMEKXHSJF-UHFFFAOYSA-N 0.000 description 2
- IGSKHXTUVXSOMB-UHFFFAOYSA-N cyclopropylmethanamine Chemical compound NCC1CC1 IGSKHXTUVXSOMB-UHFFFAOYSA-N 0.000 description 2
- VAYGXNSJCAHWJZ-UHFFFAOYSA-N dimethyl sulfate Chemical compound COS(=O)(=O)OC VAYGXNSJCAHWJZ-UHFFFAOYSA-N 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- RIFGWPKJUGCATF-UHFFFAOYSA-N ethyl chloroformate Chemical compound CCOC(Cl)=O RIFGWPKJUGCATF-UHFFFAOYSA-N 0.000 description 2
- PENFZVSMRPVDDO-UHFFFAOYSA-N ethyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclohexylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound C=1C2=CC=CC=C2N=C(N(CC)CC2CCCCC2)C=1CN(C(=O)OCC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PENFZVSMRPVDDO-UHFFFAOYSA-N 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 230000008570 general process Effects 0.000 description 2
- 239000007952 growth promoter Substances 0.000 description 2
- 230000003779 hair growth Effects 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- 239000004009 herbicide Substances 0.000 description 2
- 150000002391 heterocyclic compounds Chemical class 0.000 description 2
- 229940126904 hypoglycaemic agent Drugs 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- 229960003444 immunosuppressant agent Drugs 0.000 description 2
- 201000001881 impotence Diseases 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 2
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 239000002917 insecticide Substances 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 239000007937 lozenge Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000007721 medicinal effect Effects 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- FLLCZARJBRSAFA-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CCCC1 FLLCZARJBRSAFA-UHFFFAOYSA-N 0.000 description 2
- 239000003094 microcapsule Substances 0.000 description 2
- 108010038232 microsomal triglyceride transfer protein Proteins 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 125000002757 morpholinyl group Chemical group 0.000 description 2
- 239000003149 muscarinic antagonist Substances 0.000 description 2
- 208000031225 myocardial ischemia Diseases 0.000 description 2
- HSSKLCCHHOERGB-UHFFFAOYSA-N n,1-diethyl-5-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(C(F)(F)F)=C1 HSSKLCCHHOERGB-UHFFFAOYSA-N 0.000 description 2
- SOEINDPDOWSEPB-UHFFFAOYSA-N n-(2,5-dimethylpyrazol-3-yl)acetamide Chemical compound CC(=O)NC1=CC(C)=NN1C SOEINDPDOWSEPB-UHFFFAOYSA-N 0.000 description 2
- XQWSLHIYGMOJHI-UHFFFAOYSA-N n-(cyclohexylmethyl)ethanamine Chemical compound CCNCC1CCCCC1 XQWSLHIYGMOJHI-UHFFFAOYSA-N 0.000 description 2
- IWYCJJJQXVVZIW-UHFFFAOYSA-N n-(cyclopentylmethyl)-n-ethyl-1,3-dimethyl-5-[[(2-methyltetrazol-5-yl)-[(3,4,5-trifluorophenyl)methyl]amino]methyl]pyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(F)C(F)=C(F)C=2)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 IWYCJJJQXVVZIW-UHFFFAOYSA-N 0.000 description 2
- GVUWDIFTNXLBBB-UHFFFAOYSA-N n-benzyl-1,1,1-trifluoro-n-(trifluoromethyl)methanamine Chemical compound FC(F)(F)N(C(F)(F)F)CC1=CC=CC=C1 GVUWDIFTNXLBBB-UHFFFAOYSA-N 0.000 description 2
- QOFZICTWQWJEKJ-UHFFFAOYSA-N n-cyclohexyl-n-ethylacetamide Chemical compound CCN(C(C)=O)C1CCCCC1 QOFZICTWQWJEKJ-UHFFFAOYSA-N 0.000 description 2
- AXDLTLIKVSAPPJ-UHFFFAOYSA-N n-ethylcyclobutanecarboxamide Chemical compound CCNC(=O)C1CCC1 AXDLTLIKVSAPPJ-UHFFFAOYSA-N 0.000 description 2
- GVWISOJSERXQBM-UHFFFAOYSA-N n-methylpropan-1-amine Chemical compound CCCNC GVWISOJSERXQBM-UHFFFAOYSA-N 0.000 description 2
- 229920003052 natural elastomer Polymers 0.000 description 2
- 229920001194 natural rubber Polymers 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 125000001715 oxadiazolyl group Chemical group 0.000 description 2
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 239000003444 phase transfer catalyst Substances 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 239000011574 phosphorus Substances 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 125000004193 piperazinyl group Chemical group 0.000 description 2
- 125000003386 piperidinyl group Chemical group 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 235000015424 sodium Nutrition 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 235000010413 sodium alginate Nutrition 0.000 description 2
- 239000000661 sodium alginate Substances 0.000 description 2
- 229940005550 sodium alginate Drugs 0.000 description 2
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 2
- 239000004299 sodium benzoate Substances 0.000 description 2
- 235000010234 sodium benzoate Nutrition 0.000 description 2
- RYYKJJJTJZKILX-UHFFFAOYSA-M sodium octadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC([O-])=O RYYKJJJTJZKILX-UHFFFAOYSA-M 0.000 description 2
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 2
- 239000012265 solid product Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 229920003051 synthetic elastomer Polymers 0.000 description 2
- 239000005061 synthetic rubber Substances 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 125000001984 thiazolidinyl group Chemical group 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 235000010487 tragacanth Nutrition 0.000 description 2
- 239000000196 tragacanth Substances 0.000 description 2
- 229940116362 tragacanth Drugs 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 239000000230 xanthan gum Substances 0.000 description 2
- 235000010493 xanthan gum Nutrition 0.000 description 2
- 229920001285 xanthan gum Polymers 0.000 description 2
- 229940082509 xanthan gum Drugs 0.000 description 2
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical group CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- VNDYJBBGRKZCSX-UHFFFAOYSA-L zinc bromide Chemical compound Br[Zn]Br VNDYJBBGRKZCSX-UHFFFAOYSA-L 0.000 description 2
- 229930195724 β-lactose Natural products 0.000 description 2
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- NWZSZGALRFJKBT-KNIFDHDWSA-N (2s)-2,6-diaminohexanoic acid;(2s)-2-hydroxybutanedioic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O.NCCCC[C@H](N)C(O)=O NWZSZGALRFJKBT-KNIFDHDWSA-N 0.000 description 1
- VJNGGOMRUHYAMC-UHFFFAOYSA-N (3,5-difluorophenyl)methanamine Chemical compound NCC1=CC(F)=CC(F)=C1 VJNGGOMRUHYAMC-UHFFFAOYSA-N 0.000 description 1
- 125000000027 (C1-C10) alkoxy group Chemical group 0.000 description 1
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- IXHHLUXPMYDIHU-UHFFFAOYSA-N 1,2,3,4-tetrahydro-1,5-naphthyridin-4-amine Chemical compound N1CCC(C2=NC=CC=C12)N IXHHLUXPMYDIHU-UHFFFAOYSA-N 0.000 description 1
- 125000004605 1,2,3,4-tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 1
- UZAOPTDGCXICDB-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinolin-4-amine Chemical compound C1=CC=C2C(N)CCNC2=C1 UZAOPTDGCXICDB-UHFFFAOYSA-N 0.000 description 1
- 125000004504 1,2,4-oxadiazolyl group Chemical class 0.000 description 1
- AIUOUEPKBRDPLG-UHFFFAOYSA-N 1,3-benzoxathiole Chemical group C1=CC=C2SCOC2=C1 AIUOUEPKBRDPLG-UHFFFAOYSA-N 0.000 description 1
- OLOZBXHUXMYKEO-UHFFFAOYSA-N 1,3-dimethylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound C1=C(C=O)C=C2C(C)=NN(C)C2=N1 OLOZBXHUXMYKEO-UHFFFAOYSA-N 0.000 description 1
- RAIPHJJURHTUIC-UHFFFAOYSA-N 1,3-thiazol-2-amine Chemical class NC1=NC=CS1 RAIPHJJURHTUIC-UHFFFAOYSA-N 0.000 description 1
- ZOBPZXTWZATXDG-UHFFFAOYSA-N 1,3-thiazolidine-2,4-dione Chemical compound O=C1CSC(=O)N1 ZOBPZXTWZATXDG-UHFFFAOYSA-N 0.000 description 1
- ATLQGZVLWOURFU-UHFFFAOYSA-N 1-(bromomethyl)-3,5-bis(trifluoromethyl)benzene Chemical compound FC(F)(F)C1=CC(CBr)=CC(C(F)(F)F)=C1 ATLQGZVLWOURFU-UHFFFAOYSA-N 0.000 description 1
- 102000016752 1-Alkyl-2-acetylglycerophosphocholine Esterase Human genes 0.000 description 1
- XEOISGZDSZRTSH-UHFFFAOYSA-N 1-[3,5-bis(trifluoromethyl)phenyl]-n-[[2-[4-(cyclohexylmethyl)piperazin-1-yl]quinolin-3-yl]methyl]methanamine Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(CNCC=2C(=NC3=CC=CC=C3C=2)N2CCN(CC3CCCCC3)CC2)=C1 XEOISGZDSZRTSH-UHFFFAOYSA-N 0.000 description 1
- FAZBIANZKUQCCQ-UHFFFAOYSA-N 1-[[3,5-bis(trifluoromethyl)phenyl]methyl]-1-[(3-cyclopentylpropylamino)-quinolin-3-ylmethyl]urea Chemical compound C1CCCC1CCCNC(C=1C=C2C=CC=CC2=NC=1)N(C(=O)N)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 FAZBIANZKUQCCQ-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- JXXBNDVAWWXOIG-UHFFFAOYSA-N 1-cyclobutyl-n-(cyclopropylmethyl)methanamine Chemical compound C1CC1CNCC1CCC1 JXXBNDVAWWXOIG-UHFFFAOYSA-N 0.000 description 1
- DFDDLFCSYLTQBP-UHFFFAOYSA-N 1-cyclobutyl-n-methylmethanamine Chemical compound CNCC1CCC1 DFDDLFCSYLTQBP-UHFFFAOYSA-N 0.000 description 1
- IDCPFAYURAQKDZ-UHFFFAOYSA-N 1-nitroguanidine Chemical compound NC(=N)N[N+]([O-])=O IDCPFAYURAQKDZ-UHFFFAOYSA-N 0.000 description 1
- SIYIBWRIGSGXKY-UHFFFAOYSA-N 2-(1h-indol-2-yl)-2-oxoacetamide Chemical compound C1=CC=C2NC(C(=O)C(=O)N)=CC2=C1 SIYIBWRIGSGXKY-UHFFFAOYSA-N 0.000 description 1
- TVAHIDVDZRRRCN-UHFFFAOYSA-N 2-(1h-pyrazol-5-yloxy)pyridine Chemical class C=1C=CC=NC=1OC=1C=CNN=1 TVAHIDVDZRRRCN-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- OLKJJCVSKFYRIL-UHFFFAOYSA-N 2-[4-(cyclohexylmethyl)piperazin-1-yl]quinoline-3-carbaldehyde Chemical compound O=CC1=CC2=CC=CC=C2N=C1N(CC1)CCN1CC1CCCCC1 OLKJJCVSKFYRIL-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- HVLOGYDFABPTOC-UHFFFAOYSA-N 2-hydroxyacetamide;1h-pyrazole Chemical class C=1C=NNC=1.NC(=O)CO HVLOGYDFABPTOC-UHFFFAOYSA-N 0.000 description 1
- NJBCRXCAPCODGX-UHFFFAOYSA-N 2-methyl-n-(2-methylpropyl)propan-1-amine Chemical compound CC(C)CNCC(C)C NJBCRXCAPCODGX-UHFFFAOYSA-N 0.000 description 1
- AZUKLCJYWVMPML-UHFFFAOYSA-N 2-methyltetrazol-5-amine Chemical compound CN1N=NC(N)=N1 AZUKLCJYWVMPML-UHFFFAOYSA-N 0.000 description 1
- VRESBNUEIKZECD-UHFFFAOYSA-N 2-methyltetrazole Chemical compound CN1N=CN=N1 VRESBNUEIKZECD-UHFFFAOYSA-N 0.000 description 1
- AOPRXJXHLWYPQR-UHFFFAOYSA-N 2-phenoxyacetamide Chemical class NC(=O)COC1=CC=CC=C1 AOPRXJXHLWYPQR-UHFFFAOYSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- JMTMSDXUXJISAY-UHFFFAOYSA-N 2H-benzotriazol-4-ol Chemical compound OC1=CC=CC2=C1N=NN2 JMTMSDXUXJISAY-UHFFFAOYSA-N 0.000 description 1
- ULRPISSMEBPJLN-UHFFFAOYSA-N 2h-tetrazol-5-amine Chemical compound NC1=NN=NN1 ULRPISSMEBPJLN-UHFFFAOYSA-N 0.000 description 1
- KPKQWXGFEKRQQA-UHFFFAOYSA-N 3,5-diphenyl-1h-1,2,4-triazole Chemical class C1=CC=CC=C1C1=NNC(C=2C=CC=CC=2)=N1 KPKQWXGFEKRQQA-UHFFFAOYSA-N 0.000 description 1
- QNAXOUMUKZDEGB-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n-bis(cyclopropylmethyl)-4,6-dimethylpyridin-2-amine Chemical compound C1CC1CN(CC1CC1)C1=NC(C)=CC(C)=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 QNAXOUMUKZDEGB-UHFFFAOYSA-N 0.000 description 1
- VAEDBVAEPNYHQP-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methyl-[(1-methyltetrazol-5-yl)methyl]amino]methyl]-n-(cyclopentylmethyl)-n-ethylquinolin-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2N(N=NN=2)C)CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=1N(CC)CC1CCCC1 VAEDBVAEPNYHQP-UHFFFAOYSA-N 0.000 description 1
- KCCLGUJGEIEOKR-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methyl-[(2-methyltetrazol-5-yl)methyl]amino]methyl]-n-(cyclopentylmethyl)-n-ethylquinolin-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC2=NN(C)N=N2)CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=1N(CC)CC1CCCC1 KCCLGUJGEIEOKR-UHFFFAOYSA-N 0.000 description 1
- KLBBMLPMDFMOEE-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methyl-pyridin-2-ylamino]methyl]-n-(cyclopentylmethyl)-n-ethylquinolin-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2N=CC=CC=2)C=1N(CC)CC1CCCC1 KLBBMLPMDFMOEE-UHFFFAOYSA-N 0.000 description 1
- HETSCGCAPKPTCI-UHFFFAOYSA-N 3-[[[3,5-bis(trifluoromethyl)phenyl]methyl-pyrimidin-2-ylamino]methyl]-n-(cyclopentylmethyl)-n-ethylquinolin-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2N=CC=CN=2)C=1N(CC)CC1CCCC1 HETSCGCAPKPTCI-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- INUNLMUAPJVRME-UHFFFAOYSA-N 3-chloropropanoyl chloride Chemical compound ClCCC(Cl)=O INUNLMUAPJVRME-UHFFFAOYSA-N 0.000 description 1
- FNXYWHTZDAVRTB-UHFFFAOYSA-N 3-methyl-1,2-oxazol-5-amine Chemical compound CC=1C=C(N)ON=1 FNXYWHTZDAVRTB-UHFFFAOYSA-N 0.000 description 1
- YICAMJWHIUMFDI-UHFFFAOYSA-N 4-acetamidotoluene Chemical compound CC(=O)NC1=CC=C(C)C=C1 YICAMJWHIUMFDI-UHFFFAOYSA-N 0.000 description 1
- 150000005007 4-aminopyrimidines Chemical class 0.000 description 1
- NVPFHSKJORCPDL-UHFFFAOYSA-N 5-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,1-diethyl-N,2-dimethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CCN(C)c1nc2n(CC)c(C)cc2cc1CN(Cc1cc(F)cc(F)c1)c1nnn(C)n1 NVPFHSKJORCPDL-UHFFFAOYSA-N 0.000 description 1
- JJAVFHOWUBTLBO-UHFFFAOYSA-N 5-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,N,1,3-tetramethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CN(C)c1nc2n(C)nc(C)c2cc1CN(Cc1cc(F)cc(F)c1)c1nnn(C)n1 JJAVFHOWUBTLBO-UHFFFAOYSA-N 0.000 description 1
- MOPCEQUOIDRPDK-UHFFFAOYSA-N 5-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,1-diethyl-n,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(F)=C1 MOPCEQUOIDRPDK-UHFFFAOYSA-N 0.000 description 1
- NHFJALPQPUCRPC-UHFFFAOYSA-N 5-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n,1,2-tetramethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CN(C)C1=NC=2N(C)C(C)=CC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(F)=C1 NHFJALPQPUCRPC-UHFFFAOYSA-N 0.000 description 1
- ZNOTTYXVTJLPFD-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethyl-n,n-bis(2-methylpropyl)pyrazolo[3,4-b]pyridin-6-amine Chemical compound CC(C)CN(CC(C)C)C1=NC=2N(C)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 ZNOTTYXVTJLPFD-UHFFFAOYSA-N 0.000 description 1
- MDXWGFGMIPOELM-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,N,1-trimethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound FC(C=1C=C(CN(C=2N=NN(N2)C)CC=2C=C3C(=NC2N(C)C)N(C=C3)C)C=C(C1)C(F)(F)F)(F)F MDXWGFGMIPOELM-UHFFFAOYSA-N 0.000 description 1
- VGRONPRPOHHADW-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,1,3-triethyl-n-methylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)N=C(CC)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 VGRONPRPOHHADW-UHFFFAOYSA-N 0.000 description 1
- XZLSFOKOGSDPDF-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,1-diethyl-n,2-dimethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)C(C)=CC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XZLSFOKOGSDPDF-UHFFFAOYSA-N 0.000 description 1
- ZNHCUXNENQOUSJ-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,1-diethyl-n,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 ZNHCUXNENQOUSJ-UHFFFAOYSA-N 0.000 description 1
- NSVMRALAXXBCMA-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n,1,2-tetramethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CN(C)C1=NC=2N(C)C(C)=CC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 NSVMRALAXXBCMA-UHFFFAOYSA-N 0.000 description 1
- YRZOOTBRHNOYRX-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n,1,3-tetramethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CN(C)C1=NC=2N(C)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 YRZOOTBRHNOYRX-UHFFFAOYSA-N 0.000 description 1
- BJHZUYRKPJFRFQ-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n,1-trimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CN(C)C1=NC=2N(C)N=CC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 BJHZUYRKPJFRFQ-UHFFFAOYSA-N 0.000 description 1
- HEDBZMCYFDHDTM-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n-bis(cyclopropylmethyl)-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(CC1CC1)CC1CC1 HEDBZMCYFDHDTM-UHFFFAOYSA-N 0.000 description 1
- MEEBWKCFSYEYFR-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n-bis(cyclopropylmethyl)-1-ethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound C1CC1CN(CC1CC1)C=1N=C2N(CC)N=CC2=CC=1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 MEEBWKCFSYEYFR-UHFFFAOYSA-N 0.000 description 1
- DQKOOKBZNRFUOC-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,n-bis(cyclopropylmethyl)-1-methylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CN1N=NC(N(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)CC=2C(=NC=3N(C)N=CC=3C=2)N(CC2CC2)CC2CC2)=N1 DQKOOKBZNRFUOC-UHFFFAOYSA-N 0.000 description 1
- XTTVYHYMQBJFKZ-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(2,2-dimethylpropyl)-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CC(C)(C)CN(CC)C1=NC=2N(C)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 XTTVYHYMQBJFKZ-UHFFFAOYSA-N 0.000 description 1
- FGJXDMKKNBWBJB-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclobutylmethyl)-n,1,3-trimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(C)CC1CCC1 FGJXDMKKNBWBJB-UHFFFAOYSA-N 0.000 description 1
- ZJMSIPHNPZYBFD-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclobutylmethyl)-n,1-diethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(CC)N=CC=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCC1 ZJMSIPHNPZYBFD-UHFFFAOYSA-N 0.000 description 1
- LWMZJLFWWVYRLR-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclobutylmethyl)-n-(cyclopropylmethyl)-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(CC1CCC1)CC1CC1 LWMZJLFWWVYRLR-UHFFFAOYSA-N 0.000 description 1
- ACRSRAXOBOZWAO-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclobutylmethyl)-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCC1 ACRSRAXOBOZWAO-UHFFFAOYSA-N 0.000 description 1
- PFHGFFXODPRKKQ-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclobutylmethyl)-n-ethyl-1-methylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=CC=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCC1 PFHGFFXODPRKKQ-UHFFFAOYSA-N 0.000 description 1
- PPKJVIUMTWMSRG-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclopentylmethyl)-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 PPKJVIUMTWMSRG-UHFFFAOYSA-N 0.000 description 1
- NCMFYNKFGIFMGO-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclopentylmethyl)-n-ethyl-3-methyl-[1,2]oxazolo[5,4-b]pyridin-6-amine Chemical compound N=1C=2ON=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 NCMFYNKFGIFMGO-UHFFFAOYSA-N 0.000 description 1
- SRDYLXFAHFAOQH-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclopropylmethyl)-1,3-dimethyl-n-(2-methylpropyl)pyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC(C)C)CC1CC1 SRDYLXFAHFAOQH-UHFFFAOYSA-N 0.000 description 1
- QYRDHSXXWABZCK-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-(cyclopropylmethyl)-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CC1 QYRDHSXXWABZCK-UHFFFAOYSA-N 0.000 description 1
- PTFCUQWWGSNPOT-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-cyclopentyl-n-(cyclopropylmethyl)-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(C1CCCC1)CC1CC1 PTFCUQWWGSNPOT-UHFFFAOYSA-N 0.000 description 1
- WFTKEUZYJNWKBI-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-cyclopentyl-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)C1CCCC1 WFTKEUZYJNWKBI-UHFFFAOYSA-N 0.000 description 1
- YYMZUSZFVXGFFX-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-ethyl-1,3-dimethyl-n-(oxolan-2-ylmethyl)pyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCCO1 YYMZUSZFVXGFFX-UHFFFAOYSA-N 0.000 description 1
- PBIMALDYZWMJNS-UHFFFAOYSA-N 5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-ethyl-1,3-dimethyl-n-propan-2-ylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C(C)C)C1=NC=2N(C)N=C(C)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 PBIMALDYZWMJNS-UHFFFAOYSA-N 0.000 description 1
- FHIDNBAQOFJWCA-UAKXSSHOSA-N 5-fluorouridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(F)=C1 FHIDNBAQOFJWCA-UAKXSSHOSA-N 0.000 description 1
- FKPXGNGUVSHWQQ-UHFFFAOYSA-N 5-methyl-1,2-oxazol-3-amine Chemical compound CC1=CC(N)=NO1 FKPXGNGUVSHWQQ-UHFFFAOYSA-N 0.000 description 1
- FRLDAOLRALUIJW-UHFFFAOYSA-N 6-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,3-diethyl-N,2-dimethylimidazo[4,5-b]pyridin-5-amine Chemical compound CCN(C)c1nc2n(CC)c(C)nc2cc1CN(Cc1cc(F)cc(F)c1)c1nnn(C)n1 FRLDAOLRALUIJW-UHFFFAOYSA-N 0.000 description 1
- QNPJNDXRJLHXOZ-UHFFFAOYSA-N 6-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,N,2,3-tetramethylimidazo[4,5-b]pyridin-5-amine Chemical compound CN(C)c1nc2n(C)c(C)nc2cc1CN(Cc1cc(F)cc(F)c1)c1nnn(C)n1 QNPJNDXRJLHXOZ-UHFFFAOYSA-N 0.000 description 1
- AECMBILOSGCACI-UHFFFAOYSA-N 6-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N,N,2,3-tetramethylimidazo[4,5-b]pyridin-5-amine Chemical compound FC(C=1C=C(CN(C=2N=NN(N2)C)CC=2C=C3C(=NC2N(C)C)N(C(=N3)C)C)C=C(C1)C(F)(F)F)(F)F AECMBILOSGCACI-UHFFFAOYSA-N 0.000 description 1
- VLWWLMFBTUPLMS-UHFFFAOYSA-N 6-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,3-diethyl-n,2-dimethylimidazo[4,5-b]pyridin-5-amine Chemical compound CCN(C)C1=NC=2N(CC)C(C)=NC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 VLWWLMFBTUPLMS-UHFFFAOYSA-N 0.000 description 1
- CZOSYEQWOYPNAS-UHFFFAOYSA-N 6-chloro-1-ethylpyrazolo[3,4-b]pyridine-5-carbaldehyde Chemical compound O=CC1=C(Cl)N=C2N(CC)N=CC2=C1 CZOSYEQWOYPNAS-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 101710126783 Acetyl-hydrolase Proteins 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 229910000497 Amalgam Inorganic materials 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 102000005666 Apolipoprotein A-I Human genes 0.000 description 1
- 108010059886 Apolipoprotein A-I Proteins 0.000 description 1
- 101710095342 Apolipoprotein B Proteins 0.000 description 1
- 102100040202 Apolipoprotein B-100 Human genes 0.000 description 1
- 102000018616 Apolipoproteins B Human genes 0.000 description 1
- 108010027006 Apolipoproteins B Proteins 0.000 description 1
- 102000006996 Aryldialkylphosphatase Human genes 0.000 description 1
- 108010008184 Aryldialkylphosphatase Proteins 0.000 description 1
- 108010024976 Asparaginase Proteins 0.000 description 1
- 229940123208 Biguanide Drugs 0.000 description 1
- XNCOSPRUTUOJCJ-UHFFFAOYSA-N Biguanide Chemical compound NC(N)=NC(N)=N XNCOSPRUTUOJCJ-UHFFFAOYSA-N 0.000 description 1
- 208000020084 Bone disease Diseases 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 239000003341 Bronsted base Substances 0.000 description 1
- OQWSVCXXAYKEFF-UHFFFAOYSA-N Brucin Natural products COc1cc2N3C4C5C(CC3=O)OC=CC6CN7CCC4(C7CC56)c2cc1OC OQWSVCXXAYKEFF-UHFFFAOYSA-N 0.000 description 1
- 125000006539 C12 alkyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000006374 C2-C10 alkenyl group Chemical group 0.000 description 1
- 125000005865 C2-C10alkynyl group Chemical group 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 108010004103 Chylomicrons Proteins 0.000 description 1
- LVZWSLJZHVFIQJ-UHFFFAOYSA-N Cyclopropane Chemical compound C1CC1 LVZWSLJZHVFIQJ-UHFFFAOYSA-N 0.000 description 1
- 238000010485 C−C bond formation reaction Methods 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 1
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000008055 Heparan Sulfate Proteoglycans Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- 206010020565 Hyperaemia Diseases 0.000 description 1
- 208000031226 Hyperlipidaemia Diseases 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- 238000008214 LDL Cholesterol Methods 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 101001043818 Mus musculus Interleukin-31 receptor subunit alpha Proteins 0.000 description 1
- JIWFWTMYALQYIR-UHFFFAOYSA-N N,1,2-triethyl-5-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N-methylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CCN(C)c1nc2n(CC)c(CC)cc2cc1CN(Cc1cc(F)cc(c1)C(F)(F)F)c1nnn(C)n1 JIWFWTMYALQYIR-UHFFFAOYSA-N 0.000 description 1
- NXKFKLNYAATDKH-UHFFFAOYSA-N N,2,3-triethyl-6-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-N-methylimidazo[4,5-b]pyridin-5-amine Chemical compound CCC1=NC2=C(N1CC)N=C(C(=C2)CN(CC3=CC(=CC(=C3)F)C(F)(F)F)C4=NN(N=N4)C)N(C)CC NXKFKLNYAATDKH-UHFFFAOYSA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- RKCIVXZUCLISIX-UHFFFAOYSA-N N-[[3,5-bis(trifluoromethyl)phenyl]methyl]-N-[[2-[1-[cyclopentyl(methyl)amino]ethyl]quinolin-3-yl]methyl]-2-methyltetrazol-5-amine Chemical compound FC(C=1C=C(CN(C=2N=NN(N2)C)CC=2C(=NC3=CC=CC=C3C2)C(C)N(C)C2CCCC2)C=C(C1)C(F)(F)F)(F)F RKCIVXZUCLISIX-UHFFFAOYSA-N 0.000 description 1
- LIWAQLJGPBVORC-UHFFFAOYSA-N N-ethyl-N-methylamine Natural products CCNC LIWAQLJGPBVORC-UHFFFAOYSA-N 0.000 description 1
- XTUVJUMINZSXGF-UHFFFAOYSA-N N-methylcyclohexylamine Chemical compound CNC1CCCCC1 XTUVJUMINZSXGF-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical class CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- 208000028389 Nerve injury Diseases 0.000 description 1
- 102000002002 Neurokinin-1 Receptors Human genes 0.000 description 1
- 108010040718 Neurokinin-1 Receptors Proteins 0.000 description 1
- 102000008299 Nitric Oxide Synthase Human genes 0.000 description 1
- 108010021487 Nitric Oxide Synthase Proteins 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- 102000014190 Phosphatidylcholine-sterol O-acyltransferase Human genes 0.000 description 1
- 108010011964 Phosphatidylcholine-sterol O-acyltransferase Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000282849 Ruminantia Species 0.000 description 1
- 206010040070 Septic Shock Diseases 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 229940100389 Sulfonylurea Drugs 0.000 description 1
- 108090000054 Syndecan-2 Proteins 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 229940123464 Thiazolidinedione Drugs 0.000 description 1
- 229940122388 Thrombin inhibitor Drugs 0.000 description 1
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 description 1
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 1
- 238000007239 Wittig reaction Methods 0.000 description 1
- GRTJBNJOHNTQBO-UHFFFAOYSA-N [2-(2-diphenylphosphanylphenyl)phenyl]-diphenylphosphane Chemical group C1=CC=CC=C1P(C=1C(=CC=CC=1)C=1C(=CC=CC=1)P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 GRTJBNJOHNTQBO-UHFFFAOYSA-N 0.000 description 1
- ADHUUMWSWNPEMZ-UHFFFAOYSA-N [3-fluoro-5-(trifluoromethyl)phenyl]methanamine Chemical compound NCC1=CC(F)=CC(C(F)(F)F)=C1 ADHUUMWSWNPEMZ-UHFFFAOYSA-N 0.000 description 1
- JEDZLBFUGJTJGQ-UHFFFAOYSA-N [Na].COCCO[AlH]OCCOC Chemical compound [Na].COCCO[AlH]OCCOC JEDZLBFUGJTJGQ-UHFFFAOYSA-N 0.000 description 1
- 230000003187 abdominal effect Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000005456 alcohol based solvent Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229930013930 alkaloid Natural products 0.000 description 1
- 150000004703 alkoxides Chemical class 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 150000001409 amidines Chemical class 0.000 description 1
- 150000001414 amino alcohols Chemical class 0.000 description 1
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- YUENFNPLGJCNRB-UHFFFAOYSA-N anthracen-1-amine Chemical compound C1=CC=C2C=C3C(N)=CC=CC3=CC2=C1 YUENFNPLGJCNRB-UHFFFAOYSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 230000001088 anti-asthma Effects 0.000 description 1
- 230000000489 anti-atherogenic effect Effects 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000000947 anti-immunosuppressive effect Effects 0.000 description 1
- 239000000924 antiasthmatic agent Substances 0.000 description 1
- 239000003529 anticholesteremic agent Substances 0.000 description 1
- 229940127226 anticholesterol agent Drugs 0.000 description 1
- 229940053202 antiepileptics carboxamide derivative Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 159000000032 aromatic acids Chemical class 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 238000005574 benzylation reaction Methods 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- RRKTZKIUPZVBMF-IBTVXLQLSA-N brucine Chemical compound O([C@@H]1[C@H]([C@H]2C3)[C@@H]4N(C(C1)=O)C=1C=C(C(=CC=11)OC)OC)CC=C2CN2[C@@H]3[C@]41CC2 RRKTZKIUPZVBMF-IBTVXLQLSA-N 0.000 description 1
- RRKTZKIUPZVBMF-UHFFFAOYSA-N brucine Natural products C1=2C=C(OC)C(OC)=CC=2N(C(C2)=O)C3C(C4C5)C2OCC=C4CN2C5C31CC2 RRKTZKIUPZVBMF-UHFFFAOYSA-N 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 230000006041 cell recruitment Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 229910052729 chemical element Inorganic materials 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 239000012069 chiral reagent Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000002603 chloroethyl group Chemical group [H]C([*])([H])C([H])([H])Cl 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- 150000005753 chloropyridines Chemical class 0.000 description 1
- 125000003724 cholesterol ester group Chemical group 0.000 description 1
- 150000001840 cholesterol esters Chemical class 0.000 description 1
- 229940125881 cholesteryl ester transfer protein inhibitor Drugs 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 238000010668 complexation reaction Methods 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 239000013058 crude material Substances 0.000 description 1
- 238000007333 cyanation reaction Methods 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- JFWMYCVMQSLLOO-UHFFFAOYSA-N cyclobutanecarbonyl chloride Chemical compound ClC(=O)C1CCC1 JFWMYCVMQSLLOO-UHFFFAOYSA-N 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000004850 cyclobutylmethyl group Chemical group C1(CCC1)C* 0.000 description 1
- VZFUCHSFHOYXIS-UHFFFAOYSA-N cycloheptane carboxylic acid Natural products OC(=O)C1CCCCCC1 VZFUCHSFHOYXIS-UHFFFAOYSA-N 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000006622 cycloheptylmethyl group Chemical group 0.000 description 1
- RVOJTCZRIKWHDX-UHFFFAOYSA-N cyclohexanecarbonyl chloride Chemical compound ClC(=O)C1CCCCC1 RVOJTCZRIKWHDX-UHFFFAOYSA-N 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000006547 cyclononyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000006623 cyclooctylmethyl group Chemical group 0.000 description 1
- WEPUZBYKXNKSDH-UHFFFAOYSA-N cyclopentanecarbonyl chloride Chemical compound ClC(=O)C1CCCC1 WEPUZBYKXNKSDH-UHFFFAOYSA-N 0.000 description 1
- PYRZPBDTPRQYKG-UHFFFAOYSA-N cyclopentene-1-carboxylic acid Chemical compound OC(=O)C1=CCCC1 PYRZPBDTPRQYKG-UHFFFAOYSA-N 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000005595 deprotonation Effects 0.000 description 1
- 238000010537 deprotonation reaction Methods 0.000 description 1
- 239000007933 dermal patch Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- 230000035487 diastolic blood pressure Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- GPAYUJZHTULNBE-UHFFFAOYSA-N diphenylphosphine Chemical compound C=1C=CC=CC=1PC1=CC=CC=C1 GPAYUJZHTULNBE-UHFFFAOYSA-N 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 229940127257 dual PPAR agonist Drugs 0.000 description 1
- 239000003602 elastase inhibitor Substances 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- XWBDWHCCBGMXKG-UHFFFAOYSA-N ethanamine;hydron;chloride Chemical compound Cl.CCN XWBDWHCCBGMXKG-UHFFFAOYSA-N 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- 125000005448 ethoxyethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- 125000005745 ethoxymethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])* 0.000 description 1
- VICYTAYPKBLQFB-UHFFFAOYSA-N ethyl 3-bromo-2-oxopropanoate Chemical compound CCOC(=O)C(=O)CBr VICYTAYPKBLQFB-UHFFFAOYSA-N 0.000 description 1
- URETXXSNYYZQQR-UHFFFAOYSA-N ethyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamothioyl]carbamate Chemical compound C=1C2=CC=CC=C2N=C(N(CC)CC2CCCC2)C=1CN(C(=S)NC(=O)OCC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 URETXXSNYYZQQR-UHFFFAOYSA-N 0.000 description 1
- KQBCDCCOBIJZMN-UHFFFAOYSA-N ethyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[4-(cyclohexylmethyl)piperazin-1-yl]quinolin-3-yl]methyl]carbamate Chemical compound C=1C2=CC=CC=C2N=C(N2CCN(CC3CCCCC3)CC2)C=1CN(C(=O)OCC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 KQBCDCCOBIJZMN-UHFFFAOYSA-N 0.000 description 1
- BTDIMGSRLPOWKK-UHFFFAOYSA-N ethyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[butyl(ethyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound CCCCN(CC)C1=NC2=CC=CC=C2C=C1CN(C(=O)OCC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 BTDIMGSRLPOWKK-UHFFFAOYSA-N 0.000 description 1
- ZROXYHJBYVUARA-UHFFFAOYSA-N ethyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(propyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OCC)C=1N(CCC)CC1CCCC1 ZROXYHJBYVUARA-UHFFFAOYSA-N 0.000 description 1
- 125000004672 ethylcarbonyl group Chemical group [H]C([H])([H])C([H])([H])C(*)=O 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical compound NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 1
- 229960004413 flucytosine Drugs 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000004175 fluorobenzyl group Chemical group 0.000 description 1
- 125000003784 fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 description 1
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 239000003823 glutamate receptor agonist Substances 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- AMANDCZTVNQSNB-UHFFFAOYSA-N glyoxamide Chemical compound NC(=O)C=O AMANDCZTVNQSNB-UHFFFAOYSA-N 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 150000002366 halogen compounds Chemical class 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000002363 herbicidal effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- IKDUDTNKRLTJSI-UHFFFAOYSA-N hydrazine monohydrate Substances O.NN IKDUDTNKRLTJSI-UHFFFAOYSA-N 0.000 description 1
- BRWIZMBXBAOCCF-UHFFFAOYSA-N hydrazinecarbothioamide Chemical compound NNC(N)=S BRWIZMBXBAOCCF-UHFFFAOYSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 201000001421 hyperglycemia Diseases 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 230000001861 immunosuppressant effect Effects 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 238000007914 intraventricular administration Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000003965 isoxazolidinyl group Chemical group 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000003199 leukotriene receptor blocking agent Substances 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 230000037356 lipid metabolism Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- LVWZTYCIRDMTEY-UHFFFAOYSA-N metamizole Chemical compound O=C1C(N(CS(O)(=O)=O)C)=C(C)N(C)N1C1=CC=CC=C1 LVWZTYCIRDMTEY-UHFFFAOYSA-N 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- ZOXYUUHHWCTUMB-UHFFFAOYSA-N methyl n-[[2-[bis(cyclopropylmethyl)amino]-8-methylquinolin-3-yl]methyl]-n-[[3,5-bis(trifluoromethyl)phenyl]methyl]carbamate Chemical compound C=1C2=CC=CC(C)=C2N=C(N(CC2CC2)CC2CC2)C=1CN(C(=O)OC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 ZOXYUUHHWCTUMB-UHFFFAOYSA-N 0.000 description 1
- DZPFMXMFURUVJM-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclobutylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CCC1 DZPFMXMFURUVJM-UHFFFAOYSA-N 0.000 description 1
- GFLMCDHUEGRHMC-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]-5,6,7,8-tetrahydroquinolin-3-yl]methyl]carbamate Chemical compound N=1C=2CCCCC=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CCCC1 GFLMCDHUEGRHMC-UHFFFAOYSA-N 0.000 description 1
- FUERTWOVMCBAIC-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]-6-methylquinolin-3-yl]methyl]carbamate Chemical compound N=1C2=CC=C(C)C=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CCCC1 FUERTWOVMCBAIC-UHFFFAOYSA-N 0.000 description 1
- GITHBSDJZHOKKF-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamodithioate Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=S)SC)C=1N(CC)CC1CCCC1 GITHBSDJZHOKKF-UHFFFAOYSA-N 0.000 description 1
- FHGLFNAQIFGIIA-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopropylmethyl(ethyl)amino]quinolin-3-yl]methyl]carbamate Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CC1 FHGLFNAQIFGIIA-UHFFFAOYSA-N 0.000 description 1
- FIDYQDSSGUVCLW-UHFFFAOYSA-N methyl n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[6-[cyclopentylmethyl(ethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridin-5-yl]methyl]carbamate Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C(=O)OC)C=1N(CC)CC1CCCC1 FIDYQDSSGUVCLW-UHFFFAOYSA-N 0.000 description 1
- 125000004674 methylcarbonyl group Chemical group CC(=O)* 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- JVNLOQGGKYDYES-UHFFFAOYSA-N n,1,3-triethyl-5-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-methylpyrazolo[3,4-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)N=C(CC)C=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(C(F)(F)F)=C1 JVNLOQGGKYDYES-UHFFFAOYSA-N 0.000 description 1
- VBRGEXFOPUYJJN-UHFFFAOYSA-N n,1-diethyl-5-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,2-dimethylpyrrolo[2,3-b]pyridin-6-amine Chemical compound CCN(C)C1=NC=2N(CC)C(C)=CC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(C(F)(F)F)=C1 VBRGEXFOPUYJJN-UHFFFAOYSA-N 0.000 description 1
- NLNPFJKEOGRTFG-UHFFFAOYSA-N n,3-diethyl-6-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-n,2-dimethylimidazo[4,5-b]pyridin-5-amine Chemical compound CCN(C)C1=NC=2N(CC)C(C)=NC=2C=C1CN(C1=NN(C)N=N1)CC1=CC(F)=CC(C(F)(F)F)=C1 NLNPFJKEOGRTFG-UHFFFAOYSA-N 0.000 description 1
- GXQNOHASRMTPED-UHFFFAOYSA-N n,n-bis(cyclopropylmethyl)-5-[[(3,5-dichlorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound C=1C(Cl)=CC(Cl)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(CC1CC1)CC1CC1 GXQNOHASRMTPED-UHFFFAOYSA-N 0.000 description 1
- IJSIURRTZRNKBH-UHFFFAOYSA-N n,n-bis(cyclopropylmethyl)ethanamine Chemical compound C1CC1CN(CC)CC1CC1 IJSIURRTZRNKBH-UHFFFAOYSA-N 0.000 description 1
- BYXFJQZJRLPQDF-UHFFFAOYSA-N n-(cyclopentylmethyl)-5-[[(3,5-dichlorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(Cl)C=C(Cl)C=2)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 BYXFJQZJRLPQDF-UHFFFAOYSA-N 0.000 description 1
- XLAURLHVQSVZOF-UHFFFAOYSA-N n-(cyclopentylmethyl)-5-[[(3,5-difluorophenyl)methyl-(2-methyltetrazol-5-yl)amino]methyl]-n-ethyl-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(F)C=C(F)C=2)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 XLAURLHVQSVZOF-UHFFFAOYSA-N 0.000 description 1
- KWMFYQVWIKOKGQ-UHFFFAOYSA-N n-(cyclopentylmethyl)-n-ethyl-5-[[[3-fluoro-5-(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(F)C=2)C(F)(F)F)C2=NN(C)N=N2)C=1N(CC)CC1CCCC1 KWMFYQVWIKOKGQ-UHFFFAOYSA-N 0.000 description 1
- RLEOFPJZLSTGTA-UHFFFAOYSA-N n-(cyclopentylmethyl)propan-1-amine Chemical compound CCCNCC1CCCC1 RLEOFPJZLSTGTA-UHFFFAOYSA-N 0.000 description 1
- HCLAKJJHNUOCRL-UHFFFAOYSA-N n-(cyclopropylmethyl)-2-methylpropan-1-amine Chemical compound CC(C)CNCC1CC1 HCLAKJJHNUOCRL-UHFFFAOYSA-N 0.000 description 1
- CUJOUJDTVQIJRO-UHFFFAOYSA-N n-(cyclopropylmethyl)cyclopentanamine Chemical compound C1CC1CNC1CCCC1 CUJOUJDTVQIJRO-UHFFFAOYSA-N 0.000 description 1
- CNOCZEWICNKWKU-UHFFFAOYSA-N n-(cyclopropylmethyl)cyclopropanecarboxamide Chemical class C1CC1C(=O)NCC1CC1 CNOCZEWICNKWKU-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- BMZPGSKGYSPIQY-UHFFFAOYSA-N n-[5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-yl]-3-chloro-n-(cyclopropylmethyl)propanamide Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(C(=O)CCCl)CC1CC1 BMZPGSKGYSPIQY-UHFFFAOYSA-N 0.000 description 1
- HTSCAXMNTICSAZ-UHFFFAOYSA-N n-[5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-yl]-n-(cyclopropylmethyl)acetamide Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NN(C)N=N2)C=1N(C(=O)C)CC1CC1 HTSCAXMNTICSAZ-UHFFFAOYSA-N 0.000 description 1
- RCHSXIMOQLCWIJ-UHFFFAOYSA-N n-[5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-yl]-n-(cyclopropylmethyl)cyclohexanecarboxamide Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(C(=O)C1CCCCC1)CC1CC1 RCHSXIMOQLCWIJ-UHFFFAOYSA-N 0.000 description 1
- YLRWKOANWWCEME-UHFFFAOYSA-N n-[5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-yl]-n-(cyclopropylmethyl)cyclopentanecarboxamide Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(C(=O)C1CCCC1)CC1CC1 YLRWKOANWWCEME-UHFFFAOYSA-N 0.000 description 1
- UQVOVIJZNQRNCU-UHFFFAOYSA-N n-[5-[[[3,5-bis(trifluoromethyl)phenyl]methyl-(2-methyltetrazol-5-yl)amino]methyl]-1,3-dimethylpyrazolo[3,4-b]pyridin-6-yl]-n-(cyclopropylmethyl)cyclopropanecarboxamide Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1CN(C1=NN(C)N=N1)CC=1C=C2C(C)=NN(C)C2=NC=1N(C(=O)C1CC1)CC1CC1 UQVOVIJZNQRNCU-UHFFFAOYSA-N 0.000 description 1
- HLSDMLXXPIEJFI-ZETCQYMHSA-N n-[[(2s)-oxolan-2-yl]methyl]ethanamine Chemical compound CCNC[C@@H]1CCCO1 HLSDMLXXPIEJFI-ZETCQYMHSA-N 0.000 description 1
- UMBHFCITBNWQDQ-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[(6-chloro-1,3-dimethylpyrazolo[3,4-b]pyridin-5-yl)methyl]-2-methyltetrazol-5-amine Chemical compound C1=C2C(C)=NN(C)C2=NC(Cl)=C1CN(C1=NN(C)N=N1)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 UMBHFCITBNWQDQ-UHFFFAOYSA-N 0.000 description 1
- PGJUQBSZYJREHD-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclobutylmethyl(ethyl)amino]quinolin-3-yl]methyl]-5-methyl-1,2-oxazol-3-amine Chemical class N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NOC(C)=C2)C=1N(CC)CC1CCC1 PGJUQBSZYJREHD-UHFFFAOYSA-N 0.000 description 1
- USLSEQBDVKFJJT-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]-4,5-dihydro-1,3-oxazol-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2OCCN=2)C=1N(CC)CC1CCCC1 USLSEQBDVKFJJT-UHFFFAOYSA-N 0.000 description 1
- GUOMATWHRCHEQV-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]-4-methyl-1,3-oxazol-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2OC=C(C)N=2)C=1N(CC)CC1CCCC1 GUOMATWHRCHEQV-UHFFFAOYSA-N 0.000 description 1
- NSCLNCIGYMRLPX-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[2-[cyclopentylmethyl(ethyl)amino]quinolin-3-yl]methyl]-5-methyl-1,3,4-oxadiazol-2-amine Chemical compound N=1C2=CC=CC=C2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2OC(C)=NN=2)C=1N(CC)CC1CCCC1 NSCLNCIGYMRLPX-UHFFFAOYSA-N 0.000 description 1
- BCEGIOWPDPPWLU-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[6-[cyclobutylmethyl(ethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridin-5-yl]methyl]-5-methyl-1,2-oxazol-3-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C2=NOC(C)=C2)C=1N(CC)CC1CCC1 BCEGIOWPDPPWLU-UHFFFAOYSA-N 0.000 description 1
- VZWAUAWVFOYWNO-UHFFFAOYSA-N n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-n-[[6-[cyclopentylmethyl(ethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridin-5-yl]methyl]-4-(trifluoromethyl)-1,3-oxazol-2-amine Chemical compound N=1C=2N(C)N=C(C)C=2C=C(CN(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)C=2OC=C(N=2)C(F)(F)F)C=1N(CC)CC1CCCC1 VZWAUAWVFOYWNO-UHFFFAOYSA-N 0.000 description 1
- FHCAIEMFCZHNRK-UHFFFAOYSA-N n-[[6-[bis(cyclopropylmethyl)amino]-1,3-dimethylpyrazolo[3,4-b]pyridin-5-yl]methyl]-n-[[3,5-bis(trifluoromethyl)phenyl]methyl]-5-methyl-1,2-oxazol-3-amine Chemical compound O1C(C)=CC(N(CC=2C=C(C=C(C=2)C(F)(F)F)C(F)(F)F)CC=2C(=NC=3N(C)N=C(C)C=3C=2)N(CC2CC2)CC2CC2)=N1 FHCAIEMFCZHNRK-UHFFFAOYSA-N 0.000 description 1
- HVAAHUDGWQAAOJ-UHFFFAOYSA-N n-benzylethanamine Chemical compound CCNCC1=CC=CC=C1 HVAAHUDGWQAAOJ-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- WHXPIXBWEZSBJL-UHFFFAOYSA-N n-ethyl-2,2-dimethylpropan-1-amine Chemical compound CCNCC(C)(C)C WHXPIXBWEZSBJL-UHFFFAOYSA-N 0.000 description 1
- QHCCDDQKNUYGNC-UHFFFAOYSA-N n-ethylbutan-1-amine Chemical compound CCCCNCC QHCCDDQKNUYGNC-UHFFFAOYSA-N 0.000 description 1
- SRTHFWNTKVOSBA-UHFFFAOYSA-N n-ethylcyclopentanamine Chemical compound CCNC1CCCC1 SRTHFWNTKVOSBA-UHFFFAOYSA-N 0.000 description 1
- RIVIDPPYRINTTH-UHFFFAOYSA-N n-ethylpropan-2-amine Chemical compound CCNC(C)C RIVIDPPYRINTTH-UHFFFAOYSA-N 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- UFWIBTONFRDIAS-UHFFFAOYSA-N naphthalene-acid Natural products C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- 229940097496 nasal spray Drugs 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 230000008764 nerve damage Effects 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 230000001293 nucleolytic effect Effects 0.000 description 1
- 239000012038 nucleophile Substances 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 229940126701 oral medication Drugs 0.000 description 1
- 239000000668 oral spray Substances 0.000 description 1
- 229940041678 oral spray Drugs 0.000 description 1
- 239000007935 oral tablet Substances 0.000 description 1
- 230000008816 organ damage Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 125000000160 oxazolidinyl group Chemical group 0.000 description 1
- 125000004043 oxo group Chemical group O=* 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 238000010651 palladium-catalyzed cross coupling reaction Methods 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004344 phenylpropyl group Chemical group 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- 125000004585 polycyclic heterocycle group Chemical group 0.000 description 1
- 229940068917 polyethylene glycols Drugs 0.000 description 1
- TZLVRPLSVNESQC-UHFFFAOYSA-N potassium azide Chemical compound [K+].[N-]=[N+]=[N-] TZLVRPLSVNESQC-UHFFFAOYSA-N 0.000 description 1
- 235000015497 potassium bicarbonate Nutrition 0.000 description 1
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 1
- 239000011736 potassium bicarbonate Substances 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 229940080818 propionamide Drugs 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000004673 propylcarbonyl group Chemical group 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 208000002815 pulmonary hypertension Diseases 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 150000008318 pyrimidones Chemical class 0.000 description 1
- NGXSWUFDCSEIOO-UHFFFAOYSA-N pyrrolidin-3-amine Chemical compound NC1CCNC1 NGXSWUFDCSEIOO-UHFFFAOYSA-N 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 229940044601 receptor agonist Drugs 0.000 description 1
- 239000000018 receptor agonist Substances 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 125000000467 secondary amino group Chemical group [H]N([*:1])[*:2] 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000003001 serine protease inhibitor Substances 0.000 description 1
- 230000000862 serotonergic effect Effects 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000004946 small molecule transport Effects 0.000 description 1
- 239000012419 sodium bis(2-methoxyethoxy)aluminum hydride Substances 0.000 description 1
- 239000007962 solid dispersion Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000002732 sphingomyelin phosphodiesterase inhibitor Substances 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 230000006103 sulfonylation Effects 0.000 description 1
- 238000005694 sulfonylation reaction Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 230000035488 systolic blood pressure Effects 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 125000001302 tertiary amino group Chemical group 0.000 description 1
- 125000005207 tetraalkylammonium group Chemical group 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- 239000003868 thrombin inhibitor Substances 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 230000037317 transdermal delivery Effects 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 1
- 125000006493 trifluoromethyl benzyl group Chemical group 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 210000005167 vascular cell Anatomy 0.000 description 1
- 229940124676 vascular endothelial growth factor receptor Drugs 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 229940102001 zinc bromide Drugs 0.000 description 1
- 150000003952 β-lactams Chemical class 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/438—The ring being spiro-condensed with carbocyclic or heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/73—Unsubstituted amino or imino radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/78—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/14—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D241/20—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Diabetes (AREA)
- Heart & Thoracic Surgery (AREA)
- Hematology (AREA)
- Cardiology (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Quinoline Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Lubricants (AREA)
Abstract
본 발명은 다른 물질 사이에 신규 벤질아민 화합물, 벤질아민 화합물을 포함하는 조성물, 벤질아민 화합물의 제조 방법, 및 지단백질 대사와 관련된 다양한 증상 또는 질환을 치료하거나 또는 예방하기 위한 벤질아민 화합물의 사용 방법을 제공한다.
벤질아민 화합물, 지단백질, 콜레스테릴 에스테르-전이 단백질 (CETP), HDL, LDL
Description
본 발명은 벤질아민 화합물, 벤질아민 화합물의 제조 및 사용을 위한 방법 및 조성물, 및 지단백질 대사와 관련된 증상 또는 질환의 치료 또는 예방을 위한 조성물 및 방법에 관한 것이다.
콜레스테릴 에스테르-전이 단백질 (CETP)은 지단백질, 예컨대 고밀도 지단백질 (HDL)의 대사에서 중요한 역할을 한다. CETP는 HDL 입자와 물리적으로 회합되는 70 kDa의 혈장 당단백질이다. 이는 HDL에서 아포지단백질 B-함유 지단백질로의 콜레스테릴 에스테르의 수송을 촉진한다. 이러한 전이는 반대 방향으로 트리글리세리드의 전이를 동반한다. 따라서, CETP 활성의 감소는 HDL 콜레스테롤 수준의 증가 및 초저밀도 지단백질 (VLDL) 및 저밀도 지단백질 (LDL) 수준의 감소를 야기할 수 있다. 따라서, CETP는 동시에 전아테롬형성 (예를 들어, LDL) 및 항아테롬형성 (예를 들어, HDL) 지단백질의 농도에 영향을 미칠 수 있다.
인간 및 임상 연구는 CETP의 저해제가 HDL 수준을 30 내지 60%까지 높이는 데 효과적일 수 있다는 것을 제시한다. 또한, 전염병학적 연구는 고밀도 지단백질 콜레스테롤 (HDL-C)의 감소가 관상 동맥 질환 (CAD)에 대한 유력한 위험 요소라는 것을 제시한다 (문헌 [Gordon et al, Circulation, 79, pp. 8-15, 1989; Despres et al, Atherosclerosis 153: 263-272, 2000]). HDL-C의 증가는 이러한 위험의 감소를 제시하는데, HDL-C가 각각 1 mg/dl (0.02 mmol/l) 증가하면 관상 심장 질환 (CHD) 위험이 2-3% 감소되는 것과 관련이 있는 것으로 추정되며, 이 수치는 저밀도 지단백질 (LDL)의 감소에 대한 것과 유사하다. 혈청 HDL-C 수준이 40 mg/dl 초과가 1차 및 2차 예방에 있어서 치료 목표로 고려되는 것이 추천되었다. 이러한 목적은, 혈청 저밀도 지단백질 콜레스테롤 (LDL-C) 수준 (100 mg/dl 미만)에 대한 치료 목표가 비록 달성되었더라도, 낮은 혈청 HDL-C 수준 및 허혈성 심장 질환 (IHD) 또는 이와 대등한 질환을 앓는 환자에게 특히 중요한 것으로 보인다.
HDL의 항아테롬형성 역할은 콜레스테롤 역수송으로 불리는 과정인 세포로부터의 유리 콜레스테롤의 유출을 촉진하고, 이를 간으로 수송하는 그의 능력에 부분적으로 기인하는 것으로 여겨진다. HDL은 다른 수가지 메커니즘에 의해 아테롬성동맥경화증에 대해서 보호할 수 있다. 예를 들어, 몇 가지 연구에서 HDL은 항산화 및 항염증 효과를 갖는 것으로 나타났다. 지질 대사의 산화 생성물은 혈관 세포에서 염증 세포 동원을 야기한다. HDL 입자는 파라옥소나제, 혈소판-활성화 인자인 아세틸히드롤라제 및 레시틴-콜레스테롤 아실트랜스퍼라제를 비롯한 LDL 산화를 저지하는 효소를 운반한다. 이들 효소는 LDL에서 이들의 축적을 제한하면서 전-염증, 산화된 인지질을 분해한다. 또한, 아포A-I는 산화된 지질과 결합하여 LDL로부터 이들을 제거할 수 있다. 또한, HDL은 박테리아 지다당류 (LPS)를 비롯한 소분자용 운반 비히클로 작용할 수도 있으므로, LPS의 염증 효과를 조절한다. 내독소 성 쇼크의 동물 모델에서, HDL은 기관 손상 및 유착 분자 발현을 약화시킨다. 따라서, HDL 증가는 항아테롬형성일 뿐만 아니라 잠재적으로 항염증성일 수도 있다.
현존하는 요법, 예를 들어 HDL-증가 요법 및 항-아테롬성동맥경화증 요법은 심각한 내성 문제를 비롯한 한계가 있다. 지단백질 대사와 관련된 증상 또는 질환, 예를 들어 아테롬성동맥경화증의 예방 또는 치료 방법을 비롯한 대체적인 요법을 강구할 필요가 있다.
<발명의 개요>
본 발명은 신규 벤질아민 화합물, 상기 벤질아민 화합물을 포함하는 신규 조성물, 및 상기 벤질아민 화합물 및 그의 조성물을 사용하는 신규 방법에 관한 것이다. 본원에 개시된 것은 벤질아민 화합물, 상기 벤질아민을 포함하는 조성물의 제조 방법, 및 상기 벤질아민을 사용하는 방법 및 조성물이다. 벤질아민 화합물 및 상기 화합물을 포함하는 조성물은 다양한 질환의 치료에 유용하다. 벤질아민 화합물의 특정 측면은 PCT 공개 제WO 2004/020393호, 및 미국 특허 제6,710,089호 및 제6,723,753호에 개시되어 있다.
한 측면에서, 본 발명은 하기 화학식 I의 구조를 갖는 화합물, 및 상기 화합물 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
A는 5개 내지 10개의 고리 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭, 헤테로시클릭 잔기이고;
R1 및 R2는 1) 수소; 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로시클릴, 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 3) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 4) (CHRx)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고, Rx는 각각의 경우에서 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택되고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로시클릴 또는 헤테 로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택되거나; 또는
R1 및 R2는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 Z 이외에 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성하고;
R3은 1) 수소 또는 시아노; 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬; 3) 치환되거나 또는 비치환된 아릴, 또는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7, C(S)NR6R7, C(S)NC(O)OR8 또는 C(S)SR8로부터 선택되고;
여기서, R3이 알킬, 아릴, 헤테로시클릴 또는 헤테로아릴인 경우, R3은 할라 이드, 히드록실, 시아노, 12개 이하의 탄소 원자를 갖는 알콕시, 또는 R11로부터 독립적으로 선택된 3개 이하의 치환기로 임의로 치환되고;
R4는 각각의 경우에서 1) 할로겐, 시아노 또는 히드록시; 2) 알킬, 시클로알킬, 시클로알콕시, 알콕시, 할로알킬 또는 할로알콕시 (이들은 12개 이하의 탄소 원자를 가짐); 3) 치환되거나 또는 비치환된 아릴, 아르알킬, 아릴옥시, 헤테로아릴 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로아릴 또는 헤테로아릴옥시는 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7 또는 (CH2)qNR6R7 (여기서, q는 0 내지 5의 정수임)로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이거나; 또는
R4 m은 3개 내지 5개의 추가의 고리 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 임의로 포함하는 융합 시클릭 잔기이고;
R5는 각각의 경우에서 1) 알콕시, 할로알콕시 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) 치환되거나 또는 비치환된 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 3) 히드록실, NR6R7, CO2R6, COR8 또는 SO2R8; 또는 4) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6 및 R7은 각각의 경우에서 1) 수소; 2) 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) 치환되거나 또는 비치환된 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되거나; 또는
R6 및 R7은 함께 3개 내지 7개의 고리 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자를 R6 및 R7이 결합된 질소 원자 이외에 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성하고;
R8은 각각의 경우에서 1) 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) 치환되거나 또는 비치환된 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Z는 N 또는 CH이거나; 또는 ZR1 잔기는 S, CO 또는 SO2이거나; 또는 ZR1R2 잔기는 -C≡CR2이고;
R11은
1) 알킬, 할로알킬, 시클로알킬 또는 알콕시카르보닐 (이들은 12개 이하의 탄소 원자를 가짐);
2) 치환되거나 또는 비치환된 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하고, 여기서 임의의 치환된 헤테로아릴 또는 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 알킬, 또는 히드록실로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨); 또는
3) -CO-Z2-R13, -CO-R12, -CO-Z2-(CH2)r-CO-Z2-R13, -NR15R16, -Z2-CO-(CH2)r-Z2-R13, -Z2-CO-(CH2)r-CO-Z2-R13, -O-(CH2)r-CO-Z2-R13, -O-(CH2)r-R14, -O-R12-(CH2)r-R13, -O-R14-CO-O-R13, -O-(CH2)r-R12, -O-(CH2)r-NR'R", -O-(CH2)r-CO2-(CH2)r-R13, -O-(CH2)r-CONR'R", -O-(CH2)r-SR8, -O-(CH2)r-CO2-R13, -O-(CH2)r-O-(CH2)r-OR13, -O-(CH2)r-CONR'R", -O-(CH2)r-CONH-(CH2)r-OR13, -O-(CH2)r-SO2R8, -O-(CH2)r-R13, -O-(CH2)r-OR13, -O-(CH2)r-O-(CH2)r-OR13, -S-(CH2)r-CONR'R", -SO2-(CH2)r-OR13, -SO2-(CH2)r-CONR'R", -(CH2)r-O-CO-R8, -(CH2)r-R12, -(CH2)r-R13, -(CH2)r-N-(CH2)r-OR13, -(CH2)r-CO-Z2-R13, -(CH2)r-Z2-R13 또는 -알케닐렌-CO2-(CH2)r-R13으로부터 독립적으로 선택되고;
r은 각각의 경우에서 독립적으로 1, 2 또는 3이고;
R12는 각각의 경우에서 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로 기를 포함하는 치환되거나 또는 비치환된 헤테로시클릴 (여기서 임의의 치환된 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 아실, 알킬 또는 알콕시카르보닐로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨), 또는 -COOH로부터 독립적으로 선택되고;
R13은 각각의 경우에서 1) 수소; 또는 2) 시클로알킬, 아릴, 할로알킬, 헤테로시클릴 또는 1개 이상의 히드록실로 임의로 치환된 알킬기 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R14는 각각의 경우에서 헤테로시클릴, 시클로알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
Z2는 각각의 경우에서 >NR10 또는 O로부터 독립적으로 선택되고;
R' 및 R"는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
R15 및 R16은 각각의 경우에서 1) 수소; 2) 12개 이하의 탄소 원자를 갖는 알 킬; 또는 3) -(CH2)r-O-R13, -(CH2)r-R14, -COR13, -(CH2)r-CO-Z2-R13, -CO2R13, -CO2-(CH2)r-R13, -CO2-(CH2)r-R12, -CO2-(CH2)r-CO-Z2-R13, -CO2-(CH2)r-OR13, -CO-(CH2)r-O-(CH2)r-O-(CH2)r-R13, -CO-(CH2)r-O(CH2)r-OR13 또는 -CO-NH-(CH2)r-OR13으로부터 독립적으로 선택되거나; 또는
R15 및 R16은 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 추가의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성하고; 여기서 임의의 치환된 시클릭 잔기는 1) 히드록실; 2) 알킬 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴은 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) COOR13, -Z2-(CH2)r-R13, -COR13, -CO2-(CH2)r-R13, -CO(CH2)r-O-R13, -(CH2)r-CO2-R13, -SO2R8, -SO2NR'R", 또는 -NR'R"로부터 독립적으로 선택된 3개 이하의 치환기로 치환되고; 여기서 -(CH2)r- 연결 잔기는 임의의 경우에서 히드록실, 아미노 또는 3개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택된 1개 이상의 기로 임의로 치환되고;
A는 1) 할로겐, 시아노, 또는 히드록실; 2) 알킬, 알케닐, 알키닐, 할로알킬, 시클로알킬, 알콕시, 시클로알콕시, 할로알콕시, 아릴, 아릴옥시, 아르알킬, 헤테로아릴, 헤테로시클릴, 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴, 헤테로시클릴, 또는 헤테로아릴옥시는 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 3) CO2R6, COR8, SO2R8, SO2NR6R7, 또는 CONR6R7; 4) (CH2)qNR6R7 (여기서, q는 0 내지 5의 정수임); 또는 5) (CH2)qCO2(CH2)q (여기서, q는 0 내지 3의 정수로부터 독립적으로 선택됨)로부터 독립적으로 선택된 1개, 2개 또는 3개의 치환기로 임의로 치환되고;
R1 및 R2이 모노시클릭 또는 비시클릭 잔기를 형성하지 않는 경우, R1 및 R2는 1) 알킬, 시클로알킬, 할로알킬, 알콕시, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 할로겐, 시아노 또는 히드록실로부터 독립적으로 선택된 1개 또는 2개의 치환기로 임의로 및 독립적으로 치환되고;
R1 및 R2가 함께 모노시클릭 또는 비시클릭 잔기를 형성하는 경우, 시클릭 잔기는 1) 할로겐, 시아노, 또는 히드록실; 2) 알킬, 할로알킬, 시클로알킬, 알콕 시, 시클로알킬-치환된 알킬, 알콕시알킬, 시클로알콕시, 할로알콕시, 아릴, 아릴옥시, 아르알킬, 헤테로아릴 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로아릴옥시는 >O, >N-, >S, 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) CO2R6, COR8, SO2R8, SO2NR6R7, 또는 CONR6R7; 또는 4) (CH2)qCO2(CH2)q (여기서, q는 0 내지 3의 정수로부터 독립적으로 선택됨)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
R4, R5, R6, R7 및 R8은 1) 할라이드, 히드록시, 시아노, 또는 NR6R7; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 알콕시로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 및 독립적으로 치환된다.
본원을 통해, 달리 명시하지 않으면, 모노시클릭 또는 비시클릭 잔기, 예컨대 A의 임의의 부분 상의 치환기로서의 임의의 원자 또는 기의 표시는 원자 또는 기가 비시클릭 잔기 A의 어느 고리에 결합된 결합위치이성질체를 비롯한 모든 가능한 결합위치이성질체를 나타내고자 하는 것이다. 예를 들어, 치환기, 예컨대 Ra가 퀴놀린 잔기의 카르보시클릭 고리 상의 임의의 위치에 결합된 경우, 그러한 표시는 Ra가 헤테로시클릭 고리에 결합된 결합위치이성질체도 포함하는 것으로 이해해야 한다. 따라서, 표기 는 Ra 잔기가 헤테로사이클 상의 이용가능한 탄소 에 결합된 것, 및 Ra 잔기가 카르보사이클 및 헤테로사이클 둘 다에 결합될 수 있는 것으로 제시된 바와 같이 Ra 잔기가 카르보사이클에 결합될 수 있는 모든 결합위치이성질체를 포함하기 위해 사용된다. 추가로, 본 명세서에서 전체적으로, 달리 명시하지 않으면, 임의의 헤테로시클릴, 임의의 헤테로시클로알킬, 임의의 헤테로아릴, 및 임의의 헤테로아릴옥시는 문맥이 허용하거나 필요한 바에 따라 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함한다.
또한 본 발명의 이러한 측면에서, 본 명세서에서 전체적으로, 2개의 R-기, 예컨대 R1 및 R2가 아시클릭인 경우에는 항상, R1 및 R2가 모노시클릭 또는 비시클릭 잔기를 형성하지 않는 경우, R1 상의 치환기는 R2 상의 치환기로부터 독립적으로 선택된다. 2개의 R-기, 예컨대 R1 및 R2가 시클릭 잔기를 형성하는 경우에는 항상 선택된 임의의 치환기는 시클릭 R1-A-R2 잔기 또는 코어 상의 치환기를 구성한다. 모든 경우에서, 하나 이상의 치환기가 임의의 기로 선택된 경우에는 항상 각각의 치환기는 임의의 다른 치환기에서 독립적으로 선택된다.
또 다른 측면에서, 본 발명은 또한 화학식 I의 화합물을 비롯한 본원에 개시된 벤질아민 화합물의 제조를 위한 방법 또는 공정에 관한 것이다. 다른 측면에서, 본 발명은 또한 화학식 I의 화합물을 비롯한 본원에 개시된 벤질아민 화합물을 포함하는 조성물에 관한 것이다. 조성물이 제약 조성물인 경우, 조성물은 또한 제약상 허용되는 담체 및 본 발명에 따른 하나 이상의 화합물을 포함하고, 추가로 임의로, 제약상 허용되는 보조제; 임의로, 제약상 허용되는 보존제; 임의로, 제약상 허용되는 부형제; 임의로, 제약상 허용되는 희석제; 및 임의로, 제약상 허용되는 용매화물을 포함한다.
본 발명은 또한 인간을 비롯한 포유동물 대상체의 증상 또는 질환을 치료하는 방법에 관한 것이다. 특정 측면에서, 상기 방법은 본원에 개시된 치료 유효량의 하나 이상의 화합물 또는 제약상 허용되는 그의 염을 포함하는 조성물을 대상체에게 투여하는 것을 포함한다. 인간 대상체를 치료하는 데 유용할 뿐만 아니라, 본 발명의 방법 및 조성물은 다양한 포유동물 예를 들어, 애완 동물 예컨대 고양이 또는 개, 영장류, 반추 동물 및 설치류를 치료하는 데 유용하다.
본 발명은 또한 예방 또는 치료 유효량의 본원에 개시된 하나 이상의 화합물 또는 제약상 허용되는 그의 염을 포함하는 조성물을 대상체에게 투여하는 것을 포함하는, 인간 또는 동물 대상체에서의 증상 또는 질환을 치료하거나 예방하는 방법에 관한 것이다. 특정 측면에서, 예를 들어 본 발명은 치료 유효량의 본원에 개시된 하나 이상의 화합물을 투여하는 것을 포함하는, 인간 또는 동물에서의 증상 또는 질환 상태, 예컨대 이상지질혈증, 아테롬성동맥경화증, 말초 혈관 질환, 고중성지방혈증, 고콜레스테롤혈증, 고베타지단백혈증, 저알파지단백혈증, 심장혈관 장애 예컨대 협심증, 허혈, 뇌졸중, 심근경색증 (MI), 재관류 손상, 재협착 및 고혈압, 및 당뇨성 혈관 질환, 예컨대 당뇨성 망막병증 및 내독소혈증의 치료 및/또는 예방 을 위한 방법을 제공한다.
본 발명에 따르면, 신규 벤질아민 화합물 및 이러한 벤질아민 화합물을 포함하는 신규 조성물이 기재되어 있다. 한 측면에서, 본 발명에 따른 화합물은 하기 화학식의 구조를 갖는 벤질아민 화합물을 포함할 수 있다.
<화학식 I>
식 중, 각각의 치환기는 상기 개시된 바와 같이 정의된다.
직전에 나타낸 화학식 I의 이러한 측면에 추가로, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다: Z는 N 또는 CH이거나; 또는 ZR1R2 잔기는 -C≡CR2이다.
상기 나타낸 화학식 I의 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R1 및 R2는 수소; 6개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C6 알킬; 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; COR8; 또는 (CH2)nR5 또는 (CH2)nRdCO2Re (여기서 n은 각각의 경우에서 1 또는 2임)로부터 독립적으로 선택되거나; 또는
R1 및 R2는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N- 또는 >NR10으로부터 독립적으로 선택된 1개 또는 2개의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성하고; 여기서 시클릭 잔기 상의 임의의 치환기는 1) 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; 또는 2) 2개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C2 알킬로부터 선택된다.
상기 나타낸 화학식 I의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 상기 개시된 바와 같이 선택된다:
R3은 1) 수소 또는 시아노; 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬; 3) 치환되거나 또는 비치환된 아릴, 또는 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 4) CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7, C(S)NR6R7, C(S)NC(O)OR8 또는 C(S)SR8로부터 선택되고;
여기서 R3이 알킬, 아릴, 헤테로시클릴 또는 헤테로아릴인 경우, R3은 할라이드, 히드록실, 시아노, 12개 이하의 탄소 원자를 갖는 알콕시, 또는 R11로부터 독립적으로 선택된 3개 이하의 치환기로 임의로 치환되고;
R11은
1) 알킬, 할로알킬, 시클로알킬 또는 알콕시카르보닐 (이들은 12개 이하의 탄소 원자를 가짐);
2) 치환되거나 또는 비치환된 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하며, 여기서 임의의 치환된 헤테로아릴 또는 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 알킬, 또는 히드록실로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨); 또는
3) -CO-Z2-R13, -CO-R12, -CO-Z2-(CH2)r-CO-Z2-R13, -NR15R16, -Z2-CO-(CH2)r-Z2-R13, -Z2-CO-(CH2)r-CO-Z2-R13, -O-(CH2)r-CO-Z2-R13, -O-(CH2)r-R14, -O-R12-(CH2)r-R13, -O-R14-CO-O-R13, -O-(CH2)r-R12, -O-(CH2)r-NR'R", -O-(CH2)r-CO2-(CH2)r-R13, -O-(CH2)r-CONR'R", -O-(CH2)r-SR8, -O-(CH2)r-CO2-R13, -O-(CH2)r-O-(CH2)r-OR13, -O-(CH2)r-CONR'R", -O-(CH2)r-CONH-(CH2)r-OR13, -O-(CH2)r-SO2R8, -O-(CH2)r-R13, -O-(CH2)r-OR13, -O-(CH2)r-O-(CH2)r-OR13, -S-(CH2)r-CONR'R", -SO2-(CH2)r-OR13, -SO2-(CH2)r-CONR'R", -(CH2)r-O-CO-R8, -(CH2)r-R12, -(CH2)r-R13, -(CH2)r-N-(CH2)r-OR13, -(CH2)r-CO-Z2-R13, -(CH2)r-Z2-R13 또는 -알케닐렌-CO2-(CH2)r-R13으로부터 독립적으로 선택되고;
r은 각각의 경우에서 독립적으로 1, 2 또는 3이고;
R12는 각각의 경우에서 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클릴 (여기서 임의의 치환된 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 아실, 알킬 또는 알콕시카르보닐로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨), 또는 -COOH로부터 독립적으로 선택되고;
R13은 각각의 경우에서 1) 수소; 또는 2) 시클로알킬, 아릴, 할로알킬, 헤테로시클릴, 또는 1개 이상의 히드록실로 임의로 치환된 알킬기 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R14는 각각의 경우에서 헤테로시클릴, 시클로알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
Z2는 각각의 경우에서 >NR10 또는 O로부터 독립적으로 선택되고;
R' 및 R"는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
R15 및 R16은 각각의 경우에서 1) 수소; 2) 12개 이하의 탄소 원자를 갖는 알킬; 또는 3) -(CH2)r-O-R13, -(CH2)r-R14, -COR13, -(CH2)r-CO-Z2-R13, -CO2R13, -CO2-(CH2)r-R13, -CO2-(CH2)r-R12, -CO2-(CH2)r-CO-Z2-R13, -CO2-(CH2)r-OR13, -CO-(CH2)r-O-(CH2)r-O-(CH2)r-R13, -CO-(CH2)r-O(CH2)r-OR13, 또는 -CO-NH-(CH2)r-OR13으로부터 독립적으로 선택되거나; 또는
R15 및 R16은 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 추가의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성하고; 여기서 임의의 치환된 시클릭 잔기는 1) 히드록실; 2) 알킬 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴은 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) COOR13, -Z2-(CH2)r-R13, -COR13, -CO2-(CH2)r-R13, -CO(CH2)r-O-R13, -(CH2)r-CO2-R13, -SO2R8, -SO2NR'R" 또는 -NR'R"로부터 독립적으로 선택된 3개 이하의 치환기로 치환되고;
여기서 -(CH2)r- 연결 잔기는 임의의 경우에서 히드록실, 아미노, 또는 3개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택된 1개 이상의 기로 임의로 치환된다.
상기 나타낸 화학식 I의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 2 또는 3이다.
본 발명의 다른 측면에서, 본 발명에 따른 화합물은 하기 화학식 Ia의 구조를 갖는 화학식 I에 따른 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함할 수 있다.
식 중,
A는
로부터 선택된 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭잔기로부터 선택되고;
고리계 A에 대한 치환기를 비롯한 다른 모든 치환기 및 기는 화학식 I에서 상기 제공된 정의에 따라 선택된다.
직전에 나타낸 화학식 Ia의 이러한 측면에 추가로, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 상기 화학식에 대해 상기 개시된 바와 같이 선택된다: Z는 N 또는 CH이거나; 또는 ZR1R2 잔기는 -C≡CR2이다.
상기 나타낸 화학식 Ia의 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R1 및 R2는 1) 수소; 2) 6개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C6 알킬; 3) 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; 4) COR8; 또는 5) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐) 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되거나; 또는
R1 및 R2는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N- 또는 >NR10으로부터 독립적으로 선택된 1개 또는 2개의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성하고; 여기서 시클릭 잔기 상의 임의의 치환기는 1) 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; 또는 2) 2개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C2 알킬로부터 선택된다.
상기 나타낸 화학식 Ia의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R3은 1) 수소 또는 시아노; 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬; 3) 치환되거나 또는 비치환된 아릴, 또는 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 4) CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7, C(S)NR6R7, C(S)NC(O)OR8, 또는 C(S)SR8로부터 선택되고;
여기서, R3이 헤테로시클릴 또는 헤테로아릴인 경우, R3은 할라이드, 히드록 실, 시아노, 12개 이하의 탄소 원자를 갖는 알콕시 또는 R11로부터 독립적으로 선택된 3개 이하의 치환기로 임의로 치환되고;
R11은
1) 알킬, 할로알킬, 시클로알킬 또는 알콕시카르보닐 (이들은 12개 이하의 탄소 원자를 가짐);
2) 치환되거나 또는 비치환된 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하며, 여기서 임의의 치환된 헤테로아릴 또는 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 알킬, 또는 히드록실로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨); 또는
3) -CO-Z2-R13, -CO-R12, -CO-Z2-(CH2)r-CO-Z2-R13, -NR15R16, -Z2-CO-(CH2)r-Z2-R13, -Z2-CO-(CH2)r-CO-Z2-R13, -O-(CH2)r-CO-Z2-R13, -O-(CH2)r-R14, -O-R12-(CH2)r-R13, -O-R14-CO-O-R13, -O-(CH2)r-R12, -O-(CH2)r-NR'R", -O-(CH2)r-CO2-(CH2)r-R13, -O-(CH2)r-CONR'R", -O-(CH2)r-SR8, -O-(CH2)r-CO2-R13, -O-(CH2)r-O-(CH2)r-OR13, -O-(CH2)r-CONR'R", -O-(CH2)r-CONH-(CH2)r-OR13, -O-(CH2)r-SO2R8, -O-(CH2)r-R13, -O- (CH2)r-OR13, -O-(CH2)r-O-(CH2)r-OR13, -S-(CH2)r-CONR'R", -SO2-(CH2)r-OR13, -SO2- (CH2)r-CONR'R", -(CH2)r-O-CO-R8, -(CH2)r-R12, -(CH2)r-R13, -(CH2)r-N-(CH2)r-OR13, -(CH2)r-CO-Z2-R13, -(CH2)r-Z2-R13 또는 -알케닐렌-CO2-(CH2)r-R13으로부터 독립적으로 선택되고;
r은 각각의 경우에서 독립적으로 1, 2 또는 3이고;
R12는 각각의 경우에서 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클릴 (여기서 임의의 치환된 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 아실, 알킬, 또는 알콕시카르보닐로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨), 또는 -COOH로부터 독립적으로 선택되고;
R13은 각각의 경우에서 1) 수소; 또는 2) 시클로알킬, 아릴, 할로알킬, 헤테로시클릴 또는 1개 이상의 히드록실로 임의로 치환된 알킬기 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R14는 각각의 경우에서 헤테로시클릴, 시클로알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
Z2는 각각의 경우에서 >NR10 또는 O로부터 독립적으로 선택되고;
R' 및 R"는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
R15 및 R16은 각각의 경우에서 1) 수소; 2) 12개 이하의 탄소 원자를 갖는 알킬; 또는 3) -(CH2)r-O-R13, -(CH2)r-R14, -COR13, -(CH2)r-CO-Z2-R13, -CO2R13, -CO2-(CH2)r-R13, -CO2-(CH2)r-R12, -CO2-(CH2)r-CO-Z2-R13, -CO2-(CH2)r-OR13, -CO-(CH2)r-O-(CH2)r-O-(CH2)r-R13, -CO-(CH2)r-O(CH2)r-OR13 또는 -CO-NH-(CH2)r-OR13으로부터 독립적으로 선택되거나; 또는
R15 및 R16은 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 추가의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성하고; 여기서 임의의 치환된 시클릭 잔기는 1) 히드록실; 2) 알킬 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴은 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) COOR13, -Z2-(CH2)r-R13, -COR13, -CO2-(CH2)r-R13, -CO(CH2)r-O-R13, -(CH2)r-CO2-R13, -SO2R8, -SO2NR'R" 또는 -NR'R"로부터 독립적으로 선택된 3개 이하의 치환기로 치환되고;
여기서, -(CH2)r- 연결 잔기는 임의의 경우에서 히드록실, 아미노 또는 3개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택된 1개 이상의 기로 임의로 치환된다.
상기 나타낸 화학식 Ia의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 2 또는 3이다.
또 다른 측면에서, 본 발명에 따른 화합물은 하기 화학식 Ia'의 구조를 갖는 화학식 I에 따른 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함할 수 있다.
식 중,
A는
로부터 선택된 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기로부터 선택되고;
여기서 Ra는 각각의 경우에서 1) 할로겐; 히드록실 또는 시아노; 2) 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적 으로 선택되고;
p는 A의 구조가 허용하거나 필요한 바에 따라 0 내지 3의 정수이다.
본 발명의 이러한 측면에서, 비시클릭 잔기의 임의의 부분 상의 치환기로서 대표적인 Ra기는, Ra기가 비시클릭 잔기의 1개 고리 또는 2개 고리에 연결된 결합위치이성질체를 비롯한 가능한 모든 결합위치이성질체를 나타내고자 한다.
직전에 나타낸 화학식 Ia'의 이러한 측면에 추가로, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
Z는 N 또는 CH이거나; 또는 ZR1R2 잔기는 -C=CR2이다.
상기 나타낸 화학식 Ia'의 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R1 및 R2는 1) 수소; 2) 6개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C6 알킬; 3) 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; 4) COR8; 또는 5) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테 로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되거나; 또는
R1 및 R2는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N- 또는 >NR10으로부터 독립적으로 선택된 1개 또는 2개의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성하고; 여기서 시클릭 잔기 상의 임의의 치환기는 1) 6개 이하의 탄소 원자를 갖는 시클로알킬인 C3 내지 C6 시클로알킬; 또는 2) 2개 이하의 탄소 원자를 갖는 알킬인 C1 내지 C2 알킬로부터 선택된다.
상기 나타낸 화학식 Ia'의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R3은 1) 수소 또는 시아노; 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬; 3) 치환되거나 또는 비치환된 아릴, 또는 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 4) CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7, C(S)NR6R7, C(S)NC(O)OR8, 또는 C(S)SR8로부터 선택되고;
여기서 R3이 알킬, 아릴, 헤테로시클릴 또는 헤테로아릴인 경우, R3은 할라이드, 히드록실, 시아노, 12개 이하의 탄소 원자를 갖는 알콕시, 또는 R11로부터 독립적으로 선택된 3개 이하의 치환기로 임의로 치환되고;
R11은
1) 알킬, 할로알킬, 시클로알킬, 또는 알콕시카르보닐 (이들은 12개 이하의 탄소 원자를 가짐);
2) 치환되거나 또는 비치환된 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하며, 여기서 임의의 치환된 헤테로아릴 또는 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 알킬, 또는 히드록실로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨); 또는
3) -CO-Z2-R13, -CO-R12, -CO-Z2-(CH2)r-CO-Z2-R13, -NR15R16, -Z2-CO-(CH2)r-Z2-R13, -Z2-CO-(CH2)r-CO-Z2-R13, -O-(CH2)r-CO-Z2-R13, -O-(CH2)r-R14, -O-R12-(CH2)r-R13, -O-R14-CO-O-R13, -O-(CH2)r-R12, -O-(CH2)r-NR'R", -O-(CH2)r-CO2-(CH2)r-R13, -O-(CH2)r-CONR'R", -O-(CH2)r-SR8, -O-(CH2)r-CO2-R13, -O-(CH2)r-O-(CH2)r-OR13, -O-(CH2)r-CONR'R", -O-(CH2)r-CONH-(CH2)r-OR13, -O-(CH2)r-SO2R8, -O-(CH2)r-R13, -O-(CH2)r-OR13, -O-(CH2)r-O-(CH2)r-OR13, -S-(CH2)r-CONR'R", -SO2-(CH2)r-OR13, -SO2-(CH2)r-CONR'R", -(CH2)r-O-CO-R8, -(CH2)r-R12, -(CH2)r-R13, -(CH2)r-N-(CH2)r-OR13, -(CH2)r-CO-Z2-R13, -(CH2)r-Z2-R13 또는 -알케닐렌-CO2-(CH2)r-R13으로부터 독립적으로 선택되고;
r은 각각의 경우에서 독립적으로 1, 2 또는 3이고;
R12는 각각의 경우에서 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클릴 (여기서 임의의 치환된 헤테로시클릴은 12개 이하의 탄소 원자를 갖는 아실, 알킬 또는 알콕시카르보닐로부터 독립적으로 선택된 3개 이하의 치환기로 치환됨), 또는 -COOH로부터 독립적으로 선택되고;
R13은 각각의 경우에서 1) 수소; 또는 2) 시클로알킬, 아릴, 할로알킬, 헤테로시클릴, 또는 1개 이상의 히드록실로 임의로 치환된 알킬기 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R14는 각각의 경우에서 헤테로시클릴, 시클로알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
Z2는 각각의 경우에서 >NR10 또는 O로부터 독립적으로 선택되고;
R' 및 R"는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
R15 및 R16은 각각의 경우에서 1) 수소; 2) 12개 이하의 탄소 원자를 갖는 알킬; 또는 3) -(CH2)r-O-R13, -(CH2)r-R14, -COR13, -(CH2)r-CO-Z2-R13, -CO2R13, -CO2-(CH2)r-R13, -CO2-(CH2)r-R12, -CO2-(CH2)r-CO-Z2-R13, -CO2-(CH2)r-OR13, -CO-(CH2)r-O- (CH2)r-O-(CH2)r-R13, -CO-(CH2)r-O(CH2)r-OR13 또는 -CO-NH-(CH2)r-OR13으로부터 독립적으로 선택되거나; 또는
R15 및 R16은 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 추가의 헤테로원자 또는 헤테로기를 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성하고; 여기서 임의의 치환된 시클릭 잔기는 1) 히드록실; 2) 알킬 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴은 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) COOR13, -Z2-(CH2)r-R13, -COR13, -CO2-(CH2)r-R13, -CO(CH2)r-O-R13, -(CH2)r-CO2-R13, -SO2R8, -SO2NR'R" 또는 -NR'R"로부터 독립적으로 선택된 3개 이하의 치환기로 치환되고;
여기서 -(CH2)r- 연결 잔기는 임의의 경우에서 히드록실, 아미노, 또는 3개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택된 1개 이상의 기로 임의로 치환된다.
상기 나타낸 화학식 Ia'의 또 다른 측면에서, 화학식의 하기 치환기는 본원에 제시된 바와 같이 선택될 수 있으나, 특정되지 않은 치환기는 이 화학식에 대해 상기 개시된 바와 같이 선택된다:
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 2 또는 3이다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 II의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 그의 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴, 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬; 3) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6, C(S)SR8, 또는 C(S)NC(O)OR8로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립 적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴, 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 1) 할로겐, 히드록실, 또는 시아노; 2) 알킬, 할로알킬, 알콕시, 할로알콕시 또는 아릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적으로 선택되고;
p는 0 내지 3의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이속사졸릴로부터 선택된 치환되거나 또는 비치환된 기로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra는 메틸, 에틸, 또는 메톡시로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 III의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공 한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴, 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 1) 수소; 2) 알킬, 할로알킬, 아릴 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적으로 선택되고;
p는 0 내지 2의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치 환기에 따라 선택된다.
또 다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIIa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra는 1) 수소; 또는 2) 알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가짐)로부터 선택되고;
Ra2는 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 선택되고;
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIIb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra는 1) 수소, 또는 2) 알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가짐)로부터 선택되고;
Ra2는 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 선택되고;
R3은 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이속사졸릴로부터 선택된 치환되거나 또는 비치환된 기로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치 환기에 따라 선택된다.
또 다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IIIc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IV의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐) 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 3) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원 자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
p는 0 내지 3의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IVa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면에서, 본원은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IVb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상 이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이소옥사졸릴로부터 선택된 치환되거나 또는 비치환된 기로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IVc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 V의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 수소 또는 12개 이하의 탄소 원자를 갖는 알킬로부터 독립적으로 선택되고;
p는 0 내지 3의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 Va의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 Vb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 치환되거나 또는 비치환된 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이속사졸릴로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 Vc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VI의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 1) 할로겐, 히드록실 또는 시아노; 또는 2) 알킬, 할로알킬, 알콕시, 할로알콕시, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적으로 선택되고;
p는 0 내지 3의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호 변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 치환되거나 또는 비치환된 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴, 또는 이속사졸릴로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VII의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 1) 할로겐, 히드록실 또는 시아노; 또는 2) 알킬, 할로알킬, 알콕시, 할로알콕시, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적으로 선택되고;
p는 0 내지 3의 정수이고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호 변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 치환되거나 또는 비치환된 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이속사졸릴로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIII의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
R1 및 R2는 1) 치환되거나 또는 비치환된 알킬, 또는 치환되거나 또는 비치환된 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;
R3은 1) 수소 또는 시아노; 2) 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함); 또는 4) CO2R6으로부터 선택되고;
R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;
m은 0 내지 3의 정수이고;
R5는 각각의 경우에서 1) 치환되거나 또는 비치환된 아릴, 시클로알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬로부터 독립적으로 선택되고;
R6은 1) 수소; 또는 2) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 아르알킬, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 선택되고;
R8은 각각의 경우에서 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고;
R10은 각각의 경우에서 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
Ra는 각각의 경우에서 1) 할로겐, 히드록실 또는 시아노; 또는 2) 알킬, 할로알킬, 알콕시, 할로알콕시, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6으로부터 독립적으로 선택되고;
R3은 1) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치 환기에 따라 선택된다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIIa의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Rb는 1) 수소; 또는 2) 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIIb의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공 한다.
식 중,
R3은 치환되거나 또는 비치환된 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이속사졸릴로부터 선택되고; 여기서 R3 상의 임의의 치환기는 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
다른 측면에서, 본 발명은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 VIIIc의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra는 수소 또는 2개 이하의 탄소 원자를 갖는 알킬이고;
R3은 1) CO2R6 또는 2) 12개 이하의 탄소 원자를 가지며, >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로아릴로부터 선택되고;
특정되지 않은 임의의 기 또는 치환기는 화학식 I에 대해 본원에 개시된 치환기에 따라 선택된다.
본 발명의 추가의 측면에서, 본 발명은 수가지의 벤질아민 화합물 부류를 제공하며, 이들 각각은 본원에 개시된 화학식 I의 하위 부류이다. 이들 부류는 하기 도시된 화학식 (II-1), (IIa-1), (IIb-1), (III-1), (IIIa-1), (IIIb-1), (IV-1), (IVa-1), (IVb-1), (V-1), (Va-1), (Vb-1), (VI-1), (VIa-1), (VIb-1), (VII-1), (VIIa-1), (VIIb-1), (VIII-1), (VIIIa-1), 및 (VIIIb-1)로 나타나며, 및 각각은, 비제한적으로 Z, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, Ra, Rb, Rx 등을 비롯한 다 양한 치환기에 의해 특성화된다. 이러한 측면에서, 각각의 예에서 이들 치환기에 대한 가능한 선택은 하기 목록에 제시되어 있으며, 이러한 가능한 선택 각각의 정의, 예를 들어 R1에 대한 가능한 선택인 R1A, R1B, R1C 및 R1D의 정의는 하기에 추가로 제공된다.
화학식 (II-1), (IIa-1), (IIb-1), (III-1), (IIIa-1), (IIIb-1), (IV-1), (IVa-1), (IVb-1), (V-1), (Va-1), (Vb-1), (VI-1), (VIa-1), (VIb-1), (VII-1), (VIIa-1), (VIIb-1), (VIII-1), (VIIIa-1), 및 (VIIIb-1)로 나타낸 부류는 또한 하기 표에 제공된다. 이들 표는 각각의 부류를 표에 따른 치환기 선택에 의해 정의된 하위 부류 화학식의 목록으로 분류한다. 예를 들어, 표 A의 화학식 (A-01)에서 (A-384)는 이 경우, 표 (II-1), (III-1), (IIIb-1), (IV-1), (V-1), (VI-1), (VII-1) 및 (VIII-1)과 관련된 화합물에 적용가능하고, 각각의 화학식 (II-1), (III-1), (IIIb-1), (IV-1), (V-1), (VI-1), (VII-1) 및 (VIII-1)에 대한 384개의 상이한 하위 부류를 제공한다. 본 발명은 각각의 이들 화합물, 각각의 이들 화합물의 제조 방법, 및 각각의 화합물의 사용 방법을 제공한다.
따라서, 이러한 측면에서, 치환기 선택은 다음과 같다. 임의의 기 또는 치환기가 임의의 이들 화학식에서 특정되지 않는 한, 화학식 I에 대해 제공된 기 또는 치환기의 정의가 적용가능하다.
Z는 ZA, ZB 또는 ZC로부터 선택될 수 있다.
R1은 R1A, R1B, R1C 또는 R1D로부터 선택될 수 있다.
R2는 R2A, R2B, R2C 또는 R2D로부터 선택될 수 있다.
R3은 R3A, R3B, R3C 또는 R3D로부터 선택될 수 있다.
R4는 R4A, R4B 또는 R4C로부터 선택될 수 있다.
R5는 R5A, R5B 또는 R5C로부터 선택될 수 있다.
R6은 R6A, R6B, R6C, R6D 또는 R6E로부터 선택될 수 있다.
R7은 R7A, R7B, R7C, R7D 또는 R7E로부터 선택될 수 있다.
R8은 R8A, R8B 또는 R8C로부터 선택될 수 있다.
R9는 R9A, R9B, R9C 또는 R9D로부터 선택될 수 있다.
R10은 R10A, R10B 또는 R10C로부터 선택될 수 있다.
Ra는 Ra1 또는 Ra2로부터 선택될 수 있다.
Rb는 Rb1 또는 Rb2로부터 선택될 수 있다.
Rx는 Rx1, Rx2, Rx3 또는 Rx4로부터 선택될 수 있다.
각각의 이들 치환기 선택을 위해, 하기 정의를 제공한다.
ZA는 N 또는 CH이다.
ZB는 N이다.
ZC는 CH이다.
R1A는 a) 수소; 또는 b) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로시클릴, 헤테로아릴, 모노알킬아미노, 디알킬아미노, 알콕시알킬, 할로알콕시알킬 또는 아미노알킬 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R1B는 치환되거나 또는 비치환된 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지며, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R1C는 a) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 b) (CHRx)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rx는 각각의 경우에서 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택되고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시 클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)이다.
R1D 및 R2D는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 Z 이외에 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성한다.
R2A는 a) 수소; 또는 b) 치환되거나 또는 비치환된 알킬, 시클로알킬, 할로알킬, 아릴, 헤테로시클릴, 헤테로아릴, 모노알킬아미노, 디알킬아미노, 알콕시알킬, 할로알콕시알킬 또는 아미노알킬 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R2B는 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클릴 또는 헤테로아릴이다.
R2C는 a) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 b) (CHRx)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rx는 각각의 경우에서 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택되고; Rd는 각각의 경우에서 알킬, 시클로알킬, 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택되고; Re는 각각의 경우에서 알킬 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐), 또는 수소로부터 독립적으로 선택됨)이다.
R2D 및 R1D는 함께 12개 이하의 탄소 원자를 포함하고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 Z 이외에 임의로 포함하는 치환되거나 또는 비치환된 모노시클릭 또는 비시클릭 잔기를 형성한다.
R3A는 a) 수소 또는 시아노; 또는 2) 12개 이하의 탄소 원자를 갖는 치환되거나 또는 비치환된 알킬이다.
R3B는 치환되거나 또는 비치환된 아릴, 또는 치환되거나 또는 비치환된 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함함)이다.
R3C는 CO2R6, COR8, SO2R8, SO2NR6R7, CONR6R7, C(S)NR6R7, C(S)NC(O)OR8 또는 C(S)SR8로부터 선택된 치환되거나 또는 비치환된 기이다.
R3D는 4,5-디히드로-옥사졸릴, 테트라졸릴, 이속사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 치환되거나 또는 비치환된 기이고; 여기서 R3D 상의 임의의 치환기는 a) 알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 b) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된다.
R4A는 a) 할로겐, 시아노 또는 히드록시; 또는 b) 알킬, 시클로알킬, 시클로알콕시, 알콕시, 할로알킬 또는 할로알콕시 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R4B는 치환되거나 또는 비치환된 아릴, 아르알킬, 아릴옥시, 헤테로아릴 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가지며, 여기서 임의의 헤테로아릴 또는 헤테로아릴옥시는 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R4C는 a) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7로부터 선택된 치환되거나 또는 비치환된 기; 또는 b) (CH2)qNR6R7 (여기서, q는 0 내지 5의 정수임)이다.
R5A는 치환되거나 또는 비치환된 알콕시, 할로알콕시 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R5B는 a) 치환되거나 또는 비치환된 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 b) 3개 내지 7개의 고리 탄소 원자, 및 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 치환되거나 또는 비치환된 헤테로시클로알킬이다.
R5C는 히드록실, NR6R7, CO2R6, COR8 또는 SO2R8이다.
R6A는 수소이다.
R6B는 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가 짐)이다.
R6C는 치환되거나 또는 비치환된 아릴, 또는 치환되거나 또는 비치환된 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R6D는 치환되거나 또는 비치환된 헤테로시클릴, 또는 치환되거나 또는 비치환된 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R6E 및 R7E는 함께 3개 내지 7개의 고리 탄소 원자를 가지고, >O, >N-, >S, 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자를 R6E 및 R7E가 결합된 질소 원자 이외에 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성한다.
R7A는 수소이다.
R7B는 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R7C는 치환되거나 또는 비치환된 아릴, 또는 치환되거나 또는 비치환된 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R7D는 치환되거나 또는 비치환된 헤테로시클릴, 또는 치환되거나 또는 비치환된 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R7E 및 R6E는 함께 3개 내지 7개의 고리 탄소 원자를 가지며, >O, >N-, >S, 또는 >NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자를 R6E 및 R7E가 결합된 질소 원자 이외에 임의로 포함하는 치환되거나 또는 비치환된 시클릭 잔기를 형성한다.
R8A는 a) 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 b) 치환되거나 또는 비치환된 아릴, 헤테로시클릴 또는 헤테로아릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R8B는 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R8C는 치환되거나 또는 비치환된 아릴, 헤테로시클릴 또는 헤테로아릴 (이들 은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)이다.
R9A는 12개 이하의 탄소 원자를 갖는 알킬이다.
R9B는 8개 이하의 탄소 원자를 갖는 알킬이다.
R9C는 6개 이하의 탄소 원자를 갖는 알킬이다.
R9D는 4개 이하의 탄소 원자를 갖는 알킬이다.
R10A는 1) 수소; 또는 2) 알킬, 시클로알킬, 할로알킬, 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R10B는 알킬, 시클로알킬 또는 할로알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
R10C는 아릴 또는 아르알킬 (이들은 12개 이하의 탄소 원자를 가짐)이다.
Ra1은 할로겐이다.
Ra2는 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐)이다.
Rb1은 12개 이하의 탄소 원자를 갖는 알킬이다.
Rb2는 6개 이하의 탄소 원자를 갖는 알킬이다.
Rx1은 독립적으로: 1) 알킬 또는 알콕시 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) 수소이다.
Rx2는 12개 이하의 탄소 원자를 갖는 알킬이다.
Rx3은 12개 이하의 탄소 원자를 갖는 알콕시이다.
Rx4는 수소이다.
화학식 II-1, IIa-1, IIb-1, III-1, IIIa-1, IIIb-1, IV-1, IVa-1, IVb-1, V-1, Va-1, Vb-1, VI-1, VIa-1, VIb-1, VII-1, VIIa-1, VIIb-1, VIII-1, VIIIa-1 및 VIIIb-1에 의해 나타난 부류의 한 측면에서, 치환되거나 또는 임의로 치환된 기 상의 임의의 치환기는 화학식 I에 대해 본원에 특정된 바와 같이 선택될 수 있다. 화학식 II-1, IIa-1, IIb-1, III-1, IIIa-1, IIIb-1, IV-1, IVa-1, IVb-1, V-1, Va-1, Vb-1, VI-1, VIa-1, VIb-1, VII-1, VIIa-1, VIIb-1, VIII-1, VIIIa-1 및 VIIIb-1에 의해 나타난 부류의 다른 측면에서, 치환되거나 또는 임의로 치환된 기 상의 임의의 치환기는 하기와 같이 선택될 수 있다:
고리 A는 1) 할로겐, 시아노 또는 히드록실; 2) 알킬, 알케닐, 알키닐, 할로알킬, 시클로알킬, 알콕시, 시클로알콕시, 할로알콕시, 아릴, 아릴옥시, 아르알킬, 헤테로아릴 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가짐); 또는 3) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 4) (CH2)qNR6R7 (여기서, q는 0 내지 5의 정수임); 또는 5) (CH2)qCO2(CH2)q (여기서, q는 0 내지 3의 정수임)로부터 독립적으로 선택된 1개, 2개 또는 3개의 치환기로 임의로 치환되고;
R1 및 R2가 모노시클릭 또는 비시클릭 잔기를 형성하지 않는 경우, R1 및 R2는 1) 알킬, 시클로알킬, 할로알킬, 알콕시, 아릴, 헤테로아릴 또는 헤테로시클릴 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로시클릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 2) 할로겐, 시아노 또는 히드록실로부터 독립적으로 선택된 1개 또는 2개의 치환기로 임의로 및 독립적으로 치환되고;
R1 및 R2가 함께 모노시클릭 또는 비시클릭 잔기를 형성하는 경우, 시클릭 잔기는 1) 할로겐, 시아노 또는 히드록실; 2) 알킬, 알케닐, 알키닐, 할로알킬, 시클로알킬, 알콕시, 시클로알킬알킬, 알콕시알킬, 시클로알콕시, 할로알콕시, 아릴, 아릴옥시, 아르알킬, 헤테로아릴 또는 헤테로아릴옥시 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로아릴 또는 헤테로아릴옥시는 >O, >N-, >S 또는 >NR10으로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함); 또는 3) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 4) (CH2)qCO2(CH2)q (여 기서, q는 0 내지 3의 정수임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
R3은 1) 알킬, 할로알킬, 아릴 또는 시클로알킬 (이들은 12개 이하의 탄소 원자를 가짐); 또는 2) CO2R9 (여기서, R9는 12개 이하의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 치환되고;
R4 및 R5는 1) 할라이드, 히드록시, 시아노, 아미노 또는 옥소; 또는 2) 알킬, 알케닐, 카르복시, 시클로알킬, 아릴, 헤테로시클릴, 헤테로아릴, 알콕시, 알킬티오, 알킬옥시카르보닐, 모노알킬아미노 또는 디알킬아미노 (이들은 12개 이하의 탄소 원자를 가지고, 여기서 임의의 헤테로시클릴 또는 헤테로아릴은 >O, >N-, >S, >NR10, >SO2 또는 >CO로부터 독립적으로 선택된 1개 이상의 헤테로원자 또는 헤테로기를 포함함)로부터 독립적으로 선택된 1개 이상의 치환기로 임의로 및 독립적으로 치환되고;
R6, R7 및 R8은 알킬, 할로알킬 또는 아릴 (이들은 12개 이하의 탄소 원자를 가짐)로부터 독립적으로 선택된 1개 또는 2개의 치환기로 임의로 및 독립적으로 치환되고;
m 및 p는 0 내지, R4 및 Ra가 각각 결합된 잔기의 구조에서 허용된 최대 수의 정수이다. 한 측면에서, m은 0 내지 3의 정수일 수 있다. 다른 측면에서, p는 0 내지 3의 정수일 수 있다.
이러한 선택 및 정의에서, 다르게 제시하지 않으면, 치환기 상의 탄소 원자 수는 기본 화학 잔기 상의 탄소 원자를 나타내고, 임의의 치환기에서 탄소 원자를 포함하지 않는다. 다르게 제시하지 않으면, 치환기 크기는 치환기의 정의에 열거되어 있다.
하기 화학식에서, 특정 선택의 치환기 중 하나 이상이 제시된 분자 내에 존재하는 경우, 예를 들어 R4, Ra 또는 Rb 중 하나 이상이 주어진 분자에 존재하는 경우, 표에서 선택은 그러한 치환기의 존재 중 하나를 나타내며, 여기서 그러한 치환기의 임의의 추가적 존재는 본원에 제공된 정의에 따라 독립적으로 선택된다. 예를 들어, 1개 이상의 Ra가 화학식 II-1에 존재하는 경우, 하기 표에서 화학식 A-O1에 따라, Ra가 1개 이상 존재하면 Ra1이고, 임의의 다른 Ra가 존재하면 Ra1 및 Ra2로부터 독립적으로 선택된다.
따라서, 본 발명의 다양한 측면에 따라, 본원은 하기 화학식의 구조를 갖는 화학식 I에 따른 벤질아민 화합물 또는 이의 임의의 조합; 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2, R3, R4 및 Ra는 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 II-1, III-1, IIIb-1, IV-1, V-1, VI-1, VII-1 및 VIII-1에 적용가능한 화학식 A-01에서 A-384를 제공한다.
본 발명의 추가의 측면에 따라, 본원은 하기 화학식의 구조를 갖는 화학식 I에 따른 벤질아민 화합물 또는 이의 임의의 조합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2, Ra 및 Rb는 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 IIa-1, VIa-1, VIIa-1 및 VIIIa-1에 적용가능한 화학식 B-01에서 B-64를 제공한다.
본 발명의 다양한 측면에 따라, 하기 화학식의 구조를 갖는 본원 화학식 I에 따른 벤질아민 화합물 또는 이의 임의의 조합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2, R3 및 Ra는 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 IIb-1, VIb-1, VIIb-1 및 VIIIb-1에 적용가능한 화학식 C-01에서 C-128을 제공한다.
본 발명의 추가의 측면에 따라, 본원 하기 화학식 IIIa-1의 구조를 갖는 화학식 I에 따른 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2, R4, Ra 및 Rb는 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 IIIa-1에 적용가능한 화학식 D-01에서 D-192를 제공한다.
또한 본 발명의 추가의 측면에 따라, 본원은 하기 화학식의 구조를 갖는 화합물인 화학식 I에 따른 벤질아민 화합물 또는 이의 임의의 조합; 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2 및 Rb는 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 IVa-1 및 Va-1에 적용가능한 화학식 E-01에서 E-32를 제공한다.
또한 본 발명의 추가의 측면에 따라, 하기 화학식의 구조를 갖는 본원 화학식 I에 따른 벤질아민 화합물 또는 이의 임의의 조합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 제공한다.
식 중, R1, R2 및 R3은 하기 표에 따라 선택될 수 있으며, 상기 도시된 화합물 IVb-1 및 Vb-1에 적용가능한 화학식 F-01에서 F-32를 제공한다.
본 발명의 추가의 측면에서, 본원은 이들 표에 제공된 화합물의 임의의 조합물을 비롯한 하기 표의 임의의 화합물로부터 선택된 벤질아민 화합물을 제공한다. 이들 특정 화합물의 개시에 의해, 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 임의의 염, 임의의 전구약물, 및 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물을 비롯한 임의의 입체이성질체, 또는 개시된 화합물의 임의의 조합물을 포함하는 것으로 한다. 각각의 하기 표에서, 실시예 번호는 특정 화합물의 제조를 위해 제공한다.
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 IX의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra1은 Me 또는 Et이고;
Ra3은 H, Me 또는 Et이고;
본 발명의 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 X의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변 이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra1은 Me 또는 Et이고;
Ra3은 H, Me 또는 Et이고;
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XI의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra는 H, Me 또는 Et이고;
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XII의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되 지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra6은 H, Me 또는 Et이고;
Ra8은 H, Me 또는 Et이고;
Rb는 Me 또는 Et이다.
본 발명의 추가의 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XIII의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한 다.
식 중,
Ra6은 H, Me 또는 Et이고;
Ra8은 H, Me 또는 Et이고;
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XIV의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용 되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
Ra4는 H, Me 또는 Et이고;
Ra6은 H, Me 또는 Et이고;
본 발명의 또 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XV의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
본 발명의 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 하기 화학식 XVI의 구조를 갖는 벤질아민 화합물, 또는 제약상 허용되거나 또는 제약상 허용되지 않는 염을 비롯한 염, 전구약물, 부분입체이성질체 혼합물, 거울상이성질체, 호변이성질체, 라세미 혼합물, 또는 이의 임의의 조합물을 포함하는 조성물을 제공한다.
식 중,
본 발명의 다른 측면은 화학식 I에 따른 벤질아민 화합물, 및 벤질아민 화합물을 포함하는 조성물을 제공하며, 여기서 화합물은
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-(2,2-디메틸-프로필)-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-이소프로필-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로펜틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로펜틸-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(5-메틸-이속사졸-3-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(5-메틸-이속사졸-3-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피라졸로[3,4-b]-피리딘-6-일)-비스-시클로프로필메틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피라졸로[3,4-b]-피리딘-6-일)-시클로부틸메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(4-트리플루오로메틸-옥사졸-2-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]-피리딘-6-일)-시클로펜틸메틸-에틸-아민;
(2-{[(3,5-비스-트리플루오로메틸-벤질)-(6-시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]-피리딘-5-일메틸]-아미노}-옥사졸-4-카르복실산 에틸 에스테르;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로펜틸메틸-에틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-디이소부틸-아민;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-이소부틸-아민;
시클로프로판카르복실산 (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-아미드;
시클로펜탄카르복실산 (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로 프로필메틸-아미드;
시클로헥산카르복실산 (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-아미드;
N-(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-N-시클로프로필메틸-아세트아미드;
N-(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-3-클로로-N-시클로프로필메틸-프로피온아미드;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-(테트라히드로-푸란-2일메틸)-아민;
(3,5-비스-트리플루오로메틸-벤질)-[6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-카르밤산 메틸 에스테르;
시클로펜틸메틸-에틸-(5-{[(3,4,5-트리플루오로-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민;
시클로펜틸메틸-에틸-(5-{[(3,5-디플루오로-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민;
시클로펜틸메틸-(1,3-디메틸-5-{[(2-메틸-2H-테트라졸-5-일)-(3,5-디클로로 벤질)-아미노]-메틸}-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-아민;
시클로펜틸메틸-에틸-(5-{[(3-플루오로-5-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민;
비스-시클로프로필메틸-(5-{[(3,5-디클로로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민;
(3,5-비스-트리플루오로메틸-벤질)-[6-(시클로펜틸메틸-에틸-아미노)-3-메틸-이속사졸로[5,4-b]피리딘-5-일메틸}-카르밤산 메틸 에스테르;
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-메틸-이속사졸로[5,4-b]피리딘-6-일)-시클로펜틸메틸-에틸-아민;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(부틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로헥실메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-프로필-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로프로필메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로부틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-6-메틸-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르;
[2-(비스-시클로프로필메틸-아미노)-8-메틸-퀴놀린-3-일메틸]-(3,5-비스-트리플루오로메틸-벤질)-카르밤산 메틸 에스테르;
(3,5-비스-트리플루오로메틸-벤질)[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-디티오카르밤산 메틸 에스테르;
3-에톡시카르보닐-1-(3,5-비스-트리플루오로메틸-벤질)-1-[2-(시클로펜틸 메틸-에틸-아미노)-퀴놀린-3-일 메틸]-티오우레아;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-퀴놀린-2-일)-부틸-에틸-아민;
(3-{[3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-퀴놀린-2-일)-시클로프로필메틸-에틸-아민;
(3-{[3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-퀴놀린-2-일)-시클로부틸메틸-에틸-아민;
(3-{[3,5-비스트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-8-퀴놀린-2-일)-비스-시클로프로필메틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(5-메틸-[1,3,4]옥사디아졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
1-(3,5-비스트리플루오로메틸-벤질)-1-[(2-시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-우레아;
1-(3,5-비스-트리플루오로메틸-벤질)-1-[(2-시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일 메틸)]-O-에틸 이소우레아;
(3-{[3,5-비스-트리플루오로메틸-벤질)-(4-메틸-티아졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[3,5-비스-트리플루오로메틸-벤질-(5-메틸-이속사졸-3-일)-아미노]-메틸}-퀴놀린-2-일)-시클로부틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-피리미딘-2-일-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(4-메틸-옥사졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(4,5-디히드로-옥사졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-피리딘-2-일-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일메틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(1-메틸-1H-테트라졸-5-일메틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-피리딘-2-일)-부틸-에틸 아민;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-4,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-6,7-디히드로-5H-[1]피리딘-3-일메틸]-카르밤산 메틸 에스테르;
(3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-6,7-디히드로-5H-[1]피리딘-2-일)-시클로펜틸메틸-에틸-아민;
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르;
(3-{[3,5-비스 트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
(3-{[3,5-비스 트리플루오로메틸-벤질)-(5-메틸-[1,3,4]옥사디아졸-2-일)-아미노]-메틸}-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민;
또는 이의 임의의 조합이다.
본 발명은 또한 제약상 허용되는 및 제약상 허용되지 않는 염을 비롯한 임의의 염, 또는 이의 임의의 혼합물을 비롯한 본원에 제공된 화합물의 임의의 조합물을 포함한다. 본 발명은 또한 입체이성질체의 임의의 조합물을 비롯한 본원에 제 공된 화합물의 임의의 입체이성질체를 포함한다.
본 발명의 이러한 측면에서, 본원에 제공된 화합물은 키랄 또는 비키랄일 수 있거나, 또는 이들은 라세미 혼합물, 부분입체이성질체, 순수한 거울상이성질체, 전구약물, 호변이성질체 또는 이의 임의의 혼합물로 존재할 수 있다. 키랄 화합물에 대해서는, 개별 거울상이성질체, 개별 부분입체이성질체, 및 거울상이성질체, 부분입체이성질체의 임의의 혼합물, 또는 둘 다가 본원에 포함되며, 예를 들면, (R), (S), 또는 (R) 및 (S) 이성질체의 혼합물이 있다. 이러한 측면에서, 개별적 광학 이성질체 또는 특정 바람직한 이성질체는 키랄 시약을 사용하여 어디서든 적용가능한 분할 공정에서 단일 이성질체 형태를 얻거나, 또는 시약 또는 촉매의 존재 하에 반응을 수행함으로써 이의 단일 거울상이성질체 또는 부분입체이성질체 형태로 얻을 수 있다.
다르게 특정하지 않으면, 화학식 I의 임의의 화합물을 비롯한 본원에 도시된 임의의 화합물은 헤테로시클릭 고리 내의 헤테로원자 또는 헤테로기의 위치에서 발생하는 가능한 모든 위치 이성질체를 비롯한, 제시된 화학식에 포함될 수 있는 가능한 모든 위치 이성질체 또는 결합위치이성질체를 포함하는 것으로 한다. 예를 들어, 화학식 I의 고리 A가 피리딘인 경우, 가능한 위치 이성질체에는 이 포함되고, 각각의 이들 이성질체는 고리 A가 피리딘인 경우에 화학식 I에 포함되는 것으로 한다. 유사하게, 고리 A가 피라졸로피리 딘인 경우, 가능한 위치 이성질체에는 이 포함되며, 각각의 이들 이성질체는 고리 A가 피라졸로피리딘인 경우에 화학식 I에 포함되는 것으로 한다. 추가로, 고리 A가 비시클릭계인 경우에 본 발명은 또한 그러한 고리계의 다른 이성질체를 고려하며, 예를 들어 고리 A가 인돌인 경우에 가능한 이성질체에는 및 가 포함되고, 각각의 이들 이성질체는 고리 A가 인돌인 경우에 화학식 I에 포함되는 것으로 한다.
한 측면에서, 라세미 화합물의 분할 방법에는 비제한적으로 미생물 분할을 이용하거나; 만델산, 캄포술폰산, 타르타르산, 락트산 등과 같은 어디서든 적용가능한 키랄산과 형성된 부분입체이성질체염을 분할하거나; 또는 키랄 염기, 예컨대 브루신, 신코나 알칼로이드 및 그의 유도체와 형성된 부분입체이성질체염을 분할하는 것 등이 포함된다. 통상적으로 이용되는 방법은 문헌 [Jaques, et al. in Enantiomers, Racemates and Resolution; Wiley-Interscience, 1981]에 종합되어 있다. 예를 들어, 적합한 경우에 화학식 I의 화합물은 키랄 아민, 아미노산 또는 아미노산으로부터 유래한 아미노알코올로 처리하거나; 산을 아미드로 전환하기 위한 통상적 반응 조건을 이용하거나; 분획 결정화 또는 크로마토그래피에 의한 부분입체이성질체의 분리; 또는 순수한 부분입체이성질체 아미드를 가수분해하여 화학식 I의 입체이성질체를 제조함으로써 분할될 수 있다.
본원에 사용된 용어 "제약상 허용되는" 염 또는 "약리학적으로 허용되는" 염 은 일반적으로 화합물 또는 화합물들의 염 또는 복합체를 나타내며, 여기서 화합물은 음이온 또는 양이온일 수 있으며, 각각 일반적으로 인간 또는 동물 소비용으로 적합하다고 고려되는 상대 양이온 또는 음이온과 결합되어 있다. 예를 들어, 제약상 허용되는 염은 산의 음이온이 일반적으로 인간 또는 동물 소비용으로 적합한 것으로 고려되는 산과의 반응 또는 착체화로 형성된 본원에 개시된 화합물의 염을 나타낼 수 있다. 이러한 측면에서, 약리학적으로 허용되는 염에는 유기산 또는 무기산과의 염이 포함된다. 약리학적으로 허용되는 염의 예에는 비제한적으로 히드로클로라이드, 히드로브로마이드, 히드로요오다이드, 술페이트, 포스페이트, 프로피오네이트, 락테이트, 말레에이트, 말레이트, 숙시네이트, 타르타레이트 등이 포함된다.
염은 또한 염기, 예컨대 유기 염기, 무기 염기, 유기금속 염기, 루이스산, 브론스테드 염기, 또는 이의 임의의 조합물을 사용하여 화합물의 산 잔기, 예컨대 카르복실산 잔기, OH, 또는 NH 등을 탈양성자화시켜 형성될 수 있다. 화합물이 산성 잔기를 갖는 경우에, 적합한 제약상 허용되는 염에는 알칼리 금속염, 알칼리 토금속염, 또는 유기물 기재의 염 등이 포함될 수 있다. 이러한 측면에서, 알칼리 금속염의 예에는 비제한적으로 나트륨 및 칼륨염이 포함되고, 유기물 기재의 염의 예에는 비제한적으로 메글루민 염 등이 포함된다. 약리학적으로 허용되는 염은 통상적 수단에 의해 제조할 수 있다. 제약상 허용되는 염, 및 그러한 염의 제조 방법의 추가의 예는, 예를 들어 문헌 [Berg et.al., J. Pharma. Sci, 66, 1-19 (1977)]에서 찾아볼 수 있다.
추가의 측면에서, 본 발명은 또한 제약상 허용되는 담체 및 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하는 조성물을 비롯한 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하는 조성물을 제공한다. 이러한 측면에서, 하나 이상의 화합물은 천연 화합물, 염, 또는 이의 임의의 조합으로 존재할 수 있다. 본 발명은 또한 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하고, 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하는 조성물을 포함한다. 다른 측면에서, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하고, 추가로 화학요법제, 면역억제제, 사이토카인, 세포독성제, 항염증제, 항이상지질혈증제, 항류마티스제, 심장혈관제, 또는 이의 임의의 조합물로부터 선택되는 제제를 임의로 포함하는 제약 조성물을 포함한다.
추가로, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하며, 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하는, 정제, 캡슐제, 시럽제, 카세제, 산제, 과립제, 용액제, 현탁액제, 에멀젼, 볼루스, 로젠지, 좌제, 크림, 젤, 페이스트, 폼제, 스프레이, 에어로졸, 마이크로캡슐제, 리포좀, 또는 경피 팻치 형태인 제약 조성물을 포함한다.
전구약물
본 발명의 다른 측면에서, 별법으로, 화합물은 전구약물 형태로 제제화되고, 투여될 수 있다. 일반적으로, 전구약물은 효소적으로 활성화되거나 보다 활성있는 모 형태로 전환될 수 있는 청구된 화합물의 기능적 유도체를 포함한다. 따라서, 본 발명의 치료 방법에서, 용어 "투여하는"은 구체적으로 개시된 화합물, 또는 구체적으로 개시되지 않았지만 환자에게 투여된 후에 생체내에서 특정 화합물로 전환될 수 있는 화합물을 사용하여 기재된 다양한 장애를 치료하는 것을 포함한다. 적합한 전구약물 유도체의 선택 및 제조를 위한 통상적 절차는, 예를 들어 문헌 [Wihnan, 14 Biochem. Soc. Trans. 375-82 (1986)]; [Stella et al., Prodrugs: A Chemical Approach to Targeted Drug Delivery, in Directed Drug Delivery 247-67 (1985)]에 기재되어 있다.
따라서, 한 측면에서, 본원에 개시된 화합물의 "전구약물"은 물리적 조건 하에 종이 본원에 개시된 화합물로 되거나, 제공하거나, 방출하거나 또는 변형되는 화학적- 또는 대사적-절단가능 기를 갖는 종을 나타낸다. 이러한 방식으로, 전구약물은 본원에 개시된 제약적 생체내 활성 화합물을 방출할 수 있다. 예를 들어, 본 발명의 전구약물에는 비제한적으로 포스페이트-함유 전구약물, 티오포스페이트-함유 전구약물, 술페이트-함유 전구약물, 펩티드-함유 전구약물, D-아미노산-변형된 전구약물, 글리코실화 전구약물, β-락탐-함유 전구약물, 임의로 치환된 페녹시아세트아미드-함유 전구약물, 임의로 치환된 페닐아세트아미드-함유 전구약물, 5-플루오로시토신 또는 보다 활성이 있는 종으로 전환될 수 있는 다른 5-플루오로우리딘 전구약물 등이 포함된다. 다른 측면에서, 본 발명의 전구약물에는 비제한적으로 카르복실산, 술폰아미드, 아민, 히드록실 등의 유도체 뿐만 아니라 다른 관능기 및 이의 임의의 조합이 포함된다.
다른 측면에서, 본 발명은 상기 기재된 임의의 조합에서 임의의 화학식의 하나 이상의 화합물을 포함하고, 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하는 제약 조성물을 제공한다. 이와 연관된 측면에서, 본 발명은 본원에 개시된 바와 같은 유효량의 하나 이상의 화합물을 투여하는 것을 포함하는, 증상 또는 질환 상태, 예컨대 이상지질혈증, 아테롬성동맥경화증, 말초 혈관 질환, 고중성지방혈증, 고콜레스테롤혈증, 고베타지단백혈증, 저알파지단백혈증, 심장혈관 장애, 예컨대 협심증, 허혈, 뇌졸중, 심근경색증 (MI), 재관류 손상, 재협착 및 고혈압, 및 당뇨성 혈관 질환, 예컨대 당뇨성 망막병증, 및 내독소혈증의 치료 방법을 제공한다.
합성 방법
반응식은 본원에 개시된 벤질아민 화합물로의 합성 접근법을 상술하기 위해 본원에 제공된다. 따라서, 본원에 따른 화합물은 특정 반응식에 제시된 바와 같이 및/또는 실시예에 도시된 바와 같이, 합성 방법 및 상업적으로 입수가능하거나 또는 상업적으로 입수가능한 전구체로부터 당업계에 공지된 합성 방법을 이용하여 합성할 수 있는 출발 물질, 또는 당업자에게 인지되어 있는 그의 변형을 이용함으로써 제조될 수 있다. 하기 반응식의 각각의 변수는 본원에 제공된 화합물의 설명과 부합되는 임의의 기를 나타낸다. 제공된 각각의 합성 반응식 또는 실시예에서, 특정되지 않은 반응식 또는 실시예에 도시된 임의의 구조에서의 치환기는 본원에 제공된 화합물의 화학식에 따라 개시된 바와 같이 선택된다.
하기 일반적인 절차는 본원에 제공된 반응식 및 실시예에서 이용될 수 있다.
할로겐화는 시약, 예컨대 옥시염화인 (POCl3), 티오닐 클로라이드 (SOCl2) 등을 사용하여, 예를 들어, 약 80℃ 내지 약 120℃의 온도에서, 약 4 내지 약 8시간 동안 수행된 후, 생성된 혼합물의 pH를 약 6 내지 약 7로 조정함으로써 수행될 수 있다.
아민화는 아세톤, 아세토니트릴, 디메틸포름아미드, 디메틸아세트아미드 등으로부터 선택된 용매의 존재 하에, 염기의 존재 또는 부재 하에 아민을 사용함으로써 수행될 수 있다. 적합한 염기에는 트리에틸아민, N,N-디이소프로필 에틸 아민, 탄산칼륨, 탄산나트륨, 수소화나트륨 등이 포함된다. 반응 온도는 전형적으로 약 20℃ 내지 약 12O℃이고, 반응 시간은 전형적으로 약 4시간 내지 약 20시간의 범위이다.
따라서 본 발명의 추가의 한 측면은 본원에 제공된 화학식의 화합물의 제조 방법에 관한 것이다. 본원에 개시된 임의의 화학식의 임의의 화합물은 반응식에 제시된 절차 뿐만 아니라 실시예에 제시된 절차를 이용하여 적합한 출발 물질 및 하기 유사한 절차를 선택함으로써 수득할 수 있다. 따라서, 본원에 개시되거나 예시된 임의의 화학식의 임의의 화합물은 바람직한 치환기가 있는 적합한 출발 물질 및 적합한 시약, 및 본원에 기재된 것과 유사한 하기 절차를 이용하여 수득할 수 있다. 따라서, 본원에 개시된 반응식은 본원의 임의의 화합물을 제조하는 데 적용될 수 있음이 당업자에게 용이하게 이해될 것이며, 따라서 반응식에서 특정 단계의 임의의 논의는 그 단계를 수행하기 위해 이용될 수 있는 한 방법 또는 한 세트의 조건을 반영하려는 것이다. 특정 단계의 이러한 논의는 제한하려는 것이 아니라, 단계가 효과적일 수 있는 한 특정 방법 및 조건 세트를 예시하려는 것이다.
본 발명의 한 측면에서, 본 발명에 따른 화학식 I의 화합물은 하기 반응식 1-5 중 하나 이상에서 도시된 바와 같이 제조될 수 있다. 특정 경우에서, 관련된 시약 및 출발 물질은 상업적으로 입수가능하다. 다른 경우에서, 관련된 시약 및 출발 물질은 유기 및 헤테로시클릭 화학에서의 표준 합성 절차에 의해 제조되며, 이는 당업자에게 공지되어 있다. 이러한 기술은 공지된 구조적으로 유사한 중간체 또는 출발 물질의 합성과 유사하고, 절차는 하기 제조예 및 실시예에 기재되어 있다. 예를 들어, 하기 문헌은 반응식 1-5에 기재된 다수의 중간체의 제조를 위한 정확한 절차 또는 유사한 절차를 개시하고 있다: 문헌 [Synlett, 2001, No: 2, 251-253]; [Synthesis 2001, 1185-1196]; [Journal of Heterocyclic Chemistry, 1987, 351-355]; [Journal of Organic Chemistry Vol: 30, 1965, 3593-3596]; [Journal of Heterocyclic Chemistry 1982, 809-811]. 그러한 공지된 절차에는 알데히드의 환원, 시안화, 아민의 알킬화, 벤질화, 아민의 아실화, 아민의 술포닐화, 환원성 아민화, 니트릴의 가수분해, 카르복실산의 에스테르화 및 카르복실산에서 아미드로의 전환 등이 포함된다.
따라서, 하기 대표적인 합성 반응식에서, 출발 물질은 상업적으로 입수가능하거나, 또는 적합한 치환기를 갖는 출발 물질 및/또는 시약을 사용하는 익히 공지된 절차를 이용하여 용이하게 제조된다. 임의의 반응식 또는 실시예의 문맥이 요 구하거나 허용하는 바에 따라, 특정하지 않은 임의의 구조에서 치환기는 개시된 화합물의 일반적인 설명에서 본원에 제시된 바와 같이 선택된다.
한 측면에서, 본 발명에 따른 화합물은 하기 반응식에 따라 제조될 수 있다.
반응식 1의 대표적인 단계는 하기를 포함한다. 화학식 Ia의 화합물은 극성 용매, 예컨대 N,N-디메틸포름아미드 (DMF) 및 염기, 예컨대 탄산나트륨 또는 탄산칼륨 중에서 HNR1R2를 사용한 아민화 반응에 의해 화학식 Ib의 화합물로 전환될 수 있다. 반응은 또한 용매, 예컨대 아세토니트릴, 테트라히드로푸란 또는 톨루엔의 존재 하에 수행될 수 있다. 염기는 또한 탄산세슘, 칼륨 3차 부톡시드 등으로부터 선택될 수 있다.
환원제, 예컨대 Na(CN)BH3, Na(OAc)3BH, NaBH4 등의 존재 하에 산 예컨대 아세트산 또는 희석된 염산과 함께 (C1-C10) 알코올 용매, 예컨대 메탄올, 에탄올, 프로판올, 이소프로판올 등, 또는 염화 용매, 예컨대 디클로로메탄, 클로로포름, 1,2-디클로로에탄 등의 중에서 화학식 Ib의 화합물을 화학식 Ic의 화합물로 환원성 아민화시켜 R3이 전형적으로 수소인 화학식 I의 화합물을 수득한다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있고, 반응 시간은 전형적으로 약 30분 내지 약 5시간의 범위일 수 있다.
R3이 수소인 화학식 I의 화합물은 염기, 예컨대 탄산칼륨의 존재 하에 용매, 예컨대 테트라히드로푸란 중에서 X1이 할로겐일 수 있는 화학식 X1CO2R6 또는 X1COR8의 화합물과 반응시킴으로써, R3이 전형적으로 CO2R6 또는 COR8이고, 여기서 R6 및 R8은 본원에 정의된 바와 같은 화학식 I의 화합물로 전환될 수 있다. 반응은 또한 아세톤, 아세토니트릴 등의 존재 하에 수행될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 55℃로 유지될 수 있고, 반응 시간은 전형적으로 약 20분 내지 약 5시간의 범위일 수 있다.
Na(CN)BH3, Na(OAc)3BH, NaBH4 등과 같은 환원제의 존재 하에 아세트산 또는 희석된 염산과 같은 산과 함께 (C1-C10) 알코올 용매 매질, 예컨대 에탄올, 프로판 올, 이소프로판올 등 중에서 화학식 Ib의 화합물을 R3이 헤테로아릴, 알킬, 헤테로시클릴일 수 있는 화학식 Id의 화합물로 환원성 아민화시켜, 화학식 Ie의 화합물을 수득할 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있고, 반응 시간은 전형적으로 약 30분 내지 약 5시간의 범위일 수 있다.
화학식 Ie의 화합물은 수소화나트륨 또는 수소화칼륨과 같은 염기의 존재 하에 X1이 이탈기, 예컨대 할로겐, 메실옥시, 토실 등일 수 있는 화학식 If의 화합물과 반응시켜 R3이 알킬, 헤테로아릴, 헤테로시클릴일 수 있는 화학식 I의 화합물을 얻을 수 있다. 반응은 용매, 예컨대 N,N-디메틸포름아미드, 아세토니트릴, 테트라히드로푸란, 톨루엔 등 중에서 수행될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 55℃로 유지될 수 있고, 반응 시간은 전형적으로 약 20분 내지 약 5시간의 범위일 수 있다.
다른 측면에서, 본 발명에 따른 화합물은 하기 반응식에 따라 제조될 수 있다.
이 반응식에서, R3이 수소일 수 있는 화학식 I의 화합물은 브롬화시아노겐 (CNBr)의 존재 하에 염기, 예컨대 중탄산나트륨, 탄산나트륨, 탄산칼륨, 탄산세슘, 중탄산칼륨 등과 함께 적합한 용매, 예컨대 디메틸포름아미드, 아세토니트릴, (C1-C10) 알코올 등을 사용함으로써 R3이 CN기일 수 있는 화학식 I의 화합물로 전환될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 55℃로 유지될 수 있고, 반응 시간은 전형적으로 약 20분 내지 약 5시간의 범위일 수 있다.
R3이 시아노 (CN)기일 수 있는 화학식 I의 화합물은 아연 염, 예컨대 ZnBr2의 존재 하에 시아노 화합물을 나트륨 아지드 또는 칼륨 아지드와 반응시킴으로써 R3이 테트라졸로일기인 화학식 I의 화합물로 전환될 수 있다. 이러한 반응에 적합한 용매에는 N,N-디메틸포름아미드, 아세토니트릴, (C1-C10) 알코올 등이 포함된다.
R3이 테트라졸릴인 화학식 I의 화합물은 상-이동 촉매, 예컨대 테트라알킬암모늄할라이드 또는 테트라아릴암모늄할라이드와 함께 염기, 예컨대 수산화나트륨, 수산화칼륨, 탄산칼륨, 수소화나트륨 등의 존재 하에 용매 매질, 예컨대 물, 디메틸포름아미드, 아세토니트릴 등 중에서 테트라졸릴 화합물을 알킬화제, 예컨대 알킬 할라이드 또는 디알킬 술페이트와 반응시킴으로써 R3이 알킬-치환된 테트라졸릴인 화학식 I의 화합물로 전환될 수 있다.
R3이 테트라졸릴인 화학식 I의 화합물은 용매, 예컨대 피리딘 중에서 테트라졸릴 화합물을 상응하는 산 클로라이드와 반응시킴으로써 R3이 알킬 치환된 [1,3,4]옥사디아졸릴인 화학식 I의 화합물로 전환될 수 있다. 한 측면에서, 반응 온도는 약 120℃ 내지 약 140℃로 유지될 수 있고, 반응 시간은 전형적으로 약 2시간 내지 약 6시간의 범위일 수 있다.
R3이 시아노 (CN)기인 화학식 I의 화합물은 촉매량의 H2O2와 함께 염기, 예컨 대 KOH, NaOH 등의 존재 하에 전형적으로 약 25 내지 약 100℃ 범위의 온도에서 약 30분 내지 약 6시간의 시간 동안 가수분해시켜, R3이 CONH2인 화학식 I의 화합물을 수득할 수 있다.
R3이 CONH2기인 화학식 I의 화합물은 상 이동 촉매 예컨대 테트라알킬암모늄할라이드, 테트라알킬암모늄 수소 술페이트, 또는 테트라아릴암모늄할라이드와 함께 염기, 예컨대 수산화나트륨, 수산화칼륨, 탄산칼륨 등의 존재 하에 용매, 예컨대 벤젠, 톨루엔 등의 중에서 알킬 할라이드와 반응시킴으로써 R3이 CONR6R7 (여기서, R6 및 R7은 독립적으로 수소 또는 본원에 특정되어 있는 바와 같은 알킬일 수 있음)인 화학식 I의 화합물로 전환될 수 있다.
R3이 CONH2기일 수 있는 화학식 I의 화합물은 또한 알코올성 용매, 예컨대 tert-부탄올, 이소프로판올 등의 존재 하에 화학식 RdCOCH2X1 (여기서, Rd는 수소, 알킬, 또는 할로알킬일 수 있고, X1은 이탈기, 예컨대 할로겐일 수 있음)의 화합물과 반응시킬 수 있다. 한 측면에서, 반응 온도는 약 60℃ 내지 약 120℃로 유지될 수 있으며, R3이 Rd-치환된 옥사졸릴기일 수 있는 화학식 I의 화합물을 수득할 수 있다,
R3이 시아노 (CN)기인 화학식 I의 화합물은 용매, 예컨대 1,4-디옥산, 톨루엔 등 중에서 히드록실 아민과 반응시킨 후, 염기, 예컨대 피리딘과 함께 Rd가 알킬일 수 있고, X1이 할로겐일 수 있는 화학식 RdCOX1의 화합물을 첨가하여 R3이 Rd-치환된 1,2,4-옥사디아졸릴기일 수 있는 화학식 I의 화합물을 수득한다.
또 다른 측면에서, 본 발명에 따른 화합물은 하기 반응식에 따라 제조될 수 있다.
상기 반응식에서, 합성은 Z1이 알데히드, 아세탈, 또는 CN일 수 있고, X2가 할로겐일 수 있는 화학식 Ig의 화합물로 시작하고, 이를 문헌 (하기 참조)으로부터 당업자에게 공지된 방법을 이용하여 R1이 알킬일 수 있는 화학식 Ih의 친핵체와 반응시켜 화학식 Ii의 화합물을 얻을 수 있다. 예를 들어, 치환된 클로로피리딘으로부터의 2급 아민, 및 1급 아민 (에틸아민 히드로클로라이드)의 형성은 염기, 예컨대 N,N-디이소프로필-N-에틸아민, 및 용매, 예컨대 에탄올의 존재 하에 수행될 수 있다. 염기는 또한 다른 3차 아민, 예컨대 트리에틸 아민 (TEA), 트리부틸 아민 등으로부터 선택될 수 있다. 반응은 또한, 비제한적으로 n-부탄올, 3차 부탄올, N,N-디메틸포름아미드 (DMF), 디메톡시에탄 등을 비롯한 용매의 존재 하에 수행될 수 있다. 반응 온도는 약 50℃ 내지 사용된 용매의 비점으로 유지될 수 있다. 반응 시간은 약 3 내지 약 16시간의 범위일 수 있다 (문헌 [Cappelli, A. et. al. Journal of Medicinal Chemistry, 47(10): pp. 2574-2586 (2004)]; [Izumi, T., et. al. Bioorganic & Medicinal Chemistry, 11: 2541-2550 (pp. 2003)]).
화학식 Ik의 화합물은 염기, 예컨대 탄산칼륨의 존재 하에 극성 용매, 예컨대 테트라히드로푸란, 디에틸 에테르 등의 중에서 화학식 Ii의 화합물을 R2가 알킬, 할로알킬 또는 COR8일 수 있는 화학식 Ij의 화합물로 알킬화 또는 아실화시켜 얻을 수 있다. 한 측면에서, 반응 온도는 약 0℃ 내지 약 100℃로 유지될 수 있고, 반응 시간은 전형적으로 약 1시간 내지 약 8시간의 범위일 수 있다.
화학식 Ip의 화합물은 적합한 환원제, 예컨대 리튬 알루미늄 히드라이드 (LAH), 나트륨 비스(2-메톡시-에톡시)알루미늄히드라이드 (레드-알 (등록상표; Red-Al)) 등을 사용하여 Z1이 시아노 (CN)기일 수 있는 화학식 Ik의 화합물을 환원시켜 제조할 수 있으며, 이는 적합한 용매, 예컨대 테트라히드로푸란, 디에틸에테르 등의 중에서 수행될 수 있다. 한 측면에서, 반응 온도는 약 0℃ 내지 약 60℃로 유지될 수 있고, 반응 시간은 전형적으로 약 1시간 내지 약 14시간의 범위일 수 있다.
화학식 Ip의 화합물은 화학식 Iq의 화합물로 환원성 아민화시켜 화학식 Im의 화합물로 전환될 수 있다. 반응은 아세트산, 용매, 예컨대 메탄올, 및 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 수행될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등, 또는 그의 혼합물로부터 선택될 수 있다. 반응은 또한 다른 환원제, 예컨대 나트륨 트리아세톡시보로히드라이드 등을 사용하여 수행될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있으며, 반응 시간은 전형적으로 약 30분 내지 약 5시간의 범위일 수 있다.
화학식 Ik의 화합물, 알데히드 또는 아세탈은 화학식 Ic의 화합물로 환원성 아민화시켜 화학식 Im의 화합물로 전환될 수 있다. 반응은 아세트산, 용매, 예컨대 메탄올, 및 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 수행될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등, 또는 그의 혼합물로부터 선택될 수 있다. 반응은 또한 다른 환원제, 예컨대 나트륨 트리아세톡시보로히드라이드, 및 유사한 환원제를 사용하여 수행할 수 있다. 전형적으로, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있고, 반응 시간은 전형적으로 약 30분 내지 약 5시간일 수 있다.
화학식 Im의 화합물은 X1이 이탈기, 예컨대 할로겐, 메실옥시 등일 수 있는 화학식 In의 화합물로 아실화시켜, 전형적으로 R3이 CO2R6, COR8, SO2R8, CONR6R7 또는 알킬일 수 있는 화학식 I의 화합물로 전환된다. 예를 들어, 화합물 Im은 염기, 예컨대 탄산칼륨 및 용매, 예컨대 테트라히드로푸란의 존재 하에 주변 온도에서 에틸 클로로포르메이트와 반응시킬 수 있다. 반응은 또한 다른 아실화제, 예컨대 메틸 클로로포르메이트 등을 사용하여 수행될 수 있다. 반응은 또한 비제한적으로 아세톤, 아세토니트릴 등을 비롯한 상이한 용매의 존재 하에 수행될 수 있다. 한 측면에서, 반응 온도는 약 22℃ 내지 약 50℃로 유지될 수 있고, 반응 시간은 전형적으로 약 4시간 내지 약 12시간의 범위일 수 있다.
Z1이 알데히드 또는 아세탈일 수 있는 화학식 Ik의 화합물은 또한 아세트산, 용매, 예컨대 메탄올, 및 적합한 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 R3이 알킬, 헤테로아릴, 헤테로시클릴일 수 있는 화학식 Id의 화합물로 환원성 아민화시켜 화학식 Io의 화합물로 전환될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등 또는 그의 혼합물로부터 선택될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 50℃로 유지될 수 있고, 반응 시간은 전형적으로 약 1시간 내지 약 6시간의 범위일 수 있다.
화학식 Io의 화합물은 염기, 예컨대 수소화나트륨 및 용매, 예컨대 N,N-디메틸포름아미드의 존재 하에 X1이 이탈기, 예컨대 할로겐, 메실옥시 등일 수 있는 화학식 If의 화합물로 벤질화 반응시켜 R3이 5원 내지 7원 헤테로아릴기일 수 있는 화학식 I의 화합물로 전환될 수 있다. 염기는 또한 수소화칼륨 등을 비롯한 염기로부터 선택될 수 있다. 반응은 또한 예를 들어, 아세토니트릴, 테트라히드로푸란, 톨루엔 등을 비롯한 용매의 존재 하에 수행될 수 있다. 전형적으로, 반응 온도는 약 25℃ 내지 약 60℃의 범위일 수 있다.
또 다른 측면에서, 본 발명에 따른 화합물은 하기 반응식에 따라 제조될 수 있다.
상기 반응식에서, 팔라듐 촉매된 크로스-커플링 아미드화 반응은 화학식 It의 화합물을 제조하기 위해 사용될 수 있다. 예를 들어, X1이 할로겐일 수 있는 헤테로아릴 할라이드 (Ir), 및 R8 및 R2가 알킬 또는 아릴일 수 있는 아미드 (Is)로부터의 화학식 It의 화합물의 형성은 팔라듐 촉매, 예컨대 트리스(디벤질리덴아세톤)디팔라듐, 포스포러스 리간드, 예컨대 4,5-비스(디페닐포스피노)-9,9-디메틸크산텐 (크산트포스 (등록상표; Xantphos)), 및 염기, 예컨대 탄산세슘의 존재 하에 적합한 용매, 예컨대 톨루엔 중에서 달성될 수 있다. 반응은 또한 톨루엔, 크실렌, 디메틸포름아미드, 테트라히드로푸란, 1,4-디옥산 등 뿐만 아니라 그의 혼합물을 비 롯한 용매의 존재 하에 수행될 수 있다. 추가로, 반응은 약 1 mol% 내지 약 10 mol%의 적합한 Pd 촉매, 예컨대 Pd(OAc)2, Pd(DIPHOS)2, Pd(PPh3)4 등의 존재 하에 수행될 수 있다. 반응은 또한 리간드, 예컨대 2-디시클로헥실포스피노-2',4',6'-트리-i-프로필-1,1'-비페닐 (XPHOS), 1,1-비스(디페닐포스핀)페로센 (DPPF), 2,2'-비스(디페닐포스파닐)-1,1'-비페닐 (BINAP), 1,2-비스(디페닐포스핀)에탄 (DIPHOS) 등의 존재 하에 수행될 수 있다. 추가로, 다른 염기, 예컨대 탄산나트륨, 탄산칼륨, 나트륨 아세테이트 등이 사용될 수 있다. 반응 온도는 전형적으로 약 50℃ 내지 약 125℃의 범위일 수 있다 (문헌 [Yin, J; Buchwald, S. L. Organic Letters, 2 (8): pp. 1101-1104 (2000)] 참조).
화학식 It의 화합물은 아세트산, 적합한 용매, 예컨대 메탄올, 및 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 화학식 Ic의 화합물로 환원성 아민화시켜 화학식 Iv의 화합물로 전환될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등 또는 그의 혼합물로부터 선택될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있고, 반응 시간은 전형적으로 약 30분 내지 약 5시간의 범위일 수 있다.
화학식 Iv의 화합물은 염기, 예컨대 탄산칼륨, 및 용매, 예컨대 테트라히드로푸란의 존재 하에 X1이 할로겐일 수 있는 화학식 In의 화합물로 아실화시켜 R3이 CO2R6, COR8, SO2R8, CONR6R7 또는 알킬일 수 있고, Y가 N일 수 있는 화학식 I의 화합물로 전환될 수 있다. 반응은 또한 아세톤, 아세토니트릴 등을 비롯한 다른 적합한 용매의 존재 하에 수행될 수 있다. 한 측면에서, 반응 온도는 약 22℃ 내지 약 50℃로 유지될 수 있고, 반응 시간은 전형적으로 약 4시간 내지 약 12시간의 범위일 수 있다.
화학식 It의 화합물은 아세트산, 용매, 예컨대 메탄올, 및 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 R3이 5원 내지 7원 헤테로아릴기일 수 있는 화학식 Id의 화합물로 환원성 아민화시켜 화학식 Iu의 화합물로 전환될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등, 또는 그의 혼합물로부터 선택될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 50℃로 유지될 수 있고, 반응 시간은 전형적으로 약 1시간 내지 약 6시간의 범위일 수 있다.
화학식 Iu의 화합물은 염기, 예컨대 수소화나트륨 및 용매, 예컨대 디메틸포름아미드의 존재 하에 X1이 이탈기, 예컨대 할로겐, 메실옥시 등일 수 있는 화학식 If의 화합물로 벤질화시켜 화학식 I의 화합물로 전환될 수 있다. 염기는 또한 수소화칼륨, 다른 수화물 등으로부터 선택될 수 있다. 반응은 또한 아세토니트릴, 테트라히드로푸란, 톨루엔 등을 비롯한 용매의 존재 하에 수행될 수 있다. 전형적으로, 반응 온도는 약 25℃ 내지 약 60℃의 범위일 수 있다.
또 다른 측면에서, 본 발명은 R1이 (CHRx)nR5 (여기서, n은 1이고, 다른 모든 치환기가 상기 정의된 바와 같음)일 수 있는 화학식 I의 화합물의 제조를 위한 일반적인 공정을 제공한다. 이러한 일반적인 공정은 하기 반응식에 도시되어 있다.
상기 반응식에서, 화학식 IIp의 화합물은 아세트산, 용매, 예컨대 메탄올, 및 환원제, 예컨대 나트륨 시아노보로히드라이드의 존재 하에 화학식 Ic의 화합물로 환원성 아민화시켜 화학식 IIq의 화합물로 전환될 수 있다. 반응은 또한 희석된 염산의 존재 하에 수행될 수 있다. 사용된 용매는 또한 (C1-C10) 알코올, 예컨대 에탄올, 프로판올, 이소프로판올 등, 또는 그의 혼합물로부터 선택될 수 있다. 한 측면에서, 반응 온도는 약 25℃ 내지 약 35℃로 유지될 수 있고, 반응 시간은 전형적으로 약 30분 내지 약 5시간의 범위일 수 있다.
화학식 IIq의 화합물은 염기, 예컨대 탄산칼륨, 및 용매, 예컨대 테트라히드 로푸란의 존재 하에 화학식 IXh의 화합물로 아실화시켜 R3이 CO2R6일 수 있는 화학식 IIr의 화합물로 전환될 수 있다. 반응은 또한 다른 적합한 용매, 예컨대 테트라히드로푸란, 아세톤, 아세토니트릴 등의 존재 하에 수행될 수 있다. 한 측면에서, 반응 온도는 약 22℃ 내지 약 50℃로 유지될 수 있고, 반응 시간은 전형적으로 약 4시간 내지 약 12시간의 범위일 수 있다.
헥 (Heck)-타입 탄소-탄소 결합 형성 반응은 화학식 IIr의 화합물, 및 Rx, R2 및 R5가 독립적으로 수소, 알킬, 아릴, 헤테로아릴, 시아노, 카르브알콕시 또는 알콕시로부터 선택될 수 있는 것인 화학식 IIs의 화합물 사이에서 수행될 수 있다. 합성 방법에는, 예를 들어 팔라듐 촉매, 예컨대 팔라듐 아세테이트, 포스포러스 리간드, 예컨대 트리페닐포스핀, 염기, 예컨대 트리에틸아민 (TEA), 및 적합한 용매, 예컨대 테트라히드로푸란의 존재 하에 헤테로아릴 할라이드 (IIr) 및 올레핀 (IIs)으로부터의 화학식 IIt의 화합물의 형성이 포함된다. 반응은 또한 다른 적합한 용매, 예컨대 톨루엔, 크실렌, N,N-디메틸포름아미드, 디에틸 에테르, 1,4-디옥산 등의 존재 하에 수행될 수 있다. 추가로, 이 반응은 비제한적으로 PdCl2, Pd2(dba)3, Pd(PPh3)4 등을 비롯한 팔라듐 촉매 약 1 mol% 내지 약 10 mol%의 존재 하에 수행될 수 있다. 반응은 또한 트리부틸포스핀, 트리아릴포스핀, DPPF, BINAP, DIPHOS 등을 비롯한 리간드의 존재 하에 수행될 수 있다. 추가로, 반응은 탄산나트륨, 탄산칼륨, 나트륨 아세테이트 등을 비롯한 다른 염기의 존재 하에 수행될 수 있다. 전형적으로, 반응 온도는 약 50℃ 내지 약 125℃의 범위일 수 있다 (문헌 [Franzen, R., Canadian Journal of Chemistry, 78: pp. 957-962 (2000); Negishi, E. et al, Chemical Review, Vol. 96: pp. 365-394 (1996)] 참조).
R1이 (CHRx)nR5 (여기서, n은 1이고, 다른 모든 치환기 및 약어는 본원에 정의된 바와 같음)일 수 있는 화학식 I의 화합물은 화학식 IIt의 화합물의 환원에 의해 수행될 수 있다. 환원의 합성 방법에는 비제한적으로 수소 (전형적으로 약 1 psi 내지 약 50 psi)의 존재 하에 극성 용매, 예컨대 에탄올, 테트라히드로푸란 등 중에서, 촉매가 대략 5 내지 10% 탄소 상 팔라듐, 라니-니켈, 나트륨 (또는 다른 적합한 금속(들)) 아말감을 포함하는 것인 촉매 수소화가 포함된다. 전형적으로, 반응 온도는 약 25℃ 내지 약 60℃의 범위일 수 있다.
추가의 측면에서, R1이 (CH2)nRdCO2Re이고, R2가 알킬이고, 특정되지 않은 치환기는 화학식 I에 대해 상기 기재된 바와 같이 선택되는 화학식 I의 화합물은 전구체, 출발 물질, 및 적합한 치환기를 갖는 시약을 사용하여 반응식 1에서 5에 기재된 바와 유사한 하기 절차에 따라 제조될 수 있다.
또 다른 측면에서, 본 발명에 따른 화합물은 하기 반응식에 따라 제조될 수 있다.
상기 반응식에서, 화학식 IIy의 화합물은 Z가 (CH2)r (r은 0 내지 2의 정수임), N 또는 O이고; Re가 화학식 I에 따라 정의된 것인 화학식 IIu의 화합물로부터 출발하여 당업자에게 공지된 절차에 의해 제조될 수 있다. 적용가능한 합성 방법에는, 예를 들어 하기 일련의 반응 단계인 1) 비티그 (Wittig) 반응; 2) 환원; 3) 에스테르의 가수분해; 및 4) 아민으로의 전환이 포함된다.
화학식 IIy의 화합물은 반응식 1 또는 반응식 3의 화학식 Ia 또는 Ig의 화합물과 반응시켜 화학식 I의 상응하는 화합물을 얻을 수 있다.
추가로, 비제한적으로 화학식 I, Ia, Ia', II, IIa, IIb, IIc, III, IIIa, IIIb, IIIc, IV, IVa, IVb, IVc, V, Va, Vb, Vc, VI, VIa, VIb, VIc, VII, VIIa, VIIb, VIIc, VIII, VIIIa, VIIIb, VIIIc, II-1, IIa-1, IIb-1, III-1, IIIa-1, IIIb-1, IV-1, IVa-1, IVb-1, V-1, Va-1, Vb-1, VI-1, VIa-1, VIb-1, VII-1, VIIa-1, VIIb-1, VIII-1, VIIIa-1, 및 VIIIb-1 등의 화합물을 비롯한 본원에 제공된 화학식의 화합물은 반응식 1에서 6에 기재된 바와 같은 적합한 출발 물질 및 시약으로 하기와 유사한 절차에 의해 제조될 수 있다.
본 발명의 다른 측면에서, 하기 표에 제시된 화합물은 본원에 개시된 바와 같이, 반응식 1 내지 6 중 하나 이상에 따라 합성될 수 있다.
| 반응식 1 내지 6 중 하나 이상에 따라 제조될 수 있는 대표적인 화합물. | |
| 목록 | 화합물 |
| 1 | (5-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-디메틸-아민 |
| 2 | 에틸-(1-에틸-5-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)아미노]메틸}-3-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-메틸-아민 |
| 3 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-디메틸-아민 |
| 4 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-디메틸-아민 |
| 5 | (5-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-3-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 6 | 에틸-(1-에틸-5-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-메틸-아민 |
| 7 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-3-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 8 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 9 | (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디에틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 10 | (1,3-디에틸-5-{[(3-플루오로-5-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 11 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디에틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 12 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-메틸-아민 |
| 13 | (6-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디메틸-3H-이미다조[4,5-b]피리딘-5-일)-디메틸-아민 |
| 14 | (6-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디메틸-3H-이미다조[4,5-b]피리딘-5-일)-디메틸-아민 |
| 15 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디메틸-3H-이미다조[4,5-b]피리딘-5-일)-디메틸-아민 |
| 16 | (6-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디메틸-3H-이미다조[4,5-b]피리딘-5-일)-디메틸-아민 |
| 17 | (6-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-에틸-2-메틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 18 | 에틸-(3-에틸-6-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2-메틸-3H-이미다조[4,5-b]피리딘-5-일)-메틸-아민 |
| 19 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-에틸-2-메틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 20 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-에틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 21 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디에틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 22 | (2,3-디에틸-6-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 23 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2,3-디에틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 24 | (6-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-3-에틸-3H-이미다조[4,5-b]피리딘-5-일)-에틸-메틸-아민 |
| 25 | (5-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,2-디메틸-1H-피롤로[2,3-b]피리딘-6-일)-디메틸-아민 |
| 26 | (5-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,2-디메틸-1H-피롤로[2,3-b]피리딘-6-일)-디메틸-아민 |
| 27 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,2-디메틸-1H-피롤로[2,3-b]피리딘-6-일)-디메틸-아민 |
| 28 | (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-메틸-1H-피롤로[2,3-b]피리딘-6-일)-디메틸-아민 |
| 29 | (5-{[(3,5-디플루오로벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-2-메틸-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 30 | 에틸-(1-에틸-5-{[(3-플루오로-5-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-2-메틸-1H-피롤로[2,3-b]피리딘-6-일)-메틸-아민 |
| 31 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-2-메틸-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 32 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 33 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,2-디에틸-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 34 | (1,2-디에틸-5-{[(3-플루오로-5-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 35 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,2-디에틸-1H-피롤로[2,3-b]피리딘-6-일)-에틸-메틸-아민 |
| 36 | (5-{[(3,5-비스-트리플루오로메틸벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1-에틸-1H-피롤로[2,3-b]피리딘-6-일)에틸-메틸-아민 |
질환의 치료 방법
CETP 활성을 조절하기 위한 본원에 개시된 화합물은 다양한 증상 또는 질환, 예컨대 지단백질 대사와 관련된 것을 예방 또는 치료하기 위해 사용될 수 있다. 특정 이론을 고수하지 않고도, CETP 활성은 순환하는 콜레스테롤-함유 HDL 수준에 영향을 미칠 수 있다고 여겨진다. CETP 증가는 LDL-C 및/또는 VLDL-C 수준에 비해 HDL-C 수준을 감소시킬 수 있다. 예를 들어, CETP는 콜레스테릴 에스테르를 HDL에서 VLDL 및 LDL로 전환시키는 역할을 하므로, 순환하는 지단백질의 상대적 프로파일을 심장혈관 질환의 위험을 증가시키는 것과 관련된 것으로 바꾸게 된다 (예를 들어, HDL-C 수준의 감소 및 VLDL-C 및 LDL-C 수준의 증가). 추가로, CETP 활성 수준의 증가는 심장혈관 질환의 위험 증가의 전조가 될 수 있다. 따라서, CETP 활성의 조절 또는 저해는 심장혈관 질환, 예컨대 아테롬성동맥경화증을 비롯한 다양한 증상 또는 질환의 진행을 감소 또는 예방하거나, 퇴행을 유도하거나, 발병위험을 감소시키기 위해 지단백질의 상대적 수준을 조절하기 위한 예방 또는 치료 방법일 수 있다.
유효량은 비제한적으로 본원에 교시된 범위를 비롯한 안전하고 효과적인 투여량 및 제제로 대상체에게 투여된다. 본원에 개시된 바와 같이, 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물은 다른 예방 또는 치료제와 함께 사용되거나, 또는 비제한적으로 운동 또는 식이요법에서의 변화를 비롯한 환자 활동을 변화시키는 단계를 임의로 포함하는 방법에서 사용될 수 있다.
한 측면에서, 본 발명은 포유동물 대상체에게 예방 또는 치료 유효량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 증상 또는 질환의 치료 또는 예방 방법을 제공한다. 다양한 측면에서, 증상 또는 질환은 이상지질혈증, 아테롬성동맥경화증, 말초 혈관 질환, 고중성지방혈증, 고콜레스테롤혈증, 고베타지단백혈증, 저알파지단백혈, 심장혈관 장애 (즉, 협심증, 허혈, 뇌졸중, 심근경색증 (MI), 재관류 손상, 재협착, 고혈압) 또는 당뇨성 혈관 질환 (즉, 당뇨성 망막병증, 내독소혈증)이다.
한 다른 측면에서, 본 발명은 포유동물 대상체에게 CETP 활성을 감소 또는 저해시키기에 충분량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 CETP 활성의 감소 또는 저해 방법을 제공한다.
또 다른 측면에서, 본 발명은 포유동물 대상체에게 고밀도 지단백질 (HDL)을 증가시키기에 충분한 양의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 고밀도 지단백질 (HDL)을 증가시키는 방법을 제공한다.
다른 측면에서, 본 발명은 포유동물 대상체에게 예방 또는 치료 유효량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 순환하는 LDL, VLDL 또는 총콜레스테롤에 대한 순환하는 HDL의 비율을 증가시키는 방법을 제공한다.
또 다른 측면에서, 본 발명은 포유동물 대상체에게 HDL-콜레스테롤의 대사를 변경시킴으로써 아테롬성동맥경화 병소의 발생을 감소시키기에 충분한 양의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 아테롬성동맥경화 병소의 발달을 감소시키기 위한 HDL-콜레스테롤의 대사 변경 방법을 제공한다.
또 다른 측면에서, 본 발명은 포유동물 대상체에게 저밀도 지단백질 (LDL)을 감소시키기에 충분한 양의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 포함하는 조성물을 투여하는 것을 포함하는, 상기 대상체에서 저밀도 지단백질 (LDL)을 감소시키는 방법을 제공한다.
다른 측면에서, 본 발명은 포유동물 대상체에게 예방 또는 치료 유효량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 투여하는 것을 포함하는, 상기 대상체에서 아테롬성동맥경화증의 치료 또는 예방 방법을 제공한다.
또 다른 측면에서, 본 발명은 포유동물 대상체에게 예방 또는 치료 유효량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 투여하는 것을 포함하는, 상기 대상체에서 고지질혈증의 치료 또는 예방 방법을 제공한다.
본 발명의 다른 측면에서, 본 발명은 포유동물 대상체에게 예방 또는 치료 유효량의 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염을 투여하는 것을 포함하는, 상기 대상체에서 CETP-매개된 장애의 치료 또는 예방 방법을 제공한다.
또 다른 측면에서, 본 발명은 이상지질혈증, 아테롬성동맥경화증, 말초 혈관 질환, 고중성지방혈증, 고콜레스테롤혈증, 고베타지단백혈증, 저알파지단백혈, 심장혈관 장애, 당뇨성 혈관 질환, 또는 내독소혈증의 치료 또는 예방 방법을 제공한다. 한 측면에서, 심장혈관 장애는 협심증, 허혈, 뇌졸중, 심근경색증 (MI), 재관류 손상, 재협착 또는 고혈압이다.
본 발명의 화합물은 하나 이상의 LDL-콜레스테롤 저하제, 예컨대 HMG CoA 환원효소 저해제; 콜레스테롤 흡수 저해제; 항비만 약물; 지단백질 장애 치료 약물; 혈당강하제: 인슐린; 비구아니드; 술포닐우레아; 티아졸리딘디온; 이중 PPAR 효능제; 및/또는 그의 혼합물과 조합하여/함께 상기 질환의 치료 및/또는 예방에 유용하다. HMG CoA 환원효소 저해제, 마이크로좀 중성지방 전이 단백질 (MTP) /ApoB 분비 저해제, 콜레스테롤 흡수 저해제, 항비만 약물, 혈당강하제와 조합된 본 발명의 화합물은 함께 또는 그러한 기간 내에 상승작용하도록 투여될 수 있다.
한 측면에서, 본 발명은 본원에 개시된 화학식의 구조를 갖는 하나 이상의 화합물, 및/또는 그의 제약상 허용되는 염, 및 임의로 항고혈압제를 포함하는 예방 또는 치료 조성물을 제공한다. 고혈압은 지속적인 고혈압을 특징으로 할 수 있다. 예시적으로, 지속적으로 약 140 mmHg 이상인 심장수축 혈압 또는 약 90 mmHg 이상인 심장확장 혈압이 있는 성인은 고혈압으로 분류될 수 있다. 고지질혈증 증상, 예컨대 아테롬성동맥경화증은 고혈압에 영향을 줄 수 있다.
본 발명의 화합물을 사용한 투여량 처방 계획은 환자의 유형, 종, 연령, 체중, 성별 및 의학적 증상; 치료될 증상의 중증도; 투여 경로; 환자의 신장 및 간 기능; 및 사용된 특정 화합물 또는 그의 염을 비롯한 다양한 인자에 따라 선택된다. 숙련된 내과의, 수의사 또는 임상의는 증상을 예방, 억제 또는 저지하기 위해 필요한 약물의 유효량을 용이하게 결정하고 처방할 수 있다.
본 발명의 화합물 및 조성물은, 예를 들어 경구, 비경구, 정맥내, 피내, 근육내, 피하, 설하, 경피, 기관지, 인후, 비내, 예컨대 크림 또는 연고에 의한 국소, 직장, 관절강내, 수조내 (intracisternally), 경막내, 질내, 복막내, 안내, 협측, 또는 경구 또는 비강 스프레이로 흡입에 의한 것을 비롯한 임의의 적합한 경로로 투여될 수 있다.
본 발명의 조성물의 효과적으로 사용하는 경우 경구 투여량은 1일 당 체중 1 kg 당 약 0.01 mg (mg/kg/일) 내지 약 100 mg/kg/일의 범위일 것이다. 이롭게는, 본 발명의 화합물은 1일 단일 투여량으로 투여될 수 있거나, 또는 1일 총 투여량이 1일에 2, 3 또는 4회로 나누어 투여될 수 있다. 추가로, 본 발명에 대한 바람직한 화합물은 적합한 비내 비히클의 국소적 사용을 통해 비내 형태로 투여되거나, 또는 당업자에게 익히 공지된 경피 피부 팻치의 상기 형태를 사용하여 경피 경로를 통해 투여될 수 있다. 경피 전달 시스템의 형태로 투여하기 위해, 투여량 투여는 물론 투여량 처방 계획을 통해 간격을 두기보다 실질적으로 지속적일 것이다.
본 발명의 방법에서, 본원에 상세히 기재된 화합물은 활성 성분을 형성할 수 있고, 전형적으로 경구 정제, 캡슐제, 엘릭시르제, 시럽제 등인 의도된 투여 형태에 따라 적합하게 선택되는 적합한 제약 희석제, 부형제 또는 담체 (본원에서 '담체' 물질로 총체적으로 언급됨)와 혼합하여, 통상적 제약 관행에 부합하여 투여된다.
예를 들어, 정제 또는 캡슐제 형태의 경구 투여를 위해, 활성 약물 성분은 경구, 비독성, 제약상 허용되는, 불활성 담체, 예컨대 락토스, 전분, 수크로스, 글루코스, 메틸 셀룰로스, 마그네슘 스테아레이트, 인산이칼슘, 황산칼슘, 만니톨, 소르비톨 등과 합해질 수 있고; 액체 형태의 경구 투여를 위해, 경구 약물 성분은 임의의 경구, 비독성, 제약상 허용되는 불활성 담체, 예컨대 에탄올, 글리세롤, 물 등과 합해질 수 있다. 또한, 바람직하거나 필요한 경우, 적합한 결합제, 윤활제, 붕해제 및 착색제가 또한 혼합물에 내포될 수 있다. 적합한 결합제에는 전분, 젤라틴, 천연 당, 예컨대 글루코스 또는 베타락토스, 옥수수 감미제, 천연 및 합성 고무, 예컨대 아카시아, 트래거캔쓰 또는 나트륨 알기네이트, 카르복시메틸셀룰로스, 폴리에틸렌 글리콜, 왁스 등이 포함된다. 이러한 투약 형태에 사용되는 윤활제에는 나트륨 올레에이트, 나트륨 스테아레이트, 마그네슘 스테아레이트, 나트륨 벤조에이트, 나트륨 아세테이트, 염화나트륨 등이 포함된다. 붕해제에는 비제한적으로 녹말, 메틸 셀룰로스, 한천, 벤토나이트, 크산탄 고무 등이 포함된다.
제약 조성물
한 측면에서, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하는 조성물을 제공한다.
다른 측면에서, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하고; 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하는 제약 조성물을 제공한다.
또 다른 측면에서, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하고; 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하는 제약 조성물을 제공하며; 여기서 제약 조성물은 정제, 캡슐제, 시럽제, 카세제, 산제, 과립제, 용액제, 현탁액제, 에멀젼, 볼루스, 로젠지, 좌제, 크림, 젤, 페이스트, 폼제, 스프레이, 에어로졸, 마이크로캡슐제, 리포좀, 또는 경피 팻치의 형태이다.
또 다른 측면에서, 본 발명은 본원에 개시된 바와 같은 하나 이상의 화합물을 포함하고; 담체, 보조제, 희석제, 부형제, 보존제, 용매화물, 또는 이의 임의의 조합물로부터 선택되는 제약상 허용되는 첨가제를 임의로 포함하며; 화학요법제, 면역억제제, 사이토카인, 세포독성제, 항-염증제, 항류마티스제, 항이상지질혈증제, 심장혈관제, 또는 이의 임의의 조합물로부터 선택되는 제제를 추가로 포함하는 제약 조성물을 제공한다.
따라서, 본원에 개시된 화합물 이외에, 본 발명의 제약 조성물은 1종 이상의 임의의 적합한 보조제 예컨대, 비제한적으로 희석제, 결합제, 안정화제, 완충제, 염, 친유성 용매, 보존제, 보조제 등을 추가로 포함할 수 있다. 본 발명의 한 측면에서, 제약상 허용되는 보조제가 사용된다. 그러한 살균 용액의 예 및 방법은 당업계에 익히 공지되어 있고, 공지된 문헌, 예컨대, 비제한적으로 문헌 [REMINGTON'S PHARMACEUTICAL SCIENCES (Gennaro, Ed., 18th Edition, Mack Publishing Co. (1990))]에서 찾을 수 있다. 제약상 허용되는 담체는 투여 방식, 화합물의 용해도 및/또는 안정성에 적합한 것으로 통상적으로 선택될 수 있다.
경구 투여용 제약 조성물
정제 또는 캡슐제 형태로 경구 투여하기 위해, 화합물은 경구, 비독성 제약상 허용되는 불활성 담체, 예컨대 에탄올, 글리세롤, 물 등과 합해질 수 있다. 또한, 바람직하거나 필요한 경우, 적합한 결합제, 윤활제, 붕해제, 및 착색제는 또한 혼합물에 내포될 수 있다. 적합한 결합제에는 비제한적으로 전분; 젤라틴; 천연 당, 예컨대 글루코스 또는 베타-락토스; 옥수수 감미제; 천연 및 합성 고무, 예컨대 아카시아, 트래거캔쓰, 또는 나트륨 알기네이트, 카르복시메틸셀룰로스; 폴리에틸렌 글리콜; 왁스 등이 포함된다. 이러한 투여 형태에 사용되는 윤활제에는, 비제한적으로 나트륨 올레에이트, 나트륨 스테아레이트, 마그네슘 스테아레이트, 나트륨 벤조에이트, 나트륨 아세테이트, 염화나트륨 등이 포함된다. 붕해제에는, 비제한적으로 전분, 메틸 셀룰로스, 한천, 벤토나이트, 크산탄 고무 등이 포함된다.
제약 제제는 본원에 개시된 임의의 화학식에 의해 나타난 1개 이상의 본 발명의 화합물, 및/또는 그의 제약상 허용되는 염을, CETP 활성을 저해하고, CETP 활성에 기인한 다양한 증상 또는 질환을 예방 또는 치료하기에 효과적인 양으로 함유한다. 제제는, 예를 들어 혈압 강하제를 비롯한 다른 성분을 임의로 함유할 수 있다.
경구 투여에 적합한 본 발명의 제제는 개별 단위, 예컨대 미리 결정된 양의 활성 성분을 각각 함유하는 캡슐제, 카세제, 또는 정제; 산제 또는 과립제; 수성 액체 또는 비-수성 액체 중의 용액제 또는 현탁액제; 또는 수중유 액체 에멀젼 또는 유중수 에멀젼 및 볼루스 등으로 제공될 수 있다.
투여 경로
본 발명은 추가로 비제한적으로 경구, 비경구, 피하, 근육내, 정맥내, 관절강내, 기관지내, 복부내, 피막내, 연골내, 공동내, 복강내, 소뇌내, 뇌실내, 결장내, 경부내, 위내, 간내, 심근내, 골내, 골반내, 심막내, 복막내, 늑막내, 전립선내, 폐내, 직장내, 신장내, 망막내, 척수내, 활액내, 흉부내, 자궁내, 방광내, 볼루스, 질, 직장, 구강, 설하, 비내, 이온영동 수단, 또는 경피 수단을 비롯한 경로에 의한 본원에 개시된 하나 이상의 화합물의 투여에 관한 것이다.
투여량
본 발명의 하나 이상의 화합물을 포함하는 조성물은 치료 효과를 달성하기에 효과적인 빈도 및 기간 동안 투여될 수 있으며, 이는 그러한 빈도 및 기간에 걸친 반복 투여의 처방 계획의 맥락에서 이해되어야 한다. 특정 측면에서, 조성물은 HSPG 발현을 증가시키기에 효과적인 빈도 및 기간 동안 투여된다. 특정 측면에서, 조성물은 1일 단일 투여량으로 투여될 수 있거나, 또는 1일 총 투여량을 1일에 2회, 3회 또는 4회로 나누어서 투여될 수 있다. 전형적으로 및 가장 통상적으로, 조성물은 1일 1회 이상 투여되지만, 특정한 경우에는 덜 빈번하게, 예를 들어 1주 2회 또는 1주 1회 투여되어 투여가 효과적일 수 있다. 가장 큰 효과를 위해서는, 투여는 장기간, 예를 들어 약 3개월 이상, 또는 약 6개월 이상, 또는 약 1년 이상, 또는 약 2년 이상, 또는 약 3년 이상 동안 지속되어야 한다. 한 측면에서, 투여는 포유동물의 후속적으로 남은 수명이 시작되는 시기부터 지속된다.
개별적 화합물의 선택 및/또는 양은 경우에 따라, 투여 기간에 걸쳐 달라질 수 있다. 한 측면에서, 본 발명의 단일 조성물이 전체 투여 기간 동안 포유동물에게 투여된다. 다른 측면에서, 하나 이상의 화합물을 포함하는 상이한 조성물이 상이한 시기에 포유동물에게 투여된다.
화합물의 투여량은 체중을 기준으로 조정될 수 있으며, 따라서 대상체의 크기에 상관없이 임의의 대상체에게 적합할 수 있다.
본 발명의 한 측면에서, 1일 경구 투여량은 총 화합물의 양을 체중 1 kg 당 약 0.0001 mg 이상 포함하며, 예시적으로는 체중 1 kg 당 약 0.0001 mg 내지 약 1000 mg, 약 0.001 mg 내지 약 100 mg, 약 0.01 mg 내지 약 10 mg, 약 0.1 mg 내지 약 5 mg, 또는 약 1 내지 약 3 mg 포함한다.
다른 측면에서, 1일 정맥내 주사량은 총 화합물의 양을 체중 1 kg 당 약 0.0001 mg 이상 포함하며, 예시적으로는 체중 1 kg 당 약 0.0001 mg 내지 약 0.5 mg, 약 0.001 mg 내지 약 0.25, 또는 약 0.01 내지 약 0.03 mg 포함한다.
예시적으로는, 경구 투여용 정제는 총 화합물의 양을 약 0.001 mg, 약 0.1 mg, 약 0.2 mg, 약 0.5 mg, 약 1 mg, 약 2 mg, 약 5 mg, 약 10 mg, 약 15 mg, 약 100 mg, 약 150 mg, 약 200 mg, 약 250 mg, 약 300 mg, 약 350 mg, 약 400 mg, 약 450 mg, 약 500 mg, 약 550 mg, 약 600 mg, 약 650 mg, 약 700 mg, 약 800 mg, 약 900 mg, 또는 약 1000 mg 포함하도록 제조될 수 있다.
한 측면에서, 조성물은 활성 성분 함량을 조성물 중량에 대해 약 0.01% 이상, 예시적으로는 조성물 중량에 대해 약 0.01% 내지 약 99%, 약 0.05% 내지 약 90%, 약 0.1% 내지 약 80%, 약 0.5% 내지 약 50% 포함한다. 다른 물질과 합해져 단일 투여량 형태를 생성할 수 있는 활성 성분의 양은 치료된 대상체 및 투여의 특정 방식에 따라 달라진다.
유효량의 약물은 1일 당 약 0.1 mg/체중 kg 내지 약 20 mg/체중 kg의 투여량 수준에서 통상적으로 공급된다. 한 측면에서, 범위는 1일 당 약 0.2 mg/체중 kg 내지 약 10 mg/체중 kg이다. 다른 측면에서, 범위는 1일 당 약 0.5 mg/체중 kg 내지 약 10 mg/체중 kg이다. 화합물은 1일 당 약 1 내지 약 10회의 처방 계획으로 투여될 수 있다.
본 발명의 화합물 및 다른 치료제의 공-투여 또는 순차적 투여에는, 예컨대 화학치료제, 면역억제제, 사이토카인, 세포독성제, 핵분해성 화합물, 방사활성 동위원소, 수용체, 및 자연적으로 발생하거나 재조합 방법에 의해 제조될 수 있는 프로-약물 활성 효소가 사용될 수 있다. 조합 투여에는 개별 제제 또는 단일 제약 제제를 사용한 공-투여, 및 각각의 순서에 따른 연속 투여가 포함되며, 여기서 바람직하게는 둘 다 (또는 모두) 활성 치료제가 동시에 그의 생물학적 활성을 강화시키는 기간이 있다. 본 발명은 본원에 기재된 특정 방법, 합성, 제제, 프로토콜, 세포주, 구성, 및 시약에 제한되지 않으며, 따라서 다양할 수 있음이 이해되어야 한다. 본원에 사용된 용어가 특정 측면만을 설명하기 위한 것이며, 본 발명의 범위를 제한하려는 것이 아님이 또한 이해되어야 한다. 본원에 언급된 모든 공개, 특허, 및 다른 문헌은, 예를 들어 이들 문헌에 기재된 구성 및 방법의 설명 및 개시를 위해 제공되며, 이는 본 발명과 연관되어 사용될 수 있다.
정의 및 용어
본원의 화학식에서 사용된 다양한 기호에 대해 정의된 기 뿐만 아니라 그러한 기에서 정의된 임의의 치환기는 다음과 같이 정의될 수 있다. 다르게 특정하지 않으면, 특정기에서 탄소 원자 수의 임의의 언급은 비치환된 "기본" 기를 나타내려는 것이며, 따라서 기본 기에서 언급된 임의의 치환기는 탄소 원자 수의 그 자체의 제한을 비롯하여 그 자체의 정의에 의해 설명된다. 다르게 특정하지 않으면, 제시된 구조의 모든 구조 이성질체, 예를 들어 모든 거울상이성질체, 부분입체이성질체, 및 결합위치이성질체는 이 정의 내에 포함된다.
용어 "할로겐" 또는 "할로"에는 불소, 염소, 브롬 또는 요오드가 포함된다.
용어 "알킬"기는 직선형 및 분지형 알킬기를 둘 다 나타내기 위해 사용된다. 알킬기의 예에는, 비제한적으로 메틸, 에틸, 프로필, 부틸, 펜틸, 헥실, 헵틸, 옥틸, 노닐 또는 데실 등이 포함된다. 다르게 특정하지 않으면, 알킬기는 1개 내지 12개의 탄소 원자를 갖는다. 또한 다르게 특정하지 않으면, 제시된 구조의 모든 구조 이성질체, 예를 들어 모든 거울상이성질체 및 모든 부분입체이성질체는 이 정의 내에 포함된다. 예를 들어, 다르게 특정하지 않으면, 용어 프로필은 n-프로필 및 이소-프로필을 포함하는 것을 의미하며, 용어 부틸은 n-부틸, 이소-부틸, t-부틸, sec-부틸 등을 포함하는 것을 의미한다.
용어 "아릴"은 6개 내지 14개의 탄소 원자로 이루어진 임의로 치환된 모노시클릭 또는 폴리시클릭 방향족 고리계를 나타낸다. 그러한 기의 예에는 페닐, 나프틸, 1,2,3,4-테트라히드로나프탈렌, 인단, 플루오렌 등이 포함된다. 다르게 특정하지 않으면, 아릴기는 전형적으로 6개 내지 14개의 탄소 원자를 갖는다.
"아르알킬"은 아릴 치환된 알킬기를 나타내며, 여기서 아릴기 및 알킬기는 본원에서와 같이 정의된다. 전형적으로, 아릴기는 6개 내지 14개의 탄소 원자를 가질 수 있으며, 알킬기는 10개 이하의 탄소 원자를 가질 수 있다. 아르알킬기의 예에는, 비제한적으로 벤질, 페닐에틸, 페닐프로필, 페닐부틸, 프로필-2-페닐에틸 등이 포함된다.
용어 "할로알킬"은 1개 이상의 할로겐 및 상기 정의된 바와 같은 알킬 부분을 함유하는 기를 나타내며, 즉 할로알킬은 하나 이상의 할로겐으로 치환된 알킬기이다. 다르게 특정하지 않으면, 주어진 구조의 모든 구조 이성질체, 예를 들어 모든 거울상이성질체 및 모든 입체이성질체는 이 정의 내에 포함된다. 할로알킬기의 예에는 플루오로메틸, 클로로메틸, 플루오로에틸, 클로로에틸, 트리플루오로메틸 등이 포함된다. 다르게 특정하지 않으면, 할로알킬기는 1개 내지 12개의 탄소 원자를 갖는다.
"시클로알킬"기는 모노 또는 폴리시클릭일 수 있는 시클릭 알킬기를 나타낸다. 시클로알킬기의 예에는 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헵틸, 시클로옥틸, 시클로노닐, 및 시클로데실이 포함된다. 다르게 특정하지 않으면, 시클로알킬기는 3개 내지 12개의 탄소 원자를 갖는다.
"알콕시"기는 -O(알킬)기를 나타내며, 여기서 알킬은 본원에 정의된 바와 같다. 따라서, 다르게 특정하지 않으면, 제시된 구조의 모든 이성질체는 정의 내에 포함된다. 알콕시기의 예에는 메톡시, 에톡시, n-프로폭시, 이소-프로폭시, n-부톡시, 이소-부톡시, t-부톡시 등이 포함된다. 다르게 특정하지 않으면, 알콕시기는 1개 내지 12개의 탄소 원자를 갖는다. 다르게 특정되지 않으면, 제시된 구조의 모든 구조 이성질체, 예를 들어 모든 거울상이성질체 및 모든 부분입체이성질체는 이 정의 내에 포함된다. 예를 들어, 다르게 특정하지 않으면, 용어 프로폭시는 n-프로폭시 및 이소-프로폭시를 포함하는 것을 의미한다.
"아릴옥시"기는 -O(아릴)기를 나타내고, 여기서 아릴은 본원에 정의된 바와 같다. 따라서, 아릴옥시기의 아릴 부분은 치환되거나 또는 비치환될 수 있다. 아릴옥시기의 예에는, 비제한적으로 페녹시, 나프틸 등이 포함된다. 다르게 특정하지 않으면, 아릴옥시기는 전형적으로 6개 내지 14개의 탄소 원자를 갖는다.
"할로알콕시"는 할로 치환기가 있는 알콕시기를 나타내며, 여기서 알콕시 및 할로기는 상기 정의된 바와 같다. 할로알콕시기의 예에는 플루오로메톡시, 클로로메톡시, 트리플루오로메톡시, 트리클로로에톡시, 플루오로에톡시, 클로로에톡시, 트리플루오로에톡시, 퍼플루오로에톡시 (-OCF2CF3), 트리플루오로-t-부톡시, 헥사플루오로-t-부톡시, 퍼플루오로-t-부톡시 (-OC(CF3)3) 등이 포함된다. 다르게 특정하지 않으면, 할로알콕시기는 전형적으로 1개 내지 12개의 탄소 원자를 갖는다.
"알킬티오"는 -S(알킬)기를 나타내며, 여기서 알킬기는 상기 정의된 바와 같다. 알킬티오기의 예에는 메틸티오, 에틸티오, 프로필티오, 부틸티오, 이소-프로필티오, 이소-부틸티오 등이 포함된다. 다르게 특정하지 않으면, 알킬티오기는 전형적으로 1개 내지 12개의 탄소 원자를 갖는다.
"헤테로아릴"은 -O-, >N-, -S-, >NH 또는 NR 등 (여기서 R은 본원에 정의된 바와 같은 치환되거나 또는 비치환된 알킬, 아릴 또는 아실임)으로부터 선택된 1개 이상의 헤테로원자 또는 헤테로기를 갖는 4개 내지 10개의 탄소 원자의 방향족 모노시클릭 또는 폴리시클릭 고리계이다. 이러한 측면에서, 헤테로원자 또는 헤테로기가 >N-일 수 있는 경우, >NH 또는 NR이 포함되는 것으로 고려된다. 헤테로아릴기의 예에는 피라지닐, 이소티아졸릴, 옥사졸릴, 피라졸릴, 피롤릴, 트리아졸릴, 테트라졸릴, 옥사트리아졸릴, 옥사디아졸릴, 피리다지닐, 티에노피리미딜, 푸라닐, 인돌릴, 이소인돌릴, 벤조[1,3]디옥솔릴, 1,3-벤즈옥사티올, 퀴나졸리닐, 이소퀴놀리닐, 퀴놀리닐, 피리딜, 1,2,3,4-테트라히드로-이소퀴놀리닐, 1,2,3,4-테트라히드로-퀴놀리닐 피리딜, 티오페닐 등이 포함된다. 다르게 특정하지 않으면, 헤테로아릴기 전형적으로 4개 내지 10개의 탄소 원자를 갖는다. 또한, 헤테로아릴기는 고리 탄소 원자에서 헤테로시클릭 코어 구조에 결합될 수 있거나, N-치환된 헤테로아릴, 예컨대 피롤에 적용가능한 경우, 전형적으로 탈양성자화된 헤테로원자를 통해 헤테로시클릭 코어 구조에 결합되어 직접 헤테로원자-피리미딘 고리 결합을 형성할 수 있다.
"헤테로시클릴"은 -O-, >N-, -S-, >NR, >SO2, >CO 등 (여기서, R은 수소 또는 본원에 정의된 바와 같은 치환되거나 또는 비치환된 알킬, 아릴 또는 아실임)으로부터 선택된 1개 이상의 헤테로원자 또는 헤테로기를 갖는 3원 내지 10원의 비-방향족, 포화 또는 불포화, 모노시클릭 또는 폴리시클릭 고리계이다. 헤테로시클릴기의 예에는 아지리디닐, 이미다졸리디닐, 2,5-디히드로-[1,2,4]옥사디아졸레닐, 옥사졸리디닐, 이속사졸리디닐, 피롤리디닐, 피페리디닐, 피페라지닐, 모르폴리닐, 티오모르폴리닐, 티아졸리디닐, 1,3-디옥솔라닐, 1,4-디옥사닐, 2,5-디히드로-1H-이미다졸릴 등이 포함된다. 다르게 특정하지 않으면, 헤테로시클릴기는 전형적으로 2개 내지 10개의 탄소 원자를 갖는다. 헤테로시클릴기는 전형적으로 탈양성자화된 헤테로원자를 통해 결합될 수 있거나, 또는 헤테로시클릴기는 헤테로시클릴기의 탄소 원자를 통해 결합될 수 있다.
"헤테로시클로알킬"은 -O-, >N-, -S-, >NR, >SO2, >CO 등 (여기서 R은 수소 또는 본원에 정의된 바와 같은 치환되거나 비치환된 알킬, 아릴 또는 아실임)으로부터 선택된 1개 이상의 헤테로원자 또는 헤테로기를 갖는 3원 내지 10원의 비-방향족, 포화 모노시클릭 또는 폴리시클릭 고리계인 헤테로시클릴의 포화 집단을 나타낸다. 헤테로시클로알킬기의 예에는 아지리디닐, 피페리디닐, 피페라지닐, 모르폴리닐, 티아졸리디닐, 1,3-디옥솔라닐, 1,4-디옥사닐 등이 포함된다. 다르게 특정하지 않으면, 헤테로시클로알킬기는 전형적으로 2개 내지 10개의 탄소 원자를 가지거나, 다른 측면에서는, 2개 내지 6개의 탄소 원자를 갖는다. 헤테로시클로알킬기는 전형적으로 탈양성자화된 헤테로원자를 통해 결합될 수 있거나, 또는 헤테로시클로알킬기는 헤테로시클로알킬기의 탄소 원자를 통해 결합될 수 있다.
"헤테로아릴옥시"기는 헤테로아릴기의 아릴옥시형 유사체를 나타낸다. 따라서, 헤테로아릴옥시기는 산소 원자와 결합하여 전형적인 [O-헤테로아릴] 잔기를 형성하는 본원에 정의된 바와 같은 헤테로아릴기를 설명하려는 것이다. 다르게 특정하지 않으면, 헤테로아릴옥시기는 전형적으로 4개 내지 10개의 탄소 원자를 포함한다.
모노시클릭 잔기 또는 비시클릭 잔기를 비롯한 "시클릭" 잔기는, 다르게 특정하지 않으면 본원에 개시된 모든 시클릭기, 예를 들어 헤테로아릴기, 헤테로시클릴기, 헤테로시클로알킬기, 및/또는 헤테로아릴옥시기를 포함하는 것으로 한다.
"알콕시카르보닐"기는 -C(O)O(알킬)기를 나타내고, 여기서 알콕시카르보닐기의 알킬 부분은 본원에서와 같이 정의된다. 알콕시카르보닐기의 예에는, 비제한적으로 메톡시카르보닐, 에톡시카르보닐, t-부톡시카르보닐 등이 포함된다.
"알케닐"기는 지방족 탄화수소기 내의 알켄 관능기의 위치화학에 상관없이, 알켄 관능기를 포함하는 지방족 탄화수소기이다. 다르게 특정하지 않으면, 알케닐기 전형적으로 2개 내지 12개의 탄소 원자를 가지며, 다른 측면에서는 C2-C10 알케닐기이다. 알케닐기의 예에는 모든 위치화학을 포함하는 에테닐, 프로페닐, 부테닐 등이 포함되며, 따라서 "부테닐"은 1-부테닐, 2-부테닐, 및 3-부테닐을 포함한다.
"알키닐"기는 지방족 탄화수소기 내의 알킨 관능기의 위치화학에 상관없이, 알킨 관능기를 포함하는 지방족 탄화수소기이다. 다르게 특정하지 않으면, 알키닐기는 전형적으로 2개 내지 12개의 탄소 원자를 가지며, 다른 측면에서는 C2-C10 알키닐기이다. 알키닐기의 예에는 모든 위치화학을 포함하는 에티닐, 프로피닐, 부티닐 등이 포함된다. 따라서, "부티닐"은 1-부티닐, 2-부티닐, 및 3-부티닐을 포함한다.
"알콕시알킬"기는 알콕시-치환된 알킬기이며, 여기서 알콕시기 및 알킬기는 본원에서와 같이 정의된다. 다르게 특정하지 않으면, 알콕시알킬기는 전형적으로 2개 내지 20개의 탄소 원자를 갖는다. 한 측면에서, 알콕시알킬기는 (C1-C10) 알킬기에 결합된 (C1-C10) 알콕시기일 수 있으며, 여기서 알콕시 및 알킬기는 본원에 정의된 바와 같으며, 모든 입체화학 및 모든 위치화학을 포함한다. 알콕시알킬기의 예에는 메톡시메틸, 메톡시에틸, 메톡시프로필, 에톡시메틸, 에톡시에틸, 메톡시이소프로필, 에톡시이소부틸 등이 포함된다.
본원에 사용된 "아미노알킬"기는 아미노-치환된 알킬기를 나타내고, 여기서 알킬은 본원에서와 같이 정의된다. 다르게 특정하지 않으면, 아미노알킬기는 전형적으로 1개 내지 12개의 탄소 원자를 가지므로, 전형적인 아미노알킬기는 모든 위치화학을 포함하는 아미노 (C1-C12) 알킬일 수 있다. 아미노알킬기의 예에는, 비제한적으로 아미노메틸, 아미노에틸, 아미노프로필 등이 포함된다.
"시클로알킬-치환된 알킬"기는 또한 "시클로알킬알킬"기로도 지칭되며, 시클로알킬 치환기로 치환된 알킬기를 나타내고, 여기서 알킬 및 시클로알킬은 본원에서와 같이 정의된다. 따라서, 시클로알킬기 부분은 모노 또는 폴리시클릭 알킬기일 수 있다. 다르게 특정하지 않으면, 시클로알킬알킬기는 탄소 원자가 알킬 부분과 시클로알킬 부분 사이에 어떻게 분포하는지 상관없이, 20개 이하의 탄소 원자를 가질 수 있으며, 가능한 모든 입체화학 및 모든 위치화학을 포함한다. 예를 들어, 한 측면에서, 시클로알킬-치환된 알킬은 C1-C10 알킬기에 결합된 (C3-C10) 시클로알킬을 포함할 수 있으며, 여기서 시클로알킬 부분은 모노 또는 폴리시클릭일 수 있다. 시클로알킬알킬기의 예에는, 비제한적으로 시클로프로필메틸, 시클로프로필에틸, 시클로프로필프로필, 시클로부틸메틸, 시클로부틸에틸, 시클로부틸프로필, 시클로펜틸메틸, 시클로펜틸에틸, 시클로펜틸프로필, 시클로헥실메틸, 시클로헥실에틸, 시클로헥실프로필, 시클로헵틸메틸, 시클로헵틸에틸, 시클로옥틸메틸, 시클로옥틸에틸, 시클로옥틸프로필 등이 포함된다.
"시클로알콕시"기는 또한 "시클로알킬옥시"기로 지칭될 수 있으며, 본원에서 -O(시클로알킬) 치환기, 즉 시클로알킬기를 포함하는 알콕시드형 잔기를 나타내며 , 여기서 시클로알킬은 본원에서와 같이 정의된다. 따라서, 시클로알킬기 부분은 모노 또는 폴리시클릭 알킬기일 수 있으며, 다르게 특정하지 않으면, 시클로알킬알킬기는 20개 이하의 탄소 원자를 가질 수 있다. 한 측면에서, 시클로알콕시기는 (C3-C10) 시클로알킬-O-기일 수 있다. 시클로알콕시기의 예에는 시클로프로폭시, 시클로부톡시, 시클로펜톡시, 시클로헥속시 등이 포함된다.
"아실"기는 (C1-C10)알킬-CO-기를 나타내며, 여기서 (C1-C10)알킬기는 CO기, 및 다른 화학적 기 둘 다에 결합된 알킬-링커 잔기를 나타내기 위해 이러한 구조에서 사용된다. 아실기의 예에는, 비제한적으로 메틸카르보닐, 에틸카르보닐, 프로필카르보닐, 이소프로필카르보닐 등이 포함된다.
"알케닐렌"기는 C2-C10 쇄 내에서 1개 이상의 C=C 이중 결합을 포함하는 (C2-C10) 탄화수소 링커를 나타낸다. 알케닐렌기의 예에는, 비제한적으로 -CH=CH-, -CH2-CH=CH, -CH2-CH=CH-CH2-, -CH2-CH=CH-CH=CH- 등이 포함된다. 따라서, 다르게 특정하지 않으면, 알케닐렌기는 2개 내지 10개의 탄소 원자를 갖는다.
"할로알콕시알킬"기는 할로알킬-O-(C1-C10)알킬기, 즉 할로알콕시-치환된 알킬기를 나타내며, 여기서 할로알콕시 및 알킬은 본원에서와 같이 정의된다. 다르게 특정하지 않으면, 시클로알킬알킬기는 기의 할로알콕시 부분과 알킬 부분 사이에 탄소 원자가 어떻게 분포하든지 관계없이, 20개 이하의 탄소 원자를 가질 수 있으며, 가능한 모든 입체화학 및 모든 위치화학을 포함한다. 한 측면에서, 예를 들어 할로알콕시알킬은 할로알킬-O-(C1-C10)알킬이며, 여기서 기는 (C1-C10) 알킬 잔기에 결합된 (C1-C10) 할로알킬기일 수 있다. 할로알콕시알킬기의 예에는 트리플루오로메톡시메틸, 클로로메톡시에틸, 플루오로메톡시에틸, 클로로에톡시에틸, 트리플루오로메톡시프로필, 헥사플루오로에톡시에틸 등이 포함된다.
"모노알킬아미노"기는 단일 알킬기로 치환된 아미노기, 즉, 모노(C1-C20)알킬아미노기를 나타낸다. 다르게 특정하지 않으면, 모노알킬아미노기는 20개 이하의 탄소 원자를 가질 수 있다. 한 측면에서, 모노알킬아미노기는 (C1-C10)알킬-치환된 아미노기일 수 있다. 모노알킬아미노기의 예에는 메틸아미노, 에틸아미노, 프로필아미노, 이소프로필아미노 등이 포함된다.
"디알킬아미노"기는 2개의 독립적으로-선택된 알킬기로 치환된 아미노기, 즉, 디(C1-C10)알킬아미노기를 나타낸다. 다르게 특정하지 않으면, 디알킬아미노기는 20개 이하의 탄소 원자를 갖는다. 디알킬아미노기의 예에는 디메틸아미노, 디에틸아미노 등이 포함된다.
추가로, 명세서에 사용된 특정 추가 용어 및 어구의 의미는 하기와 같이 정의될 수 있다.
본원에 사용된, 용어 "화합물"에는 단수 및 복수가 모두 포함되고, 적어도 본원에 개시된 효과를 갖는 임의의 단일 물질 또는 합한 물질, 및 그러한 물질의 조합, 단편, 유사체 또는 유도체도 포함된다.
본원에 사용된, 용어 "물질"은 특정 종류 또는 구성의 임의의 물질을 광범위하게 나타낸다. "물질"의 예에는, 비제한적으로 화학적 요소, 분자, 화합물, 혼합물, 조성물, 에멀젼, 화학요법제, 약리학적 제제, 호르몬, 항체, 성장 인자, 세포 인자, 핵산, 단백질, 펩티드, 펩티드모방체, 뉴클레오티드, 탄수화물, 및 그러한 물질의 조합, 단편, 유사체 또는 유도체가 포함될 수 있다.
용어 "치료", "치료하는", "치료하다" 등은 일반적으로 임의의 방법, 적용, 요법 등을 나타내기 위해 본원에서 사용되며, 여기서 포유동물은 포유동물의 증상 또는 질환을 직접 또는 간접으로 개선하기에 바람직한 약리학적 및/또는 생리학적 효과를 얻기를 원하는 의학적 관점의 대상체이다. 효과는 질환에 기인하는 질환 및/또는 역효과를 부분적으로 또는 완전히 안정화하거나 또는 치료한다는 관점에서 치료적일 수 있다. 효과는 또한, 예를 들어 질환 징후의 억제 (즉, 그의 발달을 저지함) 또는 질환 징후 완화 (즉, 질환 또는 징후의 퇴행 야기)를 포함할 수 있다.
본원에 사용된 용어 "치료 유효량"은 포유동물, 계, 조직 또는 세포에서 필요한 생물학적 또는 의학적 효과를 나타내기에 충분한 본원에 개시된 하나 이상의 화합물, 또는 그의 제약상 허용되는 염의 양을 나타낸다.
용어 "예방하는", "예방하다", "예방" 등은 일반적으로 임의의 방법, 적용, 요법 등을 나타내기 위해 본원에 사용되며, 여기서 포유동물은 임상적으로 명백한 증상 또는 질환의 발병을 예방하거나, 또는 증상 또는 질환의 임상전 명백한 병기의 발병을 예방하기 위한 바람직한 약리학적 및/또는 생리학적 효과를 얻으려는 목적을 가진 의학적 관점의 대상체이다. 효과는 증상 또는 질환 또는 그의 징후의 발생 위험을 완전히 또는 부분적으로 예방하거나 감소시키는 관점에서 예방될 수 있다.
본원에 사용된 용어 "예방 유효량"은 세포, 조직, 계 또는 포유동물에서 예방하고자 하는 생물학적 또는 의학적 효과의 발생 위험을 예방하거나 감소시키는 약물 또는 제약 제제의 양을 나타낸다.
본원에 사용된, 용어 "활성화"는 신호전달 경로 또는 생물학적 반응의 임의의 변화, 예를 들어 상기 기저 수준, 억제된 상태에서 기저 수준의 회복, 및 상기 기저 수준 경로의 자극을 증가시키는 것을 나타낸다.
일반적으로 당업자는 모든 안정한 분자에 대해 원자가가 보존되어야 한다는 것을 인지한다. 따라서, 다르게 표현적으로 지시되지 않는 한, 화학식 I을 비롯한 모든 구조에서 원자가를 채우기 위해 수소 원자가 필요하며 사용될 수 있다는 것이 필요적으로 함축되어 있다.
본원에 언급된 공개물 및 특허는, 예를 들어 본 발명과 관련하여 이용될 수 있는 공개물 및 특허에 제공된 구성 및 방법을 설명하기 위해 개시된다. 본원의 발명자들이 선행 발명에 의한 그러한 공개물, 특허, 또는 다른 개시물로 인해 선행할 자격이 없다는 것으로 해석되면 안된다.
본원에 참고로 포함되는 임의의 문서에서 제시된 임의의 정의 또는 용도가 본원에 제공된 정의 또는 용도와 대립되지 않는 한, 본원에 제공된 정의 또는 용도로 쓰인다.
본 출원인이 임의의 유형의 범위, 예를 들어 온도 범위, 원자 수의 범위, 몰비 등을 개시하거나 청구하는 경우, 출원인의 의도는 그러한 범위가 합리적으로 포함할 수 있는 각각의 가능한 수 뿐만 아니라, 거기에 포함되는 임의의 하위 범위 및 하위 범위의 조합을 개별적으로 개시하거나 청구하는 것이다. 예를 들어, 출원인이 특정 수의 탄소 원자를 갖는 화학 잔기를 개시하거나 청구하는 경우, 출원인의 의도는 본원에 개시된 바와 상응하게 그러한 범위를 포함할 수 있는 가능한 모든 수를 개별적으로 개시하거나 청구하는 것이다. 예를 들어, R이 12개 이하의 탄소 원자를 갖는 알킬기, 또는 본원에 사용된 대체적 표현인 C1 내지 C12 알킬기로부터 독립적으로 선택된 것이라는 기재사항은 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 또는 12개의 탄소 원자를 갖는 히드로카르빌기, 뿐만 아니라 이들 두 수 사이의 임의의 범위를 갖는 히드로카르빌기, 예를 들어 C3 내지 C8 알킬기, 및 또한 C3 내지 C5 및 C7 내지 C10 히드로카르빌기와 같이, 이들 두 수 사이의 범위의 임의의 조합물을 갖는 히드로카르빌기로부터 독립적으로 선택된 R기를 나타낸다. 다른 실시예에서, 기재사항에 의해 몰비는 전형적으로 약 0.1 내지 약 1.1의 범위를 가지며, 출원인은 몰비가 약 0.1:1, 약 0.2:1, 약 0.3:1, 약 0.4:1, 약 0.5:1, 약 0.6:1, 약 0.7:1, 약 0.8:1, 약 0.9:1, 약 1.0:1, 또는 약 1.1:1로부터 선택될 수 있다고 언급하려는 것이다.
임의의 이유로 출원인이, 예를 들어 출원 시기에서 인지할 수 있는 문헌을 설명하기 위해 개시물의 충분한 척도 미만으로 청구하는 것을 선택하는 경우, 출원인은 단서에 대한 권리를 남겨두거나, 범위에 따라 또는 임의의 유사한 방식으로 청구될 수 있는, 기 내의 임의의 하위 범위 또는 하위 범위의 조합을 비롯한 임의의 그러한 기의 임의의 개별적 구성원을 배제하였다. 추가로, 임의의 이유로 출원인이, 예를 들어 출원인이 출원 시기에 인지할 수 있는 문헌을 설명하기 위해 개시물의 충분한 척도 미만으로 청구하는 것을 선택하는 경우, 출원인은 단서에 대한 권리를 남겨두거나, 임의의 개별적 치환기, 화합물, 리간드, 구조, 또는 그의 기, 또는 청구된 기의 임의의 구성원을 배제하였다.
하기 문헌은 특정 헤테로시클릭 화합물을 개시하고 있다.
| 헤테로시클릭 화합물을 개시한 문헌 | |
| 공개물 또는 특허 번호 | 제목 |
| WO2005097806 | 콜레스테롤 에스테르 수송 단백질의 억제제로서의 헤테로시클릭 피페리딘 유도체의 제조법 |
| WO2005095395 | 콜레스테릴 에스테르 수송 단백질의 억제제로서의 1,2,3,4-테트라히드로-1,5-나프티리딘-4-아민의 제조법 |
| WO2005095409 | 콜레스테릴 에스테르 수송 단백질의 억제제로서의 1,2,3,4-테트라히드로퀴놀린-4-아민의 제조법 |
| WO2005030185 | 잔여 지단백질 생성 억제를 위한 콜레스테릴 에스테르 수송 단백질 (CETP) 억제제의 사용 방법 |
| US2004039018 | 심장혈관 질환의 치료를 위한 콜레스테릴 에스테르 수송 단백질 (CETP) 억제제 및 항고혈압제 및 임의의 HMG-CoA 환원효소 억제제의 용도 |
| WO2000017165 | CETP 억제제로서의 4-아미노-치환된 2-치환된 1,2,3,4-테트라히드로퀴놀린의 제조법 |
| US2004053842 | 콜레스테롤 에스테르 수송 단백질 (CETP) 억제제 및 임의의 HMG-CoA 환원효소 억제제 및/또는 항고혈압제의 치료적 용도 및 제약 조성물 |
| WO2003000295 | 콜레스테릴 에스테르 수송 단백질 억제제 및 계면활성제의 자가-유화 제제 |
| WO2002011710 | 콜레스테릴 에스테르 수송 단백질 억제제의 제약 조성물 |
| US2003198674 | 콜레스테릴 에스테르 수송 단백질 억제제를 함유하는 제어된 방출 투여 형태 |
| WO2003063832 | CETP 억제제의 고체 무형 분산액을 포함하는 제약 조성물 |
| US2003104063 | 매트릭스 중 난용성 약물의 고체 분산액 및 용해도-증강 중합체를 함유하는 함유하는 제약 조성물 |
| US2003054037 | 무형 약물의 흡착제의 제약 조성물 |
| US2003170309 | 중합체 및 약물 조합을 함유하는 제약 조성물 |
| US2003072801 | 농도-증강 중합체를 포함하는 제약 조성물 |
| US2004185102 | CETP 억제제 및 HMG-CoA 환원효소 억제제를 포함하는 투여 형태 |
| WO2005000811 | 모노아민 수용의 억제제로서의 3-아미노피롤리딘의 제조법 |
| US2005049239 | 2형 글리신 수송체 (GlyT2)의 선택적 억제제로서의 아로일피페리딘 및 관련된 화합물의 제조법 |
| WO2005021525 | 2형 글리신 수송체 (GlyT2)의 선택적 억제제로서의 아로일피페리딘 및 관련된 화합물의 제조법 |
| WO2004078169 | 폐고혈압 및 다른 질환의 의학적 치료에서의 EP2 선택적 수용체 효능제의 용도 |
| WO2004078128 | 암 및 다른 질환의 치료에 유용한 피리딘-함유 디아릴 우레아의 제조법 |
| WO2004073709 | 항균제로서의 3급 아미노 화합물의 제조법 |
| WO2003087088 | 효소 Lp-PLA2의 억제제로서의 피리돈 및 피리미돈 화합물의 제조법 |
| WO2003030909 | 암의 치료에서 키나제 억제제로서 사용하기 위한 비시클릭 고리에 의해 N-치환된 2- 및 4-아미노피리미딘의 제조법 |
| WO2002090349 | VEGFR II 키나제의 억제제로서의 피리딜메틸안트라닐아미드 N-옥시드 |
| WO2002070462 | 심장혈관 질환의 치료를 위한 아미노디카르복실산의 제조법 |
| WO2002068417 | 헤테로폴리시클릭 화합물, 특히 피리딜- 및 페닐-치환된 1,2,4-옥사디아졸 및 유사체, 및 신경 손상을 억제하기 위한 대사성 글루타메이트 수용체 효능제로서의 그의 용도 |
| WO2002042273 | 세린 프로테아제 억제제로 유용한 방향족 산 유도체의 제조법 |
| WO2002022584 | 트롬빈 억제제로서의 치환된 헤테로시클릭 아릴-알킬-아릴 화합물의 제조법 |
| WO2001085671 | 혈관 내피 성장인자 수용체의 억제제로서의 (헤테로시클릴)안트라닐아미드의 제조법 |
| WO2001060458 | 항암 용도를 위한 프레닐-단백질 트랜스퍼라제의 피레라진 억제제 |
| WO2001060369 | 항암 요법용 프레닐-단백질 트랜스퍼라제의 피페라진 억제제 |
| WO2001056560 | 중성형 스핑고미엘리나제 억제제로서의 치환된 아미노산의 제조법 |
| WO2001022954 | 치료적으로 가치있는 특성을 포함하는 인돌릴-3-글리옥실산 유도체 |
| WO2001000623 | 니트로구아니딘 및 니트로엔아민 유도체의 제조 방법 |
| JP2001163779 | 남성의 발기 장애의 치료를 위한 프로스타글란딘 수용체 효능제 및 전구약물 |
| EP1108426 | 남성의 발기 장애의 치료를 위한 프로스타글란딘 수용체 효능제 및 전구약물 |
| DE19962300 | 항암제로서의 N-(피리딘-4-일)[1-(4-아미노벤질)인돌-3-일]글리옥실아미드의 제조법 |
| US2001014690 | 항암제로서의 N-(피리딘-4-일)[1-(4-아미노벤질)인돌-3-일]글리옥실아미드의 제조법 |
| US6432987 | 항암제로서의 N-(피리딘-4-일)[1-(4-아미노벤질)인돌-3-일]글리옥실아미드의 제조법 |
| CA2395259 | 항암제로서의 N-(피리딘-4-일)[1-(4-아미노벤질)인돌-3-일]글리옥실아미드의 제조법 |
| WO2001047913 | 항암제로서의 N-(피리딘-4-일)[1-(4-아미노벤질)인돌-3-일]글리옥실아미드의 제조법 |
| DE19930075 | 항바이러스제로서의 아미노아릴술폰아미드의 제조법 |
| WO2001002350 | 항바이러스제로서의 아미노아릴술폰아미드의 제조법 |
| WO2000050398 | NK-1 수용체 길항제로서 페닐 및 피리디닐 유도체의 제조법 |
| US6121271 | 인슐린 내성 또는 고혈당과 관련된 대사성 장애의 치료를 위한 나프토[2,3-b]헤테로아르-4-일 유도체의 제조법 |
| DE19845202 | 모발 성장 촉진제 |
| WO2000019969 | 모발 성장 촉진제 |
| WO9951224 | 항암제로서의 인돌릴글리옥실아미드의 제조법 |
| WO9919300 | 골 장애 치료를 위한 프로스타글란딘 효능제의 제조법 및 그의 용도 |
| US6008362 | 2-(4-클로로-1-아릴-부틸리덴)-히드라진카르보티오아미드에 의한 HDL 콜레스테롤의 상승 |
| US5977170 | HDL 콜레스테롤의 상승제로서의 4-[(아미노티옥소메틸)히드라조노]-4-아릴부틸 카르바메이트의 제조법 |
| JP11209366 | 심장 질환의 치료를 위한 크로만 및 약제의 제조법 |
| WO9857928 | 2-(4-클로로-1-아릴-부틸리덴)히드라진카르보티오아미드에 의한 HDL 콜레스테롤의 상승 |
| WO9857927 | 4-[(아미노티옥소메틸)히드라조노]-4-아릴부틸 카르바메이트에 의한 HDL 콜레스테롤의 상승 |
| WO9857925 | 2-[(아미노티옥소메틸)히드라조노]-4-아릴에틸 카르바메이트에 의한 HDL 콜레스테롤의 상승 |
| WO9827053 | 약물로서의 술폰아미드 및 카르복스아미드 유도체의 제조법 |
| WO9809946 | 항천식제, 항알러지제 및 면역억제제/면역조절제로서의 신규 N-치환된 인돌-3-글리옥실아미드의 제조법 |
| DE19615262 | 항아테롬성동맥경화증제로서의 페닐글리시놀 아미드 |
| EP802188 | 항아테롬성동맥경화증제로서의 페닐글리시놀 아미드 |
| WO9616650 | 2-아미노티아졸 유도체 및 그의 염을 포함하는 항균제 또는 살균제 |
| US5491152 | 아테롬성동맥경화증의 치료를 위한 시클릭 에테르 및 술피드의 ACAT-억제 유도체 |
| JP08092225 | 제초제로서의 O-(1,2,4-트리아졸-5-일)글리콜아미드 유도체의 제조법 |
| JP08092224 | 살충제 및 살비제로서의 3,5-디페닐-1,2,4-트리아졸 유도체의 제조법 |
| WO9505363 | 산화질소 합성효소 활성을 갖는 아미딘 유도체 |
| US5422355 | GABA 자가수용체 효능제로서의 항우울증제 (아릴알킬)아민 |
| DD294706 | GABA 자가수용체 효능제로서의 항우울증제 (아릴알킬)아민 |
| US5086073 | GABA 자가수용체 효능제로서의 항우울증제 (아릴알킬)아민 |
| US5260331 | GABA 자가수용체 효능제로서의 항우울증제 (아릴알킬)아민 |
| JP07285962 | 제초제로서의 (피리딜옥시)피라졸 유도체의 제조법 |
| WO9413636 | 엘라스타제 억제제로서의 N-카르바모일-2-[(아미노알킬)카르바모일알콕시]아제티디논 및 유사체의 제조법 |
| US5348953 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| CN1068815 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| ZA9204659 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| AU9218582 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| AU660026 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| WO9413636 | 소염제 및 항변제로서의 아제티디논의 제조법 |
| EP604798 | 살충제 및 살비제로서의 N-아릴히드라진 유도체 |
| EP585500 | 항무스카린제로서의 디아릴 피페라진아세트아미드 |
| WO9405648 | 항무스카린제로서의 디아릴 피페라진아세트아미드 |
| WO9310099 | 농약으로서의 피라졸글리콜아미드 유도체 |
| EP553016 | 나프탈렌 아미드 및 술폰아미드의 제조법, 그의 제약 제제, 및 세로토닌성 수용체에 대한 그의 친화도 |
| JP01104052 | 류코트리엔 길항제 및 혈관확장제로서의 피리딘 유도체의 제조법 |
출원인은 단서에 대한 권리를 남겨두거나, 현재 나타낸 임의의 청구항, 또는 본원에 개시된 임의의 속 또는 아속, 본원에 제공된 임의의 문헌을 비롯한 임의의 문헌에 개시된 임의의 화합물 또는 화합물의 군을 제시한 청구항을 비롯하여, 본원 또는 본원에 기초한 임의의 추가적 출원에서 나타낼 수 있는 임의의 청구항으로부터 제한한다.
하기 두문자어, 약어, 용어 및 정의가 본원에서 사용되었다. 하기 두문자어, 약어, 용어 및 정의는 실험 섹션에서 사용되었다. 두문자어 및 약어: THF (테트라히드로푸란), DMF (N,N-디메틸포름아미드), IPA (이소-프로판올), TBAB (테트라-n-부틸암모늄 브로마이드), DCM (디클로로메탄), DCE (디클로로에탄), EDCI [1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 히드로클로라이드], DIBAL (디이소부틸 알루미늄 히드라이드), TBAB (테트라부틸암모늄 브로마이드), LAH (수소화리튬알루미늄), g 또는 gm (그램), L (리터), mL (미리리터), mp (융점), rt 또는 RT (실온), aq (수성), min (분), h 또는 hr (시간), atm (대기), conc. (진한), MS 또는 mass spec (질량 분광기/분석기), NMR (핵 자기 공명), IR (적외선 분광기), RB (둥근 바닥), RBF (둥근 바닥 플라스크). 이들 약어 이외에, 화학 잔기에 대한 표준 화학 약어, 메틸은 예컨대 Me, 에틸은 Et 등이 전반에 사용되었다. NMR 약어: br (광범위), apt (분명한), s (단일선), d (이중선), t (삼중선), q (사중선), dq (사중선의 이중선), dd (이중선의 이중선), dt (삼중선의 이중선), m (다중선).
일반적인 합성 절차.
실온은 주변 온도 범위, 전형적으로 약 20℃ 내지 약 35℃로 정의된다. 빙조 (분쇄한 얼음 및 물) 온도는 전형적으로 약 -5℃ 내지 약 0℃의 범위로 정의된다. 환류 온도는 1차 반응 용매의 비점보다 15℃ 높거나 낮은 온도로 정의한다. 밤새는 약 8 내지 약 16시간의 시간 범위로 정의한다. 진공 여과 (물 흡입기)는 전형적으로 약 5 mm Hg 내지 약 15 mm Hg의 압력 범위에 걸쳐 일어나는 것으로 정의한다. 진공 하의 건조는 전형적으로 약 0.1 mm Hg 내지 약 5 mm Hg의 압력 범위에서 고진공 펌프를 사용하는 것으로 정의한다. 중화는 전형적인 산-기재 중화 방법으로 정의되고, pH-지시 종이를 사용하여 약 pH 6 내지 약 pH 8의 pH 범위로 측정된다. 염수는 포화 수성 염화나트륨으로 정의된다. 질소 대기는 오일 발포 시스템으로 드리에리트 (상표명; Drierite) 칼럼을 통과한 질소 기체의 양성 정압으로 정의된다. 농축된 수산화암모늄은 대략 15 M 용액으로 정의된다. 융점은 수은 온도계로 측정하였으며 수정하지 않았다.
칼럼 또는 박층 크로마토그래피에 대한 모든 용리액은 부피:부피 (v:v) 용액으로 제조되고 보고되었다. 용매, 시약, 및 후처리 반응 또는 생성물 단리를 위해 사용된 용매 및/또는 시약의 양은 유기 화학 합성에 관한 당업자에게 전형적으로 이용될 것일 수 있으며, 단리될 특정 반응물 또는 생성물에 대해 결정될 것이다. 예를 들어: 1) 분쇄한 얼음 양은 반응 규모에 따라 전형적으로 약 10 g 내지 약 1000 g의 범위이고; 2) 칼럼 크로마토그래피에 사용된 실리카겔 양은 물질의 양, 혼합물의 복합성, 및 사용된 크로마토그래피 칼럼의 크기에 따라 달라지며, 전형적으로 약 5 g 내지 약 1000 g의 범위이고; 3) 추출 용매 부피는 반응 규모에 따라 전형적으로 약 10 mL 내지 약 500 mL의 범위이고; 4) 화합물 단리에 사용된 세척액은 반응 규모에 따라 용매 또는 수성 시약의 약 10 mL 내지 약 100 mL의 범위이고; 5) 건조 시약 (탄산칼륨, 탄산나트륨 또는 황산마그네슘)은 건조될 용매의 양 및 그의 물 함량에 따라 약 5 g 내지 약 100 g의 범위이다.
분광기 및 다른 장치적 절차
NMR . 본원에 기재된 1H 스펙트럼은 바리안 게미니 (Varian Gemini) 200 MHz 분광계를 사용하여 얻었다. 특정 샘플에 대해 사용된 분광계 필드 강도 및 NMR 용매는 실시예, 또는 도로서 제시된 임의의 NMR 스펙트럼에 나타나있다. 전형적으로, 1H NMR 화학적 이동은 내부 표준인 테트라메틸실란 (TMS) (d = 0 ppm)으로부터 다운필드된 ppm (parts per million) 단위의 d값으로 보고하였다. 고체 또는 액체 샘플은 NMR 샘플 튜브에 든 적합한 NMR 용매 (전형적으로 CDCl3 또는 DMSO-d6)에 용해시키고, 데이터는 분광계 지시 매뉴얼에 따라 수집하였다. 대부분의 샘플은 가변성 온도 방식으로, 전형적으로 약 55℃에서 분석하였으나, 특정 샘플에 대한 특정 데이터는 주변 프로브 온도에서 프로브로 수집하였다. NMR 데이터는 바리안, VNMR 6.1 G 버젼으로 제공된 소프트웨어를 이용하여 처리하였다.
본 발명은 추가로 하기 실시예에 의해 예시되고, 이는 본원의 범위를 제한하려는 어떠한 방식으로도 이해되어서는 안 되며, 단지 예시하기 위한 것이다. 대조적으로, 그러한 분류가 다양한 다른 실시양태, 그의 변형 및 동등물을 가질 수 있으며, 본원의 명세서를 읽은 후에 이는 본 발명의 범위를 벗어나지 않으면서 당업자에게 그 자체로 제안될 수 있음이 명백하게 이해될 것이다. 따라서, 당업자는 어떻게 실험 및 실시예가 하기 실시예, 치환기, 시약, 또는 조건을 다양하게 변화시킴으로써 개시된 바와 같이 추가로 수행될 수 있는지 인지할 것이다. 하기 실시예에서, 온도, 압력, 시간, 중량, 백분율, 농도, 범위, 화학적 이동, 주파수, 몰비 등을 비롯한 임의의 측정의 기재에서, 그러한 측정치는 각각 "대략"인 것으로 이해되어야 한다.
실시예
1
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
단계 (i): 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드의 합성
아세트산 무수물 (6.62 mL, 70 mmol) 및 2,5-디메틸-2H-피라졸-3-일아민 (5.0 g, 45 mmol)의 혼합물을 4시간 동안 90 내지 100℃에서 교반하면서 가열하였다. 진공에서 휘발물질을 증발시킨 후, 옥시염화인 (18.5 mL, 200 mmol)을 첨가하고, 혼합물을 3시간 동안 90 내지 95℃에서 교반하면서 가열하였다. 그 후, 혼합물의 내부 온도를 90 내지 95℃로 유지하면서 무수 DMF (9.2 mL, 120 mmol)를 30분에 걸쳐 서서히 첨가하였다. 추가 2시간 동안 교반한 후, 반응 혼합물을 실온으로 냉각시키고, 분쇄한 얼음 (100 내지 120 g)에 부었다. 침전된 고체를 여과하고, 물로 세척하고, 진공에서 건조시켰다. 황색빛 고체 생성물을 후속적으로 메틸렌 클로라이드 (100 mL)에 용해시키고, 물로 세척하고, 황산나트륨 상에서 건조시키 고, 용매를 진공에서 증발시켜 원하는 생성물을 밝은 황색 고체로 수득하였다 (4.1 g), 수율: 44%, 융점: 152-153℃.
단계 ( ii ): 시클로부틸메틸-에틸-아민의 합성
시클로부탄카르보닐 클로라이드 (4.0 mL, 35 mmol)를 0 내지 5℃에서 질소 하에 무수 메틸렌 클로라이드 (25 mL) 중 에틸아민 [20 mL, 테트라히드로푸란 (THF) 중 2 M 용액] 및 트리에틸아민 (4.85 mL, 35 mmol)의 빙냉 용액에 서서히 첨가하였다. 20분 동안 교반한 후, 혼합물을 20 내지 25℃로 가온하고, 추가 5 내지 7시간 동안 교반하였다. 반응물을 5 내지 10% 수성 중탄산나트륨에 부어서 반응을 켄칭시켰다. 유기층을 분리하고, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 증발시켜 시클로부탄카르복실산 에틸아미드를 연한 황색 액체로 수득하고, 이를 실온에서 정치시켜 고체화하였다.
그 후, 수소화리튬알루미늄 (30 mL, THF 중 2 M 용액)을 질소 대기 하에 무수 THF (10 mL) 중 시클로부탄카르복실산 에틸아미드 (4.45 g, 35 mmol)의 용액에 서서히 첨가하였다. 20℃에서 1시간 동안 교반한 후, 반응물을 3시간 동안 온화하게 환류시켰다. 실온으로 냉각시킨 후, 1 N 수성 수산화나트륨으로 반응을 켄칭시키고, 여과하고, 침전물을 디에틸 에테르로 세척하였다. 합한 여과액을 농축시켜 시클로부틸메틸-에틸-아민을 무색 액체 (2.0 g)로 수득하였다, 수율: 50%.
단계 ( iii ): 6-(시클로부틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드의 합성
탄산칼륨 (0.83 g, 6 mmol)을 질소 하에서 무수 DMF (8 mL) 중 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (1.04 g, 5.0 mmol) 및 시클로부틸메틸-에틸-아민 (0.8 g, 7.0 mmol)의 용액에 첨가하였다. 0.5시간 동안 실온에서 교반한 후, 반응 혼합물을 14시간 동안 80℃에서 가열하였다. 그 후, 반응물을 실온으로 냉각시키고, 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 첨가하고, 유기층을 수성 혼합물로부터 분리하였다. 유기 추출물을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공에서 증발시켰다. 잔류물을 실리카겔 (200-400 메쉬)을 사용하고, 20 내지 60% 헥산:에틸 아세테이트로 용리한 크로마토그래피에 의해 정제하여 표제 화합물을 연한 황색 액체로 수득하였다 (1.23 g), 수율: 87%.
단계 ( iv ): {5-[3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-시클로부틸메틸-에틸-아민의 합성
무수 MeOH (5.0 mL) 중 6-(시클로부틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (0.38 g, 1.3 mmol) 및 비스-트리플루오로메틸-벤질아민 (0.32 g, 1.3 mmol)의 용액에 빙초산 (0.2 mL)을 첨가하고, 생성된 혼합물을 20분 동안 실온에서 교반하였다. 나트륨 시아노보로히드라이드 (0.245 g, 4 mmol)를 서서히 첨가하고, 반응물을 밤새 실온에서 교반하였다. 휘발물질을 진공에서 증발시킨 후, 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 잔류물에 첨가하고, 유기층을 분리되도록 두었다. 유기층을 수집하고, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공에서 증발시켰다. 잔류물을 실리카겔 (200-400 메쉬)을 사용하고, 1 내지 5% CH2Cl2:Me0H로 용리한 크로마토그래피로 정제하여 표제 화합물을 무색 액체로 수득하였다 (0.265 g), 수율: 40%.
단계 (v): (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
무수 탄산칼륨 (0.138 g, 1 mmol)을 실온에서 무수 MeOH 중 {5-[3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-시클로부틸메틸-에틸-아민 (0.25 g, 0.49 mmol) 및 브롬화시아노겐 (0.106 g, 1 mmol)의 용액에 첨가하였다. 2시간 동안 교반한 후, 휘발물질을 진공에서 증발시켰다. 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 잔류물에 첨가하고, 유기층을 수성 혼합물로부터 분리하였다. 유기 추출물을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공에서 증발시켰다.
조 잔류물을 무수 DMF (4.5 mL)에 용해시키고, 이 용액에, 나트륨 아지드 (0.195 g, 3.0 mmol) 및 염화암모늄 (0.16 g, 3.0 mmol)을 실온에서 첨가하였다. 실온에서 15분 동안 교반한 후, 반응 혼합물을 5시간 동안 95℃에서 가열하였다. 그 후, 반응 혼합물을 실온으로 냉각시키고, 물 (30 mL) 및 에틸 아세테이트(30 mL)를 첨가하고, 유기층을 분리하고, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공에서 증발시켰다. 수성 NaOH (1 N)를 실온에서 첨가하여 잔류물을 용해시켰다. 이 용액에 메틸렌 클로라이드 (6 mL), 디메틸 술페이트 (0.1 mL, 1 mmol), 테트라부틸암모늄 브로마이드 (0.01 내지 0.02 g)를 순차적으로 첨가하고, 생성된 혼합물을 밤새 교반하였다. 이어서, 유기층을 분리하고, 수성층을 메 틸렌 클로라이드로 역 추출 (2 x 20 mL)하였다. 합한 유기 추출물을 염수로 세척하고, 용매를 진공에서 증발시켰다. 잔류물을 실리카겔 (200-400 메쉬)을 사용하고, 5 내지 20% 헥산:EtOAc로 용리한 크로마토그래피에 의해 정제하여 표제 화합물을 무색 점성질 액체로 수득하였다 (0.06 g), 수율: 21%.
실시예
2
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 비스-시클로프로필메틸-아민 (미국 특허 제3,546,295호에 개시된 문헌 방법에 따라 제조함)을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.17 g), 수율: 28%.
실시예
3
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-에틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로프로필메틸-에틸-아민 (미국 특허 제3,546,295호에 개시된 바와 같이 제조함)을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.2 g), 수율: 37%.
실시예
4
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-메틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로부틸메틸-메틸-아민 (단계 (ii)에서 에틸아민 대신에 메틸아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 액체로 얻음)을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.23 g), 수율: 31%.
실시예
5
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
시클로부틸메틸
-
시클로프로필메
틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로부틸메틸-시클로프로필메틸-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 밝은 황색 고체로 수득하였다 (0.106 g), 수율: 15%, 융점 84-85℃.
실시예
6
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-(2,2-디메틸-프로필)-에틸-
아민
의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 2,2-디메틸 -프로필-에틸-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 고체로 수득하였다 (0.28 g), 수율: 41%, 융점 72-73℃.
실시예
7
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-이소프로필-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 에틸-이소프로필아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.23 g), 수율: 38%.
실시예
8
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로펜틸-에틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로펜틸-에틸아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 고체로 수득하였다 (0.14 g), 수율: 30%, 융점 43-44℃.
실시예
9
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
시클로펜틸
-
시클로프로필메틸
-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로펜틸-시클로프로필메틸아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 액체로 수득하였다 (0.25 g), 수율: 46%.
실시예
10
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(5-
메틸
-
이속사졸
-3-일)-아미노]-
메틸
}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
단계 (i): 시클로부틸메틸-{1,3-디메틸-5-[(5-메틸-이속사졸-3-일아미노)-메틸]-1H-피라졸로[3,4-b]피리딘-6-일}-에틸-아민의 합성
5-메틸-이속사졸-3-일아민 (0.37 g, 3.8 mmol)을 질소 하에서 무수 클로로포름 (20 mL) 및 아세트산 (0.2 mL) 중 6-(시클로부틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (0.54 g, 1.9 mmol)의 용액에 첨가하였다. 15분 동안 실온에서 교반한 후, 나트륨 트리아세톡시보로히드라이드 (1.20 g, 5.7 mmol)를 서서히 첨가하고, 이 혼합물을 실온에서 밤새 교반하였다. 클로로포름을 진공에서 증발시킨 후, 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 잔류물에 첨가하였다. 유기층을 분리하고, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 농축시켜 표제 화합물을 수득하였으며, 이를 이를 추가 정제 없이 사용하였다.
단계 ( ii ): (5-{[(3,5-비스-트리플루오로메틸-벤질)-(5-메틸-이속사졸-3-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
수소화나트륨 [0.06 g, (무기 오일 중 60% 분산액)]을 무수 DMF (3 mL) 중 시클로부틸메틸-{1,3-디메틸-5-[(5-메틸-이속사졸-3-일아미노)-메틸-1H-피라졸로[3 ,4-b]피리딘-6-일}-에틸-아민 (0.225 g, 0.6 mmol)의 용액에 실온에서 교반하면서 첨가하였다. 이 혼합물을 1시간 동안 교반한 후, 3,5-비스-트리플루오로메틸벤질 브로마이드 (0.13 mL, 0.7 mmol)를 서서히 첨가하고, 추가 12시간 동안 지속적으로 교반하였다. 에틸 아세테이트 (30 mL) 및 물 (30 mL)을 첨가하고, 층을 분리하였다. 수성층을 에틸 아세테이트로 역 추출 (2 x 30 mL)하였다. 합한 유기 추출물을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공에서 농축시켰다. 조 잔류물을 실리카겔 (200-400 메쉬)을 사용하고, 25 내지 50% 헥산:에틸 아세테이트로 용리한 크로마토그래피에 의해 정제하여 표제 화합물을 무색 점성질 액체로 수득하였다 (0.10 g), 수율: 29%.
실시예
11
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(5-
메틸
-
이속사졸
-3-일)-아미노]-
메
틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 하기를 제외하고, 실시예 10에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.03 g), 수율: 19%: 1) 단계 (i): 6-(시클로부틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 대신에 6-(비스-시클로프로필메틸아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 사용하고; 2) 단계 (ii): 수소화나트륨 및 DMF 대신에 각각 나트륨 tert-부톡시드 및 무수 THF를 사용하였다.
실시예
12
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
단계 (i): 6-클로로-1-메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드의 합성
히드라진 히드레이트 (9.7 mL, 200 mmol)를 10분에 걸쳐 무수 EtOH (105 mL) 중 아크릴로니트릴 (13.5 mL, 205 mmol)의 격렬히 교반된 용액에 5 내지 10℃에서 첨가하였다. 첨가가 완료된 후, 반응물을 24시간 동안 실온에서 교반한 후, 5 내지 10℃로 냉각시키고, 파라포름알데히드 (6.4 g, 220 mmol)를 서서히 첨가하였다. 생성된 혼합물을 추가 3시간 동안 실온에서 지속적으로 교반하였다. 에탄올을 진공에서 증발시켜 점성의 황색 오일을 수득하였으며, 이를 1-프로판올 (30 mL)로 희석하였다. 이 용액에 고체 NaOH (0.2 g)를 첨가하고, 이 혼합물을 4시간 동안 가열 환류시켰다. 휘발물질을 증발시킨 후, 암갈색 오일을 실리카겔을 통해 여과하고, 1 내지 5% CH2Cl2:Me0H로 세척하였다. 합한 여과액을 증발시켜 연한 황색 액체를 수득하였다. 액체 화합물을 아세트산 무수물 (15.2 mL)에 용해시키고, 100℃에서 3시간 동안 가열하였다. 그 후, 반응 혼합물을 실온으로 냉각시키고, 옥시염화인 (49.0 mL, 540 mmol)에 이어 DMF (31.0 mL)를 30분에 걸쳐 서서히 첨가하였다. 이 혼합물을 실온에서 30분 동안 교반한 후, 반응물을 100℃에서 5시간 동안 가열한 후, 실온으로 냉각시키고, 빙수에 서서히 붓고, CH2Cl2로 추출 (3 x 50 mL)하였다. 합한 유기 추출물을 황산나트륨 상에서 건조시키고, 여과하고, 진공에서 농축시켰다. 조 생성물을 1 내지 5% CH2Cl2:Me0H로 용리한 실리카겔 크로마토그래피에 의해 정제하여 6-클로로-1-메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 밝은 황색 오일로 수득하였다 (1.8 g), 수율: 6%.
단계 ( ii ): (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
표제 화합물을 단계 (iii)에서 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 대신에 6-클로로-1-메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 사용하는 것을 제외하고, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.49 g), 수율: 42%.
실시예
13
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1-메틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸아민 대신에 비스-시클로프로필메틸-아민을, 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 대신에 6-클로로-1-메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 사용하는 것을 제외하고, 실시예 1에 기재된 바와 같은 절차에 따라 밝은 황색 오일로 수득하였다 (0.31 g), 수율: 60%.
실시예
14
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1-에틸-1H-피라졸로[3,4-b]피리딘-6-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸아민 대신에 비스-시클로 프로필메틸-아민을, 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 대신에 6-클로로-1-에틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 사용하는 것을 제외하고, 실시예 1에 기재된 바와 같은 절차에 따라 무색 오일로 수득하였다 (0.37 g), 수율: 45%.
실시예
15
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]메틸}-1-에틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로부틸메틸-에틸-아민의 합성
표제 화합물을 단계 (iii)에서 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 대신에 6-클로로-1-에틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드를 사용하는 것을 제외하고, 실시예 1에 기재된 바와 같은 절차에 따라 무색 분말로 수득하였다 (0.36 g), 수율:36%.
융점 76-77℃.
실시예
16
(3,5-
비스
-
트리플루오로메틸
-벤질)-[6-(
시클로펜틸메틸
-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-카르밤산
메틸
에스테르의 합성
단계 (i): N-(2,5-디메틸-2H-피라졸-3-일)-아세트아미드의 합성
피리딘 (7.1 mL, 90 mmol)을 0℃에서 아세트산 무수물 (46 mL) 중 2,5-디메틸-2H-피라졸-3-일아민 (10 g, 90 mmol)의 용액에 첨가하고, 생성된 혼합물을 실온에서 30분 동안 교반하였다. 용매를 진공 하에 제거하여 표제 화합물을 갈색빛 액체로 수득하였다 (13.7 g), 수율: 100%.
단계 ( ii ): 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드의 합성
N-(2,5-디메틸-2H-피라졸-3-일)-아세트아미드 (13.7 g, 89 mmol) 및 옥시염화인 (68.4 mL, 44.5 mmol, 사용전 증류시킴)의 혼합물을 질소 대기 하에 2시간 동안 교반하면서 90 내지 95℃로 가열한 후, 동일한 온도에서 20분 동안 DMF (19.6 mL, 26.7 mmol)를 서서히 첨가하였다. 3시간 동안 교반한 후, 반응물을 0℃로 냉각시키고, 분쇄한 얼음을 서서히 첨가하고, 30분 동안 지속적으로 교반하였다. 생성된 고체를 여과하고, 물 및 석유 에테르로 세척하여 밝은 황색 고체를 수득하였다 (7.8 g), 수율: 43%.
단계 ( iii ): 6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드의 합성
DMF (75 mL) 중 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (5 g, 0.023 mol) 및 탄산칼륨 (9.9 g, 0.0717 mol)의 현탁액을 20분 동안 실온에서 교반하였다. 이어서, 시클로펜틸메틸 에틸 아민 (4.25 g, 33.0 mmol)을 첨가하고, 반응물을 8시간 동안 환류시켰다. 반응물을 실온으로 냉각시킨 후, 물 (500 mL)을 반응 혼합물에 첨가하고, 에틸 아세테이트로 추출 (3 x 400 mL)하고, 합한 유기층을 건조시키고, 농축시켰다. 잔류물을 실리카겔 (100-200 메쉬) 칼럼 크로마토그래피에 의해 정제하였다. 헥산 중 10% 에틸 아세테이트로 용리하여 순수한 생성물을 무색 점성질 덩어리로 수득하였다 (76%).
단계 ( iv ): {5-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-시클로펜틸메틸-에틸-아민의 합성
MeOH 및 아세트산 (2 방울) 중 6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (5.3 g, 17.0 mmol) 및 3,5-비스-트리플루오로메틸벤질아민 (4.7 g, 0.019 mol)의 혼합물을 실온에서 30분 동안 교반하였다. 0℃로 냉각시킨 후, 나트륨 시아노보로히드라이드 (2.2 g, 35.0 mmol)를 약 10분에 걸쳐 서서히 첨가하였다. 실온에서 30분 동안 교반한 후, 반응 혼합물을 진공에서 농축시켰다. 물 (50 mL)을 잔류물에 첨가하고, 30분 동안 교반하였다. 고체를 여과하고, 물에 이어 석유 에테르로 세척하고, 진공에서 건조시켜 무색 고체를 수득하였다 (72%).
단계 (v): (3,5-비스-트리플루오로메틸-벤질)-[6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-카르밤산 메틸 에스테르의 합성
THF (10 mL) 중 {5-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-시클로펜틸메틸-에틸-아민 (0.25 g, 0.47 mmol) 및 탄산칼륨 (0.19 g, 1.4 mmol)의 혼합물을 20분 동안 실온에서 교반하였다. 그 후, 메틸 클로로포르메이트 (0.55 mL, 0.7 mmol)를 첨가하고, 밤새 지속적으로 교반하였다. 이 혼합물에 물 (100 mL)을 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 100 mL)하였다. 유기 추출물을 합하고, 농축시키고, 잔류물을 230-400 메쉬 실리카겔 상에서 칼럼 크로마토그래피에 의해 정제하였다. 헥산 중 20% 에틸 아세테이트로 용리하여 순수한 생성물을 무색 점성질 덩어리로 수득하였다 (55%).
실시예
17
시클로펜틸메틸
-에틸-(5-{[(3,4,5-
트리플루오로
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민의 합성
단계 (i): 시클로펜틸메틸-에틸-{5-[(3,4,5-디플루오로-벤질아미노)-메틸]- 1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-아민의 합성
실시예 16의 단계 (iii)에서 수득한 6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (0.30 g, 1.00 mmol), 3,4,5-트리플루오로벤질아민 (0.161 g, 1.0 mmol) 및 아세트산 (0.120 g, 2.0 mmol)을 25 mL의 둥근 바닥 플라스크에 넣은 후, MeOH 5 mL를 첨가하였다. 이 혼합물을 25 내지 35℃에서 15분 동안 교반하였다. 이어서, 나트륨 시아노보로히드라이드 (0.189 g, 3.0 mmol)를 일부분씩 나누어 첨가하였다. 이 혼합물을 실온에서 1시간 동안 교반한 후, MeOH를 진공에서 제거하고, 물을 조 혼합물에 첨가하였다. 혼합물을 에틸 아세테이트로 추출 (3 x 50 mL)하고, 합한 유기층을 포화 중탄산나트륨 용액, 염수로 세척하고, 황산나트륨 상에서 건조시켰다. 용매를 증발시켜 생성물을 오일 로 수득하였다 (0.44 g), 수율: 90%.
단계 ( ii ): [6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸-(3,4,5-트리플루오로-벤질)-시안아미드의 합성
MeOH (15 mL) 중 시클로펜틸메틸-에틸-{5-[(3,4,5-디플루오로-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-아민 (0.450 g, 1.0 mmol)의 용액에 N2 대기 하에 중탄산나트륨 (0.168 g, 2.0 mmol)에 이어 브롬화시아노겐 (0.126 g, 1.20 mmol)을 첨가하고, 이 혼합물을 0.5시간 동안 실온에서 교반하였다. 이어서, 반응 혼합물을 진공 하에 농축시키고, 잔류물을 물에 용해시키고, 에틸 아세테이트로 추출 (3 x 20 mL)하였다. 합한 유기 추출물을 황산나트륨 상에서 건조시키고, 농축시켜 조 생성물을 수득하였다. 조 생성물을 100-200 메쉬 실리카겔 상에서 10% 에틸 아세테이트 및 석유 에테르를 사용하여 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 오일로 수득하였다 (59%).
단계 ( iii ): 시클로펜틸메틸-에틸-(5-{[(3,4,5-트리플루오로-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민의 합성
무수 DMF (10 mL) 중 [6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸-(3,4,5-트리플루오로-벤질)-시안아미드 (0.280 g, 0.590 mmol) 및 염화암모늄 (0.160 g, 2.95 mmol)의 교반된 현탁액에 나트륨 아지드 (0.195 g, 2.95 mmol)를 첨가하고, 반응 혼합물을 100℃에서 밤새 가열하였다. 반응 혼합물을 실온으로 냉각시킨 후, 빙수를 첨가하고, 이 혼합물을 30분 동안 가열한 후, 에틸 아세테이트로 추출 (3 x 50 mL)하였다. 합한 유기층을 황산나트륨 상에서 건조시키고, 증발시켜 생성물을 오일로 수득하였다 (90%).
단계 ( iv ): 시클로펜틸메틸-에틸-(5-{[(3,4,5-트리플루오로-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아 민의 합성
물 (4 mL) 중 시클로펜틸메틸-에틸-(5-{[(3,4,5-트리플루오로-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민 (0.420 g, 0.818 mmol)의 현탁액에 수산화나트륨 (0.065 g, 1.630 mmol)을 첨가하고, 생성된 혼합물을 15분 동안 실온에서 교반하였다. 그 후, DCM (5 mL), 디메틸 술페이트 (0.113 g, 0.90 mmol), 및 테트라부틸암모늄 브로마이드 (0.013 g, 0.050 mmol)를 반응 혼합물에 순차적으로 첨가하였다. 반응물을 0.5시간 동안 실온에서 교반하였다. 유기층을 수성층으로부터 분리하고, 수성층을 DCM로 역 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 농축시켰다. 잔류물을 100-200 메쉬 실리카겔 상에서 5% EtOAc 및 석유 에테르를 사용한 칼럼 크로마토그래피에 의해 정제하여 시클로펜틸메틸-에틸-(5-{[(3,4,5-트리플루오로-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민을 연한 황색 고체로 수득하였다 (45%), 융점: 100℃.
실시예
18
시클로펜틸메틸
-에틸-(5-{[(3,5-
디플루오로
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민의 합성
표제 화합물을 단계 (i)에서 3,4,5-트리플루오로벤질아민 대신에 3,5-디플루오로벤질아민을 사용하여, 실시예 17에 기재된 바와 같은 절차에 따라 수득하였다.
실시예
19
시클로펜틸메틸
-(1,3-디메틸-5-{[(2-
메틸
-2H-
테트라졸
-5-일)-(3,5-
디클로로
벤질)-아미노]-메틸}-1H-피라졸로[3,4-b]피리딘-6-일)-에틸-아민의 합성
표제 화합물을 단계 (i)에서 3,4,5-트리플루오로벤질아민 대신에 3,5-디클로로벤질아민을 사용하여, 실시예 17에 기재된 바와 같은 절차에 따라 수득하였다.
실시예
20
시클로펜틸메틸
-에틸-(5-{[(3-
플루오로
-5-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
아
민의 합성
표제 화합물을 단계 (iv)에서 3,5-비스-트리플루오로벤질아민 대신에 3-플루오로-5-트리플루오로메틸-벤질아민을 사용하고, 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로프로필메틸-에틸-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 수득하였다.
실시예
21
비스
-
시클로프로필메틸
-(5-{[(3,5-
디클로로벤질
)-(2-
메틸
-2H-
테트라졸
-5-일) -아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-아민의 합성
표제 화합물을 실시예 1의 단계 (iii)에서 시클로부틸 메틸 에틸아민 대신에 비스-시클로프로필메틸-에틸아민을 사용하고, 실시예 1의 단계 (iv)에서 비스-트리플루오로메틸-벤질아민 대신에 3,5-디클로로벤질아민을 사용하는 것을 제외하고, 실시예 1에 대한 실험 절차에 따라 제조하였다.
실시예
22
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(4-
트리플루오로메틸
-
옥사졸
-2-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로
[3,4-b]-피리딘-6-일)-
시클로펜틸메틸
-에틸-아민의 합성
단계 (i): 1-(3,5-비스-트리플루오로메틸-벤질)-1-[6-(시클로펜틸메틸-에틸- 아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-우레아의 합성
에탄올 (15 mL) 중 [6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸-(3,5-비스-트리플루오로메틸-벤질)-시안아미드 (0.50 g, 0.880 mmol)의 교반된 용액에 H2O2 (1.5 mL) 및 KOH의 포화 수용액 (0.70 g, 11.97 mmol)을 0℃에서 첨가하였다. 이 혼합물을 서서히 가열 환류시켰다. 2시간 후, 반응 혼합물을 실온으로 냉각시키고, 물 (10 mL)을 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 40 mL)하였다. 합한 유기층을 황산나트륨 상에서 건조시키고, 증발시켜 조 잔류물을 수득하였다. 조 물질을 100-200 메쉬 실리카겔 상에서 10% 에틸 아세테이트 및 석유 에테르를 사용하여 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 점성 오일로 수득하였다 (60%).
단계 ( ii ): (5-{[(3,5-비스-트리플루오로메틸-벤질)-(4-트리플루오로메틸-옥사졸-2-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]-피리딘-6-일)-시클로펜틸메틸-에틸-아민의 합성
tert-부탄올 (10 mL) 중 1-(3,5-비스-트리플루오로메틸-벤질)-1-[6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-우레아 (0.250 g, 0.430 mmol)의 교반된 용액에 1,1,1-트리플루오로메틸 아세틸 브로마이드 (0.20 g, 0.480 mmol)를 첨가하였다. 이 혼합물을 3시간 동안 환류시킨 후, 실온으로 냉각시켰다. 진공에서 농축시킨 후, 물 (10 mL)을 잔류물에 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 25 mL)하였다. 합한 유기층을 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 조 잔류물을 수득하였으며, 이를 100-200 메쉬 실리카겔 상에서 5% 에틸 아세테이트 및 석유 에테르를 사용하여 칼럼 크로마토그래피에 의해 정제하여, 표제 화합물을 백색 고체로 수득하였다 (20%), 융점: 139℃.
실시예
23
(2-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(6-
시클로펜틸메틸
-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]-피리딘-5-일메틸]-아미노}-옥사졸-4-카르복실산 에 틸 에스테르의 합성
에탄올 (10 mL) 중 1-(3,5-비스-트리플루오로메틸-벤질)-1-[6-(시클로펜틸메틸-에틸-아미노)-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸]-우레아 (1.20 gm, 2.10 mmol)의 빙냉 용액에 3-브로모-2-옥소-프로피온산 에틸 에스테르 (0.612 g, 3.150 mmol)를 첨가하였다. 이 혼합물을 실온에 도달하도록 두면서 교반한 후, 반응 혼합물을 8시간 동안 환류시키고, 이어서 실온으로 냉각시켰다. 반응 휘발물질을 증발시킨 후, 물 (10 mL)을 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 50 mL)하였다. 합한 유기층을 황산나트륨 상에서 건조시키고, 증발시켜 조 잔류물을 수득하였고, 이를 100-200 메쉬 실리카겔 상에서 5% 에틸 아세테이트 및 석유 에테르를 사용하여 칼럼 크로마토그래피에 의해 정제하여, 표제 생성물을 황색 페이스트로 수득하였다 (6%).
실시예
24
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노] -메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로펜틸메틸-에틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로펜틸메틸-에틸-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 밝은 오렌지색 고체로 수득하였다 (56%), 융점: 84-86℃.
실시예
25
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-디이소부틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 디이소부틸 -아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 점성질 액체로 수득하였다 (0.395 g), 수율: 38%.
실시예
26
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
시클로프로필메틸
-이소부틸-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 시클로프로필메틸-이소부틸-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 고체로 수득하였다 (0.35 g), 수율: 40%, 융점: 99-101℃.
실시예
27
시클로프로판카르복실산
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
시클로프로필메틸
-아미드의 합성
단계 (i): (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-아민의 합성
MeOH (75 mL) 및 아세트산 (2 방울) 중 6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-카르브알데히드 (6.3 g, 30 mmol) 및 3,5-비스-트리플루오로메틸벤질아민 (7.3 g, 30 mmol)의 혼합물을 실온에서 30분 동안 교반하였다. 이어서, 반응물을 0℃로 냉각시키고, 나트륨 시아노보로히드라이드 (3.7 g, 50 mmol)를 10 분에 걸쳐 서서히 첨가하였다. 2시간 동안 실온에서 교반한 후, 반응 혼합물을 농축시키고, 물 (50 mL)을 잔류물에 첨가하고, 생성된 혼합물을 30분 동안 교반하였다. 고체 생성물을 여과하고, 물 및 석유 에테르로 세척하고, 진공 하에 건조시켜 무색 고체를 수득하였다 (9.2 g), 수율: 70%.
단계 ( ii ): (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-시안아미드의 합성
메탄올 (150 mL) 중 화합물 (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-아민 (9.O g, 0.02 mol), 브롬화시아노겐 (2.60 g, 0.024 mole) 및 탄산수소나트륨 (3.50 g, 0.04 mole)의 혼합물을 실온에서 30분 동안 교반하였다. 이어서, 반응 혼합물을 농축시키고, 물 (10O mL)을 잔류물에 첨가하고, 이 혼합물을 추가 30분 동안 교반하였다. 생성된 고체를 여과하고, 물에 이어 석유 에테르로 세척하고, 최종적으로 진공 하에 건조시켜 무색 고체를 수득하였다 (8.70 g), 수율: 91%.
단계 ( iii ): (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-(2H-테트라졸-5-일)-아민의 합성
물 (300 mL) 중 (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-시안아미드 (8.5 g, 10 mmol), 나트륨 아지드 (1.4 g, 20 mmol) 및 브롬화아연 (4.1 g, 10 mmol)의 혼합물을 3시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 5% 염산 (50 mL) 및 에틸 아세테이트 (500 mL)를 첨가하고, 생성된 혼합물을 20분 동안 교반한 후, 유기층을 분리하였다. 이 공정을 에틸 아세테이트로 3회 반복 (3 x 50O mL)하였다. 합한 유기층을 건조시키고, 농축시키고, 잔류물을 230-400 메쉬 실리카겔 상에서 칼럼 크로마토그래피에 의해 정제하였다. 헥산 중 15% 에틸 아세테이트로 칼럼을 용리하여 순수한 생성물을 무색 고체로 수득하였다 (8.3 g), 수율: 90%.
단계 ( iv ): (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-(2-메틸-2H-테트라졸-5-일)-아민의 합성
DMF (150 mL) 중 (3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-(2H-테트라졸-5-일)-아민 (8.5 g, 10 mmol) 및 수소화나트륨 (0.81 g, 30 mmol)의 혼합물을 0℃에서 20분 동안 교반하였다. 그 후, 메틸 요오다이드 (3.5 g, 20 mmol)를 첨가하고, 생성된 혼합물을 0 내지 10℃에서 30분 동안 교반하였다. 물 (100 mL)을 반응 혼합물에 첨가한 후, 이를 에틸 아세테이트로 추출 (3 x 100 mL)하였다. 합한 유기층을 황산나트륨 상에서 건조시키고, 농축시켰다. 잔류물을 230-400 메쉬 실리카겔 상에서 칼럼 크로마토그래피에 의해 정제하였다. 헥산 중 10% 아세톤으로 칼럼을 용리하여 순수한 생성물을 무색 고체로 수득하였다 (6.3 g), 수율: 75%.
단계 (v): (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-아민의 합성
(3,5-비스-트리플루오로메틸-벤질)-(6-클로로-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-5-일메틸)-(2-메틸-2H-테트라졸-5-일)-아민 (0.5 g, 0.9 mmol), 칼륨 3차 부톡시드 (0.43 g, 3 mmol), 시클로프로필메틸 아민 (0.275 g, 3 mmol), 및 Pd(OAc)2 (0.01 g, 0.004 mmol), BINAP (0.03 g, 0.04 mmol)의 혼합물을 10 mL의 압력 바이알에 준비하였다. 압력 바이알을 초점 마이크로파 오븐 (CEM 디스커버리 (Discovery))에 두고, 20분 동안 110℃에서 250 와트 마이크로파 출력을 사용하여 조사하였다. 이 혼합물을 실온으로 냉각시킨 후, 에틸 아세테이트 (100 mL)를 상기 바이알에 첨가하였다. 유기층을 물로 세척 (3 x 100 mL)하고, 건조시키고, 농축시켰다. 생성된 오일을 실리카겔 (230 내지 400 메쉬)을 사용하고, 헥산 중 10% 에틸 아세테이트로 칼럼을 용리한 칼럼 크로마토그래피에 의해 정제하여 무색 고체를 수득하였다 (0.485 g), 수율: 90%.
단계 ( vi ): 시클로프로판카르복실산 (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-아미드의 합성
THF (5 mL) 중 (5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일)-시클로프로필메틸-아민 (0.25 g, 0,45 mmol), 트리에틸아민 (0.13 g, 1.3 mmol), 및 시클로프로판카르보닐 클로라이드 (0.28 g, 2.7 mmol)의 혼합물을 10 mL의 반응 용기에서 제조하고, 250 psi 하에 80℃에서 2시간 동안 250 와트 마이크로파 출력으로 조사하였다. 용기를 실온으로 냉각시키고, 반응 혼합물을 에틸 아세테이트 (100 mL)로 희석하였다. 에틸 아세테이트 층을 물로 세척 (3 x 100 mL)하고, 유기층을 분리하고, 황산나트륨 상에서 건조시키고, 농축시켰다. 생성된 오일을 실리카겔 (230-400 메쉬)을 사용하고, 디클로로메탄 중 1% 메탄올로 칼럼을 용리한 칼럼 크로마토그래피로 정제하여 무색 고체를 수득하였다 (0.147 g), 수율: 52.5%, 융점 120-122℃.
실시예
28
시클로펜탄카르복실산
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-
시클로
프로필메틸-아미드의 합성
표제 화합물 (순도 99%)을 단계 (vi)에서 시클로프로판카르보닐 클로라이드 대신에 시클로펜탄카르보닐 클로라이드를 사용하여, 실시예 27에 기재된 바와 같은 절차에 따라 무색 고체로 수득하였다 (0.085 g), 수율: 48.2%, 융점 88-90℃.
실시예
29
시클로헥산카르복실산
(5-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-6]피리딘
-6-일)-
시클로
프로필메틸-아미드의 합성
표제 화합물을 단계 (vi)에서 시클로프로판카르보닐 클로라이드 대신에 시클로헥산카르보닐 클로라이드를 사용하여, 실시예 27에 기재된 바와 같은 절차에 따라 무색 액체로 수득하였다 (0.13 g), 수율: 72%.
실시예
30
N-(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-N-
시클로프로필메틸
-
아세트
아미드의 합성
표제 화합물을 단계 (vi)에서 시클로프로판카르보닐 클로라이드 대신에 아세틸 클로라이드를 사용하여, 실시예 27에 기재된 바와 같은 절차에 따라 무색 액체로 수득하였다 (0.15 g), 수율: 93%.
실시예
31
N-(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-3-
클로로
-N-
시클로프로필메
틸-프로피온아미드의 합성
표제 화합물을 단계 (vi)에서 시클로프로판카르보닐 클로라이드 대신에 클로로프로피오닐 클로라이드를 사용하여, 실시예 27에 기재된 바와 같은 절차에 따라 무색 액체로 수득하였다 (0.066 g), 수율: 38%.
실시예
32
(3,5-
비스
-
트리플루오로메틸
-벤질)-[6-(
시클로펜틸메틸
-에틸-아미노)-3-
메틸
-이속사졸로[5,4-b]피리딘-5-일메틸}-카르밤산
메틸
에스테르의 합성
표제 화합물을 단계 (i)에서 1,3-디메틸-피라졸-5-일아민 대신에 3-메틸-이속사졸-5-일아민을 사용하는 것을 제외하고, 실시예 16에 대한 실험 절차에 따라 제조하였다 (65%).
실시예
33
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-3-메틸-이속사졸로[5,4-b]피리딘-6-일)-시클로펜틸메틸-에틸-아민의 합성
표제 화합물을 {5-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-1,3-디메틸-1H-피라졸로[3,4-b]피리딘-6-일}-시클로펜틸메틸-에틸-아민 대신에 {5-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-3-메틸-이속사졸로[5,4-b]피리딘-6-일}-시 클로펜틸메틸-에틸-아민을 사용하는 것을 제외하고, 실시예 24에 대한 실험 절차에 따라 제조하였다 (60%).
실시예
34
(5-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-
메틸
}-1,3-디메틸-1H-
피라졸로[3,4-b]피리딘
-6-일)-에틸-(
테트라히드로
-푸란-2-
일메틸
)-아민의 합성
표제 화합물을 단계 (iii)에서 시클로부틸메틸-에틸-아민 대신에 (S)-에틸-(테트라히드로-푸란-2-일메틸)-아민을 사용하여, 실시예 1에 기재된 바와 같은 절차에 따라 무색 점성질 액체로 수득하였다 (0.21 g), 수율: 55%.
실시예
35
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로펜틸메틸
-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산
메틸
에스테르의 합성
단계 (i): 2-클로로퀴놀린-3-카르브알데히드의 합성
디메틸포름아미드 (9.13 g, 0.125 mol)를 건조 튜브가 장착된 플라스크에서 0℃로 냉각시키고, 옥시염화인 (53.7 g, 0.35 mol)을 교반하면서 적가하였다. 이 용액에 아세트아닐라이드 (6.55 g, 0.05 mol)를 첨가하고, 혼합물을 16시간 동안 65℃에서 환류 하에 가열하였다. 과량의 옥시염화인을 증류시키고, 물을 첨가하고, 용액을 에틸 아세테이트로 추출하였다. 용매를 증발시키고, 조 물질을 실리카겔 (100-200 메쉬) 상에서 2% 에틸 아세테이트/석유 에테르를 사용하여 정제하였다. 수율: 68%, 융점: 145℃;
단계 ( ii ): N-시클로펜틸메틸 에틸아민의 합성
N-시클로펜테노일-에틸아민을 시클로펜텐산 (2 g, 17.5 mmol) 및 옥살릴 클로라이드 (2.2 g, 17.5 mmol)로부터 25 내지 35℃에서 8 내지 12시간 동안 교반한 후에 제조하였다. 여기에 에틸아민 (2,1 g, 48.7 mmol)의 벤젠 용액을 0℃에서 첨 가하고, 이 반응 혼합물을 3시간 동안 25 내지 35℃에서 교반한 후, 용매를 진공 하에 증발시켜 N-시클로펜테노일-에틸아민을 수득하였다 (1.7 g), 수율: 68.9%. 무수 테트라히드로푸란 (THF) (10 mL) 중 N-시클로펜테노일-에틸아민 (1.7 g, 13.3 mmol)의 용액을 질소 대기 하에 두고, 수소화리튬알루미늄 (LiAlH4; 1.3 g, 36.1 mmol)을 이 용액에 첨가하였다. 1시간 동안 25 내지 35℃에서 교반한 후, 반응 혼합물을 8시간 동안 온화하게 환류시켰다. 반응 혼합물을 포화 황산나트륨 용액으로 켄칭시키고, 여과하고, 침전물을 디에틸 에테르 (Et2O)로 세척하였다. 여과액을 농축시켜 N-시클로펜틸메틸 에틸아민을 수득하였다 (0.6 g), 수율: 40%.
단계 ( iii ): 2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-카르브알데히드의 합성
2-클로로퀴놀린-3-카르브알데히드 (0.27 g, 1.40 mmol) 및 탄산칼륨 (0.579 g, 1.4 mmol)을 25 mL의 2-목 둥근 바닥 플라스크에 넣었다. 이 플라스크에 N,N-디메틸포름아미드 (DMF) 3 mL를 첨가한 후, 시클로펜틸 메틸 에틸 아민의 디메틸포름아미드 용액 (0.214 g, 1.69 mmol)을 적가하였다. 생성된 혼합물을 2시간 동안 환류시킨 후, 25 내지 35℃로 냉각시키고, 이어서 혼합물을 분쇄한 얼음 (10 mL)에 붓고, 에틸 아세테이트로 추출 (3 x 50 mL)하였다. 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시켰다. 용매를 진공에서 증발시켜 생성물을 황색 오일로 수득하였다. 수율: 0.355 g (89%);
단계 ( iv ): {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민의 합성
단계 (iii)에서 수득한 2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-카르브알데히드 (0.355 g, 1.25 mmol), 3,5-비스-트리플루오로메틸벤질아민 (0.305 g, 1,25 mmol), 및 아세트산 (0.151 g, 2.51 mmol)을 25 mL의 둥근 바닥 플라스크에 넣고, 이어서 메탄올 4 mL를 첨가하고, 혼합물을 25 내지 35℃에서 15분 동안 교반하였다. 이어서, 나트륨 시아노보로히드라이드 (0,237 g, 3.77 mmol)를 일부분씩 나누어 첨가하였다. 실온에서 추가 1시간 동안 지속적으로 교반한 후, 메탄올을 진공 하에 제거하고, 물을 조 혼합물에 첨가하였다. 이 혼합물을 에틸 아세테이트로 추출 (3 x 50 mL)하고, 합한 유기층을 포화 중탄산나트륨 용액에 이어 염수로 세척한 후, 황산나트륨 상에서 건조시켰다. 용매를 증발시켜 생성물을 오일성 잔류물로 수득하였으며, 이를 4% 에틸 아세테이트/석유 에테르를 사용하여 실리카겔 (100-200) 상에서 정제하였다.
단계 (v): (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르의 합성
단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸-메틸-에틸-아민 (0.155 g, 0.304 mmol), 및 K2CO3 (0.126 g, 0.913 mmol)을 질소 대기 하에 2-목 둥근 바닥 플라스크에 넣었다. 무수 테트라히드로푸란 (3 내지 4 mL)을 상기 플라스크에 첨가하고, 혼합물을 실온에서 30분 동안 교반하였다. 이어서, 메틸클로로포르메이트 (0.035 g, 0.456 mmol)를 적가하고, 반응 혼합물을 25 내지 35℃에서 8 내지 12시간 동안 교반하였다. 그 후, 용매를 진공에서 제거하고, 여기에 물을 첨가하고, 혼합물을 에틸 아세테이트로 추출하였다. 유기층을 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 조 표제 화합물을 수득하였으며, 이를 실리카겔 (100-200 메쉬 ASTM) 상에서 3% 에틸 아세테 이트/석유 에테르를 사용하여 정제하였다. 원하는 화합물을 96.70%의 순도를 갖는 황색 점성 화합물로 수득하였다.
실시예
36
(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
디에틸아미노
-퀴놀린-3-
일메틸
)-
카르
밤산
메틸
에스테르의 합성
표제 화합물을 단계 (iii)에서 시클로펜틸메틸 에틸 아민 대신에 디에틸아민을 사용한 것을 제외하고, 실시예 35에서 이용된 것과 동일한 절차에 따라 합성하였으며, 생성물을 무색 점성 화합물로 수득하였다 (0.14 g), 수율; 60%, 순도 95.45% (HPLC: 알티마 (Alltima) C18, [0.01M KH2PO4: CH3CN], 215 nM, Rt 10.589분);
실시예
37
(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
피롤리딘
-1-일-퀴놀린-3-
일메틸
)-
카르
밤산
메틸
에스테르의 합성
표제 화합물을 단계 (iii)에서 시클로펜틸 메틸 에틸아민 대신에 피롤리딘을 사용하여, 실시예 35에 기재된 바와 같은 절차에 따라 오일로 수득하였다 (0.25 g, 59%), 순도 95.12% (HPLC: 이너트실 (Inertsil) ODS 3V, [0.01 M KH2PO4:CH3CN], 215 nM, Rt 12.410분).
실시예
38
(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-피페리딘-1-일-퀴놀린-3-
일메틸
)-
카르
밤산
메틸
에스테르의 합성
표제 화합물을 단계 (iii)에서 시클로펜틸메틸 에틸 아민 대신에 피페리딘을 사용하여, 실시예 35에 기재된 것과 동일한 절차에 따라 합성하였다. 생성물을 무 색, 점성 화합물로 수득하였다 (0.07 g), 수율: 63%, 순도 93.56% (HPLC: 이너트실 ODS 3V, [0.01 M KH2PO4: CH3CN], 215 nM, Rt 10.569분).
실시예
39
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(4-
시클로헥실메틸
-피페라진-1-일)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르의 합성
단계 (i): 2-(4-시클로헥실메틸-피페라진-1-일)-퀴놀린-3-카르브알데히드의 합성
1-(시클로헥실메틸)피페라진 (0.42 mL, 2.2 mmol)을 주변 온도에서 질소 대기 하에 무수 DMF (4 mL) 중 2-클로로-3-퀴놀린카르복스알데히드 (0.383 g, 2.0 mmol) 및 탄산칼륨 (0.7 g, 5.0 mmol)의 혼합물에 첨가하였다. 20분 동안 교반한 후, 반응 혼합물을 4.5시간 동안 110℃에서 가열하였다. 실온으로 냉각시킨 후, 이 혼합물을 물 (40 mL)로 희석하고, 에틸 아세테이트로 추출 (3 x 30 mL)하였다. 합한 유기 추출물을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과한 후, 진공 하에 농축시켜 연한 갈색 조 생성물을 수득하였다. 디클로로메탄 중 2.5% 메탄올로 용리한 실리카겔 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 수득하였다 (0.56 g), 수율: 86%.
단계 ( ii ): (3,5-비스-트리플루오로메틸-벤질)-[2-(4-시클로헥실메틸-피페라진-1-일)-퀴놀린-3-일메틸]-아민의 합성
3,5-비스(트리플루오로메틸)벤질아민 (0.305 g, 1.25 mmol)을 주변 온도에서 질소 대기 하에 메탄올 중 2-(4-시클로헥실메틸-피페라진-1-일)-퀴놀린-3-카르브알데히드 (0.4 g, 1.23 mmol)의 용액에 첨가한 후, 아세트산 (0.15 mL)을 첨가하였다. 1시간 동안 교반한 후, 나트륨 시아노보로히드라이드 (0.237 g, 3.77 mmol)를 조심스럽게 첨가하고, 반응물을 실온에서 밤새 교반하였다. 반응 혼합물을 증발 건조시키고, 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 잔류물에 첨가한 후, 이를 에틸 아세테이트로 추출 (2 x 30 mL)하였다. 합한 유기 상을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 연한 황색 조 생성물을 수득하였다. 2.5% 메탄올/디클로로메탄으로 용리한 실리카겔 칼럼 크로마토그래피로 정제하여 표제 화합물을 수득하였다 (0.468 g), 수율: 67%.
단계 ( iii ): (3,5-비스-트리플루오로메틸-벤질)-[2-(4-시클로헥실메틸-피페라진-1-일)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르의 합성
무수 탄산칼륨 (0.17 g, 1.23 mmol)을 무수 THF (5 mL) 중 (3,5-비스-트리플루오로메틸-벤질)-[2-(4-시클로헥실메틸-피페라진-1-일)-퀴놀린-3-일-메틸]-아민 (0.23 g, 0.4 mmol)의 용액에 첨가하였다. 0.5시간 동안 교반한 후, 에틸 클로로포르메이트 (0.06 mL, 0.6 mmol)를 질소 대기 하에 서서히 첨가하였다. 실온에서 밤새 교반한 후, 물 (25 mL)을 첨가하고, 혼합물을 에틸 아세테이트로 추출 (3 x 25 mL)하였다. 합한 유기 상을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공에서 농축시켜 무색 액체를 수득하였다. 10 내지 30% 에틸 아세테이트/헥산으로 용리한 실리카겔 크로마토그래피에 의해 정제하여 원하는 최종 생성물을 점성이 있는 액체로 수득하였다 (0.206 g), 수율: 81%.
실시예
40
[2-(벤질-에틸-아미노)-퀴놀린-3-
일메틸
]-(3,5-
비스
-
트리플루오로메틸
-벤질)-카르밤산 에틸 에스테르의 합성
표제 화합물을 단계 (i)에서 1-(시클로헥실메틸)피페라진 대신에 N-에틸-벤질아민을 사용하는 것을 제외하고, 실시예 39에 대한 실험 절차에 따라 제조하였으며, 점성이 있는 액체로 수득하였다 (0.218 g), 수율: 96%.
실시예
41
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(부틸-에틸-아미노)-퀴놀린-3-
일메틸
]-카르밤산 에틸 에스테르의 합성
표제 화합물을 단계 (i)에서 1-(시클로헥실메틸)피페라진 대신에 N-에틸-부틸아민을 사용하는 것을 제외하고, 실시예 39에 대한 실험 절차에 따라 제조하였으며, 점성이 있는 액체로 수득하였다 (0.223 g), 수율: 97.4%.
실시예
42
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로헥실메틸
-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르의 합성
단계 (i): N-시클로헥실메틸-에틸아민의 합성
아세틸 클로라이드 (1.1 mL, 15.4 mmol)를 피리딘 (4 mL) 중 시클로헥실메틸 아민 (1.3 mL, 10 mmol)의 빙냉 용액에 질소 대기 하에서 서서히 첨가하였다. 0 내지 5℃에서 1시간 동안 교반한 후, 반응 혼합물을 주변 온도에서 6시간 동안 유지하였다. 이어서, 이 혼합물을 물 (20 mL)에 붓고, 에틸 아세테이트로 추출 (3 x 25 mL)하였다. 합한 유기 상을 1 N HCl (2 x 10 mL)에 이어 포화 중탄산나트륨 용액 (10 mL)으로 세척하였다. 유기층을 황산나트륨 상에서 건조시키고, 여과하고, 진공에서 농축시켜 N-아세틸-시클로헥실-에틸-아민을 수득하였다 (1.50 g), 수율: 98%. 무수 THF (10 mL) 중 N-아세틸-시클로헥실-에틸-아민 (0.8 g, 5.0 mmol)의 용액을 질소 하에 준비하고, 수소화리튬알루미늄 (에테르 중 1.0 M 용액, 10 mmol)을 상기 용액에 첨가하였다. 6시간 동안 실온에서 교반한 후, 반응 혼합물을 물 (30 mL)에 붓고, 1시간 동안 교반하였다. 이어서, 무기염을 여과하고, 물 (10 mL) 및 에틸 아세테이트 (3 x 25 mL)로 세척하였다. 합한 여과액을 수집하고, 유기 상을 분리하였다. 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공에서 농축시켜 표제 화합물을 수득하였다 (0.4 g), 수율: 56%.
단계 ( ii ): (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로헥실메틸-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르의 합성
표제 화합물을 1-(시클로헥실메틸)피페라진 대신에 N-시클로헥실메틸-에틸아민을 사용하여, 실시예 39에 대한 실험 절차에 따라 무색 점성이 있는 액체로 제조 하였다 (0.268 g); 수율, 98.89%.
실시예
43
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로펜틸메틸
-프로필-아미노)-퀴놀린-3-일메틸]-카르밤산 에틸 에스테르의 합성
표제 화합물을 단계 (i)에서 1-(시클로헥실메틸)피페라진 대신에 시클로펜틸메틸 프로필아민을 사용하여, 실시예 39의 실험 절차에 따라 무색 점성이 있는 액체로 제조하였다 (0.155 g), 수율: 88%.
실시예
44
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로프로필메틸
-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산
메틸
에스테르의 합성
표제 화합물을 단계 (iii)에서 시클로펜틸메틸 에틸아민 대신에 시클로프로필메틸 에틸아민을 사용하여, 실시예 35에 대한 실험 절차에 따라 무색 점성이 있는 액체로 제조하였다 (0.085 g), 수율: 54.48%.
실시예
45
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로부틸메틸
-에틸-아미노)-퀴놀린-3-일메틸]-카르밤산
메틸
에스테르의 합성
표제 화합물은 단계 (iii)에서 시클로펜틸 메틸 에틸아민 대신에 시클로부틸메틸 에틸아민을 사용하여, 실시예 35에 대한 실험 절차에 따라 무색 점성의 액체로 제조하였다 (0.13 g), 수율: 97%.
실시예
46
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로펜틸메틸
-에틸-아미노)-6-
메틸
-퀴놀린-3-일메틸]-카르밤산
메틸
에스테르의 합성
표제 화합물을 단계 (i)에서 아세트아닐라이드 대신에 p-톨릴 아세트아미드를 사용하는 것을 제외하고, 실시예 35에 언급된 것과 동일한 실험 절차에 따라 점성이 있는 액체로 합성하였다 (0.02 g), 수율: 18%, 순도 99.59% (HPLC: 시미트리 쉴드 RP8, 22:70 [0.01 M KH2PO4:CH3CN], 220 nM, Rt 8.212분).
실시예
47
[2-(
비스
-
시클로프로필메틸
-아미노)-8-
메틸
-퀴놀린-3-
일메틸
]-(3,5-
비스
-
트리플루오로메틸
-벤질)-카르밤산
메틸
에스테르의 합성
단계 (i): 비스-시클로프로필메틸-아민의 합성
(i) a. 시클로프로판카르복실산 시클로프로필메틸-아미드의 합성:
시클로프로필 카르복실산 (1.0 g, 11.63 mmol)을 50 mL의 2-목 둥근 바닥 플라스크에 DCM (25 mL)과 함께 넣었다. 이 혼합물을 0℃로 냉각시키고, EDCI (4.15 g, 13.95 mmol)를 질소 대기 하에 교반하면서 혼합물에 일부분씩 나누어 첨가하고, 온도를 0.5시간 동안 유지하였다. 그 후, 히드록시벤조트리아졸 (1.88 g, 13.95 mmol)을 0℃의 혼합물에 첨가하고, 이를 10분 동안 교반한 후, 트리에틸아민 (1.7 g, 11.63 mmol)을 첨가하고, 혼합물을 동일한 온도에서 추가 0.5시간 동안 지속적으로 교반하였다. 이어서, 시클로프로필메틸아민 (0.825 g, 11.63 mmol)을 첨가하고, 반응물을 실온으로 도달하도록 두고, 밤새 지속적으로 교반하였다. 이어서, 용매를 진공에서 제거하고, 조 잔류물을 디클로로메탄으로 용리한 60-120 실리카겔 상에서 칼럼을 통과시켜 정제하여 표제 화합물을 수득하였다 (1.6 g), 수율: 87%.
(i) b. 비스-시클로프로필메틸-아민의 합성
무수 에테르 10 mL 중 수소화리튬알루미늄 (1.3 g, 9.35 mmol)의 현탁액에 무수 에테르 (10 mL) 중 N-시클로펜테노일-에틸아민 (1.7 g, 13.3 mmol)의 용액을 질소 대기 하에 첨가하였다. 이 반응물을 실온에서 8시간 동안 교반한 후, 반응 혼합물을 포화 황산나트륨 용액으로 켄칭시키고, 여과하고, 침전물을 디에틸 에테르로 세척하였다. 여과액을 농축시켜 표제 아민을 수득하였다 (0.8 g), 수율: 69%.
단계 ( ii ): [2-(비스-시클로프로필메틸-아미노)-8-메틸-퀴놀린-3-일메틸]- (3,5-비스-트리플루오로메틸-벤질)-카르밤산 메틸 에스테르의 합성
표제 화합물을 단계 (iii)의 아세트아닐라이드 및 비스-시클로프로필메틸 아민 대신에 단계 (i)의 o-톨릴 아세트아닐라이드를 사용하는 것을 제외하고, 실시예 35에서와 동일한 절차를 이용함으로써 합성하였으며, 원하는 생성물을 밝은 황색의 점성이 있는 액체로 수득하였다 (0.05 g), 수율:40%, 순도 98.8% (HPLC: 시미트리 쉴드 RP8, [0.01 M KH2PO4: CH3CN], 217 nM, Rt 12.719분).
실시예
48
(3,5-
비스
-
트리플루오로메틸
-벤질) [2-(
시클로펜틸메틸
-에틸-아미노)-퀴놀린-3-일메틸]-디티오카르밤산
메틸
에스테르의 합성
25 mL의 둥근 바닥 플라스크 내의 무수 THF (15 mL) 중 수소화나트륨 (0.023 g, 0.98 mmol)의 현탁액에 0℃에서 실시예 35의 단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 (0.25 g, 0.44 mmol)을 첨가하였다. 이 반응 혼합물을 동일한 온도에서 10분 동안 교반하고, 이황화탄소 (0.112 g, 0.98 mmol)를 적가한 후, 메틸 요오다이드 (0.208 g, 1.47 mmol)를 첨가하였다. 반응물을 실온에 도달하도록 두고, 0.5시간 동안 지속적으로 교반하였다. 이어서, 물을 반응물에 첨가한 후, 이를 에틸 아세테이트로 추출하였다. 합한 유기층을 염수 용액으로 세척하고, 황산나트륨 상에서 건조시켰다. 용매를 증발시켜 표제 화합물을 수득하였다 (0.250 g), 수율: 87%, 순도 98.59% (HPLC: 시미트리 쉴드 RP8, [0.01 M KH2PO4: CH3CN], 217 nM, Rt 12.221분).
실시예
49
3-
에톡시카르보닐
-1-(3,5-
비스
-
트리플루오로메틸
-벤질)-1-[2-(
시클로펜틸
메
틸-에틸-아미노)-퀴놀린-3-일
메틸
]-
티오우레아의
합성
실시예 35의 단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸-메틸-에틸-아민 (0.5 g, 0.982 mmol), 에톡시카르보닐 이소티오시아네이트 (0.141 g, 1.08 mmol)를 50 mL의 둥근 바닥 플라스크에 넣고, 클로로포름을 이 혼합물에 첨가하였다. 반응물을 질소 대기 하에 0.5시간 동안 환류시킨 후, 반응 혼합물을 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.4 g), 수율: 65%, 순도 93.7% (HPLC:시미트리 쉴드 RP8, [0.01 M KH2PO4: CH3CN], 215 nM, Rt 9.337분).
실시예
50
[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
펜트
-1-
이닐
-퀴놀린-3-
일메틸
)-아미노]-아세트산
tert
-부틸 에스테르의 합성
단계 (i): (3,5-비스-트리플루오로메틸-벤질)-(2-클로로-퀴놀린-3-일메틸)-아민의 합성
3,5-비스-(트리플루오로메틸벤질아민) (6.31 g, 26 mmol) 및 아세트산 (1.5 mL, 36.4 mmol)을 무수 THF (100 mL)에 용해시킨 2-클로로-3-퀴놀린 카르복스알데히드 (5.01 g, 26 mmol)에 첨가하였다. 생성된 혼합물을 실온에서 1시간 동안 교반하였다. 이어서, 나트륨 트리아세톡시보로히드라이드 (7.71 g, 26 mmol)를 상기 용액에 첨가하고, 이 혼합물을 실온에서 밤새 교반하였다. 그 후, 혼합물을 에테르로 희석하고, 물로 2회 및 염수로 1회 세척하였다. 유기상을 수집하고, 탄산칼 륨 상에서 건조시키고, 회전 증발에 의해 농축시켰다. 생성된 샘플을 진공 하에 건조시키고, 정제하여 (바이오티지 호라이즌 HPFC 크로마토그래피 시스템, SiO2, 70:30 헥산:에틸 아세테이트) 회백색 고체를 수득하였다 (9.5 g), 수율: 87%, 순도 97.7% (HPLC: 이너트실 ODS-3V C18, 30:70 [KH2PO4 (0.01 M, pH 3.2): CH3CN], 264 nm, Rt 12.2분).
단계 ( ii ): [(3,5-비스-트리플루오로메틸-벤질)-(2-클로로-퀴놀린-3-일메틸)-아미노]-아세트산 tert-부틸 에스테르의 합성
단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-(2-클로로-퀴놀린-3-일메틸)-아민 (972 mg, 2.3 mmol)을 THF (10 mL)에 용해시킨 후, 디-tert-부틸 디카르보네이트 (587 mg, 2.53 mmol) 및 트리에틸아민 (0.32 mL, 2.3 mmol)을 첨가하였다. 생성된 혼합물을 실온에서 밤새 교반한 후, 회전 증발기에서 농축시켜 THF를 제거하였다. 조 샘플을 디클로로메탄으로 희석하고, 물로 2회 및 염수로 1회 세척하였다. 유기상을 탄산칼륨 상에서 건조시키고, 회전 증발에 의해 농축시키고, 밤새 진공 하에 건조시켜 [(3,5-비스-트리플루오로메틸-벤질)-(2-클로로-퀴 놀린-3-일메틸)-아미노]-아세트산 tert-부틸 에스테르를 회백색 고체로 수득하였다 (1.1 g, 90%), 순도 98.4% (HPLC: 이너트실 ODS-3V C18, 20:80 [KH2PO4 (0.01 M, pH 3.2): CH3CN], 264 nm, Rt 20.9분), 융점 84℃.
단계 ( iii ): [(3,5-비스-트리플루오로메틸-벤질)-(2-펜트-1-이닐-퀴놀린-3-일메틸)-아미노]-아세트산 tert-부틸 에스테르의 합성
단계 (ii)에서 수득한 [(3,5-비스-트리플루오로메틸-벤질)-(2-클로로-퀴놀린-3-일메틸)-아미노]-아세트산 tert-부틸 에스테르 (530 mg, 1 mmol)를 무수 DMF (5 mL) 및 무수 THF (2 mL)에 용해시킨 후, PdCl2(PPh3)2 (36.7 mg, 0.05 mmol), 트리에틸아민 (0.57 mL, 4.15 mmol), 요오드화구리 (11 mg, 0.05 mmol), 및 1-펜틴 (0.12 mL, 1.2 mmol)을 상기 THF 용액에 첨가하였다. 반응 용기를 알루미늄 호일에 싸고, 생성된 혼합물을 실온에서 밤새 교반하였다. 그 후, 이 샘플을 에틸 아세테이트로 희석하고, 셀라이트 (상표명; Celite)를 통해 여과하였다. 셀라이트 (상표명)를 에틸 아세테이트로 세척하고, 여과액을 물로 2회 및 염수로 1회 세척하였다. 유기상을 건조시키고, 여과하고, 회전 증발에 의해 농축시켰다. 생성된 샘 플을 진공 하에 밤새 건조시키고, 조 잔류물을 정제하여 (바이오티지 호라이즌 HPFC 크로마토그래피 시스템, SiO2, 80:20 헥산:에틸 아세테이트) 표제 화합물을 갈색 오일로 수득하였다 (458 mg), 수율: 83%, 순도 91.3% (HPLC: 이너트실 ODS-3V C18, 20:80 [KH2PO4 (0.01 M, pH 3.2): CH3CN], 264 nm, Rt 28.6분).
실시예
51
[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
펜틸
-퀴놀린-3-
일메틸
)-아미노]-아세트산
tert
-부틸 에스테르의 합성
실시예 16에서 수득한 화합물, [(3,5-비스-트리플루오로메틸-벤질)-(2-펜트-1-이닐-퀴놀린-3-일메틸)-아미노]-아세트산 tert-부틸 에스테르 (163 mg, 0.3 mmol)를 에탄올 (3 mL)에 용해시키고, 팔라듐 [탄소 상 10% 분말 (50 mg)]을 첨가하였다. 생성된 혼합물을 H2 하에 (풍선을 이용함) 3시간 동안 교반하였다. 샘플을 에탄올로 희석하고, 셀라이트 (상표명)를 통해 여과하였다. 셀라이트 (상표명)를 에탄올로 세척하고, 여과액을 회전 증발에 의해 농축시키고, 생성된 샘플을 밤 새 진공 하에 건조시키고, 조 물질을 정제하여 (바이오티지 호라이즌 HPFC 크로마토그래피 시스템, SiO2, 80:20 헥산: 에틸 아세테이트) 표제 생성물을 무색 오일로 수득하였다 (75 mg), 수율: 45%, 순도 96.3% (HPLC: 이너트실 ODS-3V C18, 20:80 [KH2PO4 (0.01 M, pH 3.2): CH3CN], 264 nm, Rt 49.0분)
실시예
52
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸
아민의
합성
단계 (i): (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드의 합성
MeOH (10 mL) 중 실시예 35의 단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루 오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 (0.372 g, 0.73 mmol)의 용액에 N2 대기 하에 중탄산나트륨 (0.122 g, 1.46 mmol)에 이어 브롬화시아노겐 (0.138 g, 1.31 mmol)을 첨가하였다. 반응 혼합물을 실온에서 4시간 동안 교반하였다. 이어서, 용매를 진공 하에 제거하여 조 잔류물을 수득하였으며, 이를 물에 용해시키고, 에틸 아세테이트로 추출하고, 황산나트륨 상에서 건조시켰다. 용매를 증발시키고, 진공에서 농축시켜 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸-메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드를 수득하였다 (0.4 g), 수율: 99%.
IR(KBr, cm-1): 3424, 2952, 2214, 1280;
단계 ( ii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
(3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드 (0.368 g, 0.689 mmol), 나트륨 아지드 (0.049 g, 0.758 mmol), 및 브롬화아연 (0.155 g, 0.689 mmol)을 N2 대기 하에 둥근 바닥 플라스크에 넣었다. 이 반응 혼합물에 물 (8 mL)을 첨가하고, 생성된 혼합물을 24시간 동안 격렬하게 교반하면서 환류시켰다. 그 후, 반응 혼합물을 실온으로 냉각시키고, HCl (3 N, 0.92 mL) 및 에틸 아세테이트의 혼합물을 첨가하였다. 고체가 분리되지 않을 때까지 격렬하게 지속적으로 교반하고, 수성층을 pH 1에 도달하게 하였다. 유기층을 분리하고, 진공 하에 농축시켰다. 수산화나트륨 (0.25 N, 6.25 mL)의 용액을 잔류물에 첨가하고, 잔류물이 용해될 때까지 30분 동안 교반하고, 수산화아연의 현탁액을 형성하였다. 현탁액을 여과하고, NaOH (1 N)로 세척하고, 여과액에 3 N HCl을 적가하여 산성화시켜 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민을 황색 고체로 수득하였다 (0.140 g), 수율: 35%.
단계 ( iii ): (3-{[3,5-비스 트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜타메틸-에틸 아민의 합성
물 (4 mL) 중 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민 (0.133 g, 0.230 mmol)의 현탁액에 수산화나트륨 (0.009 g, 0.230 mmol)을 첨가하고, 이 혼합물을 15분 동안 실온에서 교반한 후, 디클로로메탄 (4 mL)을 첨가하였다. 이 반응 혼합물에 디메틸 술페이트 (0.030 g, 0.241 mmol)에 이어 테트라부틸암모늄 브로마이드 (0.003 g, 0.011 mmol)를 첨가하였다. 이 혼합물을 24시간 동안 교반하였다. 유기층을 수성층으로부터 분리하고, 수성층을 DCM으로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 조 잔류물을 수득하였다. 이 잔류물을 100-200 메쉬 실리카겔 상에서 8% 에틸 아세테이트 및 석유 에테르를 사용한 칼럼 크로마토그래피에 의해 정제하여 (3-{[3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸-}-퀴놀린-2-일)-시클로펜틸-메틸-에틸 아민을 수득하였다 (0.030 g), 수율: 22%.
실시예
53
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(1-
메틸
-1H-
테트라졸
-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 52의 결합위치이성질체, (3-{[3,5-비스-트리플루오로메틸-벤질)-(1-메틸-1H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸 아민의 조 물질을 100-200 메쉬 실리카겔 상에서 석유 에테르 중 18% 에틸 아세테이트로 용리한 칼럼 크로마토그래피에 의해 정제한 후, 이를 동일한 반응 혼합물로부터 분리하였다 (0.2 g), 수율: 7%.
실시예 54
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-퀴놀린-2-일)-부틸-에틸
아민의
합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 (3-{[(3,5-비스-트리플루오 로메틸-벤질아미노)-메틸]-퀴놀린-2-일)-부틸-에틸-아민을 사용하여, 실시예 52의 실험 절차에 따라 점성질의 무색 액체로 제조하였다 (0.04 g), 수율: 11%.
실시예
55
3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로프로필메틸-에틸
아민의
합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로프로필메틸-에틸-아민을 사용하여, 실시예 52의 실험 절차에 따라 무색 점성질 액체로 제조하였다 (0.045 g), 수율: 29.6%.
실시예
56
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로부틸메틸-에틸
아민의
합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로부틸메틸-에틸-아민을 사용하여, 실시예 52의 실험 절차에 따라 무색의 점성질 액체로 제조하였다 (0.064 g), 수율: 27.3%.
실시예 57
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-8-메틸-퀴놀린-2-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-8-메틸-퀴놀린-2-일}-비스-시클로프로필메틸-아민을 사용하는 것을 제외하고, 실시예 52에서와 동일한 합성 절차에 따라 오일로 제조하였다 (0.07 g), 수율: 52%.
실시예
58
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(5-
메틸
-[1,3,4]
옥사디아졸
-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 52의 단계 (ii)에서 수득한 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1H-테트라졸-5-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민 (0.30 g, 0.519 mmol)을 무수 피리딘 (5 mL)에 첨가하고, 상기 용액을 0℃로 냉각시킨 후, 아세틸 클로라이드 (0.143 g, 1.8 mmol)를 첨가하였다. 이 반응 혼합물을 3시간 동안 환류시킨 후, 이를 실온으로 도달하도록 두고, 물로 희석하고, 이어서 수산화나트륨으로 염기성화시켰다. 피리딘을 공비혼합물로 제거하고, 잔류물을 에틸 아세테이트에 용해시키고, 칼럼 크로마토그래피에 의해 정제하여 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(5-메틸-[1,3,4]옥사디아졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민을 수득하였다 (0.110 g), 수율: 36%, 순도 96.91%.
실시예
59
1-(3,5-
비스
-
트리플루오로메틸
-벤질)-1-(
시클로펜틸메틸
-에틸-아미노)-퀴놀린-3-일메틸]-우레아의 합성
실시예 52의 단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드 (0.10 g, 0.19 mmol)를 둥근 바닥 플라스크에 질소 대기 하에 넣고, 과산화수소 (325 마이크로 리터)에 이어 수산화칼륨 (0.147 g, 0.18 mmol)을 첨가하였다. 반응 혼합물을 40℃에서 2시간 동안 교반한 후, 실온으로 냉각되도록 두었다. 물을 반응 혼합물에 첨가한 후, 에틸 아세테이트로 추출하였다. 합한 유기층을 염수 용액으로 세척하고, 황산나트륨 상에서 건조시켰다. 용매를 증발시켜 표제 화합물을 수득하였다 (0.1 g), 수율: 37%, 순도 91.00%.
실시예
60
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(4-
트리플루오로메틸
-
옥사졸
-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 59의 1-(3,5-비스-트리플루오로메틸-벤질)-1-(시클로펜틸메틸-에틸- 아미노)-퀴놀린-3-일메틸]-우레아 (0.1 g, 0.181 mmol), 및 3-브로모-1,1,1-트리플루오로 프로판-2-온 (0.032 g, 0.181 mmol)을 50 mL의 2-목 둥근 바닥 플라스크에 넣은 후, tert-부탄올 (10 mL)을 첨가하였다. 이 반응 혼합물을 질소 대기 하에 12시간 동안 환류시킨 후, 진공 하에 농축시켰다. 이어서, 물을 이 혼합물에 첨가하고, 수용액을 에틸 아세테이트로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하였다. 유기 용매를 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.03 g), 수율: 27%, 순도 93.7%.
실시예
61
1-(3,5-
비스
-
트리플루오로메틸
-벤질)-1-(2-
시클로펜틸메틸
-에틸-아미노)-퀴놀린-3-일
메틸
)-2-에틸
이소우레아의
합성
실시예 59의 1-(3,5-비스-트리플루오로메틸-벤질)-1-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-우레아 (0.1 g, 0.181 mmol), 및 트리에톡시 테트라플루오로보레이트 (0.034 g, 0.181 mmol)를 아르곤 대기 하에 25 mL의 2-목 둥근 바닥 플라스크에 넣은 후, DCE 4 mL를 이 혼합물에 첨가하였다. 이 반응 혼합물을 실온에서 12시간 동안 교반한 후, 현탁액을 여과하고, 생성된 침전물을 DCE (20 mL)로 세척하고, 진공 하에 건조시켜 표제 화합물을 수득하였다 (0.1 g), 수율: 95.2%, 순도 96.42%.
실시예
62
1-(3,5-
비스
-
트리플루오로메틸
-벤질)-1-[2-(
시클로펜틸메틸
-에틸-아미노)-퀴놀린-3-일
메틸
]-
티오우레아의
합성
실시예 49에서 수득한 3-에톡시카르보닐-1-(3,5-비스-트리플루오로메틸-벤질)-1-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일 메틸]-티오우레아 (0.3 g, 0.468 mmol), 및 2 N 수산화나트륨 (20 mL)을 50 mL의 둥근 바닥 플라스크에 넣었다. 반응 혼합물을 12시간 동안 환류시키고, 6 N 염산으로 중화시키고, 수용액을 에틸 아세테이트로 추출 (3 x 20 mL)하였다. 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.2 g), 수율: 75.2%, 순도 97.5%.
실시예
63
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(4-
메틸
-티아졸-2-일)-아미노]-
메틸
}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 62에서 수득한 1-(3,5-비스-트리플루오로메틸-벤질)-1-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일 메틸]-티오우레아 (0.1 g, 0.176 mmol), 및 클로로아세톤 (0.048 g, 0.528 mmol)을 50 mL의 둥근 바닥 플라스크에 넣고, 이어서 tert-부탄올을 첨가하였다. 반응물을 질소 대기 하에 12시간 동안 환류시킨 후, 반응 혼합물을 진공 하에 농축시키고, 물을 첨가하였다. 수용액을 에틸 아세테이트로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.04 g), 수율: 40%, 순도 93.3%.
실시예
64
시클로펜틸메틸
-(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(5-
메틸
-4,5-
디히드
로-옥사졸-2-일)-아미노]-메틸}-퀴놀린-2-일)-에틸-아민의 합성
실시예 52의 단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드 (0.10 g, 0.184 mmol), 1-아미노-2-프로판올 (0.018 g, 0.257 mmol), 및 카드뮴 아세테이트 (0.02 g)를 50 mL의 둥근 바닥 플라스크에 넣었다. 이 반응 혼합물을 100℃로 0.5시간 동안 가열하고, 실온으로 냉각시키고, 포화 염화나트륨 용액을 첨가하였다. 수용액을 디클로로메탄으로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.9 g), 수율: 83%, 순도 97.7%.
실시예
65
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질-(5-
메틸
-
이속사졸
-3-일)-아미노]-
메
틸}-퀴놀린-2-일)-시클로부틸메틸-에틸-아민의 합성
단계 (i): 시클로부틸메틸-에틸-{3-[(5-메틸-이속사졸-3-일아미노)-메틸]-퀴놀린-2-일}-아민의 합성
5-메틸-이속사졸-3-일아민 (0.098 g, 1 mmol)을 무수 메탄올 (5 mL) 및 아세트산 (0.15 mL) 중 2-(시클로부틸메틸-에틸-아미노)-퀴놀린-3-카르브알데히드 (0.268 g, 1 mmol)의 용액에 질소 하에 첨가하였다. 15분 동안 주변 온도에서 교반한 후, 나트륨 시아노보로히드라이드 (0.19 g, 3 mmol)를 서서히 첨가하고, 반응 혼합물을 밤새 교반하였다. 그 후, 용매를 진공에서 증발시키고, 물 (30 mL) 및 에틸 아세테이트 (30 mL)를 잔류물에 첨가하였다. 유기층을 분리하고, 염수로 세척하고, 황산나트륨 상에서 건조시키고, 여과하고, 진공에서 농축시켰다. 잔류물을 실리카겔 상에서 디클로로메탄 중 1 내지 5% 메탄올로 용리한 크로마토그래피에 의해 정제하여 표제 화합물을 수득하였다 (0.15O g), 수율: 43%.
단계 ( ii ): (3-{[3,5-비스-트리플루오로메틸-벤질-(5-메틸-이속사졸-3-일)-아미노]-메틸}-퀴놀린-2-일)-시클로부틸메틸-에틸-아민의 합성
나트륨 메톡시드 (0.108 g, 2.0 mmol)를 주변 온도에서 교반하면서 시클로부틸메틸-에틸-{3-[(5-메틸-이속사졸-3-일아미노)-메틸]-퀴놀린-2-일}-아민 (0.14 g, 0.4 mmol)의 무수 테트라히드로푸란 (6 mL) 용액에 첨가하였다. 이 혼합물을 15분 동안 교반한 후, 3,5-비스-트리플루오로메틸벤질 브로마이드 (0.08 mL, 0.4 mmol)를 서서히 첨가하고, 밤새 지속적으로 교반하였다. 에틸 아세테이트 (30 mL) 및 물 (30 mL)을 첨가하고, 층을 분리하였다. 수성층을 에틸 아세테이트로 역 추출 (2 x 30 mL)하고, 합한 유기 추출물을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공에서 농축시켰다. 조 잔류물을 실리카겔 상에서 에틸 아세테이트 중 10 내지 70% 헥산으로 용리한 크로마토그래피에 의해 정제하여 표제 화합물을 수득하였다 (0.045 g), 수율: 20%.
실시예
66
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-피리미딘-2-일-아미노]-
메틸
}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 35의 단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 (0.96 g, 1.88 mmol), 2-브로모피리미딘 (0.1 g, 0.26 mmol) 및 탄산칼륨 (0.26 g, 1.88 mmol)을 DMSO (1 mL)가 든 튜브에 넣고, 마이크로파로 150℃에서 2시간 동안 가열하였다. 조 잔류물을 헥산 중 5% 에틸 아세테이트로 용리한 실리카겔 (60-120 메쉬) 상에서 정제하여 표제 화합물을 수득하였다 (0.035 g), 수율: 30%, 순도 97.53%.
실시예
67
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(4-
메틸
-
옥사졸
-2-일)-아미노]-
메
틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 52의 단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드 (0.1 g, 0.184 mmol), 및 2 N 수산화나트륨 (0.08 g, 0.22 mmol)을 디옥산 (10 mL)이 든 50 mL의 둥근 바닥 플라스크에 넣고, 히드록시아세톤 (0.013 g, 0.18 mmol)을 실온에서 적가하였다. 반응 혼합물을 2 내지 4시간 동안 환류시킨 후, 반응물을 실온으로 냉각시키고, 물을 첨가하였다. 수용액을 에틸 아세테이트로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.03 g), 수율: 27%, 순도 97.4%.
실시예
68
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(4,5-
디히드로
-
옥사졸
-2-일)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 52의 단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-4-일]-시안아미드 (0.5 g, 0.936 mmol), 2-아미노-에탄올 (1.2 mL, 1.3 mmol), 및 카드뮴 아세테이트 (0.02 g)를 50 mL의 둥근 바닥 플라스크에 넣었다. 이 반응 혼합물을 0.5시간 동안 100℃로 가열한 후, 반응물을 실온으로 냉각시키고, 포화 염화나트륨 용액을 상기 혼합물에 첨가하였다. 수용액을 DCM으로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 용매를 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.1 g), 수율: 18%, 순도 97.5%.
실시예
69
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-피리딘-2-일-아미노]-
메틸
}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
순도 97.45%의 표제 화합물을 단계 (i)에서 2-(시클로부틸메틸-에틸-아미노)-퀴놀린-3-카르브알데히드 대신에 2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-카르브알데히드를, 5-메틸-이속사졸-3-일아민 대신에 2-아미노 피리딘을 사용하는 것을 제외하고, 실시예 65의 실험 절차에 따라 합성하였다 (0.10 g), 수율: 31%.
실시예
70
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-
일메틸
)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
단계 (i): (3-{[3,5-비스 트리플루오로 메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-아미노}-아세토니트릴의 합성
N2 대기 하에, 탄산칼륨 (0.4 g, 2.94 mmol)을 MeOH (10 mL) 중 실시예 35의 단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 (0.5 g, 0.98 mmol)의 용액에 첨가하고, 이어서 클로로아세토니트릴 (0.64 g, 0.98 mmol)을 첨가하였다. 이 반응 혼합물을 실온에서 4시간 동안 교반하였다. 그 후, 용매를 진공 하에 제거하여 조 잔류물을 수득하였으며, 이를 물에 용해시키고, 에틸 아세테이트로 추출하고, 황산나트륨 상에서 건조시켰다. 용매를 증발시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.25 g), 수율: 47%.
단계 ( ii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1H-테트라졸-5-일메틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 19에서 수득한 (3-{[3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-퀴놀린-3-일메틸]-아미노}-아세토니트릴 (0.26 g, 0.474 mmol), 나트륨 아지드 (0.154 g, 2.37 mmol), 및 염화암모늄 (0.126 g, 2.37 mmol)을 DMF (10 mL)가 든 50 mL의 둥근 바닥 플라스크에 넣었다. 반응물을 질소 대기 하에 1시간 동안 환류시켰다. 이어서, 반응 혼합물을 실온으로 냉각시키고, 수용액을 에틸 아세테이트로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하였다. 이어서, 용매를 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.25 g), 수율: 92%.
m/z (ES-MS): 592 (M++1, 100%)
단계 ( iii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일메틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
물 (4 mL) 중 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일메 틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민 (0,25 g, 0.423 mmol)의 현탁액에 수산화나트륨 (0.033 g, 0.846 mmol)을 첨가하고, 생성된 혼합물을 15분 동안 실온에서 교반한 후, DCM (4 mL)을 첨가하였다. 이어서, 디메틸 술페이트 (0.058 g, 0.465 mmol)를 이 혼합물에 첨가한 후, 테트라부틸암모늄 브로마이드 (0.006 g, 0.021 mmol)를 첨가하고, 생성된 혼합물을 15분 동안 지속적으로 교반하였다. 이어서, 유기층을 수성층으로부터 분리하고, 수성층을 DCM으로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 잔류물을 수득하였다. 이 잔류물을 100-200 메쉬 실리카겔 상에서 석유 에테르 중 4% 에틸 아세테이트를 사용하여 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 수득하였다 (0.08 g), 수율: 31.3%.
실시예
71
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(1-
메틸
-1H-
테트라졸
-5-
일메틸
)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
실시예 70의 결합위치이성질체, (3-{[(3,5-비스-트리플루오로메틸-벤질)-(1-메틸-1H-테트라졸-5-일메틸)-아미노]-메틸}-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 조 잔류물을 100-200 메쉬 실리카겔 상에서 석유 에테르 중 15% 에틸 아세테이트를 사용하여 칼럼 크로마토그래피에 의해 정제한 후, 이를 동일한 반응 혼합물로부터 분리하였다 (0.03 g), 수율: 17%.
실시예
72
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸-}-8-에틸-퀴놀린-2-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로 메틸-벤질아미노)-메틸]-8-에틸-퀴놀린-2-일}-비스-시클로프로필메틸-아민을 사용하는 것을 제외하고, 실시예 52에 개시된 바와 동일한 합성 절차에 따라 합성하여 상기 화합물을 오일로 수득하였다 (0.60 g), 수율: 54%.
실시예
73
(3-{[3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-피리딘-2-일)-부틸-에틸
아민의
합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-퀴놀린-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-피리딘-2-일}-부틸-에틸-아민을 사용하는 것을 제외하고, 실시예 52의 실험 절차에 따라 무색 점성질 액체로 제조하였다.
실시예
74
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로펜틸메틸
-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-일메틸]-카르밤산
메틸
에스테르의 합성
단계 (i): 2-포르밀 시클로헥사논의 나트륨 염의 합성
나트륨 (2.8 g)을 1 L의 둥근 바닥 플라스크 내의 무수 에테르 300 mL에 넣고, 아세톤-무수 얼음조를 사용하여 현탁액을 0℃로 냉각시켰다. 이 냉각된 현탁액에 무수 에테르 (100 mL) 중 에틸 포르메이트 (0.21 mol) 및 시클로헥사논 (0.204 mol)의 혼합물을 첨가하였다. 반응 혼합물의 온도가 실온에 도달하도록 두고, 밤새 지속적으로 교반하였다. 조 현탁액을 여과하고, 침전물을 진공 하에 2시간 동안 건조시켜 (2-옥소-시클로헥실리덴)나트륨 메탄올레이트를 수득하였다 (16.0 g), 수율: 82%.
m/z (ES-MS): 126 (M++1, 100%), 125 (M+-1, 30%), 97 (M+-CHO, 50%).
단계 ( ii ): 2-옥소-1,2,5,6,7,8-헥사히드로-퀴놀린-3-카르보니트릴의 합성
톨루엔 (300 mL) 중 2-포르밀시클로헥사논의 나트륨 염 (16.0 g, 10.8 mmol)의 용액에 시아노아세트아미드 (22.00 g, 0.237 mol)를 첨가하고, 반응물을 실온에서 1시간 동안 교반되도록 두었다. 그 후, 디클로로메탄 (25 mL) 중 피페리딘 아세테이트의 2 M 용액을 첨가하고, 반응물을 24시간 동안 환류시켰다. 이어서, 반응 혼합물을 0℃로 냉각시키고, 아세트산으로 산성화시켰다. 생성된 현탁액을 여과하고, 침전물을 톨루엔으로 세척하였다. 여과액을 농축시켜 점성 잔류물을 수득하였으며, 이를 디에틸 에테르에 이어 에틸 아세테이트로 처리하여 2-옥소-1,2,5,6,7,8-헥사히드로-퀴놀린-3-카르보니트릴을 미세한 고체로 수득하였다 (6.00 g), 수율: 31.8%.
m/z (CI-MS): 175 (M++1, 100%)
IR (cm-1): 2227 (CN), 1664 (CO).
단계 ( iii ): 2-클로로-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴
2-옥소-1,2,5,6,7,8-헥사히드로퀴놀린-3-카르보니트릴 (6.0 g, 34.4 mmol)에 옥시염화인 (20 mL)을 첨가하고, 이 혼합물을 실온에서 1시간 동안 교반한 후, 12시간 동안 환류시켰다. 과량의 옥시염화인을 증류시키고, 잔류물을 빙냉수에 부었다. 수용액을 포화 중탄산나트륨 용액으로 염기성화시키고, 형성된 침전물을 여과하였다. 침전물을 2% 에틸 아세테이트 및 석유 에테르로 용리한 칼럼 크로마토그래피로 정제하여 2-클로로-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴을 수득하였다 (5.00 g), 수율: 75%.
단계 ( iv ): 2-(시클로펜틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴의 합성
무수 디옥산 (15 mL)을 2-클로로-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴 (3.0 g, 15.62 mmol), 탄산칼륨 (8.6 g, 62.5 mmol), CuI (5 mol%, 0.064 g), 및 트랜스-1,2-시클로헥산디아민 (5 mol%, 0.089 g)의 혼합물에 아르곤 대기 하에서 첨가하였다. 이어서, 디옥산 중 N-시클로펜틸-에틸아민 (2.3 g, 18.75 mmol)의 용액을 교반된 반응 혼합물에 첨가한 후, 이를 24시간 동안 환류시켰다. 그 후, 용매를 진공 하에 증발시키고, 잔류물을 실리카겔 (100-200 메쉬) 상에서 2% 에틸 아세테이트 및 석유 에테르로 용리한 칼럼 크로마토그래피로 정제하여 2-(시클로펜 틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴을 수득하였다 (0.3 g), 수율: 10%.
단계 (v): (3-아미노메틸-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸아민의 합성
THF (15 mL) 중 LAH (0.600 g, 16 mmol)의 현탁액에 무수 THF 중 2-(시클로펜틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-카르보니트릴 (0.300 g, 1.06 mmol)의 용액을 첨가하였다. 이 반응 혼합물을 14시간 동안 온화하게 환류시켰다. 이어서, 반응하지 않은 LAH를 황산나트륨의 포화 용액으로 켄칭시키고, 잔류물을 여과하고, 디에틸 에테르로 세척하였다. 세척액을 수집하고, 황산나트륨 상에서 건조시키고, 용매를 증발시켜 (3-아미노메틸-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸아민을 수득하였다 (0.2 g), 수율: 65%.
단계 ( vi ): {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6,7,8-테트라히드로-퀴놀린-2-일}-시클로펜틸메틸-에틸아민의 합성
MeOH (3 mL) 중 3,5-비스-트리플루오로메틸 벤즈알데히드 (0.185 g, 0.76 mmol)의 용액에 (3-아미노메틸-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸아민 (0.2 g, 0.69 mmol)에 이어 아세트산 (0.08 mL, 1.39 mmol)을 첨가하였다. 이 반응 혼합물을 실온에서 1시간 동안 교반한 후, 나트륨 시아노보로히드라이드 (0.172 g, 2.78 mmol)를 첨가하고, 추가 8시간 동안 지속적으로 교반하였다. 이어서, 용매를 진공 하에 증발시키고, 물을 첨가한 후, 생성물을 에틸 아세테이트로 추출하였다. 유기층을 포화 아황산나트륨 용액으로 세척하고, 유기층을 분리하고, 황산나트륨 상에서 건조시키고, 용매를 증발시켜 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6,7,8-테트라히드로-퀴놀린-2-일}-시클로펜틸메틸-에틸아민을 수득하였다 (0.250 g), 수율: 70%.
단계 ( vii ): (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르의 합성
무수 THF (5 mL) 중 탄산칼륨 (0.269 g, 1.949 mmol)의 현탁액에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6,7,8-테트라히드로-퀴놀린-2-일}-시클로펜틸메틸-에틸아민 (0.25 g, 0.3 mmol)의 THF 용액 (10 mL)을 첨가한 후, 이를 1시간 동안 교반하였다. 이어서, 메틸 클로로포르메이트 (0.137 g, 1.46 mmol)를 첨가하고, 실온에서 8시간 동안 지속적으로 교반하였다. 이어서, 용매를 증발시키고, 물을 첨가하고, 생성물을 에틸 아세테이트로 추출하였다. 유기층을 황산나트륨 상에서 건조시키고, 용매를 증발시켜 잔류물을 수득하였다. 이러한 조 잔류물을 실리카겔 (100-200 메쉬) 상에서 2% 에틸 아세테이트 및 석유 에테르로 용리하여 정제하여 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-5,6,7,8-테트라히드로-퀴놀린-3-일메틸]-카르밤산 메틸 에스테르를 밝은 녹색의 페이스트 같은 화합물로 수득하였다 (0.05 g), 수율: 15%.
실시예
75
(3,5-
비스
-
트리플루오로메틸
-벤질)-[2-(
시클로펜틸메틸
-에틸-아미노)-6,7-
디 히드로
-5H-[1]피리딘-3-일메틸]-카르밤산
메틸
에스테르의 합성
순도 96%의 표제 화합물을 단계 (i)에서 시클로헥사논 대신에 시클로펜타논을 사용하는 것을 제외하고, 실시예 74에 제시된 바와 동일한 실험 절차에 따라 제조하였다 (0.03 g), 수율: 13%.
실시예
76
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-6,7-디히드로-5H-[1]피리딘-2-일)-시클로펜틸메틸-에틸-아민의 합성
단계 (i): (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-6,7-테트라히드로-5H-[1]피리딘-3-일메틸]-시안아미드의 합성
실시예 2의 단계 (vi)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6,7,8-테트라히드로-퀴놀린-2-일}-시클로펜틸메틸-에틸아민과 같이 제조한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-6,7-디히드로-5H-[1]-피리딘-2-일}-시클로펜틸메틸-에틸아민 (1.20 g, 2.4 mmol)의 용액을 DMF (10 mL) 중에서 제조하고, 탄산칼륨 (0.995 g, 7.21 mmol)에 이어 브롬화시아노겐 (0.303 g, 2.88 mmol)을 첨가하였다. 이 반응 혼합물을 실온에서 밤새 교반한 후, 분쇄한 얼음을 첨가하고, 생성된 수성층을 에틸 아세테이트로 추출하고, 염수로 세척하였다. 유기층을 황산나트륨 상에서 건조시키고, 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (1.20 g), 수율: 95%.
단계 ( ii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일)-아미노]-메틸}-6,7-디히드로-5H-[1]피리딘-2-일)-시클로펜틸메틸-에틸-아민의 합성
단계 (i)에서 수득한 (3,5-비스-트리플루오로메틸-벤질)-[2-(시클로펜틸메틸-에틸-아미노)-6,7-테트라히드로-5H-[1]피리딘-3-일메틸]-시안아미드 (0.8 g, 1.526 mmol), 나트륨 아지드 (0.496 g, 7.633 mmol), 및 염화암모늄 (0.408 g, 7.633 mmol)을 50 mL의 둥근 바닥 플라스크에 무수 DMF (10 mL)와 함께 넣었다. 이 혼합물을 질소 대기 하에 1시간 동안 환류시킨 후, 실온으로 냉각시키고, 빙냉수 (15 mL)를 첨가하였다. 이 수용액을 에틸 아세테이트로 추출 (3 x 10 mL)하였다. 합한 유기층을 염수로 세척하고, 용매를 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.800 g), 수율: 92.4%.
단계 ( iii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-6,7-디히드로-5H-[1]피리딘-2-일)-시클로펜틸메틸-에틸-아민의 합성
물 8 mL 중 단계 (ii)에서 수득한 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일)-아미노]-메틸}-6,7-디히드로-5H-[1]피리딘-2-일)-시클로펜틸메틸-에틸-아민 (0.800 g, 1.446 mmol)의 수성 현탁액에 수산화나트륨 (0.115 g, 2.890 mmol)을 첨가하고, 이 혼합물을 15분 동안 실온에서 교반한 후, DCM (8 mL)을 첨가하였다. 이어서, 디메틸 술페이트 (0.200 g, 1.591 mmol)에 이어 테트라부틸암모늄 브로마이드 (0.023 g, 0.072 mmol)를 첨가하였다. 이 혼합물을 0.5시간 동안 교반한 후, 유기층을 수성층으로부터 분리하고, 수성층을 DCM으로 추출 (3 x 10 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시킨 후, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.500 g), 수율: 61%.
실시예
77
(3-{[3,5-
비스
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
표제 화합물을 단계 (i)에서 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-6,7-디히드로-5H-[1]피리딘-2-일}-시클로펜틸메틸-에틸-아민 대신에 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6,7,8-테트라히드로-퀴놀린-2-일}-시클로펜틸메틸-에틸아민을 사용하는 것을 제외하고, 실시예 76에 재시된 바와 같은 절차에 따라 제조하였다 (0.04 g), 수율: 35%.
실시예
78
(3-{[3,5-
비스
트리플루오로메틸
-벤질)-(5-
메틸
-[1,3,4]
옥사디아졸
-2-일)-아미노]-메틸}-5,6,7,8-테트라히드로퀴놀린-2-일)-시클로펜틸메틸-에틸-아민의 합성
(3-{[3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일)-아미노]-메틸}- 5,6,7,8-테트라히드로-퀴놀린-2-일)-시클로펜틸메틸-에틸-아민 (0.2 g, 0.344 mmol)을 무수 피리딘 (5 mL)에 첨가하고, 상기 용액을 0℃로 냉각시키고, 아세틸 클로라이드 (0.094 g, 1.2 mmol)를 첨가한 후, 반응물을 3시간 동안 환류시켰다. 그 후, 반응물을 실온으로 냉각되도록 두고, 물로 희석한 후, 수산화나트륨으로 염기성화시켰다. 피리딘을 공비 혼합물로 제거하고, 잔류물을 에틸 아세테이트에 용해시키고, 칼럼 크로마토그래피에 의해 정제하여 표제 화합물을 수득하였다 (0.110 g), 수율: 40%.
실시예
79
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-5,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민의 합성
단계 (i): 3-포르밀-2-부타논의 나트륨 염의 합성
나트륨 (5.80 g)을 1 L 둥근 바닥 플라스크 내의 무수 에테르 300 mL에 첨가하고, 현탁액을 아세톤-무수 얼음조를 사용하여 0℃로 냉각시켰다. 이 냉각된 현탁액에 무수 에테르 (100 mL) 중 에틸 포르메이트 (0.256 mol) 및 2-부타논 (0.232 mol)의 혼합물을 첨가하였다. 이 혼합물을 실온으로 가온되도록 두고, 밤새 지속적으로 교반하였다. 이어서, 조 현탁액을 여과하고, 침전물을 2시간 동안 진공 하에 건조시켜 표제 화합물을 수득하였다 (21.0 g), 수율: 79.2%.
단계 ( ii ): 2-옥소-1,2-디히드로-5,6-디메틸 피리딘-3-카르보니트릴의 합성
시아노 아세트아미드 (3.78 g, 0.237 mol)를 물 (100 mL) 중 3-포르밀-2-부타논의 나트륨 염 (5.00 g, 40.9 mmol)의 용액에 첨가하고, 이 반응물을 실온에서 1시간 동안 교반되도록 두었다. 그 후, 물 (10 mL) 중 피페리딘 아세테이트의 2 M 용액을 첨가하고, 반응 혼합물을 24시간 동안 환류되도록 두었다. 이 혼합물을 냉각되도록 두고, 아세트산으로 산성화시켰다. 현탁액을 여과하고, 침전물을 톨루엔 으로 세척하였다. 여과액을 수집하고, 농축시켜 점성 잔류물을 수득하였으며, 이를 디에틸 에테르에 이어 에틸 아세테이트로 세척하여 표제 화합물을 수득하였다 (2.00 g), 수율: 33%, 밝은 갈색 고체.
단계 ( iii ): 2-클로로-5,6-디메틸 피리딘-3-카르보니트릴의 합성
옥시염화인 (15 mL)을 50 mL의 2목 둥근 바닥 플라스크 내의 2-옥소-1,2-디히드로-5,6-디메틸 피리딘-3-카르보니트릴 (2.00 g, 13.5 mmol)에 첨가하고, 이 혼합물을 실온에서 1시간 동안 교반한 후, 12시간 동안 환류시켰다. 그 후, 과량의 옥시염화인을 증류시키고, 잔류물을 빙냉수에 부었다. 수용액을 포화 중탄산나트륨 용액으로 염기성화시키고, 형성된 침전물을 여과하여 표제 화합물을 수득하였다 (1.50 g), 수율: 66.7%.
단계 ( iv ): 2-(비스-시클로프로필메틸-아미노)-5,6-디메틸 피리딘-3-카르보니트릴의 합성
DMF (5 mL)를 단계 (iii)에서 수득한 2-클로로-5,6-디메틸 피리딘-3-카르보니트릴 (1,50 g, 9,0 mmol), 및 탄산칼륨 (3.70 g, 26.8 mmol)의 혼합물에 첨가하였다. DMF 중 비스-시클로프로필메틸-아민 (1.2 g, 9.6 mmol)의 용액을 교반된 반응 혼합물에 서서히 첨가한 후, 반응물을 24시간 동안 환류시켰다. 이어서, 반응물을 실온으로 냉각시키고, 분쇄한 얼음에 부은 후, 에틸 아세테이트로 추출 (3 x 20 mL)하였다. 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (0.500 g), 수율: 22.7%.
단계 (v): 2-(비스-시클로프로필메틸-아미노)-5,6-디메틸 피리딘-3-카르브알데히드의 합성
단계 (iv)에서 수득한 2-(비스-시클로프로필메틸-아미노)-5,6-디메틸 피리딘-3-카르보니트릴 (0.5 g, 1.96 mmol)을 무수 THF와 함께 50 mL의 2목 둥근 바닥 플라스크에 넣었다. 반응 혼합물을 0℃로 냉각시키고, THF 중 DIBAL (1.8 g, 12.9 mmol)의 20% (w/v) 용액을 이 혼합물에 적가하였다. 이 혼합물을 0℃에서 유지시키고, 1시간 동안 교반하였다. 그 후, 반응물을 실온으로 도달하도록 두고, 1 N HCl (10 mL)을 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 10 mL)하였다. 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (0.2 g), 수율: 40%.
단계 ( vi ): {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6-디메틸- 피리딘-2-일}-비스-시클로프로필메틸-아민의 합성
MeOH (3 mL) 중 단계 (v)에서 수득한 2-(비스-시클로프로필메틸-아미노)-5,6-디메틸 피리딘-3-카르브알데히드 (0.2 g, 0.775 mmol), 및 3,5-비스-트리플루오로메틸 벤질 아민 (0.18 g, 0.74 mmol)의 용액에 아세트산 (0.093 mL, 1.5 mmol)을 첨가하였다. 이 반응 혼합물을 실온에서 1시간 동안 교반한 후, 나트륨 시아노보로히드라이드 (0.096 g, 1.5 mmol)를 첨가하였다. 이 혼합물을 추가 2시간 동안 교반한 후, 용매를 진공 하에 증발시키고, 물을 첨가하고, 생성물을 에틸 아세테이트로 추출하였다. 유기층을 포화 중탄산나트륨 용액으로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 증발시켜 표제 화합물을 수득하였다 (0.300 g), 수율: 81 %.
단계 ( vii ): [2-(비스-시클로프로필메틸-아미노)-5,6-디메틸-피리딘-3-일메틸]-(3,5-비스-트리플루오로메틸-벤질-시안아미드의 합성
단계 (vi)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-5,6-디메틸-피리딘-2-일}-비스-시클로프로필메틸-아민 (0.300 g, 0.600 mmol)의 용액에 중탄산나트륨 (0.15 g, 1.7 mmol)을 N2 대기 하에 첨가한 후, 브롬화시아노겐 (0.13 g, 1.2 mmol)을 첨가하였다. 이 혼합물을 실온에서 0.5시간 동안 교반한 후, 진공 하에 농축시켰다. 이어서, 물을 첨가하고, 수성층을 에틸 아세테이트로 추출하고, 염수로 세척하고, 황산나트륨 상에서 건조시켰다. 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (0.297 g), 수율: 95%.
단계 ( viii ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일)- 아미노]-메틸}-5,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민의 합성
단계 (vii)에서 수득한 [2-(비스-시클로프로필메틸-아미노)-5,6-디메틸-피리딘-3-일메틸]-(3,5-비스-트리플루오로메틸-벤질-시안아미드 (0.297 g, 0.58 mmol), 나트륨 아지드 (0.18 g, 2.7 mmol), 및 염화암모늄 (0.15 g, 2.7 mmol)을 무수 DMF (10 mL)와 함께 50 mL의 둥근 바닥 플라스크에 넣었다. 반응물을 질소 대기 하에 1시간 동안 환류시킨 후, 실온으로 냉각되도록 두었다. 이어서 빙냉수 (10 mL)를 DMF 중 반응 혼합물에 첨가하고, 수용액을 에틸 아세테이트로 추출 (3 x 20 mL)하고, 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다. 이 화합물을 정제 없이 다음 단계에서 사용하였다 (0.3 g), 수율: 93.7%
m/z (CI-MS) 557 (M++1, 100%)
단계 ( ix ): (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2-메틸-2H-테트라졸-5-일)-아미노]-메틸}-5,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민의 합성
물 (4 mL) 중 단계 (viii)에서 수득한 (3-{[(3,5-비스-트리플루오로메틸-벤질)-(2H-테트라졸-5-일)-아미노]-메틸}-5,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민 (0.3 g, 0.54 mmol)의 현탁액에 수산화나트륨 (0.04 g, 1.0 mmol)을 첨가하고, 이 혼합물을 15분 동안 실온에서 교반한 후, DCM (4 mL)을 첨가하였다. 이어서, 디메틸 술페이트 (0.13 g, 1.03 mmol)를 이 혼합물에 첨가한 후, 테트라부틸암모늄 브로마이드 (0.008 g, 0.024 mmol)를 첨가하였다. 이어서, 혼합물을 0.5시간 동안 교반한 후, 유기층을 수성층으로부터 분리하고, 이를 DCM으로 추출 (3 x 10 mL)하였다. 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시킨 후, 진공 하에 농축시켜 표제 화합물을 밝은 황색 오일로 수득하였다 (0.200 g), 수율: 66.6%.
실시예
80
(3-{[(3,5-
비스
-
트리플루오로메틸
-벤질)-(2-
메틸
-2H-
테트라졸
-5-일)-아미노]-메틸}-4,6-디메틸-피리딘-2-일)-비스-시클로프로필메틸-아민의 합성
표제 화합물을 단계 (i)에서 2-부타논 대신에 펜탄-2,4-디온을 사용하는 것을 제외하고, 실시예 79에 제시된 실험 절차에 따라 제조하였다 (0.2 g) 수율: 39.1%.
실시예
81
(3,5-
비스
-
트리플루오로메틸
-벤질)-[3-(
시클로펜틸메틸
-에틸-아미노)-피라진-2-일메틸]-카르밤산
메틸
에스테르의 합성
단계 (i): 3-브로모-피라진-2-카르복실산 메틸 에스테르의 합성
브롬화구리 (1.36 g, 6.1 mmol) 및 t-부틸 니트라이트 (0.78 g, 7.6 mmol)를 아세토니트릴 (2 mL)과 함께 50 mL의 둥근 바닥 플라스크에 넣고, 이 혼합물을 60℃에서 5분 동안 가열하였다. 그 후, 3-아미노-피라진-2-카르복실산 메틸 에스테 르 (0.8 g, 5.09 mmol)를 교반하면서 일부분씩 나누어 첨가하고, 동일한 온도에서 추가 10분 동안 지속적으로 교반하였다. 이어서, 반응 혼합물을 실온으로 냉각시키고, 희석된 HCL (2 N) 100 mL에 부은 후, 디에틸 에테르로 추출 (3 x 50 mL)하였다. 합한 유기층을 희석된 HCl로 세척하고, 황산나트륨 상에서 건조시킨 후, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.139 g), 수율: 12%.
단계 ( ii ): 2-(시클로펜틸메틸-에틸-아미노)-피라진-2-카르복실산 메틸 에스테르의 합성
단계 (i)의 스케일-업 (scale-up) 반응으로부터 수득한 3-브로모-피라진-2-카르복실산 메틸 에스테르 (0.893 g, 4.11 mmol), 및 탄산칼륨 (1.7 g, 12.3 mmol)을 50 mL의 2목 둥근 바닥 플라스크에 첨가하였다. 이 플라스크에, DMF 10 mL를 첨가한 후, N-시클로펜틸메틸 에틸 아민 (0.627 g, 4.93 mmol)의 DMF 용액을 적가하였다. 이 혼합물을 밤새 환류시킨 후, 실온으로 냉각되도록 두고, 분쇄한 얼음 (10 mL)에 붓고, 에틸 아세테이트로 추출 (3 x 50 mL)하였다. 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (0.468 g), 수율: 43%.
단계 ( iii ): 3-(시클로펜틸메틸-에틸-아미노)-피라진-2-카르브알데히드의 합성
단계 (ii)에서 수득한 2-(시클로펜틸메틸-에틸-아미노)-피라진-2-카르복실산 메틸 에스테르 (0.468 g, 1.77 mmol)를 무수 DCM과 함께 50 mL의 2목 둥근 바닥 플라스크에 넣었다. 반응 혼합물을 -70℃로 냉각시키고, DIBAL (톨루엔 중 20% 용액, 0.252 g, 1.77 mmol)을 상기 혼합물에 교반하면서 적가하고, 동일한 온도에서 1시간 동안 지속적으로 교반하였다. 이 혼합물을 실온으로 가온되도록 두고, 포화 염화암모늄 용액으로 켄칭시키고, DCM으로 추출 (3 x 30 mL)하였다. 합한 유기층을 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 진공 하에 증발시켜 표제 화합물을 수득하였다 (0.082 g), 수율: 20%.
단계 ( iv ): {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-피라진-2-일}-시클로펜틸메틸-에틸-아민의 합성
단계 (iii)에서 수득한 3-(시클로펜틸메틸-에틸-아미노)-피라진-2-카르브알데히드 (0.082 g, 0.351 mmol), 3,5-비스-트리플루오로메틸벤질아민 (0.085 g, 0.351 mmol), 및 아세트산 (0.042 g, 0.70 mmol)을 25 mL의 둥근 바닥 플라스크에 넣었다. 메탄올 (4 mL)을 첨가하고, 이 혼합물을 실온에서 15분 동안 교반하였다. 이어서, 나트륨 시아노보로히드라이드 (0.066 g, 1.05 mmol)를 일부분씩 나누어 첨가하고, 실온에서 추가 1시간 동안 지속적으로 교반하였다. 메탄올을 진공 하에 제거하고, 물을 조 혼합물에 첨가하고, 생성물을 에틸 아세테이트로 추출 (3 x 25 mL)하였다. 합한 유기층을 포화 중탄산나트륨 용액에 이어 염수로 세척하고, 황산나트륨 상에서 건조시키고, 용매를 증발시켜 표제 아민을 수득하였다 (0.163 g), 수율: 90%.
단계 (v): (3,5-비스-트리플루오로메틸-벤질)-[3-(시클로펜틸메틸-에틸-아미노)-피라진-2-일메틸]-카르밤산 메틸 에스테르의 합성
단계 (iv)에서 수득한 {3-[(3,5-비스-트리플루오로메틸-벤질아미노)-메틸]-피라진-2-일}-시클로펜틸-메틸-에틸-아민 (0.155 g, 0.33 mmol), 및 K2CO3 (0,139 g, 1.0 mmol)을 N2 대기 하에 2목 둥근 바닥 플라스크에 넣었다. 무수 THF (3 내지 4 mL)를 플라스크에 첨가하고, 이 혼합물을 실온에서 30분 동안 교반하였다. 이어서, 메틸클로로포르메이트 (0.038 g, 0.404 mmol)를 상기 혼합물에 적가하고, 반응물을 실온에서 밤새 교반되도록 두었다. 용매를 진공 하에 제거하고, 물을 첨가하고, 생성물을 에틸 아세테이트로 추출하였다. 유기층을 황산나트륨 상에서 건조시키고, 진공 하에 농축시켜 표제 화합물을 수득하였다 (0.020 g), 수율: 12%.
실시예
82
시험관내
활성의 측정
CETP 저해제를 확인하기 위한 시험관내 형광-기재 분석을 문헌 [Bisgaier et al., J Lipid Res., 34(9): 1625-34 (1993)] 및 [Epps et al., Chem Phys Lipids., 77(1): 51-63 (1995)]에 개략된 프로토콜의 변형으로부터 개발하였다. 수용체 및 공여체 지질 마이크로에멀젼은, 완충액을 0.67 ug/mL 인간 HDL (칼바이오켐 (Calbiochem))로 제조한 것을 제외하고, 문헌 [Bisgaier et al, 1993]에 따라 제조하였다. 형광 콜레스테릴 에스테르 유사체 BODIPY-CE (몰레큘라 프로브스 (Molecular Probes))를 함유하는 공여체 마이크로에멀젼은 각각 503 nm 및 518 nm에서 최대 여기 및 방출로 특성화시켰다. 형광 콜레스테릴 에스테르의 수용체 입자로의 CETP-매개된 수송은 MX3000P 형광 플레이트 해독기 (스트라타진 (Stratagene))에서 FAM 필터 세트 (여기 492 nm, 방출 516 nm)를 사용하여 2시간에 걸쳐 모니터링하였다. 재조합 CETP 효소 (심장혈관 표적)는 지질 수송을 달성하기 위해 최종 농도 0.14 ng/μl에서 사용되었다. 화합물에 의한 CETP 저해를 DMSO 대조군과 비교하여, 2시간에 걸친 CETP 활성 조절을 백분율로서 그래프를 작성하였다. CETP 저해에 대한 IC50 곡선은 활성화 프로파일로부터 생성하였다. 활성 화합물은 또한 3% 인간 혈청 알부민, 분획 V (칼바이오켐)의 존재 하에, 상기와 같이 CETP 저해에 대해 시험하였다.
이러한 프로토콜을 사용하여, 실시예 35, 41, 42, 43, 44, 45, 46, 48, 49, 53, 58, 59, 61, 63, 66, 68, 69, 70, 71, 73 및 75에 제시된 화합물은 IC50값이 5 μM 이하인 CETP 활성을 나타내었고; 실시예 1, 2, 3, 4, 5, 6, 7 8, 10, 11, 12, 13, 14, 15, 18, 19, 20, 21, 22, 24, 27, 32, 33, 52, 54, 55, 56, 57, 65, 67, 74, 77, 76 및 78에 제시된 화합물은 IC50값이 1 μM 이하인 CETP 활성을 나타내었 다.
Claims (74)
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 하기 화학식 Ia'의 구조를 갖는 화합물 또는 그의 염.<화학식 Ia'>식 중,A는로부터 선택된 잔기이고;여기서 Ra는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시로부터 독립적으로 선택되고;p는 0 내지 3의 정수이고;Z는 N이고;R1 및 R2는 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 3) 6개 내지 12개의 탄소 원자를 갖는 아릴; 3개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 4) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 5) (CHRx)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고, Rx는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시, 또는 수소로부터 독립적으로 선택되고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되거나; 또는R1 및 R2는 함께, 2개 내지 12개의 탄소 원자를 포함하며 Z 이외에 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 추가로 포함할 수 있는 모노시클릭 또는 비시클릭 잔기를 형성하고;R3은 1) 시아노; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬; 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 6개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴; 4) CO2R6, CONH2, C(S)NR6R7, C(S)NC(O)OR8 또는 C(S)SR8; 또는 5) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 알킬인 경우, R3은 시아노, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로아릴 또는 헤테로시클릴로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환되고, 여기서 헤테로아릴 또는 헤테로시클릴은 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 아릴, 또는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴인 경우, R3은 1) 할라이드, 히드록실 또는 시아노, 2) 1개 내지 12개의 탄소 원자를 갖는 알콕시, 또는 3) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 4개 내지 12개의 탄소 원자를 갖는 헤테로아릴기로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 1개 내지 12개의 탄소 원자를 갖는 알콕시 또는 할로알콕시, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 3) 히드록실, NR6R7, CO2R6, COR8 또는 SO2R8; 또는 4) 3개 내지 7개의 고리 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클로알킬로부터 독립적으로 선택되고;R6 및 R7은 각각의 경우에서 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되거나; 또는R6 및 R7은 N과 함께, 3개 내지 7개의 고리 탄소 원자를 가지며 R6 및 R7이 결합된 질소 원자 이외에 O, N, S 또는 NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 더 포함할 수 있는 시클릭 잔기를 형성하고;R8은 각각의 경우에서 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택되고;R1 및 R2가 모노시클릭 또는 비시클릭 잔기를 형성하지 않는 경우, R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬, 할로알킬 또는 알콕시, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로아릴 또는 헤테로시클릴; 또는 2) 할로겐, 시아노 또는 히드록실로부터 독립적으로 선택된 1개 또는 2개의 치환기로 치환될 수 있고;R1 및 R2가 함께 모노시클릭 또는 비시클릭 잔기를 형성하는 경우, 시클릭 잔기는 1) 할로겐, 시아노 또는 히드록실; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬, 할로알킬, 알콕시 또는 할로알콕시, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬 또는 시클로알콕시, 4개 내지 12개의 탄소 원자를 갖는 시클로알킬-치환된 알킬, 2개 내지 12개의 탄소 원자를 갖는 알콕시알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴 또는 아릴옥시, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 4개 내지 12개의 탄소 원자를 가지며 O, N, S 또는 NR10으로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로아릴 또는 헤테로아릴옥시; 3) CO2R6, COR8, SO2R8, SO2NR6R7 또는 CONR6R7; 또는 4) (CH2)qCO2(CH2)q (여기서 q는 0 내지 3의 정수로부터 독립적으로 선택됨)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4, R5, R6, R7 및 R8은 1) 할라이드, 히드록시, 시아노 또는 NR6R7; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있다.
- 삭제
- 제6항에 있어서,R1 및 R2가 1) 수소; 2) 1개 내지 6개의 탄소 원자를 갖는 알킬; 3) 3개 내지 6개의 탄소 원자를 갖는 시클로알킬; 4) COR8; 또는 5) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서 n은 각각의 경우에서 1 또는 2임)로부터 독립적으로 선택되거나; 또는R1 및 R2가 함께, 2개 내지 12개의 탄소 원자를 포함하며 O, N 또는 NR10으로부터 독립적으로 선택된 1개 또는 2개의 헤테로원자 또는 헤테로기를 추가로 포함할 수 있는 모노시클릭 또는 비시클릭 잔기를 형성하고; 여기서 상기 모노시클릭 또는 비시클릭 잔기가 1) 3개 내지 6개의 탄소 원자를 갖는 시클로알킬; 또는 2) 1개 또는 2개의 탄소 원자를 갖는 알킬로부터 독립적으로 선택된 1개 내지 3개의 치환기로 추가 치환될 수 있는 것인 화합물.
- 제6항에 있어서,R3이 1) 시아노; 2) 1개 내지 6개의 탄소 원자를 갖는 알킬; 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 6개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴; 4) CO2R6, CONH2, C(S)NR6R7, C(S)NC(O)OR8 또는 C(S)SR8; 또는 5) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 알킬인 경우, R3은 시아노, 헤테로아릴 또는 헤테로시클릴로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환되고, 여기서 헤테로아릴 또는 헤테로시클릴은 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 아릴, 또는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴인 경우, R3은 할라이드, 히드록실, 시아노, 1개 내지 12개의 탄소 원자를 갖는 알콕시, 또는 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 4개 내지 12개의 탄소 원자를 갖는 헤테로아릴기로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있는 것인 화합물.
- 제6항에 있어서,R4가 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 4개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m이 2 또는 3인 화합물.
- 하기 화학식 II의 구조를 갖는 화합물 또는 그의 염.<화학식 II>식 중,R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되거나; 또는R1 및 R2는 함께, 2개 내지 12개의 탄소 원자를 포함하며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 추가로 포함할 수 있는 모노시클릭 또는 비시클릭 잔기를 형성하고;R3은 1) 시아노; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬; 3) 2개 내지 6개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴; 4) CO2R6, C(S)SR8 또는 C(S)NC(O)OR8; 또는 5) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 알킬인 경우, R3은 시아노, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로아릴 또는 헤테로시클릴로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환되고, 여기서 헤테로아릴 또는 헤테로시클릴은 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;여기서, R3이 아릴, 또는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴인 경우, R3은 1) 할라이드, 히드록실 또는 시아노, 2) 1개 내지 12개의 탄소 원자를 갖는 알콕시, 또는 3) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 4개 내지 12개의 탄소 원자를 갖는 헤테로아릴기로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R6은 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 선택되고;R8은 각각의 경우에서 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택되고;Ra는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시로부터 독립적으로 선택되고;p는 0 내지 3의 정수이다.
- 제6항에 있어서, 하기 화학식 III의 구조를 갖는 화합물 또는 그의 염.<화학식 III>식 중,R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;R3은 1) CO2R6; 또는 2) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 또는 3) 3개 내지 7개의 고리 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클로알킬로부터 독립적으로 선택되고;R6은 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 선택되고;R8은 각각의 경우에서 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택된다.
- 제6항에 있어서, 하기 화학식 IIIb의 구조를 갖는 화합물 또는 그의 염.<화학식 IIIb>식 중,Ra는 1) 수소, 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬로부터 선택되고;Ra2는 수소, 또는 1개 내지 12개의 탄소 원자를 갖는 알킬로부터 선택되고;R3은 테트라졸릴, 1,3,4-옥사디아졸릴, 옥사졸릴, 피리미디닐, 4,5-디히드로-옥사졸릴, 피리딜, 티아졸릴 또는 이소옥사졸릴로부터 선택된 기이고; 여기서 상기 기는 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있다.
- 제6항에 있어서, 하기 화학식 IV의 구조를 갖는 화합물 또는 그의 염.<화학식 IV>식 중,R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;R3은 1) CO2R6; 또는 2) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 또는 3) 3개 내지 7개의 고리 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클로알킬로부터 독립적으로 선택되고;R6은 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 선택되고;R8은 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택되고;Ra는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시로부터 독립적으로 선택되고;p는 0 내지 3의 정수이다.
- 삭제
- 제6항에 있어서, 하기 화학식 V의 구조를 갖는 화합물 또는 그의 염.<화학식 V>식 중,R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1 또는 2이고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;R3은 1) 시아노; 2) 2개 내지 6개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 5원, 6원 또는 7원 헤테로시클릴 또는 헤테로아릴; 3) CO2R6; 또는 4) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 3) 3개 내지 7개의 고리 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클로알킬로부터 독립적으로 선택되고;R6은 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 선택되고;R8은 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택되고;Ra는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 알콕시이고;p는 0 내지 3의 정수이다.
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 제6항에 있어서, 하기 화학식 VIII의 구조를 갖는 화합물 또는 그의 염.<화학식 VIII>식 중,R1 및 R2는 1) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) COR8 또는 CO2R6; 또는 3) (CH2)nR5 또는 (CH2)nRdCO2Re (여기서, n은 각각의 경우에서 1, 2 또는 3이고; Rd는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고; Re는 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 또는 수소로부터 독립적으로 선택됨)로부터 독립적으로 선택되고;R3은 1) CO2R6; 또는 2) 4,5-디히드로-옥사졸릴, 테트라졸릴, 이소옥사졸릴, 피리딜, 피리미디닐, 옥사디아졸릴, 티아졸릴 또는 옥사졸릴로부터 선택된 기로부터 선택되고; 여기서 상기 기는 a) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬; 또는 b) CO2R9 (여기서 R9는 1개 내지 12개의 탄소 원자를 갖는 알킬임)로부터 독립적으로 선택된 1개 내지 3개의 치환기로 치환될 수 있고;R4는 각각의 경우에서 1) 할로겐 또는 시아노; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬로부터 독립적으로 선택되고;m은 0 내지 3의 정수이고;R5는 각각의 경우에서 1) 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 2) 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴; 또는 3) 3개 내지 7개의 고리 탄소 원자 및 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개 내지 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클로알킬로부터 독립적으로 선택되고;R6은 1) 수소; 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 또는 3개 내지 12개의 탄소 원자를 갖는 시클로알킬; 또는 3) 6개 내지 12개의 탄소 원자를 갖는 아릴, 7개 내지 12개의 탄소 원자를 갖는 아르알킬, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 선택되고;R8은 각각의 경우에서 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 2개 내지 12개의 탄소 원자를 가지며 O, N, S, NR10, SO2 또는 CO로부터 독립적으로 선택된 1개, 2개 또는 3개의 헤테로원자 또는 헤테로기를 포함하는 헤테로시클릴 또는 헤테로아릴로부터 독립적으로 선택되고;R10은 각각의 경우에서 1) 수소; 또는 2) 1개 내지 12개의 탄소 원자를 갖는 알킬 또는 할로알킬, 3개 내지 12개의 탄소 원자를 갖는 시클로알킬, 6개 내지 12개의 탄소 원자를 갖는 아릴, 또는 7개 내지 12개의 탄소 원자를 갖는 아르알킬로부터 독립적으로 선택된다.
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US64079804P | 2004-12-31 | 2004-12-31 | |
| US60/640,798 | 2004-12-31 | ||
| PCT/US2005/047203 WO2006073973A2 (en) | 2004-12-31 | 2005-12-28 | Novel benzylamine derivatives as cetp inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20070102696A KR20070102696A (ko) | 2007-10-19 |
| KR101238525B1 true KR101238525B1 (ko) | 2013-02-28 |
Family
ID=36648035
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020077017632A KR101238525B1 (ko) | 2004-12-31 | 2005-12-28 | Cetp 저해제로서의 신규 벤질아민 유도체 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US9040558B2 (ko) |
| EP (1) | EP1848430B1 (ko) |
| JP (1) | JP5096927B2 (ko) |
| KR (1) | KR101238525B1 (ko) |
| CN (2) | CN103102303B (ko) |
| CA (1) | CA2605214C (ko) |
| DK (1) | DK1848430T3 (ko) |
| ES (2) | ES2644450T3 (ko) |
| HK (1) | HK1131055A1 (ko) |
| MX (1) | MX2007007919A (ko) |
| WO (1) | WO2006073973A2 (ko) |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101238525B1 (ko) | 2004-12-31 | 2013-02-28 | 레디 유에스 테라퓨틱스 인코포레이티드 | Cetp 저해제로서의 신규 벤질아민 유도체 |
| US8604055B2 (en) | 2004-12-31 | 2013-12-10 | Dr. Reddy's Laboratories Ltd. | Substituted benzylamino quinolines as cholesterol ester-transfer protein inhibitors |
| EP1981342B1 (en) * | 2005-12-28 | 2016-11-30 | Dr. Reddy's Laboratories Ltd. | Selective benzylamine derivatives and their utility as cholesterol ester-transfer protein inhibitors |
| CA2634833A1 (en) * | 2005-12-29 | 2007-07-05 | Novartis Ag | Pyridinyl amine derivatives as inhibitors of cholesteryl ester transfer protein (cetp) |
| UY30118A1 (es) * | 2006-01-31 | 2007-06-29 | Tanabe Seiyaku Co | Compueto amina trisustituido |
| UY30117A1 (es) | 2006-01-31 | 2007-06-29 | Tanabe Seiyaku Co | Compuesto amina trisustituido |
| US8383660B2 (en) * | 2006-03-10 | 2013-02-26 | Pfizer Inc. | Dibenzyl amine compounds and derivatives |
| GB0609268D0 (en) * | 2006-05-10 | 2006-06-21 | Novartis Ag | Organic compounds |
| CA2650954C (en) * | 2006-05-10 | 2014-02-11 | Novartis Ag | Bicyclic derivatives as cetp inhibitors |
| BRPI0711447A2 (pt) * | 2006-05-11 | 2011-11-08 | Novartis Ag | compostos orgánicos |
| RU2009108280A (ru) | 2006-08-08 | 2010-09-20 | Санофи-Авентис (Fr) | Ариламиноарилалкилзамещенные имидазолидин-2,4-дионы, способы их получения, содержащие эти соединения лекарственные средства и их применение |
| US7750019B2 (en) | 2006-08-11 | 2010-07-06 | Kowa Company, Ltd. | Pyrimidine compound having benzyl(pyridylmethyl)amine structure and medicament comprising the same |
| MX2009005249A (es) * | 2006-11-15 | 2009-05-28 | Novartis Ag | Compuestos organicos. |
| JP2010509387A (ja) * | 2006-11-15 | 2010-03-25 | ノバルティス アーゲー | Cetp阻害剤としてのヘテロ環式誘導体 |
| WO2008097976A1 (en) * | 2007-02-09 | 2008-08-14 | Kalypsys, Inc. | Heterocyclic modulators of tgr5 for treatment of disease |
| US7790737B2 (en) * | 2007-03-13 | 2010-09-07 | Kowa Company, Ltd. | Substituted pyrimidine compounds and their utility as CETP inhibitors |
| ES2559838T3 (es) | 2007-03-16 | 2016-02-16 | Concert Pharmaceuticals, Inc. | Inhibidores de proteína de transferencia de ésteres de colesterol |
| JP5244095B2 (ja) | 2007-04-13 | 2013-07-24 | 興和株式会社 | 新規なジベンジルアミン構造を有するピリミジン化合物及びこれを含有する医薬 |
| EP2155187B1 (en) * | 2007-05-07 | 2016-05-25 | Merck Sharp & Dohme Corp. | Method of treatment using fused aromatic compounds having anti-diabetic activity |
| JP4846769B2 (ja) * | 2007-07-30 | 2011-12-28 | 田辺三菱製薬株式会社 | 医薬組成物 |
| EP2025674A1 (de) | 2007-08-15 | 2009-02-18 | sanofi-aventis | Substituierte Tetrahydronaphthaline, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| DE102007054497B3 (de) | 2007-11-13 | 2009-07-23 | Sanofi-Aventis Deutschland Gmbh | Neue kristalline Diphenylazetidinonhydrate und Verfahren zu deren Herstellung |
| UY31968A (es) | 2008-07-09 | 2010-01-29 | Sanofi Aventis | Nuevos derivados heterocíclicos, sus procesos para su preparación, y sus usos terapéuticos |
| WO2010068601A1 (en) | 2008-12-08 | 2010-06-17 | Sanofi-Aventis | A crystalline heteroaromatic fluoroglycoside hydrate, processes for making, methods of use and pharmaceutical compositions thereof |
| WO2010092340A1 (en) * | 2009-02-13 | 2010-08-19 | Ucb Pharma S.A. | Fused pyridine and pyrazine derivatives as kinase inhibitors |
| SG178880A1 (en) | 2009-08-26 | 2012-04-27 | Sanofi Sa | Novel crystalline heteroaromatic fluoroglycoside hydrates, pharmaceuticals comprising these compounds and their use |
| WO2011157827A1 (de) | 2010-06-18 | 2011-12-22 | Sanofi | Azolopyridin-3-on-derivate als inhibitoren von lipasen und phospholipasen |
| US8828995B2 (en) | 2011-03-08 | 2014-09-09 | Sanofi | Branched oxathiazine derivatives, method for the production thereof, use thereof as medicine and drug containing said derivatives and use thereof |
| US8871758B2 (en) | 2011-03-08 | 2014-10-28 | Sanofi | Tetrasubstituted oxathiazine derivatives, method for producing them, their use as medicine and drug containing said derivatives and the use thereof |
| WO2012120052A1 (de) | 2011-03-08 | 2012-09-13 | Sanofi | Mit carbozyklen oder heterozyklen substituierte oxathiazinderivate, verfahren zu deren herstellung, diese verbindungen enthaltende arzneimittel und deren verwendung |
| EP2683699B1 (de) | 2011-03-08 | 2015-06-24 | Sanofi | Di- und trisubstituierte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| WO2012120054A1 (de) | 2011-03-08 | 2012-09-13 | Sanofi | Di- und trisubstituierte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| CA2845284C (en) * | 2011-08-18 | 2018-03-06 | Dr. Reddy's Laboratories Ltd. | Substituted heterocyclic amine compounds as cholesteryl ester-transfer protein (cetp) inhibitors |
| KR101803866B1 (ko) * | 2011-09-27 | 2017-12-04 | 닥터 레디스 레보러터리즈 리미티드 | 동맥경화증 치료에 유용한 콜레스테릴 에스테르-전달 단백질(cetp) 억제제로서 5-벤질아미노메틸-6-아미노피라졸로[3,4-b]피리딘 유도체 |
| US20140303198A1 (en) | 2011-11-29 | 2014-10-09 | Kowa Company, Ltd. | Agent for inhibiting expression of npc1l1 and/or lipg mrna and agent for preventing and/or treating obesity |
| JPWO2014017569A1 (ja) * | 2012-07-26 | 2016-07-11 | 興和株式会社 | 血中ldlを低下させるための医薬 |
| RU2015123632A (ru) * | 2012-11-19 | 2017-01-10 | Др. Редди'С Лабораторис Лтд. | Фармацевтические композиции ингибиторов сетр |
| WO2014128564A2 (en) | 2013-02-21 | 2014-08-28 | Dr. Reddy's Laboratories Ltd. | Pharmaceutical compositions of cetp inhibitors |
| JP2015054838A (ja) * | 2013-09-12 | 2015-03-23 | 興和株式会社 | 血中ldlコレステロールを低下させる医薬 |
| US10214502B2 (en) * | 2016-10-04 | 2019-02-26 | Mayo Foundation For Medical Education And Research | Method of inhibiting apolipoprotein-E expression while increasing expression of at least one of LDL-receptor protein or AbcA1 protein comprising administering a small compound |
| CN108329330B (zh) * | 2017-01-20 | 2021-05-04 | 复旦大学 | 2-苄氧苯基噁唑并吡啶类化合物及其药物用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004020393A1 (ja) | 2002-08-30 | 2004-03-11 | Japan Tobacco Inc. | ジベンジルアミン化合物及びその医薬用途 |
| WO2005100298A1 (en) | 2004-04-13 | 2005-10-27 | Merck & Co., Inc. | Cetp inhibitors |
Family Cites Families (118)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2965643A (en) * | 1960-12-20 | Derivatives of pyrazolo | ||
| CH273953A (de) * | 1948-05-21 | 1951-03-15 | Ciba Geigy | Verfahren zur Herstellung von Aminen. |
| US2858309A (en) * | 1956-05-07 | 1958-10-28 | Ciba Pharm Prod Inc | New aminobenzene sulfonamide |
| US3546295A (en) * | 1968-08-01 | 1970-12-08 | Exxon Research Engineering Co | N-cycloalkyl anilines |
| US3713499A (en) * | 1971-08-11 | 1973-01-30 | Gulf Research Development Co | Method and apparatus for treating drilling mud |
| DE3143016A1 (de) * | 1980-10-29 | 1982-05-27 | Nippon Kayaku K.K., Tokyo | 5,6,7,8-tetrahydro-1,6-naphthyridinderivate und verfahren zu ihrer herstellung |
| JPH01104052A (ja) | 1987-06-12 | 1989-04-21 | Yoshitomi Pharmaceut Ind Ltd | ピリジン誘導体 |
| ES2058288T3 (es) | 1987-07-08 | 1994-11-01 | American Home Prod | Composiciones de ibuprofen secadas por atomizacion. |
| US5089073A (en) * | 1988-09-26 | 1992-02-18 | W. R. Grace & Co.-Conn. | High strength laminated film for chub packaging |
| US5474989A (en) * | 1988-11-11 | 1995-12-12 | Kurita Water Industries, Ltd. | Drug composition |
| GB8912784D0 (en) | 1989-06-02 | 1989-07-19 | Wyeth John & Brother Ltd | Amines |
| US5260331A (en) * | 1989-01-02 | 1993-11-09 | John Wyeth & Brother Limited | Composition for treating depression with (S- or O-heteroaryl)alkyl amines |
| HUT58270A (en) | 1989-06-02 | 1992-02-28 | Wyeth John & Brother Ltd | Process for producing amine derivatives and pharmaceutical compositions containing them |
| US5422355A (en) * | 1989-06-02 | 1995-06-06 | John Wyeth & Brother, Limited | Composition for treating depression with (N-heteroaryl)alkylamines |
| US5260301A (en) * | 1990-03-01 | 1993-11-09 | Fujisawa Pharmaceutical Co., Ltd. | Pharmaceutical solution containing FK-506 |
| ATE159426T1 (de) * | 1991-04-16 | 1997-11-15 | Nippon Shinyaku Co Ltd | Verfahren zur herstellung einer festen dispersion |
| WO1993000332A1 (en) | 1991-06-25 | 1993-01-07 | Merck & Co., Inc. | Substituted azetidinones as anti-inflammatory and antidegenerative agents |
| ZA924659B (en) | 1991-06-25 | 1993-03-31 | Merck & Co Inc | New substituted azetidinones as anti-inflammatory and antidegenerative agents |
| US5348953A (en) * | 1991-06-25 | 1994-09-20 | Merck & Co., Inc. | Substituted azetidinones as anti-inflammatory and antidegenerative agents |
| TW225469B (ko) | 1991-11-12 | 1994-06-21 | Nissan Kagakl Kogyo | |
| FR2686339B1 (fr) | 1992-01-22 | 1994-03-11 | Adir Cie | Nouveaux amides et sulfonamides naphtaleniques, leurs procedes de preparation et les compositions pharmaceutiques qui les contiennent. |
| EP0585500A1 (en) | 1992-09-04 | 1994-03-09 | Merrell Dow Pharmaceuticals Inc. | Diaryl piperazineacetamides as antimuscarinic agents |
| ATE161530T1 (de) | 1992-09-04 | 1998-01-15 | Takeda Chemical Industries Ltd | Kondensierte heterozyklische verbindungen, deren herstellung und verwendung |
| AU5802894A (en) | 1992-12-17 | 1994-07-04 | Merck & Co., Inc. | New substituted azetidinones as anti-inflammatory and antidegenerative agents |
| MY131441A (en) | 1992-12-29 | 2007-08-30 | American Cyanamid Co | Amidrazones and their use as insecticidal and acaricidal agents |
| ATE231126T1 (de) | 1993-08-12 | 2003-02-15 | Astrazeneca Ab | Amidin-derivate mit stickstoffoxid-synthease- aktivität |
| US5491152A (en) * | 1994-03-23 | 1996-02-13 | The Du Pont Merck Pharmaceutical Company | Derivatives of cyclic ethers and sulfides for the treatment of atherosclerosis |
| JPH07285962A (ja) | 1994-04-20 | 1995-10-31 | Nissan Chem Ind Ltd | ピリジンカルボン酸アミド誘導体 |
| IT1270615B (it) * | 1994-07-14 | 1997-05-07 | Smithkline Beecham Farma | Uso di derivati di chinolina |
| JPH0892224A (ja) | 1994-09-16 | 1996-04-09 | Kumiai Chem Ind Co Ltd | 3,5−置換フェニルトリアゾール誘導体および殺虫、殺ダニ剤 |
| JPH0892225A (ja) | 1994-09-29 | 1996-04-09 | Nissan Chem Ind Ltd | トリアゾールグリコール酸アミド誘導体 |
| EP0790057B1 (en) | 1994-11-29 | 2002-06-05 | Hisamitsu Pharmaceutical Co., Inc. | Antibacterial or bactericide comprising 2-aminothiazole derivative and salts thereof |
| GB9511220D0 (en) * | 1995-06-02 | 1995-07-26 | Glaxo Group Ltd | Solid dispersions |
| JPH09235276A (ja) * | 1995-12-27 | 1997-09-09 | Takeda Chem Ind Ltd | オキサゾール誘導体、その製造法および用途 |
| US6730679B1 (en) * | 1996-03-22 | 2004-05-04 | Smithkline Beecham Corporation | Pharmaceutical formulations |
| DE19615262A1 (de) | 1996-04-18 | 1997-10-23 | Bayer Ag | Heteroverknüpfte Phenylglycinolamide |
| EP0904060B1 (en) * | 1996-05-20 | 2003-12-10 | Janssen Pharmaceutica N.V. | Antifungal compositions with improved bioavailability |
| AR008789A1 (es) | 1996-07-31 | 2000-02-23 | Bayer Corp | Piridinas y bifenilos substituidos |
| DE19636150A1 (de) | 1996-09-06 | 1998-03-12 | Asta Medica Ag | N-substituierte Indol-3-glyoxylamide mit antiasthmatischer, antiallergischer und immunsuppressiver/immunmodulierender Wirkung |
| WO1998016508A2 (en) * | 1996-10-02 | 1998-04-23 | Trustees Of Boston University | Synthesis of aromatic compounds by diels-alder reaction on solid support |
| TW523506B (en) | 1996-12-18 | 2003-03-11 | Ono Pharmaceutical Co | Sulfonamide or carbamide derivatives and drugs containing the same as active ingredients |
| AU7688398A (en) | 1997-06-16 | 1999-01-04 | American Home Products Corporation | Elevation of hdl cholesterol by 2-{(aminothioxomethyl)-hydrazono}-2-arylethyl carbamates |
| WO1998057927A1 (en) | 1997-06-16 | 1998-12-23 | American Home Products Corporation | Elevation of hdl cholesterol by 4-[(aminothioxomethyl)hydrazono]-4-arylbutyl carbamates |
| US6008362A (en) * | 1997-06-16 | 1999-12-28 | Commons; Thomas Joseph | Elevation of HDL cholesterol by 2-(-4-chlorol-1-aryl-butylidene)-hydrazinecarbothioamides |
| US5977170A (en) * | 1997-06-16 | 1999-11-02 | American Home Products Corporation | Elevation of HDL cholesterol by 4-[(aminothioxomethyl)hydrazono]-4-arylbutyl carbamates |
| AU7589598A (en) | 1997-06-16 | 1999-01-04 | American Home Products Corporation | Elevation of hdl cholesterol by 2-(4-chloro -1-aryl-butylidene) -hydrazinecarbothioamides |
| EP1741424B1 (en) | 1997-08-11 | 2018-10-03 | Pfizer Products Inc. | Solid pharmaceutical dispersions with enhanced bioavailabilty |
| UA67754C2 (uk) | 1997-10-10 | 2004-07-15 | Пфайзер, Інк. | Агоністи простагландину, фармацевтична композиція на їх основі (варіанти), спосіб нарощення та збереження кісткової маси у хребетних та спосіб лікування (варіанти) |
| JPH11209366A (ja) | 1998-01-23 | 1999-08-03 | Nissan Chem Ind Ltd | クロマン誘導体及び心不全治療薬 |
| DE19814838C2 (de) | 1998-04-02 | 2001-01-18 | Asta Medica Ag | Indolyl-3-glyoxylsäure-Derivate mit Antitumorwirkung |
| CZ20003978A3 (cs) * | 1998-04-27 | 2001-09-12 | Centre National De La Recherche Scientifique | Deriváty 3-(amino- nebo aminoalkyl) pyridinonu a jejich použití |
| US6121271A (en) * | 1998-05-12 | 2000-09-19 | American Home Products Corporation | Naphtho[2,3-B]heteroar-4-yl derivatives |
| GT199900147A (es) | 1998-09-17 | 1999-09-06 | 1, 2, 3, 4- tetrahidroquinolinas 2-sustituidas 4-amino sustituidas. | |
| US6350786B1 (en) * | 1998-09-22 | 2002-02-26 | Hoffmann-La Roche Inc. | Stable complexes of poorly soluble compounds in ionic polymers |
| DE19845202A1 (de) | 1998-10-01 | 2000-04-06 | Wella Ag | Haarwuchsmittel |
| IL143580A0 (en) * | 1998-12-11 | 2002-04-21 | Pharmasolutions Inc | Pharmaceutical compositions containing lipophilic drugs and methods for the preparation thereof |
| EP1027885B1 (en) * | 1999-02-09 | 2008-07-09 | Pfizer Products Inc. | Basic drug compositions with enhanced bioavailability |
| RU2238264C2 (ru) | 1999-02-24 | 2004-10-20 | Ф.Хоффманн-Ля Рош Аг | Производные бензола или пиридина и фармацевтическая композиция на их основе |
| CA2369404C (en) | 1999-06-23 | 2010-06-08 | Syngenta Participations Ag | Method of producing nitroguanidine- and nitroenamine derivatives |
| DE19930075A1 (de) | 1999-06-30 | 2001-01-04 | Bayer Ag | Neue Amino- und Amidosulfonamide als antivirale Mittel |
| US6479552B2 (en) * | 1999-09-23 | 2002-11-12 | G.D. Searle & Co. | Use of substituted N, N-disubstituted diamino compounds for inhibiting cholesteryl ester transfer protein activity |
| TWI269654B (en) | 1999-09-28 | 2007-01-01 | Baxter Healthcare Sa | N-substituted indole-3-glyoxylamide compounds having anti-tumor action |
| EP1108426A3 (en) | 1999-12-02 | 2002-10-02 | Pfizer Products Inc. | Use of prostaglandin agonists to treat erectile dysfunction or impotence |
| JP2003518038A (ja) * | 1999-12-20 | 2003-06-03 | ニコラス, ジェイ カークホフ, | 流動床噴霧乾燥によるナノ粒子製造方法 |
| DE19962300A1 (de) * | 1999-12-23 | 2001-06-28 | Asta Medica Ag | Substituierte N-Benzyl-Indol-3-yl-glyoxylsäure-Derivate mit Antitumorwirkung |
| US6306911B1 (en) | 2000-02-07 | 2001-10-23 | Ortho-Mcneil Pharmaceutical, Inc. | Substituted amino acids as neutral sphingomyelinase inhibitors |
| WO2001060369A1 (en) | 2000-02-18 | 2001-08-23 | Merck & Co., Inc. | Inhibitors of prenyl-protein transferase |
| WO2001060458A2 (en) | 2000-02-18 | 2001-08-23 | Merck & Co., Inc. | Inhibitors of prenyl-protein transferase |
| US20020019527A1 (en) * | 2000-04-27 | 2002-02-14 | Wei-Bo Wang | Substituted phenyl farnesyltransferase inhibitors |
| DE10023484A1 (de) | 2000-05-09 | 2001-11-22 | Schering Ag | Anthranylamide und deren Verwendung als Arzneimittel |
| HUP0303700A3 (en) * | 2000-07-17 | 2006-07-28 | Astellas Pharma Inc Chuo Ku | Pharmaceutical composition improved in peroral absorbability |
| US7115279B2 (en) | 2000-08-03 | 2006-10-03 | Curatolo William J | Pharmaceutical compositions of cholesteryl ester transfer protein inhibitors |
| US6653471B2 (en) * | 2000-08-07 | 2003-11-25 | Neurogen Corporation | Heterocyclic compounds as ligands of the GABAA receptor |
| JP2002145778A (ja) * | 2000-08-29 | 2002-05-22 | Takeda Chem Ind Ltd | Grk阻害剤 |
| US6576644B2 (en) * | 2000-09-06 | 2003-06-10 | Bristol-Myers Squibb Co. | Quinoline inhibitors of cGMP phosphodiesterase |
| WO2002022584A1 (en) | 2000-09-11 | 2002-03-21 | Merck & Co., Inc. | Thrombin inhibitors |
| JP2004509867A (ja) * | 2000-09-19 | 2004-04-02 | サントル、ナショナール、ド、ラ、ルシェルシュ、シアンティフィク、(セーエヌエルエス) | Hiv阻害特性を有するピリジノンおよびピリジンチオン誘導体 |
| HUP0400651A2 (hu) | 2000-11-07 | 2004-06-28 | Bristol-Myers Squibb Company | Szerin proteáz inhibitorokként alkalmazható savszármazékok és ezeket tartalmazó gyógyszerkészítmények |
| US7037528B2 (en) * | 2000-12-22 | 2006-05-02 | Baxter International Inc. | Microprecipitation method for preparing submicron suspensions |
| WO2002055484A1 (fr) * | 2001-01-12 | 2002-07-18 | Takeda Chemical Industries, Ltd. | Compose biaryle, procede de production de ce compose, et principe actif |
| BR0207390A (pt) | 2001-02-21 | 2004-10-13 | Nps Pharma Inc | Compostos, composições farmacêuticas e métodos de tratatamento de doença associada a ativação e a ativação do grupo i mg1ur |
| DE10110749A1 (de) | 2001-03-07 | 2002-09-12 | Bayer Ag | Substituierte Aminodicarbonsäurederivate |
| US7034013B2 (en) * | 2001-03-20 | 2006-04-25 | Cydex, Inc. | Formulations containing propofol and a sulfoalkyl ether cyclodextrin |
| EP1389201A1 (de) | 2001-05-08 | 2004-02-18 | Schering Aktiengesellschaft | N-oxidanthranylamid-derivate und deren verwendung als arzneimittel |
| BR0210505A (pt) | 2001-06-21 | 2004-05-18 | Pfizer Prod Inc | Formulações auto-emulsionantes de inibidores da proteìna de transferência de ésteres de colesterilo |
| BR0210519A (pt) * | 2001-06-22 | 2004-06-22 | Pfizer Prod Inc | Composições farmacêuticas de adsorvatos de fármaco amorfo |
| EP1401503B1 (en) * | 2001-06-22 | 2007-05-09 | Pfizer Products Inc. | Pharmaceutical compositions containing a solid dispersion of a poorly-soluble drug and a solubility-enhancing polymer |
| EP1269994A3 (en) * | 2001-06-22 | 2003-02-12 | Pfizer Products Inc. | Pharmaceutical compositions comprising drug and concentration-enhancing polymers |
| AU2002309172A1 (en) * | 2001-06-22 | 2003-01-08 | Pfizer Products Inc. | Pharmaceutical compositions containing polymer and drug assemblies |
| WO2003030909A1 (en) | 2001-09-25 | 2003-04-17 | Bayer Pharmaceuticals Corporation | 2- and 4-aminopyrimidines n-substtituded by a bicyclic ring for use as kinase inhibitors in the treatment of cancer |
| JP2003221376A (ja) * | 2001-11-21 | 2003-08-05 | Japan Tobacco Inc | Cetp活性阻害剤 |
| US6713499B2 (en) * | 2001-12-12 | 2004-03-30 | Hoffman-La Roche Inc. | 7-Amino-benzothiazole derivatives |
| AR038375A1 (es) | 2002-02-01 | 2005-01-12 | Pfizer Prod Inc | Composiciones farmaceuticas de inhibidores de la proteina de transferencia de esteres de colesterilo |
| ES2309294T3 (es) * | 2002-02-01 | 2008-12-16 | Pfizer Products Inc. | Formas de dosificacion farmaceutica de liberacion controlada de un inhibidor de la proteina de transferecncia de ester de colesterilo. |
| AU2003228419A1 (en) * | 2002-03-29 | 2003-10-13 | Neurogen Corporation | New aryl imidazoles and related compounds as c5a receptor modulators |
| GB0208280D0 (en) | 2002-04-10 | 2002-05-22 | Glaxo Group Ltd | Novel compounds |
| US20040053842A1 (en) * | 2002-07-02 | 2004-03-18 | Pfizer Inc. | Methods of treatment with CETP inhibitors and antihypertensive agents |
| US7071210B2 (en) * | 2002-07-02 | 2006-07-04 | Pfizer Inc. | CETP inhibitors in combination with antihypertensive agents and uses thereof |
| AU2003283769A1 (en) * | 2002-12-20 | 2004-07-14 | Pfizer Products Inc. | Dosage forms comprising a cetp inhibitor and an hmg-coa reductase inhibitor |
| GB0303683D0 (en) | 2003-02-18 | 2003-03-19 | Prolysis Ltd | Antimicrobial agents |
| JP4927533B2 (ja) | 2003-02-28 | 2012-05-09 | ニッポネックス インコーポレイテッド | 癌その他の疾患の治療に有用な置換ピリジン誘導体 |
| EP1601351A1 (en) | 2003-03-04 | 2005-12-07 | Pfizer Products Inc. | Use of ep2 selective receptor agonists in medical treatment |
| DE602004011221T2 (de) | 2003-06-11 | 2009-01-02 | Eli Lilly And Co., Indianapolis | 3-amino-pyrrolidine als inhibitoren der monoamin-wiederaufnahme |
| WO2005011634A1 (en) * | 2003-08-04 | 2005-02-10 | Pfizer Products Inc. | Dosage forms providing controlled release of cholesteryl ester transfer protein inhibitors and immediate release of hmg-coa reductase inhibitors |
| US7276610B2 (en) * | 2003-08-27 | 2007-10-02 | Janssen Pharaceutica, Nv | Aryl piperidine amides |
| WO2005030185A2 (en) | 2003-09-26 | 2005-04-07 | Japan Tobacco Inc. | Method of inhibiting remnant lipoprotein production |
| WO2005058037A1 (en) * | 2003-12-12 | 2005-06-30 | Syngenta Participations Ag | Picolinylpyrazoles as herbicides |
| WO2005058831A1 (en) * | 2003-12-12 | 2005-06-30 | Syngenta Participations Ag | Novel herbicides |
| PT1732933E (pt) | 2004-03-26 | 2008-10-20 | Lilly Co Eli | Compostos para o tratamento da dislipidémia |
| TWI345568B (en) | 2004-04-02 | 2011-07-21 | Mitsubishi Tanabe Pharma Corp | Tetrahydronaphthyridine derivatives and a process for preparing the same |
| UA90269C2 (ru) | 2004-04-02 | 2010-04-26 | Мицубиси Танабе Фарма Корпорейшн | Тетрагидрохинолиновые производные и способ их получения |
| MX2007006137A (es) | 2004-11-23 | 2007-07-19 | Pfizer Prod Inc | Compuestos y derivados de dibencil amina. |
| KR101238525B1 (ko) | 2004-12-31 | 2013-02-28 | 레디 유에스 테라퓨틱스 인코포레이티드 | Cetp 저해제로서의 신규 벤질아민 유도체 |
| US8828438B2 (en) * | 2005-05-31 | 2014-09-09 | Bend Research, Inc. | Pharmaceutical compositions of cholesteryl ester transfer protein inhibitors and HMG-CoA reductase |
| EP1981342B1 (en) | 2005-12-28 | 2016-11-30 | Dr. Reddy's Laboratories Ltd. | Selective benzylamine derivatives and their utility as cholesterol ester-transfer protein inhibitors |
| NZ569700A (en) * | 2006-02-09 | 2011-09-30 | Merck Sharp & Dohme | Polymer formulations of CETP inhibitors |
| CA2650954C (en) * | 2006-05-10 | 2014-02-11 | Novartis Ag | Bicyclic derivatives as cetp inhibitors |
| US7790737B2 (en) * | 2007-03-13 | 2010-09-07 | Kowa Company, Ltd. | Substituted pyrimidine compounds and their utility as CETP inhibitors |
-
2005
- 2005-12-28 KR KR1020077017632A patent/KR101238525B1/ko not_active IP Right Cessation
- 2005-12-28 DK DK05855717.4T patent/DK1848430T3/da active
- 2005-12-28 CA CA2605214A patent/CA2605214C/en not_active Expired - Fee Related
- 2005-12-28 MX MX2007007919A patent/MX2007007919A/es active IP Right Grant
- 2005-12-28 US US11/320,120 patent/US9040558B2/en not_active Expired - Fee Related
- 2005-12-28 CN CN201210404509.3A patent/CN103102303B/zh not_active Expired - Fee Related
- 2005-12-28 ES ES05855717.4T patent/ES2644450T3/es active Active
- 2005-12-28 WO PCT/US2005/047203 patent/WO2006073973A2/en active Application Filing
- 2005-12-28 JP JP2007549577A patent/JP5096927B2/ja not_active Expired - Fee Related
- 2005-12-28 EP EP05855717.4A patent/EP1848430B1/en not_active Not-in-force
- 2005-12-28 CN CN200580048913XA patent/CN101443006B/zh not_active Expired - Fee Related
-
2006
- 2006-06-29 ES ES06774300.5T patent/ES2615340T3/es active Active
-
2009
- 2009-11-13 HK HK09110597.7A patent/HK1131055A1/xx not_active IP Right Cessation
-
2015
- 2015-04-15 US US14/687,467 patent/US9782407B2/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004020393A1 (ja) | 2002-08-30 | 2004-03-11 | Japan Tobacco Inc. | ジベンジルアミン化合物及びその医薬用途 |
| WO2005100298A1 (en) | 2004-04-13 | 2005-10-27 | Merck & Co., Inc. | Cetp inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2008528447A (ja) | 2008-07-31 |
| CA2605214A1 (en) | 2006-07-13 |
| DK1848430T3 (da) | 2017-11-06 |
| CN103102303A (zh) | 2013-05-15 |
| US20060178514A1 (en) | 2006-08-10 |
| CN101443006B (zh) | 2012-10-10 |
| EP1848430B1 (en) | 2017-08-02 |
| CN103102303B (zh) | 2015-10-28 |
| HK1131055A1 (en) | 2010-01-15 |
| CA2605214C (en) | 2016-07-12 |
| EP1848430A2 (en) | 2007-10-31 |
| US9782407B2 (en) | 2017-10-10 |
| WO2006073973A3 (en) | 2008-12-04 |
| US20150216866A1 (en) | 2015-08-06 |
| EP1848430A4 (en) | 2011-12-28 |
| ES2615340T3 (es) | 2017-06-06 |
| ES2644450T3 (es) | 2017-11-29 |
| US9040558B2 (en) | 2015-05-26 |
| CN101443006A (zh) | 2009-05-27 |
| KR20070102696A (ko) | 2007-10-19 |
| JP5096927B2 (ja) | 2012-12-12 |
| MX2007007919A (es) | 2008-01-22 |
| WO2006073973A2 (en) | 2006-07-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101238525B1 (ko) | Cetp 저해제로서의 신규 벤질아민 유도체 | |
| JP5997335B2 (ja) | N含有複素環式化合物 | |
| US10022374B2 (en) | Certain protein kinase inhibitors | |
| AU2016225896B2 (en) | Heterocyclic compounds useful as PDK1 inhibitors | |
| US8178534B2 (en) | cMET inhibitors | |
| EP2114900B1 (en) | Thiopyrimidine-based compounds and uses thereof | |
| US8557830B2 (en) | RAF kinase modulators and methods of use | |
| JP4084410B2 (ja) | ヒスタミンh3受容体リガンドとして有用なテトラヒドロナフチリヂン誘導体 | |
| AU2006330072B2 (en) | Selective benzylamine derivatives and their utility as cholesterol ester-transfer protein inhibitors | |
| US20070155744A1 (en) | N-benzyl-3,4-dihyroxypyridine-2-carboxamide and n-benzyl-2,3-dihydroxypyridine-4- carboxamide compounds useful as hiv integrase inhibitors | |
| JP2010503701A (ja) | 増殖性疾患の治療に有用なキナーゼ阻害剤 | |
| EP2150544A2 (en) | Mapk/erk kinase inhibitors | |
| US20150284367A1 (en) | Inhibitors of syk | |
| JP2021519263A (ja) | 化合物及びその使用 | |
| WO2022053022A1 (zh) | 甲硫氨酸腺苷转移酶抑制剂、其制备方法及应用 | |
| US7700774B2 (en) | Heterocyclic compounds and their pharmaceutical compositions | |
| KR20200024120A (ko) | 모르피난 유도체의 오피오이드 δ 수용체 아고니스트 관련 질환의 치료를 위한 사용 | |
| TW202039446A (zh) | 雜環化合物 | |
| KR20220170766A (ko) | 단백질 키나아제 억제제로서의 신규한 화합물 | |
| NZ569415A (en) | Selective benzylamine derivatives and their utility as cholesterol ester-transfer protein inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20160205 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20180221 Year of fee payment: 6 |
|
| LAPS | Lapse due to unpaid annual fee |