JP4808785B2 - インスリン組成物および組成物の製造方法 - Google Patents
インスリン組成物および組成物の製造方法 Download PDFInfo
- Publication number
- JP4808785B2 JP4808785B2 JP2008547953A JP2008547953A JP4808785B2 JP 4808785 B2 JP4808785 B2 JP 4808785B2 JP 2008547953 A JP2008547953 A JP 2008547953A JP 2008547953 A JP2008547953 A JP 2008547953A JP 4808785 B2 JP4808785 B2 JP 4808785B2
- Authority
- JP
- Japan
- Prior art keywords
- insulin
- ethoxy
- human insulin
- acylated
- desb30 human
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 C*(*=N)OC* Chemical compound C*(*=N)OC* 0.000 description 3
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/52—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an inorganic compound, e.g. an inorganic ion that is complexed with the active ingredient
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/28—Insulins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/62—Insulins
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Diabetes (AREA)
- Endocrinology (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Toxicology (AREA)
- Inorganic Chemistry (AREA)
- Emergency Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
本発明は、遷延性の作用特性と高い亜鉛含有量を有するアシル化インスリンの製薬学的組成物に関する。さらに、本発明は、遷延性の作用特性と高い亜鉛含有量を有するアシル化インスリンの製薬学的組成物を製造するための方法、および糖尿病の治療のための組成物を製造する方法に関する。
現在、1型糖尿病および二型糖尿病の双方の糖尿病の治療は、いわゆる強化インスリン療法への信頼が高まっている。この療法によると、基礎インスリン要求性をカバーするための持続型インスリンの一または二回の毎日の注射を、食事と関連するインスリン要求性をカバーするための、即効型インスリンのボーラス注射により補充して含む多様な毎日のインスリン注射により、患者を治療する。
持続型インスリン組成物は、当技術分野において周知である。したがって、持続型インスリン組成物の主な型には、インスリン結晶または非晶質インスリンの注射可能な水性懸濁液が含まれる。これらの組成物では、使用されるインスリン化合物は、典型的には、プロタミンインスリン、亜鉛インスリンまたはプロタミン亜鉛インスリンである。
プロタミンは非免疫性であると依然は考えられていたが、現在では、プロタミンはヒトにおいて免疫性であり、且つ薬剤目的におけるそれらの使用は抗体の形成を引き起こすことが明らかとなっている。また、プロタミン−インスリン複合体がそれ自身免疫性であることがであるという証拠も見つかっている。従って、ある患者には、プロタミンを含有する持続型インスリン組成物の使用をさけなくてはならない。
インスリンは、膵臓のランゲルハンス島で生産される51アミノ酸のペプチドである。モノマーとして働き、その第一の機能は、膜貫通受容体に結合し、活性化することにより、グルコース分子の脂肪および筋肉組織の細胞膜を横切った輸送を促進することである。
ヒトインスリンが高濃度製薬学的製剤の形態で皮下組織に注射されるとき、それは自己会合しており、モノマーへの解離は比較的緩やかである。インスリンのヘキサマーおよびダイマーは、モノマーより毛細血管壁を貫通するのが遅い。
インスリン製剤は、大抵、インスリンを、酸性条件下で小体積の水に溶解することにより調製される。亜鉛は、その後、製剤に添加され、続いて中和され、フェノールおよびm−クレゾールのような保存料が添加される。これらのインスリンの製薬学的製剤は、ヘキサマーのインスリン毎に約2、3もしくは4の亜鉛原子として提供される。
国際公開第2005/012347号は、国際公開第95/07931号に開示されるアシル化インスリンと比較して追加の負電荷を含んでなるアシル化インスリン誘導体の別の群を開示する。これらのアシル化インスリンの製薬学的製剤は、ヘキサマーのインスリン毎に約2、3もしくは4の亜鉛原子として提供される。
国際公開第2003/094951号から、即効作用および持続作用の双方を有する安定可溶性インスリン製剤を製剤化することは公知である。製剤は、ヘキサマーのインスリン毎に約2.3から約4.5のZn2+の範囲の亜鉛含有量を有する。この発明のアシル化インスリンアナログはインスリンデテミル(detemir)である。
ヒトインスリンは、三つの第一級アミノ基を有する:A鎖およびB鎖のN末端基、およびLysB29のε−アミノ基。これらの基の一または複数で置換された幾つかのインスリン誘導体が、先行技術中で知られている。したがって、米国特許第3528960号(Eli Lilly)は、インスリン分子のうちの1、2または3の第一級アミノ基がカルボキシアロイル(aroyl)基を有するN−カルボキシアロイル(aroyl)インスリンに関する。
欧州特許第894095号は、B鎖のN末端および/または位置B28、B29またはB30のLysのε−アミノ基が、Wが長鎖炭化水素基であり得る式−CO−W−COOHの置換を有するこれらのインスリン誘導体を開示している。これらのインスリン誘導体は、作用の持続性を有し、生理学的pH値で可溶性である。
インスリンデテミル(detemir)の遅い吸収のメカニズムは、Havelundらにより研究されている(The mechanism of protraction of insulin detemir、a long-acting acylated analog of human insulin., Pharmaceutical Research, 21(2004)1498-1504)。インスリン製剤は、ヘキサマーのインスリン毎に2の亜鉛原子、続いてグリセロール、フェノール、m−クレゾールおよびリン酸ナトリウムを添加することにより調製される。
本発明は、先行技術の課題を解決するアシル化インスリンの製薬学的組成物に関する。
本発明は、および6分子のアシル化インスリン毎に4より多い亜鉛原子を含んでなるアシル化インスリンを含む可溶性製薬学的組成物に関する。
亜鉛含有量は、6分子のアシル化インスリン毎に最大約12の亜鉛原子であってよい。亜鉛含有量の上限は、インスリンの沈殿を起こし、溶液を懸濁液にする亜鉛含有量である。
本発明のある態様では、少なくとも90、92、95、96、97、98、99もしくは99.5%のアシル化インスリンが、アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体として存在する。
したがって、ある態様では、アシル化インスリンは、位置B1のα−アミノ基もしくはインスリン分子のAまたはB鎖中のリジン残基の遊離ε−アミノ基のどちらかにおいてアシル化される。
ある態様では、インスリンは、インスリン分子の位置B29のリジン残基の遊離ε−アミノ基においてアシル化される。
更なる態様では、脂肪酸部分は、約6から約32、6から24、8から20、12から20、12−16、10−16、10−20、14−18もしくは14−16の炭素原子を有する二カルボン酸性脂肪酸から誘導される。
アシル基は、問題の遊離アミノ基と直接結合していてよい。しかしながら、アシル基は、インスリン分子中の遊離アミノ基と、問題のアシル基とを一緒に連結するリンカーにより、アミド結合を介して結合していてもよい。
アシル化インスリンは、典型的には、ヒトインスリンと比較して、少なくとも一つ、もしくは二つの追加の負の正味荷電を有し、より典型的には、二つの追加の負の荷電を有するであろう。追加の負の荷電は、脂肪酸中の遊離カルボン酸基、あるいは、少なくとも一つが遊離カルボン酸もしくは中性pHで負に荷電する基を含む一または複数のアミノ酸残基を含み得るリンカー基によりもたらされ得る。更なる態様では、アシル基は、二カルボン酸性脂肪酸から誘導される。
−W−X−Y−Z2
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する側鎖中のカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基が、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Z2は、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
であるが、
ただし、Wが共有結合であってXが−CO−であるならば、Zは−COOHとは異なる]
の側鎖を有するもの、およびそのZn 2+ 錯体である。
ある態様では、Wは4から10の炭素原子を有するα−アミノ酸残基であり、更なる態様では、Wは、α−Asp、β−Asp、α−Glu、γ−Glu、α−hGluおよびδ−hGluからなる群から選択される。
ある態様では、Xは、−CO−である。
ある態様では、Z2は、−COOHである。
ある態様では、Yは、1、2もしくは3の−CH=CH−基と、鎖中に6から32、10から32、12から20、もしくは12−16の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖である。
ある態様では、Yは、式−(CH2)vC6H4(CH2)W−(vおよびwの合計が6から30、10から20、もしくは12−16の範囲になるように、vおよびwは整数であるか、あるいは、それらのうちの一つは0である)の二価の炭化水素鎖である。
更なる態様では、Wは、α−Asp、β−Asp、α−Glu、およびγ−Gluからなる群から選択され;Xは、−CO−もしくは−CH(COOH)COであり;Yは、mが12−18の範囲の整数である−(CH2)m−であり、かつ、Z2は、−COOHもしくは−CH(COOH)2である。
ある態様では、側鎖は、少なくとも一つの芳香族基もしくは少なくとも一つの二官能性PEG基を含んでよい。以下、略語「PEG」は、ポリエチレングリコールに対して用いる。
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
X4は、
・nが1、2、3、4、5もしくは6である−(CH2)n;
・Rが、水素もしくは−(CH2)p−COOH;−(CH2)p−SO3H;−(CH2)p−PO3H2;−(CH2)p−O−SO3H2;−(CH2)p−O−PO3H2;1又2の−(CH2)p−O−COOH基で置換されたアリーレン;−(CH2)p−テトラゾリルであるNR
{上式中、pは1から6の範囲の整数である};
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは、
・結合
であり;
W1は、−COOH、−SO3H、および−PO3H2およびテトラゾリルからなる群から選択される一または二の基で置換されていてもよいアリーレンもしくはヘテロアリーレンであるか、あるいはW1は結合であり;
mは0、1、2、3、4、5もしくは6であり;
X5は、
・−O−;
・
{Rは上記のように定義される};もしくは
・結合
であり;
Y1は、
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、結合もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−
・Rが上記のように定義されるNR;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは
・結合
であり;
Q7は、
・rが4から22の整数である−(CH2)r−;
・1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;もしくは
・式
−(CH2)s−Q8−(C6H4)v1−Q9−(CH2)W −Q10−(C6H4)v2−Q11−(CH2)t−Q12−(C6H4)v3−Q13−(CH2)z−
{Q8−Q13は、互いに独立して、O;Sもしくは結合であってよく;s、w、tおよびzは、互いに独立して、s、w、tおよびzの合計が4から22の範囲になるように、0もしくは1から10の整数であり、かつ、v1、v2、およびv3は、互いに独立して、0もしくは1であってよいが、ただし、W1が結合であるならば、Q7は式−(CH2)v4C6H4(CH2)W1 −(v4およびw1の合計が6から22の範囲になるように、v4およびw1は整数であるか、あるいは、それらのうちの一つは0である)の二価の炭化水素鎖ではない}
の二価の炭化水素鎖
であり;かつ、
Z1は、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−PO3H2;
−O−SO3H;
−O−PO3H2;
−テトラゾリルもしくは
W2が、−COOH、−SO3H、および−PO3H2およびテトラゾリルから選択される一または二の基で置換されているアリーレンもしくはヘテロアリーレンである−O−W2
であるが;
ただし、W1が結合であり、かつv1、v2およびv3が全て0であり、かつQ 1 − 6 が全て結合であれば、Z1はO−W2である]
を有するもの、およびその任意のZn 2+ 錯体である。
本発明のある態様では、Q7は、rが4から22、8から20、12から20、もしくは14−18の範囲の整数である−(CH2)r−である。ある態様では、Q8、Q9、Q12およびQ13は、全て結合であり、v2は1であり、v1およびv3は0である。ある態様では、Q10およびQ11は酸素である。
N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 13 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 15 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−C 6 H 4 CO]desB30ヒトインスリン、およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −(フラニレン)CO]desB30ヒトインスリン、N εB29 −{4−カルボキシ−4−[10−(4−カルボキシ−フェノキシ)−デカノイルアミノ]−ブチリル}desB30ヒトインスリン
からなる群から選択される。
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
それぞれのnは独立して、0、1、2、3、4、5もしくは6であり;
Q1、Q2、Q3、およびQ4は、互いに独立して、
・sが1−20である(CH2CH2O)s−;(CH2CH2CH2O)s−;(CH2CH2CH2CH2O)s−;(CH2CH2OCH2CH2CH2CH2O)s−もしくは(CH2CH2CH2OCH2CH2CH2CH2O)s−;
・rが4から22の整数である−(CH2)r−;もしくは、1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;
・tが1から6の整数である−(CH2)t−もしくは−(CH2OCH2)t−;
・R1およびR2が、互いに独立して、H、−COOH、(CH2)1−6COOHであってよく、かつ、R1およびR2が、それぞれの炭素において異なっていてよく、かつ、qが1−6である−(CR1R2)q−;
・R3およびR4が、互いに独立して、H、−COOHであってよく、かつ、R3およびR4が、それぞれの炭素において異なっていてよく、かつ、q1が1−6である−((CR3R4)q1)1−(NHCO−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−CONH)1−2−((CR3R4)q1−)−、−((CR3R4)q1)1−(NHCO−(CR3R4)q1−CONH)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1;もしくは
・結合
であってよいが;
ただし、Q1−Q4は異なっており;
X1、X2およびX3は、独立して、
・O;
・結合;もしくは
・
{上式中、
Rは、水素もしくはそれぞれのpが、残りのp'と独立して、1から6の範囲の整数である−(CH 2 ) p −COOH、−(CH2)p−SO3H、−(CH2)p−PO3H2、−(CH2)p−O−SO3H;−(CH2)p−O−PO3H2;もしくは−(CH2)p−テトラゾール−5−イルである}
であり;かつ
Zは、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−OSO3H
−OPO3H2
−PO3H2もしくは
−テトラゾール−5−イル
である]
を有するもの、およびその任意のZn 2+ 錯体である。
本発明のある態様では、Zは、−COOHである。
N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ペンタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ヘプタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−α−グルタミル)desB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−γ−グルタミル)desB30ヒトインスリン、N εB29 −3−[2−(2−{2−[2−(ω−カルボキシ−ヘプタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[7−カルボキシヘプタノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(7−カルボキシヘプタノイルアミノ)プロパ−オキシ]ブトキシ}プロピルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[9−カルボキシノナノイルアミノ]プロパ−オキシ)エトキシ]エトキシ}−プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(9−カルボキシノナノイルアミノ)プロパ−オキシ]ブトキシ}−プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(2−[3−(2−(2−{2−(7−カルボキシヘプタノイルアミノ)エトキシ}エトキシ)−エチルカルバモイル]プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル))desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(2−{2−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エチルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[ω−カルボキシペンタデカノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシウンデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシトリデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−ガンマ−γ−D−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(7−カルボキシヘプタノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル(propioniyl)−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン
からなる群から選択される。
親インスリンアナログの別の群では、位置B28のアミノ酸残基はLysであり、位置B29のアミノ酸残基はProである。親インスリンアナログのこの群の具体的な例としては、LysB28ProB29ヒトインスリンが挙げられる。
親インスリンアナログの別の群では、位置B3のアミノ酸残基はLysであり、位置B29のアミノ酸残基はGluである。親インスリンアナログのこの群の具体的な例としては、LysB3GluB29ヒトインスリンが挙げられる。
本発明の更なる態様では、治療の必要のある患者における1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態の治療のための、上記定義のアシル化インスリン誘導体の治療的有効量を、インスリンまたは作用が急速に発現するインスリンアナログと混合して、製薬学的に許容される担体および/または添加物と共に含む製薬学的組成物が提供される。
本発明のある態様では、少なくとも90、92、95、96、97、98、99、99.5%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する。
アシル化インスリン誘導体と即効型インスリンアナログとは、約90%/10%;約75%/25%、約70%/30% 約50%/50%、約25%/75%、約30%/70%もしくは約10%/90%のモル比で混合することができる。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.3より多い亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約4.5より多い亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5より多い亜鉛原子を組成物に添加する。更なる態様では、6分子のアシル化インスリン毎に約5.5より多い亜鉛原子、もしくは、6分子のアシル化インスリン毎に約6.5より多い亜鉛原子、もしくは、6分子のアシル化インスリン毎に約7.0より多い亜鉛原子、もしくは、6分子のアシル化インスリン毎に約7.5より多い亜鉛原子を組成物に添加する。
本発明のある態様では、本方法は、6分子のアシル化インスリン毎に約4.3から約12の亜鉛原子を組成物に添加することを含む。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5から約11.4の亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を組成物に添加する。
更なる態様では、6分子のアシル化インスリン毎に約6から約10.5の亜鉛原子、もしくは、6分子のアシル化インスリン毎に約6.5から約10の亜鉛原子、もしくは、6分子のアシル化インスリン毎に約7から約9の亜鉛原子を組成物に添加する。
本発明の更なる態様では、6分子のアシル化インスリン毎に約2より多い亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約3より多い亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約4より多い亜鉛原子を保存料の添加後に組成物に添加する。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5から約11.4の亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を保存料の添加後に組成物に添加する。
本発明のある態様では、本方法は、保存料の添加前に亜鉛の一部を添加し、保存料の添加後に亜鉛の一部を添加することを含む。
ある態様では、本方法は、6分子のアシル化インスリン毎に少なくとも0.5の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加後に添加することを含む。ある態様では、本方法は、6分子のアシル化インスリン毎に少なくとも0.5の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に少なくとも2、3、4、5、6、7、8、9、10もしくは11の亜鉛原子を保存料の添加後に添加することを含む。
本発明のある態様では、保存料の添加前に添加する亜鉛原子の数は、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子であり、保存料の添加後に添加する亜鉛原子の数は、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子である。ある態様では、本方法は、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に少なくとも4、5、6、7、8もしくは9の亜鉛原子を保存料の添加後に添加することを含む。
本発明のある態様では、本方法は、一工程で、製薬学的組成物に亜鉛原子の総量を添加することを含む。
本発明のある態様では、本方法は、二以上の工程で、製薬学的組成物に亜鉛原子を添加することを含む。例えば、亜鉛は、それぞれの工程が最大1Zn/6insのうちの少量の添加を含む1、2、3、4または5工程で、組成物に添加されてよい。亜鉛は、それぞれの工程が2Zn/6ins、3Zn/6ins、4Zn/6ins、5Zn/6insもしくは6Zn/6insのうちの少量の添加を含む1、2、3、4または5工程で、組成物に添加されてよい。
−W−X−Y−Z2
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する、側鎖中にカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基は、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Z2は、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
であるが、
ただし、Wが共有結合であってXが−CO−であるならば、Zは−COOHとは異なる]
の側鎖を有するアシル化インスリンを含む。
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
X4は、
・nが1、2、3、4、5もしくは6である−(CH2)n;
・Rが、水素もしくは−(CH2)p−COOH;−(CH2)p−SO3H;−(CH2)p−PO3H2;−(CH2)p−O−SO3H2;−(CH2)p−O−PO3H2;1又2の−(CH2)p−O−COOH基で置換されたアリーレン;−(CH2)p−テトラゾリルであるNR
{上式中、pは1から6の範囲の整数である};
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは、
・結合
であり;
W1は、−COOH、−SO3H、および−PO3H2およびテトラゾリルからなる群から選択される一または二の基で置換されていてもよいアリーレンもしくはヘテロアリーレンであるか、あるいはW1は結合であり;
mは0、1、2、3、4、5もしくは6であり;
X5は、
・−O−;
・
{Rは上記のように定義される};もしくは
・結合
であり;
Y1は、
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、結合もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−
・Rが上記のように定義されるNR;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは
・結合
であり;
Q7は、
・rが4から22の整数である−(CH2)r−;
・1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;もしくは
・式
−(CH2)s−Q8−(C6H4)v1−Q9−(CH2)W −Q10−(C6H4)v2−Q11−(CH2)t−Q12−(C6H4)v3−Q13−(CH2)z−
{Q8−Q13は、互いに独立して、O;Sもしくは結合であってよく;s、w、tおよびzは、互いに独立して、s、w、tおよびzの合計が4から22の範囲になるように、0もしくは1から10の整数であり、かつ、v1、v2、およびv3は、互いに独立して、0もしくは1であってよいが、ただし、W1が結合であるならば、Q7は式−(CH2)v4C6H4(CH2)W1 −(v4およびw1の合計が6から22の範囲になるように、v4およびw1は整数であるか、あるいは、それらのうちの一つは0である)の二価の炭化水素鎖ではない}
の二価の炭化水素鎖
であり;かつ、
Z1は、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−PO3H2;
O−SO3H;
O−PO3H2;
−テトラゾリルもしくは
W2が、−COOH、−SO3H、および−PO3H2およびテトラゾリルから選択される一または二の基で置換されているアリーレンもしくはヘテロアリーレンである−O−W2
であるが;
ただし、W1が結合であり、かつv1、v2およびv3が全て0であり、かつQ8−13が全て結合であれば、Z1はO−W2である]
を有するもの、およびその任意のZn 2+ 錯体である。
本発明のある態様では、Q7は、rが4から22、8から20、12から20、もしくは14−18の範囲の整数である−(CH2)r−である。ある態様では、Q8、Q9、Q12およびQ13は、全て結合であり、v2は1であり、v1およびv3は0である。ある態様では、Q10およびQ11は酸素である。
N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 13 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 15 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−C 6 H 4 CO]desB30ヒトインスリン、およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −(フラニレン)CO]desB30ヒトインスリン、N εB29 −{4−カルボキシ−4−[10−(4−カルボキシ−フェノキシ)−デカノイルアミノ]−ブチリル}desB30ヒトインスリン
からなる群から選択される。
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
それぞれのnは独立して、0、1、2、3、4、5もしくは6であり;
Q1、Q2、Q3、およびQ4は、互いに独立して、
・sが1−20である(CH2CH2O)s−;(CH2CH2CH2O)s−;(CH2CH2CH2CH2O)s−;(CH2CH2OCH2CH2CH2CH2O)s−もしくは(CH2CH2CH2OCH2CH2CH2CH2O)s−;
・rが4から22の整数である−(CH2)r−;もしくは、1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;
・tが1から6の整数である−(CH2)t−もしくは−(CH2OCH2)t−;
・R1およびR2が、互いに独立して、H、−COOH、(CH2)1−6COOHであってよく、かつ、R1およびR2が、それぞれの炭素において異なっていてよく、かつ、qが1−6である−(CR1R2)q−;
・R3およびR4が、互いに独立して、H、−COOHであってよく、かつ、R3およびR4が、それぞれの炭素において異なっていてよく、かつ、q1が1−6である−((CR3R4)q1)1−(NHCO−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−CONH)1−2−((CR3R4)q1−)−、−((CR3R4)q1)1−(NHCO−(CR3R4)q1−CONH)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1;もしくは
・結合
であってよいが;
ただし、Q1−Q4は異なっており;
X1、X2およびX3は、独立して、
・O;
・結合;もしくは
・
{上式中、
Rは、水素もしくはそれぞれのpが、残りのp'と独立して、1から6の範囲の整数である−(CH 2 ) p −COOH、−(CH2)p−SO3H、−(CH2)p−PO3H2、−(CH2)p−O−SO3H;−(CH2)p−O−PO3H2;もしくは−(CH2)p−テトラゾール−5−イルである}
であり;かつ
Zは、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−OSO3H
−OPO3H2
−PO3H2もしくは
−テトラゾール−5−イル
である]
を有するもの、およびその任意のZn 2+ 錯体である。
本発明のある態様では、Zは、−COOHである。
本発明のある態様では、アシル化インスリンを含む製薬学的組成物は、糖尿病の治療のための医薬の製造のために用いられる。
ある態様では、本発明は、製薬学的に許容される担体および/または製薬学的に許容される添加物を有する本発明の製薬学的組成物に関し、その組成物は、治療を必要とする患者における1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態の治療のために提供され得る。
本発明のある態様では、1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態の治療において用いるための製薬学的組成物の製造のための方法が提供される。
本発明のある態様では、治療の必要のある患者において、1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態を治療するための方法であって、本発明に係る製薬学的組成物の治療的有効量を患者に投与することを含む方法が提供される。
本発明のある態様では、1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態の治療において用いるための製薬学的組成物の製造のための方法が提供される。
第一または第二または第三などの単位投与がこの明細書の至るところで記述されるとき、これは投与の好ましい順序を示すものではなく、単に便宜上の目的のためになされるものである。
「連続的に」投与するとは、第一の薬剤の投与に続く、15分以上の時間間隔での第二の薬剤の投与を意味する。二つの単位投与形態のどちらが最初に投与されてもよい。好ましくは、双方の製品は、同じ静脈経路を通して注射する。
1.
アシル化インスリンを含み、6分子のアシル化インスリン毎に4より多い亜鉛原子をさらに含む可溶性製薬学的組成物。
2.
6分子のアシル化インスリン毎に最大約12の亜鉛原子を含む項1に記載の製薬学的組成物。
6分子のアシル化インスリン毎に約4.3から約12の亜鉛原子を含む項1または2に記載の製薬学的組成物。
4.
6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を含む項1ないし3の何れか一項に記載の製薬学的組成物。
5.
少なくとも85%のアシル化インスリンが、アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体として存在する項1ないし4の何れか一項に記載の製薬学的組成物。
少なくとも92%のアシル化インスリンが、アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体として存在する項1ないし5の何れか一項に記載の製薬学的組成物。
7.
少なくとも95%のアシル化インスリンが、アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体として存在する項1ないし6の何れか一項に記載の製薬学的組成物。
8.
少なくとも97%のアシル化インスリンが、アシル化インスリンドデカマー複合体もしくはアシル化インスリンドデカマーより高分子量の複合体として存在する項1ないし7の何れか一項に記載の製薬学的組成物。
組成物が界面活性剤を含む項1ないし8の何れか一項に記載の製薬学的組成物。
10.
アシル化インスリンが、親インスリン部分のB鎖中のLys残基のε−アミノ基でアシル化されたインスリンである項1ないし9の何れか一項に記載の製薬学的組成物。
11.
アシル基が、少なくとも一つの遊離カルボン酸基もしくは中性pHで負に荷電する基を含んでなる項1ないし10の何れか一項に記載の製薬学的組成物。
アシル基が、4から32の炭素原子を有する二カルボン酸性脂肪酸から誘導される項1または10−11の何れか一項に記載の製薬学的組成物。
13.
アシル基が、アミド結合を介したリンカー基を介して、インスリン分子と結合している項1または10−12の何れか一項に記載の製薬学的組成物。
14.
リンカー基が、少なくとも一つの遊離カルボキシル基もしくは中性pHで負に荷電する基を含んでなる項1または13に記載の製薬学的組成物。
インスリン分子が、親インスリン部分のB鎖のN末端アミノ酸残基のα−アミノ基もしくはB鎖中のLys残基のε−アミノ基の何れか一方とアミド結合を介して結合している側鎖であって、少なくとも一つの遊離カルボン酸基もしくは中性pHで負に荷電する基を含んでなる側鎖と、炭素鎖に約4から約32の炭素原子を有する脂肪酸部分と;あり得る、側鎖中の個々の構成成分をアミド結合を介して一緒に連結する一または複数のリンカーとを有する項1ないし14の何れか一項に記載の製薬学的組成物。
16.
側鎖が少なくとも一つの芳香族基を含んでなる項1−15に記載の製薬学的組成物。
17.
側鎖が少なくとも一つの二官能性PEG基を含んでなる項1−15に記載の製薬学的組成物。
インスリン分子が、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z2
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する、側鎖中にカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基は、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Z2は、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
であるが、
ただし、Wが共有結合であってXが−CO−であるならば、Zは−COOHとは異なる]
の側鎖を有するもの、およびそのZn 2+ 錯体である、項1−15の何れか一項に記載の製薬学的組成物。
19.
Z2が−COOHである項1−15および18の何れか一項に記載の製薬学的組成物。
アシル化インスリンが、N εB29 −(N α −(HOOC(CH 2 ) 14 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 15 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 17 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 18 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−Glu−N−(γ−Glu))desB30ヒトインスリン;N εB29 −(N α −(Asp−OC(CH 2 ) 16 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Glu−OC(CH 2 ) 14 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Glu−OC(CH 2 ) 14 CO−)desB30ヒトインスリン;N εB29 −(N α −(Asp−OC(CH 2 ) 16 CO−)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−α−Glu−N−(β−Asp))desB30ヒトインスリン;N εB29 −(N α −(Gly−OC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Sar−OC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;(N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−β−Asp)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−α−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−D−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 14 CO)−β−D−Asp)desB30ヒトインスリンN εB29 −(N α −(HOOC(CH 2 ) 14 CO)−β−D−Asp)desB30ヒトインスリン;N εB29 −(N−HOOC(CH 2 ) 16 CO−β−D−Asp)desB30ヒトインスリン;N εB29 −(N−HOOC(CH 2 ) 14 CO−IDA)desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−Gly]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−Gly]desB30ヒトインスリン;およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−β−Ala]desB30ヒトインスリンからなる群から選択される項1−15および18−19の何れか一項に記載の製薬学的組成物。
アシル化インスリンが、式
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
X4は、
・nが1、2、3、4、5もしくは6である−(CH2)n;
・Rが、水素もしくは−(CH2)p−COOH;−(CH2)p−SO3H;−(CH2)p−PO3H2;−(CH2)p−O−SO3H2;−(CH2)p−O−PO3H2;1又2の−(CH2)p−O−COOH基で置換されたアリーレン;−(CH2)p−テトラゾリルであるNR
{上式中、pは1から6の範囲の整数である};
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは、
・結合
であり;
W1は、−COOH、−SO3H、および−PO3H2およびテトラゾリルからなる群から選択される一または二の基で置換されていてもよいアリーレンもしくはヘテロアリーレンであるか、あるいはW1は結合であり;
mは0、1、2、3、4、5もしくは6であり;
X5は、
・−O−;
・
{Rは上記のように定義される};もしくは
・結合
であり;
Y1は、
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、結合もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−
・Rが上記のように定義されるNR;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは
・結合
であり;
Q7は、
・rが4から22の整数である−(CH2)r−;
・1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;もしくは
・式
−(CH2)s−Q8−(C6H4)v1−Q9−(CH2)W −Q10−(C6H4)v2−Q11−(CH2)t−Q12−(C6H4)v3−Q13−(CH2)z−
{Q8−Q13は、互いに独立して、O;Sもしくは結合であってよく;s、w、tおよびzは、互いに独立して、s、w、tおよびzの合計が4から22の範囲になるように、0もしくは1から10の整数であり、かつ、v1、v2、およびv3は、互いに独立して、0もしくは1であってよいが、ただし、W1が結合であるならば、Q7は式−(CH2)v4C6H4(CH2)W1 −(v4およびw1の合計が6から22の範囲になるように、v4およびw1は整数であるか、あるいは、それらのうちの一つは0である)の二価の炭化水素鎖ではない}
の二価の炭化水素鎖
であり;かつ、
Z1は、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−PO3H2;
−O−SO3H;
−O−PO3H2;
−テトラゾリルもしくは
W2が、−COOH、−SO3H、および−PO3H2およびテトラゾリルから選択される一または二の基で置換されているアリーレンもしくはヘテロアリーレンである−O−W2
であるが;
ただし、W1が結合であり、かつv1、v2およびv3が全て0であり、かつQ8−13が全て結合であれば、Z1はO−W2である]
を有するもの、およびその任意のZn 2+ 錯体である、項1−16に記載の製薬学的組成物。
W1がフェニレンである項1または21に記載の製薬学的組成物。
23.
W1が、窒素、酸素または硫黄を含んでなる5−7員環ヘテロ環系である項1または21に記載の製薬学的組成物。
24.
W1が、少なくとも一つの酸素を含んでなる5−7員環ヘテロ環系である項1、21および23に記載の製薬学的組成物。
本発明のある態様では、Q7は、rが4から22、8から20、12から20、もしくは14−18の範囲の整数である−(CH2)r−である項21−24に記載の製薬学的組成物。
26.
Q8、Q9、Q12およびQ13は、全て結合であり、v2は1であり、v1およびv3は0である項21−24に記載の製薬学的組成物。
27.
Q10およびQ11は酸素である項26に記載の製薬学的組成物。
X4およびY1は結合であり、X5は、
[上式中、Rは、pが1−4である−(CH2)p−COOHである]
である項21−27に記載の製薬学的組成物。
29.
Z1は、−COOHである項21−28に記載の製薬学的組成物。
アシル化インスリンが、式
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
それぞれのnは独立して、0、1、2、3、4、5もしくは6であり;
Q1、Q2、Q3、およびQ4は、互いに独立して、
・sが1−20である(CH2CH2O)s−;(CH2CH2CH2O)s−;(CH2CH2CH2CH2O)s−;(CH2CH2OCH2CH2CH2CH2O)s−もしくは(CH2CH2CH2OCH2CH2CH2CH2O)s−;
・rが4から22の整数である−(CH2)r−;もしくは、1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;
・tが1から6の整数である−(CH2)t−もしくは−(CH2OCH2)t−;
・R1およびR2が、互いに独立して、H、−COOH、(CH2)1−6COOHであってよく、かつ、R1およびR2が、それぞれの炭素において異なっていてよく、かつ、qが1−6である−(CR1R2)q−;
・R3およびR4が、互いに独立して、H、−COOHであってよく、かつ、R3およびR4が、それぞれの炭素において異なっていてよく、かつ、q1が1−6である−((CR3R4)q1)1−(NHCO−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−CONH)1−2−((CR3R4)q1−)−、−((CR3R4)q1)1−(NHCO−(CR3R4)q1−CONH)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1;もしくは
・結合
であってよいが;
ただし、Q1−Q4は異なっており;
X1、X2およびX3は、独立して、
・O;
・結合;もしくは
・
{上式中、
Rは、水素もしくはそれぞれのpが、残りのp'と独立して、1から6の範囲の整数である−(CH 2 ) p −COOH、−(CH2)p−SO3H、−(CH2)p−PO3H2、−(CH2)p−O−SO3H;−(CH2)p−O−PO3H2;もしくは−(CH2)p−テトラゾール−5−イルである}
であり;かつ
Zは、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−OSO3H
−OPO3H2
−PO3H2もしくは
−テトラゾール−5−イル
である]
を有するもの、およびその任意のZn 2+ 錯体である、項1−15および17の製薬学的組成物。
sが、2−12、2−4もしくは2−3の範囲の整数である項1または30に記載の製薬学的組成物。
32.
sが好ましくは1である項1または30に記載の製薬学的組成物。
33.
Zが−COOHである項30−32に記載の製薬学的組成物。
34.
親インスリンがdesB30ヒトインスリンアナログである項1ないし33の何れか一項に記載の製薬学的組成物。
親インスリンが、ヒトインスリン;desB1ヒトインスリン;desB30ヒトインスリン;GlyA21ヒトインスリン;GlyA21desB30ヒトインスリン;AspB28ヒトインスリン;ブタインスリン;LysB28ProB29ヒトインスリン;GlyA21ArgB31ArgB32ヒトインスリン;およびLysB3GluB29ヒトインスリンもしくはAspB28desB30ヒトインスリンからなる群から選択される項1ないし34の何れか一項に記載の製薬学的組成物。
アシル化インスリンが、
N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 13 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 15 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−C 6 H 4 CO]desB30ヒトインスリン、およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −(フラニレン)CO]desB30ヒトインスリン、N εB29 −{4−カルボキシ−4−[10−(4−カルボキシ−フェノキシ)−デカノイルアミノ]−ブチリル}desB30ヒトインスリン
からなる群から選択される項1−16、21−29および34−35に記載の製薬学的組成物。
アシル化インスリンが、N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ペンタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ヘプタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−α−グルタミル)desB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−γ−グルタミル)desB30ヒトインスリン、N εB29 −3−[2−(2−{2−[2−(ω−カルボキシ−ヘプタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[7−カルボキシヘプタノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(7−カルボキシヘプタノイルアミノ)プロパ−オキシ]ブトキシ}プロピルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[9−カルボキシノナノイルアミノ]プロパ−オキシ)エトキシ]エトキシ}−プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(9−カルボキシノナノイルアミノ)プロパ−オキシ]ブトキシ}−プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(2−[3−(2−(2−{2−(7−カルボキシヘプタノイルアミノ)エトキシ}エトキシ)−エチルカルバモイル]プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル))desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(2−{2−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エチルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[ω−カルボキシペンタデカノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシウンデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシトリデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−ガンマ−γ−D−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(7−カルボキシヘプタノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル(propioniyl)−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリンからなる群から選択される項1−15、17および30−35に記載の製薬学的組成物。
約6.5から8.5のpHを有する項1−37の何れか一項に記載の製薬学的組成物。
39.
即効型インスリンをさらに含む項1−38の何れか一項に記載の製薬学的組成物。
40.
少なくとも85%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する項1および39に記載の製薬学的組成物。
少なくとも92%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する項1および39−40に記載の製薬学的組成物。
42.
少なくとも95%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する項1および39−41に記載の製薬学的組成物。
少なくとも97%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する項1および39−42に記載の製薬学的組成物。
44.
少なくとも99%の即効型インスリンが、即効型インスリンヘキサマーもしくは即効型インスリンヘキサマーより低分子量の複合体として存在する項1および39−43に記載の製薬学的組成物。
即効型インスリンが、AspB28ヒトインスリン、LysB3GluB29ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである項39−44に記載の製薬学的組成物。
46.
6分子のアシル化インスリン毎に約4より多い亜鉛原子を組成物に添加する、アシル化インスリンを含む製薬学的組成物を製造するための方法。
47.
6分子のアシル化インスリン毎に最大約12の亜鉛原子を組成物に添加する項46に記載の方法。
6分子のアシル化インスリン毎に約4.3から約12の亜鉛原子を組成物に添加する項46−47の何れか一項に記載の方法。
49.
保存料の添加前に、亜鉛を組成物に添加する項46−48に記載の方法。
50.
6分子のアシル化インスリン毎に1より多い亜鉛原子を保存料の添加前に組成物に添加する項46−49の何れか一項に記載の方法。
6分子のアシル化インスリン毎に2より多い亜鉛原子を保存料の添加前に組成物に添加する項46−50の何れか一項に記載の方法。
52.
6分子のアシル化インスリン毎に3より多い亜鉛原子を保存料の添加前に組成物に添加する項46−51の何れか一項に記載の方法。
53.
6分子のアシル化インスリン毎に4より多い亜鉛原子を保存料の添加前に組成物に添加する項46−52の何れか一項に記載の方法。
6分子のアシル化インスリン毎に5より多い亜鉛原子を保存料の添加前に組成物に添加する項46−53の何れか一項に記載の方法。
55.
保存料の添加後に、亜鉛を組成物に添加する項46−48に記載の方法。
56.
6分子のアシル化インスリン毎に少なくとも0.5の亜鉛原子を保存料の添加後に組成物に添加する項46−48および55に記載の方法。
6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加後に組成物に添加する項46−48および55−56の何れか一項に記載の方法。
58.
保存料の添加前に亜鉛の一部を添加し、保存料の添加後に亜鉛の一部を添加する項46ないし57の何れか一項に記載の方法。
59.
保存料の添加前に添加する亜鉛原子の数は、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子であり、保存料の添加後に添加する亜鉛原子の数は、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子である項46ないし58の何れか一項に記載の方法。
保存料がフェノールおよび/またはm−クレゾールである項46ないし59の何れか一項に記載の方法。
61.
界面活性剤を製薬学的組成物と混合する項46ないし60の何れか一項に記載の方法。
アシル化インスリンが、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z2
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する、側鎖中にカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基は、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Z2は、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
であるが、
ただし、Wが共有結合であってXが−CO−であるならば、Zは−COOHとは異なる]
の側鎖を有するもの、およびそのZn 2+ 錯体である、項46ないし61の何れか一項に記載の方法。
アシル化インスリンが、N εB29 −(N α −(HOOC(CH 2 ) 14 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 15 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 17 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 18 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−Glu−N−(γ−Glu))desB30ヒトインスリン;N εB29 −(N α −(Asp−OC(CH 2 ) 16 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Glu−OC(CH 2 ) 14 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Glu−OC(CH 2 ) 14 CO−)desB30ヒトインスリン;N εB29 −(N α −(Asp−OC(CH 2 ) 16 CO−)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−α−Glu−N−(β−Asp))desB30ヒトインスリン;N εB29 −(N α −(Gly−OC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(Sar−OC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−γ−Glu)desB30ヒトインスリン;(N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−β−Asp)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 13 CO)−α−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 16 CO)−γ−D−Glu)desB30ヒトインスリン;N εB29 −(N α −(HOOC(CH 2 ) 14 CO)−β−D−Asp)desB30ヒトインスリン N εB29 −(N α −(HOOC(CH 2 ) 14 CO)−β−D−Asp)desB30ヒトインスリン;N εB29 −(N−HOOC(CH 2 ) 16 CO−β−D−Asp)desB30ヒトインスリン;N εB29 −(N−HOOC(CH 2 ) 14 CO−IDA)desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−Gly]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−Gly]desB30ヒトインスリン;およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−β−Ala]desB30ヒトインスリンからなる群から選択される項46ないし62の何れか一項に記載の方法。
アシル化インスリンが、式
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
X4は、
・nが1、2、3、4、5もしくは6である−(CH2)n;
・Rが、水素もしくは−(CH2)p−COOH;−(CH2)p−SO3H;−(CH2)p−PO3H2;−(CH2)p−O−SO3H2;−(CH2)p−O−PO3H2;1又2の−(CH2)p−O−COOH基で置換されたアリーレン;−(CH2)p−テトラゾリルであるNR
{上式中、pは1から6の範囲の整数である};
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは、
・結合
であり;
W1は、−COOH、−SO3H、および−PO3H2およびテトラゾリルからなる群から選択される一または二の基で置換されていてもよいアリーレンもしくはヘテロアリーレンであるか、あるいはW1は結合であり;
mは0、1、2、3、4、5もしくは6であり;
X5は、
・−O−;
・
{Rは上記のように定義される};もしくは
・結合
であり;
Y1は、
・R1およびR2は、互いに独立し、それぞれのqの値からも独立して、H、−COOH、結合もしくはOHであってよく、qは1−6であり、Rは上記のように定義される−(CR1R2)q−NR−CO−
・Rが上記のように定義されるNR;
・R3およびR4は、互いに独立し、それぞれのq1の値からも独立して、H、−COOH、もしくはOHであってよく、q1は1−6であり、Rは上記のように定義される−((CR3R4)q1−NR−CO)2−4−;もしくは
・結合
であり;
Q7は、
・rが4から22の整数である−(CH2)r−;
・1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;もしくは
・式
−(CH2)s−Q8−(C6H4)v1−Q9−(CH2)W −Q10−(C6H4)v2−Q11−(CH2)t−Q12−(C6H4)v3−Q13−(CH2)z−
{Q8−Q13は、互いに独立して、O;Sもしくは結合であってよく;s、w、tおよびzは、互いに独立して、s、w、tおよびzの合計が4から22の範囲になるように、0もしくは1から10の整数であり、かつ、v1、v2、およびv3は、互いに独立して、0もしくは1であってよいが、ただし、W1が結合であるならば、Q7は式−(CH2)v4C6H4(CH2)W1 −(v4およびw1の合計が6から22の範囲になるように、v4およびw1は整数であるか、あるいは、それらのうちの一つは0である)の二価の炭化水素鎖ではない}
の二価の炭化水素鎖
であり;かつ、
Z1は、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−PO3H2;
O−SO3H;
O−PO3H2;
−テトラゾリルもしくは
W2が、−COOH、−SO3H、および−PO3H2およびテトラゾリルから選択される一または二の基で置換されているアリーレンもしくはヘテロアリーレンである−O−W2
であるが;
ただし、W1が結合であり、かつv1、v2およびv3が全て0であり、かつQ8−13が全て結合であれば、Z1はO−W2である]
を有するもの、およびその任意のZn 2+ 錯体である、項46ないし61の何れか一項に記載の方法。
W1がフェニレンである項46および64に記載の方法。
66.
W1が、窒素、酸素または硫黄を含んでなる5−7員環ヘテロ環系である項46および64に記載の方法。
67.
W1が、少なくとも一つの酸素を含んでなる5員環ヘテロ環系である項66に記載の方法。
本発明のある態様では、Q7は、rが4から22、8から20、12から20、もしくは14−18の範囲の整数である−(CH2)r−である項46および64−67に記載の方法。
69.
Q8、Q9、Q12およびQ13は、全て結合であり、v2は1であり、v1およびv3は0である項46および64−68に記載の方法。
70.
Q10およびQ11は酸素である項69に記載の方法。
アシル化インスリンが、式
[上式中、
Insは、B鎖のN末端アミノ酸残基のα−アミノ基もしくはインスリン部分のB鎖中に存在するLys残基のε−アミノ基を介して、アミド結合を介して側鎖のCO−基と結合している親インスリン部分であり;
それぞれのnは独立して、0、1、2、3、4、5もしくは6であり;
Q1、Q2、Q3、およびQ4は、互いに独立して、
・sが1−20である(CH2CH2O)s−;(CH2CH2CH2O)s−;(CH2CH2CH2CH2O)s−;(CH2CH2OCH2CH2CH2CH2O)s−もしくは(CH2CH2CH2OCH2CH2CH2CH2O)s−;
・rが4から22の整数である−(CH2)r−;もしくは、1、2もしくは3の−CH=CH−基と、鎖中に4から22の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖;
・tが1から6の整数である−(CH2)t−もしくは−(CH2OCH2)t−;
・R1およびR2が、互いに独立して、H、−COOH、(CH2)1−6COOHであってよく、かつ、R1およびR2が、それぞれの炭素において異なっていてよく、かつ、qが1−6である−(CR1R2)q−;
・R3およびR4が、互いに独立して、H、−COOHであってよく、かつ、R3およびR4が、それぞれの炭素において異なっていてよく、かつ、q1が1−6である−((CR3R4)q1)1−(NHCO−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−CONH)1−2−((CR3R4)q1−)−、−((CR3R4)q1)1−(NHCO−(CR3R4)q1−CONH)1−2−((CR3R4)q1)1もしくは−((CR3R4)q1)1−(CONH−(CR3R4)q1−NHCO)1−2−((CR3R4)q1)1;もしくは
・結合
であってよいが;
ただし、Q1−Q4は異なっており;
X1、X2およびX3は、独立して、
・O;
・結合;もしくは
・
{上式中、
Rは、水素もしくはそれぞれのpが、残りのp'と独立して、1から6の範囲の整数である−(CH 2 ) p −COOH、−(CH2)p−SO3H、−(CH2)p−PO3H2、−(CH2)p−O−SO3H;−(CH2)p−O−PO3H2;もしくは−(CH2)p−テトラゾール−5−イルである}
であり;かつ
Zは、
−COOH;
−CO−Asp;
−CO−Glu;
−CO−Gly;
−CO−Sar;
−CH(COOH)2;
−N(CH2COOH)2;
−SO3H
−OSO3H
−OPO3H2
−PO3H2もしくは
−テトラゾール−5−イル
である]
を有するもの、およびその任意のZn 2+ 錯体である、項46−61に記載の方法。
sが、2−12、2−4もしくは2−3の範囲である項73に記載の方法。
75.
sが好ましくは1である項73に記載の方法。
76.
Zが−COOHである項73−75に記載の方法。
77.
親インスリンがdesB30ヒトインスリンアナログである項46ないし76の何れか一項に記載の方法。
親インスリンが、ヒトインスリン;desB1ヒトインスリン;desB30ヒトインスリン;GlyA21ヒトインスリン;GlyA21desB30ヒトインスリン;AspB28ヒトインスリン;ブタインスリン;LysB28 ProB29ヒトインスリン;GlyA21 ArgB31 ArgB32ヒトインスリン;およびLysB3 GluB29ヒトインスリンもしくはAspB28 desB30ヒトインスリンからなる群から選択される項46ないし77の何れか一項に記載の方法。
アシル化インスリンが、
N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 13 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 15 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 16 CO)−N−(カルボキシエチル)−CH 2 −C 6 H 4 CO]desB30ヒトインスリン;N εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシメチル)−C 6 H 4 CO]desB30ヒトインスリン、およびN εB29 −[N−(HOOC(CH 2 ) 14 CO)−N−(カルボキシエチル)−CH 2 −(フラニレン)CO]desB30ヒトインスリン、N εB29 −{4−カルボキシ−4−[10−(4−カルボキシ−フェノキシ)−デカノイルアミノ]−ブチリル}desB30ヒトインスリン
からなる群から選択される項46−61、64−72または77−78に記載の方法。
アシル化インスリンが、N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ペンタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −(3−[2−{2−(2−[ω−カルボキシ−ヘプタデカノイル−γ−グルタミル−(2−アミノ−エトキシ)]−エトキシ)−エトキシ}−エトキシ]−プロピノイル(propinoyl))desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−α−グルタミル)desB30ヒトインスリン、N εB29 −(ω−[2−(2−{2−[2−(2−カルボキシ−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エチルカルバモイル]−ヘプタデカノイル−γ−グルタミル)desB30ヒトインスリン、N εB29 −3−[2−(2−{2−[2−(ω−カルボキシ−ヘプタデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロピオニル−γ−グルタミルdesB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[7−カルボキシヘプタノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(7−カルボキシヘプタノイルアミノ)プロパ−オキシ]ブトキシ}プロピルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[9−カルボキシノナノイルアミノ]プロパ−オキシ)エトキシ]エトキシ}−プロピルカルバモイル)プロピオニル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(9−カルボキシノナノイルアミノ)プロパ−オキシ]ブトキシ}−プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(2−[3−(2−(2−{2−(7−カルボキシヘプタノイルアミノ)エトキシ}エトキシ)−エチルカルバモイル]プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル))desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(2−{2−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−[2−(2−{2−[2−(2−{2−[2−(ω−カルボキシ−トリデカノイルアミノ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−エトキシ)−エトキシ]−エトキシ}−プロポイオノイル(propionoyl)−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)−エトキシ]−エトキシ}−エチルカルバモイル)−プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{2−[2−(3−[ω−カルボキシペンタデカノイルアミノ]プロパ−オキシ)エトキシ]−エトキシ}プロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシウンデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(3−{4−[3−(ω−カルボキシトリデカノイルアミノ)プロパ−オキシ]ブトキシプロピルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −(3−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エチルカルバモイル)プロピオニル−γ−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシ−ペンタデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−ガンマ−γ−D−グルタミル)desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(7−カルボキシヘプタノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(9−カルボキシノナノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル(propioniyl)−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシウンデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリン、N εB29 −{3−[2−(2−{2−[2−(ω−カルボキシトリデカノイルアミノ)エトキシ]エトキシ}エトキシ)エトキシ]プロピオニル−γ−グルタミル}desB30ヒトインスリンからなる群から選択される項46−61または73−78の何れか一項に記載の方法。
即効型インスリンを組成物と混合する項46ないし80の何れか一項に記載の方法。
82.
即効型インスリンが、AspB28ヒトインスリン、LysB3GluB29ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである項46および80に記載の方法。
83.
糖尿病の治療のための医薬の製造のための、項1−45の何れか一項に記載の組成物の使用。
項1−45に記載の製薬学的組成物の治療的有効量を製薬学的に許容される担体と共に含む、治療の必要がある患者における糖尿病の治療のための製薬学的組成物。
85.
項1−45に記載の製薬学的組成物の治療的有効量を製薬学的に許容される担体と共に患者に投与することを含む、治療の必要がある患者における糖尿病の治療方法。
86.
糖尿病の肺性治療のための、項85に記載の方法。
1型糖尿病、2型糖尿病および高血糖を引き起こす他の状態の治療において使用するための製薬学的組成物の製造のための、項1−45に記載の組成物の使用。
88.
実施例に記載される組成物。
本発明の別の態様は、以下に要約される。
91.
アシル化インスリンを含み、6分子のアシル化インスリン毎に4より多い亜鉛原子をさらに含む可溶性製薬学的組成物。
アシル化インスリンを含み、6分子のアシル化インスリン毎に5より多い亜鉛原子をさらに含む項91に記載の可溶性製薬学的組成物。
93.
6分子のアシル化インスリン毎に最大約14の亜鉛原子を含む項91−92に記載の製薬学的組成物。
94.
6分子のアシル化インスリン毎に約5から約14の亜鉛原子を含む項91−93に記載の製薬学的組成物。
6分子のアシル化インスリン毎に約5から約13の亜鉛原子を含む項91−94の何れか一項に記載の製薬学的組成物。
96.
6分子のアシル化インスリン毎に約5から約12の亜鉛原子を含む項91−95の何れか一項に記載の製薬学的組成物。
97.
6分子のアシル化インスリン毎に約5.3から約12の亜鉛原子を含む項91−96の何れか一項に記載の製薬学的組成物。
6分子のアシル化インスリン毎に約5.5から約11.4の亜鉛原子を含む項91−97の何れか一項に記載の製薬学的組成物。
99.
6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を含む項91−98の何れか一項に記載の製薬学的組成物。
100.
アシル化インスリンが、LysB29(Nε−テトラデカノイル)desB30ヒトインスリンもしくはLysB29Nε−リトコロイル(lithocholoyl)−γ−Glu desB30ヒトインスリンである項91−99の何れか一項に記載の製薬学的組成物。
アシル化インスリンが、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する、側鎖中にカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基は、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Zは、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
である]
の側鎖を有さない項91−100の何れか一項に記載の製薬学的組成物。
アシル化インスリンがLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンではない0項91−101の何れか一項に記載の製薬学的組成物。
102.
約6.5から8.5のpHを有する項91ないし101の何れか一項に記載の製薬学的組成物。
103.
即効型インスリンをさらに含む項91ないし102の何れか一項に記載の製薬学的組成物。
104.
即効型インスリンが、AspB28ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである項103に記載の製薬学的組成物。
6分子のアシル化インスリン毎に約4より多い亜鉛原子を組成物に添加する、アシル化インスリンを含む製薬学的組成物を製造するための方法。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.3より多い亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約4.5より多い亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5より多い亜鉛原子を組成物に添加する。
110.
6分子のアシル化インスリン毎に最大約14の亜鉛原子を組成物に添加する項109に記載の方法。
6分子のアシル化インスリン毎に約4.3から約14の亜鉛原子を組成物に添加する項109−110の何れか一項に記載の方法。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5から約11.4の亜鉛原子を組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を組成物に添加する。
保存料の添加前に、亜鉛を組成物に添加する項109−111に記載の方法。
113.
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に1より多い亜鉛原子である項109−112の何れか一項に記載の方法。
114.
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に2より多い亜鉛原子である項109−113の何れか一項に記載の方法。
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に3より多い亜鉛原子である項109−114の何れか一項に記載の方法。
116.
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に4より多い亜鉛原子である項109−115の何れか一項に記載の方法。
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に5より多い亜鉛原子である項109−116の何れか一項に記載の方法。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を保存料の添加前に組成物に添加するか、あるいは、より好ましくは、6分子のアシル化インスリン毎に約5から約11.4の亜鉛原子を保存料の添加前に組成物に添加するか、あるいは、さらにより好ましくは6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を保存料の添加前に組成物に添加する。
保存料の添加後に、亜鉛を組成物に添加する項109−111の何れか一項に記載の方法。
119.
6分子のアシル化インスリン毎に少なくとも0.5の亜鉛原子を保存料の添加後に組成物に添加する項118に記載の方法。
6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加後に組成物に添加する項118−119に記載の方法。
本発明の更なる態様では、6分子のアシル化インスリン毎に約2より多い亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約3より多い亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、6分子のアシル化インスリン毎に約4より多い亜鉛原子を保存料の添加後に組成物に添加する。
本発明の更なる態様では、6分子のアシル化インスリン毎に約4.5から約12の亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、より好ましくは、6分子のアシル化インスリン毎に約5から約11.4の亜鉛原子を保存料の添加後に組成物に添加するか、あるいは、さらにより好ましくは、6分子のアシル化インスリン毎に約5.5から約10の亜鉛原子を保存料の添加後に組成物に添加する。
保存料の添加前に亜鉛の一部を添加し、保存料の添加後に亜鉛の一部を添加する項109−120の何れか一項に記載の方法。
ある態様では、本方法は、6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加後に添加するか、あるいは、6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に少なくとも2−3の亜鉛原子を保存料の添加後に添加するか、あるいは、6分子のアシル化インスリン毎に少なくとも1の亜鉛原子を保存料の添加前に添加し、6分子のアシル化インスリン毎に最大約11の亜鉛原子を保存料の添加後に添加することを含む。
保存料の添加前に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子であり、保存料の添加後に添加する亜鉛原子の数が、6分子のアシル化インスリン毎に少なくとも3の亜鉛原子である項121の何れか一項に記載の方法。
123.
保存料がフェノールおよび/またはm−クレゾールである項112−122の何れか一項に記載の方法。
アシル化インスリンが、LysB29(Nε−テトラデカノイル)desB30ヒトインスリンもしくはLysB29Nε−リトコロイル(lithocholoyl)−γ−Glu desB30ヒトインスリンである項109−123の何れか一項に記載の方法。
125.
アシル化インスリンが、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z
[上式中、
Wは、
・そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基と一緒になってアミド基を形成する、側鎖中にカルボン酸基を有するα−アミノ酸残基;
・アミドカルボニル結合を介して一緒に連結されている2、3または4のα−アミノ酸残基からなる鎖であって、
アミド結合−を介した鎖−は親インスリンのB鎖中に存在するLys残基のε−アミノ基と連結しており、
Wのアミノ酸残基は、Wが側鎖中にカルボン酸基を有するアミノ酸残基を少なくとも一つ有するように、中性側鎖を有するアミノ酸残基および側鎖中にカルボン酸基を有するアミノ酸残基の群から選択される鎖;もしくは、
・Xから親インスリンのB鎖中に存在するLys残基のε−アミノ基までの共有結合
であり;
Xは、
・−CO−;
・−CH(COOH)CO−;
・−CO−N(CH2COOH)CH2 CO−;
・−CO−N(CH2COOH)CH2CON(CH2COOH)CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2 CO−;
・−CO−N(CH2CH2COOH)CH2CH2CON(CH2CH2COOH)CH2CH2 CO−;
・−CO −NHCH(COOH)(CH2)4NHCO−;
・−CO−N(CH2CH2COOH)CH2 CO−;もしくは
・−CO−N(CH2COOH)CH2CH2 CO−であって、
a)Wがアミノ酸残基もしくはアミノ酸残基の鎖であるとき、下線の炭素からの結合を介して、W中のアミノ基とアミド結合を形成するか、あるいは、
b)Wが共有結合であるとき、下線のカルボニル炭素からの結合を介して、親インスリンのB鎖中に存在するLys残基のε−アミノ基とアミド結合を形成し;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
・1、2もしくは3の−CH=CH−基と、鎖中に10から32の範囲の合計数の炭素原子を与えるのに十分な数の−CH2−基とを含んでなる二価の炭化水素鎖
であり;かつ、
Zは、
・−COOH;
・−CO−Asp;
・−CO−Glu;
・−CO−Gly;
・−CO−Sar;
・−CH(COOH)2;
・−N(CH2COOH)2;
・−SO3H;もしくは
・−PO3H
である]
の側鎖を有さない項109−124の何れか一項に記載の方法。
アシル化インスリンがLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンではない項125の何れか一項に記載の方法。
127.
即効型インスリンを組成物に添加する項109−126の何れか一項に記載の方法。
128.
即効型インスリンが、AspB28ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである項127に記載の方法。
129.
糖尿病の治療のための医薬のの製造のための、項91−104の何れか一項に記載の組成物の使用。
本発明は、通常水準(6分子のアシル化インスリン毎に2から4の亜鉛原子)を超える亜鉛含有量の増加が、あるアシル化インスリン誘導体、特にアシル化インスリンLysB29Nε−ヘキサデカンジオイル−γ−GludesB30ヒトインスリンの中および高分子量インスリン複合体を増加させるという驚くべき知見に基づいたものである
本発明によれば、所望の度合いの会合を有するインスリンを含むインスリン製剤を設計することができる。
本発明は、さらに、インスリン製剤を調製するときに、保存料の添加後に亜鉛を加えることができるという驚くべき知見に基づいたものである。亜鉛は、典型的には、酢酸亜鉛、塩化亜鉛またはクエン酸亜鉛をインスリン製剤に添加することにより提供される。
典型的な等張剤は、塩化ナトリウム、マンニトール、ジメチルスルホン、1,2プロパンジオール、およびグリセロールであり、典型的な保存料は、フェノール、m−クレゾール、メチルp−ヒドロキシ安息香酸およびベンジルアルコールである。
本発明の組成物は、インスリンに感受性の状態の治療に用いることができる。したがって、それらは、1型糖尿病、2型糖尿病および、例えば重傷者および大きな手術を受けた人に時々見られるような高血糖の治療に用いることができる。任意の患者についての最適な投与レベルは、具体的なアシル化インスリンもしくはアシル化インスリンと用いられる即効型インスリンとの混合物の効率、年齢、体重、生理的活動、および患者の常食、他の薬物との有り得る組み合わせ、および治療されるべき状態の重篤さを含む種々の因子に依存する。本発明のインスリン誘導体の1日投与量は、既知のインスリン組成物と同様に、個々の患者それぞれについて、当業者により決定されることが推奨される。
本発明の組成物に含まれるアシル化インスリンもしくはインスリンアナログを調製するための出発産物は、周知のペプチド合成により、もしくは適する形質転換微生物中での周知の組み換え生産により、生産することができる。したがって、インスリン出発産物は、ポリペプチドをコードするDNAを含み、適切な栄養培地でペプチドの発現が許容される条件下でポリペプチドを発現することのできる宿主細胞、を培養し、その後、生じたペプチドを培養物から回収することを含む。
DNA配列は、簡便には、組換えDNA手順の対象となり得る任意のベクターに挿入してよく、ベクターの選択は導入すべき宿主細胞によることが多いであろう。したがって、ベクターは自己複製するベクター、すなわち染色体外の独立体として存在すし、その複製が染色体複製から独立しているベクター、例えばプラスミドであってよい。あるいは、ベクターは、宿主細胞に導入される場合、宿主細胞ゲノムに組み込まれ、組み込まれている染色体(一または複数)と共に複製されるものであってもよい。
また、ペプチドをコードするDNA配列は、必要ならば、適切なターミネーター、ポリアデニル化シグナル、転写促進因子配列および翻訳促進因子配列に作用可能に連結されてよい。さらに、本発明の組み換えベクターは、問題の宿主細胞においてベクターが複製することを可能にするDNA配列を更に含んでもよい。
ここで用いられる場合、「有効量」という用語は、治療しない場合と比較して患者に対して効果のある治療のために十分な投与量を意味する。
α−Aspは、−HNCH(CO−)CH 2 COOHのL体である。
β−Aspは、−HNCH(COOH)CH 2 CO−のL体である。
α−Gluは、−HNCH(CO−)CH 2 CH 2 COOHのL体である。
γ−Gluは、 −HNCH(COOH)CH 2 CH 2 CO−のL体である。
α−hGluは、−HNCH(CO−)CH 2 CH 2 CH 2 COOHのL体である。
δ−hGluは、−HNCH(COOH)CH 2 CH 2 CH 2 CO−のL体である。
β−Alaは、−NH−CH 2 −CH 2 −COOHである。
Sarは、サルコシン(N−メチルグリシン)である。
「中性側鎖を有するアミノ酸残基」という表現は、Gly、Ala、Val、Leu、Ile、Phe、Pro、Ser、Thr、Cys、Met、Tyr、AsnおよびGlnのようなアミノ酸残基を示す。
「中間分子量インスリン」もしくは「mmw」という表現は、ヒトインスリン複合体、インスリンアナログ、もしくはインスリン誘導体の分子量が、ほぼインスリン6量体から24〜80kダルトンのインスリン12量体までであることを意味する。
「低分子量インスリン」もしくは「lmw」なる表現は、ヒトインスリン、インスリンアナログもしくはインスリン誘導体の分子量が、24kダルトン未満であることを意味する。
hGlu ホモグルタミン酸
Sar: サルコシン(N−メチル−グリシン)
S.c. 皮下
アシルins アシル化インスリン
Ins インスリン
全ての表題および副題は、ここでは便宜的に使用され、決して本発明を限定するものと解すべきではない。
ここでの特許文献の引用および援用は単に便宜上なされているものに過ぎず、そのような特許文献の有効性、特許性、および/または権利行使性についての見解を反映させるものではない。
この発明は、適用される法律に容認される場合、ここに付加される請求項に列挙された主題事項の全ての修正点および等価物を含む。
実施例1
A:インスリンアスパルト600μM、3Zn/6インスリン、1.6%グリセロール、16mMのフェノールおよび16mMのm−クレゾール、7mMのtrisヒドロキシメチルアミノメタン、10mMのNaCl、pH7.5および8mlの体積:
31mgのインスリンアスパルトを2mlの水に懸濁し、30μLの1NのHClを加えて、溶液を得た。その後、240μLの10mMのZn(AcO) 2 を加え、続いて、3200μLの4%グリセロール、400μLの0.32Mフェノール、800μLのm−クレゾール、560μLの0.1Mtrisヒドロキシメチルアミノメタン、160μLの0.5MのNaClを加え、その後、1NのNaOHによりpHを調整し、最終的に、水で体積を8mlまで調整した。溶液を0.22μmの滅菌フィルターを通して濾過した。
58mgのLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンを2mlの水に懸濁し、溶解し、続いて、420μLの10mMのZn(AcO) 2 、2800μLの4%グリセロール、350μLの0.32Mフェノール、700μLのm−クレゾール、490μLの0.1Mtrisヒドロキシメチルアミノメタン、140μLの0.5MのNaClを加え、最終的に1NのNaOHの添加によりpH7.5に調整し、水を加え、7mlを得た。溶液を0.22μmの滅菌フィルターを通して濾過した。
製剤は、製剤Aと同様に調製した。
製剤は、製剤Cと同様に調製し、最終的に、1ml当たり20μLの10mMのZn(AcO) 2 を加え、pHを7.5に調整した。
製剤は、製剤Dと同様に調製し、最終的に、1ml当たり40μLの10mMのZn(AcO) 2 を加え、pHを7.5に調整した。
製剤は、製剤Cと同様に調製し、最終的に、1ml当たり40μLの10mMのZn(AcO) 2 を加え、pHを7.5に調整した。
製剤は、製剤Dと同様に調製し、最終的に、1ml当たり80μLの10mMのZn(AcO) 2 を加え、pHを7.5に調整した。
3および6で変化する亜鉛/インスリンのインスリンアスパルト600μM(AおよびE)からなる製剤は、単量体として溶出され(フラクション[12−13])、添加した亜鉛の少しの部分しかフォローしなかった、図面1−2を参照のこと。
インスリン180μMアスパルトおよび420μMのLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンおよび3、6、および8Zn/6インスリンで変化する亜鉛濃度からなる製剤を、上記ストック溶液AからHおよび上記媒質を同様に混合することにより得た。亜鉛/6アシル化インスリンの濃度を計算した例としては、3Zn/6インスリンを有するアスパルト180μM、および3Zn/6アシル−insを有するLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン420μMの混合が、4.3Zn/6アシル化インスリン[(180×3+420×3)/420=4.3Zn/アシル−ins]となることが挙げられる。サイズ排除カラムクロマトグラフィーにより、Superose6HRカラム上での高分子量インスリンの形成能力について、製剤を試験し、インスリンアナログと亜鉛の双方を定量するために、フラクションを同様に集めた。図面8から理解できるように、4.3Zn/6アシル−インスリンの製剤に相当する、3Zn/6インスリンと混合したアナログは、高分子量フラクション[1−8]で、主に、LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン(72.5%のLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン)および亜鉛を示したが、フラクション[9−14]の残りの平均として、インスリンアスパルトおよびLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの等価量が計測される形で、インスリンアスパルトも示した(図8)。6Zn/6insからなるインスリンアスパルトおよびLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの残りは、それぞれ図2および図5に示される。アスパルト180μM+LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン420μMに対し、6Zn/6ins(図2および図5)の二つの薬剤を混合し、8.6Zn/6アシル−insに相当するものは、高分子量および低分子量のインスリンアスパルトにおいて、LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの完全に区別されるフラクションを示した(図10)。インスリンアスパルトおよびLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの等量を12 Zn/6アシル−insに混合したものも、同様に、区別されるフラクションを示した(図12)。さらに、個々の製剤における8Zn/6insまでの亜鉛の濃度の増加は、LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンについては、図6中に、アスパルト180μM+LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン420μMの混合物につちえは、図11に示されている。
亜鉛の量の増加は、アナログが現実的な鈍化を示さないように、製薬学的処方におけるインスリンアスパルトおよびLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの分離を引き起こした。
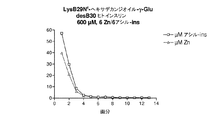
2A:フェノールおよびm−クレゾールの前に添加した3Zn/6アシル化インスリン
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン600μM、3Zn/6インスリン、1.6%グリセロール、16mMのフェノールおよび16mMのm−クレゾール、20mMのNaCl、7mMのリン酸塩、pH7.5、1.5μCiの 125 I−Tyr A14 −LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンのトレーサー、および2mlの体積。
1.2mgのLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンを400μLの水に溶解し、3μCiの 125 I−Tyr A14 −LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン トレーサーを加え、続いて、800μLの4%グリセロールを加え、10−15分間減圧遠心処理して、トレーサー溶液に含まれる添加エタノールを除去した。60μLの10mMのZn(AcO) 2 を加え、続いて、2分間隔で100μLの0.32Mフェノール、200μLの0.16Mのm−クレゾール、80μLの0.5MのNaCl、および140μLの0.1Mリン酸ナトリウムを加え、pHをpH7.5mMに調整し、合計の体積を2mlに調整した。溶液は、0.22μmの滅菌フィルターを通じて濾過し、ブタでの皮下注射の後の消失実験に用いられた。製剤例2Aから2Dのクロスオーバー研究でのアッセイ下で記載されるように、T 50% ±SEM(h)は、9.6±0.7hと決定された。
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン600μM、1.6%グリセロール、16mMのフェノールおよび16mMのm−クレゾールの前に添加した3Zn/6アシル化インスリンおよび後に添加した3Zn/6アシル化インスリン、20mMのNaCl、7mMのリン酸塩、pH7.5、1.5μCiヨウ素−I 125 −Tyr A14 −LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン トレーサー、2mlの体積。
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン600μM、1.6%グリセロール、16mMのフェノールおよび16mMのm−クレゾールの前に添加した3Zn/6アシル化インスリンおよび後に添加した3Zn/6アシル化インスリン、20mMのNaCl、pH7.5、1.5μCiの 125 I−Tyr A14 −LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン トレーサー、および2mlの体積。
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン600μM、1.6%グリセロール、16mMのフェノールおよび16mMのm−クレゾールの後に加えた6Zn/6アシル化インスリン、20mMのNaCl、7mMのリン酸塩、pH7.5、1.5μCiの 125 I−Tyr A14 −LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン トレーサー、および2mlの体積。
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンの結晶化による単離
LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンは、6molのインスリン当たり2−6molの亜鉛の亜鉛含有量および過剰のフェノール様分子(好ましくは、フェノール)を有するヘキサマー(六量体)として結晶化され得る。沈殿化剤として、イオン性の塩が用いられ、NaClが好ましい。さらに、結晶化は、少量の有機溶媒(エタノール)により促進され得る。
1.5mgの凍結乾燥LysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリンを、4mlの0.02 mol/l trisヒドロキシメチルアミノメタンバッファー(HClを用いてpH7.0に調整)に懸濁した。
1.8mlのこのLysB29Nε−ヘキサデカンジオイル−γ−Glu desB30ヒトインスリン溶液に対し、0.010mol/lのZn(OAc) 2 を含有する水溶液を69.5μlと、2mol/lのフェノールを含有するエタノール溶液18μlを添加する。
5mlの0.1Mtrisヒドロキシメチルアミノメタン含有溶液(HClを用いてpH7.5に調整)に対し、1.75gNaClおよび1mlのエタノールを加え、終体積を10mlに調整する。
結晶化:
等量(典型的には、500μl)の溶液AおよびBをガラスバイアル中で混合する。室温で12時間経過の後に、再結晶化は完全となり、生じた結晶は、濾過もしくは遠心分離により単離することができる。
製剤:
B29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリン(600μMまで)を水に懸濁し、水酸化ナトリウムの添加により溶解し、以下の順で以下のものを添加した:グリセロール1.6%、フェノールおよび16mMのm−クレゾール16mM、酢酸亜鉛0から6Zn/6ins、塩化ナトリウム10mM、リン酸塩7mM、pH7.5、および体積調整のための水。
場合によっては2mMのフェノールを加えた、37℃、pH7.3の等張の10mMのtris緩衝生理食塩水を用いた、20μLの注入体積、0.05ml/minの流量、130minのランタイムでの、Superose6PCカラム(0.32×30cm)上でのサイズ排除クロマトグラフィー(SEC)による分析。青色デキストラン(≫5MDa、K AV 0.0)、Tyroglobulin(チログロブリン)(669kDa、K AV 0.28)、Ferritin(フェリチン)(440kDa、K AV 0.39)、Ovalbumin(オバルブミン)(44.5kDa、K AV 0.56)、Ribonuclease(リボヌクレアーゼ)(13.7kDa、K AV 0.69)という第一基準およびAlbumin(アルブミン)(66kDa、K AV 0.53)、Co(III)インスリン−ヘキサマー(35kDa、K AV 0.61)、および単量体インスリンX2(6kDa、K AV 0.73)という第二基準。青色デキストランの保持時間は、17.9min(t 0 )およびカラムなしでは0.74min(t d )であり、かつ、アルブミン(HSA)の保持時間は、約34.1minであった。
t:保持時間(min)
t 0 :青色デキストランの保持時間(排除限界)
t d :カラム無しでの青色デキストランの保持時間(空隙容量)
V t :総カラム容量(mL)
f:流量(mL/min)
K AV ピーク1 x.xx
面積ピーク1(%) xxx
K AV ピーク2 x.xx
面積ピーク2(%) xxx
インスリンアスパルト(3Zn/6ins)および遷延作用型インスリン誘導体の50:50の混和性は、SECからのフラクションを集め、即効型および遷延作用型のインスリンの高分子量フラクション(ピーク1)および低分子量フラクション(ピーク2)における存在をHPLCにより定量化することにより計測する。フラクションカットは、上述した以下の積分値カットである。
溶出液にフェノールの無いSEC法では、ピーク1は、アルブミンより大きな会合形態をを含有し、ピーク2は、インスリンのジヘキサマー、ヘキサマー、ダイマーおよびモノマー携帯を含有する。
溶出液に2mMのフェノールを含むSEC法では、ピーク1は、インスリンのジヘキサマーおよび他のより大きな携帯を含有し、ピーク2は、インスリンのヘキサマー、ダイマーおよびモノマー形態を含有する。
インスリン誘導体ピーク1面積(%) xxx
インスリンアスパルトピーク2面積(%) xxx
B29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリン600μMは、一例として、0から6Zn/6insと段階的に増加する亜鉛濃度で製剤化され、亜鉛濃度が5Zn/6insの際には、SEC法によれば、超高分子量への自己会合が示され、かつ90%より多くがヒトアルブミン以上の自己会合が示された。SEC溶出液にフェノールを含ませると、二つの鋭いピークが、インスリンジヘキサマーサイズおよびインスリンモノマーサイズに観察され、4Zn/6insの際には、95%より多くがジヘキサマーサイズだった。
持続型アナログ製剤がモノマー形態の5%未満を含む場合、等モル製剤混合物の非鈍化が観察された。
B29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリンと、インスリンアスパルトとの混和性:ブタにおける正常血糖クランプ研究
製剤
B29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリン(ins.誘導体)(1200μMまで)を水に懸濁し、溶解し、グリセロール1.6%、および16mMのフェノールおよび16mMのm−クレゾールを加えた。亜鉛添加の前に、水酸化ナトリウムによりpHを7.5に調整し、最大1Zn/6insから3Zn/6insまで(ad I)、5.62Zn/6insまで(ad II)、および6Zn/6insまで(III)の少量ずつ酢酸亜鉛を添加した。その後、塩化ナトリウムを10mMまで加え、水酸化ナトリウムによりpHを7.5に調整し、水により体積を調整した。
最終的に、インスリンアスパルト(IV)は、B29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリンと、1:8のモル関係かつ合計の亜鉛濃度が3.38Zn/6ins.誘導体(I)(lowZnmix)および6Zn/6ins.誘導体(II)(highZnmix)となるように混合した。
メスのブタ(N=8、中間体重80kg)を研究の18時間前に絶食させた。インスリンアスパルトおよびB29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリンの混合の効果を調べるために、それぞれのブタに、lowZnmix(I)もしくhighZnmix(II)もしくは二つのアナログ(IIIおよびIV)の何れかを順不同で与え、同一のブタに別々に投与した。投与量は、0.9nmol/kgのインスリンアスパルトおよび7.2nmol/kgのB29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリンであった。ブタは、20%グルコース溶液の注入により、個々の空腹時血糖値における正常血糖を保たせた。血漿グルコース濃度の変化に応じて、グルコース注入速度の調整が実験的に行なわれた。血液試料は、免疫反応性のインスリンの特異的ELISA血漿分析のために、0−24hで集められ、その薬理学的特性は、図13および図14に示される。
二つの混合処方における双方のインスリン構成成分の鈍化の程度を調べた。インスリンアスパルトおよびインスリン454の双方の顕著な鈍化は、混合物中に低亜鉛濃度の場合(3.38Zn/6ins.誘導体)に観察された。しかしながら、亜鉛濃度が6亜鉛/6ins.誘導体まで増加した場合は、薬理学的特性の鈍化は観察されなかった(非鈍化が観察された)。グルコース注入速度は、個々のインスリンアナログの薬理学的特性の合計とよく匹敵した。
亜鉛バッファーとしてのクエン酸塩
B29Nε−ヘキサデカンジオイル−γ−GludesB30インスリン(ins.誘導体)(600μMまで)を水に懸濁し、溶解し、グリセロール1.6%、およびフェノール16mMおよびm−クレゾール16mMを加える。pHを水酸化ナトリウムで7.5に調整し、クエン酸塩を、酢酸亜鉛に関してそれぞれ0.6、1.8および6mMの6亜鉛/6インスリン誘導体の三つの製剤に添加した。その後、塩化ナトリウムを10mMまで加え、リン酸ナトリウム(pH7.5)を5mMまで加え、続いてpHを水酸化ナトリウムで7.5または7.8まで調整し、体積を水で調整する。
2mMフェノールを含む溶出液を用いた実施例4に記載のSEC法により、5℃保存と比較して、37℃2週間保存後で、製剤について研究した。3、5および6Zn/6ins.誘導体でクエン酸塩を有しない対照製剤も含めた。
インスリンアスパルト(3Zn/6ins)と、持続性インスリン誘導体との30:70の混和性を、SECからの分画を集め、HPLCにより即効性および持続性のインスリンを、高分子量画分(ピーク1)および低分子量画分(ピーク2)で定量化することにより測定した。画分カットと定量化は、実施例4に従った。
2mMフェノールを含むSEC生理食塩水溶出液を用いると、持続型インスリン誘導体は、主に、ジヘキサマー形態(および、より多く会合した形態)に相当するアルブミンのサイズで会合しており、モノマー形態でのインスリン誘導体の量は、3から5および6Zn/6ins.誘導体へと増加する亜鉛濃度で減少する。6Zn/6ins.誘導体の亜鉛濃度まで1、3もしくは10クエン酸塩当量を添加すると、3Zn/ins.誘導体での対照と比較して、モノマーインスリン誘導体の含有量が減少した。自己会合様式は、37℃で2週間の貯蔵の後も変化しなかった。
クエン酸塩無しで製剤化されたインスリンアスパルト(3Zn/6ins)と、本実施例の上記系に示すように製剤化された持続性インスリン誘導体との30:70の混和性を、5℃および37℃2週間保存後について、表に示す。3つのレベルでのクエン酸塩と6Zn/6insとを含むインスリン誘導体製剤は、37℃2週間保存の後も、インスリンアスパルトと混合可能であることが示され、インスリンアスパルトは、3Zn/6insにおける通常のレベルの亜鉛の高分子量画分に、部分的に含まれた。
クエン酸亜鉛を加える。
B29Nε−ヘキサデカンジオイル−γ−GludesB30インスリン(ins.誘導体)(600μMまで)を水に懸濁し、溶解し、グリセロール1.6%、およびフェノール16mMおよびm−クレゾール16mMを加える。pHを水酸化ナトリウムで7.5に調整し、クエン酸亜鉛を0.6mMの亜鉛イオンになるまで添加する。その後、塩化ナトリウムを10mMまで加え、リン酸ナトリウム(pH7.5)を5mMまで加え、続いてpHを7.5まで調整し、体積を水で調整する。
界面活性剤を添加し、即効性アナログと混合する。
B29Nε−ヘキサデカンジオイル−γ−GludesB30インスリン(ins.誘導体)(600μMまで)を水に懸濁し、溶解し、グリセロール1.6%、および16mMのフェノールおよび16mMのm−クレゾールを加える。pHを水酸化ナトリウムで7.5に調整し、酢酸亜鉛で6亜鉛/6インスリン誘導体にする(任意によって、クエン酸塩としての亜鉛)。その後、塩化ナトリウムを10mMまで加え、界面活性剤、例えばpoloxamer188またはpolysorbate20を約0.002%まで加え、リン酸ナトリウム(pH7.5)を5mMまで加え、続いてpHを7.5まで調整し、体積を水で調整する。インスリンアスパルト(AspB28ヒトインスリン)もしくはインスリンLisPro(LysB28ProB29ヒトインスリン)もしくはインスリングルリシン(LysB3GluB29ヒトインスリン)(全て600μM)を、実施例7または実施例8により製剤化されるB29Nε−ヘキサデカンジオイル−γ−Glu desB30インスリンと、約3/7から約7/3のモル比で混合する。
表3は、6のインスリン毎に2もしくは6のZn(II)を有する実施例4に記載されるようにして測定されたSECを示す。
表に記述される化合物の調製については、国際公開第2006/082204号および国際公開第2006/082205号を参照のこと。
1,16−ヘキサデカン二酸 モノベンジルエステルの調製
ヘキサデカン二酸(20.0g、69.8mmol)、n−オクタンおよびDowex(登録商標)を懸濁させ、過熱還流する。6時間後、追加のギ酸ベンジル(22.0g、162mmol)を加える。加熱を50時間続ける。反応混合液を80℃で濾過する。濾液を20℃まで冷却し、沈殿を濾過により集める。粗生成物(20.2g)をジクロロメタン(220ml)に20℃で4時間懸濁させる。懸濁液を濾過し、濾液を排出させて20−30℃で乾燥させる。結果として生じる固体(13.9g)を2−プロパノール(140ml)から再結晶する。
生成物を濾過により単離し、30−40℃で減圧下、一定重量まで乾燥させる。収量10.2g(39%)の白色物質。
1,16−ヘキサデカン二酸 モノベンジルエステル(20.0g、53.1mmol)を、35−40℃でアセトンに溶解する。N−ヒドロキシスクシンイミド(6.42g/55.8mmol)を加える。結果として生じる溶液に、ジシクロヘキシルカルボジイミド(DCC)(12.1g/58.4mmol)を加える。反応混合液を35℃で3−4時間攪拌する。結果として生じた懸濁液に、トリエチルアミン(7.40ml、53.1mmol)og L−グルタミン酸α−ベンジルエステル(12.6g/53.1mmol)を加える。反応混合液を35−40℃で8−16時間攪拌する。反応混合液を20−25℃まで冷却する。メタンスルホン酸(3.45mlの/53.1mmol)およびDCC(12.1g/53.1mmol)を加える。反応混合液を20−25℃で8−16時間攪拌する。反応混合液を濾過し、濾液を排出させて乾燥させる。残留物を、水(100ml)およびトルエン(200ml)で分画する。トルエン相を水の蒸留により乾燥させた。シリカゲル(20g)を残留物に加える。懸濁液を20−25℃で30分間攪拌し、濾過する。濾液の体積を、減圧下のエバポレーションにより約100−120mlまで減少させた。N−ヘプタン(150ml)を、15−30分間にわたって加える。結果として生じる懸濁液を2時間攪拌する。生成物を濾過により単離し、20−25℃で減圧下、一定重量まで乾燥させる。収量21g(58%)の白色物質。
L−2−(15−ベンジルオキシカルボニル−ペンタデカノイルアミノ)−ペンタン二酸 5−ベンジルエステル 1−(2,5−ジオキソ−ピロリジン−1−イル)エステル(5.0g、7.3mmol)を、トリフルオロ酢酸(95μl)を含むアセトン(95ml)に溶解する。パラジウム炭素、10%(0.50g)を加える。30−35℃で攪拌しながら水素を加える。水素の消費が停止したとき、反応混合液を濾過する。濾液を20℃に冷却し、n−ヘプタン(140ml)を15−30分間にわたって加える。結果として生じる懸濁液を2−3時間で0−5℃に冷却する。生成物を濾過により単離し、20−25℃で減圧下、一定重量まで乾燥させる。収量3g(84%)の白色物質。
生成物は、アセトン−d6を溶媒として用いてプロトンNMR(Bruker600MHz)により分析した。
4gのdesB30ヒトインスリンを64gの精製水に懸濁する。1.85mlのトリエチルアミン(TEA)を加えて、desB30ヒトインスリンを溶解させ、pHを11.4−12.0まで上げる。溶液を2−5℃まで冷却する。
448mgのPC2414を、10−15%の硫酸で安定化した3.5gのNMP(N−メチル−2−ピロリドン)に加える。
desB30ヒトインスリン溶液を攪拌し、PC2414溶液を、温度を低く保ちながら20分間にわたって加える。
希釈後、かき混ぜながら、緩やかに1M酢酸を加えることにより、pHを7.5に調整する。
HPLCによる分析により、14,22%の残留desB30ヒトインスリンを有する72,11%のLysB29(Nε−ヘキサデカンジオイル−γ−グルタミル)des(B30)ヒトインスリンの形成が示される。
オクチルジメチルシリル置換シリカを充填された、約100 Åの孔サイズと約3.5μmの粒径を有する150X4.6mm内径のカラムを、40℃で1ml/分の流速で、1:7.8%(w/w)を含むNaOH水溶液でpH5.9に調整された20mMのNaH2PO4.H2Oおよび100mmolのNa2SO4バッファー、および2:42,8%w/wのアセトニトリルを含むアセトニトリル溶媒からなり、25%(w/w)アセトニトリルとなるように調整した混合液を用いて、平衡化する。
LysB29(Nε−ヘキサデカンジオイル−γ−グルタミル)des(B30)ヒトインスリンは、約20分後にカラムから溶出した。desB30ヒトインスリンは約6分後にカラムから溶出した。
ヒトインスリンに対する本発明のインスリン誘導体の効力
実験日の体重が238-383 gであったSDオスラットを、固定(clamp)実験に用いた。ラットは、制御された環境条件下で、餌に自由に接近でき、固定実験の前一晩(3pmから)絶食した。
外科手術の前に少なくとも1週間の間、動物施設でラットを馴養した。固定実験の前に、約1週間、タイゴン(Tygon)カテーテルをハロタン麻酔下で、頚静脈(注入用)および頚動脈(血液採取用)に挿入し、首部背面で外面化して固定した。術後のラットにストレプトシリン(Streptocilin vet.)(Boehringer Ingelheim; 0.15 ml/rat, i.m.)を与え、回復期間の間、動物ケアユニット(25 ℃)に置いた。鎮痛のために、アノルフィン(Anorphin)(0.06 mg/rat, s.c.)を、麻酔の間投与し、リマディル(Rimadyl)(1.5 mg/kg, s.c.)を、麻酔から完全に回復した後(2-3 h)に投与し、2日間、日に一度投与した。
ブタにおける、本発明のインスリン誘導体のT50%の測定
T50%は、外部γ−カウンターで測定したとき、試験されるインスリンのA14Tyr[125I]標識化誘導体の注入量の50%が注入部位から消失する時間である。
実験動物ケアの原則に従い、薬物動態学的研究および薬力学的研究のために、特異的病原体の無いLYYD、非糖尿病メスブタ、Danish Landrace、YorkshireおよびDurocの交雑育種を用いた(Holmenlund、Haarloev、Denmark)。ブタには意識があり、4−5月齢で体重70−95kgであった。動物は実験の前に、一晩18時間絶食させた。
実験の開始において、60nmolの投与量の本発明に係るインスリン誘導体(試験化合物)と、60nmolの投与量インスリンデテミル(detemir)(何れもTyrA14で125I標識されている)を、それぞれのブタの首の二つの異なる位置で注射した。
図中、以下の略語が用いられる:
アスパルト: インスリンアスパルト
Zn/6Ins: 6分子のインスリン当たりの亜鉛原子
Zn/アシル−ins: 6分子のアシル化インスリン当たりの亜鉛原子
アシル−ins アシル化インスリン
Claims (14)
- アシル化インスリン、即効型インスリン、および6分子のアシル化インスリン毎に6以上最大12の亜鉛原子を含む、治療の必要がある患者における糖尿病の治療のための可溶性製薬学的組成物であって、
該アシル化インスリンは、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z2
[上式中、
Wは、
α−Asp、β−Asp、α−Glu、γ−Glu、α−hGluおよびδ−hGluからなる群から選択される側鎖中にカルボン酸基を有するα−アミノ酸残基であって、そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基またはB鎖のN末端のアミノ酸残基のα−アミノ基と一緒になってアミド基を形成するα−アミノ酸残基であり;
Xは、
・−CO−;
であり;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
であり;かつ、
Z2は、
・−COOH;
である]
の側鎖を有するインスリン分子を含んでなる、製薬学的組成物。 - 親インスリンがdesB30ヒトインスリンアナログである請求項1に記載の製薬学的組成物。
- 即効型インスリンがAspB28ヒトインスリン、LysB3GluB29ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである請求項1または2に記載の製薬学的組成物。
- アシル化インスリン、即効型インスリン、および亜鉛原子を含み、6分子のアシル化インスリン毎に6以上最大12の亜鉛原子が添加された、治療の必要がある患者における糖尿病の治療のための製薬学的組成物を製造するための方法であって、
該アシル化インスリンは、親インスリンのB鎖中に存在するLys残基のε−アミノ基と結合している側鎖であって、一般式:
−W−X−Y−Z2
[上式中、
Wは、
α−Asp、β−Asp、α−Glu、γ−Glu、α−hGluおよびδ−hGluからなる群から選択される側鎖中にカルボン酸基を有するα−アミノ酸残基であって、そのカルボン酸基のうちの一つと共に、親のインスリンのB鎖中に存在するLys残基のε−アミノ基またはB鎖のN末端のアミノ酸残基のα−アミノ基と一緒になってアミド基を形成するα−アミノ酸残基であり;
Xは、
・−CO−;
であり;
Yは、
・mが6から32の範囲の整数である−(CH2)m−;
であり;
Z2は、
・−COOH;
である]
の側鎖を有し;
該方法は、
i) 水相を提供し、
ii) 該アシル化インスリンを添加し、
iii) アシル化インスリン6分子当たり6以上最大12の亜鉛原子を添加し、
iv) 任意でさらに賦形剤を添加する
工程を含む方法。 - 保存料の添加後に、亜鉛を組成物に添加する、請求項4に記載の方法。
- 保存料の添加前に亜鉛の一部を添加し、保存料の添加後に亜鉛の一部を添加する、請求項4または5に記載の方法。
- 保存料がフェノールおよび/またはm−クレゾールである、請求項5または6に記載の方法。
- 界面活性剤を製薬学的組成物と混合する、請求項4−7の何れか一項に記載の方法。
- 親インスリンがdesB30ヒトインスリンアナログである請求項4−8の何れか一項に記載の方法。
- 即効型インスリンがAspB28ヒトインスリン、LysB3GluB29ヒトインスリンおよび/またはLysB28ProB29ヒトインスリンである請求項4−9の何れか一項に記載の方法。
- 糖尿病の治療のための医薬の製造のための、請求項1−3の何れか一項に記載の組成物の使用。
- 請求項1−3の何れか一項に記載の製薬学的組成物の治療的有効量を製薬学的に許容される担体と共に含む、治療の必要がある患者における糖尿病の治療のための製薬学的組成物。
- 請求項1−3の何れか一項に記載の製薬学的組成物の治療的有効量を製薬学的に許容される担体と共に含む、治療の必要がある患者における糖尿病の治療のための医薬。
- 1型糖尿病または2型糖尿病の治療において使用するための製薬学的組成物の製造のための、請求項1−3の何れか一項に記載の組成物の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP05113021 | 2005-12-28 | ||
| EP05113021.9 | 2005-12-28 | ||
| PCT/EP2006/070104 WO2007074133A2 (en) | 2005-12-28 | 2006-12-21 | Compositions comprising an acylated insulin and zinc and method of making the said compositions |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010174030A Division JP5026567B2 (ja) | 2005-12-28 | 2010-08-02 | インスリン組成物および組成物の製造方法 |
| JP2011008924A Division JP2011121963A (ja) | 2005-12-28 | 2011-01-19 | インスリン組成物および組成物の製造方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2009522231A JP2009522231A (ja) | 2009-06-11 |
| JP2009522231A5 JP2009522231A5 (ja) | 2010-09-16 |
| JP4808785B2 true JP4808785B2 (ja) | 2011-11-02 |
Family
ID=36888823
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008547953A Active JP4808785B2 (ja) | 2005-12-28 | 2006-12-21 | インスリン組成物および組成物の製造方法 |
| JP2010174030A Active JP5026567B2 (ja) | 2005-12-28 | 2010-08-02 | インスリン組成物および組成物の製造方法 |
| JP2011008924A Withdrawn JP2011121963A (ja) | 2005-12-28 | 2011-01-19 | インスリン組成物および組成物の製造方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010174030A Active JP5026567B2 (ja) | 2005-12-28 | 2010-08-02 | インスリン組成物および組成物の製造方法 |
| JP2011008924A Withdrawn JP2011121963A (ja) | 2005-12-28 | 2011-01-19 | インスリン組成物および組成物の製造方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US20090074882A1 (ja) |
| EP (2) | EP2505593A1 (ja) |
| JP (3) | JP4808785B2 (ja) |
| CN (1) | CN101389650B (ja) |
| AT (1) | ATE519780T1 (ja) |
| DK (1) | DK1969004T3 (ja) |
| ES (1) | ES2371361T3 (ja) |
| PL (1) | PL1969004T3 (ja) |
| PT (1) | PT1969004E (ja) |
| WO (1) | WO2007074133A2 (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011121963A (ja) * | 2005-12-28 | 2011-06-23 | Novo Nordisk As | インスリン組成物および組成物の製造方法 |
| US8828923B2 (en) | 2003-08-05 | 2014-09-09 | Novo Nordisk A/S | Insulin derivatives |
| US9034818B2 (en) | 2007-06-13 | 2015-05-19 | Novo Nordisk A/S | Pharmaceutical formulations comprising an insulin derivative |
| US9603904B2 (en) | 2008-10-30 | 2017-03-28 | Novo Nordisk A/S | Treating diabetes melitus using insulin injections with less than daily injection frequency |
| US10137172B2 (en) | 2013-04-30 | 2018-11-27 | Novo Nordisk A/S | Administration regime |
| US10335464B1 (en) | 2018-06-26 | 2019-07-02 | Novo Nordisk A/S | Device for titrating basal insulin |
| US10596229B2 (en) | 2010-10-27 | 2020-03-24 | Novo Nordisk A/S | Method of treating diabetes mellitus by administration, at specifically defined intervals, of a derivative of a naturally occurring insulin or insulin analogue, the derivative having a prolonged profile of action |
| US12343383B2 (en) | 2019-07-12 | 2025-07-01 | Novo Nordisk A/S | High concentration insulin formulation |
Families Citing this family (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006051103A2 (en) * | 2004-11-12 | 2006-05-18 | Novo Nordisk A/S | Stable formulations of peptides |
| EP1846447B1 (en) | 2005-02-02 | 2013-08-21 | Novo Nordisk A/S | Insulin derivatives |
| WO2006082204A1 (en) | 2005-02-02 | 2006-08-10 | Novo Nordisk A/S | Insulin derivatives |
| EP1991576B1 (en) * | 2006-02-27 | 2010-09-29 | Novo Nordisk A/S | Insulin derivatives |
| EP2024390B1 (en) * | 2006-05-09 | 2015-08-19 | Novo Nordisk A/S | Insulin derivative |
| MX2008014061A (es) * | 2006-05-09 | 2008-11-14 | Novo Nordisk As | Derivado de insulina. |
| DK2074141T3 (en) | 2006-09-22 | 2016-11-28 | Novo Nordisk As | The protease resistant insulin analogues. |
| US9387176B2 (en) | 2007-04-30 | 2016-07-12 | Novo Nordisk A/S | Method for drying a protein composition, a dried protein composition and a pharmaceutical composition comprising the dried protein |
| US8710000B2 (en) * | 2007-11-08 | 2014-04-29 | Novo Nordisk A/S | Insulin derivative |
| JP5241849B2 (ja) * | 2007-11-16 | 2013-07-17 | ノボ・ノルデイスク・エー/エス | インスリン及びインスリン分泌性ペプチドを含む薬学的組成物 |
| WO2009112583A2 (en) | 2008-03-14 | 2009-09-17 | Novo Nordisk A/S | Protease-stabilized insulin analogues |
| CN102037008B (zh) | 2008-03-18 | 2016-08-31 | 诺沃-诺迪斯克有限公司 | 蛋白酶稳定化的、酰化胰岛素类似物 |
| US10842951B2 (en) | 2010-01-12 | 2020-11-24 | Aerami Therapeutics, Inc. | Liquid insulin formulations and methods relating thereto |
| US9180261B2 (en) | 2010-01-12 | 2015-11-10 | Dance Biopharm Inc. | Preservative free insulin formulations and systems and methods for aerosolizing |
| US20130143803A1 (en) * | 2010-05-10 | 2013-06-06 | Novo Nordisk A/S | Process for the Preparation of Insulin-Zinc Complexes |
| CN103167878A (zh) | 2010-10-27 | 2013-06-19 | 诺沃—诺迪斯克有限公司 | 采用在不同注射时间间隔给予的胰岛素注射剂治疗糖尿病 |
| JP2013545782A (ja) | 2010-12-14 | 2013-12-26 | ノヴォ ノルディスク アー/エス | 長時間作用型インスリンと組み合わせた速効型インスリン |
| AU2012213432B2 (en) * | 2011-02-01 | 2016-10-13 | Novo Nordisk A/S | Purification of insulin |
| CN102675452B (zh) | 2011-03-17 | 2015-09-16 | 重庆富进生物医药有限公司 | 具持续降血糖和受体高结合的人胰岛素及类似物的偶联物 |
| US9481721B2 (en) | 2012-04-11 | 2016-11-01 | Novo Nordisk A/S | Insulin formulations |
| CA2872083A1 (en) | 2012-05-01 | 2013-11-07 | Novo Nordisk A/S | Pharmaceutical composition |
| WO2014064215A1 (en) | 2012-10-24 | 2014-05-01 | INSERM (Institut National de la Santé et de la Recherche Médicale) | TPL2 KINASE INHIBITORS FOR PREVENTING OR TREATING DIABETES AND FOR PROMOTING β-CELL SURVIVAL |
| EP2919804B1 (fr) | 2012-11-13 | 2018-01-31 | Adocia | Formulation à action rapide d'insuline comprenant un composé anionique substitué |
| JP6755175B2 (ja) * | 2013-03-20 | 2020-09-16 | ノヴォ ノルディスク アー/エス | インスリン投薬レジメン |
| AU2014333979B2 (en) | 2013-10-07 | 2018-02-15 | Novo Nordisk A/S | Novel derivative of an insulin analogue |
| JP6723921B2 (ja) * | 2014-01-09 | 2020-07-15 | サノフイSanofi | インスリンアナログおよび/またはインスリン誘導体の、グリセリンを含まない安定化された医薬製剤 |
| AR099569A1 (es) | 2014-02-28 | 2016-08-03 | Novo Nordisk As | Derivados de insulina y los usos médicos de estos |
| DK3006045T3 (en) | 2014-10-07 | 2017-07-17 | Cyprumed Gmbh | Pharmaceutical formulations for oral administration of peptide or protein drugs |
| EP3261648B1 (en) * | 2015-02-25 | 2023-12-06 | Aerami Therapeutics, Inc. | Liquid insulin formulations and methods relating thereto |
| US10426818B2 (en) | 2015-03-24 | 2019-10-01 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Method and pharmaceutical composition for use in the treatment of diabetes |
| JP7432361B2 (ja) * | 2016-08-02 | 2024-02-16 | 江蘇恒瑞医薬股▲ふん▼有限公司 | ヒトインスリンまたはそのアナログのアシル化誘導体 |
| TWI700091B (zh) * | 2016-12-16 | 2020-08-01 | 丹麥商諾佛 儂迪克股份有限公司 | 含胰島素醫藥組成物 |
| CN111315766B (zh) * | 2018-02-01 | 2023-05-12 | 江苏恒瑞医药股份有限公司 | 含人胰岛素类似物的酰化衍生物的药物组合物及其制备方法 |
| KR20210016400A (ko) | 2018-05-24 | 2021-02-15 | 지앙수 헨그루이 메디슨 컴퍼니 리미티드 | 재조합 인간 인슐린 또는 그 유사체의 전구체를 제조하는 방법 |
| WO2021185304A1 (zh) * | 2020-03-18 | 2021-09-23 | 东莞市东阳光生物药研发有限公司 | 制备长脂肪链二酸衍生物的方法及其应用 |
| TW202229324A (zh) * | 2020-11-27 | 2022-08-01 | 大陸商江蘇恒瑞醫藥股份有限公司 | 製備胰島素或其類似物的醯化衍生物的方法 |
| JP2024522904A (ja) * | 2021-06-25 | 2024-06-21 | ガン アンド リー ファーマシューティカルズ カンパニー リミテッド | アシル化インスリンを含む医薬組成物 |
| US20230025595A1 (en) * | 2021-07-13 | 2023-01-26 | America Great Health, a California Corporation | Formulation and Method of Preparing Divalent Cation Charged Insulin for Oral Administration |
| CN113896784B (zh) * | 2021-10-18 | 2024-04-16 | 合肥天麦生物科技发展有限公司 | 一种胰岛素结晶的制备方法及其产品 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001518915A (ja) * | 1997-03-20 | 2001-10-16 | ノボ ノルディスク アクティーゼルスカブ | インシュリンと吸収増強剤の共沈殿による治療用粉末の調整法 |
| JP2002527487A (ja) * | 1998-10-16 | 2002-08-27 | ノボ ノルディスク アクティーゼルスカブ | 肺送達のための安定に濃縮されたインスリン製剤 |
| WO2003094956A1 (en) * | 2002-05-07 | 2003-11-20 | Novo Nordisk A/S | Soluble formulations comprising monomeric insulin and acylated insulin |
| JP2004523589A (ja) * | 2001-03-23 | 2004-08-05 | アベンティス・ファーマ・ドイチユラント・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツング | 改善された安定性を有するいかなる量の亜鉛も含有しないかまたはほんの少量の亜鉛しか含有しないインスリン製剤 |
| WO2005012347A2 (en) * | 2003-08-05 | 2005-02-10 | Novo Nordisk A/S | Novel insulin derivatives |
Family Cites Families (134)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1212679B (de) | 1957-08-03 | 1966-03-17 | Novo Terapeutisk Labor As | Verfahren zur Herstellung von Insulinloesungen |
| GB1042194A (en) | 1962-04-30 | 1966-09-14 | Olin Mathieson | Insulin preparations |
| US3528960A (en) * | 1968-10-07 | 1970-09-15 | Lilly Co Eli | N-carboxyaroyl insulins |
| US3907676A (en) | 1970-07-28 | 1975-09-23 | Novo Terapeutisk Labor As | Process for purifying insulin |
| US3868358A (en) * | 1971-04-30 | 1975-02-25 | Lilly Co Eli | Protamine-insulin product |
| GB1492997A (en) | 1976-07-21 | 1977-11-23 | Nat Res Dev | Insulin derivatives |
| JPS5767548A (en) | 1980-10-14 | 1982-04-24 | Shionogi & Co Ltd | Insulin analog and its preparation |
| US4652548A (en) | 1981-08-27 | 1987-03-24 | Eli Lilly And Company | Pharmaceutical formulations comprising human insulin, human C-peptide, and human proinsulin |
| FI78616C (fi) * | 1982-02-05 | 1989-09-11 | Novo Industri As | Foerfarande foer framstaellning av en foer infusionsaendamaol avsedd stabiliserad insulinloesning, som har en foerhoejd zinkhalt. |
| US4876322A (en) | 1984-08-10 | 1989-10-24 | Siemens Aktiengesselschaft | Irradiation cross-linkable thermostable polymer system, for microelectronic applications |
| EP0174493B1 (de) | 1984-08-17 | 1988-05-25 | Bayer Ag | Thermoplastische Formmassen mit flammwidrigen Eigenschaften |
| DE3433367A1 (de) | 1984-09-12 | 1986-03-20 | Robert Bosch Gmbh, 7000 Stuttgart | Einrichtung zur steuerung der energiezufuhr zu einer heissen stelle |
| DK113585D0 (da) | 1985-03-12 | 1985-03-12 | Novo Industri As | Nye peptider |
| US5008241A (en) | 1985-03-12 | 1991-04-16 | Novo Nordisk A/S | Novel insulin peptides |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| JPS61226115A (ja) | 1985-03-30 | 1986-10-08 | Mitsubishi Metal Corp | 線条体押し出し機 |
| PH25772A (en) | 1985-08-30 | 1991-10-18 | Novo Industri As | Insulin analogues, process for their preparation |
| US4764592A (en) | 1987-04-23 | 1988-08-16 | Eli Lilly And Company | Crystalline human proinsulin and process for its production |
| US5605884A (en) | 1987-10-29 | 1997-02-25 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Factor VIII formulations in high ionic strength media |
| US4877608A (en) | 1987-11-09 | 1989-10-31 | Rorer Pharmaceutical Corporation | Pharmaceutical plasma protein formulations in low ionic strength media |
| JPH01254699A (ja) | 1988-04-05 | 1989-10-11 | Kodama Kk | インスリン誘導体及びその用途 |
| DE3827533A1 (de) * | 1988-08-13 | 1990-02-15 | Hoechst Ag | Pharmazeutische zubereitung zur behandlung des diabetes mellitus |
| KR910700262A (ko) | 1988-12-23 | 1991-03-14 | 안네 제케르 | 사람 인슐린 유사체 |
| PT93057B (pt) | 1989-02-09 | 1995-12-29 | Lilly Co Eli | Processo para a preparacao de analogos da insulina |
| IT1240314B (it) | 1989-09-28 | 1993-12-07 | Immunobiology Research Institutes, Inc. | Formulazioni acquose stabilizzate di piccoli peptidi. |
| JP3122128B2 (ja) * | 1989-12-21 | 2001-01-09 | ノボ ノルディスク アクティーゼルスカブ | ペプチド製剤 |
| DK45590D0 (ja) | 1990-02-21 | 1990-02-21 | Novo Nordisk As | |
| DK175491D0 (da) | 1991-10-18 | 1991-10-18 | Novo Nordisk As | Apparat |
| DK0618807T3 (da) | 1991-12-20 | 2003-03-03 | Novo Nordisk As | Stabiliseret farmaceutisk formulering omfattende human væksthormon og histidin |
| US5672581A (en) | 1993-01-29 | 1997-09-30 | Aradigm Corporation | Method of administration of insulin |
| US6869930B1 (en) * | 1993-09-17 | 2005-03-22 | Novo Nordisk A/S | Acylated insulin |
| CZ287945B6 (cs) | 1993-09-17 | 2001-03-14 | Novo Nordisk A/S | Inzulinový derivát a farmaceutický prostředek s jeho obsahem pro léčení diabetu |
| US6011007A (en) * | 1993-09-17 | 2000-01-04 | Novo Nordisk A/S | Acylated insulin |
| US5652216A (en) | 1994-05-26 | 1997-07-29 | Novo Nordisk A/S | Pharmaceutical preparation |
| AU3562195A (en) | 1994-10-04 | 1996-04-26 | Novo Nordisk A/S | Preparations containing aspb28 human insulin and nicotinamide |
| US5693609A (en) | 1994-11-17 | 1997-12-02 | Eli Lilly And Company | Acylated insulin analogs |
| US5646242A (en) | 1994-11-17 | 1997-07-08 | Eli Lilly And Company | Selective acylation of epsilon-amino groups |
| US5830999A (en) * | 1995-01-26 | 1998-11-03 | Regents Of The University Of California | Stabilization of insulin through ligand binding interations |
| PL183698B1 (pl) | 1995-03-17 | 2002-06-28 | Novo Nordisk As | Pochodna insuliny, kompozycja farmaceutyczna i zastosowanie pochodnej insuliny |
| US6251856B1 (en) * | 1995-03-17 | 2001-06-26 | Novo Nordisk A/S | Insulin derivatives |
| CA2226575C (en) | 1995-07-27 | 2011-10-18 | Genentech, Inc. | Stabile isotonic lyophilized protein formulation |
| US6451970B1 (en) * | 1996-02-21 | 2002-09-17 | Novo Nordisk A/S | Peptide derivatives |
| US5866538A (en) * | 1996-06-20 | 1999-02-02 | Novo Nordisk A/S | Insulin preparations containing NaCl |
| US5905140A (en) * | 1996-07-11 | 1999-05-18 | Novo Nordisk A/S, Novo Alle | Selective acylation method |
| ATE278711T1 (de) | 1996-07-11 | 2004-10-15 | Novo Nordisk As | Verfahren zur selektiven acetylierung |
| US5763401A (en) | 1996-07-12 | 1998-06-09 | Bayer Corporation | Stabilized albumin-free recombinant factor VIII preparation having a low sugar content |
| DK0821006T3 (da) | 1996-07-26 | 2004-08-16 | Aventis Pharma Gmbh | Insulinderivater med öget zinkbinding |
| IL119029A0 (en) | 1996-08-07 | 1996-11-14 | Yeda Res & Dev | Long-acting drugs and pharamaceutical compositions comprising them |
| US5898067A (en) * | 1997-02-07 | 1999-04-27 | Novo Nordisk A/S | Crystallization of proteins |
| ATE219942T1 (de) | 1997-03-20 | 2002-07-15 | Novo Nordisk As | Therapeutische pulverformulierung zur pulmonaren anwendung, welche kristallines insulin enthält |
| US7097845B2 (en) | 1997-04-23 | 2006-08-29 | Jacob Sten Petersen | Combinations of antigen and mucosal binding component for inducing specific immunological tolerance |
| DK1283051T3 (da) | 1997-06-13 | 2006-10-16 | Lilly Co Eli | Stabile insulinformuleringer |
| ZA984697B (en) | 1997-06-13 | 1999-12-01 | Lilly Co Eli | Stable insulin formulations. |
| US20020155994A1 (en) * | 1997-10-24 | 2002-10-24 | Svend Havelund | Aggregates of human insulin derivatives |
| EA200000453A1 (ru) | 1997-10-24 | 2000-10-30 | Эли Лилли Энд Компани | Композиции нерастворимого инсулина |
| CN1240718C (zh) | 1997-10-24 | 2006-02-08 | 诺沃挪第克公司 | 人胰岛素衍生物的聚集体 |
| US6451762B1 (en) * | 1997-10-24 | 2002-09-17 | Novo Nordisk A/S | Aggregates of human insulin derivatives |
| ZA989744B (en) | 1997-10-31 | 2000-04-26 | Lilly Co Eli | Method for administering acylated insulin. |
| CA2309955A1 (en) | 1997-11-12 | 1999-05-20 | Alza Corporation | Method for decreasing self-association of polypeptides |
| US6531448B1 (en) * | 1997-12-23 | 2003-03-11 | Eli Lilly And Company | Insoluble compositions for controlling blood glucose |
| EP1044016B1 (en) * | 1998-01-09 | 2005-03-16 | Novo Nordisk A/S | Stabilised insulin compositions |
| US6211144B1 (en) * | 1998-10-16 | 2001-04-03 | Novo Nordisk A/S | Stable concentrated insulin preparations for pulmonary delivery |
| ES2180511T3 (es) * | 1999-01-26 | 2003-02-16 | Lilly Co Eli | Formulaciones monodispersas de analogos de insulina acilados hexamericos. |
| EP2921180B1 (en) | 1999-02-22 | 2019-08-14 | University of Connecticut | Albumin-free factor VIII formulations |
| AU4450700A (en) | 1999-04-27 | 2000-11-10 | Eli Lilly And Company | Insulin crystals for pulmonary administration |
| GB9930882D0 (en) | 1999-12-30 | 2000-02-23 | Nps Allelix Corp | GLP-2 formulations |
| DE10022092A1 (de) | 2000-05-08 | 2001-11-15 | Aventis Behring Gmbh | Stabilisiertes Protein-Präparat und Verfahren zu seiner Herstellung |
| US6652886B2 (en) * | 2001-02-16 | 2003-11-25 | Expression Genetics | Biodegradable cationic copolymers of poly (alkylenimine) and poly (ethylene glycol) for the delivery of bioactive agents |
| JP4624600B2 (ja) * | 2001-06-08 | 2011-02-02 | トヨタ自動車株式会社 | 焼結合金、その製造方法およびバルブシート |
| AU2002316811A1 (en) | 2001-06-28 | 2003-03-03 | Novo Nordisk A/S | Stable formulation of modified glp-1 |
| JP2004537580A (ja) | 2001-08-10 | 2004-12-16 | エピックス メディカル, インコーポレイテッド | 延長された循環半減期を有するポリペプチド結合体 |
| US20030068361A1 (en) | 2001-10-09 | 2003-04-10 | Rimona Margalit | Liposome-encapsulated insulin formulations |
| PL374949A1 (en) | 2001-12-20 | 2005-11-14 | Eli Lilly And Company | Insulin molecule having protracted time action |
| US8003605B2 (en) * | 2002-03-13 | 2011-08-23 | Novo Nordisk A/S | Minimising body weight gain in insulin treatment |
| EP1506003A1 (en) | 2002-05-07 | 2005-02-16 | Novo Nordisk A/S | Soluble formulations comprising insulin aspart and insulin detemir |
| US20050232899A1 (en) | 2002-05-31 | 2005-10-20 | Aradigm Corporation | Compositions methods and systems for pulmonary delivery of recombinant human interferon alpha-2b |
| US20040002451A1 (en) | 2002-06-20 | 2004-01-01 | Bruce Kerwin | Compositions of pegylated soluble tumor necrosis factor receptors and methods of preparing |
| KR100615389B1 (ko) | 2002-08-23 | 2006-08-25 | (주)헬릭서 | 다래 추출물을 함유하는 알러지성 질환 및 비알러지성염증 질환의 예방 및 개선용 건강 기능 식품 |
| EP1562626B1 (en) | 2002-10-29 | 2007-11-28 | ALZA Corporation | Stabilized, solid-state polypeptide particles |
| US20040138099A1 (en) * | 2002-11-29 | 2004-07-15 | Draeger Eberhard Kurt | Insulin administration regimens for the treatment of subjects with diabetes |
| CN101822834A (zh) | 2003-02-07 | 2010-09-08 | 味之素株式会社 | 糖尿病治疗药 |
| CA2787820A1 (en) | 2003-02-19 | 2004-09-02 | Novartis Ag | Glycoprotein antigen sima135 expressed in metastatic human tumor cells |
| EA200501422A1 (ru) * | 2003-03-04 | 2006-04-28 | Дзе Текнолоджи Девелопмент Компани Лтд. | Длительнодействующая инъецируемая композиция инсулина и способы её изготовления и применения |
| WO2004112828A1 (en) | 2003-06-25 | 2004-12-29 | Novo Nordisk Health Care Ag | Liquid composition of factor vii polypeptides |
| US20050054818A1 (en) | 2003-07-02 | 2005-03-10 | Brader Mark Laurence | Crystalline compositions for controlling blood glucose |
| WO2005005477A2 (en) | 2003-07-11 | 2005-01-20 | Novo Nordisk A/S | Stabilised insulin compositions |
| SI2107069T1 (sl) | 2003-08-05 | 2013-04-30 | Novo Nordisk A/S | Novi inzulinski derivati |
| ES2574581T3 (es) | 2003-08-14 | 2016-06-20 | Novo Nordisk Health Care Ag | Composición farmacéutica líquida acuosa de polipéptidos de tipo Factor VII |
| JP5518282B2 (ja) | 2003-09-01 | 2014-06-11 | ノヴォ ノルディスク アー/エス | 安定なペプチドの製剤 |
| ES2229931B1 (es) | 2003-10-03 | 2006-01-16 | Grifols, S.A. | Composicion liquida bilogicamente estable de fviii, de fvw o del complejo fviii/fvw humanos. |
| EP1687428A1 (en) * | 2003-11-14 | 2006-08-09 | Novo Nordisk A/S | Processes for making acylated insulin |
| US8338374B2 (en) | 2003-12-23 | 2012-12-25 | Pharmacia Corporation | Stable growth hormone liquid formulation |
| DE602005014962D1 (de) | 2004-03-12 | 2009-07-30 | Biodel Inc | Insulinzusammensetzungen mit verbesserter wirkstoffabsorption |
| EP1750750B1 (en) | 2004-06-01 | 2012-02-01 | Ares Trading S.A. | Method of stabilizing proteins |
| WO2006008238A1 (en) | 2004-07-16 | 2006-01-26 | Novo Nordisk A/S | Method for selective acylation |
| DE602005022895D1 (de) | 2004-08-12 | 2010-09-23 | Schering Corp | Stabile pegylierte interferon-formulierung |
| PT1778723E (pt) | 2004-08-17 | 2013-01-25 | Regeneron Pharma | Formulações de antagonista de il-1 |
| WO2006051103A2 (en) | 2004-11-12 | 2006-05-18 | Novo Nordisk A/S | Stable formulations of peptides |
| ES2391776T3 (es) | 2004-11-22 | 2012-11-29 | Novo Nordisk A/S | Formulaciones solubles, estables conteniendo insulina con una sal de protamina |
| CA2593112A1 (en) | 2005-01-21 | 2006-07-27 | Alza Corporation | Therapeutic peptide formulations for coating microneedles with improved stability containing at least one counterion |
| EP1846447B1 (en) | 2005-02-02 | 2013-08-21 | Novo Nordisk A/S | Insulin derivatives |
| WO2006082204A1 (en) | 2005-02-02 | 2006-08-10 | Novo Nordisk A/S | Insulin derivatives |
| WO2007041481A1 (en) | 2005-09-29 | 2007-04-12 | Biodel, Inc. | Rapid acting and prolonged acting insulin preparations |
| JP2009512709A (ja) | 2005-10-20 | 2009-03-26 | エムディーアールエヌエー,インコーポレイテッド | 速効型インスリンの経鼻投与 |
| JP4808785B2 (ja) | 2005-12-28 | 2011-11-02 | ノボ・ノルデイスク・エー/エス | インスリン組成物および組成物の製造方法 |
| EP1991576B1 (en) * | 2006-02-27 | 2010-09-29 | Novo Nordisk A/S | Insulin derivatives |
| CN101454019A (zh) | 2006-04-12 | 2009-06-10 | 百达尔公司 | 速效和长效胰岛素联合制剂 |
| WO2007121256A2 (en) | 2006-04-12 | 2007-10-25 | Biodel, Inc. | Rapid acting and long acting insulin combination formulations |
| EP2024390B1 (en) | 2006-05-09 | 2015-08-19 | Novo Nordisk A/S | Insulin derivative |
| MX2008014061A (es) | 2006-05-09 | 2008-11-14 | Novo Nordisk As | Derivado de insulina. |
| WO2007135117A2 (en) | 2006-05-24 | 2007-11-29 | Novo Nordisk A/S | Soluble, stable insulin-containing formulations |
| DK2074141T3 (en) | 2006-09-22 | 2016-11-28 | Novo Nordisk As | The protease resistant insulin analogues. |
| US9034818B2 (en) * | 2007-06-13 | 2015-05-19 | Novo Nordisk A/S | Pharmaceutical formulations comprising an insulin derivative |
| EP2178910B1 (en) | 2007-08-15 | 2014-10-08 | Novo Nordisk A/S | Insulins with an acyl moiety comprising repeating units of alkylene glycol containing amino acids |
| EP2036539A1 (en) | 2007-09-11 | 2009-03-18 | Novo Nordisk A/S | Stable formulations of amylin and its analogues |
| US8710000B2 (en) | 2007-11-08 | 2014-04-29 | Novo Nordisk A/S | Insulin derivative |
| JP5241849B2 (ja) | 2007-11-16 | 2013-07-17 | ノボ・ノルデイスク・エー/エス | インスリン及びインスリン分泌性ペプチドを含む薬学的組成物 |
| CN102037008B (zh) | 2008-03-18 | 2016-08-31 | 诺沃-诺迪斯克有限公司 | 蛋白酶稳定化的、酰化胰岛素类似物 |
| TWI451876B (zh) | 2008-06-13 | 2014-09-11 | Lilly Co Eli | 聚乙二醇化之離脯胰島素化合物 |
| AU2009309623B9 (en) | 2008-10-30 | 2014-10-02 | Novo Nordisk A/S | Treating diabetes melitus using insulin injections with less than daily injection frequency |
| US20130143803A1 (en) | 2010-05-10 | 2013-06-06 | Novo Nordisk A/S | Process for the Preparation of Insulin-Zinc Complexes |
| AU2011202239C1 (en) | 2010-05-19 | 2017-03-16 | Sanofi | Long-acting formulations of insulins |
| EP2389945A1 (en) | 2010-05-28 | 2011-11-30 | Sanofi-Aventis Deutschland GmbH | Pharmaceutical composition comprising AVE0010 and insulin glargine |
| DK2632478T3 (da) | 2010-10-27 | 2019-10-07 | Novo Nordisk As | Behandling af diabetes melitus under anvendelse af insulinindsprøjtninger indgivet med varierende indsprøjtningsintervaller |
| CN103167878A (zh) | 2010-10-27 | 2013-06-19 | 诺沃—诺迪斯克有限公司 | 采用在不同注射时间间隔给予的胰岛素注射剂治疗糖尿病 |
| AU2012213432B2 (en) | 2011-02-01 | 2016-10-13 | Novo Nordisk A/S | Purification of insulin |
| AU2012223282B2 (en) | 2011-03-01 | 2017-02-02 | Nutrition 21, Llc | Compositions of insulin and chromium for the treatment and prevention of diabetes, hypoglycemia and related disorders |
| US10293109B2 (en) | 2011-09-13 | 2019-05-21 | Novo Nordisk A/S | Adaptive system for optimizing a drug dosage regimen over time |
| US9481721B2 (en) | 2012-04-11 | 2016-11-01 | Novo Nordisk A/S | Insulin formulations |
| CA2872083A1 (en) | 2012-05-01 | 2013-11-07 | Novo Nordisk A/S | Pharmaceutical composition |
| JP6755175B2 (ja) | 2013-03-20 | 2020-09-16 | ノヴォ ノルディスク アー/エス | インスリン投薬レジメン |
| US9839579B2 (en) | 2013-04-24 | 2017-12-12 | Corning Incorporated | Delamination resistant pharmaceutical glass containers containing active pharmaceutical ingredients |
| JP2016519127A (ja) | 2013-04-30 | 2016-06-30 | ノヴォ ノルディスク アー/エス | 新規投与レジメン |
| CN111032685A (zh) | 2017-08-17 | 2020-04-17 | 诺沃挪第克公司 | 新型酰化胰岛素类似物及其用途 |
-
2006
- 2006-12-21 JP JP2008547953A patent/JP4808785B2/ja active Active
- 2006-12-21 EP EP11156145A patent/EP2505593A1/en not_active Withdrawn
- 2006-12-21 DK DK06841562.9T patent/DK1969004T3/da active
- 2006-12-21 ES ES06841562T patent/ES2371361T3/es active Active
- 2006-12-21 US US12/096,476 patent/US20090074882A1/en not_active Abandoned
- 2006-12-21 CN CN2006800535166A patent/CN101389650B/zh not_active Ceased
- 2006-12-21 EP EP06841562A patent/EP1969004B1/en active Active
- 2006-12-21 PT PT06841562T patent/PT1969004E/pt unknown
- 2006-12-21 PL PL06841562T patent/PL1969004T3/pl unknown
- 2006-12-21 WO PCT/EP2006/070104 patent/WO2007074133A2/en not_active Ceased
- 2006-12-21 AT AT06841562T patent/ATE519780T1/de active
-
2010
- 2010-08-02 JP JP2010174030A patent/JP5026567B2/ja active Active
-
2011
- 2011-01-19 JP JP2011008924A patent/JP2011121963A/ja not_active Withdrawn
-
2014
- 2014-07-16 US US14/332,906 patent/US11167035B2/en active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001518915A (ja) * | 1997-03-20 | 2001-10-16 | ノボ ノルディスク アクティーゼルスカブ | インシュリンと吸収増強剤の共沈殿による治療用粉末の調整法 |
| JP2002527487A (ja) * | 1998-10-16 | 2002-08-27 | ノボ ノルディスク アクティーゼルスカブ | 肺送達のための安定に濃縮されたインスリン製剤 |
| JP2004523589A (ja) * | 2001-03-23 | 2004-08-05 | アベンティス・ファーマ・ドイチユラント・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツング | 改善された安定性を有するいかなる量の亜鉛も含有しないかまたはほんの少量の亜鉛しか含有しないインスリン製剤 |
| WO2003094956A1 (en) * | 2002-05-07 | 2003-11-20 | Novo Nordisk A/S | Soluble formulations comprising monomeric insulin and acylated insulin |
| WO2005012347A2 (en) * | 2003-08-05 | 2005-02-10 | Novo Nordisk A/S | Novel insulin derivatives |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8828923B2 (en) | 2003-08-05 | 2014-09-09 | Novo Nordisk A/S | Insulin derivatives |
| JP2011121963A (ja) * | 2005-12-28 | 2011-06-23 | Novo Nordisk As | インスリン組成物および組成物の製造方法 |
| US11167035B2 (en) | 2005-12-28 | 2021-11-09 | Novo Nordisk A/S | Insulin compositions and method of making a composition |
| US9034818B2 (en) | 2007-06-13 | 2015-05-19 | Novo Nordisk A/S | Pharmaceutical formulations comprising an insulin derivative |
| US9603904B2 (en) | 2008-10-30 | 2017-03-28 | Novo Nordisk A/S | Treating diabetes melitus using insulin injections with less than daily injection frequency |
| US10596229B2 (en) | 2010-10-27 | 2020-03-24 | Novo Nordisk A/S | Method of treating diabetes mellitus by administration, at specifically defined intervals, of a derivative of a naturally occurring insulin or insulin analogue, the derivative having a prolonged profile of action |
| US10137172B2 (en) | 2013-04-30 | 2018-11-27 | Novo Nordisk A/S | Administration regime |
| US10335464B1 (en) | 2018-06-26 | 2019-07-02 | Novo Nordisk A/S | Device for titrating basal insulin |
| US12226458B2 (en) | 2018-06-26 | 2025-02-18 | Novo Nordisk A/S | System for providing an up-to-date and long-acting or ultra-long-acting insulin dose guidance recommendation to treat diabetes mellitus |
| US12343383B2 (en) | 2019-07-12 | 2025-07-01 | Novo Nordisk A/S | High concentration insulin formulation |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE519780T1 (de) | 2011-08-15 |
| ES2371361T3 (es) | 2011-12-30 |
| PT1969004E (pt) | 2011-11-25 |
| EP1969004A2 (en) | 2008-09-17 |
| JP2011006428A (ja) | 2011-01-13 |
| JP5026567B2 (ja) | 2012-09-12 |
| JP2011121963A (ja) | 2011-06-23 |
| WO2007074133A2 (en) | 2007-07-05 |
| PL1969004T3 (pl) | 2012-01-31 |
| US20090074882A1 (en) | 2009-03-19 |
| JP2009522231A (ja) | 2009-06-11 |
| WO2007074133A3 (en) | 2007-10-11 |
| US20140328943A1 (en) | 2014-11-06 |
| EP1969004B1 (en) | 2011-08-10 |
| EP2505593A1 (en) | 2012-10-03 |
| DK1969004T3 (da) | 2011-11-28 |
| CN101389650B (zh) | 2012-10-10 |
| US11167035B2 (en) | 2021-11-09 |
| CN101389650A (zh) | 2009-03-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4808785B2 (ja) | インスリン組成物および組成物の製造方法 | |
| JP2009522231A5 (ja) | ||
| EP2256129B1 (en) | Insulin derivatives | |
| JP5721432B2 (ja) | アミノ酸含有アルキレングリコール反復単位を含むアシル部を有するインスリン | |
| EP2262539B1 (en) | Insulin albumin conjugates | |
| JP5550338B2 (ja) | ペグ化持続型インスリン | |
| JP5730569B2 (ja) | アシル及びアルキレングリコール部分を有するインスリンアナログ | |
| CN102037008B (zh) | 蛋白酶稳定化的、酰化胰岛素类似物 | |
| NO340925B1 (no) | Nye insulinderivater | |
| JP2013545782A (ja) | 長時間作用型インスリンと組み合わせた速効型インスリン | |
| EP2058330A1 (en) | Insulin derivative |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091218 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20100630 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100802 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20100802 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20100826 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101019 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110119 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110308 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110608 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110719 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110817 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140826 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4808785 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140826 Year of fee payment: 3 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |