JP4477879B2 - 複分解に使用される金属錯体 - Google Patents
複分解に使用される金属錯体 Download PDFInfo
- Publication number
- JP4477879B2 JP4477879B2 JP2003562130A JP2003562130A JP4477879B2 JP 4477879 B2 JP4477879 B2 JP 4477879B2 JP 2003562130 A JP2003562130 A JP 2003562130A JP 2003562130 A JP2003562130 A JP 2003562130A JP 4477879 B2 JP4477879 B2 JP 4477879B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- alkyl
- aryl
- ligand
- ylidene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System compounds of the platinum group
- C07F15/0046—Ruthenium compounds
- C07F15/0053—Ruthenium compounds without a metal-carbon linkage
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/1616—Coordination complexes, e.g. organometallic complexes, immobilised on an inorganic support, e.g. ship-in-a-bottle type catalysts
- B01J31/1625—Coordination complexes, e.g. organometallic complexes, immobilised on an inorganic support, e.g. ship-in-a-bottle type catalysts immobilised by covalent linkages, i.e. pendant complexes with optional linking groups
- B01J31/1633—Coordination complexes, e.g. organometallic complexes, immobilised on an inorganic support, e.g. ship-in-a-bottle type catalysts immobilised by covalent linkages, i.e. pendant complexes with optional linking groups covalent linkages via silicon containing groups
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2204—Organic complexes the ligands containing oxygen or sulfur as complexing atoms
- B01J31/2208—Oxygen, e.g. acetylacetonates
- B01J31/2226—Anionic ligands, i.e. the overall ligand carries at least one formal negative charge
- B01J31/2243—At least one oxygen and one nitrogen atom present as complexing atoms in an at least bidentate or bridging ligand
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2265—Carbenes or carbynes, i.e.(image)
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
- B01J31/2404—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F1/00—Compounds containing elements of Groups 1 or 11 of the Periodic System
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F1/00—Compounds containing elements of Groups 1 or 11 of the Periodic System
- C07F1/08—Copper compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F11/00—Compounds containing elements of Groups 6 or 16 of the Periodic System
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F13/00—Compounds containing elements of Groups 7 or 17 of the Periodic System
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System compounds of the platinum group
- C07F15/002—Osmium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System compounds of the platinum group
- C07F15/0046—Ruthenium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System compounds of the platinum group
- C07F15/0073—Rhodium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/02—Iron compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/04—Nickel compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/06—Cobalt compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/28—Titanium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F12/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F12/02—Monomers containing only one unsaturated aliphatic radical
- C08F12/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F12/06—Hydrocarbons
- C08F12/08—Styrene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/70—Iron group metals, platinum group metals or compounds thereof
- C08F4/7001—Iron group metals, platinum group metals or compounds thereof the metallic compound containing a multidentate ligand, i.e. a ligand capable of donating two or more pairs of electrons to form a coordinate or ionic bond
- C08F4/7003—Bidentate ligand
- C08F4/7019—Monoanionic ligand
- C08F4/7022—NO
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
- C08G61/04—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aliphatic carbon atoms
- C08G61/06—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aliphatic carbon atoms prepared by ring-opening of carbocyclic compounds
- C08G61/08—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aliphatic carbon atoms prepared by ring-opening of carbocyclic compounds of carbocyclic compounds containing one or more carbon-to-carbon double bonds in the ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/10—Polymerisation reactions involving at least dual use catalysts, e.g. for both oligomerisation and polymerisation
- B01J2231/12—Olefin polymerisation or copolymerisation
- B01J2231/125—Radical (co)polymerisation, e.g. mediators therefor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/50—Redistribution or isomerisation reactions of C-C, C=C or C-C triple bonds
- B01J2231/54—Metathesis reactions, e.g. olefin metathesis
- B01J2231/543—Metathesis reactions, e.g. olefin metathesis alkene metathesis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/02—Compositional aspects of complexes used, e.g. polynuclearity
- B01J2531/0286—Complexes comprising ligands or other components characterized by their function
- B01J2531/0288—Sterically demanding or shielding ligands
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/821—Ruthenium
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/11—Compounds covalently bound to a solid support
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1804—C4-(meth)acrylate, e.g. butyl (meth)acrylate, isobutyl (meth)acrylate or tert-butyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2438/00—Living radical polymerisation
- C08F2438/01—Atom Transfer Radical Polymerization [ATRP] or reverse ATRP
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/33—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain
- C08G2261/332—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms
- C08G2261/3322—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms derived from cyclooctene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/33—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain
- C08G2261/332—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms
- C08G2261/3324—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms derived from norbornene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/40—Polymerisation processes
- C08G2261/41—Organometallic coupling reactions
- C08G2261/418—Ring opening metathesis polymerisation [ROMP]
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/40—Polymerisation processes
- C08G2261/41—Organometallic coupling reactions
- C08G2261/419—Acyclic diene metathesis [ADMET]
Description
ジカル重合を組み合わせることは、極めて好都合なことであり、(1)原子または基の転移経路、および(2)ラジカル中間体の関与する米国特許第5,763,548号の原子(または基)転移ラジカル重合法(以後ATRPと称する)により達成されている。この種のリビング重合では転移および停止等の鎖切断反応が実質的に存在せず、分子量、分子量分布および末端官能基等の大分子構造の種々のパラメーターの制御が可能である。これはまた種々の共重合体、例えばブロックおよび星型共重合体の調製も可能とする。リビング/制御ラジカル重合は種々の不活性の種との平衡状態においてラジカルの低い定常状態濃度を要する。これは種々の遷移金属家具物と重合開始剤、例えばアルキルハライドまたはハロアルキルエステルとの間の酸化還元反応において成長中のラジカルの可逆的形成に基づいた新しい重合開始系を使用することができる。ATRPは不活性種中の炭素とハロゲンの共有結合の可逆的な遷移金属触媒性の切断を介して樹立された、増幅中のラジカルと不活性種との間の動的な平衡に基づいている。この概念を利用した重合系は、必要な平衡を樹立するために、例えば銅、ルテニウム、ニッケル、パラジウム、ロジウムおよび鉄の鎖体を用いて開発されている。
産性を改善するために、触媒量当たりのポリオレフィンの収量の増大および連続製造の期間に渡る触媒活性の維持も重要な要件である。WO02/02649号は(A)イミン構造部分を含む2座配位子を有する好ましくは遷移金属がチタン、ジルコニウムまたハフニウムである遷移金属化合物、(B−1)化合物(A)と反応して該イミン構造部分を金属アミン構造に変換できる還元能を有する化合物、および、(B−2)化合物(A)と反応してイオン対を形成する化合物を含むオレフィン重合触媒系を開示している。しかしながら、WO02/02649号は金属がカルベン配位子に対して配位している遷移金属化合物を記載していない。WO02/02649号の記載について、オレフィン重合活性とその維持を改善する必要性がなお当該分野に存在する。
本明細書においては鎖体または配位化合物という用語は、金属(アクセプター)と、それぞれが非金属の原子またはイオンを含む、配位子と呼ばれる数種の中性分子またはイオン化合物(ドナー)との間のドナー−アクセプター機序またはルイス酸−塩基反応の結果
物を指す。孤立電子対を有する原子1個以上を有する配位子を多座配位子と呼ぶ。
その最も広範な解釈において、本発明は、カルベン配位子、多座配位子および他の配位子1個以上を含み、該他の配位子の少なくとも1個がpKaが少なくとも15である制限立体障害配位子である5配位金属鎖体、その塩、その溶媒和物またはそのエナンチオマー
に関する。この5配位金属鎖体は1金属鎖体でまたは2金属鎖体であって、中性の配位子1個以上およびアニオン性の配位子1個以上に対して一方の金属が5配位であり、もう一方が4配位であるものであってよい。後者の場合には金属2個は同じかまたは異なっていてよい。多座配位子は2座配位子であってよく、その場合は本発明の金属鎖体は他の配位子2個を含み、または3座配位子であってよく、その場合は金属鎖体は他の配位子1個を含む。
本発明の5配位金属鎖体のカルベン配位子はアレニリデン配位子、クムレニリデン配位子、例えばブタン−1,2,3−トリエニリデン、ペンタ−1,2,3,4−テトラニリデン等である。
− (i)多座配位子、および、pKaが少なくとも15である制限立体障害配位子以外であり、カルベン配位子以外である他の配位子1個以上を含む4配位金属鎖体を、(ii)アルキニル化合物、ジアゾ化合物およびジアルキニル化合物からなる群より選択される反応体、ただし該反応体は金属に対するカルベン配位子を与えることができるもの、と反応させることにより5配位1金属鎖体を製造する第1の工程、および、次に、
− 第1の工程で得られた5配位1金属鎖体を、pKaが少なくとも15である制限立体障害基を含む種と、pKaが少なくとも15である該制限立体障害基を含む種がカルベン配位子以外の他の配位子の1個の変わりに金属に対して配位できるような条件下で、反応させる第2の工程、
を包含する。
− Mは周期律表の4、5、6、7、8、9、10、11および12族からなる群より選択される遷移金属、好ましくはルテニウム、オスミウム、鉄、モリブデン、タングステン、チタン、レニウム、銅、クロム、マンガン、ロジウム、バナジウム、亜鉛、金、銀、ニッケルおよびコバルトから選択される金属であり;
− Zは酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は各々、水素、C1−6アルキル、C3−10シクロアルキル、C1−6アルキル−C1−6アルコキシシリル、C1−6アルキル−アリールオキシシリル、C1−6アルキル−C3−10シクロアルコキシシリル、アリールおよびヘテロアリールからなる群より選択されるか、または、R’’およびR’’’は一緒になってアリールまたはヘテロアリール基を形成し、該基各々(水素でない場合)は、場合により、ハロゲン原子、C1−6アルキル、C1−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、C1−6アルキル−C1−6アルコキシシリル、C1−6アルキル−アリールオキシシリル、C1−6アルキル−C3−10シクロアルキルシリル、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R51個以上、好ましくは1〜3個で置換されており;
− R’は一般式(IA)を有する化合物中に含まれる場合はR’’、R’’’およびR’’’’と同様に定義され、または、一般式(IB)を有する化合物中に含まれる場合はC1−6アルキレンおよびC3−8シクロアルキレンからなる群より選択され、該アルキレンまたはシクロアルキレン基は場合により置換基R51個以上で置換されており;
− R1はpKaが少なくとも15である制限立体障害基であり;
− R2はアニオン性配位子であり;
− R3はおよびR4は各々、水素またはC1−20アルキル、C2−20アルケニル、C2−20アルキニル、C1−20カルボキシレート、C1−20アルコキシ、C2−20アルケニルオキシ、C2−20アルキニルオキシ、アリール、アリールオキシ、C1−20アルコキシカルボニル、C1−8アルキルチオ、C1−20アルキルスルホニル、C1−20アルキルスルフィニルC1−20アルキルスルホネート、アリールスルホネート、C1−20アルキルホスホネート、アリールホスホネート、C1−20アルキルアンモニウムおよびアリールアンモニウムからなる群より選択される基であり;
− R’およびR3およびR4の一方は相互に結合して2座の配位子を形成してもよく;
−R’’’およびR’’’’は相互に結合して窒素、リン、砒素およびアンチモンからなる群より選択されるヘテロ原子を含む脂肪族の環系を形成してもよく;
− R3およびR4は一緒になって縮合芳香族環系を形成してもよく、そして、
− yはMとR3およびR4を担持した炭素原子との間のsp2炭素原子の数を示し、そして0〜3の整数であるもの、その塩、溶媒和物およびエナンチオマーを提供する。
− イミダゾール−2−イリデン(pKa=24)、
− ジヒドロイミダゾール−2−イリデン(pKaは24より高値)、
− オキサゾール−2−イリデン、
− チアゾール−5−イリデン、
− チアゾール−2−イリデン、
− ピロリリデン(pKa=17.5)、
− ピラゾリリデン、
− ジヒドロピロリリデン、
− ピロリリジニリデン(pKa=44)、
− ビス(イミダゾリン−2−イリデン)およびビス(イミダゾリジン−2−イリデン)、
− インドリリデン等のベンゾ縮合誘導体(pKa=16)、および、
− 非イオン性プロホスファトラン超強塩基(スーパー塩基)、例えば米国特許第5,698,737号に記載のもの、好ましくは、Verkadeスーパー塩基として知られているトリメチリトリアザプロホスファトランP(CH3NCH2CH2)3N。
ば2,4,6−トリメチルフェニル(メシル)、2,6−ジメチルフェニル、2,4,6−トリイソプロピルフェニルまたは2,6−ジイソプロピルフェニル)またはC1-6アルキル置換基1個以上を有するヘテロアリール基(例えばピリジニル)である。
− 式R3R4R7CO≡CHを有するアルキニル化合物、ただしR3およびR4は一般式(IA)および(IB)について上記した通り定義され、そしてR7は水素、ヒドロキシルおよびR3からなる群より選択されるもの(y=2の場合)、
− 式N2CR3R4を有するジアゾ化合物、ただしただしR3およびR4は前述の通り定義されるもの(yが0である場合)、
− 式R3C≡CHを有するアルキニル化合物、ただしR3は前述の通り定義されるもの(yが1の場合)、および、
− 式R21C≡C−C≡CR22を有するジアルキニル化合物、ただしR21およびR22は各々独立して水素およびトリアルキルシリルから選択されるもの(yが3の場合)、
からなる群より選択される反応体と反応させること、を含む方法を提供する。
− 式R3R4R7CO≡CHを有するアルキニル化合物、ただしR3およびR4は式(IA)および(IB)に関して上記した通り定義され、そしてR7は水素、ヒドロキシルおよびR3からなる群より選択されるもの(y=2の場合)、
− 式N2CR3R4を有するジアゾ化合物、ただしただしR3およびR4は上記した通り定義されるもの(yが0である場合)、
− 式R3C≡CHを有するアルキニル化合物、ただしR3は上記した通り定義されるもの(yが1の場合)、および、
− 式R21C≡C−C≡CR22を有するジアルキニル化合物、ただしR21およびR22は各々独立して水素およびトリアルキルシリルから選択されるもの(yが3の場合)、
からなる群より選択される反応体と反応させること、
および、第2の工程において更に、第1の工程の反応生成物を、式R1Yを有する化合物、ただし式中R1は上記した通り定義され、Yは脱離基であるものと反応させること、を包含する上記方法を提供する。この第2の方法において、脱離基Yの適当な例は第1の方法について開示したとおりである。
− Mは周期律表の4、5、6、7、8、9、10、11および12族からなる群より選択される遷移金属、好ましくはルテニウム、オスミウム、鉄、モリブデン、タングステン、チタン、レニウム、銅、クロム、マンガン、ロジウム、バナジウム、亜鉛、金、銀、コバルトおよびニッケルから選択される金属であり;
− Zは酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は各々、水素、C1-6アルキル、C3-8シクロアルキル、アリールおよびヘテロアリールからなる群より選択されるか、または、R’’およびR’’’は一緒になってアリールまたはヘテロアリール基を形成し、該基各々は場合により、ハロゲン原子、C1-6アルキル、C1-6アルコキシ、アリール、アルキルスルホネー
ト、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R51個以上、好ましくは1〜3個で置換されており;
− R’は一般式(IIIA)を有する化合物中に含まれる場合はR’’、R’’’およびR’’’’と同様に定義され、または、一般式(IIIB)を有する化合物中に含まれる場合はC1-6アルキレンおよびC3-8シクロアルキレンからなる群より選択され、該アルキレンまたはシクロアルキレン基は場合により置換基R51個以上で置換されており;
− R1はpKaが少なくとも15である制限立体障害基であり;
− R2はアニオン性配位子である、上記鎖体、その塩、溶媒和物およびエナンチオマーを提供する。
− Mは周期律表の4、5、6、7、8、9、10、11および12族からなる群より選択される遷移金属、好ましくはルテニウム、オスミウム、鉄、モリブデン、タングステン、チタン、レニウム、銅、クロム、マンガン、ロジウム、バナジウム、亜鉛、金、銀、コバルトおよびニッケルから選択される金属であり;
− Zは酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は各々、水素、C1-6アルキル、C3-8シクロアルキル、アリールおよびヘテロアリールからなる群より選択されるか、またはR’’およびR’’’は一緒になってアリールまたはヘテロアリール基を形成し、各該基は場合によりハロゲン原子、C1-6アルキル、C1-6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R51個以上、好ましくは1〜3個で置換されているか、または、R’’およびR’’’は一緒になってアリールまたはヘテロアリール基を形成し、該基は、臭素、ヨウ素、C2-6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より選択される置換基R51個、または、ハロゲン原子、C1-6アルキル、C1-6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、C1-6アルキル−C1-6アルコキシシリル、C1-6アルキル−アリールオキシシリル、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R52個以上で置換されており;
− R’は一般式(IIA)を有する化合物中に含まれる場合はR’’、R’’’およびR’’’’と同様に定義され、または、一般式(IIB)を有する化合物中に含まれる場合はC1-6アルキレンおよびC3-8シクロアルキレンからなる群より選択され、該アルキレンまたはシクロアルキレン基は場合により置換基R51個以上で置換されており;
− R2はアニオン性配位子であり;
− R6は芳香族および不飽和の脂環族、好ましくはアリールおよびC4-20シクロアルケニル(例えばシクロオクタジエニル、ノルボルナジエニル、シクロペンタジエニルおよびシクロオクタトリエニル)基であって、該基はC1-6アルキル基1個以上で場合により置換されたものである、上記鎖体、その塩、その溶媒和物およびそのエナンチオマーを提供する。
R’’’C(OH)=C(R’’)CHO
を有するヒドロキシアルデヒド、例えばサリチルアルデヒド(Zが酸素の場合)または相当するチオアルデヒド(Zがイオウの場合)、アミノアルデヒド(ZがNR’’’’の場合)、ホスフィノアルデヒド(ZがPR’’’’の場合)、アルシノアルデヒド(ZがAsR’’’’の場合)またはスチビノアルデヒド(ZがSbR’’’’の場合)、ただしヒドロキシ、チオ、アミノ、ホスフィノ、アルシノまたはスチビノ基がアルデヒド基に対してβ位にあるものを、第1脂肪族または芳香族のアミンと縮合すること、次いで、得られたアルジミンを、例えば周期律表のIA、IIAまたはIIIA族の何れかの金属(例えばナトリウム、カリウム、マグネシウムまたはタリウム)のアルコキシドとの反応によりその炎に変換すること、次いで、該塩を例えば[RuCl2(p−クメン)]2等の不安定な配位子(例えばハロゲン)を有する金属鎖体と反応させることを包含するよく知られた方法と類似の方法で調製してよい。式(IIB)を有する中間体の第2のクラスは、所望の5員のキレート配位子を得るためには、まずベンズアルデヒド等のアルデヒドを、o−ヒドロキシアニリン(Zが酸素の場合(、アミノチオール(Zがイオウの場合)、ジアミン(ZがNR’’’’の場合)、アミノホスフィン(ZがPR’’’’の場合)、アミノアルシン(ZがAsR’’’’の場合)またはアミノスチビン(ZがSbR’’’’の場合)、ただしヒドロキシ、チオ、第2アミノ、ホスフィノ、アルシノまたはスチビノ基が第1アミノ基に対してβ位にあるもののようなアミノアルコールと縮合させること、次に得られたアミジノをその塩に変換すること、そして次に該塩を上記化合物(IA)に関して示したものと同様の方法で不安定な配位子を有する金属鎖体と反応させることにより調製してよい。
(a)前記のとおり定義される触媒活性5配位金属鎖体、および、
(b)該触媒活性5配位金属鎖体(a)を支持するのに適する担体の支持量、
を含む不均一触媒反応において使用するための支持された触媒を提供する。
晶質シリカの100〜250オングストロームの粒子よりなり(Kirk−Othmer
Encyclopedia of Chemical Technology,3rd.ed.,vol.20,766−781(1982))、多孔性は粒子間の空隙より生じるものである。
能する有機化合物の反応混合物からのその合成を記載している。別の構造要素を有する同様の組成物が欧州特許出願第293,032号に記載されている。ヘキサメチレンイミンはまた米国特許第4,954,325号において結晶性モレキュラーシーブMCM−22;米国特許第4,981,663号においてMCM−35;米国特許第5,236,575号においてMCM−49;そして米国特許第5,021,141号においてZSM−12の合成における使用について説明されている。モレキュラーシーブ組成物SSZ−25は米国特許第4,826,667号および欧州特許出願第231,860号に記載されており、該ゼオライトはアダマンタン第4アンモニウムイオンを含む反応混合物から合成されている。ゼオライト、REY、USY、REUSY、脱アルミニウム化Y、超疎水性Y、ケイ素高含有脱アルミニウム化Y、ZSM−20、Beta、L、シリコアルミオホスフェートSAPO−5、SAPO−37、SAPO−40、MCM−9、メタロアルミノホスフェートMAPO−36、アルミノホスフェートVPI−5およびメソポーラス結晶MCM−41からなる群より選択されるモレキュラーシーブ物質が本発明の支持された触媒内に含まれるのに適している。
する。本発明の金属カルベン化合物の高水準の転移活性はこれらの化合物を配意させ、そして、全種類のオレフィンの間の転移反応を触媒する。本発明の金属カルベン化合物により可能となる反応の例は、例えば、環状オレフィンの開環転移重合、非環状ジエンの閉環転移、非環状または環状のオレフィン少なくとも1種の関与する交差転移反応、および、オレフィン重合体の脱重合である。特に本発明の触媒は少なくとも3原子の環サイズの環状オレフィンを触媒することができる。このような転移反応において使用してよい環状オレフィンの例はノルボルネンおよびその機能的誘導体(例えば後述する実施例において説明するもの)、シクロブテン、ノルボルナジエン、シクロペンテン、ジシクロペンタジエン、シクロヘプタン、シクロオクタン、7−オキサノルボルネン、7−オキサノルボルナジエン、シクロオクタジエンおよびシクロドデセンを包含する。
れかであってよい。
上記式中、
aは0〜2の整数であり、
bは1および2から選択され、
cは0および1から選択され、
mおよびpは式(V)の炭化水素鎖が炭素原子10〜18個を含むようにするものであり、
rおよびtは式(IV)の2種の同じでないオレフィンの炭化水素鎖中の炭素原子の合計が12〜40となるようにするものであり、
X、X’およびX’’は水素、ハロゲン、メチル、アセチル、−CHOおよび−OR12から独立して選択され、ここでR12は水素およびテトラヒドロピラニル、テトラヒドロフラニル、t−ブチル、トリチル、エトキシエチルおよびSiR13R14R15からなる群より選択されるアルコール保護基から選択され、ここで、R13、R14およびR15は各々独立してC1-6アルキル基およびアリール基から選択される。
。この種の問題は、液体オレフィン単量体および触媒を混合し、金型内に注入、キャスティングまたは射出し、そして重合完了(即ち製品の硬化)時に成型された部分を金型から取り出した後、反応射出成型(RIM)法の場合のように必要であれば後硬化工程を行う熱硬化性重合体の成型時に起こる可能性が高い。反応速度、即ち反応混合物のポットライフを制御できる能力はより大型の部品の鋳造においてより重要となる。本発明の触媒を用いること、ポットライフを延長すること、および/または転移重合反応の速度を制御することは、種々の方法、例えば触媒/オレフィンの比率の増大、および/または重合遅延剤の反応混合物への添加等において、行ってよい。更に、これはまた下記:
(a)前述した転移触媒(場合により支持されている)をオレフィンと、反応器中、該転移触媒が実質的に非反応性(不活性)である第1の温度において接触させる第1の工程、および、
(b)反応器の温度を、該触媒が活性となる、第1の温度を超えた第2の温度とする(例えば該反応器を過熱する)第1の工程、
を包含する進歩した実施形態により達成することができる。
ニオン性配位子を抽出して得られるもの)を場合により担体の支持量と組み合わせたもの、ただしここで:
− M、Z、R’、R’’、R’’’、R’’’’、R2、R3、R4およびyは式(IA)および(IB)に関して前述のとおり定義したものであり、
− R16は中性の電子供与体であるもの、
の使用に関する。
は式R31R32C=CR33R34のものを含み、式中、
− R31およびR32は相互に独立して水素、ハロゲン、CN、CF3、C1-20アルキル(好ましくはC1-6アルキル)、α,β−不飽和C2-20アルキル(好ましくはアセチレニル)、α,β−不飽和C2-20アルケニル(好ましくはビニル)、ただし場合により(好ましくはα位において)ハロゲン、C3-8シクロアルキル、フェニルただし場合により置換基1〜5個を担持しているもの、で置換されたもの、からなる群より選択され;
− R33およびR34は独立して水素、ハロゲン(好ましくはフッ素または塩素)、C1-6アルキルおよびCOOR35(式中R35は水素、アルカリ金属またはC1-6アルキルから選択される)からなる群より選択され;そして、
− R31、R32、R33およびR34の少なくとも2つは水素またはハロゲンである。
− C1-20アルコールの(メタ)アクリル酸エステル、
− アクリロニトリル、
− C1-20アルコールのシアノアクリル酸エステル、
− C1-6アルコールのジデヒドロマトネートジエステル、
− アルキル基のα炭素原子が水素原子を担持していないビニルケトン、および、
− 場合によりビニル部分(好ましくはα炭素原子)にC1-6アルキル基およびフェニル環上に置換基1〜5個を担持したスチレン、ただし該置換基はC1-6アルキル、C1-6アルケニル(好ましくはビニル)、C1-6アルキニル(好ましくはアセチレニル)、C1-6アルコキシ、ハロゲン、ニトロ、カルボキシ、C1-6アルコキシカルボニル、C1-6アシルで保護されたヒドロキシ、シアノおよびフェニルからなる群より選択されるもの、
を包含する。
− X1はハロゲン、OR38(R38はC1-20アルキル、ポリハロC1-20アルキル、C2-20アルキニル(好ましくはアセチレニル)、C2-20アルケニル(好ましくはビニル)、場合により1〜5個のハロゲン原子またはC1-6アルキル基で置換されたフェニル、および、フェニル置換C1-6アルキルから選択される)、SR39、OC(=O)R39、OP(=O)R39、OP(=O)(OR39)2、OP(=O)OR39、O−N(R39)2およびS−C(=S)N(R39)2からなる群より選択され、ここでR39はアリールまたはC1-20アルキルであるか、または、N(R39)2基が存在する場合は、2個のR39基が一緒になって5、6または7員の複素環を形成し(上記ヘテロアリールの定義に従う)、そして、
− R35、R36およびR37は各々独立して水素、ハロゲン、C1-20アルキル(好ましくはC1-6アルキル)、C3-8シクロアルキル、C(=O)R40(ただしR40はC1-20アルキル、C1-20アルコキシ、アリールオキシまたはヘテロアリールオキシからなる群より選択さ
れる)、C(=O)NR41R42(式中R41およびR42は相互に独立して水素およびC1-20アルキルからなる群より選択されるか、または、R41とR42は一緒になって炭素原子2〜5個のアルキレン基を形成する)、COCl、OH、CN、C2-20アルケニル(好ましくはビニル)、C2-20アルキニル、オキシラニル、グリシジル、アリール、ヘテロアリール、アリールアルキルおよびアリール置換C2-20アルケニルからなる群より選択される。
懸濁法、乳化法、または沈殿法に従って実施しても良い。適当なエーテルにはジエチルエーテル、エチルプロピルエーテル、ジプロピルエーテル、メチルt−ブチルエーテル、ジ−t−ブチルエーテル、グライム(ジメトキシエタン)ジグライム(ジエチレングリコールジメチルエーテル)等が包含される。適当な環状エーテルにはテトラヒドロフランおよびジオキサンが包含される。適当なアルカンにはペンタン、ヘキサン、シクロヘキサン、オクタンおよびドデカンが包含される。適当な芳香族炭化水素にはベンゼン、トルエン、o−キシレン、m−キシレン、p−キシレンおよびクメンが包含される。選択されたハロゲン化炭化水素は反応条件下において重合開始剤として機能しないことを確認しておく必要があるが、適当なハロゲン化炭化水素には、ジクロロメタン、1,2−ジクロロエタンおよびフッ素原子/塩素原子1〜6個で置換されたベンゼンが包含される。
チレートの使用により明らかにされるとおり重合開始剤にとって要件とはならない。重合開始剤および他の反応成分の転換順序はいずれでもよいが、阻害剤を乳化前の反応混合物に添加する場合は、通常は安定なラテックスが得られる。適当な重合開始剤はATRP工程における溶媒の実施形態において前述したとおりである。重合開始剤はまたラジカル転移可能な原子または基を含む巨大分子であることができる。このような巨大分子の典型的な種類は水溶性またはむしろ両親媒性であってよく、そして、反応開始後は、重合体粒子内に取り込まれて良く、そして巨大重合開始剤の親水性セグメントにより成長中の粒子を安定させて良い。
ことによりマルチブロック共重合体を調製することができる。更にまた、ATRPはラジカル重合であるため、これらのブロックは本質的にどのような順序で調製することもできる。
(A)一般式(IB)を有する鎖体、
(B)化合物(A)と反応することによりそのイミン部分を金属アミン構造に変換する能力を有する化合物、および、
(C)化合物(A)と反応することによりイオン対を形成する能力を有する化合物、
を含む上記触媒系において使用される。
することが望ましい場合がある。
− R20はC1-6アルキレン、アリーレン、ヘテロアリーレンおよびC3-8シクロアルキレンからなる群より選択される基であり、該基は場合により、C1-20アルキル、C2-20アルケニル、C2-20アルキニル、C1-20カルボキシレート、C1-20アルコキシ、C2-20アルキルチオ、アリールオキシおよびアリールからなる群より各々が独立して選択される置換基R241個以上で置換されており;
− Dは酸素、イオウ、ケイ素、アリーレン、メチレン、CHR24、C(R24)2、NH、NR24およびPR24からなる群より選択される2価の原子または基であり;
− R21、R22およびR23は各々独立して水素、ハロゲンおよびR24からなる群より選択され;
− nは1〜20の整数であるが;
ただし、R21、R22およびR23の少なくとも1個はC1-20アルコキシ、C2-20アルケニルオキシ、C2-20アルキニルオキシ、C2-20アルコキシカルボニル、C1-20アルキルスルホニル、C1-20アルキニルスルフィニル、C1-20アルキルチオおよびアリールオキシからなる群より選択される)を有する基で置き換えられるか置換されている上記誘導体に関する。
物質を提供する。
− アリール、ポリアリール、C1-20アルキル、シクロアルキルおよび複素環シクロアルキル基、および、
− 式A(R20)nX3-n、ただしここでR20はC1-6アルキレン、アリーレン、ヘテロアリーレンおよびC3-8シクロアルキレンからなる群より選択される基であり、該基は場合により、C1-20アルキル、C2-20アルケニル、C2-20アルキニル、C1-20カルボキシレート、C1-20アルコキシ、C2-20アルケニルオキシ、C2-20アルキニルオキシ、C2-20アルコキシカルボニル、C1-20アルキスルホニル、C1-20アルキスルフィニル、C1-20アルキルチオ、アリールオキシおよびアリールからなる群より各々が独立して選択される置換基R241個以上で置換されており;Aは周期律表のIIIA族の元素(好ましくはホウ素またはアルミニウム)または窒素であるもの、または式G(R20)nX4-n、ただしGがIVA族の元素(好ましくは炭素、ケイ素またはスズ)であるもの、または、式J(R20)nX5-n、ただしJが窒素以外のVA族の元素(即ち好ましくはリン、砒素またはアンチモン)であるもの;または式E(R20)nX2-n、ただしEがVIA族の元素(好ましくは酸素またはイオウ)であるもの;ただし、該式においてXは水素またはハロゲンであるもの、を有する基、および、
− 周期律表のIIB、IIIB、IVB、VB、VIB、VIIBおよびVIIIB族の何れかの金属の遷移金族化合物、例えば4塩化チタン、3塩化バナジウム、4塩化ジルコニウム、C1-6アルキルチタネート、バナデート、ジルコネート等、
からなる群より選択される。
R’’’C(OH)=C(R’’)CHO
を有するアルデヒド、好ましくはサリチルアルデヒドを、式H2NR’を有する第1アミンと、還流温度で、有機溶媒(例えばテトラヒドロフラン)中で縮合させることにより、当該分野で知られた方法を用いて調製し、精製する。冷却後、粘稠な黄色の油状の縮合生成物をシリカゲルクロマトグラフィーで精製し、これにより式(I)の所望のサリチルアルジミン配位子を得る。第2工程においては、上記式(IIA)および(IIB)と混同してはならない式(II)を有するシッフ塩基置換ルテニウム鎖体を、金属アルコキシド、好ましくはタリウムエトキシドを式(I)の配位子の有機溶液に添加し、次に得られた固体を不活性雰囲気下に濾過し、該当するタリウム塩を定量的に得ることにより、当該分野で知られた方法を用いて調製し、精製する。次に該塩の有機溶液を室温で[RuCl2(p−クメン)]2の有機溶液と反応させた。塩化タリウム副生成物を濾過し、溶媒を蒸発させた後、残存物を結晶化し、洗浄し、乾燥し、赤茶色固体の外観を有する式(II)のシッフ塩基ルテニウム鎖体を得た。
II)を有するシッフ塩基置換ルテニウム鎖体は、まず式(III)を有するt−ブトキシル化化合物の有機溶液を式(VI)を有するシッフ塩基置換インデニリデン鎖体の有機溶液に添加し、そして混合物を1時間70〜80℃で攪拌することにより調製する。溶媒を除去した後、固体残存物を洗浄し、再結晶し、その後真空下に乾燥することにより、赤茶色の微結晶性固体として式(VII)を有する純粋な化合物を得る。
RおよびR’が添付の図の下端に示す意味を有し、MeがメチルでありiPrがイソプロピルである式(I.a)〜(I.f)を有するシッフ塩基リガンドを以下の通り調製し、精製した。第1脂肪族アミン(即ちR’が脂肪族または脂環族の基である)とのサリチルアルデヒドの縮合は、2時間還流温度でテトラヒドロフラン(以後THFと記載する)中攪拌することにより行った。室温に冷却後、粘稠な黄色の油状の縮合産物をシリカゲルクロマトグラフィーで精製し、式(I.a)〜(I.f)を有する所望のサリチルアルジミン配位子をそれぞれ95%および93%の収率で得た。芳香族第1アミンとのサリチルアルデヒドの縮合は同様に、2時間80℃でエタノール中攪拌することにより行った。0℃に冷却することにより黄色固体が反応混合物から析出した。この固体を濾過し、冷エタノールで洗浄し、次に真空下に乾燥し、式(I.a)〜(I.f)を有する所望のサリチルアルジミン配位子を90%〜93%の収率で得た。これらの配位子は物理化学的変化を起こすことなくデシケーター中数ヶ月保存できる。
添付の図に示す式(II.a)〜(II.f)を有するシッフ塩基置換ルテニウム鎖体を2工程で調製し、以下の通り精製した。第1の工程において、実施例1に従って調製した式(I.a)〜(I.f)の適切なシッフ塩基のTHF(10ml)中の溶液に、THF(5ml)中のタリウムエトキシドの溶液を室温で滴加した。添加直後、淡黄色の固体が形成し、そして反応混合物を20℃で2時間攪拌した。固体をアルゴン雰囲気下に濾過することにより、定量的収率で該当するサリチルアルジミンタリウム塩が得られ、これは更に精製することなく次の工程において即座に使用した。
THF(5ml)中のカリウムt−ブトキシドの溶液1当量をTHF(10ml)中の
1,3−ビス(2,4,6−トリメチルフェニル)−4,5−ジヒドロイミダゾリウムテトラフルオロボレートの溶液に添加し、反応混合物を室温(20℃)で5分間攪拌した後、カリウムテトラフルオロボレート副生成物を不活性雰囲気下に濾去し、式(III)を有するt−ブトキシル化化合物が定量的収率で形成した。溶媒を蒸発させた後、化合物(III)をトルエン(10ml)に溶解し、更に精製することなく次の工程において即座に使用した。トルエン(10ml)中の実施例2に従って調製した式(II.a)〜(II.f)の1つを有する適切なシッフ塩基置換ルテニウム鎖体の溶液1当量を添加した後、激しく攪拌しながら1時間反応混合物を70〜80℃に加熱した。溶媒を蒸発させた後、固体の残存物をヘキサン(3x10ml)で洗浄し、トルエン/ペンタン混合物から0℃で再結晶させた。その後真空下に乾燥して90%〜95%の範囲の収率で茶色の微結晶性固体として式(IV.a)〜(IV.f)の純粋なシッフ塩基置換ルテニウム鎖体を形成した。
式(V.a)〜(V.f)を有するシッフ塩基置換アレニリデン化合物はトルエン(15ml)中の実施例3に従って調製した式(IV.a)〜(IV.f)の1つを有する適切なシッフ塩基置換ルテニウム鎖体の溶液をトルエン(5ml)中の市販のジフェニルプロパルギルアルコールの溶液の1.2当量に添加し、次に室温(20℃)で17時間反応混合物を攪拌することにより得た。トルエンを真空下に蒸発させ、残存する固体残存物をジクロロメタン/ヘキサン混合物から再結晶し、ヘキサン(3x10ml)で洗浄して80〜90%の範囲の収率で暗茶色の微結晶性固体として所望の化合物を得た。
式(VI.a)〜(VI.f)のシッフ塩基置換インデニリデン化合物はトルエン(15ml)中の実施例2に従って調製した式(II.a)〜(II.f)の1つを有する適切なシッフ塩基置換ルテニウム鎖体の溶液をトルエン(5ml)中の市販のジフェニルプロパルギルアルコールの溶液の1.2当量に添加し、次に室温(20℃)で17時間反応混合物を攪拌することにより得た。トルエンを真空下に蒸発させ、残存する固体残存物をジクロロメタン/ヘキサン混合物から再結晶し、ヘキサン(3x10ml)で洗浄して70%より高い収率で赤茶色の微結晶性固体として所望の化合物を得た。
トルエン(10ml)中の実施例5に従って調製した式(VI.a)〜(VI.f)の1つを有する適切なシッフ塩基置換ルテニウム鎖体の溶液に、トルエン(10ml)中の実施例3の通り調製した式(III)を有するt−ブトキシル化化合物の溶液の1当量を添加した。次に70〜80℃で1時間、反応混合物を激しく攪拌した。溶媒を蒸発させた後、固体の残存物をヘキサン(3x10ml)で洗浄し、ジクロロメタン/ヘキサン混合物から再結晶した。その後真空下に乾燥し、定量的収率で赤茶色の微結晶性固体として式(VII.a)〜(VII.f)の純粋な化合物を得た。
種々の環状オレフィンの開環転移重合を溶媒としてトルエン1ml中において実施し、その際触媒としては実施例4で調製した式(V.a)を有するシッフ塩基置換アレニリデン化合物0.005モルを用いた。以下の表1はオレフィン単量体の名称、オレフィン/触媒のモル比、重合温度T(℃表示)および重合時間t(分表示)を示すものであり、そして更に時間tにおける重合収率を示している。
種々のジエンの閉環転移反応は溶媒として重水素化ベンゼン1ml中で行い(ただし塩酸ジアリルアミンの場合のみ溶媒として重水素化メタノールを使用)、その際、下記を使用した。
− 触媒として実施例4で調製した式(V.a)を有するシッフ塩基置換アレニリデン化合物0.005ミリモル、および、
− ジエン/触媒のモル比100.
以下の表2に使用したジエンの名称、反応温度T(℃表示)、反応時間t(分表示)を示し、また時間tにおける反応収率(%表示)および得られた生成物の名称も示した。
種々のオレフィンの原子転移ラジカル重合を下記に示す温度(℃表示)において下記を使用しながら8時間トルエン1ml中で行った。
− 触媒として、実施例4で調製した式(V.a)を有するシッフ塩基置換アレニリデン室温に有無鎖体0.0116モル、
− 重合開始剤として、エチル−2−メチル−2−ブロモピロピオネート(単量体がメタクリレートの場合)、メチル−2−ブロモプロピオネート(単量体がアクリレートの場合)、1−ブロモシアノエタン(単量体がアクリロニトリルの場合)または(1−ブロモエチル)ベンゼン(単量体がスチレンの場合)、
− [触媒]/[重合開始剤]/[単量体]のモル比1:2:800.
以下の表3は使用したオレフィンの名称、重合温度および重合収率(%表示)を示す。
種々のオレフィンの原子転移ラジカル重合を溶媒として水中において、下記:
− 触媒として、テトラフルオロホウ酸銀1当量であらかじめ処理しておいた実施例4において調製した式(V.a)を有するシッフ塩基置換アレニリデン化合物0.0116モル(より詳細には、化合物(V.a)の上記した量をトルエン1mlおよびトルエン中0.2MのAgBF4溶液56μlに添加し、次にAgClの濁度が観察されるまで20分間攪拌し、これによりクロリドの配位子が抽出されトルエンにより置き換えられているカチオン性ルテニウム鎖体とした)、および、
− 実施例9において既に記載したものと同様の重合開始剤、および、
− [触媒]/[重合開始剤]/[単量体]のモル比1:2:800、
を使用しながら、以下の表に示す温度で、8時間、行った。触媒および重合開始剤をトルエン中に溶解し、トルエン:水の容量比を1:1とした。以下の表4は使用したオレフィンの名称、重合温度および重合収率(%表示)を示す。
種々のビニル単量体の原子転移ラジカル重合および共重合を以下を用いて行った。
− 実施例9において使用したものと同様の重合開始剤、および、
− 触媒として、以前にChang等、Organometallics(1998)17:3460によりオレフィン転移触媒として開示されており、そして、下記式:
アルゴン雰囲気下に行った。触媒0.0117ミリモルを磁気攪拌子の入った3方向ストップコックでキャップされたガラス試験管(真空−窒素サイクル3回により脱気)に入れた。次に単量体および重合開始剤を添加することにより[触媒]/[重合開始剤]/[単量体]のモル比を1/2/800とした。全液体をアルゴン雰囲気下で乾燥シリンジを用いて取り扱った。次に反応混合物を85℃((メタ)アクリレートの場合)または110℃(スチレンの場合)の反応温度で17時間過熱した。冷却後、これをTHF中に希釈し、激しく攪拌しながらn−ヘプタン((メタ)アクリレートの場合)50mlまたはメタノール(スチレンの場合)50mlに注ぎ込んだ。次に沈殿した重合体を濾過し、一夜真空下に乾燥した。
種々のビニル単量体の原子転移ラジカル重合および共重合を溶媒S中で下記を用いて実施した。
− 実施例9において使用したものと同様の重合開始剤、および、
− 触媒として、Tosがトシレート(p−トルエンスルホネート)の略号であり、Tfがトリフレート(トリフルオロメタンスルホネート)の略号である後述するスキームに従
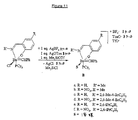
って溶媒Sの存在下において塩で適切な式(A.a)〜(A.f)を有する実施例11のルテニウムカルベン複合体を処理することにより図11に示したスキームに従って得られるカチオン性ルテニウムカルベン鎖体(B.a)〜(B.f)。
種々のビニルオレフィンのへの4塩化炭素の原子転移ラジカル付加を有機溶媒中、触媒として実施例4において調製した式(V.a)を有するシッフ塩基置換アレニリデン化合物を用いながら実施した。該触媒(0.03ミリモル)をトルエン(1ml)に溶解し、その後セプタムを通してトルエン(3ml)中のビニル単量体(9ミリモル)および4塩化炭素(13ミリモル)の卒に添加した。次に反応混合物を17時間65℃に加熱した。以下の表9は試験したビニル単量体の名称および得られた塩素化飽和付加生成物の収率(%表示)を示す。
トルエン(17ml)中の[RuCl2(p−クメン)]2(306mg、0.5ミリモル)の懸濁液に、それぞれ、トリシクロヘキシルホスフィン(0.617g、2.2ミリモル)およびフェニルアセチレンC6H5C≡CH(0.102g、1ミリモル)を添加した。混合物をゆっくり70℃に加熱し、24時間攪拌した。揮発性物質をポンピングすることにより約4mlまで混合物を濃縮した。アセトン10mlを添加し、−78℃まで冷却することにより析出した暗茶色の微結晶性固体を濾過し、真空乾燥した。収率85%で得られたこの固体はプロトンNMRスペクトル分析(CDCl3上30℃で実施)によりCl2Ru{=C=CHC6H5}(PCy3)2であることが特性化され、以下のデータが得られた。
THF(5ml)中の実施例14において得られたジクロロジシクロヘキシルホスフィンビニリデンルテニウム鎖体(3ミリモル)の溶液に実施例2の第1工程の終了時に得られたサチチルアルジミンタリウム塩のTHF(10ml)中の溶液を添加した。反応混合物を4時間20℃で攪拌し、形成した塩化タリウムを濾過して分離した。固体の残存物を−70℃でペンタンから再結晶し、式(IC)を有するシッフ塩基ビニリデンルテニウム鎖体を得た。
後に記載するスキームの6〜17の式および参照番号により識別される環状オレフィンの開環転移重合を以下の操作法に従って実施した。
種々のジエンの閉環転移反応を以下の操作法に従って実施した。10mlのSchlenck試験管中、ジエン0.095ミリモル、メシチレン13.2μl(0.095ミリモル)および実施例15に従って調製したシッフ塩基ビニリデンルテニウム鎖体50μlを重水素化ベンゼン1mlに添加し、そして、70または85℃に攪拌しながら加熱した(以下の表11に記載するとおり)。形成したエチレンを10分間間隔で真空下に除去した。2時間後、溶液を20℃に冷却し、NMR試験管内に注ぎ込んだ。生成物の収率はア
リル性プロトンの組み込みにより1H−NMRで測定する。環状異性体、オリゴマーまたはテロメアの形成は反応混合物のGC−MS分析により区別した。シリカゲルカラム上のフラッシュカラムクロマトグラフィーにより濃縮した反応混合物の精製により反応性生物を同定した(ヘキサン/酢酸エチル=6:1、Rf=0.3)。
体が係留している触媒の調製
全ての反応および操作は従来のSchlenck試験管法を用いることによりアルゴン雰囲気下で行った。アルゴンガスはP2O5(Aldrich、97%)を通して乾燥した。1H−NMRスペクトル(500MHz)はBrukerAM分光分析器上に記録した。化学シフトはppmで表示し、TMSを比較対照化合物として使用した。固相NMRスペクトルはBrukerDSX−300分光光度計を1H−NMRの場合は300.18MHz、13C−NMRの場合は75.49MHz、31P−NMRの場合は121.51MHzおよび29Si−NMRの場合は59.595MHzで操作することにより獲得した。スペクトルは12KHzまでのスピン周波数を与える慣用的な4mmのプローブヘッドを用いてMAS条件下において記録した。均一な触媒の係留はFRA106モジュールを有するラマン分光光度計Bruker Equinox 55により確認した。不均一ハイブリッド触媒の負荷はVarian Liberty ICP/MS分光光度計およびARL9400SequentialXRF分光光度計により測定した。XRDスペクトルはSiemens回折光度計D5000で記録した。元素分析はCarloErbaEA1110装置で実施した。BET分析はFlow prep060脱気装置を有するGeminiマイクロメトリック2360表面積分析器で行った。試料を423°Kで一夜乾燥し、室温に冷却してから吸着させた。空気酸化の可能性のため官能性付与された物質による特別の留意が必要であり、従って、天秤への移動および系の脱気は迅速に行った。窒素等温曲線は77℃で記録した。比表面積をBETプロットの直線部分から求めた。
XRF測定によれば、0.1069ミリモルRu鎖体/g不均一触媒5および0.054ミリモルRu鎖体/g不均一触媒11の負荷が明らかにされる。
実施例18の不均一触媒5および11の両方を使用して溶媒中の種々のオレフィンの開環転移重合を行った。市黒億点およびノルボルネン誘導体をAldrichより購入し、窒素下CaH2から蒸留した後に使用した。市販品等級の溶媒を乾燥し、窒素雰囲気下適切な乾燥剤上で24時間脱酸素処理し、蒸留した後に使用した。典型的なROMP実験において、トルエン中の触媒の懸濁液0.005ミリモルを15ml容の容器に移し、その後トルエン/ジクロロメタン中の単量体を添加した(ノルボルネンは2000当量、シクロオクテンは200当量およびノルボルネン誘導体は800当量)。反応混合物を6時間35℃で攪拌し続けた。触媒を不活性化するため、エチルビニルエーテル/2,6−ジ−t−ブチル−メチルフェノール(BHT)溶液2.5mlを添加し、完全な不活性化が起こるまで溶液を攪拌した。溶液をメタノール50ml(0.1%BHT含有)に注ぎ込み、重合体を析出させ、濾過した。重合体をCHCl3に溶解することにより触媒を濾過した。次に高粘度となるまでCHCl3を真空下に重合体溶液から除去し、その後メタノール100mlを添加することにより重合体を析出させた。次に白色の重合体を濾過紙、一夜真空下に乾燥した。重合体の数および重量平均分子量(MnおよびMw)および多分散性(Mw/Mn)をポリスチレン標準物質を用いたゲル透過クロマトグラフィー(CHCl3、25℃)により測定した。使用したGPC機材はPLゲルカラムを装着したWatersのMaxima820システムである。DSC測定はサーモメカニカル分析器(TMA2940)を使用しながらTA機器DSC−TGA(SDT2960)により行った。形成された重合体の収率[%]を以下の表12に示す。
乾燥した10ml容の容器内に触媒5モル%を計り込み、固体をベンゼン2ml中に懸濁することにより空気中のベンチトップ上で反応を行った。ベンゼン(2ml)中の適切
なジエン基質(0.1ミリモル)の溶液を内標準のドデカンとともに添加した。反応混合物を以下の表14に示す適切な温度で適切な時間攪拌した。生成物の形成およびジエンの消失はガスクロマトグラフィー(GC)でモニタリングし、アリル性メチレンのピークを積分を介して1H−NMRスペクトル分析により再現性試験において確認した(溶媒は重水素化ベンゼンであり内標準は1,3,5−メシチレンとした)。反応混合物のGC分析はまたシクロ異性体、オリゴマーまたはテロメアの形成を区別した。
従来の方法により、全試薬および溶媒を乾燥し、蒸留し、−20℃で窒素下に保存した。典型的なATRP実験においては、実施例18において製造した不均一触媒11の0.0117ミリモルを磁気攪拌子の入った3方向ストップコックでキャップしたガラス管(3回の真空−窒素サイクルにより脱気しておく)内に入れた。次にモル比[触媒]/[重合開始剤]/[単量体]が1:2:800となるようにスチレン(単量体として)および1−ブロモメチルベンゼン(重合開始剤として)を添加した。全液体を乾燥シリンジを用いながらアルゴン下に取り扱った。反応混合物を110℃で17時間加熱し、冷却した後
、THF中に希釈し、激しく攪拌しながらメタノール50ml中に注ぎ込み、その後析出したポリスチレンを吸引濾過した。最後に重合体をCHCl3に溶解することにより触媒を濾別した。次に高粘度となるまでCHCl3を重合体溶液から真空下に除去し、次にメタノール100mlを添加することにより重合体を析出させ、濾別し、15分間真空下に乾燥して分析した。重合体の収率は73%、分子量(Mn)は39,000、そして多分散性指数(Mw/Mn)は1.62であった。
従来の方法により、全試薬および溶媒を乾燥し、蒸留し、−20℃で窒素下に保存した。反応は実施例18の触媒5または11の0.01ミリモルを乾燥した10ml容の容器に計り込み、固体をトルエン2mlで懸濁することにより空気中ベンチトップ上で行った。次にトルエン(1ml)中のアルケン(3ミリモル)、CCl4(4.33ミリモル)およびドデカン(0.083ml)の溶液を添加し、反応混合物を表15に示す適切な反応温度において17時間加熱した。得られた生成物の収率は内標準としてドデカンを用いた反応混合物のGC分析により求め、以下の表5に示した。
典型的なビニル化実験において、カルボン酸(ギ酸または酢酸)4.4ミリモル、アルキン(フェニルアセチレンまたは1,7−オクタジイン)4.4ミリモルおよび実施例18の触媒5または110.04ミリモルをトルエン3mlの入った15ml容のガラス容器に移した。次に反応混合物を不活性雰囲気下100℃で4時間加熱した。総収率はフェニルアセチレンまたは1,7−オクタジインのVC≡Cの強度低下を追跡し、検量線を用いながら、ラマン分光分析により測定した。得られた生成物の立体配座は単量体の種々のフラグメント化を用いながらGC/MSにより測定した。GC/MS測定により以下に報告するもの以外の生成物の形成を区別した。
)。1,7−オクタジインを基質として使用した場合は、両方のカルボン酸の添加により、使用した触媒系にかかわらず三重結合への酸のレジオ選択的および立体選択的なアンチMarkovnikov付加に相当する(E)−アルカン−1−エニルエステルの選択的形成が起こった。しかしながら総収率は使用した触媒およびカルボン酸の種類に依存している。(E)−アルカン−1−エニルエステルの形成のほかに、低い比率の(Z)−アルカン−1−エニルエステル、Markovnikov付加産物およびジ置換エノールエステルも得られた。アルキンとしてフェニルアセチレンを使用した場合、総収率は1,7−オクタジインよりも明らかに高値となった。後者はビニル化過程において完全に異なる選択性を誘導し、即ち、不均一触媒はMarkovnikov付加産物の形成のために高い水準の反応性をもたらした。
本合成は図10に示すスキームに従って進行させた。式(2.a−f)を有するシッフ塩基置換ルテニウム鎖体を以下のとおり2工程において調製し、精製した。第1の工程においては、実施例1に従って調製した式(2.a−f)の適切なシッフ塩基のTHF(10ml)中の溶液にTHF(5ml)中のタリウムエトキシドの溶液を室温で滴加した。添加終了直後、淡黄色固体が形成し、反応混合物を20℃で2時間攪拌した。アルゴン雰囲気下に固体を濾過し、定量的収率で得られた該当するサリシルアルジミンタリウム塩を更に精製することなく即座に次の工程において使用した。
a−fを得た。該鎖体を更に核磁気共鳴(NMR)および赤外スペクトル分析(IR)で特性化し、その分析結果は以下のとおりとなった。
H5.21、N1.72;測定値:C53.23、H5.24、N1.74。
ジエチルアリルアミノエチルホスホネート0.60g(2.9ミリモル)を乾燥ジエチルエーテル50mlに溶解し、そしてトリエチルアミン1.17g(11.6ミリモル)を添加した。室温で15分間攪拌した後、アリルブロミド1.40gを滴加した。混合物を4日間還流した。水50mlを混合物に添加し、その後CH2Cl250mlで3回益した。有機層を合わせMgSO4上に乾燥した。MgSO4を濾過し、溶媒を蒸発させ、得られた生成物を高真空蒸留により更に精製し、0.1mbarの低圧力下において65℃の沸点を有するジエチルジアリルアミノメチルホスホネート0.6g(2.4ミリモル、84%収率)を得た。この生成物は以下のスペクトルにより更に特性化された。
− 質量スペクトル分析:247(M+,3)、232(M+−15.7)、206(30)、110(M+−PO(OEt)2、100)、81(14)、68(21)および41(26)。
実施例25において調製したジエチルジアリルアミノメチルホスホネート0.1g(0.41ミリモル)をクロロベンゼン2mlに溶解し、次に実施例24において調製した2
金属ルテニウム鎖体3.e0.014g(0.02ミリモル)を添加し、そして混合物を60℃で16時間攪拌した。カラムクロマトグラフィーによりクロロベンゼン蒸発後に触媒を除去し、ジエチル1H−ピロール−1−イルメチルホスホネート0.04g(0.18ミリモル、収率45%)を得た。この生成物は以下のスペクトルにより更に特性化された。
− 質量スペクトル分析:217(M+,57)、202(M+−15.17)、174(13)、107(29)、80(M+−PO(OEt)2、100)および53(14)。
塩酸グリシンメチルエステル1.5g(11.9ミリモル)を乾燥THF100mlに添加し、その後トリエチルアミン3.61g(35.8ミリモル)を添加した。室温で15分間攪拌した後、アリルブロミド4.33g(35.8ミリモル)を滴加し、そして混合物を16時間還流した。2N塩酸100mlを添加し、次にジエチルエーテル100mlで益した。水相を酸抽出後にK2CO3でアルカリ化し、そしてCH2Cl2(100ml3回)で抽出した。有機層をMgSO4上に乾燥し溶媒を蒸発させた後、生成物を更にカラムクロマトグラフィーで精製し、100%の選択性で0.78g(5.75ミリモル、収率49%)のジアリルグリシンメチルエステルを得た。この生成物は以下のスペクトルにより更に特性化された。
− 質量スペクトル分析:169(M+,−41.25)、110(M+−COOMe、100)および41(CH2=CH−CH2+、28)。
実施例27で調製したジアリルグリシンメチルエステル0.22g(1.3ミリモル)をクロロベンゼン3mlに溶解し、その後実施例24で調製した2金属ルテニウム鎖体3.e0.046g(0.064ミリモル)を添加した。混合物を65℃で16時間攪拌した。クロロベンゼン蒸発後に触媒をカラムクロマトグラフィーにより除去し、100%の選択性でメチル1H−ピロール−1−イルアセテート0.05g(0.36ミリモル、収
率28%)を得た。この生成物は以下のスペクトルにより更に特性化された。
− 質量スペクトル分析:139(M+,63)および80(M+−PO(OEt)2、100)。
Claims (7)
- ルテニウムおよびオスミウムからなる群より選ばれる金属、カルベン配位子、多座配位子、および1個以上の他の配位子を含む5配位金属錯体、その塩、その溶媒和物、またはそのエナンチオマーであって、
a)該カルベン配位子が、下記式
で表わされるカルベン配位子であり、
b)該多座配位子が、金属の配位に使用される2個のヘテロ原子を含むものであって、そのうちの少なくとも1個が窒素原子である多座配位子であり、
c)該他の配位子の少なくとも1個が、pKaが少なくとも15である制限(コンストレイント)立体障害配位子であり、
i)該制限立体障害配位子が、非イオン性プロホスファトラン超強塩基またはN−複素環カルベンであって、
ii)該N−複素環カルベンが、イミダゾール−2−イリデン、ジヒドロイミダゾール−2−イリデン、オキサゾール−2−イリデン、チアゾール−5−イリデン、チアゾール−2−イリデン、ビス(イミダゾリン−2−イリデン)、ビス(イミダゾリジン−2−イリデン)、ピロリリデン、ピラゾリリデン、ジヒドロピロリリデン、およびピロリリジニリデンからなる群より選択されるN−複素環カルベンであり、該N−複素環カルベンの複素環は、ベンゼン環に縮合したベンゾ縮合誘導体であってもよく、並びに、
iii)前記の非イオン性プロホスファトラン超強塩基またはN−複素環カルベンの1以上の水素原子が制限立体障害を与える基で置換されている
ものであり、
d)該他の配位子が、該制限立体障害配位子以外の配位子を含む場合、該配位子は、アニオン性配位子または溶媒である、
ことを特徴とする5配位金属錯体、その塩、その溶媒和物、またはそのエナンチオマー。 - 前記他の配位子の1個が、アニオン性配位子であるか、または、前記他の配位子の1個が溶媒であり、該金属錯体がアニオンと会合したカチオン性種である請求項1に記載の5配位金属錯体。
- 該5配位金属錯体が、下記一般式(IA)および(IB)
− Mは、ルテニウムおよびオスミウムからなる群より選ばれる遷移金属であり;
− Zは、酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は、各々、水素原子、C1−6アルキル、C3−10シクロアルキル、C1−6アルキル−C1−6アルコキシシリル、C1−6アルキル−アリールオキシシリル、C1−6アルキル−C3−10シクロアルコキシシリル、アリールおよびヘテロアリールからなる群より選択されるか、または、
R’’およびR’’’は、一緒になってアリール基またはヘテロアリール基を形成し、
それぞれの基は、場合により、ハロゲン原子、C1−6アルキル、C1−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、C1−6アルキル−C1−6アルコキシシリル、C1−6アルキル−アリールオキシシリル、C1−6アルキル−C3−10シクロアルキルシリル、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R5の1個以上で置換されており;
− R’は、一般式(IA)を有する化合物中に含まれる場合は、R’’、R’’’およびR’’’’と同じに定義され、一般式(IB)を有する化合物中に含まれる場合は、C1−6アルキレンおよびC3−8シクロアルキレンからなる群より選択され、該アルキレン基またはシクロアルキレン基は、場合により置換基R5の1個以上で置換されており;
− R1は、pKaが少なくとも15である制限立体障害基であり、
該制限立体障害配位子が、非イオン性プロホスファトラン超強塩基またはN−複素環カルベンであって、
該N−複素環カルベンが、イミダゾール−2−イリデン、ジヒドロイミダゾール−2−イリデン、オキサゾール−2−イリデン、チアゾール−5−イリデン、チアゾール−2−イリデン、ビス(イミダゾリン−2−イリデン)、ビス(イミダゾリジン−2−イリデン)、ピロリリデン、ピラゾリリデン、ジヒドロピロリリデン、およびピロリリジニリデンからなる群より選択されるN−複素環カルベンであり、該N−複素環カルベンの複素環は、ベンゼン環に縮合したベンゾ縮合誘導体であってもよく、
前記の非イオン性プロホスファトラン超強塩基またはN−複素環カルベンの1以上の水素原子が制限立体障害を与える基で置換されている
ものであり;
− R2は、アニオン性配位子または溶媒であり、R2が、溶媒である場合は、錯体は、アニオンに会合しており;
− R3およびR4は、各々、水素原子、または、C1−20アルキル、C2−20アルケニル、C2−20アルキニル、C1−20カルボキシレート、C1−20アルコキシ、C2−20アルケニルオキシ、C2−20アルキニルオキシ、アリール、アリールオキシ、C1−20アルコキシカルボニル、C1−8アルキルチオ、C1−20アルキルスルホニル、C1−20アルキルスルフィニル、C1−20アルキルスルホネート、アリールスルホネート、C1−20アルキルホスホネート、アリールホスホネート、C1−20アルキルアンモニウム、およびアリールアンモニウムからなる群より選択される基であり;
− R’並びにR3およびR4の一方は、相互に結合して2座の配位子を形成してもよく;
− R’’’およびR’’’’は、相互に結合して窒素、リン、砒素およびアンチモンからなる群より選択されるヘテロ原子を含む脂肪族の環系を形成してもよく;
− R3およびR4は、一緒になって縮合芳香族環系を形成してもよく、
− yは、MとR3およびR4とを担持した炭素原子との間のsp2炭素原子の数を示し、かつ、0〜3の整数である、
ことを特徴とする請求項1または2に記載の5配位金属錯体、その塩、その溶媒和物、またはそのエナンチオマー。 - R2が、C1−20アルキル、C2−20アルケニル、C2−20アルキニル、C1−20カルボキシレート、C1−20アルコキシ、C2−20アルケニルオキシ、C2−20アルキニルオキシ、アリール、アリールオキシ、C1−20アルコキシカルボニル、C1−8アルキルチオ、C1−20アルキルスルホニル、C1−20アルキルスルフィニル、C1−20アルキルスルホネート、アリールスルホネート、C1−20アルキルホスホネート、アリールホスホネート、C1−20アルキルアンモニウム、アリールアンモニウム、ハロゲン原子およびシアノからなる群より選択されるものである請求項3に記載の5配位金属錯体。
- 下記一般式(IIIA)または(IIIB)
− Mは、ルテニウムおよびオスミウムからなる群より選ばれる遷移金属であり;
− Zは、酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は、各々、水素原子、C1−6アルキル、C3−8シクロアルキル、アリールおよびヘテロアリールからなる群より選択されるか、または、R’’およびR’’’は、一緒になってアリール基またはヘテロアリール基を形成し、それぞれの基は、場合により、ハロゲン原子、C1−6アルキル、C1−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R5の1個以上で置換されており;
− R’は、一般式(IIIA)を有する化合物中に含まれる場合は、R’’、R’’’およびR’’’’と同じに定義され、または、一般式(IIIB)を有する化合物中に含まれる場合は、C1−6アルキレンおよびC3−8シクロアルキレンからなる群より選択され、前記アルキレンまたはシクロアルキレン基は、場合により置換基R5の1個以上で置換されており;
− R1は、pKaが少なくとも15である制限立体障害基であり、
該制限立体障害配位子が非イオン性プロホスファトラン超強塩基またはN−複素環カルベンであって、
該N−複素環カルベンが、イミダゾール−2−イリデン、ジヒドロイミダゾール−2−イリデン、オキサゾール−2−イリデン、チアゾール−5−イリデン、チアゾール−2−イリデン、ビス(イミダゾリン−2−イリデン)、ビス(イミダゾリジン−2−イリデン)、ピロリリデン、ピラゾリリデン、ジヒドロピロリリデン、およびピロリリジニリデンからなる群より選択されるN−複素環カルベンであり、該N−複素環カルベンの複素環は、ベンゼン環に縮合したベンゾ縮合誘導体であってもよく、
前記の非イオン性プロホスファトラン超強塩基またはN−複素環カルベンの1以上の水素原子が制限立体障害を与える基で置換されている
ものであり;
− R2は、アニオン性配位子である、
ことを特徴とする4配位金属錯体、その塩、その溶媒和物、またはそのエナンチオマー。 - 下記一般式(IIA)または(IIB)
− Mは、ルテニウムおよびオスミウムからなる群より選ばれる遷移金属であり;
− Zは、酸素、イオウ、セレン、NR’’’’、PR’’’’、AsR’’’’およびSbR’’’’からなる群より選択され;
− R’’、R’’’およびR’’’’は、各々、水素原子、C1−6アルキル、C3−8シクロアルキル、アリールおよびヘテロアリールからなる群より選択され、前記各基は、場合により、ハロゲン原子、C1−6アルキル、C1−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R5の1個以上で置換されているか、または、R’’およびR’’’は、一緒になってアリール基またはヘテロアリール基を形成し、該基は、臭素、C2−6アルキル、C2−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より選択される置換基R5の1個で置換されているか、または、ハロゲン原子、C1−6アルキル、C1−6アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R5の2個以上で置換されており;
− R’は、一般式(IIA)を有する化合物中に含まれる場合は、R’’、R’’’およびR’’’’と同じに定義され、または、一般式(IIB)を有する化合物中に含まれる場合は、C1−6アルキレンおよびC3−8シクロアルキレンからなる群より選択され、該アルキレンまたはシクロアルキレン基は、場合により、ハロゲン原子、C 1−6 アルキル、C 1−6 アルコキシ、アリール、アルキルスルホネート、アリールスルホネート、アルキルホスホネート、アリールホスホネート、アルキルアンモニウムおよびアリールアンモニウムからなる群より各々独立して選択される置換基R5の1個以上で置換されており;
− R2は、アニオン性配位子であり;
− R6は、芳香族および不飽和の脂環族基であって、該基は、1個以上のC1−6アルキル基で場合により置換されたものである、
ことを特徴とする4配位金属錯体、その塩、その溶媒和物、またはそのエナンチオマー。 - (a)請求項1乃至4のいずれか1項に記載の触媒活性5配位金属錯体、および、
(b)該触媒活性5配位金属錯体(a)を支持するのに適する量の担体、
を含む不均一触媒反応において使用するための支持された触媒。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP02075250A EP1329455A1 (en) | 2002-01-22 | 2002-01-22 | Metal carbene complexes, methods and intermediates for making them and their use in metathesis reactions |
| US34995602P | 2002-02-01 | 2002-02-01 | |
| PCT/BE2003/000008 WO2003062253A1 (en) | 2002-01-22 | 2003-01-22 | Metal complexes for use in metathesis |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009218735A Division JP5100728B2 (ja) | 2002-01-22 | 2009-09-24 | メタセシスに使用される金属錯体 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2005515260A JP2005515260A (ja) | 2005-05-26 |
| JP2005515260A5 JP2005515260A5 (ja) | 2006-01-12 |
| JP4477879B2 true JP4477879B2 (ja) | 2010-06-09 |
Family
ID=27614617
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003562130A Expired - Fee Related JP4477879B2 (ja) | 2002-01-22 | 2003-01-22 | 複分解に使用される金属錯体 |
| JP2009218735A Expired - Fee Related JP5100728B2 (ja) | 2002-01-22 | 2009-09-24 | メタセシスに使用される金属錯体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009218735A Expired - Fee Related JP5100728B2 (ja) | 2002-01-22 | 2009-09-24 | メタセシスに使用される金属錯体 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US7687635B2 (ja) |
| EP (2) | EP1743899B1 (ja) |
| JP (2) | JP4477879B2 (ja) |
| AT (2) | ATE429437T1 (ja) |
| AU (1) | AU2003236511B2 (ja) |
| CA (1) | CA2473029A1 (ja) |
| DE (2) | DE60310521T2 (ja) |
| DK (2) | DK1468004T3 (ja) |
| ES (2) | ES2279117T3 (ja) |
| WO (1) | WO2003062253A1 (ja) |
| ZA (1) | ZA200405685B (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010077128A (ja) * | 2002-01-22 | 2010-04-08 | Telene Sas | メタセシスに使用される金属錯体 |
Families Citing this family (96)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005035121A2 (en) * | 2003-10-16 | 2005-04-21 | Universiteit Gent | Schiff base metal complexes for use as catalysts in organic synthesis |
| DE102004002178A1 (de) * | 2004-01-15 | 2005-08-11 | Ivoclar Vivadent Ag | Dentalmeterialien auf der Basis von RÖMP-Kompositen |
| ATE512945T1 (de) * | 2004-02-26 | 2011-07-15 | Telene Sas | Metallkomplexe und deren verwendung in der olefinmetathese und atom- oder gruppenübertragungsreaktionen |
| US20070185343A1 (en) * | 2004-02-26 | 2007-08-09 | Universiteit Gent | Metal complexes for use in olefin metathesis and atom group transfer reactions |
| JP2006016606A (ja) * | 2004-05-31 | 2006-01-19 | Nippon Zeon Co Ltd | 環状オレフィンの付加重合用触媒、およびこれを用いた環状オレフィン付加重合体の製造方法 |
| DE102004039277A1 (de) * | 2004-08-13 | 2006-02-23 | Merck Patent Gmbh | Am Zentralatom substituierte, immoblisierbare Ruthenium(II)-Katalysatoren, Verfahren zu deren Herstellung und Verwendung |
| WO2007022945A2 (en) * | 2005-08-22 | 2007-03-01 | Viacatt N.V. | Multicoordinated metal complexes for use in metathesis reactions |
| GB0517137D0 (en) | 2005-08-22 | 2005-09-28 | Viacatt N V | Multicoordinated metal complexes for use in metalthesis reactions |
| EP1973656B1 (en) * | 2006-01-19 | 2012-05-16 | Agency for Science, Technology and Research | Heterogeneous chiral catalyst |
| US8592336B2 (en) | 2006-04-11 | 2013-11-26 | Agency For Science, Technology And Research | Catalysts for ring-closing metathesis |
| JP5612304B2 (ja) * | 2006-04-11 | 2014-10-22 | エージェンシー フォー サイエンス, テクノロジー アンド リサーチ | 閉環メタセシスのための触媒 |
| CN100465195C (zh) * | 2006-04-29 | 2009-03-04 | 中国科学院长春应用化学研究所 | 一种β-羟基丙烯亚胺钒烯烃聚合催化剂及制备方法和应用 |
| CN100424100C (zh) * | 2006-05-25 | 2008-10-08 | 中国科学院长春应用化学研究所 | 一种β-酮亚胺钒烯烃聚合催化剂及制备方法和应用 |
| CN101594937B (zh) * | 2006-11-21 | 2014-04-30 | 加州理工学院 | 含有亚噻唑-2-基配体的烯烃复分解反应引发剂 |
| WO2008067443A1 (en) * | 2006-11-29 | 2008-06-05 | Board Of Governors For Higher Education, | Aerobic oxidative coupling for the formation biaryls |
| KR101015435B1 (ko) * | 2006-12-05 | 2011-02-22 | 주식회사 엘지화학 | 중합체 제조방법 |
| FR2910004A1 (fr) * | 2006-12-14 | 2008-06-20 | Rhodia Recherches & Tech | Procede d'oligomerisation et/ou polymerisation du composes insatures |
| US8148287B2 (en) * | 2007-03-22 | 2012-04-03 | Agency For Science, Technology And Research | Catalyst immobilization on siliceous mesocellular foam via click chemistry |
| CN102027001A (zh) * | 2007-06-20 | 2011-04-20 | 新加坡科技研究局 | N-杂环卡宾金属环催化剂和方法 |
| WO2009002726A1 (en) * | 2007-06-25 | 2008-12-31 | Sun Chemical Corporation | Process for preparation of oligomeric or polymeric compounds using selective michael addition |
| WO2009009597A1 (en) * | 2007-07-09 | 2009-01-15 | The Regents Of The University Of California | Water soluble olefin metathesis |
| US8263712B2 (en) | 2007-09-04 | 2012-09-11 | Exxonmobil Research And Engineering Company | Production of elastomeric functionalized olefin polymers |
| EP2042537B1 (en) * | 2007-09-28 | 2014-05-14 | Rimtec Corporation | Polycycloolefin (PCO) thermoset assembly and process for its preparation |
| WO2009085040A1 (en) * | 2007-12-27 | 2009-07-09 | Dcb-Usa Llc | Protein kinase inhibitors |
| US8012900B2 (en) | 2007-12-28 | 2011-09-06 | Chevron Phillips Chemical Company, L.P. | Nano-linked metallocene catalyst compositions and their polymer products |
| US8080681B2 (en) | 2007-12-28 | 2011-12-20 | Chevron Phillips Chemical Company Lp | Nano-linked metallocene catalyst compositions and their polymer products |
| US7863210B2 (en) | 2007-12-28 | 2011-01-04 | Chevron Phillips Chemical Company Lp | Nano-linked metallocene catalyst compositions and their polymer products |
| DE102009017498A1 (de) | 2009-04-16 | 2010-10-28 | Süd-Chemie AG | Verwendung einer Katalysatorzusammensetzung zur Olefinmetathese in der Gasphase und Verfahren zur Olefinmetathese in der Gasphase |
| US20120035331A1 (en) * | 2009-04-28 | 2012-02-09 | Korea Institute Of Science And Technology | Polyalkylthiophene block copolymer and a method of preparing the same through a ring-opening metathesis polymerization reaction |
| US7919639B2 (en) | 2009-06-23 | 2011-04-05 | Chevron Phillips Chemical Company Lp | Nano-linked heteronuclear metallocene catalyst compositions and their polymer products |
| EP2280017B1 (en) * | 2009-07-21 | 2013-01-02 | Rimtec Corporation | Catalytic complex for olefin metathesis reactions, process for the preparation thereof and use thereof |
| US20110263870A1 (en) * | 2010-04-23 | 2011-10-27 | Helvetica Industries (P) Limited | Novel pyrrole derivatives and their synthesis |
| SG188274A1 (en) | 2010-08-23 | 2013-04-30 | Materia Inc | Vartm flow modifications for low viscosity resin systems |
| JP5738097B2 (ja) * | 2010-09-10 | 2015-06-17 | 昭和電工株式会社 | ノルボルネン系重合体の製造方法 |
| EP2620483B1 (en) | 2010-09-22 | 2016-02-10 | Zeon Corporation | Adhesive film for organic electrolyte accumulator devices |
| US8937207B2 (en) * | 2010-12-22 | 2015-01-20 | Richard Dehn | Use of supported ruthenium-carbene complexes in continuously operated reactors |
| US20120289617A1 (en) * | 2011-05-10 | 2012-11-15 | Saudi Arabian Oil Company | Hybrid Catalyst for Olefin Metathesis |
| KR20140047659A (ko) | 2011-06-17 | 2014-04-22 | 마터리아 인코포레이티드 | 올레핀 복분해 조성물을 위한 접착 촉진제 및 겔-개질제 |
| JP5916855B2 (ja) | 2011-07-12 | 2016-05-11 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | シクロヘプテンの製造法 |
| US8993819B2 (en) | 2011-07-12 | 2015-03-31 | Basf Se | Process for preparing cycloheptene |
| JP6012055B2 (ja) | 2011-09-07 | 2016-10-25 | ダウ コーニング コーポレーションDow Corning Corporation | チタン含有錯体及び縮合反応触媒、該触媒の調製方法、及び該触媒を含有する組成物 |
| EP2753663B1 (en) | 2011-09-07 | 2020-01-08 | Dow Silicones Corporation | Zirconium containing complex and condensation reaction catalysts, methods for preparing the catalysts, and compositions containing the catalysts |
| US9139699B2 (en) | 2012-10-04 | 2015-09-22 | Dow Corning Corporation | Metal containing condensation reaction catalysts, methods for preparing the catalysts, and compositions containing the catalysts |
| JP6166266B2 (ja) | 2011-10-04 | 2017-07-19 | ダウ コーニング コーポレーションDow Corning Corporation | 鉄(iii)含有の錯体及び縮合反応触媒、該触媒を調製する方法、並びに該触媒を含む組成物 |
| JP6145407B2 (ja) * | 2011-11-18 | 2017-06-14 | 株式会社Adeka | 新規化合物及びこの新規化合物を担持した担持体 |
| GB201204715D0 (en) | 2012-03-18 | 2012-05-02 | Croda Int Plc | Metathesis of olefins using ruthenium-based catalytic complexes |
| MX356142B (es) | 2012-06-13 | 2018-05-16 | Basf Se | Metodo para producir cetonas macrociclicas. |
| HUE028176T2 (en) | 2012-06-29 | 2016-12-28 | Apeiron Synthesis Sa | Metal complexes, their use, and methods for performing metathesis reactions |
| EP2695901B1 (de) | 2012-08-10 | 2016-09-14 | Basf Se | Aliphatische langkettige Polykondensate |
| EP2902428B1 (en) | 2012-09-26 | 2020-08-12 | Rimtec Corporation | Polymerizable composition and method for producing resin molded article |
| TWI485145B (zh) | 2012-10-26 | 2015-05-21 | Ind Tech Res Inst | P型有機半導體材料與光電元件 |
| US9527982B2 (en) | 2012-12-19 | 2016-12-27 | Materia, Inc. | Storage stable adhesion promoter compositions for cyclic olefin resin compositions |
| US9598531B2 (en) | 2013-02-27 | 2017-03-21 | Materia, Inc. | Olefin metathesis catalyst compositions comprising at least two metal carbene olefin metathesis catalysts |
| WO2014134333A1 (en) | 2013-02-27 | 2014-09-04 | Materia, Inc. | Metal carbene olefin metathesis two catalyst composition |
| BR112015022516A2 (pt) | 2013-03-15 | 2017-07-18 | Materia Inc | revestimento no molde de polímeros de romp |
| BR112015025850B1 (pt) | 2013-04-09 | 2021-11-03 | Materia, Inc | Método para produzir pelo menos um produto de metátese cruzada |
| MY173809A (en) | 2013-06-24 | 2020-02-24 | Materia Inc | Thermal insulation |
| MY184011A (en) | 2013-07-03 | 2021-03-17 | Materia Inc | Liquid molding compositions |
| US9890239B2 (en) * | 2013-09-04 | 2018-02-13 | California Institute Of Technology | Functionalized linear and cyclic polyolefins |
| KR20160061362A (ko) * | 2013-09-27 | 2016-05-31 | 림텍 가부시키가이샤 | 노르보르넨계 가교 중합체 및 그 제조 방법 |
| CN105829412B (zh) | 2013-12-26 | 2019-06-11 | Rimtec株式会社 | 复合成型体的制造方法 |
| CA2940338C (en) | 2014-02-27 | 2023-02-21 | Materia, Inc. | Adhesion promoter compositions for cyclic olefin resin compositions |
| EP3164409B1 (en) * | 2014-07-03 | 2021-09-01 | Guang Ming Innovation Company (Wuhan) | Group 8 transition metal catalysts and method for making same and process for use of same in metathesis reaction |
| CN106573998B (zh) * | 2014-07-24 | 2021-10-12 | 日本聚乙烯株式会社 | 烯烃聚合催化剂和烯烃聚合物的制造方法 |
| US9856352B2 (en) | 2014-08-07 | 2018-01-02 | Ppg Industries Ohio, Inc. | Glass fiber sizing compositions, sized glass fibers, and polyolefin composites |
| PL2982709T3 (pl) | 2014-08-07 | 2017-12-29 | Telene Sas | Kompozycja utwardzalna i wytwór formowany zawierający kompozycję |
| TWI688609B (zh) | 2014-11-13 | 2020-03-21 | 美商道康寧公司 | 含硫聚有機矽氧烷組成物及相關態樣 |
| JP6787907B2 (ja) | 2015-02-12 | 2020-11-18 | マテリア, インコーポレイテッド | 機能性エラストマーを含む環式オレフィン樹脂組成物 |
| CA2975259C (en) | 2015-02-14 | 2023-03-14 | Materia, Inc. | Romp polymers having improved resistance to hydrocarbon fluids |
| EP3153227A1 (de) * | 2015-10-07 | 2017-04-12 | Evonik Degussa GmbH | Verfahren zur herstellung von polyalkenameren für verpackungsanwendungen |
| EP3202813A1 (en) | 2016-02-05 | 2017-08-09 | Telene SAS | Curable composition and molded article comprising the composition |
| EP3411218A1 (en) | 2016-02-07 | 2018-12-12 | Stratasys Ltd. | Three-dimensional printing combining ring-opening metathesis polymerization and free radical polymerization |
| KR20180104314A (ko) | 2016-02-10 | 2018-09-20 | 림텍 가부시키가이샤 | 중합성 조성물 및 복합 재료 |
| US11118004B2 (en) | 2016-04-26 | 2021-09-14 | Stratasys Ltd. | Three-dimensional inkjet printing using ring-opening metathesis polymerization |
| JPWO2017204051A1 (ja) | 2016-05-27 | 2019-03-22 | Rimtec株式会社 | 複合材料成形体の製造方法 |
| CN109982995B (zh) | 2016-09-23 | 2022-09-30 | 优美科股份公司及两合公司 | 氨基酸和氨基酸衍生物的制备 |
| JP6794311B2 (ja) | 2017-05-11 | 2020-12-02 | 公益財団法人鉄道総合技術研究所 | 超電導コイル装置及びその製造方法 |
| US10245583B1 (en) * | 2017-09-12 | 2019-04-02 | Chevron Phillips Chemical Company, Lp | Use of charge-containing molecules linked with covalent bonds to enhance acetylene hydrogenation catalysts |
| CN112004598A (zh) | 2018-04-20 | 2020-11-27 | 阿朗新科德国有限责任公司 | 氢化催化剂组合物及其用于氢化丁腈橡胶的用途 |
| CN108559083B (zh) * | 2018-04-26 | 2020-07-14 | 大连理工大学 | 一种结晶性聚单硫代碳酸酯的制备方法 |
| US20210221934A1 (en) | 2018-06-07 | 2021-07-22 | Rimtec Corporation | Composite material and molded composite material |
| CN109046463B (zh) * | 2018-08-16 | 2021-05-04 | 中山大学 | 双齿氮杂卡宾锰催化剂及其制备方法和烷基化合成应用 |
| CN111068774B (zh) * | 2018-10-18 | 2022-11-04 | 中国石油化工股份有限公司 | 2,6-萘二甲酸合成所用催化剂和其应用 |
| WO2020218242A1 (ja) | 2019-04-23 | 2020-10-29 | Rimtec株式会社 | シクロオレフィン樹脂加飾成形品の製造方法 |
| EP4011613A4 (en) | 2019-08-06 | 2023-08-09 | RIMTEC Corporation | POLYMERIZABLE COMPOSITION, CYCLOOLEFIN-BASED POLYMER AND METAL/RESIN COMPOSITE |
| EP4140570A1 (en) | 2020-04-24 | 2023-03-01 | RIMTEC Corporation | Method for producing polymerization-reactive liquid formulation |
| CN115867591A (zh) | 2020-08-03 | 2023-03-28 | Rimtec株式会社 | 环烯烃系树脂固化物 |
| CN116157262A (zh) | 2020-08-28 | 2023-05-23 | Rimtec株式会社 | 阻氧性环烯烃系树脂固化物 |
| CN112250843B (zh) * | 2020-10-16 | 2023-05-30 | 湘潭大学 | 四种D-A’-(π-A)2型聚合烷基化水杨醛席夫碱衍生物合金属配合物及其制备方法与用途 |
| EP4257627A1 (en) | 2020-12-03 | 2023-10-11 | RIMTEC Corporation | Polymerizable composition and resin-impregnated superconducting coil |
| EP4331836A1 (en) | 2021-04-30 | 2024-03-06 | RIMTEC Corporation | Metal-resin layered body and method for manufacturing metal-resin layered body |
| CN115518689B (zh) * | 2021-06-24 | 2023-10-31 | 中国石油化工股份有限公司 | 一种环氧烷烃水合制二醇催化剂及其制备方法和应用 |
| US11780864B2 (en) * | 2021-07-07 | 2023-10-10 | The Hong Kong University Of Science And Technology | Rhenium(V) alkylidyne complexes and methods of use and preparation thereof |
| CN113666956B (zh) * | 2021-08-25 | 2023-04-25 | 上海橡实化学有限公司 | 一种水杨醛亚胺硅烷偶联剂及其制备方法和应用 |
| WO2023220706A2 (en) * | 2022-05-12 | 2023-11-16 | Yale University | Catalyst, system and method for mineralization of organic pollutants |
| CN116970148A (zh) * | 2023-06-15 | 2023-10-31 | 天津大学 | 一种高性能宽加工窗口的环烯烃共聚物及其制备方法 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4035032C1 (ja) | 1990-11-03 | 1992-04-30 | Degussa Ag, 6000 Frankfurt, De | |
| EP0563730A3 (en) * | 1992-03-28 | 1994-07-27 | Hoechst Ag | Alkenylaminoalkylene phosphonic acid esters and process for the preparation of copolymers comprising alkenylaminoalkylene phosphonates and ethylenic unsaturated compounds |
| US5763548A (en) * | 1995-03-31 | 1998-06-09 | Carnegie-Mellon University | (Co)polymers and a novel polymerization process based on atom (or group) transfer radical polymerization |
| US6541580B1 (en) * | 1995-03-31 | 2003-04-01 | Carnegie Mellon University | Atom or group transfer radical polymerization |
| US6410664B1 (en) * | 1997-03-24 | 2002-06-25 | Cryovac, Inc. | Catalyst compositions and processes for olefin polymers and copolymers |
| US6284852B1 (en) * | 1997-10-30 | 2001-09-04 | California Institute Of Technology | Acid activation of ruthenium metathesis catalysts and living ROMP metathesis polymerization in water |
| DE19748468A1 (de) | 1997-11-03 | 1999-05-06 | Hoechst Ag | Beschichtete Gestricke als katalytische Füllungen für Destillationskolonnen |
| US5977393A (en) * | 1997-11-21 | 1999-11-02 | California Institute Of Technology | Schiff base derivatives of ruthenium and osmium olefin metathesis catalysts |
| US6696597B2 (en) | 1998-09-01 | 2004-02-24 | Tilliechem, Inc. | Metathesis syntheses of pheromones or their components |
| JP2002020417A (ja) | 2000-07-04 | 2002-01-23 | Mitsui Chemicals Inc | オレフィンの重合方法 |
| EP1743899B1 (en) * | 2002-01-22 | 2009-04-22 | Telene SAS | Metal complexes for use in metathesis, atom transfer radical reactions, addition polymerisation and vinylation reactions, methods and intermediates for making them |
| WO2005035121A2 (en) | 2003-10-16 | 2005-04-21 | Universiteit Gent | Schiff base metal complexes for use as catalysts in organic synthesis |
| US20070185343A1 (en) * | 2004-02-26 | 2007-08-09 | Universiteit Gent | Metal complexes for use in olefin metathesis and atom group transfer reactions |
| ATE512945T1 (de) | 2004-02-26 | 2011-07-15 | Telene Sas | Metallkomplexe und deren verwendung in der olefinmetathese und atom- oder gruppenübertragungsreaktionen |
| GB0517137D0 (en) * | 2005-08-22 | 2005-09-28 | Viacatt N V | Multicoordinated metal complexes for use in metalthesis reactions |
-
2003
- 2003-01-22 EP EP06020387A patent/EP1743899B1/en not_active Expired - Lifetime
- 2003-01-22 ES ES03731638T patent/ES2279117T3/es not_active Expired - Lifetime
- 2003-01-22 DK DK03731638T patent/DK1468004T3/da active
- 2003-01-22 EP EP03731638A patent/EP1468004B1/en not_active Expired - Lifetime
- 2003-01-22 WO PCT/BE2003/000008 patent/WO2003062253A1/en active IP Right Grant
- 2003-01-22 ES ES06020387T patent/ES2323803T3/es not_active Expired - Lifetime
- 2003-01-22 DE DE60310521T patent/DE60310521T2/de not_active Expired - Lifetime
- 2003-01-22 DE DE60327378T patent/DE60327378D1/de not_active Expired - Lifetime
- 2003-01-22 AT AT06020387T patent/ATE429437T1/de active
- 2003-01-22 JP JP2003562130A patent/JP4477879B2/ja not_active Expired - Fee Related
- 2003-01-22 AU AU2003236511A patent/AU2003236511B2/en not_active Ceased
- 2003-01-22 AT AT03731638T patent/ATE348835T1/de active
- 2003-01-22 DK DK06020387T patent/DK1743899T3/da active
- 2003-01-22 CA CA002473029A patent/CA2473029A1/en not_active Abandoned
-
2004
- 2004-07-16 ZA ZA2004/05685A patent/ZA200405685B/en unknown
- 2004-07-19 US US10/894,308 patent/US7687635B2/en not_active Expired - Fee Related
-
2009
- 2009-09-24 JP JP2009218735A patent/JP5100728B2/ja not_active Expired - Fee Related
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010077128A (ja) * | 2002-01-22 | 2010-04-08 | Telene Sas | メタセシスに使用される金属錯体 |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE348835T1 (de) | 2007-01-15 |
| JP2010077128A (ja) | 2010-04-08 |
| DE60310521D1 (de) | 2007-02-01 |
| EP1468004B1 (en) | 2006-12-20 |
| WO2003062253A1 (en) | 2003-07-31 |
| DE60327378D1 (de) | 2009-06-04 |
| DE60310521T2 (de) | 2007-11-08 |
| ES2323803T3 (es) | 2009-07-24 |
| JP5100728B2 (ja) | 2012-12-19 |
| US20050043541A1 (en) | 2005-02-24 |
| DK1468004T3 (da) | 2007-04-30 |
| EP1743899A1 (en) | 2007-01-17 |
| ES2279117T3 (es) | 2007-08-16 |
| CA2473029A1 (en) | 2003-07-31 |
| ATE429437T1 (de) | 2009-05-15 |
| JP2005515260A (ja) | 2005-05-26 |
| EP1743899B1 (en) | 2009-04-22 |
| ZA200405685B (en) | 2005-10-26 |
| EP1468004A1 (en) | 2004-10-20 |
| AU2003236511B2 (en) | 2009-04-09 |
| US7687635B2 (en) | 2010-03-30 |
| DK1743899T3 (da) | 2009-06-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4477879B2 (ja) | 複分解に使用される金属錯体 | |
| AU2003236511A1 (en) | Metal complexes for use in metathesis | |
| KR100333761B1 (ko) | 고복분해활성루테늄및오스뮴금속카르벤착화합물의이용방법 | |
| JP4997096B2 (ja) | オレフィンメタセシスおよび原子またはグループ移動反応に使用するための金属錯体 | |
| EP3164409B1 (en) | Group 8 transition metal catalysts and method for making same and process for use of same in metathesis reaction | |
| US20070185343A1 (en) | Metal complexes for use in olefin metathesis and atom group transfer reactions | |
| WO2005035121A2 (en) | Schiff base metal complexes for use as catalysts in organic synthesis | |
| JP2005501936A (ja) | 2個以上のヘテロ原子を含有する架橋された二環式および多環式のオレフィンの開環メタセシス重合 | |
| Izawa et al. | (Arylimido) niobium (V)–Alkylidenes, Nb (CHSiMe3)(NAr)[OC (CF3) 3](PMe3) 2, That Enable to Proceed Living Metathesis Polymerization of Internal Alkynes | |
| JP2009511731A (ja) | 環状オレフィン重合体の製造方法 | |
| EP1937731B1 (en) | Polymerization methods using the catalysts | |
| KR100828728B1 (ko) | 고리형 올레핀 중합체 제조용 촉매 | |
| CN110114363B (zh) | 苯甲基氧基苯氧基酚配体的合成 | |
| CN109862963A (zh) | Ru亚烷基络合物的合成与表征 | |
| De Clercq et al. | Heterogenation of a shiff base substituted Grubbs catalyst and a Ru-dimer to perform romp reactions | |
| Krause | Development of new Ruthenium Catalysts for homogeneous and heterogeneous Olefin-Metathesis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20051011 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20051011 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20080722 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20080722 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090127 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090417 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20090526 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090924 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20091005 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20091007 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20091007 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100202 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100303 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100312 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130319 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130319 Year of fee payment: 3 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130319 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130319 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140319 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |