JP2014093988A - 固相担体の操作方法及び固相担体の操作装置 - Google Patents
固相担体の操作方法及び固相担体の操作装置 Download PDFInfo
- Publication number
- JP2014093988A JP2014093988A JP2012248320A JP2012248320A JP2014093988A JP 2014093988 A JP2014093988 A JP 2014093988A JP 2012248320 A JP2012248320 A JP 2012248320A JP 2012248320 A JP2012248320 A JP 2012248320A JP 2014093988 A JP2014093988 A JP 2014093988A
- Authority
- JP
- Japan
- Prior art keywords
- plug
- tube
- container
- nucleic acid
- magnetic particles
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1003—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor
- C12N15/1006—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor by means of a solid support carrier, e.g. particles, polymers
- C12N15/1013—Extracting or separating nucleic acids from biological samples, e.g. pure separation or isolation methods; Conditions, buffers or apparatuses therefor by means of a solid support carrier, e.g. particles, polymers by using magnetic beads
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6806—Preparing nucleic acids for analysis, e.g. for polymerase chain reaction [PCR] assay
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/0098—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor involving analyte bound to insoluble magnetic carrier, e.g. using magnetic separation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
- B01L2200/0668—Trapping microscopic beads
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0673—Handling of plugs of fluid surrounded by immiscible fluid
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0832—Geometry, shape and general structure cylindrical, tube shaped
- B01L2300/0838—Capillaries
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/087—Multiple sequential chambers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/043—Moving fluids with specific forces or mechanical means specific forces magnetic forces
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N2035/00346—Heating or cooling arrangements
- G01N2035/00356—Holding samples at elevated temperature (incubation)
Abstract
【解決手段】固相担体の操作方法は、容器100内に入れた液体中において、物質を担持可能、かつ磁性を有する固相担体Mを操作する固相担体の操作方法であって、容器100内において、固相担体Mに対し、磁力を印加する磁力印加部400によって、固相担体Mが容器100の長手方向及び容器100の長手方向に交わる断面方向のいずれか一方向あるいは両方向ベクトルを合成した方向へ導くことで、磁力印加部400と容器100との相対的な位置が経時的に変位するよう固相担体Mを操作する。
【選択図】図9
Description
以下では、核酸抽出キットを装着して核酸の抽出を行う固相担体の操作装置としての核酸抽出装置を一実施形態として説明する。
1.核酸抽出装置
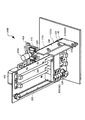
図1は、本実施形態に係る核酸抽出装置の一例を示す斜視図である。本実施形態に係る核酸抽出装置3000は、後述説明する核酸抽出キット、核酸抽出デバイス、及び核酸抽出方法に好適に適用することができる。
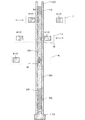
図2は、本実施形態に係る核酸抽出デバイス1000の要部を模式的に示す図である。
本実施形態の核酸抽出デバイス1000は、チューブ100と、第1プラグ10、第2プラグ20、第3プラグ30、第4プラグ40、及び第5プラグ50と、を有する。核酸抽出デバイス1000は、長手方向を有し、オイル(液体)からなる第1プラグ10、オイルと相分離する第1洗浄液(液体)からなる第2プラグ20、オイルからなる第3プラグ30、オイルと相分離する溶出液(液体)からなる第4プラグ40、及びオイルからなる第5プラグ50、が当該順で内部に配置されたチューブ(容器)100を有する。なお、チューブ100内には、第1プラグ10ないし第5プラグ50が配置された例とするが、後述する第6プラグ、第7プラグが配置されていてもよい。
チューブ100は、核酸抽出デバイス1000の要部を構成している。核酸抽出デバイス1000は、チューブ100の他に、各種の構成を含んでもよい。核酸抽出デバイス1000は、例えば、図示しないが、チューブ100に接続される配管、容器、栓、継ぎ手、ポンプ、制御装置などを含んでもよい。
第1プラグ10、第3プラグ30、及び第5プラグ50は、いずれもオイルからなる。第1プラグ10、第3プラグ30、及び第5プラグ50を構成するオイルは、互いに異なる種類のオイルであってもよい。オイルとしては、例えば、ジメチルシリコーンオイル等のシリコーン系オイル、パラフィン系オイル及びミネラルオイル並びにそれらの混合物から選択される一種を挙げることができる。また、第1プラグ10、第2プラグ20、第3プラグ30、第4プラグ40、及び第5プラグ50の隣り合うプラグを形成する液体は、互いに相分離するように選択される。
第2プラグ20は、チューブ100内の第1プラグ10と第3プラグ30との間の位置に配置される。第2プラグ20は、第1洗浄液からなる。第1洗浄液は、第1プラグ10を構成するオイル及び第3プラグ30を構成するオイルのいずれとも相分離する液体である。第1洗浄液としては、水、又は溶質濃度が10mM以下、好ましくは7mM以下、より好ましくは5mM以下の緩衝液が挙げられる。緩衝液の組成は、特に限定されないが、トリス−塩酸緩衝液などを例示することができ、EDTA(エチレンジアミン四酢酸)等を含有してもよい。このような第1洗浄液であれば、核酸が吸着した磁性粒子Mを効率よく洗浄することができる。
第4プラグ40は、チューブ100内の第3プラグ30と第5プラグ50との間の位置に配置される。第4プラグ40は、溶出液からなる。
本実施形態の核酸抽出デバイス1000は、オイル、第1洗浄液、及び溶出液がプラグ状に配置されたチューブ100を有している。そのため、チューブ100に、核酸が吸着された磁性粒子Mを第1プラグ10側から導入して、第4プラグ40まで移動させることによって、核酸の抽出を極めて短時間で容易に行うことができる。より詳細には、核酸が吸着された磁性粒子Mを、チューブ100の第1プラグ10側から導入し、第1プラグ10を構成するオイル内を通過させ、第2プラグ20を構成する第1洗浄液で洗浄し、第3プラグ30を構成するオイルを通過させ、第4プラグ40を構成する溶出液において磁性粒子Mから核酸を脱離させることができる。すなわち、本実施形態の核酸抽出デバイス1000は、核酸が吸着された磁性粒子Mをチューブ100内において移動させることによって、高い純度で核酸を含有する溶出液を得ることができる。そのため、核酸抽出デバイス1000によれば、PCRのための前処理に要する時間と手間を大幅に削減することができる。
(核酸抽出デバイスの構成等)
本実施形態の核酸抽出デバイス1000は、チューブ100と、第1プラグ10、第2プラグ20、第3プラグ30、第4プラグ40、及び第5プラグ50と、を有するが、他の機能を付加する構成を含んでもよい。本実施形態の核酸抽出デバイスは、以下に説明する構成の組合せや、各構成の変形形態を含んでもよい。
図3は、本変形例に係る核酸抽出デバイスの要部を模式的に示す図である。本実施形態の核酸抽出デバイス1010は、例えば、チューブ100の第5プラグ50側の端が開放されていてもよい。すなわち、図3に示すように、核酸抽出デバイス1010では、チューブ100の第5プラグ50側の端が、開放された状態となっている。核酸抽出デバイス1010によれば、チューブ100の第1プラグ10側からチューブ100内部に圧力を印加することにより、第5プラグ50及び第4プラグ40を順に吐出させることができる。これにより、核酸抽出デバイス1010を用いて、例えばPCRのための反応容器等に、標的核酸を含む第4プラグ40を構成する溶出液を容易に分注することができる。
図4は、本変形例に係る核酸抽出デバイスの要部を模式的に示す図である。本実施形態の核酸抽出デバイス1020は、図示のように、例えば、チューブ100の第5プラグ50側の端を封止する、脱着自在の栓110をさらに有してもよい。栓110は、例えば、ゴムやエラストマー、高分子等によりなることができる。栓110によってチューブ100が封止される場合、栓110は、第5プラグ50と接してもよいし、第5プラグ50と栓110との間に空気等の気体が配置されてもよい。また、栓110は脱着自在であるが、その機構は特に限定されない。図4の例では、栓110の一部がチューブ100内部に挿入されて固定される態様を示しているが、栓110はキャップ状であってもよい。
図5は、本変形例に係る核酸抽出デバイスを模式的に示す図である。図5に例示するように、核酸抽出デバイス1030は、チューブ100の第1プラグ10側の端に内部を連通させて接続できる、脱着自在の吸着容器(容器)120をさらに有している。
本実施形態の核酸抽出デバイスは、チューブ100内部に、第6プラグ及び第7プラグを有してもよい。
図6は、本変形例に係る核酸抽出デバイスの要部を模式的に示す図である。具体的には、チューブ100内部に、第6プラグ60及び第7プラグ70を有する核酸抽出デバイス1100を模式的に示す図である。
図7は、本実施形態に係る核酸抽出キットの一例を模式的に示す図である。図7に例示した核酸抽出キット2000は、上述した核酸抽出デバイス1000の要部を構成する部品を含む。「2.核酸抽出デバイス」の項において説明した構成と同様の構成については、同じ符号を付して詳細な説明は省略する。
上述した核酸抽出装置3000、核酸抽出キット2000、及び核酸抽出デバイス1000、並びに後述するそれらの変形形態は、いずれも本実施形態の固相担体の操作方法としての核酸抽出方法に好適に利用することができる。
以下、本実施形態の核酸抽出方法の一例として、上述の核酸抽出キット2000を利用した方法を説明する。
吸着容器120に検体を導入する工程は、例えば、綿棒に検体を付着させ、吸着容器120の開口121から、当該綿棒を差し入れ、吸着液にこれを浸漬して行うことができる。また、検体は、ピペット等によって吸着容器120の開口121から導入してもよい。また検体がペースト状や固体状であれば、例えば、吸着容器120の開口121から匙やピンセット等により吸着容器120内壁に付着させたり投入させたりしてもよい。
核酸を吸着させる工程は、吸着容器120を揺動させて行われる。この工程は、吸着容器120の開口121を封止する蓋122があれば、これを用いて吸着容器120を封止して行うとより効率的に行うことができる。この工程により、標的核酸は、カオトロピック剤の作用により、磁性粒子Mの表面に吸着される。この工程では、磁性粒子Mの表面には、標的核酸の他に標的核酸以外の核酸や蛋白質が吸着してもよい。
図8は、本実施形態に係る核酸抽出キットの一例を模式的に示す図である。
次に図8に示すように、チューブ100の第1プラグ10側の端に吸着容器120を接続する。チューブ100内の各プラグは、第1プラグ10側の栓110を外しても、第5プラグ50側の栓110がなされているため、チューブ100内を移動しにくくなっている。この工程は、チューブ100の第1プラグ10側の端に栓110が取り付けられている場合には該栓110を外して行う。そして、吸着容器120及びチューブ100は、内容物が漏出しないように接続され、吸着容器120内部とチューブ100内部との間で内容物が流通可能なように連通される。
上記工程を経ると、吸着容器120内の核酸が吸着した磁性粒子Mがチューブ100に流通できる状態となっている。チューブ100内に入れた液体中において、物質を担持可能、かつ磁性を有する磁性粒子Mを操作する。核酸が吸着した磁性粒子Mをチューブ100に導く手法としては、重力や遠心力を利用する方法を用いてもよく、特に制限されないが、本実施形態では吸着容器120及びチューブ100外部から磁力を印加して行う。磁力は、例えば、永久磁石、電磁石等により印加することができるが、発熱等を生じない点で、永久磁石を用いて印加することがより好ましい。また、永久磁石を用いる場合には、作業者の手で磁石を動かして行ってもよいし、機械装置等を利用して行ってもよい。磁性粒子Mは、磁力によって引き寄せられる性質を有しているため、この性質を利用して、吸着容器120及びチューブ100と、永久磁石の相対的な配置を変化させて、吸着容器120内からチューブ100に移動させる。チューブ100内において、磁性粒子Mに対し、磁力を印加する磁力印加部400によって、磁性粒子Mがチューブ100の長手方向及びチューブ100の長手方向に交わる断面方向のいずれか一方向あるいは両方向ベクトルを合成した方向へ導くことで、磁力印加部400と磁性粒子Mとの相対的な位置が経時的に変位するよう磁性粒子Mを操作する。これにより、第1プラグ10から順に、各プラグを通って、第4プラグ40まで磁性粒子Mが移動される。磁性粒子Mが各プラグを通過するときの各プラグにおける滞在時間は特に限定されないし、同一プラグ内でチューブ100の長手方向に沿って往復するようにして移動させてもよい。
図9〜図11は、本実施形態に係る磁性粒子Mを移動させる外部磁界印加方法について示す図である。磁力印加部400は、図9(A)に示すように、一定の間隔を介して対峙する一対の永久磁石410A,410Bを有しており、一対の永久磁石410A,410Bは、装着部300(図1参照)にチューブ100が装着された場合に、チューブ100を挟み向かい合って配置されている。
はじめに、吸着容器120内に存在する磁性粒子Mをチューブ100内に導入するため、磁力印加部400における一対の永久磁石410A,410Bの位置が、チューブ100内の第2プラグ20に対応する位置まで磁力印加部400を吸着容器120の位置から下降させる。
磁性粒子Mが第4プラグ40に到達すると、溶出液の作用により、磁性粒子Mに吸着された核酸が、第4プラグ40を構成する溶出液に溶出する。本工程を経ると、検体から溶出液に対して核酸が溶出し、検体から核酸が抽出された状態となる。
本実施形態の核酸抽出方法は、吸着容器120を変形させて、第5プラグ50及び第4プラグ40をチューブ100の吸着容器120が接続した端と反対側の端から吐出させる工程を含んでもよい。
本実施形態の核酸抽出方法によれば、核酸の抽出を極めて短時間で容易に行うことができる。本実施形態の核酸抽出方法は、核酸が吸着された磁性粒子Mをチューブ100内において移動させることによって、高い純度で核酸を含有する溶出液を得ることができる。本実施形態の核酸抽出方法によれば、PCRのための前処理に要する時間と手間を大幅に削減することができる。
以下に実験例を説明し、本発明をさらに詳細に説明するが、本発明は以下の実験例によって何ら限定されるものではない。
実験例1では、上述の核酸抽出キット2000のうち、チューブ100内部に、第1プラグ10ないし第7プラグ70を有する構成を使用した。
図12は、本実験例に係る結果を示すグラフである。なお、図12の縦軸は、蛍光輝度であり、横軸はPCRのサイクル数である。
実験例2では、一般的な核酸抽出法により核酸の抽出を行った。
実験例3では、上述の核酸抽出キット2000のうち、チューブ100内部に、第1プラグ10ないし第5プラグ50を有する構成を使用した。
(溶出温度のDNA収量に対する影響)
実験例4では、一般的な核酸抽出法により核酸の抽出を行った。
図13は、本実験例に係る溶出温度とDNA収量との関係を示すグラフである。この結果は、リアルタイムPCRの立ち上がりサイクルから計算により求めた。比較サンプルの立ち上がりサイクルをCt0、抽出サンプルの立ち上がりサイクルをCt1とすると、DNA収量は比較サンプル(1となる)の比として、式「2(Ct0-Ct1)」で表される。
上記実験例から、以下のことが判明した。
(1)PCRの前処理である核酸の抽出処理に要した時間を比較すると、検体を吸着容器120に挿入してから、PCRの反応容器に標的核酸を導入するまでの時間は、実験例1ではおよそ2分であった。実験例2ではおよそ30分であった。これにより実験例1の核酸抽出方法は、実験例2の核酸抽出方法よりも、核酸抽出に要する時間が大幅に短いことが分かった。
本発明における操作方法に係り、実施形態1とは異なる外部磁界印加方法を説明する。
図14及び図15は、本実施形態に係る永久磁石410とチューブ100との構成の一例を示す図である。図14は構成を示し、図15はその移動手順を示す。
本発明における操作方法に係り、前記実施形態とは異なる外部磁界印加方法を説明する。
図16は、本実施形態に係る永久磁石410A,410B,410Cとチューブ100との構成の一例を示す図である。(A)は構成を示し、(B)はその移動手順を示す。
上記実施形態では、永久磁石410がチューブ100の周に沿う回転運動に、永久磁石410とチューブ100の軸との距離を変化させる相対運動加えた複合運動を行う。これにより、磁性粒子Mがチューブ100の内側側面を沿う移動になるが、永久磁石410とチューブ100との距離を変えることで、チューブ100近傍の磁力の強弱が変わり、チューブ100内部の磁性粒子Mが凝縮状態と分散状態に繰り返し変化する。その結果、磁性粒子Mは試薬中で多くの領域を浮遊し洗浄の効率が上がる。
上記実施形態では、チューブ100が単一のケースで磁場の変化方法を示したが、複数のチューブ100が、並列あるいは環状に配列した場合に同様の磁力の変化方法による複数チューブ100内の磁性粒子Mの同時操作方法でもよい。
(核酸抽出装置)
図17は、本変形例に係る核酸抽出装置の一例を示す斜視図である。核酸抽出装置3100は、上述の核酸抽出装置3000とは、加熱部600を有する点で相違する以外は同様であり、作用機能の共通する部材については、同一の符号を付して説明を省略する。
(液溜部)
図18は、本変形例に係る核酸抽出デバイスを模式的に示す図である。図18に例示するように、核酸抽出デバイス1040は、チューブ100の第1プラグ10側の端に、チューブ100に連通する液溜部(容器)130が形成されている。液溜部130内部とチューブ100内部とは連通している。
(磁性粒子を移動させる工程の変形)
図19は、本変形例の核酸抽出方法を説明するための模式図である。
上述の「4.4.磁性粒子を移動させる工程」では、磁性粒子Mに対して磁力を外部から印加することによって、磁性粒子Mを第1プラグ10から各プラグを通過させて第4プラグ40まで移動させると説明した。しかし、磁性粒子Mが第2プラグ20に移動されたときに、外部から印加される磁力を変化させて、第2プラグ20内で磁性粒子Mを振動させたり、拡散凝集を繰り返したりして行ってもよい。このようにすれば、第2プラグ20を構成する第1洗浄液による磁性粒子Mの洗浄効果を高めることができる。
(核酸を溶出させる工程の変形)
上述の「4.5.核酸を溶出させる工程」では、第4プラグ40を加熱して行ってもよい。第4プラグ40を加熱する方法としては、例えば、チューブ100の第4プラグ40に対応する位置に、ヒートブロック等の熱媒体を接触させる方法や、ヒーター等の熱源を用いる方法、電磁加熱による方法などを例示することができる。
(第4プラグをチューブから吐出させる工程の変形)
上述の「4.6.第4プラグをチューブから吐出させる工程」を採用する場合、係る工程において、溶出液に対して吸着された核酸を溶出した磁性粒子Mは、第4プラグ40内に存在してもよいが、さらに、磁力を印加することによって、第1プラグ10、第2プラグ20、第3プラグ30のいずれかのプラグ、又は吸着容器120の中まで移動させてから行ってもよい。このようにすれば、溶出液に磁性粒子Mが含まれない状態で、第4プラグ40をチューブ100から吐出することができる。また、磁性粒子Mを移動させる先は、第2プラグ20又は吸着容器120とすれば、磁力を取り去っても、第3プラグ30を構成するオイル内に磁性粒子Mが進入しにくいため、第4プラグ40をチューブ100から吐出することをより容易にすることができる。
Claims (7)
- 容器内に入れた液体中において、物質を担持可能、かつ磁性を有する固相担体を操作する固相担体の操作方法であって、
前記容器内において、前記固相担体に対し、磁力を印加する磁力印加部によって、前記固相担体が前記容器の長手方向及び該容器の長手方向に交わる断面方向のいずれか一方向あるいは両方向ベクトルを合成した方向へ導くことで、前記磁力印加部と前記容器との相対的な位置が経時的に変位するよう前記固相担体を操作することを特徴とする固相担体の操作方法。 - 請求項1に記載の固相担体の操作方法において、
前記磁力印加部は、少なくとも一つの永久磁石を有することを特徴とする固相担体の操作方法。 - 請求項1又は2に記載の固相担体の操作方法において、
前記容器周面に前記永久磁石が近づいた後、前記永久磁石が前記容器周面から遠ざかることによって前記容器周面とは異なる場所に前記永久磁石が接近することで、前記固相担体が前記容器内で変位することを特徴とする固相担体の操作方法。 - 請求項1〜3のいずれか一項に記載の固相担体の操作方法において、
一定の間隔を介して対峙する2つの前記永久磁石によって前記固相担体を変位することを特徴とする固相担体の操作方法。 - 請求項1〜3のいずれか一項に記載の固相担体の操作方法において、
前記永久磁石と前記容器とが相対的に回転することによって、前記固相担体が前記容器内で変位することを特徴とする固相担体の操作方法。 - 請求項1〜3のいずれか一項に記載の固相担体の操作方法において、
前記永久磁石を少なくとも3つ以上備え、前記容器と前記永久磁石との位置が相対的に変位することによって、前記固相担体が前記容器の長手方向に直交する平面において少なくとも2方向へ変位することを特徴とする固相担体の操作方法。 - 容器内に入れた液体中において、物質を担持可能、かつ磁性を有する固相担体を操作する固体担体の操作装置であって、
前記容器内において、前記固相担体に対して磁力を印加する磁力印加部を備え、
前記固相担体を前記容器の長手方向及び該容器の長手方向に交わる断面方向のいずれか一方向あるいは両方向のベクトルを合成した方向へ導くことで、前記磁力印加部と前記容器との相対的な位置が経時的に変位するように前記固相担体を操作することを特徴とする固相担体の操作装置。
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012248320A JP2014093988A (ja) | 2012-11-12 | 2012-11-12 | 固相担体の操作方法及び固相担体の操作装置 |
| CN201380055844.XA CN104755169A (zh) | 2012-11-12 | 2013-11-12 | 操纵固体载体的方法及操纵固体载体的设备 |
| RU2015122685A RU2015122685A (ru) | 2012-11-12 | 2013-11-12 | Способ манипуляции твердыми носителями и устройство для манипуляций твердыми носителями |
| EP13827049.1A EP2916952A1 (en) | 2012-11-12 | 2013-11-12 | A method of manipulating solid carriers and an apparatus of manipulating solid carriers |
| US14/441,327 US20150284710A1 (en) | 2012-11-12 | 2013-11-12 | Method of manipulating solid carriers and an apparatus of manipulating solid carriers |
| IN1303DEN2015 IN2015DN01303A (ja) | 2012-11-12 | 2013-11-12 | |
| PCT/JP2013/006657 WO2014073218A1 (en) | 2012-11-12 | 2013-11-12 | A method of manipulating solid carriers and an apparatus of manipulating solid carriers |
| BR112015010616A BR112015010616A2 (pt) | 2012-11-12 | 2013-11-12 | método para manipular portadores sólidos e aparelho para manipular portadores sólidos |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012248320A JP2014093988A (ja) | 2012-11-12 | 2012-11-12 | 固相担体の操作方法及び固相担体の操作装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2014093988A true JP2014093988A (ja) | 2014-05-22 |
| JP2014093988A5 JP2014093988A5 (ja) | 2015-12-24 |
Family
ID=50069267
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012248320A Withdrawn JP2014093988A (ja) | 2012-11-12 | 2012-11-12 | 固相担体の操作方法及び固相担体の操作装置 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20150284710A1 (ja) |
| EP (1) | EP2916952A1 (ja) |
| JP (1) | JP2014093988A (ja) |
| CN (1) | CN104755169A (ja) |
| BR (1) | BR112015010616A2 (ja) |
| IN (1) | IN2015DN01303A (ja) |
| RU (1) | RU2015122685A (ja) |
| WO (1) | WO2014073218A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020062577A (ja) * | 2018-10-15 | 2020-04-23 | 株式会社島津製作所 | 磁性体粒子操作用装置 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015159733A (ja) * | 2014-02-26 | 2015-09-07 | セイコーエプソン株式会社 | 物質結合用固相担体の凍結乾燥体、物質含有液中の物質を物質結合用固相担体と結合させるための容器、および、物質結合用固相担体を含む凍結乾燥体の製造方法 |
| JP2015177770A (ja) * | 2014-03-19 | 2015-10-08 | セイコーエプソン株式会社 | 標的物質の精製装置、核酸精製装置、標的物質の生成方法、及び核酸増幅方法 |
| WO2021086444A1 (en) * | 2019-10-29 | 2021-05-06 | Hewlett-Packard Development Company, L.P. | Fluid preparation devices |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010147561A1 (en) * | 2009-06-16 | 2010-12-23 | Biochip Devises Pte Ltd | Method for conducting multiple reactions in a single reaction tube |
| JP2011516034A (ja) * | 2008-02-29 | 2011-05-26 | ノースウエスタン ユニバーシティ | 生物反応促進用バリア |
| JP2012152734A (ja) * | 2012-02-14 | 2012-08-16 | Tamagawa Seiki Co Ltd | 液体中の磁性粒子の集合/分散装置 |
| JP2012152213A (ja) * | 2012-02-14 | 2012-08-16 | Tamagawa Seiki Co Ltd | 液体中の磁性粒子の集合/分散装置 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3985649A (en) * | 1974-11-25 | 1976-10-12 | Eddelman Roy T | Ferromagnetic separation process and material |
| AU4927496A (en) * | 1995-02-21 | 1996-09-11 | Iqbal W. Siddiqi | Apparatus and method for mixing and separation employing magnetic particles |
| DE69839294T2 (de) * | 1997-09-29 | 2009-04-09 | F. Hoffmann-La Roche Ag | Gerät zur Abscheidung magnetischer Teilchen |
| ES2315238T3 (es) * | 1999-07-19 | 2009-04-01 | Biomerieux B.V. | Metodo para mezclar particulas magneticas con un fluido. |
| EP1621890A1 (en) * | 2004-07-26 | 2006-02-01 | bioMerieux B.V. | Device and method for separating, mixing and concentrating magnetic particles with a fluid and use thereof in purification methods |
| CN101203757A (zh) * | 2005-06-23 | 2008-06-18 | 皇家飞利浦电子股份有限公司 | 用于移动磁性粒子的设备 |
| EP1929269A2 (en) * | 2005-09-30 | 2008-06-11 | Caliper Life Sciences, Inc. | Microfluidic device for purifying a biological component using magnetic beads |
| JP4844263B2 (ja) | 2006-07-07 | 2011-12-28 | 株式会社島津製作所 | 微量化学反応方法及び装置 |
| WO2009014737A1 (en) * | 2007-07-25 | 2009-01-29 | Abbott Laboratories | Magnetic mixer |
| JP2009207459A (ja) | 2008-03-06 | 2009-09-17 | Sony Corp | 核酸抽出装置、及び核酸抽出方法 |
| WO2010038952A2 (en) * | 2008-10-01 | 2010-04-08 | Samsung Electronics Co., Ltd., | Centrifugal-based microfluid apparatus, method of fabricationg the same, and method of testing samples using the microfluidic apparatus |
| WO2012086243A1 (ja) * | 2010-12-21 | 2012-06-28 | 株式会社 島津製作所 | 管内で対象成分を操作するためのデバイス及び方法 |
-
2012
- 2012-11-12 JP JP2012248320A patent/JP2014093988A/ja not_active Withdrawn
-
2013
- 2013-11-12 WO PCT/JP2013/006657 patent/WO2014073218A1/en active Application Filing
- 2013-11-12 IN IN1303DEN2015 patent/IN2015DN01303A/en unknown
- 2013-11-12 RU RU2015122685A patent/RU2015122685A/ru unknown
- 2013-11-12 CN CN201380055844.XA patent/CN104755169A/zh active Pending
- 2013-11-12 EP EP13827049.1A patent/EP2916952A1/en not_active Withdrawn
- 2013-11-12 BR BR112015010616A patent/BR112015010616A2/pt not_active IP Right Cessation
- 2013-11-12 US US14/441,327 patent/US20150284710A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011516034A (ja) * | 2008-02-29 | 2011-05-26 | ノースウエスタン ユニバーシティ | 生物反応促進用バリア |
| WO2010147561A1 (en) * | 2009-06-16 | 2010-12-23 | Biochip Devises Pte Ltd | Method for conducting multiple reactions in a single reaction tube |
| JP2012152734A (ja) * | 2012-02-14 | 2012-08-16 | Tamagawa Seiki Co Ltd | 液体中の磁性粒子の集合/分散装置 |
| JP2012152213A (ja) * | 2012-02-14 | 2012-08-16 | Tamagawa Seiki Co Ltd | 液体中の磁性粒子の集合/分散装置 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020062577A (ja) * | 2018-10-15 | 2020-04-23 | 株式会社島津製作所 | 磁性体粒子操作用装置 |
| JP7110900B2 (ja) | 2018-10-15 | 2022-08-02 | 株式会社島津製作所 | 磁性体粒子操作用装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104755169A (zh) | 2015-07-01 |
| EP2916952A1 (en) | 2015-09-16 |
| IN2015DN01303A (ja) | 2015-07-03 |
| RU2015122685A (ru) | 2017-01-10 |
| BR112015010616A2 (pt) | 2017-07-11 |
| US20150284710A1 (en) | 2015-10-08 |
| WO2014073218A1 (en) | 2014-05-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5954532B2 (ja) | 核酸抽出用デバイス、核酸抽出用キット、核酸抽出用装置及び核酸抽出方法 | |
| JP6040268B2 (ja) | 試料破壊用ビーズを利用した生物検体の捕捉および溶出 | |
| JP2015084657A (ja) | 核酸抽出用デバイス | |
| JP2014176302A (ja) | 核酸増幅反応装置及び核酸増幅方法 | |
| JP2014176305A (ja) | 核酸増幅反応用カートリッジ | |
| JP2014176304A (ja) | 核酸増幅反応用カートリッジ | |
| JP2015104364A (ja) | 核酸増幅反応用容器、核酸増幅反応用カートリッジ、及び核酸増幅反応用カートリッジキット | |
| JP2014093988A (ja) | 固相担体の操作方法及び固相担体の操作装置 | |
| JP2016067277A (ja) | 生体関連物質抽出デバイス及び生体関連物質抽出装置 | |
| JP2015073485A (ja) | 核酸増幅方法、核酸抽出用デバイス、核酸増幅反応用カートリッジ、及び核酸増幅反応用キット | |
| JP2015188377A (ja) | 核酸増幅反応用カートリッジ及び核酸増幅装置 | |
| CN104877989A (zh) | 核酸扩增方法、核酸提取用设备、核酸扩增反应用盒、以及核酸扩增反应用套件 | |
| JP2015050968A (ja) | 核酸増幅システム | |
| JP2014033663A (ja) | 核酸抽出装置及び核酸抽出方法 | |
| JP2015073513A (ja) | 核酸抽出用デバイス、核酸抽出用キット、及び核酸抽出用装置 | |
| JP2016067274A (ja) | 物質精製デバイス及びカートリッジ | |
| JP2016214179A (ja) | 容器組立体セット | |
| JP4269002B1 (ja) | 反応装置及び方法 | |
| JP2016067273A (ja) | 容器組立体及び容器組立体キット | |
| JP2015050965A (ja) | 核酸増幅反応用カートリッジ | |
| JP2017184626A (ja) | 核酸抽出キットおよび核酸抽出カートリッジ | |
| JP2015019590A (ja) | 核酸増幅反応装置 | |
| JP2015181458A (ja) | 核酸増幅反応装置及び核酸増幅方法 | |
| JP2015097512A (ja) | 核酸抽出用デバイス | |
| US20160152969A1 (en) | Nucleic acid extraction device |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150108 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151110 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20151110 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20160610 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20160624 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160823 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20161011 |