JP2004107263A - フェナントロリン化合物及びそれを用いた有機発光素子 - Google Patents
フェナントロリン化合物及びそれを用いた有機発光素子 Download PDFInfo
- Publication number
- JP2004107263A JP2004107263A JP2002272408A JP2002272408A JP2004107263A JP 2004107263 A JP2004107263 A JP 2004107263A JP 2002272408 A JP2002272408 A JP 2002272408A JP 2002272408 A JP2002272408 A JP 2002272408A JP 2004107263 A JP2004107263 A JP 2004107263A
- Authority
- JP
- Japan
- Prior art keywords
- substituted
- group
- unsubstituted
- same
- organic light
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- -1 Phenanthroline compound Chemical class 0.000 title claims abstract description 42
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 19
- 125000003710 aryl alkyl group Chemical group 0.000 claims abstract description 19
- 125000003118 aryl group Chemical group 0.000 claims abstract description 19
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 19
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 17
- 125000005843 halogen group Chemical group 0.000 claims abstract description 15
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 claims abstract description 12
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims abstract description 10
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 claims abstract description 10
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 claims abstract description 10
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 20
- 150000002894 organic compounds Chemical class 0.000 claims description 13
- 125000003277 amino group Chemical group 0.000 claims description 10
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 9
- 150000005041 phenanthrolines Chemical class 0.000 claims description 8
- 150000001875 compounds Chemical class 0.000 abstract description 36
- 230000003287 optical effect Effects 0.000 abstract 1
- 239000010410 layer Substances 0.000 description 59
- 239000010408 film Substances 0.000 description 29
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 18
- 239000000758 substrate Substances 0.000 description 18
- 230000015572 biosynthetic process Effects 0.000 description 15
- 239000000463 material Substances 0.000 description 14
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- DVLSJPCXPNKPRJ-UHFFFAOYSA-N 2-iodo-9,9-dimethylfluorene Chemical compound C1=C(I)C=C2C(C)(C)C3=CC=CC=C3C2=C1 DVLSJPCXPNKPRJ-UHFFFAOYSA-N 0.000 description 11
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 9
- 230000005525 hole transport Effects 0.000 description 9
- 229920005989 resin Polymers 0.000 description 9
- 239000011347 resin Substances 0.000 description 9
- 239000012044 organic layer Substances 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- 238000007740 vapor deposition Methods 0.000 description 8
- 238000000034 method Methods 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- 238000001771 vacuum deposition Methods 0.000 description 7
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 238000011156 evaluation Methods 0.000 description 6
- 229910052751 metal Inorganic materials 0.000 description 6
- 239000002184 metal Substances 0.000 description 6
- DMDPAJOXRYGXCB-UHFFFAOYSA-N (9,9-dimethylfluoren-2-yl)boronic acid Chemical compound C1=C(B(O)O)C=C2C(C)(C)C3=CC=CC=C3C2=C1 DMDPAJOXRYGXCB-UHFFFAOYSA-N 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 239000012299 nitrogen atmosphere Substances 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 239000002904 solvent Substances 0.000 description 5
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 4
- 238000007789 sealing Methods 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 229910001148 Al-Li alloy Inorganic materials 0.000 description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 2
- IDWJREBUVYSPKS-UHFFFAOYSA-N 3,8-dibromo-1,10-phenanthroline Chemical compound BrC1=CN=C2C3=NC=C(Br)C=C3C=CC2=C1 IDWJREBUVYSPKS-UHFFFAOYSA-N 0.000 description 2
- AKZAIDYHEKUXBU-UHFFFAOYSA-N 4,7-dibromo-1,10-phenanthroline Chemical compound C1=CC2=C(Br)C=CN=C2C2=C1C(Br)=CC=N2 AKZAIDYHEKUXBU-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 239000004925 Acrylic resin Substances 0.000 description 2
- 229920000178 Acrylic resin Polymers 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 125000006267 biphenyl group Chemical group 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 229920000547 conjugated polymer Polymers 0.000 description 2
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N coumarin Chemical compound C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000000151 deposition Methods 0.000 description 2
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920000553 poly(phenylenevinylene) Polymers 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 229920005990 polystyrene resin Polymers 0.000 description 2
- 239000011241 protective layer Substances 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 229920002050 silicone resin Polymers 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 0 *c1c(*)nc2c(nc(*)c(*)c3*)c3c(*)c(*)c2c1* Chemical compound *c1c(*)nc2c(nc(*)c(*)c3*)c3c(*)c(*)c2c1* 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N 1,1-Diethoxyethane Chemical compound CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 1
- 229910001316 Ag alloy Inorganic materials 0.000 description 1
- VZYZZKOUCVXTOJ-UHFFFAOYSA-N CC1(C)c2cc(N(c3ccccc3)c(cc3)ccc3-c(cc3)ccc3N(c3ccccc3)c(cc3C4(C)C)ccc3-c3c4cccc3)ccc2-c2ccccc12 Chemical compound CC1(C)c2cc(N(c3ccccc3)c(cc3)ccc3-c(cc3)ccc3N(c3ccccc3)c(cc3C4(C)C)ccc3-c3c4cccc3)ccc2-c2ccccc12 VZYZZKOUCVXTOJ-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UJOBWOGCFQCDNV-UHFFFAOYSA-N Carbazole Natural products C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 239000004641 Diallyl-phthalate Substances 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229910000861 Mg alloy Inorganic materials 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004734 Polyphenylene sulfide Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 238000006069 Suzuki reaction reaction Methods 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 229920001807 Urea-formaldehyde Polymers 0.000 description 1
- 239000011354 acetal resin Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000012790 adhesive layer Substances 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- QUDWYFHPNIMBFC-UHFFFAOYSA-N bis(prop-2-enyl) benzene-1,2-dicarboxylate Chemical compound C=CCOC(=O)C1=CC=CC=C1C(=O)OCC=C QUDWYFHPNIMBFC-UHFFFAOYSA-N 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N c(cc1)cc(-c2ccc3)c1-c1c2c3ccc1 Chemical compound c(cc1)cc(-c2ccc3)c1-c1c2c3ccc1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 239000010406 cathode material Substances 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229960000956 coumarin Drugs 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- SWXVUIWOUIDPGS-UHFFFAOYSA-N diacetone alcohol Natural products CC(=O)CC(C)(C)O SWXVUIWOUIDPGS-UHFFFAOYSA-N 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- YWGBGCFJPPFOCI-UHFFFAOYSA-N fluoranthen-8-ylboronic acid Chemical compound C1=CC(C2=CC=C(C=C22)B(O)O)=C3C2=CC=CC3=C1 YWGBGCFJPPFOCI-UHFFFAOYSA-N 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000011133 lead Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000000113 methacrylic resin Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 229920001568 phenolic resin Polymers 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 229920001230 polyarylate Polymers 0.000 description 1
- 229920005668 polycarbonate resin Polymers 0.000 description 1
- 239000004431 polycarbonate resin Substances 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 229920006324 polyoxymethylene Polymers 0.000 description 1
- 229920000069 polyphenylene sulfide Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920000123 polythiophene Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 239000011669 selenium Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 1
- 229910001887 tin oxide Inorganic materials 0.000 description 1
- 125000006617 triphenylamine group Chemical group 0.000 description 1
- 238000007738 vacuum evaporation Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/311—Phthalocyanine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/321—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3]
- H10K85/324—Metal complexes comprising a group IIIA element, e.g. Tris (8-hydroxyquinoline) gallium [Gaq3] comprising aluminium, e.g. Alq3
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/621—Aromatic anhydride or imide compounds, e.g. perylene tetra-carboxylic dianhydride or perylene tetracarboxylic di-imide
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
Abstract
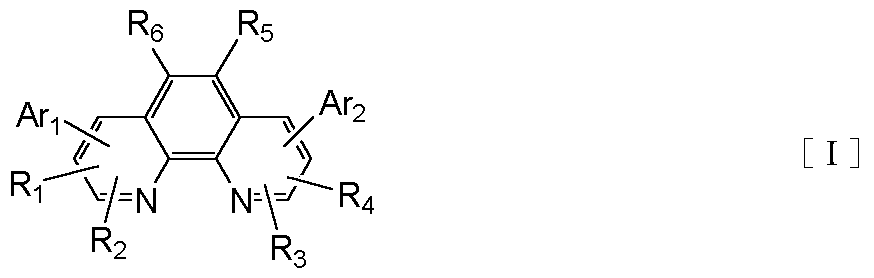
【解決手段】下記一般式[I]で示されるフェナントロリン化合物。
【化1】
(式中、R1、R2、R3、R4、R5およびR6は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基,置換あるいは無置換の複素環基またはハロゲン原子を表わし、同じであっても異なっていてもよい。Ar1およびAr2は、置換あるいは無置換のフルオレニル基、置換あるいは無置換のフルオランテニル基、置換あるいは無置換のペリレニル基または置換あるいは無置換のカルバゾリル基を表わし、同じであっても異なっていてもよい。)
【選択図】 なし
Description
【発明の属する技術分野】
本発明は、新規な有機化合物およびそれを用いた有機発光素子に関する。
【0002】
【従来の技術】
有機発光素子は、陽極と陰極間に蛍光性有機化合物または燐光性有機化合物を含む薄膜を挟持させて、各電極から電子およびホール(正孔)を注入することにより、蛍光性化合物または燐光性化合物の励起子を生成させ、この励起子が基底状態にもどる際に放射される光を利用する素子である。
【0003】
1987年コダック社の研究(非特許文献1)では、陽極にITO、陰極にマグネシウム銀の合金をそれぞれ用い、電子輸送材料および発光材料としてアルミニウムキノリノール錯体を用い、ホール輸送材料にトリフェニルアミン誘導体を用いた機能分離型2層構成の素子で、10V程度の印加電圧において1000cd/m2程度の発光が報告されている。関連の特許としては,特許文献1〜3等が挙げられる。
【0004】
また、蛍光性有機化合物の種類を変えることにより、紫外から赤外までの発光が可能であり、最近では様々な化合物の研究が活発に行われている。例えば、特許文献4〜11等に記載されている。
【0005】
近年、燐光性化合物を発光材料として用い、三重項状態のエネルギーをEL発光に用いる検討が多くなされている。プリンストン大学のグループにより、イリジウム錯体を発光材料として用いた有機発光素子が、高い発光効率を示すことが報告されている(非特許文献2)。
【0006】
さらに、上記のような低分子材料を用いた有機発光素子の他にも、共役系高分子を用いた有機発光素子が、ケンブリッジ大学のグループ(非特許文献3)により報告されている。この報告ではポリフェニレンビニレン(PPV)を塗工系で成膜することにより、単層で発光を確認している。
【0007】
共役系高分子を用いた有機発光素子の関連特許としては、特許文献12〜16等が挙げられる。
【0008】
このように有機発光素子における最近の進歩は著しく、その特徴は低印加電圧で高輝度、発光波長の多様性、高速応答性、薄型、軽量の発光デバイス化が可能であることから、広汎な用途への可能性を示唆している。
【0009】
しかしながら、現状では更なる高輝度の光出力あるいは高変換効率が必要である。また、長時間の使用による経時変化や酸素を含む雰囲気気体や湿気などによる劣化等の耐久性の面で未だ多くの問題がある。さらにはフルカラーディスプレイ等への応用を考えた場合の色純度の良い青、緑、赤の発光が必要となるが、これらの問題に関してもまだ十分でない。
【0010】
一方、フェナントロリン化合物がその優れた電子輸送性から電子輸送材料や発光材料として用いられる。フェナントロリン化合物を有機発光素子に用いた例として、特許文献17〜21などが挙げられるが、発光層材料や電子輸送材料として用いた際の特性は十分なものではない。
【0011】
【特許文献1】
米国特許第4,539,507号明細書
【特許文献2】
米国特許第4,720,432号明細書
【特許文献3】
米国特許第4,885,211号明細書
【特許文献4】
米国特許第5,151,629号明細書
【特許文献5】
米国特許第5,409,783号明細書
【特許文献6】
米国特許第5,382,477号明細書
【特許文献7】
特開平2−247278号公報
【特許文献8】
特開平3−255190号公報
【特許文献9】
特開平5−202356号公報
【特許文献10】
特開平9−202878号公報
【特許文献11】
特開平9−227576号公報
【特許文献12】
米国特許第5,247,190号明細書
【特許文献13】
米国特許第5,514,878号明細書
【特許文献14】
米国特許第5,672,678号明細書
【特許文献15】
特開平4−145192号公報
【特許文献16】
特開平5−247460号公報
【特許文献17】
特開平5−331459号公報
【特許文献18】
特開平7−82551号公報
【特許文献19】
特開平10−79297号公報
【特許文献20】
特開2001−267080号公報
【特許文献21】
特開2001−131174号公報
【非特許文献1】
Appl.Phys.Lett.51,913(1987)
【非特許文献2】
Nature,395,151(1998)
【非特許文献3】
Nature,347,539(1990)
【0012】
【発明が解決しようとする課題】
本発明の目的は、新規なフェナントロリン化合物を提供することにある。
【0013】
また本発明の目的は、特定なフェナントロリン化合物を用い、極めて高効率で高輝度な光出力を有する有機発光素子を提供することにある。
【0014】
また、極めて耐久性のある有機発光素子を提供することにある。
【0015】
さらには製造が容易でかつ比較的安価に作成可能な有機発光素子を提供する事にある。
【0016】
【課題を解決するための手段】
即ち、本発明のフェナントロリン化合物は、下記一般式[I]〜[III]のいずれかで示されることを特徴とする。
【0017】
【化8】
【0018】
(式中、R1、R2、R3、R4、R5およびR6は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基,置換あるいは無置換の複素環基またはハロゲン原子を表わし、同じであっても異なっていてもよい。Ar1およびAr2は、置換あるいは無置換のフルオレニル基、置換あるいは無置換のフルオランテニル基、置換あるいは無置換のペリレニル基または置換あるいは無置換のカルバゾリル基を表わし、同じであっても異なっていてもよい。)
【0019】
【化9】
【0020】
(式中、R7、R8、R9、R10、R11およびR12は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基,置換あるいは無置換の複素環基またはハロゲン原子を表わし、同じであっても異なっていてもよい。Ar3およびAr4は、置換あるいは無置換のフルオレニル基、置換あるいは無置換のフルオランテニル基、置換あるいは無置換のペリレニル基または置換あるいは無置換のカルバゾリル基を表わし、同じであっても異なっていてもよい。)
【0021】
【化10】
【0022】
(式中、R13、R14、R15およびR16は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基,置換あるいは無置換の複素環基またはハロゲン原子を表わす。R13およびR14は、同じであっても異なっていてもよい。Ar5、Ar6、Ar7およびAr8は、置換あるいは無置換のフルオレニル基、置換あるいは無置換のフルオランテニル基、置換あるいは無置換のペリレニル基または置換あるいは無置換のカルバゾリル基を表わし、同じであっても異なっていてもよい。)
【0023】
本発明のフェナントロリン化合物は、前記フルオレニル基が、下記一般式[IV]で示されることが好ましい。
【0024】
【化11】
【0025】
(式中、R17は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、置換あるいは無置換の複素環基、置換アミノ基、シアノ基またはハロゲン原子を表わす。R18およびR19は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基または置換あるいは無置換の複素環基を表わし、同じであっても異なっていてもよい。)
【0026】
また、前記フルオランテニル基が、下記一般式[V]で示されることが好ましい。
【0027】
【化12】
【0028】
(式中、R20は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、置換あるいは無置換の複素環基、置換アミノ基、シアノ基またはハロゲン原子を表わす。)
【0029】
また、前記ペリレニル基が、下記一般式[VI]で示されることが好ましい。
【0030】
【化13】
【0031】
(式中、R21は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、置換あるいは無置換の複素環基、置換アミノ基、シアノ基またはハロゲン原子を表わす。)
【0032】
また、前記カルバゾリル基が、下記一般式[VII]で示されることが好ましい。
【0033】
【化14】
【0034】
(式中、R22およびR23は、水素原子、置換あるいは無置換のアルキル基、置換あるいは無置換のアラルキル基、置換あるいは無置換のアリール基、置換あるいは無置換の複素環基、置換アミノ基、シアノ基またはハロゲン原子を表わし、同じであっても異なっていてもよい。)
【0035】
また、本発明の有機発光素子は、陽極及び陰極からなる一対の電極と、該一対の電極間に挟持された一または複数の有機化合物を含む層を少なくとも有する有機発光素子において、前記有機化合物を含む層の少なくとも一層が上記フェナントロリン化合物の少なくとも一種を含有することを特徴とする。
【0036】
【発明の実施の形態】
以下、本発明を詳細に説明する。
【0037】
まず、本発明のフェナントロリン化合物について説明する。
【0038】
本発明のフェナントロリン化合物は、上記一般式[I]〜[III]で示され、フルオレニル基が上記一般式[IV]、フルオランテニル基が上記一般式[V]、ペリレニル基が上記一般式[VI]、カルバゾリル基が上記一般式[VII]で示されるものであることが好ましい。
【0039】
上記一般式[I]〜[VII]における置換基の具体例を以下に示す。
【0040】
アルキル基としては、メチル基、エチル基、n−プロピル基、iso−プロピル基、n−ブチル基、ter−ブチル基、オクチル基などが挙げられる。
【0041】
アラルキル基としては、ベンジル基、フェネチル基などが挙げられる。
【0042】
アリール基としては、フェニル基、ビフェニル基、ターフェニル基などが挙げられる。
【0043】
複素環基としては、チエニル基、ピロリル基、ピリジル基、オキサゾリル基、オキサジアゾリル基、チアゾリル基、チアジアゾリル基、ターチエニル基などが挙げられる。
【0044】
置換アミノ基としては、ジメチルアミノ基、ジエチルアミノ基、ジベンジルアミノ基、ジフェニルアミノ基、ジトリルアミノ基、ジアニソリルアミノ基などが挙げられる。
【0045】
ハロゲン原子としては、フッ素、塩素、臭素、ヨウ素などが挙げられる。
【0046】
上記置換基が有してもよい置換基としては、メチル基、エチル基、プロピル基などのアルキル基、ベンジル基、フェネチル基などのアラルキル基、フェニル基、ビフェニル基などのアリール基、チエニル基、ピロリル基、ピリジル基などの複素環基、ジメチルアミノ基、ジエチルアミノ基、ジベンジルアミノ基、ジフェニルアミノ基、ジトリルアミノ基、ジアニソリルアミノ基などのアミノ基、メトキシル基、エトキシル基、プロポキシル基、フェノキシル基などのアルコキシル基、シアノ基、フッ素、塩素、臭素、ヨウ素などのハロゲン原子などが挙げられる。
【0047】
次に、本発明のフェナントロリン化合物の代表例を以下に挙げるが、本発明はこれらに限定されるものではない。
【0048】
【化15】
【0049】
【化16】
【0050】
【化17】
【0051】
【化18】
【0052】
【化19】
【0053】
【化20】
【0054】
【化21】
【0055】
【化22】
【0056】
【化23】
【0057】
【化24】
【0058】
本発明のフェナントロリン化合物は、一般的に知られている方法で合成でき、例えば、J.Org.Chem.,16,941−945(1951)、Tetrahedron,Lett.,36,3489−3490(1995)などに記載の方法でフェナントロリン化合物中間体を得て、さらにパラジウム触媒を用いたsuzuki coupling法(例えばChem.Rev.1995,95,2457−2483)などの合成法で得ることができる。
【0059】
本発明のフェナントロリン化合物は、従来の化合物に比べ電子輸送性および耐久性の優れた化合物であり、有機発光素子の有機化合物を含む層、特に、電子輸送層および発光層として有用であり、また真空蒸着法や溶液塗布法などによって形成した層は結晶化などが起こりにくく経時安定性に優れている。
【0060】
次に、本発明の有機発光素子について詳細に説明する。
【0061】
本発明の有機発光素子は、陽極及び陰極からなる一対の電極と、該一対の電極間に狭持された一または複数の有機化合物を含む層を少なくとも有する有機発光素子において、前記有機化合物を含む層の少なくとも一層が上記一般式[I]、[II]または[III]で示されるフェナントロリン化合物の少なくとも一種を含有する。
【0062】
本発明の有機発光素子は、有機化合物を含む層のうち少なくとも電子輸送層または発光層が、前記フェナントロリンの少なくとも一種を含有することが好ましい。
【0063】
本発明の有機発光素子においては、上記一般式[I]〜[III]で示されるフェナントロリン化合物を真空蒸着法や溶液塗布法により陽極及び陰極の間に形成する。その有機層の厚みは10μmより薄く、好ましくは0.5μm以下、より好ましくは0.01〜0.5μmの厚みに薄膜化することが好ましい。
【0064】
図1〜図6に本発明の有機発光素子の好ましい例を示す。
【0065】
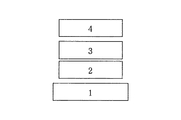
図1は、本発明の有機発光素子の一例を示す断面図である。図1は、基板1上に、陽極2、発光層3及び陰極4を順次設けた構成のものである。ここで使用する発光素子は、それ自体でホール輸送能、エレクトロン輸送能及び発光性の性能を単一で有している場合や、それぞれの特性を有する化合物を混ぜて使う場合に有用である。
【0066】
図2は、本発明の有機発光素子における他の例を示す断面図である。図2は、基板1上に、陽極2、ホール輸送層5、電子輸送層6及び陰極4を順次設けた構成のものである。この場合は、発光物質はホール輸送性かあるいは電子輸送性のいずれか、あるいは両方の機能を有している材料をそれぞれの層に用い、発光性の無い単なるホール輸送物質あるいは電子輸送物質と組み合わせて用いる場合に有用である。また、この場合、発光層は、ホール輸送層5あるいは電子輸送層6のいずれかから成る。
【0067】
図3は、本発明の有機発光素子における他の例を示す断面図である。図3は、基板1上に、陽極2、ホール輸送層5、発光層3,電子輸送層6及び陰極4を順次設けた構成のものである。これは、キャリヤ輸送と発光の機能を分離したものであり、ホール輸送性、電子輸送性、発光性の各特性を有した化合物と適時組み合わせて用いられ、極めて材料選択の自由度が増すとともに、発光波長を異にする種々の化合物が使用できるため、発光色相の多様化が可能になる。さらに、中央の発光層3に各キャリヤあるいは励起子を有効に閉じこめて、発光効率の向上を図ることも可能になる。
【0068】
図4は、本発明の有機発光素子における他の例を示す断面図である。図4は、図3に対して、ホール注入層7を陽極2側に挿入した構成であり、陽極2とホール輸送層5の密着性改善あるいはホールの注入性改善に効果があり、低電圧化に効果的である。
【0069】
図5および図6は、本発明の有機発光素子における他の例を示す断面図である。図5および図6は、図3および図4に対してホールあるいは励起子(エキシトン)を陰極4側に抜けることを阻害する層(ホールブロッキング層8)を、発光層3、電子輸送層6間に挿入した構成である。イオン化ポテンシャルの非常に高い化合物をホールブロッキング層8として用いる事により、発光効率の向上に効果的な構成である。
【0070】
ただし、図1〜図6はあくまで、ごく基本的な素子構成であり、本発明の化合物を用いた有機発光素子の構成はこれらに限定されるものではない。例えば、電極と有機層界面に絶縁性層を設ける、接着層あるいは干渉層を設ける、ホール輸送層がイオン化ポテンシャルの異なる2層から構成される、など多様な層構成をとることができる。
【0071】
本発明に用いられる一般式[I]〜[III]で示されるフェナントロリン化合物は、従来の化合物に比べ電子輸送性および耐久性の優れた化合物であり、図1〜図6のいずれの形態でも使用することができる。
【0072】
本発明は、電子輸送層または発光層の構成成分として一般式[I]〜[III]で示されるフェナントロリン化合物を用いるものであるが、これまで知られているホール輸送性化合物、発光性化合物あるいは電子輸送性化合物などを必要に応じて一緒に使用することもできる。
【0073】
以下にこれらの化合物例を挙げる。
【0074】
【化25】
【0075】
【化26】
【0076】
【化27】
【0077】
【化28】
【0078】
【化29】
【0079】
【化30】
【0080】
本発明の有機発光素子において、一般式[I]〜[III]で示されるフェナントロリン化合物を含有する層および他の有機化合物を含有する層は、一般には真空蒸着法あるいは、適当な溶媒に溶解させて塗布法により薄膜を形成する。特に塗布法で成膜する場合は、適当な結着樹脂と組み合わせて膜を形成することもできる。
【0081】
上記結着樹脂としては、広範囲な結着性樹脂より選択でき、たとえばポリビニルカルバゾール樹脂、ポリカーボネート樹脂、ポリエステル樹脂、ポリアリレート樹脂、ポリスチレン樹脂、アクリル樹脂、メタクリル樹脂、ブチラール樹脂、ポリビニルアセタール樹脂、ジアリルフタレート樹脂、フェノール樹脂、エポキシ樹脂、シリコーン樹脂、ポリスルホン樹脂、尿素樹脂等が挙げられるが、これらに限定されるものではない。また、これらは単独または共重合体ポリマーとして1種または2種以上混合してもよい。
【0082】
陽極材料としては、仕事関数がなるべく大きなものがよく、例えば、金、白金、ニッケル、パラジウム、コバルト、セレン、バナジウム等の金属単体あるいはこれらの合金、酸化錫、酸化亜鉛、酸化錫インジウム(ITO),酸化亜鉛インジウム等の金属酸化物が使用できる。また、ポリアニリン、ポリピロール、ポリチオフェン、ポリフェニレンスルフィド等の導電性ポリマーも使用できる。これらの電極物質は単独で用いてもよく、複数併用することもできる。
【0083】
一方、陰極材料としては、仕事関数の小さなものがよく、リチウム、ナトリウム、カリウム、セシウム、カルシウム、マグネシウム、アルミニウム、インジウム、銀、鉛、錫、クロム等の金属単体あるいは複数の合金として用いることができる。酸化錫インジウム(ITO)等の金属酸化物の利用も可能である。また、陰極は一層構成でもよく、多層構成をとることもできる。
【0084】
本発明で用いる基板としては、特に限定するものではないが、金属製基板、セラミックス製基板等の不透明性基板、ガラス、石英、プラスチックシート等の透明性基板が用いられる。また、基板にカラーフィルター膜、蛍光色変換フィルター膜、誘電体反射膜などを用いて発色光をコントロールする事も可能である。
【0085】
なお、作成した素子に対して、酸素や水分等との接触を防止する目的で保護層あるいは封止層を設けることもできる。保護層としては、ダイヤモンド薄膜、金属酸化物、金属窒化物等の無機材料膜、フッ素樹脂、ポリパラキシレン、ポリエチレン、シリコーン樹脂、ポリスチレン樹脂等の高分子膜、さらには、光硬化性樹脂等が挙げられる。また、ガラス、気体不透過性フィルム、金属などをカバーし、適当な封止樹脂により素子自体をパッケージングすることもできる。
【0086】
【実施例】
以下、実施例により本発明をさらに具体的に説明していくが、本発明はこれらに限定されるものではない。
【0087】
<合成例1>[例示化合物No.2の合成]
【0088】
【化31】
【0089】
300ml三ツ口フラスコに、2−ヨード−9,9−ジメチルフルオレン[1]5.8g(18.1mmol)およびジエチルエーテル80mlを入れ、窒素雰囲気中、−78度で攪拌下、n−ブチルリチウム(15%ヘキサン溶液)11.7ml(18.1mmol)を滴下した。室温まで昇温し1時間攪拌した後、−20度に冷却しバソフェナントロリン[2]1.5g(4.51mmol)のトルエン100ml分散液を滴下した。室温で12時間攪拌後、水を加え有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、アルミナカラム(ヘキサン+クロロホルム混合展開溶媒)で精製し、例示化合物No.2(黄色結晶)2.4g(収率74%)を得た。
【0090】
<合成例2>[例示化合物No.5の合成]
【0091】
【化32】
【0092】
500ml三ツ口フラスコに、4,7−ジブロモ−1,10−フェナントロリン[3]*1)1.0g(2.96mmol)、9,9−ジメチルフルオレン−2−ボロン酸[4]2.8g(11.8mmol)、トルエン140mlおよびエタノール70mlを入れ、窒素雰囲気中、室温で攪拌下、炭酸ナトリウム12g/水60mlの水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.17g(0.15mmol)を添加した。室温で30分攪拌した後、77度に昇温し3時間攪拌した。反応後、有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、アルミナカラム(ヘキサン+クロロホルム混合展開溶媒)で精製し、例示化合物No.5(白色結晶)1.5g(収率90%)を得た。
【0093】
<合成例3>[例示化合物No.20の合成]
【0094】
【化33】
【0095】
300ml三ツ口フラスコに、2−ヨード−9,9−ジメチルフルオレン[5]2.3g(7.18mmol)およびジエチルエーテル60mlを入れ、窒素雰囲気中、−78度で攪拌下、n−ブチルリチウム(15%ヘキサン溶液)4.6ml(7.18mmol)を滴下した。室温まで昇温し1時間攪拌した後、−20度に冷却し例示化合物No.5 1.0g(1.77mmol)のトルエン80ml分散液を滴下した。室温で12時間攪拌後、水を加え有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、アルミナカラム(ヘキサン+クロロホルム混合展開溶媒)で精製し、例示化合物No.20(黄色結晶)1.2g(収率73%)を得た。
【0096】
<合成例4>[例示化合物No.8の合成]
【0097】
【化34】
【0098】
500ml三ツ口フラスコに、3,8−ジブロモ−1,10−フェナントロリン[6]*2)1.0g(2.96mmol)、フルオランテン−8−ボロン酸[7]2.9g(11.8mmol)、トルエン140mlおよびエタノール70mlを入れ、窒素雰囲気中、室温で攪拌下、炭酸ナトリウム12g/水60mlの水溶液を滴下し、次いでテトラキス(トリフェニルホスフィン)パラジウム(0)0.17g(0.15mmol)を添加した。室温で30分攪拌した後、77度に昇温し3時間攪拌した。反応後、有機層をクロロホルムで抽出し無水硫酸ナトリウムで乾燥後、アルミナカラム(ヘキサン+クロロホルム混合展開溶媒)で精製し、例示化合物No.8(黄色結晶)1.4g(収率82%)を得た。
【0099】
<実施例1>
図3に示す構造の素子を作成した。
【0100】
基板1としてのガラス基板上に、陽極2としての酸化錫インジウム(ITO)をスパッタ法にて120nmの膜厚で成膜したものを透明導電性支持基板として用いた。これをアセトン、イソプロピルアルコール(IPA)で順次超音波洗浄し、次いでIPAで煮沸洗浄後、乾燥した。さらに、UV/オゾン洗浄したものを透明導電性支持基板として使用した。
【0101】
透明導電性支持基板上に下記構造式で示される化合物のクロロホルム溶液をスピンコート法により30nmの膜厚で成膜し、ホール輸送層5を形成した。
【0102】
【化35】
【0103】
さらに下記構造式で示されるIr錯体および例示化合物No.1で示されるフェナントロリン化合物(重量比5:100)を真空蒸着法により20nmの膜厚で成膜し、発光層3を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0104】
【化36】
【0105】
さらにアルミニウムトリスキノリノールを真空蒸着法により40nmの膜厚で成膜し、電子輸送層6を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0106】
次に、陰極4として、アルミニウムとリチウム(リチウム濃度1原子%)からなる蒸着材料を用いて、上記有機層の上に真空蒸着法により厚さ50nmの金属層膜を形成し、さらに真空蒸着法により厚さ150nmのアルミニウム層を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は1.0〜1.2nm/secの条件で成膜した。
【0107】
さらに、窒素雰囲気中で保護用ガラス板をかぶせ、アクリル樹脂系接着材で封止した。
【0108】
この様にして得られた素子に、ITO電極(陽極2)を正極、Al−Li電極(陰極4)を負極にして、10Vの直流電圧を印加すると18.0mA/cm2の電流密度で電流が素子に流れ、4500cd/m2の輝度で緑色の発光が観測された。
【0109】
さらに、電流密度を6.0mA/cm2に保ち100時間電圧を印加したところ、初期輝度850cd/m2から100時間後800cd/m2と輝度劣化は小さかった。
【0110】
<実施例2〜9>
例示化合物No.1に代えて、表1に示す例示化合物を用いた他は実施例1と同様に素子を作成し、同様な評価を行った。結果を表1に示す。
【0111】
<比較例1〜3>
例示化合物No.1に代えて、下記構造式で示される化合物を用いた他は実施例1と同様に素子を作成し、同様な評価を行った。結果を表1に示す。
【0112】
【化37】
【0113】
【表1】
【0114】
<実施例10>
図3に示す構造の素子を作成した。
【0115】
実施例1と同様に、透明導電性支持基板上にホール輸送層5を形成した。
【0116】
さらにクマリンおよびアルミニウムトリスキノリノール(重合比1:20)を真空蒸着法により20nmの膜厚で成膜し、発光層3を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0117】
さらに例示化合物No.3により40nmの膜厚で成膜し、電子輸送層6を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0118】
次に、実施例1と同様にして陰極4を形成した後に封止した。
【0119】
この様にして得られた素子に、ITO電極(陽極2)を正極、Al−Li電極(陰極4)を負極にして、8Vの直流電圧を印加すると1110mA/cm2の電流密度で電流が素子に流れ、95000cd/m2の輝度で緑色の発光が観測された。
【0120】
さらに、電流密度を200mA/cm2に保ち100時間電圧を印加したところ、初期輝度10000cd/m2から100時間後8500cd/m2と輝度劣化は小さかった。
【0121】
<実施例11〜18>
例示化合物No.3に代えて、表2に示す例示化合物を用いた他は実施例10と同様に素子を作成し、同様な評価を行った。結果を表2に示す。
【0122】
<比較例4〜6>
例示化合物No.3に代えて、比較化合物No.1〜3を用いた他は実施例10と同様に素子を作成し、同様な評価を行った。結果を表2に示す。
【0123】
【表2】
【0124】
<実施例19>
図3に示す構造の素子を作成した。
【0125】
実施例1と同様に、透明導電性支持基板上にホール輸送層5を形成した。
【0126】
さらに下記構造式で示されるIr錯体および下記構造式で示されるカルバゾール化合物(重合比5:100)を真空蒸着法により20nmの膜厚で成膜し、発光層3を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0127】
【化38】
【0128】
【化39】
【0129】
さらに例示化合物No.5を用い40nmの膜厚で成膜し、電子輸送層6を形成した。蒸着時の真空度は1.0×10−4Pa、成膜速度は0.2〜0.3nm/secの条件で成膜した。
【0130】
次に、実施例1と同様にして陰極4を形成した後に封止した。
【0131】
この様にして得られた素子に、ITO電極(陽極2)を正極、Al−Li電極(陰極4)を負極にして、10Vの直流電圧を印加すると20.0mA/cm2の電流密度で電流が素子に流れ、6800cd/m2の輝度で緑色の発光が観測された。
【0132】
さらに、電流密度を6.0mA/cm2に保ち100時間電圧を印加したところ、初期輝度1300cd/m2から100時間後1150cd/m2と輝度劣化は小さかった。
【0133】
<実施例20〜31>
例示化合物No.5に代えて、表3に示す例示化合物を用いた他は実施例19と同様に素子を作成し、同様な評価を行った。結果を表3に示す。
【0134】
<比較例7〜9>
例示化合物No.5に代えて、比較化合物No.1〜3を用いた他は実施例19と同様に素子を作成し、同様な評価を行った。結果を表3に示す。
【0135】
【表3】
【0136】
【発明の効果】
以上説明のように、一般式[I]〜[III]で示されるフェナントロリン化合物を用いた有機発光素子は、低い印加電圧で高輝度な発光が得られ、耐久性にも優れている。特に本発明のフェナントロリン化合物を含有する有機層は、電子輸送層として優れ、かつ発光層としても優れている。
【0137】
さらに、素子の作成も真空蒸着あるいはキャステイング法等を用いて作成可能であり、比較的安価で大面積の素子を容易に作成できる。
【図面の簡単な説明】
【図1】本発明における有機発光素子の一例を示す断面図である。
【図2】本発明における有機発光素子の他の例を示す断面図である。
【図3】本発明における有機発光素子の他の例を示す断面図である。
【図4】本発明における有機発光素子の他の例を示す断面図である。
【図5】本発明における有機発光素子の他の例を示す断面図である。
【図6】本発明における有機発光素子の他の例を示す断面図である。
【符号の説明】
1 基板
2 陽極
3 発光層
4 陰極
5 ホール輸送層
6 電子輸送層
7 ホール注入層
8 ホール/エキシトンブロッキング層
Claims (9)
- 陽極及び陰極からなる一対の電極と、該一対の電極間に挟持された一または複数の有機化合物を含む層を少なくとも有する有機発光素子において、前記有機化合物を含む層の少なくとも一層が請求項1〜7のいずれかに記載のフェナントロリン化合物の少なくとも一種を含有することを特徴とする有機発光素子。
- 前記有機化合物を含む層のうち少なくとも電子輸送層または発光層が、前記フェナントロリン化合物の少なくとも一種を含有することを特徴とする請求項8に記載の有機発光素子。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002272408A JP4261855B2 (ja) | 2002-09-19 | 2002-09-19 | フェナントロリン化合物及びそれを用いた有機発光素子 |
| AU2003260955A AU2003260955A1 (en) | 2002-09-19 | 2003-09-09 | Phenanthroline compound and organic light emitting device using same |
| US10/527,192 US7550594B2 (en) | 2002-09-19 | 2003-09-09 | Phenanthroline compound and organic light emitting device using same |
| PCT/JP2003/011485 WO2004026870A1 (en) | 2002-09-19 | 2003-09-09 | Phenanthroline compound and organic light emitting device using same |
| US12/436,507 US7982213B2 (en) | 2002-09-19 | 2009-05-06 | Phenanthroline compound and organic light emitting device using same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002272408A JP4261855B2 (ja) | 2002-09-19 | 2002-09-19 | フェナントロリン化合物及びそれを用いた有機発光素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004107263A true JP2004107263A (ja) | 2004-04-08 |
| JP4261855B2 JP4261855B2 (ja) | 2009-04-30 |
Family
ID=32024930
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002272408A Expired - Fee Related JP4261855B2 (ja) | 2002-09-19 | 2002-09-19 | フェナントロリン化合物及びそれを用いた有機発光素子 |
Country Status (4)
| Country | Link |
|---|---|
| US (2) | US7550594B2 (ja) |
| JP (1) | JP4261855B2 (ja) |
| AU (1) | AU2003260955A1 (ja) |
| WO (1) | WO2004026870A1 (ja) |
Cited By (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004171808A (ja) * | 2002-11-18 | 2004-06-17 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP2004178895A (ja) * | 2002-11-26 | 2004-06-24 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子および表示装置 |
| JP2005213348A (ja) * | 2004-01-29 | 2005-08-11 | Sony Corp | 有機発光材料および有機電界発光素子 |
| WO2006004138A1 (en) * | 2004-07-07 | 2006-01-12 | Semiconductor Energy Laboratory Co., Ltd. | Phenanthroline derivative and light emitting element and light emitting device using the same |
| JP2008205488A (ja) * | 2008-03-22 | 2008-09-04 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP2008252094A (ja) * | 2008-03-22 | 2008-10-16 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| US7517596B2 (en) * | 2004-11-29 | 2009-04-14 | Canon Kabushiki Kaisha | Phenanthroline compound and light-emitting device |
| WO2009057567A1 (ja) * | 2007-11-02 | 2009-05-07 | Toray Industries, Inc. | 発光素子材料および発光素子 |
| WO2009091231A2 (ko) | 2008-01-18 | 2009-07-23 | Lg Chem, Ltd. | 유기발광소자 및 이의 제조 방법 |
| JP2009194403A (ja) * | 2009-06-04 | 2009-08-27 | Semiconductor Energy Lab Co Ltd | 電界発光素子 |
| WO2009139607A2 (ko) | 2008-05-16 | 2009-11-19 | 주식회사 엘지화학 | 적층형 유기발광소자 |
| WO2010039009A2 (ko) | 2008-10-01 | 2010-04-08 | 주식회사 엘지화학 | 유기발광소자 및 이의 제조방법 |
| JP2010222331A (ja) * | 2009-03-25 | 2010-10-07 | Toshiba Corp | 発光層化合物および有機電界発光素子 |
| US8040044B2 (en) | 2005-07-15 | 2011-10-18 | Lg Chem, Ltd. | Organic light emitting device and method for manufacturing the same |
| JP2012505861A (ja) * | 2008-10-16 | 2012-03-08 | ソルヴェイ(ソシエテ アノニム) | 発光ダイオード用ホスト材料 |
| JP2012513679A (ja) * | 2008-12-22 | 2012-06-14 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | フェナントロリン誘導体を含む電子素子 |
| JP2012188517A (ja) * | 2011-03-10 | 2012-10-04 | National Institute For Materials Science | 配位数4の金属及びビスフェナントロリン誘導体を含む有機/金属ハイブリッドポリマー、その配位子、及びその製造方法 |
| JP2013110224A (ja) * | 2011-11-18 | 2013-06-06 | Mitsubishi Chemicals Corp | 光電変換素子、太陽電池、及び太陽電池モジュール |
| WO2013180542A1 (ko) | 2012-05-31 | 2013-12-05 | 주식회사 엘지화학 | 적층형 유기전계발광소자 |
| WO2013180540A1 (ko) | 2012-05-31 | 2013-12-05 | 주식회사 엘지화학 | 유기전계발광소자 |
| WO2014042163A1 (ja) * | 2012-09-12 | 2014-03-20 | 出光興産株式会社 | 新規化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子および電子機器 |
| JP2014509585A (ja) * | 2011-03-11 | 2014-04-21 | ベー・エル・アー・ハー・エム・エス・ゲーエムベーハー | フェナントロリン化合物を配位子とする希土類金属錯体 |
| US8748013B2 (en) | 2003-03-20 | 2014-06-10 | Semiconductor Energy Laboratory Co., Ltd. | Electroluminescent device |
| WO2014196677A1 (ko) | 2013-06-07 | 2014-12-11 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR20170105040A (ko) | 2015-01-29 | 2017-09-18 | 도레이 카부시키가이샤 | 페난트롤린 유도체, 그것을 함유하는 전자 디바이스, 발광 소자 및 광전 변환 소자 |
| US10522788B2 (en) | 2012-05-31 | 2019-12-31 | Lg Display Co., Ltd. | Organic light emitting diode |
| US11563183B2 (en) | 2017-06-21 | 2023-01-24 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11588111B2 (en) | 2017-08-04 | 2023-02-21 | Samsung Display Co., Ltd. | Condensed-cyclic compound and organic light-emitting device including the same |
| WO2024034301A1 (ja) * | 2022-08-09 | 2024-02-15 | 株式会社日本触媒 | フェナントロリン化合物およびそれを用いた有機薄膜、有機半導体素子 |
Families Citing this family (106)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3890317B2 (ja) * | 2003-04-30 | 2007-03-07 | キヤノン株式会社 | 発光素子 |
| JP4533015B2 (ja) * | 2004-06-15 | 2010-08-25 | キヤノン株式会社 | 化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2006128624A (ja) * | 2004-09-29 | 2006-05-18 | Canon Inc | 発光素子 |
| BRPI0516786A (pt) * | 2004-11-24 | 2008-09-23 | Univ Princeton | dispositivo optoeletrÈnico fotosensìvel orgánico tendo uma camada bloqueadora de éxcitons de fenantrolina |
| JP4478555B2 (ja) * | 2004-11-30 | 2010-06-09 | キヤノン株式会社 | 金属錯体、発光素子及び画像表示装置 |
| US7714501B2 (en) * | 2004-12-01 | 2010-05-11 | Semiconductor Energy Laboratory Co., Ltd. | Light emitting element, light emitting device and electronic equipment |
| JP4865258B2 (ja) * | 2005-06-21 | 2012-02-01 | キヤノン株式会社 | 1,8−ナフチリジン化合物及びそれを用いた有機発光素子 |
| US9666826B2 (en) | 2005-11-30 | 2017-05-30 | Global Oled Technology Llc | Electroluminescent device including an anthracene derivative |
| US20070122657A1 (en) * | 2005-11-30 | 2007-05-31 | Eastman Kodak Company | Electroluminescent device containing a phenanthroline derivative |
| JP4770699B2 (ja) * | 2005-12-16 | 2011-09-14 | ソニー株式会社 | 表示素子 |
| JP2007308477A (ja) * | 2006-04-20 | 2007-11-29 | Canon Inc | 化合物および有機発光素子 |
| JP4227628B2 (ja) * | 2006-04-25 | 2009-02-18 | キヤノン株式会社 | 化合物および有機発光素子 |
| US7754348B2 (en) * | 2007-04-25 | 2010-07-13 | Luminescene Technology Corp. | Phenanthroline compound and organic light emitting device using the same |
| JP5159164B2 (ja) * | 2007-05-14 | 2013-03-06 | キヤノン株式会社 | ベンゾ[ghi]フルオランテン誘導体及びこれを用いた有機発光素子 |
| US8420229B2 (en) * | 2007-10-26 | 2013-04-16 | Global OLED Technologies LLC | OLED device with certain fluoranthene light-emitting dopants |
| US8129039B2 (en) * | 2007-10-26 | 2012-03-06 | Global Oled Technology, Llc | Phosphorescent OLED device with certain fluoranthene host |
| US8076009B2 (en) * | 2007-10-26 | 2011-12-13 | Global Oled Technology, Llc. | OLED device with fluoranthene electron transport materials |
| US8431242B2 (en) | 2007-10-26 | 2013-04-30 | Global Oled Technology, Llc. | OLED device with certain fluoranthene host |
| US20090110956A1 (en) * | 2007-10-26 | 2009-04-30 | Begley William J | Oled device with electron transport material combination |
| CN101861292A (zh) * | 2007-11-19 | 2010-10-13 | 出光兴产株式会社 | 单苯并*衍生物及含有它的有机电致发光元件用材料、以及使用它的有机电致发光元件 |
| EP2072517B1 (de) * | 2007-12-21 | 2015-01-21 | Novaled GmbH | Asymmetrische Phenanthroline, deren Herstellungsverfahren und diese enthaltendes dotiertes organisches Halbleitermaterial |
| EP2161272A1 (en) | 2008-09-05 | 2010-03-10 | Basf Se | Phenanthrolines |
| US7931975B2 (en) * | 2008-11-07 | 2011-04-26 | Global Oled Technology Llc | Electroluminescent device containing a flouranthene compound |
| US8088500B2 (en) * | 2008-11-12 | 2012-01-03 | Global Oled Technology Llc | OLED device with fluoranthene electron injection materials |
| US7968215B2 (en) * | 2008-12-09 | 2011-06-28 | Global Oled Technology Llc | OLED device with cyclobutene electron injection materials |
| US8216697B2 (en) * | 2009-02-13 | 2012-07-10 | Global Oled Technology Llc | OLED with fluoranthene-macrocyclic materials |
| US20100244677A1 (en) * | 2009-03-31 | 2010-09-30 | Begley William J | Oled device containing a silyl-fluoranthene derivative |
| US9153790B2 (en) | 2009-05-22 | 2015-10-06 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| EP2477986B1 (en) * | 2009-09-14 | 2014-11-12 | B.R.A.H.M.S GmbH | Phenanthroline derivatives and their use as ligands |
| JPWO2011046182A1 (ja) | 2009-10-16 | 2013-03-07 | 出光興産株式会社 | 含フルオレン芳香族化合物、有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| WO2011086935A1 (ja) | 2010-01-15 | 2011-07-21 | 出光興産株式会社 | 含窒素複素環誘導体及びそれを含んでなる有機エレクトロルミネッセンス素子 |
| US20140217393A1 (en) * | 2011-09-09 | 2014-08-07 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| KR101722027B1 (ko) | 2012-05-03 | 2017-04-03 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| US9859517B2 (en) * | 2012-09-07 | 2018-01-02 | Nitto Denko Corporation | White organic light-emitting diode |
| KR102120894B1 (ko) | 2013-05-03 | 2020-06-10 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR102172735B1 (ko) * | 2013-10-29 | 2020-11-02 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US9698357B2 (en) | 2014-11-28 | 2017-07-04 | Luminescence Technology Corporation | Phenanthroline-based compound and use thereof |
| US9929361B2 (en) | 2015-02-16 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056657B2 (en) | 2015-02-27 | 2021-07-06 | University Display Corporation | Organic electroluminescent materials and devices |
| US9768390B2 (en) | 2015-03-26 | 2017-09-19 | Feng-wen Yen | Phenanthroline derivative for organic electroluminescent device |
| US9692003B2 (en) * | 2015-04-15 | 2017-06-27 | Feng-wen Yen | Phenanthroline derivative and use thereof |
| US9859510B2 (en) | 2015-05-15 | 2018-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418568B2 (en) | 2015-06-01 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11127905B2 (en) | 2015-07-29 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672996B2 (en) | 2015-09-03 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20170229663A1 (en) | 2016-02-09 | 2017-08-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10236456B2 (en) | 2016-04-11 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482683B2 (en) | 2016-06-20 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862054B2 (en) | 2016-06-20 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672997B2 (en) | 2016-06-20 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608186B2 (en) | 2016-09-14 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680187B2 (en) | 2016-09-23 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11196010B2 (en) | 2016-10-03 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11011709B2 (en) | 2016-10-07 | 2021-05-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20180130956A1 (en) | 2016-11-09 | 2018-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680188B2 (en) | 2016-11-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11780865B2 (en) | 2017-01-09 | 2023-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10844085B2 (en) | 2017-03-29 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944060B2 (en) | 2017-05-11 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20180370999A1 (en) | 2017-06-23 | 2018-12-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744142B2 (en) | 2017-08-10 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20190161504A1 (en) | 2017-11-28 | 2019-05-30 | University Of Southern California | Carbene compounds and organic electroluminescent devices |
| EP3492480B1 (en) | 2017-11-29 | 2021-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937503B2 (en) | 2017-11-30 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11542289B2 (en) | 2018-01-26 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR101926770B1 (ko) * | 2018-03-05 | 2018-12-07 | 주식회사 진웅산업 | 페난트롤린 화합물 및 이를 포함하는 유기발광소자 |
| US20200075870A1 (en) | 2018-08-22 | 2020-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11737349B2 (en) | 2018-12-12 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11780829B2 (en) | 2019-01-30 | 2023-10-10 | The University Of Southern California | Organic electroluminescent materials and devices |
| US20200251664A1 (en) | 2019-02-01 | 2020-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP2020158491A (ja) | 2019-03-26 | 2020-10-01 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネセンス材料及びデバイス |
| CN110144213A (zh) * | 2019-05-31 | 2019-08-20 | 北京诚志永华显示科技有限公司 | 有机电致发光材料、有机电致发光器件 |
| US20210032278A1 (en) | 2019-07-30 | 2021-02-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20210047354A1 (en) | 2019-08-16 | 2021-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20210135130A1 (en) | 2019-11-04 | 2021-05-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20210217969A1 (en) | 2020-01-06 | 2021-07-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220336759A1 (en) | 2020-01-28 | 2022-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN111574505B (zh) * | 2020-05-22 | 2021-08-03 | 西安瑞联新材料股份有限公司 | 一种以苯并[c]噌啉为受体的化合物及其应用 |
| EP3937268A1 (en) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonic oleds and vertical dipole emitters |
| US20220158096A1 (en) | 2020-11-16 | 2022-05-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220165967A1 (en) | 2020-11-24 | 2022-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220162243A1 (en) | 2020-11-24 | 2022-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220271241A1 (en) | 2021-02-03 | 2022-08-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4060758A3 (en) | 2021-02-26 | 2023-03-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4059915A3 (en) | 2021-02-26 | 2022-12-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298192A1 (en) | 2021-03-05 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298190A1 (en) | 2021-03-12 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298193A1 (en) | 2021-03-15 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220340607A1 (en) | 2021-04-05 | 2022-10-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4075531A1 (en) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonic oleds and vertical dipole emitters |
| US20220352478A1 (en) | 2021-04-14 | 2022-11-03 | Universal Display Corporation | Organic eletroluminescent materials and devices |
| US20220407020A1 (en) | 2021-04-23 | 2022-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230006149A1 (en) | 2021-04-23 | 2023-01-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230133787A1 (en) | 2021-06-08 | 2023-05-04 | University Of Southern California | Molecular Alignment of Homoleptic Iridium Phosphors |
| EP4151699A1 (en) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4212539A1 (en) | 2021-12-16 | 2023-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR102625989B1 (ko) * | 2022-02-08 | 2024-01-18 | 광주과학기술원 | 신규 페난스롤린계 화합물, 이의 제조방법 및 이를 패시베이션층으로 포함하는 광전자 소자 |
| EP4231804A3 (en) | 2022-02-16 | 2023-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230292592A1 (en) | 2022-03-09 | 2023-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230337516A1 (en) | 2022-04-18 | 2023-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230389421A1 (en) | 2022-05-24 | 2023-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4293001A1 (en) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240016051A1 (en) | 2022-06-28 | 2024-01-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240107880A1 (en) | 2022-08-17 | 2024-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN116514778A (zh) * | 2023-06-26 | 2023-08-01 | 季华实验室 | 一种有机电子传输材料、有机电致发光器件 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) * | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US4720432A (en) * | 1987-02-11 | 1988-01-19 | Eastman Kodak Company | Electroluminescent device with organic luminescent medium |
| US4885211A (en) * | 1987-02-11 | 1989-12-05 | Eastman Kodak Company | Electroluminescent device with improved cathode |
| US5130603A (en) * | 1989-03-20 | 1992-07-14 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| GB8909011D0 (en) * | 1989-04-20 | 1989-06-07 | Friend Richard H | Electroluminescent devices |
| JP2815472B2 (ja) * | 1990-01-22 | 1998-10-27 | パイオニア株式会社 | 電界発光素子 |
| DE69110922T2 (de) * | 1990-02-23 | 1995-12-07 | Sumitomo Chemical Co | Organisch elektrolumineszente Vorrichtung. |
| GB9018698D0 (en) * | 1990-08-24 | 1990-10-10 | Lynxvale Ltd | Semiconductive copolymers for use in electroluminescent devices |
| US5382477A (en) * | 1991-02-27 | 1995-01-17 | Sanyo Electric Co., Ltd. | Organic electroluminescent element and process for producing the same |
| US5151629A (en) * | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| JPH05202356A (ja) | 1991-09-11 | 1993-08-10 | Pioneer Electron Corp | 有機エレクトロルミネッセンス素子 |
| JP3328731B2 (ja) | 1991-12-05 | 2002-09-30 | 住友化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| US5393614A (en) * | 1992-04-03 | 1995-02-28 | Pioneer Electronic Corporation | Organic electroluminescence device |
| US5514878A (en) * | 1994-03-18 | 1996-05-07 | Holmes; Andrew B. | Polymers for electroluminescent devices |
| JPH0782551A (ja) | 1993-09-09 | 1995-03-28 | Nisshinbo Ind Inc | 有機エレクトロルミネッセンス素子 |
| US5409783A (en) * | 1994-02-24 | 1995-04-25 | Eastman Kodak Company | Red-emitting organic electroluminescent device |
| JPH09202878A (ja) | 1996-01-25 | 1997-08-05 | Nippon Telegr & Teleph Corp <Ntt> | 近紫外・紫外波長帯発光素子 |
| JPH09227576A (ja) | 1996-02-23 | 1997-09-02 | Sony Corp | 金属複核錯体、その製造方法及び光学的素子 |
| JPH1079297A (ja) * | 1996-07-09 | 1998-03-24 | Sony Corp | 電界発光素子 |
| PL204863B1 (pl) | 1998-07-22 | 2010-02-26 | Stichting Dienst Landbouwkundi | Zastosowanie mutanta Streptococcus, szczepionka i sposoby kontrolowania lub eliminowania choroby paciorkowcowej w populacji |
| JP2001131174A (ja) * | 1999-11-02 | 2001-05-15 | Sony Corp | バソフェナントロリン化合物及びその製造方法 |
| JP3924648B2 (ja) | 1999-11-02 | 2007-06-06 | ソニー株式会社 | 有機電界発光素子 |
| JP4876311B2 (ja) | 2000-01-14 | 2012-02-15 | 東レ株式会社 | 発光素子 |
| JP4729776B2 (ja) * | 2000-08-04 | 2011-07-20 | 東レ株式会社 | 発光素子 |
| WO2003076549A1 (fr) * | 2002-03-08 | 2003-09-18 | Canon Kabushiki Kaisha | Element electroluminescent contenant un compose de coordination metallique |
-
2002
- 2002-09-19 JP JP2002272408A patent/JP4261855B2/ja not_active Expired - Fee Related
-
2003
- 2003-09-09 US US10/527,192 patent/US7550594B2/en active Active
- 2003-09-09 AU AU2003260955A patent/AU2003260955A1/en not_active Abandoned
- 2003-09-09 WO PCT/JP2003/011485 patent/WO2004026870A1/en active Application Filing
-
2009
- 2009-05-06 US US12/436,507 patent/US7982213B2/en not_active Expired - Fee Related
Cited By (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004171808A (ja) * | 2002-11-18 | 2004-06-17 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP2004178895A (ja) * | 2002-11-26 | 2004-06-24 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子および表示装置 |
| US8748013B2 (en) | 2003-03-20 | 2014-06-10 | Semiconductor Energy Laboratory Co., Ltd. | Electroluminescent device |
| JP2005213348A (ja) * | 2004-01-29 | 2005-08-11 | Sony Corp | 有機発光材料および有機電界発光素子 |
| WO2006004138A1 (en) * | 2004-07-07 | 2006-01-12 | Semiconductor Energy Laboratory Co., Ltd. | Phenanthroline derivative and light emitting element and light emitting device using the same |
| US7750159B2 (en) | 2004-07-07 | 2010-07-06 | Semiconductor Energy Laboratory Co., Ltd. | Phenanthroline derivative and light emitting element and light emitting device using the same |
| US7517596B2 (en) * | 2004-11-29 | 2009-04-14 | Canon Kabushiki Kaisha | Phenanthroline compound and light-emitting device |
| US8040044B2 (en) | 2005-07-15 | 2011-10-18 | Lg Chem, Ltd. | Organic light emitting device and method for manufacturing the same |
| US8962155B2 (en) | 2007-11-02 | 2015-02-24 | Toray Industries, Inc. | Light emitting device based on a pyrromethene compound |
| JPWO2009057567A1 (ja) * | 2007-11-02 | 2011-03-10 | 東レ株式会社 | 発光素子材料および発光素子 |
| WO2009057567A1 (ja) * | 2007-11-02 | 2009-05-07 | Toray Industries, Inc. | 発光素子材料および発光素子 |
| WO2009091231A2 (ko) | 2008-01-18 | 2009-07-23 | Lg Chem, Ltd. | 유기발광소자 및 이의 제조 방법 |
| JP2008252094A (ja) * | 2008-03-22 | 2008-10-16 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| JP2008205488A (ja) * | 2008-03-22 | 2008-09-04 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子及び表示装置 |
| WO2009139607A2 (ko) | 2008-05-16 | 2009-11-19 | 주식회사 엘지화학 | 적층형 유기발광소자 |
| US8637854B2 (en) | 2008-05-16 | 2014-01-28 | Lg Chem, Ltd. | Stacked organic light emitting diode |
| US9587172B2 (en) | 2008-10-01 | 2017-03-07 | Lg Display Co., Ltd. | Organic light-emitting diode and method of manufacturing the same |
| WO2010039009A2 (ko) | 2008-10-01 | 2010-04-08 | 주식회사 엘지화학 | 유기발광소자 및 이의 제조방법 |
| JP2012505861A (ja) * | 2008-10-16 | 2012-03-08 | ソルヴェイ(ソシエテ アノニム) | 発光ダイオード用ホスト材料 |
| TWI468492B (zh) * | 2008-10-16 | 2015-01-11 | Solvay | 用於發光二極體之主體材料 |
| JP2012513679A (ja) * | 2008-12-22 | 2012-06-14 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | フェナントロリン誘導体を含む電子素子 |
| JP2010222331A (ja) * | 2009-03-25 | 2010-10-07 | Toshiba Corp | 発光層化合物および有機電界発光素子 |
| JP2009194403A (ja) * | 2009-06-04 | 2009-08-27 | Semiconductor Energy Lab Co Ltd | 電界発光素子 |
| JP2012188517A (ja) * | 2011-03-10 | 2012-10-04 | National Institute For Materials Science | 配位数4の金属及びビスフェナントロリン誘導体を含む有機/金属ハイブリッドポリマー、その配位子、及びその製造方法 |
| JP2014509585A (ja) * | 2011-03-11 | 2014-04-21 | ベー・エル・アー・ハー・エム・エス・ゲーエムベーハー | フェナントロリン化合物を配位子とする希土類金属錯体 |
| JP2013110224A (ja) * | 2011-11-18 | 2013-06-06 | Mitsubishi Chemicals Corp | 光電変換素子、太陽電池、及び太陽電池モジュール |
| WO2013180542A1 (ko) | 2012-05-31 | 2013-12-05 | 주식회사 엘지화학 | 적층형 유기전계발광소자 |
| WO2013180540A1 (ko) | 2012-05-31 | 2013-12-05 | 주식회사 엘지화학 | 유기전계발광소자 |
| US10522788B2 (en) | 2012-05-31 | 2019-12-31 | Lg Display Co., Ltd. | Organic light emitting diode |
| JPWO2014042163A1 (ja) * | 2012-09-12 | 2016-08-18 | 出光興産株式会社 | 新規化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子および電子機器 |
| US9871206B2 (en) | 2012-09-12 | 2018-01-16 | Idemitsu Kosan Co., Ltd. | Compound, organic electroluminescence device material, organic electroluminescence device and electronic device |
| CN110003199A (zh) * | 2012-09-12 | 2019-07-12 | 出光兴产株式会社 | 新型化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 |
| US10510964B2 (en) | 2012-09-12 | 2019-12-17 | Idemitsu Kosan Co., Ltd. | Compound, organic electroluminescence device material, organic electroluminescence device and electronic device |
| WO2014042163A1 (ja) * | 2012-09-12 | 2014-03-20 | 出光興産株式会社 | 新規化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子および電子機器 |
| CN110003199B (zh) * | 2012-09-12 | 2022-09-23 | 出光兴产株式会社 | 新型化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 |
| WO2014196677A1 (ko) | 2013-06-07 | 2014-12-11 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR20170105040A (ko) | 2015-01-29 | 2017-09-18 | 도레이 카부시키가이샤 | 페난트롤린 유도체, 그것을 함유하는 전자 디바이스, 발광 소자 및 광전 변환 소자 |
| JPWO2016121597A1 (ja) * | 2015-01-29 | 2017-11-02 | 東レ株式会社 | フェナントロリン誘導体、それを含有する電子デバイス、発光素子および光電変換素子 |
| US11563183B2 (en) | 2017-06-21 | 2023-01-24 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11844273B2 (en) | 2017-06-21 | 2023-12-12 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US11588111B2 (en) | 2017-08-04 | 2023-02-21 | Samsung Display Co., Ltd. | Condensed-cyclic compound and organic light-emitting device including the same |
| WO2024034301A1 (ja) * | 2022-08-09 | 2024-02-15 | 株式会社日本触媒 | フェナントロリン化合物およびそれを用いた有機薄膜、有機半導体素子 |
Also Published As
| Publication number | Publication date |
|---|---|
| US7550594B2 (en) | 2009-06-23 |
| AU2003260955A1 (en) | 2004-04-08 |
| US20060097227A1 (en) | 2006-05-11 |
| JP4261855B2 (ja) | 2009-04-30 |
| WO2004026870A1 (en) | 2004-04-01 |
| US7982213B2 (en) | 2011-07-19 |
| US20090218940A1 (en) | 2009-09-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4261855B2 (ja) | フェナントロリン化合物及びそれを用いた有機発光素子 | |
| JP3848224B2 (ja) | スピロ化合物及びそれを用いた有機発光素子 | |
| JP3902993B2 (ja) | フルオレン化合物及びそれを用いた有機発光素子 | |
| JP4065547B2 (ja) | フルオレン化合物及びそれを用いた有機発光素子 | |
| JP4336483B2 (ja) | ジアザフルオレン化合物及びそれを用いた有機発光素子 | |
| JP4585750B2 (ja) | 縮合多環化合物及びそれを用いた有機発光素子 | |
| JP3870102B2 (ja) | 有機発光素子 | |
| JP4865258B2 (ja) | 1,8−ナフチリジン化合物及びそれを用いた有機発光素子 | |
| JP4240841B2 (ja) | 有機発光素子 | |
| JP3848262B2 (ja) | オリゴフルオレニレン化合物及び有機発光素子 | |
| JP4871464B2 (ja) | 有機発光素子 | |
| JP4323935B2 (ja) | 有機発光素子 | |
| KR101188461B1 (ko) | 축합환 방향족 화합물 및 이것을 이용한 유기 발광소자 | |
| JP2003138251A (ja) | 有機発光素子 | |
| JP2004083513A (ja) | モノアミノ化合物およびそれを使用した有機発光素子 | |
| JP4541809B2 (ja) | 有機化合物及び有機発光素子 | |
| JP4336537B2 (ja) | 有機発光素子 | |
| JP2003109765A (ja) | 有機発光素子 | |
| JP4065552B2 (ja) | 有機発光素子 | |
| JP2003109763A (ja) | 有機発光素子 | |
| JP4950460B2 (ja) | 有機発光素子 | |
| JP2003109764A (ja) | 有機発光素子 | |
| JP2007001879A (ja) | 1,9,10−アンスリジン化合物及びそれを用いた有機発光素子 | |
| JP4035499B2 (ja) | 有機発光素子 | |
| JP4423022B2 (ja) | 2,1−ベンゾイソチアゾール化合物及びそれを用いた有機発光素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050125 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20081021 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081222 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090127 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090206 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120220 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4261855 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130220 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140220 Year of fee payment: 5 |
|
| LAPS | Cancellation because of no payment of annual fees |