DE60210697T2 - Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia - Google Patents
Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia Download PDFInfo
- Publication number
- DE60210697T2 DE60210697T2 DE60210697T DE60210697T DE60210697T2 DE 60210697 T2 DE60210697 T2 DE 60210697T2 DE 60210697 T DE60210697 T DE 60210697T DE 60210697 T DE60210697 T DE 60210697T DE 60210697 T2 DE60210697 T2 DE 60210697T2
- Authority
- DE
- Germany
- Prior art keywords
- bacterium
- amino acid
- strain
- increased
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 241000894006 Bacteria Species 0.000 title claims description 107
- 150000008575 L-amino acids Chemical class 0.000 title claims description 75
- 238000000034 method Methods 0.000 title claims description 55
- 238000004519 manufacturing process Methods 0.000 title claims description 27
- 241000588722 Escherichia Species 0.000 title claims description 18
- 230000008569 process Effects 0.000 title claims description 12
- 108090000623 proteins and genes Proteins 0.000 claims description 125
- 102000004169 proteins and genes Human genes 0.000 claims description 74
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 claims description 50
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 47
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 44
- 150000001413 amino acids Chemical group 0.000 claims description 38
- 230000000694 effects Effects 0.000 claims description 37
- 239000004473 Threonine Substances 0.000 claims description 31
- 229960002898 threonine Drugs 0.000 claims description 31
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 claims description 30
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 28
- 229960002429 proline Drugs 0.000 claims description 28
- 230000014509 gene expression Effects 0.000 claims description 27
- 229960004452 methionine Drugs 0.000 claims description 27
- 229960003136 leucine Drugs 0.000 claims description 24
- 229960004295 valine Drugs 0.000 claims description 24
- 229930182821 L-proline Natural products 0.000 claims description 22
- 239000001963 growth medium Substances 0.000 claims description 21
- 229930195722 L-methionine Natural products 0.000 claims description 20
- FFEARJCKVFRZRR-UHFFFAOYSA-N L-Methionine Natural products CSCCC(N)C(O)=O FFEARJCKVFRZRR-UHFFFAOYSA-N 0.000 claims description 19
- 239000004395 L-leucine Substances 0.000 claims description 17
- 235000019454 L-leucine Nutrition 0.000 claims description 17
- 238000003780 insertion Methods 0.000 claims description 16
- 230000037431 insertion Effects 0.000 claims description 16
- 229940024606 amino acid Drugs 0.000 claims description 15
- 210000004027 cell Anatomy 0.000 claims description 14
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 claims description 13
- 230000015572 biosynthetic process Effects 0.000 claims description 11
- 239000013598 vector Substances 0.000 claims description 11
- 238000012217 deletion Methods 0.000 claims description 10
- 230000037430 deletion Effects 0.000 claims description 10
- 238000007792 addition Methods 0.000 claims description 9
- 238000006467 substitution reaction Methods 0.000 claims description 9
- 230000009466 transformation Effects 0.000 claims description 9
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 claims description 7
- 210000000349 chromosome Anatomy 0.000 claims description 7
- 230000003028 elevating effect Effects 0.000 claims 1
- 235000018102 proteins Nutrition 0.000 description 67
- 239000002609 medium Substances 0.000 description 49
- 239000013612 plasmid Substances 0.000 description 38
- 108020004414 DNA Proteins 0.000 description 33
- 101100544070 Escherichia coli (strain K12) ygaH gene Proteins 0.000 description 23
- 241000588724 Escherichia coli Species 0.000 description 21
- 238000000855 fermentation Methods 0.000 description 16
- 230000004151 fermentation Effects 0.000 description 16
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 15
- 239000008103 glucose Substances 0.000 description 15
- 244000005700 microbiome Species 0.000 description 15
- 238000012360 testing method Methods 0.000 description 15
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 14
- 235000001014 amino acid Nutrition 0.000 description 13
- 229960000723 ampicillin Drugs 0.000 description 13
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 13
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 12
- JZRWCGZRTZMZEH-UHFFFAOYSA-N thiamine Chemical compound CC1=C(CCO)SC=[N+]1CC1=CN=C(C)N=C1N JZRWCGZRTZMZEH-UHFFFAOYSA-N 0.000 description 12
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 11
- 238000003752 polymerase chain reaction Methods 0.000 description 11
- 235000019157 thiamine Nutrition 0.000 description 11
- 239000011721 thiamine Substances 0.000 description 11
- 238000004809 thin layer chromatography Methods 0.000 description 11
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 10
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 10
- 239000012634 fragment Substances 0.000 description 10
- 229960000310 isoleucine Drugs 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- KYMBYSLLVAOCFI-UHFFFAOYSA-N thiamine Chemical compound CC1=C(CCO)SCN1CC1=CN=C(C)N=C1N KYMBYSLLVAOCFI-UHFFFAOYSA-N 0.000 description 10
- 229960003495 thiamine Drugs 0.000 description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- 229930182844 L-isoleucine Natural products 0.000 description 9
- 238000012258 culturing Methods 0.000 description 9
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 8
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 8
- 229930182817 methionine Natural products 0.000 description 8
- 229920001817 Agar Polymers 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 7
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 7
- 239000008272 agar Substances 0.000 description 7
- 238000007796 conventional method Methods 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 6
- 238000009825 accumulation Methods 0.000 description 6
- 229940041514 candida albicans extract Drugs 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 239000004474 valine Substances 0.000 description 6
- 239000012138 yeast extract Substances 0.000 description 6
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 5
- 229930064664 L-arginine Natural products 0.000 description 5
- 235000014852 L-arginine Nutrition 0.000 description 5
- 238000005273 aeration Methods 0.000 description 5
- 230000029142 excretion Effects 0.000 description 5
- 230000005764 inhibitory process Effects 0.000 description 5
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 5
- 235000019341 magnesium sulphate Nutrition 0.000 description 5
- 230000035772 mutation Effects 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- 241001646716 Escherichia coli K-12 Species 0.000 description 4
- VZUNGTLZRAYYDE-UHFFFAOYSA-N N-methyl-N'-nitro-N-nitrosoguanidine Chemical compound O=NN(C)C(=N)N[N+]([O-])=O VZUNGTLZRAYYDE-UHFFFAOYSA-N 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 4
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 4
- 235000011130 ammonium sulphate Nutrition 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 239000007791 liquid phase Substances 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- GHSJKUNUIHUPDF-UHFFFAOYSA-N s-(2-aminoethyl)-l-cysteine Chemical compound NCCSCC(N)C(O)=O GHSJKUNUIHUPDF-UHFFFAOYSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- KNTFCRCCPLEUQZ-UHFFFAOYSA-N O-Methyl-DL-serine Chemical compound COCC(N)C(O)=O KNTFCRCCPLEUQZ-UHFFFAOYSA-N 0.000 description 3
- 125000000539 amino acid group Chemical group 0.000 description 3
- 230000002950 deficient Effects 0.000 description 3
- 101150095957 ilvA gene Proteins 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 239000002504 physiological saline solution Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 101150058720 tdh gene Proteins 0.000 description 3
- -1 that is Proteins 0.000 description 3
- NYCRCTMDYITATC-QMMMGPOBSA-N 2-fluoro-L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1F NYCRCTMDYITATC-QMMMGPOBSA-N 0.000 description 2
- NYCRCTMDYITATC-UHFFFAOYSA-N 2-fluorophenylalanine Chemical compound OC(=O)C(N)CC1=CC=CC=C1F NYCRCTMDYITATC-UHFFFAOYSA-N 0.000 description 2
- LGVJIYCMHMKTPB-UHFFFAOYSA-N 3-hydroxynorvaline Chemical compound CCC(O)C(N)C(O)=O LGVJIYCMHMKTPB-UHFFFAOYSA-N 0.000 description 2
- KEZRWUUMKVVUPT-UHFFFAOYSA-N 4-azaleucine Chemical compound CN(C)CC(N)C(O)=O KEZRWUUMKVVUPT-UHFFFAOYSA-N 0.000 description 2
- YCWQAMGASJSUIP-YFKPBYRVSA-N 6-diazo-5-oxo-L-norleucine Chemical compound OC(=O)[C@@H](N)CCC(=O)C=[N+]=[N-] YCWQAMGASJSUIP-YFKPBYRVSA-N 0.000 description 2
- 229960005538 6-diazo-5-oxo-L-norleucine Drugs 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- QNAYBMKLOCPYGJ-UHFFFAOYSA-N D-alpha-Ala Natural products CC([NH3+])C([O-])=O QNAYBMKLOCPYGJ-UHFFFAOYSA-N 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 241000702191 Escherichia virus P1 Species 0.000 description 2
- 241001295925 Gegenes Species 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-UWTATZPHSA-N L-Alanine Natural products C[C@@H](N)C(O)=O QNAYBMKLOCPYGJ-UWTATZPHSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 2
- 108700026244 Open Reading Frames Proteins 0.000 description 2
- 101710201576 Putative membrane protein Proteins 0.000 description 2
- 229960003767 alanine Drugs 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 101150099953 ilvE gene Proteins 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 239000003471 mutagenic agent Substances 0.000 description 2
- 231100000707 mutagenic chemical Toxicity 0.000 description 2
- 230000003505 mutagenic effect Effects 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 108091008146 restriction endonucleases Proteins 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- IADUEWIQBXOCDZ-VKHMYHEASA-N (S)-azetidine-2-carboxylic acid Chemical compound OC(=O)[C@@H]1CCN1 IADUEWIQBXOCDZ-VKHMYHEASA-N 0.000 description 1
- PKDBCJSWQUOKDO-UHFFFAOYSA-M 2,3,5-triphenyltetrazolium chloride Chemical compound [Cl-].C1=CC=CC=C1C(N=[N+]1C=2C=CC=CC=2)=NN1C1=CC=CC=C1 PKDBCJSWQUOKDO-UHFFFAOYSA-M 0.000 description 1
- PWKSKIMOESPYIA-UHFFFAOYSA-N 2-acetamido-3-sulfanylpropanoic acid Chemical compound CC(=O)NC(CS)C(O)=O PWKSKIMOESPYIA-UHFFFAOYSA-N 0.000 description 1
- KPULXFNPTWGJQH-UHFFFAOYSA-N 3-hydroxy-4-oxo-4-propan-2-yloxybutanoic acid Chemical compound CC(C)OC(=O)C(O)CC(O)=O KPULXFNPTWGJQH-UHFFFAOYSA-N 0.000 description 1
- 101100159893 Aeromonas salmonicida yggA gene Proteins 0.000 description 1
- 102000007610 Amino-acid N-acetyltransferase Human genes 0.000 description 1
- 108010032178 Amino-acid N-acetyltransferase Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 108010055400 Aspartate kinase Proteins 0.000 description 1
- 244000063299 Bacillus subtilis Species 0.000 description 1
- 235000014469 Bacillus subtilis Nutrition 0.000 description 1
- 101100021490 Bacillus subtilis (strain 168) lnrK gene Proteins 0.000 description 1
- 238000009631 Broth culture Methods 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 241000186216 Corynebacterium Species 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 101100379641 Escherichia coli (strain K12) argO gene Proteins 0.000 description 1
- 101100117984 Escherichia coli (strain K12) eamB gene Proteins 0.000 description 1
- 101100454725 Escherichia coli (strain K12) leuE gene Proteins 0.000 description 1
- 101100319877 Escherichia coli (strain K12) yahN gene Proteins 0.000 description 1
- 241000701959 Escherichia virus Lambda Species 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 108010064711 Homoserine dehydrogenase Proteins 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- LEVWYRKDKASIDU-IMJSIDKUSA-N L-cystine Chemical compound [O-]C(=O)[C@@H]([NH3+])CSSC[C@H]([NH3+])C([O-])=O LEVWYRKDKASIDU-IMJSIDKUSA-N 0.000 description 1
- 239000004158 L-cystine Substances 0.000 description 1
- 235000019393 L-cystine Nutrition 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- JJIHLJJYMXLCOY-BYPYZUCNSA-N N-acetyl-L-serine Chemical compound CC(=O)N[C@@H](CO)C(O)=O JJIHLJJYMXLCOY-BYPYZUCNSA-N 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-N Nitrous acid Chemical compound ON=O IOVCWXUNBOPUCH-UHFFFAOYSA-N 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 239000001888 Peptone Substances 0.000 description 1
- 108010080698 Peptones Proteins 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 102000009661 Repressor Proteins Human genes 0.000 description 1
- 108010034634 Repressor Proteins Proteins 0.000 description 1
- 238000002105 Southern blotting Methods 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 108010006873 Threonine Dehydratase Proteins 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- GZCGUPFRVQAUEE-SLPGGIOYSA-N aldehydo-D-glucose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O GZCGUPFRVQAUEE-SLPGGIOYSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000009697 arginine Nutrition 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000006696 biosynthetic metabolic pathway Effects 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 238000009709 capacitor discharge sintering Methods 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229960005091 chloramphenicol Drugs 0.000 description 1
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 description 1
- 239000013611 chromosomal DNA Substances 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 229960003067 cystine Drugs 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000000994 depressogenic effect Effects 0.000 description 1
- 238000000586 desensitisation Methods 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 229940049906 glutamate Drugs 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229960002885 histidine Drugs 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 229910000358 iron sulfate Inorganic materials 0.000 description 1
- BAUYGSIQEAFULO-UHFFFAOYSA-L iron(2+) sulfate (anhydrous) Chemical compound [Fe+2].[O-]S([O-])(=O)=O BAUYGSIQEAFULO-UHFFFAOYSA-L 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 229940043046 isoleucine 50 mg Drugs 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical class O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 101150066555 lacZ gene Proteins 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000009630 liquid culture Methods 0.000 description 1
- 101150044424 lysE gene Proteins 0.000 description 1
- 229940099596 manganese sulfate Drugs 0.000 description 1
- 239000011702 manganese sulphate Substances 0.000 description 1
- 235000007079 manganese sulphate Nutrition 0.000 description 1
- SQQMAOCOWKFBNP-UHFFFAOYSA-L manganese(II) sulfate Chemical compound [Mn+2].[O-]S([O-])(=O)=O SQQMAOCOWKFBNP-UHFFFAOYSA-L 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 238000005374 membrane filtration Methods 0.000 description 1
- 101150040895 metJ gene Proteins 0.000 description 1
- 150000002741 methionine derivatives Chemical class 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 229910017464 nitrogen compound Inorganic materials 0.000 description 1
- 150000002830 nitrogen compounds Chemical class 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 235000019319 peptone Nutrition 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 101150023641 ppc gene Proteins 0.000 description 1
- 150000003147 proline derivatives Chemical class 0.000 description 1
- 101150016257 pycA gene Proteins 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 101150117659 rhtA gene Proteins 0.000 description 1
- 101150033014 rhtB gene Proteins 0.000 description 1
- 101150094644 rhtC gene Proteins 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000007480 spreading Effects 0.000 description 1
- 238000003892 spreading Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- WPLOVIFNBMNBPD-ATHMIXSHSA-N subtilin Chemical compound CC1SCC(NC2=O)C(=O)NC(CC(N)=O)C(=O)NC(C(=O)NC(CCCCN)C(=O)NC(C(C)CC)C(=O)NC(=C)C(=O)NC(CCCCN)C(O)=O)CSC(C)C2NC(=O)C(CC(C)C)NC(=O)C1NC(=O)C(CCC(N)=O)NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C1NC(=O)C(=C/C)/NC(=O)C(CCC(N)=O)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)CNC(=O)C(NC(=O)C(NC(=O)C2NC(=O)CNC(=O)C3CCCN3C(=O)C(NC(=O)C3NC(=O)C(CC(C)C)NC(=O)C(=C)NC(=O)C(CCC(O)=O)NC(=O)C(NC(=O)C(CCCCN)NC(=O)C(N)CC=4C5=CC=CC=C5NC=4)CSC3)C(C)SC2)C(C)C)C(C)SC1)CC1=CC=CC=C1 WPLOVIFNBMNBPD-ATHMIXSHSA-N 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 150000003548 thiazolidines Chemical class 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 239000012137 tryptone Substances 0.000 description 1
- 241001515965 unidentified phage Species 0.000 description 1
- 238000009423 ventilation Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/06—Alanine; Leucine; Isoleucine; Serine; Homoserine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/52—Genes encoding for enzymes or proenzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/08—Lysine; Diaminopimelic acid; Threonine; Valine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/10—Citrulline; Arginine; Ornithine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/12—Methionine; Cysteine; Cystine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P13/00—Preparation of nitrogen-containing organic compounds
- C12P13/04—Alpha- or beta- amino acids
- C12P13/24—Proline; Hydroxyproline; Histidine
Description
- Technisches Gebiet
- Die vorliegende Erfindung bezieht sich auf die Biotechnologie, speziell auf ein Verfahren zur Produktion von L-Aminosäuren durch Fermentation und insbesondere auf Gene, die sich von dem Bakterium Escherichia coli ableiten. Diese Gene eignen sich zur Verbesserung der Produktivität für L-Aminosäuren, beispielsweise L-Threonin, L-Valin, L-Prolin, L-Leucin, L-Methionin und L-Arginin.
- Technischer Hintergrund
- Konventionell werden L-Aminosäuren mit Hilfe eines Fermentationsverfahrens industriell hergestellt, wobei Mikroorganismenstämme, die aus natürlichen Quellen erhalten wurden, oder Mutanten dieser, die speziell zur Erhöhung der L-Aminosäure-produktivität modifiziert sind, verwendet werden.
- Es wurden zahlreiche Methoden zum Erhöhen der Produktivität für L-Aminosäure beschrieben, beispielsweise durch Transformation eines Mikroorganismus mit Hilfe von rekombinanter DNA (siehe zum Beispiel US-Patent Nr. 4,278,765). Diese Methoden beruhen auf der Erhöhung der Aktivität der Enzyme, die an der Aminosäure-Biosynthese beteiligt sind, und/oder der Desensibilisierung der Zielenzyme für die Rückkopplungshemmung durch die gebildete L-Aminosäure (siehe zum Beispiel Japanische Patentveröffentlichung Nr. 56-18596 (1981), WO 95/16042 oder US-Patente Nr. 5,661,012 und 6,040,160).
- Andererseits kann eine erhöhte Ausscheidung der L-Aminosäure die Produktivität eines L-Aminosäure-produzierenden Stammes erhöhen. Ein Stamm eines Bakteriums der Gattung Corynebacterium, der erhöhte Expression des L-Lysin-Exkretionsgens (lysE-Gen) zeigt, ist beschrieben (WO 9723597A2). Außerdem wurden Gene, die für die Effluxproteine codieren, die sich für die Sekretion von L-Cystein, L-Cystin, N-Acetylserin oder Thiazolidin-Derivaten eignen, beschrieben (US-Patent Nr. 5,972,663).
- Zur Zeit sind einige Gene von Escherichia coli bekannt, die für vermutliche Membranproteine codieren, welche die L-Aminosäureproduktion erhöhen. Zusätzliche Kopien des rhtB-Gens machen ein Bakterium stärker resistent gegen L-Homoserin und erhöhen die Produktion von L-Homoserin, L-Threonin, L-Alanin, L-Valin und L-Isoleucin (Europäische Patentveröffentlichung
EP994190A2 EP1013765A1 ). Zusätzliche Kopien der Gene yahN, yeaS, yfiK und yggA erhöhen die Produktion von L-Glutaminsäure, L-Lysin, L-Threonin, L-Alanin, L-Histidin, L-Prolin, L-Arginin, L-Valin und L-Isoleucin (Europäische PatentveröffentlichungEP1016710A2 ). Obwohl die vollständige Genomsequenz des Stammes Escherichia coli K-12 beschrieben ist (Blattner F. R., Plunkett G., Bloch C. A. et al., Science, 227, 1453-1474, 1997; ftp://ftp.genetics.wisc.edu/pub/sequence/ecolim52.seq.gz), gibt es viele ORFs (offene Leseraster) deren Funktion immer noch unbekannt ist. - Offenbarung der Erfindung
- Es ist Aufgabe der vorliegenden Erfindung, die Produktivität von L-Aminosäure-produzierten Stämmen zu erhöhen und ein Verfahren zur Herstellung von L-Aminosäuren, beispielsweise L- Threonin, L-Valin, L-Prolin, L-Leucin oder L-Methionin oder L-Arginin unter Verwendung dieser Stämme bereitzustellen.
- Dieses Ziel wurde erreicht, indem Gene identifiziert wurden, die für Proteine codieren, welche nicht an dem Biosyntheseweg der Ziel-L-Aminosäure beteiligt sind, sondern deren Produktion erhöhen. Ein Beispiel für ein solches Protein könnte ein Membranprotein sein, welches Aktivität für die Ausscheidung beziehungsweise Exkretion der L-Aminosäure hat. Aufgrund der Analyse der vollständigen Genomsequenz von Escherichia coli wurden Proteine mit 4 oder mehr vermutlichen Transmembransegmenten (TMS) selektiert. Als Ergebnis der intensiven Selektion haben die Erfinder unter diesen mehrere Gene identifiziert, das heißt, b2682 und b2683 und diese gründlich untersucht. Die Gene b2682 und b2683 sind als mögliche CDS bekannt, die für funktionell unbekannte Proteine codieren können (Nucleotid-Nummern 92 bis 829 und 819 bis 1154 in der Sequenz der GenBank-Hinterlegungen AE000353 beziehungsweise U00096). Das Gen b2683 ist auch als ygaH bekannt.
- Die Erfinder haben außerdem festgestellt, dass durch Erhöhen der Aktivität des durch das Gen b2682 oder das Gen b2683 codierte Protein die Produktivität eines L-Aminosäure-produzierenden Stammes erhöht wird. Die Erfindung wurde somit fertig gestellt.
- Die vorliegende Erfindung umfasst:
- 1). Ein L-Aminosäure-produzierendes Bakterium der Gattung Escherichia, welches so modifiziert worden ist, dass die L-Aminosäureproduktion durch das Bakterium durch Erhöhen der Aktivitäten der Proteine, die im Folgenden durch (A) oder (B) und (C) oder (D) definiert sind, in einer Zelle des Bakteriums erhöht ist: (A) ein Protein, welches die Aminosäuresequenz der SEQ ID NO:3 des Sequenzprotokolls umfasst; (B) ein Protein, welches die Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-24 Aminosäuren in der Aminosäuresequenz der SEQ ID NO:3 des Sequenzprotokolls umfasst und das eine Aktivität aufweist, durch die das Bakterium mit einer erhöhten Resistenz gegen L-Aminosäure und/oder deren Analoga versehen wird; (C) ein Protein, das die Aminosäuresequenz der SEQ ID NO:5 des Sequenzprotokolls umfasst; (D) ein Protein, das die Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-11 Aminosäuren in der Aminosäuresequenz der SEQ ID NO:5 des Sequenzprotokolls umfasst und das eine Aktivität aufweist, durch die das Bakterium mit einer erhöhten Resistenz gegen L-Aminosäuren und/oder deren Analoga versehen wird, wobei die Aktivitäten der Proteine durch Transformation des Bakteriums mit DNA, die für ein in (A) oder (B) und (C) oder (D) definiertes Protein codiert, oder durch Veränderung der Promotersequenz der DNA auf dem Chromosom des Bakteriums erhöht ist.
- Nachstehend werden die vorstehend unter (A) oder (B) und (C) oder (D) definierten Proteine als "Proteine der ersten Ausführungsform der vorliegenden Erfindung" bezeichnet und das Bakterium der Gattung Escherichia, in welchem die Aktivitäten der obigen Proteine erhöht sind, wird manchmal als "Bakterium der ersten Ausführungsform der vorliegenden Erfindung" bezeichnet.
- 2). Das Bakterium nach dem obigen Bakterium, wobei die Transformation mit einem Mehrkopienvektor durchgeführt ist.
- 3). Ein Verfahren zum Herstellen einer L-Aminosäure, welches das Kultivieren des vorstehend definierten Bakteriums in einem Kulturmedium und das Gewinnen der herzustellenden und anzuhäufenden L-Aminosäure aus dem Kulturmedium umfasst.
- 4). Das Verfahren nach der obigen Methode, wobei die L-Aminosäure L-Threonin ist.
- 5). Das Verfahren nach der obigen Methode, wobei das Bakterium so modifiziert worden ist, dass das Bakterium eine erhöhte Expression des Threonin-Operons aufweist.
- 6). Das Verfahren nach der obigen Methode, wobei die L-Aminosäure L-Valin ist.
- 7). Das Verfahren nach der obigen Methode, wobei das Bakterium so modifiziert worden ist, dass das Bakterium eine erhöhte Expression des ilv-Operons aufweist.
- 8). Das Verfahren nach der obigen Methode, wobei die L-Aminosäure L-Prolin ist.
- 9). Das Verfahren nach der obigen Methode, wobei das Bakterium so modifiziert worden ist, dass das Bakterium eine erhöhte Expression von Genen für die Prolin-Biosynthese aufweist.
- 10). Das Verfahren nach der obigen Methode, wobei die L-Aminosäure L-Leucin ist.
- 11). Das Verfahren nach der obigen Methode, wobei das Bakterium so modifiziert worden ist, dass das Bakterium eine erhöhte Expression des leu-Operons aufweist.
- 12). Das Verfahren nach der obigen Methode, wobei die L-Aminosäure L-Methionin ist.
- 13). Das Verfahren nach der obigen Methode, wobei das Bakterium so modifiziert worden ist, dass das Bakterium eine erhöhte Expression des met-Regulons aufweist.
- Das Verfahren zur Herstellung einer L-Aminosäure umfasst die Produktion von L-Threonin unter Verwendung eines L-Threonin-produzierenden Bakteriums, in welchem die Aktivitäten der erfindungsgemäßen Proteine, wie die mit den in SEQ ID NO:3 und SEQ ID NO:5 gezeigten Aminosäuresequenzen, erhöht sind. Das Verfahren zur Herstellung einer L-Aminosäure schließt auch die Produktion von L-Valin unter Verwendung eines L-Valin-produzierenden Bakteriums ein, in welchem die Aktivitäten der Proteine gemäß der Erfindung, wie der mit den in SEQ ID NO:3 und SEQ ID NO:5 gezeigten Aminosäuresequenzen, erhöht sind. Außerdem umfasst das Verfahren zur Herstellung einer L-Aminosäure die Produktion von L-Prolin unter Verwendung eines L-Prolin-produzierenden Bakteriums, in welchem die Aktivitäten der erfindungsgemäßen Proteine, wie der mit den in Aminosäuresequenzen, die in SEQ ID NO:3 und SEQ ID NO:5 gezeigt sind, erhöht sind. Darüber hinaus umfasst das erfindungsgemäße Verfahren zur Herstellung einer L-Aminosäure die Produktion von L-Leucin unter Verwendung eines L-Leucin-produzierenden Bakteriums, in welchem die Aktivitäten der erfindungsgemäßen Proteine, wie der, welche die in SEQ ID NO:3 und SEQ ID NO:5 gezeigten Aminosäuresequenzen aufweisen, erhöht sind. Das Verfahren zur Herstellung einer L-Aminosäure umfasst auch die Produktion von L-Methionin unter Verwendung eines L-Methionin-produzierenden Bakteriums, in dem die Aktivitäten der erfindungsgemäßen Proteine, wie der, welche die in SEQ ID NO:3 und SEQ ID NO:5 gezeigten Aminosäuresequenzen, erhöht sind.
- Die vorliegende Erfindung wird nachstehend ausführlich erläutert.
- Das erfindungsgemäße Bakterium ist ein L-Aminosäure-produzierendes Bakterium der Gattung Escherichia, welches so modifiziert ist, dass die L-Aminosäureproduktion durch das Bakterium erhöht ist, indem die Aktivitäten der erfindungsgemäßen Proteine in den Zellen des Bakteriums erhöht wurden.
- Erfindungsgemäß bedeutet "L-Aminosäure-produzierendes Bakterium" ein Bakterium, das die Fähigkeit hat, L-Aminosäuren in einem Medium anzureichern, wenn das Bakterium in dem Medium kultiviert wird. Die Fähigkeit zur Produktion von L-Aminosäure kann dem Bakterium als Eigenschaft eines Wildstammes des Bakteriums eigen sein oder kann durch Züchten verliehen oder erhöht worden sein.
- Das erfindungsgemäße Bakterium ist ein L-Aminosäure-produzierendes Bakterium der Gattung Escherichia mit erhöhter Aktivität der Proteine, welche die Produktivität der gewünschten L-Aminosäure erhöhen. Konkret ist das erfindungsgemäße Bakterium ein L-Aminosäure-produzierendes Bakterium der Gattung Escherichia, das erhöhte Aktivität mindestens eines oder zwei der erfindungsgemäßen Proteine aufweist.
- Der Ausdruck "Erhöhen der Aktivität eines Proteins" bedeutet, dass die Aktivität pro Zelle gegenüber der eines nich-tmodifizierten Stammes, beispielsweise eines Wildtyps des Bakteriums der Gattung Escherichia erhöht worden ist. So kann zum Beispiel der Fall erwähnt werden, in welchem die Anzahl der Proteinmoleküle pro Zelle erhöht ist, ein Fall, in welchem die spezifische Aktivität pro Proteinmolekül ansteigt und so weiter. Außerdem kann als Bakterium der Gattung Escherichia des Wildtyps, das als Vergleichsobjekt dient, beispielsweise der Wildstamm von Escherichia coli erwähnt werden.
- Konkret enthält das erfindungsgemäße Bakterium die DNA, die mindestens eines der Gene b2682 und b2683, vorzugsweise beide Gene, überexprimiert, auf der chromosomalen DNA oder einem Plasmid in dem Bakterium und hat erhöhte Fähigkeit zur Produktion von L-Aminosäure, beispielsweise L-Threonin, L-Valin, L-Prolin, L-Leucin oder L-Methionin.
- Die erfindungsgemäßen Proteine umfassen solche, die nachfolgend unter (A) oder (B) und (C) oder (D) definiert sind:
(A) ein Protein, welches die Aminosäuresequenz umfasst, die SEQ ID NO:3 in dem Sequenzprotokoll gezeigt ist;
(B) ein Protein, welches die Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-24 Aminosäuren in der Aminosäuresequenz, die in SEQ ID NO:3 in dem Sequenzprotokoll gezeigt ist, umfasst und das eine Aktivität aufweist, durch die dem Bakterium eine erhöhte Resistenz gegen die L-Aminosäure und/oder deren Analoga verliehen wird;
(C) ein Protein, das die Aminosäuresequenz umfasst, die in SEQ ID NO:5 des Sequenzprotokolls gezeigt ist;
(D) ein Protein, das die Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-11 Aminosäuren in der Aminosäuresequenz der SEQ ID NO:5 des Sequenzprotokolls umfasst und das eine Aktivität aufweist, durch die das Bakterium mit einer erhöhten Resistenz gegen L-Aminosäuren und/oder deren Analoga versehen wird. - Die Zahl "einige" Aminosäuren schwankt in Abhängigkeit von der Position oder der Art der Aminosäurereste in der dreidimensionalen Struktur des Proteins. Sie ist 2 bis 24, vorzugsweise 2 bis 12 und stärker bevorzugt 2 bis 5 für Protein (A) und 2 bis 11, vorzugsweise 2 bis 7, stärker bevorzugt 2 bis 5 für das Protein (C).
- Erhöhte Resistenz gegen L-Aminosäuren und/oder deren Analoga bedeutet die Fähigkeit eines Bakteriums, auf einem Minimalmedium zu wachsen, welches eine L-Aminosäure oder deren Analogon in einer Konzentration enthält, bei der der unmodifizierte Stamm oder der Wildtypstamm oder der Elternstamm des Bakteriums nicht wachsen kann, oder die Fähigkeit eines Bakteriums, auf einem Medium, welches die L-Aminosäure oder deren Analogon enthält, schneller zu wachsen, als der unmodifizierte Stamm oder der Wildtypstamm oder der Elternstamm des Bakteriums.
- Konkreter lässt sich sagen, dass ein Stamm von E. coli eine erhöhte Resistenz gegen eine L-Aminosäure oder deren Analogon hat, wenn der Stamm nach 2–4-tägiger Inkubation bei 37°C auf einer Platte mit festem Adams-Medium eine Kolonie bildet, die größer als die des unmodifizierten Stammes oder des Wildtypstammes von E. coli ist, wenn der Stamm auf einem Agarmedium, welche die L-Aminosäure oder deren Analogon enthält, unter geeigneten Bedingungen kultiviert wird. Der Ausdruck "geeignete Bedingung" bezieht sich auf die Temperatur, den pH, die Luftzufuhr oder das optionale Vorhandensein von notwendigen Nährstoffen oder dergleichen für den zu kultivierenden E. coli-Stamm.
- Beispiele für L-Aminosäure-Analoga sind 3,4-Dihydroprolin, DL-Thiaisoleucin, DL-o-Methylserin, 4-Azaleucin, Norleucin, L-o-Fluorphenylalanin und DL-o-Fluorphenylalanin, Homoserin, 6-Diazo-5-oxo-L-norleucin und DL-β-Hydroxynorvalin.
- Die erwähnte Konzentration einer L-Aminosäure oder deren Analogon, bei der der unmodifizierte Stamm oder der Wildtyp stamm des Bakteriums nicht wachsen kann, variiert sehr stark (von 0,5 μg/ml für DL-Thiaisoleucin bis 9600 μg/ml für DL-o-Methylserin) in Abhängigkeit von der Struktur der verwendeten Verbindung. So beträgt zum Beispiel diese Konzentration im Allgemeinen 7 bis 70 μg/ml, vorzugsweise 20 bis 25 μg/ml im Fall von 3,4-Dihydroprolin, im Allgemeinen 0,5 bis 5 μg/ml, vorzugsweise 0,9 bis 1,1 im Fall von DL-Thiaisoleucin, im Allgemeinen 1100 bis 9600 μg/ml, vorzugsweise 3000 bis 3500 im Fall von DL-o-Methylserin, im Allgemeinen 15 bis 150 μg/ml, vorzugsweise 40 bis 50 μg/ml im Fall von 4-Azaleucin, im Allgemeinen 150 bis 1500 μg/ml, vorzugsweise 450 bis 550 μg/ml im Fall von Norleucin, im Allgemeinen 0,6 bis 6 μg/ml, vorzugsweise 1,5 bis 2 μg/ml im Fall von L-o-Fluorphenylalanin, im Allgemeinen 2 bis 20 μg/ml, vorzugsweise 5 bis 7 μg/ml im Fall von DL-o-Fluorphenylalanin, und im Allgemeinen 330 bis 3300 μg/ml, vorzugsweise 900 bis 1100 μg/ml im Fall von Homoserin, im Allgemeinen 5 bis 50 μg/ml, vorzugsweise 12 bis 18 im Fall von 6-Diazo-5-oxo-L-norleucin, und im Allgemeinen 25 bis 250 μg/ml, vorzugsweise 70 bis 90 μg/ml im Fall von DL-β-Hydroxynorvalin.
- Empfindlichkeit gegen L-Aminosäuren und/oder deren Analoga bedeutet die Fähigkeit eines Bakteriums, in einer längeren Vermehrungszeit auf einem Minimalmedium, das eine Konzentration einer L-Aminosäure oder deren Analogon enthält, zu wachsen, als der unmodifizierte Stamm oder der Wildtypstamm.
- Alternativ bedeutet die Empfindlichkeit (Sensibilität) gegen L-Aminosäuren und/oder deren Analoga die Fähigkeit eines Bakteriums, auf einem Minimalmedium, welches eine L-Aminosäure oder deren Analogon in einer Konzentration enthält, bei welcher der unmodifizierte Stamm oder der Wildtypstamm des Bak teriums wächst, nicht zu wachsen. Ein Beispiel für ein solches L-Aminosäure-Analogon ist S-(2-Aminoethyl)-cystein. Die vorstehend erwähnte Konzentration beträgt im Allgemeinen 0,2 bis 2,0 μg/ml, vorzugsweise 0,5 bis 1,0 μg/ml im Fall von S-(2-Aminoethyl)-cystein.
- Das erfindungsgemäße Bakterium umfasst auch eines, in dem die Aktivitäten der Proteine gemäß der Erfindung durch Transformation des Bakteriums mit einer DNA, die für ein in (A) oder (B) und (C) oder (D) definiertes Protein codiert oder durch Änderung der Promotersequenz der DNA auf dem Chromosom des Bakteriums erhöht worden sind.
- Die DNA, die für die Modifizierung des erfindungsgemäßen Bakteriums verwendet wird, codiert für ein putatives Membranprotein. Konkret codiert die DNA für ein Protein, das 4 oder mehr Transmembran-Segmente aufweist. Eine solche DNA kann für Proteine mit einer Aktivität für die Exkretion von L-Aminosäure codieren. Konkreter wird die DNA durch die Gene b2682 und b2683 repräsentiert. Es ist erforderlich, festzuhalten, dass die codierende Region des Gens b2682 in Position 728-738 und die codierende Region des Gens b2683 in Position 1-11 überlappen. Beide Gene können beispielsweise durch PCR als einziges PCR-Produkt unter Verwendung von Primern erhalten werden, welche die in SEQ ID NO:1 und 2 gezeigte Nucleotidsequenz haben.
- Die Analyse der vollständigen Genomsequenz von Escherichia coli ermöglichte es, die Gene zu selektieren, die für Proteine mit 4 oder mehr putativen TMS codieren. Proteine mit bekannter Funktion und Transportproteine, die von Paulsen I. T., Sliwinski M. I., Saier M. H. (J.Mol.Biol., 1998, 277, 573) und Lipton K. J., Higgins C. F.(Molecular Microbiology, 1998, 28(1), 5) beschrieben sind, wurden aus der zu selektie renden Gruppe ausgeschlossen. Als Ergebnis einer intensiven Selektion unter den verbleibenden Genen wurden mehrere Gene ausgewählt, die für wahrscheinliche Membran-Exporter codieren. Es wurde gefunden, dass die Überexpression der Gene b2682 und b2683 die L-Aminosäureproduktion durch einen L-Aminosäure-produzierenden Stamm erhöht.
- Die DNA gemäß der vorliegenden Erfindung umfasst eine DNA, die für das Protein codiert, wobei die Deletion, Substitution, Insertion oder Addition von einer oder mehreren Aminosäuren in einer oder mehr Positionen des Proteins (A) oder (C) eingeschlossen ist, solange diese die Aktivität des Proteins nicht verlieren. Die Anzahl "mehrere" Aminosäuren differiert in Abhängigkeit von der Position oder der Art der Aminosäurereste in der dreidimensionalen Struktur des Proteins und ist 2 bis 24, vorzugsweise 2 bis 12 und stärker bevorzugt 2 bis 5 für das Protein (A), und 2 bis 11, vorzugsweise 2 bis 7, und stärker bevorzugt 2 bis 5 für das Protein (C).
- Die DNA, die für im Wesentlichen das gleiche Protein wie das in (A) oder in (C) definierte Protein codiert, kann beispielsweise durch Modifizieren der Nucleotidsequenz, die für das in (A) oder in (C) definierte Protein codiert durch ortsspezifische Mutagenese, sodass ein oder mehr Aminosäurereste entfernt, ersetzt, eingefügt oder hinzugefügt werden, erhalten werden. Eine solche modifizierte DNA kann mit Hilfe üblicher Methoden durch Behandlung mit Reagenzien und unter Bedingungen, bei der Mutationen erzeugt werden, erhalten werden. Eine solche Behandlung umfasst die Behandlung der für erfindungsgemäße Proteine codierenden DNA mit Hydroxylamin oder Behandlung des Bakteriums, welches die DNA enthält, mit UV-Strahlung oder einem Reagens, wie N-Methyl-N'-nitro-N-nitrosoguanidin oder salpetriger Säure.
- Die DNA gemäß der Erfindung umfasst Varianten, die in den verschiedenen Stämmen zu finden sind, und Varianten von Bakterien der Gattung Escherichia gemäß der natürlichen Vielfalt. Die für solche Varianten codierende DNA kann durch Isolieren der DNA, die mit dem Gen b2862 oder dem Gen b2683 oder einem Teil der Gene unter stringenten Bedingungen hybridisiert und für das Protein codiert, das die L-Aminosäureproduktion erhöht, erhalten werden. Die hier verwendete Bezeichnung "stringente Bedingungen" bedeutet Bedingungen, unter denen ein so genanntes spezifisches Hybrid gebildet wird, aber ein nicht-spezifisches Hybrid nicht gebildet wird. So umfassen beispielsweise stringente Bedingungen solche Bedinungen, unter denen DNAs mit hoher Homologie, beispielsweise DNAs mit einer Homologie von nicht weniger als 70% miteinander hybridisiert werden. Alternativ sind Beispiele für stringente Bedingungen solche Bedingungen, welche die üblichen Waschbedingungen bei der Southern-Hybridisierung, z. B. 60°C, 1 x SSC, 0,1% SDS, vorzugsweise 0,1 x SSC, 0,1% SDS, einschließen. Als Sonde für die DNA, die für Varianten codiert und mit dem Gen b2862 oder b2683 hybridisiert, kann auch eine Teilsequenz der Nucleotidsequenz SEQ ID NO:3 oder SEQ ID NO:5 verwendet werden. Eine solche Sonde kann durch PCR unter Verwendung von Oligonucleotiden hergestellt werden, die auf Basis der Nucleotidsequenz von SEQ ID NO:3 oder 5 als Primer und mit einem DNA-Fragment, welches die Nucleotidsequenz SEQ ID NO:3 oder 5 enthält, als Templat, hergestellt werden. Wenn ein DNA-Fragment einer Länge von etwa 300 bp als Sonde verwendet wird, bestehen die Waschbedingungen für die Hybridisierung beispielsweise aus den Bedingungen 50°C, 2 x SSC, und 0,1% SDS.
- Die Transformation eines Bakteriums mit der für ein Protein codierenden DNA bedeutet das Einschleusen der DNA in die Bakterienzelle beispielsweise mit konventionellen Methoden, um die Expression des für das erfindungsgemäße Protein codierenden Gens zu erhöhen und die Aktivität des Proteins in den Bakterienzellen zu verstärken.
- Methoden zum Verbessern der Genexpression umfassen Methoden, welche die Kopienzahl des Gens erhöhen. Das Einführen eines Gens in einen Vektor, der befähigt ist, in einem Bakterium der Gattung Escherichia zu wirken, erhöht die Kopienzahl des Gens. Zu diesem Zweck können vorzugsweise Mehrkopienvektoren verwendet werden. Beispiele für einen Mehrkopienvektor sind pBR322, pMW119, pUC19, pET22b oder dergleichen.
- Außerdem kann eine Erhöhung der Genexpression durch Einführen von Mehrfachkopien des Gens in das Chromosom des Bakteriums erzielt werden, beispielsweise mit Hilfe der Methode der homologen Rekombination oder dergleichen.
- Wenn die Expression von zwei oder mehr Genen erhöht wird, können die Gene zusammen in dem gleichen Plasmid oder gesondert in unterschiedlichen Plasmiden enthalten sein. Es ist außerdem möglich, dass eines der Gene auf dem Chromosom ist und das andere Gen sich in einem Plasmid befindet.
- Andererseits kann eine Erhöhung der Genexpression durch Änderung der Expressions-Regulationssequenz des Gens erreicht werden. Die Änderung der Expressions-Regulationssequenz des Gens umfasst das Einführen einer Mutation in die inhärente Expressions-Regulationssequenz des Gens, wie einen Promoter, sodass die Expression des Gens verstärkt wird (WO00/18935) und Anordnen der erfindungsgemäßen DNA unter der Kontrolle eines wirksamen Promoters. So sind als wirksame Promoter bei spielsweise der lac-Promoter, trp-Promoter, trc-Promoter, PL-Promoter des Lambdaphagen bekannt. Die Verwendung eines wirksamen Promoters kann mit einer Vermehrung der Kopien des Gens kombiniert werden.
- Das erfindungsgemäße Bakterium kann durch Einschleusen der vorstehend genannten DNAs in ein Bakterium, das eine eigene Fähigkeit zur Bildung eines L-Aminosäure hat, erhalten werden. Alternativ kann das erfindungsgemäße Bakterium dadurch erhalten werden, dass einem Bakterium, welches die DNAs bereits enthält, die Fähigkeit zur Produktion von L-Aminosäure verliehen wird. Als Elternstamm, in dem die Aktivität der erfindungsgemäßen Proteine verstärkt werden soll, können L-Threonin-produzierende Bakterien der Gattung Escherichia, wie die Stämme VL2054 (VKPM B-8067), VNIIGenetika 472T23 (US-Patent Nr. 5,631,157), VKPM B-3996 (US-Patent Nr. 5,175,107 und 5,976,843), KCCM-10132 (WO009660A1), KCCM-10133 (WO009661A1) oder dergleichen verwendet werden. Als Elternstämme, in denen die Aktivitäten der erfindungsgemäßen Proteine verstärkt werden sollen, werden auch L-Valin-produzierende Bakterien der Gattung Escherichia, wie H-81 (VKPM B-8066), NRRL B-12287 und NRRL B-12288 (US-Patent Nr. 4,391,907), VKPM B-4411 (US-Patent Nr. 5,658,766), VKPM B-7707 (Europäische Patentveröffentlichung Nr.
EP1016710A2 ) oder dergleichen verwendet. Außerdem werden als Elternstämme, in denen die Aktivitäten der erfindungsgemäßen Proteine verstärkt werden sollen, L-Prolin-produzierende Bakterien der Gattung Escherichia, wie NRRL B-12403 und NRRL B-12404 (GB2075056 DE3127361 beschrieben sind, Plasmidmutanten, die von Bloom F. R. et al. (The 15th Miami winter symposium, 1983, S. 34) beschrieben sind oder dergleichen verwendet. Außerdem werden als Eltern stamm mit erhöhter Aktivität der erfindungsgemäßen Proteine L-Leucin-produzierende Bakterien der Gattung Escherichia verwendet, wie H-9070 (FERM BP-4704) und H-9072 (FERM BP-4706) (US5744331 RU2140450 EP0872547 ) oder dergleichen. - Ebenfalls verwendet als Elternstämme, in denen die Aktivitäten der Proteine gemäß der Erfindung erhöht werden sollen, eignen sich L-Methionin-produzierende Bakterien der Gattung Escherichia, wie AJ11539 (NRRL B-12399), AJ11540 (NRRL B-12400), AJ11541 (NRRL B-12401), AJ 11542 (NRRL B-12402) (
GB2075055 - Weiterhin können als Elternstamm, in dem die Aktivität der erfindungsgemäßen Proteine verstärkt werden soll, L-Arginin-produzierende Bakterien der Gattung Escherichia verwendet werden, wie die Stämme AJ11531 und AJ11538 (
JP56106598A2 - Das erfindungsgemäße Bakterium kann außerdem mit verstärkter Expression eines oder mehrerer Gene, die an der Biosynthese von L-Aminosäuren beteiligt sind, ausgestattet werden. Beispiele für solche Gene, für L-Threonin-produzierende Bakterien sind das Threonin-Operon, das vorzugsweise ein für Aspartatkinase codierendes Gen umfasst, Homoserindehydrogenase, dessen Rückkopplungshemmung durch L-Threonin desensibilisiert ist (Japanische Patentveröffentlichung Nr. 1-29559). Beispiele für solche Gene sind das ilv-Operon, d. h. ilvGMEDA-Operon, welches nicht bevorzugt Threonindeaminase exprimiert und dessen Attenuation unterdrückt ist (Japanische offen gelegte Patentveröffentlichung Nr. 8-47397) für L-Valin produzierende Bakterien. Beispiele für solche Gene sind Gene für die L-Prolin-Biosynthese, die vorzugsweise durch das für Glutamatkinase codierende Gen proB, dessen Rückkopplungshemmung durch L-Prolin desensibilisiert ist (
DE3127361 ) repräsentiert, für L-Prolin produzierende Bakterien. Weitere Beispiele für solche Gene sind für L-Leucin-produzierende Bakterien das Leucin-Operon, d. h. leu-Operon, das vorzugsweise ein für Isopropylmalatsynthase codierendes Gen umfasst, dessen Rückkopplungshemmung durch L-Leucin desensibilisiert ist (Russische Patentveröffentlichung 2201454). Ein weiteres Beispiel für solche Gene ist das Methionin-Regulon, für L-Methionin-produzierende Bakterien. Das Methionin-Regulon kann mutierte Gene, die für Proteine codieren, aufweisen, deren Aktivität zur Repression der Aminosäure-Biosynthese vermindert ist. Ein Beispiel für ein solches Gen ist die Variante des metJ-Gens, das für ein Repressorprotein bei der Biosynthese von L-Methionin codiert, von E. coli, dessen Aktivität zur Repression der Methionin-Biosynthese vermindert ist (JP 2000-157267 A2). Ein weiteres Beispiel für ein solches Gen ist das Arginin-Regulon, das vorzugsweise ein Gen umfasst, welches für N-Acetylglutamatsynthase codiert, dessen Rückkopplungshemmung durch L-Arginin desensibilisiert ist (Rajagopal B. S. et al, Appl. Environ. Microbiol., 1998, v. 64, Nr. 5, s.1805-1811). - Das erfindungsgemäße Verfahren umfasst ein Verfahren zur Herstellung von L-Threonin, das folgende Stufen umfasst: Kultivieren des erfindungsgemäßen Bakteriums in einem Kulturmedium, um zu ermöglichen, dass L-Threonin in dem Kulturmedium gebildet und angereichert wird, und Gewinnen von L-Threonin aus dem Kulturmedium. Das erfindungsgemäße Verfahren umfasst auch ein Verfahren zur Herstellung von L-Valin, welches folgende Stufen umfasst: Kultivieren des erfindungsgemäßen Bak teriums in einem Kulturmedium, um zu ermöglichen, dass L-Valin in dem Kulturmedium gebildet und angereichert wird, und Gewinnen von L-Valin aus dem Kulturmedium. Ferner umfasst das erfindungsgemäße Verfahren ein Verfahren zur Herstellung von L-Prolin, welches folgende Stufen umfasst: Kultivieren des erfindungsgemäßen Bakteriums in einem Kulturmedium, um zu ermöglichen, dass L-Prolin in dem Kulturmedium gebildet und angereichert wird, und Gewinnen von L-Prolin aus dem Kulturmedium. Weiterhin umfasst das erfindungsgemäße Verfahren ein Verfahren zur Herstellung von L-Leucin, das folgende Stufen umfasst: Kultivieren des erfindungsgemäßen Bakteriums in einem Kulturmedium, um die Bildung und Anreicherung von L-Leucin in dem Kulturmedium zu ermöglichen und Gewinnen von L-Leucin aus dem Kulturmedium. Das erfindungsgemäße Verfahren umfasst außerdem ein Verfahren zur Herstellung von L-Methionin, das folgende Stufen umfasst: Kultivieren des erfindungsgemäßen Bakteriums in einem Kulturmedium, um die Bildung und Anreicherung von L-Methionin in dem Kulturmedium zu ermöglichen und Gewinnen von L-Methionin aus dem Kulturmedium.
- Erfindungsgemäß kann das Kultivieren, das Gewinnen und die Reinigung einer L-Aminosäure aus dem Medium und dergleichen in gleicher Weise wie bei der konventionellen Fermentationsmethode erfolgen, bei der eine Aminosäure unter Verwendung eines Mikroorganismus hergestellt wird. Das für die Kultur verwendete Medium kann entweder ein synthetisches Medium oder ein natürliches Medium sein, solange das Medium eine Kohlenstoffquelle, eine Stickstoffquelle und Mineralien und erforderlichenfalls geeignete Mengen an Nährstoffen enthält, welche die Mikroorganismen für das Wachstum benötigen. Die Kohlenstoffquelle kann verschiedene Kohlenhydrate, wie Glucose und Saccharose, und verschiedene organische Säuren umfassen. In Abhängigkeit von dem Assimilationsmodus des verwendeten Mikroorganismus kann ein Alkohol, einschließlich Ethanol und Glycerin, verwendet werden. Als Stickstoffquelle werden verschiedene Ammoniumsalze, wie Ammoniak und Ammoniumsulfat, andere Stickstoffverbindungen, wie Amine, natürliche Stickstoffquellen, wie Pepton, Sojabohnenhydrolysat und verdaute fermentative Mikroorganismen verwendet. Als Mineralien eignen sich Kaliummonophosphat, Magnesiumsulfat, Natriumchlorid, Eisensulfat, Mangansulfat, Calciumchlorid und dergleichen.
- Das Kultivieren erfolgt vorzugsweise unter aeroben Bedingungen, wie als Schüttelkultur und Rührkultur unter Belüftung bei einer Temperatur von 20 bis 40°C, vorzugsweise 30 bis 38°C. Der pH der Kultur liegt gewöhnlich zwischen 5 und 9, vorzugsweise zwischen 6,5 und 7,2. Der pH-Wert der Kultur kann mit Ammoniak, Calciumcarbonat, verschiedenen Säuren, verschiedenen Basen und Puffern eingestellt werden. Gewöhnlich führt eine 1- bis 5-tägige Kultur zur Anreicherung der gewünschten L-Aminosäure in dem flüssigen Medium.
- Nach der Kultur können Feststoffe, wie Zellen, aus dem flüssigen Kulturmedium durch Zentrifugieren oder Membranfiltration entfernt werden und die gewünschte L-Aminosäure kann gewonnen und durch Ionenaustausch, Konzentrations- und Kristallisationsmethoden gereinigt werden.
- Kurze Beschreibung der Zeichnung
-
1 zeigt die Konstruktion des Plasmids pΔlacZ. - Beste Ausführungsform der Erfindung
- Die vorliegende Erfindung wird nachstehend genauer unter Bezugnahme auf Beispiele erläutert. In den Beispielen hat eine Aminosäure die L-Konfiguration, wenn nichts anderes angegeben ist.
- Beispiel 1: Klonieren der Gene b2682 und b2683 auf dem Plasmid pΔlacZ
- Zum Klonieren der Gene b2682 und b2683 wurde der Vektor pΔlacZ verwendet. Der Vektor pΔlacZ ist ein Derivat des Vektors pET-22b(+) (Novagen, Madison, WI, USA). pET-22b(+) wurde mit BglII und XbaI behandelt und mit dem Polymerase-Kettenreaktions (PCR)-Fragment von Plasmid pMB9-lac (Fuller F., Gene, 19, 43-54, 1982) ligiert, das mit den gleichen Restriktionsendonucleasen behandelt wurde und den Plac UV5-Promoter trägt. Zum Amplifizieren des Plac UV5-Promoterfragments durch PCR wurden Primer mit den in SEQ ID NO:7 und 8 gezeigten Sequenzen verwendet. Das resultierende Plasmid wurde mit dem Strukturteil des lacZ-Gens (237 bp ohne Promoter) ergänzt, indem das Sa1I-BamHI-Fragment des Plasmids pJEL250 kloniert wurde (Dymakova E. et al., Genetika (rus), 35, 2, 181-186, 1999). Das Schema zur Herstellung des Vektors pΔlacZ ist in
1 gezeigt. - Das Ausgangsmaterial zum Klonieren der angenommenen Leseraster von E. coli b2682 und b2683 (Gene b2682 und b2683) war das PCR-Fragment, welches unter Verwendung von DNA aus E. coli-Stamm TG1 als Templat erhalten wurde. Für die Synthese dieses Fragments wurden zwei Primer mit den in SEQ ID NO:1 und 2 gezeigten Sequenzen verwendet. PCR wurde in dem "Perkin Elmer GeneAmp PCR System 2400" unter folgenden Bedingungen durchgeführt: 40 sec bei 95°C, 40 sec bei 47°C, 40 sec bei 72°C, 30 Zyklen. Somit wurde das lineare DNA-Fragment von 1158 bp, welches die Gene b2682 und b2683 enthielt, erhalten.
- Dieses PCR-Fragment wurde mit den Restriktasen XbaI und BamHI behandelt und in dem Mehrkopienvektor pΔlacZ, der vorher mit den gleichen Restriktasen behandelt worden war, eingefügt.
- Das resultierende Plasmid mit dem PCR-Fragment wurde als pYGAZH gezeichnet und enthielt beide Gene b2682 und b2683 unter der Kontrolle des Lactose-Promoters (Plac UV5).
- Beispiel 2: Einfluss der amplifizierten Gene b2682 und b2683 auf die Resistenz von E. coli-Stamm TG1 gegen Aminosäuren und deren Analoga
- E. coli-Stamm TG1(pYGAZH), TG1(pYCHE), TG1(pYHGN) und Stamm TG1 mit einem Vektor ohne Insertion (Kontrollstamm) wurden über Nacht auf einem LB-Medium, das mit Ampicillin ergänzt war (100 μg/ml) gezüchtet. Die über Nacht erhaltenen Kulturen aller Stämme wurden in frischem LB-Medium, das mit Ampicillin (100 μg/ml) und IPTG (0,5 mM) ergänzt war, auf das 25-fache verdünnt und 2 Stunden unter Belüftung bei 37°C inkubiert. Die log-Phasen-Kulturen wurden in einer 0,9%igen Lösung von NaCl verdünnt und etwa 1000 Zellen wurden auf Platten mit festem Adams-Medium, das mit Ampicillin (100 μg/ml) IPTG (0,5 mM) und einer Aminosäure oder deren Analogon supplementiert war, aufgeimpft. Nach 2-4-tägiger Inkubation bei 37°C wurden die Unterschiede in der Koloniegröße und der Koloniezahl zwischen dem Stamm TG1 mit einem Hybridplasmid und dem Kontrollstamm TG1 registriert. Die Versuchsergebnisse sind in Tabelle 1 dargestellt. Tabelle 1
- Keine:
- kein Unterschied im Vergleich zu dem Kontrollstamm
- R:
- mehr Kolonien oder erhöhte Koloniegröße
- S:
- weniger Kolonien oder geringere Koloniegröße im Vergleich zu dem Kontrollstamm
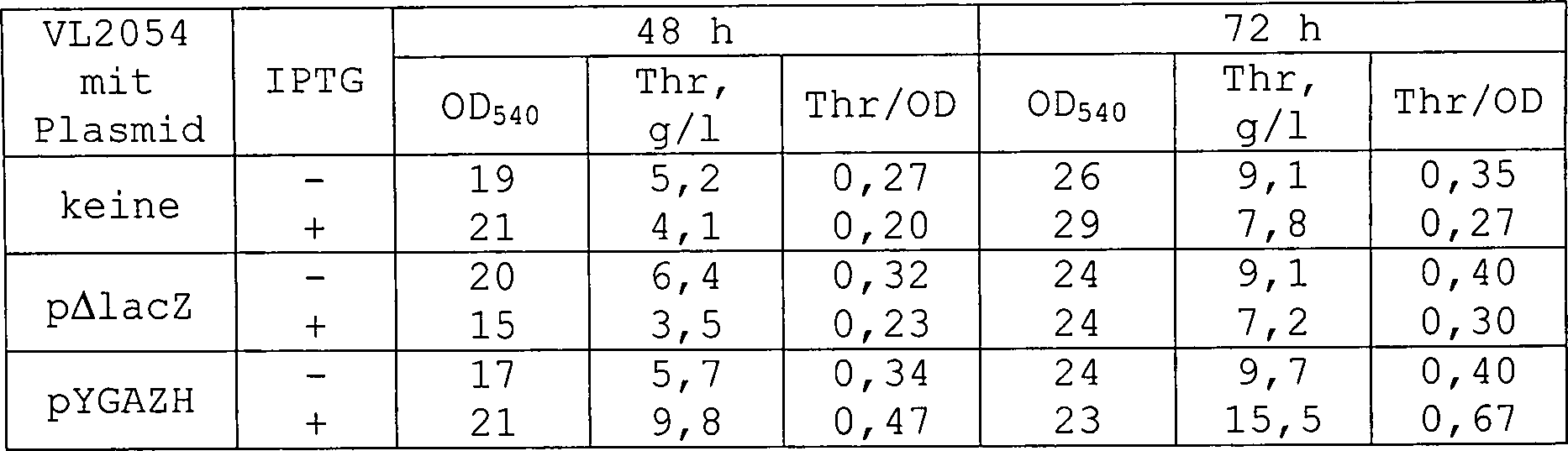
- Beispiel 3: Produktion von Threonin durch einen Stamm mit dem Plasmid pYGAZH
- Der Threonin-erzeugende Stamm VL2054 wurde durch das Plasmid pYGAZH, welches die Gene b2682 und b2683 unter der Kontrolle des Plac-UV5-Promoters trägt, transformiert. Der erhaltene Stamm wurde als VL2054(pYGAZH) bezeichnet. Der Stamm VL2054 ist ein Derivat des Stammes VKPM B-3996 und trägt auf seinem Chromosom:
- a) das integrierte Threonin-Operon unter der Kontrolle des PR-Promoters
- b) Das Wildtyp-rhtA-Gen
- c) das inaktivierte chromosomale Gen, das für Transhydrogenase codiert (tdh-Gen) und das inaktivierte Kanamycin-Resistenzgen (kan)-Gen in Tn5 (tdh:Tn5, KanS)
- d) die Mutation ilvA442.
- Der Stamm VL2054 wurde am 30. Januar 2001 unter der Hinterlegungsnummer VKPM B-8067 bei der Russischen Nationalsammlung für industrielle Mikroorganismen (VKPM) (Russia 113545, Moscow, 1 Dorozhny proezd, 1) hinterlegt und aus der ursprünglichen Hinterlegung am 1. Februar 2002 in die internationale Hinterlegung nach dem Budapester Vertrag übergeführt.
- Die 5 Kolonien jedes Stammes VL2054, des Stammes VL2054 (pΔlacZ) als Kontrollstamm der das Plasmid ohne Insertion enthält und VL2054(pYGAZH) wurden in 2 ml Minimalmedium ((NH4)2SO4 – 11 g/l; NaCl – 0,4 g/l; MgSO4 – 0,4 g/l; K2HPO4 – 1 g/l; FeSO4 – 10 mg/l; MnSO4 – 10 mg/l; Thiamin – 0,1 mg/l; Hefeextrakt – 0,5 g/l; Glucose – 40 g/l; Ampicillin – 300 mg/l falls erforderlich) in 20 ml-Reagenzgläsern suspendiert und über Nacht unter Belüftung bei 32°C inkubiert. 0,2 ml jeder der über Nacht erhaltenen Kulturen wurde in drei 20 ml- Reagenzgläser mit 2 ml frischem Medium für die Fermentation mit oder ohne IPTG übergeführt und 48 oder 72 Stunden bei 32°C mit einem Rotationsschüttler kultiviert. Zusammensetzung des Fermentationsmediums:
(NH4)2SO4 22 g/l NaCl 0,8 g/l MgSO4 0,8 g/l K2HPO4 2 g/l FeSO4 20 mg/l MnSO4 20 mg/l Thiamin 0,2 mg/l Hefeextrakt 1 g/l CaCO3 30 g/l Glucose 80 g/l Ampicillin 300 mg/l, falls erforderlich IPTG 0,5 mM, falls erforderlich - Nach dem Kultivieren wurden die Stabilität des Plasmids und die optische Absorption des Mediums bei 540 nm mit Hilfe von üblichen Methoden bestimmt. Die angereicherte Menge an Threonin in dem Medium wurde durch Dünnschichtchromatografie (TLC) bestimmt. Die Zusammensetzung der flüssigen Phase für die TLC war wie folgt: Isopropanol: 50 ml, Aceton: 50 ml, NH4OH (30%): 12 ml, H2O: 8 ml. Die Ergebnisse sind in Tabelle 2 gezeigt. Wie ersichtlich ist, verbesserte das Hybridplasmid pYGAZH die Anreicherung von Threonin durch den Threoninbildenden Stamm VL2054.
- Beispiel 4: Produktion von Valin durch einen Stamm mit dem Plasmid pYGAZH
- Der Valin-produzierende Stamm H-81 wurde durch das Plasmid pYGAZH, welches die Gene b2682 und b2683 unter der Kontrolle des Plac-UV5-Promoters trägt, transformiert. Der Stamm H-81 wurde am 30. Januar 2001 unter der Hinterlegungsnummer VKPM B-8066 bei der Russischen Nationalkollektion für industrielle Mikroorganismen (VKPM) (Russia 113545, Moscow, 1 Dorozhny proezd, 1) hinterlegt und am 1. Februar 2002 aus der ursprünglichen Hinterlegung in eine internationale Hinterlegung nach dem Budapester Vertrag übergeführt.
- 5 Kolonien jedes Stammes H-81, H-81(pΔlacZ) als Kontrollstamm, der ein Plasmid ohne Insertion enthielt und H-81 (pYGAZH) wurden in 2 ml Minimalmedium in Reagenzgläsern suspendiert ((NH4)2SO4 – 18 g/l, K2HPO4 – 1,8 g/l, MgSO4 – 1,2 g/l, Thiamin – 0,1 mg/l, Hefeextrakt – 0,5 g/l, Glucose – 60 g/l, Ampicillin – 300 mg/l, falls erforderlich) und über Nacht unter Belüftung bei 32°C inkubiert. 0,2 ml jeder der über Nacht erhaltenen Kulturen wurde in drei 20 ml-Reagenzgläser mit 2 ml frischem Fermentationsmedium mit oder ohne IPTG übergeführt und bei 32°C während 48 oder 72 Stunden mit Hilfe eines Rotationsschüttlers kultiviert. Zusammensetzung des Fermentationsmediums:
(NH4)2SO4 18 g/l K2HPO4 1,8 g/l MgSO4 1,2 g/l CaCO3 20 mg/l Thiamin 0,1 mg/l Glucose 60 g/l Ampicillin 300 mg/l, falls erforderlich IPTG 0,5 mM, falls erforderlich - Nach dem Kultivieren wurden die Stabilität des Plasmids und die optische Absorption des Mediums bei 540 nm mit Hilfe von üblichen Methoden bestimmt. Die angereicherte Menge an Valin in dem Medium wurde durch TLC bestimmt. Die Zusammensetzung der flüssigen Phase für TLC war wie folgt: Isopropanol: 80 ml, Ethylacetat: 80 ml, NH4OH (30%): 15 ml, H2O: 45 ml. Die Ergebnisse sind in Tabelle 3 gezeigt. Wie ersichtlich ist, verbesserte das Hybridplasmid pYGAZH die Anreicherung von Valin durch den Valin-produzierenden Stamm H-81.
- Referenzbeispiel 1: Produktion von L-Prolin durch einen L-Prolin-produzierenden Stamm mit ilvA-Defizienz
- Die Zellen des Wildtypstammes E. coli K12 (VKPM B-7) wurden mit einem Mutagen, N-Methyl-N'-nitro-N-nitrosoguanidin (0,1 mg/ml), 20 Minuten lang bei 37°C behandelt, gewaschen und auf ein Minimal-Agarmedium M9 aufgetragen, das mit 1,25 mg/ml Trypton, 10 mg/ml L-Prolin und 0,05 mg/ml 2,3,5-Triphenyl-tetrazoliumchlorid ergänzt war. Die meisten nach 3-tägiger Inkubation bei 37°C erschienen Kolonien waren rot gefärbt. Einige Kolonien, welche L-Prolin nicht oxidieren konnten, waren weiß. Eine dieser Kolonien wurde als Elternstamm zur Herstellung von Mutanten verwendet, die resistent gegen Prolin-Analoga (3,4-Dehydroxyprolin und Azetidin-2-carboxylat) sind, die jeweils in einer Konzentration von 2 mg/ml in M9-Agarmedium gegeben wurden.
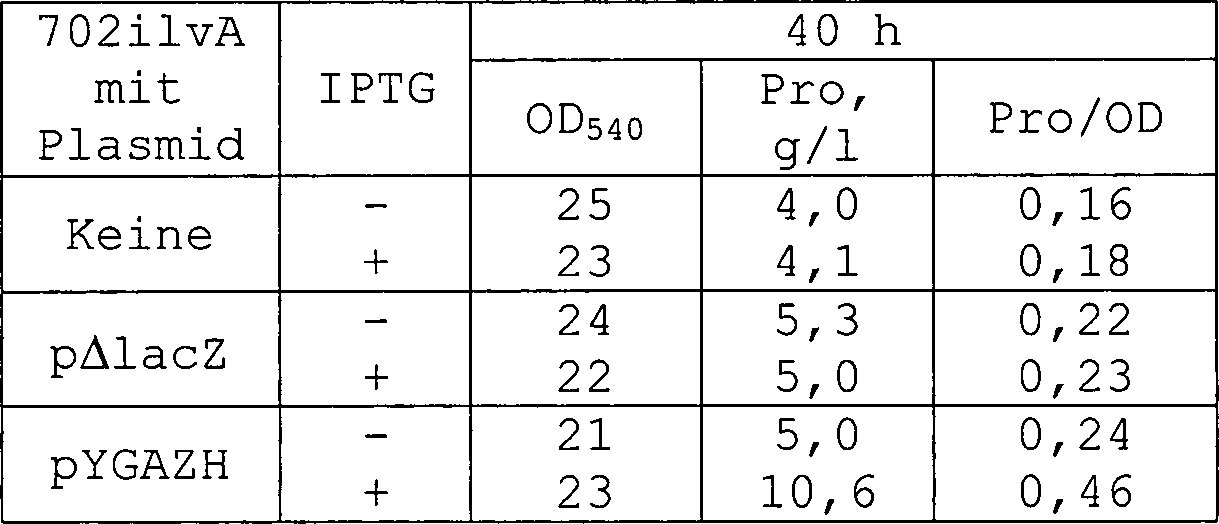
- Einige der aufgetretenen Mutanten konnten L-Prolin produzieren. Der beste L-Prolin-produzierende Stamm 702 wurde mit einem P1-Bakteriophagen behandelt, der auf Zellen des Stammes TG1 gewachsen war, in welchem das Gen ilvA durch Insertion eines Chloramphenicol (Cm)-Resistenz-Gen (Cmr) zerstört war. Eine der erhaltenen Cm-resistenten Transduktanten, 702ilvA, die sich als L-Isoleucin-auxotroph erwies, war ein weit wirksamerer L-Prolin-Erzeuger als der L-Isoleucin-prototrophe Elternstamm 702 (Tabelle 4). Das Fermentationsmedium enthielt 60 g/l Glucose, 25 g/l Ammoniumsulfat, 2 g/l KH2PO4, 1 g/l MgSO4, 0,1 mg/l Thiamin, 50 mg/l L-Isoleucin und 25 g/l Kreide (pH 7,2). Glucose und Kreide wurden separat sterilisiert. 2 ml des Mediums wurden in Reagenzgläser gegeben und mit einer Schleife des getesteten Mikroorganismus inokuliert und die Kultivierung erfolgte bei 37°C während 2 Tagen unter Schütteln.
- Die Stämme 702 und 702ilvA sind seit 25. Juli 2000 unter den Hinterlegungsnummern VKPM B-8011 und VKPM B-8012 bei der Russischen Nationalkollektion von industriellen Mikroorganismen (VKPM) hinterlegt.
- Beispiel 5: Produktion von Prolin durch einen Stamm mit dem Plasmid pYGAZH
- Der Prolin-produzierende Stamm E. coli 702ilvA wurde mit Hilfe des Plasmids pYGAZH, welches die Gene b2682 und b2683 unter der Kontrolle des Plac-UV5-Promoters trägt, transformiert.
- 5 Kolonien jedes Stammes 702ilvA, 702ilvA(pΔlacZ) als Kontrollstamm, der das Plasmid ohne Insertion enthielt, und 702ilvA(pYGAZH) wurden in 2 ml Minimalmedium ((NH4)2SO4 – 18 g/l, K2HPO4 – 1,8 g/l, MgSO4 – 1,2 g/l, Thiamin – 0,1 mg/l, Hefeextrakt – 0,5 g/l, Glucose – 60 g/l, Isoleucin – 50 mg/l, Ampicillin – 300 mg/l, falls erforderlich) in 20 ml-Reagenzgläsern suspendiert und über Nacht unter Belüftung bei 32°C inkubiert. 0,2 ml jeder der über Nacht erhaltenen Kulturen wurde in drei 20 ml-Reagenzgläser mit 2 ml frischem Fermen tationsmedium mit oder ohne IPTG übergeführt und 40 Stunden bei 32°C mit Hilfe eines Rotationsschüttlers kultiviert. Zusammensetzung des Fermentationsmediums:
(NH4)2SO4 18 g/l K2HPO4 1,8 g/l MgSO4 1,2 g/l CaCO3 20 mg/l Thiamin 0,1 mg/l Glucose 60 g/l Isoleucin 60 g/l Ampicillin 300 mg/l, falls erforderlich IPTG 0,5 mM, falls erforderlich - Nach dem Kultivieren wurden die Stabilität des Plasmids und die optische Absorption des Mediums bei 540 nm mit Hilfe von üblichen Methoden bestimmt. Die in dem Medium angereicherte Menge an Prolin wurde durch TLC bestimmt. Die Zusammensetzung der flüssigen Phase für TLC war wie folgt: Ethanol: 80 ml, NH4OH (30%): 5 ml, H2O: 25 ml. Die Ergebnisse sind in Tabelle 5 gezeigt. Wie ersichtlich ist, verbesserte das Hybridplasmid pYGAZH die Anreicherung von Prolin durch den Prolin-produzierenden Stamm 702ilvA.
- Referenzbeispiel 2: Produktion von L-Leucin durch einen ilvE-defizienten L-Leucin-produzierenden Stamm
- Die Zellen des Wildtypstamms E. coli K12 (VKPM B-7) wurden 20 Minuten bei 37°C mit einem Mutagen, N-Methyl-N'-nitro-N-nitrosoguanidin (0,05 mg/ml), behandelt, 4-mal mit physiologischer Kochsalzlösung gewaschen und auf ein Minimal-Agarmedium M9 aufplattiert, das mit 4,0 mg/ml DL-4-Azaleucin ergänzt war. Die Platten wurden 5 Tage bei 37°C inkubiert. Auf den Platten erschienene Kolonien wurden aufgenommen und durch Aufstreichen auf L-Agar-Platten gereinigt. Eine der erhaltenen gegen DL-4-Azaleucin resistenten Mutanten wurde zur Induktion der L-Isoleucin- und L-Valin-Doppelauxotrophie verwendet. Es wurden zahllose Doppelauxotrophe erhalten, die L-Isoleucin- und L-Valin zum Wachstum benötigen. Es wurde gezeigt, dass die Doppelauxotrophie für L-Isoleucin- und L-Valin durch Mutation in dem ilvE-Gen verursacht war. Unter den erhaltenen Doppelauxotrophen wurde der beste L-Leucinproduzierende Stamm, Stamm 505 selektiert, der 1,8 g/l L-Leucin produzierte. Das Fermentationsmedium enthielt 60 g/l Glucose, 25 g/l Ammoniumsulfat, 2 g/l KH2PO4, 1 g/l MgSO4, 0,1 mg/l Thiamin, 100 mg/l L-Isoleucin, 100 mg/l L-Valin und 25 g/l Kreide (pH 7,2). Glucose und Kreide wurden gesondert sterilisiert. 2 ml des Mediums wurden in Reagenzgläser gegeben und mit einer Schleife des Testmikroorganismus inokuliert und das Kultivieren erfolgte 2 Tage unter Schütteln bei 37°C.
- Der Stamm E. coli 505 wurde am 14. Mai 2001 unter der Hinterlegungsnummer VKPM B-8124 bei der Russischen Nationalkollektion für industrielle Mikroorganismen (VKPM) (Russia 113545, Moscow, 1 Dorozhny proezd, 1) hinterlegt und aus der ursprünglichen Hinterlegung am 1. Februar 2002 in die inter nationale Hinterlegung nach dem Budapester Vertrag übergeführt.
- Beispiel 6: Produktion von Leucin durch einen Stamm mit dem Plasmid pYGAZH
- Der Leucin-produzierende Stamm E. coli 505 wurde durch das Plasmids pYGAZH, der die Gene b2682 und b2683 unter der Kontrolle des Plac-UVS-Promoters enthielt, transformiert.
- 20 Kolonien jedes Stammes 505, 505(pΔlacZ) als Kontrollstamm, der das Plasmid ohne Insertion enthielt, und 505 (pYGAZH) wurden in Form einer Schleife der Kultur in 20 ml-Reagenzgläser mit L-Brühe mit oder ohne Ampicillin übergeführt und über Nacht unter Belüften bei 32°C inkubiert. 0,1 ml jeder der über Nacht erhaltenen Kulturen wurde in 20 ml-Reagenzgläser (Innendurchmesser 22 mm) übergeführt, in 2 ml Fermentationsmedium mit oder ohne IPTG suspendiert und 72 Stunden in einem Rotationsschüttler bei 32°C kultiviert. Zusammensetzung des Fermentationsmediums:
(NH4)2SO4 15 g/l K2HPO4 1,5 g/l MgSO4 × 7H2O 1,0 g/l CaCO3 20 g/l (gesondert sterilisiert) Thiamin 0,1 mg/l Glucose 60 g/l (gesondert sterilisiert) Isoleucin 0,3 g/l Valin 0,3 g/l Ampicillin 150 mg/l, falls erforderlich IPTG 0,5 mM, falls erforderlich - Nach dem Kultivieren wurde die Stabilität des Plasmids mit Hilfe einer üblichen Methode bestimmt. Die angereicherte Menge an Leucin in dem Medium wurde durch TLC bestimmt. Die Zusammensetzung der flüssigen Phase für TLC war wie folgt: Isopropanol: 80 ml, Ethylacetat: 80 ml, NH4OH (30%): 25 ml, H2O: 50 ml. Die Ergebnisse sind in Tabelle 6 gezeigt. Wie ersichtlich ist, verbesserte das Hybridplasmid pYGAZH die Leucin-Anreicherung durch den Leucin-produzierenden Stamm 505.
- Referenzbeispiel 3: Produktion von L-Methionin durch einen L-Methionin-produzierenden Stamm der gegen Norleucin resistent ist
- Der plasmidlose Threonin- und Leucin-defiziente Stamm E. coli C600 wurde als Elternstamm verwendet. Zuerst wurden Leu+-Varianten des Stammes E. coli C600 durch Transduktion mit dem Phagen P1 erhalten, der auf dem Stamm E. coli K-12 gewachsen war. Dann wurde nach der Behandlung mit N-Methyl-N'-nitro-N-nitrosoguanidin (NTG) der Mutantenstamm 44, der gegen 8 g/l L-Homoserin resistent war, erhalten. Stamm 44 ist L-Threonin-defizient und resistent gegen hohe Konzentrationen von L-Homoserin. Stamm 44 wurde bei der Russischen Nationalkollektion für industrielle Mikroorganismen (VKPM)unter der Hinterlegungsnummer VKPM B-2175 hinterlegt.
- Dann wurden aus Stamm 44 durch Mutagenese unter Verwendung von NTG Mutantenstämme induziert, die gegen ein Methionin-Analogon, Norleucin, resistent sind. Die Zellen der über Nacht in L-Brühe gewachsenen Kultur wurden abgeschleudert und erneut in physiologischer Kochsalzlösung (0,9% NaCl), die 50 μg/ml NTG enthielt, suspendiert. Nach 30 minütigem Einwirken von NTG bei 37°C wurden die Zellen abgeschleudert, viermal mit physiologischer Kochsalzlösung gewaschen und auf Minimal-Agarmedium M9 aufgestrichen, das 0,5 mg/ml Threonin und 2,5 mg/ml oder 5,0 mg/ml Norleucin enthielt. Die Platten wurden 5 Tage bei 37°C inkubiert. Auf den Platten erschienene Kolonien wurden aufgenommen und durch Aufstreichen auf L-Agar-Platten gereinigt. Der beste L-Methionin-produzierende Stamm unter diesen war Stamm 218. Das Kultivieren des neuen Stammes 218 im Reagenzglas während 3 Tagen bei 32°C unter Schütteln führt zur Anreicherung von etwa 1 g/l L-Methionin in dem Kulturmedium. Als Fermentationsmedium wurde Minimalmedium M9 verwendet, das 4% Glucose, 2,5% Ammoniumsulfat, 0,5 g/l Threonin, 25 g/l Calciumcarbonat enthielt. Glucose und Kreide wurden gesondert sterilisiert.
- Der Stamm 218 ist seit 14. Mai 2001 unter der Hinterlegungsnummer VKPM B-8124 bei der Russischen Nationalkollektion für industrielle Mikroorganismen (VKPM) hinterlegt und wurde aus der ursprünglichen Hinterlegung am 1. Februar 2002 in eine internationale Hinterlegung nach dem Budapester Vertrag übergeführt.
- Außerdem wurde die Deletion des ppc-Gens vermittels des Phagen P1 in den Stamm 218 eingeführt, wonach das pycA-Gen aus Bacillus subtilis eingefügt wurde (Russische Patentveröffentlichung 2207376). Der erhaltene Stamm 218pycA hat die Resistenz gegen Norleucin verloren. Daher wurde dem Stamm wieder Resistenz gegen Norleucin verliehen, wie oben beschrieben ist. Der beste L-Methionin-produzierende Stamm unter den erhaltenen Stämmen war Stamm E. coli 73, der unter den vorstehend beschriebenen Bedingungen etwa 1 g/l L-Methionin produzierte.
- Der Stamm E. coli 73 wurde am 14. Mai 2001 unter der Hinterlegungsnummer VKPM B-8126 in der Russischen Nationalkollektion für industrielle Mikroorganismen (VKPM) (Russia 113545, Moscow, 1 Dorozhny proezd, 1) hinterlegt und am 1. Februar 2002 aus der ursprünglichen Hinterlegung in eine internationale Hinterlegung nach dem Budapester Vertrag übergeführt.
- Beispiel 7: Produktion von Methionin durch einen Stamm mit dem Plasmid pYGAZH
- Der Methionin-produzierende Stamm E. coli 73 wurde mit Hilfe des Plasmids pYGAZH, welches die Gene b2682 und b2683 unter der Kontrolle des Plac-UV5-Promoters trägt, transformiert.
- 5 Kolonien jedes Stammes 73, 73(pΔlacZ) als Kontrollstamm, der das Plasmid ohne Insertion enthielt und 73(pYGAZH) wurden in 2 ml Minimalmedium in 20 ml-Reagenzgläsern suspendiert ((NH4)2SO4 – 18 g/l, K2HPO4 – 1,8 g/l, MgSO4 – 1,2 g/l, Thiamin – 0,1 mg/l, Hefeextrakt – 10 g/l, Glucose – 60 g/l, Threonin – 400 mg/l, Ampicillin – 300 mg/l, falls erforderlich) und über Nacht unter Belüften bei 32°C inkubiert. 0,2 ml jeder der über Nacht erhaltenen Kulturen wurde in drei 20 ml-Reagenzgläser mit 2 ml frischem Fermentationsmedium mit oder ohne IPTG übergeführt und 48 Stunden auf einem Rotationsschüttler bei 32°C kultiviert. Zusammensetzung des Fermentationsmediums:
(NH4)2SO4 18 g/l K2HPO4 1,8 g/l MgSO4 1,2 g/l CaCO3 20 g/l Thiamin 0,1 mg/l Glucose 60 g/l Threonin 400 g/l Hefeextrakt 1,0 g/l Ampicillin 300 mg/l, falls erforderlich IPTG 0,5 mM, falls erforderlich - Nach dem Kultivieren wurden die Stabilität des Plasmids und die optische Absorption des Mediums bei 540 nm mit Hilfe von üblichen Methoden bestimmt. Die angereicherte Menge an Methionin in dem Medium wurde durch TLC bestimmt. Die Zusammensetzung der flüssigen Phase für TLC war wie folgt: Isopropanol: 80 ml, Ethylacetat: 80 ml, NH4OH (30%): 15 ml, H2O: 45 ml. Die Ergebnisse sind in Tabelle 7 gezeigt. Wie ersichtlich ist, verbesserte das Hybridplasmid pYGAZH die Anreicherung von Methionin durch den Methionin-produzierenden Stamm 73.
Claims (13)
- L-Aminosäure produzierendes Bakterium der Gattung Escherichia, welches so modifiziert worden ist, daß die L-Aminosäureproduktion durch das Bakterium durch Erhöhen der Aktivitäten der Proteine, die im folgenden durch (A) oder (B) und (C) oder (D) definiert sind, in einer Zelle des Bakteriums erhöht ist: (A) ein Protein, welches die Aminosäuresequenz der SEQ ID NO:3 des Sequenzprotokolls umfaßt; (B) ein Protein, welches eine Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-24 Aminosäuren in der Aminosäuresequenz der SEQ ID NO:3 des Sequenzprotokols umfaßt und das eine Aktivität aufweist, durch die das Bakterium mit einer erhöhten Resistenz gegen L-Aminosäure und/oder deren Analoga versehen wird; (C) ein Protein, das die Aminosäuresequenz der SEQ ID NO:5 des Sequenzprotokolls umfaßt; (D) ein Protein, das die Aminosäuresequenz, einschließlich Deletion, Substitution, Insertion oder Addition von 1-11 Aminosäuren in der Aminosäuresequenz der SEQ ID NO:5 des Sequenzprotokolls umfaßt und das eine Aktivität aufweist, durch die das Bakterium mit einer erhöhten Resistenz gegen L-Aminosäuren und/oder deren Analoga versehen wird, wobei die Aktivitäten der Proteine durch Transformation des Bakteriums mit DNA, die für ein in (A) oder (B) und (C) oder (D) definiertes Protein codiert, oder durch Veränderung der Promotorsequenz der DNA auf dem Chromosom des Bakteriums erhöht ist.
- Bakterium nach Anspruch 1, wobei die Transformation mit einem Mehrkopienvektor durchgeführt wird.
- Verfahren zum Herstellen einer L-Aminosäure, welches das Kultivieren des Bakteriums nach Anspruch 1 oder 2 in einem Kulturmedium und das Gewinnen der herzustellenden und anzuhäufenden L-Aminosäure aus dem Kulturmedium umfaßt.
- Verfahren nach Anspruch 3, wobei die L-Aminosäure L-Threonin ist.
- Verfahren nach Anspruch 4, wobei das Bakterium so modifiziert worden ist, daß das Bakterium eine erhöhte Expression des Threonin-Operons aufweist.
- Verfahren nach Anspruch 3, wobei die L-Aminosäure L-Valin ist.
- Verfahren nach Anspruch 6, wobei das Bakterium so modifiziert worden ist, daß das Bakterium eine erhöhte Expression des ilv-Operons aufweist.
- Verfahren nach Anspruch 3, wobei die L-Aminosäure L-Prolin ist.
- Verfahren nach Anspruch 8, wobei das Bakterium so modifiziert worden ist, daß das Bakterium eine erhöhte Expression von Genen für die Prolin-Biosynthese aufweist.
- Verfahren nach Anspruch 3, wobei die L-Aminosäure L-Leucin ist.
- Verfahren nach Anspruch 10, wobei das Bakterium so modifiziert worden ist, daß das Bakterium eine erhöhte Expression des leu-Operons aufweist.
- Verfahren nach Anspruch 3, wobei die L-Aminosäure L-Methionin ist.
- Verfahren nach Anspruch 12, wobei das Bakterium so modifiziert worden ist, daß das Bakterium eine erhöhte Expression von Genen des met-Regulons aufweist.
Applications Claiming Priority (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2001103865 | 2001-02-13 | ||
| RU2001103865 | 2001-02-13 | ||
| RU2001104999 | 2001-02-26 | ||
| RU2001104998 | 2001-02-26 | ||
| RU2001104998A RU2215782C2 (ru) | 2001-02-26 | 2001-02-26 | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ, ШТАММ Escherichia coli - ПРОДУЦЕНТ L-АМИНОКИСЛОТЫ (ВАРИАНТЫ) |
| RU2001104999 | 2001-02-26 | ||
| RU2001117633A RU2215785C2 (ru) | 2001-06-28 | 2001-06-28 | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ, ШТАММ Escherichia coli - ПРОДУЦЕНТ L-АМИНОКИСЛОТЫ (ВАРИАНТЫ) |
| RU2001117632 | 2001-06-28 | ||
| RU2001117632A RU2215784C2 (ru) | 2001-06-28 | 2001-06-28 | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ, ШТАММ Escherichia coli - ПРОДУЦЕНТ L-АМИНОКИСЛОТЫ (ВАРИАНТЫ) |
| RU2001117633 | 2001-06-28 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60210697D1 DE60210697D1 (de) | 2006-05-24 |
| DE60210697T2 true DE60210697T2 (de) | 2007-04-05 |
Family
ID=27532689
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60219969T Expired - Lifetime DE60219969T2 (de) | 2001-02-13 | 2002-02-13 | Methode zur Production von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
| DE60210697T Expired - Lifetime DE60210697T2 (de) | 2001-02-13 | 2002-02-13 | Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
| DE60219968T Expired - Lifetime DE60219968T2 (de) | 2001-02-13 | 2002-02-13 | Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60219969T Expired - Lifetime DE60219969T2 (de) | 2001-02-13 | 2002-02-13 | Methode zur Production von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60219968T Expired - Lifetime DE60219968T2 (de) | 2001-02-13 | 2002-02-13 | Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
Country Status (6)
| Country | Link |
|---|---|
| US (3) | US7476531B2 (de) |
| EP (3) | EP1526179B9 (de) |
| JP (3) | JP5087194B2 (de) |
| CN (1) | CN100529057C (de) |
| BR (3) | BR0200350B1 (de) |
| DE (3) | DE60219969T2 (de) |
Families Citing this family (93)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9623709D0 (en) * | 1996-11-14 | 1997-01-08 | Kodak Ltd | Novel auxiliary developing agents,photographic materials incorporating them and the use thereof |
| RU2175351C2 (ru) * | 1998-12-30 | 2001-10-27 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО "АГРИ") | Фрагмент днк из escherichia coli, определяющий повышенную продукцию l-аминокислот (варианты), и способ получения l-аминокислот |
| DE60219969T2 (de) * | 2001-02-13 | 2008-01-17 | Ajinomoto Co., Inc. | Methode zur Production von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
| RU2229513C2 (ru) * | 2001-11-23 | 2004-05-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" | Способ получения l-аминокислот, штамм escherichia coli - продуцент l-аминокислоты (варианты) |
| RU2230114C2 (ru) * | 2001-11-30 | 2004-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" | Мутантная глутаминсинтетаза, фрагмент днк, штамм escherichia coli - продуцент l-глутамина и способ получения l-аминокислот |
| DE10314618A1 (de) * | 2003-04-01 | 2004-10-14 | Degussa Ag | Verfahren zur Herstellung von L-Aminosäuren unter Verwendung von Stämmen der Familie Enterobacteriaceae |
| KR100786987B1 (ko) | 2004-01-30 | 2007-12-18 | 아지노모토 가부시키가이샤 | L-아미노산 생산 미생물 및 l-아미노산 생산 방법 |
| KR100608085B1 (ko) * | 2004-02-05 | 2006-08-02 | 씨제이 주식회사 | tyrR 유전자가 불활성화된 L-쓰레오닌 생성 미생물,그를 제조하는 방법 및 상기 미생물을 이용한L-쓰레오닌의 제조방법 |
| KR100576342B1 (ko) * | 2004-02-05 | 2006-05-03 | 씨제이 주식회사 | galR 유전자가 불활성화된 L-쓰레오닌 생성 미생물,그를 제조하는 방법 및 상기 미생물을 이용한L-쓰레오닌의 제조방법 |
| KR100651220B1 (ko) | 2004-06-29 | 2006-11-29 | 씨제이 주식회사 | L-메씨오닌 생산 균주 및 상기 균주를 이용한l-메씨오닌의 생산방법 |
| RU2004124226A (ru) | 2004-08-10 | 2006-01-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Использование фосфокетолазы для продукции полезных метаболитов |
| CN1749390B (zh) * | 2004-09-17 | 2011-10-19 | 味之素株式会社 | 使用木糖利用基因表达增强的细菌进行发酵以生产l—氨基酸的方法 |
| US7915018B2 (en) | 2004-10-22 | 2011-03-29 | Ajinomoto Co., Inc. | Method for producing L-amino acids using bacteria of the Enterobacteriaceae family |
| KR100596372B1 (ko) * | 2004-12-06 | 2006-07-04 | 씨제이 주식회사 | 염색체 상의 lysR유전자가 불활성화된 L-쓰레오닌생성 미생물, 그를 제조하는 방법 및 상기 미생물을이용한 L-쓰레오닌의 제조방법 |
| RU2004137198A (ru) * | 2004-12-21 | 2006-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae, В КОТОРОЙ ИНАКТИВИРОВАН ГЕН yafA |
| RU2004137719A (ru) * | 2004-12-23 | 2006-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Способ получения l-аминокислот с использованием бактерий семейства enterobacteriaceae |
| US7422880B2 (en) * | 2005-01-19 | 2008-09-09 | Ajinomoto Co., Inc. | Method for producing an l-amino acid using a bacterium of the enterobacteriaceae family having a pathway of glycogen biosynthesis disrupted |
| EP1848810A1 (de) * | 2005-02-18 | 2007-10-31 | Ajinomoto Co., Inc. | Verfahren zur herstellung einer l-aminosäure unter verwendung eines bakteriums der familie enterobacteriaceae mit abgeschwächter expression des bola-gens |
| ATE438731T1 (de) | 2005-02-18 | 2009-08-15 | Ajinomoto Kk | Verfahren zur herstellung einer l-aminosäure unter verwendung eines bakteriums der familie enterobacteriaceae |
| DE602006015302D1 (de) * | 2005-05-16 | 2010-08-19 | Ajinomoto Kk | Verfahren zur herstellung einer l-aminosäure unter verwendung eines bakteriums der familie enterobacteriaceae mit abgeschwächter expression des kefb-gens |
| WO2007013639A1 (en) * | 2005-07-25 | 2007-02-01 | Ajinomoto Co., Inc. | A METHOD FOR PRODUCING AN L-AMINO ACID USING A BACTERIUM OF THE ENTEROBACTERIACEAE FAMILY WITH ATTENUATED EXPRESSION OF THE cpxR GENE |
| DE602006004893D1 (de) * | 2005-08-09 | 2009-03-05 | Ajinomoto Kk | VERFAHREN ZUR HERSTELLUNG EINER L-AMINOSÄURE UNTER VERWENDUNG EINES BAKTERIUMS DER FAMILIE ENTEROBACTERIACEAE MIT ABGESCHWÄCHTER EXPRESSION DES ybiV-GENS |
| WO2007086546A1 (en) * | 2006-01-26 | 2007-08-02 | Ajinomoto Co., Inc. | A method for producing an l-amino acid using a bacterium of enterobacteriaceae family with attenuated expression of the aldh gene |
| BRPI0707229B8 (pt) | 2006-01-27 | 2017-06-27 | Ajinomoto Kk | método para produzir um l-aminoácido |
| WO2007086618A1 (en) | 2006-01-30 | 2007-08-02 | Ajinomoto Co., Inc. | L-amino acid producing bacterium and method of producing l-amino acid |
| JP2009118740A (ja) | 2006-03-03 | 2009-06-04 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| EP2351830B1 (de) | 2006-03-23 | 2014-04-23 | Ajinomoto Co., Inc. | Methode zur Produktion einer L-Aminosäure unter Verwendung eines Bakteriums der Enterobacteriaceae Familie mit einer abgeschwächten Expression eines Gens kodierend für sRNA |
| EP2007873B1 (de) * | 2006-04-18 | 2015-11-18 | Ajinomoto Co., Inc. | VERFAHREN ZUR HERSTELLUNG EINER L-AMINOSÄURE UNTER VERWENDUNG EINES BAKTERIUMS DER FAMILIE ENTEROBACTERIACEAE MIT ABGESCHWÄCHTER sfmACDFH-fimZ-CLUSTER- ODER fimZ -GENEXPRESSION |
| JP2009165355A (ja) | 2006-04-28 | 2009-07-30 | Ajinomoto Co Inc | L−アミノ酸を生産する微生物及びl−アミノ酸の製造法 |
| WO2007139219A1 (en) * | 2006-06-01 | 2007-12-06 | Ajinomoto Co., Inc. | A method for producing an l-amino acid using a bacterium of the enterobacteriaceae family with attenuated expression of the rcsa gene |
| RU2337961C2 (ru) * | 2006-07-04 | 2008-11-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) | СПОСОБ ПОЛУЧЕНИЯ L-ТРЕОНИНА С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ, ПРИНАДЛЕЖАЩЕЙ К РОДУ Escherichia, В КОТОРОЙ ИНАКТИВИРОВАН ОПЕРОН rspAB |
| JP2010017082A (ja) | 2006-10-10 | 2010-01-28 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| RU2006143864A (ru) | 2006-12-12 | 2008-06-20 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА ENTEROBACTERIACEAE, В КОТОРОЙ ОСЛАБЛЕНА ЭКСПРЕССИЯ ГЕНОВ cynT, cynS, cynX, ИЛИ cynR, ИЛИ ИХ КОМБИНАЦИИ |
| JP2010041920A (ja) | 2006-12-19 | 2010-02-25 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| RU2006145712A (ru) * | 2006-12-22 | 2008-06-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Способ получения l-аминокислот методом ферментации с использованием бактерий, обладающих повышенной способностью к утилизации глицерина |
| KR100832740B1 (ko) * | 2007-01-17 | 2008-05-27 | 한국과학기술원 | 분지쇄 아미노산 생성능이 개선된 변이 미생물 및 이를이용한 분지쇄 아미노산의 제조방법 |
| JP5540504B2 (ja) | 2007-01-22 | 2014-07-02 | 味の素株式会社 | L−アミノ酸を生産する微生物及びl−アミノ酸の製造法 |
| JP2010110216A (ja) | 2007-02-20 | 2010-05-20 | Ajinomoto Co Inc | L−アミノ酸または核酸の製造方法 |
| JP2010110217A (ja) | 2007-02-22 | 2010-05-20 | Ajinomoto Co Inc | L−アミノ酸生産菌及びl−アミノ酸の製造法 |
| JP2010130899A (ja) | 2007-03-14 | 2010-06-17 | Ajinomoto Co Inc | L−グルタミン酸系アミノ酸生産微生物及びアミノ酸の製造法 |
| JP2010183841A (ja) * | 2007-05-29 | 2010-08-26 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| EP2192170B1 (de) | 2007-09-04 | 2017-02-15 | Ajinomoto Co., Inc. | Aminosäureproduzierender mikroorganismus und verfahren zur aminosäureproduktion |
| RU2396336C2 (ru) | 2007-09-27 | 2010-08-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) | СПОСОБ ПОЛУЧЕНИЯ АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ, ПРИНАДЛЕЖАЩЕЙ К РОДУ Escherichia |
| JP2011067095A (ja) | 2008-01-10 | 2011-04-07 | Ajinomoto Co Inc | 発酵法による目的物質の製造法 |
| KR20100120663A (ko) | 2008-01-23 | 2010-11-16 | 아지노모토 가부시키가이샤 | L-아미노산의 제조법 |
| RU2008105793A (ru) | 2008-02-19 | 2009-08-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Способ конструирования оперонов, содержащих трансляционно сопряженные гены, бактерия, содержащая такой оперон, способ продукции полезного метаболита и способ мониторинга экспрессии гена |
| JP5598329B2 (ja) | 2008-09-08 | 2014-10-01 | 味の素株式会社 | L−アミノ酸を生産する微生物及びl−アミノ酸の製造法 |
| JP2012029565A (ja) | 2008-11-27 | 2012-02-16 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| RU2008148283A (ru) * | 2008-12-09 | 2010-06-20 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | СПОСОБ ПОЛУЧЕНИЯ L-АРГИНИНА С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА ENTEROBACTERIACEAE, В КОТОРОЙ ОСЛАБЛЕНА ЭКСПРЕССИЯ ГЕНА artI |
| BRPI1007069A2 (pt) | 2009-01-23 | 2015-08-25 | Ajinomoto Kk | Método para produzir um l-aminoácido. |
| WO2011011391A1 (en) | 2009-07-22 | 2011-01-27 | E.I. Dupont De Nemours And Company | Sequences and their use for detection and characterization of e. coli o157:h7 |
| CN102471790B (zh) | 2009-07-29 | 2014-10-29 | 味之素株式会社 | 产生l-氨基酸的方法 |
| RU2460793C2 (ru) | 2010-01-15 | 2012-09-10 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО АГРИ) | Способ получения l-аминокислот с использованием бактерий семейства enterobacteriaceae |
| JP2013074795A (ja) | 2010-02-08 | 2013-04-25 | Ajinomoto Co Inc | 変異型rpsA遺伝子及びL−アミノ酸の製造法 |
| RU2471868C2 (ru) | 2010-02-18 | 2013-01-10 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО АГРИ) | Мутантная аденилатциклаза, днк, кодирующая ее, бактерия семейства enterobacteriaceae, содержащая указанную днк, и способ получения l-аминокислот |
| WO2011106696A2 (en) * | 2010-02-26 | 2011-09-01 | The Regents Of The University Of California | Compositions and methods for the production of l-homoalanine |
| RU2471870C2 (ru) | 2010-06-03 | 2013-01-10 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО АГРИ) | СПОСОБ ПОЛУЧЕНИЯ L-АРГИНИНА И L-ЦИТРУЛЛИНА С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА ENTEROBACTERIACEAE, В КОТОРОЙ ОСЛАБЛЕНА ЭКСПРЕССИЯ ГЕНА pepA |
| RU2501858C2 (ru) | 2010-07-21 | 2013-12-20 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО АГРИ) | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТЫ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae |
| RU2482188C2 (ru) | 2010-07-21 | 2013-05-20 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО АГРИ) | СПОСОБ ПОЛУЧЕНИЯ L-АРГИНИНА С ИСПОЛЬЗОВАНИЕМ БАКТЕРИЙ РОДА Escherichia, В КОТОРОЙ ИНАКТИВИРОВАН ОПЕРОН astCADBE |
| JP2014036576A (ja) | 2010-12-10 | 2014-02-27 | Ajinomoto Co Inc | L−アミノ酸の製造法 |
| EP2479279A1 (de) | 2011-01-20 | 2012-07-25 | Evonik Degussa GmbH | Verfahren zur fermentativen Herstellung schwefelhaltiger Aminosäuren |
| JP2014131487A (ja) | 2011-04-18 | 2014-07-17 | Ajinomoto Co Inc | L−システインの製造法 |
| RU2011134436A (ru) | 2011-08-18 | 2013-10-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО "АГРИ") | Способ получения l-аминокислоты с использованием бактерии семейства enterobacteriaceae, обладающей повышенной экспрессией генов каскада образования флагелл и клеточной подвижности |
| BR112013016373B1 (pt) | 2011-11-11 | 2021-05-18 | Ajinomoto Co., Inc | método para produzir uma substância alvo |
| RU2012112651A (ru) | 2012-04-02 | 2013-10-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО "АГРИ") | САМОИНДУЦИРУЕМАЯ ЭКСПРЕССИОННАЯ СИСТЕМА И ЕЕ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ПОЛЕЗНЫХ МЕТАБОЛИТОВ С ПОМОЩЬЮ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae |
| CN103173505B (zh) * | 2013-04-07 | 2014-07-23 | 宁夏伊品生物科技股份有限公司 | 用改变乌头酸酶调控元件的细菌发酵生产l-苏氨酸的方法 |
| CN103173504B (zh) * | 2013-04-07 | 2014-07-23 | 宁夏伊品生物科技股份有限公司 | 用乌头酸酶表达弱化和/或酶活性降低的细菌发酵生产l-苏氨酸的方法 |
| RU2013118637A (ru) | 2013-04-23 | 2014-10-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО "АГРИ") | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА ENTEROBACTERIACEAE, В КОТОРОЙ РАЗРЕГУЛИРОВАН ГЕН yjjK |
| CN105008532B (zh) | 2013-05-13 | 2017-07-21 | 味之素株式会社 | L‑氨基酸的制造方法 |
| JP2016165225A (ja) | 2013-07-09 | 2016-09-15 | 味の素株式会社 | 有用物質の製造方法 |
| RU2013140115A (ru) | 2013-08-30 | 2015-03-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО "АГРИ") | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae, В КОТОРОЙ НАРУШЕНА ЭКСПРЕССИЯ КЛАСТЕРА ГЕНОВ znuACB |
| BR112016004367B1 (pt) | 2013-08-30 | 2022-06-14 | Evonik Operations Gmbh | Microrganismo recombinante e método para a produção fermentativa de metionina e/ou seus derivados |
| RU2678757C2 (ru) * | 2013-08-30 | 2019-01-31 | Эвоник Дегусса Гмбх | Микроорганизмы для производства метионина с улучшенным выходом метионина |
| JP2016192903A (ja) | 2013-09-17 | 2016-11-17 | 味の素株式会社 | 海藻由来バイオマスからのl−アミノ酸の製造方法 |
| RU2013144250A (ru) | 2013-10-02 | 2015-04-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО "АГРИ") | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae, В КОТОРОЙ ОСЛАБЛЕНА ЭКСПРЕССИЯ ГЕНА, КОДИРУЮЩЕГО ФОСФАТНЫЙ ТРАНСПОРТЕР |
| BR112016007286B1 (pt) | 2013-10-02 | 2021-07-20 | Ajinomoto Co., Inc | Métodos de controle de amônia e para produção de uma substância alvo, e, aparelho para controle de amônia |
| WO2015060314A1 (ja) | 2013-10-21 | 2015-04-30 | 味の素株式会社 | L-アミノ酸の製造法 |
| JP6519476B2 (ja) | 2013-10-23 | 2019-05-29 | 味の素株式会社 | 目的物質の製造法 |
| RU2014105547A (ru) | 2014-02-14 | 2015-08-20 | Адзиномото Ко., Инк. | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА ENTEROBACTERIACEAE, ИМЕЮЩЕЙ СВЕРХЭКСПРЕССИРУЕМЫЙ ГЕН yajL |
| MY194223A (en) * | 2014-09-01 | 2022-11-22 | Evonik Operations Gmbh | Method and microorganism for methionine production by fermentation with improved methionine efflux |
| EP3280794B1 (de) | 2015-04-07 | 2020-05-27 | Metabolic Explorer | Modifizierter mikroorganismus zur optimierten herstellung von 2,4-dihydroxybutyrat mit verlängertem 2,4-dihydroxybutyrat-ausfluss |
| RU2015120052A (ru) | 2015-05-28 | 2016-12-20 | Аджиномото Ко., Инк. | Способ получения L-аминокислоты с использованием бактерии семейства Enterobacteriaceae, в которой ослаблена экспрессия гена gshA |
| BR112018017227A2 (pt) | 2016-02-25 | 2019-02-05 | Ajinomoto Kk | método para produzir um l-aminoácido |
| CN116218782A (zh) * | 2018-02-02 | 2023-06-06 | 隆萨有限公司 | 细胞选择和修饰细胞代谢的方法 |
| WO2020071538A1 (en) | 2018-10-05 | 2020-04-09 | Ajinomoto Co., Inc. | Method for producing target substance by bacterial fermentation |
| CN111484963A (zh) * | 2019-01-28 | 2020-08-04 | 味之素株式会社 | 用于生产l-氨基酸的方法 |
| JP2022521544A (ja) | 2019-02-22 | 2022-04-08 | 味の素株式会社 | ydiJ遺伝子を過剰発現する腸内細菌科に属する細菌を用いたL-アミノ酸の製造方法 |
| BR112021017870A2 (pt) | 2019-04-05 | 2021-12-07 | Ajinomoto Kk | Método para produzir um l-aminoácido |
| KR102183209B1 (ko) * | 2019-09-09 | 2020-11-26 | 씨제이제일제당 주식회사 | L-쓰레오닌 배출 단백질의 변이체 및 이를 이용한 l-쓰레오닌 생산 방법 |
| JP2022550084A (ja) | 2019-09-25 | 2022-11-30 | 味の素株式会社 | 細菌の発酵によるl-アミノ酸の製造方法 |
| KR102143964B1 (ko) * | 2019-12-06 | 2020-08-12 | 씨제이제일제당 주식회사 | 신규한 분지쇄 아미노산 아미노트랜스퍼라제 변이체 및 이를 이용한 류신 생산방법 |
| PE20231508A1 (es) | 2020-10-28 | 2023-09-26 | Ajinomoto Kk | Metodo de produccion de l-aminoacido |
| US20240117393A1 (en) | 2022-09-30 | 2024-04-11 | Ajinomoto Co., Inc. | Method for producing l-amino acid |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU875663A1 (ru) | 1978-06-30 | 1982-09-15 | Всесоюзный научно-исследовательский институт генетики и селекции промышленных микроорганизмов | Штаммы е.coLI ВНИИГенетика VL 334 @ N6 и ВНИИГенетика VL 334 @ N7-продуценты L-треонина и способ их получени |
| JPS575693A (en) | 1980-06-13 | 1982-01-12 | Ajinomoto Co Inc | Production of l-arginine through fermentation process |
| US5017483A (en) | 1986-02-20 | 1991-05-21 | Kyowa Hakko Kogyo Co., Ltd. | Process for producing L-threonine |
| JPS6437295A (en) * | 1987-07-31 | 1989-02-07 | Kyowa Hakko Kogyo Kk | Production of l-threonine by fermentation |
| DE3832064A1 (de) * | 1988-09-21 | 1990-03-29 | Hoechst Ag | Verfahren zur herstellung von pigmentzubereitungen der anthanthronreihe |
| US5976843A (en) | 1992-04-22 | 1999-11-02 | Ajinomoto Co., Inc. | Bacterial strain of Escherichia coli BKIIM B-3996 as the producer of L-threonine |
| US5705371A (en) | 1990-06-12 | 1998-01-06 | Ajinomoto Co., Inc. | Bacterial strain of escherichia coli BKIIM B-3996 as the producer of L-threonine |
| DE69330518T2 (de) * | 1992-11-10 | 2002-05-08 | Ajinomoto Kk | Dna, die aspartokinase iii-mutanten kodiert und ihre verwendung zur herstellung von l-threonin durch fermentation |
| JPH07155184A (ja) | 1993-12-08 | 1995-06-20 | Ajinomoto Co Inc | 発酵法によるl−リジンの製造法 |
| WO1996041871A1 (fr) * | 1995-06-13 | 1996-12-27 | Ajinomoto Co., Inc. | Procede de production de l-lysine par fermentation |
| DE19548222A1 (de) | 1995-12-22 | 1997-06-26 | Forschungszentrum Juelich Gmbh | Verfahren zur mikrobiellen Herstellung von Aminosäuren durch gesteigerte Aktivität von Exportcarriern |
| DE19726083A1 (de) | 1997-06-19 | 1998-12-24 | Consortium Elektrochem Ind | Mikroorganismen und Verfahren zur fermentativen Herstellung von L-Cystein, L-Cystin, N-Acetyl-Serin oder Thiazolidinderivaten |
| RU2144564C1 (ru) | 1998-10-13 | 2000-01-20 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" | ФРАГМЕНТ ДНК rhtB, КОДИРУЮЩИЙ СИНТЕЗ БЕЛКА RhtB, ПРИДАЮЩЕГО УСТОЙЧИВОСТЬ К L-ГОМОСЕРИНУ БАКТЕРИЯМ ESCHERICHIA COLI, И СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ |
| RU2148642C1 (ru) * | 1998-12-23 | 2000-05-10 | ЗАО "Научно-исследовательский институт АДЖИНОМОТО-Генетика" (ЗАО "АГРИ") | Фрагмент днк rhtc, кодирующий синтез белка rhtc, придающего повышенную устойчивость к l-треонину бактериям escherichia coli, и способ получения l-аминокислоты |
| RU2175351C2 (ru) * | 1998-12-30 | 2001-10-27 | Закрытое акционерное общество "Научно-исследовательский институт "Аджиномото-Генетика" (ЗАО "АГРИ") | Фрагмент днк из escherichia coli, определяющий повышенную продукцию l-аминокислот (варианты), и способ получения l-аминокислот |
| US20020028490A1 (en) | 1999-03-19 | 2002-03-07 | Douwe Molenaar | Process for the production of L-amino acids by fermentation using coryneform bacteria |
| DE19912384A1 (de) * | 1999-03-19 | 2000-09-21 | Degussa | Verfahren zur fermentativen Herstellung von L-Aminosäuren unter Verwendung coryneformer Bakterien |
| JP4273661B2 (ja) * | 1999-04-09 | 2009-06-03 | 味の素株式会社 | L−アミノ酸生産菌及びl−アミノ酸の製造法 |
| JP4245746B2 (ja) * | 1999-09-20 | 2009-04-02 | 協和発酵バイオ株式会社 | 発酵法によるアミノ酸の製造法 |
| DE60219969T2 (de) | 2001-02-13 | 2008-01-17 | Ajinomoto Co., Inc. | Methode zur Production von L-Aminosäuren mittels Bakterien der Gattung Escherichia |
| RU2229513C2 (ru) | 2001-11-23 | 2004-05-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" | Способ получения l-аминокислот, штамм escherichia coli - продуцент l-аминокислоты (варианты) |
| RU2230114C2 (ru) | 2001-11-30 | 2004-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" | Мутантная глутаминсинтетаза, фрагмент днк, штамм escherichia coli - продуцент l-глутамина и способ получения l-аминокислот |
| EP1650296B1 (de) | 2003-07-16 | 2012-04-18 | Ajinomoto Co., Inc. | Mutante serinacetyltransferase und vefahren zur herstellung von l-cystein |
| US8003367B2 (en) | 2004-03-16 | 2011-08-23 | Ajinomoto Co., Inc. | Method for producing L-amino acids by fermentation using bacteria having enhanced expression of xylose utilization genes |
| RU2004124226A (ru) | 2004-08-10 | 2006-01-27 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Использование фосфокетолазы для продукции полезных метаболитов |
| US7915018B2 (en) | 2004-10-22 | 2011-03-29 | Ajinomoto Co., Inc. | Method for producing L-amino acids using bacteria of the Enterobacteriaceae family |
| RU2004137198A (ru) | 2004-12-21 | 2006-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ИСПОЛЬЗОВАНИЕМ БАКТЕРИИ СЕМЕЙСТВА Enterobacteriaceae, В КОТОРОЙ ИНАКТИВИРОВАН ГЕН yafA |
| RU2004137719A (ru) | 2004-12-23 | 2006-06-10 | Закрытое акционерное общество "Научно-исследовательский институт Аджиномото-Генетика" (ЗАО АГРИ) (RU) | Способ получения l-аминокислот с использованием бактерий семейства enterobacteriaceae |
| US7422880B2 (en) | 2005-01-19 | 2008-09-09 | Ajinomoto Co., Inc. | Method for producing an l-amino acid using a bacterium of the enterobacteriaceae family having a pathway of glycogen biosynthesis disrupted |
-
2002
- 2002-02-13 DE DE60219969T patent/DE60219969T2/de not_active Expired - Lifetime
- 2002-02-13 BR BRPI0200350-3A patent/BR0200350B1/pt active IP Right Grant
- 2002-02-13 JP JP2002034760A patent/JP5087194B2/ja not_active Expired - Fee Related
- 2002-02-13 EP EP04028876A patent/EP1526179B9/de not_active Expired - Lifetime
- 2002-02-13 DE DE60210697T patent/DE60210697T2/de not_active Expired - Lifetime
- 2002-02-13 US US10/073,293 patent/US7476531B2/en not_active Expired - Fee Related
- 2002-02-13 EP EP04028877A patent/EP1526181B1/de not_active Expired - Lifetime
- 2002-02-13 DE DE60219968T patent/DE60219968T2/de not_active Expired - Lifetime
- 2002-02-13 BR BR122013017187A patent/BR122013017187B1/pt active IP Right Grant
- 2002-02-13 CN CNB021080860A patent/CN100529057C/zh not_active Expired - Lifetime
- 2002-02-13 EP EP02003335A patent/EP1239041B1/de not_active Expired - Lifetime
- 2002-02-13 BR BR122013017189A patent/BR122013017189B1/pt active IP Right Grant
-
2007
- 2007-10-22 JP JP2007273972A patent/JP2008067714A/ja active Pending
- 2007-10-22 JP JP2007273965A patent/JP5087362B2/ja not_active Expired - Fee Related
-
2008
- 2008-05-14 US US12/120,409 patent/US7618804B2/en not_active Expired - Fee Related
- 2008-05-14 US US12/120,404 patent/US7618803B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP1239041A3 (de) | 2003-01-15 |
| JP2002300874A (ja) | 2002-10-15 |
| EP1526181A1 (de) | 2005-04-27 |
| DE60219968D1 (de) | 2007-06-14 |
| DE60210697D1 (de) | 2006-05-24 |
| BR122013017187B1 (pt) | 2016-03-01 |
| US7618804B2 (en) | 2009-11-17 |
| DE60219969T2 (de) | 2008-01-17 |
| JP5087194B2 (ja) | 2012-11-28 |
| JP2008073053A (ja) | 2008-04-03 |
| DE60219969D1 (de) | 2007-06-14 |
| CN1373226A (zh) | 2002-10-09 |
| US20080261279A1 (en) | 2008-10-23 |
| US20050239175A1 (en) | 2005-10-27 |
| EP1526181B1 (de) | 2007-05-02 |
| JP5087362B2 (ja) | 2012-12-05 |
| US7476531B2 (en) | 2009-01-13 |
| CN100529057C (zh) | 2009-08-19 |
| EP1239041A2 (de) | 2002-09-11 |
| BR0200350B1 (pt) | 2014-10-14 |
| EP1526179B9 (de) | 2007-10-10 |
| DE60219968T2 (de) | 2008-01-17 |
| BR0200350A (pt) | 2002-10-08 |
| US20080261278A1 (en) | 2008-10-23 |
| US7618803B2 (en) | 2009-11-17 |
| EP1239041B1 (de) | 2006-04-19 |
| EP1526179A1 (de) | 2005-04-27 |
| BR122013017189B1 (pt) | 2017-02-07 |
| JP2008067714A (ja) | 2008-03-27 |
| EP1526179B1 (de) | 2007-05-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60210697T2 (de) | Verfahren zur Produktion von L-Aminosäuren mittels Bakterien der Gattung Escherichia | |
| DE69937036T2 (de) | Gen und Verfahren zur Herstellung von L-Aminosäuren | |
| DE69535674T2 (de) | Verfahren zur herstellung von l-valin und l-leucin | |
| DE60129995T2 (de) | Aminosäure-herstellende Escherichia Stämme und Verfahren zur Herstellung einer Aminosäure | |
| US6887691B2 (en) | DNA coding for protein which confers on bacterium Escherichia coli resistance to L-homoserine, and method for producing L-amino acids | |
| DE60033151T2 (de) | L-aminosäure herstellendes bakterium und verfahren zur herstellung von l-aminosäure | |
| DE69822960T2 (de) | Verfahren zur Herstellung von L-Leucin | |
| DE3891417C5 (de) | Verfahren zur Veränderung eines L-Threonin produzierenden Mikroorganismus und Verwendung eines so erhaltenen Mikroorganismus zur Herstellung von L-Threonin | |
| DE69535120T2 (de) | L-Isoleucin produzierendes Bacterium und Verfahren zur Herstellung von L-Isoleucin durch Fermentation | |
| DE60120619T2 (de) | Verfahren zur Herstellung einer Zielsubstanz durch Fermentation | |
| EP1067192A1 (de) | L-Lysin produzierende coryneforme Bakterien und Verfahren zur Herstellung von L-Lysin | |
| EP1067193A1 (de) | L-Lysin produzierende coryneforme Bakterien und Verfahren zur Herstellung von Lysin | |
| CN101597588B (zh) | 通过埃希氏菌属细菌生产l-氨基酸的方法 | |
| WO1997001637A1 (de) | Verfahren zur mikrobiellen herstellung von aminosäuren mittels rekombinanter mikroorganismen mit erhöhter sekretionsrate | |
| RU2215784C2 (ru) | СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ, ШТАММ Escherichia coli - ПРОДУЦЕНТ L-АМИНОКИСЛОТЫ (ВАРИАНТЫ) | |
| US20060040364A1 (en) | DNA coding for a protein which imparts L-homoserine resistance to Escherichia coli bacterium, and a method for producing L-amino acids | |
| DE10103778A1 (de) | Neues Fermentationsverfahren zur Herstellung von L-Threonin | |
| DE3844959B4 (de) | Stamm der Bakterien Escherichia coli BKIIM B-3996, Produzent von L-Threonin |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition |