CN109922800B - 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 - Google Patents
与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 Download PDFInfo
- Publication number
- CN109922800B CN109922800B CN201780051052.3A CN201780051052A CN109922800B CN 109922800 B CN109922800 B CN 109922800B CN 201780051052 A CN201780051052 A CN 201780051052A CN 109922800 B CN109922800 B CN 109922800B
- Authority
- CN
- China
- Prior art keywords
- day
- cromolyn
- compound
- microglial
- microglia
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 210000004027 cell Anatomy 0.000 title description 72
- 230000002025 microglial effect Effects 0.000 title description 51
- 210000002540 macrophage Anatomy 0.000 title description 25
- 230000004770 neurodegeneration Effects 0.000 title description 11
- 208000036110 Neuroinflammatory disease Diseases 0.000 title description 9
- 230000003959 neuroinflammation Effects 0.000 title description 9
- 208000015122 neurodegenerative disease Diseases 0.000 title description 5
- 230000001537 neural effect Effects 0.000 claims abstract description 15
- 208000027866 inflammatory disease Diseases 0.000 claims abstract description 11
- 208000023105 Huntington disease Diseases 0.000 claims abstract 3
- 208000018737 Parkinson disease Diseases 0.000 claims abstract 3
- 150000001875 compounds Chemical class 0.000 claims description 82
- 238000011282 treatment Methods 0.000 claims description 24
- 239000003814 drug Substances 0.000 claims description 19
- 230000003110 anti-inflammatory effect Effects 0.000 claims description 15
- 229940079593 drug Drugs 0.000 claims description 10
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 claims description 8
- 229960001680 ibuprofen Drugs 0.000 claims description 8
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 6
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 238000007912 intraperitoneal administration Methods 0.000 claims description 3
- 238000001990 intravenous administration Methods 0.000 claims 2
- IMZMKUWMOSJXDT-UHFFFAOYSA-N cromoglycic acid Chemical compound O1C(C(O)=O)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=CC=CC2=C1C(=O)C=C(C(O)=O)O2 IMZMKUWMOSJXDT-UHFFFAOYSA-N 0.000 abstract description 96
- 229960000265 cromoglicic acid Drugs 0.000 abstract description 93
- 208000024827 Alzheimer disease Diseases 0.000 abstract description 50
- -1 cromolyn derivative compound Chemical class 0.000 abstract description 20
- 238000000034 method Methods 0.000 abstract description 18
- 208000032382 Ischaemic stroke Diseases 0.000 abstract description 5
- 208000024777 Prion disease Diseases 0.000 abstract description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 123
- 210000000274 microglia Anatomy 0.000 description 61
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 48
- 230000004913 activation Effects 0.000 description 27
- 239000000203 mixture Substances 0.000 description 26
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 24
- 102000004127 Cytokines Human genes 0.000 description 23
- 108090000695 Cytokines Proteins 0.000 description 23
- 241000699670 Mus sp. Species 0.000 description 20
- 239000013543 active substance Substances 0.000 description 19
- 230000000694 effects Effects 0.000 description 16
- 210000004556 brain Anatomy 0.000 description 15
- 230000001404 mediated effect Effects 0.000 description 15
- 230000006724 microglial activation Effects 0.000 description 15
- 108090000765 processed proteins & peptides Proteins 0.000 description 14
- 108010090849 Amyloid beta-Peptides Proteins 0.000 description 13
- 102000013455 Amyloid beta-Peptides Human genes 0.000 description 13
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 13
- 239000002953 phosphate buffered saline Substances 0.000 description 13
- 230000000770 proinflammatory effect Effects 0.000 description 13
- 230000004054 inflammatory process Effects 0.000 description 12
- 230000007170 pathology Effects 0.000 description 12
- 230000014509 gene expression Effects 0.000 description 11
- 210000001616 monocyte Anatomy 0.000 description 11
- 230000004044 response Effects 0.000 description 11
- 206010061218 Inflammation Diseases 0.000 description 10
- 102000003814 Interleukin-10 Human genes 0.000 description 10
- 108090000174 Interleukin-10 Proteins 0.000 description 10
- 230000005764 inhibitory process Effects 0.000 description 10
- 239000003981 vehicle Substances 0.000 description 10
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 9
- 108090000978 Interleukin-4 Proteins 0.000 description 9
- 238000003556 assay Methods 0.000 description 9
- 229940076144 interleukin-10 Drugs 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 239000002904 solvent Substances 0.000 description 9
- RVMGXWBCQGAWBR-UHFFFAOYSA-N 4-oxo-1-benzopyran-2-carboxylic acid Chemical compound C1=CC=C2OC(C(=O)O)=CC(=O)C2=C1 RVMGXWBCQGAWBR-UHFFFAOYSA-N 0.000 description 8
- 208000037259 Amyloid Plaque Diseases 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 8
- 102000004388 Interleukin-4 Human genes 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- 238000002965 ELISA Methods 0.000 description 7
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 7
- 108010064539 amyloid beta-protein (1-42) Proteins 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 230000008018 melting Effects 0.000 description 7
- 238000002844 melting Methods 0.000 description 7
- 230000000242 pagocytic effect Effects 0.000 description 7
- 229940124597 therapeutic agent Drugs 0.000 description 7
- 241000699660 Mus musculus Species 0.000 description 6
- 125000003118 aryl group Chemical group 0.000 description 6
- 230000001419 dependent effect Effects 0.000 description 6
- VLARUOGDXDTHEH-UHFFFAOYSA-L disodium cromoglycate Chemical compound [Na+].[Na+].O1C(C([O-])=O)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=CC=CC2=C1C(=O)C=C(C([O-])=O)O2 VLARUOGDXDTHEH-UHFFFAOYSA-L 0.000 description 6
- 239000002552 dosage form Substances 0.000 description 6
- 238000011534 incubation Methods 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- 230000010287 polarization Effects 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 239000000741 silica gel Substances 0.000 description 6
- 229910002027 silica gel Inorganic materials 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 231100000419 toxicity Toxicity 0.000 description 6
- 230000001988 toxicity Effects 0.000 description 6
- 238000011830 transgenic mouse model Methods 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- 102000003777 Interleukin-1 beta Human genes 0.000 description 5
- 108090000193 Interleukin-1 beta Proteins 0.000 description 5
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 5
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 5
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 5
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 5
- 230000013629 beta-amyloid clearance Effects 0.000 description 5
- 230000015556 catabolic process Effects 0.000 description 5
- 238000006731 degradation reaction Methods 0.000 description 5
- 231100000673 dose–response relationship Toxicity 0.000 description 5
- 239000002158 endotoxin Substances 0.000 description 5
- 210000001320 hippocampus Anatomy 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 229920006008 lipopolysaccharide Polymers 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 231100000331 toxic Toxicity 0.000 description 5
- 230000002588 toxic effect Effects 0.000 description 5
- 101150053137 AIF1 gene Proteins 0.000 description 4
- 102000019034 Chemokines Human genes 0.000 description 4
- 108010012236 Chemokines Proteins 0.000 description 4
- 206010061818 Disease progression Diseases 0.000 description 4
- 238000008157 ELISA kit Methods 0.000 description 4
- 101000934338 Homo sapiens Myeloid cell surface antigen CD33 Proteins 0.000 description 4
- 108091000054 Prion Proteins 0.000 description 4
- 230000006933 amyloid-beta aggregation Effects 0.000 description 4
- 239000013592 cell lysate Substances 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000008021 deposition Effects 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 230000005750 disease progression Effects 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 230000003492 excitotoxic effect Effects 0.000 description 4
- 230000000971 hippocampal effect Effects 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- IJBVWKAGYXOMFA-UHFFFAOYSA-N 2-(2-hydroxyethyl)chromen-4-one Chemical compound C1=CC=C2OC(CCO)=CC(=O)C2=C1 IJBVWKAGYXOMFA-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 238000012286 ELISA Assay Methods 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 3
- 108010074328 Interferon-gamma Proteins 0.000 description 3
- 102000008070 Interferon-gamma Human genes 0.000 description 3
- 206010057249 Phagocytosis Diseases 0.000 description 3
- 102000029797 Prion Human genes 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 102000002689 Toll-like receptor Human genes 0.000 description 3
- 108020000411 Toll-like receptor Proteins 0.000 description 3
- 230000002776 aggregation Effects 0.000 description 3
- 238000004220 aggregation Methods 0.000 description 3
- 230000032683 aging Effects 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 229940121363 anti-inflammatory agent Drugs 0.000 description 3
- 239000002260 anti-inflammatory agent Substances 0.000 description 3
- 239000012131 assay buffer Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000012876 carrier material Substances 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 230000028993 immune response Effects 0.000 description 3
- 230000004968 inflammatory condition Effects 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 229960003130 interferon gamma Drugs 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 230000000877 morphologic effect Effects 0.000 description 3
- 210000002161 motor neuron Anatomy 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- CAMWVBRDIKKGII-UHFFFAOYSA-M n,n-dimethyl-4-(1-methylpyridin-1-ium-4-yl)aniline;iodide Chemical compound [I-].C1=CC(N(C)C)=CC=C1C1=CC=[N+](C)C=C1 CAMWVBRDIKKGII-UHFFFAOYSA-M 0.000 description 3
- 210000002569 neuron Anatomy 0.000 description 3
- 230000004112 neuroprotection Effects 0.000 description 3
- 231100000189 neurotoxic Toxicity 0.000 description 3
- 230000002887 neurotoxic effect Effects 0.000 description 3
- 230000002018 overexpression Effects 0.000 description 3
- 230000037361 pathway Effects 0.000 description 3
- 230000008782 phagocytosis Effects 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 230000011664 signaling Effects 0.000 description 3
- 230000002459 sustained effect Effects 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- BLXLFBOGYMXMHO-UHFFFAOYSA-N 1-[2-[3-(2-acetyl-3-hydroxyphenoxy)-2-fluoropropoxy]-6-hydroxyphenyl]ethanone Chemical compound CC(=O)C1=C(O)C=CC=C1OCC(F)COC1=CC=CC(O)=C1C(C)=O BLXLFBOGYMXMHO-UHFFFAOYSA-N 0.000 description 2
- 238000010175 APPswe/PSEN1dE9 Methods 0.000 description 2
- 102100037839 Acidic mammalian chitinase Human genes 0.000 description 2
- 101710178876 Acidic mammalian chitinase Proteins 0.000 description 2
- 102000002659 Amyloid Precursor Protein Secretases Human genes 0.000 description 2
- 108010043324 Amyloid Precursor Protein Secretases Proteins 0.000 description 2
- 102000009091 Amyloidogenic Proteins Human genes 0.000 description 2
- 108010048112 Amyloidogenic Proteins Proteins 0.000 description 2
- 241000167854 Bourreria succulenta Species 0.000 description 2
- 102000009058 Death Domain Receptors Human genes 0.000 description 2
- 108010049207 Death Domain Receptors Proteins 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 2
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 2
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 2
- UUSYRFWMUZILHI-UHFFFAOYSA-N FC(C(O)O)C.CC1=CC=C(C=C1)S(=O)(=O)O Chemical compound FC(C(O)O)C.CC1=CC=C(C=C1)S(=O)(=O)O UUSYRFWMUZILHI-UHFFFAOYSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000950695 Homo sapiens Mitogen-activated protein kinase 8 Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 231100000416 LDH assay Toxicity 0.000 description 2
- 208000026139 Memory disease Diseases 0.000 description 2
- 102100037808 Mitogen-activated protein kinase 8 Human genes 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 102100025243 Myeloid cell surface antigen CD33 Human genes 0.000 description 2
- 206010029350 Neurotoxicity Diseases 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- FTALBRSUTCGOEG-UHFFFAOYSA-N Riluzole Chemical compound C1=C(OC(F)(F)F)C=C2SC(N)=NC2=C1 FTALBRSUTCGOEG-UHFFFAOYSA-N 0.000 description 2
- 108020004459 Small interfering RNA Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102000008221 Superoxide Dismutase-1 Human genes 0.000 description 2
- 108010021188 Superoxide Dismutase-1 Proteins 0.000 description 2
- 108010060818 Toll-Like Receptor 9 Proteins 0.000 description 2
- 102100033117 Toll-like receptor 9 Human genes 0.000 description 2
- 206010044221 Toxic encephalopathy Diseases 0.000 description 2
- 238000010162 Tukey test Methods 0.000 description 2
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 2
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 210000001642 activated microglia Anatomy 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 208000029560 autism spectrum disease Diseases 0.000 description 2
- 230000006399 behavior Effects 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 235000019693 cherries Nutrition 0.000 description 2
- GGRHYQCXXYLUTL-UHFFFAOYSA-N chloromethyl 2,2-dimethylpropanoate Chemical compound CC(C)(C)C(=O)OCCl GGRHYQCXXYLUTL-UHFFFAOYSA-N 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 230000006720 chronic neuroinflammation Effects 0.000 description 2
- 239000000084 colloidal system Substances 0.000 description 2
- 238000004624 confocal microscopy Methods 0.000 description 2
- 210000003618 cortical neuron Anatomy 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000000593 degrading effect Effects 0.000 description 2
- 230000003828 downregulation Effects 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 231100000318 excitotoxic Toxicity 0.000 description 2
- 231100000063 excitotoxicity Toxicity 0.000 description 2
- 210000002744 extracellular matrix Anatomy 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 230000037406 food intake Effects 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- 102000056982 human CD33 Human genes 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000037456 inflammatory mechanism Effects 0.000 description 2
- 230000028709 inflammatory response Effects 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 230000015788 innate immune response Effects 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 229940028885 interleukin-4 Drugs 0.000 description 2
- 238000007917 intracranial administration Methods 0.000 description 2
- 238000002843 lactate dehydrogenase assay Methods 0.000 description 2
- 230000013016 learning Effects 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 108091070501 miRNA Proteins 0.000 description 2
- 210000004980 monocyte derived macrophage Anatomy 0.000 description 2
- 210000002864 mononuclear phagocyte Anatomy 0.000 description 2
- 210000002682 neurofibrillary tangle Anatomy 0.000 description 2
- 230000004766 neurogenesis Effects 0.000 description 2
- 230000006762 neuroinflammatory activation Effects 0.000 description 2
- 230000002314 neuroinflammatory effect Effects 0.000 description 2
- 231100000228 neurotoxicity Toxicity 0.000 description 2
- 230000007135 neurotoxicity Effects 0.000 description 2
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 2
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 230000008506 pathogenesis Effects 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000026731 phosphorylation Effects 0.000 description 2
- 238000006366 phosphorylation reaction Methods 0.000 description 2
- 229950010765 pivalate Drugs 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- 229960004181 riluzole Drugs 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 208000020431 spinal cord injury Diseases 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 108010050014 systemin Proteins 0.000 description 2
- HOWHQWFXSLOJEF-MGZLOUMQSA-N systemin Chemical compound NCCCC[C@H](N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(=O)OC(=O)[C@@H]1CCCN1C(=O)[C@H]1N(C(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H]2N(CCC2)C(=O)[C@H]2N(CCC2)C(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)N)C(C)C)CCC1 HOWHQWFXSLOJEF-MGZLOUMQSA-N 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 230000036962 time dependent Effects 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- YPTJKHVBDCRKNF-UHFFFAOYSA-N 2',6'-Dihydroxyacetophenone Chemical compound CC(=O)C1=C(O)C=CC=C1O YPTJKHVBDCRKNF-UHFFFAOYSA-N 0.000 description 1
- YEROQAQOWDWNLZ-UHFFFAOYSA-N 2-(2-hydroxyethyl)-5-[2-hydroxy-3-[2-(2-hydroxyethyl)-4-oxochromen-5-yl]oxypropoxy]chromen-4-one Chemical compound OC(COC1=C2C(C=C(OC2=CC=C1)CCO)=O)COC1=C2C(C=C(OC2=CC=C1)CCO)=O YEROQAQOWDWNLZ-UHFFFAOYSA-N 0.000 description 1
- JRMAQQQTXDJDNC-UHFFFAOYSA-M 2-ethoxy-2-oxoacetate Chemical compound CCOC(=O)C([O-])=O JRMAQQQTXDJDNC-UHFFFAOYSA-M 0.000 description 1
- IFCFLQDKQCOSRY-UHFFFAOYSA-N 4-methylbenzenesulfonic acid;propane-1,2,3-triol Chemical compound OCC(O)CO.CC1=CC=C(S(O)(=O)=O)C=C1 IFCFLQDKQCOSRY-UHFFFAOYSA-N 0.000 description 1
- SNSKDOLKXIZLDY-UHFFFAOYSA-N 5-[3-(2-carboxy-4-oxochromen-5-yl)oxy-2-fluoropropoxy]-4-oxochromene-2-carboxylic acid Chemical compound O1C(C(O)=O)=CC(=O)C2=C1C=CC=C2OCC(F)COC1=C2C(=O)C=C(C(=O)O)OC2=CC=C1 SNSKDOLKXIZLDY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- WSVLPVUVIUVCRA-KPKNDVKVSA-N Alpha-lactose monohydrate Chemical compound O.O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O WSVLPVUVIUVCRA-KPKNDVKVSA-N 0.000 description 1
- 102100034452 Alternative prion protein Human genes 0.000 description 1
- 238000010173 Alzheimer-disease mouse model Methods 0.000 description 1
- 238000009020 BCA Protein Assay Kit Methods 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 206010057248 Cell death Diseases 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 102000013717 Cyclin-Dependent Kinase 5 Human genes 0.000 description 1
- 108010025454 Cyclin-Dependent Kinase 5 Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- QXNVGIXVLWOKEQ-UHFFFAOYSA-N Disodium Chemical compound [Na][Na] QXNVGIXVLWOKEQ-UHFFFAOYSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108060003393 Granulin Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 1
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 1
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 1
- 102000000589 Interleukin-1 Human genes 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 102000004889 Interleukin-6 Human genes 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 1
- 208000029578 Muscle disease Diseases 0.000 description 1
- 208000021642 Muscular disease Diseases 0.000 description 1
- NSGDYZCDUPSTQT-UHFFFAOYSA-N N-[5-bromo-1-[(4-fluorophenyl)methyl]-4-methyl-2-oxopyridin-3-yl]cycloheptanecarboxamide Chemical compound Cc1c(Br)cn(Cc2ccc(F)cc2)c(=O)c1NC(=O)C1CCCCCC1 NSGDYZCDUPSTQT-UHFFFAOYSA-N 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102000000874 Pyrin Domain-Containing 3 Protein NLR Family Human genes 0.000 description 1
- 108010001946 Pyrin Domain-Containing 3 Protein NLR Family Proteins 0.000 description 1
- 239000012083 RIPA buffer Substances 0.000 description 1
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 102000004874 Synaptophysin Human genes 0.000 description 1
- 108090001076 Synaptophysin Proteins 0.000 description 1
- 241001247203 Syngnathidae Species 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 208000034799 Tauopathies Diseases 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical compound ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 241000700647 Variola virus Species 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 230000007792 alzheimer disease pathology Effects 0.000 description 1
- 230000003941 amyloidogenesis Effects 0.000 description 1
- 230000003942 amyloidogenic effect Effects 0.000 description 1
- 206010002022 amyloidosis Diseases 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000002768 anti-recombination Effects 0.000 description 1
- 210000000612 antigen-presenting cell Anatomy 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 229940090047 auto-injector Drugs 0.000 description 1
- 230000000035 biogenic effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000000133 brain stem Anatomy 0.000 description 1
- 210000003008 brain-resident macrophage Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 206010061592 cardiac fibrillation Diseases 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000012292 cell migration Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 230000000739 chaotic effect Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 210000001520 comb Anatomy 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Substances CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 239000003596 drug target Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000008519 endogenous mechanism Effects 0.000 description 1
- KRBBSLDXYDBFEC-UHFFFAOYSA-N ethyl 5-[3-(2-ethoxycarbonyl-4-oxochromen-5-yl)oxy-2-hydroxypropoxy]-4-oxochromene-2-carboxylate Chemical compound O1C(C(=O)OCC)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=C2C(=O)C=C(C(=O)OCC)OC2=CC=C1 KRBBSLDXYDBFEC-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 230000002600 fibrillogenic effect Effects 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 230000004914 glial activation Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 231100000171 higher toxicity Toxicity 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000037041 intracellular level Effects 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 229960001021 lactose monohydrate Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 206010027175 memory impairment Diseases 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000031990 negative regulation of inflammatory response Effects 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 230000003962 neuroinflammatory response Effects 0.000 description 1
- 230000004007 neuromodulation Effects 0.000 description 1
- 230000003961 neuronal insult Effects 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 230000000508 neurotrophic effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 239000003182 parenteral nutrition solution Substances 0.000 description 1
- 230000008807 pathological lesion Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 230000007505 plaque formation Effects 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 230000007112 pro inflammatory response Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000004224 protection Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000001012 protector Effects 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000003642 reactive oxygen metabolite Substances 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 210000005250 spinal neuron Anatomy 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000000946 synaptic effect Effects 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 238000002626 targeted therapy Methods 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- JADVWWSKYZXRGX-UHFFFAOYSA-M thioflavine T Chemical compound [Cl-].C1=CC(N(C)C)=CC=C1C1=[N+](C)C2=CC=C(C)C=C2S1 JADVWWSKYZXRGX-UHFFFAOYSA-M 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000167 toxic agent Toxicity 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 238000012301 transgenic model Methods 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- 238000009827 uniform distribution Methods 0.000 description 1
- 230000031836 visual learning Effects 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/22—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/22—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 4
- C07D311/24—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 4 with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached in position 2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
Abstract
本文描述了治疗神经元炎症病症,例如阿尔茨海默病、帕金森氏病、亨廷顿病、缺血性中风和朊病毒病的方法,包括给予治疗有效量的色甘酸或色甘酸衍生化合物。
Description
相关申请
本申请要求2016年8月31日提交的美国临时专利申请序列号62/382,192的优先权,该临时专利申请通过引用整体并入本文。
技术领域
本发明涉及治疗神经元炎症病症的方法,包括给予需要的患者治疗有效量的至少一种具有下式的化合物:
背景
已经研究了调节单核细胞和小胶质细胞活性的策略,尤其是那些可以防止小胶质细胞介导的神经毒性的策略。(参见Zhao等人,“抗炎细胞因子,白细胞介素-4,对活化小胶质细胞诱导的运动神经元毒性的保护作用(Protective effects of an anti-inflammatory cytokine,interleukin-4,on motoneuron toxicity induced byactivated microglia)”,J.Neurochem.2006,99:1176–1187;Heneka等人,“在阿尔茨海默病中被激活并导致APP/PS1小鼠的病理学的NLRP3(NLRP3is activated in Alzheimer'sdisease and contributes to pathology in APP/PS1mice)”,Nature,2013,493(7434):674-8;Theeriault等人,“阿尔茨海默病中单核细胞和小胶质细胞的动力学(The dynamicsof monocytes and microglia in Alzheimer’s disease)”,Alzheimers Res Ther.,2015,7:41;Nau等人,“提高小胶质细胞活性作为大脑抵抗感染的有效保护剂的策略(Strategies to increase the activity of microglia as efficient protectors ofthe brain against infections)”,Front Cell Neurosci.,2014,8:138。)总体来说,很明显需要更多的重点研究以更好地确定每种炎症状态如何调节神经退行性疾病如阿尔茨海默病(AD)和肌萎缩侧索硬化症(ALS)的病理学。单核细胞和小胶质细胞的早期活化有可能通过调节免疫应答从而增加单核细胞和小胶质细胞的内在吞噬能力来减缓神经变性进展,而不会引起可能恶化神经变性的促炎细胞因子的分泌。
大脑中淀粉样蛋白斑块和神经原纤维缠结的存在下神经炎症反应的作用及其在AD病理学中的相关神经元损失已经很好地建立并且被广泛研究。参见Walker等人,“人神经退行性疾病中小胶质细胞的免疫表型:检测人脑中小胶质细胞极化的挑战(Immunephenotypes of microglia in human neurodegenerative disease:challenges todetecting microglial polarization in human brains)”,Alzheimers Res Ther.,2015,7:56;Theerialut等人,2015;Wilcock,DM,“阿尔茨海默病中神经炎症的作用的变化观点(A Changing Perspective on the Role of Neuroinflammation in Alzheimer’sDisease)”,International Journal of Alzheimer’s Disease,2012,文章编号495243;McGeer等人,“针对小胶质细胞治疗阿尔茨海默病(Targeting microglia for thetreatment of Alzheimer's disease)”,Expert Opin Ther Targets,2015,19(4):497-506)。大量研究表明,小胶质细胞介导的炎症有助于AD的进展,并且发现小胶质细胞与淀粉样蛋白β(Aβ)沉积物密切相关。(参见Mandrekar等人,“阿尔茨海默病的小胶质细胞和炎症(Microglia and Inflammation in Alzheimer’s Disease)”,CNS Neurol Disord DrugTargets,2010,9(2):156–167)。
众所周知,小胶质细胞(脑驻留巨噬细胞)的性质变化取决于它们对其微环境中不同刺激物(例如细胞因子)的响应,导致一系列表型。基于细胞因子、受体和其他标志物表达的变化,单核细胞和巨噬细胞状态被定义为:经典激活(M1),替代激活(M2a),II型替代激活(M2b)和获得性失活(M2c)。(参见Walker等人,2015;Martinez等人,“巨噬细胞的替代激活:免疫功能观点(Alternative activation of macrophages:an immunologic functionalperspective)”,Annu Rev Immunol.2009,27:451-83;Mantovani等人,“趋化因子系统以多种形式的巨噬细胞激活和极化(The chemokine systemin diverse forms of macrophageactivation and polarization)”,Trends Immunol.,2004,25:677–686;Sternberg,EM.,“先天免疫的神经调节:对病原体的协调的非特异性宿主响应(Neural regulation ofinnate immunity:a coordinated nonspecific host response to pathogens)”,NatRev Immunol.,2006,6(4):318-28)。最近,许多研究试图阐明这些表型在AD脑中的作用,并确定这些细胞促成AD相关神经炎症的机制。(参见Mandrekar等人,2012;McGeer等人,2015;和Wilcock,2012)。
小胶质细胞与纤维状Aβ的相互作用导致其表型活化,并且最近已被认为在神经保护中起作用。(参见Zhao等人,2006;Figueiredo等人,“神经元-小胶质细胞串扰上调神经元FGF-2表达,通过JNK1/2介导对兴奋性毒性的神经保护作用(Neuron-microglia crosstalkup-regulates neuronal FGF-2expression which mediates neuroprotection againstexcitotoxicity via JNK1/2)”,J.Neurochem.,2008Oct.,107(1):73-85)。许多研究表明,在小鼠和人类中,神经胶质细胞通过改变其形态特征,表达大量细胞表面受体和周围病变来应对AD病理损伤(斑块和缠结)的存在。(参见Perlmutter等人,“小胶质细胞与阿兹海默病老年斑淀粉样蛋白的形态学关联(Morphologic association between microglia andsenile plaque amyloid in Alzheimer’s disease)”,Neurosci Lett.,1990,119:1,32–36;Combs等人,“鉴定小胶质细胞信号转导途径介导对β-淀粉样蛋白和朊蛋白的淀粉样蛋白形成片段的神经毒性反应(Identification of microglial signal transductionpathways mediating a neurotoxic response to amyloidogenic fragments ofβ-amyloid and prion proteins)”,J.Neurosci.,1999,19:3,928–939)。另一方面,响应于AD脑中的细胞碎片的巨噬细胞和小胶质细胞激活以及随后的促炎细胞因子的释放导致加速的神经变性。反过来,这会产生更多细胞碎片并加速疾病进展。(参见Rubio-Perez等人,“综述:阿尔茨海默病的炎症过程,细胞因子的作用(A Review:Inflammatory Process inAlzheimer's Disease,Role of Cytokines)”,Scientific World Journal,2012,756357;McGeer等人,“炎症机制在阿尔茨海默病中的重要性(The importance of inflammatorymechanisms inAlzheimer disease)”,Exp.Gerontol.1998,33:5,371–378;Akiyama等人,“炎症和阿尔茨海默病(Inflammation and Alzheimer's disease)”,Neurobiol Aging,2000,21(3),383-421;Liu等人,“TLR2是阿尔茨海默氏病淀粉样蛋白β肽的主要受体,可引发神经炎症激活(TLR2is a primary receptor for Alzheimer's amyloidβpeptide totrigger neuroinflammatory activation)”,J.Immunol.2012,188(3):1098-107)。
一些研究集中于小胶质细胞激活及其在AD病变清除中的作用,导致脑中淀粉样蛋白沉积物的减少。(参见DiCarlo等人,“海马内LPS注射减少APP+PS1转基因小鼠中的Aβ负荷(Intrahippocampal LPS injections reduce Aβload in APP+PS1transgenic mice)”,Neurobiol of Aging,2001,22:6,1007–1012;Herber等人,“在APP转基因小鼠中施用颅内LPS后Aβ水平的时间依赖性降低(Time-dependent reduction in Aβlevels afterintracranial LPS administration in APP transgenic mice)”,Exp.Neurol.,2004,190(1):245-53;Liu等人,2012)。虽然围绕Aβ斑块的常驻小胶质细胞在降解Aβ方面不如新渗入的巨噬细胞或单核细胞有效,(参见Thériault等人,2015;Varnum等人,“小胶质细胞激活表型分类对阿尔茨海默氏症中神经退行性变和再生的影响(The classification ofmicroglial activation phenotypes on neurodegeneration and regeneration inAlzheimer's disease brain)”,Arch.Immunol.Ther.Exp.(Warsz),2012,60(4):251-66),已经表明小胶质细胞确实能够内化纤维状和可溶性Aβ,但是无法处理这些肽。(参见Chung等人,“通过小胶质细胞摄取,降解和释放纤维状和可溶形式的阿尔茨海默氏淀粉样蛋白β-肽(Uptake,degradation,and release of fibrillar and soluble forms ofAlzheimer's amyloid beta-peptide by microglial cells)”,J.Biol.Chem.,1999,274:32301–8)。
此外,已经假定小胶质细胞在衰老期间经历从M2-转变为M1-倾斜激活表型。(参见Heneka等人,2013;Varnum等人,2012;Gratchev等人,“Mphi1和Mphi2可分别被Th2或Th1细胞因子重新极化,并对外源性危险信号做出响应(Mphi1and Mphi2can be re-polarizedby Th2or Th1cytokines,respectively,and respond to exogenous danger signals)”,Immunobiology,2006,211(6–8):473–486;Colton等人,“AD中和AD小鼠模型中巨噬细胞替代激活基因的表达谱(Expression profiles for macrophage alternative activationgenes in AD and in mouse models of AD)”,J.Neuroinflammation,2006,3:27)。然而,大脑中的免疫应答如何在AD中被驱动仍然是一个争论的问题,特别是神经炎症是否可以由年龄相关的全身性炎症引发。(参见Thériault等人,2015)。已经表明小胶质细胞的刺激可以增强其内在的吞噬能力,更有效地降解Aβ;已经提出了许多调节小胶质细胞响应的策略。(参见Mandrekar,2010;Kiyota等人,“CNS表达抗炎细胞因子白细胞介素-4减弱APP+PS1生物小鼠的阿尔茨海默病样发病机制(CNS expression of anti-inflammatory cytokineinterleukin-4attenuates Alzheimer’s disease-like pathogenesis in APP+PS1bigenic mice)”,FASEB J.2010,24:3093–3102;He等人,“肿瘤坏死因子死亡受体的缺失抑制淀粉样蛋白β的产生,并预防阿尔茨海默氏症小鼠的学习和记忆缺陷(Deletion oftumor necrosis factor death receptor inhibits amyloid beta generation andprevents learning and memory deficits in Alzheimer’s mice)”,J.Cell Biol.,2007,178:829–841;Varnum等人,2012)。
已经显示小胶质细胞被细胞外沉积的Aβ肽激活(Lotz等人,“在原代小鼠小胶质细胞培养物中淀粉样蛋白β肽1-40增强Toll样受体-2和-4激动剂的作用但拮抗Toll样受体-9-诱导的炎症(Amyloid beta peptide 1-40enhances the action of Toll-likereceptor-2and-4agonists but antagonizes Toll-like receptor-9-inducedinflammation in primary mouse microglial cell cultures)”,J.Neurochem.,2005,94:289–298;Reed-Geaghan等人,“CD14和toll样受体2和4是纤维状Aβ刺激的小胶质细胞激活所必需的(CD14and toll-like receptors 2and 4are required for fibrillar Aβ-stimulated microglial activation)”,J.Neurosci.,2009,29:11982–11992)。这类似于响应干扰素-γ(IFNγ),来自T细胞的肿瘤坏死因子α(TNFα)或抗原呈递细胞的存在的小胶质细胞活化。M1激活的小胶质细胞可以产生活性氧物质并导致促炎细胞因子如TNFα和白细胞介素(IL)-1β的产生增加。
小胶质细胞的M1型响应已被证明可降低淀粉样蛋白负荷,但会加剧神经原纤维缠结病理。Shaftel等人(Shaftel等人,“持续海马IL-1β过度表达介导慢性神经炎症和改善阿尔茨海默病斑块病理学(Sustained hippocampal IL-1βoverexpression mediateschronic neuroinflammation and ameliorates Alzheimer plaque pathology)”,J.Clin.Invest.,2007,117(6):1595-604)已显示IL-1β表达可能是在AD中有益的神经炎症反应的基础,并且APP/PS1转基因小鼠的海马中IL-1β过表达导致淀粉样蛋白负荷减少。作者提出,IL-1β介导的小胶质细胞活化是减少淀粉样蛋白沉积的机制。此外,Montgomery等人(Montgomery等人,“阿尔茨海默病小鼠中TNF-RI/RII表达的消除导致病理学的意外增强:对脑中慢性泛TNF-α抑制治疗策略的影响(Ablation of TNF-RI/RII expression inAlzheimer’s disease mice leads to an unexpected enhancement of pathology:implications for chronic pan-TNF-αsuppressive therapeutic strategies in thebrain)”,Am.J.Pathol.,2011,179(4):2053-70)已经表明,完整的TNF-受体信号传导对于小胶质细胞介导的细胞外淀粉样蛋白肽的摄取是至关重要的。虽然M1炎症表型似乎在许多研究中改善淀粉样蛋白病理学,但是在tau转基因小鼠或细胞培养物中诱导M1表型导致tau病理学的恶化。(参见Kitazawa等人,“脂多糖诱导的炎症通过阿尔茨海默氏病的转基因模型中的细胞周期蛋白依赖性激酶5-介导的途径加剧了tau病理学(Lipopolysaccharide-induced inflammation exacerbates tau pathology by a cyclin-dependent kinase5-mediated pathway in a transgenic model of Alzheimer’s disease”),J.Neurosci.,2005,28;25(39):8843-53.;Li等人,“Interleukin-1通过p38-MAPK途径介导小胶质细胞对皮质神经元中tau磷酸化和突触素合成的病理学影响(Interleukin-1mediates pathological effects of microglia on tau phosphorylation and onsynaptophysin synthesis in cortical neurons through a p38-MAPK pathway)”,J.Neurosci.,2003,1;23(5):1605-11)。
巨噬细胞M2激活与已知有助于抗炎作用和细胞外基质的重组的介导物相关(Zhu等人,“哮喘Th2炎症和IL-13途径激活中的酸性哺乳动物几丁质酶(Acidic mammalianchitinase in asthmatic Th2inflammation and IL-13pathway activation)”,Science,2004,304(5677):1678-82;Walker等人,2015;Wilcock等人,2012)。具有M2a表型的小胶质细胞具有增加的吞噬作用并产生生长因子,例如胰岛素样生长因子-1和抗炎细胞因子例如IL-10。IL-4和/或IL-13对巨噬细胞的刺激导致M2a状态,有时称为伤口愈合巨噬细胞(Edwards等人,“三种活化的巨噬细胞群的生物化学和功能表征(Biochemical andfunctional characterization of three activated macrophage populations)”,J.Leukoc Biol.,2006,80(6):1298-307),其通常表征为促炎细胞因子(IL-1,TNF和IL-6)的低产量。M2a响应主要在过敏反应、细胞外基质沉积和重塑中观察到。
M2b巨噬细胞的独特之处在于它们表达高水平的促炎细胞因子,这是M1活化的特征,但也表达高水平的抗炎细胞因子IL-10。(参见Moser DM.,“巨噬细胞活化的许多方面(The many faces of macrophage activation)”,J.Leukoc Biol.,2003,73(2):209-12)。
最后,M2c巨噬细胞状态被IL-10刺激,有时被称为调节性巨噬细胞。M2c巨噬细胞具有抗炎活性,其在细胞碎片的吞噬作用中起作用而没有经典的促炎反应(参见,MoserDM.,2003)。这些细胞表达TGFβ和高IL-10以及基质蛋白。(参见Mantovani等人,“多种形式的巨噬细胞活化和极化中的趋化因子系统(The chemokine systemin diverse forms ofmacrophage activation and polarization)”,Trends Immunol.,2004,25:677–686;Wilcock等人,2012)。Plunkett等人(Plunkett等人,“白细胞介素-10(IL-10)对大鼠兴奋毒性脊髓损伤后疼痛行为和基因表达的影响(Effects of interleukin-10(IL-10)on painbehavior and gene expression following excitotoxic spinal cord injury in therat)”,Exp.Neurol.,2001;168:144–154)报道IL-10介导的抗炎反应包括减少胶质细胞活化和促炎细胞因子的产生。
然而,M2小胶质细胞激活的机制及其在AD和斑块病理学中的作用尚不清楚。(参见Mandrekar等人,2010)。此外,许多研究表明,响应疾病进展小胶质细胞激活状态发生转变(Colton等人,2006;Jimenez等人,“PS1M146L/APP751SL小鼠模型阿尔茨海默氏症的海马炎症反应:年龄依赖性小胶质细胞表型转换为经典(Inflammatory response in thehippocampus of PS1M146L/APP751SL mouse model of Alzheimer’s disease:age-dependent switch in the microglial phenotype from alternative to classic)”,J.Neurosci.,2008,28:11650–11661)。在动物研究中已经报道,在疾病进展期间小胶质细胞活化表型从M2转变为M1(Jimenez等人,2008;Nolan等人,“白介素-4在调节年龄相关炎症变化中的作用(Role of interleukin-4in regulation of age-relatedinflammatorychanges in the hippocampus)”,J.Biol.Chem.,2005;280:9354–9362;Maher等人,“海马中IL-4诱导的信号传导的下调导致老年大鼠中LTP的缺陷(Downregulation of IL-4-induced signalling in hippocampus contributes to deficits in LTPin the agedrat)”,Neurobiol.Aging,2005,26:717–728),表明随着年龄的增加,替代表型的经典激活表型增加。一般认为,由细胞外沉积的Aβ激活的小胶质细胞通过触发抗炎/神经营养性M2激活和通过吞噬作用清除Aβ来保护神经元。这是新治疗目标的潜在途径。(参见He等人,2007;Yamamoto等人,“瑞典突变APP转基因小鼠中的干扰素-γ和肿瘤坏死因子-α调节淀粉样蛋白β斑块沉积和β-分泌酶表达(Interferon-gamma and tumor necrosis factor-alpharegulate amyloid-beta plaque deposition and beta-secretase expression inSwedish mutant APP transgenic mice)”,Am.J.Pathol.,2007,170:680–692;Yamamoto等人,“细胞因子介导的人单核吞噬细胞对纤维状淀粉样β肽降解的抑制(Cytokine-mediatedinhibition of fibrillar amyloid-beta peptide degradation by human mononuclearphagocytes)”,J.Immunol.,2008,181:3877–3886)。
Mantovani等人(Mantovani等人,2004)研究了IL-4作为M2a小胶质细胞激活的重要调节剂的作用。已经显示IL-4基因递送到APP+PS1小鼠中部分地抑制了海马中的胶质积聚,直接增强了神经发生,恢复了受损的空间学习,并且还减少了Aβ沉积(Kiyota等人,2010)。
Yamamoto等人(Yamamoto等人,2007,2008)在原代培养的人单核细胞衍生的巨噬细胞(MDM)和小胶质细胞中使用促炎细胞因子和抗炎细胞因子检测了巨噬细胞介导的Aβ降解。这些研究表明,抗炎和调节细胞因子导致M2a或M2c活化增加和Aβ清除增强。Kiyota等人(Kiyota等人,2011)已显示IL-4的持续表达减少了天花/小胶质细胞增生,淀粉样蛋白-β肽(Aβ)寡聚化和沉积,以及增强了神经发生。
已经提出了几种方法来调节小胶质细胞激活作为AD治疗的潜在靶标。(参见Thériault等人,2015;Cherry等人,“神经炎症和M2小胶质细胞:好的,坏的和发炎的(Neuroinflammation and M2microglia:the good,the bad,and the inflamed)”,J.Neuroinflammation,2014,11:98;Mandrekar等人,2010;Vernum等人,2012)。已提出使用抗炎药物,如非甾体抗炎药(NSAID)来阻止AD的进展,可以抑制内源性分子的促炎和抗炎活化,从而消除M2小胶质细胞功能的有益作用和斑块清除的内源性机制。(参见Wilcock等人,2012,Cherry等人,2014;Theeriault等人,2015)。
研究主要集中在两个方面:抗炎剂,以缓和促炎细胞因子的毒性作用;以及将小胶质细胞从M1状态转变为M2状态,其中毒性作用降低并且其对Aβ的吞噬活性增强。已提出(McGreer等人,2012)应在疾病进展的早期进行潜在的治疗。
已经研究了调节单核细胞和小胶质细胞活性的策略,尤其是那些可以防止小胶质细胞介导的神经毒性的策略(Zhao等人,2006;Heneka等人,2013;Therlaut等人,2015;Nau等人,2014)。总体而言,显然需要进行更集中的研究以更好地确定每种炎症状态如何调节AD的病理。通常认为单核细胞和小胶质细胞的早期活化有可能通过调节免疫应答从而增加单核细胞和小胶质细胞的内在吞噬能力来减缓AD进展,而不会引起可能使AD恶化的促炎细胞因子的分泌。
发明内容
在一些实施方式中,本发明涉及治疗神经元炎症病症的方法,包括给予需要的患者治疗有效量的至少一种具有下式的化合物:
在其他实施方案中,该方法使用以下化合物:
色甘酸二钠;
F-色甘酸二酸;
ET-色甘酸;
F-ET-色甘酸;
三醇-色甘酸;
F-三醇-色甘酸;
Ac-三醇-色甘酸;
POM-色甘酸;或
在其他实施方案中,神经元炎症病症是ALS、AD、缺血性中风或朊病毒病中的至少一种。在一个实施方案中,化合物可以腹膜内(IP)和/或静脉内(IV)给药。化合物可以每天约1mg至约1000mg的剂量给药。给药方法可以是透皮给药或通过吸入给药。
在另一个实施方案中,该方法是治疗ALS的方法,其进一步包括共同给予CD4+;siRNA;改善ALS的miRNA;胶质形态调节剂;SOD1控制物;利鲁唑;或另一种控制神经炎症的M1;M2转化活性药物。
在某些实施方案中,本发明涉及本文所述的任何方法,条件是该化合物不是色甘酸二钠。在某些实施方案中,本发明涉及本文所述的任何方法,条件是当神经元炎症病症是AD时,该化合物不是色甘酸二钠,F-色甘酸二钠,ET-色甘酸或F-ET-色甘酸。
在某些实施方案中,本发明涉及以下化合物中的任何一种:
三醇-色甘酸;
F-三醇-色甘酸;
Ac-三醇-色甘酸;
POM-色甘酸;或
附图说明
图1A说明用PBS(磷酸缓冲盐溶液)或递增剂量的色甘酸钠处理一周后Aβx-40和Aβx-42的血浆水平的定量(n=3-5只小鼠/组)。
图1B示出了在用色甘酸钠(3.15mg/kg)或PBS每天处理持续7天的小鼠中淀粉样蛋白沉积物(6E10)和小胶质细胞(Iba1)的定位的代表性图像。条形图说明了分析每只动物斑块的结果。比例尺=10μm。
图1C说明了色甘酸钠对小胶质细胞体外Aβ摄取的影响,其中在孵育后,使用AβELISA测量培养基中Aβx-40(图1C左)Aβx-42(图1C,右)的浓度。
图2显示了实施例2研究的Tg-2576小鼠中围绕这些沉积物的斑块和小胶质细胞。该图显示了淀粉样蛋白沉积物和Iba-1阳性小胶质细胞的代表性图片。
图3显示用色甘酸处理的BV2小胶质细胞的结果,并且相对于用运载体处理的BV2小胶质细胞,色甘酸和布洛芬表现出增加的Aβ42摄取水平。
图4显示了使用本文所述的各种化合物的Aβ聚集抑制测定的结果。
图5图示说明色甘酸显著影响脑TBS可溶性Aβ的水平和Aβ(42:40)的比率。
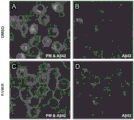
图6A显示用DMSO(对照)处理16小时的幼稚BV2小胶质细胞。然后,将细胞与荧光标记的Aβ42和DMSO或色甘酸钠一起孵育2小时。孵育后,用质膜染料(PM)标记细胞并成像。
图6B显示用DMSO(对照)处理16小时的幼稚BV2小胶质细胞。然后,将细胞与荧光标记的Aβ42和DMSO或色甘酸钠一起孵育2小时。
图6C显示用色甘酸钠(500μM)处理16小时的幼稚BV2小胶质细胞。然后,将细胞与荧光标记的Aβ42和DMSO或色甘酸钠一起孵育2小时。孵育后,用质膜染料(PM)标记细胞并成像。
图6D显示用色甘酸钠(500μM)处理16小时的幼稚BV2小胶质细胞。然后,将细胞与荧光标记的Aβ42和DMSO或色甘酸钠一起孵育2小时。
图7A图示说明色甘酸钠促进小胶质细胞Aβ42摄取。用DMSO或不同浓度的色甘酸钠处理BV2小胶质细胞16小时。然后,将细胞与可溶性未标记的Aβ42和DMSO或色甘酸钠一起孵育2小时,并收集用于ELISA分析。与用运载体(DMSO)处理的细胞相比,用色甘酸钠处理的幼稚BV2和BV2-CD33WT小胶质细胞表现出增加的Aβ42摄取水平。
图7B图示说明色甘酸钠促进小胶质细胞Aβ42摄取。将稳定表达CD33(BV2-CD33WT)的BV2细胞用DMSO或不同浓度的色甘酸钠处理16小时。然后,将细胞与可溶性未标记的Aβ42和DMSO或色甘酸钠一起孵育2小时,并收集用于ELISA分析。与用运载体(DMSO)处理的细胞相比,用色甘酸钠处理的幼稚BV2和BV2-CD33WT小胶质细胞表现出增加的Aβ42摄取水平。
图8图示说明在LDH测定中以100μM或更高浓度测试时,化合物C8显示出毒性。将幼稚BV2小胶质细胞用DMSO或色甘酸衍生物以不同浓度处理3小时。在10,50,100和150μM下测试C1,C2,C5,C6,C7和C8,而由于DMSO中的溶解度限制,在5,25,50和75μM下评估C3和C4。然后,将细胞与可溶性未标记的Aβ42肽和DMSO或色甘酸衍生物一起f孵育2小时。在处理结束时,收集细胞培养基并用乳酸脱氢酶(LDH)测定评估化合物毒性。与用运载体(DMSO)处理的细胞相比,用色甘酸衍生物C8处理的BV2小胶质细胞在100和150μM时表现出增加的毒性。
图9图示说明化合物C4促进幼稚BV2小胶质细胞中Aβ42的摄取。将BV2细胞用DMSO(运载体)或色甘酸衍生物以5至150μM的不同浓度处理3小时。然后,将细胞与可溶性未标记的Aβ42和DMSO或色甘酸衍生物一起孵育额外的2小时并收集用于ELISA分析。与用运载体处理的细胞相比,用75μM的色甘酸衍生物C4处理的BV2小胶质细胞表现出显著增加的Aβ42摄取水平。
图10图示说明化合物C4促进小胶质细胞BV2-CD33WT中Aβ42的摄取。将稳定表达CD33WT的小胶质细胞用作为对照的DMSO或不同浓度的色甘酸衍生物(C1,C3-8)处理3小时。然后,在Aβ42肽存在下将细胞与DMSO或色甘酸衍生物一起孵育额外的2小时。使用Aβ42特异性ELISA试剂盒分析细胞裂解物的细胞内Aβ42水平。与DMSO处理相比,用75μM的色甘酸衍生物C4处理导致BV2-CD33WT细胞中Aβ42的摄取增加,并且在50μM时显示出剂量依赖性效应。
图11图示说明化合物C4促进BV2-CD33WT细胞中Aβ42的摄取。用不同浓度的DMSO(运载体)或色甘酸衍生物(C1,C2和C4-7)处理BV2-CD33WT细胞3小时。然后,用DMSO或色甘酸衍生物和可溶性Aβ42肽处理细胞2小时。使用Aβ42特异性ELISA试剂盒分析细胞裂解物,并定量细胞内Aβ42水平。与用DMSO处理的细胞相比,50和75μM的色甘酸衍生物C4在BV2-CD33WT细胞中有效诱导Aβ42摄取。
具体实施方式
缺血性中风、阿尔茨海默病(AD)、肌萎缩性脊髓侧索硬化症(ALS或葛雷克氏病)、朊病毒和其他神经退行性疾病与小胶质细胞激活和肥大细胞迁移有关,也与单核细胞和产生一连串增加炎症的毒性细胞因子和碎片的其他细胞类型有关。在某些实施方案中,本发明包括抗炎化合物,通过将小胶质细胞从促炎M1状态转变为M2状态来降低促炎细胞因子的毒性作用,所述M2状态时毒性作用降低并且其对淀粉样变性、tau蛋白病和其他细胞毒性事件的吞噬活性增强。在某些实施方案中,本发明还包括化合物在影响疾病过程中的早期治疗的用途。
许多用作抗炎剂的药物在将小胶质细胞从M1转化为M2方面没有显示出效力,它们也没有增强小胶质细胞从M1到M2的调节。就本申请人所知,本文所述的化合物是具有M1至M2活性的唯一有效的、非细胞因子(例如IL-10)化合物。因此,在某些实施方案中,本发明包括化合物以及通过给予治疗有效量的至少一种所述化合物治疗神经元炎症病症的方法。
在某些实施方案中,本发明的化合物包括具有下式的那些化合物及其类似物和异构体:
此外,X可包括但不限于卤素和OCO(C1-C8烷基)。烷基包括但不限于甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基和戊基。卤素包括氟、氯、溴和碘。Y可包括但不限于-CH2OH、-CH2OAc或-CH2OMe。优选地,本发明的化合物包括在5位连接的那些化合物。
在本发明范围内的具体化合物包括:
色甘酸二钠;
F-色甘酸二酸;
ET-色甘酸;
F-ET-色甘酸;
三醇-色甘酸;
F-三醇-色甘酸;
Ac-三醇-色甘酸;或
POM-色甘酸;或
在某些实施方案中,化合物还包括5-[3-(2-羧基-4-氧代色烯-5-基)氧基-2-羟基丙氧基]-4-氧代色烯-2-羧酸衍生物和异构形式。
在某些实施方案中,本发明包括治疗多种神经元炎症病症的方法。神经元炎症病症包括但不限于诸如ALS、自闭症谱系障碍(ASD)、缺血性中风和朊病毒病的疾病。在某些实施方案中,所述化合物可用于治疗ALS,包括但不限于减缓或停止疾病的进展。在某些实施方案中,化合物可以与其他抗炎剂组合给予,以控制ALS的进行性和致命性作用的扩散。
在某些实施方案中,本发明包括针对ALS用于控制神经炎症的M1,M2转化活性药物与其他免疫靶向疗法的组合治疗,所述用于控制神经炎症的M1,M2转化活性药物例如上式中的药物,所述其他免疫靶向疗法例如CD4+,siRNA,改善ALS的miRNA,胶质形态调节剂,SOD1控制物或利鲁唑(唯一批准用于ALS的药物)。
在其他实施方案中,化合物针对位于脑干和/或脊髓、神经元或影响自发性身体肌肉的运动神经元中的神经元将减缓或停止神经元损伤。
在某些实施方案中,化合物可以使用已知的药物给药方法给药,例如IP,IV,透皮,吸入。在某些实施方案中,本发明涉及治疗或减缓神经疾病(例如AD,缺血性中风,ALS或朊病毒)的侵袭性进展的方法,并且该化合物通过输注或腹膜内给予来施用。
在某些实施方案中,本发明还提供药物组合物,其包含一种或多种本文所述的化合物以及药学上可接受的载体。优选这些组合物可以是单位剂型,例如片剂、丸剂、胶囊、粉末剂、颗粒剂、无菌胃肠外溶液剂或混悬剂、计量气溶胶或液体喷雾剂、滴剂、安瓿、自动注射器装置或栓剂,用于口服、胃肠外、鼻内、舌下或直肠给药、或者用于通过吸入或吹入给药。还设想可将化合物掺入透皮贴剂中,所述透皮贴剂设计成以连续方式递送适量的药物。
为了制备固体组合物如粉末和片剂,将主要活性成分与药学上可接受的载体如常规的压片成分如玉米淀粉、乳糖、蔗糖、山梨糖醇、滑石粉、硬脂酸、硬脂酸镁、磷酸二钙或树胶,以及其他药物稀释剂如水进行混合,以形成含有均质混合物的固体预配制组合物。这些预配制组合物是均质的描述是指活性成分均匀分散在整个组合物中,使组合物可容易地再细分成同等有效的单位剂型。
在一些实施方式中,将干粉组合物微粉化以吸入肺部。参见例如美国专利申请公开2016/0263257,其全部内容通过引用明确并入本文,特别是关于其中所述的干粉色甘酸制剂。在其他实施方案中,干粉组合物还包含至少一种赋形剂。在某些实施方案中,所述至少一种赋形剂包括乳糖一水合物和/或硬脂酸镁。
在某些实施方案中,化合物可以以治疗具体适应症的剂量给予。具体说,剂量经特别定制以使血液、脑和CSF浓度能够让药物充当M1至M2调节物的作用。这样的剂量可以包括每天约1mg至约1000mg。
活性剂的剂量通常取决于许多因素,包括化合物的药效学特征,化合物的给药方式和途径,所治疗患者的健康状况,所需治疗的程度,(如果有的话)并行治疗的性质和种类,治疗的频率和所需效果的性质。通常,化合物的剂量范围通常为每天约0.001至约250mg/kg体重。对于体重约70kg的正常成人,剂量可以为约0.1至约25mg/kg体重。然而,根据所治疗的对象的年龄和体重,预期的给药途径,所施用的特定药剂等,可能需要该常规剂量范围的一些变化。重要的是,本领域普通技术人员阅读本文后完全能够确定特定哺乳动物的剂量范围和最优剂量。
化合物的剂量可低至5ng/天。在某些实施方案中,给予约10ng/天、约15ng/天、约20ng/天、约25ng/天、约30ng/天、约35ng/天、约40ng/天、约45ng/天、约50ng/天、约60ng/天、约70ng/天、约80ng/天、约90ng/天、约100ng/天、约200ng/天、约300ng/天、约400ng/天、约500ng/天、约600ng/天、约700ng/天、约800ng/天、约900ng/天、约1μg/天、约2μg/天、约3μg/天、约4μg/天、约5μg/天、约10μg/天、约15μg/天、约20μg/天、约30μg/天、约40μg/天、约50μg/天、约60μg/天、约70μg/天、约80μg/天、约90μg/天、约100μg/天、约200μg/天、约300μg/天、约400μg/天约500μg/天、约600μg/天、约700μg/天、约800μg/天、约900μg/天、约1mg/天、约2mg/天、约3mg/天、约4mg/天、约5mg/天、约10mg/天、约15mg/天、约20mg/天、约30mg/天、约40mg/天或约50mg/天的化合物。
活性剂的剂量范围可以是5ng/天至100mg/天。在某些实施方式中,活性剂的剂量范围可以是约5ng/天至约10ng/天、约15ng/天、约20ng/天、约25ng/天、约30ng/天、约35ng/天、约40ng/天、约45ng/天、约50ng/天、约60ng/天、约70ng/天、约80ng/天、约90ng/天、约100ng/天、约200ng/天、约300ng/天、约400ng/天、约500ng/天、约600ng/天、约700ng/天、约800ng/天或约900ng/天。在某些实施方式中,化合物的剂量范围可以是约1μg/天至约2μg/天、约3μg/天、约4μg/天、约5μg/天、约10μg/天、约15μg/天、约20μg/天、约30μg/天、约40μg/天、约50μg/天、约60μg/天、约70μg/天、约80μg/天、约90μg/天、约100μg/天、约200μg/天、约300μg/天、约400μg/天、约500μg/天、约600μg/天、约700μg/天、约800μg/天或约900μg/天。在某些实施方式中,活性剂的剂量范围可以是约1mg/天至约2mg/天、约3mg/天、约4mg/天、约5mg/天、约10mg/天、约15mg/天、约20mg/天、约30mg/天、约40mg/天、约50mg/天、约60mg/天、约70mg/天、约80mg/天、约90mg/天、约100mg/天、约200mg/天、约300mg/天、约400mg/天、约500mg/天、约600mg/天、约700mg/天、约800mg/天或约900mg/天。
在某些实施方式中,以pM或nM的浓度给予化合物。在某些实施方式中,以约1pM、约2pM、约3pM、约4pM、约5pM、约6pM、约7pM、约8pM、约9pM、约10pM、约20pM、约30pM、约40pM、约50pM、约60pM、约70pM、约80pM、约90pM、约100pM、约200pM、约300pM、约400pM、约500pM、约600pM、约700pM、约800pM、约900pM、约1nM、约2nM、约3nM、约4nM、约5nM、约6nM、约7nM、约8nM、约9nM、约10nM、约20nM、约30nM、约40nM、约50nM、约60nM、约70nM、约80nM、约90nM、约100nM、约300nM、约400nM、约500nM、约600nM、约700nM、约800nM或约900nM的浓度给予化合物。
在某些实施方案中,剂型是固体剂型,并且剂型中化合物的大小是重要的。在某些实施方案中,化合物的直径小于约3μm,小于约2μm,或小于约1μm。在某些实施方案中,活性剂的直径为约0.1μm至约3.0μm。在某些实施方案中,活性剂的直径为约0.5μm至约1.5μm。在某些实施方案中,活性剂的直径为约0.2μm、约0.3μm、约0.4μm、约0.5μm、约0.6μm、约0.7μm、约0.8μm、约0.9μm、约1.0μm、约1.1μm、约1.2。μm、约1.3μm、约1.4μm、或约1.5μm。
例如,用于口服给予人的制剂可含有约0.1mg至约5g活性剂(或化合物),其与占组合物总量的约5%至约95%的合适且方便的载体材料复配。单位剂量通常含有约0.5mg至约1500mg活性剂。剂量可以是约:1mg、2mg、3mg、4mg、5mg、6mg、7mg、8mg、9mg、10mg、11mg、12mg、13mg、14mg、15mg、16mg、17mg、18mg、19mg、20mg、21mg、22mg、23mg、24mg 25mg、26mg、27mg、28mg、29mg、30mg、31mg、32mg、33mg、34mg 35mg、36mg、37mg、38mg、39mg、40mg、41mg、42mg、43mg、44mg、45mg、46mg、47mg、48mg、49mg、50mg、55mg、60mg、65、mg、70mg、75mg、80mg、85mg、90mg、95mg、100mg、200mg、300mg、400mg、500mg、600mg、800mg或100mg等,一直到约1500mg的化合物。
在某些实施方案中,本发明涉及两种活性剂的组合。在某些实施方案中,与第二组分相比,药物组合包含相对大量的第一组分可能是有利的。在某些情况下,第一活性剂与第二活性剂的比率为约:200:1、190:1、180:1、170:1、160:1、150:1、140:1、130:1、120:1、110:1、100:1、90:1、80:1、70:1、60:1、50:1、40:1、30:1、20:1、15:1、10:1、9:1、8:1、7:1、6:1或5:1。进一步优选具有更均等的药物试剂分布。在某些情况下,第一活性剂与第二活性剂的比率为约:4:1、3:1、2:1、1:1、1:2、1:3或1:4。与第一组分相比,药物组合具有相对大量的第二组分也可能是有利的。在某些情况下,第二活性剂与第一活性剂的比率为约200:1、190:1、180:1、170:1、160:1、150:1、140:1、130:1、120:1、110:1、100:1、90:1、80:1、70:1、60:1、50:1、40:1、30:1、20:1、15:1、10:1、9:1、8:1、7:1、6:1或5:1。包含第一治疗剂与第二治疗剂的上述任意组合的组合物可以每天1、2、3、4、5、6或更多次的分开剂量给予或者以提供有效于获得所需结果的释放速率的形式给予。剂型可含有第一和第二活性剂。如果剂型含有第一和第二活性剂,则每天可以给药一次。
例如,意在对人经口给予的制剂可含约0.1mg至约5g的第一治疗剂和约0.1mg至约5g的第二治疗剂,两者与合适且方便的量的载体材料混合,该载体材料占全部组合物的约5%至约95%。单位剂量通常含有约0.5mg至约1500mg的第一治疗剂和0.5mg至1500mg的第二治疗剂。剂量可以是约:25mg、50mg、100mg、200mg、300mg、400mg、500mg、600mg、800mg或100mg等,一直到约1500mg的第一治疗剂。剂量可以是约:25mg、50mg、100mg、200mg、300mg、400mg、500mg、600mg、800mg或100mg等,一直到约1500mg的第二治疗剂。
在某些实施方案中,本发明涉及治疗阿尔茨海默病的方法,包括每天通过吸入给予有需要的患者包含约1mg至100mg色甘酸二钠的微粉化干粉。
实施例
实施例1
我们在PS1/PSS动物模型中的研究表明,色甘酸钠影响小胶质细胞与淀粉样蛋白沉积物的相互作用,并最终影响小胶质细胞的Aβ清除。我们首先在用PBS或最高剂量的色甘酸钠(3.15mg/kg)处理的小鼠的脑切片中进行Aβ和小胶质细胞标记物Iba1之间的双重免疫染色。对两种染色之间重叠的系统分析显示,接受色甘酸钠的动物显示出与淀粉样蛋白重叠的较高百分比的Iba1免疫反应性(图1B),这可能表明该化合物诱导的斑块周围小胶质细胞的适度增加。
为了进一步了解这些机制,并考虑到评估小胶质细胞功能的变化在体内具有挑战性,我们使用了额外的体外Aβ小胶质细胞摄取系统。在存在或不存在色甘酸钠的情况下,将合成的Aβ40和Aβ42肽应用于培养中的小胶质细胞。
孵育16小时后,我们观察到在色甘酸钠存在下Aβ40和Aβ42水平的剂量依赖性降低,表明色甘酸钠对Aβ聚集机制的影响可通过小胶质细胞摄取促进Aβ清除(图1C)。体内和体外结果的组合可能表明,除了抑制Aβ原纤维化外,色甘酸钠还影响小胶质细胞活化和Aβ清除。
色甘酸钠不影响血浆中的Aβ水平,但促进小胶质细胞Aβ清除。图1A说明用PBS或递增剂量的色甘酸钠处理一周后对Aβx-40和Aβx-42的血浆水平的定量(n=3-5只小鼠/组)。图1B示出了在用色甘酸钠(3.15mg/kg)或PBS每天处理持续7天的小鼠中淀粉样蛋白沉积物(6E10)和小胶质细胞(Iba1)的定位的代表性图像。计算每个沉积物的Iba1阳性过程占淀粉样蛋白的百分比,其显示出在用色甘酸钠处理后Aβ和Iba1之间的重叠增加(对于PBS,n=3只小鼠,对于色甘酸钠,n=5只小鼠)。对每只动物评估20对20个斑块。比例尺=10μm。图1C显示了色甘酸钠对小胶质细胞体外Aβ摄取的影响。培养小胶质细胞并与50nM合成的Aβ40或Aβ42以及0、10nM、10μM或1mM的色甘酸钠一起孵育16小时。孵育后,使用AβELISA测量培养基中Aβx-40(图1C左)Aβx-42(图1C,右)的浓度,并用小胶质细胞数和根据PBS对照条件标准化。(n=3次实验;*,P<0.05,**,P<0.01)
实施例2
在小胶质细胞激活和M1,M2转化的其他动物研究中显示,色甘酸是测试的许多药物中唯一影响这种变化并表现出吞噬活性的药物。图2显示了该研究的Tg-2576小鼠中所有斑块和围绕这些沉积物的小胶质细胞的代表性斑块。观察与淀粉样蛋白染色共定位的Iba-1阳性过程相对于斑块周围的Iba-1信号总量的百分比的图像分析表明,与任意其他组相比,当用色甘酸钠处理小鼠时,Iba-1/淀粉样蛋白共定位更多。该结果与实施例1中的结果以及我们的体外数据相关联。
色甘酸促进小胶质细胞Aβ42摄取(但布洛芬不行),它们的组合改善了单独的布洛芬或色甘酸导致的摄取。用色甘酸和/或布洛芬(10μM,100μM,1mM)处理BV2小胶质细胞培养物16小时。然后,将细胞与可溶性Aβ42和化合物一起孵育3小时。孵育后,收集细胞用于ELISA分析。用色甘酸(100μM,1mM)以及用色甘酸和布洛芬(每种化合物100μM,1mM)处理的BV2小胶质细胞相对于用运载体处理的BV2小胶质细胞表现出增加的Aβ42摄取水平。结果来自三个独立的实验;**p<0.01,***p<0.001,单因素方差分析,Tukey检验)。数据表示为平均值±SEM。图3图示显示用色甘酸处理的BV2小胶质细胞的结果,并且相对于用运载体处理的BV2小胶质细胞,用色甘酸和布洛芬处理表现出增加的Aβ42摄取水平。
实施例3:化合物合成
5,5'-[(2-羟基-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸二乙
酯
将色甘酸钠盐(1.0g,2mmol)在EtOH(100mL)和浓盐酸(1mL)中的悬浮液在密封的反应器管中于100℃加热24小时。白色固体溶解,趁热得到澄清的无色溶液。将其冷却至室温并加入NaHCO3(1.0g)。在25℃下搅拌30分钟后,通过旋转蒸发除去溶剂。用5:95甲醇/二氯甲烷在硅胶上进行色谱分离,得到二乙酯(0.8g,产率76%);熔点154-156℃;1H NMR(CDCl3,300MHz)δ1.42(t,3H,J=7.1Hz,CH3),2.73(br s,1H,OH),4.44(q,4H,J=7.1Hz,2OCH2CH3),4.32-4.59(m,5H,CHOH,2OCH2),6.80(s,2H,2乙烯基-H),6.99(d,2H,J=8.24Hz,2Aro-H),7.12(d,2H,J=8.24Hz,2Aro-H),7.17(d,2H,J=8.24Hz,2Aro-H),7.71(t,2H,J=8.24 2Aro-H)。
5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸二乙酯
3-双(4-甲基苯磺酸酯)-2-氟丙二醇
二氯甲烷(20mL)中的1,3-双(4-甲基苯磺酸)丙三醇(2.7g,6.78mmol)溶液于0-5℃用DAST(2.18g,13.6mmol)处理。将混合物在0-5℃下搅拌30,然后温热至25℃并搅拌16小时。将混合物倒入饱和碳酸氢钠溶液(30mL)中并分层。二氯甲烷层干燥(硫酸钠)。除去溶剂后,将粗产物在硅胶上进行色谱分离(二氯甲烷),得到0.82g(30%)固体;熔点99-102℃;1HNMR(CDCl3),δ2.5(s,6H,CH3),4.15(dd,4H,J=12.3,4.6Hz,CH2,4.8(dq,1H,J=47,4.6,CHF),7.45(d,4H,J=8.1Hz,Aro-H),7.75(d,4H,J=8.4Hz,Aro-H)。
5,5’-(2-氟丙烷-1,3-二基)双(氧基)双(4-氧代-4H-色烯-2-羧酸)
1,3-双(2-乙酰基-3-羟基苯氧基)-2-氟丙烷
乙腈(40mL)中的3-双(4-甲基苯磺酸)-2-氟丙二醇(1.0,2.5mmol),2,6-二羟基苯乙酮(0.76g,5.0mmol)和碳酸钾(0.69g)的混合物回流加热16小时。过滤该反应混合物,并蒸发滤液。将粗产物在硅胶上进行色谱分离(乙腈/二氯甲烷5:95),得到0.57g(40%)产物;熔点162-165℃;1H NMR(d6-DMSO),δ2.5(s,6H,2CH3),4.38(m,4H,2CH2),5.22(br d 1H,J=49Hz,CHF),6.45(m,4H,4Aro-H),7.28(t,2H,J=4.55Hz,2Aro-H)。
5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸二乙酯
1,3-双(2-乙酰-3-羟基苯氧基)-2-氟丙烷(200mg,0.52mmol)和草酸乙酯(2mL)的混合物加入乙醇(10mL)和苯(10mL)中的乙氧基钠(87mg Na)溶液中。将混合物回流加热16小时,冷却并用醚(50mL)稀释。过滤沉淀的钠盐,用醚洗涤并干燥。然后将其溶于水中并用10%HCl酸化,得到粘性固体。将固体在乙醇(20mL)中与催化量的36%HCl一起回流1小时。混合物倒入50mL水中并用二氯甲烷(50mL)萃取两次。合并萃取物并干燥。除去溶剂后,将粗产物在硅胶上进行色谱分离(乙腈/二氯甲烷10:90),得到0.12g(45%)产物;熔点166-170℃;1H NMR(CDCl3),δ1.42(t,6H,J=7.14Hz,2CH3),4.58(q,4H,J=7.14Hz 2CH2),4.65(m,4H,2CH2),5.35(dq,1H,J=46Hz,J=4.4HZ,CHF),6.90(s,2H,乙烯基-H),6.95(d,2H,J=8.24Hz,2Aro-H),7.13(d,2H,J=8.24Hz,2Aro-H),7.17(d,2H,J=8.24Hz,2Aro-H)7.6(t,2H,J=8.24 2Aro-H)。
5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸
将5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸二乙酯(100mg,0.19mmol)在甲醇(20mL)中的悬浮液和1M氢氧化钠(2mL)在80℃加热1小时。用10%HCl酸化溶液并去除挥发物。向所述固体加入甲醇/二氯甲烷(50:50)的溶液并过滤混合物。蒸发得到76mg(85%)产物;1H NMR(d6-DMSO),δ4.65(m,4H,2CH2),5.32(br d,1H,J=46Hz,CHF),6.80(s,2H,2乙烯基-H),7.2(d,2H,J=8.24Hz,2Aro-H),7.71(t,2H,J=8.242Aro-H)。
5,5'-[(2-羟基-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃--2-乙醇
向5,5'-(2-羟基三亚甲基二氧基)双(4-氧代色烯-2-羧酸)二乙酯(1.0g,1.86mmol)在甲醇(60ml)和二氯甲烷(40mL)的悬浮液中在1小时内分批加入NaBH4(0.14g,3.72mmol)。将混合物在25℃下搅拌直至澄清(约5小时),此时通过逐滴加入1M HCl淬灭溶液直至呈酸性。蒸发溶剂,残余物用二氯甲烷萃取。将合并的有机萃取液用水洗涤并用无水硫酸钠干燥。蒸发后,残余物用柱色谱(5:95甲醇/二氯甲烷)纯化,得到0.5g(50%)三醇;1HNMR(DMSO-d6,300MHz)δ2.73(s,3H,OH),4.25-4.36(m,9H,2OCH2,CH-O),6.13(s,2H,2乙烯基H),7.04(d,2H,J=8.4Hz,芳族H),7.07(d,2H,J=8.4Hz,芳族H),7.63(t,2H,J=8.2Hz,芳族H)。
5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃--2-乙醇
使用上述制备5,5'-(2-羟基三亚甲基二氧基)双(4-氧代色烯-2-乙醇)的方法。1HNMR(DMSO-d6,300MHz)δ2.73(s,3H,OH),4.25-4.36(m,8H,2OCH2,CH-O),5.35(br d,1H,J=46Hz,CHF),6.13(s,2H,2乙烯基H),7.04(d,2H,J=8.4Hz,芳族H),7.07(d,2H,J=8.4Hz,芳族H),7.63(t,2H,J=8.2Hz,芳族H)。
5,5'-[(2-羟基-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸双
[(2,2-二甲基-1-氧代丙氧基)甲基]酯
向搅拌的色甘酸二酸(1.0g,2.7mm)在20mL DMF中的溶液中加入二异丙胺(0.7mL)和1.0g(6.5mmol)新戊酸氯甲酯。将反应混合物在60℃下搅拌4小时,加入水,分离萃取混合物,干燥(MgSO4)并真空除去溶剂。除去溶剂,残余物在硅胶4%甲醇/二氯甲烷中进行色谱分离,得到1.2g(65%)新戊酸酯化合物;mp(熔点)135-140℃;H1NMR(CDCl),δ1.24(s,18H,CH3),4.36(m,2H,OCH2),4.49(m,1H,CHOH),4.51(m,2H,OCH2),),6.00(s,4H,CH-O-CO),6.98(m,4H,2乙烯基-H,2Aro-H),7.13(d,2H,J=8.24Hz,2Aro-H),7.61(t,2H,J=8.24 2Aro-H)。
5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸双[(2,
2-二甲基-1-氧代丙氧基)甲基]酯
向搅拌的5,5'-[(2-氟-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-羧酸(1.0g,2.1mmol)在20mL DMF的溶液中加入异丙胺(0.7mL)和1.0g(6.5mmol)新戊酸氯甲酯。将反应混合物在60℃下搅拌4小时,加入水,分离萃取混合物,干燥(MgSO4)并真空除去溶剂。除去溶剂,残余物在二氧化硅上用2%甲醇的二氯甲烷溶液进行色谱分离,得到1.0g(70%)新戊酸酯化合物;熔点130-133℃;δ1.21(s,18H,CH3),4.36(m,4m,2OCH2),4.49(brd,1H,J=46Hz,CHF),6.00(s,4H,CH-O-CO),6.98(m,4H,2乙烯基-H,2Aro-H),7.13(d,2H,J=8.24Hz,2Aro-H),7.61(t,2H,J=8.24 2Aro-H)。
5,5'-[(2-羟基-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃--2-乙醇的三
乙酸酯
将乙酸酐(0.5g,4.6mmol))缓慢加入到冷却至0-5℃的5,5'-[(2-羟基-1,3-丙二基)双(氧基)]双[4-氧代-4H-1-苯并吡喃-2-乙醇(0.5g,1.14mmol)的吡啶(20mL)混合物中。将混合物在0-5℃下搅拌3小时,然后温热至室温。TLC指示反应完成。加入二氯甲烷,用10%HCl洗涤混合物直至水相呈酸性。用无水硫酸钠干燥二氯甲烷层,蒸发溶剂。用3%甲醇/二氯甲烷在硅胶上进行色谱分离,得到0.45g(72%)三乙酸酯化合物;熔点122-125℃;H1NMR(CDCl3),δ2.16(s,9H,CH3),4.58(m,2H,CH2OH),4.66(m,2H,CH2OH),4.94(s,4H,CH2OH),5.66(m,1H,CHOH),6.15(s,2H,2乙烯基-H),6.94(d,2H,2Aro-H),6.97(d,2H,J=8.24Hz,2Aro-H),7.52(t,2H,J=8.24,2Aro-H)。
实施例4:Aβ聚集抑制测定
实验设计。使3个月大的Tg2576小鼠适应2个月,然后随机分配到不同的处理组。它们包括对照组(n=10)用运载体处理,色甘酸低剂量组和色甘酸高剂量组。通过基于0.1mL/30g体重用PBS通过IP注射进行处理,每周3次,再进行3个月。所有小鼠在8个月大时处死。收获组织并处理以进行死后分析。
将最终5μM的合成Aaβ42与10、100、1,000nM的测试化合物一起孵育1小时。用最终浓度为0.5mg/ml的肝素引发聚集。测定缓冲液由125mM NaCl,2.5mM KCl,1mM MgCl2,1.25mMNa2H2PO4,2mM CaCl2,25mM葡萄糖和NaHCO3组成,将pH调节至7.4。测定缓冲液用作对照。通过硫黄素T结合的强度测量聚集,其以动力学模式检测450nm/480nm的荧光激发/发射(Spectra Max M3平板读数器,Molecular Devices)。记录聚集,通过平板读数器的软件将动力学计算为V最大。该测定一式三份进行,并表示为标准平均值±SD。蓝色虚线表示测定缓冲液对照。图4显示了测定结果。
实施例5
色甘酸显著影响脑TBS可溶性Aβ的水平和Aβ(42:40)的比率。A-B.MSD(用于测量Aβ42、40和38的混乱量表)Aβ测定应用于脑TBS可溶性样品。测定了比较各个处理组的Aβ水平和Aβ比率(42:40)的差异。*p<0.05;**p<0.01,***p<0.001,单因素方差分析,Tukey检验;平均值±SEM显示,对于低剂量和高剂量的色甘酸和布洛芬组合,较高相对水平的Aβ42/40和更高的不涉及斑块形成的Aβ38。图5图示说明了Aβ水平和Aβ比率(42:40)的单向差异结果。
实施例6-色甘酸钠对小胶质细胞中Aβ42摄取的影响
使用共聚焦显微镜和ELISA测定评估色甘酸及其衍生化合物对小胶质细胞中Aβ42摄取的影响。使用BV2小胶质细胞系,其先前被发现有效地摄取和降解外源添加的Aβ42(Jiang,Q.等人(2008)Neuron 58,681–693;Mandrekar等人,2009J.Neurosci.29,4252–4262)。在幼稚BV2小胶质细胞中测试化合物以研究它们是否调节Aβ摄取。评估化合物在稳定表达全长人CD33的BV2细胞(BV2-CD33WT)中的作用,以探究它们是否逆转CD33介导的Aβ摄取抑制(Griciuc等,2013Neuron 78,631-643)。
储备溶液的化合物编号,分子量和浓度总结在表1中。与色甘酸衍生物C1,C2,C5,C6,C7和C8相比,色甘酸衍生物C3和C4在DMSO中显示出较低的溶解度。因此,制备了除C3和C4之外的所有化合物的25mM储备溶液。分别以5mM和7.5mM的浓度制备C3和C4的储备溶液。C1是母体化合物-色甘酸二钠。
表1:在小胶质细胞中测试的化合物的总结
| 化合物编号 | 化合物名称 | 储备溶液(mM) |
| C1 | 色甘酸二钠 | 25 |
| C2 | F-色甘酸二酸 | 25 |
| C3 | ET-色甘酸 | 5 |
| C4 | F-ET-色甘酸 | 7.5 |
| C5 | 三醇-色甘酸 | 25 |
| C6 | F-三醇-色甘酸 | 25 |
| C7 | Ac-三醇-色甘酸 | 25 |
| C8 | POM-色甘酸 | 25 |
为了研究色甘酸钠对小胶质细胞中Aβ42摄取的影响,将幼稚BV2细胞用DMSO(对照)或色甘酸以500μM处理16小时。然后,用PBS洗涤细胞,并在荧光标记的Aβ42肽(400nM,红色)存在下用DMSO或色甘酸处理2小时。在处理结束时,洗涤细胞并用质膜染料(绿色)标记它们。使用共聚焦显微镜和红色通道中的荧光信号,定量细胞内Aβ42肽的水平。所有定量均由盲观察者用ImageJ软件进行。值得注意的是,色甘酸钠导致幼稚BV2小胶质细胞中Aβ42的摄取增加(图6A-图6D)。
此外,通过使用ELISA测定法测定色甘酸钠是否调节幼稚BV2小胶质细胞中的Aβ42摄取。另外,确定色甘酸钠是否导致稳定表达全长人CD33的BV2细胞(BV2-CD33WT)中Aβ42摄取水平增加。为此目的,将幼稚BV2和BV2-CD33WT细胞系用DMSO(对照)或不同浓度的色甘酸处理16小时。然后,用PBS洗涤细胞,并用DMSO或色甘酸和可溶性未标记的Aβ42肽(400nM)处理2小时。使用来自Wako的Aβ42特异性ELISA试剂盒分析收集的细胞裂解物的Aβ42摄取水平。将ELISA结果标准化为先前使用BCA测定法定量的蛋白质浓度水平。
在幼稚BV2小胶质细胞中,色甘酸钠在100μM和1mM导致Aβ42摄取增加(图7A),因此通过ELISA测定证实了免疫荧光结果。色甘酸钠还导致BV2-CD33WT细胞中在10μM和500μM的内化的Aβ42水平增加(图7B,ELISA测定)并逆转CD33介导的小胶质细胞中Aβ42摄取的抑制。总之,用色甘酸钠处理在调节幼稚BV2和BV2-CD33WT细胞系中的Aβ42摄取水平方面显示出剂量依赖性效应。
实施例7-色甘酸衍生物对小胶质细胞中Aβ42摄取的影响
为了研究色甘酸衍生物对小胶质细胞中Aβ42摄取的影响,将幼稚BV2或BV2-CD33WT细胞接种在增殖培养基中。第二天,将细胞用DMSO(对照)或不同浓度的化合物在增殖培养基中处理3小时。在10,50,100和150μM下测试C1,C2,C5,C6,C7和C8,而由于DMSO中的溶解度限制,在5,25,50和75μM下评估C3和C4。然后,用PBS洗涤细胞,并在未标记的Aβ42肽(400nM)存在下,在DMEM培养基中用DMSO或化合物处理2小时。在用CytoTox-ONETM乳酸脱氢酶(LDH)测定法评估在处理结束时收集的培养基中的化合物毒性。用冷PBS洗涤平板中剩余的细胞,并用补充有蛋白酶和磷酸酶抑制剂的RIPA缓冲液裂解。使用PierceTM BCA蛋白质测定试剂盒测定裂解物上清液中的蛋白质浓度,并使用来自Wako的Aβ42ELISA试剂盒分析来自每种裂解物的2-3μg/孔的总蛋白质的Aβ42摄取。进一步研究排除了有毒化合物浓度。
为了研究色甘酸衍生物是否在较高剂量下诱导细胞毒性,将幼稚BV2小胶质细胞与DMSO(运载体)或不同浓度的色甘酸衍生物一起孵育3小时。然后洗涤细胞并与DMSO或化合物和可溶性未标记的Aβ42一起孵育额外的2小时。然后,收集细胞培养基并测量受损细胞释放的LDH以鉴定诱导细胞溶解的化合物。LDH测定显示,当在100和150μM下测试时,色甘酸衍生物C8是唯一显示出毒性的化合物(图8)。因此,C8的100和150μM浓度被排除在Aβ42摄取测定之外。
实施例8-通过色甘酸衍生物调节小胶质细胞中Aβ42的摄取
为了测试色甘酸衍生物是否调节Aβ42摄取,将幼稚BV2小胶质细胞用DMSO(对照)或不同浓度的色甘酸衍生物化合物处理3小时。然后,洗涤细胞并在未标记的Aβ42肽存在下用DMSO或化合物处理2小时。在处理结束时,收集细胞裂解物。使用Aβ42特异性ELISA试剂盒进行细胞内Aβ42水平的分析。母体化合物C1(色甘酸钠)在100和150μM导致BV2细胞中的Aβ42摄取适度增加。与其他色甘酸衍生物一起接收的C1等分试样在DMSO中的溶解度低于首次送至我们的C1等分试样(不含色甘酸衍生物)。有趣的是,化合物C6导致BV2小胶质细胞中Aβ42摄取的强烈抑制。值得注意的是,在幼稚BV2小胶质细胞中色甘酸衍生物C4在75μM导致Aβ42肽摄取增加(图9)。
此外,通过两组独立的实验确定色甘酸衍生物是否影响BV2-CD33WT细胞中的Aβ42摄取和清除。用DMSO(对照)或浓度范围为5-150μM的色甘酸衍生物处理BV2-CD33WT细胞。
在第一组实验中,测试了色甘酸衍生物C1和C3-8。在第二组实验中用其他色甘酸衍生物测试化合物C2。与DMSO处理相比,用75μM的化合物C4处理导致Aβ42摄取增加两倍,并且在50μM时显示出剂量依赖性效应(图10)。使用GraphPad Prism 7软件,BV2-CD33WT细胞中C4的IC50为54.7μM。与DMSO处理相比,化合物C6在介导BV2-CD33WT细胞中Aβ42摄取的抑制中表现出剂量依赖性作用。
在第二组实验中,测试了BV2-CD33WT细胞中的色甘酸衍生物C1,C2和C4-7。这些结果证实了先前的结果,即与DMSO处理相比,化合物C4在75μM时增加Aβ42摄取最有效,并且在较低浓度下显示出剂量依赖性效应(图11)。因此,这些结果表明化合物C4导致BV2-CD33WT细胞中Aβ42摄取水平增加并逆转CD33介导的对Aβ摄取和清除的抑制(图10和11)。
这些结果表明,色甘酸衍生物C4诱导小胶质细胞摄取和清除Aβ42,并增强小胶质细胞从神经毒性/促炎性向神经保护/促吞噬活化表型的倾斜。
Claims (11)
2.如权利要求1所述的应用,其中,所述神经元炎症病症是肌萎缩侧索硬化症。
3.如权利要求1所述的应用,其中,所述神经元炎症病症是亨廷顿病。
4.如权利要求1所述的应用,其中,所述神经元炎症病症是帕金森病。
6.如权利要求5所述的应用,其中,所述改善肌萎缩侧索硬化的抗炎靶向药物是布洛芬。
7.如权利要求1-4中任一项所述的应用,其中,所述药物用于腹膜内(IP)和/或静脉内(IV)给药。
8.如权利要求1-4中任一项所述的应用,其中所述化合物用于透皮给药。
9.如权利要求1-4中任一项所述的应用,其中,所述化合物用于吸入给药。
10.如权利要求1-4中任一项所述的应用,其中,所述化合物以每天1mg至1000mg的剂量给药。
11.如权利要求1-4中任一项所述的应用,其中,所述化合物以每天10、20、30、50、100或500mg的剂量给药。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202310692160.6A CN116889562A (zh) | 2016-08-31 | 2017-08-31 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662382192P | 2016-08-31 | 2016-08-31 | |
| US62/382,192 | 2016-08-31 | ||
| PCT/US2017/049702 WO2018045217A1 (en) | 2016-08-31 | 2017-08-31 | Macrophages/microglia in neuro-inflammation associated with neurodegenerative diseases |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202310692160.6A Division CN116889562A (zh) | 2016-08-31 | 2017-08-31 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109922800A CN109922800A (zh) | 2019-06-21 |
| CN109922800B true CN109922800B (zh) | 2023-06-13 |
Family
ID=61309436
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780051052.3A Active CN109922800B (zh) | 2016-08-31 | 2017-08-31 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
| CN202310692160.6A Pending CN116889562A (zh) | 2016-08-31 | 2017-08-31 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202310692160.6A Pending CN116889562A (zh) | 2016-08-31 | 2017-08-31 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US20190240194A1 (zh) |
| EP (1) | EP3506894B1 (zh) |
| JP (2) | JP2019524865A (zh) |
| KR (1) | KR20190044647A (zh) |
| CN (2) | CN109922800B (zh) |
| AU (1) | AU2017321782B2 (zh) |
| CA (1) | CA3033079A1 (zh) |
| WO (1) | WO2018045217A1 (zh) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9925282B2 (en) | 2009-01-29 | 2018-03-27 | The General Hospital Corporation | Cromolyn derivatives and related methods of imaging and treatment |
| JP6499077B2 (ja) | 2012-10-25 | 2019-04-10 | ザ ジェネラル ホスピタル コーポレイション | アルツハイマー病と関連疾患の治療のための併用療法 |
| US10525005B2 (en) | 2013-05-23 | 2020-01-07 | The General Hospital Corporation | Cromolyn compositions and methods thereof |
| JP2016534063A (ja) | 2013-10-22 | 2016-11-04 | ザ ジェネラル ホスピタル コーポレイション | クロモリン誘導体ならびに関連するイメージングおよび治療方法 |
| JP2018538273A (ja) * | 2015-11-23 | 2018-12-27 | エーゼットセラピーズ, インコーポレイテッド | 虚血性脳卒中を処置するための組成物および方法 |
| CN109922800B (zh) | 2016-08-31 | 2023-06-13 | 通用医疗公司 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
| CA3068938A1 (en) * | 2017-07-08 | 2019-01-17 | The General Hospital Corporation | Screening platform to identify therapeutic drugs or agents for treatment of alzheimer's disease |
| AU2017423862A1 (en) | 2017-07-20 | 2020-02-06 | Aztherapies, Inc. | Powdered formulations of cromolyn sodium and ibuprofen |
| WO2019199776A1 (en) * | 2018-04-09 | 2019-10-17 | The General Hospital Corporation | Combination therapies for the treatment of amyotropic lateral sclerosis and related disorders |
| AU2019299347A1 (en) | 2018-07-02 | 2021-01-21 | Aztherapies, Inc. | Powdered formulations of cromolyn sodium and alpha-lactose |
| CA3111217A1 (en) * | 2018-09-05 | 2020-03-12 | The General Hospital Corporation | Methods of treating cytokine release syndrome |
| CN113727736A (zh) * | 2018-12-10 | 2021-11-30 | 通用医疗公司 | 色甘酸酯及其用途 |
| CN112375058A (zh) * | 2020-11-11 | 2021-02-19 | 杭州卢普生物科技有限公司 | 色甘酸二乙酯和色甘酸钠的制备方法 |
| WO2022146914A1 (en) * | 2020-12-28 | 2022-07-07 | The General Hospital Corporation | Cromolyn derivatives and uses thereof |
| WO2022178278A1 (en) * | 2021-02-19 | 2022-08-25 | The Trustees Of Columbia University In The City Of New York | Compositions and methods for modeling human microglia |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004071532A1 (en) * | 2003-02-13 | 2004-08-26 | Licentia Oy | Use of a mast cell activation or degranulation blocking agent in the manufacture of a medicament for the treatment of a patient subjected to thrombolyses |
| CN103347500A (zh) * | 2010-08-12 | 2013-10-09 | 利发利希奥公司 | 用于治疗tau蛋白病的组合物和方法 |
| EP2890788A1 (en) * | 2012-08-31 | 2015-07-08 | The General Hospital Corporation | Biotin complexes for treatment and diagnosis of alzheimer's disease |
| CN105061376A (zh) * | 2009-01-29 | 2015-11-18 | 通用医疗公司 | 色甘酸衍生物以及成像和治疗的相关方法 |
| CN105377037A (zh) * | 2013-05-23 | 2016-03-02 | Az治疗公司 | 用于递送色甘酸的方法 |
| CN108472275A (zh) * | 2015-11-23 | 2018-08-31 | 阿尔茨治疗方法公司 | 治疗缺血性中风的组合物及方法 |
| CN108472393A (zh) * | 2015-11-19 | 2018-08-31 | 阿尔茨治疗方法公司 | 用于治疗阿尔茨海默病和有关病症的方法 |
Family Cites Families (121)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1144905A (en) | 1965-03-25 | 1969-03-12 | Fisons Pharmaceuticals Ltd | Substituted bis-(2-carboxy-chromonyl-oxy) derivatives and preparation and pharmaceutical compositions thereof |
| US3686412A (en) | 1965-03-25 | 1972-08-22 | Colin Fitzmaurice | Compositions containing bis-chromonyl compounds for inhibiting antigen-antibody reactions |
| GB1242211A (en) | 1967-08-08 | 1971-08-11 | Fisons Pharmaceuticals Ltd | Pharmaceutical composition |
| US3957965A (en) | 1967-08-08 | 1976-05-18 | Fisons Limited | Sodium chromoglycate inhalation medicament |
| GB1257162A (zh) | 1968-02-16 | 1971-12-15 | ||
| US4405598A (en) | 1976-01-30 | 1983-09-20 | Fisons, Limited | Composition for treating asthma |
| DE3104294A1 (de) | 1981-02-07 | 1982-08-19 | Hoechst Ag, 6000 Frankfurt | Substituierte diazaspirodecane, ihre herstellung, ihre verwendung als stabilisatoren fuer organische polymere, sowie die so stabilisierten polymeren |
| US4429545A (en) | 1981-08-03 | 1984-02-07 | Ocean & Atmospheric Science, Inc. | Solar heating system |
| BE897058A (fr) | 1982-06-25 | 1983-12-16 | Sandoz Sa | Utilisation d'un derive du spiro-succinimide dans le traitement de la demence du type alzheimer |
| US4996296A (en) | 1983-07-27 | 1991-02-26 | Yeda Research & Development Co., Ltd. | Cromolyn binding protein in highly purifed form, and methods for the isolation thereof |
| US4919915A (en) | 1987-03-03 | 1990-04-24 | Paul Averback | Method for detecting the ability to prevent red-to-green congophilic birefringence |
| US5231170A (en) | 1986-08-27 | 1993-07-27 | Paul Averback | Antibodies to dense microspheres |
| ES2087911T3 (es) | 1989-04-28 | 1996-08-01 | Riker Laboratories Inc | Dispositivo de inhalacion de polvo seco. |
| US5376386A (en) | 1990-01-24 | 1994-12-27 | British Technology Group Limited | Aerosol carriers |
| DE4405387A1 (de) | 1994-02-19 | 1995-08-24 | Hoechst Ag | Verfahren zur Herstellung von Polyalkyl-1-oxa-diazaspirodecan-Verbindungen |
| US6168776B1 (en) | 1994-07-19 | 2001-01-02 | University Of Pittsburgh | Alkyl, alkenyl and alkynyl Chrysamine G derivatives for the antemortem diagnosis of Alzheimer's disease and in vivo imaging and prevention of amyloid deposition |
| CA2174583A1 (en) | 1995-05-05 | 1996-11-06 | Alexander Chucholowski | Sulfuric acid esters of sugar alcohols |
| US6026809A (en) | 1996-01-25 | 2000-02-22 | Microdose Technologies, Inc. | Inhalation device |
| US6126919A (en) | 1997-02-07 | 2000-10-03 | 3M Innovative Properties Company | Biocompatible compounds for pharmaceutical drug delivery systems |
| US6565885B1 (en) | 1997-09-29 | 2003-05-20 | Inhale Therapeutic Systems, Inc. | Methods of spray drying pharmaceutical compositions |
| US6309623B1 (en) | 1997-09-29 | 2001-10-30 | Inhale Therapeutic Systems, Inc. | Stabilized preparations for use in metered dose inhalers |
| JP2001517692A (ja) | 1997-09-29 | 2001-10-09 | インヘール セラピューティック システムズ, インコーポレイテッド | ネブライザにおける使用のための安定化調製物 |
| US5904937A (en) | 1997-10-03 | 1999-05-18 | Fmc Corporation | Taste masked pharmaceutical compositions |
| TWI239847B (en) | 1997-12-02 | 2005-09-21 | Elan Pharm Inc | N-terminal fragment of Abeta peptide and an adjuvant for preventing and treating amyloidogenic disease |
| CA2334590C (en) | 1998-06-12 | 2009-08-18 | Microdose Technologies, Inc. | Inhalation device |
| US6197963B1 (en) | 1998-08-13 | 2001-03-06 | The Trustees Of The University Of Pennsylvania | Non-peptide peptidomimetics |
| DK1283036T3 (da) | 1998-11-13 | 2008-03-25 | Jagotec Ag | Törpulver til inhalation |
| DK1140105T3 (da) | 1998-12-24 | 2004-02-23 | Janssen Pharmaceutica Nv | Galantaminpræparat med styret frigivelse |
| JP2001151673A (ja) | 1999-09-06 | 2001-06-05 | Nikken Chem Co Ltd | 吸入用粉末製剤の製造方法 |
| US20020107173A1 (en) | 1999-11-04 | 2002-08-08 | Lawrence Friedhoff | Method of treating amyloid beta precursor disorders |
| US20020009491A1 (en) | 2000-02-14 | 2002-01-24 | Rothbard Jonathan B. | Compositions and methods for enhancing drug delivery across biological membranes and tissues |
| JP5025871B2 (ja) | 2000-02-21 | 2012-09-12 | エイチ.リュンドベック エイ/エス | アミロイドの新規なダウン−レギュレート方法 |
| US20080021085A1 (en) | 2000-04-13 | 2008-01-24 | Mayo Foundation For Medical Education And Research | Method of reducing abeta42 and treating diseases |
| CA2406383A1 (en) | 2000-04-13 | 2001-10-25 | Mayo Foundation For Medical Education And Research | A.beta.42 lowering agents |
| PE20011227A1 (es) | 2000-04-17 | 2002-01-07 | Chiesi Farma Spa | Formulaciones farmaceuticas para inhaladores de polvo seco en la forma de aglomerados duros |
| MY120279A (en) | 2000-05-26 | 2005-09-30 | Pharmacia Corp | Use of a celecoxib composition for fast pain relief |
| US20020016359A1 (en) | 2000-06-29 | 2002-02-07 | Hellberg Mark R. | Compositions and methods of treating neurodegenerative diseases |
| US8519005B2 (en) | 2000-07-27 | 2013-08-27 | Thomas N. Thomas | Compositions and methods to prevent toxicity of antiinflammatory agents and enhance their efficacy |
| FR2815030A1 (fr) | 2000-10-05 | 2002-04-12 | Lipha | Derives nitroso de la diphenylamine, compositions pharmaceutiques les contenant et leur utilisation pour la preparation de medicaments |
| US6511960B2 (en) | 2001-01-05 | 2003-01-28 | Alphamed Pharmaceuticals Corp | Cromolyn for eye and ear infections |
| CN100422180C (zh) | 2001-04-23 | 2008-10-01 | 宾夕法尼亚州大学理事会 | 淀粉样斑块聚集抑制剂和诊断成像剂 |
| WO2003045331A2 (en) | 2001-11-29 | 2003-06-05 | Emisphere Technologies, Inc. | Formulations for oral administration of cromolyn sodium |
| PT1521609E (pt) | 2002-05-10 | 2010-03-03 | Oriel Therapeutics Inc | Inalador de pó seco para utilização com meios de distribuição accionados por um polímero piezoeléctrico e embalagem blister associada compreendendo um material polimérico piezoeléctrico |
| WO2004071531A1 (en) | 2003-02-13 | 2004-08-26 | Licentia Oy | Use of a mast cell activation or degranulation blocking agent in the manufacture of a medicament for the treatment of cerebral ischemia |
| US20040223918A1 (en) | 2003-05-07 | 2004-11-11 | Chrysalis Technologies Incorporated | Aerosolization of cromolyn sodium using a capillary aerosol generator |
| GB0321607D0 (en) | 2003-09-15 | 2003-10-15 | Vectura Ltd | Manufacture of pharmaceutical compositions |
| EP1686960A4 (en) | 2003-10-28 | 2007-03-07 | Glaxo Group Ltd | INHALABLE PHARMACEUTICAL PREPARATIONS EMPLOYING LACTOSE ANHYDRATE, AND METHODS OF ADMINISTERING SAID PREPARATIONS |
| GB0326632D0 (en) | 2003-11-14 | 2003-12-17 | Jagotec Ag | Dry powder formulations |
| DE10355559A1 (de) | 2003-11-21 | 2005-06-23 | Orthogen Ag | Transskin |
| WO2005063732A1 (en) | 2003-12-23 | 2005-07-14 | Microbia, Inc. | Compounds and methods for the treatment of asthma |
| WO2005077394A1 (en) | 2004-02-11 | 2005-08-25 | Ramot At Tel-Aviv University Ltd | Compositions for treatment of cancer and inflammation with curcumin and at least one nsaid |
| US20050182044A1 (en) | 2004-02-17 | 2005-08-18 | Bruinsma Gosse B. | Combinatorial therapy with an acetylcholinesterase inhibitor and (3aR)-1,3a,8-trimethyl-1,2,3,3a,8,8a-hexahydropyrrolo[2,3,-b]indol-5-yl phenylcarbamate |
| US20070293538A1 (en) | 2004-04-13 | 2007-12-20 | Myriad Genetics, Incorporated | Pharmaceutical Composition And Methods For Treating Neurodegenerative Disorders |
| CN101098678A (zh) | 2004-04-23 | 2008-01-02 | 锡德克斯公司 | 含有磺基烷基醚环糊精的dpi制剂 |
| ES2339790T3 (es) | 2004-08-30 | 2010-05-25 | Seo Hong Yoo | Efecto neuroprotector de udca solubilizado en modelo isquemico focal. |
| CA2585471A1 (en) * | 2004-11-01 | 2006-05-11 | Seo Hong Yoo | Methods and compositions for reducing neurodegeneration in amyotrophic lateral sclerosis |
| GB0426146D0 (en) | 2004-11-29 | 2004-12-29 | Bioxell Spa | Therapeutic peptides and method |
| KR20070122497A (ko) | 2005-04-22 | 2007-12-31 | 제넨테크, 인크. | Cd20 항체로 치매 또는 알츠하이머병을 치료하는 방법 |
| WO2006125324A1 (en) | 2005-05-27 | 2006-11-30 | Queen's University At Kingston | Treatment of protein folding disorders |
| CA2631493A1 (en) | 2005-12-15 | 2007-06-21 | Acusphere, Inc. | Processes for making particle-based pharmaceutical formulations for pulmonary or nasal administration |
| US8263645B2 (en) | 2006-02-03 | 2012-09-11 | Pari Pharma Gmbh | Disodium cromoglycate compositions and methods for administering same |
| AR059356A1 (es) | 2006-02-14 | 2008-03-26 | Astrazeneca Ab | Nuevos radioligandos |
| US7700618B2 (en) | 2006-03-06 | 2010-04-20 | Pfizer Inc | Sulfonyl benzimidazole derivatives |
| MX2008011553A (es) | 2006-03-09 | 2008-12-09 | Waratah Pharmaceuticals Inc | Formulacion de polialcohol de ciclohexano para el tratamiento de transtornos de agregacion de proteinas. |
| WO2008118122A2 (en) | 2006-05-08 | 2008-10-02 | Molecular Neuroimaging, Llc | Compounds and amyloid probes thereof for therapeutic and imaging uses |
| US8445437B2 (en) | 2006-07-27 | 2013-05-21 | The Brigham And Women's Hospital, Inc. | Treatment and prevention of cardiovascular disease using mast cell stabilizers |
| US20100173960A1 (en) | 2006-09-21 | 2010-07-08 | Antonio Cruz | The Combination of a Cyclohexanehexol and a NSAID for the Treatment of Neurodegenerative Diseases |
| CA2670405A1 (en) | 2006-11-24 | 2008-05-29 | Waratah Pharmaceuticals Inc. | Combination treatments for alzheimer's disease and related neurodegenerative diseases |
| DK2142513T3 (da) | 2007-04-18 | 2014-06-10 | Probiodrug Ag | Nitrovinyl-diamin-derivater som glutaminyl-cyclase-inhibitorer |
| RU2523894C2 (ru) | 2007-04-18 | 2014-07-27 | Янссен Альцгеймер Иммунотерапи | Предупреждение и лечение церебральной амилоидной ангиопатии |
| WO2008134618A2 (en) | 2007-04-27 | 2008-11-06 | The General Hospital Corporation | Novel imaging tracers for early detection and treatment of amyloid plaques caused by alzheimer's disease and related disorders |
| WO2009011782A2 (en) | 2007-07-13 | 2009-01-22 | Abbott Biotechnology Ltd. | METHODS AND COMPOSITIONS FOR PULMONARY ADMINISTRATION OF A TNFa INHIBITOR |
| GB0714134D0 (en) | 2007-07-19 | 2007-08-29 | Norton Healthcare Ltd | Dry-powder medicament |
| DK2182983T3 (da) | 2007-07-27 | 2014-07-14 | Janssen Alzheimer Immunotherap | Behandling af amyloidogene sygdomme med humaniserede anti-abeta antistoffer |
| JO3076B1 (ar) | 2007-10-17 | 2017-03-15 | Janssen Alzheimer Immunotherap | نظم العلاج المناعي المعتمد على حالة apoe |
| CA2978149C (en) | 2008-03-21 | 2019-02-12 | The General Hospital Corporation | Inositol derivatives for the detection and treatment of alzheimer's disease and related disorders |
| WO2009133128A1 (en) | 2008-04-29 | 2009-11-05 | Pharnext | Combination compositions for treating alzheimer disease and related disorders with zonisamide and acamprosate |
| MX2011007663A (es) | 2009-01-22 | 2011-08-15 | Raqualia Pharma Inc | Compuestos de sulfona heterociclica, saturada y sustituida en n, con actividad agonistica del receptor de cb2. |
| US8381454B1 (en) | 2009-01-23 | 2013-02-26 | Markus R. Robinson | Segmented, elongated, expandable, 4-season, double-walled, low-cost, rigid extruded plastic panel structures |
| US9925282B2 (en) | 2009-01-29 | 2018-03-27 | The General Hospital Corporation | Cromolyn derivatives and related methods of imaging and treatment |
| EP2810652A3 (en) | 2009-03-05 | 2015-03-11 | AbbVie Inc. | IL-17 binding proteins |
| JP2012520311A (ja) | 2009-03-11 | 2012-09-06 | プレキシコン インコーポレーテッド | Rafキナーゼの阻害のためのピロロ[2,3−b]ピリジン誘導体 |
| WO2010107702A1 (en) | 2009-03-16 | 2010-09-23 | Ipintl, Llc | Treating alzheimer's disease and osteoporosis and reducing aging |
| ES2457442T3 (es) | 2009-05-08 | 2014-04-25 | Pari Pharma Gmbh | Formulaciones farmacéuticas concentradas estabilizadoras de los mastocitos |
| EA201290041A1 (ru) * | 2009-08-06 | 2012-07-30 | Ньюралтус Фармасьютикалс, Инк. | Лечение расстройств, связанных с макрофагами |
| EP2963024B1 (en) | 2009-09-24 | 2018-07-18 | WisTa Laboratories Ltd. | Crystalline methylthioninium chloride hydrates - part 2 |
| EP2322163A1 (en) | 2009-11-03 | 2011-05-18 | Pharnext | New therapeutics approaches for treating alzheimer disease |
| US20110262442A1 (en) | 2009-11-06 | 2011-10-27 | Adenios, Inc. | Compositions for treating cns disorders |
| EP2506835B1 (en) | 2009-11-30 | 2019-06-12 | Adare Pharmaceuticals, Inc. | Compressible-coated pharmaceutical compositions and tablets and methods of manufacture |
| EP2377860A1 (en) | 2010-04-16 | 2011-10-19 | AC Immune S.A. | Novel compounds for the treatment of diseases associated with amyloid or amyloid-like proteins |
| WO2011136754A1 (en) | 2010-04-26 | 2011-11-03 | Mahmut Bilgic | A medicament developed for the treatment of respiratory diseases |
| WO2012041717A1 (en) | 2010-09-30 | 2012-04-05 | Chiesi Farmaceutici S.P.A. | Use of magnesium stearate in dry powder formulations for inhalation |
| US20120121656A1 (en) | 2010-11-15 | 2012-05-17 | Revalesio Corporation | Methods and compositions for protecting against neurotoxicity of a neurotoxic agent, and improving motor coordination associated with a neurodegenerative condition or disease |
| CN105853439A (zh) | 2011-02-11 | 2016-08-17 | 维斯塔实验室有限公司 | 吩噻嗪二胺鎓盐和其用途 |
| SG11201406142XA (en) | 2012-03-27 | 2014-10-30 | Univ Duke | Compositions and methods for the prevention and treatment of mast cell-induced vascular leakage |
| AU2013266067B2 (en) | 2012-05-25 | 2016-10-06 | Xlear, Inc. | Xylitol-based anti-mucosal compositions and related methods and compositions |
| US20150274680A1 (en) | 2012-10-23 | 2015-10-01 | Teijin Pharma Limited | Therapeutic or prophylactic agent for tumor lysis syndrome |
| JP6499077B2 (ja) | 2012-10-25 | 2019-04-10 | ザ ジェネラル ホスピタル コーポレイション | アルツハイマー病と関連疾患の治療のための併用療法 |
| US10058530B2 (en) | 2012-10-25 | 2018-08-28 | The General Hospital Corporation | Combination therapies for the treatment of Alzheimer's disease and related disorders |
| US10525005B2 (en) | 2013-05-23 | 2020-01-07 | The General Hospital Corporation | Cromolyn compositions and methods thereof |
| JP2016534063A (ja) * | 2013-10-22 | 2016-11-04 | ザ ジェネラル ホスピタル コーポレイション | クロモリン誘導体ならびに関連するイメージングおよび治療方法 |
| SI3104853T1 (sl) | 2014-02-10 | 2020-03-31 | Respivant Sciences Gmbh | Zdravljenje s stabilizatorji mastocitov za sistemske motnje |
| US20150224078A1 (en) * | 2014-02-10 | 2015-08-13 | Patara Pharma, LLC | Methods for the Treatment of Lung Diseases with Mast Cell Stabilizers |
| AU2015350142A1 (en) | 2014-11-21 | 2017-06-15 | Biohaven Pharmaceutical Holding Company Ltd. | Sublingual administration of riluzole |
| WO2016196401A1 (en) | 2015-05-29 | 2016-12-08 | The Texas A&M University System | Antimicrobial and anti-inflammatory compositions |
| US10238625B2 (en) | 2015-08-07 | 2019-03-26 | Respivant Sciences Gmbh | Methods for the treatment of mast cell related disorders with mast cell stabilizers |
| WO2017027402A1 (en) | 2015-08-07 | 2017-02-16 | Patara Pharma, LLC | Methods for the treatment of systemic disorders treatable with mast cell stabilizers, including mast cell related disorders |
| EP3368032A1 (en) * | 2015-10-28 | 2018-09-05 | AB Science | Use of masitinib and other mast cell inhibitors for treatment of parkinson's disease |
| EA038531B1 (ru) * | 2016-03-25 | 2021-09-10 | Аб Сьянс | Способ лечения амиотрофного латерального склероза, применение фармацевтической композиции, содержащей мазитиниб |
| CN109922800B (zh) | 2016-08-31 | 2023-06-13 | 通用医疗公司 | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 |
| RU2760682C2 (ru) | 2016-09-08 | 2021-11-29 | Имерго Терапьютикс, Инк. | Стабилизаторы тучных клеток лечения гиперцитокинемии и вирусной инфекции |
| AU2017423862A1 (en) | 2017-07-20 | 2020-02-06 | Aztherapies, Inc. | Powdered formulations of cromolyn sodium and ibuprofen |
| CN108164409B (zh) | 2018-01-24 | 2021-06-18 | 温州医科大学 | 一种2-亚苄基-1-茚酮类似物及应用 |
| WO2019199776A1 (en) | 2018-04-09 | 2019-10-17 | The General Hospital Corporation | Combination therapies for the treatment of amyotropic lateral sclerosis and related disorders |
| CN108403708B (zh) | 2018-05-22 | 2019-06-14 | 滨州医学院 | 秦皮苷在制备预防或治疗急性呼吸窘迫综合征药物中的应用 |
| AU2019299347A1 (en) | 2018-07-02 | 2021-01-21 | Aztherapies, Inc. | Powdered formulations of cromolyn sodium and alpha-lactose |
| CA3111217A1 (en) | 2018-09-05 | 2020-03-12 | The General Hospital Corporation | Methods of treating cytokine release syndrome |
| CN113727736A (zh) | 2018-12-10 | 2021-11-30 | 通用医疗公司 | 色甘酸酯及其用途 |
| WO2021207060A1 (en) | 2020-04-06 | 2021-10-14 | The General Hospital Corporation | Methods of treatment of coronavirus-induced inflammation conditions |
| WO2021248022A1 (en) | 2020-06-04 | 2021-12-09 | The General Hospital Corporation | Methods of treating a coronavirus infection |
| WO2022146914A1 (en) | 2020-12-28 | 2022-07-07 | The General Hospital Corporation | Cromolyn derivatives and uses thereof |
-
2017
- 2017-08-31 CN CN201780051052.3A patent/CN109922800B/zh active Active
- 2017-08-31 JP JP2019511620A patent/JP2019524865A/ja active Pending
- 2017-08-31 US US16/328,956 patent/US20190240194A1/en not_active Abandoned
- 2017-08-31 AU AU2017321782A patent/AU2017321782B2/en active Active
- 2017-08-31 CA CA3033079A patent/CA3033079A1/en active Pending
- 2017-08-31 KR KR1020197008717A patent/KR20190044647A/ko active IP Right Grant
- 2017-08-31 WO PCT/US2017/049702 patent/WO2018045217A1/en unknown
- 2017-08-31 EP EP17847576.0A patent/EP3506894B1/en active Active
- 2017-08-31 CN CN202310692160.6A patent/CN116889562A/zh active Pending
-
2021
- 2021-05-18 US US17/323,514 patent/US11679095B2/en active Active
-
2022
- 2022-08-17 JP JP2022130220A patent/JP2022171666A/ja active Pending
-
2023
- 2023-06-16 US US18/210,992 patent/US20240082207A1/en active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004071532A1 (en) * | 2003-02-13 | 2004-08-26 | Licentia Oy | Use of a mast cell activation or degranulation blocking agent in the manufacture of a medicament for the treatment of a patient subjected to thrombolyses |
| CN105061376A (zh) * | 2009-01-29 | 2015-11-18 | 通用医疗公司 | 色甘酸衍生物以及成像和治疗的相关方法 |
| CN103347500A (zh) * | 2010-08-12 | 2013-10-09 | 利发利希奥公司 | 用于治疗tau蛋白病的组合物和方法 |
| EP2890788A1 (en) * | 2012-08-31 | 2015-07-08 | The General Hospital Corporation | Biotin complexes for treatment and diagnosis of alzheimer's disease |
| CN105377037A (zh) * | 2013-05-23 | 2016-03-02 | Az治疗公司 | 用于递送色甘酸的方法 |
| CN108472393A (zh) * | 2015-11-19 | 2018-08-31 | 阿尔茨治疗方法公司 | 用于治疗阿尔茨海默病和有关病症的方法 |
| CN108472275A (zh) * | 2015-11-23 | 2018-08-31 | 阿尔茨治疗方法公司 | 治疗缺血性中风的组合物及方法 |
Non-Patent Citations (2)
| Title |
|---|
| "Mast cell stabilization reduces hemorrhage formation and mortality after administration of thrombolytics in experimental ischemic stroke";Strbian, D等;《CIRCULATION》;20070724;第116卷(第4期);参见摘要 * |
| 马英主编."生物电子等排体".《药物化学》.郑州:河南科学技术出版社,2012,第6-7页. * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN109922800A (zh) | 2019-06-21 |
| AU2017321782A1 (en) | 2019-03-07 |
| CA3033079A1 (en) | 2018-03-08 |
| AU2017321782B2 (en) | 2022-03-10 |
| WO2018045217A8 (en) | 2019-03-14 |
| US20220079914A1 (en) | 2022-03-17 |
| US11679095B2 (en) | 2023-06-20 |
| WO2018045217A1 (en) | 2018-03-08 |
| EP3506894C0 (en) | 2023-08-23 |
| EP3506894B1 (en) | 2023-08-23 |
| CN116889562A (zh) | 2023-10-17 |
| US20190240194A1 (en) | 2019-08-08 |
| EP3506894A1 (en) | 2019-07-10 |
| JP2019524865A (ja) | 2019-09-05 |
| JP2022171666A (ja) | 2022-11-11 |
| EP3506894A4 (en) | 2020-07-29 |
| KR20190044647A (ko) | 2019-04-30 |
| US20240082207A1 (en) | 2024-03-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109922800B (zh) | 与神经退行性疾病相关的神经炎症中的巨噬细胞/小胶质细胞 | |
| WO2007127448A2 (en) | Salts of pyridazine compounds | |
| JP2009535321A (ja) | Gsk−3阻害剤としてのn−(2−チアゾリル)アミド誘導体 | |
| AU2022202313A1 (en) | Method of treating neurodegenerative disorders | |
| US20230219920A1 (en) | Dimethylsulfoximine derivative | |
| JP6994939B2 (ja) | プロテオパチーの処置のためのベンジリデングアニジン誘導体の新規な治療的使用 | |
| JP4788999B2 (ja) | 分枝鎖カルボン酸化合物およびその用途 | |
| JP2015504861A (ja) | ニコチン性受容体標的化合物および組成物 | |
| WO2021067836A1 (en) | Chinone-, hydrochinome- and naphthochinone-analogues of vatiquione for treatment of mitochondrial disorder diseases | |
| WO2003055521A1 (fr) | Remedes contre les troubles cognitifs legers | |
| JP7295145B2 (ja) | 神経変性疾患を治療するための医薬及びその使用 | |
| US20230365572A1 (en) | Hydroxylbenzyl azabicyclo[2.2.1]heptan-1-ane drivatives and medical uses thereof | |
| US20120010264A1 (en) | Novel medicament for treating cognitive impairment | |
| CN117136050A (zh) | 用于使用大麻素治疗神经元病症的组合物和方法 | |
| RU2726313C1 (ru) | Применение производных N,N"-замещенных 3,7-диазабицикло[3.3.1]нонанов для терапии депрессии | |
| JP7382944B2 (ja) | 神経変性疾患を予防・治療するための新規な化合物及びその応用 | |
| WO2024003787A1 (en) | Compositions and methods for preventing and treating neurodegenerative diseases with diabetes | |
| WO2021021004A1 (ru) | Производное 3,6,9-триазатрициклотетрадекана и его применение для лечения депрессии | |
| JP2021520412A (ja) | タンパク質ミスフォールディング疾患のための療法 | |
| KR20200052938A (ko) | 테트라히드로나프틸우레아 유도체의 결정 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |