BRPI0806328B1 - Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo, seu método de preparação, composição farmacêutica, polinucleotídeo, vetor de expressão, bem como seus usos - Google Patents
Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo, seu método de preparação, composição farmacêutica, polinucleotídeo, vetor de expressão, bem como seus usos Download PDFInfo
- Publication number
- BRPI0806328B1 BRPI0806328B1 BRPI0806328-1A BRPI0806328A BRPI0806328B1 BR PI0806328 B1 BRPI0806328 B1 BR PI0806328B1 BR PI0806328 A BRPI0806328 A BR PI0806328A BR PI0806328 B1 BRPI0806328 B1 BR PI0806328B1
- Authority
- BR
- Brazil
- Prior art keywords
- antibody
- antibodies
- antigen
- binding
- amino acid
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/531—Production of immunochemical test materials
- G01N33/532—Production of labelled immunochemicals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
- G01N33/6896—Neurological disorders, e.g. Alzheimer's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/28—Neurological disorders
- G01N2800/2814—Dementia; Cognitive disorders
- G01N2800/2821—Alzheimer
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Molecular Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Psychology (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Heart & Thoracic Surgery (AREA)
Abstract
moléculas de ligação e, anticorpos ou fragmento de ligação e uso dos mesmos, antígeno, polinucleotídeo, vetor e célula hospedeira compreendo o referido polinucleotídeo, método de preparação de uma molécula de ligação beta-amilóide específica, bem como composição. a presente invenção refere-se a novas moléculas aglutinantes específicas, particularmente anticorpos humanos como também fragmentos, derivados e variantes que reconhecem neoepitopos de proteínas associadas à doença, que derivam de proteínas endógenas nativas, mas que são prevalentes no organismo de um paciente em uma forma variante e/ou fora de seu contexto fisiológico normal. além disso, estão descritas as composições farmacêuticas compreendendo tais moléculas aglutinantes, anticorpos e representações e métodos de rastreio para novas moléculas aglutinantes, que podem ou não podem ser anticorpos como também alvos no tratamento de distúrbios neurológicos tais como a doença de alzheimer.
Description
[0001] A presente invenção refere-se a novas moléculas específicas de ligação (daqui em diante denominadas como moléculas de ligação ou ligantes), particularmente anticorpos humanos, bem como fragmentos, derivados e variantes dos mesmos, que reconhecem epitopos de doenças associadas, incluindo neoepítopos, das proteínas que resultam de proteínas nativas endógenas e que são prevalentes no corpo de um paciente em uma forma variante e/ou fora do seu contexto fisiológico normal. Além disso, a presente invenção refere-se a composições farmacêuticas compreendendo tais moléculas ligantes, anticorpos e réplicas e aos métodos de rastreio para novas moléculas ligantes, que podem ou não ser anticorpos, alvos e fármacos no tratamento de diversos distúrbios, em particular, distúrbios neurológicos como a doença de Alzheimer, amiloidoses e patologia de beta-amiloide.
[0002] O sucesso na geração de anticorpos monoclonais repousa na eficiente e seletiva fusão de células B estimuladas por antígenos com uma linha de células de mieloma murino seguida pela seleção de híbridos produtores de anticorpos estáveis, conforme originalmente descrito por Kõhler e Milstein, Nature 256 (1975), 495-497. No entanto, a utilidade terapêutica em seres humanos de anticorpos com base murina é dificultada pela resposta dos anticorpos humanos anti- camundongo (HAMA) em virtude da sua origem não-humana. Abordagens para a produção de anticorpos monoclonais humanos ou similares aos humanos tornaram-se disponíveis através da engenharia genética. No entanto, os métodos disponíveis até agora sofrem a desvantagem de que não se encontram aptos a produzir anticorpos com as características daqueles produzidos no decurso de uma resposta imune humana fisiológica. Além disso, esses anticorpos não podem ser suficientemente específicos devido à reatividade cruzada com outras proteínas e/ou a proteína-alvo em contexto com funções fisiológicas normais. No caso da doença de Alzheimer ou da doença de Parkinson, por exemplo, considera-se que os anticorpos que também reagem de forma cruzada com alta afinidade com derivados fisiológicos da proteína precursora amiloide (APP) ou alfa-sinucleína exibem efeitos colaterais relacionados com as funções normais das estruturas-alvo fisiológicas. Neste aspecto, uma doença autoimune indesejável seria diretamente induzida - um risco dificilmente calculável no projeto conceituai das experiências de imunização ativa que empregam estruturas de proteínas que, na forma variante, também ocorrem fisiologicamente. Os efeitos colaterais não relacionados com a estrutura-alvo são, por exemplo, reações anafiláticas, que são de se esperar como efeitos colaterais indesejáveis e temidos da administração sistêmica das proteínas exógenas. De acordo com recentes descobertas, este também pode ser o caso nos chamados anticorpos humanizados, que originalmente provêm de organismos não-humanos, geralmente a partir de camundongos. Por outro lado, a imunização ativa com antígenos relevantes patológicos comporta o risco considerável de pacientes desenvolverem respostas a anticorpos e a células T, que também reconhecem variantes fisiológicas dessas proteínas e, consequentemente, levam a uma perigosa e incontrolável resposta autoimune.
[0003] Assim, existe uma necessidade de propiciar agentes que são específicos para um alvo envolvido em um distúrbio e que são tolerados pelo corpo humano.
[0004] Um objetivo da presente invenção é um método de identificação, validação e produção, por meio de diagnóstico e de forma terapêutica, de moléculas ligantes úteis, em especial anticorpos que são dirigidos contra variantes patológicas de proteínas endógenas. Mais especificamente, a presente invenção refere-se a um método de isolamento de uma molécula ligante de proteína específica associada à doença, compreendendo: (a) submeter um espécime obtido a partir de um paciente assintomático ou que esteja excepcionalmente clinicamente estável, mas que esteja afetado por ou com risco de desenvolver um distúrbio a um espécime de células ou tecidos patologicamente alterados com características patológicas predeterminadas; e (b) identificar e opcionalmente isolar uma molécula ligante que se liga ao dito espécime, mas não às células ou tecidos correspondentes sem tais características patológicas, uma vez que pode ser derivada de um sujeito saudável.
[0005] Conhecido é o fato de que, em caso de doenças autoimunes, os anticorpos são dirigidos contra as células autólogas e proteínas ou outros compostos, tais como glicolipídeos expressos pelas ditas células enquanto escapam dos mecanismos de tolerância conhecidos. Também conhecido é o fato de, em caso de desenvolvimentos neoplásticos endógenos, uma imunidade celular e humoral às células neoplásicas pode desenvolver-se e pode, portanto, criar mecanismo de proteção imunológica endógena contra a degeneração neoplásica dos tecidos.
[0006] A presente invenção faz uso da constatação surpreendente de que os anticorpos também podem ser dirigidos contra as variantes patofisiologicamente relevantes de proteínas endógenas, em especial contra os neoepítopos, que se formam devido à transcrição, tradução ou modificação pós-transcrição ou pós-tradução ou processamento proteolítico ou agregação patologicamente alterados. Esses anticorpos são direcionados contra proteínas endógenas que, devido à sua nova estrutura que se desvia da fisiologia normal, tornam-se patofisiologicamente relevantes por meio do desenvolvimento de efeitos patológicos. Por motivos de tolerância imunológica, os anticorpos relacionados com a resposta imune correspondente aos neoepítopos nessas variantes patológicas normalmente não apresentam, entretanto, quaisquer reações cruzadas contra as proteínas fisiologicamente funcionais, contrariamente ao caso de doenças autoimunes. Isto porque a formação de anticorpos potencialmente reativos cruzados é especificamente reprimida pelos mecanismos de tolerância conhecidos, ao passo que o desenvolvimento de uma resposta imune aos neoepítopos patológicos pode escapar à tolerância.
[0007] Assim, a presente invenção refere-se a uma nova abordagem de identificação por meio de diagnóstico, de forma terapêutica e preventiva de moléculas ligantes ativas, especialmente anticorpos e fragmentos de anticorpos de sujeitos humanos pré- selecionados por meio da interação com estruturas patológicas identificáveis.
[0008] A presente invenção é, assim, dirigida a anticorpos ou fragmentos de ligação a antígenos e moléculas de ligação a antígenos similares que são capazes de reconhecer epitopos, incluindo neoepítopos, de proteínas associadas à doença, que resultam de proteínas endógenas nativas e são prevalentes no corpo de um paciente em uma forma variante, por exemplo, como proteína patológica e/ou fora de seu contexto fisiológico normal. Além disso, a presente invenção refere-se a composições compreendendo os ditos anticorpos e a métodos imunoterapêuticos e imunodiagnósticos utilizando os mesmos.
[0009] Além disso, na identificação de anticorpos, o método de acordo com a presente invenção pode prescindir da hipótese prévia sobre a identidade de sua estrutura-alvo molecular, exclusivamente por meio de sua associação com estruturas patologicamente relevantes. Além da possibilidade de assim identificar estruturas-alvo moleculares até aqui desconhecidas para doenças específicas, outra vantagem dos anticorpos que são exclusivamente dirigidos contra estruturas patológicas baseia-se no fato de que a sua disponibilidade farmacodinâmica não é negativamente influenciada pela ligação a tecidos não-doentes de tal modo que o anticorpo é amortecido com relação a sua concentração e efeitos de submersão, impedindo deste modo a determinação de concentrações terapêutica mente eficazes. Além disso, o anticorpo e as moléculas de ligação da presente invenção são preferivelmente caracterizados pelo fato de que eles reagem com a forma variante da proteína associada à doença in vivo ou com uma célula ou membrana de célula e em uma seção de tecido com a doença caracterizado patologicamente, respectivamente, mas sem ou em uma medida significantemente menor com a variante fisiológica da proteína cognata; vide também, por exemplo, o Exemplo 2.
[00010] Uma vez que a presente invenção permite a identificação e isolamento de estruturas-alvo moleculares nas células e tecidos doentes, outra modalidade refere-se ao antígeno e à proteína patológica, ou seja, a proteína associada à doença, respectivamente, que está ligada pelo anticorpo específico do neoepítopo da presente invenção.
[00011] Uma modalidade particularmente preferida é um anticorpo humano ou um fragmento ligante de antígeno do mesmo que demonstra suas características ligantes imunológicas de qualquer dos anticorpos caracterizados pelas regiões variáveis VH e/ou VL, tal como estabelecido nas Tabelas 2 e 3, infra. Alternativamente, o anticorpo é um anticorpo humanizado, xenogênico ou um anticorpo humano- murino quimérico, sendo este último particularmente útil no caso de métodos diagnósticos e estudos em animais. Composições terapêuticas, incluindo anticorpo ou fragmentos ativos do mesmo ou agonistas e moléculas cognatas ou, alternativamente, antagonistas das mesmas e os métodos de utilização de tais composições na prevenção, diagnóstico ou tratamento de uma doença com essas composições também estão incluídos, em que uma quantidade eficaz da composição é administrada a um paciente que necessite de tal tratamento.
[00012] O fragmento ligante de antígeno do anticorpo pode ser um fragmento Fv de cadeia única, um fragmento F(ab'), um fragmento F(ab) e um fragmento F(ab')2 ou qualquer outro fragmento ligante ao antígeno. Em uma modalidade específica, infra, o anticorpo ou fragmento do mesmo é um anticorpo isótipo de IgG humano.
[00013] Naturalmente, a presente invenção abrange o linfócito de memória B e a célula B humanos imortalizados, respectivamente, que produzem o anticorpo contendo as características distintas e únicas, tal como definido abaixo.
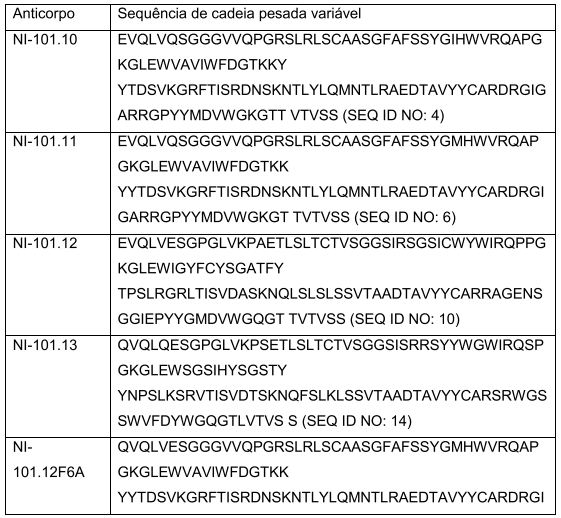
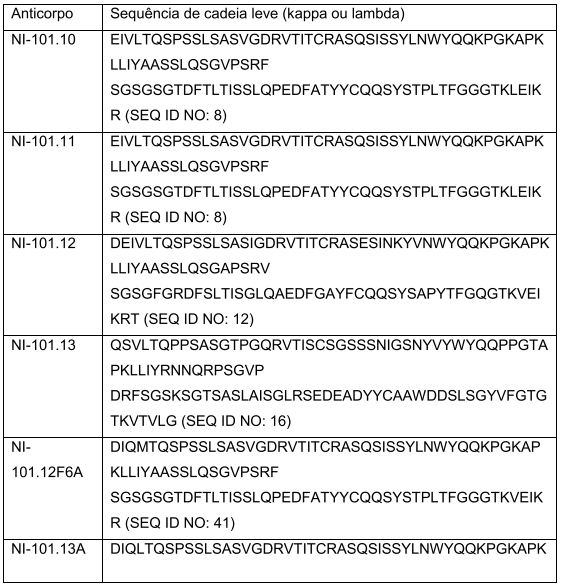
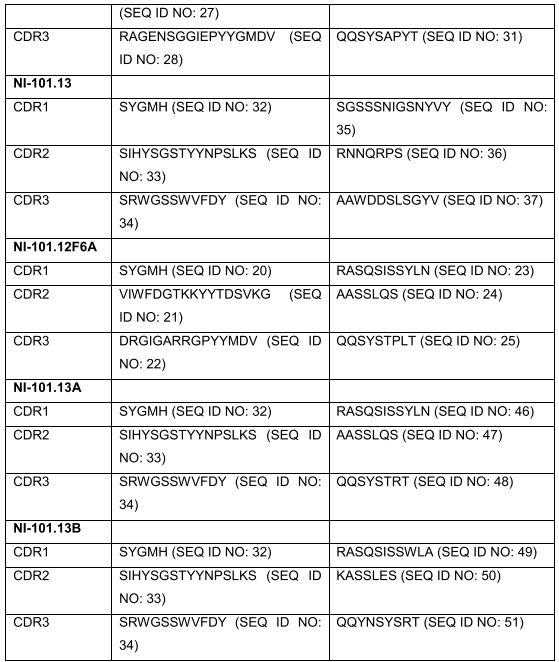
[00014] A presente invenção também se refere aos polinucleotídeos codificando pelo menos uma região variável de uma cadeia de imunoglobulina do anticorpo da invenção. Preferivelmente, a dita região variável compreende pelo menos uma região determinante de complementaridade (CDR) do VH e/ou VL da região variável conforme estabelecido nas Tabelas 2 e 3, infra. Um conjunto correspondente de CDRs é apresentado na Tabela 4, infra.
[00015] Assim, a presente invenção também engloba vetores compreendendo os ditos polinucleotídeos e as células hospedeiras transformadas conjuntamente, bem como sua utilização para a produção de um anticorpo e de moléculas de ligação equivalentes que são específicos para neoepítopos que são indicativos e/ou causadores de um distúrbio, em especial para um distúrbio do cérebro, como a doença de Alzheimer e a doença de Parkinson.
[00016] O anticorpo, a(s) cadeia(s) de imunoglobulina, seus fragmentos ligantes e o antígeno que se liga ao dito anticorpo podem ser usados em composições farmacêuticas e diagnósticas para imunoterapia e diagnóstico, respectivamente. A utilização das composições precedentes na preparação de um medicamento é, no entanto, preferida.
[00017] Portanto, é um objetivo em particular da presente invenção propiciar métodos para tratar ou prevenir um distúrbio neurológico caracterizado pelo acúmulo e/ou deposição anormal de uma proteína no sistema nervoso central, sem interferir com a função natural das respectivas proteínas. Os métodos compreendem a administração de uma concentração efetiva de um anticorpo ou derivado de anticorpo ao sujeito no qual o anticorpo liga-se à forma patológica da proteína ou do depósito da proteína com uma afinidade substancialmente maior do que a forma fisiológica normal da proteína. Em uma modalidade preferida, a presente invenção fornece métodos para tratar ou impedir ou retardar o aparecimento de doenças associadas à acumulação e deposição do peptídeo beta amiloide em um sujeito, como a doença de Alzheimer, síndrome de Down, comprometimento cognitivo leve, angiopatia amiloide cerebral, demência vascular, demência multi- infarto. Os métodos compreendem a administração de uma concentração efetiva de um anticorpo ou derivado de anticorpo ao sujeito, na qual o anticorpo liga-se à forma patológica da proteína ou ao depósito da proteína com maior afinidade do que à forma fisiológica normal da proteína. Abordagens terapêuticas similares são contempladas para o tratamento da doença de Parkinson, doença de Huntington, doença de Creutzfeldt-Jakob, fibrose cística, doença de Gaucher e similares.
[00018] Outras modalidades da presente invenção serão evidentes a partir da descrição que se segue.
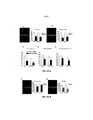
[00019] Figura 1: Anticorpo contra beta-amiloide. A: Anticorpos humanos. B: Marcação controle com anticorpos conhecidos contra beta-amiloide humano. Pacientes excepcionalmente clinicamente estáveis com doença de Alzheimer contêm anticorpos para placas beta-amiloides. A marcação imuno-histoquímica com anticorpos de pacientes excepcionalmente clinicamente estáveis nas seções do cérebro obtidas de pacientes com doença de Alzheimer confirmada patologicamente revela anticorpos que se ligam às placas beta- amiloides confirmadas por um anticorpo conhecido contra o beta- amiloide humano.
[00020] Figura 2: Anticorpo contra emaranhados neurofibrilares. A: Anticorpos humanos. B: Marcação controle com anticorpos conhecidos contra a proteína tau humana. Sujeitos humanos saudáveis contêm anticorpos para emaranhados neurofibrilares. A marcação imuno- histoquímica com anticorpos de pacientes saudáveis nas seções do cérebro obtidas de pacientes com doença de Alzheimer confirmada patologicamente revela anticorpos que se ligam aos emaranhados neurofibrilares confirmados por um anticorpo conhecido contra a proteína tau humana.
[00021] Figura 3: Anticorpo contra neurites distróficas. A: Anticorpos humanos. B: Marcação controle com anticorpos conhecidos contra a proteína tau humana. Sujeitos humanos saudáveis contêm anticorpos para neurites distróficas. A marcação imuno-histoquimica com anticorpos de pacientes saudáveis nas seções do cérebro obtidas de pacientes com doença de Alzheimer confirmada patologicamente revela anticorpos que se ligam às neurites distróficas.
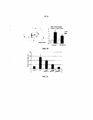
[00022] Figura 4: Anticorpo contra beta-amiloide. A figura mostra a ligação específica do anticorpo NI-101.11 recombinante humano, que foi isolado de um paciente com doença de Alzheimer excepcionalmente estável clinicamente, às placas beta-amiloides do cérebro. As seções cerebrais obtidas de um paciente com doença de Alzheimer neuropatologicamente confirmada foram marcadas com anticorpos recombinantes humanos nas concentrações indicadas. Anticorpo que se aglutina às placas beta-amiloides com concentrações de 50 pM sugere ligação de alta afinidade.
[00023] Figura 5: A ligação do anticorpo N1-101.11 humano recombinante às placas beta-amiloides não sofre concorrência dos polipeptídeos Abeta de terminação-N sintéticos lineares. A ligação do anticorpo recombinante contra o beta-amiloide (0,5 nM) cerebral não sofre concorrência do polipeptídio derivado de Abeta N-terminal representando as posições 1 a 16 em concentrações de até 1 pM.
[00024] Figura 6: O anticorpo NI-101.11 humano recombinante reconhece um epitopo Abeta conformacional que não está presente no Abeta monomérico. A ligação do NI-101.11 às placas beta-amiloides nas seções do cérebro podem sofrer concorrência das fibrilas Abetal- 42, mas não dos monômeros Abeta1-42 sintéticos lineares.
[00025] Figura 7: O anticorpo N1-101.11 humano recombinante não se liga ao Abeta sintético monomérico linear no método Western blot. Preparações de Abeta monomérico foram separadas por PAGE não- desnaturante. A proteína detectada pelo método Blotfoi examinada com o anticorpo recombinante humano contra o beta-amiloide e os anticorpos de controle contra as sequências de Abeta linear de terminação-N (6E10). Nenhuma ligação de N1-101.11 ao Abeta monomérico foi detectada. Esta constatação sugere que o anticorpo reconhece um epitopo conformacional Abeta.
[00026] Figura 8: O anticorpo NI-101.11 humano liga-se às fibrilas amiloides artificiais preparadas a partir dos peptídeos do Abeta1-42 sintéticos. As fibrilas do Abeta sintético ou do Abeta sintético monomérico cobrindo as placas ELISA em densidades de cobertura iguais foram incubadas com anticorpos humanos recombinantes contra o beta-amiloide cerebral nas concentrações indicadas. A atividade de ligação do anticorpo humano contra o beta-amiloide cerebral para fibrilas amiloides artificiais (quadrados abertos) é mais de 100 vezes superior em comparação ao Abeta monomérico (quadrados preenchidos). O anticorpo controle 22C4 liga-se preferencialmente ao Abeta monomérico (ciclos preenchidos) e menos preferencialmente às fibrilas (círculos abertos). Isto sugere que o Nl- 101.11 reconhece um epitopo conformacional, que também está presente em fibrilas amiloides artificiais preparadas a partir de peptídeos sintéticos Abeta.
[00027] Figura 9: Reatividade cruzada ausente de anticorpo Nl- 101.11 humano recombinante para APP de extensão total celular ou com qualquer de seus derivados fisiológicos ocorrendo em células expostas à cultura. Em contraste com o anticorpo controle (6E10) que se liga ao APP de superfície das células, a ligação de NI-101.11 ao APP de extensão total em superfícies celulares está ausente. Estes dados demonstram reatividade cruzada ausente de NI-101.11 para APP de extensão total celular, fisiológica.
[00028] Figura 10A-C: Ausência de ligação da NI-101.11 ao Abeta monomérico via cromatografia de exclusão de tamanho. As figuras 10A e 10B não mostram qualquer ligação do N1-101.11 ou de um anticorpo controle não relacionado ao Abeta1-42 conjugado à FITC, enquanto a Figura 10C mostra ligação proeminente do anticorpo 22C4 que reconhece um epitopo linear presente na terminação-C do Abeta.
[00029] Figura 11:0 ELISA de concorrência mostra que a ligação do anticorpo 6E10, um anticorpo dirigido contra um epitopo linear na terminação-N do Abeta, poderia ser completamente bloqueada quando da pré-incubação com concentrações superiores de peptídeos Abeta monoméricos, enquanto a pré-incubação com concentrações superiores destas preparações de peptídeos de Abeta monoméricos não aboliu a ligação do NI-101.11.
[00030] Figura 12: A ligação de NI-101.13A e NI-101.13B às seções cerebrais obtidas do modelo de camundongo transgênico Tg2676 da doença de Alzheimer.
[00031] Figura 13: ELISA mostrando ligação preferencial de Nl- 101.13A e NI-101.13B às fibrilas amiloides artificiais em comparação com o Abeta monomérico.
[00032] Figura 14A-B: A Figura 14A mostra a ligação do N1-101.12 recombinante ao peptídeo sintético Abeta1-42 através do ELISA. A Figura 14B mostra que a ligação do NI-101.12 sofreu concorrência do peptídeo Abeta1-42 em excesso.
[00033] Figura 15: Anticorpo humano recombinante NI-101.11 contra o beta-amiloide cerebral cruza a barreira hematoencefálica em um modelo de camundongo transgênico da doença de Alzheimer e se liga às placas do beta-amiloide encefálicas in vivo.
[00034] Figura 16A-B: O anticorpo NI-101.11 humano recombinante aperfeiçoa o comportamento cognitivo anormal em um modelo de camundongo transgênico da doença de Alzheimer. Camundongos arcAbeta com 24 meses de idade foram tratados semanalmente i.p. com 3 mg/kg de anticorpos por dois meses. O teste comportamental de labirinto em Y foi realizado antes e após a conclusão do tratamento.
[00035] Figura 17: A penetração na barreira hematoencefálica e a decoração das placas amiloides pela administração periférica do Nl- 101.11. O NI-101.11 pode atravessar a barreira hematoencefálica e se ligar aos depósitos beta-amiloides em camundongos tratados com Nl- 101.11 (painel esquerdo), enquanto que nenhuma dessas marcações é visível nos animais tratados com o anticorpo controle humano (painel direito). O anticorpo NI—101.11 humano recombinante reduz a carga das placas de beta-amiloides no cérebro após o tratamento sistêmico por dois meses.
[00036] Figura 18: A imunização passiva com N1-101.11 reduz a carga de beta-amiloides em camundongos arcAbeta. As análises das cargas das placas de Tioflavina S (A,B) e Vermelho de congo revelam significativas reduções de mais de 50% em comparação com os animais tratados com anticorpo controle (Mann-Whitney U, p = 0,02 para o córtex, p = 0,009 para o hipocampo para TioS e p = 0,009 para o córtex e p=0,04 para o hipocampo para a análise com Vermelho de congo). Barra graduada: 200 pm. A análise de (C-E) Tioflavina S revela uma redução significativa no peso de beta-amiloides (C), no número de placas beta-amiloides (D) e no tamanho médio das placas (E) em camundongos arcAbeta tratados com NI-101.11 em comparação com animais tratados com controle. Estatísticas em Mann-Whitney U: p = 0,02 para córtex da área da placa; p = 0,009 para hipocampo da área da placa; p = 0,047 para córtex de número da placa; p = 0,047 para hipocampo de número da placa; p = 0,009 para córtex de tamanho da placa; p = 0,009 para hipocampo de número da placa.
[00037] Figura 19: A carga reduzida de beta-amiloides é acompanhada por uma diminuição de astrocitose e microgliose: A) A quantificação da marcação para anti-GFAP revelou uma redução significativa no número de astrócitos reativos no córtex de camundongos arcAbeta tratados com NI-101.11, quando comparados com os transgênicos tratados com controle. B) A quantificação da marcação para lba-1 mostrou uma tendência para um número reduzido de microglia ativada em camundongos tratados com Nl- 101.11 no córtex e no hipocampo. Barra graduada: 200pm.
[00038] Figura 20: Não há aumento das micro-hemorragias encefálicas após dois meses de tratamento com anticorpo NI-101.11 humano recombinante. Camundongos de 24 meses de idade arcAbeta com angiopatia amiloide congofílica massiva comprovada foram tratados semanalmente i.p. com 3 mg/kg de anticorpos por dois meses. Imagem representativa de uma micro-hemorragia encefálica em camundongos arcAbeta revelada pela marcação com azul da Prússia (à esquerda). A análise quantitativa demonstra uma frequência significativamente elevada de micro-hemorragias em camundongos transgênicos arcAbeta em comparação com filhotes selvagens. O tratamento crônico com NI-101.11 não resultou em aumento da frequência de micro-hemorragias. Barra graduada: 20pm
[00039] Figura 21: O anticorpo NI-101.11 humano recombinante inibe a formação de fibrilas Abeta sintéticas in vitro.O efeito do anticorpo Nl- 101.11 humano recombinante na formação das fibrilas Abeta foi testado pela medição da Tioflavina S ligada ao Abeta agregado pela análise por fluorescência.
[00040] Figura 22: Fagocitose dependente de dosagem mediada por anticorpos das fibrilas de FITC-Abeta1-42 pelas células microgliais BV- 2 foi medida quando da inibição do sistema receptor "scavenger". O NI-101.11 desencadeia fagocitose mediada por receptor Fc gama dependente de dosagem potente de fibrilas Abeta.
[00041] Deve ser observado que o termo "um" ou "uma" entidade refere-se a uma ou mais daquela entidade; por exemplo, "um anticorpo", representa um ou mais anticorpos. Como tal, os termos "um" (ou "uma"), "um ou mais"e "pelo menos um" podem ser usados permutavelmente aqui.
[00042] Conforme utilizado aqui, o termo "polipeptídeo"destina-se a abranger um "polipeptídeo” singular, como também o plural “polipeptídeos” e refere-se a uma molécula composta de monômeros (aminoácidos) linearmente ligada por ligações amida (também conhecidos como ligações peptídicas). O termo "polipeptídeo"refere- se a qualquer cadeia ou cadeias de dois ou mais aminoácidos e não se refere a um comprimento específico do produto. Assim, os peptídeos, dipeptídeos, tripeptídeos, oligopeptídeos, "proteína", "cadeia de aminoácidos" ou qualquer outro termo utilizado para referência a uma cadeia ou cadeias de dois ou mais aminoácidos, são incluídos na definição de "polipeptídeo" e o termo "polipeptídeo" pode ser usado em vez de ou permutavelmente com qualquer um destes termos.
[00043] O termo "polipeptídeo"destina-se igualmente a fazer referência a produtos de modificações pós-expressão do polipeptídeo, incluindo, entre outros, a glicosilação, acetilação, fosforilação, amidação, derivação através de grupos de proteção/bloqueio conhecidos, clivagem proteolítica ou modificação por aminoácidos não-naturalmente ocorrentes. Um polipeptídeo pode ser derivado de uma fonte biológica natural ou produzido por tecnologia recombinante, mas não é necessariamente traduzido a partir de uma sequência de ácido nucleico designada. Ele pode ser gerado de qualquer forma, inclusive por síntese química.
[00044] Um polipeptídeo da invenção pode ser de um tamanho de cerca de 3 ou mais, 5 ou mais, 10 ou mais, 20 ou mais, 25 ou mais, 50 ou mais, 75 ou mais, 100 ou mais, 200 ou mais, 500 ou mais, 1.000 ou mais ou 2.000 ou mais aminoácidos. Os polipeptídeos podem ter uma estrutura tridimensional definida, embora não necessariamente tenham essa estrutura. Os polipeptídeos com uma estrutura tridimensional definida são referidos como dobrados, e os polipeptídeos que não possuem uma estrutura tridimensional definida, mas podem adotar um grande número de diferentes conformações, são referidos como desdobrados. Conforme utilizado aqui, o termo glicoproteína refere-se a uma proteína acoplada a, pelo menos, uma porção de carboidrato que é anexada à proteína através de uma cadeia lateral contendo oxigênio ou contendo nitrogênio de um resíduo de aminoácido, por exemplo, um resíduo de serina ou um resíduo de asparagina.
[00045] Um polipeptídeo "isolado” ou um fragmento, variante ou derivado seu, significa um polipeptídeo que não se encontra em seu meio natural. Nenhum nível particular de purificação é exigido. Por exemplo, um polipeptídeo isolado pode ser removido de seu ambiente natural ou nativo. Polipeptídeos e proteínas recombinantemente produzidos expressos em células hospedeiras são considerados isolados para fins da invenção, visto que são polipeptídeos nativos ou recombinantes que foram separados, fracionados ou substancialmente ou parcialmente purificados por qualquer técnica adequada.
[00046] Também incluídos como polipeptídeos da presente invenção estão os fragmentos, derivados, análogos ou variantes dos polipeptídeos precedentes e qualquer combinação destes. Os termos "fragmento", "variante", "derivativo" e "análogo", quando se referem a anticorpos ou polipeptídeos de anticorpos da presente invenção, incluem quaisquer polipeptídeos que retêm pelo menos algumas das propriedades de ligação a antígenos da molécula de ligação nativa, anticorpo ou polipeptídeo correspondentes. Fragmentos de polipeptídeos da presente invenção incluem fragmentos proteolíticos, bem como fragmentos de supressão, além de fragmentos de anticorpos específicos discutidos em outro lugar aqui. As variantes de anticorpos e polipeptídeos de anticorpos da presente invenção incluem fragmentos, como descritos acima, e também polipeptídeos com sequências de aminoácidos alteradas devido a substituições, supressões ou inserções. Variantes que podem ocorrer naturalmente ou não-naturalmente. As variantes que não ocorrem naturalmente podem ser produzidas utilizando as técnicas de mutagênese conhecidas na técnica. Polipeptídeos variantes podem compreender substituições, supressões ou inserções de aminoácidos conservadores e não-conservadores. Derivados de moléculas de ligação específica de neoepítopo, por exemplo, anticorpos e polipeptídeos de anticorpos da presente invenção, são polipeptídeos que foram alterados de modo a exibir características adicionais não encontradas no polipeptídeo nativo. Exemplos incluem proteínas de fusão. Os polipeptídeos variantes também podem ser aqui referidos como "análogos de polipeptídeos". Conforme utilizado aqui, um "derivado" de uma molécula ou fragmento de ligação, um anticorpo ou um polipeptídeo de anticorpo se refere a um polipeptídeo de sujeito contendo um ou mais resíduos quimicamente derivados pela reação de um grupo lateral funcional. Também incluídos como "derivados" são os peptídeos que contêm um ou mais derivados de aminoácidos de ocorrência natural dentre os vinte aminoácidos-padrão. Por exemplo, a 4-hidroxiprolina pode ser substituída por prolina; 5-hidroxilisina pode ser substituída por lisina; 3-metil-histidina pode ser usada em lugar da histidina; homesserina pode ser substituída por serina; ornitina pode ser substituída por lisina.
[00047] O termo "polinucleotídeo"destina-se a abranger um ácido nucleico singular, bem como ácidos nucleicos plurais, e refere-se a uma molécula de ácido nucleico isolada ou construtora, por exemplo, RNA mensageiro (mRNA) ou DNA de plasmídeo (pDNA). Um polinucleotídeo pode incluir uma ligação fosfodiéster convencional ou uma ligação não-convencional (por exemplo, uma ligação de amidas, tais como encontradas nos ácidos nucleicos de peptídeos (PNA)). O termo "ácido nucleico" refere-se a qualquer um ou mais segmentos de ácido nucleico, por exemplo, fragmentos de DNA ou RNA, presentes em um polinucleotídeo. Ácido nucleico ou polinucleotídeo "isolado” significa uma molécula de ácido nucleico, DNA ou RNA, que foi removida de seu ambiente nativo. Por exemplo, um polinucleotídeo recombinante codificando um anticorpo contido em um vetor é considerado isolado para efeitos da presente invenção. Outros exemplos de um polinucleotídeo isolado incluem polinucleotídeos recombinantes mantidos em células hospedeiras heterólogas ou polinucleotídeos (parcial ou substancialmente) purificados em solução. Moléculas de RNA isoladas incluem transcrições de RNA in vivo ou in vitrode polinucleotídeos da presente invenção. Polinucleotídeos ou ácidos nucleicos isolados, de acordo com a presente invenção, além disso, incluem tais moléculas produzidas sinteticamente. Além disso, o polinucleotídeo ou o ácido nucleico pode ser ou pode incluir um elemento regulador, como promotor, sítio de ligação de ribossomos ou um terminador de transcrição.
[00048] Conforme utilizado aqui, uma "região de codificação" é uma porção de ácido nucleico, que consiste em códons traduzidos em aminoácidos. Embora um "códon de parada"(TAG, TGA ou TAA) não seja traduzido em um aminoácido, este pode ser considerado como parte de uma região codificadora, mas quaisquer sequências flanqueadora ("flanking sequence"), por exemplo, promotores, sítios de ligação de ribossomos, terminadores transcricionais, íntron e similares, não fazem parte de uma região codificadora. Duas ou mais regiões codificadores da presente invenção podem estar presentes em um único constructo de polinucleotídeos, por exemplo, em um único vetor ou constructos de polinucleotídeos separados, por exemplo, em vetores (diferentes) separados. Além disso, qualquer vetor pode conter uma única região codificadora ou pode incluir duas ou mais regiões codificadoras, por exemplo, um único vetor pode codificar separadamente uma região variável de cadeia pesada de imunoglobulinas e uma região variável de cadeia leve de imunoglobulina. Além disso, um vetor, polinucleotídeo ou ácido nucleico da invenção podem codificar regiões de codificação heterólogas, quer fundidas ou não fundidas a um ácido nucleico que codifica uma molécula de ligação, um anticorpo ou fragmento, variante ou seu derivado. Regiões codificadoras heterólogas incluem, sem limitação, elementos ou motivos especializados, tais como peptídeo de sinal secretor ou um domínio funcional hetérólogo.
[00049] Em certas modalidades, o polinucleotídeo ou ácido nucleico é o DNA. No caso do DNA, uma polinucleotídeo compreendendo um ácido nucleico que codifica um polipeptídeo normalmente pode incluir um promotor e/ou outros elementos de transcrição ou tradução operavelmente associados a uma ou mais regiões codificadoras. Uma associação operável se dá quando uma região codificadora de um produto de gene, por exemplo, um polipeptídeo, é associado a uma ou mais sequências reguladoras de tal modo que coloque a expressão do produto do gene sob a influência ou o controle da(s) sequência(s) reguladora(s). Dois fragmentos de DNA (como uma região codificadora de polipeptídeo e um promotor associado) são "operavelmente associados" se a indução da função do promotor resultar na transcrição do mRNA que codifica o produto do gene desejado e se a natureza da ligação entre os dois fragmentos de DNA não interfere com a capacidade das sequências reguladoras de expressão de direcionar a expressão do produto do gene ou interfere com a capacidade do modelo de DNA ser transcrito. Assim, a região do promotor seria operavelmente associada com um ácido nucleico codificando um polipeptídeo se o promotor for capaz de efetuar a transcrição daquele ácido nucleico. O promotor pode ser um promotor de célula específica que direciona a transcrição substancial do DNA apenas em células predeterminadas. Outros elementos de controle de transcrição, além de um promotor, por exemplo, os potencializadores, operadores, repressores e sinais de término de transcrição, podem ser operavelmente associados com o polinucleotídeo para direcionar a transcrição específica das células. Promotores adequados e outras regiões de controle de transcrição são descritos aqui.
[00050] Uma variedade de regiões de controle de transcrição é conhecida daqueles versados na técnica. Estas incluem, entre outras, regiões de controle de transcrição que funcionam em células de vertebrados, tais como, mas não limitados a, segmentos promotores e intensificadores de citomegalovírus (o promotor antecipado imediato, em conjunto com íntron-A), vírus símio 40 (o promotor antecipado) e retrovirus (como vírus Rous sarcoma). Outras regiões de controle de transcrição incluem aquelas derivadas de genes de vertebrados tais como actinia, proteína de choque térmico, vertebrados, como a actinia, proteínas de choque térmico, hormônio de crescimento bovino e B- globina de coelhos, como também outras sequências capazes de controlar a expressão dos genes em células eucarióticas. Outras regiões de controle de transcrição adequadas incluem promotores específicos de tecidos e potencializadores, como também promotores induzíveis de linfocina (por exemplo, promotores induzíveis por interferons ou interleucinas).
[00051] Da mesma forma, uma variedade de elementos de controle de tradução é conhecida por aqueles versados na técnica. Estes incluem, mas não estão limitados a, sítios de ligação de ribossomos, códons de iniciação e término de tradução e elementos derivados de picornavírus (especialmente um sítio de entrada de ribossomo interno, ou IRES, também referido como uma sequência CITE).
[00052] Em outras modalidades, um polinucleotídeo da presente invenção é o RNA, por exemplo, sob a forma de RNA mensageiro (MRNA).
[00053] As regiões codificadoras de polinucleotídeos e ácidos nucleicos da presente invenção podem estar associadas a outras regiões codificadoras que codificam peptídeos secretores e de sinalização, que direcionam a secreção de um polipeptídio codificado por um polinucleotídeo da presente invenção. De acordo com a hipótese de sinal, as proteínas secretadas pelas células mamíferas têm uma sequência de peptídeo ou de líder secretor de sinal que é clivada da proteína madura, uma vez que a exportação da crescente cadeia de proteínas através do retículo endoplásmico grosso tiver sido iniciada. Aqueles versados na técnica têm conhecimento que os polipeptídeos secretados pelas células de vertebrados geralmente têm um peptídeo de sinal fundido não N-terminal do polipeptídeo, que é clivado do polipeptídeo completo ou de “comprimento total” para produzir uma forma secretada ou “madura” do polipeptídeo. Em certas modalidades, o peptídeo de sinal nativo, por exemplo, um peptídeo de sinal de cadeia pesada de imunoglobulina ou de cadeia leve é usado ou um derivado funcional dessa sequência que retém a capacidade de direcionar a secreção do polipeptídeo que é operavelmente associado com este. Alternativamente, um peptídeo de sinal mamífero heterólogo ou derivado seu, pode ser usado. Por exemplo, a sequência líder do tipo selvagem pode ser substituída pela sequência líder do ativador de plasminogênio de tecido humano (TPA) ou de B-glucuronidase de camundongos.
[00054] Salvo disposição em contrário, os termos "distúrbio" e "doença" são utilizados alternadamente aqui. Uma "molécula de ligação", conforme utilizada no contexto da presente invenção relaciona-se principalmente a anticorpos e seus fragmentos, mas também pode referir-se a outras moléculas não de anticorpos que se ligam a um neoepítopo, incluindo, entre outros, hormônios, receptores, ligantes, grandes moléculas (MHC) do complexo de histocompatibilidade, acompanhantes tais como proteínas de choque térmico (HPSs), bem como moléculas de aderência célula-célula tais como membros da super família (lg) da caderina, intergrina, lecitina do tipo C e imunoglobulina. Assim, por uma questão de clareza e sem restringir o âmbito da presente invenção, a maioria das modalidades seguintes é discutida com relação aos anticorpos e moléculas similares a anticorpos que representam as moléculas de ligação preferidas para o desenvolvimento de agentes terapêuticos e diagnósticos.
[00055] Os termos "anticorpos" e "imunoglobulina" são utilizados alternadamente aqui. Um anticorpo ou imunoglobulina é uma molécula de ligação a antígeno que inclui pelo menos o domínio variável de uma cadeia pesada e, normalmente, compreende, pelo menos, os domínios variáveis de uma cadeia pesada e uma cadeia leve. As estruturas de imunoglobulinas básicas em sistemas de vertebrados sistemas são relativamente bem compreendidas. Vide, por exemplo, Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988).
[00056] Conforme será discutido em maior detalhe abaixo, o termo “imunoglobulina” compreende várias classes amplas de polipeptídeos que podem ser distinguidos bioquimicamente. Aqueles versados na técnica observarão que as cadeias pesadas são classificadas como gama, mu, alfa, delta ou épsilon, (y, p, (, (, () com algumas subclasses entre eles (por exemplo, (y1-y4). É característica desta cadeia determinar a “classe” do anticorpo como IgG, IgM, IgA IgG ou IgE, respectivamente. As subclasses de imunoglobulina (isotipos), por exemplo, lgG1, lgG2, lgG3, lgG4, lgA1, etc. são bem caracterizadas e são conhecidas por conferir especialização funcional. Versões modificadas de dada dessas classes e isotipos são prontamente discerníveis àqueles versados na técnica em vista da descrição presente e, consequentemente, estão dentro do âmbito da presente invenção. Todas as classes de imunoglobulinas estão claramente dentro do âmbito da presente invenção, a discussão seguinte será geralmente dirigida à classe IgG das moléculas de imunoglobulina. Com relação à IgG, uma molécula de imunogobulina-padrão compreende dois polipeptídeos de cadeia leve idênticos de peso molecular de aproximadamente 23.000 Dáltons e dois polipeptídeos de cadeia pesada idênticos de peso molecular de 53.000-7000. As quatro cadeias são normalmente unidas pelas ligações dissulfeto em uma configuração em “Y” na qual as cadeias leves envolvem as cadeias pesadas iniciando na abertura do "Y" e continuando através da região variável.
[00057] Cadeias leves são classificadas como kappa ou lambda (K, X). Cada classe de cadeia pesada pode estar ligada com uma cadeia leve kappa ou lambda. Em geral, as cadeias leves e pesadas estão covalentemente ligadas umas às outras e as porções da "cauda" das duas cadeias pesadas estão ligadas entre si por ligações covalentes dissulfeto ou ligações não covalentes quando as imunoglobulinas são geradas quer por hibridomas, células B ou células hospedeiras projetadas geneticamente. Na cadeia pesada, as sequências de aminoácidos percorrem a partir do N-terminal nas terminações bifurcadas da configuração em U até o C-terminal na base de cada cadeia.
[00058] Tanto as cadeias leves e pesadas são divididas em regiões de homologia estrutural e funcional. Os termos "constante" e "variável" são utilizados funcionalmente. Neste contexto, será observado que os domínios variáveis tanto das porções de cadeia leve (VL) e pesada (VH) determinam o reconhecimento e a especificidade do antígeno. Inversamente, os domínios constantes da cadeia leve (CL) e de cadeia pesada (CH1, CH2 ou CH3) conferem importantes propriedades biológicas tais como a secreção, mobilidade transplacentária, ligação do receptor Fc, ligação complementar e similar. Por convenção, a numeração dos domínios das regiões constantes aumenta à medida que se tornam mais distantes do sítio de ligação do antígeno ou da terminação amino do anticorpo. A porção do N-terminal é uma região variável e na porção do C-terminal é uma região constante; os domínios CH3 e CL realmente compreendem o terminal carbóxi da cadeia pesada e leve, respectivamente.
[00059] Conforme indicado acima, a região variável permite que o anticorpo seletivamente reconheça e especificamente ligue epitopos sobre antígenos. Isto é, o domínio VL e o domínio VH ou subgrupo de regiões determinantes da complementaridade (CDRs), de um anticorpo se combinam para formar a região variável que define um sítio tridimensional de ligação aos antígenos. Esta estrutura de anticorpos quaternária forma o sítio de ligação aos antígenos presentes no final de cada braço do Y. Mais especificamente, o sítio de ligação aos antígenos é definido por três CDRs em cada uma das cadeias VH e VL. Qualquer anticorpo ou fragmento de imunoglobulina que contém estrutura suficiente para especificamente se ligar a um antígeno é denotado aqui permutavelmente como um "fragmento de ligação a antígenos" ou um "fragmento imunoespecífico".
[00060] Em anticorpos ocorrendo naturalmente, as seis "regiões determinantes de complementaridade" ou "CDRs" presentes em cada domínio de ligação a antígeno são sequências curtas, não contíguas de aminoácidos que são especificamente posicionados para formar o domínio de ligação a antígeno já que o anticorpo assume a sua configuração tridimensional em um ambiente aquoso. O restante dos aminoácidos nos domínios de ligação dos antígenos, referidos como regiões de "estrutura", mostram menor variabilidade intermolecular. As regiões de estrutura de trabalho adotam uma conformação de folha-p e as CDRs formam alças que ligam a estrutura em folha-p e, em alguns casos, formam parte dela. Assim, regiões de estrutura atuam de modo a formar um andaime que propicia o posicionamento das CDRs na correta orientação através de interações intercadeias, não covalentes. O domínio de ligação dos antígenos formado pelas CDRs posicionadas define uma superfície complementar ao epitopo no antígeno imunorreativo. Esta superfície complementar promove a ligação não-covalente do anticorpo ao seu epitopo cognato. Os aminoácidos compreendendo as CDRs e as regiões de estrutura, respectivamente, podem ser facilmente identificados por qualquer região dada variável de cadeia pesada ou leve por alguém ordinariamente versado na técnica, desde que tenham sido definidos com precisão (Vide "Sequences of Proteins of Immunological Interest", Kabat, E., et al., E.U. Department of Health and Human Services, (1983); e Chothia and Lesk, J. Mol. BioL, 196:901-917 (1987), que são incorporados neste documento por referência em sua totalidade).
[00061] No caso de haver duas ou mais definições de um termo que é utilizado e/ou aceito na técnica, a definição do termo, tal como é utilizada neste documento destina-se a incluir todos esses significados a menos que explicitamente afirmado o contrário. Um exemplo específico é a utilização do termo "região determinante de complementaridade" ("CDR") para descrever os sítios combinantes de antígenos não-contíguos dentro da região variável de polipeptídeos de cadeia leve e pesada. Esta região em particular foi descrita por Kabat et al., E.U. Dept, of Health and Human Services, "Sequences of Proteins of Immunological Interest" (1983) e por Chothia et al., J. Mol. Biol. 196:901-917 (1987), que são incorporados por referência neste documento, em que as definições incluem sobreposição ou subconjuntos de resíduos de aminoácidos quando comparados uns com os outros. No entanto, a aplicação de qualquer uma das duas definições para se referir a uma CDR de um anticorpo ou suas variantes, destina-se a estar dentro do âmbito do termo conforme definido e usado aqui. Os resíduos de aminoácidos apropriados que abrangem as CDRs, tal como definido por cada uma das referências acima citadas estão apresentados na Tabela I abaixo como comparação. Os números exatos dos resíduos que abrangem uma determinada CDR irão variar dependendo da sequência e tamanho do CDR. Aqueles versados na técnica poderão rotineiramente determinar quais resíduos compreendem uma CDR especial, dada a sequência de aminoácidos da região variável do anticorpo.
[00062] 1 A numeração de todas as definições de CDRs na Tabela 1 está de acordo com as convenções de numeração apresentadas por Kabat et al. (vide abaixo).
[00063] Kabat et al. também definiram um sistema de numeração para as sequências de domínios variáveis que é aplicável a qualquer anticorpo. Alguém com habilidade ordinária na técnica designa este sistema de “numeração de Kabat” a qualquer sequência de domínio variável, sem dependência de quaisquer dados experimentais além da sequência em si. Conforme utilizado aqui, a "numeração de Kabat" refere-se ao sistema de numeração estabelecidos por Kabat et al., E.U. Dept, of Health and Human Services, "Sequence of Proteins of Immunological Interest" (1983). Salvo disposição em contrário, as referências à numeração das posições de resíduos de aminoácidos específicos em um anticorpo ou fragmento de ligação ao antígeno, variante ou seu derivado da presente invenção estão de acordo com o sistema de numeração de Kabat.
[00064] Anticorpos ou fragmentos de ligação aos antígenos, fragmentos imunoespecíficos, variantes ou seus derivados da invenção incluem, entre outros, anticorpos policlonais, monoclonais, multi específicos, humanos, humanizados, primatizados ou anticorpos quiméricos, anticorpos de cadeia única, fragmentos de ligação aos epitopos, por exemplo, Fab, Fab'e F(ab')2, Fd, Fvs, Fvs de cadeia única (scFv), anticorpos de cadeia única, Fvs ligados aos bissulfetos (sdFv), fragmentos compreendendo quer um domínio VL ou VH, fragmentos produzidos por uma biblioteca de expressões de Fab e anticorpos antiidiotípicos (anti-ld), (incluindo, por exemplo, anticorpos anti-ld para os anticorpos descritos aqui). As moléculas ScFv são conhecidas na técnica e são descritas, por exemplo, na patente U.S. N°. 5.892.019. A imunoglobulina ou as moléculas de anticorpos da invenção podem ser de qualquer tipo (por exemplo, IgG, IgE, IgM, IGD, IgA e IgY), classe (por exemplo, lgG1, lgG2, lgG3, lgG4, lgA1 e lgA2) ou subclasse de molécula de imunoglobulina.
[00065] Em uma modalidade, o anticorpo da presente invenção não é IgM ou um de seus derivados com uma estrutura pentavalente. Particulares, em aplicações específicas da presente invenção, especialmente no uso terapêutico, os IgMs são menos úteis do que o IgG e outros anticorpos bivalentes ou moléculas de ligação correspondentes visto que os IgMs, devido à sua estrutura pentavalente e a falta de maturação da afinidade apresentam frequentemente reatividades cruzadas inespecíficas e com afinidade muito baixa.Fragmentos de anticorpos, incluindo anticorpos de cadeia única, podem compreender região(ões) variável(eis) separadamente ou em combinação com a totalidade ou uma parte do seguinte: região de dobradiça (hinge) e domínios CH1, CH2 e CH3. Também incluídos na invenção estão os fragmentos de ligação ao antígeno também compreendendo qualquer combinação de região(ões) variável(eis) com uma região de dobradiça e domínios CH1, CH2 e CH3. Anticorpos ou seus fragmentos imunoespecíficos da presente invenção podem ser de origem de qualquer animal incluindo aves e mamíferos. Preferivelmente, os anticorpos são humanos, murinos, asininos, de coelho, cabra, porco da Guiné, camelo, lhama, cavalo ou galinha. Em outra modalidade, a região variável pode ser condrictioide em sua origem (por exemplo, de tubarões). Conforme usado aqui, os anticorpos “humanos” incluem anticorpos contendo sequência de aminoácidos de uma imunoglobulina humana e incluem anticorpos isolados de pacientes humanos, conjuntos de imunoglobulina humana ou de animais transgênicos para uma ou mais imunoglobulinas e que não expressam imunoglobulinas endógenas, conforme descrito abaixo e, por exemplo, na Patente U.S. N°. 5.939.598 de Kucherlapati et al. Um anticorpo humano é ainda “humano” mesmo se as substituições de aminoácidos forem feitas no anticorpo, por exemplo, para melhorar as características de ligação.
[00067] Conforme usado aqui, o termo “parte de cadeia pesada” inclui sequências de aminoácidos derivadas de uma cadeia pesada de imunoglobulina. Um polipeptídeo compreendendo uma parte de cadeia pesada compreende pelo menos um dos seguintes: um domínio CH1, um domínio de dobradiça (por exemplo, região de dobradiça superior, mediana e/ou inferior), um domínio CH2, um domínio CH3 ou uma variante ou seu fragmento. Por exemplo, um polipeptídeo de ligação para uso na invenção pode compreender uma cadeia de polipeptídeos compreendendo um domínio CH1; uma cadeia de polipeptídeos compreendendo um domínio CH1 e pelo menos uma parte de um domínio de dobradiça e um domínio CH2; uma cadeia de polipeptídeos compreendendo um domínio CH1 e um domínio CH3; uma cadeia de polipeptídeos compreendendo um domínio CH1, pelo menos uma parte de um domínio de dobradiça e um domínio CH3 ou uma cadeia de polipeptídeos compreendendo um domínio CH1, pelo menos uma parte de um domínio de dobradiça, um domínio CH2 e um domínio CH3. Em outra modalidade, um polipeptídeo da invenção compreende uma cadeia de polipeptídeos compreendendo um domínio CH3. Além disso, um polipeptídeo de ligação para uso na invenção pode ser desprovido de pelo menos uma parte de um domínio CH2 (por exemplo, todo ou parte de um domínio CH2). Conforme estabelecido acima, será compreendido por alguém com habilidade ordinária na técnica que esses domínios (por exemplo, partes de cadeia pesada) podem ser modificados de tal modo que eles variem na sequência de aminoácidos a partir da molécula de imunoglobulina ocorrente naturalmente.
[00068] Em certos anticorpos ou fragmentos de ligação ao antígeno, variantes ou seus derivados descritos aqui, as partes de cadeia pesada de uma cadeia de polipeptídeo de um multímero são idênticas àquelas em uma segunda cadeia de polipeptídeos do multímero. Alternativamente, os monômeros contendo a parte de cadeia pesada da invenção não são idênticos. Por exemplo, cada monômero pode incluir um sítio de ligação a alvos diferentes, formando, por exemplo, um anticorpo biespecífico.
[00069] As partes de cadeia pesada de um polipeptídeo de ligação para utilização nos métodos de diagnóstico e tratamento descritos neste documento podem ser derivadas de moléculas de imunoglobulinas diferentes. Por exemplo, uma parte da cadeia pesada de um polipeptídeo pode incluir um domínio de CH1 derivado de uma molécula de lgG1 e de uma região de dobradiça derivada de uma molécula de lgG3. Em outro exemplo, uma parte de cadeia pesada pode incluir uma região de dobradiça derivada, em parte, de uma molécula de lgG1, e, em parte, de uma molécula de lgG3. Em outro exemplo, uma parte de cadeia pesada pode incluir uma região de dobradiça derivada, em parte, de uma molécula lgG1 e, em parte, de uma molécula lgG3. Em outro exemplo, uma parte de cadeia pesada pode incluir uma região de dobradiça quimérica derivada, em parte, de uma molécula lgG1 e, em parte, de uma molécula lgG4.
[00070] Conforme utilizado aqui, o termo "parte de cadeia leve" inclui sequências de aminoácidos provenientes de uma cadeia leve de imunoglobulina. Preferencialmente, a parte de cadeia leve inclui pelo menos um domínio de VL ou CL.
[00071] Considera-se que o tamanho mínimo de um epitopo de peptídeo ou polipeptídeo seja de cerca de quatro a cinco aminoácidos. Os epitopos de peptídeos ou polipeptídeos contêm pelo menos sete, mais preferivelmente pelo menos nove e mais preferivelmente entre pelo menos cerca de 15 a cerca de 30 aminoácidos. Uma vez que um CDR pode reconhecer um peptídeo ou polipeptídeo antigênico na sua forma terciária, os aminoácidos compreendendo um epitopo não precisam estar contíguos e, em alguns casos, podem mesmo não estar na mesma cadeia de peptídeos. Na presente invenção, o epitopo de peptídeo ou polipeptídeo reconhecido por anticorpos da presente invenção contém uma sequência de pelo menos 4, pelo menos 5, pelo menos 6, pelo menos 7, mais preferivelmente, pelo menos 8, pelo menos 9, pelo menos 10, pelo menos 15, pelo menos 20, pelo menos 25 ou entre cerca de 15 a cerca de 30 aminoácidos A3 contíguos ou não-contíguos.
[00072] O termo "neoepítopo", em conformidade com a presente invenção denota um epitopo que é único para o padrão de uma doença e contido em ou formado por uma proteína associada à distúrbio, que é uma variante patológica de uma de uma proteína diferentemente não patológica e/ou em desvio da fisiologia do estado saudável. As ditas variantes patofisiológicas podem ser formadas por meio de transcrição patologicamente alterada, tradução patologicamente alterada, modificação pós-tradução, processamento proteolítico alterado patologicamente, formação complexa alterada patologicamente com parceiros ou estruturas celulares em interação fisiológica ou patofisiológica no sentido de uma co-localização alterada ou conformação estrutural alterada patologicamente, como, por exemplo agregação, oligomerização ou fibrilação, cuja estrutura tridimensional ou tetradimensional difere da estrutura da molécula fisiologicamente ativa. Além disso, uma variante patofisiológica pode também ser caracterizada, na medida em que não se situe no seu ambiente fisiológico ou compartimento subcelular habituais. Como exemplo, neoepítopos podem estar localizados nas estruturas patologicamente conspícuas nas áreas dos tecidos encefálicos que obviamente experimentam ou já experimentaram danos funcionais. Se uma determinada estrutura, por exemplo, célula ou tecido ou proteína exibindo um neoepítopo, puder ser verificada ou não pela inversão do método descrito a seguir para isolamento e caracterização de uma molécula de ligação específica à proteína associada ao distúrbio na medida em que uma molécula de ligação, por exemplo, um anticorpo identificado pelo dito método usado para rastrear uma espécime para ligação ao dito anticorpo, deste modo determinando a presença de um neoepítopo.
[00073] As expressões "específico de proteína associada à doença"e "específico de neoepítopo” são utilizados alternadamente aqui com o termo "especificamente reconhecendo um neoepítopo". Como aqui usados termos tais como "ausência de reatividade cruzada", "específicos", "especificamente reconhecendo", "especificamente de ligação", "preferencialmente de ligação" e similares referem-se à capacidade da molécula de ligação discriminar entre o neoepítopo de uma proteína associada ao distúrbio e a proteína nativa e da proteína em sua forma e tipo selvagem e no contexto natural. Assim, a molécula de ligação da presente invenção tem uma afinidade de ligação preferencial para o neoepítopo sobre o antígeno da proteína nativa por um fator de, pelo menos, dois, de preferência, pelo menos 5, geralmente mais de um fator de 10, particularmente preferida por um fator de 50 e ainda mais preferida acima de 100. Além disso, a KD relativa da molécula de ligação, por exemplo, o anticorpo para o epitopo alvo específico, por exemplo, o neoepítopo, é preferencialmente pelo menos 10 vezes menos, mais preferencialmente pelo menos 100 vezes menos ou mais do que a KD para ligação daquele anticorpo a outros ligantes ou à contraparte nativa da proteína associada à doença.
[00074] As frases "especificamente liga-se"ou "especificamente reconhece," utilizadas permutavelmente aqui. Significam que uma molécula de ligação, por exemplo, um anticorpo se liga a um epitopo via seu domínio de ligação ao antígeno e que a ligação implica alguma complementaridade entre o domínio de ligação do antígeno e o epitopo. Segundo esta definição, é dito que um anticorpo "liga-se especificamente"a um epitopo quando este se liga a esse epitopo, através do seu domínio de ligação ao antígeno mais prontamente do que este se ligaria a um epitopo aleatório, não relacionado. O termo "especificidade" é aqui utilizado para qualificar a afinidade relativa pela qual certo anticorpo liga-se a certo epitopo. Por exemplo, o anticorpo "A" pode ser considerado como tendo uma maior especificidade para um determinado epitopo do que o anticorpo "B" ou pode ser dito que o anticorpo "A" liga-se ao epitopo "C", com uma maior especificidade do que este tem para o epitopo "D” relacionado.
[00075] A frase "preferencialmente liga-se" significa que a molécula de ligação, por exemplo, o anticorpo especificamente liga-se a um epitopo mais prontamente do que ela se ligaria a um epitopo relacionado, similar, homólogo ou análogo. Assim, um anticorpo que "preferencialmente liga-se" a um determinado epitopo mais provavelmente se ligaria a esse epitopo do que a um epitopo relacionado, embora tal anticorpo possa reagir de forma cruzada com o epitopo relacionado.
[00076] Por meio de exemplo não-limitante, uma molécula de ligação, por exemplo, um anticorpo, pode ser considerado que se liga a um primeiro epitopo, preferencialmente se ligar o dito primeiro epitopo com um constante de dissociação (KD) que é menor do que a KD do anticorpo para o segundo epitopo. Em outro exemplo não- limitante, um anticorpo pode ser considerado que se liga a um primeiro antígeno preferencialmente se ligar o primeiro epitopo com uma afinidade que tenha pelo menos uma ordem de magnitude menor do que a KD do anticorpo para o segundo epitopo. Em outro exemplo não- limitante, um anticorpo pode ser considerado que se liga a um primeiro epitopo preferencialmente se ligar o primeiro epitopo com uma afinidade que tenha pelo menos duas ordens de magnitude menores do que a KD do anticorpo para o segundo epitopo.
[00077] Em outro exemplo não-limitante, uma molécula de ligação, por exemplo, um anticorpo pode ser considerado que liga um primeiro epitopo preferencialmente se ligar ao primeiro epitopo com uma taxa off (k(off)) que seja menor do que a (k(off)) do anticorpo para o segundo epitopo. Em outro exemplo não-limitante, pode-se considerar que um anticorpo ligue um primeiro epitopo preferencialmente se ligar ao primeiro epitopo com uma afinidade que tenha pelo menos uma ordem de magnitude menor do que a k(off) do anticorpo para o segundo epitopo. Em outro exemplo não-limitante, pode-se considerar que um anticorpo ligue um primeiro epitopo preferencialmente se este ligar ao primeiro epitopo com uma afinidade que tenha pelo menos duas ordens de magnitude menores do a k(off) do anticorpo para o segundo epitopo.
[00078] Pode-se dizer que uma molécula de ligação, por exemplo, um anticorpo ou fragmento de ligação ao antígeno, variante, descrita neste documento, aglutine um polipeptídeo alvo aqui ou um fragmento ou variante seu com uma taxa off (k(off)) inferior ou igual a 5 X 10-2 seg-1, 10-2 seg-1, 5 X 10-3 seg1 ou 10-3 seg-1. Mais preferencialmente, pode-se dizer que um anticorpo da invenção ligue um polipeptídeo alvo descrito aqui ou um fragmento ou variante sua, com uma taxa off (k(off)) inferior ou igual a 5 x 10-4 seg1,10-4 seg1, 5 X 10-5 seg1 ou 10-5 seg-1, 5 X 10-6 seg-1, 10-6 seg1, 5 X 10-7 seg1 ou 107 seg1.
[00079] Pode-se dizer que uma molécula de ligação, por exemplo, um anticorpo ou fragmento, variante, derivado de ligação ao antígeno, descrita neste documento, liga um polipeptídeo alvo descrito aqui ou um fragmento ou variante deste com uma taxa on (k(on)), superior ou igual a 103 M-1 seg-1, 5 x 103 M-1 seg1, 104 M-1 seg-1 ou 5 X 104 M-1 seg-1. Mais preferivelmente, pode-se dizer que um anticorpo da invenção ligue um polinucleotídeo alvo descrito aqui ou um fragmento ou variante sua, com uma taxa on (k(on)) igual ou superior a 105 M-1 seg-1, 5 x 105 M-1 seg-1, 106 M-1 seg-1 ou 5 x 106 M-1 seg1 ou 107 M-1 seg-1.
[00080] É dito que uma molécula de ligação, por exemplo, um anticorpo, inibe de forma concorrente a ligação de um anticorpo de referência a um epitopo dado se este preferencial mente se ligar a esse epitopo na medida em que ele bloqueia, em algum grau, a ligação do anticorpo de referência ao epitopo. A inibição competitiva pode ser determinada por qualquer método conhecido na técnica, por exemplo, os ensaios de concorrência ELISA. Pode-se dizer que um anticorpo inibe de forma concorrente a ligação do anticorpo de referência a um determinado epitopo em pelo menos 90%, pelo menos 80%, pelo menos 70%, pelo menos 60% ou, pelo menos, 50%.
[00081] Conforme utilizado aqui, o termo "afinidade"refere-se a uma medida da força da ligação de um epitopo individual à CDR de uma molécula de ligação, por exemplo, uma molécula de imunoglobulina. Vide, por exemplo, Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988) páginas 27-28. Conforme utilizado aqui, o termo "avidez"refere- se à estabilidade geral do complexo entre uma população de imunoglobulinas e um antígeno ou seja, a força de combinação funcional de uma mistura de imunoglobulinas com o antígeno. Vide, por exemplo, Harlow nas páginas 29-34. Avidez está relacionada com a afinidade das moléculas individuais de imunoglobulinas na população com epitopos específicos e também as valências das imunoglobulinas e do antígeno. Por exemplo, a interação entre um anticorpo monoclonal bivalente e um antígeno com uma estrutura de epitopos altamente repetitiva, como um polímero, seria de alta avidez.
[00082] Moléculas de ligação, por exemplo, anticorpos ou fragmentos, variantes ou seus derivados de ligação ao antígeno da invenção também podem ser descritos ou especificados em termos de sua reatividade cruzada. Conforme utilizado aqui, o termo "reatividade cruzada"refere-se à capacidade de um anticorpo, específico para um antígeno, de reagir com um segundo antígeno; uma medida da relação entre duas diferentes substâncias antigênicas. Assim, um anticorpo tem reatividade cruzada se este se liga a um epitopo diferente daquele que induziu sua formação. O epitopo de reatividade cruzada geralmente contém muitas das mesmas características estruturais complementares que o epitopo indutor, e, em alguns casos, pode realmente ser mais adequado do que o original.
[00083] Por exemplo, alguns anticorpos têm algum grau de reatividade cruzada, na medida em que eles ligam epitopos relacionados, mas não idênticos, por exemplo, epitopos com pelo menos 95%, pelo menos 90%, pelo menos 85%, pelo menos 80%, pelo menos 75%, pelo menos 70%, pelo menos 65%, pelo menos 60%, pelo menos 55% e pelo menos 50% de identidade (como calculado por meio de métodos conhecidos na técnica e descritos a seguir) a um epitopo de referência. Pode-se dizer que um anticorpo tem pouca ou nenhuma reatividade cruzada se não ligar epitopos com menos de 95%, menos de 90%, menos de 85%, menos de 80%, menos de 75%, menos de 70%, menos de 65%, menos de 60%, menos de 55% e menos de 50% de identidade (conforme calculado por meio de métodos conhecidos na técnica e descritos a seguir) a um epitopo de referência. Um anticorpo pode ser considerado "muito específico" em relação a um determinado epitopo, se ele não liga qualquer outro análogo, ortológo ou homólogo daquele epitopo.
[00084] Moléculas de ligação, por exemplo, anticorpos ou fragmentos de ligação ao antígeno, variantes ou seus derivados da invenção também podem ser descritas ou especificadas em termos da sua afinidade de ligação a um polipeptídeo da invenção. Afinidades de ligação preferidas incluem aquelas com um constante de dissociação ou Kd inferior a 5 x 10-2 M, W2 M, 5 x 10-3 M, 10-3 M, 5 x 10-4 M, 10-4 M, 5 x 10-5 M, 10-5 M, 5 x 10-6 M, 10-6 M, 5 x W7 M, 10-7 M, 5 x 10-8 M, 10-8 M, 5 x 10-9 M, 10-9 M, 5 x 10-10 M, 10-10 M, 5 x 10-11 M, 10-11 M, 5 x 10-12 M, 10-12 M, 5 x 10-13 M, 10-13 M, 5 x 10-14 M, 10-14 M, 5 x 10-15 M ou 10-15 M,
[00085] Conforme indicado anteriormente, as estruturas das subunidades e a configuração tridimensional regiões dos constantes das várias classes de imunoglobulinas são bem-conhecidas. Conforme utilizado aqui, o termo "domínio VH" inclui o domínio variável terminal de uma cadeia pesada de imunoglobulina e o termo "domínio CH1" inclui o primeiro domínio da região constante (mais amino-terminal) de uma cadeia pesada de imunoglobulina. O domínio CH1 é adjacente ao domínio VH e é amino-terminal para a região dependente de uma molécula de cadeia pesada de imunoglobulina.
[00086] Conforme utilizado aqui o termo "domínio CH2" inclui a parte de uma molécula de cadeia pesada que se estenda, por exemplo, de cerca do resíduo 244 para resíduo de 360 de um anticorpo usando esquemas de numeração convencional (resíduos 244 a 360, sistema de numeração de Kabat e resíduos 231-340, sistema de numeração da UE; vide Kabat EA et al. op. cit. O domínio CH2 é único na medida em que ele não está intimamente ligado a outro domínio. Em vez disso, duas cadeias de carboidratos ramificadas ligadas em N são interpostas entre os dois domínios CH2 de uma molécula de IgG nativa intacta. Também é bem documentado que o domínio CH3 estende-se desde o domínio CH2 até o terminal C da molécula do IgG e inclui cerca de 108 resíduos.
[00087] Conforme utilizado aqui, o termo "região hinge"(região de dobradiça) inclui a parte de uma molécula de cadeia pesada que una o domínio CH1 ao domínio CH2. Esta região de dobradiça compreende aproximadamente 25 resíduos e é flexível, permitindo assim que as duas regiões de ligação ao antígeno do N-terminal movam-se independentemente. As regiões de dobradiças podem ser subdivididas em três domínios distintos: domínios de dobradiça superior, médio e inferior (Roux etal., J. Immunol.761:4083 (1998)).
[00088] Conforme utilizado aqui o termo "ligação dissulfeto" inclui a ligação covalente formada entre dois átomos de enxofre. A cisteína de aminoácido compreende um grupo tiol que pode formar uma ponte ou ligação dissulfeto com um segundo grupo tiol. Na maioria das moléculas de IgG que ocorrem naturalmente, as regiões CH1 e CL estão ligadas por uma ligação dissulfeto e as duas cadeias pesadas estão ligados por duas ligações dissulfeto nas posições correspondentes a 239 e 242 usando o sistema de numeração de Kabat (posição 226 ou 229, sistema de numeração da UE).
[00089] Conforme utilizado aqui, o termo "anticorpo projetado" refere-se a um anticorpo no qual o domínio variável na cadeia pesada e leve ou em ambas é alterado pelo menos pela substituição parcial de uma ou mais CDRs de um anticorpo de especificidade conhecida e, se necessário, pela substituição parcial da região de estrutura e pela mudança de sequência. Embora as CDRs possam ser derivadas de um anticorpo da mesma classe ou mesma subclasse que o anticorpo do qual as regiões de estrutura são derivadas, é previsto que as CDRs serão derivadas de um anticorpo de classe diferente e, de preferência, de um anticorpo de uma espécie diferente. Um anticorpo projetado em que uma ou mais CDRs “doadoras” de um anticorpo não humano de especificidade conhecida é enxertado em uma região de estrutura de cadeia pesada ou leve humana é aqui referido como "um anticorpo humanizado". Pode não ser necessário substituir todas as CDRs pelas CDRs completas a partir da região variável doadora para transferir a capacidade de ligação do antígeno de um domínio variável para outro. Pelo contrário, pode ser necessário somente transferir os resíduos que são necessários para manter a atividade do sítio de ligação alvo. Dadas as explicações apresentadas em, por exemplo nas patentes do EUA de N° 5.585.089, 5.693.761, 5.693.762 e 6.180.370, estará bem enquadrado na competência daqueles versados na técnica, quer pela realização da experimentação rotineira ou por teste de tentativa e erro para obter um anticorpo funcional projetado ou humanizado.
[00090] Conforme utilizado aqui, o termo "polipeptídeo devidamente dobrado” inclui polipeptídeos nos quais todos os domínios funcionais compreendendo o polipeptídeo são distintamente ativos. Conforme utilizado aqui, o termo "polipeptídeo indevidamente dobrado” inclui polipeptídeo nos quais pelo menos um dos domínios funcionais do polipeptídeo não é ativo. Em uma modalidade, um polipeptídeo devidamente dobrado compreende cadeias de polipeptídeos ligadas por pelo menos uma ligação dissulfeto e, inversamente, um polipeptídeo dobrado indevidamente compreende cadeias de polipeptídeos não ligadas por pelo menos uma ligação dissulfeto.
[00091] Conforme utilizado aqui, o termo "projetado" inclui a manipulação de moléculas de ácido nucleico ou de polipeptídeos por meios sintéticos (por exemplo, por técnicas recombinantes, síntese de peptídeo in vitro,por acoplamento enzimático ou químico de peptídeos ou alguma combinação destas técnicas).
[00092] Conforme utilizado aqui, os termos "ligado", "fundido" ou "fusão" são utilizados alternadamente. Estes termos referem-se à junção de mais dois elementos ou componentes, seja por que meio for, incluindo conjugação química ou meio recombinante. Uma "fusão em estrutura"refere-se à junção de duas ou mais estruturas de leitura abertas de polinucleotídeos (ORFs) para formar uma ORF maior contínua, de forma que se mantenha a estrutura de leitura de tradução correta das ORFs originais. Assim, uma proteína de fusão recombinante é uma proteína única contendo dois ou mais segmentos que correspondem a polipeptídeos codificados pelas ORFs originais (cujos segmentos não são normalmente unidos desta forma por natureza). Embora a estrutura de leitura quadro seja, portanto, contínua ao longo dos segmentos fundidos, os segmentos podem ser fisicamente ou espacialmente separados, por exemplo, sequência de ligadores na estrutura. Por exemplo, os polinucleotídeos que codificam as CDRs de uma região variável de imunoglobulina podem ser fundidos, na estrutura, mas podem ser separados por um polinucleotídeo que codifica pelo menos uma região de estrutura de imunoglobulinas ou regiões de CDRs adicionais, contanto que as CDRs “fundidas” sejam co-traduzidas como parte de um polipeptídeo contínuo.
[00093] No contexto de polipeptídeos, uma "sequência linear" ou uma "sequência" é uma ordem de aminoácidos em um polipeptídeo em uma direção terminal de amino para carboxila na qual os resíduos que estão próximos uns dos outros na sequência são contíguos na estrutura primária do polipeptídeo.
[00094] O termo "expressão", conforme utilizado neste documento refere-se a um processo pelo qual um gene produz um bioquímico, por exemplo, um RNA ou polipeptídeo. O processo inclui qualquer manifestação da presença funcional do gene dentro da célula, incluindo, entre outros, redução de genes, como também a expressão temporária e a expressão estável. Esta inclui, entre outros, a transcrição do gene em RNA mensageiro (mRNA), RNA de transferência (tRNA), RNA na forma de um pequeno grampo de cabelo (shRNA), RNA pequeno de interferência (siRNA) ou qualquer outro produto de RNA e a tradução desse mRNA em polipeptídeo(s). Se o produto final pretendido for um bioquímico, a expressão inclui a criação desse bioquímico e quaisquer bioquímicos precursores. A expressão de um gene produz um "produto de gene". Conforme utilizado aqui, um produto de gene pode ser um ácido nucleico, por exemplo, um RNA mensageiro produzido pela transcrição de um gene ou um polipeptídeo, que é traduzido de uma transcrição. Os produtos de genes descritos neste documento, além disso, incluem ácidos nucleicos com modificações pós-transcricionais, por exemplo, poliadenilação ou polipeptídeos com modificações pós-tradução, por exemplo, metilação, glicosilação, adição de lipídios, associação com outras subunidades de proteínas, clivagem proteolítica e similares.
[00095] Conforme utilizado aqui, os termos "tratar" ou "tratamento"referem-se tanto a um tratamento terapêutico e a medidas profiláticas ou preventivas, onde o objetivo é prevenir ou desacelerar (diminuir) uma alteração ou distúrbio fisiológico indesejado, tal como o desenvolvimento ou a propagação do câncer. Resultados clínicos benéficos ou desejados incluem, entre outros, alívio dos sintomas, diminuição da extensão da doença, estabilização do estado da doença (ou seja, não agravamento), atraso ou abrandamento da progressão da doença, melhora ou alívio do estado da doença e diminuição temporária da gravidade da doença (parcial ou total), quer seja detectável ou não detectável. "Tratamento" pode também significar sobrevida prolongada em comparação com a sobrevida esperada sem receber tratamento. Aqueles que necessitam de tratamento incluem aqueles já com a condição ou o distúrbio, bem como aqueles propensos a ter a condição ou o distúrbio ou aqueles em que a manifestação da condição ou distúrbio deva ser evitada.
[00096] Por "sujeito" ou "individual" ou "animal" ou "paciente" ou "mamífero", entende-se qualquer sujeito, particularmente um sujeito mamífero, por exemplo, um paciente humano, para o qual se pretende o diagnóstico, prognóstico, prevenção ou terapia. II. Métodos para identificar moléculas de ligação
[00097] A presente invenção geralmente está relacionada com os meios e os métodos para descobrir anticorpos terapeuticamente eficazes a partir de sujeitos humanos clinicamente pré-selecionados. Tal como demonstrado nos exemplos, anticorpos humanos contra estruturas anormais em doenças no cérebro humano podem ser isolados de pacientes fenotipicamente saudáveis ou clinicamente excepcionalmente estáveis e os anticorpos recombinantes correspondentes podem ser utilizados com sucesso para o tratamento, melhora da patologia e prevenção do comprometimento da função cerebral sem efeitos colaterais substanciais. A estabilidade clínica ou a não-progressão da doença pode ser identificada por exemplo, por meio da medição ao longo do tempo dos rastreios clínicos, por exemplo, cognitivo, de status (por testes neuropsicológicos, por exemplo); avaliação do nível funcional global, avaliação das capacidades da vida diária ou déficits comportamentais; análise volumétrica das estruturas cerebrais; medição in vivo dos depósitos patológicos das proteínas anormais no cérebro (por exemplo, rastreios por imagem PET beta-amiloide) ou variáveis bioquímicas nos fluidos corporais (por exemplo, proteínas tau ou peptídeos Abeta) e por comparação com o curso natural/histórico da doença. Assim, a presente invenção fornece anticorpos e moléculas de ligação que são capazes de reconhecer neoepítopos de proteínas associadas a doenças que se originam das proteínas endógenas nativas e são prevalentes no corpo de um paciente em uma forma variante, por exemplo, proteína patológica e/ou fora do seu contexto fisiológico normal. Em particular, anticorpos e seus fragmentos de ligação aos antígenos são propiciados, que demonstram características de ligação imunológica e/ou propriedades biológicas conforme indicado para o anticorpo ilustrado nos exemplos. Onde presente, o termo "características de ligação imunológica" ou outras características de ligação de um anticorpo com um antígeno, em todas as suas formas gramaticais, refere-se à especificidade, afinidade, reatividade cruzada e outras características de ligação de um anticorpo. Naturalmente, a presente invenção estende-se a linhas de produção de anticorpos e células recombinantes também. A presente invenção ainda refere-se a ensaios e kits de diagnóstico que compõem a molécula de ligação da presente invenção e a métodos terapêuticos e avaliações terapêuticas com base nelas.
[00098] A presente invenção é baseada na observação de que, em sujeitos humanos e pacientes pré-selecionados de acordo com critérios clínicos específicos, que têm o risco de desenvolver um distúrbio neurológico como a doença de Alzheimer, devido à sua idade, em relação à defesa humoral, anticorpos endógenos para patofisiológicas variantes como os agregados de peptídeos Abeta, emaranhados neurofibrilares, neurites distróficas e outras estruturas celulares também podem ser encontradas, que são neuropatologicamente características da doença. Estas estruturas podem ser encontradas isoladamente ou em combinação com outras estruturas patológicas e podem, como no caso dos agregados Abeta e dos precursores dos emaranhados neurofibrilares, desenvolver efeitos patológicos. No entanto, esses anticorpos especificamente reconhecendo as ditas estruturas não apresentam nenhuma reatividade cruzada ou reatividade cruzada significativamente inferior às formas funcionais fisiologicamente normais das proteínas subjacentes às estruturas patológicas, ao contrário do caso conhecido de uma resposta autoimune.
[00099] Sem intenção de estar preso à teoria, com base nos experimentos realizados em conformidade com a presente invenção, acreditava-se que um distúrbio não tem que se tornar manifesto e fenotipicamente perceptível, como no caso de uma infecção, a fim de resultar em uma atividade experimentalmente mensurável do sistema imune-humoral como a geração ou ativação de células B ou células B de memória específicas. No caso de células tumorais ou células diferenciadas, que têm de ser fisiologicamente eliminadas, os mecanismos já são conhecidos, onde parceiros como as células auxiliares T4 e as células T citotóxicas e as células assassinas naturais do sistema imuno-celular cooperam na indução de apoptose. Deve-se supor que, também em um ser humano saudável, as células tumorais ou suas precursoras sejam formadas em uma base diária, por meio de mutação. Entretanto, estas são imediatamente levadas à apoptose por meio dos mecanismos humoral e celular, para que um tumor não seja detectável. Neste sentido, de um “paciente saudável ou excepcionalmente clinicamente estável" não se depreende um indivíduo no qual não ocorra nenhum evento de doença, mas sim um indivíduo no qual diversos eventos de doença são controlados por mecanismos de bloqueio ou defesa antes de eles próprios se manifestarem fenotipicamente.
[000100] Em face do exposto, foi hipotetizado em conformidade com a presente invenção que deveria ser possível identificar um anticorpo ou uma célula produtora de anticorpos a partir de coletivos de pacientes específicos ou sujeitos saudáveis, que foram pré- selecionados de acordo com os critérios clínicos, sem pré-cognição de natureza molecular de um epitopo de estrutura-alvo, por exemplo, neoepítopo, onde o anticorpo, no caso de tolerância já prevalecente no corpo do doador, o qual é, por exemplo, provado pela ausência de auto-imunidade, poderia ser empregado com sucesso contra uma doença na forma de um agente produzido recombinantemente. A identificação de tal anticorpo pode assim ser conduzida sem a pré- cognição do epitopo molecular da estrutura-alvo, mas, em vez disso, somente por meio da ligação aos neoepítopos de estruturas patologicamente conspícuas em seções de tecido clínica- patologicamente bem caracterizadas derivadas de pacientes humanos ou de modelos animais da respectiva doença.
[000101] Assim, em um primeiro aspecto, a presente invenção refere-se a um método de isolar uma molécula de ligação específica à proteína associada à doença, compreendendo: (a) submeter uma espécime obtida a partir de um paciente que não apresenta sintomas ou que se apresente excepcionalmente clinicamente estável, mas que esteja afetado por ou com risco de desenvolver um distúrbio ou efetivamente suprimir a manifestação ou o surto de um distúrbio, a um espécime de células patologicamente ou fisiologicamente alteradas ou a tecido de características clínicas pré- determinadas; e (b) identificar e opcionalmente isolar uma molécula de ligação que preferencialmente se liga ao dito espécime, mas sem afinidade ou com afinidade significativamente inferior às células correspondentes ou tecidos sem tais características patológicas, já que podem vir a ser obtidos de um sujeito saudável.
[000102] O método da presente invenção pode ser executado conforme descrito na seção Exemplos com meios bem-conhecidos para alguém versado na técnica. Por exemplo, uma espécime de líquido obtida do paciente pode ser passada através de uma primeira abertura de um canal que está em contato com a estrutura da espécime alvo firmemente fixada em um suporte de objeto, deste modo permitindo a suposta ligação das moléculas presentes na espécime, quer na forma solúvel ou expressa na superfície e membrana da célula, respectivamente, para ligação à dita estrutura- alvo. A espécime de líquido pode conter, por exemplo linfócitos e/ou anticorpos, enquanto o espécime pode ser uma seção de tecido ou uma membrana revestida com moléculas ou combinações moleculares que são distintas para uma estrutura patológica alvo.
[000103] Qualquer matéria não ligante pode ser removida via a segunda abertura do canal. Ao mesmo tempo, a temperatura do suporte de objeto pode ser controlada por um termostato do suporte de objeto, por exemplo, a uma temperatura na qual a ligação natural da suposta molécula de ligação ao neoepítopo do antígeno específico para o espécime ocorra no corpo humano. Por meio do movimento do fluxo, por exemplo, poderá ser simulada a passagem da espécime de líquido, contendo moléculas preferivelmente na temperatura corporal, sobre os sistemas naturais da estrutura-alvo. Entretanto, outros métodos de incubação da espécime com o espécime, como por meio de um agitador ou mesa rotativa podem ser utilizados também. Uma vantagem especial do mencionado sistema é que este permite uma interrupção de processos metabólicos, a qualquer momento, pela diminuição da temperatura do suporte de objeto por meio do termostato do suporte de objeto. Ao fazê-lo, a temperatura do objeto titular pode ser reduzida para, por exemplo 2-10° C, em particular 4o C. Um dispositivo correspondente que pode ser utilizado de acordo com o método da presente invenção é descrito no pedido da patente européia EP 1 069 431 A2. Assim, o método da presente invenção permitirá a identificação e a caracterização dos parceiros de ligação, bem como, ao mesmo tempo, identificar e caracterizar as classes moleculares, os grupos moleculares e/ou as partes moleculares necessárias para o processo de ligação ou seja, as estruturas-alvo do espécime, que até o presente podem ser desconhecidas. Isto não só irá abrir novos possíveis meios de diagnóstico, mas também irá fornecer um novo sistema de teste para abordagens terapêuticas, em um nível molecular.
[000104] Como um paciente pode se habilitar, de acordo com a presente invenção, a um grupo de voluntários saudáveis se marcadores substitutos específicos com uma elevada probabilidade de um estado de uma doença, que surpreendentemente e, possivelmente, devido a uma resposta endógena imuno específica endógena não se manifestar clinicamente, contudo. Neste sentido, em relação a diversas doenças, um idoso saudável seria um indivíduo no qual uma doença neurodegenerativa como a doença de Alzheimer ou a doença de Parkinson ainda não se manifestou clinicamente, mas no qual o desenvolvimento pré-clínico das variantes das proteínas patofisiológicas ou seja, proteínas associadas à doença e no sentido acima mencionado, por meio da intervenção precoce do sistema imune humoral com ou sem o envolvimento dos componentes celulares do sistema imune, foi restringido ou retardado a tal ponto que, até o momento em que o paciente saudável, mas não pré-clinico, participou no estudo, a manifestação clínica da doença ainda não ocorreu. Preferencialmente, voluntários não óbvios, nos quais nem os processos autoimunológicos foram diagnosticados nem ocorreram outras possíveis condições patológicas como efeitos secundários, são recrutados como doadores para a espécime na primeira instância.
[000105] Em princípio, podem ser utilizadas amostras de pacientes que tenham sido submetidos a uma imunização ativa com variantes de proteínas ou peptídeos fisiológicos, em que o desenvolvimento do anticorpo foi impulsionado pela imunização. Anticorpos, por exemplo, podem ser identificados e isolados de pacientes com doença de Alzheimer que tenham sido vacinados com peptídeo Abeta. Vide, por exemplo, Hock et al.,Nature Medicine 8:1280-1275 (2002), Hock et al. Neuron38:547-554 (2003) e WO 2004/095031, cada um incorporado neste documento por referência em suas totalidades. No entanto, pode ser preferida a utilização de amostras de voluntários que não tenham recebido essa imunização ou medicação correspondente relativa à doença à qual a proteína patológica variante está associada e/ou é causadora de tal doença.
[000106] De acordo com a presente invenção, as amostras de um paciente, por exemplo, de indivíduos que tenham sido clinicamente pré-selecionados são analisadas quanto à presença de moléculas de ligação especificamente reconhecendo estruturas patologicamente evidentes, por exemplo, em tecido ex vivo de pacientes humanos clínico-patologicamente caracterizados ou modelos animais como, por exemplo, camundongos transgênicos ou estruturas celulares in vitroou em tecido alogênico ou xenogênico patológico. Preferencialmente, o dito paciente e/ou o dito sujeito que fornece o espécime é ser humano, mais preferivelmente ambos o são.
[000107] A espécime patologicamente ou fisiologicamente alterada característica, a célula ou espécime de tecido, são preferivelmente exibidos pela detecção ótica após a reação com uma molécula de ligação, por exemplo, o anticorpo da presente invenção. O espécime pode ser obtido como/a partir de um espécime de células, seção de tecidos, teste de esfregaço celular, espécime de células ou tecidos de um modelo animal de uma doença humana ou de material celular ou de tecido exposto à cultura in vitro.Preferivelmente, pelo menos um exemplar do dito espécime está presente em um suporte de objeto na forma de posicionador para varredura, no qual cada posição de varredura corresponde a uma estrutura patológica específica e, pelo menos, duas posições de varredura são concomitantemente expostas para detecção de uma reação com o anticorpo. A título de exemplo, os anticorpos para as marcas neuropatológicas de tais doenças neurodegenerativas como a doença de Alzheimer, doença de Parkinson ou tauopatias, incluindo placas de beta-amiloides, corpos de Lewy, emaranhados neurofibrilares e neurite distrófica, podem ser detectados em seções obtidas de tecidos encefálicos humanos post-mortemcom diagnóstico confirmado clínico-patologicamente das respectivas entidades das doenças. Isto é feito pela colocação de pequenos bastonetes de tecido incrustados em parafina sobre lâminas de vidro que são então analisadas com amostras de um paciente ou doador saudável. A detecção de uma reação com o anticorpo é feita seguindo procedimentos padrão de imuno-histoquímica e varredura microscópica.
[000108] Múltiplas microsseções de tecido contendo vários tecidos com várias doenças humanas podem ser colocados sobre a lâmina de vidro para formar um microarranjo de múltiplos tecidos. Da mesma forma, espécimes adicionais de amostras de tecido de modelos animais de doença humana, esfregaço celular ou células podem ser incrustados em parafina e colocados sobre lâminas de vidro isoladamente ou em combinação com os arranjos de tecidos ou tecido encefálico com doença de Alzheimer post-mortem humano acima descrito. Assim, uma única posição de teste sobre a lâmina de vidro pode incluir arranjos misturados de tecido e outros espécimes exibindo estruturas evidentes patologicamente.
[000109] A fim de aumentar o resultado do ensaio, mais de uma posição de ensaio é colocada sobre uma lâmina de vidro. Preferencialmente, oito posições de ensaio são colocadas em lâminas de vidro em formato de dois por quatro ajustando-se ao formato de 96 cavidades ou de microtitulação. Uma descrição mais detalhada deste microarranjo de tecidos compatível com a micro titulação pode ser encontrada na seção de métodos complementar abaixo.
[000110] Conforme mencionado, a espécime a ser analisada pode incluir um fluido corporal, uma espécime de célula ou o sobrenadante de uma espécime de células ou um derivado deles. Fluidos corporais, tais como o líquido cefalorraquidiano (LCR) lombar, plasma ou urina podem ser coletados seguindo os procedimentos clínicos padrão após consentimento expresso dos pacientes. Mais preferivelmente, a espécime compreende ou é obtida a partir de células-B ou células B de e/ou inclui anticorpos.
[000111] Preferivelmente, determinou-se que o dito paciente é afetado por um distúrbio não ainda manifestado ou em risco de desenvolver o distúrbio pela presença ou ausência de um marcador substituto ou por um curso de doença excepcionalmente estável. Critérios clínicos deverão ser considerados com relação aos marcadores substitutos com uma maior probabilidade de ocorrência ou manifestação de uma doença, de acordo com a presente invenção, no sentido de uma condição pré-clínica, ou, vice-versa, a qual atesta a improbabilidade de tal doença já ter ocorrido, como, por exemplo, a existência de uma constelação genética promovendo a doença ou uma exposição extrema ou modo de vida tornar provável o desenvolvimento fenotípico de uma doença. No caso da doença de Alzheimer, isto significa que, de acordo com a presente invenção, tais voluntários humanos são investigados quanto a células B ou células B de memória contra complexos de proteína associados à neuropatologia como agregados Abeta, espécie Abeta oligoméricos e fibrilas de beta-amiloide em placas de beta-amiloide, quanto a filamentos tau em emaranhados neurofibrilares, quanto à alfa- sinucleina em corpos de Lewy ou componentes até então não identificada molecularmente que, com relação à idade, pertencem a um grupo de indivíduos nos quais a prevalência da doença de Alzheimer é particularmente elevada ou cujos indivíduos se originam geneticamente de uma população que ostenta um alto risco para a doença de Alzheimer. Estas são, por exemplo, pessoas com mais de 75 anos que não tenham nenhum comprometimento ou que tenham apenas comprometimentos cognitivos neuropsicologicamente mensuráveis marginais, ou em caso de indicações de tumor, pessoas com marcadores de tumor altamente indicativos, por exemplo, de marcadores de tumores genéticos, mas que não têm a doença (Alloul et al.,Arch. Gerontology Geriatrics 27 (1998), 189; Dunn et al., Immunity 21 (2004) 137-148). No caso do comprometimento cognitivo leve, estes são pacientes que permaneceram clinicamente, neuropsicologicamente ou cognitivamente estáveis durante anos, apesar do seu risco estatístico anual de mais de 20% para o desenvolvimento de uma doença neurodegenerativa que se apresente clinicamente manifesta e progressiva mais adiante. Assim, em uma modalidade, o dito marcador substituto é selecionado do grupo constituído por velhice, carga amiloide cerebral, genótipo ApoE, genótipo APP, genótipo PS1, níveis nos fluidos corporais de peptídeo Abeta, isoprostanos, Tau e fosfo-Tau.
[000112] Uma abordagem em particular no emprego do método de acordo com a presente invenção consiste em testar as amostras de células B e de células de memória B de voluntários pré-selecionados clinicamente contra arranjos de espécimes de tecidos evidentes patologicamente de doenças inteiramente diferentes ou primárias relacionadas. Em especial, esses tecidos patológicos originam-se de pacientes humanos que sofrem de doenças neurodegenerativas, doenças de falso dobramento de proteínas, amiloidoses de tecidos e outras doenças relacionadas com depósitos patológicos, distúrbios autoimunes, doenças inflamatórias, doenças hiperproliferativas e neoplásicas, como por exemplo, tumores, doenças de armazenamento e doenças de inclusão bem como de modelos animais de doenças humanas, em especial de camundongos alterados com genes humanos relevantes patologicamente.
[000113] Em uma modalidade particularmente preferida, a presente invenção concentra-se na doença de Alzheimer. Nesta modalidade, a espécime é obtida a partir de um sujeito que preferivelmente preencha os seguintes critérios: a) Tenha 65, preferivelmente 70 e mais preferivelmente mais de 75 anos de idade ou mais; b) tenha plena capacidade cognitiva e boa saúde e c) não tenha sinais clínicos de demência ou d) tendo taxas de progressão da doença invulgarmente lentas, apesar da presença de um diagnóstico clínico de provável doença de Alzheimer ou e) Tenha taxas de conversão excepcionalmente baixas, desde um Comprometimento Cognitivo Leve (MCI) até doença de Alzheimer profunda.
[000114] Em uma outra modalidade, o método da presente invenção ainda compreende as etapas de: a) depuração de células B ou células B de memória a partir de uma espécime que tenha sido identificada como contendo moléculas de ligação, por exemplo, anticorpos que preferencialmente se ligam ao dito espécime mas sem afinidade ou com afinidade significativamente mais baixa para células ou tecido correspondentes de um sujeito saudável; b) obtenção de repertório de genes de imunoglobulina que codificam os anticorpos das ditas células B ou das células de memória B;e c) utilização do dito repertório para expressar os ditos anticorpos e opcionalmente onde o passo (b) compreender as etapas de: d) obtenção do mRNA das ditas células B ou das células B de memória; e) obtenção de cDNA a partir do mRNA da etapa (iv) e f) utilização de uma reação de extensão para multiplicar, a partir do dito cDNA, os fragmentos correspondentes às cadeias pesadas (HC) e às cadeias leves (LC) de kappa/lambda dos referidos anticorpos.
[000115] Métodos de produção de clones de uma célula B e linfócito B de memória humanos imortalizados, consistindo na etapa de transformação dos linfócitos B de memória humanos utilizando o Vírus Epstein Barr (EBV) na presença de um ativador de células B policlonais estão resumidos no pedido internacional W02004/076677. Este pedido internacional também descreve métodos para a obtenção de uma sequência de ácido nucleico que codifica um anticorpo de interesse, compreendendo as etapas de preparação de um clone de células B imortalizadas e de obtenção/sequenciamento de ácidos nucleicos de clone de células B que codifica o anticorpo de interesse e, em seguida, a inserção da ácido nucleico ou o uso do ácido nucleico para preparar um hospedeiro de expressão que possa expressar o anticorpo de interesse, expor à cultura ou a sub-expor à cultura o hospedeiro de expressão sob condições nas quais o anticorpo de interesse seja expresso e, opcionalmente, purificar o anticorpo de interesse. Obviamente o ácido nucleico pode ser manipulado neste ínterim para introduzir os sítios de restrição, para alterar o uso do códon, e/ou para adicionar ou otimizar as sequências reguladoras de transcrição e/ou tradução. Por exemplo, as sequências de ácidos nucleicos podem ser geradas por retro-tradução das sequências polipeptídicas do presente invenção usando software como o software NTI vetor para gerar as sequências de ácidos nucleicos que são otimizadas por códon e otimizadas para estabilidade do RNA. Todas estas técnicas são do estado da técnica e podem ser executadas por pessoa versada na técnica sem dificuldade. Métodos adicionais de imortalização de células B humanas são bem-conhecidos na técnica, por exemplo, a construção de hibridomas humanos ou hibridomas quiméricos murino-humanos.
[000116] Em outro aspecto, a presente invenção refere-se a uma molécula de ligação que é capaz de reconhecer seletivamente um epitopo de uma proteína associada à doença, incluindo um neoepítopo de uma proteína associada à doença, que pode ser preferivelmente obtido ou validado pelo método da presente invenção previamente aqui descrito e ilustrado nos exemplos. Com vantagem, a molécula de ligação da presente invenção não reconhece substancialmente a dita proteína em sua forma não associada ao distúrbio; vide também supra.
[000117] Meios e métodos para a produção de recombinantes das moléculas de ligação, em particular seus anticorpos e réplicas como também métodos de varredura para moléculas de ligação em competição, que podem ou não podem ser anticorpos, são conhecidos na técnica e estão sumarizados, por exemplo, no pedido internacional W02006/103116 com relação aos anticorpos contra o beta-amiloide e ao tratamento/diagnóstico da doença de Alzheimer, cujo conteúdo da descrição está incorporado aqui como referência para este propósito de projeto e administração de anticorpos para aplicações terapêuticas ou diagnósticas.
[000118] Entretanto, conforme descrito aqui, em particular com relação às aplicações terapêuticas em seres humanos, o anticorpo da presente invenção é um anticorpo humano. Neste contexto, a proteína patológica variante reconhecida pelo anticorpo é preferivelmente associada com um distúrbio neurológico, preferivelmente um distúrbio do cérebro.
[000119] Além disso, como demonstrado nos exemplos 3 a 5, a molécula de ligação da presente invenção, em particular um anticorpo, possui várias propriedades biológicas vantajosas, uma ou mais das quais foram consumadas pela presente invenção pela primeira vez. Por exemplo, ela é capaz de: (i) atravessar a barreira hematoencefálica, por exemplo, no local do evento patológico; (ii) ligar placas de beta-amiloides, amiloide cérebro- vascular, depósitos Abeta difusos, emaranhados neurofibrilares, tau hiperfosforilatados, corpos de Lewy positivos de alfa-sinucleina ou agregados de proteína associados com neurites distróficas; (iii) remover placas de beta-amiloide no cérebro e/ou prevenir a formação de placas amiloides no cérebro; (iv) substancialmente restaurar um comportamento normal e/ou; (v) não causar nenhuma micro-hemorragia.
[000120] Em uma modalidade particular preferida, o anticorpo ou a molécula de ligação equivalente da presente invenção pode ser distinguido de outros anticorpos por uma ou mais das seguintes propriedades, por exemplo, eles são capazes de: 1. atravessar, pelo menos em pequenas quantidades, a barreira hematoencefálica no local dos eventos patológicos; 2. ligar-se a uma ou mais estruturas extracelulares ou celulares patofisiologicamente relevantes; 3. levar à redução da estrutura patofisiologicamente relevante in vitroou in vivo\ 4. levar à redução da estrutura patofisiologicamente relevante e à redução de uma toxicidade associada aos mesmos; 5. levar ao bloqueio ou retardo de um processo de doença; 6. levar à regeneração das funções celulares e específicas de órgãos e orgânicas e, possivelmente, a uma prevenção secundária da recorrência da fisiopatologia original após degradação da toxicidade relacionada com a estrutura patofisiologicamente relevante e/ou; 7. não estarem associados com o aumento de micro- hemorragias.
[000121] Além disso, a ausência de reatividade cruzada com precursores fisiológicos ou derivados leva à consequência de que, em primeiro lugar, as concentrações são previsíveis, visto que os efeitos dissipadores nas estruturas dos tecidos sadios são evitados e, em segundo lugar, a ausência substancial das respostas autoimunes no sentido de efeitos colaterais indesejados. Além disso, os relatórios anteriores sugeriram uma associação de angiopatia amiloide cerebral (AAC) com reatividade vascular comprometida em um modelo de camundongo transgênico com AAC (Mueggler et al.,J Neurosci 22 (2002), 7218-24.). A AAC grave ocorrendo em camundongos velhos arcAB. (Knobloch et al. Neurobiol. Aging 28:1297-1306 (2007) Epub 31 de julho de 2006) poderia, assim, limitar a flexibilidade vasodilatadora dos vasos sanguíneos afetados. De acordo com a presente invenção, é prudente esperar que o tratamento com os anticorpos da presente invenção possa melhorar a vasoreatividade e o fluxo sanguíneo cerebral em camundongos transgênicos APP velhos. Isto pode ser validado usando o modelo de camundongos arcAB descrito em Knobloch et al. (2006), supra e descritos no pedido U.S. "Transgenic animal model for Alzheimer’s Disease", de Grimm et al.,Número de série 60/934.291 protocolado em 11 de junho de 2007, cujo conteúdo da descrição está incorporado neste documento como referência. III. Anticorpos
[000122] A presente invenção é ainda direcionada às moléculas de ligação, por exemplo, anticorpos e moléculas de ligação, variantes e seus derivados apresentados na Tabela 2 e 3. A presente invenção é mais especificamente dirigida a um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados, onde o anticorpo liga-se especificamente ao mesmo neoepítopo de uma proteína associada ao distúrbio como um anticorpo de referência selecionado do grupo consistindo em NI-101.10, NI-101.11, 101.12, NI-101.13, Nl- 101.12F6A, NI-101.13AeNI-101.13B.
[000123] A invenção é ainda dirigida a um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados, onde o anticorpo inibe competitivamente um anticorpo de referência selecionado a partir do grupo consistindo em NI-101.10, NI-101.11, NI-101.12, NI-101.13, Nl- 101.12F6A, NI-101.13A e NI-101.13B da ligação ao neoepítopo de uma proteína associada ao distúrbio.
[000124] A invenção é também dirigida a um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados, onde o anticorpo compreende um domínio de ligação a antígeno idêntico ao de um anticorpo selecionado a partir do grupo consistindo em N1-101.10, Nl- 101.11, NI-101.12, NI-101.13, NI-101.12F6A, NI-101.13A e Nl- 101.13B.
[000125] A presente invenção ainda exemplifica várias dessas moléculas de ligação, por exemplo, anticorpos e seus fragmentos de ligação, que podem ser caracterizados por incluir em sua região variável, por exemplo, no domínio de ligação, pelo menos, uma região determinante de complementaridade (CDR), da região variável VH e/ou VL região variável compreendendo qualquer uma das sequências de aminoácidos representadas na Tabela 2 (VH) e Tabela 3 (VL).
[000126] As sequências de nucleotídeos correspondentes codificando as regiões variáveis acima identificadas estão estabelecidas na listagem de sequências, em anexo. Um conjunto exemplar de CDRs das sequências de aminoácidos acima da região VH e/ou VL conforme ilustrado nas tabelas 2 e 3 é apresentado na Tabela 4. No entanto, como discutido a seguir, aqueles versados na técnica tem pleno conhecimento de que, além disso ou alternativamente, CDRs podem ser usadas, as quais diferem em sua sequência de aminoácidos daquelas apresentadas na Tabela 4, em um, dois, três ou ainda mais aminoácidos no caso de CDR2 e CDR3.
[000127] Em uma modalidade, o anticorpo da presente invenção é qualquer um dos anticorpos compreendendo uma sequência de aminoácidos da região VH e/ou VL como demonstrado nas Tabelas 2 e 3. Alternativamente, o anticorpo da presente invenção é um anticorpo ou fragmento de ligação a antígeno, que compete pela ligação ao neoepítopo com pelo menos um dos anticorpos contendo a região VH e/ou VL conforme ilustrado nas Tabelas 2 e 3. Estes anticorpos podem ser murinos também, no entanto, anticorpos humanizados, xenogênicos ou humano-murinos quiméricos são preferidos, em especial para aplicações terapêuticas. Um fragmento de ligação a antígeno do anticorpo pode ser, por exemplo, um fragmento Fv de cadeia única (scFv), um fragmento F (ab'), um fragmento F(ab) e um fragmento F(ab')2. Para algumas aplicações, apenas as regiões variáveis dos anticorpos são necessários, o que pode ser conseguido pelo tratamento do anticorpo reagentes adequados, de modo a gerar partes de Fab', Fab ou F (ab")2. Esses fragmentos são suficientes para a utilização, por exemplo, em procedimentos imunodiagnósticos envolvendo o acoplamento das partes imunoespecíficas de imunoglobulinas a reagentes detectores tais como radioisótopos.
[000128] A presente invenção é ainda dirigida a polipeptídeos isolados que compõem os anticorpos da presente invenção. Anticorpos do presente invenção compreendem polipeptídeos, por exemplo, sequências de aminoácidos codificando regiões de ligação a antígeno específicos derivados das moléculas de imunoglobulina. Um polipeptídeo ou sequência de aminoácidos "derivado de" uma proteína designada refere-se à origem do polipeptídeo contendo uma certa sequência de aminoácidos. Em certos casos, o polipeptídeo ou a sequência de aminoácidos é derivado de um determinado polipeptídeo ou sequência de aminoácidos de partida que possui uma sequência de aminoácidos essencialmente idêntica àquela da sequência de partida ou uma parte dela, na qual a parte consiste em pelo menos 10-20 aminoácidos, pelo menos 20-30 aminoácidos, pelo menos 30-50 aminoácidos ou que seja, de outro modo, identificável a alguém versado na técnica como tendo sua origem na sequência de partida.
[000129] Em outra modalidade, a presente invenção propicia um polipeptídeo isolado, consistindo essencialmente em, ou consistindo em uma região variável de cadeia pesada de imunoglobulina (VH), onde pelo menos um dos VH-CDRs da região variável da cadeia pesada ou pelo menos duas das VH-CDRs da região variável da cadeia pesada são, pelo menos, 80%, 85%, 90% ou 95% idênticas às sequências de aminoácidos de VH-CDR1, VH-CDR2 ou VH-CDR3 da cadeia pesada de referência dos anticorpos descritos aqui. Alternativamente, as regiões VH-CDR1, VH-CDR2 e VH-CDR3 do VH são pelo menos 80%, 85%, 90% ou 95% idênticas às sequências de aminoácidos de CDR1-VH, VH-CDR2 e VH-CDR3 da cadeia pesada de referência dos anticorpos descritos aqui. Assim, de acordo com esta modalidade, uma região variável de cadeia pesada da invenção possui sequências de polipeptídeos de VH-CDR1, VH-CDR2 e VH- CDRS relacionadas com os grupos apresentados na Tabela 4, supra. Enquanto a Tabela 4 ilustra as VH-CDRs definidas pelo sistema Kabat, outras definições de CDR, como por exemplo, VH-CDRs definidas pelo sistema Chothia, também estão incluídas na presente invenção e podem ser facilmente identificadas por uma pessoa de habilidade ordinária na técnica usando os dados apresentados nas Tabelas 2 e 3.
[000130] Em outra modalidade, a presente invenção propicia um polipeptídeo composto isolado, compreendendo, consistindo essencialmente em ou consistindo em uma região variável de cadeia pesada de imunoglobulinas (VH) na qual as regiões de VH-CDR1, VH- CDR2 e VH-CDR3 possuem sequências de polipeptídeos que são idênticas aos grupos de VH-CDR1, VH-CDR2 e VH-CDR3 ilustrados na Tabela 4.
[000131] Em outra modalidade, a presente invenção propicia um polipeptídeo isolado, consistindo essencialmente em ou consistindo em uma região variável de cadeia pesada de imunoglobulina (VH) em que as regiões de VH-CDR1, VH-CDR2 e VH-CDR3 possuem sequências de polipeptídeos que são idênticas aos grupos de VH- CDR1, VH-CDR2 e VH-CDR3 apresentados na Tabela 4, à exceção de um, dois, três, quatro, cinco, seis substituições de aminoácidos em qualquer uma VH-CDR. Em certas modalidades, as substituições de aminoácidos são conservadoras.
[000132] Em outra modalidade, a presente invenção propicia um polipeptídeo isolado, compreendendo, consistindo essencialmente em ou consistindo em uma região variável de cadeia leve de imunoglobulinas (VL), onde pelo menos uma das VL-CDRs da região variável de cadeia leve ou pelo menos duas das VL-CDRs da região variável de cadeia leve são, pelo menos, 80%, 85%, 90% ou 95% idênticas às sequências de aminoácidos de VL-CDR1, VL-CDR2 ou VL-CDR3 de cadeia leve de referência dos anticorpos descritos aqui. Alternativamente, as regiões de VL-CDR1, VL-CDR2 e VL-CDR3 da VL são pelo menos 80%, 85%, 90% ou 95% idênticas às sequências de aminoácidos de VL-CDR1, VL-CDR2 e VL-CDR3 de cadeia leve de referência dos anticorpos descritos aqui. Assim, de acordo com esta modalidade, uma região variável de cadeia leve da invenção possui sequências de polipeptídeos relacionadas com os polipeptídeos mostrados na Tabela 4, supra. Enquanto a Tabela 4 mostra as VL- CDRs definidas pelo sistema Kabat, outras definições de CDR, por exemplo, VL-CDRs definidas no sistema Chotia, estão também incluídas na presente invenção.
[000133] Em outra modalidade, a presente invenção propicia um polipeptídeo isolado compreendendo, consistindo essencialmente em ou consistindo em uma região variável de cadeia leve de imunoglobulina (VL) na qual as regiões VL-CDR1, VL-CDR2 e VL- CDRS possuem sequências de polipeptídeos que são idênticas aos grupos VL-CDR1, VL-CDR2 e VL-CDR3 mostrados na Tabela 4.
[000134] Em outra modalidade, a presente invenção propicia um polipeptídeo isolado compreendendo, consistindo essencialmente em ou consistindo em uma região variável de cadeia [s/c:] pesada de imunoglobulina (VL) na qual as regiões VL-CDR1, VL-CDR2 e VL- CDR3 possuem sequências de polipeptídeos que são idênticas aos grupos VL-CDR1, VL-CDR2 e VL-CDR3 mostrados na Tabela 4, exceto por uma, duas, três, quatro, cinco ou seis substituições de aminoácidos em qualquer VL-CDR. Em certas modalidades, as substituições de aminoácidos são conservadoras.
[000135] Uma imunoglobulina ou seus cDNAs de codificação pode ainda ser modificada. Assim, em uma nova modalidade, o método da presente invenção compreende qualquer uma das etapas de produção de um anticorpo quimérico, anticorpo humanizado, anticorpo de cadeia única, anticorpo de Fab-fragmento, anticorpo biespecífico, anticorpo de fusão, anticorpo marcado ou análogo de qualquer um desses. Métodos correspondentes são conhecidos à pessoa versada na técnica e são descritos, em Harlow e Lane "Antibodies, A Laboratory Manual", CSH Press, Cold Spring Harbor, 1988. Quando derivados desses ditos anticorpos são obtidos através da técnica de exibição de fagos, a ressonância de plásmon superficial conforme empregada no sistema BIAcore pode ser utilizada para aumentar a eficiência dos anticorpos do fago que se ligam ao mesmo epitopo como o de qualquer um dos anticorpos aqui descritos (Schier, Human Antibodies Hybridomas 7 (1996), 97-105; Malmborg, J. Immunol. Methods 183 (1995), 7-13). A produção de anticorpos quiméricos é descrita, por exemplo, no pedido internacional WO89/09622. Métodos para a produção de anticorpos humanizados são descritos, por exemplo, no pedido de patente europeia EP-A1 0 239 400 e no pedido internacional W090/07861. Uma outra fonte de anticorpos a ser utilizada em conformidade com a presente invenção são os chamados anticorpos xenogênicos. O princípio geral para a produção de anticorpos xenogênicos, tal como anticorpos humanos em camundongos é descrito, por exemplo, nos pedidos internacionais WO91/10741, W094/02602, WO96/34096 e WO 96/33735. Conforme discutido anteriormente, o anticorpo da invenção pode existir em uma variedade de formas, além dos anticorpos completos, incluindo, por exemplo, Fv, Fab e F(ab)2, assim como em cadeias únicas; vide, por exemplo, o pedido internacional WO88/09344.
[000136] Os anticorpos da presente invenção ou sua(s) correspondente(s) cadeia(s) de imunoglobulinas ainda podem ser modificados utilizando técnicas convencionais conhecidas na técnica, por exemplo, usando exclusão(ões), inserção(ões), substituição(ões), adição(ões), e/ou recombinação(ões) e/ou qualquer(quaisquer) outra(s) modificação(ões) conhecida(s) na técnica quer independentemente ou em combinação. Métodos de introdução de tais modificações na sequência de DNAs subjacentes, a sequência de aminoácidos de uma cadeia de imunoglobulinas são bem-conhecidos pela pessoa versada na técnica; vide, por exemplo, Sambrook, Molecular Cloning A Laboratory Manual, Cold Spring Harbor Laboratory (1989) e NY Ausubel, Protocols in Molecular Biology, Green Publishing Associates and Wiley Interscience, N.Y (1994). Modificações do anticorpo da invenção incluem derivatizações químicas e/ou enzimáticas em um ou mais aminoácidos constituintes, incluindo as modificações da cadeia lateral, as modificações da espinha dorsal e as modificações dos radicais N- e C-, incluindo acetilação, hidroxilação, metilação, amidação e a ligação das porções de carboidrato ou lipídios, co-fatores e similares. Do mesmo modo, a presente invenção engloba a produção de proteínas quiméricas que compõem o anticorpo descrito ou algum fragmento deste no radical do grupo amina fundido à molécula heteróloga, como um ligante imunoestimulatório no radical do grupo carboxila; ver, por exemplo, pedido internacional WO00/30680 para detalhes técnicos correspondentes.
[000137] Além disso, a presente invenção abrange pequenos peptídeos incluindo aqueles que contêm uma molécula de ligação, conforme descrito acima, por exemplo, contendo a região CDR3 da região variável de qualquer um dos anticorpos mencionados, em particular a CDR3 da cadeia pesada, visto que tem sido frequentemente observado que a CDR3 de cadeia pesada (HCDR3) é a região que possui um grau maior de variabilidade e uma participação predominante na interação de anticorpos-antígeno. Esses peptídeos podem facilmente ser sintetizados ou produzidos por meio de recombinação para produzir um agente de ligação útil de acordo com a invenção. Esses métodos são bem-conhecidos por aqueles versados na técnica. Peptídeos podem ser sintetizados, por exemplo, utilizando sintetizadores de peptídeos automatizados que estão comercialmente disponíveis. Os peptídeos podem ser produzidos por técnicas de recombinação pela incorporação do DNA expressando o peptídeo em um vetor de expressão e transformando células com o vetor de expressão para produzir o peptídeo.
[000138] Assim, a presente invenção refere-se a qualquer molécula de ligação, por exemplo, um anticorpo ou fragmento de ligação que é obtido de acordo com os meios descritos e exibe as propriedades mencionadas ou seja, aquelas que especificamente reconhecem um neoepítopo. Esses anticorpos e moléculas de ligação podem ser testados quanto a sua especificidade e afinidade de ligação, por exemplo, utilizando o método de isolamento das moléculas de ligação específicas do neoepítopo descritas anteriormente neste documento.
[000139] Como uma alternativa para a obtenção de imunoglobulinas diretamente a partir da cultura de células B ou células B de memória imortalizadas, as células imortalizadas podem ser usadas como uma fonte de cadeia pesada rearranjada e de locide cadeia leve para posterior expressão e/ou manipulação genética. Genes de anticorpos rearranjados podem transcritos inversamente a partir de mRNAs apropriados para a produção de cDNA. Se desejado, a região constante da cadeia pesada pode ser trocada por aquela com um isótopo diferente ou totalmente eliminado. As regiões variáveis podem ser ligadas para codificar as regiões de cadeia única Fv. Múltiplas regiões Fv podem ser ligadas para conferir capacidade de ligação a mais de um alvo ou podem ser empregadas combinações quiméricas de cadeia leve e pesada. Uma vez que o material genético está disponível, a concepção de análogos, como descrito acima, que conservam a sua capacidade de ligar ao alvo desejado, é simples. Métodos de clonagem de regiões variáveis de anticorpos e geração de anticorpos recombinantes são conhecidos pela pessoa versada na técnica e são descritos, por exemplo, em Gilliland et al.Tissue Antigens 47 (1996), 1-20; Doenecke et al.Leukemia 11 (1997), 1787- 1792.
[000140] Uma vez que o material genético adequado é obtido e, se desejado, modificado para codificar um análogo, as sequências de codificação, incluindo aquelas que codificam, no mínimo, as regiões variáveis da cadeia leve e pesada, podem ser inseridas em sistemas de expressão contidos em vetores que podem ser transfectados em células hospedeiras recombinantes-padrão. Uma variedade de tais células hospedeiras pode ser utilizada, para um processamento eficiente, no entanto, células de mamíferos são preferidas. As linhas de células mamíferas típicas úteis para esta finalidade incluem, entre outras, células CHO, células HEK 293 ou células NSO.
[000141] A produção do anticorpo ou análogo é então realizada pela exposição à cultura de hospedeiro recombinante modificado sob condições de cultura apropriadas para o crescimento das células hospedeiras e a expressão das sequências de codificação. Os anticorpos são então recuperados pelo isolamento deles da cultura. Os sistemas de expressão são preferivelmente projetados para incluir peptídeos de sinal de modo que os anticorpos resultantes são secretados no meio; no entanto, a produção intracelular também é possível.
[000142] Uma vez que a estrutura-alvo, por exemplo, a proteína associada à doença tiver sido marcada pela molécula de ligação respectiva ali, ela poderá ser identificada por meios e métodos bem- conhecidos na técnica, por exemplo, utilizando técnicas de espectrometria de massa (MS), tais como aquelas descritas no pedido internacional WO00/11208 e especificamente aquelas descritas em Hock et al.,Nat Med 8 (2002), 1270-1275; Hock et al. Neuron 38 (2003), 547-554. Assim, caso o anticorpo identificado em conformidade com a presente invenção produzido in vitrose ligar às estruturas, patológicas, por exemplo, às placas beta-amiloides nas seções da área patológica do cérebro, mas não de forma significativa aos tecidos saudáveis, um anticorpo candidato promissor foi identificado cuja estrutura-alvo molecular pode ser posteriormente enriquecida e purificada através de suas propriedades de ligação ao anticorpo de tecidos patológicos e, como resultado, pode ser identificada e caracterizada por meio de métodos de espectrometria de massa e analíticos de proteínas, como por exemplo MALDI/TOF (Williams, Methods Cell. Biol. 62 (2000), 449-453; Yates, J. Mass Spectrom. 33 (1998), 1-19).
[000143] Assim, em outra modalidade, a presente invenção refere-se a um antígeno que é reconhecido pela molécula de ligação, especialmente o anticorpo do presente invenção descrito anteriormente neste documento, o qual, preferivelmente, é pelo menos parte de uma proteína associada ao distúrbio.
[000144] De acordo com o acima exposto, a presente invenção também refere-se a um polinucleotídeo que codifica o antígeno ou a molécula de ligação da presente invenção, caso o anticorpo, preferivelmente, pelo menos uma região variável de uma cadeia de imunoglobulinas do anticorpo descrito acima. Normalmente, a dita região variável codificada pelos polinucleotídeos inclui pelo menos uma região de determinação de complementaridade (CDR), de VH e/ou VL da região variável do dito anticorpo. A pessoa versada na técnica sabe que cada domínio variável (o VH de cadeia pesada e o VL de cadeia leve) de um anticorpo hipervariável compreende três regiões hipervariaveis, às vezes denominadas regiões de determinação de complementaridade ou "CDRs" ladeadas por quatro regiões de estrutura de suporte relativamente conservadas ou “FRs" e referem-se aos resíduos de aminoácidos de um anticorpo que são responsáveis pela ligação a antígeno. As regiões hipervariáveis ou CDRs do subtipo de IgG humano compreendem resíduos de aminoácidos dos resíduos 24-34 (L1), 50-56 (L2) e 89-97 (L3), no domínio variável de cadeia leve e 31-35 (H1), 50-65 (H2) e 95-102 (H3) no domínio variável de cadeia pesada como descrito por Kabat et al.,Sequences of Proteins of Immunological Interest, 5th Ed Public Health Service, National Institutes of Health, Bethesda, Md (1991) e/ou os resíduos provenientes de uma alça hipervariável, por exemplo, resíduos 26-32 (L1), 50-52 (L2) e 91-96 (L3), no domínio variável de cadeia leve e 26- 32 (H1), 53-55 (H2) e 96-101 (H3), no domínio variável de cadeia pesada conforme descrito por Chothia et al.,J. Mol. Biol. 196 (1987), 901-917. Resíduos da estrutura ou FR são os resíduos de domínio variável diferentes e que incluem as regiões hipervariáveis. O termo "ligação específica"refere-se à ligação do anticorpo a um antígeno predeterminado. Normalmente, o anticorpo liga-se com uma constante de dissociação (KD), de 10 -7 M ou menos, e liga-se ao antígeno predeterminado com uma KD que seja pelo menos duas vezes menor que sua KD para ligação a um antígeno não específico (por exemplo, BSA, caseína ou qualquer outro polipeptídeo especificado), com exceção do antígeno predeterminado. As frases "um anticorpo reconhece um antígeno" e "um anticorpo específico para um antígeno" são utilizadas alternadamente aqui com o termo "um anticorpo que se liga especificamente a um antígeno". Conforme utilizado aqui ligação "altamente específica" significa que a KD relativa do anticorpo para o epitopo alvo específico, por exemplo, neoepítopo é, pelo menos, 10 vezes menor do que a KD para ligação daquele anticorpo a outros ligantes ou à contraparte nativa da proteína associada à doença.
[000145] A afinidade ou avidez de um anticorpo para um antígeno pode ser determinada experimentalmente usando qualquer método adequado; vide, por exemplo, Berzofsky et al."Antibody-Antigen Interactions"In Fundamental Immunology, Paul, W. E., ed., Raven Press New York, NY (1984), Kuby, Janis Immunology, W. H. Freeman and Company New York, NY (1992) e os métodos descritos aqui. As técnicas gerais para medição da afinidade de um anticorpo para um antígeno incluem ELISA, RIA e ressonância de plásmon de superfície. A afinidade medida de uma interação de anticorpo-antígeno em particular pode variar, se medida sob diferentes condições, por exemplo, concentração de sal, pH. Assim, as medições de afinidade e outros parâmetros de ligação a antígenos, por exemplo, KD, IC50, são realizados de preferência com soluções padronizadas de anticorpo e antígeno e uma solução-tampão padrão.
[000146] A pessoa versada na técnica facilmente reconhecerá que o domínio variável do anticorpo que contém o domínio variável acima descrito pode ser usado para a construção de outros polipeptídeos ou anticorpos da especificidade e função biológica pretendida. Assim, a presente invenção também engloba polipeptídeos e anticorpos compreendendo pelo menos uma CDR do domínio variável acima descrito e que, com vantagem, possuem basicamente as mesmas propriedades de ligação, ou semelhante, que do anticorpo descrito nos exemplos anexados. A pessoa versada na técnica facilmente reconhecerá que com o uso dos domínios variáveis ou CDRs aqui descritos, os anticorpos podem ser construídos de acordo com métodos conhecidos na técnica, por exemplo, tal como descritos no pedido da patente européia EP 0 451 216 A1 e EP 0 549 581 A1. Além disso, a pessoa versada na técnica sabe que a afinidade de ligação pode ser aumentada através de substituições de aminoácidos nas CDRs ou nas alças hipervariáveis (Chothia e Lesk, J. Mol. Biol. 196 (1987), 901-917), que se sobrepõem parcialmente com as CDRs, tal como definido por Kabat. Assim, a presente invenção também refere- se aos anticorpos em que uma ou mais das CDRs mencionadas incluem uma ou mais, de preferência não mais de duas substituições de aminoácidos. Preferencialmente, os anticorpos da invenção incluem em uma ou ambas das suas cadeias de imunoglobulinas duas ou todas as três CDRs das regiões variáveis, tal como apresentadas na Tabela 4.
[000147] As moléculas de ligação, por exemplo, anticorpos ou fragmentos de ligação ao antígeno, variantes ou seus derivados da invenção, tal como do conhecimento daqueles versados na técnica, podem compreender uma região constante que media uma ou mais funções da molécula executora. Por exemplo, a ligação do componente C1 do complemento de uma região constante de anticorpos pode ativar o sistema de complemento. A ativação do complemento é importante na opsonização e lise dos patógenos de células. A ativação do complemento também estimula a resposta inflamatória e pode também estar envolvido na hipersensibilidade autoimune. Além disso, os anticorpos se ligam aos receptores nas diferentes células através da região Fc, com um sítio de ligação ao receptor FC na região Fc do anticorpo que se liga a um receptor Fc (FCR) em uma célula. Há um número de receptores Fc que são específicos para as diferentes classes de anticorpos, incluindo anticorpos IgG (receptores gama), IgE (receptores epsilon), IgA (receptores alfa) e IgM (receptores mu). A ligação dos anticorpos aos receptores Fc nas superfícies das células desencadeia uma série de respostas biológicas incluindo absorção e destruição de partículas revestidas com anticorpos, depuração de complexos imunes, lise de células-alvo revestidas de anticorpos pelas células assassinas (processo chamado de citotoxicidade mediada por células dependentes de anticorpos ou ADCC), liberação de mediadores inflamatórios, transferência placentária e controle de produção de imunoglobulina.
[000148] Assim, certas modalidades da invenção incluem um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados, nos quais pelo menos uma porção de um ou mais dos domínios das regiões constantes foi eliminada ou, de outro modo, alterada, de modo a proporcionar as características bioquímicas desejadas tais como funções reduzidas da molécula executora, a capacidade de dimerização de modo não covalente, capacidade aumentada para localizar no sítio de um tumor, redução na meia-vida do soro ou aumento da meia-vida do soro em comparação com um anticorpo total, inalterado com aproximadamente a mesma imunogenicidade. Por exemplo, alguns anticorpos para utilização nos métodos de diagnóstico e tratamento descritos aqui são anticorpos excluídos do domínio que compreendem uma cadeia de polipeptídeo similar a uma cadeia pesada de imunoglobulina, mas que não possui pelo menos uma porção de um ou mais domínios de cadeia pesada. Por exemplo, em determinados anticorpos, um domínio inteiro da região constante do anticorpo modificado será excluído, por exemplo, o todo ou parte do domínio de CH2 domínio será excluído. Em outras modalidades, certos anticorpos para utilização nos métodos de diagnóstico e tratamento descritos aqui possuem uma região constante, por exemplo, uma região do constante de cadeia pesada, que é alterada para eliminar a glicosilação, referidos aqui como em outros locais como anticorpos aglicosilatados ou “agli”. Tais anticorpos “agli” podem ser preparados enzimaticamente, bem como pela engenharia do(s) sítio(s) de glicosilação de consenso na região constante. Embora não preso à teoria, acredita-se que anticorpos “agli” possam ter um perfil de maior segurança e estabilidade in vivo. Métodos de produção de anticorpos aglicosilatados, tendo função desejada de moléculas executoras são encontrados por exemplo em WO 2005/018572, que se acha incorporada como referência, na sua totalidade.
[000149] Em certos anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados aqui descritos, a parte Fc pode ser modificada para diminuir a função das moléculas executoras utilizando técnicas conhecidas na técnica. Por exemplo, a eliminação ou desativação (através de mutações pontuais ou por outros meios), de um domínio de região constante poderá reduzir a ligação do receptor Fc do anticorpo modificado circulante, aumentando assim a localização do tumor. Em outros casos, pode ser que as modificações da região constante coerentes com a invenção presente, moderem a ligação do complemente e, assim, reduzam a meia-vida do soro e a associação não específica de uma citotoxina conjugada. Mas outras modificações da região constante podem ser usadas para modificar os elos dissulfeto ou as porções de oligossacarídeos que permitem melhor localização devido à especificidade dos antígenos ou à flexibilidade dos anticorpos. O perfil fisiológico resultante, a biodisponibilidade e outros efeitos bioquímicos das modificações, tais como localização do tumor, biodistribuição e meia-vida do soro, podem ser facilmente medidos e quantificados utilizando técnicas imunológicas bastante conhecidas sem experimentação indevida.
[000150] Formas modificadas de anticorpos ou fragmentos de ligação a antígenos, variantes ou seus derivados da invenção podem ser criadas a partir dos anticorpos precursores ou totais usando técnicas conhecidas na técnica. Técnicas exemplares são discutidas em mais detalhes aqui.
[000151] Em certas modalidades as regiões variáveis e constantes dos anticorpos ou fragmentos de ligação ao antígeno, variantes ou seus derivados da invenção são integralmente humanas. Anticorpos totalmente humanos podem ser produzidos usando técnicas que são conhecidas na técnica e conforme descrito aqui. Por exemplo, anticorpos totalmente humanos contra um antígeno específico podem ser preparados pela administração do antígeno a um animal transgênico que foi modificado para produzir esses anticorpos em resposta ao desafio antigênico, mas cujos loci endógenos foram desativados. Técnicas exemplares que podem ser utilizadas para fabricar tais anticorpos são descritas nas patentes U.S.: 6.150.584, 6.458.592, 6.420.140. Outras técnicas são conhecidas na técnica. Anticorpos totalmente humanos podem também ser produzidos por diferentes tecnologias de exibição, por exemplo, exibição de bacteriófagos ou outros sistemas de exibição de vírus, conforme descrito em maior detalhe noutro lugar aqui.
[000152] Anticorpos ou fragmentos de ligação ao antígeno, variantes ou seus derivados da invenção podem ser produzidos ou fabricados usando técnicas que são conhecidas na técnica. Em certas modalidades, moléculas de anticorpos ou seus fragmentos são “produzidas recombinantemente", ou seja, são produzidas usando a tecnologia do DNA recombinante. Técnicas exemplares para fabricação de moléculas de anticorpos ou seus fragmentos são discutidas em mais detalhe noutro lugar aqui.
[000153] Anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção também incluem os derivados que são modificados, por exemplo, a fixação covalente de qualquer tipo de molécula ao anticorpo, de modo tal que a fixação covalente não impede o anticorpo de especificamente ligar-se ao seu epitopo cognato. Por exemplo, mas não por meio de limitação, os derivados de anticorpos incluem anticorpos que foram modificados, por exemplo, por glicosilação, acetilação, prelação, fosforilação, amidação, derivação por grupos de proteção/bloqueio conhecidos, clivagem proteolítica, ligação a um ligante celular ou a outra proteína, etc. Quaisquer das inúmeras modificações químicas podem ser realizadas por técnicas conhecidas, incluindo entre outras, a clivagem química específica, acetilação, formilação, síntese metabólica da tunicamicina, etc. Além disso, os derivados podem conter um ou mais aminoácidos não clássicos.
[000154] Em certas modalidades, os anticorpos ou fragmentos de ligação a antígeno ou seus derivados da invenção não irão suscitar uma resposta imune deletéria no animal a ser tratado, por exemplo, em um ser humano. Em certas modalidades, moléculas de ligação, por exemplo, anticorpos ou fragmentos de ligação a antígeno da invenção são derivados de um paciente, por exemplo, um paciente humano, e são posteriormente utilizadas na mesma espécie da qual foram obtidas, por exemplo, de um ser humano, aliviando ou minimizando a ocorrência de respostas imunes deletéria.
[000155] A desimunização também pode ser usada para diminuir a imunogenicidade de um anticorpo. Conforme utilizado aqui, o termo "desimunização" inclui a modificação de um anticorpo para modificar epitopos de células T (vide, por exemplo, WO9852976A1, W00034317A2). Por exemplo, as sequências VH e VL do anticorpo de partida são analisadas e um “mapa” dos epitopos das células T humanas de cada região V mostra a localização dos epitopos com relação às regiões determinantes de complementaridade (CDRs) e outros resíduos-chave dentro da sequência. Epitopos de células T individuais do mapa dos epitopos de células T são analisados para identificar as substituições de aminoácidos com um baixo risco de alterar a atividade do anticorpo final. Uma série de sequências VH e VL alternativas é concebida compreendendo combinações de substituições de aminoácidos e essas sequências são posteriormente incorporadas em uma variedade de polipeptídeos de ligação, por exemplo, anticorpos específicos de neoepítopos ou seus fragmentos imunoespecíficos para uso nos métodos de diagnóstico e tratamento métodos descritos aqui, que são, então, testados quanto à função. Normalmente, entre 12 e 24 anticorpos variantes são produzidos e testados. Os genes da cadeia leve e pesada completos, compreendendo regiões C humanas e V modificadas, são então clonados em vetores de expressão e os plasmídeos subsequentes introduzidos nas linhas de células para a produção do anticorpo total. Os anticorpos são então comparados em ensaios biológicos e bioquímicos adequados e a variante ideal é identificada.
[000156] Os anticorpos monoclonais podem ser preparados com uma grande variedade de técnicas conhecidas na técnica, incluindo a utilização de hibridomas, recombinante e tecnologias de exibição de bacteriófago ou uma combinação dos mesmos. Por exemplo, os anticorpos monoclonais podem ser produzidos utilizando técnicas de hibridomas incluindo aquelas conhecidas na técnica e ensinadas, por exemplo, em Harlow et al., Antibodies'. A Laboratory Manual, Cold Spring Harbor Laboratory Press, 2nd ed. (1988); Hammerling et al., Em: Monoclonal Antibodies and T-Cell Hybridomas Elsevier, NY, 563- 681 (1981) (as ditas referências incorporadas como referência em sua totalidade). O termo "anticorpos monoclonais", como utilizado neste documento não se limita aos anticorpos produzidos através de tecnologia de hibridomas. O termo "anticorpo monoclonal"refere-se a um anticorpo que é obtido a partir de um único clone, incluindo qualquer clone eucariótico, procariótico ou de bacteriófago e não o método pelo qual ele é produzido. Assim, o termo "anticorpos monoclonais" não se limita aos anticorpos produzidos através da tecnologia de hibridomas. Os anticorpos monoclonais podem ser preparados usando uma grande variedade de técnicas conhecidas na técnica. Em certas modalidades, os anticorpos da presente invenção são derivados de células humanas B que tenham sido imortalizadas através da transformação com o vírus Epstein-Barr, conforme descrito aqui.
[000157] No processo bem-conhecido de hibridomas (Kohler et al., Nature256:495 (1975)), os linfócitos de relativa vida curta ou mortais, de um mamífero, por exemplo, as células B derivadas de um sujeito humano como aqui descrito, são combinadas com uma linha de células tumorais imortais (por exemplo, uma linha de células de mieloma), assim, produzindo células híbridas ou "hibridomas" que são imortais e capazes de produzir anticorpo geneticamente codificado da célula B. Os híbridos resultantes são segregados em cepas genéticas únicas por seleção, diluição e recrescimento com dada cepa individual compreendendo genes específicos para a formação de um único anticorpo. Eles produzem anticorpos, que são homogêneos contra um antígeno desejado e, em referência à sua ascendência genética pura, são denominados "monoclonais".
[000158] As células de hibridomas assim preparados são semeadas e cultivadas em um meio de cultura adequado que preferivelmente contém uma ou mais substâncias que inibem o crescimento ou sobrevivência das células parentais de mieloma, não fundidas. Aqueles versados na técnica observarão que reagentes, linhas de células e meio para a formação, seleção e crescimento de hibridomas são comercialmente disponíveis a partir de um certo número de fontes e protocolos padronizados estão bem estabelecidos. Geralmente, o meio de cultura no qual as células de hibridomas estão crescendo é testado quanto à produção de anticorpos monoclonais contra o antígeno desejado. A especificidade de ligação dos anticorpos monoclonais produzidos por células de hibridomas é determinada por ensaios in vitro,como a imunoprecipitação, radioimunoensaio (RIA) ou ensaio imunoabsorvente ligado a enzimas (ELISA) ou ensaios de ligação de neoepítopos tal como descrito aqui. Após as células de hibridomas serem identificadas, as quais produzem anticorpos da especificidade, afinidade e/ou atividade desejadas, os clones podem ser subclonados pelos procedimentos de diluição limitadores e cultivados pelos métodos-padrão (Goding, Monoclonal Antibodies'. Principles and Practice, Academic Press, pp 59-103 (1986)). Será ainda observado que os anticorpos monoclonais secretados pelos subclones podem ser separados do meio de cultura, o fluido de ascite ou soro por processos convencionais de purificação, como, por exemplo, proteína-A, cromatografia de hidroxilapatita, eletroforese em gel, diálise ou cromatografia por afinidade.
[000159] Fragmentos de anticorpos que reconhecem epitopos específicos poderão ser gerados pelas técnicas conhecidas. Por exemplo, fragmentos Fab e F(ab')2 podem ser produzidos recombinantemente ou por clivagem proteolítica de moléculas de imunoglobulina, utilizando enzimas como a papaína (para produzir fragmentos Fab) ou pepsina (para a produção de fragmentos F(ab')2). Os fragmentos F(ab')2 contêm a região variável, a região constante de cadeia leve e o domínio CH1 da cadeia pesada.
[000160] Anticorpos completamente humanos, tais como aqui descritos, são particularmente desejáveis para tratamento terapêutico de pacientes humanos. Anticorpos humanos podem ser produzidos por uma variedade de métodos conhecidos na técnica, incluindo métodos de exibição de bacteriófago descritos acima usando bibliotecas de anticorpos derivadas de sequências de imunoglobulinas humanas. Vide também a patente dos EUA N°. 4.444.887 e 4.716.111; e publicações PCT WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735 e WO 91/10741, cada um dos quais é incorporado aqui como referência na sua totalidade. Anticorpos humanos da presente invenção são isolados, por exemplo, de pacientes sem sintomas mas afetados com o risco de desenvolvimento de um distúrbio como, por exemplo, a doença de Alzheimer ou de um paciente com o distúrbio, mas com um curso da doença excepcionalmente estável.
[000161] Em outra modalidade, anticorpos monoclonais desejados codificadores de DNA podem ser prontamente isolados e sequenciados utilizando procedimentos convencionais (por exemplo, usando sondas de oligonucleotídeos que são capazes de se ligar especificamente aos genes codificadores das cadeias pesadas e leves de anticorpos murinos). As células de hibridomas isoladas e subclonadas servem como uma fonte preferida de tal DNA. Uma vez isolado, o DNA pode ser colocado em vetores de expressão, que são então transfectados em células procarióticas ou eucarióticas, tais como, entre outras, células E. coli, células COS símias, células ovarianas de hamster chinês (CHO) ou células de mieloma que, de outro modo, não produzem imunoglobulinas. Mais particularmente, o isolamento do DNA (que pode ser sintético, como descrito aqui) pode ser utilizado para clonar sequências de regiões constantes e variáveis para a fabricação dos anticorpos, tal como descrito em Newman et a!., patente dos EUA N°. 5.658.570, depositada em 25 de janeiro de 1995, que é incorporada como referência neste documento. Essencialmente, isso implica a extração de RNA de células selecionadas, conversão para cDNA e amplificação por PCR utilizando iniciadores específicos de lg. Iniciadores adequados para esta finalidade também são descritas na Patente U.S. N°. 5.658.570. Como será discutido com mais detalhe a seguir, células transformadas expressando o anticorpo desejado podem ser produzidas em quantidades relativamente grandes para propiciar suprimentos clínicos e comerciais de imunoglobulina.
[000162] Em uma modalidade, um anticorpo da invenção inclui pelo menos uma CDR de cadeia pesada ou leve de uma molécula de anticorpo. Em outra modalidade, um anticorpo da invenção compreende pelo menos duas CDRs de uma ou mais moléculas de anticorpos. Em outra modalidade, um anticorpo da invenção inclui pelo menos três CDRs de uma ou mais moléculas de anticorpos. Em outra modalidade, um anticorpo da invenção inclui pelo menos quatro CDRs de uma ou mais moléculas de anticorpos. Em outra modalidade, um anticorpo da invenção compreende pelo menos cinco CDRs de uma ou mais moléculas de anticorpos. Em outra modalidade, um anticorpo da invenção inclui pelo menos seis CDRs de uma ou mais moléculas de anticorpos. Moléculas exemplares de anticorpos compreendendo pelo menos uma CDR que podem ser incluídas nos anticorpos do sujeito são descritas aqui.
[000163] Em uma modalidade específica, a sequência de aminoácidos dos domínios variáveis de cadeia pesada e/ou leve pode ser inspecionada para identificar as sequências das regiões de determinação de complementaridade (CDRs) através de métodos que são bem-conhecidos na técnica, por exemplo, por comparação com sequências de aminoácidos conhecidos de outras regiões variáveis de cadeia leve e pesada para determinar as regiões de hipervariabilidade das sequências. Usando técnicas de DNA recombinantes de rotina, uma ou mais CDRs podem ser inseridas nas regiões de estrutura, por exemplo, nas regiões de estrutura humana. As regiões de estrutura podem ser regiões de estrutura que ocorrem naturalmente ou de consenso e, preferivelmente, regiões de estrutura humana (vide, por exemplo, Chothia etal., J. Mol. Biol. 278:457-479 (1998) para uma lista de regiões de estrutura humana). Em certas modalidades, o polinucleotídeo gerado pela combinação das regiões de estrutura e CDRs codifica um anticorpo específico que se liga especificamente a pelo menos um epitopo de um polipeptídeo desejado. Em certas modalidades, uma ou mais substituições de aminoácidos podem ser feitas nas regiões de estrutura para, por exemplo, melhorar a ligação do anticorpo ao seu antígeno. Além disso, esses métodos podem ser usados para fazer substituições de aminoácidos ou exclusões de um ou mais resíduos de cisteína da região variável que fazem parte de uma ligação dissulfetos intra-cadeias para gerar moléculas de anticorpos que não possuem uma ou mais ligações dissulfetos intra- cadeias. Outras alterações nos polinucleotídeos são abrangidas pela presente invenção e na habilidade da técnica.
[000164] Alternativamente, as técnicas descritas para a produção de anticorpos de cadeia única (patente dos EUA N°. 4.694.778; Bird, Science 242:423-442 (1988); Huston et al., Proc. Natl. Acad. Sei. E.U.A. 85:5879-5883 (1988) e Ward etal.,Nature 334:544-554 (1989)) podem ser adaptadas para produzir anticorpos de cadeia única. Os anticorpos de cadeia única são formados pela ligação dos fragmentos de cadeia pesada e leve da região Fv através de uma ponte de aminoácidos, resultando em um anticorpo de cadeia única. Técnicas para a montagem de fragmentos Fv funcionais em E colltambém podem ser utilizadas (Skerra etal., Science 242:1038-1041 (1988)).
[000165] Em outra modalidade, linfócitos podem ser selecionados pela micromanipulação e pelos genes variáveis isolados. Por exemplo, células mononucleares sanguíneas periféricas podem ser isoladas de um mamífero imunizado ou naturalmente imune, por exemplo, um humano e expostos à cultura por cerca de 7 dias, in vitro.As culturas podem passar por varredura quanto a IgGs específicas que satisfaçam os critérios de varredura. Células de cavidades positivas podem ser isoladas. Células B produtoras de lg individuais podem ser isoladas por FACS ou por sua identificação em um ensaido de placas hemolíticas mediadas por complemento. Células B produtoras de lg podem ser micromanipuladas para um tubo e os genes VH e VL podem ser amplificados, utilizando, por exemplo, TR-PCR. Os genes VH e VL podem ser clonados em um vetor de expressão de anticorpo e transfectados para células (por exemplo, células procarióticas ou eucarióticas) para expressão.
[000166] Alternativamente, linhas produtoras de anticorpos podem ser selecionadas e expostas à cultura através de técnicas bem- conhecidas para o artesão versado. Essas técnicas são descritas em uma variedade de manuais de laboratório e publicações primárias. Neste contexto, as técnicas adequadas para o uso da invenção, tal como descrito abaixo estão descritas no documento Current Protocols in Immunology, Coligan et al., Eds., Green Publishing Associates and Wiley-lnterscience, John Wiley and Sons, New York (1991), que é aqui incorporado como referência na sua totalidade, incluindo os suplementos.
[000167] Anticorpos da presente invenção podem ser produzidos por qualquer método conhecido na técnica para a síntese de anticorpos, em particular, através da síntese química ou de preferência, pelas técnicas de expressão recombinantes como descrito aqui.
[000168] Em uma modalidade, um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado da invenção compreende uma região constante sintética onde um ou mais domínios são parcialmente ou totalmente eliminados ("anticorpos de domínio excluído"). Em certas modalidades, anticorpos modificados compatíveis compreenderão constructos de domínio excluído ou variantes onde todo o domínio CH2 foi removido (constructos ACH2). Para outras modalidades, um peptídeo de ligação curta pode ser usado em lugar do domínio excluído para propiciar flexibilidade e liberdade de movimento para a região variável. Aqueles versados na técnica irão observar que tais constructos são particularmente preferidas devido às propriedades regulatórias do domínio CH2 na taxa catabólica do anticorpo. Constructos de domínios excluídos podem ser obtidos usando-se um vetor que codifica um domínio constante humano IgGi (vide, por exemplo, WO 02/060955A2 e WO02/096948A2). Este vetor é projetado para eliminar o domínio CH2 e fornecer um vetor sintético que expressa uma região constante de lgG1 de domínio excluído.
[000169] Em certas modalidades, anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da presente invenção são minicorpos. Minicorpos podem ser fabricados usando os métodos descritos na técnica (Vide, por exemplo, a patente U.S. 5.837.821 ou WO 94/09817A1).
[000170] Em uma modalidade, um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado da invenção compreende uma cadeia pesada de imunoglobulina contendo exclusão ou substituição de alguns ou até mesmo de um único aminoácido, desde que permita a associação entre as subunidades monoméricas. Por exemplo, a mutação de um único aminoácido em áreas selecionadas do domínio CH2 pode ser suficiente para reduzir substancialmente a ligação de Fc e assim aumentar a localização do tumor. Do mesmo modo, pode ser desejável simplesmente excluir aquela parte de um ou mais domínios de regiões constantes que controlam a função da molécula executora (por exemplo, ligação de complementos) a ser modulada. Estas exclusões parciais das regiões constantes podem melhorar as características selecionadas do anticorpo (meia-vida do soro), deixando intactas outras funções desejáveis associadas com o domínio da região constante do sujeito. Além disso, conforme mencionado anteriormente, as regiões constantes dos anticorpos descritos podem ser sintéticas através da mutação ou substituição de um ou mais aminoácidos, o que reforça o perfil da construção resultante. A este respeito, pode ser possível para interromper a atividade propiciada por um sítio de ligação conservado (por exemplo, ligação de Fc), enquanto que substancialmente mantém a configuração e o perfil imunogênico do anticorpo modificado. Mas outras modalidades incluem a adição de um ou mais aminoácidos para a região constante para melhorar as características desejáveis, tais como função da molécula executora ou propiciar maior fixação da citotoxina ou carboidrato. Em tais modalidades, pode ser desejável inserir ou replicar sequências específicas derivadas dos domínios de região constante selecionados.
[000171] A presente invenção também propicia anticorpos que compreendem, consistem essencialmente em ou consistem em, variantes (incluindo derivados) de moléculas de anticorpos (por exemplo, as regiões VH e/ou regiões VL) aqui descritas, cujos anticorpos ou seus fragmentos se ligam imunoespecificamente a um polipeptídeo associado ao distúrbio ou fragmento ou variante seu. Normas técnicas-padrão por aqueles de habilidade na técnica podem ser usadas para introduzir mutações na sequência de nucleotídeos que codificam um anticorpo, incluindo, entre outros, meutagênese dirigida pelo sítio e mutagênese mediada pela PCR que resultam em substituições de aminoácidos. Preferivelmente, as variantes (incluindo derivados) codificam menos de 50 substituições de aminoácidos, menos de 40 substituições de aminoácidos, menos de 30 substituições de aminoácidos, menos de 25 substituições de aminoácidos, menos de 20 substituições de aminoácidos, menos de 15 substituições de aminoácidos, menos de 10 substituições de aminoácidos, menos de 5 substituições de aminoácidos, menos de 4 substituições de aminoácidos, menos de 3 substituições de aminoácidos ou menos de 2 substituições de aminoácidos em relação à região de referência VH: CDR1-VH, VH-CDR2, VH-CDR3; região VL, VL-CDR1, VL-CDR2 ou VL-CDR3. A "substituição de aminoácidos conservadora" é aquela em que o resíduo de aminoácido é substituído por um resíduo de aminoácido contendo uma cadeia lateral com uma carga similar. Famílias de resíduos de aminoácidos com cadeias laterais com cargas similares foram definidas na técnica. Essas famílias incluem aminoácidos com cadeias laterais básicas (por exemplo, lisina, arginina, histidina), cadeias laterais acídicas (por exemplo, ácido aspártico, ácido glutâmico), cadeias laterais polares não carregadas (por exemplo, glicínia, asparagina, glutamina, serina, treonina, tirosina, cisteína), cadeias laterais não polares (por exemplo, alanina, valina, leucina, isoleucina, prolina, fenilalanina, metionina, triptofano), cadeias laterais beta-ramificadas (por exemplo, treonina, valina, isoleucina) e cadeias laterais aromáticas (por exemplo, tirosina, fenilalanina, triptofano, histidina). Alternativamente, mutações podem ser introduzidas aleatoriamente ao longo de todo ou parte da sequência de codificação, como por mutagénese de saturação e os mutantes resultantes podem sofrer varredura quanto à atividade biológica para identificar mutantes que retenham atividade (por exemplo, a capacidade de vincular um polipeptídeo associado ao distúrbio).
[000172] Por exemplo, é possível introduzir mutações somente nas regiões de estrutura ou somente nas regiões CDR de uma molécula de anticorpo. Mutações introduzidas podem ser mutações de falso sentido silenciosas ou neutras, por exemplo, têm pouco ou nenhum efeito sobre a capacidade de um anticorpo ligar-se ao antígeno, na verdade, algumas dessas mutações não alteram qualquer que seja a sequência de aminoácidos. Esses tipos de mutações podem ser úteis para otimizar o uso do códon ou melhorar a produção de anticorpos do hibridoma. As regiões de codificação otimizadas pelo códon que codificam os anticorpos da presente invenção estão descritas em outro lugar neste documento. Alternativamente, mutações de sentido falso não neutras poderão alterar a capacidade do anticorpo de se ligar ao antígeno. A localização da maioria das mutações de sentido falso e neutras provavelmente deverá ser nas regiões de estrutura, enquanto a localização da maioria das mutações de sentido falso não neutras deverá ser na CDR, embora esta não seja uma exigência absoluta. Alguém versado na técnica seria capaz de conceber e testar moléculas mutantes com as propriedades desejadas tais como nenhuma alteração na atividade de ligação ao antígeno ou alteração na atividade de ligação (por exemplo, melhorias na atividade de ligação ao antígeno ou mudança na especificidade do anticorpo). Após a mutagênese, a proteína codificada poderá rotineiramente ser expressa e a atividade funcional e/ou biológica da proteína codificada (por exemplo, a capacidade de ligar imunoespecificamente pelo menos um epitopo de um polipeptídeo associado ao distúrbio) pode ser determinada através de técnicas descritas aqui ou por rotineiramente modificar as técnicas conhecidas na técnica. IV. Polinucletoídeos que Codificam Anticorpos
[000173] De acordo com o acima exposto, a presente invenção também refere-se a um polinucleotídeo que codifica uma molécula de ligação da presente invenção, como por exemplo, um anticorpo. No caso do anticorpo, o polinucleotídeo pode codificar pelo menos uma região variável de uma cadeia de imunoglobulina do anticorpo descrito acima. O polinucleotídeo da invenção que codifica o anticorpo acima descrito pode ser, por exemplo, o DNA, cDNA, RNA ou DNA ou RNA produzido sinteticamente ou uma molécula de ácido nucleico quimérica produzida recombinantemente compreendendo qualquer desses polinucleotídeos isoladamente ou em combinação. Preferivelmente o dito polinucleotídeo é parte de um vetor. Esses vetores podem incluir mais genes, tais como genes marcadores que permitem a seleção do dito vetor em uma célula hospedeira adequada e sob condições adequadas. Preferivelmente, o polinucleotídeo da invenção está operativamente ligado às sequências de controle da expressão permitindo a expressão nas células procarióticas ou eucarióticas. A expressão do dito polinucleotídeo compreende a transcrição do polinucleotídeo para um mRNA traduzível. Os elementos reguladores que asseguram a expressão em células eucarióticas, preferivelmente células mamíferas, são bem-conhecidos daqueles versados na técnica. Eles geralmente incluem sequências reguladoras que asseguram a iniciação da transcrição e, opcionalmente, sinais de poli-A que asseguram o término da transcrição e a estabilização do transcrito. Elementos reguladores adicionais podem incluir elementos transcricionais, bem como potenciadores traducionais e/ou regiões de promotores naturalmente associadas ou heterólogas.
[000174] Um polinucleotídeo que codifica um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados pode ser composto de qualquer polirribonucleotídeo ou polidesoxirribonucleotídeo, que pode ser RNA ou DNA inalterado ou RNA ou DNA modificado. Por exemplo, um polinucleotídeo que codifica um anticorpo ou fragmento de ligação a antígeno ou seu derivado pode ser composto de um DNA de fita única ou dupla, DNA que é uma mistura de regiões de fita única e dupla, RNA de fita única e dupla e RNA que é uma mistura de regiões de fita única e dupla, moléculas híbridas compreendendo DNA e RNA que podem ser de fita única ou, mais normalmente, de fita dupla ou uma mistura de regiões de fita única e dupla. Além disso, um polinucleotídeo que codifica um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado pode ser composto de regiões de fita tripla compreendendo RNA ou DNA ou RNA e DNA. Um polinucleotídeo que codifica um anticorpo ou fragmento de ligação ao antígeno, variante ou seu derivado pode também conter uma ou mais bases modificadas ou espinhas dorsais de DNA ou RNA modificadas para estabilidade ou por outras razões. Bases "modificadas" incluem, por exemplo, bases tritiladas e bases incomuns tais como inosina. Uma variedade de alterações pode ser feita ao DNA e RNA, assim, o "polinucleotídeo" engloba formas quimicamente, enzimaticamente ou metabolicamente modificadas.
[000175] Um polinucleotídeo isolado que codifica uma variante não natural de um polipeptídeo derivado de uma imunoglobulina (por exemplo, uma parte de cadeia pesada ou parte de cadeia leve de imunoglobulina) pode ser criado pela introdução de uma ou mais substituições de nucleotídeos, adições ou exclusões na sequência nucleotídica da imunoglobulina tal que uma ou mais substituições, adições ou exclusões de aminoácidos são introduzidas na proteína codificada. As mutações podem ser introduzidas por técnicas-padrão, como a mutagênese dirigida ao sítio e mutagênese mediada pela PCR. Preferivelmente, as substituições conservadoras de aminoácidos são feitas em um ou mais resíduos de aminoácidos não essenciais.
[000176] Como é sabido, o RNA pode ser isolado a partir das células de hibridomas originais ou de outras células transformadas pelas técnicas-padrão, tais como a extração e precipitação de isotiocianato de guanidínio seguidas da centrifugação ou cromatografia. Onde desejável, o mRNA pode ser isolado do RNA total por técnicas-padrão tais como a cromatografia em celulose-oligo dT. Técnicas adequadas são familiares na técnica.
[000177] Em uma modalidade, cDNAs que codificam as cadeias leves e pesadas do anticorpo podem ser produzidos, simultaneamente ou separadamente, por meio da transcriptase reversa e polimerase do DNA em conformidade com métodos bem-conhecidos. A PCR pode ser iniciada pelos iniciadoresde região constante de consenso ou por iniciadoresmais específicos com base nas sequências de aminoácidos e de DNA de cadeia leve e pesada publicadas. Conforme discutido acima, a PCR também pode ser utilizada para isolar clones de DNA que codificam as cadeias leves e pesadas de anticorpos. Neste caso, as bibliotecas podem passar por uma varredura pelos iniciadores de consenso ou sondas homólogas maiores, tal como sondas de região constante dos camundongos.
[000178] O DNA, normalmente o DNA plasmidial, pode ser isolado das células através de técnicas conhecidas na técnica, restrição mapeada e sequenciada, em conformidade com as técnicas-padrão bem-conhecidas apresentadas em detalhe, por exemplo, nas referências precedentes relativas às técnicas de DNA recombinante. Evidentemente, o DNA pode ser sintético, de acordo com a presente invenção, em qualquer ponto durante o processo de isolamento ou posterior análise.
[000179] Em uma modalidade, a presente invenção propicia um polinucleotídeo isolado compreendendo, consistindo essencialmente em ou consistindo em um ácido nucleico que codifica uma região variável de cadeia pesada de imunoglobulina (VH), onde pelo menos uma das CDRs da região variável de cadeia pesada ou pelo menos duas CDRs-VH da região variável de cadeia pesada são, pelo menos, 80%, 85%, 90% ou 95% idênticos às sequências de referência de aminoácidos CDR1-VH, VH-CDR2 ou VH-CDR3 dos anticorpos descritos aqui. Alternativamente, as regiões VH-CDR1, VH-CDR2 e VH-CDR3 da VH são pelo menos 80%, 85%, 90% ou 95% idênticas às sequências de referência de aminoácidos VH-CDR1, VH-CDR2 e VH- CDR3 de cadeia pesada descritas aqui. Assim, de acordo com esta modalidade, uma região variável de cadeia pesada da invenção tem sequências de polipeptídeos VH-CDR1, VH-CDR2 ou VH-CDR3 relacionadas às sequências de polipeptídeos mostradas na Tabela 4.
[000180] Em outra modalidade, a presente invenção propicia um polinucleotídeo isolado compreendendo, consistindo essencialmente em ou consistindo em um ácido nucleico que codifica uma região variável de cadeia leve de imunoglobulina (VL), onde pelo menos uma das VL-CDRs da região variável de cadeia leve ou pelo menos duas das VL-CDRs da região variável de cadeia leve são pelo menos 80%, 85%, 90% ou 95% idênticas às sequências de referência de aminoácidos VL-CDR1, VL-CDR2 ou VL-CDR3 de cadeia leve dos anticorpos descritos aqui. Alternativamente, as regiões VL-CDR1, VL- CDR2 e VL-CDR3 da VL são pelo menos 80%, 85%, 90% ou 95% idênticas às sequências de referência de aminoácidos VL-CDR1, VL- CDR2 e VL-CDR3 de cadeia leve dos anticorpos descritos aqui. Assim, de acordo com esta modalidade, uma região variável de cadeia leve da invenção tem sequências de polipeptídeos VL-CDR1, VL- CDR2 ou VL-CDR3 relacionadas às sequências de polipeptídeos mostradas na Tabela 4.
[000181] Em outra modalidade, a presente invenção propicia um polinucleotídeo isolado, compreendendo, consistindo essencialmente em, ou consistindo em um ácido nucleico codificando uma região variável de cadeia pesada de imunoglobulina (VH) na qual as regiões VH-CDR1, VH-CDR2 e VH-CDR3 têm sequências de polipeptídeos que são idênticos aos grupos VH-CDR1, VH-CDR2 e VH-CDR3 apresentados na Tabela 4.
[000182] Tal como é conhecida na técnica, a “identidade de sequência" entre os dois polipeptídeos ou dois polinucleotídeos é determinada pela comparação da sequência de aminoácidos ou ácidos nucleicos de um polipeptídeo ou polinucleotídeo com a sequência de um segundo polipeptídeo ou polinucleotídeo. Quando discutido aqui, se um determinado polipeptídio é pelo menos cerca de 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% ou 95% idêntico a outro polipeptídeo, pode ser determinado por meio de métodos e programas de computador/software conhecidos na técnica, como o seguinte, mas não limitado a este: BESTFIT program (Wisconsin Sequence Analysis Package, Version 8 for Unix, Genetics Computer Group, University Research Park, 575 Science Drive, Madison, Wl 53711). O BESTFIT utiliza o algoritmo de homologia local de Smith e Waterman, Advances in Applied Mathematics 2:482-489 (1981), para encontrar o melhor segmento de homologia entre as duas sequências. Ao utilizar o BESTFIT ou qualquer outro programa de alinhamento de sequência para determinar se uma determinada sequência, por exemplo, é 95% idêntica a uma sequência de referência, de acordo com a presente invenção, os parâmetros são definidos, naturalmente, de tal forma que o percentual de identidade é calculado ao longo de todo o comprimento da sequência de polipeptídeos de referência e que as lacunas na homologia de até 5% do número total de aminoácidos na sequência de referência são permitidas.
[000183] A este respeito, a pessoa versada na técnica facilmente reconhecerá que os polinucleotídeos que codificam pelo menos o domínio variável da cadeia leve e/ou pesada podem codificar os domínios variáveis de ambas as cadeias de imunoglobulina ou de somente uma. Da mesma forma, os ditos polinucleotídeos podem estar sob o controle do mesmo promotor ou podem ser separadamente controlados pela expressão. Elementos reguladores possíveis que permitem a expressão em células hospedeiras procarióticas compreendem, por exemplo, o promotor PL, 1ac, trp ou tac em E. coli e exemplos para elementos reguladores que permitem a expressão em células hospedeiras eucarióticas são o promotor AOX1 ou GAL1 em levedo ou o promotor CMV-, SV40-.RSV-, o potencializador CMV-, SV40- ou um íntron da globina em mamíferos e outras células de animais. Elementos lado a lado que são responsáveis pela iniciação da transcrição de tais elementos reguladores podem também compreender os sinais de término de transcrição, tais como o sítio SV40-poli-A ou o sítio tk-poli-A, a jusante do polinucleotídeo. Além disso, dependendo do sistema de expressão usado, as sequências líderes capazes de direcionar o polipeptídeo para um compartimento celular ou secretá-lo para o meio podem ser adicionadas à sequência codificadora do polinucleotídeo da invenção e são bem-conhecidos na técnica. A(s) sequência(s) líder(es) é(são) montada(s) na fase apropriada com sequências de tradução, iniciação e término, e, preferivelmente, uma sequência líder capaz de direcionar a secreção da proteína traduzida ou uma porção sua, para o espaço periplásmico ou meio extracelular. Opcionalmente, a sequência heteróloga poderá codificar uma proteína de fusão incluindo um peptídeo de identificação com N- ou C-terminal imprimindo as características desejadas, por exemplo, a estabilização ou a purificação simplificada do produto recombinante expresso. Neste contexto, vetores de expressão adequados são conhecidos na técnica, tais como o vetor de expressão cDNA Okayama-Berg pcDV1 (Pharmacia), pCDM8, pRc/CMV, pcDNAI, pcDNA3 (Invitrogen) ou pSPORTI (GIBCO BRL). Preferivelmente, as sequências de controle da expressão serão os sistemas do promotor eucariótico em vetores capazes de transformar ou transfectar células hospedeiras eucarióticas, mas as sequências de controle para hospedeiros procarióticos podem também ser usadas. Uma vez que o vetor tenha sido incorporado no hospedeiro apropriado, o hospedeiro é mantido sob condições adequadas para expressão de alto nível das sequências de nucleotídeos e, conforme desejado, a coleta e a purificação das cadeias leves de imunoglobulina, das cadeias pesadas, dos dímeros das cadeias leves/pesadas e dos anticorpos intactos, dos fragmentos de ligação ou de outras formas de imunoglobulina podem seguir; vide, Beychok, Cells of Immunoglobulin Synthesis, Academic Press, N.Y., (1979).
[000184] A presente invencao tambem inclui fragmentos dos polinucleotídeos da invenção, conforme descrito em outro lugar neste documento. Além disso, os polinucleotídeos que codificam os polinucleotídeos de fusão, os fragmentos Fab e outros derivados, conforme descrito aqui, são também contemplados pela invenção.
[000185] Os polinucleotídeos podem ser produzidos ou fabricados por qualquer método conhecido na técnica. Por exemplo, se a sequência de nucleotídeos do anticorpo for conhecida, um polinucleotídeo codificador do anticorpo pode ser montado a partir de oligonucleotídeos sintetizados quimicamente (por exemplo, conforme descrito em Kutmeier et ai., BioTechniques77:242 (1994)), o que, resumidamente, envolve a síntese de sobreposição das porções contendo oligonucleotídeos da sequência codificadora do anticorpo, o recozimento e a ligação daqueles oligonucleotídeos, e então a amplificação dos oligonucleotídeos ligados pela PCR.
[000186] Alternativamente, um polinucleotídeo codificador de um anticorpo ou um fragmento de ligação a antígeno, variante ou seu derivado, pode ser gerado de um ácido nucleico a partir de uma fonte adequada. Se um clone contendo um ácido nucleico codificador de um anticorpo em particular não estiver disponível, mas a sequência da molécula do anticorpo for conhecida, um ácido nucleico codificador do anticorpo pode ser quimicamente sintetizado ou obtido de uma fonte adequada (por exemplo, uma biblioteca de cDNA de anticorpo ou uma biblioteca de cDNA gerada de ou ácido nucleico, preferivelmente poli A+RNA, isolado de qualquer tecido ou células expressando o anticorpo específico de neoantígeno, tais como células de hibridomas selecionadas para expressar um anticorpo) pela amplificação da PCR utilizando iniciadores sintéticos hibridizáveis para as terminações 3' e 5' da sequência ou pela clonagem usando uma sonda de oligonucleotídeo específica para a sequência de genes em particular para identificar, por exemplo, um clone de cDNA a partir de uma biblioteca de cDNA que codifica o anticorpo. Os ácidos nucleicos amplificados gerados pela PCR podem então ser clonados nos vetores de clonagem replicáveis usando qualquer método bem-conhecido na técnica.
[000187] Uma vez que a sequência de nucleotídeos e a sequência de aminoácidos correspondente do anticorpo ou do fragmento de ligação ao antígeno, variante ou seu derivado for determinada, sua sequência de nucleotídeos pode ser manipulada usando métodos bem-conhecidos na técnica para a manipulação da sequência de nucleotídeos, por exemplo, técnicas de DNA recombinantes, mutagênese direcionada ao sítio, PCR, etc. (vide, por exemplo, as técnicas descritas em Sambrook et al., Molecular Cloning, A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y. (1990) e Ausubel et al., eds., Current Protocols in Molecular Biology, John Wiley & Sons, NY (1998), que são ambos incorporados por referência aqui em sua totalidade) para gerar anticorpos contendo uma sequência de aminoácidos diferente, por exemplo, para criar substituições de aminoácidos, exclusões e/ou inserções de aminoácidos. V. Expressão de Polipeptídeos de Anticorpos
[000188] A presente invenção também envolve um método para produção de células capazes de expressar um anticorpo da invenção ou sua(s) cadeia(s) de imunoglobulina(s) correspondente(s), compreendendo células geneticamente de engenharia com o polinucleotídeo ou com o vetor da invenção. As células obtidas pelo método da invenção podem ser usadas, por exemplo, para testar a interação do anticorpo da invenção com seu antígeno.
[000189] Em seguida à manipulação do material genético isolado para propiciar anticorpos ou fragmentos de ligação de antígenos, variantes ou seus derivados da invenção, os polinucleotídeos codificadores dos anticorpos são normalmente inseridos em um vetor de expressão para introdução nas células hospedeiras que podem ser usados para produzir a quantidade desejada do anticorpo.
[000190] A expressão recombinante de um anticorpo ou fragmento, derivado ou seu análogo, por exemplo, uma cadeia pesada ou leve de um anticorpo que se liga a uma molécula-alvo descrita aqui. Uma vez que o polinucleotídeo codificador de uma molécula de anticorpo ou uma cadeia pesada ou leve de um anticorpo ou sua porção (preferivelmente contendo o domínio variável da cadeia pesada ou leve) da invenção tiver sido obtido, o vetor para a produção da molécula do anticorpo poderá ser produzido pela tecnologia do DNA recombinante usando técnicas bem-conhecidas na técnica. Assim, os métodos para preparação de uma proteína pela expressão de um polinucleotídeo contendo um anticorpo codificador da sequência de nucleotídeos estão descritos aqui. Os métodos que são bem- conhecidos por aqueles versados na técnica podem ser usados para construir vetores de expressão contendo sequências de codificação de anticorpos e sinais de controle de transcrição e de tradução apropriados. Esses métodos incluem, por exemplo, técnicas de DNA recombinantes in vitro,técnicas sintéticas e recombinação genética in vivo. A invenção, portanto, propicia vetores replicáveis compreendendo uma sequência codificadora de uma molécula de anticorpo da invenção ou uma cadeia pesada ou leve sua, ou um domínio variável de cadeia pesada ou leve, operavelmente ligados a um promotor. Tais vetores podem incluir a sequência de nucleotídeos codificadores da região constante da molécula do anticorpo (vide, por exemplo, PCT Publication WO 86/05807; PCT Publication WO 89/01036; e Patente U.S. N°. 5.122.464) e o domínio variável do anticorpo pode ser clonado em tal vetor para expressão da cadeia pesada ou leve inteira.
[000191] A presente invenção refere-se a vetores, particularmente plasmídeos, cosmídeos, vírus e bacteriófagos usados convencionalmente na engenharia genética, que compreende um polinucleotídeo codificador do antígeno ou preferivelmente um domínio variável de uma cadeia de imunoglobulina de um anticorpo da invenção; opcionalmente em combinação com um polinucleotídeo da invenção que codifica o domínio variável de outra cadeia de imunoglobulinas do anticorpo da invenção. Preferivelmente, o dito vetor é um vetor de expressão e/ou um vetor de transferência ou de direcionamento de genes. Os vetores de expressão derivados dos vírus tais como retrovirus, vírus vaccinia, vírus associados a adeno, vírus da herpes ou vírus papiloma bovino, podem ser usados para entrega dos polinucleotídeos ou vetor da invenção na população de células direcionadas. Métodos que são bem-conhecidos por aqueles versados na técnica podem ser usados para construir vetores virais; vide, por exemplo, as técnicas descritas em Sambrook, Molecular Cloning A Laboratory Manual, Cold Spring Harbor Laboratory (1989) N.Y. e Ausubel, Current Protocols in Molecular Biology, Green Publishing Associates and Wiley Interscience, N.Y. (1994). Alternativamente, os polinucleotídeos e os vetores da invenção podem ser reconstituídos em lipossomas para a entrega das células-alvo. Os vetores contendo os polinucleotídeos da invenção (por exemplo, o(s) domínio(s) variável(eis) pesado(s) e/ou leve(s) das sequências de codificação e das sequências de controle de expressão das cadeias de imunoglobulinas) podem ser transferidos para a célula hospedeira por métodos bem-conhecidos, que variam dependendo do tipo de hospedeiro celular. Por exemplo, a transfecção de cloreto de cálcio é comumente utilizada para células procarióticas, ao passo que o tratamento com fosfato de cálcio ou a eletroporação pode ser utilizado para outros hospedeiros celulares; vide Sambrook, supra.
[000192] O termo "vetor" ou "vetor de expressão" é usado aqui com o significado de vetores usados em conformidade com a presente invenção como veículo para introdução em expressão de um gene desejado em uma célula hospedeira. Conforme de conhecimento daqueles versados na técnica, tais vetores podem facilmente ser selecionados do grupo consistindo em plasmídeos, fagos, vírus e retro-vírus. Em geral, os vetores compatíveis com a presente invenção compreenderão um marcador de seleção, sítios de restrição apropriados para facilitar a clonagem do gene desejado e a capacidade de entrar e/ou replicar em células eucarióticas ou procarióticas.
[000193] Para os fins desta invenção, inúmeros sistemas de vetores de expressão podem ser empregados. Por exemplo, uma classe de vetor utiliza elementos do DNA que são derivados de vírus de animais tais como o vírus papiloma bovino, vírus polioma, adenovirus, vírus vaccinia, baculovírus, retro-vírus (RSV, MMTV ou MOMLV) ou vírus SV40. Outros envolvem o uso de sistemas policistrônicos com sítios de ligação de ribossomos internos. Além disso, as células que integraram o DNA em seus cromossomos podem ser selecionadas pela introdução de um ou mais marcadores que permitem a seleção de células hospedeiras transfectadas. O marcador pode propiciar a prototrofia para um hospedeiro auxotrófico, resistência ao biocídio (por exemplo, antibióticos) ou resistência a metais pesados tais como cobre. O gene do marcador selecionável pode ser diretamente ligado às sequências do DNA para ser expresso ou introduzido na mesma célula pela co-transformação. Elementos adicionais podem também ser necessários para a síntese ideal do mRNA. Estes elementos podem incluir sequências de sinais, sinais de divisão, como também promotores de transcrição, potencializadores e sinais de término.
[000194] Em modalidades particularmente preferidas, os genes das regiões variáveis clonadas são inseridos em um vetor de expressão em conjunto com os genes das regiões constantes de cadeia pesada e leve sintéticos (preferivelmente humanos), conforme discutido acima. Em uma modalidade, isto é efetuado usando um vetor de expressão patenteado da Biogen IDEC, Inc., denominado NEOSPLA (descrito na patente U.S. 6.159.730). Este vetor contém o promotor/potencializador do citomegalovírus, o promotor principal da betaglobina de camundongos, a origem SV40 de réplica, a sequência de poliadenilação de hormônios de crescimento bovino, o éxon 1 e o éxon 2 de fosfotransferase de neomicina, o gene de reductase de di- hidrofolato e a sequência líder. Descobriu-se que este vetor resulta em expressão de nível muito alto de anticorpos quando da incorporação de genes de regiões variáveis e constantes, transfecção em células CHO, seguido pela seleção em meio contendo G418 e amplificação de metotrexato. É claro que qualquer vetor de expressão que for capaz de elicitar a expressão em células eucarióticas pode ser usado na presente invenção. Exemplos de vetores adequados incluem, mas não estão limitados a plasmídeos pcDNA3, pHCMV/Zeo, pCR3.1, pEFI/His, pIND/GS, pRc/HCMV2, pSV40/Zeo2, pTRACER-HCMV, pUB6/V5-His, pVAX1 e pZeoSV2 (disponíveis pela Invitrogen, San Diego, CA), e plasmídeo pCI (disponível pela Promega, Madison, Wl). Em geral, a varredura de grandes números de células transformadas para aquelas que expressam níveis adequadamente altos se as cadeias pesada e leve de imunoglobulina for experimentação de rotina, a qual pode ser realizada, por exemplo, por sistemas robóticos. Os sistemas de vetores são também ensinados nas patentes U.S. N°. 5.736.137 e 5.658.570, cada qual está incorporada aqui como referência em sua totalidade. Este sistema propicia altos níveis de expressão, por exemplo, >30 pg/célula/dia. Outros sistemas de vetores exemplares são descritos, por exemplo, na patente U.S. 6.413.777.
[000195] Em outras modalidades preferidas, os anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção podem ser expressos usando constructos policistrônicos tais como aqueles descritos na Publicação do Pedido de Patente U.S. N°. 2003-0157641 A1, depositado em 18 de novembro de 2002 e incorporado aqui em sua totalidade. Nesses novos sistemas de impressão, múltiplos produtos de genes de interesse tais como cadeias pesadas e leves de anticorpos podem ser produzidos a partir de um único constructo policistrônico. Esses sistemas com vantagem usam um sítio de entrada de ribossomo interno (IRES) para propiciar níveis relativamente altos de anticorpos. Sequências IRES compatíveis estão descritas na Patente U.S. N°. 6.193.980 que se encontra também incorporada aqui. Aqueles versados na técnica observarão que tais sistemas de expressão podem ser usados para efetivamente produzir a faixa ampla de anticorpos descrita no pedido presente.
[000196] Mais geralmente, uma vez que o vetor ou sequência de DNA codificadora de uma subunidade monomérica do anticorpo foi elaborada, o vetor de expressão pode ser introduzido em uma célula hospedeira apropriada. A introdução do plasmídeo na célula hospedeira pode ser realizada através de várias técnicas bem- conhecidas por aqueles versados na técnica. Estas incluem, mas não estão limitadas à transfecção (incluindo eletroforese e eletroporação), fusão de protoplastos, precipitação de fosfato de cálcio, fusão de células com DNA envelopado, microinjeção e infecção com vírus intacto. Vide Ridgway, A. A. G. "Mammalian Expression Vectors"Vectors, Rodriguez and Denhardt, Eds., Butterworths, Boston, Mass., Chapter 24.2, pp. 470-472 (1988). Normalmente, a introdução de plasmídeos no hospedeiro se dá via eletroporação. As células hospedeiras que acolhem o constructo da expressão são cultivadas sob condições apropriadas à prodção das cadeias leves e das cadeias pesadas e testadas quanto à síntese das proteínas da cadeia pesada e/ou leve. Técnicas de ensaio exemplares incluem ensaio imunosorbente ligado a enzimas (ELISA), radioimunoensaio (RIA) ou análise de selecionador de células ativadas por fluorescênica (FACS), imuno-histoquímica e similar.
[000197] O vetor de expressão é transferido para uma célula hospedeira pelas técnicas convencionais e as células transfectadas são então expostas à cultura através de técnicas convencionais para produzir um anticorpo para uso nos métodos descritos aqui. Assim, a invenção inclui células hospedeiras contendo um polinucleotídeo codificador de um anticorpo da invenção ou uma cadeia pesada ou leve sua, operavelmente ligada a um promotor heterólogo. Em modalidades preferidas para a expressão de anticorpos de cadeia dupla os vetores codificadores de ambas cadeias pesada e leve podem ser co-expressos na célula hospedeira para expressão da molécula de imunoglobulina inteira, conforme detalhado abaixo.
[000198] A presente invenção ainda refere-se a células hospedeiras transformadas com um polinucleotídeo ou vetor da invenção. A dita célula hospedeira pode ser uma célula procariótica ou eucariótica. O polinucleotídeo ou vetor da invenção que está presente na célula hospedeira pode ser integrado ao genoma da célula hospedeira ou pode ser mantido extracromossomalmente. A célula hospedeira pode ser qualquer célula procariótica ou eucariótica, tal como uma célula de inseto, fungo, planta, animal ou ser humano. As células de fungos preferidas, por exemplo, aquelas do genus Saccharomyces, em particular aquelas da espécie S. cerevisiae. O termo “procariótico” significa incluir todas as bactérias que possam ser transformadas ou transfectadas com as moléculas de DNA ou RNA para a expressão de um anticorpo da invenção ou das cadeias de imunoglobulinas correspondentes. Os hospedeiros procarióticos podem incluir bactérias gram negativas como gram positivas tais como, por exemplo, E. coli, S. typhimurium, Serratia marcescens e Bacillus subtilis. O termo “eucariótico” significa incluir levedo, planta vascular, inseto e preferivelmente células mamíferas, mais preferivelmente células HEK 293, NSO e CHO. Dependendo do hospedeiro empregado em um procedimento de produção recombinante, os anticorpos ou cadeias de imunoglobulinas codificados pelo polinucleotídeo da presente invenção podem ser glicosilados ou podem ser não glicosilados. Anticorpos da invenção ou das cadeias de imunoglobulinas correspondentes podem também incluir um resíduo de aminoácido de metionina inicial. Um polinucleotídeo da invenção pode ser usado para transformar ou transfectar o hospedeiro usando qualquer uma das técnicas comumente conhecidas por aqueles versados na técnica. Além disso, métodos para preparação de genes fundidos, operavelmente ligados e para expressão dos mesmos em, por exemplo, células mamíferas e bactérias são bem-conhecidos na técnica (Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, 1989). Os constructos e métodos genéticos descritos ali podem ser utilizados para expressão do anticorpo da invenção ou de cadeias de imunoglobulinas correspondentes em hospedeiros eucarióticos ou procarióticos. Em geral, vetores de expressão contendo sequências de promotores que facilitam a transcrição eficiente do polinucleotídeo inserido são usados em relação com o hospedeiro. O vetor de expressão normalmente contém uma origem de replicação, um promotor e um exterminador, como também genes específicos que são capazes de propiciar a seleção fenotípica das células transformadas. As células de fontes adequadas para as sequências de DNA e as células hospedeiras para a expressão e secreção da imunoglobulina podem ser obtidas a partir de inúmeras fontes, tais como a publicação American Type Culture Collection ("Catalogue of Cell Lines and Hybridomas", Fifth edition (1985) Rockville, Maryland, EUA, que está incorporada aqui como referência). Além disso, animais transgênicos, preferivelmente mamíferos, compreendendo células da invenção podem ser usados para a produção em larga escala de anticorpos da invenção.
[000199] Assim, em outra modalidade, a presente invenção refere-se a um método para a produção de uma molécula de ligação específica à proteína associada ao distúrbio, por exemplo, um anticorpo ou um fragmento de ligação ou sua(s) cadeia(s) de imunoglobulinas, o dito método compreendendo (a) Exposição de uma célula à cultura conforme descrito acima; e (b) Isolamento do dito antígeno, da molécula de ligação, do anticorpo ou do fragmento de ligação ou de sua(s) cadeia(s) de imunoglobulina da cultura.
[000200] Hospedeiros transformados podem ser cultivados em fermentadores e expostos à cultura de acordo com as técnicas conhecidas na técnica para obtenção do crescimento ideal das células. Uma vez expressos, os anticorpos totais, seus dímeros, cadeias leves e pesadas individuais ou outras formas de imunoglobulinas da presente invenção, podem ser purificados de acordo com os procedimentos padrão da técnica, incluindo precipitação de sulfato de amónio, colunas de afinidade, cromatografia de colunas, eletroforese de gel e similares; ver, Scopes, "Protein Purification", Springer Verlag, N.Y. (1982). O anticorpo ou sua(s) cadeia(s) de imunoglobulina(s) correspondente(s) da invenção podem então ser isolados do meio de cultivo, dos lisatos celulares ou das porções das membranas celulares. O isolamento e a purificação dos, por exemplo, anticorpos ou cadeias de imunoglobulinas expressos recombinantemente da invenção podem se dar através de qualquer meio convencional tais como, por exemplo, separações cromatográficas preparatórias ou separações imunológicas tais como aquelas envolvendo o uso de anticorpos monoclonais ou policlonais direcionados, por exemplo, contra a região constante do anticorpo da invenção. Será evidente àqueles versados na técnica que os anticorpos da invenção podem ser ainda acoplados as outras porções para, por exemplo, aplicações de direcionamento e formação da imagem em fármaco. Tal acoplamento pode ser conduzido quimicamente após a expressão do anticorpo ou do antígeno ao sítio de fixação ou o produto do equipamento pode ser projetado para o anticorpo ou antígeno da invenção no nível do DNA. Os DNAs são então expressos em um sistema de hospedeiros adequado e as proteínas expressas são coletadas e recaracterizadas, se necessário.
[000201] As imunoglobulinas substancialmente puras de pelo menos cerca de 90 a 95% de homogeneidade são preferidas e de 98 a 99% ou mais de homogeneidade mais preferidas, para usos farmacêuticos. Uma vez purificados, parcialmente ou até a homogeneidade, conforme desejado, os anticorpos podem, então, ser usados terapeuticamente (incluindo extra corporalmente) ou no desenvolvimento ou realização de procedimentos de ensaios.
[000202] A célula hospedeira pode ser co-transfectada com dois vetores de expressão da invenção, o primeiro vetor codificando um polipeptídeo derivado de cadeia pesada e o segundo vetor codificando um polipeptídeo derivado de cadeia leve. Os dois vetores podem conter marcadores selecionáveis idênticos que possibilitam a expressão igual de polipeptídeos de cadeia pesada e leve. Alternativamente, um vetor único pode ser usado que codifica ambos polipeptídeos de cadeia pesada e leve. Em tais situações, a cadeia leve é colocada com vantagem antes da cadeia pesada para impedir um excesso de cadeia pesada sem toxicidade (Proudfoot, Nature 322:52 (1986); Kohler, Proc. Natl. Acad. Sci. USA 77:2197 (1980)). As sequências codificadoras para as cadeias pesada e leve podem compreender o cDNA ou o DNA genômico.
[000203] Conforme usado aqui, o termo “células hospedeiras"refere- se a células que acolhem vetores construídos usando técnicas de DNA recombinante e codificando pelo menos um gene heterólogo. Em descrições dos processos para isolamento de anticorpos dos hospedeiros recombinantes, os termos "célula" e "cultura de células" são usados intercambiavelmente para denotar a fonte do anticorpo, a menos que esta esteja claramente especificada de outro modo. Em outras palavras, a recuperação do polipeptídeo das “células” pode significar a partir das células totais dilatadas ou de cultura de células contendo ambas as células do meio e suspensas.
[000204] Uma variedade de sistemas de vetor de expressão de hospedeiro pode ser utilizada para expressar moléculas de anticorpos para uso nos métodos descritos aqui. Tais sistemas de expressão de hospedeiros representam veículos pelos quais as sequências codificadoras podem ser produzidas e subsequentemente purificadas, mas também representam células que podem, quando transformadas ou transfectadas com as sequências codificadoras de nucleotídeos apropriados, expressar uma molécula de anticorpo da invenção in situ. Estas incluem, entre outras, a micro-organismos tais como bactérias (por exemplo, E. coli, B. subtilis) transformados com vetores de expressão de DNA de bacteriófago recombinante, DNA plasmídeo ou DNA cosmídeo contendo sequências de codificação de anticorpos; levedo (por exemplo, Saccharomyces, Pichia) transformados com vetores de expressão de levedo recombinantes contendo sequências codificadoras de anticorpos; sistemas de células de insetos infectados com vetores de expressão de vírus recombinante (por exemplo, baculovírus) contendo sequências codificadoras de anticorpos; sistemas de células de plantas infectadas com vetores de expressão de vírus recombinante (por exemplo, vírus mosaico de couve-flor, CaMV; vírus mosaico de tabaco, TMV) ou transformados com vetores de expressão de plasmídeo recombinante (por exemplo, plasmídeo Ti) contendo sequências codificadoras de anticorpos; ou sistemas de células mamíferas (por exemplo, células COS, CHO, BLK, 293, 3T3) acolhendo constructos de expressão recombinantes contendo promotores derivados do genoma das células mamíferas (por exemplo, promotor de metalotioneína) ou de vírus mamíferos (por exemplo, o promotor tardio do adenovirus, o promotor 7,5K do vírus vaccinia). Preferivelmente, células bacterianas tais como Escherichia coli e mais preferivelmente, células eucarióticas, especialmente para a expressão da molécula de anticorpo recombinante total, são usadas para a expressão de uma molécula de anticorpo recombinante. Por exemplo, células mamíferas tais como células ovarianas de hamster chinês, em conjunto com um vetor tal como o elemento promotor do gene precoce intermediário principal do citomegalovírus humano são um sistema de expressão eficaz para anticorpos (Foecking et ai., Gene 45:101 (1986); Cockett et ai., Bio/Technology 8:2 (1990)).
[000205] A linha de células hospedeiras usada para expressão da proteína é frequentemente de origem mamífera: aqueles versados na técnica têm a capacidade de preferencialmente determinar linhas de células hospedeiras em particular que são mais adaptadas ao produto de gene desejado a ser expresso ali. Linhas de células hospedeiras exemplares incluem, entre outras, CHO (Ovário de Hamster Chinês), DG44 e DUXB11 (linhas de Ovários de Hamster Chinês, DHFR menos), HELA (carcinoma cervical humano), CVI (linha de rim de macaco), COS (um derivado de CVI com antígeno SV40 T), VERY, BHK (rim de hamster bebê), MDCK, 293, WI38, R1610 (fibroblasto de hamster chinês) BALBC/3T3 (fibroblasto de camundongo), HAK (linha de rim de hamster), SP2/O (mieloma de camundongo), P3x63-Ag3.653 (mieloma de camundongo), BFA-1c1BPT (células endoteliais bovinas), RAJI (linfócito humano) e 293 (rim humano). Células CHO são particularmente preferidas. As linhas de células hospedeiras encontram-se normalmente disponíveis através dos serviços comerciais, da The American Tissue Culture Collection ou da literatura publicada.
[000206] Além disso, uma cepa de células hospedeiras pode ser escolhida que module a expressão das sequências inseridas ou modifique e processe o produto de genes no modo específico desejado. Tais modificações (por exemplo, a glicosilação) e o processamento (por exemplo, a clivagem) dos produtos proteicos podem ser importantes para a função da proteína. Células hospedeiras diferentes possuem características e mecanismos específicos para o processamento pós-tradução e modificação das proteínas e produtos de genes. As linhas de células apropriadas ou sistemas hospedeiros podem ser escolhidos para assegurar a modificação e o processamento corretos da proteína estrangeira expressa. Para esta finalidade, as células hospedeiras eucarióticas que possuem o maquinário celular para processamento apropriado do transcrito primário, da glicosilação e fosforilação do produto dos genes podem ser usadas.
[000207] Para produção de longo prazo, de alto rendimento de proteínas recombinantes, a expressão estável é preferida. Por exemplo, linhas das células que expressam estavelmente a molécula do anticorpo podem ser projetadas. Em vez de usar vetores de expressão que contenham origens vitais de replicação, as células hospedeiras podem ser transformadas com o DNA controlado pelos elementos de controle de expressão apropriados (por exemplo, promotor, potencializador, sequências, exterminadores de transcrição, sítios de polidadenilação, etc.) e um marcador selecionável. Em seguida à introdução do DNA estrangeiro, pode se deixar as células projetadas crescerem por 1-2 dias em meios enriquecidos, e então, serem comutadas para meios seletivos. O marcador selecionável no plasmídeo recombinante confere resistência à seleção e permite que as células estavelmente integrem o plasmídeo em seus cromossomas e cresçam para formar focique, por sua vez, podem ser clonados e expandidos para linhas de células. Este método pode, com vantagem, ser usado para projetar linhas de células que estavelmente expressam a molécula do anticorpo.
[000208] Inúmeros sistemas de seleção podem ser usados, incluindo, entre outros, a cinase de timidina de vírus herpes simplex (Wigler et al., Cell11:223 (1977)), fosforribosiltransferase de ipoxantina-guanina (Szybalska &Szybalski, Proc. Natl. Acad. Sei. USA 48:202 (1992)) e os genes de fosforribosiltransferase de adenina (Lowy et al., Cell22:817 1980) podem ser empregados em células tk-, hgprt- ou aprt, respectivamente. Também, a resistência antimetabólito pode ser usada como base da seleção para os genes seguintes: dfr, que confere resistência ao metrotrexato (Wigler et al., Natl. Acad. Sei. USA 77:357 (1980); O'Hare et al., Proc. Natl. Acad. Sei. USA 78:1527 (1981)); gpt, que confere resistência ao ácido micofenólico (Mulligan &Berg, Proc. Natl. Acad. Sei. USA 78:2072 (1981)); neo, que confere resistência ao aminoglicosídeo G-418 Clinical Pharmacy12:488-505; Wu and Wu, Biotherapy 3:87-95 (1991); Tolstoshev, Ann. Rev. Pharmacol. Toxicol. 32:573-596 (1993); Mulligan, Science 260:926-932 (1993); and Morgan and Anderson, Ann. Rev. Biochem. 62:191-217 (1993); TIB TECH 11(5): 155-215 (May, 1993); e hygro, que confere resistênica à higromicina (Santerre et al., Gene 30:147 (1984). Métodos comumente conhecidos na técnica da tecnologia do DNA recombinante que podem ser usados, são descritos em Ausubel et al. (eds.), Current Protocols in Molecular Biology, John Wiley & Sons, NY (1993); Kriegler, Gene Transfer and Expression, A Laboratory Manual, Stockton Press, NY (1990); e nos capítulos 12 e 13, Dracopoli et al. (eds.), Current Protocols in Human Genetics, John Wiley & Sons, NY (1994); Colberre-Garapin et al. J. Mol. Biol. 150A (1981), que são incorporados neste documento como referência em sua totalidade.
[000209] Os níveis de expressão de uma molécula de anticorpo podem ser aumentados pela amplificação do vetor (para uma revisão, ver Bebbington and Hentschel, The use of vectors based on gene amplification for the expression of cloned genes in mammalian cells in DNA cloning, Academic Press, New York, Vol. 3. (1987)). Quando urn marcador no sistema de vetores que expressa o anticorpo for amplificável, o aumento no nível do inibidor presente na cultura da célula hospedeira aumentar o número de cópias do gene do marcador. Visto que a região amplificada é associada com o gene do anticorpo, a produção do anticorpo também aumentará (Crouse et al., Mol. Cell. Biol.3:257 (1983)).
[000210] A produção in vitropermite a escala ascendente para propiciar grandes quantidades dos polipeptídeos desejados. Técnicas para cultivo de células mamíferas sob condições de cultura de tecidos são conhecidas na técnica e incluem cultura de suspensão homogênea, por exemplo, em um reator suspenso ou em um reator contínuo de agitador ou cultura celular imobilizada ou presa, por exemplo, em fibras ocas, microcápsulas, em microesferas de agarose ou cartuchos de cerâmica. Se necessário, e/ou desejado, as soluções de polipeptídeos pode ser purificada pelos métodos usuais de cromatografia como, por exemplo, filtração em gel, cromatografia de troca iônica, cromatografia sobre DEAE-celulose ou cromatografia de (imuno-)afinidade, por exemplo, após a biossíntese preferencial de um polipeptídeo de região de dependência sintética ou antes de ou após a etapa de cromatografia HIC exposta aqui.
[000211] Genes que codificam anticorpos ou fragmentos de ligação a antígenos, variantes ou seus derivados da invenção podem também ser expressos de células não-mamíferas tais como de bactérias ou insetos ou fungos ou células de plantas. As bactérias que facilmente absorvem ácidos nucleicos incluem membros do Enterobacteriaceae, como cepas de Escherichia coli e Salmonella;Bacillaceae, tais como Bacillus subtilis; Pneumococcus; Streptococcuse Haemophilus influenzae.Será ainda observado que, quando expresso em bactérias, os polipeptídeos heterólogos normalmente tornam-se parte dos corpos de inclusão. Os polipeptídeos heterólogos devem ser isolados, purificados e posteriormente agrupados em moléculas funcionais. Quando as formas tetravalentes dos anticorpos forem desejadas, as subunidades se auto-agruparão em anticorpos tetravalentes (WO02/096948A2).
[000212] Em sistemas bacterianos, inúmeros vetores de expressão podem ser, com vantagem, selecionados dependendo do uso pretendido para a molécula de anticorpo sendo expressa. Por exemplo, quando uma grande quantidade deste tipo de proteína deve ser produzida, para a geração de composições farmacêuticas de uma molécula de anticorpo, vetores que direcionam a expressão de altos níveis de produtos de proteínas de fusão que são prontamente purificados podem ser desejáveis. Esses vetores incluem, entre outros, o vetor pUR278 de expressão do E. coli, mas não se limitam a este. (Ruther et al., EMBO J. 2:1791 (1983)), no qual o anticorpo que codifica a sequência pode ser ligado individualmente no vetor na moldura com a região de codificação 1acZ, de modo que a proteína de fusão é produzida; vetores pIN (Inouye & Inouye, Nucleic Acids Res. 73:3101-3109 (1985); Van Heeke & Schuster, J. Biol. Chem. 24:5503- 5509 (1989)) e similares. Os vetores pGEX podem também ser usados para expressar os polipeptídeos estrangeiros como proteínas de fusão com a glutationa S-transferase (GST). Em geral, essas proteínas de fusão são solúveis e podem facilmente ser purificadas a partir de células lisadas por adsorção e com ligação às esferas de glutationa- agarose da matriz seguido pela extração na presença de glutationa livre. Os vetores pGEX são projetados para incluir sítios de trombina ou clivagem de protease de fator Xa de modo que o produto do gene alvo clonado pode ser liberado de uma porção de GST.
[000213] Além de procariontes, micróbios eucarióticos também podem ser utilizados. Saccharomyces cerevisiae ou levedo comum de padaria, é o mais comumente usado dentre os micro-organismos eucarióticos, embora uma série de outras cepas seja comumente disponível, por exemplo, Pichia pastoris.
[000214] Para a expressão em Saccharomyces, o plasmídeo YRp7, por exemplo, (Stinchcomb et al., Nature 282:39 (1979); Kingsman et ai., Gene 7:141 (1979); Tschemper et al., Gene 10A57 (1980)) é comumente utilizado. Este plasmídeo já contém o gene TRP1 que determina um marcador de seleção para uma cepa mutante de levedo sem a capacidade de crescer em triptofano, por exemplo ATCC N°. 44076 ou PEP4-1 (Jones, Genetics85:12 (1977)). A presença da lesão trpl como uma característica do genoma da célula hospedeira do levedo então propicia um ambiente eficaz para detectar a transformação pelo crescimento na ausência de triptofano.
[000215] Em um sistema de insetos, o vírus Autographa californica da poliedrose nuclear (AcNPV) é normalmente usado como um vetor para expressar genes estranhos. O vírus cresce em células de Spodoptera frugiperda. A sequência de codificação do anticorpo pode ser clonada individualmente em regiões não-essenciais (por exemplo, o gene poliedrina) do vírus e colocados sob controle de um promotor AcNPV (por exemplo, o promotor poliedrina).
[000216] Uma vez que a molécula de um anticorpo da invenção tenha sido recombinantemente expressa, ela pode ser purificada por qualquer método conhecido na técnica para a purificação de uma molécula imunoglobulina, por exemplo, por cromatografia (por exemplo, troca iônica, afinidade, especialmente por afinidade para o antígeno específico após a Proteína A e pela cromatografia de coluna dimensionadora), centrifugação, solubilidade diferencial ou por qualquer outra técnica-padrão para a purificação de proteínas. Alternativamente, um método preferido para o aumento da afinidade de anticorpos da invenção é descrito em E.U. 2002 0123057 A1. VI. Proteínas de fusão e conjugados
[000217] Os anticorpos da presente invenção podem incluir um novo domínio, o dito domínio sendo ligado por ligações covalentes ou não covalentes. A ligação pode ser baseada na fusão genética de acordo com os métodos conhecidos na técnica e descritos acima ou pode ser realizada através, por exemplo, da ligação cruzada química, conforme descrição, por exemplo, no pedido internacional WO94/04686. O domínio adicional presente na proteína de fusão que inclui o anticorpo da invenção pode ser preferencialmente ser ligado por um ligador flexível, com vantagem um ligador de polipeptídeo, em que o dito ligador de polipeptídeo compreende aminoácidos ligados a peptídeos, hidrofílicos, plurais de comprimento suficiente para abranger a distância entre a extremidade de terminação-C do dito outro domínio e a extremidade N-terminal do anticorpo da invenção ou vice-versa. O agente terapêutico ou diagnosticamente ativo pode ser acoplado ao anticorpo da invenção ou a um fragmento de ligação a antígeno seu por diversos meios. Isto inclui, por exemplo, proteínas de fusão de cadeia única compreendendo as regiões variáveis do anticorpo da invenção acopladas por métodos covalentes, tais como ligações peptídicas, ao agente terapêutica ou diagnosticamente ativo. Outros exemplos são moléculas que incluem pelo menos um fragmento de ligação a antígeno acoplado às moléculas adicionais, covalentemente ou não covalentemente incluem aqueles na lista ilustrativa não- limitantea seguinte. Traunecker, Int. J. Cancer Surp. SuDP 7 (1992), 51-52, descrevem o reagente bioespecífico janusin no qual a região Fv dirigida ao CD3 é acoplada ao CD4 solúvel ou a outros ligantes, tais como OVCA e IL-7. Do mesmo modo, as regiões variáveis do anticorpo da invenção podem ser construídas nas moléculas Fv e acopladas a ligantes alternativos tais como aqueles ilustrados no citado artigo. Higgins, J. Infect Disease 166 (1992), 198-202, descreveu um anticorpo hetero-conjugado composto de OKT3 ligado de forma cruzada a um anticorpo direcionado a uma sequência específica na região V3 do GP120. Tais anticorpos hetero-conjugados podem também ser construídos usando pelo menos as regiões variáveis contidas no anticorpo dos métodos da invenção. Exemplos adicionais de anticorpos específicos incluem aqueles descritos por Fanger, Cancer Treat. Res. 68 (1993), 181-194 e por Fanger, Crit. Rev. Immunol. 12 (1992), 101-124.
[000218] Em uma nova modalidade da presente invenção, a molécula de ligação, o anticorpo, a cadeia de imunoglobulina ou um fragmento de ligação seu ou o antígeno é marcado de forma detectável. Agentes de marcação podem ser acoplados quer direta ou indiretamente aos anticorpos ou antígenos da invenção. Um exemplo de acoplamento indireto se dá através da utilização de uma porção espaçadora.
[000219] Assim, a atividade biológica das moléculas de ligação, por exemplo, anticorpos aqui identificados, sugere que eles tenham afinidade suficiente para torná-los candidatos potenciais à localização do fármaco para células expressando as estruturas superficiais da célula e do tecido doentes, respectivamente. Este direcionamento e ligação às células poderíam ser úteis para a produção de agentes terapeuticamente ou diagnosticamente ativos e para a produção de genes/terapia de genes. As moléculas/partículas com um anticorpo da invenção se ligariam especificamente às células/tecidos expressando a forma variante da proteína patológica e, portanto, poderíam ter uso diagnóstico e terapêutico. Assim, a molécula de ligação, por exemplo, o anticorpo ou seu fragmento de ligação ao antígeno da presente invenção poderíam ser marcados (por exemplo, metal fluorescente, radioativo, enzima, magnético nuclear, pesado) e usados para detectar alvos in vivo ou in vitro,incluindo “imunoquímica” como testes in vitro. In vivo, eles poderíam ser usados de forma similar às técnicas de imagem de medicina nuclear para detectar tecidos, células ou outros materiais expressando o neoepítopo. Assim, em outra modalidade, a presente invenção refere-se ao uso de uma molécula de ligação ou a um anticorpo da presente invenção ou ao seu fragmento de ligação para a preparação de uma composição para detecção in vivo de direcionamento ou de um agente terapêutico e/ou diagnóstico para uma proteína associada ao distúrbio sem cérebro, detectando, suprimindo ou reduzindo a formação de agregados de proteínas ou conformações patológicas em um sujeito, para aperfeiçoamento da cognição ou retardamento ou reversão do declínio cognitivo associado a doenças ou para extração extra-corpórea de compostos patológicos ou seus precursores dos fluidos corporais.
[000220] Em certas modalidades, o polipeptídeo do anticorpo compreende uma sequência de aminoácidos ou uma ou mais porções não normalmente associadas com um anticorpo. Modificações exemplares são descritas mais detalhadamente abaixo. Por exemplo, um fragmento de anticorpo fv de cadeia única da invenção pode compreender uma sequência de ligadores flexíveis ou pode ser modificado para adicionar uma metade funcional (por exemplo, PEG, um fármaco, uma toxina ou um rótulo.)
[000221] Um polipeptídeo de anticorpo da invenção pode compreender, consistir essencialmente em ou consistir em uma proteína de fusão. As proteínas de fusão são moléculas quiméricas, que incluem, por exemplo, um domínio de ligação a antígeno de imunoglobulina com pelo menos um sítio de ligação de alvo e pelo menos uma porção heteróloga, isto é, uma porção com a qual ela não está naturalmente ligada na natureza. As sequências de aminoácidos podem normalmente existir em proteínas separadas que são reunidas no polipeptídeo de fusão ou podem normalmente existir na mesma proteína, mas são colocadas em um novo arranjo no polipeptídeo de fusão. As proteínas de fusão podem ser criadas, por exemplo, por síntese química ou através da criação e tradução de um polinucleotídeo em que as regiões de peptídeos são codificadas na relação desejada.
[000222] O termo "heterólogos", tal como aplicado a um polinucleotídeo ou a um polipeptídeo, significa que o polinucleotídeo ou o polipeptídeo é derivado de uma entidade distinta daquela do restante da entidade à qual ele está sendo comparado. Por exemplo, tal como utilizado aqui, um "polipetídeo heterólogo" a ser fundido a um anticorpo ou um fragmento de ligação a antígeno, variante ou análogo seu, é derivado de um polipeptídeo não de imunoglobulina da mesma espécie ou de um polipeptídeo de imunoglobulina ou não de imunoglobulina de uma espécie diferente.
[000223] Conforme discutido em mais detalhes em outros pontos aqui, os anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção poderão ser ainda recombinantemente fundidos a um polipeptídeo heterólogo no N- ou C-terminal ou quimicamente conjugados (incluindo conjugações covalentes e não covalentes) aos polipeptídeos ou outras composições. Por exemplo, os anticorpos podem ser recombinantemente fundidos ou conjugados a moléculas úteis como rótulos nos ensaios de detecção e nas moléculas executoras tais como polipeptídeos heterólogos, fármacos, radionuclídeos ou toxinas. Vide por exemplo, as publicações PCT WO 92/08495, WO 91/14438, WO 89/12624; Patente dos EUA N°. 5.314.995; e PE 396.387.
[000224] Anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção podem ser compostos de aminoácidos unidos uns aos outros pelas ligações de peptídeos ou por ligações de peptídeos modificados, ou seja, isósteres de peptídeos e podem conter aminoácidos diferentes dos 20 aminoácidos codificados com gene. Os anticorpos podem ser modificados por processos naturais, tais como processamento pós-tradução ou por técnicas de modificação química que são bem-conhecidas na técnica. Tais alterações são bem descritas em textos básicos e em monografias mais detalhadas, bem como em volumosa literatura de investigação. As alterações podem ocorrer em qualquer lugar do anticorpo, incluindo a espinha dorsal do peptídeo, as cadeias laterais de aminoácidos e as terminações amino e carboxila ou em porções tais como carboidratos. Será observado que o mesmo tipo de alteração pode estar presente no mesmo grau ou em diferentes graus em diversos sites em um determinado anticorpo. Além disso, um dado anticorpo pode conter vários tipos de modificações. Os anticorpos podem ser ramificados, por exemplo, como um resultado de ubiquitinação e eles podem ser cíclicos, com ou sem ramificação. Anticorpos cíclicos, ramificados e cíclicos ramificados podem resultar de processos naturais pós-tradução ou podem ser produzidos pelos métodos sintéticos. As modificações incluem acetilação, acilação, ribosilação-ADP, amidação, fixação covalente de flavina, fixação covalente de uma porção heme, fixação covalente de um nucleotídeo ou derivado de nucleotídeo, fixação covalente de um lipídio ou derivado de lipídio, fixação covalente de fosfatidilinositol, ligação cruzada, ciclização, formação de ligação dissulfeto, desmetilação, formação de ligações covalentes cruzadas, formação de cisteína, formação de piroglutamato, formilação, gama-carboxilação, glicosilação, formação de âncora de GPI, hidroxilação, iodinação, metilação, miristoilação, oxidação, pegilação, processamento proteolítico, fosforilação, prenilação, racemização, selenoilação, sulfatação, adição mediada de RNA-de-transferência de aminoácidos para proteínas tais como arginilação e utiquitinação. (Vide por exemplo, Proteins -Structures and molecular properties,T. E. Creighton, W. H. Freeman and Company, New York, 2nd Ed. (1993); Postranslational Covalent Modification Of Proteins, B. C. Johnson, Ed. Academic Press, New York, pgs. 1-12 (1983) ; Seifter et al., Meth Enzymol 182: 626-646 (1990); Rattan et al., Ann NY Acad Sci 663:448- 62 (1992).
[000225] A presente invenção também propicia proteínas de fusão compreendendo um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado e polipeptídeo heterólogo. Em uma modalidade, uma proteína de fusão da invenção compreende, consiste essencialmente em ou consiste em um polipeptídeo contendo a sequência de aminoácidos de qualquer uma ou mais das regiões VH de um anticorpo da invenção ou a sequência de aminoácidos de qualquer uma ou mais das regiões VL de um anticorpo da invenção ou fragmentos ou variantes suas e uma sequência heteróloga de polipeptídeos. Em outra modalidade, uma proteína de fusão para uso em métodos de diagnóstico e tratamento aqui descritos compreende, consiste essencialmente em ou consiste em um polipeptídeo tendo a sequência de aminoácidos de qualquer uma, duas, três das VH-CDRs de um anticorpo ou de fragmentos, variantes, ou derivados seus ou a sequência de aminoácidos de qualquer uma, duas, três das VL-CDRs de um anticorpo ou fragmentos, variantes ou seus derivados e uma sequência de polipeptídeos heterólogos. Em uma modalidade, a proteína de fusão compreende um polipeptídeo tendo a sequência de aminoácidos, uma VH-CDR3 de um anticorpo da presente invenção ou fragmento, derivado ou variante e uma sequência heteróloga de polipeptídeos, que especificamente se liga a proteínas de fusão em menos um neoepítopo de um distúrbio associado à proteína. Em outra modalidade, uma proteína de fusão compreende um polipeptídeo tendo a sequência de aminoácidos de pelo menos uma região de VH de um anticorpo da invenção e a sequência de pelo menos uma região de VL de um anticorpo da invenção ou fragmentos, derivados ou variantes seus e uma sequência de polipeptídeos heterólogos. Preferencialmente, as regiões VH e VL da proteína de fusão correspondem a um anticorpo de única fonte (ou fragmento de scFv ou Fab), que especificamente liga pelo menos um neoepítopo de uma proteína associada ao distúrbio. Em outra modalidade, uma proteína de fusão para uso nos métodos de diagnóstico e tratamento descritos aqui compreende um polipeptídeo tendo a sequência de aminoácidos de qualquer uma, duas, três ou mais das VH CDRs de um anticorpo e a sequência de aminoácidos de qualquer uma, duas, três ou mais das VL CDRs de um anticorpo ou fragmentos ou variantes e uma sequência heteróloga de polipeptídeos. Preferivelmente, duas, três, quatro, cinco, seis ou mais das VH-CDR (s) ou LV-CDR (s) correspondem a um anticorpo de uma única fonte (ou fragmento de scFv ou Fab) da invenção. Moléculas de ácido nucleico que codificam estas proteínas de fusão são também contempladas pela invenção.
[000226] Proteínas de fusão exemplares reportadas na literatura incluem fusões do receptor de células T (Gascoigne et al., Proc. Natl. Acad. Sei. USA 84:2936-2940 (1987)); CD4 (Capon et al., Nature 337:525-531 (1989); Traunecker et al., Nature339:68-70 (1989); Zettmeissl et al., DNA Cell Biol. USA 9:347-353 (1990); e Byrn et al., Nature 344:667-670 (1990)); L-selectin (receptor homing) (Watson et al., J. Cell. Biol. 110:2221-2229 (1990); e Watson et al., Nature 349:164-167 (1991)); CD44 (Aruffo et al., Cell 67:1303-1313 (1990)); CD28 e B7 (Linsley et al., J. Exp. Med. 773:721-730 (1991)); CTLA-4 (Lisley et al., J. Exp. Med. 774:561-569 (1991)); CD22 (Stamenkovic et al., Cell 66:1133-1144 (1991)); receptor TNF (Ashkenazi et al., Proc. Natl. Acad. Sci. USA 88:10535-10539 (1991); Lesslauer et al., Eur. J. Immunol. 27:2883-2886 (1991); e Peppel et al., J. Exp. Med. 774:1483- 1489 (1991)); e IgE receptor a (Ridgway e Gorman, J. Cell. Biol. Vol. 115, Abstract No. 1448 (1991)).
[000227] Conforme discutido noutro lugar neste relatório, os anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção podem ser fundidos aos polipeptídeos heterólogos para aumentar a meia vida in vivo dos polipeptídeos ou para uso em imunoensaios usando métodos conhecidos na técnica. Por exemplo, em uma modalidade, PEG pode ser conjugado aos anticorpos da invenção para aumentar sua meia vida in vivo. Leong, S.R., et al., Cytokine76:106 (2001); Adv. in Drug Deliv. Rev. 54:531 (2002); ou Weir et al., Biochem. Soc. Transactions 30:512 (2002).
[000228] Além disso, os anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção podem ser fundidos às sequências de marcador, tal como um peptídeo para facilitar sua purificação ou detecção. Em modalidades preferidas, a sequência de aminoácidos de marcador é um peptídeo de hexa- histidina, tal como o rótulo propiciado em um vetor pQE (QIAGEN, Inc., 9259 Eton Avenue, Chatsworth, Califórnia, 91311), entre outros, muitos dos quais são comercialmente disponíveis. Conforme descrito em Gentz et al., Proc. Natl. Acad. Sci. E.U.A. 86:821-824 (1989), por exemplo, a hexa-histidina propicia a purificação conveniente da proteína de fusão. Outros rótulos de peptídeos úteis para purificação incluem, entre outros, o rótulo "HA", o qual corresponde a um epitopo derivado da proteína hemaglutinina da gripe (Wilson et al., Cell 37.767 (1984)) e ao rótulo "bandeira".
[000229] As proteínas de fusão podem ser preparadas usando métodos que são bem-conhecidos na técnica (ver, por exemplo, Patente U.S. nos. 5.116.964 e 5.225.538). O local exato no qual se dá a fusão pode ser selecionado empiricamente para otimizar as características de secreção ou ligação da proteína de fusão. O DNA que codifica a proteína de fusão é, então, transfectado para uma célula hospedeira para a expressão.
[000230] Os anticorpos da presente invenção podem ser usados em forma não conjugada ou podem ser conjugados com pelo menos uma de uma variedade de moléculas, por exemplo, para melhorar as propriedades terapêuticas da molécula, para facilitar a detecção alvo ou a formação de imagem ou terapia do paciente. Os anticorpos ou fragmentos de ligação a antígeno ou seus derivados da invenção podem ser marcados ou conjugados que antes ou após a purificação, quando a purificação for realizada.
[000231] Em particular, os anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção podem ser conjugados com agentes terapêuticos, pró-farmacos, peptídeos, proteínas, enzimas, vírus, lipídios, modificadores da resposta biológica, agentes farmacêuticos ou PEG.
[000232] Conjugados que são imunotoxinas incluindo anticorpos convencionais foram amplamente descritos na técnica. As toxinas podem ser acopladas aos anticorpos pelas técnicas convencionais de acoplamento ou imunotoxinas contendo porções de toxinas de proteínas podem ser produzidas como proteínas de fusão. Os anticorpos da presente invenção podem ser usados em uma forma correspondente para obter tais imunotoxinas. Exemplos de tais imunotoxinas sâo aqueles descritos por Byers, Seminars Cell. Biol. 2 (1991), 59-70 e por Fanger, Immunol. Today 12 (1991), 51-54
[000233] A proteína de fusão descrita acima pode ainda compreender um ligante clivável ou sítio de clivagem para proteinases. Estas porções espaçadoras, por sua vez, podem ser solúveis ou insolúveis (Diener et al., Science 231 (1986), 148) e podem ser selecionadas para permitir a liberação do fármaco do antígeno no sítio alvo. Exemplos de agentes terapêuticos que podem ser acoplados aos anticorpos ou antígenos da presente invenção para imunoterapia são fármacos, radiosótopos, lectinas e toxinas. Os fármacos com as quais pode haver a conjugação com os anticorpos ou antígenos da presente invenção incluem compostos que são classicamente referidos como fármacos tais como mitomicina C, daunorrubicina e vinblastina. Na utilização de anticorpos ou antígenos conjugados radioisotopicamente da invenção para, por exemplo, imunoterapia, certos isótopos podem ser mais preferíveis do que outros dependendo de tais fatores como a distribuição de leucócitos como também a estabilidade ou emissão. Dependendo da resposta autoimune, alguns emissores podem ter preferência sobre outros. Em geral, radioisótopos emissores de partículas a e B são preferidos na imunoterapia. Preferidos são os emissores de alta energia, e de curta faixa tais como 212Bi. Exemplos de radioisótopos que podem ser ligados a anticorpos ou antígenos da 125 131 90 invenção para fins terapêuticos incluem, entre outros, I, I, Y, 67 64 212 212 211 47 109 188 Cu, Cu, Bi, At, Pb, Sc, Pd e Re. Outros agentes terapêuticos que podem ser acoplados à molécula de ligação, por exemplo, o anticorpo ou o fragmento de ligação a antígeno seu da invenção, como também protocolos terapêuticos ex vivoe in vivo, são conhecidos ou podem ser facilmente verificados por aqueles versados na técnica. Sempre que apropriado, a pessoa versada na técnica poderá usar um polinucleotídeo da invenção que codifica um dos anticorpos acima descritos, antígenos ou os vetores correspondentes em vez do próprio material proteico.
[000234] Aqueles versados na técnica observarão que os conjugados também podem ser agrupados usando uma variedade de técnicas dependendo do agente selecionado a ser conjugado. Por exemplo, os conjugados com biotina são preparados, por exemplo, pela reação de um polipeptídeo ligante com um éster de biotina ativado tal como o éster de N-hidroxissucinimida de biotina. Similarmente, os conjugados com um marcador fluorescente podem ser preparados na presença de um agente de acoplamento, por exemplo, aqueles listados neste relatório ou pela reação com isotiocianato, preferivelmente isotiocianato-fluoresceína. Os conjugados dos anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção são preparados de forma análoga.
[000235] A presente invenção ainda abrange anticorpos ou fragmentos de ligação a antígeno, variantes ou seus derivados da invenção conjugados com um agente de diagnóstico ou terapêutico. Os anticorpos podem ser usados diagnosticamente para, por exemplo, monitorar o desenvolvimento ou progressão de uma doença neurológica como parte de um procedimento de teste clínico para, por exemplo, determinar a eficácia de um dado regime de prevenção e/ou tratamento. A detecção pode ser facilitada pelo acoplamento do anticorpo ou fragmento de ligação de antígeno, variante ou seu derivado a uma substância detectável. Exemplos de substâncias detectáveis incluem várias enzimas, grupos prostéticos, materiais fluorescentes, materiais luminescentes, materiais bioluminescentes, materiais radioativos, metais emissores de positron usando várias tomografias de emissão de positron e íons metálicos paramagnéticos não radioativos. Vide por exemplo, a patente dos U.S. N°. 4.741.900 para íons metálicos que podem ser conjugados com anticorpos para uso como diagnósticos de acordo com a presente invenção. Exemplos de enzimas adequadas incluem peroxidase de raiz forte, fosfatase alcalina, (B-galactosidase ou acetilcolinesterase; exemplos de complexos de grupos prostéticos incluem streptavidin/biotin e avidin/biotin; exemplos de materiais fluorescentes adequados incluem umbeliferona, fluoresceína, isotiocianato de fluoresceína, rodamina, fluoresceína de diclorotriazinilamina, cloreto de dansila ou ficoeritrina; um exemplo de um material luminescente inclui luminol; exemplos de materiais bioluminescentes incluem luciferase, luciferina e aquorina; e exemplos de material radioativo adequado incluem 125l, 131l, 111ln ou "Tc.
[000236] Um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado também pode ser marcado de forma detectável através seu acoplamento a um composto quimioluminescente. A presença do anticorpo marcado como quimioluminescente é então determinada pela detecção da presença de luminescência que surge durante o curso de uma reação química. Exemplos de compostos marcadores quimioluminescentes particularmente úteis são o luminol, isoluminol, éster de acridínio teromático, imidazole, sal de acridínio e éster de oxalato.
[000237] Um dos meios pelos quais um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado pode ser marcado de forma detectável é através da ligação do mesmo a uma enzima e pelo uso de um produto ligado em um imunoensaio de enzimas (EIA) (Voller, A., "The Enzyme Linked Immunosorbent Assay (ELISA)" Microbiological Associates Quarterly Publication, Walkersville, Md., Diagnostic Horizons 2:1-7 (1978)); Voller et al., J. Clin. 'Pathol. 37:507- 520 (1978); Butler, J. E., Meth. Enzymol. 73:482-523 (1981); Maggio, E. (ed.), Enzyme Immunoassay, CRC Press, Boca Raton, Fla., (1980); Ishikawa, E. et al., (eds.), Enzyme Immunoassay, Kgaku Shoin, Tóquio (1981). A enzima, que está ligada ao anticorpo irá reagir com um substrato adequado, de preferência um substrato cromogênico, de forma a produzir uma porção química que pode ser detectada, por exemplo, por espectrofotometria, fluorimetria ou por meios visuais. As enzimas que podem ser usadas para marcar de forma detectável o anticorpo incluem, entre outras, desidrogenase de malato, nuclease estafilococcal, isomerase delta-5-esteroide, desidrogenase de álcool de levedo, alfa-glicerofosfato, desidrogenase, isomerase fosfato de triose, peroxidase de raiz forte, fosfatase alcalina, asparaginase, oxidase de glicose, beta-galactosidase, ribonuclease, urease, catalase, desidrogenase de glicose-6-fosfato, glucoamilase e acetilcolinesterase. Além disso, a detecção pode ser realizada por métodos colori métricos que empregam um substrato cromogênico para a enzima. A detecção também pode ser realizada por comparação visual da extensão da reação enzimática de um substrato, em comparação com padrões igualmente preparados.
[000238] A detecção também pode ser realizada usando qualquer um dentre uma variedade de outros imunoensaios. Por exemplo, através da marcação de forma radioativa do anticorpo ou do fragmento de ligação a antígeno, variante ou seu derivado, é possível detectar o anticorpo através da utilização de um radioimunoensaio (RIA) (vide, por exemplo, Weintraub, B., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, (March, 1986)), que são incorporados por referência neste documento). O isótopo radioativo pode ser detectado por meio de, entre outros, um contador gama, um contador de cintilação ou autorradiografia.
[000239] Um anticorpo ou fragmento de ligação a antígeno, variante ou seu derivado, pode também ser marcado de forma detectável usando metais emissores de fluorescência tal como o 152Eu ou outros da série de lantanida. Estes metais podem ser afixados ao anticorpo utilizando tais grupos quelantes como ácido dietilenotria- minopentacético (DTPA) ou ácido etilenodiaminotetracético (EDTA).
[000240] Técnicas para conjugar várias porções a um anticorpo ou fragmento de ligação a antígeno, variante ou seus derivados deles são bem-conhecidos; vide por exemplo, Arnon et al.,"Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", in Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. (1985); Hellstrom et al.,"Antibodies For Drug Delivery", in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), Marcel Dekker, Inc., pp. 623-53 (1987); Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", in Monoclonal Antibodies '84: Biological And Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); "Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", in Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), Academic Press pp. 303-16 (1985), and Thorpe et al., "The Preparation And Cytotoxic Properties Of Antibody-Toxin Conjugates", Immunol. Rev. 62:119-58 (1982).
[000241] Em certas modalidades, uma porção que aumenta a estabilidade ou eficácia de uma molécula de ligação, por exemplo, um polipeptídeo de ligação, por exemplo, um anticorpo ou seu fragmento imunoespecífico, pode ser conjugado. Por exemplo, em uma modalidade, o PEG pode ser conjugado com as moléculas de ligação da invenção para aumentar a sua meia vida in vivo. Leong, S.R., et al., Cytokine76:106 (2001); Adv. in Drug Deliv. Rev. 54:531 (2002); ou Weir et al., Biochem. Soc. Transactions 30:512 (2002). VII. Composições e métodos de uso
[000242] Ademais, a presente invenção refere-se às composições compreendendo a referida molécula de ligação, por exemplo, anticorpo ou seu fragmento de ligação ao antígeno da presente invenção ou seus derivados químicos ou o polinucleotídeo, vetor ou célula da invenção. A composição da presente invenção pode ainda compreender um veículo farmaceuticamente aceitável. O termo “derivado químico” descreve uma molécula que contém porções químicas adicionais que não são normalmente uma parte da molécula de base. Tais porções podem melhorar a solubilidade, a meia vida, absorção, etc. da molécula de base. Alternativamente, as porções podem atenuar os efeitos colaterais indesejáveis da molécula de base ou diminuir a toxicidade da molécula de base. Além disso, a composição farmacêutica da presente invenção pode compreender outros agentes tais como interleucinas ou interferons dependendo do uso pretendido da composição farmacêutica. Por exemplo, para uso no tratamento da doença de Alzheimer, o agente adicional pode ser selecionado a partir do grupo constituído de pequenas moléculas orgânicas, anticorpos anti-Abeta e suas combinações. Assim, em uma determinada modalidade, a presente invenção refere-se ao uso da molécula de ligação, por exemplo, anticorpo ou seu fragmento de ligação do antígeno da presente invenção ou de uma molécula de ligação contendo substancialmente as mesmas especificidades de qualquer um destes, o polinucleotídeo, o vetor ou a célula da presente invenção para a preparação de uma composição farmacêutica ou de diagnóstico para tratar ou impedir a progressão da doença de Alzheimer, para a melhora dos sintomas associados com a doença de Alzheimer; para o diagnóstico ou varredura de um sujeito quanto à presença da doença de Alzheimer ou para determinar o risco de um sujeito de desenvolver a doença de Alzheimer. A dita composição farmacêutica pode ser projetada para ser administrada por via intravenosa, intramuscular, subcutânea, intraperitoneal, intranasal, parentérica ou em aerossol; ver também infra.
[000243] Assim, em uma modalidade, a presente invenção refere-se a um método de tratamento de um distúrbio neurológico caracterizado pelo acúmulo anormal e/ou deposição de uma proteína no sistema nervoso central, cujo método compreende a administração a um sujeito com esta necessidade de uma quantidade terapeuticamente eficaz de qualquer uma das moléculas de ligação, anticorpos, antígenos, polinucleotídeos, vetores ou células da presente invenção. O termo "distúrbio neurológico" inclui, entre outros, Doença de Alzheimer, comprometimento cognitivo leve, demência fronto-temporal, doença de corpos de Lewy, doença de Parkinson, doença de Pick, doença de Binswanger; angiopatia amiloide congofílica, angiopatia amiloide cerebral, síndrome de Down, demência de multi-infarto, Doença de Huntington, doença de Creutzfeldt-Jakob, demência de AIDS complexa, depressão, ansiedade, fobia, a paralisia de Bell, epilepsia, encefalite, esclerose múltipla, doenças neuromusculares, distúrbios neuro-oncológicos, tumores cerebrais, distúrbios neurovasculares incluindo derrame, distúrbios neuroimunológicos, doença neuro-otológica, neurotrauma incluindo lesão da medula espinhal, dor, incluindo dor neuropática, doenças pediátricas, neurológicas e neuropsiquiátricas, distúrbios do sono, síndrome de Tourette, comprometimento cognitivo leve, demência vascular, demência multi-infarto, fibrose cística, doença de Gaucher, outros distúrbios do movimento e doenças do sistema nervoso central (SNC) em geral. Salvo disposição em contrário, os termos neurodegenerativas, neurológicas ou neuropsiquiátricos são utilizados indiferentemente aqui.
[000244] No âmbito da presente invenção, um método é descrito para caracterizar anticorpos humanos para um grande número de doenças e para também produzir os ditos anticorpos subsequentemente para empregá-los em forma de diagnóstico, terapeuticamente ou como prevenção em tais pacientes cujo imunosistema não reagiu com a imunoresposta correspondente ao desenvolvimento da patologia da doença. Em particular, isto terá que ser esperado em doenças que ocorrem em idade avançada porque, como se sabe, a reatividade do sistema imune diminui de forma contínua e significativa conforme a idade aumenta. Nestes casos, anticorpos ativos terapêutica ou preventivamente poderiam compensar as restrições relacionadas com a idade do sistema imune, no que refere-se ao bloqueio do enriquecimento das variantes da proteína patofisiológica endógena e poderiam, assim, contribuir para um melhor estado de saúde na idade avançada. Assim, o uso médico da presente invenção é particularmente válido para o grupo dos pacientes acima descritos, por exemplo, na idade de 60, 65, 70, 75, 80 ou mais velhos e, em princípio, refere-se a todas as doenças manifestando-se em forma de descarrilamento de qualquer espécie, como por exemplo endoproteólise, alterações de conformação, alterações de modificações pós-tradução, mutações somáticas ou combinações dos mesmos, fenotipicamente por meio do desenvolvimento de variantes patofisiológicas da proteína endógena. No âmbito da presente invenção, variantes patofisiológicas são consideradas como sendo variantes contendo neoepítopos patológicos que se desviam da fisiologia, vide supra.
[000245] Em particular, as aplicações terapêuticas incluem doenças tumorais, doenças inflamatórias e doenças do sistema nervoso central, como a doença de Alzheimer, doença de Parkinson, doença de Pick, demência com corpos de Lewy, doenças de Prion, incluindo doença de Creutzfeldt-Jakob, paralisia supra nuclear progressiva, atrofia de múltiplos sistemas, degeneração corticobasal, degeneração fronto- temporal com Parkinsonismo similar à doença de Huntington de cromossoma 17, demência fronto-temporal, angiopatia amiloide cerebral, comprometimento cognitivo leve, síndrome de Down, hemorragia cerebral hereditária com amiloidose tipo holandês e tipo islandês, ataxia espinocerebelar e esclerose lateral amiotróica como também glaucoma, miosite corporal de inclusão, polineuropatia amiloide familial e amiloidose compreendendo proteínas fibrilares derivadas de pelo menos uma das seguintes proteínas precursoras: SAA (do inglês Serum-Amyloíd-Protein A, proteína sérica amiloide A), AL (cadeias k or l-leves de imunoglobulinas), AH (cadeias g1 lg pesadas), ATTR (transtiretina, prealbumina sérica), AApo-A-1 (Apolipoproteína A1), AApoA2 (Apolipoproteína A2), AGel (Gelsolina), ACys (Cistatina C), ALys (Lisozima), AFib (Fibrinógeno), Beta-amiloide (proteína precursora de amiloide), Beta-amiloide 2M (beta2- microglobulina), APrP (proteína Prion), ACal (Procalcitonina), AIAPP (polipeptídeo amiloide da ilhota); APro (Prolactina), Alns (Insulina); AMed (Lactaderina); Aker (cerato-epitelina); ALac (Lactoferrina), Abri (AbriPP), ADan (ADanPP); ou AANP (peptídeo natriurético atrial), (Skovronsky at al., Annu. Rev. Pathol. Mech. Dis. 2006; 1:151-70; Buxbaum, Curr Opin Rheumatol 2003; 16: 67-75.
[000246] Uma vantagem em particular da abordagem terapêutica da presente invenção reside no fato de que os anticorpos derivados das células B e das células de memória B a partir de organismo excepcionalmente estável pré-clinicamente ou clinicamente saudável são, com uma certa probabilidade, capazes de evitar a manifestação clínica da doença ou de diminuir o risco da ocorrência de uma doença manifesta clinicamente ou de retardar o momento da ocorrência de uma doença manifesta clinicamente. Normalmente, esses anticorpos também já passaram com sucesso através da maturação somática ou seja, da otimização com relação à seletividade e eficácia na ligação de alta afinidade à molécula-alvo por meio de variação somática das regiões variáveis do anticorpo.
[000247] O conhecimento de que tais células in vivo, por exemplo, em um ser humano, não foram ativadas por meio de proteínas relacionadas ou outras proteínas fisiológicas ou estruturas de células no sentido de uma reação alérgica ou autoimunológica é também de grande importância médica pois isso significa um considerável aumento da chance de passar com sucesso pelas fases dos testes clínicos. Por assim dizer, a eficácia, tolerabilidade e aceitabilidade já foram demonstradas antes do desenvolvimento pré-clínico do anticorpo terapêutico ou profilático em pelo menos um sujeito humano. Pode ser esperado então que com um procedimento de acordo com a presente invenção, a eficácia específica da estrutura-alvo de um anticorpo como agente terapêutico e a diminuição da probabilidade de efeitos colaterais aumentam significativamente sua probabilidade clínica de sucesso.
[000248] Do exposto, é evidente que a presente invenção engloba qualquer utilização de uma molécula de ligação específica da doença compreendendo pelo menos uma CDR do anticorpo acima descrito, em particular para diagnóstico e/ou tratamento de um distúrbio relacionado com a doença de Alzheimer e a deposição Abeta, respectivamente. Preferivelmente, a dita molécula de ligação é um anticorpo da presente invenção ou sua cadeia de imunoglobulinas. Além disso, a presente invenção refere-se a anticorpos anti-idiotípicos de qualquer um dos anticorpos mencionados descritos anteriormente neste documento. Existem anticorpos ou outras moléculas de ligação que se ligam à sequência de peptídeos antigênicos únicos localizados em uma região variável do anticorpo próxima ao sítio de ligação ao antígeno.
[000249] Em outra modalidade a presente invencao refere-se a uma composição de diagnóstico compreendendo qualquer uma das moléculas de ligação descritas acima, anticorpos, fragmentos de ligação a antígeno, polinucleotídeos, vetores ou células da invenção e, opcionalmente, meios adequados para a detecção, tais como reagentes convencionalmente usados em métodos de diagnóstico baseados em ácido imuno ou nucleico. Os anticorpos da invenção são, por exemplo, adequados para uso em imunoensaios nos quais eles podem ser utilizados na fase líquida ou ligados a um veículo da fase sólida. Exemplos de imunoensaios que podem utilizar os anticorpos da invenção são imunoensaios concorrentes e não concorrentes em um formato direto ou indireto. Exemplos desses imunoensaios são o radioimunoensaio (RIA), o sanduíche (ensaio imunométrico), a citometria de fluxo e o ensadio pelo método Western blot.Os antígenos e anticorpos da invenção podem ser ligados a muitos veículos diferentes e utilizados para isolar células especificamente ligadas aos mesmos. Exemplos de veículos bem-conhecidos incluem o vidro, poliestireno, cloreto de polivinila, polipropileno, polietileno, policarbonato, dextram, nylon, amiloses, celuloses naturais e modificadas, poliacrilamidas, agaroses e magnetita. A natureza do veículo pode ser solúvel ou insolúvel para fins da invenção. Há muitos rótulos e métodos diferentes de marcação conhecidos daqueles versados na técnica. Exemplos dos tipos de rótulos que podem ser utilizados na presente invenção incluem enzimas, radioisótopos, metais coloidais, compostos fluorescentes, compostos quimioluminescentes e compostos bioluminescentes; ver também as modalidades discutidas anteriormente neste documento.
[000250] Por uma nova modalidade, as moléculas de ligação, em especial anticorpos da presente invenção também podem ser utilizadas em um método para o diagnóstico de um distúrbio em um indivíduo para obter uma espécime de fluido corporal da pessoa testada, que pode ser uma espécime de sangue, uma espécime linfática ou qualquer outra espécime de fluido corporal e promover o contato da espécime de fluido corporal com um anticorpo da presente invenção sob condições que permitam a formação de complexos antigeno-anticorpo. O nível desses complexos é então determinado por métodos conhecidos na técnica, um nível significativamente mais elevado do que o formado em uma espécime de controle que indica a doença no indivíduo testado. Da mesma forma, o antígeno específico ligado aos anticorpos da invenção também pode ser usado. Assim, a presente invenção refere-se a um imunoensaio in vitro compreendendo a molécula de ligação, por exemplo, seu fragmento de ligação a anticorpo ou antígeno da invenção.
[000251] Neste contexto, a presente invenção também refere-se aos meios especificamente projetados para esta finalidade. Por exemplo, uma disposição com base em proteínas ou em anticorpos pode ser utilizada, a qual, por exemplo, é carregada com quaisquer antígenos derivados da referida proteína associada ao distúrbio e que contém o neoepítopo para detectar autoanticorpos que podem estar presentes em pacientes que sofrem de, por exemplo, um distúrbio neurológico, em especial a doença de Alzheimer ou com anticorpos ou moléculas equivalentes de ligação a antígeno da presente invenção que reconhecem especificamente qualquer uma dessas proteínas. Por exemplo, perfil de microdisposição de antígenos de anticorpos na artrite reumatoide foi relatado por Hueber et al. Arthritis Rheum. 52 (2005), 2645-2655. O projeto dos imunoensaios de micro disposições é resumido em Kusnezow et al., Mol. Cell Proteomics 5 (2006), 1681- 1696. Assim, a presente invenção também se refere com as microdisposições carregadas com moléculas ou antígenos de ligação identificados em conformidade com a presente invenção.
[000252] A presente invencao tambem fornece um pacote ou kit farmacêutico e de diagnostico, respectivamente, compreendendo um ou mais recipientes cheios com um ou mais dos ingredientes acima descritos, por exemplo, molécula de ligação, anticorpo ou fragmento de ligação, antígeno, polinucleotídeo, vetor ou célula da presente invenção. Associado com esse(s) recipiente (s) poderá estar um anúncio na forma prescrita por uma agência governamental que regulamenta a fabricação, uso ou venda de produtos farmacêuticos ou de produtos biológicos, cujo anúncio reflete a aprovação pela agência de fabricação, utilização ou venda para administração em seres humanos. Além disso ou alternativamente, o kit inclui reagentes e/ou instruções de uso em ensaios de diagnóstico apropriados. A composição, por exemplo, o kit da presente invenção é, certamente, particularmente adequada para o diagnóstico, prevenção e tratamento de um distúrbio que vem acompanhado da presença de uma proteína associada à doença conforme definido acima, especialmente a amiloidose e, em particular, aplicável ao tratamento da doença de Alzheimer (dC).
[000253] Os termos "tratamento", "que trata" e similares, são aqui usados geralmente para obter um efeito farmacológico e/ou fisiológico desejado. O efeito pode ser profilático em termos de totalmente ou parcialmente prevenir uma doença ou seu sintoma e/ou pode ser terapêutico em termos de parcialmente ou completamente curar uma doença e/ou seu efeito adverso atribuído à doença. O termo "tratamento", como utilizado neste documento abrange qualquer tratamento de uma doença em um mamífero, especialmente um ser humano e inclui: (a) impedir a ocorrência da doença em um sujeito que pode estar predisposto à doença, mas não foi diagnosticado ainda como veículo dela; (b) inibir a doença, por exemplo, interrompendo seu desenvolvimento; ou (c) aliviar a doença, por exemplo, causando sua regressão.
[000254] Além disso, o termo "sujeito" ou "paciente" refere-se a um mamífero, de preferência humano, que necessita de tratamento para uma condição, distúrbio ou doença.
[000255] As composições farmacêuticas da presente invenção podem ser formuladas de acordo com métodos bem-conhecidos na técnica; ver, por exemplo Remington: The Science and Practice of Pharmacy (2000) by the University of Sciences in Philadelphia, ISBN 0-683-306472. Exemplos de veículos farmacêuticos adequados são bem-conhecidos na técnica e incluem soluções-tampão salinas de fosfato, água, emulsões, tais como emulsões de óleo/água, diversos tipos de umidificantes, soluções estéreis, etc. Composições compreendendo tais veículos podem ser formuladas por métodos convencionais bastante conhecidos. Estas composições farmacêuticas podem ser administradas ao sujeito em dose adequada. A administração de composições adequadas pode ser efetuada por diferentes meios, por exemplo, por via intravenosa, intraperitoneal, subcutânea, intramuscular, administração tópica e intradérmica. As formulações em aerossol, como formulações em spray nasal incluem soluções aquosas purificadas ou outras soluções do agente ativo com agentes conservantes e agentes isotônicos. Tais formulações são de preferência ajustadas até um pH e estado isotônico compatível com as membranas mucosas nasais. Formulações para administração retal ou vaginal podem ser apresentadas na forma de supositório com um veículo adequado.
[000256] Além disso, enquanto a presente invenção inclui o corrente procedimento padrão (embora afortunadamente raro) de perfurar um pequeno orifício no crânio para administrar um fármaco da presente invenção, em um aspecto preferido, a molécula de ligação, especialmente o anticorpo ou o fármaco com base no anticorpo da presente invenção pode atravessar a barreira hematoencefálica, o que permite a administração intravenosa ou oral.
[000257] A posologia deverá ser determinada pelo médico assistente e por fatores clínicos. Como é bastante sabido nas técnicas médicas, as dosagens para qualquer paciente dependem de muitos fatores, incluindo a altura do paciente, a área de superfície do corpo, a idade, o composto particular a ser administrado, gênero, hora e via de administração, saúde geral e outros fármacos sendo administrados simultaneamente. Uma dose típica pode ser, por exemplo, na faixa de 0,001 a 1,000 pg (ou do ácido nucleico para expressão ou inibição de expressão neste intervalo); no entanto, doses abaixo ou acima desta faixa exemplar são visualizadas, especialmente considerando os fatores acima mencionados. Geralmente, a dosagem pode variar, por exemplo, de cerca de 0,0001 a 100 mg/kg e mais geralmente de 0,01 a 5 mg/kg (por exemplo, 0,02 mg/kg, 0,25 mg/kg, 0,5 mg/kg, 0,75 mg/kg, 1 mg/kg de 2 mg/kg, etc), do peso corporal do hospedeiro. Por exemplo, as doses podem ser de 1 mg/kg de peso corporal ou 10 mg/kg de peso corporal ou dentro da faixa de 1-10 mg/kg, de preferência, pelo menos, 1 mg/kg. Doses intermediárias nas faixas acima são também destinadas a estar dentro do âmbito da invenção. Os sujeitos podem receber tais doses diárias, em dias alternativos, semanalmente ou de acordo com qualquer outra programação determinada pela análise empírica. Um tratamento exemplar envolve a administração em doses múltiplas durante um período prolongado, por exemplo, de pelo menos seis meses. Regimes de tratamentos exemplares adicionais envolvem a administração uma vez a cada duas semanas ou uma vez por mês ou uma vez a cada 3 a 6 meses. Programações de dosagens exemplares incluem 1-10 mg/kg ou 15 mg/kg em dias consecutivos, 30 mg/kg em dias alternados ou 60 mg/kg semanalmente. Em alguns métodos, dois ou mais anticorpos monoclonais com diferentes especificidades de ligação são administrados simultaneamente, em cujo caso a dosagem de cada anticorpo administrado se enquadra dentro das faixas indicadas. O progresso pode ser monitorado pela avaliação periódica. Preparações para administração parenteral incluem soluções aquosas ou não aquosas, suspensões e emulsões. Exemplos de solventes não aquosos são propileno glicol, polietileno glicol, óleos vegetais, como o azeite de oliva, ésteres orgânicos injetáveis tais como o oelato de etila. Veículos aquosos incluem a água, soluções alcoólicas/aquosas, emulsões ou suspensões, incluindo meios salinos e tamponados. Veículos parenterais incluem solução de cloreto de sódio, dextrose de Ringer, dextrose e cloreto de sódio, lactato de Ringer ou óleos fixos. Veículos intravenosos incluem reabastecedores de fluidos e nutrientes reabastecedores de eletrólitos (tais como aqueles baseados na dextrose de Ringer) e similares. Conservantes e outros aditivos podem também estar presentes, como, por exemplo, antibióticos, antioxidantes, quelantes e gases inertes e outros do gênero. Além disso, a composição farmacêutica da invenção pode incluir mais agentes como a dopamina ou fármacos psicofarmacológicos, dependendo da utilização pretendida da composição farmacêutica. Além disso, a composição farmacêutica também pode ser formulada como uma vacina, por exemplo, se a composição farmacêutica da invenção compreende um anticorpo anti-A0 para a imunização passiva.
[000258] Além disso, a co-administração ou a administração sequencial de outros agentes podem ser desejável. Uma dose ou quantidade terapeuticamente eficaz refere-se àquela quantidade de ingrediente ativo suficiente para aliviar os sintomas ou a condição. A eficácia terapêutica e a toxicidade desses compostos podem ser determinadas pelos procedimentos farmacêuticos-padrão nas culturas de células ou em animais cobaias, por exemplo, ED50 (a dose terapeuticamente eficaz em 50% da população) e LD50 (a dose letal para 50% da população). A relação entre a dose terapêutica e efeitos tóxicos é o índice terapêutico e pode ser expressa como a razão, LD50/ED50. Preferivelmente, o agente terapêutico na composição está presente em uma quantidade suficiente para restabelecer um comportamento normal e/ou as propriedades cognitivas no caso da doença de Alzheimer.
[000259] As composições farmacêuticas em conformidade com a presente invenção podem de preferência ser usadas para o tratamento dos distúrbios neurológicos, incluindo, entre outros, a doença de Alzheimer, doença de Parkinson, doença de Pick, demência com corpos de Lewy, doenças de Prion, incluindo doença de Creutzfeldt- Jakob, paralisia supra nuclear progressiva, atrofia de múltiplos sistemas, degeneração corticobasal, degeneração fronto-temporal com Parkinsonismo similar à doença de Huntington de cromossoma 17, demência fronto-temporal, angiopatia amiloide cerebral, comprometimento cognitivo leve, síndrome de Down, hemorragia cerebral hereditária com amiloidose tipo holandês e tipo islandês, ataxia espinocerebelar e esclerose lateral amiotróica como também glaucoma, miosite corporal de inclusão, polineuropatia amiloide familial e amiloidose compreendendo proteínas fibrilares derivadas de pelo menos uma das seguintes proteínas precursoras: SAA (proteína sérica amiloide A), AL (cadeias k or l-leves de imunoglobulinas), AH (cadeias g1 lg pesadas), ATTR (transtiretina, prealbumina sérica), AApo-A-1 (Apolipoproteína A1), AApoA2 (Apolipoproteína A2), AGel (Gelsolina), ACys (Cistatina C), ALys (Lisozima), AFib (Fibrinogêneo), Beta- amiloide (proteína precursora de amiloide), Beta-amiloide 2M (beta2- microglobulina), APrP (proteína Prion), ACal (Procalcitonina), AIAPP (polipeptídeo amiloide da ilhota); APro (Prolactina), Alns (Insulina); AMed (Lactaderina); Aker (cerato-epitelina); ALac (Lactoferrina), Abri (AbriPP), ADan (ADanPP); ou AANP (peptídeo natriurético atrial), (Skovronsky at al., Annu. Rev. Pathol. Meeh. Dis. 2006; 1:151-70; Buxbaum, Curr Opin Rheumatol 2003; 16: 67-75., neuro-oncologia, neuro-imunologia, dor neuro-otológica, neurologia pediátrica, fobia, distúrbios afetivos, distúrbios do sono, Síndrome de Tourette, outros distúrbios do movimento e doenças do sistema nervoso central (CNS) em geral.
[000260] Estas e outras modalidades são descritas e abrangidas pela descrição e exemplos da presente invenção. Outra literatura a respeito de qualquer um dos materiais, métodos, usos e compostos a ser empregados em conformidade com a presente invenção podem ser encontrados em bibliotecas públicas e bancos de dados, usando, por exemplo, dispositivos eletrônicos. Por exemplo, o banco de dados público "Medline"pode ser utilizado, o qual é hospedado pelas seguintes instituições: National Center for Biotechnology Information e/ou National Library of Medicine alocadas nos Institutos Nacionais de Saúde (National Institutes of Health). Outros bancos de dados e endereços da internet, tais como aqueles do European Bioinformatics Institute (EBI), que é parte do European Molecular Biology Laboratory (EMBL) são conhecidos daqueles versados na técnica e podem também ser obtidos usando ferramentas de busca na internet. Uma visão geral das informações de patentes em biotecnologia e um levantamento das fontes de informações de patentes úteis para busca retrospectiva e para conhecimento atual são apresentados em Berks, Tibtech 12 (1994), 352-364.
[000261] A descrição acima geralmente descreve a presente invenção. Salvo indicação em contrário, um termo conforme usado aqui observa a definição encontrada no Oxford Dictionary of Biochemistry and Molecular Biology, Oxford University Press, 1997, revisto em 2000 e reimpresso em 2003, ISBN 0 19 850673 2. Vários documentos são citados em todo o texto do presente relatório descritivo. Citações bibliográficas completas podem ser encontradas no final da especificação imediatamente precedente às reivindicações. O conteúdo de todas as referências citadas (incluindo referências de literatura, patentes emitidas, pedidos de patentes publicados conforme citados neste pedido e nos relatórios descritivos, instruções do fabricante) é aqui incorporado expressamente como referênica; entretanto, não existe admissão de que qualquer documento seja, de fato, técnica anterior com relação à presente invenção.
[000262] Um entendimento mais completo pode ser obtido através da consulta aos exemplos específicos seguintes que são fornecidos aqui para fins de ilustração somente e não se destinam a limitar o âmbito da invenção.
[000263] Os exemplos que seguem ilustram mais ainda a invenção, mas não deverão ser interpretados como limitadores do âmbito da invenção sob nenhum aspecto. Descrições detalhadas de métodos convencionais, tais como aqueles empregados neste documento podem ser encontradas na literatura citada, ver também "The Merck Manual of Diagnosis and Therapy" Seventeenth Ed. by Beers and Berkow (Merck & Co., Inc. 2003).
[000264] A prática da presente invenção empregará, salvo indicado em contrário, técnicas convencionais de biologia celular, cultura celular, biologia molecular, biologia transgênica, microbiologia, DNA recombinante e imunologia, que estão dentro da habilidade da técnica. Para mais detalhes das técnicas gerais úteis na prática desta invenção, o profissional poderá consultar os livros-texto-padrão e revisões sobre biologia celular e cultura de tecidos; ver também as referências citadas nos exemplos. Métodos gerais em bioquímica molecular e celular podem ser encontrados em tais livros-texto-padrão como: Molecular Cloning: A Laboratory Manual, 3rd ed. (Sambrook et al. Harbor Laboratory Press 2001); Short Protocols in Molecular Biology, 4th Ed. (Ausubel et al. Eds., John Wiley & Sons 1999); DNA Cloning, Volumes I and II (Glover ed., 1985); Oligonucleotide Synthesis (Gait ed., 1984); Nucleic Acid Hybridization (Hames and Higgins eds. 1984); Transcription And Translation (Hames and Higgins eds. 1984); Culture Of Animal Cells (Freshney and Alan, Liss, Inc., 1987); Gene Transfer Vectors for Mammalian Cells (Miller and Calos, eds.); Current Protocols in Molecular Biology and Short Protocols in Molecular Biology, 3rd Edition (Ausubel et al., eds.); e Recombinant DNA Methodology (Wu, ed., Academic Press). Gene Transfer Vectors For Mammalian Cells (Miller and Calos, eds., 1987, Cold Spring Harbor Laboratory); Methods In Enzymology, Vols. 154 and 155 (Wu et al., eds.); Immobilized Cells And Enzymes (IRL Press, 1986); Perbal, A Practical Guide To Molecular Cloning (1984); o tratado, Methods In Enzymology (Academic Press, Inc., N.Y.); Immunochemical Methods In Cell And Molecular Biology (Mayer and Walker, eds., Academic Press, London, 1987); Handbook Of Experimental Immunology, Volumes l-IV (Weir and Blackwell, eds., 1986). Protein Methods (Bollag et al., John Wiley & Sons 1996); Non-viral Vectors for Gene Therapy (Wagner et al. eds., Academic Press 1999); Viral Vectors (Kaplitt & Loewy eds., Academic Press 1995); Immunology Methods Manual (Lefkovits ed., Academic Press 1997); and Cell and Tissue Culture: Laboratory Procedures in Biotechnology (Doyle & Griffiths, John Wiley & Sons 1998). Os reagentes, vetores de clonagem e kits para manipulação genética mencionados neste dodumento podem ser adquiridos de fornecedores comerciais tais como BioRad, Stratagene, Invitrogen, Sigma-Aldrich e ClonTech. Técnicas gerais em cuoura celular e colecao de meios estão apresentados em Large Scale Mammalian Cell Culture (Hu et al., Curr. Opin. Biotechnol. 8 (1997), 148); Serum-free Media (Kitano, Biotechnology 17 (1991), 73); Large Scale Mammalian Cell Culture (Curr. Opin. Biotechnol. 2 (1991), 375); and Suspension Culture of Mammalian Cells (Birch et al., Bioprocess Technol. 19 (1990), 251); Extracting information from cDNA arrays, Herzel eta!., CHAOS 11 (2001), 98-107.
[000265] Os seguintes experimentos são ilustrados e descritos com relação ao anticorpo NI-101.11. Entretanto, os outros anticorpos da série NI 101, em especial NI 101.10 são estruturalmente similares e, portanto, deles se pode esperar que apresentem resultados comparáveis.
[000266] Sujeitos humanos selecionados cuidadosamente clinicamente que são caracterizados por cursos clínicos excepcionalmente positivos, por exemplo, ausência de sinais clínicos da doença na presença de fatores de risco ou de cursos estáveis de sinais suaves ou prodrômicos sem nenhum desenvolvimento da doença ou de não progressores de longo prazo são recrutados para propiciar linfócitos sanguíneos periféricos como material de partida para o isolamento das células B de memória. A estratégia está baseada no conceito estabelecido na imunologia da infecção de que um conjunto de células B de memória do sujeito preserva as especificidades do anticorpo e, possivelmente, também as frequências de anticorpos geradas durante os encontros de antígenos anteriores (McHeyzer-Williams e Ahmed Curr. Opin. Immunol. Opin. 11 (1999), 172-179, Bernasconi et a!., Science 298 (2002), 2199-202; Traggiai et a!., Nat. Med. 10 (2004), 871-875). Este conceito foi desenvolvido para explicar a imunidade versátil contra os agentes infecciosos, como também para descrever a imunidade mediada pelo anticorpo após a primeira infecção. Segundo esta teoria, o complemento total dos anticorpos contra todos os antígenos que haviam induzido uma resposta do anticorpo no histórico do sujeito, seja naturalmente ou após a vacinação, deve ser plenamente representado no conjunto das células B de memória. De acordo com a presente invenção esta teoria é aplicada aos antígenos endógenos gerados como resultado da agregação ou conformação anormal de uma outra proteína de outro modo relevante fisiológica e que, como tal, não está sujeita à tolerância imunológica fisiológica e, assim, pode adquirir propriedades antigênicas e induzir uma resposta imune contra os neoepítopos conformacionais. (neoepítopos).
[000267] As células B de memória são isoladas com marcadores de superfície incluindo o marcador de célula B pan CD22, em combinação com a seleção negativa das células B não experimentadas com antígeno que expressaram IgM, IgD, IgE e IgA. Com esta técnica, aproximadamente 10.000 a 150.000 células de memória B podem ser obtidas a partir de 30 ml de sangue humano. Estas são imortalizadas, por exemplo com o vírus Epstein Barr e expostas à cultura oligo- clonalmente em camadas de alimentador de fibroblasto humano irradiado (Zubler et al.,J Immunol. 134 (1985), 3662-3668; Traggiai et al., Nat. Med. 10 (2004), 871-875). Para melhorar a eficácia da transformação e da imortalização das células B de memória secretoras do anticorpo, CpG 2006 que imita as atividades dos CpG- binucleotídeos não metilatados bacterianos (Hartmann and Krieg J Immunol 164(2) (2000), 944-953) podem ser usados. Protocolo experimental:
[000268] A seleção de células B do volume de PBL foi realizada utilizando a tecnologia MACS e microesferas CD22 (Miltenyi, Bergisch Gladbach, Alemanha). PBL foi marcado com MACS anti-humano CD22, IgD anti-humano conjugado com ficoeritrina e anticorpos conjugados com APC antihumanos IgM, IgA, CD3, CD8, CD56 (Becton Dickinson, Basel, Suíça). Células positivas-CD22 foram isoladas usando colunas LS e dispositivo Midi MACS (Miltenyi), seguido pela seleção de células negativas-APC e ficoeritrina usando um selecionador de células MoFIo. (Dako, Fort Collins, E.U.A.). Células B CD22-positivas, IgM, IGD-, IgA-, IgE-negativas foram então incubadas com vírus Epstein Barr contendo sobrenadante obtido a partir das células B95-8 e CpG 2006 (Sigma, Buchs, Suíça), na concentração de 2,5 mg/l em meio de células B (RPMI 1640 complementado com 10% de soro bovino fetal (Hyclone, Perbio, Lausanne, Suíça). 5-50 células foram cultivadas por cavidade em placas de 96 cavidades de base redonda Costar (Corning, Vitaris, Baar, Suíça) em meio de células B, em 30.000 PBL humano irradiado preparado de doadores voluntários. As culturas das células B de memória foram mantidas a 37°C e 5% de CO2 em uma incubadora de cultura celular umidificada por 2-4 semanas após cujo período, o meio condicionado das culturas foi testado em ELISA e em disposições de tecidos.
[000269] Os anticorpos em meios condicionados passam por varredura quanto à ligação a epitopos patológicos incluindo agregados de proteínas e estruturas relevantes patologicamente, anormais em cortes de tecidos obtidas de pacientes humanos com diagnósticos confirmados patologicamente incluindo, entre outros, a doença de Alzheimer ou obtidos de cortes de tecidos de modelos de camundongos transgênicos da doença humana ou de cortes de tecidos obtidos de modelos animais da doença humana incluindo primatas não-humanos idosos ou pelo ELISA de preparações de peptídeos sintéticos agregados. Estruturas anormais, patológicas no sentido desta invenção incluem, mas não estão restritas a, placas B- amiloide, emaranhados neurofibrilares, agregados de alfa-sinucleínas em corpos de Lewy e agregados de proteínas depositados em neurites distróficas. Tecidos humanos também são usados para excluir reatividades cruzadas de anticorpos com estruturas de tecido supercelular ou celular normal. Anticorpos escolhidos são ainda analisados quanto à determinação de classe e subclasse de cadeia leve. Mensagens selecionadas de anticorpos relevantes para a patologia das culturas de células B de memória são transcritas usando TR-PCR, clonadas e combinadas em vetores de expressão para a produção recombinante.
[000270] Varredura do meio condicionado de células B usando microdisposições de tecidos compatíveis com microtitulação.
[000271] Tecidos cerebrais de seres humanos com doença de Alzheimer pós-morte inseridos em parafina foram cortados em bastões de 1-2 mm de diâmetro e 10 mm de comprimento. Quatro bastões foram inseridos verticalmente em parafina de modo a formar um quadrado que coubesse no formato do microtitulação de 9 por 9 mm. Fatias de tecido de 5 pm foram cortadas a partir deste conjunto com um micrótomo e duas fatias foram agrupadas adjacentes uma à outra nos slides de vidro resultantes em um conjunto de bastões de 2 por 4 adaptados ao formato do microtitulação de 96 cavidades. Alternativamente, tecidos de camundongos transgênicos APP foram usados para preparar as disposições dos tecidos.
[000272] Meio condicionado das culturas de células B de memória foi transferido para lâminas de disposições de tecidos usando uma pipeta de multicanais e incubado por 2 h em temperatura ambiente. Após uma etapa de lavagem, a ligação de anticorpos humanos para cortes de tecidos foi analisada usando anticorpos secundários conjugados de Ci-3 quanto ao IgG humano (Jackson ImmunoResearch Europe Ltd., Suffolk, Reino Unido). A análise da fluorescência foi realizada em um microscópio invertido de fluorescência (Leica, Heerbrugg, Suíça).
[000273] Microplacas de 96 cavidades com meia área (Corning) foram revestidas com peptídeo Abeta sintético em uma concentração- padrão de 1pg/ml em tampão de revestimento (15 mM Na2CO3, 35 mM NaHCO3, pH 9.42) durante a noite a 4°C. As placas foram lavadas e sítios de ligação não específicos foram bloqueados por 1 h em temperatura ambiente com PBS contendo 2% BSA (Sigma, Buchs, Suíça). O meio condicionado de células B foi transferido das placas de cultura de células B de memória para placas de ELISA e foi incubado por 2 h em temperatura ambiente. A ligação dos anticorpos humanos foi determinada utilizando anticorpos policlonais de burro anti-lgG humano conjugados à peroxidase de raiz forte (HRP) (Jackson ImmunoResearch Europe Ltd., Cambridgeshire, UK), seguida da medição da atividade de HRP em um ensaio colorimétrico-padrão.
[000274] Células B vivas de culturas de células B de memória são cultivadas usando um selecionador de células. O mRNA é preparado e sequências de cadeia leve e pesada de imunoglobulina são obtidas usando iniciadores específicos de estrutura-lg para toda família de estrutura 1 (FR1) da cadeia leve e pesada variável humana como iniciadoresde 5' em combinação com iniciadoresespecíficos para todos os segmentos J-H humanos como iniciadores3’ (Marks et al., Mol. Biol. 222 (1991), 581-597). Alternativamente, o TR-PCR de células únicas de células selecionadas únicas da cultura de células B de memória pode ser usado como fonte desequências de cadeia leve e pesada de lg (Babcook et al.,Proc. Natl. Acad. Sei. USA 93 (1996), 7843-7848; Brezinschek et al.,J. Immunol. 155 (1995), 190-202; Coronella et al., Nucleic Acids Research 28 (2000); Owens, et al., J. Immunol. 171 (2003), 2725-2733). A seleção de células únicas conserva o emparelhamento correto das cadeias leve e pesada de imunoglobulinas dos clones de anticorpos originalmente produzidos na cultura das células B.
[000275] A identificação do clone de anticorpo com a especificidade desejada é realizada através da revarredura em microdisposição de tecidos compatíveis com o microtitulação e a ELISA quando da expressão recombinante de anticorpos completos. A expressão recombinante de anticorpos de lgG1 completos é obtida quando da inserção das sequências de cadeia leve e pesada variáveis "na estrutura de leitura correta" para vetores de expressão que complementam a sequência de regiões variáveis com uma sequência codificadora de um peptídeo de sinal na ponta do prime-5e na Ponta-s'com uma sequência codificadora do(s) domínio(s) constantes apropriados. Para esse efeito, os iniciadorescontinham sítios de restrição projetados para facilitar a clonagem de sequências de cadeia leve e pesada variável para vetores de expressão de anticorpos. A imunoglobulina de cadeia pesada é expressa pela inserção do produto TR-PCR da cadeia pesada da imunoglobulina na estrutura em um vetor de expressão de cadeia pesada comportando um peptídeo de sinal e domínios constantes da imunoglobulina humana. A imunoglobulina da cadeia leve kappa é expressa pela inserção do produto TR-PCR da cadeia leve kappa em estrutura em um vetor de expressão de cadeia leve propiciando um peptídeo de sinal e o domínio constante 1 da imunoglobulina de cadeia leve kappa humana. Alternativamente, a imunoglobulina de cadeia leve lambda é expressa pela inserção do produto TR-PCR de cadeia leve lambda em estrutura em um vetor de expressão de cadeia leve lambda propiciando um peptídeo de sinal e o domínio constante 1 da imunoglobulina de cadeia leve lambda humana.
[000276] Os anticorpos monoclonais recombinantes funcionais são obtidos quando da co-transfecção em células HEK 293 (ou qualquer outra linha de célula de recipiente apropriado) de um vetor de expressão de cadeia pesada de lg e um vetor de expressão de cadeia leve lg lambda ou kappa. O anticorpo monoclonal humano recombinante é posteriormente purificado do meio condicionado usando uma purificação da coluna A da proteína-padrão. O anticorpo monoclonal humano recombinante pode ser produzido em quantidades ilimitadas usando células transientemente ou estavelmente transfectadas. Linhas de células produtoras de anticorpos monoclonais humanos recombinantes podem ser estabelecidas usando vetores de expressão-lg diretamente ou pela re-clonagem das regiões variáveis de lg em diferentes vetores de expressão. Derivados, tais como F (ab), F (ab)2 e scFv também podem ser gerados a partir destas regiões variáveis de lg.
[000277] As células vivas conforme identificadas por suas propriedades de dispersão da luz para os lados e para frente de culturas de células B de memória foram selecionadas em partes de 100-2000 células diretamente em tubos de 0,2 ml de PCR tubos enchidos com 20pl de RNAIater (Ambion, Huntingdon, Reino Unido), utilizando um selecionador de células MoFIo. mRNA foi preparado utilizando o kit micro de mRNA-direto (Dynal, Invitrogen, Basel, Suíça). cDNA foi preparado usando o kit “TR para PCR” (Clontech BectonDickinson, Basel, Suíça) e a PCR das sequências variáveis de cadeia leve e pesada (lg) de imunoglobulina foi realizada usando o Kit Advantage 2 PCR (Clontech) usando iniciadoresespecíficos para todas as famílias de trabalho de estrutura 1 (FR1) de cadeia leve e pesada variável humana em combinação com os iniciadores específicos para os domínios constantes de cadeias leves lambda lg ou kappa lg ou pesada lg como iniciadores 3'. Iniciadores foram adquiridos da Microsynth (Balgach, Suíça).
[000278] Um peptídeo de sinal que foi usado em todos os vetores de expressão foi derivado da sequência 1 L5 de famílias de cadeia leve kappa de imunoglobulina humana (MDMRVPAQLLGLLLLWFPGSRC; SEQ ID NO: 2) conforme descrito em Base-V e projetado para propiciar o sítio de restrição Xba para facilitar a clonagem das regiões variáveis amplificadas de PCR
[000279] (ATGGACATGCGGGTGCCCGCCCAGCTGCTGGGCCTG CTGCTGCTGTGGTTCCCCGGCTCTAGATGC: SEQ ID NO: 1). Xba1 foi introduzido pela mutagênese silenciosa. Como um sítio de restrição 3 usado para a clonagem de regiões de cadeia pesada variáveis Sail foi introduzido no C1 do lgG1 propiciado pelo vetor. Do mesmo modo, o sítio de restrição BsiW1 foi introduzido no C1 da cadeia leve kappa e Xho1 foi introduzido no C1 da cadeia leve lambda. O resumo da restrição de PCR e ligadura ao destinatário em vetores foi realizada de acordo com procedimentos normais. O DNA de Plasmídeo foi preparado utilizando kits-padrão (Quiagen, Hombrechtikon, Suiça). Os vetores recebedores continham um promotor CMV para expressão dos genes de anticorpos em células mamíferas.
[000280] Para o TR-PCR de células únicas de regiões variáveis de cadeia leve e pesada de lg de células B cultivadas, foi usada uma modificação do método descrito por Owens et al. (Owens et al., 2003). Células únicas foram depositadas diretamente em cada tubo de uma disposição de tubos PCR de 0,2 ml utilizando o selecionador de células MoFIo. Cada tubo foi preparado para conter 10 pl de tampão de TR para transcriptase reverso do Superscrit II (Invitrogen). Tubos de PCR foram congelados por choque em gelo seco e descongelados imediatamente antes de TR-PCR. O cDNA foi preparado utilizando hexâmeros aleatórios (Clontech) e transcriptase reversa do Superscript II (Invitrogen). O 1o ciclo de PCR das regiões variáveis de cadeia pesada e leve de imunoglobulina foi realizada usando, como iniciadores5’, um conjunto de iniciadoresque foram preparados para uso em todos os peptídeos de sinal conservados entre as famílias de regiões variáveis de lg. Na posição 3’, iniciadoresúnicos específicos para a região constante da cadeia pesada de C1 lg ou a cadeia leve lambda de lg ou kappa de lg foram usados. O 2o ciclo de PCR foi realizado em produtos de PCR obtidos durante o primeiro ciclo de PCR usando os iniciadores conforme descrito para TR-PCR de células B em volume. A clonagem em vetores recebedores foi, portanto, realizada.
[000281] A clonagem foi realizada usando o método de diluição limitado-padrão ou através de deposição de células únicas em chapas de cultura de 96 cavidades utilizando um selecionador de células (MoFIo, Dako, Fort Collins, EUA). Para limitar a diluição, células de uma cultura de células B de memória foram colhidas, passaram por uma malha de náilon de 30 pm (Falcon, Becton Dickinson, Basel, Suíça), ressuspensas em meio e semeadas em placas de 96 cavidades ou placas de 384 cavidades em uma concentração de 0,3 células por cavidade.
[000282] Para semeadura com o selecionador de células, o dispositivo foi configurado para depositar uma célula única (modo único 1) por cavidade diretamente em placas de 96 cavidades complementadas com meio de células B. O meio de cultura foi complementado com meio condicionado por células T ativadas. Alternativamente, 30.000 células de alimentador irradiadas foram adicionadas ao meio. O meio de cultura foi complementado com meio condicionado por células T ativadas.
[000283] O sequenciamento das sequências das regiões variáveis de imunoglobulinas clonadas foi realizado usando iniciadores específicos para o promotor de CMV presente 5’ das sequências das regiões variáveis de lg inseridas. Alternativamente, iniciadores que foram preparados para uso nos domínios constantes das cadeias leve e pesada de lg foram utilizados. Sequências obtidas foram analisadas e alinhadas usando software Vector NTI (Informax-lnvitrogen). Plasmídeos contendo sequências que codificaram as regiões variáveis de imunoglobulinas completas em consonância com o peptídeo líder e o domínio constante foram usadas para expressão.
[000284] Os anticorpos podem ser produzidos em quantidades suficientes pela expressão recombinante usando tecnologias conhecidas na técnica (Trill et ai., Curr. Opin. Biotechnol. 6 (1995), 553-601). O anticorpo monoclonal humano recombinante de até 1 mg foi produzido quando da transfecção transitória de células HEK-293. O anticorpo monoclonal humano recombinante de até 100 mg foi produzido mediante a transdução estável de células HEK-293 ou de células murinas NOS usando vetores lentivírus recombinantes.
[000285] Vetor de cadeia pesada de lg e vetores de cadeia leve de lg foram co-transfectados para células HEK-293 usando o método- padrão de co-precipitação de fosfato de cálcio. Anticorpos recombinantes foram purificados a partir do meio condicionado por células HEK-293 utilizando purificação da coluna A de proteínas (GE- Healthcare, Otelfingen, Suíça). Produção em grande escala de anticorpos recombinantes humanos por transdução estável
[000286] Aqui, um sistema de transfecção com base em lentivírus foi empregado para gerar linhas de células convertidas estavelmente produzindo anticorpo recombinante humano (Zufferey et al.,Virol. 72 (1998), 9873-9880). Células HEK-293 foram co-convertidas com dois lentivetores distintos, um portando um cassette de expressão para a cadeia pesada de lg, o outro um cassette para cadeia leve de lg de um anticorpo recombinante. Este método de transdução pode ser utilizado em uma ampla gama de linhas de células de mamíferos, tais como células CHO e NSO.
[000287] Camundongos transgênicos foram gerados como descrito anteriormente (Knobloch et al.Neurobiol. Aging July 28 (2006)) sobre um fundo híbrido C57B1/6 e DBA2. O grupo de teste foi retrocruzado uma vez quanto a C57BL/6. Os camundongos foram mantidos sob condições habitacionais-padrão, em um ciclo claro/escuro de 12h:12h invertido e tiveram livre acesso à alimentação e água. Os grupos de tratamento foram equilibrados por idade (24 meses no primeiro ensaio, 26 meses no 2o teste) e gênero. Camundongos são tratados com anticorpos (3mg/kg de peso corporal), com injeções intraperitoneais uma vez por semana, durante um período de 2 meses, resultando em 8 injecções por animal.
[000288] A taxa de alternação espontânea é avaliada usando um labirinto de plástico em forma de Y, com braços medindo 40 x 20 x 10 cm. Durante sessões de 5 minutos, as sequências de entradas de braços são registradas; a alternância foi definida como entradas sucessivas nos três braços, em conjuntos trigêmeos de sobreposição. A alternância de percentual foi calculada como a razão das alternâncias reais a possíveis. Após 2 meses de tratamento de anticorpos, os camundongos são retestados no labirinto em Y. Os experimentadores são sempre mantidos cegos para ambos os tratamentos e genótipos durante todo o experimento.
[000289] Para avaliar se os anticorpos ou seus fragmentos selecionados podem penetrar na barreira hematoencefálica e se ligar aos seus alvos de proteínas anormalmente agregados ou de conformação alterada no cérebro, uma dose eficaz do anticorpo é administrada sistemicamente, intraperitonealmente, por via intravenosa, intramuscular, subcutânea ou intranasal a um animal transgênico que é caracterizado pelo acúmulo não fisiológico do alvo de proteína agregado ou de conformação alterada no cérebro. A ligação do anticorpo às estruturas específicas da patologia no cérebro é então avaliada pela imunomarcação com um anticorpo secundário de anti-lg humano seguido da detecção imuno-histoquímica padrão. Protocolo experimental:
[000290] Camundongos do modelo transgênico PS-1/APPswe para a doença de Alzheimer receberam duas injeções periféricas de 150 pg de NI-101.11 no dia 1 e no dia 3. Os camundongos foram sacrificados 24 h após a segunda injeção e pulverizados com PBS. Os cérebros foram congelados e as fatias de tecido foram preparadas a partir do tecido congelado usando o criostato. A presença de anticorpo humano nas seções criostáticas foi testada pela marcação com anticorpo anti- IgG humana conjugado à Cy3 (Jackson ImmunoResearch Europe, Suffolk, Reino Unido). A localização das placas amiloides foi realizada através da co-marcação das seções criostáticas com o anticorpo controle específico para Abeta murino 6E10 (disponível pela Covance, Catálogo Número SIG-39320), seguido pelo anticorpo IgG anticamundongo conjugado à FITC. Alternativamente, a marcação com anticorpo anti-lgG humano conjugado à Cy3 foi utilizada isoladamente. A análise da fluorescência foi realizada em um microscópio invertido de fluorescência (Leica).
[000291] Os efeitos do tratamento com o anticorpo nos níveis de alvos de proteínas agregados ou de conformação alterada no cérebro foram avaliados pelo tratamento sistêmico ou pela produção pelo cérebro alvo do anticorpo (intracraniano, intratecal ou intraventricular) e pelo controle de um anticorpo não relacionado para animais transgênicos com acúmulo não fisiológico característico do alvo de proteína agregado ou de conformação alterada no cérebro. Os efeitos do tratamento são avaliados pela imunomarcação ou marcação histoquímica dos alvos de proteína alterados ou agregados e pela medição da área coberta por tais agregados, pelo tamanho dos agregados e pelo número de agregados e pela quantificação bioquímica das concentrações dos alvos de proteínas em diferentes áreas do cérebro.
[000292] Os efeitos potenciais adversos relacionados com o alvo do tratamento com o anticorpo serão avaliados pela administração sistêmica ou pela produção pelo cérebro alvo do anticorpo (intracraniano, intratecal ou intraventricular) e um controle do anticorpo não relacionado com animais transgênicos com acúmulo não fisiológico característico do alvo de proteína agregado ou de conformação alterada no cérebro. Os efeitos colaterais em potencial serão avaliados pela imunomarcação ou marcação histoquímica (por exemplo, azul prussiano para micro-hemorragias, hematoxilina-eosina, células sanguíneas brancas ativadas) e quantificação bioquímica (por exemplo, níveis de citocinas pelo ELISA).
[000293] Células HEK-293 células foram transfectadas temporariamente com um vetor que expressa APP selvagem humano fundido no C-terminal intracelular com a variante amarelo citrina fluorescente da proteína. 24 horas após a transfecção, as células foram incubadas com anticorpos recombinantes humanos ou com anticorpos de controle a 4°C durante 30 minutos. Após uma etapa de lavagem, a célula foi fixada e o anticorpo ligado à superfície foi detectado usando anticorpos secundários IgG humano ou de camundongo conjugados à Cy-3 (Jackson ImmunoResearch). A análise de fluorescência foi realizada em um microscópio confocal (Leica).
[000294] O peptídeo Abeta foi adquirido da Bachem (Bubendorf, Suíça). O peptídeo liofilizado foi reconstituído em TFA e resuspenso em PBS imediatamente antes de sua utilização como Abeta monomérico nos ensaios. As fibrilas Abeta foram preparadas pela incubação de peptídeo Abeta1-42 peptídeo monomérico em uma concentração de lOOpg/ml em PBS a 37°C por 24h. As preparações de peptídeos Abeta monoméricos e fibrilas foram também usados como substrato para cobrir placas ELISA.
[000295] O peptídeo Abeta monomérico foi misturado com corante de carregamento, desnaturado a quente e carregado com 0,2 pg por via, e separado em um gradiente SDS-PAGE. As bandas foram incubadas com anticorpo primário por 2 h. A ligação do anticorpo monoclonal humano primário ou anticorpo controle de camundongos 6E10 foi revelada utilizando anticorpos anti-humanos ou anticamundongos secundários conjugados com a peroxidase de raiz- forte (HRP). Bandas foram desenvolvidas usando Substrato de Sensibilidade Máxima SuperSignal West Femto (Pierce, Fisher Scientific, Wohlen, Suíça).
[000296] O anticorpo NI-101.11 humano recombinante foi incubado por 2 h com preparações de peptídeos Abeta. As preparações de anticorpos/Abeta foram então usadas para marcação imuno- histoquímica da seção do cérebro obtida de um paciente com a doença de Alzheimer neuropatologicamente confirmada. Crio-seções- de 5 pm foram preparadas, bloqueadas com 4% BSA, 5% de soro de cabra e 5% de soro de cavalo em PBS por 1h em TA e marcadas com preparações de NI-101.11/Abeta por 1 h em temperatura ambiente. Após uma etapa de lavagem, a ligação dos anticorpos humanos às seções de tecidos foi analisada usando anticorpos secundários IgG humano conjugados à Cy3 (Jackson ImmunoResearch Europe Ltd). A análise da fluorescência foi realizada em um microscópio invertido de fluorescência (Leica, Heerbrugg, Suíça).
[000297] Detecção de anticorpos humanos contra estruturas anormais prevalentes em doenças do cérebro humano
[000298] Anticorpos a partir de indivíduos fenotipicamente saudáveis ou extraordinariamente clinicamente estáveis com a doença de Alzheimer foram testados por imuno-histoquímica nas seções cerebrais obtidas de pacientes com doença de Alzheimer patologicamente confirmada. A figura demonstra a presença de anticorpos em um paciente clinicamente excepcionalmente estável que se ligam a placas beta-amiloides conforme foi confirmado pela co- marcação com um anticorpo conhecido contra o beta-amiloide humano (anticorpo 4G8; Figura 1B). A presença em um sujeito humano saudável de anticorpos para emaranhados neurofibrilares em uma seção de tecido obtido de um paciente com doença de Alzheimer é mostrada na figura 2A. Este resultado foi confirmado pela co-marcação com um anticorpo conhecido contra tau humano (HT7). A figura 3A revela a presença em um sujeito humano saudável de anticorpos contra neurites distróficas em uma seção de tecido obtida de um paciente com doença de Alzheimer. Marcação controle com anticorpo conhecido contra o tau humano (HT7) é ilustrada na Figura 3 B. Esses resultados demonstram a presença, em pacientes fenotipicamente saudáveis ou excepcionalmente clinicamente estáveis, de anticorpos contra estruturas patológicas identificáveis em amostras de tecido humano com diagnóstico histopatologicamente confirmado.
[000299] Anticorpos humanos recombinantes mantêm especificidade para estrutura anormal in vivo e reconhecem epitopo conformacional de protepina beta-amiloide associada à doença em placas de amiloides do cérebro mas não seu precursor fisiológico ou derivado não patogênico.
[000300] Anticorpos NI-101.11, N1-101,12, NI-101.13A e NI-101.13B foram obtidos de pacientes com a doença de Alzheimer excepcionalmente clinicamente estáveis com uma taxa significantemente reduzida de declínio cognitivo. O isolamento dos anticorpos e a produção de recombinantes foram realizados conforme especificado nos métodos complementares. NI-101.11
[000301] O NI-101.11 recombinante foi testado quanto à ligação às placas beta-amiloides do cérebro. As seções cerebrais obtidas de um paciente com doença de Alzheimer neuropatologicamente confirmada foram marcadas nas concentrações indicadas. A ligação do anticorpo às placas beta-amiloides com concentrações de 50 pM sugere ligação de alta afinidade. A ligação do anticorpo NI-101.11 às placas beta- amiloides em uma concentração de 0,5 nM não pode sofrer concorrência pela adição de quantidades excessivas de polipeptídeo derivado de Abeta N-terminal sintético linear representando posições de 1 a 16 em concentrações de até 1 pM (Figura 5). Além disso, a ligação de NI-101.11 às placas beta-amiloides nas seções do cérebro em concentração de 8 nM sofre concorrência de quantidades excessivas de fibrilas de Abeta1-42 (4 pM) mas não de monômeros de Abeta1-42 sintéticos lineares a uma concentração de 4 pM, sugerindo que NI -101.11 reconhece um epitopo conformacional que não está presente no Abeta monomérico (Figura 6).
[000302] Para melhor avaliar a ligação do anticorpo NI-101.11 recombinante humano ao Abeta sintético monomérico linear, preparações de Abeta monomérico foram separadas pelo PAGE não- desnaturante. Proteína marcada foi examinada com anticorpo Nl- 101.11 recombinante humano e um com um anticorpo controle contra as sequências Abeta lineares N-terminais (6E10). Enquanto que o 6E10 produziu marcação proeminente do peptídeo Abeta monomérico, nenhuma ligação foi detectada para N1-101.11 sugerindo que Nl- 101.11 não se aglutina ao peptídeo Abeta monomérico linear mas reconhece um epitopo Abeta conformacional. (Figura 7)
[000303] A ligação do recombinante N1-101.11 às fibrilas amiloides artificiais preparadas a partir de peptídeos Abeta1-42 sintéticos e do Abeta monomérico foi determinada pelo ELISA (Figura 8). Fibrilas Abeta ou Abeta sintéticas monoméricas pintadas sobre placas ELISA em iguais densidades de cobertura foram incubadas com N1-101.11 nas concentrações indicadas. A ligação às fibrilas amiloides artificiais (quadrados abertos) é mais do que 100 vezes superior conforme comparado com o Abeta monomérico (quadrados preenchidos). O anticorpo controle 22C4 contra o C-terminal do Abeta preferencialmente se liga ao Abeta monomérico (círculos preenchidos) e menos preferencialmente às fibrilas (círculos abertos). Isso sugere que o NI-101-10 reconhece um epitopo conformacional, que também está presente nas fibrilas amiloides preparadas a partir de peptídeos Abeta sintéticos.
[000304] A reatividade cruzada do anticorpo NI-101.11 humano recombinante contra o AP de comprimento total celular ou com qualquer de seus derivados fisiológicos foi determinada pelos testes de ligação das células (Figura 9).
[000305] As células HEK-293 vivas que estavelmente expressam o APP humano fundido ao Citrin como um marcador foram incubadas por 30 minutos a 4°C, para evitar a internalização, com o anticorpo Nl- 101.11 humano recombinante ou com o anticorpo controle 6E10 contra a sequência Abeta linear N-terminal. Sinais de Cintrin-positivo indicam células que expressam APP. Em contraste com o anticorpo controle (6E10) que se liga ao APP de superfície da célula em todas as células que expressam o padrão de fusão, nenhuma ligação de anticorpo Nl- 101.11 humano recombinante ao APP de comprimento total é detectada. Estes dados demonstram a ausência de reatividade cruzada de NI-101.11 para APP de celular fisiológico.
[000306] A falta de ligação de NI-101.11 ao Abeta monomérico foi ainda demonstrada pela cromatografia de exclusão do tamanho. Nenhuma algutinação do NI-101.11 ou de um anticorpo controle não relacionado foi observada para o Abeta1-42 monomérico Conjugado à FITC (Figura 10A, 10B). Em contraste, o anticorpo 22C4 dirigido contra um epitopo linear presente no C-terminal do Abeta co-eluiu com os monômeros Abeta 1-42-FITC (Figura 10 C).
[000307] Em um ELISA de concorrência, a ligação de 6E10, um anticorpo dirigido contra um epitopo linear no N-terminal do Abeta, poderia ser completamente bloqueado quando da pré-incubação com concentrações em excesso de peptídeos Abeta1-16, Abeta1-28 e Abeta1-40 monoméricos. Em contraposição, a pré-incubação com concentrações em excesso de peptídeos Abeta lineares não aboliu a ligação do N1-101.11, sugerindo que o N1-101.11 requer um epitopo conformacional (Figura 11). NI-101.13Ae 13B
[000308] Os anticorpos NI-101.13A e 13B humanos recombinantes foram testados quanto à ligação às seções cerebrais obtidas de um modelo de camundongo APP transgênico de doença de Alzheimer (Tg2576). NI-101.13A e NI-101.13B produziram marcação proeminente de placas beta-amiloides na concentração de 10 nM (Figura 12). Ligação dos NI-101.13A e NI-101.13B recombinantes às fibrilas amiloides artificiais preparadas dos peptídeos Abetal-42 sintéticos e do Abeta monomérico foi determinada pelo ELISA. As fibrilas Abeta sintéticas ou Abeta sintético monomérico pintados sobre as placas ELISA em iguais densidades de revestimento foram incubadas com NI-101.13A e NI-101.13B nas concentrações indicadas. Ligação preferencial para fibrilas amiloides artificiais em comparação com monoméricas Abeta foi observado para ambos os anticorpos testados (Figura 13). NI-101.12
[000309] A ligação do N1-101.12 recombinante ao peptídeo Abetal- 42 sintético foi confirmada pelo ELISA (Figura 14A). A ligação do Nl- 101.12 em concentração de 133 nM sofreu concorrência pelo excesso de peptídeo Abeta1-42 (Figura 14 B).
[000310] O anticorpo humano recombinante contra o beta-amiloide do cérebro cruza a barreira hematoencefálica em um modelo de camundongo transgênico da doença de Alzheimer e se liga às placas do beta-amiloide encefálicas in vivo.
[000311] Para determinar se o anticorpo NI-101.11 humano recombinante cruza a barreira hematoencefálica e se liga às placas beta-amiloides do cérebro in vivo, os camundongos do modelo da doença de Alzheimer PS-1/APPswe transgênicos receberam duas injeções periféricas de 150 pg de N1-101.11 no dia 1 e no dia 3. Os camundongos foram sacrificados 24 h após a segunda injeção e perfundidos com PBS. Os cérebros foram colhidos e as seções dos cérebros foram marcadas com anticorpos contra IgG humano conjugados à FITC ou com anticorpo 6E10 de anticorpo Abeta monoclonal de camundongo seguido por um anticorpo contra IgG de camundongo conjugado à FITC para confirmar a presença das placas beta-amiloide do cérebro. A intensa marcação das placas amiloides com IgG anti-humano indicou que o anticorpo N1-101.11 humano recombinante pode cruzar a barreira hematoencefálica dos camundongos transgênicos e se ligar às placas beta-amiloides em animais vivos. (Figura 15).
[000312] O anticorpo humano recombinante contra o beta-amiloide melhora o comportamento cognitivo anormal e confere a redução de carga de placas beta-amiloides, astrogiose e microgliose em um modelo de camundongo transgênico da doença de Alzheimer sem aumentar a frequência das micro-hemorragias.
[000313] Camundongos com arcAbeta de 24 meses de idade e filhotes do tipo selvagem com a mesma idade foram tratados semanalmente i.p. com 3 mg/kg de anticorpo NI-101.11 humano recombinante ou com um anticorpo controle humano combinado com isotipo durante 2 meses. Para avaliar o efeito do tratamento sobre o comportamento anormal em camundongos transgênicos, o teste comportamental de labirinto em Y, foi realizado antes e após a conclusão do tratamento. A taxa espontânea de alternação foi avaliada usando um labirinto de plástico em forma de Y, com braços medindo de 40 x 20 x 10 cm. Durante sessões de 5 minutos, as sequências de entradas de braços são registradas; a alternância foi definida como entradas sucessivas nos três braços, em conjuntos trigêmeos de sobreposição. A alternância de percentual foi calculada como a razão das alternâncias reais para possíveis (definido como o número total de entradas de braços - 2) multiplicado por 100%. O desempenho do labirinto em forma de Y de camundongos arcAbeta não tratados e de controle de filhotes do tipo selvagem foi comparado usando um teste-t não emparelhado. Um teste não-paramétrico de Kruskal-Wallis foi utilizado para comparar a melhora após o tratamento em todos os 4 grupos. O teste U de Mann-Whitney não-paramétrico foi escolhido para comparação em forma de par dos diferentes grupos. Os executores-zero (isto é, camundongos que não deixaram o braço em que eles estavam) foram excluídos da análise.
[000314] Como foi observado nos estudos anteriores, camundongos arcAbeta de 24 meses de idade demonstraram estar significativamente incapacitados em comparação com seus irmãos do tipo selvagem (Figura 16A, antes do tratamento; teste t não emparelhado, p = 0,0007).
[000315] Camundongos arcAbeta tratados com NI-101.11 mostraram claramente níveis de alteração elevados em comparação com camundongos de controle do tipo selvagem tratados com NI-101.11 após 2 meses de tratamento. Análise da melhoria (ou seja, o desempenho após o tratamento menos desempenho antes do tratamento) mostrou uma diferença significativa entre os quatro grupos (Figura 16 B, teste de Kruskal-Wallis, p = 0,03). Uma análise post-hoc em forma de par entre todos os grupos mostrou que os camundongos arcAbeta tratados com NI-101.11 melhorou seu desempenho cognitivo significativamente mais do que os camundongos do tipo selvagem (U de Mann-Whitney, p = 0,05 N1-101.11 tg em contraposição ao NI 101.11 wt, p = 0,008 N1-101.11 tg em contraposição ao controle wt). Este grupo de camundongos também mostrou uma forte tendência para o desempenho melhorado em comparação com os filhotes transgênicos tratados com anticorpo controle (U de Mann-Whitney; p=0.08 NI-101.11 tg em contraposição ao controle tg). Todos os camundongos mostraram uma melhora de ~10% no desempenho na repetição do teste, o que foi ocorreu provavelmente devido ao ambiente familiar da tarefa.
[000316] Os efeitos do tratamento com NI-101.11 por 2 meses em peso amiloide, astrogliose e microgliose foram analisados pela análise histoquímica e imuno-histoquímica quantitativa. Para essa finalidade, os camundongos foram anestesiados após a conclusão dos testes comportamentais e foram perfundidos transcardialmente com PBS. Um hemisfério cerebral foi fixado em 4% de paraformaldeído e incrustado em parafina. Seções sagitais de 5 pm foram cortadas com um micrótomo Leica RM 2135 (Bannockburn, Illinois). A carga de placa beta-amiloide em córtex e o hipocampo foram quantificados nas seções do cérebro marcadas com Tioflavina S e Vermelho de congo, de acordo com o protocolo padrão. Para imunofluorescência, fatias foram desparafinadas, bloqueadas com 4% BSA, 5% de soro de cabra e 5% de soro de cavalo em PBS por 1 h em TR. Os anticorpos foram incubados durante a noite a 4°C utilizando as seguintes diluições: anti- GFAP (Advanced Immunochemicals) 1:500, anti IBA1 (Wako) 1:500. Anticorpos secundários acoplados com fluoróforo foram incubados em TR por 2 h. 2-3 seções por cérebro de camundongo com 75 pm de espaçamento foram usadas para cada marcação. 2 imagens por seção foram tomadas na ampliação de 10x para análise córtex (região frontal e parietal). Toda a área do hipocampo (5x de ampliação cortada para ROI) foi levada para a análise do hipocampo. A análise da imagem automatizada foi feita com o software ImageJ.
[000317] Dupla marcação de seções de cérebro de camundongos arcAbeta imunizados com 6E10 e ligação revelada de IgG anti- humano de N1-101.11 para depósitos Abeta (Figura 17, painel esquerdo), indicando que o NI-101.11 pode atravessar a barreira hematoencefálica e se ligar às placas beta-amiloides. Nenhuma ligação como esta do anticorpo humano aos depósitos Abeta foi observada em camundongos arcAbeta tratados com anticorpo controle (Figura 17 painel direito).
[000318] O tratamento crônico com 3mg/kg de N1-101.11 resultou em uma redução significativa da carga da placa amiloide como foi revelado pela Tioflavina S e marcação com Vermelho de congo. Esta redução atingiu níveis superiores a 50% no córtex e no hipocampo em comparação aos camundongos arcAbeta tratados com anticorpo controle (Figura 18 A, B). Além da área da placa (Fig 18 C), reduções significativas foram também observadas para o número de placas (Figura 18 D) e o tamanho medido da placa (Figura 18 E).
[000319] Para testar se o tratamento crônico com NI-101.11 afeta a resposta neuroinflamatória nos camundongos arcAbeta, astrócitos reativos e microglia foram quantificados após a marcação imuno- histológica. A redução no número de astrócitos reativos (anti-mancha GFAP) foi observada no córtex de camundongos arcAbeta tratados com NI-101.11 em comparação com animais tratados com anticorpos controle (Figura 19A; U deMann-Whitney, p = 0,047). Nenhuma alteração foi detectada no hipocampo. A marcação com um anticorpo contra um marcador de microglia e macrófagos (anti-lba1) também revelou uma tendência estatística para inflamação reduzida (Figura 19 B; U de Mann-Whitney, p = 0,075 tanto para o córtex como para o hipocampo). A diminuição na astrocitose e microgliose está alinhada com a carga beta-amiloide reduzida observada após o tratamento com NI-101.11.
[000320] A imunoterapia passiva com certos anticorpos monoclonais dirigidos contra o Abeta pode ser associada com frequência aumentada de micro-hemorragias no cérebro (Pfeifer et al., Science 298 (2002), 1379; Wilcock et al., J Neuroinflammation 1 (2004), 24). Para avaliar os efeitos da terapia crônica com Nl- 101.11, a marcação com azul da Prússia de Perl foi realizada nas seções do cérebro de camundongos do tipo selvagem e arcAbeta aos tratamento com NI-101.11 crônico. Esta marcação revela a presença de hemossiderina, um produto de divisão da hemoglobina e marcador de micro-hemorragias anteriores (Figura 20). Em camundongos arcAbeta idosos tratados com um anticorpo controle, a frequência dos perfis positivos de azul prussiano foi significativamente elevada em comparação aos filhotes do tipo selvagem (U de Mann-Whitney, p = 0,001). O tratamento com o Nl- 101.11 não levou a um aumento do número de micro-hemorragias quando comparado com os camundongos arcAbeta tratados com anticorpo controle (U de Mann-Whitney, p = 0,347), indicando que os efeitos terapêuticos benéficos do tratamento NI-101.11 ocorreram na ausência deste efeito colateral frequentemente observado de imunoterapia passiva ao Abeta.
[000321] Anticorpo humano recombinante contra o beta-amiloide do cérebro inibe a formação das fibrilas abeta sintéticas in vitro.
[000322] O efeito do anticorpo NI-101.11 humano recombinante na formação das fibrilas-Abeta foi testado pela medição da ligação de Tioflavina S ao Abeta agregado pela análise de fluorescência. Soluções Abeta monoméricas foram incubadas a 37°C durante 24 h, quando da ausência do aumento da concentração de NI-101.11. A formação de fibrilas Abeta sintéticas in vitrofoi inibida pelo NI-101.11 humano recombinante de maneira dependente da concentração (Figura 21).
[000323] Os efeitos do NI-101.11 na fagocitose mediada pelo receptor Fc gama das fibrilas Abeta foram estudados na linha de células derivadas de microglias BV-2. As células BV-2 foram mantidas em DMEM complementado com 5% de FBS, Etapa/Pen e glutamina. As células foram tripisinizadas e cavidades/120.000 células BV-2 foram cultivadas em placas de 24 cavidades de base plana. Após 12 h, o meio foi substituído por 400 ul de DMEM/F12/cavidade completado com de 20 mM de HEPES (pH 7,3), 1% BSA, 10 mg/ml Etapa/Pen. 100 pg/ml de Fucoidan, um inibidor do receptor "scavenger", foi adicionado 30 minutos antes da experiência. 50 pM de fibrilas Abeta conjugadas à FITC foram pré-incubadas com concentrações indicadas de anticorpos durante 30 minutos a 37°C, lavadas duas vezes seguido de centrifugação por 5 min. a 14.000 x g. Esta suspensão foi adicionada às placas de cultura do tecido. Após 30 min, as células BV- 2 foram lavadas duas vezes com HBSS para remover Abeta fibrilar não associado.
[000324] As células foram tratadas com 250 pg/m de tripsina/EDTA por 20 min a 4°C e lavadas duas vezes por centrifugação a 500 x g por 5 min a 4°C. As células foram fixadas durante 20 min. em FACS-Fix (PBS, 2U, 2% de glicose, 5 mM NaN) e lavadas duas vezes com lavagem FACS (PBS, 5 pM EDTA, 0,2% BSA). A fluorescência (FL-1) de 10.000 células foi determinada pela análise FACS (com base em Webster SD et ai., Jl 2001).
[000325] Fagocitose dependente do receptor Fc gama de fibrilas Abeta1-42 conjugadas à FITC foi medida quando da inibição do sistema do receptor "scavenger". A análise comparativa de um anticorpo NI-101.11 humano e um anticorpo disponível comercialmente com um epitopo linear no N-terminal do peptídeo Abeta (6E10) demonstrou a indução dependente de dose de fagocitose das fibrilas Abeta. A aceitação das fibrilas mediadas por Nl- 101.11 é até 3 vezes maior que a observada para o anticorpo 6E10 (Figura 22). Esses dados indicam que o NI-101.11 dispara fagocitose mediada por receptor Fc gama dependente de dose potente de fibrilas Abeta pelas células microgliais.
[000326] Conforme demonstrado nos experimentos acima realizados em conformidade com a presente invenção, foi surpreendentemente possível detectar os anticorpos ativos protetores e terapêuticos e as células-B produtoras de anticorpos em sujeitos humanos fenotipicamente saudáveis, assintomáticos, como também em pacientes com cursos de doença clínicos excepcionalmente estáveis a despeito de um diagnóstico de incapacidade cognitiva ou doença de Alzheimer. Mais especificamente, uma nova classe de anticorpos humanos poderia ser detectada e isolada, que discrimina a forma fisiologicamente funcional de um antígeno, minimizando, assim, o risco de efeitos secundários autoimunogênicos, até aqui representando um problema na imunoterapia. Assim, anticorpos e moléculas de ligação equivalentes são propiciados de modo que especificamente reconhecem uma variante do antígeno em uma estrutura patofisiologicamente relevante, à qual o anticorpo deverá se ligar para diminuir sua toxicidade ou para reduzir sua concentração ou para promover sua degradação, por meio de, por exemplo, tornar o patógeno visível para macrófagos que expressam FcR ou células de microglia e, portanto, torná-lo inócuo. Como ainda demonstrado nos exemplos, tais anticorpos são terapeuticamente eficazes e são capazes de suspender como também impedir efeitos prejudiciais de proteínas patológicas anormais e seus agregados sem aumentar a frequência das micro-hemorragias do cérebro.
Claims (19)
1. Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo, caracterizado pelo fato de que se liga a beta-amiloide e que compreende uma região variável de cadeia pesada (VH) e uma região variável de cadeia leve (VL), em que a VH compreende uma primeira região determinante de complementariedade (VHCDR1) com a sequência de aminoácido como estabelecido na SEQ ID NO: 20, uma VHCDR2 com a sequência de aminoácido como estabelecido na SEQ ID NO: 21, e uma VHCDR3 com a sequência de aminoácido como estabelecido na SEQ ID NO: 22, e em que a VL compreende uma VLCDR1 com a sequência de aminoácido como estabelecido na SEQ ID NO: 23, uma VLCDR2 com a sequência de aminoácido como estabelecido na SEQ ID NO: 24, e uma VLCDR3 com a sequência de aminoácido como estabelecido na SEQ ID NO: 25, em que o anticorpo ou fragmento do mesmo compreende ainda uma região constante de lgG1 humana ou fragmento da mesma.
2. Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo de acordo com a reivindicação 1, caracterizado pelo fato de que compreende ainda uma cadeia leve capa humana.
3. Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que é um anticorpo humano ou um fragmento do mesmo.
4. Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de que se liga a placas beta-amiloides, depósitos amiloide cerebrovascular ou Abeta difuso.
5. Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo de acordo com qualquer uma das reivindicações 1 a 4, caracterizado pelo fato de que a VH compreende a sequência de aminoácido como estabelecida na SEQ ID NO: 39, e a VL compreende a sequência de aminoácido como estabelecida na SEQ ID NO: 41.
6. Composição farmacêutica, caracterizada pelo fato de que compreende o anticorpo ou fragmento de ligação ao antígeno do mesmo, como definido em qualquer uma das reivindicações 1 a 5, e um veículo farmaceuticamente aceitável.
7. Composição farmacêutica de acordo com a reivindicação 6, caracterizada pelo fato de que compreende ainda um agente adicional útil para o tratamento da doença de Alzheimer selecionado a partir do grupo consistindo em moléculas orgânicas pequenas, anticorpos anti-Abeta e combinações dos mesmos.
8. Anticorpo isolado que se liga a beta-amiloide e que compreende uma região VH e uma VL, caracterizado pelo fato de que a VH compreende uma VHCDR1 com a sequência de aminoácido como estabelecido na SEQ ID NO: 20, uma VHCDR2 com a sequência de aminoácido como estabelecido na SEQ ID NO: 21, e uma VHCDR3 com a sequência de aminoácido como estabelecido na SEQ ID NO: 22, a VL compreende uma VLCDR1 com a sequência de aminoácido como estabelecido na SEQ ID NO: 23, uma VLCDR2 com a sequência de aminoácido como estabelecido na SEQ ID NO: 24, e uma VLCDR3 com a sequência de aminoácido como estabelecido na SEQ ID NO: 25, e o anticorpo compreende ainda uma região constante de lgG1 humana.
9. Anticorpo de acordo com a reivindicação 8, caracterizado pelo fato de que compreende ainda uma cadeia leve capa humana.
10. Anticorpo de acordo com a reivindicação 8 ou 9, caracterizado pelo fato de que a VH compreende a sequência de aminoácido como estabelecida na SEQ ID NO: 39, e a VL compreende a sequência de aminoácido como estabelecida na SEQ ID NO: 41.
11. Composição farmacêutica, caracterizada pelo fato de que compreende o anticorpo, como definido em qualquer uma das reivindicações 8 a 10, e um veículo farmaceuticamente aceitável.
12. Composição farmacêutica, de acordo com a reivin-dicação 11, caracterizada pelo fato de que compreende ainda um agente adicional útil para o tratamento da doença de Alzheimer selecionado a partir do grupo consistindo em moléculas orgânicas pequenas, anticorpos anti-Abeta e combinações dos mesmos.
13. Polinucleotídeo isolado, caracterizado pelo fato de que compreende a sequência de nucleotídeos como demonstrada em: (i) SEQ ID NO: 38; ou (ii) SEQ ID NO: 40, em que a sequência de nucleotídeos é ligada a um elemento regulador heterólogo.
14. Vetor de expressão ou vetores de expressão, carac-terizados pelo fato de que compreendem o polinucleotídeo ou polinucleotídeos, como definidos na reivindicação 13, em que o polinucleotídeo ou polinucleotídeos é/são ligado(s) a um elemento regulador heterólogo.
15. Método para preparação de um anticorpo anti-beta- amiloide ou um fragmento de ligação ao antígeno do mesmo, caracterizado pelo fato de que compreende: (a) cultivar a célula hospedeira que compreende o polinu-cleotídeo ou polinucleotídeos, como definidos na reivindicação 13, ou o vetor de expressão, como definido na reivindicação 14, em uma cultura de células sob condições que levam a expressão do anticorpo anti-beta-amiloide ou fragmento de ligação ao antígeno do mesmo; e (b) isolar o referido anticorpo anti-beta-amiloide ou frag-mento de ligação ao antígeno do mesmo a partir da cultura de células.
16. Método de acordo com a reivindicação 15, caracterizado pelo fato de que compreende ainda formular o anticorpo isolado anti-beta-amiloide ou fragmento de ligação ao antígeno do mesmo em uma composição farmacêutica estéril.
17. Uso do anticorpo anti-beta-amiloide ou fragmento de ligação ao antígeno do mesmo, como definido em qualquer uma das reivindicações 1 a 5 e 9 a 11, caracterizado pelo fato de que é para a preparação de um medicamento para tratamento da doença de Alzheimer, deficiência cognitiva branda ou acumulação ou deposição anormal de beta-amiloide no sistema nervoso central em um indivíduo humano.
18. Composição, caracterizada pelo fato de que compre-ende o anticorpo anti-beta-amiloide ou um fragmento de ligação ao antígeno do mesmo, como definido em qualquer uma das reivindicações 1 a 5 e 9 a 11, em que o anticorpo anti-beta-amiloide ou um fragmento de ligação ao antígeno do mesmo está ligado a um marcador detectável.
19. Composição, de acordo com a reivindicação 18, carac-terizada pelo fato de que o marcador detectável é uma enzima, um grupo prostético, um material fluorescente, um material luminescente, um material bioluminescente, um material radioativo, um metal emissor de positrons ou um íon de metal paramagnético não-radioativo.
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87883107P | 2007-01-05 | 2007-01-05 | |
| EP07000211 | 2007-01-05 | ||
| EP07000211.8 | 2007-01-05 | ||
| US60/878,831 | 2007-01-05 | ||
| US93429107P | 2007-06-11 | 2007-06-11 | |
| US60/934,291 | 2007-06-11 | ||
| EP07020341.9 | 2007-10-17 | ||
| EP07020341 | 2007-10-17 | ||
| PCT/EP2008/000053 WO2008081008A1 (en) | 2007-01-05 | 2008-01-07 | Method of providing disease-specific binding molecules and targets |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0806328A2 BRPI0806328A2 (pt) | 2011-09-06 |
| BRPI0806328B1 true BRPI0806328B1 (pt) | 2020-07-14 |
| BRPI0806328B8 BRPI0806328B8 (pt) | 2021-05-25 |
Family
ID=39186163
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0806328A BRPI0806328B8 (pt) | 2007-01-05 | 2008-01-07 | anticorpo isolado ou fragmento de ligação ao antígeno do mesmo, seu método de preparação, composição farmacêutica, polinucleotídeo, vetor de expressão, bem como seus usos |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US8906367B2 (pt) |
| EP (5) | EP2426143B1 (pt) |
| JP (1) | JP5398545B2 (pt) |
| KR (4) | KR20120017469A (pt) |
| CN (3) | CN102603893A (pt) |
| AU (1) | AU2008203703C1 (pt) |
| BR (1) | BRPI0806328B8 (pt) |
| CA (2) | CA2674140C (pt) |
| CY (1) | CY1119197T1 (pt) |
| DK (3) | DK2436696T3 (pt) |
| EA (2) | EA029481B1 (pt) |
| ES (3) | ES2439490T3 (pt) |
| HU (2) | HUE033325T2 (pt) |
| LT (1) | LT2436696T (pt) |
| MX (1) | MX2009007136A (pt) |
| PL (3) | PL2426143T3 (pt) |
| PT (3) | PT2436696T (pt) |
| SG (1) | SG177954A1 (pt) |
| SI (2) | SI2099826T1 (pt) |
| WO (1) | WO2008081008A1 (pt) |
Families Citing this family (105)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2674140C (en) * | 2007-01-05 | 2018-05-15 | University Of Zurich | Method of providing disease-specific binding molecules and targets |
| HRP20140049T1 (hr) | 2007-01-05 | 2014-02-28 | University Of Zürich | Anti beta-amiloid antitijela i njihova upotreba |
| KR101570702B1 (ko) | 2007-03-13 | 2015-11-23 | 유니버시티 오브 취리히 | 단일클론 인간 종양-특이적 항체 |
| JP2011527338A (ja) * | 2008-07-09 | 2011-10-27 | ユニバーシティー オブ チューリッヒ | 神経新生を促進する方法 |
| EP2186827A1 (en) | 2008-11-14 | 2010-05-19 | HS LifeSciences Ltd. | Surrogate marker directed cDNA cloning of selectively induced mRNAs |
| KR101781228B1 (ko) | 2008-12-19 | 2017-09-22 | 바이오겐 인터내셔널 뉴로사이언스 게엠베하 | 인간 항-알파-시누클레인 자가항체 |
| FR2945538B1 (fr) * | 2009-05-12 | 2014-12-26 | Sanofi Aventis | Anticorps humanises specifiques de la forme protofibrillaire du peptide beta-amyloide. |
| CA2807244A1 (en) | 2010-08-27 | 2012-03-01 | University Of Zurich | A novel diagnostic and therapeutic target in inflammatory and/or cardiovascular diseases |
| EP2609431B1 (en) | 2010-08-27 | 2017-05-10 | University of Zurich | Method for target and drug validation in inflammatory and/or cardiovascular diseases |
| SG189174A1 (en) | 2010-10-11 | 2013-05-31 | Biogen Idec Internat Neuroscience Gmbh | Human anti-tau antibodies |
| SG10201509790YA (en) | 2010-11-30 | 2015-12-30 | Chugai Pharmaceutical Co Ltd | Antigen-Binding Molecule Capable Of Binding To Plurality Of Antigen Molecules Repeatedly |
| CN103380145B (zh) | 2010-12-17 | 2016-10-12 | 生物控股有限公司 | 人类抗-sod1抗体 |
| US20140044644A1 (en) | 2011-02-21 | 2014-02-13 | University Of Zurich | Ankyrin g and modulators thereof for the treatment of neurodegenerative disorders |
| WO2012133782A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| WO2012142301A2 (en) | 2011-04-12 | 2012-10-18 | Quanterix Corporation | Methods of determining a treatment protocol for and/or a prognosis of a patients recovery from a brain injury |
| MX357193B (es) | 2011-06-23 | 2018-06-29 | Univ Zuerich | Moleculas de union anti-alfa sinucleina. |
| US20140335089A1 (en) | 2011-09-30 | 2014-11-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting elimination of antigens |
| TW201817745A (zh) | 2011-09-30 | 2018-05-16 | 日商中外製藥股份有限公司 | 具有促進抗原清除之FcRn結合域的治療性抗原結合分子 |
| SG11201401100UA (en) | 2011-09-30 | 2014-07-30 | Chugai Pharmaceutical Co Ltd | Antigen-binding molecule inducing immune response to target antigen |
| JP6322411B2 (ja) | 2011-09-30 | 2018-05-09 | 中外製薬株式会社 | 複数の生理活性を有する抗原の消失を促進する抗原結合分子 |
| US20150299313A1 (en) | 2011-10-05 | 2015-10-22 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting clearance from plasma of antigen comprising suger chain receptor-binding domain |
| US20130095118A1 (en) * | 2011-10-11 | 2013-04-18 | Vaccinex, Inc. | Use of Semaphorin-4D Binding Molecules for Modulation of Blood Brain Barrier Permeability |
| CA2853100A1 (en) * | 2011-10-24 | 2013-05-02 | Intellect Neurosciences, Inc. | Compositions and methods for treatment of proteinopathies |
| KR101961508B1 (ko) * | 2011-10-28 | 2019-03-25 | 바이오겐 인터내셔널 뉴로사이언스 게엠베하 | Tdp-43 특이적 결합 분자 |
| AU2012332814B2 (en) | 2011-11-02 | 2017-12-14 | Biogen International Neuroscience Gmbh | Use of an anti-alpha-synuclein antibody to diagnose an elevated level of alpha-synuclein in the brain |
| CN113416257A (zh) | 2011-11-30 | 2021-09-21 | 中外制药株式会社 | 包含进入细胞内以形成免疫复合体的搬运体(载体)的药物 |
| DE102011057019A1 (de) * | 2011-12-23 | 2013-06-27 | Forschungszentrum Jülich GmbH | Standard zur Quantifizierung von pathogenen Aggregaten aus körpereigenen Proteinen |
| TWI593705B (zh) | 2011-12-28 | 2017-08-01 | Chugai Pharmaceutical Co Ltd | Humanized anti-epiregulin antibody and cancer therapeutic agent containing the antibody as an active ingredient |
| HUE037186T2 (hu) * | 2011-12-28 | 2018-08-28 | Immunoqure Ag | Eljárás humán antitestek izolálására |
| US10131709B2 (en) | 2011-12-28 | 2018-11-20 | Immunoqure Ag | Nucleic acid molecules encoding monoclonal antibodies specific for IL-22 |
| IN2014DN07149A (pt) * | 2012-01-27 | 2015-04-24 | Neotope Biosciences Ltd | |
| CN104204204A (zh) | 2012-02-09 | 2014-12-10 | 中外制药株式会社 | 抗体的Fc区变异体 |
| KR102219987B1 (ko) | 2012-02-24 | 2021-02-25 | 추가이 세이야쿠 가부시키가이샤 | FcγRIIB를 매개로 항원의 소실을 촉진하는 항원 결합 분자 |
| CN104487457B (zh) | 2012-05-30 | 2018-01-26 | 中外制药株式会社 | 靶组织特异性抗原结合分子 |
| EP2857419B1 (en) | 2012-05-30 | 2021-01-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for eliminating aggregated antigens |
| CA2894178A1 (en) * | 2012-12-07 | 2014-06-12 | Biogen International Neuroscience Gmbh | A method of reducing brain amyloid plaques using anti-a.beta. antibodies |
| KR102234324B1 (ko) | 2012-12-21 | 2021-03-31 | 바이오젠 엠에이 인코포레이티드 | 인간 항-타우 항체 |
| PL2970378T3 (pl) | 2013-03-15 | 2021-12-06 | Biogen Ma Inc. | Chromatografia oddziaływań hydrofobowych białek w warunkach bez soli |
| KR20160022354A (ko) | 2013-06-24 | 2016-02-29 | 추가이 세이야쿠 가부시키가이샤 | 인간화 항에피레귤린 항체를 유효성분으로서 포함하는 선암 이외의 비소세포폐암의 치료제 |
| AU2014284809B2 (en) * | 2013-07-03 | 2016-12-15 | Seoul National University R&Db Foundation | Chicken antibody transformed into cysteine and site-specific conjugation using same |
| WO2015006475A1 (en) * | 2013-07-12 | 2015-01-15 | Biogen Idec International Neuroscience Gmbh | Genetic and image biomarkers associated with decline in cognitive measures and brain glucose metabolism in populations with alzheimer's disease or those susceptible to developing alzheimer's disease |
| WO2015041310A1 (ja) | 2013-09-20 | 2015-03-26 | 中外製薬株式会社 | 抗プロテインc抗体による出血性疾患の治療 |
| MY176237A (en) * | 2013-11-21 | 2020-07-24 | Hoffmann La Roche | Anti-alpha-synuclein antibodies and methods of use |
| EP3078744B1 (en) | 2013-12-04 | 2020-08-26 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecules, the antigen-binding activity of which varies according to the concentration of compounds, and libraries of said molecules |
| NZ721048A (en) | 2013-12-20 | 2020-08-28 | Neurimmune Holding Ag | Antibody-based therapy of transthyretin (ttr) amyloidosis and human-derived antibodies therefor |
| CA2952745A1 (en) * | 2014-06-26 | 2015-12-30 | Janssen Vaccines & Prevention B.V. | Antibodies and antigen-binding fragments that specifically bind to microtubule-associated protein tau |
| ZA201608812B (en) | 2014-06-26 | 2019-08-28 | Janssen Vaccines & Prevention Bv | Antibodies and antigen-binding fragments that specifically bind to microtubule-associated protein tau |
| WO2016016278A2 (en) * | 2014-07-29 | 2016-02-04 | Neurimmune Holding Ag | Human-derived anti-huntingtin (htt) antibodies and uses thereof |
| AU2015326911C1 (en) | 2014-09-30 | 2025-12-18 | Neurimmune Holding Ag | Human-derived anti-dipeptide repeats (DPRs) antibody |
| MA41115A (fr) | 2014-12-02 | 2017-10-10 | Biogen Int Neuroscience Gmbh | Procédé de traitement de la maladie d'alzheimer |
| US20190099475A1 (en) | 2015-04-08 | 2019-04-04 | Nantomics, Llc | Cancer neoepitopes |
| CA3172682A1 (en) * | 2015-04-23 | 2016-10-27 | Nantomics, Llc | Cancer neoepitopes |
| CN108604257B (zh) * | 2015-10-12 | 2022-12-13 | 南托米克斯有限责任公司 | 产生特异性免疫治疗组合物及其相关核酸构建体的方法 |
| JP2018532736A (ja) | 2015-10-12 | 2018-11-08 | ナントミクス,エルエルシー | チェックポイント阻害物質への感受性を予測するmsiおよびネオエピトープの探索のための系、組成物、および方法 |
| EP3430397B1 (en) * | 2016-03-14 | 2022-02-23 | Biogen International Neuroscience GmbH | Antibody-dependent cell-mediated phagocytosis assay for reliably measuring uptake of aggregated proteins |
| US11542332B2 (en) | 2016-03-26 | 2023-01-03 | Bioatla, Inc. | Anti-CTLA4 antibodies, antibody fragments, their immunoconjugates and uses thereof |
| EP3448874A4 (en) | 2016-04-29 | 2020-04-22 | Voyager Therapeutics, Inc. | COMPOSITIONS FOR TREATING A DISEASE |
| US10889638B2 (en) | 2016-05-02 | 2021-01-12 | Prothena Biosciences Limited | Antibodies recognizing tau |
| AU2017259039B2 (en) | 2016-05-02 | 2024-05-09 | Prothena Biosciences Limited | Antibodies recognizing tau |
| MX2018015022A (es) | 2016-06-07 | 2019-08-14 | Biogen Int Neuroscience Gmbh | Métodos para el tratamiento de la enfermedad de alzheimer. |
| CN109641028A (zh) * | 2016-06-29 | 2019-04-16 | 加利福尼亚大学董事会 | α-突触核蛋白聚集的基于结构的肽抑制剂 |
| JP2018035137A (ja) | 2016-07-13 | 2018-03-08 | マブイミューン ダイアグノスティックス エイジーMabimmune Diagnostics Ag | 新規な抗線維芽細胞活性化タンパク質(fap)結合薬剤およびその使用 |
| US20190330318A1 (en) | 2016-07-25 | 2019-10-31 | Biogen Ma Inc. | Anti-hspa5 (grp78) antibodies and uses thereof |
| US10662226B2 (en) | 2016-10-28 | 2020-05-26 | The Regents of the University of Caiifomia | Synthetic beta-amyloid peptides capable of forming stable antigenic oligomers |
| MA47163A (fr) | 2016-12-16 | 2019-11-06 | Biogen Ma Inc | Facteur 11 de différenciation de croissance activé protéolytiquement stabilisé |
| JP2020508054A (ja) | 2017-02-17 | 2020-03-19 | デナリ セラピューティクス インコーポレイテッドDenali Therapeutics Inc. | 抗タウ抗体及びその使用方法 |
| KR101989383B1 (ko) * | 2017-04-04 | 2019-06-14 | 조선대학교산학협력단 | 알츠하이머성 치매의 조기진단을 위한 펩타이드 프로브 |
| AU2018263935B2 (en) | 2017-05-02 | 2024-09-26 | Prothena Biosciences Limited | Antibodies recognizing tau |
| CN109201128A (zh) | 2017-07-05 | 2019-01-15 | 京东方科技集团股份有限公司 | 微流控芯片、化学发光免疫分析系统和分析方法 |
| CN118370815A (zh) * | 2017-08-22 | 2024-07-23 | 渤健马萨诸塞州股份有限公司 | 含有抗β淀粉样蛋白抗体的药物组合物 |
| CN108484761B (zh) * | 2018-03-10 | 2021-04-30 | 吉林大学 | 一种特异性识别并诱导Aβ42的寡聚体及原纤维解聚的单链抗体、单链抗体基因及其应用 |
| CN108874749B (zh) * | 2018-06-22 | 2022-10-14 | 西南科技大学 | 一种高考志愿录取概率模型的建立方法 |
| MY203453A (en) | 2018-07-17 | 2024-06-28 | Shanghai hengrui pharmaceutical co ltd | Anti-abeta antibody, antigen-binding fragment thereof and application thereof |
| US12259395B2 (en) | 2018-08-17 | 2025-03-25 | Ab Studio Inc. | Catabodies and methods of use thereof |
| EP3861023A1 (en) * | 2018-10-04 | 2021-08-11 | Georg-August-Universität Göttingen Stiftung Öffentlichen Rechts, Universitätsmedizin | Humanised anti-n-truncated amyloid beta monoclonal antibody |
| CN113508135A (zh) | 2018-10-29 | 2021-10-15 | 比奥根Ma公司 | 增强血脑屏障转运的人源化和稳定化的fc5变体 |
| CN111518206B (zh) * | 2019-02-01 | 2022-03-29 | 长春金赛药业有限责任公司 | 人源化抗Aβ单克隆抗体及其应用 |
| CN111518205B (zh) * | 2019-02-01 | 2022-03-29 | 长春金赛药业有限责任公司 | 人源化抗Aβ单克隆抗体及其应用 |
| CN111518207B (zh) * | 2019-02-01 | 2022-03-29 | 长春金赛药业有限责任公司 | 人源化抗Aβ单克隆抗体及其应用 |
| KR102135130B1 (ko) * | 2019-02-15 | 2020-07-17 | 충북대학교 산학협력단 | 트랜스타이레틴 단백질에 특이적으로 결합하는 dna 앱타머 및 이의 용도 |
| TWI859197B (zh) | 2019-03-03 | 2024-10-21 | 愛爾蘭商普羅帝納生物科學公司 | 識別tau之抗體 |
| US11851487B2 (en) * | 2019-04-01 | 2023-12-26 | Rensselaer Polytechnic Institute | Methods and systems for detecting peptide aggregates |
| KR20220084095A (ko) | 2019-10-22 | 2022-06-21 | 바이오젠 엠에이 인코포레이티드 | 알츠하이머병의 치료를 위한 항-베타-아밀로이드 항체 |
| BR112022006534A2 (pt) | 2019-10-24 | 2022-07-05 | Novago Therapeutics Ag | Anticorpos anti-nogo-a |
| WO2021108861A1 (en) * | 2019-12-03 | 2021-06-10 | The University Of Queensland | Treatment of neurodegenerative diseases using ultrasound and amyloid-beta antibodies |
| KR20210095781A (ko) | 2020-01-24 | 2021-08-03 | 주식회사 에이프릴바이오 | 항원결합 단편 및 생리활성 이펙터 모이어티로 구성된 융합 컨스트럭트를 포함하는 다중결합항체 및 이를 포함하는 약학조성물 |
| JP7735291B2 (ja) | 2020-02-21 | 2025-09-08 | エーアールエス ファーマシューティカルズ、インコーポレイテッド | ネクチン-4抗体コンジュゲートおよびその使用 |
| IL298215A (en) | 2020-05-19 | 2023-01-01 | Othair Prothena Ltd | A multi-epitope vaccine for the treatment of Alzheimer's disease |
| WO2021245184A1 (en) | 2020-06-02 | 2021-12-09 | Neurimmune Ag | HUMAN ANTIBODIES AGAINST SEVERE ACUTE RESPIRATORY SYNDROME CORONAVIRUS-2 (SARS-CoV-2) |
| KR20230026489A (ko) | 2020-06-24 | 2023-02-24 | 프로테나 바이오사이언시즈 리미티드 | 소르틸린을 인지하는 항체 |
| EP4175673A1 (en) | 2020-07-01 | 2023-05-10 | ARS Pharmaceuticals Inc. | Anti-asgr1 antibody conjugates and uses thereof |
| UY39337A (es) | 2020-07-23 | 2022-02-25 | Othair Prothena Ltd | Anticuerpos anti-abeta |
| IL300347A (en) | 2020-08-07 | 2023-04-01 | Othair Prothena Ltd | Multi-shot vaccine for the treatment of Alzheimer's disease |
| CN114252628A (zh) * | 2020-09-24 | 2022-03-29 | 首都医科大学附属北京世纪坛医院 | 尿液再生蛋白及其多肽片段在过敏性疾病中的应用 |
| CN114252607A (zh) * | 2020-09-24 | 2022-03-29 | 首都医科大学附属北京世纪坛医院 | 尿液v-atpase亚基s1及其多肽片段在过敏性疾病中的应用 |
| US20240101654A1 (en) | 2020-12-29 | 2024-03-28 | Neurimmune Ag | Human anti-tau antibodies |
| TW202300517A (zh) | 2021-03-12 | 2023-01-01 | 美商美國禮來大藥廠 | 抗類澱粉β抗體及其用途 |
| CA3216353A1 (en) * | 2021-04-08 | 2022-10-13 | Sana Biotechnology, Inc. | Cd8-specific antibody constructs and compositions thereof |
| WO2022251048A1 (en) | 2021-05-24 | 2022-12-01 | Eli Lilly And Company | Anti-amyloid beta antibodies and uses thereof |
| EP4351588A1 (en) | 2021-06-11 | 2024-04-17 | Sage Therapeutics, Inc. | Neuroactive steroid for the treatment of alzheimer's disease |
| CA3239708A1 (en) | 2021-12-03 | 2023-06-08 | Aubin MICHALON | Novel potency assay for antibody-based drugs and useful means therefor |
| CN117586388A (zh) * | 2022-08-09 | 2024-02-23 | 深圳智源生物医药有限公司 | 改进的β淀粉样蛋白寡聚体特异性结合抗体 |
| WO2024087430A1 (zh) * | 2023-02-28 | 2024-05-02 | 湖南乾康科技有限公司 | 一种用于定量检测尿液淀粉样前体蛋白片段的酶联免疫检测方法 |
| EP4704814A1 (en) | 2023-05-02 | 2026-03-11 | Sage Therapeutics, LLC | Neuroactive steroid formulations and methods of use thereof |
| WO2025064824A1 (en) | 2023-09-22 | 2025-03-27 | Biogen Ma Inc. | Methods for treating alzheimer's disease |
Family Cites Families (125)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4444887A (en) | 1979-12-10 | 1984-04-24 | Sloan-Kettering Institute | Process for making human antibody producing B-lymphocytes |
| US4716111A (en) | 1982-08-11 | 1987-12-29 | Trustees Of Boston University | Process for producing human antibodies |
| US4741900A (en) | 1982-11-16 | 1988-05-03 | Cytogen Corporation | Antibody-metal ion complexes |
| US4694778A (en) | 1984-05-04 | 1987-09-22 | Anicon, Inc. | Chemical vapor deposition wafer boat |
| AU584417B2 (en) | 1985-04-01 | 1989-05-25 | Lonza Group Ag | Transformed myeloma cell-line and a process for the expression of a gene coding for a eukaryotic polypeptide employing same |
| GB8601597D0 (en) | 1986-01-23 | 1986-02-26 | Wilson R H | Nucleotide sequences |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| ATE243754T1 (de) | 1987-05-21 | 2003-07-15 | Micromet Ag | Multifunktionelle proteine mit vorbestimmter zielsetzung |
| US5892019A (en) | 1987-07-15 | 1999-04-06 | The United States Of America, As Represented By The Department Of Health And Human Services | Production of a single-gene-encoded immunoglobulin |
| GB8717430D0 (en) | 1987-07-23 | 1987-08-26 | Celltech Ltd | Recombinant dna product |
| EP0362371A4 (en) | 1988-04-15 | 1990-10-24 | Protein Design Labs, Inc. | Il-2 receptor-specific chimeric antibodies |
| DE68921982T4 (de) | 1988-06-14 | 1996-04-25 | Cetus Oncology Corp | Kupplungsmittel und sterisch gehinderte, mit disulfid gebundene konjugate daraus. |
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5225538A (en) | 1989-02-23 | 1993-07-06 | Genentech, Inc. | Lymphocyte homing receptor/immunoglobulin fusion proteins |
| US5116964A (en) | 1989-02-23 | 1992-05-26 | Genentech, Inc. | Hybrid immunoglobulins |
| ZA902949B (en) | 1989-05-05 | 1992-02-26 | Res Dev Foundation | A novel antibody delivery system for biological response modifiers |
| US6150584A (en) | 1990-01-12 | 2000-11-21 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| JP3068180B2 (ja) | 1990-01-12 | 2000-07-24 | アブジェニックス インコーポレイテッド | 異種抗体の生成 |
| US5314995A (en) | 1990-01-22 | 1994-05-24 | Oncogen | Therapeutic interleukin-2-antibody based fusion proteins |
| ATE158615T1 (de) | 1990-03-20 | 1997-10-15 | Univ Columbia | Chimäre antikörper mit rezeptor-bindenden liganden anstelle ihrer konstanten region |
| GB9020282D0 (en) | 1990-09-17 | 1990-10-31 | Gorman Scott D | Altered antibodies and their preparation |
| DE69133036T2 (de) | 1990-11-09 | 2003-02-06 | Stephen D. Gillies | Cytokine immunokonjugate |
| IE922437A1 (en) | 1991-07-25 | 1993-01-27 | Idec Pharma Corp | Recombinant antibodies for human therapy |
| NZ255101A (en) | 1992-07-24 | 1997-08-22 | Cell Genesys Inc | A yeast artificial chromosome (yac) vector containing an hprt minigene expressible in murine stem cells and genetically modified rodent therefor |
| EP2000536A3 (en) | 1992-08-21 | 2010-06-30 | Biogen Idec MA, Inc. | Tat-derived transport polypeptides |
| US5837821A (en) | 1992-11-04 | 1998-11-17 | City Of Hope | Antibody construct |
| US5736137A (en) | 1992-11-13 | 1998-04-07 | Idec Pharmaceuticals Corporation | Therapeutic application of chimeric and radiolabeled antibodies to human B lymphocyte restricted differentiation antigen for treatment of B cell lymphoma |
| DE69332859T2 (de) | 1992-11-13 | 2003-12-18 | Idec Pharmaceuticals Corp., San Diego | Konsensus-kozak-sequenzen zur säugetier-exprimierung |
| US5876950A (en) * | 1995-01-26 | 1999-03-02 | Bristol-Myers Squibb Company | Monoclonal antibodies specific for different epitopes of human GP39 and methods for their use in diagnosis and therapy |
| US6130364A (en) | 1995-03-29 | 2000-10-10 | Abgenix, Inc. | Production of antibodies using Cre-mediated site-specific recombination |
| DE69637481T2 (de) | 1995-04-27 | 2009-04-09 | Amgen Fremont Inc. | Aus immunisierten Xenomäusen stammende menschliche Antikörper gegen IL-8 |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US5875396A (en) * | 1995-11-13 | 1999-02-23 | Wytec, Incorporated | Multichannel radio frequency transmission system to deliver wideband digital data into independent sectorized service areas |
| GB9524973D0 (en) | 1995-12-06 | 1996-02-07 | Lynxvale Ltd | Viral vectors |
| US5916771A (en) | 1996-10-11 | 1999-06-29 | Abgenix, Inc. | Production of a multimeric protein by cell fusion method |
| US6420140B1 (en) | 1996-10-11 | 2002-07-16 | Abgenix, Inc. | Production of multimeric protein by cell fusion method |
| JP4215172B2 (ja) | 1996-12-03 | 2009-01-28 | アムジェン フレモント インク. | 複数のV▲下H▼およびV▲下κ▼領域を含むヒトIg遺伝子座を有するトランスジェニック哺乳動物、ならびにそれから産生される抗体 |
| CN1175111C (zh) | 1997-03-14 | 2004-11-10 | 艾德药品公司 | 将基因整合至哺乳动物细胞特定位点的方法及所用载体 |
| US8173127B2 (en) * | 1997-04-09 | 2012-05-08 | Intellect Neurosciences, Inc. | Specific antibodies to amyloid beta peptide, pharmaceutical compositions and methods of use thereof |
| DE69839808D1 (de) | 1997-04-09 | 2008-09-11 | Intellect Neurosciences Inc | Für die termini des beta-amyloids spezifische, rekombinante antikörper, dafür kodierende dna und verfahren zu ihrer verwendung |
| US20020086847A1 (en) * | 1997-04-09 | 2002-07-04 | Mindset Biopharmaceuticals (Usa) | Recombinant antibodies specific for beta-amyloid ends, DNA encoding and methods of use thereof |
| EP0970126B1 (en) | 1997-04-14 | 2001-04-18 | Micromet AG | Novel method for the production of antihuman antigen receptors and uses thereof |
| US6235883B1 (en) | 1997-05-05 | 2001-05-22 | Abgenix, Inc. | Human monoclonal antibodies to epidermal growth factor receptor |
| AU736549B2 (en) | 1997-05-21 | 2001-08-02 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Method for the production of non-immunogenic proteins |
| US6703015B1 (en) * | 1999-09-03 | 2004-03-09 | Ramot At Tel-Aviv University Ltd. | Filamentous bacteriophage displaying an β-amyloid epitope |
| US7179892B2 (en) | 2000-12-06 | 2007-02-20 | Neuralab Limited | Humanized antibodies that recognize beta amyloid peptide |
| TWI239847B (en) * | 1997-12-02 | 2005-09-21 | Elan Pharm Inc | N-terminal fragment of Abeta peptide and an adjuvant for preventing and treating amyloidogenic disease |
| US6710226B1 (en) | 1997-12-02 | 2004-03-23 | Neuralab Limited | Transgenic mouse assay to determine the effect of Aβ antibodies and Aβ Fragments on alzheimer's disease characteristics |
| US20080050367A1 (en) * | 1998-04-07 | 2008-02-28 | Guriq Basi | Humanized antibodies that recognize beta amyloid peptide |
| US6743427B1 (en) | 1997-12-02 | 2004-06-01 | Neuralab Limited | Prevention and treatment of amyloidogenic disease |
| US6913745B1 (en) | 1997-12-02 | 2005-07-05 | Neuralab Limited | Passive immunization of Alzheimer's disease |
| US6761888B1 (en) * | 2000-05-26 | 2004-07-13 | Neuralab Limited | Passive immunization treatment of Alzheimer's disease |
| US7964192B1 (en) * | 1997-12-02 | 2011-06-21 | Janssen Alzheimer Immunotherapy | Prevention and treatment of amyloidgenic disease |
| US6750324B1 (en) * | 1997-12-02 | 2004-06-15 | Neuralab Limited | Humanized and chimeric N-terminal amyloid beta-antibodies |
| US7462605B2 (en) * | 1998-01-23 | 2008-12-09 | Celmed Oncology (Usa), Inc. | Phosphoramidate compounds and methods of use |
| WO2000011208A1 (en) | 1998-08-25 | 2000-03-02 | University Of Washington | Rapid quantitative analysis of proteins or protein function in complex mixtures |
| AU1631700A (en) | 1998-11-23 | 2000-06-13 | Idec Pharmaceuticals Corporation | Tumor antigen-specific antibody-gp39 chimeric protein constructs |
| JP2002534959A (ja) | 1998-12-08 | 2002-10-22 | バイオベーション リミテッド | 免疫原性タンパク質の改変方法 |
| US6361973B1 (en) * | 1999-03-22 | 2002-03-26 | Novozymes Biotech, Inc. | Promoters for expressing genes in a fungal cell |
| US6787637B1 (en) * | 1999-05-28 | 2004-09-07 | Neuralab Limited | N-Terminal amyloid-β antibodies |
| UA81216C2 (en) | 1999-06-01 | 2007-12-25 | Prevention and treatment of amyloid disease | |
| DE19932958C2 (de) | 1999-07-14 | 2003-08-07 | Walter Schubert | Vorrichtung zur Bindung von Molekülen, Molekülgruppen, Molekülteilen und/oder Zellen |
| ES2344189T3 (es) | 1999-09-03 | 2010-08-20 | RAMOT UNIVERSITY AUTHORITY FOR APPLIED RESEARCH & INDUSTRIAL DEVELOPMENT LTD. | Agentes, composiciones y metodos que los utilizan utiles en el tratamiento o la prevencion de la enfermedad de alzheimer. |
| US6187309B1 (en) | 1999-09-14 | 2001-02-13 | Milkaus Laboratory, Inc. | Method for treatment of symptoms of central nervous system disorders |
| US6294171B2 (en) * | 1999-09-14 | 2001-09-25 | Milkhaus Laboratory, Inc. | Methods for treating disease states comprising administration of low levels of antibodies |
| US6713058B2 (en) * | 1999-09-14 | 2004-03-30 | Milkhaus Laboratory, Inc. | Methods for alleviating symptoms associated with neuropathic conditions comprising administration of low levels of antibodies |
| US6436401B1 (en) * | 1999-09-14 | 2002-08-20 | Milkhaus Laboratory, Inc. | Methods for alleviating symptoms associated with diabetes and diabetic neuropathy comprising administration of low levels of antibodies |
| WO2002003911A2 (en) * | 2000-07-07 | 2002-01-17 | Lars Lannfelt | Prevention and treatment of alzheimer's disease |
| EP1172378A1 (en) | 2000-07-12 | 2002-01-16 | Richard Dr. Dodel | Human beta-amyloid antibody and use thereof for treatment of alzheimer's disease |
| JP4368196B2 (ja) | 2000-11-17 | 2009-11-18 | ユニバーシティー オブ ロチェスター | 真核細胞において免疫グロブリン分子を製造および同定するインビトロにおける方法 |
| US6716226B2 (en) * | 2001-06-25 | 2004-04-06 | Inscope Development, Llc | Surgical clip |
| TWI255272B (en) | 2000-12-06 | 2006-05-21 | Guriq Basi | Humanized antibodies that recognize beta amyloid peptide |
| US7700751B2 (en) * | 2000-12-06 | 2010-04-20 | Janssen Alzheimer Immunotherapy | Humanized antibodies that recognize β-amyloid peptide |
| CA2436092A1 (en) | 2001-01-29 | 2002-08-08 | Idec Pharmaceutical Corporation | Modified antibodies and methods of use |
| AU2002327164A1 (en) | 2001-01-29 | 2002-12-09 | Idec Pharmaceuticals Corporation | Engineered tetravalent antibodies and methods of use |
| US7771722B2 (en) * | 2001-08-17 | 2010-08-10 | Eli Lilly And Company | Assay method for alzheimer's disease |
| US20030157641A1 (en) | 2001-11-16 | 2003-08-21 | Idec Pharmaceuticals Corporation | Polycistronic expression of antibodies |
| US7390885B2 (en) * | 2001-11-26 | 2008-06-24 | Cell Matrix, Inc. | Humanized collagen antibodies and related methods |
| MY139983A (en) * | 2002-03-12 | 2009-11-30 | Janssen Alzheimer Immunotherap | Humanized antibodies that recognize beta amyloid peptide |
| US20110200609A1 (en) * | 2002-09-12 | 2011-08-18 | The Regents Of The University Of California | Monoclonal antibodies specific for pathological amyloid aggregates common to amyloids formed from proteins of differing sequence |
| TW200509968A (en) | 2002-11-01 | 2005-03-16 | Elan Pharm Inc | Prevention and treatment of synucleinopathic disease |
| US8506959B2 (en) | 2002-11-01 | 2013-08-13 | Neotope Biosciences Limited | Prevention and treatment of synucleinopathic and amyloidogenic disease |
| EP1571211B1 (en) * | 2002-11-22 | 2010-01-20 | Chugai Seiyaku Kabushiki Kaisha | Antibodies against lesional tissues |
| EP1597280B2 (en) | 2003-02-26 | 2016-08-24 | Institute for Research in Biomedicine | Monoclonal antibody production by ebv transformation of b cells |
| WO2004095031A1 (en) | 2003-04-24 | 2004-11-04 | Universität Zürich | Method of monitoring immunotherapy |
| TWI374893B (en) | 2003-05-30 | 2012-10-21 | Janssen Alzheimer Immunotherap | Humanized antibodies that recognize beta amyloid peptide |
| WO2005018424A2 (en) * | 2003-08-18 | 2005-03-03 | Research Foundation For Mental Hygiene, Inc. | Antibodies specific for fibrillar amyloid and a procedure to detect fibrillar amyloid deposits |
| NZ545776A (en) | 2003-08-22 | 2009-05-31 | Biogen Idec Inc | Improved antibodies having altered effector function and methods for making the same |
| KR20090005410A (ko) | 2004-02-23 | 2009-01-13 | 일라이 릴리 앤드 캄파니 | 항-Aβ 항체 |
| JPWO2005105998A1 (ja) | 2004-04-27 | 2008-07-31 | 財団法人化学及血清療法研究所 | ヒト抗アミロイドβペプチド抗体およびその抗体フラグメント |
| DE602005022871D1 (de) | 2004-06-07 | 2010-09-23 | Univ Ramot | Verfahren zur passiven immunisierung gegen eine durch amyloidaggregation gekennzeichnete krankheit oder erkrankung mit vermindertem nervenentzündungsrisiko |
| SE0401601D0 (sv) * | 2004-06-21 | 2004-06-21 | Bioarctic Neuroscience Ab | Protofibril specific antibodies and uses thereof |
| MX2007001679A (es) | 2004-08-09 | 2007-05-23 | Elan Pharm Inc | Prevencion y tratamiento de la enfermedad sinucleinopatica y amiloidogenica. |
| WO2006050041A2 (en) | 2004-10-28 | 2006-05-11 | Ramot At Tel Aviv University Ltd. | Methods for reducing or inhibiting brain inflammation or for promoting neurogenesis |
| PE20061401A1 (es) * | 2004-12-15 | 2006-12-23 | Neuralab Ltd | ANTICUERPOS Aß PARA MEJORAR LA COGNICION |
| WO2006094724A2 (en) * | 2005-03-05 | 2006-09-14 | Abbott Gmbh & Co. Kg | Screening method, process for purifying of non-diffusible a-beta oligomers, selective antibodies against said non-diffusible a-beta oligomers and a process for manufacturing of said antibodies |
| JP2006265189A (ja) | 2005-03-24 | 2006-10-05 | Kyoto Univ | βアミロイドペプチド、及びそれを用いたアルツハイマー病治療薬又は予防薬のスクリーニング方法 |
| ES2318918B1 (es) | 2005-04-01 | 2010-02-16 | Biotherapix Molecular Medicines, S.L.U. | Anticuerpos humanos con capacidad de union al peptido beta-amiloide y sus aplicaciones. |
| PE20061323A1 (es) * | 2005-04-29 | 2007-02-09 | Rinat Neuroscience Corp | Anticuerpos dirigidos contra el peptido amiloide beta y metodos que utilizan los mismos |
| US9133267B2 (en) * | 2005-11-22 | 2015-09-15 | The Trustees Of The University Of Pennsylvania | Antibody treatment of Alzheimer's and related diseases |
| CA2637472A1 (en) * | 2005-11-30 | 2007-06-07 | Abbott Laboratories | Methods of preparation of recombinant forms of human beta-amyloid protein and uses of these proteins |
| EP2289909B1 (en) * | 2005-11-30 | 2014-10-29 | AbbVie Inc. | Screening method, process for purifying of non-diffusible a-beta oligomers, selective antibodies against said non-diffusible a-beta oligomers and a process for manufacturing of said antibodies |
| KR101667623B1 (ko) * | 2005-11-30 | 2016-10-19 | 애브비 인코포레이티드 | 아밀로이드 베타 단백질에 대한 모노클로날 항체 및 이의 용도 |
| RS53291B (sr) | 2005-12-12 | 2014-08-29 | Ac Immune S.A. | Beta 1-42 specifična monoklonska antitela sa terapeutskim svojstvima |
| US8784810B2 (en) * | 2006-04-18 | 2014-07-22 | Janssen Alzheimer Immunotherapy | Treatment of amyloidogenic diseases |
| US8455626B2 (en) * | 2006-11-30 | 2013-06-04 | Abbott Laboratories | Aβ conformer selective anti-aβ globulomer monoclonal antibodies |
| CA2674140C (en) * | 2007-01-05 | 2018-05-15 | University Of Zurich | Method of providing disease-specific binding molecules and targets |
| DK3067066T3 (da) | 2007-02-23 | 2019-05-20 | Prothena Biosciences Ltd | Forebyggelse og behandling af synukleinopatisk og amyloidogenisk sygdom |
| US8003097B2 (en) * | 2007-04-18 | 2011-08-23 | Janssen Alzheimer Immunotherapy | Treatment of cerebral amyloid angiopathy |
| CN101970000A (zh) * | 2007-04-18 | 2011-02-09 | 杨森阿尔茨海默氏症免疫治疗公司 | 脑淀粉样血管病的预防和治疗 |
| EP2182983B1 (en) * | 2007-07-27 | 2014-05-21 | Janssen Alzheimer Immunotherapy | Treatment of amyloidogenic diseases with humanised anti-abeta antibodies |
| EP2185160B1 (en) * | 2007-08-31 | 2019-02-13 | Neurimmune Holding AG | Method of providing patient specific immune response in amyloidoses and protein aggregation disorders |
| WO2009033743A1 (en) | 2007-09-13 | 2009-03-19 | University Of Zurich Prorektorat Forschung | Monoclonal amyloid beta (abeta)-specific antibody and uses thereof |
| WO2009043103A1 (en) * | 2007-10-02 | 2009-04-09 | Csl Limited | Therapeutic antibody purification method and method of use |
| EP2210901A4 (en) | 2007-10-19 | 2012-04-25 | Immunas Pharma Inc | FOR THE SPECIFIC BINDING TO AN OLIGOMICALLY ABLE ANTIBODY AND ITS USE |
| GB0720912D0 (en) * | 2007-10-25 | 2007-12-05 | Univ Cardiff | Monoclonal Anitbody for APP |
| MY155144A (en) * | 2007-10-29 | 2015-09-15 | Inst Nat Sante Rech Med | NEW ANTIBODIES SPECIFIC OF THE ß-AMYLOID PEPTIDES AND THEIR USES AS DIAGNOSTIC AGENTS OR DRUGS |
| MX2010003828A (es) * | 2007-11-16 | 2010-04-27 | Univ Rockefeller | Anticuerpos especificos para la forma de protofibrillas de la proteina beta-amiloide. |
| PT2246427T (pt) * | 2008-02-08 | 2017-03-03 | Immunas Pharma Inc | Anticorpos capazes de se ligar especificamente a oligómeros beta amilóides e a sua utilização |
| JP2011527338A (ja) * | 2008-07-09 | 2011-10-27 | ユニバーシティー オブ チューリッヒ | 神経新生を促進する方法 |
| CA2742771A1 (en) * | 2008-11-13 | 2010-05-20 | Modgene, Llc | Modification of amyloid-beta load in non-brain tissue |
| EP2419447B1 (en) * | 2009-04-17 | 2017-08-23 | Immunas Pharma, Inc. | Antibodies that specifically bind to a beta oligomers and use thereof |
| DK2462161T3 (en) * | 2009-08-06 | 2017-06-06 | Immunas Pharma Inc | Antibodies specifically binding to A-beta oligomers and their use |
| EP2462162B1 (en) * | 2009-08-06 | 2016-10-12 | Immunas Pharma, Inc. | Antibodies that specifically bind to a beta oligomers and use thereof |
-
2008
- 2008-01-07 CA CA2674140A patent/CA2674140C/en active Active
- 2008-01-07 EP EP11184418.9A patent/EP2426143B1/en active Active
- 2008-01-07 BR BRPI0806328A patent/BRPI0806328B8/pt active IP Right Grant
- 2008-01-07 EP EP08700998.1A patent/EP2099826B1/en active Active
- 2008-01-07 CN CN2012100468084A patent/CN102603893A/zh active Pending
- 2008-01-07 EP EP11185486.5A patent/EP2436696B8/en active Active
- 2008-01-07 KR KR1020127000738A patent/KR20120017469A/ko not_active Ceased
- 2008-01-07 KR KR1020167021950A patent/KR101735257B1/ko active Active
- 2008-01-07 MX MX2009007136A patent/MX2009007136A/es active IP Right Grant
- 2008-01-07 ES ES08700998.1T patent/ES2439490T3/es active Active
- 2008-01-07 PL PL11184418T patent/PL2426143T3/pl unknown
- 2008-01-07 CN CN201310282725.XA patent/CN103408661B/zh active Active
- 2008-01-07 EP EP17174176.2A patent/EP3239175A1/en not_active Withdrawn
- 2008-01-07 DK DK11185486.5T patent/DK2436696T3/en active
- 2008-01-07 CN CN2008800062941A patent/CN101622275B/zh active Active
- 2008-01-07 HU HUE11185486A patent/HUE033325T2/en unknown
- 2008-01-07 ES ES11185486.5T patent/ES2635317T3/es active Active
- 2008-01-07 CA CA2764852A patent/CA2764852C/en active Active
- 2008-01-07 SI SI200831130T patent/SI2099826T1/sl unknown
- 2008-01-07 AU AU2008203703A patent/AU2008203703C1/en active Active
- 2008-01-07 PL PL11185486T patent/PL2436696T3/pl unknown
- 2008-01-07 ES ES11184418.9T patent/ES2641897T3/es active Active
- 2008-01-07 DK DK08700998.1T patent/DK2099826T3/da active
- 2008-01-07 LT LTEP11185486.5T patent/LT2436696T/lt unknown
- 2008-01-07 PT PT111854865T patent/PT2436696T/pt unknown
- 2008-01-07 DK DK11184418.9T patent/DK2426143T3/en active
- 2008-01-07 EA EA201201067A patent/EA029481B1/ru not_active IP Right Cessation
- 2008-01-07 EA EA200900954A patent/EA017611B1/ru not_active IP Right Cessation
- 2008-01-07 JP JP2009544399A patent/JP5398545B2/ja active Active
- 2008-01-07 HU HUE11184418A patent/HUE034512T2/en unknown
- 2008-01-07 KR KR1020097016340A patent/KR20090114388A/ko not_active Withdrawn
- 2008-01-07 KR KR1020167002281A patent/KR101700073B1/ko active Active
- 2008-01-07 SI SI200831845T patent/SI2436696T1/sl unknown
- 2008-01-07 PL PL08700998T patent/PL2099826T3/pl unknown
- 2008-01-07 PT PT111844189T patent/PT2426143T/pt unknown
- 2008-01-07 WO PCT/EP2008/000053 patent/WO2008081008A1/en not_active Ceased
- 2008-01-07 PT PT87009981T patent/PT2099826E/pt unknown
- 2008-01-07 US US12/522,031 patent/US8906367B2/en active Active
- 2008-01-07 EP EP17169749.3A patent/EP3239174A1/en not_active Withdrawn
- 2008-01-07 SG SG2012000758A patent/SG177954A1/en unknown
-
2017
- 2017-08-08 CY CY20171100850T patent/CY1119197T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220403011A1 (en) | Method of providing disease-specific binding molecules and targets | |
| BRPI0806328B1 (pt) | Anticorpo isolado ou fragmento de ligação ao antígeno do mesmo, seu método de preparação, composição farmacêutica, polinucleotídeo, vetor de expressão, bem como seus usos | |
| AU2013204620B2 (en) | Method of Providing Disease-Specific Binding Molecules and Targets | |
| AU2011265453B9 (en) | Method of providing disease-specific binding molecules and targets | |
| HK1167150A (en) | Method of providing disease-specific binding molecules and targets | |
| HK1167150B (en) | Method of providing disease-specific binding molecules and targets |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07E | Notice of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] |
Free format text: NOTIFICACAO DE ANUENCIA RELACIONADA COM O ART 229 DA LPI |
|
| B06T | Formal requirements before examination [chapter 6.20 patent gazette] | ||
| B06A | Notification to applicant to reply to the report for non-patentability or inadequacy of the application [chapter 6.1 patent gazette] | ||
| B06A | Notification to applicant to reply to the report for non-patentability or inadequacy of the application [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 14/07/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 07/01/2008 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |