WO2021182575A1 - 白血球濃縮分離デバイス、血液採取容器及び白血球の分離方法 - Google Patents
白血球濃縮分離デバイス、血液採取容器及び白血球の分離方法 Download PDFInfo
- Publication number
- WO2021182575A1 WO2021182575A1 PCT/JP2021/009804 JP2021009804W WO2021182575A1 WO 2021182575 A1 WO2021182575 A1 WO 2021182575A1 JP 2021009804 W JP2021009804 W JP 2021009804W WO 2021182575 A1 WO2021182575 A1 WO 2021182575A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- blood
- collection container
- blood collection
- osmotic pressure
- container body
- Prior art date
Links
- 210000004369 blood Anatomy 0.000 title claims abstract description 353
- 239000008280 blood Substances 0.000 title claims abstract description 353
- 238000000926 separation method Methods 0.000 title claims abstract description 153
- 210000000265 leukocyte Anatomy 0.000 title claims abstract description 151
- 238000000034 method Methods 0.000 title claims description 29
- 210000000601 blood cell Anatomy 0.000 claims abstract description 153
- 230000003204 osmotic effect Effects 0.000 claims abstract description 134
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 105
- 239000000243 solution Substances 0.000 claims abstract description 42
- 230000005484 gravity Effects 0.000 claims abstract description 36
- 239000002504 physiological saline solution Substances 0.000 claims abstract description 19
- 239000000203 mixture Substances 0.000 claims description 91
- 239000000463 material Substances 0.000 claims description 70
- 101710154606 Hemagglutinin Proteins 0.000 claims description 57
- 101710093908 Outer capsid protein VP4 Proteins 0.000 claims description 57
- 101710135467 Outer capsid protein sigma-1 Proteins 0.000 claims description 57
- 101710176177 Protein A56 Proteins 0.000 claims description 57
- 239000000185 hemagglutinin Substances 0.000 claims description 57
- 239000003963 antioxidant agent Substances 0.000 claims description 28
- 230000003078 antioxidant effect Effects 0.000 claims description 28
- 235000006708 antioxidants Nutrition 0.000 claims description 28
- 239000003146 anticoagulant agent Substances 0.000 claims description 27
- 229940127219 anticoagulant drug Drugs 0.000 claims description 27
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 claims description 12
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical group [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 12
- 229920001612 Hydroxyethyl starch Polymers 0.000 claims description 10
- 229940050526 hydroxyethylstarch Drugs 0.000 claims description 10
- 229920002307 Dextran Polymers 0.000 claims description 9
- 239000002202 Polyethylene glycol Substances 0.000 claims description 9
- 229920001223 polyethylene glycol Polymers 0.000 claims description 9
- 235000010323 ascorbic acid Nutrition 0.000 claims description 6
- 239000011668 ascorbic acid Substances 0.000 claims description 6
- 229960005070 ascorbic acid Drugs 0.000 claims description 6
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 5
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 claims description 5
- 239000008103 glucose Substances 0.000 claims description 5
- 239000011780 sodium chloride Substances 0.000 claims description 5
- 229910017053 inorganic salt Inorganic materials 0.000 claims description 3
- 210000003743 erythrocyte Anatomy 0.000 abstract description 51
- 238000011084 recovery Methods 0.000 abstract description 18
- 238000009530 blood pressure measurement Methods 0.000 abstract description 5
- 238000005054 agglomeration Methods 0.000 abstract 1
- 230000002776 aggregation Effects 0.000 abstract 1
- 239000000843 powder Substances 0.000 description 73
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 71
- 239000000377 silicon dioxide Substances 0.000 description 35
- 239000007788 liquid Substances 0.000 description 34
- 229920005989 resin Polymers 0.000 description 29
- 239000011347 resin Substances 0.000 description 29
- -1 polyethylene terephthalate Polymers 0.000 description 27
- 230000000694 effects Effects 0.000 description 22
- 238000005119 centrifugation Methods 0.000 description 19
- ZSWFCLXCOIISFI-UHFFFAOYSA-N cyclopentadiene Chemical compound C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 19
- 239000011259 mixed solution Substances 0.000 description 18
- 239000000178 monomer Substances 0.000 description 14
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 12
- ARCGXLSVLAOJQL-UHFFFAOYSA-N anhydrous trimellitic acid Natural products OC(=O)C1=CC=C(C(O)=O)C(C(O)=O)=C1 ARCGXLSVLAOJQL-UHFFFAOYSA-N 0.000 description 11
- 238000011109 contamination Methods 0.000 description 11
- 239000002253 acid Substances 0.000 description 8
- 150000002894 organic compounds Chemical class 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 206010018910 Haemolysis Diseases 0.000 description 7
- 125000005907 alkyl ester group Chemical group 0.000 description 7
- 210000004027 cell Anatomy 0.000 description 7
- 230000008588 hemolysis Effects 0.000 description 7
- 239000011812 mixed powder Substances 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 238000004820 blood count Methods 0.000 description 6
- CYIDZMCFTVVTJO-UHFFFAOYSA-N pyromellityc acid Natural products OC(=O)C1=CC(C(O)=O)=C(C(O)=O)C=C1C(O)=O CYIDZMCFTVVTJO-UHFFFAOYSA-N 0.000 description 6
- 230000009974 thixotropic effect Effects 0.000 description 6
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 5
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 5
- 229920005549 butyl rubber Polymers 0.000 description 5
- 229920001971 elastomer Polymers 0.000 description 5
- 229920000139 polyethylene terephthalate Polymers 0.000 description 5
- 239000005020 polyethylene terephthalate Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 239000002904 solvent Substances 0.000 description 5
- 239000004925 Acrylic resin Substances 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 229920000178 Acrylic resin Polymers 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 210000001072 colon Anatomy 0.000 description 3
- 229920001577 copolymer Polymers 0.000 description 3
- 239000011888 foil Substances 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 150000004676 glycans Chemical class 0.000 description 3
- 230000001771 impaired effect Effects 0.000 description 3
- 239000003208 petroleum Substances 0.000 description 3
- 229920001225 polyester resin Polymers 0.000 description 3
- 239000004645 polyester resin Substances 0.000 description 3
- 229920001282 polysaccharide Polymers 0.000 description 3
- 239000005017 polysaccharide Substances 0.000 description 3
- 229920005749 polyurethane resin Polymers 0.000 description 3
- 239000005060 rubber Substances 0.000 description 3
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 3
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Chemical compound C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- 229910002012 Aerosil® Inorganic materials 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 229920001283 Polyalkylene terephthalate Polymers 0.000 description 2
- 239000004721 Polyphenylene oxide Substances 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- RXKJFZQQPQGTFL-UHFFFAOYSA-N dihydroxyacetone Chemical compound OCC(=O)CO RXKJFZQQPQGTFL-UHFFFAOYSA-N 0.000 description 2
- 239000000806 elastomer Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- 239000003349 gelling agent Substances 0.000 description 2
- 238000003703 image analysis method Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 238000007561 laser diffraction method Methods 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 229920001515 polyalkylene glycol Polymers 0.000 description 2
- 229920000570 polyether Polymers 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 238000000790 scattering method Methods 0.000 description 2
- 238000007789 sealing Methods 0.000 description 2
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical compound OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 description 2
- 229920002545 silicone oil Polymers 0.000 description 2
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- LRTOHSLOFCWHRF-UHFFFAOYSA-N 1-methyl-1h-indene Chemical compound C1=CC=C2C(C)C=CC2=C1 LRTOHSLOFCWHRF-UHFFFAOYSA-N 0.000 description 1
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical compound CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 1
- 239000004808 2-ethylhexylester Substances 0.000 description 1
- JLBJTVDPSNHSKJ-UHFFFAOYSA-N 4-Methylstyrene Chemical compound CC1=CC=C(C=C)C=C1 JLBJTVDPSNHSKJ-UHFFFAOYSA-N 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- DQEFEBPAPFSJLV-UHFFFAOYSA-N Cellulose propionate Chemical compound CCC(=O)OCC1OC(OC(=O)CC)C(OC(=O)CC)C(OC(=O)CC)C1OC1C(OC(=O)CC)C(OC(=O)CC)C(OC(=O)CC)C(COC(=O)CC)O1 DQEFEBPAPFSJLV-UHFFFAOYSA-N 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 229920000209 Hexadimethrine bromide Polymers 0.000 description 1
- 229920001479 Hydroxyethyl methyl cellulose Polymers 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- NZKCUAOWWJCEEU-UHFFFAOYSA-N O.O.[K].[K].OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O Chemical compound O.O.[K].[K].OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O NZKCUAOWWJCEEU-UHFFFAOYSA-N 0.000 description 1
- 108010089814 Plant Lectins Proteins 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000004373 Pullulan Substances 0.000 description 1
- 229920001218 Pullulan Polymers 0.000 description 1
- KRADHMIOFJQKEZ-UHFFFAOYSA-N Tri-2-ethylhexyl trimellitate Chemical compound CCCCC(CC)COC(=O)C1=CC=C(C(=O)OCC(CC)CCCC)C(C(=O)OCC(CC)CCCC)=C1 KRADHMIOFJQKEZ-UHFFFAOYSA-N 0.000 description 1
- 108010059993 Vancomycin Proteins 0.000 description 1
- 235000010724 Wisteria floribunda Nutrition 0.000 description 1
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000004520 agglutination Effects 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 239000005388 borosilicate glass Substances 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 238000003320 cell separation method Methods 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 229920006218 cellulose propionate Polymers 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 229940120503 dihydroxyacetone Drugs 0.000 description 1
- FPAFDBFIGPHWGO-UHFFFAOYSA-N dioxosilane;oxomagnesium;hydrate Chemical compound O.[Mg]=O.[Mg]=O.[Mg]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O FPAFDBFIGPHWGO-UHFFFAOYSA-N 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000010528 free radical solution polymerization reaction Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 229920005555 halobutyl Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- DNIAPMSPPWPWGF-UHFFFAOYSA-N monopropylene glycol Natural products CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 1
- 125000005487 naphthalate group Chemical group 0.000 description 1
- 239000000025 natural resin Substances 0.000 description 1
- XNGIFLGASWRNHJ-UHFFFAOYSA-N o-dicarboxybenzene Natural products OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 239000003726 plant lectin Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920000233 poly(alkylene oxides) Polymers 0.000 description 1
- 229920001308 poly(aminoacid) Polymers 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920001281 polyalkylene Polymers 0.000 description 1
- 229920001707 polybutylene terephthalate Polymers 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- KCTAWXVAICEBSD-UHFFFAOYSA-N prop-2-enoyloxy prop-2-eneperoxoate Chemical compound C=CC(=O)OOOC(=O)C=C KCTAWXVAICEBSD-UHFFFAOYSA-N 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 235000019423 pullulan Nutrition 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000005368 silicate glass Substances 0.000 description 1
- 229920002050 silicone resin Polymers 0.000 description 1
- 239000005361 soda-lime glass Substances 0.000 description 1
- PPASLZSBLFJQEF-RKJRWTFHSA-M sodium ascorbate Substances [Na+].OC[C@@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RKJRWTFHSA-M 0.000 description 1
- 235000010378 sodium ascorbate Nutrition 0.000 description 1
- 229960005055 sodium ascorbate Drugs 0.000 description 1
- PPASLZSBLFJQEF-RXSVEWSESA-M sodium-L-ascorbate Chemical compound [Na+].OC[C@H](O)[C@H]1OC(=O)C(O)=C1[O-] PPASLZSBLFJQEF-RXSVEWSESA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- KKEYFWRCBNTPAC-UHFFFAOYSA-L terephthalate(2-) Chemical compound [O-]C(=O)C1=CC=C(C([O-])=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-L 0.000 description 1
- 229920002725 thermoplastic elastomer Polymers 0.000 description 1
- 229920005992 thermoplastic resin Polymers 0.000 description 1
- 229920006337 unsaturated polyester resin Polymers 0.000 description 1
- 229960003165 vancomycin Drugs 0.000 description 1
- MYPYJXKWCTUITO-UHFFFAOYSA-N vancomycin Natural products O1C(C(=C2)Cl)=CC=C2C(O)C(C(NC(C2=CC(O)=CC(O)=C2C=2C(O)=CC=C3C=2)C(O)=O)=O)NC(=O)C3NC(=O)C2NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(CC(C)C)NC)C(O)C(C=C3Cl)=CC=C3OC3=CC2=CC1=C3OC1OC(CO)C(O)C(O)C1OC1CC(C)(N)C(O)C(C)O1 MYPYJXKWCTUITO-UHFFFAOYSA-N 0.000 description 1
- MYPYJXKWCTUITO-LYRMYLQWSA-O vancomycin(1+) Chemical compound O([C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=C2C=C3C=C1OC1=CC=C(C=C1Cl)[C@@H](O)[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@H]3C(=O)N[C@H]1C(=O)N[C@H](C(N[C@@H](C3=CC(O)=CC(O)=C3C=3C(O)=CC=C1C=3)C([O-])=O)=O)[C@H](O)C1=CC=C(C(=C1)Cl)O2)=O)NC(=O)[C@@H](CC(C)C)[NH2+]C)[C@H]1C[C@](C)([NH3+])[C@H](O)[C@H](C)O1 MYPYJXKWCTUITO-LYRMYLQWSA-O 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/49—Blood
- G01N33/491—Blood by separating the blood components
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5021—Test tubes specially adapted for centrifugation purposes
- B01L3/50215—Test tubes specially adapted for centrifugation purposes using a float to separate phases
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0631—Purification arrangements, e.g. solid phase extraction [SPE]
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/16—Reagents, handling or storing thereof
Abstract
Description
上記白血球濃縮分離デバイスは、上記容器本体内に収容された血球分離材を備える。上記血液採取容器は、上記血液採取容器本体内に収容された血球分離材を備える。上記血球分離材の25℃での比重は、1.075以上1.093以下である。上記血球分離材としては、血球分離用組成物、及び血球分離用冶具等が挙げられる。血球分離材の作製が容易であることから、上記血球分離材は、上記血球分離用組成物であることが好ましい。
上記血球分離用組成物は、遠心分離時に白血球と赤血球との間に移動して隔壁を形成する組成物である。また、上記血球分離用組成物は、遠心分離後に白血球層に赤血球が混入することを防止する目的で用いられる。上記血球分離用組成物は、チクソトロピー性を有することが好ましく、チクソトロピー性を有するゲル状組成物であることがより好ましい。上記白血球濃縮分離デバイスにおいて、上記血球分離用組成物は、上記容器本体の底部に収容されていてもよく、内壁面上に配置されていてもよい。本発明の効果をより一層効果的に発揮する観点から、上記血球分離用組成物は、上記容器本体の底部に収容されていることが好ましい。上記血液採取容器において、上記血球分離用組成物は、上記血液採取容器本体の底部に収容されていてもよく、内壁面上に配置されていてもよい。本発明の効果をより一層効果的に発揮する観点から、上記血球分離用組成物は、上記血液採取容器本体の底部に収容されていることが好ましい。
上記「25℃で流動性を有する」とは、25℃での粘度が500Pa・s以下であることを意味する。
上記無機微粉末としては、微粉末シリカ、酸化チタン粉末、酸化亜鉛粉末、炭酸カルシウム粉末、アルミナ粉末、ガラス微粉末、タルク粉末、カオリン粉末、ベントナイト粉末、チタニア粉末、及びジルコニウム粉末等が挙げられる。
上記血球分離用組成物は、本発明の効果を損なわない限り、上述した成分以外の他の成分を含んでいてもよい。上記血球分離用組成物は、例えば、上記他の成分として、有機ゲル化剤、熱可塑性エラストマー、ポリアルキレングリコール、シリコーンオイル、補助溶媒、酸化防止剤、着色剤及び水等を含んでいてもよい。上記他の成分はそれぞれ、1種のみが用いられてもよく、2種以上が併用されてもよい。
上記血球分離用組成物の25℃での比重は、1.075以上1.093以下である。上記血球分離用組成物の25℃での比重は、好ましくは1.077以上、より好ましくは1.082以上、好ましくは1.090以下、より好ましくは1.088以下である。上記比重が上記下限以上及び上記上限以下であると、白血球の回収率がより一層高く、赤血球の混入量がより一層少ない検体を良好に得ることができる。
上記血球分離用冶具は、遠心分離時に白血球と赤血球との間に移動して隔壁を形成する冶具である。また、上記血球分離用冶具は、遠心分離後に白血球層に赤血球が混入することを防止する目的で用いられる。
上記構成A1を備える白血球濃縮分離デバイスは、上記容器本体内に収容された赤血球凝集剤を備える。上記構成A2を備える血液採取容器は、上記血液採取容器本体内に収容された赤血球凝集剤を備える。上記赤血球凝集剤として、従来公知の赤血球凝集剤を用いることができる。上記赤血球凝集剤は、1種のみが用いられてもよく、2種以上が併用されてもよい。
上記構成B1を備える白血球濃縮分離デバイスは、上記容器本体内に収容された浸透圧調整剤を備える。上記構成B2を備える血液採取容器は、上記血液採取容器本体内に収容された浸透圧調整剤を備える。上記浸透圧調整剤として、従来公知の浸透圧調整剤を用いることができる。上記浸透圧調整剤は、1種のみが用いられてもよく、2種以上が併用されてもよい。
上記白血球濃縮分離デバイスは、上記容器本体内に収容された抗凝固剤を備えることが好ましい。上記血液採取容器は、上記血液採取容器本体内に収容された抗凝固剤を備えることが好ましい。上記抗凝固剤として、従来公知の抗凝固剤を用いることができる。上記抗凝固剤は、1種のみが用いられてもよく、2種以上が併用されてもよい。
上記白血球濃縮分離デバイスは、上記容器本体内に収容された酸化防止剤を備えることが好ましい。上記血液採取容器は、上記血液採取容器本体内に収容された酸化防止剤を備えることが好ましい。上記酸化防止剤を備えることにより、上記白血球濃縮分離デバイス及び上記血液採取容器を放射線滅菌する際の変性を効果的に抑えることができる。上記酸化防止剤として、従来公知の酸化防止剤を用いることができる。上記酸化防止剤は、1種のみが用いられてもよく、2種以上が併用されてもよい。
上記容器本体及び上記血液採取容器本体の形状としては、特に限定されないが、有底の管状容器であることが好ましい。
上記白血球濃縮分離デバイス及び上記血液採取容器は、栓体を備えることが好ましい。上記栓体として、従来公知の栓体を用いることができる。上記栓体は、容器本体の開口又は血液採取容器本体の開口に、気密的かつ液密的に取付けることが可能な素材、形状からなる栓体であることが好ましい。上記栓体は、採血針が刺通され得るように構成されていることが好ましい。
上記血液採取容器は、採血管であることが好ましい。上記血液採取容器本体は、採血管本体であることが好ましい。
本発明に係る白血球の分離方法は、上述した血液採取容器を用いた白血球の分離方法であって、上記血液採取容器内に血液を採取する工程と、上記血液が採取された上記血液採取容器を遠心分離する工程とを備える。上記白血球の分離方法は、血液から白血球を分離する方法である。上記白血球の分離方法は、血液から白血球を濃縮分離する方法である。
本発明に係る白血球濃縮分離システムは、所定量の血液由来試料が採取され、上記血液由来試料中に存在する白血球を濃縮分離するための白血球濃縮分離システムであって、25℃での比重が1.075以上1.093以下である血球分離材を備え、以下の構成A3、又は、構成B3を備える。
(メタ)アクリル系樹脂:
アクリル酸-2-エチルヘキシルとアクリル酸ブチルとをアゾ系重合開始剤の存在下で溶液重合法によりラジカル重合させ、25℃で流動性を有する(メタ)アクリル酸エステル系樹脂を得た。
石油樹脂(イーストマンケミカル社製「リガライトS5090」)
ジシクロペンタジエン樹脂1(コロン社製「スコレッツSU500」)
ジシクロペンタジエン樹脂2(コロン社製「スコレッツSU90」)
トリメリット酸エステル(ベンゼンポリカルボン酸アルキルエステル誘導体、DIC社製「モノサイザーW700」)
親水性シリカ(微粉末シリカ、日本アエロジル社製「200CF」)
疎水性シリカ(微粉末シリカ、日本アエロジル社製「R974」)
酸化チタン粉末(石原産業社製「A-100」)
シリコーンオイル(東レダウコーニング社製「SF8410」)
有機ゲル化剤(新日本理化社製「ゲルオールD」)
1-メチル-2-ピロリドン(補助溶媒)
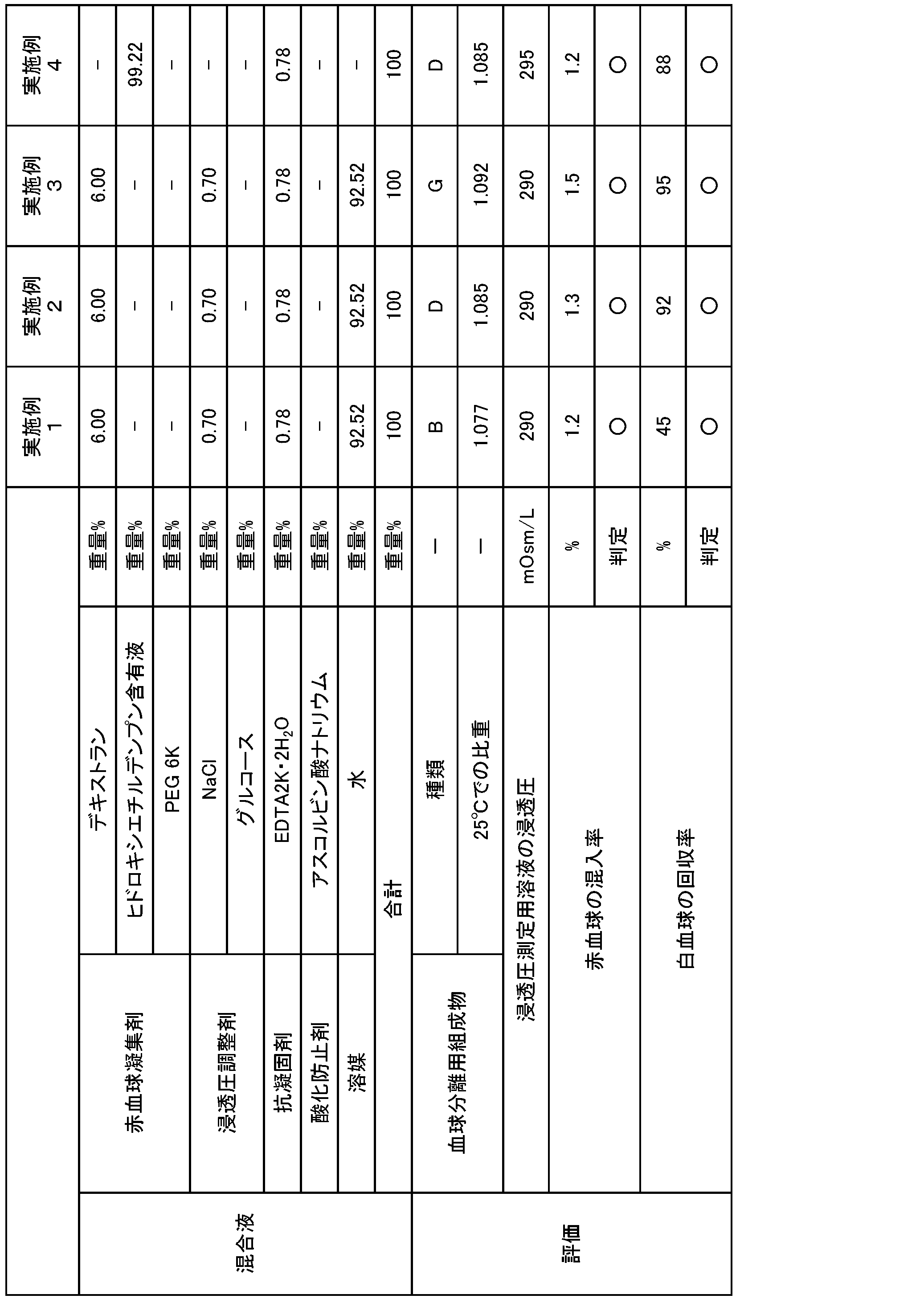
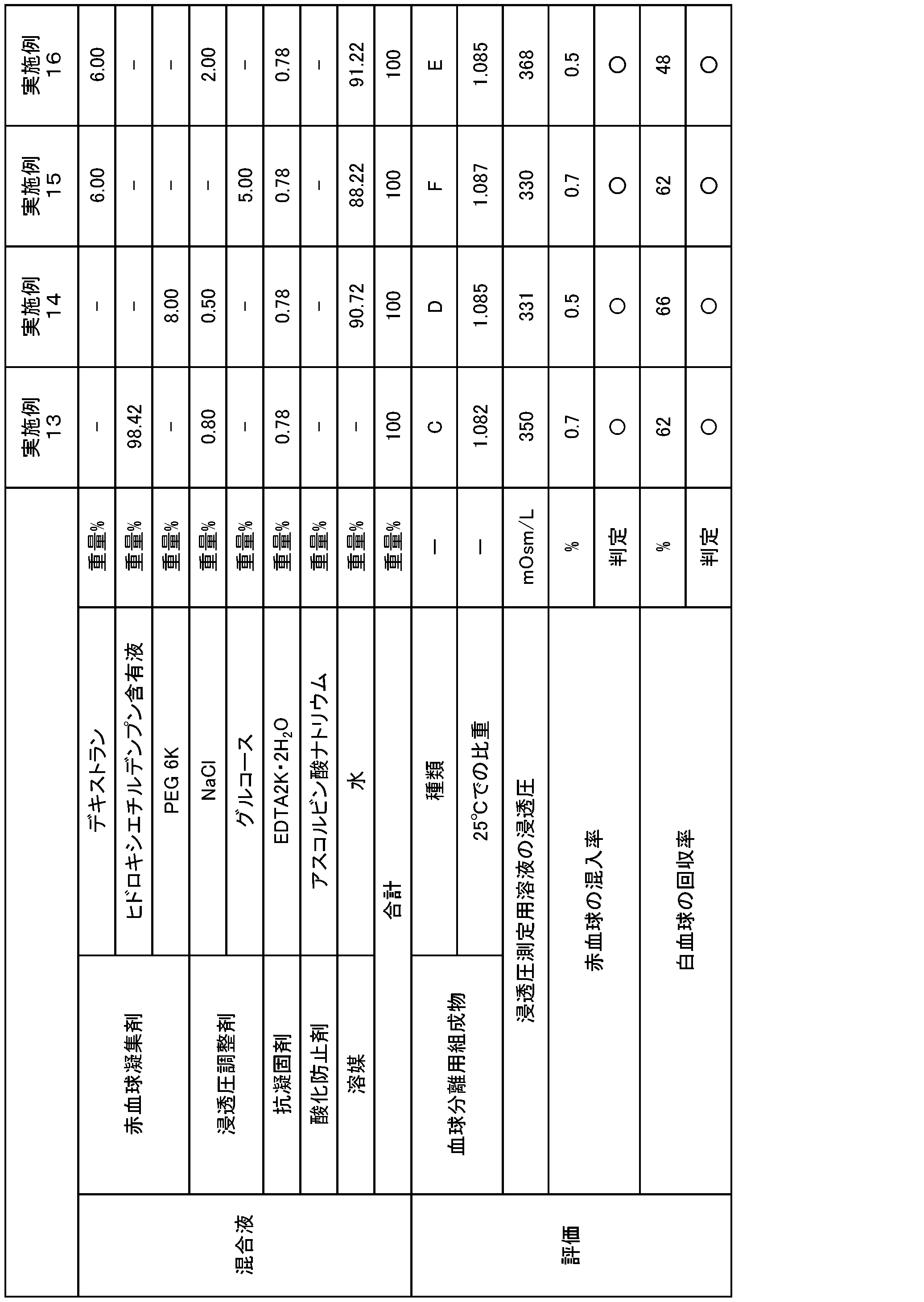
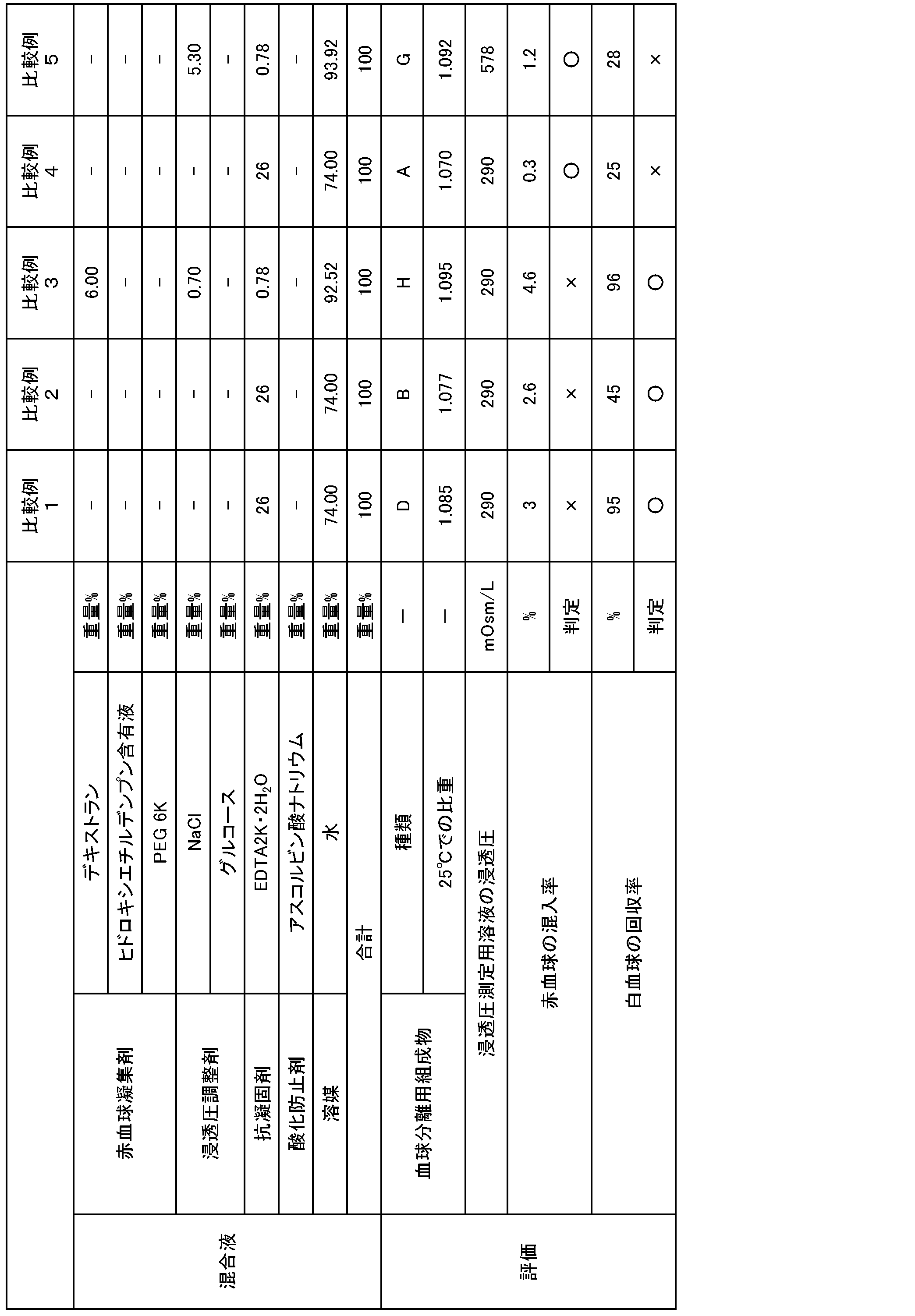
表1,2に記載の配合割合で、25℃で流動性を有する有機成分と無機微粉末とその他の成分とを混合し、チクソトロピー性を有する血球分離用組成物A~Hを作製した。
デキストラン(重量平均分子量200000)
ヒドロキシエチルデンプン含有液(ニプロ社製「HES40」、重量平均分子量約40万のヒドロキシエチルデンプンを6w/v%の濃度で含有する水溶液)
ポリエチレングリコール(PEG 6K、富士フィルム和光純薬社製)
塩化ナトリウム
グルコース
エチレンジアミン四酢酸二カリウム塩二水和物(EDTA2K・2H2O)
アスコルビン酸ナトリウム
赤血球凝集剤、浸透圧調整剤、及び抗凝固剤を、水に溶解して、混合液を得た。得られた混合液の配合成分の種類及び配合量を表3に示す。なお、得られた混合液の浸透圧は血液と等張に調整されている。
血球分離用組成物の種類、並びに赤血球凝集剤、抗凝固剤、酸化防止剤及び浸透圧調整剤の配合量を表3~7のように変更したこと以外は、実施例1と同様にして、血液採取容器を作製した。なお、表中、ヒドロキシエチルデンプン含有液の配合量は、ヒドロキシエチルデンプンの含有量ではなく、ヒドロキシエチルデンプン含有液(市販品)の配合量で示した。また、得られた混合液の浸透圧は、血液と等張、もしくは高張に調整されている。
抗凝固剤を、水に溶解して、混合液を得た。
血球分離用組成物の種類を表7のように変更したこと以外は、比較例1と同様にして、血液採取容器を作製した。
(1)血球分離用組成物の25℃での比重
得られた血球分離用組成物1滴を、比重を0.002の間隔で段階的に調整した25℃の食塩水中に順次滴下し、食塩水中における浮沈により比重を測定した。
得られた血液採取容器に生理食塩水4mLを添加した。添加後、転倒混和して、生理食塩水で水溶性成分を溶解し、浸透圧測定用溶液を得た。得られた浸透圧測定用溶液の浸透圧を、浸透圧計(アークレイ社製「OM-6060」)を用いて、氷点降下法により測定した。
3名の血液を用意し、以下の工程を順に行った。
得られた血液採取容器の上記血液採取容器本体内に血液4mLを採取した。
血液採取容器を1500Gで15分間遠心分離した。
○:赤血球の混入率が2%以下
×:赤血球の混入率が2%を超える
○:白血球の回収率が40%以上
×:白血球の回収率が40%未満
2…血液採取容器本体
2a…内壁面
3…血球分離用組成物
4…混合液
4A…混合粉末
5…栓体
Claims (17)
- 所定量の血液由来試料が添加され、前記血液由来試料中に存在する白血球を濃縮分離するための白血球濃縮分離デバイスであって、
容器本体と、
前記容器本体内に収容された血球分離材とを備え、
前記血球分離材の25℃での比重が1.075以上1.093以下であり、
以下の構成A1、又は、構成B1を備える、白血球濃縮分離デバイス。
構成A1:前記容器本体内に収容された赤血球凝集剤を備える。
構成B1:前記容器本体内に収容された浸透圧調整剤を備え、前記白血球濃縮分離デバイスに添加される血液由来試料の所定量と等量の生理食塩水で、前記容器本体内に収容された水溶性成分を溶解して、浸透圧測定用溶液を得たときに、前記浸透圧測定用溶液の浸透圧が300mOsm/L以上500mOsm/L以下である。 - 所定量の血液が採取される血液採取容器であって、
血液採取容器本体と、
前記血液採取容器本体内に収容された血球分離材とを備え、
前記血球分離材の25℃での比重が1.075以上1.093以下であり、
以下の構成A2、又は、構成B2を備える、血液採取容器。
構成A2:前記血液採取容器本体内に収容された赤血球凝集剤を備える。
構成B2:前記血液採取容器本体内に収容された浸透圧調整剤を備え、前記血液採取容器に採取される血液の所定量と等量の生理食塩水で、前記血液採取容器本体内に収容された水溶性成分を溶解して、浸透圧測定用溶液を得たときに、前記浸透圧測定用溶液の浸透圧が300mOsm/L以上500mOsm/L以下である。 - 前記血球分離材が、チクソトロピー性を有する血球分離用組成物である、請求項2に記載の血液採取容器。
- 前記構成A2を備える、請求項2又は3に記載の血液採取容器。
- 前記赤血球凝集剤が、デキストラン、ヒドロキシエチルデンプン又はポリエチレングリコールである、請求項4に記載の血液採取容器。
- 前記デキストランの重量平均分子量が、50000以上である、請求項5に記載の血液採取容器。
- 前記構成B2を備える、請求項2又は3に記載の血液採取容器。
- 前記浸透圧測定用溶液の浸透圧が320mOsm/L以上360mOsm/L以下である、請求項7に記載の血液採取容器。
- 前記血球分離材の25℃での比重が1.082以上1.090以下であり、
前記浸透圧測定用溶液の浸透圧が320mOsm/L以上360mOsm/L以下である、請求項7又は8に記載の血液採取容器。 - 前記浸透圧調整剤が、塩化ナトリウム、又はグルコースである、請求項7~9のいずれか1項に記載の血液採取容器。
- 前記構成A2と前記構成B2とを備える、請求項2~10のいずれか1項に記載の血液採取容器。
- 前記血液採取容器本体内に収容された抗凝固剤を備える、請求項2~11のいずれか1項に記載の血液採取容器。
- 前記血液採取容器本体内に収容された酸化防止剤を備える、請求項2~12のいずれか1項に記載の血液採取容器。
- 前記酸化防止剤が、アスコルビン酸、又はアスコルビン酸の無機塩である、請求項13に記載の血液採取容器。
- 請求項1に記載の白血球濃縮分離デバイスを用いた白血球の分離方法であって、
前記白血球濃縮分離デバイスに血液由来試料を添加する工程と、
前記血液由来試料が添加された前記白血球濃縮分離デバイスを遠心分離する工程とを備える、白血球の分離方法。 - 請求項2~14のいずれか1項に記載の血液採取容器を用いた白血球の分離方法であって、
前記血液採取容器内に血液を採取する工程と、
前記血液が採取された前記血液採取容器を遠心分離する工程とを備える、白血球の分離方法。 - 所定量の血液由来試料が採取され、前記血液由来試料中に存在する白血球を濃縮分離するための白血球濃縮分離システムであって、
25℃での比重が1.075以上1.093以下である血球分離材を備え、
以下の構成A3、又は、構成B3を備える、白血球濃縮分離システム。
構成A3:赤血球凝集剤を備える。
構成B3:浸透圧調整剤を備え、前記血液由来試料の所定量と等量の生理食塩水で、前記血液由来試料と混合される水溶性成分を溶解して、浸透圧測定用溶液を得たときに、前記浸透圧測定用溶液の浸透圧が300mOsm/L以上500mOsm/L以下である。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202180020430.8A CN115280145A (zh) | 2020-03-11 | 2021-03-11 | 白细胞浓缩分离设备、血液采集容器和白细胞的分离方法 |
| KR1020227024973A KR20220151158A (ko) | 2020-03-11 | 2021-03-11 | 백혈구 농축 분리 디바이스, 혈액 채취 용기 및 백혈구의 분리 방법 |
| JP2022507279A JPWO2021182575A1 (ja) | 2020-03-11 | 2021-03-11 | |
| CA3170079A CA3170079A1 (en) | 2020-03-11 | 2021-03-11 | Leukocyte concentration separation device, blood collection container, and method for separating leukocytes |
| EP21767156.9A EP4119943A4 (en) | 2020-03-11 | 2021-03-11 | LEUKOCYTE CONCENTRATION SEPARATION DEVICE, BLOOD COLLECTION CONTAINER AND LEUKOCYTE SEPARATION METHOD |
| US17/908,407 US20230090675A1 (en) | 2020-03-11 | 2021-03-11 | Leukocyte concentration separation device, blood collection container, and method for separating leukocytes |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020-042080 | 2020-03-11 | ||
| JP2020042080 | 2020-03-11 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021182575A1 true WO2021182575A1 (ja) | 2021-09-16 |
Family
ID=77671614
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/009804 WO2021182575A1 (ja) | 2020-03-11 | 2021-03-11 | 白血球濃縮分離デバイス、血液採取容器及び白血球の分離方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20230090675A1 (ja) |
| EP (1) | EP4119943A4 (ja) |
| JP (1) | JPWO2021182575A1 (ja) |
| KR (1) | KR20220151158A (ja) |
| CN (1) | CN115280145A (ja) |
| CA (1) | CA3170079A1 (ja) |
| WO (1) | WO2021182575A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023181468A1 (ja) * | 2022-03-25 | 2023-09-28 | 積水メディカル株式会社 | 循環腫瘍細胞分離キット、循環腫瘍細胞分離容器及び循環腫瘍細胞の分離方法 |
| WO2024070504A1 (ja) * | 2022-09-29 | 2024-04-04 | 積水メディカル株式会社 | 血液保存用組成物及び血液採取容器 |
Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS54238Y2 (ja) * | 1973-02-12 | 1979-01-08 | ||
| JPS5737259A (en) * | 1980-08-14 | 1982-03-01 | Sherwood Medical Ind Inc | Covering of stopper for anticoagulation |
| JPS5754860A (en) * | 1980-09-17 | 1982-04-01 | Fuerante Antonio | Blood density separation |
| JPS5854130B2 (ja) * | 1978-03-17 | 1983-12-02 | 旭化成株式会社 | 白血球分離法 |
| JPS603367B2 (ja) * | 1979-10-09 | 1985-01-28 | 旭化成株式会社 | 白血球分離法および白血球分離材 |
| JPS6184557A (ja) | 1984-09-24 | 1986-04-30 | ベクトン・デイツキンソン・アンド・カンパニー | 血液分離方法 |
| JPH0442627B2 (ja) * | 1983-02-18 | 1992-07-14 | Technicon Instr | |
| JPH08510322A (ja) * | 1993-04-26 | 1996-10-29 | インターナショナル リモート イメージング システムズ,インコーポレーテッド | ヒト全血から白血球細胞を濃縮するための組成物及び方法 |
| JPH102898A (ja) * | 1996-03-12 | 1998-01-06 | Johnson & Johnson Clinical Diagnostics Inc | 白血球の選択的調製方法及びポリメラーゼ連鎖反応用キット |
| JPH10160731A (ja) * | 1996-11-22 | 1998-06-19 | Stephen C Wardlaw | 赤血球層と顆粒球層間の明確な界面形成方法 |
| JP2004003920A (ja) * | 2002-03-26 | 2004-01-08 | Kawasumi Lab Inc | 血液成分の分離方法及び血液成分の分離装置 |
| WO2010132783A1 (en) | 2009-05-15 | 2010-11-18 | Becton, Dickinson And Company | Density phase separation device |
| US20130045852A1 (en) * | 2011-08-19 | 2013-02-21 | John R. Chapman | Centrifuge separation method and apparatus using a medium density fluid |
| WO2013168767A1 (ja) * | 2012-05-10 | 2013-11-14 | コニカミノルタ株式会社 | 赤血球除去方法および採血用遠沈管 |
| JP2017102114A (ja) * | 2015-12-01 | 2017-06-08 | ゼネラル・エレクトリック・カンパニイ | 赤血球凝集および白血球単離 |
| JP2017129429A (ja) * | 2016-01-19 | 2017-07-27 | 稲田 捷也 | 多白血球血漿の調整方法 |
| JP2017523385A (ja) * | 2014-04-16 | 2017-08-17 | ゼネラル・エレクトリック・カンパニイ | ガンマ線照射安定化デキストラン溶液及び使用方法 |
| JP2018059791A (ja) * | 2016-10-05 | 2018-04-12 | デンカ生研株式会社 | 赤血球の凝集方法及び分離方法並びに赤血球凝集用試薬 |
| US20180120295A1 (en) * | 2015-05-01 | 2018-05-03 | Mesotex, Inc. | Process for separating nucleated cells from non-nucleated red blood cells |
| US20180195938A1 (en) * | 2015-06-16 | 2018-07-12 | Tascom Co., Ltd. | Biological material measuring instrument |
| US20190162716A1 (en) * | 2017-11-28 | 2019-05-30 | Canon Virginia, Inc. | Methods and devices for separation of blood components |
| WO2019131613A1 (ja) | 2017-12-27 | 2019-07-04 | 積水メディカル株式会社 | 血清または血漿分離用組成物、血液採取容器、及び血清または血漿の分離方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4640785A (en) * | 1984-12-24 | 1987-02-03 | Becton Dickinson And Company | Separation of lymphocytes and monocytes from blood samples |
| US7927810B2 (en) * | 2002-11-19 | 2011-04-19 | Katsuya Togawa | Plasma or serum separation membrane and filter apparatus including the plasma or serum separation membrane |
-
2021
- 2021-03-11 CA CA3170079A patent/CA3170079A1/en active Pending
- 2021-03-11 KR KR1020227024973A patent/KR20220151158A/ko active Search and Examination
- 2021-03-11 CN CN202180020430.8A patent/CN115280145A/zh active Pending
- 2021-03-11 JP JP2022507279A patent/JPWO2021182575A1/ja active Pending
- 2021-03-11 EP EP21767156.9A patent/EP4119943A4/en active Pending
- 2021-03-11 US US17/908,407 patent/US20230090675A1/en active Pending
- 2021-03-11 WO PCT/JP2021/009804 patent/WO2021182575A1/ja unknown
Patent Citations (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS54238Y2 (ja) * | 1973-02-12 | 1979-01-08 | ||
| JPS5854130B2 (ja) * | 1978-03-17 | 1983-12-02 | 旭化成株式会社 | 白血球分離法 |
| JPS603367B2 (ja) * | 1979-10-09 | 1985-01-28 | 旭化成株式会社 | 白血球分離法および白血球分離材 |
| JPS5737259A (en) * | 1980-08-14 | 1982-03-01 | Sherwood Medical Ind Inc | Covering of stopper for anticoagulation |
| JPS5754860A (en) * | 1980-09-17 | 1982-04-01 | Fuerante Antonio | Blood density separation |
| JPH0442627B2 (ja) * | 1983-02-18 | 1992-07-14 | Technicon Instr | |
| JPS6184557A (ja) | 1984-09-24 | 1986-04-30 | ベクトン・デイツキンソン・アンド・カンパニー | 血液分離方法 |
| JPH0465981B2 (ja) * | 1984-09-24 | 1992-10-21 | Becton Dickinson Co | |
| JPH08510322A (ja) * | 1993-04-26 | 1996-10-29 | インターナショナル リモート イメージング システムズ,インコーポレーテッド | ヒト全血から白血球細胞を濃縮するための組成物及び方法 |
| JPH102898A (ja) * | 1996-03-12 | 1998-01-06 | Johnson & Johnson Clinical Diagnostics Inc | 白血球の選択的調製方法及びポリメラーゼ連鎖反応用キット |
| JPH10160731A (ja) * | 1996-11-22 | 1998-06-19 | Stephen C Wardlaw | 赤血球層と顆粒球層間の明確な界面形成方法 |
| JP2004003920A (ja) * | 2002-03-26 | 2004-01-08 | Kawasumi Lab Inc | 血液成分の分離方法及び血液成分の分離装置 |
| WO2010132783A1 (en) | 2009-05-15 | 2010-11-18 | Becton, Dickinson And Company | Density phase separation device |
| US20130045852A1 (en) * | 2011-08-19 | 2013-02-21 | John R. Chapman | Centrifuge separation method and apparatus using a medium density fluid |
| WO2013168767A1 (ja) * | 2012-05-10 | 2013-11-14 | コニカミノルタ株式会社 | 赤血球除去方法および採血用遠沈管 |
| JP2017523385A (ja) * | 2014-04-16 | 2017-08-17 | ゼネラル・エレクトリック・カンパニイ | ガンマ線照射安定化デキストラン溶液及び使用方法 |
| US20180120295A1 (en) * | 2015-05-01 | 2018-05-03 | Mesotex, Inc. | Process for separating nucleated cells from non-nucleated red blood cells |
| US20180195938A1 (en) * | 2015-06-16 | 2018-07-12 | Tascom Co., Ltd. | Biological material measuring instrument |
| JP2017102114A (ja) * | 2015-12-01 | 2017-06-08 | ゼネラル・エレクトリック・カンパニイ | 赤血球凝集および白血球単離 |
| JP2017129429A (ja) * | 2016-01-19 | 2017-07-27 | 稲田 捷也 | 多白血球血漿の調整方法 |
| JP2018059791A (ja) * | 2016-10-05 | 2018-04-12 | デンカ生研株式会社 | 赤血球の凝集方法及び分離方法並びに赤血球凝集用試薬 |
| US20190162716A1 (en) * | 2017-11-28 | 2019-05-30 | Canon Virginia, Inc. | Methods and devices for separation of blood components |
| WO2019131613A1 (ja) | 2017-12-27 | 2019-07-04 | 積水メディカル株式会社 | 血清または血漿分離用組成物、血液採取容器、及び血清または血漿の分離方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP4119943A4 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023181468A1 (ja) * | 2022-03-25 | 2023-09-28 | 積水メディカル株式会社 | 循環腫瘍細胞分離キット、循環腫瘍細胞分離容器及び循環腫瘍細胞の分離方法 |
| JP7355473B1 (ja) | 2022-03-25 | 2023-10-03 | 積水メディカル株式会社 | 循環腫瘍細胞分離キット、循環腫瘍細胞分離容器及び循環腫瘍細胞の分離方法 |
| WO2024070504A1 (ja) * | 2022-09-29 | 2024-04-04 | 積水メディカル株式会社 | 血液保存用組成物及び血液採取容器 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20230090675A1 (en) | 2023-03-23 |
| EP4119943A4 (en) | 2024-04-10 |
| CA3170079A1 (en) | 2021-09-16 |
| CN115280145A (zh) | 2022-11-01 |
| KR20220151158A (ko) | 2022-11-14 |
| EP4119943A1 (en) | 2023-01-18 |
| JPWO2021182575A1 (ja) | 2021-09-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6901194B1 (ja) | 血液採取容器及び血漿の分離方法 | |
| CA1178257A (en) | Apparatus for separating blood | |
| WO2021182575A1 (ja) | 白血球濃縮分離デバイス、血液採取容器及び白血球の分離方法 | |
| JP6535050B2 (ja) | 循環腫瘍細胞濃縮分離デバイス及び循環腫瘍細胞の濃縮分離方法 | |
| CN110753843B (zh) | 血清或血浆分离用组合物、血液采取容器以及血清或血浆的分离方法 | |
| JP2023110819A (ja) | 血液採取容器、血漿の分離方法、細胞外遊離核酸の分離方法及び細胞外小胞の分離方法 | |
| JP7355473B1 (ja) | 循環腫瘍細胞分離キット、循環腫瘍細胞分離容器及び循環腫瘍細胞の分離方法 | |
| JP6809747B1 (ja) | 単核球含有血漿分離用組成物及び血液採取容器 | |
| WO2023145137A1 (ja) | 血液採取容器、血漿の分離方法、細胞外遊離核酸の分離方法及び細胞外小胞の分離方法 | |
| WO2022250142A1 (ja) | 血液採取容器、血漿の分離方法、細胞外遊離核酸の分離方法及び細胞外小胞の分離方法 | |
| JP3420855B2 (ja) | 血液検査用容器及び担体 | |
| JP7309108B2 (ja) | 血液分離用組成物、血液採取容器及び白血球の分離方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21767156 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2022507279 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 3170079 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2021767156 Country of ref document: EP Effective date: 20221011 |