WO2020004316A1 - リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 - Google Patents
リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 Download PDFInfo
- Publication number
- WO2020004316A1 WO2020004316A1 PCT/JP2019/024930 JP2019024930W WO2020004316A1 WO 2020004316 A1 WO2020004316 A1 WO 2020004316A1 JP 2019024930 W JP2019024930 W JP 2019024930W WO 2020004316 A1 WO2020004316 A1 WO 2020004316A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- lithography
- film
- mass
- forming material
- film forming
- Prior art date
Links
- 238000001459 lithography Methods 0.000 title claims abstract description 356
- 239000000463 material Substances 0.000 title claims abstract description 267
- 238000000034 method Methods 0.000 title claims abstract description 89
- 239000000203 mixture Substances 0.000 title claims description 168
- 150000001875 compounds Chemical class 0.000 claims abstract description 137
- 238000005530 etching Methods 0.000 claims abstract description 60
- 239000000758 substrate Substances 0.000 claims abstract description 57
- 229920002120 photoresistant polymer Polymers 0.000 claims abstract description 25
- LLHKCFNBLRBOGN-UHFFFAOYSA-N propylene glycol methyl ether acetate Chemical compound COCC(C)OC(C)=O LLHKCFNBLRBOGN-UHFFFAOYSA-N 0.000 claims description 102
- 150000003949 imides Chemical class 0.000 claims description 99
- 239000002904 solvent Substances 0.000 claims description 81
- -1 isocyanate compounds Chemical class 0.000 claims description 61
- 229920005989 resin Polymers 0.000 claims description 60
- 239000011347 resin Substances 0.000 claims description 60
- 230000015572 biosynthetic process Effects 0.000 claims description 59
- ZLPORNPZJNRGCO-UHFFFAOYSA-N 3-methylpyrrole-2,5-dione Chemical compound CC1=CC(=O)NC1=O ZLPORNPZJNRGCO-UHFFFAOYSA-N 0.000 claims description 41
- 125000004432 carbon atom Chemical group C* 0.000 claims description 40
- 239000007864 aqueous solution Substances 0.000 claims description 37
- 125000005842 heteroatom Chemical group 0.000 claims description 35
- 238000004132 cross linking Methods 0.000 claims description 34
- 239000003431 cross linking reagent Substances 0.000 claims description 28
- 238000012644 addition polymerization Methods 0.000 claims description 27
- 125000000217 alkyl group Chemical group 0.000 claims description 24
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 claims description 23
- 239000002253 acid Substances 0.000 claims description 23
- 229910052710 silicon Inorganic materials 0.000 claims description 23
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 20
- 238000000605 extraction Methods 0.000 claims description 19
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 claims description 18
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 18
- 239000010703 silicon Substances 0.000 claims description 18
- 230000002378 acidificating effect Effects 0.000 claims description 15
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 15
- 229910052760 oxygen Inorganic materials 0.000 claims description 15
- 239000001301 oxygen Substances 0.000 claims description 15
- 239000012074 organic phase Substances 0.000 claims description 13
- 239000007870 radical polymerization initiator Substances 0.000 claims description 13
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 12
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 12
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 11
- 229910052731 fluorine Inorganic materials 0.000 claims description 11
- 239000011737 fluorine Substances 0.000 claims description 11
- 239000003505 polymerization initiator Substances 0.000 claims description 11
- 238000000746 purification Methods 0.000 claims description 11
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 claims description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims description 9
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 claims description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 9
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 9
- 238000011161 development Methods 0.000 claims description 8
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 8
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 claims description 7
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 claims description 6
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 claims description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 6
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 claims description 6
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 claims description 6
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 claims description 6
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 claims description 6
- CATSNJVOTSVZJV-UHFFFAOYSA-N heptan-2-one Chemical compound CCCCCC(C)=O CATSNJVOTSVZJV-UHFFFAOYSA-N 0.000 claims description 6
- 229910052500 inorganic mineral Inorganic materials 0.000 claims description 6
- 230000001678 irradiating effect Effects 0.000 claims description 6
- 239000011707 mineral Substances 0.000 claims description 6
- 150000007524 organic acids Chemical class 0.000 claims description 6
- 235000006408 oxalic acid Nutrition 0.000 claims description 6
- 230000005855 radiation Effects 0.000 claims description 6
- 239000011975 tartaric acid Substances 0.000 claims description 6
- 235000002906 tartaric acid Nutrition 0.000 claims description 6
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims description 6
- 239000004593 Epoxy Chemical class 0.000 claims description 5
- 150000001412 amines Chemical class 0.000 claims description 5
- 150000001913 cyanates Chemical class 0.000 claims description 5
- 150000002460 imidazoles Chemical class 0.000 claims description 5
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 4
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 4
- 235000011054 acetic acid Nutrition 0.000 claims description 4
- 239000012535 impurity Substances 0.000 claims description 4
- 229940098779 methanesulfonic acid Drugs 0.000 claims description 4
- 229910017604 nitric acid Inorganic materials 0.000 claims description 4
- 150000003003 phosphines Chemical class 0.000 claims description 4
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 4
- WHOZNOZYMBRCBL-OUKQBFOZSA-N (2E)-2-Tetradecenal Chemical compound CCCCCCCCCCC\C=C\C=O WHOZNOZYMBRCBL-OUKQBFOZSA-N 0.000 claims description 3
- VZXTWGWHSMCWGA-UHFFFAOYSA-N 1,3,5-triazine-2,4-diamine Chemical class NC1=NC=NC(N)=N1 VZXTWGWHSMCWGA-UHFFFAOYSA-N 0.000 claims description 3
- 239000002841 Lewis acid Substances 0.000 claims description 3
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 claims description 3
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 claims description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 claims description 3
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 3
- 150000005130 benzoxazines Chemical class 0.000 claims description 3
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 claims description 3
- 239000001530 fumaric acid Substances 0.000 claims description 3
- 239000003999 initiator Substances 0.000 claims description 3
- 239000012948 isocyanate Substances 0.000 claims description 3
- 150000007517 lewis acids Chemical class 0.000 claims description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 claims description 3
- 239000011976 maleic acid Substances 0.000 claims description 3
- 150000007974 melamines Chemical class 0.000 claims description 3
- 229940044654 phenolsulfonic acid Drugs 0.000 claims description 3
- 235000019260 propionic acid Nutrition 0.000 claims description 3
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 claims description 3
- 150000003672 ureas Chemical class 0.000 claims description 3
- 150000002576 ketones Chemical class 0.000 claims description 2
- 150000001451 organic peroxides Chemical class 0.000 claims description 2
- 150000002989 phenols Chemical class 0.000 claims description 2
- 125000001183 hydrocarbyl group Chemical group 0.000 claims 2
- 125000001046 glycoluril group Chemical class [H]C12N(*)C(=O)N(*)C1([H])N(*)C(=O)N2* 0.000 claims 1
- 238000011156 evaluation Methods 0.000 description 126
- 239000010410 layer Substances 0.000 description 122
- 238000002411 thermogravimetry Methods 0.000 description 45
- 239000000243 solution Substances 0.000 description 33
- 238000006243 chemical reaction Methods 0.000 description 30
- 229910052757 nitrogen Inorganic materials 0.000 description 28
- 239000007789 gas Substances 0.000 description 24
- 239000003960 organic solvent Substances 0.000 description 24
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 23
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 18
- 239000000126 substance Substances 0.000 description 18
- 238000003786 synthesis reaction Methods 0.000 description 14
- URLKBWYHVLBVBO-UHFFFAOYSA-N Para-Xylene Chemical group CC1=CC=C(C)C=C1 URLKBWYHVLBVBO-UHFFFAOYSA-N 0.000 description 12
- 230000007547 defect Effects 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 11
- 150000002430 hydrocarbons Chemical group 0.000 description 11
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Natural products OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 10
- 229910004298 SiO 2 Inorganic materials 0.000 description 10
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 238000012545 processing Methods 0.000 description 9
- 238000005160 1H NMR spectroscopy Methods 0.000 description 8
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 8
- 239000008346 aqueous phase Substances 0.000 description 8
- 238000000576 coating method Methods 0.000 description 8
- 229910052751 metal Inorganic materials 0.000 description 8
- 239000002184 metal Substances 0.000 description 8
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 8
- 238000002156 mixing Methods 0.000 description 8
- 229920003986 novolac Polymers 0.000 description 8
- 229920000642 polymer Polymers 0.000 description 8
- 239000002994 raw material Substances 0.000 description 8
- 229910052717 sulfur Inorganic materials 0.000 description 8
- 239000011593 sulfur Substances 0.000 description 8
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 7
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 7
- 150000007514 bases Chemical class 0.000 description 7
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 7
- 229910052794 bromium Inorganic materials 0.000 description 7
- 238000005229 chemical vapour deposition Methods 0.000 description 7
- 239000000460 chlorine Substances 0.000 description 7
- 229910052801 chlorine Inorganic materials 0.000 description 7
- 238000010438 heat treatment Methods 0.000 description 7
- 238000004528 spin coating Methods 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- CMLFRMDBDNHMRA-UHFFFAOYSA-N 2h-1,2-benzoxazine Chemical compound C1=CC=C2C=CNOC2=C1 CMLFRMDBDNHMRA-UHFFFAOYSA-N 0.000 description 6
- 125000003118 aryl group Chemical group 0.000 description 6
- 238000001723 curing Methods 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- KJIFKLIQANRMOU-UHFFFAOYSA-N oxidanium;4-methylbenzenesulfonate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1 KJIFKLIQANRMOU-UHFFFAOYSA-N 0.000 description 6
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 5
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 5
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 5
- XLJMAIOERFSOGZ-UHFFFAOYSA-M cyanate group Chemical group [O-]C#N XLJMAIOERFSOGZ-UHFFFAOYSA-M 0.000 description 5
- 229910001882 dioxygen Inorganic materials 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 229910052740 iodine Inorganic materials 0.000 description 5
- 239000011630 iodine Substances 0.000 description 5
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 5
- 230000003287 optical effect Effects 0.000 description 5
- 239000004065 semiconductor Substances 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 229910052814 silicon oxide Inorganic materials 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 238000003860 storage Methods 0.000 description 5
- QNODIIQQMGDSEF-UHFFFAOYSA-N (1-hydroxycyclohexyl)-phenylmethanone Chemical compound C=1C=CC=CC=1C(=O)C1(O)CCCCC1 QNODIIQQMGDSEF-UHFFFAOYSA-N 0.000 description 4
- SDDBCEWUYXVGCQ-UHFFFAOYSA-N 1,5-dimethylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1C SDDBCEWUYXVGCQ-UHFFFAOYSA-N 0.000 description 4
- RNIPJYFZGXJSDD-UHFFFAOYSA-N 2,4,5-triphenyl-1h-imidazole Chemical compound C1=CC=CC=C1C1=NC(C=2C=CC=CC=2)=C(C=2C=CC=CC=2)N1 RNIPJYFZGXJSDD-UHFFFAOYSA-N 0.000 description 4
- AYKYXWQEBUNJCN-UHFFFAOYSA-N 3-methylfuran-2,5-dione Chemical compound CC1=CC(=O)OC1=O AYKYXWQEBUNJCN-UHFFFAOYSA-N 0.000 description 4
- WOCGGVRGNIEDSZ-UHFFFAOYSA-N 4-[2-(4-hydroxy-3-prop-2-enylphenyl)propan-2-yl]-2-prop-2-enylphenol Chemical compound C=1C=C(O)C(CC=C)=CC=1C(C)(C)C1=CC=C(O)C(CC=C)=C1 WOCGGVRGNIEDSZ-UHFFFAOYSA-N 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N DMSO Substances CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 229910002091 carbon monoxide Inorganic materials 0.000 description 4
- 238000001312 dry etching Methods 0.000 description 4
- 239000003822 epoxy resin Substances 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 229920000647 polyepoxide Polymers 0.000 description 4
- 229920000734 polysilsesquioxane polymer Polymers 0.000 description 4
- 238000007650 screen-printing Methods 0.000 description 4
- 239000002356 single layer Substances 0.000 description 4
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 4
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 3
- KCKAGGPNSPNAOR-UHFFFAOYSA-N 2,3-dimethylnaphthalene-1-carbaldehyde Chemical compound C1=CC=C2C(C=O)=C(C)C(C)=CC2=C1 KCKAGGPNSPNAOR-UHFFFAOYSA-N 0.000 description 3
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 3
- YBRVSVVVWCFQMG-UHFFFAOYSA-N 4,4'-diaminodiphenylmethane Chemical compound C1=CC(N)=CC=C1CC1=CC=C(N)C=C1 YBRVSVVVWCFQMG-UHFFFAOYSA-N 0.000 description 3
- YXHKONLOYHBTNS-UHFFFAOYSA-N Diazomethane Chemical compound C=[N+]=[N-] YXHKONLOYHBTNS-UHFFFAOYSA-N 0.000 description 3
- 229910052581 Si3N4 Inorganic materials 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- KYKAJFCTULSVSH-UHFFFAOYSA-N chloro(fluoro)methane Chemical compound F[C]Cl KYKAJFCTULSVSH-UHFFFAOYSA-N 0.000 description 3
- 235000015165 citric acid Nutrition 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical group C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 3
- 239000012153 distilled water Substances 0.000 description 3
- 238000010894 electron beam technology Methods 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 238000005227 gel permeation chromatography Methods 0.000 description 3
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- HQVNEWCFYHHQES-UHFFFAOYSA-N silicon nitride Chemical compound N12[Si]34N5[Si]62N3[Si]51N64 HQVNEWCFYHHQES-UHFFFAOYSA-N 0.000 description 3
- 239000002002 slurry Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- MDEDKSYUWOWMHU-UHFFFAOYSA-N 1-[2-ethyl-4-[[3-ethyl-5-methyl-4-(3-methyl-2,5-dioxopyrrol-1-yl)phenyl]methyl]-6-methylphenyl]-3-methylpyrrole-2,5-dione Chemical compound C(C)C=1C=C(C=C(C=1N1C(C(C)=CC1=O)=O)C)CC1=CC(=C(C(=C1)C)N1C(C(C)=CC1=O)=O)CC MDEDKSYUWOWMHU-UHFFFAOYSA-N 0.000 description 2
- BTFWJAUZPQUVNZ-UHFFFAOYSA-N 1-methyl-3-[(3-methylphenyl)methyl]benzene Chemical compound CC1=CC=CC(CC=2C=C(C)C=CC=2)=C1 BTFWJAUZPQUVNZ-UHFFFAOYSA-N 0.000 description 2
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical compound C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 2
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 229910004541 SiN Inorganic materials 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000010908 decantation Methods 0.000 description 2
- 230000006866 deterioration Effects 0.000 description 2
- 125000003700 epoxy group Chemical group 0.000 description 2
- LZCLXQDLBQLTDK-UHFFFAOYSA-N ethyl 2-hydroxypropanoate Chemical compound CCOC(=O)C(C)O LZCLXQDLBQLTDK-UHFFFAOYSA-N 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- VPVSTMAPERLKKM-UHFFFAOYSA-N glycoluril Chemical class N1C(=O)NC2NC(=O)NC21 VPVSTMAPERLKKM-UHFFFAOYSA-N 0.000 description 2
- 125000005462 imide group Chemical group 0.000 description 2
- 239000011261 inert gas Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 229920003192 poly(bis maleimide) Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 238000010526 radical polymerization reaction Methods 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 230000004580 weight loss Effects 0.000 description 2
- WZKZYRSMAQLVTF-UHFFFAOYSA-N (2-butylphenyl)-phenyliodanium Chemical group C(CCC)C1=C(C=CC=C1)[I+]C1=CC=CC=C1 WZKZYRSMAQLVTF-UHFFFAOYSA-N 0.000 description 1
- FDYDISGSYGFRJM-UHFFFAOYSA-N (2-methyl-2-adamantyl) 2-methylprop-2-enoate Chemical compound C1C(C2)CC3CC1C(OC(=O)C(=C)C)(C)C2C3 FDYDISGSYGFRJM-UHFFFAOYSA-N 0.000 description 1
- QSUJHKWXLIQKEY-UHFFFAOYSA-N (2-oxooxolan-3-yl) 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC1CCOC1=O QSUJHKWXLIQKEY-UHFFFAOYSA-N 0.000 description 1
- OOIBFPKQHULHSQ-UHFFFAOYSA-N (3-hydroxy-1-adamantyl) 2-methylprop-2-enoate Chemical compound C1C(C2)CC3CC2(O)CC1(OC(=O)C(=C)C)C3 OOIBFPKQHULHSQ-UHFFFAOYSA-N 0.000 description 1
- LJHFIVQEAFAURQ-ZPUQHVIOSA-N (NE)-N-[(2E)-2-hydroxyiminoethylidene]hydroxylamine Chemical class O\N=C\C=N\O LJHFIVQEAFAURQ-ZPUQHVIOSA-N 0.000 description 1
- WNQSKPOIYILBMI-UHFFFAOYSA-N 1-[butylsulfonyl(diazo)methyl]sulfonylbutane Chemical compound CCCCS(=O)(=O)C(=[N+]=[N-])S(=O)(=O)CCCC WNQSKPOIYILBMI-UHFFFAOYSA-N 0.000 description 1
- GLYOFBNLYMTEPS-UHFFFAOYSA-N 1-[diazo(2-methylpropylsulfonyl)methyl]sulfonyl-2-methylpropane Chemical compound CC(C)CS(=O)(=O)C(=[N+]=[N-])S(=O)(=O)CC(C)C GLYOFBNLYMTEPS-UHFFFAOYSA-N 0.000 description 1
- WUYAQJZXAJBVFT-UHFFFAOYSA-N 1-[diazo(propylsulfonyl)methyl]sulfonylpropane Chemical compound CCCS(=O)(=O)C(=[N+]=[N-])S(=O)(=O)CCC WUYAQJZXAJBVFT-UHFFFAOYSA-N 0.000 description 1
- GYQQFWWMZYBCIB-UHFFFAOYSA-N 1-[diazo-(4-methylphenyl)sulfonylmethyl]sulfonyl-4-methylbenzene Chemical compound C1=CC(C)=CC=C1S(=O)(=O)C(=[N+]=[N-])S(=O)(=O)C1=CC=C(C)C=C1 GYQQFWWMZYBCIB-UHFFFAOYSA-N 0.000 description 1
- FFKFRQVYUILJCW-UHFFFAOYSA-N 1-hydroxypyrrolidine-2,5-dione;methanesulfonic acid Chemical compound CS(O)(=O)=O.ON1C(=O)CCC1=O FFKFRQVYUILJCW-UHFFFAOYSA-N 0.000 description 1
- XAJXGUBHPFWEIH-UHFFFAOYSA-N 1-hydroxypyrrolidine-2,5-dione;pentane-1-sulfonic acid Chemical compound ON1C(=O)CCC1=O.CCCCCS(O)(=O)=O XAJXGUBHPFWEIH-UHFFFAOYSA-N 0.000 description 1
- QPAWHGVDCJWYRJ-UHFFFAOYSA-N 1-hydroxypyrrolidine-2,5-dione;trifluoromethanesulfonic acid Chemical compound ON1C(=O)CCC1=O.OS(=O)(=O)C(F)(F)F QPAWHGVDCJWYRJ-UHFFFAOYSA-N 0.000 description 1
- SQAINHDHICKHLX-UHFFFAOYSA-N 1-naphthaldehyde Chemical compound C1=CC=C2C(C=O)=CC=CC2=C1 SQAINHDHICKHLX-UHFFFAOYSA-N 0.000 description 1
- AFTPEBDOGXRMNQ-UHFFFAOYSA-N 2,2,4-Trimethylhexane Chemical compound CCC(C)CC(C)(C)C AFTPEBDOGXRMNQ-UHFFFAOYSA-N 0.000 description 1
- KJXSTIJHXKFZKV-UHFFFAOYSA-N 2-(cyclohexylmethylsulfanyl)cyclohexan-1-one;trifluoromethanesulfonic acid Chemical compound [O-]S(=O)(=O)C(F)(F)F.O=C1CCCCC1[SH+]CC1CCCCC1 KJXSTIJHXKFZKV-UHFFFAOYSA-N 0.000 description 1
- PXXUHFVEJQHLSK-UHFFFAOYSA-N 2-[[2-aminoethyl(dimethyl)silyl]oxy-dimethylsilyl]ethanamine Chemical compound NCC[Si](C)(C)O[Si](C)(C)CCN PXXUHFVEJQHLSK-UHFFFAOYSA-N 0.000 description 1
- ZTJDHPJOEXLRHO-UHFFFAOYSA-N 2-[[2-aminoethyl(diphenoxy)silyl]oxy-diphenoxysilyl]ethanamine Chemical compound C=1C=CC=CC=1O[Si](O[Si](CCN)(OC=1C=CC=CC=1)OC=1C=CC=CC=1)(CCN)OC1=CC=CC=C1 ZTJDHPJOEXLRHO-UHFFFAOYSA-N 0.000 description 1
- IQMVIUWWZGWTLG-UHFFFAOYSA-N 2-[[2-aminoethyl(diphenyl)silyl]oxy-diphenylsilyl]ethanamine Chemical compound C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(CCN)O[Si](CCN)(C=1C=CC=CC=1)C1=CC=CC=C1 IQMVIUWWZGWTLG-UHFFFAOYSA-N 0.000 description 1
- DRYBUHKBBRHEAE-UHFFFAOYSA-N 2-[diazo(propan-2-ylsulfonyl)methyl]sulfonylpropane Chemical compound CC(C)S(=O)(=O)C(=[N+]=[N-])S(=O)(=O)C(C)C DRYBUHKBBRHEAE-UHFFFAOYSA-N 0.000 description 1
- SAFWZKVQMVOANB-UHFFFAOYSA-N 2-[tert-butylsulfonyl(diazo)methyl]sulfonyl-2-methylpropane Chemical compound CC(C)(C)S(=O)(=O)C(=[N+]=[N-])S(=O)(=O)C(C)(C)C SAFWZKVQMVOANB-UHFFFAOYSA-N 0.000 description 1
- QIRNGVVZBINFMX-UHFFFAOYSA-N 2-allylphenol Chemical compound OC1=CC=CC=C1CC=C QIRNGVVZBINFMX-UHFFFAOYSA-N 0.000 description 1
- QFABNUVNDKOIEH-UHFFFAOYSA-N 2-methylsulfanylcyclohexan-1-one Chemical compound CSC1CCCCC1=O QFABNUVNDKOIEH-UHFFFAOYSA-N 0.000 description 1
- WHGXZPQWZJUGEP-UHFFFAOYSA-N 2-prop-1-enylphenol Chemical compound CC=CC1=CC=CC=C1O WHGXZPQWZJUGEP-UHFFFAOYSA-N 0.000 description 1
- WMIVYXHTTYBDLD-UHFFFAOYSA-N 3-[[3-[(2,5-dioxopyrrol-3-yl)methyl]-4-methylphenyl]methyl]pyrrole-2,5-dione Chemical compound CC1=C(C=C(C=C1)CC=1C(=O)NC(C=1)=O)CC=1C(=O)NC(C=1)=O WMIVYXHTTYBDLD-UHFFFAOYSA-N 0.000 description 1
- RVFQOYLBPXHFKR-UHFFFAOYSA-N 3-[[3-[(2,5-dioxopyrrol-3-yl)methyl]phenyl]methyl]pyrrole-2,5-dione Chemical compound O=C1NC(=O)C(CC=2C=C(CC=3C(NC(=O)C=3)=O)C=CC=2)=C1 RVFQOYLBPXHFKR-UHFFFAOYSA-N 0.000 description 1
- GPXCORHXFPYJEH-UHFFFAOYSA-N 3-[[3-aminopropyl(dimethyl)silyl]oxy-dimethylsilyl]propan-1-amine Chemical compound NCCC[Si](C)(C)O[Si](C)(C)CCCN GPXCORHXFPYJEH-UHFFFAOYSA-N 0.000 description 1
- XRAAFZNZEZFTCV-UHFFFAOYSA-N 3-[[3-aminopropyl(diphenyl)silyl]oxy-diphenylsilyl]propan-1-amine Chemical compound C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(CCCN)O[Si](CCCN)(C=1C=CC=CC=1)C1=CC=CC=C1 XRAAFZNZEZFTCV-UHFFFAOYSA-N 0.000 description 1
- AAOTXAXPBHMDLB-UHFFFAOYSA-N 3-[[[3-aminopropyl(diethyl)silyl]oxy-diethylsilyl]oxy-diethylsilyl]propan-1-amine Chemical compound NCCC[Si](CC)(CC)O[Si](CC)(CC)O[Si](CC)(CC)CCCN AAOTXAXPBHMDLB-UHFFFAOYSA-N 0.000 description 1
- ZWRBLCDTKAWRHT-UHFFFAOYSA-N 3-[[[3-aminopropyl(dimethyl)silyl]oxy-dimethylsilyl]oxy-dimethylsilyl]propan-1-amine Chemical compound NCCC[Si](C)(C)O[Si](C)(C)O[Si](C)(C)CCCN ZWRBLCDTKAWRHT-UHFFFAOYSA-N 0.000 description 1
- JKWTWAKSRCPWLP-UHFFFAOYSA-N 3-[[[3-aminopropyl(diphenyl)silyl]oxy-dimethylsilyl]oxy-diphenylsilyl]propan-1-amine Chemical compound C=1C=CC=CC=1[Si](CCCN)(C=1C=CC=CC=1)O[Si](C)(C)O[Si](CCCN)(C=1C=CC=CC=1)C1=CC=CC=C1 JKWTWAKSRCPWLP-UHFFFAOYSA-N 0.000 description 1
- UDNAFHBSEWJPEB-UHFFFAOYSA-N 3-methyl-1-[3-[3-[3-(3-methyl-2,5-dioxopyrrol-1-yl)phenoxy]phenoxy]phenyl]pyrrole-2,5-dione Chemical compound CC1=CC(=O)N(C1=O)C1=CC(OC2=CC=CC(OC3=CC(=CC=C3)N3C(=O)C=C(C)C3=O)=C2)=CC=C1 UDNAFHBSEWJPEB-UHFFFAOYSA-N 0.000 description 1
- XJUPXVIODOCNGA-UHFFFAOYSA-N 3-methyl-1-[3-[4-[3-(3-methyl-2,5-dioxopyrrol-1-yl)phenoxy]phenoxy]phenyl]pyrrole-2,5-dione Chemical compound CC1=CC(=O)N(C1=O)C2=CC(=CC=C2)OC3=CC=C(C=C3)OC4=CC=CC(=C4)N5C(=O)C=C(C5=O)C XJUPXVIODOCNGA-UHFFFAOYSA-N 0.000 description 1
- ZRFGTTGUHYTSSV-UHFFFAOYSA-N 3-methyl-1-[4-[3-[4-(3-methyl-2,5-dioxopyrrol-1-yl)phenoxy]phenoxy]phenyl]pyrrole-2,5-dione Chemical compound CC1=CC(=O)N(C1=O)C2=CC=C(C=C2)OC3=CC(=CC=C3)OC4=CC=C(C=C4)N5C(=O)C=C(C5=O)C ZRFGTTGUHYTSSV-UHFFFAOYSA-N 0.000 description 1
- IJSMGUHRHSUAQM-UHFFFAOYSA-N 3-methyl-1-[4-[4-[4-(3-methyl-2,5-dioxopyrrol-1-yl)phenoxy]phenoxy]phenyl]pyrrole-2,5-dione Chemical compound CC1=CC(=O)N(C1=O)C2=CC=C(C=C2)OC3=CC=C(C=C3)OC4=CC=C(C=C4)N5C(=O)C=C(C5=O)C IJSMGUHRHSUAQM-UHFFFAOYSA-N 0.000 description 1
- ZZMBONADFMYLJG-UHFFFAOYSA-N 3-silyloxysilyloxysilylpropan-1-amine Chemical compound NCCC[SiH2]O[SiH2]O[SiH3] ZZMBONADFMYLJG-UHFFFAOYSA-N 0.000 description 1
- QEQVCPKISCKMOQ-UHFFFAOYSA-N 3h-benzo[f][1,2]benzoxazine Chemical compound C1=CC=CC2=C(C=CNO3)C3=CC=C21 QEQVCPKISCKMOQ-UHFFFAOYSA-N 0.000 description 1
- MTMKZABGIQJAEX-UHFFFAOYSA-N 4,4'-sulfonylbis[2-(prop-2-en-1-yl)phenol] Chemical compound C1=C(CC=C)C(O)=CC=C1S(=O)(=O)C1=CC=C(O)C(CC=C)=C1 MTMKZABGIQJAEX-UHFFFAOYSA-N 0.000 description 1
- QJENIOQDYXRGLF-UHFFFAOYSA-N 4-[(4-amino-3-ethyl-5-methylphenyl)methyl]-2-ethyl-6-methylaniline Chemical compound CC1=C(N)C(CC)=CC(CC=2C=C(CC)C(N)=C(C)C=2)=C1 QJENIOQDYXRGLF-UHFFFAOYSA-N 0.000 description 1
- IDLYVPNAAUXRPW-UHFFFAOYSA-N 4-[(4-aminobutyl-methoxy-methylsilyl)oxy-methoxy-methylsilyl]butan-1-amine Chemical compound NCCCC[Si](C)(OC)O[Si](C)(CCCCN)OC IDLYVPNAAUXRPW-UHFFFAOYSA-N 0.000 description 1
- IYTXQZMZTQHONB-UHFFFAOYSA-N 4-[(4-aminophenoxy)-dimethylsilyl]oxyaniline Chemical compound C=1C=C(N)C=CC=1O[Si](C)(C)OC1=CC=C(N)C=C1 IYTXQZMZTQHONB-UHFFFAOYSA-N 0.000 description 1
- DVJCVFJDBHWFNC-UHFFFAOYSA-N 4-[[(4-aminophenoxy)-dimethylsilyl]oxy-dimethylsilyl]oxyaniline Chemical compound C=1C=C(N)C=CC=1O[Si](C)(C)O[Si](C)(C)OC1=CC=C(N)C=C1 DVJCVFJDBHWFNC-UHFFFAOYSA-N 0.000 description 1
- ILCGTNBULCHWOE-UHFFFAOYSA-N 4-[[4-aminobutyl(dimethyl)silyl]oxy-dimethylsilyl]butan-1-amine Chemical compound NCCCC[Si](C)(C)O[Si](C)(C)CCCCN ILCGTNBULCHWOE-UHFFFAOYSA-N 0.000 description 1
- RAXMFFZNRKLKLH-UHFFFAOYSA-M 4-methylbenzenesulfonate;[4-[(2-methylpropan-2-yl)oxy]phenyl]-phenyliodanium Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.C1=CC(OC(C)(C)C)=CC=C1[I+]C1=CC=CC=C1 RAXMFFZNRKLKLH-UHFFFAOYSA-M 0.000 description 1
- YXZXRYDYTRYFAF-UHFFFAOYSA-M 4-methylbenzenesulfonate;triphenylsulfanium Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 YXZXRYDYTRYFAF-UHFFFAOYSA-M 0.000 description 1
- MJGQMEJOQAULGB-UHFFFAOYSA-M 4-methylbenzenesulfonate;tris[4-[(2-methylpropan-2-yl)oxy]phenyl]sulfanium Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.C1=CC(OC(C)(C)C)=CC=C1[S+](C=1C=CC(OC(C)(C)C)=CC=1)C1=CC=C(OC(C)(C)C)C=C1 MJGQMEJOQAULGB-UHFFFAOYSA-M 0.000 description 1
- ZEYFKFIBCCPTAM-UHFFFAOYSA-N 4-silyloxysilylaniline Chemical compound NC1=CC=C(C=C1)[SiH2]O[SiH3] ZEYFKFIBCCPTAM-UHFFFAOYSA-N 0.000 description 1
- 229910018125 Al-Si Inorganic materials 0.000 description 1
- 102100033806 Alpha-protein kinase 3 Human genes 0.000 description 1
- 101710082399 Alpha-protein kinase 3 Proteins 0.000 description 1
- 229910018520 Al—Si Inorganic materials 0.000 description 1
- 0 CC(C(N1*N(C(C=C2C)=O)C2=O)=O)=CC1=O Chemical compound CC(C(N1*N(C(C=C2C)=O)C2=O)=O)=CC1=O 0.000 description 1
- UNOCKGDBXCJFAN-UHFFFAOYSA-N CO[SiH](CCCCN)O[SiH](OC)O[SiH2]CCCCN Chemical compound CO[SiH](CCCCN)O[SiH](OC)O[SiH2]CCCCN UNOCKGDBXCJFAN-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 102100028829 Heat shock 70 kDa protein 4L Human genes 0.000 description 1
- 101001078634 Homo sapiens Heat shock 70 kDa protein 4L Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 229920000877 Melamine resin Polymers 0.000 description 1
- XYVQFUJDGOBPQI-UHFFFAOYSA-N Methyl-2-hydoxyisobutyric acid Chemical compound COC(=O)C(C)(C)O XYVQFUJDGOBPQI-UHFFFAOYSA-N 0.000 description 1
- GHBBMBXBLDQHCB-UHFFFAOYSA-N NC1=CC=C(C=C1)[SiH2]O[SiH2]O[SiH3] Chemical compound NC1=CC=C(C=C1)[SiH2]O[SiH2]O[SiH3] GHBBMBXBLDQHCB-UHFFFAOYSA-N 0.000 description 1
- 101100380548 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) apg-2 gene Proteins 0.000 description 1
- XQUPVDVFXZDTLT-UHFFFAOYSA-N O=C(C=CC1=O)N1c1ccc(Cc(cc2)ccc2N(C(C=C2)=O)C2=O)cc1 Chemical compound O=C(C=CC1=O)N1c1ccc(Cc(cc2)ccc2N(C(C=C2)=O)C2=O)cc1 XQUPVDVFXZDTLT-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 229910008938 W—Si Inorganic materials 0.000 description 1
- HKKMPPDCCCBZHM-UHFFFAOYSA-M [4-[(2-methylpropan-2-yl)oxy]phenyl]-diphenylsulfanium;trifluoromethanesulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C1=CC(OC(C)(C)C)=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 HKKMPPDCCCBZHM-UHFFFAOYSA-M 0.000 description 1
- ISFXMNADAJKIEG-UHFFFAOYSA-M [4-[(2-methylpropan-2-yl)oxy]phenyl]-phenyliodanium;trifluoromethanesulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C1=CC(OC(C)(C)C)=CC=C1[I+]C1=CC=CC=C1 ISFXMNADAJKIEG-UHFFFAOYSA-M 0.000 description 1
- QFKJMDYQKVPGNM-UHFFFAOYSA-N [benzenesulfonyl(diazo)methyl]sulfonylbenzene Chemical compound C=1C=CC=CC=1S(=O)(=O)C(=[N+]=[N-])S(=O)(=O)C1=CC=CC=C1 QFKJMDYQKVPGNM-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical class C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- 238000007259 addition reaction Methods 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000007754 air knife coating Methods 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 125000002723 alicyclic group Chemical group 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229910003481 amorphous carbon Inorganic materials 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 238000007611 bar coating method Methods 0.000 description 1
- 229920005601 base polymer Polymers 0.000 description 1
- PLGBRGZNHLWMKD-UHFFFAOYSA-N bis[2-aminoethyl(dimethyl)silyl] dimethyl silicate Chemical compound NCC[Si](C)(C)O[Si](OC)(OC)O[Si](C)(C)CCN PLGBRGZNHLWMKD-UHFFFAOYSA-N 0.000 description 1
- AOMMCEXPXYKABF-UHFFFAOYSA-N bis[4-aminobutyl(dimethyl)silyl] dimethyl silicate Chemical compound NCCCC[Si](C)(C)O[Si](OC)(OC)O[Si](C)(C)CCCCN AOMMCEXPXYKABF-UHFFFAOYSA-N 0.000 description 1
- JQDSSRRIHBKYPJ-UHFFFAOYSA-N bis[5-aminopentyl(dimethyl)silyl] dimethyl silicate Chemical compound NCCCCC[Si](C)(C)O[Si](OC)(OC)O[Si](C)(C)CCCCCN JQDSSRRIHBKYPJ-UHFFFAOYSA-N 0.000 description 1
- OOJITEPTYTVULX-UHFFFAOYSA-N bis[5-aminopentyl(diphenyl)silyl] dimethyl silicate Chemical compound C=1C=CC=CC=1[Si](CCCCCN)(C=1C=CC=CC=1)O[Si](OC)(OC)O[Si](CCCCCN)(C=1C=CC=CC=1)C1=CC=CC=C1 OOJITEPTYTVULX-UHFFFAOYSA-N 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- MZUPWNMULGRONZ-UHFFFAOYSA-N cyclohexylsulfonylcyclohexane Chemical group C1CCCCC1S(=O)(=O)C1CCCCC1 MZUPWNMULGRONZ-UHFFFAOYSA-N 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- UMIKAXKFQJWKCV-UHFFFAOYSA-M diphenyliodanium;4-methylbenzenesulfonate Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.C=1C=CC=CC=1[I+]C1=CC=CC=C1 UMIKAXKFQJWKCV-UHFFFAOYSA-M 0.000 description 1
- SBQIJPBUMNWUKN-UHFFFAOYSA-M diphenyliodanium;trifluoromethanesulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C=1C=CC=CC=1[I+]C1=CC=CC=C1 SBQIJPBUMNWUKN-UHFFFAOYSA-M 0.000 description 1
- CZZYITDELCSZES-UHFFFAOYSA-N diphenylmethane Chemical compound C=1C=CC=CC=1CC1=CC=CC=C1 CZZYITDELCSZES-UHFFFAOYSA-N 0.000 description 1
- LTYMSROWYAPPGB-UHFFFAOYSA-O diphenylsulfanium Chemical compound C=1C=CC=CC=1[SH+]C1=CC=CC=C1 LTYMSROWYAPPGB-UHFFFAOYSA-O 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000010981 drying operation Methods 0.000 description 1
- 238000000609 electron-beam lithography Methods 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000005677 ethinylene group Chemical group [*:2]C#C[*:1] 0.000 description 1
- 229940116333 ethyl lactate Drugs 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- NBVXSUQYWXRMNV-UHFFFAOYSA-N fluoromethane Chemical compound FC NBVXSUQYWXRMNV-UHFFFAOYSA-N 0.000 description 1
- 238000007756 gravure coating Methods 0.000 description 1
- 238000013007 heat curing Methods 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- WSFSSNUMVMOOMR-NJFSPNSNSA-N methanone Chemical compound O=[14CH2] WSFSSNUMVMOOMR-NJFSPNSNSA-N 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 229930015698 phenylpropene Natural products 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 238000001020 plasma etching Methods 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 150000003139 primary aliphatic amines Chemical class 0.000 description 1
- 238000007639 printing Methods 0.000 description 1
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical group CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 150000005619 secondary aliphatic amines Chemical class 0.000 description 1
- 150000003377 silicon compounds Chemical class 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 150000003459 sulfonic acid esters Chemical class 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 150000003510 tertiary aliphatic amines Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 238000005979 thermal decomposition reaction Methods 0.000 description 1
- 238000012719 thermal polymerization Methods 0.000 description 1
- 238000010023 transfer printing Methods 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- TUODWSVQODNTSU-UHFFFAOYSA-M trifluoromethanesulfonate;tris[4-[(2-methylpropan-2-yl)oxy]phenyl]sulfanium Chemical compound [O-]S(=O)(=O)C(F)(F)F.C1=CC(OC(C)(C)C)=CC=C1[S+](C=1C=CC(OC(C)(C)C)=CC=1)C1=CC=C(OC(C)(C)C)C=C1 TUODWSVQODNTSU-UHFFFAOYSA-M 0.000 description 1
- WLOQLWBIJZDHET-UHFFFAOYSA-N triphenylsulfonium Chemical compound C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 WLOQLWBIJZDHET-UHFFFAOYSA-N 0.000 description 1
- 239000012953 triphenylsulfonium Substances 0.000 description 1
- FAYMLNNRGCYLSR-UHFFFAOYSA-M triphenylsulfonium triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 FAYMLNNRGCYLSR-UHFFFAOYSA-M 0.000 description 1
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 1
- UKRDPEFKFJNXQM-UHFFFAOYSA-N vinylsilane Chemical class [SiH3]C=C UKRDPEFKFJNXQM-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/09—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers
- G03F7/11—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers having cover layers or intermediate layers, e.g. subbing layers
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/09—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers
- G03F7/094—Multilayer resist systems, e.g. planarising layers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F122/00—Homopolymers of compounds having one or more unsaturated aliphatic radicals each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides or nitriles thereof
- C08F122/36—Amides or imides
- C08F122/40—Imides, e.g. cyclic imides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/46—Polymerisation initiated by wave energy or particle radiation
- C08F2/48—Polymerisation initiated by wave energy or particle radiation by ultraviolet or visible light
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/46—Polymerisation initiated by wave energy or particle radiation
- C08F2/48—Polymerisation initiated by wave energy or particle radiation by ultraviolet or visible light
- C08F2/50—Polymerisation initiated by wave energy or particle radiation by ultraviolet or visible light with sensitising agents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F22/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides or nitriles thereof
- C08F22/36—Amides or imides
- C08F22/40—Imides, e.g. cyclic imides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F267/00—Macromolecular compounds obtained by polymerising monomers on to polymers of unsaturated polycarboxylic acids or derivatives thereof as defined in group C08F22/00
- C08F267/10—Macromolecular compounds obtained by polymerising monomers on to polymers of unsaturated polycarboxylic acids or derivatives thereof as defined in group C08F22/00 on to polymers of amides or imides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/04—Azo-compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/28—Oxygen or compounds releasing free oxygen
- C08F4/32—Organic compounds
- C08F4/38—Mixtures of peroxy-compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F6/00—Post-polymerisation treatments
- C08F6/008—Treatment of solid polymer wetted by water or organic solvents, e.g. coagulum, filter cakes
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
- G03F7/2022—Multi-step exposure, e.g. hybrid; backside exposure; blanket exposure, e.g. for image reversal; edge exposure, e.g. for edge bead removal; corrective exposure
- G03F7/2026—Multi-step exposure, e.g. hybrid; backside exposure; blanket exposure, e.g. for image reversal; edge exposure, e.g. for edge bead removal; corrective exposure for the removal of unwanted material, e.g. image or background correction
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/26—Processing photosensitive materials; Apparatus therefor
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/26—Esters containing oxygen in addition to the carboxy oxygen
- C08F220/28—Esters containing oxygen in addition to the carboxy oxygen containing no aromatic rings in the alcohol moiety
- C08F220/283—Esters containing oxygen in addition to the carboxy oxygen containing no aromatic rings in the alcohol moiety and containing one or more carboxylic moiety in the chain, e.g. acetoacetoxyethyl(meth)acrylate
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
- H01L21/0271—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising organic layers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
- H01L21/033—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising inorganic layers
- H01L21/0332—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising inorganic layers characterised by their composition, e.g. multilayer masks, materials
Definitions
- the present invention relates to a film forming material for lithography, a composition for forming a film for lithography containing the material, an underlayer film for lithography formed using the composition, and a pattern forming method using the composition (for example, a resist pattern). Method or circuit pattern method).
- the light source for lithography used for forming the resist pattern has been shortened from a KrF excimer laser (248 nm) to an ArF excimer laser (193 nm).
- a KrF excimer laser (248 nm)
- an ArF excimer laser (193 nm)
- simply reducing the thickness of the resist makes it difficult to obtain a sufficient resist pattern thickness for processing the substrate. Therefore, not only a resist pattern, but also a process of forming a resist underlayer film between the resist and the semiconductor substrate to be processed, and giving the resist underlayer film a function as a mask at the time of substrate processing has been required.
- a resist underlayer film material containing a polymer having a specific repeating unit has been proposed to realize a resist underlayer film for lithography having a selectivity of a dry etching rate smaller than that of a resist (see Patent Document 2). .). Furthermore, to realize a resist underlayer film for lithography having a selectivity of a dry etching rate smaller than that of a semiconductor substrate, a repeating unit of acenaphthylenes and a repeating unit having a substituted or unsubstituted hydroxy group are copolymerized. A resist underlayer film material containing a polymer has been proposed (see Patent Document 3).
- an amorphous carbon underlayer film formed by CVD using methane gas, ethane gas, acetylene gas or the like as a raw material is well known.
- the present inventors have developed a lower layer for lithography containing a naphthalene formaldehyde polymer containing a specific structural unit and an organic solvent as a material that is excellent in optical properties and etching resistance, is soluble in a solvent, and is applicable to a wet process.
- a film forming composition (see Patent Documents 4 and 5) has been proposed.
- Patent Document 6 a method of forming a silicon nitride film (see Patent Document 6) and a method of forming a silicon nitride film by CVD (Patent Document 7) Cf.) is known.
- Patent Document 7 a material containing a silsesquioxane-based silicon compound is known (see Patent Documents 8 and 9).
- the present invention has been made in view of the above-described problems, and has as its object the purpose of applying a wet process to a photoresist lower layer which is excellent in heat resistance, etching resistance, characteristics of embedding in a stepped substrate, and film flatness.
- An object of the present invention is to provide a film forming material for lithography useful for forming a film, a composition for forming a film for lithography containing the material, and an underlayer film and a pattern forming method for lithography using the composition. .
- a group of the following formula (0) A film forming material for lithography, comprising a compound having the formula: [2] The film forming material for lithography according to [1], wherein the compound having the group of the formula (0) is at least one selected from the group consisting of a polycitraconimide compound and a citraconic imide resin.
- X is each independently a single bond, —O—, —CH 2 —, —C (CH 3 ) 2 —, —CO—, —C (CF 3 ) 2 —, —CONH— or —COO—;
- A is a divalent hydrocarbon group having 1 to 80 carbon atoms which may contain a single bond, an oxygen atom, or a hetero atom;
- R 1 is each independently a group having 0 to 30 carbon atoms which may contain a hetero atom;
- m1 is each independently an integer of 0 to 4.
- X is each independently a single bond, —O—, —CO—, or —COO—;
- X is a single bond
- A is- (CH 2 ) n1- , n1 is an integer of 1 to 10, R 1 is each independently an alkyl group; m1 is each independently an integer of 0 to 4,
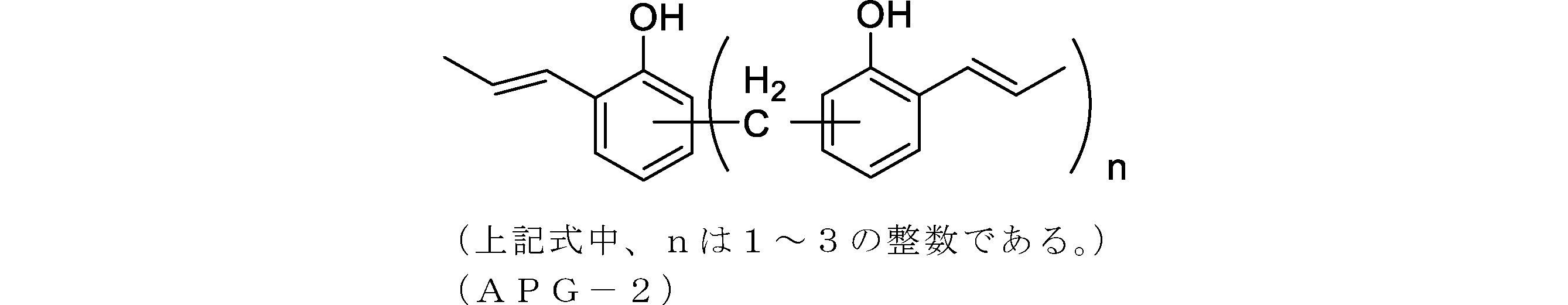
- [6-3] The film forming material for lithography according to the above [6-2], wherein n1 is an integer of 1 to 6.
- [6-4] The film forming material for lithography according to the above [6-2], wherein n1 is an integer of 1 to 3.
- X is each independently -CO- or -COO-
- A is- (O (CH 2 ) n2 ) n3-
- n2 is an integer of 1 to 4
- n3 is an integer of 1 to 20
- R 1 is each independently an alkyl group
- m1 is each independently an integer of 0 to 4,
- [6-6] The film-forming material for lithography according to the above [6-5], wherein -X-AX- is -CO- (O (CH 2 ) n2 ) n3 -COO-.
- X is -O-, A has the following structure
- Y is —C (CH 3 ) 2 — or —C (CF 3 ) 2 —, R 1 is each independently an alkyl group;
- m1 is each independently an integer of 0 to 4,
- A has the following structure The film forming material for lithography according to the above [6-7].
- [6-9] The film forming material for lithography according to any one of the above [5A] to [6-8], wherein R 1 is independently an alkyl group having 1 to 6 carbon atoms.
- R 3 and R 4 are each independently a group having 0 to 10 carbon atoms which may contain a hetero atom; m3 is each independently an integer of 0 to 4, m4 is each independently an integer of 0 to 4, n is an integer of 1 to 4.
- R 3 and R 4 are each independently a group having 0 to 10 carbon atoms which may contain a hetero atom; m3 is each independently an integer of 0 to 4, m4 is each independently an integer of 0 to 4, n is an integer of 1 to 4.
- [7-1] The film forming material for lithography according to the above [7], wherein R 2 or R 3 and R 4 are an alkyl group.
- [7-2] The film forming material for lithography according to any one of the above [4] to [7-1], wherein the hetero atom is selected from the group consisting of oxygen, fluorine and silicon.
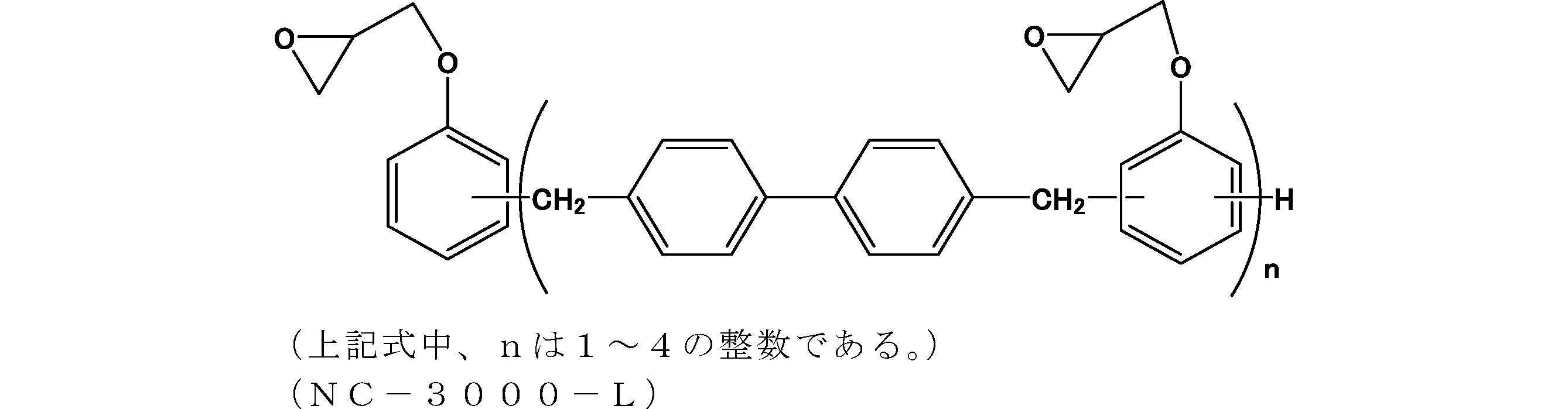
- the crosslinking agent is at least one selected from the group consisting of phenol compounds, epoxy compounds, cyanate compounds, amino compounds, benzoxazine compounds, melamine compounds, guanamine compounds, glycoluril compounds, urea compounds, isocyanate compounds and azide compounds.
- a composition for forming a film for lithography comprising the material for forming a film for lithography according to any one of [1] to [17] and a solvent.
- a lower layer film for lithography formed using the composition for forming a film for lithography according to [20].
- a method for forming a resist pattern comprising: [23] Forming a lower layer film on a substrate using the composition for forming a film for lithography according to the above [20], Forming an intermediate layer film on the lower layer film using a resist intermediate layer film material containing silicon atoms; Forming at least one photoresist layer on the intermediate layer film, Irradiating a predetermined area of the photoresist layer with radiation and developing to form a resist pattern; Etching the intermediate layer film using the resist pattern as a mask, Etching the lower layer film using the obtained intermediate layer film pattern as an etching mask, A step of forming a pattern on the substrate by etching the substrate using the obtained lower layer film pattern as an etching mask, And a circuit pattern forming method.
- the acidic aqueous solution is a mineral acid aqueous solution or an organic acid aqueous solution
- the mineral acid aqueous solution contains at least one selected from the group consisting of hydrochloric acid, sulfuric acid, nitric acid and phosphoric acid
- the organic acid aqueous solution is a group consisting of acetic acid, propionic acid, oxalic acid, malonic acid, succinic acid, fumaric acid, maleic acid, tartaric acid, citric acid, methanesulfonic acid, phenolsulfonic acid, p-toluenesulfonic acid, and trifluoroacetic acid.
- the solvent that is arbitrarily immiscible with water is one or more solvents selected from the group consisting of toluene, 2-heptanone, cyclohexanone, cyclopentanone, methyl isobutyl ketone, propylene glycol monomethyl ether acetate, and ethyl acetate. 24] or the purification method according to [25]. [27] Any of [24] to [26] above, further comprising a second extraction step of bringing the organic phase into contact with water after the first extraction step to extract impurities in the lithographic film-forming material. Purification method as described.
- a film forming material for lithography to which a wet process can be applied and which is useful for forming a photoresist underlayer film having excellent heat resistance, etching resistance, characteristics of embedding in a step substrate, and excellent film flatness, is provided.
- a composition for forming a film for lithography containing the material, and an underlayer film for lithography and a method for forming a pattern using the composition is provided.
- a film forming material for lithography includes a group represented by the following formula (0): (Hereinafter, sometimes referred to as “citraconimide compound” in the present specification).
- the citraconic imide compound can be obtained, for example, by a dehydration ring-closing reaction between a compound having one or more primary amino groups in the molecule and citraconic anhydride.
- Examples of the citraconic imide compound include a polycitraconic imide compound and a citraconic imide resin.
- the content of the citraconic imide compound in the film forming material for lithography of the present embodiment is preferably 0.1 to 100% by mass, more preferably 0.5 to 100% by mass, and 1 to 100% by mass. More preferably, it is mass%. Further, from the viewpoint of heat resistance and etching resistance, the content is preferably 51 to 100% by mass, more preferably 60 to 100% by mass, further preferably 70 to 100% by mass, and more preferably 80 to 100% by mass. It is particularly preferred that the content is mass%.
- the citraconic imide compound of the present embodiment can be used in combination with a conventional underlayer film forming composition in order to improve the heat resistance of the conventional underlayer film forming composition.
- the content of the citraconic imide compound in the underlayer film forming composition (excluding the solvent) is preferably from 1 to 50% by mass, more preferably from 1 to 30% by mass.
- the conventional underlayer film forming composition include, for example, those described in WO 2013/024779, but are not limited thereto.
- the citraconic imide compound in the film forming material for lithography of the present embodiment is characterized in that it has a function other than an acid generator or a basic compound for forming a film for lithography.
- a biscitraconic imide compound and an addition-polymerized citraconic imide resin are preferable from the viewpoint of availability of raw materials and production corresponding to mass production.
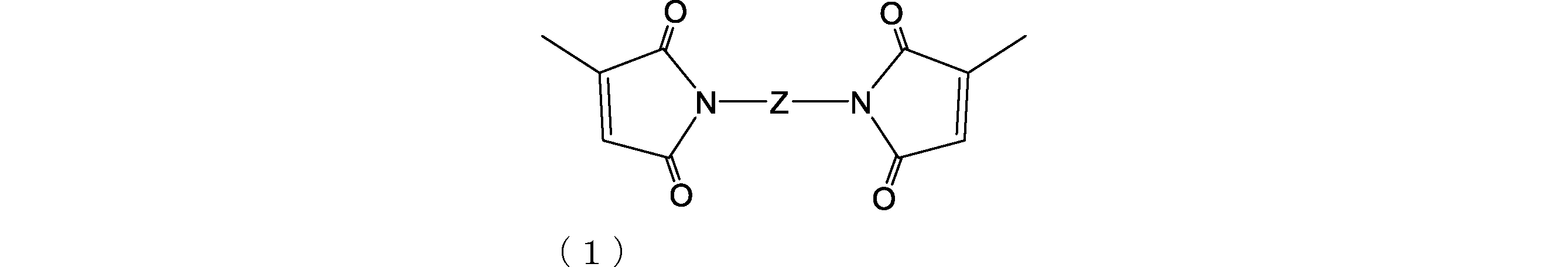
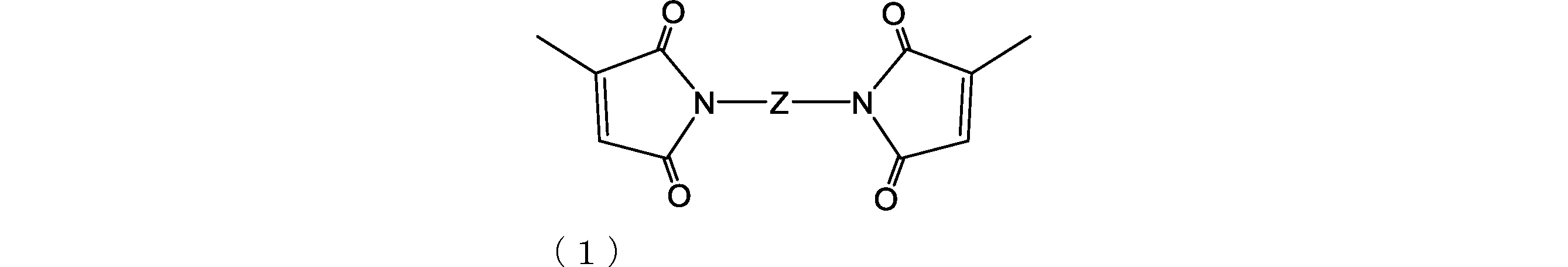
- the biscitraconimide compound is preferably a compound represented by the following formula (1).
- Z is a divalent hydrocarbon group having 1 to 100 carbon atoms which may contain a hetero atom.
- the hydrocarbon group may have 1 to 80, 1 to 60, 1 to 40, 1 to 20, etc. carbon atoms.
- Examples of the hetero atom include oxygen, nitrogen, sulfur, fluorine, silicon and the like.
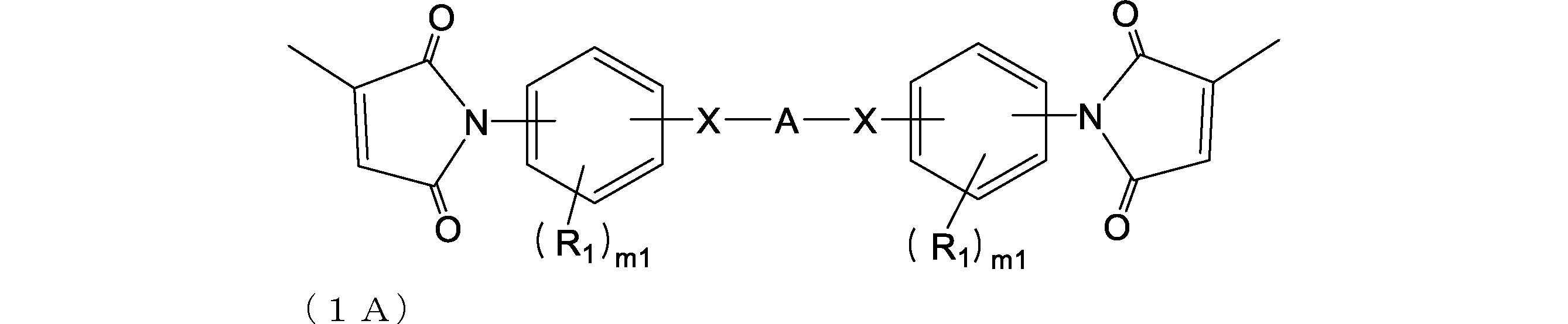
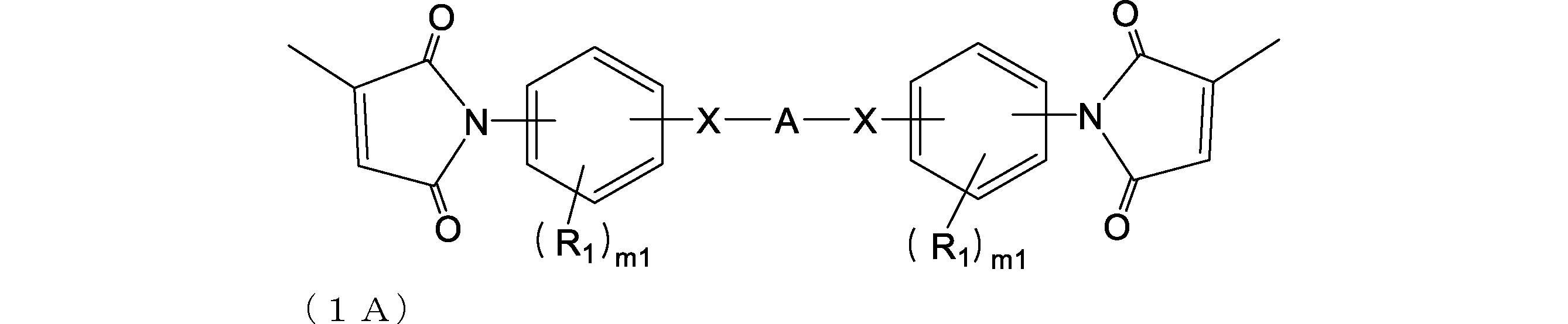
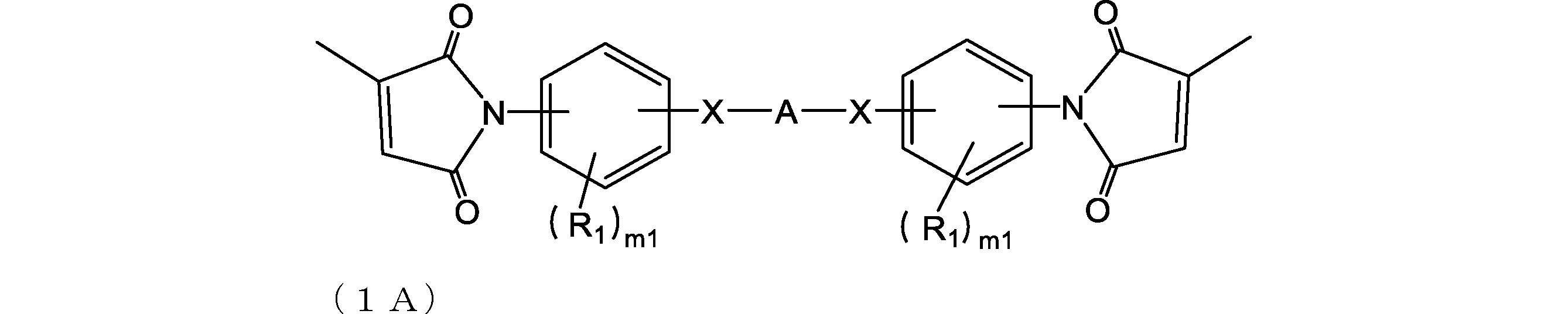
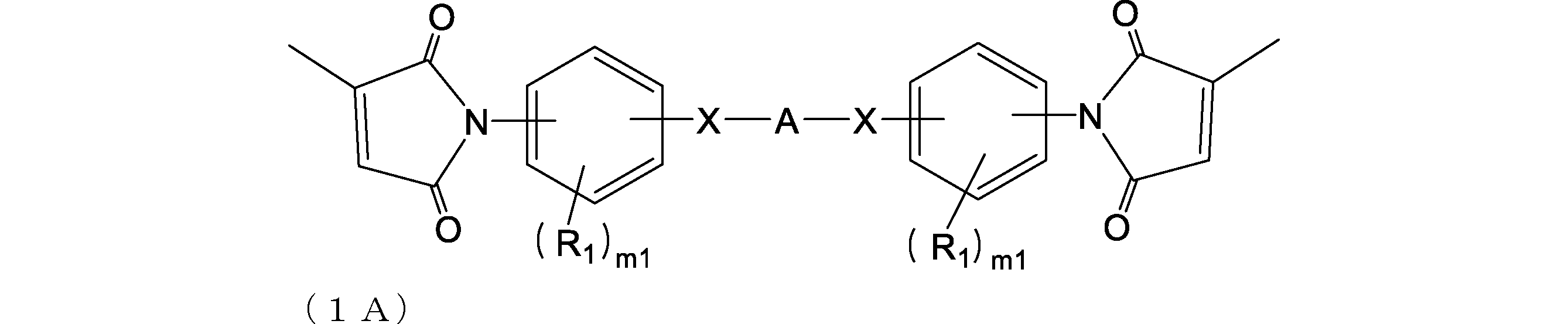
- the biscitraconimide compound is more preferably a compound represented by the following formula (1A).
- X is each independently a single bond, —O—, —CH 2 —, —C (CH 3 ) 2 —, —CO—, —C (CF 3 ) 2 —, —CONH— or —COO—;
- A is a divalent hydrocarbon group having 1 to 80 carbon atoms which may contain a single bond, an oxygen atom, and a hetero atom (eg, oxygen, nitrogen, sulfur, fluorine);
- R 1 is each independently a group having 0 to 30 carbon atoms which may contain a hetero atom (eg, oxygen, nitrogen, sulfur, fluorine, chlorine, bromine, iodine);
- m1 is each independently an integer of 0 to 4.
- X is each independently a single bond, —O—, —CH 2 —, —C (CH 3 ) 2 —, —CO—, —C (CF 3 ) 2 —, —CONH— or —COO—;
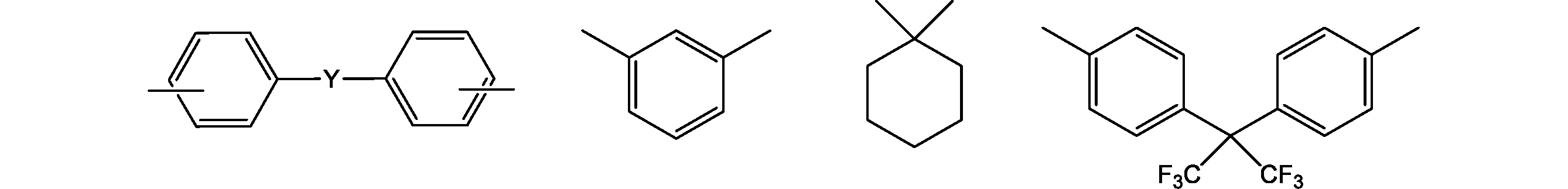
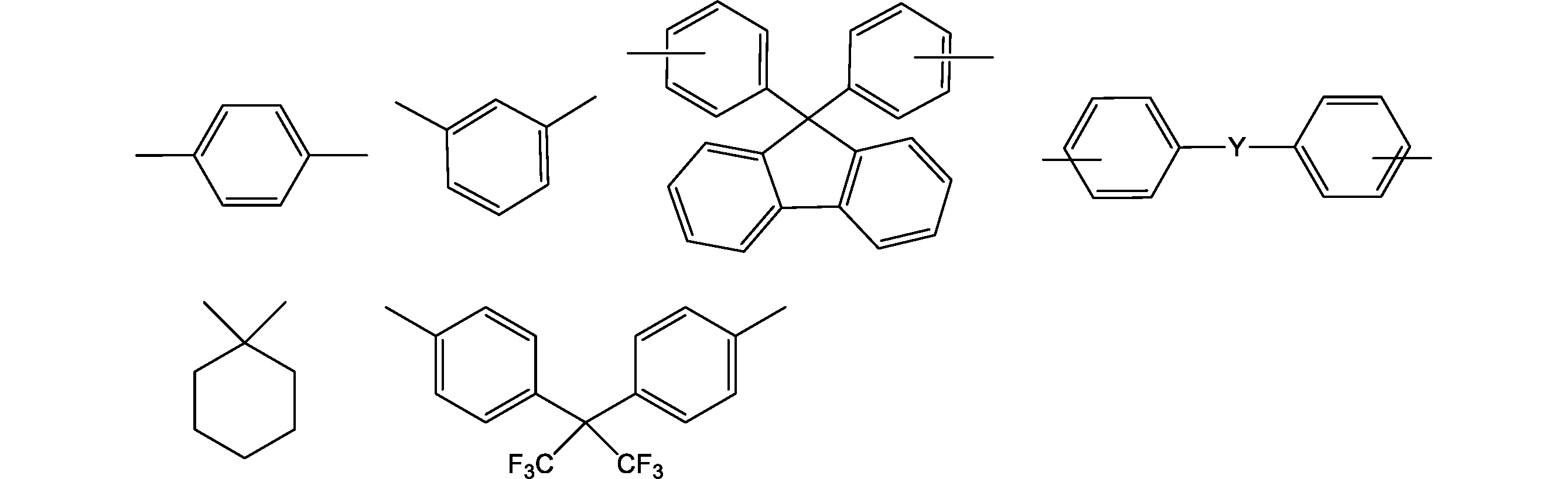
- A is a single bond, an oxygen atom,-(CH 2 ) n- , -CH 2 C (CH 3 ) 2 CH 2 -,-(C (CH 3 ) 2 ) n -,-(O (CH 2 ) m2 ) N -,-( ⁇ (C 6 H 4 )) n- , or one of the following structures:
- Y is a single bond, —O—, —CH 2 —, —C (CH 3 ) 2 —, —C (CF 3 ) 2 —,
- R 1 is each independently a group having 0 to 30 carbon atoms which may contain a hetero atom (eg,
- X is preferably a single bond from the viewpoint of heat resistance, and is preferably -COO- from the viewpoint of solubility.
- Y is preferably a single bond from the viewpoint of improving heat resistance.
- R 1 is preferably a group having 0 to 20 or 0 to 10 carbon atoms which may contain a hetero atom (eg, oxygen, nitrogen, sulfur, fluorine, chlorine, bromine, iodine).
- R 1 is preferably a hydrocarbon group from the viewpoint of improving solubility in an organic solvent.
- R 1 includes an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms) and the like, and specifically, a methyl group and an ethyl group.
- n1 is preferably an integer of 0 to 2, and more preferably 1 or 2 from the viewpoints of improving raw material availability and solubility.
- m2 is preferably an integer of 2 to 4.
- n is preferably an integer of 0 to 2, and more preferably an integer of 1 to 2 from the viewpoint of improving heat resistance.
- X is each independently a single bond, —O—, —CO—, or —COO—;
- A is a single bond, an oxygen atom, — (CH 2 ) n1 —, —CH 2 C (CH 3 ) 2 CH 2 —, — (O (CH 2 ) n2 ) n3 —, or the following structure: n1 is an integer of 1 to 10, n2 is an integer of 1 to 4, n3 is an integer of 1 to 20, Y is —C (CH 3 ) 2 — or —C (CF 3 ) 2 —, R 1 is each independently an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms); m1 is each independently an integer of 0 to 4.
- X is a single bond
- A is- (CH 2 ) n1-
- n1 is an integer of 1 to 10
- R 1 is each independently an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms)
- m1 is each independently an integer of 0 to 4.
- n1 is preferably 1 to 6 or 1 to 3.
- X is each independently -CO- or -COO-;
- A is- (O (CH 2 ) n2 ) n3- ,
- n2 is an integer of 1 to 4,
- n3 is an integer of 1 to 20,
- R 1 is each independently an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms);
- m1 is each independently an integer of 0 to 4.
- -X-AX- is preferably -CO- (O (CH 2 ) n2 ) n3 -COO-.
- X is -O-
- A has the following structure
- Y is —C (CH 3 ) 2 — or —C (CF 3 ) 2 —
- R 1 is each independently an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms);
- m1 is each independently an integer of 0 to 4.
- A has the following structure It is preferable that
- the biscitraconimide compound is preferably a compound represented by the following formula (1B).
- Z1 is a divalent linear, branched or cyclic hydrocarbon group having 1 to 100 carbon atoms which may contain a hetero atom.
- the hetero atom include oxygen, nitrogen, sulfur, fluorine, silicon and the like.
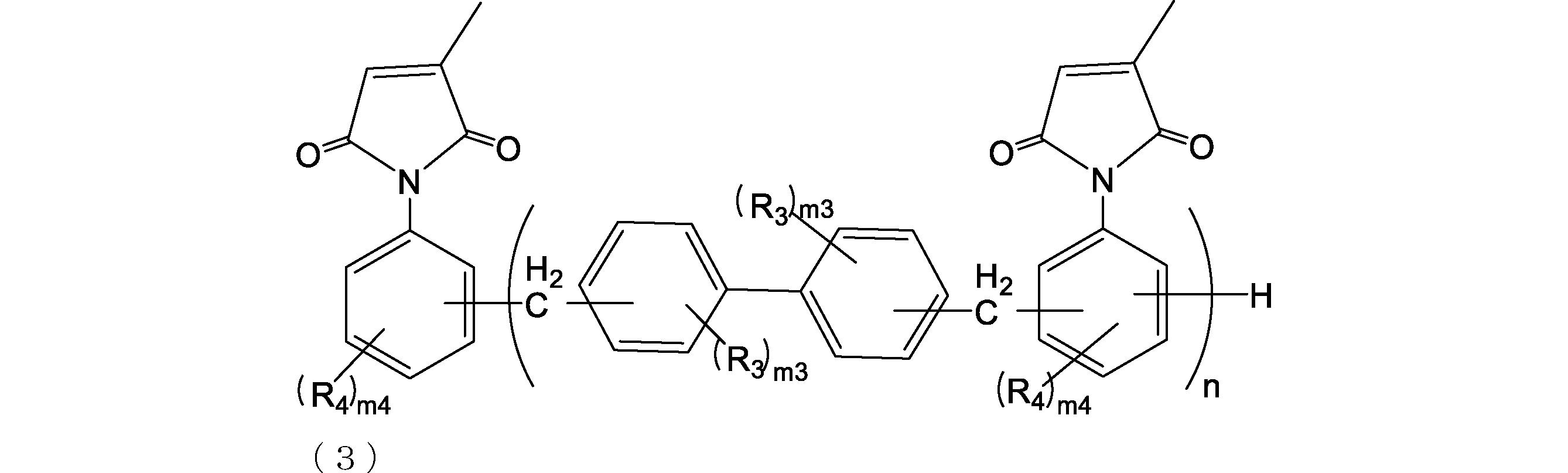
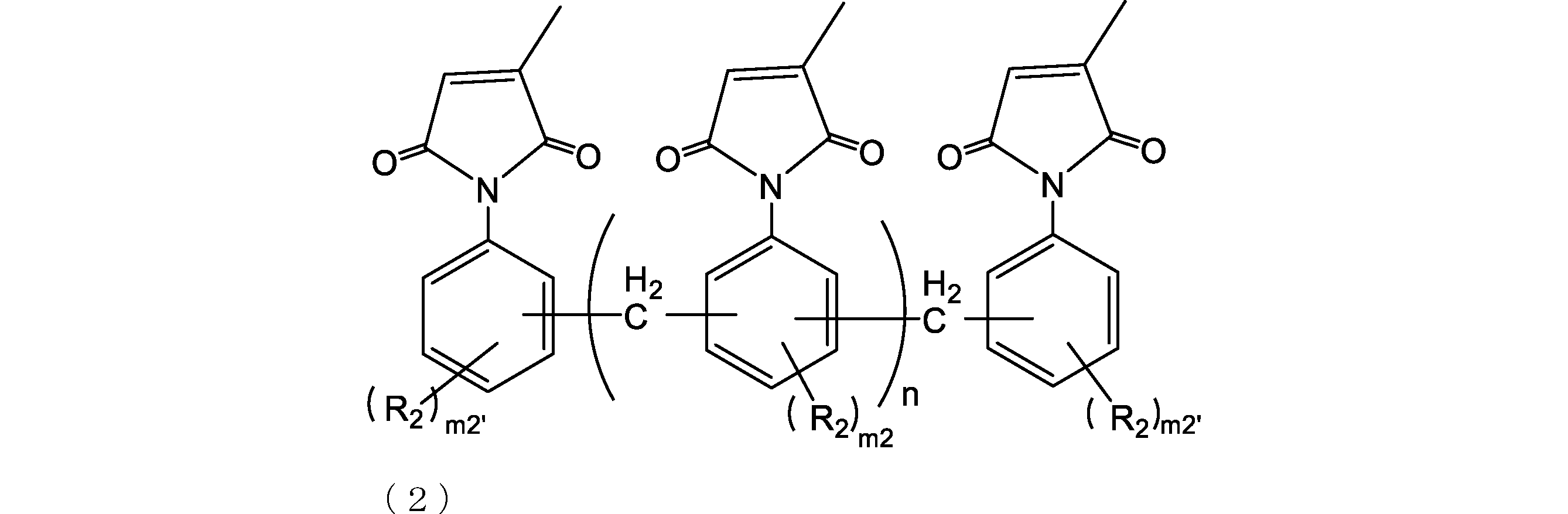
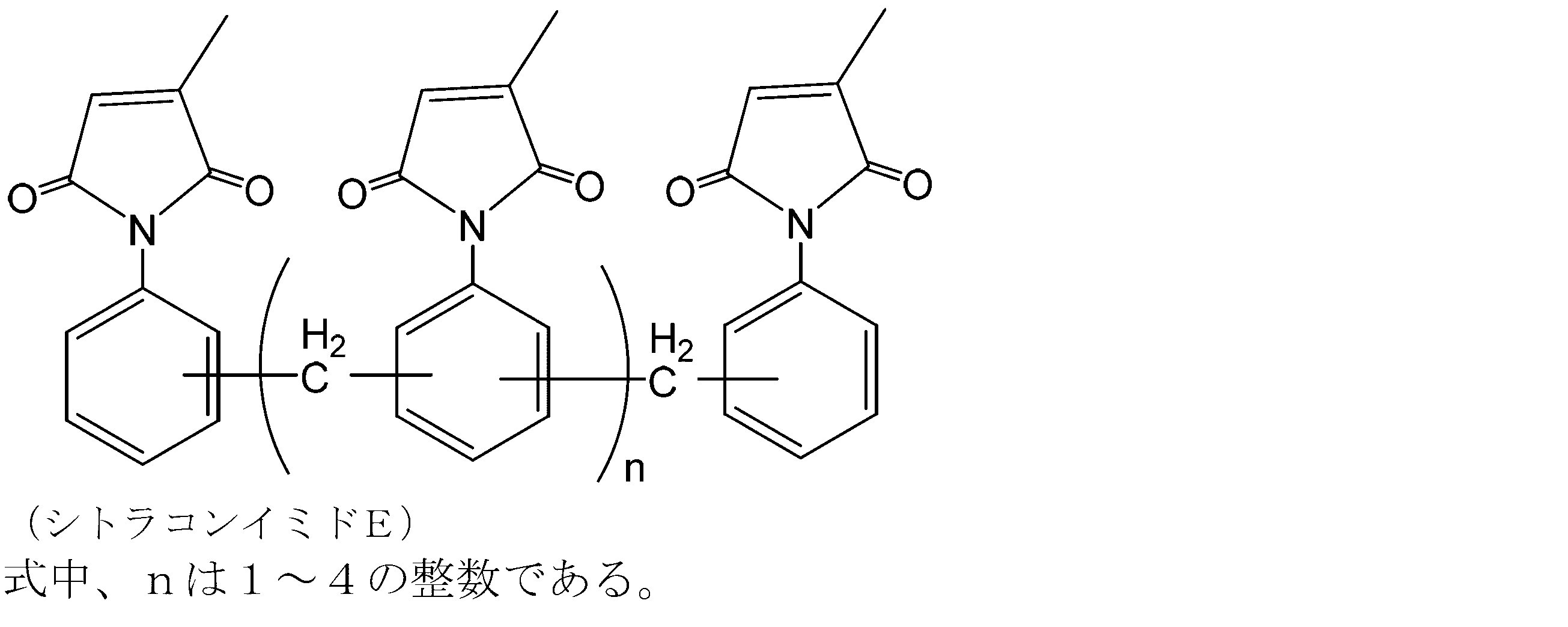
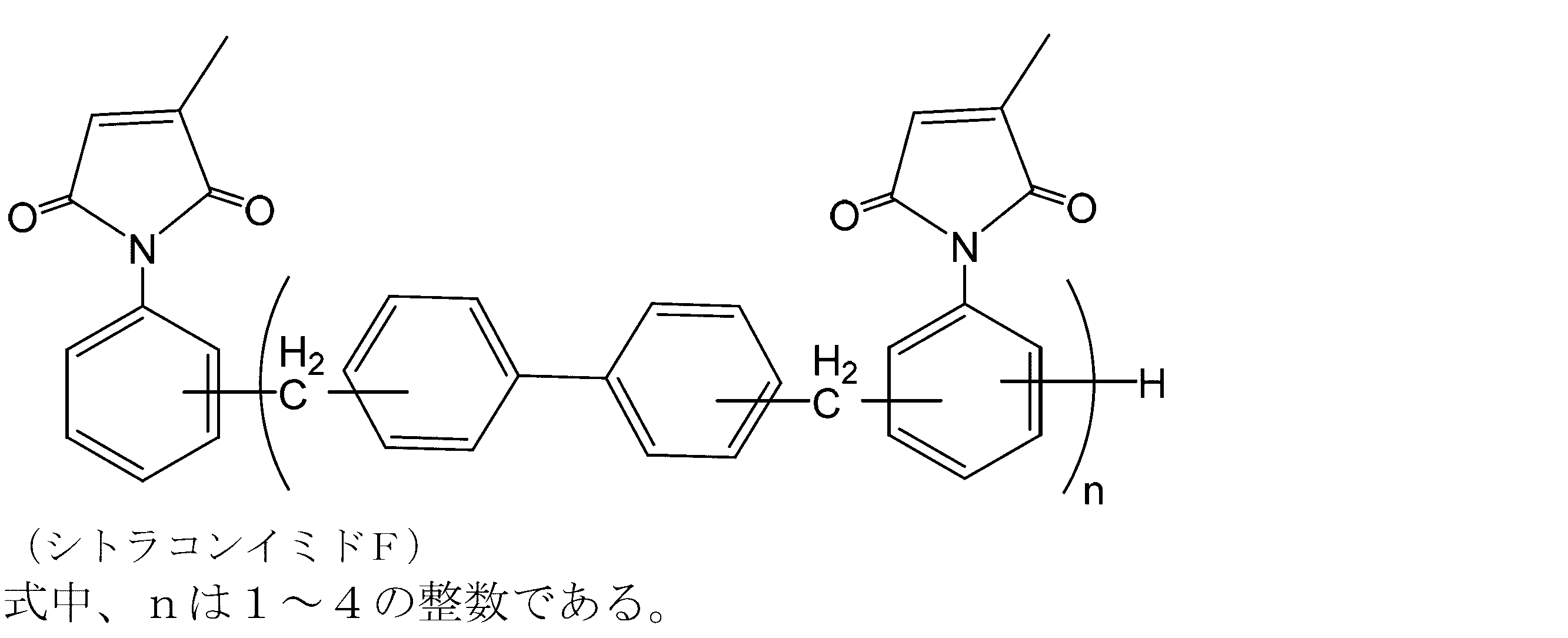
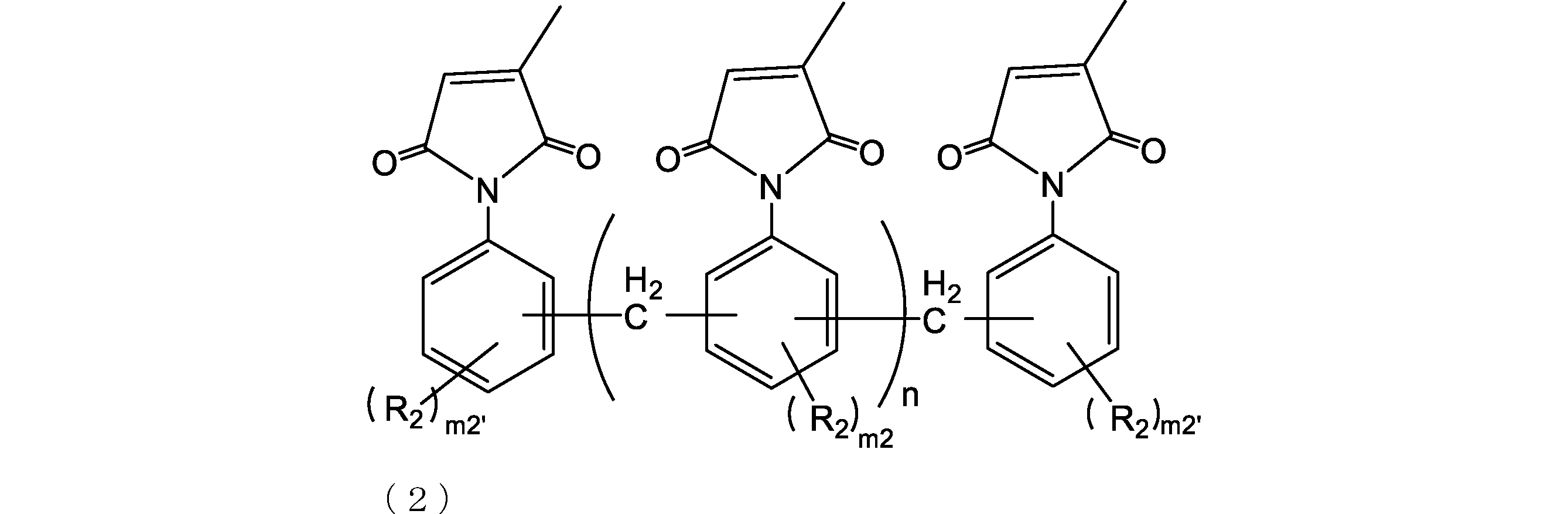
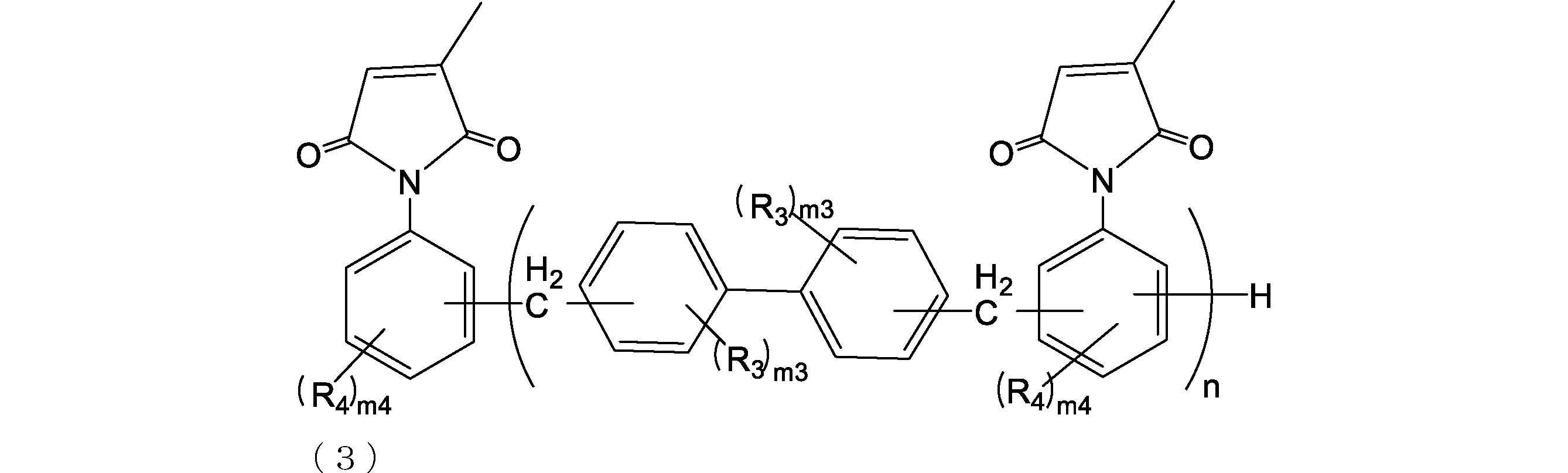
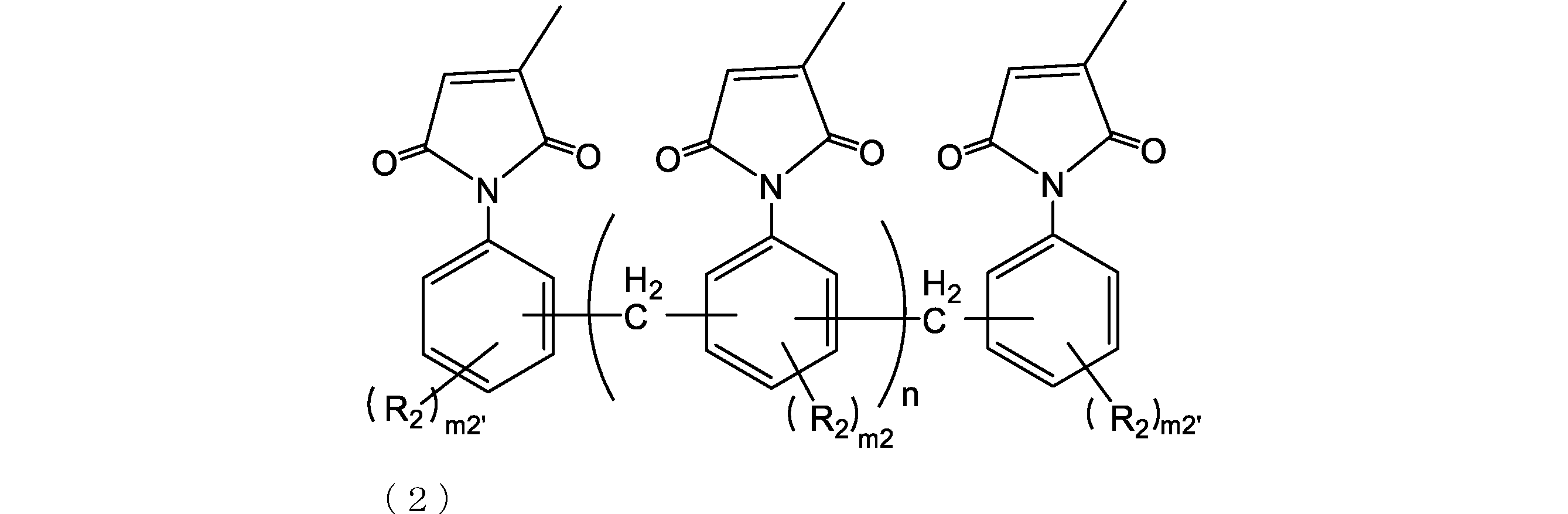
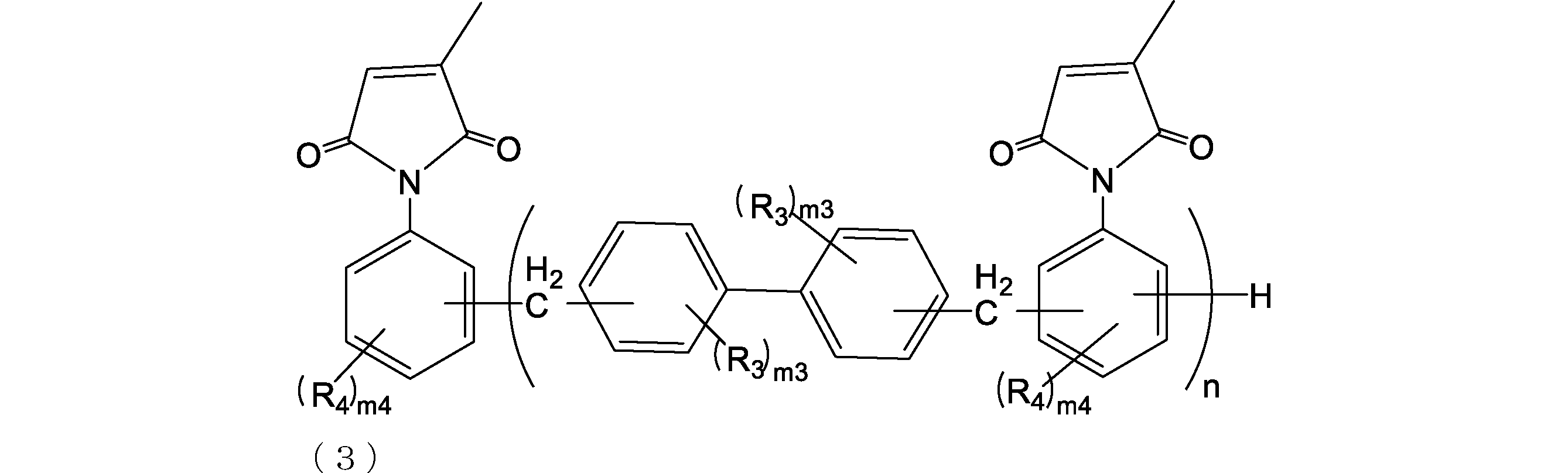
- the addition polymerization type citraconic imide resin is preferably a resin represented by the following formula (2) or (3) from the viewpoint of improving etching resistance.
- R 2 is independently a group having 0 to 10 carbon atoms which may contain a hetero atom (eg, oxygen, nitrogen, sulfur, fluorine, chlorine, bromine, iodine). Further, R 2 is preferably a hydrocarbon group from the viewpoint of improving the solubility in an organic solvent.
- R 2 includes an alkyl group (for example, an alkyl group having 1 to 6 or 1 to 3 carbon atoms) and the like, and specifically, a methyl group and an ethyl group.
- m2 is each independently an integer of 0 to 3.
- M2 is preferably 0 or 1, and more preferably 0 from the viewpoint of raw material availability.
- m2 ′ is an integer of 0 to 4 each independently.
- n2 ' is preferably 0 or 1, and more preferably 0 from the viewpoint of raw material availability.
- n is an integer of 0 to 4. Further, n is preferably an integer of 1 to 4 or 0 to 2, and more preferably an integer of 1 to 2 from the viewpoint of improving heat resistance.
- R 3 and R 4 are each independently a group having 0 to 10 carbon atoms which may contain a hetero atom (eg, oxygen, nitrogen, sulfur, fluorine, chlorine, bromine, iodine). is there. Further, R 3 and R 4 are preferably a hydrocarbon group from the viewpoint of improving the solubility in an organic solvent.
- R 3 and R 4 an alkyl group (eg, an alkyl group having 1 to 6 or 1 to 3 carbon atoms) and the like can be mentioned, and specifically, a methyl group, an ethyl group and the like can be mentioned.
- n is an integer of 0 to 4. Further, n is preferably an integer of 1 to 4 or 0 to 2, and more preferably an integer of 1 to 2 from the viewpoint of raw material availability.
- the film forming material for lithography of the present embodiment can be applied to a wet process.
- the film forming material for lithography of the present embodiment has an aromatic structure, and also has a rigid citraconic imide skeleton, and the citraconic imide group causes a crosslinking reaction by high-temperature baking alone, Develop high heat resistance. As a result, deterioration of the film during high-temperature baking is suppressed, and a lower layer film having excellent etching resistance to oxygen plasma etching or the like can be formed.
- the film forming material for lithography of the present embodiment has high solubility in an organic solvent and high solubility in a safe solvent, despite having an aromatic structure.
- the lower layer film for lithography composed of the composition for forming a film for lithography of the present embodiment described later has excellent embedding characteristics into a stepped substrate and excellent flatness of the film, not only good product quality stability, but also a resist. Since the adhesiveness between the layer and the resist intermediate layer film material is also excellent, an excellent resist pattern can be obtained.
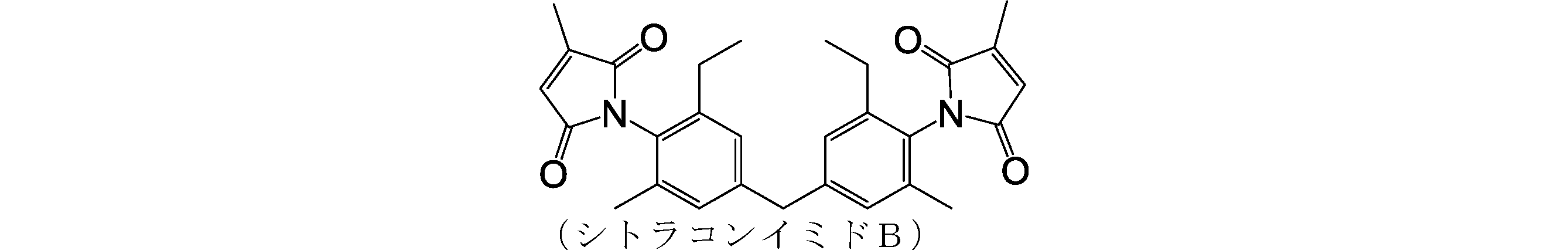
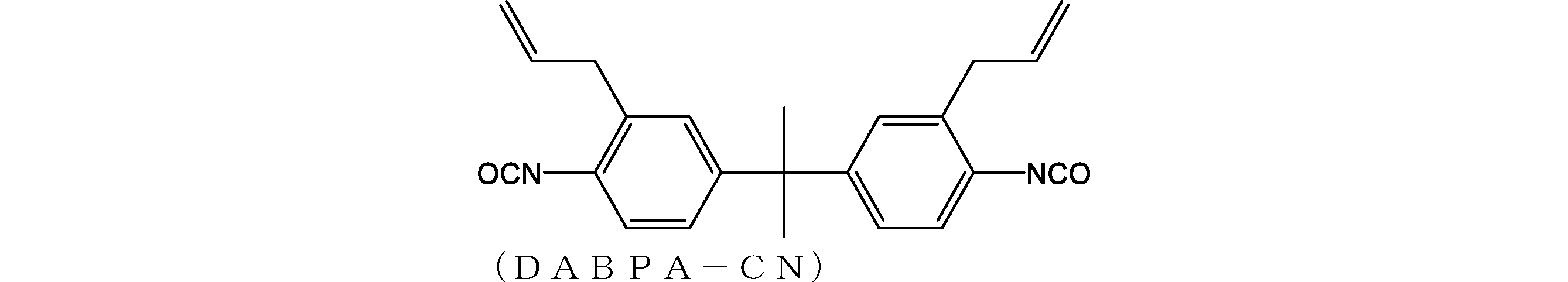
- the biscitraconimide compound used in the present embodiment is specifically m-phenylenebiscitraconimide, 4-methyl-1,3-phenylenebiscitraconimide, 4,4-diphenylmethanebiscitraconimide, 4,4 '-Diphenylsulfone biscitraconimide, 1,3-bis (3-citraconimidophenoxy) benzene, 1,3-bis (4-citraconimidophenoxy) benzene, 1,4-bis (3-citraconimidophenoxy) benzene, Bis citraconimide having a phenylene skeleton such as 1,4-bis (4-citraconimidophenoxy) benzene; bis (3-ethyl-5-methyl-4-citraconimidophenyl) methane, 1,1-bis (3-ethyl-) 5-methyl-4-citraconimidophenyl) ethane, 2,2 Bis (3-e
- biscitraconimide compounds bis (3-ethyl-5-methyl-4-citraconimidophenyl) methane, N, N'-4,4 '-[3,3'-dimethyl-diphenylmethane] biscitraconimide, N , N'-4,4 '-[3,3'-Diethyldiphenylmethane] biscitraconimide is preferred because of its excellent solvent solubility and heat resistance.
- the addition polymerization type from the viewpoint of the heat resistance of the film for lithography, the adhesion to the resist intermediate layer, and the difficulty of film defects.
- Citraconimide resin is more preferred.
- the film-forming material for lithography of the present embodiment contains a crosslinking agent as necessary from the viewpoint of lowering the curing temperature and suppressing intermixing, in addition to the biscitraconimide compound and / or the addition polymerization type citraconic imide resin. It may be.
- the crosslinking agent is not particularly limited as long as it undergoes a crosslinking reaction with citraconimide, and any known crosslinking system can be applied.
- Specific examples of the crosslinking agent that can be used in the present embodiment include, for example, a phenol compound, an epoxy compound, Examples include, but are not limited to, cyanate compounds, amino compounds, benzoxazine compounds, acrylate compounds, melamine compounds, guanamine compounds, glycoluril compounds, urea compounds, isocyanate compounds, azide compounds, and the like.
- These crosslinking agents can be used alone or in combination of two or more. Among these, a benzoxazine compound, an epoxy compound or a cyanate compound is preferable, and a benzoxazine compound is more preferable from the viewpoint of improving etching resistance.
- the phenolic hydroxyl group, epoxy group, cyanate group, amino group, or phenolic group formed by opening the alicyclic site of benzoxazine may be used as the active group of these cross-linking agents.
- the hydroxyl group undergoes an addition reaction with the carbon-carbon double bond constituting the citraconic imide group to form a crosslink, and the two carbon-carbon double bonds of the biscitraconimide compound of the present embodiment polymerize and crosslink.
- phenol compound known compounds can be used.
- those described in WO2018-016614 can be mentioned.
- an aralkyl-type phenol resin is desirable from the viewpoint of heat resistance and solubility.
- epoxy compound known compounds can be used and selected from compounds having two or more epoxy groups in one molecule. For example, those described in WO2018-016614 can be mentioned. These epoxy resins may be used alone or in combination of two or more. From the viewpoint of heat resistance and solubility, epoxy resins obtained from phenol aralkyl resins and biphenyl aralkyl resins are preferably solid epoxy resins at room temperature.
- the cyanate compound is not particularly limited as long as it has two or more cyanate groups in one molecule, and a known compound can be used. For example, those described in WO 2011108524 are exemplified.
- preferred cyanate compounds have a structure in which a hydroxyl group of a compound having two or more hydroxyl groups in one molecule is substituted with a cyanate group.
- the cyanate compound preferably has an aromatic group, and a compound having a structure in which a cyanate group is directly connected to an aromatic group can be suitably used. Examples of such a cyanate compound include those described in International Publication WO2018-016614. These cyanate compounds may be used alone or in appropriate combination of two or more. Further, the above-mentioned cyanate compound may be in any form of a monomer, an oligomer and a resin.
- amino compound examples include those described in International Publication No. 2018-016614.
- the structure of the oxazine of the benzoxazine compound is not particularly limited, and examples thereof include structures of an oxazine having an aromatic group including a condensed polycyclic aromatic group, such as benzoxazine and naphthoxazine.
- benzoxazine compound examples include compounds represented by the following general formulas (a) to (f).
- a bond displayed toward the center of the ring indicates that the bond forms a ring and is bonded to any carbon to which a substituent can be bonded.
- R1 and R2 independently represent an organic group having 1 to 30 carbon atoms.
- R3 to R6 independently represent hydrogen or a hydrocarbon group having 1 to 6 carbon atoms.
- X is independently a single bond, -O-, -S-, -SS-, -SO 2- , -CO-,-.
- Y is independently a single bond, -O-, -S-, -CO-, -C (CH 3 ) 2- , -C (CF 3 ) 2- Or an alkylene having 1 to 3 carbon atoms.
- the benzoxazine compound includes an oligomer or polymer having an oxazine structure in a side chain, and an oligomer or polymer having a benzoxazine structure in a main chain.
- the benzoxazine compound can be produced by a method similar to the method described in WO 2004/09708 pamphlet, JP-A-11-12258 and JP-A-2004-352670.
- melamine compound examples include, for example, those described in WO2018-016614.
- guanamine compound examples include, for example, those described in International Publication No. 2018-016614.
- glycoluril compound examples include, for example, those described in WO2018-016614.
- urea compound examples include, for example, those described in International Publication WO2018-016614.
- a crosslinking agent having at least one allyl group may be used from the viewpoint of improving the crosslinking property.
- Specific examples of the crosslinking agent having at least one allyl group include those described in WO2018-016614, but are not limited to those exemplified. These may be used alone or as a mixture of two or more. Among these, 2,2-bis (3-allyl-4-hydroxyphenyl) propane, 1,1,1,2, and 3,2,2-bis (3-allyl-4-hydroxyphenyl) propane are preferred from the viewpoint of excellent compatibility with the biscitraconimide compound and / or the addition polymerization type citraconimide resin.
- the film-forming material for lithography of the present embodiment is obtained by crosslinking and curing a biscitraconimide compound and / or an addition-polymerized citraconic imide resin alone or after blending the above-mentioned crosslinking agent by a known method. Can be formed.
- the cross-linking method include techniques such as heat curing and light curing.
- the content of the cross-linking agent is usually in the range of 0.1 to 10000 parts by mass, when the total mass of the biscitraconimide compound and the addition polymerization type citraconimide resin is 100 parts by mass, From the viewpoint of solubility and solubility, it is in the range of 0.1 to 1000 parts by mass, more preferably in the range of 0.1 to 100 parts by mass, and still more preferably in the range of 1 to 50 parts by mass. Preferably it is in the range of 1 to 30 parts by mass.
- a crosslinking accelerator for promoting a crosslinking and curing reaction can be used as necessary.
- the crosslinking accelerator is not particularly limited as long as it promotes crosslinking and curing reactions, and examples thereof include amines, imidazoles, organic phosphines, and Lewis acids.
- One of these crosslinking accelerators can be used alone, or two or more can be used in combination.
- imidazoles or organic phosphines are preferable, and imidazoles are more preferable from the viewpoint of lowering the crosslinking temperature.
- the crosslinking accelerator is not limited to the following, but includes, for example, those described in WO2018-016614.
- the compounding amount of the crosslinking accelerator is usually in the range of 0.1 to 10 parts by mass, when the total mass of the biscitraconimide compound and the addition polymerization type citraconimide resin is 100 parts by mass. Preferably, it is in the range of 0.1 to 5 parts by mass, more preferably 0.1 to 3 parts by mass from the viewpoint of controllability and economy.
- the film forming material for lithography of the present embodiment may contain a radical polymerization initiator as needed.
- the radical polymerization initiator may be a photopolymerization initiator that initiates radical polymerization by light, or a thermal polymerization initiator that initiates radical polymerization by heat.
- radical polymerization initiator is not particularly limited, and a conventionally used one can be appropriately used. For example, those described in WO2018-016614 can be mentioned. As the radical polymerization initiator in the present embodiment, one of these may be used alone, or two or more of them may be used in combination, or other known polymerization initiators may be further used in combination.
- the content of the radical polymerization initiator may be any amount stoichiometrically necessary with respect to the total mass of the biscitraconimide compound and the addition polymerization type citraconic imide resin.
- the amount is preferably 0.05 to 25 parts by mass, more preferably 0.1 to 10 parts by mass when the total mass with the addition polymerization type citraconimide resin is 100 parts by mass.
- the content of the radical polymerization initiator is 0.05 parts by mass or more, the curing of the biscitraconimide compound and / or the citraconic imide resin tends to be prevented from becoming insufficient.
- the content of the polymerization initiator is 25 parts by mass or less, there is a tendency that the long-term storage stability at room temperature of the film forming material for lithography can be prevented from being impaired.
- the film forming material for lithography can be purified by washing with an acidic aqueous solution.
- the purification method comprises dissolving a film forming material for lithography in an organic solvent immiscible with water to obtain an organic phase, contacting the organic phase with an acidic aqueous solution, and performing an extraction treatment (first extraction step). And transferring a metal component contained in an organic phase containing a film forming material for lithography and an organic solvent to an aqueous phase, and then separating the organic phase and the aqueous phase.
- the organic solvent that is not arbitrarily miscible with water is not particularly limited, but is preferably an organic solvent that can be safely applied to a semiconductor manufacturing process.
- the amount of the organic solvent used is usually about 1 to 100 times by mass the compound used.
- organic solvent used include, for example, those described in International Publication No. 2015/080240.
- toluene, 2-heptanone, cyclohexanone, cyclopentanone, methyl isobutyl ketone, propylene glycol monomethyl ether acetate, ethyl acetate and the like are preferable, and cyclohexanone and propylene glycol monomethyl ether acetate are particularly preferable.
- These organic solvents can be used alone or in combination of two or more.
- the acidic aqueous solution is appropriately selected from aqueous solutions in which generally known organic and inorganic compounds are dissolved in water. For example, those described in International Publication No. 2015/080240 are exemplified. These acidic aqueous solutions can be used alone or in combination of two or more.
- the acidic aqueous solution include a mineral acid aqueous solution and an organic acid aqueous solution.
- the mineral acid aqueous solution include an aqueous solution containing at least one selected from the group consisting of hydrochloric acid, sulfuric acid, nitric acid, and phosphoric acid.
- organic acid aqueous solution examples include acetic acid, propionic acid, oxalic acid, malonic acid, succinic acid, fumaric acid, maleic acid, tartaric acid, citric acid, methanesulfonic acid, phenolsulfonic acid, p-toluenesulfonic acid and trifluoroacetic acid.
- the acidic aqueous solution is preferably an aqueous solution of sulfuric acid, nitric acid, and a carboxylic acid such as acetic acid, oxalic acid, tartaric acid, and citric acid.
- an aqueous solution of sulfuric acid, oxalic acid, tartaric acid, and citric acid is preferable.
- polyvalent carboxylic acids such as oxalic acid, tartaric acid, and citric acid coordinate with metal ions and generate a chelating effect, so that more metals can be removed.
- the water used here is preferably one having a low metal content, such as ion-exchanged water, for the purpose of the present invention.
- the pH of the acidic aqueous solution is not particularly limited. However, if the acidity of the aqueous solution is too high, the compound or resin used may be adversely affected, which is not preferable. Usually, the pH range is about 0-5, more preferably about 0-3.
- the use amount of the acidic aqueous solution is not particularly limited, but if the amount is too small, it is necessary to increase the number of extractions for removing the metal. The above problems may occur.
- the amount of the aqueous solution to be used is generally 10 to 200 parts by mass, preferably 20 to 100 parts by mass, based on the solution of the film forming material for lithography.
- the metal component can be extracted by bringing the acidic aqueous solution into contact with a solution (B) containing a film forming material for lithography and an organic solvent immiscible with water.
- the temperature at the time of performing the above-mentioned extraction treatment is usually 20 to 90 ° C, preferably 30 to 80 ° C.
- the extraction operation is performed by, for example, mixing well by stirring or the like, and then allowing the mixture to stand. Thereby, the metal component contained in the solution containing the compound and the organic solvent to be used is transferred to the aqueous phase. In addition, by this operation, the acidity of the solution is reduced, and deterioration of the compound used can be suppressed.
- a solution phase containing the compound and the organic solvent to be used is separated into an aqueous phase, and a solution containing the organic solvent is recovered by decantation or the like.
- the standing time is not particularly limited. However, if the standing time is too short, the separation of the aqueous phase containing the organic solvent from the aqueous phase becomes poor, which is not preferable. Usually, the standing time is 1 minute or more, more preferably 10 minutes or more, and further preferably 30 minutes or more.
- the extraction process may be performed only once, but it is also effective to repeat the operations of mixing, standing, and separating a plurality of times.
- the organic phase containing the organic solvent extracted and recovered from the aqueous solution after the treatment is further subjected to an extraction treatment with water (second extraction).
- Step) is preferably performed.
- the extraction operation is performed by mixing well by stirring or the like, and then allowing the mixture to stand.
- the resulting solution is separated into a solution phase containing a compound and an organic solvent and an aqueous phase, and the solution phase is recovered by decantation or the like.
- the water used here is preferably one having a low metal content, such as ion-exchanged water, for the purpose of the present invention.
- the extraction process may be performed only once, but it is also effective to repeat the operations of mixing, standing, and separating a plurality of times. Further, the conditions such as the ratio of use of the two, the temperature, the time, and the like in the extraction treatment are not particularly limited, but may be the same as in the case of the contact treatment with the acidic aqueous solution.
- Water mixed in the solution containing the film forming material for lithography and the organic solvent thus obtained can be easily removed by performing an operation such as distillation under reduced pressure. Further, the concentration of the compound can be adjusted to an arbitrary concentration by adding an organic solvent as needed.
- a method for obtaining only a film forming material for lithography from a solution containing the obtained organic solvent can be performed by a known method such as removal under reduced pressure, separation by reprecipitation, and a combination thereof. If necessary, known processes such as a concentration operation, a filtration operation, a centrifugation operation, and a drying operation can be performed.
- composition for forming a film for lithography contains the material for forming a film for lithography and a solvent.
- the film for lithography is, for example, a lower film for lithography.
- the composition for forming a film for lithography of the present embodiment is applied to a substrate, and then, if necessary, after heating to evaporate the solvent, may be heated or irradiated with light to form a desired cured film. it can.
- the method of applying the composition for forming a film for lithography of the present embodiment is optional, for example, a spin coating method, a dipping method, a flow coating method, an ink jet method, a spray method, a bar coating method, a gravure coating method, a slit coating method, Methods such as a roll coating method, a transfer printing method, a brush coating, a blade coating method, and an air knife coating method can be appropriately employed.
- the heating temperature of the film is not particularly limited for the purpose of evaporating the solvent, and may be, for example, 40 to 400 ° C.
- the heating method is not particularly limited, and for example, evaporation may be performed using a hot plate or an oven under an appropriate atmosphere such as air, an inert gas such as nitrogen, or a vacuum.
- the heating temperature and the heating time may be selected under conditions suitable for the target process of the electronic device, and the heating conditions may be selected so that the physical properties of the obtained film conform to the required characteristics of the electronic device.
- the conditions for light irradiation are not particularly limited, and appropriate irradiation energy and irradiation time may be employed depending on the lithography film forming material to be used.
- the solvent used for the composition for forming a film for lithography of the present embodiment is not particularly limited as long as at least the biscitraconimide and / or the addition polymerization type citraconic imide resin can be dissolved, and a known one is appropriately used. Can be.
- the solvent include, for example, those described in International Publication 2013/024779. These solvents can be used alone or in combination of two or more.
- cyclohexanone propylene glycol monomethyl ether, propylene glycol monomethyl ether acetate, ethyl lactate, methyl hydroxyisobutyrate, and anisole are particularly preferred from the viewpoint of safety.
- the content of the solvent is not particularly limited, but from the viewpoint of solubility and film formation, the total mass of the biscitraconimide compound and the addition-polymerized citraconic imide resin in the film forming material for lithography is 100 parts by mass. In this case, the amount is preferably 25 to 9,900 parts by mass, more preferably 400 to 7,900 parts by mass, and even more preferably 900 to 4,900 parts by mass.
- the composition for forming a film for lithography of the present embodiment may contain an acid generator as necessary from the viewpoint of further accelerating the crosslinking reaction.
- an acid generator those which generate an acid by thermal decomposition, those which generate an acid by light irradiation, and the like are known, and any of them can be used.
- Examples of the acid generator include those described in International Publication 2013/024779. Among these, ditertiary butyl diphenyliodonium nonafluoromethanesulfonate, trifluoromethanesulfonic acid diphenyliodonium, trifluoromethanesulfonic acid (p-tert-butoxyphenyl) phenyliodonium, p-toluenesulfonic acid diphenyliodonium, p- Toluenesulfonic acid (p-tert-butoxyphenyl) phenyliodonium, trifluoromethanesulfonic acid triphenylsulfonium, trifluoromethanesulfonic acid (p-tert-butoxyphenyl) diphenylsulfonium, trifluoromethanesulfonic acid tris (p-tert-butoxyphenyl) Sulfonium, triphenylsulfonium,
- the content of the acid generator is not particularly limited, and the total mass of the biscitraconimide compound and the addition polymerization type citraconic imide resin in the film forming material for lithography is 100%.
- the amount is preferably from 0 to 50 parts by mass, more preferably from 0 to 40 parts by mass.
- composition for forming an underlayer film for lithography of the present embodiment may contain a basic compound from the viewpoint of improving storage stability and the like.
- the basic compound serves as a quencher for the acid to prevent a small amount of the acid generated from the acid generator from advancing the crosslinking reaction.
- a basic compound include, but are not limited to, primary, secondary and tertiary aliphatic amines, mixed amines, and aromatic amines described in WO2013-024779.
- the content of the basic compound is not particularly limited, and the total mass of the biscitraconimide compound and the addition polymerization type citraconic imide resin in the film forming material for lithography is 100. In the case of parts by mass, it is preferably from 0 to 2 parts by mass, more preferably from 0 to 1 part by mass. When the content is in the above-mentioned preferable range, storage stability tends to be improved without excessively impairing the crosslinking reaction.
- composition for forming a film for lithography of the present embodiment may contain a known additive.
- Known additives are not limited to the following, but include, for example, ultraviolet absorbers, defoamers, coloring agents, pigments, nonionic surfactants, anionic surfactants, and cationic surfactants.
- the lower layer film for lithography of the present embodiment is formed using the composition for forming a film for lithography of the present embodiment.
- the pattern forming method of the present embodiment includes a step (A-1) of forming an underlayer film on a substrate by using the composition for forming a film for lithography of the present embodiment, and forming at least one layer on the underlayer film.
- a step (B-1) of forming an underlayer film on a substrate by using the composition for forming a film for lithography of the present embodiment includes the steps of: A step of forming an intermediate layer film using a resist intermediate layer film material containing silicon atoms (B-2), and a step of forming at least one photoresist layer on the intermediate layer film (B-3) After the step (B-3), irradiating a predetermined area of the photoresist layer with radiation and developing to form a resist pattern (B-4); Thereafter, the intermediate layer film is etched using the resist pattern as a mask, the lower layer film is etched using the obtained intermediate layer film pattern as an etching mask, and the substrate is etched using the obtained lower layer film pattern as an etching mask. Having a step (B-5) to form a pattern on the substrate by.
- the method of forming the lower layer film for lithography of the present embodiment is not particularly limited as long as it is formed from the composition for forming a film for lithography of the present embodiment, and a known method can be applied.
- a known method can be applied.
- an underlayer film can be formed.
- the baking temperature is not particularly limited, but is preferably in the range of 80 to 450 ° C., and more preferably 200 to 400 ° C.
- the baking time is not particularly limited, but is preferably in the range of 10 to 300 seconds.
- the thickness of the lower layer film can be appropriately selected according to the required performance, and is not particularly limited, but is usually preferably 30 to 20,000 nm, more preferably 50 to 15,000 nm, More preferably, it is 50 to 1000 nm.
- a silicon-containing resist layer is formed thereon in the case of a two-layer process, or a single-layer resist made of a normal hydrocarbon, and a silicon-containing intermediate layer is formed thereon in the case of a three-layer process. It is preferable to form a single-layer resist layer containing no silicon thereon. In this case, a known photoresist material for forming the resist layer can be used.
- a silicon-containing resist material for a two-layer process from the viewpoint of oxygen gas etching resistance, a silicon atom-containing polymer such as a polysilsesquioxane derivative or a vinylsilane derivative is used as a base polymer, and further, an organic solvent, an acid generator, If necessary, a positive photoresist material containing a basic compound or the like is preferably used.
- the silicon atom-containing polymer a known polymer used in this type of resist material can be used.
- a polysilsesquioxane-based intermediate layer is preferably used as the silicon-containing intermediate layer for the three-layer process.
- the intermediate layer By giving the intermediate layer an effect as an antireflection film, there is a tendency that reflection can be effectively suppressed.
- the k value tends to be high and the substrate reflection tends to be high. Thereby, substrate reflection can be reduced to 0.5% or less.
- the intermediate layer having such an antireflection effect is not limited to the following, but for exposure at 193 nm, an acid or heat-crosslinked polysilsesquioxe into which a phenyl group or a light-absorbing group having a silicon-silicon bond is introduced. Sun is preferably used.
- an intermediate layer formed by a Chemical Vapor Deposition (CVD) method can be used.
- An intermediate layer having a high effect as an antireflection film manufactured by the CVD method is not limited to the following, but, for example, an SiON film is known.
- formation of an intermediate layer by a wet process such as spin coating or screen printing has a simpler and more cost-effective merit than a CVD method.
- the upper resist in the three-layer process may be either a positive type or a negative type, and the same resist as a commonly used single-layer resist can be used.
- the lower layer film of the present embodiment can be used as an antireflection film for a normal single-layer resist or as a base material for suppressing pattern collapse. Since the lower layer film of the present embodiment has excellent etching resistance for underlying processing, it can also be expected to function as a hard mask for underlying processing.
- a wet process such as spin coating or screen printing is preferably used, as in the case of forming the lower layer film.
- prebaking is usually performed.
- the prebaking is performed at 80 to 180 ° C. for 10 to 300 seconds.
- exposure is performed, post-exposure bake (PEB), and development are performed according to a conventional method to obtain a resist pattern.
- the thickness of the resist film is not particularly limited, but is generally preferably from 30 to 500 nm, more preferably from 50 to 400 nm.
- the exposure light may be appropriately selected and used depending on the photoresist material used. Generally, high energy rays having a wavelength of 300 nm or less, specifically, excimer lasers of 248 nm, 193 nm, and 157 nm, soft X-rays of 3 to 20 nm, electron beams, X-rays, and the like can be given.
- the resist pattern formed by the above-described method has the pattern collapse suppressed by the lower layer film of the present embodiment. Therefore, by using the lower layer film of the present embodiment, a finer pattern can be obtained, and the exposure amount necessary to obtain the resist pattern can be reduced.
- gas etching is preferably used.
- gas etching etching using oxygen gas is preferable.
- an inert gas such as He or Ar, or CO, CO 2 , NH 3 , SO 2 , N 2 , NO 2 , or H 2 gas can be added.
- gas etching can be performed only with CO, CO 2 , NH 3 , N 2 , NO 2 and H 2 gas without using oxygen gas.
- the latter gas is preferably used for protecting the side wall of the pattern to prevent undercut of the side wall.
- gas etching is also preferably used in the etching of the intermediate layer in the three-layer process.
- the gas etching the same gas etching as that described in the above-described two-layer process can be applied.
- the processing of the intermediate layer in the three-layer process is preferably performed using a fluorocarbon-based gas and a resist pattern as a mask.
- the lower layer film can be processed by performing, for example, oxygen gas etching using the intermediate layer pattern as a mask.
- a silicon oxide film, a silicon nitride film, and a silicon oxynitride film are formed by a CVD method, an ALD method, or the like.
- the method for forming the nitride film is not limited to the following.
- a method described in JP-A-2002-334869 (Patent Document 6) and WO 2004/066377 (Patent Document 7) can be used.
- a photoresist film can be formed directly on such an intermediate layer film, an organic anti-reflection film (BARC) is formed on the intermediate layer film by spin coating, and a photoresist film is formed thereon. May be.
- a polysilsesquioxane-based intermediate layer is also preferably used as the intermediate layer.
- the resist intermediate layer film By giving the resist intermediate layer film an effect as an antireflection film, there is a tendency that reflection can be effectively suppressed.
- Specific materials for the polysilsesquioxane-based intermediate layer are not limited to the following, but are described in, for example, JP-A-2007-226170 (Patent Document 8) and JP-A-2007-226204 (Patent Document 9). What was done can be used.
- the etching of the next substrate can also be performed by a conventional method.
- etching is mainly performed with a chlorofluorocarbon-based gas
- p-Si, Al or W a chlorine-based or bromine-based is used.
- Etching mainly using gas can be performed.
- the silicon-containing resist layer or the silicon-containing intermediate layer is separated separately, and generally, dry etching separation with a chlorofluorocarbon-based gas is performed after processing the substrate. .
- the lower layer film of the present embodiment is characterized in that these substrates have excellent etching resistance.
- a known substrate can be appropriately selected and used, and is not particularly limited. Examples of the substrate include Si, ⁇ -Si, p-Si, SiO 2 , SiN, SiON, W, TiN, and Al. .
- the substrate may be a laminate having a film to be processed (substrate to be processed) on a substrate (support).
- various Low-k films such as Si, SiO 2 , SiON, SiN, p-Si, ⁇ -Si, W, W-Si, Al, Cu, and Al-Si, and a stopper film thereof.
- a material different from the base material (support) is used.
- the thickness of the substrate to be processed or the film to be processed is not particularly limited, but is usually preferably about 50 to 1,000,000 nm, and more preferably 75 to 500,000 nm.
- the molecular weight of the synthesized compound was measured by LC (GPC) -MS analysis using Acquity UPLC / MALDI-Synapt HDMS manufactured by Water.
- thermogravimetric loss at 400 ° C. is less than 10%
- thermogravimetric loss at 400 ° C. is 10% to 25%
- Thermal weight loss at 400 ° C. exceeds 25%
- reaction solution 60R, manufactured by WANHUA CHEMICAL GROUP CO., LTD.
- 10.0 g of a solution of 30 g of dimethylformamide and 30 g of p-xylene were added to prepare a reaction solution.
- 3.0 g of p-toluenesulfonic acid monohydrate was added, and the mixture was stirred at 140 ° C. for 6 hours to carry out a reaction. Collected in a Stark trap.
- the reaction solution was cooled to 40 ° C., and then dropped into a beaker containing 300 ml of distilled water to precipitate a product.
- a target resin represented by the following formula. 8.20 g were obtained.
- the obtained resin was measured for polystyrene-equivalent molecular weight by the above method, and as a result, was 1416.
- Example 1 As a biscitraconimide compound, 10 parts by mass of citraconimide A was used alone to prepare a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B), and the obtained lithography film-forming material was evaluated to have sufficient solubility.
- thermogravimetric measurement was similarly performed by changing citraconic imide A to citraconic imide B, citraconic imide C, and citraconic imide D.
- the thermal weight loss at 400 ° C. of the obtained lithographic film forming material was 10%.
- evaluation A the thermal weight loss at 400 ° C. of the obtained lithographic film forming material was 10%.
- evaluation B the solubility in PGMEA
- citraconic imide B and citraconic imide C were 5% by mass or more and less than 10% by mass (evaluation B)
- citraconic imide D was 20% by mass or more (evaluation S). It was very excellent, and the obtained film forming material for lithography was evaluated as having sufficient solubility.
- Example 5 10 parts by mass of citraconic imide A and 0.1 parts by mass of 2,4,5-triphenylimidazole (TPIZ) as a crosslinking accelerator were used as a film forming material for lithography.
- TPIZ 2,4,5-triphenylimidazole
- thermogravimetry the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated.
- the result was 5% by mass or more and less than 10% by mass (evaluation B), and the obtained lithography film-forming material was evaluated to have sufficient solubility.
- Example 6 10 parts by mass of citraconic imide A was used. Further, 0.1 part by mass of triphenylphosphine (TPP) was blended as a crosslinking accelerator to obtain a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B). The obtained lithography film-forming material was evaluated to have excellent solubility. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- TPP triphenylphosphine
- Example 7 10 parts by mass of citraconic imide A was used. Further, as a cross-linking agent, 2 parts by mass of benzoxazine (BF-BXZ; manufactured by Konishi Chemical Industry Co., Ltd.) represented by the following formula is used, and 2,4,5-triphenylimidazole (TPIZ) is used as a cross-linking accelerator. 0.1 part by mass was blended to obtain a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated.
- BF-BXZ benzoxazine
- TPIZ 2,4,5-triphenylimidazole
- the result was 5% by mass or more and less than 10% by mass (evaluation B).
- the obtained lithography film-forming material was evaluated to have excellent solubility.
- 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- Example 8 10 parts by mass of citraconic imide A was used.
- a crosslinking agent 2 parts by mass of a biphenylaralkyl-type epoxy resin (NC-3000-L; manufactured by Nippon Kayaku Co., Ltd.) represented by the following formula is used, and 0.1 part by mass of TPIZ is compounded as a crosslinking accelerator.
- TPIZ 0.1 part by mass of TPIZ is compounded as a crosslinking accelerator.
- a film forming material for lithography was obtained.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B).
- the obtained lithography film-forming material was evaluated to have excellent solubility.
- 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- Example 9 10 parts by mass of citraconic imide A was used. Further, 2 parts by mass of diallyl bisphenol A type cyanate (DABPA-CN; manufactured by Mitsubishi Gas Chemical) represented by the following formula is used as a crosslinking agent, and 2,4,5-triphenylimidazole (TPIZ) is used as a crosslinking accelerator. was blended in an amount of 0.1 part by mass to obtain a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- DABPA-CN diallyl bisphenol A type cyanate
- TPIZ 2,4,5-triphenylimidazole
- the solubility in PGMEA was evaluated to be 10% by mass or more and less than 20% by mass (evaluation A), and the obtained film-forming material for lithography was evaluated to have excellent solubility.
- 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- Example 10 10 parts by mass of citraconic imide A was used. Further, as a cross-linking agent, 2 parts by mass of diallyl bisphenol A (BPA-CA; manufactured by Konishi Chemical) represented by the following formula was used, and 2,4,5-triphenylimidazole (TPIZ) was used as a cross-linking accelerator. One part by mass was blended to obtain a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B).
- BPA-CA diallyl bisphenol A
- TPIZ 2,4,5-triphenylimidazole
- the obtained lithography film-forming material was evaluated to have excellent solubility.
- 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- Example 11 10 parts by mass of citraconic imide A, 2 parts by mass of benzoxazine BF-BXZ represented by the above formula as a cross-linking agent, and 0.1 part by mass of TPIZ as a cross-linking accelerator are blended to form a film for lithography.
- Material As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B). The obtained lithography film-forming material was evaluated to have excellent solubility.
- Example 12 10 parts by mass of citraconic imide A and 2 parts by mass of benzoxazine BF-BXZ represented by the above formula as a crosslinking agent, and an acid generator ditertiarybutyldiphenyliodonium nonafluoromethanesulfonate for promoting crosslinking.
- 0.1 parts by mass of DTDPI manufactured by Midori Kagaku Co., Ltd.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated.
- the result was 5% by mass or more and less than 10% by mass (evaluation B).
- the obtained lithography film-forming material was evaluated to have excellent solubility.
- 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the biscitraconimide compound, and the mixture was stirred at room temperature for at least 3 hours with a stirrer to prepare a composition for film formation for lithography.
- Example 13 10 parts by mass of citraconic imide A was used.
- As a crosslinking agent 2 parts by mass of a diphenylmethane-type allylphenol resin (APG-1; manufactured by Gunei Chemical Industry) represented by the following formula was used as a film forming material for lithography.
- APG-1 diphenylmethane-type allylphenol resin
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated.
- the result was 5% by mass or more and less than 10% by mass (evaluation B).
- the obtained lithography film-forming material was evaluated to have excellent solubility.
- Example 14 10 parts by mass of citraconic imide A was used. Further, as a cross-linking agent, 2 parts by mass of a diphenylmethane-type propenylphenol resin (APG-2; manufactured by Gunei Chemical Industry) represented by the following formula was used as a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B). The obtained lithography film-forming material was evaluated to have excellent solubility.
- APG-2 diphenylmethane-type propenylphenol resin
- Example 15 10 parts by mass of citraconic imide A was used. Further, as a cross-linking agent, 2 parts by mass of 4,4'-diaminodiphenylmethane (DDM; manufactured by Tokyo Chemical Industry) represented by the following formula was used as a film forming material for lithography. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B). The obtained lithography film-forming material was evaluated to have excellent solubility. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the citraconic imide compound, and the mixture was stirred with a stirrer at room temperature for at least 3 hours to prepare a composition for film formation for lithography.
- DDM 4,4'-diaminodiphenylmethane
- thermogravimetry Using 20 parts by mass of citraconimide A alone, a film forming material for lithography was used. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B), and the obtained lithography film-forming material was evaluated as having necessary solubility.
- Example 17 A film forming material for lithography was used in the same manner as in Example 5 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 18 A film forming material for lithography was used in the same manner as in Example 6, except that citraconic imide D was used instead of citraconic imide A. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 19 A film forming material for lithography was used in the same manner as in Example 7, except that citraconic imide D was used instead of citraconic imide A. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 20 A film forming material for lithography was used in the same manner as in Example 8, except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 21 A film forming material for lithography was used in the same manner as in Example 9 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 22 A film forming material for lithography was used in the same manner as in Example 10 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 23 A film forming material for lithography was used in the same manner as in Example 11, except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 24 A film forming material for lithography was used in the same manner as in Example 12 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 25 A film forming material for lithography was used in the same manner as in Example 13 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 26 A film forming material for lithography was used in the same manner as in Example 14 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 27 A film forming material for lithography was used in the same manner as in Example 15 except that citraconic imide D was used instead of citraconic imide A.
- thermogravimetry the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 28 A film forming material for lithography was used in the same manner as in Example 16 except that citraconic imide D was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 29> A film forming material for lithography was used in the same manner as in Example 1 except that citraconic imide E was used instead of citraconic imide A. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 30 A film forming material for lithography was used in the same manner as in Example 1 except that citraconic imide F was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 31 A film forming material for lithography was used in the same manner as in Example 5 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 32 A film forming material for lithography was used in the same manner as in Example 6, except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 33 A film forming material for lithography was used in the same manner as in Example 7, except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 34 A film forming material for lithography was used in the same manner as in Example 8, except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 35 A film forming material for lithography was used in the same manner as in Example 9 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 36 A film forming material for lithography was used in the same manner as in Example 10 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 37 A film forming material for lithography was used in the same manner as in Example 11 except that citraconimide E was used instead of citraconimide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 38 A film forming material for lithography was used in the same manner as in Example 12 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 39 A film forming material for lithography was used in the same manner as in Example 13 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 40> A film forming material for lithography was used in the same manner as in Example 14 except that citraconic imide E was used instead of citraconic imide A. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 41 A film forming material for lithography was used in the same manner as in Example 15 except that citraconic imide E was used instead of citraconic imide A.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- Example 42 10 parts by mass of citraconic imide A and 0.1 part by mass of IRGACURE 184 (manufactured by BASF) represented by the following formula as a photoradical polymerization initiator were blended to obtain a film forming material for lithography. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the biscitraconimide compound, and the mixture was stirred at room temperature for at least 3 hours with a stirrer to prepare a composition for film formation for lithography.
- Example 43 10 parts by mass of citraconimide D and 0.1 part by mass of IRGACURE 184 (manufactured by BASF) as a photoradical polymerization initiator were used as a film forming material for lithography. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the biscitraconimide compound, and the mixture was stirred at room temperature for at least 3 hours with a stirrer to prepare a composition for film formation for lithography.
- Example 44 10 parts by mass of citraconic imide E and 0.1 part by mass of IRGACURE 184 (manufactured by BASF) as a photoradical polymerization initiator were blended to obtain a film forming material for lithography. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the biscitraconimide compound, and the mixture was stirred at room temperature for at least 3 hours with a stirrer to prepare a composition for film formation for lithography.
- Example 45 10 parts by mass of citraconic imide F and 0.1 part by mass of IRGACURE 184 (manufactured by BASF) as a photoradical polymerization initiator were blended to obtain a film forming material for lithography. 90 parts by mass of PGMEA as a solvent was added to 10 parts by mass of the biscitraconimide compound, and the mixture was stirred at room temperature for at least 3 hours with a stirrer to prepare a composition for film formation for lithography.
- ethylbenzene (reagent grade, manufactured by Wako Pure Chemical Industries, Ltd.) was added to the reaction solution as a diluting solvent, and after standing, the lower aqueous phase was removed. Further, neutralization and washing were performed, and ethylbenzene and unreacted 1,5-dimethylnaphthalene were distilled off under reduced pressure to obtain 1.25 kg of a light brown solid dimethylnaphthalene formaldehyde resin.
- the molecular weight of the obtained dimethylnaphthalene formaldehyde resin was a number average molecular weight (Mn): 562, a weight average molecular weight (Mw): 1168, and a degree of dispersion (Mw / Mn): 2.08.
- a 0.5-L four-necked flask equipped with a Dimroth condenser, a thermometer, and a stirring blade was prepared.
- 100 g (0.51 mol) of the dimethylnaphthalene formaldehyde resin obtained above and 0.05 g of paratoluenesulfonic acid were charged into the four-necked flask and heated to 190 ° C. After heating for an hour, the mixture was stirred. Thereafter, 52.0 g (0.36 mol) of 1-naphthol was further added, and the mixture was further heated to 220 ° C. and reacted for 2 hours.
- a modified resin (CR-1) had Mn: 885, Mw: 2220, and Mw / Mn: 4.17.
- TG thermogravimetry
- the amount of thermogravimetric loss at 400 ° C. of the obtained resin was more than 25% (evaluation C). Therefore, it was evaluated that application to high-temperature baking was difficult.
- solubility in PGMEA it was 10 mass% or more (evaluation A), and it was evaluated that it had excellent solubility.
- a phenol compound (BisN-1) represented by the following formula described in International Publication 2013/024779 As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated. The result was 5% by mass or more and less than 10% by mass (evaluation B), and the obtained lithography film-forming material was evaluated as having necessary solubility.
- Example 47 To a phenol compound (BisN-1) represented by the above formula, 2 parts by mass of citraconimide D as a biscitraconimide compound was added to 8 parts by mass to obtain a lithography film forming material. As a result of the thermogravimetry, the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A). The solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- the thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 20% by mass or more (evaluation S), and the obtained lithography film-forming material was evaluated to have necessary solubility.
- thermogravimetric loss at 400 ° C. of the obtained film forming material for lithography was less than 10% (evaluation A).
- the solubility in PGMEA was evaluated to be 10% by mass or more and less than 20% by mass (evaluation A), and the obtained lithographic film-forming material was evaluated to have necessary solubility.
- Examples 1 to 41, Comparative Examples 1 and 2 Using the lithographic film-forming materials obtained in Examples 1 to 41, the lithographic film-forming compositions corresponding to Examples 1 to 41 and Comparative Examples 1 and 2 so that the compositions shown in Table 1 were obtained. Was prepared respectively. Next, the compositions for forming a film for lithography of Examples 1 to 41 and Comparative Examples 1 and 2 were spin-coated on a silicon substrate, and then baked at 240 ° C. for 60 seconds and further at 400 ° C. for 120 seconds to form a film. Each lower layer film of 200 nm was produced. A film thickness reduction rate (%) was calculated from the difference in film thickness before and after baking at 400 ° C., and the film heat resistance of each lower layer film was evaluated. Then, the etching resistance was evaluated under the following conditions. Further, under the following conditions, the embedding property into the stepped substrate and the flatness were evaluated.
- Examples 42 to 45 Lithographic film forming compositions corresponding to Examples 42 to 45 were each prepared so as to have the composition shown in Table 2.
- the composition for forming a film for lithography of Examples 42 to 45 was spin-coated on a silicon substrate, and then baked at 110 ° C. for 60 seconds to remove the solvent of the coating film.
- the composition was cured at an amount of 600 mJ / cm 2 and an irradiation time of 20 seconds, and baked at 400 ° C. for 120 seconds, thereby producing each lower layer film having a thickness of 200 nm.
- a film thickness reduction rate (%) was calculated from the difference in film thickness before and after baking at 400 ° C., and the film heat resistance of each lower layer film was evaluated.
- the etching resistance was evaluated under the following conditions. Further, under the following conditions, the embedding property into the stepped substrate and the flatness were evaluated.
- compositions for forming a film for lithography corresponding to Examples 46 to 49 and Reference Example 1 were prepared so as to have the compositions shown in Table 3. Then, the composition for forming a film for lithography of Examples 46 to 49 and Reference Example 1 was spin-coated on a silicon substrate, baked at 110 ° C. for 60 seconds to remove the solvent of the coating, and then subjected to a high-pressure mercury lamp. To cure at an integrated exposure dose of 600 mJ / cm 2 and an irradiation time of 20 seconds, and further baked at 400 ° C. for 120 seconds. Each lower layer film having a thickness of 200 nm was produced.
- a film thickness reduction rate (%) was calculated from the difference in film thickness before and after baking at 400 ° C., and the film heat resistance of each lower layer film was evaluated. Then, the etching resistance was evaluated under the following conditions. Further, under the following conditions, the embedding property into the stepped substrate and the flatness were evaluated.
- the etching resistance was evaluated according to the following evaluation criteria. From the practical viewpoint, the following S evaluation is particularly preferable, and the A evaluation and the B evaluation are preferable.
- S evaluation is particularly preferable, and the A evaluation and the B evaluation are preferable.
- the above-mentioned composition for forming a film is formed on a SiO 2 step substrate in which a trench (aspect ratio: 1.5) having a width of 100 nm, a pitch of 150 nm, and a depth of 150 nm (aspect ratio: 1.5) and a trench (open space) having a width of 5 ⁇ m and a depth of 180 nm are mixed. Objects were applied respectively. Thereafter, baking was performed at 240 ° C. for 120 seconds in an air atmosphere to form a resist underlayer film having a thickness of 200 nm.
- Example 50 The composition for forming a film for lithography in Example 5 was coated on a SiO 2 substrate having a thickness of 300 nm and baked at 240 ° C. for 60 seconds and further at 400 ° C. for 120 seconds to form a lower layer film having a thickness of 70 nm. did. A resist solution for ArF was applied on the lower layer film and baked at 130 ° C. for 60 seconds to form a photoresist layer having a thickness of 140 nm.
- the resist solution for ArF is prepared by mixing 5 parts by mass of the compound of the following formula (22), 1 part by mass of triphenylsulfonium nonafluoromethanesulfonate, 2 parts by mass of tributylamine, and 92 parts by mass of PGMEA. What was used was used.
- the compound of the following formula (22) was prepared as follows. That is, 4.15 g of 2-methyl-2-methacryloyloxyadamantane, 3.00 g of methacryloyloxy- ⁇ -butyrolactone, 2.08 g of 3-hydroxy-1-adamantyl methacrylate, 0.38 g of azobisisobutyronitrile were added to tetrahydrofuran.
- the reaction solution was dissolved in 80 mL. This reaction solution was polymerized under a nitrogen atmosphere at a reaction temperature of 63 ° C. for 22 hours, and then the reaction solution was dropped into 400 mL of n-hexane. The resulting resin thus obtained was coagulated and purified, and the resulting white powder was filtered and dried under reduced pressure at 40 ° C. overnight to obtain a compound represented by the following formula.
- the photoresist layer was exposed to light using an electron beam lithography apparatus (manufactured by Elionix; ELS-7500, 50 keV), baked at 115 ° C. for 90 seconds (PEB), and then subjected to 2.38% by mass of tetramethylammonium hydroxide (PEB).
- ELS-7500 electron beam lithography apparatus
- PEB baked at 115 ° C. for 90 seconds
- PEB tetramethylammonium hydroxide
- TMAH tetramethylammonium hydroxide
- Example 51 A positive resist pattern was obtained in the same manner as in Example 50 except that the composition for forming a lower layer film for lithography in Example 6 was used instead of the composition for forming a lower layer film for lithography in Example 5 described above. . Table 4 shows the evaluation results.
- Example 52> A positive resist pattern was obtained in the same manner as in Example 50 except that the composition for forming a lower layer film for lithography in Example 7 was used instead of the composition for forming a lower layer film for lithography in Example 5 described above. . Table 4 shows the evaluation results.
- Example 53 A positive resist pattern was obtained in the same manner as in Example 50 except that the composition for forming a lower layer film for lithography in Example 8 was used instead of the composition for forming a lower layer film for lithography in Example 5. .
- Table 4 shows the evaluation results.
- Examples 54 to 57 The compositions for forming a film for lithography in Examples 16 and 28 to 30 were applied on a 300 nm-thick SiO 2 substrate and baked at 240 ° C. for 60 seconds and further at 400 ° C. for 120 seconds to obtain a film thickness. A lower layer film of 70 nm was formed. Thereafter, the film surface was observed with an optical microscope to confirm the presence or absence of a defect. Table 5 shows the evaluation results.
- Examples 54 to 57 using the film forming composition for lithography of the present embodiment including the biscitraconimide compound showed a comparison with Comparative Examples 4 and 5 including the bismaleimide compound. It was confirmed that a film with reduced defects was obtained. Although the cause is not clear, the biscitraconimide compound has higher solubility stability in a solvent than the bismaleimide compound, and / or self-reaction between the compounds is hard to occur, and it is difficult to generate minute particles that cause defects. It is estimated that.
- the film forming material for lithography of the present embodiment has relatively high heat resistance and relatively high solvent solubility, has excellent embedding characteristics in a stepped substrate and excellent flatness of a film, and is applicable to a wet process. Therefore, the composition for forming a film for lithography containing the material for forming a film for lithography can be widely and effectively used in various applications requiring these properties. In particular, the present invention can be effectively used particularly in the field of an underlayer film for lithography and an underlayer film for a multilayer resist.
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- General Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Architecture (AREA)
- Structural Engineering (AREA)
- Materials Engineering (AREA)
- Manufacturing & Machinery (AREA)
- Computer Hardware Design (AREA)
- Microelectronics & Electronic Packaging (AREA)
- Power Engineering (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Materials For Photolithography (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Polymerisation Methods In General (AREA)
Abstract
本発明は、湿式プロセスが適用可能であり、耐熱性、エッチング耐性、段差基板への埋め込み特性及び膜の平坦性に優れるフォトレジスト下層膜を形成するために有用な、リソグラフィー用膜形成材料等を提供することを課題とする。前記課題は、下記式(0)の基: を有する化合物を含有する、リソグラフィー用膜形成材料によって解決することができる。
Description
本発明は、リソグラフィー用膜形成材料、該材料を含有するリソグラフィー用膜形成用組成物、該組成物を用いて形成されるリソグラフィー用下層膜及び該組成物を用いるパターン形成方法(例えば、レジストパターン方法又は回路パターン方法)に関する。
半導体デバイスの製造において、フォトレジスト材料を用いたリソグラフィーによる微細加工が行われている。近年、LSIの高集積化と高速度化に伴い、パターンルールによる更なる微細化が求められている。そして、現在汎用技術として用いられている光露光を用いたリソグラフィーにおいては、光源の波長に由来する本質的な解像度の限界に近づきつつある。
レジストパターン形成の際に使用するリソグラフィー用の光源は、KrFエキシマレーザー(248nm)からArFエキシマレーザー(193nm)へと短波長化されている。しかしながら、レジストパターンの微細化が進むと、解像度の問題若しくは現像後にレジストパターンが倒れるといった問題が生じてくるため、レジストの薄膜化が望まれるようになる。ところが、単にレジストの薄膜化を行うと、基板加工に十分なレジストパターンの膜厚を得ることが難しくなる。そのため、レジストパターンだけではなく、レジストと加工する半導体基板との間にレジスト下層膜を作製し、このレジスト下層膜にも基板加工時のマスクとしての機能を持たせるプロセスが必要になってきた。
現在、このようなプロセス用のレジスト下層膜として、種々のものが知られている。例えば、従来のエッチング速度の速いレジスト下層膜とは異なり、レジストに近いドライエッチング速度の選択比を持つリソグラフィー用レジスト下層膜を実現するものとして、所定のエネルギーが印加されることにより末端基が脱離してスルホン酸残基を生じる置換基を少なくとも有する樹脂成分と溶媒とを含有する多層レジストプロセス用下層膜形成材料が提案されている(特許文献1参照。)。また、レジストに比べて小さいドライエッチング速度の選択比を持つリソグラフィー用レジスト下層膜を実現するものとして、特定の繰り返し単位を有する重合体を含むレジスト下層膜材料が提案されている(特許文献2参照。)。さらに、半導体基板に比べて小さいドライエッチング速度の選択比を持つリソグラフィー用レジスト下層膜を実現するものとして、アセナフチレン類の繰り返し単位と、置換又は非置換のヒドロキシ基を有する繰り返し単位とを共重合してなる重合体を含むレジスト下層膜材料が提案されている(特許文献3参照。)。
一方、この種のレジスト下層膜において高いエッチング耐性を持つ材料としては、メタンガス、エタンガス、アセチレンガス等を原料に用いたCVDによって形成されたアモルファスカーボン下層膜がよく知られている。
また、本発明者らは、光学特性及びエッチング耐性に優れるとともに、溶媒に可溶で湿式プロセスが適用可能な材料として、特定の構成単位を含むナフタレンホルムアルデヒド重合体及び有機溶媒を含有するリソグラフィー用下層膜形成組成物(特許文献4及び5参照。)を提案している。
なお、3層プロセスにおけるレジスト下層膜の形成において用いられる中間層の形成方法に関しては、例えば、シリコン窒化膜の形成方法(特許文献6参照。)や、シリコン窒化膜のCVD形成方法(特許文献7参照。)が知られている。また、3層プロセス用の中間層材料としては、シルセスキオキサンベースの珪素化合物を含む材料が知られている(特許文献8及び9参照。)。
上述したように、従来数多くのリソグラフィー用膜形成材料が提案されているが、スピンコート法やスクリーン印刷等の湿式プロセスが適用可能な高い溶媒溶解性を有するのみならず、耐熱性、エッチング耐性、段差基板への埋め込み特性及び膜の平坦性を高い次元で両立させたものはなく、新たな材料の開発が求められている。
本発明は、上述の課題を鑑みてなされたものであり、その目的は、湿式プロセスが適用可能であり、耐熱性、エッチング耐性、段差基板への埋め込み特性及び膜の平坦性に優れるフォトレジスト下層膜を形成するために有用な、リソグラフィー用膜形成材料、該材料を含有するリソグラフィー用膜形成用組成物、並びに、該組成物を用いたリソグラフィー用下層膜及びパターン形成方法を提供することにある。
本発明者らは、前記課題を解決するために鋭意検討を重ねた結果、特定構造を有する化合物を用いることにより、前記課題を解決できることを見出し、本発明を完成するに到った。すなわち、本発明は次のとおりである。
[1]
下記式(0)の基:
を有する化合物を含有する、リソグラフィー用膜形成材料。
[2]
前記式(0)の基を有する化合物が、ポリシトラコンイミド化合物及びシトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、[1]に記載のリソグラフィー用膜形成材料。
[3]
前記式(0)の基を有する化合物が、ビスシトラコンイミド化合物及び付加重合型シトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、前記[1]又は[2]に記載のリソグラフィー用膜形成材料。
[4]
前記ビスシトラコンイミド化合物が下記式(1)で表される、前記[3]に記載のリソグラフィー用膜形成材料。
(式(1)中、Zはヘテロ原子を含んでいてもよい炭素数1~100の2価の炭化水素基である。)
[5A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]又は[4]に記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、又はヘテロ原子を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。)
[5B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[5A]のいずれかに記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aはヘテロ原子を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[5B]のいずれかに記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n-、-CH2C(CH3)2CH2-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
Yは単結合、-O-、-CH2-、-C(CH3)2-、-C(CF3)2-、
であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。)
[6B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6A]のいずれかに記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは-(CH2)n-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
Yは単結合、-O-、-CH2-、-C(CH3)2-、-C(CF3)2-、
であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。)
[6-1A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6B]のいずれかに記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n1-、-CH2C(CH3)2CH2-、-(O(CH2)n2)n3-、又は以下の構造であり、
n1は1~10の整数であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6-1B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6-1A]のいずれかに記載のリソグラフィー用膜形成材料。
(式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは-(CH2)n1-、-(O(CH2)n2)n3-、又は以下の構造であり、
n1は1~10の整数であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6-2]
Xが単結合であり、
Aが-(CH2)n1-であり、
n1が1~10の整数であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-3]
n1が1~6の整数である、前記[6-2]に記載のリソグラフィー用膜形成材料。
[6-4]
n1が1~3の整数である、前記[6-2]に記載のリソグラフィー用膜形成材料。
[6-5]
Xがそれぞれ独立に、-CO-又は-COO-であり、
Aが-(O(CH2)n2)n3-であり、
n2が1~4の整数であり、
n3が1~20の整数であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-6]
-X-A-X-が-CO-(O(CH2)n2)n3-COO-である、前記[6-5]に記載のリソグラフィー用膜形成材料。
[6-7]
Xが-O-であり、
Aが以下の構造
であり、
Yが-C(CH3)2-又は-C(CF3)2-であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-8]
Aが以下の構造
である、前記[6-7]に記載のリソグラフィー用膜形成材料。
[6-9]
R1がそれぞれ独立に、炭素数1~6のアルキル基である、前記[5A]~[6-8]のいずれかに記載のリソグラフィー用膜形成材料。
[6-10]
R1がそれぞれ独立に、炭素数1~3のアルキル基である、前記[5A]~[6-8]のいずれかに記載のリソグラフィー用膜形成材料。
[7]
前記付加重合型シトラコンイミド樹脂が下記式(2)又は下記式(3)で表される、前記[3]に記載のリソグラフィー用膜形成材料。
(式(2)中、
R2はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m2はそれぞれ独立に0~3の整数であり、
m2´はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
(式(3)中、
R3及びR4はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m3はそれぞれ独立に0~4の整数であり、
m4はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
[7-1]
R2、又はR3及びR4が、アルキル基である、前記[7]に記載のリソグラフィー用膜形成材料。
[7-2]
ヘテロ原子が酸素、フッ素、及びケイ素からなる群より選ばれる、前記[4]~[7-1]のいずれかに記載のリソグラフィー用膜形成材料。
[7-3]
ヘテロ原子が酸素である、前記[4]~[7-2]のいずれかに記載のリソグラフィー用膜形成材料。
[8]
架橋剤をさらに含有する、前記[1]~[7-3]のいずれかに記載のリソグラフィー用膜形成材料。
[9]
前記架橋剤が、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物及びアジド化合物からなる群より選ばれる少なくとも1種である、前記[8]に記載のリソグラフィー用膜形成材料。
[10]
前記架橋剤が、少なくとも1つのアリル基を有する、前記[8]又は[9]に記載のリソグラフィー用膜形成材料。
[11]
前記架橋剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~100質量部である、前記[8]~[10]のいずれかに記載のリソグラフィー用膜形成材料。
[12]
架橋促進剤をさらに含有する、前記[1]~[11]のいずれかに記載のリソグラフィー用膜形成材料。
[13]
前記架橋促進剤が、アミン類、イミダゾール類、有機ホスフィン類、及びルイス酸からなる群より選ばれる少なくとも1種である、前記[12]に記載のリソグラフィー用膜形成材料。
[14]
前記架橋促進剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~5質量部である、前記[12]又は[13]に記載のリソグラフィー用膜形成材料。
[15]
ラジカル重合開始剤をさらに含有する、前記[1]~[14]のいずれかに記載のリソグラフィー用膜形成材料。
[16]
前記ラジカル重合開始剤が、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種である、前記[15]に記載のリソグラフィー用膜形成材料。
[17]
前記ラジカル重合開始剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.05~25質量部である、前記[15]又は[16]に記載のリソグラフィー用膜形成材料。
[18]
前記[1]~[17]のいずれかに記載のリソグラフィー用膜形成材料と溶媒とを含有する、リソグラフィー用膜形成用組成物。
[19]
酸発生剤をさらに含有する、前記[18]に記載のリソグラフィー用膜形成用組成物。
[20]
リソグラフィー用膜がリソグラフィー用下層膜である、前記[18]又は[19]に記載のリソグラフィー用膜形成用組成物
[21]
前記[20]に記載のリソグラフィー用膜形成用組成物を用いて形成される、リソグラフィー用下層膜。
[22]
基板上に、前記[20]に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、少なくとも1層のフォトレジスト層を形成する工程、及び
該フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程、
を含む、レジストパターン形成方法。
[23]
基板上に、前記[20]に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、珪素原子を含有するレジスト中間層膜材料を用いて中間層膜を形成する工程、
該中間層膜上に、少なくとも1層のフォトレジスト層を形成する工程、
該フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成する工程、
該レジストパターンをマスクとして前記中間層膜をエッチングする工程、
得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングする工程、
得られた下層膜パターンをエッチングマスクとして基板をエッチングすることで基板にパターンを形成する工程、
を含む、回路パターン形成方法。
[24]
前記[1]~[17]のいずれかに記載のリソグラフィー用膜形成材料を、溶媒に溶解させて有機相を得る工程と、
前記有機相と酸性の水溶液とを接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第一抽出工程と、
を含み、
前記有機相を得る工程で用いる溶媒が、水と任意に混和しない溶媒を含む、精製方法。
[25]
前記酸性の水溶液が、鉱酸水溶液又は有機酸水溶液であり、
前記鉱酸水溶液が、塩酸、硫酸、硝酸及びリン酸からなる群より選ばれる1種以上を含み、
前記有機酸水溶液が、酢酸、プロピオン酸、蓚酸、マロン酸、コハク酸、フマル酸、マレイン酸、酒石酸、クエン酸、メタンスルホン酸、フェノールスルホン酸、p-トルエンスルホン酸及びトリフルオロ酢酸からなる群より選ばれる1種以上を含む、前記[24]に記載の精製方法。
[26]
前記水と任意に混和しない溶媒が、トルエン、2-ヘプタノン、シクロヘキサノン、シクロペンタノン、メチルイソブチルケトン、プロピレングリコールモノメチルエーテルアセテート及び酢酸エチルからなる群より選ばれる1種以上の溶媒である、前記[24]又は[25]に記載の精製方法。
[27]
前記第一抽出工程後、前記有機相を、水に接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第二抽出工程をさらに含む、前記[24]~[26]のいずれかに記載の精製方法。
[28]
下記式(2)又は下記式(3)で表される付加重合型シトラコンイミド樹脂。
(式(2)中、
R2はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m2はそれぞれ独立に0~3の整数であり、
m2´はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
(式(3)中、
R3及びR4はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m3はそれぞれ独立に0~4の整数であり、
m4はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
[29]
R2、又はR3及びR4が、アルキル基である、前記[28]に記載の付加重合型シトラコンイミド樹脂。
[30]
ヘテロ原子が酸素、フッ素、及びケイ素からなる群より選ばれる、前記[28]又は[29]に記載の付加重合型シトラコンイミド樹脂。
[31]
ヘテロ原子が酸素である、前記[28]~[30]のいずれかに記載の付加重合型シトラコンイミド樹脂。
[1]
下記式(0)の基:
[2]
前記式(0)の基を有する化合物が、ポリシトラコンイミド化合物及びシトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、[1]に記載のリソグラフィー用膜形成材料。
[3]
前記式(0)の基を有する化合物が、ビスシトラコンイミド化合物及び付加重合型シトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、前記[1]又は[2]に記載のリソグラフィー用膜形成材料。
[4]
前記ビスシトラコンイミド化合物が下記式(1)で表される、前記[3]に記載のリソグラフィー用膜形成材料。
[5A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]又は[4]に記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、又はヘテロ原子を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。)
[5B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[5A]のいずれかに記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aはヘテロ原子を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[5B]のいずれかに記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n-、-CH2C(CH3)2CH2-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。)
[6B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6A]のいずれかに記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは-(CH2)n-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。)
[6-1A]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6B]のいずれかに記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n1-、-CH2C(CH3)2CH2-、-(O(CH2)n2)n3-、又は以下の構造であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6-1B]
前記ビスシトラコンイミド化合物が下記式(1A)で表される、前記[3]~[6-1A]のいずれかに記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは-(CH2)n1-、-(O(CH2)n2)n3-、又は以下の構造であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基であり、
m1はそれぞれ独立に、0~4の整数である。)
[6-2]
Xが単結合であり、
Aが-(CH2)n1-であり、
n1が1~10の整数であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-3]
n1が1~6の整数である、前記[6-2]に記載のリソグラフィー用膜形成材料。
[6-4]
n1が1~3の整数である、前記[6-2]に記載のリソグラフィー用膜形成材料。
[6-5]
Xがそれぞれ独立に、-CO-又は-COO-であり、
Aが-(O(CH2)n2)n3-であり、
n2が1~4の整数であり、
n3が1~20の整数であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-6]
-X-A-X-が-CO-(O(CH2)n2)n3-COO-である、前記[6-5]に記載のリソグラフィー用膜形成材料。
[6-7]
Xが-O-であり、
Aが以下の構造
Yが-C(CH3)2-又は-C(CF3)2-であり、
R1がそれぞれ独立に、アルキル基であり、
m1がそれぞれ独立に、0~4の整数である、
前記[6-1B]に記載のリソグラフィー用膜形成材料。
[6-8]
Aが以下の構造
[6-9]
R1がそれぞれ独立に、炭素数1~6のアルキル基である、前記[5A]~[6-8]のいずれかに記載のリソグラフィー用膜形成材料。
[6-10]
R1がそれぞれ独立に、炭素数1~3のアルキル基である、前記[5A]~[6-8]のいずれかに記載のリソグラフィー用膜形成材料。
[7]
前記付加重合型シトラコンイミド樹脂が下記式(2)又は下記式(3)で表される、前記[3]に記載のリソグラフィー用膜形成材料。
R2はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m2はそれぞれ独立に0~3の整数であり、
m2´はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
R3及びR4はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m3はそれぞれ独立に0~4の整数であり、
m4はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
[7-1]
R2、又はR3及びR4が、アルキル基である、前記[7]に記載のリソグラフィー用膜形成材料。
[7-2]
ヘテロ原子が酸素、フッ素、及びケイ素からなる群より選ばれる、前記[4]~[7-1]のいずれかに記載のリソグラフィー用膜形成材料。
[7-3]
ヘテロ原子が酸素である、前記[4]~[7-2]のいずれかに記載のリソグラフィー用膜形成材料。
[8]
架橋剤をさらに含有する、前記[1]~[7-3]のいずれかに記載のリソグラフィー用膜形成材料。
[9]
前記架橋剤が、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物及びアジド化合物からなる群より選ばれる少なくとも1種である、前記[8]に記載のリソグラフィー用膜形成材料。
[10]
前記架橋剤が、少なくとも1つのアリル基を有する、前記[8]又は[9]に記載のリソグラフィー用膜形成材料。
[11]
前記架橋剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~100質量部である、前記[8]~[10]のいずれかに記載のリソグラフィー用膜形成材料。
[12]
架橋促進剤をさらに含有する、前記[1]~[11]のいずれかに記載のリソグラフィー用膜形成材料。
[13]
前記架橋促進剤が、アミン類、イミダゾール類、有機ホスフィン類、及びルイス酸からなる群より選ばれる少なくとも1種である、前記[12]に記載のリソグラフィー用膜形成材料。
[14]
前記架橋促進剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~5質量部である、前記[12]又は[13]に記載のリソグラフィー用膜形成材料。
[15]
ラジカル重合開始剤をさらに含有する、前記[1]~[14]のいずれかに記載のリソグラフィー用膜形成材料。
[16]
前記ラジカル重合開始剤が、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種である、前記[15]に記載のリソグラフィー用膜形成材料。
[17]
前記ラジカル重合開始剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.05~25質量部である、前記[15]又は[16]に記載のリソグラフィー用膜形成材料。
[18]
前記[1]~[17]のいずれかに記載のリソグラフィー用膜形成材料と溶媒とを含有する、リソグラフィー用膜形成用組成物。
[19]
酸発生剤をさらに含有する、前記[18]に記載のリソグラフィー用膜形成用組成物。
[20]
リソグラフィー用膜がリソグラフィー用下層膜である、前記[18]又は[19]に記載のリソグラフィー用膜形成用組成物
[21]
前記[20]に記載のリソグラフィー用膜形成用組成物を用いて形成される、リソグラフィー用下層膜。
[22]
基板上に、前記[20]に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、少なくとも1層のフォトレジスト層を形成する工程、及び
該フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程、
を含む、レジストパターン形成方法。
[23]
基板上に、前記[20]に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、珪素原子を含有するレジスト中間層膜材料を用いて中間層膜を形成する工程、
該中間層膜上に、少なくとも1層のフォトレジスト層を形成する工程、
該フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成する工程、
該レジストパターンをマスクとして前記中間層膜をエッチングする工程、
得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングする工程、
得られた下層膜パターンをエッチングマスクとして基板をエッチングすることで基板にパターンを形成する工程、
を含む、回路パターン形成方法。
[24]
前記[1]~[17]のいずれかに記載のリソグラフィー用膜形成材料を、溶媒に溶解させて有機相を得る工程と、
前記有機相と酸性の水溶液とを接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第一抽出工程と、
を含み、
前記有機相を得る工程で用いる溶媒が、水と任意に混和しない溶媒を含む、精製方法。
[25]
前記酸性の水溶液が、鉱酸水溶液又は有機酸水溶液であり、
前記鉱酸水溶液が、塩酸、硫酸、硝酸及びリン酸からなる群より選ばれる1種以上を含み、
前記有機酸水溶液が、酢酸、プロピオン酸、蓚酸、マロン酸、コハク酸、フマル酸、マレイン酸、酒石酸、クエン酸、メタンスルホン酸、フェノールスルホン酸、p-トルエンスルホン酸及びトリフルオロ酢酸からなる群より選ばれる1種以上を含む、前記[24]に記載の精製方法。
[26]
前記水と任意に混和しない溶媒が、トルエン、2-ヘプタノン、シクロヘキサノン、シクロペンタノン、メチルイソブチルケトン、プロピレングリコールモノメチルエーテルアセテート及び酢酸エチルからなる群より選ばれる1種以上の溶媒である、前記[24]又は[25]に記載の精製方法。
[27]
前記第一抽出工程後、前記有機相を、水に接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第二抽出工程をさらに含む、前記[24]~[26]のいずれかに記載の精製方法。
[28]
下記式(2)又は下記式(3)で表される付加重合型シトラコンイミド樹脂。
R2はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m2はそれぞれ独立に0~3の整数であり、
m2´はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
R3及びR4はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~10の基であり、
m3はそれぞれ独立に0~4の整数であり、
m4はそれぞれ独立に0~4の整数であり、
nは1~4の整数である。)
[29]
R2、又はR3及びR4が、アルキル基である、前記[28]に記載の付加重合型シトラコンイミド樹脂。
[30]
ヘテロ原子が酸素、フッ素、及びケイ素からなる群より選ばれる、前記[28]又は[29]に記載の付加重合型シトラコンイミド樹脂。
[31]
ヘテロ原子が酸素である、前記[28]~[30]のいずれかに記載の付加重合型シトラコンイミド樹脂。
本発明によれば、湿式プロセスが適用可能であり、耐熱性、エッチング耐性、段差基板への埋め込み特性及び膜の平坦性に優れるフォトレジスト下層膜を形成するために有用な、リソグラフィー用膜形成材料、該材料を含有するリソグラフィー用膜形成用組成物、並びに、該組成物を用いたリソグラフィー用下層膜及びパターン形成方法を提供することができる。
以下、本発明の実施の形態について説明する。なお、以下の実施の形態は、本発明を説明するための例示であり、本発明はその実施の形態のみに限定されない。
[リソグラフィー用膜形成材料]
本発明の実施形態のひとつであるリソグラフィー用膜形成材料は、以下の下記式(0)の基:
を有する化合物(以下、本明細書において「シトラコンイミド化合物」ということがある。)を含有する。シトラコンイミド化合物は、例えば、分子内に1個以上の第1級アミノ基を有する化合物と無水シトラコン酸との脱水閉環反応により得ることができる。シトラコンイミド化合物としては、例えば、ポリシトラコンイミド化合物及びシトラコンイミド樹脂を挙げることができる。
本発明の実施形態のひとつであるリソグラフィー用膜形成材料は、以下の下記式(0)の基:
本実施形態のリソグラフィー用膜形成材料中の、シトラコンイミド化合物の含有量は、0.1~100質量%であることが好ましく、0.5~100質量%であることがより好ましく、1~100質量%であることがさらに好ましい。また、耐熱性及びエッチング耐性の観点からは、51~100質量%であることが好ましく、60~100質量%であることがより好ましく、70~100質量%であることがさらに好ましく、80~100質量%であることが特に好ましい。
本実施形態のシトラコンイミド化合物は、従来の下層膜形成組成物の耐熱性を向上させるために従来の下層膜形成組成物と併用することができる。その場合の下層膜形成組成物中(溶媒を除く)のシトラコンイミド化合物の含有量としては、1~50質量%が好ましく、1~30質量%がより好ましい。
従来の下層膜形成組成物としては、例えば、国際公開2013/024779に記載のものが挙げられるが、これらに制限されることはない。
従来の下層膜形成組成物としては、例えば、国際公開2013/024779に記載のものが挙げられるが、これらに制限されることはない。
本実施形態のリソグラフィー用膜形成材料中の、シトラコンイミド化合物はリソグラフィー用膜形成用の酸発生剤あるいは塩基性化合物としての機能以外を有することを特徴とする。
本実施形態のリソグラフィー用膜形成材料に用いられるポリシトラコンイミド化合物及びシトラコンイミド樹脂としては、原料入手性と量産化に対応した製造の観点からビスシトラコンイミド化合物及び付加重合型シトラコンイミド樹脂が好ましい。
<ビスシトラコンイミド化合物>
ビスシトラコンイミド化合物は、下記式(1)で表される化合物であることが好ましい。
式(1)中、Zはヘテロ原子を含んでいてもよい炭素数1~100の2価の炭化水素基である。炭化水素基の炭素数は、1~80、1~60、1~40、1~20等であってもよい。ヘテロ原子としては、酸素、窒素、硫黄、フッ素、ケイ素等を挙げることができる。
ビスシトラコンイミド化合物は、下記式(1)で表される化合物であることが好ましい。
ビスシトラコンイミド化合物は、下記式(1A)で表される化合物であることがより好ましい。
式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素)を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素)を含んでいてもよい炭素数1~80の2価の炭化水素基であり、
R1はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~30の基であり、
m1はそれぞれ独立に、0~4の整数である。
より好ましくは、耐熱性及びエッチング耐性向上の観点から、式(1A)中、
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n-、-CH2C(CH3)2CH2-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
Yは単結合、-O-、-CH2-、-C(CH3)2-、-C(CF3)2-、
であり、
R1はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n-、-CH2C(CH3)2CH2-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
R1はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~30の基であり、
nは、0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。
Xは、耐熱性の観点から、単結合であることが好ましく、溶解性の観点から、-COO-であることが好ましい。
Yは、耐熱性向上の観点から、単結合であることが好ましい。
R1は、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~20又は0~10の基であることが好ましい。R1は、有機溶媒への溶解性向上の観点から、炭化水素基であることが好ましい。例えば、R1として、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)等が挙げられ、具体的にはメチル基、エチル基等が挙げられる。
m1は、0~2の整数であることが好ましく、原料入手性及び溶解性向上の観点から、1又は2であることがより好ましい。
m2は、2~4の整数であることが好ましい。
nは、0~2の整数であることが好ましく、耐熱性向上の観点から、1~2の整数であることがより好ましい。
Yは、耐熱性向上の観点から、単結合であることが好ましい。
R1は、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~20又は0~10の基であることが好ましい。R1は、有機溶媒への溶解性向上の観点から、炭化水素基であることが好ましい。例えば、R1として、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)等が挙げられ、具体的にはメチル基、エチル基等が挙げられる。
m1は、0~2の整数であることが好ましく、原料入手性及び溶解性向上の観点から、1又は2であることがより好ましい。
m2は、2~4の整数であることが好ましい。
nは、0~2の整数であることが好ましく、耐熱性向上の観点から、1~2の整数であることがより好ましい。
式(1A)で表される化合物の一実施形態としては、
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n1-、-CH2C(CH3)2CH2-、-(O(CH2)n2)n3-、又は以下の構造であり、
n1は1~10の整数であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
Xはそれぞれ独立に、単結合、-O-、-CO-、又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n1-、-CH2C(CH3)2CH2-、-(O(CH2)n2)n3-、又は以下の構造であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
式(1A)で表される化合物の一実施形態としては、
Xは単結合であり、
Aは-(CH2)n1-であり、
n1は1~10の整数であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、n1は1~6又は1~3であることが好ましい。
Xは単結合であり、
Aは-(CH2)n1-であり、
n1は1~10の整数であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、n1は1~6又は1~3であることが好ましい。
式(1A)で表される化合物の一実施形態としては、
Xはそれぞれ独立に、-CO-又は-COO-であり、
Aは-(O(CH2)n2)n3-であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、-X-A-X-は-CO-(O(CH2)n2)n3-COO-であることが好ましい。
Xはそれぞれ独立に、-CO-又は-COO-であり、
Aは-(O(CH2)n2)n3-であり、
n2は1~4の整数であり、
n3は1~20の整数であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、-X-A-X-は-CO-(O(CH2)n2)n3-COO-であることが好ましい。
式(1A)で表される化合物の一実施形態としては、
Xは-O-であり、
Aは以下の構造
であり、
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、Aは以下の構造
であることが好ましい。
Xは-O-であり、
Aは以下の構造
Yは-C(CH3)2-又は-C(CF3)2-であり、
R1はそれぞれ独立に、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)であり、
m1はそれぞれ独立に、0~4の整数である。
ここで、Aは以下の構造
ビスシトラコンイミド化合物は、下記式(1B)で表される化合物であることが好ましい。
式(1B)中、Z1はヘテロ原子を含んでいてもよい炭素数1~100の2価の直鎖状、分岐状、あるいは環状の炭化水素基である。ヘテロ原子としては、酸素、窒素、硫黄、フッ素、ケイ素等を挙げることができる。
前記式(2)中、R2はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~10の基である。また、R2は、有機溶媒への溶解性向上の観点から、炭化水素基であることが好ましい。例えば、R2として、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)等が挙げられ、具体的にはメチル基、エチル基等が挙げられる。
m2はそれぞれ独立に0~3の整数である。また、m2は、0又は1であることが好ましく、原料入手性の観点から、0であることがより好ましい。
m2´はそれぞれ独立に、0~4の整数である。また、m2´は、0又は1であることが好ましく、原料入手性の観点から、0であることがより好ましい。
nは、0~4の整数である。また、nは、1~4又は0~2の整数であることが好ましく、耐熱性向上の観点から、1~2の整数であることがより好ましい。
m2はそれぞれ独立に0~3の整数である。また、m2は、0又は1であることが好ましく、原料入手性の観点から、0であることがより好ましい。
m2´はそれぞれ独立に、0~4の整数である。また、m2´は、0又は1であることが好ましく、原料入手性の観点から、0であることがより好ましい。
nは、0~4の整数である。また、nは、1~4又は0~2の整数であることが好ましく、耐熱性向上の観点から、1~2の整数であることがより好ましい。
前記式(3)中、R3及びR4はそれぞれ独立に、ヘテロ原子(例えば、酸素、窒素、硫黄、フッ素、塩素、臭素、ヨウ素)を含んでいてもよい炭素数0~10の基である。また、R3及びR4は、有機溶媒への溶解性向上の観点から、炭化水素基であることが好ましい。例えば、R3及びR4として、アルキル基(例えば、炭素数1~6又は1~3のアルキル基)等が挙げられ、具体的にはメチル基、エチル基等が挙げられる。
m3はそれぞれ独立に0~4の整数である。また、m3は、0~2の整数であることが好ましく、原料入手性の観点から、0であることがより好ましい。
m4はそれぞれ独立に、0~4の整数である。また、m4は、0~2の整数であることが好ましく、原料入手性の観点から、0であることがより好ましい。
nは、0~4の整数である。また、nは、1~4又は0~2の整数であることが好ましく、原料入手性の観点から、1~2の整数であることがより好ましい。
m3はそれぞれ独立に0~4の整数である。また、m3は、0~2の整数であることが好ましく、原料入手性の観点から、0であることがより好ましい。
m4はそれぞれ独立に、0~4の整数である。また、m4は、0~2の整数であることが好ましく、原料入手性の観点から、0であることがより好ましい。
nは、0~4の整数である。また、nは、1~4又は0~2の整数であることが好ましく、原料入手性の観点から、1~2の整数であることがより好ましい。
本実施形態のリソグラフィー用膜形成材料は、湿式プロセスへの適用が可能である。また、本実施形態のリソグラフィー用膜形成材料は、芳香族構造を有しており、また剛直なシトラコンイミド骨格を有しており、単独でも高温ベークによって、そのシトラコンイミド基が架橋反応を起こし、高い耐熱性を発現する。その結果、高温ベーク時の膜の劣化が抑制され、酸素プラズマエッチング等に対するエッチング耐性に優れた下層膜を形成することができる。さらに、本実施形態のリソグラフィー用膜形成材料は、芳香族構造を有しているにも関わらず、有機溶媒に対する溶解性が高く、安全溶媒に対する溶解性が高い。さらに、後述する本実施形態のリソグラフィー用膜形成用組成物からなるリソグラフィー用下層膜は段差基板への埋め込み特性及び膜の平坦性に優れ、製品品質の安定性が良好であるだけでなく、レジスト層やレジスト中間層膜材料との密着性にも優れるので、優れたレジストパターンを得ることができる。
本実施形態で使用されるビスシトラコンイミド化合物は、具体的には、m-フェニレンビスシトラコンイミド、4-メチル-1,3-フェニレンビスシトラコンイミド、4,4-ジフェニルメタンビスシトラコンイミド、4,4‘-ジフェニルスルホンビスシトラコンイミド、1,3-ビス(3-シトラコンイミドフェノキシ)ベンゼン、1,3-ビス(4-シトラコンイミドフェノキシ)ベンゼン、1,4-ビス(3-シトラコンイミドフェノキシ)ベンゼン、1,4-ビス(4-シトラコンイミドフェノキシ)ベンゼン等のフェニレン骨格含有ビスシトラコンイミド;ビス(3-エチル-5-メチル-4-シトラコンイミドフェニル)メタン、1,1-ビス(3-エチル-5-メチル-4-シトラコンイミドフェニル)エタン、2,2-ビス(3-エチル-5-メチル-4-シトラコンイミドフェニル)プロパン、N,N'-4,4'-[3,3'-ジメチル-ジフェニルメタン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジメチル-1,1-ジフェニルエタン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジメチル-1,1-ジフェニルプロパン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジエチル-ジフェニルメタン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジn-プロピル-ジフェニルメタン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジn-ブチル-ジフェニルメタン]ビスシトラコンイミド等のジフェニルアルカン骨格含有ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジメチル-ビフェニレン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジエチル-ビフェニレン]ビスシトラコンイミド等のビフェニル骨格含有ビスシトラコンイミド、1,6-ヘキサンビスシトラコンイミド、1,6-ビスシトラコンイミド(2,2,4-トリメチル)ヘキサン、1,3-ジメチレンシクロヘキサンビスシトラコンイミド、1,4-ジメチレンシクロヘキサンビスシトラコンイミドなどの脂肪族骨格ビスシトラコンイミド、及び1,3-ビス(3-アミノプロピル)-1,1,2,2-テトラメチルジシロキサン、1,3-ビス(3-アミノブチル)-1,1,2,2-テトラメチルジシロキサン、ビス(4-アミノフェノキシ)ジメチルシラン、1,3-ビス(4-アミノフェノキシ)テトラメチルジシロキサン、1,1,3,3-テトラメチル-1,3-ビス(4-アミノフェニル)ジシロキサン、1,1,3,3-テトラフェノキシ-1,3-ビス(2-アミノエチル)ジシロキサン、1,1,3,3-テトラフェニル-1,3-ビス(2-アミノエチル)ジシロキサン、1,1,3,3-テトラフェニル-1,3-ビス(3-アミノプロピル)ジシロキサン、1,1,3,3-テトラメチル-1,3-ビス(2-アミノエチル)ジシロキサン、1,1,3,3-テトラメチル-1,3-ビス(3-アミノプロピル)ジシロキサン、1,1,3,3-テトラメチル-1,3-ビス(4-アミノブチル)ジシロキサン、1,3-ジメチル-1,3-ジメトキシ-1,3-ビス(4-アミノブチル)ジシロキサン、1,1,3,3,5,5-ヘキサメチル-1,5-ビス(4-アミノフェニル)トリシロキサン、1,1,5,5-テトラフェニル-3,3-ジメチル-1,5-ビス(3-アミノプロピル)トリシロキサン、1,1,5,5-テトラフェニル-3,3-ジメトキシ-1,5-ビス(4-アミノブチル)トリシロキサン、1,1,5,5-テトラフェニル-3,3-ジメトキシ-1,5-ビス(5-アミノペンチル)トリシロキサン、1,1,5,5-テトラメチル-3,3-ジメトキシ-1,5-ビス(2-アミノエチル)トリシロキサン、1,1,5,5-テトラメチル-3,3-ジメトキシ-1,5-ビス(4-アミノブチル)トリシロキサン、1,1,5,5-テトラメチル-3,3-ジメトキシ-1,5-ビス(5-アミノペンチル)トリシロキサン、1,1,3,3,5,5-ヘキサメチル-1,5-ビス(3-アミノプロピル)トリシロキサン、1,1,3,3,5,5-ヘキサエチル-1,5-ビス(3-アミノプロピル)トリシロキサン、1,1,3,3,5,5-ヘキサプロピル-1,5-ビス(3-アミノプロピル)トリシロキサン等のジアミノシロキサンからなるビスシトラコンイミド化合物等が挙げられる。
ビスシトラコンイミド化合物の中でも特にビス(3-エチル-5-メチル-4-シトラコンイミドフェニル)メタン、N,N'-4,4'-[3,3'-ジメチル-ジフェニルメタン]ビスシトラコンイミド、N,N'-4,4'-[3,3'-ジエチルジフェニルメタン]ビスシトラコンイミドが、溶剤溶解性や耐熱性にも優れるため、好ましい。
本実施形態で使用されるビスシトラコンイミド化合物及び/又は付加重合型シトラコンイミド樹脂のうち、リソグラフィー用膜の耐熱性、レジスト中間層との密着性、膜欠陥の出来にくさの観点から付加重合型シトラコンイミド樹脂がより好ましい。
<架橋剤>
本実施形態のリソグラフィー用膜形成材料は、ビスシトラコンイミド化合物及び/又は付加重合型シトラコンイミド樹脂に加え、硬化温度の低下やインターミキシングを抑制する等の観点から、必要に応じて架橋剤を含有していてもよい。
本実施形態のリソグラフィー用膜形成材料は、ビスシトラコンイミド化合物及び/又は付加重合型シトラコンイミド樹脂に加え、硬化温度の低下やインターミキシングを抑制する等の観点から、必要に応じて架橋剤を含有していてもよい。
架橋剤としてはシトラコンイミドと架橋反応すれば特に限定されず、公知のいずれの架橋システムを適用できるが、本実施形態で使用可能な架橋剤の具体例としては、例えば、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、アクリレート化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物、アジド化合物等が挙げられるが、これらに特に限定されない。これらの架橋剤は、1種を単独で、或いは2種以上を組み合わせて用いることができる。これらの中でもベンゾオキサジン化合物、エポキシ化合物又はシアネート化合物が好ましく、エッチング耐性向上の観点から、ベンゾオキサジン化合物がより好ましい。
シトラコンイミドと架橋剤との架橋反応では、例えば、これらの架橋剤が有する活性基(フェノール性水酸基、エポキシ基、シアネート基、アミノ基、又はベンゾオキサジンの脂環部位が開環してなるフェノール性水酸基)が、シトラコンイミド基を構成する炭素-炭素二重結合と付加反応して架橋する他、本実施形態のビスシトラコンイミド化合物が有する2つの炭素-炭素二重結合が重合して架橋する。
前記フェノール化合物としては、公知のものが使用できる。例えば、国際公開2018-016614号に記載のものが挙げられる。好ましくは、耐熱性及び溶解性の点から、アラルキル型フェノール樹脂が望ましい。
前記エポキシ化合物としては、公知のものが使用でき、1分子中にエポキシ基を2個以上有するものの中から選択される。例えば、国際公開2018-016614号に記載のものが挙げられる。これらのエポキシ樹脂は、単独でもよいし、2種以上を併用してもよい。好ましくは、耐熱性と溶解性という点から、フェノールアラルキル樹脂類、ビフェニルアラルキル樹脂類から得られるエポキシ樹脂等の常温で固体状エポキシ樹脂である。
前記シアネート化合物としては、1分子中に2個以上のシアネート基を有する化合物であれば特に制限なく、公知のものを使用することができる。例えば、WO 2011108524に記載されているものが挙げられるが、本実施形態において、好ましいシアネート化合物としては、1分子中に2個以上の水酸基を有する化合物の水酸基をシアネート基に置換した構造のものが挙げられる。また、シアネート化合物は、芳香族基を有するものが好ましく、シアネート基が芳香族基に直結した構造のものを好適に使用することができる。このようなシアネート化合物としては、例えば、国際公開2018-016614号に記載のものが挙げられる。これらのシアネート化合物は、単独で又は2種以上を適宜組み合わせて使用してもよい。また、上記したシアネート化合物は、モノマー、オリゴマー及び樹脂のいずれの形態であってもよい。
前記アミノ化合物としては、例えば、国際公開2018-016614号に記載のものが挙げられる。
前記ベンゾオキサジン化合物のオキサジンの構造は特に限定されず、ベンゾオキサジンやナフトオキサジン等の、縮合多環芳香族基を含む芳香族基を有するオキサジンの構造が挙げられる。
ベンゾオキサジン化合物としては、例えば下記一般式(a)~(f)に示す化合物が挙げられる。なお下記一般式において、環の中心に向けて表示されている結合は、環を構成しかつ置換基の結合が可能ないずれかの炭素に結合していることを示す。
一般式(a)~(c)中、R1及びR2は独立して炭素数1~30の有機基を表す。また一般式(a)~(f)中、R3乃至R6は独立して水素又は炭素数1~6の炭化水素基を表す。また前記一般式(c)、(d)及び(f)中、Xは独立して、単結合、-O-、-S-、-S-S-、-SO2-、-CO-、-CONH-、-NHCO-、-C(CH3)2-、-C(CF3)2-、-(CH2)m-、-O-(CH2)m-O-、-S-(CH2)m-S-を表す。ここでmは1~6の整数である。また一般式(e)及び(f)中、Yは独立して、単結合、-O-、-S-、-CO-、-C(CH3)2-、-C(CF3)2-又は炭素数1~3のアルキレンを表す。
また、ベンゾオキサジン化合物には、オキサジン構造を側鎖に有するオリゴマーやポリマー、ベンゾオキサジン構造を主鎖中に有するオリゴマーやポリマーが含まれる。
ベンゾオキサジン化合物は、国際公開2004/009708号パンフレット、特開平11-12258号公報、特開2004-352670号公報に記載の方法と同様の方法で製造することができる。
前記メラミン化合物の具体例としては、例えば、国際公開2018-016614号に記載のものが挙げられる。
前記グアナミン化合物の具体例としては、例えば、国際公開2018-016614号に記載のものが挙げられる。
前記グリコールウリル化合物の具体例としては、例えば、国際公開2018-016614号に記載のものが挙げられる。
前記ウレア化合物の具体例としては、例えば、国際公開2018-016614号に記載のものが挙げられる。
また、本実施形態において、架橋性向上の観点から、少なくとも1つのアリル基を有する架橋剤を用いてもよい。少なくとも1つのアリル基を有する架橋剤の具体例としては、国際公開2018-016614号に記載のものが挙げられるが、これら例示されたものに限定されるものではない。これらは単独でも、2種類以上の混合物であってもよい。これらの中でも、ビスシトラコンイミド化合物及び/又は付加重合型シトラコンイミド樹脂との相溶性に優れるという観点から、2,2-ビス(3-アリル-4-ヒドロキシフェニル)プロパン、1,1,1,3,3,3-ヘキサフルオロ-2,2-ビス(3-アリル-4-ヒドロキシフェニル)プロパン、ビス(3-アリル-4-ヒドロキシフェニル)スルホン、ビス(3-アリル-4-ヒドロキシフェニル)スルフィド、ビス(3-アリル-4-ヒドロキシフェニル)エ-テル等のアリルフェノール類が好ましい。
本実施形態のリソグラフィー用膜形成材料はビスシトラコンイミド化合物及び/又は付加重合型シトラコンイミド樹脂を単独で、あるいは前記架橋剤を配合させた後、公知の方法で架橋、硬化させて、本実施形態のリソグラフィー用膜を形成することができる。架橋方法としては、熱硬化、光硬化等の手法が挙げられる。
前記架橋剤の含有割合は、通常、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~10000質量部の範囲であり、好ましくは、耐熱性及び溶解性の観点から0.1~1000質量部の範囲であり、より好ましくは、0.1~100質量部の範囲であり、さらに好ましくは、1~50質量部の範囲であり、最も好ましくは1~30質量部の範囲である。
本実施形態のリソグラフィー用膜形成材料には、必要に応じて架橋、硬化反応を促進させるための架橋促進剤を用いることができる。
前記架橋促進剤としては、架橋、硬化反応を促進させるものであれば、特に限定されないが、例えば、アミン類、イミダゾール類、有機ホスフィン類、ルイス酸等が挙げられる。これらの架橋促進剤は、1種を単独で、或いは2種以上を組み合わせて用いることができる。これらの中でもイミダゾール類又は有機ホスフィン類が好ましく、架橋温度の低温化の観点から、イミダゾール類がより好ましい。
前記架橋促進剤としては、以下に限定されないが、例えば、国際公開2018-016614号に記載のものが挙げられる。
架橋促進剤の配合量としては、通常、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、好ましくは0.1~10質量部の範囲であり、より好ましくは、制御のし易さ及び経済性の観点からの0.1~5質量部の範囲であり、さらに好ましくは0.1~3質量部の範囲である。
架橋促進剤の配合量としては、通常、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、好ましくは0.1~10質量部の範囲であり、より好ましくは、制御のし易さ及び経済性の観点からの0.1~5質量部の範囲であり、さらに好ましくは0.1~3質量部の範囲である。
<ラジカル重合開始剤>
本実施形態のリソグラフィー用膜形成材料には、必要に応じてラジカル重合開始剤を配合することができる。ラジカル重合開始剤としては、光によりラジカル重合を開始させる光重合開始剤であってもよいし、熱によりラジカル重合を開始させる熱重合開始剤であってもよい。
本実施形態のリソグラフィー用膜形成材料には、必要に応じてラジカル重合開始剤を配合することができる。ラジカル重合開始剤としては、光によりラジカル重合を開始させる光重合開始剤であってもよいし、熱によりラジカル重合を開始させる熱重合開始剤であってもよい。
このようなラジカル重合開始剤としては、特に制限されず、従来用いられているものを適宜採用することができる。例えば、国際公開2018-016614号に記載のものが挙げられる。本実施形態におけるラジカル重合開始剤としては、これらのうちの1種を単独で用いても2種以上を組み合わせて用いてもよく、他の公知の重合開始剤をさらに組み合わせて用いてもよい。
前記ラジカル重合開始剤の含有量としては、前記ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量に対して化学量論的に必要な量であればよいが、前記ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に0.05~25質量部であることが好ましく、0.1~10質量部であることがより好ましい。ラジカル重合開始剤の含有量が0.05質量部以上である場合には、ビスシトラコンイミド化合物及び/又はシトラコンイミド樹脂の硬化が不十分となることを防ぐことができる傾向にあり、他方、ラジカル重合開始剤の含有量が25質量部以下である場合には、リソグラフィー用膜形成材料の室温での長期保存安定性が損なわれることを防ぐことができる傾向にある。
[リソグラフィー用膜形成材料の精製方法]
前記リソグラフィー用膜形成材料は酸性水溶液で洗浄して精製することが可能である。前記精製方法は、リソグラフィー用膜形成材料を水と任意に混和しない有機溶媒に溶解させて有機相を得て、その有機相を酸性水溶液と接触させ抽出処理(第一抽出工程)を行うことにより、リソグラフィー用膜形成材料と有機溶媒とを含む有機相に含まれる金属分を水相に移行させたのち、有機相と水相とを分離する工程を含む。該精製により本発明のリソグラフィー用膜形成材料の種々の金属の含有量を著しく低減させることができる。
前記リソグラフィー用膜形成材料は酸性水溶液で洗浄して精製することが可能である。前記精製方法は、リソグラフィー用膜形成材料を水と任意に混和しない有機溶媒に溶解させて有機相を得て、その有機相を酸性水溶液と接触させ抽出処理(第一抽出工程)を行うことにより、リソグラフィー用膜形成材料と有機溶媒とを含む有機相に含まれる金属分を水相に移行させたのち、有機相と水相とを分離する工程を含む。該精製により本発明のリソグラフィー用膜形成材料の種々の金属の含有量を著しく低減させることができる。
水と任意に混和しない前記有機溶媒としては、特に限定されないが、半導体製造プロセスに安全に適用できる有機溶媒が好ましい。使用する有機溶媒の量は、使用する該化合物に対して、通常1~100質量倍程度使用される。
使用される有機溶媒の具体例としては、例えば、国際公開2015/080240に記載のものが挙げられる。これらの中でも、トルエン、2-ヘプタノン、シクロヘキサノン、シクロペンタノン、メチルイソブチルケトン、プロピレングリコールモノメチルエーテルアセテート、酢酸エチル等が好ましく、特にシクロヘキサノン、プロピレングリコールモノメチルエーテルアセテートが好ましい。これらの有機溶媒はそれぞれ単独で用いることもできるし、また2種以上を混合して用いることもできる。
前記酸性の水溶液としては、一般に知られる有機、無機系化合物を水に溶解させた水溶液の中から適宜選択される。例えば、国際公開2015/080240に記載のものが挙げられる。これら酸性の水溶液は、それぞれ単独で用いることもできるし、また2種以上を組み合わせて用いることもできる。酸性の水溶液としては、例えば、鉱酸水溶液及び有機酸水溶液を挙げることができる。鉱酸水溶液としては、例えば、塩酸、硫酸、硝酸及びリン酸からなる群より選ばれる1種以上を含む水溶液を挙げることができる。有機酸水溶液としては、例えば、酢酸、プロピオン酸、蓚酸、マロン酸、コハク酸、フマル酸、マレイン酸、酒石酸、クエン酸、メタンスルホン酸、フェノールスルホン酸、p-トルエンスルホン酸及びトリフルオロ酢酸からなる群より選ばれる1種以上を含む水溶液を挙げることができる。また、酸性の水溶液としては、硫酸、硝酸、及び酢酸、蓚酸、酒石酸、クエン酸等のカルボン酸の水溶液が好ましく、さらに、硫酸、蓚酸、酒石酸、クエン酸の水溶液が好ましく、特に蓚酸の水溶液が好ましい。蓚酸、酒石酸、クエン酸等の多価カルボン酸は金属イオンに配位し、キレート効果が生じるために、より金属を除去できると考えられる。また、ここで用いる水は、本発明の目的に沿って、金属含有量の少ないもの、例えばイオン交換水等が好ましい。
前記酸性の水溶液のpHは特に制限されないが、水溶液の酸性度があまり大きくなると、使用する化合物又は樹脂に悪影響を及ぼすことがあり好ましくない。通常、pH範囲は0~5程度であり、より好ましくはpH0~3程度である。
前記酸性の水溶液の使用量は特に制限されないが、その量があまりに少ないと、金属除去のための抽出回数多くする必要があり、逆に水溶液の量があまりに多いと全体の液量が多くなり操作上の問題を生ずることがある。水溶液の使用量は、通常、リソグラフィー用膜形成材料の溶液に対して10~200質量部であり、好ましくは20~100質量部である。
前記酸性の水溶液と、リソグラフィー用膜形成材料及び水と任意に混和しない有機溶媒を含む溶液(B)とを接触させることにより金属分を抽出することができる。
前記抽出処理を行う際の温度は通常、20~90℃であり、好ましくは30~80℃の範囲である。抽出操作は、例えば、撹拌等により、よく混合させたあと、静置することにより行われる。これにより、使用する該化合物と有機溶媒を含む溶液に含まれていた金属分が水相に移行する。また本操作により、溶液の酸性度が低下し、使用する該化合物の変質を抑制することができる。
抽出処理後、使用する該化合物及び有機溶媒を含む溶液相と、水相とに分離させ、デカンテーション等により有機溶媒を含む溶液を回収する。静置する時間は特に制限されないが、静置する時間があまりに短いと有機溶媒を含む溶液相と水相との分離が悪くなり好ましくない。通常、静置する時間は1分間以上であり、より好ましくは10分間以上であり、さらに好ましくは30分間以上である。また、抽出処理は1回だけでもかまわないが、混合、静置、分離という操作を複数回繰り返して行うのも有効である。
酸性の水溶液を用いてこのような抽出処理を行った場合は、処理を行ったあとに、該水溶液から抽出し、回収した有機溶媒を含む有機相は、さらに水との抽出処理(第二抽出工程)を行うことが好ましい。抽出操作は、撹拌等により、よく混合させたあと、静置することにより行われる。そして得られる溶液は、化合物と有機溶媒とを含む溶液相と、水相とに分離するのでデカンテーション等により溶液相を回収する。また、ここで用いる水は、本発明の目的に沿って、金属含有量の少ないもの、例えばイオン交換水等が好ましい。抽出処理は1回だけでもかまわないが、混合、静置、分離という操作を複数回繰り返して行うのも有効である。また、抽出処理における両者の使用割合や、温度、時間等の条件は特に制限されないが、先の酸性の水溶液との接触処理の場合と同様で構わない。
こうして得られた、リソグラフィー用膜形成材料と有機溶媒とを含む溶液に混入する水分は減圧蒸留等の操作を施すことにより容易に除去できる。また、必要により有機溶媒を加え、化合物の濃度を任意の濃度に調整することができる。
得られた有機溶媒を含む溶液から、リソグラフィー用膜形成材料のみを得る方法は、減圧除去、再沈殿による分離、及びそれらの組み合わせ等、公知の方法で行うことができる。必要に応じて、濃縮操作、ろ過操作、遠心分離操作、乾燥操作等の公知の処理を行うことができる。
[リソグラフィー用膜形成用組成物]
本実施形態のリソグラフィー用膜形成用組成物は、前記リソグラフィー用膜形成材料と溶媒とを含有する。リソグラフィー用膜は、例えば、リソグラフィー用下層膜である。
本実施形態のリソグラフィー用膜形成用組成物は、前記リソグラフィー用膜形成材料と溶媒とを含有する。リソグラフィー用膜は、例えば、リソグラフィー用下層膜である。
本実施形態のリソグラフィー用膜形成用組成物は、基材に塗布し、その後、必要に応じて加熱して溶媒を蒸発させた後、加熱又は光照射して所望の硬化膜を形成することができる。本実施形態のリソグラフィー用膜形成用組成物の塗布方法は任意であり、例えば、スピンコート法、ディップ法、フローコート法、インクジェット法、スプレー法、バーコート法、グラビアコート法、スリットコート法、ロールコート法、転写印刷法、刷毛塗り、ブレードコート法、エアーナイフコート法等の方法を適宜採用できる。
前記膜の加熱温度は、溶媒を蒸発させる目的では特に限定されず、例えば、40~400℃で行うことができる。加熱方法としては、特に限定されるものではなく、例えば、ホットプレートやオーブンを用いて、大気、窒素等の不活性ガス、真空中等の適切な雰囲気下で蒸発させればよい。加熱温度及び加熱時間は、目的とする電子デバイスのプロセス工程に適合した条件を選択すればよく、得られる膜の物性値が電子デバイスの要求特性に適合するような加熱条件を選択すればよい。光照射する場合の条件も特に限定されるものではなく、用いるリソグラフィー用膜形成材料に応じて、適宜な照射エネルギー及び照射時間を採用すればよい。
<溶媒>
本実施形態のリソグラフィー用膜形成用組成物に用いる溶媒としては、ビスシトラコンイミド及び/又は付加重合型シトラコンイミド樹脂が少なくとも溶解するものであれば、特に限定されず、公知のものを適宜用いることができる。
本実施形態のリソグラフィー用膜形成用組成物に用いる溶媒としては、ビスシトラコンイミド及び/又は付加重合型シトラコンイミド樹脂が少なくとも溶解するものであれば、特に限定されず、公知のものを適宜用いることができる。
溶媒の具体例としては、例えば、国際公開2013/024779に記載のものが挙げられる。これらの溶媒は、1種を単独で、或いは2種以上を組み合わせて用いることができる。
前記溶媒の中で、安全性の点から、シクロヘキサノン、プロピレングリコールモノメチルエーテル、プロピレングリコールモノメチルエーテルアセテート、乳酸エチル、ヒドロキシイソ酪酸メチル、アニソールが特に好ましい。
前記溶媒の含有量は、特に限定されないが、溶解性及び製膜上の観点から、リソグラフィー用膜形成用材料中のビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、25~9,900質量部であることが好ましく、400~7,900質量部であることがより好ましく、900~4,900質量部であることがさらに好ましい。
<酸発生剤>
本実施形態のリソグラフィー用膜形成用組成物は、架橋反応をさらに促進させる等の観点から、必要に応じて酸発生剤を含有していてもよい。酸発生剤としては、熱分解によって酸を発生するもの、光照射によって酸を発生するもの等が知られているが、いずれのものも使用することができる。
本実施形態のリソグラフィー用膜形成用組成物は、架橋反応をさらに促進させる等の観点から、必要に応じて酸発生剤を含有していてもよい。酸発生剤としては、熱分解によって酸を発生するもの、光照射によって酸を発生するもの等が知られているが、いずれのものも使用することができる。
酸発生剤としては、例えば、国際公開2013/024779に記載のものが挙げられる。これらのなかでも、特に、ジターシャリーブチルジフェニルヨードニウムノナフルオロメタンスルホナート、トリフルオロメタンスルホン酸ジフェニルヨードニウム、トリフルオロメタンスルホン酸(p-tert-ブトキシフェニル)フェニルヨードニウム、p-トルエンスルホン酸ジフェニルヨードニウム、p-トルエンスルホン酸(p-tert-ブトキシフェニル)フェニルヨードニウム、トリフルオロメタンスルホン酸トリフェニルスルホニウム、トリフルオロメタンスルホン酸(p-tert-ブトキシフェニル)ジフェニルスルホニウム、トリフルオロメタンスルホン酸トリス(p-tert-ブトキシフェニル)スルホニウム、p-トルエンスルホン酸トリフェニルスルホニウム、p-トルエンスルホン酸(p-tert-ブトキシフェニル)ジフェニルスルホニウム、p-トルエンスルホン酸トリス(p-tert-ブトキシフェニル)スルホニウム、トリフルオロメタンスルホン酸トリナフチルスルホニウム、トリフルオロメタンスルホン酸シクロヘキシルメチル(2-オキソシクロヘキシル)スルホニウム、トリフルオロメタンスルホン酸(2-ノルボニル)メチル(2-オキソシクロヘキシル)スルホニウム、1,2'-ナフチルカルボニルメチルテトラヒドロチオフェニウムトリフレート等のオニウム塩;ビス(ベンゼンスルホニル)ジアゾメタン、ビス(p-トルエンスルホニル)ジアゾメタン、ビス(シクロヘキシルスルホニル)ジアゾメタン、ビス(n-ブチルスルホニル)ジアゾメタン、ビス(イソブチルスルホニル)ジアゾメタン、ビス(sec-ブチルスルホニル)ジアゾメタン、ビス(n-プロピルスルホニル)ジアゾメタン、ビス(イソプロピルスルホニル)ジアゾメタン、ビス(tert-ブチルスルホニル)ジアゾメタン等のジアゾメタン誘導体;ビス-(p-トルエンスルホニル)-α-ジメチルグリオキシム、ビス-(n-ブタンスルホニル)-α-ジメチルグリオキシム等のグリオキシム誘導体、ビスナフチルスルホニルメタン等のビススルホン誘導体;N-ヒドロキシスクシンイミドメタンスルホン酸エステル、N-ヒドロキシスクシンイミドトリフルオロメタンスルホン酸エステル、N-ヒドロキシスクシンイミド1-プロパンスルホン酸エステル、N-ヒドロキシスクシンイミド2-プロパンスルホン酸エステル、N-ヒドロキシスクシンイミド1-ペンタンスルホン酸エステル、N-ヒドロキシスクシンイミドp-トルエンスルホン酸エステル、N-ヒドロキシナフタルイミドメタンスルホン酸エステル、N-ヒドロキシナフタルイミドベンゼンスルホン酸エステル等のN-ヒドロキシイミド化合物のスルホン酸エステル誘導体等が好ましく用いられる。
本実施形態のリソグラフィー用膜形成用組成物において、酸発生剤の含有量は、特に限定されないが、リソグラフィー用膜形成材料中のビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0~50質量部であることが好ましく、より好ましくは0~40質量部である。上述の好ましい範囲にすることで、架橋反応が高められる傾向にあり、また、レジスト層とのミキシング現象の発生が抑制される傾向にある。
<塩基性化合物>
さらに、本実施形態のリソグラフィー用下層膜形成用組成物は、保存安定性を向上させる等の観点から、塩基性化合物を含有していてもよい。
さらに、本実施形態のリソグラフィー用下層膜形成用組成物は、保存安定性を向上させる等の観点から、塩基性化合物を含有していてもよい。
前記塩基性化合物は、酸発生剤より微量に発生した酸が架橋反応を進行させるのを防ぐための、酸に対するクエンチャーの役割を果たす。このような塩基性化合物としては、以下に限定されないが、例えば、国際公開2013-024779に記載されている、第一級、第二級又は第三級の脂肪族アミン類、混成アミン類、芳香族アミン類、複素環アミン類、カルボキシ基を有する含窒素化合物、スルホニル基を有する含窒素化合物、水酸基を有する含窒素化合物、ヒドロキシフェニル基を有する含窒素化合物、アルコール性含窒素化合物、アミド誘導体又はイミド誘導体等が挙げられる。
本実施形態のリソグラフィー用膜形成用組成物において、塩基性化合物の含有量は、特に限定されないが、リソグラフィー用膜形成材料中のビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0~2質量部であることが好ましく、より好ましくは0~1質量部である。上述の好ましい範囲にすることで、架橋反応を過度に損なうことなく保存安定性が高められる傾向にある。
さらに、本実施形態のリソグラフィー用膜形成用組成物は、公知の添加剤を含有していてもよい。公知の添加剤としては、以下に限定されないが、例えば、紫外線吸収剤、消泡剤、着色剤、顔料、ノニオン系界面活性剤、アニオン系界面活性剤、カチオン系界面活性剤等が挙げられる。
[リソグラフィー用下層膜及びパターンの形成方法]
本実施形態のリソグラフィー用下層膜は、本実施形態のリソグラフィー用膜形成用組成物を用いて形成される。
本実施形態のリソグラフィー用下層膜は、本実施形態のリソグラフィー用膜形成用組成物を用いて形成される。
また、本実施形態のパターン形成方法は、基板上に、本実施形態のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程(A-1)と、前記下層膜上に、少なくとも1層のフォトレジスト層を形成する工程(A-2)と、前記工程(A-2)の後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程(A-3)と、を有する。
さらに、本実施形態の他のパターン形成方法は、基板上に、本実施形態のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程(B-1)と、前記下層膜上に、珪素原子を含有するレジスト中間層膜材料を用いて中間層膜を形成する工程(B-2)と、前記中間層膜上に、少なくとも1層のフォトレジスト層を形成する工程(B-3)と、前記工程(B-3)の後、前記フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成する工程(B-4)と、前記工程(B-4)の後、前記レジストパターンをマスクとして前記中間層膜をエッチングし、得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングし、得られた下層膜パターンをエッチングマスクとして基板をエッチングすることで基板にパターンを形成する工程(B-5)と、を有する。
本実施形態のリソグラフィー用下層膜は、本実施形態のリソグラフィー用膜形成用組成物から形成されるものであれば、その形成方法は特に限定されず、公知の手法を適用することができる。例えば、本実施形態のリソグラフィー用膜形成用組成物をスピンコートやスクリーン印刷等の公知の塗布法或いは印刷法等で基板上に付与した後、有機溶媒を揮発させる等して除去することで、下層膜を形成することができる。
下層膜の形成時には、上層レジストとのミキシング現象の発生を抑制するとともに架橋反応を促進させるために、ベークをすることが好ましい。この場合、ベーク温度は、特に限定されないが、80~450℃の範囲内であることが好ましく、より好ましくは200~400℃である。また、ベーク時間も、特に限定されないが、10~300秒間の範囲内であることが好ましい。なお、下層膜の厚さは、要求性能に応じて適宜選定することができ、特に限定されないが、通常、30~20,000nmであることが好ましく、より好ましくは50~15,000nmであり、さらに好ましくは50~1000nmである。
基板上に下層膜を作製した後、2層プロセスの場合はその上に珪素含有レジスト層、或いは通常の炭化水素からなる単層レジスト、3層プロセスの場合はその上に珪素含有中間層、さらにその上に珪素を含まない単層レジスト層を作製することが好ましい。この場合、このレジスト層を形成するためのフォトレジスト材料としては公知のものを使用することができる。
2層プロセス用の珪素含有レジスト材料としては、酸素ガスエッチング耐性の観点から、ベースポリマーとしてポリシルセスキオキサン誘導体又はビニルシラン誘導体等の珪素原子含有ポリマーを使用し、さらに有機溶媒、酸発生剤、必要により塩基性化合物等を含むポジ型のフォトレジスト材料が好ましく用いられる。ここで珪素原子含有ポリマーとしては、この種のレジスト材料において用いられている公知のポリマーを使用することができる。
3層プロセス用の珪素含有中間層としてはポリシルセスキオキサンベースの中間層が好ましく用いられる。中間層に反射防止膜として効果を持たせることによって、効果的に反射を抑えることができる傾向にある。例えば、193nm露光用プロセスにおいて、下層膜として芳香族基を多く含み基板エッチング耐性が高い材料を用いると、k値が高くなり、基板反射が高くなる傾向にあるが、中間層で反射を抑えることによって、基板反射を0.5%以下にすることができる。このような反射防止効果がある中間層としては、以下に限定されないが、193nm露光用としてはフェニル基又は珪素-珪素結合を有する吸光基を導入された、酸或いは熱で架橋するポリシルセスキオキサンが好ましく用いられる。
また、Chemical Vapour Deposition(CVD)法で形成した中間層を用いることもできる。CVD法で作製した反射防止膜としての効果が高い中間層としては、以下に限定されないが、例えば、SiON膜が知られている。一般的には、CVD法よりスピンコート法やスクリーン印刷等の湿式プロセスによる中間層の形成の方が、簡便でコスト的なメリットがある。なお、3層プロセスにおける上層レジストは、ポジ型でもネガ型でもどちらでもよく、また、通常用いられている単層レジストと同じものを用いることができる。
さらに、本実施形態の下層膜は、通常の単層レジスト用の反射防止膜或いはパターン倒れ抑制のための下地材として用いることもできる。本実施形態の下層膜は、下地加工のためのエッチング耐性に優れるため、下地加工のためのハードマスクとしての機能も期待できる。
前記フォトレジスト材料によりレジスト層を形成する場合においては、前記下層膜を形成する場合と同様に、スピンコート法やスクリーン印刷等の湿式プロセスが好ましく用いられる。また、レジスト材料をスピンコート法等で塗布した後、通常、プリベークが行われるが、このプリベークは、80~180℃で10~300秒の範囲で行うことが好ましい。その後、常法にしたがい、露光を行い、ポストエクスポジュアーベーク(PEB)、現像を行うことで、レジストパターンを得ることができる。なお、レジスト膜の厚さは特に制限されないが、一般的には、30~500nmが好ましく、より好ましくは50~400nmである。
また、露光光は、使用するフォトレジスト材料に応じて適宜選択して用いればよい。一般的には、波長300nm以下の高エネルギー線、具体的には248nm、193nm、157nmのエキシマレーザー、3~20nmの軟X線、電子ビーム、X線等を挙げることができる。
上述の方法により形成されるレジストパターンは、本実施形態の下層膜によってパターン倒れが抑制されたものとなる。そのため、本実施形態の下層膜を用いることで、より微細なパターンを得ることができ、また、そのレジストパターンを得るために必要な露光量を低下させ得る。
次に、得られたレジストパターンをマスクにしてエッチングを行う。2層プロセスにおける下層膜のエッチングとしては、ガスエッチングが好ましく用いられる。ガスエッチングとしては、酸素ガスを用いたエッチングが好適である。酸素ガスに加えて、He、Ar等の不活性ガスや、CO、CO2、NH3、SO2、N2、NO2、H2ガスを加えることも可能である。また、酸素ガスを用いずに、CO、CO2、NH3、N2、NO2、H2ガスだけでガスエッチングを行うこともできる。特に後者のガスは、パターン側壁のアンダーカット防止のための側壁保護のために好ましく用いられる。
一方、3層プロセスにおける中間層のエッチングにおいても、ガスエッチングが好ましく用いられる。ガスエッチングとしては、上述の2層プロセスにおいて説明したものと同様のものが適用可能である。とりわけ、3層プロセスにおける中間層の加工は、フロン系のガスを用いてレジストパターンをマスクにして行うことが好ましい。その後、上述したように中間層パターンをマスクにして、例えば酸素ガスエッチングを行うことで、下層膜の加工を行うことができる。
ここで、中間層として無機ハードマスク中間層膜を形成する場合は、CVD法やALD法等で、珪素酸化膜、珪素窒化膜、珪素酸化窒化膜(SiON膜)が形成される。窒化膜の形成方法としては、以下に限定されないが、例えば、特開2002-334869号公報(特許文献6)、WO2004/066377(特許文献7)に記載された方法を用いることができる。このような中間層膜の上に直接フォトレジスト膜を形成することができるが、中間層膜の上に有機反射防止膜(BARC)をスピンコートで形成して、その上にフォトレジスト膜を形成してもよい。
中間層として、ポリシルセスキオキサンベースの中間層も好ましく用いられる。レジスト中間層膜に反射防止膜として効果を持たせることによって、効果的に反射を抑えることができる傾向にある。ポリシルセスキオキサンベースの中間層の具体的な材料については、以下に限定されないが、例えば、特開2007-226170号(特許文献8)、特開2007-226204号(特許文献9)に記載されたものを用いることができる。
また、次の基板のエッチングも、常法によって行うことができ、例えば、基板がSiO2、SiNであればフロン系ガスを主体としたエッチング、p-SiやAl、Wでは塩素系、臭素系ガスを主体としたエッチングを行うことができる。基板をフロン系ガスでエッチングする場合、2層レジストプロセスの珪素含有レジストと3層プロセスの珪素含有中間層は、基板加工と同時に剥離される。一方、塩素系或いは臭素系ガスで基板をエッチングした場合は、珪素含有レジスト層又は珪素含有中間層の剥離が別途行われ、一般的には、基板加工後にフロン系ガスによるドライエッチング剥離が行われる。
本実施形態の下層膜は、これら基板のエッチング耐性に優れる特徴がある。なお、基板は、公知のものを適宜選択して使用することができ、特に限定されないが、Si、α-Si、p-Si、SiO2、SiN、SiON、W、TiN、Al等が挙げられる。また、基板は、基材(支持体)上に被加工膜(被加工基板)を有する積層体であってもよい。このような被加工膜としては、Si、SiO2、SiON、SiN、p-Si、α-Si、W、W-Si、Al、Cu、Al-Si等種々のLow-k膜及びそのストッパー膜等が挙げられ、通常、基材(支持体)とは異なる材質のものが用いられる。なお、加工対象となる基板或いは被加工膜の厚さは、特に限定されないが、通常、50~1,000,000nm程度であることが好ましく、より好ましくは75~500,000nmである。
以下、本発明を合成実施例、実施例、製造例、参考例及び比較例によりさらに詳細に説明するが、本発明は、これらの例によってなんら限定されるものではない。
[分子量]
合成した化合物の分子量は、Water社製Acquity UPLC/MALDI-Synapt HDMSを用いて、LC(GPC)-MS分析により測定した。
合成した化合物の分子量は、Water社製Acquity UPLC/MALDI-Synapt HDMSを用いて、LC(GPC)-MS分析により測定した。
[耐熱性の評価]
エスアイアイ・ナノテクノロジー社製EXSTAR6000TG-DTA装置を使用し、試料約5mgをアルミニウム製非密封容器に入れ、窒素ガス(100ml/min)気流中昇温速度10℃/minで500℃まで昇温することにより熱重量減少量を測定した。実用的観点からは、下記A又はB評価が好ましい。A又はB評価であれば、高い耐熱性を有し、高温ベークへの適用が可能である。
<評価基準>
A:400℃での熱重量減少量が、10%未満
B:400℃での熱重量減少量が、10%~25%
C:400℃での熱重量減少量が、25%超
エスアイアイ・ナノテクノロジー社製EXSTAR6000TG-DTA装置を使用し、試料約5mgをアルミニウム製非密封容器に入れ、窒素ガス(100ml/min)気流中昇温速度10℃/minで500℃まで昇温することにより熱重量減少量を測定した。実用的観点からは、下記A又はB評価が好ましい。A又はB評価であれば、高い耐熱性を有し、高温ベークへの適用が可能である。
<評価基準>
A:400℃での熱重量減少量が、10%未満
B:400℃での熱重量減少量が、10%~25%
C:400℃での熱重量減少量が、25%超
[溶解性の評価]
50mlのスクリュー瓶にプロピレングリコールモノメチルエーテルアセテート(PGMEA)と化合物及び/又は樹脂を仕込み、23℃にてマグネチックスターラーで1時間撹拌後に、化合物及び/又は樹脂のPGMEAに対する溶解量を測定し、その結果を以下の基準で評価した。実用的観点からは、下記S、A又はB評価が好ましい。S、A又はB評価であれば、溶液状態で高い保存安定性を有し、半導体微細加工プロセスで広く用いられるエッジビートリムーバー液(PGME/PGMEA混合液)にも十分に適用が可能である。S評価であれば、長期保存安定性に非常に優れ、シェルフライフの長い下層膜形成組成物を製造できる。
<評価基準>
S:20質量%以上
A:10質量%以上20質量%未満
B:5質量%以上10質量%未満
C:5質量%未満
50mlのスクリュー瓶にプロピレングリコールモノメチルエーテルアセテート(PGMEA)と化合物及び/又は樹脂を仕込み、23℃にてマグネチックスターラーで1時間撹拌後に、化合物及び/又は樹脂のPGMEAに対する溶解量を測定し、その結果を以下の基準で評価した。実用的観点からは、下記S、A又はB評価が好ましい。S、A又はB評価であれば、溶液状態で高い保存安定性を有し、半導体微細加工プロセスで広く用いられるエッジビートリムーバー液(PGME/PGMEA混合液)にも十分に適用が可能である。S評価であれば、長期保存安定性に非常に優れ、シェルフライフの長い下層膜形成組成物を製造できる。
<評価基準>
S:20質量%以上
A:10質量%以上20質量%未満
B:5質量%以上10質量%未満
C:5質量%未満
(合成実施例1) シトラコンイミドAの合成
攪拌機、冷却管及びビュレットを備えた内容積200mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)9.19g(82.0mmol)、ジメチルフォルムアミド20gおよびp-キシレン40gとを仕込み80℃に加熱後、4,4’-ジアミノジフェニルメタン(東京化成工業(株)製)7.92(40.0mmol)のジメチルフォルムアミド20gおよびp-キシレン40gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物1.5gを加えて、140℃にて7時間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、カラムクロマトによる分離精製を行うことにより、下記式で示される目的化合物(シトラコンイミドA)4.20gを得た。
なお、400MHz-1H-NMRにより以下のピークが見出され、上記式の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.3~7.4(8H,Ph-H)、6.8(2H,=CH-)、4.0(2H,-CH2-)、2.1(6H,-CH3(シトラコンイミド環))
得られた化合物について、前記方法により分子量を測定した結果、386であった。
攪拌機、冷却管及びビュレットを備えた内容積200mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)9.19g(82.0mmol)、ジメチルフォルムアミド20gおよびp-キシレン40gとを仕込み80℃に加熱後、4,4’-ジアミノジフェニルメタン(東京化成工業(株)製)7.92(40.0mmol)のジメチルフォルムアミド20gおよびp-キシレン40gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物1.5gを加えて、140℃にて7時間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、カラムクロマトによる分離精製を行うことにより、下記式で示される目的化合物(シトラコンイミドA)4.20gを得た。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.3~7.4(8H,Ph-H)、6.8(2H,=CH-)、4.0(2H,-CH2-)、2.1(6H,-CH3(シトラコンイミド環))
得られた化合物について、前記方法により分子量を測定した結果、386であった。
(合成実施例2) シトラコンイミドBの合成
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-ジアミノ-3,3’-ジエチル-5,5’-ジメチルジフェニルメタン(東京化成工業(株)製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドB)4.50gを得た。
なお、400MHz-1H-NMRにより以下のピークが見出され、上記式の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.1(4H,Ph-H)、6.8(2H,=CH-)、3.9(2H,-CH2-)、2.3(4H,CH3-CH2-Ph)、2.1(6H,CH3-Ph)、1.9(6H,-CH3(シトラコンイミド環))、1.0(6H,CH3-CH2-Ph)
得られた化合物について、前記方法により分子量を測定した結果、470であった。
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-ジアミノ-3,3’-ジエチル-5,5’-ジメチルジフェニルメタン(東京化成工業(株)製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドB)4.50gを得た。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.1(4H,Ph-H)、6.8(2H,=CH-)、3.9(2H,-CH2-)、2.3(4H,CH3-CH2-Ph)、2.1(6H,CH3-Ph)、1.9(6H,-CH3(シトラコンイミド環))、1.0(6H,CH3-CH2-Ph)
得られた化合物について、前記方法により分子量を測定した結果、470であった。
(合成実施例3) シトラコンイミドCの合成
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-ジアミノ-3,3’ジメチルジフェニルメタン(東京化成工業(株)製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドC)4.35gを得た。
なお、400MHz-1H-NMRにより以下のピークが見出され、上記式の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.1~7.3(6H,Ph-H)、6.8(2H,=CH-)、4.0(2H,-CH2-)、2.0(6H,CH3-Ph)、1.9(6H,-CH3(シトラコンイミド環))
得られた化合物について、前記方法により分子量を測定した結果、414であった。
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-ジアミノ-3,3’ジメチルジフェニルメタン(東京化成工業(株)製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドC)4.35gを得た。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.1~7.3(6H,Ph-H)、6.8(2H,=CH-)、4.0(2H,-CH2-)、2.0(6H,CH3-Ph)、1.9(6H,-CH3(シトラコンイミド環))
得られた化合物について、前記方法により分子量を測定した結果、414であった。
(合成実施例4) シトラコンイミドDの合成
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-(4,4’-イソプロピリデンジフェニル-1,1’-ジイルジオキシ)ジアニリン(シグマアルドリッチ社製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドD)4.35gを得た。
なお、400MHz-1H-NMRにより以下のピークが見出され、上記式の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.0~7.3(16H,Ph-H)、6.8(2H,=CH-)、2.0(6H,-CH3(シトラコンイミド環))、1.7(6H,-CH3)
得られた化合物について、前記方法により分子量を測定した結果、598であった。
4,4’-ジアミノジフェニルメタンの代わりに、4,4’-(4,4’-イソプロピリデンジフェニル-1,1’-ジイルジオキシ)ジアニリン(シグマアルドリッチ社製)を用いた以外、合成実施例1と同様に反応し、下記式で示される目的化合物(シトラコンイミドD)4.35gを得た。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.0~7.3(16H,Ph-H)、6.8(2H,=CH-)、2.0(6H,-CH3(シトラコンイミド環))、1.7(6H,-CH3)
得られた化合物について、前記方法により分子量を測定した結果、598であった。
(合成実施例5) シトラコンイミドEの合成
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)19.38g(164.0mmol)、ジメチルフォルムアミド40gおよびp-キシレン80gを仕込み80℃に加熱後、ポリジアミノジフェニルメタン(WANAMINE MDA-60R,WANHUA CHEMICAL GROUP CO.,LTD製)10.0gのジメチルフォルムアミド30gおよびp-キシレン30gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物3.0gを加えて、140℃にて6時間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、減圧ろ過を行い、得られた固体を60℃にて減圧下乾燥を行うことにより、下記式で示される目的樹脂(シトラコンイミドE)8.20gを得た。
得られた樹脂について、前記方法によりポリスチレン換算分子量を測定した結果、1416であった。
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)19.38g(164.0mmol)、ジメチルフォルムアミド40gおよびp-キシレン80gを仕込み80℃に加熱後、ポリジアミノジフェニルメタン(WANAMINE MDA-60R,WANHUA CHEMICAL GROUP CO.,LTD製)10.0gのジメチルフォルムアミド30gおよびp-キシレン30gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物3.0gを加えて、140℃にて6時間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、減圧ろ過を行い、得られた固体を60℃にて減圧下乾燥を行うことにより、下記式で示される目的樹脂(シトラコンイミドE)8.20gを得た。
得られた樹脂について、前記方法によりポリスチレン換算分子量を測定した結果、1416であった。
(合成実施例6) シトラコンイミドFの合成
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)19.38g(164.0mmol)、ジメチルフォルムアミド40gおよびp-キシレン60を仕込み80℃に加熱後、ビフェニルアラルキル型ポリアミン(製品名:BAN,日本化薬(株)製)12.0gのジメチルフォルムアミド30gおよびp-キシレン30gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物3.0gを加えて、140℃にて8間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、減圧ろ過を行い、得られた固体を60℃にて減圧下乾燥を行うことにより、下記式で示される目的樹脂(シトラコンイミドF)10.5gを得た。
得られた樹脂について、前記方法によりポリスチレン換算分子量を測定した結果、1582であった。
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器を準備した。この容器に、シトラコン酸無水物(東京化成工業(株)製)19.38g(164.0mmol)、ジメチルフォルムアミド40gおよびp-キシレン60を仕込み80℃に加熱後、ビフェニルアラルキル型ポリアミン(製品名:BAN,日本化薬(株)製)12.0gのジメチルフォルムアミド30gおよびp-キシレン30gの溶液を加えて、反応液を調製した。この反応液を80℃で10分撹拌後、p-トルエンスルホン酸一水和物3.0gを加えて、140℃にて8間撹拌して反応を行ない、共沸脱水にて生成水をディーンスタークトラップにて回収した。次に、反応液を40℃に冷却した後、蒸留水300mlを入れたビーカーに滴下し、生成物を析出させた。得られたスラリー溶液をろ過後、残渣をメタノールで洗浄し、減圧ろ過を行い、得られた固体を60℃にて減圧下乾燥を行うことにより、下記式で示される目的樹脂(シトラコンイミドF)10.5gを得た。
得られた樹脂について、前記方法によりポリスチレン換算分子量を測定した結果、1582であった。
<実施例1>
ビスシトラコンイミド化合物として、シトラコンイミドA10質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
ビスシトラコンイミド化合物として、シトラコンイミドA10質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例2~4>
シトラコンイミドAを、シトラコンイミドB、シトラコンイミドCおよびシトラコンイミドDに変更して同様に熱重量測定を行なった結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、シトラコンイミドBおよびシトラコンイミドCは、5質量%以上10質量%未満(評価B)であり、シトラコンイミドDは、20質量%以上(評価S)と非常に優れ、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
シトラコンイミドAを、シトラコンイミドB、シトラコンイミドCおよびシトラコンイミドDに変更して同様に熱重量測定を行なった結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、シトラコンイミドBおよびシトラコンイミドCは、5質量%以上10質量%未満(評価B)であり、シトラコンイミドDは、20質量%以上(評価S)と非常に優れ、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
<実施例5>
シトラコンイミドAを10質量部、また、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部、また、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は十分な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例6>
シトラコンイミドAを10質量部使用した。また、架橋促進剤としてトリフェニルホスフィン(TPP)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋促進剤としてトリフェニルホスフィン(TPP)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例7>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるベンゾオキサジン(BF-BXZ;小西化学工業株式会社製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるベンゾオキサジン(BF-BXZ;小西化学工業株式会社製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例8>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるビフェニルアラルキル型エポキシ樹脂(NC-3000-L;日本化薬株式会社製)2質量部を使用し、架橋促進剤としてTPIZを0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるビフェニルアラルキル型エポキシ樹脂(NC-3000-L;日本化薬株式会社製)2質量部を使用し、架橋促進剤としてTPIZを0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例9>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジアリルビスフェノールA型シアネート(DABPA-CN;三菱ガス化学製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、10質量%以上20質量%未満(評価A)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジアリルビスフェノールA型シアネート(DABPA-CN;三菱ガス化学製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例10>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジアリルビスフェノールA(BPA-CA;小西化学製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジアリルビスフェノールA(BPA-CA;小西化学製)2質量部を使用し、架橋促進剤として2,4,5-トリフェニルイミダゾール(TPIZ)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例11>
シトラコンイミドAを10質量部、また、架橋剤として、上記式で表されるベンゾオキサジンBF-BXZを2質量部使用し、架橋促進剤としてTPIZを0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部、また、架橋剤として、上記式で表されるベンゾオキサジンBF-BXZを2質量部使用し、架橋促進剤としてTPIZを0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例12>
シトラコンイミドAを10質量部、また、架橋剤として、上記式で表されるベンゾオキサジンBF-BXZを2質量部使用し、架橋促進のため、酸発生剤ジターシャリーブチルジフェニルヨードニウムノナフルオロメタンスルホナート(DTDPI;みどり化学(株)製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部、また、架橋剤として、上記式で表されるベンゾオキサジンBF-BXZを2質量部使用し、架橋促進のため、酸発生剤ジターシャリーブチルジフェニルヨードニウムノナフルオロメタンスルホナート(DTDPI;みどり化学(株)製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例13>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジフェニルメタン型アリルフェノール樹脂(APG-1;群栄化学工業製)2質量部を使用し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジフェニルメタン型アリルフェノール樹脂(APG-1;群栄化学工業製)2質量部を使用し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例14>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジフェニルメタン型プロペニルフェノール樹脂(APG-2;群栄化学工業製)2質量部を使用し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表されるジフェニルメタン型プロペニルフェノール樹脂(APG-2;群栄化学工業製)2質量部を使用し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例15>
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表される4,4´-ジアミノジフェニルメタン(DDM;東京化成製)2質量部を使用し、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は優れた溶解性を有するものと評価された。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部使用した。また、架橋剤として、下記式で表される4,4´-ジアミノジフェニルメタン(DDM;東京化成製)2質量部を使用し、リソグラフィー用膜形成材料とした。
前記シトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例16>
シトラコンイミドAを20質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料20質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを20質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料20質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例17>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例5と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例5と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例18>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例6と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例6と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例19>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例7と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例7と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例20>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例8と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例8と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例21>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例9と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例9と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例22>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例10と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例10と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例23>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例11と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例11と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例24>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例12と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例12と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例25>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例13と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例13と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例26>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例14と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例14と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例27>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例15と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例15と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例28>
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例16と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドDを用いた以外は実施例16と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例29>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例1と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例1と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例30>
シトラコンイミドAの代わりにシトラコンイミドFを用いた以外は実施例1と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドFを用いた以外は実施例1と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例31>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例5と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例5と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例32>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例6と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例6と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例33>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例7と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例7と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例34>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例8と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例8と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例35>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例9と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例9と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例36>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例10と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例10と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例37>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例11と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例11と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例38>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例12と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例12と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例39>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例13と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例13と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例40>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例14と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例14と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例41>
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例15と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAの代わりにシトラコンイミドEを用いた以外は実施例15と同様に、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例42>
シトラコンイミドAを10質量部、また、光ラジカル重合開始剤として、下記式で表されるイルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドAを10質量部、また、光ラジカル重合開始剤として、下記式で表されるイルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例43>
シトラコンイミドDを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドDを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例44>
シトラコンイミドEを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドEを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例45>
シトラコンイミドFを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
シトラコンイミドFを10質量部、また、光ラジカル重合開始剤として、イルガキュア(IRGACURE)184(BASF社製)を0.1質量部配合し、リソグラフィー用膜形成材料とした。
前記ビスシトラコンイミド化合物10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<製造例1>
ジムロート冷却管、温度計及び攪拌翼を備えた、底抜きが可能な内容積10Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流中、1,5-ジメチルナフタレン1.09kg(7mol、三菱ガス化学(株)製)、40質量%ホルマリン水溶液2.1kg(ホルムアルデヒドとして28mol、三菱ガス化学(株)製)及び98質量%硫酸(関東化学(株)製)0.97mlを仕込み、常圧下、100℃で還流させながら7時間反応させた。その後、希釈溶媒としてエチルベンゼン(和光純薬工業(株)製、試薬特級)1.8kgを反応液に加え、静置後、下相の水相を除去した。さらに、中和及び水洗を行い、エチルベンゼン及び未反応の1,5-ジメチルナフタレンを減圧下で留去することにより、淡褐色固体のジメチルナフタレンホルムアルデヒド樹脂1.25kgを得た。
得られたジメチルナフタレンホルムアルデヒド樹脂の分子量は、数平均分子量(Mn):562、重量平均分子量(Mw):1168、分散度(Mw/Mn):2.08であった。
ジムロート冷却管、温度計及び攪拌翼を備えた、底抜きが可能な内容積10Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流中、1,5-ジメチルナフタレン1.09kg(7mol、三菱ガス化学(株)製)、40質量%ホルマリン水溶液2.1kg(ホルムアルデヒドとして28mol、三菱ガス化学(株)製)及び98質量%硫酸(関東化学(株)製)0.97mlを仕込み、常圧下、100℃で還流させながら7時間反応させた。その後、希釈溶媒としてエチルベンゼン(和光純薬工業(株)製、試薬特級)1.8kgを反応液に加え、静置後、下相の水相を除去した。さらに、中和及び水洗を行い、エチルベンゼン及び未反応の1,5-ジメチルナフタレンを減圧下で留去することにより、淡褐色固体のジメチルナフタレンホルムアルデヒド樹脂1.25kgを得た。
得られたジメチルナフタレンホルムアルデヒド樹脂の分子量は、数平均分子量(Mn):562、重量平均分子量(Mw):1168、分散度(Mw/Mn):2.08であった。
続いて、ジムロート冷却管、温度計及び攪拌翼を備えた内容積0.5Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流下で、上述のようにして得られたジメチルナフタレンホルムアルデヒド樹脂100g(0.51mol)とパラトルエンスルホン酸0.05gとを仕込み、190℃まで昇温させて2時間加熱した後、攪拌した。その後さらに、1-ナフトール52.0g(0.36mol)を加え、さらに220℃まで昇温させて2時間反応させた。溶剤希釈後、中和及び水洗を行い、溶剤を減圧下で除去することにより、黒褐色固体の変性樹脂(CR-1)126.1gを得た。
得られた樹脂(CR-1)は、Mn:885、Mw:2220、Mw/Mn:4.17であった。
熱重量測定(TG)の結果、得られた樹脂の400℃での熱重量減少量は25%超(評価C)であった。そのため、高温ベークへの適用が困難であるものと評価された。
PGMEAへの溶解性を評価した結果、10質量%以上(評価A)であり、優れた溶解性を有するものと評価された。
なお、上記のMn、Mw及びMw/Mnについては、以下の条件にてゲル浸透クロマトグラフィー(GPC)分析を行い、ポリスチレン換算の分子量を求めることにより測定した。
装置:Shodex GPC-101型(昭和電工(株)製)
カラム:KF-80M×3
溶離液:THF 1mL/min
温度:40℃
得られた樹脂(CR-1)は、Mn:885、Mw:2220、Mw/Mn:4.17であった。
熱重量測定(TG)の結果、得られた樹脂の400℃での熱重量減少量は25%超(評価C)であった。そのため、高温ベークへの適用が困難であるものと評価された。
PGMEAへの溶解性を評価した結果、10質量%以上(評価A)であり、優れた溶解性を有するものと評価された。
なお、上記のMn、Mw及びMw/Mnについては、以下の条件にてゲル浸透クロマトグラフィー(GPC)分析を行い、ポリスチレン換算の分子量を求めることにより測定した。
装置:Shodex GPC-101型(昭和電工(株)製)
カラム:KF-80M×3
溶離液:THF 1mL/min
温度:40℃
<実施例46>
国際公開2013/024779に記載されている下記式で表されるフェノール化合物(BisN-1)8質量部に、ビスシトラコンイミド化合物として、シトラコンイミドAを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
国際公開2013/024779に記載されている下記式で表されるフェノール化合物(BisN-1)8質量部に、ビスシトラコンイミド化合物として、シトラコンイミドAを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、5質量%以上10質量%未満(評価B)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例47>
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドDを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドDを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例48>
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドEを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドEを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例49>
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドFを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
上記式で表されるフェノール化合物(BisN-1)8質量部にビスシトラコンイミド化合物として、シトラコンイミドFを2質量部加え、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、20質量%以上(評価S)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<参考例1>
上記式で表されるフェノール化合物(BisN-1)10質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、10質量%以上20質量%未満(評価A)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
上記式で表されるフェノール化合物(BisN-1)10質量部を単独で用いて、リソグラフィー用膜形成材料とした。
熱重量測定の結果、得られたリソグラフィー用膜形成材料の400℃での熱重量減少量は10%未満(評価A)であった。また、PGMEAへの溶解性を評価した結果、10質量%以上20質量%未満(評価A)であり、得られたリソグラフィー用膜形成材料は必要な溶解性を有するものと評価された。
前記リソグラフィー用膜形成材料10質量部に対し、溶媒としてPGMEAを90質量部加え、室温下、スターラーで少なくとも3時間以上攪拌させることにより、リソグラフィー用膜形成用組成物を調製した。
<実施例1~41、比較例1~2>
表1に示す組成となるように、前記実施例1~41で得られたリソグラフィー用膜形成材料を用いて、実施例1~41及び比較例1~2に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例1~41、比較例1~2のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、240℃で60秒間、さらに400℃で120秒間ベークして、膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
表1に示す組成となるように、前記実施例1~41で得られたリソグラフィー用膜形成材料を用いて、実施例1~41及び比較例1~2に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例1~41、比較例1~2のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、240℃で60秒間、さらに400℃で120秒間ベークして、膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
<実施例42~45>
表2に示す組成となるように、前記実施例42~45に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例42~45のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、110℃で60秒間ベークして塗膜の溶媒を除去した後、高圧水銀ランプにより、積算露光量600mJ/cm2、照射時間20秒で硬化させて、さらに400℃で120秒間ベークして、膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
表2に示す組成となるように、前記実施例42~45に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例42~45のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、110℃で60秒間ベークして塗膜の溶媒を除去した後、高圧水銀ランプにより、積算露光量600mJ/cm2、照射時間20秒で硬化させて、さらに400℃で120秒間ベークして、膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
<実施例46~49並びに参考例1>
表3に示す組成となるように、前記実施例46~49並びに参考例1に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例46~49並びに参考例1のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、110℃で60秒間ベークして塗膜の溶媒を除去した後、高圧水銀ランプにより、積算露光量600mJ/cm2、照射時間20秒で硬化させて、さらに400℃で120秒間ベークして、
膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
表3に示す組成となるように、前記実施例46~49並びに参考例1に対応するリソグラフィー用膜形成用組成物を各々調製した。次いで、実施例46~49並びに参考例1のリソグラフィー用膜形成用組成物をシリコン基板上に回転塗布し、その後、110℃で60秒間ベークして塗膜の溶媒を除去した後、高圧水銀ランプにより、積算露光量600mJ/cm2、照射時間20秒で硬化させて、さらに400℃で120秒間ベークして、
膜厚200nmの下層膜を各々作製した。前記400℃でベーク前後の膜厚差から膜厚減少率(%)を算出して、各下層膜の膜耐熱性を評価した。そして、下記に示す条件にてエッチング耐性を評価した。
また、下記に示す条件にて、段差基板への埋め込み性、及び平坦性を評価した。
[膜耐熱性の評価]
<評価基準>
S:400℃ベーク前後の膜厚減少率≦10%
A:400℃ベーク前後の膜厚減少率≦15%
B:400℃ベーク前後の膜厚減少率≦20%
C:400℃ベーク前後の膜厚減少率>20%
<評価基準>
S:400℃ベーク前後の膜厚減少率≦10%
A:400℃ベーク前後の膜厚減少率≦15%
B:400℃ベーク前後の膜厚減少率≦20%
C:400℃ベーク前後の膜厚減少率>20%
[エッチング試験]
エッチング装置:サムコインターナショナル社製 RIE-10NR
出力:50W
圧力:4Pa
時間:2min
エッチングガス
CF4ガス流量:O2ガス流量=5:15(sccm)
エッチング装置:サムコインターナショナル社製 RIE-10NR
出力:50W
圧力:4Pa
時間:2min
エッチングガス
CF4ガス流量:O2ガス流量=5:15(sccm)
[エッチング耐性の評価]
エッチング耐性の評価は、以下の手順で行った。
まず、実施例1におけるリソグラフィー用膜形成材料に代えてノボラック(群栄化学社製PSM4357)を用い、乾燥温度を110℃にすること以外は、実施例1と同様の条件で、ノボラックの下層膜を作製した。そして、このノボラックの下層膜を対象として、上述のエッチング試験を行い、そのときのエッチングレートを測定した。
次に、実施例1~49、比較例1及び2並びに参考例1の下層膜を対象として、前記エッチング試験を同様に行い、そのときのエッチングレートを測定した。
そして、ノボラックの下層膜のエッチングレートを基準として、以下の評価基準でエッチング耐性を評価した。実用的観点からは、下記S評価が特に好ましく、A評価及びB評価が好ましい。
<評価基準>
S:ノボラックの下層膜に比べてエッチングレートが、-30%未満
A:ノボラックの下層膜に比べてエッチングレートが、-30%以上~-20%未満
B:ノボラックの下層膜に比べてエッチングレートが、-20%以上~-10%未満
C:ノボラックの下層膜に比べてエッチングレートが、-10%以上0%以下
エッチング耐性の評価は、以下の手順で行った。
まず、実施例1におけるリソグラフィー用膜形成材料に代えてノボラック(群栄化学社製PSM4357)を用い、乾燥温度を110℃にすること以外は、実施例1と同様の条件で、ノボラックの下層膜を作製した。そして、このノボラックの下層膜を対象として、上述のエッチング試験を行い、そのときのエッチングレートを測定した。
次に、実施例1~49、比較例1及び2並びに参考例1の下層膜を対象として、前記エッチング試験を同様に行い、そのときのエッチングレートを測定した。
そして、ノボラックの下層膜のエッチングレートを基準として、以下の評価基準でエッチング耐性を評価した。実用的観点からは、下記S評価が特に好ましく、A評価及びB評価が好ましい。
<評価基準>
S:ノボラックの下層膜に比べてエッチングレートが、-30%未満
A:ノボラックの下層膜に比べてエッチングレートが、-30%以上~-20%未満
B:ノボラックの下層膜に比べてエッチングレートが、-20%以上~-10%未満
C:ノボラックの下層膜に比べてエッチングレートが、-10%以上0%以下
[段差基板埋め込み性の評価]
段差基板への埋め込み性の評価は、以下の手順で行った。
リソグラフィー用下層膜形成用組成物を膜厚80nmの60nmラインアンドスペースのSiO2基板上に塗布して、240℃で60秒間ベークすることにより90nm下層膜を形成した。得られた膜の断面を切り出し、電子線顕微鏡にて観察し、段差基板への埋め込み性を評価した。
<評価基準>
A:60nmラインアンドスペースのSiO2基板の凹凸部分に欠陥無く下層膜が埋め込まれている。
C:60nmラインアンドスペースのSiO2基板の凹凸部分に欠陥があり下層膜が埋め込まれていない。
段差基板への埋め込み性の評価は、以下の手順で行った。
リソグラフィー用下層膜形成用組成物を膜厚80nmの60nmラインアンドスペースのSiO2基板上に塗布して、240℃で60秒間ベークすることにより90nm下層膜を形成した。得られた膜の断面を切り出し、電子線顕微鏡にて観察し、段差基板への埋め込み性を評価した。
<評価基準>
A:60nmラインアンドスペースのSiO2基板の凹凸部分に欠陥無く下層膜が埋め込まれている。
C:60nmラインアンドスペースのSiO2基板の凹凸部分に欠陥があり下層膜が埋め込まれていない。
[平坦性の評価]
幅100nm、ピッチ150nm、深さ150nmのトレンチ(アスペクト比:1.5)及び幅5μm、深さ180nmのトレンチ(オープンスペース)が混在するSiO2段差基板上に、上記得られた膜形成用組成物をそれぞれ塗布した。その後、大気雰囲気下にて、240℃で120秒間焼成して、膜厚200nmのレジスト下層膜を形成した。このレジスト下層膜の形状を走査型電子顕微鏡(日立ハイテクノロジーズ社の「S-4800」)にて観察し、トレンチ又はスペース上におけるレジスト下層膜の膜厚の最大値と最小値の差(ΔFT)を測定した。
<評価基準>
S:ΔFT<10nm(平坦性最良)
A:10nm≦ΔFT<20nm(平坦性良好)
B:20nm≦ΔFT<40nm(平坦性やや良好)
C:40nm≦ΔFT(平坦性不良)
幅100nm、ピッチ150nm、深さ150nmのトレンチ(アスペクト比:1.5)及び幅5μm、深さ180nmのトレンチ(オープンスペース)が混在するSiO2段差基板上に、上記得られた膜形成用組成物をそれぞれ塗布した。その後、大気雰囲気下にて、240℃で120秒間焼成して、膜厚200nmのレジスト下層膜を形成した。このレジスト下層膜の形状を走査型電子顕微鏡(日立ハイテクノロジーズ社の「S-4800」)にて観察し、トレンチ又はスペース上におけるレジスト下層膜の膜厚の最大値と最小値の差(ΔFT)を測定した。
<評価基準>
S:ΔFT<10nm(平坦性最良)
A:10nm≦ΔFT<20nm(平坦性良好)
B:20nm≦ΔFT<40nm(平坦性やや良好)
C:40nm≦ΔFT(平坦性不良)
<実施例50>
実施例5におけるリソグラフィー用膜形成用組成物を膜厚300nmのSiO2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚70nmの下層膜を形成した。この下層膜上に、ArF用レジスト溶液を塗布し、130℃で60秒間ベークすることにより、膜厚140nmのフォトレジスト層を形成した。ArF用レジスト溶液としては、下記式(22)の化合物:5質量部、トリフェニルスルホニウムノナフルオロメタンスルホナート:1質量部、トリブチルアミン:2質量部、及びPGMEA:92質量部を配合して調製したものを用いた。
なお、下記式(22)の化合物は、次のように調製した。すなわち、2-メチル-2-メタクリロイルオキシアダマンタン4.15g、メタクリルロイルオキシ-γ-ブチロラクトン3.00g、3-ヒドロキシ-1-アダマンチルメタクリレート2.08g、アゾビスイソブチロニトリル0.38gを、テトラヒドロフラン80mLに溶解させて反応溶液とした。この反応溶液を、窒素雰囲気下、反応温度を63℃に保持して、22時間重合させた後、反応溶液を400mLのn-ヘキサン中に滴下した。このようにして得られる生成樹脂を凝固精製させ、生成した白色粉末をろ過し、減圧下40℃で一晩乾燥させて下記式で表される化合物を得た。
実施例5におけるリソグラフィー用膜形成用組成物を膜厚300nmのSiO2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚70nmの下層膜を形成した。この下層膜上に、ArF用レジスト溶液を塗布し、130℃で60秒間ベークすることにより、膜厚140nmのフォトレジスト層を形成した。ArF用レジスト溶液としては、下記式(22)の化合物:5質量部、トリフェニルスルホニウムノナフルオロメタンスルホナート:1質量部、トリブチルアミン:2質量部、及びPGMEA:92質量部を配合して調製したものを用いた。
なお、下記式(22)の化合物は、次のように調製した。すなわち、2-メチル-2-メタクリロイルオキシアダマンタン4.15g、メタクリルロイルオキシ-γ-ブチロラクトン3.00g、3-ヒドロキシ-1-アダマンチルメタクリレート2.08g、アゾビスイソブチロニトリル0.38gを、テトラヒドロフラン80mLに溶解させて反応溶液とした。この反応溶液を、窒素雰囲気下、反応温度を63℃に保持して、22時間重合させた後、反応溶液を400mLのn-ヘキサン中に滴下した。このようにして得られる生成樹脂を凝固精製させ、生成した白色粉末をろ過し、減圧下40℃で一晩乾燥させて下記式で表される化合物を得た。
前記式(22)中、40、40、20とあるのは各構成単位の比率を示すものであり、ブロック共重合体を示すものではない。
次いで、電子線描画装置(エリオニクス社製;ELS-7500,50keV)を用いて、フォトレジスト層を露光し、115℃で90秒間ベーク(PEB)し、2.38質量%テトラメチルアンモニウムヒドロキシド(TMAH)水溶液で60秒間現像することにより、ポジ型のレジストパターンを得た。評価結果を表4に示す。
<実施例51>
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例6におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例6におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
<実施例52>
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例7におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例7におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
<実施例53>
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例8におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
前記実施例5におけるリソグラフィー用下層膜形成用組成物の代わりに実施例8におけるリソグラフィー用下層膜形成用組成物を用いること以外は、実施例50と同様にして、ポジ型のレジストパターンを得た。評価結果を表4に示す。
<比較例3>
下層膜の形成を行わないこと以外は、実施例33と同様にして、フォトレジスト層をSiO2基板上に直接形成し、ポジ型のレジストパターンを得た。評価結果を表4に示す。
下層膜の形成を行わないこと以外は、実施例33と同様にして、フォトレジスト層をSiO2基板上に直接形成し、ポジ型のレジストパターンを得た。評価結果を表4に示す。
[評価]
実施例50~53、及び比較例3のそれぞれについて、得られた55nmL/S(1:1)及び80nmL/S(1:1)のレジストパターンの形状を(株)日立製作所製の電子顕微鏡(S-4800)を用いて観察した。現像後のレジストパターンの形状については、パターン倒れがなく、矩形性が良好なものを良好とし、そうでないものを不良として評価した。また、当該観察の結果、パターン倒れが無く、矩形性が良好な最小の線幅を解像性として評価の指標とした。さらに、良好なパターン形状を描画可能な最小の電子線エネルギー量を感度として、評価の指標とした。
実施例50~53、及び比較例3のそれぞれについて、得られた55nmL/S(1:1)及び80nmL/S(1:1)のレジストパターンの形状を(株)日立製作所製の電子顕微鏡(S-4800)を用いて観察した。現像後のレジストパターンの形状については、パターン倒れがなく、矩形性が良好なものを良好とし、そうでないものを不良として評価した。また、当該観察の結果、パターン倒れが無く、矩形性が良好な最小の線幅を解像性として評価の指標とした。さらに、良好なパターン形状を描画可能な最小の電子線エネルギー量を感度として、評価の指標とした。
表4から明らかなように、ビスシトラコンイミド化合物を含む本実施形態のリソグラフィー用膜形成用組成物を用いた実施例50~53は、比較例3と比較して、解像性及び感度ともに有意に優れていることが確認された。また、現像後のレジストパターン形状もパターン倒れがなく、矩形性が良好であることが確認された。さらに、現像後のレジストパターン形状の相違から、実施例5~8のリソグラフィー用膜形成用組成物から得られる実施例50~53の下層膜は、レジスト材料との密着性が良いことが示された。
<実施例54~57>
実施例16、実施例28~30におけるリソグラフィー用膜形成用組成物を膜厚300nmのSiO2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚70nmの下層膜を形成した。
その後、光学顕微鏡にて膜表面を観察し、欠陥の有無を確認した。評価結果を表5に示す。
実施例16、実施例28~30におけるリソグラフィー用膜形成用組成物を膜厚300nmのSiO2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚70nmの下層膜を形成した。
その後、光学顕微鏡にて膜表面を観察し、欠陥の有無を確認した。評価結果を表5に示す。
<評価基準>
A:欠陥無し
B:欠陥がほぼ無い
C:欠陥あり
なお、欠陥とは光学顕微鏡による膜表面の観察において確認される異物の存在をいう。
A:欠陥無し
B:欠陥がほぼ無い
C:欠陥あり
なお、欠陥とは光学顕微鏡による膜表面の観察において確認される異物の存在をいう。
表5から明らかなように、ビスシトラコンイミド化合物を含む本実施形態のリソグラフィー用膜形成用組成物を用いた実施例54~57は、ビスマレイミド化合物を含む比較例4及び5と比較して、欠陥が低減された膜が得られることが確認された。
この原因は定かではないが、ビスマレイミド化合物より、ビスシトラコンイミド化合物の方が溶媒に対する溶解安定性が高く、および/または化合物同士の自己反応が起こり辛く、欠陥原因となる微小パーティクルが生成し難いためと推定している。
この原因は定かではないが、ビスマレイミド化合物より、ビスシトラコンイミド化合物の方が溶媒に対する溶解安定性が高く、および/または化合物同士の自己反応が起こり辛く、欠陥原因となる微小パーティクルが生成し難いためと推定している。
本実施形態のリソグラフィー用膜形成材料は、耐熱性が比較的に高く、溶媒溶解性も比較的に高く、段差基板への埋め込み特性及び膜の平坦性に優れ、湿式プロセスが適用可能である。そのため、リソグラフィー用膜形成材料を含むリソグラフィー用膜形成用組成物はこれらの性能が要求される各種用途において、広く且つ有効に利用可能である。とりわけ、本発明は、リソグラフィー用下層膜及び多層レジスト用下層膜の分野において、特に有効に利用可能である。
Claims (31)
- 前記式(0)の基を有する化合物が、ポリシトラコンイミド化合物及びシトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、請求項1に記載のリソグラフィー用膜形成材料。
- 前記式(0)の基を有する化合物が、ビスシトラコンイミド化合物及び付加重合型シトラコンイミド樹脂からなる群より選ばれる少なくとも1種である、請求項1又は2に記載のリソグラフィー用膜形成材料。
- 前記ビスシトラコンイミド化合物が下記式(1A)で表される、請求項3~5のいずれか一項に記載のリソグラフィー用膜形成材料。
Xはそれぞれ独立に、単結合、-O-、-CH2-、-C(CH3)2-、-CO-、-C(CF3)2-、-CONH-又は-COO-であり、
Aは、単結合、酸素原子、-(CH2)n-、-CH2C(CH3)2CH2-、-(C(CH3)2)n-、-(O(CH2)m2)n-、-(О(C6H4))n-、又は以下の構造のいずれかであり、
R1はそれぞれ独立に、ヘテロ原子を含んでいてもよい炭素数0~30の基であり、
nは0~20の整数であり、
m1及びm2はそれぞれ独立に、0~4の整数である。) - 架橋剤をさらに含有する、請求項1~7のいずれか一項に記載のリソグラフィー用膜形成材料。
- 前記架橋剤が、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物及びアジド化合物からなる群より選ばれる少なくとも1種である、請求項8に記載のリソグラフィー用膜形成材料。
- 前記架橋剤が、少なくとも1つのアリル基を有する、請求項8又は9に記載のリソグラフィー用膜形成材料。
- 前記架橋剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~100質量部である、請求項8~10のいずれか一項に記載のリソグラフィー用膜形成材料。
- 架橋促進剤をさらに含有する、請求項1~11のいずれか一項に記載のリソグラフィー用膜形成材料。
- 前記架橋促進剤が、アミン類、イミダゾール類、有機ホスフィン類、及びルイス酸からなる群より選ばれる少なくとも1種である、請求項12に記載のリソグラフィー用膜形成材料。
- 前記架橋促進剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.1~5質量部である、請求項12又は13に記載のリソグラフィー用膜形成材料。
- ラジカル重合開始剤をさらに含有する、請求項1~14のいずれか一項に記載のリソグラフィー用膜形成材料。
- 前記ラジカル重合開始剤が、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種である、請求項15に記載のリソグラフィー用膜形成材料。
- 前記ラジカル重合開始剤の含有割合が、ビスシトラコンイミド化合物と付加重合型シトラコンイミド樹脂との合計質量を100質量部とした場合に、0.05~25質量部である、請求項15又は16に記載のリソグラフィー用膜形成材料。
- 請求項1~17のいずれか一項に記載のリソグラフィー用膜形成材料と溶媒とを含有する、リソグラフィー用膜形成用組成物。
- 酸発生剤をさらに含有する、請求項18に記載のリソグラフィー用膜形成用組成物。
- リソグラフィー用膜がリソグラフィー用下層膜である、請求項18又は19に記載のリソグラフィー用膜形成用組成物
- 請求項20に記載のリソグラフィー用膜形成用組成物を用いて形成される、リソグラフィー用下層膜。
- 基板上に、請求項20に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、少なくとも1層のフォトレジスト層を形成する工程、及び
該フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程、
を含む、レジストパターン形成方法。 - 基板上に、請求項20に記載のリソグラフィー用膜形成用組成物を用いて下層膜を形成する工程、
該下層膜上に、珪素原子を含有するレジスト中間層膜材料を用いて中間層膜を形成する工程、
該中間層膜上に、少なくとも1層のフォトレジスト層を形成する工程、
該フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成する工程、
該レジストパターンをマスクとして前記中間層膜をエッチングする工程、
得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングする工程、及び
得られた下層膜パターンをエッチングマスクとして基板をエッチングすることで基板にパターンを形成する工程、
を含む、回路パターン形成方法。 - 請求項1~17のいずれか一項に記載のリソグラフィー用膜形成材料を、溶媒に溶解させて有機相を得る工程と、
前記有機相と酸性の水溶液とを接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第一抽出工程と、
を含み、
前記有機相を得る工程で用いる溶媒が、水と任意に混和しない溶媒を含む、精製方法。 - 前記酸性の水溶液が、鉱酸水溶液又は有機酸水溶液であり、
前記鉱酸水溶液が、塩酸、硫酸、硝酸及びリン酸からなる群より選ばれる1種以上を含み、
前記有機酸水溶液が、酢酸、プロピオン酸、蓚酸、マロン酸、コハク酸、フマル酸、マレイン酸、酒石酸、クエン酸、メタンスルホン酸、フェノールスルホン酸、p-トルエンスルホン酸及びトリフルオロ酢酸からなる群より選ばれる1種以上を含む、請求項24に記載の精製方法。 - 前記水と任意に混和しない溶媒が、トルエン、2-ヘプタノン、シクロヘキサノン、シクロペンタノン、メチルイソブチルケトン、プロピレングリコールモノメチルエーテルアセテート及び酢酸エチルからなる群より選ばれる1種以上の溶媒である、請求項24又は25に記載の精製方法。
- 前記第一抽出工程後、前記有機相を、水に接触させて、前記リソグラフィー用膜形成材料中の不純物を抽出する第二抽出工程をさらに含む、請求項24~26のいずれか一項に記載の精製方法。
- R2、又はR3及びR4が、アルキル基である、請求項28に記載の付加重合型シトラコンイミド樹脂。
- ヘテロ原子が酸素、フッ素、及びケイ素からなる群より選ばれる、請求項28又は29に記載の付加重合型シトラコンイミド樹脂。
- ヘテロ原子が酸素である、請求項28~30のいずれかに記載の付加重合型シトラコンイミド樹脂。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201980041635.7A CN112400138A (zh) | 2018-06-26 | 2019-06-24 | 光刻用膜形成材料、光刻用膜形成用组合物、光刻用下层膜和图案形成方法 |
| US17/255,745 US20210278767A1 (en) | 2018-06-26 | 2019-06-24 | Film forming material for lithography, composition for film formation for lithography, underlayer film for lithography, and method for forming pattern |
| EP19825077.1A EP3816728A4 (en) | 2018-06-26 | 2019-06-24 | FILM-FORMING MATERIAL FOR LITHOGRAPHY, FILM-FORMING COMPOSITION FOR LITHOGRAPHY, UNDER-LAYER FILM FOR LITHOGRAPHY AND METHOD FOR FORMING PATTERNS |
| KR1020207035825A KR102703439B1 (ko) | 2018-06-26 | 2019-06-24 | 리소그래피용 막형성재료, 리소그래피용 막형성용 조성물, 리소그래피용 하층막 및 패턴 형성방법 |
| JP2020527503A JP7336078B2 (ja) | 2018-06-26 | 2019-06-24 | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018120815 | 2018-06-26 | ||
| JP2018-120815 | 2018-06-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020004316A1 true WO2020004316A1 (ja) | 2020-01-02 |
Family
ID=68985466
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2019/024930 WO2020004316A1 (ja) | 2018-06-26 | 2019-06-24 | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20210278767A1 (ja) |
| EP (1) | EP3816728A4 (ja) |
| JP (1) | JP7336078B2 (ja) |
| KR (1) | KR102703439B1 (ja) |
| CN (1) | CN112400138A (ja) |
| TW (1) | TWI826475B (ja) |
| WO (1) | WO2020004316A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2022076516A (ja) * | 2020-11-10 | 2022-05-20 | 信越化学工業株式会社 | 低誘電樹脂組成物 |
| JP2022147022A (ja) * | 2021-03-23 | 2022-10-06 | 信越化学工業株式会社 | 熱硬化性シトラコンイミド樹脂組成物 |
| JPWO2022270529A1 (ja) * | 2021-06-25 | 2022-12-29 | ||
| JP2023526687A (ja) * | 2020-06-24 | 2023-06-22 | アークサーダ・アー・ゲー | 改善された特性を有する新規な組成物 |
| JP7523871B2 (ja) | 2021-08-02 | 2024-07-29 | 信越化学工業株式会社 | 熱硬化性樹脂組成物 |
Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02300223A (ja) * | 1989-05-16 | 1990-12-12 | Mitsubishi Petrochem Co Ltd | ポリイミド |
| JPH1112258A (ja) | 1997-06-20 | 1999-01-19 | Shikoku Chem Corp | 3−アリールジヒドロ−1,3−ベンゾオキサジン化合物の製法 |
| JPH11258802A (ja) * | 1998-03-16 | 1999-09-24 | Fuji Photo Film Co Ltd | ネガ型レジスト組成物 |
| JP2001220414A (ja) * | 2000-02-07 | 2001-08-14 | Toagosei Co Ltd | 活性エネルギー線硬化性組成物 |
| JP2002334869A (ja) | 2001-02-07 | 2002-11-22 | Tokyo Electron Ltd | シリコン窒化膜の形成方法、形成装置及びこの形成装置の洗浄前処理方法 |
| WO2004009708A1 (ja) | 2002-07-19 | 2004-01-29 | Nippon Steel Chemical Co., Ltd. | 硬化性樹脂組成物 |
| JP2004177668A (ja) | 2002-11-27 | 2004-06-24 | Tokyo Ohka Kogyo Co Ltd | 多層レジストプロセス用下層膜形成材料およびこれを用いた配線形成方法 |
| WO2004066377A1 (ja) | 2003-01-24 | 2004-08-05 | Tokyo Electron Limited | 被処理基板上にシリコン窒化膜を形成するcvd方法 |
| JP2004271838A (ja) | 2003-03-07 | 2004-09-30 | Shin Etsu Chem Co Ltd | レジスト下層膜材料ならびにパターン形成方法 |
| JP2004352670A (ja) | 2003-05-29 | 2004-12-16 | Shikoku Chem Corp | ベンゾオキサジン化合物、プリプレグ、積層板及びプリント配線板 |
| JP2005250434A (ja) | 2004-02-04 | 2005-09-15 | Shin Etsu Chem Co Ltd | レジスト下層膜材料ならびにパターン形成方法 |
| JP2007226170A (ja) | 2006-01-27 | 2007-09-06 | Shin Etsu Chem Co Ltd | 反射防止膜材料、反射防止膜を有する基板及びパターン形成方法 |
| JP2007226204A (ja) | 2006-01-25 | 2007-09-06 | Shin Etsu Chem Co Ltd | 反射防止膜材料、基板、及びパターン形成方法 |
| WO2009072465A1 (ja) | 2007-12-07 | 2009-06-11 | Mitsubishi Gas Chemical Company, Inc. | リソグラフィー用下層膜形成組成物及び多層レジストパターン形成方法 |
| WO2011034062A1 (ja) | 2009-09-15 | 2011-03-24 | 三菱瓦斯化学株式会社 | 芳香族炭化水素樹脂及びリソグラフィー用下層膜形成組成物 |
| WO2011108524A1 (ja) | 2010-03-02 | 2011-09-09 | 三菱瓦斯化学株式会社 | 樹脂組成物、プリプレグ、および積層板 |
| JP2012107087A (ja) * | 2010-11-16 | 2012-06-07 | Jnc Corp | 硬化性組成物 |
| WO2013024779A1 (ja) | 2011-08-12 | 2013-02-21 | 三菱瓦斯化学株式会社 | リソグラフィー用下層膜形成材料、リソグラフィー用下層膜及びパターン形成方法 |
| WO2015080240A1 (ja) | 2013-11-29 | 2015-06-04 | 三菱瓦斯化学株式会社 | 化合物又は樹脂の精製方法 |
| JP2015534598A (ja) * | 2012-09-25 | 2015-12-03 | プロメラス, エルエルシー | マレイミド含有シクロオレフィンポリマーおよびその利用 |
| WO2016129679A1 (ja) * | 2015-02-12 | 2016-08-18 | 三菱瓦斯化学株式会社 | 化合物、樹脂、リソグラフィー用下層膜形成材料、リソグラフィー用下層膜形成用組成物、リソグラフィー用下層膜、レジストパターン形成方法、回路パターン形成方法及び化合物又は樹脂の精製方法 |
| WO2018016614A1 (ja) | 2016-07-21 | 2018-01-25 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物及びパターン形成方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5638319A (en) * | 1979-09-06 | 1981-04-13 | Mitsubishi Electric Corp | Heat-resistant resin composition |
| FR2859730A1 (fr) * | 2003-09-15 | 2005-03-18 | Michelin Soc Tech | Composition de caoutchouc comportant un citracomaleimide. |
| TWI391788B (zh) * | 2007-04-06 | 2013-04-01 | 羅門哈斯電子材料有限公司 | 塗覆組成物 |
| WO2017126536A1 (ja) * | 2016-01-20 | 2017-07-27 | 三菱瓦斯化学株式会社 | 樹脂組成物、支持体付き樹脂シート、多層プリント配線板及び半導体装置 |
| JP7360630B2 (ja) * | 2018-02-28 | 2023-10-13 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物及びそれを用いたリソグラフィー用膜形成材料 |
-
2019
- 2019-06-24 CN CN201980041635.7A patent/CN112400138A/zh active Pending
- 2019-06-24 EP EP19825077.1A patent/EP3816728A4/en not_active Withdrawn
- 2019-06-24 WO PCT/JP2019/024930 patent/WO2020004316A1/ja unknown
- 2019-06-24 US US17/255,745 patent/US20210278767A1/en active Pending
- 2019-06-24 KR KR1020207035825A patent/KR102703439B1/ko active IP Right Grant
- 2019-06-24 JP JP2020527503A patent/JP7336078B2/ja active Active
- 2019-06-26 TW TW108122245A patent/TWI826475B/zh active
Patent Citations (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02300223A (ja) * | 1989-05-16 | 1990-12-12 | Mitsubishi Petrochem Co Ltd | ポリイミド |
| JPH1112258A (ja) | 1997-06-20 | 1999-01-19 | Shikoku Chem Corp | 3−アリールジヒドロ−1,3−ベンゾオキサジン化合物の製法 |
| JPH11258802A (ja) * | 1998-03-16 | 1999-09-24 | Fuji Photo Film Co Ltd | ネガ型レジスト組成物 |
| JP2001220414A (ja) * | 2000-02-07 | 2001-08-14 | Toagosei Co Ltd | 活性エネルギー線硬化性組成物 |
| JP2002334869A (ja) | 2001-02-07 | 2002-11-22 | Tokyo Electron Ltd | シリコン窒化膜の形成方法、形成装置及びこの形成装置の洗浄前処理方法 |
| WO2004009708A1 (ja) | 2002-07-19 | 2004-01-29 | Nippon Steel Chemical Co., Ltd. | 硬化性樹脂組成物 |
| JP2004177668A (ja) | 2002-11-27 | 2004-06-24 | Tokyo Ohka Kogyo Co Ltd | 多層レジストプロセス用下層膜形成材料およびこれを用いた配線形成方法 |
| WO2004066377A1 (ja) | 2003-01-24 | 2004-08-05 | Tokyo Electron Limited | 被処理基板上にシリコン窒化膜を形成するcvd方法 |
| JP2004271838A (ja) | 2003-03-07 | 2004-09-30 | Shin Etsu Chem Co Ltd | レジスト下層膜材料ならびにパターン形成方法 |
| JP2004352670A (ja) | 2003-05-29 | 2004-12-16 | Shikoku Chem Corp | ベンゾオキサジン化合物、プリプレグ、積層板及びプリント配線板 |
| JP2005250434A (ja) | 2004-02-04 | 2005-09-15 | Shin Etsu Chem Co Ltd | レジスト下層膜材料ならびにパターン形成方法 |
| JP2007226204A (ja) | 2006-01-25 | 2007-09-06 | Shin Etsu Chem Co Ltd | 反射防止膜材料、基板、及びパターン形成方法 |
| JP2007226170A (ja) | 2006-01-27 | 2007-09-06 | Shin Etsu Chem Co Ltd | 反射防止膜材料、反射防止膜を有する基板及びパターン形成方法 |
| WO2009072465A1 (ja) | 2007-12-07 | 2009-06-11 | Mitsubishi Gas Chemical Company, Inc. | リソグラフィー用下層膜形成組成物及び多層レジストパターン形成方法 |
| WO2011034062A1 (ja) | 2009-09-15 | 2011-03-24 | 三菱瓦斯化学株式会社 | 芳香族炭化水素樹脂及びリソグラフィー用下層膜形成組成物 |
| WO2011108524A1 (ja) | 2010-03-02 | 2011-09-09 | 三菱瓦斯化学株式会社 | 樹脂組成物、プリプレグ、および積層板 |
| JP2012107087A (ja) * | 2010-11-16 | 2012-06-07 | Jnc Corp | 硬化性組成物 |
| WO2013024779A1 (ja) | 2011-08-12 | 2013-02-21 | 三菱瓦斯化学株式会社 | リソグラフィー用下層膜形成材料、リソグラフィー用下層膜及びパターン形成方法 |
| JP2015534598A (ja) * | 2012-09-25 | 2015-12-03 | プロメラス, エルエルシー | マレイミド含有シクロオレフィンポリマーおよびその利用 |
| WO2015080240A1 (ja) | 2013-11-29 | 2015-06-04 | 三菱瓦斯化学株式会社 | 化合物又は樹脂の精製方法 |
| WO2016129679A1 (ja) * | 2015-02-12 | 2016-08-18 | 三菱瓦斯化学株式会社 | 化合物、樹脂、リソグラフィー用下層膜形成材料、リソグラフィー用下層膜形成用組成物、リソグラフィー用下層膜、レジストパターン形成方法、回路パターン形成方法及び化合物又は樹脂の精製方法 |
| WO2018016614A1 (ja) | 2016-07-21 | 2018-01-25 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物及びパターン形成方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3816728A4 |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023526687A (ja) * | 2020-06-24 | 2023-06-22 | アークサーダ・アー・ゲー | 改善された特性を有する新規な組成物 |
| JP7381778B2 (ja) | 2020-06-24 | 2023-11-16 | アークサーダ・アー・ゲー | 改善された特性を有する新規な組成物 |
| JP2022076516A (ja) * | 2020-11-10 | 2022-05-20 | 信越化学工業株式会社 | 低誘電樹脂組成物 |
| JP7383357B2 (ja) | 2020-11-10 | 2023-11-20 | 信越化学工業株式会社 | 低誘電樹脂組成物 |
| JP2022147022A (ja) * | 2021-03-23 | 2022-10-06 | 信越化学工業株式会社 | 熱硬化性シトラコンイミド樹脂組成物 |
| JP7451058B2 (ja) | 2021-03-23 | 2024-03-18 | 信越化学工業株式会社 | 熱硬化性シトラコンイミド樹脂組成物 |
| US12012485B2 (en) | 2021-03-23 | 2024-06-18 | Shin-Etsu Chemical Co., Ltd. | Heat-curable citraconimide resin composition |
| JPWO2022270529A1 (ja) * | 2021-06-25 | 2022-12-29 | ||
| JP7409564B2 (ja) | 2021-06-25 | 2024-01-09 | 住友ベークライト株式会社 | ネガ型感光性ポリマー、ポリマー溶液、ネガ型感光性樹脂組成物、硬化膜および半導体装置 |
| JP7523871B2 (ja) | 2021-08-02 | 2024-07-29 | 信越化学工業株式会社 | 熱硬化性樹脂組成物 |
| US12110356B2 (en) | 2021-08-02 | 2024-10-08 | Shin-Etsu Chemical Co., Ltd. | Heat-curable resin composition |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20210023845A (ko) | 2021-03-04 |
| EP3816728A4 (en) | 2021-08-11 |
| CN112400138A (zh) | 2021-02-23 |
| US20210278767A1 (en) | 2021-09-09 |
| JPWO2020004316A1 (ja) | 2021-08-02 |
| KR102703439B1 (ko) | 2024-09-06 |
| TW202014407A (zh) | 2020-04-16 |
| JP7336078B2 (ja) | 2023-08-31 |
| TWI826475B (zh) | 2023-12-21 |
| EP3816728A1 (en) | 2021-05-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI761512B (zh) | 微影用膜形成材料、微影用膜形成用組成物、微影用下層膜及圖型形成方法 | |
| KR102703439B1 (ko) | 리소그래피용 막형성재료, 리소그래피용 막형성용 조성물, 리소그래피용 하층막 및 패턴 형성방법 | |
| JP7438483B2 (ja) | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 | |
| JP7256482B2 (ja) | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 | |
| JP6889873B2 (ja) | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 | |
| JP7258279B2 (ja) | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 | |
| WO2021029320A1 (ja) | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 | |
| US20240319600A1 (en) | Film forming material for lithography, composition, underlayer film for lithography, and method for forming pattern | |
| WO2023032998A1 (ja) | スピンオンカーボン膜形成用組成物、スピンオンカーボン膜形成用組成物の製造方法、リソグラフィー用下層膜、レジストパターン形成方法、及び回路パターン形成方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 19825077 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2020527503 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2019825077 Country of ref document: EP Effective date: 20210126 |