WO2019082964A1 - 硬化性組成物 - Google Patents
硬化性組成物Info
- Publication number
- WO2019082964A1 WO2019082964A1 PCT/JP2018/039650 JP2018039650W WO2019082964A1 WO 2019082964 A1 WO2019082964 A1 WO 2019082964A1 JP 2018039650 W JP2018039650 W JP 2018039650W WO 2019082964 A1 WO2019082964 A1 WO 2019082964A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- curable composition
- compound
- meth
- agent
- composition according
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/06—Metallic compounds other than hydrides and other than metallo-organic compounds; Boron halide or aluminium halide complexes with organic compounds containing oxygen
- C08F4/10—Metallic compounds other than hydrides and other than metallo-organic compounds; Boron halide or aluminium halide complexes with organic compounds containing oxygen of alkaline earth metals, zinc, cadmium, mercury, copper or silver
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K6/00—Preparations for dentistry
- A61K6/70—Preparations for dentistry comprising inorganic additives
- A61K6/71—Fillers
- A61K6/73—Fillers comprising sulfur-containing compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F222/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides, or nitriles thereof
- C08F222/10—Esters
- C08F222/1006—Esters of polyhydric alcohols or polyhydric phenols
- C08F222/106—Esters of polycondensation macromers
- C08F222/1065—Esters of polycondensation macromers of alcohol terminated (poly)urethanes, e.g. urethane(meth)acrylates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/06—Metallic compounds other than hydrides and other than metallo-organic compounds; Boron halide or aluminium halide complexes with organic compounds containing oxygen
- C08F4/20—Metallic compounds other than hydrides and other than metallo-organic compounds; Boron halide or aluminium halide complexes with organic compounds containing oxygen of antimony, bismuth, vanadium, niobium or tantalum
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/40—Redox systems
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/10—Metal compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/10—Metal compounds
- C08K3/105—Compounds containing metals of Groups 1 to 3 or Groups 11 to 13 of the Periodic system
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/10—Metal compounds
- C08K3/11—Compounds containing metals of Groups 4 to 10 or Groups 14 to 16 of the Periodic system
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/15—Heterocyclic compounds having oxygen in the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/15—Heterocyclic compounds having oxygen in the ring
- C08K5/151—Heterocyclic compounds having oxygen in the ring having one oxygen atom in the ring
- C08K5/1535—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/16—Nitrogen-containing compounds
- C08K5/34—Heterocyclic compounds having nitrogen in the ring
- C08K5/35—Heterocyclic compounds having nitrogen in the ring having also oxygen in the ring
- C08K5/353—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/36—Sulfur-, selenium-, or tellurium-containing compounds
- C08K5/41—Compounds containing sulfur bound to oxygen
- C08K5/42—Sulfonic acids; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/36—Sulfur-, selenium-, or tellurium-containing compounds
- C08K5/45—Heterocyclic compounds having sulfur in the ring
- C08K5/46—Heterocyclic compounds having sulfur in the ring with oxygen or nitrogen in the ring
- C08K5/47—Thiazoles
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
- C08K2003/2248—Oxides; Hydroxides of metals of copper
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K2201/00—Specific properties of additives
- C08K2201/019—Specific properties of additives the composition being defined by the absence of a certain additive
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/16—Halogen-containing compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/0091—Complexes with metal-heteroatom-bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/05—Alcohols; Metal alcoholates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/09—Carboxylic acids; Metal salts thereof; Anhydrides thereof
- C08K5/098—Metal salts of carboxylic acids
Definitions
- the present invention relates to a curable composition.
- the technology to give a curable composition by polymerizing a polymerizable monomer is widely used industrially, and specifically, thermal polymerization, photo polymerization, normal temperature chemical polymerization can be mentioned, and a polymerizable monomer It is implemented by the method corresponding to the various polymerization catalysts mix
- These polymerization methods are also widely used in the dental treatment field, and, for example, dental adhesive resin cements classified as resin restoration materials, dental composite resins (including those having self-adhesiveness), dental adhesives Materials, dental cold polymerization resin, dental composite resin, dental backing, dental root filling, orthodontic adhesive, shaking tooth fixing material, tooth pit and fissure sealing material (dental sealant), etc. It is practically used as a polymerization technology for various adhesive materials and filling materials.
- the polymerization initiator to be mixed with the curable composition widely used for dental treatment materials mainly includes a photopolymerization initiator that is polymerized and cured by irradiating visible light, and two or more agents that are stored separately.
- chemical polymerization initiators that are mixed and polymerized / cured just before use, and recently, there are increasing cases of using materials in combination of both initiators in dental practice.
- the chemical polymerization initiator starts the polymerization reaction only by mixing and kneading the polymerization catalyst component at around normal temperature, and furthermore, it is necessary to polymerize and cure the polymerizable monomer at around normal temperature, Higher polymerization activity is required compared to the initiator system of
- An example of a general chemical polymerization initiator system widely used in the dental field is a redox polymerization initiator in which an oxidizing agent and a reducing agent are combined.
- the curable composition containing a redox polymerization initiator is generally used as a plurality of compositions divided into a first agent containing an oxidizing agent and a second agent containing a reducing agent, as a so-called packageable curable composition
- the chemical polymerization reaction is initiated by mixing the first agent and the second agent at the time of use, and the curing of the mixture proceeds. Therefore, since a combination of an oxidizing agent and a reducing agent that can cause a redox reaction can not usually be stored in the same preparation, they are stored as a packaged curable composition divided into three or more parts in some cases. There is a need.
- a curable composition containing a highly active chemical polymerization initiator for example, a redox polymerization initiator system in which a peroxide and a reducing substance are combined is known, and is also widely used in the field of dental materials.
- a dental curable composition comprising a first agent containing a diacyl peroxide compound such as benzoyl peroxide as the peroxide and a second agent containing an aromatic amine compound as the reducing material is known.
- Patent Document 1 A curable composition containing this chemical polymerization initiator is conventionally and widely used in the field of dental materials as it is possible to prepare a mixture in which the curing reaction proceeds smoothly even in the oral cavity at ordinary temperature.
- the curable composition containing benzoyl peroxide is often decomposed during storage at normal temperature to generate radicals due to the high polymerization activity of benzoyl peroxide, the composition cures during storage. Or, there is a problem that it is inactivated by the decomposition and can not maintain sufficient polymerizability after long-term storage.
- thermodynamically stable hydroperoxide compound As a curable composition which mix
- This chemically polymerizable curable composition has the feature of being excellent in storage stability at normal temperature compared with a composition using benzoyl peroxide by using a thermally stable peroxide. There is. However, its activity is lower than that of benzoyl peroxide and the like, and its curing time has room for improvement.
- Patent Documents 4 and 5 use a hydroperoxide compound as a peroxide, a curable composition including a chemical polymerization initiator composed of a thiourea compound as a reducing agent, and a transition metal compound as an accelerator. Proposed.
- These curable compositions are characterized by relatively high thermal stability and high storage stability at room temperature.
- these chemical polymerization initiator systems still have lower polymerization reactivity and longer curing time as compared with conventional chemical polymerization catalyst systems composed of benzoyl peroxide-aromatic amine compounds.
- these curable compositions have a large change with time of the operable time after storage, and there is a problem that the mixture obtained by mixing the first agent and the second agent after storage tends to solidify.
- Patent Document 6 also proposes a chemical polymerization initiator substantially composed of a peroxide, which is composed of a Lewis acidic compound, a tertiary amine compound and a sulfinic acid compound.
- the curable composition containing this chemical polymerization initiator is substantially free of peroxides, so that the storage stability is not influenced by the chemical stability of the peroxide, and it can be stored at ordinary temperature. Storage stability is greatly improved.
- the curable composition does not contain peroxide, its curing time is long, and its polymerizability has room for improvement.
- the curable composition In order for the curable composition to exhibit the desired performance, it is desired to have the polymerizability which ensures polymerization in the use environment of each material to give a cured product.
- an object of the present invention is to provide a curable composition having sufficient polymerizability even under acidic conditions.
- the present invention includes the matters described in the following [1] to [19].
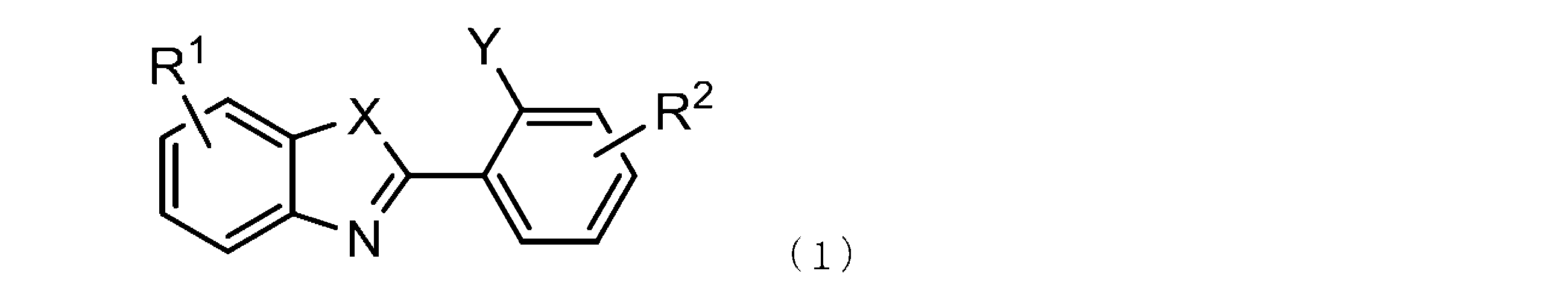
- X represents an oxygen atom or a sulfur atom
- Y represents a hydroxyl group or an amino group
- R 1 and R 2 each independently represent a hydrogen atom, a halogen atom, or a hydrocarbon having 1 to 4 carbon atoms
- the transition metal compound (b) is at least one selected from a copper compound and a vanadium compound.
- the total of the transition metal compound (b), the compound (c) and the reducing agent (d) is 0.1 to 40 parts by mass with respect to 100 parts by mass of the polymerizable monomer
- the curable composition according to any one of [1] to [10].
- a dental composition which is a base filling material, an orthodontic adhesive, a swaying tooth fixing material, a dental sealant, a temporary adhesive cement or a dental filling material.
- a kit for initiating polymerization comprising a first agent (A) and a second agent (B), wherein the first agent (A) is a transition from a polymerizable monomer (a) having an acidic group, Polymerization which contains a metal compound (b) and the second agent (B) contains at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds, and a reducing agent (d) Start kit.
- the curable composition of the present invention has sufficient polymerizability as a chemically polymerizable curable composition.
- (meth) acrylic means acrylic or methacrylic
- (meth) acrylic acid means “acrylic acid” or “methacrylic acid”.
- (meth) acryloyl means “acryloyl” or “methacryloyl”
- (meth) acrylate means “acrylate” or "methacrylate”.
- the curable composition of the present invention comprises a polymerizable monomer (a) having an acidic group, a transition metal compound (b), and at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds. And a reducing agent (d), and, if necessary, at least one selected from the components (e) to (j) described below and other components.
- the curable composition of the present invention has sufficient polymerizability as a chemically polymerizable curable composition.
- the curable composition of the present invention can give a cured product having sufficient strength as a cured product for dental materials.
- the curable composition of the present invention contains a chemical polymerization initiator.
- the curable composition of the present invention may be an embodiment comprising one agent and containing all the components in the agent, and a plurality of agents such as the first agent (A) and the second agent (B). It may be an embodiment in which it is packaged (packaged curable composition).
- the mixture obtained by mixing the plurality of agents packaged in the former aspect and the latter aspect in the latter aspect is particularly referred to as a "polymerizable mixture".
- a polymerizable mixture prepared by mixing and storing the above-mentioned respective agents for a long time at normal temperature or higher can give a curable composition which maintains sufficient polymerization activity.
- polymerizable monomer (a) which has an acidic group an acidic group containing radically polymerizable monomer is mentioned, for example, The polymerizable monomer conventionally used as a dental adhesive monomer is used it can.
- a radically polymerizable unsaturated group contained in an acidic group containing radically polymerizable monomer a (meth) acryloyl group, a (meth) acrylamide group, a styryl group, a vinyl group, an allyl group is mentioned, for example.
- a (meth) acryloyl group and a (meth) acrylamide group are preferable, and a methacryloyl group from the viewpoint of ease of elimination of the polymerizable group by hydrolysis etc. in the oral cavity, etc.
- a (meth) acrylamide group is more preferable, and a methacryloyl group is more preferable.
- an acidic group contained in the polymerizable monomer (a) having an acidic group for example, a carboxylic acid group, a carboxylic acid anhydride group, a phosphoric acid group, a thiophosphoric acid group, a pyrophosphoric acid group, a thiophosphoric acid group, a phosphonic acid Groups, thiophosphonic acid groups and sulfonic acid groups.
- acidic groups may be in the form of acid chlorides, alkali metal salts, alkaline earth metal salts, ammonium salts and the like.
- polymerizable monomer having a phosphoric acid group for example, 2- (meth) acryloyloxyethyl dihydrogen phosphate, 3- (meth) acryloyloxypropyl dihydrogen phosphate, 4- (meth) acryloyloxybutyl di- Hydrogen phosphate, 5- (meth) acryloyloxypentyl dihydrogen phosphate, 6- (meth) acryloyloxyhexyl dihydrogen phosphate, 7- (meth) acryloyloxyheptyl dihydrogen phosphate, 8- (meth) acryloyloxy Octyl dihydrogen phosphate, 9- (meth) acryloyloxynonyl dihydrogen phosphate, 10- (meth) acryloyl oxydecyl dihydrogen phosphate, 11- (meth) Acryloyl oxyundecyl dihydrogen phosphate, 12- (meth) acryloyloxybut
- Examples of the polymerizable monomer having a pyrophosphate group include bis [2- (meth) acryloyloxyethyl] pyrophosphate, bis [4- (meth) acryloyloxybutyl] pyrophosphate, and bis [6- (pyrophosphate). Meta) acryloyloxyhexyl], bis [8- (meth) acryloyloxyoctyl] pyrophosphate, bis [10- (meth) acryloyloxydecyl] pyrophosphate, and their acid chlorides, alkali metal salts, alkaline earth metals Salts and ammonium salts can be mentioned. Moreover, the compound which substituted the pyrophosphate group in these compounds to the thio pyrophosphate group is also mentioned.
- a polymerizable monomer having a phosphonic acid group for example, 2- (meth) acryloyloxyethyl phenylphosphonate, 5- (meth) acryloyloxypentyl-3-phosphonopropionate, 6- (meth) acryloyloxy Hexyl-3-phosphonopropionate, 10- (meth) acryloyloxydecyl-3-phosphonopropionate, 6- (meth) acryloyloxyhexyl-3-phosphonoacetate, 10- (meth) acryloyloxydecyl -3-phosphonoacetate, and their acid chlorides, alkali metal salts, alkaline earth metal salts, ammonium salts. Moreover, the compound which substituted the phosphonic acid group in these compounds to the thiophosphonic acid group is also mentioned.
- polymerizable monomer having a sulfonic acid group for example, 2-sulfoethyl (meth) acrylate, 2-sulfo-1-propyl (meth) acrylate, 1-sulfo-2-propyl (meth) acrylate, 1-sulfo -2-butyl (meth) acrylate, 3-sulfo-2-butyl (meth) acrylate, 3-bromo-2-sulfo-2-propyl (meth) acrylate, 3-methoxy-1-sulfo-2-propyl (meth) Acrylate, 1,1-dimethyl-2-sulfoethyl (meth) acrylamide, and their acid chlorides, alkali metal salts, alkaline earth metal salts, ammonium salts.
- Examples of the polymerizable monomer having a carboxylic acid group or a carboxylic acid anhydride group include, for example, monocarboxylic acid, dicarboxylic acid, tricarboxylic acid and tetracarboxylic acid or derivatives thereof.
- polymerizable monomers (a) having an acidic group 4-methacryloyloxyethyltrimellitic acid, 4-methacryloyloxyethyltrimellitic anhydride, 10-methacryloyloxydecyldihydrate from the viewpoint of adhesion to tooth substances.
- Hydrogen phosphate is preferred.
- the polymerizable monomer (a) having an acidic group may be used alone or in combination of two or more.
- the content of the polymerizable monomer (a) having an acidic group in the curable composition of the present invention is preferably 1 to 50 parts by mass, more preferably 3 with respect to 100 parts by mass of the total of the polymerizable monomers.
- the amount is about 35 parts by mass, more preferably 5 to 25 parts by mass. It exists in the tendency which is excellent in the polymerizability of a polymerizable mixture, and excellent in the adhesive strength and mechanical physical property of the cured
- the polymerizable monomer includes a polymerizable monomer (a) having an acidic group, and a polymerizable monomer (e) having no acidic group described later.
- each component is described in the present specification, in the case of the after-packing type curable composition described later, when the respective component amounts in the plurality of divided and packaged agents are totaled The total amount of each component may fall within the range described herein.
- the polymerizable composition of the present invention can be provided with sufficient polymerizability.
- a transition metal compound (b) a copper compound, a vanadium compound, a cobalt compound, a nickel compound, an iron compound, a molybdenum compound is mentioned, for example.
- copper compound for example, copper acetylacetonate, copper oleate, copper acetate, copper gluconate, copper citrate, copper phthalate, copper naphthenate, copper hydroxide, copper methoxide, copper ethoxide, copper isopropoxide, Examples thereof include monovalent or divalent copper compounds such as copper chloride and copper bromide.
- the vanadium compound is preferably at least one compound selected from trivalent to pentavalent vanadium compounds, for example, vanadium (III) acetylacetonate, vanadium (III) naphthenate, vanadyl stearate, vanadium benzoylacetonate, Bis (maltolate) oxovanadium (IV), oxobis (1-phenyl-1,3-butanedionate) vanadium (IV), vanadyl (IV) acetylacetonate, vanadium (IV) tetraoxide, vanadyl oxalate (IV) ), Vanadyl sulfate (IV), oxobis (1-phenyl-1,3-butanedionate) vanadium (IV), bis (maltolate) oxovanadium (IV), vanadium (V) oxytriisopropoxide, vanadium pentoxide (V), Metabana Sodium phosphate
- cobalt compounds include cobalt acetylacetonate, cobalt acetate, cobalt naphthenate, cobalt oleate, cobalt stearate, cobalt 2-ethylhexanoate, cobalt benzoate, cobalt oxalate, cobalt citrate, cobalt carbonate, nitrate Cobalt, cobalt sulfate, cobalt phosphate, cobalt perchlorate, cobalt thiocyanate, cobalt oxide, cobalt sulfide, cobalt fluoride, cobalt chloride, cobalt bromide, cobalt hydroxide, cobalt isopropoxide and the like.
- nickel compounds include nickel acetylacetonate, bis (dithiobenzyl) nickel, bis (cyclopentadienyl) nickel, nickel formate acetate, nickel acetate, nickel lactate, nickel naphthenate, nickel 2-ethylhexanoate, Acid, nickel citrate, nickel stearate, nickel perchlorate, nickel oxide, nickel sulfide, nickel fluoride, nickel chloride, nickel bromide, nickel iodide, nickel iodide, nickel carbonate, nickel nitrate, nickel sulfate, nickel hydroxide, Nickel ethoxide is mentioned.
- iron compound examples include iron acetylacetonate, ferrocene, iron acetate, iron stearate, iron 2-ethylhexanoate, iron oxalate, iron citrate, iron gluconate, iron nitrate, iron sulfate, iron phosphate, Examples thereof include iron perchlorate, iron oxide, iron sulfide, iron fluoride, iron chloride, iron bromide, potassium hexacyanoferrate and iron ethoxide.
- molybdenum compound examples include molybdenum oxide, molybdenum acetylacetonate oxide, molybdenium ethoxide, bis (2,4-pentadionato) molybdate molybdenium, molybdenil diethyl dithiocarbamate.
- transition metal compounds (b) it is preferable to use at least one selected from a copper compound and a vanadium compound, from the viewpoint of being excellent in the polymerizability of the polymerizable mixture and the stability during storage.
- a copper compound and a vanadium compound from the viewpoint of being excellent in the polymerizability of the polymerizable mixture and the stability during storage.
- monovalent or divalent copper chloride, copper bromide, copper acetate, vanadium (III) acetylacetonate, and vanadyl (IV) acetylacetonate are preferable from the viewpoint of solubility in a polymerizable monomer and handling.
- the transition metal compounds (b) may be used alone or in combination of two or more.
- the content of the transition metal compound (b) in the curable composition of the present invention is preferably 0.001 to 5 parts by mass, more preferably 0.005 to 3 with respect to 100 parts by mass of the polymerizable monomer. It is preferably in an amount of 0.01 to 1 part by mass. If the content of the transition metal compound (b) is less than the lower limit value, the effect of including the transition metal compound (b) may not be obtained, and if it is more than the upper limit value.
- the polymerizable monomer contained in the first agent (A) described later tends to be easily polymerized during storage.
- the curable composition of the present invention contains at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds.
- the compound (c) has an effect of enhancing the polymerization catalytic activity of the transition metal compound (b).
- the compound (c) By blending the compound (c) into the curable composition of the present invention, the polymerizability of the polymerizable mixture is improved.
- a cured product having good mechanical strength can be obtained, and discoloration of the cured product is less likely to occur, and an aesthetically good cured product can be obtained.
- the reason is that at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds functions as a ligand for the transition metal compound (b) to improve the polymerizability. It is guessed.
- reducing agents (d) when a compound that can also be classified as a compound (c) is used as the reducing agent (d), at least one selected from benzooxazole compounds and benzothiazole compounds other than the compound Species compounds can be used as compound (c). In one embodiment, when a compound that can be classified as a reducing agent (d) among the compounds (c) is used as the compound (c), a reducing agent (d) other than the compound is selected and used be able to.
- the compound having a mercapto group at the 2-position of the benzoxazole ring and the compound having a mercapto group at the 2-position of the benzothiazole ring have thiol-derived reactivity, and the polymerizable unit amount in the curable composition There is a risk of reaction between the body and the thiol. Therefore, it is preferable to remove a compound having a mercapto group at the 2-position of the benzoxazole ring and a compound having a mercapto group at the 2-position of the benzothiazole ring from the compound (c).
- the curable composition of the present invention also includes, as compound (c), a compound having a mercapto group at the 2-position of the benzoxazole ring and a compound having a mercapto group at the 2-position of the benzothiazole ring. Good.
- the compound (c) may be unsubstituted or may have any functional group as long as it has a benzoxazole ring and / or a benzothiazole ring, and known compounds can be used without limitation. .
- benzoxazole 2-methylbenzoxazole, 2-phenylbenzoxazole, 2- (2-benzoxazolyl) acetic acid, 2- (2-benzoxazolyl) maleic acid, 7 -Aminobenzoxazole, benzoxazole 4-carboxylic acid, benzoxazole 7-carboxylic acid, 2- (2-hydroxyphenyl) benzoxazole, 2- (2-aminophenyl) benzoxazole, benzothiazole, 2-methylbenzothiazole, 2-phenylbenzothiazole, 2- (2-benzothiazolyl) acetic acid, 2- (2-benzothiazolyl) maleic acid, 7-aminobenzothiazole, benzothiazole 4-carboxylic acid, benzothiazole 7-carboxylic acid, 2- (2- Hydroxyphenyl) benzoti Tetrazole, 2- (2-aminophenyl) benzothiazole.
- the compound (c) is preferably a compound represented by the following formula (1).
- X represents an oxygen atom or a sulfur atom
- Y represents a hydroxyl group or an amino group
- R 1 and R 2 each independently represent a hydrogen atom, a halogen atom, or a hydrocarbon group having 1 to 4 carbon atoms.
- the halogen atom includes a fluorine atom, a chlorine atom, a bromine atom and an iodine atom.
- hydrocarbon group having 1 to 4 carbon atoms examples include alkyl groups such as methyl group, ethyl group, n-propyl group, isopropyl group, n-butyl group, isobutyl group and tert-butyl group.
- Specific examples of the compound represented by the formula (1) include 2- (2-hydroxyphenyl) benzoxazole, 2- (2-aminophenyl) benzoxazole, 2- (2-hydroxyphenyl) benzothiazole, 2- (2- (2-hydroxyphenyl) benzothiazole) And 2-aminophenyl) benzothiazole.
- benzoxazole benzothiazole, and a compound represented by the formula (1) are preferable, and benzoxazole, 2- (2-hydroxyphenyl) benzoxazole , Benzothiazole and 2- (2-hydroxyphenyl) benzothiazole are more preferred.
- the compound (c) may be used alone or in combination of two or more.
- the content of the compound (c) in the curable composition of the present invention is preferably 0.1 to 20 parts by mass, more preferably 0.5 to 10 parts by mass with respect to 100 parts by mass of the polymerizable monomer. And more preferably 1 to 5 parts by mass.
- the curable composition of the present invention may not have the effect of improving the sufficient polymerizability.
- Reducing agent (d) examples include sulfur-based reducing agents, boron-based reducing agents, ascorbic acid or salts thereof, aldehydes, oxalic acid or salts thereof, and aromatic amine compounds.
- sulfur-based reducing agents include sulfinic acid or a salt thereof, sulfites such as sodium sulfite, bisulfites such as sodium bisulfite, pyrosulfites such as sodium metabisulfite, thiosulfates such as sodium thiosulfate, etc.
- boron-based reducing agent examples include aryl borate compounds such as tetraalkylboron, trialkylphenylboron, dialkyldiphenylboron, monoalkyltriphenylboron, tetraphenylboron and the like, or salts thereof.
- Aldehydes include, for example, terephthalaldehyde and benzaldehyde derivatives.
- At least one selected from sulfinic acid, salts of sulfinic acid, ascorbic acid and salts of ascorbic acid is preferable because it is possible to particularly improve the polymerizability.
- the salt examples include alkali metal salts such as sodium salt, potassium salt and lithium salt, alkaline earth metal salts such as magnesium salt, calcium salt and barium salt, amine salt, ammonium salt and pyridinium salt.
- the aromatic amine compound has an excellent polymerization promoting effect when it is added to the curable composition as a reducing agent.
- the aromatic amine compound when used together with the polymerizable monomer (a) having an acidic group, the aromatic amine compound may be deactivated by neutralization, and the polymerization promoting effect may be reduced.
- the curable composition of the present invention can exhibit sufficient polymerizability even in such an embodiment, but it is preferable to use a reducing agent other than the aromatic amine compound from the viewpoint of the above-mentioned deactivation.
- sulfinic acid or a salt thereof is particularly preferable because it improves the polymerizability, suppresses discoloration and the like to be good in aesthetics and is suitable for dental use.
- the sulfinic acid or a salt thereof is described in detail below.
- At least one compound selected from sulfinic acid and a salt thereof (d1) >> By including at least one compound (d1) selected from sulfinic acid and a salt thereof in the curable composition, the effect of improving the polymerizability of the curable composition of the present invention is obtained.
- At least one compound (d1) selected from sulfinic acid and its salt for example, methanesulfinic acid, ethanesulfinic acid, propanesulfinic acid, hexanesulfinic acid, octanesulfinic acid, decanesulfinic acid, dodecanesulfinic acid and the like Alkanesulfinic acids; Cycloaliphatic sulfinic acids such as cyclohexanesulfinic acid and cyclooctanesulfinic acid; Benzenesulfinic acid, o-toluenesulfinic acid, p-toluenesulfinic acid, ethylbenzenesulfinic acid, decylbenzenesulfinic acid, dodecylbenzenesulfinic acid, Aromatics such as 2,4,6-trimethylbenzenesulfinic acid, 2,4,6-triethylbenzenesulfinic acid, 2,4,
- the reducing agent (d) may be used alone or in combination of two or more.
- the content of the reducing agent (d) in the curable composition of the present invention is preferably 0.01 to 20 parts by mass, more preferably 0.1 to 10 parts by mass with respect to 100 parts by mass of the polymerizable monomer. Part, more preferably 1 to 5 parts by mass. If it is such an aspect, it tends to be excellent in polymerization nature in consideration of hardening time of a polymerization mixture, and operation possible time, and adhesive strength of a hardened material obtained.
- the reducing agent (d) is at least one compound (d1) selected from sulfinic acid and a salt thereof, the above content is preferable.
- the total of the transition metal compound (b), the compound (c) and the reducing agent (d) in the curable composition of the present invention is preferably 0.1 to 100 parts by mass of the polymerizable monomer.
- the amount is 40 parts by mass, more preferably 0.5 to 23 parts by mass, and still more preferably 1 to 10 parts by mass.
- the polymerizability and storage stability of the curable composition and the mechanical strength of the cured product provided by the curable composition tend to be excellent.
- Polymerizable monomer having no acidic group (e) By including the polymerizable monomer (e) having no acidic group in the curable composition, various physical properties of the resulting cured product, such as mechanical strength and adhesive strength, can be improved. Moreover, the fluidity
- a polymerizable monomer (e) which does not have an acidic group the radically polymerizable monomer which does not have an acidic group is mentioned, for example.
- a (meth) acryloyl group, a (meth) acrylamide group, a styryl group, a vinyl group, an allyl group is mentioned, for example .
- a (meth) acryloyl group and a (meth) acrylamide group are preferable, and a methacryloyl group from the viewpoint of ease of elimination of the polymerizable group by hydrolysis etc. in the oral cavity, etc.
- a (meth) acrylamide group is more preferable, and a methacryloyl group is more preferable.
- Hydroxyalkyl (meth) such as 2-hydroxyethyl (meth) acrylate, 3-hydroxypropyl (meth) acrylate, 4-hydroxybutyl (meth) acrylate, 6-hydroxyhexyl (meth) acrylate, 10-hydroxydecyl (meth) acrylate ) Acrylate, 2- (dimethylamino) ethyl (meth) acrylate, N-methyl-N-phenylaminoethyl (meth) acrylate, N-ethyl-N-phenylaminoethyl (meth) acrylate, propylene glycol mono (meth) acrylate , Glycerol mono (meth) acrylate, erythritol mono (meth) acrylate, N-methylol (meth) acrylamide, N-hydroxyethyl (meth) acrylamide, N, N- (
- radical polymerizable monomers (e) having no acidic group 1,6-bis (methacryloxyethyloxycarbonylamino) -2,2,4-trimethylhexane from the viewpoint of physical properties and handling ease
- UDMA bisphenol A diglycidyl methacrylate
- Bis-GMA bisphenol A diglycidyl methacrylate
- 2,2-bis (4-methacryloyloxypolyethoxyphenyl) propane generally called “ D-2.6 E ′ ′
- 2-hydroxyethyl methacrylate (HEMA), glycerol dimethacrylate (GDMA), triethylene glycol dimethacrylate (TEGDMA) are preferred.
- the polymerizable monomers (e) having no acidic group may be used alone or in combination of two or more.
- the content of the polymerizable monomer (e) having no acidic group in the curable composition of the present invention is preferably 50 to 99 parts by mass, and more preferably 100 parts by mass in total of the polymerizable monomers. Is 65 to 97 parts by mass, more preferably 75 to 95 parts by mass. With such an embodiment, the flowability of the curable composition can be improved, and the mechanical strength, adhesive strength, etc. of the cured product obtained from the polymerizable mixture can be improved.
- the curable composition of the present invention may be substantially free of peroxide (f), but may contain peroxide (f) depending on the embodiment.
- peroxide (f) peroxide (f)
- the curable composition of the present invention may be substantially free of peroxide (f), but may contain peroxide (f) depending on the embodiment.
- peroxides (f) known compounds can be used without any limitation.
- diasilver oxide compounds such as benzoyl peroxide, peroxy ester compounds such as t-butylperoxybenzoate, alkyl peroxides such as 1,1-di (t-butylperoxy) cyclohexane, 1,1,3 And hydroperoxide compounds such as 2,3-tetramethylbutyl hydroperoxide, and inorganic peroxides such as persulfates.
- Peroxy ester compounds and hydroperoxide compounds are particularly preferable in terms of the effect obtained when they are added to the curable composition of the present invention.
- a vanadium compound is used as the transition metal compound (b)
- Any peroxy ester compound may be used without any limitation as long as it has an acyl group on one side of the peroxy group (-OO- group) and a hydrocarbon group (or an organic group similar thereto) on the other side.
- Can. Specifically, t-butyl peroxyisobutyrate, t-butyl peroxy laurate, t-butyl peroxy-2-ethylhexyl monocarbonate, t-butyl peroxy isononanoate, t-butyl peroxy acetate, t-Butyl peroxybenzoate, t-butyl peroxy-3,5,5-trimethylhexanoate, 2,5-dimethyl-2,5-bis (2-ethylhexanoyl peroxy) hexane, cumyl peroxy neo Decanoate, 1,1,3,3-Tetramethylbutylperoxy neodecanoate, 2,5-Dimethyl-2,5-bis (m-
- hydroperoxide compound any known peroxy group (-OO- group) having a hydrocarbon group (or an organic group similar thereto) on one side and a hydrogen on the other side may be used without any limitation. it can.
- p-menthane hydroperoxide, diisopropylbenzene hydroperoxide, 1,1,3,3-tetramethylbutyl hydroperoxide, cumene hydroperoxide, t-hexyl hydroperoxide, t-amyl hydroperoxide Peroxide is mentioned.
- 1,1,3,3-tetramethylbutyl hydroperoxide and cumene hydroperoxide are preferable from the viewpoint of storage stability and polymerization activity.
- the peroxide (f) may be used singly or in combination of two or more.
- the peroxide (f) When the peroxide (f) is added to the curable composition of the present invention, it may be added in such a range that the curing time of the polymerizable mixture, the operable time, and the color stability of the obtained cured product are not adversely affected.
- the content of the peroxide (f) in the curable composition of the present invention is preferably 0.01 to 5 parts by mass, more preferably 0.05 to 3 parts by mass with respect to 100 parts by mass of the polymerizable monomer. It is preferably in an amount of 0.1 to 1 part by mass.
- the curable composition of the present invention may be substantially free of peroxide (f).
- the content of the peroxide (f) in the curable composition of the present invention is that the curable composition of the present invention does not substantially contain the peroxide (f). It means that it is less than 0.01 mass part with respect to 100 mass parts of monomers.
- the curable composition of the present invention is one preferred embodiment that the photopolymerization initiator (g) contains.
- a photopolymerization initiator (g) into the curable composition of the present invention, it becomes possible to provide a dual cure type curable composition, and it becomes possible to cure the composition by light irradiation.
- photopolymerization initiator (g) known ones can be used without any limitation, and examples thereof include ⁇ -diketone / reducing agent, ketal / reducing agent, thioxanthone / reducing agent, and acyl phosphine oxide compound.
- the ⁇ -diketone / reducing agent means a combination of ⁇ -diketone and a reducing agent, and the other examples are also the same.
- “reducing agent” in the ⁇ -diketone / reducing agent means a reducing agent in the photopolymerization initiator (g), and the above-mentioned reducing agent (d) used as a reducing agent in the chemical polymerization initiator is included Absent. The other examples are also the same.
- the photopolymerization initiator (g) is an ⁇ -diketone / aromatic amine compound
- at least one of the hydrogen atoms bonded to the aromatic ring of the aromatic amine compound is substituted with an electron-withdrawing group (including a halogen group) It is further preferable to include the aromatic amine compound.
- ⁇ -diketones include diacetyl, 2,3-pentadione, 2,3-hexadione, benzyl, 4,4′-dimethoxybenzyl, 4,4′-diethoxybenzyl, 4,4′-oxybenzyl, 4 , 4'-Dichlorobenzyl, 4-nitrobenzyl, ⁇ -naphthyl, ⁇ -naphthyl, camphorquinone (CQ), camphorquinone sulfonic acid, camphorquinone carboxylic acid, 1,2-cyclohexanedione, methylglyoxal, phenylglyoxal And pyruvic acid, benzoylformic acid, phenylpyruvic acid, methyl pyruvate, ethyl benzoylformate, methyl phenylpyruvate and butyl phenylpyruvate.
- ketals examples include benzyl dimethyl ketal and benzyl diethyl ketal.
- thioxanthone for example, 2-chlorothioxanthone, 2,4-diethylthioxanthone, 2-hydroxy-3- (9-oxy-9H-thioxanthen-4-yloxy) -N, N, N-trimethyl-propanaminium Chloride, 2-hydroxy-3- (1-methyl-9-oxy-9H-thioxanthen-4-yloxy) -N, N, N-trimethyl-propanaminium chloride, 2-hydroxy-3- (9-oxo -9H-thioxanthen-2-yloxy) -N, N, N-trimethyl-propanaminium chloride, 2-hydroxy-3- (3,4-dimethyl-9-oxo-9H-thioxanthen-2-yloxy) -N, N, N-trimethyl-1-propaneaminium chloride, 2-hydroxy-3- (3,4 Dimethyl-9H-thioxanthen-2-yloxy) -N, N, N-trimethyl-1-propaneaminium
- acyl phosphine oxide compound for example, benzoyldimethoxyphosphine oxide, benzoylethoxyphenylphosphine oxide, benzoyldiphenylphosphine oxide, 2-methylbenzoyldiphenylphosphine oxide, 2,4,6-trimethylbenzoyldiphenylphosphine oxide, bis (2,6 And -dimethoxybenzoyl) -2,4,4-trimethylpentylphosphine oxide and bis (2,4,6-trimethylbenzoyl) -phenylphosphine oxide.
- the reducing agent examples include peroxides such as hydrogen peroxide, Michler's ketone; Aldehydes such as citronellal, lauryl aldehyde, phthaldialdehyde, dimethylamino benzaldehyde and terephthalaldehyde; Mercaptans such as decanethiol, 3-mercaptopropyltrimethoxysilane, 4-mercaptoacetophenone, thiosalicylic acid, thiobenzoic acid; N, N-Dimethylaminobenzoic acid and its alkyl esters such as methyl N, N-dimethylaminobenzoate, ethyl N, N-dimethylaminobenzoate (DMABAE), butoxyethyl N, N-dimethylaminobenzoate (DMABABE) And aromatic rings of N, N-diethylaminobenzoic acid (DEABA) and its alkyl ester, N, N-di
- photopolymerization initiators (g) preferred are photopolymerization initiators containing a camphor quinone and / or an acyl phosphine oxide compound from the viewpoint of having an absorption wavelength in the visible light region and being capable of polymerizing by visible light.
- a photopolymerization initiator containing camphorquinone having an absorption wavelength at 468 nm is more preferable.
- Examples of the photopolymerization initiator containing a camphor quinone / reducing agent include a polymerization initiator containing a camphor quinone / aromatic amine compound, and a photo polymerization initiator containing a peroxide such as camphor quinone / hydrogen peroxide Examples thereof include a polymerization initiator containing camphorquinone / aldehydes, and a polymerization initiator containing camphorquinone / mercaptans. Among these, a polymerization initiator containing camphorquinone / aromatic amine compound is preferable.
- the aromatic amine compound to be used DMABAE and DMABABE are preferable from the viewpoint of the polymerization promoting effect of photopolymerization and handling.
- the photopolymerization initiator (g) may be used alone or in combination of two or more.
- the content of the photopolymerization initiator (g) in the curable composition of the present invention is preferably 0.001 to 5 parts by mass, more preferably 0.005 to 5 parts by mass with respect to 100 parts by mass of the polymerizable monomer.
- the amount is 2 parts by mass, more preferably 0.01 to 1 part by mass.
- the content of the photopolymerization initiator (g) is less than the above lower limit, curing of the curable composition by light irradiation may not proceed sufficiently, and when it is more than the above upper limit, the polymerizable mixture is a light
- the color tone may be derived from the polymerization initiator (g), or the composition may be cured during storage.
- the curable composition of the present invention may contain a filler (h).
- a filler (h) By containing the filler (h) in the curable composition, for example, the flowability, consistency, color tone and curability of the curable composition can be adjusted, and the X-ray opaqueness is imparted, The mechanical strength of the cured product can be improved.
- the filler (h) commonly known and widely used fillers can be used without limitation.
- Fillers (h) are usually roughly classified into organic fillers and inorganic fillers.
- the organic filler is obtained, for example, by polymerizing a filler of a powdery polymer obtained by pulverizing a polymer or dispersing and polymerizing a polymerizable monomer, and a polymerizable monomer containing a crosslinking agent, followed by pulverization. Fillers are included.
- the organic filler for example, polymethyl methacrylate (PMMA), polyethyl methacrylate, polypropyl methacrylate, polybutyl methacrylate (PBMA), polyvinyl acetate (PVAc), polyethylene glycol (PEG) and polypropylene glycol (PPG) ), Polyvinyl alcohol (PVA), polyurethane, polyurea, methyl methacrylate-ethyl methacrylate copolymer, crosslinked polymethyl methacrylate, crosslinked polyethyl methacrylate, ethylene-vinyl acetate copolymer and styrene-butadiene copolymer
- the fine powder of the homopolymer or copolymer of polymeric monomers, such as a coalescence etc. is mentioned.
- the organic filler may be one obtained by adding a known pigment, a biologically active component, a component such as a polymerization initiator at the time of preparation of the organic filler.
- various glasses containing silicon dioxide as a main component and optionally containing oxides such as heavy metals, boron and aluminum
- various ceramics diatomaceous earth, kaolin, clay minerals (montmorillonite etc.)
- Activated clay synthetic zeolite, mica, calcium fluoride, ytterbium fluoride, calcium carbonate, calcium phosphate, aluminum sulfate, barium sulfate, calcium sulfate, zirconium sulfate, zirconium dioxide, titanium dioxide, aluminum oxide, aluminum oxide, boron oxide, barium oxide, lanthanum oxide, oxide Strontium, zinc oxide, calcium oxide, lithium oxide, sodium oxide, bismuth oxide, yttrium oxide, calcium phosphate, hydroxyapatite, aluminum hydroxide, sodium fluoride, potassium fluoride, monofluo Sodium phosphate, lithium fluoride, and a fine powder such as ytterbium fluoride.
- inorganic fillers include, for example, barium borosilicate glass fine powder (Kimble laysorb T3000, shot 8235, shot GM27884, shot G018-053 and shot GM39923, etc.), strontium boroaluminosilicate glass fine powder (Raysorb) T4000, shot G018-093, shot G018-163 and shot GM32087 etc.) fine powder of lanthanum glass (eg shot GM31684), fine powder of fluoroaluminosilicate glass (eg shot G018-091 and shot G018-117), zirconium and / or Cesium-containing boroaluminosilicate glass fine powder (shots G018-307, G018-308 and G018-31 And the like).
- barium borosilicate glass fine powder Kimble laysorb T3000, shot 8235, shot GM27884, shot G018-053 and shot GM39923, etc.
- a polymerizable monomer may be added to these inorganic fillers in advance to form a paste, which may be polymerized and cured, and then an organic-inorganic composite filler obtained by grinding may be used.
- the organic-inorganic composite filler is obtained, for example, by polymerizing and coating fine powder silica or zirconium oxide of the inorganic filler with a polymerizable monomer having trimethylolpropane tri (meth) acrylate (TMPT) as a main component. And fillers obtained by grinding the polymer (TMPT ⁇ f).
- a dental material containing a microfiller having a particle size of 0.1 ⁇ m or less is one of the preferred embodiments for a dental composite resin.
- a material of the filler having such a small particle diameter silica (for example, trade name Aerosil), alumina, zirconia, titania and the like are preferable.
- the incorporation of such a small particle size inorganic filler is advantageous in obtaining the abrasion resistance and the abrasion resistance of the cured product.
- fillers are surface-treated with a silane coupling agent or the like according to the purpose.
- a silane coupling agent or the like according to the purpose.
- a surface treatment agent known silane coupling agents can be used without limitation.
- ⁇ -methacryloxyalkyltrimethoxysilane (number of carbons between methacryloxy group and silicon atom: 3 to 12)
- ⁇ -methacryloxyalkyltriethoxysilane (number of carbon atoms between methacryloxy group and silicon atom) 3-12)
- organosilicon compounds such as vinyltrimethoxysilane, vinylethoxysilane and vinyltriacetoxysilane are used.
- concentration of the surface treating agent is usually in the range of 0.1 to 20 parts by mass, preferably 0.5 to 10 parts by mass, with respect to 100 parts by mass of the filler.
- silane coupling agent In addition to the silane coupling agent, it may be surface-treated with a titanate coupling agent, an aluminate coupling agent, a zirco-aluminate coupling agent or the like. Furthermore, the radical polymerizable monomer may be graft-polymerized on the surface of the filler particles.
- a method of surface treatment known methods can be used without particular limitation.
- fillers (h) can be suitably added according to the use of the curable composition of the present invention.
- the filler (h) may be used alone or in combination of two or more.
- the content of the filler (h) can be appropriately set according to the application.
- the content of the filler (h) is based on 100 parts by mass of the total of the polymerizable monomers contained in the first agent (A) and the second agent (B).
- the amount is preferably 10 to 900 parts by mass, more preferably 40 to 400 parts by mass, and still more preferably 60 to 240 parts by mass.
- Such a mode is preferable when the packaged curable composition of the present invention is used as a dental adhesive resin cement or a dental composite resin.
- the curable composition of the present invention may contain an organic solvent (i).
- the organic solvent (i) include acetone, ethanol, isopropanol, tetrahydrofuran, acetonitrile, acetonitrile, hexane, toluene, ethyl acetate and dichloromethane.
- a water-soluble organic solvent such as acetone, ethanol or isopropanol from the viewpoint of adhesiveness and affinity to tooth surfaces.
- the water-soluble organic solvent is an organic solvent which forms a uniform solution with water at an arbitrary ratio.
- the curable composition of the present invention may contain water (j).
- water (j) it is preferable to use distilled water or ion exchange water so that there is no impurity that adversely affects the polymerizability and adhesion.
- the content thereof is preferably 100 parts by mass in total of the polymerizable monomer, the organic solvent (i) and water (j). Is 5 to 95 parts by mass, more preferably 10 to 90 parts by mass, and still more preferably 20 to 75 parts by mass. In such an embodiment, the uniformity, flowability, and adhesive strength of the curable composition of the present invention can be improved.
- the content thereof is preferably 100 parts by mass in total of the polymerizable monomer, the organic solvent (i) and water (j).
- the amount is 0.5 to 50 parts by mass, more preferably 1 to 40 parts by mass, and still more preferably 5 to 30 parts by mass. In such an embodiment, the uniformity, flowability, and adhesive strength of the curable composition of the present invention can be improved.
- the curable composition of the present invention may appropriately contain other components other than the above depending on the purpose, as long as the storage stability and the function as the curable composition are not impaired.
- various stabilizers such as a polymerization inhibitor and an ultraviolet light absorber may be contained, and in order to adjust the color tone, known pigments, dyes, and fluorescence You may contain an agent etc.
- calcium-containing compounds such as calcium chloride, fluorine-containing compounds such as sodium fluoride, fungicides, antibacterial agents, therapeutic and biologically active ingredients, and the like may be contained.
- reinforcements such as a well-known fiber.
- the content of each of the other components described above is preferably 0.00001 to 10 with respect to 100 parts by mass of the polymerizable monomer from the viewpoints of not impairing the effects of the present invention and exhibiting the characteristics of the other components.
- the amount is preferably in the range of 0.00005 to 5 parts by mass, and more preferably 0.0001 to 1 parts by mass.
- the curable composition of the present invention may be, for example, a plurality of agents such as the first agent (A) and the second agent (B), that is, a packaged curable composition,
- the form of each of these agents may be, for example, the form of a paste, a liquid or the like.
- both the first agent (A) and the second agent (B) be in the form of paste or liquid from the viewpoint of easy handling.
- the curable composition of the present invention is a two-paste composition in which both the first agent (A) and the second agent (B) are a paste-like preparation, it is suitable for dental adhesive resin cement.
- the curable composition of the present invention is a two-component composition in which both the first agent (A) and the second agent (B) are liquid preparations, it is suitable for a dental adhesive.
- the packaged curable composition may have other agents such as the third agent (C).
- the curable composition of the present invention is usually composed of a first agent (A) and a second agent (B), and each component is stored separately in each preparation as needed.
- Each component contained in the first agent (A) may be further packaged in a plurality of agents.
- Each component contained in the second agent (B) may be further packaged in a plurality of agents.
- the first agent (A) preferably contains a polymerizable monomer (a) having an acidic group and a transition metal compound (b).
- the first agent (A) contains the polymerizable monomer (a) having an acidic group and the transition metal compound (b), so that the performance is not impaired during storage, and the second agent There is no adverse effect on the components contained in (B).
- the second agent (B) comprises at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds, and a reducing agent (d) (for example, at least one compound selected from sulfinic acid and salts thereof ( It is preferable to contain d1).
- a reducing agent (d) for example, at least one compound selected from sulfinic acid and salts thereof ( It is preferable to contain d1).
- the polymerizable monomer (e) having no acidic group may be contained in either or both of the first agent (A) and the second agent (B). Preferably, it is included.
- the polymerizable monomer (e) having no acidic group is contained in both the first agent (A) and the second agent (B), one contained in the first agent (A) Those contained in the agent (B) may be the same or different.
- the peroxide (f) is preferably contained in the second agent (B).
- the peroxide (f) does not adversely affect the components in the first agent (A) during storage, and its activity tends not to decrease during storage .
- the photopolymerization initiator (g) is preferably contained in the second agent (B) from the viewpoint of storage stability.
- a photoinitiator (g) in another agent (for example, 3rd agent (C)) other than 1st agent (A) and 2nd agent (B).
- a photoinitiator (g) in another agent (for example, 3rd agent (C)) other than 1st agent (A) and 2nd agent (B).
- a photoinitiator (g) in another agent (for example, 3rd agent (C)) other than 1st agent (A) and 2nd agent (B).
- camphorquinone an acyl phosphine oxide compound is contained in the third agent (C) as a photopolymerization initiator (g), a polymerizable unit having no acidic group which can be contained in the second agent (B)
- the storage stability of the body (e) can be further improved.
- the filler (h), the organic solvent (i) and the water (j) may be contained in one or both of the first agent (A) and the second agent (B).
- both the first agent (A) and the second agent (B) contain the filler (h) and / or the organic solvent (i)
- the agent contained in the first agent (A) and the second agent Those included in B) may be the same or different.
- the mixing mass ratio of the first agent (A) to the second agent (B) can be appropriately set based on the curability of the resulting polymerizable mixture and the time (operable time) which can be used for the adhesion operation, etc. -10: 1 is preferable, 1: 5-5: 1 is more preferable, and 1: 2-2: 1 is more preferable.
- the curable composition of the present invention can be obtained by curing the polymerizable mixture obtained by mixing the packaged agents at 20 to 50 ° C., for example, at normal temperature or around body temperature (37 ° C.).
- the cured products can be used in dental applications such as dental treatment applications.
- the curable composition of the present invention can be cured at normal temperature or more.
- the curable composition of the present invention can also be cured at, for example, 10 to 120 ° C.
- a photoinitiator (g) when contained as a component of a curable composition, after processing the polymerizable mixture obtained by mixing each packaged agent into a predetermined shape, a well-known light is obtained.
- a desired cured product can be obtained by irradiating visible light for a predetermined time using an irradiation apparatus.
- the conditions such as the irradiation intensity and the irradiation time can be appropriately changed in accordance with the curability of the package-type curable composition of the present invention.
- cured material obtained can also be improved by heat-processing the hardened
- the curable composition of the present invention can be suitably used in dental applications such as various dental treatment applications.
- the curable composition of the present invention is, for example, a dental adhesive resin cement, a dental composite resin (including self-adhesive ones, the same shall apply hereinafter), a dental bonding material, a dental backing, a dental root. It can be used as a filler, an adhesive for orthodontic treatment, a tooth locking material, a tooth pit and fissure sealant (a dental sealant), a temporary adhesive cement for dental use, a dental filling material and the like.
- the curable composition of the present invention can be used in a method generally known as a method of using a dental material.
- a dental adhesive resin cement e.g., a dental adhesive resin cement
- a dental composite resin e.g., a dental composite resin
- the curable composition of the present invention is obtained by mixing the agents contained in the packaged curable composition.
- the polymerizable mixture can be used alone by coating it on the adhesive surface.
- the curable composition of the present invention when used as a dental material, it may be used together with other dental materials.
- a polymerizable mixture prepared from the curable composition of the present invention can be applied and used.
- the curable composition of the present invention is directly applied to the adherend surface of the adherend as a bonding material, it may be used by filling it with another curable composition such as a dental composite resin. .
- the curable composition of the present invention has good polymerizability.
- a curable composition can be prepared which gives a cured product having sufficient mechanical strength.
- the curable composition which is excellent in long-term storage stability over normal temperature can also be prepared.
- the curing time of the curable composition of the present invention at 37 ° C. is preferably 0.5 to 4 minutes, more preferably 0.8 to 3.5 minutes, and still more preferably 1 to 3 minutes.
- 50 MPa or more is preferable, as for the three-point bending strength of the hardened
- the higher three-point bending strength is preferable, and the upper limit thereof is not particularly limited, and may be, for example, 240 MPa.
- the curing time at 37 ° C. after storing the curable composition of the present invention at 55 ° C. for 3 weeks is preferably 3 minutes or less, and more preferably 1 to 3 minutes.
- kits for initiating polymerization contains the first agent (A) and the second agent (B).
- the first agent (A) contains a polymerizable monomer (a) having an acidic group and a transition metal compound (b).
- the second agent (B) contains at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds, and a reducing agent (d).
- the first agent (A) and the second agent (B) are usually housed in separate containers. Each component contained in the first agent (A) may be further packaged in a plurality of agents. Each component contained in the second agent (B) may be further packaged in a plurality of agents.
- each component contained in a 1st agent (A) may be accommodated in the same container, and may be accommodated in a separate container.
- the polymerizable monomer (a) having an acidic group and the transition metal compound (b) contained in the first agent (A) may be housed in the same container, and are housed in separate containers.
- each component contained in a 2nd agent (B) may be accommodated in the same container, and may be accommodated in a separate container.
- the compound (c) and the reducing agent (d) contained in the second agent (B) may be housed in the same container, or may be housed in separate containers.
- kit for initiation of polymerization of the present invention can be used for the same application as the curable composition of the present invention described above, and the preferred application is also the same.
- the second agent (B) in the above-described separately packaged curable composition of the present invention may be used as a polymerization initiator. That is, the polymerization initiator of the present invention can contain at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds, and a reducing agent (d).
- R812 Fine particle silica (manufactured by Nippon Aerosil Co., Ltd., trade name “Aerosil R812”) [Organic solvent (i)] Acetone: Acetone (manufactured by Fuji Film Wako Pure Chemical Industries, Ltd.) EtOH: ethanol (manufactured by Fujifilm Wako Pure Chemical Industries, Ltd.) [Water (j)] Distilled water: manufactured with distilled water production equipment (manufactured by Tokyo Rika Kikai Co., Ltd.) [Other ingredients: polymerization inhibitor] BHT: 2,6-di-t-butyl-4-methylphenol (made by Tokyo Chemical Industry Co., Ltd.) MEHQ: 4-Methoxyphenol (Fuji Film Wako Pure Chemical Industries, Ltd.)
- the first agent (A) and the second agent (B) are prepared by mixing the respective components according to the respective formulations described in the
- ⁇ Curing time measurement method (according to ISO 4049)> The curing time of each example and comparative example was measured by differential thermal analysis using a differential scanning calorimeter (DSC).
- DSC 3500 Sirius (made by NETZSCH) was used as a measuring apparatus.
- the first agent (A) and the second agent (B) collected in equal amounts (mass basis) on a dental kneading paper at room temperature set at 20-25 ° C. are mixed with a dental spatula for 10 seconds Then, a polymerizable mixture was obtained, and the obtained polymerizable mixture was filled in an Al sample pan for DSC measurement.
- a sample pan made of Al filled with a polymerizable mixture was placed in a thermostat of a DSC set at 37 ⁇ 1 ° C. immediately before measurement, and measurement was started 40 seconds after the start of kneading. The temperature was raised by the curing reaction of the polymerizable mixture, and the time until reaching the maximum temperature was recorded as the curing time.
- ⁇ Three-point bending strength measurement method (according to ISO 4049)>
- the first agent (A) and the second agent (B) collected in equal amounts (mass basis) on a dental drawing paper at room temperature set at 20 to 25 ° C. are mixed with a dental spatula for 10 seconds to make uniform It was a polymerizable mixture.
- the obtained polymerizable mixture was filled into a 2 mm ⁇ 2 mm ⁇ 25 mm test body action mold, pressed from both sides with a mirror film, and polymerized by the corresponding polymerization method.
- a cured product obtained by polymerizing a mold filled with the polymerizable mixture for 1 hour in a thermostat set at 37 ⁇ 1 ° C. was used as a test body.
- a cured product obtained by irradiating light for 1 minute and 30 seconds on each side with a technical LED irradiator at room temperature was used as a test body.
- the technical LED irradiator is "Alpha light V (Morita Co., Ltd./light source: LED lamp, 400 to 408 nm; 465 to 475 nm)", and an integrated UV light meter "UIT-250 / Ushio Electric Co., Ltd.”
- test body is removed from the mold and immersed in distilled water, and stored for 18 hours in a thermostat at 37 ⁇ 1 ° C. After that, the test body is taken out and three-pointed using a universal tester (Intesco Co., Ltd.) The flexural strength was measured.
- the breaking strength measurement test was carried out by applying a load at a crosshead speed of 1 mm / min until the test body broke, and the strength of the cured product was calculated from the obtained maximum point stress. Further, in this test, the elastic modulus of the cured product obtained by the curable composition of the present invention was also calculated.
- the measurement result of bending strength and an elastic modulus is calculated as an average value of each measured value which measured using a some test body on the same conditions.
- the curing time is within 3 minutes, it can be judged that the evaluated polymerizable mixture has sufficient curability. In addition, if the three-point bending strength of the obtained cured product is 80 MPa or more, it can be determined that a cured product having sufficient strength is obtained. Furthermore, if the curing time of the polymerizable mixture evaluated for storage stability is within 3 minutes after the storage stability test, the curable composition maintains sufficient polymerizability and is judged to be excellent for storage stability. it can.
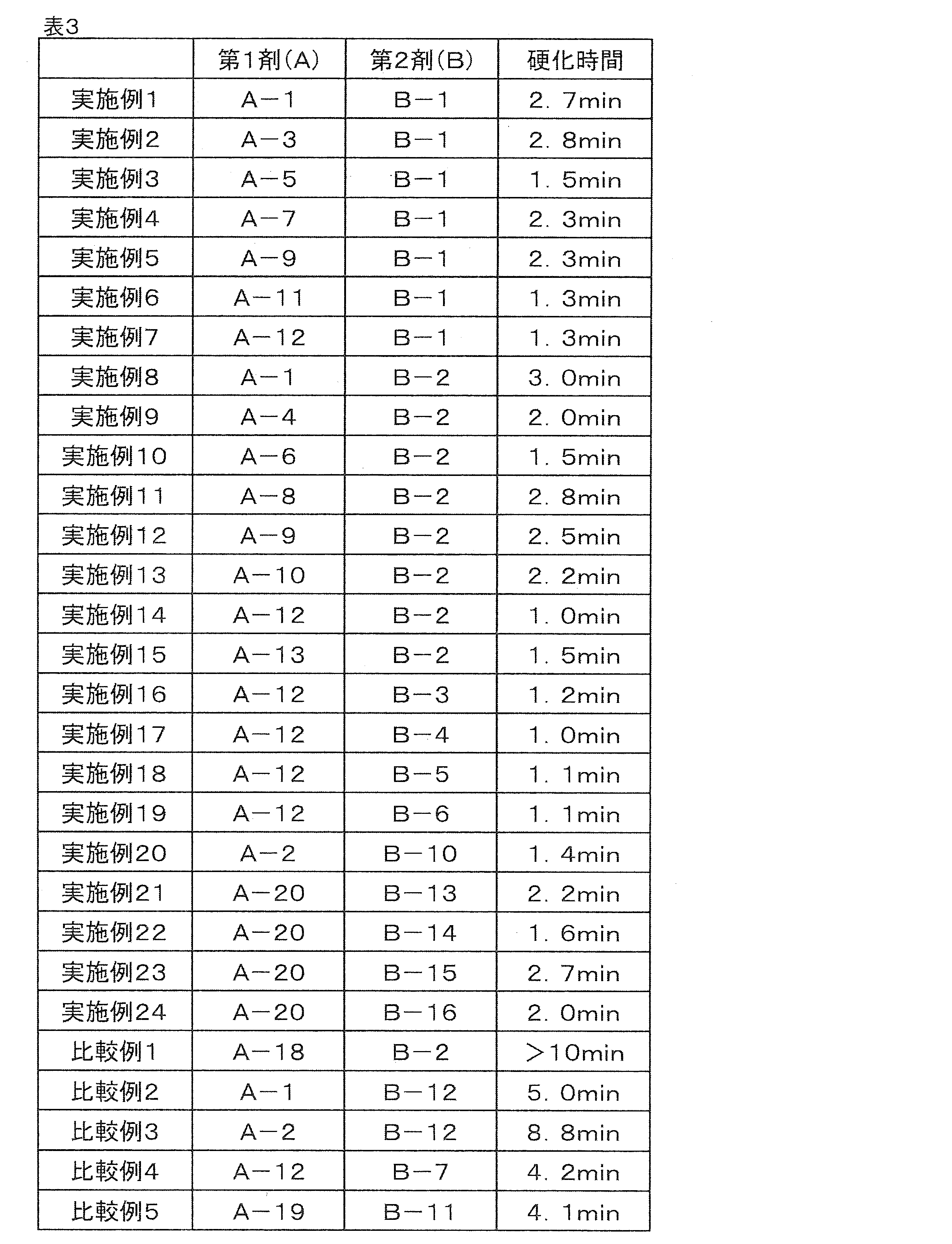
- Examples 1-19 which do not contain peroxide (f), showed good cure times.
- Comparative Example 1 which does not contain the transition metal compound (b) does not cure within 10 minutes, and does not contain at least one compound (c) selected from benzoxazole compounds and benzothiazole compounds.
- the polymerizability decreased.
- the comparative example 4 which used the benzimidazole compound which is not a compound (c) was not able to acquire sufficient polymerization promotion effect.
- Comparative Example 5 even in the case of a curable composition containing a peroxide-based chemical polymerization initiator containing a small amount of peroxide (f), sufficient polymerizability was not exhibited.
- Example 20 which mix
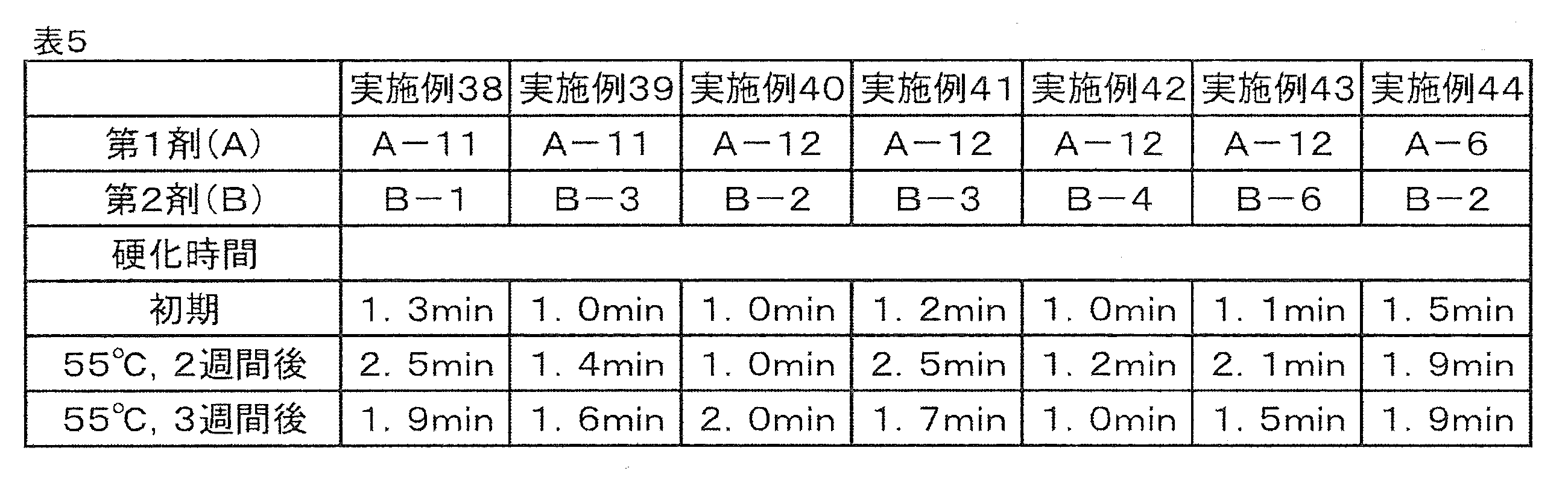
- Examples 38 to 44 As shown in Table 5, the storage stability of each of the curable compositions of the combination of the first agent (A) and the second agent (B) prepared in Table 1 and Table 2 was evaluated by the above-mentioned method.
- the curable compositions prepared in Examples 38 to 44 maintained sufficient polymerizability even after storage at 55 ° C. for 3 weeks, and showed excellent storage stability.
Abstract
本発明は、酸性条件においても充分な重合性を有する硬化性組成物を提供することを課題とし、本発明は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)と、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する硬化性組成物である。
Description
本発明は、硬化性組成物に関する。
重合性単量体を重合することにより硬化性組成物を与える技術は、産業的に広く用いられており、具体的には、熱重合、光重合、常温化学重合が挙げられ、重合性単量体を含む組成物に配合される各種重合触媒に対応する手法により実施される。これら重合手法は歯牙治療分野においても広く利用されており、例えば、レジン系修復材料に分類される歯科用接着性レジンセメント、歯科用コンポジットレジン(自己接着性を有するものを含む)、歯科用接着材、歯科用常温重合レジン、歯科用コンポジットレジン、歯科用裏層材、歯科用根幹充填材、歯列矯正用接着材、動揺歯固定材、歯牙小窩裂溝封鎖材(歯科用シーラント)等の各種接着性材料および充填材料の重合技術として実際に使用されている。
歯牙治療用材料に汎用される硬化性組成物に配合される重合開始剤には、主に可視光線を照射して重合・硬化させる光重合開始剤と、別々に保存した2種以上の剤を使用直前に混合して重合・硬化させる化学重合開始剤があり、最近では、その両方の開始剤を併用した材料を歯科臨床に使用する例も増加している。これらのうち化学重合開始剤は、常温付近で重合触媒成分を混合・練和することのみにより重合反応を開始し、さらには常温付近で重合性単量体を重合・硬化させる必要があり、他の開始剤系と比較して高い重合活性が要求される。
歯科分野において汎用される一般的な化学重合開始剤系の一例として、酸化剤と還元剤を組み合わせたレドックス重合開始剤が挙げられる。レドックス重合開始剤を配合した硬化性組成物は、通常は酸化剤を含む第1剤と還元剤を含む第2剤とに分割した複数の組成物、いわゆる分包型硬化性組成物として、使用する直前まで保存され、使用時に第1剤と第2剤とを混合させることにより化学重合反応が開始し、混合物の硬化が進行する。そのため、レドックス反応を生起しうる酸化剤と還元剤との組み合わせを、通常、同一製剤中に保存することができないため、場合によっては3剤以上に分割した分包型硬化性組成物として保存する必要がある。
高活性な化学重合開始剤を含む硬化性組成物として、例えば、過酸化物と還元性物質とを組み合わせたレドックス重合開始剤系が知られ、歯科材料分野においても汎用されている。例えば、前記過酸化物として過酸化ベンゾイル等のジアシルパーオキサイド化合物を含む第1剤と、前記還元性物質として芳香族アミン化合物を含む第2剤とから構成される歯科用硬化性組成物が知られている(特許文献1)。この化学重合開始剤を含む硬化性組成物は、常温の口腔内でも硬化反応が円滑に進行する混合物が調製できることから、歯科材料分野においても従来から広く使用されている。
しかし、過酸化ベンゾイルを含む硬化性組成物は、過酸化ベンゾイルの重合活性の高さから、常温での保管中に分解してラジカルを生成する場合が多いため、保管中に組成物が硬化する、あるいは前記分解により失活して長期保管後の充分な重合性を維持できないという問題があった。
上記問題を解決する化学重合開始剤を配合した硬化性組成物として、過酸化物を熱力学的に安定なハイドロパーオキサイド化合物を使用したものが提案されている(特許文献2および3)。この化学重合型硬化性組成物は、熱的に安定な過酸化物を使用することにより、過酸化ベンゾイルを使用した組成物と比較して常温での保存安定性に優れるという特徴を有している。しかしながら、過酸化ベンゾイル等と比較すると活性が低く、その硬化時間には改良の余地があった。
また、特許文献4および5には、過酸化物としてハイドロパーオキサイド化合物を使用し、還元剤としてチオ尿素化合物、促進剤として遷移金属化合物から構成される化学重合開始剤を含む硬化性組成物が提案されている。これらの硬化性組成物は熱に対する安定性が比較的高く、室温での保存安定性が高い特徴を有している。一方、これら化学重合開始剤系は、過酸化ベンゾイル-芳香族アミン化合物で構成される従来の化学重合触媒系と比較すると、依然として重合反応性が低く、硬化時間も長い。さらに、これら硬化性組成物は保存後の操作可能時間の経時的な変化が大きく、保存後の第1剤および第2剤を混合して得られる混合物は固化しやすくなるという問題があった。
特許文献6には、ルイス酸性化合物、第三級アミン化合物およびスルフィン酸化合物から構成される、過酸化物を実質含まない化学重合開始剤も提案されている。この化学重合開始剤を含む硬化性組成物は、実質的に過酸化物を含まないことにより、その保存安定性が過酸化物の化学的安定性に左右されることが無く、常温保管時の保存安定性が大きく改善されている。しかしながら、前記硬化性組成物は過酸化物を含まないために、その硬化時間が長く、その重合性には改善の余地があった。
硬化性組成物が所望の性能を発揮するためには、夫々の材料の使用環境において確実に重合し、硬化物を与える重合性を有することが望まれている。
すなわち、本発明の目的は、酸性条件においても充分な重合性を有する硬化性組成物を提供することにある。
本発明者らは、上記課題を解決すべく鋭意検討した結果、下記構成を有する硬化性組成物が、上記課題を解決できることを見出し、本発明を完成するに至った。
本発明は以下[1]~[19]に記載の事項を含む。
[1]酸性基を有する重合性単量体(a)と、遷移金属化合物(b)と、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する硬化性組成物。
[2]前記化合物(c)が、ベンゾオキサゾール環の2位にメルカプト基を有する化合物およびベンゾチアゾール環の2位にメルカプト基を有する化合物を含まない、前記[1]に記載の硬化性組成物。
[3]前記還元剤(d)が、スルフィン酸、スルフィン酸の塩、アスコルビン酸およびアスコルビン酸の塩から選ばれる少なくとも1種の化合物を含む、前記[1]又は[2]に記載の硬化性組成物。
[4]前記化合物(c)が、ベンゾオキサゾール、ベンゾチアゾール、および下記式(1)で示される化合物から選ばれる少なくとも1種である、前記[1]~[3]のいずれかに記載の硬化性組成物。
[式(1)中、Xは酸素原子または硫黄原子を表し、Yは水酸基またはアミノ基を表し、R1およびR2はそれぞれ独立に水素原子、ハロゲン原子、または炭素数1~4の炭化水素基を表す。]
[5]前記遷移金属化合物(b)が、銅化合物およびバナジウム化合物から選ばれる少なくとも1種である、前記[1]~[4]のいずれかに記載の硬化性組成物。
[5]前記遷移金属化合物(b)が、銅化合物およびバナジウム化合物から選ばれる少なくとも1種である、前記[1]~[4]のいずれかに記載の硬化性組成物。
[6]酸性基を有さない重合性単量体(e)をさらに含有する、前記[1]~[5]のいずれかに記載の硬化性組成物。
[7]過酸化物(f)を実質的に含有しない、前記[1]~[6]のいずれかに記載の硬化性組成物。
[8]過酸化物(f)をさらに含有する、前記[1]~[6]のいずれかに記載の硬化性組成物。
[9]前記過酸化物(f)が、ハイドロパーオキサイド化合物およびパーオキシエステル化合物から選ばれる少なくとも1種である、前記[8]に記載の硬化性組成物。
[10]光重合開始剤(g)、フィラー(h)、有機溶剤(i)および水(j)から選ばれる少なくとも1種をさらに含有する、前記[1]~[9]のいずれかに記載の硬化性組成物。
[11]前記遷移金属化合物(b)、前記化合物(c)および前記還元剤(d)の合計が、重合性単量体100質量部に対して、0.1~40質量部である、前記[1]~[10]のいずれかに記載の硬化性組成物。
[12]前記遷移金属化合物(b)の含有量が、重合性単量体100質量部に対して、0.001~5質量部である、前記[1]~[11]のいずれかに記載の硬化性組成物。
[13]前記化合物(c)の含有量が、重合性単量体100質量部に対して、0.1~20質量部である、前記[1]~[12]のいずれかに記載の硬化性組成物。
[14]前記還元剤(d)の含有量が、重合性単量体100質量部に対して、0.01~20質量部である、前記[1]~[13]のいずれかに記載の硬化性組成物。
[15]歯科用途に用いられる、前記[1]~[14]のいずれかに記載の硬化性組成物。
[16]前記[1]~[15]のいずれかに記載の硬化性組成物を含有し、歯科用接着性レジンセメント、歯科用コンポジットレジン、歯科用ボンディング材、歯科用裏層材、歯科用根幹充填材、歯列矯正用接着材、動揺歯固定材、歯科用シーラント、歯科用仮着セメントまたは歯科用充填材料である、歯科用組成物。
[17]前記[1]~[15]のいずれかに記載の硬化性組成物または前記[16]に記載の歯科用組成物の硬化物。
[18]第1剤(A)と第2剤(B)とを含む重合開始用キットであり、前記第1剤(A)が、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)とを含有し、前記第2剤(B)が、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する、重合開始用キット。
[19]ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する重合開始剤。
本発明の硬化性組成物は、化学重合型の硬化性組成物として充分な重合性を有する。
以下、本発明について詳細に説明する。なお、本明細書において「(メタ)アクリル」とは、アクリルまたはメタクリルを意味し、例えば「(メタ)アクリル酸」は「アクリル酸」または「メタクリル酸」の意味である。同様に、「(メタ)アクリロイル」とは「アクリロイル」または「メタクリロイル」を意味し、「(メタ)アクリレート」とは「アクリレート」または「メタクリレート」を意味する。
[硬化性組成物]
本発明の硬化性組成物は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)と、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有し、必要に応じて以下に説明する(e)~(j)の成分およびその他の成分から選ばれる少なくとも1種を含有する。
本発明の硬化性組成物は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)と、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有し、必要に応じて以下に説明する(e)~(j)の成分およびその他の成分から選ばれる少なくとも1種を含有する。
本発明の硬化性組成物は、化学重合型の硬化性組成物として充分な重合性を有する。また、本発明の硬化性組成物は、歯科材料用硬化物として充分な強度を有する硬化物を与えることができる。さらに、本発明によると、光重合開始剤を併用するデュアルキュア型の硬化性組成物を提供することも可能である。
本発明において、遷移金属化合物(b)、化合物(c)および還元剤(d)の全部又はこれらのうち一部の組合せは、いわゆる化学重合開始剤として作用する。したがって、本発明の硬化性組成物は、化学重合開始剤を含有する。
本発明の硬化性組成物は、一つの剤からなり、当該剤中に前記各成分を全て含有する態様でもよく、第1剤(A)および第2剤(B)のように複数の剤に分包されている態様(分包型硬化性組成物)でもよい。前者の態様、および後者の態様において分包された前記複数の剤を混合して得られた混合物を、特に「重合性混合物」ともいう。本発明では、常温以上において前記各剤を長期間保存した後に混合して調製される重合性混合物が、充分な重合活性を維持する硬化性組成物を与えることができる。
(酸性基を有する重合性単量体(a))
酸性基を有する重合性単量体(a)が硬化性組成物に含まれることにより、接着性に優れる本発明の硬化性組成物が得られる。
酸性基を有する重合性単量体(a)が硬化性組成物に含まれることにより、接着性に優れる本発明の硬化性組成物が得られる。
酸性基を有する重合性単量体(a)としては、例えば、酸性基含有ラジカル重合性単量体が挙げられ、歯科用接着性単量体として従来用いられている重合性単量体が使用できる。
酸性基含有ラジカル重合性単量体に含まれるラジカル重合可能な不飽和基としては、例えば、(メタ)アクリロイル基、(メタ)アクリルアミド基、スチリル基、ビニル基、アリル基が挙げられる。口腔内における加水分解等による重合性基の脱離のし易さなどの点から、これらのラジカル重合可能な不飽和基の中でも、(メタ)アクリロイル基および(メタ)アクリルアミド基が好ましく、メタクリロイル基および(メタ)アクリルアミド基がより好ましく、メタクリロイル基がさらに好ましい。
酸性基を有する重合性単量体(a)に含まれる酸性基としては、例えば、カルボン酸基、カルボン酸無水物基、リン酸基、チオリン酸基、ピロリン酸基、チオピロリン酸基、ホスホン酸基、チオホスホン酸基およびスルホン酸基が挙げられる。なお、これらの酸性基は、酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩等の形態になっていてもよい。
リン酸基を有する重合性単量体としては、例えば、2-(メタ)アクリロイルオキシエチルジハイドロジェンホスフェート、3-(メタ)アクリロイルオキシプロピルジハイドロジェンホスフェート、4-(メタ)アクリロイルオキシブチルジハイドロジェンホスフェート、5-(メタ)アクリロイルオキシペンチルジハイドロジェンホスフェート、6-(メタ)アクリロイルオキシヘキシルジハイドロジェンホスフェート、7-(メタ)アクリロイルオキシヘプチルジハイドロジェンホスフェート、8-(メタ)アクリロイルオキシオクチルジハイドロジェンホスフェート、9-(メタ)アクリロイルオキシノニルジハイドロジェンホスフェート、10-(メタ)アクリロイルオキシデシルジハイドロジェンホスフェート、11-(メタ)アクリロイルオキシウンデシルジハイドロジェンホスフェート、12-(メタ)アクリロイルオキシドデシルジハイドロジェンホスフェート、16-(メタ)アクリロイルオキシヘキサデシルジハイドロジェンホスフェート、20-(メタ)アクリロイルオキシイコシルジハイドロジェンホスフェート等の(メタ)アクリロイルオキシアルキルジハイドロジェンホスフェート、ビス〔2-(メタ)アクリロイルオキシエチル〕ハイドロジェンホスフェート、ビス〔4-(メタ)アクリロイルオキシブチル〕ハイドロジェンホスフェート、ビス〔6-(メタ)アクリロイルオキシヘキシル〕ハイドロジェンホスフェート、ビス〔8-(メタ)アクリロイルオキシオクチル〕ハイドロジェンホスフェート、ビス〔9-(メタ)アクリロイルオキシノニル〕ハイドロジェンホスフェート、ビス〔10-(メタ)アクリロイルオキシデシル〕ハイドロジェンホスフェート等のビス〔(メタ)アクリロイルオキシアルキル〕ハイドロジェンホスフェート、1,3-ジ(メタ)アクリロイルオキシプロピルジハイドロジェンホスフェート、2-(メタ)アクリロイルオキシエチルフェニルハイドロジェンホスフェート、2-(メタ)アクリロイルオキシエチル-2-ブロモエチルハイドロジェンホスフェート、ビス〔2-(メタ)アクリロイルオキシ-(1-ヒドロキシメチル)エチル〕ハイドロジェンホスフェート、ペンタアクリロイルジペンタエリスリトールハイドロジェンホスフェート、およびこれらの酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩が挙げられる。また、これらの化合物におけるリン酸基をチオリン酸基に置き換えた化合物も挙げられる。
ピロリン酸基を有する重合性単量体としては、例えば、ピロリン酸ビス〔2-(メタ)アクリロイルオキシエチル〕、ピロリン酸ビス〔4-(メタ)アクリロイルオキシブチル〕、ピロリン酸ビス〔6-(メタ)アクリロイルオキシヘキシル〕、ピロリン酸ビス〔8-(メタ)アクリロイルオキシオクチル〕、ピロリン酸ビス〔10-(メタ)アクリロイルオキシデシル〕、およびこれらの酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩が挙げられる。また、これらの化合物におけるピロリン酸基をチオピロリン酸基に置き換えた化合物も挙げられる。
ホスホン酸基を有する重合性単量体としては、例えば、2-(メタ)アクリロイルオキシエチルフェニルホスホネート、5-(メタ)アクリロイルオキシペンチル-3-ホスホノプロピオネート、6-(メタ)アクリロイルオキシヘキシル-3-ホスホノプロピオネート、10-(メタ)アクリロイルオキシデシル-3-ホスホノプロピオネート、6-(メタ)アクリロイルオキシヘキシル-3-ホスホノアセテート、10-(メタ)アクリロイルオキシデシル-3-ホスホノアセテート、およびこれらの酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩が挙げられる。また、これらの化合物におけるホスホン酸基をチオホスホン酸基に置き換えた化合物も挙げられる。
スルホン酸基を有する重合性単量体としては、例えば、2-スルホエチル(メタ)アクリレート、2-スルホ-1-プロピル(メタ)アクリレート、1-スルホ-2-プロピル(メタ)アクリレート、1-スルホ-2-ブチル(メタ)アクリレート、3-スルホ-2-ブチル(メタ)アクリレート、3-ブロモ-2-スルホ-2-プロピル(メタ)アクリレート、3-メトキシ-1-スルホ-2-プロピル(メタ)アクリレート、1,1-ジメチル-2-スルホエチル(メタ)アクリルアミド、およびこれらの酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩が挙げられる。
カルボン酸基またはカルボン酸無水物基を有する重合性単量体としては、例えば、モノカルボン酸、ジカルボン酸、トリカルボン酸およびテトラカルボン酸またはこれらの誘導体が挙げられ、これらの例としては、(メタ)アクリル酸、マレイン酸、p-ビニル安息香酸、11-(メタ)アクリロイルオキシ-1,1-ウンデカンジカルボン酸(メタクリレートの場合:「MAC10」)、1,4-ジ(メタ)アクリロイルオキシエチルピロメリット酸、6-(メタ)アクリロイルオキシエチルナフタレン-1,2,6-トリカルボン酸、4-(メタ)アクリロイルオキシメチルトリメリット酸およびその無水物、4-(メタ)アクリロイルオキシエチルトリメリット酸(メタクリレートの場合:「4-MET」)およびその無水物(メタクリレートの場合:4-META)、4-(メタ)アクリロイルオキシブチルトリメリット酸およびその無水物、4-[2-ヒドロキシ-3-(メタ)アクリロイルオキシ]ブチルトリメリット酸およびその無水物、2,3-ビス(3,4-ジカルボキシベンゾイルオキシ)プロピル(メタ)アクリレート、N,O-ジ(メタ)アクリロイルチロシン、O-(メタ)アクリロイルチロシン、N-(メタ)アクリロイルチロシン、N-(メタ)アクリロイルフェニルアラニン、N-(メタ)アクリロイル-p-アミノ安息香酸、N-(メタ)アクリロイル-O-アミノ安息香酸、N-(メタ)アクリロイル-5-アミノサリチル酸(メタクリレートの場合:「5-MASA」)、N-(メタ)アクリロイル-4-アミノサリチル酸、2または3または4-(メタ)アクリロイルオキシ安息香酸、2-ヒドロキシエチル(メタ)アクリレートとピロメリット酸二無水物の付加生成物(メタクリレートの場合:「PMDM」)、2-ヒドロキシエチル(メタ)アクリレートと無水マレイン酸または3,3',4,4'-ベンゾフェノンテトラカルボン酸二無水物(メタクリレートの場合:「BTDA」)または3,3',4,4'-ビフェニルテトラカルボン酸二無水物の付加反応物、2-(3,4-ジカルボキシベンゾイルオキシ)-1,3-ジ(メタ)アクリロイルオキシプロパン、N-フェニルグリシンまたはN-トリルグリシンとグリシジル(メタ)アクリレートとの付加物、4-[(2-ヒドロキシ-3-(メタ)アクリロイルオキシプロピル)アミノ]フタル酸、3または4-[N-メチル-N-(2-ヒドロキシ-3-(メタ)アクリロイルオキシプロピル)アミノ]フタル酸、およびこれらの酸塩化物、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩が挙げられる。
酸性基を有する重合性単量体(a)の中でも、歯質に対する接着性の観点から、4-メタクリロイルオキシエチルトリメリット酸、4-メタクリロイルオキシエチルトリメリット酸無水物、10-メタクリロイルオキシデシルジハイドロジェンホスフェートが好ましい。
酸性基を有する重合性単量体(a)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の酸性基を有する重合性単量体(a)の含有量は、重合性単量体の合計100質量部中、好ましくは1~50質量部、より好ましくは3~35質量部、さらに好ましくは5~25質量部である。このような態様であると、重合性混合物の重合性に優れ、かつ得られる硬化物の接着強度および機械的物性に優れる傾向にある。
前記重合性単量体とは、酸性基を有する重合性単量体(a)、および後述する酸性基を有さない重合性単量体(e)を包含する。
なお、本明細書において各成分の含有量を記載しているが、後述する分包型硬化性組成物の場合は、分包された前記複数の剤中のそれぞれの成分量を合計したときの各成分の合計量が本明細書に記載する範囲に入ればよい。
(遷移金属化合物(b))
遷移金属化合物(b)が硬化性組成物に含まれることにより、本発明の硬化性組成物に充分な重合性を付与することができる。遷移金属化合物(b)としては、例えば、銅化合物、バナジウム化合物、コバルト化合物、ニッケル化合物、鉄化合物、モリブデン化合物が挙げられる。
遷移金属化合物(b)が硬化性組成物に含まれることにより、本発明の硬化性組成物に充分な重合性を付与することができる。遷移金属化合物(b)としては、例えば、銅化合物、バナジウム化合物、コバルト化合物、ニッケル化合物、鉄化合物、モリブデン化合物が挙げられる。
銅化合物としては、例えば、銅アセチルアセトナート、オレイン酸銅、酢酸銅、グルコン酸銅、クエン酸銅、フタル酸銅、ナフテン酸銅、水酸化銅、銅メトキシド、銅エトキシド、銅イソプロポキシド、塩化銅、臭化銅等の1価または2価の銅化合物が挙げられる。
バナジウム化合物としては、3価~5価のバナジウム化合物から選ばれる少なくとも1種の化合物が好ましく、例えば、バナジウム(III)アセチルアセトナート、ナフテン酸バナジウム(III)、バナジルステアレート、バナジウムベンゾイルアセトネート、ビス(マルトラート)オキソバナジウム(IV)、オキソビス(1-フェニル-1,3-ブタンジオネート)バナジウム(IV)、バナジル(IV)アセチルアセトナート、四酸化二バナジウム(IV)、シュウ酸バナジル(IV)、硫酸バナジル(IV)、オキソビス(1-フェニル-1,3-ブタンジオネート)バナジウム(IV)、ビス(マルトラート)オキソバナジウム(IV)、バナジウム(V)オキシトリイソプロポキシド、五酸化バナジウム(V)、メタバナジン酸ナトリウム(V)、メタバナジン酸アンモニウム(V)が挙げられる。
コバルト化合物としては、例えば、コバルトアセチルアセトナート、酢酸コバルト、ナフテン酸コバルト、オレイン酸コバルト、ステアリン酸コバルト、2-エチルヘキサン酸コバルト、安息香酸コバルト、シュウ酸コバルト、クエン酸コバルト、炭酸コバルト、硝酸コバルト、硫酸コバルト、リン酸コバルト、過塩素酸コバルト、チオシアン酸コバルト、酸化コバルト、硫化コバルト、フッ化コバルト、塩化コバルト、臭化コバルト、水酸化コバルト、コバルトイソプロポキシドが挙げられる。
ニッケル化合物としては、例えば、ニッケルアセチルアセトナート、ビス(ジチオベンジル)ニッケル、ビス(シクロペンタジエニル)ニッケル、ギ酸酢酸ニッケル、酢酸ニッケル、乳酸ニッケル、ナフテン酸ニッケル、2-エチルヘキサン酸ニッケル、シュウ酸ニッケル、クエン酸ニッケル、ステアリン酸ニッケル、過塩素酸ニッケル、酸化ニッケル、硫化ニッケル、フッ化ニッケル、塩化ニッケル、臭化ニッケル、ヨウ化ニッケル、炭酸ニッケル、硝酸ニッケル、硫酸ニッケル、水酸化ニッケル、ニッケルエトキシドが挙げられる。
鉄化合物としては、例えば、鉄アセチルアセトナート、フェロセン、酢酸鉄、ステアリン酸鉄、2-エチルヘキサン酸鉄、シュウ酸鉄、クエン酸鉄、グルコン酸鉄、硝酸鉄、硫酸鉄、リン酸鉄、過塩素酸鉄、酸化鉄、硫化鉄、フッ化鉄、塩化鉄、臭化鉄、ヘキサシアノ鉄酸カリウム、鉄エトキシドが挙げられる。
モリブデン化合物としては、例えば、酸化モリブデン、酸化モリブデンアセチルアセトナート、モリブデニウムエトキシド、ビス(2,4-ペンタジオナト)酸化モリブデニウム、モリブデニルジエチルジチオカルバメートが挙げられる。
遷移金属化合物(b)の中でも、重合性混合物の重合性および保管中の安定性に優れる点から、銅化合物およびバナジウム化合物から選ばれる少なくとも1種を使用することが好ましい。また、重合性単量体への溶解度および取り扱いの観点から、1価または2価の塩化銅、臭化銅、酢酸銅、バナジウム(III)アセチルアセトナート、バナジル(IV)アセチルアセトナートが好ましい。
遷移金属化合物(b)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の遷移金属化合物(b)の含有量は、重合性単量体100質量部に対して、好ましくは0.001~5質量部、より好ましくは0.005~3質量部、さらに好ましくは0.01~1質量部である。遷移金属化合物(b)の含有量が前記下限値よりも少ない場合には、遷移金属化合物(b)を含ませたことによる効果が得られないおそれがあり、前記上限値よりも多い場合には、後述する第1剤(A)に含まれる重合性単量体が保存中に重合しやすくなる傾向がある。
(ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c))
本発明の硬化性組成物は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)を含有する。化合物(c)は、遷移金属化合物(b)の重合触媒活性を高める効果を有している。化合物(c)を本発明の硬化性組成物に配合することにより、重合性混合物の重合性が向上する。さらに、機械的強度の良好な硬化物が得られるとともに、硬化物の変色も起こりにくくなり、審美的に良好な硬化物が得られる。その理由は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)が、遷移金属化合物(b)に対して配位子として機能し、重合性を向上させているからであると推測される。
本発明の硬化性組成物は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)を含有する。化合物(c)は、遷移金属化合物(b)の重合触媒活性を高める効果を有している。化合物(c)を本発明の硬化性組成物に配合することにより、重合性混合物の重合性が向上する。さらに、機械的強度の良好な硬化物が得られるとともに、硬化物の変色も起こりにくくなり、審美的に良好な硬化物が得られる。その理由は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)が、遷移金属化合物(b)に対して配位子として機能し、重合性を向上させているからであると推測される。
一実施態様において、還元剤(d)のうち、化合物(c)にも分類されえる化合物を還元剤(d)として使用する場合、当該化合物以外のベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物を化合物(c)として使用することができる。また、一実施態様において、化合物(c)のうち、還元剤(d)にも分類されえる化合物を化合物(c)として使用する場合、当該化合物以外の還元剤(d)を選択して使用することができる。
また、ベンゾオキサゾール環の2位にメルカプト基を有する化合物およびベンゾチアゾール環の2位にメルカプト基を有する化合物は、チオール由来の反応性を有しており、硬化性組成物中の重合性単量体とチオールとの反応物が生じるおそれがある。そのため、化合物(c)からは、ベンゾオキサゾール環の2位にメルカプト基を有する化合物およびベンゾチアゾール環の2位にメルカプト基を有する化合物を除くことが好ましい。
ただし、本発明の硬化性組成物は、一実施態様において、化合物(c)として、ベンゾオキサゾール環の2位にメルカプト基を有する化合物およびベンゾチアゾール環の2位にメルカプト基を有する化合物を含んでもよい。
化合物(c)は、ベンゾオキサゾール環および/またはベンゾチアゾール環を有していれば無置換であってもいずれの官能基を有していてもよく、公知の化合物を制限無く使用することができる。
化合物(c)としては、例えば、ベンゾオキサゾール、2-メチルベンゾオキサゾール、2-フェニルベンゾオキサゾール、2-(2-ベンゾオキサゾリル)酢酸、2-(2-ベンゾオキサゾリル)マレイン酸、7-アミノベンゾオキサゾール、ベンゾオキサゾール4-カルボン酸、ベンゾオキサゾール7-カルボン酸、2-(2-ヒドロキシフェニル)ベンゾオキサゾール、2-(2-アミノフェニル)ベンゾオキサゾール、ベンゾチアゾール、2-メチルベンゾチアゾール、2-フェニルベンゾチアゾール、2-(2-ベンゾチアゾリル)酢酸、2-(2-ベンゾチアゾリル)マレイン酸、7-アミノベンゾチアゾール、ベンゾチアゾール4-カルボン酸、ベンゾチアゾール7-カルボン酸、2-(2-ヒドロキシフェニル)ベンゾチアゾール、2-(2-アミノフェニル)ベンゾチアゾールが挙げられる。
化合物(c)は、下記式(1)で示される化合物であることが好ましい。
式(1)中、Xは酸素原子または硫黄原子を表し、Yは水酸基またはアミノ基を表す。R1およびR2はそれぞれ独立に水素原子、ハロゲン原子、または炭素数1~4の炭化水素基を表す。
ハロゲン原子としては、フッ素原子、塩素原子、臭素原子、ヨウ素原子が挙げられる。
炭素数1~4の炭化水素基としては、例えば、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、イソブチル基、tert-ブチル基等のアルキル基が挙げられる。
式(1)で示される化合物の具体例としては、2-(2-ヒドロキシフェニル)ベンゾオキサゾール、2-(2-アミノフェニル)ベンゾオキサゾール、2-(2-ヒドロキシフェニル)ベンゾチアゾール、2-(2-アミノフェニル)ベンゾチアゾールが挙げられる。
化合物(c)の中でも、組成物の重合性や保存安定性の観点から、ベンゾオキサゾール、ベンゾチアゾール、式(1)で示される化合物が好ましく、ベンゾオキサゾール、2-(2-ヒドロキシフェニル)ベンゾオキサゾール、ベンゾチアゾール、2-(2-ヒドロキシフェニル)ベンゾチアゾールがより好ましい。
化合物(c)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の化合物(c)の含有量は、重合性単量体100質量部に対して、好ましくは0.1~20質量部、より好ましくは0.5~10質量部、さらに好ましくは1~5質量部である。前記下限値よりも化合物(c)の含有量が少ない場合には、本発明の硬化性組成物に充分な重合性の向上の効果が得られないおそれがある。
(還元剤(d))
本発明において使用される還元剤(d)としては、例えば、硫黄系還元剤、ホウ素系還元剤、アスコルビン酸又はその塩、アルデヒド類、シュウ酸又はその塩、芳香族アミン化合物が挙げられる。
本発明において使用される還元剤(d)としては、例えば、硫黄系還元剤、ホウ素系還元剤、アスコルビン酸又はその塩、アルデヒド類、シュウ酸又はその塩、芳香族アミン化合物が挙げられる。
硫黄系還元剤としては、例えば、スルフィン酸又はその塩、亜硫酸ナトリウム等の亜硫酸塩、亜硫酸水素ナトリウム等の亜硫酸水素塩、ピロ亜硫酸ナトリウム等のピロ亜硫酸塩、チオ硫酸ナトリウム等のチオ硫酸塩が挙げられる。
ホウ素系還元剤としては、例えば、テトラアルキルホウ素、トリアルキルフェニルホウ素、ジアルキルジフェニルホウ素、モノアルキルトリフェニルホウ素、テトラフェニルホウ素等のアリールボレート化合物又はその塩が挙げられる。
アルデヒド類としては、例えば、テレフタルアルデヒドおよびベンズアルデヒド誘導体が挙げられる。
これらのうち、特に重合性を向上させることが可能であることから、スルフィン酸、スルフィン酸の塩、アスコルビン酸およびアスコルビン酸の塩から選ばれる少なくとも1種が好ましい。
前記塩としては、例えば、ナトリウム塩、カリウム塩、リチウム塩等のアルカリ金属塩、マグネシウム塩、カルシウム塩、バリウム塩等のアルカリ土類金属塩、アミン塩、アンモニウム塩、ピリジニウム塩が挙げられる。
また、芳香族アミン化合物は、還元剤として硬化性組成物に配合した場合に、優れた重合促進効果を有している。しかしながら、酸性基を有する重合性単量体(a)とともに芳香族アミン化合物を用いると、前記芳香族アミン化合物が中和により失活し、その重合促進効果が低下することがある。本発明の硬化性組成物は、このような態様であっても充分な重合性を示すことができるが、前記失活の観点から、芳香族アミン化合物以外の還元剤を用いることが好ましい。
また、重合性を向上させつつ、変色等を抑制して審美性が良好となり、歯科用途に適していることから、スルフィン酸又はその塩が特に好ましい。スルフィン酸又はその塩について、下記に詳述する。
《スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)》
スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)が硬化性組成物に含まれることにより、本発明の硬化性組成物の重合性が向上する効果が得られる。
スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)が硬化性組成物に含まれることにより、本発明の硬化性組成物の重合性が向上する効果が得られる。
スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)としては、例えば、メタンスルフィン酸、エタンスルフィン酸、プロパンスルフィン酸、ヘキサンスルフィン酸、オクタンスルフィン酸、デカンスルフィン酸、ドデカンスルフィン酸等のアルカンスルフィン酸;シクロヘキサンスルフィン酸、シクロオクタンスルフィン酸等の脂環族スルフィン酸;ベンゼンスルフィン酸、o-トルエンスルフィン酸、p-トルエンスルフィン酸、エチルベンゼンスルフィン酸、デシルベンゼンスルフィン酸、ドデシルベンゼンスルフィン酸、2,4,6-トリメチルベンゼンスルフィン酸、2,4,6-トリエチルベンゼンスルフィン酸、2,4,6-トリイソプロピルベンゼンスルフィン酸、ナフタリンスルフィン酸等の芳香族スルフィン酸;およびこれらのナトリウム塩、カリウム塩、リチウム塩等のアルカリ金属塩、マグネシウム塩、カルシウム塩、バリウム塩等のアルカリ土類金属塩、アミン塩、アンモニウム塩、ピリジニウム塩等の前記スルフィン酸の塩が挙げられる。これらの中でも、硬化性組成物の保存安定性と重合性混合物の重合活性の観点で、芳香族スルフィン酸およびその塩が好ましい。
還元剤(d)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の還元剤(d)の含有量は、重合性単量体100質量部に対して、好ましくは0.01~20質量部、より好ましくは0.1~10質量部、さらに好ましくは1~5質量部である。このような態様であると、重合性混合物の硬化時間、操作可能時間を考慮した重合性、得られる硬化物の接着強度に優れる傾向にある。特に、還元剤(d)が、スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)である場合、上記の含有量であることが好ましい。
また、本発明の硬化性組成物中の遷移金属化合物(b)、化合物(c)および還元剤(d)の合計は、重合性単量体100質量部に対して、好ましくは0.1~40質量部、より好ましくは0.5~23質量部、さらに好ましくは1~10質量部である。このような態様であると、硬化性組成物の重合性および保存安定性、硬化性組成物が与える硬化物の機械的強度に優れる傾向にある。
(酸性基を有さない重合性単量体(e))
酸性基を有さない重合性単量体(e)が硬化性組成物に含まれることにより、得られる硬化物の様々な物性、例えば機械的強度や接着強度を向上させることができる。また、酸性基を有さない重合性単量体(e)が硬化性組成物に含まれていることにより、本発明の硬化性組成物の流動性を向上させることができる。
酸性基を有さない重合性単量体(e)が硬化性組成物に含まれることにより、得られる硬化物の様々な物性、例えば機械的強度や接着強度を向上させることができる。また、酸性基を有さない重合性単量体(e)が硬化性組成物に含まれていることにより、本発明の硬化性組成物の流動性を向上させることができる。
酸性基を有さない重合性単量体(e)としては、例えば、酸性基を有さないラジカル重合性単量体が挙げられる。酸性基を有さないラジカル重合性単量体に含まれるラジカル重合可能な不飽和基としては、例えば、(メタ)アクリロイル基、(メタ)アクリルアミド基、スチリル基、ビニル基、アリル基が挙げられる。口腔内における加水分解等による重合性基の脱離のし易さなどの点から、これらのラジカル重合可能な不飽和基の中でも、(メタ)アクリロイル基および(メタ)アクリルアミド基が好ましく、メタクリロイル基および(メタ)アクリルアミド基がより好ましく、メタクリロイル基がさらに好ましい。
酸性基を有さないラジカル重合性単量体としては、例えば、
2-ヒドロキシエチル(メタ)アクリレート、3-ヒドロキシプロピル(メタ)アクリレート、4-ヒドロキシブチル(メタ)アクリレート、6-ヒドロキシヘキシル(メタ)アクリレート、10-ヒドロキシデシル(メタ)アクリレート等のヒドロキシアルキル(メタ)アクリレート、2-(ジメチルアミノ)エチル(メタ)アクリレート、N-メチル-N-フェニルアミノエチル(メタ)アクリレート、N-エチル-N-フェニルアミノエチル(メタ)アクリレート、プロピレングリコールモノ(メタ)アクリレート、グリセロールモノ(メタ)アクリレート、エリスリトールモノ(メタ)アクリレート、N-メチロール(メタ)アクリルアミド、N-ヒドロキシエチル(メタ)アクリルアミド、N、N-(ジヒドロキシエチル)(メタ)アクリルアミド、メチル(メタ)アクリレート、エチル(メタ)アクリレート、プロピル(メタ)アクリレート、イソプロピル(メタ)アクリレート、ブチル(メタ)アクリレート、イソブチル(メタ)アクリレート、ベンジル(メタ)アクリレート、ラウリル(メタ)アクリレート、2,3-ジブロモプロピル(メタ)アクリレート、3-(メタ)アクリロイルオキシプロピルトリメトキシシラン、11-(メタ)アクリロイルオキシウンデシルトリメトキシシラン、(メタ)アクリルアミド、ジメチルアミノエチル(メタ)アクリレート、ジメチルアミノプロピル(メタ)アクリレート、ジメチルアミノブチル(メタ)アクリレート、(メタ)アクリロイルオキシドデシルピリジニウムブロマイド、(メタ)アクリロイルオキシドデシルピリジニウムクロライドおよび(メタ)アクリロイルオキシヘキサデシルピリジニウムクロライド等の1官能性単量体;
2,2-ビス((メタ)アクリロイルオキシフェニル)プロパン、2,2-ビス〔4-(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)フェニル〕プロパン(通称「Bis-GMA」)、2,2-ビス(4-(メタ)アクリロイルオキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシポリエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシジエトキシフェニル)プロパン)、2,2-ビス(4-(メタ)アクリロイルオキシテトラエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシペンタエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシジプロポキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシエトキシフェニル)-2-(4-(メタ)アクリロイルオキシジエトキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシジエトキシフェニル)-2-(4-(メタ)アクリロイルオキシトリエトキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシジプロポキシフェニル)-2-(4-(メタ)アクリロイルオキシトリエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシプロポキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシイソプロポキシフェニル)プロパン、1,4-ビス(2-(メタ)アクリロイルオキシエチル)ピロメリテート等の芳香環を有する2官能性単量体;
グリセロールジ(メタ)アクリレート、エチレングリコールジ(メタ)アクリレート、ジエチレングリコールジ(メタ)アクリレート、トリエチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、ブチレングリコールジ(メタ)アクリレート、ネオペンチルグリコールジ(メタ)アクリレート等のアルキレングリコールジ(メタ)アクリレート、ポリエチレングリコールジ(メタ)アクリレート、1,3-ブタンジオールジ(メタ)アクリレート、1,5-ペンタンジオールジ(メタ)アクリレート、1,6-ヘキサンジオールジ(メタ)アクリレート、1,10-デカンジオールジ(メタ)アクリレート、1,12-ドデカンジオールジ(メタ)アクリレート、1,2-ビス(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)エタン、1,6-ビス(メタクリロキシエチルオキシカルボニルアミノ)-2,2,4-トリメチルヘキサン(通称「UDMA」)、1,2-ビス(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)エタン等の脂肪族炭素鎖を有する2官能性単量体;
トリメチロールプロパントリ(メタ)アクリレート、トリメチロールエタントリ(メタ)アクリレート、トリメチロールメタントリ(メタ)アクリレート、トリス(2-(メタ)アクリロキシエチル)イソシアヌレート、ペンタエリスリトールトリ(メタ)アクリレート、ペンタエリスリトールテトラ(メタ)アクリレート、ジペンタエリスリトールペンタ(メタ)アクリレート、N,N-(2,2,4-トリメチルヘキサメチレン)ビス〔2-(アミノカルボキシ)プロパン-1,3-ジオール〕テトラメタクリレート、1,7-ジアクリロイルオキシ-2,2,6,6-テトラアクリロイルオキシメチル-4-オキシヘプタン等の3官能以上の多官能性単量体;
ヘキサメチレンジイソシアネート(HDI)、トリレンジイソシアネート(TDI)、キシリレンジイソシアネート(XDI)、ジフェニルメタンジイソシアネート(MDI)、イソホロンジイソシアネート(IPDI)、トリメチルヘキサメチレンジイソシアネート(TMHMDI)等のイソシアネート基(-NCO)を有する化合物と、2-ヒドロキシエチル(メタ)アクリレート、2-ヒドロキシプロピル(メタ)アクリレート、2-ヒドロキシブチル(メタ)アクリレート、6-ヒドロキシヘキシル(メタ)アクリレート、10-ヒドロキシデシル(メタ)アクリレート、3-クロロ-2-ヒドロキシプロピル(メタ)アクリレート、2-ヒドロキシ-3-フェノキシプロピル(メタ)アクリレート、グリセリンモノ(メタ)アクリレート、N-ヒドロキシエチル(メタ)アクリルアミド、N、N-(ジヒドロキシエチル)(メタ)アクリルアミド、ビスフェノールAジグリシジル(メタ)アクリレート、2-ヒドロキシ-3アクリロイルオキシプロピル(メタ)アクリレート、2,2-ビス[4-〔3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ〕フェニル]プロパン、1,2-ビス〔3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ〕エタン、ペンタエリスリトールトリ(メタ)アクリレート、ジペンタエリスリールのトリまたはテトラ(メタ)クリレート等の水酸基(-OH)を有する(メタ)アクリレート化合物とを付加反応させることにより合成される重合性単量体(例えば、国際公開第2012/157566号、国際公開第2015/015220号、国際公開第2015/015221号、特開2016-094482号公報に記載);
が挙げられる。
2-ヒドロキシエチル(メタ)アクリレート、3-ヒドロキシプロピル(メタ)アクリレート、4-ヒドロキシブチル(メタ)アクリレート、6-ヒドロキシヘキシル(メタ)アクリレート、10-ヒドロキシデシル(メタ)アクリレート等のヒドロキシアルキル(メタ)アクリレート、2-(ジメチルアミノ)エチル(メタ)アクリレート、N-メチル-N-フェニルアミノエチル(メタ)アクリレート、N-エチル-N-フェニルアミノエチル(メタ)アクリレート、プロピレングリコールモノ(メタ)アクリレート、グリセロールモノ(メタ)アクリレート、エリスリトールモノ(メタ)アクリレート、N-メチロール(メタ)アクリルアミド、N-ヒドロキシエチル(メタ)アクリルアミド、N、N-(ジヒドロキシエチル)(メタ)アクリルアミド、メチル(メタ)アクリレート、エチル(メタ)アクリレート、プロピル(メタ)アクリレート、イソプロピル(メタ)アクリレート、ブチル(メタ)アクリレート、イソブチル(メタ)アクリレート、ベンジル(メタ)アクリレート、ラウリル(メタ)アクリレート、2,3-ジブロモプロピル(メタ)アクリレート、3-(メタ)アクリロイルオキシプロピルトリメトキシシラン、11-(メタ)アクリロイルオキシウンデシルトリメトキシシラン、(メタ)アクリルアミド、ジメチルアミノエチル(メタ)アクリレート、ジメチルアミノプロピル(メタ)アクリレート、ジメチルアミノブチル(メタ)アクリレート、(メタ)アクリロイルオキシドデシルピリジニウムブロマイド、(メタ)アクリロイルオキシドデシルピリジニウムクロライドおよび(メタ)アクリロイルオキシヘキサデシルピリジニウムクロライド等の1官能性単量体;
2,2-ビス((メタ)アクリロイルオキシフェニル)プロパン、2,2-ビス〔4-(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)フェニル〕プロパン(通称「Bis-GMA」)、2,2-ビス(4-(メタ)アクリロイルオキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシポリエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシジエトキシフェニル)プロパン)、2,2-ビス(4-(メタ)アクリロイルオキシテトラエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシペンタエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシジプロポキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシエトキシフェニル)-2-(4-(メタ)アクリロイルオキシジエトキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシジエトキシフェニル)-2-(4-(メタ)アクリロイルオキシトリエトキシフェニル)プロパン、2-(4-(メタ)アクリロイルオキシジプロポキシフェニル)-2-(4-(メタ)アクリロイルオキシトリエトキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシプロポキシフェニル)プロパン、2,2-ビス(4-(メタ)アクリロイルオキシイソプロポキシフェニル)プロパン、1,4-ビス(2-(メタ)アクリロイルオキシエチル)ピロメリテート等の芳香環を有する2官能性単量体;
グリセロールジ(メタ)アクリレート、エチレングリコールジ(メタ)アクリレート、ジエチレングリコールジ(メタ)アクリレート、トリエチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、ブチレングリコールジ(メタ)アクリレート、ネオペンチルグリコールジ(メタ)アクリレート等のアルキレングリコールジ(メタ)アクリレート、ポリエチレングリコールジ(メタ)アクリレート、1,3-ブタンジオールジ(メタ)アクリレート、1,5-ペンタンジオールジ(メタ)アクリレート、1,6-ヘキサンジオールジ(メタ)アクリレート、1,10-デカンジオールジ(メタ)アクリレート、1,12-ドデカンジオールジ(メタ)アクリレート、1,2-ビス(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)エタン、1,6-ビス(メタクリロキシエチルオキシカルボニルアミノ)-2,2,4-トリメチルヘキサン(通称「UDMA」)、1,2-ビス(3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ)エタン等の脂肪族炭素鎖を有する2官能性単量体;
トリメチロールプロパントリ(メタ)アクリレート、トリメチロールエタントリ(メタ)アクリレート、トリメチロールメタントリ(メタ)アクリレート、トリス(2-(メタ)アクリロキシエチル)イソシアヌレート、ペンタエリスリトールトリ(メタ)アクリレート、ペンタエリスリトールテトラ(メタ)アクリレート、ジペンタエリスリトールペンタ(メタ)アクリレート、N,N-(2,2,4-トリメチルヘキサメチレン)ビス〔2-(アミノカルボキシ)プロパン-1,3-ジオール〕テトラメタクリレート、1,7-ジアクリロイルオキシ-2,2,6,6-テトラアクリロイルオキシメチル-4-オキシヘプタン等の3官能以上の多官能性単量体;
ヘキサメチレンジイソシアネート(HDI)、トリレンジイソシアネート(TDI)、キシリレンジイソシアネート(XDI)、ジフェニルメタンジイソシアネート(MDI)、イソホロンジイソシアネート(IPDI)、トリメチルヘキサメチレンジイソシアネート(TMHMDI)等のイソシアネート基(-NCO)を有する化合物と、2-ヒドロキシエチル(メタ)アクリレート、2-ヒドロキシプロピル(メタ)アクリレート、2-ヒドロキシブチル(メタ)アクリレート、6-ヒドロキシヘキシル(メタ)アクリレート、10-ヒドロキシデシル(メタ)アクリレート、3-クロロ-2-ヒドロキシプロピル(メタ)アクリレート、2-ヒドロキシ-3-フェノキシプロピル(メタ)アクリレート、グリセリンモノ(メタ)アクリレート、N-ヒドロキシエチル(メタ)アクリルアミド、N、N-(ジヒドロキシエチル)(メタ)アクリルアミド、ビスフェノールAジグリシジル(メタ)アクリレート、2-ヒドロキシ-3アクリロイルオキシプロピル(メタ)アクリレート、2,2-ビス[4-〔3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ〕フェニル]プロパン、1,2-ビス〔3-(メタ)アクリロイルオキシ-2-ヒドロキシプロポキシ〕エタン、ペンタエリスリトールトリ(メタ)アクリレート、ジペンタエリスリールのトリまたはテトラ(メタ)クリレート等の水酸基(-OH)を有する(メタ)アクリレート化合物とを付加反応させることにより合成される重合性単量体(例えば、国際公開第2012/157566号、国際公開第2015/015220号、国際公開第2015/015221号、特開2016-094482号公報に記載);
が挙げられる。
酸性基を有さないラジカル重合性単量体(e)の中でも、物性や取扱いの容易さの観点から、1,6-ビス(メタクリロキシエチルオキシカルボニルアミノ)-2,2,4-トリメチルヘキサン(UDMA)、ビスフェノールAジグリシジルメタクリレート(Bis-GMA)、2,2-ビス(4-メタクリロイルオキシポリエトキシフェニル)プロパンのうち、エトキシ基の平均付加モル数が2.6である化合物(通称「D-2.6E」)、2-ヒドロキシエチルメタクリレート(HEMA)、グリセロールジメタクリレート(GDMA)、トリエチレングリコールジメタクリレート(TEGDMA)が好ましい。
酸性基を有さない重合性単量体(e)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の酸性基を有さない重合性単量体(e)の含有量は、重合性単量体の合計100質量部中、好ましくは50~99質量部、より好ましくは65~97質量部、さらに好ましくは75~95質量部である。このような態様であると、硬化性組成物の流動性を向上でき、その重合性混合物から得られる硬化物の機械的強度や接着強度などを向上させることができる。
(過酸化物(f))
本発明の硬化性組成物は、過酸化物(f)を実質的に含有しなくてもよいが、実施形態次第では過酸化物(f)を含有していてもよい。硬化性組成物に過酸化物(f)を配合することにより、その重合性混合物の重合性が向上し、得られる硬化物の機械的強度や接着強度に優れる傾向にある。
本発明の硬化性組成物は、過酸化物(f)を実質的に含有しなくてもよいが、実施形態次第では過酸化物(f)を含有していてもよい。硬化性組成物に過酸化物(f)を配合することにより、その重合性混合物の重合性が向上し、得られる硬化物の機械的強度や接着強度に優れる傾向にある。
過酸化物(f)としては、公知の化合物を何の制限を受けることなく使用することができる。例えば、過酸化ベンゾイル等のジアシルバーオキサイド化合物、t-ブチルパーオキシベンゾエート等のパーオキシエステル化合物、1,1-ジ(t-ブチルパーオキシ)シクロヘキサン等のアルキル過酸化物、1,1,3,3-テトラメチルブチルハイドロパーオキサイド等のハイドロパーオキサイド化合物、過流酸塩等の無機過酸化物が挙げられる。本発明の硬化性組成物へ配合した場合に得られる効果の高さから、特にパーオキシエステル化合物およびハイドロパーオキサイド化合物が好ましい。遷移金属化合物(b)としてバナジウム化合物を用いる場合は、特にハイドロパーオキサイド化合物を用いることが好ましい。
パーオキシエステル化合物としては、ペルオキシ基(-OO-基)の一方にアシル基、もう一方に炭化水素基(またはそれに類する有機基)を有するものであれば公知のものを何ら制限なく使用することができる。具体的には、t-ブチルパーオキシイソブチレート、t-ブチルパーオキシラウレート、t-ブチルパーオキシ-2-エチルヘキシルモノカーボネート、t-ブチルパーオキシイソノナノエート、t-ブチルパーオキシアセテート、t-ブチルパーオキシベンゾエート、t-ブチルパーオキシ-3,5,5-トリメチルヘキサノエート、2,5-ジメチル-2,5-ビス(2-エチルヘキサノイルパーオキシ)ヘキサン、クミルパーオキシネオデカノエート、1,1,3,3-テトラメチルブチルパーオキシネオデカノエート、2,5-ジメチル-2,5-ビス(m-トルオイルパーオキシ)ヘキサン、2,5-ジメチル-2,5-ビス(ベンゾイルパーオキシ)ヘキサン等が挙げられる。これらの中でも、保存安定性と重合活性の観点から、t-ブチルパーオキシベンゾエート、t-ブチルパーオキシイソノナノエートが好ましい。
ハイドロパーオキサイド化合物としては、ペルオキシ基(-OO-基)の一方に炭化水素基(またはそれに類する有機基)、もう一方に水素を有するものであれば公知のものを何ら制限なく使用することができる。具体的には、p-メンタンハイドロパーオキサイド、ジイソプロピルベンゼンハイドロパーオキサイド、1,1,3,3-テトラメチルブチルハイドロパーオキサイド、クメンハイドロパーオキサイド、t-へキシルハイドロパーオキサイド、t-アミルハイドロパーオキサイドが挙げられる。これらの中でも、保存安定性と重合活性の観点から、1,1,3,3-テトラメチルブチルハイドロパーオキサイド、クメンハイドロパーオキサイドが好ましい。
過酸化物(f)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物に過酸化物(f)を配合する場合、重合性混合物の硬化時間、操作可能時間、得られる硬化物の色調安定性に悪い影響を与えない範囲で配合することが好ましい。本発明の硬化性組成物中の過酸化物(f)の含有量は、重合性単量体100質量部に対して、好ましくは0.01~5質量部、より好ましくは0.05~3質量部、さらに好ましくは0.1~1質量部である。
いくつかの実施形態では、本発明の硬化性組成物は、過酸化物(f)を実質的に含有しなくてよい。本発明の硬化性組成物が過酸化物(f)を実質的に含有しないとは、具体的には、本発明の硬化性組成物中の過酸化物(f)の含有量が、重合性単量体100質量部に対して、0.01質量部未満であることを意味する。
(光重合開始剤(g))
本発明の硬化性組成物は、光重合開始剤(g)が含有することが好ましい一態様である。本発明の硬化性組成物に光重合開始剤(g)を配合することにより、デュアルキュア型の硬化性組成物の提供が可能となり、光照射による組成物の硬化が可能になる。
本発明の硬化性組成物は、光重合開始剤(g)が含有することが好ましい一態様である。本発明の硬化性組成物に光重合開始剤(g)を配合することにより、デュアルキュア型の硬化性組成物の提供が可能となり、光照射による組成物の硬化が可能になる。
光重合開始剤(g)としては、公知のものを何ら制限なく使用することができ、例えば、α-ジケトン/還元剤、ケタール/還元剤、チオキサントン/還元剤、アシルホスフィンオキサイド化合物が挙げられる。α-ジケトン/還元剤とは、α-ジケトンと還元剤との組合せを意味し、その他の用例も同様である。また、α-ジケトン/還元剤中の「還元剤」は、光重合開始剤(g)における還元剤を意味し、化学重合開始剤における還元剤として使用される上述の還元剤(d)は含まない。その他の用例も同様である。
光重合開始剤(g)がα-ジケトン/芳香族アミン化合物である場合、芳香族アミン化合物は芳香環に結合する水素原子のうち少なくともひとつが電子求引性基(ハロゲン基を含む)で置換された芳香族アミン化合物を含むことがさらに好ましい。
α-ジケトンとしては、例えば、ジアセチル、2,3-ペンタジオン、2,3-ヘキサジオン、ベンジル、4,4'-ジメトキシベンジル、4,4'-ジエトキシベンジル、4,4'-オキシベンジル、4,4'-ジクロルベンジル、4-ニトロベンジル、α-ナフチル、β-ナフチル、カンファーキノン(CQ)、カンファーキノンスルホン酸、カンファーキノンカルボン酸、1,2-シクロへキサンジオン、メチルグリオキザール、フェニルグリオキザール、ピルビン酸、ベンゾイルギ酸、フェニルピルビン酸、ピルビン酸メチル、ベンゾイルギ酸エチル、フェニルピルビン酸メチル、フェニルピルビン酸ブチルが挙げられる。
ケタールとしては、例えば、ベンジルジメチルケタール、ベンジルジエチルケタールが挙げられる。
チオキサントンとしては、例えば、2-クロロチオキサントン、2,4-ジエチルチオキサントン、2-ヒドロキシ-3-(9-オキシ-9H-チオキサンテン-4-イルオキシ)-N,N,N-トリメチル-プロパンアミニウムクロライド、2-ヒドロキシ-3-(1-メチル-9-オキシ-9H-チオキサンテン-4-イルオキシ)-N,N,N-トリメチル-プロパンアミニウムクロライド、2-ヒドロキシ-3-(9-オキソ-9H-チオキサンテン-2-イルオキシ)-N,N,N-トリメチル-プロパンアミニウムクロライド、2-ヒドロキシ-3-(3,4-ジメチル-9-オキソ-9H-チオキサンテン-2-イルオキシ)-N,N,N-トリメチル-1-プロパンアミニウムクロライド、2-ヒドロキシ-3-(3,4-ジメチル-9H-チオキサンテン-2-イルオキシ)-N,N,N-トリメチル-1-プロパンアミニウムクロライド、2-ヒドロキシ-3-(1,3,4-トリメチル-9-オキソ-9H-チオキサンテン-2-イルオキシ)-N,N,N-トリメチル-1-プロパンアミニウムクロライドが挙げられる。
アシルホスフィンオキサイド化合物としては、例えば、ベンゾイルジメトキシホスフィンオキシド、ベンゾイルエトキシフェニルホスフィンオキシド、ベンゾイルジフェニルホスフィンオキシド、2-メチルベンゾイルジフェニルホスフィンオキシド、2,4,6-トリメチルベンゾイルジフェニルホスフィンオキシド、ビス(2,6-ジメトキシベンゾイル)-2,4,4-トリメチルペンチルフォスフィンオキシド、ビス(2,4,6-トリメチルベンゾイル)-フェニルホスフィンオキシドが挙げられる。
上記還元剤としては、例えば、過酸化水素等の過酸化物、ミヒラーケトン;
シトロネラール、ラウリルアルデヒド、フタルジアルデヒド、ジメチルアミノベンズアルデヒドおよびテレフタルアルデヒド等のアルデヒド類;
デカンチオール、3-メルカプトプロピルトリメトキシシラン、4-メルカプトアセトフェノン、チオサリチル酸、チオ安息香酸等のメルカプタン類;
N,N-ジメチルアミノ安息香酸メチル、N,N-ジメチルアミノ安息香酸エチル(DMABAE)、N,N-ジメチルアミノ安息香酸ブトキシエチル(DMABABE)などのN,N-ジメチルアミノ安息香酸およびそのアルキルエステル、N,N-ジエチルアミノ安息香酸(DEABA)およびそのアルキルエステル、N,N-ジメチルアミノベンズアルデヒド(DMABAd)、N,N-ジメチルアミノベンゾフェノン、N,N-ジメチル-p-フルオロアニリン等の、芳香環に結合する水素原子のうち少なくともひとつが電子求引性基(ハロゲン原子を含む)で置換された芳香族アミン化合物;
が挙げられる。
シトロネラール、ラウリルアルデヒド、フタルジアルデヒド、ジメチルアミノベンズアルデヒドおよびテレフタルアルデヒド等のアルデヒド類;
デカンチオール、3-メルカプトプロピルトリメトキシシラン、4-メルカプトアセトフェノン、チオサリチル酸、チオ安息香酸等のメルカプタン類;
N,N-ジメチルアミノ安息香酸メチル、N,N-ジメチルアミノ安息香酸エチル(DMABAE)、N,N-ジメチルアミノ安息香酸ブトキシエチル(DMABABE)などのN,N-ジメチルアミノ安息香酸およびそのアルキルエステル、N,N-ジエチルアミノ安息香酸(DEABA)およびそのアルキルエステル、N,N-ジメチルアミノベンズアルデヒド(DMABAd)、N,N-ジメチルアミノベンゾフェノン、N,N-ジメチル-p-フルオロアニリン等の、芳香環に結合する水素原子のうち少なくともひとつが電子求引性基(ハロゲン原子を含む)で置換された芳香族アミン化合物;
が挙げられる。
光重合開始剤(g)の中でも、可視光領域に吸収波長を有し、可視光線で重合させることが可能な観点から、カンファーキノンおよび/またはアシルホスフィンオキサイド化合物を含有する光重合開始剤が好ましく、特に、468nmに吸収波長を有するカンファーキノンを含有する光重合開始剤がより好ましい。
カンファーキノン/還元剤を含有する光重合開始剤としては、例えば、カンファーキノン/芳香族アミン化合物を含有する重合開始剤、カンファーキノン/過酸化水素等の過酸化物を含有する光重合開始剤、カンファーキノン/アルデヒド類を含有する重合開始剤、カンファーキノン/メルカプタン類を含有する重合開始剤が挙げられる。これらの中でも、カンファーキノン/芳香族アミン化合物を含有する重合開始剤が好ましい。用いる芳香族アミン化合物としては、光重合の重合促進効果と取り扱いの観点から、DMABAE、DMABABEが好ましい。
光重合開始剤(g)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
本発明の硬化性組成物中の光重合開始剤(g)の含有量は、重合性単量体100質量部に対して、好ましくは0.001~5質量部、より好ましくは0.005~2質量部、さらに好ましくは0.01~1質量部である。光重合開始剤(g)の含有量が前記下限値よりも少ないと、硬化性組成物の光照射による硬化が充分に進行しない場合があり、前記上限値よりも多いと、重合性混合物が光重合開始剤(g)由来の色調に呈色したり、保存中に組成物が硬化したりする場合がある。
(フィラー(h))
本発明の硬化性組成物は、フィラー(h)を含有してもよい。硬化性組成物にフィラー(h)が含まれていることにより、例えば、硬化性組成物の流動性、稠度、色調および硬化性などを調整することができ、X線不透過性の付与、得られた硬化物の機械的強度を向上させることができる。フィラー(h)としては、一般的に汎用される公知のフィラーを制限無く使用することができる。
本発明の硬化性組成物は、フィラー(h)を含有してもよい。硬化性組成物にフィラー(h)が含まれていることにより、例えば、硬化性組成物の流動性、稠度、色調および硬化性などを調整することができ、X線不透過性の付与、得られた硬化物の機械的強度を向上させることができる。フィラー(h)としては、一般的に汎用される公知のフィラーを制限無く使用することができる。
フィラー(h)は、通常、有機フィラーと無機フィラーに大別される。
有機フィラーとしては、例えば、重合体の粉砕または重合性単量体の分散重合によって得られた粉末重合体のフィラーや、架橋剤を含む重合性単量体を重合させた後、粉砕して得られるフィラーが挙げられる。有機フィラーとしては、例えば、ポリメタクリル酸メチル(PMMA)、ポリメタクリル酸エチル、ポリメタクリル酸プロピル、ポリメタクリル酸ブチル(PBMA)、ポリ酢酸ビニル(PVAc)、ポリエチレングリコール(PEG)やポリプロピレングリコール(PPG)、ポリビニルアルコール(PVA)、ポリウレタン、ポリウレア、メタクリル酸メチル-メタクリル酸エチル共重合体、架橋型ポリメタクリル酸メチル、架橋型ポリメタクリル酸エチル、エチレン-酢酸ビニル共重合体およびスチレン-ブタジエン共重合体等の重合性単量体の単独重合体または共重合体の微粉末が挙げられる。また、有機フィラーは、有機フィラーの調製時に、公知の色素や生物活性成分、重合開始剤などの成分を添加して得られた物であってもよい。
無機フィラーとしては、例えば、各種ガラス類(二酸化珪素を主成分とし、必要に応じ、重金属、ホウ素およびアルミニウム等の酸化物を含有する)、各種セラミック類、珪藻土、カオリン、粘土鉱物(モンモリロナイト等)、活性白土、合成ゼオライト、マイカ、フッ化カルシウム、フッ化イッテルビウム、炭酸カルシウム、リン酸カルシウム、硫酸アルミニウム、硫酸バリウム、硫酸カルシウム、二酸化ジルコニウム、二酸化チタン、酸化アルミニウム、酸化ホウ素、酸化バリウム、酸化ランタン、酸化ストロンチウム、酸化亜鉛、酸化カルシウム、酸化リチウム、酸化ナトリウム、酸化ビスマス、酸化イットリウム、リン酸カルシウム、ヒドロキシアパタイト、水酸化アルミニウム、フッ化ナトリウム、フッ化カリウム、モノフルオロリン酸ナトリウム、フッ化リチウム、フッ化イッテルビウム等の微粉末が挙げられる。このような無機フィラーの具体例としては、例えば、バリウムボロシリケートガラス微粉末(キンブルレイソーブT3000、ショット8235、ショットGM27884、ショットG018-053およびショットGM39923など)、ストロンチウムボロアルミノシリケートガラス微粉末(レイソーブT4000、ショットG018-093、ショットG018-163およびショットGM32087など)、ランタンガラス微粉末(ショットGM31684など)、フルオロアルミノシリケートガラス微粉末(ショットG018-091およびショットG018-117など)、ジルコニウムおよび/またはセシウム含有のボロアルミノシリケートガラス微粉末(ショットG018-307、G018-308およびG018-310など)が挙げられる。
また、これら無機フィラーに重合性単量体を予め添加し、ペースト状にした後、重合・硬化させ、粉砕して得られる有機無機複合フィラーを用いても差し支えない。有機無機複合フィラーとしては、例えば、無機質フィラーのうちの微粉末シリカまたは酸化ジルコニウムなどをトリメチロールプロパントリ(メタ)アクリレート(TMPT)を主成分とする重合性単量体で重合被覆し、得られた重合体を粉砕したフィラー(TMPT・f)が挙げられる。
粒径が0.1μm以下のミクロフィラーが配合された歯科材料は、歯科用コンポジットレジンに好適な態様の一つである。かかる粒径の小さなフィラーの材質としては、シリカ(例えば、商品名アエロジル)、アルミナ、ジルコニア、チタニアなどが好ましい。このような粒径の小さい無機フィラーの配合は、硬化物の研磨滑沢性および耐摩耗性を得る上で有利である。
これらのフィラーに対して、目的に応じて、シランカップリング剤などにより表面処理が施される。無機フィラーまたは有機無機複合フィラーを用いる場合、本発明に使用される重合性単量体との親和性や分散性を良好にするため、公知の表面処理剤でフィラー表面を処理して用いるのが好ましい。かかる表面処理剤としては、公知のシランカップリング剤を制限無く使用することができる。例えば、γ-メタクリルオキシアルキルトリメトキシシラン(メタクリルオキシ基とケイ素原子との間の炭素数:3~12)、γ-メタクリルオキシアルキルトリエトキシシラン(メタクリルオキシ基と珪素原子との間の炭素数:3~12)、ビニルトリメトキシシラン、ビニルエトキシシランおよびビニルトリアセトキシシラン等の有機珪素化合物が使用される。表面処理剤の濃度は、フィラー100質量部に対して、通常0.1~20質量部、好ましくは0.5~10質量部の範囲で使用される。また、シランカップリング剤以外にも、チタネート系カップリング剤、アルミネート系カップリング剤、ジルコ-アルミネート系カップリング剤等により表面処理して用いてもよい。さらには、充填材粒子表面に前記ラジカル重合性単量体をグラフト重合させて用いてもよい。表面処理の方法としては、公知の方法を特に限定されずに用いることができる。
これらのフィラー(h)は、本発明の硬化性組成物の用途に応じて、適宜添加することができる。フィラー(h)は1種単独で用いても、2種以上を組み合わせて用いてもよい。
フィラー(h)の含有量はその用途に応じて適宜設定できる。例えば分包型硬化性組成物の場合には、フィラー(h)の含有量は、第1剤(A)および第2剤(B)に含まれる重合性単量体の合計100質量部に対して、好ましくは10~900質量部、より好ましくは40~400質量部、さらに好ましくは60~240質量部である。このような態様であると、本発明の分包型硬化性組成物を歯科用接着性レジンセメントまたは歯科用コンポジットレジン等として用いる場合に好ましい。
(有機溶剤(i)及び/又は水(j))
本発明の硬化性組成物は、有機溶剤(i)を含有してもよい。有機溶剤(i)としては、例えば、アセトン、エタノール、イソプロパノール、テトラヒドロフラン、アセトニトリル、ヘキサン、トルエン、酢酸エチル、ジクロロメタンが挙げられる。本発明の硬化性組成物を歯科材料用途に使用する場合、接着性および歯面に対する親和性の観点から、アセトン、エタノール、イソプロパノール等の水溶性有機溶剤を用いることが好ましい。水溶性有機溶剤とは、任意の割合で水と均一な溶液を形成する有機溶剤のことである。
本発明の硬化性組成物は、有機溶剤(i)を含有してもよい。有機溶剤(i)としては、例えば、アセトン、エタノール、イソプロパノール、テトラヒドロフラン、アセトニトリル、ヘキサン、トルエン、酢酸エチル、ジクロロメタンが挙げられる。本発明の硬化性組成物を歯科材料用途に使用する場合、接着性および歯面に対する親和性の観点から、アセトン、エタノール、イソプロパノール等の水溶性有機溶剤を用いることが好ましい。水溶性有機溶剤とは、任意の割合で水と均一な溶液を形成する有機溶剤のことである。
本発明の硬化性組成物は、水(j)を含有してもよい。水(j)としては、重合性ならびに接着性に悪影響を与える不純物が無いように、蒸留水やイオン交換水を用いることが好ましい。
本発明の硬化性組成物に有機溶剤(i)を配合する場合、その含有量は、重合性単量体と、有機溶剤(i)と、水(j)との合計100質量部中、好ましくは5~95質量部、より好ましくは10~90質量部、さらに好ましくは20~75質量部である。このような態様であると、本発明の硬化性組成物の均一性や流動性、接着強度を向上することができる。
本発明の硬化性組成物に水(j)を配合する場合、その含有量は、重合性単量体と、有機溶剤(i)と、水(j)との合計100質量部中、好ましくは0.5~50質量部、より好ましくは1~40質量部、さらに好ましくは5~30質量部である。このような態様であると、本発明の硬化性組成物の均一性や流動性、接着強度を向上することができる。
(その他の成分)
本発明の硬化性組成物には、硬化性組成物としての保存安定性や機能を損なわない限り、上記以外のその他の成分を、目的に応じて適宜含有してもよい。
本発明の硬化性組成物には、硬化性組成物としての保存安定性や機能を損なわない限り、上記以外のその他の成分を、目的に応じて適宜含有してもよい。
例えば、硬化性組成物の保存安定性等を向上させるために、重合禁止剤、紫外線吸収剤等の各種安定剤を含有してもよく、色調を調整するために、公知の顔料、染料、蛍光剤等を含有してもよい。また、塩化カルシウム等のカルシウム含有化合物、フッ化ナトリウム等のフッ素含有化合物、防カビ剤、抗菌剤、治療および生物活性成分などを含有してもよい。さらに、得られる硬化物の機械的強度を向上させるために、公知のファイバー等の補強材を含有してもよい。
上記その他の成分それぞれの含有量は、本発明の効果を損なわないこと、およびその他の成分の特性を発揮する観点から、重合性単量体100質量部に対して、好ましくは0.00001~10質量部、より好ましくは0.00005~5質量部、さらに好ましくは0.0001~1質量部である。
[分包型硬化性組成物]
本発明の硬化性組成物は、例えば、第1剤(A)および第2剤(B)のように複数の剤に分包されていてもよく、すなわち分包型硬化性組成物であってもよく、これら各剤の形態としては、例えば、ペースト、液等の形態が挙げられる。
本発明の硬化性組成物は、例えば、第1剤(A)および第2剤(B)のように複数の剤に分包されていてもよく、すなわち分包型硬化性組成物であってもよく、これら各剤の形態としては、例えば、ペースト、液等の形態が挙げられる。
取り扱いの容易性の観点から、第1剤(A)および第2剤(B)ともにペースト状または液状であることが好ましい。本発明の硬化性組成物が、第1剤(A)および第2剤(B)ともにペースト状製剤である2ペースト型組成物である場合は、歯科用接着性レジンセメントに好適である。また、本発明の硬化性組成物が、第1剤(A)および第2剤(B)ともに液状製剤である2液型組成物である場合は、歯科用接着材に好適である。分包型硬化性組成物は、第3剤(C)等のその他の剤を有してもよい。
本発明の硬化性組成物は、通常、第1剤(A)と第2剤(B)とから構成され、夫々の成分が必要に応じて各々の製剤に別々に保存される。第1剤(A)に含まれる各成分が複数の剤にさらに分包されていてもよい。第2剤(B)に含まれる各成分が複数の剤にさらに分包されていてもよい。
(第1剤(A))
第1剤(A)は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)とを含有することが好ましい。また、第1剤(A)に酸性基を有する重合性単量体(a)、および遷移金属化合物(b)が含まれることにより、保存中にその性能が損なわれることがなく、第2剤(B)に含まれる成分に悪影響を与えることがない。
第1剤(A)は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)とを含有することが好ましい。また、第1剤(A)に酸性基を有する重合性単量体(a)、および遷移金属化合物(b)が含まれることにより、保存中にその性能が損なわれることがなく、第2剤(B)に含まれる成分に悪影響を与えることがない。
(第2剤(B))
第2剤(B)は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)(例えば、スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1))とを含有することが好ましい。
第2剤(B)は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)(例えば、スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1))とを含有することが好ましい。
酸性基を有さない重合性単量体(e)は、第1剤(A)および第2剤(B)のどちらか一方に含まれていても両方に含まれていてもよく、両方に含まれていることが好ましい。第1剤(A)と第2剤(B)の両方に酸性基を有さない重合性単量体(e)が含まれる場合には、第1剤(A)に含まれるものと第2剤(B)に含まれるものとは同一でも異なっていてもよい。
本発明の硬化性組成物に過酸化物(f)が含まれる場合には、過酸化物(f)は第2剤(B)に含まれることが好ましい。第2剤(B)中で過酸化物(f)を保存することにより、保存中に第1剤(A)中の成分に悪い影響を与えず、保存中にその活性が低下しない傾向にある。
本発明の硬化性組成物に光重合開始剤(g)が含まれる場合には、保存安定性の観点から、光重合開始剤(g)は第2剤(B)に含まれることが好ましい。また、光重合開始剤(g)は、第1剤(A)および第2剤(B)以外の別の剤(例えば第3剤(C))に含ませることも好ましい態様である。例えば、光重合開始剤(g)としてカンファーキノン、アシルホスフィンオキサイド化合物が第3剤(C)等に含まれる場合、第2剤(B)に含まれ得る酸性基を有さない重合性単量体(e)の保存安定性をより向上することができる。
フィラー(h)、有機溶剤(i)および水(j)は、第1剤(A)および第2剤(B)のどちらか一方または両方に含まれていてもよい。第1剤(A)と第2剤(B)の両方にフィラー(h)および/または有機溶剤(i)が含まれる場合には、第1剤(A)に含まれるものと第2剤(B)に含まれるものとは同一でも異なっていてもよい。
第1剤(A)と第2剤(B)との混和質量比は、得られる重合性混合物の硬化性および接着操作に使用できる時間(操作可能時間)などから適宜設定できるが、1:10~10:1が好ましく、1:5~5:1がより好ましく、1:2~2:1がさらに好ましい。
本発明の硬化性組成物は、分包された各剤を混合して得られた重合性混合物を、20~50℃、例えば、常温または体温(37℃)付近で硬化させることができ、得られる硬化物は、歯科治療用途等の歯科用途に用いることができる。また、本発明の硬化性組成物は、常温以上でも硬化させることができる。一実施態様では、本発明の硬化性組成物は、例えば10~120℃で硬化させることもできる。
また、硬化性組成物の成分として光重合開始剤(g)が含まれる場合は、分包された各剤を混合して得られた重合性混合物を所定の形状に加工したのち、公知の光照射装置を用いて所定の時間可視光を照射することにより、所望の硬化物を得ることができる。照射強度、照射時間等の条件は、本発明の分包型硬化性組成物の硬化性に合わせて適切に変更することができる。また、光照射後の硬化物を、さらに適切な条件で熱処理をすることにより、得られる硬化物の機械的物性を向上させることもできる。
本発明の硬化性組成物は、種々の歯科治療用途等の歯科用途に好適に用いることができる。本発明の硬化性組成物は、例えば、歯科用接着性レジンセメント、歯科用コンポジットレジン(自己接着性を有するものを含む。以下同じ)、歯科用ボンディング材、歯科用裏層材、歯科用根幹充填材、歯列矯正用接着材、動揺歯固定材、歯牙小窩裂溝封鎖材(歯科用シーラント)、歯科用仮着セメント、歯科用充填材料などとして用いることができる。
本発明の硬化性組成物は、歯科材料の使用方法として一般に知られている方法で使用することができる。例えば、本発明の分包型硬化性組成物を、歯科用接着性レジンセメント、歯科用コンポジットレジン等として使用する場合には、分包型硬化性組成物に含まれる各剤を混合して得た重合性混合物を単独で接着面に塗布して用いることができる。また、本発明の硬化性組成物を歯科材料として使用する場合には、さらに他の歯科材料とともに使用してもよい。例えば、被着体の接着面にボンディング材やプライマー等の他の組成物で処理した後に、本発明の硬化性組成物から調製される重合性混合物を塗布して用いることもできる。さらには、本発明の硬化性組成物をボンディング材として、被着体の被着面に対して直接塗布した後、歯科用コンポジットレジン等の他の硬化性組成物を充填して用いることもできる。
本発明の硬化性組成物は、良好な重合性を有する。また、過酸化物を実質的に含有しない硬化性組成物である場合も充分な機械的強度を有する硬化物を与える硬化性組成物を調製することができる。さらに、常温以上の長期保存安定性に優れる硬化性組成物を調製することもできる。
本発明の硬化性組成物の37℃における硬化時間は、0.5~4分が好ましく、0.8~3.5分がより好ましく、1~3分がさらに好ましい。また、本発明の硬化性組成物から形成された硬化物の三点曲げ強度は、50MPa以上が好ましく、70MPa以上がより好ましく、80MPa以上がさらに好ましい。三点曲げ強度は高い方が好ましく、その上限は特に限定されないが、例えば240MPa等であってもよい。さらに、本発明の硬化性組成物を55℃で3週間保存した後の37℃における硬化時間が3分以内であることが好ましく、1~3分がより好ましい。なお、本発明の硬化性組成物の硬化時間、三点曲げ強度、保存安定性の評価は実施例に記載された方法により求めたものである。
[重合開始用キット]
上述の本発明の分包型硬化性組成物は、重合開始用キットとして用いることができる。すなわち、本発明の重合開始用キットは、第1剤(A)と第2剤(B)とを含む。第1剤(A)は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)を含有する。第2剤(B)は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する。
上述の本発明の分包型硬化性組成物は、重合開始用キットとして用いることができる。すなわち、本発明の重合開始用キットは、第1剤(A)と第2剤(B)とを含む。第1剤(A)は、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)を含有する。第2剤(B)は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する。
本発明の重合開始用キットにおいて、第1剤(A)および第2剤(B)は、通常、別々の容器に収容される。第1剤(A)に含まれる各成分が複数の剤にさらに分包されていてもよい。第2剤(B)に含まれる各成分が複数の剤にさらに分包されていてもよい。
すなわち、第1剤(A)に含まれる各成分は、同一の容器に収容されていてもよく、別々の容器に収容されていてもよい。例えば、第1剤(A)に含まれる酸性基を有する重合性単量体(a)および遷移金属化合物(b)が、同一の容器に収容されていてもよく、別々の容器に収容されていてもよい。また、第2剤(B)に含まれる各成分は、同一の容器に収容されていてもよく、別々の容器に収容されていてもよい。例えば、第2剤(B)に含まれる化合物(c)および還元剤(d)が、同一の容器に収容されていてもよく、別々の容器に収容されていてもよい。
本発明の重合開始用キットは、上述の本発明の硬化性組成物同様の用途に使用でき、好適な用途も同様である。
[重合開始剤]
上述の本発明の分包型硬化性組成物における第2剤(B)は、重合開始剤として用いてもよい。すなわち、本発明の重合開始剤は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含むことができる。
上述の本発明の分包型硬化性組成物における第2剤(B)は、重合開始剤として用いてもよい。すなわち、本発明の重合開始剤は、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含むことができる。
以下、実施例および比較例を挙げて本発明を詳細に説明するが、本発明はこれら実施例に限定されるものではない。実施例に使用した化合物の略号を以下に示す。
[酸性基を有する重合性単量体(a)]
4-MET:4-メタクリロイルオキシエチルトリメリット酸
(サンメディカル株式会社製)
MDP:10-メタクリロイルオキシデシルジハイドロジェンホスフェート(富士フィルム和光純薬株式会社製)
[遷移金属化合物(b)]
VO(acac)2:バナジル(IV)アセチルアセトナート
(東京化成工業株式会社製、使用前に乳鉢で粉砕したものを使用)
V(acac)3:バナジウム(III)アセチルアセトナート
(シグマ-アルドリッチ社製)
Cu(OAc)2:酢酸銅(II)(富士フィルム和光純薬株式会社製)
CuCl:塩化銅(I)(富士フィルム和光純薬株式会社製)
CuCl2:塩化銅(II)(富士フィルム和光純薬株式会社製)
CuBr2:臭化銅(II)(シグマ-アルドリッチ社製)
[ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)]
HPBO:2-(2-ヒドロキシフェニル)ベンゾオキサゾール
(東京化成工業株式会社製)
HPBT:2-(2-ヒドロキシフェニル)ベンゾチアゾール
(東京化成工業株式会社製)
BO:ベンゾオキサゾール(東京化成工業株式会社製)
BT:ベンゾチアゾール(富士フィルム和光純薬株式会社製)
PBT:2-フェニルベンゾチアゾール(東京化成工業株式会社製)
APBT:2-(2-アミノフェニル)ベンゾチアゾール
(シグマ-アルドリッチ社製)
[ベンゾイミダゾール化合物]
HPBI:2-(2-ヒドロキシフェニル)ベンゾイミダゾール
(シグマ-アルドリッチ社製)
[還元剤(d)]
[スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)]
p-TSS:p-トルエンスルフィン酸ナトリウム(富士フィルム和光純薬株式会社製、購入後70℃で減圧乾燥し、乳鉢で粉砕したもの)
[芳香族アミン化合物]
DEPT:N,N-ジエタノール-p-トルイジン
(富士フィルム和光純薬株式会社製)
[酸性基を有さない重合性単量体(e)]
UDMA:1,6-ビス(メタクリロキシエチルオキシカルボニルアミノ)-2,2,4-トリメチルヘキサン(公知のウレタン化反応の手法に従い、HEMAと2,2,4-トリメチルヘキシルジイソシアネートとの2:1とで自製した化合物)
TEGDMA:トリエチレングリコールジメタクリレート
(新中村化学工業株式会社製)
HEMA:2-ヒドロキシエチルメタクリレート
(三菱ケミカル株式会社製)
[過酸化物(f)]
TMBHP:1,1,3,3-テトラメチルブチルハイドロパーオキサイド(アルケマ吉富株式会社製、商品名「ルペロックス215」)
BPO:過酸化ベンゾイル(東京化成工業株式会社製)
[光重合開始剤(g)]
CQ:d,l-カンファーキノン(富士フィルム和光純薬株式会社製)
DMABAE:N,N-ジメチルアミノ安息香酸エチル
(富士フィルム和光純薬株式会社製)
[フィラー(h)]
F1:シラン処理バリウムガラス粉、シラン処理フルオロアルミノシリケート粉など(SCHOTT社製、商品名「GM8235」、「G018-117」など)
R812:微粒子シリカ
(日本アエロジル株式会社製、商品名「エアロジルR812」)
[有機溶剤(i)]
Acetone:アセトン(富士フィルム和光純薬株式会社製)
EtOH:エタノール(富士フィルム和光純薬株式会社製)
[水(j)]
蒸留水:蒸留水製造装置(東京理化器械株式会社製)により製造したもの
[その他の成分:重合禁止剤]
BHT:2,6-ジ-t-ブチル-4-メチルフェノール
(東京化成工業株式会社製)
MEHQ:4-メトキシフェノール(富士フィルム和光純薬株式会社製)
下記表1および表2に記載の各配合(表の各数値は質量部)にしたがって、各成分を混合して第1剤(A)および第2剤(B)を調製し、これら2剤の総質量比が1:1の分包型硬化性組成物を作製した。
4-MET:4-メタクリロイルオキシエチルトリメリット酸
(サンメディカル株式会社製)
MDP:10-メタクリロイルオキシデシルジハイドロジェンホスフェート(富士フィルム和光純薬株式会社製)
[遷移金属化合物(b)]
VO(acac)2:バナジル(IV)アセチルアセトナート
(東京化成工業株式会社製、使用前に乳鉢で粉砕したものを使用)
V(acac)3:バナジウム(III)アセチルアセトナート
(シグマ-アルドリッチ社製)
Cu(OAc)2:酢酸銅(II)(富士フィルム和光純薬株式会社製)
CuCl:塩化銅(I)(富士フィルム和光純薬株式会社製)
CuCl2:塩化銅(II)(富士フィルム和光純薬株式会社製)
CuBr2:臭化銅(II)(シグマ-アルドリッチ社製)
[ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)]
HPBO:2-(2-ヒドロキシフェニル)ベンゾオキサゾール
(東京化成工業株式会社製)
HPBT:2-(2-ヒドロキシフェニル)ベンゾチアゾール
(東京化成工業株式会社製)
BO:ベンゾオキサゾール(東京化成工業株式会社製)
BT:ベンゾチアゾール(富士フィルム和光純薬株式会社製)
PBT:2-フェニルベンゾチアゾール(東京化成工業株式会社製)
APBT:2-(2-アミノフェニル)ベンゾチアゾール
(シグマ-アルドリッチ社製)
[ベンゾイミダゾール化合物]
HPBI:2-(2-ヒドロキシフェニル)ベンゾイミダゾール
(シグマ-アルドリッチ社製)
[還元剤(d)]
[スルフィン酸およびその塩から選ばれる少なくとも1種の化合物(d1)]
p-TSS:p-トルエンスルフィン酸ナトリウム(富士フィルム和光純薬株式会社製、購入後70℃で減圧乾燥し、乳鉢で粉砕したもの)
[芳香族アミン化合物]
DEPT:N,N-ジエタノール-p-トルイジン
(富士フィルム和光純薬株式会社製)
[酸性基を有さない重合性単量体(e)]
UDMA:1,6-ビス(メタクリロキシエチルオキシカルボニルアミノ)-2,2,4-トリメチルヘキサン(公知のウレタン化反応の手法に従い、HEMAと2,2,4-トリメチルヘキシルジイソシアネートとの2:1とで自製した化合物)
TEGDMA:トリエチレングリコールジメタクリレート
(新中村化学工業株式会社製)
HEMA:2-ヒドロキシエチルメタクリレート
(三菱ケミカル株式会社製)
[過酸化物(f)]
TMBHP:1,1,3,3-テトラメチルブチルハイドロパーオキサイド(アルケマ吉富株式会社製、商品名「ルペロックス215」)
BPO:過酸化ベンゾイル(東京化成工業株式会社製)
[光重合開始剤(g)]
CQ:d,l-カンファーキノン(富士フィルム和光純薬株式会社製)
DMABAE:N,N-ジメチルアミノ安息香酸エチル
(富士フィルム和光純薬株式会社製)
[フィラー(h)]
F1:シラン処理バリウムガラス粉、シラン処理フルオロアルミノシリケート粉など(SCHOTT社製、商品名「GM8235」、「G018-117」など)
R812:微粒子シリカ
(日本アエロジル株式会社製、商品名「エアロジルR812」)
[有機溶剤(i)]
Acetone:アセトン(富士フィルム和光純薬株式会社製)
EtOH:エタノール(富士フィルム和光純薬株式会社製)
[水(j)]
蒸留水:蒸留水製造装置(東京理化器械株式会社製)により製造したもの
[その他の成分:重合禁止剤]
BHT:2,6-ジ-t-ブチル-4-メチルフェノール
(東京化成工業株式会社製)
MEHQ:4-メトキシフェノール(富士フィルム和光純薬株式会社製)
下記表1および表2に記載の各配合(表の各数値は質量部)にしたがって、各成分を混合して第1剤(A)および第2剤(B)を調製し、これら2剤の総質量比が1:1の分包型硬化性組成物を作製した。
<硬化時間測定法(ISO4049準拠)>
各実施例および比較例の硬化時間は、示差走査熱量計(DSC)を用いた示差熱分析法により測定した。なお、測定装置としては、DSC 3500 Sirius(NETZSCH社製)を用いた。
各実施例および比較例の硬化時間は、示差走査熱量計(DSC)を用いた示差熱分析法により測定した。なお、測定装置としては、DSC 3500 Sirius(NETZSCH社製)を用いた。
具体的には、20~25℃に設定した室温下、歯科用練和紙上に等量(質量基準)採取した第1剤(A)と第2剤(B)を歯科用スパチュラで10秒間混合して、重合性混合物を得て、得られた重合性混合物をDSC測定用のAl製サンプルパンに充填した。
重合性混合物を充填したAl製サンプルパンを、37±1℃に設定したDSCの恒温槽に測定直前に設置し、練和開始40秒後に測定を開始した。重合性混合物の硬化反応によって温度が上昇し、最高温度に達した時点までの時間を硬化時間として記録した。
<三点曲げ強度測定法(ISO4049準拠)>
20~25℃に設定した室温下、歯科用練和紙上に等量(質量基準)採取した第1剤(A)と第2剤(B)を歯科用スパチュラで10秒間混合して、均一な重合性混合物とした。得られた重合性混合物を2mm×2mm×25mmの試験体作用の型に充填し、裏表両面からルミラーフィルムで圧接し、対応する重合方法で重合させた。
20~25℃に設定した室温下、歯科用練和紙上に等量(質量基準)採取した第1剤(A)と第2剤(B)を歯科用スパチュラで10秒間混合して、均一な重合性混合物とした。得られた重合性混合物を2mm×2mm×25mmの試験体作用の型に充填し、裏表両面からルミラーフィルムで圧接し、対応する重合方法で重合させた。
化学重合のみで試験体を作成する場合、重合性混合物を充填した型を37±1℃に設定した恒温器で1時間重合させて得られた硬化物を試験体とした。
光重合により試験体を作成する場合、前記室温下において技工用LED照射器により裏表1分30秒ずつ光照射して得られた硬化物を試験体とした。尚、技工用LED照射器は「アルファライトV(株式会社モリタ社製/光源:LEDランプ、400~408nm;465~475nm)」であり、紫外線積算光量計「UIT-250/ウシオ電機株式会社製」で測定した光源405nmの照度:60mW/cm2及び1分30秒間の集積光量:5,100mJ/cm2の装置を使用した。
各々の試験体を型から外して蒸留水に浸漬して、37±1℃の恒温器中で18時間保管後、試験体を取り出し、万能試験機(株式会社インテスコ社製)を用いて三点曲げ破壊強度を測定した。前記破壊強度測定試験はクロスヘッドスピード1mm/minの荷重速度で試験体が破折するまで荷重を加えて実施し、得られた最大点応力より硬化物の強度を算出した。また、この試験において、本発明の硬化性組成物により得られた硬化物の弾性率も併せて算出した。尚、曲げ強度および弾性率の測定結果は、同一条件で複数の試験体を用いて、測定した各測定値の平均値として算出したものである。
<保存安定性試験>
調製直後の第1剤(A)と第2剤(B)について、上述の方法で硬化時間を測定した後、これとは別に準備した第1剤(A)と第2剤(B)を55℃に設定した恒温器内に3週間保存した。2週間または3週間後にそれぞれの第1剤(A)および第2剤(B)を取り出し、上述した方法に従って硬化時間を測定した。
調製直後の第1剤(A)と第2剤(B)について、上述の方法で硬化時間を測定した後、これとは別に準備した第1剤(A)と第2剤(B)を55℃に設定した恒温器内に3週間保存した。2週間または3週間後にそれぞれの第1剤(A)および第2剤(B)を取り出し、上述した方法に従って硬化時間を測定した。
硬化時間が3分以内であれば、評価した重合性混合物が充分な硬化性を有すると判断することができる。また、得られた硬化物の三点曲げ強度が、80MPa以上であれば充分な強度を有する硬化物を与えると判断できる。さらに、保存安定性を評価した重合性混合物の硬化時間が、保存安定性試験後に3分以内であれば、硬化性組成物は充分な重合性を維持しており、保存安定性に優れると判断できる。
[実施例1~24、比較例1~5]
表3に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、上述の方法にしたがって、硬化時間を測定した。
表3に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、上述の方法にしたがって、硬化時間を測定した。
過酸化物(f)を含有しない実施例1~19は、良好な硬化時間を示した。一方、遷移金属化合物(b)を含有しない比較例1は、10分以内に硬化せず、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)を含有しない比較例2、3は、重合性が低下した。化合物(c)ではないベンゾイミダゾール化合物を用いた比較例4は、充分な重合促進効果は得られなかった。また、比較例5のように、過酸化物(f)の配合量が少ない過酸化物系の化学重合開始剤を含む硬化性組成物においても、充分な重合性を示さなかった。
過酸化物(f)を配合した実施例20は、重合性が向上した。さらに、有機溶剤(i)および水(j)を配合した実施例21~24においても、良好な硬化時間を与えた。
[実施例25~37、比較例6]
表4に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、上述の方法にしたがって、三点曲げ強度および弾性率を測定した。表4の括弧内には、各測定結果の標準偏差を記述した。
表4に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、上述の方法にしたがって、三点曲げ強度および弾性率を測定した。表4の括弧内には、各測定結果の標準偏差を記述した。
化学重合で硬化させた実施例25~31の硬化物は、良好な機械的強度を示した。また、光重合開始剤(g)を配合したデュアルキュア材料である実施例32~37の硬化物も、充分な機械的強度を示した。一方、比較例6のように、過酸化物(f)の配合量が少ない過酸化物系の化学重合開始剤を含む硬化性組成物からなる硬化物の機械的強度は、実施例25~37と比較して低下した。
[実施例38~44]
表5に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、前述の方法により保存安定性を評価した。実施例38~44で作成した硬化性組成物は、55℃、3週間保管後も充分な重合性を維持しており、優れた保存安定性を示した。
表5に示すように、表1および表2で作成した第1剤(A)および第2剤(B)の組み合せの硬化性組成物それぞれについて、前述の方法により保存安定性を評価した。実施例38~44で作成した硬化性組成物は、55℃、3週間保管後も充分な重合性を維持しており、優れた保存安定性を示した。
Claims (19)
- 酸性基を有する重合性単量体(a)と、
遷移金属化合物(b)と、
ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、
還元剤(d)と
を含有する硬化性組成物。 - 前記化合物(c)が、ベンゾオキサゾール環の2位にメルカプト基を有する化合物およびベンゾチアゾール環の2位にメルカプト基を有する化合物を含まない、請求項1に記載の硬化性組成物。
- 前記還元剤(d)が、スルフィン酸、スルフィン酸の塩、アスコルビン酸およびアスコルビン酸の塩から選ばれる少なくとも1種の化合物を含む、請求項1又は2に記載の硬化性組成物。
- 前記遷移金属化合物(b)が、銅化合物およびバナジウム化合物から選ばれる少なくとも1種である、請求項1~4のいずれか1項に記載の硬化性組成物。
- 酸性基を有さない重合性単量体(e)をさらに含有する、請求項1~5のいずれか1項に記載の硬化性組成物。
- 過酸化物(f)を実質的に含有しない、請求項1~6のいずれか1項に記載の硬化性組成物。
- 過酸化物(f)をさらに含有する、請求項1~6のいずれか1項に記載の硬化性組成物。
- 前記過酸化物(f)が、ハイドロパーオキサイド化合物およびパーオキシエステル化合物から選ばれる少なくとも1種である、請求項8に記載の硬化性組成物。
- 光重合開始剤(g)、フィラー(h)、有機溶剤(i)および水(j)から選ばれる少なくとも1種をさらに含有する、請求項1~9のいずれか1項に記載の硬化性組成物。
- 前記遷移金属化合物(b)、前記化合物(c)および前記還元剤(d)の合計が、重合性単量体100質量部に対して、0.1~40質量部である、請求項1~10のいずれか1項に記載の硬化性組成物。
- 前記遷移金属化合物(b)の含有量が、重合性単量体100質量部に対して、0.001~5質量部である、請求項1~11のいずれか1項に記載の硬化性組成物。
- 前記化合物(c)の含有量が、重合性単量体100質量部に対して、0.1~20質量部である、請求項1~12のいずれか1項に記載の硬化性組成物。
- 前記還元剤(d)の含有量が、重合性単量体100質量部に対して、0.01~20質量部である、請求項1~13のいずれか1項に記載の硬化性組成物。
- 歯科用途に用いられる、請求項1~14のいずれか1項に記載の硬化性組成物。
- 請求項1~15のいずれか1項に記載の硬化性組成物を含有し、歯科用接着性レジンセメント、歯科用コンポジットレジン、歯科用ボンディング材、歯科用裏層材、歯科用根幹充填材、歯列矯正用接着材、動揺歯固定材、歯科用シーラント、歯科用仮着セメントまたは歯科用充填材料である、歯科用組成物。
- 請求項1~15のいずれか1項に記載の硬化性組成物または請求項16に記載の歯科用組成物の硬化物。
- 第1剤(A)と第2剤(B)とを含む重合開始用キットであり、
前記第1剤(A)が、酸性基を有する重合性単量体(a)と、遷移金属化合物(b)とを含有し、
前記第2剤(B)が、ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する、
重合開始用キット。 - ベンゾオキサゾール化合物およびベンゾチアゾール化合物から選ばれる少なくとも1種の化合物(c)と、還元剤(d)とを含有する重合開始剤。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019551235A JP7046971B2 (ja) | 2017-10-26 | 2018-10-25 | 硬化性組成物 |
| US16/753,086 US11306160B2 (en) | 2017-10-26 | 2018-10-25 | Curable composition |
| EP18870893.7A EP3702377A4 (en) | 2017-10-26 | 2018-10-25 | CURING COMPOSITION |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017-207083 | 2017-10-26 | ||
| JP2017207083 | 2017-10-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019082964A1 true WO2019082964A1 (ja) | 2019-05-02 |
Family
ID=66247907
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2018/039650 WO2019082964A1 (ja) | 2017-10-26 | 2018-10-25 | 硬化性組成物 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11306160B2 (ja) |
| EP (1) | EP3702377A4 (ja) |
| JP (1) | JP7046971B2 (ja) |
| WO (1) | WO2019082964A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020083802A (ja) * | 2018-11-21 | 2020-06-04 | クラレノリタケデンタル株式会社 | 歯科用コンポジットレジン |
| WO2021049269A1 (ja) * | 2019-09-13 | 2021-03-18 | 株式会社ジーシー | ガラス粉末及び化学重合開始剤 |
| WO2022014492A1 (ja) * | 2020-07-15 | 2022-01-20 | 三井化学株式会社 | 重合開始剤、硬化性組成物調製用キット、硬化性組成物、硬化物及び歯科材料 |
| WO2023058773A1 (ja) * | 2021-10-08 | 2023-04-13 | クラレノリタケデンタル株式会社 | 歯科用硬化性組成物及び歯科用キット |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5160690B1 (ja) * | 2012-04-03 | 2013-03-13 | 株式会社J−オイルミルズ | 粒状物およびその製造方法、ならびにこれを用いた食品、飼料および食肉製品 |
| KR101907382B1 (ko) * | 2016-12-28 | 2018-10-12 | 롯데제과 주식회사 | 크리스피한 식감을 가진 얇은 칩 스타일의 크래커 조성물과 이의 제조방법 |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5846883B2 (ja) | 1975-10-04 | 1983-10-19 | ソニー株式会社 | Am受信機 |
| JPH09157124A (ja) * | 1995-12-11 | 1997-06-17 | Kuraray Co Ltd | 操作性の優れた歯科用接着剤システム |
| JP2009144054A (ja) | 2007-12-14 | 2009-07-02 | Gc Corp | 重合性組成物 |
| JP4646264B1 (ja) | 2009-10-16 | 2011-03-09 | 日本歯科薬品株式会社 | 歯科用硬化性組成物 |
| JP2012157566A (ja) | 2011-02-01 | 2012-08-23 | Sammy Corp | 遊技機および遊技盤 |
| JP2014152107A (ja) * | 2013-02-05 | 2014-08-25 | Tokuyama Dental Corp | 歯科用硬化性組成物 |
| JP2015015220A (ja) | 2013-07-08 | 2015-01-22 | トヨタ自動車株式会社 | 燃料電池スタック |
| JP2015015221A (ja) | 2013-07-08 | 2015-01-22 | 株式会社オートネットワーク技術研究所 | ツイストペア電線および該ツイストペア電線の形成方法 |
| JP5683337B2 (ja) | 2011-03-17 | 2015-03-11 | 株式会社トクヤマデンタル | 化学重合型歯科用接着性組成物 |
| JP5773557B2 (ja) | 2005-08-19 | 2015-09-02 | ヘレーウス クルツァー ゲゼルシャフト ミット ベシュレンクテル ハフツングHeraeus Kulzer GmbH | 貯蔵安定性および酸系のための特別な適性 |
| JP2016094482A (ja) | 2011-05-16 | 2016-05-26 | 三井化学株式会社 | 歯科材料、歯科材料組成物、歯科修復材料および硬化物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2233150A1 (en) * | 1997-03-31 | 1998-09-30 | Kuraray Co., Ltd. | Resinous composition for dental use |
| JP4947831B2 (ja) | 2000-09-18 | 2012-06-06 | 電気化学工業株式会社 | 硬化性樹脂組成物、硬化体、接着剤組成物及び接合体 |
| JP4244274B2 (ja) * | 2001-09-27 | 2009-03-25 | 富士フイルム株式会社 | 光重合性組成物及び記録材料 |
| JP4948914B2 (ja) * | 2006-06-20 | 2012-06-06 | 富士フイルム株式会社 | 金属微粒子含有黒色分散物、着色組成物、感光性転写材料、遮光画像付き基板、カラーフィルター、及び液晶表示装置 |
| JP5282406B2 (ja) * | 2008-02-06 | 2013-09-04 | 三菱化学株式会社 | ホログラム記録媒体 |
| US9365658B2 (en) * | 2010-11-15 | 2016-06-14 | Eastman Kodak Company | Method of photocuring acrylate compositions |
| JP5846883B2 (ja) | 2011-02-17 | 2016-01-20 | 株式会社トクヤマデンタル | 化学重合触媒およびその用途 |
| US10231905B2 (en) * | 2013-03-26 | 2019-03-19 | Kuraray Noritake Dental Inc. | Dental curable composition |
| GB2519055A (en) | 2013-08-01 | 2015-04-15 | Calla Lily Personal Care Ltd | Drug delivery device |
| GB201313850D0 (en) | 2013-08-02 | 2013-09-18 | Johnson Matthey Plc | Getter composition |
| CN107073914A (zh) * | 2014-09-30 | 2017-08-18 | 东丽株式会社 | 显示器用支承基板、使用其的滤色片及其制造方法、有机el元件及其制造方法以及柔性有机el显示器 |
-
2018
- 2018-10-25 JP JP2019551235A patent/JP7046971B2/ja active Active
- 2018-10-25 US US16/753,086 patent/US11306160B2/en active Active
- 2018-10-25 EP EP18870893.7A patent/EP3702377A4/en active Pending
- 2018-10-25 WO PCT/JP2018/039650 patent/WO2019082964A1/ja unknown
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5846883B2 (ja) | 1975-10-04 | 1983-10-19 | ソニー株式会社 | Am受信機 |
| JPH09157124A (ja) * | 1995-12-11 | 1997-06-17 | Kuraray Co Ltd | 操作性の優れた歯科用接着剤システム |
| JP3449843B2 (ja) | 1995-12-11 | 2003-09-22 | 株式会社クラレ | 操作性の優れた歯科用接着剤システム |
| JP5773557B2 (ja) | 2005-08-19 | 2015-09-02 | ヘレーウス クルツァー ゲゼルシャフト ミット ベシュレンクテル ハフツングHeraeus Kulzer GmbH | 貯蔵安定性および酸系のための特別な適性 |
| JP2009144054A (ja) | 2007-12-14 | 2009-07-02 | Gc Corp | 重合性組成物 |
| JP4646264B1 (ja) | 2009-10-16 | 2011-03-09 | 日本歯科薬品株式会社 | 歯科用硬化性組成物 |
| JP2012157566A (ja) | 2011-02-01 | 2012-08-23 | Sammy Corp | 遊技機および遊技盤 |
| JP5683337B2 (ja) | 2011-03-17 | 2015-03-11 | 株式会社トクヤマデンタル | 化学重合型歯科用接着性組成物 |
| JP2016094482A (ja) | 2011-05-16 | 2016-05-26 | 三井化学株式会社 | 歯科材料、歯科材料組成物、歯科修復材料および硬化物 |
| JP2014152107A (ja) * | 2013-02-05 | 2014-08-25 | Tokuyama Dental Corp | 歯科用硬化性組成物 |
| JP2015015220A (ja) | 2013-07-08 | 2015-01-22 | トヨタ自動車株式会社 | 燃料電池スタック |
| JP2015015221A (ja) | 2013-07-08 | 2015-01-22 | 株式会社オートネットワーク技術研究所 | ツイストペア電線および該ツイストペア電線の形成方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3702377A4 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020083802A (ja) * | 2018-11-21 | 2020-06-04 | クラレノリタケデンタル株式会社 | 歯科用コンポジットレジン |
| JP7237543B2 (ja) | 2018-11-21 | 2023-03-13 | クラレノリタケデンタル株式会社 | 歯科用コンポジットレジン |
| WO2021049269A1 (ja) * | 2019-09-13 | 2021-03-18 | 株式会社ジーシー | ガラス粉末及び化学重合開始剤 |
| WO2022014492A1 (ja) * | 2020-07-15 | 2022-01-20 | 三井化学株式会社 | 重合開始剤、硬化性組成物調製用キット、硬化性組成物、硬化物及び歯科材料 |
| WO2023058773A1 (ja) * | 2021-10-08 | 2023-04-13 | クラレノリタケデンタル株式会社 | 歯科用硬化性組成物及び歯科用キット |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3702377A4 (en) | 2021-08-25 |
| JP7046971B2 (ja) | 2022-04-04 |
| EP3702377A1 (en) | 2020-09-02 |
| US11306160B2 (en) | 2022-04-19 |
| US20200291157A1 (en) | 2020-09-17 |
| JPWO2019082964A1 (ja) | 2020-09-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7046971B2 (ja) | 硬化性組成物 | |
| JP5224255B2 (ja) | ラジカル重合触媒 | |
| JP5622867B2 (ja) | 歯科用硬化性組成物 | |
| EP1454921B1 (en) | Radical polymerization catalysts and adhesive kit for dental use | |
| JP5577037B2 (ja) | 分包型のレドックス硬化型組成物 | |
| AU2016373755B2 (en) | Dental adhesive material kit | |
| JPWO2016159219A1 (ja) | 歯科材料用重合性モノマー、組成物、接着性歯科材料、及びキット | |
| JP6346086B2 (ja) | 2ペースト型歯科用硬化性組成物 | |
| JP5101072B2 (ja) | 歯科用組成物 | |
| JP5622558B2 (ja) | 分包型の歯科用硬化性組成物 | |
| JP6526042B2 (ja) | チオ尿素誘導体に基づく光重合性およびデュアルキュア型歯科用材料 | |
| JP5191486B2 (ja) | 反応硬化性接着性組成物および歯科用接着材キット | |
| JP5325633B2 (ja) | 2液型の歯科用接着剤 | |
| JP6298758B2 (ja) | 歯科用硬化性組成物 | |
| US11744782B2 (en) | Separately packed curable composition | |
| JPH069327A (ja) | 歯質の接着性組成物および接着方法 | |
| JP5415167B2 (ja) | 歯科用組成物 | |
| JP5350109B2 (ja) | 歯科用組成物 | |
| JP6548661B2 (ja) | 歯科用材料を調製するためのモノマー混合物 | |
| JP7044885B2 (ja) | 重合開始剤、硬化性組成物、歯科材料および硬化性組成物の調製用キット | |
| JP2023098835A (ja) | 酸処理充填材をベースにした良好な透明度を持つ自己接着型歯科用コンポジットセメント |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 18870893 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2019551235 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2018870893 Country of ref document: EP Effective date: 20200526 |