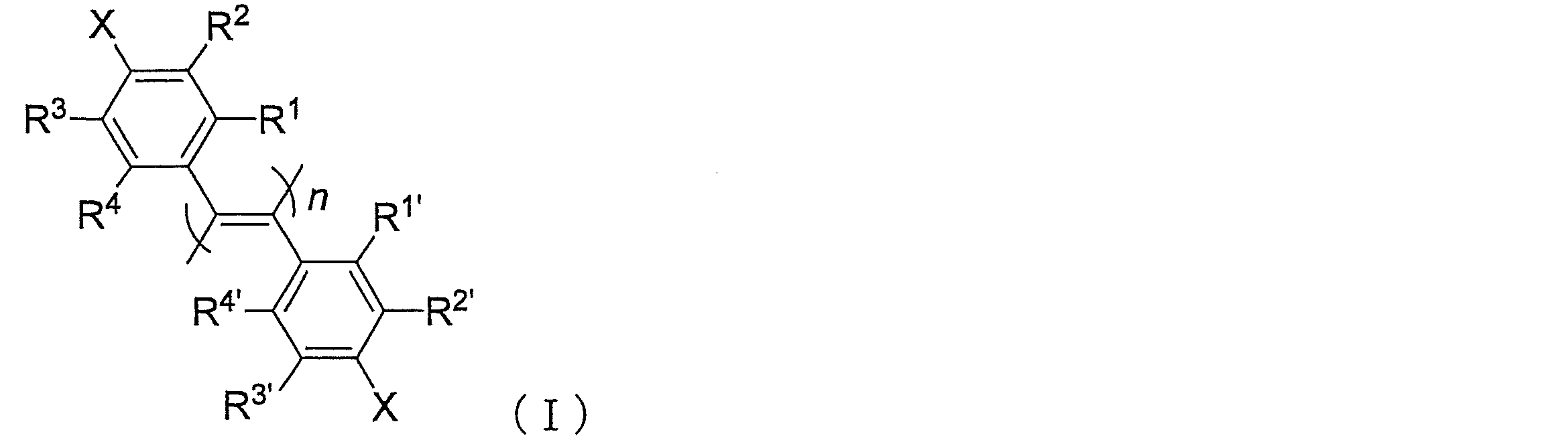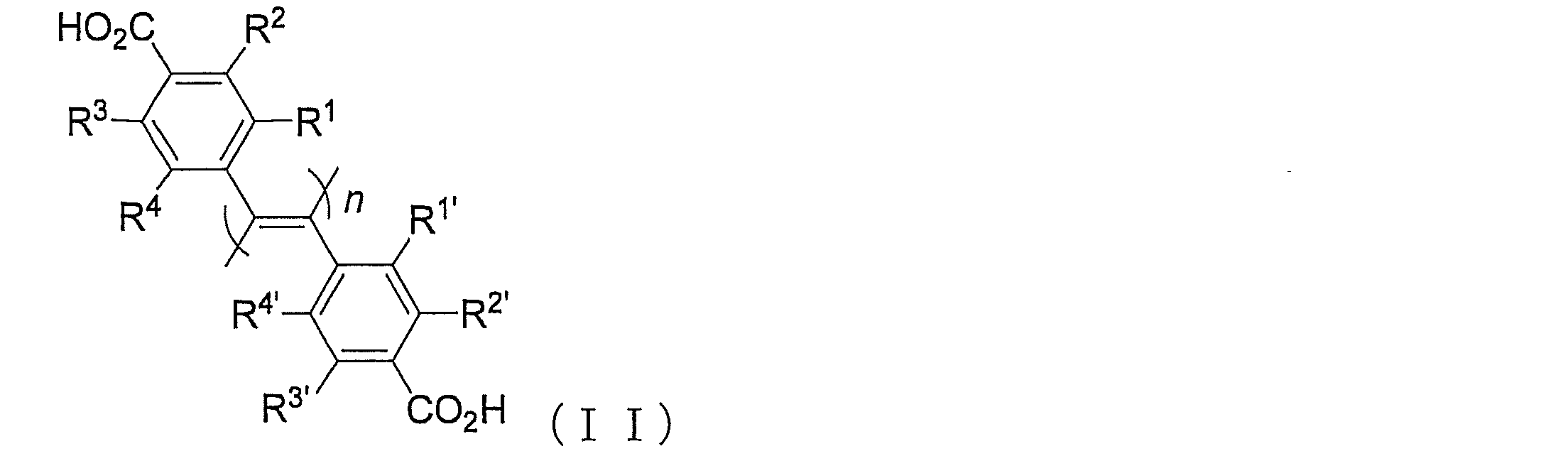WO2014126028A1 - 光学活性ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 - Google Patents
光学活性ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 Download PDFInfo
- Publication number
- WO2014126028A1 WO2014126028A1 PCT/JP2014/053001 JP2014053001W WO2014126028A1 WO 2014126028 A1 WO2014126028 A1 WO 2014126028A1 JP 2014053001 W JP2014053001 W JP 2014053001W WO 2014126028 A1 WO2014126028 A1 WO 2014126028A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- compound
- amino
- ethylamine
- optionally substituted
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F138/00—Homopolymers of compounds having one or more carbon-to-carbon triple bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/281—Sorbents specially adapted for preparative, analytical or investigative chromatography
- B01J20/29—Chiral phases
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3204—Inorganic carriers, supports or substrates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3206—Organic carriers, supports or substrates
- B01J20/3208—Polymeric carriers, supports or substrates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3231—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the coating or impregnating layer
- B01J20/3242—Layers with a functional group, e.g. an affinity material, a ligand, a reactant or a complexing group
- B01J20/3268—Macromolecular compounds
- B01J20/327—Polymers obtained by reactions involving only carbon to carbon unsaturated bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3231—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the coating or impregnating layer
- B01J20/3242—Layers with a functional group, e.g. an affinity material, a ligand, a reactant or a complexing group
- B01J20/3268—Macromolecular compounds
- B01J20/328—Polymers on the carrier being further modified
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F238/00—Copolymers of compounds having one or more carbon-to-carbon triple bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F38/00—Homopolymers and copolymers of compounds having one or more carbon-to-carbon triple bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
- C08F8/14—Esterification
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
- G01N2030/8809—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample
- G01N2030/8877—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample optical isomers
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Analytical Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Polymers & Plastics (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
Description
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよいアルコキシ基、置換されていてもよいアルキルチオ基、トリ置換シリル基、トリ置換シロキシ基又は置換されていてもよいアシルオキシ基を示し;
Xは、光学活性キラル化合物との縮合によりアミド化又はエステル化されたカルボキシ基を示し;並びに
nは、10以上の整数を示す。]
で表される光学活性なポリ(ジフェニルアセチレン)化合物(以下、「化合物(I)」と称することもある。)又はその塩、或いはその溶媒和物、並びに化合物(I)の主鎖に一方向巻きのらせん構造を有するポリ(ジフェニルアセチレン)化合物(以下、単に「化合物(I-h)」と称することもある。)又はその塩、或いはその溶媒和物が、広範なキラル化合物の光学異性体混合物の分離剤として有用であることを初めて見出し、本発明を完成するに至った。
すなわち、本発明は以下の通りである。
[1]式(I):
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよいアルコキシ基、置換されていてもよいアルキルチオ基、トリ置換シリル基、トリ置換シロキシ基又は置換されていてもよいアシルオキシ基を示し;
Xは、光学活性キラル化合物との縮合によりアミド化又はエステル化されたカルボキシ基を示し;並びに
nは、10以上の整数を示す。]
で表されるポリ(ジフェニルアセチレン)化合物又はその塩、或いはその溶媒和物。
[2]一方向巻きのらせん構造を有することを特徴とする、上記[1]記載の化合物又はその塩、或いはその溶媒和物。
[3]R1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基である、上記[1]又は[2]に記載の化合物又はその塩、或いはその溶媒和物。
[4]Xが、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-メチル-2-(1-ピペリジノメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン、1-フェニルエチルアルコール、1-フェニル-2-プロパノール、1,2,3,4-テトラヒドロ-1-ナフトール、1-アセチル-3-ピロリジノール、1-ベンジル-3-ピロリジノール、2-ブタノール、α-ヒドロキシ-γ-ブチロラクトン、3-ヒドロキシテトラヒドロフラン、1-メチル-3-ピロリジノール、2-オクタノール、2-ペンタノール、1-(2-ナフチル)エタノール、メントール、ボルネオール、キニジン、キニン、キンコリン、キンコリジン、シンコニジン、シンコニン及びカルボキシ基を保護したアミノ酸からなる群より選択されるキラル化合物の光学活性体との縮合によりアミド化又はエステル化されたカルボキシ基である、上記[1]~[3]のいずれかに記載の化合物又はその塩、或いはその溶媒和物。
[5]R1、R1’、R2、R2’、R3、R3’、R4及びR4’が、独立してそれぞれ水素原子、ハロゲン原子、ハロゲン原子により置換されていてもよいC1-6アルキル基、ハロゲン原子により置換されていてもよいC1-6アルコキシ基、トリC1-6アルキルシリル基又はトリC1-6アルキルシロキシ基であって、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xが、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン及びカルボキシ基を保護したアミノ酸からなる群より選択される化合物の光学活性体との縮合によりアミド化されたカルボキシ基であり;並びに
nが、10以上10000以下の整数である、上記[1]又は[2]に記載の化合物又はその塩、或いはその溶媒和物。
[6]R1、R1’、R2、R2’、R3、R3’、R4及びR4’が、独立してそれぞれ水素原子又はハロゲン原子であって、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xが、(S)-(-)-1-フェニルエチルアミン又は(R)-(+)-1-フェニルエチルアミンとの縮合によりアミド化されたカルボキシ基であり;並びに
nが、100以上10000以下の整数である、上記[1]又は[2]に記載の化合物又はその塩、或いはその溶媒和物。
[7]上記[1]~[6]のいずれかに記載のポリ(ジフェニルアセチレン)化合物からなる光学異性体分離剤。
[8]上記[7]記載の光学異性体分離剤を担体に担持してなる充填剤。
[9]担体がシリカゲルである、上記[8]記載の充填剤。
[10]上記[8]又は[9]に記載の充填剤を充填して調製されるキラルカラム。
[11]光学異性体の混合物の純度測定用又は分離用として使用する、上記[10]記載のキラルカラム。
[12]上記[2]記載の化合物又はその塩、或いはその溶媒和物の製造方法であって、式(II):
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよいアルコキシ基、置換されていてもよいアルキルチオ基、トリ置換シリル基、トリ置換シロキシ基又は置換されていてもよいアシルオキシ基を示し;並びに
nは、10以上の整数を示す。]
で表されるポリ(ジフェニルアセチレン)化合物のカルボキシ基を光学活性キラル化合物と縮合させて、アミド化又はエステル化する工程、及び
前記アミド化又はエステル化された化合物を加熱処理する工程を含むことを特徴とする、方法。
[13]加熱処理が、約90℃で行われることを特徴とする、上記[12]記載の方法。
[14]光学活性キラル化合物が、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-メチル-2-(1-ピペリジノメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン、1-フェニルエチルアルコール、1-フェニル-2-プロパノール、1,2,3,4-テトラヒドロ-1-ナフトール、1-アセチル-3-ピロリジノール、1-ベンジル-3-ピロリジノール、2-ブタノール、α-ヒドロキシ-γ-ブチロラクトン、3-ヒドロキシテトラヒドロフラン、1-メチル-3-ピロリジノール、2-オクタノール、2-ペンタノール、1-(2-ナフチル)エタノール、メントール、ボルネオール、キニジン、キニン、キンコリン、キンコリジン、シンコニジン、シンコニン及びカルボキシ基を保護したアミノ酸からなる群より選択される化合物の光学活性体である、上記[12]又は[13]に記載の方法。
[15]アミド化又はエステル化する工程が、アミド化する工程である、上記[12]~[14]のいずれかに記載の方法。
[16]光学活性キラル化合物が、(S)-(-)-1-フェニルエチルアミン又は(R)-(+)-1-フェニルエチルアミンである、上記[15]記載の方法。
(定義)
本発明の化合物(I)は、下記式(I):
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよいアルコキシ基、置換されていてもよいアルキルチオ基、トリ置換シリル基、トリ置換シロキシ基又は置換されていてもよいアシルオキシ基を示し;
Xは、光学活性キラル化合物との縮合によりアミド化又はエステル化されたカルボキシ基を示し;並びに
nは、10以上の整数を示す。]
で表されるポリ(ジフェニルアセチレン)化合物であり、また本発明の化合物(I-h)は、化合物(I)のうち、そのポリマー主鎖に一方向巻きのらせん構造を有する化合物である。
有機酸との塩として、例えば、シュウ酸、マレイン酸、クエン酸、フマル酸、乳酸、リンゴ酸、コハク酸、酒石酸、酢酸、トリフルオロ酢酸、グルコン酸、アスコルビン酸、メタンスルホン酸、ベンゼンスルホン酸、p-トルエンスルホン酸等との塩が挙げられる。
無機塩基との塩として、例えば、ナトリウム塩、カリウム塩、カルシウム塩、マグネシウム塩、アンモニウム塩等が挙げられる。
有機塩基との塩として、例えば、メチルアミン、ジエチルアミン、トリメチルアミン、トリエチルアミン、エタノールアミン、ジエタノールアミン、トリエタノールアミン、エチレンジアミン、トリス(ヒドロキシメチル)メチルアミン、ジシクロヘキシルアミン、N,N’-ジベンジルエチレンジアミン、グアニジン、ピリジン、ピコリン、コリン、シンコニン、メグルミン等との塩が挙げられる。
アミノ酸との塩として、例えば、リジン、アルギニン、アスパラギン酸、グルタミン酸等との塩が挙げられる。
本発明の化合物(I)の塩(若しくは化合物(I-h)の塩)は、好ましくは、無機塩基または有機塩基との塩である。
[化合物(IA)]
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいアルコキシ基、トリアルキルシリル基又はトリアルキルシロキシ基であり、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xは、光学活性キラルアミン(例、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン、カルボキシ基を保護したアミノ酸等の光学活性体)との縮合によりアミド化されたカルボキシ基であり;並びに
nが、10以上の整数である、化合物(I)。
[化合物(IB)]
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、ハロゲン原子により置換されていてもよいC1-6アルキル基、ハロゲン原子により置換されていてもよいC1-6アルコキシ基、トリC1-6アルキルシリル基又はトリC1-6アルキルシロキシ基であり、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xは、光学活性キラルアミン(前記例示した化合物)との縮合によりアミド化されたカルボキシ基であり;並びに
nが、10以上10000以下の整数である、化合物(I)。
[化合物(IC)]
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子又はハロゲン原子であり、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xは、(R)-(+)-1-フェニルエチルアミン又は(S)-(-)-1-フェニルエチルアミンとの縮合によりアミド化されたカルボキシ基であり;並びに
nが、100以上10000以下の整数である、化合物(I)。
本発明の化合物(I)及び化合物(I-h)の製造方法としては、特に限定されないが、例えば、以下のような反応を経て合成することができる。
当該工程は、化合物1をエステル化して、化合物2を製造する工程である。
当該反応は、自体公知の方法(例えば、酸ハライドへと変換後、アルコール(R7OH)と反応させる方法、縮合剤及び塩基存在下でアルコール(R7OH)と反応させる方法等)により行われる。
溶媒としては、例えば、トルエン、キシレン等の芳香族炭化水素類;ジエチルエーテル、テトラヒドロフラン、ジオキサン等のエーテル類;クロロホルム、ジクロロメタン等のハロゲン化炭化水素類等あるいはそれらの混合物が挙げられる。
反応温度は、通常-10℃~30℃、好ましくは0℃~20℃であり、反応時間は、通常1~30時間である。
縮合剤の使用量は、化合物1(1当量)に対して、1~10当量使用することができ、好ましくは1~5モルである。
溶媒としては、例えば、トルエン、キシレン等の芳香族炭化水素類;ジエチルエーテル、テトラヒドロフラン、ジオキサン等のエーテル類;クロロホルム、ジクロロメタン等のハロゲン化炭化水素類等あるいはそれらの混合物が挙げられ、中でも、トルエン、テトラヒドロフラン等が好ましい。
反応温度は、通常-10℃~30℃、好ましくは0℃~20℃であり、反応時間は、通常1~30時間である。
当該工程は、化合物2の脱離基Y(好ましくは、ヨウ素)を薗頭カップリング条件下でトリメチルシリルエチニル基に置換して、化合物3へと変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中、塩基存在下、金属触媒を用いて行われる。
該金属触媒の使用量は、化合物2(1当量)に対して、通常0.001~1当量である。
該塩基は、溶媒として使用することもでき、該塩基の使用量は、化合物2(1当量)に対して、通常10~1000当量である。
反応時間は、通常0.5~24時間である。
当該工程は、化合物3のトリメチルシリル基を除去することにより、化合物4へと変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中、塩基又はフッ化テトラ-n-ブチルアンモニウム等のフッ化物イオン源を用いて行われる。
該塩基の使用量は、化合物3(1当量)に対して、通常1~10当量である。
反応時間は、通常0.5~24時間である。
当該工程は、化合物2’の脱離基Y’(好ましくは、ヨウ素)を薗頭カップリング条件下で化合物4とカップリング反応を行い、化合物5へと変換する工程である。
当該工程は、化合物5を重合させることにより、化合物6へと変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中、窒素雰囲気下、金属触媒を用いて行われる。
該金属触媒の使用量は、化合物5(1当量)に対して、通常0.0001~0.2当量、好ましくは、0.001~0.1当量である。
反応時間は、通常0.5~30時間である。
当該工程は、化合物6のエステルを加水分解して、化合物(II)に変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中、塩基を用いて行われる。
該塩基の使用量は、化合物6(1当量)に対して、通常1~100当量である。
反応時間は、通常0.5~30時間である。
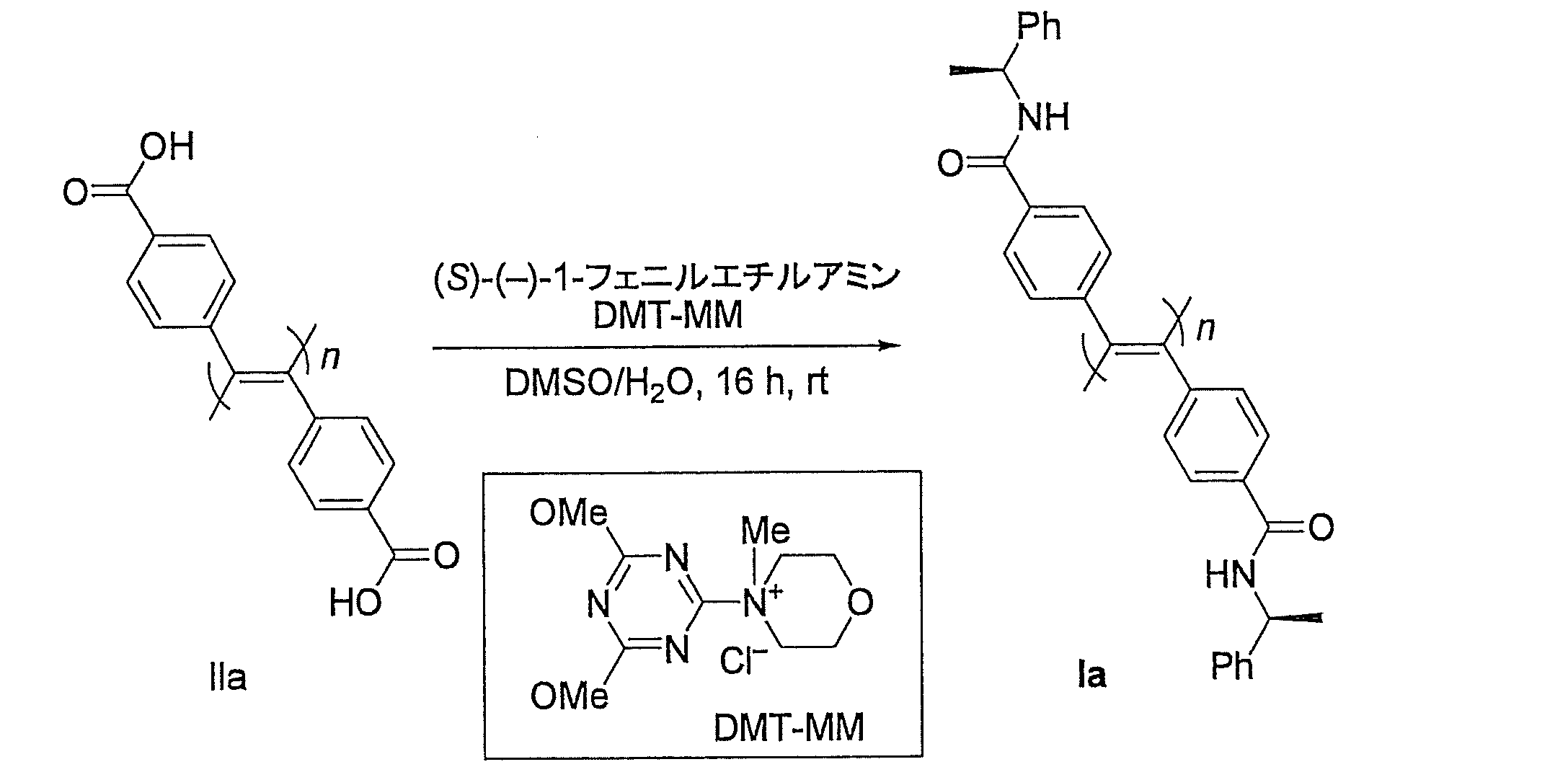
当該工程は、化合物(II)のカルボキシ基を光学活性キラル化合物との縮合反応によりアミド化又はエステル化して化合物(I)に変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中、必要に応じて縮合添加剤存在下、縮合剤を用いて行われる。
縮合添加剤の使用量は、化合物(II)1当量に対して、好ましくは0.05~1.5当量である。
縮合剤の使用量は、化合物(II)1当量に対して、1~10当量使用することができ、好ましくは1~5当量である。
溶媒としては、例えば、水;ジメチルスルホキシド(DMSO);トルエン、キシレン等の芳香族炭化水素類;ジエチルエーテル、テトラヒドロフラン、ジオキサン等のエーテル類;クロロホルム、ジクロロメタン等のハロゲン化炭化水素類等あるいはそれらの混合物が挙げられ、中でも、水とDMSOの混合溶媒等が好ましい。
反応温度は、通常0~40℃、好ましくは0℃~室温であり、反応時間は、通常1~30時間である。
当該工程は、化合物(I)の主鎖に一方向巻きのらせん構造を形成させて、化合物(I-h)に変換する工程である。
当該反応は、反応に影響を及ぼさない溶媒中で化合物(I)を加熱処理して行われる。
反応温度は、通常10℃~200℃、好ましくは80℃~100℃であり、反応時間は、通常1~30時間である。
本発明の化合物(I)又は化合物(I-h)は、それ自体を光学異性体分離剤として使用することもできるが、通常、多孔質有機担体又は多孔質無機担体等の担体に担持させることが好ましい。
1H及び13C-NMRスペクトルは、JEOL ECA500を用い、重クロロホルム、重ジメチルスルホキシド及び重水を溶媒として測定した。1H-NMRについてのデータは、化学シフト(δppm)、多重度(s=シングレット、d=ダブレット、t=トリプレット、q=カルテット、quint=クインテット、m=マルチプレット、dd=ダブルダブレット、dt=ダブルトリプレット、brs=ブロードシングレット)、カップリング定数(Hz)、積分及び割当てとして報告する。
フラッシュクロマトグラフィーは、関東化学株式会社(日本、東京)のシリカゲル60Nを用いて行った。
平均分子量はゲル浸透クロマトグラフィー(日本分光製高速液体クロマトグラフィーポンプ PU-2080、日本分光製紫外可視検出器 UV-970、日本分光製カラムオーブン CO-1560、Shodex製カラム KF-805L)によりポリスチレン換算で算出した。
調製した本発明の化合物(I)の分離能の測定には日本分光製高速液体クロマトグラフィーポンプPU-2080、日本分光製紫外可視検出器 MD-910、日本分光製旋光検出器 OR-990を用いた。円二色性(CD)測定は日本分光製円二色性分散計 J-725、紫外可視吸収測定は日本分光製紫外可視分光光度計 V-570、赤外吸収測定は、日本分光製赤外分光光度計 FT/IR-460を用いて行った。
以下の実施例中の「室温」は通常約10℃ないし約25℃を示す。混合溶媒において示した比は、特に断らない限り容量比を示す。%は、特に断らない限り重量%を示す。
化合物(Ia)の合成
mp:61.3-62.4℃;
IR(KBr,cm-1):1943(C≡C),1707(C=O);
1H NMR(500MHz,CDCl3,rt):δ8.04(d,J=8.6Hz,4H,Ar-H),7.60(d,J=8.0Hz,4H,Ar-H),4.33(t,J=6.6Hz,4H,2OCH2CH2),1.76(quint,J=6.6Hz,4H,2OCH2CH2),1.25-1.47(m,16H,8CH2),0.90(t,J=6.9Hz,6H,2CH3);
13C NMR(125MHz,CDCl3,rt):δ166.19,131.76,130.46,129.68,127.38,91.49,65.56,31.88,29.11,28.85,26.15,22.75,14.23;
元素分析:Calcd for C30H38O4:C,77.89;H,8.28.Found:C,77.60;H,8.37.
IR(KBr,cm-1):1721(C=O);
1H NMR(500MHz,CDCl3,50℃):δ7.16-7.28(br,4H,Ar-H),6.41-6.71(br,2H,Ar-H),5.92-6.15(br,2H,Ar-H),4.03-4.48(br,4H,2OCH2CH2),1.60-1.93(br,4H,2OCH2CH2),1.25-1.47(br,16H,8CH2),0.79-1.04(br,6H,2CH3);
元素分析:Calcd for C30H38O4:C,77.89;H,8.28.Found:C,77.40;H,8.42.
IR(KBr,cm-1):1701(C=O);
1H NMR(500MHz,d6-DMSO/D2O(1:1,v/v),80℃):δ7.19-6.88(br,4H,Ar-H),6.53-6.31(br,2H,Ar-H),6.12-5.82(br,2H,Ar-H);
元素分析:Calcd for (C16H10O4・2.1H2O)n:C,63.20;H,4.71.Found:C,63.04;H,4.55.
カラムの調製と不斉識別能評価
化合物(Ia)(150mg)をアセトン/テトラヒドロフラン(4:1,v/v)(5mL)に溶解し、メンブランフィルター(0.2μm)によりろ過を行った後、HPLC用のシリカゲル(ダイソー製:粒径7μm)に担持した。得られたポリマー担持ゲルをスラリー法(溶媒:ヘキサン)により長さ25cm、内径0.20cmのステンレスカラムに充填した。
化合物(Ia-h)(150mg)をアセトン/テトラヒドロフラン(2:1,v/v)(5mL)に溶解し、メンブランフィルター(0.2μm)によりろ過を行った後、HPLC用のシリカゲル(ダイソー製:粒径7μm)に担持した。得られたポリマー担持ゲルをスラリー法(溶媒:ヘキサン)により長さ25cm、内径0.20cmのステンレスカラムに充填した。
上記(1)、(2)の操作で調製されたキラルカラム(A)、(B)を用いて、1,1’-ビ-2-ナフトールのラセミ体の光学分割をHPLCにより行った(室温:約20℃)。溶離液にはヘキサン/2-プロパノール=90/10(v/v)を用いて、流速は0.1mL/分とした。また、溶離液がカラムを素通りする時間t0は1,3,5-トリ-tert-ブチルベンゼンの溶出時間から求めた。その結果、キラルカラム(A)を用いた場合には、k1=1.52、α=1.34と見積もられ、キラルカラム(B)を用いた場合には、k1=0.80、α=1.53と見積もられた(表1、図2(キラルカラム(B)による分離結果))。
上記(1)、(2)の操作で調製されたキラルカラム(A)、(B)を用いて、様々な化合物のラセミ体の光学分割をHPLC(流速は、0.1mL/分(ヘキサン/2-プロパノール=90/10又は99/1)により行った。その分離条件と結果を表1に示した。いずれのカラムを用いても光学分割は可能であるが、キラルカラム(B)を用いた方が、分離係数(α)の値が増加していることから、加熱処理により主鎖にらせんのキラリティーを誘起することにより光学分割能がより顕著に向上することが確認できた。
Claims (16)
- 一方向巻きのらせん構造を有することを特徴とする、請求項1記載の化合物又はその塩、或いはその溶媒和物。
- R1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基である、請求項1又は2に記載の化合物又はその塩、或いはその溶媒和物。
- Xが、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-メチル-2-(1-ピペリジノメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン、1-フェニルエチルアルコール、1-フェニル-2-プロパノール、1,2,3,4-テトラヒドロ-1-ナフトール、1-アセチル-3-ピロリジノール、1-ベンジル-3-ピロリジノール、2-ブタノール、α-ヒドロキシ-γ-ブチロラクトン、3-ヒドロキシテトラヒドロフラン、1-メチル-3-ピロリジノール、2-オクタノール、2-ペンタノール、1-(2-ナフチル)エタノール、メントール、ボルネオール、キニジン、キニン、キンコリン、キンコリジン、シンコニジン、シンコニン及びカルボキシ基を保護したアミノ酸からなる群より選択されるキラル化合物の光学活性体との縮合によりアミド化又はエステル化されたカルボキシ基である、請求項1~3のいずれか一項に記載の化合物又はその塩、或いはその溶媒和物。
- R1、R1’、R2、R2’、R3、R3’、R4及びR4’が、独立してそれぞれ水素原子、ハロゲン原子、ハロゲン原子により置換されていてもよいC1-6アルキル基、ハロゲン原子により置換されていてもよいC1-6アルコキシ基、トリC1-6アルキルシリル基又はトリC1-6アルキルシロキシ基であって、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xが、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン及びカルボキシ基を保護したアミノ酸からなる群より選択される化合物の光学活性体との縮合によりアミド化されたカルボキシ基であり;並びに
nが、10以上10000以下の整数である、請求項1又は2に記載の化合物又はその塩、或いはその溶媒和物。 - R1、R1’、R2、R2’、R3、R3’、R4及びR4’が、独立してそれぞれ水素原子又はハロゲン原子であって、且つR1とR1’、R2とR2’、R3とR3’及びR4とR4’が、それぞれ同一の基であり;
Xが、(S)-(-)-1-フェニルエチルアミン又は(R)-(+)-1-フェニルエチルアミンとの縮合によりアミド化されたカルボキシ基であり;並びに
nが、100以上10000以下の整数である、請求項1又は2に記載の化合物又はその塩、或いはその溶媒和物。 - 請求項1~6のいずれか一項に記載のポリ(ジフェニルアセチレン)化合物からなる光学異性体分離剤。
- 請求項7記載の光学異性体分離剤を担体に担持してなる充填剤。
- 担体がシリカゲルである、請求項8記載の充填剤。
- 請求項8又は9に記載の充填剤を充填して調製されるキラルカラム。
- 光学異性体の混合物の純度測定用又は分離用として使用する、請求項10記載のキラルカラム。
- 請求項2記載の化合物又はその塩、或いはその溶媒和物の製造方法であって、式(II):
R1、R1’、R2、R2’、R3、R3’、R4及びR4’は、独立してそれぞれ水素原子、ハロゲン原子、置換されていてもよいアルキル基、置換されていてもよいシクロアルキル基、置換されていてもよいアルコキシ基、置換されていてもよいアルキルチオ基、トリ置換シリル基、トリ置換シロキシ基又は置換されていてもよいアシルオキシ基を示し;並びに
nは、10以上の整数を示す。]
で表されるポリ(ジフェニルアセチレン)化合物のカルボキシ基を光学活性キラル化合物と縮合させて、アミド化又はエステル化する工程、及び
前記アミド化又はエステル化された化合物を加熱処理する工程を含むことを特徴とする、方法。 - 加熱処理が、約90℃で行われることを特徴とする、請求項12記載の方法。
- 光学活性キラル化合物が、1-フェニルエチルアミン、1-シクロヘキシルエチルアミン、1-(1-ナフチル)エチルアミン、1-(2-ナフチル)エチルアミン、sec-ブチルアミン、1-フェニル-2-(p-トリル)エチルアミン、1-(p-トリル)エチルアミン、1-(4-メトキシフェニル)エチルアミン、β-メチルフェネチルアミン、2-アミノ-1-ブタノール、2-アミノ-1,2-ジフェニルエタノール、1-アミノ-2-インダノール、2-アミノ-1-フェニル-1,3-プロパンジオール、2-アミノ-1-プロパノール、ロイシノール、フェニルアラニノール、2-フェニルグリシノール、バリノール、ノルエフェドリン、メチオニノール、1-ベンジル-3-アミノピロリジン、2-(メトキシメチル)ピロリジン、1-メチル-2-(1-ピペリジノメチル)ピロリジン、1-(2-ピロリジノメチル)ピロリジン、1-フェニルエチルアルコール、1-フェニル-2-プロパノール、1,2,3,4-テトラヒドロ-1-ナフトール、1-アセチル-3-ピロリジノール、1-ベンジル-3-ピロリジノール、2-ブタノール、α-ヒドロキシ-γ-ブチロラクトン、3-ヒドロキシテトラヒドロフラン、1-メチル-3-ピロリジノール、2-オクタノール、2-ペンタノール、1-(2-ナフチル)エタノール、メントール、ボルネオール、キニジン、キニン、キンコリン、キンコリジン、シンコニジン、シンコニン及びカルボキシ基を保護したアミノ酸からなる群より選択される化合物の光学活性体である、請求項12又は13に記載の方法。
- アミド化又はエステル化する工程が、アミド化する工程である、請求項12~14のいずれか一項に記載の方法。
- 光学活性キラル化合物が、(S)-(-)-1-フェニルエチルアミン又は(R)-(+)-1-フェニルエチルアミンである、請求項15記載の方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015500220A JP6083832B2 (ja) | 2013-02-12 | 2014-02-10 | 光学活性ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 |
| US14/766,853 US9562121B2 (en) | 2013-02-12 | 2014-02-10 | Optically active poly(diphenylacetylene) compound, preparation method therefor, and use thereof as optical isomer separating agent |
| EP14751643.9A EP2957575B1 (en) | 2013-02-12 | 2014-02-10 | Optically active poly(diphenylacetylene) compound, preparation method therefor, and use thereof as optical isomer separating agent |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013024421 | 2013-02-12 | ||
| JP2013-024421 | 2013-02-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014126028A1 true WO2014126028A1 (ja) | 2014-08-21 |
Family
ID=51354031
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/053001 WO2014126028A1 (ja) | 2013-02-12 | 2014-02-10 | 光学活性ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9562121B2 (ja) |
| EP (1) | EP2957575B1 (ja) |
| JP (1) | JP6083832B2 (ja) |
| WO (1) | WO2014126028A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019045267A (ja) * | 2017-08-31 | 2019-03-22 | 国立大学法人金沢大学 | 比色検出型キラルセンサーを用いる光学活性キラルアミン化合物のキラリティー及び光学純度の決定方法 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107670643B (zh) * | 2017-09-18 | 2020-04-28 | 安徽良臣硅源材料有限公司 | 一种d-(-)-3-磷酸甘油酸酯键合硅胶油脂吸附剂 |
| CN109470803B (zh) * | 2019-01-10 | 2021-08-10 | 通标标准技术服务(上海)有限公司 | 一种同时测定染料或颜料中多种色酚含量的方法 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS57150432A (en) | 1981-03-11 | 1982-09-17 | Daicel Chem Ind Ltd | Adsorbent deposited with optically active high polymer used in separation |
| JPS6040952A (ja) | 1983-08-17 | 1985-03-04 | Daicel Chem Ind Ltd | 光学分割用充填剤 |
| JPS6082858A (ja) | 1983-10-13 | 1985-05-11 | Daicel Chem Ind Ltd | 光学分割用吸着剤 |
| JPS60108751A (ja) | 1983-11-18 | 1985-06-14 | Daicel Chem Ind Ltd | 分離剤 |
| JPS62210053A (ja) | 1986-03-07 | 1987-09-16 | Agency Of Ind Science & Technol | 光学異性体分離用充填剤 |
| JPS63307829A (ja) | 1986-04-02 | 1988-12-15 | Eisai Co Ltd | 光学異性体用分離剤 |
| JPH05271338A (ja) * | 1992-03-27 | 1993-10-19 | Nippon Zeon Co Ltd | 二置換ジフェニルアセチレン系重合体 |
| JPH08133991A (ja) * | 1994-11-04 | 1996-05-28 | Daicel Chem Ind Ltd | 光学活性ポリアセチレン誘導体を用いた光学分割剤 |
| JP2005239863A (ja) * | 2004-02-26 | 2005-09-08 | Japan Science & Technology Agency | キラル配向構造を有する有機/無機複合体及びその製造法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4598228B2 (ja) | 2000-04-13 | 2010-12-15 | 独立行政法人科学技術振興機構 | ポリアセチレン誘導体の新規製造法 |
| JP4898498B2 (ja) * | 2007-03-09 | 2012-03-14 | キヤノン株式会社 | 置換ポリアセチレン、複合体およびデバイス構造 |
-
2014
- 2014-02-10 WO PCT/JP2014/053001 patent/WO2014126028A1/ja active Application Filing
- 2014-02-10 EP EP14751643.9A patent/EP2957575B1/en not_active Not-in-force
- 2014-02-10 JP JP2015500220A patent/JP6083832B2/ja not_active Expired - Fee Related
- 2014-02-10 US US14/766,853 patent/US9562121B2/en not_active Expired - Fee Related
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS57150432A (en) | 1981-03-11 | 1982-09-17 | Daicel Chem Ind Ltd | Adsorbent deposited with optically active high polymer used in separation |
| JPS6040952A (ja) | 1983-08-17 | 1985-03-04 | Daicel Chem Ind Ltd | 光学分割用充填剤 |
| JPS6082858A (ja) | 1983-10-13 | 1985-05-11 | Daicel Chem Ind Ltd | 光学分割用吸着剤 |
| JPS60108751A (ja) | 1983-11-18 | 1985-06-14 | Daicel Chem Ind Ltd | 分離剤 |
| JPS62210053A (ja) | 1986-03-07 | 1987-09-16 | Agency Of Ind Science & Technol | 光学異性体分離用充填剤 |
| JPS63307829A (ja) | 1986-04-02 | 1988-12-15 | Eisai Co Ltd | 光学異性体用分離剤 |
| JPH05271338A (ja) * | 1992-03-27 | 1993-10-19 | Nippon Zeon Co Ltd | 二置換ジフェニルアセチレン系重合体 |
| JPH08133991A (ja) * | 1994-11-04 | 1996-05-28 | Daicel Chem Ind Ltd | 光学活性ポリアセチレン誘導体を用いた光学分割剤 |
| JP2005239863A (ja) * | 2004-02-26 | 2005-09-08 | Japan Science & Technology Agency | キラル配向構造を有する有機/無機複合体及びその製造法 |
Non-Patent Citations (3)
| Title |
|---|
| KENGO HASHIMOTO: "Kogaku Fukassei na Suiyosei Poly(diphenyl acetylene) Yudotai eno Chirality Yuki", POLYMER PREPRINTS, vol. 61, no. 2, 2012, JAPAN, pages 2561 * |
| OKAMOTO, Y.; KAWASHIMA, M.; HATADA, K., J. AM. CHEM. SOC., vol. 106, 1984, pages 5357 |
| See also references of EP2957575A4 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019045267A (ja) * | 2017-08-31 | 2019-03-22 | 国立大学法人金沢大学 | 比色検出型キラルセンサーを用いる光学活性キラルアミン化合物のキラリティー及び光学純度の決定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9562121B2 (en) | 2017-02-07 |
| EP2957575A1 (en) | 2015-12-23 |
| JPWO2014126028A1 (ja) | 2017-02-02 |
| JP6083832B2 (ja) | 2017-02-22 |
| EP2957575B1 (en) | 2017-10-18 |
| US20150376308A1 (en) | 2015-12-31 |
| EP2957575A4 (en) | 2016-10-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ueki et al. | Rational application of self-disproportionation of enantiomers via sublimation—a novel methodological dimension for enantiomeric purifications | |
| JP6083832B2 (ja) | 光学活性ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 | |
| Li et al. | Novel enantioselective fluorescent sensors for malate anion based on acridine | |
| JP6086512B2 (ja) | 新規ポリ(ジフェニルアセチレン)化合物及びその製造方法、並びにその光学異性体分離剤としての用途 | |
| FI120876B (fi) | Kiraalit adsorbentit ja niiden valmistus sekä adsorbenttien pohjana olevat yhdisteet ja niiden valmistus | |
| CN102667466B (zh) | 光学异构体用分离剂 | |
| JP5757602B2 (ja) | 不斉選択性の切り替えが可能なクロマトグラフィー用充填剤 | |
| Nakamura et al. | Chemical modification of diamond powder with optically active functionalities and its chiral recognition behavior | |
| JP6109604B2 (ja) | オクタヒドロビナフチル誘導体 | |
| CN107011180B (zh) | 2,6-二氨基三蝶烯的两种对映异构体及其检测分离方法 | |
| CN110684043B (zh) | 一种c-n轴手性芳胺化合物及其制备方法 | |
| JP6501297B2 (ja) | 比色検出型キラルセンサー | |
| Hirose et al. | Resolution of α-methylbenzylamine via diastereomeric salt formation using the naturally based reagent N-tosyl-(S)-phenylalanine together with a solvent switch technique | |
| JP6460816B2 (ja) | 固体状態で不斉選択性の切り替えが可能な光学異性体分離剤 | |
| JP6095129B2 (ja) | 光学異性体用分離剤 | |
| CN105452221B (zh) | 2,3,4,9-四氢-1h-咔唑-4-甲酰胺衍生物的对映异构体分离和纯化 | |
| JP4417161B2 (ja) | 置換シクロデキストリンおよびその製法 | |
| US8362237B2 (en) | Optical-isomer separating agent for chromatography and process for producing the same | |
| JP2019182971A (ja) | キラル固定相 | |
| CN108164480B (zh) | 一种二芳基呋喃化合物的合成方法 | |
| CN108164449B (zh) | 一种吡咯衍生物的合成方法 | |
| CN115772115A (zh) | 一种芳基吡啶溴代衍生物的合成方法 | |
| CN116969871A (zh) | 一种二氟甲基硒醚类化合物的合成方法 | |
| JP2016199692A (ja) | 多糖誘導体、及びその蛍光性キラルセンサーとしての用途 | |
| JP2018177907A (ja) | キラルアミンセンサー |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14751643 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015500220 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14766853 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2014751643 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014751643 Country of ref document: EP |