WO2014051103A1 - 熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 - Google Patents
熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 Download PDFInfo
- Publication number
- WO2014051103A1 WO2014051103A1 PCT/JP2013/076396 JP2013076396W WO2014051103A1 WO 2014051103 A1 WO2014051103 A1 WO 2014051103A1 JP 2013076396 W JP2013076396 W JP 2013076396W WO 2014051103 A1 WO2014051103 A1 WO 2014051103A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- compound
- gallium
- group
- silanol
- epoxy
- Prior art date
Links
- YXALYBMHAYZKAP-UHFFFAOYSA-N O=C(C1CC2OC2CC1)OCC1CC2OC2CC1 Chemical compound O=C(C1CC2OC2CC1)OCC1CC2OC2CC1 YXALYBMHAYZKAP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/24—Acids; Salts thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/54—Silicon-containing compounds
- C08K5/541—Silicon-containing compounds containing oxygen
- C08K5/5415—Silicon-containing compounds containing oxygen containing at least one Si—O bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/68—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the catalysts used
- C08G59/681—Metal alcoholates, phenolates or carboxylates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/68—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the catalysts used
- C08G59/70—Chelates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/10—Metal compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/54—Silicon-containing compounds
- C08K5/541—Silicon-containing compounds containing oxygen
- C08K5/5415—Silicon-containing compounds containing oxygen containing at least one Si—O bond
- C08K5/5419—Silicon-containing compounds containing oxygen containing at least one Si—O bond containing at least one Si—C bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/56—Organo-metallic compounds, i.e. organic compounds containing a metal-to-carbon bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L63/00—Compositions of epoxy resins; Compositions of derivatives of epoxy resins
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L83/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon only; Compositions of derivatives of such polymers
- C08L83/04—Polysiloxanes
- C08L83/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/14—Polysiloxanes containing silicon bound to oxygen-containing groups
- C08G77/16—Polysiloxanes containing silicon bound to oxygen-containing groups to hydroxyl groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L2201/00—Properties
- C08L2201/02—Flame or fire retardant/resistant
Definitions
- the present invention relates to a novel thermosetting resin composition, a method for producing the same, a method for producing a cured resin, and a method for generating self-polymerization of an epoxy compound.
- An epoxy resin or a silicone resin (also referred to as a polysiloxane resin) is used as a sealing material for semiconductor devices such as light emitting diodes (LEDs) and as a matrix for supporting phosphors in white LEDs or the like.
- an epoxy-silicone resin in which an epoxy resin is hybridized with a silicone resin has been developed (Patent Documents 1, 2, and 3). Furthermore, mixing an additive such as silica with the above-described resin according to the application has been studied.
- polyamine curing agents As typical curing agents for epoxy resins, polyamine curing agents, carboxylic anhydride curing agents, and phenol resin curing agents are well known. These curing agents are compounds having a functional group that reacts with an epoxy group.
- another curing agent there is a type that catalyzes a self-polymerization reaction (cation polymerization reaction accompanied by ring opening) of an epoxy group.
- a combination of silanol and a metal complex (a complex containing Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Al, or Zr) is known (patent) References 4, 5).
- Gallium compounds are known as curing catalysts for condensation-curing silicone resins (Patent Document 6).
- the main object of the present invention is to produce a novel thermosetting resin composition using an epoxy compound, a method for producing the same, a method for producing a novel resin cured product using an epoxy compound, and self-polymerization of the epoxy compound And / or providing at least one of the novel methods. Furthermore, it aims at provision of the resin composition which contributes to provision of the hardened
- thermosetting resin composition containing an epoxy compound, a gallium compound, and a silanol source compound.
- the manufacturing method of a thermosetting resin composition which has a step which mixes a gallium compound and a silanol source compound with an epoxy compound.
- a method for producing a cured resin comprising a step of heating an epoxy compound in the presence of a gallium compound and silanol.
- a novel thermosetting resin composition using an epoxy compound, a production method thereof, a production method of a novel resin cured product using an epoxy compound, and self-polymerization of an epoxy compound At least one of the novel methods is provided.
- the cured product can be provided with functions such as high strength, heat resistance, stable linear expansion coefficient and elasticity in a wide temperature range.
- the 1 H-NMR spectrum of Sample 1 is shown.
- the 1 H-NMR spectrum of Sample 2 is shown.
- the 1 H-NMR spectrum of Sample 3 is shown.
- the 1 H-NMR spectrum of Sample 4 is shown. It is sectional drawing showing the one aspect
- thermosetting resin composition of the present invention contains (A) an epoxy compound, (B) a gallium compound, and (C) a silanol source compound.
- This thermosetting resin composition may contain components other than the above (A) to (C) as necessary.
- thermosetting resin composition a self-polymerization reaction of an epoxy compound catalyzed by a gallium compound and silanol supplied from a silanol source compound is involved in at least a part of the curing mechanism.
- This thermosetting resin composition can be cured only by the self-polymerization reaction, but is not limited thereto.
- each component of this thermosetting resin composition will be described.
- Epoxy Compound is a compound having an epoxy group in the molecule, and preferably an alicyclic epoxy compound having a cyclohexyl epoxy group. Structural examples of typical alicyclic epoxy compounds are shown in formulas (1) to (3).
- the epoxy compound may be a compound having a glycidyl group, but the activity of the self-polymerization reaction may be lower than that of the alicyclic epoxy compound.
- Preferred examples of the epoxy compound having a glycidyl group include a glycidyl ether containing an alicyclic structure as shown in formulas (4) to (8), or an ester compound, and no alicyclic structure as shown in formula (9).
- glycidyl ether compounds glycidyl ether compounds having a disiloxane skeleton as shown in formula (10), and glycidyl amide compounds having an isocyanuric acid skeleton as shown in formula (11).
- the epoxy compound may be an aromatic epoxy compound.
- epoxy compounds include bisphenol A, bisphenol F, bisphenol AD, bisphenol S, tetramethyl bisphenol A, tetramethyl bisphenol F, tetramethyl bisphenol AD, tetramethyl bisphenol S, tetrafluoro as shown in formula (12).
- Bivalent phenols such as bisphenol type epoxy resins obtained by glycidylation of bisphenols such as bisphenol A, biphenyl type epoxy resins represented by the formula (13), dihydroxynaphthalene, 9,9-bis (4-hydroxyphenyl) fluorene, etc.
- Glycidylated epoxy resins 1,1,1-tris (4-hydroxyphenyl) methane and other trisphenols glycidylated epoxy resins, 1,1,2,2-tetrakis (4-H Rokishifeniru) tetrakis phenols glycidylated epoxy resins such as ethane, phenol novolac, cresol novolac, bisphenol A, novolac, novolac type epoxy resins and novolacs and glycidyl of such brominated bisphenol A novolak and the like.
- the epoxy compound may be an epoxy compound having an alicyclic structure obtained by hydrogenating an aromatic epoxy compound.
- the epoxy compound may be a silicon-containing compound having an epoxy group.
- the silicon-containing compound is a silane compound or a siloxane compound.
- Examples of the silicon-containing compound having an epoxy group include ⁇ -glycidoxypropyltrimethoxysilane, ⁇ -glycidoxypropyltriethoxysilane, 2- (3,4-epoxycyclohexyl) ethyltrimethoxysilane, 2- (3, 4-epoxycyclohexyl) ethyltriethoxysilane, ( ⁇ -glycidoxypropyl) (methyl) dimethoxysilane, ( ⁇ -glycidoxypropyl) (ethyl) dimethoxysilane, ( ⁇ -glycidoxypropyl) (methyl) di Ethoxysilane, ( ⁇ -glycidoxypropyl) (ethyl) diethoxysilane, [2- (3,4-epoxycyclohexylethyl) (methyl) dimethoxysilane, [2- (3,4-epoxycyclohexyl) ethyl] ( Ethyl)
- the organopolysiloxane represented by Formula (14) is also contained in the silicon compound containing an epoxy group. (R 11 3 SiO 1/2 ) a1 (R 12 2 SiO 2/2 ) b1 (R 13 SiO 3/2 ) c1 (SiO 4/2 ) d1 (O 1/2 H) e1 (14)
- R 11 , R 12 and R 13 each independently represent a monovalent organic group, and at least one is an organic group containing an epoxy group in one molecule.
- R 11 3 SiO 1/2 represents an M unit
- R 12 2 SiO 2/2 represents a D unit
- R 13 SiO 3/2 represents a T unit
- SiO 4/2 represents a Q unit.
- a1, b1, c1, and d1 are each integers of 0 or more, and a1 + b1 + c1 + d1 ⁇ 3.
- R 11 , R 12 and R 13 are preferably hydrocarbon groups having 1 to 10 carbon atoms. Specific examples thereof include a methyl group, an ethyl group, a propyl group, a butyl group, and pentyl.
- Alkyl groups such as hexyl and heptyl groups; alkenyl groups such as vinyl, allyl, butenyl, pentenyl and hexenyl; aryl groups such as phenyl, tolyl and xylyl; benzyl and phenethyl And substituted alkyl groups such as chloromethyl group, 3-chloropropyl group, 3,3,3-trifluoropropyl group, and nonafluorobutylethyl group.
- examples of the organic group containing an epoxy group include epoxy alkyl groups such as 2,3-epoxypropyl group, 3,4-epoxybutyl group, and 4,5-epoxypentyl group; 2-glycidoxyethyl Groups, glycidoxyalkyl groups such as 3-glycidoxypropyl group, 4-glycidoxybutyl group; ⁇ - (or 2-) (3,4-epoxycyclohexyl) ethyl group, ⁇ - (or 3-) Examples include epoxycyclohexylalkyl groups such as (3,4-epoxycyclohexyl) propyl group.
- e1 is an integer of 0 or more, and represents the number of hydroxyl groups (silanol) directly bonded to the silicon atom.
- the epoxy compound has a hydrolyzable group bonded to a silicon atom.
- the organopolysiloxane represented by the formula (14) (however, e1 ⁇ 1)
- generates may be sufficient.
- the organopolysiloxane represented by the formula (14) (however, e1 ⁇ 1) it may be a compound in which all or part of hydroxyl groups directly bonded to silicon atoms are replaced with hydrolyzable groups. .
- the hydrolyzable group is a group that generates a hydroxyl group (silanol) bonded to a silicon atom by hydrolysis.
- a hydroxy group an alkoxy group, hydrogen, an acetoxy group, an enoxy group, an oxime group, A halogen group is mentioned.
- a preferred hydrolyzable group is an alkoxy group, particularly an alkoxy group having 1 to 3 carbon atoms, that is, a methoxy group, an ethoxy group, or a propoxy group.
- the organopolysiloxane type epoxy compound represented by the above formula (14) can be produced, for example, by the following method.
- Method 1 A method of cohydrolyzing and polycondensing a silane compound having an epoxy group and a silane compound having no epoxy group and / or an oligomer thereof.
- Method 2 A method of adding an organic compound having an epoxy group and a carbon-carbon double bond group to a polysiloxane having a hydrosilyl group.
- Method 3) A method in which the double bond portion of the polysiloxane having an organic group containing a carbon-carbon double bond is oxidized and converted to an epoxy group.
- the raw materials that can be used in the production of the polysiloxane type epoxy compound by the method 1 are as follows.
- Examples of raw materials for introducing the M unit include trimethylmethoxysilane, trimethylethoxysilane, triphenylmethoxysilane, and triphenylsilanol.
- dialkylsiloxane oligomers having hydroxyl groups at both ends compounds having silanol-modified compounds such as polydimethylsiloxane, polymethylphenylsiloxane, dimethylsiloxane-diphenylsiloxane copolymer, and polydiphenylsiloxane are commercially available.
- Raw materials for introducing T unit include methyltrimethoxysilane, methyltriethoxysilane, ethyltrimethoxysilane, ethyltriethoxysilane, vinyltrimethoxysilane, phenyltrimethoxysilane, 3,3,3-trifluoropropyl Examples include trimethoxysilane and hydrolytic condensates thereof.
- raw materials for introducing the Q unit include tetramethoxysilane, tetraethoxysilane, tetrapropoxysilane, and hydrolytic condensates thereof.
- gallium Compound A gallium compound is a component that acts as a catalyst for a self-polymerization reaction of an epoxy compound in combination with a silanol supplied from a silanol source compound described in detail later.
- the gallium compound is not particularly limited as long as it exhibits the above action, and can be selected from the following candidate compounds: gallium complex having a chelate ligand, gallium acetate, gallium oxyacetate, triethoxygallium, tris (8-quinolinolato) Gallium, gallium oxalate, gallium ethyl xanthate, diethyl ethoxy gallium, gallium maleate and the like. gallium salts of long chain carboxylic acids such as n-octylic acid, 2-ethylhexanoic acid and naphthenic acid. *
- chelate ligands examples include ⁇ -diketone type compounds and o-ketophenol type compounds.
- Some ⁇ -diketone type compounds have structures represented by the following formulas (15) to (17).
- R represents an alkyl group or a halogen-substituted alkyl group.
- Specific examples of the compound of the formula (15) include acetylacetone, trifluoroacetylacetone, pentafluoroacetylacetone, hexafluoroacetylacetone and the like.
- Specific examples of the compound of the formula (16) include ethylacetoacetate and the compound of the formula (17). Specific examples of such include diethyl malonate.
- the O-ketophenol type compound is a compound represented by the following formula (18).
- R ′ represents a hydrogen atom, an alkyl group, a halogen-substituted alkyl group or an alkoxy group.
- Specific examples of the compound of formula (18) include salicylaldehyde, ethyl-O-hydroxyphenyl ketone and the like.
- a gallium complex having a chelate ligand is a preferred example of a gallium compound, and among them, gallium acetylacetonate can be particularly preferably used.
- the weight loss due to heating of the cured product is less than that of an Al catalyst.
- the weight loss due to heating of the cured product is less than that of the Al catalyst.
- the weight loss is preferably 20% by mass or less before heating at 150 to 200 ° C. ⁇ 500 hours, and more preferably 10% by mass or less.
- the (B) gallium compound is usually 0.001 part by weight or more, preferably 0.01 part by weight or more, and 5.0 part by weight or less, preferably 1.0 part by weight based on 100 parts by weight of the (A) epoxy compound. It is as follows.
- silanol source compound is a compound which is a supply source of silanol.
- Silanol in combination with the aforementioned gallium compound, acts as a catalyst for the self-polymerization reaction of the epoxy compound.
- silanol is considered to be a cation source necessary for the initiation of the self-polymerization reaction of the epoxy compound.
- an aromatic group such as a phenyl group is bonded to the silicon atom of the silanol source compound, this aromatic group functions to increase the acidity of the silanol hydroxyl group, that is, to enhance the action of silanol as a cation source. it seems to do.
- the silanol source compound may be a potential silanol source.
- it is a compound which has a silicon atom to which a hydrolyzable group is bonded and which produces silanol when the hydrolyzable group is hydrolyzed.
- the hydrolyzable group include a hydroxy group, an alkoxy group, hydrogen, an acetoxy group, an enoxy group, an oxime group, and a halogen group.
- a preferred hydrolyzable group is an alkoxy group, particularly an alkoxy group having 1 to 3 carbon atoms, that is, a methoxy group, an ethoxy group, or a propoxy group.
- silanol source compound is a silicon atom to which hydroxyl groups such as phenyldimethylsilanol, diphenylmethylsilanol, triphenylsilanol, dihydroxydiphenylsilane (diphenyldisilanol), trimethylsilanol, triethylsilanol, dihydroxydimethylsilane, and trihydroxymethylsilane are bonded.
- It is a monosilane compound having Another example of the silanol source compound is an organopolysiloxane represented by the formula (19) having a silicon atom to which a hydroxyl group is bonded.
- R 21 , R 22 and R 23 each independently represent a monovalent organic group.
- R 21 3 SiO 1/2 represents an M unit
- R 22 2 SiO 2/2 represents a D unit
- R 23 SiO 3/2 represents a T unit
- SiO 4/2 represents a Q unit.
- a2, b2, c2, and d2 are each integers of 0 or more, and a2 + b2 + c2 + d2 ⁇ 3.
- e2 is a natural number of 1 or more, and represents the number of hydroxyl groups (silanol) directly bonded to the silicon atom.
- R 21 , R 22 and R 23 in the formula (19) are usually hydrocarbon groups having 1 to 10 carbon atoms. Specific examples thereof include a methyl group, an ethyl group, a propyl group, a butyl group, a pentyl group, Alkyl groups such as hexyl group and heptyl group; alkenyl groups such as vinyl group, allyl group, butenyl group, pentenyl group and hexenyl group; aryl groups such as phenyl group, tolyl group and xylyl group; aralkyl groups such as benzyl group and phenethyl group Groups; substituted alkyl groups such as chloromethyl group, 3-chloropropyl group, 3,3,3-trifluoropropyl group, nonafluorobutylethyl group and the like.
- the silanol source compound has a hydrolyzable group bonded to a silicon atom, and produces a organopolysiloxane represented by the formula (19) when the hydrolyzable group is hydrolyzed. Also good.
- the organopolysiloxane represented by the formula (19) may be a compound in which all or part of the hydroxyl groups directly bonded to the silicon atom are replaced with hydrolyzable groups.
- the silanol source compound is an organopolysiloxane and is used together with an epoxy compound not containing a siloxane structure
- the organopolysiloxane is silicon from the viewpoint of ensuring compatibility between the organopolysiloxane and the epoxy compound. It preferably has an aromatic group bonded to an atom.
- the weight average molecular weight is preferably 500 or more and more preferably 700 or more so that it does not volatilize during or after curing of the thermosetting resin composition.
- the weight average molecular weight is preferably 20,000 or less, more preferably 15,000 or less.
- the silanol source compound may be an organopolysiloxane or a silane compound having two or more silicon atoms bonded to a hydroxyl group or a hydrolyzable group in one molecule.
- a silanol source compound is polycondensed by the action of the gallium compound to increase the molecular weight when heated, so that it does not bleed out after curing.
- the organopolysiloxane represented by the formula (22) includes a compound represented by the formula (2) and a compound represented by the formula (24) (dihydroxydimethylsilane or polydimethylsiloxane having hydroxyl groups at both ends), It can be obtained by polycondensation.
- a polycondensation catalyst a metal catalyst can be used in addition to an acid and a base, and a gallium compound such as gallium acetoacetonate can also be used.
- the organopolysiloxane represented by the formula (23) can be obtained by polycondensation of the compound represented by the formula (21) and the compound represented by the formula (24).
- a polycondensation catalyst a metal catalyst can be used in addition to an acid and a base, and a gallium compound such as gallium acetoacetonate can also be used.
- m, n, M, N, m1, and m2 are each an integer of 1 or more.
- the degree of polymerization so that the viscosity of the organopolysiloxane or the viscosity of the thermosetting resin composition obtained using the organopolysiloxane is 10,000 mPa ⁇ s or less, particularly 5000 mPa ⁇ s or less. Is preferably set.
- Organopolysiloxanes represented by formula (2), formula (20) to formula (23) are also a suitable example of the (C) silanol source compound.
- a polycondensation catalyst a metal catalyst can be used in addition to an acid and a base, and a gallium compound such as gallium acetoacetonate can also be used.
- Such organopolysiloxanes have the property of being cured by the action of a condensation catalyst such as an acid, a base or a metal compound such as a gallium compound.
- a monosilane compound and an organopolysiloxane may be used in combination.
- the (C) silanol source compound is usually 0.05 parts by weight or more, preferably 0.5 parts by weight or more, and 500 parts by weight or less, preferably 200 parts by weight or less based on 100 parts by weight of the (A) epoxy compound. .
- the content ratio of the (B) gallium compound and the (C) silanol source compound is preferably 1: 0.05 to 0.001: 100, more preferably 1:10 to 0.01: 100, by weight.
- either one or both of the epoxy compound and the silanol source compound may have an organopolysiloxane structure portion.
- the gallium compound acts as a dehydration condensation catalyst between the silanols, so that both the self-polymerization reaction of the epoxy compound and the silanol condensation reaction are involved in curing.
- a good thermosetting resin composition is obtained. Since the gallium compound also serves as a catalyst for the dealcoholization condensation reaction between silanol and alkoxy group, the same effect can be obtained when silanol and alkoxy group are introduced into the organopolysiloxane structure.
- a hydrosilyl group is introduced into one of the organopolysiloxane structure part of the epoxy compound and the organopolysiloxane structure part of the silanol source compound, and a vinylsilyl group is introduced into the other, and a hydrosilylation reaction catalyst such as a platinum compound is used.
- a thermosetting resin composition having good curability in which both the self-polymerization reaction and hydrosilylation reaction of the epoxy compound are involved in curing can be obtained.
- thermosetting resin composition in which both the self-polymerization reaction and hydrosilylation reaction are involved in curing is obtained.
- This example may be modified such that a vinylsilyl group is introduced into the organopolysiloxane structure part of either one or both of the epoxy compound and the silanol source compound, and the organopolysiloxane to be added is introduced with a hydrosilyl group.
- thermosetting resin composition includes a dispersant, an antioxidant, a defoaming agent, It may further contain additives such as colorants, modifiers, leveling agents, light diffusing agents, thermal conductivity, flame retardants, reactive or non-reactive diluents, adhesion and adhesion improvers, and various fillers. .
- both general organic fillers and inorganic fillers can be used.
- the organic filler include styrene polymer particles, methacrylate polymer particles, ethylene polymer particles, propylene polymer particles, synthetic polymer particles such as polyamide, starch, natural products such as wood flour, cellulose that may be modified, Examples include various organic pigments.
- the inorganic filler is not particularly limited as long as it is an inorganic substance or a compound containing an inorganic substance. Specifically, for example, quartz, fumed silica, precipitated silica, anhydrous silicic acid, fused silica, crystalline silica, ultrafine powder amorphous silica.
- Silica-based inorganic fillers such as alumina, zircon, iron oxide, zinc oxide, titanium oxide, silicon nitride, boron nitride, aluminum nitride, silicon carbide, glass fiber, glass flake, alumina fiber, carbon fiber, mica, graphite, carbon black , Ferrite, graphite, diatomaceous earth, clay, talc, aluminum hydroxide, calcium carbonate, manganese carbonate, magnesium carbonate, barium sulfate, potassium titanate, calcium silicate, inorganic balloon, silver powder and the like.
- Silica-based inorganic fillers such as alumina, zircon, iron oxide, zinc oxide, titanium oxide, silicon nitride, boron nitride, aluminum nitride, silicon carbide, glass fiber, glass flake, alumina fiber, carbon fiber, mica, graphite, carbon black , Ferrite, graphite, diatomaceous earth, clay, talc, aluminum hydroxide, calcium carbonate
- a surface treatment suitably.
- the surface treatment include alkylation treatment, trimethylsilylation treatment, silicone treatment, treatment with a silane coupling agent, and the like, but are not particularly limited.
- the amount of filler added is not particularly limited.
- the strength, hardness, elastic modulus, thermal expansion coefficient, thermal conductivity, heat dissipation, electrical properties, light reflectance, flame retardancy, fire resistance, thixotropy, and gas barrier of the molded product obtained Various physical properties such as properties can be improved.
- the order of mixing the filler is not particularly limited, but the epoxy compound is used in the absence of a catalyst used for curing a gallium compound, silanol source compound, or other epoxy resin in order to prevent the curing reaction from proceeding due to heat generation during mixing. It is desirable to mix with.
- the means for mixing the filler is not particularly limited. Specifically, for example, a two-roll or three-roll, a planetary stirring and defoaming device, a homogenizer, a dissolver, a planetary mixer, etc., a plastmill Such as a melt kneader. Mixing may be performed at normal temperature, may be performed by heating, may be performed under normal pressure, or may be performed under reduced pressure. If the temperature during mixing is high, the composition may be cured before molding. *
- an inorganic filler particularly silica fine particles
- an inorganic filler may be added mainly for the purpose of suppressing a difference in thermal expansion coefficient generated between adjacent members.
- a higher effect can be obtained by increasing the amount added, and it is desirable to add 40 parts by weight or more, preferably 70 parts by weight or more, and more preferably 80 parts by weight or more with respect to 100 parts by weight of the epoxy resin.
- control of the particle size distribution is often used.
- a higher filling rate can be obtained by mixing fillers having different particle sizes.
- the viscosity of the composition increases significantly.
- the viscosity can be kept low.
- the interaction between the particles and between the matrix composition composed of particles and epoxy resin can be controlled to obtain an appropriate viscosity.
- thermosetting resin composition according to the embodiment of the present invention may contain an antioxidant in order to suppress yellowing under the use environment.
- Phenol-based antioxidants phosphorus-based antioxidants, hindered amines, and the like are preferably used. Of these, hindered phenol-based antioxidants having an alkyl group at one or both ortho positions of the phenolic hydroxyl group are particularly preferred. Used.
- a catalyst used for curing ordinary epoxy resin can be used in combination.
- tertiary amines such as benzyldimethylamine, 2,4,6-tris (dimethylaminomethyl) phenol, cyclohexyldimethylamine, triethanolamine; 2-methylimidazole, 2-n-heptylimidazole, 2-n- Undecylimidazole, 2-phenylimidazole, 2-phenyl-4-methylimidazole, 1-benzyl-2-methylimidazole, 1-benzyl-2-phenylimidazole, 1,2-dimethylimidazole, 2-ethyl-4-methyl Imidazole, 1- (2-cyanoethyl) -2-methylimidazole, 1- (2-cyanoethyl) -2-n-n-
- thermosetting resin composition according to the embodiment of the present invention may contain an acid anhydride as a curing aid.
- an acid anhydride as a curing aid.
- Examples of the alicyclic carboxylic acid anhydride include compounds represented by formulas (25) to (30), 4-methyltetrahydrophthalic acid anhydride, methyl nadic acid anhydride, dodecenyl succinic acid anhydride, Examples thereof include Diels-Alder reaction products of alicyclic compounds having a conjugated double bond such as ⁇ -terpinene and alloocimene and maleic anhydride, and hydrogenated products thereof.
- arbitrary structural isomers and arbitrary geometric isomers can be used as the Diels-Alder reaction product and hydrogenated products thereof.
- the alicyclic carboxylic acid anhydride can be used after being appropriately chemically modified as long as the curing reaction is not substantially hindered.
- effects such as control of the epoxy reaction rate, handling, improvement of leveling, and prevention of coloring may be obtained.
- content of an acid anhydride It is preferable that it is 1.5 equivalent or less with respect to the amount of epoxy. More preferably, it is 1 equivalent or less, More preferably, it is 0.8 equivalent or less.
- thermosetting resin composition of the present invention can contain a silane coupling agent in order to improve the adhesion to metal parts and inorganic fillers.
- Examples include 2- (3,4-epoxycyclohexyl) ethyltrimethoxysilane, vinyltriethoxysilane, vinyltrimethoxysilane, 3-glycidoxypropyltrimethoxysilane, ⁇ -methacryloxypropyltrimethoxysilane, ⁇ - Examples include aminopropyltrimethoxysilane and N-phenyl-3-aminopropyltrimethoxysilane.
- a catalyst used for ordinary silanol curing can be used in combination as long as it does not inhibit the epoxy reaction by the catalytic action of the gallium compound and the silanol supplied from the silanol source compound.
- Specific examples include a dehydration / dealcohol condensation reaction catalyst.
- the reaction catalyst preferably contains at least one selected from the group consisting of an organometallic complex catalyst, a salt of a metal and an organic acid, and a Lewis acid / Lewis base catalyst.
- the metal component contained in the dehydration / dealcohol condensation reaction catalyst it is preferable to use one or more selected from Sn, Zn, Fe, Ti, Zr, Bi, Hf, Y, Al, B, Ga, etc.
- Ti, Al, Zn, Zr, Hf, and Ga are preferable in that they have high reaction activity.
- they When used as a light emitting device member, they have moderate catalytic activity with little electrode corrosion and light absorption.
- Zr and Hf are particularly preferable because unnecessary cutting deterioration hardly occurs.
- thermosetting resin composition includes the above components (A) to (C) and, if necessary, fillers, diluents, antioxidants and the like. It can be produced by mixing other components.
- This thermosetting resin composition may be a two-component curable type in consideration of storage stability.
- the liquid A can be a liquid containing an epoxy compound
- the liquid B can be a liquid containing a gallium compound and a silanol source compound.
- the liquid A can be a liquid containing an epoxy compound and a silanol source compound
- the liquid B can be a liquid containing a gallium compound.
- the liquid A can be a liquid containing an epoxy compound and a gallium compound
- the liquid B can be a liquid containing a silanol source compound.
- thermosetting resin composition The heating method for curing the thermosetting resin composition according to the embodiment of the present invention is not particularly limited, and examples thereof include hot air circulation heating and infrared rays. Conventionally known methods such as heating and high-frequency heating can be employed.
- the heat treatment conditions are not particularly limited as long as the thermosetting resin composition can be brought into a desired cured state.
- thermosetting resin composition is not particularly limited, and as a sealing material or the like for various semiconductor devices including light emitting devices such as LED devices. Can be used.
- a sealing material for a semiconductor light emitting element for example, a sealing material for a semiconductor light emitting element, an adhesive (die bond agent) for fixing the semiconductor light emitting element to a package, a lead frame, etc., a structural material constituting the package, a highly reflective coating material, etc.
- an adhesive die bond agent for fixing the semiconductor light emitting element to a package, a lead frame, etc.
- a structural material constituting the package for example, a highly reflective coating material, etc.
- phosphor when used as a wavelength conversion element, phosphor, fumed silica, spherical silica and the like can be added.
- a heat conductive agent when used as a die bond agent, a heat conductive agent, fumed silica, or the like can be added.
- titania particles, alumina particles, and the like when used as a structural material for a package or a highly reflective coating material, titania particles, alumina particles, and the like can be added.
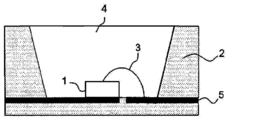
- the LED device includes an LED element 1, a resin molded body 2, a bonding wire 3, a sealing material 4 containing a phosphor, and a lead frame 5.
- the LED element 1 is an InGaN-based LED that emits light having a wavelength in the near ultraviolet region, the violet region, or the blue region.
- the resin molded body 2 is molded together with the lead frame 5 and has a cup shape.
- the lead frame 5 is made of a conductive metal and is a structural member, and at the same time plays a role of transmitting current supplied to the LED device from the outside to the LED element 1.
- the bonding wire 3 electrically connects the LED element 1 and one side of the lead frame.
- the LED element 1 is bonded and fixed to the other side of the lead frame using a die bonding agent imparted with conductivity by adding conductive particles, and then sealed with a sealing material 4 mixed with a phosphor.
- thermosetting resin composition according to the embodiment of the present invention can be used as a material for the resin molding 2, the sealing material 4, and the die bond agent (not shown) in the LED device shown in FIG.
- thermosetting resin composition was identified.
- silanol polymethylphenylsiloxane having a weight average molecular weight of about 900 in terms of polystyrene (BLUESTARS SILICONES Co., Ltd., FLD516: SOL, represented by the formula (31), having silicon atoms bonded to hydroxyl groups at both ends. -1) was used.
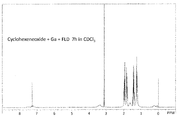
- Samples 1 to 4 were prepared as follows. Sample 1 was obtained by adding 0.59 g of SOL-1 to 5.03 g of cyclohexene oxide and mixing.
- Sample 1 (mixture of 5.03 g of cyclohexene oxide and 0.59 g of SOL-1) was stirred at 120 ° C. for 7 hours under a nitrogen stream to obtain Sample 2.
- sample 3 was obtained by stirring a mixture of 5.00 g of cyclohexene oxide and 0.002 g of gallium acetylacetonate (Ga (acac) 3 ) at 120 ° C. for 7 hours under a nitrogen stream. It was.
- the content of SOL-1 in Sample 4 is 12 parts by weight per 100 parts by weight of cyclohexene oxide, as in Samples 1 and 2.
- the content of Ga (acac) 3 in sample 4 is 0.04 parts by weight with respect to 100 parts by weight of cyclohexene oxide, as in sample 3.
- the 1 H-NMR spectrum was measured using an AVANCE400 manufactured by Bruker BioSpin Corporation under the conditions of a magnetic field of 400 MHz and a temperature of 25 ° C. Deuterated chloroform was used as the solvent, and the sample concentration was about 5 wt%. Tetramethylsilane was used as a reference material. 1.4 Results of 1 H-NMR Spectroscopy 1 H-NMR spectra of Samples 1 to 4 are shown in FIGS.
- a signal group of 3.1 ppm derived from the epoxymethine group of cyclohexene oxide and a signal group of 1 to 2 ppm derived from the methylene group of cyclohexene oxide were observed in all four samples.
- gallium acetylacetonate made by Strem Chemicals, Inc.
- This compound may also be referred to as gallium triacetylacetonate, tris (acetylacetonato) gallium, tris (2,4-pentanedionato) gallium and the like. It may also be expressed as Ga (acac) 3 .
- the first silanol compound is polymethylphenylsiloxane (FLD516 manufactured by BLUESTAR SILICONES) having a weight average molecular weight of about 900 in terms of polystyrene, which has a silicon atom bonded to a hydroxyl group at both ends, represented by the formula (33). (Hereinafter, this compound is abbreviated as SOL-1).
- the second silanol compound is dihydroxydiphenylsilane (manufactured by Shin-Etsu Chemical Co., Ltd., LS-4320) (hereinafter, this compound is abbreviated as SOL-2).
- the third silanol compound is a polydimethylsiloxane represented by formula (34) having a hydroxyl group-bonded silicon atom at both ends and having a weight average molecular weight of about 500 in terms of polystyrene [Momentive Performance Materials Japan ( XC96-723] (hereinafter, this compound is abbreviated as SOL-3).
- compositions 1 to 7 having compositions shown in Table 1 were prepared.
- the Ga (acac) 3 solution is a 2.0% by weight gallium acetylacetonate solution obtained by dissolving 0.047 g of gallium acetylacetonate in 2.36 g of SOL-1. is there.
- This Ga (acac) 3 solution was mixed with EPC-1 during the preparation of compositions 1 and 2, whereas solid gallium acetylacetonate was directly dissolved in EPC-1 during the preparation of compositions 3-5.
- the amount of gallium acetylacetonate used in reference to the amount of EPC-1 is the same in any of compositions 1 to 5.
- ⁇ Heat treatment> About 2 g of the epoxy composition was put in an aluminum cup having an inner diameter of 5 cm, and first held at 120 ° C. for 30 minutes in a thermostatic bath, and then held at 150 ° C. for 150 minutes.
- compositions 1 to 4 lost fluidity by heat treatment, and in these compositions, the gelation rate exceeded 90%.
- a common feature of compositions 1-4 is that they contain both gallium acetylacetonate and silanol.
- compositions 5 containing gallium acetylacetonate but not silanol compositions 6 and 7 containing silanol but not gallium acetylacetonate remained fluid after heat treatment.
- the gelation rate was also 0%.
- compositions 1 to 4 were thermally cured mainly due to the polycondensation of SOL-1, SOL-2 and SOL-3 catalyzed by gallium acetylacetonate.
- the reason is that the contents of SOL-1, SOL-2 and SOL-3 in compositions 1 to 4 are 1/10 or less of EPC-1 by weight.
- SOL-1, SOL-2, and SOL-3 all have two silanol hydroxyl groups in one molecule, and are compounds that do not form a three-dimensional crosslinked structure even when polycondensed.
- the possibility of polycondensation of SOL-1, SOL-2 and SOL-3 in compositions 1 to 4 is not denied.
- reaction solution is neutralized with an aqueous sodium dihydrogen phosphate solution (10% by mass), washed with water until the washed water becomes neutral, and then the volatile components are removed under reduced pressure to remove polysiloxane EPSi-1 Got.
- Siloxane EPSi-2 was obtained.
- YX-4000H manufactured by Mitsubishi Chemical Corporation having a structure represented by the formula (35) was used. (Hereinafter this compound is called EPC-2)
- compositions 8 to 12 having compositions shown in Table 3 were prepared.
- a spherical filler MSR-SF630 manufactured by Tatsumori Co., Ltd. was used.
- Example 1 Evaluation of fluidity was performed according to Example 1 described above.
- the hardness after heat treatment was also measured.
- the hardness is measured by Asker rubber hardness tester A type (manufactured by Kobunshi Keiki Co., Ltd.) as the hardness meter, and constant pressure loader CL-150 for rubber hardness meter (stock of polymer meter stock) as the loader Was used to measure Shore A hardness.
- compositions 8 to 12 lost fluidity due to the heat treatment, and the hardness (shore A) of these compositions after the heat treatment exceeded 90.
- polysiloxane having an epoxy group polysiloxane having an aromatic group, an acid anhydride compound, and an epoxy compound are blended at a ratio (weight ratio) shown in Table 5 and mixed at room temperature in an air atmosphere. After stirring until uniform, the (C) gallium compound was added and further stirred. The obtained liquid was heated at 80 ° C. for 0.5 hours and then at 150 ° C. for 2.5 hours to perform a curing test.
- thermosetting resin composition described in Table 5 was cured by the method described above, and the cured state of the obtained cured product was observed. The results are shown in Table 6.
- Siloxane EPSi-3 was obtained.
- the above-mentioned polysiloxane and acid anhydride compound are blended as shown in Table 7, mixed at room temperature in an air atmosphere, stirred until the whole becomes uniform, and then a gallium compound or an aluminum compound is added. Further stirring was performed.
- the obtained liquid was heated at 80 ° C. for 0.5 hours and then at 150 ° C. for 2.5 hours to perform a curing test.
- the fluidity and gelation rate were evaluated according to Example 1 described above. The results are shown in Table 8.
- the cured state was good even when gallium acetate was used instead of gallium acetylacetonate, but in the composition using aluminum ethylacetylacetonate, the curing reaction was too early, Gelation was observed during stirring at room temperature. When gallium acetylacetonate was removed, the fluidity remained after heating and the gelation rate was zero%.
Abstract
エポキシ化合物を用いた新規な熱硬化性樹脂組成物、その製造方法、エポキシ化合物を用いた新規な樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させるための新規な方法の、少なくともいずれかを提供することを課題とし、熱硬化性樹脂組成物は、エポキシ化合物と、ガリウム化合物と、シラノール源化合物とを含有する。熱硬化性樹脂組成物の製造方法は、エポキシ化合物に、ガリウム化合物およびシラノール源化合物を混合するステップを有する。樹脂硬化物の製造方法は、エポキシ化合物を、ガリウム化合物およびシラノールの存在下で加熱するステップを含む。エポキシ化合物の自己重合を発生させる方法は、ガリウム化合物およびシラノールを触媒に用いることを特徴とする。
Description
本発明は、新規な熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法に関する。
発光ダイオード(LED)等の半導体デバイスの封止材料として、また、白色LED等において蛍光体を担持するマトリックスとして、エポキシ樹脂やシリコーン樹脂(ポリシロキサン樹脂ともいう)が用いられている。また、シリコーン樹脂にエポキシ樹脂をハイブリッド化したエポキシ-シリコーン樹脂も開発されている(特許文献1、2、3)。さらには、用途に応じて、上記の樹脂にシリカ等の添加物を混合することも検討されている。
エポキシ樹脂の代表的な硬化剤として、ポリアミン系硬化剤、カルボン酸無水物系硬化剤、フェノール樹脂系硬化剤がよく知られている。これらの硬化剤はエポキシ基と反応する官能基を有する化合物である。その他の硬化剤として、エポキシ基の自己重合反応(開環を伴うカチオン重合反応)を触媒するタイプのものがある。この種の硬化剤として、シラノールと、金属錯体(Ti、V、Cr、Mn、Fe、Co、Ni、Cu、Zn、AlまたはZrを含む錯体)とを組合せたものが知られている(特許文献4、5)。
縮合硬化型のシリコーン樹脂のための硬化触媒としてガリウム化合物が知られている(特許文献6)。
縮合硬化型のシリコーン樹脂のための硬化触媒としてガリウム化合物が知られている(特許文献6)。
本発明の主たる目的は、エポキシ化合物を用いた新規な熱硬化性樹脂組成物、その製造方法、エポキシ化合物を用いた新規な樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させるための新規な方法の、少なくともいずれかを提供することにある。さらには新規な熱硬化性樹脂組成物の提供に新たに機能付与された硬化物の提供に資する樹脂組成物の提供を目的とする。
本発明者らは、2官能の脂環式エポキシ化合物に対して触媒量のガリウムアセチルアセトネートと、シラノールを含有する化合物とを添加した組成物が熱硬化性を示すことを見出し、本発明を完成させた。
すなわち本発明は以下に存する。
(1)エポキシ化合物と、ガリウム化合物と、シラノール源化合物とを含有する熱硬化性樹脂組成物。
(2)エポキシ化合物に、ガリウム化合物およびシラノール源化合物を混合するステップを有する、熱硬化性樹脂組成物の製造方法。
(3)エポキシ化合物を、ガリウム化合物およびシラノールの存在下で加熱するステップを含む、樹脂硬化物の製造方法。
(4)エポキシ化合物の自己重合を発生させる方法であって、ガリウム化合物およびシラノールを触媒として添加するステップを含む方法。
すなわち本発明は以下に存する。
(1)エポキシ化合物と、ガリウム化合物と、シラノール源化合物とを含有する熱硬化性樹脂組成物。
(2)エポキシ化合物に、ガリウム化合物およびシラノール源化合物を混合するステップを有する、熱硬化性樹脂組成物の製造方法。
(3)エポキシ化合物を、ガリウム化合物およびシラノールの存在下で加熱するステップを含む、樹脂硬化物の製造方法。
(4)エポキシ化合物の自己重合を発生させる方法であって、ガリウム化合物およびシラノールを触媒として添加するステップを含む方法。
本発明によれば、エポキシ化合物を用いた新規な熱硬化性樹脂組成物、その製造方法、エポキシ化合物を用いた新規な樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させるための新規な方法の、少なくともいずれかが提供される。そのような組成物の提供により、硬化物としては、高強度、耐熱性、幅広い温度領域での安定した線膨張率および弾性といった機能を付与することができる。
以下、本発明を実施の形態に即して説明するが、本発明は本明細書に明示的または黙示的に記載された実施の形態により限定されるものではなく、その要旨を逸脱しない限りにおいて種々に変更して実施することができる。
1.熱硬化性樹脂組成物
本発明の熱硬化性樹脂組成物は、(A)エポキシ化合物、(B)ガリウム化合物、および(C)シラノール源化合物を含有する。この熱硬化性樹脂組成物には、必要に応じて上記(A)~(C)以外の成分を含有させてもよい。
本発明の熱硬化性樹脂組成物は、(A)エポキシ化合物、(B)ガリウム化合物、および(C)シラノール源化合物を含有する。この熱硬化性樹脂組成物には、必要に応じて上記(A)~(C)以外の成分を含有させてもよい。
この熱硬化性樹脂組成物は、その硬化機構の少なくとも一部に、ガリウム化合物とシラノール源化合物から供給されるシラノールとによって触媒されるエポキシ化合物の自己重合反応が関与するものである。この熱硬化性樹脂組成物は、該自己重合反応のみにより硬化するものであり得るが、限定されるものではない。
以下、この熱硬化性樹脂組成物の各成分について説明する。
以下、この熱硬化性樹脂組成物の各成分について説明する。
1.1(A)エポキシ化合物
エポキシ化合物は、分子中にエポキシ基を有する化合物であり、好ましくはシクロヘキシルエポキシ基を有する脂環式エポキシ化合物である。典型的な脂環式エポキシ化合物の構造例を式(1)~(3)に示す。
エポキシ化合物は、分子中にエポキシ基を有する化合物であり、好ましくはシクロヘキシルエポキシ基を有する脂環式エポキシ化合物である。典型的な脂環式エポキシ化合物の構造例を式(1)~(3)に示す。
グリシジル基を有するエポキシ化合物の好適例として、式(4)~式(8)に示すような脂環構造を含むグリシジルエーテル、またはエステル化合物、式(9)に示すような脂環構造を含まないグリシジルエーテル化合物、式(10)に示すようなジシロキサン骨格を有するグリシジルエーテル化合物、式(11)に示すようなイソシアヌル酸骨格を有するグリシジルアミド化合物がある。
また、エポキシ化合物は、芳香族エポキシ化合物であってもよい。かかるエポキシ化合物の例としては、式(12)に示すようなビスフェノールA、ビスフェノールF、ビスフェノールAD、ビスフェノールS、テトラメチルビスフェノールA、テトラメチルビスフェノールF、テトラメチルビスフェノールAD、テトラメチルビスフェノールS、テトラフルオロビスフェノールAなどのビスフェノール類をグリシジル化したビスフェノール型エポキシ樹脂、式(13)に示すようなビフェニル型のエポキシ樹脂、ジヒドロキシナフタレン、9,9-ビス(4-ヒドロキシフェニル)フルオレン等の2価のフェノール類をグリシジル化したエポキシ樹脂、1,1,1-トリス(4-ヒドロキシフェニル)メタン等のトリスフェノール類をグリシジル化したエポキシ樹脂、1,1,2,2-テトラキス(4-ヒドロキシフェニル)エタン等のテトラキスフェノール類をグリシジル化したエポキシ樹脂、フェノールノボラック、クレゾールノボラック、ビスフェノールA、ノボラック、臭素化ビスフェノールAノボラック等のノボラック類をグリシジル化したノボラック型エポキシ樹脂等が挙げられる。
エポキシ化合物は、エポキシ基を有するケイ素含有化合物であってもよい。ケイ素含有化合物とは、シラン化合物やシロキサン化合物である。
エポキシ基を有するケイ素含有化合物には、γ-グリシドキシプロピルトリメトキシシラン、γ-グリシドキシプロピルトリエトキシシラン、2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン、2-(3,4-エポキシシクロヘキシル)エチルトリエトキシシラン、(γ-グリシドキシプロピル)(メチル)ジメトキシシラン、(γ-グリシドキシプロピル)(エチル)ジメトキシシラン、(γ-グリシドキシプロピル)(メチル)ジエトキシシラン、(γ-グリシドキシプロピル)(エチル)ジエトキシシラン、〔2-(3,4-エポキシシクロヘキシルエチル〕(メチル)ジメトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エチル)ジメトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メチル)ジエトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エチル)ジエトキシシラン、(γ-グリシドキシプロピル)(メトキシ)ジメチルシラン、(γ-グリシドキシプロピル)(メトキシ)ジエチルシラン、(γ-グリシドキシプロピル)(エトキシ)ジメチルシラン、(γ-グリシドキシプロピル)(エトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メトキシ)ジメチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エトキシ)ジメチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(ジメチル)ジシロキサン、3-エポキシプロピル(フェニル)ジメトキシシランなどがある。
また、エポキシ基を含有するケイ素化合物には、式(14)で表されるオルガノポリシロキサンも含まれる。
(R11 3SiO1/2)a1(R12 2SiO2/2)b1(R13SiO3/2)c1(SiO4/2)d1(O1/2H)e1 ・・・(14)
また、エポキシ基を含有するケイ素化合物には、式(14)で表されるオルガノポリシロキサンも含まれる。
(R11 3SiO1/2)a1(R12 2SiO2/2)b1(R13SiO3/2)c1(SiO4/2)d1(O1/2H)e1 ・・・(14)
式(14)において、R11、R12、R13はそれぞれ独立して1価の有機基を示し、かつ、1分子中において少なくとも1つがエポキシ基を含む有機基である。
式(14)において、R11
3SiO1/2はMユニット、R12
2SiO2/2はDユニット、R13SiO3/2はTユニット、SiO4/2はQユニットを、それぞれ表している。a1、b1、c1およびd1は、それぞれが0以上の整数であり、かつ、a1+b1+c1+d1≧3である。
式(14)において、R11、R12、R13は、好ましくは、炭素数1~10の炭化水素基であり、その具体例としては、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基などのアルキル基;ビニル基、アリル基、ブテニル基、ペンテニル基、ヘキセニル基などのアルケニル基;フェニル基、トリル基、キシリル基などのアリール基;ベンジル基、フェネチル基などのアラルキル基;クロロメチル基、3-クロロプロピル基、3,3,3-トリフルオロプロピル基、ノナフルオロブチルエチル基などの置換アルキル基が挙げられる。
式(14)において、エポキシ基を含む有機基としては、2,3-エポキシプロピル基、3,4-エポキシブチル基、4,5-エポキシペンチル基などのエポキシアルキル基;2-グリシドキシエチル基、3-グリシドキシプロピル基、4-グリシドキシブチル基などのグリシドキシアルキル基;β-(または2-)(3,4-エポキシシクロヘキシル)エチル基、γ-(または3-)(3,4-エポキシシクロヘキシル)プロピル基などのエポキシシクロヘキシルアルキル基が例示される。
式(14)においてe1は0以上の整数であり、ケイ素原子に直接結合する水酸基(シラノール)の個数を表している。
式(14)においてe1は0以上の整数であり、ケイ素原子に直接結合する水酸基(シラノール)の個数を表している。
エポキシ化合物は、ケイ素原子に結合する加水分解性基を有するものであって、該加水分解性基を加水分解したときに、式(14)で表されるオルガノポリシロキサン(ただし、e1≧1)を生じる化合物であってもよい。換言すれば、式(14)で表されるオルガノポリシロキサン(ただし、e1≧1)において、ケイ素原子に直接結合した水酸基の全部または一部を加水分解性基に置き換えた化合物であってもよい。
ここで、加水分解性基とは、加水分解によってケイ素原子に結合した水酸基(シラノール)を生じる基であり、具体例としては、ヒドロキシ基、アルコキシ基、水素、アセトキシ基、エノキシ基、オキシム基、ハロゲン基が挙げられる。好ましい加水分解性基はアルコキシ基であり、特に炭素数1~3のアルコキシ基、すなわち、メトキシ基、エトキシ基、プロポキシ基である。
上記式(14)で表されるオルガノポリシロキサン型のエポキシ化合物は、例えば、次の方法で製造することができる。
(方法1)エポキシ基を有するシラン化合物と、エポキシ基を有しないシラン化合物および/またはそのオリゴマーとを、共加水分解および重縮合させる方法。
(方法2)ヒドロシリル基を有するポリシロキサンに、エポキシ基と炭素-炭素二重結合基を有する有機化合物を付加させる方法。
(方法3)炭素-炭素二重結合を含む有機基を有するポリシロキサンの該二重結合部分を酸化させて、エポキシ基に変換する方法。
上記方法1でポリシロキサン型のエポキシ化合物を製造する際に用いることのできる原料は次の通りである。
(方法1)エポキシ基を有するシラン化合物と、エポキシ基を有しないシラン化合物および/またはそのオリゴマーとを、共加水分解および重縮合させる方法。
(方法2)ヒドロシリル基を有するポリシロキサンに、エポキシ基と炭素-炭素二重結合基を有する有機化合物を付加させる方法。
(方法3)炭素-炭素二重結合を含む有機基を有するポリシロキサンの該二重結合部分を酸化させて、エポキシ基に変換する方法。
上記方法1でポリシロキサン型のエポキシ化合物を製造する際に用いることのできる原料は次の通りである。
Mユニットを導入するための原料としては、トリメチルメトキシシラン、トリメチルエトキシシラン、トリフェニルメトキシシラン、トリフェニルシラノールなどが例示される。
Dユニットを導入するための原料としては、ジメチルジメトキシシラン、メチルフェニルジメトキシシラン、メチルビニルジメトキシシラン、ジフェニルジメトキシシラン、ジメチルジエトキシシラン、メチルフェニルジエトキシシランおよびこれらの加水分解縮合物(オリゴマー)が例示される。
両末端に水酸基を有するジアルキルシロキサンオリゴマーとして、ポリジメチルシロキサン、ポリメチルフェニルシロキサン、ジメチルシロキサン-ジフェニルシロキサン共重合体、ポリジフェニルシロキサンなどの両末端をシラノール変性した化合物が市販されている。
Tユニットを導入するための原料としては、メチルトリメトキシシラン、メチルトリエトキシシラン、エチルトリメトキシシラン、エチルトリエトキシシラン、ビニルトリメトキシシラン、フェニルトリメトキシシラン、3,3,3-トリフルオロプロピルトリメトキシシランおよびこれらの加水分解縮合物が例示される。
Qユニットを導入するための原料としては、テトラメトキシシラン、テトラエトキシシラン、テトラプロポキシシランおよびこれらの加水分解縮合物が例示される。
エポキシ基を導入するための原料としては、γ-グリシドキシプロピルトリメトキシシラン、γ-グリシドキシプロピルトリエトキシシラン、2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン、2-(3,4-エポキシシクロヘキシル)エチルトリエトキシシラン、(γ-グリシドキシプロピル)(メチル)ジメトキシシラン、(γ-グリシドキシプロピル)( エチル)ジメトキシシラン、(γ-グリシドキシプロピル)(メチル)ジエトキシシラン、(γ-グリシドキシプロピル)(エチル)ジエトキシシラン、〔2-(3,4-エポキシシクロヘキシルエチル〕(メチル)ジメトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エチル)ジメトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メチル)ジエトキシシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エチル)ジエトキシシラン、(γ-グリシドキシプロピル)(メトキシ)ジメチルシラン、(γ-グリシドキシプロピル)(メトキシ)ジエチルシラン、(γ-グリシドキシプロピル)(エトキシ)ジメチルシラン、(γ-グリシドキシプロピル)(エトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メトキシ)ジメチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(メトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エトキシ)ジメチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(エトキシ)ジエチルシラン、〔2-(3,4-エポキシシクロヘキシル)エチル〕(ジメチル)ジシロキサン、3-エポキシプロピル(フェニル)ジメトキシシランなどが例示される。
1.2(B)ガリウム化合物
ガリウム化合物は、後段で詳述するシラノール源化合物から供給されるシラノールと組み合わされて、エポキシ化合物の自己重合反応の触媒として作用する成分である。
ガリウム化合物は、後段で詳述するシラノール源化合物から供給されるシラノールと組み合わされて、エポキシ化合物の自己重合反応の触媒として作用する成分である。
ガリウム化合物は上記作用を示すものであればよく、次の候補化合物から選択することができる:キレート配位子を有するガリウム錯体、酢酸ガリウム、オキシ酢酸ガリウム、トリエトキシガリウム、トリス(8-キノリノラト)ガリウム、シュウ酸ガリウム、エチルキサントゲン酸ガリウム、ジエチルエトキシガリウム、マレイン酸ガリウム等。n-オクチル酸、2-エチルヘキサン酸、ナフテン酸などの長鎖カルボン酸のガリウム塩等。
キレート配位子としては、β-ジケトン型化合物と、o-ケトフェノール型化合物が挙げられる。β-ジケトン型化合物には、次の式(15)~式(17)に示す構造を有するものがある。
式(15)の化合物の具体例としてはアセチルアセトン、トリフルオロアセチルアセトン、ペンタフルオロアセチルアセトン、ヘキサフルオロアセチルアセトン等が、式(16)の化合物の具体例としてはエチルアセトアセテート等が、式(17)の化合物の具体例としてはジエチルマロネート等が挙げられる。
O-ケトフェノール型化合物は、次の式(18)で表される化合物である。
O-ケトフェノール型化合物は、次の式(18)で表される化合物である。
式(18)の化合物の具体例としては、サリチルアルデヒド、エチル-O-ヒドロキシフェニルケトン等が挙げられる。
キレート配位子を有するガリウム錯体はガリウム化合物の好適例であり、その中でもガリウムアセチルアセトネートは特に好適に使用することができる。
Ga触媒を用いるとAl触媒に比べて硬化物の加熱による重量減少が少ない。特に硬化物がシロキサン構造を含む場合にはAl触媒に比べて硬化物の加熱による重量減少が少ない。
具体的には、150~200℃×500時間で、重量減少が加熱前の20質量%以下が好ましく、10質量%以下が更に好ましい。
(B)ガリウム化合物は、(A)エポキシ化合物100重量部に対して通常0.001重量部以上、好ましくは0.01重量部以上、また5.0重量部以下、好ましくは1.0重量部以下である。
1.3(C)シラノール源化合物
シラノール源化合物はシラノールの供給源たる化合物である。シラノールは、前述のガリウム化合物と組み合わされて、エポキシ化合物の自己重合反応の触媒として作用する。
シラノール源化合物はシラノールの供給源たる化合物である。シラノールは、前述のガリウム化合物と組み合わされて、エポキシ化合物の自己重合反応の触媒として作用する。
シラノールの役割は、エポキシ化合物の自己重合反応の開始に必要なカチオン源であると考えられる。シラノール源化合物のケイ素原子にフェニル基等の芳香族基が結合している場合には、この芳香族基はシラノール水酸基の酸性度を高める働き、つまり、シラノールのカチオン源としての作用を強める働きをしていると考えられる。
シラノール源化合物は、潜在的なシラノール源であってもよい。例えば、加水分解性基が結合したケイ素原子を有しており、該加水分解基が加水分解されたときにシラノールを生じる化合物である。加水分解性基の具体例としては、ヒドロキシ基、アルコキシ基、水素、アセトキシ基、エノキシ基、オキシム基、ハロゲン基が挙げられる。好ましい加水分解性基はアルコキシ基であり、特に炭素数1~3のアルコキシ基、すなわち、メトキシ基、エトキシ基、プロポキシ基である。
シラノール源化合物の一例は、フェニルジメチルシラノール、ジフェニルメチルシラノール、トリフェニルシラノール、ジヒドロキシジフェニルシラン(ジフェニルジシラノール)、トリメチルシラノール、トリエチルシラノール、ジヒドロキシジメチルシラン、トリヒドロキシメチルシランなどの水酸基が結合したケイ素原子を有するモノシラン化合物である。
シラノール源化合物の他の一例は、水酸基が結合したケイ素原子を有する、式(19)で表されるオルガノポリシロキサンである。
(R21 3SiO1/2)a2(R22 2SiO2/2)b2(R23SiO3/2)c2(SiO4/2)d2(O1/2H)e2 ・・・(19)
式(19)において、R21、R22、R23はそれぞれ独立して1価の有機基を示す。
シラノール源化合物の他の一例は、水酸基が結合したケイ素原子を有する、式(19)で表されるオルガノポリシロキサンである。
(R21 3SiO1/2)a2(R22 2SiO2/2)b2(R23SiO3/2)c2(SiO4/2)d2(O1/2H)e2 ・・・(19)
式(19)において、R21、R22、R23はそれぞれ独立して1価の有機基を示す。
式(19)において、R21
3SiO1/2はMユニット、R22
2SiO2/2はDユニット、R23SiO3/2はTユニット、SiO4/2はQユニットを、それぞれ表している。a2、b2、c2およびd2は、それぞれが0以上の整数であり、かつ、a2+b2+c2+d2≧3である。e2は1以上の自然数であり、ケイ素原子に直接結合する水酸基(シラノール)の個数を表している。
式(19)のR21、R22、R23は、通常、炭素数1~10の炭化水素基であり、その具体例としては、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基などのアルキル基;ビニル基、アリル基、ブテニル基、ペンテニル基、ヘキセニル基などのアルケニル基;フェニル基、トリル基、キシリル基などのアリール基;ベンジル基、フェネチル基などのアラルキル基;クロロメチル基、3-クロロプロピル基、3,3,3-トリフルオロプロピル基、ノナフルオロブチルエチル基などの置換アルキル基が挙げられる。
シラノール源化合物は、ケイ素原子に結合する加水分解性基を有するものであって、該加水分解性基を加水分解したときに、式(19)で表されるオルガノポリシロキサンを生じる化合物であってもよい。換言すれば、式(19)で表されるオルガノポリシロキサンにおいて、ケイ素原子に直接結合した水酸基の全部または一部を加水分解性基に置き換えた化合物であってもよい。
シラノール源化合物がオルガノポリシロキサンであって、これをシロキサン構造を含まないエポキシ化合物と共に用いる場合には、該オルガノポリシロキサンと該エポキシ化合物との相溶性を確保する観点から、該オルガノポリシロキサンはケイ素原子に結合した芳香族基を有するものであることが好ましい。
シラノール源化合物がオルガノポリシロキサンである場合、その重量平均分子量については、熱硬化性樹脂組成物の硬化中あるいは硬化後に揮発しないように、500以上であることが好ましく、700以上であることがより好ましい。一方、重合度が高過ぎると粘度が高くなって取り扱い性が悪くなることから、該重量平均分子量は20,000以下であることが好ましく、15,000以下であることがより好ましい。
好適な実施形態では、シラノール源化合物は水酸基または加水分解性基が結合したケイ素原子を1分子中に2個以上有するオルガノポリシロキサンまたはシラン化合物であってもよい。かかるシラノール源化合物は、加熱されたときにガリウム化合物の作用により重縮合して高分子量化するので、硬化後にブリードアウトすることがない。
シラノール源化合物として好適に使用できるオルガノポリシロキサンとして、上記式(2)、式(20)~式(23)で表される構造を有するものが挙げられる。
式(22)で表されるオルガノポリシロキサンは、式(2)で表される化合物と式(24)で表される化合物(ジヒドロキシジメチルシランまたは両末端に水酸基を有するポリジメチルシロキサン)とを、重縮合することにより得ることができる。重縮合触媒としては、酸、塩基の他、金属触媒を用いることができ、ガリウムアセトアセトネートのようなガリウム化合物を用いることもできる。
式(23)で表されるオルガノポリシロキサンは、式(21)で表される化合物と式(24)で表される化合物とを、重縮合することにより得ることができる。重縮合触媒としては、酸、塩基の他、金属触媒を用いることができ、ガリウムアセトアセトネートのようなガリウム化合物を用いることもできる。
式(20)~式(24)において、m、n、M、N、m1、m2は、それぞれ、1以上の整数である。これらの数を大きくし過ぎた場合、すなわちポリシロキサンの重合度を高くし過ぎた場合、粘度が高くなり過ぎてハンドリングが容易でなくなる他、シラノールの含有率が下がるために触媒能が低下する傾向が生じることに注意すべきである。ハンドリング性の観点からは、当該オルガノポリシロキサンの粘度あるいは当該オルガノポリシロキサンを用いて得られる熱硬化性樹脂組成物の粘度が10000mPa・s以下、特に5000mPa・s以下となるように、その重合度を設定することが好ましい。
式(2)、式(20)~式(23)で表されるオルガノポリシロキサンから選ばれる1種以上を、メチルトリメトキシシラン、フェニルトリメトキシシランなどの3官能シラン化合物とともに重縮合させて得られるオルガノポリシロキサンも、(C)シラノール源化合物の好適例である。重縮合触媒としては、酸、塩基の他、金属触媒を用いることができ、ガリウムアセトアセトネートのようなガリウム化合物を用いることもできる。かかるオルガノポリシロキサンは、更に酸、塩基またはガリウム化合物などの金属化合物のような縮合触媒を作用させることにより硬化する性質を有する。シラノール源として、モノシラン化合物とオルガノポリシロキサンを併せて用いてもよい。
(C)シラノール源化合物は、(A)エポキシ化合物100重量部に対して通常0.05重量部以上、好ましくは0.5重量部以上、また500重量部以下、好ましくは200重量部以下である。
また、(B)ガリウム化合物と(C)シラノール源化合物の含有比は重量比で1:0.05~0.001:100が好ましく、より好ましくは1:10~0.01:100である。
また、(B)ガリウム化合物と(C)シラノール源化合物の含有比は重量比で1:0.05~0.001:100が好ましく、より好ましくは1:10~0.01:100である。
1.4 エポキシシリコーン樹脂
本発明の実施形態に係る熱硬化性樹脂組成物においては、エポキシ化合物とシラノール源化合物のいずれか一方、または両方が、オルガノポリシロキサン構造部分を有し得る。その場合に、オルガノポリシロキサン構造部分にシラノールを導入すると、ガリウム化合物がシラノール間の脱水縮合触媒として作用するので、エポキシ化合物の自己重合反応とシラノール縮合反応の両方が硬化に関与する、耐熱性の良好な熱硬化性樹脂組成物が得られる。ガリウム化合物はシラノールとアルコキシ基の間の脱アルコール縮合反応の触媒にもなるので、オルガノポリシロキサン構造部分にシラノールとアルコキシ基を導入した場合も同様の効果が得られる。
本発明の実施形態に係る熱硬化性樹脂組成物においては、エポキシ化合物とシラノール源化合物のいずれか一方、または両方が、オルガノポリシロキサン構造部分を有し得る。その場合に、オルガノポリシロキサン構造部分にシラノールを導入すると、ガリウム化合物がシラノール間の脱水縮合触媒として作用するので、エポキシ化合物の自己重合反応とシラノール縮合反応の両方が硬化に関与する、耐熱性の良好な熱硬化性樹脂組成物が得られる。ガリウム化合物はシラノールとアルコキシ基の間の脱アルコール縮合反応の触媒にもなるので、オルガノポリシロキサン構造部分にシラノールとアルコキシ基を導入した場合も同様の効果が得られる。
他の一例では、エポキシ化合物が有するオルガノポリシロキサン構造部分とシラノール源化合物が有するオルガノポリシロキサン構造部分の一方にヒドロシリル基、他方にビニルシリル基を導入するとともに、白金化合物のようなヒドロシリル化反応触媒を添加することにより、エポキシ化合物の自己重合反応とヒドロシリル化反応の両方が硬化に関与する、硬化性の良好な熱硬化性樹脂組成物が得られる。
あるいは、エポキシ化合物とシラノール源化合物のいずれか一方または両方が有するオルガノポリシロキサン構造部分にヒドロシリル基を導入するとともに、ビニルシリル基を有するオルガノポリシロキサンとヒドロシリル化反応触媒を添加することによっても、エポキシ化合物の自己重合反応とヒドロシリル化反応の両方が硬化に関与する熱硬化性樹脂組成物が得られる。この例を変形して、エポキシ化合物とシラノール源化合物のいずれか一方または両方が有するオルガノポリシロキサン構造部分にビニルシリル基を導入し、添加するオルガノポリシロキサンをヒドロシリル基が導入されたものとしてもよい。
1.5 その他の成分
本発明の実施形態に係る熱硬化性樹脂組成物には、上述の成分の他に、物性改善、機能付与等の観点から、分散剤、酸化防止剤、消泡剤、着色剤、変性剤、レベリング剤、光拡散剤、熱伝導性、難燃剤、反応性または非反応性の希釈剤、接着、密着性向上剤等の添加剤または各種フィラーをさらに含有してもよい。
本発明の実施形態に係る熱硬化性樹脂組成物には、上述の成分の他に、物性改善、機能付与等の観点から、分散剤、酸化防止剤、消泡剤、着色剤、変性剤、レベリング剤、光拡散剤、熱伝導性、難燃剤、反応性または非反応性の希釈剤、接着、密着性向上剤等の添加剤または各種フィラーをさらに含有してもよい。
1.5.1 フィラー
フィラーとしては、一般的な有機フィラー、無機フィラーのいずれも使用することができる。有機フィラーとしては、スチレン系ポリマー粒子、メタクリレート系ポリマー粒子、エチレン系ポリマー粒子、プロピレン系ポリマー粒子、ポリアミド系等の合成ポリマー粒子、デンプン、木粉等の天然物、変性されていてもよいセルロース、各種有機顔料などが挙げられる。無機フィラーとしては、無機物もしくは無機物を含む化合物であれば特に限定されないが、具体的に例えば、石英、ヒュームドシリカ、沈降性シリカ、無水ケイ酸、溶融シリカ、結晶性シリカ、超微粉無定型シリカ等のシリカ系無機フィラー、アルミナ、ジルコン、酸化鉄、酸化亜鉛、酸化チタン、窒化ケイ素、窒化ホウ素、窒化アルミ、炭化ケイ素、ガラス繊維、ガラスフレーク、アルミナ繊維、炭素繊維、マイカ、黒鉛、カーボンブラック、フェライト、グラファイト、ケイソウ土、白土、クレー、タルク、水酸化アルミニウム、炭酸カルシウム、炭酸マンガン、炭酸マグネシウム、硫酸バリウム、チタン酸カリウム、ケイ酸カルシウム、無機バルーン、銀粉等を挙げることができる。
フィラーとしては、一般的な有機フィラー、無機フィラーのいずれも使用することができる。有機フィラーとしては、スチレン系ポリマー粒子、メタクリレート系ポリマー粒子、エチレン系ポリマー粒子、プロピレン系ポリマー粒子、ポリアミド系等の合成ポリマー粒子、デンプン、木粉等の天然物、変性されていてもよいセルロース、各種有機顔料などが挙げられる。無機フィラーとしては、無機物もしくは無機物を含む化合物であれば特に限定されないが、具体的に例えば、石英、ヒュームドシリカ、沈降性シリカ、無水ケイ酸、溶融シリカ、結晶性シリカ、超微粉無定型シリカ等のシリカ系無機フィラー、アルミナ、ジルコン、酸化鉄、酸化亜鉛、酸化チタン、窒化ケイ素、窒化ホウ素、窒化アルミ、炭化ケイ素、ガラス繊維、ガラスフレーク、アルミナ繊維、炭素繊維、マイカ、黒鉛、カーボンブラック、フェライト、グラファイト、ケイソウ土、白土、クレー、タルク、水酸化アルミニウム、炭酸カルシウム、炭酸マンガン、炭酸マグネシウム、硫酸バリウム、チタン酸カリウム、ケイ酸カルシウム、無機バルーン、銀粉等を挙げることができる。
これらは、単独で用いてもよく、2種類以上併用してもよい。また、適宜表面処理をほどこしてもよい。表面処理としては、アルキル化処理、トリメチルシリル化処理、シリコーン処理、シランカップリング剤による処理等が挙げられるが、特に限定されるものではない。
フィラーの添加量は特に限定されない。
フィラーの添加量は特に限定されない。
フィラーを用いることにより、得られる成形体の強度、硬度、弾性率、熱膨張率、熱伝導率、放熱性、電気的特性、光の反射率、難燃性、耐火性、チキソトロピー性、およびガスバリア性等の諸物性を改善することができる。
フィラーの混合の順序としては、特に限定されないが、混合時の発熱による硬化反応の進行を防ぐため、ガリウム化合物、シラノール源化合物、その他のエポキシ樹脂硬化に使用される触媒の非存在下でエポキシ化合物と混合することが望ましい。
フィラーを混合する手段としては、特に限定されるものではないが、具体的に例えば、2本ロールあるいは3本ロール、遊星式撹拌脱泡装置、ホモジナイザー、ディゾルバー、プラネタリーミキサー等の撹拌機、プラストミル等の溶融混練機等が挙げられる。混合は、常温で行ってもよいし加熱して行ってもよく、また、常圧下で行ってもよいし減圧状態で行ってもよい。混合する際の温度が高いと、成型する前に組成物が硬化する場合がある。
本樹脂組成物を封止材として使用する場合、隣接する部材との間に生じる熱膨張率差を抑えることを主目的として、無機フィラー、特に、シリカ微粒子を添加することがある。添加量を増やすことでより高い効果が得られ、エポキシ樹脂100重量部に対し、40重量部以上、好ましくは70重量部以上、さらに好ましくは80重量部以上の添加が望ましい。添加量を増やす手段として、粒径分布の制御がよく用いられる。粒径の異なるフィラーを混合することで、より高い充填率が得られる。
また、添加量が増加すると、組成物の粘度上昇が顕著になる。用途、成型法によっては、粘度上昇を抑制する必要があるが、その場合、フィラーの形状、表面構造が大きく影響する。形状は、繊維状、不定形のものよりも、球状のものを選択することで、粘度を低く抑えることが出来る。また、粒子表面官能基の種類、量により、粒子間および粒子-エポキシ樹脂等からなるマトリックス組成物間の相互作用を制御し、適当な粘度を得ることが出来る。
1.5.2 酸化防止剤
本発明の実施形態に係る熱硬化性樹脂組成物には、使用環境下での黄変を抑制するために、酸化防止剤を含有させることができる。
本発明の実施形態に係る熱硬化性樹脂組成物には、使用環境下での黄変を抑制するために、酸化防止剤を含有させることができる。
フェノール系酸化防止剤、リン系酸化防止剤、ヒンダードアミン系等が好適に用いられるが、なかでも、フェノール水酸基の片側あるいは両側のオルト位にアルキル基を有するヒンダードフェノール系酸化防止剤が特に好適に用いられる。
1.5.3 エポキシ樹脂の硬化触媒
ガリウム化合物と、シラノール源化合物から供給されるシラノールの触媒作用を阻害しない限りにおいて、通常のエポキシ樹脂硬化に使用される触媒を併用することができる。例えば、ベンジルジメチルアミン、2,4,6-トリス(ジメチルアミノメチル)フェノール、シクロヘキシルジメチルアミン、トリエタノールアミン等の3級アミン類;2-メチルイミダゾール、2-n-ヘプチルイミダゾール、2-n-ウンデシルイミダゾール、2-フェニルイミダゾール、2-フェニル-4-メチルイミダゾール、1-ベンジル-2-メチルイミダゾール、1-ベンジル-2-フェニルイミダゾール、1,2-ジメチルイミダゾール、2-エチル-4-メチルイミダゾール、1-(2-シアノエチル)-2-メチルイミダゾール、1-(2-シアノエチル)-2-n-ウンデシルイミダゾール、1-(2-シアノエチル)-2-フェニルイミダゾール、1-(2-シアノエチル)-2-エチル-4-メチルイミダゾール、2-フェニル-4-メチル-5-ヒドロキシメチルイミダゾール、2-フェニル-4,5-ジ(ヒドロキシメチル)イミダゾール、1-(2-シアノエチル)-2-フェニル-4,5-ジ〔(2’-シアノエトキシ)メチル〕イミダゾール、1-(2-シアノエチル)-2-n-ウンデシルイミダゾリウムトリメリテート、1-(2-シアノエチル)-2-フェニルイミダゾリウムトリメリテート、1-(2-シアノエチル)-2-エチル-4-メチルイミダゾリウムトリメリテート、2,4-ジアミノ-6-〔2 ’-メチルイミダゾリル-(1’)〕エチル-s-トリアジン、2,4-ジアミノ-6-(2 ’-n-ウンデシルイミダゾリル)エチル-s-トリアジン、2,4-ジアミノ-6-〔2’-エチル-4’-メチルイミダゾリル-(1’)〕エチル-s-トリアジン、2-メチルイミダゾールのイソシアヌル酸付加物、2-フェニルイミダゾールのイソシアヌル酸付加物、2,4-ジアミノ-6-〔2’-メチルイミダゾリル-(1’)〕エチル-s-トリアジンのイソシアヌル酸付加物等のイミダゾール類;ジフェニルフォスフィン、トリフェニルフォスフィン、亜リン酸トリフェニル等の有機リン系化合物;ベンジルトリフェニルフォスフォニウムクロライド、テトラ-n-ブチルフォスフォニウムブロマイド、メチルトリフェニルフォスフォニウムブロマイド、エチルトリフェニルフォスフォニウムブロマイド、n-ブチルトリフェニルフォスフォニウムブロマイド、テトラフェニルフォスフォニウムブロマイド、エチルトリフェニルフォスフォニウムヨーダイド、エチルトリフェニルフォスフォニウムアセテート、メチルトリブチルホスホニウムジメチルホスフェート、テトラブチルホスホニウムジエチルホスホジチオネート、テトラ-n-ブチルフォスフォニウムベンゾトリアゾレート、テトラ-n-ブチルフォスフォニウムテトラフルオロボレート、テトラ-n-ブチルフォスフォニウムテトラフェニルボレート、テトラフェニルフォスフォニウムテトラフェニルボレート等の4級フォスフォニウム塩類;1,8-ジアザビシクロ[5.4.0]ウンデセン-7やその有機酸塩等のジアザビシクロアルケン類;オクチル酸亜鉛、アクチル酸錫、アルミニウムアセチルアセトン錯体等の有機金属化合物;テトラエチルアンモニウムブロマイド、テトラ-n-ブチルアンモニウムブロマイド等の4級アンモニウム塩類;三フッ化ホウ素、ホウ酸トリフェニル等のホウ素化合物;塩化亜鉛、塩化第二錫等の金属ハロゲン化合物のほか、ジシアンジアミドやアミンとエポキシ樹脂との付加物等のアミン付加型促進剤等の高融点分散型潜在性硬化促進剤;前記イミダゾール類、有機リン系化合物や4級フォスフォニウム塩類等の硬化促進剤の表面をポリマーで被覆したマイクロカプセル型潜在性硬化促進剤;アミン塩型潜在性硬化剤促進剤;ガリウム化合物以外のルイス酸塩、ブレンステッド酸塩等の高温解離型の熱カチオン重合型潜在性硬化促進剤等の潜在性硬化促進剤等を挙げることができる。
ガリウム化合物と、シラノール源化合物から供給されるシラノールの触媒作用を阻害しない限りにおいて、通常のエポキシ樹脂硬化に使用される触媒を併用することができる。例えば、ベンジルジメチルアミン、2,4,6-トリス(ジメチルアミノメチル)フェノール、シクロヘキシルジメチルアミン、トリエタノールアミン等の3級アミン類;2-メチルイミダゾール、2-n-ヘプチルイミダゾール、2-n-ウンデシルイミダゾール、2-フェニルイミダゾール、2-フェニル-4-メチルイミダゾール、1-ベンジル-2-メチルイミダゾール、1-ベンジル-2-フェニルイミダゾール、1,2-ジメチルイミダゾール、2-エチル-4-メチルイミダゾール、1-(2-シアノエチル)-2-メチルイミダゾール、1-(2-シアノエチル)-2-n-ウンデシルイミダゾール、1-(2-シアノエチル)-2-フェニルイミダゾール、1-(2-シアノエチル)-2-エチル-4-メチルイミダゾール、2-フェニル-4-メチル-5-ヒドロキシメチルイミダゾール、2-フェニル-4,5-ジ(ヒドロキシメチル)イミダゾール、1-(2-シアノエチル)-2-フェニル-4,5-ジ〔(2’-シアノエトキシ)メチル〕イミダゾール、1-(2-シアノエチル)-2-n-ウンデシルイミダゾリウムトリメリテート、1-(2-シアノエチル)-2-フェニルイミダゾリウムトリメリテート、1-(2-シアノエチル)-2-エチル-4-メチルイミダゾリウムトリメリテート、2,4-ジアミノ-6-〔2 ’-メチルイミダゾリル-(1’)〕エチル-s-トリアジン、2,4-ジアミノ-6-(2 ’-n-ウンデシルイミダゾリル)エチル-s-トリアジン、2,4-ジアミノ-6-〔2’-エチル-4’-メチルイミダゾリル-(1’)〕エチル-s-トリアジン、2-メチルイミダゾールのイソシアヌル酸付加物、2-フェニルイミダゾールのイソシアヌル酸付加物、2,4-ジアミノ-6-〔2’-メチルイミダゾリル-(1’)〕エチル-s-トリアジンのイソシアヌル酸付加物等のイミダゾール類;ジフェニルフォスフィン、トリフェニルフォスフィン、亜リン酸トリフェニル等の有機リン系化合物;ベンジルトリフェニルフォスフォニウムクロライド、テトラ-n-ブチルフォスフォニウムブロマイド、メチルトリフェニルフォスフォニウムブロマイド、エチルトリフェニルフォスフォニウムブロマイド、n-ブチルトリフェニルフォスフォニウムブロマイド、テトラフェニルフォスフォニウムブロマイド、エチルトリフェニルフォスフォニウムヨーダイド、エチルトリフェニルフォスフォニウムアセテート、メチルトリブチルホスホニウムジメチルホスフェート、テトラブチルホスホニウムジエチルホスホジチオネート、テトラ-n-ブチルフォスフォニウムベンゾトリアゾレート、テトラ-n-ブチルフォスフォニウムテトラフルオロボレート、テトラ-n-ブチルフォスフォニウムテトラフェニルボレート、テトラフェニルフォスフォニウムテトラフェニルボレート等の4級フォスフォニウム塩類;1,8-ジアザビシクロ[5.4.0]ウンデセン-7やその有機酸塩等のジアザビシクロアルケン類;オクチル酸亜鉛、アクチル酸錫、アルミニウムアセチルアセトン錯体等の有機金属化合物;テトラエチルアンモニウムブロマイド、テトラ-n-ブチルアンモニウムブロマイド等の4級アンモニウム塩類;三フッ化ホウ素、ホウ酸トリフェニル等のホウ素化合物;塩化亜鉛、塩化第二錫等の金属ハロゲン化合物のほか、ジシアンジアミドやアミンとエポキシ樹脂との付加物等のアミン付加型促進剤等の高融点分散型潜在性硬化促進剤;前記イミダゾール類、有機リン系化合物や4級フォスフォニウム塩類等の硬化促進剤の表面をポリマーで被覆したマイクロカプセル型潜在性硬化促進剤;アミン塩型潜在性硬化剤促進剤;ガリウム化合物以外のルイス酸塩、ブレンステッド酸塩等の高温解離型の熱カチオン重合型潜在性硬化促進剤等の潜在性硬化促進剤等を挙げることができる。
1.5.4 酸無水物
本発明の実施形態に係る熱硬化性樹脂組成物には、硬化助剤として酸無水物を含有させることができる。酸無水物の種類に特に制限はないが、該樹脂組成物を光半導体デバイスに使用する場合には、耐光性の観点から脂環式カルボン酸無水物を使用することが好ましい。
本発明の実施形態に係る熱硬化性樹脂組成物には、硬化助剤として酸無水物を含有させることができる。酸無水物の種類に特に制限はないが、該樹脂組成物を光半導体デバイスに使用する場合には、耐光性の観点から脂環式カルボン酸無水物を使用することが好ましい。
脂環式カルボン酸無水物としては、例えば、式(25)~式(30)で表される化合物や、4-メチルテトラヒドロフタル酸無水物、メチルナジック酸無水物、ドデセニルコハク酸無水物のほか、α-テルピネン、アロオシメン等の共役二重結合を有する脂環式化合物と無水マレイン酸とのディールス・アルダー反応生成物やこれらの水素添加物等を挙げることができる。
また、前記脂環式カルボン酸無水物は、硬化反応を実質的に妨げない限り、適宜に化学的に変性して使用することもできる。
酸無水物を含有することで、エポキシ反応速度の制御、ハンドリング、レベリングの向上、着色防止等の効果が得られる場合がある。酸無水物の含有量としては特に制限はないが、エポキシ量に対して1.5当量以下であることが好ましい。より好ましくは1当量以下、更に好ましくは0.8当量以下である。
1.5.5 シランカップリング剤
本発明の熱硬化性樹脂組成物には、金属部品や無機フィラーに対する接着性を良好にするためにシランカップリング剤を含有させることができる。
本発明の熱硬化性樹脂組成物には、金属部品や無機フィラーに対する接着性を良好にするためにシランカップリング剤を含有させることができる。
具体例として、2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン、ビニルトリエトキシシラン、ビニルトリメトキシシラン、3-グリシドキシプロピルトリメトキシシラン、γ-メタクリロキシプロピルトリメトキシシラン、γ-アミノプロピルトリメトキシシラン、N-フェニル-3-アミノプロピルトリメトキシシラン等が挙げられる。
1.5.6 シラノールの縮合触媒
ガリウム化合物と、シラノール源化合物から供給されるシラノールの触媒作用によるエポキシの反応を阻害しない限りにおいて、通常のシラノール硬化に使用される触媒を併用することができる。
具体例として、脱水・脱アルコール縮合反応触媒が挙げられる。前記反応触媒には、有機金属錯体触媒、金属と有機酸の塩、ルイス酸・ルイス塩基触媒からなる群から選ばれる少なくとも1つを含有することが好ましい。脱水・脱アルコール縮合反応触媒に含まれる金属成分としては、Sn、Zn、Fe、Ti、Zr、Bi、Hf、Y、Al、B、Gaなどから選ばれる1以上を用いるのが好ましく、中でもSn、Ti、Al、Zn、Zr、Hf、Gaは反応活性が高いという点で好ましく、発光デバイス用部材として用いる場合に電極腐食や光吸収が少なく適度な触媒活性を有し、ジメチルポリシロキサン鎖の不要な切断劣化が起こりにくいZrやHfが特に好ましい。
ガリウム化合物と、シラノール源化合物から供給されるシラノールの触媒作用によるエポキシの反応を阻害しない限りにおいて、通常のシラノール硬化に使用される触媒を併用することができる。
具体例として、脱水・脱アルコール縮合反応触媒が挙げられる。前記反応触媒には、有機金属錯体触媒、金属と有機酸の塩、ルイス酸・ルイス塩基触媒からなる群から選ばれる少なくとも1つを含有することが好ましい。脱水・脱アルコール縮合反応触媒に含まれる金属成分としては、Sn、Zn、Fe、Ti、Zr、Bi、Hf、Y、Al、B、Gaなどから選ばれる1以上を用いるのが好ましく、中でもSn、Ti、Al、Zn、Zr、Hf、Gaは反応活性が高いという点で好ましく、発光デバイス用部材として用いる場合に電極腐食や光吸収が少なく適度な触媒活性を有し、ジメチルポリシロキサン鎖の不要な切断劣化が起こりにくいZrやHfが特に好ましい。
2.熱硬化性樹脂組成物の製造方法
本発明の実施形態に係る上記熱硬化性樹脂組成物は、上記成分(A)~(C)と、必要に応じてフィラー、希釈剤、酸化防止剤などのその他の成分を混合することにより製造することができる。
この熱硬化性樹脂組成物は、保存安定性を考慮して2液硬化型としてもよい。
本発明の実施形態に係る上記熱硬化性樹脂組成物は、上記成分(A)~(C)と、必要に応じてフィラー、希釈剤、酸化防止剤などのその他の成分を混合することにより製造することができる。
この熱硬化性樹脂組成物は、保存安定性を考慮して2液硬化型としてもよい。
2液硬化型とする場合は、例えば、A液をエポキシ化合物を含む液とし、B液をガリウム化合物とシラノール源化合物を含む液とすることができる。また、A液をエポキシ化合物とシラノール源化合物を含む液とし、B液をガリウム化合物を含む液とすることもできる。また、A液をエポキシ化合物とガリウム化合物を含む液とし、B液をシラノール源化合物を含む液とすることもできる。
3.熱硬化性樹脂組成物の硬化方法
本発明の実施形態に係る上記熱硬化性樹脂組成物を硬化させるために行う加熱の方法は、特に限定されるものではなく、例えば、熱風循環式加熱、赤外線加熱、高周波加熱等の従来公知の方法を採用することができる。
熱処理条件は、熱硬化性樹脂組成物を所望の硬化状態にすることができればよく、特に制限はない。
本発明の実施形態に係る上記熱硬化性樹脂組成物を硬化させるために行う加熱の方法は、特に限定されるものではなく、例えば、熱風循環式加熱、赤外線加熱、高周波加熱等の従来公知の方法を採用することができる。
熱処理条件は、熱硬化性樹脂組成物を所望の硬化状態にすることができればよく、特に制限はない。
4.熱硬化性樹脂組成物の用途
本発明の実施形態に係る上記熱硬化性樹脂組成物の用途は特に限定されず、LEDデバイスのような発光デバイスを含む各種の半導体デバイスに、封止材等として用いることができる。
本発明の実施形態に係る上記熱硬化性樹脂組成物の用途は特に限定されず、LEDデバイスのような発光デバイスを含む各種の半導体デバイスに、封止材等として用いることができる。
発光デバイスにおいては、例えば、半導体発光素子の封止材料、半導体発光素子をパッケージ、リードフレーム等に固定するための接着剤(ダイボンド剤)、パッケージを構成する構造材料、高反射コーティング材など、各種の用途に使用することができる。
用途に応じて、その他の成分を添加することができ、例えば、波長変換素子として用いる場合は蛍光体、フュームドシリカ、球状シリカなどを添加できる。ダイボンド剤として用いる場合は熱伝導剤、フュームドシリカなどを添加できる。パッケージ用の構造材料や高反射コーティング材として用いる場合はチタニア粒子やアルミナ粒子などを添加することができる。
LEDデバイスは、例えば図5に断面図を示す様に、LED素子1、樹脂成形体2、ボンディングワイヤ3、蛍光体を含有する封止材4、リードフレーム5から構成される。
LED素子1は、近紫外領域、紫領域または青領域の波長の光を発するInGaN系LEDである。
樹脂成形体2はリードフレーム5と共に成形されており、カップ型を呈している。
リードフレーム5は導電性の金属からなり、構造部材であると同時に、外部からLEDデバイスに供給される電流をLED素子1に伝える役割を果たす。
ボンディングワイヤ3は、LED素子1とリードフレームの一方側とを電気的に接続している。
LED素子1は、近紫外領域、紫領域または青領域の波長の光を発するInGaN系LEDである。
樹脂成形体2はリードフレーム5と共に成形されており、カップ型を呈している。
リードフレーム5は導電性の金属からなり、構造部材であると同時に、外部からLEDデバイスに供給される電流をLED素子1に伝える役割を果たす。
ボンディングワイヤ3は、LED素子1とリードフレームの一方側とを電気的に接続している。
LED素子1は導電性粒子の添加により導電性を付与されたダイボンド剤を用いてリードフレームの他方側に接着固定されたうえ、蛍光体を混合した封止材4により封止されている。
本発明の実施形態に係る熱硬化性樹脂組成物は、図5に示すLEDデバイスにおいて、樹脂成形体2、封止材4、およびダイボンド剤(図示せず)の材料として用いることができる。
以下、実施例により本発明を詳細に説明する。まず、熱硬化性樹脂組成物の硬化機構の同定を行った。
1.硬化機構の同定
ガリウム化合物およびシラノール源化合物の存在下でエポキシ化合物を加熱したときに生じる反応の同定を試みた。以下に詳細を記す。
ガリウム化合物およびシラノール源化合物の存在下でエポキシ化合物を加熱したときに生じる反応の同定を試みた。以下に詳細を記す。
1.1 材料
エポキシ化合物として、シクロヘキセンオキシド(和光純薬工業社製)を用いた。この化合物は単官能エポキシ化合物であり、重合したときに3次元架橋構造を形成しない。
ガリウム化合物としては、ガリウムアセチルアセトネートを用いた。
エポキシ化合物として、シクロヘキセンオキシド(和光純薬工業社製)を用いた。この化合物は単官能エポキシ化合物であり、重合したときに3次元架橋構造を形成しない。
ガリウム化合物としては、ガリウムアセチルアセトネートを用いた。
シラノールとしては、式(31)で表される、水酸基が結合しているケイ素原子を両末端に有する、ポリスチレン換算の重量平均分子量約900のポリメチルフェニルシロキサン(BLUESTARS SILICONES社製 FLD516:以下、SOL-1と称す)を用いた。
1.2 サンプル
下記のようにしてサンプル1~4を準備した。
5.03gのシクロヘキセンオキシドに0.59gのSOL-1を加え混合することによりサンプル1を得た。
下記のようにしてサンプル1~4を準備した。
5.03gのシクロヘキセンオキシドに0.59gのSOL-1を加え混合することによりサンプル1を得た。
シュレンク管を用いて、サンプル1(5.03gのシクロヘキセンオキシドと0.59gのSOL-1の混合物)を窒素気流下、120℃で7時間撹拌することによりサンプル2を得た。
シュレンク管を用いて、5.00gのシクロヘキセンオキシドに0.002gのガリウムアセチルアセトネート(Ga(acac)3)を加えた混合物を窒素気流下、120℃で7時間撹拌することによりサンプル3を得た。
0.047gのガリウムアセトアセトナートを2.36gのSOL-1に溶解して2.0%のGa(acac)3溶液を得た。
シュレンク管を用いて、5.02gのシクロヘキセンオキシドに、上述のGa(acac)3溶液0.104gと、0.498gのSOL-1を加えた混合物を窒素気流下、120℃で7時間撹拌することによりサンプル4を得た。
シュレンク管を用いて、5.02gのシクロヘキセンオキシドに、上述のGa(acac)3溶液0.104gと、0.498gのSOL-1を加えた混合物を窒素気流下、120℃で7時間撹拌することによりサンプル4を得た。
サンプル4におけるSOL-1の含有量はサンプル1および2と同じく、シクロヘキセンオキシド100重量部に対して12重量部である。また、サンプル4におけるGa(acac)3の含有量はサンプル3と同じく、シクロヘキセンオキシド100重量部に対して0.04重量部である。
1.3 測定
サンプル1~4のそれぞれについて、1H-NMR分光法を用いてエポキシ基の反応率を評価するとともに、GPC(ゲル浸透クロマトグラフィ)によりシクロヘキセンオキシドの重合体が含有されるか否かを調べた。
サンプル1~4のそれぞれについて、1H-NMR分光法を用いてエポキシ基の反応率を評価するとともに、GPC(ゲル浸透クロマトグラフィ)によりシクロヘキセンオキシドの重合体が含有されるか否かを調べた。
1H-NMRスペクトルの測定はブルカーバイオスピン(株)製AVANCE400を用いて、磁場400MHz、温度25℃という条件で行った。溶媒には重クロロホルムを用い、試料濃度は約5wt%とした。基準物質にはテトラメチルシランを用いた。
1.4 1H-NMR分光分析結果
サンプル1~4の1H-NMRスペクトルを、図1~4にそれぞれ示す。
1.4 1H-NMR分光分析結果
サンプル1~4の1H-NMRスペクトルを、図1~4にそれぞれ示す。
シクロヘキセンオキシドのエポキシメチン基に由来する3.1ppmのシグナル、および、シクロヘキセンオキシドのメチレン基に由来する1~2ppmのシグナル群は、4つのサンプルの全てで観測された。
サンプル1、2および4では、SOL-1のメチル基に由来する0~0.4ppmのシグナル、および、SOL-1のフェニル基に由来する7.0~7.6ppmのシグナルが観測された。
サンプル4では3.4ppmにオキシメチン基に由来するシグナルが観測された。3.1ppmのシグナルと3.4ppmのシグナルの積分強度比から、シクロヘキセンオキシドのエポキシ基の反応率(エポキシメチンからオキシメチンへの転化率)は38%と見積もられた。
1.5 GPC結果
サンプル1および2ではGPCチャートにシクロヘキセンオキシド単量体のピークとSOL-1のピークが現れた。また、サンプル3ではシクロヘキセンオキシド単量体のピークのみが観察された。
一方、サンプル4ではGPCチャートにシクロヘキセンオキシドの重合体のピークが観測され、その重量平均分子量(Mw)は1800であった。
サンプル1および2ではGPCチャートにシクロヘキセンオキシド単量体のピークとSOL-1のピークが現れた。また、サンプル3ではシクロヘキセンオキシド単量体のピークのみが観察された。
一方、サンプル4ではGPCチャートにシクロヘキセンオキシドの重合体のピークが観測され、その重量平均分子量(Mw)は1800であった。
1.6 考察
GPC結果は、ガリウムアセチルアセトネートおよびSOL-1の存在下で加熱処理を行ったサンプル4においてのみ、シクロヘキセンオキシドの重合が起こったことを示している。そして、1H-NMRスペクトルにオキシメチン基に由来するシグナル(3.4ppm)が観測されたのは、そのサンプル4のみであった。このことは、ガリウムアセチルアセトネートおよびSOL-1の存在下で生じたシクロヘキセンオキシドの重合反応が、エポキシ基の開環を伴う自己重合反応であった可能性が高いことを示している。
GPC結果は、ガリウムアセチルアセトネートおよびSOL-1の存在下で加熱処理を行ったサンプル4においてのみ、シクロヘキセンオキシドの重合が起こったことを示している。そして、1H-NMRスペクトルにオキシメチン基に由来するシグナル(3.4ppm)が観測されたのは、そのサンプル4のみであった。このことは、ガリウムアセチルアセトネートおよびSOL-1の存在下で生じたシクロヘキセンオキシドの重合反応が、エポキシ基の開環を伴う自己重合反応であった可能性が高いことを示している。
[実施例1~4、比較例1~3]
1.硬化性の評価
1.1 材料
この実験では以下に記す材料を使用した。
<2官能エポキシ化合物>
2官能エポキシ化合物として、式(32)で表される構造を有する3,4-エポキシシクロヘキシルメチル‐3’,4’-エポキシシクロヘキサンカルボキシレート[(株)ダイセル製 CEL2021P]を用いた(以下ではこの化合物をEPC-1と略して呼ぶ)。
1.硬化性の評価
1.1 材料
この実験では以下に記す材料を使用した。
<2官能エポキシ化合物>
2官能エポキシ化合物として、式(32)で表される構造を有する3,4-エポキシシクロヘキシルメチル‐3’,4’-エポキシシクロヘキサンカルボキシレート[(株)ダイセル製 CEL2021P]を用いた(以下ではこの化合物をEPC-1と略して呼ぶ)。
<ガリウム化合物>
ガリウム化合物としては、3価ガリウムのアセチルアセトン錯体であるガリウムアセチルアセトネート(Strem Chemicals, Inc.製)を用いた。この化合物は、ガリウムトリアセチルアセトネート、トリス(アセチルアセトナト)ガリウム、トリス(2,4-ペンタンジオナト)ガリウムなどとも呼ばれることがある。また、Ga(acac)3と表記されることがある。
ガリウム化合物としては、3価ガリウムのアセチルアセトン錯体であるガリウムアセチルアセトネート(Strem Chemicals, Inc.製)を用いた。この化合物は、ガリウムトリアセチルアセトネート、トリス(アセチルアセトナト)ガリウム、トリス(2,4-ペンタンジオナト)ガリウムなどとも呼ばれることがある。また、Ga(acac)3と表記されることがある。
<シラノール>
3種類のシラノール化合物を用いた。
一番目のシラノール化合物は、式(33)で表される、水酸基が結合したケイ素原子を両末端に有する、ポリスチレン換算の重量平均分子量約900のポリメチルフェニルシロキサン(BLUESTAR SILICONES社製 FLD516)である(以下ではこの化合物をSOL-1と略して呼ぶ)。
3種類のシラノール化合物を用いた。
一番目のシラノール化合物は、式(33)で表される、水酸基が結合したケイ素原子を両末端に有する、ポリスチレン換算の重量平均分子量約900のポリメチルフェニルシロキサン(BLUESTAR SILICONES社製 FLD516)である(以下ではこの化合物をSOL-1と略して呼ぶ)。
二番目のシラノール化合物は、ジヒドロキシジフェニルシラン[信越化学工業(株)製 LS-4320]である(以下ではこの化合物をSOL-2と略して呼ぶ)。
三番目のシラノール化合物は、式(34)で表される、水酸基が結合したケイ素原子を両末端に有する、ポリスチレン換算の重量平均分子量約500のポリジメチルシロキサン[モメンティブ・パフォーマンス・マテリアルズ・ジャパン(同)製 XC96-723]である(以下ではこの化合物をSOL-3と略して呼ぶ)。
なお、表1において、Ga(acac)3溶液とは、0.047gのガリウムアセチルアセトネートを2.36gのSOL-1に溶解して得た、2.0重量%のガリウムアセチルアセトネート溶液である。
組成物1及び2の調製時にはこのGa(acac)3溶液をEPC-1と混合したのに対し、組成物3~5の調製時には固体のガリウムアセチルアセトネートを直接EPC-1に溶解させた。なお、EPC-1の量を基準としたガリウムアセチルアセトネートの使用量は、組成物1~5のいずれにおいても同じである。
1.3 硬化性の評価
硬化性を評価するために、表1に示す7種類のエポキシ組成物に対して下記の熱処理を行いゲル化率を測定した。
ゲル化率については、EPC-1がTHF(テトラヒドロフラン)に対して高い溶解性を示すことから、熱処理後のエポキシ組成物に含まれるTHF不溶成分の重量比とすることにした。
熱処理およびゲル化率測定の手順は下記の通りである。
硬化性を評価するために、表1に示す7種類のエポキシ組成物に対して下記の熱処理を行いゲル化率を測定した。
ゲル化率については、EPC-1がTHF(テトラヒドロフラン)に対して高い溶解性を示すことから、熱処理後のエポキシ組成物に含まれるTHF不溶成分の重量比とすることにした。
熱処理およびゲル化率測定の手順は下記の通りである。
<熱処理>
約2gのエポキシ組成物を内径5cmのアルミカップに入れ、恒温槽中にて、まず120℃で30分間保持し、次いで150℃で150分間保持した。
約2gのエポキシ組成物を内径5cmのアルミカップに入れ、恒温槽中にて、まず120℃で30分間保持し、次いで150℃で150分間保持した。
<ゲル化率の測定>
上記熱処理後のエポキシ組成物1.0gに対し50gのTHF(テトラヒドロフラン)を加え、室温下で撹拌した。1時間の撹拌後、THFに溶解しなかった成分を吸引濾過によって回収し、80℃にて真空乾燥したうえでその重量を測定した。このTHF不溶成分の重量を、THFを加える前のエポキシ組成物の重量(1.0g)で除算することにより、ゲル化率を算出した。
上記熱処理後のエポキシ組成物1.0gに対し50gのTHF(テトラヒドロフラン)を加え、室温下で撹拌した。1時間の撹拌後、THFに溶解しなかった成分を吸引濾過によって回収し、80℃にて真空乾燥したうえでその重量を測定した。このTHF不溶成分の重量を、THFを加える前のエポキシ組成物の重量(1.0g)で除算することにより、ゲル化率を算出した。
<熱処理後の流動性の評価>
エポキシ組成物が入ったアルミカップを恒温槽から取り出し、温度が室温まで下がったところで該アルミカップを約45度傾けたときに、内部のエポキシ組成物が流動した場合には「流動性あり」、流動しなかった場合には「流動性なし」と判定した。
結果は表2に示す。
エポキシ組成物が入ったアルミカップを恒温槽から取り出し、温度が室温まで下がったところで該アルミカップを約45度傾けたときに、内部のエポキシ組成物が流動した場合には「流動性あり」、流動しなかった場合には「流動性なし」と判定した。
結果は表2に示す。
1.4 考察
表2に示すように、熱処理により流動性が喪失したのは組成物1~4であり、これらの組成物においてはゲル化率が90%を超える値となった。
組成物1~4の共通点は、ガリウムアセチルアセトネートとシラノールの両方を含有することである。
表2に示すように、熱処理により流動性が喪失したのは組成物1~4であり、これらの組成物においてはゲル化率が90%を超える値となった。
組成物1~4の共通点は、ガリウムアセチルアセトネートとシラノールの両方を含有することである。
対照的に、ガリウムアセチルアセトネートを含有するがシラノールを含有しない組成物5、シラノールを含有するがガリウムアセチルアセトネートを含有しない組成物6及び7は、熱処理の後も流動性を保ったままであり、ゲル化率もゼロ%であった。
この結果は、ガリウムアセチルアセトネートおよびシラノールの両方の存在が、2官能エポキシ化合物であるEPC-1が重合して3次元架橋構造を形成するための必要十分条件であることを証拠付けるものといえる。
補足すると、ガリウムアセチルアセトネートに触媒されるSOL-1、SOL-2及びSOL-3の重縮合が主たる要因となって、組成物1~4が熱硬化した可能性は無いと考えられる。その理由として、組成物1~4におけるSOL-1、SOL-2及びSOL-3の含有量が、重量比でEPC-1の10分の1以下であることが挙げられる。また、SOL-1、SOL-2及びSOL-3はいずれも1分子中のシラノール水酸基の数が2個であり、重縮合しても3次元架橋構造を形成しない化合物であることが挙げられる。ただし、組成物1~4において、SOL-1、SOL-2及びSOL-3の重縮合が生じた可能性を否定するものではない。
[実施例5~9]
<合成例1>
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン23.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン60g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.250g、トルエン50gを混合した後、50℃で9時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してポリシロキサンEPSi-1を得た。
<合成例1>
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン23.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン60g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.250g、トルエン50gを混合した後、50℃で9時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してポリシロキサンEPSi-1を得た。
<合成例2>
2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン64.8g、トリメチルエトキシシラン40.1g、イソプロピルアルコール45g及び1N塩酸24.39gを混合し、室温で3h攪拌し、さらに水酸化カリウム1.51gとイソプロピルアルコール148gを加えてイソプロピルアルコールの還流条件で4時間過熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=1000のポリシロキサンEPSi-2を得た。
また、式(35)で表される構造を有するYX-4000H(三菱化学株式会社製)を用いた。(以下ではこの化合物をEPC-2と呼ぶ)
2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン64.8g、トリメチルエトキシシラン40.1g、イソプロピルアルコール45g及び1N塩酸24.39gを混合し、室温で3h攪拌し、さらに水酸化カリウム1.51gとイソプロピルアルコール148gを加えてイソプロピルアルコールの還流条件で4時間過熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=1000のポリシロキサンEPSi-2を得た。
また、式(35)で表される構造を有するYX-4000H(三菱化学株式会社製)を用いた。(以下ではこの化合物をEPC-2と呼ぶ)
流動性の評価は、上述の実施例1に準じて行った。また、本実施例では、熱処理後の硬度も測定した。硬度の測定は、JIS K6253に準拠して、硬度計としてアスカーゴム硬度計A型(高分子計器株式会社製測定器)を、荷重器としてゴム硬度計用定圧荷重器CL-150(高分子計器株式会社製)を用いて、ショアA硬さを測定した。
<合成例3>
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン50.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン3.45g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.250g、トルエン5.94gを混合した後、50℃で9時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=20000のポリシロキサン(A)-1を得た。
得られたポリシロキサン(A)-1は式(36)において、a=0、b=0.963、c=0.0367、d=0であった。
(R1R2R3SiO1/2)a(R4R5SiO2/2)b(R6SiO3/2)c(SiO4/2)d(O1/2R7)e ・・・(36)
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン50.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン3.45g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.250g、トルエン5.94gを混合した後、50℃で9時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=20000のポリシロキサン(A)-1を得た。
得られたポリシロキサン(A)-1は式(36)において、a=0、b=0.963、c=0.0367、d=0であった。
(R1R2R3SiO1/2)a(R4R5SiO2/2)b(R6SiO3/2)c(SiO4/2)d(O1/2R7)e ・・・(36)
<合成例4>
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン50.0g、フェニルトリメトキシシラン0.91g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.25g、トルエン21.8gを混合した後、80℃で6時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=13000のポリシロキサン(B)-1を得た。
得られたポリシロキサン(B)-1は式(37)において、al=0、bl=0.987、cl=0.0132、dl=0であった。
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン50.0g、フェニルトリメトキシシラン0.91g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.25g、トルエン21.8gを混合した後、80℃で6時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=13000のポリシロキサン(B)-1を得た。
得られたポリシロキサン(B)-1は式(37)において、al=0、bl=0.987、cl=0.0132、dl=0であった。
(R8R9R10SiO1/2)al(R11R12SiO2/2)bl(R13SiO3/2)cl(SiO4/2)dl(O1/2R14)el ・・・(37)
<合成例5>
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン40.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン7.90g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.400g、2-プロパノール17.0gを混合した後、80℃で5時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=2500のポリシロキサン(A)-2を得た。
得られたポリシロキサン(A)-2は前記式(36)において、a=0、b=0.902、c=0.0984、d=0であった。
Mw=900のヒドロキシ末端メチルフェニルポリシロキサン40.0g、エポキシ基含有アルコキシシランとして2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン7.90g、1,8-ジアザビシクロ[5.4.0]-7-ウンデセン0.400g、2-プロパノール17.0gを混合した後、80℃で5時間加熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=2500のポリシロキサン(A)-2を得た。
得られたポリシロキサン(A)-2は前記式(36)において、a=0、b=0.902、c=0.0984、d=0であった。
[実施例10~14、比較例4,5]
以下に示す各成分を表5に示す割合で配合し、以下に示す方法にしたがって熱硬化性樹脂組成物を調製した。なお、各成分としては、以下に示すものを用いた。
(A) エポキシ基を有するポリシロキサン
(A)-1:合成例3で作成したポリシロキサン
(A)-2:合成例5で作成したポリシロキサン
(B) 芳香族基を有するポリシロキサン
(B)-1:合成例4で作成したポリシロキサン
(B)-2:ヒドロキシ末端メチルフェニルポリシロキサン(Mw=900)
(C) ガリウム化合物((C)-2はその他の硬化触媒)
(C)-1:ガリウムアセチルアセトナート
(C)-2:アルミニウムエチルアセチルアセトナート
(D) 酸無水物化合物
(D)-1:4-メチルヘキサヒドロ無水フタル酸/ヘキサヒドロ無水フタル酸混合物 MH700(新日本理化株式会社)
(表5において、fの値は、組成物中のエポキシ総量に対する酸無水物のモル比を示す。)
(E) エポキシ化合物
(E)-1:3,4-エポキシシクロヘキシルメチル-3′,4′-エポキシシクロヘキサンカルボキシレート
以下に示す各成分を表5に示す割合で配合し、以下に示す方法にしたがって熱硬化性樹脂組成物を調製した。なお、各成分としては、以下に示すものを用いた。
(A) エポキシ基を有するポリシロキサン
(A)-1:合成例3で作成したポリシロキサン
(A)-2:合成例5で作成したポリシロキサン
(B) 芳香族基を有するポリシロキサン
(B)-1:合成例4で作成したポリシロキサン
(B)-2:ヒドロキシ末端メチルフェニルポリシロキサン(Mw=900)
(C) ガリウム化合物((C)-2はその他の硬化触媒)
(C)-1:ガリウムアセチルアセトナート
(C)-2:アルミニウムエチルアセチルアセトナート
(D) 酸無水物化合物
(D)-1:4-メチルヘキサヒドロ無水フタル酸/ヘキサヒドロ無水フタル酸混合物 MH700(新日本理化株式会社)
(表5において、fの値は、組成物中のエポキシ総量に対する酸無水物のモル比を示す。)
(E) エポキシ化合物
(E)-1:3,4-エポキシシクロヘキシルメチル-3′,4′-エポキシシクロヘキサンカルボキシレート
上述のエポキシ基を有するポリシロキサン、芳香族基を有するポリシロキサン、酸無水物化合物、エポキシ化合物を、表5に示す割合(重量比)で配合し、室温、大気雰囲気下で混合し、全体が均一になるまで撹拌を行ったのちに、(C)ガリウム化合物を加えてさらに撹拌をおこなった。
得られた液を80℃で0.5時間、次いで、150℃で2.5時間加熱し、硬化試験を行った。
得られた液を80℃で0.5時間、次いで、150℃で2.5時間加熱し、硬化試験を行った。
表6の結果から明らかなとおり、(C)-1:ガリウムアセチルアセトナートの代わりに(C)-2 :アルミニウムエチルアセチルアセトナートを用いた組成物では、膜の硬化が不良であったり、硬化反応が早すぎて、室温での攪拌時にゲル化が認められた。
<合成例6>
2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン37.6g、Mw=700のヒドロキシ末端ジメチルポリシロキサン14.6g、イソプロピルアルコール22.5g及び1N塩酸11.00gを混合し、室温で3h攪拌し、さらに水酸化カリウム0.74gとイソプロピルアルコール160gを加えてイソプロピルアルコールの還流条件で4時間過熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=2000のポリシロキサンEPSi-3を得た。
上述のポリシロキサン、酸無水物化合物を、表7に示す通りに配合し、室温、大気雰囲気下で混合し、全体が均一になるまで撹拌を行ったのちに、ガリウム化合物またはアルミニウム化合物を加えてさらに撹拌をおこなった。
2-(3,4-エポキシシクロヘキシル)エチルトリメトキシシラン37.6g、Mw=700のヒドロキシ末端ジメチルポリシロキサン14.6g、イソプロピルアルコール22.5g及び1N塩酸11.00gを混合し、室温で3h攪拌し、さらに水酸化カリウム0.74gとイソプロピルアルコール160gを加えてイソプロピルアルコールの還流条件で4時間過熱攪拌操作を行った。その後、リン酸二水素ナトリウム水溶液(10質量%)で反応液を中和してから、洗浄後の水が中性になるまで水洗後、減圧下で揮発成分を除去してMw=2000のポリシロキサンEPSi-3を得た。
上述のポリシロキサン、酸無水物化合物を、表7に示す通りに配合し、室温、大気雰囲気下で混合し、全体が均一になるまで撹拌を行ったのちに、ガリウム化合物またはアルミニウム化合物を加えてさらに撹拌をおこなった。
1 LED素子
2 樹脂成形体
3 ボンディングワイヤ
4 封止材
5 リードフレーム
2 樹脂成形体
3 ボンディングワイヤ
4 封止材
5 リードフレーム
Claims (24)
- エポキシ化合物と、ガリウム化合物と、シラノール源化合物とを含有する熱硬化性樹脂組成物。
- 上記エポキシ化合物が脂環式エポキシ化合物を含む、請求項1に記載の熱硬化性樹脂組成物。
- 上記シラノール源化合物がオルガノポリシロキサンを含む、請求項1または請求項2に記載の熱硬化性樹脂組成物。
- 上記シラノール源化合物が、モノシラン化合物を含む、請求項1~3のいずれかに記載の熱硬化性樹脂組成物。
- 上記ガリウム化合物が、キレート配位子を有するガリウム錯体を含む、請求項1~4のいずれかに記載の熱硬化性樹脂組成物。
- 上記キレート配位子を有するガリウム錯体が、ガリウムトリアセチルアセトネートを含む、請求項5に記載の熱硬化性樹脂組成物。
- エポキシ化合物に、ガリウム化合物およびシラノール源化合物を混合するステップを有する、熱硬化性樹脂組成物の製造方法。
- 上記エポキシ化合物が脂環式エポキシ化合物を含む、請求項7に記載の製造方法。
- 上記シラノール源化合物がオルガノポリシロキサンを含む、請求項7または8に記載の製造方法。
- 上記シラノール源化合物が、モノシラン化合物を含む、請求項7~9のいずれかに記載の製造方法。
- 上記ガリウム化合物が、キレート配位子を有するガリウム錯体を含む、請求項7~10のいずれかに記載の製造方法。
- 上記キレート配位子を有するガリウム錯体が、ガリウムトリアセチルアセトネートを含む、請求項11に記載の製造方法。
- エポキシ化合物を、ガリウム化合物およびシラノールの存在下で加熱するステップを含む、樹脂硬化物の製造方法。
- 上記エポキシ化合物が脂環式エポキシ化合物を含む、請求項13に記載の製造方法。
- 上記シラノールの供給源としてオルガノポリシロキサンを用いる、請求項13または14に記載の製造方法。
- 上記シラノールの供給源として、モノシラン化合物を用いる、請求項13~15のいずれかに記載の製造方法。
- 上記ガリウム化合物として、キレート配位子を有するガリウム錯体を用いる、請求項13~16いずれかに記載の製造方法。
- 上記キレート配位子を有するガリウム錯体が、ガリウムトリアセチルアセトネートを含む、請求項17に記載の製造方法。
- エポキシ化合物の自己重合を発生させる方法であって、ガリウム化合物およびシラノールを触媒として添加するステップを含む方法。
- 上記エポキシ化合物が脂環式エポキシ化合物を含む、請求項19に記載の方法。
- 上記シラノールの供給源としてオルガノポリシロキサンを用いる、請求項19または20に記載の方法。
- 上記シラノールの供給源として、モノシラン化合物を用いる、請求項19~21のいずれかに記載の方法。
- 前記ガリウム化合物が、キレート配位子を有するガリウム錯体を含む、請求項19~22のいずれかに記載の方法。
- 上記キレート配位子を有するガリウム錯体が、ガリウムトリアセチルアセトネートを含む、請求項23に記載の方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201380050393.0A CN104662086B (zh) | 2012-09-28 | 2013-09-27 | 热固性树脂组合物、其制造方法、树脂固化物的制造方法以及使环氧化合物发生自聚合的方法 |
| JP2013558831A JP5549789B1 (ja) | 2012-09-28 | 2013-09-27 | 熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 |
| EP13840504.8A EP2902441A4 (en) | 2012-09-28 | 2013-09-27 | A HEAT-RESISTANT RESIN COMPOSITION, METHOD FOR THE PRODUCTION THEREOF, METHOD FOR THE PRODUCTION OF A CURED RESIN PRODUCT, AND DEVICE FOR DETERMINING THE SELF-POLYMERIZATION OF AN EPOXY COMPOUND |
| US14/643,799 US9550877B2 (en) | 2012-09-28 | 2015-03-10 | Thermosetting resin composition, method for producing same, method for producing cured resin product, and method for causing self-polymerization of epoxy compound |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012217279 | 2012-09-28 | ||
| JP2012-217279 | 2012-09-28 | ||
| JP2013175645 | 2013-08-27 | ||
| JP2013-175645 | 2013-08-27 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US14/643,799 Continuation US9550877B2 (en) | 2012-09-28 | 2015-03-10 | Thermosetting resin composition, method for producing same, method for producing cured resin product, and method for causing self-polymerization of epoxy compound |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014051103A1 true WO2014051103A1 (ja) | 2014-04-03 |
Family
ID=50388494
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/076396 WO2014051103A1 (ja) | 2012-09-28 | 2013-09-27 | 熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9550877B2 (ja) |
| EP (1) | EP2902441A4 (ja) |
| JP (2) | JP5549789B1 (ja) |
| CN (1) | CN104662086B (ja) |
| TW (1) | TWI637020B (ja) |
| WO (1) | WO2014051103A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016117879A (ja) * | 2014-12-19 | 2016-06-30 | 三菱化学株式会社 | 液状樹脂組成物 |
| JP2016166279A (ja) * | 2015-03-09 | 2016-09-15 | 三菱化学株式会社 | 熱硬化性樹脂組成物およびその成形体 |
| JP2016180088A (ja) * | 2014-07-24 | 2016-10-13 | 三菱化学株式会社 | 熱硬化性樹脂組成物及びその成形体 |
| CN106574038A (zh) * | 2014-07-24 | 2017-04-19 | 三菱化学株式会社 | 热固性树脂组合物及其成形体 |
| JP2019099609A (ja) * | 2017-11-29 | 2019-06-24 | Dic株式会社 | 繊維強化成形材料及びそれを用いた成形品 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6543991B2 (ja) * | 2014-03-26 | 2019-07-17 | 三菱ケミカル株式会社 | 熱硬化性樹脂組成物 |
| DE102016106031A1 (de) * | 2016-04-01 | 2017-10-05 | Dr. Neidlinger Holding Gmbh | Heißhärtendes Zweikomponenten-Epoxidharz |
| KR20170123394A (ko) * | 2016-04-28 | 2017-11-08 | 주식회사 네패스신소재 | 방열 특성이 향상된 코팅 조성물 및 이를 이용한 도막의 형성 방법 |
| JPWO2018025850A1 (ja) * | 2016-08-03 | 2019-06-06 | 三菱ケミカル株式会社 | 樹脂組成物 |
| CN107312177A (zh) * | 2017-08-02 | 2017-11-03 | 王琪宇 | 一种制切削液用聚醚改性硅油的制备方法 |
| WO2019219608A1 (en) * | 2018-05-16 | 2019-11-21 | Huntsman Advanced Materials Licensing (Switzerland) Gmbh | Accelerator composition for the cure of polyfunctional isocyanates with epoxy resins |
| CN108641517A (zh) * | 2018-05-29 | 2018-10-12 | 芜湖市元奎新材料科技有限公司 | 建筑用隔热涂料及其制备方法 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5618643A (en) | 1979-07-25 | 1981-02-21 | Toshiba Corp | Preparation of epoxy resin composition |
| JPS5817537A (ja) | 1981-07-22 | 1983-02-01 | Sony Corp | 薄膜磁気記録媒体 |
| JPH03287627A (ja) * | 1990-04-05 | 1991-12-18 | Nippon Telegr & Teleph Corp <Ntt> | ポリシロキサン |
| JPH0841168A (ja) | 1994-07-27 | 1996-02-13 | Matsushita Electric Works Ltd | 液状エポキシ樹脂組成物及び半導体装置 |
| JP2000017149A (ja) * | 1998-07-02 | 2000-01-18 | Nippon Kayaku Co Ltd | 封止材用液状エポキシ樹脂組成物及びその硬化物 |
| JP2007332314A (ja) | 2006-06-16 | 2007-12-27 | Jsr Corp | 熱硬化性樹脂組成物および光半導体用接着剤 |
| JP2010090196A (ja) * | 2008-10-03 | 2010-04-22 | Yokohama Rubber Co Ltd:The | 光拡散性シリコーン樹脂組成物およびこれを用いる光半導体封止体 |
| JP2010111756A (ja) | 2008-11-05 | 2010-05-20 | Yokohama Rubber Co Ltd:The | 加熱硬化性光半導体封止用樹脂組成物およびこれを用いる光半導体封止体 |
| JP2012092172A (ja) | 2010-10-25 | 2012-05-17 | Jsr Corp | 光半導体封止用組成物および発光素子 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1402899A (en) * | 1971-10-28 | 1975-08-13 | Gen Electric | Curable epoxy resin compositons |
| US3812214A (en) * | 1971-10-28 | 1974-05-21 | Gen Electric | Hardenable composition consisting of an epoxy resin and a metal acetylacetonate |
| JPS5817537B2 (ja) | 1979-06-25 | 1983-04-07 | 株式会社東芝 | エポキシ樹脂系組成物 |
| JP4300418B2 (ja) * | 2004-04-30 | 2009-07-22 | 信越化学工業株式会社 | エポキシ・シリコーン混成樹脂組成物及び発光半導体装置 |
| JP2008056857A (ja) * | 2006-09-01 | 2008-03-13 | Sekisui Chem Co Ltd | 光半導体用熱硬化性組成物、光半導体素子用封止剤、光半導体素子用ダイボンド材、光半導体素子用アンダーフィル材及び光半導体装置 |
-
2013
- 2013-09-27 WO PCT/JP2013/076396 patent/WO2014051103A1/ja active Application Filing
- 2013-09-27 JP JP2013558831A patent/JP5549789B1/ja active Active
- 2013-09-27 TW TW102135268A patent/TWI637020B/zh active
- 2013-09-27 EP EP13840504.8A patent/EP2902441A4/en active Pending
- 2013-09-27 CN CN201380050393.0A patent/CN104662086B/zh active Active
-
2014
- 2014-05-22 JP JP2014105886A patent/JP2015063656A/ja active Pending
-
2015
- 2015-03-10 US US14/643,799 patent/US9550877B2/en active Active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5618643A (en) | 1979-07-25 | 1981-02-21 | Toshiba Corp | Preparation of epoxy resin composition |
| JPS5817537A (ja) | 1981-07-22 | 1983-02-01 | Sony Corp | 薄膜磁気記録媒体 |
| JPH03287627A (ja) * | 1990-04-05 | 1991-12-18 | Nippon Telegr & Teleph Corp <Ntt> | ポリシロキサン |
| JPH0841168A (ja) | 1994-07-27 | 1996-02-13 | Matsushita Electric Works Ltd | 液状エポキシ樹脂組成物及び半導体装置 |
| JP2000017149A (ja) * | 1998-07-02 | 2000-01-18 | Nippon Kayaku Co Ltd | 封止材用液状エポキシ樹脂組成物及びその硬化物 |
| JP2007332314A (ja) | 2006-06-16 | 2007-12-27 | Jsr Corp | 熱硬化性樹脂組成物および光半導体用接着剤 |
| JP2010090196A (ja) * | 2008-10-03 | 2010-04-22 | Yokohama Rubber Co Ltd:The | 光拡散性シリコーン樹脂組成物およびこれを用いる光半導体封止体 |
| JP2010111756A (ja) | 2008-11-05 | 2010-05-20 | Yokohama Rubber Co Ltd:The | 加熱硬化性光半導体封止用樹脂組成物およびこれを用いる光半導体封止体 |
| JP2012092172A (ja) | 2010-10-25 | 2012-05-17 | Jsr Corp | 光半導体封止用組成物および発光素子 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP2902441A4 |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016180088A (ja) * | 2014-07-24 | 2016-10-13 | 三菱化学株式会社 | 熱硬化性樹脂組成物及びその成形体 |
| CN106574038A (zh) * | 2014-07-24 | 2017-04-19 | 三菱化学株式会社 | 热固性树脂组合物及其成形体 |
| US20170130006A1 (en) * | 2014-07-24 | 2017-05-11 | Mitsubishi Chemical Corporation | Thermosetting resin composition and molded body thereof |
| EP3173434A4 (en) * | 2014-07-24 | 2017-06-28 | Mitsubishi Chemical Corporation | Thermosetting resin composition and molded body thereof |
| JP2016117879A (ja) * | 2014-12-19 | 2016-06-30 | 三菱化学株式会社 | 液状樹脂組成物 |
| JP2016166279A (ja) * | 2015-03-09 | 2016-09-15 | 三菱化学株式会社 | 熱硬化性樹脂組成物およびその成形体 |
| JP2019099609A (ja) * | 2017-11-29 | 2019-06-24 | Dic株式会社 | 繊維強化成形材料及びそれを用いた成形品 |
| JP7087358B2 (ja) | 2017-11-29 | 2022-06-21 | Dic株式会社 | 繊維強化成形材料及びそれを用いた成形品 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104662086A (zh) | 2015-05-27 |
| EP2902441A4 (en) | 2015-09-30 |
| US9550877B2 (en) | 2017-01-24 |
| TWI637020B (zh) | 2018-10-01 |
| JP2015063656A (ja) | 2015-04-09 |
| CN104662086B (zh) | 2018-04-17 |
| US20150240070A1 (en) | 2015-08-27 |
| JP5549789B1 (ja) | 2014-07-16 |
| TW201422709A (zh) | 2014-06-16 |
| EP2902441A1 (en) | 2015-08-05 |
| JPWO2014051103A1 (ja) | 2016-08-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5549789B1 (ja) | 熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 | |
| JPWO2005100445A1 (ja) | 光半導体封止用組成物、光半導体封止材および光半導体封止用組成物の製造方法 | |
| TWI666250B (zh) | 熱硬化性樹脂組成物及其成形體 | |
| JP5891617B2 (ja) | 熱硬化性樹脂組成物、半導体デバイス用部材、及びそれを用いた半導体デバイス | |
| JP6031739B2 (ja) | 熱硬化性樹脂組成物、半導体デバイス用部材、及びそれを用いた半導体デバイス | |
| JP2016180088A (ja) | 熱硬化性樹脂組成物及びその成形体 | |
| JP2012241059A (ja) | 熱硬化性樹脂組成物、半導体デバイス用部材、及びそれを用いた半導体デバイス | |
| JP6299328B2 (ja) | 熱硬化性樹脂組成物、その製造方法、樹脂硬化物の製造方法、および、エポキシ化合物の自己重合を発生させる方法 | |
| JP2016166279A (ja) | 熱硬化性樹脂組成物およびその成形体 | |
| JP2016117822A (ja) | 液状樹脂組成物 | |
| JP6543991B2 (ja) | 熱硬化性樹脂組成物 | |
| JP6311399B2 (ja) | 熱硬化性樹脂組成物、およびその成形体 | |
| JP2016194059A (ja) | エポキシ基含有樹脂組成物およびその成形体 | |
| JP6405663B2 (ja) | 熱硬化性樹脂組成物 | |
| JP2017066364A (ja) | 樹脂組成物 | |
| JP6609935B2 (ja) | 樹脂組成物 | |
| JP2017092258A (ja) | リモートフォスファー型半導体発光装置及びその製法 | |
| JP6657566B2 (ja) | 低粘度樹脂組成物 | |
| JP6349858B2 (ja) | 熱硬化性樹脂組成物 | |
| JP6421427B2 (ja) | 熱硬化性樹脂組成物 | |
| JP6691475B2 (ja) | シリコーン樹脂組成物及び光半導体装置 | |
| JP2015187210A (ja) | 熱硬化性樹脂組成物 | |
| JP2015189936A (ja) | 1液型熱硬化性樹脂組成物 | |
| JP2015189920A (ja) | 樹脂組成物 | |
| WO2018025850A1 (ja) | 樹脂組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2013558831 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13840504 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013840504 Country of ref document: EP |