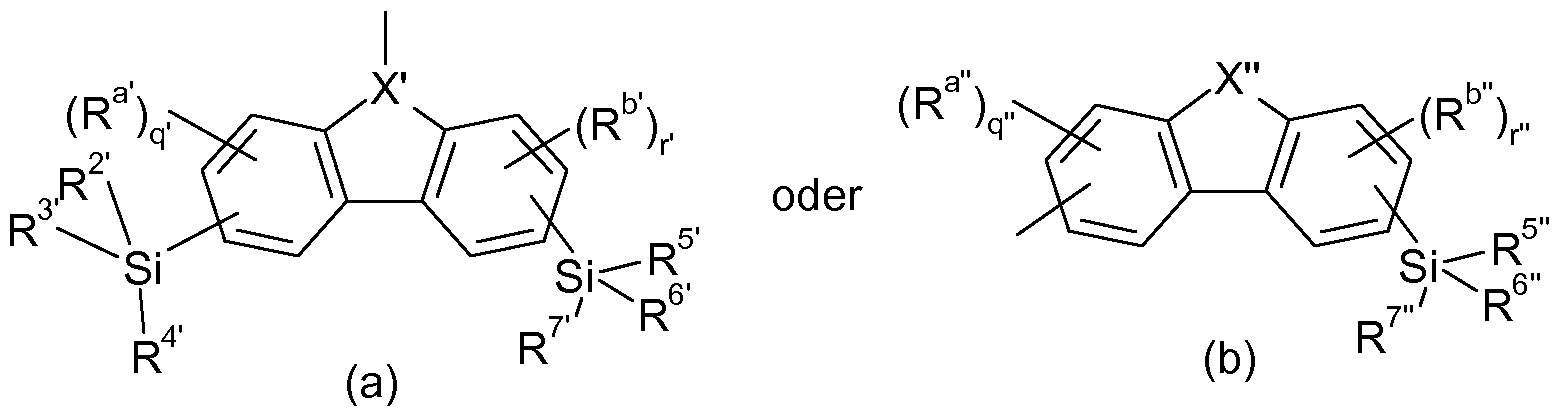WO2009003898A1 - Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden - Google Patents
Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden Download PDFInfo
- Publication number
- WO2009003898A1 WO2009003898A1 PCT/EP2008/058106 EP2008058106W WO2009003898A1 WO 2009003898 A1 WO2009003898 A1 WO 2009003898A1 EP 2008058106 W EP2008058106 W EP 2008058106W WO 2009003898 A1 WO2009003898 A1 WO 2009003898A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- substituted
- unsubstituted
- radicals
- aryl
- alkyl
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 174
- -1 carbene transition metal Chemical class 0.000 title claims description 131
- 229910052723 transition metal Inorganic materials 0.000 title description 5
- 239000000463 material Substances 0.000 claims abstract description 104
- HZVOZRGWRWCICA-UHFFFAOYSA-N methanediyl Chemical compound [CH2] HZVOZRGWRWCICA-UHFFFAOYSA-N 0.000 claims abstract description 77
- 239000004020 conductor Substances 0.000 claims abstract description 58
- 239000011159 matrix material Substances 0.000 claims abstract description 49
- 238000002347 injection Methods 0.000 claims abstract description 36
- 239000007924 injection Substances 0.000 claims abstract description 36
- 238000000034 method Methods 0.000 claims abstract description 31
- 238000002360 preparation method Methods 0.000 claims abstract description 31
- 230000008569 process Effects 0.000 claims abstract description 7
- 150000003254 radicals Chemical class 0.000 claims description 186
- 125000001424 substituent group Chemical group 0.000 claims description 73
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 66
- 239000003446 ligand Substances 0.000 claims description 57
- 125000003118 aryl group Chemical group 0.000 claims description 55
- 125000000217 alkyl group Chemical group 0.000 claims description 43
- 125000001072 heteroaryl group Chemical group 0.000 claims description 42
- 125000006413 ring segment Chemical group 0.000 claims description 42
- 229910052739 hydrogen Inorganic materials 0.000 claims description 40
- 239000001257 hydrogen Substances 0.000 claims description 40
- 229910052736 halogen Inorganic materials 0.000 claims description 30
- 229910052751 metal Inorganic materials 0.000 claims description 30
- 239000002184 metal Substances 0.000 claims description 29
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 29
- 150000002431 hydrogen Chemical group 0.000 claims description 28
- 229910052717 sulfur Inorganic materials 0.000 claims description 26
- 229910052760 oxygen Inorganic materials 0.000 claims description 22
- 230000000694 effects Effects 0.000 claims description 21
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 21
- 229910005965 SO 2 Inorganic materials 0.000 claims description 20
- 238000004519 manufacturing process Methods 0.000 claims description 17
- 229910052757 nitrogen Inorganic materials 0.000 claims description 17
- 125000005842 heteroatom Chemical group 0.000 claims description 16
- 239000002243 precursor Substances 0.000 claims description 15
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims description 12
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 11
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 10
- 150000005840 aryl radicals Chemical group 0.000 claims description 9
- 125000004429 atom Chemical group 0.000 claims description 9
- 125000005708 carbonyloxy group Chemical group [*:2]OC([*:1])=O 0.000 claims description 9
- OAKJQQAXSVQMHS-UHFFFAOYSA-N hydrazine group Chemical group NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 claims description 9
- 150000002739 metals Chemical class 0.000 claims description 9
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 9
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims description 9
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 9
- 125000003368 amide group Chemical group 0.000 claims description 8
- 229910019142 PO4 Inorganic materials 0.000 claims description 7
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 claims description 7
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 claims description 7
- 125000001841 imino group Chemical group [H]N=* 0.000 claims description 7
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 claims description 7
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 claims description 7
- 230000000737 periodic effect Effects 0.000 claims description 7
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims description 7
- 239000010452 phosphate Substances 0.000 claims description 7
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 claims description 7
- 229940124530 sulfonamide Drugs 0.000 claims description 7
- 150000003456 sulfonamides Chemical class 0.000 claims description 7
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 claims description 7
- 150000003462 sulfoxides Chemical class 0.000 claims description 7
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 claims description 7
- 150000001642 boronic acid derivatives Chemical class 0.000 claims description 6
- 230000007935 neutral effect Effects 0.000 claims description 6
- 125000000018 nitroso group Chemical group N(=O)* 0.000 claims description 6
- 230000003647 oxidation Effects 0.000 claims description 6
- 238000007254 oxidation reaction Methods 0.000 claims description 6
- 229910052698 phosphorus Inorganic materials 0.000 claims description 6
- 229910000073 phosphorus hydride Inorganic materials 0.000 claims description 6
- 125000005555 sulfoximide group Chemical group 0.000 claims description 6
- 229910000086 alane Inorganic materials 0.000 claims description 5
- 125000002577 pseudohalo group Chemical group 0.000 claims description 5
- 229910052747 lanthanoid Inorganic materials 0.000 claims description 4
- 150000002602 lanthanoids Chemical class 0.000 claims description 4
- 241000837181 Andina Species 0.000 claims description 3
- 125000005110 aryl thio group Chemical group 0.000 claims description 3
- UORVGPXVDQYIDP-BJUDXGSMSA-N borane Chemical group [10BH3] UORVGPXVDQYIDP-BJUDXGSMSA-N 0.000 claims 2
- 125000005597 hydrazone group Chemical group 0.000 claims 2
- 150000002923 oximes Chemical group 0.000 claims 2
- 238000005286 illumination Methods 0.000 abstract 1
- 239000010410 layer Substances 0.000 description 237
- GBXQPDCOMJJCMJ-UHFFFAOYSA-M trimethyl-[6-(trimethylazaniumyl)hexyl]azanium;bromide Chemical class [Br-].C[N+](C)(C)CCCCCC[N+](C)(C)C GBXQPDCOMJJCMJ-UHFFFAOYSA-M 0.000 description 94
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 80
- 229910052741 iridium Inorganic materials 0.000 description 59
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 57
- 239000000243 solution Substances 0.000 description 56
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 55
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 53
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 53
- 239000000203 mixture Substances 0.000 description 44
- 239000000370 acceptor Substances 0.000 description 33
- 239000000758 substrate Substances 0.000 description 31
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 30
- HAKJPFBYGDBEEA-UHFFFAOYSA-N triphenyl-(9-phenyl-6-triphenylsilylcarbazol-3-yl)silane Chemical compound C1=CC=CC=C1N1C2=CC=C([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)C=C2C2=CC([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)=CC=C21 HAKJPFBYGDBEEA-UHFFFAOYSA-N 0.000 description 30
- 239000000460 chlorine Substances 0.000 description 28
- 239000000047 product Substances 0.000 description 27
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 24
- 150000002367 halogens Chemical class 0.000 description 21
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 19
- 230000015572 biosynthetic process Effects 0.000 description 19
- 229910052731 fluorine Inorganic materials 0.000 description 19
- 238000003756 stirring Methods 0.000 description 19
- 238000003786 synthesis reaction Methods 0.000 description 19
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 18
- 230000009471 action Effects 0.000 description 16
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 15
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 238000005160 1H NMR spectroscopy Methods 0.000 description 14
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 14
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 14
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 14
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 13
- 229910052794 bromium Inorganic materials 0.000 description 13
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 12
- 0 Cc1cc([S+](c2ccccc2)(c2ccccc2)c2ccc(*c(c-3c4)ccc4[Si](c4ccccc4)(c4ccccc4)c4cc(C(F)(F)F)ccc4)c-3c2)ccc1 Chemical compound Cc1cc([S+](c2ccccc2)(c2ccccc2)c2ccc(*c(c-3c4)ccc4[Si](c4ccccc4)(c4ccccc4)c4cc(C(F)(F)F)ccc4)c-3c2)ccc1 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 229910052786 argon Inorganic materials 0.000 description 12
- 229910052801 chlorine Inorganic materials 0.000 description 12
- 238000004440 column chromatography Methods 0.000 description 12
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 12
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 11
- 238000006254 arylation reaction Methods 0.000 description 11
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 11
- 238000004770 highest occupied molecular orbital Methods 0.000 description 11
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 11
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 11
- 239000002904 solvent Substances 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 10
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 10
- 150000001716 carbazoles Chemical class 0.000 description 9
- 239000000706 filtrate Substances 0.000 description 9
- YUCFVHQCAFKDQG-UHFFFAOYSA-N fluoromethane Chemical compound F[CH] YUCFVHQCAFKDQG-UHFFFAOYSA-N 0.000 description 9
- 238000006884 silylation reaction Methods 0.000 description 9
- 230000032258 transport Effects 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 8
- 239000011368 organic material Substances 0.000 description 8
- 239000002244 precipitate Substances 0.000 description 8
- 125000006239 protecting group Chemical group 0.000 description 8
- STTGYIUESPWXOW-UHFFFAOYSA-N 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline Chemical compound C=12C=CC3=C(C=4C=CC=CC=4)C=C(C)N=C3C2=NC(C)=CC=1C1=CC=CC=C1 STTGYIUESPWXOW-UHFFFAOYSA-N 0.000 description 7
- GEQBRULPNIVQPP-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 GEQBRULPNIVQPP-UHFFFAOYSA-N 0.000 description 7
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- MNKYQPOFRKPUAE-UHFFFAOYSA-N chloro(triphenyl)silane Chemical compound C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(Cl)C1=CC=CC=C1 MNKYQPOFRKPUAE-UHFFFAOYSA-N 0.000 description 7
- 239000012459 cleaning agent Substances 0.000 description 7
- 229940043397 deconex Drugs 0.000 description 7
- 238000001194 electroluminescence spectrum Methods 0.000 description 7
- 235000019439 ethyl acetate Nutrition 0.000 description 7
- 230000006870 function Effects 0.000 description 7
- 230000003472 neutralizing effect Effects 0.000 description 7
- 239000012074 organic phase Substances 0.000 description 7
- 239000000741 silica gel Substances 0.000 description 7
- 229910002027 silica gel Inorganic materials 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 7
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 7
- JBWRZTKHMKVFMQ-UHFFFAOYSA-N 3,6-dibromo-9-phenylcarbazole Chemical compound C12=CC=C(Br)C=C2C2=CC(Br)=CC=C2N1C1=CC=CC=C1 JBWRZTKHMKVFMQ-UHFFFAOYSA-N 0.000 description 6
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 6
- 229910004298 SiO 2 Inorganic materials 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 230000000903 blocking effect Effects 0.000 description 6
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 5
- 229960000583 acetic acid Drugs 0.000 description 5
- 229910052783 alkali metal Inorganic materials 0.000 description 5
- 125000003545 alkoxy group Chemical group 0.000 description 5
- 125000004104 aryloxy group Chemical group 0.000 description 5
- 229910000085 borane Inorganic materials 0.000 description 5
- 239000012362 glacial acetic acid Substances 0.000 description 5
- 125000000168 pyrrolyl group Chemical group 0.000 description 5
- 229910000080 stannane Inorganic materials 0.000 description 5
- 125000001544 thienyl group Chemical group 0.000 description 5
- UORVGPXVDQYIDP-UHFFFAOYSA-N trihydridoboron Substances B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 5
- DBDJXGIDPXHUGS-UHFFFAOYSA-N triphenyl-(6-triphenylsilyl-9h-carbazol-3-yl)silane Chemical compound C1=CC=CC=C1[Si](C=1C=C2C3=CC(=CC=C3NC2=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 DBDJXGIDPXHUGS-UHFFFAOYSA-N 0.000 description 5
- FIHILUSWISKVSR-UHFFFAOYSA-N 3,6-dibromo-9h-carbazole Chemical compound C1=C(Br)C=C2C3=CC(Br)=CC=C3NC2=C1 FIHILUSWISKVSR-UHFFFAOYSA-N 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 4
- 125000003860 C1-C20 alkoxy group Chemical group 0.000 description 4
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 4
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 4
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical group CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- WIHKEPSYODOQJR-UHFFFAOYSA-N [9-(4-tert-butylphenyl)-6-triphenylsilylcarbazol-3-yl]-triphenylsilane Chemical compound C1=CC(C(C)(C)C)=CC=C1N1C2=CC=C([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)C=C2C2=CC([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)=CC=C21 WIHKEPSYODOQJR-UHFFFAOYSA-N 0.000 description 4
- 150000001340 alkali metals Chemical class 0.000 description 4
- 125000004414 alkyl thio group Chemical group 0.000 description 4
- 239000008346 aqueous phase Substances 0.000 description 4
- 150000001502 aryl halides Chemical class 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 230000031709 bromination Effects 0.000 description 4
- 238000005893 bromination reaction Methods 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 239000002800 charge carrier Substances 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 238000010511 deprotection reaction Methods 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 238000005401 electroluminescence Methods 0.000 description 4
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 4
- 239000011737 fluorine Substances 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 239000011777 magnesium Substances 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 4
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 3
- 238000007126 N-alkylation reaction Methods 0.000 description 3
- BGECDVWSWDRFSP-UHFFFAOYSA-N borazine Chemical compound B1NBNBN1 BGECDVWSWDRFSP-UHFFFAOYSA-N 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 230000008878 coupling Effects 0.000 description 3
- 238000010168 coupling process Methods 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- MGNCLNQXLYJVJD-UHFFFAOYSA-N cyanuric chloride Chemical compound ClC1=NC(Cl)=NC(Cl)=N1 MGNCLNQXLYJVJD-UHFFFAOYSA-N 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 230000005595 deprotonation Effects 0.000 description 3
- 238000010537 deprotonation reaction Methods 0.000 description 3
- 150000002390 heteroarenes Chemical class 0.000 description 3
- 150000004693 imidazolium salts Chemical class 0.000 description 3
- 125000002883 imidazolyl group Chemical group 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- WPHGSKGZRAQSGP-UHFFFAOYSA-N methylenecyclohexane Natural products C1CCCC2CC21 WPHGSKGZRAQSGP-UHFFFAOYSA-N 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- 239000012044 organic layer Substances 0.000 description 3
- 125000002971 oxazolyl group Chemical group 0.000 description 3
- 229910000027 potassium carbonate Inorganic materials 0.000 description 3
- 125000003226 pyrazolyl group Chemical group 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 229910052707 ruthenium Inorganic materials 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 125000004149 thio group Chemical group *S* 0.000 description 3
- 150000003624 transition metals Chemical class 0.000 description 3
- 125000001425 triazolyl group Chemical group 0.000 description 3
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 3
- IVQMKRVPLRKRLZ-UHFFFAOYSA-N (3,6-dibromocarbazol-9-yl)-triphenylsilane Chemical compound C12=CC=C(Br)C=C2C2=CC(Br)=CC=C2N1[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 IVQMKRVPLRKRLZ-UHFFFAOYSA-N 0.000 description 2
- POILWHVDKZOXJZ-ARJAWSKDSA-M (z)-4-oxopent-2-en-2-olate Chemical compound C\C([O-])=C\C(C)=O POILWHVDKZOXJZ-ARJAWSKDSA-M 0.000 description 2
- ZAYUOSICZWFJSW-UHFFFAOYSA-N 10h-phenothiazine 5,5-dioxide Chemical class C1=CC=C2S(=O)(=O)C3=CC=CC=C3NC2=C1 ZAYUOSICZWFJSW-UHFFFAOYSA-N 0.000 description 2
- QPTWWBLGJZWRAV-UHFFFAOYSA-N 2,7-dibromo-9-H-carbazole Natural products BrC1=CC=C2C3=CC=C(Br)C=C3NC2=C1 QPTWWBLGJZWRAV-UHFFFAOYSA-N 0.000 description 2
- GTVLPQMCDKDSLC-UHFFFAOYSA-N 3,6-dibromo-9-(3-methoxyphenyl)carbazole Chemical compound COC1=CC=CC(N2C3=CC=C(Br)C=C3C3=CC(Br)=CC=C32)=C1 GTVLPQMCDKDSLC-UHFFFAOYSA-N 0.000 description 2
- ZVFQEOPUXVPSLB-UHFFFAOYSA-N 3-(4-tert-butylphenyl)-4-phenyl-5-(4-phenylphenyl)-1,2,4-triazole Chemical compound C1=CC(C(C)(C)C)=CC=C1C(N1C=2C=CC=CC=2)=NN=C1C1=CC=C(C=2C=CC=CC=2)C=C1 ZVFQEOPUXVPSLB-UHFFFAOYSA-N 0.000 description 2
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 229910052693 Europium Inorganic materials 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- WARVYMSBKRUHKT-UHFFFAOYSA-N [3,6-bis(triphenylsilyl)carbazol-9-yl]-triphenylsilane Chemical compound C1=CC=CC=C1[Si](C=1C=C2C3=CC(=CC=C3N(C2=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 WARVYMSBKRUHKT-UHFFFAOYSA-N 0.000 description 2
- YPNPQQWPICNIRO-UHFFFAOYSA-N [9-[4,6-bis[3,6-bis(triphenylsilyl)carbazol-9-yl]-1,3,5-triazin-2-yl]-6-triphenylsilylcarbazol-3-yl]-triphenylsilane Chemical compound C1=CC=CC=C1[Si](C=1C=C2C3=CC(=CC=C3N(C=3N=C(N=C(N=3)N3C4=CC=C(C=C4C4=CC(=CC=C43)[Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)[Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)N3C4=CC=C(C=C4C4=CC(=CC=C43)[Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)[Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)C2=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 YPNPQQWPICNIRO-UHFFFAOYSA-N 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 150000001350 alkyl halides Chemical class 0.000 description 2
- 238000010719 annulation reaction Methods 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 2
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- XZCJVWCMJYNSQO-UHFFFAOYSA-N butyl pbd Chemical compound C1=CC(C(C)(C)C)=CC=C1C1=NN=C(C=2C=CC(=CC=2)C=2C=CC=CC=2)O1 XZCJVWCMJYNSQO-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 238000005229 chemical vapour deposition Methods 0.000 description 2
- DCFKHNIGBAHNSS-UHFFFAOYSA-N chloro(triethyl)silane Chemical compound CC[Si](Cl)(CC)CC DCFKHNIGBAHNSS-UHFFFAOYSA-N 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 239000012043 crude product Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000004987 dibenzofuryl group Chemical group C1(=CC=CC=2OC3=C(C21)C=CC=C3)* 0.000 description 2
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 2
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical class C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 2
- 125000005509 dibenzothiophenyl group Chemical group 0.000 description 2
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 230000005525 hole transport Effects 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- 150000002466 imines Chemical class 0.000 description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 2
- 238000000816 matrix-assisted laser desorption--ionisation Methods 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 229940078552 o-xylene Drugs 0.000 description 2
- 125000002524 organometallic group Chemical group 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 238000005240 physical vapour deposition Methods 0.000 description 2
- SIOXPEMLGUPBBT-UHFFFAOYSA-M picolinate Chemical compound [O-]C(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-M 0.000 description 2
- 239000003880 polar aprotic solvent Substances 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- KWYUFKZDYYNOTN-UHFFFAOYSA-M potassium hydroxide Substances [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000011241 protective layer Substances 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 230000008707 rearrangement Effects 0.000 description 2
- 238000006462 rearrangement reaction Methods 0.000 description 2
- 238000005215 recombination Methods 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 229910052703 rhodium Inorganic materials 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000002210 silicon-based material Substances 0.000 description 2
- NDVLTYZPCACLMA-UHFFFAOYSA-N silver oxide Chemical compound [O-2].[Ag+].[Ag+] NDVLTYZPCACLMA-UHFFFAOYSA-N 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 238000004611 spectroscopical analysis Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- MDDUHVRJJAFRAU-YZNNVMRBSA-N tert-butyl-[(1r,3s,5z)-3-[tert-butyl(dimethyl)silyl]oxy-5-(2-diphenylphosphorylethylidene)-4-methylidenecyclohexyl]oxy-dimethylsilane Chemical compound C1[C@@H](O[Si](C)(C)C(C)(C)C)C[C@H](O[Si](C)(C)C(C)(C)C)C(=C)\C1=C/CP(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 MDDUHVRJJAFRAU-YZNNVMRBSA-N 0.000 description 2
- 238000007740 vapor deposition Methods 0.000 description 2
- XOHVSPABFDSRQC-UHFFFAOYSA-N (4-methoxyphenyl)-[6-[(4-methoxyphenyl)-dimethylsilyl]-9-phenylcarbazol-3-yl]-dimethylsilane Chemical compound C1=CC(OC)=CC=C1[Si](C)(C)C1=CC=C(N(C=2C=CC=CC=2)C=2C3=CC(=CC=2)[Si](C)(C)C=2C=CC(OC)=CC=2)C3=C1 XOHVSPABFDSRQC-UHFFFAOYSA-N 0.000 description 1
- PIFHBODBJYQXMD-UHFFFAOYSA-N (6-bromo-9-phenylcarbazol-3-yl)-triphenylsilane Chemical compound C12=CC=C([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)C=C2C2=CC(Br)=CC=C2N1C1=CC=CC=C1 PIFHBODBJYQXMD-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- PAAZPARNPHGIKF-UHFFFAOYSA-N 1,2-dibromoethane Chemical compound BrCCBr PAAZPARNPHGIKF-UHFFFAOYSA-N 0.000 description 1
- AZUYLZMQTIKGSC-UHFFFAOYSA-N 1-[6-[4-(5-chloro-6-methyl-1H-indazol-4-yl)-5-methyl-3-(1-methylindazol-5-yl)pyrazol-1-yl]-2-azaspiro[3.3]heptan-2-yl]prop-2-en-1-one Chemical compound ClC=1C(=C2C=NNC2=CC=1C)C=1C(=NN(C=1C)C1CC2(CN(C2)C(C=C)=O)C1)C=1C=C2C=NN(C2=CC=1)C AZUYLZMQTIKGSC-UHFFFAOYSA-N 0.000 description 1
- UTQUFKAPHZAOQK-UHFFFAOYSA-N 1-n,1-n,2-n,2-n,3-n,3-n,4-n,4-n-octakis-phenylbenzene-1,2,3,4-tetramine Chemical compound C1=CC=CC=C1N(C=1C(=C(N(C=2C=CC=CC=2)C=2C=CC=CC=2)C(N(C=2C=CC=CC=2)C=2C=CC=CC=2)=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 UTQUFKAPHZAOQK-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- XNCMQRWVMWLODV-UHFFFAOYSA-N 1-phenylbenzimidazole Chemical compound C1=NC2=CC=CC=C2N1C1=CC=CC=C1 XNCMQRWVMWLODV-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- XKLNOVWDVMWTOB-UHFFFAOYSA-N 2,3,4,9-tetrahydro-1h-carbazole Chemical class N1C2=CC=CC=C2C2=C1CCCC2 XKLNOVWDVMWTOB-UHFFFAOYSA-N 0.000 description 1
- MGNCLNQXLYJVJD-VMIGTVKRSA-N 2,4,6-trichloro-1,3,5-triazine Chemical class Cl[13C]1=N[13C](Cl)=N[13C](Cl)=N1 MGNCLNQXLYJVJD-VMIGTVKRSA-N 0.000 description 1
- UFCZRCPQBWIXTR-UHFFFAOYSA-N 2,8-dibromodibenzofuran Chemical compound C1=C(Br)C=C2C3=CC(Br)=CC=C3OC2=C1 UFCZRCPQBWIXTR-UHFFFAOYSA-N 0.000 description 1
- WNEXSUAHKVAPFK-UHFFFAOYSA-N 2,8-dibromodibenzothiophene Chemical compound C1=C(Br)C=C2C3=CC(Br)=CC=C3SC2=C1 WNEXSUAHKVAPFK-UHFFFAOYSA-N 0.000 description 1
- RIKNNBBGYSDYAX-UHFFFAOYSA-N 2-[1-[2-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]-n,n-bis(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C(=CC=CC=1)C1(CCCCC1)C=1C(=CC=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 RIKNNBBGYSDYAX-UHFFFAOYSA-N 0.000 description 1
- IXHWGNYCZPISET-UHFFFAOYSA-N 2-[4-(dicyanomethylidene)-2,3,5,6-tetrafluorocyclohexa-2,5-dien-1-ylidene]propanedinitrile Chemical compound FC1=C(F)C(=C(C#N)C#N)C(F)=C(F)C1=C(C#N)C#N IXHWGNYCZPISET-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000389 2-pyrrolyl group Chemical group [H]N1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- JAERGRPXCBTKNT-UHFFFAOYSA-N 3,6-dibromo-9-(3,4,5-trimethoxyphenyl)carbazole Chemical compound COC1=C(OC)C(OC)=CC(N2C3=CC=C(Br)C=C3C3=CC(Br)=CC=C32)=C1 JAERGRPXCBTKNT-UHFFFAOYSA-N 0.000 description 1
- FLLMODIOUCBEQC-UHFFFAOYSA-N 3-(3,6-dibromocarbazol-9-yl)benzonitrile Chemical compound C12=CC=C(Br)C=C2C2=CC(Br)=CC=C2N1C1=CC=CC(C#N)=C1 FLLMODIOUCBEQC-UHFFFAOYSA-N 0.000 description 1
- YPVKVRFKWOXUQF-UHFFFAOYSA-N 3-carbazol-9-ylbenzonitrile Chemical compound N#CC1=CC=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=C1 YPVKVRFKWOXUQF-UHFFFAOYSA-N 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000001397 3-pyrrolyl group Chemical group [H]N1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- YGBCLRRWZQSURU-UHFFFAOYSA-N 4-[(diphenylhydrazinylidene)methyl]-n,n-diethylaniline Chemical compound C1=CC(N(CC)CC)=CC=C1C=NN(C=1C=CC=CC=1)C1=CC=CC=C1 YGBCLRRWZQSURU-UHFFFAOYSA-N 0.000 description 1
- KBXXZTIBAVBLPP-UHFFFAOYSA-N 4-[[4-(diethylamino)-2-methylphenyl]-(4-methylphenyl)methyl]-n,n-diethyl-3-methylaniline Chemical compound CC1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=CC=1)N(CC)CC)C)C1=CC=C(C)C=C1 KBXXZTIBAVBLPP-UHFFFAOYSA-N 0.000 description 1
- HTNLTVXRWGAUAB-UHFFFAOYSA-N 4-benzyl-2-[3,5-bis(4-benzyl-1-phenylimidazol-2-yl)phenyl]-1-phenylimidazole Chemical compound C=1C=CC=CC=1CC(N=1)=CN(C=2C=CC=CC=2)C=1C(C=1)=CC(C=2N(C=C(CC=3C=CC=CC=3)N=2)C=2C=CC=CC=2)=CC=1C(N(C=1)C=2C=CC=CC=2)=NC=1CC1=CC=CC=C1 HTNLTVXRWGAUAB-UHFFFAOYSA-N 0.000 description 1
- 125000004860 4-ethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])C([H])([H])[H] 0.000 description 1
- ZOKIJILZFXPFTO-UHFFFAOYSA-N 4-methyl-n-[4-[1-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C1(CCCCC1)C=1C=CC(=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 ZOKIJILZFXPFTO-UHFFFAOYSA-N 0.000 description 1
- MVIXNQZIMMIGEL-UHFFFAOYSA-N 4-methyl-n-[4-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C=1C=CC(=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 MVIXNQZIMMIGEL-UHFFFAOYSA-N 0.000 description 1
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- BZTPLMLVTRAIRP-UHFFFAOYSA-N 9-[3,5-bis(trifluoromethyl)phenyl]-3,6-dibromocarbazole Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(N2C3=CC=C(Br)C=C3C3=CC(Br)=CC=C32)=C1 BZTPLMLVTRAIRP-UHFFFAOYSA-N 0.000 description 1
- PVAFQJRITXZPCL-UHFFFAOYSA-N 9-[3,5-bis(trifluoromethyl)phenyl]carbazole Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=C1 PVAFQJRITXZPCL-UHFFFAOYSA-N 0.000 description 1
- 229910017008 AsF 6 Inorganic materials 0.000 description 1
- NJQFCQXFOHVYQJ-PMACEKPBSA-N BF 4 Chemical compound C1([C@@H]2CC(=O)C=3C(O)=C(C)C4=C(C=3O2)[C@H](C(C)C)C2=C(O4)C(C)=C(C(C2=O)(C)C)OC)=CC=CC=C1 NJQFCQXFOHVYQJ-PMACEKPBSA-N 0.000 description 1
- 238000005615 Borsche-Drechsel cyclization reaction Methods 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 229910052772 Samarium Inorganic materials 0.000 description 1
- 229910018286 SbF 6 Inorganic materials 0.000 description 1
- 229910004020 SiCz Inorganic materials 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 238000006887 Ullmann reaction Methods 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- GFUZZRQHGZIBNY-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenyl]-[6-[[3,5-bis(trifluoromethyl)phenyl]-dimethylsilyl]-9-phenylcarbazol-3-yl]-dimethylsilane Chemical compound C=1C(C(F)(F)F)=CC(C(F)(F)F)=CC=1[Si](C)(C)C(C=C1C2=CC(=CC=C22)[Si](C)(C)C=3C=C(C=C(C=3)C(F)(F)F)C(F)(F)F)=CC=C1N2C1=CC=CC=C1 GFUZZRQHGZIBNY-UHFFFAOYSA-N 0.000 description 1
- JZWDIKPZWMXPMG-UHFFFAOYSA-N [3,5-bis(trifluoromethyl)phenyl]-chloro-dimethylsilane Chemical compound C[Si](C)(Cl)C1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 JZWDIKPZWMXPMG-UHFFFAOYSA-N 0.000 description 1
- LBQUWRKTAHGYNR-UHFFFAOYSA-N [6-[dimethyl-(2,3,4,5,6-pentafluorophenyl)silyl]-9-phenylcarbazol-3-yl]-dimethyl-(2,3,4,5,6-pentafluorophenyl)silane Chemical compound FC=1C(F)=C(F)C(F)=C(F)C=1[Si](C)(C)C(C=C1C2=CC(=CC=C22)[Si](C)(C)C=3C(=C(F)C(F)=C(F)C=3F)F)=CC=C1N2C1=CC=CC=C1 LBQUWRKTAHGYNR-UHFFFAOYSA-N 0.000 description 1
- SPTKHRGYZHAHPT-UHFFFAOYSA-N [9-(3-methoxyphenyl)-6-triphenylsilylcarbazol-3-yl]-triphenylsilane Chemical compound COC1=CC=CC(N2C3=CC=C(C=C3C3=CC(=CC=C32)[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SPTKHRGYZHAHPT-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 229910052768 actinide Inorganic materials 0.000 description 1
- 150000001255 actinides Chemical class 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910000102 alkali metal hydride Inorganic materials 0.000 description 1
- 150000008046 alkali metal hydrides Chemical class 0.000 description 1
- 229910000272 alkali metal oxide Inorganic materials 0.000 description 1
- 229910001860 alkaline earth metal hydroxide Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical compound [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 150000003851 azoles Chemical class 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- LYGCVUNYPAISNJ-UHFFFAOYSA-N benzene 2-benzyl-1-phenylimidazole Chemical compound c1ccccc1.C(c1nccn1-c1ccccc1)c1ccccc1 LYGCVUNYPAISNJ-UHFFFAOYSA-N 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- RTYNSTRFACIKRL-UHFFFAOYSA-N chloro-(4-methoxyphenyl)-dimethylsilane Chemical compound COC1=CC=C([Si](C)(C)Cl)C=C1 RTYNSTRFACIKRL-UHFFFAOYSA-N 0.000 description 1
- OJZNZOXALZKPEA-UHFFFAOYSA-N chloro-methyl-diphenylsilane Chemical compound C=1C=CC=CC=1[Si](Cl)(C)C1=CC=CC=C1 OJZNZOXALZKPEA-UHFFFAOYSA-N 0.000 description 1
- CWJSHJJYOPWUGX-UHFFFAOYSA-N chlorpropham Chemical compound CC(C)OC(=O)NC1=CC=CC(Cl)=C1 CWJSHJJYOPWUGX-UHFFFAOYSA-N 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000002243 cyclohexanonyl group Chemical class *C1(*)C(=O)C(*)(*)C(*)(*)C(*)(*)C1(*)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexyloxide Natural products O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 1
- 125000006547 cyclononyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000004855 decalinyl group Chemical group C1(CCCC2CCCCC12)* 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- BYYOSGSRLZDICO-UHFFFAOYSA-N dimethyl-bis(9-phenyl-3-triphenylsilylcarbazol-1-yl)silane Chemical compound C=1C([Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=CC(C2=CC=CC=C2N2C=3C=CC=CC=3)=C2C=1[Si](C)(C)C1=CC([Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=CC(C2=CC=CC=C22)=C1N2C1=CC=CC=C1 BYYOSGSRLZDICO-UHFFFAOYSA-N 0.000 description 1
- LIKFHECYJZWXFJ-UHFFFAOYSA-N dimethyldichlorosilane Chemical compound C[Si](C)(Cl)Cl LIKFHECYJZWXFJ-UHFFFAOYSA-N 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000000295 emission spectrum Methods 0.000 description 1
- 238000005265 energy consumption Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- DQYBDCGIPTYXML-UHFFFAOYSA-N ethoxyethane;hydrate Chemical compound O.CCOCC DQYBDCGIPTYXML-UHFFFAOYSA-N 0.000 description 1
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 230000001815 facial effect Effects 0.000 description 1
- 229910000078 germane Inorganic materials 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- SHFJWMWCIHQNCP-UHFFFAOYSA-M hydron;tetrabutylazanium;sulfate Chemical compound OS([O-])(=O)=O.CCCC[N+](CCCC)(CCCC)CCCC SHFJWMWCIHQNCP-UHFFFAOYSA-M 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 230000026045 iodination Effects 0.000 description 1
- 238000006192 iodination reaction Methods 0.000 description 1
- SNHMUERNLJLMHN-UHFFFAOYSA-N iodobenzene Chemical compound IC1=CC=CC=C1 SNHMUERNLJLMHN-UHFFFAOYSA-N 0.000 description 1
- MILUBEOXRNEUHS-UHFFFAOYSA-N iridium(3+) Chemical class [Ir+3] MILUBEOXRNEUHS-UHFFFAOYSA-N 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- WGOPGODQLGJZGL-UHFFFAOYSA-N lithium;butane Chemical compound [Li+].CC[CH-]C WGOPGODQLGJZGL-UHFFFAOYSA-N 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 238000001906 matrix-assisted laser desorption--ionisation mass spectrometry Methods 0.000 description 1
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- WGOCMDOCWBEEOG-UHFFFAOYSA-N methyl-[6-[methyl(diphenyl)silyl]-9-phenylcarbazol-3-yl]-diphenylsilane Chemical compound C=1C=CC=CC=1[Si](C=1C=C2C3=CC(=CC=C3N(C=3C=CC=CC=3)C2=CC=1)[Si](C)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C)C1=CC=CC=C1 WGOCMDOCWBEEOG-UHFFFAOYSA-N 0.000 description 1
- 230000011987 methylation Effects 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 229910003455 mixed metal oxide Inorganic materials 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- JGOAZQAXRONCCI-SDNWHVSQSA-N n-[(e)-benzylideneamino]aniline Chemical compound C=1C=CC=CC=1N\N=C\C1=CC=CC=C1 JGOAZQAXRONCCI-SDNWHVSQSA-N 0.000 description 1
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 1
- ISGOGUQCGJYLRY-UHFFFAOYSA-N n-phenyl-n-phosphanylaniline Chemical compound C=1C=CC=CC=1N(P)C1=CC=CC=C1 ISGOGUQCGJYLRY-UHFFFAOYSA-N 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229910052758 niobium Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 238000010534 nucleophilic substitution reaction Methods 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- CBHCDHNUZWWAPP-UHFFFAOYSA-N pecazine Chemical compound C1N(C)CCCC1CN1C2=CC=CC=C2SC2=CC=CC=C21 CBHCDHNUZWWAPP-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000003444 phase transfer catalyst Substances 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- 229940067157 phenylhydrazine Drugs 0.000 description 1
- 150000004031 phenylhydrazines Chemical class 0.000 description 1
- 125000003356 phenylsulfanyl group Chemical group [*]SC1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 1
- 229920000548 poly(silane) polymer Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 229910052702 rhenium Inorganic materials 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- KZUNJOHGWZRPMI-UHFFFAOYSA-N samarium atom Chemical compound [Sm] KZUNJOHGWZRPMI-UHFFFAOYSA-N 0.000 description 1
- 125000001824 selenocyanato group Chemical group *[Se]C#N 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 229910001923 silver oxide Inorganic materials 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 229910052713 technetium Inorganic materials 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 230000008646 thermal stress Effects 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 1
- VUPBSZJVARHEPI-UHFFFAOYSA-N triphenyl-(1-phenyl-6-triphenylsilyl-9h-carbazol-3-yl)silane Chemical compound C1=CC=CC=C1C1=CC([Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=CC2=C1NC1=CC=C([Si](C=3C=CC=CC=3)(C=3C=CC=CC=3)C=3C=CC=CC=3)C=C12 VUPBSZJVARHEPI-UHFFFAOYSA-N 0.000 description 1
- COHQQWZJNAJBJP-UHFFFAOYSA-N triphenyl-(8-triphenylsilyldibenzofuran-2-yl)silane Chemical compound C1=CC=CC=C1[Si](C=1C=C2C3=CC(=CC=C3OC2=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 COHQQWZJNAJBJP-UHFFFAOYSA-N 0.000 description 1
- RXKXRKMEOMPFJD-UHFFFAOYSA-N triphenyl-(8-triphenylsilyldibenzothiophen-2-yl)silane Chemical compound C1=CC=CC=C1[Si](C=1C=C2C3=CC(=CC=C3SC2=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 RXKXRKMEOMPFJD-UHFFFAOYSA-N 0.000 description 1
- HJSCEGYFGVNHSR-UHFFFAOYSA-N triphenyl-[9-(3,4,5-trimethoxyphenyl)-6-triphenylsilylcarbazol-3-yl]silane Chemical compound COC1=C(OC)C(OC)=CC(N2C3=CC=C(C=C3C3=CC(=CC=C32)[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)[Si](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 HJSCEGYFGVNHSR-UHFFFAOYSA-N 0.000 description 1
- AKQNYQDSIDKVJZ-UHFFFAOYSA-N triphenylsilane Chemical class C1=CC=CC=C1[SiH](C=1C=CC=CC=1)C1=CC=CC=C1 AKQNYQDSIDKVJZ-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 229910006400 μ-Cl Inorganic materials 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2102/00—Constructional details relating to the organic devices covered by this subclass
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02B—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO BUILDINGS, e.g. HOUSING, HOUSE APPLIANCES OR RELATED END-USER APPLICATIONS
- Y02B20/00—Energy efficient lighting technologies, e.g. halogen lamps or gas discharge lamps
- Y02B20/30—Semiconductor lamps, e.g. solid state lamps [SSL] light emitting diodes [LED] or organic LED [OLED]
Definitions
- the present invention relates to an organic light-emitting diode comprising an anode An and a cathode Ka and arranged between the anode An and the cathode Ka light-emitting layer E containing at least one carbene complex, and optionally at least one further layer, wherein the light E-emitting layer E and / or the at least one further layer comprises at least one compound selected from disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzophospholes, disilyldibenzothiophene-S-oxides and disilyldibenzothiophene-S, S-dioxides, a light-emitting layer containing at least one of the above compounds and at least one carbene complex, the use of the abovementioned compounds as matrix material, hole / exciton blocker material, electron / exciton blocker material, hole
- Injection material electron injection material, hole conductor material and / or electrical conductor material and a device selected from the group consisting of stationary screens, mobile screens and lighting units containing at least one organic light-emitting diode according to the invention; selected disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzophospholes, disilyldibenzothiophene-S-oxides and disilyldibenzothiophene-S, S-dioxides and methods for their preparation.
- OLEDs organic light emitting diodes
- the property of materials is used to emit light when excited by electric current.
- OLEDs are of particular interest as an alternative to cathode ray tubes and to liquid crystal displays for the production of flat panel displays. Due to the very compact design and the intrinsically low power consumption, devices containing OLEDs are particularly suitable for mobile applications, for example for applications in mobile phones, laptops, etc., as well as for lighting.
- the basic principles of the functioning of OLEDs and suitable structures (layers) of OLEDs are known to the person skilled in the art and are mentioned, for example, in WO 2005/113704 and the literature cited therein.
- phosphorescent materials can be used in addition to fluorescent materials (fluorescence emitters).
- the phosphorescence emitters are usually organometallic complexes which, in contrast to the fluorescence emitters which exhibit singlet emission, exhibit triplet emission (triplet emitters) (MA Baldow et al., Appl. Phys. Lett. 1999, 75, 4 to 6).
- triplet emission triplet emission
- Triplet emitter phosphorescence emitter
- Such device compositions may contain, for example, special matrix materials in which the actual light emitter is present in distributed form. Furthermore, the compositions may contain blocking materials, whereby hole, excitation and / or electron blockers may be present in the device compositions. Alternatively or alternatively, the device compositions may further comprise hole injection materials and / or electron injection materials and / or hole conductor materials and / or electron conductor materials. The selection of the above-mentioned materials, which are used in combination with the actual light emitter, has a significant influence, inter alia, on the efficiency and the lifetime of the OLEDs.
- US 2005/0238919 A1 relates to an organic light-emitting diode which contains at least one aryl compound which contains two or more silicon atoms.
- the materials mentioned in US 2005/0238919 A1 are preferably used as matrix materials in the light-emitting layer.
- emitter materials phosphorescence emitters are preferably used according to US 2005/0238919 A1. These are preferably ortho-metalated transition metal complexes. More detailed information regarding the emitter material used are made in US 2005/0238919 A1 only in the examples.
- Organic light-emitting diodes which contain at least one carbene complex as emitter material in addition to the silicon atoms containing aryl compounds are not disclosed in US 2005/0238919 A1.
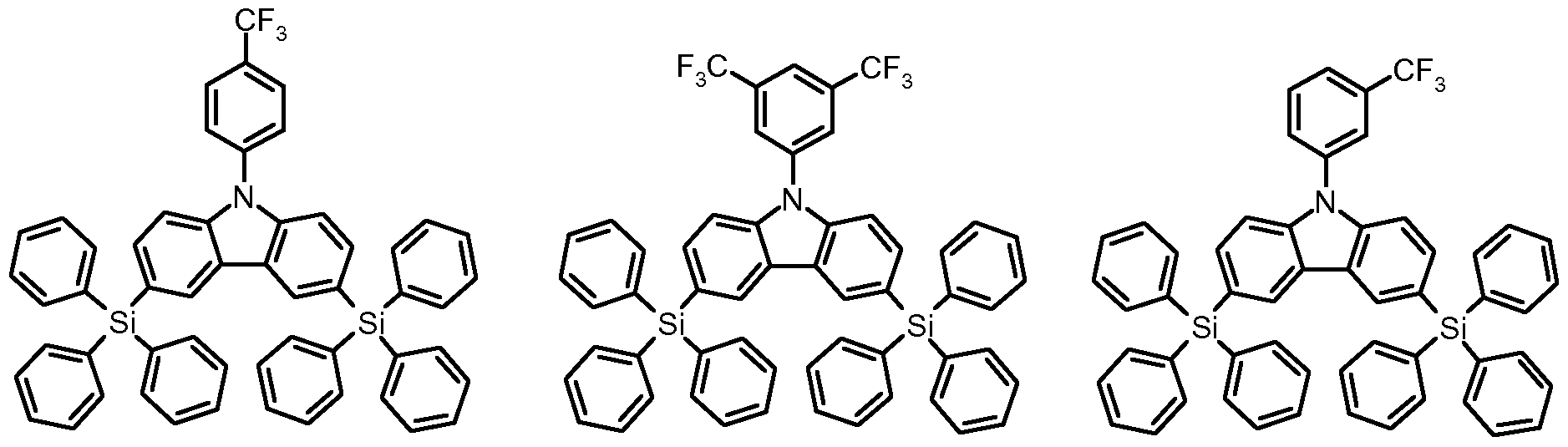
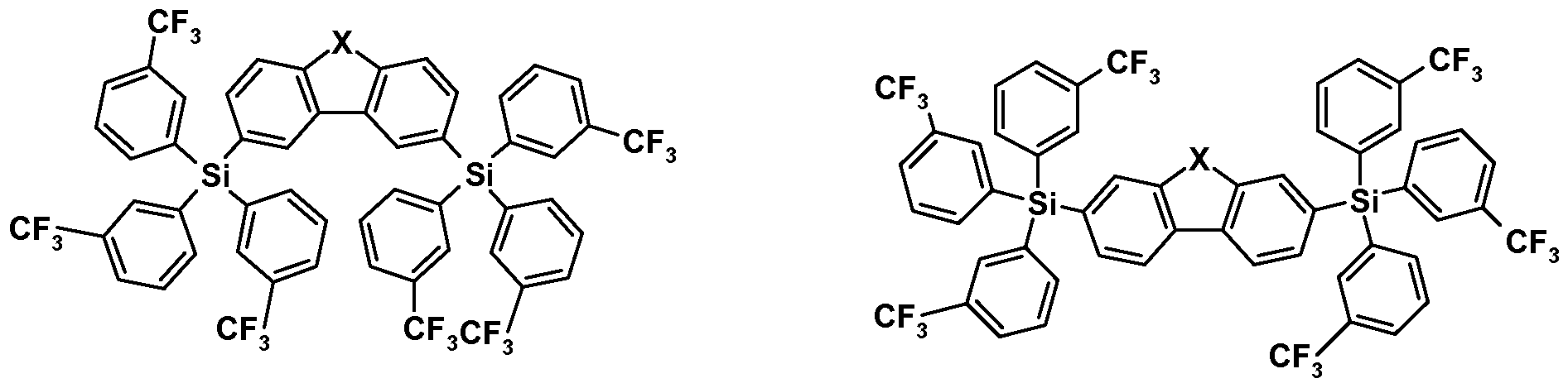
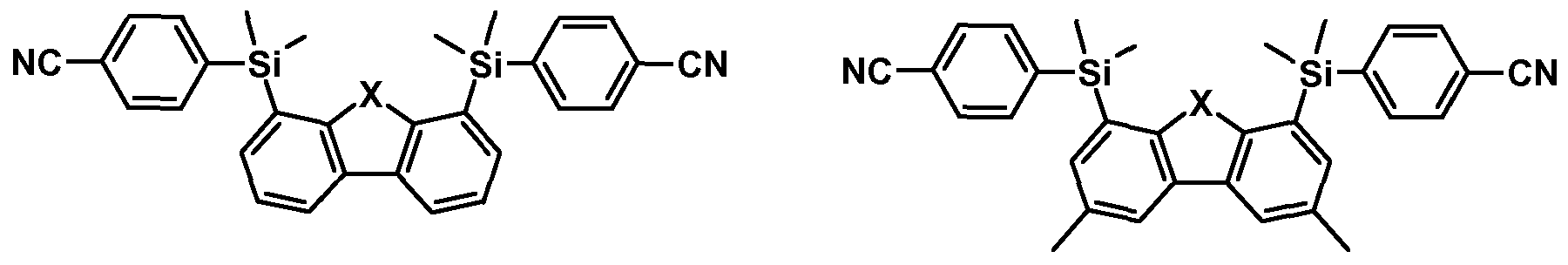
- US 200570238919 A1 mentions a large number of differently substituted silicon-containing compounds, but in the examples of the present application, only silicon-containing compounds of formulas (1-1) and (I-2) having the following formulas
- Tsai et al. Adv. Mater., 2006, Vol. 18, No. 9, pages 1216 to 1220 discloses blue light-emitting organic light-emitting diodes comprising 9- (4-tert-butylphenyl) -3,6-bis ( tris-phenylsilyl) carbazole as matrix material.
- As emitter materials according to Tsai et al. no carbene complexes used.
- Yang et al., Angew. Chem. 2007, 1 19, 2470 to 2473 relates to blue light-emitting heteroleptic iridium (III) complexes which are suitable for use in phosphorescent OLEDs.
- III heteroleptic iridium
- hole transport material and exciton blocker material in the examples according to Yang et al. 9- (4-tert-butylphenyl) -3,6-bis (triphenylsilyl) carbazole used.
- the use of carbene complexes as emitter materials is described in Yang et al. not revealed.
- JP 2004253298 A relates to white light-emitting organic light-emitting diodes in which substituted triphenylsilanes are used as matrix materials.
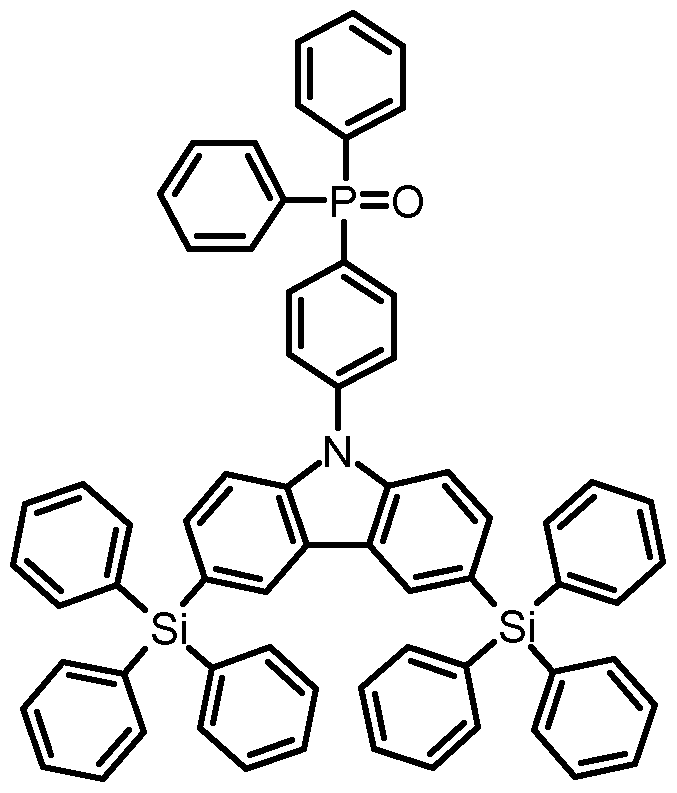
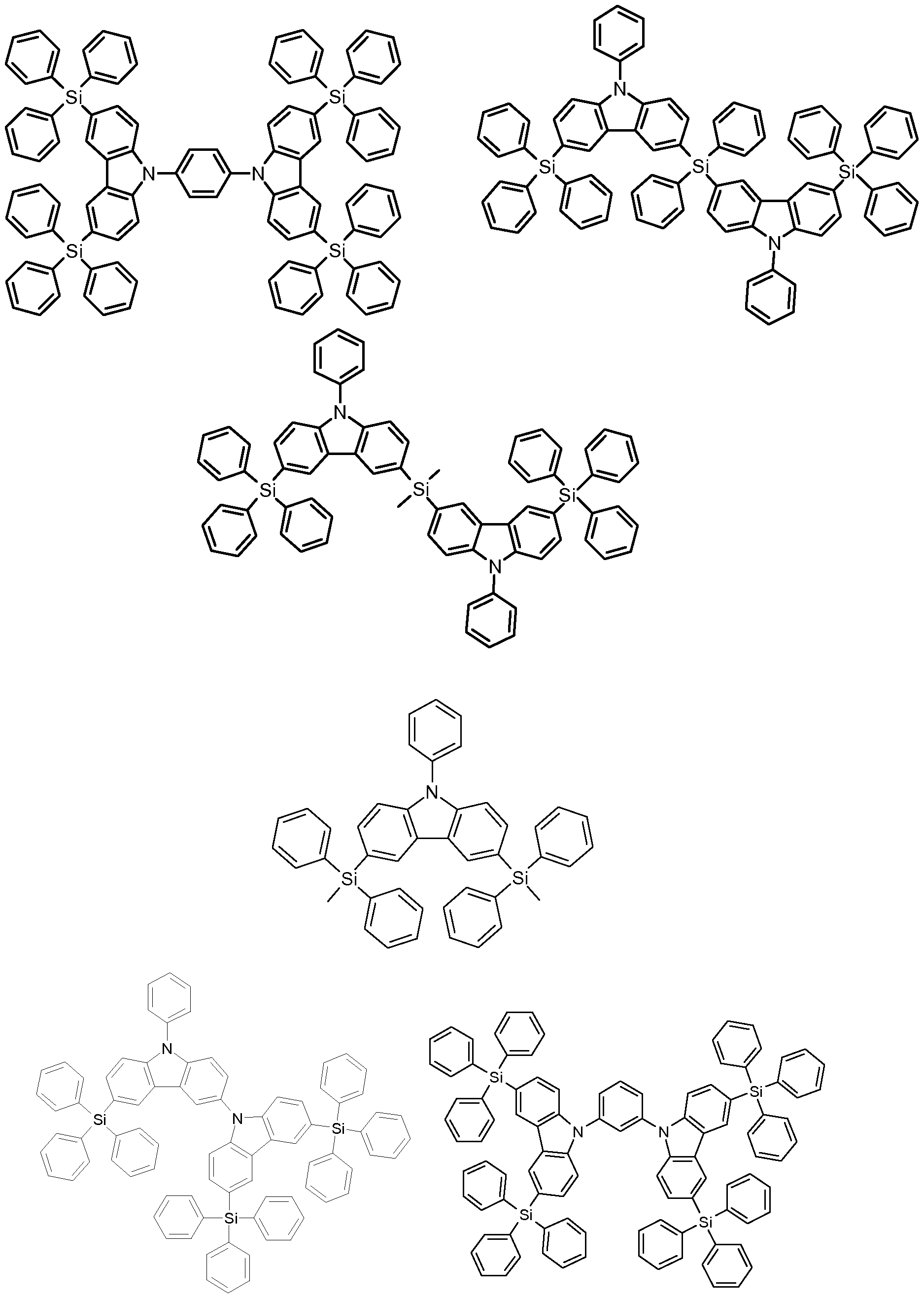
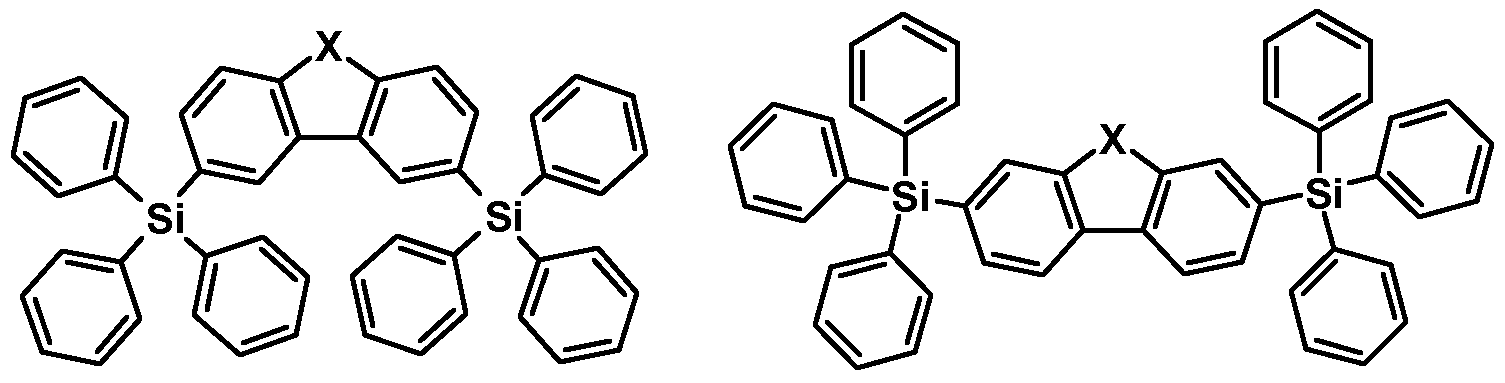
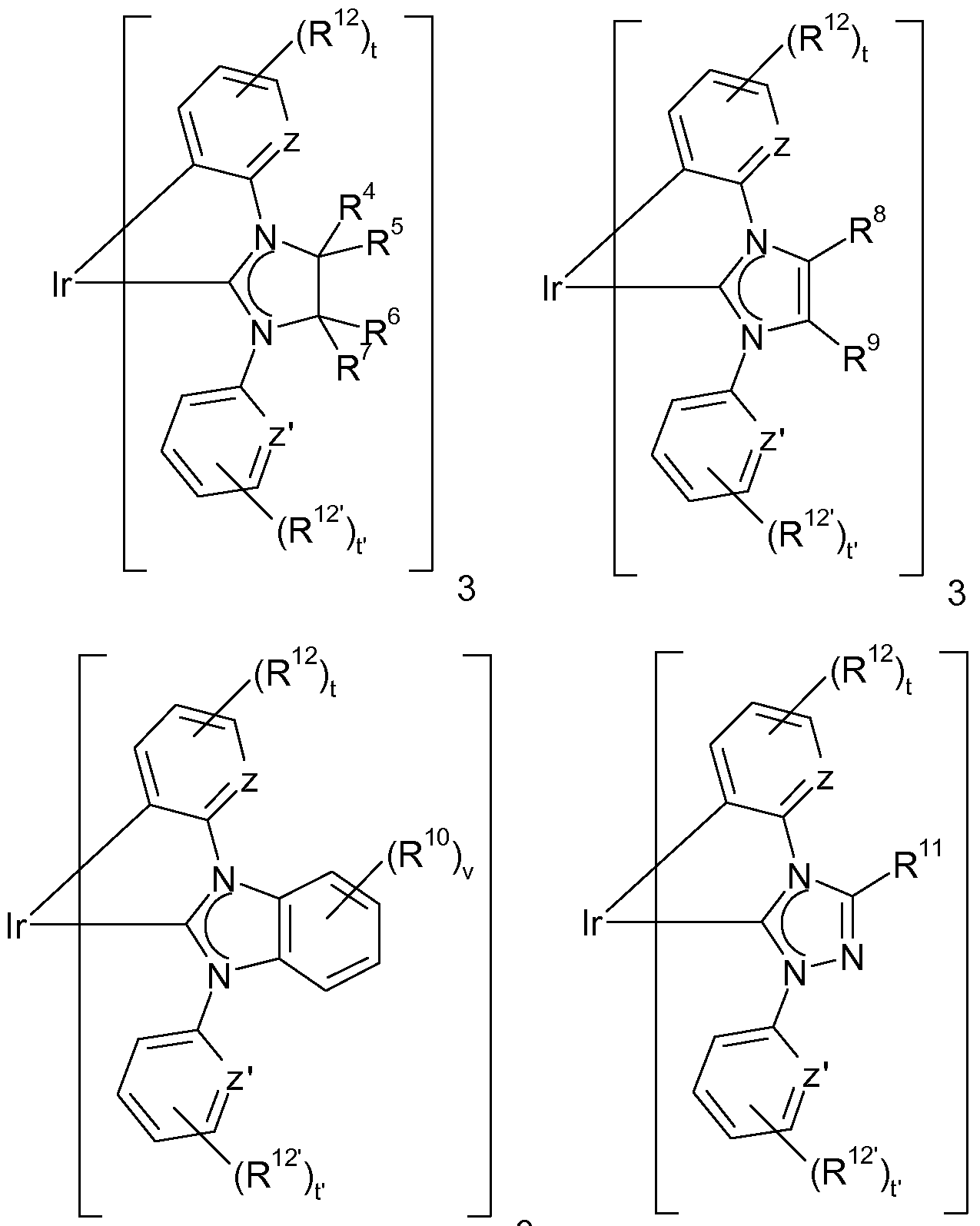
- an organic light-emitting diode comprising an anode An and a cathode Ka and a light-emitting layer E which is arranged between the anode An and the cathode Ka and contains at least one carbene complex of the general formula I
- M 1 metal atom selected from the group consisting of metals of group IB, IIB, HIB, IVB, VB, VIB, VIIB, the lanthanides and INA of the Periodic Table of the Elements (CAS version) in each of the corresponding metal atom is possible oxidation state; preferably selected from the group consisting of groups IIB, HIB, IVB, VB, VIB, VIIB, VIII of the periodic table of the elements (CAS version), Cu and Eu, particularly preferably selected from the groups IB, VIB, VIIB, VIII and Eu, most preferably selected from Cr, Mo, W, Mn, Tc, Re, Ru, Os, Co, Rh, Ir, Fe, Nb, Pd, Pt, Cu, Ag, Au and Eu, further very particularly preferably Os, Rh, Ir, Ru, Pd and Pt, in particular very particular preference Ru, Rh, Ir and Pt, and even more preferably Ir and Pt; carbene carbene ligand which
- L mono or dianionic ligand, preferably monoanionic ligand, which may be mono- or didentate;
- n 0 or> 1
- ligands L can be the same or different at m> 1;
- o Number of ligands K, where o can be 0 or> 1, and the ligands K can be the same or different at o> 1;
- p charge of the complex 0, 1, 2, 3 or 4; preferably 0, 1 or 2, more preferably 0;
- W monoanionic counterion preferably halide, pseudohalide, BF 4 " , PF 6 “ , AsF 6 “ , SbF 6 “ or OA C “ , particularly preferably Cl “ , Br “ , I “ , CN “ or OAc “ very particularly preferably Br “ or I “ ;
- n + m + o and the charge p depend on the oxidation state and coordination number of the metal atom used, the charge of the complex and on the toughness of the carbene, L and K ligands, and on the charge of the ligands carbene and L, with the condition that n is at least 1;
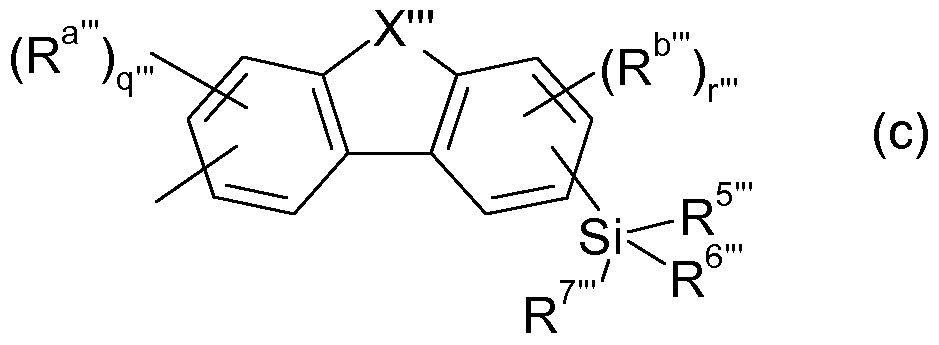
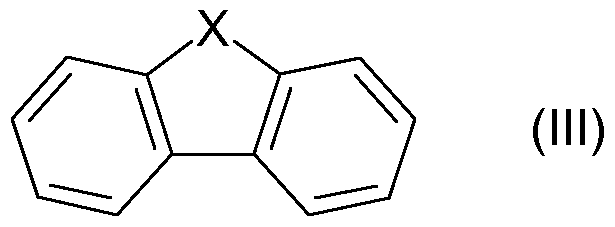
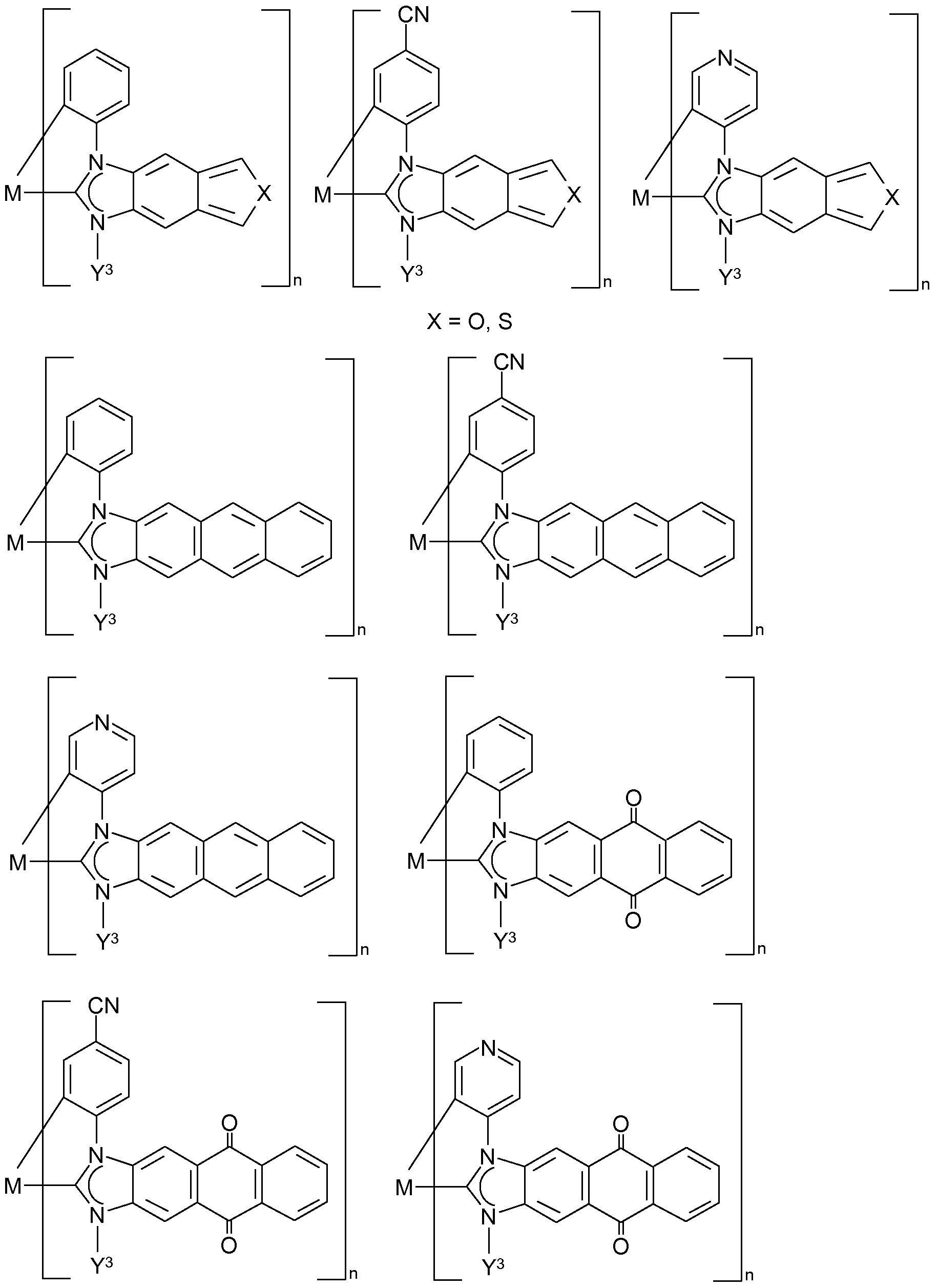
- the organic light-emitting diode contains at least one compound of the general formula II which is present in the light-emitting layer E and / or in the at least one further layer,
- X is NR 1 , S, O, PR 1 , SO 2 or SO;
- R 1 is substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C 6 -C 30 -aryl or substituted or unsubstituted heteroaryl having 5 to 30 ring atoms;
- R 2, R 3, R 4, R 5, R 6, R 7 are each independently substituted or unsubstituted Ci-C 2 o alkyl or substituted or unsubstituted C 6 -C 30 -aryl or a structure of the general formula (c)
- R 14 , R 15 , R 16 are independently substituted or unsubstituted C 1 -C 20 alkyl or substituted or unsubstituted C 6 -C 30 aryl;
- q, r independently of one another are O, 1, 2 or 3; in which case, when q and r are O, all substitutable positions of the aryl radical are substituted by hydrogen,
- radicals and indices in the group of the formula (c) X '", R 5 '", R 6 '", R 7 '", R a '", R b '", q '"and r'" independently each have the meanings given for the radicals and indices of the compounds of the general formula (II) X, R 5 , R 6 , R 7 , R a , R b , q and r.
- the compounds of the general formula (II) are readily available and, both when used as matrix materials in the light-emitting layer E and when used in at least one of the further layers of an OLED containing at least one carbene complex of the formula (I) as a light emitter Combined with the actual emitter (s) of the general formula (I) good efficiencies when used in OLEDs and are suitable for providing OLEDs with a long service life.
- the compounds of the formula (II) can be used either as a matrix in the light-emitting layer E, as a hole / exciton blocker, as an electron / exciton blocker, as hole injection materials, as electron injection materials, as a hole conductor and / or or used as an electron conductor.
- a hole / exciton blocker as an electron / exciton blocker
- hole injection materials as electron injection materials
- hole conductor and / or or used as an electron conductor are known to the person skilled in the art and are mentioned, for example, in WO 2005/113704 or WO 2005/019373.
- the organic light-emitting diode (OLED) according to the invention has the following structure:
- Suitable further layers of the OLED according to the invention are the layers which are known to the person skilled in the art and are usually present in OLEDs.
- the OLED according to the invention preferably contains at least one further layer selected from the group consisting of: at least one block layer for electrons / excitons, at least one block layer for holes / excitons, at least one hole injection layer, at least one hole conductor layer, at least one electron injection layer and at least one electron conductor layer.
- the individual of the abovementioned layers of the OLED can in turn be made up of two or more layers.
- the Hole conductor layer may be constructed of a layer, in which holes are injected from the electrode, and a layer which transports the holes away from the hole-injecting layer in the light-emitting layer.
- the electron conduction layer may also consist of several layers, for example a layer in which electrons are injected through the electrode and a layer which receives electrons from the electron injection layer and transports them into the light-emitting layer. These layers are selected in each case according to factors such as energy level, temperature resistance and charge carrier mobility, as well as energy difference of said layers with the organic layers or the metal electrodes.
- the person skilled in the art is able to choose the structure of the OLEDs in such a way that it is optimally adapted to the organic compounds used according to the invention as emitter substances.
- the HOMO (highest occupied molecular orbital) of the hole conductor layer should be aligned with the work function of the anode
- the LUMO (lowest unoccupied molecular orbital) of the electron conductor layer should be aligned with the work function of the cathode, as far as the aforementioned layers in the inventive OLEDs are present.
- the inventive OLED can, for. B. - in a preferred embodiment - be composed of the following layers:
- the OLED does not have all of the layers mentioned, for example, an OLED having the layers (1) (anode), (3) (light-emitting layer), and (6) (cathode) is also suitable the functions of the layers (2) (hole conductor layer) and (4) (hole / exciton block layer) and (5) (electron conductor layer) are taken over by the adjacent layers.
- OLEDs comprising layers (1), (2), (3) and (6) or layers (1), (3), (4), (5) and (6) are also suitable.
- the OLEDs between the anode (1) and the hole conductor layer (2) may have a block layer for electrons / excitons.
- the anode (1) is an electrode that provides positive charge carriers.
- it may be constructed of materials including a metal, a mixture of various metals, a metal alloy, a metal oxide, or a mixture of various metal oxides.
- the anode may be a conductive polymer.
- Suitable metals include the metals of groups Ib, IVa, Va and VIa of the Periodic Table of the Elements and the transition metals of the group Villa.
- mixed metal oxides of groups IIb, INb and IVb of the Periodic Table of the Elements for example indium tin oxide (ITO), are generally used.
- the anode (1) contains an organic material, for example polyaniline, as described, for example, in Nature, Vol. 357, pages 477 to 479 (June 1, 1992). At least either the anode or the cathode should be at least partially transparent in order to be able to decouple the light formed.
- the material used for the anode (1) is preferably ITO.
- Suitable hole conductor materials for the layer (2) of the OLEDs according to the invention are disclosed, for example, in Kirk-Othmer Encyclopedia of Chemical Technology, 4th Edition, Vol. 18, pages 837 to 860, 1996. Both hole transporting molecules and polymers can be used as hole transport material.
- Commonly used hole-transporting molecules are selected from the group consisting of tris- [N- (1-naphthyl) -N- (phenylamino)] triphenylamine (1-naphDATA), 4,4'-bis [N- (1) naphthyl) -N-phenyl-amino] biphenyl ( ⁇ -NPD), N, N'-diphenyl-N, N'-bis (3-methylphenyl) - [1, 1'-biphenyl] -4,4'-diamine (TPD), 1, 1-bis [(di-4-tolylamino) phenyl] cyclohexane (TAPC), N, N'-bis (4-methylphenyl) -N, N'-bis (4-ethylphenyl) - [ 1, 1 '- (3,3'-dimethyl) biphenyl] -4,4'-diamine (ETPD), tetrakis (3-methylphenyl)
- hole transporting polymers are selected from the group consisting of polyvinyl carbazoles, (phenylmethyl) polysilanes and polyanilines. It is also possible to obtain hole transporting polymers by doping hole transporting molecules into polymers such as polystyrene and polycarbonate. Suitable hole-transporting molecules are the molecules already mentioned above.
- the carbene complexes of the formula (I) mentioned above as emitter materials can be used as hole conductor materials, the band gap of the at least one hole conductor material generally being greater than the band gap of the emitter material used. It is Under band gap in the context of the present application, the triplet energy to understand.
- the light-emitting layer (3) contains at least one carbene complex of the formula (I) as emitter material. This may be present alone or together with at least one matrix material in the light-emitting layer. Suitable matrix materials are e.g. Phenothiazine-S, S-dioxide derivatives or compounds which contain aromatic or heteroaromatic rings connected via carbonyl groups, as disclosed in WO2006 / 100298.
- another carbene complex of the formula (I) is used as matrix material, wherein the band gap of the carbene complex used as matrix material is generally greater than the band gap of the emitter material.
- a compound of the formula (II) is used as the matrix material, compounds of the formula (II) which may be mentioned below being preferred as the matrix material.
- the block layer for holes / excitons (4) can typically comprise hole blocker materials used in OLEDs, such as 2,9-dimethyl-4,7-diphenyl-1, 10-phenanthroline (bathocuproine, (BCP)), bis (2-methyl-8 -quinolinato) -4-phenyl-phenylato) -aluminium (III) (BAIq), phenothiazine-S, S-dioxide derivatives and 1,3,5-tris (N-phenyl-2-benzylimidazole) -benzene) (TPBI), wherein TPBI is also suitable as electron-conducting material.
- hole blocker materials used in OLEDs such as 2,9-dimethyl-4,7-diphenyl-1, 10-phenanthroline (bathocuproine, (BCP)), bis (2-methyl-8 -quinolinato) -4-phenyl-phenylato) -aluminium (III) (BAIq), phenothiazine
- the block layer for holes / excitons may comprise a compound of the general formula (II), wherein compounds of the formula (II) which are suitable as hole-blocking / exciton-blocking materials are mentioned below.
- the present invention relates to an OLED according to the invention comprising the layers (1) anode, (2) hole conductor layer, (3) light-emitting layer, (4) block layer for holes / excitons, (5) electron conductor layer and (6 ) Cathode, and optionally further layers, wherein the light-emitting layer (3) contains at least one carbene complex of the formula (I) and the block layer for holes / excitons at least one compound of the formula (II).
- the present invention relates to an OLED according to the invention comprising the layers (1) anode, (2) hole conductor layer, (3) light-emitting layer, (4) block layer for holes / excitons, (5) electron layer and 6) cathode, and optionally further layers, wherein the light-emitting layer (3) at least one carbene complex of the formula (I) and at least one compound of the formula (II) and the block layer for holes / excitons at least one compound of the formula (II) contains.
- the present invention relates to an OLED according to the invention comprising the layers (1) anode, (2) hole conductor layer and / or (2 ') blocking layer for electrons / excitons (the OLED can comprise both the layers (2) and (2') and either the layer (2) or the layer (2 ')), (3) light-emitting layer, (4) block layer for holes / excitons, (5) electron conductor layer and (6) cathode, and optionally further layers, wherein the block layer for electrons / excitons and / or the hole conductor layer and optionally the light-emitting layer (3) contains at least one compound of the formula (II).
- hole conductor materials and electron conductor materials some may fulfill several functions.
- some of the electron-conducting materials are simultaneously hole-blocking materials if they have a deep HOMO. These can be z. B. in the block layer for holes / excitons (4) are used.
- the function as a hole / exciton blocker of the layer (5) is taken over, so that the layer (4) may be omitted.
- the charge transport layers can also be electronically doped in order to improve the transport properties of the materials used, on the one hand to make the layer thicknesses more generous (avoidance of pinholes / short circuits) and on the other hand to minimize the operating voltage of the device.
- the hole conductor materials can be doped with electron acceptors, for example phthalocyanines or arylamines such as TPD or TDTA can be doped with tetrafluorotetracyanchinodimethane (F4-TCNQ).
- the electron conductor materials can be doped, for example, with alkali metals, for example Alq 3 with lithium.
- the electronic doping is known to the person skilled in the art and described, for example, in W. Gao, A. Kahn, J.
- the cathode (6) is an electrode which serves to introduce electrons or negative charge carriers.
- Suitable materials for the cathode are selected from the group consisting of alkali metals of group Ia, for example Li, Cs, alkaline earth metals of group IIa, for example calcium, barium or magnesium, metals of group IIb of the Periodic Table of the Elements (old ILJPAC version) comprising the lanthanides and actinides, for example samarium.
- metals such as aluminum or indium, as well as combinations of all the metals mentioned.
- lithium-containing organometallic compounds or LiF can be applied between the organic layer and the cathode to reduce the operating voltage.
- the OLED according to the present invention may additionally contain further layers which are known to the person skilled in the art.
- a layer can be applied between the layer (2) and the light-emitting layer (3), which facilitates the transport of the positive charge and / or adapts the band gap of the layers to one another.
- this further layer can serve as a protective layer.
- additional layers may be present between the light-emitting layer (3) and the layer (4) to facilitate the transport of the negative charge and / or to match the band gap between the layers.
- this layer can serve as a protective layer.
- the OLED according to the invention contains at least one of the further layers mentioned below:
- Suitable materials for the individual layers are known to the person skilled in the art and disclosed, for example, in WO 00/70655. Furthermore, it is possible that some of the layers used in the OLED according to the invention are surface-treated in order to increase the efficiency of the charge carrier transport. The choice of materials for each of these layers is preferably determined by obtaining an OLED having a high efficiency and a lifetime.
- the preparation of the OLED according to the invention can be carried out by methods known to the person skilled in the art.
- the inventive OLED is produced by successive vapor deposition of the individual layers onto a suitable substrate.
- Suitable substrates are for example glass, inorganic semiconductors or polymer films.
- vapor deposition conventional techniques can be used such as thermal evaporation, chemical vapor deposition (CVD), physical vapor deposition (PVD) and others.
- the organic layers of the OLED can be applied from solutions or dispersions in suitable solvents, using coating techniques known to those skilled in the art.
- the various layers have the following thicknesses: anode (1) 50 to 500 nm, preferably 100 to 200 nm; Hole-conductive layer (2) 5 to 100 nm, preferably 20 to 80 nm, light-emitting layer (3) 1 to 100 nm, preferably 10 to 80 nm, Block layer for holes / excitons (4) 2 to 100 nm, preferably 5 to 50 nm, electron-conducting layer (5) 5 to 100 nm, preferably 20 to 80 nm, cathode (6) 20 to 1000 nm, preferably 30 to 500 nm.
- a. be influenced by the relative thickness of each layer.
- the thickness of the electron transport layer should preferably be chosen such that the position of the recombination zone is tuned to the optical resonator property of the diode and thus to the emission wavelength of the emitter.
- the ratio of the layer thicknesses of the individual layers in the OLED depends on the materials used.
- the layer thicknesses of optionally used additional layers are known to the person skilled in the art. It is possible that the electron-conducting layer and / or the hole-conducting layer have larger thicknesses than the specified layer thicknesses when they are electrically doped.
- the light-emitting layer E and / or at least one of the further layers optionally present in the OLED according to the invention contains at least one compound of the general formula (II). While the at least one compound of the general formula (II) is present in the light-emitting layer E as matrix material together with at least one carbene complex of the general formula (I), the at least one compound of the general formula (II) in the at least one further layer the OLEDs according to the invention are used in each case alone or together with at least one of the other materials mentioned above suitable for the corresponding layers. From substituted or unsubstituted Ci-C2 o alkyl radicals having 1 to 20 carbon atoms are to be understood.
- C 1 - to C 10 -alkyl radicals particularly preferably C 1 to C 6 -alkyl radicals.
- the alkyl radicals can be straight-chain as well as branched or cyclic, the alkyl radicals having at least 3 carbon atoms in the case of cyclic alkyl radicals.
- the alkyl radicals may be selected from the group with one or more substituents consisting of C 1 -C 20 - alkoxy, halogen, preferably F, and C 6 -C 3 o-aryl which may in turn be substituted or unsub- stituiert substituted, be. Suitable aryl substituents as well as suitable alkoxy and halogen substituents are mentioned below.
- kyl group Al examples include methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl and octyl, as well as C 6 -C 3 o-aryl, -C 2 o-alkoxy and / or halogen, especially F, substituted derivatives the said alkyl groups, for example CF 3 .
- n-isomers of the radicals mentioned and branched isomers such as isopropyl, isobutyl, isopentyl, sec-butyl, tert-butyl, neopentyl, 3,3-dimethylbutyl, 3-ethylhexyl, etc. are included.
- Preferred alkyl groups are methyl, ethyl, tert-butyl and CF 3 .
- Suitable cyclic alkyl groups which may also be unsubstituted or substituted by the radicals mentioned above with respect to the alkyl groups, are cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl, cyclononyl and cyclodecyl.
- it may also be polycyclic ring systems, such as decalinyl, norbornyl, bornanyl or adamantyl.
- Suitable CrC 2 O AIkOXy- and -C 2 o-alkylthio groups derived respectively from the above-mentioned -C 20 -alkyl radicals from.
- SC 2 H 5 , SC 3 H 7 , SC 4 H 9 and SC 8 H 17 may be mentioned here
- C 3 H 7 , C 4 H 9 and C 8 H 17 include both the n-isomers and branched isomers such as isopropyl, isobutyl, sec-butyl, tert-butyl and 2-ethylhexyl.
- Particularly preferred alkoxy or alkylthio groups are methoxy, ethoxy, n-octyloxy, 2-ethylhexyloxy and SCH 3 .
- Suitable halogen radicals or halogen substituents for the purposes of the present application are fluorine, chlorine, bromine and iodine, preferably fluorine, chlorine and bromine, particularly preferably fluorine and chlorine, very particularly preferably fluorine.
- Suitable pseudohalogen radicals in the context of the present application are CN, SCN, OCN, N 3 and SeCN, CN and SCN being preferred. Most preferred is CN.
- C 6 -C 3 -aryl residues of cyclic mono-, bicyclic or tricyclic aromatic compounds are derived that do not contain ring heteroatoms.
- the term aryl for the second ring also includes the saturated form (perhydroform) or the partially unsaturated form (for example, the dihydroform or tetrahyroform), as far as the respective forms are known and stable. That is, the term aryl in the present invention includes, for example, bicyclic or tricyclic radicals in which both both and all three radicals are aromatic, as well as bicyclic or tricyclic radicals in which only one ring is aromatic, and tricyclic radicals wherein two rings are aromatic.
- aryl examples include: phenyl, naphthyl, indanyl, 1, 2-dihydronaphthenyl, 1, 4-dihydronaphthenyl, indyl, anthracenyl, phenanthrenyl or 1, 2,3,4-tetrahydronaphthyl.
- Particularly preferred are C 6 -C 0 -aryl, for example phenyl or naphthyl, very particularly preferably C 6 -aryl, for example phenyl.
- the C ⁇ -Cso-aryl radicals may be unsubstituted or substituted by one or more further radicals.
- Suitable other radicals are selected from the group consisting of -C 2 -alkyl, C 6 -C 3 -aryl or substituents having donor or acceptor action, suitable substituents are mentioned with donor or acceptor below.
- the C 6 -C 30 -aryl radicals are unsubstituted or substituted by one or more CrC 2 o-alkoxy groups, CN, CF 3 , F or amino groups (NR 14 R 15 , suitable radicals R 14 and R 15 are mentioned above) , Further preferred substitutions of the C 6 -C 30 -aryl radicals depend on the intended use of the compounds of the general formula (II) and are mentioned below.
- Suitable C 6 -C 3 o-aryloxy, C 6 -C 30 -alkyl kylthioreste derive correspondingly from the aforementioned C 6 -C 30 -aryl radicals from. Particularly preferred are phenoxy and phenylthio.
- Unsubstituted or substituted heteroaryl having 5 to 30 ring atoms are to be understood as meaning monocyclic, bicyclic or tricyclic heteroaromatics, some of which can be derived from the abovementioned aryl in which at least one carbon atom in the aryl skeleton is replaced by a heteroatom.
- Preferred heteroatoms are N, O and S.
- the heteroaryl radicals have 5 to 13 ring atoms.
- the backbone of the heteroaryl radicals selected from systems such as pyridine and five-membered heteroaromatics such as thiophene, pyrrole, imidazole or furan.
- backbones may optionally be fused with one or two six-membered aromatic radicals.
- Suitable fused heteroaromatics are carbazolyl, benzimidazolyl, benzofuryl, dibenzofuryl or dibenzothiophenyl.
- the backbone may be substituted at one, several or all substitutable positions, suitable substituents being the same as those already mentioned under the definition of C 6 -C 30 -aryl.
- the heteroaryl radicals are unsubstituted.
- Suitable heteroaryl radicals are, for example, pyridin-2-yl, pyridin-3-yl, pyridin-4-yl, thiophen-2-yl, thiophen-3-yl, pyrrol-2-yl, pyrrol-3-yl, furan-2 - yl, furan-3-yl and imidazol-2-yl and the corresponding benzanellated radicals, in particular particular carbazolyl, benzimidazolyl, benzofuryl, dibenzofuryl or dibenzothiophenyl.
- Preferred substituents with donor or acceptor action are selected from the group consisting of: C 1 - to C 20 -alkoxy, preferably C 1 -C 6 -alkoxy, more preferably ethoxy or methoxy; C6-C 30 -aryloxy preferably, C 6 -C 0 aryloxy, most preferably phenyloxy; SiR 14 R 15 R 16 , wherein R 14 , R 15 and R 16 are preferably each independently substituted or unsubstituted alkyl or substituted or unsubstituted phenyl; more preferably at least one of R 14 , R 15 or R 16 is substituted or unsubstituted phenyl, most preferably at least one of R 14 , R 15 and R 16 is substituted phenyl, suitable substituents being mentioned above; Halogen radicals, preferably F, Cl, Br, particularly preferably F or Cl, very particularly preferably F, halogenated C 1 -C 20 -alkyl radicals, preferably
- CF 3 CH 2 F, CHF 2 or C 2 F 5 ;
- Amino preferably dimethylamino, diethylamino or diphenylamino;
- OH pseudohalogen radicals, preferably CN, SCN or OCN, more preferably CN, -C (O) OC r C 4 alkyl, preferably -C (O) OMe, P (O) R 2 , preferably P (O) Ph 2 or SO 2 R 2 , preferably SO 2 Ph.
- Very particularly preferred substituents having donor or acceptor selected from the group consisting of methoxy, phenyloxy, halogenated CrC 4 - alkyl, preferably CF 3, CH 2 F, CHF 2, C 2 F 5, halogen, preferably F, CN, SiR 14 R 15 R 16 , where suitable radicals R 14 , R 15 and R 16 are already mentioned, diphenylamino, -C (O) O-C 4 -alkyl, preferably -C (O) OMe, P (O) Ph 2 , SO 2 Ph.
- the above-mentioned groups with donor or acceptor effect should not be ruled out that also further of the aforementioned radicals and Groups may have a donor or acceptor effect.
- the above-mentioned heteroaryl radicals are also donor or acceptor groups and the dC 2 o-alkyl radicals are donor-donating groups.
- radicals R 14 , R 15 and R 16 mentioned in the abovementioned groups with donor or acceptor action have the meanings already mentioned above, ie R 14 , R 15 , R 16 independently of one another
- Substituted or unsubstituted C 1 -C 20 -alkyl or substituted or unsubstituted C 6 -C 30 -aryl suitable and preferred alkyl and aryl radicals being mentioned above.
- the radicals R 14 , R 15 and R 16 Ci-C ⁇ -alkyl, z.
- R 15 R 16 - R 14 , R 15 and R 16 are preferably each independently substituted or unsubstituted CrC 2 o-alkyl or substituted or unsubstituted phenyl; at least one of R 14 , R 15 or R 16 is particularly preferably substituted or unsubstituted phenyl, very particularly preferably at least one of R 14 , R 15 and R 16 is substituted phenyl, suitable substituents being mentioned above.
- electron-donating substituents and electron-withdrawing substituents further used in the present application are donor-action substituents (electron-donating substituents) and acceptor-action substituents (electron-withdrawing substituents), respectively.
- Suitable electron-donating and electron-withdrawing substituents are thus those already mentioned above with respect to the substituents with donor or acceptor effect substituents.
- the compounds of the formula (II) are disilyl compounds in which the radicals and indices have the following meanings:
- X is NR 1 , S, O, PR 1 , SO 2 , or SO, preferably NR 1 , S, O;
- R 1 is substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C 6 -C 3 o-aryl, or substituted or unsubstituted heteroaryl having 5 to 30 ring atoms; preferably substituted or unsubstituted Cr C2o-alkyl or substituted or unsubstituted C 6 -C 3 -aryl more preferably substituted or unsubstituted C 6 -C 0 aryl or unsubstituted C 2 o alkyl, most preferably substituted or unsubstituted phenyl, suitable substituents being mentioned above;
- R 2 , R 3 , R 4 , R 5 , R 6 , R 7 independently substituted or unsubstituted Ci-C 2 o-alkyl or substituted or unsubstitute
- R 6 or R 7 is substituted or unsubstituted C 6 -C 30 -aryl, more preferably substituted or unsubstituted C 6 -C 0 -Aryl, most preferably substituted or unsubstituted phenyl, wherein suitable substituents are mentioned above, and / or one of R 2 , R 3 or R 4 and / or one of R 5 , R 6 or R 7 is a radical of Structure (c);
- R a , R b independently of one another are substituted or unsubstituted C 1 -C 20 -alkyl, substituted or unsubstituted C 6 -C 30 -aryl, substituted or unsubstituted heteroaryl having 5 to 30 ring atoms, or a substituent with donor or acceptor action, where suitable and preferred substituents with donor or acceptor are mentioned above;
- R 14, R 15, R 16 are each independently substituted or unsubstituted Ci-C 20 alkyl or substituted or unsubstituted C 6 -C 30 aryl, preferably substituted or unsubstituted C 6 alkyl or substituted or unsubstituted C 6 -C 0 -aryl wherein R 14 , R 15 and R 16 particularly preferably independently represent substituted or unsubstituted dC 20 alkyl or substituted or unsubstituted phenyl; at least one of R 14 , R 15 or R 16 is particularly preferably substituted or unsubstituted phenyl, very particularly preferably at least one of R 14 , R 15 and R 16 is substituted phenyl, suitable substituents being mentioned above;
- q, r are each independently 0, 1, 2 or 3, where, when q or r are 0, all substitutable positions of the aryl radical carry hydrogen atoms, preferably 0.
- the present invention relates to an organic light emitting diode according to the invention, wherein the group X is NR 1 , wherein the radical R 1 has already been defined above, wherein at least one of R 1 to R 7 , R a or R b in the compounds of Formula (II) contains at least one heteroatom.
- Preferred heteroatoms are N, Si, halogen, in particular F or Cl, O, S or P.
- the heteroatom may be in the form of a substituent on at least one of the radicals R 1 to R 7 , R a or R b or in the form of part of a substituent or present in the backbone of at least one of R 1 to R 7 , R a or R b .
- Suitable substituents or basic skeletons are known to the person skilled in the art and are mentioned under the definitions of the radicals R 1 to R 7 , R a or R b .
- a preferred embodiment of the present invention relates to an organic light emitting diode according to the present invention, wherein at least one of R 2 , R 3 or R 4 and / or at least one of R 5 , R 6 or R 7 in the compounds of formula (II ) substituted or unsubstituted C 6 -C 30 -ArVl mean.
- Preferred aryl radicals and their substituents have already been mentioned above.
- a further embodiment of the present invention relates to an organic light-emitting diode according to the invention, in which the compound of the general formula (II) is a 3,6-disilyl-substituted compound of the general formula (IIa):
- NR 1 S, O, PR 1 , SO 2 or SO preferably NR 1 , S or O; particularly preferably NR 1 ;
- R 1 is substituted or unsubstituted C 1 -C 20 -alkyl, substituted or unsubstituted C 6 -C 30 -arVl or substituted or unsubstituted heteroaryl having 5 to 30 ring atoms; preferably substituted or unsubstituted C 6 -
- R 2 , R 3 , R 4 , R 5 , R 6 , R 7 are independently substituted or unsubstituted dC 20 alkyl or substituted or unsubstituted C 6 -C 30 aryl or a structure of general formula (c); at least one of R 2 , R 3 or R 4 and / or at least one of R 5 , R 6 or R 7 preferably denotes substituted or unsubstituted C 6 -C 30 -aryl, particularly preferably substituted or unsubstituted C 6 - Ci 0 -ArVl, most preferably substituted or unsubstituted phenyl, wherein suitable substituents are mentioned above, and / or one of the radicals R 2 , R 3 or R 4 and / or one of the radicals R 5 , R 6 or R 7 is a Remainder of the structure (c);
- R 8 , R 9 , R 10 , R 11 , R 12 , R 13 independently of one another are hydrogen or those mentioned for R a and R b
- Phenyl more preferably at least one of R 14 , R 15 or R 16 is substituted or unsubstituted phenyl, most preferably at least one of R 14 , R 15 and R 16 is substituted phenyl, suitable substituents being mentioned above;
- the compounds of the formula (II) used in the organic light-emitting diodes according to the invention for the radicals R 1 to R 7 , R a and R b and the group X have the following meanings:
- R 1 is substituted or unsubstituted C 6 -C 30 aryl or substituted or unsubstituted heteroaryl group having 5 to 30 ring atoms, preferably substituted or unsubstituted C 6 -C 0 -aryl, more preferably substituted or unsubstituted phenyl, suitable substituents are specified above;
- R 2, R 3, R 4, R 5, R 6, R 7 are each independently substituted or unsubstituted Ci-C 2 o alkyl or substituted or unsubstituted C 6 -C 30 aryl, or a structure of the general formula (c) , preferably independently of one another substituted or unsubstituted CrC ⁇ -alkyl or substituted or unsubstituted
- C 6 -C 0 -aryl more preferably substituted or unsubstituted C C ⁇ alkyl, or substituted or unsubstituted phenyl; wherein in one embodiment at least one of R 2 , R 3 or R 4 and / or at least one of R 5 , R 6 or R 7 is substituted or unsubstituted C 6 -C 30 -aryl, preferably substituted or unsubstituted C 6 -C 12 0 -aryl, more preferably substituted or unsubstituted phenyl group; preferred substituents being mentioned above;
- R 8 , R 9 , R 10 , R 11 , R 12 , R 13 independently of one another are hydrogen or those mentioned for R a and R b
- R 14, R 15, R 16 each independently substituted or unsubstituted C 20 alkyl or substituted or unsubstituted C 6 -C 30 aryl, preferably substituted or unsubstituted Ci-C 6 alkyl or substituted or unsubstituted C 6 -C 0 -Aryl, wherein R 14 , R 15 and R 16 particularly preferably independently represent substituted or unsubstituted C 1 -C 20 alkyl or substituted or unsubstituted phenyl; at least one of R 14 , R 15 or R 16 is particularly preferably substituted or unsubstituted phenyl, very particularly preferably at least one of R 14 , R 15 and R 16 is substituted phenyl, suitable substituents being mentioned above.
- X in the formulas mentioned under iia) and (iv) is preferably O, S, SO or SO 2 .
- the present invention relates to an organic light emitting diode in which a compound of formula (II) is used, wherein the radical R 1 , and / or at least one of the radicals R 2 , R 3 and R 4 and or at least one of the radicals from the group R 5 , R 6 and R 7 is independently of one another substituted or unsubstituted C 6 -aryl of the following formula:
- R 5 17 hydrogen, substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C ⁇ -Cso-aryl, substituted or unsubstituted heteroaryl having 5 to 30 ring atoms, a substituent having donor or acceptor action, overall suitable substituents with donor or acceptor action are mentioned above, or a radical of the general formula a or b
- X ' is N or P
- the radicals and indices X ", R 2' , R 3 ' , R 4' , R 5 ' , R 5" , R 6' , R 6 " , R 7 ' , R 7" , R a ' , R a " , R b' , R b" , q ⁇ q ", r 'and r" independently represent the radicals and indices X, R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R a , R b , q and r have the meanings mentioned; or one of the radicals R 2 , R 3 or R 4 and / or one of the radicals R 5 , R 6 or R 7 is a radical of the general formula c
- radicals and indices X '', R 5 , R 6 , R 7 , R a , R b , q '''andr''independently of one another denote the radicals and indices X, R 5 , R 6 , R 7 , R a , R b , q and r have mentioned meanings.
- Preferred radicals R 17 are selected from the group consisting of hydrogen, substituted or unsubstituted Ci-C 6 alkyl, substituted or unsubstituted C 6 -C 0 aryl, substituted or unsubstituted heteroaryl group having 5 to 13 ring atoms, preferably carbazolyl, a substituent having Donor or acceptor action selected from the group consisting of C 1 - to C 2 o-alkoxy, preferably C 1 -C 6 -alkoxy, more preferably ethoxy or methoxy; C 6 to C 3 o-aryloxy, preferably C 6 -C 0 aryloxy, most preferably phenyloxy; SiR 14 R 15 R 16 ; Halogen radicals, preferably F, Cl, Br, more preferably F or Cl, most preferably F, halogenated CrC 2 O- Alkyl radicals, preferably halogenated C 1 -C 6 -alkyl radicals, very particularly preferably fluorinated C
- R 14 , R 15 and R 16 are each independently substituted or unsubstituted d- to C 6 - Alkyl or substituted or unsubstituted Ce- to Cio-aryl and - in the case of SiR 14 R 15 R 16 - preferably independently substituted or unsubstituted alkyl or substituted or unsubstituted phenyl; at least one of R 14 , R 15 or R 16 is particularly preferably substituted or unsubstituted phenyl, very particularly preferably at least
- the radicals R 17 are independently selected from the group consisting of methoxy, phenyloxy, unsubstituted Ci-C 4 alkyl, preferably as methyl, halogenated C r C 4 alkyl, preferably CF 3, CHF 2, CH 2 F , C 2 F 5, CN, halogen, preferably F, -C (O) OC r C 4 alkyl, preferably -C (O) OMe, P (O) Ph 2 , and substituted or unsubstituted heteroaryl having 5 to 13 ring atoms , preferably carbazolyl.
- the indices r and q in the compounds of the formula (II) denote O, d. H. all substitutable positions of the aryl groups carry hydrogen atoms. For all other radicals and indices, the meanings given above apply.
- the compounds of the formula (II) used according to the invention can be used in various layers of the organic light-emitting diode according to the invention, suitable and preferred layer sequences being mentioned above in the OLEDs according to the invention.
- the present invention relates to organic light-emitting diodes, wherein the compounds of formula (II) are used in the light-emitting layer E as a matrix.
- the present invention relates to an organic light-emitting diode according to the invention, in which the compounds of the formula (II) are used in the block layer for electrons as electron / exciton blocker and / or in the hole injection layer and / or in the hole conductor layer. It is also possible that the compounds of the formula (II) are further present in the light-emitting layer E and / or one or more of the layers mentioned below.
- the present invention relates to an organic light-emitting diode according to the invention, in which the compounds of the formula (II) are present in the block layer for holes as hole / exciton blocker and / or in the electron Injection layer and / or be used in the electron conductor layer. It is also possible that the compounds of the formula (II) are present in the light-emitting layer E and / or one or more of the abovementioned layers.
- the compounds of the formula (II) have different preferred radicals R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R a and R b and different groups X on.
- the LUMO of the block layer for electrons is higher in energy than the LUMO of the materials used in the light-emitting layer (both of the emitter material and optionally used matrix materials).
- Suitable substitution patterns of the compounds of the formula (II) which are suitable as electron and / or exciton blocker materials are thus dependent inter alia on the electronic properties (in particular the position of the LUMO) of the materials used in the light-emitting layer.
- the HOMO of the block layer for electrons is higher in energy than the HOMOs of the materials present in the light-emitting layer (both of the emitter materials and of the optionally present matrix materials).
- Suitable substitution patterns of the compounds of the formula (II) which are suitable as hole and / or exciton blocker materials are thus dependent inter alia on the electrochemical properties (in particular the position of the HOMOs) of the materials present in the light-emitting layer.
- radicals R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R a and R b of the compounds of the formula (II) depending on their use in different layers of the inventive OLED are mentioned below . It should be noted that other than the below-mentioned preferred substitutions of the compounds of formula (II) for use in the various layers - depending on the electronic properties of the other layers of the OLED, in particular depending on the electronic properties of the light emitting layer - may be suitable in principle.
- a preferred embodiment of the present invention relates to an organic light-emitting diode, wherein the compounds of the formula (II) in a block layer for electrons, in a hole injection layer and / or in a hole conductor layer and / or in the light-emitting layer E as matrix materials be used.
- Preferred compounds of the formula (II) which can be employed in at least one of the abovementioned layers have at least one radical R 1 , R 2 , R 3 , R 4 , R 5 , R 6 or R 7 which is substituted or unsubstituted C 1 -C 20 -alkyl, heteroaryl having 5 to 30 ring atoms, substituted or unsubstituted C 6 -C 30 -arVl, alkyl-substituted C 6 -C 30 -aryl (where "alkyl-substituted” is substituted by C 1 -C 20 -alkyl C 6 - C 30 aryl group), with at least one substituent having a donor action substituted C 6 -C 30 aryl or heteroaryl having 5 to 30 ring atoms substituted C 6 -C 30 aryl or a substituent with donor or, in the case of R 2 , R 3 , R 4 , R 5 , R 6 or R 7 , is
- Suitable substituents with donor are preferably selected from the group consisting of substituted or unsubstituted 6 -alkyl, preferably methyl, substituted or unsubstituted C 6 -C 0 aryl, substituted or unsubstituted electron-rich heteroaryl having five to 30 ring atoms, preferably selected from the group consisting of carbazolyl, pyrrolyl, imidazolyl, pyrazolyl, triazolyl, oxazolyl, thiophenyl, preferably carbazolyl, pyrrolyl and thiophenyl, especially preferably carbazolyl, Ci-C2 o alkoxy, preferably -C 6 - alkoxy, particularly preferably methoxy and ethoxy, C 6 -C 30 -aryloxy, preferably C 6 -C 0 - aryloxy, most preferably phenyloxy, Ci- C 20 alkylthio, dC
- the at least one radical which is used in the abovementioned layers is particularly preferably a C 6 -aryl radical of the formula (d) which is substituted by at least one donor-active substituent and / or at least one heteroaryl radical having from 5 to 30 ring atoms.
- R 18 are each independently substituted or unsubstituted C 1 -C 6 -alkyl, preferably methyl, substituted or unsubstituted C 6 -C 10 -aryl, C 1 -C 20 -alkoxy, preferably C 1 -C 6 -alkoxy, more preferably methoxy and ethoxy, C 6 - C 30 - aryloxy, preferably C 6 -C 0 aryloxy, most preferably phenyloxy, -C 20 - alkylthio, preferably C 6 alkylthio, more preferably -SCH 3, C 6 -C 30 -arylthio, preferably C 6 -C 0 - Arylthio, particularly preferably -SPh, SiR 14 R 15 R 16 , where R 14 , R 15 and R 16 have the abovementioned meanings and preferably denote donor-substituted phenyl groups, amino (-NR 14 R 15 ), preferably diphenylamino
- Preferred groups R 18 are selected from the group consisting of methoxy, ethoxy, phenoxy, with methoxy being particularly particularly preferred, carbazolyl, pyrrolyl, imidazolyl, pyrazolyl, triazolyl, oxazolyl and thiophenyl, where methoxy, phenyloxy, carbazolyl and NR 14 R 15 where R 14 and R 15 are phenyl or ToIyI are very particularly preferred.
- the compounds of the formula (II) used in the abovementioned layers particularly preferably have at least one radical R 1 , R 2 , R 3 , R 4 , R 5 , R 6 or R 7 selected from the group consisting of
- At least the radical R 1 is a C 6 -aryl radical of the formula (d) which is substituted by at least one substituent having a donor effect and / or at least one heteroaryl radical having from 5 to 30 ring atoms;
- R 2 , R 3 , R 4 , R 5 , R 6 and R 7 are preferably phenyl, methyl or phenyl substituted with methoxy or phenyloxy.
- Another object of the present invention relates to an organic light-emitting diode according to the invention, wherein at least one compound of formula (II) is present in at least one of the layers selected from light-emitting layer E, block layer for holes, electron injection layer and electron conductor layer.
- Preferred compounds of the formula (II) used in the abovementioned layers have at least one radical R 1 , R 2 , R 3 , R 4 , R 5 , R 6 or R 7 which has at least one substituent with acceptor action (electron-withdrawing radical).
- Substituted d- to C 2 o-alkyl, with at least one substituent with acceptor C 6 -C 3 o-substituted aryl, with at least one heteroaryl radical having 5 to 30 ring atoms substituted C 6 -C 30 -aryl or a substituent with acceptor is.
- Suitable substituents with acceptor action are selected from the group consisting of electron-poor heteroaryls having 5 to 30
- Halogen substituted CrC 2 o-alkyl, pseudohalogen radicals, amido (-C O (NR 14 ),
- R 14, R 15 and R 16 is substituted or unsubstituted Cr C 20 alkyl, preferably substituted or unsubstituted Ci-C 6 alkyl, or substituted or unsubstituted C 6 -C 3 o-aryl, preferably substituted or unsubstituted C 6 -Ci 0 -
- the at least one radical which is used in the abovementioned layers is a substituted C ⁇ -aryl radical of the formula (e)
- p is 1, 2, 3, 4 or 5, preferably 1, 2 or 3, more preferably 1 or 2, and
- R 14 represents substituted or unsubstituted electron-poor heteroaryl having five to 30 ring atoms, preferably selected from the group consisting of pyridine, pyrimidine and triazine.
- the compounds of the formula (II) used in the abovementioned layers particularly preferably have at least one radical R 1 , R 2 , R 3 , R 4 , R 5 , R 6 or R 7 selected from the group consisting of:
- the present invention relates to compounds of general formula (II) as defined above, wherein in the event that X is NR 1 , at least one of R 1 to R 7 , R a or R b in the compounds of formula (II) contains at least one heteroatom.
- X is NR 1 , S, O, PR 1 , SO 2 or SO;
- R 1 is substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C ⁇ -aryl or substituted or unsubstituted heteroaryl having 5 to 30 ring atoms;
- R 2, R 3, R 4, R 5, R 6, R 7 are each independently substituted or unsubstituted CrC 2O -alkyl or substituted or unsubstituted C ⁇ -aryl or a structure of the general formula NEN (c)
- R 14 , R 15 , R 16 are independently substituted or unsubstituted C 1 -C 20 alkyl or substituted or unsubstituted C 6 -C 30 aryl; q, r independently of one another are O, 1, 2 or 3; in which case, when q or r is O, all substitutable positions of the aryl radical are substituted by hydrogen, where the radicals and indices in the group of the formula (c) X '', R 5 '', R 6 '', R 7 '", R a '", R b '", q'" and r '"independently represent the radicals and indices of the compounds of general formula (II) X, R 5 , R 6 , R 7 , R a , R b , q and r have the meanings mentioned;
- At least one of the radicals R 1 to R 7 , R a or R b in the compounds of the formula (II) contains at least one heteroatom.
- at least one of the radicals R 2 , R 3 or R 4 and / or at least one of the radicals R 5 , R 6 or R 7 preferably denotes substituted or unsubstituted C 6 -C 3 O-ArVl.
- the compound of general formula (II) is particularly preferably a 3,6-disilyl-substituted compound of general formula (IIa):
- NR 1 S, O, PR 1 , SO 2 or SO preferably NR 1 , S or O; particularly preferably NR 1 ;
- R 1 is substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C 6 -C 30 -aryl or substituted or unsubstituted heteroaryl having 5 to 30 ring atoms; preferably substituted or unsubstituted C 6 -C 30 aryl or substituted or unsubstituted C 20 -alkyl more preferably substituted or unsubstituted C 6 -C 0 -C 20 -alkyl or unsubstituted aryl very particularly preferably substituted or unsubstituted phenyl;
- R 2 , R 3 , R 4 , R 5 , R 6 , R 7 are independently substituted or unsubstituted C 1 -C 20 -alkyl or substituted or unsubstituted C 6 -C 30 -aryl or a structure of general formula (c);
- At least one of the radicals R 2, R 3 or R 4 and / or at least one of the radicals R 5, R 6 or R 7 is substituted or unsubstituted C 6 -C 30 - aryl, more preferably substituted or unsubstituted C 6 -C 0 -Aryl, very particularly preferably substituted or unsubstituted phenyl, and / or one of the radicals R 2 , R 3 or R 4 and / or one of the radicals R 5 , R 6 or R 7 is a radical of the structure (c);
- radical R 1 and / or at least one of the radicals from the group R 2 , R 3 and R 4 and / or at least one of the radicals from the group R 5 , R 6 and R 7 are preferred in the compounds of the formula (II) independently substituted or unsubstituted C ⁇ -aryl of the following formula:
- p is 0, 1, 2, 3, 4 or 5, preferably 0, 1, 2 or 3, particularly preferably 0, 1 or 2;
- R 17 is hydrogen, substituted or unsubstituted C 2 o alkyl, substituted or unsubstituted C ⁇ -Cso-aryl, substituted or unsubstituted heteroaryl having 5 to 30 ring atoms, a substituent having a donor or acceptor, or a radical of general formula A or B
- X 'N or P means, and the radicals and indices X ", R 2 ' , R 3' , R 4 ' , R 5' , R 5" , R 6 ' , R 6 " , R 7' , R 7" , R a ' , R a " , R b ' , R b " , q ⁇ q", r' and r "independently of one another represent the radicals and indices X, R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R a , R b , q and r have the meanings mentioned;
- radicals R 2 , R 3 or R 4 and / or one of the radicals R 5 , R 6 or R 7 is a radical of the general formula c
- radicals and indices X '", R 5'" , R 6 '" , R 7'" , R a '" , R b'" , q '"and r'" independently of one another represent the radicals and indices X , R 5 , R 6 , R 7 , R a , R b , q and r have mentioned meanings.
- Particularly preferred compounds of the formula (II) correspond to the abovementioned compounds of the formula (II) which are preferably used in the OLEDs according to the invention, where, in the event that X denotes NR 1 , at least one of the radicals R 1 to R 7 , R a or R b in the compounds of formula (II) contains at least one heteroatom.
- a typical carbazole synthesis is the Borsche-Drechsel cyclization (Borsche, Ann., 359, 49 (1908); Drechsel, J. prakt. Chem., [2], 38, 69, 1888).
- tetrahydrocarbocoles can be prepared according to methods known to those skilled in the art, e.g. B. by condensation of optionally suitably substituted phenylhydrazine with optionally suitably substituted cyclohexanone, wherein the corresponding imine is obtained.
- an acid-catalyzed rearrangement and ring closure reaction takes place to give the corresponding tetrahydrocarbozole.
- X is NR 1 , SO, SO 2 , S, O or PR 1 or NH or PH or PPh.
- radicals R 1 in the case that X is NH or PH, before or after the introduction of the radicals R a , R b , SiR 2 R 3 R 4 and SiR 5 R 6 R 7 , as far as the radicals R a and R b in the compounds of the formula (II), or for introducing the radicals R a , R b , SiR 2 R 3 R 4 and SiR 5 R 6 R 7 suitable precursor compounds are introduced.
- X NR 1 and PR 1 :
- Variant b) is particularly preferred when R 1 is substituted or unsubstituted C 1 -C 20 -alkyl or C 6 -C 30 -arVl or C 1 -C 20 -alkyl-substituted C 6 -C 30 -aryl.
- the present invention therefore relates to a process for preparing the compounds of the formula (II) according to the invention and used according to the invention,
- Suitable precursor compounds for introducing the radicals R a , R b , SiR 2 R 3 R 4 and SiR 5 R 6 R 7 are in particular the corresponding halogenated, preferably brominated compounds of the general formula (IV):
- Hal is halogen, preferably bromine or iodine, particularly preferably bromine
- n is 0, 1 or 2 (the sum of both n in formula (IV) being at least 1), preferably 1 in each case and X in step ia) and ic)
- X is NH or PH
- X in step ib) is NR 1 or PR 1
- X in step id) is NR 1 , SO, SO 2 , S, O or PR 1 .
- halogenation can be carried out according to methods known to the person skilled in the art.
- bromination or iodination takes place in the 3- and 6-positions of the skeleton of the formula (III).
- bromination with Br 2 is carried out in glacial acetic acid or chloroform at low temperatures, for example 0 0 C.
- the introduction of the radical is preferably carried out by reacting the skeleton of the formula (III) or the compound of the formula (IV) with an alkyl halide or aryl halide or heteroaryl halide of the formula R 1 -Hal, where R 1 is already defined above and HaI is F, Cl, Br or I, preferably Br, I or F.
- Suitable bases are known to the person skilled in the art and are preferably selected from the group consisting of alkali metal and alkaline earth metal hydroxides such as NaOH, KOH, Ca (OH) 2 , alkali metal hydrides such as NaH, KH, alkali metal amides such as NaNH 2 , alkali metal or alkaline earth metal carbonates such as K 2 CO 3 or Cs 2 COs, and alkali metal alkoxides such as NaOMe, NaOEt. Furthermore, mixtures of the abovementioned bases are suitable. Particularly preferred are NaOH, KOH, NaH, or K 2 CO 3 .
- N-alkylation for example disclosed in M. Tosa et al., Heterocyclic Communications, Vol. 7, No. 3, 2001, pp. 277-282
- N-arylation or N-heteroarylation for example (N -Arylation) disclosed in H. Gilman and DA Shirley, J. Am. Chem. Soc. 66 (1944) 888; D. Li et al., Dyes and Pigments 49 (2001) 181-186
- Suitable solvents are, for example, polar aprotic solvents such as dimethyl sulfoxide, dimethylformamide or alcohols.
- reaction may further be carried out in a non-polar aprotic solvent, eg, toluene, if a phase transfer catalyst, eg, tetra-n-butylammonium hydrogensulfate, is present (as described, for example, in I. Gozlan et al., J. Heterocycl. 21 (1984) 613-614).
- a phase transfer catalyst eg, tetra-n-butylammonium hydrogensulfate
- the N- (hetero) arylation can be carried out, for example, by copper-catalyzed coupling of the compound of the formula (III) or (IV) with a (hetero) aryl halide, for example an arylidide (Ullmann reaction).
- the introduction of the radical R 1 preferably takes place by reacting the compound of the formula (III) or (IV) with an alkyl, aryl or heteroaryl fluoride in the presence of NaH in DMF (nucleophilic substitution) or by reaction with an alkyl, aryl or heteroaryl bromide or iodide under Cu / base (Ullmann, supra) or Pd catalysis.
- the molar ratio of the compound of the formula (III) or (IV) to the alkyl halide or (hetero) aryl halide of the formula R 1 -Hal is generally 1: 1 to 1:15, preferably 1: 1 to 1: 6, especially preferably 1: 4.
- the N-alkylation or N- (hetero) arylation is generally carried out at a temperature from 0 to 220 0 C., preferably 20 to 200 0 C.
- the reaction time is generally 0.5 to 48 hours, preferably 1 to 24 hours.
- the N-alkylation or N-arylation is carried out at atmospheric pressure.
- the crude product obtained is worked up in accordance with methods known to the person skilled in the art.
- the preparation of the desired silylated compounds of the formula (II) is carried out starting from the halogenated precursor compounds of the formula (IV) generally by halogen / metal exchange and subsequent silylation by methods known to the person skilled in the art.
- the preparation is carried out in a first step by halogen / metal exchange by reacting the halogenated compounds of formula (IV) with alkyl lithium or Mg at temperatures of generally -80 0 C to + 80 0 C, preferably at -78 ° C to 0 0 C. (for Alkyllithiumverbinguen) or 0 0 C to 80 0 C (for Mg), more preferably from 0 0 C to 40 0 C (for Mg).
- alkyllithium compounds in particular n-BuLi or tert. -BuLi used.
- the reaction is generally carried out in a solvent, preferably in THF (or ether, preferably diethyl ether).
- the silylation is generally carried out in a solvent. Preferred solvents are THF or ether, preferably diethyl ether.
- the silylation is carried out in direct connection to the reaction in the first step, without working up or isolation of the product obtained after the first step.
- halogen / metal exchange and subsequent silylation are generally repeated until all n halo radicals in the compound of formula (IV) have been replaced by silyl groups.
- the introduction of the protective group is carried out in accordance with methods known in the art. In general, a deprotonation first takes place and then the introduction of a protective group.
- the deprotonation is usually carried out with bases, for example with NaH, nBuLi or tert. -BuLi.
- deprotection is likewise carried out according to methods known to the person skilled in the art. Suitable reagents for deprotection depend on the protective groups used. When SiR 3 is used as a protective group, deprotection is generally carried out with an acid or TBAF (tetrabutylammonium fluoride).
- TBAF tetrabutylammonium fluoride
- the organic light-emitting diode contains at least one carbene complex of the general formula (I) in addition to at least one compound of the formula (II).
- M 1 metal atom selected from the group consisting of transition metals of group IB, IIB, HIB, IVB, VB, VIB, VIIB, VIII, the lanthanides and INA of the Periodic Table of the Elements (CAS version), in each possible oxidation state for the corresponding metal atom ; preferred metal atoms are already mentioned above;
- carbene carbene ligand which may be neutral or monoanionic and mono-, bi- or tridentate; the carbene ligand may also be a bis- or tris-color ligand;
- L mono- or dianionic ligand, preferably monoanionic ligand, which may be mono- or bidentate;
- n number of carbene ligands where n is at least 1, preferably 1 to 6, and the carbene ligands in the complex of formula I may be the same or different at n> 1;
- n 0 or ⁇ 1, preferably 0 to 5, and the ligands L can be the same or different at m> 1;
- o can be 0 or ⁇ 1, preferably 0 to 5, and the ligands K o> 1 can be the same or different;
- Preferred carbene complexes of the formula (I) which are preferably used are mentioned in WO 2005/019373, WO 2005/1 13704, WO 06/018292, WO 06/056418 and the non-prepublished European applications with the file references 06112198.4, 061 12228.9, 06116100.6 and 061 16093.3 , Particularly preferred carbene complexes are mentioned in WO 05/019373 and WO 06/056148.
- the disclosure of said WO and EP applications is hereby explicitly incorporated by reference, and these disclosures are to be considered incorporated into the content of the present application.
- suitable carbene complexes of the formula (I) for use in the OLEDs of the invention contain carbene ligands of the structures disclosed below, inter alia in WO 2005/019373 A2 (the designation of the variables used below was taken from the application WO 2005/019373 A2; with regard to the more precise definition of the variables, reference is expressly made to this application):
- z, z are the same or different, CH or N;
- R 12 , R 12 are identical or different, an alkyl, aryl, heteroaryl or alkenyl radical, preferably an alkyl or aryl radical or in each case 2 radicals R 12 or R 12 together form a fused ring which optionally has at least one heel teroatom, preferably N, may contain, preferably in each case 2 radicals R 12 or R 12 together form a fused aromatic C 6 ring, which may be fused to this, preferably six-membered, aromatic ring optionally one or more further aromatic rings, each conceivable annulation is possible, and the fused radicals may in turn be substituted; or R 12 or R 12 is a radical with donor or acceptor action, preferably selected from the group consisting of halogen radicals, preferably F, Cl, Br, particularly preferably F; Alkoxy, aryloxy, carbonyl, ester, amino, amide, CHF 2 , CH 2 F, CF 3 , CN, thio groups and SCN;
- halogen radicals
- t and t ' are identical or different, preferably equal to 0 to 3, where, when t or t'> 1, the radicals R 12 and R 12 may be identical or different, preferably t or t 'is 0 or 1, the radical R 12 or R 12 is, when t or t 'is 1, in the ortho, meta or para position to the point of attachment to the nitrogen atom adjacent to the carbene carbon atom;
- R 4 , R 5 , R 6 , R 7 , R 8 , R 9 and R 11 are hydrogen, alkyl, aryl, heteroaryl, alkenyl or a substituent with donor or acceptor action, preferably selected from halogen radicals, preferably F, Cl, Br, particularly preferably F, alkoxy radicals, aryloxy radicals, carbonyl radicals, ester radicals, amine radicals, amide radicals, CH 2 F groups, CHF 2 groups, CF 3 groups, CN groups, thio groups and SCN groups, preferably hydrogen, alkyl , Heteroaryl or aryl,
- R 10 is alkyl, aryl, heteroaryl or alkenyl, preferably alkyl, heteroaryl or aryl, or in each case 2 radicals R 10 together form a fused ring which may optionally contain at least one heteroatom, preferably nitrogen, preferably form in each case 2 radicals R 10 together fused aromatic C ⁇ ring, which may be fused to this, preferably six-membered aromatic ring optionally one or more further aromatic rings, wherein any conceivable annulation is possible, and the fused radicals may in turn be substituted; or R 10 is a radical having a donor or acceptor action, preferably selected from
- halogen radicals preferably F, Cl, Br, particularly preferably F
- Alkoxy, aryloxy, carbonyl, ester, amino, amide, CHF 2 , CH 2 F, CF 3 , CN, thio groups and SCN v is 0 to 4, preferably 0, 1 or 2, most preferably 0, wherein when v
- the four carbon atoms of the aryl group in formula c, optionally substituted with R 10 carry hydrogen atoms.
- carbene complexes of the formula (I) for use in the OLEDs according to the invention are Ir carbene complexes of the following structures disclosed in WO 2005/019373 A2:
- carbene complexes of the formula (I) are, in particular, also structures disclosed in WO 2006/056418 A2 (the designation of the variables used in the following was taken from the application WO 2006/056418 A2, which expressly becomes more precise referred to this application): ⁇
- M is Ru (III), Rh (III), Ir (III), Pd (II) or Pt (II)
- n Ru (III), Rh (III) and Ir (III) is 3, for Pd (II) and Pt (II) assumes the value 2 and Y 2 and Y 3 signify hydrogen, methyl, ethyl, n-propyl, isopropyl or tert-butyl.
- M is Ir (III) with n equal to 3.
- Y 3 is preferably methyl, ethyl, n-propyl, iso-propyl or tert-butyl.
- carbene complexes of the formula (I) are in particular also:
- M is Ru (III), Rh (III), Ir (III), Pd (II) or Pt (II)
- n Ru (III), Rh (III) and Ir (III) is 3, for Pd (II) and Pt (II) is 2 and Y 3 is hydrogen, methyl, ethyl, n-propyl, iso-propyl or tert-butyl.
- M is Ir (III) with n equal to 3.
- Y 3 is preferably methyl, ethyl, n-propyl, iso-propyl or tert-butyl.
- carbene complexes of the formula (I) are in particular also:
- M is Ru (III), Rh (III) and especially Ir (III), Pd (II) or Pt (II), n is Ru (III), Rh (III) and Ir (III) is 3 and for Pd (II) and Pt (II) assumes the value 2.
- carbene complexes of the formula (I) are in particular also:
- M is Ru (III), Rh (III) and especially Ir (III), Pd (II) or Pt (II), n is Ru (III), Rh (III) and Ir (III) is 3 and for Pd (II) and Pt (II) assumes the value 2.
- complexes with different carbene ligands and / or with mono- or dianionic ligands which may be both mono- and bidentate, are also suitable.
- M is, for example, Ru (III), Rh (III) or Ir (III), in particular Ir (III), and L ' and L "are , for example, ligands selected from the group of ligands L 1 to L 7
- YY 22 is hydrogen, methyl, ethyl, n-propyl, isopropyl or tert-butyl and Y 3 is methyl, ethyl, n-propyl, iso-propyl or tert-butyl. designated.
- LML ' L " examples of complexes of trivalent metal centers M with ligands L (here monoanionic, bidentate ligand) as “spectator ligands” are LML ' L “ , LM (L ' ) 2 and L 2 ML ' , where M is approximately Ru (III), Rh (III) or Ir (III), in particular Ir (III), and L ' and L "have the meaning given above.
- L ' and L " in the complexes LML ' L " this yields:
- Suitable ligands L are, in particular, the acetylacetonate and its derivatives, the picolinate, Schiff's bases, amino acids and the bidentate monoanionic ligands mentioned in WO 02/15645 A1; In particular, the acetylacetonate and Picolinate of interest. In the case of complexes L 2 ML ' , the ligands L may be the same or different.
- Y 3 denotes hydrogen, methyl, ethyl, n-propyl, isopropyl or tert-butyl, in particular methyl, ethyl, n-propyl or iso-propyl.
- R is hydrogen, alkyl or aryl, preferably methyl, ethyl, n-propyl, iso-propyl, tert-butyl or phenyl, and also
- M is Ru (III), Rh (III), Ir (III), Pd (II) or Pt (II),
- n in the case where M is Ru (III), Rh (III) and Ir (III) means the value 3 and in the case where M is Pd (II) and Pt (II) assumes the value 2 and Y 2 and Y 3 are hydrogen, methyl, ethyl, n-propyl, iso-propyl or tert. Butyl mean.
- M is Ir (III) with n equal to 3.
- Y 3 is preferably methyl, ethyl, n-propyl, iso-propyl or tert-butyl.
- the compounds of the formula (II) according to the invention as matrix materials in the light-emitting layer and / or in at least one further layer of the OLEDs according to the invention, it is possible to obtain OLEDs with high efficiency and lifetime.
- the efficiency of the OLEDs according to the invention can be further improved by optimizing the other layers.
- Shaped substrates and new hole-transporting materials, which cause a reduction in the operating voltage or an increase in the quantum efficiency, can also be used in the inventive OLEDs.
- additional layers may be present in the OLEDs to adjust the energy levels of the various layers and to facilitate electroluminescence.
- the OLEDs according to the invention can be used in all devices in which electroluminescence is useful. Suitable devices are preferably selected from stationary and mobile screens and lighting units. Stationary screens are e.g. Screens of computers, televisions, screens in printers, kitchen appliances and billboards, lights and signboards. Mobile screens are e.g. Screens in cell phones, laptops, digital cameras, vehicles, and destination displays on buses and trains.
- the compounds of the formula (II) can be used together with the carbene complex of the formula (I) in OLEDs with inverse structure.
- the compounds of the formula (II) used according to the invention in these inverse OLEDs are preferably used in turn as matrix materials in the light-emitting layer together with at least one carbene complex of the formula (I) and / or in at least one further layer of the OLED.
- the construction of inverse OLEDs and the materials usually used therein are known to the person skilled in the art.
- Another object of the present invention relates to a light-emitting layer containing at least one compound of formula (II) according to the present invention and at least one carbene complex of general formula (I) according to the present invention.
- Preferred compounds of the formula (II) and carbene complexes of the formula (I) are mentioned above.
- the proportion of the at least one compound of the formula (II) in the light-emitting layer of the OLED according to the invention is 10 to 99% by weight, preferably 50 to 99% by weight, particularly preferably 70 to 97% by weight.
- the proportion of the at least one carbene complex of the general formula (I) as emitter material in the light-emitting layer is generally from 1 to 90% by weight, preferably from 1 to 50% by weight, particularly preferably from 3 to 30% by weight. %, wherein the proportions of the at least one compound of the formula (II) and the at least one carbene complex of the general formula (I) used as the emitter compound give 100% by weight.
- the light-emitting layer in addition to the at least one compound of the general formula (II) and the at least one carbene complex of the general formula (I) contains further substances, for. B. further Thinner, further from the compounds of formula (II) different matrix material, wherein z. B. further diluent material is mentioned below.
- a further subject of the present invention is the use of compounds of the general formula II according to the present application as matrix material, hole / exciton blocker material and / or electron / exciton blocker material and / or hole injection material and / or electron injection material and / or Hole conductor material and / or electron conductor material in an organic light-emitting diode containing at least one carbene complex of the general formula I according to the present application.
- the compounds of the formula (II) are preferably used as matrix materials and / or hole / exciton blocker materials in the OLED according to the invention.
- the present invention relates to a device selected from the group consisting of stationary screens such as screens of computers, televisions, screens in printers, kitchen appliances and billboards, lights, billboards and mobile screens such as screens in mobile phones, laptops, digital cameras, vehicles and target displays Buses and trains and lighting units comprising at least one organic light-emitting diode according to the invention or at least one light-emitting layer according to the invention.
- Example 1a Synthesis of 9- (3,5-bis (trifluoromethyl) phenyl) -3,6-dibromo-carbazole
- Carbazole (1 eq), phenyl halide A, potassium carbonate and copper powder are heated to 160-200 0 C and stirred overnight at this temperature. After cooling to room temperature, it is extracted with acetone or methylene chloride. The precipitate is filtered off and purified by column chromatography (silica gel, methylene chloride / cyclohexane).
- Carbazole (1 eq), phenyl iodide B, potassium carbonate and copper powder are heated to 130-160 0C and stirred for 48 h at this temperature. After cooling to room temperature, it is extracted with methylene chloride. Recrystallization from EtOH gives the desired product.
- Example 4c Synthesis of 9- (3,4,5-trimethoxyphenyl) -3,6-bis (triphenylsilyl) carbazole
- Example 4d Synthesis of 3,6-bis - [(3,5-bis (trifluoromethyl) phenyl) -dimethyl-silyl] -9-phenyl-carbazole
- Reaction method 6.02 g (18.47 mmol) of 2,8-dibromodibenzofuran are suspended in 120 ml of THF and carefully added at -78 ° C with 22.9 ml (36.64 mmol) of n-BuLi (1, 6M in hexane). Subsequently, the mixture is stirred at -78 ° C. for 3 h. The reaction mixture is treated with a solution of 10.91 g (37.00 mmol) of chlorotriphenylsilane in 120 ml of THF, to room temperature Allow to warm and stir for 16 h at room temperature. It is cautiously quenched with 10 ml of methanol and then concentrated to dryness.
- the residue is first digested in methanol, then in water and then again in methanol, filtered off and dried.
- the crude product is dissolved in methylene chloride, filtered through silica gel and crystallized by blanketing with cyclohexane. The crystals are filtered off and dried. 9.28 g (73%) of white powder are obtained.
- the imidazolium salt is prepared by deprotonation of dibenzothiophene with nBuLi in THF and subsequent bromination with 1,2-dibromoethane.
- the brominated dibenzothiophene is coupled with imidazole with the addition of CuI, K 2 CO 3 in NMP.
- the imidazolium salt is formed by methylation with MeI in THF.
- Example 1 Preparation of an OLED containing 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) as matrix material (65% by weight) and as hole-ZExcitonenblocker
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment also improves the hole injection properties of the ITO.
- the following organic materials are vapor-deposited on the cleaned substrate at a rate of about 0.5-5 nm / min at about 10 -8 mbar and the hole conductor and exciton blocker is lr (dpbic) 3 (V1) having a thickness of 30 nm applied to the substrate.
- Example 4b 65% by weight of the compound 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) in a thickness of 40 nm, the former compound acting as emitter, the latter as matrix material.
- the material Example 4b is evaporated with a thickness of 5 nm as Excitonen- and hole blocker.
- V2 The synthesis of V2 is described in WO 2006/056418.
- an electron transporter TPBI (1,3,5-tris (N-phenylbenzylimidazol-2-yl) benzene) in a thickness of 50 nm, a 0.75 nm thick lithium fluoride layer, and finally a 110 nm thick Al electrode evaporated.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities. To determine the lifetime, the OLED is operated at a constant current density and recorded the decrease in light output. Lifespan is defined as the time that elapses to one-half of the initial luminance to decrease the luminance.
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment also improves the hole injection properties of the ITO.
- the former compound acts as an emitter, the latter as a matrix material.
- the material 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) is vapor-deposited to a thickness of 10 nm as exciton and hole blocker.
- an electron transporter BCP 2,9-dimethyl-4,7-diphenyl-1, 10-phenanthroline in a thickness of 50 nm, a 0.75 nm thick lithium fluoride layer and finally a 110 nm thick Al electrode are evaporated.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities. To determine the lifetime, the OLED is operated at a constant current density and recorded the decrease in light output. Lifespan is defined as the time that elapses to one-half of the initial luminance to decrease the luminance. For the described OLED, the following electro-optical data result:
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment also improves the hole injection properties of the ITO.
- the material 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) is vapor-deposited to a thickness of 10 nm as exciton and hole blocker.
- an electron transporter TPBI in a thickness of 40 nm, a 0.75 nm thick lithium fluoride layer and finally a 110 nm thick Al electrode are vapor-deposited.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities. To determine the lifetime, the OLED is operated at a constant current density and recorded the decrease in light output. Lifespan is defined as the time that elapses to one-half of the initial luminance to decrease the luminance.
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To eliminate possible organic residues, the substrate is in an ozone furnace for a further 25 minutes a continuous ozone flow. This treatment also improves the hole injection properties of the ITO.
- the material UGH3 is evaporated with a thickness of 10 nm as Excitonen- and hole blocker.
- a combination of materials is 4 nm of 9-phenyl-3,6-bis (triphenylsilyl) -carbazole (Example 4b) and 36 nm TPBI as the electron transporter, a 0.75 nm thick lithium fluoride layer, and finally a 1 10 nm thick Al Electrode evaporated.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities. To determine the lifetime, the OLED is operated at a constant current density and recorded the decrease in light output. Lifespan is defined as the time that elapses to one-half of the initial luminance to decrease the luminance.
- the ratio of the lifetimes of the OLED according to Example 3 and the OLED according to Example 4 is 4: 1.
- Example 5 Typical work instruction 1 for the production of an OLED:
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment also improves the hole injection properties of the ITO.
- an electron transporter BCP (2,9-dimethyl-4,7-diphenyl-1, 10-phenanthroline) in a thickness of 50 nm, a 0.75 nm thick lithium fluoride layer and finally a 110 nm thick Al electrode evaporated.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities.
- the structure of the respective OLED is given in the right column of Table 1 (Device Structure).
- the production of the respective OLED takes place in accordance with the above-mentioned typical working instructions.
- the values for the current efficiency, quantum efficiency (QE) and voltage given in Table 1 are relative values, in each case based on a reference OLED, which is identical in construction to the respective OLED and differs from the respective inventive OLED in that both Matrix as well as exciton and hole blocker 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) are used.
- the values for the current efficiency, quantum efficiency (QE) and voltage given in Table 1 are defined as 100% for the respective reference OLED.
- the OLED used in each case as a reference OLED which has 9-phenyl-3,6-bis (triphenylsilyl) carbazole (Example 4b) both as matrix and as exciton and hole blocker, also serves as a reference for an OLED, the 9- (4-tert-butylphenyl) -3,6-bis (triphenylsilyl) carbazole, both as a matrix and as an exciton and hole blocker.
- the OLEDs listed below in Table 2 are prepared according to the typical procedure described in Example 5.
- the following table shows the electroluminescence data (current efficiency, quantum efficiency (QE) and voltage) for various OLEDs according to the invention.
- the OLEDs mentioned below instead of the material 9-phenyl-3,6-bis (triphenylsilyl) -carbazole (Example 4b) according to the typical procedure of Example 5, in each case another compound of the formula II was used as matrix material and / or blocking material. Otherwise, the OLEDs mentioned below do not differ from those described above
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment further improves the hole injection properties of the ITO.
- the material 9- (4-phenyl) -3,6-bis (triphenylsilyl) -9H-carbazole (4b) is evaporated with a thickness of 10 nm as exciton and hole blocker.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities.
- the ITO substrate used as the anode is first cleaned with commercial cleaning agents for LCD production (Deconex 20NS ® and neutralizing agent 25ORGAN- ACI D ®) and subsequently cleaned in an acetone / isopropanol mixture in an ultrasonic bath. To remove possible organic residues, the substrate is exposed to a continuous flow of ozone for another 25 minutes in an ozone furnace. This treatment further improves the hole injection properties of the ITO.
- the following organic and inorganic materials are vapor-deposited on the cleaned substrate at a rate of about 0.1-5 nm / min at about 10 -8 mbar: as a doped hole conductor, lr (dpbic) 3 is doped to 10% with MoO 3 and with a thickness of 35 nm and applied to the substrate Further 10 nm undoped lr (dpbic) 3 follow as a hole conductor and exciton blocker.
- the material 9- (4-phenyl) -3,6-bis (triphenylsilyl) -9H-carbazole (4b) is evaporated with a thickness of 10 nm as exciton and hole blocker.
- an electron transporter BCP 2,9-dimethyl-4,7-diphenyl-1, 10-phenanthroline in a thickness of 40 nm, a 0.75 nm thick lithium fluoride layer and finally a 110 nm thick Al electrode are evaporated.
- electroluminescence spectra are recorded at different currents or voltages. Furthermore, the current-voltage characteristic is measured in combination with the radiated light output. The light output can be converted by calibration with a luminance meter into photometric quantities.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
Claims
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010513911A JP5675349B2 (ja) | 2007-07-05 | 2008-06-25 | カルベン遷移金属錯体発光体、ならびにジシリルカルバゾール、ジシリルジベンゾフラン、ジシリルジベンゾチオフェン、ジシリルジベンゾホスホール、ジシリルジベンゾチオフェンs−オキシドおよびジシリルジベンゾチオフェンs,s−ジオキシドから選択される少なくとも1つの化合物を含む有機発光ダイオード |
| CN200880104631.0A CN101878552B (zh) | 2007-07-05 | 2008-06-25 | 包含卡宾-过渡金属配合物发射体和至少一种选自二甲硅烷基咔唑、二甲硅烷基二苯并呋喃、二甲硅烷基二苯并噻吩、二甲硅烷基二苯并磷杂环戊二烯、二甲硅烷基二苯并噻吩s-氧化物和二甲硅烷基二苯并噻吩s,s-二氧化物的化合物的有机发光二极管 |
| US12/667,619 US8373159B2 (en) | 2007-07-05 | 2008-06-25 | Organic light-emitting diodes comprising carbene-transition metal complex emitter, and at least one compound selected from disilylcarbazoles, disilyldibenzofurans, disilyldibenzothiophenes, disilyldibenzophospholes, disilyldibenzothiophene s-oxides and disilyldibe |
| EP08774297.9A EP2165377B1 (de) | 2007-07-05 | 2008-06-25 | Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07111809.5 | 2007-07-05 | ||
| EP07111809 | 2007-07-05 | ||
| EP08153309.3 | 2008-03-26 | ||
| EP08153309 | 2008-03-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009003898A1 true WO2009003898A1 (de) | 2009-01-08 |
Family
ID=39766891
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2008/058106 WO2009003898A1 (de) | 2007-07-05 | 2008-06-25 | Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8373159B2 (de) |
| EP (1) | EP2165377B1 (de) |
| JP (1) | JP5675349B2 (de) |
| KR (1) | KR101577465B1 (de) |
| CN (1) | CN101878552B (de) |
| WO (1) | WO2009003898A1 (de) |
Cited By (588)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010184910A (ja) * | 2009-02-13 | 2010-08-26 | Chemiprokasei Kaisha Ltd | 新規なトリアリールホスフィンオキシド誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
| WO2011045337A1 (de) | 2009-10-14 | 2011-04-21 | Basf Se | Dinukleare platin-carben-komplexe und deren verwendung in oleds |
| WO2011051404A1 (de) | 2009-10-28 | 2011-05-05 | Basf Se | Heteroleptische carben-komplexe und deren verwendung in der organischen elektronik |
| WO2011073149A1 (de) | 2009-12-14 | 2011-06-23 | Basf Se | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds |
| WO2011155508A1 (ja) | 2010-06-08 | 2011-12-15 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| WO2011155507A1 (ja) | 2010-06-08 | 2011-12-15 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| WO2011157790A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a dibenzofurane compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| WO2011157779A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a pyridine compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| JP2012036164A (ja) * | 2010-06-17 | 2012-02-23 | ▲いく▼▲雷▼光電科技股▲分▼有限公司 | 有機エレクトロルミネッセンス装置に用いられる化合物及び有機エレクトロルミネッセンス装置 |
| WO2012045710A1 (en) | 2010-10-07 | 2012-04-12 | Basf Se | Phenanthro[9,10-b]furans for electronic applications |
| CN102439111A (zh) * | 2009-05-27 | 2012-05-02 | 檀国大学校产学协力团 | 咔唑系氧化膦化合物和包含该化合物的有机电致发光器件 |
| WO2012080052A1 (en) | 2010-12-13 | 2012-06-21 | Basf Se | Bispyrimidines for electronic applications |
| WO2012111548A1 (ja) | 2011-02-16 | 2012-08-23 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| US8258297B2 (en) | 2007-10-17 | 2012-09-04 | Basf Se | Transition metal complexes with bridged carbene ligands and use thereof in OLEDs |
| WO2012172482A1 (en) * | 2011-06-14 | 2012-12-20 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in oleds |
| US8362246B2 (en) | 2010-12-13 | 2013-01-29 | Basf Se | Bispyrimidines for electronic applications |
| CN102939295A (zh) * | 2010-04-16 | 2013-02-20 | 巴斯夫欧洲公司 | 桥联苯并咪唑-卡宾配合物及其在oled中的用途 |
| EP2582770A1 (de) * | 2010-06-18 | 2013-04-24 | Basf Se | Organische elektronische vorrichtungen mit einer schicht aus mindestens einer metalloorganischen verbindung und mindestens einem metalloxid |
| WO2013104649A1 (en) | 2012-01-12 | 2013-07-18 | Basf Se | Metal complexes with dibenzo[f,h]quinoxalines |
| US8618533B2 (en) | 2008-10-07 | 2013-12-31 | Osram Opto Semiconductors Gmbh | Siloles substituted by fused ring systems and use thereof in organic electronics |
| WO2014012972A1 (en) | 2012-07-19 | 2014-01-23 | Basf Se | Dinuclear metal complexes comprising carbene ligands and the use thereof in oleds |
| WO2014030666A1 (ja) | 2012-08-24 | 2014-02-27 | コニカミノルタ株式会社 | 透明電極、電子デバイス、および透明電極の製造方法 |
| US8692241B1 (en) | 2012-11-08 | 2014-04-08 | Universal Display Corporation | Transition metal complexes containing triazole and tetrazole carbene ligands |
| US8691401B2 (en) | 2010-04-16 | 2014-04-08 | Basf Se | Bridged benzimidazole-carbene complexes and use thereof in OLEDS |
| US8709615B2 (en) | 2011-07-28 | 2014-04-29 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US8716484B1 (en) | 2012-12-05 | 2014-05-06 | Universal Display Corporation | Hole transporting materials with twisted aryl groups |
| US8754232B2 (en) | 2011-02-23 | 2014-06-17 | Universal Display Corporation | Methods of making bis-tridentate carbene complexes of ruthenium and osmium |
| US8822708B2 (en) | 2007-08-08 | 2014-09-02 | Universal Display Corporation | Benzo-fused thiophene / triphenylene hybrid materials |
| WO2014147134A1 (en) | 2013-03-20 | 2014-09-25 | Basf Se | Azabenzimidazole carbene complexes as efficiency booster in oleds |
| WO2014157618A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それを具備した照明装置及び表示装置 |
| WO2014157494A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| US8871361B2 (en) | 2011-02-23 | 2014-10-28 | Universal Display Corporation | Tetradentate platinum complexes |
| WO2014177518A1 (en) | 2013-04-29 | 2014-11-06 | Basf Se | Transition metal complexes with carbene ligands and the use thereof in oleds |
| US8884316B2 (en) | 2011-06-17 | 2014-11-11 | Universal Display Corporation | Non-common capping layer on an organic device |
| US8883322B2 (en) | 2011-03-08 | 2014-11-11 | Universal Display Corporation | Pyridyl carbene phosphorescent emitters |
| US8889864B2 (en) | 2006-02-10 | 2014-11-18 | Universal Display Corporation | Metal complexes of cyclometallated imidazo[1,2-f]phenanthridine and diimidazo[1,2-a:1′,2′-c]quinazoline ligands and isoelectronic and benzannulated analogs thereof |
| US8927749B2 (en) | 2013-03-07 | 2015-01-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8927308B2 (en) | 2011-05-12 | 2015-01-06 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| US8926119B2 (en) | 2011-08-04 | 2015-01-06 | Universal Display Corporation | Extendable light source with variable light emitting area |
| WO2015000955A1 (en) | 2013-07-02 | 2015-01-08 | Basf Se | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| US8932734B2 (en) | 2010-10-08 | 2015-01-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8946697B1 (en) | 2012-11-09 | 2015-02-03 | Universal Display Corporation | Iridium complexes with aza-benzo fused ligands |
| US8952363B2 (en) | 2009-01-16 | 2015-02-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8952362B2 (en) | 2012-08-31 | 2015-02-10 | The Regents Of The University Of Michigan | High efficiency and brightness fluorescent organic light emitting diode by triplet-triplet fusion |
| US8963132B2 (en) | 2010-03-25 | 2015-02-24 | Universal Display Corporation | Solution processable doped triarylamine hole injection materials |
| US8969592B2 (en) | 2012-01-10 | 2015-03-03 | Universal Display Corporation | Heterocyclic host materials |
| US8968887B2 (en) | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| US8987451B2 (en) | 2012-01-03 | 2015-03-24 | Universal Display Corporation | Synthesis of cyclometallated platinum(II) complexes |
| US9005772B2 (en) | 2011-02-23 | 2015-04-14 | Universal Display Corporation | Thioazole and oxazole carbene metal complexes as phosphorescent OLED materials |
| WO2015063046A1 (en) | 2013-10-31 | 2015-05-07 | Basf Se | Azadibenzothiophenes for electronic applications |
| US9040962B2 (en) | 2010-04-28 | 2015-05-26 | Universal Display Corporation | Depositing premixed materials |
| US9054344B2 (en) | 2010-01-20 | 2015-06-09 | Universal Display Corporation | Electroluminescent devices for lighting applications |
| US9054343B2 (en) | 2011-06-17 | 2015-06-09 | Universal Display Corporation | Fine tuning of emission spectra by combination of multiple emitter spectra |
| US9054323B2 (en) | 2012-03-15 | 2015-06-09 | Universal Display Corporation | Secondary hole transporting layer with diarylamino-phenyl-carbazole compounds |
| US9059412B2 (en) | 2012-07-19 | 2015-06-16 | Universal Display Corporation | Transition metal complexes containing substituted imidazole carbene as ligands and their application in OLEDs |
| US9076973B2 (en) | 2008-09-03 | 2015-07-07 | Universal Display Corporation | Phosphorescent materials |
| US9079872B2 (en) | 2010-10-07 | 2015-07-14 | Basf Se | Phenanthro[9, 10-B]furans for electronic applications |
| US9118017B2 (en) | 2012-02-27 | 2015-08-25 | Universal Display Corporation | Host compounds for red phosphorescent OLEDs |
| US9123903B2 (en) | 2007-12-28 | 2015-09-01 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| US9130177B2 (en) | 2011-01-13 | 2015-09-08 | Universal Display Corporation | 5-substituted 2 phenylquinoline complexes materials for light emitting diode |
| US9140428B2 (en) | 2010-06-11 | 2015-09-22 | Universal Display Corporation | Triplet-triplet annihilation up-conversation for display and lighting applications |
| US9142786B2 (en) | 2007-03-08 | 2015-09-22 | Universal Display Corporation | Phosphorescent materials |
| US9142792B2 (en) | 2010-06-18 | 2015-09-22 | Basf Se | Organic electronic devices comprising a layer comprising at least one metal organic compound and at least one metal oxide |
| US9142788B2 (en) | 2011-11-14 | 2015-09-22 | Universal Display Corporation | Host materials for OLEDs |
| US9156870B2 (en) | 2010-02-25 | 2015-10-13 | Universal Display Corporation | Phosphorescent emitters |
| US9163174B2 (en) | 2012-01-04 | 2015-10-20 | Universal Display Corporation | Highly efficient phosphorescent materials |
| US9166175B2 (en) | 2012-11-27 | 2015-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9175211B2 (en) | 2010-03-03 | 2015-11-03 | Universal Display Corporation | Phosphorescent materials |
| US9181270B2 (en) | 2014-02-28 | 2015-11-10 | Universal Display Corporation | Method of making sulfide compounds |
| US9184399B2 (en) | 2012-05-04 | 2015-11-10 | Universal Display Corporation | Asymmetric hosts with triaryl silane side chains |
| US9190621B2 (en) | 2007-03-08 | 2015-11-17 | Universal Display Corporation | Materials for organic light emitting diode |
| US9190623B2 (en) | 2012-11-20 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190620B2 (en) | 2014-03-01 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9196860B2 (en) | 2012-12-04 | 2015-11-24 | Universal Display Corporation | Compounds for triplet-triplet annihilation upconversion |
| US9193745B2 (en) | 2011-11-15 | 2015-11-24 | Universal Display Corporation | Heteroleptic iridium complex |
| US9209411B2 (en) | 2012-12-07 | 2015-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9212197B2 (en) | 2011-05-19 | 2015-12-15 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants |
| US9217004B2 (en) | 2011-11-21 | 2015-12-22 | Universal Display Corporation | Organic light emitting materials |
| US9224958B2 (en) | 2013-07-19 | 2015-12-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9231218B2 (en) | 2012-07-10 | 2016-01-05 | Universal Display Corporation | Phosphorescent emitters containing dibenzo[1,4]azaborinine structure |
| US9252377B2 (en) | 2011-07-14 | 2016-02-02 | Universal Display Corporation | Inorganic hosts in OLEDs |
| US9252363B2 (en) | 2012-10-04 | 2016-02-02 | Universal Display Corporation | Aryloxyalkylcarboxylate solvent compositions for inkjet printing of organic layers |
| WO2016016791A1 (en) | 2014-07-28 | 2016-02-04 | Idemitsu Kosan Co., Ltd (Ikc) | 2,9-functionalized benzimidazolo[1,2-a]benzimidazoles as hosts for organic light emitting diodes (oleds) |
| US9257658B2 (en) | 2011-05-19 | 2016-02-09 | Universal Display Corporation | Method of making organic electroluminescent materials |
| EP2982676A1 (de) | 2014-08-07 | 2016-02-10 | Idemitsu Kosan Co., Ltd. | Benzimidazo[2,1-b]benzoxazole für elektronische Anwendungen |
| EP2993215A1 (de) | 2014-09-04 | 2016-03-09 | Idemitsu Kosan Co., Ltd. | Azabenzimidazo[2,1-a]benzimidazole für elektronische Anwendungen |
| US9287513B2 (en) | 2012-09-24 | 2016-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9293712B2 (en) | 2013-10-11 | 2016-03-22 | Universal Display Corporation | Disubstituted pyrene compounds with amino group containing ortho aryl group and devices containing the same |
| US9306179B2 (en) | 2013-11-08 | 2016-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312499B1 (en) | 2015-01-05 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312505B2 (en) | 2012-09-25 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9315724B2 (en) | 2011-06-14 | 2016-04-19 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in OLEDs |
| US9318710B2 (en) | 2012-07-30 | 2016-04-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9324949B2 (en) | 2013-07-16 | 2016-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3015469A1 (de) | 2014-10-30 | 2016-05-04 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazole für elektronische anwendungen |
| WO2016079169A1 (en) | 2014-11-18 | 2016-05-26 | Basf Se | Pt- or pd-carbene complexes for use in organic light emitting diodes |
| WO2016079667A1 (en) | 2014-11-17 | 2016-05-26 | Idemitsu Kosan Co., Ltd. | Indole derivatives for electronic applications |
| EP3034506A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 4-funktionalisierte Carbazolderivate für elektronische Anwendungen |
| EP3034507A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 1-funktionalisierte Dibenzofurane und Dibenzothiophene für organische Leuchtdioden (OLEDS) |
| US9386657B2 (en) | 2012-03-15 | 2016-07-05 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| US9397302B2 (en) | 2014-10-08 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9397309B2 (en) | 2014-03-13 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent devices |
| US9397310B2 (en) | 2011-07-14 | 2016-07-19 | Universal Display Corporation | Organice electroluminescent materials and devices |
| US9397312B2 (en) | 2011-05-11 | 2016-07-19 | Universal Display Corporation | Process for fabricating metal bus lines for OLED lighting panels |
| EP3053918A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd | 2-Carbazol substituierte Benzimidazole für elektronische Anwendungen |
| EP3054498A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd. | Bisimidazodiazozine |
| US9419225B2 (en) | 2013-03-14 | 2016-08-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3056504A1 (de) | 2015-02-16 | 2016-08-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3061763A1 (de) | 2015-02-27 | 2016-08-31 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3061759A1 (de) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrilsubstituierte dibenzofurane |
| US9435021B2 (en) | 2010-07-29 | 2016-09-06 | University Of Southern California | Co-deposition methods for the fabrication of organic optoelectronic devices |
| US9444075B2 (en) | 2014-11-26 | 2016-09-13 | Universal Display Corporation | Emissive display with photo-switchable polarization |
| US9450198B2 (en) | 2014-04-15 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9450195B2 (en) | 2014-12-17 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3070144A1 (de) | 2015-03-17 | 2016-09-21 | Idemitsu Kosan Co., Ltd. | Siebengliedrige ringverbindungen |
| US9455411B2 (en) | 2008-09-25 | 2016-09-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9455417B2 (en) | 2011-12-13 | 2016-09-27 | Universal Display Corporation | Split electrode for organic devices |
| EP3072943A1 (de) | 2015-03-26 | 2016-09-28 | Idemitsu Kosan Co., Ltd. | Dibenzofuran/carbazol-substituierte benzonitrile |
| US9461254B2 (en) | 2012-01-03 | 2016-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3075737A1 (de) | 2015-03-31 | 2016-10-05 | Idemitsu Kosan Co., Ltd | Benzimidazolo[1,2-a]benzimidazol mit aryl- oder heteroarylnitrilgruppen für organische leuchtdioden |
| US9478758B1 (en) | 2015-05-08 | 2016-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9484541B2 (en) | 2014-10-20 | 2016-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9493698B2 (en) | 2011-08-31 | 2016-11-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502656B2 (en) | 2014-02-24 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502672B2 (en) | 2012-06-21 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3098229A1 (de) | 2015-05-15 | 2016-11-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9512355B2 (en) | 2011-12-09 | 2016-12-06 | Universal Display Corporation | Organic light emitting materials |
| US9512136B2 (en) | 2012-11-26 | 2016-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3101021A1 (de) | 2015-06-01 | 2016-12-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2016193243A1 (en) | 2015-06-03 | 2016-12-08 | Udc Ireland Limited | Highly efficient oled devices with very short decay times |
| US9537106B2 (en) | 2013-05-09 | 2017-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9543532B2 (en) | 2010-06-11 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9540329B2 (en) | 2012-07-19 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9553274B2 (en) | 2013-07-16 | 2017-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3124488A1 (de) | 2015-07-29 | 2017-02-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9590180B2 (en) | 2007-06-23 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590195B2 (en) | 2014-02-28 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590194B2 (en) | 2014-02-14 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3150604A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazol mit benzimidazolo[1,2-a]benzimidazolylgruppen, carbazolylgruppen, benzofurangruppen oder benzothiophengruppen für organische leuchtdioden |
| EP3150606A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole mit benzofuran- oder benzothiophen- gruppen für organische licht emittierende dioden. |
| WO2017056055A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying triazine groups for organic light emitting diodes |
| WO2017056053A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying benzimidazolo[1,2-a]benzimidazolyl groups, carbazolyl groups, benzofurane groups or benzothiophene groups for organic light emitting diodes |
| US9634264B2 (en) | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634265B2 (en) | 2009-04-28 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3159350A1 (de) | 2015-09-03 | 2017-04-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9647217B2 (en) | 2014-02-24 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647221B2 (en) | 2011-07-14 | 2017-05-09 | Universal Display Corporation | Organic light-emitting devices |
| US9647227B2 (en) | 2005-04-13 | 2017-05-09 | Universal Display Corporation | Organic light emitting devices |
| US9647218B2 (en) | 2013-11-14 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017078182A1 (en) | 2015-11-04 | 2017-05-11 | Idemitsu Kosan Co., Ltd. | Benzimidazole fused heteroaryls |
| US9653691B2 (en) | 2012-12-12 | 2017-05-16 | Universal Display Corporation | Phosphorescence-sensitizing fluorescence material system |
| US9663544B2 (en) | 2012-07-25 | 2017-05-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673406B2 (en) | 2009-05-20 | 2017-06-06 | Universal Display Corporation | Metal complexes with boron-nitrogen heterocycle containing ligands |
| US9673407B2 (en) | 2014-02-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9670404B2 (en) | 2012-06-06 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673401B2 (en) | 2013-06-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017093958A1 (en) | 2015-12-04 | 2017-06-08 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole derivatives for organic light emitting diodes |
| US9685617B2 (en) | 2012-11-09 | 2017-06-20 | Universal Display Corporation | Organic electronuminescent materials and devices |
| US9691993B2 (en) | 2014-04-09 | 2017-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017109727A1 (en) | 2015-12-21 | 2017-06-29 | Idemitsu Kosan Co., Ltd. | Hetero-condensed phenylquinazolines and their use in electronic devices |
| US9711730B2 (en) | 2015-01-25 | 2017-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3200255A2 (de) | 2016-01-06 | 2017-08-02 | Konica Minolta, Inc. | Organisches elektrolumineszenzelement, verfahren zur herstellung eines organischen elektrolumineszenzelements, sowie anzeige und beleuchtungsvorrichtung |
| US9725476B2 (en) | 2012-07-09 | 2017-08-08 | Universal Display Corporation | Silylated metal complexes |
| US9735373B2 (en) | 2013-06-10 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9735377B2 (en) | 2005-05-06 | 2017-08-15 | Universal Display Corporation | Phosphorescent emitters and host materials with improved stability |
| US9735378B2 (en) | 2013-09-09 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3205658A1 (de) | 2016-02-09 | 2017-08-16 | Universal Display Corporation | Organische elektrolumineszenzmaterialien und vorrichtungen |
| US9741941B2 (en) | 2014-04-29 | 2017-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748503B2 (en) | 2013-09-13 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748500B2 (en) | 2015-01-15 | 2017-08-29 | Universal Display Corporation | Organic light emitting materials |
| US9748504B2 (en) | 2014-03-25 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755159B2 (en) | 2014-01-23 | 2017-09-05 | Universal Display Corporation | Organic materials for OLEDs |
| US9755164B2 (en) | 2011-06-08 | 2017-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9761814B2 (en) | 2014-11-18 | 2017-09-12 | Universal Display Corporation | Organic light-emitting materials and devices |
| US9761807B2 (en) | 2013-07-15 | 2017-09-12 | Universal Display Corporation | Organic light emitting diode materials |
| US9773986B2 (en) | 2009-11-19 | 2017-09-26 | The University Of Southern California | Copper(I)-carbene complexes and organic electroluminescent devices |
| US9773985B2 (en) | 2012-05-21 | 2017-09-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9783564B2 (en) | 2011-07-25 | 2017-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3231809A2 (de) | 2016-04-11 | 2017-10-18 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| WO2017178864A1 (en) | 2016-04-12 | 2017-10-19 | Idemitsu Kosan Co., Ltd. | Seven-membered ring compounds |
| EP3239161A1 (de) | 2013-07-31 | 2017-11-01 | UDC Ireland Limited | Lumineszente diazabenzimidazol-carben-metall-komplexe |
| US9831447B2 (en) | 2013-10-08 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831437B2 (en) | 2013-08-20 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847498B2 (en) | 2014-04-14 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847496B2 (en) | 2013-12-23 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847497B2 (en) | 2014-02-18 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9853229B2 (en) | 2013-10-23 | 2017-12-26 | University Of Southern California | Organic electroluminescent materials and devices |
| EP3261147A1 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3261146A2 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9862739B2 (en) | 2014-03-31 | 2018-01-09 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| US9871214B2 (en) | 2015-03-23 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871212B2 (en) | 2014-11-14 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3270435A2 (de) | 2016-06-20 | 2018-01-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9876173B2 (en) | 2013-12-09 | 2018-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9882151B2 (en) | 2014-11-14 | 2018-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9899612B2 (en) | 2006-12-08 | 2018-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905784B2 (en) | 2013-11-15 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911931B2 (en) | 2014-06-26 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911928B2 (en) | 2015-03-19 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3297051A1 (de) | 2016-09-14 | 2018-03-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9929357B2 (en) | 2014-07-22 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929360B2 (en) | 2016-07-08 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929353B2 (en) | 2014-04-02 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9935277B2 (en) | 2014-01-30 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9935276B2 (en) | 2013-02-21 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9932359B2 (en) | 2013-08-30 | 2018-04-03 | University Of Southern California | Organic electroluminescent materials and devices |
| EP3301088A1 (de) | 2016-10-03 | 2018-04-04 | Universal Display Corporation | Kondensierte pyridine als organische elektrolumineszente materialien und vorrichtungen |
| EP3305796A1 (de) | 2016-10-07 | 2018-04-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9954180B2 (en) | 2010-08-20 | 2018-04-24 | Universal Display Corporation | Bicarbazole compounds for OLEDs |
| EP3318566A1 (de) | 2012-09-20 | 2018-05-09 | UDC Ireland Limited | Azadibenzofurane für elektronische anwendungen |
| EP3321258A1 (de) | 2016-11-09 | 2018-05-16 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| US9978958B2 (en) | 2012-08-24 | 2018-05-22 | Universal Display Corporation | Phosphorescent emitters with phenylimidazole ligands |
| US9978961B2 (en) | 2014-01-08 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978956B2 (en) | 2015-07-15 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3323822A1 (de) | 2016-09-23 | 2018-05-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9997712B2 (en) | 2013-03-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997716B2 (en) | 2014-05-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003034B2 (en) | 2013-09-30 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003033B2 (en) | 2014-02-18 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008679B2 (en) | 2014-04-14 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008678B2 (en) | 2008-12-12 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008677B2 (en) | 2011-01-13 | 2018-06-26 | Universal Display Corporation | Materials for organic light emitting diode |
| EP3345914A1 (de) | 2017-01-09 | 2018-07-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10033004B2 (en) | 2015-06-01 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10038151B2 (en) | 2014-11-12 | 2018-07-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3354654A2 (de) | 2016-11-11 | 2018-08-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10043987B2 (en) | 2014-09-29 | 2018-08-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10056565B2 (en) | 2013-11-20 | 2018-08-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10069090B2 (en) | 2012-11-20 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10074806B2 (en) | 2013-08-20 | 2018-09-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10079349B2 (en) | 2011-05-27 | 2018-09-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10084143B2 (en) | 2008-09-16 | 2018-09-25 | Universal Display Corporation | Phosphorescent materials |
| EP3381927A1 (de) | 2017-03-29 | 2018-10-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10109799B2 (en) | 2015-05-21 | 2018-10-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10121975B2 (en) | 2013-07-03 | 2018-11-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3401318A1 (de) | 2017-05-11 | 2018-11-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10135007B2 (en) | 2014-09-29 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135008B2 (en) | 2014-01-07 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135006B2 (en) | 2016-01-04 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10144867B2 (en) | 2015-02-13 | 2018-12-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10147892B2 (en) | 2010-12-07 | 2018-12-04 | The University Of Southern California | Organic electroluminescent materials and devices |
| US10153443B2 (en) | 2016-07-19 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153445B2 (en) | 2016-11-21 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10158089B2 (en) | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3418285A1 (de) | 2017-06-20 | 2018-12-26 | Idemitsu Kosan Co., Ltd. | Zusammensetzung mit einem substituierten ir-komplex und einem mit einem heteroatom verbrückten phenylchinazolin |
| EP3418286A1 (de) | 2017-06-23 | 2018-12-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10177316B2 (en) | 2015-02-09 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10177318B2 (en) | 2015-10-29 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10181564B2 (en) | 2015-08-26 | 2019-01-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10199581B2 (en) | 2013-07-01 | 2019-02-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10199582B2 (en) | 2013-09-03 | 2019-02-05 | University Of Southern California | Organic electroluminescent materials and devices |
| US10205105B2 (en) | 2016-08-15 | 2019-02-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10211413B2 (en) | 2012-01-17 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10208026B2 (en) | 2014-03-18 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3444258A2 (de) | 2017-08-10 | 2019-02-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| KR20190020182A (ko) * | 2009-12-14 | 2019-02-27 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| US10236458B2 (en) | 2016-10-24 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256419B2 (en) | 2014-05-08 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10253252B2 (en) | 2014-12-30 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256411B2 (en) | 2015-05-21 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256427B2 (en) | 2014-04-15 | 2019-04-09 | Universal Display Corporation | Efficient organic electroluminescent devices |
| US10270046B2 (en) | 2015-03-06 | 2019-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10276809B2 (en) | 2016-04-05 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297770B2 (en) | 2015-03-27 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297762B2 (en) | 2014-07-09 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10301338B2 (en) | 2014-05-08 | 2019-05-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3489243A1 (de) | 2017-11-28 | 2019-05-29 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| EP3492528A1 (de) | 2017-11-30 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3492480A2 (de) | 2017-11-29 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10340464B2 (en) | 2016-11-10 | 2019-07-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10347851B2 (en) | 2013-12-20 | 2019-07-09 | Udc Ireland Limited | Highly efficient OLED devices with very short decay times |
| US10355222B2 (en) | 2015-02-06 | 2019-07-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10355227B2 (en) | 2013-12-16 | 2019-07-16 | Universal Display Corporation | Metal complex for phosphorescent OLED |
| US10361375B2 (en) | 2014-10-06 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388892B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388893B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10400163B2 (en) | 2013-02-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403830B2 (en) | 2014-05-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403826B2 (en) | 2015-05-07 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403825B2 (en) | 2014-02-27 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411201B2 (en) | 2014-11-12 | 2019-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411200B2 (en) | 2014-08-07 | 2019-09-10 | Universal Display Corporation | Electroluminescent (2-phenylpyridine)iridium complexes and devices |
| US10418569B2 (en) | 2015-01-25 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418562B2 (en) | 2015-02-06 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457699B2 (en) | 2014-05-02 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457864B2 (en) | 2016-02-09 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10461260B2 (en) | 2014-06-03 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10468609B2 (en) | 2016-06-02 | 2019-11-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10476010B2 (en) | 2015-11-30 | 2019-11-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10490753B2 (en) | 2016-12-15 | 2019-11-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10505127B2 (en) | 2016-09-19 | 2019-12-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10522769B2 (en) | 2015-08-18 | 2019-12-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10529931B2 (en) | 2015-03-24 | 2020-01-07 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| US10566547B2 (en) | 2016-07-11 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566552B2 (en) | 2016-04-13 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566546B2 (en) | 2014-07-14 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3613751A1 (de) | 2018-08-22 | 2020-02-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10593892B2 (en) | 2015-10-01 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593890B2 (en) | 2015-04-06 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10600966B2 (en) | 2015-02-27 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10600967B2 (en) | 2016-02-18 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608185B2 (en) | 2016-10-17 | 2020-03-31 | Univeral Display Corporation | Organic electroluminescent materials and devices |
| US10608188B2 (en) | 2017-09-11 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10629820B2 (en) | 2017-01-18 | 2020-04-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636983B2 (en) | 2014-05-08 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636978B2 (en) | 2014-12-30 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644247B2 (en) | 2015-02-06 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644251B2 (en) | 2013-12-04 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10651403B2 (en) | 2016-06-20 | 2020-05-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10662196B2 (en) | 2016-11-17 | 2020-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672998B2 (en) | 2017-03-23 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680183B2 (en) | 2015-02-15 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686143B2 (en) | 2015-03-05 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686140B2 (en) | 2016-06-20 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102013200085B4 (de) | 2012-01-06 | 2020-06-18 | Universal Display Corporation | Hocheffiziente phosphoreszierende Materialien |
| US10707423B2 (en) | 2014-02-21 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10707427B2 (en) | 2016-02-09 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10720587B2 (en) | 2016-07-19 | 2020-07-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10727423B2 (en) | 2016-06-20 | 2020-07-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3689889A1 (de) | 2019-02-01 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3690973A1 (de) | 2019-01-30 | 2020-08-05 | University Of Southern California | Organische elektrolumineszente materialien und vorrichtungen |
| US10741780B2 (en) | 2017-03-10 | 2020-08-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10745431B2 (en) | 2017-03-08 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749113B2 (en) | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10770664B2 (en) | 2015-09-21 | 2020-09-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777754B2 (en) | 2017-04-11 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777749B2 (en) | 2015-05-07 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3709376A1 (de) | 2019-03-12 | 2020-09-16 | Universal Display Corporation | Oled mit triplett-emitter und einer lebensdauer des angeregten zustands von unter 200 ns |
| US10790455B2 (en) | 2017-05-18 | 2020-09-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3715353A1 (de) | 2019-03-26 | 2020-09-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10804475B2 (en) | 2017-01-11 | 2020-10-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10811618B2 (en) | 2016-12-19 | 2020-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822361B2 (en) | 2017-02-22 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10825997B2 (en) | 2015-06-25 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822362B2 (en) | 2017-05-11 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10833276B2 (en) | 2016-11-21 | 2020-11-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840458B2 (en) | 2016-05-25 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840459B2 (en) | 2017-05-18 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10847728B2 (en) | 2015-10-01 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10854826B2 (en) | 2014-10-08 | 2020-12-01 | Universal Display Corporation | Organic electroluminescent compounds, compositions and devices |
| US10862055B2 (en) | 2017-05-05 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862046B2 (en) | 2017-03-30 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10868261B2 (en) | 2014-11-10 | 2020-12-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3750897A1 (de) | 2019-06-10 | 2020-12-16 | Universal Display Corporation | Organische elektrolumineszente materialien und geräte |
| US10870668B2 (en) | 2017-05-05 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873036B2 (en) | 2015-07-07 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873037B2 (en) | 2017-03-28 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10897016B2 (en) | 2016-11-14 | 2021-01-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910577B2 (en) | 2017-03-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910570B2 (en) | 2017-04-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3771717A1 (de) | 2019-07-30 | 2021-02-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3778614A1 (de) | 2019-08-16 | 2021-02-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10930866B2 (en) | 2013-07-25 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930862B2 (en) | 2017-06-01 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930864B2 (en) | 2017-05-10 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10934293B2 (en) | 2017-05-18 | 2021-03-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944062B2 (en) | 2017-05-18 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10941170B2 (en) | 2017-05-03 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10950803B2 (en) | 2014-10-13 | 2021-03-16 | Universal Display Corporation | Compounds and uses in devices |
| US10957861B2 (en) | 2015-12-29 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957866B2 (en) | 2016-06-30 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957870B2 (en) | 2012-09-07 | 2021-03-23 | Universal Display Corporation | Organic light emitting device |
| US10964904B2 (en) | 2017-01-20 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964893B2 (en) | 2016-11-17 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10971687B2 (en) | 2017-12-14 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10968226B2 (en) | 2017-06-23 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978647B2 (en) | 2017-02-15 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10975113B2 (en) | 2017-04-21 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10991895B2 (en) | 2015-10-06 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10998507B2 (en) | 2015-11-23 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3816175A1 (de) | 2019-11-04 | 2021-05-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3823055A1 (de) | 2019-11-14 | 2021-05-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11018309B2 (en) | 2015-08-03 | 2021-05-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024808B2 (en) | 2015-12-29 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038137B2 (en) | 2017-04-28 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038117B2 (en) | 2017-04-11 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038115B2 (en) | 2017-05-18 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and device |
| US11050028B2 (en) | 2017-01-24 | 2021-06-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056658B2 (en) | 2017-03-29 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11053268B2 (en) | 2017-01-20 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3845545A1 (de) | 2020-01-06 | 2021-07-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11081647B2 (en) | 2016-04-22 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081659B2 (en) | 2018-01-10 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081658B2 (en) | 2016-10-03 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858945A1 (de) | 2020-01-28 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11084838B2 (en) | 2017-04-21 | 2021-08-10 | Universal Display Corporation | Organic electroluminescent materials and device |
| US11094891B2 (en) | 2016-03-16 | 2021-08-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11101434B2 (en) | 2017-04-21 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11108000B2 (en) | 2014-08-07 | 2021-08-31 | Unniversal Display Corporation | Organic electroluminescent materials and devices |
| US11117897B2 (en) | 2017-05-01 | 2021-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11127906B2 (en) | 2016-10-03 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11139443B2 (en) | 2017-03-31 | 2021-10-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11142538B2 (en) | 2018-03-12 | 2021-10-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11152579B2 (en) | 2016-12-28 | 2021-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11158820B2 (en) | 2017-03-29 | 2021-10-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11165028B2 (en) | 2018-03-12 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11168103B2 (en) | 2017-11-17 | 2021-11-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11174259B2 (en) | 2017-06-23 | 2021-11-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11180519B2 (en) | 2018-02-09 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183642B2 (en) | 2016-10-03 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183646B2 (en) | 2017-11-07 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11189804B2 (en) | 2016-10-03 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11201298B2 (en) | 2017-01-09 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11201299B2 (en) | 2017-05-04 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11214587B2 (en) | 2017-11-07 | 2022-01-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11217757B2 (en) | 2018-03-12 | 2022-01-04 | Universal Display Corporation | Host materials for electroluminescent devices |
| EP3937268A1 (de) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228003B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228002B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228004B2 (en) | 2018-06-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233203B2 (en) | 2018-09-06 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233205B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233204B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239434B2 (en) | 2018-02-09 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239433B2 (en) | 2017-07-26 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239432B2 (en) | 2016-10-14 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11261207B2 (en) | 2018-06-25 | 2022-03-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11271177B2 (en) | 2018-01-11 | 2022-03-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11276829B2 (en) | 2017-03-31 | 2022-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11279722B2 (en) | 2018-03-12 | 2022-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11296283B2 (en) | 2018-06-04 | 2022-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11302872B2 (en) | 2015-09-09 | 2022-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11322691B2 (en) | 2017-07-26 | 2022-05-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11325932B2 (en) | 2019-02-08 | 2022-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342513B2 (en) | 2018-05-04 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11339182B2 (en) | 2018-06-07 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342509B2 (en) | 2018-02-09 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4001287A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001286A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11349083B2 (en) | 2017-08-10 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11367840B2 (en) | 2018-01-26 | 2022-06-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4016659A1 (de) | 2020-11-16 | 2022-06-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11374181B2 (en) | 2019-08-14 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11370809B2 (en) | 2019-02-08 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4019526A1 (de) | 2018-01-26 | 2022-06-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11390639B2 (en) | 2018-04-13 | 2022-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4039692A1 (de) | 2021-02-03 | 2022-08-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11424420B2 (en) | 2017-09-07 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11437591B2 (en) | 2017-08-24 | 2022-09-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4053137A1 (de) | 2021-03-05 | 2022-09-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11444249B2 (en) | 2017-09-07 | 2022-09-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4056578A1 (de) | 2021-03-12 | 2022-09-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11450822B2 (en) | 2018-05-25 | 2022-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4059915A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4060758A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059941A1 (de) | 2021-03-15 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11459349B2 (en) | 2018-05-25 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11462697B2 (en) | 2017-08-22 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469384B2 (en) | 2018-11-02 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469382B2 (en) | 2017-07-12 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469383B2 (en) | 2018-10-08 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11476430B2 (en) | 2018-10-15 | 2022-10-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4075531A1 (de) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| EP4074723A1 (de) | 2021-04-05 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4075530A1 (de) | 2021-04-14 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4079743A1 (de) | 2021-04-23 | 2022-10-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11485706B2 (en) | 2018-09-11 | 2022-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495757B2 (en) | 2017-06-23 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495756B2 (en) | 2019-05-07 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495752B2 (en) | 2018-10-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495749B2 (en) | 2015-04-06 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4086266A1 (de) | 2021-04-23 | 2022-11-09 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11508913B2 (en) | 2017-08-10 | 2022-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11512093B2 (en) | 2019-03-04 | 2022-11-29 | Universal Display Corporation | Compound used for organic light emitting device (OLED), consumer product and formulation |
| US11515494B2 (en) | 2018-05-04 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515489B2 (en) | 2018-11-28 | 2022-11-29 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11515482B2 (en) | 2018-10-23 | 2022-11-29 | Universal Display Corporation | Deep HOMO (highest occupied molecular orbital) emitter device structures |
| US11515493B2 (en) | 2018-01-11 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11522140B2 (en) | 2015-08-17 | 2022-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545636B2 (en) | 2016-12-15 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545637B2 (en) | 2017-01-13 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4112701A2 (de) | 2021-06-08 | 2023-01-04 | University of Southern California | Molekulare ausrichtung homoleptischer iridiumphosphore |
| US11552261B2 (en) | 2017-06-23 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11548905B2 (en) | 2016-12-15 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557738B2 (en) | 2019-02-22 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11555048B2 (en) | 2016-12-01 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557733B2 (en) | 2018-03-12 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11560398B2 (en) | 2019-05-07 | 2023-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11569480B2 (en) | 2019-03-12 | 2023-01-31 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| US11600787B2 (en) | 2019-08-30 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11605791B2 (en) | 2017-09-01 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11608321B2 (en) | 2017-06-23 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4151699A1 (de) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11616203B2 (en) | 2018-04-17 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11613550B2 (en) | 2019-04-30 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices comprising benzimidazole-containing metal complexes |
| US11623936B2 (en) | 2018-12-11 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11637261B2 (en) | 2019-03-12 | 2023-04-25 | Universal Display Corporation | Nanopatch antenna outcoupling structure for use in OLEDs |
| US11637251B2 (en) | 2009-03-23 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11634445B2 (en) | 2019-05-21 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11639363B2 (en) | 2019-04-22 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11647667B2 (en) | 2019-06-14 | 2023-05-09 | Universal Display Corporation | Organic electroluminescent compounds and organic light emitting devices using the same |
| US11672165B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11672176B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11678565B2 (en) | 2017-06-23 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11690285B2 (en) | 2018-11-28 | 2023-06-27 | Universal Display Corporation | Electroluminescent devices |
| US11685754B2 (en) | 2019-07-22 | 2023-06-27 | Universal Display Corporation | Heteroleptic organic electroluminescent materials |
| US11696492B2 (en) | 2017-09-07 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697653B2 (en) | 2019-10-21 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11700765B2 (en) | 2018-01-10 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11706972B2 (en) | 2015-09-08 | 2023-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4212539A1 (de) | 2021-12-16 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11708355B2 (en) | 2019-08-01 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716900B2 (en) | 2018-05-30 | 2023-08-01 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11716899B2 (en) | 2018-11-28 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11718634B2 (en) | 2018-09-14 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11723269B2 (en) | 2017-08-22 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11725022B2 (en) | 2017-06-23 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11739081B2 (en) | 2019-03-11 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744141B2 (en) | 2017-08-09 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753427B2 (en) | 2018-05-04 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758804B2 (en) | 2017-06-23 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753425B2 (en) | 2018-07-11 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4242285A1 (de) | 2022-03-09 | 2023-09-13 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11765965B2 (en) | 2019-10-30 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765970B2 (en) | 2017-07-26 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765968B2 (en) | 2017-01-23 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778897B2 (en) | 2017-09-20 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11773320B2 (en) | 2019-02-21 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778895B2 (en) | 2020-01-13 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11793073B2 (en) | 2018-05-06 | 2023-10-17 | Universal Display Corporation | Host materials for electroluminescent devices |
| EP4265626A2 (de) | 2022-04-18 | 2023-10-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11802136B2 (en) | 2017-06-23 | 2023-10-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4271160A2 (de) | 2015-02-13 | 2023-11-01 | Merck Patent GmbH | Aromatisches heterocyclisches derivat und organisches elektrolumineszenzelement, beleuchtungsvorrichtung und anzeigevorrichtung mit dem aromatischen heterocyclischen derivat |
| US11812624B2 (en) | 2019-01-30 | 2023-11-07 | The University Of Southern California | Organic electroluminescent materials and devices |
| US11812622B2 (en) | 2015-09-25 | 2023-11-07 | Universal Display Corporation | Organic electroluminescent compounds and devices |
| US11814403B2 (en) | 2017-06-23 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818949B2 (en) | 2015-04-06 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11825735B2 (en) | 2017-11-28 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11820783B2 (en) | 2019-09-06 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11825736B2 (en) | 2018-11-19 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11827651B2 (en) | 2019-05-13 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832510B2 (en) | 2017-06-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4282863A1 (de) | 2022-05-24 | 2023-11-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11834459B2 (en) | 2018-12-12 | 2023-12-05 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11845764B2 (en) | 2018-01-26 | 2023-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4293001A1 (de) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11864458B2 (en) | 2019-10-08 | 2024-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4299693A1 (de) | 2022-06-28 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11871653B2 (en) | 2019-02-22 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11882759B2 (en) | 2018-04-13 | 2024-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11889708B2 (en) | 2019-11-14 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11903305B2 (en) | 2018-09-24 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910700B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11910702B2 (en) | 2017-11-07 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent devices |
| US11910699B2 (en) | 2017-08-10 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4326030A1 (de) | 2022-08-17 | 2024-02-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11917900B2 (en) | 2020-01-28 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917843B2 (en) | 2017-07-26 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925103B2 (en) | 2018-06-05 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925105B2 (en) | 2019-08-26 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11919914B2 (en) | 2019-10-25 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11920070B2 (en) | 2019-07-12 | 2024-03-05 | The University Of Southern California | Luminescent janus-type, two-coordinated metal complexes |
| US11925102B2 (en) | 2015-06-04 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11930699B2 (en) | 2019-08-15 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11926638B2 (en) | 2019-07-22 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11932660B2 (en) | 2020-01-29 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937494B2 (en) | 2019-08-28 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11944000B2 (en) | 2013-10-29 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11950493B2 (en) | 2019-10-15 | 2024-04-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11957050B2 (en) | 2018-02-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963441B2 (en) | 2018-11-26 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963438B2 (en) | 2019-03-26 | 2024-04-16 | The University Of Southern California | Organic electroluminescent materials and devices |
| US11968883B2 (en) | 2017-07-26 | 2024-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11970508B2 (en) | 2020-04-22 | 2024-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4362645A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4362630A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4362631A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11976086B2 (en) | 2019-03-06 | 2024-05-07 | Samsung Display Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and apparatus including the organic light-emitting device |
| US11985888B2 (en) | 2019-08-12 | 2024-05-14 | The Regents Of The University Of Michigan | Organic electroluminescent device |
| EP4369898A1 (de) | 2022-10-27 | 2024-05-15 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4376583A2 (de) | 2022-10-27 | 2024-05-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11999886B2 (en) | 2019-09-26 | 2024-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12010859B2 (en) | 2019-05-24 | 2024-06-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4386065A1 (de) | 2022-12-14 | 2024-06-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US12018035B2 (en) | 2020-03-23 | 2024-06-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12029055B2 (en) | 2018-01-30 | 2024-07-02 | The University Of Southern California | OLED with hybrid emissive layer |
| US12035613B2 (en) | 2020-05-26 | 2024-07-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12048237B2 (en) | 2016-05-05 | 2024-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12058929B2 (en) | 2015-06-04 | 2024-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12065451B2 (en) | 2020-08-19 | 2024-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12075690B2 (en) | 2017-12-14 | 2024-08-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12075691B2 (en) | 2019-04-30 | 2024-08-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12077550B2 (en) | 2019-07-02 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12089486B2 (en) | 2017-02-08 | 2024-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12084465B2 (en) | 2020-02-24 | 2024-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12103942B2 (en) | 2019-05-13 | 2024-10-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12122793B2 (en) | 2020-03-26 | 2024-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3457452B1 (de) * | 2006-09-21 | 2022-11-02 | UDC Ireland Limited | Oled-anzeige mit verlängerter lebensdauer |
| KR101642030B1 (ko) * | 2007-10-17 | 2016-07-25 | 바스프 에스이 | 가교된 카르벤 리간드를 포함하는 전이 금속 착물 및 이의 용도 |
| DE102008015773A1 (de) * | 2008-03-26 | 2009-10-01 | Albert-Ludwigs-Universität Freiburg | Verfahren zur decarboxylativen Hydroformylierung alpha,beta-ungesättigter Carbonsäuren |
| JP5808252B2 (ja) * | 2009-01-07 | 2015-11-10 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | カルバゾール、ジベンゾフラン、ジベンゾチオフェンおよびジベンゾホスホールから選択されたシリル置換およびヘテロ原子置換された化合物および該化合物の有機エレクトロニクスへの使用 |
| WO2010097433A1 (de) | 2009-02-26 | 2010-09-02 | Basf Se | Chinonverbindungen als dotierstoff in der organischen elektronik |
| KR102044134B1 (ko) | 2012-12-03 | 2019-12-02 | 엘지디스플레이 주식회사 | 인광 화합물 및 이를 이용한 유기발광다이오드소자 |
| JP5630511B2 (ja) * | 2013-02-06 | 2014-11-26 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP5626384B2 (ja) * | 2013-02-06 | 2014-11-19 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2014208632A (ja) * | 2013-03-28 | 2014-11-06 | 日本合成化学工業株式会社 | 新規イミダゾール化合物、電子デバイス用材料、発光素子、電子デバイス及びその製造方法 |
| JP6119375B2 (ja) * | 2013-03-29 | 2017-04-26 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| CN105646459A (zh) * | 2014-11-13 | 2016-06-08 | 上海和辉光电有限公司 | 一种化合物及其制备方法和应用 |
| CN106749375B (zh) * | 2016-11-30 | 2019-04-05 | 长春海谱润斯科技有限公司 | 一种三苯基硅基相连苯并噻吩衍生物及使用该衍生物的有机发光器件 |
| CN107746384A (zh) * | 2017-11-14 | 2018-03-02 | 东南大学 | 一种基于三氟甲基的紫色荧光材料晶体及制备方法 |
| CN108586539B (zh) * | 2018-04-13 | 2020-06-05 | 苏州科技大学 | 含二苯并噻吩环金属铱配合物及其作为有机电致发光器件发光层掺杂材料的应用 |
| CN109390487A (zh) * | 2018-09-30 | 2019-02-26 | 云谷(固安)科技有限公司 | 一种有机发光二极管、显示面板和显示装置 |
| JP7060490B2 (ja) * | 2018-10-31 | 2022-04-26 | メルク パテント ゲーエムベーハー | 非イオン性有機エレクトロニクス材料、電子デバイス、有機エレクトロルミネッセンス素子及び有機エレクトロルミネッセンス素子作製用溶液 |
| CN110078757B (zh) * | 2019-05-24 | 2021-07-02 | 南京邮电大学 | 一种芳基硅有机光电材料及其制备方法与应用 |
| WO2022191609A1 (ko) * | 2021-03-08 | 2022-09-15 | 고려대학교 세종산학협력단 | 이리듐 착물 및 이를 포함하는 유기 전계 발광 소자 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005019373A2 (de) * | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2008034758A2 (de) * | 2006-09-21 | 2008-03-27 | Basf Se | Oled-anzeige mit verlängerter lebensdauer |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100913568B1 (ko) | 1999-05-13 | 2009-08-26 | 더 트러스티즈 오브 프린스턴 유니버시티 | 전계인광에 기초한 고 효율의 유기 발광장치 |
| CN100505375C (zh) | 2000-08-11 | 2009-06-24 | 普林斯顿大学理事会 | 有机金属化合物和发射转换有机电致磷光 |
| JP4590825B2 (ja) | 2003-02-21 | 2010-12-01 | コニカミノルタホールディングス株式会社 | 白色発光有機エレクトロルミネッセンス素子 |
| JP4869565B2 (ja) | 2004-04-23 | 2012-02-08 | 富士フイルム株式会社 | 有機電界発光素子 |
| WO2005113704A2 (en) | 2004-05-18 | 2005-12-01 | The University Of Southern California | Luminescent compounds with carbene ligands |
| DE102004040005A1 (de) | 2004-08-18 | 2006-02-23 | Basf Ag | In Polymermatrices eingebettete Übergangsmetallcarbenkomplexe zur Verwendung in OLEDs |
| DE102004057072A1 (de) | 2004-11-25 | 2006-06-01 | Basf Ag | Verwendung von Übergangsmetall-Carbenkomplexen in organischen Licht-emittierenden Dioden (OLEDs) |
| DE102005014284A1 (de) | 2005-03-24 | 2006-09-28 | Basf Ag | Verwendung von Verbindungen, welche aromatische oder heteroaromatische über Carbonyl-Gruppen enthaltende Gruppen verbundene Ringe enthalten, als Matrixmaterialien in organischen Leuchtdioden |
| DE102005040285A1 (de) | 2005-08-25 | 2007-03-01 | Basf Ag | Weiße organische Leuchtdioden (OLEDs) auf der Basis von Exciplexen zweier blau fluoreszierender Verbindungen |
| JP5199887B2 (ja) | 2006-01-31 | 2013-05-15 | ビーエーエスエフ ソシエタス・ヨーロピア | 遷移金属カルベン錯体の製造方法 |
| US20070224446A1 (en) * | 2006-03-24 | 2007-09-27 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device using the same |
| EP2007781B1 (de) | 2006-04-04 | 2012-09-12 | Basf Se | Übergangsmetallkomplexe, enthaltend einen nicht-carben- und ein oder zwei carbenliganden und deren verwendung in oleds |
| WO2007115970A1 (de) | 2006-04-05 | 2007-10-18 | Basf Se | Heteroleptische übergangsmetall-carben-komplexe und deren verwendung in organischen leuchtdioden (oleds) |
| US8563145B2 (en) * | 2006-06-02 | 2013-10-22 | Idemitsu Kosan Co., Ltd. | Material containing two or three dibenzofuran groups, dibenzothiophene groups, or a combination thereof, which is operable for organic electroluminescence elements, and organic electroluminescence elements using the material |
| JP4871689B2 (ja) * | 2006-09-27 | 2012-02-08 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP5049711B2 (ja) * | 2006-09-27 | 2012-10-17 | 富士フイルム株式会社 | 有機電界発光素子 |
| KR101642030B1 (ko) | 2007-10-17 | 2016-07-25 | 바스프 에스이 | 가교된 카르벤 리간드를 포함하는 전이 금속 착물 및 이의 용도 |
-
2008
- 2008-06-25 JP JP2010513911A patent/JP5675349B2/ja active Active
- 2008-06-25 WO PCT/EP2008/058106 patent/WO2009003898A1/de active Application Filing
- 2008-06-25 US US12/667,619 patent/US8373159B2/en active Active
- 2008-06-25 CN CN200880104631.0A patent/CN101878552B/zh active Active
- 2008-06-25 EP EP08774297.9A patent/EP2165377B1/de active Active
- 2008-06-25 KR KR1020107002592A patent/KR101577465B1/ko active IP Right Grant
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005019373A2 (de) * | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2008034758A2 (de) * | 2006-09-21 | 2008-03-27 | Basf Se | Oled-anzeige mit verlängerter lebensdauer |
Non-Patent Citations (4)
| Title |
|---|
| E. B. SCHWARTZ, C. B. KNOBLER, D. J. CRAM, J. AM. CHEM. SOC., vol. 114, 1992, pages 10775 - 10784, XP002497619 * |
| MING-HAN TSAI ET AL: "11.4: Highly Efficient Blue Organic Electrophosphorescent Devices Based on 3,6-Bis(triphenylsilyl)Carbazole as the Host Material", SID 2006, 2006 SID INTERNATIONAL SYMPOSIUM, SOCIETY FOR INFORMATION DISPLAY, LO, vol. XXXVII, 24 May 2005 (2005-05-24), pages 139 - 141, XP007012646, ISSN: 0006-966X * |
| MING-HAN TSAI ET AL: "Highly Efficient Organic Blue Electrophosphorescent Devices Based on 3,6-Bis(triphenylsilyl)carbazole as the Host Material", ADVANCED MATERIALS, WILEY VCH, WEINHEIM, DE, vol. 18, 24 April 2006 (2006-04-24), pages 1216 - 1220, XP002483366, ISSN: 0935-9648 * |
| PETER ERK ET AL: "11.2: Efficient Deep Blue Triplet Emitters for OLEDs", SID 2006, 2006 SID INTERNATIONAL SYMPOSIUM, SOCIETY FOR INFORMATION DISPLAY, LO, vol. XXXVII, 24 May 2005 (2005-05-24), pages 131 - 133, XP007012644, ISSN: 0006-966X * |
Cited By (895)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9647227B2 (en) | 2005-04-13 | 2017-05-09 | Universal Display Corporation | Organic light emitting devices |
| US9871219B2 (en) | 2005-04-13 | 2018-01-16 | Universal Display Corporation | Organic light emitting devices |
| US9735377B2 (en) | 2005-05-06 | 2017-08-15 | Universal Display Corporation | Phosphorescent emitters and host materials with improved stability |
| US9893306B2 (en) | 2006-02-10 | 2018-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9065063B2 (en) | 2006-02-10 | 2015-06-23 | Universal Display Corporation | Metal complexes of cyclometallated imidazo[1,2-f]phenanthridine and diimidazo[1,2-a:1′,2′-c]quinazoline ligands and isoelectronic and benzannulated analogs thereof |
| US10158090B2 (en) | 2006-02-10 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978649B2 (en) | 2006-02-10 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749121B2 (en) | 2006-02-10 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8889864B2 (en) | 2006-02-10 | 2014-11-18 | Universal Display Corporation | Metal complexes of cyclometallated imidazo[1,2-f]phenanthridine and diimidazo[1,2-a:1′,2′-c]quinazoline ligands and isoelectronic and benzannulated analogs thereof |
| US9548462B2 (en) | 2006-02-10 | 2017-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403831B2 (en) | 2006-02-10 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9281483B2 (en) | 2006-02-10 | 2016-03-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9899612B2 (en) | 2006-12-08 | 2018-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10230060B2 (en) | 2007-03-08 | 2019-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911930B2 (en) | 2007-03-08 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9853227B2 (en) | 2007-03-08 | 2017-12-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9577201B2 (en) | 2007-03-08 | 2017-02-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190621B2 (en) | 2007-03-08 | 2015-11-17 | Universal Display Corporation | Materials for organic light emitting diode |
| US10600975B2 (en) | 2007-03-08 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495755B2 (en) | 2007-03-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9142786B2 (en) | 2007-03-08 | 2015-09-22 | Universal Display Corporation | Phosphorescent materials |
| US9590180B2 (en) | 2007-06-23 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10312450B2 (en) | 2007-08-08 | 2019-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11690286B2 (en) | 2007-08-08 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9608206B2 (en) | 2007-08-08 | 2017-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12082493B2 (en) | 2007-08-08 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9153786B2 (en) | 2007-08-08 | 2015-10-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10374171B2 (en) | 2007-08-08 | 2019-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997727B2 (en) | 2007-08-08 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9577200B2 (en) | 2007-08-08 | 2017-02-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957858B2 (en) | 2007-08-08 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8822708B2 (en) | 2007-08-08 | 2014-09-02 | Universal Display Corporation | Benzo-fused thiophene / triphenylene hybrid materials |
| US8258297B2 (en) | 2007-10-17 | 2012-09-04 | Basf Se | Transition metal complexes with bridged carbene ligands and use thereof in OLEDs |
| US9123903B2 (en) | 2007-12-28 | 2015-09-01 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| US9997726B2 (en) | 2007-12-28 | 2018-06-12 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| US11482685B2 (en) | 2008-09-03 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593896B2 (en) | 2008-09-03 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10186672B2 (en) | 2008-09-03 | 2019-01-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9630983B2 (en) | 2008-09-03 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent material and devices |
| US9076973B2 (en) | 2008-09-03 | 2015-07-07 | Universal Display Corporation | Phosphorescent materials |
| US10892426B2 (en) | 2008-09-03 | 2021-01-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10084143B2 (en) | 2008-09-16 | 2018-09-25 | Universal Display Corporation | Phosphorescent materials |
| US9455411B2 (en) | 2008-09-25 | 2016-09-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8618533B2 (en) | 2008-10-07 | 2013-12-31 | Osram Opto Semiconductors Gmbh | Siloles substituted by fused ring systems and use thereof in organic electronics |
| US10008678B2 (en) | 2008-12-12 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8952363B2 (en) | 2009-01-16 | 2015-02-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831442B2 (en) | 2009-01-16 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9067947B2 (en) | 2009-01-16 | 2015-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9518063B2 (en) | 2009-01-16 | 2016-12-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP2010184910A (ja) * | 2009-02-13 | 2010-08-26 | Chemiprokasei Kaisha Ltd | 新規なトリアリールホスフィンオキシド誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
| US11637251B2 (en) | 2009-03-23 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9184397B2 (en) | 2009-03-23 | 2015-11-10 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11380854B2 (en) | 2009-03-23 | 2022-07-05 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US11910701B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10312458B2 (en) | 2009-03-23 | 2019-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910700B2 (en) | 2009-03-23 | 2024-02-20 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US10374173B2 (en) | 2009-04-28 | 2019-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634265B2 (en) | 2009-04-28 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673406B2 (en) | 2009-05-20 | 2017-06-06 | Universal Display Corporation | Metal complexes with boron-nitrogen heterocycle containing ligands |
| CN102439111A (zh) * | 2009-05-27 | 2012-05-02 | 檀国大学校产学协力团 | 咔唑系氧化膦化合物和包含该化合物的有机电致发光器件 |
| US9108998B2 (en) | 2009-10-14 | 2015-08-18 | Basf Se | Dinuclear platinum-carbene complexes and the use thereof in OLEDs |
| WO2011045337A1 (de) | 2009-10-14 | 2011-04-21 | Basf Se | Dinukleare platin-carben-komplexe und deren verwendung in oleds |
| US11871654B2 (en) | 2009-10-28 | 2024-01-09 | Udc Ireland Limited | Heteroleptic carbene complexes and the use thereof in organic electronics |
| CN102741265B (zh) * | 2009-10-28 | 2015-12-09 | 巴斯夫欧洲公司 | 杂配卡宾配合物及其在有机电子品中的用途 |
| US11189806B2 (en) | 2009-10-28 | 2021-11-30 | Udc Ireland Limited | Heteroleptic carbene complexes and the use thereof in organic electronics |
| CN102741265A (zh) * | 2009-10-28 | 2012-10-17 | 巴斯夫欧洲公司 | 杂配卡宾配合物及其在有机电子品中的用途 |
| JP2013509380A (ja) * | 2009-10-28 | 2013-03-14 | ビーエーエスエフ ソシエタス・ヨーロピア | ヘテロレプティックなカルベン錯体及び該錯体を有機エレクトロニクスで用いる使用 |
| WO2011051404A1 (de) | 2009-10-28 | 2011-05-05 | Basf Se | Heteroleptische carben-komplexe und deren verwendung in der organischen elektronik |
| US9773986B2 (en) | 2009-11-19 | 2017-09-26 | The University Of Southern California | Copper(I)-carbene complexes and organic electroluminescent devices |
| KR102231266B1 (ko) * | 2009-12-14 | 2021-03-24 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| CN102762582A (zh) * | 2009-12-14 | 2012-10-31 | 巴斯夫欧洲公司 | 包含二氮杂苯并咪唑卡宾配体的金属配合物及其在oled中的用途 |
| KR101838199B1 (ko) * | 2009-12-14 | 2018-04-26 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| US11444254B2 (en) | 2009-12-14 | 2022-09-13 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDs |
| US10916716B2 (en) | 2009-12-14 | 2021-02-09 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDS |
| WO2011073149A1 (de) | 2009-12-14 | 2011-06-23 | Basf Se | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds |
| US10090476B2 (en) | 2009-12-14 | 2018-10-02 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDs |
| KR20190020182A (ko) * | 2009-12-14 | 2019-02-27 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| KR20180027648A (ko) * | 2009-12-14 | 2018-03-14 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| KR101951851B1 (ko) * | 2009-12-14 | 2019-02-26 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| US11839140B2 (en) | 2009-12-14 | 2023-12-05 | Udc Ireland Limited | Metal complexes comprising diazabenzmidazolocarbene ligands and the use thereof in OLEDS |
| US9487548B2 (en) | 2009-12-14 | 2016-11-08 | Udc Ireland Limited | Metal complexes comprising diazabenzimidazolocarbene ligands and the use thereof in OLEDs |
| KR102128072B1 (ko) * | 2009-12-14 | 2020-06-30 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| CN102762582B (zh) * | 2009-12-14 | 2015-11-25 | 巴斯夫欧洲公司 | 包含二氮杂苯并咪唑卡宾配体的金属配合物及其在oled中的用途 |
| KR20200080326A (ko) * | 2009-12-14 | 2020-07-06 | 유디씨 아일랜드 리미티드 | 디아자벤즈이미다졸로카르벤 리간드를 포함하는 금속 착물 및 oled에서의 그의 용도 |
| US9054344B2 (en) | 2010-01-20 | 2015-06-09 | Universal Display Corporation | Electroluminescent devices for lighting applications |
| US9156870B2 (en) | 2010-02-25 | 2015-10-13 | Universal Display Corporation | Phosphorescent emitters |
| US9175211B2 (en) | 2010-03-03 | 2015-11-03 | Universal Display Corporation | Phosphorescent materials |
| US8963132B2 (en) | 2010-03-25 | 2015-02-24 | Universal Display Corporation | Solution processable doped triarylamine hole injection materials |
| CN102939295A (zh) * | 2010-04-16 | 2013-02-20 | 巴斯夫欧洲公司 | 桥联苯并咪唑-卡宾配合物及其在oled中的用途 |
| CN102939295B (zh) * | 2010-04-16 | 2017-05-24 | Udc 爱尔兰有限责任公司 | 桥联苯并咪唑‑卡宾配合物及其在oled中的用途 |
| US8691401B2 (en) | 2010-04-16 | 2014-04-08 | Basf Se | Bridged benzimidazole-carbene complexes and use thereof in OLEDS |
| US9040962B2 (en) | 2010-04-28 | 2015-05-26 | Universal Display Corporation | Depositing premixed materials |
| US8968887B2 (en) | 2010-04-28 | 2015-03-03 | Universal Display Corporation | Triphenylene-benzofuran/benzothiophene/benzoselenophene compounds with substituents joining to form fused rings |
| WO2011155507A1 (ja) | 2010-06-08 | 2011-12-15 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| WO2011155508A1 (ja) | 2010-06-08 | 2011-12-15 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| US9543532B2 (en) | 2010-06-11 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9140428B2 (en) | 2010-06-11 | 2015-09-22 | Universal Display Corporation | Triplet-triplet annihilation up-conversation for display and lighting applications |
| JP2012036164A (ja) * | 2010-06-17 | 2012-02-23 | ▲いく▼▲雷▼光電科技股▲分▼有限公司 | 有機エレクトロルミネッセンス装置に用いられる化合物及び有機エレクトロルミネッセンス装置 |
| JP2013537701A (ja) * | 2010-06-18 | 2013-10-03 | ビーエーエスエフ ソシエタス・ヨーロピア | 少なくとも1種の金属有機化合物及び少なくとも1種の金属酸化物を含有する層を含む有機電子デバイス |
| JP2013535106A (ja) * | 2010-06-18 | 2013-09-09 | ビーエーエスエフ ソシエタス・ヨーロピア | ジベンゾフラン化合物と8−ヒドロキシキノリノラトアルカリ土類金属錯体または8−ヒドロキシキノリノラトアルカリ金属錯体との層を含む、有機電子デバイス |
| WO2011157790A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a dibenzofurane compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| CN107698622B (zh) * | 2010-06-18 | 2021-06-29 | Udc 爱尔兰有限责任公司 | 包含含有至少一种金属有机化合物和至少一种金属氧化物的层的有机电子器件 |
| EP2582770A4 (de) * | 2010-06-18 | 2014-06-18 | Basf Se | Organische elektronische vorrichtungen mit einer schicht aus mindestens einer metalloorganischen verbindung und mindestens einem metalloxid |
| KR101806586B1 (ko) | 2010-06-18 | 2017-12-07 | 유디씨 아일랜드 리미티드 | 하나 이상의 금속 유기 화합물 및 하나 이상의 금속 산화물을 함유하는 층을 포함하는 유기 전자 소자 |
| WO2011157779A1 (en) | 2010-06-18 | 2011-12-22 | Basf Se | Organic electronic devices comprising a layer of a pyridine compound and a 8-hydroxyquinolinolato earth alkaline metal, or alkali metal complex |
| JP2013538436A (ja) * | 2010-06-18 | 2013-10-10 | ビーエーエスエフ ソシエタス・ヨーロピア | ピリジン化合物と8−ヒドロキシキノリノラトアルカリ土類金属又はアルカリ金属錯体の層を含む有機電子デバイス |
| JP2016197744A (ja) * | 2010-06-18 | 2016-11-24 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | 少なくとも1種の金属有機化合物及び少なくとも1種の金属酸化物を含有する層を含む有機電子デバイス |
| EP2582770A1 (de) * | 2010-06-18 | 2013-04-24 | Basf Se | Organische elektronische vorrichtungen mit einer schicht aus mindestens einer metalloorganischen verbindung und mindestens einem metalloxid |
| CN107698622A (zh) * | 2010-06-18 | 2018-02-16 | Udc 爱尔兰有限责任公司 | 包含含有至少一种金属有机化合物和至少一种金属氧化物的层的有机电子器件 |
| US9142792B2 (en) | 2010-06-18 | 2015-09-22 | Basf Se | Organic electronic devices comprising a layer comprising at least one metal organic compound and at least one metal oxide |
| US9435021B2 (en) | 2010-07-29 | 2016-09-06 | University Of Southern California | Co-deposition methods for the fabrication of organic optoelectronic devices |
| US11289659B2 (en) | 2010-08-20 | 2022-03-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9954180B2 (en) | 2010-08-20 | 2018-04-24 | Universal Display Corporation | Bicarbazole compounds for OLEDs |
| US11316113B2 (en) | 2010-08-20 | 2022-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9079872B2 (en) | 2010-10-07 | 2015-07-14 | Basf Se | Phenanthro[9, 10-B]furans for electronic applications |
| WO2012045710A1 (en) | 2010-10-07 | 2012-04-12 | Basf Se | Phenanthro[9,10-b]furans for electronic applications |
| US9401482B2 (en) | 2010-10-08 | 2016-07-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8932734B2 (en) | 2010-10-08 | 2015-01-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10147892B2 (en) | 2010-12-07 | 2018-12-04 | The University Of Southern California | Organic electroluminescent materials and devices |
| US8362246B2 (en) | 2010-12-13 | 2013-01-29 | Basf Se | Bispyrimidines for electronic applications |
| WO2012080052A1 (en) | 2010-12-13 | 2012-06-21 | Basf Se | Bispyrimidines for electronic applications |
| US11997918B2 (en) | 2011-01-13 | 2024-05-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008677B2 (en) | 2011-01-13 | 2018-06-26 | Universal Display Corporation | Materials for organic light emitting diode |
| US11374180B2 (en) | 2011-01-13 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9130177B2 (en) | 2011-01-13 | 2015-09-08 | Universal Display Corporation | 5-substituted 2 phenylquinoline complexes materials for light emitting diode |
| US10680189B2 (en) | 2011-01-13 | 2020-06-09 | Universal Display Corporation | Materials for organic light emitting diodes |
| WO2012111548A1 (ja) | 2011-02-16 | 2012-08-23 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| US9923154B2 (en) | 2011-02-16 | 2018-03-20 | Konica Minolta, Inc. | Organic electroluminescent element, lighting device, and display device |
| US10388890B2 (en) | 2011-02-23 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent heterocyclic carbene metal complexes and devices containing the same |
| US9947880B2 (en) | 2011-02-23 | 2018-04-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8754232B2 (en) | 2011-02-23 | 2014-06-17 | Universal Display Corporation | Methods of making bis-tridentate carbene complexes of ruthenium and osmium |
| US9005772B2 (en) | 2011-02-23 | 2015-04-14 | Universal Display Corporation | Thioazole and oxazole carbene metal complexes as phosphorescent OLED materials |
| US10381580B2 (en) | 2011-02-23 | 2019-08-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8871361B2 (en) | 2011-02-23 | 2014-10-28 | Universal Display Corporation | Tetradentate platinum complexes |
| US8883322B2 (en) | 2011-03-08 | 2014-11-11 | Universal Display Corporation | Pyridyl carbene phosphorescent emitters |
| US10873038B2 (en) | 2011-03-08 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600791B2 (en) | 2011-03-08 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9972793B2 (en) | 2011-03-08 | 2018-05-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9397312B2 (en) | 2011-05-11 | 2016-07-19 | Universal Display Corporation | Process for fabricating metal bus lines for OLED lighting panels |
| US9450027B2 (en) | 2011-05-12 | 2016-09-20 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| US8927308B2 (en) | 2011-05-12 | 2015-01-06 | Universal Display Corporation | Method of forming bus line designs for large-area OLED lighting |
| US9212197B2 (en) | 2011-05-19 | 2015-12-15 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants |
| US9257658B2 (en) | 2011-05-19 | 2016-02-09 | Universal Display Corporation | Method of making organic electroluminescent materials |
| US10158089B2 (en) | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10079349B2 (en) | 2011-05-27 | 2018-09-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11189805B2 (en) | 2011-05-27 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297769B2 (en) | 2011-06-08 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9812656B2 (en) | 2011-06-08 | 2017-11-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847495B2 (en) | 2011-06-08 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11063229B2 (en) | 2011-06-08 | 2021-07-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978648B2 (en) | 2011-06-08 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755164B2 (en) | 2011-06-08 | 2017-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2012172482A1 (en) * | 2011-06-14 | 2012-12-20 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in oleds |
| CN103732603B (zh) * | 2011-06-14 | 2017-05-31 | Udc 爱尔兰有限责任公司 | 包含氮杂苯并咪唑碳烯配体的金属配合物及其在oled中的用途 |
| US9315724B2 (en) | 2011-06-14 | 2016-04-19 | Basf Se | Metal complexes comprising azabenzimidazole carbene ligands and the use thereof in OLEDs |
| CN103732603A (zh) * | 2011-06-14 | 2014-04-16 | 巴斯夫欧洲公司 | 包含氮杂苯并咪唑碳烯配体的金属配合物及其在oled中的用途 |
| EP3415521A1 (de) | 2011-06-14 | 2018-12-19 | UDC Ireland Limited | Metallkomplexe mit azabenzimidazolcarbenliganden und verwendung davon in oleds |
| CN107501330A (zh) * | 2011-06-14 | 2017-12-22 | Udc 爱尔兰有限责任公司 | 包含氮杂苯并咪唑碳烯配体的金属配合物及其在oled中的用途 |
| US9054343B2 (en) | 2011-06-17 | 2015-06-09 | Universal Display Corporation | Fine tuning of emission spectra by combination of multiple emitter spectra |
| US8884316B2 (en) | 2011-06-17 | 2014-11-11 | Universal Display Corporation | Non-common capping layer on an organic device |
| US11751455B2 (en) | 2011-06-17 | 2023-09-05 | Universal Display Corporation | Non-common capping layer on an organic device |
| US10340313B2 (en) | 2011-06-17 | 2019-07-02 | Universal Display Corporation | Non-common capping layer on an organic device |
| US9397310B2 (en) | 2011-07-14 | 2016-07-19 | Universal Display Corporation | Organice electroluminescent materials and devices |
| US9647221B2 (en) | 2011-07-14 | 2017-05-09 | Universal Display Corporation | Organic light-emitting devices |
| US9252377B2 (en) | 2011-07-14 | 2016-02-02 | Universal Display Corporation | Inorganic hosts in OLEDs |
| US10214551B2 (en) | 2011-07-25 | 2019-02-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9783564B2 (en) | 2011-07-25 | 2017-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8709615B2 (en) | 2011-07-28 | 2014-04-29 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US8926119B2 (en) | 2011-08-04 | 2015-01-06 | Universal Display Corporation | Extendable light source with variable light emitting area |
| US9313857B2 (en) | 2011-08-04 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9493698B2 (en) | 2011-08-31 | 2016-11-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9142788B2 (en) | 2011-11-14 | 2015-09-22 | Universal Display Corporation | Host materials for OLEDs |
| US9193745B2 (en) | 2011-11-15 | 2015-11-24 | Universal Display Corporation | Heteroleptic iridium complex |
| US9217004B2 (en) | 2011-11-21 | 2015-12-22 | Universal Display Corporation | Organic light emitting materials |
| US10454046B2 (en) | 2011-12-09 | 2019-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482684B2 (en) | 2011-12-09 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9512355B2 (en) | 2011-12-09 | 2016-12-06 | Universal Display Corporation | Organic light emitting materials |
| US9455417B2 (en) | 2011-12-13 | 2016-09-27 | Universal Display Corporation | Split electrode for organic devices |
| US9461254B2 (en) | 2012-01-03 | 2016-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8987451B2 (en) | 2012-01-03 | 2015-03-24 | Universal Display Corporation | Synthesis of cyclometallated platinum(II) complexes |
| US9163174B2 (en) | 2012-01-04 | 2015-10-20 | Universal Display Corporation | Highly efficient phosphorescent materials |
| DE102013200085B4 (de) | 2012-01-06 | 2020-06-18 | Universal Display Corporation | Hocheffiziente phosphoreszierende Materialien |
| US8969592B2 (en) | 2012-01-10 | 2015-03-03 | Universal Display Corporation | Heterocyclic host materials |
| US9447113B2 (en) | 2012-01-10 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10167303B2 (en) | 2012-01-12 | 2019-01-01 | Udc Ireland Limited | Iridium organometallic complex containing a substituted dibenzo[f,h]quinoxaline and an electronic device having an emitting layer containing the iridium complex |
| US9472762B2 (en) | 2012-01-12 | 2016-10-18 | Udc Ireland Limited | Iridium organometallic complex containing a substituted dibenzo[f,h]quinoxaline and an electronic device having an emitting layer containing the iridium complex |
| WO2013104649A1 (en) | 2012-01-12 | 2013-07-18 | Basf Se | Metal complexes with dibenzo[f,h]quinoxalines |
| US10211413B2 (en) | 2012-01-17 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9118017B2 (en) | 2012-02-27 | 2015-08-25 | Universal Display Corporation | Host compounds for red phosphorescent OLEDs |
| US9386657B2 (en) | 2012-03-15 | 2016-07-05 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| US9548459B2 (en) | 2012-03-15 | 2017-01-17 | Universal Display Corporation | Organic materials for organic light emitting devices |
| DE102013003605B4 (de) | 2012-03-15 | 2023-08-17 | Universal Display Corporation | Sekundäre Lochtransportschicht mit Tricarbazolverbindungen |
| US9054323B2 (en) | 2012-03-15 | 2015-06-09 | Universal Display Corporation | Secondary hole transporting layer with diarylamino-phenyl-carbazole compounds |
| US9184399B2 (en) | 2012-05-04 | 2015-11-10 | Universal Display Corporation | Asymmetric hosts with triaryl silane side chains |
| US9773985B2 (en) | 2012-05-21 | 2017-09-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9670404B2 (en) | 2012-06-06 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502672B2 (en) | 2012-06-21 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9725476B2 (en) | 2012-07-09 | 2017-08-08 | Universal Display Corporation | Silylated metal complexes |
| US9231218B2 (en) | 2012-07-10 | 2016-01-05 | Universal Display Corporation | Phosphorescent emitters containing dibenzo[1,4]azaborinine structure |
| US9059412B2 (en) | 2012-07-19 | 2015-06-16 | Universal Display Corporation | Transition metal complexes containing substituted imidazole carbene as ligands and their application in OLEDs |
| WO2014012972A1 (en) | 2012-07-19 | 2014-01-23 | Basf Se | Dinuclear metal complexes comprising carbene ligands and the use thereof in oleds |
| US9590196B2 (en) | 2012-07-19 | 2017-03-07 | Udc Ireland Limited | Dinuclear metal complexes comprising carbene ligands and the use thereof in OLEDs |
| DE102013214144B4 (de) | 2012-07-19 | 2023-02-16 | Universal Display Corp. | Diarylamino-substituierte Metallkomplexe |
| EP3133079A1 (de) | 2012-07-19 | 2017-02-22 | UDC Ireland Limited | Dinukleare metallkomplexe mit carbenliganden und verwendung davon in oleds |
| US9540329B2 (en) | 2012-07-19 | 2017-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9663544B2 (en) | 2012-07-25 | 2017-05-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9318710B2 (en) | 2012-07-30 | 2016-04-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9627631B2 (en) | 2012-07-30 | 2017-04-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978958B2 (en) | 2012-08-24 | 2018-05-22 | Universal Display Corporation | Phosphorescent emitters with phenylimidazole ligands |
| WO2014030666A1 (ja) | 2012-08-24 | 2014-02-27 | コニカミノルタ株式会社 | 透明電極、電子デバイス、および透明電極の製造方法 |
| US8952362B2 (en) | 2012-08-31 | 2015-02-10 | The Regents Of The University Of Michigan | High efficiency and brightness fluorescent organic light emitting diode by triplet-triplet fusion |
| US11696459B2 (en) | 2012-09-07 | 2023-07-04 | Universal Display Corporation | Phosphorescence-sensitized delayed fluorescence light emitting system |
| US10957870B2 (en) | 2012-09-07 | 2021-03-23 | Universal Display Corporation | Organic light emitting device |
| EP3318566A1 (de) | 2012-09-20 | 2018-05-09 | UDC Ireland Limited | Azadibenzofurane für elektronische anwendungen |
| US10249827B2 (en) | 2012-09-20 | 2019-04-02 | Udc Ireland Limited | Azadibenzofurans for electronic applications |
| US9287513B2 (en) | 2012-09-24 | 2016-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917902B2 (en) | 2012-09-25 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312505B2 (en) | 2012-09-25 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388894B2 (en) | 2012-09-25 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9252363B2 (en) | 2012-10-04 | 2016-02-02 | Universal Display Corporation | Aryloxyalkylcarboxylate solvent compositions for inkjet printing of organic layers |
| US8692241B1 (en) | 2012-11-08 | 2014-04-08 | Universal Display Corporation | Transition metal complexes containing triazole and tetrazole carbene ligands |
| US9685617B2 (en) | 2012-11-09 | 2017-06-20 | Universal Display Corporation | Organic electronuminescent materials and devices |
| US10033002B2 (en) | 2012-11-09 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11380855B2 (en) | 2012-11-09 | 2022-07-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634264B2 (en) | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10510968B2 (en) | 2012-11-09 | 2019-12-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8946697B1 (en) | 2012-11-09 | 2015-02-03 | Universal Display Corporation | Iridium complexes with aza-benzo fused ligands |
| US10069090B2 (en) | 2012-11-20 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10847729B2 (en) | 2012-11-20 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190623B2 (en) | 2012-11-20 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11145831B2 (en) | 2012-11-20 | 2021-10-12 | Universal Display Corporation | Osmium(IV) complexes for OLED materials |
| US9512136B2 (en) | 2012-11-26 | 2016-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9166175B2 (en) | 2012-11-27 | 2015-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9196860B2 (en) | 2012-12-04 | 2015-11-24 | Universal Display Corporation | Compounds for triplet-triplet annihilation upconversion |
| US8716484B1 (en) | 2012-12-05 | 2014-05-06 | Universal Display Corporation | Hole transporting materials with twisted aryl groups |
| US9209411B2 (en) | 2012-12-07 | 2015-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716902B2 (en) | 2012-12-07 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10069081B2 (en) | 2012-12-07 | 2018-09-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910564B2 (en) | 2012-12-07 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9670185B2 (en) | 2012-12-07 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9653691B2 (en) | 2012-12-12 | 2017-05-16 | Universal Display Corporation | Phosphorescence-sensitizing fluorescence material system |
| US10400163B2 (en) | 2013-02-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102014001468B4 (de) | 2013-02-08 | 2024-08-08 | Universal Display Corporation | Heteroleptischer phenylbenzimidazol-komplex |
| US9935276B2 (en) | 2013-02-21 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11871652B2 (en) | 2013-02-21 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10367154B2 (en) | 2013-02-21 | 2019-07-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8927749B2 (en) | 2013-03-07 | 2015-01-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9419225B2 (en) | 2013-03-14 | 2016-08-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014147134A1 (en) | 2013-03-20 | 2014-09-25 | Basf Se | Azabenzimidazole carbene complexes as efficiency booster in oleds |
| US9997712B2 (en) | 2013-03-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2014157618A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、それを具備した照明装置及び表示装置 |
| WO2014157494A1 (ja) | 2013-03-29 | 2014-10-02 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2014177518A1 (en) | 2013-04-29 | 2014-11-06 | Basf Se | Transition metal complexes with carbene ligands and the use thereof in oleds |
| US9537106B2 (en) | 2013-05-09 | 2017-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9735373B2 (en) | 2013-06-10 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9673401B2 (en) | 2013-06-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10199581B2 (en) | 2013-07-01 | 2019-02-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10991896B2 (en) | 2013-07-01 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3266789A1 (de) | 2013-07-02 | 2018-01-10 | UDC Ireland Limited | Monosubstituierte diazabenzimidazolcarben-metall-komplexe zur verwendung in organischen leuchtdioden |
| US11605790B2 (en) | 2013-07-02 | 2023-03-14 | Udc Ireland Limited | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| EP3608329A1 (de) | 2013-07-02 | 2020-02-12 | UDC Ireland Limited | Monosubstituierte diazabenzimidazolcarben-metall-komplexe zur verwendung in organischen leuchtdioden |
| WO2015000955A1 (en) | 2013-07-02 | 2015-01-08 | Basf Se | Monosubstituted diazabenzimidazole carbene metal complexes for use in organic light emitting diodes |
| US10121975B2 (en) | 2013-07-03 | 2018-11-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9761807B2 (en) | 2013-07-15 | 2017-09-12 | Universal Display Corporation | Organic light emitting diode materials |
| US9324949B2 (en) | 2013-07-16 | 2016-04-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9553274B2 (en) | 2013-07-16 | 2017-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9224958B2 (en) | 2013-07-19 | 2015-12-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930866B2 (en) | 2013-07-25 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3239161A1 (de) | 2013-07-31 | 2017-11-01 | UDC Ireland Limited | Lumineszente diazabenzimidazol-carben-metall-komplexe |
| US10749114B2 (en) | 2013-08-20 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831437B2 (en) | 2013-08-20 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10074806B2 (en) | 2013-08-20 | 2018-09-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11611042B2 (en) | 2013-08-20 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9932359B2 (en) | 2013-08-30 | 2018-04-03 | University Of Southern California | Organic electroluminescent materials and devices |
| US10199582B2 (en) | 2013-09-03 | 2019-02-05 | University Of Southern California | Organic electroluminescent materials and devices |
| US9735378B2 (en) | 2013-09-09 | 2017-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748503B2 (en) | 2013-09-13 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003034B2 (en) | 2013-09-30 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9831447B2 (en) | 2013-10-08 | 2017-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9293712B2 (en) | 2013-10-11 | 2016-03-22 | Universal Display Corporation | Disubstituted pyrene compounds with amino group containing ortho aryl group and devices containing the same |
| US10128450B2 (en) | 2013-10-23 | 2018-11-13 | University Of Southern California | Organic electroluminescent materials and devices |
| US9853229B2 (en) | 2013-10-23 | 2017-12-26 | University Of Southern California | Organic electroluminescent materials and devices |
| US11944000B2 (en) | 2013-10-29 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015063046A1 (en) | 2013-10-31 | 2015-05-07 | Basf Se | Azadibenzothiophenes for electronic applications |
| US9306179B2 (en) | 2013-11-08 | 2016-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647218B2 (en) | 2013-11-14 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10033000B2 (en) | 2013-11-15 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905784B2 (en) | 2013-11-15 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10056565B2 (en) | 2013-11-20 | 2018-08-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10644251B2 (en) | 2013-12-04 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9876173B2 (en) | 2013-12-09 | 2018-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11653558B2 (en) | 2013-12-16 | 2023-05-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10355227B2 (en) | 2013-12-16 | 2019-07-16 | Universal Display Corporation | Metal complex for phosphorescent OLED |
| EP3916822A1 (de) | 2013-12-20 | 2021-12-01 | UDC Ireland Limited | Hocheffiziente oled-vorrichtungen mit sehr kurzer abklingzeit |
| US11765967B2 (en) | 2013-12-20 | 2023-09-19 | Udc Ireland Limited | Highly efficient OLED devices with very short decay times |
| US10347851B2 (en) | 2013-12-20 | 2019-07-09 | Udc Ireland Limited | Highly efficient OLED devices with very short decay times |
| US11075346B2 (en) | 2013-12-20 | 2021-07-27 | Udc Ireland Limited | Highly efficient OLED devices with very short decay times |
| US9847496B2 (en) | 2013-12-23 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135008B2 (en) | 2014-01-07 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11943999B2 (en) | 2014-01-07 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749122B2 (en) | 2014-01-07 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10985331B2 (en) | 2014-01-07 | 2021-04-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11005051B2 (en) | 2014-01-08 | 2021-05-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978961B2 (en) | 2014-01-08 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9755159B2 (en) | 2014-01-23 | 2017-09-05 | Universal Display Corporation | Organic materials for OLEDs |
| US9935277B2 (en) | 2014-01-30 | 2018-04-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590194B2 (en) | 2014-02-14 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024816B2 (en) | 2014-02-18 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10003033B2 (en) | 2014-02-18 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847497B2 (en) | 2014-02-18 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10707423B2 (en) | 2014-02-21 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9647217B2 (en) | 2014-02-24 | 2017-05-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9502656B2 (en) | 2014-02-24 | 2016-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403825B2 (en) | 2014-02-27 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600782B2 (en) | 2014-02-27 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9590195B2 (en) | 2014-02-28 | 2017-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9181270B2 (en) | 2014-02-28 | 2015-11-10 | Universal Display Corporation | Method of making sulfide compounds |
| US9673407B2 (en) | 2014-02-28 | 2017-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9190620B2 (en) | 2014-03-01 | 2015-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9397309B2 (en) | 2014-03-13 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent devices |
| US10208026B2 (en) | 2014-03-18 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748504B2 (en) | 2014-03-25 | 2017-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10370396B2 (en) | 2014-03-31 | 2019-08-06 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometallated aryl group and their use in organic light emitting diodes |
| US9862739B2 (en) | 2014-03-31 | 2018-01-09 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an O-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| US10118939B2 (en) | 2014-03-31 | 2018-11-06 | Udc Ireland Limited | Metal complexes, comprising carbene ligands having an o-substituted non-cyclometalated aryl group and their use in organic light emitting diodes |
| US9929353B2 (en) | 2014-04-02 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9691993B2 (en) | 2014-04-09 | 2017-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9905785B2 (en) | 2014-04-14 | 2018-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10825998B2 (en) | 2014-04-14 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10008679B2 (en) | 2014-04-14 | 2018-06-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9847498B2 (en) | 2014-04-14 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11793066B2 (en) | 2014-04-14 | 2023-10-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11005052B2 (en) | 2014-04-14 | 2021-05-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9450198B2 (en) | 2014-04-15 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256427B2 (en) | 2014-04-15 | 2019-04-09 | Universal Display Corporation | Efficient organic electroluminescent devices |
| US9741941B2 (en) | 2014-04-29 | 2017-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11427607B2 (en) | 2014-05-02 | 2022-08-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10457699B2 (en) | 2014-05-02 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11919916B2 (en) | 2014-05-02 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10263198B2 (en) | 2014-05-08 | 2019-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256419B2 (en) | 2014-05-08 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495754B2 (en) | 2014-05-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10276805B2 (en) | 2014-05-08 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10301338B2 (en) | 2014-05-08 | 2019-05-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403830B2 (en) | 2014-05-08 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636983B2 (en) | 2014-05-08 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9997716B2 (en) | 2014-05-27 | 2018-06-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10461260B2 (en) | 2014-06-03 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10700293B2 (en) | 2014-06-26 | 2020-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9911931B2 (en) | 2014-06-26 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11456423B2 (en) | 2014-07-09 | 2022-09-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10297762B2 (en) | 2014-07-09 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11957047B2 (en) | 2014-07-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024811B2 (en) | 2014-07-09 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566546B2 (en) | 2014-07-14 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929357B2 (en) | 2014-07-22 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016016791A1 (en) | 2014-07-28 | 2016-02-04 | Idemitsu Kosan Co., Ltd (Ikc) | 2,9-functionalized benzimidazolo[1,2-a]benzimidazoles as hosts for organic light emitting diodes (oleds) |
| US12029108B2 (en) | 2014-08-07 | 2024-07-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11108000B2 (en) | 2014-08-07 | 2021-08-31 | Unniversal Display Corporation | Organic electroluminescent materials and devices |
| EP2982676A1 (de) | 2014-08-07 | 2016-02-10 | Idemitsu Kosan Co., Ltd. | Benzimidazo[2,1-b]benzoxazole für elektronische Anwendungen |
| US10411200B2 (en) | 2014-08-07 | 2019-09-10 | Universal Display Corporation | Electroluminescent (2-phenylpyridine)iridium complexes and devices |
| EP2993215A1 (de) | 2014-09-04 | 2016-03-09 | Idemitsu Kosan Co., Ltd. | Azabenzimidazo[2,1-a]benzimidazole für elektronische Anwendungen |
| US11641774B2 (en) | 2014-09-29 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10043987B2 (en) | 2014-09-29 | 2018-08-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10749113B2 (en) | 2014-09-29 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135007B2 (en) | 2014-09-29 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342510B2 (en) | 2014-10-06 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361375B2 (en) | 2014-10-06 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10854826B2 (en) | 2014-10-08 | 2020-12-01 | Universal Display Corporation | Organic electroluminescent compounds, compositions and devices |
| US10998508B2 (en) | 2014-10-08 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342516B2 (en) | 2014-10-08 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9799838B2 (en) | 2014-10-08 | 2017-10-24 | Universal Display Corporation | Fluorinated organic electroluminescent materials and devices |
| US9397302B2 (en) | 2014-10-08 | 2016-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12082485B2 (en) | 2014-10-08 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10950803B2 (en) | 2014-10-13 | 2021-03-16 | Universal Display Corporation | Compounds and uses in devices |
| US9484541B2 (en) | 2014-10-20 | 2016-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016067261A1 (en) | 2014-10-30 | 2016-05-06 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazoles for electronic applications |
| EP3015469A1 (de) | 2014-10-30 | 2016-05-04 | Idemitsu Kosan Co., Ltd. | 5-((benz)imidazol-2-yl)benzimidazo[1,2-a]benzimidazole für elektronische anwendungen |
| US10868261B2 (en) | 2014-11-10 | 2020-12-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10411201B2 (en) | 2014-11-12 | 2019-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832507B2 (en) | 2014-11-12 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11043641B2 (en) | 2014-11-12 | 2021-06-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10038151B2 (en) | 2014-11-12 | 2018-07-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871212B2 (en) | 2014-11-14 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9882151B2 (en) | 2014-11-14 | 2018-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016079667A1 (en) | 2014-11-17 | 2016-05-26 | Idemitsu Kosan Co., Ltd. | Indole derivatives for electronic applications |
| US9761814B2 (en) | 2014-11-18 | 2017-09-12 | Universal Display Corporation | Organic light-emitting materials and devices |
| WO2016079169A1 (en) | 2014-11-18 | 2016-05-26 | Basf Se | Pt- or pd-carbene complexes for use in organic light emitting diodes |
| US9444075B2 (en) | 2014-11-26 | 2016-09-13 | Universal Display Corporation | Emissive display with photo-switchable polarization |
| US9825260B2 (en) | 2014-11-26 | 2017-11-21 | Universal Display Corporation | Emissive display with photo-switchable polarization |
| EP3034506A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 4-funktionalisierte Carbazolderivate für elektronische Anwendungen |
| EP3034507A1 (de) | 2014-12-15 | 2016-06-22 | Idemitsu Kosan Co., Ltd | 1-funktionalisierte Dibenzofurane und Dibenzothiophene für organische Leuchtdioden (OLEDS) |
| WO2016097983A1 (en) | 2014-12-15 | 2016-06-23 | Idemitsu Kosan Co., Ltd. | 1-functionalized dibenzofurans and dibenzothiophenes for organic light emitting diodes (oleds) |
| US9680113B2 (en) | 2014-12-17 | 2017-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9450195B2 (en) | 2014-12-17 | 2016-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10000517B2 (en) | 2014-12-17 | 2018-06-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10253252B2 (en) | 2014-12-30 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10636978B2 (en) | 2014-12-30 | 2020-04-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9312499B1 (en) | 2015-01-05 | 2016-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9748500B2 (en) | 2015-01-15 | 2017-08-29 | Universal Display Corporation | Organic light emitting materials |
| US10418569B2 (en) | 2015-01-25 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9711730B2 (en) | 2015-01-25 | 2017-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3053918A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd | 2-Carbazol substituierte Benzimidazole für elektronische Anwendungen |
| US10644247B2 (en) | 2015-02-06 | 2020-05-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3054498A1 (de) | 2015-02-06 | 2016-08-10 | Idemitsu Kosan Co., Ltd. | Bisimidazodiazozine |
| US11245081B2 (en) | 2015-02-06 | 2022-02-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418562B2 (en) | 2015-02-06 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10355222B2 (en) | 2015-02-06 | 2019-07-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016125110A1 (en) | 2015-02-06 | 2016-08-11 | Idemitsu Kosan Co., Ltd. | Bisimidazolodiazocines |
| US10177316B2 (en) | 2015-02-09 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4271160A2 (de) | 2015-02-13 | 2023-11-01 | Merck Patent GmbH | Aromatisches heterocyclisches derivat und organisches elektrolumineszenzelement, beleuchtungsvorrichtung und anzeigevorrichtung mit dem aromatischen heterocyclischen derivat |
| US11795385B2 (en) | 2015-02-13 | 2023-10-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10144867B2 (en) | 2015-02-13 | 2018-12-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10889754B2 (en) | 2015-02-13 | 2021-01-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11535797B2 (en) | 2015-02-13 | 2022-12-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680183B2 (en) | 2015-02-15 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3056504A1 (de) | 2015-02-16 | 2016-08-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US9929361B2 (en) | 2015-02-16 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3061759A1 (de) | 2015-02-24 | 2016-08-31 | Idemitsu Kosan Co., Ltd | Nitrilsubstituierte dibenzofurane |
| EP3061763A1 (de) | 2015-02-27 | 2016-08-31 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10600966B2 (en) | 2015-02-27 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11678567B2 (en) | 2015-02-27 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056657B2 (en) | 2015-02-27 | 2021-07-06 | University Display Corporation | Organic electroluminescent materials and devices |
| US10686143B2 (en) | 2015-03-05 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10270046B2 (en) | 2015-03-06 | 2019-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3070144A1 (de) | 2015-03-17 | 2016-09-21 | Idemitsu Kosan Co., Ltd. | Siebengliedrige ringverbindungen |
| US9911928B2 (en) | 2015-03-19 | 2018-03-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9871214B2 (en) | 2015-03-23 | 2018-01-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10529931B2 (en) | 2015-03-24 | 2020-01-07 | Universal Display Corporation | Organic Electroluminescent materials and devices |
| EP3072943A1 (de) | 2015-03-26 | 2016-09-28 | Idemitsu Kosan Co., Ltd. | Dibenzofuran/carbazol-substituierte benzonitrile |
| US10297770B2 (en) | 2015-03-27 | 2019-05-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2016157113A1 (en) | 2015-03-31 | 2016-10-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying aryl- or heteroarylnitril groups for organic light emitting diodes |
| EP3075737A1 (de) | 2015-03-31 | 2016-10-05 | Idemitsu Kosan Co., Ltd | Benzimidazolo[1,2-a]benzimidazol mit aryl- oder heteroarylnitrilgruppen für organische leuchtdioden |
| US10593890B2 (en) | 2015-04-06 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495749B2 (en) | 2015-04-06 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11672175B2 (en) | 2015-04-06 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11245080B2 (en) | 2015-04-06 | 2022-02-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818949B2 (en) | 2015-04-06 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10693082B2 (en) | 2015-04-06 | 2020-06-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10403826B2 (en) | 2015-05-07 | 2019-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744151B2 (en) | 2015-05-07 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777749B2 (en) | 2015-05-07 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9478758B1 (en) | 2015-05-08 | 2016-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9859510B2 (en) | 2015-05-15 | 2018-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| USRE48809E1 (en) | 2015-05-15 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11335864B2 (en) | 2015-05-15 | 2022-05-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10547013B2 (en) | 2015-05-15 | 2020-01-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3098229A1 (de) | 2015-05-15 | 2016-11-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US12035614B2 (en) | 2015-05-15 | 2024-07-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10109799B2 (en) | 2015-05-21 | 2018-10-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10256411B2 (en) | 2015-05-21 | 2019-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3101021A1 (de) | 2015-06-01 | 2016-12-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10033004B2 (en) | 2015-06-01 | 2018-07-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418568B2 (en) | 2015-06-01 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4060757A1 (de) | 2015-06-03 | 2022-09-21 | UDC Ireland Limited | Hocheffiziente oled-vorrichtungen mit sehr kurzer abklingzeit |
| WO2016193243A1 (en) | 2015-06-03 | 2016-12-08 | Udc Ireland Limited | Highly efficient oled devices with very short decay times |
| US12058929B2 (en) | 2015-06-04 | 2024-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925102B2 (en) | 2015-06-04 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10825997B2 (en) | 2015-06-25 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873036B2 (en) | 2015-07-07 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9978956B2 (en) | 2015-07-15 | 2018-05-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3124488A1 (de) | 2015-07-29 | 2017-02-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11127905B2 (en) | 2015-07-29 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11018309B2 (en) | 2015-08-03 | 2021-05-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11522140B2 (en) | 2015-08-17 | 2022-12-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10522769B2 (en) | 2015-08-18 | 2019-12-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10181564B2 (en) | 2015-08-26 | 2019-01-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3760635A1 (de) | 2015-09-03 | 2021-01-06 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11605789B2 (en) | 2015-09-03 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361381B2 (en) | 2015-09-03 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672996B2 (en) | 2015-09-03 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3159350A1 (de) | 2015-09-03 | 2017-04-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11626563B2 (en) | 2015-09-03 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11706972B2 (en) | 2015-09-08 | 2023-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11302872B2 (en) | 2015-09-09 | 2022-04-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10770664B2 (en) | 2015-09-21 | 2020-09-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11812622B2 (en) | 2015-09-25 | 2023-11-07 | Universal Display Corporation | Organic electroluminescent compounds and devices |
| US10847728B2 (en) | 2015-10-01 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12063853B2 (en) | 2015-10-01 | 2024-08-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10593892B2 (en) | 2015-10-01 | 2020-03-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11889747B2 (en) | 2015-10-01 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017056053A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying benzimidazolo[1,2-a]benzimidazolyl groups, carbazolyl groups, benzofurane groups or benzothiophene groups for organic light emitting diodes |
| EP3150604A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazol mit benzimidazolo[1,2-a]benzimidazolylgruppen, carbazolylgruppen, benzofurangruppen oder benzothiophengruppen für organische leuchtdioden |
| WO2017056055A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying triazine groups for organic light emitting diodes |
| EP3150606A1 (de) | 2015-10-01 | 2017-04-05 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole mit benzofuran- oder benzothiophen- gruppen für organische licht emittierende dioden. |
| WO2017056052A1 (en) | 2015-10-01 | 2017-04-06 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole carrying benzimidazolo[1,2-a]benzimidazolyl groups, carbazolyl groups, benzofurane groups or benzothiophene groups for organic light emitting diodes |
| US10991895B2 (en) | 2015-10-06 | 2021-04-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388892B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11349087B2 (en) | 2015-10-29 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10177318B2 (en) | 2015-10-29 | 2019-01-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10388893B2 (en) | 2015-10-29 | 2019-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017078182A1 (en) | 2015-11-04 | 2017-05-11 | Idemitsu Kosan Co., Ltd. | Benzimidazole fused heteroaryls |
| US11832456B2 (en) | 2015-11-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10998507B2 (en) | 2015-11-23 | 2021-05-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10476010B2 (en) | 2015-11-30 | 2019-11-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017093958A1 (en) | 2015-12-04 | 2017-06-08 | Idemitsu Kosan Co., Ltd. | Benzimidazolo[1,2-a]benzimidazole derivatives for organic light emitting diodes |
| WO2017109727A1 (en) | 2015-12-21 | 2017-06-29 | Idemitsu Kosan Co., Ltd. | Hetero-condensed phenylquinazolines and their use in electronic devices |
| WO2017109722A1 (en) | 2015-12-21 | 2017-06-29 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocyclic compounds and organic electroluminescence devices containing them |
| US10957861B2 (en) | 2015-12-29 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024808B2 (en) | 2015-12-29 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818948B2 (en) | 2015-12-29 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10135006B2 (en) | 2016-01-04 | 2018-11-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3200255A2 (de) | 2016-01-06 | 2017-08-02 | Konica Minolta, Inc. | Organisches elektrolumineszenzelement, verfahren zur herstellung eines organischen elektrolumineszenzelements, sowie anzeige und beleuchtungsvorrichtung |
| US10457864B2 (en) | 2016-02-09 | 2019-10-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11692132B2 (en) | 2016-02-09 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858842A1 (de) | 2016-02-09 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11098245B2 (en) | 2016-02-09 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3205658A1 (de) | 2016-02-09 | 2017-08-16 | Universal Display Corporation | Organische elektrolumineszenzmaterialien und vorrichtungen |
| US11716898B2 (en) | 2016-02-09 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10707427B2 (en) | 2016-02-09 | 2020-07-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10600967B2 (en) | 2016-02-18 | 2020-03-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11094891B2 (en) | 2016-03-16 | 2021-08-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10276809B2 (en) | 2016-04-05 | 2019-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4122941A1 (de) | 2016-04-11 | 2023-01-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3231809A2 (de) | 2016-04-11 | 2017-10-18 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10236456B2 (en) | 2016-04-11 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2017178864A1 (en) | 2016-04-12 | 2017-10-19 | Idemitsu Kosan Co., Ltd. | Seven-membered ring compounds |
| US11825734B2 (en) | 2016-04-13 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566552B2 (en) | 2016-04-13 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342515B2 (en) | 2016-04-13 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228002B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081647B2 (en) | 2016-04-22 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228003B2 (en) | 2016-04-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12048237B2 (en) | 2016-05-05 | 2024-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10840458B2 (en) | 2016-05-25 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10985328B2 (en) | 2016-05-25 | 2021-04-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11711977B2 (en) | 2016-05-25 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10468609B2 (en) | 2016-06-02 | 2019-11-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10651403B2 (en) | 2016-06-20 | 2020-05-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3261146A2 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3843171A1 (de) | 2016-06-20 | 2021-06-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3270435A2 (de) | 2016-06-20 | 2018-01-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11683981B2 (en) | 2016-06-20 | 2023-06-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672997B2 (en) | 2016-06-20 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11588121B2 (en) | 2016-06-20 | 2023-02-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11903306B2 (en) | 2016-06-20 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10686140B2 (en) | 2016-06-20 | 2020-06-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3261147A1 (de) | 2016-06-20 | 2017-12-27 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US12101999B2 (en) | 2016-06-20 | 2024-09-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11690284B2 (en) | 2016-06-20 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10727423B2 (en) | 2016-06-20 | 2020-07-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11839139B2 (en) | 2016-06-20 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11424419B2 (en) | 2016-06-20 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482683B2 (en) | 2016-06-20 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3920254A1 (de) | 2016-06-20 | 2021-12-08 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11114624B2 (en) | 2016-06-20 | 2021-09-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4349935A2 (de) | 2016-06-20 | 2024-04-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3758084A1 (de) | 2016-06-20 | 2020-12-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10862054B2 (en) | 2016-06-20 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10957866B2 (en) | 2016-06-30 | 2021-03-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9929360B2 (en) | 2016-07-08 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680184B2 (en) | 2016-07-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10566547B2 (en) | 2016-07-11 | 2020-02-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10720587B2 (en) | 2016-07-19 | 2020-07-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153443B2 (en) | 2016-07-19 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10205105B2 (en) | 2016-08-15 | 2019-02-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3297051A1 (de) | 2016-09-14 | 2018-03-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10608186B2 (en) | 2016-09-14 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11024807B2 (en) | 2016-09-14 | 2021-06-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10505127B2 (en) | 2016-09-19 | 2019-12-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680187B2 (en) | 2016-09-23 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3323822A1 (de) | 2016-09-23 | 2018-05-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11196010B2 (en) | 2016-10-03 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11711969B2 (en) | 2016-10-03 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183642B2 (en) | 2016-10-03 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3301088A1 (de) | 2016-10-03 | 2018-04-04 | Universal Display Corporation | Kondensierte pyridine als organische elektrolumineszente materialien und vorrichtungen |
| US11127906B2 (en) | 2016-10-03 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081658B2 (en) | 2016-10-03 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11189804B2 (en) | 2016-10-03 | 2021-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11711968B2 (en) | 2016-10-07 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3305796A1 (de) | 2016-10-07 | 2018-04-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11011709B2 (en) | 2016-10-07 | 2021-05-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3858844A1 (de) | 2016-10-07 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11239432B2 (en) | 2016-10-14 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608185B2 (en) | 2016-10-17 | 2020-03-31 | Univeral Display Corporation | Organic electroluminescent materials and devices |
| US10236458B2 (en) | 2016-10-24 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3789379A1 (de) | 2016-11-09 | 2021-03-10 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| EP3321258A1 (de) | 2016-11-09 | 2018-05-16 | Universal Display Corporation | 4-phenylbenzo[g]quinazolin oder 4-(3,5-dimethylphenylbenzo[g]quinazoline iridiumkomplexe zur verwendung als nah-infrarot oder infrarot emittierende materialien in oleds |
| US10340464B2 (en) | 2016-11-10 | 2019-07-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680188B2 (en) | 2016-11-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4092036A1 (de) | 2016-11-11 | 2022-11-23 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3354654A2 (de) | 2016-11-11 | 2018-08-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11069864B2 (en) | 2016-11-11 | 2021-07-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11980094B2 (en) | 2016-11-14 | 2024-05-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10897016B2 (en) | 2016-11-14 | 2021-01-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10662196B2 (en) | 2016-11-17 | 2020-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964893B2 (en) | 2016-11-17 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10833276B2 (en) | 2016-11-21 | 2020-11-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10153445B2 (en) | 2016-11-21 | 2018-12-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11555048B2 (en) | 2016-12-01 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545636B2 (en) | 2016-12-15 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10490753B2 (en) | 2016-12-15 | 2019-11-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11548905B2 (en) | 2016-12-15 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10811618B2 (en) | 2016-12-19 | 2020-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11152579B2 (en) | 2016-12-28 | 2021-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3345914A1 (de) | 2017-01-09 | 2018-07-11 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11201298B2 (en) | 2017-01-09 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3689890A1 (de) | 2017-01-09 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4212540A1 (de) | 2017-01-09 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11780865B2 (en) | 2017-01-09 | 2023-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10804475B2 (en) | 2017-01-11 | 2020-10-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11545637B2 (en) | 2017-01-13 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10629820B2 (en) | 2017-01-18 | 2020-04-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11053268B2 (en) | 2017-01-20 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964904B2 (en) | 2017-01-20 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11566034B2 (en) | 2017-01-20 | 2023-01-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765968B2 (en) | 2017-01-23 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765966B2 (en) | 2017-01-24 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11050028B2 (en) | 2017-01-24 | 2021-06-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12089486B2 (en) | 2017-02-08 | 2024-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10978647B2 (en) | 2017-02-15 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10844084B2 (en) | 2017-02-22 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822361B2 (en) | 2017-02-22 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697661B2 (en) | 2017-02-22 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11254697B2 (en) | 2017-02-22 | 2022-02-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11760770B2 (en) | 2017-02-22 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10745431B2 (en) | 2017-03-08 | 2020-08-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10741780B2 (en) | 2017-03-10 | 2020-08-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672998B2 (en) | 2017-03-23 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910577B2 (en) | 2017-03-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10873037B2 (en) | 2017-03-28 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12041846B2 (en) | 2017-03-29 | 2024-07-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11158820B2 (en) | 2017-03-29 | 2021-10-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3730506A1 (de) | 2017-03-29 | 2020-10-28 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10844085B2 (en) | 2017-03-29 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11678563B2 (en) | 2017-03-29 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3985012A1 (de) | 2017-03-29 | 2022-04-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3381927A1 (de) | 2017-03-29 | 2018-10-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11056658B2 (en) | 2017-03-29 | 2021-07-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11192910B2 (en) | 2017-03-29 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11725021B2 (en) | 2017-03-29 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862046B2 (en) | 2017-03-30 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11139443B2 (en) | 2017-03-31 | 2021-10-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11276829B2 (en) | 2017-03-31 | 2022-03-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038117B2 (en) | 2017-04-11 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10777754B2 (en) | 2017-04-11 | 2020-09-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11084838B2 (en) | 2017-04-21 | 2021-08-10 | Universal Display Corporation | Organic electroluminescent materials and device |
| US11101434B2 (en) | 2017-04-21 | 2021-08-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10975113B2 (en) | 2017-04-21 | 2021-04-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11591356B2 (en) | 2017-04-21 | 2023-02-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11566035B2 (en) | 2017-04-21 | 2023-01-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10910570B2 (en) | 2017-04-28 | 2021-02-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038137B2 (en) | 2017-04-28 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11702420B2 (en) | 2017-05-01 | 2023-07-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11117897B2 (en) | 2017-05-01 | 2021-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10941170B2 (en) | 2017-05-03 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11201299B2 (en) | 2017-05-04 | 2021-12-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11377459B2 (en) | 2017-05-05 | 2022-07-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862055B2 (en) | 2017-05-05 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10870668B2 (en) | 2017-05-05 | 2020-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930864B2 (en) | 2017-05-10 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10822362B2 (en) | 2017-05-11 | 2020-11-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944060B2 (en) | 2017-05-11 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4141010A1 (de) | 2017-05-11 | 2023-03-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3401318A1 (de) | 2017-05-11 | 2018-11-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US10944062B2 (en) | 2017-05-18 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10934293B2 (en) | 2017-05-18 | 2021-03-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11038115B2 (en) | 2017-05-18 | 2021-06-15 | Universal Display Corporation | Organic electroluminescent materials and device |
| US10840459B2 (en) | 2017-05-18 | 2020-11-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10790455B2 (en) | 2017-05-18 | 2020-09-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10930862B2 (en) | 2017-06-01 | 2021-02-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3418285A1 (de) | 2017-06-20 | 2018-12-26 | Idemitsu Kosan Co., Ltd. | Zusammensetzung mit einem substituierten ir-komplex und einem mit einem heteroatom verbrückten phenylchinazolin |
| EP3418286A1 (de) | 2017-06-23 | 2018-12-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11725022B2 (en) | 2017-06-23 | 2023-08-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495757B2 (en) | 2017-06-23 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11958825B2 (en) | 2017-06-23 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12098157B2 (en) | 2017-06-23 | 2024-09-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10968226B2 (en) | 2017-06-23 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11678565B2 (en) | 2017-06-23 | 2023-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11174259B2 (en) | 2017-06-23 | 2021-11-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11802136B2 (en) | 2017-06-23 | 2023-10-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11731975B2 (en) | 2017-06-23 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11814403B2 (en) | 2017-06-23 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11552261B2 (en) | 2017-06-23 | 2023-01-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11608321B2 (en) | 2017-06-23 | 2023-03-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758804B2 (en) | 2017-06-23 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11832510B2 (en) | 2017-06-23 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469382B2 (en) | 2017-07-12 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11322691B2 (en) | 2017-07-26 | 2022-05-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4185086A1 (de) | 2017-07-26 | 2023-05-24 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11239433B2 (en) | 2017-07-26 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765970B2 (en) | 2017-07-26 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11917843B2 (en) | 2017-07-26 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11968883B2 (en) | 2017-07-26 | 2024-04-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12096681B2 (en) | 2017-07-26 | 2024-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744141B2 (en) | 2017-08-09 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3444258A2 (de) | 2017-08-10 | 2019-02-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3783006A1 (de) | 2017-08-10 | 2021-02-24 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11910699B2 (en) | 2017-08-10 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11349083B2 (en) | 2017-08-10 | 2022-05-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744142B2 (en) | 2017-08-10 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11508913B2 (en) | 2017-08-10 | 2022-11-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11462697B2 (en) | 2017-08-22 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11723269B2 (en) | 2017-08-22 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11437591B2 (en) | 2017-08-24 | 2022-09-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11605791B2 (en) | 2017-09-01 | 2023-03-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11444249B2 (en) | 2017-09-07 | 2022-09-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11424420B2 (en) | 2017-09-07 | 2022-08-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11696492B2 (en) | 2017-09-07 | 2023-07-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12069949B2 (en) | 2017-09-07 | 2024-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10964895B2 (en) | 2017-09-11 | 2021-03-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608188B2 (en) | 2017-09-11 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11778897B2 (en) | 2017-09-20 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11183646B2 (en) | 2017-11-07 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910702B2 (en) | 2017-11-07 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent devices |
| US11214587B2 (en) | 2017-11-07 | 2022-01-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11685756B2 (en) | 2017-11-07 | 2023-06-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11168103B2 (en) | 2017-11-17 | 2021-11-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3878855A1 (de) | 2017-11-28 | 2021-09-15 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| US11825735B2 (en) | 2017-11-28 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3489243A1 (de) | 2017-11-28 | 2019-05-29 | University of Southern California | Carbenverbindungen und organische elektrolumineszente vorrichtungen |
| EP3492480A2 (de) | 2017-11-29 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11937503B2 (en) | 2017-11-30 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3492528A1 (de) | 2017-11-30 | 2019-06-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11233204B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12075690B2 (en) | 2017-12-14 | 2024-08-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10971687B2 (en) | 2017-12-14 | 2021-04-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11233205B2 (en) | 2017-12-14 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11700765B2 (en) | 2018-01-10 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081659B2 (en) | 2018-01-10 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11818946B2 (en) | 2018-01-11 | 2023-11-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11271177B2 (en) | 2018-01-11 | 2022-03-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515493B2 (en) | 2018-01-11 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11542289B2 (en) | 2018-01-26 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11367840B2 (en) | 2018-01-26 | 2022-06-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4019526A1 (de) | 2018-01-26 | 2022-06-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11845764B2 (en) | 2018-01-26 | 2023-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12029055B2 (en) | 2018-01-30 | 2024-07-02 | The University Of Southern California | OLED with hybrid emissive layer |
| US11180519B2 (en) | 2018-02-09 | 2021-11-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697662B2 (en) | 2018-02-09 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11239434B2 (en) | 2018-02-09 | 2022-02-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11910708B2 (en) | 2018-02-09 | 2024-02-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11957050B2 (en) | 2018-02-09 | 2024-04-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342509B2 (en) | 2018-02-09 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11746122B2 (en) | 2018-03-12 | 2023-09-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11217757B2 (en) | 2018-03-12 | 2022-01-04 | Universal Display Corporation | Host materials for electroluminescent devices |
| US12108668B2 (en) | 2018-03-12 | 2024-10-01 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11557733B2 (en) | 2018-03-12 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11700766B2 (en) | 2018-03-12 | 2023-07-11 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11279722B2 (en) | 2018-03-12 | 2022-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11165028B2 (en) | 2018-03-12 | 2021-11-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11142538B2 (en) | 2018-03-12 | 2021-10-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11882759B2 (en) | 2018-04-13 | 2024-01-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11390639B2 (en) | 2018-04-13 | 2022-07-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11616203B2 (en) | 2018-04-17 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11839142B2 (en) | 2018-05-04 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11342513B2 (en) | 2018-05-04 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515494B2 (en) | 2018-05-04 | 2022-11-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753427B2 (en) | 2018-05-04 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11793073B2 (en) | 2018-05-06 | 2023-10-17 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11459349B2 (en) | 2018-05-25 | 2022-10-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11450822B2 (en) | 2018-05-25 | 2022-09-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11844267B2 (en) | 2018-05-25 | 2023-12-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11716900B2 (en) | 2018-05-30 | 2023-08-01 | Universal Display Corporation | Host materials for electroluminescent devices |
| US12022727B2 (en) | 2018-06-04 | 2024-06-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11404653B2 (en) | 2018-06-04 | 2022-08-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11296283B2 (en) | 2018-06-04 | 2022-04-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11925103B2 (en) | 2018-06-05 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11339182B2 (en) | 2018-06-07 | 2022-05-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228004B2 (en) | 2018-06-22 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11261207B2 (en) | 2018-06-25 | 2022-03-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11753425B2 (en) | 2018-07-11 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3613751A1 (de) | 2018-08-22 | 2020-02-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4206210A1 (de) | 2018-08-22 | 2023-07-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11233203B2 (en) | 2018-09-06 | 2022-01-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11939293B2 (en) | 2018-09-11 | 2024-03-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11485706B2 (en) | 2018-09-11 | 2022-11-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11718634B2 (en) | 2018-09-14 | 2023-08-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11903305B2 (en) | 2018-09-24 | 2024-02-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11495752B2 (en) | 2018-10-08 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469383B2 (en) | 2018-10-08 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11476430B2 (en) | 2018-10-15 | 2022-10-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515482B2 (en) | 2018-10-23 | 2022-11-29 | Universal Display Corporation | Deep HOMO (highest occupied molecular orbital) emitter device structures |
| US11839141B2 (en) | 2018-11-02 | 2023-12-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11469384B2 (en) | 2018-11-02 | 2022-10-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11825736B2 (en) | 2018-11-19 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11963441B2 (en) | 2018-11-26 | 2024-04-16 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11515489B2 (en) | 2018-11-28 | 2022-11-29 | Universal Display Corporation | Host materials for electroluminescent devices |
| US12048246B2 (en) | 2018-11-28 | 2024-07-23 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11672165B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11706980B2 (en) | 2018-11-28 | 2023-07-18 | Universal Display Corporation | Host materials for electroluminescent devices |
| US12035618B2 (en) | 2018-11-28 | 2024-07-09 | Universal Display Corporation | Electroluminescent devices |
| US11716899B2 (en) | 2018-11-28 | 2023-08-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11672176B2 (en) | 2018-11-28 | 2023-06-06 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11690285B2 (en) | 2018-11-28 | 2023-06-27 | Universal Display Corporation | Electroluminescent devices |
| US11623936B2 (en) | 2018-12-11 | 2023-04-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11737349B2 (en) | 2018-12-12 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11834459B2 (en) | 2018-12-12 | 2023-12-05 | Universal Display Corporation | Host materials for electroluminescent devices |
| US11780829B2 (en) | 2019-01-30 | 2023-10-10 | The University Of Southern California | Organic electroluminescent materials and devices |
| EP3690973A1 (de) | 2019-01-30 | 2020-08-05 | University Of Southern California | Organische elektrolumineszente materialien und vorrichtungen |
| US11812624B2 (en) | 2019-01-30 | 2023-11-07 | The University Of Southern California | Organic electroluminescent materials and devices |
| EP4301117A2 (de) | 2019-02-01 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3689889A1 (de) | 2019-02-01 | 2020-08-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11370809B2 (en) | 2019-02-08 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11325932B2 (en) | 2019-02-08 | 2022-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11773320B2 (en) | 2019-02-21 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11758807B2 (en) | 2019-02-22 | 2023-09-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11557738B2 (en) | 2019-02-22 | 2023-01-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11871653B2 (en) | 2019-02-22 | 2024-01-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11512093B2 (en) | 2019-03-04 | 2022-11-29 | Universal Display Corporation | Compound used for organic light emitting device (OLED), consumer product and formulation |
| US11976086B2 (en) | 2019-03-06 | 2024-05-07 | Samsung Display Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and apparatus including the organic light-emitting device |
| US11739081B2 (en) | 2019-03-11 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11637261B2 (en) | 2019-03-12 | 2023-04-25 | Universal Display Corporation | Nanopatch antenna outcoupling structure for use in OLEDs |
| US11963389B2 (en) | 2019-03-12 | 2024-04-16 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| US11569480B2 (en) | 2019-03-12 | 2023-01-31 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| EP3709376A1 (de) | 2019-03-12 | 2020-09-16 | Universal Display Corporation | Oled mit triplett-emitter und einer lebensdauer des angeregten zustands von unter 200 ns |
| US11968851B2 (en) | 2019-03-12 | 2024-04-23 | Universal Display Corporation | Organic electroluminescent devices |
| EP4134371A2 (de) | 2019-03-26 | 2023-02-15 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11963438B2 (en) | 2019-03-26 | 2024-04-16 | The University Of Southern California | Organic electroluminescent materials and devices |
| EP3715353A1 (de) | 2019-03-26 | 2020-09-30 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11639363B2 (en) | 2019-04-22 | 2023-05-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12006333B2 (en) | 2019-04-30 | 2024-06-11 | Universal Display Corporation | Organic electroluminescent materials and devices comprising imidazole-containing metal complexes |
| US12075691B2 (en) | 2019-04-30 | 2024-08-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11613550B2 (en) | 2019-04-30 | 2023-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices comprising benzimidazole-containing metal complexes |
| US11495756B2 (en) | 2019-05-07 | 2022-11-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11560398B2 (en) | 2019-05-07 | 2023-01-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11827651B2 (en) | 2019-05-13 | 2023-11-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12103942B2 (en) | 2019-05-13 | 2024-10-01 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11634445B2 (en) | 2019-05-21 | 2023-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12010859B2 (en) | 2019-05-24 | 2024-06-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3750897A1 (de) | 2019-06-10 | 2020-12-16 | Universal Display Corporation | Organische elektrolumineszente materialien und geräte |
| US11647667B2 (en) | 2019-06-14 | 2023-05-09 | Universal Display Corporation | Organic electroluminescent compounds and organic light emitting devices using the same |
| US12077550B2 (en) | 2019-07-02 | 2024-09-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11920070B2 (en) | 2019-07-12 | 2024-03-05 | The University Of Southern California | Luminescent janus-type, two-coordinated metal complexes |
| US12018036B2 (en) | 2019-07-22 | 2024-06-25 | Universal Display Corporation | Heteroleptic organic electroluminescent materials and devices |
| US11685754B2 (en) | 2019-07-22 | 2023-06-27 | Universal Display Corporation | Heteroleptic organic electroluminescent materials |
| US11926638B2 (en) | 2019-07-22 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3771717A1 (de) | 2019-07-30 | 2021-02-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4219515A1 (de) | 2019-07-30 | 2023-08-02 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11708355B2 (en) | 2019-08-01 | 2023-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11985888B2 (en) | 2019-08-12 | 2024-05-14 | The Regents Of The University Of Michigan | Organic electroluminescent device |
| US11374181B2 (en) | 2019-08-14 | 2022-06-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11930699B2 (en) | 2019-08-15 | 2024-03-12 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3778614A1 (de) | 2019-08-16 | 2021-02-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11925105B2 (en) | 2019-08-26 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937494B2 (en) | 2019-08-28 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11600787B2 (en) | 2019-08-30 | 2023-03-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11820783B2 (en) | 2019-09-06 | 2023-11-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11999886B2 (en) | 2019-09-26 | 2024-06-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11864458B2 (en) | 2019-10-08 | 2024-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11950493B2 (en) | 2019-10-15 | 2024-04-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11697653B2 (en) | 2019-10-21 | 2023-07-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11919914B2 (en) | 2019-10-25 | 2024-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11765965B2 (en) | 2019-10-30 | 2023-09-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3816175A1 (de) | 2019-11-04 | 2021-05-05 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3823055A1 (de) | 2019-11-14 | 2021-05-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11889708B2 (en) | 2019-11-14 | 2024-01-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3845545A1 (de) | 2020-01-06 | 2021-07-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4151644A1 (de) | 2020-01-06 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11778895B2 (en) | 2020-01-13 | 2023-10-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4294157A2 (de) | 2020-01-28 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP3858945A1 (de) | 2020-01-28 | 2021-08-04 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US11917900B2 (en) | 2020-01-28 | 2024-02-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11932660B2 (en) | 2020-01-29 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12084465B2 (en) | 2020-02-24 | 2024-09-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12018035B2 (en) | 2020-03-23 | 2024-06-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12122793B2 (en) | 2020-03-26 | 2024-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11970508B2 (en) | 2020-04-22 | 2024-04-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12035613B2 (en) | 2020-05-26 | 2024-07-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3937268A1 (de) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| US12065451B2 (en) | 2020-08-19 | 2024-08-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4016659A1 (de) | 2020-11-16 | 2022-06-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001287A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4329463A2 (de) | 2020-11-24 | 2024-02-28 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4001286A1 (de) | 2020-11-24 | 2022-05-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4039692A1 (de) | 2021-02-03 | 2022-08-10 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059915A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4060758A2 (de) | 2021-02-26 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4053137A1 (de) | 2021-03-05 | 2022-09-07 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4056578A1 (de) | 2021-03-12 | 2022-09-14 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4059941A1 (de) | 2021-03-15 | 2022-09-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4074723A1 (de) | 2021-04-05 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4075531A1 (de) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonische oleds und vertikale dipolstrahler |
| EP4075530A1 (de) | 2021-04-14 | 2022-10-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4401530A2 (de) | 2021-04-14 | 2024-07-17 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4079743A1 (de) | 2021-04-23 | 2022-10-26 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4086266A1 (de) | 2021-04-23 | 2022-11-09 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4112701A2 (de) | 2021-06-08 | 2023-01-04 | University of Southern California | Molekulare ausrichtung homoleptischer iridiumphosphore |
| EP4151699A1 (de) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4212539A1 (de) | 2021-12-16 | 2023-07-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4242285A1 (de) | 2022-03-09 | 2023-09-13 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4265626A2 (de) | 2022-04-18 | 2023-10-25 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4282863A1 (de) | 2022-05-24 | 2023-11-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4293001A1 (de) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4299693A1 (de) | 2022-06-28 | 2024-01-03 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4326030A1 (de) | 2022-08-17 | 2024-02-21 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US12127470B2 (en) | 2022-09-16 | 2024-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4369898A1 (de) | 2022-10-27 | 2024-05-15 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4362645A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4376583A2 (de) | 2022-10-27 | 2024-05-29 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4362631A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4362630A2 (de) | 2022-10-27 | 2024-05-01 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| EP4386065A1 (de) | 2022-12-14 | 2024-06-19 | Universal Display Corporation | Organische elektrolumineszente materialien und vorrichtungen |
| US12122794B2 (en) | 2023-05-25 | 2024-10-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
Also Published As
| Publication number | Publication date |
|---|---|
| US20100219403A1 (en) | 2010-09-02 |
| CN101878552A (zh) | 2010-11-03 |
| KR20100045462A (ko) | 2010-05-03 |
| EP2165377B1 (de) | 2021-04-28 |
| JP5675349B2 (ja) | 2015-02-25 |
| JP2010532400A (ja) | 2010-10-07 |
| CN101878552B (zh) | 2015-07-15 |
| EP2165377A1 (de) | 2010-03-24 |
| KR101577465B1 (ko) | 2015-12-14 |
| US8373159B2 (en) | 2013-02-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2165377B1 (de) | Organische leuchtdioden enthaltend carben-übergangsmetall-komplex-emitter und mindestens eine verbindung ausgewählt aus disilylcarbazolen; disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s,s-dioxiden | |
| EP3345983B1 (de) | Verbindungen enthaltend mindestens eine disilylverbindung ausgewählt aus disilylcarbazolen, disilyldibenzofuranen, disilyldibenzothiophenen, disilyldibenzophospholen, disilyldibenzothiophen-s-oxiden und disilyldibenzothiophen-s, s-dioxiden | |
| EP2393819B1 (de) | Silyl- und heteroatom-substituierte verbindungen ausgewählt aus carbazolen, dibenzofuranen, dibenzothiophenen und dibenzophospholen und ihre anwendung in der organischen elektronik | |
| EP2150556B1 (de) | Silane enthaltend phenothiazin-s-oxid oder phenothiazin-s,s-dioxid-gruppen und deren verwendung in oleds | |
| EP3457452B1 (de) | Oled-anzeige mit verlängerter lebensdauer | |
| EP2513125B1 (de) | Metallkomplexe, enthaltend diazabenzimidazolcarben-liganden und deren verwendung in oleds | |
| DE112011101663B4 (de) | Azaborinverbindungen als Hostmaterialien und Dotiermittel für Pholeds | |
| DE112011103404B4 (de) | Neuartige 3,9-verknüpfte Oligocarbazole und OLEDs, die diese neuartigen Oligocarbazole enthalten | |
| EP2556075B1 (de) | Substituierte carbazolderivate und ihre verwendung in organischen elektronikelementen | |
| EP2488540B1 (de) | Dinukleare platin-carben-komplexe und deren verwendung in oleds | |
| TWI647233B (zh) | 聯伸三苯矽烷主體 | |
| DE112012002237T5 (de) | Host Materialien für OLEDS | |
| WO2011051404A1 (de) | Heteroleptische carben-komplexe und deren verwendung in der organischen elektronik | |
| EP1817805A1 (de) | Verwendung von phenothiazin-s-oxiden und -s,s-dioxiden als matrixmaterialien f]r organische leuchtdioden | |
| EP2301091B1 (de) | Verwendung von cyclischen phosphazenverbindungen in organischen leuchtdioden | |
| EP2207865A1 (de) | Verwendung von substituierten tris(diphenylamino)-triazinverbindungen in oleds | |
| WO2009053346A1 (de) | Verwendung von diphenylamino-bis(phenoxy)- und bis(diphenylamino)-phenoxytriazinverbindungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200880104631.0 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 08774297 Country of ref document: EP Kind code of ref document: A1 |
|
| DPE1 | Request for preliminary examination filed after expiration of 19th month from priority date (pct application filed from 20040101) | ||
| DPE1 | Request for preliminary examination filed after expiration of 19th month from priority date (pct application filed from 20040101) | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2010513911 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2008774297 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 20107002592 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12667619 Country of ref document: US |