JP6986965B2 - 抗pd−1抗体 - Google Patents
抗pd−1抗体 Download PDFInfo
- Publication number
- JP6986965B2 JP6986965B2 JP2017525309A JP2017525309A JP6986965B2 JP 6986965 B2 JP6986965 B2 JP 6986965B2 JP 2017525309 A JP2017525309 A JP 2017525309A JP 2017525309 A JP2017525309 A JP 2017525309A JP 6986965 B2 JP6986965 B2 JP 6986965B2
- Authority
- JP
- Japan
- Prior art keywords
- homology
- seq
- amino acid
- antibody
- variable region
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/04—Drugs for disorders of the respiratory system for throat disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
- A61P31/06—Antibacterial agents for tuberculosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/06—Antimalarials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/10—Anthelmintics
- A61P33/12—Schistosomicides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/64—General methods for preparing the vector, for introducing it into the cell or for selecting the vector-containing host
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/74—Inducing cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/32—Fusion polypeptide fusions with soluble part of a cell surface receptor, "decoy receptors"
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/599—Cell markers; Cell surface determinants with CD designations not provided for elsewhere
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Immunology (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Oncology (AREA)
- Biochemistry (AREA)
- Communicable Diseases (AREA)
- Molecular Biology (AREA)
- Pulmonology (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Cell Biology (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Mycology (AREA)
- Dermatology (AREA)
- Otolaryngology (AREA)
- Epidemiology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
Description
本出願は、2014年7月22日出願の国際出願第PCT/CN2014/082721号明細書の優先権を主張し、その全体があらゆる目的のために参照によって本明細書に組み込まれる。
本発明は、PD−1に結合する抗体及びその抗原結合断片、ならびにこのような抗体及び抗原結合断片を使用する方法に関する。
本明細書と共に電子的に提出されるテキストファイルの内容は、その全体が参照によって本明細書に組み込まれる:配列表のコンピュータ可読形式コピー(ファイル名称:CRBI_006_01WO_SeqList_ST25);記録日:2015年7月14日;ファイルサイズ:147KB)。
プログラム死受容体1(PD−1)は、主としてリンパ球上で発現され、2つのリガンド、すなわちPD−L1及びPD−L2を有する。PD−1は、遺伝子Pdcd1によってコードされる55kDaのタンパク質であり、リガンドとの結合によって抗原受容体シグナル伝達の下方制御が促進されることが示された(Freeman et al.(2000)J Exp Med 192:1027−34(非特許文献1);Latchman,et.al.(2001)Nat Immunol 2:261−8(非特許文献2);Carter et al.(2002)Eur J Immunol 32:634−43(非特許文献3))。PD−1は、CD28、CTLA−4、ICOS及びBTLAなどのメンバーを含む免疫グロブリンスーパーファミリーに属する。PD−1は、リガンド結合のためのIg可変型(V型)ドメイン及びシグナル伝達分子の結合のための細胞質尾部を含有するI型膜貫通糖タンパク質である。PD−1は、2つの細胞質チロシンベースのシグナル伝達モチーフ、すなわち免疫受容体抑制性チロシンモチーフ(ITIM)及び免疫受容体スイッチ性チロシンモチーフ(ITSM)を含有する。T細胞の刺激後、PD−1は、その細胞質尾部内のITSMモチーフにチロシンホスファターゼSHP−2を動員し、CD3T細胞シグナル伝達カスケードに関与するエフェクター分子、例えばCD3ゼータ、PKCシータ及びZAP70などの脱リン酸化をもたらす。対照的に、PD−1のリガンド(PD−L1及びPD−L2)は、未知の機能を有する2つの短い細胞質領域を有する。このリガンドは、IgV様及びIgC様ドメインを含有する細胞外領域を有し、構成的に発現される、または非造血組織に加えて種々の腫瘍型を含む、様々な細胞型で誘導され得る。PD−L1は、B細胞、T細胞、骨髄性細胞及び樹状細胞(DC)上で発現されるだけでなく、微小血管内皮細胞及び心臓、肺などのような非リンパ器官のような末梢細胞上にも発現される。対照的に、PD−L2は、マクロファージ及びDC上でのみ見出される。PD−1リガンドの発現パターンは、末梢寛容の維持におけるPD−1の役割を示唆し、末梢において自己反応性T細胞及びB細胞の応答を制御するのに役立つ場合がある。今日までに、多数の研究が、PD−1とそのリガンドとの相互作用が、インビトロ及びインビボでリンパ球増殖の阻害をもたらすことを示してきた。PD−1/PDL1相互作用を妨げると、T細胞増殖を増加させ、サイトカイン産生を促進することが示されている。
[本発明1001]
PD−1に結合する単離された抗体またはその断片であって、
配列番号24、34、45、55、65、75、85、95、105、及び115から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する軽鎖CDR1配列;
配列番号25、35、46、56、66、76、86、96、106、及び116から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する軽鎖CDR2配列;
配列番号26、36、47、57、67、77、87、97、107、及び117から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する軽鎖CDR3配列;
配列番号19、29、40、50、60、70、80、90、100、及び110から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する重鎖CDR1配列;
配列番号20、30、41、51、61、71、81、91、101、及び111から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する重鎖CDR2配列;及び
配列番号21、31、42、52、62、72、82、92、102、及び112から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有する重鎖CDR3配列
を含む、前記単離された抗体またはその断片。
[本発明1002]
配列番号24、34、45、55、65、75、85、95、105、及び115から成る群から選択されるアミノ酸配列から成る軽鎖CDR1;
配列番号25、35、46、66、76、86、96、106、及び116から成る群から選択されるアミノ酸配列から成る軽鎖CDR2;
配列番号26、36、47、57、67、77、87、97、107、及び117から成る群から選択されるアミノ酸配列から成る軽鎖CDR3;
配列番号19、29、40、50、60、70、80、90、100、及び110から成る群から選択されるアミノ酸配列から成る重鎖CDR1;
配列番号20、30、41、51、61、71、81、91、101、及び111から成る群から選択されるアミノ酸配列から成る重鎖CDR2;及び
配列番号21、31、42、52、62、72、82、92、102、及び112から成る群から選択されるアミノ酸配列から成る重鎖CDR3
を含む、本発明1001の抗体またはその断片。
[本発明1003]
それぞれ配列番号24、25、及び26のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号19、20、及び21のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1004]
それぞれ配列番号34、35、及び36のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号29、30、及び31のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1005]
それぞれ配列番号45、46、及び47のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号40、41、及び42のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1006]
それぞれ配列番号55、56、及び57のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号50、51、及び52のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1007]
それぞれ配列番号65、66、及び67のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号60、61、及び62のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1008]
それぞれ配列番号75、76、及び77のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号70、71、及び72のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1009]
それぞれ配列番号85、86、及び87のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号80、81、及び82のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1010]
それぞれ配列番号95、96、及び97のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号90、91、及び92のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1011]
それぞれ配列番号105、106、及び107のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号100、101、及び102のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1012]
それぞれ配列番号115、116、及び117のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号110、111、及び112のアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3
を含む、本発明1001の抗体または断片。
[本発明1013]
キメラである、またはヒト化されている、本発明1001〜1012のいずれかの単離された抗体またはその断片。
[本発明1014]
PD−1に結合する単離された抗体またはその断片であって、
配列番号23、33、44、54、64、74、84、94、104、114、133、及び143から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む軽鎖可変領域;及び
配列番号18、28、39、49、59、69、79、89、99、109、131、及び141から成る群から選択されるアミノ酸配列と少なくとも80%の相同性を有するアミノ酸配列を含む重鎖可変領域
を含む、前記単離された抗体またはその断片。
[本発明1015]
配列番号23、33、44、54、64、74、84、94、104、114、133、及び143から成る群から選択されるアミノ酸配列を含む軽鎖可変領域;及び
配列番号18、28、39、49、59、69、79、89、99、109、131、及び141から成る群から選択されるアミノ酸配列を含む重鎖可変領域
を含む、本発明1014の単離された抗体またはその断片。
[本発明1016]
PD−1に結合する単離された抗体またはその断片であって、
配列番号133または152の軽鎖可変領域;及び
配列番号131の重鎖可変領域
を含む、前記単離された抗体またはその断片。
[本発明1017]
PD−1に結合する単離された抗体またはその断片であって、
配列番号143の軽鎖可変領域;及び
配列番号141の重鎖可変領域
を含む、前記単離された抗体またはその断片。
[本発明1018]
PD−1に結合する単離された抗体またはその断片であって、
配列番号139または153の軽鎖;及び
配列番号135の重鎖
を含む、前記単離された抗体またはその断片。
[本発明1019]
PD−1に結合する単離された抗体またはその断片であって、
配列番号139または153の軽鎖;及び
配列番号137の重鎖
を含む、前記単離された抗体またはその断片。
[本発明1020]
PD−1に結合する単離された抗体またはその断片であって、
配列番号149の軽鎖;及び
配列番号145の重鎖
を含む、前記単離された抗体またはその断片。
[本発明1021]
PD−1に結合する単離された抗体またはその断片であって、
配列番号149の軽鎖;及び
配列番号147の重鎖
を含む、前記単離された抗体またはその断片。
[本発明1022]
本発明1001〜1021のいずれかの抗体またはその断片と同じエピトープに結合する、単離された抗体またはその断片。
[本発明1023]
本発明1001〜1021のいずれかの抗体またはその断片とPD−1への結合について競合し、前記競合が、ELISA、フローサイトメトリー、または表面プラズモン共鳴(SPR)アッセイにより測定される、単離された抗体またはその断片。
[本発明1024]
モノクローナル抗体、scFv、Fab断片、Fab’断片、及びF(ab)’断片から成る群から選択される、本発明1001〜1021のいずれかの単離された抗体またはその断片。
[本発明1025]
治療剤に連結される、または治療剤と複合体化される、本発明1001〜1021のいずれかの抗体またはその断片。
[本発明1026]
前記治療剤が、細胞傷害性薬物、放射性同位体、免疫調節剤、または抗体である、本発明1025の抗体またはその断片。
[本発明1027]
PD−1に結合する単離された抗体またはその断片であって、PD−1に対して約1nM〜約0.01nMの親和性を有する、前記単離された抗体またはその断片。
[本発明1028]
PD−1に対して約1nM以下の親和性を有する、本発明1027の単離された抗体またはその断片。
[本発明1029]
PD−1に対して約0.1nM以下の親和性を有する、本発明1027の単離された抗体またはその断片。
[本発明1030]
PD−1に結合する単離された抗体またはその断片であって、前記抗体が、約5ng/mL〜約1000ng/mLの結合EC50を有する、前記単離された抗体またはその断片。
[本発明1031]
PD−1に結合する単離された抗体またはその断片であって、前記抗体が、PD−1とPD−L1との結合をブロックする、前記単離された抗体またはその断片。
[本発明1032]
約5ng/mL〜約1000ng/mLのIC50でPD−1とPD−L1またはPD−L2との結合をブロックする、本発明1031の単離された抗体またはその断片。
[本発明1033]
PD−1に結合する単離された抗体またはその断片であって、炎症性サイトカインの産生により測定されるT細胞活性化を増加させる、前記単離された抗体またはその断片。
[本発明1034]
IL−2及びIFNγのT細胞による産生を増加させる、本発明1028の単離された抗体またはその断片。
[本発明1035]
PD−1に結合する単離された抗体またはその断片であって、10D1、4C10、7D3、13F1、15H5、14A6、22A5、6E1、5A8、7A4、及び/または7A4Dから成る群から選択されるハイブリドーマによって産生される、前記単離された抗体またはその断片。
[本発明1036]
本発明1001〜1035のいずれかの抗体またはその断片と、
薬学的に許容される担体と
を含む組成物。
[本発明1037]
本発明1001〜1035のいずれかの抗体またはその断片をコードする、単離されたポリヌクレオチド。
[本発明1038]
本発明1037の単離されたポリヌクレオチドを含む、発現ベクター。
[本発明1039]
本発明1038の発現ベクターを含む、宿主細胞。
[本発明1040]
10D1、4C10、7D3、13F1、15H5、14A6、22A5、6E1、5A8、7A4及び7A4Dから成る群から選択される、単離されたハイブリドーマ細胞株。
[本発明1041]
T細胞活性化を増加させるための方法であって、T細胞を本発明1001〜1035のいずれかの抗体またはその断片と接触させる段階を含む、前記方法。
[本発明1042]
対象における腫瘍を減少させるための方法または腫瘍細胞の増殖を阻害するための方法であって、前記対象に治療有効量の本発明1001〜1035のいずれかの単離された抗体またはその断片を投与する段階を含む、前記方法。
[本発明1043]
癌の処置を必要とする対象において癌を処置するための方法であって、治療有効量の本発明1001〜1035のいずれかの単離された抗体またはその断片を前記対象に投与する段階を含む、前記方法。
[本発明1044]
前記癌が、リンパ腫、白血病、黒色腫、神経膠腫、乳癌、肺癌、結腸癌、骨癌、卵巣癌、膀胱癌、腎臓癌、肝臓癌、胃癌、直腸癌、精巣癌、唾液腺癌、甲状腺癌、胸腺癌、上皮癌、頭頸部癌、胃の癌、膵臓癌、またはこれらの組み合わせから成る群から選択される、本発明1043の方法。
[本発明1045]
感染症の処置を必要とする対象において感染症を処置するための方法であって、治療有効量の本発明1001〜1035のいずれかの単離された抗体またはその断片を前記対象に投与する段階を含む、前記方法。
[本発明1046]
前記感染症が、カンジダ症、カンジダ血症、アスペルギルス症、連鎖球菌性肺炎、連鎖球菌性の皮膚及び口咽頭の状態、グラム陰性菌による敗血症、結核、単核球症、インフルエンザ、呼吸器合胞体ウイルスにより引き起こされる呼吸器病、マラリア、住血吸虫症、ならびにトリパノソーマ症から成る群から選択される、本発明1045の方法。
プログラム死受容体1(PD−1)は、免疫系のチェックポイント受容体である。PD−1は、主として活性化T細胞及びB細胞上で発現され、単球ならびに胸腺発達中にCD4−CD8−ダブルネガティブT細胞及びNK−T細胞上にも生じる(上記のAgata et al.,Okazaki et al.(2002)Curr.Opin.Immunol.14:391779−82;Bennett et al.(2003)J Immunol 170:711−8)。PD−1は、2つのリガンド、すなわちPD−L1及びPD−L2を有する。PD−1と2つのリガンドのいずれかとの相互作用は、インビトロ及びインビボでT細胞応答を減弱させることが示されているが、これはPD−1とPD−L1との局所的相互作用を阻害することにより反転され得、その効果は、PD−1とPD−L2との相互作用も同様にブロックされる場合、相加的である(Iwai et al.(2002)Proc.Nat’l.Acad Sci.USA 99:12293−7;Brown et al.(2003)J.Immunol.170:1257−66)。
ヒトPD−1に対する抗体を生成するために、hPD−1をヒスチジンタグ(hPD−1−Hisタグ、配列番号1)、マウスFc(hPD−L1−mFc、配列番号13)、及びヒトFcタグ(hPD−1−hFc、配列番号5)と融合して、その細胞外ドメインのオープンリーディングフレームをコードするcDNAをPCRにより得て、それぞれ発現ベクターのpcDNA3.1(Invitrogenカタログ番号V−790)にサブクローニングした。freestyle293細胞での一過性発現後、hPD−1−HisタグをNTAカラム(GE healthcare)で精製し、hPD−1−mFc及びhPD−1−hFcをプロテインGカラム(GE healthcare)で精製した。
ELISA結合分析を、ヒトPD−1−hFcタンパク質に基づいて実施した。96ウェルプレート(Costar、カタログ番号9018)を、コーティング緩衝液(PBS、Hyclone、カタログ番号SH30256.01B)中、2μg/mlのPD1−hFc(CrownBio)を100μL用いて4℃で一晩コーティングした。ウェルを吸引し、非特異的結合部位を、1%(w/v)のウシ血清アルブミン(BSA、Roche、カタログ番号738328)を用いた200μLのブロッキング緩衝液を添加して、37℃で1時間インキュベートすることによりブロックした。プレートを洗浄緩衝液(0.05%(v/v)のTween20(Sigma、カタログ番号P1379)を加えたPBSで3回洗浄した後、ブロッキング緩衝液中のハイブリドーマ上清の好適な希釈物を100μL/ウェルで添加し、室温で1時間インキュベートした。プレートを洗浄し、100μL/ウェルの、ブロッキング緩衝液中のヤギ抗マウスIgG(H+L)(Thermo、カタログ番号31432)で60分間インキュベートした。プレートを洗浄した後、100μL/ウェルの基質溶液(TMB(eBioscience、カタログ番号00−4201−56)を添加し、プレートを室温で2分間インキュベートした。100μL/ウェルの停止溶液(2NのH2SO4)を添加して、反応を停止させた。比色シグナルが生じたら、Auto Plate SpectraMax Plus(供給業者:Molecular Devices;モデル:MNR0643;ソフトウェア:SoftMax Pro v5.4)を使用して450nmで読み取った。この方法により、ヒトPD−1タンパク質と高度に特異的に結合する抗体を産生するハイブリドーマ細胞株を、繰り返し選択した。
サブクローニングは限界希釈法の手順に基づき、モノクローナル抗体を産生する個々のハイブリドーマクローンを得るように設計する。ハイブリドーマの各々を複数回(4回)の限界希釈法に供した。サブクローニングの各回について、クローンをELISA及びFACSに基づく妨害分析により試験した。
精製したハイブリドーマ抗体を、ELISA及びFACS分析に基づいてさらに特徴付けた。使用した方法は、実施例2で上に記載したものと同様であったが、ただし、この場合は精製抗体を量及び濃度で測定し、その結果を使用してEC50値及びIC50値を計算した。以下の表、すなわち表1〜5は、10種の抗体の結果を示す。
抗体の結合特性をさらに特徴付けるために、10種のハイブリドーマ抗体をBiacore(Biacore 3000、GE)を使用して特性を明らかにし、結合速度を明らかにして平衡結合定数を計算した。このアッセイを、mouse antibody capture kit(BR−1008−38、GE)を使用して、捕捉方法により実施した。抗マウスFc mabをpH5.0の固定化緩衝液中で25μg/mlまで希釈した後、5μl/分の流速で表6に示すパラメータを用いて固定化を実施した。速度論的実行は、1)リガンドを典型的には0.5〜1分間、10μl/分の流速で注入し;2)好適な分析物を典型的には3分間注入し、続いて典型的には5〜10分間、30μl/分の流速でのランニング緩衝液(1倍のPBS−P20)中で解離させて;3)再生溶液の10mMのグリシンをpH1.7で典型的には1〜2分間、10μl/分の流速で注入することにより行った。
抗体の種交差反応を評価するために、マウス及びカニクイザルPD−1受容体をPCRによりクローニングし、安定にトランスフェクトした293T−PD−1細胞を生成した。抗体を、タンパク質に基づくELISAを使用して、カニクイザル受容体への結合について試験した。試験の結果は、抗体がヒト及びカニクイザルPD−1に等しい親和性で結合し、ヒトPD−1と比較した場合に類似した有効性でhPD−L1/Fc及びhPD−L2/Fcと、カニクイザルPD−1との結合をブロックすることを示した。選択した抗体で、使用したアッセイのいずれにおいても、検出可能な親和性でマウスPD−1と結合したものはなかった。ヒトCTLA4、ICOS及びCD28と交差反応するものはない(表8を参照のこと)。
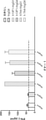
混合リンパ球反応を使用して、リンパ球エフェクター細胞に対する、PD−1経路をブロックすることの効果を実証した。アッセイでは、マウス抗ヒトPD−1モノクローナル抗体の存在下または非存在下における増殖、IFN−γ分泌及びIL−2分泌についてT細胞を試験した。アッセイでは、ヒトCD4+T細胞を、CD4+の陰性選択(Miltenyi Biotech、カタログ番号130−091−155)を使用してPBMCから精製した。成熟樹状細胞(DC)は、精製した単球(Miltenyi、Mo−DC Generation Toolbox、カタログ番号130−093−568)をMo−DC分化培地で7日間培養し;次いで、DC成熟をMo−Dc Maturationで2日間誘導して得た。各培養物は、200μlの総体積中、105個の精製T細胞及び104個の同種異系樹状細胞を含有した。抗PD−1モノクローナル抗体の4C10、5A8、6E1、7D3、7A4、10D1、13F1、14A6、15H5、または22A5を各培養物に異なる抗体濃度で添加した。抗体なし、またはアイソタイプ対照抗体のいずれかを陰性対照として使用した。細胞を37℃で5日間培養した。5日目に、50μlの培地をIL−2及びIFN−γの測定のために収集した。培養液中のIFN−γ及びIL−2のレベルを、EIA hIFN−γ ELISA kit(R&D、カタログ番号DY285)及びIL−2 ELISAキット(eBioscience)を使用して測定した。試験の結果を図2(IL−2分泌)及び図3(IFN−γ分泌)に提供し、これは抗ヒトPD−1モノクローナル抗体が、濃度依存的様式でT細胞増殖、IFN−γ分泌及びIL−2分泌を促進したことを示す。対照的に、アイソタイプ対照抗体を含有する培養物は、T細胞増殖、IFN−γまたはIL−2分泌の増加を示さなかった。
精製して、特徴付けた10種の抗PD1モノクローナル抗体の特性を表8にまとめる。これらの抗体は、PD−1に(20uM〜3nMの範囲の解離定数で)強力に結合し、異なるIC50値でPD−L1及びPD−L2の両方との相互作用をブロックすることができた。抗体の各々は、IL2及びIFNγ産生を誘導した。10種の抗体には、CTLA4、ICOS、またはCD28と交差反応したものはなかった。抗体の各々は、カニクイザルPD−1と結合した。抗体の各々は、溶液に添加した場合に受容体アンタゴニストとして機能し、最終的にT細胞応答を増強した(実施例5を参照のこと)。
免疫グロブリンcDNAのクローニング
RNeasy Mini Kit(Qiagen、カタログ番号74104)により、hPD−1抗体を産生するハイブリドーマ細胞株から単離した全RNAを鋳型として使用し、SuperScript(登録商標)II Reverse Transcriptase(Life Technology、カタログ番号18064−14)をメーカーの指示に従って用いて第1鎖cDNAを合成した。次いで、cDNA産物を、50μl体積の反応混合物において縮重マウスIgGプライマー(Kettleborough CA,et al,European Journal of Immunology 23:206−211(1993)、Strebe N,et al,Antibody Engineering 1:3−14(2010))を使用してPCRに供した。反応は、S1000(商標)サーマルサイクラー(Bio−Rad、カタログ番号184−2000)において、94℃で1.5分間の変性;50℃で1分間のアニーリング;及び72℃で1分間の合成を30サイクル行って実施した。30回目のサイクルの最後に、反応混合物を伸張するためにさらに7分間72℃でインキュベートした。
7A4及び13F1キメラ軽鎖(それぞれ配列番号123及び129)は、PCRでクローニングしたマウスVL領域のcDNAを、それぞれヒトカッパ及びIgG1に連結することにより構築した。7A4及び13F1キメラIgG1重鎖(それぞれ配列番号119及び125)は、PCRでクローニングしたマウスVH領域のcDNAをヒトIgG1定常領域に連結することにより構築した。7A4及び13F1キメラIgG4重鎖(それぞれ配列番号121及び127)は、PCRでクローニングしたマウスVH領域のcDNAをヒトIgG4定常領域に連結することにより構築した。マウスcDNA配列の5’末端を、軽鎖及び重鎖の両方にリーダー配列を付加するように設計されたPCRプライマーを使用して修飾した。
7A4及び13F1抗体を、CDR移植手法(その全体が参照によって本明細書に組み込まれる、米国特許第5,225,539号明細書)を使用してヒト化する。マウス抗体7A4及び13F1の軽鎖及び重鎖可変鎖配列を、NCBIデータベースhttp://www.ncbi.nlm.nih.gov/igblast/igblast.cgiを検索することにより、構造バイオインフォマティクス研究共同体(RCSB)のタンパク質構造データバンクで入手可能な配列と比較した。7A4及び13F1のモデルを、それぞれ最も高い配列相同性を有するVH及びVL構造に基づいて生成した。
ヒト化7A4、7A4D及び13F1抗体の軽鎖及び重鎖をコードするDNAを合成し、発現ベクターのpcDNA3.1(Invitrogen、カタログ番号V−790)にクローニングした。Freestyle293細胞(106個/mLで200mL)に、100μgのヒト化重鎖及び軽鎖発現プラスミドの各々をトランスフェクトし、6日間培養した。次いで、上清中のヒト化抗体をプロテインGカラム(GE healthcare)で精製した。
ヒト化13F1−hIgG1、13F1−hIgG4、7A4−IgG1及び7A4−hIgG4抗体の生成及び精製後、抗体の結合及び特異性を、ELISAに基づく結合及びPD−1妨害分析、加えてFACSに基づく結合及びPD−L1妨害分析に基づいて決定した。使用した方法は、実施例2及び4で上に記載したものと同様であった。
ヒト化抗体の結合特性を特徴付けるために、PD−1とPD−1抗体との間の結合速度をBiacore3000により測定し、1Hzのデータ収集速度で記録した。ポリクローナルウサギ抗マウスIgG(GE、BR−1008−38)を10mMのpH5.0の酢酸ナトリウムで希釈し、およそ15000RUでCM5バイオセンサーチップの参照用及び実験用フローセルにamine coupling kit(GE、BR10050)を使用して固定化した。各サイクルの開始時に、希釈した試験抗体(1.5μg/ml)を、捕捉するために1分間実験フローセルに注入した。PD−1分析物系列は、ストックをランニング緩衝液で100nMまで希釈し、続いて同じ緩衝液中で0.78nMに至るまで連続2倍希釈を行って調製した。分析物を30μL/分の流速で3分間、参照用及び実験用フローセルに連続して注入した。次いで、ランニング緩衝液(0.05%のP20を加えたPBS)を30μL/分の流速で10分間にわたって流した。各サイクルの最後に、バイオセンサー表面を、10μL/分の流速で10mMのpH1.7のグリシン−HCl緩衝液を3分間注入して再生した。各分析物試料の注入(すなわち、各サイクル)について、同時に記録した参照表面での応答を差し引き、続いて単一参照用のランニング緩衝液試料での応答をさらに差し引いて、実験バイオセンサー表面から得られた結合応答を二重参照した。結合及び解離速度定数(ka及びkd)を、Biaevaluation 4.0ソフトウェアを使用して、力価測定系列全体の二重参照したセンサーグラムをラングミュアモデル(1:1)にフィッティングすることにより同時に決定した。解離定数、すなわちKDを、決定した速度定数から関係KD=kd/kaによって計算した。図10及び図17Aに示すように、ヒト化抗PD−1抗体の13F1、7A4、及び7A4Dは、高い親和性でヒトPD−1と結合した。Biocore結合曲線を図10及び図17Aの上部パネルに示し、定量化結合データを図10及び図17Aの下部パネルにまとめる。図17Bは、7A4D−hIgG4抗体による、293T−PD1細胞に対するPD−L1の結合の妨害IC50を示す。
混合リンパ球反応(MLR)を用いて、ヒト化抗体がリンパ球エフェクター細胞のPD−1経路をブロックする能力を実証した。アッセイでは、抗PD−1抗体の存在下または非存在下におけるIFNγ及びIL−2分泌についてT細胞を試験した。ヒトCD4+T細胞を、CD4の陰性選択アイソレーションキット(Mitenyi Biotech、カタログ番号130−091−155)を使用してヒトPBMCから精製した。未熟樹状細胞(DC)を、Mo−DC Generation Toolbox(Miltenyi、カタログ番号130−093−568)を使用してヒトPBMCから単離した単球から得た。細胞をMo−DC分化培地で7日間培養し、次いで成熟DCとなるようにMo−Dc Maturation mediumで2日間誘導した。MLRを設定するために、105個の精製T細胞及び104個の同種異系成熟DC細胞を各ウェルに添加し、総体積を200μlとした。試験する抗体を、20μg/ml〜0.002μg/mlの濃度範囲でアッセイした。抗体なし、またはアイソタイプ対照抗体(hIgG4)のいずれかを陰性対照として使用した。細胞を37℃で5日間培養した。6日目に、培地中のIFN−γ及びIL−2のレベルを、IL−2 ELISAキット(eBioscience)及びhIFN−γ ELISA kit(R&D、カタログ番号DY285)を使用して測定した。ヒト化13F1抗体について、結果を図11(IL−2産生)及び図12(IFNγ産生)に示す。ヒト化13F1抗体の各々は、濃度依存的様式でIL−2及びIFNγ産生を促進した。同様に、ヒト化7A4及び7A4D抗体は、濃度依存的様式でIL−2(図13及び18)及びIFNγ(図14及び19)産生を促進した。アイソタイプ対照抗体を含有する培養物は、IFN−γ及びIL−2分泌の増加を示さなかった。したがって、試験の結果は、ヒト化PD−1抗体がPD−1経路をブロックし、T細胞免疫応答を刺激することを示した。
抗原特異的T細胞受容体の誘発が、PD−1/PD−L1経路を抗PD−1抗体でブロックすることにより調節されたか否かを調査するために、ヒトT細胞リコールアッセイを用いて、破傷風トキソイド(TT)抗原を使用し、健康なTT免疫化ドナーの血中における既存のメモリーT細胞を刺激した。この目的のために、TT免疫化ドナーから最近採取した新鮮なPBMC(1年未満に採取した試料)を、80U/mlのペニシリン、80g/mlのストレプトマイシン及び30%の自己血清を補充したRPMI1640(Invitrogen、カタログ番号A10491−01)を使用して、4×105個の細胞/ウェルで96ウェル丸底プレート(costar、カタログ番号3799)に播種した。ヒト化13F1または7A4抗体を種々の濃度で添加し、0.1ug/mlのSEB及び1ug/mlのTT(Astarte Biologies)で刺激した。37℃、5%CO2で7日間の共培養後、上清を採取してIFN−γの濃度を測定した。試験の結果を図15に示し、これはTT抗原単独と比較して、抗PD−1抗体でのPD−L1妨害が、メモリーT細胞によるIFN−γ分泌の増強をもたらしたことを実証する。
本実施例では、T細胞活性化に対する、ヒト化抗PD−1抗体によりPD−/PD−L1経路をブロックすることの効果を検査した。精製したヒトCD4+T細胞(Mitenyi Biotech、カタログ番号130−091−155)を、自己単球由来樹状細胞(DC)の存在下で1μg/mlの可溶性抗CD3抗体(R&D、カタログ番号MAB100)で活性化した。力価測定用抗PD−1抗体の存在下または非存在下における活性化から3日後、培地を採取してIFNγの濃度をELISAで測定した。結果を図16に示し、これは抗PD−1抗体によるPD−L1妨害が、T細胞によるIFN−γ分泌を増強したことを示している。
Claims (15)
- i)それぞれ配列番号115、116、及び117のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号110、111、及び112のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
ii)それぞれ配列番号24、25、及び26のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号19、20、及び21のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
iii)それぞれ配列番号34、35、及び36のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号29、30、及び31のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
iv)それぞれ配列番号45、46、及び47のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号40、41、及び42のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
v)それぞれ配列番号55、56、及び57のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号50、51、及び52のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
vi)それぞれ配列番号65、66、及び67のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号60、61、及び62のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
vii)それぞれ配列番号75、76、及び77のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号70、71、及び72のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
viii)それぞれ配列番号85、86、及び87のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号80、81、及び82のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
ix)それぞれ配列番号95、96、及び97のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号90、91、及び92のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;または
x)それぞれ配列番号105、106、及び107のアミノ酸配列を含む軽鎖CDR1、CDR2、及びCDR3;及び
それぞれ配列番号100、101、及び102のアミノ酸配列を含む重鎖CDR1、CDR2、及びCDR3;
を含む、1nM以下の親和性でPD−1に結合する単離された抗体またはその抗原結合断片であって、任意で前記抗体またはその抗原結合断片はキメラである、またはヒト化されている、単離された抗体またはその抗原結合断片。 - 1nM以下の親和性でPD−1に結合する単離された抗体またはその抗原結合断片であって、
(i)配列番号152と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号131と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(ii)配列番号133と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号131と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(iii)配列番号23と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号18と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(iv)配列番号33と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号28と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(v)配列番号44と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号39と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(vi)配列番号54と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号49と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(vii)配列番号64と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号59と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(viii)配列番号74と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号69と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(ix)配列番号84と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号79と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(x)配列番号94と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号89と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(xi)配列番号104と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号99と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;
(xii)配列番号114と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号109と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域;または
(xiii)配列番号143と少なくとも95%の相同性を有するアミノ酸配列を含む軽鎖可変領域、および配列番号141と少なくとも95%の相同性を有するアミノ酸配列を含む重鎖可変領域
を含む、前記単離された抗体またはその抗原結合断片。 - PD−1に結合する単離された抗体またはその抗原結合断片であって、
i)配列番号152または133の軽鎖可変領域;及び
配列番号131の重鎖可変領域;
ii)配列番号143の軽鎖可変領域;及び
配列番号141の重鎖可変領域;
iii)配列番号139または153の軽鎖;及び
配列番号135の重鎖;
iv)配列番号139または153の軽鎖;及び
配列番号137の重鎖;
v)配列番号149の軽鎖;及び
配列番号145の重鎖;または
vi)配列番号149の軽鎖;及び
配列番号147の重鎖
を含む、前記単離された抗体またはその抗原結合断片。 - モノクローナル抗体、scFv、Fab断片、Fab’断片、及びF(ab’)2断片から成る群から選択される、請求項1〜3のいずれか1項に記載の単離された抗体またはその抗原結合断片。
- 治療剤に連結される、または治療剤と複合体化される、請求項1〜3のいずれか1項に記載の抗体またはその抗原結合断片。
- 請求項1〜3のいずれか1項に記載の単離された抗体またはその抗原結合断片であって、PD−1に対して1nM〜0.01nMの親和性を有する、単離された抗体またはその抗原結合断片。
- 請求項1〜3のいずれか1項に記載の単離された抗体またはその抗原結合断片であって、前記抗体が、5ng/mL〜1000ng/mLの結合EC50を有する、またはPD−1とPD−L1との結合をブロックする、前記単離された抗体またはその抗原結合断片。
- 請求項1〜7のいずれか1項に記載の抗体またはその抗原結合断片と、
薬学的に許容される担体と
を含む組成物。 - 請求項1〜7のいずれか1項に記載の抗体またはその抗原結合断片をコードする、単離されたポリヌクレオチド。
- 請求項9に記載の単離されたポリヌクレオチドを含む、発現ベクター。
- 請求項10に記載の発現ベクターを含む、宿主細胞。
- 治療有効量の請求項1〜7のいずれか1項に記載の単離された抗体またはその抗原結合断片を含む、それを必要とする対象において癌または感染症を処置するための医薬組成物であって、
前記癌が、リンパ腫、白血病、黒色腫、神経膠腫、乳癌、肺癌、結腸癌、骨癌、卵巣癌、膀胱癌、腎臓癌、肝臓癌、胃癌、直腸癌、精巣癌、唾液腺癌、甲状腺癌、胸腺癌、上皮癌、頭頸部癌、胃の癌、膵臓癌、またはこれらの組み合わせから成る群から選択され、または
前記感染症が、カンジダ症、カンジダ血症、アスペルギルス症、連鎖球菌性肺炎、連鎖球菌性の皮膚及び口咽頭の状態、グラム陰性菌による敗血症、結核、単核球症、インフルエンザ、呼吸器合胞体ウイルスにより引き起こされる呼吸器病、マラリア、住血吸虫症、ならびにトリパノソーマ症から成る群から選択される、前記医薬組成物。 - 前記治療剤が、細胞傷害性薬物、放射性同位体、免疫調節剤、または抗体である、請求項5に記載の抗体またはその抗原結合断片。
- PD−1に対して1nM以下、または0.1nM以下の親和性を有する、請求項6に記載の抗体またはその抗原結合断片。
- 5ng/mL〜1000ng/mLのIC50でPD−1とPD−L1またはPD−L2との結合をブロックする、請求項7に記載の抗体またはその抗原結合断片。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNPCT/CN2014/082721 | 2014-07-22 | ||
| CN2014082721 | 2014-07-22 | ||
| PCT/US2015/041575 WO2016014688A2 (en) | 2014-07-22 | 2015-07-22 | Anti-pd-1 antibodies |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020085029A Division JP2020188760A (ja) | 2014-07-22 | 2020-05-14 | 抗pd−1抗体 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017530722A JP2017530722A (ja) | 2017-10-19 |
| JP2017530722A5 JP2017530722A5 (ja) | 2018-08-30 |
| JP6986965B2 true JP6986965B2 (ja) | 2021-12-22 |
Family
ID=55163959
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017525309A Active JP6986965B2 (ja) | 2014-07-22 | 2015-07-22 | 抗pd−1抗体 |
| JP2020085029A Pending JP2020188760A (ja) | 2014-07-22 | 2020-05-14 | 抗pd−1抗体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020085029A Pending JP2020188760A (ja) | 2014-07-22 | 2020-05-14 | 抗pd−1抗体 |
Country Status (16)
| Country | Link |
|---|---|
| US (3) | US10428146B2 (ja) |
| EP (1) | EP3171892B1 (ja) |
| JP (2) | JP6986965B2 (ja) |
| KR (1) | KR102524920B1 (ja) |
| CN (1) | CN106573052B (ja) |
| AU (2) | AU2015292678B2 (ja) |
| BR (2) | BR112017001385B1 (ja) |
| CA (1) | CA2955788C (ja) |
| ES (1) | ES2905301T3 (ja) |
| IL (2) | IL250222B (ja) |
| MX (1) | MX388181B (ja) |
| NZ (1) | NZ728688A (ja) |
| RU (1) | RU2711141C2 (ja) |
| SG (2) | SG11201700496WA (ja) |
| WO (1) | WO2016014688A2 (ja) |
| ZA (1) | ZA201700551B (ja) |
Families Citing this family (65)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2746805T3 (es) | 2013-12-12 | 2020-03-06 | Shanghai hengrui pharmaceutical co ltd | Anticuerpo de PD-1, fragmento de unión a antígeno del mismo y aplicación médica del mismo |
| TWI693232B (zh) | 2014-06-26 | 2020-05-11 | 美商宏觀基因股份有限公司 | 與pd-1和lag-3具有免疫反應性的共價結合的雙抗體和其使用方法 |
| JP6986965B2 (ja) | 2014-07-22 | 2021-12-22 | アポロミクス インコーポレイテッド | 抗pd−1抗体 |
| WO2016022630A1 (en) | 2014-08-05 | 2016-02-11 | Jiping Zha | Anti-pd-l1 antibodies |
| TWI773646B (zh) | 2015-06-08 | 2022-08-11 | 美商宏觀基因股份有限公司 | 結合lag-3的分子和其使用方法 |
| CN114591433A (zh) | 2015-07-13 | 2022-06-07 | 西托姆克斯治疗公司 | 抗pd-1抗体、可活化抗pd-1抗体及其使用方法 |
| HUE055207T2 (hu) | 2015-07-30 | 2021-11-29 | Macrogenics Inc | PD-1 és LAG-3 kötõ molekulák és eljárások azok alkalmazására |
| CN114605548A (zh) | 2015-09-01 | 2022-06-10 | 艾吉纳斯公司 | 抗-pd-1抗体及其使用方法 |
| HK1251158A1 (zh) | 2015-09-29 | 2019-01-25 | 细胞基因公司 | Pd-1结合蛋白及其使用方法 |
| US12030942B2 (en) | 2015-10-02 | 2024-07-09 | Les Laboratoires Servier | Anti-PD-1 antibodies and compositions |
| SMT202200118T1 (it) | 2015-11-03 | 2022-05-12 | Janssen Biotech Inc | Anticorpi che legano specificamente pd-1 e loro usi |
| EA201891178A1 (ru) | 2015-12-14 | 2019-01-31 | Макродженикс, Инк. | Биспецифичные молекулы, обладающие иммунореактивностью в отношении pd-1 и ctla-4, и способы их применения |
| CN107286242B (zh) * | 2016-04-01 | 2019-03-22 | 中山康方生物医药有限公司 | 抗pd-1的单克隆抗体 |
| US11299751B2 (en) | 2016-04-29 | 2022-04-12 | Voyager Therapeutics, Inc. | Compositions for the treatment of disease |
| EP3448875A4 (en) * | 2016-04-29 | 2020-04-08 | Voyager Therapeutics, Inc. | COMPOSITIONS FOR TREATING A DISEASE |
| TWI640536B (zh) | 2016-06-20 | 2018-11-11 | 克馬伯有限公司 | 抗體 |
| JP7164528B2 (ja) | 2016-09-14 | 2022-11-01 | ベイジン・ハンミ・ファーマシューティカル・カンパニー・リミテッド | Pd-1に特異的に結合する可能な抗体及びその機能的断片 |
| AU2017329024A1 (en) | 2016-09-19 | 2019-03-21 | Celgene Corporation | Methods of treating immune disorders using pd-1 binding proteins |
| WO2018053401A1 (en) | 2016-09-19 | 2018-03-22 | Celgene Corporation | Methods of treating vitiligo using pd-1 binding proteins |
| US10597454B2 (en) * | 2016-10-15 | 2020-03-24 | Innovent Biologics (Suzhou) Co., Ltd | PD-1 antibodies |
| EP3541841B1 (en) * | 2016-11-18 | 2024-09-11 | Les Laboratoires Servier | Anti-pd-1 antibodies and compositions |
| CN118634323A (zh) | 2016-12-07 | 2024-09-13 | 艾吉纳斯公司 | 抗体和其使用方法 |
| CN106519034B (zh) * | 2016-12-22 | 2020-09-18 | 鲁南制药集团股份有限公司 | 抗pd-1抗体及其用途 |
| WO2018119474A2 (en) * | 2016-12-23 | 2018-06-28 | Remd Biotherapeutics, Inc. | Immunotherapy using antibodies that bind programmed death 1 (pd-1) |
| WO2018133842A1 (zh) * | 2017-01-20 | 2018-07-26 | 大有华夏生物医药集团有限公司 | 人程序性死亡受体pd-1的单克隆抗体及其片段 |
| CN108341871A (zh) | 2017-01-24 | 2018-07-31 | 三生国健药业(上海)股份有限公司 | 抗pd-1单克隆抗体及其制备方法和应用 |
| SG11201907753TA (en) | 2017-02-24 | 2019-09-27 | Macrogenics Inc | Bispecific binding molecules that are capable of binding cd137 and tumor antigens, and uses thereof |
| US11483810B2 (en) * | 2017-04-03 | 2022-10-25 | Huawei Technologies Co., Ltd. | Methods and systems for resource configuration of wireless communication systems |
| CA3185303A1 (en) | 2017-04-05 | 2018-10-11 | Symphogen A/S | Combination therapies targeting pd-a, tim-3, and lag-3 |
| CA3058966A1 (en) | 2017-04-14 | 2018-10-18 | Tollnine, Inc. | Immunomodulating polynucleotides, antibody conjugates thereof, and methods of their use |
| WO2018231339A2 (en) * | 2017-04-20 | 2018-12-20 | Dana-Farber Cancer Institute, Inc. | Anti-phosphotyrosinylated pd-1 antibodies and uses thereof |
| EP3645740A4 (en) * | 2017-06-25 | 2021-08-18 | Systimmune, Inc. | ANTI-PD-1 ANTIBODIES AND METHOD OF MANUFACTURING AND USE |
| US11021540B2 (en) * | 2017-09-07 | 2021-06-01 | Augusta University Research Institute, Inc. | Antibodies to programmed cell death protein 1 |
| KR20190065234A (ko) * | 2017-11-30 | 2019-06-11 | 그리폴스 다이어그노스틱 솔루션즈 인크. | 면역 관문 억제제인 pd-1 및 pd-l1에 대한 항체 치료를 모니터링하기 위한 면역분석 및 조작된 단백질 |
| CN111356702B (zh) * | 2017-12-06 | 2022-07-26 | 正大天晴药业集团南京顺欣制药有限公司 | 抗pd-l1抗体及其抗原结合片段 |
| CN108059677B (zh) * | 2017-12-08 | 2020-05-22 | 浙江大学 | 全人源抗pdl-1单链抗体b36及其应用 |
| CN107880127B (zh) * | 2017-12-08 | 2020-05-22 | 浙江大学 | 全人源抗pdl-1单链抗体b129及其应用 |
| CN108059678B (zh) * | 2017-12-08 | 2020-05-22 | 浙江大学 | 全人源抗pdl-1单链抗体b30及其应用 |
| US12398209B2 (en) | 2018-01-22 | 2025-08-26 | Janssen Biotech, Inc. | Methods of treating cancers with antagonistic anti-PD-1 antibodies |
| CA3091373A1 (en) * | 2018-02-17 | 2019-08-22 | Apollomics Inc. | Cancer treatment using combination of neutrophil modulator with modulator of immune checkpoint |
| US11814434B2 (en) * | 2018-03-13 | 2023-11-14 | Tusk Therapeutics Ltd. | Anti-CD25 for tumour specific cell depletion |
| JP7054573B2 (ja) * | 2018-04-15 | 2022-04-14 | イムヴィラ・カンパニー・リミテッド | Pd-1結合抗体及びその用途 |
| EP3794039A4 (en) * | 2018-05-17 | 2022-05-04 | Nanjing Leads Biolabs Co., Ltd. | PD-1 BINDING ANTIBODIES AND USE |
| TWI806870B (zh) * | 2018-05-23 | 2023-07-01 | 中國大陸商大有華夏生物醫藥集團有限公司 | 抗pd-1抗體及其用途 |
| CN120714023A (zh) | 2018-06-20 | 2025-09-30 | 因赛特公司 | 抗pd-1抗体及其用途 |
| CN110624106A (zh) * | 2018-06-22 | 2019-12-31 | 嘉和生物药业有限公司 | Pd-1信号通路拮抗剂与艾滋病疫苗的联合应用 |
| EP3823991A4 (en) | 2018-07-19 | 2022-08-03 | Tayu Huaxia Biotech Medical Group Co., Ltd. | ANTI-PD-1 ANTIBODIES, DOSAGE FORMS AND USES THEREOF |
| CN111423510B (zh) * | 2019-01-10 | 2024-02-06 | 迈威(上海)生物科技股份有限公司 | 重组抗人pd-1抗体及其应用 |
| JP7604379B2 (ja) * | 2019-02-03 | 2024-12-23 | ジエンス ヘンルイ メデイシンカンパニー リミテッド | 抗pd-1抗体、その抗原結合フラグメントおよびそれらの医薬用途 |
| CA3143218A1 (en) * | 2019-06-10 | 2020-12-17 | Apollomics Inc. (Hangzhou) | Antibody-interleukin fusion protein and methods of use |
| EP3998081A4 (en) | 2019-07-05 | 2023-07-12 | Ono Pharmaceutical Co., Ltd. | TREATMENT OF BLOOD CANCER WITH PD-1/CD3 DUAL SPECIFICITY PROTEIN |
| JP7771749B2 (ja) | 2019-08-08 | 2025-11-18 | 小野薬品工業株式会社 | 二重特異性タンパク質 |
| EP4039704A4 (en) * | 2019-09-30 | 2023-09-20 | Sichuan Kelun-Biotech Biopharmaceutical Co., Ltd. | ANTI-PD-1 ANTIBODIES AND USE THEREOF |
| WO2021095599A1 (ja) * | 2019-11-13 | 2021-05-20 | 国立大学法人京都大学 | Pd-1シグナル阻害剤の併用療法 |
| CN113134080A (zh) * | 2020-01-17 | 2021-07-20 | 嘉和生物药业有限公司 | 抗pd-1抗体和呋喹替尼联合在制备治疗癌症的药物中的用途 |
| IL295759A (en) | 2020-02-28 | 2022-10-01 | Tallac Therapeutics Inc | Transglutaminase mediated coupling |
| WO2022068891A1 (zh) * | 2020-09-30 | 2022-04-07 | 苏州沙砾生物科技有限公司 | Pd-1抗体及其制备方法与应用 |
| GB202107994D0 (en) | 2021-06-04 | 2021-07-21 | Kymab Ltd | Treatment of cancer |
| CN115611981A (zh) * | 2021-07-12 | 2023-01-17 | 嘉和生物药业有限公司 | 抗pd-1抗体在治疗外周t细胞淋巴瘤中的应用 |
| CN115607664A (zh) * | 2021-07-15 | 2023-01-17 | 嘉和生物药业有限公司 | 抗pd-1抗体在治疗宫颈癌中的应用 |
| WO2023147470A2 (en) | 2022-01-28 | 2023-08-03 | Georgiamune Inc. | Antibodies to programmed cell death protein 1 that are pd-1 agonists |
| EP4626474A2 (en) * | 2022-12-02 | 2025-10-08 | Ohio State Innovation Foundation | S100a7 as a diagnostic marker and therapeutic target for disorders |
| JP2026504180A (ja) | 2023-01-30 | 2026-02-03 | カイマブ・リミテッド | 抗体 |
| WO2024228167A1 (en) | 2023-05-03 | 2024-11-07 | Iox Therapeutics Inc. | Inkt cell modulator liposomal compositions and methods of use |
| WO2025128264A1 (en) * | 2023-12-15 | 2025-06-19 | Pharmaessentia Corporation | Anti-pd-1 monoclonal antibody and methods of use thereof |
Family Cites Families (103)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| AU600575B2 (en) | 1987-03-18 | 1990-08-16 | Sb2, Inc. | Altered antibodies |
| US5859205A (en) | 1989-12-21 | 1999-01-12 | Celltech Limited | Humanised antibodies |
| US5994514A (en) | 1991-08-14 | 1999-11-30 | Genentech, Inc. | Immunoglobulin variants |
| WO1993022332A2 (en) | 1992-04-24 | 1993-11-11 | Board Of Regents, The University Of Texas System | Recombinant production of immunoglobulin-like domains in prokaryotic cells |
| WO1994029351A2 (en) | 1993-06-16 | 1994-12-22 | Celltech Limited | Antibodies |
| US5595756A (en) * | 1993-12-22 | 1997-01-21 | Inex Pharmaceuticals Corporation | Liposomal compositions for enhanced retention of bioactive agents |
| CA2143491C (en) | 1994-03-01 | 2011-02-22 | Yasumasa Ishida | A novel peptide related to human programmed cell death and dna encoding it |
| US6194551B1 (en) | 1998-04-02 | 2001-02-27 | Genentech, Inc. | Polypeptide variants |
| US6528624B1 (en) | 1998-04-02 | 2003-03-04 | Genentech, Inc. | Polypeptide variants |
| GB9809951D0 (en) | 1998-05-08 | 1998-07-08 | Univ Cambridge Tech | Binding molecules |
| KR101077001B1 (ko) | 1999-01-15 | 2011-10-26 | 제넨테크, 인크. | 효과기 기능이 변화된 폴리펩티드 변이체 |
| US6737056B1 (en) | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| CA2383424C (en) | 1999-08-23 | 2011-02-15 | Gordon Freeman | Novel b7-4 molecules and uses therefor |
| WO2001014557A1 (en) | 1999-08-23 | 2001-03-01 | Dana-Farber Cancer Institute, Inc. | Pd-1, a receptor for b7-4, and uses therefor |
| US20040038339A1 (en) | 2000-03-24 | 2004-02-26 | Peter Kufer | Multifunctional polypeptides comprising a binding site to an epitope of the nkg2d receptor complex |
| EP2264072A1 (en) | 2000-04-13 | 2010-12-22 | The Rockefeller University | Enhancement of antibody-mediated cytotoxicity. |
| JP3871326B2 (ja) | 2000-11-15 | 2007-01-24 | 小野薬品工業株式会社 | Pd−1欠損マウスおよびその用途 |
| PT1355919E (pt) | 2000-12-12 | 2011-03-02 | Medimmune Llc | Moléculas com semivida longa, composições que as contêm e suas utilizações |
| US20030133939A1 (en) | 2001-01-17 | 2003-07-17 | Genecraft, Inc. | Binding domain-immunoglobulin fusion proteins |
| EP1389203B8 (en) | 2001-02-27 | 2010-03-10 | The Governement of the United States of America, represented by The Secretary Department of Health and Human services | Analogs of thalidomide as angiogenesis inhibitors |
| KR100900176B1 (ko) | 2001-03-07 | 2009-06-02 | 메르크 파텐트 게엠베하 | 하이브리드 이소타입 항체 부분구조를 포함하는 단백질을위한 발현 기술 |
| AR036993A1 (es) | 2001-04-02 | 2004-10-20 | Wyeth Corp | Uso de agentes que modulan la interaccion entre pd-1 y sus ligandos en la submodulacion de respuestas inmunologicas |
| US7317091B2 (en) | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| US7662925B2 (en) | 2002-03-01 | 2010-02-16 | Xencor, Inc. | Optimized Fc variants and methods for their generation |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| AU2003287345A1 (en) | 2002-10-31 | 2004-06-07 | Genentech, Inc. | Methods and compositions for increasing antibody production |
| CN1753912B (zh) | 2002-12-23 | 2011-11-02 | 惠氏公司 | 抗pd-1抗体及其用途 |
| US7960512B2 (en) | 2003-01-09 | 2011-06-14 | Macrogenics, Inc. | Identification and engineering of antibodies with variant Fc regions and methods of using same |
| EP2368578A1 (en) | 2003-01-09 | 2011-09-28 | Macrogenics, Inc. | Identification and engineering of antibodies with variant Fc regions and methods of using same |
| US7563869B2 (en) | 2003-01-23 | 2009-07-21 | Ono Pharmaceutical Co., Ltd. | Substance specific to human PD-1 |
| US8084582B2 (en) | 2003-03-03 | 2011-12-27 | Xencor, Inc. | Optimized anti-CD20 monoclonal antibodies having Fc variants |
| NZ545776A (en) | 2003-08-22 | 2009-05-31 | Biogen Idec Inc | Improved antibodies having altered effector function and methods for making the same |
| US20060134105A1 (en) | 2004-10-21 | 2006-06-22 | Xencor, Inc. | IgG immunoglobulin variants with optimized effector function |
| WO2005077981A2 (en) | 2003-12-22 | 2005-08-25 | Xencor, Inc. | Fc POLYPEPTIDES WITH NOVEL Fc LIGAND BINDING SITES |
| GB0400440D0 (en) | 2004-01-09 | 2004-02-11 | Isis Innovation | Receptor modulators |
| WO2006033386A1 (ja) | 2004-09-22 | 2006-03-30 | Kirin Beer Kabushiki Kaisha | 安定化されたヒトIgG4抗体 |
| TW200639163A (en) | 2005-02-04 | 2006-11-16 | Genentech Inc | RAF inhibitor compounds and methods |
| CN1296385C (zh) | 2005-03-30 | 2007-01-24 | 王哲 | 抗猪生长激素单克隆抗体及制备方法及应用 |
| ES2720160T3 (es) | 2005-05-09 | 2019-07-18 | Ono Pharmaceutical Co | Anticuerpos monoclonales humanos contra muerte programada 1(PD-1) y métodos para tratar el cáncer usando anticuerpos dirigidos contra PD-1 solos o junto con otras sustancias inmunoterapéuticas |
| EA019344B1 (ru) | 2005-07-01 | 2014-03-31 | МЕДАРЕКС, Эл.Эл.Си. | Человеческие моноклональные антитела против лиганда-1 запрограммированной гибели клеток (pd-l1) и их применения |
| KR20180058863A (ko) | 2005-11-30 | 2018-06-01 | 애브비 인코포레이티드 | 아밀로이드 베타 단백질에 대한 모노클로날 항체 및 이의 용도 |
| ZA200804679B (en) | 2005-12-08 | 2010-02-24 | Millenium Pharmaceuticals Inc | Bicyclic compounds with kinase inhibitory activity |
| PL2004688T5 (pl) | 2006-03-23 | 2014-09-30 | Bioarctic Neuroscience Ab | Ulepszone przeciwciała wobec protofibryli oraz ich zastosowania |
| WO2007136572A2 (en) | 2006-05-15 | 2007-11-29 | Merck & Co., Inc. | Antidiabetic bicyclic compounds |
| CN101563105B (zh) | 2006-07-10 | 2013-01-23 | 拜奥根Idec马萨诸塞公司 | 用于抑制smad4-缺陷癌症的组合物和方法 |
| CN101104640A (zh) | 2006-07-10 | 2008-01-16 | 苏州大学 | 抗人pd-l1单克隆抗体制备及应用 |
| US20080227704A1 (en) | 2006-12-21 | 2008-09-18 | Kamens Joanne S | CXCL13 binding proteins |
| CA2673870A1 (en) | 2006-12-27 | 2008-07-10 | Emory University | Compositions and methods for the treatment of infections and tumors |
| EP2666787B1 (en) | 2007-05-31 | 2022-02-09 | Genmab A/S | STABLE IgG4 ANTIBODIES |
| US7615883B2 (en) | 2007-06-06 | 2009-11-10 | Meheen H Joe | Wind driven venturi turbine |
| AU2014201367B2 (en) | 2007-06-18 | 2016-01-28 | Merck Sharp & Dohme B.V. | Antibodies to human programmed death receptor pd-1 |
| JP5191537B2 (ja) | 2007-06-18 | 2013-05-08 | エム・エス・ディー・オス・ベー・フェー | ヒトのプログラムされたデスレセプターpd−1に対する抗体 |
| WO2009024531A1 (en) | 2007-08-17 | 2009-02-26 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Method for treating and diagnosing hematologic malignancies |
| KR20100090258A (ko) | 2007-10-16 | 2010-08-13 | 에스비아이 바이오테크 가부시키가이샤 | 항bst2 항체 |
| JO3076B1 (ar) | 2007-10-17 | 2017-03-15 | Janssen Alzheimer Immunotherap | نظم العلاج المناعي المعتمد على حالة apoe |
| EP2262837A4 (en) * | 2008-03-12 | 2011-04-06 | Merck Sharp & Dohme | PD-1 BINDING PROTEINS |
| EP2328920A2 (en) | 2008-08-25 | 2011-06-08 | Amplimmune, Inc. | Targeted costimulatory polypeptides and methods of use to treat cancer |
| AU2009290543B2 (en) | 2008-09-12 | 2015-09-03 | Oxford University Innovation Limited | PD-1 specific antibodies and uses thereof |
| US8927697B2 (en) | 2008-09-12 | 2015-01-06 | Isis Innovation Limited | PD-1 specific antibodies and uses thereof |
| BRPI0919377A2 (pt) | 2008-09-26 | 2016-09-27 | Dana Farber Cancer Inst Inc | anticorpo isolado ou um fragmento ligante de antígeno do memso, ácido nucleico isolado, vetor, célula hospedeira, composição farmacêutica, método de produzir o referido anticorpo ou fragmento, uso dos mesmos, e composição compreendendo o referido anticorpo ou fragmento |
| KR101050829B1 (ko) | 2008-10-02 | 2011-07-20 | 서울대학교산학협력단 | 항 pd-1 항체 또는 항 pd-l1 항체를 포함하는 항암제 |
| EP2370593B1 (en) | 2008-11-28 | 2016-03-30 | Emory University | Methods for determining the efficacy of pd-1 antagonists |
| HUE065752T2 (hu) | 2008-12-09 | 2024-06-28 | Hoffmann La Roche | Anti-PD-L1 antitestek és felhasználásuk T-sejt funkció elõsegítésére |
| US20100197924A1 (en) | 2008-12-22 | 2010-08-05 | Millennium Pharmaceuticals, Inc. | Preparation of aminotetralin compounds |
| ES2629337T3 (es) | 2009-02-09 | 2017-08-08 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos contra PD-1 y anticuerpos contra PD-L1 y usos de los mismos |
| AU2010224160A1 (en) | 2009-03-10 | 2011-09-22 | Biogen Idec Ma Inc. | Anti-BCMA antibodies |
| US9493578B2 (en) | 2009-09-02 | 2016-11-15 | Xencor, Inc. | Compositions and methods for simultaneous bivalent and monovalent co-engagement of antigens |
| US8389689B2 (en) | 2009-10-28 | 2013-03-05 | Janssen Biotech, Inc. | Anti-GLP-1R antibodies and their uses |
| US10053513B2 (en) | 2009-11-30 | 2018-08-21 | Janssen Biotech, Inc. | Antibody Fc mutants with ablated effector functions |
| HUE050768T2 (hu) | 2010-02-19 | 2021-01-28 | Xencor Inc | Új CTLA4-IG immunadhezinek |
| CA2791930A1 (en) * | 2010-03-11 | 2011-09-15 | Kerry Louise Tyson | Pd-1 antibody |
| MX341925B (es) | 2010-03-29 | 2016-09-07 | Zymeworks Inc | Anticuerpos con funcion efectora suprimida o mejorada. |
| US20120100166A1 (en) | 2010-07-15 | 2012-04-26 | Zyngenia, Inc. | Ang-2 Binding Complexes and Uses Thereof |
| BR112013024574B1 (pt) | 2011-03-29 | 2022-08-09 | Roche Glycart Ag | Anticorpo e uso do anticorpo |
| CA2830806C (en) | 2011-03-31 | 2020-05-12 | Merck Sharp & Dohme Corp. | Stable formulations of antibodies to human programmed death receptor pd-1 and related treatments |
| JP6072771B2 (ja) | 2011-04-20 | 2017-02-01 | メディミューン,エルエルシー | B7−h1およびpd−1に結合する抗体およびその他の分子 |
| AP2013007281A0 (en) | 2011-05-02 | 2013-11-30 | Ym Biosciences Australia Pty | Multiple myeloma treatment |
| CN103596982B (zh) | 2011-06-06 | 2016-11-02 | 诺沃—诺迪斯克有限公司 | 治疗性抗体 |
| EA026924B1 (ru) | 2011-08-01 | 2017-05-31 | Дженентек, Инк. | Способы лечения рака с использованием антагонистов, связывающихся с осью pd-1, и ингибиторов mek |
| KR101981873B1 (ko) | 2011-11-28 | 2019-05-23 | 메르크 파텐트 게엠베하 | 항-pd-l1 항체 및 그의 용도 |
| JP6226752B2 (ja) | 2012-02-09 | 2017-11-08 | 中外製薬株式会社 | 抗体のFc領域改変体 |
| WO2013165690A1 (en) | 2012-04-30 | 2013-11-07 | Medimmune, Llc | Molecules with reduced effector function and extended half-lives, compositions, and uses thereof |
| US9212224B2 (en) | 2012-05-15 | 2015-12-15 | Bristol-Myers Squibb Company | Antibodies that bind PD-L1 and uses thereof |
| CN104736168B (zh) | 2012-05-31 | 2018-09-21 | 索伦托治疗有限公司 | 与pd-l1结合的抗原结合蛋白 |
| RU2689760C2 (ru) | 2012-05-31 | 2019-05-30 | Дженентек, Инк. | Способы лечения рака с применением антагонистов аксиального связывания pd-1 и vegf антагонистов |
| MX2014015744A (es) | 2012-07-03 | 2015-06-05 | Janssen Sciences Ireland Uc | Anticuerpos a-beta de epítopo de terminal c y central. |
| CN104936982B (zh) | 2012-08-03 | 2020-04-24 | 丹娜法伯癌症研究院 | 抗-pd-l1和pd-l2双结合抗体单一试剂及其使用方法 |
| CA2886433C (en) | 2012-10-04 | 2022-01-04 | Dana-Farber Cancer Institute, Inc. | Human monoclonal anti-pd-l1 antibodies and methods of use |
| EP2911669B1 (en) | 2012-10-26 | 2024-04-10 | The University of Chicago | Synergistic combination of immunologic inhibitors for the treatment of cancer |
| EP2934577A1 (en) | 2012-12-19 | 2015-10-28 | Adimab, LLC | Multivalent antibody analogs, and methods of their preparation and use |
| AR093984A1 (es) | 2012-12-21 | 2015-07-01 | Merck Sharp & Dohme | Anticuerpos que se unen a ligando 1 de muerte programada (pd-l1) humano |
| TWI635098B (zh) | 2013-02-01 | 2018-09-11 | 再生元醫藥公司 | 含嵌合恆定區之抗體 |
| LT2840892T (lt) | 2013-02-20 | 2018-07-25 | Regeneron Pharmaceuticals, Inc. | Nežmogaus tipo gyvūnai su modifikuotomis imunoglobulino sunkiųjų grandinių sekomis |
| KR20150127591A (ko) | 2013-03-15 | 2015-11-17 | 리제너론 파아마슈티컬스, 인크. | Il-33 길항제 및 이의 용도 |
| US9676853B2 (en) | 2013-05-31 | 2017-06-13 | Sorrento Therapeutics, Inc. | Antigen binding proteins that bind PD-1 |
| JP6623353B2 (ja) | 2013-09-13 | 2019-12-25 | ベイジーン スウィッツァーランド ゲーエムベーハー | 抗pd−1抗体並びにその治療及び診断のための使用 |
| KR102003754B1 (ko) | 2014-07-03 | 2019-07-25 | 베이진 엘티디 | Pd-l1 항체와 이를 이용한 치료 및 진단 |
| JP6986965B2 (ja) | 2014-07-22 | 2021-12-22 | アポロミクス インコーポレイテッド | 抗pd−1抗体 |
| WO2016022630A1 (en) | 2014-08-05 | 2016-02-11 | Jiping Zha | Anti-pd-l1 antibodies |
| US9139653B1 (en) | 2015-04-30 | 2015-09-22 | Kymab Limited | Anti-human OX40L antibodies and methods of treatment |
| CN114591433A (zh) * | 2015-07-13 | 2022-06-07 | 西托姆克斯治疗公司 | 抗pd-1抗体、可活化抗pd-1抗体及其使用方法 |
| WO2017024465A1 (en) | 2015-08-10 | 2017-02-16 | Innovent Biologics (Suzhou) Co., Ltd. | Pd-1 antibodies |
-
2015
- 2015-07-22 JP JP2017525309A patent/JP6986965B2/ja active Active
- 2015-07-22 AU AU2015292678A patent/AU2015292678B2/en active Active
- 2015-07-22 MX MX2017000985A patent/MX388181B/es unknown
- 2015-07-22 KR KR1020177005011A patent/KR102524920B1/ko active Active
- 2015-07-22 US US15/328,225 patent/US10428146B2/en active Active
- 2015-07-22 NZ NZ728688A patent/NZ728688A/en unknown
- 2015-07-22 SG SG11201700496WA patent/SG11201700496WA/en unknown
- 2015-07-22 BR BR112017001385-1A patent/BR112017001385B1/pt active IP Right Grant
- 2015-07-22 RU RU2017105915A patent/RU2711141C2/ru active
- 2015-07-22 CN CN201580040301.XA patent/CN106573052B/zh active Active
- 2015-07-22 ES ES15824277T patent/ES2905301T3/es active Active
- 2015-07-22 WO PCT/US2015/041575 patent/WO2016014688A2/en not_active Ceased
- 2015-07-22 SG SG10201900571YA patent/SG10201900571YA/en unknown
- 2015-07-22 CA CA2955788A patent/CA2955788C/en active Active
- 2015-07-22 BR BR122020025583-8A patent/BR122020025583B1/pt active IP Right Grant
- 2015-07-22 EP EP15824277.6A patent/EP3171892B1/en active Active
-
2017
- 2017-01-22 IL IL250222A patent/IL250222B/en active IP Right Grant
- 2017-01-24 ZA ZA2017/00551A patent/ZA201700551B/en unknown
-
2019
- 2019-08-12 US US16/538,448 patent/US10981994B2/en active Active
-
2020
- 2020-05-14 JP JP2020085029A patent/JP2020188760A/ja active Pending
-
2021
- 2021-01-18 AU AU2021200264A patent/AU2021200264B2/en active Active
- 2021-03-08 US US17/195,226 patent/US11560429B2/en active Active
- 2021-04-18 IL IL282403A patent/IL282403B2/en unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6986965B2 (ja) | 抗pd−1抗体 | |
| US11827707B2 (en) | Anti PD-L1 antibodies | |
| JP7520072B2 (ja) | Pd-l1特異的抗体およびそれを使用する方法 | |
| JP2014532074A (ja) | IL7受容体のα鎖に対する抗体‐薬剤候補物質の製造におけるこれらの使用 | |
| JP7352007B2 (ja) | ヒト化抗vegfモノクローナル抗体 | |
| US20240269276A1 (en) | Specific binding protein targeting pd-l1 and cd73 | |
| RU2809746C2 (ru) | Гуманизированное моноклональное антитело против vegf | |
| HK40112828A (zh) | 抗pd-l1抗体 | |
| HK1242960B (en) | Anti-pd-1 antibodies | |
| BR112017002234B1 (pt) | Anticorpo isolado que se liga a pd-l1 ou fragmento do mesmo, uso do anticorpo ou fragmento, composição, polinucleotídeo isolado e vetor de expressão | |
| BR122020026802B1 (pt) | Anticorpo isolado que se liga a pd-l1 ou fragmento do mesmo, uso do anticorpo ou fragmento, composição, polinucleotídeo isolado e vetor de expressão |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180723 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180723 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190603 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190830 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20190830 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20200115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200514 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20200514 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200520 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20200515 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20200701 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20200706 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20200904 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20200909 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20201223 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20201223 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20210215 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20210408 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20210719 |
|
| C13 | Notice of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: C13 Effective date: 20210811 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210922 |
|
| C23 | Notice of termination of proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C23 Effective date: 20211007 |
|
| C03 | Trial/appeal decision taken |
Free format text: JAPANESE INTERMEDIATE CODE: C03 Effective date: 20211108 |
|
| C30A | Notification sent |
Free format text: JAPANESE INTERMEDIATE CODE: C3012 Effective date: 20211108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211130 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6986965 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |