JP5677972B2 - ヒト血清アルブミンリンカーおよびそのコンジュゲート - Google Patents
ヒト血清アルブミンリンカーおよびそのコンジュゲート Download PDFInfo
- Publication number
- JP5677972B2 JP5677972B2 JP2011536365A JP2011536365A JP5677972B2 JP 5677972 B2 JP5677972 B2 JP 5677972B2 JP 2011536365 A JP2011536365 A JP 2011536365A JP 2011536365 A JP2011536365 A JP 2011536365A JP 5677972 B2 JP5677972 B2 JP 5677972B2
- Authority
- JP
- Japan
- Prior art keywords
- hsa linker
- hsa
- cancer
- binding
- trastuzumab
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/76—Albumins
- C07K14/765—Serum albumin, e.g. HSA
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/38—Albumins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/42—Proteins; Polypeptides; Degradation products thereof; Derivatives thereof, e.g. albumin, gelatin or zein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/76—Albumins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/31—Fusion polypeptide fusions, other than Fc, for prolonged plasma life, e.g. albumin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/70—Fusion polypeptide containing domain for protein-protein interaction
- C07K2319/74—Fusion polypeptide containing domain for protein-protein interaction containing a fusion for binding to a cell surface receptor
Description
ヒト血清アルブミン(HSA)リンカーコンジュゲート、ならびにその結合用、診断用、および治療用のコンジュゲートを提供する。一態様では、HSAリンカーは、2つのアミノ酸置換を包含する。別の態様は、第一および第二の単鎖Fv分子(scFv)であるアミノ末端およびカルボキシ末端の結合部分にHSAリンカーが共有結合している、コンジュゲートである。例示的なコンジュゲートは、例えば治療用途等のために腫瘍細胞の増殖を低下させるのに有用である。診断用および治療用のHSAリンカーコンジュゲートの製造および投与のための方法を、さらに提供する。
抗体様結合部分(無傷の抗体、抗体断片、およびscFv内のものを含む)は、治療用途のためにしばしば使用される。一般に抗体断片およびscFvは無傷の抗体よりも短い血清半減期を呈し、一部の治療用途においては、そのような断片およびscFvの機能を保有する治療剤に関してインビボ半減期の延長が望ましいことがあり得る。
に相当する34merのヒトAFPペプチドに対して90%の配列同一性を有するAFPポリペプチドリンカー配列は、SEQ ID NO: 58の446〜479セグメントから改変されたアミノ酸を最大3個含みうる。生物学的に活性なヒトAFP断片における配列変更のこのような例の一つは、米国特許第5,707,963号(参照により本明細書に組み入れられる)で見出され、これは例えば、2つのアミノ酸残基(SEQ ID NO: 59のアミノ酸9および22)に柔軟性(flexibility)を有するヒトAFPの34アミノ酸断片(SEQ ID NO: 59)を開示している。AFPポリペプチドリンカー配列のその他の例としては、例えば、SEQ ID NO: 58のアミノ酸19〜198(ヒトAFPドメインI)、SEQ ID NO: 58のアミノ酸217〜408(ヒトAFPドメインII)、SEQ ID NO: 58のアミノ酸409〜609(ヒトAFPドメインIII)、SEQ ID NO: 58のアミノ酸19〜408(ヒトAFPドメインI+II)、SEQ ID NO: 58のアミノ酸217〜609(ヒトAFPドメインII+III)、およびSEQ ID NO: 58のアミノ酸285〜609(ヒトAFP断片I)が挙げられる。別の態様では、ヒトAFPポリペプチドリンカー配列は、SEQ ID NO: 58のアミノ酸489〜496を含む8アミノ酸の配列(すなわち、EMTPVNPG)である。
「抗体」という用語は、本明細書において互換的に用いる場合、抗体または免疫グロブリンの全体および、任意の抗原結合断片またはその単鎖を包含する。抗体とは、本明細書において用いる場合、哺乳動物(例えば、ヒトまたはマウス)のものでもよく、ヒト化されても、キメラであっても、組み換えられていても、合成的に作製されても、または天然から単離されてもよい。ヒトを含むほとんどの哺乳動物では、抗体全体とは、ジスルフィド結合によって接続された少なくとも2つの重(H)鎖および2つの軽(L)鎖を有する。各々の重鎖は、重鎖可変領域(本明細書においてVHと省略される)および重鎖定常領域からなる。重鎖定常領域は、3つのドメインであるCH1、CH2、およびCH3、ならびにCH1とCH2との間のヒンジ領域からなる。各軽鎖は、軽鎖可変領域(本明細書においてVLと省略される)および軽鎖定常領域からなる。軽鎖定常領域は、一つのドメインであるCLからなる。VHおよびVL領域はさらに、相補性決定領域(CDR)と呼ばれる超可変性の領域と、より保存された、散在するフレームワーク領域(FR)と呼ばれる領域に細分することができる。VHおよびVLは各々、3つのCDRと4つのFRから構成され、これらは、アミノ末端からカルボキシ末端まで以下の順序で、整列されている:FR1、CDR1、FR2、CDR2、FR3、CDR3、FR4。重鎖および軽鎖の可変領域は、抗原と相互作用する結合ドメインを含む。抗体の定常領域は、免疫系の種々の細胞(例えば、エフェクター細胞)、および古典的な補体系の第一成分(Clq)などを含む宿主の組織または因子への免疫グロブリンの結合を媒介し得る。本発明の抗体には、全ての公知の形態の抗体および抗体様特性を有するその他のタンパク質骨格が挙げられる。例えば抗体は、ヒト抗体、ヒト化抗体、二重特異性抗体、キメラ抗体、または抗体様特性を有するタンパク質骨格、例えばフィブロネクチンまたはアンキリンリピートであってもよい。抗体はまた、Fab、Fab'2、scFv、SMIP、ダイアボディ、ナノボディ、アプタマー、またはドメイン抗体であってもよい。抗体は、以下のアイソタイプのいずれを有してもよい:IgG(例えば、IgG1、IgG2、IgG3、およびIgG4)、IgM、IgA(例えば、IgA1、IgA2、およびIgAsec)、IgD、またはIgE。本明細書において規定される結合部分として、HSAリンカーと組み合わせて使用可能な抗体には、これらに限定されるわけではないが、ナタリズマブ、インフリキシマブ、アダリムマブ、リツキシマブ、アレムツズマブ、ベバシズマブ、ダクリズマブ、エファリズマブ、ゴリムマブ、セルトリズマブ、トラスツズマブ、アバタセプト、エタネルセプト、ペルツズマブ、セツキシマブ、およびパニツムマブが含まれる。
[本発明1001]
以下を含む、HSAリンカーコンジュゲート:
(i) SEQ ID NO: 6〜15のいずれか一つに示されるアミノ酸配列を含む、ヒト血清アルブミン(HSA)リンカー;ならびに
(ii) 抗体、単鎖Fv分子、二重特異性単鎖Fv((scFv') 2 )分子、ドメイン抗体、ダイアボディ、トリアボディ(triabody)、ホルモン、Fab断片、F(ab') 2 分子、タンデムscFv(taFv)断片、レセプター、リガンド、アプタマー、およびこれらの生物学的に活性な断片からなる群より選択される第一および第二の結合部分であって、該第一の結合部分が、該HSAリンカーのアミノ末端に結合し、かつ該第二の結合部分が、該HSAリンカーのカルボキシ末端に結合している、第一および第二の結合部分。
[本発明1002]
前記HSAリンカーが、SEQ ID NO: 1に示されるアミノ酸配列を含む、本発明1001のHSAリンカーコンジュゲート。
[本発明1003]
前記第一の結合部分がErbB3に特異的に結合し、かつ前記第二の結合部分がErbB2に特異的に結合する、本発明1001のHSAリンカーコンジュゲート。
[本発明1004]
SEQ ID NO: 16であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-1。
[本発明1005]
SEQ ID NO: 17であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-2。
[本発明1006]
SEQ ID NO: 18であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-3。
[本発明1007]
SEQ ID NO: 19であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-4。
[本発明1008]
SEQ ID NO: 20であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-5。
[本発明1009]
SEQ ID NO: 21であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-6。
[本発明1010]
SEQ ID NO: 22であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-7。
[本発明1011]
SEQ ID NO: 23であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-8。
[本発明1012]
SEQ ID NO: 24であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-9。
[本発明1013]
SEQ ID NO: 25であるアミノ酸配列を有するまたは含む、HSAリンカーコンジュゲートB2B3-10。
[本発明1014]
薬学的に許容される担体、賦形剤、または希釈剤と混合された、本発明1001〜1013のいずれかのHSAリンカーコンジュゲート。
[本発明1015]
本発明1001〜1013のいずれかのHSAリンカーコンジュゲートの有効量を哺乳動物に投与する工程を含む、疾患または障害を有する患者を治療するための方法。
[本発明1016]
シクロホスファミド、カンプトテシン、ホモカンプトテシン、コルヒチン、コンブレスタチン(combrestatin)、コンブレスタチン、リゾキシン、ドリスタチン(dolistatin)、アンサマイトシンp3、メイタンシノイド、アウリスタチン、カリチアマイシン(caleachimicin)、メトトレキサート、5-フルオロウラシル(5-FU)、ドキソルビシン、パクリタキセル、ドセタキセル、シスプラチン、カルボプラチン、タモキシフェン、ラロキシフェン、レトロゾール、エピルビシン、ベバシズマブ、ペルツズマブ、トラスツズマブ、およびこれらの誘導体からなる群より選択される1つまたは複数の治療剤と組み合わせた、本発明1001〜1013のいずれかのHSAリンカーコンジュゲートを含む、組成物。
[本発明1017]
前記治療剤がトラスツズマブである、本発明1016の組成物。
[本発明1018]
前記HSAリンカーコンジュゲートが、SEQ ID NO: 16であるアミノ酸配列を有するまたは含むHSAリンカーコンジュゲートB2B3-1である、本発明1016の組成物。
[本発明1019]
前記治療剤がトラスツズマブであり、かつ前記HSAリンカーコンジュゲートが、SEQ ID NO: 16であるアミノ酸配列を有するまたは含むHSAリンカーコンジュゲートB2B3-1である、本発明1016の組成物。
[本発明1020]
ヒト乳房腫瘍細胞を用いたヒト異種移植モデルのヌードマウスにおいて第一の用量の治療剤および第二の用量のHSAリンカーコンジュゲートにより試験した場合に、同一モデルにおいて第一の用量の治療剤のみまたは第二の用量のHSAリンカーコンジュゲートのみにより提供されるよりも大きな効果が該組み合わせによって提供される、本発明1019の組成物。
[本発明1021]
少なくとも3 mg/kgのB2B3-1および少なくとも0.1 mg/kgのトラスツズマブを提供するように対象に投与することが可能な剤形である、本発明1020の組成物。
[本発明1022]
3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブを提供するように対象に投与されるのに適合化された剤形である、本発明1021の組成物。
[本発明1023]
10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブを提供するように対象に投与されるのに適合化された剤形である、本発明1021の組成物。
[本発明1024]
3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブを提供するように対象に投与された場合に、対応する対象の3 mg/kgのB2B3-1のみまたは0.1 mg/kgのトラスツズマブのみによる処理よりも効果的である、本発明1022の組成物。
[本発明1025]
10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブを提供するように対象に投与された場合に、対応する対象の10 mg/kgのみまたは1 mg/kgのトラスツズマブのみによる処理よりも効果的である、本発明1023の組成物。
[本発明1026]
3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブをそれぞれに提供するように複数の対象に投与された場合に、20日後に該対象の10%超において腫瘍の退縮を誘導する、本発明1022の組成物。
[本発明1027]
10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブをそれぞれに提供するように複数の対象に投与された場合に、20日後に該対象の少なくとも50%において腫瘍の退縮を誘導する、本発明1023の組成物。
[本発明1028]
前記治療剤がラパチニブである、本発明1016の組成物。
[本発明1029]
前記治療剤がタキサンである、本発明1016の組成物。
[本発明1030]
タキサンがパクリタキセルまたはドセタキセルである、本発明1029の組成物。
[本発明1031]
前記治療剤がレトロゾールである、本発明1016の組成物。
[本発明1032]
前記第一の結合部分が約16 nMのK d でErbB3に結合し、かつ前記第二の結合部分が約0.3 nMのK d でErbB2に結合する、本発明1003のHSAリンカーコンジュゲート。
[本発明1033]
対象を治療する方法であって、該対象が腫瘍の治療を必要としており、該治療が、本発明1001〜1014および1032のいずれかのHSAリンカーコンジュゲートの有効量を該対象に投与する工程を含む、方法。
[本発明1034]
対象を治療する方法であって、該対象が腫瘍の治療を必要としており、該治療が、本発明1016〜1030のいずれかの組成物の有効量を該対象に投与する工程を含む、方法。
[本発明1035]
腫瘍の治療のための医薬の調製における、本発明1001〜1014および1032のいずれかのHSAリンカーコンジュゲートの使用。
[本発明1036]
腫瘍の治療のための医薬の調製における、本発明1016〜1030のいずれかの組成物の使用。
本発明は、ヒト血清アルブミン(HSA)リンカー、ならびに、HSAリンカーと1つまたは複数のさらなる部分、例えば結合部分とを含むHSAリンカーコンジュゲート(例えば、結合剤、診断剤、または治療剤)を提供する。そのようなHSAリンカーコンジュゲートは、例えば6時間〜7日間という延長されたインビボ半減期などの望ましい特性を有し、かつ、哺乳動物(例えばヒト)にインビボで投与されても、体液性または細胞媒介性の有意な免疫応答を誘導しない。一局面では、本発明は、2つの所定のアミノ酸置換(すなわち、SEQ ID NO: 1に示される「C34S」および「N503Q」の置換)を有する変異HSAリンカーを提供する。別の局面では、本発明は、インビボでの哺乳動物(例えば、ヒト)における診断用途もしくは治療用途のための、または哺乳動物の細胞、組織、もしくは器官と関連したインビトロでの使用のための、1つまたは複数の結合部分(例えば、抗体、抗体断片、レセプター/リガンド、または低分子)に結合したHSAリンカーを提供する。さらなる局面において、哺乳動物における(または哺乳動物の細胞、組織、または器官と関連した)診断用途または治療用途のために、HSAリンカーを1つまたは複数の免疫調節剤、細胞毒性剤または細胞増殖抑制剤、検出可能標識、または放射性剤と連結してもよい。HSAリンカーを含むHSAリンカーコンジュゲートは任意で、1つまたは複数の薬学的に許容される担体または賦形剤と組み合わされてもよく、かつ、静脈内に、筋肉内に、経口的に、吸入によって、非経口的に、腹腔内に、動脈内に、経皮的に、舌下に、経鼻的に、座剤の使用を通じて、経頬的に、リポソームで、脂肪に(adiposally)、眼球に(opthalmically)、眼内に、皮下に、髄腔内に、局部的に、または局所的に投与されるように製剤化されてもよい。HSAリンカーコンジュゲートは、1つまたは複数の生物学的活性剤(例えば、生物学的または化学的な剤、例えば化学療法剤および抗腫瘍剤)と組み合わせたり同時投与することができるが、必ずしもその必要はない。さらなる局面において本発明は、結合部分(例えば、抗体、抗体断片、レセプター、またはリガンド)、免疫調節剤、細胞毒性剤または細胞増殖抑制剤、検出可能標識、または放射性剤をHSAリンカーに結合させて、診断または治療の用途に使用できるHSAリンカーコンジュゲートを調製するための、説明書を備えたキットを提供する。
HSAリンカーは、SEQ ID NO: 3に示される野生型HSAアミノ酸配列を含みうる。あるいは、HSAリンカーは、改変配列または変異配列を含んでもよい。1つの変異HSAリンカーは、SEQ ID NO: 3に示される野性型HSAアミノ酸配列を基準として34位および503位に2つのアミノ酸変異を含む。34位のシステイン残基(すなわち、C34)はシステイン以外の任意のアミノ酸残基(例えば、セリン、トレオニン、またはアラニン)に変異してもよい。同様に、503位のアスパラギン残基(すなわち、N503)はアスパラギン以外の任意のアミノ酸残基(例えば、グルタミン、セリン、ヒスチジン、またはアラニン)に変異してもよい。一態様では、HSAリンカーは、それぞれSEQ ID NO: 1およびSEQ ID NO: 2に示されるアミノ酸配列および対応するヌクレオチド配列を有する。この変異HSAリンカーは、2つのアミノ酸置換(すなわち、アミノ酸残基34のシステインの代わりにセリン(「C34S」)、およびアミノ酸残基503のアスパラギンの代わりにグルタミン(「N503Q」))を含む。1つまたは複数の結合部分(例えば、抗体、抗体断片(例えば、単鎖抗体)、または他の標的化剤もしくは生物学的に活性な剤(例えば、レセプターおよびリガンド))に結合させた場合、HSAリンカーは、これらのコンジュゲートに対して、および、同じく結合させた追加の診断剤もしくは治療剤(例えば、免疫調節剤、細胞毒性剤、もしくは細胞増殖抑制剤、検出可能標識、または放射性剤)に対して、該HSAリンカーの非存在下におけるこれらの剤の薬理学的特性と比べて有益な、いくつかの薬理学的特性を付与する。哺乳動物(例えば、ヒト)への投与の場合、これらの恩典には、免疫原性の低下(例えば、リンカー-抗体コンジュゲートの宿主抗体中和反応の低減)、(例えば、質量分析による)HSAリンカーコンジュゲートの検出の増大、および薬理学的半減期の延長(例えば、6時間超、8時間超、12時間超、24時間超、36時間超、2日超、3日超、4日超、5日超、6日超、または7日超の半減期)が含まれる。具体的には、アミノ酸残基34のシステインをセリンで置換することにより、HSAリンカーの酸化およびタンパク質不均一性が低減する。野性型HSAにおいて、アミノ酸残基503のアスパラギンは脱アミノ反応に感受性であり、これは薬理学的半減期の低下をもたらす可能性が高い。アミノ酸残基503のアスパラギンをグルタミンで置換することにより、HSAリンカーの薬理学的半減期の延長と、それに対応して、哺乳動物(例えば、ヒト)またはその細胞、組織、または器官に投与された場合のHSAリンカーを含むコンジュゲート剤の薬理学的半減期の延長をもたらすことができる。
HSAリンカーに対する、本明細書において定義される結合部分の結合を容易にするために、短い(例えば、2〜20アミノ酸長の)ペプチドコネクターを、HSAリンカーのアミノ末端またはカルボキシ末端に結合させることができる(例えば、共有結合(例えば、ペプチド結合)、イオン結合、または疎水性結合させるか、または高親和性のタンパク質-タンパク質結合相互作用を介する(例えば、ビオチンとアビジン))。これらのコネクターは、本明細書に記載の任意の結合部分が結合可能である、柔軟なテザーを提供する。ペプチドコネクターは、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20またはそれ以上のアミノ酸長であってもよい。一態様では、コネクターは、例えばグリシン、アラニン、セリン、グルタミン、ロイシン、またはバリン残基の配列である。本明細書において具体的に列挙されてはいないが、コネクターは、グリシン、アラニン、セリン、グルタミン、ロイシン、もしくはバリン残基のみであってもよく、または最大約20アミノ酸長までのこれらの残基の任意の組み合わせであってもよい。好ましい態様では、HSAリンカーのアミノ末端に結合したコネクターはアミノ酸配列AASまたはAAQを有し、カルボキシ末端に結合したコネクターはアミノ酸配列「AAAL」(SEQ ID NO: 5)を有する。コネクターは、HSAリンカー内のアミノ酸残基に対して、HSAリンカーのアミノ末端もしくはカルボキシ末端と共有結合してもよいし、または存在する場合には1つまたは複数の結合部分の間に含まれてもよい。
1つまたは複数の上述のペプチドコネクター、1つまたは複数の後述の結合部分、ポリペプチドベースの検出可能標識、および他のポリペプチドベースの治療剤を含むまたは含まない、HSAリンカーは、組み換えにより作製することができる。例えば、HSAリンカー(および1つまたは複数の任意のエレメント)をコードするヌクレオチド配列は、細菌(例えば、大腸菌)、昆虫、酵母、もしくは哺乳動物の細胞(例えば、CHO細胞)、または、哺乳動物の組織、器官、もしくは生物体(例えば、トランスジェニックのげっ歯類、有蹄類(例えば、ヤギ)または非ヒト霊長類)において、(例えば、プラスミド内で、ウイルスベクター内で、または遺伝子導入により)発現させてもよい。宿主の細胞、組織、または器官でHSAリンカーを発現させた後、当業者は、標準的なタンパク質精製法(例えば、FPLCまたはアフィニティクロマトグラフィー)を用いて該HSAリンカーを単離および精製し得る。2つの結合部分と組み合わせたHSAリンカーの産生のための組み換え発現系を図1に図示する。
HSAリンカーコンジュゲートはまた、標的の細胞、組織、または器官へのHSAリンカーコンジュゲートの選択的かつ特異的な結合を可能にする、1つまたは複数の結合部分、例えば、抗体、抗体断片(本明細書記載のとおり、例えば、単鎖Fv(scFv))、またはレセプター/リガンド(すなわち、タンパク質または糖タンパク質のリガンドまたはレセプター)を含んでもよい。結合部分を、(例えば、共有結合(例えば、ペプチド結合)、イオン結合、もしくは疎水性結合を介して、または高親和性のタンパク質-タンパク質の結合相互作用を介して(例えば、ビオチンとアビジン))HSAリンカーに結合させることができる。
抗体には、IgG、IgA、IgM、IgD、およびIgEアイソタイプが含まれる。抗体またはその抗体断片は、本明細書において用いる場合、標的細胞の外側上にまたは内部に存在する標的タンパク質、糖タンパク質、またはエピトープに結合する、1つまたは複数の相補性決定領域(CDR)または結合ペプチドを含む。
またヒト化抗体をHSAリンカーと組み合わせて使用してもよく、ここで、該抗体CDRの1つまたは複数は非ヒト抗体配列由来であり、該CDRの1つまたは複数(ただし好ましくは全て)は、抗原(例えば、タンパク質、糖タンパク質、または他の適切なエピトープ)に特異的に結合する。
特定のHSAリンカーコンジュゲート内部では、タンパク質または糖タンパク質のレセプターまたはリガンドがHSAリンカーと結合している。レセプターまたはリガンドと結合したHSAリンカーを用いて、例えば、分泌タンパク質、細胞(例えば、癌細胞)、組織、または器官を特異的に標的してもよい。さらにHSAリンカー-レセプターまたは-リガンドコンジュゲートと、同起源の標的レセプターまたはリガンドとの特異的結合によって、細胞内または細胞間のシグナル伝達経路における生物学的な作動/拮抗活性を生じさせることができる。本明細書に記載の他の結合部分と同様に、レセプターおよびリガンドまたはこれらの断片を、HSAリンカーのアミノ末端および/もしくはカルボキシ末端に、HSAリンカーに連結したペプチドコネクターに、またはHSAリンカー内のアミノ酸残基に、結合させることができる。
HSAリンカー、またはそれに結合した任意の結合部分(例えば、抗体、抗体断片、レセプター、またはリガンド)を、キレート剤または検出可能標識に連結して、診断剤をすることができる。また、本明細書に記載のような検出可能標識と、1つまたは複数の本明細書に記載の治療剤または結合部分とを含む、HSAリンカーコンジュゲートも意図される。
HSAリンカー、またはそれに結合した任意の分子もしくは部分を任意の公知の細胞毒性部分または治療部分に連結して、疾患(例えば、癌、自己免疫疾患、または心血管系の疾患)または疾患の1つまたは複数の症状を治療、阻害、軽減、または緩和するために投与可能な剤(HSAリンカーコンジュゲート)を形成させることができる。例としては、これらに限定されるわけではないが、抗腫瘍剤、例えば:アシビシン;アクラルビシン;塩酸アコダゾール;アクロニン;アドゼレシン;アドリアマイシン;アルデスロイキン;アルトレタミン;アンボマイシン(ambomycin);酢酸アメタントロン;アミノグルテチミド;アムサクリン;アナストロゾール;アントラマイシン;アスパラギナーゼ;アスペルリン(asperlin);アザシチジン;アゼテパ(azetepa);アゾトマイシン(azotomycin);バチマスタット;ベンゾデパ;ビカルタミド;塩酸ビサントレン;ビスナフィドジメシレート(bisnafide dimesylate);ビゼレシン;硫酸ブレオマイシン;ブレキナルナトリウム;ブロピリミン;ブスルファン;カクチノマイシン;カルステロン;カンプトテシン;カラセミド;カルベチマー;カルボプラチン;カルムスチン;塩酸カルビシン;カルゼレシン;セデフィンゴール;クロラムブシル;シロレマイシン;シスプラチン;クラドリビン;コンブレテスタチンa-4;クリスナトールメシレート;シクロホスファミド;シタラビン;ダカルバジン;ダカ(n-[2-(ジメチル-アミノ)エチル]アクリジン-4-カルボキサミド);ダクチノマイシン;塩酸ダウノルビシン;ダウノマイシン;デシタビン;デキソルマプラチン;デザグアニン;デザグアニンメシレート;ジアジクオン(diaziquone);ドセタキセル;ドラサチン;ドキソルビシン;塩酸ドキソルビシン;ドロロキシフェン;クエン酸ドロロキシフェン;プロピオン酸ドロモスタノロン;デュアゾマイシン;エダトレキサート;塩酸エフロールニチン;エリプチシン;エルサミトルシン;エンロプラチン;エンプロマート;エピプロピジン;塩酸エピルビシン;エルブロゾール;塩酸エソルビシン;エストラムスチン;リン酸エストラムスチンナトリウム;エタニダゾール;ヨード化ケシ油エチルエステルi131;エトポシド;リン酸エトポシド;エトプリン;塩酸ファドロゾール;ファザラビン;フェンレチニド;フロクスウリジン;リン酸フルダラビン;フルオロウラシル;5-fdump;フルオロシタビン;ホスキドン;ホストリエシンナトリウム;ゲムシタビン;塩酸ゲムシタビン;金au198;ホモカンプトテシン;ヒドロキシ尿素;塩酸イダルビシン;イホスファミド;イルモホシン;インターフェロンα-2a;インターフェロンα-2b;インターフェロンα-n1;インターフェロンα-n3;インターフェロンβ-ia;インターフェロンγ-ib;イプロプラチン;塩酸イリノテカン;ランレオチド酢酸;レトロゾール;酢酸リュープロリド;塩酸リアロゾール;ロメトレキソールナトリウム;ロムスチン;塩酸ロソキサントロン;マソプロコール;メイタンシン;塩酸メクロレタミン;酢酸メゲストロール;メレンゲストロール酢酸;メルファラン;メノガリル;メルカプトプリン;メトトレキサート;メトトレキサートナトリウム;メトプリン;メツレデパ;ミチンドミド;ミトカルシン(mitocarcin);ミトクロミン;ミトジリン(mitogillin);ミトマルシン(mitomalcin);マイトマイシン;ミトスペル(mitosper);ミトタン;塩酸ミトキサントロン;ミコフェノール酸;ノコダゾール;ノガラマイシン;オルマプラチン;オキシスラン;パクリタキセル;ペガスパルガーゼ;ペリオマイシン(peliomycin);ペンタムスチン;硫酸ペプロイシン;ペルホスファミド;ピポブロマン;ピポスルファン;塩酸ピロキサントロン;プリカマイシン;プロメスタン;ポルフィマーナトリウム;ポルフィロマイシン;プレドニムスチン;塩酸プロカルバジン;ピューロマイシン;塩酸ピューロマイシン;ピラゾフリン;リゾキシン;リゾキシンd;リボプリン;ログレチミド;サフィンゴール;塩酸サフィンゴール;セムスチン;シムトラゼン;スパルホサートナトリウム;スパルソマイシン;塩酸スピロゲルマニウム;スピロムスチン;スピロプラチン;ストレプトニグリン;ストレプトゾシン;塩化ストロンチウムsr89;スロフェヌル;タリソマイシン;タキサン;タキソイド;テコガラン(tecogalan)ナトリウム;テガフール;塩酸テロキサントロン;テモポルフィン;テニポシド;テロキシロン;テストラクトン;チアミプリン;チオグアニン;チオテパ;チミタック(thymitaq);チアゾフリン;チラパザミン;トムデックス;top53;塩酸トポテカン;クエン酸トレミフェン;酢酸トレストロン;リン酸トリシリビン;トリメトレキサート;グルクロン酸トリメトレキサート;トリプトレリン;塩酸ツブロゾール;ウラシルマスタード;ウレデパ;バプレオチド;ベルテポルフィン;ビンブラスチン;硫酸ビンブラスチン;ビンクリスチン;硫酸ビンクリスチン;ビンデシン;硫酸ビンデシン;硫酸ビネピジン;硫酸ビングリシナート;硫酸ビンロイロシン;酒石酸ビノレルビン;硫酸ビンロシジン(vinrosidine);硫酸ビンゾリジン;ボロゾール;ゼニプラチン;ジノスタチン;塩酸ゾルビシン;2-クロロデオキシアデノシン;2'-デオキシホルマイシン;9-アミノカンプトテシン;ラルチトレキセド;N-プロパルギル-5,8-ジデアザ葉酸;2-クロロ-2'-アラビノ-フルオロ-2'-デオキシアデノシン;2-クロロ-2'-デオキシアデノシン;アニソマイシン;トリコスタチンA;hPRL-G129R;CEP-751;リノミド(linomide);硫黄マスタード;ナイトロジェンマスタード(メクロレタミン);シクロホスファミド;メルファラン;クロラムブシル;イホスファミド;ブスルファン;N-メチル-N-ニトロソ尿素(MNU);N,N'-ビス(2-クロロエチル)-N-ニトロソ尿素(BCNU);N-(2-クロロエチル)-N'-シクロヘキシル-N-ニトロソ尿素(CCNU);N-(2-クロロエチル)-N'-(トランス-4-メチルシクロヘキシル-N-ニトロソ尿素(MeCCNU);N-(2-クロロエチル)-N'-(ジエチル)エチルホスホン酸-N-ニトロソ尿素(フォテムスチン);ストレプトゾトシン;ジアカルバジン(DTIC);ミトゾロミド;テモゾロミド;チオテパ;マイトマイシンC;AZQ;アドゼレシン;シスプラチン;カルボプラチン;オルマプラチン;オキサリプラチン;C1-973;DWA2114R;JM216;JM335;ビス(白金);トムデックス;アザシチジン;シタラビン;ゲムシタビン;6-メルカプトプリン;6-チオグアニン;ヒポキサンチン;テニポシド9-アミノカンプトテシン;トポテカン;CPT-11;ドキソルビシン;ダウノマイシン;エピルビシン;ダルビシン;ミトキサントロン;ロソキサントロン;ダクチノマイシン(アクチノマイシンD);アムサクリン;ピラゾロアクリジン;オールトランスレチノール;14-ヒドロキシ-レトロ-レチノール;オールトランスレチノイン酸;N-(4-ヒドロキシフェニル)レチナミド;13-シス-レチノイン酸;3-メチルTTNEB;9-シス-レチノイン酸;フルダラビン(2-F-アラ-AMP);または2-クロロデオキシアデノシン(2-Cda)が挙げられる。
本発明はまた、結合剤、診断剤、または治療剤の形成における、天然の野性型HSAリンカーを包含し、そのアミノ酸配列およびヌクレオチド配列をそれぞれSEQ ID NO: 3および4に示す。SEQ ID NO: 3に列挙されるアミノ酸配列を有するHSAリンカーを利用する全ての態様では、1つまたは複数の上記のペプチドコネクターを、該HSAリンカーのアミノ末端および/もしくはカルボキシ末端に共有結合させるか、または該HSAリンカー配列内のアミノ酸残基に共有結合させて、1つまたは複数の結合部分の結合を容易にする。
本発明はさらに、1つまたは複数のペプチドコネクターまたは結合部分と組み合わせてもよい、短縮した野性型HSAポリペプチドを用いて形成される、HSAリンカーコンジュゲートを提供する。野性型の全長HSAアミノ酸配列(すなわち、SEQ ID NO: 3)のアミノ酸のうち1個、2個、3個、4個、5個、10個、15個、20個、50個、100個、200個、またはそれ以上を欠いている野性型HSAポリペプチドを、本明細書において記載されるような任意の結合部分または診断剤または治療剤のいずれかに結合させることができる。短縮は、HSAリンカーの一端または両端で行うことができ、または内部残基の欠失を含むことができる。2つ以上のアミノ酸残基の短縮は一列に並んでいる(すなわち、連続的である)必要はない。野性型HSAリンカーの例としては、1つまたは複数のペプチドコネクターまたは結合部分、1つまたは複数のドメインI(SEQ ID NO: 56;SEQ ID NO: 3の残基1〜197)、ドメインII(SEQ ID NO: 54;SEQ ID NO: 3の残基189〜385)、もしくはドメインIII(SEQ ID NO: 57;;SEQ ID NO: 3の残基381〜585)、またはこれらの組み合わせを有するもお、例えば、ドメインIとII、IとIII、およびIIとIIIを組み合わせて有するものが挙げられる。
HSAリンカーを、該HSAリンカーのアミノ酸残基の部位特異的化学的修飾によって修飾してもよいが、必須ではない。正確に折り畳まれた三次構造のHSAは、該タンパク質の外面上に特定のアミノ酸残基を提示している。化学的反応性を有するアミノ酸残基(例えば、システイン)を、表面露出したこれらの残基に対して置換することができ、これによって診断剤または治療剤の部位特異的結合が可能になる。
HSAリンカーの表面露出アミノ酸残基は、診断剤、治療剤、または細胞毒性剤の化学結合を可能にするためにシステイン残基で置換されてもよい。(その天然の三次構造に折り畳まれている場合に)HSAリンカーの表面上に露出したシステイン残基は、マレイミドまたはハロアセチルなどのチオール反応性基に対する診断剤、治療剤、または細胞毒性剤の特異的結合を可能にする。マレイミド基に対するシステイン残基のチオール官能基の求核反応性は、リジン残基のアミノ基またはN末端アミノ基などのタンパク質内の他の全てのアミノ酸官能基と比較して約1000倍高い。ヨードアセチル試薬およびマレイミド試薬におけるチオール特異的な官能性はアミン基と反応し得るが、より高いpH(>9.0)およびより長い反応時間が必要である(Garman, 1997, Non-Radioactive Labelling: A Practical Approach, Academic Press, London)。タンパク質中の遊離チオールの量は、標準的なエルマンアッセイを用いて推定され得る。反応性の遊離チオールを生成するために、ジチオスレイトール(DTT)またはセレノールなどの試薬によるジスルフィド結合の還元(Singhら、Anal. Biochem. 304:147〜156(2002))が必要である場合もある。
さらに、血清クリアランス速度の改変は、HSAリンカー内部にグリコシル化部位を設計することによって達成できる。特定の態様では、HSAリンカーはグリコシル化されている。ポリペプチドのグリコシル化は、典型的にはN結合型かO結合型のどちらかである。N結合とは、アスパラギン残基の側鎖への糖質部分の結合を指す。トリペプチド配列であるアスパラギン-X-セリンおよびアスパラギン-X-トレオニン(ここでXはプロリン以外の任意のアミノ酸を表す)は、アスパラギン側鎖に対する糖質部分の酵素的結合に対する認識配列である。従って、ポリペプチド内にこれらのトリペプチド配列のどちらかが存在することによって、可能性のあるグリコシル化部位が作製される。O結合型グリコシル化とは、糖であるN-アセチルガラクトサミン(aceylgalactosamine)、ガラクトース、またはキシロースのうち一つの、ヒドロキシアミノ酸に対する、最も一般的にはセリンまたはトレオニンに対する結合を指すが、5-ヒドロキシプロリンまたは5-ヒドロキシリジンを用いてもよい。
本明細書に記載のHSAリンカーコンジュゲートを、本明細書に記載の治療剤、細胞毒性剤、または細胞増殖抑制剤の1つまたは複数と共に投与してもよい。例えば、乳癌に罹患している患者に、ErbB2およびErbB3 scFv(例えば、B2B3-1)を含むHSAリンカーを投与することができ、これは、乳癌の治療のための一般的な化学療法レジメンである、例えばドキソルビシン、シクロホスファミド、およびパクリタキセルと同時投与することができる。この点に関して使用のために好ましい治療剤は、トラスツズマブである。この組み合わせに関するデータは、後述の実施例42〜44に示される。癌治療に有用である追加の生物学的および化学的な剤は、本明細書に、例えば付表2に示される。
放射線療法または外科手術の前に、それと同時に、またはその後に、HSAリンカーコンジュゲートを投与してもよい。例えば、増殖性障害(例えば、乳癌)に罹患している患者に、HSAリンカーコンジュゲートを単独で、または、癌性組織の部位における標的放射線療法または外科的処置(例えば、乳腺腫瘍摘出術または乳房切除術)と同時に本明細書に記載のその他の治療剤、細胞毒性剤、もしくは細胞毒性剤と組み合わせて、投与することができる。HSAリンカーコンジュゲートとの組み合わせに適した放射線療法としては、近接照射療法および標的術中放射線療法(TARGIT)が挙げられる。
本明細書で提供される薬学的組成物は、1つまたは複数の結合部分(例えば、抗体または抗体断片)、診断剤(例えば、放射性核種またはキレート剤)、または治療剤(例えば、細胞毒性剤または免疫調節剤)を含むHSAリンカーコンジュゲートの、治療上有効量または診断上有効量を包含する。活性成分であるHSAリンカーコンジュゲート(1つまたは複数の結合部分、診断剤、または治療剤と共に調製される)は、種々の薬物送達系における使用のために製剤化することができる。1つまたは複数の生理学的に許容可能な賦形剤または担体を、適切な製剤化のために組成物に含めることができる。本発明での使用に適した製剤は、Remington’s Pharmaceutical Sciences, Mack Publishing Company, Philadelphia, PA, 第17版(1985)に見出される。薬物送達のための方法の概説については、Langer Science 249:1527〜1533(1990)を参照のこと。
HSAリンカーコンジュゲートは、例えば、増殖性疾患(例えば、黒色腫、明細胞肉腫、および腎臓癌などの癌)、および自己免疫疾患(例えば、多発性硬化症、関節リウマチ、およびブドウ膜炎)の診断または治療を含む、ヒトにおける診断用途および治療用途に用いることができる。ヒトの増殖性疾患および自己免疫疾患についての以下の記載は、診断用途および治療用途においてHSAリンカーコンジュゲートをどのように適用できるのかについての全体的な理解を当業者に与えるためのものであり、本発明の範囲を限定する意図はない。
HSAリンカーコンジュゲートは、これらに限定されるわけではないが、乳癌、黒色腫、明細胞肉腫、腎臓癌(例えば、腎細胞癌)、前立腺癌、肺癌、胃癌、および卵巣癌などの増殖性疾患を、診断、治療、予防、または除去するために使用できる。増殖性疾患を有することが疑われるまたはそれに罹患している患者における診断用途または治療用途のためにHSAリンカーと結合させる結合部分は、増殖性疾患に関連する標的分子(例えば、チロシンキナーゼレセプターなどの細胞表面レセプター)を特異的に結合させるか、アゴナイズするか、活性化するか、拮抗するか、または阻害する能力に基づいて、選択され得る。例えば、インスリン様成長因子レセプター(IGFR、例えば、IGF1RおよびIGF2R)、線維芽細胞成長因子レセプター(FGFR)、血小板由来成長因子レセプター(PDGFR)、血管内皮成長因子レセプター(VEGFR)、腫瘍壊死因子レセプター(TNFR)、上皮細胞成長因子レセプター(EGFR、例えば、ErbB2(HER2/neu))、Fcレセプター、c-kitレセプター、または間葉上皮移行因子レセプター(c-met;肝細胞成長因子レセプター(HGFR)としても公知)を標的する結合部分をHSAリンカーに結合させて、増殖性疾患を診断または治療することができる。HSAリンカーコンジュゲートによる癌細胞の特異的結合は、結合された癌細胞の検出(例えば、本明細書で定義したような検出可能標識に結合させたHSAリンカー)または破壊(例えば、細胞毒性剤に結合させたHSAリンカー)を可能にし得る。乳癌および腎臓癌の治療に関するHSAリンカーコンジュゲートの具体的な用途を、下記に記載する。
一般的な形態の乳癌としては、浸潤性の乳管癌つまり乳管の悪性癌、および浸潤性の小葉癌つまり乳腺小葉の悪性癌が挙げられる。ある種の乳癌細胞は、高レベルの上皮細胞成長因子レセプター、特にErbB2(すなわち、HER2/neu)を発現することが公知である。EGFRの異常なシグナル伝達または無秩序な活性化は、乳癌を含む多くの癌の発達および進行に関連づけられている。機能不全EGFR経路を介して媒介される無制限細胞増殖は、上皮由来の多種多様な固形腫瘍で見出され、データによって、腫瘍のEGFR発現、過剰発現、および調節不全と、疾患の進行、転移の表現型、化学療法に対する耐性、および全体的な予後不良とが関連付けられている。
腎臓癌、例えば腎細胞癌は、従来の放射線療法および化学療法に対して特に耐性である。そういう訳で、HSAリンカーと結合させた生物学的治療剤の適用は、これらの癌に罹患している患者にとっての魅力的な選択肢に相当する。例えば、腎癌を治療するために、I型インターフェロンまたはインターロイキン2レセプターをアゴナイズする結合部分と結合させたHSAリンカーを用いることができる。固形腫瘍として、腫瘍血管新生を標的および阻害する結合部分(例えば、ベバシズマブなどの抗血管内皮成長因子(VEGF)抗体)も、治療効果のために用いることができる。
HSAリンカーコンジュゲートを用いて、例えばヒト患者における自己免疫疾患および自己免疫障害、例えば、多発性硬化症(MS)、インスリン依存性糖尿病(IDDM)、関節リウマチ(RA)、ブドウ膜炎、シェーグレン症候群、グレーブス病、乾癬、および重症筋無力症などを、診断、治療、予防、または安定化することができる。自己免疫疾患および自己免疫障害は、免疫系の自己反応性要素(例えば、T細胞、B細胞、および自己反応性抗体)によって生じる。そういう訳で、自己反応性の免疫細胞および抗体を阻害、遮断、拮抗、または枯渇させる結合部分(例えば、抗リンパ球または抗胸腺細胞グロブリン;モノクローナル抗体であるバシリキシマブ、ダクリズマブ、またはムロモナブ-CD3)を、治療用途のためにHSAリンカーと結合させることができる。本明細書で定義された、炎症性シグナル伝達インヒビター(ISI)として機能する結合部分を、自己免疫の治療のためにHSAリンカーに結合させることができる。さらに、インテグリン機能を阻害またはこれに拮抗する結合部分(例えば、本明細書で定義されたインテグリンアンタゴニスト)は、疾患の進行を回復または停止できる。
多発性硬化症(MS)は、中枢神経系(CNS)の神経の不可逆的な変性を特徴とする神経学的疾患である。根源的な原因は不明であるが、MSにおける神経変性は、脱髄すなわち、通常は外層を裏打ちして神経を絶縁するタンパク質であるミエリンの剥離の直接的結果である。T細胞は、MSの発症に重要な役割を果たしている。正常な白質でない、炎症を起こしたMS病変は、ヒトHLA-DR2などのMHCクラスII関連分子によって提示される自己抗原に応答する、浸潤性CD4+T細胞を有し得る。浸潤性CD4T細胞(TH1細胞)は、炎症促進性サイトカインIL-2、IFN-γ、およびTNF-αを産生し、これが、マクロファージなどの抗原提示細胞(APC)を活性化して、さらなる炎症促進性サイトカイン(例えば、IL-1β、IL-6、IL-8、およびIL-12)を産生させる。IL-12はさらにIFN-γ合成を誘導する。その結果、神経鞘の進行性脱髄が起こり、これがヒト疾患につながる。
関節リウマチ(RA)は、免疫系による関節の攻撃が起こっている慢性的な炎症性自己免疫障害である。これは、日常生活に支障を来し(disabling)かつ疼痛性の炎症状態であり、疼痛および関節破壊によって運動機能の実質的な喪失をもたらし得る。RAは全身性の疾患であって、皮膚、血管、心臓、肺、および筋肉を含む身体全体にわたって関節外組織に影響を与える場合が多い。
ブドウ膜炎とは、具体的には眼球の中間層の炎症を指すが、眼球の内部に関与する任意の炎症性プロセスを指す場合もある。ブドウ膜炎は、自己免疫性原因によっても特発性原因によってもよい。
本発明はさらに、HSAリンカーならびに1つまたは複数の結合部分(例えば、抗体または抗体断片)、診断剤(例えば、放射性核種またはキレート剤)、および治療剤(例えば、細胞毒性剤または免疫調節剤)と共に、必要に応じて、これらを該HSAリンカーに結合させるために使用可能である試薬を含む、薬学的組成物と、薬学的に許容される担体とを、疾患または病態(例えば、癌、自己免疫疾患、または心血管疾患)を治療するための治療上有効量で含む、キットを提供する。キットは、それに含まれる組成物を実施者(例えば、医師、看護師、または患者)が投与することを可能にするための説明書を含む。
HSAに対する薬物の特異的結合のための部位を特定するために、結晶構造を調査して、表面に露出したセリン残基およびトレオニン残基を同定する。これらの特定の表面露出したアミノ酸をその後システインに変異させることができ、これによって、マレイミドのようなチオール特異的結合を用いた、置換されたシステインへの薬物の結合が可能になる。薬物結合の前には、温和な還元が必要であり得る。結合させる薬物の数は、HSAに導入される、表面露出したシステイン残基の数によって、制御される。どちらも大部分の構造がシステインと同一であるので、セリンおよびトレオニンは変異のための最も適切な残基として選択されるが、他の表面露出した残基を変異させてシステインとしてもよく、細胞増殖抑制薬または細胞毒性薬に対して成功裏に結合しうる。
HSA中のアスパラギン連結グリコシル化部位の導入のための領域を特定するために、結晶構造を調査して、表面露出した(>30%)アスパラギン、セリン、およびトレオニンの残基が変異に適しているとする。コンセンサス配列であるアスパラギン-x-セリン/トレオニン(ここで、xはプロリンではない)が存在する場合、グリコシル化はアスパラギン残基で起こる。表2は、アスパラギン連結グリコシル化の導入のためのHSA中の可能な変異部位を列挙している。
*これらの変異がHSA内で起こることは滅多に無いことも、報告されている(Carlson et al., “Alloalbuminemia in Sweden: Structural study and phenotypic distribution of nine albumin variants,” Proc. Nat. Acad. Sci. USA 89:8225- 8229 (1992); Madison et al., “Genetic variants of human serum albumin in Italy: point mutants and a carboxyl-terminal variant,” Proc. Nat. Acad. Sci. USA 91:6476-6480 (1994); Hutchinson et al., “The N-terminal sequence of albumin Redhill, a variant of human serum albumin,” FEBS Lett. 193:211-212 (1985); Brennan et al., “Albumin Redhill (-1 Arg, 320 Ala-Thr): a glycoprotein variant of human serum albumin whose precursor has an aberrant signal peptidase cleavage site,” Proc. Nat. Acad. Sci. USA 87:26-30 (1990); Minchiotti et al., “Structural characterization of four genetic variants of human serum albumin associated with alloalbuminemia in Italy,” Eur. J. Biochem. 247:476-482 (1997); Peach et al., “Structural characterization of a glycoprotein variant of human serum albumin: albumin Casebrook (494 Asp-Asn),” Biochim. Biophys. Acta 1097:49-54 (1991))。
B2B3-1は、ヒト抗ErbB2 scFv抗体であるB1D2(SEQ ID NO: 27)、および、ヒト抗ErbB3 scFvであるH3(SEQ ID NO: 26)を含む、二重特異性scFv抗体融合分子である。2つのscFvは、修飾されたヒト血清アルブミン(HSA)リンカーによって連結されている。抗ErbB3 scFvであるH3は、短いコネクターポリペプチドを組み込んでいるHSAリンカーのアミノ末端に組み換えによって融合されており、抗ErbB2 scFvであるB1D2は、さらなる短いコネクターポリペプチドを組み込んでいる該修飾HSAリンカーのカルボキシ末端に組み換えによって融合されている。各々のコネクターポリペプチドは、プロテアーゼ耐性の特性に基づいて選択される。該修飾HSAリンカーは2つのアミノ酸置換を含む。天然HSAの34位のシステイン残基を、この部位での酸化に起因する潜在的なタンパク質の不均一性を低下させるために、セリンに変異させる。薬理学的半減期を低下させ得る脱アミドに対して天然HSAでは感受性であり得る、天然HSAのアミノ酸503のアスパラギン残基を、グルタミンに変異させる。その抗ErbB2 scFv結合部分の高い親和性(10.0nM〜0.01nMの範囲のkD、より好ましくは約0.3nMのkDを有する)のために、B2B3-1は、ErbB2を過剰発現している腫瘍に選択的に結合すると考えられている。続いて50〜1nMの範囲、より好ましくは約16nMのkDを有する抗ErbB3 scFvによりErbB3が結合することによって、ErbB3のHRG誘導性リン酸化が阻害される。修飾HSAリンカーは、該二重特異性分子の循環半減期を延長させる。B2B3-1は分子量119.6kDaを有し、好ましくはグリコシル化されていない。
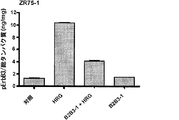
図2に示されるとおり、B2B3-1変異体は、ZR75-1乳癌細胞においてHRG誘導性のpErbB3を阻害する。ZR75-1乳癌細胞を、ある用量範囲のB2B3-1変異体で24時間処理した後、HRG刺激を行う。ELISAによって細胞溶解物中でpErbB3レベルを測定し、パーセント阻害と共にIC50値を算出する。繰り返し実験を表すエラーバーと共にIC50平均値(Y軸)を示す。対応するバーの上にパーセント阻害値を示す。
特記しない限り、全ErbB3およびリン酸化ErbB3のELISAのためのELISA試薬は、R&D Systemsより購入したDUOSETキットである。96ウェルのNUNC MAXISORBプレートを抗体50μlで被覆し、室温で一晩インキュベーションする。翌朝、カルシウムおよびマグネシウムを含まないDulbeccoリン酸緩衝生理食塩水(PBS)にTween界面活性剤を含めたもの(PBST)(0.05% Tween-20)を用いるBIOTEKプレートウォッシャー内で1000μl/ウェルでプレートを3回洗浄する。続いて、2% BSAを含むPBSを用いて、室温で約1時間プレートをブロッキングする。PBSTを用いるBIOTEKプレートウォッシャー内で1000μl/ウェルでプレートを3回洗浄する。細胞は、37℃および5%二酸化炭素で増殖させ、冷PBSで洗浄した後、150mM NaCl、5mMピロリン酸ナトリウム、10uM bpV(phen)、50uMフェニルアルシン、1mMオルトバナジン酸ナトリウム、およびプロテアーゼインヒビターカクテル(Sigma、P2714)を添加した哺乳動物タンパク質抽出(MPER)溶解緩衝液(Pierce, 78505)を用いて回収する。さらなる処理に関しては、50%溶解緩衝液および1% BSAで希釈した50μLの細胞溶解物および標準を2つ組で使用する。試料を4℃で2時間、プレートシェーカー上でインキュベーションし、上述のように洗浄する。約50μlの検出抗体を2% BSAで希釈し、PBSTを添加し、室温で約1〜2時間インキュベーションする。リン酸化ErbB3については検出抗体を西洋ワサビペルオキシダーゼ(HRP)に直接結合させるが、全ErbB3についてはビオチン化マウス抗ヒトErbB3二次検出抗体を使用する。プレートを上述のように洗浄する。全ErbB3については約50μlのストレプトアビジン-HRPを添加して30分間インキュベーションし、プレートを上述のように洗浄する。約50μlのSUPERSIGNAL ELISA Pico(Thermo Scientific)基質を添加し、FUSIONプレートリーダーを用いてプレートを読み取る。2つ組の試料は平均され、存在する場合、エラーバーは2つの複製物の間の標準偏差を表す。
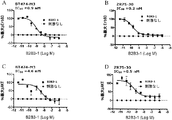
B2B3-1変異体A5-HSA-B1D2(図3〜5のパネルA)、H3-HSA-B1D2(図3〜5のパネルB)、H3-HSA-F5B6H2(図3〜5のパネルC)、およびF4-HSA-F5B6H2(図3〜5のパネルD)による24時間の前処理の後に、リン酸化ErbB3(図3A〜D)、AKT(図4A〜D)、およびERK(図5A〜D)の阻害を測定する。BT474乳癌細胞を、ある用量範囲のB2B3-1変異体で24時間処理した後、HRG刺激を行う。ELISAによって細胞溶解物中でpErbB3、pAKT、およびpERKのレベルを測定し、パーセント阻害と共にIC50値を算出する。これらの結果は、10-8モルおよびそれ以上の濃度においてAKT、ERK、およびErbB3のHRG誘導性リン酸化を50%超阻害するHSAリンカーコンジュゲートは、試験したものの中でB1B2-1のみであることを実証するものである。
図6に示すとおり、B2B3-1変異体によるBT474乳房腫瘍細胞の処理は、G1細胞周期停止、およびS期の細胞群の減少を引き起こす。BT474細胞を、1μMのB2B3-1変異体および対照を用いて72時間処理する。処理の終了後、細胞をトリプシン処理して、ヨウ化プロピジウムを含む低張液中に穏やかに再懸濁し、単一の細胞をフローサイトメトリーによって解析する。G1期およびS期の細胞周期分布は、細胞周期分析のために設計された曲線あてはめアルゴリズム(FlowJoソフトウェア細胞周期プラットフォーム)を用いて測定する。
B2B3-1(SEQ ID NO: 16)は、その二量体化パートナーであるErbB2の大量発現を利用してErbB3活性化を阻害し、腫瘍細胞を標的する。高親和性抗ErbB2 scFv抗体であるB1D2は、ErbB2を過剰発現している腫瘍細胞をB2B3-1が標的とするのを容易にする。修飾HSAリンカーによってB1D2を低親和性の抗ErbB3 scFv抗体であるH3に接続し、これが、ErbB3のリガンドであるHRGの結合を遮断する。B2B3-1によって媒介される、ErbB3リン酸化および下流のAKTシグナル伝達の阻害は、この遮断によるものと考えられる。ErbB2結合性scFvであるB1D2は、作動作用も拮抗作用も有さない親scFvのC6.5に由来する。従ってB1D2は、単なる標的剤として機能する可能性が高い。ErbB3結合性scFvの比較的低い結合親和性により、ErbB3を発現しているがErbB2はほとんどまたは全く発現していない正常な非癌性組織とB2B3-1との強い結合が妨害されると考えられ、それによって非特異的な毒性の可能性が低下する。ErbB2とErbB3の両方を発現している腫瘍細胞では、両方のレセプターに結合する二重特異性B2B3-1の結合活性の影響が存在し、これによって、ErbB3 scFvの親和性の低さが克服され、ErbB3レセプター複合体とのHRG相互作用の強力な阻害が可能になる。
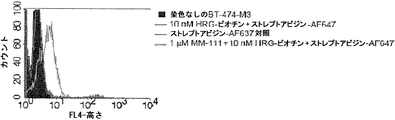
ErbB3に対するHRGの結合を遮断できるB2B3-1の能力を実証した後、ErbB3を発現しかつErbB2を過剰発現している2つの細胞株におけるインビトロErbB3シグナル伝達に対するB2B3-1の効果を調査する。ヒト乳癌細胞株BT-474-M3(例えばDrummond et al. (2005) Clin. Cancer Res. 11:3392; Park et al. (2002) Clin. Cancer Res. 8:1172; Kirpotin et al. (2006) Cancer Res. 66:6732に記載)およびZR7530(US NIH Lawrence Berkeley National Laboratory breast cancer cell collectionより入手可能)を、一晩にわたり血清飢餓処理し、24時間にわたりB2B3-1の用量滴定で前処理した後、10分間にわたり5 nMのHRG 1β EGFドメインで刺激する。その後、ほぼ上述したとおりにELISAアッセイを用いてErbB3およびAKTのリン酸化状態を調べる。その結果、両細胞株において、用量依存的様式で、かつ強力なIC50で、ErbB3およびAKT両方のリン酸化のHRG誘導性活性化をB2B3-1が阻害することが示される(図8A〜D)。
図9は、BT474乳癌細胞におけるシグナル伝達タンパク質に対するB2B3-1処理の効果を示す。細胞を、ある用量範囲のB2B3-1を用いて24時間処理した後、ヘレグリン刺激を行う。pErbB2、pErbB3、pErk、およびpAKTのレベル、ならびにこれらの対応する総タンパク質レベルを、細胞溶解物についてウエスタンブロット分析によって測定する。少なくともpErbB2およびpErbB3のレベルはB2B3-1処理によって用量依存的様式で低下することが、結果により示される。
図10は、B2B3-1処理したBT474乳癌細胞の免疫沈降-ウエスタンブロット分析を示す。細胞を、ある用量範囲のB2B3-1を用いて24時間処理した後、ヘレグリン刺激を行う。ErbB2に会合した複合体を、抗ErbB2抗体を用いて細胞溶解物から単離した後、ウエスタンブロット分析によってpErbB2およびpErbB3、ならびに対応する総タンパク質のレベルを検出する。抗ErbB2抗体によって実質的により多くのErbB3およびリン酸化ErbB3が沈降するように、B2B3-1がErbB2をErbB3に架橋させていることが、結果により示される。
B2B3-1の抗腫瘍活性を、いくつかのアッセイを用いてインビトロで調べる。第一のアッセイでは、G1期のBT-474細胞またはSKBR3細胞の蓄積に対するB2B3-1の影響、ならびに随伴するS期の細胞周期の減少を調べる。簡潔に言うと、細胞を1μMのB2B3-1またはPBSビヒクルを用いて72時間処理する。処理の終了後、細胞をトリプシン処理して、ヨウ化プロピジウムを含む低張液中に穏やかに再懸濁し、単一の細胞をフローサイトメトリーによって解析する。G1期およびS期の細胞周期分布は、細胞周期分析のために設計された曲線あてはめアルゴリズム(FlowJoソフトウェア細胞周期プラットフォーム, Tree Star, Inc.)を用いて測定する。B2B3-1は、S期の細胞の割合をわずかに低下させ、G1期の細胞群を増大させることが見出された(図11A)。第二の実験では、B2B3-1による処理の後に形成された細胞コロニーの数を調べる。乳癌細胞BT-474およびSKBR3を1μMのB2B3-1の存在下でプレーティングし、培地のみにプレーティングした細胞と比較する。培地のみまたは処理を含む培地は、3日毎に補充する。14日後、コロニー数を計数して、処理なしの細胞と比較する。図11Bは、B2B3-1で細胞を処理した場合に形成されるコロニーの数が対照細胞と比較して40〜45%低下することを示している。最後に、B2B3-1が細胞増殖を阻害する能力を、Real-Time Cell Electronic Sensing System(RT-CES;ACEA Biosciences)を用いる細胞インピーダンスアッセイで評価する。BT-474細胞を、マイクロエレクトロニクスセンサーアレイを組み込んだプレート上に播種して、B2B3-1または培地のみの用量滴定で72時間処理する。細胞-電極インピーダンス応答の発生を表すデータを72時間にわたり1時間毎に収集し、IC50値を処理から68時間後に算出する。図11Cは、B2B3-1がBT-474細胞のインピーダンスを33nMのIC50で阻害できたことを示す。
本発明者らはまた、B2B3-1が、ErbB2レセプターとErbB3レセプターに同時に結合して架橋できるその能力に基づいて、アゴニスト活性を呈するか否かも検討した。血清飢餓処理したZR75-1乳癌細胞を1μMのB2B3-1またはPBSビヒクルとともに24時間インキュベーションする。また細胞を、B2B3-1またはPBSビヒクルで24時間処理した後、5nMのHRG 1β EGFドメインを用いて10分間刺激する。細胞を溶解し、ほぼ上述したとおりのELISAによって、溶解物のpErbB3含量を評価する。図12は、B2B3-1のみで処理した細胞が、処理なしの細胞のレベルと同等レベルのリン酸化ErbB3を含んでいたことを示し、これにより、B2B3-1はErbB3リン酸化を促進するアゴニストとしては作用しないことが示される。
ErbB2およびErbB3に対して特異的に結合でき、関連するErbBファミリーメンバーであるEGFRおよびErbB4には結合できないB2B3-1の能力を、ELISAによって調べる。プレートを、ErbB2またはErbB3いずれかの組み換え細胞外ドメインで被覆する。プレートをブロッキングして、競合するEGFR、ErbB2、ErbB3、またはErbB4の組み換え細胞外ドメインの連続希釈物の存在下で、半最大結合濃度のB2B3-1を用いてインキュベーションする。ErbB2被覆プレートに対するB2B3-1結合を遮断したのは可溶性ErbB2細胞外ドメインだけであったことが、結果により示される(図13A)。同様に、ErbB3被覆プレートに対するB2B3-1結合を遮断したのは、可溶性ErbB3細胞外ドメインだけであった(図13B)。これらの結果は、ErbB2に対する、抗ErbB2アームであるB1D2の特異性、およびErbB3に対する、抗ErbB3アームであるH3の特異性を実証するものと考えられる。ErbB3被覆プレート上でB2B3-1と共に可溶性ErbB2細胞外ドメインをインキュベーションした場合に観察されたシグナルの増大は、該プレート上でのErbB2-ErbB3-B2B3-1複合体の形成によるものと考えられる。
B2B3-1の単特異性変異体を用いて、ErbB2およびErbB3の両方を発現している腫瘍細胞に結合できるB2B3-1の能力を調査した。SKO-2(SEQ ID NO: 67)およびSKO-3(SEQ ID NO: 68)は、それぞれErbB2またはErbB3と相互作用できる能力を欠いた、B2B3-1の変異体である。
および
と、以下の温度サイクルを用いて、変異c295gおよびa296cを作成する:95℃1分間の後、95℃1分間、55℃分間、および65℃17.2分間を30サイクル。プラスミドDNAのDNA配列決定によって、変異を確認する。t334g、g335c、およびa341cに変異を導入するために、c295gおよびa296cに配列確認済みの変異を有するプラスミドに対して、プライマー
および
と以下の温度サイクルを用いて、2回目の部位特異的突然変異誘発を実施する:95℃30秒間ならびに、95℃30秒間、55℃1分間、および68℃17.2分間を18サイクル。得られるプラスミドDNAのDNA配列決定によって、変異を確認する。
および
を用いて、変異B1D2 scFvをSKO-2から単離し、Kas I/ Not I制限消化B2B3-1プラスミドへのサブクローニングのためにKas I制限部位およびNot I制限部位を導入する。PCRは以下の通り実施する:変異B1D2の増幅のため、94℃1分間の後、94℃30秒間、58℃1分間、72℃1分間を30サイクル、その後72℃5分間を1サイクル。クローニングの成功は、DNA配列決定によりモニタリングする。SKO-2およびSKO-3プラスミドは、振とうフラスコまたは10L WAVEバッグ中のCHO-K1細胞より安定に発現され、Blue SEPHAROSEおよび陽イオン交換クロマトグラフィーを用いて調整培地から精製される。
100nMのB2B3-1を、ヒト、カニクイザル、またはマウスの血清中で120時間にわたり37℃でインキュベーションすることによって、生理学的条件下でのB2B3-1の安定性を評価する。試料を0、24、48、72、96、および120時間目に取り出して、B2B3-1がErbB2およびErbB3の両方に結合する能力をELISAによって測定する。このELISAは、組み換えErbB2細胞外ドメインで96ウェルプレートを一晩被覆する工程、引き続くブロッキング工程、およびその後のB2B3-1の連続希釈物とのインキュベーションを伴う。次いで、プレートをFc-ErbB3細胞外ドメイン融合タンパク質と共に、続いてヤギ抗ヒトFc-HRPコンジュゲートと共に、インキュベーションする。スーパーシグナル化学発光基質の添加によって、プレートを現像する。図15A〜Cは、B2B3-1が、3つの種全てに由来する血清において生理学的条件下で安定であり続け、測定した全ての時点でErbB2およびErbB3の両方に結合できる同等の能力を維持していることを示している。
ヒトBT-474-M3異種移植片を保有しているヌードマウスを用いて、インビボでのB2B3-1の効果を評価する。1群あたり10匹のマウスを、0.3、1、3、10、30、または90mg/kgのB2B3-1で12回、3日毎に処理する。対照群には、90mg/kgのB2B3-1用量と等モル用量のPBSビヒクルまたはHSAを投与する。全ての用量を腹腔内(i.p.)投与する。腫瘍の大きさを週2回測定して、相当する腫瘍容積を算出する。B2B3-1処理は、対照群と比較してBT-474-M3腫瘍の大きさを有意に低下させることが、結果により示される(図16)。最低用量のB2B3-1(0.1mg/kg)で処理されたマウス以外のB2B3-1処理群の各々で、完全退縮が観察された。
図17A〜図17Eで示されるとおり、B2B3-1は複数の異種移植モデルにおいて、腫瘍の大きさをErbB2依存的様式で低下させる。B2B3-1は、ErbB2をレセプター>1×105個/細胞で発現しているCalu-3(図17A)、SKOV-3(図17B)、NCI-N87(図17C)、およびMDA-MB-361(図17E)の異種移植モデルでは有効であったが、4.5×104個/細胞のErbB2レセプターを発現するACHN(図17D)異種移植モデルではそれほど作用しなかった。マウスは、30mg/kgのB2B3-1で3日毎に処理した。
ErbB2の過剰発現によって、B2B3-1不応答のADRr乳癌異種移植モデルがB2B3-1に対する応答モデルに変換される(図18Aおよび18B)。ErbB2は、レトロウイルス発現系を用いてADRr乳癌細胞で過剰発現する。高レベルのErbB2を発現しているトランスフェクト細胞(ADRr-E2)をFACSを用いて選択し、続いてヌードマウス中に皮下注射して、異種移植腫瘍を樹立する。マウスは、30mg/kgのB2B3-1で3日毎に処理する。野性型ADRr異種移植片(図18A)ではB2B3-1に対する応答は観察されなかったが、ADRr-E2異種移植片(図18B)はB2B3-1に応答した。
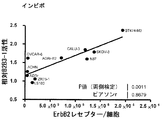
図19A〜Bに示すように、B2B3-1活性は、インビトロ(図19A)およびインビボ(図19B)においてErbB2発現レベルと正に相関する。B2B3-1によるErbB3リン酸化の阻害を、ErbB2発現レベルがレセプター5×104個/細胞〜レセプター2.4×106個/細胞の範囲である9種類の腫瘍細胞株において、ELISAアッセイを用いて判定する。B2B3-1がErbB3リン酸化を基底レベル(%pErbB3阻害)まで阻害する能力の程度は、ErbB2発現レベルと正に相関していることが見出された。同様に、低〜高レベルのErbB2を発現している10種類の異種移植モデルにおいてB2B3-1活性を評価する。異種移植片応答は同じく、ErbB2発現レベルと正に相関していた。
BT474-M3乳房腫瘍細胞のB2B3-1処理によって、核に対するp27kip1の転位が生じる(図20A)。BT474-M3細胞を1μMのB2B3-1で6時間処理する。p27kip1の細胞内位置を、免疫蛍光技術を用いて評価する。B2B3-1で処理した細胞において、p27kip1は核へと転位し、これは細胞増殖の阻害をもたらすことが示されている。p27kip1は処理なしの細胞の細胞質内に残存した。
図21A〜Bに示すように、BT474-M3乳房腫瘍異種移植片のB2B3-1処理によって核へのp27kip1の転位が起こる。BT474乳房腫瘍異種移植片を、用量30mg/kgのB2B3-1(図21A)、または等モル用量のHSA(図21B)で3日毎に計4回処理する。HSA対照腫瘍と比較して、B2B3-1処理した腫瘍においてp27kip1に関する核染色の増大が観察され、このことはインビボにおけるB2B3-1の抗増殖効果を示した。
B2B3-1処理によって、BT474乳癌異種移植腫瘍における増殖マーカーKi67の減少がもたらされる。BT474-M3乳房腫瘍異種移植片を、用量30mg/kgのB2B3-1(図22A)または等モル用量のHSA(図22B)で3日毎に計4回処理する。その後のKi67に対する腫瘍切片の染色により、HSA処理腫瘍と比較して、B2B3-1処理腫瘍に関する発現パターンの低下が実証された。
CD31発現に関するアッセイによって判定されるように(図23A〜図23B)、B2B3-1処理は、BT474-M3乳癌異種移植腫瘍において血管密度の低下をもたらす。BT474乳房腫瘍異種移植片を、用量30mg/kgのB2B3-1(図23A)または等モル用量のHSA(図23B)で、3日毎に計4回処理する。腫瘍を、血管マーカーCD31の存在について染色する。B2B3-1で処理した腫瘍は、HSAで処理した対照腫瘍と比較して、血管密度の顕著な低下を示す。
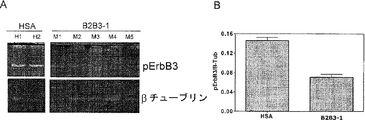
BT-474-M3異種移植腫瘍を30mg/kgのB2B3-1または17.5 mg/kgのHSAで、3日毎に計4回処理して、最後の投与から24時間後に腫瘍を回収する。腫瘍を溶解し、SDS-PAGE、続いてウエスタン分析に供して、B2B3-1の標的であるErbB3のリン酸化の相対レベルを評価する。等量のタンパク質を各レーンにロードし、βチューブリンについてプローブすることによって総タンパク質レベルを制御する。リン酸化ErbB3に特異的な抗体を用いるウエスタンブロット分析によって、B2B3-1処理腫瘍が含むpErbB3は、HSA処理腫瘍よりも少ないことが示される(図24A)。ウエスタンブロット分析の濃度測定と、その後の、βチューブリン積分バンド強度平均値に対するpErbB3積分バンド強度平均値の正規化によって、B2B3-1処理腫瘍が含むpErbB3は対照のHSA処理腫瘍よりも有意に少ないことが、実証された(図24B)。これらのデータによって、B2B3-1はインビボにおいてその標的ErbB3のリン酸化を阻害することが確認された。
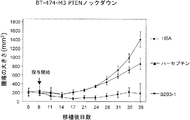
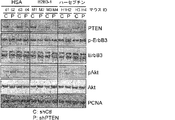
BT-474-M3乳癌細胞において腫瘍サプレッサー遺伝子であるホスファターゼ・テンシンホモログ(PTEN)の活性をノックアウトするために、shRNA技術を適用する。簡潔に言うと、レトロウイルストランスフェクションによって、shPTENまたはshControl RNAでBT-474-M3培養細胞をトランスフェクトする。PTENが減少したトランスフェクト細胞を、FACSを用いて選択し、続いてヌードマウスの右側腹部に皮下注射して異種移植腫瘍を樹立する。対照ベクターでトランスフェクトした細胞を、同じマウスの左側腹部に注射する。30mg/kgのB2B3-1で3日毎に、または10mg/kgのトラスツズマブで毎週、マウスを処理する。B2B3-1と等モル用量のHSAを対照として注射する。全て、腹腔内(i.p.)注射とする。
腫瘍異種移植片でシグナル伝達するErbB3のリン酸化をB2B3-1が阻害する能力を、上述のPTEN欠損BT-474-M3モデルを用いて調査する。操作された細胞株または対照細胞株の異種移植腫瘍を、30mg/kgのB2B3-1、17.5mg/kgのHSAで3日毎に、または10mg/kgのトラスツズマブで毎週処理して、腫瘍を最終回の24時間後に回収する。腫瘍を溶解し、SDS-PAGEに続いてウエスタン分析に供し、B2B3-1の標的であるErbB3、AKTのリン酸化の相対レベル、および総PTENレベルを評価する。等量のタンパク質を各レーンにロードし、PCNAについてプローブすることによって総タンパク質レベルを制御する。リン酸化ErbB3特異的な抗体を用いるウエスタンブロット分析によって、B2B3-1処理腫瘍が含むpAKTは、HSA処理腫瘍やハーセプチン処理腫瘍よりも少ないことが示される(図26A)。ウエスタンブロット分析の濃度測定と、その後の、PCNA積分バンド強度平均値に対するpAKT積分バンド強度平均値の正規化によって、B2B3-1処理腫瘍が含むpAKTは、対照のHSA処理腫瘍およびハーセプチン処理腫瘍よりも有意に少ないことが実証された(図26B)。
B2B3-1の薬物動態学的パラメーターをnu/nuマウスで調べる。動物を無作為にグループ分けし、単一用量5、15、30、または45mg/kgのB2B3-1を静脈内(IV)投与する(それぞれ、図27A〜図27D)。投与前、ならびに投与から0.5、4、8、24、48、72、および120時間後に、採血する。各時点について3匹のマウスを用いる。B2B3-1の血清レベルを、2つのELISA方法を用いて測定する。第一の方法は、ErbB2およびErbB3の両方に対するB2B3-1の機能的な結合を要するが、第二の方法は、血清中のB2B3-1のHSA成分しか測定しない。HSAのELISAは、ポリクローナル抗HSA捕捉抗体およびHRP結合ポリクローナル抗HSA検出抗体を利用する。HSA法に対してErbB2/ErbB3結合法を用いて測定したB2B3-1血清濃度が低下していることは、機能性B2B3-1の損失を示しうる。図27A〜Dは、いずれのELISA法を用いて評価した場合にもB2B3-1の薬物動態特性が同等であることを示しており、これは、B2B3-1がマウスの循環中で安定であることを示している。
B2B3-1血清濃度は、2コンパートメントの双指数関数モデルを用いてあてはめられ、二相性の配置を示す。5、15、30、または45mg/kg用量に対して、終末半減期はそれぞれ17、16、23、および18時間と算出され、これを表4に示す。B2B3-1用量の増加によって、曝露の直線的な増大がもたらされた(図28)。
薬物動態分析のための血液試料は、雌性カニクイザルにおける用量範囲決定用の毒性試験からも得る。この試験では、動物に4、20、または200mg/kgのB2B3-1を3日毎に4回、注入投与する。サンプリングは、投与前濃度およびピーク/トラフ濃度を得るために、各投与日(試験1日目、4日目、7日目、および10日目)における投与の前および5分後に、ならびに、1日目の初回注入から1、2、4、8、24、および48時間後と、10日目の最終注入から1、2、4、8、24、48、72、および120時間後とに行った。200mg/kgを投与した動物の回復に関しては、最終注入から168、336、および456時間後にも血清試料を採取する。
B2B3-1二重特異性scFv抗体融合タンパク質をコードするプラスミドは、固有のヒト抗ErbB3 scFv(「H3」と命名される)、ヒト抗ErbB2 scFv(「B1D2」と命名される)、および改変されたヒト血清アルブミン(HSA)リンカーの遺伝子配列を組み合わせて作製される。抗ErbB3 scFvであるH3は、接続用ペプチド(Ala-Ala-Ser)を介してHSAリンカーのアミノ末端に組み換え的に連結され、抗ErbB2 scFvであるB1D2は接続用ペプチド(Ala-Ala-Ala-Leu;SEQ ID NO: 5)を介してHSAリンカーのカルボキシ末端に遺伝子的に連結される。ペプチドコネクターは、哺乳動物の発現ベクター構築の際に制限部位を導入することによって形成され、単鎖抗体断片およびHSAリンカーと一緒に哺乳動物で発現するのに適したコドン使用頻度で合成される。
標準的な分子生物学的技術を用いてB2B3-1コード配列をpMP10kベースのベクター中にクローニングし、図30に示されるプラスミドpMP10k4H3-mHSA-B1D2を作製する。この構築物は大部分が、一般に用いられる遺伝子エレメントを使用している。B2B3-1発現は、ヒトGAPDプロモーターによって駆動される。このベクターは、マトリックス付着領域またはMARエレメントと呼ばれる遺伝子エレメントを利用している。MAR遺伝子レエレメントは、クロマチンの動的な機構を制御し、隣接する遺伝子を周囲のクロマチンの影響から遮断することによって、遺伝子のコピー数依存性、位置独立性、発現を増大させる。MARエレメントは、組み換えタンパク質の産生に関して所望のレベルの発現を呈しているクローンの単離確率を向上させ、かつ産生の安定性を増大させることが示されている。B2B3-1構築物で用いられるMARエレメントは非コードヒトMARエレメントである。B2B3-1プラスミドに加えて、ネオマイシン抗生物質耐性プラスミド(図31)およびハイグロマイシン耐性プラスミド(図32)も、安定な形質転換体を選択するために用いられる。
チャイニーズハムスター卵巣CHO-K1細胞は、ATCC(ATCC # CCL-61)から購入する。CHO-K1細胞株は、T. T. Puckが作製した、親CHO細胞株の血清依存的かつプロリン依存的な接着性サブクローンである。B2B3-1トランスフェクションに用いるCHO-K1細胞は、トランスフェクションの前に無血清培地での懸濁増殖について予め適合させる。B2B3-1細胞株を発生させるために、反復トランスフェクション手順を用いる。トランスフェクションの24時間前に、CHO-K1細胞を、8mMのL-グルタミン、0.1mMのヒポキサンチンナトリウム、および0.016mMのチミジンを補充したSFM4CHO(無血清)培地(HyClone, Logan, UT)中で、細胞1.0×106個/mLまで事前継代(sub passage)する。トランスフェクション当日、細胞をOptiMEM培地(Invitrogen Corp, Carlsbad, CA)中に再懸濁し、細胞40,000個を24ウェルプレートの各ウェル中に入れる。最初のトランスフェクションでは、B2B3-1発現プラスミド(pMP10k4H3-mHSA-B1D2)およびネオマイシン耐性プラスミド(図30;pSV2-neo(Selexis, Inc., Marlborough, MA)を、プラスミドモル比75:1(B2B3-1:ネオマイシン耐性)で一緒に混合する。該プラスミド混合物を次に、陽イオン性脂質トランスフェクション試薬(Lipofectamine LTX, Invitrogen Corp, Carlsbad, CA)と混合し、30分間にわたり脂質/DNA複合体を形成させる。その後、該DNA/脂質複合体をCHO-K1細胞に添加して、24ウェルプレートを37℃、5%CO2のインキュベーター内に入れる。
各トランスフェクションウェルの内容物をPBSで洗浄し、トリプシン処理して、2つの96ウェルプレートに分配する。用いる増殖培地は、10%FBS(Invitrogen Corp, Carlsbad, CA)および500mg/Lのジェネティシン(G418;Invitrogen Corp, Carlsbad, CA)を含むDMEM/F12(Invitrogen Corp, Carlsbad, CA)からなる。96ウェルプレート中の培地を、4日目に、8mMのL-グルタミン、0.1mMのヒポキサンチンナトリウム、0.016mMのチミジン、および500mg/Lのジェネティシンを補充したSFM4CHO培地に交換する。選択培地中でさらに2週間培養した後、生存細胞は明確なコロニーを形成している。該クローンを、定量用スポットブロット技術を用いて評価する。産生性最大のコロニーをトリプシン処理して、24ウェルプレートの単一ウェルに広げる。
初回のトランスフェクション(前記)から決定された産生性最大の細胞プールを、産生を増大させるために2回目のトランスフェクションに供する。トランスフェクションの24時間前、細胞プールを、8mMのL-グルタミン、0.1mMのヒポキサンチンナトリウム、および0.016mMのチミジンを補充したSFM4CHO(無血清)培地中で細胞1.0×106個/mLまで事前継代する。トランスフェクション当日、細胞をOptiMEM培地(Invitrogen Corp, Carlsbad, CA)中に再懸濁し、細胞40,000個を24ウェルプレートの各ウェル中に再度入れる。最初のトランスフェクションでは、B2B3-1およびハイグロマイシン耐性プラスミド(図32;pTK-Hyg(Clontech, Mountain View, CA))を50:1(B2B3-1:ハイグロマイシン耐性)というプラスミドモル比で一緒に混合する。該プラスミド混合物を次に、陽イオン性脂質トランスフェクション試薬(Lipofectamine LTX, Invitrogen Corp)と混合し、30分間にわたり脂質/DNA複合体を形成させる。その後、該DNA/脂質複合体を前記細胞プールに添加して、24ウェルプレートを37℃、5%CO2のインキュベーター内に配置する。
各トランスフェクションウェルの内容物をPBSで洗浄し、トリプシン処理して、2つの96ウェルプレートに分配する。用いる増殖培地は、10%のFBSおよび400mg/LのハイグロマイシンB(Invitrogen Corp)を補充したDMEM/F12からなる。96ウェルプレート中の培地を、4日目に、8mMのL-グルタミン、0.1mMのヒポキサンチンナトリウム、0.016mMのチミジン、および400 mg/LのハイグロマイシンBを補充したHyclone SFM4CHO培地に交換する。さらに2週間の選択の後、生存細胞は明確なコロニーを形成している。該クローンを、定量用スポットブロット技術を用いて評価する。産生性最大のコロニーをトリプシン処理して、24ウェルプレートの単一ウェルに広げる。
前記産生分析によって特定される、増殖性が最高でB2B3-1産生性が最大であるコロニーを、125mLの振とうフラスコから移して、5つの96ウェルプレート中に、細胞1個/ウェルとなるよう算出した細胞濃度でプレーティングする。96ウェルプレートを37℃かつ5%CO2のインキュベーター内に配置する。ウェルを週2回試験して、コロニーの形成を追跡する。単一細胞から生じるコロニーを、該コロニーの対称形状に基づいて特定する。そのようなコロニーを含むウェルを、24ウェルでの7日間の評価、および125mL振とうスラスコでの7日間の評価による、さらなるスクリーニングのために選び出す。
B2B3-1は、患者の耐容度に応じて、60分間または90分間にわたる点滴静注によって週1回投与される。B2B3-1は、患者(例えば、ヒト)への投与用に、20mMのL-ヒスチジン塩酸塩、150mMの塩化ナトリウム、pH6.5の滅菌溶液中に25mg/mLの濃度で処方される。
患者の癌が、ErbB2(HER2/neu)を含む上皮細胞成長因子レセプターを高レベルで発現していると考えられる場合、ErbB2結合部分と結合したHSAリンカー、例えばB2B3-1、B2B3-2、v-3、B2B3-4、B2B3-5、B2B3-6、B2B3-7、B2B3-8、B2B3-9、またはB3B3-10(後述の表6を参照のこと)による治療が適応であり得る。癌生検の遺伝型スクリーニングまたは組織学的スクリーニングによって患者腫瘍におけるErbB2高発現が明らかになる場合も該当しうる。
患者の癌がErbB2(HER2/neu)を含む上皮細胞成長因子レセプターを高レベルで発現していると考えられる場合、ErbB2結合部分と結合させたHSAリンカー、例えばB2B3-1、B2B3-2、v-3、B2B3-4、B2B3-5、B2B3-6、B2B3-7、B2B3-8、B2B3-9、またはB3B3-10(後述の表6を参照のこと)による治療が適応であり得る。癌生検の遺伝型スクリーニングまたは組織学的スクリーニングによって患者腫瘍におけるErbB2高発現が明らかになる場合も該当しうる。
HSAリンカーコンジュゲートは、後述の表5で列挙する1つまたは複数のエレメント(グループA〜E)を用いて構築される。特に、後述の表5でグループCとして示されるHSAリンカーコンジュゲートは、表5に示されるグループAおよびEから選択される1つまたは複数の結合部分を組み込んでいる。さらに、HSAリンカーコンジュゲートはまた、表5のグループBおよびDから選択される1つまたは複数のペプチドコネクターを、HSAリンカーのアミノ末端およびカルボキシ末端の各々に含んでもよい。ペプチドコネクターは、コネクター配列の長さを増大または減少させるために、繰り返されてもよいし短縮されてもよい。
q7d(7日毎に1回)投与レジメンを使用したB2B3-1の効果を、ヒト乳癌細胞株BT-474-M3の異種移植腫瘍を有する、Charles River Labsより入手した5〜6週齢の雌性無胸腺ヌードマウス(nu/nu)において測定する(図33)。PBS中のヒトBT-474-M3細胞20×106個を注射する24時間前に、マウスの反対側腹部にエストロゲン放出インプラントを皮下移植する(0.72 mgペレット、60日、遅延放出、Innovative Research of America, Sarasota, FL)。腫瘍増殖(腫瘍容積約400 mm3)が確認されたら投与を開始し、試験全体にわたって30 mg/kgを3日毎に1回(q3d)、あるいは、22 mg/kg、66 mg/kg、132 mg/kg、または198 mg/kgを7日毎に1回、1群あたり10匹のマウスに腹腔内注射によりB2B3-1を投与する。デジタル式キャリパーを用いて、1週間に2回、腫瘍を計測する。腫瘍容積は下記式を用いて算出する:π/6 x (W2 x L)、式中、Wは短径であり、Lは長径である。異種移植腫瘍に対して、66 mg/kgのq7d投与によって与えられるB2B3-1の曝露は、30 mg/kgのq3d投与と類似していることが、薬物動態の算出によって示唆される。PBSビヒクルを陰性対照として用いる。B2B3-1の効果は、B2B3-1の30 mg/kg、q3d投与および高い順に3種類の用量のq7d投与について同等であった。このことは、B2B3-1に関するq7d投与スケジュールが本モデルに適していることを示す。
B2B3-1がヘレグリン誘導性ErbB3活性を阻害する能力を、ウエスタンブロット解析を用いて試験する。血清飢餓させたBT-474-M3細胞の単層を100 nM B2B3-1またはトラスツズマブで24時間処理した後、5 nM HRG 1β EGFで10分間刺激する。細胞は、10nMおよび100 nMのB2B3-1または10nMおよび100 nMのトラスツズマブでも処理し、刺激せずに放置する。溶解物を、ErbB3、pErbB3、AKT、およびpAKTに対する免疫ブロット解析に供する。B2B3-1処理はリガンド依存的様式でpErbB3およびpAKTの阻害をもたらすことがウエスタンブロット解析(図34)によって実証されたが、一方、トラスツズマブによるpErbB3およびpAKTの阻害はリガンド非存在下でしか認められなかった。
4種類の異なる乳癌細胞株を用いて、B2B3-1、トラスツズマブ、および両薬物の組み合わせが癌細胞スフェロイドの増殖に与える効果を調べた。ヒト乳癌細胞BT-474-M3、SKBR3(ATCC)、またはMDA-MB-361(ATCC)2,000個を低接着性の丸底96ウェルプレート(Corning(登録商標) 96 Well Clear Round Bottom Ultra Low Attachment Microplate - Product #7007)に播種し、翌日、スフェロイドを計測して、ある用量範囲のB2B3-1、トラスツズマブ、または、トラスツズマブに対してB2B3-1が3倍モル過剰である両者の組み合わせで処理した。増殖の12日後、スフェロイドの表面積を計測し、処理なしの細胞と比較した。図35A〜Cで認められるように、ある濃度範囲にわたるB2B3-1とトラスツズマブの組み合わせは、最低濃度を除く全ての薬物濃度で試験した全細胞株において、単一の剤を上回るスフェロイド増殖阻害をもたらした。またこれらの結果は、ErbB2(HER2)への結合に関してB2B3-1がトラスツズマブとは競合しないことも示す。
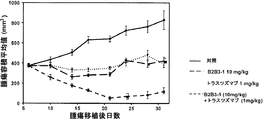
トラスツズマブと同時投与された場合のB2B3-1のインビボにおける効果を、Charles River Labsより入手した5〜6週齢の雌性無胸腺ヌードマウス(nu/nu)において、BT-474-M3異種移植モデルを用いて調べる。PBS中のヒトBT-474-M3細胞20×106個を注射する24時間前に、マウスの反対側腹部にエストロゲン放出インプラントを皮下移植する(0.72 mgペレット、60日、遅延放出、Innovative Research of America, Sarasota, FL)。腫瘍増殖(腫瘍容積約400 mm3)が確認されたら投与を開始する。デジタル式キャリパーを用いて、1週間に2回、腫瘍を計測する。腫瘍容積は下記式を用いて算出する:π/6 x (W2 x L)、式中、Wは短径であり、Lは長径である。1群あたり10匹のマウスに、B2B3-1を3 mg/kgまたは10 mg/kgでq3d投与するか、トラスツズマブを1 mg/kgまたは0.1 mg/kgでq7d投与するか、あるいは両薬物の組み合わせを、試験全体にわたって腹腔内注射により投与する。B2B3-1とトラスツズマブの組み合わせ(10 mg/kg B2B3-1 + 1 mg/kgトラスツズマブ、10 mg/kg B2B3-1 + 0.1 mg/kgトラスツズマブ、3 mg/kg B2B3-1 + 1 mg/kgトラスツズマブ、3 mg/kg B2B3-1 + 0.1 mg/kgトラスツズマブ)は全て、対応する単一の剤と同様に投与する。
本発明をその特定の態様を参酌して記載してきたが、さらなる改変が可能であること、および、概して本発明の原理に従い、かつ本発明が属する技術分野内で公知のまたは慣例の実施に近くかつ本明細書で上述される本質的な特徴に適用され得るような本発明の開示からの逸脱を含む、本発明の任意の改変、用途、または適応を、本出願が包含することを意図していることが理解されるであろう。
Claims (27)
- SEQ ID NO: 16であるアミノ酸配列を含む、ヒト血清アルブミン(HSA)リンカーコンジュゲートB2B3-1。
- 16 nMのKdでErbB3に結合し、かつ0.3 nMのKdでErbB2に結合する、請求項1記載のHSAリンカーコンジュゲート。
- 前記HSAリンカーが、SEQ ID NO: 1に示されるアミノ酸配列を含む、請求項1記載のHSAリンカーコンジュゲート。
- 薬学的に許容される担体、賦形剤、または希釈剤と混合された、請求項1〜3のいずれか一項記載のHSAリンカーコンジュゲート。
- 請求項1〜4のいずれか一項記載のHSAリンカーコンジュゲートを含む医薬。
- シクロホスファミド、カンプトテシン、ホモカンプトテシン、コルヒチン、コンブレタスタチン、リゾキシン、ドリスタチン(dolistatin)、アンサマイトシンp3、メイタンシノイド、アウリスタチン、カリチアマイシン(caleachimicin)、メトトレキサート、5-フルオロウラシル(5-FU)、ドキソルビシン、パクリタキセル、ドセタキセル、シスプラチン、カルボプラチン、タモキシフェン、ラロキシフェン、レトロゾール、エピルビシン、ベバシズマブ、ペルツズマブ、トラスツズマブ、およびこれらの誘導体からなる群より選択される1つまたは複数の治療剤と組み合わせて使用するための、請求項1〜4のいずれか一項記載のHSAリンカーコンジュゲートを含む、組成物。
- 前記治療剤がトラスツズマブである、請求項6記載の組成物。
- 前記HSAリンカーコンジュゲートが、SEQ ID NO: 16であるアミノ酸配列を含むHSAリンカーコンジュゲートB2B3-1である、請求項6記載の組成物。
- ヒト乳房腫瘍細胞を用いたヒト異種移植モデルのヌードマウスにおいて第一の用量の治療剤および第二の用量のHSAリンカーコンジュゲートにより試験した場合に、同一モデルにおいて第一の用量の治療剤のみまたは第二の用量のHSAリンカーコンジュゲートのみにより提供されるよりも大きな効果が該組み合わせによって提供される、請求項8記載の組成物。
- 少なくとも3 mg/kgのB2B3-1および少なくとも0.1 mg/kgのトラスツズマブを提供するように対象に投与することが可能な剤形である、請求項9記載の組成物。
- 3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブを提供するように対象に投与されるのに適合化された剤形である、請求項10記載の組成物。
- 10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブを提供するように対象に投与されるのに適合化された剤形である、請求項10記載の組成物。
- 3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブを提供するように対象に投与された場合に、対応する対象の3 mg/kgのB2B3-1のみまたは0.1 mg/kgのトラスツズマブのみによる処理よりも効果的である、請求項11記載の組成物。
- 10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブを提供するように対象に投与された場合に、対応する対象の10 mg/kgのB2B3-1のみまたは1 mg/kgのトラスツズマブのみによる処理よりも効果的である、請求項12記載の組成物。
- 3 mg/kgのB2B3-1および0.1 mg/kgのトラスツズマブをそれぞれに提供するように複数の対象に投与された場合に、20日後に該対象の10%超において腫瘍の退縮を誘導する、請求項11記載の組成物。
- 10 mg/kgのB2B3-1および1 mg/kgのトラスツズマブをそれぞれに提供するように複数の対象に投与された場合に、20日後に該対象の少なくとも50%において腫瘍の退縮を誘導する、請求項12記載の組成物。
- 前記治療剤がラパチニブである、請求項6記載の組成物。
- 前記治療剤がタキサンである、請求項6記載の組成物。
- タキサンがパクリタキセルまたはドセタキセルである、請求項18記載の組成物。
- 前記治療剤がレトロゾールである、請求項6記載の組成物。
- 疾患または障害を有する患者を治療するための医薬の製造における、請求項1〜4のいずれか一項記載のHSAリンカーコンジュゲートまたは請求項5〜20のいずれか一項記載の組成物の使用。
- 前記疾患または障害が増殖性疾患である、請求項21記載の使用。
- 前記増殖性疾患が、細胞表面レセプターを通じた細胞シグナル伝達に関連する、請求項22記載の使用。
- 前記増殖性疾患が、黒色腫、明細胞肉腫、リンパ腫、頭頸部癌、膀胱癌、乳癌、結腸癌、直腸癌、卵巣癌、子宮内膜癌、胃癌、食道癌、膵臓癌、腎臓癌、前立腺癌、唾液腺癌、肺癌、肝臓癌、皮膚癌、または脳癌である、請求項22記載の使用。
- 前記医薬が、シクロホスファミド、カンプトテシン、ホモカンプトテシン、コルヒチン、コンブレタスタチン、リゾキシン、ドリスタチン(dolistatin)、アンサマイトシンp3、メイタンシノイド、アウリスタチン、カリチアマイシン(caleachimicin)、メトトレキサート、5-フルオロウラシル(5-FU)、ドキソルビシン、パクリタキセル、ドセタキセル、シスプラチン、カルボプラチン、タモキシフェン、ラロキシフェン、レトロゾール、エピルビシン、ベバシズマブ、ペルツズマブ、トラスツズマブ、およびこれらの誘導体からなる群より選択される1つまたは複数の治療剤と組み合わせて投与することによって哺乳類を治療するためのものである、請求項21〜24のいずれか一項記載の使用。
- 前記1つまたは複数の治療剤がトラスツズマブである、請求項25記載の使用。
- 前記哺乳類がヒトである、請求項21〜26のいずれか一項記載の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11579708P | 2008-11-18 | 2008-11-18 | |
| US61/115,797 | 2008-11-18 | ||
| PCT/US2009/040259 WO2009126920A2 (en) | 2008-04-11 | 2009-04-10 | Human serum albumin linkers and conjugates thereof |
| USPCT/US2009/040259 | 2009-04-10 | ||
| PCT/US2009/060721 WO2010059315A1 (en) | 2008-11-18 | 2009-10-14 | Human serum albumin linkers and conjugates thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012509259A JP2012509259A (ja) | 2012-04-19 |
| JP2012509259A5 JP2012509259A5 (ja) | 2013-05-23 |
| JP5677972B2 true JP5677972B2 (ja) | 2015-02-25 |
Family
ID=42198443
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011536365A Expired - Fee Related JP5677972B2 (ja) | 2008-11-18 | 2009-10-14 | ヒト血清アルブミンリンカーおよびそのコンジュゲート |
Country Status (6)
| Country | Link |
|---|---|
| US (4) | US8927694B2 (ja) |
| JP (1) | JP5677972B2 (ja) |
| KR (1) | KR20110112301A (ja) |
| CN (1) | CN102282168A (ja) |
| BR (1) | BRPI0921586A2 (ja) |
| WO (1) | WO2010059315A1 (ja) |
Families Citing this family (134)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7332585B2 (en) | 2002-04-05 | 2008-02-19 | The Regents Of The California University | Bispecific single chain Fv antibody molecules and methods of use thereof |
| US20040067532A1 (en) | 2002-08-12 | 2004-04-08 | Genetastix Corporation | High throughput generation and affinity maturation of humanized antibody |
| US8580263B2 (en) * | 2006-11-21 | 2013-11-12 | The Regents Of The University Of California | Anti-EGFR family antibodies, bispecific anti-EGFR family antibodies and methods of use thereof |
| EP3248617A3 (en) | 2007-02-16 | 2018-02-21 | Merrimack Pharmaceuticals, Inc. | Antibodies against erbb3 and uses thereof |
| US8877688B2 (en) | 2007-09-14 | 2014-11-04 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| EP3753947A1 (en) | 2007-09-14 | 2020-12-23 | Adimab, LLC | Rationally designed, synthetic antibody libraries and uses therefor |
| CN102282168A (zh) * | 2008-11-18 | 2011-12-14 | 梅里麦克制药股份有限公司 | 人血清白蛋白接头以及其结合物 |
| SG2014012918A (en) | 2009-02-11 | 2014-04-28 | Novozymes Biopharma Dk As | Albumin variants and conjugates |
| CA2769619C (en) | 2009-08-17 | 2019-04-30 | Roche Glycart Ag | Targeted immunoconjugates |
| GB2488077A (en) * | 2009-10-30 | 2012-08-15 | Novozymes Biopharma Dk As | Albumin variants |
| CN102781960B (zh) | 2010-02-16 | 2014-12-10 | 米迪缪尼有限公司 | Hsa相关组合物及使用方法 |
| WO2011112953A2 (en) | 2010-03-11 | 2011-09-15 | Merrimack Pharmaceuticals, Inc. | Use of erbb3 inhibitors in the treatment of triple negative and basal-like breast cancers |
| KR20130070576A (ko) | 2010-04-09 | 2013-06-27 | 노보자임스 바이오파마 디케이 에이/에스 | 알부민 유도체 및 변이체 |
| WO2011139681A1 (en) | 2010-04-26 | 2011-11-10 | Merrimack Pharmaceuticals | Assays for anti-drug antibodies in the presence of abundant endogenous protein counterpart of the drug |
| KR20130066631A (ko) | 2010-05-06 | 2013-06-20 | 노파르티스 아게 | 치료적 저밀도 지단백질-관련 단백질 6 (lrp6) 다가 항체에 대한 조성물 및 사용 방법 |
| EP4234698A3 (en) | 2010-05-06 | 2023-11-08 | Novartis AG | Compositions and methods of use for therapeutic low density lipoprotein-related protein 6 (lrp6) antibodies |
| WO2011146902A1 (en) | 2010-05-21 | 2011-11-24 | Merrimack Pharmaceuticals, Inc. | Bi-specific fusion proteins |
| TW201302793A (zh) | 2010-09-03 | 2013-01-16 | Glaxo Group Ltd | 新穎之抗原結合蛋白 |
| DK2635607T3 (da) | 2010-11-05 | 2019-11-18 | Zymeworks Inc | Stabilt heterodimert antistofdesign med mutationer i fc-domænet |
| EP2648738A2 (en) | 2010-12-06 | 2013-10-16 | Merrimack Pharmaceuticals, Inc. | Dosage and administration for preventing cardiotoxicity in treatment with erbb2-targeted immunoliposomes comprising anthracyclin chemotherapeutic agents |
| EP2658872B1 (en) * | 2010-12-27 | 2020-09-30 | Apo-T B.V. | A polypeptide that binds aberrant cells and induces apoptosis |
| US9045564B2 (en) | 2011-02-15 | 2015-06-02 | Medimmune, Llc | HSA-related compositions and methods of use |
| CN103547598A (zh) * | 2011-02-24 | 2014-01-29 | 梅里麦克制药股份有限公司 | 包含抗-erbb3药剂的联合治疗 |
| AU2012222833B2 (en) | 2011-03-03 | 2017-03-16 | Zymeworks Inc. | Multivalent heteromultimer scaffold design and constructs |
| CA2828075A1 (en) * | 2011-03-11 | 2012-09-20 | Merrimack Pharmaceuticals, Inc. | Use of inhibitors of egfr-family receptors in the treatment of hormone refractory breast cancers |
| US20150231238A1 (en) * | 2011-03-15 | 2015-08-20 | Merrimack Pharmaceuticals, Inc. | Overcoming resistance to erbb pathway inhibitors |
| GB2491006A (en) | 2011-05-05 | 2012-11-21 | Novozymes Biopharma Uk Ltd | Albumin variants |
| EP2760892A1 (en) | 2011-09-29 | 2014-08-06 | Apo-T B.V. | Multi-specific binding molecules targeting aberrant cells |
| CN109897103A (zh) | 2011-11-04 | 2019-06-18 | 酵活有限公司 | 在Fc结构域中具有突变的稳定异源二聚的抗体设计 |
| WO2013067355A1 (en) * | 2011-11-04 | 2013-05-10 | Novartis Ag | Low density lipoprotein-related protein 6 (lrp6) - half life extender constructs |
| WO2013075066A2 (en) | 2011-11-18 | 2013-05-23 | Eleven Biotherapeutics, Inc. | Proteins with improved half-life and other properties |
| WO2013096939A1 (en) * | 2011-12-23 | 2013-06-27 | Sri International | Selective binding compounds |
| US20130165628A1 (en) * | 2011-12-23 | 2013-06-27 | Sri International | Double Binding Constructs |
| EP3470434A1 (en) | 2012-01-13 | 2019-04-17 | Apo-T B.V. | Aberrant cell-restricted immunoglobulins provided with a toxic moiety |
| US9944691B2 (en) | 2012-03-16 | 2018-04-17 | Albumedix A/S | Albumin variants |
| AU2013259053A1 (en) * | 2012-05-11 | 2015-01-15 | Merrimack Pharmaceuticals, Inc. | Dosage and administration of bispecific scFv conjugates in combination with anti-cancer therapeutics |
| AU2013202947B2 (en) | 2012-06-13 | 2016-06-02 | Ipsen Biopharm Ltd. | Methods for treating pancreatic cancer using combination therapies comprising liposomal irinotecan |
| US9717724B2 (en) | 2012-06-13 | 2017-08-01 | Ipsen Biopharm Ltd. | Methods for treating pancreatic cancer using combination therapies |
| US9499634B2 (en) | 2012-06-25 | 2016-11-22 | Zymeworks Inc. | Process and methods for efficient manufacturing of highly pure asymmetric antibodies in mammalian cells |
| WO2014012082A2 (en) | 2012-07-13 | 2014-01-16 | Zymeworks Inc. | Multivalent heteromultimer scaffold design an constructs |
| US20150202287A1 (en) | 2012-08-30 | 2015-07-23 | Merrimack Pharmaceuticals, Inc. | Combination therapies comprising anti-erbb3 agents |
| BR112015010318A2 (pt) | 2012-11-08 | 2017-08-22 | Albumedix As | Variantes de albumina |
| US9914785B2 (en) | 2012-11-28 | 2018-03-13 | Zymeworks Inc. | Engineered immunoglobulin heavy chain-light chain pairs and uses thereof |
| KR20150091116A (ko) | 2012-12-03 | 2015-08-07 | 메리맥 파마슈티컬즈, 인크. | Her2-양성 암을 치료하기 위한 병용요법 |
| WO2014098464A1 (ko) * | 2012-12-18 | 2014-06-26 | 이화여자대학교 산학협력단 | 인간혈청알부민 열안정화용 조성물 및 이를 이용한 열안정화된 인간혈청알부민의 제조방법 |
| WO2014121033A1 (en) * | 2013-02-04 | 2014-08-07 | Fl Therapeutics Llc | Soluble complexes of drug analogs and albumin |
| JP2016519108A (ja) | 2013-04-18 | 2016-06-30 | アルモ・バイオサイエンシーズ・インコーポレイテッド | インターロイキン−10を疾病及び疾患の治療に用いる方法 |
| CA2910945A1 (en) | 2013-05-08 | 2014-11-13 | Zymeworks Inc. | Bispecific her2 and her3 antigen binding constructs |
| MA38571B1 (fr) | 2013-05-13 | 2018-10-31 | Vision Global Holdings Ltd | Composition pharmaceutique comprenant un agent thérapeutique à base d'hémoglobine modifiée pour un traitement de ciblage du cancer et imagerie diagnostique |
| WO2014186905A1 (en) * | 2013-05-24 | 2014-11-27 | Zymeworks Inc. | Modular protein drug conjugate therapeutic |
| JP2016528879A (ja) | 2013-06-17 | 2016-09-23 | アルモ・バイオサイエンシーズ・インコーポレイテッド | タンパク質の同一性および安定性を評価する方法 |
| JP6509867B2 (ja) | 2013-08-30 | 2019-05-08 | アルモ・バイオサイエンシーズ・インコーポレイテッド | 疾患及び障害を治療するためにインターロイキン−10を使用する方法 |
| JP2016540993A (ja) * | 2013-09-30 | 2016-12-28 | 第一三共株式会社 | タンパク質生体マーカー及びその使用 |
| RU2016122957A (ru) | 2013-11-11 | 2017-12-19 | Армо Байосайенсиз, Инк. | Способы применения интерлейкина-10 для лечения заболеваний и расстройств |
| SG11201605215YA (en) | 2013-12-25 | 2016-08-30 | Daiichi Sankyo Co Ltd | Anti-trop2 antibody-drug conjugate |
| EP3087394A2 (en) | 2013-12-27 | 2016-11-02 | Merrimack Pharmaceuticals, Inc. | Biomarker profiles for predicting outcomes of cancer therapy with erbb3 inhibitors and/or chemotherapies |
| US10487140B2 (en) | 2014-01-14 | 2019-11-26 | Integrated Biotherapeutics, Inc. | Targeting immunological functions to the site of bacterial infections using cell wall targeting domains of bacteriolysins |
| WO2015115091A1 (ja) | 2014-01-31 | 2015-08-06 | 第一三共株式会社 | 抗her2抗体-薬物コンジュゲート |
| EP3470435B1 (en) | 2014-02-28 | 2020-08-05 | Merus N.V. | Antibody that binds erbb-2 and erbb-3 |
| SG11201607109QA (en) | 2014-02-28 | 2016-09-29 | Merus Nv | Antibodies that bind egfr and erbb3 |
| AU2015244814B2 (en) * | 2014-04-07 | 2020-12-24 | Chugai Seiyaku Kabushiki Kaisha | Immunoactivating antigen-binding molecule |
| JP6612738B2 (ja) | 2014-04-10 | 2019-11-27 | 第一三共株式会社 | 抗her2抗体−薬物コンジュゲート |
| US11473080B2 (en) * | 2014-04-30 | 2022-10-18 | The Board Of Trustees Of The University Of Illinois | Method for generating high affinity, bivalent binding agents for sandwich assays |
| AU2015260230A1 (en) | 2014-05-13 | 2016-11-17 | Chugai Seiyaku Kabushiki Kaisha | T cell-redirected antigen-binding molecule for cells having immunosuppression function |
| BR112016025056A2 (pt) * | 2014-05-14 | 2018-02-20 | F. Hoffmann-La Roche Ag | uso de pelo menos um polipeptídeo, anticorpo biespecífico, anticorpo biespecífico isolado, anticorpo her3/her2 biespecífico, célula hospedeira, método de produção do anticorpo biespecífico her3/her2, imunoconjugado e formulação farmacêutica |
| US9937259B2 (en) | 2014-06-27 | 2018-04-10 | Zhuhai Beihai Biotech Co., Ltd. | Abiraterone derivatives and non-covalent complexes with albumin |
| WO2016022723A1 (en) | 2014-08-05 | 2016-02-11 | Merrimack Pharmaceuticals, Inc. | Combination therapies for treating her2-positive cancers that are resistant to her2-targeted therapies |
| GB201417067D0 (en) * | 2014-09-26 | 2014-11-12 | South African Nuclear Energy | Radiopharmaceutical conjugate |
| EP3223858A4 (en) * | 2014-10-31 | 2018-07-11 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Tlr9 targeted cytotoxic agents |
| US11318131B2 (en) | 2015-05-18 | 2022-05-03 | Ipsen Biopharm Ltd. | Nanoliposomal irinotecan for use in treating small cell lung cancer |
| JP7121496B2 (ja) | 2015-05-28 | 2022-08-18 | アルモ・バイオサイエンシーズ・インコーポレイテッド | 癌治療で使用するためのペグ化インターロイキン-10 |
| US10184006B2 (en) | 2015-06-04 | 2019-01-22 | Merrimack Pharmaceuticals, Inc. | Biomarkers for predicting outcomes of cancer therapy with ErbB3 inhibitors |
| AU2016286898B2 (en) | 2015-06-29 | 2022-12-08 | Daiichi Sankyo Company, Limited | Method for selectively manufacturing antibody-drug conjugate |
| IL310467A (en) | 2015-07-15 | 2024-03-01 | Genmab As | Human CD3 antibodies or chimeras |
| CA2987322C (en) * | 2015-08-11 | 2020-02-11 | Coherent Biopharma | Multi-ligand drug conjugates and uses thereof |
| SI3337467T1 (sl) | 2015-08-20 | 2021-03-31 | Ipsen Biopharm Ltd. Ash Road | Kombinacijska terapija, ki vsebuje liposomski irinotekan in zaviralec PARP za zdravljenje raka |
| JP7007261B2 (ja) | 2015-08-20 | 2022-01-24 | アルブミディクス リミティド | アルブミン変異体及びコンジュゲート |
| EP3791876A1 (en) | 2015-08-21 | 2021-03-17 | Ipsen Biopharm Ltd. | Methods for treating metastatic pancreatic cancer using combination therapies comprising liposomal irinotecan and oxaliplatin |
| CN108025040A (zh) | 2015-08-25 | 2018-05-11 | 阿尔莫生物科技股份有限公司 | 使用白介素-10治疗疾病和病症的方法 |
| CA2999756A1 (en) * | 2015-09-24 | 2017-03-30 | The University Of North Carolina At Chapel Hill | Methods and compositions for reducing metastases |
| US10040840B2 (en) * | 2015-10-02 | 2018-08-07 | Silver Creek Pharmaceuticals, Inc. | Bi-specific annexin A5/IGF-1 proteins and methods of use thereof to promote regeneration and survival of tissue |
| CN108366965B (zh) | 2015-10-16 | 2021-10-01 | 易普森生物制药有限公司 | 稳定喜树碱药物组合物 |
| ES2865482T3 (es) | 2015-10-23 | 2021-10-15 | Merus Nv | Moléculas de unión que inhiben el crecimiento del cáncer |
| JP6931329B2 (ja) | 2015-11-18 | 2021-09-01 | 中外製薬株式会社 | 免疫抑制機能を有する細胞に対するt細胞リダイレクト抗原結合分子を用いた併用療法 |
| US11649293B2 (en) | 2015-11-18 | 2023-05-16 | Chugai Seiyaku Kabushiki Kaisha | Method for enhancing humoral immune response |
| KR101746152B1 (ko) | 2015-12-07 | 2017-06-13 | 주식회사 이수앱지스 | ErbB3에 특이적으로 결합하는 항체 및 그의 용도 |
| BR112018012851A2 (pt) | 2015-12-22 | 2018-12-26 | Albumedix Ltd | cepas de expressão de proteína melhoradas |
| EP3430034A1 (en) | 2016-03-16 | 2019-01-23 | Merrimack Pharmaceuticals, Inc. | Engineered trail for cancer therapy |
| SG11201811431VA (en) | 2016-07-14 | 2019-01-30 | Genmab As | Multispecific antibodies against cd40 and cd137 |
| MX2019004783A (es) | 2016-11-02 | 2019-08-12 | Ipsen Biopharm Ltd | Tratamiento de cancer gastrico usando terapias de combinacion que comprenden irinotecan liposomico oxaliplatino, 5-fluoruracilo (y leucovorina). |
| JP2020500306A (ja) | 2016-11-04 | 2020-01-09 | オーフス ウニベルシテット | 新生児Fc受容体の過剰発現により特徴づけられる腫瘍の同定と治療 |
| TW201828993A (zh) | 2016-12-12 | 2018-08-16 | 日商第一三共股份有限公司 | 抗體-藥物結合物與免疫檢查點抑制劑之組合 |
| KR102537651B1 (ko) | 2017-01-17 | 2023-05-26 | 다이이찌 산쿄 가부시키가이샤 | 항 gpr20 항체 및 항 gpr20 항체-약물 콘쥬게이트 |
| US20200239579A1 (en) | 2017-03-09 | 2020-07-30 | Genmab A/S | Antibodies against pd-l1 |
| MX2019011660A (es) | 2017-03-31 | 2019-11-18 | Merus Nv | Anticuerpos biespecificos que se unen al receptor 2 del factor de crecimiento humano (erbb-2) y receptor 3 del factor de crecimiento humano (erbb3) para usarse en el tratamiento de celulas que tienen un gen de fusion de neuregulina-1 (nrg1). |
| TW202330036A (zh) | 2017-05-15 | 2023-08-01 | 日商第一三共股份有限公司 | 抗體-藥物結合物之製造方法 |
| JP7282693B2 (ja) | 2017-06-20 | 2023-05-29 | アルブミディクス リミティド | 改良されたタンパク質発現株 |
| AU2018309339A1 (en) | 2017-08-04 | 2020-02-20 | BioNTech SE | Binding agents binding to PD-L1 and CD137 and use thereof |
| MX2020001432A (es) | 2017-08-09 | 2020-03-20 | Merus Nv | Anticuerpos que se unen al receptor del factor de crecimiento epidermico (egfr) y tirosina-proteina cinasa met (cmet). |
| CN117838881A (zh) | 2017-08-31 | 2024-04-09 | 第一三共株式会社 | 制备抗体-药物缀合物的新方法 |
| KR20200041993A (ko) | 2017-08-31 | 2020-04-22 | 다이이찌 산쿄 가부시키가이샤 | 항체-약물 콘주게이트의 개량 제조 방법 |
| WO2019096226A1 (en) * | 2017-11-16 | 2019-05-23 | Chengdu Easton Biopharmaceuticals Co., Ltd. | Pasylated vegfr/pdgfr fusion proteins and their use in therapy |
| CN117815404A (zh) | 2018-05-18 | 2024-04-05 | 第一三共株式会社 | 抗-muc1抗体-药物缀合物 |
| CA3113605A1 (en) | 2018-09-19 | 2020-03-26 | Lava Therapeutics B.V. | Novel bispecific antibodies for use in the treatment of hematological malignancies |
| KR20210124959A (ko) | 2018-11-06 | 2021-10-15 | 젠맵 에이/에스 | 항체 제제 |
| CN109627337B (zh) * | 2018-12-29 | 2023-07-21 | 上海复宏汉霖生物技术股份有限公司 | 一种抗prlr的单克隆抗体及其制备方法和应用 |
| CN113993893A (zh) | 2019-02-01 | 2022-01-28 | 拉法医疗有限公司 | 新cd40结合抗体 |
| NL2022494B1 (en) | 2019-02-01 | 2020-08-19 | Lava Therapeutics B V | Novel CD40-binding antibodies |
| EP3946631A1 (en) * | 2019-03-26 | 2022-02-09 | Shimadzu Corporation | Photoimmunotherapy and pharmaceutical agent used therefor |
| EP3792283A1 (en) | 2019-09-16 | 2021-03-17 | Lava Therapeutics B.V. | Treatment of cancer comprising administration of vgamma9vdelta2 t cell receptor binding antibodies |
| EP4069200A1 (en) | 2019-12-04 | 2022-10-12 | Albumedix Ltd | Methods and compositions produced thereby |
| WO2021155916A1 (en) | 2020-02-04 | 2021-08-12 | BioNTech SE | Treatment involving antigen vaccination and binding agents binding to pd-l1 and cd137 |
| ES2934984T3 (es) * | 2020-02-13 | 2023-02-28 | Orano Med | Procedimiento para la modificación específica del sitio de un anticuerpo |
| BR112022015572A2 (pt) | 2020-03-18 | 2022-09-27 | Genmab As | Anticorpo, composição, composição farmacêutica, anticorpo para uso como um medicamento, métodos para tratar uma doença e para produzir um anticorpo, ácido nucléico, um ou mais ácidos nucléicos, célula, e, kit de partes |
| WO2021205184A1 (en) | 2020-04-09 | 2021-10-14 | Autolus Limited | Polypeptide |
| GB202007441D0 (en) | 2020-05-19 | 2020-07-01 | Autolus Ltd | Polypeptide |
| KR20230042035A (ko) | 2020-07-08 | 2023-03-27 | 라바 테라퓨틱스 엔.브이. | Psma와 감마-델타 t 세포 수용체에 결합할 수 있는 항체 |
| CA3187061A1 (en) | 2020-08-06 | 2022-02-10 | Karsten Beckmann | Binding agents for coronavirus s protein |
| BR112023004321A2 (pt) | 2020-09-10 | 2023-04-04 | Genmab As | Método para tratar linfoma de célula b grande difusa em um sujeito humano |
| JP2023541858A (ja) | 2020-09-10 | 2023-10-04 | ジェンマブ エー/エス | 慢性リンパ球性白血病を治療するためのcd3及びcd20に対する二重特異性抗体 |
| AU2021377232A1 (en) * | 2020-11-10 | 2023-06-15 | New York University | Macropinocytosis selective monobody-drug conjugates |
| KR20230157933A (ko) | 2020-12-10 | 2023-11-17 | 라바 테라퓨틱스 엔.브이. | 감마-델타 t 세포 수용체에 결합하는 항체 |
| EP4263600A1 (en) | 2020-12-18 | 2023-10-25 | Century Therapeutics, Inc. | Chimeric antigen receptor systems with adaptable receptor specificity |
| EP4298125A1 (en) | 2021-02-26 | 2024-01-03 | LAVA Therapeutics N.V. | Antibodies that bind cd123 and gamma-delta t cell receptors |
| CN117396509A (zh) | 2021-05-07 | 2024-01-12 | 健玛保 | 包含结合b7h4和cd3的双特异性抗体的药物组合物 |
| BR112023027006A2 (pt) | 2021-06-21 | 2024-03-12 | BioNTech SE | Método para reduzir ou prevenir a progressão de um tumor ou tratar um câncer em um sujeito, e, agente de ligação |
| CA3229822A1 (en) | 2021-09-13 | 2023-03-16 | Patrick John DOONAN | Cd33 x v?2 multispecific antibodies for the treatment of cancer |
| AU2022361691A1 (en) | 2021-10-08 | 2024-03-28 | Genmab A/S | Antibodies binding to cd30 and cd3 |
| WO2023067138A1 (en) | 2021-10-21 | 2023-04-27 | LAVA Therapeutics N.V. | Uses of gamma delta t cell activating antibodies |
| WO2023174521A1 (en) | 2022-03-15 | 2023-09-21 | Genmab A/S | Binding agents binding to epcam and cd137 |
| EP4285926A1 (en) | 2022-05-30 | 2023-12-06 | LAVA Therapeutics N.V. | Combination treatment for chronic lymphocytic leukemia |
| EP4292610A1 (en) | 2022-06-15 | 2023-12-20 | LAVA Therapeutics N.V. | Variant antibodies that bind gamma-delta t cell receptors |
| EP4292609A1 (en) | 2022-06-15 | 2023-12-20 | LAVA Therapeutics N.V. | Compositions comprising antibodies that bind gamma-delta t cell receptors |
| NL2032398B1 (en) | 2022-07-06 | 2024-01-23 | Academisch Ziekenhuis Leiden | Bispecific antibody and uses thereof |
Family Cites Families (148)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6009A (en) * | 1849-01-09 | Improvement in machines for gathering pea-vines | ||
| US5800815A (en) | 1903-05-05 | 1998-09-01 | Cytel Corporation | Antibodies to P-selectin and their uses |
| US4450103A (en) | 1982-03-01 | 1984-05-22 | Cetus Corporation | Process for recovering human IFN-β from a transformed microorganism |
| US4588585A (en) | 1982-10-19 | 1986-05-13 | Cetus Corporation | Human recombinant cysteine depleted interferon-β muteins |
| US4737462A (en) | 1982-10-19 | 1988-04-12 | Cetus Corporation | Structural genes, plasmids and transformed cells for producing cysteine depleted muteins of interferon-β |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4959314A (en) | 1984-11-09 | 1990-09-25 | Cetus Corporation | Cysteine-depleted muteins of biologically active proteins |
| US5168062A (en) | 1985-01-30 | 1992-12-01 | University Of Iowa Research Foundation | Transfer vectors and microorganisms containing human cytomegalovirus immediate-early promoter-regulatory DNA sequence |
| US5260203A (en) | 1986-09-02 | 1993-11-09 | Enzon, Inc. | Single polypeptide chain binding molecules |
| US6121424A (en) | 1991-11-25 | 2000-09-19 | Enzon, Inc. | Multivalent antigen-binding proteins |
| ATE87659T1 (de) | 1986-09-02 | 1993-04-15 | Enzon Lab Inc | Bindungsmolekuele mit einzelpolypeptidkette. |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| US5869620A (en) | 1986-09-02 | 1999-02-09 | Enzon, Inc. | Multivalent antigen-binding proteins |
| US4704692A (en) | 1986-09-02 | 1987-11-03 | Ladner Robert C | Computer based system and method for determining and displaying possible chemical structures for converting double- or multiple-chain polypeptides to single-chain polypeptides |
| DE3856559T2 (de) | 1987-05-21 | 2004-04-29 | Micromet Ag | Multifunktionelle Proteine mit vorbestimmter Zielsetzung |
| US5258498A (en) | 1987-05-21 | 1993-11-02 | Creative Biomolecules, Inc. | Polypeptide linkers for production of biosynthetic proteins |
| US5132405A (en) | 1987-05-21 | 1992-07-21 | Creative Biomolecules, Inc. | Biosynthetic antibody binding sites |
| US5091513A (en) | 1987-05-21 | 1992-02-25 | Creative Biomolecules, Inc. | Biosynthetic antibody binding sites |
| US5753627A (en) | 1988-12-05 | 1998-05-19 | Novartis Ag | Use of certain complexed somatostatin peptides for the invivo imaging of somatostatin receptor-positive tumors and metastasis |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5705363A (en) | 1989-03-02 | 1998-01-06 | The Women's Research Institute | Recombinant production of human interferon τ polypeptides and nucleic acids |
| US5766883A (en) | 1989-04-29 | 1998-06-16 | Delta Biotechnology Limited | Polypeptides |
| ATE92107T1 (de) | 1989-04-29 | 1993-08-15 | Delta Biotechnology Ltd | N-terminale fragmente von menschliches serumalbumin enthaltenden fusionsproteinen. |
| FR2650598B1 (fr) | 1989-08-03 | 1994-06-03 | Rhone Poulenc Sante | Derives de l'albumine a fonction therapeutique |
| US5730978A (en) | 1989-09-01 | 1998-03-24 | Fred Hutchinson Cancer Research Center | Inhibition of lymphocyte adherence with α4β1-specific antibodies |
| US6033665A (en) | 1989-09-27 | 2000-03-07 | Elan Pharmaceuticals, Inc. | Compositions and methods for modulating leukocyte adhesion to brain endothelial cells |
| US5292658A (en) | 1989-12-29 | 1994-03-08 | University Of Georgia Research Foundation, Inc. Boyd Graduate Studies Research Center | Cloning and expressions of Renilla luciferase |
| DE69233068T2 (de) | 1991-02-27 | 2004-01-22 | Micromet Ag | Serin-reiche peptidlinker |
| US5525491A (en) | 1991-02-27 | 1996-06-11 | Creative Biomolecules, Inc. | Serine-rich peptide linkers |
| CA2122732C (en) | 1991-11-25 | 2008-04-08 | Marc D. Whitlow | Multivalent antigen-binding proteins |
| FR2686620B1 (fr) | 1992-01-27 | 1995-06-23 | Rhone Poulenc Rorer Sa | Serum-albumine humaine, preparation et utilisation. |
| FR2686899B1 (fr) | 1992-01-31 | 1995-09-01 | Rhone Poulenc Rorer Sa | Nouveaux polypeptides biologiquement actifs, leur preparation et compositions pharmaceutiques les contenant. |
| ATE503496T1 (de) | 1992-02-06 | 2011-04-15 | Novartis Vaccines & Diagnostic | Biosynthetisches bindeprotein für tumormarker |
| WO1994012520A1 (en) | 1992-11-20 | 1994-06-09 | Enzon, Inc. | Linker for linked fusion polypeptides |
| NZ261259A (en) | 1993-01-12 | 1996-12-20 | Biogen Inc | Humanised recombinant anti-vla4 antibody and diagnostic compositions and medicaments |
| CN1074243A (zh) | 1993-02-06 | 1993-07-14 | 北京中化生物技术研究所 | 白介素6-白介素2融合蛋白及其制法和用途 |
| US5780594A (en) | 1993-03-01 | 1998-07-14 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Biologically active protein fragments containing specific binding regions of serum albumin or related proteins |
| US5928904A (en) | 1993-09-07 | 1999-07-27 | Smithkline Beecham Corporation | DNA encoding recombinant IL4 antibodies useful in treatment of IL4 mediated disorders |
| US5914110A (en) | 1993-09-07 | 1999-06-22 | Smithkline Beecham Corporation | Recombinant IL4 antibodies useful in treatment of IL4 mediated disorders |
| US5631158A (en) | 1993-10-25 | 1997-05-20 | Creative Biomolecules, Inc. | Methods and compositions for high protein production from non-native DNA |
| US5936065A (en) | 1993-12-06 | 1999-08-10 | Cytel Corporation | CS-1 peptidomimetics, compositions and methods of using the same |
| US5821231A (en) | 1993-12-06 | 1998-10-13 | Cytel Corporation | CS-1 peptidomimetics, compositions and methods of using same |
| US5840299A (en) | 1994-01-25 | 1998-11-24 | Athena Neurosciences, Inc. | Humanized antibodies against leukocyte adhesion molecule VLA-4 |
| US8715645B2 (en) | 1994-05-27 | 2014-05-06 | The Regents Of The University Of Colorado | Viral vectors encoding apoptosis-inducing proteins and methods for making and using the same |
| US5622701A (en) | 1994-06-14 | 1997-04-22 | Protein Design Labs, Inc. | Cross-reacting monoclonal antibodies specific for E- and P-selectin |
| US5811391A (en) | 1994-08-25 | 1998-09-22 | Cytel Corporation | Cyclic CS-1 peptidomimetics, compositions and methods of using same |
| US5874540A (en) | 1994-10-05 | 1999-02-23 | Immunomedics, Inc. | CDR-grafted type III anti-CEA humanized mouse monoclonal antibodies |
| US5763733A (en) | 1994-10-13 | 1998-06-09 | Enzon, Inc. | Antigen-binding fusion proteins |
| US5670356A (en) | 1994-12-12 | 1997-09-23 | Promega Corporation | Modified luciferase |
| US6306840B1 (en) | 1995-01-23 | 2001-10-23 | Biogen, Inc. | Cell adhesion inhibitors |
| US5656730A (en) | 1995-04-07 | 1997-08-12 | Enzon, Inc. | Stabilized monomeric protein compositions |
| AU6113396A (en) | 1995-06-14 | 1997-01-15 | Regents Of The University Of California, The | Novel high affinity human antibodies to tumor antigens |
| GB9526733D0 (en) | 1995-12-30 | 1996-02-28 | Delta Biotechnology Ltd | Fusion proteins |
| US5968511A (en) * | 1996-03-27 | 1999-10-19 | Genentech, Inc. | ErbB3 antibodies |
| US6686350B1 (en) | 1996-07-25 | 2004-02-03 | Biogen, Inc. | Cell adhesion inhibitors |
| US6423512B1 (en) | 1996-07-26 | 2002-07-23 | Novartis Ag | Fusion polypeptides |
| PE99498A1 (es) | 1996-07-26 | 1999-01-21 | Novartis Ag | Polipeptidos de fusion |
| CA2288992C (en) | 1997-04-30 | 2012-06-12 | Enzon, Inc. | Single-chain antigen-binding proteins capable of glycosylation, production and uses thereof |
| US6191269B1 (en) | 1997-05-30 | 2001-02-20 | The Regents Of The University Of California | Selective induction of cell death by delivery of amino-terminal interleukin-1-α pro-piece polypeptide |
| AU8163398A (en) | 1997-06-23 | 1999-01-04 | Pharmacia & Upjohn Company | Inhibitors of alpha4beta1mediated cell adhesion |
| US6229011B1 (en) | 1997-08-22 | 2001-05-08 | Hoffman-La Roche Inc. | N-aroylphenylalanine derivative VCAM-1 inhibitors |
| US6455550B1 (en) | 1997-08-22 | 2002-09-24 | Hoffmann-La Roche Inc. | N-alkanoylphenylalanine derivatives |
| US6197794B1 (en) | 1998-01-08 | 2001-03-06 | Celltech Therapeutics Limited | Phenylalanine derivatives |
| US6329372B1 (en) | 1998-01-27 | 2001-12-11 | Celltech Therapeutics Limited | Phenylalanine derivatives |
| US6171809B1 (en) | 1998-01-29 | 2001-01-09 | Packard Instrument Company | Method and compositions for detecting luciferase biological samples |
| CA2325346A1 (en) | 1998-04-03 | 1999-10-14 | Chugai Seiyaku Kabushiki Kaisha | Humanized antibody against human tissue factor (tf) and process for constructing humanized antibody |
| GB9811159D0 (en) | 1998-05-22 | 1998-07-22 | Celltech Therapeutics Ltd | Chemical compounds |
| EA002988B1 (ru) | 1998-05-28 | 2002-12-26 | Байоджен, Инк. | (r)-n-[[4-[[(2-метилфениламино)карбонил]амино]фенил]ацетил]-l-пропил-3- метил- бета-аланин и его применение в качестве ингибитора клеточной адгезии, опосредуемой интегрином альфа4бета1 |
| GB9812088D0 (en) | 1998-06-05 | 1998-08-05 | Celltech Therapeutics Ltd | Chemical compounds |
| US6685617B1 (en) | 1998-06-23 | 2004-02-03 | Pharmacia & Upjohn Company | Inhibitors of α4β1 mediated cell adhesion |
| US6355678B1 (en) | 1998-06-29 | 2002-03-12 | Parker Hughes Institute | Inhibitors of the EGF-receptor tyrosine kinase and methods for their use |
| GB9821061D0 (en) | 1998-09-28 | 1998-11-18 | Celltech Therapeutics Ltd | Chemical compounds |
| DK1656952T3 (da) | 1998-10-16 | 2014-01-20 | Biogen Idec Inc | Polyalkylenglycolkonjugater af interferon beta-1A og anvendelser deraf |
| US6333396B1 (en) | 1998-10-20 | 2001-12-25 | Enzon, Inc. | Method for targeted delivery of nucleic acids |
| JP3180906B2 (ja) | 1998-11-12 | 2001-07-03 | 日本電気株式会社 | 磁気抵抗効果型複合ヘッドの製造方法 |
| EP1154993B1 (en) | 1999-02-18 | 2004-10-06 | F. Hoffmann-La Roche Ag | Thioamide derivatives |
| US8236159B2 (en) * | 1999-04-13 | 2012-08-07 | Applied Materials Inc. | Electrolytic process using cation permeable barrier |
| US6265572B1 (en) | 1999-04-20 | 2001-07-24 | Hoffmann-La Roche Inc. | Pyrrolidincarbonylamino cyclic disulfide anti-inflammatory agents |
| US7534866B2 (en) | 2005-10-19 | 2009-05-19 | Ibc Pharmaceuticals, Inc. | Methods and compositions for generating bioactive assemblies of increased complexity and uses |
| US6579857B1 (en) * | 1999-06-11 | 2003-06-17 | Evanston Northwestern Healthcare Research Institute | Combination cancer therapy comprising adenosine and deaminase enzyme inhibitors |
| US6756378B2 (en) | 1999-06-30 | 2004-06-29 | Pharmacopeia Drug Discovery, Inc. | VLA-4 inhibitor compounds |
| US7067313B1 (en) | 1999-07-14 | 2006-06-27 | D. Collen Research Foundation | Ligands for use in therapeutic compositions for the treatment of hemostasis disorders |
| US6365619B1 (en) | 1999-07-22 | 2002-04-02 | Novartis Ag | Treatment of arteriosclerosis |
| SK287075B6 (sk) | 1999-08-13 | 2009-11-05 | Biogen Idec Ma Inc. | Inhibítory bunkovej adhézie a farmaceutické prostriedky, ktoré ich obsahujú |
| US6531122B1 (en) | 1999-08-27 | 2003-03-11 | Maxygen Aps | Interferon-β variants and conjugates |
| EP1094110A1 (en) | 1999-10-21 | 2001-04-25 | Leadd B.V. | Apoptosis inducing proteinaceous substance |
| AU1416501A (en) | 1999-11-18 | 2001-05-30 | Ajinomoto Co., Inc. | Novel phenylalanine derivatives |
| US6380387B1 (en) | 1999-12-06 | 2002-04-30 | Hoffmann-La Roche Inc. | 4-Pyrimidinyl-n-acyl-l phenylalanines |
| US6388084B1 (en) | 1999-12-06 | 2002-05-14 | Hoffmann-La Roche Inc. | 4-pyridinyl-n-acyl-l-phenylalanines |
| DE19962936A1 (de) | 1999-12-24 | 2001-06-28 | Bayer Ag | Neue beta-Aminosäureverbindungen als Integrinantagonisten |
| OA12126A (en) | 1999-12-28 | 2006-05-05 | Pfizer Prod Inc | Non-peptidyl inhibitors of VLA-4 dependent cell binding useful in treating inflammatory, autoimmune,and respiratory diseases. |
| US7446174B2 (en) | 2001-03-02 | 2008-11-04 | Xencor, Inc. | Protein based TNF-α variants for the treatment of TNF-α related disorders |
| WO2001070670A1 (fr) | 2000-03-23 | 2001-09-27 | Ajinomoto Co., Inc. | Nouveau derive de phenylalanine |
| US6946134B1 (en) | 2000-04-12 | 2005-09-20 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| CA2747325A1 (en) | 2000-04-12 | 2001-10-25 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| US20050100991A1 (en) | 2001-04-12 | 2005-05-12 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| DE60118362T2 (de) | 2000-05-19 | 2007-05-24 | The Center for Blood Research, Inc., Boston | VERFAHREN ZUR BEHANDLUNG VON HÄMOSTATISCHEN STÖRUNGEN DURCH LöSLICHES P-SELECTIN |
| GB0027328D0 (en) | 2000-06-23 | 2000-12-27 | Aventis Pharma Inc | Bioengineered vehicles for targeted nucleic acid delivery |
| US6787636B1 (en) | 2000-07-14 | 2004-09-07 | New Century Pharmaceuticals, Inc. | Modified serum albumin with reduced affinity for nickel and copper |
| US20040247565A1 (en) | 2000-07-19 | 2004-12-09 | Chih-Ping Liu | Method of treatment using interferon-tau |
| AU2001278986A1 (en) | 2000-07-21 | 2002-02-05 | Elan Pharmaceuticals, Inc. | 3-amino-2-(4-aminocarbonyloxy)phenyl-propionic acid derivatives as alpha-4- integrin inhibitors |
| US7015216B2 (en) | 2000-07-21 | 2006-03-21 | Elan Pharmaceuticals, Inc. | Heteroaryl-β-alanine derivatives as alpha 4 integrin inhibitors |
| MXPA03001495A (es) | 2000-08-18 | 2003-06-06 | Ajinomoto Kk | Derivados de fenilalanina novedosos. |
| AU2001286242A1 (en) | 2000-09-14 | 2002-03-26 | Toray Industries, Inc | Urea derivative and adhesive-molecule inhibitor containing the same as active ingredient |
| CA2423007C (en) | 2000-09-25 | 2010-06-01 | Toray Industries, Inc. | Spiro derivatives and adhesion molecule inhibitors containing the same as effective ingredients |
| US6818216B2 (en) | 2000-11-28 | 2004-11-16 | Medimmune, Inc. | Anti-RSV antibodies |
| NZ540232A (en) | 2001-02-22 | 2007-06-29 | Celltech R&D Ltd | Phenylalanine enamide derivatives possessing a cyclobutene group, for use as integrin inhibitors |
| ES2180416B1 (es) | 2001-03-12 | 2004-06-01 | BIOTOOLS BIOTECHNOLOGICAL & MEDICAL LABORATORIES, S.A. | Procedimiento para la preparacion de mezclas de reaccion estabilizadas, total o parcialmente desecadas, que comprenden, al menos, una enzima, mezclas de reaccion y kits que las contienen. |
| WO2003007889A2 (en) | 2001-07-17 | 2003-01-30 | Research Development Foundation | Therapeutic agents comprising pro-apoptotic proteins |
| JP4164871B2 (ja) | 2001-07-26 | 2008-10-15 | 味の素株式会社 | 新規フェニルプロピオン酸誘導体 |
| US6900292B2 (en) | 2001-08-17 | 2005-05-31 | Lee-Hwei K. Sun | Fc fusion proteins of human erythropoietin with increased biological activities |
| EP1454898A4 (en) | 2001-12-13 | 2006-12-13 | Ajinomoto Kk | NEW PHENYL ALANIDE DERIVATIVES |
| KR101271635B1 (ko) | 2001-12-21 | 2013-06-12 | 휴먼 게놈 사이언시즈, 인코포레이티드 | 알부민 융합 단백질 |
| EP1463752A4 (en) | 2001-12-21 | 2005-07-13 | Human Genome Sciences Inc | ALBUMIN FUSION PROTEINS |
| EP1463751B1 (en) | 2001-12-21 | 2013-05-22 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| EP1576088A4 (en) | 2002-01-04 | 2006-09-06 | Xencor Inc | DOMINANT NEGATIVE PROTEINS AND METHOD THEREFOR |
| CN1656095A (zh) | 2002-03-22 | 2005-08-17 | 东丽株式会社 | 螺衍生物和包含其作为活性组分的粘着分子抑制剂 |
| US7332580B2 (en) | 2002-04-05 | 2008-02-19 | The Regents Of The University Of California | Bispecific single chain Fv antibody molecules and methods of use thereof |
| US7332585B2 (en) | 2002-04-05 | 2008-02-19 | The Regents Of The California University | Bispecific single chain Fv antibody molecules and methods of use thereof |
| GB0216571D0 (en) | 2002-07-17 | 2002-08-28 | Celltech R&D Ltd | Chemical compounds |
| GB0216568D0 (en) | 2002-07-17 | 2002-08-28 | Celltech R&D Ltd | Chemical compounds |
| US7314613B2 (en) | 2002-11-18 | 2008-01-01 | Maxygen, Inc. | Interferon-alpha polypeptides and conjugates |
| US20040115204A1 (en) | 2002-12-11 | 2004-06-17 | Fanger Gary R. | Antibodies to treat cancer |
| WO2004082640A2 (en) | 2003-03-19 | 2004-09-30 | New Century Pharmaceuticals, Inc. | Human serum albumin conjugates with therapeutic compounds |
| US7446125B2 (en) | 2003-04-09 | 2008-11-04 | Universidad Del Pais Vasco | Derivatives of nitroproline compounds, processes of manufacture and uses in the treatment of integrin mediated disorders |
| WO2005035719A2 (en) | 2003-10-03 | 2005-04-21 | Board Of Control Of Michigan Technological University | Modified luciferase |
| US7638331B2 (en) | 2004-01-02 | 2009-12-29 | The Administration of the Tulane Rducation Fund | Directed apoptosis in COX-2 overexpressing cancer cells through expression targeted gene delivery |
| EP2067789A1 (en) | 2004-04-13 | 2009-06-10 | F. Hoffmann-La Roche Ag | Anti-P selectin antibodies |
| EP1778270A4 (en) | 2004-05-05 | 2009-09-02 | Merrimack Pharmaceuticals Inc | BIS-SPECIFIC BINDER FOR MODULATING BIOLOGICAL ACTIVITY |
| KR20070039911A (ko) | 2004-06-01 | 2007-04-13 | 도만티스 리미티드 | 증강된 혈청 반감기를 가지는 이특이성 융합 항체 |
| TW200610754A (en) | 2004-06-14 | 2006-04-01 | Daiichi Seiyaku Co | Vla-4 inhibitor |
| US7196112B2 (en) | 2004-07-16 | 2007-03-27 | Biogen Idec Ma Inc. | Cell adhesion inhibitors |
| US20060018859A1 (en) | 2004-07-16 | 2006-01-26 | Carter Daniel C | Modified human serum albumin with reduced or eliminated affinity to chemical or biological contaminants at Cys 34 |
| ZA200703478B (en) | 2004-10-05 | 2008-07-30 | Genentech Inc | Therapeutic agents with decreased toxicity |
| MX2007008017A (es) | 2004-12-31 | 2007-09-12 | Genentech Inc | Polipeptidos que se ligan a br3 y usos de los mismos. |
| AU2005327973A1 (en) | 2005-02-23 | 2006-08-31 | Merrimack Pharmaceuticals, Inc. | Bispecific binding agents for modulating biological activity |
| US20070243163A1 (en) | 2006-02-17 | 2007-10-18 | Chih-Ping Liu | Respiratory tract delivery of interferon-tau |
| JP5840345B2 (ja) | 2006-09-08 | 2016-01-06 | アンブルックス, インコーポレイテッドAmbrx, Inc. | 修飾ヒト血漿ポリペプチドまたは修飾ヒトFc足場タンパク質ならびにこれらの利用 |
| BRPI0716744A2 (pt) * | 2006-09-14 | 2016-10-04 | Human Genome Sciences Inc | proteínas de fusão de albumina |
| US8580263B2 (en) | 2006-11-21 | 2013-11-12 | The Regents Of The University Of California | Anti-EGFR family antibodies, bispecific anti-EGFR family antibodies and methods of use thereof |
| US8343950B2 (en) * | 2006-12-15 | 2013-01-01 | Concert Pharmaceuticals, Inc. | Quinazoline derivatives and methods of treatment |
| PL2288715T3 (pl) | 2008-04-11 | 2015-03-31 | Merrimack Pharmaceuticals Inc | Łączniki będące albuminą surowicy ludzkiej i ich koniugaty |
| UA104868C2 (uk) * | 2008-08-15 | 2014-03-25 | Меррімак Фармасьютікалз, Інк. | Спосіб лікування пацієнта, що має неопластичну пухлину, відповідно до спрогнозованої реакції |
| CN102282168A (zh) | 2008-11-18 | 2011-12-14 | 梅里麦克制药股份有限公司 | 人血清白蛋白接头以及其结合物 |
| WO2011133668A2 (en) | 2010-04-20 | 2011-10-27 | President And Fellows Of Harvard College | Methods and compositions for the treatment of cancer |
| WO2011146902A1 (en) * | 2010-05-21 | 2011-11-24 | Merrimack Pharmaceuticals, Inc. | Bi-specific fusion proteins |
| WO2013067355A1 (en) * | 2011-11-04 | 2013-05-10 | Novartis Ag | Low density lipoprotein-related protein 6 (lrp6) - half life extender constructs |
| US20150202287A1 (en) * | 2012-08-30 | 2015-07-23 | Merrimack Pharmaceuticals, Inc. | Combination therapies comprising anti-erbb3 agents |
-
2009
- 2009-10-14 CN CN2009801545099A patent/CN102282168A/zh active Pending
- 2009-10-14 JP JP2011536365A patent/JP5677972B2/ja not_active Expired - Fee Related
- 2009-10-14 KR KR1020117014075A patent/KR20110112301A/ko not_active Application Discontinuation
- 2009-10-14 WO PCT/US2009/060721 patent/WO2010059315A1/en active Application Filing
- 2009-10-14 BR BRPI0921586A patent/BRPI0921586A2/pt not_active IP Right Cessation
- 2009-10-14 US US13/130,007 patent/US8927694B2/en not_active Expired - Fee Related
-
2010
- 2010-04-09 US US12/757,801 patent/US20110059076A1/en not_active Abandoned
-
2014
- 2014-12-24 US US14/582,719 patent/US20150191545A1/en not_active Abandoned
-
2016
- 2016-08-30 US US15/251,158 patent/US20170204192A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110112301A (ko) | 2011-10-12 |
| BRPI0921586A2 (pt) | 2019-09-24 |
| JP2012509259A (ja) | 2012-04-19 |
| US20120003221A1 (en) | 2012-01-05 |
| US20150191545A1 (en) | 2015-07-09 |
| US20170204192A1 (en) | 2017-07-20 |
| US8927694B2 (en) | 2015-01-06 |
| CN102282168A (zh) | 2011-12-14 |
| US20110059076A1 (en) | 2011-03-10 |
| WO2010059315A1 (en) | 2010-05-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5677972B2 (ja) | ヒト血清アルブミンリンカーおよびそのコンジュゲート | |
| JP5863926B2 (ja) | ヒト血清アルブミンリンカーおよびそのコンジュゲート | |
| JP7348349B2 (ja) | B細胞成熟抗原結合タンパク質 | |
| JP5068270B2 (ja) | 癌を処置するためのil−17アンタゴニスト抗体 | |
| CN107849142B (zh) | 拮抗性抗肿瘤坏死因子受体超家族抗体 | |
| JP7425049B2 (ja) | Dll3結合タンパク質および使用方法 | |
| US20230383003A1 (en) | Antagonistic anti-tumor necrosis factor receptor superfamily polypeptides | |
| CN108235685A (zh) | Pd-1拮抗剂与egfr抑制剂的组合 | |
| US20230295326A1 (en) | Antagonistic anti-tumor necrosis factor receptor superfamily polypeptides | |
| JP2015110558A (ja) | ヒトox40受容体に対する結合分子 | |
| US20240101693A1 (en) | Antagonistic anti-tumor necrosis factor receptor superfamily antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120329 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120329 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130325 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131216 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140313 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140320 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140529 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141126 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141224 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150105 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5677972 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |