JP2017520575A - 二重特異的ヘテロ二量体ダイアボディおよびその使用 - Google Patents
二重特異的ヘテロ二量体ダイアボディおよびその使用 Download PDFInfo
- Publication number
- JP2017520575A JP2017520575A JP2016575335A JP2016575335A JP2017520575A JP 2017520575 A JP2017520575 A JP 2017520575A JP 2016575335 A JP2016575335 A JP 2016575335A JP 2016575335 A JP2016575335 A JP 2016575335A JP 2017520575 A JP2017520575 A JP 2017520575A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- cad
- sequence
- subdomain
- heterodimer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/524—CH2 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/626—Diabody or triabody
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/72—Increased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Abstract
Description
本出願は、2014年7月1日に出願された米国仮特許出願第62/019,762号および2015年4月17日に出願された米国仮特許出願第62/148,920号の利益を主張し、その全体が参照により本明細書に組み込まれる。
本出願は、EFS−Webにより電子出願され、.txt形式で電子的に提出された配列表を含む。.txtファイルは、2015年6月12日に作成された「PC72054A_Sequence_Listing.txt」の表題の、248KBのサイズを有する配列表を含有する。この.txtファイルに含有される配列表は、本明細書の一部であり、その全体が参照により本明細書に組み込まれる。
本発明は、二重特異的ヘテロ二量体ダイアボディおよびがんの処置におけるその使用に関する。
一度、本発明の分子(すなわち、結合ドメイン)をコードする核酸配列が得られたら、分子の産生のためにベクターを、当技術分野で周知の技術を使用する組換えDNA技術によって産生することができる。
以前に述べた通り、二重特異的ヘテロ二量体ダイアボディとは、両抗体結合ドメインが単一のポリペプチド鎖内に含まれ、それぞれのポリペプチド鎖中のVLおよびVHドメインが異なる抗体に由来する、それぞれ、少なくとも1つの抗体VLドメインと1つの抗体VHドメインまたはそれらの断片を含む、2つ以上のポリペプチド鎖またはタンパク質の複合体を指す。特定の態様において、二重特異的ヘテロ二量体ダイアボディは、VLとVHドメインの両方を含有するポリペプチド鎖の二量体または四量体を含む。多量体タンパク質を含む個々のポリペプチド鎖は、鎖間ジスルフィド結合によって多量体の少なくとも1つの他のペプチドに共有結合していてもよい。
位の免疫特異性に基づいて容易に管理される。
二重特異的ヘテロ二量体ダイアボディのポリペプチド鎖は、様々なリンカーおよびペプチドを含んでもよい。リンカーおよびペプチドは、0、1、2、3、4、5、6、7、8、9個以上のアミノ酸であってもよい。ある特定の態様において、二重特異的ヘテロ二量体ダイアボディのポリペプチド鎖は、グリシン−セリンリンカー(リンカー1)を含んでもよい。別の態様において、リンカー1は、限定されるものではないが、GGGSGGGG(配列番号68)およびGGGGSGGGG(配列番号69)の配列を含んでもよい。
本発明の態様において、図2および図3に示されるような、VF−DARTとして知られる二重特異的ヘテロ二量体ダイアボディは、第1のポリペプチド鎖(1)と第2のポリペプチド鎖(2)とを含む。
また、二重特異的ヘテロ二量体ダイアボディの2つの異なるポリペプチド鎖のヘテロ二量体形成を、反対のメンバーに対する親和性およびそれ自身に対する反発力を有するドメインの使用によって促進することもできる。そのようなドメインの例は、コイルドコイルドメインである。例えば、第1のポリペプチド鎖(1)は、負に荷電したアルファ−ヘリックスコイル(E−コイル)を形成するグルタミン酸リッチ領域を有する第1のヘテロ二量体促進ドメインを含んでもよく、第2のポリペプチド鎖(2)は、正に荷電したヘリックスコイル(K−コイル)を形成するリシンリッチ領域を有する第2のヘテロ二量体促進ドメインを含んでもよく、これは、ヘテロ二量体形成を促進する静電的相互作用を可能にする。E−コイルは別のE−コイル含有ポリペプチドに対する反発力を有する、およびK−コイルについてはその逆であるため、ホモ二量体形成を減少させることができる。
本発明は、Fc領域もしくはドメイン、またはその一部を含む二重特異的ヘテロ二量体ダイアボディを包含する。ある特定の態様において、Fc領域、またはその一部は、IgG1、IgG2、IgG3またはIgG4のFc領域の1つまたは複数の定常ドメイン(例えば、CH2またはCH3ドメイン)を含む。他の態様において、本発明は、Fc領域またはその一部が同等の野生型Fc領域またはその一部と比較して少なくとも1つのアミノ酸改変(例えば、置換)を含む、Fc領域またはその一部を含む分子を包含する。バリアントFc領域は、当技術分野で周知であり、当技術分野で周知の任意の結合活性またはエフェクター機能アッセイ、例えば、ELISA、SPR分析、またはADCCにおいてアッセイされるバリアントFc領域を含む抗体の表現型を変化させるために主として使用される。そのようなバリアントFc領域、またはその一部は、Fc領域またはその一部を含む本発明のダイアボディ分子により示される血漿半減期および安定性を延長させることができる。他の態様において、本発明は、当技術分野で公知の任意のFcバリアントの使用を包含する。
本発明の態様において、LP−DARTと呼ばれる、Fc領域を有する二重特異的ヘテロ二量体ダイアボディが図1および図5に示される。LP−DARTは、IgGのFcドメインに融合された、標的抗原とCD3とに結合する2つのscFvドメインを含んでもよい。本発明の一態様において、二重特異的ヘテロ二量体ダイアボディは、IgG1のFcドメインに融合された、P−カドヘリンとCD3イプシロンとに結合する2つのscFvドメインを含んでもよい。特に、図1Aおよび図1Bは、抗P−カドヘリン/抗ヒトCD3 LP−DARTの4つの代替表示を示し、図5は、構築されたLP−DARTの一般図を示す。LP−DARTは、第1および第2のヘテロ二量体促進ドメインが、CH2および/またはCH3ドメインがノブ(突起)またはホール(空洞)を含むように変化された、免疫グロブリンFc領域のCH2および/またはCH3ドメインを有する免疫グロブリンFc領域を含むことを除いて、VF−DARTまたはEK−DARTについて上記された構造と類似する。LP−DARTのFc部分に対する改変を、以下に記載する。
ヒトIgG1のFc領域を改変して、翻訳後に切断されることが多いC末端リシン残基を除去し、ならびに、FcγRIIIへの結合のためエフェクター機能をオブラート(oblate)する標準的なプライマー特異的PCR突然変異誘発を使用して突然変異L234A、L235AおよびG237Aを導入した(エフェクターヌル表現型)。
「ノブインホール」は、ヘテロ二量体化のために抗体重鎖ホモ二量体を操作するための当技術分野で公知の有効な設計戦略である。この手法においては、「ノブ」バリアントを、IgG1のFc領域の一方の鎖中で、小さいアミノ酸をより大きいもの、例えば、Y349CおよびT366Wに置き換えることにより取得した。「ノブ」を、大きい残基をより小さいもの、例えば、S354C、T366S、L368AおよびY408Vに置き換えることにより作出されたFc領域の相補鎖のCH3ドメイン中、「ホール」に挿入するように設計した。
図6および図7は、それぞれ、N末端MP3−DARTおよびC末端MP3−DART二重特異的ヘテロ二量体ダイアボディの略図である。そのようなMP3−DARTタンパク質は、3つのポリペプチド鎖:第1のポリペプチド鎖(1)、第2のポリペプチド鎖(2)および第3のポリペプチド鎖(3)から構成される。
ある特定の態様において、二重特異的ヘテロ二量体ダイアボディのそれぞれのポリペプチド鎖を、本発明の別のポリペプチド鎖上の対応するシステイン残基と相互作用して、鎖間ジスルフィド結合を形成することができる少なくとも1つのシステイン残基を含むように操作することができる。鎖間ジスルフィド結合は、ダイアボディ分子を安定化するのに役立ち、組換え系における発現および回収を改善し、安定で一貫した製剤をもたらし、ならびに、in vivoでの単離および/または精製された産物の安定性を改善することができる。システイン残基を、ポリペプチド鎖の任意の部分に、単一のアミノ酸として、またはより大きいアミノ酸配列、例えば、ヒンジ領域の一部として導入することができる。特定の態様において、少なくとも1つのシステイン残基を、ポリペプチド鎖のC末端に存在するように操作する。
本発明は、対象におけるがんの処置、防止または管理のための方法および組成物であって、治療有効量の本発明に従って操作された二重特異的ヘテロ二量体ダイアボディを対象に投与することを含み、この分子はがん抗原にさらに結合する、方法および組成物を包含する。本発明の分子は、原発性腫瘍およびがん細胞の転移の防止、阻害、増殖の減少および/または退縮にとって特に有効であり得る。特定の作用機構によって束縛されることを意図するものではないが、本発明の分子は、腫瘍消失、腫瘍減少またはその組合せをもたらし得るエフェクター機能を媒介することができる。
本発明の代表的な材料を、2013年12月20日にAmerican Type Culture Collection、10801 University Boulevard、Manassas、Va.20110−2209、USA(ATCC)に寄託した。ATCC受託番号PTA−120809を有するベクター153 LP−DART Aは、P−カドヘリンLP−DART(Fc融合ダイアボディ)A鎖をコードする組換えヒトDNA挿入物を含み、ATCC受託番号PTA−120810を有するベクター153 LP−DART Bは、P−カドヘリンLP−DART(Fc融合ダイアボディ)B鎖をコードする組換えヒトDNA挿入物を含む。寄託物は、Budapest Treaty on the International Recognition of the Deposit of Microorganisms for the Purpose of Patent Procedure and Regulations thereunder (Budapest Treaty)の条項の下で作製した。これは、寄託日から30年間にわたって寄託物の生きた培養物の維持を確保するものである。寄託物は、ブダペスト条約の条項の下でATCCにより利用可能となり、Pfizer IncとATCCとの合意を受け、いずれが第1であっても、関連する米国特許の保証の際または任意の米国もしくは外国特許出願の公開の際に寄託物の培養物の子孫の永続的かつ無制限の利用可能性を公衆に保証し、35U.S.C.Section 122およびそれに準拠する委員会の規則(886OG638を特に参照する37C.F.R.Section 1.14を含む)に従って権利を与えられる米国特許商標庁長官によって決定される者にその子孫の利用を保証する。
P−カドヘリン抗体および二重特異的ヘテロ二量体ダイアボディの生成
二重特異的ヘテロ二量体ダイアボディを、それぞれの組換え産生、精製および結合特性を評価するために構築した。アフィニティ精製された二重特異的ヘテロ二量体ダイアボディを、本明細書に記載の組換え発現系によって産生した。ELISAおよびSPR分析により、共有結合による二重特異的ヘテロ二量体ダイアボディが、両方の標的抗原、P−カドヘリンおよびCD−3に対する親和性を示し、両抗原に同時に結合することができることがさらに示された。
P−カドヘリンの細胞外ドメイン(ECD)に結合する一本鎖断片可変(scFv)部分を、当技術分野で公知の技術を利用して、非免疫化ヒトドナーに由来するscFvから構成されるファージディスプレイライブラリーを用いて同定した。標準的なELISA技術により、ファージ表面上に発現されるscFvの結合を、P−カドヘリンタンパク質構築物およびP−カドヘリン発現細胞上で測定した。
scFv断片を、従来の方法を使用して、未精製の細菌グリセロールストックとして、または精製されたプラスミドとして、プライマー5’GGAGATTTTCAACGTGAA3’(配列番号58)および5’CTCTTCTGAGATGAGTTTTTG3’(配列番号59)を用いて配列決定した。
強い組換えP−カドヘリンまたは細胞表面結合(バックグラウンドまたは陰性細胞結合の3倍を超える)を示したscFv断片を、DARTタンパク質中へのサブクローニングのために選択した。DARTの設計およびクローニング方法は、以前に記載されている(Johnsonら、J Mol Biol、399:436〜449、2010;Mooreら、Blood、117(17):4542〜51、2011)。ファージディスプレイライブラリーから新規抗P−カドヘリンscFvを適合させるための方法は、以下の通りである:VHについてはBamHI/BspEIおよびVLについてはBssHII/BamHIを組み込むプライマーを用いる標準的なポリメラーゼ連鎖反応(PCR)により、断片を増幅した。製造業者の仕様書(New England Biolabs)に従って対応する制限酵素で断片を切断した。
抗P−カドヘリン/抗ヒトCD3 LP−DARTの構築
抗P−カドヘリン/抗ヒトCD3 DARTタンパク質を、それぞれのDARTタンパク質が哺乳動物発現ベクター中へのクローニングのためのそれぞれの末端に制限酵素クローニング部位を含有するようにPCRによって増幅した。表11ならびに図33Aおよび図33Bを参照されたい。
P−カドヘリンscFv−FcおよびDARTタンパク質の結合特性
P−カドヘリンタンパク質構築物およびP−カドヘリン発現細胞に対する、P−カドヘリンscFv−Fc構築物(ヒトIgG Fc領域に融合したP−カドヘリンVHおよびVL)およびDARTタンパク質の結合特性を、標準的なELISA技術を使用して分析した。表12中のデータは、ファージ由来P−カドヘリンscFv−Fc構築物が、組換えヒトP−カドヘリンには強く結合するが、マウスP−カドヘリンには検出可能に結合しなかったことを示す。
DARTタンパク質の表面プラズモン共鳴(SPR)分析
P−カドヘリンおよびCD3に対するEK−DARTタンパク質の結合親和性を、BIACORE(登録商標)3000バイオセンサー(GE Healthcare)を使用するSPRによって分析した。抗原huCD3εδおよびヒトP−カドヘリン−Fcまたはヒト/カニクイザル/マウスP−カドヘリン−ECDを、製造業者により推奨されるようにアミンカップリングキットによってCM−5センサーチップ上に固定した。表15は、カニクイザル(「cyno」)P−カドヘリンECDに対するファージ由来EK−DARTタンパク質の結合親和性を示し、表16は、ヒト可溶性CD3タンパク質に対するファージ由来EK−DARTタンパク質の結合親和性を示す。表15および表16中の全てのEK−DARTタンパク質はCD3−2を含む。
P−カドヘリンDARTタンパク質の特徴付け
示差走査熱量測定(DSC)分析を使用して、ファージ由来EK−DARTタンパク質の熱安定性を特徴付けた。表21は、P−カドヘリンEK−DARTタンパク質が65℃より高いTm1遷移を有する好ましい温度プロファイルを有していたことを示す。強制凝集分析は、40℃でP−カドヘリンEK−DARTタンパク質の温度ストレスに対する耐性を示す。表21中の全てのEK−DARTタンパク質は、CD3−2を含む。
P−カドヘリンLP−DARTタンパク質の特徴付け
表23は、親クローンP−CAD 35およびCD3−2を用いて生成された8つの異なるP−カドヘリンLP−DART構築物(番号1〜番号8)に関する様々な機能的および生物物理学的データをまとめる。
P−カドヘリン発現の定量
A.in vitro試験のためにルシフェラーゼを発現するように操作されたがん細胞株上でのP−カドヘリン発現の定量
フローサイトメトリー実験を行って、10種のがん細胞株のパネルにわたる内因性細胞表面P−カドヘリン発現の相対レベルを決定するために抗P−カドヘリンmAb(PF−03732010)結合を評価した。in vitroでの試験のために全ての腫瘍細胞株を、ルシフェラーゼを発現するように操作した。一定範囲のP−カドヘリン受容体発現を示す腫瘍細胞株を、飽和FACS結合について記載されたように収集した。試料あたり2.5x105個の細胞を、96ウェル丸底ポリプロピレンプレートに移した。1:1のmAb:PE(eBioscience)比でコンジュゲートされた5μg/mlおよび10μg/mlのフィコエリトリン(PE)標識された抗ヒトP−カドヘリンmAb(PF−03732010)または対照マウスIgG1 mAb(Biolegend)にコンジュゲートされたPEを用いて、室温で30分間、細胞を染色した。細胞を洗浄し、FACSバッファー+10ng/mlヨウ化プロピジウムを用いて再懸濁した後、FACS Divaソフトウェアを含むLSRIIを用いて取得した。QuantiBRITE PEビーズ(BD Pharmingen)を、0.5mLのFACSバッファーを使用して再構成し、腫瘍細胞試料と同じ電圧設定を用いるLSRIIを使用して取得した。両ビーズおよび腫瘍細胞のPE幾何平均蛍光強度を使用して、QuantiBRITE PE Bead Kitに関する製造業者に処方されたプロトコールに従って細胞あたりに結合したPE標識抗体の数(ABC)を算出した。受容体密度と細胞傷害性EC50との間の線形回帰曲線のフィッティングを、それぞれの腫瘍細胞株に関する5μg/mLおよび10μg/mLのPE標識抗P−カドヘリンmAbでのQuantibriteアッセイにより決定された平均受容体密度のLog10値と、GraphPad Prism 5.0ソフトウェアを使用した同じ標的腫瘍細胞株に関する平均in vitro細胞傷害性EC50のLog10値とをプロットすることにより決定した。
フローサイトメトリー実験を行って、in vivo試験のためのがん細胞株のパネルにわたる内因性細胞表面P−カドヘリン発現の相対レベルを決定するために抗P−カドヘリンmAb(Pfizer PF−03732010)結合を評価した。一定範囲のP−カドヘリン受容体発現を示す腫瘍細胞株を、飽和FACS結合のために記載されたように収集した。試料あたり2.5x105個の細胞を、96ウェル丸底ポリプロピレンプレートに移した。1:1のmAb:PE(eBioscience)比でコンジュゲートされた5μg/mlおよび10μg/mlのフィコエリトリン(PE)標識された抗ヒトP−カドヘリンmAbまたは対照マウスIgG1 mAb(Biolegend)にコンジュゲートされた7.5μg/mLのPEを用いて、室温で30分間、細胞を染色した。細胞を洗浄し、FACSバッファー+10ng/mlヨウ化プロピジウムを用いて再懸濁した後、FACS Divaソフトウェアを含むLSRIIを用いて取得した。QuantiBRITE PEビーズ(BD Pharmingen)を、0.5mlのFACSバッファーを使用して再構成し、腫瘍細胞試料と同じ電圧設定を用いるLSRIIを使用して取得した。両ビーズおよび腫瘍細胞の平均PE幾何平均蛍光強度を使用して、QuantiBRITE PE Bead Kitに関する製造業者に処方されたプロトコールに従って細胞あたりに結合したPE標識抗体の数(ABC)を算出した。
in vitro細胞傷害アッセイ
A.EK−DART細胞傷害性Tリンパ球(CTL)アッセイ
強力な組換えP−カドヘリン/CD3タンパク質結合および強力な結合シグナル(バックグラウンドまたはEC50の3倍を超える≒PF03732010−DART)を示すEK−DARTタンパク質を、以前に記載された、T細胞により指向化された細胞殺傷アッセイ(Mooreら、Blood、117(17):4542〜4551、2011)においてスクリーニングした。表29は、本発明のP−カドヘリンEK−DARTタンパク質に関する効率的な、T細胞により指向化された細胞傷害性を示す。30:1のE:T比でのヒトPBMCの存在下で、ヒトP−カドヘリンを過剰発現するように操作されたCHO細胞および高レベルのP−カドヘリンを内因的に発現するがん細胞株(H1650)は、LDH放出アッセイを使用して測定された場合、24時間のインキュベーション後にEK−DARTタンパク質によって両方とも効率的に溶解された。40時間までのインキュベーション時間の延長は、P−カドヘリンEK−DART分子を用いて再指向化されたT細胞による殺傷の作用機構によって予測された通り細胞殺傷の効力をさらに増加させた。対照的に、P−カドヘリン発現の欠如に基づいて予測された通り、親CHO細胞株上で殺傷は観察されなかった。表29中の全てのEK−DARTタンパク質は、CD3−2を含む。
153 LP−DARTの媒介性細胞殺傷を、細胞傷害性Tリンパ球(CTL)アッセイによって評価した。エフェクター(T細胞)の標的(CHO細胞)に対する比が10:1であるCHO親細胞およびCHO P−カドヘリン細胞を、増大する濃度の153 LP−DARTの存在下でCD3+ T細胞と共にインキュベートした。細胞生存能力を48時間後に測定し、半数効果濃度(EC50)を算出したところ、0.41pMであった。その結果、153 LP−DARTはCHO P−カドヘリン細胞上では強力な殺傷を示すが、CHO親細胞上では陰性対照を超える活性は検出されないことが示された。したがって、CTL活性は、P−カドヘリン発現に依存していた。
一定範囲のP−カドヘリン受容体発現を示すセクションAからの腫瘍細胞株を収集し、試料あたり2.5x105個の細胞を、96ウェル丸底ポリプロピレンプレートに移した。1:1のmAb:PE(eBioscience)比でコンジュゲートされた5μg/mlおよび10μg/mlのフィコエリトリン(PE)標識された抗ヒトP−カドヘリンmAb(Pfizer PF−03732010)または対照マウスIgG1 mAb(Biolegend)にコンジュゲートされたPEを用いて、室温で30分間、細胞を染色した。細胞を洗浄し、FACSバッファー+10ng/mlヨウ化プロピジウムを用いて再懸濁した後、FACS Divaソフトウェアを含むLSRIIを用いて取得した。QuantiBRITE PEビーズ(BD Pharmingen)を、0.5mLのFACSバッファーを使用して再構成し、腫瘍細胞試料と同じ電圧設定を用いるLSRIIを使用して取得した。両ビーズおよび腫瘍細胞のPE幾何平均蛍光強度を使用して、QuantiBRITE PE Bead Kitに関する製造業者に処方されたプロトコールに従って細胞あたりに結合したPE標識抗体の数(ABC)を算出した。
ヒトPBMC再構成異種移植試験
強力な、T細胞により指向化された細胞傷害性(10ng/mL未満のEC50)を示す様々なDARTタンパク質を、以下に記載されるような異種移植再構成実験においてin vivoで試験した。
健康なヒトドナーに由来するPBMCを、Ficoll勾配遠心分離を使用することによって全血から単離した。簡単に述べると、全血を、滅菌PBSで1:1に希釈した。35mLの希釈された血液を、50mLチューブ中の15mLのFICOLL−PAQUE(商標)Plus上に載せ、チューブを1400rpmで20分間、ブレーキをオフにして遠心分離した。2つの相の間の淡黄色の被覆層を、50mLチューブ中に収集し、600xg(1620rpm)で5分間、チューブを遠心分離することによって、45mLのPBSで洗浄した。上清を廃棄し、細胞ペレットをPBSで1回洗浄し、Trypan Blue色素排除法により生細胞数を決定した。PBMCを、完全培地(RPMI1640、10%FBS、2mMグルタミン、10mM HEPES、100μ/100μ/mLペニシリン/ストレプトマイシン(P/S))中、2.5x106細胞/mLの最終濃度に再懸濁した。
ヒトT細胞を、RosettaSep T細胞単離キット中に提供される製造業者のプロトコールに従ってヘパリン処理された全血から単離した。次いで、精製されたT細胞を、細胞を抗CD3(OKT−3;1μg/mL)および抗CD28(66μg/mL)抗体に48時間曝露することによって活性化した。刺激後、細胞を、IL−2(7.6ng/mL)の存在下で最大3週間、10%FBSおよび1%ペニシリン/ストレプトマイシンを含むRPMI1640培地中で増殖させた。
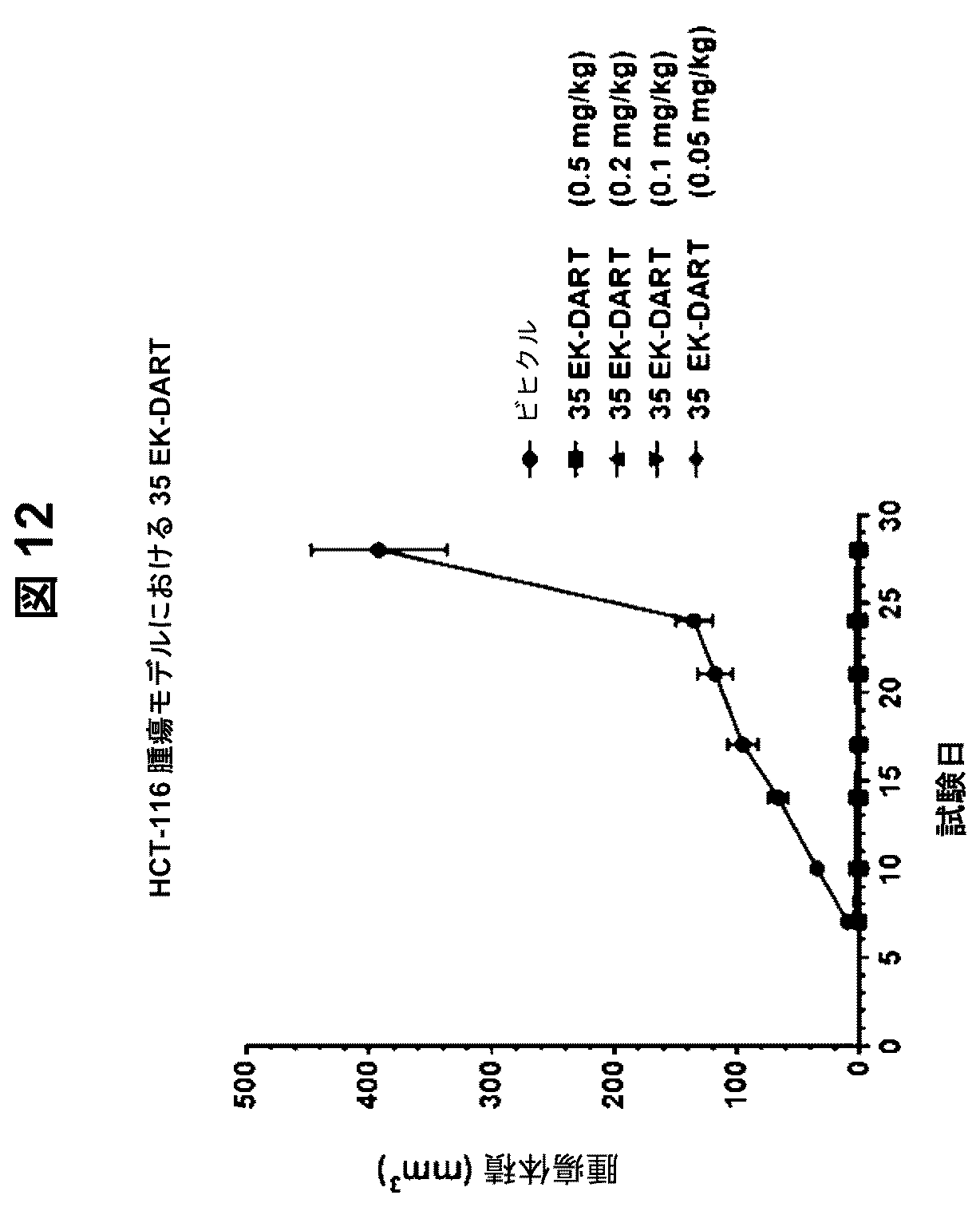
ヒトT細胞と腫瘍細胞(HCT116、Du145またはH1650)を1:5の比(それぞれ、1x106個および5x106個)で混合し、200μLの滅菌生理食塩水中に懸濁し、試験0日目(SD0)に皮下注射した。様々なP−カドヘリンEK−DART(CD3−2)、LP−DART(CD3−1)または対照DART(CD3−2)タンパク質を、対照と共に、SD0、1、2、および3に、100μLの尾静脈注射により静脈内(IV)投与した。それぞれの処置群は8匹の動物を含有していた。
動物の体重:腫瘍細胞注射の時点で開始して試験完了まで週に2回、個々の動物の体重を記録した。
HCT116細胞株を、活性化T細胞と予め混合し、上記で詳述されたように試験0日目(SD0)にNOD/SCIDガンマノックアウトマウス(N=8匹/群)中に皮下(SC)的に埋め込んだ。様々なP−カドヘリンEK−DART、LP−DARTまたは対照DARTタンパク質を用いる処置を、腫瘍細胞/T細胞混合物を埋め込んだのと同じ日[(SD0)]に開始した後、合計4回の毎日の注射のためにさらに3日間、毎日の注射を行った。動物を、4つの用量レベル(0.5、0.2、0.1、および0.05mg/kg)でP−カドヘリンEK−DART、LP−DARTまたは対照DARTタンパク質で処置した。結果を、図9〜図14に示す。
Du145細胞株を活性化T細胞と予め混合し、上記で詳述されたようにSD0にNOD/SCIDガンマノックアウトマウス(N=8匹/群)にSC的に埋め込んだ。153 LP−DARTによる処置を、腫瘍細胞/T細胞混合物を埋め込んだのと同じ日[(SD0)]に開始した後、合計4回の毎日の注射のためにさらに3日間、毎日の注射を行った。動物を、5つの用量レベル(100、10、1、0.1、および0.01μg/kg)の153 LP−DARTで処置した。結果を図15に示す。
H1650細胞株を活性化T細胞と予め混合し、上記で詳述されたようにSD0にNOD/SCIDガンマノックアウトマウス(N=8匹/群)にSC的に埋め込んだ。153 LP−DARTによる処置を、腫瘍細胞/T細胞混合物を埋め込んだのと同じ日[(SD0)]に開始した後、合計4回の毎日の注射のためにさらに3日間、毎日の注射を行った。動物を、5つの用量レベル(100、10、1、0.1、および0.01μg/kg)の153 LP−DARTで処置した。結果を図16に示す。
確立された腫瘍ヒトPBMC生着モデル
定量的フローサイトメトリー分析に基づいてP−カドヘリン高(HCT116)、中(SW480)、低(Ls174T)および陰性(SW620)発現と分類されるヒト結腸直腸がんの4つの別々の異種移植腫瘍モデルを確立した。HCT116は、最も高い相対レベルの細胞表面P−カドヘリン発現(43,801ABC、表28)を示し、SW480は相対的に中レベルの細胞表面P−カドヘリン発現(12,665ABC、表28)を示し、Ls174Tは相対的に低レベルの細胞表面P−カドヘリン発現(4,160ABC、表28)を示す。
確立された腫瘍ヒトT細胞養子移入モデル
HCT116(結腸)およびSUM149(乳)のヒトT細胞の養子移入を用いる腫瘍増殖阻害を分析した。HCT116は、最も高い相対レベルの細胞表面P−カドヘリン発現(43,801ABC、表28)を示し、SUM149は相対的に中レベルの細胞表面P−カドヘリン発現(15,426ABC、表28)を示す。T細胞を、2X GlutaMax−1、1%PenStrep、および20ng/ml組換えヒトIL−2(Life Technologies、Carlsbad、CA)を補充したOpTmizer CTS T Cell Expansion Serum−Free Mediaを用いて0.5x106細胞/mlに再懸濁した。次いで、Dynabeads Human T−Expander CD3/CD28磁気ビーズ(Life Technologies)を、1x106個のビーズ/ml(2個のビーズ/細胞)でT細胞に添加し、製造業者のプロトコールに従って細胞を1週間培養した。回収の時点で、ビーズを磁石で除去し、in vivoでの接種のために1x107細胞/mlでDPBS中に細胞を再懸濁した。
P−カドヘリン陽性患者由来異種移植(PDX)
P−カドヘリン陽性PDXのin vivoでの腫瘍増殖阻害を分析した。P−カドヘリン陽性患者由来結腸直腸腫瘍異種移植片、PDX−CRX−11260を、抗P−カドヘリン抗体を用いるFFPE腫瘍試料の陽性染色によって同定した。PDX−CRX−11260腫瘍組織をNSG動物に埋め込み、大まかに100mm3まで増殖させた。動物をn=7の用量群に無作為化し、ビヒクル、0.05mg/kgの153 LP−DART(CD3−1)、または0.5mg/kgの153 LP−DART(CD3−1)を毎週投与した。初回投与の1日後、全ての動物に2x106個のin vitroで増加させたヒトT細胞を投与した。
腫瘍浸潤リンパ球(TIL)の用量依存的蓄積
ヒト末梢血単核細胞(PBMC)が生着し、変化するレベルの153 LP−DART(CD3−1)(n=3)を投与したHCT116腫瘍があるマウスを、投与の6日後に安楽死させて、腫瘍浸潤ヒトCD3+リンパ球を評価した。腫瘍試料を、ヒト腫瘍細胞解離バッファーを含有するgentleMACS Cチューブ(Miltenyi Biotech)中に収集し、gentleMACS組織解離装置(Miltenyi Biotech)を使用する柔らかいヒト腫瘍のための製造業者に提言されたプロトコールを使用して単一細胞懸濁にかけた。次いで、細胞懸濁液を、2mM EDTAを含有するDPBSを用いて洗浄し、生細胞数をトリパンブルー色素排除および血球計により決定した。各試料から1x106個の生細胞を、2%FBSおよび0.02%アジ化ナトリウムを含有するPBS中に収集し、氷上で30min、CD3 FITC(BD Pharmingen)で染色した。洗浄後、ヨウ化プロピジウムを、FACS Divaソフトウェアを含むLSRII(BD Pharmingen)を使用する分析の直前に各試料に添加した。
FMT画像化を使用するP−カドヘリンLP−DARTの生体分布および腫瘍標的化
皮下HCT116異種移植が確立されたNSGまたは無胸腺ヌードマウスを使用した。T細胞の生着を含む試験は、健康なヒトボランティアから単離されたT細胞を受けた。腫瘍が300〜500mm3に達した時、生体分布試験を開始した。P−カドヘリン153 LP−DART(CD3−1)または陰性対照−DART(非標的化ドメインxCD3結合ドメイン)を、1〜2.75のフルオロフォアの二重特異的標識に対する比で、近赤外フルオロフォアVivoTag680XL(VT680)とコンジュゲートさせ、P−カドヘリン153 LP−DART−VivoTag680XLおよび対照−LP−DART−VivoTag680XLを得た。
VT680標識化が分子特性に影響したかどうかを決定するために、品質対照試験を実施した:FACS分析および分子活性のための細胞傷害アッセイによる細胞へのin vitroでの結合。この特性をVT680標識された、および標識されていない対照LP−DARTおよびP−カドヘリン153 LP−DARTについて比較した。CV815で標識されたT細胞について、T細胞増加およびまたエフェクター細胞に対する細胞傷害性を評価した。表41は、生体分布試験のために使用された分子を示す。DOL=標識化の程度。
HCT116異種移植モデルにおけるP−カドヘリン153 LP−DARTの生体分布および標的化を、縦方向のFMT画像化を使用して分析した。50%マトリゲル中の100万個のHCT116細胞を、メスのnu/nuマウス(8週齢)のSQ脇腹に注射した。腫瘍を、約300〜500mm3のサイズまで増殖させた。動物に、1nモルのVT680に等しいプローブ(VT680で標識された生物分子)を注射した(表41)。in vivoでのFMT画像化(全身)を、注射後5min、24h、48h、96hおよび240hで縦方向に実施した。血液(血漿)試料を、それぞれの時点で収集した。断続的な時点および試験の終わりに、動物を安楽死させ、PBS/生理食塩水をかん流させて、血管区画から血液を除去した。組織(腫瘍、肝臓、脾臓、腎臓、肺および脳)をex vivoで画像化した。FMTデータを、TrueQuantソフトウェアを使用して分析した。ex vivoでの画像化の後、将来のPK分析のために組織を簡易凍結した。血漿および組織試料のPK分析を、ELISAにより実施した。T細胞の生着を、生体分布試験においては実施しなかった。
FMT画像化を使用するHCT116モデルにおける生着したT細胞の細胞追跡を行った。50%マトリゲル中の100万個のHCT116細胞を、メスのNSGマウス(8週齢)のSQ脇腹に注射した。腫瘍が約300〜500mm3のサイズであった時、P−カドヘリン153 LP−DART(VT680で標識された、または標識されていない)を、SQ経路により注射した。薬物を注射した24時間後、CV815で標識された500万個のT細胞をIV経路により注射した。細胞生着後、FMT画像化を縦方向に実施した。P−カドヘリン153 LP−DART−VT680およびT細胞−CV815群について680nmおよび800nmレーザーを使用して連続画像化を実施した。
結晶および構造の決定
結晶化試験のために、図25に示される精製されたDARTタンパク質を使用した。特に、ヘテロ二量体促進ドメインを含まず、P−CAD 35 VHドメインに共有結合された「6XHIS」と指定されたC末端HisタグHHHHHH(配列番号78)およびCD3 VHドメインに共有結合された「FLAG」と指定されたC末端FLAG配列GGCGGDYKDDDDK(配列番号79)を有するDARTタンパク質(クローン35 P−CAD VL/VH結合ドメインとクローンCD3結合ドメインとを有する)を、結晶解析のために設計した(以後、「結晶35DART」と指定する)。
P−カドヘリン153 LP−DARTのエピトープマッピング
P−カドヘリン153 LP−DARTの結合エピトープを同定するために、可溶性P−カドヘリン−細胞外ドメイン(ECD)−Fc融合タンパク質構築物を生成した。それぞれのP−カドヘリン−Fc構築物は、図34に示されるように、シグナルペプチド、プロペプチドおよびヒンジに遺伝的に融合されたP−カドヘリンECDサブドメイン領域(ECD1、ECD1−2、ECD1−3、ECD1−4、またはECD1−5)ならびに切断性リンカーを介してヒトIgG1のCH2およびCH3ドメインを含んでいた。ECD−Fc構築物を生成するために使用されるECD1、ECD2、ECD3、ECD4およびECD5 P−カドヘリンサブドメイン断片は、図35に示され、表42にさらに特徴付けられるように、完全長p−カドヘリンエピトープ(UniProt P22223、CADH3、ヒトカドヘリン−3)中で同定された配列と一致する。
抗P−カドヘリンCDRのパラトープマッピング
相補性決定領域(CDR)中のどのアミノ酸(AA)残基がヒトP−カドヘリンへのscFv 153結合に関与するかをさらに理解するために、全ての非アラニンCDR AAを、平行部位特異的突然変異誘発によって個別にアラニンに突然変異させた。
63のオリゴ(長さ33〜45塩基)を設計した(表45)。オリゴの長さを、同等の融点(Tm)予測値を有するようにそれぞれのオリゴについて調整した。それぞれのオリゴを、クローン153 scFvのセンス鎖の逆相補体であり、「AGC」(アラニンコドンの逆相補体、GCT)のいずれかの側の15〜21塩基に隣接するように設計した。
scFvを、ファージ粒子の表面上で発現させることができる。表面上にscFvを発現するファージを調製するために、2%グルコース/100μg/mLアンピシリンと共に1mLの2X TY培地を含有する96ディープウェルプレートに、QPix(商標)2コロニーピッカー(Molecular Devices、Sunnyvale CA)を使用して解凍されたグリセロールストック(1ウェルあたり1個のクローン)からの0.5〜1μLを接種し、37℃(900rpm)で約4時間増殖させた。次に、5μLの1:29ヘルパーファージ希釈液(8.3x1013pfu)を添加し、プレートを振盪せずに37℃でさらに30分間インキュベートした後、300rpmで1時間インキュベートした。プレートを遠心分離し、培地を、カナマイシン/非グルコース含有培地(50μg/mLのカナマイシンおよび100μg/mLのアンピシリンを含む2X TY)と交換した。プレートを25℃(900rpm)で一晩増殖させ、遠心分離後、上清中にファージを回収した。
P−カドヘリン−ECD1−3−Fcタンパク質または陰性対照タンパク質を、PBS+Ca2+およびMg2+中2μg/mLの濃度で、96ウェルNunc Maxisorp(登録商標)プレート(Thermo Fisher Scientific、Madison、CT)上に4℃で一晩コーティングした。PBS+Ca2+およびMg2+を使用してプレートを3回洗浄し、3%ミルク/PBS+Ca2+およびMg2+中、室温で1時間ブロックした。上記のように調製されたファージ試料を室温で1時間、ブロックされたプレートに添加した。PBS+Ca2+およびMg2+で3回、プレートを洗浄した後、二次抗体(抗M13−HRP 1:2000、GE Healthcare、Piscataway、NJ)を添加した。プレートを室温でさらに1時間インキュベートし、PBS+Ca2+およびMg2+で6回洗浄した。TMB(SurModics、Eden Prairie、MN)を使用してシグナルを展開し、H2SO4で反応を停止させ、EnVision(登録商標)プレートリーダー(Perkin Elmer、Waltham、MA)上、450nmで吸光度を読み取った。
ヒトP−カドヘリン−Fcタンパク質への抗P−カドヘリンscFv 153アラニン突然変異体のファージ調製物の結合を、ELISAによって試験した。データを総結合シグナル(OD450)および親クローン153と比較した結合のパーセントとしてプロットした。次いで、Z−スコアを、クローン153の結合パーセントの標準偏差に基づいて算出した。このアッセイに関するデータを、表46および表47に提示する。
Claims (76)
- P−カドヘリンのエピトープとCD3のエピトープとに特異的に結合することができる二重特異的ヘテロ二量体ダイアボディであって、第1のポリペプチド鎖および第2のポリペプチド鎖を含み、
a.第1のポリペプチドが、N末端からC末端の方向に、
i.サブドメイン1Aとサブドメイン1Bとを含むドメイン1、および
ii.第1のヘテロ二量体促進ドメイン
を含み、
b.第2のポリペプチド鎖が、N末端からC末端の方向に、
i.サブドメイン2Aとサブドメイン2Bとを含むドメイン2、および
ii.第2のヘテロ二量体促進ドメイン
を含み、
サブドメイン1Aとサブドメイン2Aが、抗P−カドヘリン抗体の可変重鎖(VH)ドメイン(P−CAD VH)と、抗P−カドヘリン抗体の可変軽鎖(VL)ドメイン(P−CAD VL)とを含むP−カドヘリンVL/VH結合ドメインを形成し、サブドメイン1Bとサブドメイン2Bが、抗CD3抗体のVLドメイン(CD3 VL)と、抗CD3抗体のVH結合ドメイン(CD3 VH)とを含むCD3 VL/VH結合ドメインを形成する、または
サブドメイン1Aとサブドメイン2Aが、CD3 VLとCD3 VHとを含むCD3 VL/VH結合ドメインを形成し、サブドメイン1Bとサブドメイン2BがP−CAD VHとP−CAD VLとを含むP−カドヘリンVL/VH結合ドメインを形成する、二重特異的ヘテロ二量体ダイアボディ。 - サブドメイン1AがP−CAD VLまたはCD3 VLを含み、サブドメイン1Bが、サブドメイン1AがCD3 VLを含む場合、P−CAD VH、またはサブドメイン1AがP−CAD VLを含む場合、CD3 VHを含み、サブドメイン2Bがサブドメイン1Aについて選択されるVLドメインに応じてP−CAD VLまたはCD3 VLを含み、サブドメイン2Aが、サブドメイン2BがCD3 VLを含む場合、P−CAD VH、またはサブドメイン2BがP−CAD VLを含む場合、CD3 VHを含む、請求項1に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1AがP−CAD VLを含み、サブドメイン1BがCD3 VHを含み、サブドメイン2BがCD3 VLを含み、サブドメイン2AがP−CAD VHを含む、請求項1または2に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1AがCD3 VLを含み、サブドメイン1BがP−CAD VHを含み、サブドメイン2BがP−CAD VLを含み、サブドメイン2AがCD3 VHを含む、請求項1または2に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1AがP−CAD VHまたはCD3 VHを含み、サブドメイン1Bが、サブドメイン1AがCD3 VHを含む場合、P−CAD VL、またはサブドメイン1AがP−CAD VHを含む場合、CD3 VLを含み、サブドメイン2Bが、サブドメイン1Aについて選択されるVHドメインに応じてP−CAD VHまたはCD3 VHを含み、サブドメイン2Aが、サブドメイン2BがCD3 VHを含む場合、P−CAD VL、またはサブドメイン2BがP−CAD VHを含む場合、CD3 VLを含む、請求項1に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1AがP−CAD VHを含み、サブドメイン1BがCD3 VLを含み、サブドメイン2BがCD3 VHを含み、サブドメイン2AがP−CAD VLを含む、請求項1または5に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1AがCD3 VHを含み、サブドメイン1BがP−CAD VLを含み、サブドメイン2BがP−CAD VHを含み、サブドメイン2AがCD3 VLを含む、請求項1または5に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインと第2のヘテロ二量体促進ドメインが、CH2およびCH3ドメインを含むIgG Fc領域を含み、CH2ドメインおよび/またはCH3ドメインのアミノ酸配列が、ノブまたはホールを形成するように、野生型IgG Fc領域と比較して、少なくとも1つのアミノ酸改変を含み、請求項1から7のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインと第2のヘテロ二量体促進ドメインが両方ともノブもしくは両方ともホールではなく、および/または第1のヘテロ二量体促進ドメインと第2のヘテロ二量体促進ドメインがIgG免疫グロブリンFc領域を形成する、請求項8に記載の二重特異的ヘテロ二量体ダイアボディ。
- ノブを形成するIgG Fc領域が配列番号63の配列を含み、ホールを形成するIgG Fc領域が配列番号64の配列を含む、請求項8または9のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインと第2のヘテロ二量体促進ドメインが、グルタミン酸および負に荷電したアルファ−ヘリックスコイルを含むE−コイル領域またはリシンおよび正に荷電したヘリックスコイルを含むK−コイル領域を含み、第1のヘテロ二量体促進ドメインと第2のヘテロ二量体促進ドメインが両方ともE−コイル領域または両方ともK−コイル領域ではない、請求項1から7のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- E−コイル領域が配列番号61の配列を含み、および/またはK−コイル領域が配列番号62の配列を含む、請求項11に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1Aとサブドメイン1Bが、グリシン−セリンリンカー(リンカー1)によって連結され、サブドメイン2Bとサブドメイン2Aが、グリシン−セリンリンカー(リンカー1)によって連結されている、請求項1から12のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- グリシン−セリンリンカー(リンカー1)が、配列番号68または配列番号69の配列を含む、請求項13に記載の二重特異的ヘテロ二量体ダイアボディ。
- サブドメイン1Aとサブドメイン1Bが結合してVL/VHエピトープ結合ドメインを形成せず、サブドメイン2Bとサブドメイン2Aが結合してVL/VHエピトープ結合ドメインを形成しない、請求項1から14のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインがサブドメイン1B上にシステインリンカー(リンカー2)を含む、および/または第2のヘテロ二量体促進ドメインがサブドメイン2A上にシステインリンカー(リンカー2)を含む、請求項1から15のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインおよび/または第2のヘテロ二量体促進ドメインのリンカー2が、少なくとも1つのグリシン残基をさらに含む、請求項16に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインおよび/または第2のヘテロ二量体促進ドメインのリンカー2が、GFNRGEC(配列番号70)、GVEPKSC(配列番号71)、GGCGGG(配列番号72)、GCPPCP(配列番号73)、GGTGGCPPCP(配列番号74)、GEPKSSDKTHTCPPCP(配列番号75)またはGGTGGGEPKSSDKTHTCPPCP(配列番号76)の配列を含む、請求項17に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインのリンカー2が、GCPPCP(配列番号73)、GGTGGCPPCP(配列番号74)、GEPKSSDKTHTCPPCP(配列番号75)またはGGTGGGEPKSSDKTHTCPPCP(配列番号76)を含み、第2のヘテロ二量体促進ドメインのリンカー2が、GCPPCP(配列番号73)、GGTGGCPPCP(配列番号74)、GEPKSSDKTHTCPPCP(配列番号75)またはGGTGGGEPKSSDKTHTCPPCP(配列番号76)の配列を含む、請求項18に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインのリンカー2が、GGCGGG(配列番号72)の配列を含み、第2のヘテロ二量体促進ドメインのリンカー2が、GGCGGG(配列番号72)の配列を含む、請求項18に記載の二重特異的ヘテロ二量体ダイアボディ。
- 第1のヘテロ二量体促進ドメインのリンカー2が、GFNRGEC(配列番号70)の配列を含み、第2のヘテロ二量体促進ドメインのリンカー2が、GVEPKSC(配列番号71)を含み、または第1のヘテロ二量体促進ドメインのリンカー2が、GVEPKSC(配列番号71)の配列を含み、第2のヘテロ二量体促進ドメインのリンカー2が、GFNRGEC(配列番号70)の配列を含む、請求項18に記載の二重特異的ヘテロ二量体ダイアボディ。
- a.ヒトP−カドヘリンの細胞外ドメイン3(ECD3)に結合する、
b.P−カドヘリン上のエピトープに結合するが、E−カドヘリンもしくはVE−カドヘリン上のエピトープには結合しない、
c.ヒトP−カドヘリン上のエピトープに結合するが、マウスP−カドヘリン上のエピトープには結合しない、
d.長い血清および腫瘍半減期を示す、または
e.増大したP−カドヘリン発現レベルもしくは増大した受容体密度レベルの存在下で、より低いEC50を示す、
請求項1から21のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。 - a.XL1.1−XL1.2−XL1.3−XL1.4−XL1.5−XL1.6−XL1.7−XL1.8−XL1.9−XL1.10−XL1.11−XL1.2−XL1.13を含むP−CAD VL CDR1配列、
b.XL2.1−XL2.2−XL2.3−XL2.4−XL2.5−XL2.6−XL2.7を含むP−CAD VL CDR2配列、
c.P−CAD VL CDR3配列 XL3.1−XL3.2−XL3.3−XL3.4−XL3.5−XL3.6−XL3.7−XL3.8−XL3.9−XL3.10−XL3.11、
d.XH1.1−XH1.2−XH1.3−XH1.4−XH1.5−XH1.6−XH1.7−XH1.8−XH1.9−XH1.10またはXH1.5、XH1.6−XH1.7−XH1.8−XH1.9−XH1.10を含むP−CAD VH CDR1配列、
e.XH2.1−XH2.2−XH2.3−XH2.4−XH2.5−XH2.6−XH2.7−XH2.8−XH2.9−XH2.10またはXH2.1−XH2.2−XH2.3−XH2.4−XH2.5−XH2.6−XH2.7−XH2.8−XH2.9−XH2.10−XH2.11−XH2.12−XH2.13−XH2.14−XH2.15−XH2.16−XH2.17を含むP−CAD VH CDR2配列、および
f.XH3.1−XH3.2−XH3.3−XH3.4−XH3.5−XH3.6−XH3.7−XH3.8−XH3.9を含むP−CAD VH CDR3配列
を含み、ここで、XL3.3がWであり、XH1.8がGであり、XH2.5がYであり、XH3.1がIであり、XH3.7がFである、請求項1から22のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。 - XL1.8がGであり、XL2.2がNであり、XL2.3がNであり、XL3.2がTであり、XH2.6がNであり、XH2.16がQであり、XH3.5がNであり、XH3.9がIである、請求項23に記載の二重特異的ヘテロ二量体ダイアボディ。
- a.配列番号1、3、5、7、9、11、13、15、17、19、21もしくは23の配列を含むP−CAD VLのP−CAD VL CDR1、P−CAD VL CDR2、およびP−CAD VL CDR3、
b.配列番号45もしくは46の配列を含むCD3 VHのCD3 VH CDR1、CD3 VH CDR2、およびCD3 VH CDR3
c.配列番号47の配列を含むCD3 VLのCD3 VL CDR1、CD3 VL CDR2、およびCD3 VL CDR3、ならびに/または
d.配列番号2、4、6、8、10、12、14、16、18、20、22もしくは24の配列を含むP−CAD VHのP−CAD VH CDR1、P−CAD VH CDR2、およびP−CAD VH CDR3
を含む、請求項1から24のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。 - a.P−CAD VL CDR1が配列番号35もしくは36の配列を含み、P−CAD VL CDR2が配列番号37もしくは38の配列を含み、P−CAD VL CDR3が配列番号39、40、41、42、43もしくは44の配列を含む、
b.CD3 VH CDR1が配列番号48の配列を含み、CD3 VH CDR2が配列番号49もしくは50の配列を含み、CD3 VH CDR3が配列番号51の配列を含む、
c.CD3 VL CDR1が配列番号55の配列を含み、CD3 VL CDR2が配列番号56の配列を含み、CD3 VL CDR3が配列番号57の配列を含む、および/または
d.P−CAD VH CDR1が配列番号25もしくは33の配列を含み、P−CAD VH CDR2が配列番号26もしくは34の配列を含み、P−CAD VH CDR3が配列番号27、28、29、30、31、もしくは32の配列を含む、
請求項25に記載の二重特異的ヘテロ二量体ダイアボディ。 - P−CAD VL CDR1が配列番号35の配列を含み、P−CAD VL CDR2が配列番号37の配列を含み、P−CAD VL CDR3が配列番号41の配列を含み、P−CAD VH CDR1が配列番号25の配列を含み、P−CAD VH CDR2が配列番号26の配列を含み、P−CAD VH CDR3が配列番号28の配列を含む、請求項25または26に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VL CDR1が配列番号35の配列を含み、P−CAD VL CDR2が配列番号37の配列を含み、P−CAD VL CDR3が配列番号42の配列を含み、P−CAD VH CDR1が配列番号25の配列を含み、P−CAD VH CDR2が配列番号26の配列を含み、P−CAD VH CDR3が配列番号29の配列を含む、請求項25または26に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VL CDR1が配列番号35の配列を含み、P−CAD VL CDR2は配列番号37の配列を含み、P−CAD VL CDR3が配列番号43の配列を含み、P−CAD VH CDR1が配列番号25の配列を含み、P−CAD VH CDR2が配列番号26の配列を含み、P−CAD VH CDR3が配列番号30の配列を含む、請求項25または26に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VL CDR1が配列番号35の配列を含み、P−CAD VL CDR2が配列番号37の配列を含み、P−CAD VL CDR3が配列番号39の配列を含み、P−CAD VH CDR1が配列番号25の配列を含み、P−CAD VH CDR2が配列番号26の配列を含み、P−CAD VH CDR3が配列番号31の配列を含む、請求項25または26に記載の二重特異的ヘテロ二量体ダイアボディ。
- a.P−CAD VLが配列番号1、3、5、7、9、11、13、15、17、19、21または23の配列を含み、
b.CD3 VHが配列番号45または46の配列を含み、
c.CD3 VLが配列番号47の配列を含み、
d.P−CAD VHが配列番号2、4、6、8、10、12、14、16、18、20、22または24の配列を含む、
請求項1から30のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。 - P−CAD VLが配列番号5の配列を含み、P−CAD VHが配列番号6の配列を含む、請求項31に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VLが配列番号7の配列を含み、P−CAD VHが配列番号8の配列を含む、請求項31に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VLが配列番号9の配列を含み、P−CAD VHが配列番号10の配列を含む、請求項31に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−CAD VLが配列番号15の配列を含み、P−CAD VHが配列番号16の配列を含む、請求項31に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンのエピトープとCD3のエピトープとに特異的に結合することができる二重特異的ヘテロ二量体ダイアボディであって、第1のポリペプチド鎖および第2のポリペプチド鎖を含み、第1のポリペプチド鎖が配列番号90の配列を含み、第2のポリペプチド鎖が配列番号91の配列を含む、二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンのエピトープとCD3のエピトープとに特異的に結合することができる二重特異的ヘテロ二量体ダイアボディであって、第1のポリペプチド鎖および第2のポリペプチド鎖を含み、第1のポリペプチド鎖が配列番号92の配列を含み、第2のポリペプチド鎖が配列番号93の配列を含む、二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンのエピトープとCD3のエピトープとに特異的に結合することができる二重特異的ヘテロ二量体ダイアボディであって、第1のポリペプチド鎖および第2のポリペプチド鎖を含み、第1のポリペプチド鎖が配列番号88の配列を含み、第2のポリペプチド鎖が配列番号89の配列を含む、二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンのエピトープとCD3のエピトープとに特異的に結合することができる二重特異的ヘテロ二量体ダイアボディであって、第1のポリペプチド鎖および第2のポリペプチド鎖を含み、第1のポリペプチド鎖および第2のポリペプチド鎖が図30A、図30B、図31A、図31B、図32Aまたは図32Bに記載の配列を含む二重特異的ヘテロ二量体ダイアボディ。
- 第1および第2のポリペプチド鎖が、少なくとも1つのジスルフィド結合によって互いに共有結合している、請求項1から39のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンに結合し、請求項1から40のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディと競合する、二重特異的ヘテロ二量体ダイアボディ。
- 治療有効量の請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディと、薬学的に許容できる担体とを含む医薬組成物。
- それを必要とする患者に、請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディまたは請求項42に記載の医薬組成物を投与することを含む、患者におけるP−カドヘリン関連障害を処置する方法。
- P−カドヘリン関連障害ががんである、請求項43に記載の方法。
- がんが、乳がん、結腸直腸がん、卵巣がん、胃がん、甲状腺がん、前立腺がん、子宮頸がん、膵臓がん、肺がん、膀胱がん、肝臓がん、子宮内膜がん、頭頸部がん、精巣がん、およびグリア芽腫からなる群から選択される、請求項44に記載の方法。
- それを必要とする患者に、請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体または請求項42に記載の医薬組成物を投与することを含み、細胞溶解性T細胞応答が活性化される、患者におけるP−カドヘリン関連障害を処置する方法。
- 療法における使用のための請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- 療法における使用のための医薬品の製造における請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディの使用。
- 療法が、P−カドヘリン関連障害の処置である、請求項47または48に記載の使用のための二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリン関連障害ががんである、請求項49に記載の使用のための二重特異的ヘテロ二量体ダイアボディ。
- がんが、乳がん、結腸直腸がん、卵巣がん、胃がん、甲状腺がん、前立腺がん、子宮頸がん、膵臓がん、肺がん、膀胱がん、肝臓がん、子宮内膜がん、頭頸部がん、精巣がん、およびグリア芽腫からなる群から選択される、請求項50に記載の使用のための二重特異的ヘテロ二量体ダイアボディ。
- 療法が細胞溶解性T細胞応答を活性化する、請求項47または48に記載の使用のための二重特異的ヘテロ二量体ダイアボディ。
- 請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディを組換え産生する単離された宿主細胞。
- 請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディをコードするヌクレオチド配列を含む単離されたポリヌクレオチド。
- 請求項54に記載のポリヌクレオチドを含むベクター。
- 二重特異的ヘテロ二量体ダイアボディの産生をもたらす条件下で請求項53に記載の宿主細胞を培養すること、および培養上清から二重特異的ヘテロ二量体ダイアボディを精製することを含む、二重特異的ヘテロ二量体ダイアボディを産生する方法。
- 結晶構造が、サブドメイン1Bの239位のシステイン残基(Cys239)およびサブドメイン2Aの246位のシステイン残基(Cys246)を含むシステイン残基対の間のジスルフィド結合によって安定化される小型の球状構造として構築されており、結晶が原子座標の決定のためにX線を回折して、約2.0オングストロームより良好な分解能を提供する、請求項1から41のいずれか一項に記載の二重特異的ヘテロ二量体ダイアボディ。
- P−カドヘリンに結合する抗体であって、
a.XL1.1−XL1.2−XL1.3−XL1.4−XL1.5−XL1.6−XL1.7−XL1.8−XL1.9−XL1.10−XL1.11−XL1.2−XL1.13を含むP−CAD VL CDR1配列、
b.XL2.1−XL2.2−XL2.3−XL2.4−XL2.5−XL2.6−XL2.7を含むP−CAD VL CDR2配列、
c.P−CAD VL CDR3配列 XL3.1−XL3.2−XL3.3−XL3.4−XL3.5−XL3.6−XL3.7−XL3.8−XL3.9−XL3.10−XL3.11、
d.XH1.1−XH1.2−XH1.3−XH1.4−XH1.5−XH1.6−XH1.7−XH1.8−XH1.9−XH1.10またはXH1.5、XH1.6−XH1.7−XH1.8−XH1.9−XH1.10を含むP−CAD VH CDR1配列、
e.XH2.1−XH2.2−XH2.3−XH2.4−XH2.5−XH2.6−XH2.7−XH2.8−XH2.9−XH2.10またはXH2.1−XH2.2−XH2.3−XH2.4−XH2.5−XH2.6−XH2.7−XH2.8−XH2.9−XH2.10−XH2.11−XH2.12−XH2.13−XH2.14−XH2.15−XH2.16−XH2.17を含むP−CAD VH CDR2配列、および
f.XH3.1−XH3.2−XH3.3−XH3.4−XH3.5−XH3.6−XH3.7−XH3.8−XH3.9を含むP−CAD VH CDR3配列
を含み、ここで、XL3.3がWであり、XH1.8がGであり、XH2.5がYであり、XH3.1がIであり、XH3.7がFである、抗体。 - XL1.8がGであり、XL2.2がNであり、XL2.3がNであり、XL3.2がTであり、XH2.6がNであり、XH2.16がQであり、XH3.5がNであり、XH3.9がIである、請求項58に記載の抗体。
- 配列番号1、3、5、7、9、11、13、15、17、19、21もしくは23の配列を含む軽鎖可変領域のP−CAD VL CDR1、P−CAD VL CDR2およびP−CAD VL CDR3ならびに/または配列番号2、4、6、8、10、12、14、16、18、20、22もしくは24の配列を含む重鎖可変領域のP−CAD VH CDR1、P−CAD VH CDR2およびP−CAD VH CDR3を含む、請求項58または59に記載の抗体。
- a.配列番号35または36の配列を含むP−CAD VL CDR1、
b.配列番号37または38の配列を含むP−CAD VL CDR2、
c.配列番号39、40、41、42、43または44の配列を含むP−CAD VL CDR3、
d.配列番号25または33の配列を含むP−CAD VH CDR1、
e.配列番号26または34の配列を含むP−CAD VH CDR2、および
f.配列番号27、28、29、30、31または32の配列を含むP−CAD VH CDR3
を含む、請求項58から60のいずれか一項に記載の抗体。 - a.配列番号35または36の配列を含むP−CAD VL CDR1、
b.配列番号37または38の配列を含むP−CAD VL CDR2、
c.配列番号39、40、41、42、43または44の配列を含むP−CAD VL CDR3、
d.配列番号25の配列を含むP−CAD VH CDR1、
e.配列番号26の配列を含むP−CAD VH CDR2、および
f.配列番号27、28、29、30、31または32の配列を含むP−CAD VH CDR3
を含む、請求項58から61のいずれか一項に記載の抗体。 - a.配列番号35の配列を含むP−CAD VL CDR1、
b.配列番号37の配列を含むP−CAD VL CDR2、
c.配列番号42の配列を含むP−CAD VL CDR3、
d.配列番号25の配列を含むP−CAD VH CDR1、
e.配列番号26の配列を含むP−CAD VH CDR2、および
f.配列番号29の配列を含むP−CAD VH CDR3
を含む、請求項58から62のいずれか一項に記載の抗体。 - 配列番号1、3、5、7、9、11、13、15、17、19、21および23の配列を含む軽鎖可変領域、ならびに/または配列番号2、4、6、8、10、12、14、16、18、20、22もしくは24の配列を含む重鎖可変領域を含む、請求項58から63のいずれか一項に記載の抗体。
- 配列番号5の配列を含む軽鎖可変領域アミノ酸および/または配列番号6の配列を含む重鎖可変領域を含む、請求項64に記載の抗体。
- 配列番号7の配列を含む軽鎖可変領域および/または配列番号8の配列を含む重鎖可変領域を含む、請求項64に記載の抗体。
- 配列番号9の配列を含む軽鎖可変領域および/または配列番号10の配列を含む重鎖可変領域を含む、請求項64に記載の抗体。
- 配列番号15の配列を含む軽鎖可変領域および/または配列番号16の配列を含む重鎖可変領域を含む、請求項64に記載の抗体。
- P−カドヘリンに結合し、請求項58から68のいずれか一項に記載の抗体とP−カドヘリンへの結合について競合する抗体。
- 治療有効量の請求項58から69のいずれか一項に記載の抗体と、薬学的に許容できる担体とを含む医薬組成物。
- それを必要とする患者に、請求項58から69のいずれか一項に記載の抗体または請求項70に記載の医薬組成物を投与することを含む、患者におけるP−カドヘリン陽性がんを処置する方法。
- 療法における使用のための請求項58から69のいずれか一項に記載の抗体。
- 療法における使用のための医薬品の製造における請求項58から69のいずれか一項に記載の抗体の使用。
- 請求項58から69のいずれか一項に記載の抗体をコードする核酸。
- 請求項74に記載の核酸を含むベクター。
- 請求項75に記載のベクターを含む宿主細胞。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462019762P | 2014-07-01 | 2014-07-01 | |
| US62/019,762 | 2014-07-01 | ||
| US201562148920P | 2015-04-17 | 2015-04-17 | |
| US62/148,920 | 2015-04-17 | ||
| PCT/IB2015/054829 WO2016001810A1 (en) | 2014-07-01 | 2015-06-26 | Bispecific heterodimeric diabodies and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017520575A true JP2017520575A (ja) | 2017-07-27 |
| JP2017520575A5 JP2017520575A5 (ja) | 2018-08-02 |
Family
ID=53718063
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016575335A Pending JP2017520575A (ja) | 2014-07-01 | 2015-06-26 | 二重特異的ヘテロ二量体ダイアボディおよびその使用 |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US9884921B2 (ja) |
| EP (1) | EP3164417A1 (ja) |
| JP (1) | JP2017520575A (ja) |
| KR (1) | KR20170010863A (ja) |
| CN (1) | CN106661119A (ja) |
| AU (2) | AU2015283704A1 (ja) |
| BR (1) | BR112016030740A2 (ja) |
| CA (1) | CA2895659A1 (ja) |
| CO (1) | CO2017000016A2 (ja) |
| IL (1) | IL249889A0 (ja) |
| MX (1) | MX2016017393A (ja) |
| PE (1) | PE20170286A1 (ja) |
| PH (1) | PH12016502491A1 (ja) |
| RU (1) | RU2016151645A (ja) |
| SG (1) | SG11201609707WA (ja) |
| TW (2) | TW201936638A (ja) |
| WO (1) | WO2016001810A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021525080A (ja) * | 2018-05-23 | 2021-09-24 | ファイザー・インク | GUCY2cに特異的な抗体及びその使用 |
Families Citing this family (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SG10202007326QA (en) | 2014-12-05 | 2020-08-28 | Memorial Sloan Kettering Cancer Center | Chimeric antigen receptors targeting g-protein coupled receptor and uses thereof |
| EP3227324A4 (en) * | 2014-12-05 | 2018-08-29 | Memorial Sloan Kettering Cancer Center | Antibodies targeting g-protein coupled receptor and methods of use |
| FI3283524T3 (fi) * | 2015-04-17 | 2023-05-05 | Amgen Res Munich Gmbh | Bispesifisiä vasta-ainekonstrukteja cdh3:lle ja cd3:lle |
| EP3322735A4 (en) * | 2015-07-15 | 2019-03-13 | Zymeworks Inc. | BISPECIFIC ANTIGEN-BINDING CONSTRUCTS CONJUGATED TO A MEDICINAL PRODUCT |
| US20190185578A1 (en) * | 2016-07-29 | 2019-06-20 | Chugai Seiyaku Kabushiki Kaisha | Bispecific antibody exhibiting increased alternative fviii-cofactor-function activity |
| CN106496331B (zh) * | 2016-11-08 | 2020-03-13 | 北京智岭生物医药科技有限公司 | 一种FSH-Fc融合蛋白及其制备方法和用途 |
| SG11201907299XA (en) | 2017-02-08 | 2019-09-27 | Dragonfly Therapeutics Inc | Multi-specific binding proteins for activation of natural killer cells and therapeutic uses thereof to treat cancer |
| WO2018178055A1 (en) * | 2017-03-29 | 2018-10-04 | F. Hoffmann-La Roche Ag | Bispecific antigen binding molecule for a costimulatory tnf receptor |
| AU2018243114C1 (en) * | 2017-03-29 | 2022-05-05 | Cytoarm Co., Ltd. | Antigen-specific T cells and uses thereof |
| JP7205995B2 (ja) * | 2017-03-29 | 2023-01-17 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | 共刺激性tnf受容体に対する二重特異性抗原結合分子 |
| CN108866635B (zh) * | 2017-05-09 | 2021-11-26 | 安升(上海)医药科技有限公司 | 多特异性蛋白药物及其文库、以及制备方法和应用 |
| JP7018458B2 (ja) * | 2017-06-02 | 2022-02-10 | ファイザー・インク | 組換えrobo2タンパク質、組成物、方法およびそれらの使用 |
| TWI690539B (zh) * | 2017-06-22 | 2020-04-11 | 財團法人生物技術開發中心 | 一個需依賴標靶細胞使T細胞接合及活化之不對稱異二聚Fc-ScFv融合抗體形式及其在癌症治療上之應用 |
| JP6496095B1 (ja) | 2017-09-29 | 2019-04-03 | 中外製薬株式会社 | 血液凝固第viii因子(fviii)補因子機能代替活性を有する多重特異性抗原結合分子および当該分子を有効成分として含有する薬学的製剤 |
| KR101973060B1 (ko) * | 2017-10-20 | 2019-04-26 | 주식회사 녹십자 | 항-cd3 항체 및 이를 포함하는 암 치료용 약학적 조성물 |
| CN109706164A (zh) * | 2017-10-26 | 2019-05-03 | 深圳新诺微环生物科技有限公司 | 微环dna表达连接人和猴cd20与效应细胞抗原的桥接分子及其应用 |
| CN109706163A (zh) * | 2017-10-26 | 2019-05-03 | 深圳新诺微环生物科技有限公司 | 微环dna表达连接人与动物靶细胞与效应细胞的桥接分子及其应用 |
| CN112368012A (zh) | 2018-02-08 | 2021-02-12 | 蜻蜓疗法股份有限公司 | 靶向nkg2d受体的抗体可变结构域 |
| RU2020128440A (ru) | 2018-02-28 | 2022-03-28 | Пфайзер Инк. | Варианты il-15 и их применения |
| JP2021523140A (ja) * | 2018-05-07 | 2021-09-02 | ドラゴンフライ セラピューティクス, インコーポレイテッド | Nkg2d、cd16、及び腫瘍関連抗原に結合するタンパク質 |
| JP7384835B2 (ja) | 2018-05-23 | 2023-11-21 | ファイザー・インク | Cd3に特異的な抗体及びその使用 |
| WO2020128893A1 (en) | 2018-12-21 | 2020-06-25 | Pfizer Inc. | Combination treatments of cancer comprising a tlr agonist |
| CN113260379B (zh) * | 2018-12-21 | 2022-09-02 | 浙江时迈药业有限公司 | 蛋白酶可切割的双特异性抗体及其用途 |
| CN110357969B (zh) * | 2019-05-27 | 2022-03-08 | 北京志道生物科技有限公司 | 一种GLP1-EGFa异源二聚体蛋白、功能及方法 |
| US11339159B2 (en) | 2019-07-17 | 2022-05-24 | Pfizer Inc. | Toll-like receptor agonists |
| CN113416258B (zh) * | 2019-10-24 | 2023-08-29 | 北京免疫方舟医药科技有限公司 | 一种多特异性抗体及其制备方法和用途 |
| EP4077387A1 (en) | 2019-12-17 | 2022-10-26 | Pfizer Inc. | Antibodies specific for cd47, pd-l1, and uses thereof |
| TW202128176A (zh) | 2019-12-18 | 2021-08-01 | 美商輝瑞股份有限公司 | 使用蛋白精胺酸甲基轉移酶5(prmt5)抑制劑之每日一次癌症治療方案 |
| EP4118105A2 (en) | 2020-03-09 | 2023-01-18 | Pfizer Inc. | Cd80-fc fusion protein and uses thereof |
| JP2023524854A (ja) | 2020-05-13 | 2023-06-13 | ファイザー・インク | がんを処置するための方法、治療、および使用 |
| PE20231565A1 (es) | 2020-07-17 | 2023-10-04 | Pfizer | Anticuerpos terapeuticos y sus usos |
| TW202224703A (zh) | 2020-09-14 | 2022-07-01 | 美商輝瑞股份有限公司 | 治療癌症之方法、治療劑及用途 |
| WO2022153161A1 (en) | 2021-01-14 | 2022-07-21 | Pfizer Inc. | Treatment of cancer using a prmt5 inhibitor |
| CN114539420A (zh) * | 2022-01-20 | 2022-05-27 | 同济大学苏州研究院 | 抗b7-h3单克隆抗体、抗b7-h3×cd3双特异性抗体、制备方法及其应用 |
| WO2023218320A1 (en) | 2022-05-11 | 2023-11-16 | Pfizer Inc. | Anti-lymphotoxin beta receptor antibodies and methods of use thereof |
| WO2023242769A1 (en) | 2022-06-17 | 2023-12-21 | Pfizer Inc. | Il-12 variants, anti-pd1 antibodies, fusion proteins, and uses thereof |
| WO2024003773A1 (en) | 2022-07-01 | 2024-01-04 | Pfizer Inc. | 2,7-naphthyridine compounds as mastl inhibitors |
| WO2024009191A1 (en) | 2022-07-05 | 2024-01-11 | Pfizer Inc. | Pyrido[4,3-d]pyrimidine compounds |
| WO2024074977A1 (en) | 2022-10-04 | 2024-04-11 | Pfizer Inc. | Substituted 1 h-pyrazolo-pyridine and-pyrimidine compounds |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006515318A (ja) * | 2002-10-29 | 2006-05-25 | ファルマシア・コーポレーション | 特異的に発現する癌関連遺伝子、それによってコードされるポリペプチドおよびその使用方法 |
| JP2009508466A (ja) * | 2005-04-15 | 2009-03-05 | マクロジェニクス,インコーポレーテッド | 共有結合型ダイアボディとその使用 |
| JP2011526583A (ja) * | 2008-06-30 | 2011-10-13 | オンコセラピー・サイエンス株式会社 | 放射性同位体標識で標識された抗cdh3抗体およびその使用 |
Family Cites Families (193)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3382317D1 (de) | 1982-03-15 | 1991-07-25 | Schering Corp | Hybride dns, damit hergestellte bindungszusammensetzung und verfahren dafuer. |
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US5869620A (en) | 1986-09-02 | 1999-02-09 | Enzon, Inc. | Multivalent antigen-binding proteins |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| US5091513A (en) | 1987-05-21 | 1992-02-25 | Creative Biomolecules, Inc. | Biosynthetic antibody binding sites |
| WO1991001752A1 (en) | 1989-07-27 | 1991-02-21 | Fred Hutchinson Cancer Research Center | Immunosuppressive monoclonal antibodies, hybridomas and methods of transplantation |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US5811267A (en) | 1990-10-29 | 1998-09-22 | Chiron Corporation | Isolated nucleic acid molecules encoding antigen binding sites of antibody molecules specific for cancer antigens |
| DE4118120A1 (de) | 1991-06-03 | 1992-12-10 | Behringwerke Ag | Tetravalente bispezifische rezeptoren, ihre herstellung und verwendung |
| US6129914A (en) | 1992-03-27 | 2000-10-10 | Protein Design Labs, Inc. | Bispecific antibody effective to treat B-cell lymphoma and cell line |
| WO1994007921A1 (en) | 1992-09-25 | 1994-04-14 | Commonwealth Scientific And Industrial Research Organisation | Target binding polypeptide |
| AU5670194A (en) | 1992-11-20 | 1994-06-22 | Enzon, Inc. | Linker for linked fusion polypeptides |
| US5837242A (en) | 1992-12-04 | 1998-11-17 | Medical Research Council | Multivalent and multispecific binding proteins, their manufacture and use |
| ATE187494T1 (de) | 1992-12-11 | 1999-12-15 | Dow Chemical Co | Multivalente einkettige antikörper |
| DE69432744T2 (de) | 1993-02-04 | 2004-03-25 | Borean Pharma A/S | Verbessertes verfahren zur rückfaltung der proteine |
| US5747654A (en) | 1993-06-14 | 1998-05-05 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant disulfide-stabilized polypeptide fragments having binding specificity |
| US6476198B1 (en) | 1993-07-13 | 2002-11-05 | The Scripps Research Institute | Multispecific and multivalent antigen-binding polypeptide molecules |
| WO1995009917A1 (en) | 1993-10-07 | 1995-04-13 | The Regents Of The University Of California | Genetically engineered bispecific tetravalent antibodies |
| IT1271461B (it) | 1993-12-01 | 1997-05-28 | Menarini Ricerche Sud Spa | Anticorpo monoclonale bispecifico anti-cd3/anti-egfr,processo per la produzione e suo uso. |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| WO1997014719A1 (en) | 1995-10-16 | 1997-04-24 | Unilever N.V. | A bifunctional or bivalent antibody fragment analogue |
| AU722985B2 (en) | 1996-07-12 | 2000-08-17 | Mcgill University | Compounds and methods for modulating cell adhesion |
| CA2267620A1 (en) | 1996-07-16 | 1998-01-22 | Andreas Pluckthun | Immunoglobulin superfamily domains and fragments with increased solubility |
| AU6537798A (en) | 1997-03-14 | 1998-10-12 | Denise Casentini-Borocz | Targeted cytolysis of cancer cells |
| US7951917B1 (en) | 1997-05-02 | 2011-05-31 | Genentech, Inc. | Method for making multispecific antibodies having heteromultimeric and common components |
| US20020062010A1 (en) | 1997-05-02 | 2002-05-23 | Genentech, Inc. | Method for making multispecific antibodies having heteromultimeric and common components |
| US6670453B2 (en) | 1997-10-27 | 2003-12-30 | Unilever Patent Holdings B.V. | Multivalent antigen-binding proteins |
| US6485910B1 (en) | 1998-02-09 | 2002-11-26 | Incyte Genomics, Inc. | Ras association domain containing protein |
| ID26964A (id) | 1998-02-19 | 2001-02-22 | Xcyte Therapies Inc | Komposisi dan metode untuk pengaturan pengaktifan limfosit |
| CZ121599A3 (cs) | 1998-04-09 | 1999-10-13 | Aventis Pharma Deutschland Gmbh | Jednořetězcová molekula vázající několik antigenů, způsob její přípravy a léčivo obsahující tuto molekulu |
| US6783961B1 (en) | 1999-02-26 | 2004-08-31 | Genset S.A. | Expressed sequence tags and encoded human proteins |
| ID27512A (id) | 1998-04-21 | 2001-04-12 | Microment Ges Fur Biomedizinis | Polipeptid tetapan cd19xcd3 dan kegunaan-kegunaannya |
| DE19819846B4 (de) | 1998-05-05 | 2016-11-24 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Multivalente Antikörper-Konstrukte |
| GB9812545D0 (en) | 1998-06-10 | 1998-08-05 | Celltech Therapeutics Ltd | Biological products |
| WO2000006605A2 (en) | 1998-07-28 | 2000-02-10 | Micromet Ag | Heterominibodies |
| ES2293748T3 (es) | 1998-10-21 | 2008-03-16 | Altor Bioscience Corporation | Moleculas de fijacion poliespecificas y usos de las mismas. |
| WO2001057188A2 (en) | 2000-02-03 | 2001-08-09 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| US20020142000A1 (en) | 1999-01-15 | 2002-10-03 | Digan Mary Ellen | Anti-CD3 immunotoxins and therapeutic uses therefor |
| DE19905048A1 (de) | 1999-02-08 | 2000-08-10 | Gsf Forschungszentrum Umwelt | Verwendung depletorisch oder mitogen wirkender Antikörper in der Immuntherapie |
| CN101289511A (zh) | 2000-04-11 | 2008-10-22 | 杰南技术公司 | 多价抗体及其应用 |
| JP2004506408A (ja) | 2000-04-26 | 2004-03-04 | イルーシス セラポーティクス,インコーポレーテッド | 二重特異性分子及びその用途 |
| US20040047854A1 (en) | 2001-07-27 | 2004-03-11 | Black Roy A. | Human disintegrin protein |
| GB0025307D0 (en) | 2000-10-16 | 2000-11-29 | Celltech Chiroscience Ltd | Biological products |
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| US20030133939A1 (en) | 2001-01-17 | 2003-07-17 | Genecraft, Inc. | Binding domain-immunoglobulin fusion proteins |
| US7319139B2 (en) | 2001-01-29 | 2008-01-15 | Biogen Idec, Inc. | TAG-72 specific CH2 domain deleted antibodies |
| US20040053245A1 (en) | 2001-02-05 | 2004-03-18 | Tang Y. Tom | Novel nucleic acids and polypeptides |
| AU2002240751A1 (en) | 2001-03-09 | 2002-09-24 | William Herman | Targeted ligands |
| AU2002247826A1 (en) | 2001-03-13 | 2002-09-24 | University College London | Specific binding members |
| EP1402256A4 (en) | 2001-05-31 | 2006-09-13 | Chiron Corp | USE OF P-CADHERIN AS TARGET IN ANTICANCER THERAPY |
| US7189507B2 (en) | 2001-06-18 | 2007-03-13 | Pdl Biopharma, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| EP1399484B1 (en) | 2001-06-28 | 2010-08-11 | Domantis Limited | Dual-specific ligand and its use |
| WO2003022987A2 (en) | 2001-07-26 | 2003-03-20 | Eos Biotechnology, Inc. | Methods of diagnosis of hepatitis c infection, compositions and methods of screening for modulators of hepatitis c infection |
| US6833441B2 (en) | 2001-08-01 | 2004-12-21 | Abmaxis, Inc. | Compositions and methods for generating chimeric heteromultimers |
| US20040142325A1 (en) | 2001-09-14 | 2004-07-22 | Liat Mintz | Methods and systems for annotating biomolecular sequences |
| EP1293514B1 (en) | 2001-09-14 | 2006-11-29 | Affimed Therapeutics AG | Multimeric single chain tandem Fv-antibodies |
| US20040241703A1 (en) | 2002-08-19 | 2004-12-02 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| EP2075256A2 (en) | 2002-01-14 | 2009-07-01 | William Herman | Multispecific binding molecules |
| US7317091B2 (en) | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| US8030461B2 (en) | 2002-04-15 | 2011-10-04 | Chugai Seiyaku Kabushiki Kaisha | Methods for constructing scDb libraries |
| EP1354600A1 (en) | 2002-04-19 | 2003-10-22 | Affimed Therapeutics AG | Antibody combination useful for tumor therapy |
| US20040018493A1 (en) | 2002-07-12 | 2004-01-29 | Anastasio Alison E. | Haplotypes of the CD3E gene |
| JP4330532B2 (ja) | 2002-07-18 | 2009-09-16 | 株式会社セルフリーサイエンス | 単鎖抗体およびその利用 |
| US7820166B2 (en) | 2002-10-11 | 2010-10-26 | Micromet Ag | Potent T cell modulating molecules |
| US9701754B1 (en) | 2002-10-23 | 2017-07-11 | City Of Hope | Covalent disulfide-linked diabodies and uses thereof |
| WO2004044000A2 (en) | 2002-11-14 | 2004-05-27 | Adherex Technologies, Inc. | Compounds and methods for modulating functions of classical cadherins |
| EP2311870A1 (en) | 2002-11-26 | 2011-04-20 | Genentech, Inc. | Compositions and methods for the treatment of immune related diseases |
| CA2525519A1 (en) | 2003-05-08 | 2004-12-02 | Xcyte Therapies, Inc. | Generation and isolation of antigen-specific t cells |
| WO2004106380A2 (en) | 2003-05-31 | 2004-12-09 | Micromet Ag | Human-anti-human cd3 binding molecules |
| EP1629012B1 (en) | 2003-05-31 | 2018-11-28 | Amgen Research (Munich) GmbH | Pharmaceutical compositions comprising bispecific anti-cd3, anti-cd19 antibody constructs for the treatment of b-cell related disorders |
| RU2403262C2 (ru) | 2003-06-11 | 2010-11-10 | Уайт | Выделенный полипептид ib альфа гликопротеина тромбоцитов человека, слитый белок, молекула днк (варианты), экспрессирующий вектор (варианты), клетка (варианты), способ экспрессии полипептида, способ экспрессии слитого белка, фармацевтическая композиция (варианты), способ ингибирования прикрепления клетки крови к биологической ткани в биологической системе, способ ингибирования прикрепления белка к биологической ткани в биологической системе и способ лечения нарушения |
| US20050163782A1 (en) | 2003-06-27 | 2005-07-28 | Biogen Idec Ma Inc. | Modified binding molecules comprising connecting peptides |
| PT1639011E (pt) | 2003-06-30 | 2009-01-20 | Domantis Ltd | Anticorpos (dab) de domínio único peguilados |
| US7754209B2 (en) | 2003-07-26 | 2010-07-13 | Trubion Pharmaceuticals | Binding constructs and methods for use thereof |
| US20070037204A1 (en) | 2003-08-08 | 2007-02-15 | Hiroyuki ABURANTAI | Gene overexpressed in cancer |
| WO2005019258A2 (en) | 2003-08-11 | 2005-03-03 | Genentech, Inc. | Compositions and methods for the treatment of immune related diseases |
| WO2005028507A1 (en) | 2003-09-24 | 2005-03-31 | Monash University | CRYSTAL STRUCTURE OF CD3ϵϜ/OKT3 COMPLEX |
| US7235641B2 (en) | 2003-12-22 | 2007-06-26 | Micromet Ag | Bispecific antibodies |
| ATE435238T1 (de) | 2004-05-05 | 2009-07-15 | Micromet Ag | Herstellung eines einkettigen fv antikörperfragments |
| WO2005118635A2 (en) | 2004-06-03 | 2005-12-15 | Novimmune S.A. | Anti-cd3 antibodies and methods of use thereof |
| EP1786918A4 (en) | 2004-07-17 | 2009-02-11 | Imclone Systems Inc | NEW BISPECIFIC ANTIBODY TETRAVALENT |
| CA2577082A1 (en) | 2004-09-02 | 2006-03-16 | Genentech, Inc. | Heteromultimeric molecules |
| PT1699826E (pt) | 2005-01-05 | 2009-06-17 | F Star Biotech Forsch & Entw | Domínios de imunoglobulina sintética com propriedades de ligação construídos em regiões da molécula diferentes das regiões determinantes de complementaridade |
| JP5109131B2 (ja) | 2005-02-10 | 2012-12-26 | オンコセラピー・サイエンス株式会社 | 膀胱癌を診断する方法 |
| US20120237442A1 (en) | 2005-04-06 | 2012-09-20 | Ibc Pharmaceuticals, Inc. | Design and Construction of Novel Multivalent Antibodies |
| US9963510B2 (en) | 2005-04-15 | 2018-05-08 | Macrogenics, Inc. | Covalent diabodies and uses thereof |
| US9284375B2 (en) | 2005-04-15 | 2016-03-15 | Macrogenics, Inc. | Covalent diabodies and uses thereof |
| UA95775C2 (uk) | 2005-04-26 | 2011-09-12 | Пфайзер Инк. | Антитіло, яке специфічно зв'язується з р-кадгерином |
| WO2006116737A2 (en) | 2005-04-28 | 2006-11-02 | Mcgill University | Compounds and methods for modulating cadherin-mediated processes |
| KR101360671B1 (ko) | 2005-06-10 | 2014-02-07 | 추가이 세이야쿠 가부시키가이샤 | sc(Fv)2를 함유하는 의약조성물 |
| JP2006345852A (ja) | 2005-06-16 | 2006-12-28 | Virxsys Corp | 抗体複合体 |
| EA014025B1 (ru) | 2005-09-12 | 2010-08-30 | Новиммун С.А. | Композиции антитела против cd3 |
| EP1940881B1 (en) | 2005-10-11 | 2016-11-30 | Amgen Research (Munich) GmbH | Compositions comprising cross-species-specific antibodies and uses thereof |
| KR101287777B1 (ko) | 2005-12-21 | 2013-07-23 | 암젠 리서치 (뮌헨) 게엠베하 | 가용성 cea에 대한 내성을 가지는 약학적 조성물 |
| WO2007075672A2 (en) | 2005-12-23 | 2007-07-05 | Lankenau Institute For Medical Research | Prognostic cancer markers |
| EP2004687A1 (en) | 2006-02-28 | 2008-12-24 | Oncotherapy Science, Inc. | Methods for damaging cells using effector functions of anti-cdh3 antibodies |
| WO2007106507A2 (en) | 2006-03-14 | 2007-09-20 | Petrie Howard T | Detection of gene expression in mixed sample or tissue |
| CN103073639A (zh) | 2006-03-17 | 2013-05-01 | 比奥根艾迪克Ma公司 | 稳定的多肽组合物 |
| AR060070A1 (es) | 2006-03-24 | 2008-05-21 | Merck Patent Gmbh | Dominios proteicos heterodimericos obtenidos por ingenieria |
| US8535677B2 (en) | 2006-06-06 | 2013-09-17 | Oxford Biotherapeutics, Ltd. | Antibody drug conjugate treatment of colorectal cancer |
| TWI438207B (zh) | 2007-02-21 | 2014-05-21 | Oncotherapy Science Inc | 表現腫瘤相關抗原之癌症的胜肽疫苗 |
| HUE040467T2 (hu) | 2007-04-03 | 2019-03-28 | Amgen Res Munich Gmbh | Keresztfaj-specifikus kötõdomén |
| CN101687915B8 (zh) * | 2007-04-03 | 2018-08-03 | 安进研发(慕尼黑)股份有限公司 | 跨物种特异性CD3-ε结合结构域 |
| WO2008124858A2 (en) | 2007-04-11 | 2008-10-23 | F-Star Biotechnologische Forschungs- Und Entwicklungsges. M.B.H. | Targeted receptor |
| ES2456963T3 (es) | 2007-06-04 | 2014-04-24 | Rappaport Family Institute For Research In The Medical Sciences | Agentes para el tratamiento de enfermedades inflamatorias y métodos para usar los mismos |
| CN101952312A (zh) | 2007-07-31 | 2011-01-19 | 米迪缪尼有限公司 | 多特异性表位结合蛋白及其应用 |
| JP5485152B2 (ja) | 2007-08-15 | 2014-05-07 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツング | 単一特異性および多特異性抗体ならびに使用方法 |
| CN104356225B (zh) | 2007-08-20 | 2018-02-13 | 肿瘤疗法科学股份有限公司 | Cdh3 肽以及含有cdh3 肽的药剂 |
| CA2700714C (en) | 2007-09-26 | 2018-09-11 | Ucb Pharma S.A. | Dual specificity antibody fusions |
| CA2740310A1 (en) | 2007-11-01 | 2009-05-07 | The Royal Institution For The Advancement Of Learning/Mcgill University | Altered cadherin processing in tumor cells |
| UY31504A1 (es) | 2007-11-30 | 2009-07-17 | Construcciones de union de antigenos | |
| US20090162359A1 (en) | 2007-12-21 | 2009-06-25 | Christian Klein | Bivalent, bispecific antibodies |
| US9266967B2 (en) | 2007-12-21 | 2016-02-23 | Hoffmann-La Roche, Inc. | Bivalent, bispecific antibodies |
| US8227577B2 (en) | 2007-12-21 | 2012-07-24 | Hoffman-La Roche Inc. | Bivalent, bispecific antibodies |
| EP2080812A1 (en) | 2008-01-18 | 2009-07-22 | Transmedi SA | Compositions and methods of detecting post-stop peptides |
| US9029508B2 (en) | 2008-04-29 | 2015-05-12 | Abbvie Inc. | Dual variable domain immunoglobulins and uses thereof |
| TW201008574A (en) | 2008-08-19 | 2010-03-01 | Oncotherapy Science Inc | INHBB epitope peptides and vaccines containing the same |
| AU2009299791B2 (en) | 2008-10-01 | 2016-02-25 | Amgen Research (Munich) Gmbh | Cross-species-specific PSCAxCD3, CD19xCD3, C-METxCD3, EndosialinxCD3, EpCAMxC D3, IGF-1RxCD3 or FAPalpha xCD3 bispecific single chain antibody |
| MX2011003502A (es) | 2008-10-01 | 2011-09-01 | Micromet Ag | Anticuerpo de cadena sencilla biespecifica de psmaxcd3 especifico a traves de especies. |
| EP3375790A1 (en) | 2008-10-01 | 2018-09-19 | Amgen Research (Munich) GmbH | Cross-species-specific single domain bispecific single chain antibody |
| DK2352763T4 (da) | 2008-10-01 | 2022-10-17 | Amgen Res Munich Gmbh | Bispecifikke enkeltkædede antistoffer med specificitet for højmolekylære målantigener |
| WO2010040545A1 (en) | 2008-10-06 | 2010-04-15 | Novoplant Gmbh | Proteolytically stable antibody formats |
| CN102292352A (zh) | 2008-10-10 | 2011-12-21 | 新兴产品开发西雅图有限公司 | Tcr复合物免疫治疗剂 |
| US20110020221A1 (en) | 2009-04-09 | 2011-01-27 | The Johns Hopkins University | Cancer stem cell expression patterns and compounds to target cancer stem cells |
| CA2760642A1 (en) | 2009-05-01 | 2010-11-04 | The University Of Tokyo | Anti-cadherin antibody |
| SG176219A1 (en) | 2009-05-27 | 2011-12-29 | Hoffmann La Roche | Tri- or tetraspecific antibodies |
| US8703132B2 (en) | 2009-06-18 | 2014-04-22 | Hoffmann-La Roche, Inc. | Bispecific, tetravalent antigen binding proteins |
| JP2013503607A (ja) | 2009-09-01 | 2013-02-04 | アボット・ラボラトリーズ | 二重可変ドメイン免疫グロブリンおよびその使用 |
| US9493578B2 (en) | 2009-09-02 | 2016-11-15 | Xencor, Inc. | Compositions and methods for simultaneous bivalent and monovalent co-engagement of antigens |
| US20110064743A1 (en) | 2009-09-09 | 2011-03-17 | Hammond Philip W | Human anti-cancer antibodies |
| WO2011030107A1 (en) | 2009-09-10 | 2011-03-17 | Ucb Pharma S.A. | Multivalent antibodies |
| WO2011038301A2 (en) | 2009-09-25 | 2011-03-31 | Xoma Technology Ltd. | Screening methods |
| EP2490714A4 (en) | 2009-10-20 | 2013-11-13 | Glaxo Group Ltd | ASSAY OF ANTI-CD3 ANTIBODIES IN AUTOIMMUNE DISEASES |
| EP2496600A1 (en) | 2009-11-04 | 2012-09-12 | Fabrus LLC | Methods for affinity maturation-based antibody optimization |
| GB0920127D0 (en) | 2009-11-17 | 2009-12-30 | Ucb Pharma Sa | Antibodies |
| WO2011071541A2 (en) | 2009-12-11 | 2011-06-16 | The Scripps Research Institute | Cadherin modulatory agents |
| CA2785139A1 (en) | 2009-12-22 | 2011-06-30 | Novartis Ag | Tetravalent cd47-antibody constant region fusion protein for use in therapy |
| US20110165161A1 (en) | 2009-12-23 | 2011-07-07 | Shih-Yao Lin | Anti-epcam antibodies that induce apoptosis of cancer cells and methods using same |
| ES2701626T3 (es) | 2009-12-28 | 2019-02-25 | Oncotherapy Science Inc | Anticuerpos anti-CDH3 y sus usos |
| CN102014475B (zh) | 2010-01-08 | 2012-01-04 | 华为技术有限公司 | 资源映射、码分复用方法及装置 |
| US20120294857A1 (en) | 2010-01-11 | 2012-11-22 | Trustees Of Dartmouth College | Monomeric Bi-Specific Fusion Protein |
| US8815211B2 (en) | 2010-02-10 | 2014-08-26 | Fujifilm Ri Pharma Co., Ltd. | Radioactive metal-labeled anti-cadherin antibody |
| LT2361936T (lt) | 2010-02-25 | 2016-09-12 | Affimed Gmbh | Antigeną rišanti molekulė ir jos panaudojimas |
| WO2011109588A1 (en) | 2010-03-03 | 2011-09-09 | Health Research Inc. | Novel cd3 epsilon immunogens and antibodies |
| TWI653333B (zh) | 2010-04-01 | 2019-03-11 | 安進研究(慕尼黑)有限責任公司 | 跨物種專一性之PSMAxCD3雙專一性單鏈抗體 |
| SG185027A1 (en) | 2010-05-03 | 2012-11-29 | Genentech Inc | Compositions and methods for the diagnosis and treatment of tumor |
| CA2807127C (en) * | 2010-08-02 | 2019-02-12 | Leslie S. Johnson | Covalent diabodies and uses thereof |
| JP2013535508A (ja) | 2010-08-13 | 2013-09-12 | ベイラー リサーチ インスティテュート | 抗体付きアジュバントを抗原提示細胞に直接的に標的化することをベースにした新規ワクチンアジュバント |
| JP6147665B2 (ja) | 2010-08-14 | 2017-06-14 | アッヴィ・インコーポレイテッド | アミロイドベータ結合タンパク質 |
| US9834615B2 (en) | 2010-08-16 | 2017-12-05 | Novimmune Sa | Methods for the generation of multispecific and multivalent antibodies |
| CA2814040C (en) | 2010-10-08 | 2021-03-23 | Joshua Michael Donaldson | A monoclonal antibody framework binding interface for meditopes, meditope delivery systems and methods for their use |
| PT2634194T (pt) | 2010-10-29 | 2018-10-19 | Perseus Proteomics Inc | Anticorpos anti-cdh3 possuidores de elevada capacidade de internalização |
| JP2014015396A (ja) | 2010-10-29 | 2014-01-30 | Perseus Proteomics Inc | 高い親和性を有する抗cdh3抗体 |
| EP4303237A3 (en) | 2010-11-30 | 2024-03-27 | Chugai Seiyaku Kabushiki Kaisha | Cytotoxicity-inducing therapeutic agent |
| UY33827A (es) | 2010-12-22 | 2012-07-31 | Abbott Lab | Proteínas de unión a media-inmunoglobulina y sus usos |
| UY33826A (es) | 2010-12-22 | 2012-07-31 | Abbott Lab | Proteínas de unión con dominios trivariables y sus usos |
| US10689447B2 (en) | 2011-02-04 | 2020-06-23 | Genentech, Inc. | Fc variants and methods for their production |
| US20120231023A1 (en) | 2011-03-08 | 2012-09-13 | Baylor Research Institute | Novel Vaccine Adjuvants Based on Targeting Adjuvants to Antibodies Directly to Antigen-Presenting Cells |
| US20140056897A1 (en) | 2011-03-10 | 2014-02-27 | Hco Antibody, Inc. | Bispecific three-chain antibody-like molecules |
| JP5972915B2 (ja) | 2011-03-16 | 2016-08-17 | アムジエン・インコーポレーテツド | Fc変異体 |
| JP6130307B2 (ja) | 2011-03-17 | 2017-05-17 | ザ ユニバーシティ オブ バーミンガム | 再指向性免疫療法 |
| US9624291B2 (en) | 2011-03-17 | 2017-04-18 | Ramot At Tel-Aviv University Ltd. | Bi- and monospecific, asymmetric antibodies and methods of generating the same |
| WO2012129227A1 (en) | 2011-03-22 | 2012-09-27 | Baylor Research Institute | Dendritic cells (dcs) targeting for tuberculosis (tb) vaccine |
| EP2688592A4 (en) | 2011-03-25 | 2015-07-22 | Baylor Res Inst | COMPOSITIONS AND METHODS FOR IMMUNIZATION AGAINST HEPATITIS C VIRUS |
| TWI671315B (zh) | 2011-03-28 | 2019-09-11 | 法商賽諾菲公司 | 具有交叉結合區定向之雙重可變區類抗體結合蛋白 |
| US20140178368A1 (en) | 2011-04-19 | 2014-06-26 | Leslie Lynne SHARP | Combinations of anti-4-1bb antibodies and adcc-inducing antibodies for the treatment of cancer |
| US20140161800A1 (en) | 2011-04-22 | 2014-06-12 | John W. Blankenship | Prostate-Specific Membrane Antigen Binding Proteins and Related Compositions and Methods |
| CN103842383B (zh) * | 2011-05-16 | 2017-11-03 | 健能隆医药技术(上海)有限公司 | 多特异性fab融合蛋白及其使用方法 |
| KR102030531B1 (ko) | 2011-05-21 | 2019-10-10 | 마크로제닉스, 인크. | 탈면역화된 혈청-결합 도메인 및 혈청 반감기를 연장하기 위한 그것의 용도 |
| KR102060389B1 (ko) | 2011-05-21 | 2019-12-31 | 마크로제닉스, 인크. | 사람 및 비-사람 cd3에 결합할 수 있는 cd3-결합 분자 |
| CN103857699B (zh) | 2011-05-24 | 2016-08-31 | 泽恩格尼亚股份有限公司 | 多价和单价多特异性复合物及其用途 |
| WO2012162583A1 (en) | 2011-05-26 | 2012-11-29 | Ibc Pharmaceuticals, Inc. | Design and construction of novel multivalent antibodies |
| PL2726510T3 (pl) | 2011-05-27 | 2023-05-29 | F.Hoffmann-La Roche Ag | Kierowanie podwójne |
| BR112013031762A2 (pt) | 2011-06-16 | 2016-09-13 | Novartis Ag | proteínas solúveis para utilização como terapêuticos |
| JPWO2012176765A1 (ja) | 2011-06-24 | 2015-02-23 | 株式会社ペルセウスプロテオミクス | 抗ヒトp−カドへリン(cdh3)遺伝子組み換え抗体 |
| US20140242081A1 (en) | 2011-07-18 | 2014-08-28 | Micromet Ag | Dosing regimens for treatment of cea-expressing cancers |
| WO2013013700A1 (en) | 2011-07-22 | 2013-01-31 | Affimed Therapeutics Ag | Multivalent antigen-binding fv molecule |
| BR112014004168A2 (pt) | 2011-08-23 | 2017-12-12 | Roche Glycart Ag | anticorpo biespecífico, composição farmacêutica, uso do anticorpo biespecífico, célula hospedeira procariótica ou eucariótica, método de produção de anticorpo e invenção |
| EP3321286B1 (en) | 2011-08-23 | 2021-01-06 | Roche Glycart AG | Bispecific t cell activating antigen binding molecules |
| WO2013026835A1 (en) | 2011-08-23 | 2013-02-28 | Roche Glycart Ag | Fc-free antibodies comprising two fab fragments and methods of use |
| SG2014008577A (en) | 2011-08-23 | 2014-04-28 | Roche Glycart Ag | Bispecific antigen binding molecules |
| US20130058947A1 (en) | 2011-09-02 | 2013-03-07 | Stem Centrx, Inc | Novel Modulators and Methods of Use |
| WO2013041865A1 (en) | 2011-09-22 | 2013-03-28 | Immunocore Limited | T cell receptors |
| WO2013041687A1 (en) | 2011-09-23 | 2013-03-28 | Amgen Research (Munich) Gmbh | Bispecific binding molecules for 5t4 and cd3 |
| TWI679212B (zh) | 2011-11-15 | 2019-12-11 | 美商安進股份有限公司 | 針對bcma之e3以及cd3的結合分子 |
| US9718893B2 (en) | 2011-12-19 | 2017-08-01 | Synimmune Gmbh | Bispecific antibody molecule |
| GB201203442D0 (en) | 2012-02-28 | 2012-04-11 | Univ Birmingham | Immunotherapeutic molecules and uses |
| EP2820047B1 (en) | 2012-03-01 | 2018-04-25 | Amgen Research (Munich) GmbH | Long life polypeptide binding molecules |
| KR20150003251A (ko) | 2012-04-04 | 2015-01-08 | 가부시키가이샤 페르세우스 프로테오믹스 | 항 cdh3(p-카드헤린) 항체의 약물 콘쥬게이트 |
| US10202452B2 (en) | 2012-04-20 | 2019-02-12 | Aptevo Research And Development Llc | CD3 binding polypeptides |
| EA039663B1 (ru) * | 2012-05-03 | 2022-02-24 | Амген Инк. | Применение антитела против pcsk9 для снижения сывороточного холестерина лпнп и лечения связанных с холестерином расстройств |
| US10647756B2 (en) * | 2015-05-18 | 2020-05-12 | Pfizer Inc. | Humanized antibodies |
-
2015
- 2015-06-26 PE PE2016002813A patent/PE20170286A1/es unknown
- 2015-06-26 CA CA2895659A patent/CA2895659A1/en not_active Abandoned
- 2015-06-26 EP EP15741347.7A patent/EP3164417A1/en not_active Withdrawn
- 2015-06-26 SG SG11201609707WA patent/SG11201609707WA/en unknown
- 2015-06-26 MX MX2016017393A patent/MX2016017393A/es unknown
- 2015-06-26 BR BR112016030740-2A patent/BR112016030740A2/pt not_active Application Discontinuation
- 2015-06-26 RU RU2016151645A patent/RU2016151645A/ru not_active Application Discontinuation
- 2015-06-26 AU AU2015283704A patent/AU2015283704A1/en not_active Abandoned
- 2015-06-26 CN CN201580035515.8A patent/CN106661119A/zh active Pending
- 2015-06-26 WO PCT/IB2015/054829 patent/WO2016001810A1/en active Application Filing
- 2015-06-26 JP JP2016575335A patent/JP2017520575A/ja active Pending
- 2015-06-26 KR KR1020167036814A patent/KR20170010863A/ko active Search and Examination
- 2015-06-26 US US14/751,704 patent/US9884921B2/en not_active Expired - Fee Related
- 2015-06-29 TW TW107142295A patent/TW201936638A/zh unknown
- 2015-06-29 TW TW104120955A patent/TWI659042B/zh not_active IP Right Cessation
-
2016
- 2016-12-13 PH PH12016502491A patent/PH12016502491A1/en unknown
-
2017
- 2017-01-01 IL IL249889A patent/IL249889A0/en unknown
- 2017-01-03 CO CONC2017/0000016A patent/CO2017000016A2/es unknown
- 2017-12-13 US US15/840,019 patent/US20180155452A1/en not_active Abandoned
-
2018
- 2018-12-05 AU AU2018274919A patent/AU2018274919A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006515318A (ja) * | 2002-10-29 | 2006-05-25 | ファルマシア・コーポレーション | 特異的に発現する癌関連遺伝子、それによってコードされるポリペプチドおよびその使用方法 |
| JP2009508466A (ja) * | 2005-04-15 | 2009-03-05 | マクロジェニクス,インコーポレーテッド | 共有結合型ダイアボディとその使用 |
| JP2011526583A (ja) * | 2008-06-30 | 2011-10-13 | オンコセラピー・サイエンス株式会社 | 放射性同位体標識で標識された抗cdh3抗体およびその使用 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021525080A (ja) * | 2018-05-23 | 2021-09-24 | ファイザー・インク | GUCY2cに特異的な抗体及びその使用 |
| JP7057843B2 (ja) | 2018-05-23 | 2022-04-20 | ファイザー・インク | GUCY2cに特異的な抗体及びその使用 |
| JP2022106751A (ja) * | 2018-05-23 | 2022-07-20 | ファイザー・インク | GUCY2cに特異的な抗体及びその使用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3164417A1 (en) | 2017-05-10 |
| KR20170010863A (ko) | 2017-02-01 |
| SG11201609707WA (en) | 2017-01-27 |
| IL249889A0 (en) | 2017-03-30 |
| MX2016017393A (es) | 2017-09-05 |
| CO2017000016A2 (es) | 2017-05-19 |
| PE20170286A1 (es) | 2017-03-30 |
| BR112016030740A2 (pt) | 2018-02-20 |
| AU2018274919A1 (en) | 2019-01-03 |
| TWI659042B (zh) | 2019-05-11 |
| PH12016502491A1 (en) | 2017-03-22 |
| TW201936638A (zh) | 2019-09-16 |
| CN106661119A (zh) | 2017-05-10 |
| US20180155452A1 (en) | 2018-06-07 |
| RU2016151645A (ru) | 2018-08-03 |
| CA2895659A1 (en) | 2016-01-01 |
| US20160002357A1 (en) | 2016-01-07 |
| US9884921B2 (en) | 2018-02-06 |
| RU2016151645A3 (ja) | 2019-02-20 |
| TW201612194A (en) | 2016-04-01 |
| WO2016001810A1 (en) | 2016-01-07 |
| AU2015283704A1 (en) | 2016-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9884921B2 (en) | Bispecific heterodimeric diabodies and uses thereof | |
| US11603405B2 (en) | Anti-CD3 antibodies and uses thereof | |
| JP2020018298A (ja) | Cldn18.2及びcd3に対する抗体コンストラクト | |
| CN113286634A (zh) | 对gucy2c特异性的抗体及其用途 | |
| JP7447208B2 (ja) | 抗体 | |
| JP2024510098A (ja) | 抗GPRC5DxBCMAxCD3三重特異性抗体およびその使用 | |
| US20230357398A1 (en) | Novel human antibodies binding to human cd3 epsilon | |
| EP4245317A1 (en) | Bispecific antibody for claudin 18a2 and cd3 and application of bispecific antibody | |
| KR20240014058A (ko) | 항-cea 항체 및 항-cd137 다중 특이적 항체 및 사용 방법 | |
| WO2022242679A1 (en) | Anti-cd137 antibodies and methods of use | |
| WO2022242682A1 (en) | Anti-gpc3 and anti-cd137 multispecific antibodies and methods of use | |
| TWI830761B (zh) | 針對cldn18.2和cd3之抗體構建體 | |
| WO2024078558A1 (zh) | 抗cd100抗体及其用途 | |
| EP4219553A1 (en) | Anti-tigit antibody and double antibody and their application | |
| JP2024054405A (ja) | 抗体 | |
| JP2023547662A (ja) | Cldn6及びcd3に選択的に結合するポリペプチド構築物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170314 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180622 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180622 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190520 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190718 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20191216 |