JP2010090129A - Glp−1、exendin−4、そのペプチド・アナログ及びその使用 - Google Patents
Glp−1、exendin−4、そのペプチド・アナログ及びその使用 Download PDFInfo
- Publication number
- JP2010090129A JP2010090129A JP2009262568A JP2009262568A JP2010090129A JP 2010090129 A JP2010090129 A JP 2010090129A JP 2009262568 A JP2009262568 A JP 2009262568A JP 2009262568 A JP2009262568 A JP 2009262568A JP 2010090129 A JP2010090129 A JP 2010090129A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- polypeptide
- glp
- pharmaceutical composition
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/12—Antidiuretics, e.g. drugs for diabetes insipidus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/57563—Vasoactive intestinal peptide [VIP]; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/2278—Vasoactive intestinal peptide [VIP]; Related peptides (e.g. Exendin)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/26—Glucagons
Abstract
【解決手段】GLP-1及びexendin-4の新規ポリペプチド・アナログ。
【効果】ポリペプチドのインシュリン分泌刺激効果は、等量のGLP-1又はexendin-4の効果と同程度か又はそれを超える。糖尿病の治療及び神経障害、例えばアルツハイマー病及びパーキンソン病の治療、並びに2型糖尿病に関連した末梢神経障害の治療に用いることができる。
【選択図】なし
Description
当該出願は、2001年7月31日に出願された米国特許出願番号第60/309,076号に対して優先権を主張する。
膵臓のベータ細胞機能不全及び付随するインシュリン産生の減少は、糖尿病をもたらす恐れがある。1型糖尿病において、ベータ細胞は、免疫系によって完全に破壊され、インシュリン産生細胞の欠如をもたらす(インシュリン依存型[1型]糖尿病に対する内科医のガイド:Diagnosis and Treatment, American Diabetes Association, 1988(非特許文献1))。2型糖尿病において、ターゲット組織がグルコース摂取においてインシュリンの効果に抵抗性をもつようになると、ベータ細胞が徐々に能率的でなくなる。よって、ベータ細胞は、1型糖尿病の人々において不存在であり、そして2型糖尿病の人々において機能的に十分な機能を果たしていない。
本願発明の目的に従って、本明細書中に含まれ、かつ、全体的に記載されているとおり、1の側面において、本願発明は、GLP-1及びexendin-4の新規ポリペプチド・アナログに関する。好ましい態様において、前記ポリペプチドは、インシュリン分泌刺激性及び長期作用性である。好ましくは、前記ポリペプチドのインシュリン分泌刺激効果は、等モル量のGLP-1又はexendin-4の効果に匹敵するか又はそれを超える。
本発明は、以下の、本発明の好ましい態様の詳細な説明及びそこに含まれる実施例、並びに図面及びそれらの上記及び下記の説明を参照することによってより容易に理解される。
よって、例えば、「a polypeptide」への言及は、複数のポリペプチドの混合物を含み、「a pharmaceutical carrier」への言及は、2以上のそのような担体の混合物を含む、そのほかも同様。
「任意に」又は「場合により」は、その後に記載された事件又は情況が生じるかもしれず、そしてこの記載は、上記事件又は状況が生じる場合と生じない場合を含むことを意味する。
以下の実施例は、本明細書中で主張される化合物、組成物、物品、デバイス、及び/又は方法がどのように作製され、そして評価されるのかについての完璧な開示及び説明を当業者に提供するためになされ、そして本発明の純粋な例示として意図され、当該発明者が彼ら発明とみなすものの範囲を制限することはない。数(例えば、数量、温度等)に関して正確度を確保するために努力がなされたが、しかしいくつかの誤り及び偏りが明らかにされるであろう。別段の指示のない限り、部分は、重量による部分であり、温度は、℃又は気温であり、圧力は、大気又はその付近である。
exendin-4及びGLP-1の基本的な特徴を取り入れた一連のキメラ・ペプチドを、設計した。35のペプチドの配列を、GLP-1(第7〜第36残基)、及びexendin-4(番号付けされたGLP-1残基を用いたexendin-4のアラインメントに従って番号を付けた第7〜第45残基)の配列とともに図1に示す。それらは、(i)第8と第9アミノ酸の間のDDP1Vの切断作用を最小限にし、(ii)インシュリン分泌刺激作用のための最小限の要件を評価し、そして(iii)exendin-4とGLP-1の間のアミノ酸の差異がGLP-1に対する効果における前者の13倍増の原因となることを評価するように設計した。図1に示されたペプチドは、それらの合成にL-及びD-アミノ酸を利用した。
他のペプチドを、2-アミノヘキサン酸(6-アミノヘキサン酸)を使ってDPP1Vによる切断を減らすように設計した。表2を参照のこと。
Dr. Samuel A. Clark(Bio Hybrid Technologies, Shrewsbury, MA)から贈与物であるRIN1048-36細胞を、インシュリン分泌に対するGLP-1、exendin-4、及びアナログの作用を観察するために使用した。細胞を、12ウェル皿の底に置いたガラス・カバースリップ上に、2.5×105細胞/cm2の密度で播種し、48時間培養した。その後、それらを、37℃の加湿インキュベータ内で、それぞれグルコース不含緩衝液(mMの:140 NaCl、5 KCl、1 NaPO4、1 MgSO4、2 CaCl、20 HEPES緩衝液(pH 7.4)及び0.1%のウシ血清アルブミンを含む)を用いて30分で2期間プレインキュベートした。その後、細胞を、5 mMのグルコース及びペプチド(1×10-8 M)を伴う同じ緩衝液1 mLの存在下、37℃で1時間インキュベートした。GLP-1とexendin-4(1×10-8 M)を、全てのアッセイの標準として使用した。1時間後、培地を取り除き、そしてEIA(Crystal Chem, Dhicago II)によるインシュリンレベルの定量化の前に−80℃で保存し、そして標準としてウシγ-グロブリンを用いたブラッドフォード法(Bio-Rad, Richmond, CA)を使った総タンパク質の測定のために、HCl(300 μl、0.1 M、20分、RT)を用いて細胞を溶解した。
ヒトGLP-1受容体を安定的にトランスフェクトされたCHO細胞、GLP-1R細胞を、12ウェル・プレート上に60〜70%集密まで育て、クレブズ-リンガー・リン酸塩緩衝物質(KRP)で3回洗浄し、そして加湿気インキュベータ内、37℃で2時間、0.1%のウシ血清アルブミン含有KRP(BSA)1 mlと一緒にインキュベートした。次に細胞を、研究中のペプチドの存在又は不存在下、イソブチルメチルキサンチン(IBMX)(1 mM;Calbiochem, La Jolla, CA)を伴う、0.1%のBSAを補った1 mlのKRP中でインキュベートした。氷冷リン酸緩衝生理食塩水(PBS)で無傷の細胞を3回洗浄することによって30分後に反応を止めた。氷冷過塩素酸(0.6 M、1 ml、5分)中で細胞をインキュベートすることによって細胞内のcAMPを抽出した。炭酸カリウム(5M、84 μl)を使ってサンプルのpHを7に調整した後、試料管をボルテックスし、形成された沈殿を、遠心分離(5分、2000×g、4℃)で沈殿させた。上清を、真空で乾燥させ、4 mMのEDTA含有0.05 MのTris(pH7.5)(300 μl)中に可溶化した。炭酸ナトリウム(0.15 μM)と硫酸亜鉛(0.15 μM)を加えたサンプルを、次に氷上で15分間インキュベートした。得られた塩沈殿物を、遠心分離(5分、2000×g、4℃)によって除去した。サンプルを、[3H]cAMP競合的タンパク質結合アッセイ・キット(Amersham, Philadelphia, PA)を使って、二重のアリコート(50 μl)でアッセイした。
結合研究を、Montrose-Rafizadeh et al., (1997b) J. Biol. Chem. 272:21201-206のやり方で実施した。要するに、CHO/GLP-1R細胞を、12ウェル・プレート上で集密まで育て、実験の2時間前に無血清Ham F-12培地で洗浄した。0.5 mlの結合緩衝液(10)により2回洗浄した後、細胞を、2% BSA、17 mg/LのDiprotin A(Bachem, Torence, CA)、10 mMのグルコース、1〜1000 nMのGLP-1又は他のペプチド、及び30,000 cpmのSI-GLP-1(Amersham, Philadelphia, PA)を含む0.5 mlの緩衝液と一緒に、4℃で一晩インキュベートした。インキュベーション終了後に、上清を捨て、細胞を氷冷PBSで3回洗浄し、そして0.5 mlの0.5 NのNaOH及び0.1%のドデシル硫酸ナトリウムと一緒に室温で10分間インキュベートした。細胞ライセートの放射活性を、ICN Apec-Series g-counterで計測した。総結合から、大過剰の非標識GLP-1(1 μM)の存在下でインキュベートした細胞に関する放射活性を差し引いて、特定の結合を決定した。
急性最大インシュリン応答を、静中ペプチド投与後のズッカーラットにおける血漿インシュリン・レベルの定量によって測定した。特に、一晩の絶食後の体重約400 gの糖尿病雄ラットを、50 mg/kgのペントバルビタールにより麻酔し、そして採血のためにカテーテルをそれらの右大腿動脈に結んだ。その後、exendin-4、GLP-1、又はペプチド(0.4 nmol/kg)のボーラスを、それらの左伏在静脈中に30秒で投与した(1つのペプチドにつきN=6)。ペプチド投与前、及びその後5、15、30、60及び90分で採集した血液を、インシュリン定量のために、EDTA及びアプロチニンを含むヘパリン処理管内に注いだ。血漿を、分離し、取り除き、そして直ちに-70℃に冷凍した。次にラット・インシュリンELISAキット(Crystal Chem Inc., Chicago, IL)を使ってインシュリン・レベルを定量した。
インシュリン分泌刺激作用の時間依存的な継続時間を、腹膜内(i.p.)ペプチド投与後のズッカーラットにおける血漿インシュリン及びグルコース・レベルの定量によって評価した。具体的には、一晩に絶食した、体重約400gの糖尿病雄ラットを、50 mg/kgのペントバルビタールで麻酔し、そして採血のためにカテーテルを右大腿動脈に結んだ。その後、exendin-4、GLP-1、又はペプチド(0.4 nmol/kg)のボーラスをi.p.投与した。(1ペプチドにつきN≧2)。ペプチド投与前、及びその後30及び60分、そして2、4、6及び24時間に採集した血液を、インシュリン定量のために、EDTA及びアプロチニンを含むヘパリン処理管内に注ぎ、そして分離したサンプルで、グルコースを計測することにした。血漿を分離し、取り除き、そして直ちに-70℃に冷凍した。次にラット・インシュリンELISAキット(Crystal Chem Inc., Chicago, IL)を使ってインシュリン・レベルを定量し、血漿グルコースをグルコース酸化酵素法によって定量した。
GLP-1(2 μM)とGLP-1Aha8(配列番号8)(2 μM)を、PBS中、5 mUの組み換えDPP1V(Calbiochem, La Jolla, CA)と一緒に、37℃でそれぞれ10分間と2時間インキュベートした。両化合物(100 μM、100 μl)を、同等の量のヒト血清中、37℃で2時間インキュベートした。全てのケースについて、酸素反応を、トリフルオロ酢酸(0.1%v/vの終濃度)の添加によって止めた。マトリックス支援レーザー脱離イオン化法−飛行時間型質量分析法(MALDI-TOF)を使って、サンプルを直ちに分析した。MicromassMALDI-TOF(Micromass, Beverly, MA)リフレクトロン機器を、1スペクトルにつき5レーザー・ショットを用いて、1000〜6000 Daの質量範囲にわたり15〜25%のレーザー・エネルギーで使用した。α-シアノ-4-ヒドロキシシンナミック酸(Sigma, St.Louis, MO)を、マトリックスとして使用し、8 mg/mlの炭酸アンモニウム(Sigma, St.Louis, MO)バッファー中、10 mg/mlの濃度に調製した。MALDIプレートに移す前に、1 μlのサンプルを、マトリックスで50/50 v/vに希釈した。
6ヶ月齢の雄ズッカーfa/faラット(Harlan, Indianapolis, IN)、及び6ヶ月齢のウィスターラットを、この研究で使用した。それらを、食べ物と水を自由摂取させ、12時間の明、12時間の暗のサイクル(午前7時に点灯)の状態にした。ズッカーラットの床敷きは、紙ベースの製品「Carefresh」(Absorption Co., Belingham、WA)であった。実験の前一晩、床敷きの不存在の状態で、ズッカーラットをワイヤー上で絶食させた。ウィスターラットを、それらの通常の床敷き上で絶食させた。ペントバルビタール(50mg/kg)の腹膜内の注射によって全身麻酔を誘発した。採血のために大腿動脈にカニューレを取り付け、そしてポリペプチド(GLP-1Aha8(配列番号8)及びGLP-1Gly8(配列番号3)、24 nmol/kg)を、動物の首筋に皮下注射した(各処置群についてn=5)。血糖値を、Glucometer Elite(Bayer Corp. Diagnostics, Tarrytown, NY)を使っやグルコース酸化酵素法によって計測した。
この研究は、Ex-4の生物活性に対する、第9C末端アミノ酸の重要性を判断するために実施した。切詰められたEx-4アナログの配列と、第9C末端配列を付加したGLP-1アナログを当該研究に使用した。
先に記載のとおり、ペプチドを合成した。全てのペプチドが、95%超の純度であった。表4は、研究したGLP-1及びexendin-4アナログの配列を示す。イソブチルメチルキサンチン(IBMX)は、Calbiochem(La Jolla, CA)から購入した。Exendin-4及びGLP-1-(7-36)アミドを、Bachem(Torrance, CA)から入手した。クローン化したラット・インスリノーマ細胞系RIN1046-38は、Dr. Samuel A. Clark(BioHybrid Technologies, Shrewsbury, MA)からの贈与物であり、37℃の加湿5%CO2-95%エアー・インキュベーター内で、グルコース(11 mM)、50 U/mlのペニシリン、50 μg/mlのストレプトマイシン及びグルタミン(2 mM)を補充したEarle's塩(Mediatech, Inc., Herndon, VA)を伴うM199中で、日常的に培養された。GLP-1受容体遺伝子により安定的にトランスフェクトされたチャイニーズハムスター卵巣(CHO)細胞、CHO/GLP-1R細胞を、先に記載した。血漿インシュリン・レベルをELISAによって計測した(Crystal Chem Inc., Chicago ILL)。HbA1cを、Greig et al., 1999に記載のとおり計測した。血糖値を、Glucometer Elite(Bayer Diagnostics, Tarrytown, NY)を使って計測した。
下線を引かれたアミノ酸が、試験されるexendin-4配列由来のアミノ酸を表す。
6ヶ月齢の雄ズッカー(fa/fa)ラット(Harlan, Indianapolis, IN)、2ヶ月齢のC57BLKS/J-Leprdb/Leprdbマウス(Jackson Laboratories, Bar Haror, MA)、及び2ヶ月齢のフィッシャーラット(Harlan, Indianapolis, IN)を、急性及び慢性の実験で使用した。全ての動物に、食べ物と水を自由摂取させた。動物を、12時間の明-暗いサイクル(午前7時に点灯)の状態のおいた。ズッカーラット及びdb/dbマウスのための床敷きは、紙ベースの製品、Carefresh(Absorption Co., Belingham, WA)であり、そしてフィッシャーラットを、通常の床敷きの上に収容した。
12ウェル・プレート上で60から70%集密まで培養したRIN1046-38細胞を、実施例3に記載のとおり処理し、そして適宜にcAMP定量を実施した。用量反応曲線を図21に示す。
実施例4に記載のとおり結合試験を実施した。表5は、それぞれCHO GLP-1R細胞における競合的結合及びRIN 1046-38細胞におけるcAMPアッセイから得たIC50及びEC50値を示す。
全ての値を平均±SEMとして示し、群間の差を、ANOVAを使って分析した。図1及び2の曲線を、反復コンピュータプログラム(20)を使って4因子S字状ロジスティック回帰方程式に適合させ、そして表2のEC50及びIC50値を適合データから計算した。
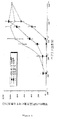
10 nmol/kgのペプチドを、0.1%のBSAを含むPBS溶液で投与したことを除き、実施例5で先に記載したとおり、6ヶ月齢の雄ズッカーfa/faラット(Harlan, Indianapolis, IN)をこの研究で使用した。Ex(1-36)及びEx(1-35)のsc注射後の血糖値を、図22に示す。
動物を、実験開始前にそれらの環境順化を容易にするために、2.5ヶ月間我々の施設に収容した。処理の最初の20日間、毎日午前9時に、動物にEx(1-30)(1 nmol/kg)を腹膜内(ip)注射で与えた。その後、次の32日間、午前9時と午後9時位に、動物は、ipでEx(1-30)(1 nmol/kg)を受けた。処理プリトコールの最初の20日の終了時点で、血糖値及びHbA1cを計測した。食物摂取及び動物体重を、毎日午前9時の注射時に測定した。スケジュールの中で失敗した日はない。磁気共鳴像(MRI)を、51日目で取り、そしてIPGTTを、52日目に実施した。
1.9 T、ボア31 cmのBruker BioSpecシステム(Bruker Medizintechnik GmbH, Ettlingen, Germany)、内径20 cmのシールド型グラジエント・セット、及び直径5 cmのボリューム共鳴器を使って、磁気共鳴イメージを得た。慢性の研究で使用した動物を、イソフルオラン知覚麻痺下に置き、標準T1強調多重スライス・スピン−エコー法(TR=500 ms、TE=8.5 ms)を、腹部全体を含む領域をカバーする、各2.1mmの厚さの20の隣接するスライスにわたって得られた。視野は、128×128画素より高く5×5 cmであった。各々のイメージを、約9分の総撮像時間にわたり、8回の収集を使って収集した。全ての動物において、撮像を2つの時点(0日目と51日目)で実施した。
アルツハイマー症(AD)の重要な病理的な特徴の1つは、主にアミロイド-βペプチド(Aβ)より成る老人斑の脳血管沈着である。Aβは、より大きなグリコシル化膜結合タンパク質β-アミロイド前駆体タンパク質(βAPP)から誘導される。大部分のβAPPは、Aβドメインにタンパク質分解によって切断されて、アミロイド生成性断片の形成を防ぐ可溶性誘導体(sAPP)を産生する。この研究は、β-アミロイド前駆体タンパク質のプロセッシングに対するGLP-1及び2つのアナログの効果を測定するために実施した。
ラット褐色細胞腫(PC12)細胞系において、ニューロンの増殖と分化、及びニューロンタンパク質の代謝に対するGLP-1とその長期作用性アナログ2種類、exendin-4、及びexendin-4 WOTの効果を、試験した。GLP-1及びexendin-4は、神経突起の伸長を誘発し、それは、選択的GLP-1受容体拮抗薬、exendin(9-39)との同時インキュベーションによって覆された。さらに、exendin-4は、神経成長因子(NGF)によって開始された分化を促進し、かつ、NGF介在撤回に続く細胞の変性を救う。
7S NGFを、Promega(Madison, WI)から購入した。GLP-1及びexendin(9-39)を、Bachem(Torrance, CA)から入手した。Exendin-4及びそのアナログ、exendin-4WOTを合成し、先に記載のとおりHPLC分析によって>95%の純度であることを評価した。全ての他の化学薬品は、別段の記載のない限り、高純度であって、Sigma Chemicals(St.Louis, MO)から入手した。
統計分析を、必要に応じて実施した。結果を平均±SEM(SEM=平均間の差異の標準誤差)と表現した。SPSSバージョンVIIを使って、分散分析(ANOVA)を実行し、p<0.05を、統計的に有意であるとみなした。有意な主効果に続いて、Tukey's Honestly Significant Difference test(テューキーのHSD)を使って計画比較を行った。
褐色細胞腫細胞を、Dr. D. K. Lahiri(Indianapolis)から入手し、RIN1046-38細胞(クローン・ラット・インスリノーマ細胞株)は、Dr. Samuel A. Clark(Bio Hybrid Technology, Shrewsbury, MA)からの贈与物である。PC12細胞を、10%の熱不活化ウマ血清、5%の熱不活化胎児ウシ血清、25 mMのHepesバッファー、及び1×抗生物質−抗真菌溶液を補ったRPMI1640中で培養した。RIN1046-38細胞を、12 mMのグルコースを含み、5%の熱不活化胎児ウシ血清、0.03%のグルタミン、50 U/mlのペニシリン、及び50 mg/mlのストレプトマイシンを補った培地199中で培養した。細胞培養培地及び血清を、MediaTech(Cellgro) Inc.(Herndon, VA)から入手した。細胞を、5.0%のCO2を含む加湿雰囲気中で培養した。それらを、1枚の60 mm皿につき約2.0×106細胞にて播種した。PC12細胞を、ラットの尾のコラーゲンで覆われた培養器(Roche Molecular Biochemicals, Indianapolis)上で培養した。7S NGFを、100 mg/mlの濃度で成長培地中への希釈によって調製し、-20℃で保存した。GLP-1及びアナログの原液を、滅菌水中で新たに作製し、-20℃で保存した。
イムノブロッティング法によるタンパク質分析のために、調整培地及び細胞ペレットを毎日採集した。細胞ライセートを以下のとおり調製した。プレートからの細胞を、そっと回収し、10分間800 gで遠心分離した。細胞ペレットを、10 mMのTris-HCl(pH7.4)、1%のSDS、0.174 mg/mlのフッ化フェニルメチルスルホニル(PMSF)、各々1 mg/mlのアプロチニン、ロイペプチン、ペプスタチンA、及び45.98 mg/mlバナジン酸ナトリウムと10.5 mg/mlフッ化ナトリウムの混合物4 mlを含む溶解バッファー中に懸濁した。懸濁した細胞を、粉砕し、15分間14,000 gで遠心分離した。上清溶液のタンパク質(細胞ライセート)を、計測し(Bradford, 1976)、イムノブロッティング法によって分析した。
2.6%のビスアクリルアミド(Novex、サンディエゴCA)を含む10%のTris−グリシン・ゲルを使って、各細胞ライセート及び調整培地からのタンパク質10 μgを用いて、ウェスタンブロット分析を実施した。タンパク質を、PVDF紙上にブロットした。5%の酢酸(Sigma)中、0.1%のPonceau S溶液を用いて膜を染色することによって、移したタンパク質を可視化した。
PC12細胞を、上記のとおり60 mm皿上で培養し、4日間培養した。この間神経突起の伸長を毎日定量した。1枚の皿につき、5つの無作為な細胞領域を評価し、そして神経突起をもつ細胞の割合が測定した。1つの領域につき約100細胞を、細胞体のそれと同等以上の長さの神経突起について記録した。1つの細胞につき1以上の突起をもっていたかもしれないが、1つの細胞を一度だけ記録した。
exendin-4(100 ng/ml)を、10 ng/ml又は30 ng/mlのNGFのいずれかと同時処理したとき、神経突起伸長の有意な増加を、未処理対照細胞に対して観察した(それぞれ、596%及び819%増加、ともにp<0.01)。NGF処理単独に対する神経突起伸長の増加は、30 ng/mlで有意であるのみだった(p<0.01)。類似した結果を、単独で又はNGFと組み合わせて、他の投与量のexendin-4によって観察した。これらのデータは、exendin-4が分化を開始することができて、かつ、NGFに誘発された分化を促進することができることを示唆している。
50 ng/mlのNGFの存在/不存在下、又はexendin-4(1又は5 mg/ml)存在/不存在下、PC12細胞を、完全培地(RPMI1640+5%のウシ胎仔血清+10%のウマ血清)中で培養した。4又は7日後に、細胞を採集し、続いてさらに3日間、通常培地中で回復させた。最終日に、細胞を採集し、生細胞の割合を測定するためにMTTアッセイを実施した。2番目の組の実験(阻止)において、4又は7日間、細胞を、50 ng/mlのNGF及びexendin-4(1又は5 mg/ml)の存在下で培養した。細胞を採集し、前記のとおり回復させた。3番目の組の実験(救済)において、細胞を、50 ng/mlのNGFの存在下で4日間培養した。さらに3日間、5 mg/mlのExendin-4を、培地に加えた。7日目に細胞を採集し、前記のとおり回復させた。
Promega(Madison, WI)製のCellTiter96(登録商標)Aqueous One Solution Cell Proliferation Assay Reagentを、修飾MTTアッセイにおける生細胞数の測定のための比色分析手順で使用した。この試薬は、新規テトラゾリウム化合物[3-(4,5-ジメチル-2-yl)-5-(3-カルボキシメトキシフェニル)-2-(4-スルフォフェニル)-2H-テトラゾリウム、内部塩;MTS]、及び電子共役試薬(フェナジン・エトスルフェート;PES)を含む。PESは化学安定性を高め、それはMTSとの組み合わせを可能にし、安定した溶液を形成した。MTSテトラゾリウム化合物は、組織培養培地に溶解する、有色のホルマザン産物へと細胞によって生物学的に還元される。代謝的に活性な細胞中のデヒドロゲナーゼ酵素によって産生されるNADPH又はNADHによって、この転換は恐らく達成される(Berridge and Tan, 1993)。アッセイを、直接的に培養したウェルへの少量の試薬の追加、1〜4時間のインキュベーション、続く96ウェルプレート・リーダーによる490 nmの吸光度によって実施される。490 nmの吸光度の値によって計測されるホルマザン産物の量を、培養物中の生細胞の数に直接に比例している。MTSホルマザン産物は組織培地に溶解するので、本手順は、MTTのようなテトラゾリウム成分を使う手順よりわずかなステップしか必要としない。
GLP-1及びexendin-4誘発神経突起伸長の機構を決定するために、分化した培養物を、それぞれERK MAPKとPI3-Kを阻害する50 μMのPD98059又は40 μMのLY294002で処理する。cAMPに依存したMAPKリン酸化がPKAによって制御されたかどうかを決定するために、GLP-1及びNGFによって誘発した神経突起をPKAの特異的阻害薬、H89で処理した。
GLP-1、exendin-4又はexendin-WOTの誘発したPC12細胞の分化の間に生じている分子の変化を検討するために、シナプス小胞膜でよく発現されているリン酸化された37 kDaのタンパク質である、シナプトフィジンの特徴を試験した。PC12細胞の神経分泌液胞を染色するシナプトフィジン・モノクローナル抗体(Oncogene Research Products, San Diego, CA)を使用した。膜を、20 mMのTris、500 mMのNaCl pH7.4、1%(w/v)のカゼイン(BioRad, San Diego, CA)によって37℃で1時間ブロックした。一次抗体を、ブロック中に希釈し、そして4℃で一晩タンパク質と一緒にインキュベートした。前記膜を、20 mMのTris pH7.4、150 mMのNaCl、及び0.05%のTween-20(TBST)で3回、室温で15分間強く洗浄した。ブロック中、ペルオキシダーゼ連結二次抗体を、膜と一緒に室温で2時間インキュベートした。ペルオキシダーゼ連結抗マウスIgM(Chemicon, Tenecula, CA)を、シナプトフィジンに対する二次抗体として使用した。過剰な抗体を、TBSTで3回強く洗い落とし、その後ECLプラス(Amersham, Philadelphia, PA)中で5分間インキュベーションした。続いて膜を写真用フィルムに焼き付けた。Molecular Analystソフトウェア(BioRad, Hercules, CA)を使ってタンパク質バンドの濃度測定による定量化を実施した。
PC12細胞を、35 mm培養皿内のポリ-L-リジン・コート・ガラス・カバースリップ上に移し、(先に記載のとおり)標準的な条件下で培養した。細胞を、30分間、0.25%のグルタルアルデヒドを用いて固定した。内性ペルオキシダーゼ活性を、0.3%のH2O2でクエンチし、GLP-1受容体のN末端に対して産生された一次ポリクローナル抗体(Dr. Joel F. Habener, Massachusetts GeneralHospital, MAからの贈与物)(希釈係数1:1500)中でのインキュベーションを、室温で1時間実行した。可視化は、ビオチン化抗ウサギIgG二次抗体中でのインキュベーションに続く、ジアミノベンジジン・ジヒドロクロライド(DAB)による発色を伴う、アビジン−ビオチン・ペルオキシダーゼ法を使った。
RT-PCRを、GLP-1受容体mRNAに関する高感度アッセイとして実施した。ラット・インスリノーマ細胞(RIN細胞)を、正の対照として使用した。全RNAを、ChomczynskiとSaccchi(1987)の方法を使ってPC12細胞から分離した。2.5 mgのRNAを我々のRT-PCR反応に使用した。50 mMのKCl、10 mMのTris-HCl、3.5 mMのMgCl2、200 mMのdNTP、並びに各々0.4 mMのラットGLP-1Rセンス(5'ACAGGTCTCTTCTGCAACC 3')及びアンチセンス(5'AAGATGACTTCATGCGTGCC 3')オリゴヌクレオチド・プライマー(膵臓のGLP-1受容体配列の5'及び3'末端)を含むバッファー50 mlの量でRT-PCRを行った。[a-32P]dCTPの存在下、30サイクルで増幅を行った。ラット島細胞を、正の対照として使用した。RT-PCR産物(10 ml)を、適当なサイズマーカーと一緒に4〜20%のポリアクリルアミドゲルで分離した。続いて、真空下80℃で1時間ゲルを乾燥させて、そしてX線フィルムに焼き付けた。
cAMPの測定の前に、PC12細胞を、3日間、33 μg/mlのGLP-1で処理した。トリプリケートの培養物を、処理開始後、合計期間30分の間、5分の間隔で採集した。処理開始時(ゼロ分)に採集した細胞を、cAMPの基礎レベルに使用した。サイクリックAMPを、Monte-Rafizadeh et al.,(1997a)の方法に従って計測した。
exendin-4の考えられる毒性効果を、インビトロにて2つの方法:LDH分析及びトリパンブルー排除法によって試験した。LDHアッセイを、Sigmaキットを使って実施した。処理後に異なる時間間隔で回集した調整培地サンプルを、高感度乳酸デヒドロゲナーゼ(LDH)アッセイに供した。LDHアッセイは、総細胞質内LDHを通して又は培地中に放出された細胞質内LDHの量の関数としての膜の完全性によって、細胞数の尺度を提供した。放出されたLDHの測定は、LDHの作用によるNADの減少に基づいた。得られた減少したNAD(NADH)を、テトラゾリウム色素の化学量論的変換に利用した。最終有色化合物を、分光光学的にに計測した。培地をアッセイするより前に細胞が溶解された場合、細胞数の増加又は減少が、変換された基質の量の付随する変化をもたらす。これは、試験物質によって引き起こされた胞傷害反応又は膜損傷(細胞毒性)の程度を示した。
GLP-1が培養においてPC12細胞の増殖に影響するかどうかを測定するために、5-ブロモ-2'-デオキシウリジン(BrdU)の取り込みを観察することによって低血清培地中の細胞増殖を評価した。標識後の抗BrdU抗体を用いた免疫細胞化学を、標識の時点で活発にDNAを複製していた細胞を確認するために使用した。PC12細胞を、33 μg/mlのGLP-1又は50 ng/mlのNGFの存在下又は不存在下で3日間培養した。細胞DNAを標識するために、4%のパラホルムアルデヒド中に固定する6時間前に、10 μMのBrdUを培地に加えた。方法の残りの部分は、増殖キット(Roche, Indianapolis, IN)に従って行った。増殖している細胞(BrdU標識の時点でDNA複製を受けてた細胞)は、クロモゲン反応により暗染された核を示した。BrdU取り込みを、処理の1、2及び3日目に定量した。各々の処理条件について3枚の皿をカウントし、細胞総数に対する標識された細胞のパーセンテージとして表した。PC12細胞は、NGFによる処理(未処理に対して9%の上昇)及びGLP-1による処理(未処理に対して18%)後、1日目にBrdUの取り込みの増加を示した。
グルタミン酸によって誘発した細胞死から培養海馬ニューロンを保護する、並びに、成体ラットイにおけるボテン酸で誘発したコリン作用性マーカー欠損を軽減する、GLP-1及びその長期作用性アナログ、exendin-4の能力を試験した。
海馬ニューロン培養物を、前記(Mattson et al., 1995)に類似した方法を使って18日齢の胎仔Sprague Dawleyラットから調製した。要するに、細胞を、軽いトリプシン処理及び粉砕によって解離させ、そして10%のFBS及び1%の抗生物質溶液(104 U/mlのペニシリンG、10 mg/mlのストレプトマイシン及び25 μg/mlのアムホテリシンB;Sigma Chemicals, St. Louis, MO)を含む最小必須培地中に蒔いた。海馬ニューロンを、25 mmの直径のポリ-D-リジン・コート・ガラス・カバースリップ上に、100,000細胞/mlの密度で蒔いた。細胞を蒔いた3時間後に、培地を、1%のB27-サプリメント(Gibco/Life Technologies, Carlsbad, CA)を含む無血清Neurobasal培地によって交換した。
結合の検討を、Montrose-Rafizadeh(1997b)に記載のとおり実施した。デュプリケートの海馬ニューロン培養物を、0.5 mlの結合バッファーで洗浄し、続いて
2%のBSA、17 mg/lのdiprotinA(Bachem, Torrance, CA)、10 mMのグルコース、0.001〜1000 nMのGLP-1、及び30,000 cpmの125I-GLP-1(Amersham Pharmacia Biotech, Little Chalfont, UK)を含む0.5 mlのバッファー中、4℃で一晩インキュベートした。インキュベーション終了の時点で、上清を捨て、そして細胞を氷冷PBSで3回洗浄し、そして0.5mlの、0.5MのNaOH及び0.1%のSDS中、室温で10分間インキュベートした。細胞ライセート中の放射活性を、Apecシリーズγカウンター(ICN Biomedicals, Inc., Costa Mesa, CA)えにより計測した。総結合から、大過剰の非標識GLP-1(1 μM)の存在でインキュベートした細胞に関する放射活性を差し引いたものとして、特異的結合を測定した。50%の結合、EC50に関係しているGLP-1濃度を、ロジット・プロット分析によって測定した。
機能性GLP-1受容体の存在を証明するために、サイクリックAMPを、Montrose-Rafizadeh et al.,の方法に従って計測した(1997a)。トリプリケートの海馬ニューロンの細胞培養を、10 nMのGLP-1で処理し、合計で30分間、薬物処理開始後5分間隔で採集した。薬物処理の開始時(ゼロ分)で採集された細胞を、cAMPの基礎レベルに使用した。
蛍光性DNA結合色素Hoescht 33342を、アポトーシス細胞死を計測するために使用した。ニューロンを、グルタミン酸(10 μM)の存在又は不存在下、GLP-1(10 nM)又はexendin-4(0.3 μM)を伴ったLocke'sバッファー中で16時間インキュベートした。使用したGLP-1の濃度は、cAMPの放出を刺激することが証明され、かつ、我々の先のニューロン細胞研究において細胞死を引き起こすことなく分化を誘発した、結合実験によって得られたEC50値を基にした。細胞を、PBS中、4%のパラホルムアルデヒド溶液中で固定し、膜を0.2%のTritionX-100によって透過処理した。Hoechst 33342(1 μM)との30分間のインキュベーションに続いて、40×油浸対物レンズを使ってエピ蛍光照明(340 nm励起、510 nmバリア・フィルター)下で核を可視化した。約200の細胞を、各々の処理条件について少なくとも3枚の別々の皿でカウントし、そして実験を少なくとも2度繰り返した。核DNAが断片化されるか又は凝集された場合、細胞はアポトーシスであると考えられ、それに対しより拡散した、及び均一な分布の核DNAをもつ細胞は生き残ったものとみなした。カウントの時点で、調査員は処理群の正体に気付かなかった。凝集又は断片化された核をもつ細胞のパーセンテージを、各々の培養物で測定した。
各々約300gの体重がある35匹の生体雄フィッシャー-344ラットを、食物及び水を自由摂取できる、制御された明/暗、及び温度条件下で収容した。ラットを、ケタミン(90 mg/kg)とアセプロマジン(0.91 mg/kg)で麻酔をかけた。先に記載のとおり定位の手術が実行した。0.1 Mのリン酸緩衝生理食塩水(PBS)中に溶解したイボテン酸を、10 μg/μl(0.5 μl、2箇所)で、内側前脳束の左側支部に注入した;Paxinos & Watson(1998)によって大脳核と呼ばれた、参考文献を参照のこと。毒素のこの特定の一団の効能に関する先の試験的な調査が、この投与量が、皮質への突起の同程度の減少と共に、脳基底におけるコリン・アセチルトランスフェラーゼ(ChAT)陽性免疫反応性の60%減少を引き起こしたことを証明した。媒質の注入を受けた2番目のシリーズを、対照として使用した。各々の注入を、2.5分にわたり行い、そしてさらに2.5分がカニューレを引き抜く前の拡散のために与えられた。2週間後、動物を、再度麻酔し、脳室内カニューレを定位的に右側脳室に植え込んだ(AP=-0.8 mm、L=+1.4 mm、V=-4.0mm)。
隣接する前頭面に沿った脳切片を、病変部位を通して40 μmの厚さで得、そして処理したChATについて;1:100希釈のポリクローナル・ヤギ抗ChAT抗体(Chemicon、International Inc., Temecula, CA)を使って、及びグリア繊維酸性タンパク質(GFAP)について;1:750希釈のポリクローナル・ウサギ抗GFAP抗体(Chemicon)を使って、比較的自由に処理した。アビジン-ビオチン/セイヨウワサビペルオキシダーゼ・プロトコルを使って、陽性の免疫反応性の可視化を行った。さらに、一組の切片を、Geula and Mesulam, 1989によって、修飾された方法を使って前脳基底核のコリン作用性ニューロンについて細胞化学的マーカーとしてのアセチルコリンエステラーゼ(AChE)活性について染色した。追加の一組の切片を、ゼラチン・コートされたスライド上へのせ、クレシル・バイオレットで染色して細胞体を可視化した。
コリン・アセチルトランスフェラーゼ免疫反応性を、前脳基底核全体にわたるコリン作用性ニューロンのマーカーとして使用した。ChAT抗体は、類似したサイズとアセチルコリンエステラーゼ(AChE)陽性細胞への分布をもつ非常に多数の大きな多極ニューロンを染色した。免疫細胞化学的染色は、低いバックグラウンドをもち、かつ、細胞形態の明確な写真を提供した(図17)。媒質の連続注入を伴うイボテン酸の注入は、左大脳核の注射部位から約1 mm半径のChAT-免疫反応性ニューロンの大幅な(43%)損失をもたらした(図18、棒グラフ4)。媒質注入を受けたシャム手術対照群は、右大脳核に対する左大脳核のChAT陽性細胞体のパーセンテージの増加を示した(図18、棒グラフ1)。GLP-1又はexendin-4注入を受けたイボテン酸損傷動物は、媒質の注入を受けたそれらの損傷動物に対して左大脳核におけるChAT-免疫反応性細胞体の損失の減少をもたらした。より特に、exendin-4の注入は、媒質注入に続いて現れた43%から大脳核のそれのたった24%未満まで、左大脳核のChAT-免疫反応性細胞体の損失の減少をもたらした(図18、棒グラフ5)。さらに、GLP-1注入は、右大脳核のそれのたった6%未満まで左大脳核のChAT陽性免疫反応性細胞体の損失を減少させる、より多くの顕著な逆転を成し遂げた(図18、棒グラフ6)。標準ANOVAは、処理条件についての全体的な有意な効果を証明した(F=21.363、df=5,28、p<0.001)。ペプチド、対、媒質処理の多重比較(Tc=14.14及び19.71)は、イボテン酸による病変の後のexendin-4(p<0.05)、及びGLP-1(p<0.01)の注入を受けて左大脳核におけるChAT免疫反応性の有意な改善を明らかにした。イボテン酸による病変後のGLP-1注入であっても、右側とほぼ対等の値を実現するまで、左大脳核のChAT陽性細胞の損失を減少させ、全体的なパーセント差異は、シャム媒質群より有意に低いままであった(p<0.001)。媒質注入を受けたシャム群(sham group)のChAT-免疫反応性のかなりの増加のため、これは適当である(図18、棒グラフ1)。
Aβ1-42又はFe2+で誘発した細胞死に続くGLP-1及び/又はexendin-4の保護効果、並びにインビトロにおける、分泌型と細胞内型の間のβAPPプロセッシングに対するGLP-1、exendin-4、及びexendin-4WOTの効果、そして最終的に、対照マウスにおけるインビボでのAβペプチドのレベルを試験した。
他の箇所で記載のとおり、PC12細胞を、10%の熱不活化ウマ血清、5%の熱不活化ウシ胎仔血清(FBS)、及び25 mMのHepesバッファーを補ったRPMI 1640中で培養した(Labiri et. al., 2000)。全ての培地及び血清を、MediaTech Inc. (Herndon, VA)から入手した。細胞を、ラットの尾のコラーゲンでコートした培養器(Roche Molecular Biochemicals, Indianapolis, IN)に、約2.0×106細胞/60 mmで蒔いた。細胞が十分に接着するとすぐに、播種した24時間後に処理をトリプリケートで開始した。前記培地を吸引し、適当な化合物を伴った0.5%のFBSを含む、3 mlの新鮮な低血清培地を加えた。細胞を、GLP-1(3.3、33及び330 μg/ml)(Bachem, Torrence, CA)、及び2つのGLP-1アナログ、exendin-4(0.1、1.0及び10 μg/ml)及びexendin4-WOT(0.1及び1.0 μg/ml)で処理した。NGF(5、10、25及び50 ng/ml)(Promega, Madison, WI)によるPC12細胞の処理を、正の対照として使用した。さらに、5 ng/mlのNGFと0.1 μg/mlのexendin-4を、組み合わせて同時に加えた。Exendin-4及びそのアナログのexendin4-WOTを、合成し、そして高速液体クロマトグラフィー分析によって95%超純粋であると評価した。
処理が誘発した細胞毒性を、処理及び未処理のPC12細胞由来の調整培地の両方で(Sigma, St.Louis, MO製のLDHキットを使って)分泌された乳酸デヒドロゲナーゼ(LDH)レベルの分析によって検査した。予想どおり、LDHレベルは、薬物処理の開始時点で採取した培地標準に対して上昇した(図19A)。分散分析は、LDH分泌に対する処理の全体的な有意な効果を証明した(F=2.22、df=11,35、p<0.001)。チューキーのHSD検定(Tc=0.42,及び0.51)を使った対照との帰納的な連続した多重比較が、10 μg/mlのEx4処理に続くLDH分泌の単一の有意な増加を明らかにした(1.65倍上昇;p<0.01)。使用した投与量及び時点での、GLP-1及びアナログでの処理の結果としての毒性の可能性は;10 μg/mlのexendin-4を除いて、外されうる。これは、合計細胞数で全く有意な変化を証明しなかったGLP-1処理前後に実行した(トリパンブルーによる染色後の)細胞カウントによってさらに実証された。
3日間の処理に続いて、未処理(低血清培地のみ)及び処理PC12細胞由来の調整培地及び(前記のとおり調製された)細胞ライセートを、モノクローナル抗体、22C11(Roche Molecular Biochemicals, Indianapolis, IN)を使ったウエスタン免疫ブロット分析に供した。そのエピトープ部位が外形質のシステイン含有ドメイン内の第66〜81残基に割り当てられたE.コリ(E.coli)産生βAPPに対して産生された抗体は、細胞膜で見出されるβAPPの全ての成熟型、及び調整培地中に分泌されるカルボキシル切り詰め可溶性型及びβAPP様タンパク質(APLP)を認識する。免疫反応産物の可視化を、化学発光によって行い、ゆえに分子量マーカーは写真用フィルム上で見えなかった。PVDF膜上に目に見える標準分子量マーカーを重ねることによって発光性の産物の分子量の特定を達成した。NIHイメージを使ってタンパク質バンドの濃度測定による定量化を実施した。
サンドイッチELISAを使って等量の調整培地及び脳全体のホモジェネートを、Aβ1-40についてアッセイした(Suzuki et. al., 1994)。モノクローナル抗体BAN50(Aβ1-16に対して産生された)を全ての種類のAβ(Aβ1-40とAβ1-42)のための捕獲抗体として使用し、モノクローナル抗体BA27を、Aβ1-40レベルの特異的な検出のために使用した。アッセイと並行して行なわれた適当な標準曲線から推論されるように、Aβ1-40のレベルを、調整培地サンプルに関するpM濃度で、そしてマウス脳ホモジェネートに関してfmol/gで表した。
海馬を発生初期18日目のSprague-Dawleyラットから取り出し、細胞を軽いトリプシン処理及び粉砕によって分離し、そして約150細胞/mm2培養面積の密度で、ポリエチレンイミンによって表面をコートしたプラスチック製の直径35 mmの皿上に播種した。培養物を、37℃で、6%のCO2/94%の大気雰囲気中、B-27サプリメン(GibcoBRL ,Carlsbad, CA)、2 mMのL-グルタミン、1 mMのHepes、及び0.001%の硫酸ゲンタマイシン(Sigma, St.Louis, MO)を含むNeurobasal培地中で維持した。これらの条件下で維持されるとき、ニューロン抗原NeuN及び神経膠星状細胞タンパク質グリア繊維酸性タンパク質に対する抗体で免疫染色することによって測定されるように、この海馬培養物は、約95%のニューロンと5%の神経膠星状細胞から成る。Aβ1-42を、Bachem(Torrance, CA)から購入し、滅菌水中に1 mMの原液として調製した。FeSO4を、滅菌水中に200 μMの原液として調製した。GLP-1及びexendin-4を、生理食塩液中に500×の原液として調製した。
Claims (51)
- ニューロンの死滅を減少させるための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、1以上のニューロンが該ポリペプチドと接触させられることによってニューロンの死滅が減少させられるものである、使用。
- 前記接触ステップがインビボにおいてである、請求項1に記載の使用。
- 前記接触ステップがインビトロにおいてである、請求項1に記載の方法。
- 前記ニューロンの死滅が神経変性症状によって引き起こされる、請求項1に記載の方法。
- 前記ニューロンの死滅が毒素によって引き起こされる、請求項1に記載の方法。
- 前記ニューロンの死滅が損傷によって引き起こされる、請求項1に記載の方法。
- ニューロンの分化又は増殖を促進するための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、1以上のニューロンが該ポリペプチドと接触させられることによってニューロンの分化又は増殖が促進させられるものである、使用。
- 前記接触ステップがインビボにおいてである、請求項7に記載の方法。
- 前記接触ステップがインビトロにおいてである、請求項7に記載の方法。
- アミロイドタンパク質の形成又は蓄積を減少させるための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、1以上のニューロンが該ポリペプチドと接触させられることによってアミロイドタンパク質の形成又は蓄積が減少させられるものである、使用。
- 神経突起の発達を促進するための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、1以上のニューロンが該ポリペプチドと接触させられることによって神経突起の発達が促進されるものである、使用。
- 前記接触ステップがインビボにおいてである、請求項11に記載の方法。
- 前記接触ステップがインビトロにおいてである、請求項11に記載の方法。
- 神経変性症状の患者を治療するか、又は患者の神経変性症状の1以上の徴候を軽減させるための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、治療として有効な量の該ポリペプチドが患者に投与されることによって、神経変性症状の患者が治療されるか、又は患者の神経変性症状の1以上の徴候が軽減されるものである、使用。
- 前記神経変性症状が、アルツハイマー病、パーキンソン病、ハンチントン病、筋萎縮性側索硬化症、脳卒中、多発性硬化症、脳の損傷、脊髄損傷、及び末梢神経障害から成る群から選ばれる、請求項14に記載の使用。
- 神経毒性損傷の患者を治療するか、又は患者の神経毒性損傷の1以上の徴候を軽減させるための医薬の製造のための、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドの使用であって、治療として有効な量の該ポリペプチドが患者に投与されることによって、神経毒性損傷の患者が治療されるか、又は患者の神経毒性損傷の1以上の徴候が軽減されるものである、使用。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項1、7、10、11、14または16のいずれか1項に記載の使用。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項1、7、10、11、14または16のいずれか1項に記載の使用。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項1、7、10、11、14または16のいずれか1項に記載の使用。
- 配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む、ニューロンの死滅を減少させるための医薬組成物。
- 前記ニューロンの死滅が神経変性症状によって引き起こされる、請求項20に記載の医薬組成物。
- 前記ニューロンの死滅が毒素によって引き起こされる、請求項20に記載の医薬組成物。
- 前記ニューロンの死滅が損傷によって引き起こされる、請求項20に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項20に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項20に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項20に記載の医薬組成物。
- 配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む、ニューロンの分化又は増殖を促進するための医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項27に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項27に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項27に記載の医薬組成物。
- 配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む、アミロイドタンパク質の形成又は蓄積を減少させるための医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項31に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項31に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項31に記載の医薬組成物。
- 配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む、神経突起の発達を促進するための医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項35に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項35に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項35に記載の医薬組成物。
- 配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む、ニューロン突起を成長させるための医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項39に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項39に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項39に記載の医薬組成物。
- 神経変性症状の患者を治療するか、又は患者の神経変性症状の1以上の徴候を軽減させるための医薬組成物であって、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む医薬組成物。
- 前記神経変性症状が、アルツハイマー病、パーキンソン病、ハンチントン病、筋萎縮性側索硬化症、脳卒中、多発性硬化症、脳の損傷、脊髄損傷、及び末梢神経障害から成る群から選ばれる、請求項43に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項43に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項43に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項43に記載の医薬組成物。
- 神経毒性損傷の患者を治療するか、又は患者の神経毒性損傷の1以上の徴候を軽減させるための医薬組成物であって、配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列を含むポリペプチドを含む医薬組成物。
- 該ポリペプチドが配列番号:2の配列を含むものである、請求項48に記載の医薬組成物。
- 該ポリペプチドが配列番号:1、2、5、6、7、8、9、10、11、12、13、14、15、25および33からなる群より選択される配列からなるものである、請求項48に記載の医薬組成物。
- 該ポリペプチドが配列番号:2の配列からなるものである、請求項48に記載の医薬組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US30907601P | 2001-07-31 | 2001-07-31 | |
| US60/309,076 | 2001-07-31 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003517083A Division JP2005501058A (ja) | 2001-07-31 | 2002-07-30 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013007734A Division JP5695097B2 (ja) | 2001-07-31 | 2013-01-18 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010090129A true JP2010090129A (ja) | 2010-04-22 |
| JP5631578B2 JP5631578B2 (ja) | 2014-11-26 |
Family
ID=23196575
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003517083A Revoked JP2005501058A (ja) | 2001-07-31 | 2002-07-30 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
| JP2009262568A Expired - Lifetime JP5631578B2 (ja) | 2001-07-31 | 2009-11-18 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
| JP2013007734A Expired - Lifetime JP5695097B2 (ja) | 2001-07-31 | 2013-01-18 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003517083A Revoked JP2005501058A (ja) | 2001-07-31 | 2002-07-30 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013007734A Expired - Lifetime JP5695097B2 (ja) | 2001-07-31 | 2013-01-18 | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 |
Country Status (8)
| Country | Link |
|---|---|
| US (4) | US7576050B2 (ja) |
| EP (3) | EP2022505B1 (ja) |
| JP (3) | JP2005501058A (ja) |
| AT (2) | ATE536881T1 (ja) |
| AU (2) | AU2002317599B2 (ja) |
| CA (1) | CA2455963C (ja) |
| DE (1) | DE60228972D1 (ja) |
| WO (1) | WO2003011892A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20180096733A (ko) * | 2015-12-23 | 2018-08-29 | 더 존스 홉킨스 유니버시티 | 신경계 및 신경변성 상태의 요법으로서 장기간 작용하는 glf-1r 작용제 |
| WO2020175570A1 (ja) * | 2019-02-28 | 2020-09-03 | 新田ゼラチン株式会社 | 脳機能調整剤、およびこれを含む飲食品 |
Families Citing this family (135)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050272652A1 (en) * | 1999-03-29 | 2005-12-08 | Gault Victor A | Peptide analogues of GIP for treatment of diabetes, insulin resistance and obesity |
| ATE346093T1 (de) * | 2000-06-16 | 2006-12-15 | Lilly Co Eli | Analoge des glucagon ähnlichen peptid-1 |
| EP2022505B1 (en) | 2001-07-31 | 2011-12-14 | The Government of the United States of America, as represented by the Secretary of the Department of Health and Human Services | GLP-1, exendin-4, peptide analogs and uses thereof |
| ES2545090T3 (es) | 2001-12-21 | 2015-09-08 | Human Genome Sciences, Inc. | Proteínas de fusión de albúmina y GCSF |
| CA2468700A1 (en) * | 2002-01-08 | 2003-07-17 | Eli Lilly And Company | Extended glucagon-like peptide-1 analogs |
| GB0205693D0 (en) * | 2002-03-09 | 2002-04-24 | Astrazeneca Ab | Chemical compounds |
| US7731947B2 (en) | 2003-11-17 | 2010-06-08 | Intarcia Therapeutics, Inc. | Composition and dosage form comprising an interferon particle formulation and suspending vehicle |
| AU2004231461B2 (en) * | 2003-03-19 | 2009-11-12 | Eli Lilly And Company | Polyethelene glycol linked GLP-1 compounds |
| CN102174102A (zh) * | 2003-05-15 | 2011-09-07 | 塔夫茨大学信托人 | 肽和多肽药物的稳定类似物 |
| US7329725B1 (en) | 2003-10-29 | 2008-02-12 | Nastech Pharmaceutical Company Inc. | Phage displayed Trp cage ligands |
| AU2005203925A1 (en) | 2004-01-08 | 2005-07-21 | Theratechnologies Inc. | Glucagon-Like Peptide-1 analogs with long duration of action |
| CA2555894A1 (en) | 2004-02-11 | 2005-08-25 | Amylin Pharmaceuticals, Inc. | Pancreatic polypeptide family motifs and polypeptides comprising the same |
| US8076288B2 (en) | 2004-02-11 | 2011-12-13 | Amylin Pharmaceuticals, Inc. | Hybrid polypeptides having glucose lowering activity |
| JP2008515856A (ja) | 2004-10-07 | 2008-05-15 | ノボ ノルディスク アクティーゼルスカブ | 遅延性glp−1化合物 |
| WO2006037811A2 (en) | 2004-10-07 | 2006-04-13 | Novo Nordisk A/S | Protracted exendin-4 compounds |
| EP1838336A2 (en) * | 2004-12-24 | 2007-10-03 | Amylin Pharmaceuticals, Inc. | Use of glp-1 and agonists thereof to prevent cardiac myocyte apoptosis |
| WO2006083761A2 (en) | 2005-02-03 | 2006-08-10 | Alza Corporation | Solvent/polymer solutions as suspension vehicles |
| US11246913B2 (en) | 2005-02-03 | 2022-02-15 | Intarcia Therapeutics, Inc. | Suspension formulation comprising an insulinotropic peptide |
| CA2597649A1 (en) | 2005-02-11 | 2006-08-17 | Amylin Pharmaceuticals, Inc. | Gip analog and hybrid polypeptides with selectable properties |
| US8263545B2 (en) | 2005-02-11 | 2012-09-11 | Amylin Pharmaceuticals, Inc. | GIP analog and hybrid polypeptides with selectable properties |
| KR20080021636A (ko) * | 2005-05-05 | 2008-03-07 | 카딜라 핼쓰캐어 리미티드 | Glp-1 아고니스트인 신규 화합물 |
| CN100429227C (zh) | 2005-06-29 | 2008-10-29 | 常州制药厂有限公司 | Exendin4多肽片段 |
| EP1922336B1 (en) * | 2005-08-11 | 2012-11-21 | Amylin Pharmaceuticals, LLC | Hybrid polypeptides with selectable properties |
| EA014647B1 (ru) * | 2005-08-11 | 2010-12-30 | Амилин Фармасьютикалз, Инк. | Гибридные полипептиды с селектируемыми свойствами |
| US20090286722A1 (en) * | 2005-09-08 | 2009-11-19 | Utech Limited | Analogs of Gastric Inhibitory Polypeptide as a Treatment for Age Related Decreased Pancreatic Beta Cell Function |
| WO2007028633A2 (en) * | 2005-09-08 | 2007-03-15 | Uutech Limited | Treatment of diabetes related obesity |
| CN101262874A (zh) * | 2005-09-08 | 2008-09-10 | 塔夫茨大学信托人 | 稳定化的glp-1类似物 |
| EA015169B1 (ru) | 2005-09-14 | 2011-06-30 | Такеда Фармасьютикал Компани Лимитед | Применение ингибиторов дипептидилпептидазы |
| CN102675221A (zh) | 2005-09-16 | 2012-09-19 | 武田药品工业株式会社 | 用于制备嘧啶二酮衍生物的方法中的中间体 |
| DE602005017628D1 (de) | 2005-09-22 | 2009-12-24 | Biocompatibles Uk Ltd | Fusionspolypeptide vom glp-1 (glucagon-like peptide-1) mit erhöhten peptidaseresistenz |
| CN101534846B (zh) | 2005-11-07 | 2014-11-05 | 印第安纳大学研究及科技有限公司 | 显示生理学溶解性和稳定性的胰高血糖素类似物 |
| WO2007112347A1 (en) | 2006-03-28 | 2007-10-04 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| EP2004213A1 (en) * | 2006-04-03 | 2008-12-24 | Novo Nordisk A/S | Glp-1 peptide agonists |
| CA2648936C (en) * | 2006-04-20 | 2013-07-09 | Amgen Inc. | Glp-1 compounds |
| DE602006009631D1 (de) | 2006-05-10 | 2009-11-19 | Biocompatibles Uk Ltd | GLP-1 Peptide enthaltende kugelförmige Mikrokapseln, deren Produktion und deren Verwendung |
| JP5143131B2 (ja) | 2006-05-30 | 2013-02-13 | インターシア セラピューティクス,インコーポレイティド | 浸透圧送出システムの二片構成内部チャネル型の流れモジュレータ |
| PL2359808T3 (pl) | 2006-08-09 | 2013-10-31 | Intarcia Therapeutics Inc | Osmotyczne systemy dostawcze i zespoły tłokowe |
| US8497240B2 (en) | 2006-08-17 | 2013-07-30 | Amylin Pharmaceuticals, Llc | DPP-IV resistant GIP hybrid polypeptides with selectable properties |
| US8324383B2 (en) | 2006-09-13 | 2012-12-04 | Takeda Pharmaceutical Company Limited | Methods of making polymorphs of benzoate salt of 2-[[6-[(3R)-3-amino-1-piperidinyl]-3,4-dihydro-3-methyl-2,4-dioxo-1(2H)-pyrimidinyl]methyl]-benzonitrile |
| TW200838536A (en) | 2006-11-29 | 2008-10-01 | Takeda Pharmaceutical | Polymorphs of succinate salt of 2-[6-(3-amino-piperidin-1-yl)-3-methyl-2,4-dioxo-3,4-dihydro-2H-pyrimidin-1-ylmethy]-4-fluor-benzonitrile and methods of use therefor |
| US8669228B2 (en) | 2007-01-05 | 2014-03-11 | Indiana University Research And Technology Corporation | Glucagon analogs exhibiting enhanced solubility in physiological pH buffers |
| RU2413528C2 (ru) | 2007-01-18 | 2011-03-10 | Открытое Акционерное Общество "Валента Фармацевтика" | Лекарственный препарат для лечения сахарного диабета на основе экзенатида и даларгина, применение и способ лечения |
| AU2008216265B2 (en) | 2007-02-15 | 2014-04-03 | Indiana University Research And Technology Corporation | Glucagon/GLP-1 receptor co-agonists |
| US8093236B2 (en) | 2007-03-13 | 2012-01-10 | Takeda Pharmaceuticals Company Limited | Weekly administration of dipeptidyl peptidase inhibitors |
| EP1972349A1 (en) * | 2007-03-21 | 2008-09-24 | Biocompatibles UK Limited | GLP-1 fusion peptides conjugated to polymer(s), their production and use |
| EP1975176A1 (en) * | 2007-03-27 | 2008-10-01 | Biocompatibles UK Limited | Novel glp-1 fusion peptides, their production and use |
| MX2009011123A (es) | 2007-04-23 | 2009-11-02 | Intarcia Therapeutics Inc | Formulaciones de suspensiones de peptidos insulinotropicos y sus usos. |
| ES2550363T3 (es) * | 2007-09-05 | 2015-11-06 | Novo Nordisk A/S | Derivados truncados de GLP-1 y su uso terapéutico |
| EP2190460B1 (en) * | 2007-09-05 | 2014-12-17 | Novo Nordisk A/S | Peptides derivatized with a-b-c-d- and their therapeutical use |
| EP2679597A1 (en) | 2007-09-05 | 2014-01-01 | Novo Nordisk A/S | Glucagon-like peptide-1 derivatives and their pharmaceutical use |
| GB0717388D0 (en) | 2007-09-07 | 2007-10-17 | Uutech Ltd | Use of GIP for the treatment of disorders associated with dysfunctional synaptic transmission |
| GB0717399D0 (en) | 2007-09-07 | 2007-10-17 | Uutech Ltd | Use of GLP-1 analogues for the treatment of disorders associated with dysfunctional synaptic transmission |
| CA2707861A1 (en) | 2007-10-30 | 2009-05-07 | Indiana University Research And Technology Corporation | Glucagon antagonists |
| JP5771005B2 (ja) | 2007-10-30 | 2015-08-26 | インディアナ ユニバーシティー リサーチ アンド テクノロジー コーポレーションIndiana University Research And Technology Corporation | グルカゴンアンタゴニスト及びglp−1アゴニスト活性を示す化合物 |
| EP2240155B1 (en) | 2008-02-13 | 2012-06-06 | Intarcia Therapeutics, Inc | Devices, formulations, and methods for delivery of multiple beneficial agents |
| US20110245173A1 (en) * | 2008-06-03 | 2011-10-06 | Bachovchin William W | Long-Acting GLP-1 Derivatives, and Methods of Treating Cardiac Dysfunction |
| CN102088989B (zh) | 2008-06-17 | 2014-11-26 | 印第安纳大学研究及科技有限公司 | 在生理pH缓冲液中具有增强的溶解性和稳定性的胰高血糖素类似物 |
| TWI474835B (zh) | 2008-06-17 | 2015-03-01 | Univ Indiana Res & Tech Corp | 用於治療代謝病症及肥胖症之基於gip之混合激動劑 |
| PE20100255A1 (es) | 2008-06-17 | 2010-04-25 | Univ Indiana Res & Tech Corp | Co-agonistas del receptor de glucagon/glp-1 |
| KR101939557B1 (ko) | 2008-10-17 | 2019-01-17 | 사노피-아벤티스 도이칠란트 게엠베하 | 인슐린과 glp-1 효능제의 병용물 |
| JP2012512903A (ja) | 2008-12-19 | 2012-06-07 | インディアナ ユニバーシティー リサーチ アンド テクノロジー コーポレーション | アミド系グルカゴンスーパーファミリーペプチドプロドラッグ |
| WO2010076809A2 (en) * | 2008-12-29 | 2010-07-08 | Panacea Biotec Ltd | Glp-1 analogs and uses thereof |
| US8642544B2 (en) | 2009-04-01 | 2014-02-04 | Amylin Pharmaceuticals, Llc | N-terminus conformationally constrained GLP-1 receptor agonist compounds |
| WO2010118034A2 (en) * | 2009-04-06 | 2010-10-14 | Board Of Regents, The University Of Texas System | Cyclic peptide analogues for non-invasive imaging of pancreatic beta-cells |
| AU2010260058B2 (en) | 2009-06-16 | 2015-09-24 | Indiana University Research And Technology Corporation | GIP receptor-active glucagon compounds |
| US20120148586A1 (en) * | 2009-08-27 | 2012-06-14 | Joyce Ching Tsu Chou | Glucagon-like protein-1 receptor (glp-1r) agonists for treating autoimmune disorders |
| NZ598686A (en) | 2009-09-28 | 2014-05-30 | Intarcia Therapeutics Inc | Rapid establishment and/or termination of substantial steady-state drug delivery |
| RU2537239C2 (ru) | 2009-11-13 | 2014-12-27 | Санофи-Авентис Дойчланд Гмбх | Фармацевтическая композиция, включающая агонист glp-1, инсулин и метионин |
| AU2010317994B2 (en) | 2009-11-13 | 2014-03-06 | Sanofi-Aventis Deutschland Gmbh | Pharmaceutical composition comprising a GLP-1 agonist and methionine |
| US8703701B2 (en) | 2009-12-18 | 2014-04-22 | Indiana University Research And Technology Corporation | Glucagon/GLP-1 receptor co-agonists |
| CA2788304A1 (en) | 2010-01-27 | 2011-08-04 | Indiana University Research And Technology Corporation | Glucagon antagonist - gip agonist conjugates and compositions for the treatment of metabolic disorders and obesity |
| KR20130062931A (ko) | 2010-05-13 | 2013-06-13 | 인디애나 유니버시티 리서치 앤드 테크놀로지 코퍼레이션 | 핵 호르몬 수용체 활성을 나타내는 글루카곤 슈퍼패밀리 펩티드 |
| WO2011143208A1 (en) | 2010-05-13 | 2011-11-17 | Indiana University Research And Technology Corporation | Glucagon superfamily peptides exhibiting g protein-coupled receptor activity |
| RU2580317C2 (ru) | 2010-06-24 | 2016-04-10 | Индиана Юниверсити Рисерч Энд Текнолоджи Корпорейшн | Пептидные пролекарства, принадлежащие к суперсемейству амид-содержащих глюкагонов |
| CN103179978A (zh) | 2010-08-30 | 2013-06-26 | 赛诺菲-安万特德国有限公司 | Ave0010用于制造供治疗2型糖尿病用的药物的用途 |
| US9023986B2 (en) | 2010-10-25 | 2015-05-05 | Hoffmann-La Roche Inc. | Glucose-dependent insulinotropic peptide analogs |
| DK3326620T3 (da) | 2010-12-16 | 2020-05-25 | Novo Nordisk As | Faste sammensætninger omfattende en glp-1-agonist og et salt af n-(8-(2- hydroxybenzoyl)amino)caprylsyre |
| EA201390941A1 (ru) | 2010-12-22 | 2013-12-30 | Индиана Юниверсити Рисерч Энд Текнолоджи Корпорейшн | Аналоги глюкагона, проявляющие активность на рецепторе gip |
| US9050347B2 (en) | 2011-01-25 | 2015-06-09 | Viviabiotech, S.L. | 1,2,4-oxadiazole derivatives as drugs modulating the GLP-1 peptide receptor |
| US20120208755A1 (en) | 2011-02-16 | 2012-08-16 | Intarcia Therapeutics, Inc. | Compositions, Devices and Methods of Use Thereof for the Treatment of Cancers |
| MX355361B (es) | 2011-04-12 | 2018-04-17 | Novo Nordisk As | Derivados de peptido 1 tipo glucagon (glp-1) doblemente acilados. |
| WO2012145523A2 (en) | 2011-04-20 | 2012-10-26 | The United States Of America, As Represented By The Secretary, Department Of Health & Human Services | Aav mediated exendin-4 gene transfer to salivary glands to protect subjects from diabetes or obesity |
| US9821032B2 (en) | 2011-05-13 | 2017-11-21 | Sanofi-Aventis Deutschland Gmbh | Pharmaceutical combination for improving glycemic control as add-on therapy to basal insulin |
| US20140221283A1 (en) | 2011-06-22 | 2014-08-07 | Indiana University Research And Technology Corporation | Glucagon/glp-1 receptor co-agonists |
| US9309301B2 (en) | 2011-06-22 | 2016-04-12 | Indiana University Research And Technology Corporation | Glucagon/GLP-1 receptor co-agonists |
| JP6367115B2 (ja) | 2011-08-29 | 2018-08-01 | サノフィ−アベンティス・ドイチュラント・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツング | 2型糖尿病患者の血糖コントロールに使用する組合せ医薬 |
| AR087744A1 (es) | 2011-09-01 | 2014-04-16 | Sanofi Aventis Deutschland | Composicion farmaceutica para uso en el tratamiento de una enfermedad neurodegenerativa |
| CA2847246A1 (en) | 2011-11-17 | 2013-05-23 | Indiana University Research And Technology Corporation | Glucagon superfamily peptides exhibiting glucocorticoid receptor activity |
| US9388212B2 (en) | 2013-02-21 | 2016-07-12 | Chemical & Biopharmaceutical Laboratories Of Patras S.A. | Solid phase peptide synthesis via side chain attachment |
| AU2013234496B2 (en) | 2012-03-22 | 2017-07-27 | Novo Nordisk A/S | Compositions of GLP-1 peptides and preparation thereof |
| HUE042757T2 (hu) | 2012-03-22 | 2019-07-29 | Novo Nordisk As | Szállító szert tartalmazó készítmények és elõállításuk |
| ES2871328T3 (es) | 2012-06-20 | 2021-10-28 | Novo Nordisk As | Formulación de comprimido que comprende un péptido y un agente de suministro |
| ES2602486T3 (es) | 2012-06-21 | 2017-02-21 | Indiana University Research And Technology Corporation | Análogos de glucagón que muestran actividad de receptor de GIP |
| UA116217C2 (uk) | 2012-10-09 | 2018-02-26 | Санофі | Пептидна сполука як подвійний агоніст рецепторів glp1-1 та глюкагону |
| WO2014088631A1 (en) * | 2012-12-06 | 2014-06-12 | Stealth Peptides International, Inc. | Peptide therapeutics and methods for using same |
| JP2016503046A (ja) * | 2012-12-19 | 2016-02-01 | ノヴォ ノルディスク アー/エス | コレステロール流出活性を有する新規glp−1受容体アゴニスト |
| AU2013366691A1 (en) | 2012-12-21 | 2015-07-09 | Sanofi | Exendin-4 derivatives |
| JP6382488B2 (ja) * | 2013-02-21 | 2018-08-29 | ケミカル アンド バイオファーマシューティカル ラボラトリーズ オブ パトラ エス.エー. | 側鎖結合を介する固相ペプチド合成 |
| WO2015070050A1 (en) | 2013-11-08 | 2015-05-14 | Baylor Research Institute | Nuclear loclization of glp-1 stimulates myocardial regeneration and reverses heart failure |
| WO2015081891A1 (en) | 2013-12-06 | 2015-06-11 | Baikang (Suzhou) Co., Ltd | Bioreversable promoieties for nitrogen-containing and hydroxyl-containing drugs |
| TW201609797A (zh) | 2013-12-13 | 2016-03-16 | 賽諾菲公司 | 雙重glp-1/升糖素受體促效劑 |
| TW201609796A (zh) | 2013-12-13 | 2016-03-16 | 賽諾菲公司 | 非醯化之艾塞那肽-4(exendin-4)胜肽類似物 |
| EP3080150B1 (en) | 2013-12-13 | 2018-08-01 | Sanofi | Exendin-4 peptide analogues as dual glp-1/gip receptor agonists |
| TW201609799A (zh) | 2013-12-13 | 2016-03-16 | 賽諾菲公司 | 雙重glp-1/gip受體促效劑 |
| TW201625668A (zh) | 2014-04-07 | 2016-07-16 | 賽諾菲公司 | 作為胜肽性雙重glp-1/昇糖素受體激動劑之艾塞那肽-4衍生物 |
| TW201625670A (zh) | 2014-04-07 | 2016-07-16 | 賽諾菲公司 | 衍生自exendin-4之雙重glp-1/升糖素受體促效劑 |
| TW201625669A (zh) | 2014-04-07 | 2016-07-16 | 賽諾菲公司 | 衍生自艾塞那肽-4(Exendin-4)之肽類雙重GLP-1/升糖素受體促效劑 |
| US9932381B2 (en) | 2014-06-18 | 2018-04-03 | Sanofi | Exendin-4 derivatives as selective glucagon receptor agonists |
| GB201415598D0 (en) * | 2014-09-03 | 2014-10-15 | Univ Birmingham | Elavated Itercranial Pressure Treatment |
| US9889085B1 (en) | 2014-09-30 | 2018-02-13 | Intarcia Therapeutics, Inc. | Therapeutic methods for the treatment of diabetes and related conditions for patients with high baseline HbA1c |
| NZ733670A (en) | 2014-12-12 | 2021-12-24 | Sanofi Aventis Deutschland | Insulin glargine/lixisenatide fixed ratio formulation |
| US11135271B2 (en) | 2014-12-30 | 2021-10-05 | Hanmi Pharm. Co., Ltd. | Glucagon derivatives with improved stability |
| TWI748945B (zh) | 2015-03-13 | 2021-12-11 | 德商賽諾菲阿凡提斯德意志有限公司 | 第2型糖尿病病患治療 |
| TW201705975A (zh) | 2015-03-18 | 2017-02-16 | 賽諾菲阿凡提斯德意志有限公司 | 第2型糖尿病病患之治療 |
| US10993993B2 (en) | 2015-05-28 | 2021-05-04 | Immunoforge Co., Ltd. | Pharmaceutical composition for treating muscle atrophy or sarcopenia including glucagon-like peptide (GLP-1) or GLP-1 receptor agonist |
| KR101661332B1 (ko) * | 2015-05-28 | 2016-09-29 | (의료)길의료재단 | 글루카곤 유사 펩타이드-1 수용체 항진제를 포함하는 근감소증 치료용 약학 조성물 |
| AU2016270984B2 (en) | 2015-06-03 | 2021-02-25 | Intarcia Therapeutics, Inc. | Implant placement and removal systems |
| AR105319A1 (es) | 2015-06-05 | 2017-09-27 | Sanofi Sa | Profármacos que comprenden un conjugado agonista dual de glp-1 / glucagón conector ácido hialurónico |
| MA49545B1 (fr) | 2015-06-30 | 2022-03-31 | Hanmi Pharm Ind Co Ltd | Dérivé de glucagon et composition comprenant un conjugué à action prolongée de celui-ci |
| TW201706291A (zh) | 2015-07-10 | 2017-02-16 | 賽諾菲公司 | 作為選擇性肽雙重glp-1/升糖素受體促效劑之新毒蜥外泌肽(exendin-4)衍生物 |
| CN116063454A (zh) * | 2015-12-31 | 2023-05-05 | 韩美药品株式会社 | 胰高血糖素/glp-1/gip受体三重激动剂 |
| CN109310743A (zh) | 2016-05-16 | 2019-02-05 | 因塔西亚制药公司 | 胰高血糖素受体选择性多肽及其使用方法 |
| USD840030S1 (en) | 2016-06-02 | 2019-02-05 | Intarcia Therapeutics, Inc. | Implant placement guide |
| USD860451S1 (en) | 2016-06-02 | 2019-09-17 | Intarcia Therapeutics, Inc. | Implant removal tool |
| UA126662C2 (uk) | 2016-06-29 | 2023-01-11 | Ханмі Фарм. Ко., Лтд. | Похідна глюкагону, її кон'югат, композиція, яка її містить, та її терапевтичне застосування |
| CA3040906A1 (en) | 2016-10-20 | 2018-04-26 | Peptron, Inc. | Methods of delivering a neuroprotective polypeptide to the central nervous system |
| EP3565580B1 (en) | 2017-01-03 | 2024-03-06 | i2o Therapeutics, Inc. | Continuous administration of exenatide and co-adminstration of acetaminophen, ethinylestradiol or levonorgestrel |
| IL275778B2 (en) | 2018-02-02 | 2023-12-01 | Novo Nordisk As | Solid compounds that make up glp-1 agonist n-8-2-hydroxybenzoyl salt |
| CN110452952B (zh) * | 2018-05-08 | 2024-01-16 | 宜昌东阳光长江药业股份有限公司 | 一种glp-1类似物生物活性的检测方法 |
| KR101921085B1 (ko) | 2018-05-21 | 2018-11-22 | 이뮤노포지 주식회사 | 글루카곤 유사 펩타이드-1(glp-1), glp-1 유래 펩타이드, 또는 glp-1 분해 억제제를 포함하는 근감소증 또는 근위축증 치료용 약학 조성물 |
| KR102119188B1 (ko) * | 2018-11-13 | 2020-06-08 | 이뮤노포지 주식회사 | 글루카곤 유사 펩타이드-1(glp-1), glp-1 유래 펩타이드, 또는 glp-1 분해 억제제를 포함하는 근감소증 또는 근위축증 치료용 약학 조성물 |
| WO2020214012A1 (ko) * | 2019-04-19 | 2020-10-22 | 한미약품 주식회사 | 글루카곤, glp-1 및 gip 수용체 모두에 활성을 갖는 삼중 활성체 또는 이의 결합체를 포함하는 고지혈증 예방 또는 치료용 약학적 조성물 및 예방 또는 치료 방법 |
| WO2020214013A1 (ko) * | 2019-04-19 | 2020-10-22 | 한미약품 주식회사 | 글루카곤, glp-1 및 gip 수용체 모두에 활성을 갖는 삼중 활성체 또는 이의 결합체의 고지혈증에 대한 치료적 용도 |
| AU2020331939A1 (en) | 2019-08-16 | 2022-03-24 | Applied Molecular Transport Inc. | Compositions, formulations, and interleukin production and purification |
| CA3164565A1 (en) * | 2020-01-13 | 2021-07-22 | Seon Myeong Lee | Therapeutic use of long-acting conjugate of triple agonist having activities to all of glucagon/glp-1/gip receptors for lung disease |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013139477A (ja) | 2005-09-28 | 2013-07-18 | Ventria Bioscience | 経口投与される剤 |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3710795A (en) | 1970-09-29 | 1973-01-16 | Alza Corp | Drug-delivery device with stretched, rate-controlling membrane |
| US5424286A (en) * | 1993-05-24 | 1995-06-13 | Eng; John | Exendin-3 and exendin-4 polypeptides, and pharmaceutical compositions comprising same |
| CA2137206A1 (en) * | 1993-12-09 | 1995-06-10 | John A. Galloway | Glucagon-like insulinotropic peptides, compositions and methods |
| GB9409496D0 (en) | 1994-05-12 | 1994-06-29 | London Health Ass | Method for improving glycaemic control in diabetes |
| US5574008A (en) * | 1994-08-30 | 1996-11-12 | Eli Lilly And Company | Biologically active fragments of glucagon-like insulinotropic peptide |
| ATE316100T1 (de) * | 1996-06-05 | 2006-02-15 | Roche Diagnostics Gmbh | Exendin-analoga, verfahren zu deren herstellung und diese enthaltende arzneimittel |
| ES2425559T5 (es) * | 1997-01-07 | 2018-02-02 | Amylin Pharmaceuticals, Llc | Composiciones farmacéuticas que comprenden las exendinas y los agonistas de las mismas |
| US6268479B1 (en) * | 1997-03-12 | 2001-07-31 | The Trustees Of Columbia University In The City Of New York | Intracellular amyloid-beta peptide binding (ERAB) polypeptide |
| WO1999038501A2 (en) * | 1998-02-02 | 1999-08-05 | Trustees Of Tufts College | Method of regulating glucose metabolism, and reagents related thereto |
| ATE366115T1 (de) | 1998-02-13 | 2007-07-15 | Amylin Pharmaceuticals Inc | Inotropische und diuretische effekte von exendin und glp-1 |
| EP1056774A1 (en) | 1998-02-27 | 2000-12-06 | Novo Nordisk A/S | N-terminally truncated glp-1 derivatives |
| JP4394279B2 (ja) | 1998-03-09 | 2010-01-06 | ジーランド ファーマ アクティーゼルスカブ | 酵素加水分解に対する傾向が減少した薬理学的に活性なペプチド複合体 |
| DE19828113A1 (de) | 1998-06-24 | 2000-01-05 | Probiodrug Ges Fuer Arzneim | Prodrugs von Inhibitoren der Dipeptidyl Peptidase IV |
| CA2339326A1 (en) | 1998-08-10 | 2000-02-24 | Josephine Egan | Differentiation of non-insulin producing cells into insulin producing cells by glp-1 or exendin-4 and uses thereof |
| MY155270A (en) * | 1998-09-24 | 2015-09-30 | Lilly Co Eli | Use of glp-1 or analogs in treatment of stroke |
| US6429197B1 (en) * | 1998-10-08 | 2002-08-06 | Bionebraska, Inc. | Metabolic intervention with GLP-1 or its biologically active analogues to improve the function of the ischemic and reperfused brain |
| KR100458748B1 (ko) * | 1998-12-07 | 2004-12-03 | 더 어드미니스트레이터즈 오브 더 튜래인 어듀케이셔널 훤드 | Glp-1 유사체 |
| EP2322545A1 (en) * | 1998-12-07 | 2011-05-18 | Ipsen Pharma | Analogues of GLP-1 |
| JP3136356B2 (ja) | 1998-12-15 | 2001-02-19 | 農林水産省家畜衛生試験場長 | 改変型シグナルペプチドをコードするdna |
| CA2356706C (en) * | 1999-01-14 | 2014-09-30 | Amylin Pharmaceuticals, Inc. | Novel exendin agonist formulations and methods of administration thereof |
| DK1189629T3 (da) | 1999-02-10 | 2011-01-03 | Curis Inc | Peptid YY (PYY) til behandling af glucosestofskiftesygdomme |
| SI1180121T1 (en) * | 1999-05-17 | 2004-04-30 | Conjuchem, Inc. | Long lasting insulinotropic peptides |
| US6506724B1 (en) * | 1999-06-01 | 2003-01-14 | Amylin Pharmaceuticals, Inc. | Use of exendins and agonists thereof for the treatment of gestational diabetes mellitus |
| EP1076066A1 (en) * | 1999-07-12 | 2001-02-14 | Zealand Pharmaceuticals A/S | Peptides for lowering blood glucose levels |
| WO2001034200A1 (fr) * | 1999-11-10 | 2001-05-17 | Takeda Chemical Industries, Ltd | Inhibiteurs de prise de poids |
| US6278018B1 (en) | 1999-12-14 | 2001-08-21 | Surmodics, Inc. | Surface coating agents |
| US20030036504A1 (en) | 2000-01-10 | 2003-02-20 | Amylin Pharmaceuticals, Inc. | Use of exendins and agonists thereof for modulation of triglyceride levels and treatment of dyslipidemia |
| AU2001232337A1 (en) * | 2000-02-18 | 2001-08-27 | Kanagawa Academy Of Science And Technology | Pharmaceutical composition, reagent and method for intracerebral delivery of pharmaceutically active ingredient or labeling substance |
| EP1136071A3 (en) * | 2000-03-22 | 2003-03-26 | Pfizer Products Inc. | Use of glycogen phosphorylase inhibitors |
| EP1313767A2 (en) * | 2000-08-24 | 2003-05-28 | Thomas Jefferson University | Peptide with effects on cerebral health |
| CA2434237C (en) * | 2000-12-07 | 2012-05-15 | Eli Lilly And Company | Glp-1 fusion proteins |
| EP2022505B1 (en) | 2001-07-31 | 2011-12-14 | The Government of the United States of America, as represented by the Secretary of the Department of Health and Human Services | GLP-1, exendin-4, peptide analogs and uses thereof |
| ES2343061T3 (es) * | 2002-05-24 | 2010-07-22 | Medtronic, Inc. | Metodos y constructos de dna para produccion de polipeptidos con rendimiento alto. |
| US6969702B2 (en) * | 2002-11-20 | 2005-11-29 | Neuronova Ab | Compounds and methods for increasing neurogenesis |
| DOP2006000008A (es) * | 2005-01-10 | 2006-08-31 | Arena Pharm Inc | Terapia combinada para el tratamiento de la diabetes y afecciones relacionadas y para el tratamiento de afecciones que mejoran mediante un incremento de la concentración sanguínea de glp-1 |
| JP2013007734A (ja) | 2011-01-17 | 2013-01-10 | Nippon Dempa Kogyo Co Ltd | 外力検出装置及び外力検出センサー |
-
2002
- 2002-07-30 EP EP08162544A patent/EP2022505B1/en not_active Expired - Lifetime
- 2002-07-30 AT AT08162544T patent/ATE536881T1/de active
- 2002-07-30 DE DE60228972T patent/DE60228972D1/de not_active Expired - Lifetime
- 2002-07-30 CA CA2455963A patent/CA2455963C/en not_active Expired - Lifetime
- 2002-07-30 AT AT02748271T patent/ATE408414T1/de not_active IP Right Cessation
- 2002-07-30 AU AU2002317599A patent/AU2002317599B2/en not_active Expired
- 2002-07-30 EP EP10177860.3A patent/EP2275117B1/en not_active Expired - Lifetime
- 2002-07-30 US US10/485,140 patent/US7576050B2/en active Active
- 2002-07-30 JP JP2003517083A patent/JP2005501058A/ja not_active Revoked
- 2002-07-30 WO PCT/US2002/024141 patent/WO2003011892A2/en active Application Filing
- 2002-07-30 EP EP02748271A patent/EP1411968B1/en not_active Expired - Lifetime
-
2008
- 2008-07-01 AU AU2008202893A patent/AU2008202893B2/en not_active Expired
- 2008-12-18 US US12/317,042 patent/US8278272B2/en not_active Expired - Lifetime
-
2009
- 2009-11-18 JP JP2009262568A patent/JP5631578B2/ja not_active Expired - Lifetime
-
2012
- 2012-08-24 US US13/594,313 patent/US8853160B2/en not_active Expired - Lifetime
-
2013
- 2013-01-18 JP JP2013007734A patent/JP5695097B2/ja not_active Expired - Lifetime
-
2014
- 2014-08-27 US US14/470,528 patent/US10941187B2/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013139477A (ja) | 2005-09-28 | 2013-07-18 | Ventria Bioscience | 経口投与される剤 |
Non-Patent Citations (4)
| Title |
|---|
| JPN4007010041; Jpn. J. Pharmacol. Vol. 85, No. Supplement 1, 20010301, p. 276P * |
| JPN4007010042; 第22回日本神経科学大会プログラム抄録集 , 1999, p. 146 * |
| JPN4007010043; Brain Research Vol. 878, 2000, p. 194-198 * |
| JPN6013015849; The Journal of Biological Chemistry 272, 34, 1997, p.21201-21206 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20180096733A (ko) * | 2015-12-23 | 2018-08-29 | 더 존스 홉킨스 유니버시티 | 신경계 및 신경변성 상태의 요법으로서 장기간 작용하는 glf-1r 작용제 |
| JP7026044B2 (ja) | 2015-12-23 | 2022-02-25 | ザ・ジョンズ・ホプキンス・ユニバーシティー | 神経性状態および神経変性状態の治療としての長時間作用型GLP-1rアゴニスト |
| KR102508651B1 (ko) | 2015-12-23 | 2023-03-13 | 더 존스 홉킨스 유니버시티 | 신경계 및 신경변성 상태의 요법으로서 장기간 작용하는 glf-1r 작용제 |
| WO2020175570A1 (ja) * | 2019-02-28 | 2020-09-03 | 新田ゼラチン株式会社 | 脳機能調整剤、およびこれを含む飲食品 |
Also Published As
| Publication number | Publication date |
|---|---|
| US8853160B2 (en) | 2014-10-07 |
| EP2275117B1 (en) | 2016-10-26 |
| ATE408414T1 (de) | 2008-10-15 |
| EP1411968B1 (en) | 2008-09-17 |
| US8278272B2 (en) | 2012-10-02 |
| EP2022505A2 (en) | 2009-02-11 |
| ATE536881T1 (de) | 2011-12-15 |
| JP5695097B2 (ja) | 2015-04-01 |
| EP2022505A3 (en) | 2009-05-27 |
| EP1411968A4 (en) | 2005-06-15 |
| JP2013139447A (ja) | 2013-07-18 |
| CA2455963A1 (en) | 2003-02-13 |
| WO2003011892A2 (en) | 2003-02-13 |
| EP1411968A2 (en) | 2004-04-28 |
| JP2005501058A (ja) | 2005-01-13 |
| US20090253625A1 (en) | 2009-10-08 |
| EP2275117A1 (en) | 2011-01-19 |
| US20150072930A1 (en) | 2015-03-12 |
| US7576050B2 (en) | 2009-08-18 |
| US10941187B2 (en) | 2021-03-09 |
| AU2008202893B2 (en) | 2012-01-12 |
| JP5631578B2 (ja) | 2014-11-26 |
| DE60228972D1 (de) | 2008-10-30 |
| AU2008202893A1 (en) | 2008-07-24 |
| US20120329715A1 (en) | 2012-12-27 |
| AU2002317599B2 (en) | 2008-04-03 |
| US20040242853A1 (en) | 2004-12-02 |
| WO2003011892A3 (en) | 2004-02-26 |
| EP2022505B1 (en) | 2011-12-14 |
| CA2455963C (en) | 2017-07-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5631578B2 (ja) | Glp−1、exendin−4、そのペプチド・アナログ及びその使用 | |
| AU2002317599A1 (en) | GLP-1 exendin-4 peptide analogs and uses thereof | |
| EP1988100B1 (en) | Derivatives of glucagon-like peptide-2 and their therapeutic use | |
| US5424286A (en) | Exendin-3 and exendin-4 polypeptides, and pharmaceutical compositions comprising same | |
| US7049284B2 (en) | Glucagon-like peptide-2 and its therapeutic use | |
| EP1932535A2 (en) | Stimulation of beta cell profileration | |
| JP2002522068A (ja) | GLP−1またはExendin−4による、非インスリン産生細胞のインスリン産生細胞への分化、およびその使用 | |
| AU2014277804B2 (en) | Glp-1 exendin-4 peptide analogs and uses thereof | |
| AU2012202081B2 (en) | GLP-1 Exendin-4 peptide analogs and uses thereof | |
| CN112759640B (zh) | 一类glp-1/胃泌素受体双重激动剂及其应用 | |
| Class et al. | Patent application title: GLP-1, EXENDIN-4, PEPTIDE ANALOGS AND USES THEREOF Inventors: Nigel H. Greig (Phoenix, MD, US) Nigel H. Greig (Phoenix, MD, US) Josephine M. Egan (Baltimore, MD, US) Maire Doyle (Baltimore, MD, US) Harold W. Holloway (Middle River, MD, US) Tracy Perry (Baltimore, MD, US) | |
| Greig et al. | GLP-1 exendin-4 peptide analogs and uses thereof | |
| WO2008062420A2 (en) | Use of glucagon and insulin in methods and compositions for the treatment of acute brain injury and neurodegenerative disorders |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100106 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20120309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120529 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120918 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130118 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130318 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20130405 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20141008 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5631578 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |