DE60009155T2 - Substituierte phenyl-piperazin-derivate, deren herstellung und verwendung - Google Patents
Substituierte phenyl-piperazin-derivate, deren herstellung und verwendung Download PDFInfo
- Publication number
- DE60009155T2 DE60009155T2 DE60009155T DE60009155T DE60009155T2 DE 60009155 T2 DE60009155 T2 DE 60009155T2 DE 60009155 T DE60009155 T DE 60009155T DE 60009155 T DE60009155 T DE 60009155T DE 60009155 T2 DE60009155 T2 DE 60009155T2
- Authority
- DE
- Germany
- Prior art keywords
- piperazine
- indol
- phenyl
- propyl
- methoxyphenoxy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000002360 preparation method Methods 0.000 title claims description 3
- YZTJYBJCZXZGCT-UHFFFAOYSA-N phenylpiperazine Chemical class C1CNCCN1C1=CC=CC=C1 YZTJYBJCZXZGCT-UHFFFAOYSA-N 0.000 title description 4
- 150000001875 compounds Chemical class 0.000 claims description 57
- -1 1-homopiperidinyl Chemical group 0.000 claims description 42
- 229910052739 hydrogen Inorganic materials 0.000 claims description 27
- 239000001257 hydrogen Substances 0.000 claims description 25
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 claims description 23
- 125000000217 alkyl group Chemical group 0.000 claims description 21
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 19
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 15
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 11
- 150000002431 hydrogen Chemical class 0.000 claims description 10
- 239000002253 acid Substances 0.000 claims description 9
- 229910052736 halogen Inorganic materials 0.000 claims description 9
- 150000002367 halogens Chemical class 0.000 claims description 9
- 150000003839 salts Chemical class 0.000 claims description 9
- 125000003118 aryl group Chemical group 0.000 claims description 8
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 claims description 7
- JCXYIZHUALZKGZ-UHFFFAOYSA-N 3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-fluoro-1h-indole Chemical compound O1CCOC2=C1C=CC=C2OC1=CC=CC=C1N(CC1)CCN1CCCC1=CNC2=CC=C(F)C=C21 JCXYIZHUALZKGZ-UHFFFAOYSA-N 0.000 claims description 6
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 claims description 6
- QHIPGMYRQRWNRR-UHFFFAOYSA-N 4-[3-[2-[4-[3-(5-fluoro-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]phenyl]morpholine Chemical compound C12=CC(F)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC(C=1)=CC=CC=1N1CCOCC1 QHIPGMYRQRWNRR-UHFFFAOYSA-N 0.000 claims description 5
- YULASTKKEXFGFD-UHFFFAOYSA-N 5-fluoro-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(F)=CC=C3NC=2)CC1 YULASTKKEXFGFD-UHFFFAOYSA-N 0.000 claims description 5
- 208000024827 Alzheimer disease Diseases 0.000 claims description 5
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 5
- 208000028017 Psychotic disease Diseases 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 208000019906 panic disease Diseases 0.000 claims description 5
- OWEYIAFRYKPGTI-UHFFFAOYSA-N 3-[2-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]ethyl]-6-chloro-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCC=2C3=CC=C(C=C3NC=2)Cl)=C1 OWEYIAFRYKPGTI-UHFFFAOYSA-N 0.000 claims description 4
- JJWGGTBCCAPKEC-UHFFFAOYSA-N 3-[2-[4-[2-(6-chloro-1h-indol-3-yl)ethyl]piperazin-1-yl]phenoxy]-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCC=3C4=CC=C(Cl)C=C4NC=3)CC2)=C1 JJWGGTBCCAPKEC-UHFFFAOYSA-N 0.000 claims description 4
- XHYDHLYHMNFUCR-UHFFFAOYSA-N 3-[2-[4-[3-(5-fluoro-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(F)=CC=C4NC=3)CC2)=C1 XHYDHLYHMNFUCR-UHFFFAOYSA-N 0.000 claims description 4
- NBNANZDPAUVZCM-UHFFFAOYSA-N 3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C=1NC2=CC=CC=C2C=1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 NBNANZDPAUVZCM-UHFFFAOYSA-N 0.000 claims description 4
- IWCRVEQTMBSESW-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-1h-pyrrolo[3,2-h]quinoline Chemical compound C1=CC2=CC=CN=C2C2=C1C(CCCN1CCN(CC1)C=1C(=CC=CC=1)OC=1C=C3OCOC3=CC=1)=CN2 IWCRVEQTMBSESW-UHFFFAOYSA-N 0.000 claims description 4
- SJNOCZFKZOJIQV-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-bromo-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC2=CNC3=CC=C(C=C32)Br)=C1 SJNOCZFKZOJIQV-UHFFFAOYSA-N 0.000 claims description 4
- VDUCKTWNZRHCIM-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-methyl-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC2=CNC3=CC=C(C=C32)C)=C1 VDUCKTWNZRHCIM-UHFFFAOYSA-N 0.000 claims description 4
- OSBODECQQSOMJP-UHFFFAOYSA-N 3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-5-yloxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound C1=CC=C2C(CCCN3CCN(CC3)C=3C(=CC=CC=3)OC=3C=4OCCOC=4C=CC=3)=CNC2=C1 OSBODECQQSOMJP-UHFFFAOYSA-N 0.000 claims description 4
- YWFVVSIGTZAXMZ-UHFFFAOYSA-N 3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-methyl-1h-indole Chemical compound O1CCOC2=C1C=CC=C2OC1=CC=CC=C1N(CC1)CCN1CCCC1=CNC2=CC=C(C)C=C21 YWFVVSIGTZAXMZ-UHFFFAOYSA-N 0.000 claims description 4
- HRVYGCMPBMUWFJ-UHFFFAOYSA-N 3-[3-[4-[2-(2,6-dimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-5-fluoro-1h-indole Chemical compound COC1=CC=CC(OC)=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(F)=CC=C3NC=2)CC1 HRVYGCMPBMUWFJ-UHFFFAOYSA-N 0.000 claims description 4
- HCGIKUSNRRBOND-UHFFFAOYSA-N 3-[3-[4-[2-(2,6-dimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-5-iodo-1h-indole Chemical compound COC1=CC=CC(OC)=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(I)=CC=C3NC=2)CC1 HCGIKUSNRRBOND-UHFFFAOYSA-N 0.000 claims description 4
- VHWXQDZLKFTBDL-UHFFFAOYSA-N 3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC=CC=C3NC=2)CC1 VHWXQDZLKFTBDL-UHFFFAOYSA-N 0.000 claims description 4
- MYFLIGNTKZLKLG-UHFFFAOYSA-N 3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-pyrrolo[3,2-h]quinoline Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=C(C4=NC=CC=C4C=C3)NC=2)CC1 MYFLIGNTKZLKLG-UHFFFAOYSA-N 0.000 claims description 4
- FEMNAJICUFEEAB-UHFFFAOYSA-N 3-[3-[4-[2-(3-ethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-5-methyl-1h-indole Chemical compound CCOC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(C)=CC=C4NC=3)CC2)=C1 FEMNAJICUFEEAB-UHFFFAOYSA-N 0.000 claims description 4
- MYUVRBSMTUTXRR-UHFFFAOYSA-N 3-[3-[4-[2-(3-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC=CC=C4NC=3)CC2)=C1 MYUVRBSMTUTXRR-UHFFFAOYSA-N 0.000 claims description 4
- FVIHVLPVKPYXBS-UHFFFAOYSA-N 3-[3-[4-[2-(4-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound C1=CC(OC)=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC=CC=C3NC=2)CC1 FVIHVLPVKPYXBS-UHFFFAOYSA-N 0.000 claims description 4
- QEZZAYHWJOLDBB-UHFFFAOYSA-N 3-[4-[4-(2-phenoxyphenyl)piperazin-1-yl]butyl]-1h-indole Chemical compound C=1NC2=CC=CC=C2C=1CCCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 QEZZAYHWJOLDBB-UHFFFAOYSA-N 0.000 claims description 4
- AWVHHHMYGYTECD-UHFFFAOYSA-N 3-[4-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]butyl]-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCCC=2C3=CC=CC=C3NC=2)=C1 AWVHHHMYGYTECD-UHFFFAOYSA-N 0.000 claims description 4
- IAAPLRAZMTUWGR-UHFFFAOYSA-N 4-[3-[2-[4-[3-(5-iodo-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]phenyl]morpholine Chemical compound C12=CC(I)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC(C=1)=CC=CC=1N1CCOCC1 IAAPLRAZMTUWGR-UHFFFAOYSA-N 0.000 claims description 4
- SPZHZXUYAUSLEZ-UHFFFAOYSA-N 5,7-difluoro-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(F)=CC(F)=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 SPZHZXUYAUSLEZ-UHFFFAOYSA-N 0.000 claims description 4
- CSMJLNZSFBNWGG-UHFFFAOYSA-N 5,7-dimethyl-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(C)=CC(C)=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 CSMJLNZSFBNWGG-UHFFFAOYSA-N 0.000 claims description 4
- ITUPHCUEMUPHHZ-UHFFFAOYSA-N 5-bromo-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(Br)=CC=C3NC=2)CC1 ITUPHCUEMUPHHZ-UHFFFAOYSA-N 0.000 claims description 4
- YNNHQUNIYAHJNE-UHFFFAOYSA-N 5-bromo-3-[3-[4-[2-(3,4,5-trimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=C(OC)C(OC)=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(Br)=CC=C4NC=3)CC2)=C1 YNNHQUNIYAHJNE-UHFFFAOYSA-N 0.000 claims description 4
- VNGSIPURRUXSRM-UHFFFAOYSA-N 5-chloro-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(Cl)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 VNGSIPURRUXSRM-UHFFFAOYSA-N 0.000 claims description 4
- ZQCXOBLVWVJECD-UHFFFAOYSA-N 5-chloro-3-[3-[4-[2-(2,6-dimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC)=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(Cl)=CC=C3NC=2)CC1 ZQCXOBLVWVJECD-UHFFFAOYSA-N 0.000 claims description 4
- BYPGLVLRQYFMDE-UHFFFAOYSA-N 5-chloro-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(Cl)=CC=C3NC=2)CC1 BYPGLVLRQYFMDE-UHFFFAOYSA-N 0.000 claims description 4
- IMMGOHFIDQMRJW-UHFFFAOYSA-N 5-chloro-3-[3-[4-[2-(3-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(Cl)=CC=C4NC=3)CC2)=C1 IMMGOHFIDQMRJW-UHFFFAOYSA-N 0.000 claims description 4
- BAEARRMUMJRQJS-UHFFFAOYSA-N 5-fluoro-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(F)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 BAEARRMUMJRQJS-UHFFFAOYSA-N 0.000 claims description 4
- OINDAPWTNMMZPX-UHFFFAOYSA-N 5-iodo-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(I)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 OINDAPWTNMMZPX-UHFFFAOYSA-N 0.000 claims description 4
- XEZVUHUDOCQKML-UHFFFAOYSA-N 5-iodo-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(I)=CC=C3NC=2)CC1 XEZVUHUDOCQKML-UHFFFAOYSA-N 0.000 claims description 4
- BJNYRUIABYCUEN-UHFFFAOYSA-N 5-methyl-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(C)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 BJNYRUIABYCUEN-UHFFFAOYSA-N 0.000 claims description 4
- ZAGYUVDFLFKSSF-UHFFFAOYSA-N 6-chloro-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC=C(Cl)C=C3NC=2)CC1 ZAGYUVDFLFKSSF-UHFFFAOYSA-N 0.000 claims description 4
- HRIZKEVNKGMQNZ-UHFFFAOYSA-N 6-chloro-3-[3-[4-[2-(3-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC=C(Cl)C=C4NC=3)CC2)=C1 HRIZKEVNKGMQNZ-UHFFFAOYSA-N 0.000 claims description 4
- TWVWLMZPWYEJMU-UHFFFAOYSA-N 7-chloro-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C=1NC=2C(Cl)=CC=CC=2C=1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 TWVWLMZPWYEJMU-UHFFFAOYSA-N 0.000 claims description 4
- 208000019901 Anxiety disease Diseases 0.000 claims description 4
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 4
- 208000021384 Obsessive-Compulsive disease Diseases 0.000 claims description 4
- 206010039966 Senile dementia Diseases 0.000 claims description 4
- 206010041250 Social phobia Diseases 0.000 claims description 4
- 229910052799 carbon Inorganic materials 0.000 claims description 4
- 208000028867 ischemia Diseases 0.000 claims description 4
- GWXJVSCULKGPCF-UHFFFAOYSA-N n,n-diethyl-3-[2-[4-[3-(5-fluoro-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]aniline Chemical compound CCN(CC)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(F)=CC=C4NC=3)CC2)=C1 GWXJVSCULKGPCF-UHFFFAOYSA-N 0.000 claims description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 4
- BCRYPVTXFYJJFK-UHFFFAOYSA-N 3-[2-[4-[4-(1h-indol-3-yl)butyl]piperazin-1-yl]phenoxy]-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCCC=3C4=CC=CC=C4NC=3)CC2)=C1 BCRYPVTXFYJJFK-UHFFFAOYSA-N 0.000 claims description 3
- FSEDYOZYCMHMQU-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-fluoro-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC2=CNC3=CC=C(C=C32)F)=C1 FSEDYOZYCMHMQU-UHFFFAOYSA-N 0.000 claims description 3
- HXXYEEZKEAZAQO-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-iodo-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC2=CNC3=CC=C(C=C32)I)=C1 HXXYEEZKEAZAQO-UHFFFAOYSA-N 0.000 claims description 3
- MZFKVLBXPSVKGQ-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-6-chloro-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC=2C3=CC=C(C=C3NC=2)Cl)=C1 MZFKVLBXPSVKGQ-UHFFFAOYSA-N 0.000 claims description 3
- XFJPTURVHIBMTM-UHFFFAOYSA-N 4-[3-[2-[4-[3-(5-chloro-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]phenyl]morpholine Chemical compound C12=CC(Cl)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC(C=1)=CC=CC=1N1CCOCC1 XFJPTURVHIBMTM-UHFFFAOYSA-N 0.000 claims description 3
- STABULDVAWQBJU-UHFFFAOYSA-N 5,7-difluoro-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(F)=CC(F)=C3NC=2)CC1 STABULDVAWQBJU-UHFFFAOYSA-N 0.000 claims description 3
- XSKSCLXXLRGKGP-UHFFFAOYSA-N 5-bromo-3-[3-[4-(2-phenoxyphenyl)piperazin-1-yl]propyl]-1h-indole Chemical compound C12=CC(Br)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 XSKSCLXXLRGKGP-UHFFFAOYSA-N 0.000 claims description 3
- RBEAPCNJKIRGQK-UHFFFAOYSA-N 5-bromo-3-[3-[4-[2-(2,6-dimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC)=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(Br)=CC=C3NC=2)CC1 RBEAPCNJKIRGQK-UHFFFAOYSA-N 0.000 claims description 3
- UKTVNKZIUFMCFK-UHFFFAOYSA-N 6-chloro-3-[2-[4-(2-phenoxyphenyl)piperazin-1-yl]ethyl]-1h-indole Chemical compound C=1NC2=CC(Cl)=CC=C2C=1CCN(CC1)CCN1C1=CC=CC=C1OC1=CC=CC=C1 UKTVNKZIUFMCFK-UHFFFAOYSA-N 0.000 claims description 3
- SNUOPPWSZMNHHF-UHFFFAOYSA-N 6-chloro-3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-5-yloxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound O1CCOC2=C1C=CC=C2OC1=CC=CC=C1N(CC1)CCN1CCCC1=CNC2=CC(Cl)=CC=C21 SNUOPPWSZMNHHF-UHFFFAOYSA-N 0.000 claims description 3
- LDYDUAZTRIFSCI-UHFFFAOYSA-N 7-chloro-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC=CC(Cl)=C3NC=2)CC1 LDYDUAZTRIFSCI-UHFFFAOYSA-N 0.000 claims description 3
- 208000030814 Eating disease Diseases 0.000 claims description 3
- 208000019454 Feeding and Eating disease Diseases 0.000 claims description 3
- 125000002252 acyl group Chemical group 0.000 claims description 3
- 230000016571 aggressive behavior Effects 0.000 claims description 3
- 235000014632 disordered eating Nutrition 0.000 claims description 3
- 125000001072 heteroaryl group Chemical group 0.000 claims description 3
- DRVVXAZBMOYBLW-UHFFFAOYSA-N n,n-dimethyl-3-[2-[4-[3-(5-methyl-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]aniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC(C)=CC=C4NC=3)CC2)=C1 DRVVXAZBMOYBLW-UHFFFAOYSA-N 0.000 claims description 3
- 239000008194 pharmaceutical composition Substances 0.000 claims description 3
- 125000004076 pyridyl group Chemical group 0.000 claims description 3
- 125000000168 pyrrolyl group Chemical group 0.000 claims description 3
- 125000001424 substituent group Chemical group 0.000 claims description 3
- HNDDEJSHBYUIQF-UHFFFAOYSA-N 3-[1-[4-[2-(1h-indol-3-yl)ethyl]piperazin-1-yl]cyclohexa-2,4-dien-1-yl]oxy-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC2(C=CC=CC2)N2CCN(CCC=3C4=CC=CC=C4NC=3)CC2)=C1 HNDDEJSHBYUIQF-UHFFFAOYSA-N 0.000 claims description 2
- GAWDQCKEXSAHTB-UHFFFAOYSA-N 3-[1-[4-[3-(1h-indol-3-yl)propyl]piperazin-1-yl]cyclohexa-2,4-dien-1-yl]oxy-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC2(C=CC=CC2)N2CCN(CCCC=3C4=CC=CC=C4NC=3)CC2)=C1 GAWDQCKEXSAHTB-UHFFFAOYSA-N 0.000 claims description 2
- LUJPWQVJKPZNSK-UHFFFAOYSA-N 3-[2-[4-[1-(1,3-benzodioxol-5-yloxy)cyclohexa-2,4-dien-1-yl]piperazin-1-yl]ethyl]-1h-indole Chemical compound C=1NC2=CC=CC=C2C=1CCN(CC1)CCN1C1(OC=2C=C3OCOC3=CC=2)CC=CC=C1 LUJPWQVJKPZNSK-UHFFFAOYSA-N 0.000 claims description 2
- XTNQUASOAVCWFR-UHFFFAOYSA-N 3-[3-[4-[1-(1,3-benzodioxol-5-yloxy)cyclohexa-2,4-dien-1-yl]piperazin-1-yl]propyl]-1h-indole Chemical compound C=1NC2=CC=CC=C2C=1CCCN(CC1)CCN1C1(OC=2C=C3OCOC3=CC=2)CC=CC=C1 XTNQUASOAVCWFR-UHFFFAOYSA-N 0.000 claims description 2
- 208000007848 Alcoholism Diseases 0.000 claims description 2
- 206010001584 alcohol abuse Diseases 0.000 claims description 2
- 208000025746 alcohol use disease Diseases 0.000 claims description 2
- 239000003085 diluting agent Substances 0.000 claims description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 2
- 125000005322 morpholin-1-yl group Chemical group 0.000 claims description 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims description 2
- 229910052760 oxygen Inorganic materials 0.000 claims description 2
- 239000000825 pharmaceutical preparation Substances 0.000 claims description 2
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000003226 pyrazolyl group Chemical group 0.000 claims description 2
- 229910052717 sulfur Inorganic materials 0.000 claims description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 claims 2
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims 1
- RDSVSEFWZUWZHW-UHFFFAOYSA-N 7-bromo-1h-indole Chemical compound BrC1=CC=CC2=C1NC=C2 RDSVSEFWZUWZHW-UHFFFAOYSA-N 0.000 claims 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims 1
- 208000035475 disorder Diseases 0.000 claims 1
- 239000003937 drug carrier Substances 0.000 claims 1
- 230000005032 impulse control Effects 0.000 claims 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 75
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 66
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 45
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 40
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 33
- 238000000034 method Methods 0.000 description 33
- 229920005989 resin Polymers 0.000 description 33
- 239000011347 resin Substances 0.000 description 33
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 32
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 28
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 27
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 27
- 108020003175 receptors Proteins 0.000 description 25
- 102000005962 receptors Human genes 0.000 description 25
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 24
- 239000000203 mixture Substances 0.000 description 18
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 16
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 16
- 239000000243 solution Substances 0.000 description 15
- 238000005160 1H NMR spectroscopy Methods 0.000 description 14
- 239000002904 solvent Substances 0.000 description 14
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 229960003638 dopamine Drugs 0.000 description 12
- 239000011541 reaction mixture Substances 0.000 description 11
- 239000005557 antagonist Substances 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 9
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 8
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 8
- 229910000027 potassium carbonate Inorganic materials 0.000 description 8
- 150000003335 secondary amines Chemical class 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 230000000561 anti-psychotic effect Effects 0.000 description 7
- 210000004556 brain Anatomy 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 230000005764 inhibitory process Effects 0.000 description 7
- 230000003287 optical effect Effects 0.000 description 7
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 239000000543 intermediate Substances 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 6
- 208000012902 Nervous system disease Diseases 0.000 description 5
- 208000025966 Neurological disease Diseases 0.000 description 5
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 238000010828 elution Methods 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 239000002464 receptor antagonist Substances 0.000 description 5
- 229940044551 receptor antagonist Drugs 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 4
- 150000001241 acetals Chemical class 0.000 description 4
- 230000027455 binding Effects 0.000 description 4
- 239000012043 crude product Substances 0.000 description 4
- 150000002009 diols Chemical class 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 239000012038 nucleophile Substances 0.000 description 4
- 230000003389 potentiating effect Effects 0.000 description 4
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 238000010898 silica gel chromatography Methods 0.000 description 4
- 238000010561 standard procedure Methods 0.000 description 4
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 4
- XEPRNSDBSCSQII-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-7-bromo-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC=2C=3C=CC=C(C=3NC=2)Br)=C1 XEPRNSDBSCSQII-UHFFFAOYSA-N 0.000 description 3
- HGGGPQXRYFVAIT-UHFFFAOYSA-N 3-[3-[4-[2-(2,6-dimethoxyphenoxy)phenyl]piperazin-1-yl]propyl]-5-methyl-1h-indole Chemical compound COC1=CC=CC(OC)=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC(C)=CC=C3NC=2)CC1 HGGGPQXRYFVAIT-UHFFFAOYSA-N 0.000 description 3
- TVRRHNHAQUPMKC-UHFFFAOYSA-N 3-[3-[4-[2-(3-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-pyrrolo[3,2-h]quinoline Chemical compound COC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=C(C5=NC=CC=C5C=C4)NC=3)CC2)=C1 TVRRHNHAQUPMKC-UHFFFAOYSA-N 0.000 description 3
- DJMWBNWFBCHEOX-UHFFFAOYSA-N 6-chloro-3-[2-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]ethyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCC=2C3=CC=C(Cl)C=C3NC=2)CC1 DJMWBNWFBCHEOX-UHFFFAOYSA-N 0.000 description 3
- CAURJXXIHPFLBP-UHFFFAOYSA-N 6-chloro-3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-6-yloxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound O1CCOC2=CC(OC3=CC=CC=C3N3CCN(CC3)CCCC=3C4=CC=C(C=C4NC=3)Cl)=CC=C21 CAURJXXIHPFLBP-UHFFFAOYSA-N 0.000 description 3
- KIFNFFBTSDIOQZ-UHFFFAOYSA-N 7-bromo-3-[3-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCC=2C3=CC=CC(Br)=C3NC=2)CC1 KIFNFFBTSDIOQZ-UHFFFAOYSA-N 0.000 description 3
- DDYLGNDOBMGFCI-UHFFFAOYSA-N 7-fluoro-3-[3-[4-[2-(3-methoxyphenoxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound COC1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC=CC(F)=C4NC=3)CC2)=C1 DDYLGNDOBMGFCI-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical class OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 208000019022 Mood disease Diseases 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 3
- 239000004793 Polystyrene Substances 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical class CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 150000001408 amides Chemical class 0.000 description 3
- 239000000010 aprotic solvent Substances 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 230000007278 cognition impairment Effects 0.000 description 3
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 3
- 239000007791 liquid phase Substances 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 3
- 229920002223 polystyrene Polymers 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 208000020016 psychiatric disease Diseases 0.000 description 3
- 238000012552 review Methods 0.000 description 3
- 201000000980 schizophrenia Diseases 0.000 description 3
- 230000000697 serotonin reuptake Effects 0.000 description 3
- 239000012312 sodium hydride Substances 0.000 description 3
- 229910000104 sodium hydride Inorganic materials 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 3
- 239000003039 volatile agent Substances 0.000 description 3
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- YMDZDFSUDFLGMX-UHFFFAOYSA-N 2-chloro-n-(2-chloroethyl)ethanamine;hydron;chloride Chemical compound [Cl-].ClCC[NH2+]CCCl YMDZDFSUDFLGMX-UHFFFAOYSA-N 0.000 description 2
- GOLXRNDWAUTYKT-UHFFFAOYSA-N 3-(1H-indol-3-yl)propanoic acid Chemical compound C1=CC=C2C(CCC(=O)O)=CNC2=C1 GOLXRNDWAUTYKT-UHFFFAOYSA-N 0.000 description 2
- LYPSVQXMCZIRGP-UHFFFAOYSA-N 3-(1h-indol-3-yl)propan-1-ol Chemical compound C1=CC=C2C(CCCO)=CNC2=C1 LYPSVQXMCZIRGP-UHFFFAOYSA-N 0.000 description 2
- YUBXEUBNYOBJMQ-UHFFFAOYSA-N 3-(3-bromopropyl)-1h-indole Chemical compound C1=CC=C2C(CCCBr)=CNC2=C1 YUBXEUBNYOBJMQ-UHFFFAOYSA-N 0.000 description 2
- VTKNDBXCWMSEIO-UHFFFAOYSA-N 3-[2-[4-[3-(1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCN(CCCC=3C4=CC=CC=C4NC=3)CC2)=C1 VTKNDBXCWMSEIO-UHFFFAOYSA-N 0.000 description 2
- XKYRGHFKHNICJW-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-5-chloro-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCCC2=CNC3=CC=C(C=C32)Cl)=C1 XKYRGHFKHNICJW-UHFFFAOYSA-N 0.000 description 2
- NRGTXEUWAJRJMT-UHFFFAOYSA-N 3-[3-[4-[2-(2,3-dihydro-1,4-benzodioxin-6-yloxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound C1=CC=C2C(CCCN3CCN(CC3)C=3C(=CC=CC=3)OC=3C=C4OCCOC4=CC=3)=CNC2=C1 NRGTXEUWAJRJMT-UHFFFAOYSA-N 0.000 description 2
- YCXQDIPLCFFZRS-UHFFFAOYSA-N 4-[3-[2-[4-[3-(5-bromo-1h-indol-3-yl)propyl]piperazin-1-yl]phenoxy]phenyl]morpholine Chemical compound C12=CC(Br)=CC=C2NC=C1CCCN(CC1)CCN1C1=CC=CC=C1OC(C=1)=CC=CC=1N1CCOCC1 YCXQDIPLCFFZRS-UHFFFAOYSA-N 0.000 description 2
- ZNLHWEDEIKEQDK-UHFFFAOYSA-N 5-chloropentanal Chemical compound ClCCCCC=O ZNLHWEDEIKEQDK-UHFFFAOYSA-N 0.000 description 2
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 0 C*1(C)CCCC1 Chemical compound C*1(C)CCCC1 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 208000020401 Depressive disease Diseases 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 2
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000002168 alkylating agent Substances 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 230000008485 antagonism Effects 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical compound FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- QZUDBNBUXVUHMW-UHFFFAOYSA-N clozapine Chemical compound C1CN(C)CCN1C1=NC2=CC(Cl)=CC=C2NC2=CC=CC=C12 QZUDBNBUXVUHMW-UHFFFAOYSA-N 0.000 description 2
- 229960004170 clozapine Drugs 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 2
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 2
- 150000002475 indoles Chemical class 0.000 description 2
- 238000005342 ion exchange Methods 0.000 description 2
- 230000002197 limbic effect Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- XKQRIBXKPQGCPO-UHFFFAOYSA-N n,n-dimethyl-3-(2-piperazin-1-ylphenoxy)aniline Chemical compound CN(C)C1=CC=CC(OC=2C(=CC=CC=2)N2CCNCC2)=C1 XKQRIBXKPQGCPO-UHFFFAOYSA-N 0.000 description 2
- 230000010807 negative regulation of binding Effects 0.000 description 2
- 150000002828 nitro derivatives Chemical class 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- KJIFKLIQANRMOU-UHFFFAOYSA-N oxidanium;4-methylbenzenesulfonate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1 KJIFKLIQANRMOU-UHFFFAOYSA-N 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 125000004193 piperazinyl group Chemical group 0.000 description 2
- 229920000642 polymer Chemical class 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- 239000000018 receptor agonist Substances 0.000 description 2
- 229940044601 receptor agonist Drugs 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000004007 reversed phase HPLC Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 229940076279 serotonin Drugs 0.000 description 2
- 239000003772 serotonin uptake inhibitor Substances 0.000 description 2
- DKGZKTPJOSAWFA-UHFFFAOYSA-N spiperone Chemical compound C1=CC(F)=CC=C1C(=O)CCCN1CCC2(C(NCN2C=2C=CC=CC=2)=O)CC1 DKGZKTPJOSAWFA-UHFFFAOYSA-N 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 210000003568 synaptosome Anatomy 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 2
- HJUGFYREWKUQJT-UHFFFAOYSA-N tetrabromomethane Chemical compound BrC(Br)(Br)Br HJUGFYREWKUQJT-UHFFFAOYSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 239000011592 zinc chloride Substances 0.000 description 2
- 235000005074 zinc chloride Nutrition 0.000 description 2
- FANCTJAFZSYTIS-IQUVVAJASA-N (1r,3s,5z)-5-[(2e)-2-[(1r,3as,7ar)-7a-methyl-1-[(2r)-4-(phenylsulfonimidoyl)butan-2-yl]-2,3,3a,5,6,7-hexahydro-1h-inden-4-ylidene]ethylidene]-4-methylidenecyclohexane-1,3-diol Chemical compound C([C@@H](C)[C@@H]1[C@]2(CCCC(/[C@@H]2CC1)=C\C=C\1C([C@@H](O)C[C@H](O)C/1)=C)C)CS(=N)(=O)C1=CC=CC=C1 FANCTJAFZSYTIS-IQUVVAJASA-N 0.000 description 1
- KRVOJOCLBAAKSJ-RDTXWAMCSA-N (2R,3R)-nemonapride Chemical compound C1=C(Cl)C(NC)=CC(OC)=C1C(=O)N[C@H]1[C@@H](C)N(CC=2C=CC=CC=2)CC1 KRVOJOCLBAAKSJ-RDTXWAMCSA-N 0.000 description 1
- SHAHPWSYJFYMRX-GDLCADMTSA-N (2S)-2-(4-{[(1R,2S)-2-hydroxycyclopentyl]methyl}phenyl)propanoic acid Chemical compound C1=CC([C@@H](C(O)=O)C)=CC=C1C[C@@H]1[C@@H](O)CCC1 SHAHPWSYJFYMRX-GDLCADMTSA-N 0.000 description 1
- FEKUXLUOKFSMRO-UHFFFAOYSA-N (4-fluorophenyl)hydrazine;hydron;chloride Chemical compound Cl.NNC1=CC=C(F)C=C1 FEKUXLUOKFSMRO-UHFFFAOYSA-N 0.000 description 1
- VIMMECPCYZXUCI-MIMFYIINSA-N (4s,6r)-6-[(1e)-4,4-bis(4-fluorophenyl)-3-(1-methyltetrazol-5-yl)buta-1,3-dienyl]-4-hydroxyoxan-2-one Chemical compound CN1N=NN=C1C(\C=C\[C@@H]1OC(=O)C[C@@H](O)C1)=C(C=1C=CC(F)=CC=1)C1=CC=C(F)C=C1 VIMMECPCYZXUCI-MIMFYIINSA-N 0.000 description 1
- BFCFYVKQTRLZHA-UHFFFAOYSA-N 1-chloro-2-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1Cl BFCFYVKQTRLZHA-UHFFFAOYSA-N 0.000 description 1
- PWKNBLFSJAVFAB-UHFFFAOYSA-N 1-fluoro-2-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1F PWKNBLFSJAVFAB-UHFFFAOYSA-N 0.000 description 1
- IGXSSRPZRAIXQF-UHFFFAOYSA-N 2,3-dihydro-1,4-benzodioxin-5-ol Chemical compound O1CCOC2=C1C=CC=C2O IGXSSRPZRAIXQF-UHFFFAOYSA-N 0.000 description 1
- HBAHZZVIEFRTEY-UHFFFAOYSA-N 2-heptylcyclohex-2-en-1-one Chemical compound CCCCCCCC1=CCCCC1=O HBAHZZVIEFRTEY-UHFFFAOYSA-N 0.000 description 1
- NTLAICDKHHQUGC-UHFFFAOYSA-N 3-(2-bromoethyl)-1h-indole Chemical compound C1=CC=C2C(CCBr)=CNC2=C1 NTLAICDKHHQUGC-UHFFFAOYSA-N 0.000 description 1
- MESJRHHDBDCQTH-UHFFFAOYSA-N 3-(dimethylamino)phenol Chemical compound CN(C)C1=CC=CC(O)=C1 MESJRHHDBDCQTH-UHFFFAOYSA-N 0.000 description 1
- YZZDGFRDDLGQII-UHFFFAOYSA-N 3-[2-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]ethyl]-1h-indole Chemical compound C1=C2OCOC2=CC(OC2=CC=CC=C2N2CCN(CC2)CCC=2C3=CC=CC=C3NC=2)=C1 YZZDGFRDDLGQII-UHFFFAOYSA-N 0.000 description 1
- JQRDSRJCMZLTBE-UHFFFAOYSA-N 3-[3-[4-[2-(1,3-benzodioxol-5-yloxy)phenyl]piperazin-1-yl]propyl]-1h-indole Chemical compound C1=CC=C2C(CCCN3CCN(CC3)C=3C(=CC=CC=3)OC=3C=C4OCOC4=CC=3)=CNC2=C1 JQRDSRJCMZLTBE-UHFFFAOYSA-N 0.000 description 1
- KQXNDOJNIPWLPE-UHFFFAOYSA-N 3-[4-[4-[2-(2-methoxyphenoxy)phenyl]piperazin-1-yl]butyl]-1h-indole Chemical compound COC1=CC=CC=C1OC1=CC=CC=C1N1CCN(CCCCC=2C3=CC=CC=C3NC=2)CC1 KQXNDOJNIPWLPE-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- DOQLCJMCQWQQHK-UHFFFAOYSA-N 4-chlorobutanal Chemical compound ClCCCC=O DOQLCJMCQWQQHK-UHFFFAOYSA-N 0.000 description 1
- 102100022738 5-hydroxytryptamine receptor 1A Human genes 0.000 description 1
- 101710138638 5-hydroxytryptamine receptor 1A Proteins 0.000 description 1
- GVIQYWPEJQUXLX-UHFFFAOYSA-N 6-chlorohexanal Chemical compound ClCCCCCC=O GVIQYWPEJQUXLX-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- SKTFQHRVFFOHTQ-UHFFFAOYSA-N 8-bromo-1,3-dimethyl-7h-purine-2,6-dione Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC(Br)=N2 SKTFQHRVFFOHTQ-UHFFFAOYSA-N 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 229910015900 BF3 Inorganic materials 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical group NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- 208000026331 Disruptive, Impulse Control, and Conduct disease Diseases 0.000 description 1
- 102000004073 Dopamine D3 Receptors Human genes 0.000 description 1
- 108090000525 Dopamine D3 Receptors Proteins 0.000 description 1
- 108050004812 Dopamine receptor Proteins 0.000 description 1
- 102000015554 Dopamine receptor Human genes 0.000 description 1
- 238000006783 Fischer indole synthesis reaction Methods 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 208000030990 Impulse-control disease Diseases 0.000 description 1
- 238000003109 Karl Fischer titration Methods 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- 229920001367 Merrifield resin Polymers 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 102000003946 Prolactin Human genes 0.000 description 1
- 108010057464 Prolactin Proteins 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 241000220304 Prunus dulcis Species 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 239000003875 Wang resin Substances 0.000 description 1
- NERFNHBZJXXFGY-UHFFFAOYSA-N [4-[(4-methylphenyl)methoxy]phenyl]methanol Chemical compound C1=CC(C)=CC=C1COC1=CC=C(CO)C=C1 NERFNHBZJXXFGY-UHFFFAOYSA-N 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 230000002152 alkylating effect Effects 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 235000020224 almond Nutrition 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 150000001448 anilines Chemical class 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000000164 antipsychotic agent Substances 0.000 description 1
- 229940054051 antipsychotic indole derivative Drugs 0.000 description 1
- 229940005529 antipsychotics Drugs 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical compound C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 210000003710 cerebral cortex Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 125000000000 cycloalkoxy group Chemical group 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- PUSKHXMZPOMNTQ-UHFFFAOYSA-N ethyl 2,1,3-benzoselenadiazole-5-carboxylate Chemical compound CCOC(=O)C1=CC=C2N=[Se]=NC2=C1 PUSKHXMZPOMNTQ-UHFFFAOYSA-N 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 230000008570 general process Effects 0.000 description 1
- LHGVFZTZFXWLCP-UHFFFAOYSA-N guaiacol Chemical compound COC1=CC=CC=C1O LHGVFZTZFXWLCP-UHFFFAOYSA-N 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 150000007857 hydrazones Chemical class 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 239000002917 insecticide Substances 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000011968 lewis acid catalyst Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- WZHJKEUHNJHDLS-QTGUNEKASA-N metergoline Chemical compound C([C@H]1CN([C@H]2[C@@H](C=3C=CC=C4N(C)C=C(C=34)C2)C1)C)NC(=O)OCC1=CC=CC=C1 WZHJKEUHNJHDLS-QTGUNEKASA-N 0.000 description 1
- 229960004650 metergoline Drugs 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 210000001577 neostriatum Anatomy 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 210000001009 nucleus accumben Anatomy 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N palmitic acid group Chemical group C(CCCCCCCCCCCCCCC)(=O)O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 239000004031 partial agonist Substances 0.000 description 1
- 210000002442 prefrontal cortex Anatomy 0.000 description 1
- 229940097325 prolactin Drugs 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 230000000698 schizophrenic effect Effects 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000012896 selective serotonin reuptake inhibitor Substances 0.000 description 1
- 239000003723 serotonin 1A agonist Substances 0.000 description 1
- 239000003727 serotonin 1A antagonist Substances 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 108010092215 spiroperidol receptor Proteins 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 150000003892 tartrate salts Chemical class 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 150000003577 thiophenes Chemical class 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/32—Alcohol-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/14—Radicals substituted by nitrogen atoms, not forming part of a nitro radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Neurosurgery (AREA)
- Medicinal Chemistry (AREA)
- Neurology (AREA)
- Psychiatry (AREA)
- Addiction (AREA)
- Hospice & Palliative Care (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Description
- Substituierte Phenyl-piperazin-Derivate, ihre Herstellung und Verwendung
- Die vorliegende Erfindung betrifft neue substituierte Phenyl-piperazin-Derivate, die wirksam an den 5-HT1A-Rezeptor binden, diese Verbindungen enthaltende pharmazeutische Zusammensetzungen und ihre Verwendung zur Behandlung bestimmter psychiatrischer und neurologischer Störungen. Viele der Verbindungen der Erfindung sind ebenfalls wirksame Serotoninwiederaufnahmehinibitoren und/oder D3/D4-Liganden und werden daher als besonders nützlich zur Behandlung von Depression und Psychose erachtet.
- Stand der Technik
- Klinische und pharmakologische Studien haben gezeigt, daß 5-HT1A-Agonisten und Partialagonisten nützlich in der Behandlung einer Reihe von affektiven Störungen sind, wie allgemeine Angststörung, Panikstörung, Zwangsstörung, Depression und Aggression.
- Es wurde ebenfalls berichtet, daß 5-HT1A-Liganden nützlich in der Behandlung von Ischämie sein können.
- Eine Übersicht über 5-HT1A-Antagonisten und vorgeschlagene potentielle therapeutische Ziele für die Antagonisten auf Basis von vorklinischen und klinischen Daten wird von Schechter et al. dargestellt, Serotonin, 1997, Bd. 2, Ausgabe 7. Es wird angegeben, daß 5-HT1A-Antagonisten nützlich in der Behandlung von Schizophrenie, Altersdemenz, mit Alzheimer-Krankheit verbundener Demenz und in Kombination mit SSRI-Antidepressiva ebenfalls nützlich in der Behandlung von Depression sein können.
- 5-HT-Wiederaufnahmeinhibitoren sind allgemein bekannte Antidepressiva und nützlich zur Behandlung von Panikstörungen und Sozialphobie.
- Die Wirkung der kombinierten Verabreichung einer Verbindung, die die Serotoninwiederaufnahme hemmt, und eines 5-HT1A-Rezeptorantagonisten wurde in mehreren Untersuchungen ausgewertet (Innis, R.B. et al., Eur. J. Pharmacol., 1987, 143, S. 195–204 und Gartside, S.E., Br. J. Pharmacol. 1995, 115, S. 1064–1070, Blier, P. et al., Trends Pharmacol. Sci. 1994, 15, 220). In diesen Untersuchungen wurde festgestellt, daß kombinierte 5-HT1A- Rezeptorantagonisten und Serotoninwiederaufnahmeinhibitoren ein schnelleres Einsetzen der therapeutischen Wirkung erzeugen würden.
- Dopamin D4-Rezeptoren gehören zur Dopamin D2-Unterfamilie von Rezeptoren, die als verantwortlich für die antipsychotischen Wirkungen von Neuroleptika betrachtet wird. Die Nebenwirkungen von Neuroleptika, die primär ihre Wirkung über einen Antagonismus von D2-Rezeptoren ausüben, sind dafür bekannt, daß sie auf einen D2-Rezeptorantagonismus in den striären Regionen der Hirns zurückzuführen sind. Jedoch befinden sich Dopamin D4-Rezeptoren primär in anderen Bereichen des Hirns als im Striatum, was nahelegt, daß Antagonisten des Dopamin D4-Rezeptors extrapyramidale Nebenwirken fehlen werden. Dies wird durch das Antipsychotikum Clozapin veranschaulicht, das eine höhere Affinität für D4- als für D2-Rezeptoren ausübt, und dem extrapyramidale Nebenwirkungen fehlen (Van Tol et al., Nature 1991, 350, 610; Hadley, Medicinal Research Reviews 1996, 16, 507–526 und Sanner, Exp. Opin. Ther. Patents 1998, 8, 383–393).
- Es wurde gezeigt, daß eine Anzahl von D4-Liganden, die als selektive D4-Rezeptorantagonisten postuliert wurden (L-745,879 und U-101958), antipsychotisches Potential besitzen (Mansbach et al., Psychopharmacology 1998, 135, 194–200). Jedoch wurde kürzlich berichtet, daß diese Verbindungen partielle D4-Rezeptoragonisten in verschiedenen in-vitro-Wirksamkeitstests sind (Gazi et al., Br. J. Pharmacol. 1998, 124, 889–896 und Gazi et al., Br. J. Pharmacol. 1999, 128, 613–620). Außerdem wurde gezeigt, daß Clozapin, das ein wirksames Antipsychotikum ist, ein stummer Antagonist ist (Gazi et al., Br. J. Pharmacol. 1999, 128, 613–620).
- Entsprechend können D4-Liganden, die partielle D4-Rezeptoragonisten oder -antagonisten sind, vorteilhafte Wirkungen gegen Psychosen aufweisen.
- Dopamin D4-Antagonisten können ebenfalls nützlich zur Behandlung von kognitiven Defiziten sein (Jentsch et al., Psychopharmacology 1999, 142, 78–84).
- Es wurde ebenfalls nahegelegt, daß Dopamin D4-Antagonisten nützlich zur Reduzierung von Dyskinäsie sein können, die als Ergebnis der Behandlung von Parkinson-Krankheit mit L-Dopa auftritt (Tahar et al., Eur. J. Pharmacol. 2000, 399, 183–186).
- Dopamin D3-Rezeptoren gehören ebenfalls zur Dopamin D2-Unterfamilie von Rezeptoren, und sie finden sich vorzugsweise in den limbischen Regionen des Hirns (Sokoloff et al., Nature, 1990, 347, 146–151), wie im Nucleus accumbens, wo die Dopamin-Rezeptorblockade mit einer antipsychotischen Aktivität in Verbindung gebracht wurde (Willner, Int. Clinical Psychopharmacology 1997, 12, 297–308). Außerdem wurde eine Erhöhung der Spiegel von D3-Rezeptoren im limbischen Teil von schizophrenen Gehirnen berichtet (Gurevich et al., Arch. Gen. Psychiatry 1997, 54, 225–32). Deshalb können D3-Rezeptorantagonisten das Potential für eine effektive antipsychotische Therapie bieten, die frei von den extrapyramidalen Nebenwirkungen der klassischen Antipsychotika sind, die ihre Wirkung primär durch Blockade von D2-Rezeptoren ausüben (Shafer et al., Psychopharmacology 1998, 135, 1–16; Schwartz et al., Brain Research Reviews 2000, 31, 277–287).
- Außerdem führt die D3-Rezeptorblockade zu einer schwachen Stimulierung des präfrontalen Cortex (Merchant et al., Cerebral Cortex 1996, 6, 561–570), was nützlich gegen negative Symptome und kognitive Defizite sein könnte, die mit Schizophrenie verbunden sind. Zusätzlich können Dopamin D3-Antagonisten D2-Antagonisten-induzierte extrapyramidale Nebenwirkungen umkehren (Millan et al., Eur. J. Pharmacol. 1997, 321, R7–R9) und verursachen keine Veränderung im Prolactin (Reavill et al., J. Pharmacol. Exp. Ther. 2000, 294, 1154–1165). Entsprechend könnten D3-antagonistische Eigenschaften eines Antipsychotikums die negativen Symptome und kognitiven Defizite reduzieren und zu einem verbesserten Nebenwirkungsprofil in bezug auf extrapyramidale Nebenwirkungen und hormonale Veränderungen führen.
- Dopamin D3-Agonisten wurden ebenfalls als relevant in der Behandlung von Schizophrenie erachtet (Wustow et al., Current Pharmaceutical Design, 1997, 3, 391–404).
- Entsprechend wird angenommen, daß Mittel, die auf den 5-HT1A-Rezeptor wirken, sowohl Agonisten als auch Antagonisten, von potentiellem Nutzen in der Therapie von psychiatrischen und neurologischen Störungen und somit hocherwünscht sind. Außerdem können Antagonisten, die gleichzeitig eine wirksame Serotoninwiederaufnahme-Inhibierungsaktivität und/oder D4- und/oder D3-Aktivität aufweisen, besonders nützlich zur Behandlung verschiedener psychiatrischer und neurologischer Krankheiten sein.
- Mit den Verbindungen der vorliegenden Erfindung strukturell ähnliche Verbindungen wurden zuvor beschrieben. Thiophen-Derivate werden in WO 99/02516 als Liganden für den 5-HT1A-Rezeptor beschrieben. WO 97/26252 beschreibt Piperazinyl-Derivate als Insektizide. WO 95/14004 beschreibt substituierte Alkylamino-indol-Derivate als 5-HT1A-, 5-HT1B- und 5-HT1D-Derivate.
- Es wurde jetzt gefunden, daß Verbindungen einer bestimmten Klasse von Phenyl-piperazin-Derivaten an den 5-HT1A-Rezeptor mit hohen Affinitäten binden. Außerdem wurde festgestellt, daß viele dieser Verbindungen andere höchst vorteilhafte Eigenschaften besitzen, wie z.B. eine wirksame Serotoninwiederaufnahme-Inhibierungsakvitität und/oder Affinität für den D4- und/oder D3-Rezeptor.
- Zusammenfassung der Erfindung
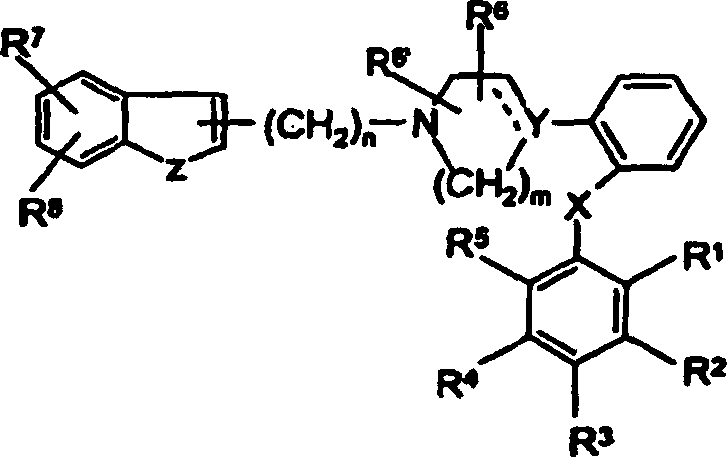
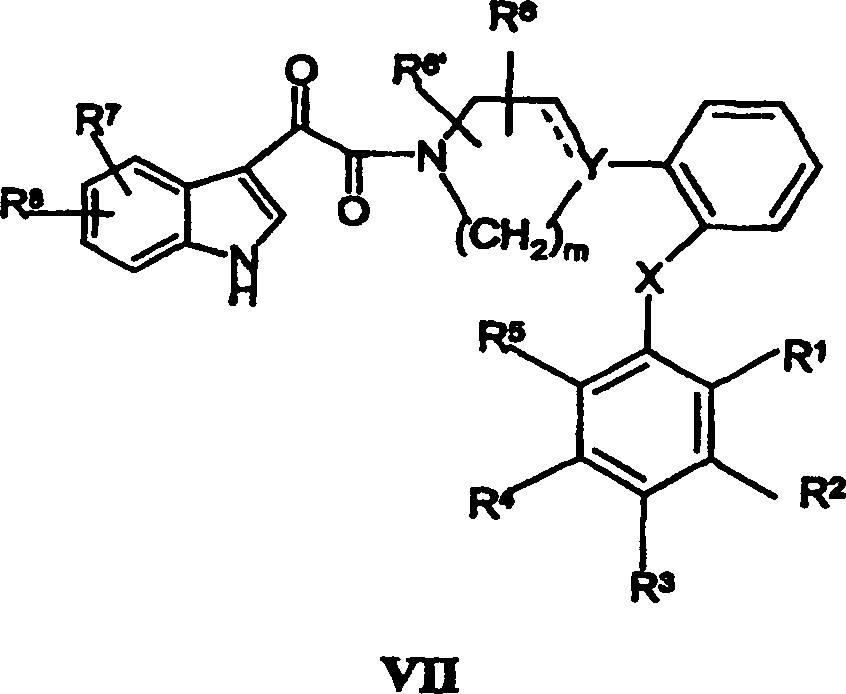
- Entsprechend betrifft die vorliegende Erfindung neue Verbindungen der allgemeinen Formel (I): worin Z NH, NR''', O oder S darstellt; R''' Wasserstoff oder C1-6-Alkyl darstellt;
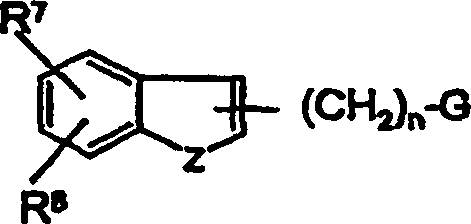
R7 und R8 unabhängig Wasserstoff, Halogen, C1-6-Alkyl, C3-8-Cycloalkyl, CN, CF3 oder C1-6-Alkoxy darstellen; oder R7 und R8 zusammen einen an den Benzol-Ring kondensierten 5- oder 6-gliedrigen Aryl- oder Heteroaryl-Ring bilden;
Y N, C oder CH darstellt;
die gestrichelte Linie eine optionale Bindung darstellt;
R6 und R6' H oder C1-6-Alkyl darstellen;
X -O- oder -S- darstellt; n 2, 3, 4 oder 5 ist;
m 2 oder 3 ist;
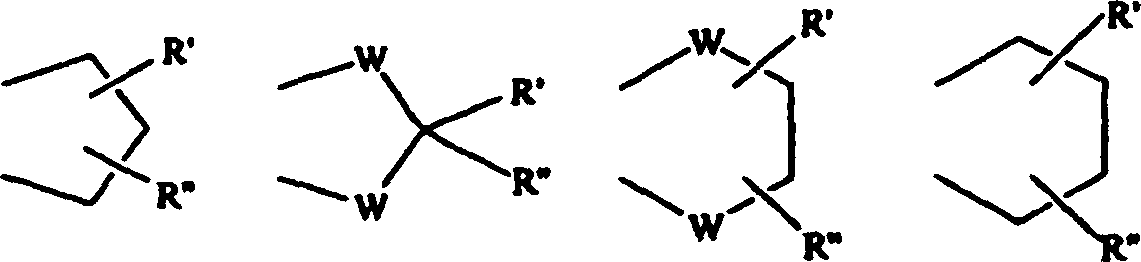
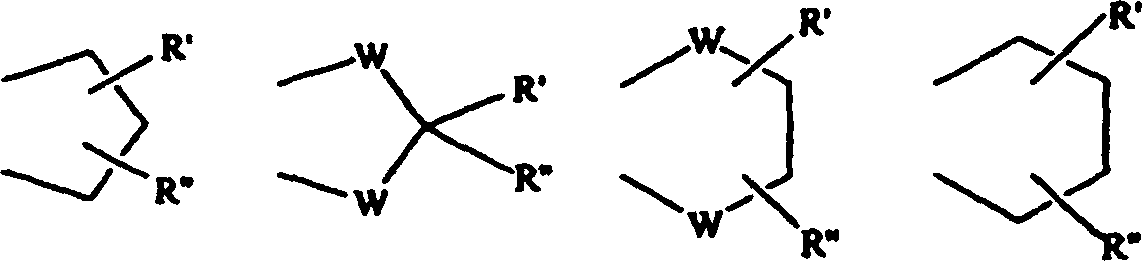
R1, R2, R3, R4 und R5 unabhängig aus einer Gruppe ausgewählt sind, die aus Wasserstoff, Halogen, C1-6-Alkyl, C2-6-Alkenyl, C1-6-Alkinyl, C3-8-Cycloalkyl, Aryl, Hydroxy, Hydroxy-C1-6-alkyl, C1-6-Alkoxy, C3-8-Cycloalkoxy, C1-6-Alkylsulfanyl, Acyl und NR9R10 besteht, worin R9 und R10 unabhängig Wasserstoff, C1-6-Alkyl, C2-6-Alkenyl, C2-6-Alkinyl, C3-8-Cycloalkyl oder Aryl darstellen; oder R9 und R10 zusammen mit dem Stickstoff, an den sie gebunden sind, einen 1-Morpholinyl-, 1-Piperidinyl-, 1-Homopiperidinyl-, 1-Piperazinyl-, 1-Homopiperazinyl-, 1-Imidazolyl-, 1-Pyrrolyl- oder Pyrazolyl-Ring bilden, von denen alle weiter mit C1-6-Alkyl substituiert sein können; oder zwei benachbarte Substituenten aus R1–R5 zusammen einen an den Phenyl-Ring kondensierten Ring bilden, der aus der Gruppe ausgewählt ist, die aus besteht, worin W O oder S ist und R' und R'' Wasserstoff oder C1-6-Alkyl sind. - Die Verbindungen der Erfindung besitzen Affinität für den 5-HT1A-Rezeptor. Entsprechend sieht die Erfindung vor:
Eine Verbindung wie oben als Medikament. - Eine pharmazeutische Zusammensetzung, die wenigstens eine Verbindung der Formel (I) wie oben definiert oder ein pharmazeutisch akzeptables Säureadditionssalz davon oder einen Prodrug davon in einer therapeutisch wirksamen Menge und in Kombination mit einem oder mehreren pharmazeutisch akzeptablen Trägern oder Verdünnungsmitteln umfaßt.
- Die vorliegende Erfindung stellt die Verwendung einer Verbindung der Formel (I) wie oben definiert oder eines Säureadditionssalzes oder Prodrugs davon zur Herstellung einer pharmazeutischen Zubereitung zur Behandlung der oben genannten Störungen bereit.
- Die Erfindung stellt ein Verfahren zur Behandlung von Krankheiten und Störungen in Menschen bereit, die durch Abnormalitäten im Serotoninsystem des zentralen Nervensystems verursacht werden, umfassend die Verabreichung einer wirksamen Menge einer Verbindung der Formel (I) wie oben.
- Die Verbindungen der Erfindung werden als nützlich zur Behandlung von affektiven Störungen, wie Depression, allgemeine Angststörung, Panikstörung, Zwangsstörungen, Sozialphobie, Eßstörung, Impulskontrollstörungen, Alkoholmißbrauch und Aggression, Psychose und neurologischen Störungen, wie Ischämie und Altersdemenz, erachtet.
- Ausführliche Beschreibung der Erfindung
- Eine bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin Z NH ist und das resultierende Indol in Position 3 gebunden ist;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin R7 und R8 unabhängig aus Wasserstoff, Halogen und C1-6-Alkyl ausgewählt sind oder R7 und R8 zusammen einen kondensierten Pyridyl-Ring bilden;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin n 2, 3 oder 4 ist;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin m 2 ist;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin R6 und R6' beide Wasserstoff sind;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin Y N ist;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin R1, R2, R3, R4 und R5 unabhängig aus Wasserstoff, Alkoxy und NR3R4 ausgewählt sind, worin R3 und R4 unabhängig Wasserstoff oder C1-6-Alkyl darstellen; oder R3 und R4 zusammen 1-Morpholino bilden; oder zwei benachbarte Vertreter aus R1, R2, R3, R4 und R5 zusammen einen kondensierten Ring bilden, der aus -O-CH2-O-, -O-CH2-CH2-O- oder -CH2-CH2-CH2- besteht;
eine andere bevorzugte Ausführungsform der Erfindung ist die Verbindung der Formel (I) wie oben, worin ein oder zwei Vertreter aus R1, R2, R3, R4 und R5 nicht Wasserstoff sind;
die am meisten bevorzugte Ausführungsform der Erfindung ist die Verbindung gemäß Formel (2) wie oben, wobei die Verbindung eine der folgenden ist:
1-{1-[3-(Dimethylamino)phenoxy]phenyl}-4-[2-(1H-indol-3-yl)ethyl]piperazin;
1-[1-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(1H-indol-3-yl)ethyl]piperazin;
1-{1-[3-(Dimethylamino)phenoxy]phenyl}-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[1-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl)piperazin;
1-[2-(1,4-Benzodioxan-6-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,4-Benzodioxan-6-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[4-(1H-indol-3-yl)butyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin;
1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin;
1-[2-(4-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin;
1-(2-Phenoxyphenyl)-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin;
1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin;
1-[2-(2,6-Dimethoxyphenoxy)phenyl)-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl)-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl)-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin;
1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin;
1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin;
1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin;
1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-Ethoxyphenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-(Diethylamino)phenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin;
1-{2-[3-(Morpholin-4-yl)phenoxy)phenyl}-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin;
1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin;
1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(7-fluor-1H-indol-3-yl)propyl]piperazin;
1-(2-Phenoxyphenyl)-4-[3-(5,7-dimethyl-1H-indol-3-yl)propyl]piperazin;
1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin;
1-[2-(3,4,5-Trimethoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin. - Einige der Verbindungen der allgemeinen Formel (I) können als optische Isomer davon existieren, und solche optischen Isomere sind ebenfalls von der Erfindung umfaßt.
- Der Begriff C1-6-Alkyl bezeichnet eine verzweigte oder unverzweigte Alkyl-Gruppe mit 1 bis einschließlich 6 Kohlenstoffatomen, wie Methyl, Ethyl, 1-Propyl, 2-Propyl, 1-Butyl, 2-Butyl, 2-Methyl-2-propyl und 2-Methyl-1-propyl.
- In ähnlicher Weise bezeichnen C2-6-Alkenyl bzw. C2-6-Alkinyl solche Gruppen mit 2 bis einschließlich 6 Kohlenstoffatomen, und die Gruppen besitzen wenigstens eine Doppelbindung bzw. Dreifachbindung.
- Halogen bedeutet Fluor, Chlor, Brom oder Iod.
- Der Begriff C3-8-Cycloalkyl bezeichnet einen monocyclischen oder bicyclischen Carbocyclus mit 3 bis 8 C-Atomen, wie Cyclopropyl, Cyclopentyl, Cyclohexyl, Cycloheptyl und Cyclooctyl. Bevorzugte Ausführungsformen sind Cyclopropyl, Cyclopentyl und Cyclohexyl.
- Die Begriffe C1-6-Alkoxy, C1-6-Alkylsulfanyl und C3-8-Cycloalkoxy bezeichnen solche Gruppe, in denen die Alkyl-Gruppe C1-6-Alkyl wie oben definiert ist.
- Acyl bedeutet CHO und -CO-Alkyl, worin die Alkyl-Gruppe C1-6-Alkyl wie oben definiert ist.
- 5- oder 6-gliedrige Ringe, die Aryl oder Heteroaryl sind, bezeichnen Gruppen wie Phenyl, Pyrrolyl, Pyridyl, Pyrimidyl, Furanyl und Thienyl. Exemplarisch für organische Säureadditionssalze gemäß der Erfindung sind diejenigen mit Maleinsäure, Fumarsäure, Benzoesäure, Ascorbinsäure, Bernsteinsäure, Oxalsäure, Bis-methylensalicylsäure, Methansulfonsäure, Ethandisulfonsäure, Essigsäure, Propionsäure, Weinsäure, Salicylsäure, Zitronensäure, Gluconsäure, Milchsäure, Äpfelsäure, Mandelsäure, Zimtsäure, Citraconsäure, Asparaginsäure, Stearinsäure, Palmitinsäure, Itaconsäure, Glykolsäure, p-Aminobenzoesäure, Glutaminsäure, Benzolsulfonsäure und Theopyllinessigsäure sowie die 8-Halogentheophylline, z.B. 8-Bromtheophyllin. Exemplarisch für anorganische Säureadditionssalze gemäß der Erfindung sind diejenigen mit Chlorwasserstoffsäure, Bromwasserstoffsäure, Schwefelsäure, Sulfaminsäure, Phosphorsäure und Salpetersäure. Die Säureadditionssalze der Erfindung sind bevorzugt pharmazeutisch akzeptable Salze, die mit nicht-toxischen Säuren gebildet werden.
- Außerdem können die Verbindungen dieser Erfindung in unsolvatisierten sowie solvatisierten Formen mit pharmazeutisch akzeptablen Lösungsmitteln wie Wasser, Ethanol und dgl. existieren. Allgemein werden die solvatisierten Formen als äquivalent mit den unsolvatisierten Formen für die Zwecke dieser Erfindung betrachtet.
- Einige der Verbindungen der vorliegenden Erfindung enthalten chirale Zentren, und solche Verbindungen existieren in Form von Isomeren (z.B. Enantiomeren). Die Erfindung schließt alle solche Isomere und beliebige Mischungen daraus ein, einschließlich racemischer Mischungen.
- Racemische Formen können in die optischen Antipoden durch bekannte Verfahren aufgetrennt werden, z.B. durch Trennung der diastereomeren Salze davon mit einer optisch aktiven Säure und durch Freisetzung der optisch aktiven Amin-Verbindung durch Behandlung mit einer Base. Ein anderes Verfahren zur Auftrennung von Racematen in die optischen Antipoden beruht auf der Chromatographie an einer optisch aktiven Matrix. Racemische Verbindungen der vorliegenden Erfindung können so in ihre optischen Antipoden aufgetrennt werden, z.B. durch fraktionierte Kristallisation von z.B. d- oder l-Salzen (Tartrate, Mandelate oder Kampfersulfonat). Die Verbindungen der vorliegenden Erfindung können ebenfalls durch die Bildung diastereomerer Derivate aufgetrennt werden.
- Zusätzliche Verfahren für die Auftrennung optischer Isomere, die den Fachleuten bekannt sind, können verwendet werden. Solche Verfahren schließen diejenigen ein, die von J. Jaques, A. Collet und S. Wilen erörtert werden in "Enantiomers, Racemates and Resolutions", John Wiley and Sons, New York (1981).
- Optisch aktive Verbindungen können auch aus optisch aktiven Ausgangsstoffen hergestellt werden.
- Die Verbindungen der Erfindung können durch eines der folgenden Verfahren hergestellt werden, umfassend:
- a) Umsetzen eines sekundären Amins der Formel worin R1–R6', X, Y und m wie oben definiert sind, mit einem Alkylierungsmittel der allgemeinen Formel: worin R7, R8, Z und n wie oben definiert sind und G eine geeignete Abgangsgruppe ist, wie z.B. Halogen, Mesylat oder Tosylat;
- b) Umsetzen einer Verbindung der Formel: worin R1–R6', X, Y, n und m wie oben definiert sind und Q(OH)2 ein Diol ist, wie z.B. substituiertes Ethylenglykol oder Propylenglykol, oder ein Polymer-gebundenes Diol; mit einem Hydrazin der Formel:
- c) Reduzieren eines Amids der Formel: worin Z, R1–R8, X, Y, n und m wie oben definiert sind;
- d) Reduzieren einer Verbindung der Formel: worin R1–R8, Y, X und m wie oben definiert sind.
- Die Alkylierungen gemäß Verfahren a werden allgemein durch Sieden der Reaktanden im Rückfluß oder durch Erwärmen auf eine feste Temperatur in einem geeigneten Lösungsmittel, wie z.B. Aceton, Acetonitril, Methylisobutylketon, Tetrahydrofuran, Dioxan, Ethanol, 2-Propanol, Ethylacetat, N,N-Dimethylformamid, Dimethylsulfoxid oder 1-Methyl-2-pyrrolidinon, in Gegenwart einer Base, wie z.B. Triethylamin oder Kaliumcarbonat, und gegebenenfalls einer katalytischen Menge Kaliumiodid durchgeführt.
- Sekundäre Amine der Formel (III) werden durch die oben umrissene Reaktionssequenz hergestellt. 2-Fluornitrobenzol wird mit einem Nukleophil der Formel (VIII) in einem aprotischen Lösungsmittel wie N,N-Dimethylformamid unter Verwendung organischer oder anorganischer Basen bei erhöhter Temperatur umgesetzt. Nach Reduktion der intermediären Nitro-Verbindung (IX) unter Verwendung von Standardbedingungen, wie z.B. Palladium-katalysierte Hydrierung oder mit Eisen in sauren Lösungsmitteln, wurde das Anilin-Derivat (X) zum gewünschten sekundären Amin der Formel (III) umgewandelt. Die Piperazin-Bildung wurde entweder durch Reaktion mit Bis(2-chlorethyl)amin-hydrochlorid bei erhöhter Temperatur oder in einer Mehrstufensynthese gemäß veröffentlichten Verfahren durchgeführt (Kruse et al., Recl. Trav. Chim. Pays-Bas, 1988, 107, 303–309).
- Alternativ werden sekundäre Amine der Formel (III) unter Verwendung der monosubstituierten cyclischen Diamine der Formel (XII) als Schlüsselzwischenstufe hergestellt. Der Substituent R ist eine angemessene Schutzgruppe, wie z.B. eine Ethoxy-, Methoxy- oder 2-Methyl-2-propyloxycarbonyl-Gruppe oder eine Benzyl-Gruppe, oder ein geeigneter fester Träger wie ein Merrifield-Harz oder eine Feststoff-geträgerte Carbamat-Gruppe, wie z.B. der Carbamatlinker auf Wang-Harz-Basis (Zaragoza, Tetrahedron Lett., 1995, 36, 8677–8678). Die monosubstituierten cyclischen Diamine der Formel (XII) werden aus handelsüblichen Ausgangsstoffen oder durch Verfahren hergestellt, die für den fachlich versierten Chemiker naheliegend sind. Die monosubstituierten cyclischen Diamine der Formel (XII) werden mit η6-1,2-Dichlorbenzol-η5-cyclopentadienyleisen(II)-hexafluorophosphat bei erhöhter Temperatur in einem aprotischen Lösungsmittel wie trockenem Tetrahydrofuran unter Verwendung einer angemessenen Base wie Kaliumcarbonat umgesetzt. η6-1,2-Dichlorbenzol-η5-cyclopentadienyleisen(II)-hexafluorophosphat wird in Analogie zu Literaturverfahren hergestellt (Pearson und Gelormani, J. Org. Chem. 1994, 59, 4561–4570). Das so gebildete Monochlor-Derivat der Formel (XIII) wird anschließend mit einem Nukleophil der Formel (VIII) in einem aprotischen Lösungsmittel wie trockenem Tetrahydrofuran entweder durch Verwendung einer angemessenen Base wie Kaliumcarbonat oder durch Entschützen des Nukleophils der Formel (VIII) unter Verwendung einer Base wie Natriumhydrid vor der Reaktion umgesetzt. Entkomplexierung, durchgeführt gemäß Literaturverfahren (Pearson et al., J. Org. Chem. 1996, 61, 1297–1305), gefolgt von Entschützen durch dem fachmännischen Chemiker naheliegende Verfahren oder Spaltung vom festen Träger gemäß Literaturverfahren (Zaragoza, Tetrahedron Lett., 1995, 36, 8677–8678 und Conti et al., Tetrahedron Lett., 1997, 38, 2915–2918) lieferte die gewünschten sekundären Amine der Formel (III), entsprechend den sekundären Aminen der Formel (XV), R=H. Nukleophile der Formel (VIII) sind kommerziell erhältlich oder werden durch dem fachlich versierten Chemiker naheliegende Verfahren oder gemäß Literaturverfahren hergestellt (Guillaumet und Hretani, J. Heterocyclic Chem , 26, 193–196, 1989).
- Die Alkylierungsmittel der Formel: werden gemäß Literaturverfahren (J. Med. Chem. 1983, 26, 1470–1477, Brodfuehrer et al., J. Org. Chem. 1997, 62, 9192–9202, Anelli et al., J. Org. Chem. 1987, 52, 2559–2562, Brodfuehrer et al., J. Org. Chem. 1997, 62, 9192–9202) oder durch dem fachlich versierten Chemiker naheliegende Verfahren hergestellt.
- Die Indolbildung gemäß Verfahren b wird durch Reaktion von Acetalen der Formel (IV) mit Arylhydrazinen der Formel (V) durchgeführt, was zu den entsprechenden Hydrazonen führt, die anschließend zu Indolen mittels der Fischer-Indol-Synthese umgewandelt werden. Die Synthesesequenz wird bevorzugt als Eintopfverfahren unter Verwendung von Lewis-Säure-Katalysatoren, bevorzugt Zinkchlorid oder Bortrifluorid, oder Protonensäuren, bevorzugt Schwefelsäure oder Phosphorsäure, in einem geeigneten Lösungsmittel wie Essigsäure oder Ethanol bei erhöhter Temperatur durchgeführt. Acetale der Formel (IV) werden durch die oben umrissene Reaktionssequenz 2) unter Verwendung von mono-substituierten cyclischen Diaminen der Formel (XII) mit als Schlüsselzwischenstufen hergestellt. Die Schlüsselzwischenstufen der Formel (XII) werden durch Alkylierung von cyclischen Diaminen der Formel (XI) mit Acetalen der Formel: unter Verwendung der oben für Verfahren a beschriebenen Bedingungen hergestellt. Polymergebundene Acetale der Formel (XVI) werden durch Reaktion von Aldehyden der Formel G-(CH2)n+1-CHO mit handelsüblichem 2,2-Dimethyl-1,3-dioxolan-4-yl-methoxymethylpolystyrol in einem geeigneten Lösungsmittel wie Toluol unter Verwendung von p-Toluolsulfonsäure als Katalysator bei erhöhter Temperatur hergestellt. 4-Chlorbutanal, 5-Chlorpentanal und 6-Chlorhexanal wurden in Analogie zum von Normant et al. beschrieben Verfahren hergestellt, Tetrahedron 1994, 50 (40), 11665.
- Die Reduktionen gemäß Verfahren c und d werden allgemein durch Verwendung von LiAlH4, AlH3 oder Diboran in einem inerten Lösungsmittel wie Tetrahydrofuran, Dioxan oder Diethylether bei Raumtemperatur oder bei geringfügig erhöhter Temperatur durchgeführt. Die Amide der Formel (VI) werden aus sekundären Aminen der Formel (III) und substituierten Indol-3-ylalkylcarbonsäuren oder -carbonsäurechloriden durch dem fachlich versierten Chemiker naheliegende Verfahren hergestellt. Die Amide der Formel (VII) werden aus 3-unsubstituierten Indolen und sekundären Aminen der Formel (III) gemäß mehrstufigen Literaturverfahren hergestellt (Nichols et al., Synthesis 1999, 6, 935–938 und Speeter und Anthony, J. Am. Chem. Soc. 1954, 76, 6208–6210).
- Beispiele
- Alle Reaktionen wurden unter einem positiven Stickstoffdruck durchgeführt. Schmelzpunkte wurden an einer Vorrichtung Büchi SMP-20 bestimmt und sind unkorrigiert. Analytische LC-MS-Daten wurden an einem PE Sciex API 150EX-Instrument erhalten, das mit einer IonSpray-Quelle und einem Shimadzu LC-8A/SLC-10A LC-System ausgerüstet war. Die LC-Bedingungen (50 × 4,6 mm YMC ODS-A mit 5 μm Teilchengröße) waren eine Elution mit linearem Gradienten mit Wasser/Acetonitril/Trifluoressigsäure (90:10:0,05) zu Wasser/Acetonitril/Trifluoressigsäure (10:90:0,03) in 7 min mit 2 ml/min. Für die Verbindungen 3c, 3e, 3f und 3l waren die LC-Bedingungen (Waters Symmetry, 30 × 4,6 mm, Cl8, 3,5 μm Teilchengröße) eine Elution mit linearem Gradienten mit Wasser/Acetonitril/Trifluoressigsäure (90:10:0,05) zu Wasser/Acetonitril/Trifluoressigsäure (10:90:0,03) in 4 min mit 2 ml/min. Reinheit wurde durch Integration der UV-Spur (254 nm) bestimmt. Die Retentionszeiten Rt sind in Minuten ausgedrückt. Präparative LC-MS-Trennung wurde am gleichen Instrument durchgeführt. Die LC-Bedingungen (50 × 20 mm YMC ODS-A mit 5 μμm Teilchengröße) waren eine Elution mit linearem Gradienten mit Wasser/Acetonitril/Trifluoressigsäure (80:20:0,05) zu Wasser/Acetonitril/Trifluoressigsäure (10:90:0,03) in 7 min mit 22,7 ml/min. Die Fraktionssammlung wurde durch "Split-Flow"-MS-Detektion durchgeführt. 1H-NMR-Spektren wurden bei 500,13 MHz an einem Bruker Avance DRX500-Instrument oder bei 250,13 MHz an einem Bruker AC 250-Instrument aufgezeichnet. Deuteriertes Chloroform (99,8% D) oder Dimethylsulfoxid (99,9% D) wurden als Lösungsmittel verwendet. TMS wurde als interner Referenzstandard verwendet. Werte der chemischen Verschiebung sind in ppm ausgedrückt. Die folgenden Abkürzungen werden für die Multiplizität der NMR-Signale verwendet: s = Singulett, d = Dublett, t = Triplett, q = Quartett, qui = Quintett, h = Heptett, dd = Dublett von Dubletts, dt = Dublett von Tripletts, dq = Dublett von Quartetts, tt = Triplett von Tripletts, m = Multiplett und b = breites Singulett. NMR-Signale, die sauren Protonen entsprechen, sind allgemein ausgelassen. Der Wassergehalt in kristallinen Verbindungen wurde durch Karl-Fischer-Titration bestimmt. Standard-Aufarbeitungsverfahren bezeichnen die Extraktion mit dem angegebenen organischen Lösungsmittel aus geeigneten wäßrigen Lösungen, Trocknen der kombinierten organischen Extrakte (wasserfreies MgSO4 oder Na2SO4), Filtrieren und Verdampfen des Lösungsmittels im Vakuum. Zur Säulenchromatographie wurde Kieselgel vom Typ Kieselgel 60, 230–400 mesh ASTM verwendet. Zur Ionenaustauschchromatographie wurde das folgende Material verwendet: SCX-Säulen (1 g) von Varian Mega Bond Elut®, Chrompack Kat. Nr. 220776. Vor der Verwendung wurden die SCX-Säulen mit einer 10%igen Lösung von Essigsäure in Methanol (3 ml) vorkonditioniert. Zur Umkehrphasenchromatographie wurde das folgende Material verwendet: C-18-Säulen (1 g) von Varian Mega Bond Elut®, Chrompack Kat. Nr. 220508. Vor der Verwendung wurden die C-18-Säulen mit Methanol (3 ml) und Wasser (3 ml) vorkonditioniert. Zum Entkomplexieren durch Bestrahlung wurde eine UV-Lichtquelle (300 W) von Philipps verwendet.
- Beispiel 1
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[2-(1H-indol-3-yl)ethyl)piperazin, Oxalat (1a)
- 1-Chlor-2-nitrobenzol (15,0 g), 3-(Dimethylamino)phenol (13,0 g) und Kaliumhydroxid (11,8 g) wurden in N,N-Dimethylformamid (350 ml) gelöst und für 18 h unter Rückfluß gekocht. Die Reaktion wurde dann abgekühlt und in Wasser gegossen und durch ein Standardverfahren unter Verwendung von Ethylacetat aufgearbeitet. Das Rohprodukt wurde durch Kieselgelchromatographie (Heptan: Ethylacetat:Triethylamin/80:10:10) gereinigt. Die reine Zwischenstufe wurde in einer Mischung aus Ethanol (200 ml) und Essigsäure (20 ml) gelöst. Nach Zugabe von Pd/C (5%, 4,5 g) wurde die Reaktionsmischung unter einer Wasserstoffatmosphäre (3 bar) für 3 h geschüttelt. Die Reaktionsmischung wurde filtriert und nach Neutralisation durch ein Standardverfahren unter Verwendung von Ethylacetat aufgearbeitet, was das reine Anilin (11,2 g) lieferte. Die rohe Anilin, Bis-(2-chlorethyl)amin-hydrochlorid (8,6 g) und Chlorbenzol (200 ml) wurden unter Rückfluß für 48 h gekocht. Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt und die flüchtigen Lösungsmittel im Vakuum zum Erhalt des rohen 1-{[3-(Dimethylamino)phenoxy]phenyl}piperazins (18,6 g) verdampft. Eine Lösung aus dem rohen Piperazin, Di-tert-butyldicarbonat (32 g) und Kaliumcarbonat (68 g) in Tetrahydrofuran:Wasser/1:1 wurde für 18 h auf 50°C erwärmt. Die organische Schicht wurde abgetrennt und die wäßrige Phase mit Ethylacetat extrahiert. Die vereinigten organischen Phasen wurden durch ein Standardverfahren gefolgt von Reinigung durch Kieselgelchromatographie (Heptan:Ethylacetat/8:2) aufgearbeitet, was reines BOC-geschütztes 1-{[3-Dimethyl)phenoxy]phenyl}piperazin (9,4 g) lieferte. Eine Lösung aus dem BOC-Derivat in einer Mischung aus trockenem THF (30 ml) und Trifluoressigsäure (30 ml) wurde bei Raumtemperatur für 1 h gerührt. Die flüchtigen Lösungsmittel wurden im Vakuum verdampft, und Ethylacetat und 1N wäßriges Natriumhydroxid wurden hinzugegeben. Die organische Phase wurde aufgefangen und durch ein Standardverfahren aufgearbeitet, um 1-{[3-(Dimethylamino)phenoxy]phenyl}piperazin (6,0 g) zu ergeben. Eine Mischung aus einem Teil des reinen Piperazins (1,37 g), 3-(2-Bromethyl)-1H-indol (1,0 g), Kaliumcarbonat (2,2 g), Kaliumiodid (katalytisch) und Methylisobutylketon wurde unter Rückfluß für 24 h gekocht. Die Mischung wurde auf Raumtemperatur abgekühlt, filtriert und die flüchtigen Lösungsmittel im Vakuum unter Erhalt eines Öls verdampft, das durch Kieselgelchromatographie (Heptan:Ethylacetat:Triethylamin/26:70:4) unter Erhalt der Titelverbindung als Öl gereinigt wurde. Die Titelverbindung wurde als ihr Oxalat aus Aceton kristallisiert (1,27 g). Smp. 210–206°C.
- 1H-NMR/250 MHz (DMSO-d6): 2,85 (s, 6H); 3,00–3,35 (m, 12H); 6,15 (d, 1H); 6,35 (s, 1H); 6,45 (d, 1H); 6,85 (d, 1H); 6,95–7,15 (m, 6H); 7,20 (s, 1H); 7,35 (d, 1H); 7,55 (d, 1H); 10,90 (s, 1H). MS (m/z): 441 (MH+), 144. Analyse Berechnet für C28H32N4O: C, 67,89; H, 6,47; N, 10,56. Gefunden: C, 67,34; H, 6,59; N, 10,30.
- Die folgenden Verbindungen wurden unter Verwendung des gleichen allgemeinen Verfahrens hergestellt:
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(1H-indol-3-yl)ethyl]piperazin, Oxalat (1b).
-
- Smp. 221–228°C. 1H-NMR (250 MHz, DMSO-d6): 3,00–3,35 (m, 12H); 6,00 (s, 2H); 6,40 (dd, 1H); 6,65 (d, 1H9; 6,80–6,90 (m, 2H); 6,95–7,15 (m, 5H); 7,20 (d, 1H); 7,35 (d, 1H); 7,55 (d, 1H); 10,90 (s, 1H). MS (m/z): 443 (MH+), 311, 131. Analyse Berechnet für C27H27N3O3: C, 65,10; H, 5,54; N, 7,86. Gefunden: C, 64,86; H, 5,55; N, 7,60.
- Beispiel 2
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[3-(1H-indol-3-yl)propyl]piperazin (2a)
- Zu einer Suspension aus Lithiumaluminiumhydrid (8,0 g) in Tetrahydrofuran (500 ml) wurde eine Lösung aus 3-Indolpropionsäure (20 g) in Tetrahydrofuran (100 ml) getropft. Die Reaktionsmischung wurde für 1 h bei Raumtemperatur gerührt und anschließend auf 5°C abgekühlt. Nach aufeinanderfolgender Zugabe von Wasser (16 ml), 15%igem wäßrigem Natriumhydroxid (8,0 ml) und Wasser (40 ml) wurde die Reaktionsmischung bei Raumtemperatur über Nacht gerührt und filtriert. Verdampfen der flüchtigen Lösungsmittel ergab reines 3-(1H-Indol-3-yl)propanol (19,1 g) als Öl. 3-(1H-Indol-3-yl)propanol (18,6 g) und Kohlenstofftetrabromid (42,1 g) wurden in Acetonitril (1 l) gelöst und auf 0°C abgekühlt, und Triphenylphosphin (30,7 g) wurde in kleinen Portionen hinzugegeben. Die Reaktion wurde für weitere 3 h bei Raumtemperatur gerührt, die flüchtigen Lösungsmittel im Vakuum verdampft und das verbleibende Öl durch Kieselgelchromatographie (Heptan:Ethylacetat/2:1) unter Erhalt von 3-(3-Brompropyl)-1H-indol gereinigt (25,6 g). Diese Zwischenstufe wurde an die Piperazin-Einheiten unter Verwendung des in Beispiel 1 beschriebenen Verfahrens gekuppelt, um die Titelverbindung als isolierten amorphen Feststoff zu ergeben.
- 1H-NMR (250 MHz, DMSO-d6): 1,80 (q, 2H); 2,25–2,40 (m, 6H); 2,65 (t, 2H); 2,85 (s, 6H); 3,05 (m, 4H); 6,10 (dd, 1H); 6,30 (t, 1H); 6,45 (dd, 1H); 6,80–7,10 (m, 8H); 7,30 (d, 1H); 7,50 (d, 1H); 10,70 (b, 1H); MS (m/z): 455 (MH+), 295, 239, 201, 130.
- Die folgenden Verbindungen wurden analog hergestellt:
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin, Oxalat (2b).
-
- Smp. 156–162°C. 1H-NMR (250 MHz, DMSO-d6): 1,80 (q, 2H); 2,25–2,40 (m, 6H); 2,70 (t, 2H); 3,05 (m, 4H); 6,00 (s, 2H); 6,35 (dd, 1H); 6,55 (d, 1H); 6,85 (d, 2H); 6,90–7,15 (m, 6H); 7,30 (d, 1H); 7,50 (d, 1H); 10,75 (s, 1H). MS (m/z): 456 (MH+), 297, 201, 130. Analyse Berechnet für C28H29N3O3: C, 73,81; H, 6,43; N, 9,23. Gefunden: C, 73,28; H, 6,45; N, 9,00.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin, Dihydrochlorid (2c).
-
- Smp.: 165°C (Zersetzung). 1H-NMR (250 MHz, DMSO-d6): 2,08 (m, 2H); 2,73 (t, 2H); 3,02 (m, 2H); 3,15 (t, 4H); 3,55 (t, 4H); 6,00 (s, 2H); 6,40 (d, 1H); 6,65 (s, 1H); 6,80 (d, 1H); 6,85 (d, 1H); 7,00 (m, 2H); 7,05 (m, 2H); 7,25 (d, 1H); 7,38 (s, 1H); 7,55 (dd, 1H); 10,45 (s, 1H); 11,00 (s, 1H). MS (m/z): 490 (MH+). Analyse Berechnet für C28H30Cl3N3O3: C, 59,73; H, 5,38; N, 7,47. Gefunden: C, 59,13; H, 5,36; N, 7,26.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin, Dihydrochlorid (2d).
-
- Smp.: 183–189°C. 1H-NMR (500 MHz, DMSO-d6): 2,12 (m, 2H); 2,73 (t, 2H); 3,05–3,25 (m, 6H); 3,55 (d, 2H); 3,65 (d, 2H); 3,75 (s, 3H); 6,53 (m, 1H); 6,88–7,20 (m, 9H); 7,27–7,40 (m, 3H); 11,05 (s, 2H). MS (m/z): 460 (MH+). Analyse Berechnet für C28H32Cl2FN3O2: C, 63,16; H, 6,06; N, 7,89. Gefunden: C, 63,04; H, 6,07; N, 7,88.
- 1-[2-(1,4-Benzodioxan-6-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin (2e).
-
- 1H-NMR (250 MHz, CDCl3): 1,90 (qui, 2H); 2,40–2,60 (m, 6H); 2,79 (t, 2H); 3,15 (t, 4H); 4,22 (s, 4H); 6,45 (m, 2H); 6,77 (d, 1H); 6,85–7,22 (m, 7H); 7,35 (d, 1H); 7,60 (d, 1H); 7,92 (s, 1H). MS (m/z): 470 (MH+).
- 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (2f)
-
- 1H-NMR (250 MHz, CDCl3): 1,90 (qui, 2H); 2,38–2,53 (m, 6H); 2,73 (t, 2H); 3,16 (t, 4H); 4,26 (s, 4H); 6,38 (dd, 1H); 6,60–6,75 (m, 2H); 6,83–7,10 (m, 6H); 7,23–7,30 (m, 3H); 7,92 (s, 1H). LC/MS (m/z): 488 (MH+), Rt = 2,53, Reinheit 99,8%.
- 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin (2g)
-
- 1H-NMR (250 MHz, CDCl3): 1,90 (qui, 2H); 2,35–2,50 (m, 6H); 2,75 (t, 2H); 3,18 (t, 4H); 4,28 (s, 4H); 6,40 (dd, 1H); 6,60–6,75 (m, 3H); 6,80–7,08 (m, 6H); 7,32 (d, 1H); 7,50 (d, 1H); 7,95 (s, 1H). LC/MS (m/z): 504 (MH+), Rt = 2,60, Reinheit 99,6%.
- 1-[2-(1,4-Benzodioxan-6-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin (2h)
-
- 1H-NMR (250 MHz, CDCl3): 1,90 (qui, 2H); 2,35–2,55 (m, 6H); 2,75 (t, 2H); 3,15 (t, 4H); 4,23 (s, 4H); 6,45 (m, 2H); 6,78–6,15 (m, 7H); 7,32 (d, 1H); 7,50 (d, 1H); 7,92 (s, 1H). LC/MS (m/z): 504 (MH+), Rt = 2,62, Reinheit 99,7%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin (2i)
-
- 6-Chlor-3-(3-{4-[2-(2-methoxy-phenoxy)-phenyl]-piperazin-1-yl}propyl)-1H-indol 1H-NMR (250 MHz, CDCl3): 1,90 (qui, 2H); 2,35–2,50 (m, 6H); 2,73 (t, 2H); 3,19 (t, 4H); 3,83 (s, 3H); 6,70–7,08 (m, 10H); 7,32 (d, 1H); 7,49 (d, 1H); 7,94 (s, 1H). LC/MS (m/z): 476 (MH+), Rt = 2,59, Reinheit 99,8%.
- 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin (2j)
-
- 1H-NMR (250 MHz, CDCl3): 1,89 (qui, 2H); 2,33–2,60 (m, 6H); 2,73 (t, 2H); 3,13 (t, 4H); 3,75 (s, 3H); 6,49 (m, 2H); 6,58 (dd, 1H); 6,95–7,20 (m, 7H); 7,32 (d, 1H); 7,49 (d, 1H); 7,92 (s, 1H). LC/MS (m/z): 476 (MH+), Rt = 2,64, Reinheit 99,7%.
- Beispiel 3
- 1[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin (3a)
- 4-[(4-Nitrophenoxy)carbonyloxymethyl)phenoxyphenyl-polystyrol (267,0 g, 235 mmol) wurde in trockenem N,N-Dimethylformamid (2 l) suspendiert. N-Methylmorpholin (238,0 g, 2,35 mol) und Piperazin (102,0 g, 1,17 mol) wurden hinzugegeben, und die Mischung wurde bei Raumtemperatur für 16 h gerührt. Das Harz wurde abfiltriert und mit N,N-Dimethylformamid (2 × 1 l), Tetrahydrofuran (2 × 1 l), Wasser (1 × 500 ml), Methanol (2 × 1 l), Tetrahydrofuran (2 × 1 l) und Methanol (1 × 1 l) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 500 ml) gewaschen und im Vakuum (25°C, 36 h) zum Erhalt eines fast farblosen Harzes getrocknet (240,0 g). Ein Teil des so erhaltenen Harzes (115,1 g, 92 mmol) wurden in trockenem Tetrahydrofuran (1,6 l) suspendiert, und η6-1,2-Dichlorbenzol-η5-cyclopentadienyleisen(II)-hexafluorophosphat (76,0 g, 184 mmol) wurde hinzugegeben, gefolgt von Kaliumcarbonat (50,9 g, 368 mmol). Die Reaktionsmischung wurde für 16 h bei 60°C gerührt. Nach Abkühlen auf Raumtemperatur wurde das Harz abfiltriert und mit Tetrahydrofuran (2 × 500 ml), Wasser (2 × 250 ml), Tetrahydrofuran (2 × 500 ml), Wasser (2 × 250 ml), Methanol (2 × 250 ml), Dichlormethan (2 × 500 ml) und Methanol (2 × 250 ml) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 500 ml) gewaschen und im Vakuum getrocknet (25°C, 36 h), um ein dunkel-orangefarbenes Harz (142 g) zu liefern.
- Zu einer Lösung aus 2-Hydroxyanisol (2,2 g, 17,7 mmol) in Tetrahydrofuran (50 ml) wurde vorsichtig unverdünntes Natriumhydrid (15,5 ml) bei Raumtemperatur gegeben (Vorsicht: Erzeugung von Wasserstoff). Die Mischung wurde weitere 30 min gerührt, nachdem die Entwicklung von Wasserstoff aufgehört hatte. Anschließend wurde ein Teil des oben erhaltenen Harzes (2,8 g, 1,72 mmol) hinzugegeben, und die Mischung wurde für 12 h bei 40°C gerührt. Nach Abkühlen auf Raumtemperatur wurde das Harz abfiltriert und mit Tetrahydrofuran (2 × 50 ml), Tetrahydrofuran/Wasser (1:1) (2 × 50 ml), N,N-Dimethylformamid (2 × 50 ml), Wasser (2 × 50 ml), Methanol (3 × 50 ml) und Tetrahydrofuran (3 × 50 ml) und anschließend mit Methanol und Tetrahydrofuran (jeweils 50 ml, 5 Durchläufe) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 50 ml) gewaschen und im Vakuum getrocknet (25°C, 12 h).
- Das so erhaltene Harz (3,0 g, 1,84 mmol) und eine 0,5 M Lösung von 1,10-Phenanthrolin in einer 3:1-Mischung aus Pyridin/Wasser (20 ml) wurde in ein lichtdurchlässiges Reagenzglas gegeben. Zum Entkomplexieren wurde die Suspension verwirbelt und mit sichtbarem Licht für 12 h bestrahlt. Ein sehr charakteristisches Merkmal des Schrittes zum Entkomplexieren ist das Erscheinen der intensiven roten Farbe der flüssigen Phase während der Bestrahlung. Das Harz wurde abfiltriert und mit Methanol (2 × 25 ml), Wasser (2 × 25 ml) und Tetrahydrofuran (3 × 25 ml) gewaschen, bis die Waschlösungen farblos blieben (5 Durchläufe), und das Bestrahlungsverfahren wurde wiederholt, bis das Entkomplexieren vollständig war (5 Durchläufe). Nach vollständigem Entkomplexieren wurde das Harz mit Dichlormethan (3 × 25 ml) gewaschen und im Vakuum getrocknet (25°C, 12 h).
- Das Harz (ca. 2,5 g, 1,84 mmol) wurde in einer 1:1-Mischung aus Trifluoressigsäure und Dichlormethan (25 ml) suspendiert und bei Raumtemperatur für 2 h gerührt. Das Harz wurde abfiltriert und mit Methanol (1 × 5 ml) und Dichlormethan (1 × 5 ml) gewaschen. Die flüssigen Phasen wurden vereinigt, und die flüchtigen Lösungsmittel wurden unter Erhalt eines dunkelbraunen Öls (1,5 g) verdampft.
- Das Öl wurde in Acetonitril (10 ml) gelöst. Zur so erhaltenen Lösung wurden Kaliumcarbonat (46 mg, 0,33 mmol) und 3-(3-Brompropyl)-1H-indol (33 mg, 0,14 mmol) gegeben, und die Mischung wurde für 12 h auf 80°C erwärmt. Isocyanomethylpolystyrol (250 mg, 0,29 mmol) wurde hinzugegeben, und die Mischung wurde langsam auf Raumtemperatur abgekühlt. Das Harz wurde abfiltriert und mit Methanol (1 × 2 ml) und Dichlormethan (1 × 2 ml) gewaschen. Die kombinierten flüssigen Phasen wurden von den flüchtigen Lösungsmitteln abgedampft, um ein dunkelbraunes Öl zu liefern. Das Rohprodukt wurde durch präparative Umkehrphasen-HPLC-Chromatographie gereinigt. Die resultierende Lösung wurde anschließend auf eine vorkonditionierte Ionenaustauschsäule aufgetragen. Die Säule wurde mit Methanol (4 ml) und Acetonitril (4 ml) gewaschen, gefolgt von Elution des Rohprodukts mit einer 4N-Lösung von Ammoniak in Methanol (4,5 ml). Verdampfen der flüchtigen Lösungsmittel liefert die Titelverbindung 3a als gelbes Öl (66 mg).
LC/MS (m/z): 442 (MH+), Rt = 4,15, Reinheit: 93%. - Die folgenden Verbindungen wurden analog hergestellt:
- 1-(2-Phenoxyphenyl)-4-[4-(1H-indol-3-yl)butyl]piperazin (3b):
-
- LC/MS (m/z): 426 (MH+), Rt = 4,36, Reinheit: 79%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin (3c)
-
- LC/MS (m/z): 470 (MH+), Rt = 2,62, Reinheit: 89%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin (3d):
-
- LC/MS (m/z): 462 (MH+), Rt = 4,35, Reinheit: 76%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin (3e):
-
- LC/MS (m/z): 476 (MH+), Rt = 2,64, Reinheit: 89%.
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin (3f):
-
- LC/MS (m/z): 475 (MH+), Rt = 2,32, Reinheit: 91%.
- 1[(2-(2-Methoxyphenoxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin (3g):
-
- LC/MS (m/z): 456 (MH+), Rt = 4,31, Reinheit: 90%.
- 1-[2-(4-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin (3h):
-
- LC/MS (m/z): 442 (MH+), Rt = 4,18, Reinheit: 90%.
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[4-(1H-indol-3-yl)butyl]piperazin (3i):
-
- LC/MS (m/z): 469 (MH+), Rt = 2,27, Reinheit: 88%.
- 1-(2-Phenoxyphenyl)-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin (3j):
-
- LC/MS (m/z): 432 (MH+), Rt = 4,40, Reinheit: 70%.
- Beispiel 4
- 2-(4-Chlorbutyl)-1,3-dioxolan-4-ylmethoxymethylpolystyrol (4a)
- Ein 2 l-Rundkolben wurde mit 2,2-Dimethyl-1,3-dioxolan-4-ylmethoxymethylpolystyrol gefüllt (90 g, 72 mmol, kommerziell erhältlich als (±)-1-(2,3-Isopropyliden)glycerolpolystyrol von Calbiochem-Novabiochem, Kat.-Nr. 01-64-0291). Toluol (900 ml), gefolgt von p-Toluolsulfonsäuremonohydrat (5,0 g, 26 mmol), Natriumsulfat (25 g) und 5-Chlorpentanal (25,5 g, 211 mmol) wurden hinzugegeben, und die Mischung wurde unter Rückfluß für 12 h gekocht. Der Rückflußkondensator wurde gegen eine Dean-Stark-Vorrichtung ausgetauscht, und die Mischung wurde unter Rückfluß für weitere 3 h gekocht. Nach Abkühlen der Reaktionsmischung auf 60°C wurde das Harz abfiltriert und mit Toluol (200 ml), Tetrahydrofuran/Pyridin (1:1, 200 ml), Tetrahydrofuran/Wasser/Pyridin (10:10:1, 200 ml), Methanol (200 ml), Wasser (200 ml), Tetrahydrofuran (200 ml), Dichlormethan (200 ml), Methanol (3 × 200 ml) und Dichlormethan (3 × 200 ml) gewaschen. Das Harz wurde im Vakuum getrocknet (55°C, 12 h), um die Titelverbindung 4a zu liefern (97 g).
- Die folgenden Verbindungen wurden analog hergestellt:
- 2-(3-Chlorpropyl)-1,3-dioxolan-4-ylmethoxymethylpolystyrol (4b)
- 2-(5-Chlorpentyl)-1,3-dioxolan-4-ylmethoxymethylpolystyrol (4c)
- Beispiel 5
- 1-(2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5a)
- 2-(3-Chlorbutyl)-1,3-dioxolan-4-ylmethoxymethylpolystyrol (70 g, 90,3 mmol) wurde in trockenem N,N-Dimethylformamid (700 ml) suspendiert.
- Natriumiodid (68 g, 452 mmol) wurde hinzugegeben, gefolgt Diisopropylethylamin (232 ml, 1,36 mol) und Piperazin (117 g, 1,36 mol). Die Reaktionsmischung wurde unter Rühren für 12 h auf 80°C erwärmt. Nach Abkühlen auf Raumtemperatur wurde das Harz abfiltriert und mit N,N-Dimethylformamid (3 × 500 ml), Methanol (3 × 500 ml) und Tetrahydrofuran (3 × 500 ml) und anschließend mit Methanol und Tetrahydrofuran (jeweils 250 ml, 5 Durchläufe) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 500 ml) gewaschen und im Vakuum getrocknet (25°C, 36 h), um ein fast farbloses Harz zu liefern (76 g).
- Ein Teil des erhaltenen Harzes (50 g, 60,6 mmol) wurde dann in trockenem Tetrahydrofuran (600 ml) suspendiert. η6-1,2-Dichlorbenzol-η5-cyclopentadienyleisen(II)-hexafluorophosphat (48 g, 116,2 mmol) wurde hinzugegeben, gefolgt von Kaliumcarbonat (32 g, 233 mmol). Die Reaktionsmischung wurde für 12 h bei 60°C gerührt. Nach Abkühlen auf Raumtemperatur wurde das Harz abfiltriert und mit Tetrahydrofuran (2 × 500 ml), Wasser (2 × 250 ml), Tetrahydrofuran (2 × 500 ml), Methanol (2 × 250 ml), Dichlormethan (2 × 500 ml) und Methanol (2 × 250 ml) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 500 ml) gewaschen und im Vakuum getrocknet (25°C, 36 h), um ein dunkel-orangefarbenes Harz zu liefern (70 g).
- Zu einer Lösung aus 5-Hydroxy-1,4-benzodioxan (2,8 g, 18,4 mmol) in Tetrahydrofuran (50 ml) wurde vorsichtig unverdünntes Natriumhydrid (15,5 mmol) bei Raumtemperatur gegeben (Vorsicht: Erzeugung von Wasserstoff). Die Mischung wurde für weitere 30 min gerührt, nachdem die Wasserstofferzeugung aufgehört hatte. Anschließend wurde ein Teil des oben erhaltenen Harzes (2,8 g, 2,3 mmol) hinzugegeben, und die Mischung wurde für 12 h bei 40°C gerührt. Nach Abkühlen auf Raumtemperatur wurde das Harz abfiltriert und mit Tetrahydrofuran (2 × 50 ml), Tetrahydrofuran/Wasser (1:1) (2 × 50 ml), N,N-Dimethylformamid (2 × 50 ml), Wasser (2 × 50 ml), Methanol (3 × 50 ml) und Tetrahydrofuran (3 × 50 ml) und anschließend mit Methanol und Tetrahydrofuran (jeweils 50 ml, 5 Durchläufe) gewaschen. Schließlich wurde das Harz mit Dichlormethan (3 × 50 ml) gewaschen und im Vakuum getrocknet (25°C, 12 h).
- Ein Teil des erhaltenen Harzes (200 mg, 0,15 mmol) und eine 0,5 M-Lösung von 1,10-Phenanthrolin in einer (3:1)-Mischung aus Pyridin/Wasser (10 ml) wurde in ein lichtdurchlässiges Reagenzglas gegeben. Die Suspension wurde verwirbelt und für 12 h bestrahlt. Ein sehr charakteristisches Merkmal des Entkomplexierungsschrittes ist das Erscheinen der intensiven roten Farbe der flüssigen Phase während der Bestrahlung. Das Harz wurde ab filtriert und mit Methanol (2 × 10 ml), Wasser (2 × 10 ml) und Tetrahydrofuran (3 × 10 ml) gewaschen, bis die Waschlösungen farblos blieben (ca. 5 Durchläufe), und das Bestrahlungsverfahren wurde wiederholt, bis die Entkomplexierung vollständig war (ca. 4 Durchläufe). Nach dem vollständigen Entkomplexieren wurde das Harz mit Dichlormethan (3 × 10 ml) gewaschen und im Vakuum getrocknet (25°C, 12 h).
- Das erhaltene Harz (160 mg, 0,15 mmol) und 4-Fluorphenylhydrazinhydrochlorid (35 mg, 0,21 mmol) wurden in einem Reagenzglas vermischt. Eine 0,5 M Lösung von wasserfreiem Zinkchlorid in Essigsäure (1,5 ml) wurde hinzugegeben, und das Reagenzglas wurde versiegelt. Die Reaktionsmischung wurde für 12 h bei 70°C gerührt. Nach Abkühlen auf Raumtemperatur wurde die Reaktionsmischung filtriert und das zurückbleibende Harz mit Dimethylsulfoxid (1,5 ml) gewaschen. Gesättigte wäßrige Natriumcarbonat-Lösung (1,5 ml) wurde vorsichtig zu den kombinierten Filtraten hinzugegeben (Vorsicht: Erzeugung von Kohlendioxid). Die Lösung wurde auf eine vorkonditionierte Umkehrphasen-C-18-Säule aufgetragen. Die Säule wurde mit Wasser (4 ml) gewaschen, und das Produkt wurde mit Methanol (4,5 ml) eluiert. Nach Verdampfen der flüchtigen Lösungsmittel wurde das Rohprodukt durch präparative Umkehrphasen-HPLC-Chromatographie gereinigt. Die resultierende Lösung wurde anschließend auf eine vorkonditionierte Ionenaustauschsäule aufgetragen. Die Säule wurde mit Methanol (4 ml) und Acetonitril (4 ml) gewaschen, gefolgt von Elution des Produkts mit einer 4 N Ammoniak-Lösung in Methanol (4,5 ml). Verdampfen der flüchtigen Lösungsmittel lieferte die Titelverbindung 5a als gelbes Öl (2 mg).
- LC/MS (m/z): 488 (MH+), Rt = 4,22, Reinheit: 84%.
- Die folgenden Verbindungen wurden analog hergestellt:
- 1-(2-Phenoxyphenyl)-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5b):
-
- LC/MS (m/z): 426 (MH+), Rt = 4,44, Reinheit: 88%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5c):
-
- LC/MS (m/z): 476 (MH+), Rt = 4,46, Reinheit: 95%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin (5d):
-
- LC/MS (m/z): 522 (MH+), Rt = 4,52, Reinheit: 91%.
- 1-(2-Phenoxyphenyl)-4-[3-(1H-indol-3-yl)propyl]piperazin (5e):
-
- LC/MS (m/z): 412 (MH+), Rt = 4,25, Reinheit: 98%.
- 1-(2-Phenoxyphenyl)-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5f):
-
- LC/MS (m/z): 430 (MH+), Rt = 4,32, Reinheit: 96%.
- 1-(2-Phenoxyphenyl)-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin (5g):
-
- LC/MS (m/z): 492 (MH+), Rt = 4,60, Reinheit: 84%.
- 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin (5h):
-
- LC/MS (m/z): 552 (MH+), Rt = 4,49, Reinheit: 86%.
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5i):
-
- LC/MS (m/z): 469 (MH+), Rt = 3,73, Reinheit: 86%.
- 1-(2-Phenoxyphenyl)-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5j)
-
- LC/MS (m/z): 446 (MH+), Rt = 4,52, Reinheit: 88%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5k):
-
- LC/MS (m/z): 470 (MH+), Rt = 4,38, Reinheit: 70%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5l)
-
- LC/MS (m/z): 460 (MH+), Rt = 4,24, Reinheit: 87%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin (5m)
-
- LC/MS (m/z): 476 (MH+), Rt = 4,42, Reinheit: 96%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5n):
-
- LC/MS (m/z): 474 (MH+), Rt = 4,25, Reinheit: 99%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin (5o):
-
- LC/MS (m/z): 582 (MH+), Rt = 4,58, Reinheit: 85%.
- 1-(2-Phenoxyphenyl)-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin (5p):
-
- LC/MS (m/z): 430 (MH+), Rt = 4,3%, Reinheit: 87%.
- 1-(2-Phenoxyphenyl)-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin (5q):
-
- LC/MS (m/z): 448 (MH+), Rt = 4,44, Reinheit: 84%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin (5r):
-
- LC/MS (m/z): 520 (MH+), Rt = 4,50, Reinheit: 77%.
- 1-{2-[3-(Dimethylamino)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5s):
-
- LC/MS (m/z): 473 (MH+), Rt = 3,63, Reinheit: 96%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin (5t):
-
- LC/MS (m/z): 568 (MH+), Rt = 4,63, Reinheit: 82%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5u):
-
- LC/MS (m/z): 490 (MH+), Rt = 4,45, Reinheit: 90%.
- 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5v):
-
- LC/MS (m/z): 506 (MH+), Rt = 4,46, Reinheit: 83%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin (5w):
-
- LC/MS (m/z): 507 (MH+), Rt = 3,30, Reinheit: 97%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin (5x):
-
- LC/MS (m/z): 478 (MH+), Rt = 4,36, Reinheit: 75%.
- 1-(2-Phenoxyphenyl)-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin (5y):
-
- LC/MS (m/z): 5,38 (MH+), Rt = 4,69, Reinheit: 92%.
- 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin (5z):
-
- LC/MS (m/z): 493,2 (MH+), Rt = 3,29, Reinheit: 96%.
- 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin (5aa):
-
- LC/MS (m/z): 493 (MH+), Rt = 3,38, Reinheit: 96%.
- 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5ab):
-
- LC/MS (m/z): 484 (MH+), Rt = 4,35, Reinheit: 84%.
- 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5ac):
-
- LC/MS (m/z): 486 (MH+), Rt = 4,38, Reinheit: 80%.
- 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin (5ad):
-
- LC/MS (m/z): 442 (MH+), Rt = 4,25, Reinheit: 85%.
- 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin (5ae):
-
- LC/MS (m/z): 471 (MH+), Rt = 4,13, Reinheit: 83%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-Brom-1H-indol-3-yl)propyl]piperazin (5af):
-
- LC/MS (m/z): 536 (MH+), Rt = 4,49, Reinheit: 88%.
- 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5ag):
-
- LC/MS (m/z): 515 (MH+), Rt = 4,17, Reinheit: 94%.
- 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5ah):
-
- LC/MS (m/z): 476 (MH+), Rt = 4,53, Reinheit: 92%.
- 1-[2-(3-Ethoxyphenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin (5ai):
-
- LC/MS (m/z): 470 (MH+), Rt = 4,68, Reinheit: 85%.
- 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin (5aj):
-
- LC/MS (m/z): 598 (MH+), Rt = 4,61, Reinheit: 70%.
- 1-{2-[3-(Diethylamino)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5ak):
-
- LC/MS (m/z): 501 (MH+), Rt = 3,18, Reinheit: 87%.
- 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin (5al):
-
- LC/MS (m/z): 490 (MH+), Rt = 4,26, Reinheit: 88%.
- 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin (5am):
-
- LC/MS (m/z): 475 (MH+), Rt = 4,42, Reinheit: 78%.
- 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin (5an):
-
- LC/MS (m/z): 531 (MH+), Rt = 4,34, Reinheit: 81%.
- 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin (5ao):
-
- LC/MS (m/z): 623 (MH+), Rt = 4,56, Reinheit: 71%.
- 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(7-fluor-1H-indol-3-yl)propyl]piperazin (5aq):
-
- LC/MS (m/z): 460 (MH+), Rt = 4,38, Reinheit: 70%.
- 1-(2-Phenoxyphenyl)-4-[3-(5,7-dimethyl-1H-indol-3-yl)propyl]piperazin (5ar):
-
- LC/MS (m/z): 440 (MH+), Rt = 4,64, Reinheit: 78%.
- 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin (5as):
-
- LC/MS (m/z): 534 (MH+), Rt = 4,46, Reinheit: 75%.
- 1-[2-(3,4,5-Trimethoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin (5at):
-
- LC/MS (m/z): 580 (MH+), Rt = 4,34, Reinheit: 81%.
- Pharmakologische Untersuchung
- Die Verbindungen der Erfindung wurden in allgemein anerkannten und verläßlichen Verfahren untersucht. Die Untersuchungen waren wie folgt:
- Inhibierung der Bindung von 3H-YM-09151-2 an humane Dopamin-D4-Rezeptoren
- Durch dieses Verfahren wird die Inhibierung der Bindung von [3H]YM-09151-2 (0,06 nM) an Membranen von humanen klonierten Dopamin D4.2-Rezeptoren, exprimiert in CHO-Zellen, durch Wirkstoffe in vitro bestimmt. Verfahren modifiziert aus NEN Life Science Products, Inc., technisches Datenzertifikat PC2533-10/96. Die Ergebnisse sind in der folgenden Tabelle 1 als IC50-Werte angegeben.
- Inhibierung der Bindung von [3H]-Spiperon an humane D3-Rezeptoren
- Durch dieses Verfahren wird die Inhibierung der Bindung von [3H]-Spiperon (0,3 nM) an Membranen von humanen klonierten Dopamin D3-Rezeptoren, exprimiert in CHO-Zellen, durch Wirkstoffe in vitro bestimmt. Verfahren modifiziert aus R.G. MacKenzie et al., Eur. J. Pharm.-Mol. Pharm. Sec., 1994, 266, 79–85. Die Ergebnisse sind in der folgenden Tabelle 1 als IC50-Werte angegeben.
- Die Affinität der Verbindungen der Erfindung zu 5-HT1A-Rezeptoren wurde durch Messung der Inhibierung der Bindung eines radioaktiven Liganden an 5-HT1A-Rezeptoren wie im folgenden Test beschrieben bestimmt:
- Inhibierung der 3H-5-CT-Bindung an humane 5-HT1A-Rezeptoren
- Durch dieses Verfahren wird die Inhibierung der Bindung des 5-HT1A-Agonisten 3H-5-Carboxamidotryptamin (3H-5-CT) an klonierte humane 5-HT1A-Rezeptoren, die stabil in transfizierten HeLa-Zellen (HA7) exprimiert werden (A. Fargin et al., J. Biol. Chem., 1989, 264, 14848), durch Wirkstoffe in vitro bestimmt. Der Test wurde als Modifikation des von M.A. Harrington et al. beschriebenen Verfahrens durchgeführt, J. Pharmcol. Exp. Ther., 1994, 268, 1098. Humane 5-HT1A-Rezeptoren (40 μg Zellhomogenat) wurden für 15 Minuten bei 37°C in 50 mM Tris-Puffer bei pH 7,7 in Gegenwart von 3H-5-CT inkubiert. Die nicht-spezifische Bindung wurde durch Einschließen von 10 μM Metergolin bestimmt. Die Reaktion wurde durch schnelle Filtration durch Unifilter GF/B-Filter an einem Tomtec Cell Harvester beendet. Die Filter wurden in einem Packard Top Counter gezählt. Die erhaltenen Ergebnisse sind nachfolgend in Tabelle 1 dargestellt.
- Inhibierung der 3H-5-HT-Aufnahme in Synaptosomen aus Rattenhirn
- Unter Verwendung dieses Verfahren wird die Fähigkeit von Wirkstoffen zur Hemmung der Akkumulierung von 3H-5-HT in Synaptosomen aus Rattenvollhirn in vitro bestimmt. Der Test wurde wie von J. Hyttel beschrieben durchgeführt, J. Psychopharmacology 1978, 60, 13. Die erhaltenen Ergebnisse sind in Tabelle 1 dargestellt: Tabelle 1:
- Entsprechend zeigen die Verbindungen der Erfindung Affinitäten in den beschriebenen Untersuchungen, sie werden als nützlich erachtet in der Behandlung von affektiven Störungen, wie Depression, allgemeine Angststörung, Panikstörung, Zwangsstörungen, Sozialphobie und Eßstörungen, Psychose und neurologischen Störungen wie Ischämie und Altersdemenz.
Claims (12)
- Verbindung, die durch die allgemeine Formel (I) dargestellt wird: worin Z NH, NR''', O oder S darstellt; R''' Wasserstoff oder C1-6-Alkyl darstellt; R7 und R8 unabhängig Wasserstoff, Halogen, C1-6-Alkyl, C3-8-Cycloalkyl, CN, CF3 oder C1-6-Alkoxy darstellen; oder R7 und R8 zusammen einen an den Benzol-Ring kondensierten 5- oder 6-gliedrigen Aryl- oder Heteroaryl-Ring bilden; Y N, C oder CH darstellt; die gestrichelte Linie eine optionale Bindung darstellt; R6 und R6' H oder C1-6-Alkyl darstellen; X -O- oder -S- darstellt; n 2, 3, 4 oder 5 ist; m 2 oder 3 ist; R1, R2, R3, R4 und R5 unabhängig aus einer Gruppe ausgewählt sind, die aus Wasserstoff, Halogen, C1-6-Alkyl, C2-6-Alkenyl, C2-6-Alkinyl, C3-8-Cycloalkyl, Aryl, Hydroxy, Hydroxy-C1-6-alkyl, C1-6-Alkoxy, C3-8-Cycloalkoxy, C1-6-Alkylsulfanyl, Acyl und NR9R10 besteht, worin R9 und R10 unabhängig Wasserstoff, C1-6-Alkyl, C2-6-Alkenyl, C2-6-Alkinyl, C3-8-Cycloalkyl oder Aryl darstellen; oder R9 und R10 zusammen mit dem Stickstoff, an den sie gebunden sind, einen 1-Morpholinyl-, 1-Piperidinyl-, 1-Homopiperidinyl-, 1-Piperazinyl-, 1-Homopiperazinyl-, 1-Imidazolyl-, 1-Pyrrolyl- oder Pyrazolyl-Ring bilden, von denen alle weiter mit C1-6-Alkyl substituiert sein können; oder zwei benachbarte Substituenten aus R1–R5 zusammen einen an den Phenyl-Ring kondensierten Ring bilden, der aus der Gruppe ausgewählt ist, die aus besteht, worin W O oder S ist und R' und R'' Wasserstoff oder C1-6-Alkyl sind.
- Verbindung gemäß Anspruch 1, worin Z NH ist und der Aryl-Ring in Position 3 gebunden ist.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin R7 und R8 unabhängig aus Wasserstoff, Halogen und C1-6-Alkyl ausgewählt sind oder R7 und R8 zusammen einen kondensierten Pyridyl-Ring bilden.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin n 2, 3 oder 4 ist.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin m 2 ist.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin R6 und R6' beide Wasserstoff sind.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin Y N ist.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin R1, R2, R3, R4 und R5 unabhängig aus Wasserstoff, Alkoxy und NR9R10 ausgewählt sind, worin R9 und R10 unabhängig Wasserstoff oder C1-6-Alkyl darstellen; oder R9 und R10 zusammen einen 1-Morpholino-Ring bilden; oder zwei benachbarte Vertreter aus R1, R2, R3, R4 und R5 zusammen einen kondensierten Ring bilden, der aus -O-CH2-O-, -O-CH2-CH2-O- oder -CH2-CH2-CH2- besteht.
- Verbindung gemäß einem der vorhergehenden Ansprüche, worin ein oder zwei Vertreter aus R1, R2, R3, R4 und R5 nicht Wasserstoff sind.
- Verbindung gemäß einem der vorhergehenden Ansprüche, wobei die Verbindung eine der folgenden ist: 1-{1-[3-(Dimethylamino)phenoxy]phenyl}-4-[2-(1H-indol-3-yl)ethyl]piperazin; 1-[1-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(1H-indol-3-yl)ethyl]piperazin; 1-{1-[3-(Dimethylamino)phenoxy]phenyl}-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[1-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-b-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-b-yloxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(6-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[4-(1H-indol-3-yl}butyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin; 1-(2-(2-Methoxyphenoxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin; 1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin; 1-[2-(4-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[4-(1H-indol-3-yl)butyl]piperazin; 1-(2-Phenoxyphenyl)-4-[2-(6-chlor-1H-indol-3-yl)ethyl]piperazin; 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(7-chlor-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-(Dimethylamino)phenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(5,7-difluor-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin; 1-[2-(2-Methoxyphenoxy)phenyl]-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin; 1-[2-(3-Methoxyphenoxy)phenyl)-4-[3-(1H-pyrrolo[3,2-h]chinolin-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3=(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[2-(1,4-Benzodioxan-5-yloxy)phenyl]-4-[3-(1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin; 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-Methoxyphenoxy)phenyl]-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-Ethoxyphenoxy)phenyl]-4-[3-(5-methyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin; 1-[2-(3-(Diethylamino)phenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-[2-(2,6-Dimethoxyphenoxy)phenyl]-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-fluor-1H-indol-3-yl)propyl]piperazin; 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-chlor-1H-indol-3-yl)propyl]piperazin; 1-{2-[3-(Morpholin-4-yl)phenoxy]phenyl}-4-[3-(5-iod-1H-indol-3-yl)propyl]piperazin; 1-(2-(3-Methoxyphenoxy)phenyl]-4-[3-(7-fluor-1H-indol-3-yl)propyl]piperazin; 1-(2-Phenoxyphenyl)-4-[3-(5,7-dimethyl-1H-indol-3-yl)propyl]piperazin; 1-[2-(1,3-Benzodioxolan-5-yloxy)phenyl]-4-[3-(7-brom-1H-indol-3-yl)propyl]piperazin; oder 1-[2-(3,4,5-Trimethoxyphenoxy)phenyl]-4-[3-(5-brom-1H-indol-3-yl)propyl]piperazin.
- Pharmazeutische Zusammensetzung, die wenigstens eine Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 10 oder ein pharmazeutisch akzeptables Säureadditionssalz davon in einer therapeutisch wirksamen Menge und in Kombination mit einem oder mehreren pharmazeutisch akzeptablen Trägern oder Verdünnungsmitteln umfaßt.
- Verwendung einer Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 10 oder eines Säureadditionssalzes davon zur Herstellung einer pharmazeutischen Zubereitung zur Behandlung von Depression, Psychose, allgemeiner Angststörung, Panikstörung, Zwangsstörung, Störung der Impulskontrolle, Alkoholmißbrauch, Aggression, Ischämie, Altersdemenz, Sozialphobie oder Eßstörung.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DKPA199901885 | 1999-12-30 | ||
| DK188599 | 1999-12-30 | ||
| PCT/DK2000/000721 WO2001049678A1 (en) | 1999-12-30 | 2000-12-20 | Substituted phenyl-piperazine derivatives, their preparation and use |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60009155D1 DE60009155D1 (de) | 2004-04-22 |
| DE60009155T2 true DE60009155T2 (de) | 2005-01-05 |
Family
ID=8108803
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60009155T Expired - Fee Related DE60009155T2 (de) | 1999-12-30 | 2000-12-20 | Substituierte phenyl-piperazin-derivate, deren herstellung und verwendung |
Country Status (28)
| Country | Link |
|---|---|
| US (1) | US6699864B2 (de) |
| EP (1) | EP1246816B1 (de) |
| JP (1) | JP2003519224A (de) |
| KR (1) | KR100790916B1 (de) |
| CN (1) | CN1230432C (de) |
| AR (1) | AR029428A1 (de) |
| AT (1) | ATE261959T1 (de) |
| AU (1) | AU2152101A (de) |
| BG (1) | BG65262B1 (de) |
| BR (1) | BR0016952A (de) |
| CA (1) | CA2395705C (de) |
| CZ (1) | CZ20022319A3 (de) |
| DE (1) | DE60009155T2 (de) |
| EA (1) | EA006071B1 (de) |
| ES (1) | ES2213634T3 (de) |
| HU (1) | HUP0203722A3 (de) |
| IL (2) | IL150241A0 (de) |
| IS (1) | IS2174B (de) |
| MX (1) | MXPA02006223A (de) |
| NO (1) | NO322666B1 (de) |
| NZ (1) | NZ519647A (de) |
| PL (1) | PL199351B1 (de) |
| PT (1) | PT1246816E (de) |
| SK (1) | SK9442002A3 (de) |
| TR (2) | TR200400645T4 (de) |
| UA (1) | UA72948C2 (de) |
| WO (1) | WO2001049678A1 (de) |
| ZA (1) | ZA200204814B (de) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA81749C2 (uk) | 2001-10-04 | 2008-02-11 | Х. Луннбек А/С | Фенілпіперазинові похідні як інгібітори зворотного захоплення серотоніну |
| DE10259244A1 (de) * | 2002-12-17 | 2004-07-01 | Merck Patent Gmbh | N-(Indolethyl-)cycloamin-Verbindungen |
| UA81300C2 (en) * | 2003-04-04 | 2007-12-25 | Lundbeck & Co As H | Derivates of 4-(2-fenilsulfanilfenil)-1,2,3,6-tetrahydropiridin as retarding agents of serotonin recapture |
| AU2004226838B8 (en) | 2003-04-04 | 2009-06-11 | H. Lundbeck A/S | 4-(2-phenylsulfanyl-phenyl)-piperidine derivatives as serotonin reuptake inhibitors |
| DE602004014190D1 (de) | 2003-12-23 | 2008-07-10 | Lundbeck As Valby H | 2-(1h-indolylsulfanyl)-benzylaminderivate als ssri |
| SE0400441D0 (sv) | 2004-02-25 | 2004-02-25 | Active Biotech Ab | Novel Benzofurans and Indols |
| AR052308A1 (es) | 2004-07-16 | 2007-03-14 | Lundbeck & Co As H | Derivados de 2-(1h-indolilsulfanil)-arilamina y una composicion farmaceutica que contiene al compuesto |
| AR054393A1 (es) | 2005-06-17 | 2007-06-20 | Lundbeck & Co As H | Derivados de benzo(b)furano y benzo(b)tiofeno, composiciones farmaceuticas que los contienen y su uso en la fabricacion de un medicamento para el tratamiento de enfermedades mediadas por la inhibicion de la reabsorcion de neurotransmisores de amina biogenicos. |
| US7629473B2 (en) | 2005-06-17 | 2009-12-08 | H. Lundbeck A/S | 2-(1H-indolylsulfanyl)-aryl amine derivatives |
| WO2007144005A1 (en) | 2006-06-16 | 2007-12-21 | H. Lundbeck A/S | 1- [2- (2, 4-dimethylphenylsulfanyl) -phenyl] piperazine as a compound with combined serotonin reuptake, 5-ht3 and 5-ht1a activity for the treatment of cognitive impairment |
| EP2209380A4 (de) * | 2007-10-09 | 2011-09-14 | Mark T Hamann | Verfahren zur verwendung von zusammensetzungen mit antidepressiver wirksamkeit, stimmungsaufhellender wirksamkeit und sonstiger neurologischer wirksamkeit und diesbezügliche zusammensetzungen |
| EA201001425A1 (ru) * | 2008-03-14 | 2011-06-30 | Мерк Патент Гмбх | Азаиндольные соединения для лечения заболеваний центральной нервной системы |
| SI2981520T1 (sl) * | 2013-04-04 | 2019-07-31 | Lek Pharmaceuticals D.D. | Novi proces za sintezo 1-(2-((2,4-dimetilfenil)tio)fenil)piperazina |
| CN105085482B (zh) * | 2014-05-04 | 2018-08-10 | 广东东阳光药业有限公司 | 取代的哌嗪化合物及其使用方法和用途 |
| CN105085491B (zh) * | 2014-05-05 | 2019-06-25 | 广东东阳光药业有限公司 | 取代的吲哚化合物及其使用方法和用途 |
| US10316025B2 (en) | 2015-06-03 | 2019-06-11 | Sunshine Lake Pharma Co., Ltd. | Substituted piperazine compounds and methods of use and use thereof |
| CN106795160B (zh) * | 2015-07-23 | 2019-04-19 | 广东东阳光药业有限公司 | 取代的吲哚化合物及其使用方法和用途 |
| AU2018340376B2 (en) * | 2017-09-29 | 2022-09-01 | Sunshine Lake Pharma Co., Ltd. | Substituted pyrimidine piperazine compound and use thereof |
| CN111518012A (zh) * | 2020-05-27 | 2020-08-11 | 中国药科大学 | 含苯硫醚结构的化合物或其药学上可接受的盐、制备方法和用途 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2138865A1 (de) * | 1970-08-15 | 1973-02-22 | Sumitomo Chemical Co | 3-indolylpiperazine, verfahren zu ihrer herstellung und arzneimittel |
| GB8830312D0 (en) * | 1988-12-28 | 1989-02-22 | Lundbeck & Co As H | Heterocyclic compounds |
| AU6435594A (en) * | 1993-04-15 | 1994-11-08 | Merck Sharp & Dohme Limited | Indole derivatives as dopamine d4 antagonists |
| FR2712591B1 (fr) * | 1993-11-19 | 1996-02-09 | Pf Medicament | Nouvelles arylpipérazines dérivées d'indole, leur préparation et leur utilisation thérapeutique. |
| WO1997019039A1 (en) | 1995-11-17 | 1997-05-29 | Novartis Ag | Solid phase synthesis of heterocyclic compounds and combinatorial compound library |
| USH2007H1 (en) * | 1996-01-19 | 2001-12-04 | Fmc Corporation | Insecticidal N-heterocyclylalkyl-or N-[(polycyclyl)alkyl]-N′substituted piperazines |
| ES2128266B1 (es) * | 1997-07-08 | 2000-01-16 | Vita Invest Sa | Compuestos derivados de tiofeno y benzotiofeno y utilizacion y composicion correspondientes. |
| AU5486600A (en) | 1999-06-15 | 2001-01-02 | Aventis Pharmaceuticals Products Inc. | Solid phase synthesis of n,n-disubstituted diazacycloalkylcarboxy derivatives |
| AU2351701A (en) * | 1999-12-30 | 2001-07-16 | H. Lundbeck A/S | A method for the preparation of substituted benzene derivatives |
-
2000
- 2000-12-20 AU AU21521/01A patent/AU2152101A/en not_active Abandoned
- 2000-12-20 MX MXPA02006223A patent/MXPA02006223A/es active IP Right Grant
- 2000-12-20 EA EA200200732A patent/EA006071B1/ru not_active IP Right Cessation
- 2000-12-20 TR TR2004/00645T patent/TR200400645T4/xx unknown
- 2000-12-20 PL PL355539A patent/PL199351B1/pl not_active IP Right Cessation
- 2000-12-20 PT PT00984924T patent/PT1246816E/pt unknown
- 2000-12-20 BR BR0016952-8A patent/BR0016952A/pt not_active Application Discontinuation
- 2000-12-20 CA CA002395705A patent/CA2395705C/en not_active Expired - Fee Related
- 2000-12-20 ES ES00984924T patent/ES2213634T3/es not_active Expired - Lifetime
- 2000-12-20 CZ CZ20022319A patent/CZ20022319A3/cs unknown
- 2000-12-20 KR KR1020027008608A patent/KR100790916B1/ko not_active Expired - Fee Related
- 2000-12-20 IL IL15024100A patent/IL150241A0/xx unknown
- 2000-12-20 AT AT00984924T patent/ATE261959T1/de not_active IP Right Cessation
- 2000-12-20 UA UA2002065260A patent/UA72948C2/uk unknown
- 2000-12-20 EP EP00984924A patent/EP1246816B1/de not_active Expired - Lifetime
- 2000-12-20 JP JP2001550218A patent/JP2003519224A/ja active Pending
- 2000-12-20 WO PCT/DK2000/000721 patent/WO2001049678A1/en not_active Ceased
- 2000-12-20 NZ NZ519647A patent/NZ519647A/en unknown
- 2000-12-20 TR TR2002/01683T patent/TR200201683T2/xx unknown
- 2000-12-20 DE DE60009155T patent/DE60009155T2/de not_active Expired - Fee Related
- 2000-12-20 SK SK944-2002A patent/SK9442002A3/sk unknown
- 2000-12-20 CN CNB008192057A patent/CN1230432C/zh not_active Expired - Fee Related
- 2000-12-20 HU HU0203722A patent/HUP0203722A3/hu unknown
- 2000-12-28 AR ARP000106987A patent/AR029428A1/es unknown
-
2002
- 2002-06-13 IS IS6420A patent/IS2174B/is unknown
- 2002-06-14 ZA ZA200204814A patent/ZA200204814B/xx unknown
- 2002-06-16 IL IL150241A patent/IL150241A/en not_active IP Right Cessation
- 2002-06-20 US US10/177,261 patent/US6699864B2/en not_active Expired - Fee Related
- 2002-06-28 NO NO20023146A patent/NO322666B1/no not_active IP Right Cessation
- 2002-07-17 BG BG106930A patent/BG65262B1/bg unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60009155T2 (de) | Substituierte phenyl-piperazin-derivate, deren herstellung und verwendung | |
| DE60225162T2 (de) | Phenylpiperazinderivate als serotonin wiederaufnahmehemmer | |
| DE69108461T2 (de) | 1-Indolylalkyl-4-(alkoxy-pyrimidinyl)piperazine. | |
| EP1246815B1 (de) | Phenylpiperazinyl-derivate | |
| DE60011817T2 (de) | 4-phenyl-1-piperazinyl, -piperidinyl und -tetrahydropyridyl-derivate | |
| DE3878371T2 (de) | Psychotropische bizyklische imide. | |
| DE68905845T2 (de) | Tetrazolverbindungen als antagonisten der excitatorischen aminosaeurerezeptoren. | |
| JPH11504921A (ja) | ニューロキニンアンタゴニストとしてのピペラジノ誘導体 | |
| DE69610793T2 (de) | 6-Subsitituierte-1,2,3,4-tetrahydro-9H-Carbazole und 7-substituierte-1OH-Cyclohepta(7,6-B)-Indole | |
| DE60130691T2 (de) | Indolderivate zur Behandlung von Erkrankungen des Zentralnervensystems | |
| DE3688397T2 (de) | 3-(2-aminoethyl)indol und -indolinderivate, verfahren zu ihrer herstellung und diese derivate enthaltende pharmazeutische zusammensetzungen. | |
| DE69501791T2 (de) | Indol-derivate als 5-ht1-like agonisten | |
| DE69614491T2 (de) | 5HT1Dalpha und 5HT2A Ligande | |
| DE60102471T2 (de) | Indolderivate zur verwendung in der behandlung von zns-störungen | |
| DE69724000T2 (de) | Indan- oder dihydroindol-derivate | |
| DE69609707T2 (de) | Phenoxyethylamin-derivate mit hoher affinität fur den 5-ht1a-rezeptor, verfahren zu ihrer herstellung, ihre verwendung als medikamente und sie enthaltende pharmazeutische zusammensetzungen | |
| DE69431441T2 (de) | Trizyklische verbindungen mit affinität für den 5-ht1a rezeptor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8339 | Ceased/non-payment of the annual fee |