WO2020067560A1 - 外用剤 - Google Patents
外用剤 Download PDFInfo
- Publication number
- WO2020067560A1 WO2020067560A1 PCT/JP2019/038448 JP2019038448W WO2020067560A1 WO 2020067560 A1 WO2020067560 A1 WO 2020067560A1 JP 2019038448 W JP2019038448 W JP 2019038448W WO 2020067560 A1 WO2020067560 A1 WO 2020067560A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- monomer
- component
- mass
- less
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/14—Methyl esters, e.g. methyl (meth)acrylate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
- A61K8/06—Emulsions
- A61K8/062—Oil-in-water emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/0241—Containing particulates characterized by their shape and/or structure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/34—Alcohols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/34—Alcohols
- A61K8/345—Alcohols containing more than one hydroxy group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/36—Carboxylic acids; Salts or anhydrides thereof
- A61K8/361—Carboxylic acids having more than seven carbon atoms in an unbroken chain; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/37—Esters of carboxylic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/39—Derivatives containing from 2 to 10 oxyalkylene groups
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/40—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing nitrogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
- A61K8/608—Derivatives containing from 2 to 10 oxyalkylene groups
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/81—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- A61K8/8105—Compositions of homopolymers or copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond; Compositions of derivatives of such polymers
- A61K8/8117—Homopolymers or copolymers of aromatic olefines, e.g. polystyrene; Compositions of derivatives of such polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/81—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- A61K8/8141—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides or nitriles thereof; Compositions of derivatives of such polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/81—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- A61K8/8141—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides or nitriles thereof; Compositions of derivatives of such polymers
- A61K8/8147—Homopolymers or copolymers of acids; Metal or ammonium salts thereof, e.g. crotonic acid, (meth)acrylic acid; Compositions of derivatives of such polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/81—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions involving only carbon-to-carbon unsaturated bonds
- A61K8/8141—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides or nitriles thereof; Compositions of derivatives of such polymers
- A61K8/8152—Homopolymers or copolymers of esters, e.g. (meth)acrylic acid esters; Compositions of derivatives of such polymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/86—Polyethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/89—Polysiloxanes
- A61K8/891—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q5/00—Preparations for care of the hair
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F212/02—Monomers containing only one unsaturated aliphatic radical
- C08F212/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F212/06—Hydrocarbons
- C08F212/08—Styrene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F218/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid or of a haloformic acid
- C08F218/02—Esters of monocarboxylic acids
- C08F218/04—Vinyl esters
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F218/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid or of a haloformic acid
- C08F218/02—Esters of monocarboxylic acids
- C08F218/04—Vinyl esters
- C08F218/08—Vinyl acetate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D131/00—Coating compositions based on homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid, or of a haloformic acid; Coating compositions based on derivatives of such polymers
- C09D131/02—Homopolymers or copolymers of esters of monocarboxylic acids
- C09D131/04—Homopolymers or copolymers of vinyl acetate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/10—General cosmetic use
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/54—Polymers characterized by specific structures/properties
- A61K2800/542—Polymers characterized by specific structures/properties characterized by the charge
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/60—Particulates further characterized by their structure or composition
- A61K2800/65—Characterized by the composition of the particulate/core
- A61K2800/654—The particulate/core comprising macromolecular material
Definitions
- the present invention relates to an external preparation.
- Patent Literature 1 discloses that an aqueous polymer emulsion obtained by emulsion polymerization of a specific monomer has excellent storage stability and excellent water resistance and adhesion of a coating film.
- Patent Literature 2 discloses that a cosmetic resin obtained by emulsion polymerization of a specific monomer mixture has excellent transparency and excellent balance of properties such as water resistance, adhesiveness, cosmetic durability, and a feeling of tightness. It has been disclosed.
- Patent Document 3 discloses a water-in-oil type skin cosmetic containing a specific resin emulsion, a partially crosslinked organopolysiloxane polymer, and a volatile silicone, and substantially not containing a surfactant. It is disclosed that it has excellent transparency, water resistance, and sebum resistance, has a smooth feel, and has good storage stability.
- Patent Literature 4 discloses that a soap-free polymer emulsion for cosmetics having a glass transition temperature of 5 to -50 ° C obtained by copolymerizing a specific hydrophobic monomer and a specific hydrophilic monomer forms a flexible film. It is disclosed that the composition is excellent in blending stability (ethanol resistance) and coating properties (dirt resistance).
- the present invention relates to an external preparation containing the following components (A) and (B).
- Component (A) (A) one or more hydrophobic monomers selected from the group consisting of styrene and its derivatives, vinyl esters, and hydrophobic acrylic monomers; and (b) a structural unit derived from an ionic hydrophilic monomer or a salt thereof.
- An ionic polymer particle component having a mass ratio (a) / (b) of (a) / (b) of 99.5 / 0.5 to 80/20 and a glass transition temperature of more than 5 ° C. and 120 ° C.
- B Phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), benzyl alcohol (B3), sorbitol (B4), oxyalkylene derivatives (B5) represented by the following general formula (I), polyoxyalkylenealkyl glucosides ( B6), oleic acid (B7), alkyl benzoate (B8), xylitol (B9), (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10), and One or more compounds selected from the group consisting of methylphenylpolysiloxane (B11) Z- ⁇ O (PO) l (EO) m- (BO) n H ⁇ a (I)
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropy
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1.
- the external preparation of the present invention contains the following components (A) and (B).
- Component (A) (A) one or more hydrophobic monomers selected from the group consisting of styrene and its derivatives, vinyl esters, and hydrophobic acrylic monomers; and (b) a structural unit derived from an ionic hydrophilic monomer or a salt thereof.
- Ionic polymer particle component having a mass ratio (a) / (b) of 99.5 / 0.5 to 80/20 between (a) and (b) and a glass transition temperature of more than 5 ° C. and 120 ° C.
- B Phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), benzyl alcohol (B3), sorbitol (B4), oxyalkylene derivatives (B5) represented by the following general formula (I), polyoxyalkylenealkyl glucosides ( B6), oleic acid (B7), alkyl benzoate (B8), xylitol (B9), (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10), and One or more compounds selected from the group consisting of methylphenylpolysiloxane (B11) Z- ⁇ O (PO) l (EO) m- (BO) n H ⁇ a (I)
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropy
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1. Since the external preparation of the present invention contains the above-mentioned components (A) and (B), it has less stickiness, is excellent in use feeling, has high film-forming ability, and is excellent in abrasion resistance.
- an acrylic polymer emulsion or an external preparation containing the same is an improvement in compatibility between low stickiness and excellent usability, and excellent film forming ability, and good abrasion resistance of the formed film.
- An object of the present invention is to provide an external preparation which has a low stickiness, is excellent in use feeling, and has a high film-forming ability and excellent abrasion resistance.
- the present inventors have found that the above problem can be solved by using an external preparation containing a combination of predetermined ionic polymer particles and a predetermined compound.
- the external preparation of the present invention is useful as, for example, a skin cosmetic because it has a low stickiness, is excellent in use feeling, and has a high film-forming ability and excellent abrasion resistance.
- the reason that the above effects can be obtained by the external preparation of the present invention is considered as follows.
- the ionic polymer can be used for various external preparations such as skin cosmetics by forming an ionic polymer particle by emulsion in water.
- Tg glass transition temperature
- the polymer becomes very sticky and the feeling of use deteriorates.
- the Tg of the polymer is too high, the film-forming ability tends to decrease, and the formed film tends to have poor abrasion resistance and water resistance.
- the external preparation of the present invention by using ionic polymer particles having a Tg of more than 5 ° C. as the component (A), it is possible to suppress stickiness and improve the usability.
- the component (A) has a structural unit derived from a predetermined hydrophobic monomer, the component (A) has a good affinity for the component (B) described later, and the component (A) and the component (B) can be used in combination. Even when the component (A) has a relatively high Tg of more than 5 ° C., the obtained external preparation has high film-forming ability, and the formed film is considered to have good abrasion resistance and water resistance. Further, when the Tg of the component (A) is 120 ° C. or lower, the film forming ability of the obtained external preparation can be favorably maintained.
- the external preparation of the present invention can be, for example, an external preparation applied to hair and skin.
- the external preparation of the present invention is preferably a cosmetic, more preferably a skin cosmetic. preferable.
- the dosage form of the external preparation there is no particular limitation on the dosage form of the external preparation, and any dosage form such as liquid, foam, paste, cream, and solid can be used.
- the external preparation of the present invention is preferably an oil-in-water external preparation in which the component (A) and the component (B) form an oil-in-water emulsion.
- the external preparation of the present invention comprises, as component (A): (A) one or more hydrophobic monomers selected from the group consisting of styrene and its derivatives, vinyl esters, and hydrophobic acrylic monomers; and (b) a structural unit derived from an ionic hydrophilic monomer or a salt thereof.
- Ionic polymer particles having a mass ratio of (a) / (b) of 99.5 / 0.5 to 80/20 and a glass transition temperature of more than 5 ° C. and not more than 120 ° C. contains.
- the external preparation of the present invention becomes an external preparation having less stickiness, excellent feeling in use, and excellent abrasion resistance of the formed film due to the above-mentioned effects.
- hydrophobic monomer refers to a monomer having a homopolymer solubility of 1% by mass or less in water at 20 ° C.
- hydrophilic monomer refers to a monomer at 20 ° C. A monomer having a solubility in water of more than 1% by mass. Specific examples of the hydrophobic monomer and the hydrophilic monomer will be described later.
- the ionic polymer particles as the component (A) have a glass transition temperature (Tg) of more than 5 ° C and 120 ° C or less.
- Tg glass transition temperature
- the Tg of the ionic polymer particles is preferably 10 ° C. or higher, more preferably 15 ° C. or higher, still more preferably 20 ° C. or higher, and still more preferably 30 ° C. or higher.
- the viewpoint of improving abrasion resistance it is preferably 105 ° C or less, more preferably 100 ° C or less, further preferably 95 ° C or less, still more preferably 70 ° C or less, still more preferably 50 ° C or less, and still more preferably 45 ° C. It is as follows.
- the specific range of the Tg of the ionic polymer particles is preferably from 10 to 105 ° C, more preferably from 10 to 100 ° C, still more preferably from 15 to 100 ° C, even more preferably from 20 to 100 ° C, and still more preferably from 30 to 100 ° C.
- the temperature is 95 ° C., more preferably 30 to 70 ° C., even more preferably 30 to 50 ° C., and even more preferably 30 to 45 ° C.
- the glass transition temperature of the ionic polymer particles may be measured by a general differential scanning calorimeter (DSC) using sufficiently dried polymer particles.
- DSC differential scanning calorimeter
- the Tg can be calculated from the following equation (1). w 1 , w 2 ,...: weight fraction of each monomer (total of weight fraction is 1) Tg 1 , Tg 2 ,...: Tg (° C.) of homopolymer of each monomer
- the glass transition temperature of the homopolymer of each monomer is described in, for example, “J. Brandrup. Et. Al.,“ Polymer Handbook, Fourth Edition ”, John Wiley & Sons. Inc.”.
- Component (A) is (a) one or more hydrophobic monomers selected from the group consisting of styrene and its derivatives, vinyl esters, and hydrophobic acrylic monomers (hereinafter, also simply referred to as “hydrophobic monomer (a)”). ).
- Styrene and its derivatives Styrene and its derivatives used as the hydrophobic monomer (a) include styrene, ⁇ -methylstyrene, methylstyrene, butylstyrene, t-butylstyrene, dimethylstyrene, divinylbenzene and the like. More than one species can be used. Among them, styrene is preferred from the viewpoints of easiness, availability, and economy of emulsion polymerization in the production of polymer particles.
- vinyl ester examples of the vinyl ester used as the hydrophobic monomer (a) include vinyl acetate, vinyl propionate, vinyl butyrate, vinyl hexanoate, vinyl octanoate, vinyl decanoate, vinyl laurate, vinyl palmitate, and vinyl stearate. Examples thereof include vinyl esters having an alkyl group or an alkenyl group, and one or more of these can be used. Among them, vinyl acetate is preferable from the viewpoints of easiness, availability, and economy of emulsion polymerization in the production of polymer particles.
- (meth) acrylic acid ester As the hydrophobic acrylic monomer used as the hydrophobic monomer (a), (meth) acrylic acid ester is preferable.
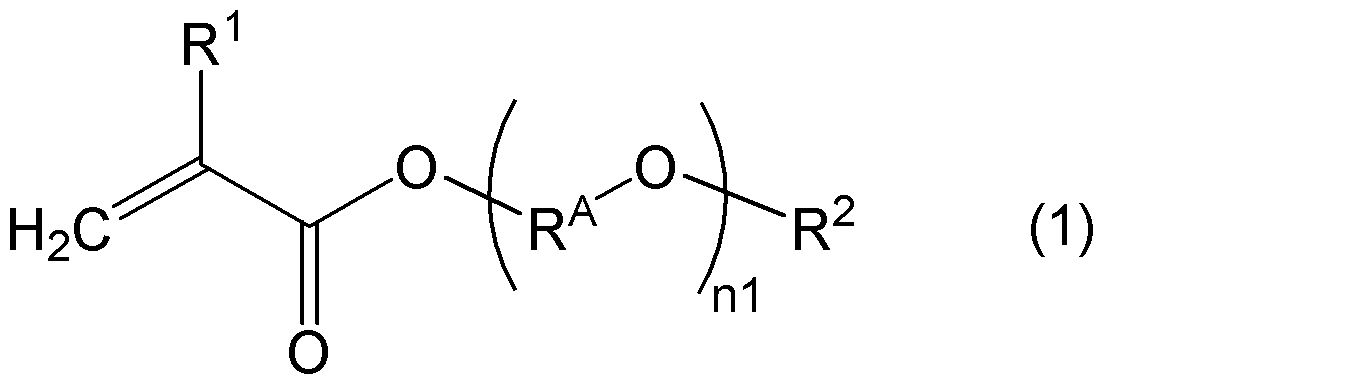
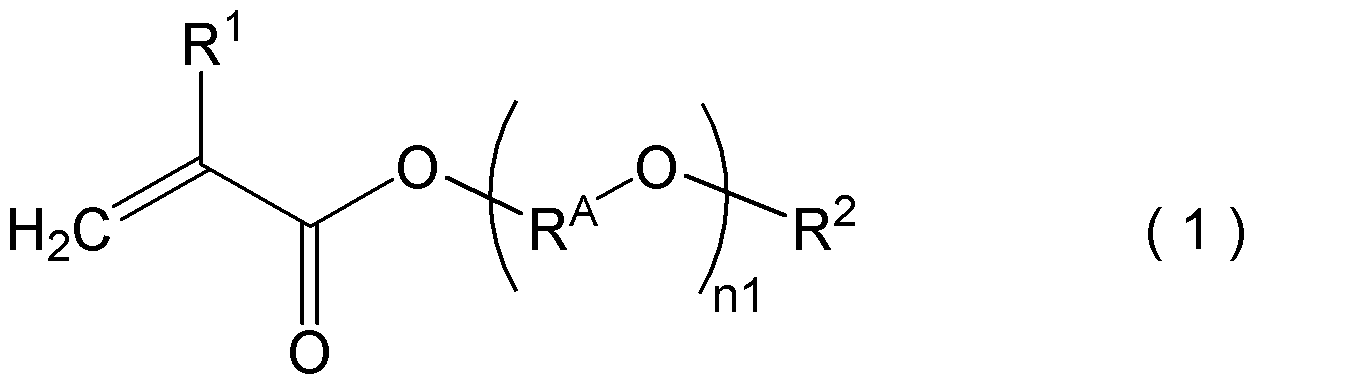
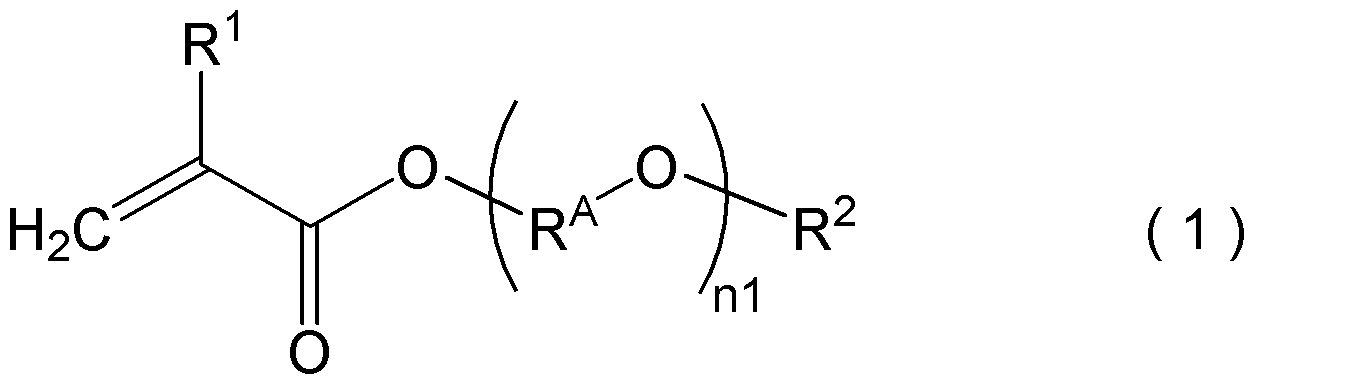
- (meth) acrylic acid ester represented by the following general formula (1) Polymers in which the amount of the polymer dissolved in water at 20 ° C. is 1% by mass or less are exemplified.
- “(meth) acrylic acid” means methacrylic acid or acrylic acid.
- R 1 represents a hydrogen atom or a methyl group
- R 2 may have a hydroxy group, a chain aliphatic group having 1 to 24 carbon atoms, and a chain aliphatic group having 5 to 24 carbon atoms.
- n1 is an integer of 0 or more and 30 or less.
- R 1 represents a hydrogen atom or a methyl group
- R 2 may have a hydroxy group, a chain aliphatic group having 1 to 24 carbon atoms, and a chain aliphatic group having 5 to 24 carbon atoms. It represents a cyclic aliphatic group, an aryl group having 6 to 24 carbon atoms, or an aralkyl group having 7 to 24 carbon atoms.
- the chain aliphatic group may be any of a linear aliphatic group and a branched aliphatic group.
- R 2 is preferably a linear aliphatic group having 1 to 24 carbon atoms, and more preferably carbon atom, from the viewpoints of tackiness suppression, ease of emulsion polymerization in the production of polymer particles, availability, and economy.
- An alkyl group having a number of 1 to 24, more preferably an alkyl group having 1 to 12 carbon atoms, still more preferably an alkyl group having 1 to 8 carbon atoms, and still more preferably an alkyl group having 1 to 6 carbon atoms. is there.
- R A represents an alkylene group having 2 to 4 carbon atoms, from the viewpoint of availability and economy, it is preferably an ethylene group or a propylene group, when n1 is 2 or more, each R A presence of a plurality of identical But they may be different.
- n1 is preferably an integer of 0 or more and 10 or less, and more preferably 0 from the viewpoint of suppressing stickiness, the ease of emulsion polymerization in the production of polymer particles, the availability, and the economic efficiency.
- (meth) Acrylic acid alkyl esters are preferred.
- the carbon number of the alkyl is preferably 1 or more and 24 or less, more preferably 1 or more and 12 or less, further preferably 1 or more and 8 or less, and further more preferably 1 or more and 6 or less.
- alkyl (meth) acrylate examples include methyl (meth) acrylate, ethyl (meth) acrylate, n-propyl (meth) acrylate, isopropyl (meth) acrylate, and n- (meth) acrylate.
- decyl, isodecyl (meth) acrylate, and lauryl (meth) acrylate are exemplified.
- hydrophobic monomer (a) styrene, vinyl acetate and (meth) are preferably used from the viewpoint of improving the abrasion resistance of the film and suppressing the stickiness, the ease of emulsion polymerization in the production of polymer particles, the availability and the economic efficiency.
- the hydrophobic monomer (a) preferably contains the following monomer (a1) and monomer (a2) from the viewpoint of controlling Tg of the ionic polymer particles as the component (A).
- (A1) at least one selected from the group consisting of styrene, vinyl acetate, and a (meth) acrylate ester having a homopolymer having a glass transition temperature of more than 5 ° C, and a (a2) homopolymer having a glass transition temperature of 5 ° C or less.
- the monomer (a1) is at least one selected from the group consisting of styrene, vinyl acetate, and a (meth) acrylate having a glass transition temperature of a homopolymer of more than 5 ° C.
- the (meth) acrylate having a glass transition temperature of the homopolymer of more than 5 ° C. is preferably a homopolymer of the (meth) acrylate represented by the general formula (1). Having a glass transition temperature of more than 5 ° C.
- the monomer (a1) is preferably at least one selected from the group consisting of styrene and alkyl (meth) acrylate,
- the number is preferably 1 or more and 24 or less, more preferably 1 or more and 12 or less, further preferably 1 or more and 8 or less, and still more preferably 1 or more and 6 or less.
- the monomer (a1) examples include styrene (100 ° C.), vinyl acetate (32 ° C.), methyl acrylate (10 ° C.), tert-butyl acrylate (107 ° C.), isobornyl acrylate (94 ° C.), methacryl Methyl acrylate (105 ° C.), ethyl methacrylate (65 ° C.), n-butyl methacrylate (20 ° C.), isobutyl methacrylate (53 ° C.), sec-butyl methacrylate (60 ° C.), tert-butyl methacrylate (118 C), cyclohexyl methacrylate (83 C), benzyl methacrylate (54 C), isobornyl methacrylate (170 C), 2-hydroxyethyl methacrylate (75 C), and one or more of these.
- the temperature in parentheses is the Tg of the homopolymer of each monomer.
- styrene, vinyl acetate, methyl methacrylate, and ethyl methacrylate in terms of Tg control of ionic polymer particles, ease of emulsion polymerization in production of polymer particles, availability and economy.
- At least one selected from the group consisting of styrene, methyl methacrylate, and ethyl methacrylate is more preferred, and one or more selected from the group consisting of styrene and methyl methacrylate is more preferred.
- the monomer (a2) is a (meth) acrylic acid ester having a homopolymer having a glass transition temperature of 5 ° C. or less, and is preferably a homopolymer of the (meth) acrylic acid ester represented by the general formula (1). Those having a glass transition temperature of 5 ° C. or less are mentioned. From the viewpoints of easiness, availability, and economy of emulsion polymerization in the production of polymer particles, among (meth) acrylates, alkyl (meth) acrylates are preferable, and the number of carbon atoms of the alkyl is preferably 1 or more and 24 or less. And more preferably 1 or more and 12 or less, further preferably 1 or more and 8 or less, and further more preferably 1 or more and 6 or less.
- the monomer (a2) examples include ethyl acrylate ( ⁇ 24 ° C.), n-butyl acrylate ( ⁇ 54 ° C.), 2-ethylhexyl acrylate ( ⁇ 50 ° C.), and 2-ethylhexyl methacrylate ( ⁇ 10 ° C.) ), Isodecyl methacrylate (-41 ° C), lauryl methacrylate (-65 ° C) and the like, and one or more of these can be used.
- the temperature in parentheses is the Tg of the homopolymer of each monomer.
- ethyl acrylate, n-butyl acrylate, and acrylic acid 2 are preferred from the viewpoint of controlling the Tg of the ionic polymer particles, the ease of emulsion polymerization in the production of the polymer particles, the availability, and the economy.
- One or more selected from the group consisting of -ethylhexyl is preferable, and n-butyl acrylate is more preferable.
- the glass transition temperature of the homopolymer of the monomer (a1) and the glass transition temperature of the homopolymer of the monomer (a2) are determined.
- the difference is 15 ° C. or more.
- the difference in the glass transition temperature is more preferably 50 ° C. or more, further preferably 80 ° C. or more, still more preferably 100 ° C. or more, and still more preferably 120 ° C. or more. More preferably, it is 140 ° C. or higher.
- the difference in the glass transition temperature is preferably 200 ° C. or lower, more preferably 180 ° C. or lower, further more preferably 170 ° C. It is as follows.
- the specific range of the difference between the glass transition temperature of the homopolymer of the monomer (a1) and the glass transition temperature of the homopolymer of the monomer (a2) is preferably 15 to 200 ° C., more preferably 50 to 200 ° C., and still more preferably.
- the temperature is 50 to 180 ° C, more preferably 80 to 180 ° C, still more preferably 100 to 180 ° C, still more preferably 120 to 180 ° C, and even more preferably 140 to 170 ° C.
- the mass ratio (a1) / (a2) is preferably 50/50 to 99/1, more preferably 50/50. 9090/10, more preferably 54/46 to 85/15, even more preferably 54/46 to 80/20, even more preferably 60/40 to 80/20, even more preferably 65/35 to 80/20. 20.
- the Tg of the ionic polymer particles can be easily adjusted to a range of more than 5 ° C. and 120 ° C. or less, and the sticky suppressing effect and the abrasion resistance improving effect are excellent.
- the total amount of the monomer (a1) and the monomer (a2) in the hydrophobic monomer (a) is preferably from the viewpoint of controlling the Tg of the ionic polymer particles and from the viewpoint of the ease of emulsion polymerization in the production of the polymer particles. It is 50% by mass or more, more preferably 70% by mass or more, still more preferably 80% by mass or more, and still more preferably 90% by mass or more. The upper limit is 100% by mass.
- the component (A) has a structural unit derived from an ionic hydrophilic monomer or a salt (b) thereof.
- the component (A) having the constituent unit can be used as emulsion particles dispersed in an aqueous medium.
- Examples of the ionic hydrophilic monomer or a salt thereof include an anionic hydrophilic monomer having an anionic group or a salt thereof, and a cationic hydrophilic monomer having a cationic group or a salt thereof.
- anionic group in the anionic hydrophilic monomer examples include a carboxy group, a sulfonic acid group, a phosphoric acid group, and the like.From the viewpoint of easiness of emulsion polymerization in the production of polymer particles, availability, and economy, carboxy group and One or more selected from the group consisting of sulfonic acid groups is preferred.
- anionic hydrophilic monomer or a salt thereof examples include vinyl compounds having a carboxy group such as (meth) acrylic acid, maleic acid, fumaric acid, itaconic acid, crotonic acid, and styrene carboxylic acid, and salts thereof; 2- ( Vinyl compounds having a sulfonic acid group such as (meth) acrylamide-2-methylpropanesulfonic acid, styrenesulfonic acid, (meth) acryloyloxyethylsulfonic acid or salts thereof; vinylphosphonic acid, (meth) acryloyloxyethylphosphoric acid, etc.
- a vinyl compound having a phosphoric acid group or a salt thereof; and one or more of these can be used.
- Examples of the cationic hydrophilic monomer or a salt thereof have a dialkylamino group such as dimethylaminoethyl (meth) acrylate, diethylaminoethyl (meth) acrylate, dimethylaminopropyl (meth) acrylamide, and diethylaminopropyl (meth) acrylamide (meth).
- the ionic hydrophilic monomer or its salt (b) is an anionic hydrophilic monomer.
- Monomer or a salt thereof is preferable, and a monomer having at least one anionic group selected from the group consisting of a carboxy group and a sulfonic acid group or a salt thereof is more preferable, acrylic acid, methacrylic acid, a sulfonic acid group-containing monomer, and One or more selected from the group consisting of these salts are more preferable, and acrylic acid, methacrylic acid, styrene sulfonic acid, and salts thereof from the viewpoints of ease, availability, and economy of emulsion polymerization in the production of polymer particles.
- At least one member selected from the group consisting of acrylic acid, methacrylic acid, and salts thereof Al is even more preferably one or more selected, acrylic acid or a salt thereof is even more preferable.
- the component (A) contains a structural unit derived from a hydrophobic monomer (a) and an ionic hydrophilic monomer or a salt thereof (b), and has a mass ratio (a) / (b) of (a) and (b). Is 99.5 / 0.5 to 80/20.
- the mass ratio (a) / (b) is within this range, the Tg of the ionic polymer particles as the component (A) can be easily controlled to a desired range, and the emulsion stability is good.
- the mass ratio (a) / (b) is preferably 99/1 to 85/15, more preferably 99/1 to 90/10, still more preferably 99/1 to 95/5, and still more preferably. Is from 98.5 / 1.5 to 95/5, and even more preferably from 98/2 to 95/5.
- the component (A) may further have a constitutional unit derived from a monomer other than the hydrophobic monomer (a) and the ionic hydrophilic monomer or a salt thereof (b).
- the total amount of the hydrophobic monomer (a) and the ionic hydrophilic monomer or its salt (b) in all the monomers constituting the component (A) is preferably 80% by mass or more. And more preferably 90% by mass or more, further preferably 95% by mass or more, and still more preferably 98% by mass or more.
- the upper limit is 100% by mass.
- the ionic polymer particles as the component (A) can be produced by polymerizing the above monomer component and forming the particles into fine particles.
- Polymerization and microparticulation methods include (1) a method in which monomer components are polymerized into fine particles by an emulsion polymerization method, a suspension polymerization method, a dispersion polymerization method, and the like; After obtaining the polymer by the above method, there is a method in which the fine particles are formed by a phase inversion emulsification method, a suspension method, or the like.
- the method (1) is preferable from the viewpoint of ease of production, and the emulsion polymerization method is more preferable.
- a soap-free emulsion polymerization method in which a surfactant is not added is preferable from the viewpoints of the skin irritation of the obtained component (A) and the water resistance.
- the soap-free emulsion polymerization method is a method in which a monomer component is emulsion-polymerized in the presence of a polymerization initiator without using an emulsifier such as a surfactant, a polymer-type emulsifier, and a reactive surfactant. It can be carried out.
- the main component of the solvent used is water, and in some cases, a hydrophilic solvent such as a lower alcohol may be mixed.
- the reaction temperature is set below the boiling point of the solvent.
- the monomer concentration in the reaction system is not particularly limited, but is preferably 1 to 60% by mass from the viewpoints of production efficiency and suppression of aggregates.
- the component (A) is obtained as an aqueous dispersion (emulsion) of ionic polymer particles. It is preferable to mix this form with the external preparation of the present invention from the viewpoint of stability and handling.
- the reaction is preferably a radical polymerization reaction from the viewpoint of ease of production and flexibility of the monomer composition.
- radical polymerization initiator used in the radical polymerization reaction known compounds can be used, and examples thereof include peroxide initiators such as ammonium persulfate, sodium persulfate, potassium persulfate, benzoyl peroxide, and lauroyl peroxide.
- Azo start such as 2,2'-azobis (2-methylpropionamidine) dihydrochloride, 2,2'-azobis (2,4-dimethylvaleronitrile), 2,2'-azobisisobutyronitrile Agents and the like.
- a water-soluble radical polymerization initiator is preferable, and one or more selected from the group consisting of ammonium persulfate, sodium persulfate, and potassium persulfate is more preferable.
- the amount of the radical polymerization initiator used can be appropriately selected depending on the type and concentration of the monomer component, the type of the radical polymerization initiator, the polymerization temperature, and the like. % By mass, more preferably 0.1% by mass or more and 5% by mass or less.
- the average particle size of the component (A) is preferably 150 nm or more, more preferably 200 nm or more, and still more preferably 300 nm or more, from the viewpoint of improving the abrasion resistance and water resistance of the coating. Further, from the viewpoint of emulsion stability, the average particle size of the component (A) is preferably 800 nm or less, more preferably 700 nm or less, further preferably 600 nm or less, and still more preferably 550 nm or less. The specific range of the average particle size of the component (A) is preferably from 150 to 800 nm, more preferably from 200 to 700 nm, further preferably from 300 to 600 nm, and still more preferably from 300 to 550 nm.
- the average particle diameter of the component (A) means a median diameter (D50).
- the average particle size is a value measured at 25 ° C. using a laser diffraction / scattering type particle size distribution analyzer, and can be specifically measured by the method described in Examples.
- the component (A) is produced by the above-described soap-free emulsion polymerization method, the average particle size is easily adjusted to the above range. Further, in the soap-free emulsion polymerization method, since it is not necessary to use a surfactant, the component (A) obtained is also preferable in that the skin irritation is reduced.
- the content of the component (A) in the external preparation is preferably 0.1% by mass or more, more preferably 0.3% by mass or more, and still more preferably 0.1% by mass, from the viewpoint of improving the abrasion resistance of the film and suppressing stickiness. It is at least 5% by mass, more preferably at least 0.8% by mass, even more preferably at least 1.2% by mass. In addition, from the viewpoint of suppressing stickiness, preferably 5% by mass or less, more preferably 4% by mass or less, still more preferably 3.5% by mass or less, still more preferably 3% by mass or less, and still more preferably 2.5% by mass or less. % By mass or less.
- the specific range of the content of the component (A) in the external preparation is preferably 0.1 to 5% by mass, more preferably 0.3 to 4% by mass, and still more preferably 0.5 to 3.5% by mass. , More preferably 0.8 to 3% by mass, even more preferably 1.2 to 2.5% by mass.
- Component (B) The external preparation of the present invention is represented by the following general formula (I) as a component (B), phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), benzyl alcohol (B3), sorbitol (B4).
- Z- ⁇ O (PO) l (EO) m- (BO) n H ⁇ a (I)
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropylene group
- EO represents an oxyethylene group
- BO represents a carbon atom.
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1.
- the use of the component (B) in the external preparation of the present invention improves the film forming ability of the obtained external preparation even when the component (A) has a relatively high Tg of more than 5 ° C. due to the above-mentioned effects. This is considered to improve the wear resistance and water resistance of the formed film.
- the component (B) one type or two or more types can be used.
- oxyalkylene derivatives (B5), polyoxyalkylenealkyl glucosides (B6), alkyl benzoates (B8), (RS) -2-cyano-3 represented by the following general formula (I) , 3-Diphenylprop-2-enoic acid-2-ethylhexyl ester (B10) and methylphenylpolysiloxane (B11) will be described.
- Component (B5) is an oxyalkylene derivative represented by the following general formula (I).
- Component (B5) a mixture of different oxyalkylene derivatives among the oxyalkylene derivatives represented by the following general formula (I) may be used.
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropylene group
- EO represents an oxyethylene group
- BO represents a carbon atom.
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1.
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 to 9 hydroxy groups.
- a is in the range of 3 or more and 9 or less.
- the compound containing three or more and nine or less hydroxy groups include glycerin and trimethylolpropane when the number of hydroxy groups is three, and erythritol, pentaerythritol and sorbitol when the number of hydroxy groups is four. Alkyl glycosides, and diglycerin.
- Xylitol when the number of hydroxy groups is 5, dipentaerythritol, sorbitol and inositol when the number is 6; sucrose and trehalose when the number is 8; and maltitol when the number is 9;
- the compounds containing 3 to 9 hydroxy groups compounds containing 3 to 6 hydroxy groups are preferable, and the compounds containing 3 to 6 hydroxy groups are preferable, from the viewpoints of improving the abrasion resistance of the film of the external preparation and suppressing stickiness.
- Compounds containing no more than three hydroxy groups are more preferred, and compounds containing three hydroxy groups are even more preferred. That is, the compound is preferably at least one selected from the group consisting of glycerin and trimethylolpropane, and more preferably glycerin.
- the component (B5) in a compound containing 3 or more and 9 or less hydroxy groups, all the hydroxy groups are substituted with- ⁇ O (PO) l (EO) m- (BO) n H ⁇ . Is preferred.
- PO represents an oxypropylene group.
- 1 represents the average number of moles of PO units added, and is preferably 0.5 or more, more preferably 2 or more, from the viewpoint of improving the abrasion resistance of the film and suppressing stickiness. In addition, from the same viewpoint, it is preferably 10 or less, more preferably 5 or less.
- the specific range of 1 is preferably 0.5 to 10, more preferably 2 to 10, and even more preferably 2 to 5.
- EO represents an oxyethylene group.
- m represents the average number of moles of EO unit added, and is preferably 1 or more, more preferably 2 or more, from the viewpoints of solubility in water, improvement in abrasion resistance of the film, and suppression of stickiness.
- it is preferably 20 or less, more preferably 10 or less, and still more preferably 8 or less.
- the specific range of m is preferably 1 to 20, more preferably 2 to 10, and still more preferably 2 to 8.
- the mass ratio (PO / EO) is preferably 1/5 to 5/1, more preferably 1/4 to 4 from the viewpoints of improving the abrasion resistance of the film, suppressing stickiness, dissolving in water, and moisture retention. / 1 range.
- the order in which the PO and EO units are added is not particularly limited, and they may be added in any form of random or block. From the viewpoint of improving the abrasion resistance of the coating, random addition is preferred.
- BO represents an oxyalkylene group having 4 carbon atoms, for example, an oxybutylene group and an oxytetramethylene group, and preferably an oxybutylene group.
- butylene is here, -CH 2 -CH (C 2 H 5) -, - CH (CH 3) -CH (CH 3) -, and -CH 2 -C (CH 3) 2 - And one or more of these may be used.
- n represents an average number of added moles of BO units, and is preferably 0.5 or more, more preferably 0.8 or more, and still more preferably 1 or more, from the viewpoint of improving the abrasion resistance of the film and suppressing stickiness. From the viewpoint of moisture retention, it is preferably 5 or less, more preferably 4 or less.
- the specific range of n is preferably 0.5 to 5, more preferably 0.8 to 4, and still more preferably 1 to 4.
- the (BO) n unit is bonded to a terminal hydrogen atom of the oxyalkylene derivative.
- Examples of commercially available products of the oxyalkylene derivative represented by the general formula (I) include "WILBRIDE @ S-753" (PEG / PPG / polybutylene glycol-8 / 5/5 glycerin) manufactured by NOF Corporation. .
- polyoxyalkylene alkyl glucoside (B6) examples include compounds in which an alkyl glucoside is added with an alkylene oxide.
- the oxyalkylene is preferably oxyalkylene having 2 or 3 carbon atoms, more preferably one or more selected from the group consisting of oxyethylene and oxypropylene, from the viewpoint of improving the wear resistance of the film and suppressing stickiness. More preferably, it is oxyethylene.
- the alkyl group in the alkyl glucoside is preferably an alkyl group having 1 to 3 carbon atoms, and more preferably a methyl group, from the viewpoint of improving abrasion resistance of the film and suppressing stickiness.
- the average number of moles of the alkylene oxide added is preferably 5 or more, more preferably 10 or more, and also preferably 30 or less, more preferably 20 or less, from the viewpoint of improving the wear resistance of the film and suppressing stickiness. .
- Examples of commercially available polyoxyalkylene alkyl glucosides include “Macbiobrid MG-10E” (Methyl Gluces-10), “McBiobrid MG-20E” (Methyl Gluces-20), and “McBiobrid” manufactured by NOF Corporation.
- MG-10P PPG-10 methyl glucose
- Macbiobrid MG-20P PPG-20 methyl glucose
- Alkyl benzoate (B8) As the alkyl benzoate of the component (B8), an alkyl ester of benzoic acid having 12 to 15 carbon atoms may be mentioned from the viewpoint of improving the abrasion resistance of the film and suppressing stickiness.
- alkyl benzoate examples include "Finsolve TN” (alkyl benzoate (C12-15)) manufactured by Innospec Active Chemicals LLC.
- the component (B10) is a compound also referred to as octocrylene, and examples of commercially available products include “PARSOL 340” manufactured by DSM Corporation.
- the methylphenylpolysiloxane of the component (B11) is a compound also referred to as diphenylsiloxyphenyltrimethicone, and examples of commercially available products include “KF-56A” manufactured by Shin-Etsu Chemical Co., Ltd.
- component (B) one type or two or more types can be used.
- component (B) is preferably phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), or the oxyalkylene derivative (B5) represented by the general formula (I). ), Alkyl benzoate (B8), (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10), and methylphenylpolysiloxane (B11).
- the content of the component (B) in the external preparation is preferably 0.1% by mass or more, more preferably 0.3% by mass or more, and still more preferably 0.5% by mass, from the viewpoint of improving the abrasion resistance of the film.
- the content is more preferably 0.8% by mass or more, and even more preferably 1.2% by mass or more.
- it is preferably 20% by mass or less, more preferably 12% by mass or less, still more preferably 8% by mass or less, still more preferably 5% by mass or less, and still more preferably 3% by mass or less. is there.
- the specific range of the content of the component (B) in the external preparation is preferably 0.1 to 20% by mass, more preferably 0.3 to 12% by mass, and still more preferably 0.5 to 8% by mass. More preferably, it is 0.5 to 5% by mass, still more preferably 0.8 to 5% by mass, and still more preferably 1.2 to 3% by mass.
- the content of the component (A) and the component (B) in the external preparation is preferably such that the content of the component (A) is 0.1 to 5% by mass and the content of the component (B) is 0.1 to 5% by mass. 20% by mass, more preferably the content of component (A) is 0.3 to 4% by mass and the content of component (B) is 0.3 to 12% by mass, still more preferably the content of component (A)
- the content is 0.5 to 3.5% by mass and the content of component (B) is 0.5 to 8% by mass, and more preferably, the content of component (A) is 0.5 to 3.5%.
- the content ratio of component (A) to component (B) in the external preparation can be appropriately selected depending on the types of component (A) and component (B). : 1 to 1: 5, preferably 4: 1 to 1: 4, more preferably 2: 1 to 1: 2.
- the external preparation of the present invention can contain an aqueous medium.
- the aqueous medium include water; lower alcohols such as ethanol and isopropyl alcohol; low molecular weight diols and triols having 6 or less carbon atoms such as 1,3-butylene glycol, glycerin, ethylene glycol, and propylene glycol; and water and lower alcohols. At least one selected from the group consisting of water and ethanol is more preferred, and it is preferable that at least water is contained.
- the content of the aqueous medium in the external preparation can be appropriately selected according to the dosage form of the external preparation, but is usually in the range of 1 to 99.8% by mass.
- the content of the aqueous medium in the external preparation may be the balance of all the active ingredients in the external preparation.
- the external preparation of the present invention includes, in addition to the above-mentioned components, cosmetic ingredients and medicinal ingredients used according to the use of the external preparation, and components usually used in external preparations such as skin cosmetics, for the purpose of the present invention. You may contain suitably if it does not impair.
- the component include, other than the component (B), an antioxidant, an ultraviolet absorber, a surfactant, a thickener, an oil agent, a pH adjuster, a bactericide, an anti-inflammatory agent, a preservative, a coloring agent, and a chelate. Agents, humectants, pearlescent agents, ceramides, fragrances and the like.
- the method for producing the external preparation of the present invention is not particularly limited. For example, it can be produced by blending the component (A), the component (B), and other components used as required by the method described in the examples, and mixing using a known stirring device or the like.
- the present invention further discloses the following composition.
- An external preparation containing the following components (A) and (B).
- An ionic polymer particle component having a mass ratio (a) / (b) of (a) / (b) of 99.5 / 0.5 to 80/20 and a glass transition temperature of more than 5 ° C. and 120 ° C.
- B Phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), benzyl alcohol (B3), sorbitol (B4), oxyalkylene derivatives (B5) represented by the following general formula (I), polyoxyalkylenealkyl glucosides ( B6), oleic acid (B7), alkyl benzoate (B8), xylitol (B9), (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10), and One or more compounds selected from the group consisting of methylphenylpolysiloxane (B11) Z- ⁇ O (PO) l (EO) m- (BO) n H ⁇ a (I)
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropy
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1.
- the glass transition temperature (Tg) of the component (A) is preferably from 10 ° C to 105 ° C, more preferably from 10 ° C to 100 ° C, still more preferably from 15 ° C to 100 ° C, even more preferably from 20 ° C to 100 ° C. C. to 100 ° C., more preferably 30 ° C. to 95 ° C., still more preferably 30 ° C. to 70 ° C., still more preferably 30 ° C. to 50 ° C., even more preferably 30 ° C. to 45 ° C.
- R 1 represents a hydrogen atom or a methyl group
- R 2 may have a hydroxy group, a chain aliphatic group having 1 to 24 carbon atoms, and a chain aliphatic group having 5 to 24 carbon atoms. It represents a cyclic aliphatic group, an aryl group having 6 to 24 carbon atoms, or an aralkyl group having 7 to 24 carbon atoms
- RA represents an alkylene group having 2 to 4 carbon atoms.
- n1 is an integer of 0 or more and 30 or less.
- ionic hydrophilic monomer or a salt thereof is at least one selected from the group consisting of acrylic acid, methacrylic acid, styrenesulfonic acid, and salts thereof.
- hydrophobic monomer (a) contains the following monomer (a1) and monomer (a2).
- A1 at least one selected from the group consisting of styrene, vinyl acetate, and a (meth) acrylate ester having a homopolymer having a glass transition temperature of more than 5 ° C, and a (a2) homopolymer having a glass transition temperature of 5 ° C or less.
- Method acrylate
- the difference between the glass transition temperature of the homopolymer of the monomer (a1) and the glass transition temperature of the homopolymer of the monomer (a2) is preferably from 15 ° C to 200 ° C, more preferably from 50 ° C to 200 ° C, More preferably 50 ° C or more and 180 ° C or less, still more preferably 80 ° C or more and 180 ° C or less, still more preferably 100 ° C or more and 180 ° C or less, still more preferably 120 ° C or more and 180 ° C or less, even more preferably 140 ° C or more.
- the external preparation according to ⁇ 5> which is 170 ° C or lower.
- the average particle size of the component (A) is preferably 150 nm or more and 800 nm or less, more preferably 200 nm or more and 700 nm or less, further preferably 300 nm or more and 600 nm or less, and still more preferably 300 nm or more and 550 nm or less.
- the external preparation according to any one of to ⁇ 6>.
- the mass ratio (a1) / (a2) of the monomer (a1) to the monomer (a2) is preferably 50/50 to 99/1, more preferably 50/50 to 90/10, and even more preferably 54/50. 46 to 85/15, more preferably 54/46 to 80/20, even more preferably 60/40 to 80/20, even more preferably 65/35 to 80/20, ⁇ 5> to ⁇ 7.
- the external preparation according to any one of>.
- the total amount of the hydrophobic monomer (a) and the ionic hydrophilic monomer or its salt (b) in all the monomers constituting the component (A) is preferably 80% by mass or more, more preferably 90% by mass.
- the total amount of the monomer (a1) and the monomer (a2) in the hydrophobic monomer (a) is preferably 50% by mass or more, more preferably 70% by mass or more, further preferably 80% by mass or more, and further more
- the content of the component (A) is preferably 0.1 to 5% by mass, more preferably 0.3 to 4% by mass, still more preferably 0.5 to 3.5% by mass, and still more preferably.
- the component (B) is preferably phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), an oxyalkylene derivative (B5) represented by the above general formula (I), and an alkyl benzoate (B8) , (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10), and methylphenyl polysiloxane (B11), and Preferably, a group consisting of phenoxyethanol (B1), 2-ethylhexyl paramethoxycinnamate (B2), and (RS) -2-cyano-3,3-diphenylprop-2-enoic acid-2-ethylhexyl ester (B10).
- At least one member selected from the group consisting of phenoxyethanol (B1) and paramethoxycinnamate At least one member selected from the group consisting of 2-ethylhexyl (B2), ⁇ 1> ⁇ external preparation according to any one of ⁇ 11>.
- the content of the component (B) is preferably 0.1 to 20% by mass, more preferably 0.3 to 12% by mass, still more preferably 0.5 to 8% by mass, and still more preferably 0.1 to 8% by mass.
- the content of component (A) and component (B) in the external preparation is preferably 0.1 to 5% by mass of component (A) and 0% by mass of component (B). 1 to 20% by mass, more preferably 0.3 to 4% by mass of component (A) and 0.3 to 12% by mass of component (B), still more preferably
- the content of A) is 0.5 to 3.5% by mass and the content of component (B) is 0.5 to 8% by mass, and more preferably, the content of component (A) is 0.5 to 3.5% by mass.
- component (B) is 0.5 to 5% by mass, even more preferably the content of component (A) is 0.8 to 3% by mass and the content of component (B) The content is 0.8 to 5% by mass, and still more preferably, the content of component (A) is 1.2 to 2.5% by mass and the content of component (B) is 1.2 to 3% by mass.
- the content ratio of the component (A) to the component (B) in the external preparation is preferably from 5: 1 to 1: 5, more preferably from 4: 1 to 1: 4, more preferably by mass ratio.
- An external preparation containing the following components (A) and (B).
- An ionic polymer particle component (B) having a mass ratio (a) / (b) of (a) / (b) of 99/1 to 95/5 and a glass transition temperature of 10 ° C. or more and 105 ° C.
- Z represents a residue obtained by removing a hydroxy group from a compound containing 3 or more and 9 or less hydroxy groups
- PO represents an oxypropylene group
- a is in the range of 3 or more and 9 or less.
- l, m, and n each represent the average addition mole number of PO, EO, and BO units, where l is 0.5 or more and 10 or less, m is 1 or more and 20 or less, and n is 0.5 or more and 5 or less.
- the mass ratio (PO / EO) is in the range of 1/5 to 5/1.
- ⁇ 20> The content according to any one of ⁇ 16> to ⁇ 19>, wherein the content ratio of the component (A) to the component (B) in the external preparation is 5: 1 to 1: 5 by mass ratio. External preparation.
- Glass transition temperature (Tg) Glass transition temperature of the polymer particles was determined from the following equation (1) using the Tg value of the homopolymer of each monomer used in the examples. w 1 , w 2 ,...: weight fraction of each monomer (total of weight fraction is 1) Tg 1 , Tg 2 ,...: Tg (° C.) of homopolymer of each monomer
- Tg of the homopolymer of each monomer used in the examples is as follows. Polymethyl methacrylate: 105 ° C Polystyrene: 100 ° C Polyvinyl acetate: 32 ° C N-butyl polyacrylate: -54 ° C Polyacrylic acid: 106 ° C
- the average particle diameter (median diameter: D50) of the polymer particles was measured using a laser diffraction / scattering particle size distribution analyzer “LA-920” manufactured by HORIBA, Ltd. at 25 ° C. using water as a dispersion medium and relative refraction. The ratio was measured as 1.200-0.000i.
- Production Example 1 (Production of dispersion liquid of polymer particles 1) 510 g of ion-exchanged water was placed in a 1 L glass separable flask, and stirred for 30 minutes under a nitrogen atmosphere. The temperature of the flask was raised to around 70 ° C., and after the temperature in the system reached 70 ° C., a solution in which 1.5 g of ammonium persulfate was dissolved in 15 g of ion-exchanged water was added. Next, a monomer solution obtained by uniformly mixing 204 g of methyl methacrylate, 87 g of n-butyl acrylate, and 9 g of acrylic acid was dropped into the system at a constant rate over 3 hours.
- the mixture was maintained at about 70 ° C. for 1 hour, and then heated to about 75 ° C. and maintained for 3 hours to carry out polymerization and ripening.
- 43.7 g of a 1N aqueous solution of sodium hydroxide was added to neutralize the solution.
- aggregates were removed by mesh filtration (200 mesh) to obtain a dispersion of the polymer particles 1 having a solid content of 35% by mass.
- the glass transition temperature of the polymer particles 1 was 39 ° C., and the average particle size was 450 nm.
- Production Examples 2 and 3 (Production of dispersion liquid of polymer particles 2 and 3) A dispersion liquid of polymer particles 2 and 3 was produced in the same manner as in Production Example 1 except that the total amount of 291 g of methyl methacrylate and n-butyl acrylate was changed to the monomer composition (mass ratio) shown in Table 1. did.
- Table 1 shows the glass transition temperature and the average particle size of the polymer particles 2 and 3.
- Production Example 4 (Production of dispersion liquid of polymer particles 6) 510 g of ion-exchanged water was placed in a 1 L glass separable flask, and stirred for 30 minutes under a nitrogen atmosphere. The temperature of the flask was raised to around 70 ° C., and after the temperature in the system reached 70 ° C., a solution in which 1.5 g of ammonium persulfate was dissolved in 15 g of ion-exchanged water was added. Next, a monomer solution obtained by uniformly mixing 285 g of styrene, 6 g of n-butyl acrylate, and 9 g of acrylic acid was dropped into the system at a constant rate over 3 hours.
- the mixture was maintained at about 70 ° C. for 1 hour, and then heated to about 75 ° C. and maintained for 3 hours to carry out polymerization and ripening.
- 43.7 g of a 1N aqueous solution of sodium hydroxide was added to neutralize the solution. Further, aggregates were removed by mesh filtration (200 mesh) to obtain a dispersion of polymer particles 6 having a solid content of 35% by mass.
- Table 1 shows the glass transition temperature and the average particle size of the polymer particles 6.
- Production Example 5 (Production of dispersion liquid of polymer particles 7) 510 g of ion-exchanged water was placed in a 1 L glass separable flask, and stirred for 30 minutes under a nitrogen atmosphere. The temperature of the flask was raised to around 70 ° C., and after the temperature in the system reached 70 ° C., a solution in which 1.5 g of ammonium persulfate was dissolved in 15 g of ion-exchanged water was added. Next, a monomer solution obtained by uniformly mixing 225 g of vinyl acetate, 66 g of n-butyl acrylate, and 9 g of acrylic acid was dropped into the system at a constant rate over 3 hours.
- the mixture was maintained at about 70 ° C. for 1 hour, and then heated to about 75 ° C. and maintained for 3 hours to carry out polymerization and ripening.
- 43.7 g of a 1N aqueous solution of sodium hydroxide was added to neutralize the solution. Aggregates were further removed by mesh filtration (200 mesh) to obtain a dispersion of polymer particles 7 having a solid content of 35% by mass.
- Table 1 shows the glass transition temperature and the average particle size of the polymer particles 7.
- Production Example 6 (Production of dispersion liquid of polymer particles 8) A dispersion of polymer particles 8 was obtained in the same manner as in Production Example 4 except that the total amount of 291 g of styrene and n-butyl acrylate was changed to the monomer composition (mass ratio) shown in Table 1.
- Table 1 shows the glass transition temperature and the average particle size of the polymer particles 8.
- Comparative Production Examples 1 and 2 (Production of Dispersions of Polymer Particles 4 and 5) Except that the total amount of 291 g of methyl methacrylate and n-butyl acrylate was changed to the monomer composition (mass ratio) shown in Table 1, polymer particles 4 and 5 for comparative examples were produced in the same manner as in Production Example 1. Was prepared. Table 1 shows the glass transition temperature and the average particle size of the polymer particles.
- the external preparation of the present invention is useful as, for example, a skin cosmetic because it has a low stickiness and is excellent in use feeling, and has a high film-forming ability and excellent abrasion resistance.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Chemical & Material Sciences (AREA)
- Emergency Medicine (AREA)
- Organic Chemistry (AREA)
- Polymers & Plastics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Dermatology (AREA)
- Dispersion Chemistry (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Wood Science & Technology (AREA)
- Cosmetics (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
Description
例えば特許文献1には、特定のモノマーを乳化重合して得られる水系ポリマーエマルションが、保存安定性が良好で、且つ塗膜の耐水性、密着性に優れることが開示されている。
特許文献2には、特定の単量体混合物を乳化重合することによって得られる化粧料樹脂が、透明性に優れ、耐水性、密着性、化粧持ち及びツッパリ感等の特性のバランスが優れることが開示されている。
特許文献3には、特定の樹脂エマルジョン、部分架橋型オルガノポリシロキサン重合物、及び揮発性シリコーンを含有し、界面活性剤を実質的に含有しないことを特徴とする油中水型皮膚化粧料が、透明性、耐水性、耐皮脂性に優れ、滑らかな感触を有し、かつ保存安定性が良好であることが開示されている。
特許文献4には、特定の疎水性モノマーと特定の親水性モノマーを共重合して得られる、ガラス転移温度が5~-50℃の化粧料用ソープフリーポリマーエマルションが、柔軟な皮膜を形成し、配合安定性(耐エタノール性)、塗布性(耐ヨレ性)に優れることが開示されている。
成分(A):
(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)イオン性親水性モノマー又はその塩
に由来する構成単位を含み、
(a)と(b)の質量比(a)/(b)が99.5/0.5~80/20であり、ガラス転移温度が5℃超120℃以下であるイオン性ポリマー粒子
成分(B):
フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
本発明の外用剤は、下記成分(A)及び成分(B)を含有する。
成分(A):
(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)イオン性親水性モノマー又はその塩
に由来する構成単位を含み、(a)と(b)の質量比(a)/(b)が99.5/0.5~80/20であり、ガラス転移温度が5℃超120℃以下であるイオン性ポリマー粒子
成分(B):
フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
本発明の外用剤は上記成分(A)及び成分(B)を含有することにより、べたつきが少なく使用感に優れ、かつ皮膜形成能が高く耐摩耗性に優れる。
本発明の課題は、べたつきが少なく使用感に優れ、かつ皮膜形成能が高く耐摩耗性に優れる外用剤を提供することにある。
本発明の外用剤は、べたつきが少なく使用感に優れ、かつ皮膜形成能が高く耐摩耗性に優れることから、例えば皮膚化粧料として有用である。
イオン性ポリマーは、水中でエマルション化してイオン性ポリマー粒子とすることにより、皮膚化粧料等の各種外用剤に用いることができる。しかしながら、使用するポリマーのガラス転移温度(Tg)が低いと非常にべたつき、使用感が悪くなる。一方で、当該ポリマーのTgが高すぎると皮膜形成能が低下し、形成される皮膜の耐摩耗性及び耐水性が劣る傾向がある。
本発明の外用剤においては、成分(A)としてTgが5℃超のイオン性ポリマー粒子を用いることで、べたつきを抑え、使用感を向上させることができる。また、成分(A)は所定の疎水性モノマーに由来する構成単位を有するため後述する成分(B)との親和性が良好であり、成分(A)と成分(B)とを併用することにより、成分(A)のTgが5℃超と比較的高い範囲であっても得られる外用剤の皮膜形成能が高く、形成される皮膜の耐摩耗性、耐水性が良好になると考えられる。さらに、成分(A)のTgが120℃以下であると、得られる外用剤の皮膜形成能を良好に維持できる。
外用剤の剤型には特に制限はなく、例えば液体状、泡状、ペースト状、クリーム状、固形状等、任意の剤型とすることが可能である。
また本発明の外用剤は、成分(A)及び成分(B)が水中油型エマルションを形成している水中油型の外用剤であることが好ましい。
本発明の外用剤は、成分(A)として、
(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)イオン性親水性モノマー又はその塩
に由来する構成単位を含み、(a)と(b)の質量比(a)/(b)が99.5/0.5~80/20であり、ガラス転移温度が5℃超120℃以下であるイオン性ポリマー粒子を含有する。
本発明の外用剤は成分(A)を含有することで、前述した作用効果により、べたつきが少なく使用感に優れ、かつ形成される皮膜の耐摩耗性が良好な外用剤となる。
成分(A)であるイオン性ポリマー粒子は、ガラス転移温度(Tg)が5℃超120℃以下である。Tgが5℃超であることで、外用剤のべたつきを抑制して使用感を向上させることができ、120℃以下であることで、皮膜形成能を良好に維持できる。
べたつき抑制の観点から、イオン性ポリマー粒子のTgは、好ましくは10℃以上、より好ましくは15℃以上、更に好ましくは20℃以上、より更に好ましくは30℃以上であり、皮膜形成能すなわち皮膜の耐摩耗性向上の観点から、好ましくは105℃以下、より好ましくは100℃以下、更に好ましくは95℃以下、より更に好ましくは70℃以下、より更に好ましくは50℃以下、より更に好ましくは45℃以下である。
イオン性ポリマー粒子のTgの具体的範囲は、好ましくは10~105℃、より好ましくは10~100℃、更に好ましくは15~100℃、より更に好ましくは20~100℃、より更に好ましくは30~95℃、より更に好ましくは30~70℃、より更に好ましくは30~50℃、より更に好ましくは30~45℃である。
w1、w2、・・・:各モノマーの重量分率(重量分率の合計は1)
Tg1、Tg2、・・・:各モノマーのホモポリマーのTg(℃)
成分(A)は、(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー(以下、単に「疎水性モノマー(a)」ともいう)に由来する構成単位を有する。
疎水性モノマー(a)として用いられるスチレン及びその誘導体としては、スチレン、α-メチルスチレン、メチルスチレン、ブチルスチレン、t-ブチルスチレン、ジメチルスチレン、ジビニルベンゼン等が挙げられ、これらを1種又は2種以上用いることができる。上記の中でも、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、スチレンが好ましい。
疎水性モノマー(a)として用いられるビニルエステルとしては、酢酸ビニル、プロピオン酸ビニル、酪酸ビニル、ヘキサン酸ビニル、オクタン酸ビニル、デカン酸ビニル、ラウリン酸ビニル、パルミチン酸ビニル、ステアリン酸ビニル等の、アルキル基又はアルケニル基を有するビニルエステルが挙げられ、これらを1種又は2種以上用いることができる。上記の中でも、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、酢酸ビニルが好ましい。
疎水性モノマー(a)として用いられる疎水性アクリル系モノマーとしては、(メタ)アクリル酸エステルが好ましく、例えば、下記一般式(1)で表される(メタ)アクリル酸エステルであって、そのホモポリマーの20℃の水への溶解量が1質量%以下であるものが挙げられる。なお本明細書において「(メタ)アクリル酸」とは、メタクリル酸又はアクリル酸を意味する。
式(1)中、R1は水素原子又はメチル基を示し、R2はヒドロキシ基を有していてもよい、炭素数1以上24以下の鎖状脂肪族基、炭素数5以上24以下の環状脂肪族基、炭素数6以上24以下のアリール基、又は炭素数7以上24以下のアラルキル基を示し、RAは炭素数2以上4以下のアルキレン基を示す。n1は0以上30以下の整数である。
R2は、べたつき抑制の観点、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、好ましくは炭素数1以上24以下の鎖状脂肪族基であり、より好ましくは炭素数1以上24以下のアルキル基、更に好ましくは炭素数1以上12以下のアルキル基、より更に好ましくは炭素数1以上8以下のアルキル基、より更に好ましくは炭素数1以上6以下のアルキル基である。
RAは炭素数2以上4以下のアルキレン基を示し、入手性及び経済性の観点から、エチレン基又はプロピレン基であることが好ましく、n1が2以上のとき、複数存在するRAはそれぞれ同一でも異なっていてもよい。
n1は0以上10以下の整数が好ましく、べたつき抑制の観点、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、0がより好ましい。
(メタ)アクリル酸アルキルエステルの具体例としては、(メタ)アクリル酸メチル、(メタ)アクリル酸エチル、(メタ)アクリル酸n-プロピル、(メタ)アクリル酸イソプロピル、(メタ)アクリル酸n-ブチル、(メタ)アクリル酸イソブチル、(メタ)アクリル酸sec-ブチル、(メタ)アクリル酸tert-ブチル、(メタ)アクリル酸2-エチルヘキシル、(メタ)アクリル酸イソオクチル、(メタ)アクリル酸n-デシル、(メタ)アクリル酸イソデシル、及び(メタ)アクリル酸ラウリルからなる群から選ばれる1種以上が挙げられる。
(a1)スチレン、酢酸ビニル、及び、ホモポリマーのガラス転移温度が5℃超の(メタ)アクリル酸エステルからなる群から選ばれる1種以上
(a2)ホモポリマーのガラス転移温度が5℃以下の(メタ)アクリル酸エステル
モノマー(a1)は、スチレン、酢酸ビニル、及び、ホモポリマーのガラス転移温度が5℃超の(メタ)アクリル酸エステルからなる群から選ばれる1種以上である。
モノマー(a1)のうち、ホモポリマーのガラス転移温度が5℃超の(メタ)アクリル酸エステルとしては、好ましくは、前記一般式(1)で表される(メタ)アクリル酸エステルのうちホモポリマーのガラス転移温度が5℃超のものが挙げられる。
ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、モノマー(a1)としてはスチレン及び(メタ)アクリル酸アルキルエステルからなる群から選ばれる1種以上が好ましく、アルキルの炭素数は、好ましくは1以上24以下、より好ましくは1以上12以下、更に好ましくは1以上8以下、より更に好ましくは1以上6以下である。
これらの中でも、イオン性ポリマー粒子のTg制御の観点、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、スチレン、酢酸ビニル、メタクリル酸メチル、及びメタクリル酸エチルからなる群から選ばれる1種以上が好ましく、スチレン、メタクリル酸メチル、及びメタクリル酸エチルからなる群から選ばれる1種以上がより好ましく、スチレン及びメタクリル酸メチルからなる群から選ばれる1種以上が更に好ましい。
モノマー(a2)は、ホモポリマーのガラス転移温度が5℃以下の(メタ)アクリル酸エステルであり、好ましくは、前記一般式(1)で表される(メタ)アクリル酸エステルのうちホモポリマーのガラス転移温度が5℃以下のものが挙げられる。
ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、(メタ)アクリル酸エステルの中でも(メタ)アクリル酸アルキルエステルが好ましく、アルキルの炭素数は、好ましくは1以上24以下、より好ましくは1以上12以下、更に好ましくは1以上8以下、より更に好ましくは1以上6以下である。
これらの中でも、イオン性ポリマー粒子のTg制御の観点、ポリマー粒子の製造における乳化重合の容易性、入手性及び経済性の観点から、好ましくはアクリル酸エチル、アクリル酸n-ブチル、及びアクリル酸2-エチルヘキシルからなる群から選ばれる1種以上が好ましく、アクリル酸n-ブチルがより好ましい。
イオン性ポリマー粒子のTg制御の観点から、当該ガラス転移温度の差は、より好ましくは50℃以上、更に好ましくは80℃以上、より更に好ましくは100℃以上、より更に好ましくは120℃以上、より更に好ましくは140℃以上である。また、イオン性ポリマー粒子のTg制御の観点、モノマーの入手性及び経済性の観点からは、当該ガラス転移温度の差は、好ましくは200℃以下、より好ましくは180℃以下、更に好ましくは170℃以下である。
モノマー(a1)のホモポリマーのガラス転移温度とモノマー(a2)のホモポリマーとのガラス転移温度の差の具体的範囲は、好ましくは15~200℃、より好ましくは50~200℃、更に好ましくは50~180℃、より更に好ましくは80~180℃、より更に好ましくは100~180℃、より更に好ましくは120~180℃、より更に好ましくは140~170℃である。
成分(A)は、イオン性親水性モノマー又はその塩(b)に由来する構成単位を有する。成分(A)は当該構成単位を有することで、水性媒体に分散されたエマルション粒子とすることができる。
上記観点から、質量比(a)/(b)は、好ましくは99/1~85/15、より好ましくは99/1~90/10、更に好ましくは99/1~95/5、より更に好ましくは98.5/1.5~95/5、より更に好ましくは98/2~95/5である。
成分(A)であるイオン性ポリマー粒子は、前記モノマー成分を重合し、微粒子化することにより製造できる。重合及び微粒子化の方法としては、(1)乳化重合法、懸濁重合法、分散重合法等によりモノマー成分を重合しながら微粒子化する方法、(2)溶液重合法等によりモノマー成分を重合してポリマーを得た後、転相乳化法、懸濁法等により微粒子化する方法、が挙げられる。これらのうち、製造容易性の観点からは(1)の方法が好ましく、乳化重合法がより好ましい。乳化重合法の中でも、得られる成分(A)の皮膚刺激性の少なさ及び耐水性の観点から、界面活性剤を添加しないソープフリー乳化重合法が好ましい。
ソープフリー乳化重合法は、モノマー成分を、重合開始剤の存在下、界面活性剤、高分子型乳化剤、反応型界面活性剤等の乳化剤を用いずに乳化重合する方法であり、公知の方法で行うことができる。乳化重合の場合、用いる溶媒の主成分は水であり、場合によっては低級アルコールなどの親水性溶剤を混合してもよい。反応温度は、溶媒の沸点以下に設定される。反応系内のモノマー濃度は特に限定されないが、生産効率と凝集物抑制の観点から、1~60質量%が望ましい。
上記方法によれば、成分(A)はイオン性ポリマー粒子の水分散体(エマルション)として得られる。この形態で本発明の外用剤に配合することが、安定性や取り扱いの観点からは好ましい。
ラジカル重合反応に用いられるラジカル重合開始剤としては、公知の化合物を用いることができ、例えば、過硫酸アンモニウム、過硫酸ナトリウム、過硫酸カリウム、ベンゾイルパーオキサイド、ラウロイルパーオキサイド等の過酸化物系開始剤;2,2’-アゾビス(2-メチルプロピオンアミジン)二塩酸塩、2,2’-アゾビス(2,4-ジメチルバレロニトリル)、2,2’-アゾビスイソブチロニトリル等のアゾ系開始剤等が挙げられる。ソープフリー乳化重合を行う観点からは、水溶性のラジカル重合開始剤が好ましく、過硫酸アンモニウム、過硫酸ナトリウム、及び過硫酸カリウムからなる群から選ばれる1種以上がより好ましい。
ラジカル重合開始剤の使用量は、モノマー成分の種類及び濃度、ラジカル重合開始剤の種類、重合温度等により適宜選択できるが、通常、全モノマー量に対して好ましくは0.01質量%以上、10質量%以下であり、より好ましくは0.1質量%以上、5質量%以下である。
本明細書において、成分(A)の平均粒径とはメジアン径(D50)を意味する。当該平均粒径はレーザー回折/散乱式粒子径分布測定装置を用いて25℃で測定した値であり、具体的には実施例に記載の方法で測定できる。
本発明の外用剤は、成分(B)として、フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物を含有する。
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
成分(B)のうち、以下に、一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、安息香酸アルキル(B8)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)について説明する。
成分(B5)は、下記一般式(I)で示されるオキシアルキレン誘導体である。成分(B5)として、下記一般式(I)で示されるオキシアルキレン誘導体のうち、異なるオキシアルキレン誘導体の混合物を用いてもよい。
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
3個以上9個以下のヒドロキシ基を含む化合物としては、例えばヒドロキシ基が3個である場合はグリセリン、トリメチロールプロパンが挙げられ、ヒドロキシ基が4個である場合はエリスリトール、ペンタエリスリトール、ソルビトール、アルキルグリコシド、及びジグリセリンが挙げられる。ヒドロキシ基が5個である場合はキシリトール、6個である場合はジペンタエリスリトール、ソルビトール、及びイノシトール、8個である場合はスクロース及びトレハロース、9個である場合はマルチトールが挙げられる。
また、成分(B5)は、3個以上9個以下のヒドロキシ基を含む化合物において、すべてのヒドロキシ基が-{O(PO)l(EO)m-(BO)nH}に置換されていることが好ましい。
PO及びEO単位を付加する順序は特に限定されず、ランダム、ブロックのいずれの形態で付加してもよい。皮膜の耐摩耗性向上の観点からは、好ましくはランダム付加である。
成分(B6)のポリオキシアルキレンアルキルグルコシドとしては、アルキルグルコシドにアルキレンオキサイドが付加した化合物が挙げられる。
上記オキシアルキレンとしては、皮膜の耐摩耗性向上及びべたつき抑制の観点から、好ましくは炭素数2又は3のオキシアルキレンであり、より好ましくはオキシエチレン及びオキシプロピレンからなる群から選ばれる1種以上、更に好ましくはオキシエチレンである。
上記アルキルグルコシドにおけるアルキル基としては、皮膜の耐摩耗性向上及びべたつき抑制の観点から、好ましくは炭素数1以上3以下のアルキル基であり、より好ましくはメチル基である。
上記アルキレンオキサイドの平均付加モル数は、皮膜の耐摩耗性向上及びべたつき抑制の観点から、好ましくは5以上、より好ましくは10以上であり、また、好ましくは30以下、より好ましくは20以下である。
ポリオキシアルキレンアルキルグルコシドの市販品としては、日油(株)製の「マクビオブライド MG-10E」(メチルグルセス-10)、「マクビオブライド MG-20E」(メチルグルセス-20)、「マクビオブライド MG-10P」(PPG-10 メチルグルコース)、「マクビオブライド MG-20P」(PPG-20 メチルグルコース)等を例示できる。
成分(B8)の安息香酸アルキルとしては、皮膜の耐摩耗性向上及びべたつき抑制の観点から、安息香酸の炭素数12以上15以下のアルキルエステルが挙げられる。安息香酸アルキルの市販品としては、Innospec Active Chemicals LLC社製の「フィンソルブ TN」(安息香酸アルキル(C12-15))等を例示できる。
成分(B10)は、オクトクリレンとも称される化合物であり、市販品としては、DSM(株)製の「パルソール340」等を例示できる。
成分(B11)のメチルフェニルポリシロキサンは、ジフェニルシロキシフェニルトリメチコンとも称される化合物であり、市販品としては、信越化学工業(株)製の「KF-56A」等を例示できる。
上記のうち、成分(B)としては、べたつき抑制の観点から、好ましくはフェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、前記一般式(I)で示されるオキシアルキレン誘導体(B5)、安息香酸アルキル(B8)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上であり、より好ましくはフェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、及び(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)からなる群から選ばれる1種以上であり、更に好ましくはフェノキシエタノール(B1)及びパラメトキシケイ皮酸2-エチルヘキシル(B2)からなる群から選ばれる1種以上である。
外用剤中の成分(A)と成分(B)との含有量比は、成分(A)及び成分(B)の種類により適宜選択することができるが、べたつき抑制の観点から、質量比で5:1~1:5が好ましく、4:1~1:4がより好ましく、2:1~1:2が更に好ましい。
本発明の外用剤は、水性媒体を含有することができる。水性媒体としては、水;エタノール、イソプロピルアルコール等の低級アルコール;1,3-ブチレングリコール、グリセリン、エチレングリコール、プロピレングリコール等の炭素数6以下の低分子ジオール及びトリオールが挙げられ、水及び低級アルコールからなる群から選ばれる1種以上が好ましく、水及びエタノールからなる群から選ばれる1種以上がより好ましく、少なくとも水を含有することが好ましい。
外用剤中の水性媒体の含有量は、外用剤の剤型により適宜選択することができるが、通常、1~99.8質量%の範囲である。外用剤中の水性媒体の含有量は、外用剤中のすべての有効成分の残部であってよい。
本発明の外用剤は、前記成分の他、外用剤の用途に応じて使用される美容成分や薬効成分、並びに、皮膚化粧料等の外用剤に通常使用される成分を、本発明の目的を損なわない範囲で適宜含有してもよい。当該成分としては、例えば、成分(B)以外の、酸化防止剤、紫外線吸収剤、界面活性剤、増粘剤、油剤、pH調整剤、殺菌剤、抗炎症剤、防腐剤、着色剤、キレート剤、保湿剤、パール剤、セラミド類、香料等が挙げられる。
成分(A):
(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)イオン性親水性モノマー又はその塩
に由来する構成単位を含み、
(a)と(b)の質量比(a)/(b)が99.5/0.5~80/20であり、ガラス転移温度が5℃超120℃以下であるイオン性ポリマー粒子
成分(B):
フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
式(1)中、R1は水素原子又はメチル基を示し、R2はヒドロキシ基を有していてもよい、炭素数1以上24以下の鎖状脂肪族基、炭素数5以上24以下の環状脂肪族基、炭素数6以上24以下のアリール基、又は炭素数7以上24以下のアラルキル基を示し、RAは炭素数2以上4以下のアルキレン基を示す。n1は0以上30以下の整数である。
(a1)スチレン、酢酸ビニル、及び、ホモポリマーのガラス転移温度が5℃超の(メタ)アクリル酸エステルからなる群から選ばれる1種以上
(a2)ホモポリマーのガラス転移温度が5℃以下の(メタ)アクリル酸エステル
成分(A):
(a)スチレン、酢酸ビニル並びに(メタ)アクリル酸アルキルエステルからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)アクリル酸、及びメタクリル酸からなる群から選ばれる1種以上のイオン性親水性モノマー又はその塩
に由来する構成単位を含み、
(a)と(b)の質量比(a)/(b)が99/1~95/5であり、ガラス転移温度が10℃以上105℃以下であるイオン性ポリマー粒子
成分(B):
フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。
ポリマー粒子のガラス転移温度は、実施例で使用した各モノマーのホモポリマーのTgの値を使用して下記式(1)から求めた。
w1、w2、・・・:各モノマーの重量分率(重量分率の合計は1)
Tg1、Tg2、・・・:各モノマーのホモポリマーのTg(℃)
ポリメタクリル酸メチル:105℃
ポリスチレン:100℃
ポリ酢酸ビニル:32℃
ポリアクリル酸n-ブチル:-54℃
ポリアクリル酸:106℃
ポリマー粒子の平均粒径(メジアン径:D50)は、(株)堀場製作所製のレーザー回折/散乱式粒子径分布測定装置「LA-920」を用い、25℃において、水を分散媒として相対屈折率:1.200-0.000iとして測定した。
専門パネラー5名により、前腕内側に直径5cmの円に各例で得られた外用剤を20μL塗布し、25℃、57RH%下で20秒間かけて塗り延ばした。その後、使用感(べたつき感)を、下記評価基準に従い評価し、5名の平均スコアを求めた。
5:べたつきをまったく感じない
4:べたつきを感じない
3:べたつきをやや感じる
2:べたつきを感じる
1:べたつきを非常に感じる
3cm×10cmのガラス板に、各例で得られた外用剤を100μL塗布し、25℃で60分乾燥させて皮膜を形成した。この皮膜の上に、15gf/cm2の圧力がかかる重りを乗せた人工皮革を載置して、ガラス板面に対し平行に、100mm/秒の速度で引っ張り、皮膜が壊れなければ「良好」、壊れれば「不良」と評価した。
イオン交換水510gを1Lのガラス製セパラブルフラスコに入れ、窒素雰囲気下で30分攪拌した。フラスコを70℃付近まで昇温し、系内が70℃に達した後、過硫酸アンモニウム1.5gをイオン交換水15gに溶解した溶液を添加した。次いで、メタクリル酸メチル204g、アクリル酸n-ブチル87g、及びアクリル酸9gを均一に混合したモノマー溶液を、3時間かけて系内に一定速度で滴下した。滴下終了後、70℃付近で1時間保持した後、75℃付近まで昇温し3時間保持することで重合及び熟成を行った。得られた反応溶液を冷却した後、1N-水酸化ナトリウム水溶液43.7gを添加して中和した。さらに凝集物をメッシュ濾過(200mesh)で取り除き、固形分35質量%のポリマー粒子1の分散液を得た。ポリマー粒子1のガラス転移温度は39℃、平均粒径は450nmであった。
メタクリル酸メチル及びアクリル酸n-ブチルの合計量291gを、表1に示すモノマー組成(質量比)に変更したこと以外は、製造例1と同様の方法でポリマー粒子2,3の分散液を製造した。ポリマー粒子2,3のガラス転移温度、平均粒径を表1に示す。
イオン交換水510gを1Lのガラス製セパラブルフラスコに入れ、窒素雰囲気下で30分攪拌した。フラスコを70℃付近まで昇温し、系内が70℃に達した後、過硫酸アンモニウム1.5gをイオン交換水15gに溶解した溶液を添加した。次いで、スチレン285g、アクリル酸n-ブチル6g、及びアクリル酸9gを均一に混合したモノマー溶液を、3時間かけて系内に一定速度で滴下した。滴下終了後、70℃付近で1時間保持した後、75℃付近まで昇温し3時間保持することで重合及び熟成を行った。得られた反応溶液を冷却した後、1N-水酸化ナトリウム水溶液43.7gを添加して中和した。さらに凝集物をメッシュ濾過(200mesh)で取り除き、固形分35質量%のポリマー粒子6の分散液を得た。ポリマー粒子6のガラス転移温度、平均粒径を表1に示す。
イオン交換水510gを1Lのガラス製セパラブルフラスコに入れ、窒素雰囲気下で30分攪拌した。フラスコを70℃付近まで昇温し、系内が70℃に達した後、過硫酸アンモニウム1.5gをイオン交換水15gに溶解した溶液を添加した。次いで、酢酸ビニル225g、アクリル酸n-ブチル66g、及びアクリル酸9gを均一に混合したモノマー溶液を、3時間かけて系内に一定速度で滴下した。滴下終了後、70℃付近で1時間保持した後、75℃付近まで昇温し3時間保持することで重合及び熟成を行った。得られた反応溶液を冷却した後、1N-水酸化ナトリウム水溶液43.7gを添加して中和した。さらに凝集物をメッシュ濾過(200mesh)で取り除き、固形分35質量%のポリマー粒子7の分散液を得た。ポリマー粒子7のガラス転移温度、平均粒径を表1に示す。
スチレン及びアクリル酸n-ブチルの合計量291gを、表1に示すモノマー組成(質量比)に変更したこと以外は、製造例4と同様の方法で、ポリマー粒子8の分散液を得た。ポリマー粒子8のガラス転移温度、平均粒径を表1に示す。
メタクリル酸メチル及びアクリル酸n-ブチルの合計量291gを、表1に示すモノマー組成(質量比)に変更したこと以外は、製造例1と同様の方法で、比較例用のポリマー粒子4,5の分散液を製造した。ポリマー粒子のガラス転移温度、平均粒径を表1に示す。
表2に示す各成分を混合し、各例の水中油型の外用剤を得た。表2に記載した配合量は各成分の有効成分量(質量%)である。得られた外用剤を用いて、前記方法によりべたつき及び耐摩耗性の評価を行った。結果を表2に示す。
なお、比較例5~18は耐摩耗性が劣るため、べたつきの評価は行わなかった。
*1 パラメトキシケイ皮酸2-エチルヘキシル:ユビナールMC80(BASF SE社製)
*2 式(I)で示されるオキシアルキレン誘導体(PEG/PPG/ポリブチレングリコール-8/5/3グリセリン):WILBRIDE S-753(日油(株)製)
*3 ポリオキシアルキレンアルキルグルコシド(メチルグルセス-20):マクビオブライド MG-20E(日油(株)製)
*4 安息香酸アルキル(C12-15):フィンソルブ TN(Innospec Active Chemicals LLC社製)
*5 オクトクリレン:パルソール340(DSM(株)製)
*6 メチルフェニルポリシロキサン:KF-56A(信越化学工業(株)製)
*7 ポリエチレングリコール:PEG-1540(三洋化成工業(株)製)
*8 ジメチルポリシロキサン:シリコーンKF-96L-2CS(信越化学工業(株)製)
*9 水添ポリイソブテン:パールリーム4(日油(株)製)
*10 オリーブ油:クロピュア OL(クローダジャパン(株)製)
*11 パルミチン酸イソプロピル:エキセパール IPP(花王(株)製)
*12 ジカプリン酸ネオペンチルグリコール:エステモール N-01(日清オイリオグループ(株)製)
*13 イソノナン酸イソノニル:サラコス99(日清オイリオグループ(株)製)
*14 ミリスチン酸イソプロピル:エキセパール IPM(花王(株)製)
*15 カプリリルメチコン:SS-3408(東レ・ダウコーニング(株)製)
*16 トリエチルヘキサノイン:T.I.O(日清オイリオグループ(株)製)
Claims (11)
- 下記成分(A)及び成分(B)を含有する外用剤。
成分(A):
(a)スチレン及びその誘導体、ビニルエステル、並びに疎水性アクリル系モノマーからなる群から選ばれる1種以上の疎水性モノマー、及び
(b)イオン性親水性モノマー又はその塩
に由来する構成単位を含み、
(a)と(b)の質量比(a)/(b)が99.5/0.5~80/20であり、ガラス転移温度が5℃超120℃以下であるイオン性ポリマー粒子
成分(B):
フェノキシエタノール(B1)、パラメトキシケイ皮酸2-エチルヘキシル(B2)、ベンジルアルコール(B3)、ソルビトール(B4)、下記一般式(I)で示されるオキシアルキレン誘導体(B5)、ポリオキシアルキレンアルキルグルコシド(B6)、オレイン酸(B7)、安息香酸アルキル(B8)、キシリトール(B9)、(RS)-2-シアノ-3,3-ジフェニルプロパ-2-エン酸-2-エチルヘキシルエステル(B10)、及びメチルフェニルポリシロキサン(B11)からなる群から選ばれる1種以上の化合物
Z-{O(PO)l(EO)m-(BO)nH}a (I)
式中、Zは3個以上9個以下のヒドロキシ基を含む化合物からa個のヒドロキシ基を除いた残基を表し、POはオキシプロピレン基を表し、EOはオキシエチレン基を表し、BOは炭素数4のオキシアルキレン基を表す。aは3以上9以下の範囲である。l、m、及びnはそれぞれPO、EO、及びBO単位の平均付加モル数を表し、lは0.5以上10以下、mは1以上20以下、nは0.5以上5以下である。但し、質量比(PO/EO)は1/5~5/1の範囲である。 - イオン性親水性モノマー又はその塩(b)がアクリル酸、メタクリル酸、スチレンスルホン酸、及びこれらの塩からなる群から選ばれる1種以上である、請求項1又は2に記載の外用剤。
- 疎水性モノマー(a)が下記モノマー(a1)及びモノマー(a2)を含有する、請求項1~3のいずれか1項に記載の外用剤。
(a1)スチレン、酢酸ビニル、及び、ホモポリマーのガラス転移温度が5℃超の(メタ)アクリル酸エステルからなる群から選ばれる1種以上
(a2)ホモポリマーのガラス転移温度が5℃以下の(メタ)アクリル酸エステル - モノマー(a1)のホモポリマーのガラス転移温度とモノマー(a2)のホモポリマーとのガラス転移温度の差が15℃以上である、請求項4に記載の外用剤。
- 成分(A)の平均粒径が150nm以上800nm以下である、請求項1~5のいずれか1項に記載の外用剤。
- モノマー(a1)とモノマー(a2)の質量比(a1)/(a2)が50/50~99/1である、請求項4~6のいずれか1項に記載の外用剤。
- 成分(A)を構成する全モノマー中の疎水性モノマー(a)及びイオン性親水性モノマー又はその塩(b)の合計量が80質量%以上である、請求項1~7のいずれか1項に記載の外用剤。
- 疎水性モノマー(a)中のモノマー(a1)及びモノマー(a2)の合計量が80質量%以上である、請求項4~8のいずれか1項に記載の外用剤。
- 成分(A)の含有量が0.1質量%以上5質量%以下でかつ成分(B)の含有量が0.1質量%以上20質量%以下である、請求項1~9のいずれか1項に記載の外用剤。
- 成分(A)と成分(B)との含有量比が、質量比で5:1~1:5である、請求項1~10のいずれか1項に記載の外用剤。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19864331.4A EP3858324A4 (en) | 2018-09-28 | 2019-09-30 | EXTERNAL PREPARATION |
| KR1020217008321A KR20210047329A (ko) | 2018-09-28 | 2019-09-30 | 외용제 |
| US17/279,977 US20210386632A1 (en) | 2018-09-28 | 2019-09-30 | External preparation |
| CN201980061957.8A CN112739313A (zh) | 2018-09-28 | 2019-09-30 | 外用剂 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018-185465 | 2018-09-28 | ||
| JP2018185465 | 2018-09-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020067560A1 true WO2020067560A1 (ja) | 2020-04-02 |
Family
ID=69953187
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2019/038448 WO2020067560A1 (ja) | 2018-09-28 | 2019-09-30 | 外用剤 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20210386632A1 (ja) |
| EP (1) | EP3858324A4 (ja) |
| JP (1) | JP2020055807A (ja) |
| KR (1) | KR20210047329A (ja) |
| CN (1) | CN112739313A (ja) |
| TW (1) | TW202027722A (ja) |
| WO (1) | WO2020067560A1 (ja) |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02262512A (ja) * | 1989-04-01 | 1990-10-25 | Shionogi & Co Ltd | 皮膚の保護剤組成物 |
| US5614049A (en) * | 1993-11-10 | 1997-03-25 | Wacker Chemie Gmbh | Use of aqueous dispersions of two-phase emulsion graft copolymers as binders for stiffening materials in the textile and leather industry |
| JPH09125091A (ja) * | 1995-10-30 | 1997-05-13 | Kao Corp | 皮膚洗浄料 |
| JPH1067617A (ja) * | 1996-07-05 | 1998-03-10 | Basf Ag | 化粧用又は医薬用組成物 |
| JP2002327019A (ja) | 2001-03-02 | 2002-11-15 | Shiseido Co Ltd | 水系ポリマーエマルション、及びそれを用いた化粧料 |
| JP2005002207A (ja) | 2003-06-11 | 2005-01-06 | Nippon Nsc Ltd | 化粧料用樹脂 |
| JP2006008585A (ja) | 2004-06-25 | 2006-01-12 | Kanebo Cosmetics Inc | 油中水型皮膚用化粧料 |
| JP2006008561A (ja) | 2004-06-24 | 2006-01-12 | Kao Corp | 化粧料用ポリマーエマルション |
| JP2011037727A (ja) * | 2009-08-07 | 2011-02-24 | Kao Corp | 皮膚洗浄剤組成物 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000119171A (ja) * | 1998-10-12 | 2000-04-25 | Kao Corp | 崩壊性粒子 |
| US8545859B2 (en) * | 2003-11-26 | 2013-10-01 | Akzo Nobel N.V. | Use of acrylates copolymer as waterproofing agent in personal care applications |
| JP2008303207A (ja) * | 2007-05-07 | 2008-12-18 | Kao Corp | エーテルカルボキシレートの製造方法 |
| JP5818564B2 (ja) * | 2011-08-03 | 2015-11-18 | 花王株式会社 | 毛髪化粧料組成物 |
| WO2013048919A1 (en) * | 2011-09-30 | 2013-04-04 | L'oreal S.A. | Cosmetic compositions comprising latex film formers |
| BR112018004731B1 (pt) * | 2015-09-28 | 2021-10-26 | Rohm And Haas Company | Composição para cuidados com a pele, método para aumentar a absorção de spf ou uv de uma composição de cuidados com a pele |
| WO2017222570A1 (en) * | 2016-06-22 | 2017-12-28 | Rohm And Haas Company | Compositions containing latex particles and uv absorbers |
-
2019
- 2019-09-30 WO PCT/JP2019/038448 patent/WO2020067560A1/ja active Application Filing
- 2019-09-30 KR KR1020217008321A patent/KR20210047329A/ko unknown
- 2019-09-30 EP EP19864331.4A patent/EP3858324A4/en not_active Withdrawn
- 2019-09-30 US US17/279,977 patent/US20210386632A1/en not_active Abandoned
- 2019-09-30 JP JP2019180390A patent/JP2020055807A/ja active Pending
- 2019-09-30 CN CN201980061957.8A patent/CN112739313A/zh active Pending
- 2019-10-01 TW TW108135528A patent/TW202027722A/zh unknown
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02262512A (ja) * | 1989-04-01 | 1990-10-25 | Shionogi & Co Ltd | 皮膚の保護剤組成物 |
| US5614049A (en) * | 1993-11-10 | 1997-03-25 | Wacker Chemie Gmbh | Use of aqueous dispersions of two-phase emulsion graft copolymers as binders for stiffening materials in the textile and leather industry |
| JPH09125091A (ja) * | 1995-10-30 | 1997-05-13 | Kao Corp | 皮膚洗浄料 |
| JPH1067617A (ja) * | 1996-07-05 | 1998-03-10 | Basf Ag | 化粧用又は医薬用組成物 |
| JP2002327019A (ja) | 2001-03-02 | 2002-11-15 | Shiseido Co Ltd | 水系ポリマーエマルション、及びそれを用いた化粧料 |
| JP2005002207A (ja) | 2003-06-11 | 2005-01-06 | Nippon Nsc Ltd | 化粧料用樹脂 |
| JP2006008561A (ja) | 2004-06-24 | 2006-01-12 | Kao Corp | 化粧料用ポリマーエマルション |
| JP2006008585A (ja) | 2004-06-25 | 2006-01-12 | Kanebo Cosmetics Inc | 油中水型皮膚用化粧料 |
| JP2011037727A (ja) * | 2009-08-07 | 2011-02-24 | Kao Corp | 皮膚洗浄剤組成物 |
Non-Patent Citations (2)
| Title |
|---|
| J. BRANDRUP: "Polymer Handbook", JOHN WILEY & SONS. INC. |
| See also references of EP3858324A4 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3858324A4 (en) | 2022-05-18 |
| CN112739313A (zh) | 2021-04-30 |
| US20210386632A1 (en) | 2021-12-16 |
| KR20210047329A (ko) | 2021-04-29 |
| TW202027722A (zh) | 2020-08-01 |
| EP3858324A1 (en) | 2021-08-04 |
| JP2020055807A (ja) | 2020-04-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4099310B2 (ja) | ポリシロキサン含有ポリマーの化粧品処方物のための使用 | |
| JP6869942B2 (ja) | 油中水型乳化化粧料 | |
| JP2002201111A (ja) | 界面活性剤不含化粧用、皮膚用及び医薬用剤 | |
| JP2004522833A (ja) | 水溶性単位及びlcstを有する単位を含むポリマーによって、4から50℃の温度で安定化された分散物 | |
| EP3459978B1 (en) | Cosmetic for correcting bumps and dips | |
| JP6434218B2 (ja) | アイライナー化粧料 | |
| JP2022511674A (ja) | ミネラル日焼け止め組成物 | |
| WO2020067560A1 (ja) | 外用剤 | |
| TWI762819B (zh) | 化妝料 | |
| JP2000290459A (ja) | アクリルターポリマーを具備する水中油型エマルジョン形態の組成物、及びその使用、特にその化粧的使用 | |
| JP2002523532A (ja) | カチオン性ポリマーとその使用 | |
| JP6467127B2 (ja) | 樹脂及び化粧料用基材 | |
| WO2013064599A1 (en) | Hair styling composition | |
| KR20140007889A (ko) | 증점제로서 수-비용해성 양친매성 공중합체를 함유하는 미용 제제 | |
| JPH10265344A (ja) | 油中水型乳化毛髪化粧料 | |
| JP2022504559A (ja) | 水膨潤性架橋エラストマーおよび調製方法および使用 | |
| JPH10175829A (ja) | 乳化型毛髪セット剤組成物 | |
| JP2000290154A (ja) | 日焼け止め化粧料 | |
| CN111031997A (zh) | 用于除去皮肤上的化妆品的包含疏水性聚合物的组合物 | |
| JP4498838B2 (ja) | ポリマー組成物 | |
| JP2004238325A (ja) | 分散安定剤及び水性乳化液とこれを用いた化粧料 | |
| JPH10265345A (ja) | 毛髪化粧料 | |
| JP6705082B2 (ja) | 毛髪化粧料用基剤、毛髪化粧料、整髪料 | |
| JP2024044680A (ja) | 水中油型乳化組成物 | |
| JP2023133017A (ja) | 皮膜形成性組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 19864331 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20217008321 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2101001740 Country of ref document: TH |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2019864331 Country of ref document: EP Effective date: 20210428 |