WO2019131987A1 - 脂質微粒子分散物 - Google Patents
脂質微粒子分散物 Download PDFInfo
- Publication number
- WO2019131987A1 WO2019131987A1 PCT/JP2018/048404 JP2018048404W WO2019131987A1 WO 2019131987 A1 WO2019131987 A1 WO 2019131987A1 JP 2018048404 W JP2018048404 W JP 2018048404W WO 2019131987 A1 WO2019131987 A1 WO 2019131987A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- mass
- less
- lipid
- component
- preferable
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/34—Alcohols
- A61K8/345—Alcohols containing more than one hydroxy group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/0241—Containing particulates characterized by their shape and/or structure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/02—Cosmetics or similar toiletry preparations characterised by special physical form
- A61K8/04—Dispersions; Emulsions
- A61K8/06—Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/33—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing oxygen
- A61K8/34—Alcohols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/40—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing nitrogen
- A61K8/42—Amides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/40—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing nitrogen
- A61K8/44—Aminocarboxylic acids or derivatives thereof, e.g. aminocarboxylic acids containing sulfur; Salts; Esters or N-acylated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/46—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing sulfur
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/46—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing sulfur
- A61K8/466—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing sulfur containing sulfonic acid derivatives; Salts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/63—Steroids; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/68—Sphingolipids, e.g. ceramides, cerebrosides, gangliosides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/92—Oils, fats or waxes; Derivatives thereof, e.g. hydrogenation products thereof
- A61K8/922—Oils, fats or waxes; Derivatives thereof, e.g. hydrogenation products thereof of vegetable origin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/412—Microsized, i.e. having sizes between 0.1 and 100 microns
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/413—Nanosized, i.e. having sizes below 100 nm
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/60—Particulates further characterized by their structure or composition
- A61K2800/65—Characterized by the composition of the particulate/core
- A61K2800/652—The particulate/core comprising organic material
Definitions
- the present invention relates to a lipid particulate dispersion and a skin cosmetic.
- stratum corneum intercellular lipid In the interstices of keratinocytes constituting the stratum corneum present in the outermost layer of the skin, a lipid called stratum corneum intercellular lipid is present.
- the lipid composition of this stratum corneum intercellular lipid is about 50% of ceramide, and further consists of cholesterol, cholesterol ester, fatty acid and the like.
- ceramide is deeply involved in rough skin, dry skin and the like, and it is known that the state of the stratum corneum can be improved by supplementing ceramide with external use.
- ceramides various cosmetic compositions containing solid fat such as ceramides have been reported.
- these solid fats have high crystallinity and high melting point, it is difficult to stabilize them in a preparation, and various stabilization techniques have been developed.
- a ceramide dispersion comprising a ceramide-containing particle, a fatty acid having a melting point of 30 ° C.
- Patent Document 1 International Publication WO 2010/38814 Pamphlet
- Patent Document 2 Japanese Patent Application Publication No. 2007-15972
- Patent Document 3 Japanese Patent Application Publication No. 2004-331595
- Patent Document 4 Japanese Patent Application Publication No. 2-191208
- Patent Document 5 Unexamined-Japanese-Patent No. 9-124432
- the present invention is a lipid fine particle dispersion containing the following components (A) to (E) and having a pH of 3.5 to 8.0, and the temperature of the lipid fine particles in the temperature range of 45 ° C. to 80: It is an object of the present invention to provide a lipid particulate dispersion having a heat of fusion of 0.30 J / g or less and an average particle size of less than 200 nm.
- A Lipids solid or semi-solid at 25 ° C. other than component (A) selected from sterols and derivatives thereof
- B (C) anionic surfactant
- D water-soluble solvent
- water-soluble solvent water
- Solid fats such as ceramides are crystallized in the composition, and the crystals are relatively large and unstable, often unstable in the liquid crystal state in the preparation, and the like. In the cosmetic using the composition, the action of solid fat such as ceramides could not be sufficiently exhibited over time. On the other hand, the skin surface is kept weakly acidic as part of maintaining homeostasis. Therefore, in designing a mild skin cosmetic preparation, it is preferred to adjust the preparation to a weak acidity as a pH close to the skin.
- the present invention is to provide a lipid fine particle dispersion stably emulsified and dispersed as fine particles without crystallization of solid fat such as ceramides under acidic conditions.
- the present inventors combined use of sterols and solid fat such as ceramides to obtain an anionic surfactant and a water-soluble solvent.
- a specific anionic surfactant is used, not only from neutral to alkaline but also under acidic conditions, the crystallinity of solid fats such as ceramides is low, and it is stably emulsified as fine particles. It was found that a dispersion of lipid microparticles was obtained.
- the lipid fine particle dispersion of the present invention has low crystallinity of solid fat such as ceramides even under acidic conditions, is stably emulsified and dispersed as fine particles, and has crystallinity of solid fat such as ceramides. By stably emulsifying and dispersing as low, fine particles, the action of these solid fats on the skin is sufficiently exerted.
- Component (A) used for the lipid particulate dispersion of the present invention is at least one selected from sterols and their derivatives.
- the component (A) contributes to lowering the crystallinity of the lipid of the component (B) and reducing the particle size in the lipid microparticle dispersion of the present invention.
- Component (A) includes cholesterol, phytosterols and their derivatives. Derivatives of cholesterol and phytosterols include fatty acid cholesterol esters and fatty acid phytosterol esters.
- fatty acid cholesterol ester a cholesterol ester with a fatty acid having 12 to 24 carbon atoms is preferable.
- cholesteryl laurate cholesteryl palmitate, cholesteryl myristate, cholesteryl oleate, cholesteryl isostearate and cholesteryl linoleate are preferred.
- N-lauroyl-L-glutamic acid di (cholesteryl / behenyl / octyldodecyl), N-lauroyl-L-glutamic acid di (cholesteryl / octyldodecyl), N-lauroyl-L-glutamic acid di (phytosteryl / behenyl / octyldodecyl) N-Lauroyl-L-glutamic acid di (phytosteryl / octyldodecyl), N-lauroyl-L-glutamic acid di (phytosteryl / octyldodecyl), N-lauroyl-L-glutamic acid di (phytoste
- sterol esters of N-acyl amino acids are “ELDU PS-203” and “Plandool-LG2” (N-lauroyl-L-glutamic acid di (phytosteryl / octyldecyl) sold by Ajinomoto Co., Japan Seisei Co., Ltd.
- the content is preferably 0.003% by mass or more and 5.0% by mass or less, more preferably 0.08% by mass or more and 1.0% by mass or less, and more preferably 0.2% by mass or more. 8 mass% or less is further preferable, 0.3 mass% or more and 0.8 mass% or less is still more preferable, and 0.4 mass% or more and 0.6 mass% or less is still more preferable. .
- Component (B) is a solid or semi-solid lipid at 25 ° C. other than component (A).
- solid or semi-solid at 25 ° C. means that the viscosity at 25 ° C. is greater than 10000 mPa ⁇ s.
- the viscosity was measured using a B-type viscometer (VISCOMETER TVB-10, manufactured by Toki Sangyo Co., Ltd.), rotor No. It measures at 4, 12 rpm and 1 minute.
- the said component (B) shows a moisturizing effect, a barrier function improvement effect, etc. with respect to skin, and is an active ingredient of cosmetics.
- the solid or semi-solid lipid includes a lipid having a melting point of 50 to 150 ° C.
- R 1b is a hydrocarbon group having 10 to 26 carbon atoms
- R 2b is a hydrocarbon group having 9 to 25 carbon atoms
- X is — (CH 2 ) n — (wherein n is 2 to 6) Indicates an integer).
- R 1 and R 2 are the same or different and each represents a hydrocarbon group having 1 to 40 carbon atoms which may be hydroxylated, and R 3 represents an alkylene group having 1 to 6 carbon atoms or a single bond, R 4 represents a hydrogen atom, an alkoxy group having 1 to 12 carbon atoms, or a 2,3-dihydroxypropyloxy group, provided that when R 3 is a single bond, R 4 is a hydrogen atom.
- the hydrocarbon group is preferably an alkyl group or an alkenyl group.
- Examples of the compound of the general formula (1) include N- (hexadecyloxyhydroxypropyl) -N-hydroxyethyl hexadecanamide, and examples of the compound of the general formula (2) include long chain dibasic acid Bis 3-methoxypropylamide is mentioned.
- these components (B) natural ceramides, synthetic ceramides such as those represented by the general formulas (1) and (2), and aliphatic alcohols having 12 to 30 carbon atoms are preferable from the viewpoint of moisturizing action and barrier function improving action. These lipids can be used alone or in combination of two or more.
- Component (B) is preferably contained in the lipid fine particle dispersion of the present invention in an amount of 0.01% by mass or more, more preferably 0.1% by mass or more, from the viewpoint of moisturizing action and barrier function improving action. 3% by mass or more is more preferable, and 5.0% by mass or less is preferable, 3.0% by mass or less is more preferable, and 1.0% by mass from the viewpoint of lowering the crystallinity and stabilizing the particle diameter small. The following are more preferable. As a specific range, 0.01 mass% or more and 5.0 mass% or less is preferable, 0.1 mass% or more and 3.0 mass% or less is more preferable, and 0.3 mass% or more and 1.0 mass% or less More preferable.
- the mass ratio (A / B) of the component (A) to the component (B) in the lipid fine particle dispersion of the present invention is preferably 0.1 or more from the viewpoint of lowering crystallinity of the component (B) and stabilizing it.
- 0.2 or more is more preferable, 0.3 or more is more preferable, 1.0 or less is preferable, 0.8 or less is more preferable, and 0.6 or less is more preferable.
- 0.1 or more and 1.0 or less are preferable, 0.2 or more and 0.8 or less are more preferable, and 0.3 or more and 0.6 or less are more preferable.
- Component (C) is an anionic surfactant.
- an anionic surfactant N-acyl amino acid salt, N-acyl methyl taurine, from the viewpoint of expression of sufficient surface activity at pH 3.5 to 8.0 including not only alkaline conditions but neutral conditions as well as acidic conditions. Salts, alkyl phosphates, polyoxyethylene alkyl ether phosphates, fatty acid salts, alkyl sulfates, polyoxyethylene alkyl ether sulfates, alkyl ether carboxylates, dialkyl sulfosuccinates, diacyl amino acid lysine salts, etc. preferable.
- N-acyl amino acid salt N-acyl methyl taurine salt, polyoxyethylene alkyl ether phosphate, fatty acid salt, diacyl amino acid lysine salt, alkyl sulfate ester salt, polyoxyethylene alkyl ether sulfate ester salt, alkyl ether carboxylic acid
- acid salts and dialkyl sulfosuccinates are preferred.
- One or more selected from salts are more preferable.
- one or more selected from N-acyl amino acid salt, N-acyl methyl taurine salt, polyoxyethylene alkyl ether phosphate, fatty acid salt and diacyl amino acid lysine salt are more preferable
- N-acyl amino acid salt and One or more selected from N-acylmethyl taurine salts are more preferable.
- N-acyl amino acid salts include sodium N-lauroyl-L-glutamate, sodium N-stearoyl-L-glutamate, arginine N-stearoyl-L-glutamate, sodium N-myristoyl-L-glutamate, sodium N-lauroyl sarcosine, etc.
- Examples of the N-acylmethyl taurine salt include N-myristoyl-N-methyl taurine sodium, N-lauroyl-N-methyl taurine sodium, N-stearoyl-N-methyl taurine sodium and the like.
- alkyl phosphate examples include sodium monomyristyl phosphate, sodium monostearyl phosphate, sodium di (C12-C15) palace-8-phosphate and the like.
- polyoxyethylene alkyl phosphates examples include sodium polyoxyethylene oleyl ether phosphate, sodium polyoxyethylene cetyl ether phosphate, sodium polyoxyethylene stearyl ether phosphate and the like.
- fatty acid salt examples include fatty acid salts having 12 to 24 carbon atoms such as sodium laurate, potassium palmitate and arginine stearate.
- alkyl sulfate ester salt examples include sodium lauryl sulfate, potassium lauryl sulfate and the like.
- polyoxyethylene alkyl ether sulfate ester salt examples include polyoxyethylene lauryl sulfate triethanolamine salt and the like.
- alkyl ether carboxylate examples include polyoxyethylene lauryl ether acetate and the like.
- dialkyl sulfosuccinates examples include sodium di-2-ethylhexyl sulfosuccinate and the like.
- diacyl amino acid lysine salt include sodium dilauroyl glutamate and the like.
- the content of the component (C) in the lipid fine particle dispersion of the present invention is preferably 0.002% by mass or more, and 0.05% by mass or more from the viewpoint of stability of the preparation and homeostasis of the skin surface used.
- 0.1 mass% or more is more preferable, 3.0 mass% or less is preferable, 1.0 mass% or less is more preferable, and 0.5 mass% or less is more preferable.
- 0.002% by mass or more and 3.0% by mass or less is preferable, 0.05% by mass or more and 1.0% by mass or less is more preferable, 0.1% by mass or more and 0.5% by mass or less preferable.
- the ratio (A + B / C) of the total mass of the component (A) to the component (B) and the mass of the component (C) in the lipid particle dispersion of the present invention is 0 from the viewpoint of moisturizing action, barrier function improving action and stability. .05 or more is preferable, 0.5 or more is more preferable, 1.0 or more is further preferable, 2.0 or more is further more preferable, 6.0 or less is preferable, 5.5 or less is more preferable, 5.0 The following are more preferable. As a specific range, 0.05 or more and 6.0 or less are preferable, 0.5 or more and 5.5 or less are more preferable, 1.0 or more and 5.5 or less are more preferable, and 2.0 or more and 5.5 or less Is even more preferred.
- (D) Water-soluble solvents such as ethylene glycol, diethylene glycol, triethylene glycol, polyethylene glycol (average molecular weight less than 1000), propylene glycol, dipropylene glycol, polypropylene glycol (average molecular weight: less than 1000), glycerin, diglycerin, poly Glycerin, isoprene glycol, 1,2-pentanediol, 1,3-propanediol, 1,3-butylene glycol, hexylene glycol, polyhydric alcohols such as methyl cellulose, lower alcohols such as methanol and ethanol, and the like can be mentioned. .
- glycerin, 1,3-butylene glycol, dipropylene glycol, 1,3-propanediol and the like are particularly preferable.
- These components (D) can be used alone or in combination of two or more.
- the content of the component (D) is that the component (A) and the component (B), or the component (A), the component (B), and the component (C) be efficiently and uniformly dissolved, the stability and the feeling of use From the point of point of view, 1.0% by mass or more is preferable, 2.0% by mass or more is more preferable, 3.0% by mass or more is more preferable, 30% by mass or less is preferable in the lipid fine particle dispersion of the present invention.
- the mass% or less is more preferable, and the 20 mass% or less is more preferable.
- 1.0 mass% or more and 30 mass% or less are preferable, 2.0 mass% or more and 25 mass% or less are more preferable, and 3.0 mass% or more and 20 mass% or less are more preferable.
- the lipid particulate dispersion of the present invention further contains component (E) water.
- component (E) water is preferably 50% by mass or more, more preferably 70% by mass or more, and still more preferably 80% by mass or more 97 mass% or less is preferable, 95 mass% or less is more preferable, and 90 mass% or less is more preferable.
- 50 to 97 mass% is preferable, 70 to 95 mass% is more preferable, and 80 to 90 mass% is more preferable.
- the lipid microparticle dispersion of the present invention preferably further contains Component (F) a nonionic surfactant from the viewpoint of stability.
- a nonionic surfactant HLB 10 to 20 nonionic surfactants are preferable, HLB 12 to 15 nonionic surfactants are more preferable, and HLB 12.5 to 14.5 are preferable.
- Nonionic surfactants are more preferred.
- HLB hydrophilic-lipophilic balance
- HLB hydrophilic-lipophilic balance
- [HLB] 7 + 1.171 log (Mw / Mo) (Wherein, Mw represents the molecular weight of the hydrophilic group of the surfactant, Mo represents the molecular weight of the hydrophobic group of the surfactant, and log represents the base 10 logarithm.)
- nonionic surfactant of the component (F) for example, glycerin fatty acid ester, sorbitan fatty acid ester, propylene glycol fatty acid ester, polyethylene glycol fatty acid ester, sucrose fatty acid ester, polyoxyethylene fatty acid ester, polyoxyethylene sorbitan fatty acid Ester, polyoxyethylene alkyl ether, polyoxyethylene sorbitol fatty acid ester, polyoxyethylene glycerin fatty acid ester, polyoxyethylene propylene glycol fatty acid ester, polyoxyethylene castor oil, polyoxyethylene hydrogenated castor oil, polyoxyethylene hydrogenated castor oil fatty acid Ester, polyoxyethylene phytostanol ether, polyoxyethylene phytosterose ether, polyoxyethylene Nko less ethanol ether, polyoxyethylene cholesteryl ether, polyoxyalkylene-modified organopolysiloxane, polyoxyalkylene-alkyl co-modified organopolysiloxanes, and the like
- polyoxyethylene hydrogenated castor oil having an average added mole number of oxyethylene groups of 25 to 80, polyoxyethylene fatty acid ester having an average added mole number of oxyethylene groups of 10 to 140, carbon Polyoxyethylene sorbitan fatty acid ester having 12 to 18 alkyl groups and having an average added mole number of oxyethylene groups of 20, and an average added mole number of an alkyl group having 16 to 22 carbon atoms and an oxyethylene group having 15 to 25 carbon atoms
- polyoxyethylene / methylpolysiloxane copolymers having an average addition mole number of 10 to 20 of oxyethylene groups
- polyoxyethylenes having an average addition mole number of oxyethylene groups of 25 to 80.
- Hardened castor oil a carbon number of 16 to 22 alkyl group and the level of oxyethylene group More preferably, polyoxyethylene alkyl ether having an addition mole number of 15 to 25 and polyoxyethylene hardened hydrogenated castor oil having an average addition mole number of oxyethylene group of 35 to 65, an alkyl group having 16 to 20 carbon atoms and an oxyethylene group Further preferred is a polyoxyethylene alkyl ether having an average added mole number of from 20 to 25.
- ком ⁇ онент (F) as a component (40EO), Emanon CH-40 (HLB12.5, Kao Corp. make), as a polyoxyethylene hydrogenated castor oil (60EO), an Emalone CH-60 ( K) (HLB 14.0, manufactured by Kao Corporation), as polyoxyethylene isocetyl ether (20 EO), EMALEX 1620 (HLB 14, manufactured by Nippon Emulsion Co., Ltd.), as polyoxyethylene isostearyl ether (25 EO), EMALEX 18 25 (HLB 14, Japan emulsion)
- Commercial products, such as company-made can be used.
- One or two of these components (F) can be used.
- the lipid fine particle dispersion of the present invention is in a form in which the component (A) and the component (B) are dispersed and emulsified in water, and the pH thereof is 3.5 or more and 8.0 or less.
- the lipid fine particle dispersion of the present invention has low crystallinity including acidic conditions with a pH of 3.5 or more and 8.0 or less, and stably exists as fine particles. Therefore, the feeling of use is maintained while maintaining the homeostasis of the skin surface. It is good.
- the pH is preferably 3.5 or more and 7.0 or less, more preferably 3.5 or more and 6.0 or less, and still more preferably 3.5 or more and 5.5 or less from the viewpoint of skin surface homeostasis and feeling of use. .
- the lipid microparticle dispersion of the present invention may further contain a base and / or an acid in order to adjust the pH to the above range.
- the base is not particularly limited, and may be an organic base or an inorganic base.
- the organic base is preferably one or more selected from basic amino acids and alkanolamines. Specifically, basic amino acids such as L-arginine, lysine and histidine; alkanols such as monoethanolamine, diethanolamine, triethanolamine, aminomethylpropanol, aminomethylpropanediol, aminoethylpropanediol and trishydroxymethylaminoethane One or more selected from amines are preferred.
- the inorganic base is preferably one or more selected from calcium hydroxide, sodium hydroxide and potassium hydroxide. Among these, one or more selected from L-arginine, calcium hydroxide, sodium hydroxide and potassium hydroxide are more preferable.
- the inorganic acid is preferably one or more selected from hydrochloric acid, nitric acid, nitrous acid, sulfuric acid, sulfurous acid, phosphoric acid, phosphonic acid and phosphinic acid. Among these, one or more selected from adipic acid and phosphoric acid are more preferable.
- the base and / or the acid is preferably contained in such an amount that the pH of the lipid microparticle dispersion of the present invention falls within the above range.
- the lipid fine particle dispersion of the present invention further comprises, in addition to the above components, components used for ordinary cosmetics, such as oil components, moisturizers, antioxidants, preservatives, chelating agents, whitening agents, UV absorbers, Vitamins, plant extracts, various other medicinal ingredients, powders, flavors, coloring materials and the like can be contained.
- components used for ordinary cosmetics such as oil components, moisturizers, antioxidants, preservatives, chelating agents, whitening agents, UV absorbers, Vitamins, plant extracts, various other medicinal ingredients, powders, flavors, coloring materials and the like can be contained.
- the lipid fine particle dispersion of the present invention is prepared, for example, by mixing oil components including components (A) to (D), heating and dissolving at 80 to 95 ° C., adding (E) water thereto and stirring to uniformly emulsify.
- oil components including components (A) to (D), heating and dissolving at 80 to 95 ° C., adding (E) water thereto and stirring to uniformly emulsify.
- the oil component and the aqueous component are individually heated and dissolved, each is made to flow in a fixed amount, and they are merged. It can also be manufactured by an emulsification method (described in Japanese Patent No. 5086583) using a micromixer in which the mixture is allowed to flow through pores with a diameter of 0.03 mm or more and 20 mm or less.
- the average particle diameter of the lipid fine particles emulsified and dispersed in the lipid fine particle dispersion of the present invention is less than 200 nm, and in terms of stability, it is more preferably less than 150 nm, and less than 130 nm. More preferable.
- the fine lipid fine particles are uniformly emulsified and dispersed in water in a low crystalline state, and therefore, they only enhance the feeling of use as a feeling of use as compared with a conventional preparation containing no lipid fine particles.
- it is useful as a skin cosmetic since it provides a smooth and smooth touch without giving stickiness while the skin after application is mochimochi.
- lipid microparticles are uniformly emulsified and dispersed in water with low crystallinity, it is considered that the membrane fluidity of the lipid microparticles is high, and the permeability of the active ingredient to the stratum corneum and the high barrier function improvement effect Can also be expected.
- the present invention further discloses the following composition.
- a lipid particulate dispersion containing the following components (A) to (E) and having a pH of 3.5 to 8.0, and at a temperature range of 45 ° C to 80 ° C of the lipid particulates A lipid microparticle dispersion having a heat of fusion of 0.30 J / g or less and an average particle size of less than 200 nm.
- A Lipids solid or semi-solid at 25 ° C. other than component (A) selected from sterols and derivatives thereof
- B) (C) anionic surfactant (D) water-soluble solvent (E) water
- the content of the ⁇ 3> component (A) is preferably 0.003% by mass or more, more preferably 0.08% by mass or more, still more preferably 0.2% by mass or more, still more preferably 0.3% by mass Or more, more preferably 0.4% by mass or more, preferably 5.0% by mass or less, more preferably 1.0% by mass or less, still more preferably 0.8% by mass or less, still more preferably 0 .6 mass% or less, preferably 0.003 mass% or more and 5.0 mass% or less, more preferably 0.08 mass% or more and 1.0 mass% or less, still more preferably 0.2 mass% or more.
- the lipid according to ⁇ 1> or ⁇ 2> which is 8% by mass or less, more preferably 0.3% by mass to 0.8% by mass, and still more preferably 0.4% by mass to 0.6% by mass Fine particle dispersion.
- the component (B) contains one or more selected from ceramides, sphingosines, fatty acids having 16 to 22 carbon atoms, and aliphatic alcohols having 12 to 30 carbon atoms
- the lipid fine particle dispersion according to any one of the above.
- the lipid microparticle dispersion of the ⁇ 4> description in which ⁇ 5> ceramides contain the compound chosen from following General formula (1) and (2).
- R 1b is a hydrocarbon group having 10 to 26 carbon atoms
- R 2b is a hydrocarbon group having 9 to 25 carbon atoms
- X is — (CH 2 ) n — (wherein n is 2 to 6) Indicates an integer).
- R 1 and R 2 are the same or different and each represents a hydrocarbon group having 1 to 40 carbon atoms which may be hydroxylated, and R 3 represents an alkylene group having 1 to 6 carbon atoms or a single bond, R 4 represents a hydrogen atom, an alkoxy group having 1 to 12 carbon atoms, or a 2,3-dihydroxypropyloxy group, provided that when R 3 is a single bond, R 4 is a hydrogen atom.
- the content of the ⁇ 6> component (B) is preferably 0.01% by mass or more, more preferably 0.1% by mass or more, still more preferably 0.3% by mass or more, and preferably 5.0 % By mass or less, more preferably 3.0% by mass or less, still more preferably 1.0% by mass or less, preferably 0.01% by mass or more and 5.0% by mass or less, more preferably 0.1% by mass
- the mass ratio (A / B) of the ⁇ 7> component (A) to the component (B) is preferably 0.1 or more, more preferably 0.2 or more, still more preferably 0.3 or more, and preferably 1.0 or less, more preferably 0.8 or less, still more preferably 0.6 or less, preferably 0.1 or more and 1.0 or less, more preferably 0.2 or more and 0.8 or less, more preferably
- the component (C) is preferably N-acylamino acid salt, N-acylmethyl taurine salt, alkyl phosphate, polyoxyethylene alkyl ether phosphate, fatty acid salt, alkyl sulfate, polyoxyethylene alkyl ester.
- N-acyl amino acid salts N-acyl methyl taurine salts, poly Oxyethylene alkyl ether phosphate, fatty acid salt, diacyl amino acid lysine salt, alkyl sulfate ester salt, polyoxyethylene alkyl ether sulfate ester salt, alkyl ether carboxylate and dialkyl sulfosuccinate selected from one or more kinds
- the content of the ⁇ 9> component (C) is preferably 0.002% by mass or more, more preferably 0.05% by mass or more, still more preferably 0.1% by mass or more, and preferably 3.0% by mass. % Or less, more preferably 1.0% by mass or less, still more preferably 0.5% by mass or less, preferably 0.02% by mass or more and 3.0% by mass or less, more preferably 0.05% by mass.
- the total mass of the ⁇ 10> component (A), the component (B) and the component (C) is preferably 0.015% by mass or more, more preferably 0.33% by mass or more, still more preferably 0.5% by mass or more And preferably 13.0% by mass or less, more preferably 5.0% by mass or less, still more preferably 2.0% by mass or less, and preferably 0.015% by mass or more and 13.0% by mass
- the ratio (A + B / C) of the total mass of the component (A) and the component (B) to the mass of the component (C) is preferably 0.05 or more, more preferably 0.5 or more, still more preferably 1 0 or more, more preferably 2.0 or more, preferably 6.0 or less, more preferably 5.5 or less, still more preferably 5.0 or less, and preferably 0.05 or more. .0 or less, more preferably 0.5 or more and 5.5 or less, still more preferably 1.0 or more and 5.5 or less, still more preferably 2.0 or more and 5.5 or less of ⁇ 1> to ⁇ 10>
- the lipid microparticle dispersion according to any of the above.
- the ⁇ 12> component (D) contains one or more selected from polyhydric alcohols and lower alcohols, and more preferably selected from ethanol, glycerin, 1,3-butylene glycol, dipropylene glycol and 1,3-propanediol
- the content of the ⁇ 13> component (D) is preferably 1.0% by mass or more, more preferably 2.0% by mass or more, still more preferably 3.0% by mass or more, and preferably 30% by mass or less It is more preferably 25% by mass or less, still more preferably 20% by mass or less, preferably 1.0% by mass to 30% by mass, more preferably 2.0% by mass to 25% by mass, still more preferably
- the content of the ⁇ 14> component (E) is preferably 50% by mass or more, more preferably 70% by mass or more, still more preferably 80% by mass or more, and preferably 97% by mass or less, more preferably 95% by mass. % By mass or less, more preferably 90% by mass or less, preferably 50% by mass to 97% by mass, more preferably 70% by mass to 95% by mass, still more preferably 80% by mass to 90% by mass.
- ⁇ 15> The lipid fine particle dispersion according to any one of ⁇ 1> to ⁇ 14>, which further contains a component (F) a nonionic surfactant.
- the ⁇ 16> component (F) is preferably a nonionic surfactant of HLB 10 to 20, more preferably a nonionic surfactant of HLB 12 to 15, further preferably a nonionic surfactant of HLB 12.5 to 14.5.
- the ⁇ 17> component (F) is glycerine fatty acid ester, sorbitan fatty acid ester, propylene glycol fatty acid ester, polyethylene glycol fatty acid ester, sucrose fatty acid ester, polyoxyethylene fatty acid ester, polyoxyethylene sorbitan fatty acid ester, polyoxyethylene alkyl ether , Polyoxyethylene sorbitol fatty acid ester, polyoxyethylene glycerin fatty acid ester, polyoxyethylene propylene glycol fatty acid ester, polyoxyethylene castor oil, polyoxyethylene hydrogenated castor oil, polyoxyethylene cured castor oil fatty acid ester, polyoxyethylene phytostanol Ether, polyoxyethylene phytosterose ether, polyoxyethylene cholestanol ether, Polyoxyethylene cholesteryl ethers and polyoxyalkylene-modified organopolysiloxane, selected from polyoxyalkylene-alkyl co-modified organopolysiloxane comprises one or more ⁇
- the content of the ⁇ 18> component (F) is preferably 0.01% by mass or more, more preferably 0.05% by mass or more, still more preferably 0.1% by mass or more, and preferably 10% by mass Or less, more preferably 5.0% by mass or less, still more preferably 1.0% by mass or less, and preferably 0.01% by mass or more and 10% by mass or less, more preferably 0.05% by mass or more
- the lipid microparticle dispersion according to any one of ⁇ 15> to ⁇ 17>, which is 0 mass% or less, more preferably 0.1 mass% to 1.0 mass%.
- the pH is preferably 3.5 to 7.0, more preferably 3.5 to 6.0, and still more preferably 3.5 to 5.5.
- the lipid fine particle dispersion according to any one of the above The lipid fine particle according to any one of ⁇ 1> to ⁇ 19>, wherein the lipid fine particle containing the ⁇ 20> component (A) and the component (B) has low crystallinity and is uniformly emulsified and dispersed in water as fine particles. Dispersion. ⁇ 21> The average particle diameter of the lipid fine particles containing the component (A) and the component (B) emulsified and dispersed in the lipid fine particle dispersion is preferably less than 150 nm, more preferably less than 130 nm. 20. The lipid microparticle dispersion according to any one of 20>. ⁇ 22> A skin cosmetic containing the lipid fine particle dispersion according to any one of ⁇ 1> to ⁇ 21>.
- Micromixer method For the compositions described in Tables 1 to 4 and 7 to 8 and Example 17 described in Table 6, first, Components A, B, D, and F are heated and dissolved at 85 ° C., and uniform oil is obtained. Phase mixture X was prepared. Next, components C and E were heated and dissolved at 85 ° C. to prepare a homogeneous aqueous phase mixture Y. The mixtures X and Y are heated at 85 ° C. while flowing a constant amount of each under a pressure of 0.2 MPa ⁇ s, and they are combined to flow through the pores having a pore size of 0.4 mm to make the lotion-like uniform An emulsified product Z was obtained. The components other than the components D and E and the components A to F were mixed, and homogeneous dissolution was confirmed, and then added to the emulsion Z to obtain each sample.
- a differential scanning calorimeter manufactured by ⁇ DSCVIIevo RIGAKU Co., Ltd.
- the heat of fusion was determined from the total endotherm in the temperature range of 45 ° C to 80 ° C in the melting curve obtained by the measurement (heating rate: 0.3 ° C / min), and applied to the evaluation of A to D below. .
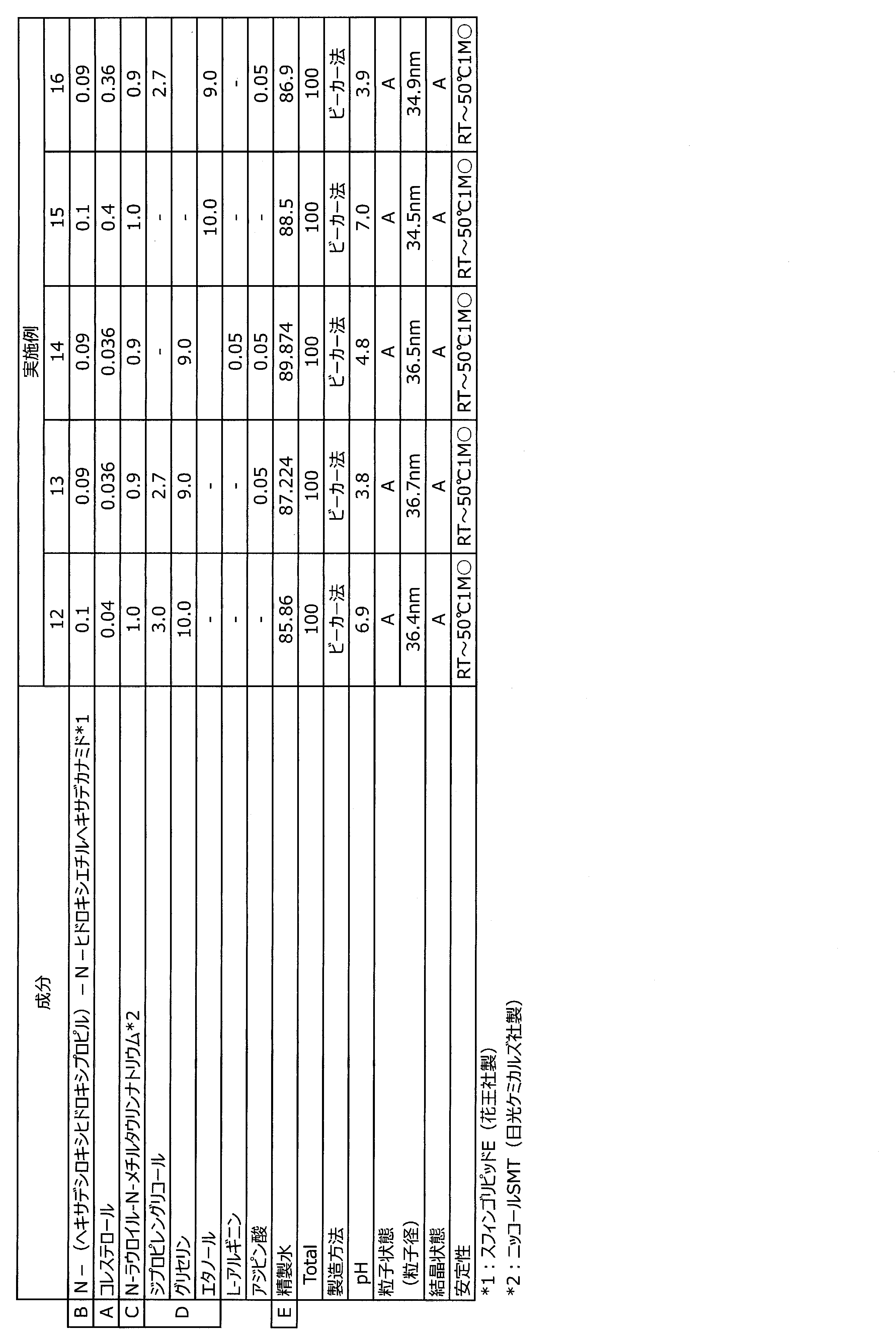
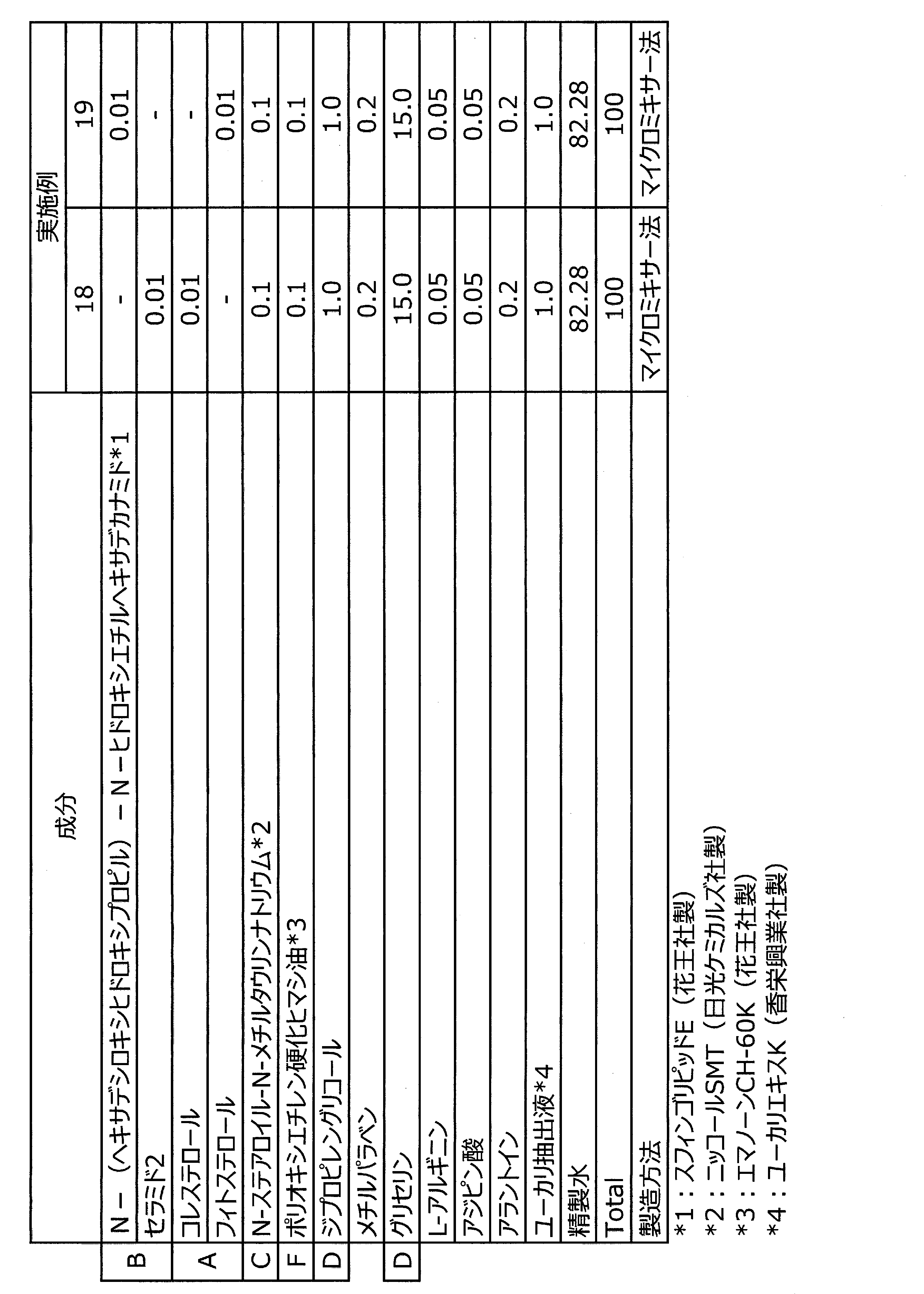
- the lipid fine particle dispersions listed in Tables 1 to 8 were produced, and their physical properties, stability and feeling in use were evaluated. The results are also shown in Tables 1 to 8.
- the lipid fine particle dispersion shown in Table 7 also has low crystallinity of solid fat such as ceramides, is stably emulsified and dispersed as fine particles, and is excellent in stability and feeling in use.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Chemical & Material Sciences (AREA)
- Dispersion Chemistry (AREA)
- Dermatology (AREA)
- Emergency Medicine (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Cosmetics (AREA)
Abstract
セラミド類等の固体脂を結晶化させることなく、微細な粒子として安定に乳化分散させた組成物の提供。 次の成分(A)~(E)を含有し、pHが3.5以上8.0以下である脂質微粒子分散物であり、当該脂質微粒子の45℃以上80℃以下の温度範囲における融解熱量が0.30J/g以下であり、平均粒子径が200nm未満である脂質微粒子分散物。
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水
Description
本発明は、脂質微粒子分散物及び皮膚化粧料に関する。
皮膚の最外層に存在する角質層を構成する角質細胞の間隙には、角層細胞間脂質と呼ばれる脂質が存在している。この角層細胞間脂質の脂質組成は、約50%がセラミドであり、その他コレステロール、コレステロールエステル、脂肪酸等からなる。このうちセラミドは、荒れ肌、乾燥肌等に深く関与しており、セラミドを外用で補うことにより角質層の状態を改善できることが知られている。
かかる観点から、セラミド類等の固体脂を配合した化粧料が種々報告されている。ところが、これらの固体脂は、結晶性が高く、また融点が高いため製剤中での安定化が難しいことから、種々の安定化技術が開発されている。例えば、セラミド含有粒子、融点が30℃以下の脂肪酸、非イオン性界面活性剤、アニオン性界面活性剤等を組み合わせたセラミド分散物(特許文献1)、非イオン性界面活性剤と油分とポリオキシプロピレン・ポリオキシエチレン共重合体ジアルキルエーテルと水を含有する一相マイクロエマルション組成物(特許文献2)、セラミド類と炭素数12~30の脂肪族アルコールを配合して、90℃で相溶化した脂質組成物(特許文献3)、コレステロール脂肪酸エステル等5種を含有する感温性コレステリック液晶組成物(特許文献4)、セラミドとコレステロール等とを相転移温度以上に加熱し、多価アルコールを添加し、その後冷却して液晶型エマルションとする技術(特許文献5)が報告されている。
(特許文献1)国際公開第2010/38814号パンフレット
(特許文献2)特開2007-15972号公報
(特許文献3)特開2004-331595号公報
(特許文献4)特開平2-191208号公報
(特許文献5)特開平9-124432号公報
(特許文献2)特開2007-15972号公報
(特許文献3)特開2004-331595号公報
(特許文献4)特開平2-191208号公報
(特許文献5)特開平9-124432号公報
本発明は、次の成分(A)~(E)を含有し、pHが3.5以上8.0以下である脂質微粒子分散物であり、当該脂質微粒子の45℃以上80以下の温度範囲における融解熱量が0.30J/g以下であり、平均粒子径が200nm未満である脂質微粒子分散物を提供するものである。
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水
前記組成物中においてセラミド類等の固体脂は、結晶化してしまう、当該結晶は比較的大きく不安定である、製剤中において液晶状態では不安定であることが多い等の問題があり、これらの組成物を用いた化粧料では経時的にセラミド類等の固体脂の作用を充分発揮させることができなかった。
一方で皮膚の表面は恒常性を維持する一環で弱酸性に保たれている。そのため、低刺激な皮膚化粧料を設計する上では製剤を肌に近いpHとして弱酸性に調整することが好まれる。しかし、セラミド等の固体脂を安定に乳化分散させるために特定のアニオン性界面活性剤を用いる場合には、アルカリ環境下で特に高い界面活性能を発現し、弱酸性から中性のpHではその界面活性能が失活してしまうという問題がある。
従って、本発明は、酸性条件下においてもセラミド類等の固体脂を結晶化させることなく、微細な粒子として安定に乳化分散させた脂質微粒子分散物を提供することにある。
一方で皮膚の表面は恒常性を維持する一環で弱酸性に保たれている。そのため、低刺激な皮膚化粧料を設計する上では製剤を肌に近いpHとして弱酸性に調整することが好まれる。しかし、セラミド等の固体脂を安定に乳化分散させるために特定のアニオン性界面活性剤を用いる場合には、アルカリ環境下で特に高い界面活性能を発現し、弱酸性から中性のpHではその界面活性能が失活してしまうという問題がある。
従って、本発明は、酸性条件下においてもセラミド類等の固体脂を結晶化させることなく、微細な粒子として安定に乳化分散させた脂質微粒子分散物を提供することにある。
そこで本発明者は、セラミド類等の固体脂の微細分散化及び結晶化防止手段につき種々検討した結果、ステロール類とセラミド類等の固体脂とを併用し、アニオン性界面活性剤と水溶性溶媒を含有させることにより、特定のアニオン性界面活性剤を用いた時に中性からアルカリ性に限らず、酸性条件下においても、セラミド類等の固体脂の結晶性が低く、微細な粒子として安定に乳化分散する脂質微粒子分散物が得られることを見出した。
本発明の脂質微粒子分散物は、酸性条件下においても、セラミド類等の固体脂の結晶性が低く、微細な粒子として安定に乳化分散しており、かつセラミド類等の固体脂の結晶性が低く、微細な粒子として安定に乳化分散することで、これらの固体脂の皮膚に対する作用が十分に発揮される。
本発明の脂質微粒子分散物に用いられる成分(A)は、ステロール及びその誘導体から選ばれる1種以上である。成分(A)は、本発明の脂質微粒子分散物中において、成分(B)の脂質の結晶性を低くし、粒子径を小さく安定化するのに寄与する。
成分(A)としては、コレステロール、フィトステロール及びそれらの誘導体が挙げられる。コレステロール及びフィトステロールの誘導体としては、脂肪酸コレステロールエステル、脂肪酸フィトステロールエステルが挙げられる。ここで、脂肪酸コレステロールエステルとしては、炭素数12~24の脂肪酸とのコレステロールエステルが好ましい。より具体的には、ラウリン酸コレステリル、パルミチン酸コレステリル、ミリスチン酸コレステリル、オレイン酸コレステリル、イソステアリン酸コレステリル、リノール酸コレステリルから選ばれる1種又は2種以上が好ましい。また、N-ラウロイル-L-グルタミン酸ジ(コレステリル/ベヘニル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(コレステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/ベヘニル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)、N-ミリストイル-N-メチルアラニン(フィトステリル/デシルテトラデシル)等のN-アシルアミノ酸のステロールエステルを用いることもでき、N-ラウロイル-L-グルタミン酸ジ(コレステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)が好適に例示できる。N-アシルアミノ酸のステロールエステルの市販品としては味の素社、日本精化社より販売されている「エルデュウPS-203」「Plandool-LG2」(N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルデシル))、「エルデュウCL-301」(N-ラウロイルグルタミン酸ジ(コレステリル/ベヘニル/オクチルドデシル))、「エルデュウCL-202」(N-ラウロイルグルタミン酸ジ(コレステリル/オクチルドデシル))、「エルデュウPS-304」「エルデュウPS-306」「Plandool-LG1」「Plandool-LG3」「Plandool-LG4」(N-ラウロイルグルタミン酸ジ(フィトステリル/ベヘニル/オクチルドデシル))、「エルデュウAPS-307」(N-ミリストイル-N-メチルアラニン(フィトステリル/デシルテトラデシル))等が例示できる。
成分(A)としては、コレステロール、フィトステロール及びそれらの誘導体が挙げられる。コレステロール及びフィトステロールの誘導体としては、脂肪酸コレステロールエステル、脂肪酸フィトステロールエステルが挙げられる。ここで、脂肪酸コレステロールエステルとしては、炭素数12~24の脂肪酸とのコレステロールエステルが好ましい。より具体的には、ラウリン酸コレステリル、パルミチン酸コレステリル、ミリスチン酸コレステリル、オレイン酸コレステリル、イソステアリン酸コレステリル、リノール酸コレステリルから選ばれる1種又は2種以上が好ましい。また、N-ラウロイル-L-グルタミン酸ジ(コレステリル/ベヘニル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(コレステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/ベヘニル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)、N-ミリストイル-N-メチルアラニン(フィトステリル/デシルテトラデシル)等のN-アシルアミノ酸のステロールエステルを用いることもでき、N-ラウロイル-L-グルタミン酸ジ(コレステリル/オクチルドデシル)、N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルドデシル)が好適に例示できる。N-アシルアミノ酸のステロールエステルの市販品としては味の素社、日本精化社より販売されている「エルデュウPS-203」「Plandool-LG2」(N-ラウロイル-L-グルタミン酸ジ(フィトステリル/オクチルデシル))、「エルデュウCL-301」(N-ラウロイルグルタミン酸ジ(コレステリル/ベヘニル/オクチルドデシル))、「エルデュウCL-202」(N-ラウロイルグルタミン酸ジ(コレステリル/オクチルドデシル))、「エルデュウPS-304」「エルデュウPS-306」「Plandool-LG1」「Plandool-LG3」「Plandool-LG4」(N-ラウロイルグルタミン酸ジ(フィトステリル/ベヘニル/オクチルドデシル))、「エルデュウAPS-307」(N-ミリストイル-N-メチルアラニン(フィトステリル/デシルテトラデシル))等が例示できる。
成分(A)は、1種以上を用いることができ、成分(B)の結晶性を低くし、粒子径を小さく安定化する観点から、本発明の脂質微粒子分散物中に、0.003質量%以上含有するのが好ましく、0.08質量%以上含有するのがより好ましく、0.2質量%以上含有するのがさらに好ましく、0.3質量%以上含有するのがよりさらに好ましく、0.4質量%以上含有するのがよりさらに好ましい。また、同様の観点から5.0質量%以下含有するのが好ましく、1.0質量%以下含有するのがより好ましく、0.8質量%以下含有するのがさらに好ましく、0.6質量%以下含有するのがよりさらに好ましい。具体的には、0.003質量%以上5.0質量%以下含有するのが好ましく、0.08質量%以上1.0質量%以下含有するのがより好ましく、0.2質量%以上0.8質量%以下含有するのがさらに好ましく、0.3質量%以上0.8質量%以下含有するのがよりさらに好ましく、0.4質量%以上0.6質量%以下含有するのがよりさらに好ましい。
成分(B)は、成分(A)以外の25℃で固体又は半固体の脂質である。ここで、25℃で固体又は半固体とは、25℃における粘度が10000mPa・sより大きいことをいう。粘度は、B型粘度計(VISCOMETER TVB-10、東機産業社製)、ローターNo.4、12rpm、1分で測定するものである。当該成分(B)は、皮膚に対して保湿作用、バリア機能改善作用等を示し、化粧料の有効成分である。ここで、固体又は半固体の脂質としては、融点が50~150℃である脂質が挙げられる。成分(B)としては、セラミド類、スフィンゴシン類(天然物と合成物を含む)などのスフィンゴ脂質;ステアリン酸、ベヘン酸等の炭素数16~22の脂肪酸;セチルアルコール、ステアリルアルコール、ベヘニルアルコール、バチルアルコール、キミルアルコールなどの炭素数12~30の脂肪族アルコールなどが挙げられる。
セラミド類としては、天然セラミド、スフィンゴシン誘導体などの他、特開昭62-228048号公報、特開昭63-216812号公報、特開昭63-227513号公報、特開昭64-29347号公報、特開昭64-31752号公報、特開平8-319263号公報などに記載のセラミド類似構造物質(合成セラミド)が例示される。具体的には、次の一般式(1)及び(2)から選ばれる化合物が好ましく、特に一般式(1)の化合物が好ましい。
〔式中、R1bは炭素数10~26の炭化水素基、R2bは炭素数9~25の炭化水素基を示し、Xは-(CH2)n-(ここでnは2~6の整数を示す)を示す。〕
(式中、R1及びR2は同一又は異なって炭素数1~40のヒドロキシル化されていてもよい炭化水素基を示し、R3は炭素数1~6のアルキレン基又は単結合を示し、R4は水素原子、炭素数1~12のアルコキシ基又は2,3-ジヒドロキシプロピルオキシ基を示す。ただし、R3が単結合のとき、R4は水素原子である。)
なお、前記一般式(1)及び(2)中、炭化水素基としてはアルキル基又はアルケニル基が好ましい。
一般式(1)の化合物の例としては、N-(ヘキサデシロキシヒドロキシプロピル)-N-ヒドロキシエチルヘキサデカナミドが挙げられ、一般式(2)の化合物の例としては長鎖二塩基酸ビス3-メトキシプロピルアミドが挙げられる。
これらの成分(B)のうち、保湿作用、バリア機能改善作用の観点から、天然セラミド、前記一般式(1)及び(2)等の合成セラミド、炭素数12~30の脂肪族アルコールが好ましい。これらの脂質は、1種又は2種以上を組み合わせて用いることができる。
これらの成分(B)のうち、保湿作用、バリア機能改善作用の観点から、天然セラミド、前記一般式(1)及び(2)等の合成セラミド、炭素数12~30の脂肪族アルコールが好ましい。これらの脂質は、1種又は2種以上を組み合わせて用いることができる。
成分(B)は、保湿作用、バリア機能改善作用の観点から、本発明の脂質微粒子分散物中に0.01質量%以上含有するのが好ましく、0.1質量%以上がより好ましく、0.3質量%以上がさらに好ましく、また、結晶性を低くし、粒子径を小さく安定化する観点から、5.0質量%以下が好ましく、3.0質量%以下がより好ましく、1.0質量%以下がさらに好ましい。具体的な範囲としては0.01質量%以上5.0質量%以下が好ましく、0.1質量%以上3.0質量%以下がより好ましく、0.3質量%以上1.0質量%以下がさらに好ましい。
本発明の脂質微粒子分散物における成分(A)と成分(B)の質量比(A/B)は、成分(B)の結晶性を低くし安定化させる観点から、0.1以上が好ましく、0.2以上がより好ましく、0.3以上がさらに好ましく、また1.0以下が好ましく、0.8以下がより好ましく、0.6以下がさらに好ましい。具体的な範囲としては0.1以上1.0以下が好ましく、0.2以上0.8以下がより好ましく、0.3以上0.6以下がさらに好ましい。
成分(C)は、アニオン性界面活性剤である。アニオン性界面活性剤としては、アルカリ、中性条件のみならず酸性条件も含むpH3.5から8.0において十分な界面活性能の発現の観点から、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、アルキルリン酸塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩、ジアルキルスルホコハク酸塩、ジアシルアミノ酸リシン塩等が好ましい。このうち、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上が好ましい。さらに、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上がより好ましい。また、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩及びジアシルアミノ酸リシン塩から選ばれる1種又は2種以上がさらに好ましく、N-アシルアミノ酸塩及びN-アシルメチルタウリン塩から選ばれる1種又は2種以上がよりさらに好ましい。
N-アシルアミノ酸塩としては、N-ラウロイル-L-グルタミン酸ナトリウム、N-ステアロイル-L-グルタミン酸ナトリウム、N-ステアロイル-L-グルタミン酸アルギニン、N-ミリストイル-L-グルタミン酸ナトリウム、N-ラウロイルサルコシンナトリウム等のN-アシルグルタミン酸塩、N-アシルサルコシン塩等が挙げられる。N-アシルメチルタウリン塩としては、N-ミリストイル-N-メチルタウリンナトリウム、N-ラウロイル-N-メチルタウリンナトリウム、N-ステアロイル-N-メチルタウリンナトリウム等が挙げられる。アルキルリン酸塩としては、モノミリスチルリン酸ナトリウム、モノステアリルリン酸ナトリウム、ジ(C12-C15)パレス-8-リン酸ナトリウム等が挙げられる。ポリオキシエチレンアルキルリン酸塩としては、ポリオキシエチレンオレイルエーテルリン酸ナトリウム、ポリオキシエチレンセチルエーテルリン酸ナトリウム、ポリオキシエチレンステアリルエーテルリン酸ナトリウム等が挙げられる。脂肪酸塩としては、ラウリン酸ナトリウム、パルミチン酸カリウム、ステアリン酸アルギニン塩等の炭素数12~24の脂肪酸塩が挙げられる。アルキル硫酸エステル塩としては、ラウリル硫酸ナトリウム、ラウリル硫酸カリウム等が挙げられる。ポリオキシエチレンアルキルエーテル硫酸エステル塩としては、ポリオキシエチレンラウリル硫酸トリエタノールアミン塩等が挙げられる。アルキルエーテルカルボン酸塩としては、ポリオキシエチレンラウリルエーテル酢酸塩等が挙げられる。ジアルキルスルホコハク酸塩としては、ジ-2-エチルヘキシルスルホコハク酸ナトリウム等が挙げられる。ジアシルアミノ酸リシン塩としては、ジラウロイルグルタミン酸リシンナトリウム等が挙げられる。これらのアニオン性界面活性剤は1種又は2種以上を使用することができる。
N-アシルアミノ酸塩としては、N-ラウロイル-L-グルタミン酸ナトリウム、N-ステアロイル-L-グルタミン酸ナトリウム、N-ステアロイル-L-グルタミン酸アルギニン、N-ミリストイル-L-グルタミン酸ナトリウム、N-ラウロイルサルコシンナトリウム等のN-アシルグルタミン酸塩、N-アシルサルコシン塩等が挙げられる。N-アシルメチルタウリン塩としては、N-ミリストイル-N-メチルタウリンナトリウム、N-ラウロイル-N-メチルタウリンナトリウム、N-ステアロイル-N-メチルタウリンナトリウム等が挙げられる。アルキルリン酸塩としては、モノミリスチルリン酸ナトリウム、モノステアリルリン酸ナトリウム、ジ(C12-C15)パレス-8-リン酸ナトリウム等が挙げられる。ポリオキシエチレンアルキルリン酸塩としては、ポリオキシエチレンオレイルエーテルリン酸ナトリウム、ポリオキシエチレンセチルエーテルリン酸ナトリウム、ポリオキシエチレンステアリルエーテルリン酸ナトリウム等が挙げられる。脂肪酸塩としては、ラウリン酸ナトリウム、パルミチン酸カリウム、ステアリン酸アルギニン塩等の炭素数12~24の脂肪酸塩が挙げられる。アルキル硫酸エステル塩としては、ラウリル硫酸ナトリウム、ラウリル硫酸カリウム等が挙げられる。ポリオキシエチレンアルキルエーテル硫酸エステル塩としては、ポリオキシエチレンラウリル硫酸トリエタノールアミン塩等が挙げられる。アルキルエーテルカルボン酸塩としては、ポリオキシエチレンラウリルエーテル酢酸塩等が挙げられる。ジアルキルスルホコハク酸塩としては、ジ-2-エチルヘキシルスルホコハク酸ナトリウム等が挙げられる。ジアシルアミノ酸リシン塩としては、ジラウロイルグルタミン酸リシンナトリウム等が挙げられる。これらのアニオン性界面活性剤は1種又は2種以上を使用することができる。
本発明の脂質微粒子分散物中の成分(C)の含有量は、製剤の安定性と使用する皮膚表面の恒常性の観点から、0.002質量%以上が好ましく、0.05質量%以上がより好ましく、0.1質量%以上がさらに好ましく、また、3.0質量%以下が好ましく、1.0質量%以下がより好ましく、0.5質量%以下がさらに好ましい。具体的には、0.002質量%以上3.0質量%以下が好ましく、0.05質量%以上1.0質量%以下がより好ましく、0.1質量%以上0.5質量%以下がさらに好ましい。
本発明の脂質微粒子分散物における成分(A)、成分(B)及び成分(C)の合計質量は、保湿作用、バリア機能改善作用の点から、脂質微粒子分散物総量の0.015質量%以上が好ましく、0.33質量%以上がより好ましく、0.5質量%以上がさらに好ましく、また13.0質量%以下が好ましく、5.0質量%以下がより好ましく、2.0質量%以下がさらに好ましい。具体的な範囲としては、0.015質量%以上13.0質量%以下が好ましく、0.33質量%以上5.0質量%以下がより好ましく、0.5質量%以上2.0質量%以下がさらに好ましい。
本発明の脂質微粒子分散物における成分(A)と成分(B)の合計質量と成分(C)の質量の比(A+B/C)は、保湿作用、バリア機能改善作用や安定性の点から0.05以上が好ましく、0.5以上がより好ましく、1.0以上がさらに好ましく、2.0以上がよりさらに好ましく、また6.0以下が好ましく、5.5以下がより好ましく、5.0以下がさらに好ましい。具体的な範囲としては、0.05以上6.0以下が好ましく、0.5以上5.5以下がより好ましく、1.0以上5.5以下がさらに好ましく、2.0以上5.5以下がよりさらに好ましい。
成分(D)は、水溶性溶媒である。水溶性溶媒は、本発明の脂質微粒子分散物において、成分(A)及び成分(B)、あるいは成分(A)、成分(B)、及び成分(C)を効率的に均一溶解することや、安定性の向上、使用感の調整に寄与する。(D)水溶性溶媒としては、エチレングリコール、ジエチレングリコール、トリエチレングリコール、ポリエチレングリコール(平均分子量1000未満)、プロピレングリコール、ジプロピレングリコール、ポリプロピレングリコール(平均分子量:1000未満)、グリセリン、ジグリセリン、ポリグリセリン、イソプレングリコール、1,2-ペンタンジオール、1,3-プロパンジオール、1,3-ブチレングリコール、ヘキシレングリコール、メチルグルセス等の多価アルコール、メタノール、エタノール等の低級アルコール等を挙げることができる。このうち、グリセリン、1,3-ブチレングリコール、ジプロピレングリコール、1,3-プロパンジオール等が特に好ましい。これらの成分(D)は1種又は2種以上を使用することができる。
成分(D)の含有量は、成分(A)及び成分(B)、あるいは成分(A)、成分(B)、及び成分(C)を効率的に均一溶解することや、安定性、使用感の点から、本発明の脂質微粒子分散物中に1.0質量%以上が好ましく、2.0質量%以上がより好ましく、3.0質量%以上がさらに好ましく、30質量%以下が好ましく、25質量%以下がより好ましく、20質量%以下がさらに好ましい。具体的な範囲としては、1.0質量%以上30質量%以下が好ましく、2.0質量%以上25質量%以下がより好ましく、3.0質量%以上20質量%以下がさらに好ましい。
本発明の脂質微粒子分散物は、さらに成分(E)水を含有する。本発明の脂質微粒子分散物中の(E)水の含有量は、安定性、使用感の点から50質量%以上が好ましく、70質量%以上がより好ましく、80質量%以上がさらに好ましく、また、97質量%以下が好ましく、95質量%以下がより好ましく、90質量%以下がさらに好ましい。具体的な範囲としては、50質量%以上97質量%以下が好ましく、70質量%以上95質量%以下がより好ましく、80質量%以上90質量%以下がさらに好ましい。
本発明の脂質微粒子分散物は、さらに成分(F)非イオン性界面活性剤を含有するのが、安定性の点で好ましい。このような(F)非イオン性界面活性剤としては、HLB10~20の非イオン性界面活性剤が好ましく、HLB12~15の非イオン性界面活性剤がより好ましく、HLB12.5~14.5の非イオン性界面活性剤がさらに好ましい。
ここで、HLB(親水性親油性バランス)は、例えば下記式により求めることができるものである。
ここで、HLB(親水性親油性バランス)は、例えば下記式により求めることができるものである。
式:〔HLB〕=7+1.171log(Mw/Mo)
(式中、Mwは界面活性剤の親水性基の分子量、Moは界面活性剤の疎水性基の分子量、logは底が10の対数を示す。)
(式中、Mwは界面活性剤の親水性基の分子量、Moは界面活性剤の疎水性基の分子量、logは底が10の対数を示す。)
また非イオン性界面活性剤として、界面活性剤Xと界面活性剤Yの2種類を併用する場合、それぞれのHLBをHLBX及びHLBYとした時、両者を混合した非イオン性界面活性剤のHLBは、それぞれの質量分率をWX、WYとすると、
式:〔HLB〕=〔(WX×HLBX)+(WY×HLBY)〕÷(WX+WY)
に基づいて求められる。また、非イオン性界面活性剤として3種類以上を併用する場合、前記と同様にしてそれらを混合した非イオン性界面活性剤のHLBを求めることができる。尚、本発明においては、混合した非イオン性界面活性剤のHLBが上記の範囲となることが好ましく、HLB10~20以外の非イオン性界面活性剤も用いることができる。
式:〔HLB〕=〔(WX×HLBX)+(WY×HLBY)〕÷(WX+WY)
に基づいて求められる。また、非イオン性界面活性剤として3種類以上を併用する場合、前記と同様にしてそれらを混合した非イオン性界面活性剤のHLBを求めることができる。尚、本発明においては、混合した非イオン性界面活性剤のHLBが上記の範囲となることが好ましく、HLB10~20以外の非イオン性界面活性剤も用いることができる。
成分(F)の非イオン性界面活性剤としては、例えば、グリセリン脂肪酸エステル、ソルビタン脂肪酸エステル、プロピレングリコール脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ショ糖脂肪酸エステル、ポリオキシエチレン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンソルビトール脂肪酸エステル、ポリオキシエチレングリセリン脂肪酸エステル、ポリオキシエチレンプロピレングリコール脂肪酸エステル、ポリオキシエチレンヒマシ油、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレン硬化ヒマシ油脂肪酸エステル、ポリオキシエチレンフィトスタノールエーテル、ポリオキシエチレンフィトステロースエーテル、ポリオキシエチレンコレスタノールエーテル、ポリオキシエチレンコレステリルエーテル、ポリオキシアルキレン変性オルガノポリシロキサン、ポリオキシアルキレン・アルキル共変性オルガノポリシロキサン等が挙げられる。
これらのうち、安定性の点から、オキシエチレン基の平均付加モル数が25~80のポリオキシエチレン硬化ヒマシ油、オキシエチレン基の平均付加モル数が10~140のポリオキシエチレン脂肪酸エステル、炭素数が12~18のアルキル基でありオキシエチレン基の平均付加モル数が20のポリオキシエチレンソルビタン脂肪酸エステル、炭素数が16~22のアルキル基とオキシエチレン基の平均付加モル数が15~25のポリオキシエチレンアルキルエーテル、オキシエチレン基の平均付加モル数が10~20であるポリオキシエチレン・メチルポリシロキサン共重合体が好ましく、オキシエチレン基の平均付加モル数が25~80のポリオキシエチレン硬化ヒマシ油、炭素数が16~22のアルキル基とオキシエチレン基の平均付加モル数が15~25のポリオキシエチレンアルキルエーテルがより好ましく、オキシエチレン基の平均付加モル数が35~65のポリオキシエチレン硬化ヒマシ油、炭素数が16~20のアルキル基とオキシエチレン基の平均付加モル数が20~25のポリオキシエチレンアルキルエーテルがさらに好ましい。
また、成分(F)としては、ポリオキシエチレン硬化ヒマシ油(40EO)として、エマノーンCH-40(HLB12.5、花王社製)、ポリオキシエチレン硬化ヒマシ油(60EO)として、エマノーンCH-60(K)(HLB14.0、花王社製)、ポリオキシエチレンイソセチルエーテル(20EO)として、EMALEX1620(HLB14、日本エマルジョン社製)、ポリオキシエチレンイソステアリルエーテル(25EO)として、EMALEX1825(HLB14、日本エマルジョン社製)などの市販品を使用することができる。
これらの成分(F)は1種又は2種を使用することができる。
これらの成分(F)は1種又は2種を使用することができる。
本発明の脂質微粒子分散物中の成分(F)の含有量は、安定性の点から、0.01質量%以上が好ましく、0.05質量%以上がより好ましく、0.1質量%以上がさらに好ましく、また、10質量%以下が好ましく、5.0質量%以下がより好ましく、1.0質量%以下がさらに好ましい。具体的な範囲としては0.01質量%以上10質量%以下が好ましく、0.05質量%以上5.0質量%以下がより好ましく、0.1質量%以上1.0質量%以下がさらに好ましい。
本発明の脂質微粒子分散物は、前記成分(A)及び成分(B)が水中に分散乳化した形態であり、そのpHは3.5以上8.0以下である。本発明の脂質微粒子分散物は、pHが3.5以上8.0以下と酸性条件も含め結晶性が低く、微細な粒子として安定に存在するため、皮膚表面の恒常性を保ちながら使用感が良好である。当該pHは、皮膚表面の恒常性、使用感の点から3.5以上7.0以下がより好ましく、3.5以上6.0以下がより好ましく、3.5以上5.5以下がさらに好ましい。
本発明の脂質微粒子分散物は、pHを前記範囲に調整するため、更に、塩基及び/又は酸を含有することができる。
塩基としては、特に制限されず、有機塩基であっても無機塩基であっても良い。
有機塩基は、塩基性アミノ酸、アルカノールアミンから選ばれる1種又は2種以上が好ましい。具体的には、L-アルギニン、リジン、ヒスチジン等の塩基性アミノ酸;モノエタノールアミン、ジエタノールアミン、トリエタノールアミン、アミノメチルプロパノール、アミノメチルプロパンジオール、アミノエチルプロパンジオール、トリスヒドロキシメチルアミノエタン等のアルカノールアミンから選ばれる1種又は2種以上が好ましい。
また、無機塩基は、水酸化カルシウム、水酸化ナトリウム、水酸化カリウムから選ばれる1種又は2種以上が好ましい。
これらのうち、L-アルギニン、水酸化カルシウム、水酸化ナトリウム、水酸化カリウムから選ばれる1種又は2種以上がより好ましい。
塩基としては、特に制限されず、有機塩基であっても無機塩基であっても良い。
有機塩基は、塩基性アミノ酸、アルカノールアミンから選ばれる1種又は2種以上が好ましい。具体的には、L-アルギニン、リジン、ヒスチジン等の塩基性アミノ酸;モノエタノールアミン、ジエタノールアミン、トリエタノールアミン、アミノメチルプロパノール、アミノメチルプロパンジオール、アミノエチルプロパンジオール、トリスヒドロキシメチルアミノエタン等のアルカノールアミンから選ばれる1種又は2種以上が好ましい。
また、無機塩基は、水酸化カルシウム、水酸化ナトリウム、水酸化カリウムから選ばれる1種又は2種以上が好ましい。
これらのうち、L-アルギニン、水酸化カルシウム、水酸化ナトリウム、水酸化カリウムから選ばれる1種又は2種以上がより好ましい。
また、酸は、有機酸、無機酸のいずれでも良い。
有機酸はモノカルボン酸、ジカルボン酸、オキシカルボン酸、酸性アミノ酸から選ばれる1種又は2種以上が好ましい。具体的には、酢酸、プロピオン酸、酪酸等のモノカルボン酸;コハク酸、フタル酸、フマル酸、シュウ酸、マロン酸、グルタル酸、アジピン酸等のジカルボン酸;グリコール酸、クエン酸、乳酸、ピルビン酸、リンゴ酸、酒石酸等のオキシカルボン酸;グルタミン酸、アスパラギン酸等の酸性アミノ酸から選ばれる1種又は2種以上が好ましい。
また、無機酸は、塩酸、硝酸、亜硝酸、硫酸、亜硫酸、リン酸、ホスホン酸、ホスフィン酸から選ばれる1種又は2種以上が好ましい。
これらの中で、アジピン酸及びリン酸から選ばれる1種又は2種以上がより好ましい。
有機酸はモノカルボン酸、ジカルボン酸、オキシカルボン酸、酸性アミノ酸から選ばれる1種又は2種以上が好ましい。具体的には、酢酸、プロピオン酸、酪酸等のモノカルボン酸;コハク酸、フタル酸、フマル酸、シュウ酸、マロン酸、グルタル酸、アジピン酸等のジカルボン酸;グリコール酸、クエン酸、乳酸、ピルビン酸、リンゴ酸、酒石酸等のオキシカルボン酸;グルタミン酸、アスパラギン酸等の酸性アミノ酸から選ばれる1種又は2種以上が好ましい。
また、無機酸は、塩酸、硝酸、亜硝酸、硫酸、亜硫酸、リン酸、ホスホン酸、ホスフィン酸から選ばれる1種又は2種以上が好ましい。
これらの中で、アジピン酸及びリン酸から選ばれる1種又は2種以上がより好ましい。
これらの塩基及び/又は酸は、本発明の脂質微粒子分散物のpHが前記範囲になるような量を含有するのが好ましい。
本発明の脂質微粒子分散物には、さらに前記成分以外に、通常の化粧料に用いられる成分、例えば、油性成分、保湿剤、酸化防止剤、防腐剤、キレート剤、美白剤、紫外線吸収剤、ビタミン類、植物抽出物、その他各種薬効成分、粉体、香料、色材などを含有させることができる。
本発明の脂質微粒子分散物は、例えば成分(A)~(D)を含む油性成分を混合し、80~95℃で加熱溶解し、これに(E)水を加えて撹拌し均一に乳化させることにより製造できる。また、成分(A)~(E)、及び必要に応じて用いられるその他の成分の内、油性成分と水性成分とをそれぞれ個別に加熱溶解し、それぞれを一定量で流動させると共に、それらを合流させ、孔径が0.03mm以上20mm以下の細孔に流通させるマイクロミキサーを利用した乳化方法(特許第5086583号公報記載)によっても製造することができる。
本発明の脂質微粒子分散物は、成分(A)及び成分(B)を含む微細化された脂質微粒子が、結晶性が低い状態で水中に均一に乳化分散している組成物である。当該脂質微粒子が微細且つ結晶性の低い状態で存在するか否かは、動的光散乱法及び示差走査熱量測定により確認することができる。すなわち、まず、脂質微粒子の存在とその粒子径は動的光散乱法により測定されるキュムラント径により測定できる。また、その脂質微粒子の結晶性が低いものであることについては、示差走査熱量測定で45℃以上80℃以下の温度域における融解熱量が0.30J/g以下であることにより確認できる。
また、本発明の脂質微粒子分散物中に乳化分散している脂質微粒子の平均粒子径は、200nm未満であり、安定性の点で、150nm未満であるのがより好ましく、130nm未満であるのがさらに好ましい。
また、本発明の脂質微粒子分散物中に乳化分散している脂質微粒子の平均粒子径は、200nm未満であり、安定性の点で、150nm未満であるのがより好ましく、130nm未満であるのがさらに好ましい。
本発明の脂質微粒子分散物は、微細な脂質微粒子が、結晶性の低い状態で水中に均一に乳化分散しているため、従来の脂質微粒子を含まない製剤に比べ使用感としてしっとり感を高めるのみならず、同時に塗布後の肌をモチモチとしながらべたつきを与えずさっぱり滑らかな肌触りにするため、皮膚化粧料として有用である。また、脂質微粒子が結晶性が低い状態で水中に均一に乳化分散しているため、脂質微粒子の膜流動性が高いと考えられ、有効成分の角層への高い浸透性や高いバリア機能改善効果も期待できる。
上述した実施形態に関し、本発明はさらに以下の組成物を開示する。
<1>次の成分(A)~(E)を含有し、pHが3.5以上8.0以下である脂質微粒子分散物であり、当該脂質微粒子の45℃以上80℃以下の温度範囲における融解熱量が0.30J/g以下であり、平均粒子径が200nm未満である脂質微粒子分散物。
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水
<2>成分(A)が、コレステロール、フィトステロール及びそれらの誘導体から選ばれる1種以上であり、より好ましくはコレステロール、脂肪酸コレステロールエステル、脂肪酸フィトステロールエステル、N-アシルアミノ酸コレステロールエステル及びN-アシルアミノ酸フィトステロールエステルから選ばれる1種以上を含む<1>記載の脂質微粒子分散物。
<3>成分(A)の含有量が、好ましくは0.003質量%以上、より好ましくは0.08質量%以上、さらに好ましくは0.2質量%以上、よりさらに好ましくは0.3質量%以上、よりさらに好ましくは0.4質量%以上であり、また好ましくは5.0質量%以下、より好ましくは1.0質量%以下、さらに好ましくは0.8質量%以下、よりさらに好ましくは0.6質量%以下であり、好ましくは0.003質量%以上5.0質量%以下、より好ましくは0.08質量%以上1.0質量%以下、さらに好ましくは0.2質量%以上0.8質量%以下、よりさらに好ましくは0.3質量%以上0.8質量%以下、よりさらに好ましくは0.4質量%以上0.6質量%以下である<1>又は<2>記載の脂質微粒子分散物。
<4>成分(B)が、セラミド類、スフィンゴシン類、炭素数16~22の脂肪酸、及び炭素数12~30の脂肪族アルコールから選ばれる1種以上を含む<1>~<3>のいずれかに記載の脂質微粒子分散物。
<5>セラミド類が、次の一般式(1)及び(2)から選ばれる化合物を含む<4>記載の脂質微粒子分散物。
<3>成分(A)の含有量が、好ましくは0.003質量%以上、より好ましくは0.08質量%以上、さらに好ましくは0.2質量%以上、よりさらに好ましくは0.3質量%以上、よりさらに好ましくは0.4質量%以上であり、また好ましくは5.0質量%以下、より好ましくは1.0質量%以下、さらに好ましくは0.8質量%以下、よりさらに好ましくは0.6質量%以下であり、好ましくは0.003質量%以上5.0質量%以下、より好ましくは0.08質量%以上1.0質量%以下、さらに好ましくは0.2質量%以上0.8質量%以下、よりさらに好ましくは0.3質量%以上0.8質量%以下、よりさらに好ましくは0.4質量%以上0.6質量%以下である<1>又は<2>記載の脂質微粒子分散物。
<4>成分(B)が、セラミド類、スフィンゴシン類、炭素数16~22の脂肪酸、及び炭素数12~30の脂肪族アルコールから選ばれる1種以上を含む<1>~<3>のいずれかに記載の脂質微粒子分散物。
<5>セラミド類が、次の一般式(1)及び(2)から選ばれる化合物を含む<4>記載の脂質微粒子分散物。
〔式中、R1bは炭素数10~26の炭化水素基、R2bは炭素数9~25の炭化水素基を示し、Xは-(CH2)n-(ここでnは2~6の整数を示す)を示す。〕
(式中、R1及びR2は同一又は異なって炭素数1~40のヒドロキシル化されていてもよい炭化水素基を示し、R3は炭素数1~6のアルキレン基又は単結合を示し、R4は水素原子、炭素数1~12のアルコキシ基又は2,3-ジヒドロキシプロピルオキシ基を示す。ただし、R3が単結合のとき、R4は水素原子である。)
<6>成分(B)の含有量が、好ましくは0.01質量%以上、より好ましくは0.1質量%以上、さらに好ましくは0.3質量%以上であり、また、好ましくは5.0質量%以下、より好ましくは3.0質量%以下、さらに好ましくは1.0質量%以下であり、また、好ましくは0.01質量%以上5.0質量%以下、より好ましくは0.1質量%以上3.0質量%以下、さらに好ましくは0.3質量%以上1.0質量%以下である<1>~<5>のいずれかに記載の脂質微粒子分散物。
<7>成分(A)と成分(B)の質量比(A/B)が好ましくは0.1以上、より好ましくは0.2以上、さらに好ましくは0.3以上であり、また、好ましくは1.0以下、より好ましくは0.8以下、さらに好ましくは0.6以下であり、また好ましくは0.1以上1.0以下、より好ましくは0.2以上0.8以下、さらに好ましくは0.3以上0.6以下である<1>~<6>のいずれかに記載の脂質微粒子分散物。
<8>成分(C)が、好ましくはN-アシルアミノ酸塩、N-アシルメチルタウリン塩、アルキルリン酸塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩、ジアルキルスルホコハク酸塩及びジアシルアミノ酸リシン塩から選ばれる1種又は2種以上を含み、より好ましくは、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上を含み、さらに好ましくは、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上を含み、さらにより好ましくはN-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩及びジアシルアミノ酸リシン塩から選ばれる1種又は2種以上を含み、特に好ましくはN-アシルアミノ酸塩及びN-アシルメチルタウリン塩から選ばれる1種又は2種以上を含む<1>~<7>のいずれかに記載の脂質微粒子分散物。
<9>成分(C)の含有量が、好ましくは0.002質量%以上、より好ましくは0.05質量%以上、さらに好ましくは0.1質量%以上であり、また好ましくは3.0質量%以下、より好ましくは1.0質量%以下、さらに好ましくは0.5質量%以下であり、また、好ましくは0.02質量%以上3.0質量%以下、より好ましくは0.05質量%以上1.0質量%以下、さらに好ましくは0.1質量%以上0.5質量%以下である<1>~<8>のいずれかに記載の脂質微粒子分散物。
<10>成分(A)、成分(B)及び成分(C)の合計質量が、好ましくは0.015質量%以上、より好ましくは0.33質量%以上、さらに好ましくは0.5質量%以上であり、また好ましくは13.0質量%以下、より好ましくは5.0質量%以下、さらに好ましくは2.0質量%以下であり、また、好ましくは0.015質量%以上13.0質量%以下、より好ましくは0.33質量%以上5.0質量%以下、さらに好ましくは0.5質量%以上2.0質量%以下である<1>~<9>のいずれかに記載の脂質微粒子分散物。
<11>成分(A)と成分(B)の合計質量と成分(C)の質量の比(A+B/C)が、好ましくは0.05以上、より好ましくは0.5以上、さらに好ましくは1.0以上、よりさらに好ましくは2.0以上であり、また、好ましくは6.0以下、より好ましくは5.5以下、さらに好ましくは5.0以下であり、また好ましくは0.05以上6.0以下、より好ましくは0.5以上5.5以下、さらに好ましくは1.0以上5.5以下、よりさらに好ましくは2.0以上5.5以下である<1>~<10>のいずれかに記載の脂質微粒子分散物。
<12>成分(D)が、多価アルコール及び低級アルコールから選ばれる1種以上を含み、より好ましくはエタノール、グリセリン、1,3-ブチレングリコール、ジプロピレングリコール及び1,3-プロパンジオールから選ばれる1種以上を含む<1>~<11>のいずれかに記載の脂質微粒子分散物。
<13>成分(D)の含有量が、好ましくは1.0質量%以上、より好ましくは2.0質量%以上、さらに好ましくは3.0質量%以上であり、また好ましくは30質量%以下、より好ましくは25質量%以下、さらに好ましくは20質量%以下であり、また好ましくは1.0質量%以上30質量%以下、より好ましくは2.0質量%以上25質量%以下、さらに好ましくは3.0質量%以上20質量%以下である<1>~<12>のいずれかに記載の脂質微粒子分散物。
<14>成分(E)の含有量が、好ましくは50質量%以上、より好ましくは70質量%以上、さらに好ましくは80質量%以上であり、また、好ましくは97質量%以下、より好ましくは95質量%以下、さらに好ましくは90質量%以下であり、また、好ましくは50質量%以上97質量%以下、より好ましくは70質量%以上95質量%以下、さらに好ましくは80質量%以上90質量%以下である<7>~<13>のいずれかに記載の脂質微粒子分散物。
<15>さらに成分(F)非イオン性界面活性剤を含有する<1>~<14>のいずれかに記載の脂質微粒子分散物。
<16>成分(F)が、好ましくはHLB10~20の非イオン性界面活性剤、より好ましくはHLB12~15の非イオン性界面活性剤、さらに好ましくはHLB12.5~14.5の非イオン性界面活性剤を含む<15>記載の脂質微粒子分散物。
<17>成分(F)が、グリセリン脂肪酸エステル、ソルビタン脂肪酸エステル、プロピレングリコール脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ショ糖脂肪酸エステル、ポリオキシエチレン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンソルビトール脂肪酸エステル、ポリオキシエチレングリセリン脂肪酸エステル、ポリオキシエチレンプロピレングリコール脂肪酸エステル、ポリオキシエチレンヒマシ油、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレン硬化ヒマシ油脂肪酸エステル、ポリオキシエチレンフィトスタノールエーテル、ポリオキシエチレンフィトステロースエーテル、ポリオキシエチレンコレスタノールエーテル、ポリオキシエチレンコレステリルエーテル及びポリオキシアルキレン変性オルガノポリシロキサン、ポリオキシアルキレン・アルキル共変性オルガノポリシロキサンから選ばれる1種以上を含む<15>又は<16>記載の脂質微粒子分散物。
<18>成分(F)の含有量が、好ましくは0.01質量%以上、より好ましくは0.05質量%以上、さらに好ましくは0.1質量%以上であり、また、好ましくは10質量%以下、より好ましくは5.0質量%以下、さらに好ましくは1.0質量%以下であり、また好ましくは0.01質量%以上10質量%以下であり、より好ましくは0.05質量%以上5.0質量%以下、さらに好ましくは0.1質量%以上1.0質量%以下である<15>~<17>のいずれかに記載の脂質微粒子分散物。
<19>pHが好ましくは3.5以上7.0以下、より好ましくは3.5以上6.0以下、さらに好ましくは3.5以上5.5以下である<1>~<18>のいずれかに記載の脂質微粒子分散物。
<20>成分(A)及び成分(B)を含む脂質微粒子の結晶性が低く、微細な粒子として水中に均一に乳化分散している<1>~<19>のいずれかに記載の脂質微粒子分散物。
<21>脂質微粒子分散物中に乳化分散している成分(A)及び成分(B)を含む脂質微粒子の平均粒子径が、好ましくは150nm未満、より好ましくは130nm未満である<1>~<20>のいずれかに記載の脂質微粒子分散物。
<22><1>~<21>のいずれかに記載の脂質微粒子分散物を含有する皮膚化粧料。
<6>成分(B)の含有量が、好ましくは0.01質量%以上、より好ましくは0.1質量%以上、さらに好ましくは0.3質量%以上であり、また、好ましくは5.0質量%以下、より好ましくは3.0質量%以下、さらに好ましくは1.0質量%以下であり、また、好ましくは0.01質量%以上5.0質量%以下、より好ましくは0.1質量%以上3.0質量%以下、さらに好ましくは0.3質量%以上1.0質量%以下である<1>~<5>のいずれかに記載の脂質微粒子分散物。
<7>成分(A)と成分(B)の質量比(A/B)が好ましくは0.1以上、より好ましくは0.2以上、さらに好ましくは0.3以上であり、また、好ましくは1.0以下、より好ましくは0.8以下、さらに好ましくは0.6以下であり、また好ましくは0.1以上1.0以下、より好ましくは0.2以上0.8以下、さらに好ましくは0.3以上0.6以下である<1>~<6>のいずれかに記載の脂質微粒子分散物。
<8>成分(C)が、好ましくはN-アシルアミノ酸塩、N-アシルメチルタウリン塩、アルキルリン酸塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩、ジアルキルスルホコハク酸塩及びジアシルアミノ酸リシン塩から選ばれる1種又は2種以上を含み、より好ましくは、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、アルキル硫酸エステル塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上を含み、さらに好ましくは、N-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩、ジアシルアミノ酸リシン塩、ポリオキシエチレンアルキルエーテル硫酸エステル塩、アルキルエーテルカルボン酸塩及びジアルキルスルホコハク酸塩から選ばれる1種又は2種以上を含み、さらにより好ましくはN-アシルアミノ酸塩、N-アシルメチルタウリン塩、ポリオキシエチレンアルキルエーテルリン酸塩、脂肪酸塩及びジアシルアミノ酸リシン塩から選ばれる1種又は2種以上を含み、特に好ましくはN-アシルアミノ酸塩及びN-アシルメチルタウリン塩から選ばれる1種又は2種以上を含む<1>~<7>のいずれかに記載の脂質微粒子分散物。
<9>成分(C)の含有量が、好ましくは0.002質量%以上、より好ましくは0.05質量%以上、さらに好ましくは0.1質量%以上であり、また好ましくは3.0質量%以下、より好ましくは1.0質量%以下、さらに好ましくは0.5質量%以下であり、また、好ましくは0.02質量%以上3.0質量%以下、より好ましくは0.05質量%以上1.0質量%以下、さらに好ましくは0.1質量%以上0.5質量%以下である<1>~<8>のいずれかに記載の脂質微粒子分散物。
<10>成分(A)、成分(B)及び成分(C)の合計質量が、好ましくは0.015質量%以上、より好ましくは0.33質量%以上、さらに好ましくは0.5質量%以上であり、また好ましくは13.0質量%以下、より好ましくは5.0質量%以下、さらに好ましくは2.0質量%以下であり、また、好ましくは0.015質量%以上13.0質量%以下、より好ましくは0.33質量%以上5.0質量%以下、さらに好ましくは0.5質量%以上2.0質量%以下である<1>~<9>のいずれかに記載の脂質微粒子分散物。
<11>成分(A)と成分(B)の合計質量と成分(C)の質量の比(A+B/C)が、好ましくは0.05以上、より好ましくは0.5以上、さらに好ましくは1.0以上、よりさらに好ましくは2.0以上であり、また、好ましくは6.0以下、より好ましくは5.5以下、さらに好ましくは5.0以下であり、また好ましくは0.05以上6.0以下、より好ましくは0.5以上5.5以下、さらに好ましくは1.0以上5.5以下、よりさらに好ましくは2.0以上5.5以下である<1>~<10>のいずれかに記載の脂質微粒子分散物。
<12>成分(D)が、多価アルコール及び低級アルコールから選ばれる1種以上を含み、より好ましくはエタノール、グリセリン、1,3-ブチレングリコール、ジプロピレングリコール及び1,3-プロパンジオールから選ばれる1種以上を含む<1>~<11>のいずれかに記載の脂質微粒子分散物。
<13>成分(D)の含有量が、好ましくは1.0質量%以上、より好ましくは2.0質量%以上、さらに好ましくは3.0質量%以上であり、また好ましくは30質量%以下、より好ましくは25質量%以下、さらに好ましくは20質量%以下であり、また好ましくは1.0質量%以上30質量%以下、より好ましくは2.0質量%以上25質量%以下、さらに好ましくは3.0質量%以上20質量%以下である<1>~<12>のいずれかに記載の脂質微粒子分散物。
<14>成分(E)の含有量が、好ましくは50質量%以上、より好ましくは70質量%以上、さらに好ましくは80質量%以上であり、また、好ましくは97質量%以下、より好ましくは95質量%以下、さらに好ましくは90質量%以下であり、また、好ましくは50質量%以上97質量%以下、より好ましくは70質量%以上95質量%以下、さらに好ましくは80質量%以上90質量%以下である<7>~<13>のいずれかに記載の脂質微粒子分散物。
<15>さらに成分(F)非イオン性界面活性剤を含有する<1>~<14>のいずれかに記載の脂質微粒子分散物。
<16>成分(F)が、好ましくはHLB10~20の非イオン性界面活性剤、より好ましくはHLB12~15の非イオン性界面活性剤、さらに好ましくはHLB12.5~14.5の非イオン性界面活性剤を含む<15>記載の脂質微粒子分散物。
<17>成分(F)が、グリセリン脂肪酸エステル、ソルビタン脂肪酸エステル、プロピレングリコール脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ショ糖脂肪酸エステル、ポリオキシエチレン脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンソルビトール脂肪酸エステル、ポリオキシエチレングリセリン脂肪酸エステル、ポリオキシエチレンプロピレングリコール脂肪酸エステル、ポリオキシエチレンヒマシ油、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレン硬化ヒマシ油脂肪酸エステル、ポリオキシエチレンフィトスタノールエーテル、ポリオキシエチレンフィトステロースエーテル、ポリオキシエチレンコレスタノールエーテル、ポリオキシエチレンコレステリルエーテル及びポリオキシアルキレン変性オルガノポリシロキサン、ポリオキシアルキレン・アルキル共変性オルガノポリシロキサンから選ばれる1種以上を含む<15>又は<16>記載の脂質微粒子分散物。
<18>成分(F)の含有量が、好ましくは0.01質量%以上、より好ましくは0.05質量%以上、さらに好ましくは0.1質量%以上であり、また、好ましくは10質量%以下、より好ましくは5.0質量%以下、さらに好ましくは1.0質量%以下であり、また好ましくは0.01質量%以上10質量%以下であり、より好ましくは0.05質量%以上5.0質量%以下、さらに好ましくは0.1質量%以上1.0質量%以下である<15>~<17>のいずれかに記載の脂質微粒子分散物。
<19>pHが好ましくは3.5以上7.0以下、より好ましくは3.5以上6.0以下、さらに好ましくは3.5以上5.5以下である<1>~<18>のいずれかに記載の脂質微粒子分散物。
<20>成分(A)及び成分(B)を含む脂質微粒子の結晶性が低く、微細な粒子として水中に均一に乳化分散している<1>~<19>のいずれかに記載の脂質微粒子分散物。
<21>脂質微粒子分散物中に乳化分散している成分(A)及び成分(B)を含む脂質微粒子の平均粒子径が、好ましくは150nm未満、より好ましくは130nm未満である<1>~<20>のいずれかに記載の脂質微粒子分散物。
<22><1>~<21>のいずれかに記載の脂質微粒子分散物を含有する皮膚化粧料。
次に実施例を挙げて本発明を更に詳細に説明する。
(製造方法)
(1)マイクロミキサー法
表1~4、7~8に記載の組成物及び表6記載の実施例17については、まず成分A、B、D、Fを85℃で加熱溶解し、均一な油相混合物Xを調製した。次に成分C、Eを85℃で加熱溶解し、均一な水相混合物Yを調製した。混合物X及びYを85℃で加熱しながら0.2MPa・sの圧力下でそれぞれを一定量で流動させると共に、それらを合流させ、孔径が0.4mmの細孔に流通させ化粧水状の均一な乳化物Zを得た。一部の成分D、E及び成分A~F以外の成分は混合し、均一溶解を確認した後に乳化物Zに添加することで各試料を得た。
(1)マイクロミキサー法
表1~4、7~8に記載の組成物及び表6記載の実施例17については、まず成分A、B、D、Fを85℃で加熱溶解し、均一な油相混合物Xを調製した。次に成分C、Eを85℃で加熱溶解し、均一な水相混合物Yを調製した。混合物X及びYを85℃で加熱しながら0.2MPa・sの圧力下でそれぞれを一定量で流動させると共に、それらを合流させ、孔径が0.4mmの細孔に流通させ化粧水状の均一な乳化物Zを得た。一部の成分D、E及び成分A~F以外の成分は混合し、均一溶解を確認した後に乳化物Zに添加することで各試料を得た。
(2)ビーカー法
表5に記載の組成物及び表6記載の比較例6については、成分A、B、C、D、Fを85℃で加熱溶解し、均一な油相混合物を得た。この油相混合物に成分Eを撹拌しながら滴下することで乳化物を得た。一部の成分E及び成分A~F以外の成分は混合し、均一溶解を確認した後に乳化物へ添加することで各試料を得た。
表5に記載の組成物及び表6記載の比較例6については、成分A、B、C、D、Fを85℃で加熱溶解し、均一な油相混合物を得た。この油相混合物に成分Eを撹拌しながら滴下することで乳化物を得た。一部の成分E及び成分A~F以外の成分は混合し、均一溶解を確認した後に乳化物へ添加することで各試料を得た。
(評価方法)
(1)粒子状態
実施例及び比較例の脂質微粒子分散物について、粒子径分析装置(ゼータサイザーナノZS マルバーン社製)を用いた動的光散乱法による測定(20倍希釈液)により得られたキュムラント径を求め、以下のA~Dの評価に当てはめた。
A:130nm未満
B:130nm以上150nm未満
C:150nm以上200nm未満
D:200nm以上
(2)結晶状態
実施例及び比較例の脂質微粒子分散物について、示差走査熱量分析装置(μDSCVIIevo リガク社製)を用いた測定(昇温速度:0.3℃/min)により得られた融解曲線の45℃以上80℃以下の温度範囲における全吸熱量から融解熱量を求め、以下のA~Dの評価に当てはめた。
A:熱量0.05J/g未満
B:熱量0.05J/g以上0.15J/g未満
C:熱量0.15J/g以上0.30J/g以下
D:熱量0.30J/gを超える
(1)粒子状態
実施例及び比較例の脂質微粒子分散物について、粒子径分析装置(ゼータサイザーナノZS マルバーン社製)を用いた動的光散乱法による測定(20倍希釈液)により得られたキュムラント径を求め、以下のA~Dの評価に当てはめた。
A:130nm未満
B:130nm以上150nm未満
C:150nm以上200nm未満
D:200nm以上
(2)結晶状態
実施例及び比較例の脂質微粒子分散物について、示差走査熱量分析装置(μDSCVIIevo リガク社製)を用いた測定(昇温速度:0.3℃/min)により得られた融解曲線の45℃以上80℃以下の温度範囲における全吸熱量から融解熱量を求め、以下のA~Dの評価に当てはめた。
A:熱量0.05J/g未満
B:熱量0.05J/g以上0.15J/g未満
C:熱量0.15J/g以上0.30J/g以下
D:熱量0.30J/gを超える
(3)安定性
実施例及び比較例の脂質微粒子分散物について、規格ガラス容器(マイティバイアルNo.7 アズワン社製)に充填し室温及び50℃の環境にて1ヵ月保管し、外観の変化を観察し、評価した。観察時においては製剤に相分離がないこと、クリーミングが起こらないこと、沈殿物あるいは析出物のないことを確認し、いずれの変化も見られなかった場合のみ合格「○」とした。
実施例及び比較例の脂質微粒子分散物について、規格ガラス容器(マイティバイアルNo.7 アズワン社製)に充填し室温及び50℃の環境にて1ヵ月保管し、外観の変化を観察し、評価した。観察時においては製剤に相分離がないこと、クリーミングが起こらないこと、沈殿物あるいは析出物のないことを確認し、いずれの変化も見られなかった場合のみ合格「○」とした。
(4)使用感
表6に記載の実施例及び比較例を等量肌に使用した時について、専門パネラにより「しっとり感」、「もちもち感」及び「滑らかさ」について使用感の良い順で4段階評価を行った。評価基準を以下に示す。
A:とても感じる
B:やや感じる
C:僅かに感じる
D:全く感じない
表6に記載の実施例及び比較例を等量肌に使用した時について、専門パネラにより「しっとり感」、「もちもち感」及び「滑らかさ」について使用感の良い順で4段階評価を行った。評価基準を以下に示す。
A:とても感じる
B:やや感じる
C:僅かに感じる
D:全く感じない
表1~8記載の脂質微粒子分散物を製造し、その物性、安定性及び使用感を評価した。その結果も表1~8に併せて示す。
表7記載の脂質微粒子分散物についても、セラミド類等の固体脂の結晶性が低く、微細な粒子として安定に乳化分散しており、安定性及び使用感についても優れたものである。
Claims (7)
- 次の成分(A)~(E)を含有し、pHが3.5以上8.0以下である脂質微粒子分散物であり、当該脂質微粒子の45℃以上80℃以下の温度範囲における融解熱量が0.30J/g以下であり、平均粒子径が200nm未満である脂質微粒子分散物。
(A)ステロール及びその誘導体から選ばれる1種以上
(B)成分(A)以外の25℃で固体又は半固体の脂質
(C)アニオン性界面活性剤
(D)水溶性溶媒
(E)水 - 成分(A)と成分(B)の合計質量と成分(C)の質量の比(A+B/C)が0.05以上6.0以下である請求項1記載の脂質微粒子分散物。
- 成分(A)がコレステロール及びフィトステロールから選ばれる1種以上を含む請求項1又は2記載の脂質微粒子分散物。
- 成分(B)が天然セラミド、合成セラミド及び炭素数12~30の脂肪族アルコールから選ばれる1種以上を含む請求項1~3のいずれか1項記載の脂質微粒子分散物。
- 成分(C)がN-アシルアミノ酸塩及びN-アシルメチルタウリン塩から選ばれる1種以上である請求項1~4のいずれか1項記載の脂質微粒子分散物。
- さらに、成分(F)非イオン性界面活性剤を含有する請求項1~5のいずれか1項記載の脂質微粒子分散物。
- 請求項1~6のいずれか1項記載の脂質微粒子分散物を含有する皮膚化粧料。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18893406.1A EP3733159A4 (en) | 2017-12-28 | 2018-12-28 | LIPID PARTICLE DISPERSION |
| KR1020207015850A KR20200103652A (ko) | 2017-12-28 | 2018-12-28 | 지질 미립자 분산물 |
| US16/958,541 US11564871B2 (en) | 2017-12-28 | 2018-12-28 | Dispersion of fine lipid particle dispersion |
| CN201880081069.8A CN111511345B (zh) | 2017-12-28 | 2018-12-28 | 脂质微粒分散物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017254874 | 2017-12-28 | ||
| JP2017-254874 | 2017-12-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019131987A1 true WO2019131987A1 (ja) | 2019-07-04 |
Family
ID=67067593
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2018/048404 WO2019131987A1 (ja) | 2017-12-28 | 2018-12-28 | 脂質微粒子分散物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11564871B2 (ja) |
| EP (1) | EP3733159A4 (ja) |
| JP (1) | JP7278769B2 (ja) |
| KR (1) | KR20200103652A (ja) |
| CN (1) | CN111511345B (ja) |
| TW (1) | TWI793240B (ja) |
| WO (1) | WO2019131987A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021049483A1 (ja) * | 2019-09-13 | 2021-03-18 | 味の素株式会社 | 粉体の表面処理方法、それに使用する表面処理剤組成物、および表面処理された粉体 |
| JP7411421B2 (ja) | 2020-01-16 | 2024-01-11 | 株式会社ファンケル | 化粧料 |
Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62228048A (ja) | 1985-12-20 | 1987-10-06 | Kao Corp | アミド誘導体及びそれを含有する皮膚外用剤 |
| JPS63216812A (ja) | 1987-03-06 | 1988-09-09 | Kao Corp | 皮膚外用剤 |
| JPS63227513A (ja) | 1987-03-16 | 1988-09-21 | Kao Corp | 皮膚外用剤 |
| JPS6429347A (en) | 1987-07-24 | 1989-01-31 | Kao Corp | Amide derivative and external agent for skin containing said derivative |
| JPS6431752A (en) | 1987-07-27 | 1989-02-02 | Kao Corp | Amide derivative and skin external preparation containing said derivative |
| JPH02191208A (ja) | 1989-01-18 | 1990-07-27 | Pola Chem Ind Inc | 化粧料 |
| JPH08319263A (ja) | 1995-05-24 | 1996-12-03 | Kao Corp | アミド誘導体、この製造中間体並びに該アミド誘導体を含有する皮膚外用剤及び毛髪化粧料 |
| JPH09124432A (ja) | 1995-10-26 | 1997-05-13 | Kanebo Ltd | 液晶型エマルションの製造方法および該製造方法によって得られる液晶型エマルション組成物 |
| JP2001316217A (ja) * | 2000-05-11 | 2001-11-13 | Takasago Internatl Corp | 水性透明組成物 |
| WO2004045566A1 (ja) * | 2002-11-15 | 2004-06-03 | Kose Corporation | 半透明化粧料 |
| JP2004331595A (ja) | 2003-05-09 | 2004-11-25 | Takasago Internatl Corp | 脂質組成物およびそれを含有する皮膚外用剤 |
| JP2006335693A (ja) * | 2005-06-02 | 2006-12-14 | Kao Corp | 乳化組成物 |
| JP2007015972A (ja) | 2005-07-07 | 2007-01-25 | Shiseido Co Ltd | 一相マイクロエマルション組成物、及びo/w超微細エマルション外用剤の製造方法 |
| WO2010038814A1 (ja) | 2008-09-30 | 2010-04-08 | 富士フイルム株式会社 | セラミド分散物及びその製造方法 |
| JP5086583B2 (ja) | 2006-08-10 | 2012-11-28 | 花王株式会社 | セラミド微粒子分散液の製造方法 |
| JP2013227294A (ja) * | 2012-03-30 | 2013-11-07 | Kose Corp | 半透明性乃至透明性組成物 |
| JP2015093840A (ja) * | 2013-11-08 | 2015-05-18 | 株式会社ミリオナ化粧品 | セラミド類含有液状透明組成物、皮膚外用剤、およびセラミド類含有液状透明組成物の製造方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4185240B2 (ja) | 2000-09-13 | 2008-11-26 | 花王株式会社 | 水中油型乳化化粧料 |
| JP4886204B2 (ja) | 2005-03-31 | 2012-02-29 | 花王株式会社 | 水中油型乳化組成物の製造方法 |
| JP6510177B2 (ja) * | 2014-04-01 | 2019-05-08 | ロレアル | ナノ又はマイクロエマルションの形態の組成物 |
| WO2018123883A1 (ja) | 2016-12-27 | 2018-07-05 | 花王株式会社 | セラミド微粒子分散物の製造方法 |
-
2018
- 2018-12-28 EP EP18893406.1A patent/EP3733159A4/en active Pending
- 2018-12-28 JP JP2018246370A patent/JP7278769B2/ja active Active
- 2018-12-28 TW TW107147778A patent/TWI793240B/zh active
- 2018-12-28 WO PCT/JP2018/048404 patent/WO2019131987A1/ja unknown
- 2018-12-28 CN CN201880081069.8A patent/CN111511345B/zh active Active
- 2018-12-28 US US16/958,541 patent/US11564871B2/en active Active
- 2018-12-28 KR KR1020207015850A patent/KR20200103652A/ko not_active Application Discontinuation
Patent Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62228048A (ja) | 1985-12-20 | 1987-10-06 | Kao Corp | アミド誘導体及びそれを含有する皮膚外用剤 |
| JPS63216812A (ja) | 1987-03-06 | 1988-09-09 | Kao Corp | 皮膚外用剤 |
| JPS63227513A (ja) | 1987-03-16 | 1988-09-21 | Kao Corp | 皮膚外用剤 |
| JPS6429347A (en) | 1987-07-24 | 1989-01-31 | Kao Corp | Amide derivative and external agent for skin containing said derivative |
| JPS6431752A (en) | 1987-07-27 | 1989-02-02 | Kao Corp | Amide derivative and skin external preparation containing said derivative |
| JPH02191208A (ja) | 1989-01-18 | 1990-07-27 | Pola Chem Ind Inc | 化粧料 |
| JPH08319263A (ja) | 1995-05-24 | 1996-12-03 | Kao Corp | アミド誘導体、この製造中間体並びに該アミド誘導体を含有する皮膚外用剤及び毛髪化粧料 |
| JPH09124432A (ja) | 1995-10-26 | 1997-05-13 | Kanebo Ltd | 液晶型エマルションの製造方法および該製造方法によって得られる液晶型エマルション組成物 |
| JP2001316217A (ja) * | 2000-05-11 | 2001-11-13 | Takasago Internatl Corp | 水性透明組成物 |
| WO2004045566A1 (ja) * | 2002-11-15 | 2004-06-03 | Kose Corporation | 半透明化粧料 |
| JP2004331595A (ja) | 2003-05-09 | 2004-11-25 | Takasago Internatl Corp | 脂質組成物およびそれを含有する皮膚外用剤 |
| JP2006335693A (ja) * | 2005-06-02 | 2006-12-14 | Kao Corp | 乳化組成物 |
| JP2007015972A (ja) | 2005-07-07 | 2007-01-25 | Shiseido Co Ltd | 一相マイクロエマルション組成物、及びo/w超微細エマルション外用剤の製造方法 |
| JP5086583B2 (ja) | 2006-08-10 | 2012-11-28 | 花王株式会社 | セラミド微粒子分散液の製造方法 |
| WO2010038814A1 (ja) | 2008-09-30 | 2010-04-08 | 富士フイルム株式会社 | セラミド分散物及びその製造方法 |
| JP2013227294A (ja) * | 2012-03-30 | 2013-11-07 | Kose Corp | 半透明性乃至透明性組成物 |
| JP2015093840A (ja) * | 2013-11-08 | 2015-05-18 | 株式会社ミリオナ化粧品 | セラミド類含有液状透明組成物、皮膚外用剤、およびセラミド類含有液状透明組成物の製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3733159A4 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20200103652A (ko) | 2020-09-02 |
| EP3733159A1 (en) | 2020-11-04 |
| EP3733159A4 (en) | 2021-10-27 |
| TWI793240B (zh) | 2023-02-21 |
| CN111511345B (zh) | 2023-03-31 |
| TW201929835A (zh) | 2019-08-01 |
| US20210059910A1 (en) | 2021-03-04 |
| JP7278769B2 (ja) | 2023-05-22 |
| JP2019119742A (ja) | 2019-07-22 |
| US11564871B2 (en) | 2023-01-31 |
| CN111511345A (zh) | 2020-08-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4767352B1 (ja) | 乳化組成物 | |
| KR101337811B1 (ko) | O/w 미세 에멀젼 외용제의 제조 방법 | |
| US9839588B2 (en) | Skin external preparation comprising an aqueous dispersion of finely dispersed wax, nonionic surfactant, and ionic water-soluble thickener | |
| CN1723872B (zh) | 水包油型乳化组合物 | |
| JP2014073991A (ja) | 乳化組成物 | |
| JP5244989B2 (ja) | O/w乳化組成物の製造方法 | |
| JP7278769B2 (ja) | 脂質微粒子分散物 | |
| JP2003095956A (ja) | 微細エマルション組成物 | |
| JP3715223B2 (ja) | 水中油型乳化組成物の製造方法 | |
| JPH09165317A (ja) | 水中油型乳化組成物 | |
| JP3662513B2 (ja) | 乳化化粧料 | |
| CN100473375C (zh) | 水包油型乳化化妆品 | |
| JP2010222317A (ja) | 水中油型乳化化粧料 | |
| JP2006290751A (ja) | 水中油型エマルション及びその製造方法 | |
| JP2005103421A (ja) | 微細エマルションおよびその製造方法 | |
| JP5395817B2 (ja) | ベシクル組成物およびその製造方法ならびにその用途 | |
| JP2006281038A (ja) | 水中油型乳化組成物の製造方法 | |
| JP2003095845A (ja) | 半透明液状化粧料 | |
| JP2007070329A (ja) | マイクロエマルション組成物およびその製造方法 | |
| JP5226088B2 (ja) | 皮膚外用医薬乳化製剤 | |
| JPH08245370A (ja) | 水中油型乳化組成物 | |
| JP2015124218A (ja) | 毛髪化粧料用組成物及びその製造方法、並びに毛髪化粧料用組成物を含有する毛髪化粧料 | |
| JP2007169174A (ja) | O/w型乳化組成物 | |
| JP2005320257A (ja) | 皮膚外用医薬乳化製剤およびその製造方法 | |
| JPS596938A (ja) | 乳化組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 18893406 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2018893406 Country of ref document: EP Effective date: 20200728 |