WO2012002464A1 - ω3脂肪酸の配合製剤 - Google Patents
ω3脂肪酸の配合製剤 Download PDFInfo
- Publication number
- WO2012002464A1 WO2012002464A1 PCT/JP2011/064976 JP2011064976W WO2012002464A1 WO 2012002464 A1 WO2012002464 A1 WO 2012002464A1 JP 2011064976 W JP2011064976 W JP 2011064976W WO 2012002464 A1 WO2012002464 A1 WO 2012002464A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- capsule
- gelatin
- film
- statin
- epa
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4891—Coated capsules; Multilayered drug free capsule shells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/202—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids having three or more double bonds, e.g. linolenic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/23—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin of acids having a carboxyl group bound to a chain of seven or more carbon atoms
- A61K31/232—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin of acids having a carboxyl group bound to a chain of seven or more carbon atoms having three or more double bonds, e.g. etretinate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Emergency Medicine (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
脂質異常症治療においてスタチン投与患者を対象とした、エパデールの虚血性心疾患の発症抑制効果を調べた無作為化比較大規模臨床試験(JELIS試験)が行われ、その主解析において、主要冠動脈イベントの発症率がエパデール投与併用群と非投与群を比較した際、投与群で有意に低いというエビデンスが得られている。(非特許文献5)生活習慣病の治療に焦点を当てた場合、上記記載のω3PUFAおよびスタチンの臨床効果に注目し、両医薬品の配合剤の開発を行うことは、薬物治療上、意義のあるものと考えられる。
2.ω3PUFA類から選ばれる少なくとも1つがカプセル内容物に含有され、スタチン化合物から選ばれる少なくとも1つがカプセル皮膜に含有されている、上記1に記載の軟カプセル。
3.炭酸塩、メタケイ酸アルミン酸塩およびリン酸塩からなる群から選択される少なくとも1つがカプセル皮膜に含有されている、上記1または2の何れかに記載の軟カプセル。
4.炭酸塩および/またはメタケイ酸アルミン酸塩がカプセル皮膜に含有されている、上記1ないし3の何れかに記載の軟カプセル。
5.炭酸水素ナトリウムおよび/またはメタケイ酸アルミン酸マグネシウムがカプセル皮膜に含有されている、上記1ないし4の何れかに記載の軟カプセル。
6.カプセル皮膜がゼラチンを含有する、上記1ないし5の何れかに記載の軟カプセル。
7.カプセル皮膜がコハク化ゼラチン、有機酸、加水分解ゼラチンおよびトレハロースからなる群から選ばれる少なくとも1つを含有する、上記1ないし6の何れかに記載の軟カプセル。
8.有機酸が酒石酸である、上記7に記載の軟カプセル。
9.水溶性ポリマーによりカプセル皮膜の内面に被膜が形成されている、上記1ないし8の何れかに記載の軟カプセル。
10.水溶性ポリマーがHPMCである、上記9に記載の軟カプセル。
11.スタチン化合物が水溶性スタチン化合物である、上記1ないし10の何れかに記載の軟カプセル。
12.スタチン化合物がプラバスタチンおよびロスバスタチン、ならびにそれらの塩および水和物からなる群から選択される少なくとも1つである、上記1ないし11の何れかに記載の軟カプセル。
14.ω3PUFA類が、EPAおよびDHA、ならびに、それらの塩およびエステルからなる群から選択される少なくとも1つである、上記1ないし12の何れかに記載の軟カプセル。
15.ω3PUFA類が、EPA-Eおよび/またはDHA-Eである、上記1ないし14の何れかに記載の軟カプセル。
16.上記1ないし15の何れかに記載の軟カプセルの形態である配合製剤。
1)カプセルの皮膜液のpHを7.0~9.5に調整する工程、
2)カプセルの皮膜液にスタチン化合物を溶解する工程、
3)ω3PUFA類を含有するカプセル内容物を調製する工程、および、
4)カプセルの内容物とカプセルの皮膜液から軟カプセルを得る工程。
18.炭酸塩および/またはメタケイ酸アルミン酸塩をカプセル皮膜液に添加する工程を含む、上記17の製法。
19.炭酸水素ナトリウムおよび/またはメタケイ酸アルミン酸マグネシウムをカプセル皮膜液に添加する工程を含む、上記17または18の何れかに記載の製法。
20.カプセル皮膜液にゼラチンを添加する工程を含む、上記17ないし19の何れかに記載の製法。
21.以下の工程を含む、上記17ないし20の何れかに記載の製法;
カプセル皮膜液にコハク化ゼラチン、有機酸、加水分解ゼラチンおよびトレハロースからなる群から選ばれる少なくとも1つを添加する工程。
22.有機酸が酒石酸である、上記17ないし21の何れかに記載の製法。
23.さらに、以下の工程を含む、上記17ないし22の何れかに記載の製法;
1)水溶性ポリマーをω3PUFA類(カプセル内容物)中に添加する工程、および/または、
2)カプセル皮膜内面に水溶性ポリマーの被膜を形成させる工程。
24.水溶性ポリマーがHPMCである、上記23に記載の製法。
25.スタチン化合物が水溶性スタチン化合物である、上記17ないし24の何れかに記載の製法。
26.スタチン化合物がプラバスタチンおよびロスバスタチン、ならびにそれらの塩および水和物からなる群から選択される少なくとも1つである、上記17ないし25の何れかに記載の製法。
27.スタチン化合物がプラバスタチンナトリウムおよび/またはロスバスタチンカルシウムである、上記17ないし26の何れかに記載の製法。
28.ω3PUFA類が、EPAおよびDHA、ならびに、それらの塩およびエステルからなる群から選択される少なくとも1つである、上記17ないし27の何れかに記載の製法。
29.ω3PUFA類が、EPA-Eおよび/またはDHA-Eである、上記17ないし28の何れかに記載の製法。
従って、本発明の軟カプセルおよび配合製剤は、製造時安定性のみならず長期保存に適すること、カプセル皮膜、特にゼラチン皮膜の変性または不溶化の抑制により各配合成分の良好なバイオアベイラビリティを示す等の利点を有する。さらに、本発明の軟カプセルおよび配合製剤の製法は、製造工程数を低減でき、製造が容易であること、各配合成分の配合量を適切に調整しうること、歩留まりが良いこと等の利点を有する。
本発明の配合製剤は、脂質異常症等の疾患の予防・治療薬等として使用しうる。
本発明において、「ω3PUFA」とは、分子内に複数の炭素-炭素の二重結合を有し、メチル基側から数えて3番目の位置に最初の二重結合を有する脂肪酸である。代表的なものとして、α-リノレン酸、EPA、DHA、エイコサトリエン酸、ステアリドン酸、エイコサテトラエン酸、イワシ酸、テトラコサペンタエン酸およびニシン酸などが例示される。本発明における「ω3PUFA類」の語は、特に断らない限りは、ω3PUFAだけでなく、その製薬上許容される塩およびエステルなども含む意味で用いられる。
本発明で用いられるω3PUFA類は、合成品、半合成品または天然品のいずれでもよく、これらを含有する天然油の形態でもよい。ここで、天然品とは、ω3PUFA類を含有する天然油から公知の方法によって抽出されたもの、粗精製されたもの、あるいはそれらを更に高度に精製したものを意味する。半合成品は、微生物などにより産生されたω3PUFA類を含み、また該ω3PUFA類あるいは天然のω3PUFA類にエステル化、エステル交換等の化学処理を施したものも含まれる。本発明では、ω3PUFA類として、これらのうちの1種を単独で、あるいは2種以上を組み合わせて用いることができる。
本発明では、ω3PUFA類としてEPAおよび/またはDHAが好ましい例として挙げられ、EPAが更に好ましい例として挙げられる。また、ω3PUFAの製薬学上許容しうる塩としてナトリウム塩、カリウム塩などの無機塩基、ベンジルアミン塩、ジエチルアミン塩などの有機塩基、アルギニン塩、リジン塩などの塩基性アミノ酸との塩およびエステルとしてエチルエステル等のアルキルエステルやモノ-、ジ-およびTG等のエステルが例示される。好ましくはエチルエステルまたはTGエステルが挙げられ、エチルエステルが更に好ましい例として挙げられる。すなわち、EPA-E、EPAのTGエステル、DHA-E、およびDHAのTGエステルが好ましい例として挙げられ、EPA-EおよびDHA-Eが更に好ましい例として挙げられ、EPA-Eがより好ましい例として挙げられる。
例えば、EPA-EとDHA-Eを用いる場合、EPAの本剤組成物の純度が上記であれば、EPA-E/DHA-Eの組成比および全脂肪酸中のEPA-E+DHA-Eの含量比は特に問わないが、好ましい組成比として、EPA-E/DHA-Eは、0.8以上であることが好ましく、更に好ましくは、1.0以上、より好ましくは、1.2以上である。
また、本剤組成物はリノール酸、γリノレン酸、ジホモ-γ-リノレン酸などのω3PUFA類以外の多価不飽和脂肪酸、それらの製薬学上許容される塩またはエステルを含んでいても良いが、アラキドン酸含量は少ないことが望まれ、2質量%未満が好ましく、1質量%未満がさらに好ましく、アラキドン酸を実質的に含まない態様がとくに好ましい。
本発明の配合製剤のω3PUFA類の含量は特に限定されないが、通常、カプセル内容物の50質量%以上、好ましくは80質量%以上、より好ましくは85質量%以上、さらに好ましくは90質量%以上である。
ω3PUFA類として、精製魚油も使用できる。また、ω3PUFA類のモノグリセリド、ジグリセリド、TG誘導体またはこれらの組合せなども好ましい態様の一つである。例えばインクロメガ製(lncromega)F2250、F2628、E2251、F2573、TG2162、TG2779、TG2928、TG3525およびE5015(クローダ インターナショナル ピーエルシー製(Croda International PLC, Yorkshire, England))、および EPAX6000FA、EPAX5000TG、EPAX4510TG、EPAX2050TG、EPAX7010EE、K85TG、K85EEおよびK80EE(プロノバ バイオファーマ製(Pronova Biopharma, Lysaker, Norway) )などの種々のω3PUFA類を含有する製品が市販されており、これらを入手して使用することもできる。
好ましくは、水溶性スタチン化合物であり、具体的には、プラバスタチンナトリウムまたはロスバスタチンカルシウムである。
本発明において、「スタチン」の配合形態は必ずしも限定されない。例えば、「スタチン」を、ω3PUFA類を含有するカプセル内容物中に溶解または分散する、公知の適当な方法によりカプセル皮膜にコーティングする、または、カプセル皮膜中に溶解または分散することができるが、好ましくは、カプセルの皮膜液中に溶解し、公知の適当な方法によりカプセルを成形することによりカプセル皮膜中に配合した形態である。
本発明の配合製剤のスタチンの含量は特に限定されないが、通常、配合製剤の0.01%ないし20質量%、好ましくは0.01%ないし10質量%、さらに好ましくは0.01%ないし5質量%である。
「ゼラチン」としては、軟カプセル剤の製造において通常使用されるもの、例えば、第16改正日本薬局方で規定される医薬用ゼラチン(ゼラチンおよび精製ゼラチン)が挙げられる。ゼラチンは、2種以上を組合せて用いてもよい。カプセル皮膜はその他に可塑剤等を含有しうる。
「可塑剤」としては、軟カプセル剤の製造において通常使用されるもの、例えば、グリセリン(例、濃グリセリン)、エチレングリコール、ポリエチレングリコール、プロピレングリコール、ポリプロピレングリコール等の多価アルコール、ソルビトール、マンニトール、キシリトール等の糖アルコールなどが好ましい。これらの可塑剤は、2種以上を組合せて用いてもよい。中でも、グリセリン、ソルビトールが好ましい。また、グリセリンとソルビトールとの組み合わせを使用することも好ましい。この場合、グリセリンとソルビトールとの質量比を、1:5~5:1の範囲で使用することが好ましく、1:3~3:1の範囲で使用することがより好ましい。
本発明の軟カプセル剤、特にシームレスカプセルにおいて、カプセル皮膜液は、ゼラチンと可塑剤とを、その重量比において、10:1~1:10の範囲で含有することが好ましく、10:1~1:1の範囲で含有することがより好ましい。
カプセル皮膜液とカプセル内容物との重量比は、通常10:1~1:10で、好ましくは3:1~1:10である。
さらに、必要に応じて、カプセル皮膜に一般に用いられる各種添加剤、例えば、アミノ酸、クエン酸、グリセリン、ソルビトール、等の可塑剤、防腐剤、色素や酸化チタン等の着色剤、有機酸等を添加することができる。
カプセル皮膜の成形と、内容物充填のタイミングは、カプセル剤のタイプによって異なる。
本発明の軟カプセルおよび配合製剤において、カプセル皮膜のpHを弱アルカリ性にすることで、スタチンの安定性が向上する。pHは例えばpH7.0~9.5、好ましくは7.0~9.0、より好ましくは7.0~8.0、特に好ましくは7.5~8.0である。カプセル皮膜のpHとは、通常、カプセル皮膜液のpHであり、また、カプセル皮膜のpHの実測値でもよい。カプセル皮膜のpHの実測値とは、カプセル皮膜をその重量比0.5~10倍の水に溶解した時のpHである。
さらに、スタチンの安定性を向上させるために、種々の添加剤の成分を適用でき、例えば、リン酸一水素カルシウム、リン酸一水素ナトリウム、リン酸三ナトリウム、リン酸水素ナトリウム、リン酸水素カルシウム、リン酸水素ナトリウム、リン酸二カリウム、リン酸二水素カリウム、リン酸二水素カルシウム、リン酸二水素ナトリウムなどのリン酸塩およびその水和物、炭酸カリウム、炭酸カルシウム、炭酸水素カリウム、炭酸水素ナトリウム、炭酸マグネシウムなどの炭酸塩およびその水和物、メタケイ酸アルミン酸マグネシウムなどのメタケイ酸アルミン酸塩、ケイ酸アルミン酸マグネシウムなどのケイ酸アルミン酸塩などが挙げられるが、好ましくは炭酸塩、リン酸塩またはメタケイ酸アルミン酸塩であり、より好ましくは炭酸塩またはメタケイ酸アルミン酸塩であり、さらに好ましくは炭酸塩である。これらの添加剤の皮膜中の含有量は通常0.2~8質量%、より好ましくは0.5~5質量%である。
ここで、有機酸としては、必ずしも限定されず、酒石酸、クエン酸、アミノ酸、フィチン等のリン酸化イノシトール、フマル酸、コハク酸、乳酸、リンゴ酸、マレイン酸等が例示されるが、酒石酸が好ましい。これらの有機酸の皮膜中の含有量は、通常0.2~10質量%、好ましくは1.0~5質量%である。コハク化ゼラチンの皮膜中の含有量は、通常1~40質量%、より好ましくは5~20質量%である。加水分解ゼラチンの皮膜中の含有量は、通常1~50質量%、より好ましくは5~25質量%である。トレハロースの皮膜中の含有量は、通常1~35質量%、より好ましくは4~16質量%である。また、前記化合物を2種以上添加する場合は、各々の化合物の添加量は前記の好ましい範囲よりさらに減量することもできる。
水溶性ポリマーとしては、通常医薬製剤に汎用されるHPMC、ヒドロキシプロピルセルロース(以下、HPCと記す)、メチルセルロース(以下、MCと記す)、ポリビニルピロリドン(以下、PVPと記す)の何れか1つまたはその組み合わせを用いることができ、HPMC、HPCおよびPVPが耐油性の観点から好ましいが、HPMCが特に好ましい。カプセル内容物中にこれらの水溶性ポリマーを懸濁し、カプセルを形成することで、カプセル皮膜の内面に被膜を形成することができる。これらの水溶性ポリマーのカプセル内容物中の含有量は、通常0.5~20質量%、好ましくは1.0~10質量%である。
また、カプセル皮膜液にコハク化ゼラチン、有機酸、加水分解ゼラチンおよびトレハロースからなる群から選ばれる少なくとも1つを添加することと、水溶性ポリマーをω3PUFA類(カプセル内容物)中に添加することおよび/または水溶性ポリマーをカプセル皮膜内面に展延することを組み合わせることもでき、その場合は各々の化合物の添加量は前記の好ましい範囲よりさらに減量することもできる。
(実施例1)
ゼラチン(ニッピ社製)310.5g、ソルビトール33.0g、濃グリセリン31.5g、無水エタノール3.0g、炭酸水素ナトリウム9.6gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム9.0gと精製水を加え溶解し、全量を1500gとしたものをpHが8.5~9.0の皮膜液とし、EPA-Eを内容液とした。皮膜液と内容液について、同心二重ノズルを用いた液中滴下法にて、カプセル化を行った。次にこれらのカプセルを乾燥し、EPA-Eとプラバスタチンナトリウムの配合比率が90:1である、直径約4mmのシームレスカプセルを得た。製造したシームレスカプセルはアルミラミネート袋に入れ、袋内を窒素置換して密封して保存した。表1に皮膜液の処方を示す。
ゼラチン310.5g、ソルビトール33.0g、濃グリセリン31.5g、無水エタノール3.0g、メタケイ酸アルミン酸マグネシウム18.0g、リン酸二水素ナトリウム二水和物12.0gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム9.0gおよび精製水を加え溶解し、全量を1500gとしたものをpHが8.5~9.0の皮膜液とし、EPA-Eを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表2に皮膜液の処方を示す。
ゼラチン310.5g、ソルビトール33.0g、濃グリセリン31.5g、無水エタノール3.0g、リン酸二水素ナトリウム二水和物12.0gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム9.0gおよび精製水を加え溶解し、全量を1500gとしたものをpHが8.5~9.5の皮膜液とし、EPA-Eを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表3に皮膜液の処方を示す。
ゼラチン375.0g、ソルビトール33.0g、濃グリセリン31.5g、無水エタノール3.0g、炭酸水素ナトリウム9.6gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、精製水を加えて1500gとしたものをpHが8.5~9.0の皮膜液とした。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表4に皮膜液の処方を示す。
ゼラチン414.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gおよび精製水を加え溶解し、全量を2000gとしたものをpHが7.5~8.0の皮膜液とした。別に、EPA-Eに無水エタノール1.3質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表5に皮膜液の処方を示す。
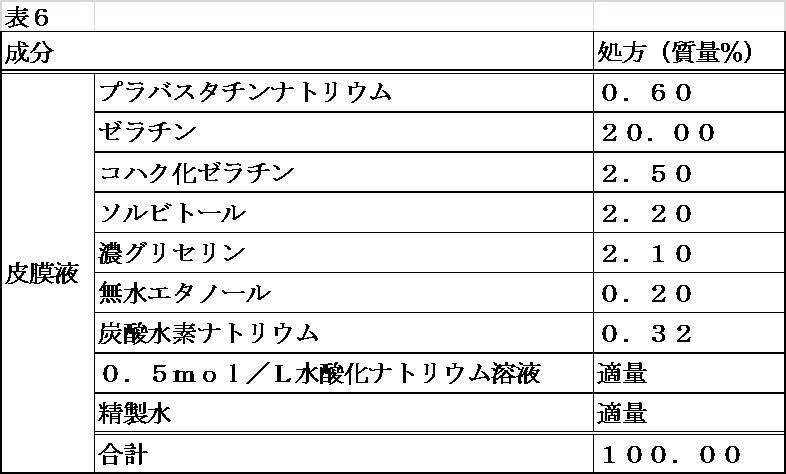
ゼラチン400.0g、コハク化ゼラチン(ニッピ社製)50.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gと精製水を加え溶解し、全量を2000gとしたものをpHが7.5~8.0の皮膜液とした。別に、EPA-Eに無水エタノール1.3質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表6に皮膜液の処方を示す。
ゼラチン400.0g、コハク化ゼラチン50.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gおよび精製水を加え溶解し、全量を2000gとしたものをpHが8.0~8.5の皮膜液とした。別に、EPA-Eに無水エタノール1.3質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表7に皮膜液の処方を示す。
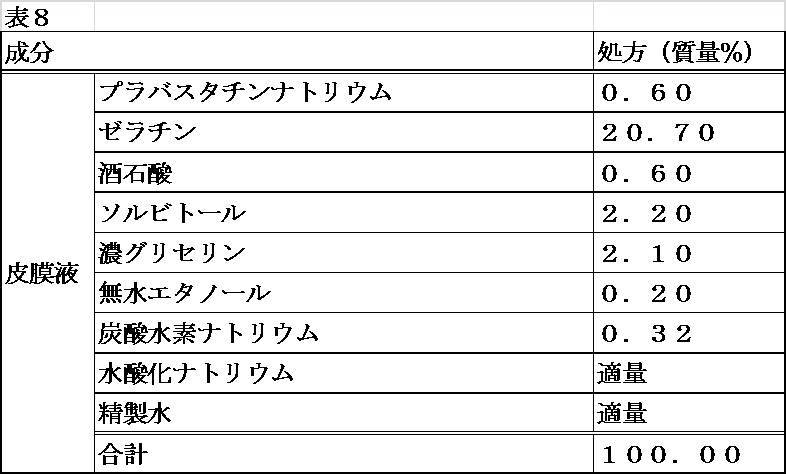
ゼラチン414.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、酒石酸12.0gおよび水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gと精製水を加え溶解し、全量を2000gとしたものをpHが7.5~8.0の皮膜液とした。別に、EPA-Eに無水エタノール1.3質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表8に皮膜液の処方を示す。
ゼラチン400.0g、コハク化ゼラチン50.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、酒石酸12.0gおよび水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gおよび精製水を加え溶解し、全量を2000gとしたものをpHが7.5~8.0の皮膜液とした。別に、EPA-Eに無水エタノール1.3質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表9に皮膜液の処方を示す。
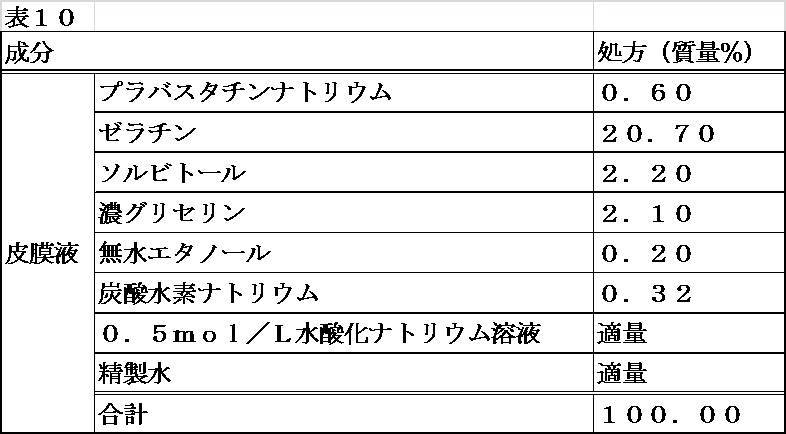
ゼラチン414.0g、ソルビトール44.0g、濃グリセリン42.0g、無水エタノール4.0g、炭酸水素ナトリウム6.4gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム12.0gおよび精製水を加え溶解し、全量を2000gとしたものをpHが7.5~8.0の皮膜液とした。別に、EPA-E970gにHPMC(信越化学工業社製、TC-5E)30gを分散したものを内容液とした。以下、実施例1と同様の方法にて調製し、ゼラチン皮膜と内容液の間に、HPMCの膜が形成された、2層皮膜のシームレスカプセルを得た。シームレスカプセルはアルミラミネート袋に入れ、袋内を窒素置換して密封し、保存した。表10に皮膜液の処方を示す。
ゼラチン69.0kg、濃グリセリン30.3kg、炭酸水素ナトリウム2.07kgおよび精製水を混合した後、水酸化ナトリウムおよび精製水を加えてpHを調節し、全量を160kgとしたものをpH8.5~9.0の皮膜液とした。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とした。皮膜液を用いてゼラチンシートを作成し、鋳型を用いてこれを打ち抜きながら内容液を充てんし、ロータリー法により軟カプセルを得た。製造した軟カプセルはアルミラミネート袋に入れ、密封した。表11に皮膜液の処方を示す。
ゼラチン33.2kg、コハク化ゼラチン33.2kg、濃グリセリン19.9kg、炭酸水素ナトリウム1.99kgおよび精製水を加えて混合し、水酸化ナトリウムおよび精製水を加えてpHを調節し、全量を160kgとしたものをpHが8.5~9.0の皮膜液とした。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とした。以下、実施例11と同様の方法にて調製し、保存した。表12に皮膜液の処方を示す。
ゼラチン33.2kg、コハク化ゼラチン33.2kg、濃グリセリン19.9kg、炭酸水素ナトリウム1.99kg、メタケイ酸アルミン酸マグネシウム3.85kgおよび精製水を混合し、水酸化ナトリウムおよび精製水を加えてpHを調節し、全量を160kgとしたものをpHが8.5~9.0の皮膜液とした。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とした。以下、実施例11と同様の方法にて調製し、保存した。表13に皮膜液の処方を示す。
ゼラチン33.2kg、コハク化ゼラチン33.2kg、濃グリセリン19.9kg、炭酸水素ナトリウム1.99kgおよび精製水を加えて混合し、水酸化ナトリウムおよび精製水を加えてpHを調節し、全量を160kgとしたものをpHが7.5~8.5の皮膜液とする。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とする。以下、実施例11と同様の方法にて調製し、保存する。表14に皮膜液の処方を示す。
ゼラチン310.5g、ソルビトール33.0g、濃グリセリン31.5g、無水エタノール3.0gおよび精製水を混合した後、0.5mol/L水酸化ナトリウムを添加してpHを調節し、プラバスタチンナトリウム9.0gと精製水を加え溶解し、全量を1500gとしたものをpH8.5~9.0の皮膜液とし、EPA-Eを内容液とした。以下、実施例1と同様の方法にて調製し、保存した。表15に皮膜液の処方を示す。
プラバスタチンナトリウムをロスバスタチンカルシウムに置き換え、EPA-Eとロスバスタチンカルシウムの配合比率を720:1とした以外は、実施例1~15に記載されている方法に準じて、直径約4mmのシームレスカプセルまたはロータリー式軟カプセルを得る。以下、実施例1と同様の方法にてカプセルを保存する。表16に各皮膜液の処方を示す。
ゼラチン372.6g、ソルビトール39.6g、濃グリセリン37.8g、無水エタノール3.6g、精製水を混合した後、プラバスタチンナトリウム10.8gと精製水を加え溶解し、全量を1800gとしたものをpH7.0以下の皮膜液とした。別に、EPA-Eに無水エタノール1.5質量%相当量を混和させたものを内容液とした。以下、実施例1と同様の方法に調製し、保存した。表17に皮膜液の処方を示す。
ゼラチン77.29kg、濃グリセリン34.16kgおよび精製水を加えて混合し、全量を180kgとしたものをpHが7.0以下の皮膜液とした。別に、EPA-E900.0gにプラバスタチンナトリウム10.0gを懸濁したものを内容液とした。以下、実施例11と同様の方法にて調製し、保存した。表18に皮膜液の処方を示す。
*プラバスタチンナトリウムの安定化(シームレスカプセル)
実施例1~9、15および比較例1の各シームレスカプセルを40℃または50℃に保存し、経時試験を行った。初期、および40℃相対湿度75%(表中で75%RHのように表記する)に4週間(表中で4Wのように表記する)保存後または50℃に10日保存後に、シームレスカプセルからプラバスタチンナトリウムの類縁物質を抽出し、常法により高速液体クロマトグラフ法(以下、HPLCと記す)にて分析した。各シームレスカプセルの類縁物質の合計量を表19に示す。
*ゼラチンの変性抑制
・皮膜A、皮膜B
表20に示す処方の皮膜液を調製し、シャーレに展延し、乾燥を行い、ゼラチン皮膜を作成した。作成したゼラチン皮膜をEPA-Eに浸して、窒素置換を行い密封し、60℃で10日間保存した後の皮膜の外観を評価した。
・皮膜C、皮膜D
表20に示す処方の皮膜液を調製し、シリンジを用いて棒状に成形し、乾燥を行い、約0.3gの棒状のゼラチン皮膜を作成した。作成したゼラチン皮膜はEPA-Eに浸して、窒素置換を行い密封し、50℃で10日間保存した。保存後の皮膜を37℃の温水900mL中で溶解し、溶解後の液をフィルター(孔径:1μm)にてろ過し、フィルター上の不溶化物の乾燥後の質量より、以下の式にて不溶化率(%)を算出した。
不溶化率(%)={不溶化物乾燥質量(mg)/試験に用いた皮膜の質量(mg)}×100
不溶化率の評価:○不溶化率0.3%未満、×不溶化率0.3%以上
コハク化ゼラチンや酒石酸を添加した皮膜Aおよび皮膜Bでは、60℃で10日間保存後も皮膜の外観の変化は認められなかった。また、加水分解ゼラチン末やトレハロースを添加した皮膜Cおよび皮膜Dでは、50℃で10日間保存後も不溶化率は0.3%未満であった。即ち、本発明の軟カプセルの皮膜中にコハク化ゼラチン、酒石酸、加水分解ゼラチン末またはトレハロースを添加することで、保存時の皮膜変性または不溶化抑制効果を示した。
*プラバスタチンナトリウムの安定化(ロータリー法軟カプセル)
実施例11~13および比較例2の各軟カプセルを40℃に保存し、経時試験を行った。初期および40℃相対湿度75%に2週間または4週間保存後に軟カプセルからプラバスタチンナトリウムの類縁物質を抽出し、常法によりHPLCにて測定した。各軟カプセルの類縁物質の合計量を表21に示す。
Claims (5)
- ω3多価不飽和脂肪酸およびその製薬学上許容しうる塩およびエステルからなる群から選ばれる少なくとも1つ、ならびに、水溶性スタチン化合物からなる群から選ばれる少なくとも1つを含有し、カプセル皮膜のpHが7.0~9.5に調整された、軟カプセルの形態である配合製剤。
- ω3多価不飽和脂肪酸およびその製薬学上許容しうる塩およびエステルからなる群から選ばれる少なくとも1つがカプセル内容物に含有され、水溶性スタチン化合物からなる群から選ばれる少なくとも1つがカプセル皮膜に含有されている、請求項1に記載の配合製剤。
- 炭酸塩および/またはメタケイ酸アルミン酸マグネシウムが前記カプセル皮膜に含有されている、請求項1または2に記載の配合製剤。
- 前記カプセル皮膜がゼラチンを含有し、かつ、コハク化ゼラチン、酒石酸、加水分解ゼラチンおよびトレハロースからなる群から選ばれる少なくとも1つを含有する、請求項1ないし3の何れかに記載の配合製剤。
- 前記水溶性スタチン化合物が、プラバスタチンおよびロスバスタチン、ならびにそれらの塩および水和物からなる群から選択される少なくとも1つである請求項1ないし4の何れかに記載の配合製剤。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES11800926T ES2710540T5 (es) | 2010-06-30 | 2011-06-29 | Preparación de compuesto de ácido graso omega-3 |
| US13/806,032 US8609138B2 (en) | 2010-06-30 | 2011-06-29 | ω3 fatty acid compound preparation |
| JP2012522678A JP5829607B2 (ja) | 2010-06-30 | 2011-06-29 | ω3脂肪酸の配合製剤 |
| EP11800926.5A EP2664328B2 (en) | 2010-06-30 | 2011-06-29 | Omega3 fatty acid compound preparation |
| CA2803558A CA2803558C (en) | 2010-06-30 | 2011-06-29 | .omega.3 fatty acid compound preparation |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010150611 | 2010-06-30 | ||
| JP2010-150611 | 2010-06-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012002464A1 true WO2012002464A1 (ja) | 2012-01-05 |
Family
ID=45402168
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/064976 WO2012002464A1 (ja) | 2010-06-30 | 2011-06-29 | ω3脂肪酸の配合製剤 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8609138B2 (ja) |
| EP (1) | EP2664328B2 (ja) |
| JP (1) | JP5829607B2 (ja) |
| CA (1) | CA2803558C (ja) |
| ES (1) | ES2710540T5 (ja) |
| WO (1) | WO2012002464A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014095628A1 (en) * | 2012-12-17 | 2014-06-26 | Sigma-Tau Industrie Farmaceutiche Riunite S.P.A. | Oral formulation containing a statin in omega-3 polyunsaturated fatty acids (n-3 pufa) |
| EP2844257A4 (en) * | 2012-05-01 | 2016-06-01 | Catabasis Pharmaceuticals Inc | Fatty Acid Conjugates from Statin and FXR Agonists; COMPOSITIONS AND METHODS OF USE |
| US20190099422A1 (en) * | 2013-03-15 | 2019-04-04 | Amarin Pharmaceuticals Ireland Limited | Pharmaceutical composition comprising eicosapentaenoic acid and derivatives thereof and a statin |
| WO2022215753A1 (ja) * | 2021-04-09 | 2022-10-13 | アリメント工業株式会社 | ゼラチンカプセル剤 |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20110236476A1 (en) | 2008-09-02 | 2011-09-29 | Amarin Corporation Plc. | Pharmaceutical composition comprising eicosapentaenoic acid and nicotinic acid and methods of using same |
| NZ624963A (en) | 2009-04-29 | 2016-07-29 | Amarin Pharmaceuticals Ie Ltd | Pharmaceutical compositions comprising epa and a cardiovascular agent and methods of using the same |
| NZ627238A (en) | 2009-04-29 | 2016-02-26 | Amarin Pharmaceuticals Ie Ltd | Stable pharmaceutical composition comprising ethyl eicosapentaenoate |
| MY172372A (en) | 2009-06-15 | 2019-11-21 | Amarin Pharmaceuticals Ie Ltd | Compositions and methods for lowering triglycerides |
| WO2011038122A1 (en) | 2009-09-23 | 2011-03-31 | Amarin Corporation Plc | Pharmaceutical composition comprising omega-3 fatty acid and hydroxy-derivative of a statin and methods of using same |
| NZ744990A (en) | 2010-11-29 | 2019-10-25 | Amarin Pharmaceuticals Ie Ltd | Low eructation composition and methods for treating and/or preventing cardiovascular disease in a subject with fish allergy/hypersensitivity |
| US11712429B2 (en) | 2010-11-29 | 2023-08-01 | Amarin Pharmaceuticals Ireland Limited | Low eructation composition and methods for treating and/or preventing cardiovascular disease in a subject with fish allergy/hypersensitivity |
| US20130131170A1 (en) | 2011-11-07 | 2013-05-23 | Amarin Pharmaceuticals Ireland Limited | Methods of treating hypertriglyceridemia |
| US11291643B2 (en) | 2011-11-07 | 2022-04-05 | Amarin Pharmaceuticals Ireland Limited | Methods of treating hypertriglyceridemia |
| EP2793867B1 (en) | 2011-12-22 | 2021-01-20 | Baes, Erik | Gelatin/alginate delayed release capsules comprising omega-3 fatty acids, and methods and uses thereof |
| EP2800469B1 (en) | 2012-01-06 | 2021-08-25 | Amarin Pharmaceuticals Ireland Limited | Compositions and methods for lowering levels of high-sensitivity (hs-crp) in a subject |
| WO2013192109A1 (en) | 2012-06-17 | 2013-12-27 | Matinas Biopharma, Inc. | Omega-3 pentaenoic acid compositions and methods of use |
| EP2866801A4 (en) | 2012-06-29 | 2016-02-10 | Amarin Pharmaceuticals Ie Ltd | METHODS OF REDUCING THE RISK OF A CARDIOVASCULAR EVENT IN A SUBJECT SUBJECTED TO STATIN TREATMENT |
| WO2014074552A2 (en) | 2012-11-06 | 2014-05-15 | Amarin Pharmaceuticals Ireland Limited | Compositions and methods for lowering triglycerides without raising ldl-c levels in a subject on concomitant statin therapy |
| US20140187633A1 (en) | 2012-12-31 | 2014-07-03 | Amarin Pharmaceuticals Ireland Limited | Methods of treating or preventing nonalcoholic steatohepatitis and/or primary biliary cirrhosis |
| US9452151B2 (en) | 2013-02-06 | 2016-09-27 | Amarin Pharmaceuticals Ireland Limited | Methods of reducing apolipoprotein C-III |
| US9624492B2 (en) | 2013-02-13 | 2017-04-18 | Amarin Pharmaceuticals Ireland Limited | Compositions comprising eicosapentaenoic acid and mipomersen and methods of use thereof |
| US10966968B2 (en) | 2013-06-06 | 2021-04-06 | Amarin Pharmaceuticals Ireland Limited | Co-administration of rosiglitazone and eicosapentaenoic acid or a derivative thereof |
| US20150065572A1 (en) | 2013-09-04 | 2015-03-05 | Amarin Pharmaceuticals Ireland Limited | Methods of treating or preventing prostate cancer |
| US9585859B2 (en) | 2013-10-10 | 2017-03-07 | Amarin Pharmaceuticals Ireland Limited | Compositions and methods for lowering triglycerides without raising LDL-C levels in a subject on concomitant statin therapy |
| US10561631B2 (en) | 2014-06-11 | 2020-02-18 | Amarin Pharmaceuticals Ireland Limited | Methods of reducing RLP-C |
| WO2015195662A1 (en) | 2014-06-16 | 2015-12-23 | Amarin Pharmaceuticals Ireland Limited | Methods of reducing or preventing oxidation of small dense ldl or membrane polyunsaturated fatty acids |
| BR112017013445B1 (pt) * | 2014-12-23 | 2021-11-23 | Evonik Operations Gmbh | Processo para aumentar a estabilidade de uma composição que compreende ácidos graxos ômega 6 poli-insaturados e uso da composição de produto |
| PL3236782T3 (pl) * | 2014-12-23 | 2020-06-29 | Evonik Operations Gmbh | Sposób zwiększania stabilności kompozycji zawierającej wielonienasycone kwasy tłuszczowe omega-3 |
| US10406130B2 (en) | 2016-03-15 | 2019-09-10 | Amarin Pharmaceuticals Ireland Limited | Methods of reducing or preventing oxidation of small dense LDL or membrane polyunsaturated fatty acids |
| WO2018213663A1 (en) | 2017-05-19 | 2018-11-22 | Amarin Pharmaceuticals Ireland Limited | Compositions and methods for lowering triglycerides in a subject having reduced kidney function |
| CN107422021B (zh) * | 2017-07-14 | 2019-11-19 | 北京朗阅科技有限公司 | 琼脂糖胶囊及其制备方法与应用 |
| US11058661B2 (en) | 2018-03-02 | 2021-07-13 | Amarin Pharmaceuticals Ireland Limited | Compositions and methods for lowering triglycerides in a subject on concomitant statin therapy and having hsCRP levels of at least about 2 mg/L |
| KR102296068B1 (ko) | 2018-09-24 | 2021-09-02 | 애머린 파마슈티칼스 아일랜드 리미티드 | 대상체에서 심혈관 사건의 위험도를 감소시키는 방법 |
Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS55138457A (en) * | 1979-04-18 | 1980-10-29 | Tokai Capsule Co Ltd | Fusible soft capsule |
| JPH026406A (ja) | 1988-03-31 | 1990-01-10 | E R Squibb & Sons Inc | 安定性良好な医薬組成物 |
| JPH038435A (ja) * | 1989-06-06 | 1991-01-16 | Riyouei Shoji:Kk | 水溶性軟カプセル |
| JPH05246844A (ja) | 1991-12-12 | 1993-09-24 | Sandoz Ag | HMG−CoAリダクターゼ禁止剤化合物を含んでなる安定化された製薬学的組成物 |
| JPH11502838A (ja) * | 1995-03-29 | 1999-03-09 | ザ、プロクター、エンド、ギャンブル、カンパニー | キサンチン誘導体を含むゼラチン外殻を有するソフトゼラチンカプセル |
| JP2003002829A (ja) | 2001-04-17 | 2003-01-08 | Toyo Pharmar Kk | 医薬組成物 |
| JP2003073270A (ja) | 2001-08-30 | 2003-03-12 | Nisshin Seiyaku Kk | 安定性および溶出性の良好なプラバスタチンナトリウム錠 |
| JP2004002473A (ja) | 1998-12-07 | 2004-01-08 | Towa Yakuhin Kk | プラバスタチンナトリウム錠 |
| JP2004196706A (ja) * | 2002-12-18 | 2004-07-15 | Hayashibara Biochem Lab Inc | 食感が改善されたシームレスカプセルとその製造方法 |
| WO2006045865A1 (es) | 2004-10-19 | 2006-05-04 | Gp Pharm S.A. | Formulación farmacéutica que comprende microcapsulas de estatinas suspendidas en ester alquílicos de ácidos grasos poliinsaturados (pufa) |
| WO2006096806A2 (en) | 2005-03-08 | 2006-09-14 | Reliant Pharmaceutiacals, Inc. | Treatment with statin and omega-3 fatty acids and a combination product thereof |
| WO2007103557A2 (en) | 2006-03-09 | 2007-09-13 | Reliant Pharmaceuticals, Inc. | Coating capsules with active pharmaceutical ingredients |
| WO2007130714A1 (en) * | 2006-02-01 | 2007-11-15 | Transform Pharmaceuticals, Inc. | Novel statin pharmaceutical compositions and related methods of treatment |
| WO2009087938A1 (ja) | 2008-01-10 | 2009-07-16 | Takeda Pharmaceutical Company Limited | カプセル製剤 |
| JP2010513351A (ja) * | 2006-12-20 | 2010-04-30 | ノバルティス アーゲー | 酸を含むゼラチンカプセル剤 |
| JP2010260812A (ja) * | 2009-05-01 | 2010-11-18 | Nakanihon Capsule Co Ltd | ソフトカプセル |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI20109A (sl) * | 1998-12-16 | 2000-06-30 | LEK, tovarna farmacevtskih in kemi�nih izdelkov, d.d. | Stabilna farmacevtska formulacija |
| JP2002080430A (ja) * | 2000-06-23 | 2002-03-19 | Sankyo Co Ltd | プラバスタチンを含有する医薬組成物を安定させる方法 |
| CA2483099A1 (en) | 2002-05-03 | 2003-11-13 | Hexal Ag | Stable pharmaceutical formulation for a combination of a statin and an ace inhibitor |
| GB0217306D0 (en) | 2002-07-25 | 2002-09-04 | Novartis Ag | Compositions comprising organic compounds |
| JP2008509154A (ja) | 2004-08-06 | 2008-03-27 | トランスフオーム・フアーマシユーチカルズ・インコーポレーテツド | 新規なスタチン薬剤組成物および関連治療方法 |
| EP1905424A3 (en) | 2006-02-02 | 2008-04-30 | Ranbaxy Laboratories Limited | Process for the preparation of a pharmaceutical composition comprising stabilized statin particles |
| US8784886B2 (en) | 2006-03-09 | 2014-07-22 | GlaxoSmithKline, LLC | Coating capsules with active pharmaceutical ingredients |
| JP2009541433A (ja) * | 2006-06-26 | 2009-11-26 | ヴァルファルマ ソチエタ アノニマ | オメガポリエン脂肪酸の経口投与のための医薬品の組成物、及び1又はそれ以上の配合禁忌の有効成分、並びにその調剤の工程 |
| US20080038332A1 (en) | 2006-08-10 | 2008-02-14 | Cai Gu Huang | Stable pharmaceutical formulation comprising atorvastatin calcium |
| ITMI20072142A1 (it) | 2007-11-08 | 2009-05-09 | Yervant Zarmanian | Composizioni farmaceutiche contenenti statine e derivati di acidi grassi omega-3 |
| EP2306982B1 (en) * | 2008-06-27 | 2015-01-07 | Abdi Ibrahim Ilac Sanayi ve Ticaret Anonim Sirketi | Pharmaceutical compositions of rosuvastatin calcium |
| WO2010010579A1 (en) | 2008-07-19 | 2010-01-28 | Lupin Limited | Multiple unit dosage form of niacin |
-
2011
- 2011-06-29 ES ES11800926T patent/ES2710540T5/es active Active
- 2011-06-29 CA CA2803558A patent/CA2803558C/en active Active
- 2011-06-29 WO PCT/JP2011/064976 patent/WO2012002464A1/ja active Application Filing
- 2011-06-29 EP EP11800926.5A patent/EP2664328B2/en active Active
- 2011-06-29 US US13/806,032 patent/US8609138B2/en active Active
- 2011-06-29 JP JP2012522678A patent/JP5829607B2/ja active Active
Patent Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS55138457A (en) * | 1979-04-18 | 1980-10-29 | Tokai Capsule Co Ltd | Fusible soft capsule |
| JPH026406A (ja) | 1988-03-31 | 1990-01-10 | E R Squibb & Sons Inc | 安定性良好な医薬組成物 |
| JPH038435A (ja) * | 1989-06-06 | 1991-01-16 | Riyouei Shoji:Kk | 水溶性軟カプセル |
| JPH05246844A (ja) | 1991-12-12 | 1993-09-24 | Sandoz Ag | HMG−CoAリダクターゼ禁止剤化合物を含んでなる安定化された製薬学的組成物 |
| JPH11502838A (ja) * | 1995-03-29 | 1999-03-09 | ザ、プロクター、エンド、ギャンブル、カンパニー | キサンチン誘導体を含むゼラチン外殻を有するソフトゼラチンカプセル |
| JP2004002473A (ja) | 1998-12-07 | 2004-01-08 | Towa Yakuhin Kk | プラバスタチンナトリウム錠 |
| JP3719679B2 (ja) | 1998-12-07 | 2005-11-24 | 三共株式会社 | プラバスタチンナトリウム錠 |
| JP2003002829A (ja) | 2001-04-17 | 2003-01-08 | Toyo Pharmar Kk | 医薬組成物 |
| JP2003073270A (ja) | 2001-08-30 | 2003-03-12 | Nisshin Seiyaku Kk | 安定性および溶出性の良好なプラバスタチンナトリウム錠 |
| JP2004196706A (ja) * | 2002-12-18 | 2004-07-15 | Hayashibara Biochem Lab Inc | 食感が改善されたシームレスカプセルとその製造方法 |
| WO2006045865A1 (es) | 2004-10-19 | 2006-05-04 | Gp Pharm S.A. | Formulación farmacéutica que comprende microcapsulas de estatinas suspendidas en ester alquílicos de ácidos grasos poliinsaturados (pufa) |
| JP2008517040A (ja) | 2004-10-19 | 2008-05-22 | デフィアンテ ファルマセウティカ,リミタダ. | ポリ不飽和脂肪酸(pufa)アルキルエステルに分散されたスタチンのマイクロカプセルを含む医薬組成物 |
| WO2006096806A2 (en) | 2005-03-08 | 2006-09-14 | Reliant Pharmaceutiacals, Inc. | Treatment with statin and omega-3 fatty acids and a combination product thereof |
| JP2008533029A (ja) | 2005-03-08 | 2008-08-21 | レリアント ファーマスーティカルズ インコーポレイテッド | スタチン及びω−3脂肪酸による治療方法、並びにそれらの複合生成物 |
| WO2007130714A1 (en) * | 2006-02-01 | 2007-11-15 | Transform Pharmaceuticals, Inc. | Novel statin pharmaceutical compositions and related methods of treatment |
| WO2007103557A2 (en) | 2006-03-09 | 2007-09-13 | Reliant Pharmaceuticals, Inc. | Coating capsules with active pharmaceutical ingredients |
| JP2009529531A (ja) | 2006-03-09 | 2009-08-20 | レリアント ファーマスーティカルズ インコーポレイテッド | 医薬成分を含有するコーティングカプセル |
| JP2010513351A (ja) * | 2006-12-20 | 2010-04-30 | ノバルティス アーゲー | 酸を含むゼラチンカプセル剤 |
| WO2009087938A1 (ja) | 2008-01-10 | 2009-07-16 | Takeda Pharmaceutical Company Limited | カプセル製剤 |
| JP2010260812A (ja) * | 2009-05-01 | 2010-11-18 | Nakanihon Capsule Co Ltd | ソフトカプセル |
Non-Patent Citations (6)
| Title |
|---|
| "Drug Interview Form", January 2011, ASTRAZENECA K.K., SHIONOGI & CO., LTD., article "Crestor" |
| "Drug Interview Form", July 2010, DAIICHI SANKYO CO., LTD., article "Mevalotin" |
| "Drug Interview Form", June 2010, ASTELLAS PHARMA INC., article "Lipitor" |
| LANCET, vol. 369, 2007, pages 1090 - 1098 |
| PHARMACOLOGY & THERAPEUTICS, vol. 113, 2007, pages 378 - 393 |
| See also references of EP2664328A4 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2844257A4 (en) * | 2012-05-01 | 2016-06-01 | Catabasis Pharmaceuticals Inc | Fatty Acid Conjugates from Statin and FXR Agonists; COMPOSITIONS AND METHODS OF USE |
| WO2014095628A1 (en) * | 2012-12-17 | 2014-06-26 | Sigma-Tau Industrie Farmaceutiche Riunite S.P.A. | Oral formulation containing a statin in omega-3 polyunsaturated fatty acids (n-3 pufa) |
| US20190099422A1 (en) * | 2013-03-15 | 2019-04-04 | Amarin Pharmaceuticals Ireland Limited | Pharmaceutical composition comprising eicosapentaenoic acid and derivatives thereof and a statin |
| US11547710B2 (en) * | 2013-03-15 | 2023-01-10 | Amarin Pharmaceuticals Ireland Limited | Pharmaceutical composition comprising eicosapentaenoic acid and derivatives thereof and a statin |
| WO2022215753A1 (ja) * | 2021-04-09 | 2022-10-13 | アリメント工業株式会社 | ゼラチンカプセル剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2664328B1 (en) | 2018-11-21 |
| US20130115284A1 (en) | 2013-05-09 |
| CA2803558A1 (en) | 2012-01-05 |
| JP5829607B2 (ja) | 2015-12-09 |
| US8609138B2 (en) | 2013-12-17 |
| EP2664328A1 (en) | 2013-11-20 |
| ES2710540T5 (es) | 2022-08-26 |
| CA2803558C (en) | 2018-05-29 |
| EP2664328B2 (en) | 2022-04-27 |
| JPWO2012002464A1 (ja) | 2013-08-29 |
| EP2664328A4 (en) | 2014-01-22 |
| ES2710540T3 (es) | 2019-04-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5829607B2 (ja) | ω3脂肪酸の配合製剤 | |
| KR101310710B1 (ko) | 오메가-3 지방산 에스테르 및 HMG-CoA 환원효소 억제제를 포함하는 경구용 복합 조성물 | |
| US20210128510A1 (en) | Self-emulsifying composition of omega3 fatty acid | |
| RU2709612C2 (ru) | САМОЭМУЛЬГИРУЮЩАЯСЯ КОМПОЗИЦИЯ ω3 ЖИРНОЙ КИСЛОТЫ | |
| US20190231731A1 (en) | Self-emulsifying composition of omega3 fatty acid | |
| JP2009502950A (ja) | ジヒドロピリジンカルシウムチャネルブロッカー及びω3脂肪酸を用いた治療法、並びにそれらの混合生成物 | |
| JP2010506841A (ja) | 抗不整脈薬およびオメガ−3脂肪酸およびそれらの組合せ品による治療法 | |
| JP2009541433A (ja) | オメガポリエン脂肪酸の経口投与のための医薬品の組成物、及び1又はそれ以上の配合禁忌の有効成分、並びにその調剤の工程 | |
| US10512611B2 (en) | Millicapsule formulations comprising polyunsaturated free fatty acids | |
| KR101466617B1 (ko) | 오메가-3 지방산 및 HMG-CoA 환원효소 억제제를 포함하는 안정성이 증가된 경구용 복합 제제 | |
| KR102108154B1 (ko) | 개선된 생체이용률을 갖는 오메가-3 지방산 및 HMG-CoA 환원효소 억제제를 포함하는 약제학적 복합제제 | |
| KR101830977B1 (ko) | 오메가-3 지방산 또는 이의 에스테르 및 하이드록시메틸글루타닐 코엔자임에이 환원효소 억제제를 포함하는 경구용 복합 제제 | |
| KR20130003501A (ko) | 오메가-3 지방산 또는 이의 에스테르 및 하이드록시메틸글루타닐 코엔자임에이 환원효소 억제제를 포함하는 경구용 복합 제제 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11800926 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2012522678 Country of ref document: JP |
|
| ENP | Entry into the national phase |
Ref document number: 2803558 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13806032 Country of ref document: US Ref document number: 2011800926 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |