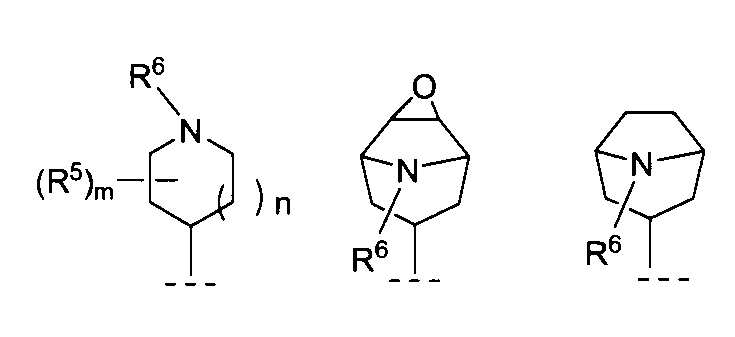WO2010126025A1 - 四級アンモニウム塩化合物 - Google Patents
四級アンモニウム塩化合物 Download PDFInfo
- Publication number
- WO2010126025A1 WO2010126025A1 PCT/JP2010/057422 JP2010057422W WO2010126025A1 WO 2010126025 A1 WO2010126025 A1 WO 2010126025A1 JP 2010057422 W JP2010057422 W JP 2010057422W WO 2010126025 A1 WO2010126025 A1 WO 2010126025A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- unsubstituted
- group
- methyl
- carbamoyl
- phenylphenyl
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/18—Bridged systems
Definitions
- the present invention relates to novel compounds having ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity.
- the invention also relates to pharmaceutical compositions comprising such compounds, processes and intermediates for preparing such compositions, and methods of using such compounds to treat pulmonary disease.
- Bronchodilator drugs are commonly used for the treatment of chronic lung diseases such as asthma and chronic obstructive pulmonary disease (COPD).
- chronic lung diseases such as asthma and chronic obstructive pulmonary disease (COPD).
- COPD chronic obstructive pulmonary disease
- beta 2 adrenergic receptor (adrenoceptor) agonists such as albuterol, formoterol and salmeterol
- muscarinic receptor antagonists such as anticholinergic compounds such as ipratropium and tiotropium. These compounds are mainly administered by inhalation.
- a compound having both ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity produces bronchodilation by two distinct modes of action while being a single molecule.
- Such disadvantages can be eliminated by making the drug into a single molecule having two actions.
- having a single molecule is useful for patients who are being treated as it is easier to formulate with other therapeutic agents to create triple therapy combinations.
- Pharmacologically these two actions can be expressed synchronously, as the two actions are based on the pharmacokinetics of a single molecule in the lung tissue administered.
- side effects can be reduced by providing pharmacokinetic characteristics that can not be achieved by the combination of two agents or their combination depending on the structural design.
- Compounds having two functions in such a single molecule are reported, for example, in Patent Documents 1 to 6 and the like. However, these compounds are clearly different in structure from the compounds disclosed in the present invention.
- An object of the present invention is to provide quaternary ammonium salt compounds having both ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity.
- R 1 represents a hydrogen atom or an unsubstituted C1-C8 alkyl group
- R 2 is a single bond, C 1 -C 8 alkylene (unsubstituted or carbon atom substituted by 1 to 2 oxygen atoms), unsubstituted C 2 -C 4 alkenylene, or unsubstituted —O—C 1 -C 4 alkylene
- X represents a single bond, -O-, -CONR 3- , -NR 3 CO-, or -NR 3 CO-CH 2 -O-
- R 3 represents a hydrogen atom or unsubstituted C 1 Represents a C8 alkyl group
- a 1 is a single bond, unsubstituted or (halogen atom, hydroxyl group, cyano group, nitro group, carboxyl group, trifluoromethyl group, unsubstituted C 1 to C
- R 4 represents unsubstituted C 1 -C 10 alkylene
- R 8 and R 9 each independently represent a halogen atom, a cyano group, an unsubstituted C 1 to C 6 alkyl group, a nitro group, or -NR 10 R 11 (wherein R 10 and R 11 each independently represent A hydrogen atom or an unsubstituted C1-C6 alkyl group), an unsubstituted C1-C6 alkoxy group, a carboxyl group, an unsubstituted C1-C6 alkoxycarbonyl group, a hydroxyl group, a trifluoromethyl group, a mercapto group or Represents an unsubstituted C1-C6 alkylthio group
- a and b each independently represent an integer of
- a quaternary ammonium salt compound represented by or a pharmaceutically acceptable salt thereof (2) The quaternary ammonium salt compound or the pharmaceutically acceptable salt thereof according to (1), wherein R 2 , X and A 1 are any of the following (i) to (iv): (I) R 2 is a single bond, C 1 -C 4 alkylene (carbon atom is substituted by one oxygen atom), unsubstituted C 1 -C 8 alkylene, or unsubstituted —O—C 1 -C 4 alkylene; X Is -O-; A 1 represents a single bond or unsubstituted phenylene.
- R 2 is unsubstituted C 1 -C 4 alkylene, unsubstituted C 2 -C 4 alkenylene, or unsubstituted -O-C 1 -C 4 alkylene;
- X is -CONR 3- ;
- a 1 is a single bond, unsubstituted And C 1 -C 4 alkylene-unsubstituted phenylene or unsubstituted C 6 -C 8 cycloalkylene.
- R 2 is unsubstituted C 1 -C 4 alkylene;
- X is —NR 3 CO— or —NR 3 CO—CH 2 —O—;
- a 1 is unsubstituted phenylene.
- R 2 , X and A 1 represent a single bond.
- R 2 is a single bond; X is -O-; A 1 is a single bond: R 4 represents unsubstituted C1-C10 alkylene.
- R 2 is (unsubstituted or carbon atom is replaced by one oxygen atom) C1 ⁇ C8 alkylene; X is -O-; A 1 is a single bond; R 4 is an unsubstituted C1 ⁇ C10 alkylene Represents (Vii) R 2 is C1 ⁇ C8 alkylene unsubstituted; X is -O-; A 1 is an unsubstituted phenylene -; R 4 represents a C1 ⁇ C4 alkylene unsubstituted.
- R 2 is —O-unsubstituted C 1 -C 4 alkylene; X is —O—; A 1 is unsubstituted phenylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted C 1 to C 4 alkylene; X is -CONR 3- ; A 1 is unsubstituted C 1 to C 4 alkylene-unsubstituted phenylene; R 4 is unsubstituted C 1 to C 4 alkylene.
- (Xi) R 2 is unsubstituted C 1 -C 4 alkylene; X is -CONR 3- ; A 1 is unsubstituted C 6 -C 8 cycloalkylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted C 1 -C 4 alkylene; X is -CONR 3- ; A 1 is unsubstituted phenylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted —O—C 1 -C 4 alkylene; X is —CONR 3 —; A 1 is unsubstituted phenylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted C 2 -C 4 alkenylene; X is -CONR 3- ; A 1 is unsubstituted phenylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted C 2 -C 4 alkenylene; X is -CONR 3- ; A 1 is unsubstituted C 1 -C 4 alkylene-unsubstituted phenylene; R 4 is unsubstituted C 1 -C 4 alkylene.
- R 2 is unsubstituted C1-C4 alkylene; X is -NR 3 CO-; A 1 is unsubstituted phenylene; R 4 is unsubstituted C1-C4 alkylene.
- R 2 is unsubstituted C1-C4 alkylene; X is -NR 3 CO-CH 2 -O-; A 1 is unsubstituted phenylene; R 4 is unsubstituted C1-C4 alkylene.
- R 2 is a single bond; X is a single bond; A 1 is a single bond; R 4 represents unsubstituted C 1 -C 8 alkylene.
- R 2 is (unsubstituted or carbon atom is replaced by one oxygen atom) C1 ⁇ C6 alkylene, or unsubstituted -O-C1 ⁇ C4 alkylene;
- X is -CONR 3- or -NR 3 CO-CH 2 -O-; 1 to 3 substituents selected from the group consisting of A 1 is unsubstituted or (halogen atom, hydroxyl group, unsubstituted C 1 to C 4 alkyl group, unsubstituted C 1 to C 4 alkoxy group, and trifluoromethyl group) (C6-C10 arylene or 5- to 10-membered heteroarylene); and R 4 is unsubstituted C1-C6 alkylene,
- R 2 is unsubstituted C 1 -C 6 alkylene;
- X is -CONR 3- ;
- a 1 is 1 to 4 substituents selected from the group consisting of unsubstituted or (halogen atom, hydroxy group, unsubstituted C1 to C4 alkyl group, unsubstituted C1 to C4 alkoxy group, and trihalomethyl group) Substituted (phenylene or naphthylene); and R 4 is unsubstituted C 1 -C 6 alkylene, The quaternary ammonium salt compound as described in (1) or a pharmaceutically acceptable salt thereof.
- R 2 is unsubstituted C 1 -C 6 alkylene; X is -CONH-; A 1 is unsubstituted or phenylene substituted with 1 to 2 substituents selected from the group consisting of halogen and methoxy; and R 4 is substituted or unsubstituted C 1 -C 6 alkylene
- R 1 represents a hydrogen atom, A quaternary ammonium salt compound or a pharmaceutically acceptable salt thereof according to any one of (1) to (6), wherein a represents an integer of 0.
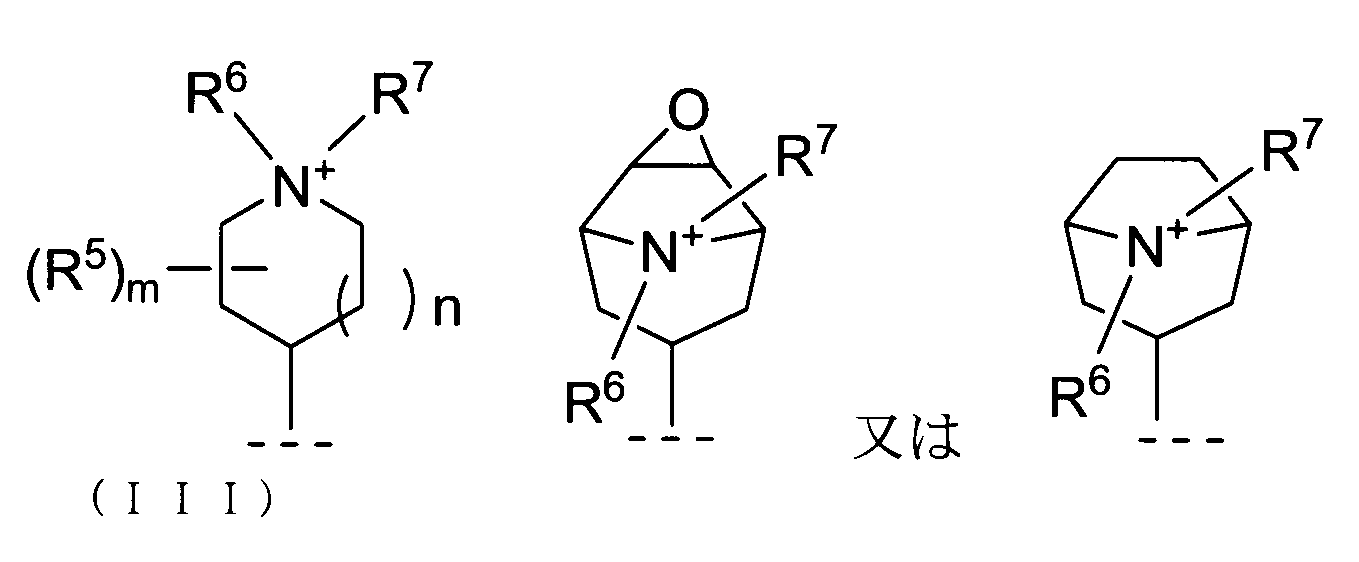
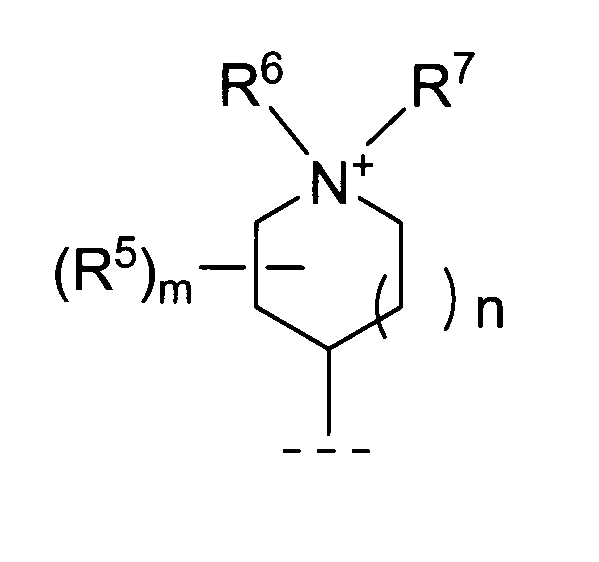
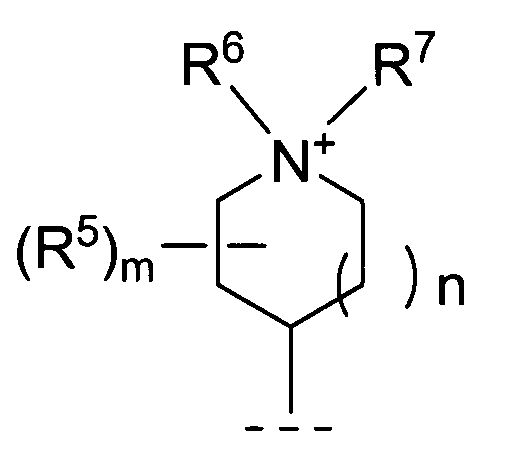
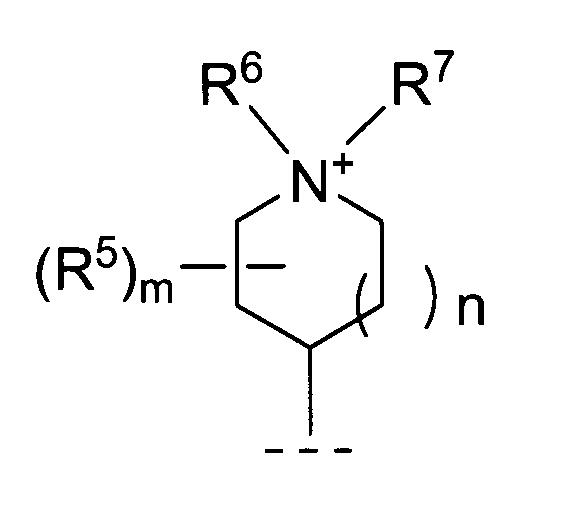
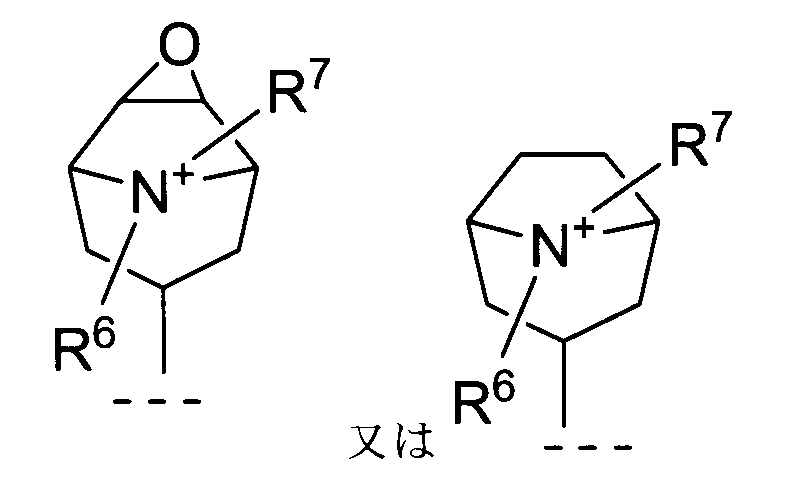
- Q is A group represented by R 6 and R 7 each independently represent a methyl group or a phenoxyethyl group, n represents an integer of 1 and The quaternary ammonium salt compound or the pharmaceutically acceptable salt thereof according to (7), wherein m represents an integer of 0. (9)
- Q A group represented by The quaternary ammonium salt compound according to (7) or a pharmaceutically acceptable salt thereof, wherein R 6 and R 7 each represent a methyl group.
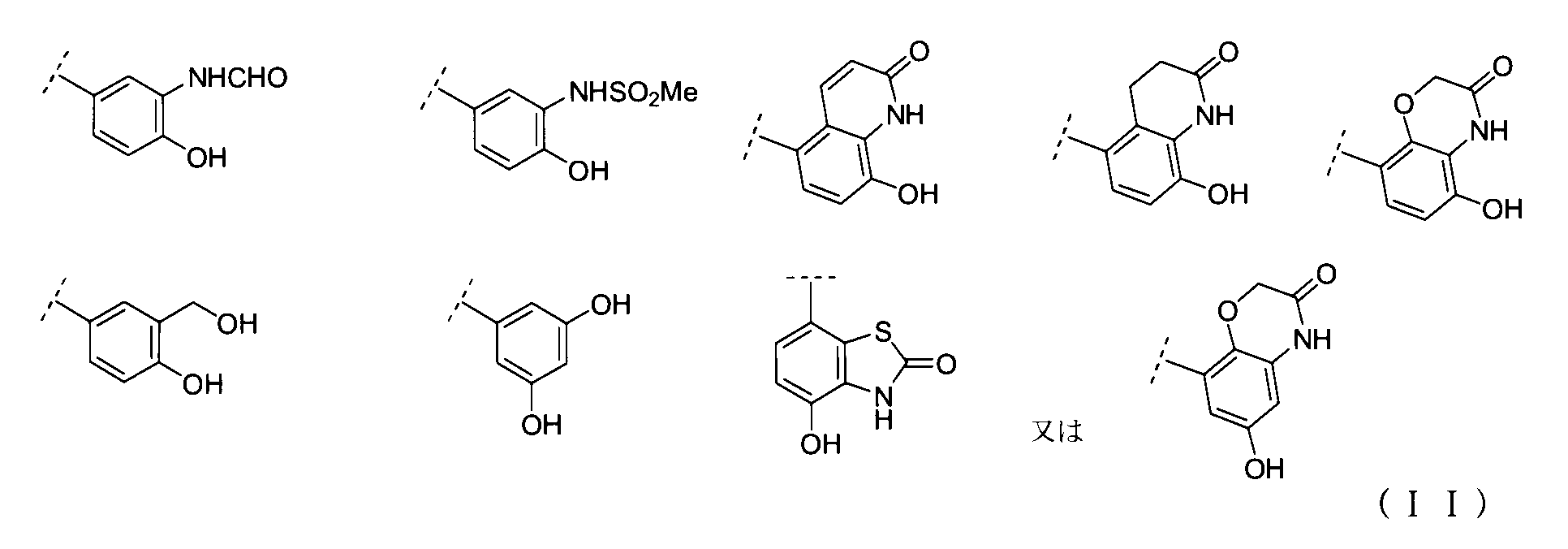
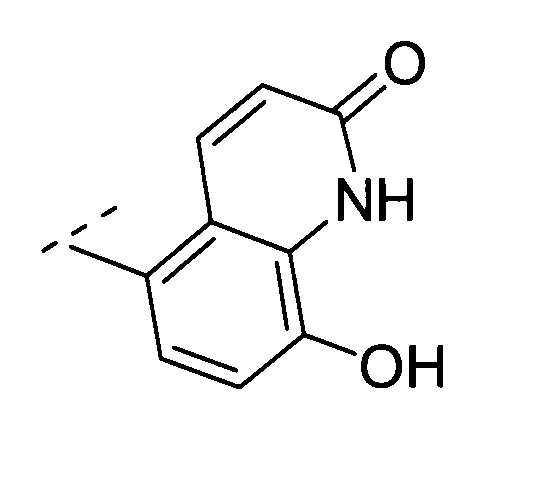
- Y is And the quaternary ammonium salt compound according to any one of (1) to (9) or a pharmaceutically acceptable salt thereof.
- a pharmaceutical composition comprising the compound according to any one of (1) to (10) or a pharmaceutically acceptable salt thereof, and a pharmaceutically acceptable carrier.
- a pharmaceutical composition having ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity comprising the compound according to any one of (1) to (10) or a pharmaceutically acceptable salt thereof as an active ingredient.
- a preventive or therapeutic agent for pulmonary disease which comprises the compound according to any one of (1) to (10) or a pharmaceutically acceptable salt thereof as an active ingredient.
- a prophylactic or therapeutic agent comprising the compound according to (13) or a pharmaceutically acceptable salt thereof as an active ingredient, wherein the pulmonary disease is chronic obstructive pulmonary disease or asthma.
- the compound represented by the formula (I) of the present invention or a pharmaceutically acceptable salt thereof has excellent ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity, and therefore has chronic obstructive pulmonary disease (COPD) or asthma Etc. are useful as preventive and therapeutic agents for inflammatory diseases.
- the compounds of the present invention have high bronchodilator activity by placing a quaternary ammonium structure at the terminal part of the molecule. Furthermore, it is possible to have excellent action duration, low side effects such as saliva suppression, and also have stability and ease of production.
- each group of the compound represented by the general formula (I) of the present invention is defined as follows.
- the order of description in each group represents the order of bonding in formula (I).
- C1 to C4 alkylene-substituted or unsubstituted arylene” of A 1 is such that “C1 to C4 alkylene” at the left end is bonded to X and “substituted or unsubstituted arylene” at the right end is bonded to R 4
- the number on the right of the carbon atom represents the number of carbon atoms, and for example, “C1 to C6” represents one having “carbon number 1 to 6”.
- the "C1-C8 alkyl group" in R 1 means a linear or branched carbon chain having 1 to 8 carbon atoms, and examples thereof include a methyl group, an ethyl group, a propyl group, an isopropyl group and a butyl group.
- those having 1 to 4 carbon atoms are preferable, and methyl group or ethyl group is particularly preferable.
- R 1 hydrogen is preferred.
- the "C1-C8 alkylene” in R 2 means a linear or branched carbon chain having 1 to 8 carbon atoms, and specifically, methylene, ethylene, propylene, isopropylene, butylene, Isobutylene, tert-butylene, pentylene, neopentylene, isopentylene, 1,2-dimethylpropylene, hexylene, isohexylene, 1,1-dimethylbutylene, 2,2-dimethylbutylene, octylene, nonylene, etc., among which 1 carbon atom It is preferable that 6 to 6 carbon atoms, more preferably 2 to 5 carbon atoms, and ethylene, propylene or butylene is particularly preferable.
- the C1 to C8 alkylene in R 2 may have a carbon atom substituted with one or two oxygen atoms at any chemically possible position.
- C2-C4 alkenylene in R 2 means a carbon chain containing an unsaturated double bond, and specifically includes vinylene, propenylene, butenylene, 2-methyl-1-propenylene etc., and vinylene, Or propenylene is preferred.
- C1-C4 alkylene in “-O-C1-C4 alkylene” for R 2 means a linear or branched carbon chain having 1 to 4 carbon atoms, and specifically, Methylene, ethylene, propylene, isopropylene, butylene and the like.
- Preferred as "-O-C1-C4 alkylene” is -O-ethylene, -O-propylene or -O-butylene.
- R 2 unsubstituted C 1 -C 6 alkylene is preferable, and ethylene, propylene or butylene is particularly preferable.
- the "C1-C8 alkyl group" in R 3 of X means a linear or branched carbon chain having 1 to 8 carbon atoms, and specifically, a methyl group, an ethyl group, a propyl group Isopropyl, butyl, isobutyl, tert-butyl, pentyl, neopentyl, isopentyl, 1,2-dimethylpropyl, hexyl, isohexyl, 1,1-dimethylbutyl, 2, 2- A dimethylbutyl group, a 1-ethylbutyl group, a 2-ethylbutyl group, an isoheptyl group, an octyl group, an isooctyl group and the like are shown, among which those having 1 to 4 carbon atoms are preferable, and a methyl group or an ethyl group is particularly preferable.
- -O- or -CONR 3 - is preferable, and particularly preferably -O- or -CONH-.
- C6 ⁇ C10 arylene in A 1, means an aromatic hydrocarbon ring C6 ⁇ C10, specifically, represents phenylene, and the hydrocarbon ring arylene naphthylene, preferably phenylene, or naphthylene is there.
- a 5- to 10-membered heteroarylene in A 1 means a 5- to 10-membered aromatic heterocycle containing 1 to 4 heteroatoms selected from a sulfur atom, a nitrogen atom and an oxygen atom, Specifically, pyridinene, thienylene, thiazolylene, benzothiazolylene, benzothiophenylene and the like are represented, preferably thienylene or pyridinene.
- C1 ⁇ C4 alkylene substituted or unsubstituted C6 ⁇ C10 arylene means a straight or branched carbon chain having 1 to 4 carbon atoms Specifically, it represents methylene, ethylene, propylene, isopropylene, butylene and the like, and among them, methylene or ethylene is preferable.
- C6-C10 arylene means a C6-C10 aromatic hydrocarbon ring, and specific examples thereof include phenylene and naphthylene and the like, with preference given to phenylene.
- C1 ⁇ C4 alkylene substituted or unsubstituted 5- to 10-membered heteroarylene refers to a straight-chain or branched carbon chain having 1 to 4 carbon atoms And specifically represent methylene, ethylene, propylene, isopropylene, butylene and the like, among which methylene or ethylene is preferable.
- 5- to 10-membered heteroarylene means a 5- to 10-membered aromatic heterocycle containing 1 to 3 hetero atoms selected from sulfur atom, nitrogen atom and oxygen atom, and specifically And pyridinene, thienylene, thiazolylene, benzothiazolylene, benzothiophenylene and the like, preferably thienylene.
- a halogen atom As a substituent of “arylene” or “heteroarylene” in A 1 , a halogen atom, a hydroxyl group, a cyano group, a nitro group, a carboxyl group, a trifluoromethyl group, a C1 to C6 alkyl group, a C3 to C8 cycloalkyl group, C1 -C6 alkoxy group, C3-C8 cycloalkyloxy group, mercapto group, C1-C6 alkylthio group, C3-C8 cycloalkylthio group, amino group, mono (C1-C6 alkyl) amino group, and di (C1-C6 alkyl) Examples thereof include an amino group and the like, preferably a halogen atom, a C1 to C6 alkyl group, a C1 to C6 alkoxy group, or a trifluoromethyl group.
- Examples of the “C3-C8 cycloalkylene” of A 1 include cyclopropylene, cyclobutylene, cyclopentylene, cyclohexylene and the like, and specifically, cyclohexylene is preferable.
- Examples of the substituent of “C3-C8 cycloalkylene” in A 1 include halogen and C1-C6 alkyl group, preferably a methyl group.
- halogen atom as a substituent of “arylene”, “heteroarylene” or “C3 to C8 cycloalkylene” in A 1 means a fluorine atom, a chlorine atom, a bromine atom, an iodine atom or the like, preferably It is a fluorine atom, a chlorine atom or a bromine atom.
- Arylene in A 1, as a substituent of "heteroarylene” or “C3 ⁇ C8 cycloalkylene” as “C1 ⁇ C6 alkyl group", straight chain, or branched having 1 to 6 carbon atoms It means a carbon chain, and specifically, methyl group, ethyl group, propyl group, isopropyl group, butyl group, isobutyl group, tert-butyl group, pentyl group, neopentyl group, isopentyl group, 1,2-dimethylpropyl group And hexyl, isohexyl, 1,1-dimethylbutyl, 2,2-dimethylbutyl, 1-ethylbutyl, 2-ethylbutyl, hexyl and the like, preferably methyl or ethyl .
- C3-C8 cycloalkyl group as a substituent of "arylene” or “heteroarylene” in A 1 include cyclic groups such as cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl and cyclooctyl.
- the alkyl group is preferably a cyclopropyl group, a cyclopentyl group or a cyclohexyl group.
- C 1 to C 6 alkoxy group as a substituent of “arylene” or “heteroarylene” in A 1 means methoxy, ethoxy, n-propoxy, n-butoxy, isopropoxy, isobutoxy, sec-butoxy, tert-butoxy It means a C1-C6 linear or branched alkoxy group such as 1-ethylpropoxy and 2-propylbutoxy, preferably a methoxy group, an ethoxy group or an isopropoxy group.
- the "arylene” or "C3 ⁇ C8 cycloalkyl group” as the substituent of the "heteroarylene” in A 1, means a group consisting of the C3 ⁇ C8 cycloalkyl group and oxy group, the preferred specific Examples include a cyclopropyloxy group, a cyclopentyloxy group, or a cyclohexyloxy group and the like.
- C1-C6 alkylthio group as a substituent of “arylene” or “heteroarylene” in A 1 means a group consisting of the C1-C6 alkyl group and a thio group, and preferred specific examples thereof are And a methylthio group or an ethylthio group.
- arylene or "C3 ⁇ C8 cycloalkylthio group” as a substituent of "heteroarylene” in A 1, means a group consisting of the C3 ⁇ C8 cycloalkyl group and a thio group, the preferred embodiment And cyclopropylthio and the like.
- the "mono (C1 to C6 alkyl) amino group” as a substituent of "arylene” or “heteroarylene” in A 1 means an amino group monosubstituted by a C1 to C6 alkyl group, and preferred specific examples thereof Examples include methylamino and the like.
- di (C1 to C6 alkyl) amino group as a substituent of “arylene” or “heteroarylene” in A 1 means an amino group disubstituted by the same or different C1 to C6 alkyl group, and Preferred specific examples include dimethylamino group and the like.
- phenylene substituted with one to three substituents selected from the group consisting of unsubstituted or (halogen, hydroxyl group, C1 to C4 alkyl group, C1 to C4 alkoxy group, and trifluoromethyl group) is preferable. Further, phenylene substituted with one or two substituents selected from the group consisting of unsubstituted or halogen atoms and methoxy groups is more preferable.
- the "C1-C10 alkylene” in R 4 means a linear or branched carbon chain having 1 to 10 carbon atoms, and specifically, methylene, ethylene, propylene, butylene, isopropylene, Pentylene, isobutylene, hexylene, tert-butylene, 1,1-dimethylethylene, hexylene, isohexylene, 1,1-dimethylpropylene, 2,2-dimethylbutylene, 1-ethylbutylene, 2-ethylbutylene, isoheptylene, octylene, isooctylene And nonylene and the like, among which those having 1 to 5 carbon atoms are preferable, and methylene, ethylene, propylene or 1,1-dimethylethylene is particularly preferable.
- halogen atom in R 8 and R 9 means a fluorine atom, a chlorine atom, a bromine atom, an iodine atom and the like, and as a preferable specific example thereof, a fluorine atom, a chlorine atom, a bromine atom and an iodine atom It can be mentioned.
- the "C1-C6 alkyl group" in R 8 and R 9 means a linear or branched carbon chain having 1 to 6 carbon atoms, and specifically, a methyl group, an ethyl group, a propyl group Group, isopropyl group, butyl group, isobutyl group, tert-butyl group, pentyl group, neopentyl group, isopentyl group, 1,2-dimethylpropyl group, hexyl group, isohexyl group, 1,1-dimethylbutyl group, 2,2 And represents -dimethylbutyl group, 1-ethylbutyl group, 2-ethylbutyl group, etc. Among them, those having 1 to 4 carbon atoms are preferable, and methyl group or ethyl group is particularly preferable.
- the “C1 to C6 alkyl group” in “R 10 , R 11 ” of R 8 and R 9 means a linear or branched carbon chain having 1 to 6 carbon atoms, for example, a methyl group , Ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, pentyl, neopentyl, isopentyl, 1,2-dimethylpropyl, hexyl, isohexyl, 1,1-dimethylbutyl And a 2, 2-dimethylbutyl group, a 1-ethylbutyl group, a 2-ethylbutyl group, etc.
- those having 1 to 4 carbon atoms are preferable, and a methyl group is particularly preferable.
- the "C1-C6 alkoxy group" in R 8 and R 9 means an alkoxy group having 1 to 6 carbon atoms, and specifically, a methoxy group, an ethoxy group, a propoxy group, an isopropoxy group, a butoxy group , Isobutoxy group, sec-butoxy group, tert-butoxy group, pentyloxy group, neopentyloxy group, tert-pentyloxy group, 2-methylbutoxy group, hexyloxy group, isohexyloxy group, etc.
- Those having 1 to 4 carbon atoms are preferable, and a methoxy group or an ethoxy group is most preferable.
- C1-C6 alkoxycarbonyl group for R 8 and R 9 include methoxycarbonyl group, ethoxycarbonyl group, propoxycarbonyl group, isopropoxycarbonyl group, butoxycarbonyl group, isobutoxycarbonyl group, sec-butoxy group A carbonyl group, a tert-butoxycarbonyl group, a pentyloxycarbonyl group, an isopentyloxycarbonyl group, a neopentyloxycarbonyl group, a hexyloxycarbonyl group etc., preferably a methoxycarbonyl group, an ethoxycarbonyl group or an isopropoxycarbonyl group And more preferably a methoxycarbonyl group.
- the "C1-C6 alkylthio group" in R 8 and R 9 means an alkylthio group having 1 to 6 carbon atoms, and specifically, a methylthio group, an ethylthio group, a propylthio group, an isopropylthio group, a butylthio group Isobutylthio, sec-butylthio, tert-butylthio, pentylthio, neopentylthio, tert-pentylthio, 2-methylbutylthio, hexylthio, isohexylthio and the like, among which carbon
- the number is preferably 1 to 4, and most preferably a methylthio group or an ethylthio group.
- R 8 and R 9 each independently, a halogen atom or a hydroxyl group is preferable.
- a and b each independently represent an integer of 0 to 3, and a and b are each preferably 0 or 1. When a or b is 0, it means that there is no substituent as R 8 or R 9 .
- C1-C6 alkyl group in R 6 and R 7 of Q means a linear or branched carbon chain having 1 to 6 carbon atoms, and specifically, methyl group, ethyl group Group, propyl group, isopropyl group, butyl group, isobutyl group, tert-butyl group, pentyl group, neopentyl group, isopentyl group, 1,2-dimethylpropyl group, hexyl group, 1,1-dimethylbutyl group, or 2, Among them, one having 1 to 4 carbon atoms is preferable, and a methyl group or an ethyl group is particularly preferable.
- the “C8 to C10 phenoxyalkyl group” in R 6 and R 7 means a group consisting of a phenoxy group and a C 2 to C 4 alkyl group, and specifically, a phenoxyethyl group, a phenoxypropyl group, or a phenoxybutyl group etc. Among them, phenoxyethyl group or phenoxypropyl group is particularly preferable.
- halogen atom as a substituent of the "C1-C6 alkyl group” or the "C8-C10 phenoxyalkyl group” in R 6 and R 7 means a fluorine atom, a chlorine atom, a bromine atom, an iodine atom, etc.
- a fluorine atom a chlorine atom or a bromine atom.
- the "C1-C6 alkyl group” as a substituent of the "C8-C10 phenoxyalkyl group” in R 6 and R 7 means a linear or branched carbon chain having 1 to 6 carbon atoms Specifically, methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, pentyl, neopentyl, isopentyl, 1,2-dimethylpropyl, hexyl, isohexyl And a 1,1-dimethylbutyl group, a 2,2-dimethylbutyl group, a 1-ethylbutyl group, a 2-ethylbutyl group, a hexyl group or the like, preferably a methyl group or an ethyl group.
- C 1 to C 6 alkoxy group as a substituent of “C 1 to C 6 alkyl group” or “C 8 to C 10 phenoxyalkyl group” in R 6 and R 7 is methoxy, ethoxy, n-propoxy, n-butoxy, iso C1 to C6 straight or branched alkoxy group such as propoxy, isobutoxy, sec-butoxy, tert-butoxy, 1-ethylpropoxy and 2-propylbutoxy is meant, preferably a methoxy group.
- the substituent of the “C1-C6 alkyl group” in R 6 and R 7 includes a halogen atom or a hydroxyl group, preferably a halogen atom.
- the "C1-C6 alkyl group" in R 5 means a linear or branched carbon chain having 1 to 6 carbon atoms, and examples thereof include a methyl group, an ethyl group, a propyl group, an isopropyl group and a butyl group.
- those having 1 to 4 carbon atoms are preferable, and a methyl group or an ethyl group is particularly preferable.
- R 5 , R 6 and R 7 may be combined with each other to form a ring” means, for example, R 6 and R 7 combine to form butylene, pentylene or hexylene It is. Preferably, pentylene or hexylene is used.
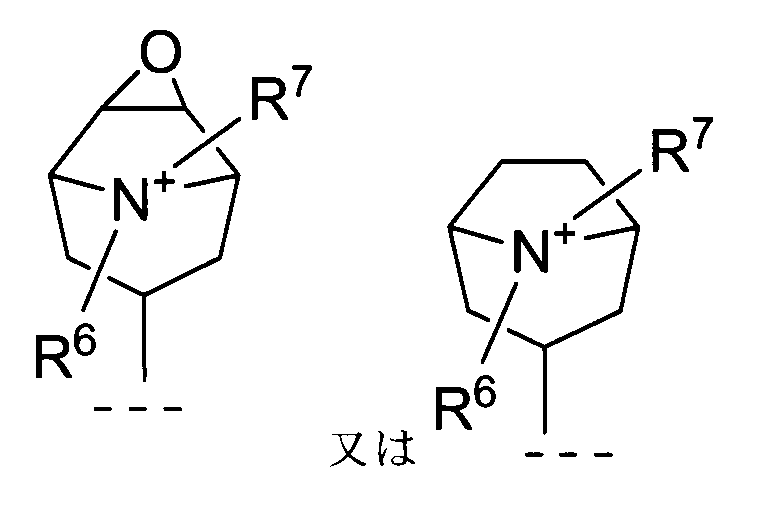
- R 5 is bonded to R 6 or R 7 to form an azabicyclo ring or an azatricyclo ring together with the original heterocycle.
- Such azabicyclo rings include quinuclidine rings.
- R 6 and R 7 are each independently a methyl group or a C 2 phenoxyalkyl group.
- N represents an integer of 0 to 2, preferably 1.
- n represents an integer of 0 to 3, preferably 0. When m is 0, it means that there is no substituent as R 5 .
- n is an integer of 1 and m is particularly preferably an integer of 0.
- R 6 and R 7 each independently represent a methyl group.
- W - as the anion expressed as, specifically, fluorine ion, chlorine ion, bromine ion, iodine ion, sulfate ion, phosphate ion, nitrate ion, carbonate ion, acetate ion, lactate ion, tartrate ion Benzoate, citrate, trifluoroacetate, methanesulfonate, ethanesulfonate, methylsulfate, benzenesulfonate, p-toluenesulfonate, isethionate, adipate, ethane 1,2-disulfonic acid ion, 1,5-naphthalenedisulfonic acid ion, naphthalene-2-sulfonic acid ion, malate ion, maleate ion, malonic acid ion, fumaric acid ion, succinic acid ion, 1-hydroxy-2 -Na
- the following compounds are also more preferable quaternary ammonium salt compounds.
- a salt may be formed with a base.
- a salt is not particularly limited as long as it is a pharmaceutically acceptable salt, and specifically, a hydrogen fluoride salt, a hydrochloride, a hydrobromide, a hydroiodide, a phosphate, Mineral acid salts such as nitrate and sulfate; methanesulfonate, ethanesulfonate, 2-hydroxyethanesulfonate, p-toluenesulfonate, benzenesulfonate, ethane-1,2-disulfonate ion, Organic sulfonates such as 1,5-naphthalenedisulfonate ion, naphthalene-2-sulfonate ion; and acetate, trifluoroacetate, propionate, oxalate, fumarate, phthalate, malonic acid Acid addition of organic carboxylates such as salts
- the compounds of formula (I) according to the invention may have isomers.
- isomers in the ring, fused ring (E, Z, cis, trans form), isomers due to the presence of asymmetric carbon, etc. (R, S form, ⁇ , ⁇ configuration, enantiomers, diastereomers), Optically active form (D, L, d, l form), tautomer, polar form by chromatographic separation (high polar form, low polar form), equilibrium compound, rotamer, mixture of any ratio of these And racemic mixtures and the like.
- the reaction when the raw material compound or the reaction intermediate has a substituent such as a hydroxyl group, an amino group or a carboxyl group which can affect the reaction, the reaction is carried out by appropriately protecting such functional group. It is desirable to release the
- the protective group is not particularly limited as long as it is a protective group generally used for each substituent and does not adversely affect other parts in the steps of protection and deprotection.
- examples of the protecting group for hydroxyl group include trialkylsilyl group, C1 to C4 alkoxymethyl group, tetrahydropyranyl group, acyl group, C1 to C4 alkoxycarbonyl group and the like
- examples of protecting group for amino group include C1 to C4 Examples thereof include a C4 alkoxycarbonyl group, a benzyloxycarbonyl group, and an acyl group
- a protecting group for a carboxyl group includes a C1 to C4 alkyl group.
- the compounds of the present invention represented by the general formula (I) can be produced by any of the following general production methods.
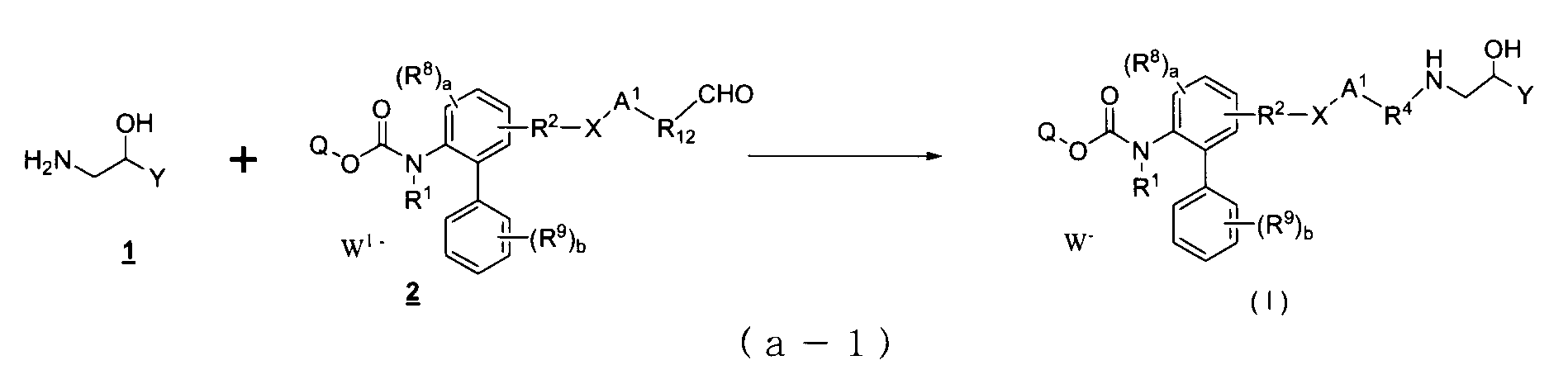
- ⁇ Manufacturing method 1> (Wherein, A 1, R 4, R 8, R 9, Y, Q, W - is equal to the definitions in the general formula (I), R 12 is a carbon number one less than R 4 alkylene (R 4 Indicates a single bond) when it is methylene)
- the reaction represented by the above reaction formula (a-1) can be carried out by using well-known conditions of reductive amination reaction.
- the reductive amination is performed by using an inert solvent (eg, dimethylsulfoxide, etc.) in the presence of the compound 1 and the compound 2 in the formula in the presence of a reducing agent (including a borohydride reducing agent (eg, sodium triacetoxyborohydride)).
- a reducing agent including a borohydride reducing agent (eg, sodium triacetoxyborohydride)
- the reaction is carried out by reaction in N, N-dimethylformamide and the like. It is a counter ion of the compound 2 W 1-is W - same as either the, or after the reaction, by known methods W - is substituted.
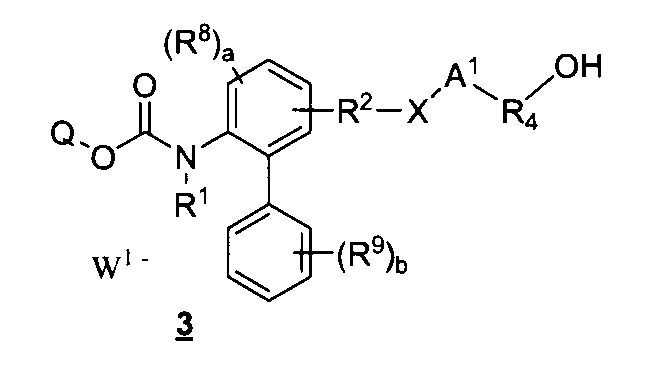
- the compound 2 in the above reaction formula (a-1) is a compound of the following formula 3 :
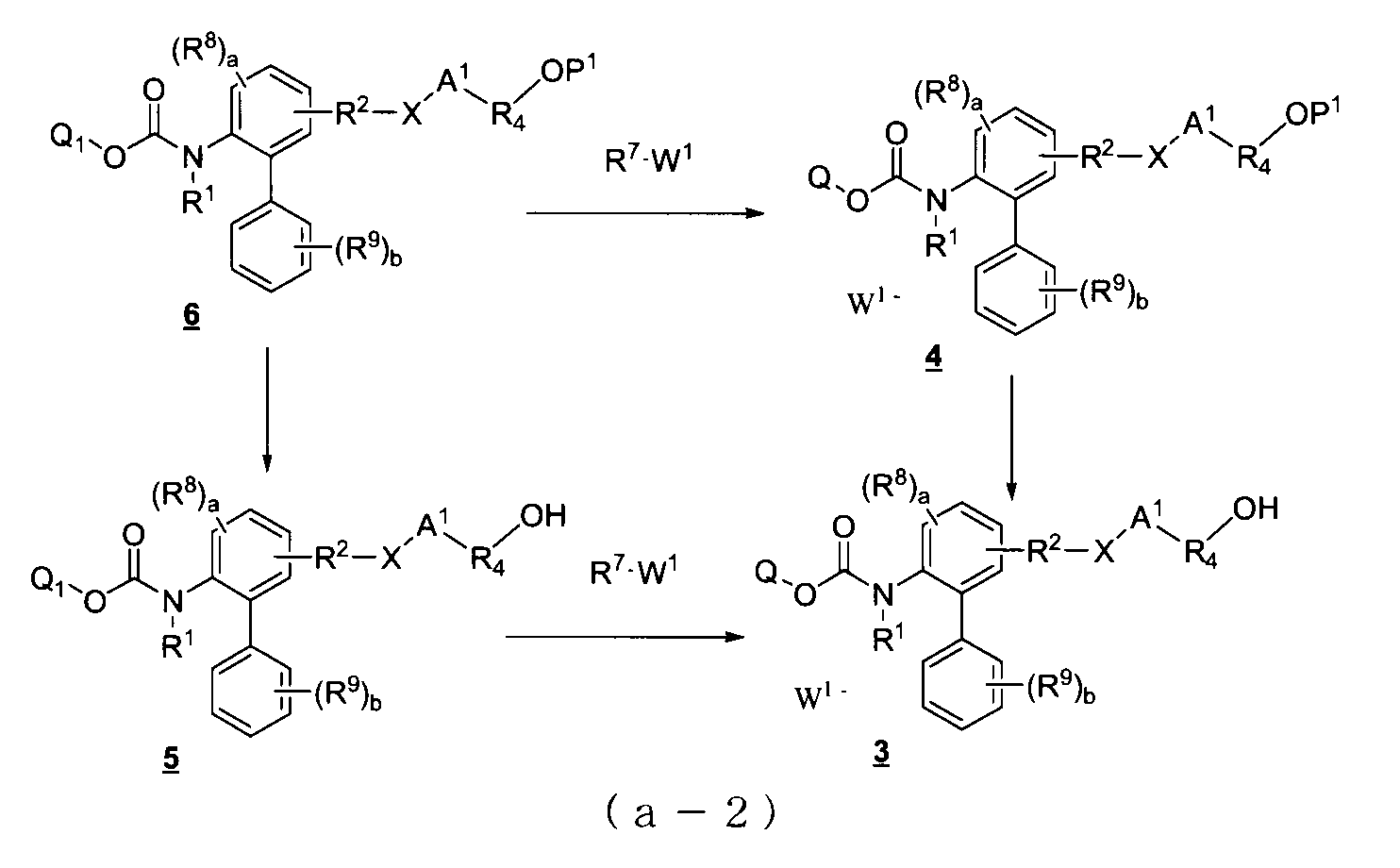
- Compound 3 of the above formula can be prepared by the two methods shown in the following reaction formula (a-2).
- P 1 represents a general hydroxyl group protecting group
- Q 1 represents any of the following formulas.
- the reactions from compound 6 to compound 4 and from compound 5 to compound 3 are N-alkylation reactions that convert tertiary amines into quaternary ammonium salts.
- the N-alkylation reaction is carried out under ice-cooling to room temperature or in a tertiary amine compound in an alkylating agent (eg, alkyl halide etc.) and an inert solvent (eg acetonitrile, N, N-dimethylformamide etc.) It can be carried out under heating.
- an alkylating agent eg, alkyl halide etc.
- an inert solvent eg acetonitrile, N, N-dimethylformamide etc.
- the reaction from compound 6 to compound 5 and from compound 4 to compound 3 is a general deprotecting reaction of a protecting group for hydroxyl group.
- a protecting group for hydroxyl group For example, when P 1 is a trialkylsilyl group, it may be treated with trifluoroacetic acid, hydrogen fluoride-triethylamine complex or the like, and when P 1 is an acyl group, it may be treated under general alkaline hydrolysis conditions. Can be done by
- the compound 6 of the reaction formula (a-2) can be prepared in the step shown in the following reaction formula (a-3).
- L 1 represents a leaving group.
- the reaction is carried out in the presence of a base (eg pyridine, triethylamine etc.), in an inert solvent (eg acetonitrile, N, N-dimethylformamide etc) or without solvent, under ice-cooling to room temperature or optionally under heating.
- a base eg pyridine, triethylamine etc.
- an inert solvent eg acetonitrile, N, N-dimethylformamide etc
- examples of the leaving group include halogen, methanesulfonyloxy, and benzenesulfonyloxy.
- Compound 6 can also be prepared in the step shown in the following reaction formula (a-4) when X is —CONR 3 —.
- R 12 represents an alkylene having one carbon shorter than R 2 (a single bond when R 4 is methylene, and P 2 represents a general carboxyl group protecting group).
- the reaction from the compound 8 and the compound 7a to the compound 9 can be carried out under the same conditions as the reaction formula (a-3).
- the reaction from compound 9 to compound 10 is a deprotection reaction of the protecting group of the carboxyl group. This deprotection reaction can be carried out under general acid hydrolysis conditions, alkali hydrolysis conditions, catalytic reduction conditions or the like.
- the reaction from compound 10 to compound 6 can be carried out by using well-known conditions for amidation reaction.
- amidation reaction can be carried out by condensation reaction of amines and carboxylic acids in the presence of a condensing agent such as carbodiimides.
- a condensing agent such as carbodiimides.
- halogenated hydrocarbons such as N, N-dimethylformamide and chloroform are suitable as the solvent
- N, N-dicyclohexylcarbodiimide and 1-ethyl- (3- (N, N-) are suitable as the condensing agent.
- Dimethylamino) propyl) carbodiimide, carbonyl diimidazole, diphenyl phosphoryl azide, diethyl phosphoryl cyanide, etc. are used.
- the reaction is usually carried out under cooling to room temperature or optionally under heating.
- R 2 in compound 7 represents a single bond
- X represents -O-
- a 1 represents a single bond
- R 4 represents C1-C10 alkylene, or R 2 represents -O-C1.
- X is —O—
- a 1 is phenylene
- R 4 is C 1 -C 4 alkylene
- it can be prepared in the step shown in the following reaction formula (a-5).
- L 2 represents a leaving group.
- the reaction from compound 13 to compound 12 is an O-alkylation reaction.
- a phenolic hydroxyl group-containing compound is mixed with an alkylating agent (eg, alkyl halide etc.) and an inert solvent (eg, acetonitrile, N, N-dimethylformamide etc.), a base (eg, potassium carbonate etc.) It can be carried out in the presence, at room temperature or optionally with heating.
- the reaction from compound 12 to compound 11 is a hydroxyl protection reaction and can be carried out by a known method.
- the reaction from compound 11 to compound 7b is a reduction reaction of a nitro group and can be performed under general conditions such as catalytic reduction and tin chloride treatment.
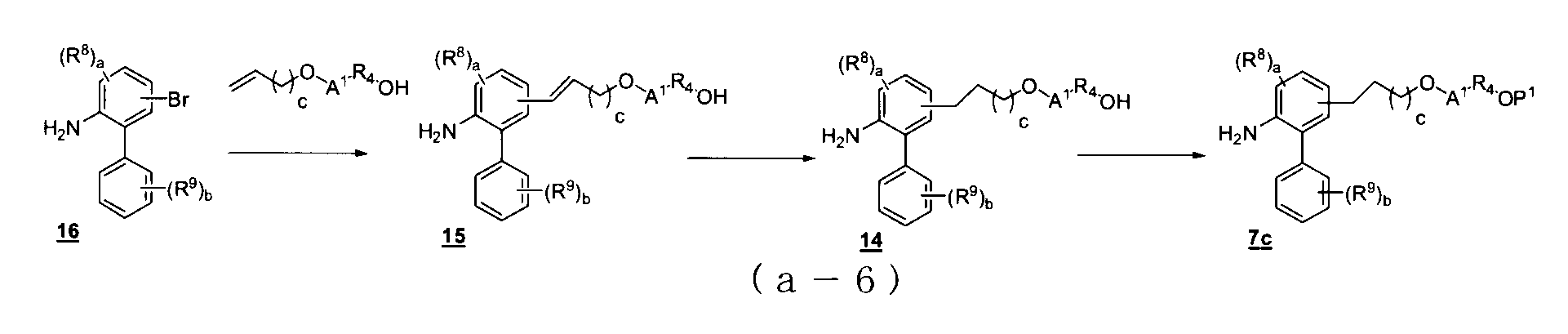
- reaction formula (a-3) when R 2 in the compound 7 is C 1 to C 8 alkylene, X is -O-, A 1 is phenylene, and R 4 -is phenylene-C 3-C 4 alkylene, the following reaction It can be prepared by the process shown in Formula (a-6).
- c represents an integer of 1 or 2.
- the reaction from compound 16 to compound 15 is a so-called Heck reaction in which an aryl halide is reacted with an alkene.
- the reaction can be carried out by heating and stirring in an inert solvent in the presence of palladium, a phosphine ligand and a base.
- the reaction from compound 15 to compound 14 is a double bond reduction reaction, and can be carried out by a known method such as catalytic reduction.
- the reaction from compound 14 to compound 7c is a hydroxyl protection reaction and can be carried out by a known method.
- the reaction can be carried out in an inert solvent (eg, acetonitrile, N, N-dimethylformamide, etc.), at room temperature, or optionally with warming.
- an inert solvent eg, acetonitrile, N, N-dimethylformamide, etc.
- the counter ion W 1 ⁇ of the compound 3 is the same as W 1 ⁇ or after reaction is replaced by W 2 ⁇ by a known method.
- Compound 17 can be prepared from compound 3 above by known methods.
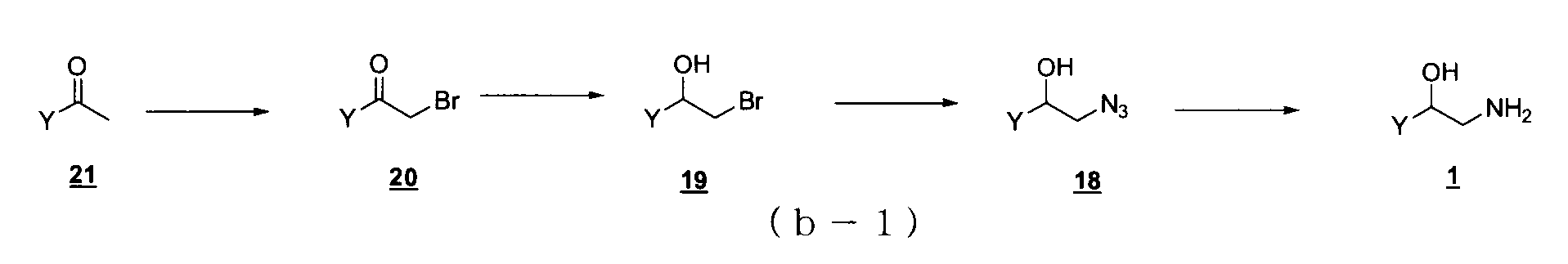
- the reaction formula (a-1), can be prepared by the steps shown in compound 1 of (a-7) in the following reaction formula (b-1).
- the reaction from compound 21 to compound 20 is a halogenation reaction, and the compound of compound 21 is reacted with a compound of compound 21 in the presence of a Lewis acid (eg, boron trifluoride diethyl etherate) It can be carried out by reacting with bromine.
- a Lewis acid eg, boron trifluoride diethyl etherate
- the reaction from compound 20 to compound 19 is a reduction reaction and can be carried out by reacting compound 20 with a reducing agent (eg, borane).
- Such reduction can be carried out in the presence of a chiral catalyst (an optically active compound 1 is provided, for example a chiral catalyst such as (R)-(+)- ⁇ , ⁇ .
- a chiral catalyst such as (R)-(+)- ⁇ , ⁇ .
- the reaction from compound 19 to compound 18 is an azidation reaction and can be carried out by reacting compound 19 with sodium azide
- the reaction from compound 19 to compound 18 is a reduction a reaction by treating compound 18 under the conditions of a typical catalytic reduction, or.
- compound 21 can be carried out, are well known in the art, also Using commercially available starting materials and reagents can be prepared by procedures well known.
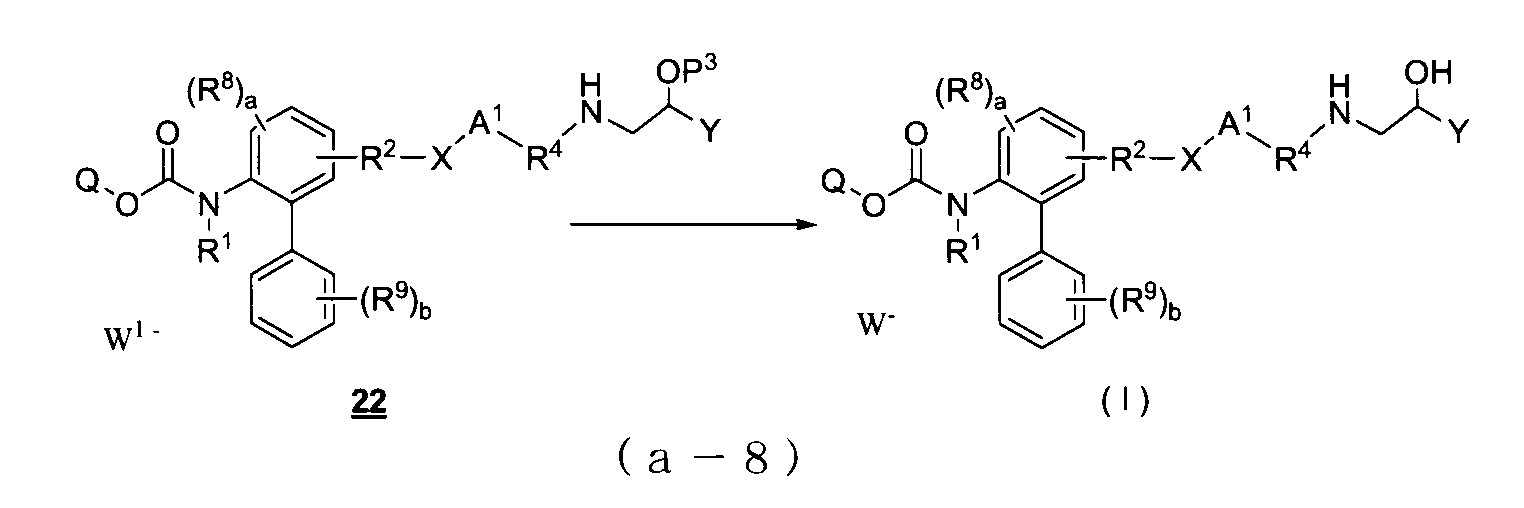
- a 1 , R 4 , R 8 , R 9 , Y, Q, and W ⁇ are the same as in the general formula (I), and P 3 represents a general hydroxyl group protecting group).
- the reaction represented by the above reaction formula (a-8) is a deprotecting reaction of a hydroxyl protecting group.
- P 3 is a tert- butyldimethylsilyl group, it can be carried out by treatment with tetrabutylammonium fluoride or trifluoroacetic acid and the like.
- the compound 1a of the above formula can be produced by carrying out a general protective group introduction reaction to a hydroxyl group during any step of the reaction formula (b-1).
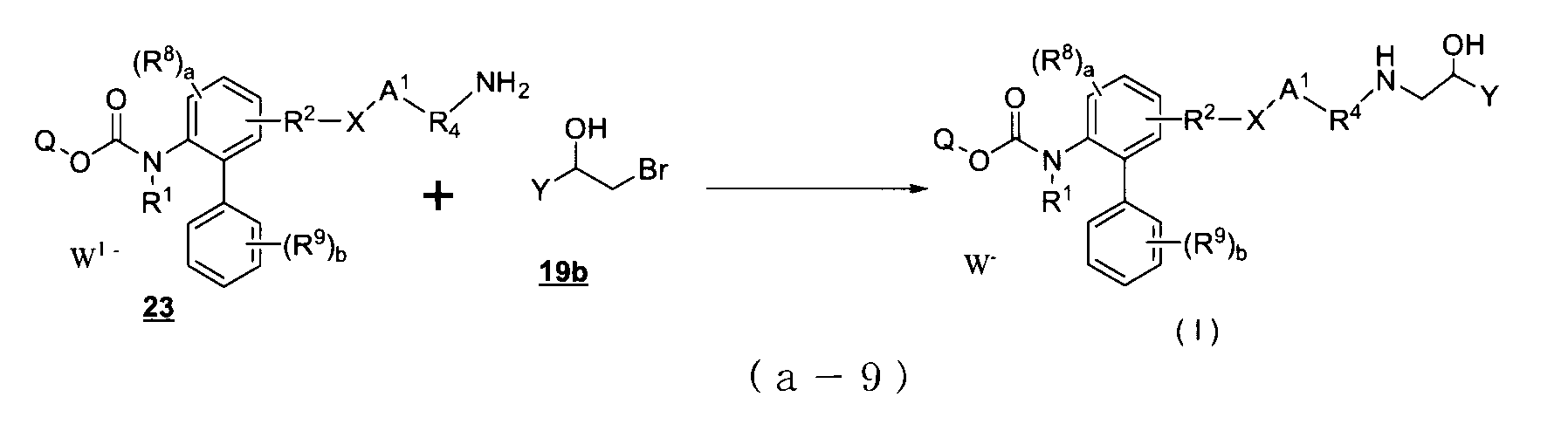
- Production Example 4 In the above reaction formula (a-9), the reaction of the compound 23 and the compound 19b is an N-alkylation reaction.
- the N-alkylation reaction can be carried out in an inert solvent (for example, acetonitrile, N, N-dimethylformamide or the like), in the presence of a base (for example, potassium carbonate or the like), at room temperature or optionally under heating.
- a base for example, potassium carbonate or the like
- This protective group can be deprotected under conditions of general deprotecting reaction (eg, catalytic reduction etc.) after the N-alkylation reaction.
- the counter ion W 1 ⁇ of the compound 23 is the same as W 1 ⁇ or after reaction is replaced by W 2 ⁇ by a known method.
- the compounds of formula (I) are isolated and purified as substances, such as free compounds, their salts, hydrates or solvates.
- the salt of the compound of formula (I) can also be produced by subjecting it to a standard salt formation or salt exchange reaction.
- the isolation or purification is carried out by applying ordinary chemical operations such as extraction and / or various fractional chromatography.
- the compounds of the present invention have ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity, and have sustained bronchodilatory activity by topical administration, so that the pathologies mediated by ⁇ 2 adrenergic receptor or muscarinic receptor (ie ⁇ 2 adrenaline It is useful for treating conditions that are ameliorated by treatment with receptor agonists or muscarinic receptor antagonists.
- Such conditions may include, for example, pulmonary disorders associated with reversible airway obstruction or pulmonary diseases (eg, chronic obstructive pulmonary disease (eg, chronic and wheezing). And emphysema), asthma, pulmonary fibrosis etc.).
- Conditions that may be treated include preterm birth, depression, congestive heart failure, skin disorders (eg inflammatory skin disorders, allergic skin disorders, psoriatic skin disorders and proliferative skin disorders, reducing the acidity of pepsin) Conditions where it is desirable (eg, peptic ulcer and gastric ulcer) and muscle fatigue disease.
- skin disorders eg inflammatory skin disorders, allergic skin disorders, psoriatic skin disorders and proliferative skin disorders, reducing the acidity of pepsin
- Conditions where it is desirable eg, peptic ulcer and gastric ulcer
- muscle fatigue disease e.g, peptic ulcer and gastric ulcer
- the present invention also relates to a pharmaceutical comprising a pharmaceutically acceptable carrier and a compound of formula (I) or a pharmaceutically acceptable salt thereof, a solvate thereof, a hydrate thereof, or a stereoisomer thereof Providing a composition.
- a pharmaceutical composition may be administered as a co-agent, in combination with other therapeutic agents, as needed, for the purpose of enhancing the preventive and / or therapeutic effects, etc.
- the combination of the pharmaceutical composition of the present invention and the other agent may be administered in the form of a combined preparation in which both components are combined in one preparation, or may be administered in separate preparations.
- the administration in separate preparations includes simultaneous administration and administration by time difference.
- the pharmaceutical composition of the present invention may be administered first, and other agents may be administered later, or other agents may be administered first, and the pharmaceutical composition of the present invention is later applied.
- the administration may be performed, and each administration method may be the same or different.
- the other drug may be a low molecular weight compound, and may be a high molecular weight protein, a polypeptide, a polynucleotide (DNA, RNA, gene), an antisense, a decoy, an antibody, a vaccine, etc. Also good.
- the dose of the other drug can be appropriately selected based on the dose clinically used. For example, 0.01 to 100 parts by mass of another agent may be used with respect to 1 part by mass of the compound of the present invention.
- other drugs may be administered in combination of two or more at an appropriate ratio.
- agents that enhance the preventive and / or therapeutic effect of the therapeutic agent of the present invention include not only those which have been found so far based on the mechanism described above, but also those which will be found in the future.
- the disease which exerts the preventive and / or therapeutic effect by the combination drug is not particularly limited, and it may be a disease which enhances the preventive and / or therapeutic effect of the therapeutic agent of the present invention.
- agents for enhancing the preventive and / or therapeutic effect of the therapeutic agent of the present invention for example, ⁇ 2 adrenergic receptor agonist, muscarinic receptor antagonist, leukotriene receptor antagonist, antihistamine, antiallergic agent, steroid Anti-inflammatory drugs, vaccine agents, herbal medicines, non-steroidal anti-inflammatory drugs, 5-lipoxygenase inhibitors, 5-lipoxygenase activated protein antagonists, leukotriene synthesis inhibitors, prostaglandins, cannabinoid-2 receptor stimulants, antitussives
- Representative ⁇ 2 adrenergic receptor agonists which can be used in combination with the compounds of the present invention include salmeterol, salbutamol, formoterol, indacaterol, salmefamol, fenoterol, terbutaline, albuterol, isoetharine, metaproterenol, bitolterol, pirvuterol, revalve Terol et al., Or pharmaceutically acceptable salts thereof, including, but not limited to.
- muscarinic antagonists that can be used in combination with the compounds of the present invention include atropine, atropine sulfate, atropine oxide, methylatropine sulfate, homatropine hydrobromide, hyostyamine hydrobromide (d, l), scopolamine hydrobromide , Ipratropium hydrobromide, oxytropium hydrobromide, tiotropium bromide, methanethelin, propanthelin hydrobromide, methyl anisotropine methyl bromide, cladinium bromide, copyrrolate, isopropamide iodide, mepenzolate bromide, tolydichloride Xyl, methylhexosulfate, cyclopentrate hydrochloride, tropicamide, trihexyphenidyl hydrochloride, pirenzepine, modzepine, methoctolamine etc., or pharmaceutically acceptable salts thereof (for compounds listed
- leukotriene receptor antagonists that can be used in combination with the compounds of the present invention include pranlukast hydrate, montelukast sodium, zafirlukast etc., or pharmaceutically acceptable salts thereof (for the compounds listed as salts, they And pharmaceutically acceptable salts), but is not limited thereto.
- antihistamines that can be used in combination with the compounds of the present invention include carbinoxamine maleate, clemastine fumarate, diphenylhydramine hydrochloride, dimenhydrinate hydrochloride, dimenhydrinate maleate pyrilamine maleate, triperenamine hydrochloride, triperenamine citrate, chlorpheniramine and acrivastine, Hydroxyzine hydrochloride, hydroxyidine hydroxy acid hydrochloride, cyclidine hydrochloride, cyclidine hydrochloride, meclidine hydrochloride and cetirizine hydrochloride, astemizole, levocabastine hydrochloride, loratadine or its descarbethoxy analog, terfenadine hydrochloride, fexofenadine hydrochloride, azelastine hydrochloride etc., or their pharmaceuticals Examples thereof include, but are not limited to, pharmaceutically acceptable salts (for compounds listed as salts, salts in which those salts are substituted for
- Representative anti-allergic agents which can be used in combination with the compound of the present invention include sodium cromoglycate, tranilast, anlexanox, repirinast, ibudilast, permirolast potassium, tazanolast, ozagrel hydrochloride, imitrodast sodium, seratrodast, lamatroban calcium And the like, or pharmaceutically acceptable salts thereof (for compounds listed as salts, salts obtained by replacing those salts with pharmaceutically acceptable salts), but are not limited thereto.
- Representative steroidal anti-inflammatory agents that can be used in combination with the compounds of the present invention include methylprednisolone, prednisolone, dexamethasone, fluticasone, beclomethasone propionate, budesonide, flunisolide, ciclesonide etc., or pharmaceutically acceptable salts thereof (salts Examples of the compounds listed as include, but are not limited to, salts in which their salts are replaced with pharmaceutically acceptable salts.
- Representative vaccine therapeutic agents that can be used in combination with the compounds of the present invention include Paspart, Astremezin Bronkasma Berna, and the like.
- non-steroidal anti-inflammatory agents that can be used in combination with the compounds of the present invention include aspirin, loxonine, diclofenac, celecoxib, aluminoprofen, pranoprofen, ibuprofen, droxicam, aceclofenac, ketoprofen, piroxicam, emorfazone, aurano It includes, but is not limited to, fin, piroxicam, lornoxicam, emorfazone, etc., or pharmaceutically acceptable salts thereof.
- leukotriene synthesis inhibitors that can be used in combination with the compounds of the present invention include, but are not limited to, auranofin, progematocine maleate, etc., or pharmaceutically acceptable salts thereof.
- antitussives that can be used in combination with the compounds of the present invention include, but are not limited to, codeine phosphate, dihydrocodeine phosphate, oxymetebanol, noscapine etc, or pharmaceutically acceptable salts thereof.
- Typical expectorants which can be used in combination with the compound of the present invention include ammonia vicinal extract, bromohexine hydrochloride, cherry skin extract, carbocysteine, ambroxol hydrochloride, methylcysteine hydrochloride, acetylcysteine, L-ethylcysteine hydrochloride and the like, or These include, but are not limited to, pharmaceutically acceptable salts thereof (for compounds listed as salts, salts in which those salts are substituted for pharmaceutically acceptable salts).
- Representative phosphodiesterase inhibitors that can be used in combination with the compounds of the present invention include, but are not limited to, doxophilin, roflumilast, cilomilast, etc., or pharmaceutically acceptable salts thereof.
- the compounds of the present invention are optionally administered in combination with other therapeutic agents.
- a steroidal anti-inflammatory agent eg, a corticosteroid
- the pharmaceutical composition of the present invention uses only two active ingredients and Therapeutics may be provided (ie, ⁇ 2 adrenergic receptor agonists, muscarinic receptor antagonists and anti-inflammatory activity).
- Therapeutics ie, ⁇ 2 adrenergic receptor agonists, muscarinic receptor antagonists and anti-inflammatory activity.
- Such a two-component composition can be prepared from a single triple agent, as a pharmaceutical composition comprising two active ingredients is usually easily formulated as compared to a composition comprising three active ingredients.
- the pharmaceutical compositions and methods of the present invention further comprise a therapeutically effective amount of a steroidal anti-inflammatory agent.
- the compound of the present invention can be formulated, if necessary, using pharmaceutically acceptable additives and widely used techniques as a single preparation or a combination preparation.
- the compound of the present invention In order to use the compound of the present invention or a combination of the compound of the present invention and another agent for the above-mentioned purpose, it is usually administered topically and in a parenteral form.
- the dose of the compound of the present invention varies depending on the age, body weight, symptoms, therapeutic effect, administration method and the like, but it is usually about 0.1 ⁇ g to 10 mg per adult per dose, and the administration frequency is once a day to Two times is preferred.
- parenteral agents examples include inhalants and the like. These preparations may be controlled release agents such as immediate release preparations and sustained release preparations. These preparations can be produced by known methods, such as the method described in the Japanese Pharmacopoeia.
- Inhalants for parenteral administration include aerosols, powders for inhalation, solutions for inhalation (for example, solutions for inhalation, suspensions for inhalation, etc.), or capsule-like inhalants, and the corresponding inhalation solutions May be in the form of solution or suspension in water or other suitable medium at the time of use.
- These inhalants can be operated using a suitable inhaled container, and, for example, when administering inhalable solutions, use a sprayer (atomizer, nebulizer) or the like, or in the case of administering inhalable powders, powder
- an inhalation administration device can be used.
- the compound of the present invention is formulated into a powder or liquid, inhalable propellant and / or carrier, and powdered according to a conventional method.
- the powder is pulverized with lactose, starch, magnesium stearate and the like to form a uniform mixture or granulated to prepare a powder.
- the compound of interest may be dissolved in a liquid carrier such as water, physiological saline or an organic solvent.
- propellant for example, chlorofluorocarbon, liquefied gas propellant (for example, fluorinated hydrocarbon, liquefied petroleum, diethyl ether, dimethyl ether etc.), compressed gas (carbon dioxide gas, nitrous oxide gas, nitrogen, etc.) Gas etc. are used.
- chlorofluorocarbon for example, fluorinated hydrocarbon, liquefied petroleum, diethyl ether, dimethyl ether etc.
- compressed gas carbon dioxide gas, nitrous oxide gas, nitrogen, etc.
- additives may be added to the inhalant as appropriate.
- the additive may be any commonly used additive, for example, solid excipients (eg lactose, sucrose, glucose, cellulose etc.), liquid excipients (eg propylene glycol etc.), binders (Eg, starch, dextrin, methyl cellulose, hydroxypropyl cellulose, polyethylene glycol etc.), lubricant (eg, magnesium stearate, light anhydrous silicic acid, talc, sodium lauryl acid etc.), flavoring agent (eg, citric acid, Menthol, glycyrrhizin ammonium salt, glycine, orange powder, etc., preservative (eg, sodium benzoate, sodium bisulfite, methyl parapen, propyl parapen, etc.), stabilizer (eg, citric acid, sodium citrate etc.), suspension Or emulsifying agents (eg methyl cellulose, Livinyl pyrrolidone, lec
- preservatives for example, in the case of a liquid for inhalation, preservatives, suspending agents or emulsifying agents, solvents, solubilizers, preservatives, stabilizers, coloring agents, buffering agents, pH adjusters, tonicity agents, A thickener and the like are appropriately selected and prepared as required.
- a solid excipient, a binder, a lubricant, a preservative, a stabilizer, a preservative, and the like are appropriately selected and prepared as necessary.
- the inhalant may contain a biodegradable polymer.
- biodegradable polymers include fatty acid ester polymers or copolymers thereof, polyacrylates, polyhydroxybutyrates, polyalkylene oxalates, polyorthoesters, polycarbonates and polyamines, and these include 1 Types or more may be mixed and used.
- phospholipids such as egg yolk lecithin, chitosan and the like may be used.
- fatty acid ester polymers or copolymers thereof examples include polylactic acid, polyglycolic acid, polycitric acid, polymalic acid and lactic acid-glycolic acid copolymers, and one or more of these may be mixed and used.
- a biodegradable polymer such as lactic acid-glycolic acid copolymer may be used to prepare a drug-encapsulated microsphere or nanosphere.
- the obtained solid was dissolved in a mixed solution of benzyl 4- (3-amino-4-phenylphenyl) butyrate (31.1 g, 60.0 mmol) in pyridine (50 mL) and N, N-dimethylformamide (150 mL). Add and stir at room temperature for 2 hours. The reaction was quenched by adding purified water under ice water cooling, and extracted with ethyl acetate. The organic layer was washed with dilute aqueous sodium hydroxide solution and saturated brine, dried over anhydrous sodium sulfate and concentrated under reduced pressure.
- the reaction was quenched by adding a saturated aqueous solution of Rochelle salt under cooling with ice water, and extracted with ethyl acetate.
- the organic layer was washed with saturated Rochelle salt aqueous solution and brine, dried over anhydrous magnesium sulfate and concentrated under reduced pressure.
- the obtained solid is washed with a hexane-ethyl acetate mixed solvent (ratio 4: 1), collected by filtration, and dried under reduced pressure to give 4-amino-5-chloro-2-methoxybenzyl alcohol (11.8 g). Got).
- reaction solution was filtered through celite, and the filtrate was concentrated under reduced pressure to give 5- ⁇ [8- (tert-butyldimethylsilanoyloxy) octyl] oxy ⁇ -2-phenylaniline as a crude product.
- Nonan-7-yl N- (5- ⁇ 2-[(6- ⁇ [(tert-butyldimethylsilyl) oxy] methyl ⁇ naphthalen-2-yl) carbamoyl] ethyl ⁇ -2-phenylphenyl) carbamate (77 mg 0.13 mmol) to (1R, 2R, 4S, 5S, 7S) -7-( ⁇ [5- (2- ⁇ [6-( ⁇ [(2R) -2-hydroxy-2- (8-hydroxy) -2-Oxo-1,2-dihydroquinolin-5-yl) ethyl] amino ⁇ methyl) naphthalen-2-yl] carbamoyl ⁇ ethyl) -2-phenylphenyl] carbamoyl ⁇ oxy) -9,9-dimethyl-3 -Oxa-9-azatricyclo [3.3.1.0 2, 4 Nonan-9-ium trifluoroacetate (19.5 mg) was obtained.
- Example 66 4-[( ⁇ 5- [3-( ⁇ [4-( ⁇ [(2R) -2-hydroxy-2- (8-hydroxy-2-oxo-1,2-dihydroquinolin-5-yl) ethyl] Synthesis of amino ⁇ methyl) phenyl] methyl ⁇ carbamoyl) propyl] -2-phenylphenyl ⁇ carbamoyl) oxy] -1,1-dimethylpiperidin-1-ium trifluoroacetate According to Example 65, Reference Example 15-62 The obtained 1-methylpiperidin-4-yl N- (5- ⁇ 3-[( ⁇ 4-[(tert-butoxycarbonyl) amino] phenyl ⁇ methyl) carbamoyl] propyl ⁇ -2-phenylphenyl) carbamate (86 mg, 0.14 mmol) to 4-[( ⁇ 5- [3-( ⁇ [(2R) -2-hydroxy-2- (8
- the residue was dissolved in methanol (10 mL), a catalytic amount of palladium on carbon hydroxide was added, and the solution was placed under a hydrogen atmosphere and stirred for 4 days.
- the reaction solution was filtered through celite and concentrated under reduced pressure.
- To the residue was added 5% hydrobromic acid methanol solution (10 mL), and the mixture was stirred at 80 ° C. for 2 hours, and then the reaction solution was concentrated under reduced pressure.
- Nonane-9-ium trifluoroacetate (1R, 2R, 4S, 5S, 7S) -9-methyl- obtained in Reference Example 15-69 according to Example 58 3-oxa-9-azatricyclo [3.3.1.0 2,4 ] nonan-7-yl N- ⁇ 5- [2-( ⁇ 4- [3- (tert-butyldimethylsilanoyloxy) propyl] Phenyl ⁇ carbamoyl) d [L, 2R, 4S, 5S, 7S) -7-( ⁇ [5- (2- ⁇ [4- (3- ⁇ [)]) from -2-phenylphenyl ⁇ carbamate (100.5 mg, 0.15 mmol).
- Example 74 4-( ⁇ [5- (2- ⁇ [5- ⁇ [(2R) -2-hydroxy-2- (8-hydroxy-2-oxo-1,2-dihydroquinolin-5-yl) ethyl] amino ⁇ Synthesis of pentyl] carbamoyl ⁇ ethyl) -2-phenylphenyl] carbamoyl ⁇ oxy) -1,1-dimethylpiperidin-1-ium trifluoroacetate
- Example 58 the 1-methyl compound obtained in Reference Example 15-70 From piperidin-4-yl N- ⁇ 5- [2- (5-[(tert-butyldimethylsilanoyloxy) pentyl] carbamoyl) ethyl] -2-phenylphenyl ⁇ carbamate (163.1 mg, 0.28 mmol), 4-( ⁇ [5- (2- ⁇ [5- ⁇ [(2R) -2-hydroxy-2- (8-hydroxy
- reaction solution was filtered through Celite, alumina and Florisil, and extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate and concentrated under reduced pressure to give 3-nitro-4-phenylbenzoic acid as a crude product.
- reaction solution was filtered through celite, and the filtrate was concentrated under reduced pressure to give tert-butyl N- [9- (4-phenyl 3-amino-phenyl) -8-nonen-1-yl] carbamate as a crude product.
- reaction solution is filtered, concentrated and purified by HPLC preparative, 4-( ⁇ [5- (9-[ ⁇ (2R)-[8- (benzyloxy) -2-oxo-1,2- Dihydroquinolin-5-yl] -2-hydroxyethyl ⁇ amino] nonyl) -2-phenylphenyl] carbamoyl ⁇ oxy) -1,1-dimethylpiperidin-1-ium trifluoroacetate was obtained.
- reaction solution was extracted with ethyl acetate, and the organic layer was washed with saturated aqueous ammonium chloride solution and saturated brine, dried over anhydrous magnesium sulfate and concentrated under reduced pressure.
- the residue was purified by flash column chromatography to obtain tert-butyl N- [2- (4-hydroxyphenyl) ethyl] carbamate (4.97 g).
- Example 77 4- ⁇ [(5- ⁇ 3- [4- (2- ⁇ [(2R) -2-hydroxy-2- (8-hydroxy-2-oxo-1,2-dihydroquinolin-5-yl) ethyl] Synthesis of amino ⁇ ethyl) phenoxy] propyl ⁇ -2-phenylphenyl) carbamoyl] oxy ⁇ -1,1-dimethylpiperidin-1-ium trifluoroacetate The 1-methylpiperidine obtained in Reference Example 49 according to Example 76.
- reaction solution was quenched with water and extracted with ethyl acetate.
- the organic layer was washed with saturated aqueous sodium hydrogen carbonate solution and saturated brine, dried over anhydrous sodium sulfate and concentrated under reduced pressure.
- the residue was dissolved in N, N-dimethylformamide (5 mL) and potassium carbonate (207.0 mg, 1.5 mmol) and 4- (hydroxymethyl) phenol (161.2 mg, 1.3 mmol) were added.
- the reaction solution was extracted with ethyl acetate.
- the organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate and concentrated under reduced pressure.
- the reaction was terminated by rapid filtration on a GF / B glass fiber filtration plate (PerkinElmer) previously soaked in 0.2% polyethyleneimine.
- the filter plate was washed three times with washing solution (50 mM Tris-HCl pH 7.4, 0.9% sodium chloride) to remove unbound radioactivity. Plates were then dried and 40 ⁇ L of MicroScint-20 Liquid Top Count Microplate scintillation cocktail (PerkinElmer) was added and counted on a Packard Topcount liquid scintillation counter (PerkinElmer).
- the binding inhibition rate of the test compound was calculated by the following formula.
- Binding inhibition rate (%) [(radioactivity-nonspecific binding amount of test compound-added sample) / (total binding amount-nonspecific binding amount)] ⁇ 100
- the 50% inhibitory concentrations (IC 50 values) of the test compounds were analyzed by non-linear regression analysis of one-site competitive binding, using the GraphPad Prism Software package (GraphPad Software), for the binding inhibition rates of the test compounds at different concentrations.
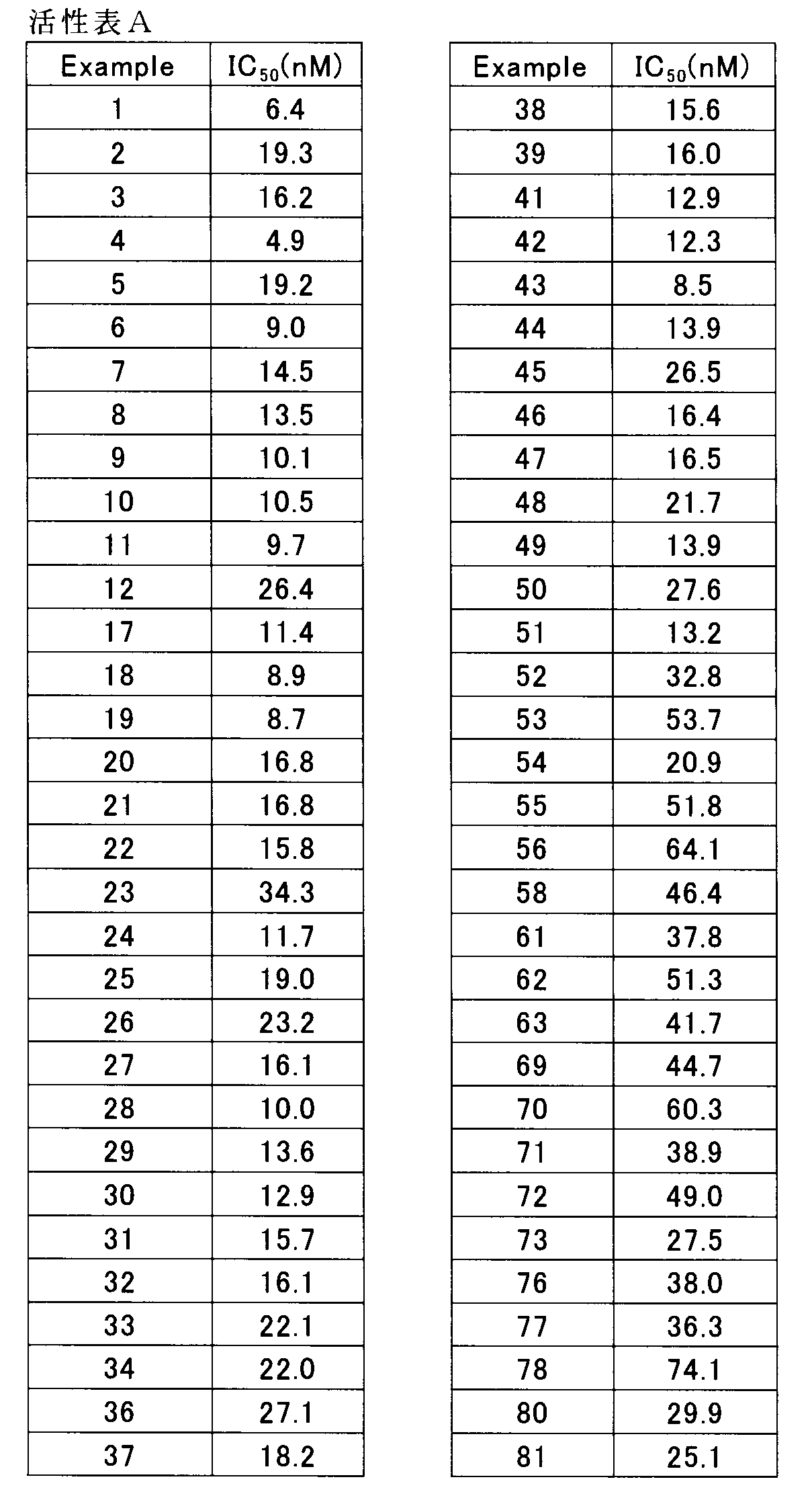
- Exemplary compounds of the invention tested in this assay were found to have an IC 50 value of less than about 10 nM for human M3 muscarinic receptor.
- the compounds of Examples 1, 48 and 51 were found to have IC 50 values less than 10 nM.
- Example 83 Evaluation of inhibitory effect on methacholine-induced calcium influx using FLIPR assay Muscarinic receptor subtypes (M1, M3 and M5 receptors) to be coupled to Gq protein are phospholipase C (A) due to binding to an agonist receptor PLC) activate the pathway. As a result, activated PLC hydrolyses phosphatidylinositol diphosphate (PIP2) into diacylglycerol (DAG) and phosphatidyl-1,4,5-triphosphate (IP3), which in turn That is, release of calcium from the endoplasmic reticulum and sarcoplasmic reticulum.
- the FLIPR (Molecular devices) assay can measure the increase in intracellular calcium by changing the fluorescence intensity by using a calcium-sensitive dye (Component A) that fluoresces when free calcium is bound .
- CHO-K1 cells stably expressing human M3 muscarinic receptor suspended in Ham's F-12 medium (Invitrogen) containing 10% fetal bovine serum (FBS) at a volume of 100 ⁇ L / well in 96 wells Were seeded on FLIPR plates. On the next day, cells were added with 60 ⁇ L / well of Non-wash-dye solution (Hanks buffer saline HBSS containing 20 mM HEPES and 6.5 mM probenecid), and incubated at 37 ° C. for 1 hour in the presence of 5% carbon dioxide.
- Non-wash-dye solution Hanks buffer saline HBSS containing 20 mM HEPES and 6.5 mM probenecid
- test compound solution HBSS containing 1% DMSO, 20 mM HEPES, 2.5 mM probenecid and 0.05% bovine serum albumin BSA
- concentration range 0.01-1000 nM
- Add 20 ⁇ L of 30 nM methacholine solution HBSS containing 20 mM HEPES, 2.5 mM probenecid and 0.05% bovine serum albumin BSA
- trace the fluorescence intensity for 170 seconds by the intracellular calcium influx measurement device FLIPR 96 (Molecular Devices) did.
- the difference between the lowest value and the highest value of the fluorescence intensity (FI) within the measurement time is taken as the measured value, and the measured value of the sample without the test compound added with the methacholine (FIpositive), the measured value with the sample without the methacholine added without the test compound
- the inhibition rate of the test compound was calculated from the measured value (FItest) of the measured value of the sample (FInegative) and the methacholine-added / test compound-added sample according to the following equation.
- Inhibition rate of test compound (%) [1-(FItest-FInegative) / (FI positive-FInegative)] x 100
- the 50% inhibitory concentrations (IC 50 values) of the test compounds were analyzed by a 4-parameter logistic model using XLfit 4 (IDBS) for the inhibition rates of the test compounds at different concentrations.
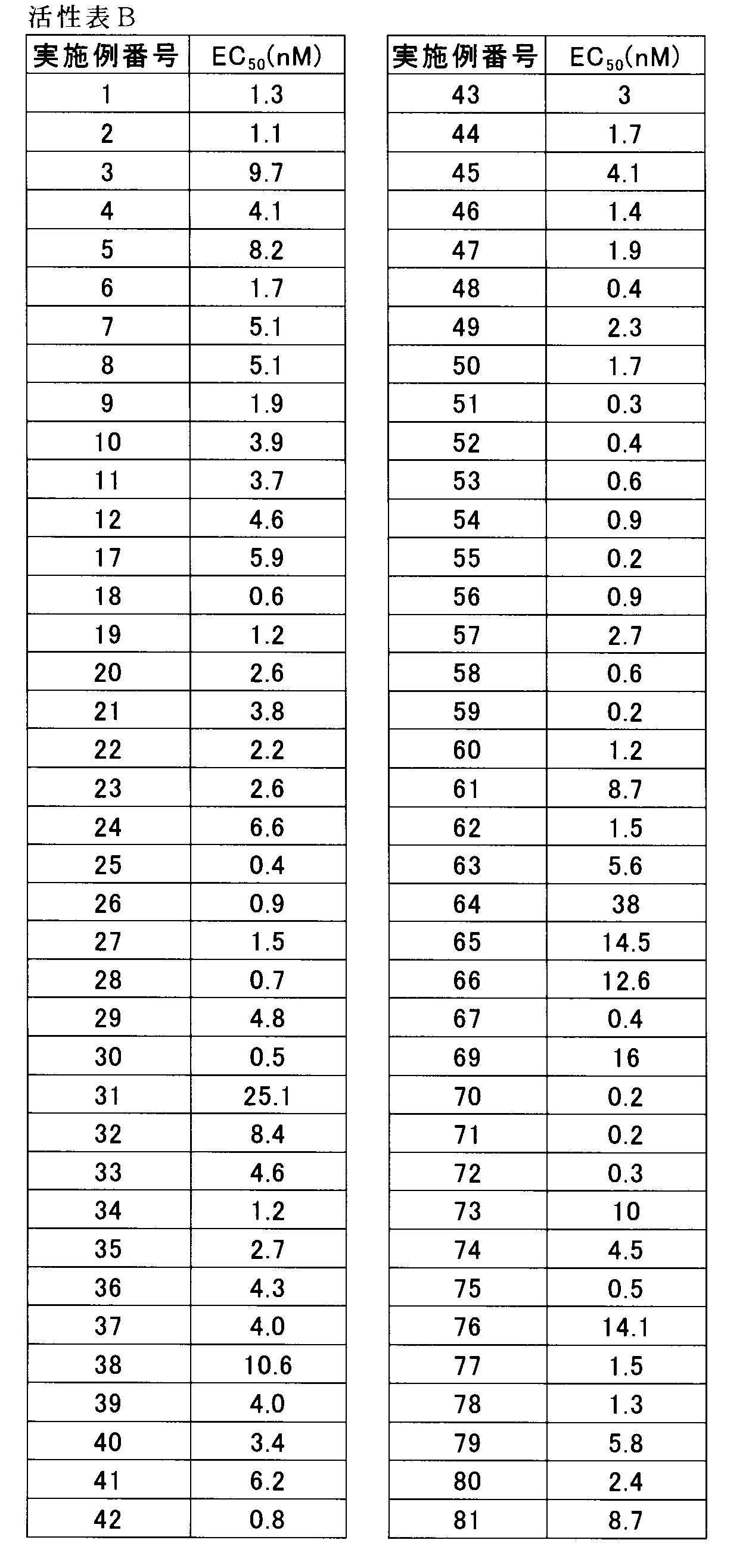
- Example 84 Evaluation by whole cell cAMP flash plate assay using CHO-K1 cells stably expressing human ⁇ 2 adrenergic receptor ⁇ 2 adrenergic receptor coupled to Gs protein is adenyl by binding to agonist receptor Activate acid cyclase. As a result, cAMP is produced intracellularly. It is possible to measure the activating ability of the ⁇ 2 adrenergic receptor by measuring this amount of cAMP using a cAMP-Screen System (Applied Biosystems).
- CHO-K1 cells expressing human ⁇ 2 adrenergic receptor suspended in Ham's F-12 medium containing 10% FBS were seeded in 96 well plates at a volume of 100 ⁇ L / well. The next day, the cells were washed with 200 ⁇ L of PBS (-), 80 ⁇ L of 0.5 mM IBMX solution (Ham's F-12 medium containing 0.05% BSA) was added, and 20 minutes at 37 ° C. in the presence of 5% carbon dioxide Incubated.
- test compound solution 0.5 mM IBMX solution containing 1% DMSO
- test compound solution 0.5 mM IBMX solution containing 1% DMSO
- Assay / Lysis Buffer cAMP Screen System accessory reagent
- the cells were lysed by pipetting, and further incubated at 37 ° C. for 30 minutes, and then frozen at -80 ° C.
- thawed samples at room temperature were processed according to the cAMP Screen System protocol and chemiluminescence was measured by EnVision (PerkinElmer). The amount of cAMP was calculated from a standard curve of a standard product attached to cAMP Screen System.
- the concentration (EC 50 value) reaching 50% of the maximum effect of the test compound was analyzed by a 4-parameter logistic model using XLfit 4 (IDBS) for the amount of cAMP produced by the test compound at different concentrations.
- Example 85 Evaluation of duration of action in guinea pig isolated trachea
- a ring-shaped guinea pig isolated trachea is fixed in a water bath while applying a constant tension, and contracted by acetylcholine, histamine or electrical stimulation or the like. Induce a reaction.
- the change in tension is output to a portable recorder through a versatile preamp device (Nippon Denso Corp.) and a carrier amplifier (Nippon Denso Corp.) and recorded.
- a versatile preamp device Nippon Denso Corp.
- a carrier amplifier Nippon Denso Corp.
- a Hartley male guinea pig (Japan SLC Co., Ltd.) having a weight of about 400 to 500 g was used.
- the animals were anesthetized by intraperitoneal administration of 33% urethane / 0.8% ⁇ -chloralose at a dose of 3 mL / kg, and then the neck was incised for blood removal and death.
- the tracheal ring was prepared by cutting at 2 tracheal cartilage intervals in glucose / 4.7 mM potassium chloride / 1.2 mM monobasic potassium phosphate / 2.5 mM calcium chloride).
- the sample was fixed by applying 1 g of tension to a magnus tank (UFER 5 mL chamber, Iwashi and Kishimoto Medical Industry Co., Ltd.) filled with a magnus reaction solution warmed to 37 ° C. through 95% oxygen / 5% carbon dioxide. . After stabilization by incubation for 60 minutes, it was washed 3-4 times with the Magnus reaction solution. After filling the Magnus tank with 4410 ⁇ L of the Magnus reaction, 90 ⁇ L of a 15 ⁇ M carbamoyl chloride solution was added and the contraction reaction was recorded for 15 minutes. After completion of the reaction, the reaction was washed twice with the Magnus reaction solution, and it was confirmed that the contraction reaction had returned to the baseline, and was used for the experiment.
- a magnus tank UFER 5 mL chamber, Iwashi and Kishimoto Medical Industry Co., Ltd.
- magnus reaction solution After filling the magnus tank with 4410 ⁇ L of the magnus reaction solution, 90 ⁇ L of 150 ⁇ M acetylcholine solution or 150 ⁇ M histamine solution was added, and tracheal contraction reaction was recorded for 15 minutes. After completion of the reaction, the reaction mixture was washed twice with the magnus reaction solution, replaced with the magnus reaction solution again, and allowed to return to the baseline. The Magnus bath was replaced with 4.5 mL of the test compound solution adjusted to 0.01-1000 nM, and incubated for 3 hours.
- the 50% inhibitory concentrations (IC 50 values) of the test compounds at each time were analyzed by the sigmoidal logistic model using XLfit 4 (IDBS) for the inhibition rates of the test compounds at different concentrations. Furthermore, the duration of action of the test compound was evaluated by comparing the difference between the IC 50 value immediately after the test compound removal (0 hour) and 5 hours after the test compound removal.
- the exemplary compounds of the present invention tested in this assay were found to have a strong inhibitory effect on acetylcholine-stimulated and histamine-stimulated tracheal contraction responses even 5 hours after compound removal. It was done.
- the compound is an IC 50 value of an IC 50 value after 5 hours 0 hours of Examples 2,6,12,18,19,23,25,32,33,34,48,51,77 and 78 was found to be less than 50 times.
- Example 86 Effect on acetylcholine or histamine-induced bronchoconstriction in guinea pig These in vivo assays are used to evaluate the bronchoprotective effect based on M3 muscarinic receptor antagonist activity and ⁇ 2 adrenergic receptor agonist activity of test compounds .
- a Hartley male guinea pig (Nippon SLC Co., Ltd.) weighing 400 g to 500 g was used.
- the animals were anesthetized by inhaling Flusen (Takeda Pharmaceutical Co., Ltd.) in a plastic box.
- the test compound was dissolved in saline containing DMSO, and a dose of 0.04-25 ⁇ g / kg was administered intratracheally through the nasal cavity in a volume of 0.4 mL / kg.
- a solvent containing no test compound was administered.
- the animals were anesthetized by intraperitoneal administration of 33% urethane / 0.8% ⁇ -chloralose at a dose of 3 mL / kg.
- a catheter was inserted into the jugular vein for intravenous administration of acetylcholine or histamine.
- the trachea was also cannulated to measure artificial respiration and airway airway pressure.
- the animals were ventilated at a frequency of 60 times / min at a volume of 10 mL / kg using a ventilator (Harvard Apparatus).
- the airway pressure was measured by the Konzett-Roessler method using an integrated respiratory function measurement apparatus (M ⁇ I ⁇ P ⁇ S). Airway airway pressure was measured and baseline values were recorded prior to acetylcholine or histamine administration.
- the above-mentioned doses of acetylcholine or histamine are administered 1 hour, 6 hours, 12 hours, 18 hours, 24 hours after administration of the test compound, and airway communication is performed in the same manner.
- the barometric pressure was measured.
- the inhibition ratio of the test compound to the airway contraction response was calculated by the following formula.
- Airway contraction inhibition rate (%) (Airway ventilation pressure of acetylcholine- or histamine-administered animal in test compound-administered animal-baseline value) / (Airway ventilation pressure of acetylcholine- or histamine-administered animal-baseline value) x 100
- the 50% inhibitory dose (ID 50 value) of the test compound was analyzed by the sigmoidal logistic model using XLfit 4 (IDBS) for the airway contraction suppression rate of the test compound with different doses.
- An exemplary compound of the invention tested in this assay was found to have an ID 50 value of less than about 5 ⁇ g / kg, respectively, for acetylcholine stimulated and airway stimulated airway contraction responses.
- the compounds of Examples 1, 48 and 51 were found to have an ID 50 value of less than 1 ⁇ g / kg against airway contraction response to acetylcholine and histamine stimulation one hour after compound administration. .
- the airway contraction suppression rate to acetylcholine stimulation after 24 hours when the compound is administered at 25 ⁇ g / kg is, for example, as described in Examples 1, 2, 6, 12, 18, 19, 20, 25, 34, 36, 46. , 48, 51, 55, 57, 58, 70, 71 and 77 were 50% or more.
- the airway contraction suppression rate to histamine stimulation after 6 hours when the compound is administered at 25 ⁇ g / kg can be obtained, for example, by Example 1, 18, 19, 20, 23, 25, 33, 34, 35, 36 , 37, 40, 41, 42, 46, 48, 51, 55, 56 and 71 were 30% or more.
- the compound represented by the formula (I) of the present invention or a pharmaceutically acceptable salt thereof has excellent ⁇ 2 adrenergic receptor agonist activity and muscarinic receptor antagonist activity, and therefore has chronic obstructive pulmonary disease (COPD) or asthma Etc. are useful as preventive and therapeutic agents for inflammatory diseases.
- COPD chronic obstructive pulmonary disease
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pulmonology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Hydrogenated Pyridines (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
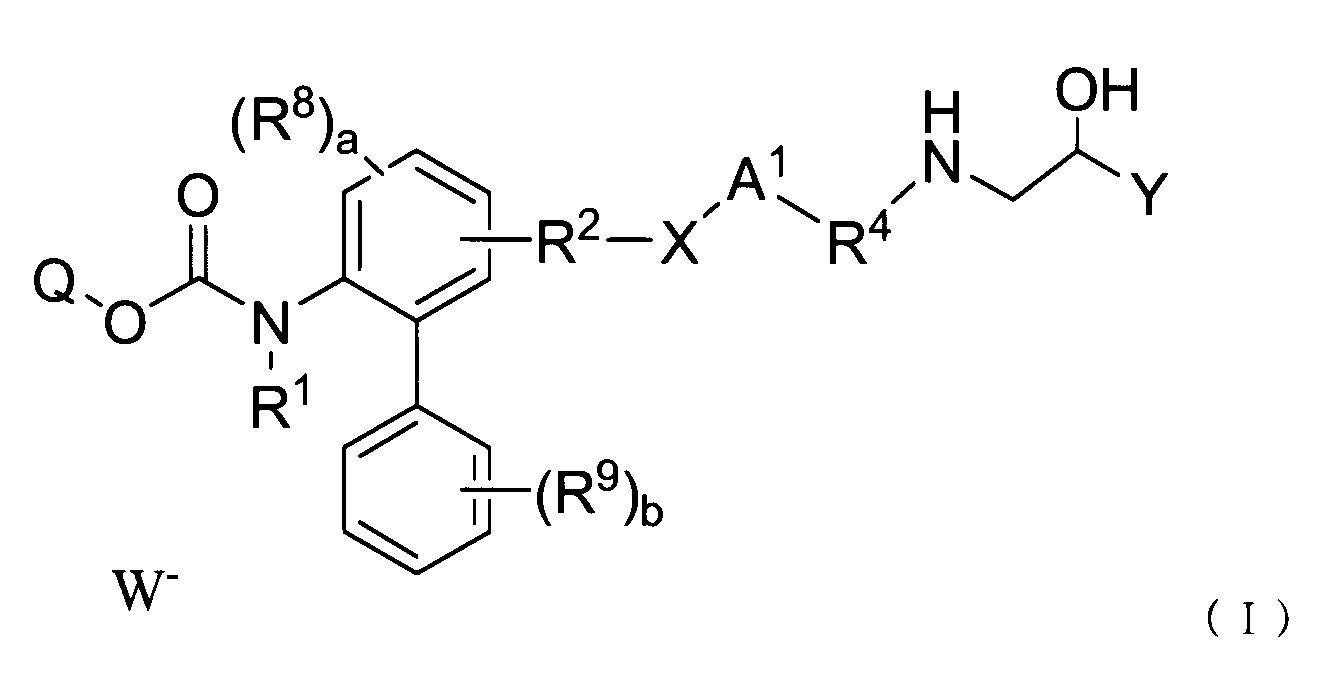
(1)一般式(I)
R1は、水素原子、又は無置換のC1~C8アルキル基を表し;
R2は、単結合、(無置換もしくは炭素原子が1~2個の酸素原子により置換された)C1~C8アルキレン、無置換のC2~C4アルケニレン、又は無置換の-O-C1~C4アルキレンを表し;
Xは、単結合、-O-、-CONR3-、-NR3CO-、又は-NR3CO-CH2-O-を表し(ここで、R3は、水素原子、又は無置換のC1~C8アルキル基を表す。);
A1は、単結合、無置換もしくは(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~4個の置換基で置換されたC6~C10アリーレン、無置換もしくは(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~4個の置換基で置換された5~10員のヘテロアリーレン、無置換のC1~C4アルキレン-置換もしくは無置換のC6~C10アリーレン(このC6~C10アリーレンの置換基としては、(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~3個の置換基である。)、無置換のC1~C4アルキレン-置換もしくは無置換の5~10員ヘテロアリーレン(この5~10員ヘテロアリーレンの置換基としては、(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~3個の置換基である。)、又は無置換もしくは(ハロゲン及び無置換のC1~C6アルキル基)からなる群から選ばれる1~3個の置換基で置換されたC3~C8シクロアルキレンを表し;
R4は、無置換のC1~C10アルキレンを表し;
R8及びR9は、それぞれ独立して、ハロゲン原子、シアノ基、無置換のC1~C6アルキル基、ニトロ基、-NR10R11(ここで、R10及びR11は、それぞれ独立して、水素原子、又は無置換のC1~C6アルキル基を表す。)、無置換のC1~C6アルコキシ基、カルボキシル基、無置換のC1~C6アルコキシカルボニル基、水酸基、トリフルオロメチル基、メルカプト基又は無置換のC1~C6アルキルチオ基を表し;
a及びbは、それぞれ独立して、0~3の整数を表し;
Yは式(II)
Qは、式(III)
R5は、無置換もしくは(ハロゲン原子、水酸基、及び無置換のC1~C6アルコキシ基)からなる群から選ばれる1~4個の置換基で置換されたC1~C6アルキル基を表し、あるいは
R5、R6、及びR7は任意の2つが結合して環を形成してもよく、
nは0~2の整数を表し、
mは0~3の整数を表す。)を表し;
W-は陰イオンを表す。]
で表される四級アンモニウム塩化合物又はその薬学的に許容される塩。
(2)R2、X、及びA1が、下記の(i)~(iv)のいずれかである、(1)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(i)R2が、単結合、(炭素原子が1個の酸素原子により置換された)C1~C4アルキレン、無置換のC1~C8アルキレン、又は無置換の-O-C1~C4アルキレン;Xが-O-;A1が単結合又は無置換のフェニレンを表す。
(ii)R2が無置換のC1~C4アルキレン、無置換のC2~C4アルケニレン、又は無置換の-O-C1~C4のアルキレン;Xが-CONR3-;A1が単結合、無置換のフェニレン、無置換のC1~C4アルキレン-無置換のフェニレン、又は無置換のC6~C8のシクロアルキレンを表す。
(iii)R2が無置換のC1~C4アルキレン;Xが-NR3CO-又は-NR3CO-CH2-O-;A1が無置換のフェニレンを表す。
(iv)R2、X、A1が単結合を表す。
(3)R2、X、A1、及びR4が、下記の(v)~(xviii)のいずれかである、(1)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(v)R2が単結合;Xが-O-;A1が単結合:R4が無置換のC1~C10アルキレンを表す。
(vi)R2が(無置換もしくは炭素原子が1個の酸素原子により置換された)C1~C8アルキレン;Xが-O-;A1が単結合;R4が無置換のC1~C10アルキレンを表す。
(vii)R2が無置換のC1~C8アルキレン;Xが-O-;A1が無置換のフェニレン-;R4が無置換のC1~C4アルキレンを表す。
(viii)R2が-O-無置換のC1~C4アルキレン;Xが-O-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(ix)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が単結合;R4が無置換のC1~C8アルキレンを表す。
(x)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のC1~C4アルキレン-無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xi)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のC6~C8シクロアルキレン;R4が無置換のC1~C4アルキレンを表す。
(xii)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xiii)R2が無置換の-O-C1~C4アルキレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xiv)R2が無置換のC2~C4アルケニレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xv)R2が無置換のC2~C4アルケニレン;Xが-CONR3-;A1が無置換のC1~C4アルキレン-無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xvi)R2が無置換のC1~C4アルキレン;Xが-NR3CO-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xvii)R2が無置換のC1~C4アルキレン;Xが-NR3CO-CH2-O-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xviii)R2が単結合;Xが単結合;A1が単結合;R4が無置換のC1~C8アルキレンを表す。
(4)R2が、(無置換もしくは炭素原子が1個の酸素原子により置換された)C1~C6アルキレン、又は無置換の-O-C1~C4アルキレン;
Xが、-CONR3-、又は-NR3CO-CH2-O-;
A1が、無置換もしくは(ハロゲン原子、水酸基、無置換のC1~C4アルキル基、無置換のC1~C4アルコキシ基、及びトリフルオロメチル基)からなる群から選ばれる1~3個の置換基で置換された(C6~C10アリーレン又は5~10員のヘテロアリーレン);及び
R4が、無置換のC1~C6アルキレンである、
(1)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(5)R2が、無置換のC1~C6アルキレン;
Xが、-CONR3-;
A1が、無置換もしくは(ハロゲン原子、水酸基、無置換のC1~C4アルキル基、無置換のC1~C4アルコキシ基、及びトリハロメチル基)からなる群から選ばれる1~4個の置換基で置換された(フェニレン又はナフチレン);及び
R4が、無置換のC1~C6アルキレンである、
(1)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(6)R2が、無置換のC1~C6アルキレン;
Xが、-CONH-;
A1が、無置換もしくはハロゲン及びメトキシ基からなる群から選ばれる1~2個の置換基で置換されたフェニレン;及び
R4が、置換もしくは無置換のC1~C6アルキレンである、
(1)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(7)R1が、水素原子を表し、
aが0の整数を表す、(1)~(6)のいずれかに記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(8)Qが
R6及びR7は、それぞれ独立して、メチル基又はフェノキシエチル基を表し、
nは1の整数を表し、
mは0の整数を表す、(7)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(9)Qが、
R6及びR7は、メチル基を表す、(7)に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(10)Yが
(11)(1)~(10)のいずれかに記載の化合物又はその薬学的に許容される塩と、薬学的に許容される担体を含む医薬組成物。
(12)(1)~(10)のいずれかに記載の化合物又はその薬学的に許容される塩を有効成分として含有する、β2アドレナリンレセプターアゴニスト活性及びムスカリンレセプターアンタゴニスト活性を有する医薬組成物。
(13)(1)~(10)のいずれかに記載の化合物又はその薬学的に許容される塩を有効成分として含有する、肺疾患の予防剤又は治療剤。
(14)前記肺疾患が、慢性閉塞性肺疾患又は喘息である、(13)に記載の化合物もしくはその薬学的に許容される塩を有効成分として含有する予防剤又は治療剤。
本発明の一般式(I)で示される化合物の各基については、次のように定義される。各基における表記の順は、式(I)において結合している順を表す。例えば、A1の「C1~C4アルキレン-置換もしくは無置換のアリーレン」は、左端の「C1~C4アルキレン」がXに、右端の「置換もしくは無置換のアリーレン」がR4に結合し、「C1~C4アルキレン」と「置換もしくは無置換のアリーレン」が結合している基を表す。また、炭素原子の右にある数字が炭素数の数を表し、例えば「C1~C6」であれば「炭素数1~6」のものを表す。
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[3-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2,5-ジフルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[2-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ベンゾチオフェン-5-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル](メチル)カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)チオフェン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[3-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[2-クロロ-5-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[3-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-(トリフルオロメチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[3-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[3-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,2R,4S,5S,7S)-7-({[4-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
(1R,3R)-3-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-8,8-ジメチル-8-アザトリシクロ[3.2.1]オクタン-8-イウム、
4-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
4-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
4-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1-メチル-1-(2-フェノキシエチル)ピペリジン-1-イウム、
4-[({5-[(8-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}オクチル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[(6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘキシル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[(9-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ノニル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[(4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ブチル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}メトキシ)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[2-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]メチル}カルバモイル)エチル]-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[3-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]メチル}カルバモイル)プロピル]-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-[({5-[(1E)-2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}-1-エテン-1-イル]-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}-2-メチルプロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[4-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウム、
4-{[(5-{2-[5-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ペンチル)カルバモイル]エチル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウム、
4-{[(5-{[7-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘプチル)オキシ]カルボニル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(9-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ノニル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-{[(5-{3-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウム、
4-{[(5-{3-[(5-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ペンチル)オキシ]プロピル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウム、
4-{[(5-{2-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]エトキシ}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウム、
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]フォルムアミド}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム、
4-({[5-({2-[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェノキシ]アセタミド}メチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウム
本発明の化合物(I)は、酸付加塩を形成する場合がある。また、置換基の種類によっては、塩基との塩を形成する場合もある。このような塩は、医薬的に許容できる塩であれば特に限定されないが、具体的には、フッ化水素酸塩、塩酸塩、臭化水素酸塩、ヨウ化水素酸塩、リン酸塩、硝酸塩、硫酸塩等の鉱酸塩類;メタンスルホン酸塩、エタンスルホン酸塩、2-ヒドロキシエタンスルホン酸塩、p-トルエンスルホン酸塩、ベンゼンスルホン酸塩、エタン-1,2-ジスルホン酸イオン、1,5-ナフタレンジスルホン酸イオン、ナフタレン-2-スルホン酸イオン等の有機スルホン酸塩;並びに酢酸塩、トリフルオロ酢酸塩、プロピオン酸塩、シュウ酸塩、フマル酸塩、フタル酸塩、マロン酸塩、コハク酸塩、グルタル酸塩、アジピン酸塩、酒石酸塩、マレイン酸塩、リンゴ酸塩、マンデル酸塩、1-ヒドロキシ-2-ナフトエ酸塩等の有機カルボン酸塩類が酸付加塩として含まれ、ナトリウム塩、カリウム塩、マグネシウム塩、カルシウム塩、アルミニウム塩等の無機塩基との塩や、メチルアミン塩、エチルアミン塩、リジン塩、オルニチン塩等の有機塩基との塩が、塩基との塩として挙げられる。
<製造法1>
上記反応式(a-1)で示される反応は周知の還元的アミノ化反応の条件を用いることにより行うことができる。還元的アミノ化は、式中の化合物1と化合物2を、還元剤(ホウ化水素還元剤(例えば、トリアセトキシホウ化水素ナトリウム)を含む)の存在下、不活性溶媒(例えば、ジメチルスルホキシド、N,N-ジメチルホルムアミド等)中で反応させることによって行われる。化合物2のカウンターイオンであるW1-はW-と同じであるか、あるいは反応後、公知の方法によってW-に置換される。
反応は塩基(例えば、ピリジン、トリエチルアミン等)の存在下、不活性溶媒(例えば、アセトニトリル、N,N-ジメチルホルムアミド等)中又は無溶媒で、氷冷下から室温下、又は場合により加温下で行うことができる。ここで、脱離基としてはハロゲン、メタンスルホニルオキシ、及びベンゼンスルホニルオキシ等を挙げることができる。
上記反応式(a-4)において、化合物8及び化合物7aから化合物9への反応は、前記反応式(a-3)と同様の条件で行うことができる。化合物9から化合物10への反応は、カルボキシル基の保護基の脱保護反応である。この脱保護反応は、一般的な酸加水分解条件、アルカリ加水分解条件、又は接触還元条件等によって行うことができる。化合物10から化合物6への反応は周知のアミド化反応の条件を用いることにより行うことができる。通常、このようなアミド化反応はカルボジイミド類等の縮合剤存在下、アミン類とカルボン酸とを縮合反応させることによって行うことができる。この場合、溶媒としてはN,N-ジメチルホルムアミドやクロロホルム等のハロゲン化炭化水素類が適しており、縮合剤としては、N,N-ジシクロヘキシルカルボジイミドや1-エチル-(3-(N,N-ジメチルアミノ)プロピル)カルボジイミドやカルボニルジイミダゾール、ジフェニルホスホリルアジドやジエチルホスホリルシアニド等が用いられる。反応は通常、冷却ないし室温下、又は場合により加温下で行われる。
上記反応式(a-5)において、化合物13から化合物12への反応は、O-アルキル化反応である。O-アルキル化反応は、フェノール性水酸基含有化合物をアルキル化剤(例えば、アルキルハライド等)と不活性溶媒(例えば、アセトニトリル、N,N-ジメチルホルムアミド等)中、塩基(例えば、炭酸カリウム等)存在下、室温又は場合により加温下で行うことができる。化合物12から化合物11への反応は、水酸基の保護反応であり、周知の方法で行うことができる。化合物11から化合物7bへの反応は、ニトロ基の還元反応であり、接触還元や塩化スズ処理等の一般的な条件で行うことができる。
上記反応式(a-6)において、化合物16から化合物15への反応は、アリールハライドとアルケンを反応させる、いわゆるHeck反応である。反応は、パラジウム、ホスフィン配位子及び塩基存在下、不活性溶媒中、加温攪拌することで行うことができる。化合物15から化合物14への反応は、二重結合の還元反応であり、周知の接触還元等の方法で行うことができる。化合物14から化合物7cへの反応は、水酸基の保護反応であり、周知の方法で行うことができる。
<製造法2>
上記反応式(a-7)で示される反応は、N-アルキル化反応である。好ましいL3としては、ハロゲン原子(例えば、塩素原子、臭素原子、ヨウ素原子)、スルホニルオキシ基、ベンゼンスルホニルオキシ基が挙げられる。反応は不活性溶媒(例えば、アセトニトリル、N,N-ジメチルホルムアミド等)中、室温下、又は場合により加温下で行うことができる。化合物3のカウンターイオンであるW1-はW-と同じであるか、あるいは反応後、公知の方法によってW-に置換される。化合物17は、前記の化合物3から公知の方法で調製できる。
<製造法3>
上記反応式(a-8)で示される反応は、水酸基の保護基の脱保護反応である。公知の方法によって脱保護することができ、例えば、P3がtert-ブチルジメチルシリル基の場合、テトラブチルアンモニウムフルオリドやトリフルオロ酢酸等で処理することにより行うことができる。
<製造例4>
[参考例1]
8-ヒドロキシキノリン-N-オキシドの合成
8-キノリノール(351g、2.42mol)をジクロロメタン(3.5L)に溶解し、氷水冷却下、メタクロロ過安息香酸(675.3g、2.74mol)を分割添加し、室温で2時間攪拌した。不溶物をろ去し、ジクロロメタンで洗浄した。ろ液と洗液を混合し、減圧濃縮した。残渣に2%アンモニア水(2.1L)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、8-ヒドロキシキノリン-N-オキシド(318.4g)を得た。
1H-NMR(400MHz,DMSO-d6) δ8.51(d,J=8.0Hz,1H),8.06(d,J=8.0Hz,1H),7.43-7.56(m,2H),7.39(d,J=8.0Hz,1H),6.98(d,J=8.0Hz,1H)
[参考例2]
8-アセトキシ-1H-キノリン-2-オンの合成
8-ヒドロキシキノリン-N-オキシド(640g、3.97mol)を無水酢酸(2.0L)に懸濁し、70℃で2.5時間攪拌した。氷水冷却下、10℃以下で1時間攪拌後、析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、8-アセトキシ-1H-キノリン-2-オン(570.6g)を得た
1H-NMR(400MHz,DMSO-d6) δ11.6(s,1H),7.94(d,J=9.6Hz,1H),7.56(d,J=8.0Hz,1H),7.28(d,J=8.0Hz,1H),7.17(t,J=8.0Hz,1H),6.53(d,J=9.6Hz,1H),2.36(s,3H)
[参考例3]
5-アセチル-8-ヒドロキシ-1H-キノリン-2-オンの合成
8-アセトキシ-1H-キノリン-2-オン(570.6g、2.81mol)をジクロロエタン(5.8L)に懸濁し、氷水冷却下、20℃以下で、塩化アルミニウム(925g、6.94mol)を分割添加し、70℃~80℃で3時間攪拌した。反応溶液を減圧濃縮し、残渣に1M塩酸(10L)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、5-アセチル-8-ヒドロキシ-1H-キノリン-2-オン(584g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 11.3(s,1H),10.6(s,1H),8.66(d,J=10.0Hz,1H),7.67(d,J=8.4Hz,1H),6.91(d,J=8.4Hz,1H),6.52(d,J=10.0Hz,1H),2.41(s,3H)
[参考例4]
5-アセチル-8-ベンジルオキシ-1H-キノリン-2-オンの合成
5-アセチル-8-ヒドロキシ-1H-キノリン-2-オン(430g 、2.12mol)を、N,N-ジメチルホルムアミド(3.3L)に懸濁し、炭酸カリウム(298g、2.16mol)を加え、続いて、臭化ベンジル(298g、2.11mol)を加え、室温で2 時間攪拌した。不溶物をろ去し、N,N-ジメチルホルムアミド洗浄した。ろ液と洗浄液を混合し、減圧濃縮した。残渣に精製水(3.3L)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、5-アセチル-8-ベンジルオキシ-1H-キノリン-2-オン(541g)を得た。
1H-NMR(400MHz,CDCl3) δ 9.23(s,1H),8.93(d,J=10.0Hz,1H),7.69(d,J=8.0Hz,1H),7.43(s,5H),7.04(d,J=8.0Hz,1H),6.77(d,J=10.0Hz,1H),5.26(s,2H),2.65(s,3H)
[参考例5]
8-ベンジルオキシ-5-(2-ブロモアセチル)-1H-キノリン-2-オンの合成
5-アセチル-8-ベンジルオキシ-1H-キノリン-2-オン(372g 、1.27 mol)をテトラヒドロフラン(3.6L) に溶解し、そして0℃まで冷却した。三臭化ピリジニウム(453g、1.27mol) を分割投入し、3時間加熱還流した後、テトラヒドロフラン(3.1L)を加え、一晩加熱還流した。析出物をろ取、テトラヒドロフランで洗浄した。固体をテトラヒドロフラン(2.3L)で懸濁洗浄した後、精製水(3L)で洗浄した。別途、テトラヒドロフランろ液と洗浄液を混合し、減圧濃縮した後、テトラヒドロフラン(1L)で懸濁洗浄した。固体を合わせて減圧下にて乾燥して、8-ベンジルオキシ-5-(2-ブロモアセチル)-1H-キノリン-2-オン(387g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 11.1(s,1H),8.49(d,J=9.0Hz,1H),7.86(d,J=9.0Hz,1H),7.58(d,J=8.0Hz,2H),7.25-7.45(m,5H),6.67(d,J=9.0Hz,1H),5.42(s,2H),4.91(s,2H)
[参考例6]
8-ベンジルオキシ-5-((R)-2-ブロモ-1-ヒドロキシエチル)-1H-キノリン-2-オンの合成
アルゴン気流下、8-ベンジルオキシ-5-(2-ブロモアセチル)-1H-キノリン-2-オン(374g 、1.00mol)を脱水テトラヒドロフラン(3.8L)に懸濁 し、CBS触媒(27.8g)を加え、-55~-45℃で40分間攪拌した。0.9M ボラン-テトラヒドロフラン錯体テトラヒドロフラン溶液(1.27L)を同温度下で滴下した後、徐々に0℃まで昇温した。メタノール(1.3L)を滴下した後、不溶物をろ去し、テトラヒドロフランで洗浄した。ろ液と洗浄液を混合し、減圧濃縮した。残渣に精製水(6.3L)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄した。さらに、酢酸エチル(4.8L)で懸濁洗浄し、ろ取、減圧下にて乾燥して、8-ベンジルオキシ-5-((R)-2-ブロモ-1-ヒドロキシエチル)-1H-キノリン-2-オン(278g)を得た。
1H-NMR(400MHz,CDCl3) δ 9.26(s,1H),8.08(d,J=10.0Hz,1H),7.37-7.45(m,5H),7.28(d,J=8.0Hz,1H),7.05(d,J=8.0Hz,1H),6.72(d,J=10.0Hz,1H),5.33(dd,J=9.0Hz,4.0Hz,1H),5.19(s,2H)
3.71-3.74(m,2H)
[参考例7]
5-((R)-2-アジド-1-ヒドロキシエチル)-8-ベンジルオキシ-1H - キノリン-2-オンの合成
8-ベンジルオキシ-5-((R)-2-ブロモ-1-ヒドロキシエチル)-1H-キノリン-2-オン(20.8g、55.6 mmol)とアジ化ナトリウム(3.61g、55.5 mmol)をN,N-ジメチルホルムアミド(100mL)に懸濁 し、65℃で3時間攪拌した。アジ化ナトリウム(1.81g、27.8mmol)を加え、同温で一晩攪拌した。反応溶液に精製水を加え、室温で1時間攪拌した。析出物をろ取、精製水で洗浄した。減圧下にて乾燥して、5-((R)-2-アジド-1-ヒドロキシエチル)-8-ベンジルオキシ-1H-キノリン-2-オン(16.8g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 10.7(s,1H),8.19(d,J=12.0Hz,1H),7.56(d,J=8.0Hz,2H),7.34-7.41(m,1H),7.26-7.33(m,1H),7.20(s,2H),6.54(d,J=8.0Hz,1H),5.90(d,J=8.0Hz,1H),5.30(s,2H),5.18-5.26(m,1H),3.44(dd,J=12.0Hz,8.0Hz,1H),
3.30(dd,J=16.0Hz,4.0Hz,1H)
[参考例8]
5-((R)-2-アミノ-1-ヒドロキシエチル)-8-ヒドロキシ-1H-キノリン- 2-オン酢酸塩の合成
5-((R)-2-アジド-1-ヒドロキシエチル)-8-ベンジルオキシ-1H-キノリン-2-オン(16.8g、49.9mmol)を酢酸(50mL)に懸濁し、触媒量の水酸化パラジウム炭素を加え、水素雰囲気下に溶液をおいて一晩攪拌した。触媒をろ過により除去し減圧濃縮した。残渣に室温でメタノール(100mL)と酢酸エチル(100mL)を加え、攪拌した。析出物をろ取し乾燥して、5-((R)-2-アミノ-1-ヒドロキシエチル)-8-ヒドロキシ-1H-キノリン-2-オン酢酸塩(12.5g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 8.16(d,J=8.0Hz,1H),7.05(d,J=8.0Hz,1H),6.91(d,J=8.0Hz,1 H),6.49(d,J=8.0Hz,1 H)5.06(dd,J=8.0Hz,4.0Hz,1H),2.85(dd,J=12.0Hz,4.0Hz,1H),2.73(dd,J=12.0Hz,8.0Hz,1H),1.84(s,3H)
[参考例9]
trans-3-(4-ブロモ-3-ニトロフェニル)アクリル酸tertブチルの合成
窒素気流下、水素化ナトリウム(ミネラルオイル40%添加、1.70g、42.6mmol)をテトラヒドロフラン(80mL)に懸濁させ、氷水冷却下、ジエチルホスホノ酢酸tertブチルエステル(8.59g、34.1mmol)を加えた。氷水冷却下で1時間攪拌した後、4-ブロモ-3-ニトロ-ベンズアルデヒド(6.53g、28.4mmol)のN,N-ジメチルホルムアミド(50mL)溶液を加え、ゆっくりと室温に戻しながら16時間攪拌した。氷水冷却下、飽和塩化アンモニア水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、trans-3-(4-ブロモ-3-ニトロフェニル)アクリル酸tertブチル(7.07g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.95(d,J=2.0Hz,1H),7.75(d,J=8.3Hz,1H),7.52(dd,J=8.3Hz,2.0Hz,1H),7.51(d,J=16.1Hz,1H),6.45(d,J=16.1Hz,1H),1.54(s,9H)
[参考例10]
trans-3-(3-ニトロ-4-フェニルフェニル)アクリル酸tertブチルの合成
trans-3-(4-ブロモ-3-ニトロフェニル)アクリル酸tertブチル(7.07g、21.5mmol)を1,4-ジオキサン(200mL)に溶解し、フェニルホウ酸(5.25g、42.1mmol)、炭酸セシウム(56.1g、172.2mmol)、1,1-[ビス(ジフェニルフォスフィノ)フェロセン]ジクロロパラジウム(II)ジクロロメタン錯体(0.88g、1.1mmol)、精製水(50mL)を加え、窒素気流下80℃で4時間攪拌した。反応溶液をセライト、アルミナ、フローリジルでろ過後、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、trans-3-(3-ニトロ-4-フェニルフェニル)アクリル酸tertブチル(6.52g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.96(d,J=1.7Hz,1H),7.71(dd,J=7.8Hz,1.7Hz,1H),7.60(d,J=16.1Hz,1H),7.40-7.49(m,4H),7.29-7.36(m,2H),6.48(d,J=16.1,1H),1.55(s,9H)
[参考例11]
3-(3-アミノ-4-フェニルフェニル)プロピオン酸tertブチルの合成
trans-3-(3-ニトロ-4-フェニルフェニル)アクリル酸tertブチル(6.52g、20.0mmol)をメタノール(100mL)と酢酸エチル(100mL)に溶解し、10%パラジウム炭素(500mg)を加え、水素雰囲気下室温で16時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、3-(3-アミノ-4-フェニルフェニル)プロピオン酸tertブチル(5.94g)を得た。
LC/MS:M+1=338.3
[参考例12]
3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸tertブチルの合成
窒素気流下、4-ヒドロキシ-1-メチルピペリジン(2.88g、25.0mmol)をアセトニトリル(80mL)に溶解させ、氷水冷却下、ジホスゲン(9.89g、50mmol)のアセトニトリル(20mL)溶液を加えた。室温で1時間攪拌した後、減圧濃縮し、固体を得た。得られた固体を、3-(3-アミノ-4-フェニルフェニル)プロピオン酸tertブチル(2.97g、10.0mmol)のピリジン(50mL)溶液に加え、室温で16時間攪拌した。氷水冷却下、希水酸化ナトリウム水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸tertブチル(5.08g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.99(s,1H),7.45-7.50(m,2H),7.39-7.43(m,1H),7.33-7.37(m,2H),7.13(d,J=7.8Hz,1H),6.97(dd,J=7.8Hz,1.7Hz,1H),6.59(s,1H),4.69-4.74(m,1H),2.95(t,J=7.9Hz,2H),2.60-2.74(m,2H),2.60(t,J=7.5Hz,2H),2.26(s,3H),2.16-2.25(m,2H),1.89-1.99(m,2H),1.66-1.82(m,2H), 1.44(s,9H)
[参考例12-2]
3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸tertブチルの合成
参考例12に従い、トロペノール(310mg、2.0mmol)と3-(3-アミノ-4-フェニルフェニル)プロピオン酸tertブチル(297mg、1.0mmol)から3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸tertブチル(121mg)を得た。
LC/MS:M+1=479.3
[参考例13]
3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩の合成
3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸tertブチル(5.08g、11.6mmol)に4M塩化水素ジオキサン溶液(70mL)を添加、70℃で2時間攪拌した。反応溶液を減圧濃縮し、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(5.49g)を得た。
[参考例13-2]
3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩の合成
参考例13に従い、参考例12-2で得られた3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸tert-ブチル(121mg、0.25mmol)から3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(105mg)を得た。
LC/MS:M+1=423.3
[参考例14]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリンの合成
4-アミノベンジルアルコール(5.00g、40.6mmol)とイミダゾール(5.52g、81.2mmol)をテトラヒドロフラン(30mL)に溶解させ、tert-ブチルジメチルクロロシラン(9.14g、60.9mmol)のテトラヒドロフラン(10mL)溶液を加えた。室温で1時間攪拌した後、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(9.94g)を得た。
[参考例15]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(191mg、0.5mmol)をN,N-ジメチルホルムアミド(10mL)に溶解し、そこにN-エチル-N’-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(1.0mmol)、N-ヒドロキシベンゾトリアゾール(1.0mmol)、トリエチルアミン(5.0mmol)、4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(1.0mmol)を加え、室温で16時間攪拌した。反応液を酢酸エチルにて抽出し、有機層を飽和食塩水で洗浄、硫酸ナトリウムにて乾燥後、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(121.7mg)を得た。
1H-NMR(400MHz,CDCl3) δ 8.03(s,1H),7.39-8.05(m,5H),7.32-7.36(m,2H),7.22-7.29(m,3H),7.13(d,J=7.8Hz,1H),7.02(d,J=7.8Hz,1H),6.62(s,1H),4.68-4.75(m,1H),4.69(s,2H),3.09(t,J=7.6Hz,2H),2.71(t,J=7.6Hz,2H),2.62-2.71(m,2H),2.29(s,3H),2.19-2.31(m,2H),1.92-2.00(m,2H),1.68-1.78(m,2H),0.93(s,9H),0.08(s,6H)
[参考例16]
3-(4-ブロモ-3-ニトロベンゾイル)プロピオン酸の合成
塩氷冷却下、発煙硝酸(200mL)に3-(4-ブロモベンゾイル)プロピオン酸(75.0g、291.7mmol)を反応溶液温度が-5℃以下に保たれる速度で分割添加した。-12℃~-10℃で1時間攪拌後、反応溶液を氷にあけ、析出した固体をろ取、精製水で洗浄後、減圧下にて乾燥して、3-(4-ブロモ-3-ニトロベンゾイル)プロピオン酸(91.0g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 8.43(d,J=2.0Hz,1H),7.96-8.06(m,2H),3.20(t,J=6.2Hz,2H),2.51(t,J=6.2Hz,2H)
[参考例17]
3-(3-ニトロ-4-フェニルベンゾイル)プロピオン酸の合成
3-(4-ブロモ-3-ニトロベンゾイル)プロピオン酸(45.3g、150.0mmol)を1,4-ジオキサン(400mL)に溶解し、フェニルホウ酸(27.4g、225.0mmol)、炭酸セシウム(146.6g、450.0mmol)、1,1-[ビス(ジフェニルフォスフィノ)フェロセン]ジクロロパラジウム(II)ジクロロメタン錯体(3.7g、4.5mmol)、精製水(150mL)を加え、窒素気流下80℃で18時間攪拌した。反応溶液をセライト、アルミナ、フローリジルでろ過後、水層を分離した。有機層を希水酸化ナトリウム水溶液で抽出した。水層を合わせて酢酸エチルで洗浄した後、氷水冷却下、6M塩酸で酸性にし、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥、減圧濃縮し、3-(3-ニトロ-4-フェニルベンゾイル)プロピオン酸(39.4g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 12.22(s,1H),8.48(d,J=0.9Hz,1H),8.30(dd,J=8.2Hz,0.9Hz,1H),7.73(d,J=8.2Hz,1H),7.45-7.50(m,3H),7.37-7.41(m,2H),3.34(t,J=6.2Hz,2H),2.63(t,J=6.2Hz,2H)
[参考例18]
4-(3-アミノ-4-フェニルフェニル)酪酸の合成
3-(3-ニトロ-4-フェニルベンゾイル)プロピオン酸(18.6g、69.0mmol)を酢酸(200mL)とトリフルオロ酢酸(20mL)に溶解し、10%水酸化パラジウム炭素(5g)を加え、水素雰囲気下70℃で16時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮した。
1H-NMR(400MHz、DMSO-d6) δ 7.35-7.44(m,4H),7.27-7.33(m,1H),6.90(d,J=7.8Hz,1H),6.60(d,J=1.0Hz,1H),6.48(dd,J=7.8Hz,1.0Hz,1H),2.47(d,J=7.8Hz,2H),2.24(d,J=7.4Hz,2H),1.74-1.82(m,2H)
[参考例19]
4-(3-アミノ-4-フェニルフェニル)酪酸ベンジル トシル酸塩の合成
4-(3-アミノ-4-フェニルフェニル)酪酸(21.6g、84.6mmol)のトルエン(300mL)懸濁液に、ベンジルアルコール(50mL)、トシル酸一水和物(17.7g、93.0mmol)を加え、ディーンスタークで脱水しながら5時間加熱還流した。反応溶液を減圧濃縮し、得られた固体をヘキサン-酢酸エチルの混合溶媒(4:1)で洗浄し、ろ取、減圧下にて乾燥して、4-(3-アミノ-4-フェニルフェニル)酪酸ベンジル トシル酸塩(41.2g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 7.44-7.53(m,5H),7.30 -7.39(m,7H),7.28(d,J=7.8Hz,2H),7.19-7.27(m,1H),7.11(d,J=7.8Hz,2H),5.10(s,2H),4.49(s,3H),2.65(t,J=7.7Hz,2H),2.42(d,J=7.4Hz,2H),1.83-1.90(m,2H)
[参考例20]
4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸ベンジルの合成
窒素気流下、4-ヒドロキシ-1-メチルピペリジン(10.4g、90.0mmol)をアセトニトリル(100mL)に溶解させ、氷水冷却下、ジホスゲン(35.6g、180mmol)のアセトニトリル(50mL)溶液を加えた。室温で5時間攪拌した後、減圧濃縮し、固体を得た。得られた固体を、4-(3-アミノ-4-フェニルフェニル)酪酸ベンジル トシル酸塩(31.1g、60.0mmol)のピリジン(50mL)、N,N-ジメチルホルムアミド(150mL)混合溶液に加え、室温で2時間攪拌した。氷水冷却下、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を希水酸化ナトリウム水溶液、飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸ベンジル(25.8g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.96(s,1H),7.43-7.50(m,2H),7.39-7.42(m,1H),7.30-7.38(m,7H),7.12(d,J=7.8Hz,1H),6.93(dd,J=7.7Hz,1.6Hz,1H),6.58(s,1H),5.13(s,2H),4.65-4.75(m,1H),2.69(t,J=7.6Hz,2H),2.60-2.68(m,2H),2.42(t,J=7.4Hz,2H),2.26(s,3H),2.16-2.21(m,2H),2.98-1.08(m,2H),1.68-1.88(m,2H),1.64-1.75(m,2H)
[参考例20-2]
4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジルの合成
参考例20に従い、スコピン(Shanghai FWD Chemcials Co., Ltd.より購入、9.31g、60.0mmol)と4-(3-アミノ-4-フェニルフェニル)酪酸ベンジル トシル酸塩(31.1g、60.0mmol)から4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジル(9.14g)を得た。
LC/MS:M+1=527.3
[参考例20-3]
4-(3-{[({(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジルの合成
参考例20に従い、トロピン(2.82g、20.0mmol)、と4-(3-アミノ-4-フェニルフェニル)酪酸ベンジルトシル酸塩(5.17g、10.0mmol)から4-(3-{[({(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジル(4.37g)を得た。
LC/MS:M+1=513.3
[参考例21]
4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸の合成
4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸ベンジル(25.8g、5.30mmol)を酢酸エチル(250mL)に溶解し、10%水酸化パラジウム炭素(5g)を加え、水素雰囲気下室温で3日間攪拌した後、50℃で6時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(21.3g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 7.94(s,1H),7.43-7.48(m,5H),7.27(d,J=7.8Hz,1H),7.26(s,1H),7.16(dd,J=7.8Hz,1.2Hz,1H),4.46-4.54(m,1H),2.66(t,J=7.7Hz,2H),2.55-2.62(m,2H),2.30(t,J=7.3Hz,2H),2.20(s,3H),2.12-2.23(m,2H),1.82-1.92(m,2H),1.72-1.79(m,2H),1.48-1.58(m,2H)
[参考例21-2]
4-(3-{[({(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸の合成
参考例21に従い、参考例20-3で得られた4-(3-{[({(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジルの合成(2.09g、3.98mmol)から4-(3-{[({(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(706mg)を得た。
LC/MS:M+1=423.3
[参考例21-3]
4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸の合成
参考例21に従い、参考例20-2で得られた4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸ベンジル(2.09g、3.98mmol)から4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(1.55g)を得た。
LC/MS:M+1=437.3
[参考例21-6]
4-(4-ブロモベンゾイル)酪酸の合成
塩化アルミニウム(8g、60mmol)とブロモベンゼン(30mL)の混合物に、氷水冷却下、エチルグルタリルクロリド(5g、28.0mmol)を加え、室温で2時間攪拌した。反応溶液を氷にあけて反応を停止した後、混合物を酢酸エチルにて抽出した。有機層を飽和食塩水、飽和炭酸水素ナトリウム水溶液、飽和食塩水の順にて洗浄し、無水硫酸マグネシウムで乾燥した後、減圧濃縮した。
1H-NMR(400MHz、DMSO-d6) δ 12.08(s,1H),7.87(dt,J=8.8Hz,2.0Hz,2H),7.71(dt,J=8.8Hz,2.0Hz,2H),3.03(t,J=7.2Hz,2H),2.28(t,J=7.4Hz,2H),1.75-1.86(m,2H)
[参考例16-2]
4-(4-ブロモ-3-ニトロベンゾイル)酪酸の合成
参考例16に従い、参考例21-6で得られた4-(4-ブロモベンゾイル)酪酸(5.95g、21.9mmol)から、4-(4-ブロモ-3-ニトロベンゾイル)プロピオン酸(6.76g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 8.48(d,J=1.7Hz,1H),8.03-8.10(m,2H),3.10(t,J=7.2Hz,2H),2.29(t,J=7.4Hz,2H),1.76-1.86(m,2H)
[参考例17-2]
4-(3-ニトロ-4-フェニルベンゾイル)酪酸の合成
参考例17に従い、参考例16-2で得られた4-(4-ブロモ-3-ニトロベンゾイル)酪酸(6.76g、19.0mmol)から、4-(3-ニトロ-4-フェニルベンゾイル)酪酸(5.94g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 12.11(s,1H), 8.45(d,J=2.0Hz,1H),8.27(dd,J=8.0Hz,2.0Hz 1H),7.72(d,J=8.0Hz,1H),7.44-7.50(m,3H),7.36-7.40(m,2H),3.16(t,J=7.1Hz,2H),2.32(t,J=7.3Hz,2H),1.81-1.90(m,2H)
[参考例18-2]
5-(3-アミノ-4-フェニルフェニル)吉草酸の合成
参考例18に従い、参考例17-2で得られた4-(3-ニトロ-4-フェニルベンゾイル)酪酸(2.93g、10.0mmol)から、5-(3-アミノ-4-フェニルフェニル)吉草酸(1.52g)を得た。
[参考例19-2]
5-(3-アミノ-4-フェニルフェニル)吉草酸ベンジル トシル酸塩の合成
参考例19に従い、参考例18-2で得られた5-(3-アミノ-4-フェニルフェニル)吉草酸(1.37g、5.10mmol)から、5-(3-アミノ-4-フェニルフェニル)吉草酸ベンジル トシル酸塩(3.53g)を得た。
1H-NMR(400MHz、DMSO-d6) δ 7.43-7.53(m,5H),7.29-7.39(m,9H),7.19-7.24(m,1H),7.11(d,J=7.8Hz,2H),5.08(s,2H),4.48(s,3H),2.63(t,J=6.8Hz,2H),2.41(d,J=8.8Hz,2H),1.56-1.61(m,4H)
[参考例20-4]
5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸ベンジルの合成
参考例20に従い、参考例19-2で得られた5-(3-アミノ-4-フェニルフェニル)吉草酸ベンジル トシル酸塩(1.32g、2.5mmol)と4-ヒドロキシ-1-メチルピペリジン(0.58mg、5.0mmol)から、5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸ベンジル(985mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.95(s,1H),7.46-7.50(m,2H),7.26-7.42(m,8H),7.11(d,J=7.8Hz,1H),6.92(dd,J=7.8Hz,1.5Hz,1H),6.60(s,1H),5.12(s,2H),4.67-4.74(m,1H),2.66(t,J=7.0Hz,2H),2.62-2.70(m,2H),2.40(t,J=7.3Hz,2H),2.26(s,3H),2.18-2.21(m,2H),1.90-2.00(m,2H),1.66-1.83(m,6H)
[参考例20-5]
5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸ベンジルの合成
参考例20に従い、参考例19-2で得られた5-(3-アミノ-4-フェニルフェニル)吉草酸ベンジル トシル酸塩(1.32g、2.5mmol)とスコピン(0.95g、5.0mmol)から、5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸ベンジル(985mg)を得た。
LC/MS:M+1=541.3
[参考例21-4]
5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸の合成
参考例21に従い、参考例20-4で得られた5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸ベンジル(500mg、0.5mmol)から、5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸(410mg)を得た。
LC/MS:M+1=411.3
[参考例21-5]
5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸の合成
参考例21に従い、参考例20-4で得られた5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸ベンジル(540mg、1.0mmol)から、5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸(450mg)を得た。
LC/MS:M+1=451.3
[参考例22]
1-(2-フェノキシエチル)ピペリジン-4-オールの合成
4-ヒドロキシピペリジン(5.06g、50mmol)をN,N-ジメチルホルムアミド(200mL)に溶解し、炭酸カリウム(13.8g、100mmol)と(2-ブロモエトキシ)ベンゼン(12.9g、60mmol)を加え、70℃で18時間攪拌した。反応溶液を酢酸エチルで抽出し、有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、1-(2-フェノキシエチル)ピペリジン-4-オール(8.48g)を得た。
LC/MS:M+1=222.3
[参考例23]
4-アミノ-5-クロロ-2-メトキシベンジルアルコールの合成
水素化リチウムアルミニウム(25.0g、116mmol)のテトラヒドロフラン(150mL)懸濁液に、氷水冷却下、4-アミノ-5-クロロ-2-メトキシ安息香酸(5g、28.0mmol)を分割添加し、5時間加熱還流した。氷水冷却下、飽和ロシェル塩水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和ロシェル塩水溶液、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。得られた固形物をヘキサン-酢酸エチル混合溶媒(比4:1)で洗浄、ろ取し、減圧下にて乾燥して、4-アミノ-5-クロロ-2-メトキシベンジルアルコール(11.8g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.13(s,1H),6.31(s,1H),4.53(d,J=2.4Hz,2H),4.02-4.08(broad,2H),3.80(s,3H)
[参考例14-2]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリンの合成
参考例14に従い、参考例23で得られた4-アミノ-5-クロロ-2-メトキシベンジルアルコール(11.8g、62.9mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(18.1g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.25(s,1H),6.26(s,1H),4.61(s,2H),3.92-4.02(broad,2H),3.74(s,3H),0.94(s,9H),0.08(s,6H)
[参考例14-3]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロ-アニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-2-クロロ安息香酸(858mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロ-アニリン(1.3g)を得た。
LC/MS:M+1=271.2
[参考例14-4]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-3-フルオロ安息香酸(776mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロアニリン(0.66g)を得た。
LC/MS:M+1=256.2
[参考例14-5]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-2,5-ジフルオロ安息香酸(406mg、2.0mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロアニリン(94.2mg)を得た。
LC/MS:M+1=274.2
[参考例14-6]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-2-メトキシ安息香酸(836mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリン(0.30g)を得た。
LC/MS:M+1=268.2
[参考例14-7]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-2-フルオロ安息香酸(776mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロアニリン(0.45g)を得た。
LC/MS:M+1=256.2
[参考例14-8]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルアニリンの合成
2-メチル-4-ニトロ安息香酸(741mg、5mmol)をメタノール(20mL)に溶解し、10%パラジウム炭素(100mg)を加え、水素雰囲気下室温で16時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、4-アミノ-2-メチル安息香酸を粗体として得た。得られた4-アミノ-2-メチル安息香酸から、参考例23、及び、参考例14に従い、4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルアニリン(0.33g)を得た。
LC/MS:M+1=252.2
[参考例14-9]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-3-クロロ安息香酸(858mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(0.49g)を得た。
LC/MS:M+1=272.2
[参考例14-10]
5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-3-メトキシ安息香酸(836mg、5mmol)から5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(0.45g)を得た。
LC/MS:M+1=268.2
[参考例14-11]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-3-メチル安息香酸(756mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリン(0.17g)を得た。
LC/MS:M+1=252.2
[参考例14-12]
6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミンの合成
参考例23、及び、参考例14に従い、2-アミノ-6-ナフトエ酸(936mg、5mmol)から、6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(0.97g)を得た。
LC/MS:M+1=288.2
[参考例14-13]
2-[(tert-ブチルジメチルシラノイルオキシ)メチル]-1-ベンゾチオフェン-5-アミンの合成
参考例23、及び、参考例14に従い、5-アミノ-1-ベンゾチオフェン-2-カルボン酸メチル(1.04g、5mmol)から、2-[(tert-ブチルジメチルシラノイルオキシ)メチル]-1-ベンゾチオフェン-5-アミンの合成(0.64g)を得た。
LC/MS:M+1=294.1
[参考例14-14]
3-[(tert-ブチルジメチルシラノイルオキシ)メチル]-4-メトキシアニリンの合成
参考例23、及び、参考例14に従い、5-アミノ-2-メトキシ安息香酸(836mg、5mmol)から3-[(tert-ブチルジメチルシラノイルオキシ)メチル]-4-メトキシアニリン(0.89g)を得た。
LC/MS:M+1=268.2
[参考例14-15]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-N-メチルアニリンの合成
参考例23、及び、参考例14に従い、4-メチルアミノ安息香酸(756mg、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-N-メチルアニリン(0.84g)を得た。
LC/MS:M+1=252.2
[参考例14-16]
5-[(tert-ブチルジメチルシラノイルオキシ)メチル]チオフェン-2-アミンの合成
5-ニトロ-2-チオフェンカルバルデヒド(15.7g、10.0mmol)をテトラヒドロフランに溶解し、氷水冷却下、ボラン-テトラヒドロフラン錯体(1M、テトラヒドロフラン溶液、25.0mmol)を滴下し、室温で2時間攪拌した。氷水冷却下、飽和ロシェル塩水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和ロシェル塩水溶液、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。得られた固形物をメタノール(20mL)に溶解し、ラネーニッケルを触媒量加え、水素雰囲気下室温で2時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、(5-アミノチオフェン-2-イル)メタノールを租体として得た。得られた(5-アミノチオフェン-2-イル)メタノールから、参考例14に従い、5-[(tert-ブチルジメチルシラノイルオキシ)メチル]チオフェン-2-アミン(170mg)を得た。
LC/MS:M+1=244.3
[参考例14-17]
5-[(tert-ブチルジメチルシラノイルオキシ)メチル]ピリジン-2-アミンの合成
参考例23、及び、参考例14に従い、6-アミノニコチン酸(691mg、5mmol)から、5-[(tert-ブチルジメチルシラノイルオキシ)メチル]ピリジン-2-アミン(0.14g)を得た。
LC/MS:M+1=239.2
[参考例14-18]
2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシ-アニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-5-ブロモ-2-メトキシ安息香酸メチル(500mg、2mmol)から2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシ-アニリン(0.35g)を得た。
LC/MS:M+1=347.1
[参考例14-19]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシ-アニリンの合成
参考例23及び参考例14に従い、4-アミノ-5-クロロ-2-エトキシ安息香酸(863mg、4mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシ-アニリン(0.87g)を得た。
LC/MS:M+1=316.1
[参考例14-20]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシ-アニリンの合成
参考例14-8に従い、2-エトキシ-4-ニトロ安息香酸(702mg、3.32mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシ-アニリン(0.65g)を得た。
LC/MS:M+1=282.3
[参考例14-21]
2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリンの合成
参考例23、及び、参考例14に従い、4-アミノ-2-ブロモ安息香酸(460mg、2mmol)から2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(0.59g)を得た。
LC/MS:M+1=317.1
[参考例14-22]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)アニリンの合成
参考例14-8に従い、4-ニトロ-2-(トリフルオロメチル)安息香酸(1.18g、5mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)アニリン(0.94g)を得た。
LC/MS:M+1=306.2
[参考例15-2]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(191mg、0.5mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(188mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(20mg)を得た。
LC/MS:M+1=666.3
[参考例15-3]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-3で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロ-アニリン(544mg、2.0mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(340mg)を得た。
LC/MS:M+1=636.3
[参考例15-4]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-4で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロアニリン(383mg、1.5mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(266mg)を得た。
LC/MS:M+1=620.3
[参考例15-5]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(126mg、0.3mmol)と参考例14-5で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロアニリン(94.2mg、0.35mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(44mg)を得た。
LC/MS:M+1=637.3
[参考例15-6]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(181mg、0.5mmol)と参考例14-6で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリン(201mg、0.75mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(89mg)を得た。
LC/MS:M+1=632.3
[参考例15-7]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(419mg、1.1mmol)と参考例14-7で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロアニリン(383mg、1.5mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(308mg)を得た。
LC/MS:M+1=620.3
[参考例15-8]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(419mg、1.1mmol)と参考例14-8で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルアニリン(330mg、1.3mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(250mg)を得た。
LC/MS:M+1=616.3
[参考例15-9]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-9で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(360mg、1.3mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(195mg)を得た。
LC/MS:M+1=636.2
[参考例15-10]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-10で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(401mg、1.5mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(340mg)を得た。
LC/MS:M+1=632.3
[参考例15-11]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(260mg、0.68mmol)と参考例14-11で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリン(170mg、0.68mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(82mg)を得た。
LC/MS:M+1=616.3
[参考例15-12]
1-メチルピペリジン-4-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-12で得られた6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(431mg、1.5mmol)から1-メチルピペリジン-4-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(279mg)を得た。
LC/MS:M+1=652.3
[参考例15-13]
1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}-1-ベンゾチオフェン-5-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(419mg、1.1mmol)と参考例14-13で得られた2-[(tert-ブチルジメチルシラノイルオキシ)メチル]-1-ベンゾチオフェン-5-アミン(440mg、1.5mmol)から1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}-1-ベンゾチオフェン-5-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(204mg)を得た。
LC/MS:M+1=685.3
[参考例15-14]
1-メチルピペリジン-4-イル N-{5-[2-({5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-14で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(401mg、1.5mmol)から1-メチルピペリジン-4-イル N-{5-[2-({5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(322mg)を得た。
LC/MS:M+1=632.3
[参考例15-15]
1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}{メチル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(419mg、1.1mmol)と参考例14-15で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-N-メチルアニリン(377mg、1.5mmol)から1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}{メチル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(172mg)を得た。
LC/MS:M+1=616.3
[参考例15-16]
1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}チオフェン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(293mg、0.7mmol)と参考例14-16で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]チオフェン-2-アミン(170mg、0.7mmol)から1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}チオフェン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(105.7mg)を得た。
LC/MS:M+1=608.3
[参考例15-17]
1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(209mg、0.5mmol)と参考例14-17で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]ピリジン-2-アミン(179mg、0.75mmol)から1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(120mg)を得た。
LC/MS:M+1=603.3
[参考例15-18]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(173.2mg、0.4mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(181.1mg、0.6mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(108.5mg)を得た。
LC/MS:M+1=680.3
[参考例15-19]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-9で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(203.9mg、0.75mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(192mg)を得た。
LC/MS:M+1=650.3
[参考例15-20]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-6で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリン(200.6mg、0.75mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(172mg)を得た。
LC/MS:M+1=646.3
[参考例15-21]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-10で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(200.6mg、0.75mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(212mg)を得た。
LC/MS:M+1=646.3
[参考例15-22]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-11で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリン(188.6mg、0.75mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(212mg)を得た。
LC/MS:M+1=630.3
[参考例15-23]
1-メチルピペリジン-4-イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-12で得られた6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(215.6mg、0.75mmol)から1-メチルピペリジン-4-イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(214mg)を得た。
LC/MS:M+1=666.3
[参考例15-24]
1-メチルピペリジン-4-イル N-(5-{3-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-17で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]ピリジン-2-アミン(179mg、0.75mmol)から1-メチルピペリジン-4-イル N-(5-{3-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(175mg)を得た。
LC/MS:M+1=617.3
[参考例15-25]
1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(303mg、0.7mmol)と参考例14-18で得られた2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシアニリン(363mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(124mg)を得た。
LC/MS:M+1=726.2
[参考例15-26]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-19で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシアニリン(316mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(53mg)を得た。
LC/MS:M+1=694.4
[参考例15-27]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(217mg、0.50mmol)と参考例14-20で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシアニリン(106mg、0.38mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(145mg)を得た。
LC/MS:M+1=660.4
[参考例15-28]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-4で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロアニリン(255mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(173mg)を得た。
LC/MS:M+1=634.3
[参考例15-29]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-3で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロアニリン(272mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(157mg)を得た。
LC/MS:M+1=650.3
[参考例15-30]
1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216mg、0.5mmol)と参考例14-21で得られた2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(316mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(110mg)を得た。
LC/MS:M+1=696.3
[参考例15-31]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(216.5mg、0.5mmol)と参考例14-22で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)アニリン(305mg、1.0mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(172mg)を得た。
LC/MS:M+1=684.3
[参考例15-32]
1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸(161mg、0.4mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(142mg、0.6mmol)から1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(122mg)を得た。
LC/MS:M+1=616.3
[参考例15-33]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(161mg、0.4mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(142mg、0.6mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(122mg)を得た。
LC/MS:M+1=656.3
[参考例15-34]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(173mg、0.40mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(181.1mg、0.6mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(108.5mg)を得た。
LC/MS:M+1=720.3
[参考例15-35]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(218mg、0.5mmol)と参考例14-12で得られた6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(287mg、1.0mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(181mg)を得た。
LC/MS:M+1=706.3
[参考例15-36]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(218mg、0.5mmol)と参考例14-6で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリン(266.6mg、1.0mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(251mg)を得た。
LC/MS:M+1=686.3
[参考例15-37]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(218mg、0.5mmol)と参考例14-9で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(270mg、1.0mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(161mg)を得た。
LC/MS:M+1=690.3
[参考例15-38]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(218mg、0.5mmol)と参考例14-10で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(267mg、1.0mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(311mg)を得た。
LC/MS:M+1=686.3
[参考例15-39](1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(218mg、0.5mmol)と参考例14-10で得られた5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリン(250mg、1.0mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(149mg)を得た。
LC/MS:M+1=670.3
[参考例15-40]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(382mg、1.0mmol)と参考例14-12で得られた6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(250mg、0.87mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(311mg)を得た。
LC/MS:M+1=692.3
[参考例15-41]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(230mg、0.5mmol)と参考例14-10で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシアニリン(200mg、0.75mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(281mg)を得た。
LC/MS:M+1=672
[参考例15-42]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(230mg、0.5mmol)と参考例14-6で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシアニリン(200mg、0.75mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(239mg)を得た。
LC/MS:M+1=672.3
[参考例15-43]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(206mg、0.45mmol)と参考例14-11で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルアニリン(170mg、0.68mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(296mg)を得た。
LC/MS:M+1=656.3
[参考例15-44]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(165mg、0.36mmol)と参考例14-9で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(294mg、1.08mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(96mg)を得た。
LC/MS:M+1=676.2
[参考例15-45]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(156mg、0.34mmol)と参考例14-3で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロ-アニリン(137mg、0.51mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(156mg)を得た。
LC/MS:M+1=676.2
[参考例15-46]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(138mg、0.3mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(151mg、0.5mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(52mg)を得た。
LC/MS:M+1=706.3
[参考例15-47]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(174mg、0.38mmol)と参考例14-20で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシアニリン(160mg、0.57mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(216mg)を得た。
LC/MS:M+1=687.3
[参考例15-48]
(1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例21-3で得られた4-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)酪酸(173mg、0.40mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(181.1mg、0.60mmol)から1R,3R)-8-メチル-8-アザビシクロ[3.2.1]オクタン-3-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(108.5mg)を得た。
LC/MS:M+1=720.3
[参考例15-49]
1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例21-4で得られた5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸(205mg、0.50mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(237mg、1.00mmol)から1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(137mg)を得た。
LC/MS:M+1=630.3
[参考例15-50]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例21-5で得られた5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸(225mg、0.50mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(237mg、1.00mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(64mg)を得た。
LC/MS:M+1=670.3
[参考例15-51]
1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例21-4で得られた5-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]吉草酸(205mg、0.50mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(181.1mg、0.60mmol)から1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(60.5mg)を得た。
LC/MS:M+1=694.3
[参考例15-52]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例21-5で得られた5-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)吉草酸(225mg、0.50mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(181.1mg、0.60mmol)から、(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(76.5mg)を得た。
LC/MS:M+1=734.3
[参考例24]
2-フェニル-N-アセチルアニリンの合成
2-フェニルアニリン(5g、29.55mmol)を酢酸(30mL)に溶解させ、氷浴下、無水酢酸(3.62g、35.45mmol)を加え、氷浴下で2時間撹拌した。溶液を減圧濃縮し残渣に水(15mL)を加え、室温で3時間撹拌した。析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、2-フェニル-N-アセチルアニリン(6.21 g)を得た。
1H-NMR(400MHz,CDCl3) δ 8.27(d,J=8.0Hz,1H)、7.12-7.51(m,8H)、2.02(s,3H)
[参考例25]
2-フェニル-4-ブロモ-N-アセチルアニリンの合成
2-フェニル-N-アセチルアニリン(6.21g、29.40mmol)を酢酸(70mL)に溶解させ、氷浴下、別途調整した、四塩化炭素(19.21mL)に溶解させた臭化水素(6.14g、38.42mmol)を滴下し、室温で終夜撹拌した。溶液を減圧濃縮し、残渣に水(20mL)加え、続いてエタノール(30mL)を加えて、氷浴下1時間撹拌した。析出物をろ取、エタノール/水=1:1で洗浄し、減圧下にて乾燥して、2-フェニル-4-ブロモ-N-アセチルアニリン(7.79g)を得た。
1H-NMR(400MHz,CDCl3) δ 8.22(d,J=8.8 Hz,1H)、7.44-7.52(m,4H)、7.34-7.38(m,3H)、2.01(s,3H)
[参考例26]
2-フェニル-4-ブロモアニリンの合成
2-フェニル-4-ブロモ-N-アセチルアニリン(7.79g、26.85mmol)をエタノール(100mL)に溶解させ、氷浴下、2N塩酸(33.56mmol、67.12mL)を滴下し、一晩加熱還流した。溶液を減圧濃縮して酢酸エチル(50mL)と水(40mL)で抽出し、硫酸ナトリウムで乾燥、ろ過させた後、減圧濃縮した。残渣をシリカゲルカラムにて精製し2-フェニル-4-ブロモアニリン(6.58g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.40-7.47(m,4H)、7.36-7.39(m,1H)、7.22-7.24(m,2H)、6.65(dd,J=6.6Hz,2.4 Hz,1H)、3.76(bs,1H)
[参考例27]
4-(4-アミノ-3-フェニルフェニル)-3-ブテン酸tertブチルの合成
2-フェニル-4-ブロモアニリン(564.7mg、2.28mmol)をN,N-ジメチルホルムアミド(25mL)に溶解させ、室温でtert-ブチル-3-ブテノエート(582.5mg、4.10mmol)、トリ-(o-トリル)ホスフィン(1.87 g、6.16mmol)、ジイソプロピルエチルアミン(0.78mL,4.56mmol)を加え脱気し、酢酸パラジウム(67.4mg、0.30mmol)を加え再び脱気した。90℃にて終夜撹拌した後、セライトにてろ過し酢酸エチル(120mL)で洗浄した。有機層を飽和食塩水(50mL)で洗浄した後、硫酸ナトリウムで乾燥、ろ過、減圧濃縮した。残渣をシリカゲルカラムにて精製し、4-(4-アミノ-3-フェニルフェニル)-3-ブテン酸tertブチル(555.8mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.45(d,J=4.4Hz,1H)7.33-7.38(m,1H)7.18(dt,J=12.5Hz,4.5Hz,2H)6.71(d,J=8.3Hz,1H)6.38(d,J=15.9Hz,1H)6.05-6.14(m,1H)3.79(bs,1H)3.12(dd,J=7.2Hz,1.3Hz,1H)、1.46(s,9H)
[参考例11-2]
4-(4-アミノ-3-フェニルフェニル)酪酸tertブチルの合成
参考例11に従い、4-(4-アミノ-3-フェニルフェニル)-3-ブテン酸tertブチル(555.8mg、1.80mmol)から4-(4-アミノ-3-フェニルフェニル)酪酸tertブチル(450.1mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.44-7.47(m,4H)7.30-7.38(m,1H)6.94-7.00(m,2H)6.71(d,J=8.0Hz,1H)2.56(t,J=7.6Hz,2H)2.24(t,J=7.6Hz,2H)1.84-1.92(m,2H)1.44(s,9H)
[参考例12-3]4-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸tertブチルの合成
参考例12に従い、4-(4-アミノ-3-フェニルフェニル)酪酸tertブチル(158.2mg、0.51mmol)から4-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸tertブチル(224.7mg)を得た。
LC/MS:M+1=453.2
[参考例12-4]
4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸tertブチルの合成
参考例12に従い、スコピン(118.3mg、0.76mmol)と4-(4-アミノ-3-フェニルフェニル)酪酸tertブチル(158.2mg、0.51mmol)から4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸tertブチル(181.2mg、0.37mmol)を得た。
LC/MS:M+1=493.2
[参考例13-3]
4-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸塩酸塩の合成
参考例13に従い、4-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸tertブチル(224.7mg、0.50mmol)から4-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸塩酸塩を得た。
LC/MS:M+1=397.1
[参考例13-4]
4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩の合成
参考例13に従い、4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸tertブチル(181.2mg、0.37mmol)から4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩を得た。
LC/MS:M+1=437.1
[参考例15-53]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.37mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(66.5mg、0.28mmol)から、(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(70.1mg)を得た。
LC/MS:M+1=656.3
[参考例15-54]
1-メチルピペリジン-4-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-3で得られた4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]酪酸(161mg、0.4mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(90.2mg、0.38mmol)から1-メチルピペリジン-4-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(88.2mg)を得た。
LC/MS:M+1=616.3
[参考例15-55]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.75mmol)と参考例14-2で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシアニリン(339.6mg、1.13mmol)から、((1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(201.2mg)を得た。
LC/MS:M+1=720.2
[参考例15-56]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(4-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.23mmol)と参考例14-12で得られた6-[(tert-ブチルジメチルシラノイルオキシ)メチル]ナフタレン-2-アミン(99.2mg、0.35mmol)から(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(4-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートを得た。
LC/MS:M+1=706.2
[参考例12-5]
3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸tertブチルの合成
参考例12に従い、参考例22で得た1-(2-フェノキシエチル)ピペリジン-4-オール(712mg、3.22mmol)と3-(3-アミノ-4-フェニルフェニル)プロピオン酸tertブチル(239mg、0.80mmol)から3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸tertブチル(471mg)を得た。
LC/MS:M+1=545.3
[参考例13-5]
3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸塩酸塩の合成
参考例13に従い、参考例12-5で得た3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸tertブチル(471mg、0.86mmol)から3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸塩酸塩(422mg)を得た。
LC/MS:M+1=489.3
[参考例15-57]
1-(2-フェノキシエチル)ピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-5で得た3-{3-[({[1-(2-フェノキシエチル)ピペリジン-4-イル]オキシ}カルボニル)アミノ]-4-フェニルフェニル}プロピオン酸塩酸塩(227,1mg、0.43mmol)から1-(2-フェノキシエチル)ピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(237mg)を得た。
LC/MS:M+1=708.3
[参考例28]
4-メトキシ-2-ニトロ-1-フェニルベンゼンの合成
1-ブロモ-4-メトキシ-2-ニトロベンゼン(2.32g、10mmol)を1,4-ジオキサン(30mL)に溶解し、フェニルホウ酸(2.44g、20mmol)、炭酸セシウム(26g、80mmol)、1,1-[ビス(ジフェニルフォスフィノ)フェロセン]ジクロロパラジウム(II)ジクロロメタン錯体(0.82g、1mmol)、精製水(12mL)を加え、窒素気流下80℃で18時間攪拌した。反応溶液をセライト、アルミナ、フローリジルでろ過後、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、4-メトキシ-2-ニトロ-1-フェニルベンゼン(1.86g)を得た。
[参考例29]
3-ニトロ-4-フェニルフェノールの合成
4-メトキシ-2-ニトロ-1-フェニルベンゼン(1.86g、8.31mmol)をジクロロメタン(40mL)に溶解させ、氷水冷却下、三臭化ホウ素(2mL)のジクロロメタン(10mL)溶液を加えた。室温で18時間攪拌した後、反応溶液を氷にあけて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮し、3-ニトロ-4-フェニルフェノールを粗体として得た。
[参考例30]
8-(3-ニトロ-4-フェニルフェノキシ)オクタン-1-オールの合成
3-ニトロ-4-フェニルフェノール(860mg、4.0mmol)をN,N-ジメチルホルムアミド(40mL)に溶解させ、8-ブロモ-1-オクタノール(1.86g、6.0mmol)を加えた。50℃で5時間攪拌した後、反応溶液を酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、8-(3-ニトロ-4-フェニルフェノキシ)オクタン-1-オール(1.23g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.34-7.44(m,5H),7.26-7.33(m,2H),7.13(dd,J=8.5Hz,2.4Hz,1H),4.03(t,J=6.5Hz,2H),3.65(t,J=6.5Hz,2H),1.78-1.87(m,2H),1.44-1.65(m,4H),1.31-1.42(m,6H)
[参考例31]
tert-ブチルジメチル{[8-(3-ニトロ-4-フェニルフェノキシ)オクチル]オキシ}シランの合成
8-(3-ニトロ-4-フェニルフェノキシ)オクタン-1-オール(1.23g、3.5mmol)とイミダゾール(408mg、6.0mmol)をテトラヒドロフラン(15mL)に溶解させ、tert-ブチルジメチルクロロシラン(750mg、5.0mmol)のテトラヒドロフラン(5mL)溶液を加えた。室温で18時間攪拌した後、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化アンモニウム水溶液、飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチルジメチル{[8-(3-ニトロ-4-フェニルフェノキシ)オクチル]オキシ}シラン(1.38g)を得た。
1H-NMR(400MHz,CDCl3) δ 7.32-7.44(m,5H),7.26-7.30(m,2H),7.13(dd,J=8.5Hz,2.7Hz,1H),4.03(t,J=6.5 Hz,2H),3.61(t,J=6.5 Hz,2H),1.78-1.87(m,2H),1.44-1.65(m,4H),1.31-1.42(m,6H),0.90(s,9H),0.05(s,6H)
[参考例32]
5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルアニリンの合成
{[8-(3-ニトロ-4-フェニルフェノキシ)オクチル]オキシ}シラン(1.38g、3.02mmol)をメタノール(20mL)に溶解し、10%パラジウム炭素(50mg)を加え、水素雰囲気下室温で2時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルアニリンを粗体として得た。
LC/MS:M+1=428.3
[参考例32-2]
5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルアニリンの合成
参考例30、31、32に従い、6-ブロモ-1-ヘキサノール(543mg、3.0mmol)と3-ニトロ-4-フェニルフェノール(430mg、2.0mmol)から、5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルアニリンを得た。
LC/MS:M+1=316.3
[参考例32-3]
5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルアニリンの合成
参考例30、31、32に従い、9-ブロモ-1-ノナノール(669mg、3.0mmol)と3-ニトロ-4-フェニルフェノール(430mg、2.0mmol)から、5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルアニリンを得た。
LC/MS:M+1=358.3
[参考例12-6]
1-メチルピペリジン-4-イル N-(5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルフェニル)カルバメートの合成
参考例12に従い、1-メチルピペリジノール(1.15g、10mmol)と参考例32で得られた5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルアニリン(777mg、1.82mmol)から、1-メチルピペリジン-4-イル N-(5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルフェニル)カルバメート(283mg)を得た。
LC/MS:M+1=589.3
[参考例12-7]
1-メチルピペリジン-4-イル N-(5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルフェニル)カルバメートの合成
参考例12に従い、1-メチルピペリジノール(865mg、7.5mmol)と参考例32-2で得られた5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルアニリンから、1-メチルピペリジン-4-イル N-(5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルフェニル)カルバメート(626mg)を得た。
LC/MS:M+1=540.3
[参考例12-8]
1-メチルピペリジン-4-イル N-(5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルフェニル)カルバメートの合成
参考例12に従い、1-メチルピペリジノール(865mg、7.5mmol)と参考例32-3で得られた5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルアニリンから、1-メチルピペリジン-4-イル N-(5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルフェニル)カルバメート(408mg)を得た。
LC/MS:M+1=583.3
[参考例33]
3-ブロモ-5-フェニルアニリンの合成
4-ブロモ-2-ニトロ-1-フェニルベンゼン(1.15g、4.1mmol)を酢酸エチル(10mL)とエタノール(10mL)に溶解し、塩化スズ(2.85g、15mmol)を加え、80℃で18時間攪拌した。反応溶液を室温に戻し、飽和炭酸水素ナトリウム水溶液で中和した後、セライト、アルミナ、フローリジルでろ過し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、3-ブロモ-5-フェニルアニリン(533mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.32-7.46(m,5H),6,90-6.97(m,3H),3.65-3.85(broad,2H)
[参考例34]
[4-(2-プロペノイルオキシ)フェニル]メタノールの合成
4-(ヒドロキシメチル)フェノール(620mg、5.0mmol)をN,N-ジメチルホルムアミド(25mL)に溶解させ、炭酸カリウム(1.38g、10.0mmol)、4-ブロモ-1-ブテン(1.08g、8.0mmol)を加えた。70℃で4時間攪拌した後、反応溶液を酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、[4-(2-プロペノイルオキシ)フェニル]メタノール(267mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.26-7.30(m,2H),6.86-6.92(m,2H),5.85-5.95(m,1H),5.09-5,20(m,2H),4.61(s,2H),4.02(t,J=6.8Hz,2H),2.50-2.58(m,2H)
[参考例35]
(4-[{(3E)-4-(3-アミノ-4-フェニルフェニル)-3-ブテン-1-イル}オキシ] フェニル)メタノールの合成
参考例33で得た3-ブロモ-5-フェニルアニリン(248mg、1.0mmol)をN,N-ジメチルホルムアミド(10mL)に溶解させ、参考例34で得た[4-(2-プロペノイルオキシ)フェニル]メタノール(267mg、1.5mmol)、トリ-(o-トリル)ホスフィン(913mg、3.0mmol)、ジイソプロピルエチルアミン(258mg、2.0mmol)、酢酸パラジウム(45mg、0.2mmol)を加え、120℃にて18時間撹拌した。反応溶液を酢酸エチルで希釈した後、セライトにてろ過し、有機層を飽和食塩水で洗浄、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、(4-[{(3E)-4-(3-アミノ-4-フェニルフェニル)-3-ブテン-1-イル}オキシ]フェニル)メタノール(268mg)を得た。
[参考例36]
[4-{4-(3-アミノ-4-フェニルフェニル)ブトキシ}フェニル]メタノールの合成
参考例35で得た(4-[{(3E)-4-(3-アミノ-4-フェニルフェニル)-3-ブテン-1-イル}オキシ]フェニル)メタノール(268mg、0.78mmol)をメタノール(5mL)に溶解し、10%パラジウム炭素(10mg)を加え、水素雰囲気下室温で3時間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、[4-{4-(3-アミノ-4-フェニルフェニル)ブトキシ}フェニル]メタノールを粗体として得た。
[参考例37]
5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルアニリンの合成
参考例35で得た[4-{4-(3-アミノ-4-フェニルフェニル)ブトキシ}フェニル]メタノールとイミダゾール(170mg、2.5mmol)をテトラヒドロフラン(15mL)に溶解させ、tert-ブチルジメチルクロロシラン(300mg、2.0mmol)のテトラヒドロフラン(5mL)溶液を加えた。室温で1時間攪拌した後、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルアニリン(260mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.40-7.46(m,4H),7.30-7.34(m,1H),7.19-7.23(m,2H),7.85(d,J=7.8Hz,1H),6.83-6.88(m,2H),6.66-6.69(m,1H),6.61(s,1H),4,67(s,2H),3.94-4.01(m,2H),2.63(t,J=7.2Hz,2H),1.75-1.89(m,4H),0.92(s,9H),0.08(s,6H)
[参考例12-9]
1-メチルピペリジン-4-イル N-[5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルフェニル]カルバメートの合成
参考例12に従い、1-メチルピペリジノール(144mg、1.25mmol)と参考例37で得られた5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルアニリン(115mg、0.25mmol)から、1-メチルピペリジン-4-イル N-[5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルフェニル]カルバメート(129mg)を得た。
LC/MS:M+1=603.3
[参考例14-23]
4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]アニリンの合成
参考例23、及び、参考例14に従い、3-(4-アミノフェニル)プロピオン酸(991mg、6mmol)から4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]アニリン(1.31g)を得た。
LC/MS:M+1=266.3
[参考例15-58]
1-メチルピペリジン-4-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(191mg、0.5mmol)と参考例14-23で得られた4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]アニリンから、1-メチルピペリジン-4-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメート(155mg)を得た。
LC/MS:M+1=630.3
[参考例14-24]
4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]アニリンの合成
参考例23、及び参考例14に従い、2-(4-アミノフェニル)エチルアルコール(1.37g、10mmol)から4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]アニリン(2.25g)を得た。
LC/MS:M+1=252.3
[参考例15-59]
1-メチルピペリジン-4-イル N-{5-[2-({4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(76mg、0.2mmol)と参考例14-24で得られた4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]アニリンから、1-メチルピペリジン-4-イル N-{5-[2-({4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメート(188mg)を得た。
LC/MS:M+1=616.3
[参考例38]
2-(3-ニトロ-4-フェニルフェノキシ)酢酸tert-ブチルの合成
3-ニトロ-4-フェニルフェノール(215mg、1.0mmol)をN,N-ジメチルホルムアミド(5mL)に溶解させ、2-ブロモ酢酸tert-ブチル(292mg、1.5mmol)を加えた。80℃で18時間攪拌した後、反応溶液を酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、2-(3-ニトロ-4-フェニルフェノキシ)酢酸tert-ブチル(370mg)を得た。
[参考例39]
2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸tertブチルの合成
参考例11、12に従い、参考例38で得られた2-(3-ニトロ-4-フェニルフェノキシ)酢酸tert-ブチル(329mg、1.0mmol)から、2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸tertブチル(531mg)を得た。
[参考例13-6]
2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸塩酸塩の合成
参考例13に従い、参考例39で得た2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸tertブチル(531mg、1.2mmol)から、2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸塩酸塩(509mg)を得た。
LC/MS:M+1=384.3
[参考例15-60]
4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル 2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]アセテートの合成
参考例15に従い、参考例13-6で得られた2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェノキシ]酢酸塩酸塩(210mg、0.5mmol)と参考例14で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(237mg、1.0mmol)から4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル 2-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]アセテート(28mg)を得た。
LC/MS:M+1=603.3
[参考例15-61]
1-メチルピペリジン-4-イル N-(5-{2-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]エチル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(50mg、0.12mmol)と1-(N-Boc-アミノメチル)-4-(アミノメチル)ベンゼン(94mg、0.4mmol)から、1-メチルピペリジン-4-イル N-(5-{2-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(94mg)を得た。
LC/MS:M+1=601.3
[参考例4-2]
5-アセチル-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン- 2-オンの合成
5-アセチル-8-ヒドロキシ-1H-キノリン-2-オン(29.5g、0.15mol)を、N,N-ジメチルホルムアミド(145mL)に懸濁し、炭酸カリウム(22.2g、0.16mol)を加え、続いて、4-メトキシベンジルクロライド(22.7g、0.15mol)を加え、90℃で一晩攪拌した。反応液に精製水(0.5L)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄し、減圧下にて乾燥して、5-アセチル-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オン(26.1g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 10.90(s,1H),8.67(dJ=8.0Hz,1H),7.78(d,J=8.0Hz,1H),7.51(d,J=8.0Hz,2H),7.27(d,J=8.0Hz,1H),6.92(d,J=8.0Hz,2H),6.62(d,J=8.0Hz,1H),5.32(s,2H)3.73(s,3H)
[参考例5-2]
5-(2-ブロモアセチル)-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オンの合成
5-アセチル-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オン(1.25g、3.87mmol)をテトラヒドロフラン(10mL)に溶解し、そして0℃まで冷却した。三臭化ピリジニウム(1.51g、4.25mmol)を分割投入し、一晩加熱還流した。析出物をろ取、テトラヒドロフランで洗浄した。ろ液を減圧濃縮した後、精製水(20mL)で懸濁洗浄した。析出物をろ取、精製水で洗浄した。酢酸エチル(20mL)で懸濁洗浄し、ろ取、減圧下にて乾燥して、5-(2-ブロモアセチル)-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オン(515mg)を得た。
1H-NMR(400MHz,DMSO-d6) δ 11.00(s,1H),8.49(d,J=8.0Hz,1H),7.85(d,J=8.0Hz,1H),7.52(d,J=8.0Hz,2H),7.30(d,J=8.0Hz,1H),6.93(d,J=8.0Hz,2H),6.56(d,J=8.0Hz,1H),5.34(s,2H),4.91(s,2H),3.73(s,2H)
[参考例6-2]
5-[(1R)-2-ブロモ-1-ヒドロキシエチル]-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オンの合成
アルゴン気流下、5-(2-ブロモアセチル)-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オン(7.15g、17.8mmol)を脱水テトラヒドロフラン(40mL)に懸濁し、CBS触媒(493mg)を加え、-20℃で40分間攪拌した。1.0M ボラン-テトラヒドロフラン錯体テトラヒドロフラン溶液(21.4mL)を同温度下で滴下した後、徐々に0℃まで昇温した。メタノール(20mL)を滴下した後、不溶物をろ去し、テトラヒドロフランで洗浄した。ろ液と洗浄液を混合し、減圧濃縮した。残渣に精製水(100mL)を加え、室温で一晩攪拌した。析出物をろ取、精製水で洗浄した。さらに、酢酸エチル(200mL)で懸濁洗浄し、ろ取、減圧下にて乾燥して、5-[(1R)-2-ブロモ-1-ヒドロキシエチル]-8-[(4-メトキシフェニル)メトキシ]-1,2-ジヒドロキノリン-2-オン(3.06g)を得た。
1H-NMR(400MHz,DMSO-d6) δ 10.60(s,1H),8.17(dJ=8.0Hz,1H),7.49(d,J=8.0Hz,2H),7.20(d,J=8.0Hz,1H),6.92(d,J=8.0Hz,2H),6.54(d,J=8.0Hz,1H),5.93(d,J=8.0Hz,1H)5.18-5.24(m,3H),3.67(dd,J=12.0Hz,8.0Hz,1H),3.60(dd,J=12.0Hz,8.0Hz,1H)
[参考例15-62]
1-メチルピペリジン-4-イル N-(5-{3-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例15に従い、4-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]酪酸塩酸塩(86mg、0.2mmol)と1-(N-Boc-アミノメチル)-4-(アミノメチル)ベンゼン(118mg、0.5mmol)から、1-メチルピペリジン-4-イル N-(5-{3-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(86mg)を得た。
LC/MS:M+1=615.3
[参考例40]
trans-3-(3-アミノ-4-フェニルフェニル)アクリル酸tertブチルの合成
参考例10で得られたtrans-3-(3-ニトロ-4-フェニルフェニル)アクリル酸tertブチル(325mg、1.0mmol)をテトラヒドロフラン(15mL)に溶解し、水冷下亜鉛末(196mg、3.0mmol)と酢酸(0.2mL)を加え、室温で3時間攪拌した。反応溶液を酢酸エチルで希釈した後、飽和炭酸水素ナトリウム水溶液で中和し、セライトろ過した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥、減圧濃縮し、trans-3-(3-アミノ-4-フェニルフェニル)アクリル酸tertブチルを粗体として得た。
LC/MS:M+1=296.3
[参考例12-10]
(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸tertブチルの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(172mg、1.5mmol)と参考例40で得られたtrans-3-(3-アミノ-4-フェニルフェニル)アクリル酸tertブチル(150mg、0.5mmol)から、(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸tertブチル(117mg)を得た。
LC/MS:M+1=437.3
[参考例13-7]
(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸塩酸塩の合成
参考例13に従い、参考例39で得た(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸tertブチル(117mg、0.27mmol)から、(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸塩酸塩(112mg)を得た。
LC/MS:M+1=381.3
[参考例15-63]
1-メチルピペリジン-4-イル N-{5-[(1E)-2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)-1-エテン-1-イル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-7で得た(2E)-3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]-2-プロペン酸塩酸塩(112mg、0.27mmol)と4-[(tert-ブチルジメチルシラノイルオキシ)メチル]アニリン(1.0mmol)から、1-メチルピペリジン-4-イル N-{5-[(1E)-2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)-1-エテン-1-イル]-2-フェニルフェニル}カルバメート(57mg)を得た。
LC/MS:M+1=600.3
[参考例41]
1-(2-メチル-2-ニトロプロピル)-4-ニトロベンゼンの合成
ナトリウムエトキシド(3.5g、50mmol)のエタノール(100mL)溶液に、室温で1-(クロロメチル)-4-ニトロベンゼン(8.6g、50mmol)と2-ニトロプロパン(2.2g、250mmol)を加え、18時間加熱還流した。反応溶液をろ過、減圧濃縮し、酢酸エチルで希釈した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、1-(2-メチル-2-ニトロプロピル)-4-ニトロベンゼン(8.52g)を得た。
1H-NMR(400MHz,CDCl3) δ 8.17(d,J=8.5Hz,2H),7.29(d,J=8.5Hz,2H),3.32(s,2H),1.59(s,6H)
[参考例42]
4-(2-メチル-2-ニトロプロピル)アニリンの合成
参考例41で得た1-(2-メチル-2-ニトロプロピル)-4-ニトロベンゼン(673mg、3.0mmol)をメタノール(20mL)に溶解し、触媒量のパラジウム炭素を加え、水素雰囲気下に溶液をおいて6時間攪拌した。反応溶液をセライトろ過し、減圧濃縮し、4-(2-メチル-2-ニトロプロピル)アニリンを粗体として得た。
LC/MS:M+1=195.3
[参考例15-64]
1-メチルピペリジン-4-イル N-[5-(2-{[4-(2-メチル-2-ニトロプロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバメートの合成
参考例15に従い、3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(418mg、1.0mmol)と4-(2-メチル-2-ニトロプロピル)アニリン(582mg、3.0mmol)から、1-メチルピペリジン-4-イル N-[5-(2-{[4-(2-メチル-2-ニトロプロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバメート(193.5mg)を得た。
LC/MS:M+1=559.3
[参考例9-2]
trans-3-(3-ブロモ-4-ニトロフェニル)アクリル酸tertブチルの合成
参考例9に従い、ジエチルホスホノ酢酸tertブチルエステル(920mg、4.0mmol)と3-ブロモ-4-ニトロ-ベンズアルデヒド(1.0g、3.9mmol)から、trans-3-(3-ブロモ-4-ニトロフェニル)アクリル酸tertブチル(777mg)を得た。
1H-NMR(400MHz,CDCl3) δ 8.17(d,J=8.5Hz,1H),7.86(d,J=1.7Hz,1H),7.55(dd,J=8.5Hz,1.7Hz,1H),7.50(d,J=15.9Hz,1H),6.46(d,J=15.9Hz,1H),1.54(s,9H)
[参考例10-2]
trans-3-(4-ニトロ-3-フェニルフェニル)アクリル酸tertブチルの合成
参考例10に従い、参考例9-2で得られたtrans-3-(3-ブロモ-4-ニトロフェニル)アクリル酸tertブチル(777mg、2.37mmol)から、trans-3-(4-ニトロ-3-フェニルフェニル)アクリル酸tertブチル(802mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.88(d,J=8.3Hz,1H),7.55-7.66(m,3H),7.42-7.46(m,3H),7.30-7.36(m,2H),6.48(d,J=15.9Hz,1H),1.54(s,9H)
[参考例11-3]
3-(4-アミノ-3-フェニルフェニル)プロピオン酸tertブチル
参考例11に従い、trans-3-(4-ニトロ-3-フェニルフェニル)アクリル酸tertブチル(802mg、2.5mmol)から、3-(4-アミノ-3-フェニルフェニル)プロピオン酸tertブチル(742mg)を得た。
LC/MS:M+1=298.3
[参考例12-11]
3-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]プロピオン酸tertブチルの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(450mg、15.0mmol)と参考例11-3で得た3-(4-アミノ-3-フェニルフェニル)プロピオン酸tertブチル(742mg、2.5mmol)から、3-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]プロピオン酸tertブチル(878mg)を得た。
1H-NMR(400MHz,CDCl3) δ 7.97(s,1H),7.38-7.49(m,3H),7.34-7.38(m,2H),7.19(dd,J=8.5Hz,2.0Hz,1H),7.06(d,J=2.0Hz,1H),6.54(s,1H),4.70-4.74(m,1H),2.90(t,J=7.8Hz,1H),2.62-2.70(m,2H),2.54(t,J=7.8Hz,1H),2.29(s,3H),2.23-2.30(m,2H),1.92-2.00(m,2H),1.66-1.75(m,2H),1.41(s,9H)
LC/MS:M+1=439.3
[参考例15-65]
1-メチルピペリジン-4-イル N-{4-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例13、15に従い、参考例12-11で得た3-[4-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-3-フェニルフェニル]プロピオン酸tertブチル(219mg、0.5mmol)から、1-メチルピペリジン-4-イル N-{4-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(235mg)を得た。
1H-NMR(400MHz,CDCl3) δ 8.01(s,1H),7.37-7.48(m,5H),7.29-7.32(m,2H),7.21-7.25(m,3H),7.15(s,1H),7.09(d,J=2.0Hz,1H),6.54(s,1H),4.68(s,2H),4.70-4.73(m,1H),3.04(t,J=7.4Hz,1H),2.62-2.66(m,2H),2.64(t,J=7.6Hz,1H),2.26(s,3H),2.16-2.22(m,2H),1.91-1.96(m,2H),1.64-1.74(m,2H),0.93(s,9H),0.09(s,6H)
LC/MS:M+1=602.3
[実施例1]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例15で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(178.1mg、0.296mmol)をテトラヒドロフラン(10mL)に溶解し、そこに三フッ化水素トリエチルアミン錯体(0.3mL)を加え、70℃で1.5時間攪拌した。反応液を酢酸エチルにて抽出し、有機層を希水酸化ナトリウム水溶液、飽和食塩水で洗浄、硫酸ナトリウムにて乾燥後、減圧濃縮した。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),10.14(s,1H),9.07(d,J=50.5Hz,1H),8.75(s,1H),8.05(d,J=10.0Hz,1H),7.63(d,J=8.5Hz,2H),7.44(d,J=8.5Hz,2H),7.27-7.40(m,6H),7.24(d,J=8.0Hz,1H),7.19(d,J=8.0Hz,1H),7.10(d,J=8.0Hz,1H),6.96(d,J=8.0Hz,1H),6.53(d,J=10.0Hz,1H),5.28-5.33(m,1H),4.58-4.66(m,1H),4.12-4.18 (m 2H),3.35-3.43(m,2H),3.25-3.35(m,2H),3.07(s,3H),3.06(s,3H),3.05-3.09(m,2H),2.94(t,J=7.5Hz,2H),2.68(t,J=7.5Hz,2H),1.94-2.04(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=704.3
[実施例2]
4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-2で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(17mg、0.03mmol)から、4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(11.6mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.46(s,1H),9.61(s,1H),8.87(d,J=25.0Hz,1H), 8.74(s,1H),8.09(d,J=10.0Hz 1H),7.58(s,1H),7.57(s,1H),7.29-7.44(m,6H),7.16-7.29(m,2H),7.13(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.56(d,J=10.0Hz,1H),5.32-5.37(m,1H),4.57-4.66(m,1H),4.12-4.18(m,2H),3.80(s,3H),3.35-3.43(m,2H),3.25-3.35(m,2H),3.04-3.09(m,2H),3.07(s,3H),3.06(s,3H),2.95(t,J=7.7Hz,2H),2.79(t,J=7.7Hz,2H),1.95-2.04(m,2H),1.69-1.81(m,2H)
LC/MS:[M]+=768.3
[実施例3]
4-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-3で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(64.2mg、0.12mmol)から、4-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(10.6mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.32(s,1H),9.12-9.02(broad,1H),8.72(s,1H),8.10(d,J=10.0Hz,1H),7.91(d,J=2.0Hz,1H),7.58(d,J=8.5Hz,1H),7.51(dd,J=8.5Hz,2.0Hz,1H),7.28-7.44(m,5H),7.25(d,J=7,8 Hz,1H),7.19(d,J=7,8Hz,1H),7.13(d,J=8.3 Hz,1H),6.97(d,J=8.3 Hz,1H),6.55(d,J=10.0 Hz,1H),5.32-5.38(m,1H),4.57-4.66(m,1H),4.22-4.40(m,2H),3.34-3.42(m,2H),3.26-3.34(m,2H),3.06-3.14(m,2H),3.07(s,3H),3.06(s,3H),2.94(t,J=7.7Hz,2H),2.70(t,J=7.7Hz,2H),1.95-2.05(m,2H),1.68-1.81(m,2H)
LC/MS:[M]+=738.2
[実施例4]
4-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-4で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(104mg、0.20mmol)から、4-({[5-(2-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(29.4mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),9.89(s,1H),9.11(d,J=33.4Hz,1H),8.73(s,1H),8.07(d,J=10.0Hz,1H),7.94-8.00(m,1H),7.28-7.46(m,6H),7.31(d,J=8.0Hz,1H),7.20(d,J=8.0Hz,1H),7.11(d,J=8.0Hz,1H),6.96(d,J=8.0Hz,1H),6.55(d,J=10.0Hz,1H),5.30-5.35(m,1H),4.58-4.66(m,1H),4.18-4.25(m,2H),3.34-3.42(m,2H),3.26-3.34(m,2H),3.03-3.08(m,2H),3.07(s,3H),3.06(s,3H),2.93(t,J=7.7 Hz,2H),2.75(t,J=7.7Hz,2H),1.95-2.05(m,2H),1.68-1.81(m,2H)
LC/MS:[M]+=722.3
[実施例5]
4-({[5-(2-{[2,5-ジフルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-5で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2,5-ジフルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(44.7mg、0.07mmol)から、4-({[5-(2-{[2,5-ジフルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(16.8mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.10(s,1H),9.02-9.18(broad,1H),8.72(s,1H),8.12(d,J=10.0Hz,1H),8.01(dd,J=11.6Hz,6.7Hz,1H),7.54(dd,J=11.6Hz,6.7Hz,1H),7.27-7.44(m,6H),7.18-7.27(m,2H),7.13(d,J=8.0Hz,1H),6.97(d,J=8.0Hz,1H),6.56(d,J=10.0Hz,1H),5.31-5.36(m,1H),4.58-4.65(m,1H),4.18-4.26 (m 2H),3.35-3.43(m,2H),3.26-3.35(m,2H),3.07-3.15(m,2H),3.07(s,3H),3.06(s,3H),2.93(t,J=7.4Hz,2H),2.79(t,J=7.4Hz,2H),1.93-2.04(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=740.3
[実施例6]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-6で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(74.3mg、0.14mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(19.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.14(s,1H),8.72(s,1H),8.60-8.80(broad,1H),8.04(d,J=10.0Hz,1H),7.14-7.48(m,11H),7.11(d,J=8.3 Hz,1H),6.96(d,J=8.3Hz,1H),6.55(d,J=10.0 Hz,1H),5.28-5.34(m,1H),4.58-4.64(m,1H),4.12-4.22(m,2H),3.34-3.43(m,2H),3.26-3.34(m,2H),3.79(s,3H),3.07(s,3H),3.06(s,3H),2.97-3.02(m,2H),2.94(t,J=7.6Hz,2H),2.68(t,J=7.6Hz,2H),1.92-2.04(m,2H),1.68-1.80(m,2H)
LC/MS:[M]+=734.3
[実施例7]
4-({[5-(2-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-7で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-フルオロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(155.6mg、0.30mmol)から、4-({[5-(2-{[3-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(27.2mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),10.38(s,1H),9.13(d,J=48.8 Hz,1H),8.75(s,1H),8.11(d,J=9.8Hz,1H),7.64-7.71(m,1H),7.52(t,J=8.5Hz,1H),7.28-7.44(m,5H),7.24(d,J=8.0Hz,1H),7.19(dd,J=8.0Hz,1.5Hz,1H),7.12(d,J=8.3Hz,1H),6.98(d,J=8.3Hz,1H),6.54(d,J=9.8Hz,1H),5.30-5.37(m,1H),4.58-4.64(m,1H),4.18-4.29(m,2H),3.34-3.43(m,2H),3.26-3.34(m,2H),3.03-3.08(m,2H),3.07(s,3H),3.06(s,3H),2.94(t,J=7.6Hz,2H),2.70(t,J=7.6Hz,2H),1.95-2.04(m,2H),1.68-1.80(m,2H)
LC/MS:[M]+=722.3
[実施例8]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-8で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(102.9mg、0.20mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(7.3mg)を得た。
LC/MS:[M]+=718.3
[実施例9]
4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-9で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(107mg、0.20mmol)から、4-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(27.2mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),9.65(s,1H),8.80-9.18(broad,1H),8.74(s,1H),8.07(d,J=10.0 Hz,1H),7.78(d,J=8.5 Hz,1H),7.69(d,J=2.0Hz,1H),7.45(dd,J=8.5Hz,2.0Hz,1H),7.28-7.45(m,6H),7.18-7.27(m,2H),7.12(d,J=8.3Hz,1H),6.96(d,J=8.3Hz,1H),6.56(d,J=9.8Hz,1H),5.28-5.34(m,1H),4.58-4.66(m,1H),4.16-4.23(m,2H),3.33-3.42(m,2H),3.26-3.33(m,2H),3.07(s,3H),3.06(s,3H),2.90-2.98(m,2H),2.94(t,J=8.0Hz,2H),2.76(t,J=8.0Hz,2H),1.92-2.04(m,2H),1.68-1.80(m,2H)
LC/MS:[M]+=738.2
[実施例10]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-10で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(106.1mg、0.20mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(18.5mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),9.27(s,1H),9.00-9.22(broad,1H),8.74(s,1H),8.06(d,J=9.8Hz,1H),8.01(d,J=7.8 Hz,1H),7.28-7.44(m,6H),7.18-7.27(m,3H),7.11(d,J=8.3Hz,1H),7.01-7.06(m,1H),6.97(d,J=8.3Hz,1H),6.56(d,J=9.8Hz,1H),5.32-5.36(m,1H),4.58-4.66(m,1H),4.16-4.23(m,2H),3.83(s,3H),3.34-3.43(m,2H),3.27-3.34(m,2H),3.07(s,3H),3.06(s,3H),2.90-2.98(m,2H),2.92(t,J=7.6Hz,2H),2.76(t,J=7.6Hz,2H),1.94-2.06(m,2H),1.67-1.80(m,2H)
LC/MS:[M]+=734.3
[実施例11]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-11で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(66.9mg、0.13mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(8.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),9.38(s,1H),8.80-9.20(broad,1H),8.73(s,1H),8.05(d,J=10,0Hz,1H),8.47(d,J=8.0Hz,1H),7.20-7.44(m,10H),7.11(d,J=8.3Hz,1H),6.97(d,J=8.0Hz,1H),6.56(d,J=10,0Hz,1H),5.30-5.33(m,1H),4.58-4.64(m,1H),4.13-4.18(m,2H),3.34-3.42(m,2H),3.26-3.34(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.08(m,2H),2.95(t,J=7.7 Hz,2H),2.71(t,J=7.7Hz,2H),2.16(s,3H),1.94-2.06(m,2H),1.68-1.82(m,2H)
LC/MS:[M]+=718.3
[実施例12]
4-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-12で得られた1-メチルピペリジン-4-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(110.1mg、0.20mmol)から、4-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(8.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.44(s,1H),10.26(s,1H),9.16(d,J=23.7Hz,1H),8.72(s,1H),8.36(s,1H),8.04(d,J=10.0Hz,1H),7.96(s,1H),7.88(d,J=6.0Hz,1H),7.85(d,J=6.0Hz,1H),7.58-7.65(m,2H),7.28-7.44(m,6H),7.19-7.27(m,2H),7.10(d,J=8.3Hz,1H),6.95(d,J=8.0Hz,1H),6.56(d,J=10.0Hz,1H),5.32-5.36(m,1H),4.57-4.66(m,1H),4.33-4.38(m,2H),3.34-3.43(m,2H),3.27-3.34(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.07(m,2H),2.98(t,J=7.7Hz,2H),2.75(t,J=7.7Hz,2H),1.94-2.05(m,2H),1.68-1.80(m,2H)
LC/MS:[M]+=754.3
[実施例13]
4-({[5-(2-{[2-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-1-ベンゾチオフェン-5-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-13で得られた1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}-1-ベンゾチオフェン-5-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(105.8mg、0.19mmol)から、4-({[5-(2-{[2-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-1-ベンゾチオフェン-5-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(13.3mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.46(s,1H),10.12(s,1H),9.22-9.30(broad,1H),8.71(s,1H),8.27(d,J=1.7Hz,1H),8,07(d,J=9.8Hz,1H),7.91(d,J=8.5Hz,1H),7.56(s,1H),7.28-7.44(m,6H),7.19-7.27(m,2H),7.11(d,J=8.3Hz,1H),6.96(d,J=8.0Hz,1H),6.51(d,J=9.8Hz,1H),5.32-5.36(m,1H),4.57-4.62(m,1H),4.51-4.56(m,2H),3.34-3.43(m,2H),3.27-3.34(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.07(m,2H),2.96(t,J=8.2Hz,2H),2.70(t,J=8.2Hz,2H),1.92-2.04(m,2H),1.68-1.81(m,2H)
LC/MS:[M]+=760.3
[実施例14]
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-14で得られた1-メチルピペリジン-4-イル N-{5-[2-({5-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(138.0mg、0.26mmol)から、4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(28.2mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.45(s,1H),9.26(s,1H),8.98(d,J=24.4Hz,1H),8.74(s,1H),8.19(s,1H),8.06(d,J=10.0Hz,1H),7.20-7.44(m,6H),7.18-7.25(m,3H),7.06-7.13(m,2H),6.96(d,J=8.0 Hz,1H),6.56(d,J=10.0Hz,1H),4.98-5.36(m,1H),4.58-4.66(m,1H),4.13-4.18(m,2H),3.84(s,3H),3.34-3.42(m,2H),3.26-3.34(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.08(m,2H),2.92(t,J=7.6 Hz,2H),2.78(t,J=7.6Hz,2H),1.94-2.05(m,2H),1.67-1.81(m,2H)
LC/MS:[M]+=734.3
[実施例15]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル](メチル)カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-15で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}{メチル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(139.0mg、0.27mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル](メチル)カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(45.7mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),9.12(d,J=40.7Hz,1H),8.72(s,1H),8.04(d,J=10.0Hz,1H),7.51(d,J=8.0Hz,2H),7.24-7.38(m,6H),7.07-7.12(m,1H),7.70(d,J=8.0Hz,2H),7.06-7.13(m,2H),6.92(d,J=8.0 Hz,1H),6.49(d,J=10.0Hz,1H),5.27-5.32(m,1H),4.55-4.60(m,1H),4.16-4.22(m,2H),3.33-3.38(m,2H),3.24-3.33(m,2H),3.12(s,3H),3.12-3.15(m,2H),3.03(s,3H),3.02(s,3H),3.00-3.04(m,2H),2.73-2.80(m,2H),1.90-2.00(m,2H),1.65-1.75(m,2H)
LC/MS:[M]+=718.3
[実施例16]
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)チオフェン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-16で得られた1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}チオフェン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(40.5mg、0.08mmol)から、4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)チオフェン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(15.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 11.35(s,1H),10.46(s,1H),9.07(broad,1H),8.71(s,1H),8.02(d,J=10.0Hz,1H),7.25-7.39(m,5H),7.17-7.25(m,2H),7.12-7.16(m,1H),7.06(d,J=8.0Hz,1H),6.97(d,J=3.9Hz,1H),6.92(d,J=8.0Hz,1H),6.52(d,J=3.9Hz,1H),6.51(d,J=10.0Hz,1H),5.23-5.28(m,1H),4.55-4.62(m,1H),4.25-4.33 (m 2H),3.33-3.40(m,2H),3.20-3.33(m,2H),3.03(s,3H),3.02(s,3H),2.95-3.02(m,2H),2.90(t,J=7.6Hz,2H),2.65(t,J=7.6Hz,2H),1.90-2.00(m,2H),1.65-1.75(m,2H)
LC/MS:[M]+=710.2
[実施例17]
4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-17で得られた1-メチルピペリジン-4-イル N-(5-{2-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(90.3mg、0.18mmol)から、4-({[5-(2-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(37.0mg)を得た。
LC/MS:[M]+=705.3
[実施例18]
4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-18で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(10.9mg、0.16mmol)から、4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(45mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),9.60(s,1H),8.94(d,J=58.8Hz,1H),8.76(s,1H),8.09(d,J=10.0Hz,1H),7.56(d,J=15.6Hz,2H),7.25-7.48(m,4H),7.28-7.35(m,1H),7.26(s,1H),7.24(d,J=8.0Hz,1H),7.17(dd,J=8.0Hz,1.5Hz,1H),7.13(d,J=8.0Hz,1H),6.98(d,J=8.0Hz,1H),6.55(d,J=10.0Hz,1H),5.28-5.33(m,1H),4.60-4.65(m,1H),4.24-4.15(m,2H),3.79(s,3H),3.34-3.42(m,2H),3.28-3.38(m,2H),3.07-3.09(m,2H),3.07(s,3H),3.06(s,3H),2.67(t,J=7.6Hz,2H),2.49-2.50(m,2H),1.97-2.06(m,2H),1.90-1.97(m,2H),1.73-1.79(m,2H)
LC/MS:[M]+=782.3
[実施例19]
4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-19で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(164.7mg、0.3mmol)から、4-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(79.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.46(s,1H),9.62(s,1H),9.20(d,J=62.4Hz,1H),8.73(s,1H),8.09(d,J=10.0Hz,1H),7.75(d,J=8.3Hz,1H),7.70(d,J=1.7Hz,1H),7.45(dd,J=8.3Hz,1.7Hz,1H),7.35-7.42(m,4H),7.29-7.34(m,1H),7.26(s,1H),7.25(d,J=8.0Hz,1H),7.17(dd,J=8.0Hz,1.5Hz,1H),7.12(d,J=8.3Hz,1H),6.98(d,J=8.3Hz,1H),6.55(d,J=10,0Hz,1H),5.32-5.37(m,1H),4.59-4.65(m,1H),4.13-4.18(m,2H),3.35-3.42(m,2H),3.28-3.35(m,2H),3.08(s,3H),3.07(s,3H),2.96-3.02(m,2H),2.67(t,J=7.6Hz,2H),2.46(t,J=7.4Hz,2H),1.97-2.06(m,2H),1.88-1.97(m,2H),1.72-1.81(m,2H)
LC/MS:[M]+=752.3
[実施例20]
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-20で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(147.1mg、0.27mmol)から、4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(103.2mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.46(s,1H),10.12(s,1H),8.80(d,J=51.2Hz,1H),8.73(s,1H),8.05(d,J=10.0Hz,1H),7.47(d,J=1.5Hz,1H),7.35-7.44(m,4H),7.29-7.34(m,2H),7.26(s,1H),7.25(d,J=8.0 Hz,1H),7.17(dd,J=8.0Hz,1.5Hz,2H),7.11(d,J=8.0Hz,1H),6.97(d,J=8.0Hz,1H),6.53(d,J=10,0Hz,1H),5.30-5.35(m,1H),4.59-4.65(m,1H),4.09-4.23(m,2H),3.77(s,3H),3.35-3.42(m,2H),3.26-3.35(m,2H),3.08(s,3H),3.07(s,3H),2.96-3.02(m,2H),2.65(t,J=7.6Hz,2H),2.39(t,J=7.4Hz,2H),1.97-2.06(m,2H),1.88-1.96(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=748.2
[実施例21]
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-21で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(179.7mg、0.33mmol)から、4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(218mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),9.20(s,1H),9.24(d,J=95.2Hz,1H),8.75(s,1H),8.09(d,J=10.0Hz,1H),7.99(d,J=8.0Hz,1H),7.36-7.44(m,4H),7.22-7.34(m,4H)7.16(dd,J=7.8Hz,1.3Hz,1H),7.13(d,J=8.0Hz,1H),7.02(dd,J=8.0Hz,1.3Hz,1H),6.99(d,J=8.0Hz,1H),6.52(d,J=10,0Hz,1H),5.32-5.38(m,1H),4.60-4.68(m,1H),4.16-4.22(m,2H),3.84(s,3H),3.37-3.44(m,2H),3.28-3.37(m,2H),3.08(s,3H),3.07(s,3H),2.96-3.04(m,2H),2.65(t,J=7.8Hz,2H),2.47(t,J=7.6Hz,2H),1.96-2.04(m,2H),1.86-1.95(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=748.3
[実施例22]
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-22で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(111mg、0.21mmol)から、4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(72.9mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),9.39(s,1H),9.10(d,J=51.5Hz,1H),8.74(s,1H),8.06(d,J=10.0Hz,1H),7.29-7.48(m,8H),7.26(s,1H),7.25(d,J=8.0Hz,1H),7.17(d,J=8.0Hz,1H),7.11(d,J=8.3Hz,1H),6.97(d,J=8.3,Hz,1H),6.54(d,J=10,0Hz,1H),5.31-5.36(m,1H),4.59-4.66(m,1H),4.13-4.18(m,2H),3.36-3.42(m,2H),3.28-3.36(m,2H),3.08(s,3H),3.07(s,3H),2.92-3.02(m,2H),2.67(t,J=7.6Hz,2H),2.34(t,J=7.4Hz,2H),2.21(s,3H),1.97-2.04(m,2H),1.90-1.97(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=732.2
[実施例23]
4-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-23で得られた1-メチルピペリジン-4-イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(180.7mg、0.32mmol)から、4-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(109mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),10.26(s,1H),9.27(d,J=66.8Hz,1H),8.75(s,1H),8.38(s,1H),8.06(d,J=9.8Hz,1H),7.96(s,1H),7.85(d,J=8.0Hz,2H),7.59-7.66(m,2H),7.36-7.44(m,4H),7.27-7.36(m,2H),7.25(d,J=7.8Hz,1H),7.18(dd,J=7.8Hz,1.3Hz,1H),7.11(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.54(d,J=9,8Hz,1H),5.35-5.39(m,1H),4.58-4.68(m,1H),4.34-4.38(m,2H),3.35-3.43(m,2H),3.27-3.35(m,2H),3.08(s,3H),3.07(s,3H),2.96-3.06(m,2H),2.68(t,J=7.6Hz,2H),2.45(t,J=7.4Hz,2H),2.21(s,3H),1.92-2.05(m,4H),1.70-1.82(m,2H)
LC/MS:[M]+=768.3
[実施例24]
4-({[5-(3-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-24で得られた1-メチルピペリジン-4-イル N-(5-{3-[(5-{[(tert-ブチルジメチルシリル)オキシ]メチル}ピリジン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(139.2mg、0.27mmol)から、4-({[5-(3-{[5-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ピリジン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(101mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.60(s,1H),10.49(s,1H),9.23(d,J=77.8Hz,1H),8.75(s,1H),8.40(d,J=2.2Hz,1H),8.13(d,J=8.3Hz,1H),8.12(d,J=10.0Hz,1H),7.92(dd,J=8.7Hz,2.2Hz,1H),7.29-7.48(m,5H),7.25(s,1H),7.24(d,J=8.0Hz,1H),7.14-7.16(m,1H),7.12(d,J=8.3Hz,1H),6.98(d,J=8.3,Hz,1H),6.54(d,J=10,0Hz,1H),5.33-5.38(m,1H),4.59-4.66(m,1H),4.18-4.24(m,2H),3.36-3.42(m,2H),3.28-3.36(m,2H),3.08(s,3H),3.07(s,3H),2.92-3.02(m,2H),2.64(t,J=7.7Hz,2H),2.47(t,J=7.3Hz,2H),1.96-2.04(m,2H),1.89-1.96(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=719.3
[実施例25]
4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-25で得られた1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(106.2mg、0.17mmol)から、4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(56.2mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),9.53(s,1H),8.90(d,J=38.3Hz,1H),8.75(s,1H),8.08(d,J=10.0Hz,1H),7.73(s,1H),7.29-7.44(m,6H),7.26(s,1H),7.25(d,J=8.0Hz,1H),7.15-7.19(m,1H),7.13(d,J=8.0Hz,1H),6.97(d,J=8.0,Hz,1H),6.56(d,J=10,0Hz,1H),5.32-5.37(m,1H),4.58-4.64(m,1H),4.14-4.24(m,2H),3.79(s,3H),3.28-3.43(m,4H),3.07(s,3H),3.06(s,3H),2.98-3.06(m,2H),2.67(t,J=7.7Hz,2H),2.46(t,J=7.4Hz,2H),1.96-2.04(m,2H),1.89-1.96(m,2H),1.70-1.82(m,2H)LC/MS:[M]+=826.3
[実施例26]
4-({[5-(3-{[2-クロロ-5-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-26で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(45mg、0.076mmol)から、4-({[5-(3-{[2-クロロ-5-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(18mg)を得た。
LC/MS:[M]+=796.4
[実施例27]
4-({[5-(3-{[5-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-27で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(123mg、0.22mmol)から、4-({[5-(3-{[5-エトキシ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(48mg)を得た。
LC/MS:[M]+=762.4
[実施例28]
4-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-28で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-フルオロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(144mg、0.27mmol)から、4-({[5-(3-{[2-フルオロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(102mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),9.88(s,1H),9.21(d,J=82.7Hz,1H),8.74(s,1H),8.09(d,J=9.8Hz,1H),7.92(t,J=8.3Hz,1H),7.28-7.47(m,7H),7.25(s,1H),7.23(d,J=8.0Hz,1H),7.15-7.18(m,1H),7.11(d,J=8.0Hz,1H),6.97(d,J=8.0,Hz,1H),6.54(d,J=9,8Hz,1H),5.32-5.37(m,1H),4.58-4.64(m,1H),4.16-4.23(m,2H),3.26-3.43(m,4H),3.08(s,3H),3.07(s,3H),2.94-3.02(m,2H),2.65(t,J=7.7Hz,2H),2.46(t,J=7.4Hz,2H),1.96-2.04(m,2H),1.87-1.95(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=736.3
[実施例29]
4-({[5-(3-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-29で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(131.8mg、0.24mmol)から、4-({[5-(3-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(108mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.31(s,1H),9.18(d,J=54.1Hz,1H),8.75(s,1H),8.12(d,J=10.0Hz,1H),7.92(d,J=2.0Hz,1H),7.59(d,J=8.5Hz,1H),7.52(dd,J=8.5Hz,2.0Hz,1H),7.29-7.44(m,5H),7.25(s,1H),7.24(d,J=8.0Hz,1H),7.14-7.18(m,1H),7.13(d,J=8.5Hz,1H),6.98(d,J=8.5,Hz,1H),6.54(d,J=10,0Hz,1H),5.34-5.40(m,1H),4.58-4.68(m,1H),4.24-4.40(m,2H),3.28-3.44(m,4H),3.08(s,3H),3.07(s,3H),3.04-3.15(m,2H),2.65(t,J=7.6Hz,2H),2.40(t,J=7.3Hz,2H),1.96-2.04(m,2H),1.87-1.95(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=752.3
[実施例30]
4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-25で得られた1-メチルピペリジン-4-イル N-{5-[3-({2-ブロモ-4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(95mg、0.16mmol)から、4-({[5-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(34mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),9.58(s,1H),9.16(d,J=42.4Hz,1H),8.74(s,1H),8.09(d,J=10.0Hz,1H),7.86(d,J=1.7Hz,1H),7.63(d,J=8.3Hz,1H),7.50(dd,J=8.3Hz,1.7Hz,1H),7.29-7.44(m,5H),7.26(s,1H),7.25(d,J=8.0Hz,1H),7.14-7.18(m,1H),7.12(d,J=8.0Hz,1H),6.97(d,J=8.0,Hz,1H),6.56(d,J=10,0Hz,1H),5.30-5.38(m,1H),4.58-4.68(m,1H),4.18-4.25(m,2H),3.28-3.42(m,4H),3.07(s,3H),3.06(s,3H),2.98-3.05(m,2H),2.67(t,J=7.6Hz,2H),2.44(t,J=7.3Hz,2H),1.96-2.04(m,2H),1.87-1.95(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=796.3
[実施例31]
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-(トリフルオロメチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-31で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-(トリフルオロメチル)フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(145.2mg、0.25mmol)から、4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-(トリフルオロメチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(98mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),9.34(d,J=78.3Hz,1H),8.76(s,1H),8.13(s,1H),8.13(d,J=10.0Hz,1H),7.88-7.93(m,1H),7.77(d,J=8.5Hz,1H),7.29-7.44(m,5H),7.26(s,1H),7.25(d,J=8.0Hz,1H),7.14-7.18(m,1H),7.14(d,J=8.0Hz,1H),6.99(d,J=8.0,Hz,1H),6.54(d,J=10,0Hz,1H),5.36-5.43(m,1H),4.58-4.68(m,1H),4.30-4.44(m,2H),3.26-3.44(m,4H),3.08(s,3H),3.07(s,3H),2.98-3.05(m,2H),2.66(t,J=7.6Hz,2H),2.43(t,J=7.3Hz,2H),1.96-2.04(m,2H),1.90-1.96(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=786.3
[実施例32]
4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-32で得られた1-メチルピペリジン-4-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(122mg、0.2mmol)から、4-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(40mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.45(s,1H),10.06(s,1H),9.02(d,J=38.8Hz,1H),8.70(s,1H),8.09(d,J=10.0Hz,1H),7.63(d,J=8.5Hz,2H),7.35-7.45(m,6H),7.28-7.35(m,1H),7.25(s,1H),7.24(d,J=7.8Hz,1H),7.14-7.18(m,1H),7.10(d,J=8.0Hz,1H),6.96(d,J=8.0Hz,1H),6.54(d,J=10,0Hz,1H),5.28-5.33(m,1H),4.59-4.66(m,1H),4.13-4.18(m,2H),3.34-3.42(m,2H),3.28-3.34(m,2H),3.07(s,3H),3.06(s,3H),2.90-3.09(m,2H),2.65(t,J=7.6Hz,2H),2.38(t,J=7.3Hz,2H),1.97-2.06(m,2H),1.88-1.97(m,2H),1.73-1.81(m,2H)
LC/MS:[M]+=718.3
[実施例33]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-33で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(57.6mg、0.088mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(25mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),10.06(s,1H),8.99(d,J=18.5Hz,1H),8.75(s,1H),8.03(d,J=10.0Hz,1H),7.63(d,J=8.5Hz,2H),7.31-7.46(m,7H),7.27(s,1H),7.25(d,J=7.8Hz,1H),7.13-7.18(m,1H),7.10(d,J=8.3Hz,1H),6.95(d,J=8.3Hz,1H),6.54(d,J=10.0Hz,1H),5.28-5.34(m,1H),4.79(t,J=5.6Hz,1H),4.13-4.19(m,2H),4.08-4.12(m,2H),3.76-3.95(broad,2H),3.25(s,3H),3.01(s,3H),2.92-3.02(m,2H),2.94(t,J=7.8 Hz,2H),2.53(dt,J=16.9Hz,5.2Hz,2H),2.38(t,J=7.3Hz,2H),1.88-1.96(m,2H),1.79(d,J=17.1Hz,2H)
LC/MS:[M]+=758.3
[実施例34]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-18で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(136.8mg、0.2mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(87mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.54(s,1H),9.60(s,1H),8.92(d,J=48.0Hz,1H),8.78(s,1H),8.08(d,J=10.0Hz,1H),7.58(s,1H),7.54(s,1H),7.31-7.46(m,5H),7.28(s,1H),7.25(d,J=7.8Hz,1H),7.13-7.18(m,1H),7.12(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.55(d,J=10.0Hz,1H),5.32-5.37(m,1H),4.78(t,J=5.2Hz,1H),4.14-4.24(m,2H),4.08-4.12(m,2H),3.82-3.98(broad,2H),3.79(s,3H),3.25(s,3H),3.01(s,3H),2.94-3.07(m,2H),2.65(t,J=7.6Hz,2H),2.53-2.58(m,2H),2.43-2.50(m,2H),1.88-1.96(m,2H),1.79(d,J=12.9Hz,2H)
LC/MS:[M]+=822.3
[実施例35]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-35で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(5-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(181mg、0.26mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(26mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),10.23(s,1H),9.17(d,J=22.2Hz,1H),8.78(s,1H),8.38(s,1H),8.03(d,J=10.0Hz,1H),7.95(s,1H),7.83-7.89(m,2H),7.58-7.66(m,2H),7.31-7.46(m,5H),7.29(s,1H),7.26(d,J=7.8Hz,1H),7.16-7.20(m,1H),7.10(d,J=8.0Hz,1H),6.95(d,J=8.0Hz,1H),6.48(d,J=10.0Hz,1H),5.31-5.36(m,1H),4.79(t,J=6.0Hz,1H),4.32-4.38(m ,2H),4.07-4.13(m,2H),3.78-4.00(broad,2H),3.25(s,3H),3.05-3.13(m,2H),3.01(s,3H),2.67(t,J=7.6Hz,2H),2.49-2.58(m,2H),2.44(t,J=7.3Hz,2H),1.92-2.00(m,2H),1.79(d,J=14.1Hz,2H)
LC/MS:[M]+=808.3
[実施例36]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9- イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-36で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(251mg、0.36mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(81mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),10.14(s,1H),8.79(d,J=52.9Hz,1H),8.78(s,1H),8.05(d,J=10.0Hz,1H),7.31-7.46(m,7H),7.28(s,1H),7.25(d,J=7.8Hz,1H),7.13-7.19(m,2H),7.11(d,J=8.0Hz,1H),6.97(d,J=8.0Hz,1H),6.53(d,J=10.0Hz,1H),5.29-5.35(m,1H),4.79(t,J=5.4 Hz,1H),4.10-4.23 (m,2H),4.07-4.13(m,2H),3.78-4.0(broad,2H),3.78(s,3H),3.26(s,3H),3.02(s,3H),2.94-3.04(m,2H),2.64(t,J=7.7Hz,2H),2.49-2.57(m,2H),2.38(t,J=7.3Hz,2H),1.88-1.96(m,2H),1.78(d,J=13.2Hz,2H)
LC/MS:[M]+=788.3
[実施例37]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-37で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(116.1mg、0.23mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(19.7mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.52(s,1H),9.63(s,1H),9.02-9.15(broad,1H),8.77(s,1H),8.07(d,J=10.0Hz,1H),7.75(d,J=8.3Hz,1H),7.69(d,J=2.0Hz,1H),7.31-7.47(m,6H),7.28(s,1H),7.25(d,J=7.8Hz,1H),7.14-7.18(m,1H),7.12(d,J=8.3Hz,1H),6.96(d,J=8.3Hz,1H),6.53(d,J=10.0Hz,1H),5.29-5.34(m,1H),4.78(t,J=5.7 Hz,1H),4.16-4.24(m,2H),4.07-4.13(m,2H),3.78-4.00(broad,2H),3.25(s,3H),3.02-3.12(m,2H),3.01(s,3H),2.65(t,J=7.4Hz,2H),2.49-2.57(m,2H),2.46(t,J=7.3Hz,2H),1.88-1.96(m,2H),1.78(d,J=13.3Hz,2H)LC/MS:[M]+=792.3
[実施例38]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-38で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(311.2mg、0.45mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9- イウムトリフルオロアセテート(61mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),9.21(s,1H),9.15(d,J=67.6Hz,1H),8.77(s,1H),8.07(d,J=10.0Hz,1H),7.98(d,J=8.0Hz,1H),7.31-7.47(m,5H),7.22-7.28(m,3H),7.15(d,J=8.5Hz,1H),7.11(d,J=8.3Hz,1H),7.01-7.06(m,1H),6.97(d,J=8.3Hz,1H),6.53(d,J=10.0Hz,1H),5.30-5.38(m,1H),4.78(t,J=5.6Hz,1H),4.14-4.22 (m ,2H),4.07-4.13(m,2H),3.82-4.02(broad,2H),3.83(s,3H),3.25(s,3H),3.01(s,3H),2.90-3.08(m,2H),2.63(t,J=7.6Hz,2H),2.49-2.58(m,2H),2.46(t,J=7.3Hz,2H),1.88-1.96(m,2H),1.78(d,J=13.2Hz,2H)
LC/MS:[M]+=788.3
[実施例39]
(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-39で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(149mg、0.22mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(38mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.51(s,1H),9.39(s,1H),9.07(d,J=41.2Hz,1H),8.78(s,1H),8.05(d,J=10.0Hz,1H),7.30-7.48(m,8H),7.28(s,1H),7.25(d,J=7.8Hz,1H),7.16(d,J=7.8Hz,1H),7.11(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.55(d,J=10.0Hz,1H),5.30-5.36(m,1H),4.79(t,J=5.5 Hz,1H),4.12-4.18(m,2H),4.07-4.12(m,2H),3.82-4.02(broad,2H),3.83(s,3H),3.25(s,3H),3.01(s,3H),2.90-3.06(m,2H),2.65(t,J=7.6Hz,2H),2.49-2.58(m,2H),2.41(t,J=7.1Hz,2H),1.87-1.97(m,2H),1.78(d,J=17.1Hz,2H)
LC/MS:[M]+=772.3
[実施例40]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-40で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(5-{2-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(77mg、0.13mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(19.5mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),10.27(s,1H),9.07-9.15(broad,1H),8.77(s,1H),8.37(s,1H),8.02(d,J=10.0Hz,1H),7.95(s,1H),7.84-7.90(m,2H),7.57-7.65(m,2H),7.31-7.46(m,6H),7.20-7.28(m,2H),7.10(d,J=8.3Hz,1H),6.94(d,J=8.3Hz,1H),6.49(d,J=10.0Hz,1H),5.30-5.36(m,1H),4.79(t,J=5.4Hz,1H),4.33-4.38 (m,2H),4.07-4.12(m,2H),3.78-3.98(broad,2H),3.24(s,3H),3.05-3.14(m,2H),3.00(s,3H),2.97(t,J=8.0Hz,2H),2.75(t,J=8.0 Hz,2H),2.46-2.58(m,2H),1.78(d,J=16.8Hz,2H)
LC/MS:[M]+=794.3
[実施例41]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-41で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(50mg、0.08mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(10.5mg)を得た。
LC/MS:[M]+=774.3
[実施例42]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-42で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(64.3mg、0.11mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(11.4mg)を得た。
LC/MS:[M]+=774.3
[実施例43]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-43で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-メチルフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメー(196mg、0.3mmol)から、((1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-2-メチルフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(128mg)を得た。
LC/MS:[M]+=758.3
[実施例44]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-44で得られた1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(95mg、0.14mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(25.5mg)を得た。
LC/MS:[M]+=779.4
[実施例45]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-45で得られた1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-クロロフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(256mg、0.23mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[3-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(45mg)を得た。
LC/MS:[M]+=778.3
[実施例46]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-46で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(52mg、0.074mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(25.6mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),9.60(s,1H),8.86(d,J=29.3Hz,1H),8.77(s,1H),8.08(d,J=10.0Hz,1H),7.58(s,1H),7.57(s,1H),7.30-7.46(m,5H),7.18-7.28(m,2H),7.13(d,J=8.3Hz,2H),6.97(d,J=8.3Hz,1H),6.56(d,J=10.0Hz,1H),5.34(dd,J=9.1Hz,3.5Hz,1H),4.79(t,J=5.6 Hz,1H),4.14-4.24 (m,2H),4.07-4.13(m,2H),3.80-3.98(broad,2H),3.80(s,3H),3.26(s,3H),3.01(s,3H),2.98-3.08(m,2H),2.94(t,J=7.7Hz,2H),2.78(t,J=7.7Hz,2H),2.54(dt,J=17.7Hz,5.2Hz,2H),1.77(d,J=11.0Hz,2H)
LC/MS:[M]+=808.3
[実施例47]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-エトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-47で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-エトキシフェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(219mg、0.32mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-3-エトキシフェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(109mg)を得た。
LC/MS:[M]+=788.3
[実施例48]
(1R,3R)-3-{[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-8,8-ジメチル-8-アザビシクロ[3.2.1]ノナン-8-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-48で得られた(1R,3R)-8-メチル-8- アザビシクロ[3.2.1]オクタン-3-イル N-{5-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(488mg、0.69mmol)から、((1R,3R)-3-{[5-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-8,8-ジメチル-8-アザビシクロ[3.2.1]ノナン-8-イウムトリフルオロアセテート(285mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),9.59(s,1H),8.99(d,J=39.8Hz,1H),8.90(s,1H),8.08(d,J=9.8Hz,1H),7.58(s,1H),7.54(s,1H),7.31-7.46(m,8H),7.13(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.56(d,J=9.8Hz,1H),5.30-5.36(m,1H),4.72(t,J=5.2 Hz,1H),4.12-4.26(m,2H),3.80(s,3H),3.77(s,3H),3.00-3.12 (m,4H),2.99(s,3H),2.67(t,J=7.0Hz,2H),2.36-2,56(m,4H),2.12-2,28(m,2H),1.86-1.96(m,2H),1.67(d,J=16.1Hz,2H)
LC/MS:[M]+=808.3
[実施例49]
4-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-49で得られた1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-3-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(137mg、0.218mmol)から、4-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(64mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.08(s,1H),9.10(d,J=68.8 Hz,1H),8.73(s,1H),8.06(d,J=10.0Hz,1H),7.62(d,J=8.8Hz,2H),7.28-7.45(m,7H),7.23(s,1H),7.23(d,J=7.6Hz,1H),7.14(dd,J=7.9Hz,1.3Hz,1H),7.10(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.53(d,J=10,0Hz,1H),5.30-5.35(m,1H),4.57-4.62(m,1H),4.12-4.18(m,2H),3.36-3.42(m,2H),3.26-3.36(m,2H),3.07(s,3H),3.06(s,3H),2.88-3.09(m,2H),2.63(t,J=7.0 Hz,2H),2.36(t,J=7.0Hz,2H),1.94-2.06(m,2H),1.69-1.82(m,2H),1.60-1.68(m,4H)
LC/MS:[M]+=732.3
[実施例50]
(1R,2R,4S,5S,7S)-7-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-50で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(64mg、0.1mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(4-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(21.4mg)を得た。
LC/MS:[M]+=772.3
[実施例51]
4-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-51で得られた1-メチルピペリジン-4-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(60.5mg、0.087mmol)から、4-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(17mg)を得た。
LC/MS:[M]+=796.3
[実施例52]
(1R,2R,4S,5S,7S)-7-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9- イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-52で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[4-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)ブチル]-2-フェニルフェニル}カルバメート(76mg、0.1mmol)から、(1R,2R,4S,5S,7S)-7-({[5-(4-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}ブチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(11.9mg)を得た。
LC/MS:[M]+=836.3
[実施例53]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-53で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(70.1mg、0.11mmol)から、(1R,2R,4S,5S,7S)-7-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(30.9mg)を得た。
LC/MS:[M]+=758.3
[実施例54]
4-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-54で得られた1-メチルピペリジン-4-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(88.2mg、0.14mmol)から、4-({[4-(3-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(45mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),10.03(s,1H),8.88-8.98(broad,1H),8.70(s,1H),8.02(d,J=10.0Hz,1H),7.61(d,J=8.3Hz,2H),7.26-7.44(m,8H),7.20(d,J=8.5Hz,1H),7.15(s,1H),7.09(d,J=8.3Hz,1H),6.94(d,J=8.3Hz,1H),6.54(d,J=10.0Hz,1H),5.26-5.34(m,1H),4.58-4.66(m,1H),4.12-4.17(m,2H),3.34-3.42(m,2H),3.26-3.34(m,2H),3.07(s,3H),3.06(s,3H),2.90-3.06(m,2H),2.65(t,J=7.2 Hz,2H),2.38(t,J=7.7Hz,2H),1.94-2.04(m,2H),1.87-1.94(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=718.3
[実施例55]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-55で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(201mg、0.28mmol)から、(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(59mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.49(s,1H),9.55(s,1H),8.75-8.84(broad,1H),8.73(s,1H),8.07(d,J=10.0Hz,1H),7.57(s,1H),7.53(s,1H),7.31-7.46(m,6H),7.21(d,J=8.3Hz,1H),7.17(s,1H),7.12(d,J=8.3Hz,1H),6.96(d,J=8.3Hz,1H),6.57(d,J=10.0Hz,1H),5.28-5.34(m,1H),4.78(t,J=5.9Hz,1H),4.14-4.22(m,2H),4.07-4.12(m,2H),3.79(s,3H),3.82-3.98(broad,2H),3.25(s,3H),3.01-3.07(m,2H),3.01(s,3H),2.66(t,J=7.3Hz,2H),2.49-2.58(m,2H),2.43-2.49(m,2H),1.87-1.96(m,2H),1.77(d,J=17.1Hz,2H)
LC/MS:[M]+=822.3
[実施例56]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-56で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-(4-{3-[(6-{[(tert-ブチルジメチルシリル)オキシ]メチル}ナフタレン-2-イル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメートから、(1R,2R,4S,5S,7S)-7-({[4-(3-{[6-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)ナフタレン-2-イル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(59.9mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.19(s,1H),9.02-9.14(broad,1H),8.74(s,1H),8.37(s,1H),8.02(d,J=10.0Hz,1H),7.94(s,1H),7.83-7.90(m,2H),7.57-7.62(m,2H),7.31-7.47(m,6H),7.22(d,J=8.8Hz,1H),7.18(s,1H),7.10(d,J=8.3Hz,1H),6.94(d,J=8.3Hz,1H),6.49(d,J=10.0Hz,1H),5.28-5.35(m,1H),4.78(t,J=5.5Hz,1H),4.32-4.37(m,2H),4.07-4.12(m,2H),3.82-3.98(broad,2H),3.25(s,3H),3.06-3.14(m,2H),3.00(s,3H),2.68(t,J=7.8Hz,2H),2.49-2.58(m,2H),2.42(t,J=7.2Hz,2H),1.92-1.99(m,2H),1.77(d,J=18.0Hz,2H)
LC/MS:[M]+=808.3
[実施例57]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1-メチル-1-(2-フェノキシエチル)ピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-57で得られた1-(2-フェノキシエチル)ピペリジン-4-イル N-{5-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(227mg、0.43mmol)から、(4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1-メチル-1-(2-フェノキシエチル)ピペリジン-1-イウムトリフルオロアセテート(82.5mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.48(s,1H),10.14(s,1H),9.07(d,J=51.7Hz,1H),8.75(d,J=6.1Hz,1H),8.06(d,J=10.0Hz,1H),7.63(d,J=8.5Hz,2H),7.44(d,J=8.5Hz,2H),7.27-7.42(m,8H),7.18-7.27(m,2H)7.10(d,J=8.3Hz,1H),6.95-7.04(m,3H),6.97(d,J=8.3Hz,1H),6.53(d,J=10.0Hz,1H),5.29-5.34(m,1H),4.62-4.71(m,1H),4.46-4.50 (m 2H),4.12-4.20 (m 2H),3.80-3.86(m,2H)3.47-3.60(m,2H),3.40-3.52(m,2H),3.15(s,3H),2.96-3.05(m,2H),2.94(t,J=7.5Hz,2H),2.68(t,J=7.5Hz,2H),2.02-2.12(m,2H),1.73-1.86(m,2H)
LC/MS:[M]+=810.3
[実施例58]
4-[({5-[(8-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}オクチル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例12-6で得られた1-メチルピペリジン-4-イル N-(5-{[8-(tert-ブチルジメチルシラノイルオキシ)オクチル]オキシ}-2-フェニルフェニル)カルバメート(283mg、0.50mmol)をテトラヒドロフラン(10mL)に溶解し、そこに三フッ化水素トリエチルアミン錯体(0.4mL)を加え、室温で18時間攪拌した。反応液を酢酸エチルにて抽出し、有機層を希水酸化ナトリウム水溶液、飽和食塩水で洗浄、硫酸ナトリウムにて乾燥後、減圧濃縮した。
1H-NMR(400MHz、DMSO-d6) δ 10.54(s,1H),8.67(s,1H),8.54-8.72(broad,1H),8.15(d,J=10.0Hz,1H),7.27-7.43(m,5H),7.21(d,J=8.5Hz,1H),7.14(d,J=8.0Hz,1H),7.00(s,1H),6.98(d,J=8.0Hz,1H),6.86(dd,J=8.5Hz,2.4Hz,1H),6.56(d,J=10.0Hz,1H),5.27-5.32(m,1H),4.58-4.66(m,1H),3.97(t,J=7.1 Hz,2H),3.25-3.43(m,4H),3.07(s,3H),3.06(s,3H),3.00-3.12(m,2H),2.92-3.00(m,2H),1.94-2.04(m,2H),1.67-1.82(m,4H),1.54-1.67(m,2H),1.34-1.46(m,2H),1.20-1.34(m,6H)
LC/MS:[M]+=671.3
[実施例59]
4-[({5-[(6-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘキシル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例12-7で得られた1-メチルピペリジン-4-イル N-(5-{[6-(tert-ブチルジメチルシラノイルオキシ)ヘキシル]オキシ}-2-フェニルフェニル)カルバメート(163mg、0.30mmol)から、4-[({5-[(6-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘキシル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(30.1mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.50(s,1H),8.68(s,1H),8.65(d,J=24.6Hz,1H),8.16(d,J=10.0Hz,1H),7.27-7.43(m,5H),7.21(d,J=8.5Hz,1H),7.14(d,J=8.5Hz,1H),7.00(s,1H),6.98(d,J=8.0Hz,1H),6.86(dd,J=8.5Hz,2.4Hz,1H),6.56(d,J=10.0Hz,1H),5.28-5.33(m,1H),4.58-4.66(m,1H),3.98(t,J=6.2 Hz,2H),3.26-3.44(m,4H),3.07-3.14(m,2H),3.07(s,3H),3.06(s,3H),2.94-3.02(m,2H),1.94-2.04(m,2H),1.60-1.82(m,6H),1.30-1.48(m,4H)
LC/MS:[M]+=643.3
[実施例60]
4-[({5-[(9-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ノニル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例12-8で得られた1-メチルピペリジン-4-イル N-(5-{[9-(tert-ブチルジメチルシラノイルオキシ)ノニル]オキシ}-2-フェニルフェニル)カルバメート(175mg、0.30mmol)から、4-[({5-[(9-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ノニル)オキシ]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(31.8mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.47(s,1H),8.65(s,1H),8.54-8.72(broad,1H),8.15(d,J=10.0Hz,1H),7.27-7.43(m,5H),7.21(d,J=8.5Hz,1H),7.14(d,J=8.5Hz,1H),7.00(s,1H),6.98(d,J=8.0Hz,1H),6.86(dd,J=8.4Hz,2.6Hz,1H),6.56(d,J=10.0Hz,1H),5.28-5.33(m,1H),4.58-4.66(m,1H),3.97(t,J=6.7 Hz,2H),3.25-3.43(m,4H),3.07(s,3H),3.06(s,3H),3.00-3.12(m,2H),2.92-3.00(m,2H),1.94-2.04(m,2H),1.60-1.82(m,4H),1.55-1.66(m,2H),1.34-1.46(m,2H),1.20-1.34(m,8H)
LC/MS:[M]+=685.3
[実施例61]
4-{[(5-{4-[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェノキシ]ブチル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例12-9で得た1-メチルピペリジン-4-イル N-[5-(4-{4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェノキシ}ブチル)-2-フェニルフェニル]カルバメート(115mg、0.25mmol)から、4-{[(5-{4-[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェノキシ]ブチル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(102mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.45(s,1H),9.02(d,J=59.3Hz,1H),8.95(s,1H),8.06(d,J=9.8Hz,1H),7.27-7.44(m,6H),7.25(s,1H),7.24(d,J=7.8Hz,2H),7.14-7.20(m,1H),7.10(d,J=8.3Hz,2H),6.95-6.99(m,2H),6.53(d,J=9.8Hz,1H),5.29-5.34(m,1H),4.58-4.66(m,1H),4.12-4.17(m,2H),4.01(t,J=5.5Hz,2H),3.25-3.43(m,4H),3.07(s,3H),3.06(s,3H),2.88-3.05(m,2H),2.67(t,J=6.6Hz,2H),1.96-2.08(m,2H),1.70-1.82(m,6H)
LC/MS:[M]+=705.3
[実施例62]
4-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例15-58で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメート(63mg、0.1mmol)から、4-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(16mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.45(s,1H),9.91(s,1H),8.70(s,1H),8.56-8.66(broad,1H),8.05(d,J=10.0Hz,1H),7.49-7.55(m,2H),7.27-7.43(m,6H),7.11-7.26(m,5H),6.97(d,J=8.0Hz,1H),6.56(d,J=10.0Hz,1H),5.25-5.31(m,1H),4.58-4.66(m,1H),3.35-3.43(m,2H),3.25-3.35(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.06(m,2H),2.93(t,J=7.7 Hz,2H),2.64(t,J=7.7 Hz,2H),2.57(t,J=7.4 Hz,2H),1.94-2.04(m,2H),1.84-1.94(m,2H),1.68-1.80(m,2H)
LC/MS:[M]+=732.3
[実施例63]
4-({[5-(2-{[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例15-59で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[2-(tert-ブチルジメチルシラノイルオキシ)エチル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメート(61mg、0.1mmol)から、4-({[5-(2-{[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(4.4mg)を得た。
LC/MS:[M]+=718.3
[実施例64]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}メトキシ)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例15-60で得られた1-メチルピペリジン-4-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)エチル]フェニル}カルバモイル)]エチル}-2-フェニルフェニル}カルバメート(61mg、0.1mmol)から、4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}メトキシ)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(15mg)を得た。
LC/MS:[M]+=706.3
[実施例65]
4-[({5-[2-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]メチル}カルバモイル)エチル]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例15-61で得た1-メチルピペリジン-4-イル N-(5-{2-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]エチル}-2-フェニルフェニル)カルバメート(94mg、0.16mmol)をアセトニトリル(5mL)に溶解し、そこにヨウ化メチル(1mL)を加え、室温で1時間攪拌した後、反応溶液を減圧濃縮した。
LC/MS:[M]+=718.3
[実施例66]
4-[({5-[3-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]メチル}カルバモイル)プロピル]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例65に従い、参考例15-62で得た1-メチルピペリジン-4-イル N-(5-{3-[({4-[(tert-ブトキシカルボニル)アミノ]フェニル}メチル)カルバモイル]プロピル}-2-フェニルフェニル)カルバメート(86mg、0.14mmol)から、4-[({5-[3-({[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]メチル}カルバモイル)プロピル]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(3.3mg)を得た。
LC/MS:[M]+=732.3
[実施例67]
4-[({5-[(1E)-2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}-1-エテン-1-イル]-2-フェニルフェニル}カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-63で得た1-メチルピペリジン-4-イル N-{5-[(1E)-2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)-1-エテン-1-イル]-2-フェニルフェニル}カルバメート(57mg、0.095mmol)から、4-[({5-[(1E)-2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}-1-エテン-1-イル]-2-フェニルフェニル}カルバモイル)オキシ]-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(29.9mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.45(s,1H),9.07(d,J=43.7Hz,1H),8.89(s,1H),8.06(d,J=10.0Hz,1H),8.75(d,J=8.8Hz,2H),7.70(s,1H),7.61(d,J=15.6Hz,1H),7.57(d,J=8.3Hz,1H),7.49(d,J=8.8Hz,2H),7.27-7.46(m,6H),7.11(d,J=8.3Hz,1H),6.97(d,J=8.3Hz,1H),6.90(d,J=15.6Hz,1H),6.54(d,J=10.0Hz,1H),5.30-5.35(m,1H),4.62-4.68(m,1H),4.15-4.21(m,2H),3.25-3.43(m,4H),3.07(s,3H),3.06(s,3H),2.88-3.05(m,2H),1.96-2.08(m,2H),1.70-1.82(m,2H)
LC/MS:[M]+=702.3
[実施例68]
4-({[5-(2-{[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}-2-メチルプロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例15-64で得た1-メチルピペリジン-4-イル N-[5-(2-{[4-(2-メチル-2-ニトロプロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバメート(193mg、0.35mmol)をアセトニトリル(10mL)に溶解し、そこにヨウ化メチル(2mL)を加え、室温で1時間攪拌した後、反応溶液を減圧濃縮した。
残渣をメタノール(10mL)に溶解し、触媒量の水酸化パラジウム炭素 を加え、水素雰囲気下に溶液をおいて4日間攪拌した。反応溶液をセライトろ過し、減圧濃縮した。
残渣に5%臭化水素酸メタノール溶液(10mL)を加え、80℃で2時間攪拌した後、反応溶液を減圧濃縮した。
LC/MS:[M]+=746.3
[実施例69]
4-({[4-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート
実施例1に従い、参考例15-65で得た1-メチルピペリジン-4-イル N-{4-[2-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(227mg、0.377mmol)から、4-({[4-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(87mg)を得た。
1H-NMR(400MHz、DMSO-d6) δ 10.46(s,1H),10.10(s,1H),9.06(d,J=52.0Hz,1H),8.70(s,1H),8.06(d,J=10.0Hz,1H),7.61(d,J=8.5Hz,2H),7.43(d,J=8.5Hz,2H),7.27-7.40(m,6H),7.20-7.25(m,2H),7.10(d,J=8.0Hz,1H),6.97(d,J=8.0Hz,1H),6.53(d,J=10.0Hz,1H),5.28-5.34(m,1H),4.58-4.66(m,1H),4.12-4.18(m 2H),3.34-3.43(m,2H),3.25-3.35(m,2H),3.07(s,3H),3.06(s,3H),3.00-3.05(m,2H),2.94(t,J=7.4 Hz,2H),2.67(t,J=7.4 Hz,2H),1.94-2.04(m,2H),1.68-1.80(m,2H)
LC/MS:M+1=704.3
[参考例15-66]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.50mmol)と参考例14-18で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモ-5-メトキシアニリン(346.35mg、1.0mmol)から、(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(196.3mg)を得た。
LC/MS:[M]+=765.3
[参考例15-67]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7- イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.50mmol)と参考例14-9で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロアニリン(163.1mg、1.0mmol)から、((1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-クロロフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(137.2mg)を得た。
LC/MS:M+1=692.3
[参考例15-68]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-4で得られた4-(4-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル}オキシ)カルボニル]アミノ}-3-フェニルフェニル)酪酸塩酸塩(0.50mmol)と参考例14-21で得られた4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモアニリン(237.2mg、1.0mmol)から、(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(168.8mg)を得た。
LC/MS:M+1=736.3
[実施例70]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-66で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7- イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(196.3mg、0.257mmol)から、(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)-5-メトキシフェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(24.6mg)を得た。
LC/MS:[M]+=866.3
[実施例71]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-67で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモ-5-メトキシフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(137.2mg、0.199mmol)から、(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-クロロ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(34.19mg)を得た。
LC/MS:[M]+=792.3
[実施例72]
(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例1に従い、参考例15-66で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{4-[3-({4-[(tert-ブチルジメチルシラノイルオキシ)メチル]-2-ブロモフェニル}カルバモイル)プロピル]-2-フェニルフェニル}カルバメート(168.8mg、0.230mmol)から、(1R,2R,4S,5S,7S)-7-({[4-(3-{[2-ブロモ-4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]カルバモイル}プロピル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(9.16mg)を得た。
LC/MS:[M]+=836.3
[参考例15-69]
(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13-2で得られた3-(3-{[({[1R,2R,4S,5S,7S]-9-メチル-3-オキサ-9- アザトリシクロ[3.3.1.02,4]ノナン-9-イル}オキシ)カルボニル]アミノ}-4-フェニルフェニル)プロピオン酸塩酸塩(137.3mg、0.3mmol)と参考例14-23で得られた4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]アニリン(132.7mg、0.5mmol)から、(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(165.3mg)を得た。
LC/MS:M+1=670.3
[実施例73]
(1R,2R,4S,5S,7S)-7-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテートの合成
実施例58に従い、参考例15-69で得られた(1R,2R,4S,5S,7S)-9-メチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-7-イル N-{5-[2-({4-[3-(tert-ブチルジメチルシラノイルオキシ)プロピル]フェニル}カルバモイル)エチル]-2-フェニルフェニル}カルバメート(100.5mg、0.15mmol)から、1R,2R,4S,5S,7S)-7-({[5-(2-{[4-(3-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}プロピル)フェニル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-9,9-ジメチル-3-オキサ-9-アザトリシクロ[3.3.1.02,4]ノナン-9-イウムトリフルオロアセテート(7.9mg)を得た。
LC/MS:[M]+=772.3
[参考例15-70]
1-メチルピペリジン-4-イル N-{5-[2-(5-[(tert-ブチルジメチルシラノイルオキシ)ペンチル]カルバモイル)エチル]-2-フェニルフェニル}カルバメートの合成
参考例15に従い、参考例13で得られた3-[3-({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]プロピオン酸塩酸塩(242mg、0.59mmol)と[(5-アミノペンチル)オキシ](tert-ブチル)ジメチルシラン(217.4mg、1.0mmol)から、1-メチルピペリジン-4-イル N-{5-[2-(5-[(tert-ブチルジメチルシラノイルオキシ)ペンチル]カルバモイル)エチル]-2-フェニルフェニル}カルバメート(163.1mg)を得た。
LC/MS:M+1=582.3
[実施例74]
4-({[5-(2-{[5-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ペンチル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例15-70で得られた1-メチルピペリジン-4-イル N-{5-[2-(5-[(tert-ブチルジメチルシラノイルオキシ)ペンチル]カルバモイル)エチル]-2-フェニルフェニル}カルバメート(163.1mg、0.28mmol)から、4-({[5-(2-{[5-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ペンチル]カルバモイル}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(3.27mg)を得た。
LC/MS:[M]+=684.3
[参考例43]
7-ヒドロキシヘプチル 4-ブロモ-3-ニトロベンゾエートの合成
4-ブロモ-3-ニトロ安息香酸(1.0g、2.5mmol)を1,4-ジオキサン(30mL)に溶解し、フェニルホウ酸(610mg、5.0mmol)、炭酸セシウム(6.5g、20.0mmol)、1,1-[ビス(ジフェニルフォスフィノ)フェロセン]ジクロロパラジウム(II)ジクロロメタン錯体(204mg、0.10mmol)、及び精製水(10mL)を加え、窒素気流下80℃で終夜攪拌した。反応溶液をセライト、アルミナ、及びフローリジルでろ過後、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥、減圧濃縮し、3-ニトロ-4-フェニル安息香酸を粗体として得た。
[参考例44]
7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-ニトロ-4-フェニルベンゾエートの合成
参考例43で得られた4-ブロモ-3-ニトロベンゾエート(824.9mg、2.3mmol)とイミダゾール(1.3g、4.0mmol)をテトラヒドロフラン(10mL)に溶解させ、tert-ブチルジメチルクロロシラン(450mg、3.0mmol)のテトラヒドロフラン(5mL)溶液を加えた。室温で終夜攪拌した後、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化アンモニウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸マグネシウムで乾燥後、減圧濃縮した。残渣をメタノール(20mL)に溶解し、10%パラジウム炭素(50mg)を加え、水素雰囲気下室温で4日間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-ニトロ-4-フェニルベンゾエートを粗体として得た。
LC/MS:M+1=442.3
[参考例12-12]
7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-({[(1-メチルピペリジン-4-イル)オキシ]カルバモイル}アミノ)-4-フェニルベンゾエートの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(576mg、5.0mmol)と参考例44で得た7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-ニトロ-4-フェニルベンゾエートから、7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-({[(1-メチルピペリジン-4-イル)オキシ]カルバモイル}アミノ)-4-フェニルベンゾエート(491.3mg)を得た。
LC/MS:M+1=583.3
[実施例75]
4-{[5-({[(7-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘプチル)オキシ]カルボニル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例12-12で得られた7-(tert-ブチルジメチルシラノイルオキシ)ヘプチル 3-({[(1-メチルピペリジン-4-イル)オキシ]カルバモイル}アミノ)-4-フェニルベンゾエート(491.3mg、0.84mmol)から、4-{[5-({[(7-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ヘプチル)オキシ]カルボニル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(27.6mg)を得た。
LC/MS:[M]+=685.3
[参考例44]
tert-ブチル N-(8-ブロモオクチル)-N-[(tert-ブトキシ)カルボニル]カルバメートの合成
窒素気流下、水素化ナトリウム(ミネラルオイル40%添加、935mg、17mmol)をN ,N-ジメチルホルムアミド(160mL)に懸濁させ、氷水冷却下、ジ-tert-ブチル イミノジカルボキシレート(3.26g、15mmol)を加えた。氷水冷却下で1時間攪拌した後、1,8-ジブロモオクタン(8.16g、30mmol)のN ,N-ジメチルホルムアミド(10mL)溶液を加え、ゆっくりと室温に戻しながら16時間攪拌した。氷水冷却下、飽和塩化アンモニア水溶液を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチル N-(8-ブロモオクチル)-N-[(tert-ブトキシ)カルボニル]カルバメート(4.26g)を得た。
[参考例45]
tert-ブチル N-[9-(4-ブロモ-3-ニトロフェニル)-8-ノネン-1-イル]-N[(tert-ブトキシ)カルボニル]カルバメートの合成
参考例44で得たtert-ブチル N-(8-ブロモオクチル)-N-[(tert-ブトキシ)カルボニル]カルバメート(1.02g、2.5mmol)とトリフェニルフォスフィン(1.18g、4.5mmol)をアセトニトリル(50mL)に溶解し、加熱還流下,終夜攪拌した後、反応溶液を減圧濃縮した。残渣をテトラヒドロフラン(50mL)に溶解し、窒素気流下、-78℃に冷却し、n-ブチルリチウム(2.5Mヘキサン溶液、1.08mL、2.7mmol)を滴下した。氷水冷却下で1時間攪拌した後、-78℃に冷却し、4-ブロモ-3-ニトロベンズアルデヒド(575mg、2.5mmol)のテトラヒドロフラン溶液を加え、ゆっくりと室温に戻しながら16時間攪拌した。水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチル N-[9-(4-ブロモ-3-ニトロフェニル)-8-ノネン-1-イル]-N[(tert-ブトキシ)カルボニル]カルバメート(375mg)を得た。
[参考例46]
tert-ブチル N-[9-(3-ニトロ-4-フェニルフェニル)-8-ノネン-1-イル]カルバメートの合成
参考例45で得たtert-ブチル N-[9-(4-ブロモ-3-ニトロフェニル)-8-ノネン-1-イル]-N[(tert-ブトキシ)カルボニル]カルバメート(375mg、0.7mmol)を1,4-ジオキサン(30mL)に溶解し、フェニルホウ酸(244mg、2.0mmol)、炭酸セシウム(2.6g、8.0mmol)、1,1-[ビス(ジフェニルフォスフィノ)フェロセン]ジクロロパラジウム(II)ジクロロメタン錯体(82mg、0.10mmol)、及び精製水(10mL)を加え、窒素気流下80℃で3日間攪拌した。反応溶液をセライト、アルミナ、及びフローリジルでろ過後、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチル N-[9-(3-ニトロ-4-フェニルフェニル)-8-ノネン-1-イル]カルバメート(305mg)を得た。
[参考例47]
tert-ブチル N-[9-(4-フェニル3-アミノ-フェニル)-8-ノネン-1-イル]カルバメートの合成
参考例46で得たtert-ブチル N-[9-(3-ニトロ-4-フェニルフェニル)-8-ノネン-1-イル]カルバメート(305mg、0.7mmol)を酢酸エチル(15mL)とメタノール(5mL)に溶解し、10%パラジウム炭素(50mg)を加え、水素雰囲気下室温で終夜攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、tert-ブチル N-[9-(4-フェニル3-アミノ-フェニル)-8-ノネン-1-イル]カルバメートを粗体として得た。
LC/MS:M+1=411.2
[参考例12-13]
1-メチルピペリジン-4-イル N-[5-(9-{[(tert-ブトキシ)カルボニル]アミノ}ノニル)-2-フェニルフェニル]カルバメートの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(460mg、4.0mmol)と参考例47で得たtert-ブチル N-[9-(4-フェニル3-アミノ-フェニル)-8-ノネン-1-イル]カルバメートから、1-メチルピペリジン-4-イル N-[5-(9-{[(tert-ブトキシ)カルボニル]アミノ}ノニル)-2-フェニルフェニル]カルバメート(351.7mg)を得た。
LC/MS:M+1=552.3
[実施例76]
4-({[5-(9-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ノニル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例12-13で得た1-メチルピペリジン-4-イル N-[5-(9-{[(tert-ブトキシ)カルボニル]アミノ}ノニル)-2-フェニルフェニル]カルバメート(110.4mg、0.2mmol)をアセトニトリル(5mL)に溶解し、そこにヨウ化メチル(1mL)を加え、室温で1時間攪拌した後、反応溶液を減圧濃縮した。残渣に5%臭化水素酸メタノール溶液(5mL)を加え、80℃で3時間攪拌した後、反応溶液を減圧濃縮した。残渣をプロピオニトリル(3mL)とアセトニトリル(5mL)に溶解し、8-ベンジルオキシ-5-((R)-2-ブロモ-1-ヒドロキシエチル)-1H-キノリン-2-オン(56.1mg、0.15mmol)、ヨウ化カリウム(50mg、0.3mmol)、及び炭酸水素ナトリウム(168mg、2.0mmol)を加え、100℃で終夜攪拌した。反応溶液をろ過して、濃縮後、HPLC分取にて精製し、4-({[5-(9-[{(2R)-[8-(ベンジルオキシ)-2-オキソ-1,2-ジヒドロキノリン-5-イル]-2-ヒドロキシエチル}アミノ]ノニル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートを得た。
LC/MS:[M]+=669.4
[参考例48]
tert-ブチル N-[2-(4-ヒドロキシフェニル)エチル]カルバメートの合成
4-(2-アミノエチル)フェノール(2.74g、20.0mmol)をテトラヒドロフラン(30mL)と水(30mL)に溶解し、ジ-tert-ブチルジカルボネート(6.50g、30.0mmol)と炭酸水素ナトリウム(4.20g、50.0mmol)を加え、室温で3時間攪拌した。反応溶液を酢酸エチルで抽出し、有機層を飽和塩化アンモニウム水溶液と飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチル N-[2-(4-ヒドロキシフェニル)エチル]カルバメート(4.97g)を得た。
[参考例34-2]
tert-ブチル N-{2-[4-(2-プロペン-1-イルオキシ)フェニル]エチル}カルバメートの合成
参考例34に従い、参考例48で得たtert-ブチル N-[2-(4-ヒドロキシフェニル)エチル]カルバメート(2.37g、10.0mmol)と3-ブロモ-1-ブテン(1.81g、15.0mmol)から、tert-ブチル N-{2-[4-(2-プロペン-1-イルオキシ)フェニル]エチル}カルバメート(2.49g)を得た。
[参考例35-2]
tert-ブチル N-[2-(4-{[(2E)-3-(3-アミノ-4-フェニルフェニル)-2-プロペン-1-イル]オキシ}フェニル)エチル]カルバメートの合成
参考例35に従い、参考例34-2で得たtert-ブチル N-{2-[4-(2-プロペン-1-イルオキシ)フェニル]エチル}カルバメート(832.1mg、3.0mmol)から、tert-ブチル N-[2-(4-{[(2E)-3-(3-アミノ-4-フェニルフェニル)-2-プロペン-1-イル]オキシ}フェニル)エチル]カルバメート(288.0mg)を得た。
[参考例12-14]
1-メチルピペリジン-4-イル N-{5-[(1E)-3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]-1-プロペン-1-イル]-2-フェニルフェニル}カルバメートの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(345.5mg、3.0mmol)と参考例44で得たtert-ブチル N-[2-(4-{[(2E)-3-(3-アミノ-4-フェニルフェニル)-2-プロペン-1-イル]オキシ}フェニル)エチル]カルバメート(288.0mg、0.7mmol)から、1-メチルピペリジン-4-イル N-{5-[(1E)-3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]-1-プロペン-1-イル]-2-フェニルフェニル}カルバメート(321.9mg)を得た。
LC/MS:M+1=586.2
[参考例49]
1-メチルピペリジン-4-イル N-(5-{3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例12-14で得た1-メチルピペリジン-4-イル N-{5-[(1E)-3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]-1-プロペン-1-イル]-2-フェニルフェニル}カルバメート(321.9mg、0.49mmol)をメタノール(10mL)に溶解し、10%パラジウム炭素(20mg)を加え、水素雰囲気下室温で終夜攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、1-メチルピペリジン-4-イル N-(5-{3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバメート(265.7mg)を粗体として得た。
[実施例77]
4-{[(5-{3-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例76に従い、参考例49で得た1-メチルピペリジン-4-イル N-(5-{3-[4-(2-{[(tert-ブトキシ)カルボニル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバメート(117.6mg、0.20mmol)と8-ベンジルオキシ-5-((R)-2-ブロモ-1-ヒドロキシエチル)-1H-キノリン-2-オン(29.9mg、0.08mmol)から、4-{[(5-{3-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]プロピル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(11.1mg)を得た。
LC/MS:[M]+=705.3
[参考例34-3]
({[5-(2-プロペン-1-イルオキシ)ペンチル]オキシ}メチル)ベンゼンの合成
参考例34に従い、5-(ベンジルオキシ)プロペン-1-オール(1.91g、10.0mmol)と3-ブロモ-1-ブテン(1.45g、12.0mmol)から、({[5-(2-プロペン-1-イルオキシ)ペンチル]オキシ}メチル)ベンゼン(1.67g)を得た。
[参考例35-3]
5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルアニリンの合成
参考例35に従い、参考例33で得た3-ブロモ-5-フェニルアニリン(496.3mg,2.0mmol)と参考例34-3で得た[({[5-(2-プロペン-1-イルオキシ)ペンチル]オキシ}メチル)ベンゼン(703.0mg、3.0mmol)から、5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルアニリン(483.4mg)を得た。
[参考例12-15]
1-メチルピペリジン-4-イル N-{5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルフェニル}カルバメートの合成
参考例12に従い、4-ヒドロキシ-1-メチルピペリジン(230.4mg、2.0mmol)と参考例35-3で得た5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルアニリン(240.9mg、0.6mmol)から、1-メチルピペリジン-4-イル N-{5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルフェニル}カルバメート(403.4mg)を得た。
LC/MS:M+1=543.3
[参考例50]
1-メチルピペリジン-4-イル N-(5-{3-[(5-ヒドロキシペンチル)オキシ]プロピル}-2-フェニルフェニル)カルバメートの合成
参考例12-15で得た1-メチルピペリジン-4-イル N-{5-[(1E)-3-{[5-(ベンジルオキシ)ペンチル]オキシ}-1-プロペン-1-イル]-2-フェニルフェニル}カルバメート(403.4mg、0.74mmol)をメタノール(20mL)に溶解し、20%水酸化パラジウム炭素(50mg)を加え、水素雰囲気下室温で4日間攪拌した。反応温度を90℃にし、更に1日間攪拌した。反応溶液をセライトろ過後、ろ液を減圧濃縮し、1-メチルピペリジン-4-イル N-(5-{3-[(5-ヒドロキシペンチル)オキシ]プロピル}-2-フェニルフェニル)カルバメートを粗体として得た。
[実施例78]
4-{[(5-{3-[(5{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}ペンチル)オキシ]プロピル}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例50で得られた1-メチルピペリジン-4-イル N-(5-{3-[(5-ヒドロキシペンチル)オキシ]プロピル}-2-フェニルフェニル)カルバメート(113.6mg、0.25mmol)をアセトニトリル(10mL)に溶解し、そこにヨウ化メチル(2mL)を加え、室温で1時間攪拌した後、反応溶液を減圧濃縮した。
LC/MS:[M]+=671.3
[参考例51]
2-[4-(2-ブロモエトキシ)フェニル]-1-エタノールの合成
4-(ヒドロキシエチル)フェノール(2.7g、20.0mmol)をN,N-ジメチルホルムアミド(50mL)に溶解させ、炭酸カリウム(6.90g、50.0mmol)、1,2-ジブロモエタン(15.03g、80.0mmol)を加えた。80℃で6時間攪拌した後、反応溶液を酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、2-[4-(2-ブロモエトキシ)フェニル]-1-エタノール(750.0mg)を得た。
[参考例52]
2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}-1-エタノールの合成
参考例38に従い、3-ニトロ-4-フェニルフェノール(215mg、1.0mmol)と参考例50で得られた2-[4-(2-ブロモエトキシ)フェニル]-1-エタノールから、2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}-1-エタノール(263.1mg)を得た。
[参考例53]
tert-ブチルジメチル(2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}エトキシ)シランの合成
参考例52で得た2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}-1-エタノール(263.1mg、0.69mmol)とイミダゾール(115.6mg、17.3mmol)をテトラヒドロフラン(10mL)に溶解させ、tert-ブチルジメチルクロロシラン(207.9mg、1.39mmol)のテトラヒドロフラン(5mL)溶液を加えた。室温で16時間攪拌した後、精製水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、tert-ブチルジメチル(2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}エトキシ)シラン(336.2mg)を得た。
[参考例54]
1-メチルピペリジン-4-イル N-{5-[2-(4-{2-[(tert-ブチルジメチルシリル)オキシ]エチル}フェノキシ)エトキシ]-2-フェニルフェニル}カルバメートの合成
参考例11、12に従い、参考例53で得られたtert-ブチルジメチル(2-{4-[2-(3-ニトロ-4-フェニルフェノキシ)エトキシ]フェニル}エトキシ)シラン(336.2mg、0.68mmol)から、1-メチルピペリジン-4-イル N-{5-[2-(4-{2-[(tert-ブチルジメチルシリル)オキシ]エチル}フェノキシ)エトキシ]-2-フェニルフェニル}カルバメート(164.3mg)を得た。
[実施例79]
4-{[(5-{2-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]エトキシ}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例58に従い、参考例54で得られた1-メチルピペリジン-4-イル N-{5-[2-(4-{2-[(tert-ブチルジメチルシリル)オキシ]エチル}フェノキシ)エトキシ]-2-フェニルフェニル}カルバメート(81.7mg、0.135mmol)から、4-{[(5-{2-[4-(2-{[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}エチル)フェノキシ]エトキシ}-2-フェニルフェニル)カルバモイル]オキシ}-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(11.7mg)を得た。
LC/MS:[M]+=707.3
[参考例55]
N-[2-(4-ブロモ-3-ニトロフェニル)エチル]-2,2,2-トリフルオロアセタミドの合成
2-(4-ブロモフェニル)エタン-1-アミン(5.0g、25.0mmol)のジクロロエタン(100mL)溶液に、氷冷下、トリエチルアミン(7.0mL)とトリフルオロ酢酸無水物(7.88g、37.5mmol)を加え、1時間攪拌した後、室温で更に3時間攪拌した。氷冷下、反応溶液に水を加え、20分攪拌した後、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化アンモニウム水溶液、及び飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣を酢酸(15mL)に溶解し、氷冷下、発煙硝酸(30mL)をゆっくり滴下した後、氷冷下で1時間、室温で16時間攪拌した。反応溶液を氷にあけ、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、及び飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、N-[2-(4-ブロモ-3-ニトロフェニル)エチル]-2,2,2-トリフルオロアセタミド(5.17g)を得た。
[参考例56]
2,2,2-トリフルオロ-N-[2-(3-ニトロ-4-フェニルフェニル)エチル]-アセタミドの合成
参考例10に従い、参考例55で得たN-[2-(4-ブロモ-3-ニトロフェニル)エチル]-2,2,2-トリフルオロアセタミド(5.17g、15.1mmol)から、2,2,2-トリフルオロ-N-[2-(3-ニトロ-4-フェニルフェニル)エチル]-アセタミド(3.34g)を得た。
LC/MS:M+1=339.2
[参考例57]
酢酸(4-{[2-(3-ニトロ-4-フェニルフェニル)エチル]カルバモイル}フェニル)メチルの合成
参考例56で得られた2,2,2-トリフルオロ-N-[2-(3-ニトロ-4-フェニルフェニル)エチル]-アセタミド(338.3mg、1.0mmol)をメタノール(1mL)とテトラヒドロフラン(10mL)に溶解し、水酸化ナトリウム水溶液(5M、0.5mL)を加え、室温で5時間攪拌した。反応溶液を酢酸エチルで抽出し、有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、減圧濃縮した。
[参考例58]
酢酸[4-({2-[3({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]エチル}カルバモイル)フェニル]メチルの合成
参考例11、12に従い、参考例57で得られた酢酸(4-{[2-(3-ニトロ-4-フェニルフェニル)エチル]カルバモイル}フェニル)メチル(379.7mg、0.91mmol)から、酢酸[4-({2-[3({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]エチル}カルバモイル)フェニル]メチル(209.0mg)を得た。
[実施例80]
4-({[5-(2-{[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェニル]フォルムアミド}エチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
参考例58で得られた酢酸[4-({2-[3({[(1-メチルピペリジン-4-イル)オキシ]カルボニル}アミノ)-4-フェニルフェニル]エチル}カルバモイル)フェニル]メチル(53.0mg、0.10mmol)をメタノール(1mL)とテトラヒドロフラン(10mL)に溶解し、水酸化ナトリウム水溶液(5M、0.1mL)を加え、室温で1時間攪拌した。反応溶液を酢酸エチルで抽出し、有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥し、減圧濃縮した。
LC/MS:[M]+=704.3
[参考例59]
(3-ニトロ-4-フェニルフェニル)メタンアミンの合成
4-(ブロモエチル)-2-ニトロ-1-フェニルベンゼン(584.3mg、2.0mmol)とフタルイミドカリウム(555.0mg、3.0mmol)をN,N-ジメチルホルムアミド(8mL)に溶解し、110℃で3時間攪拌した。反応液を酢酸エチルにて抽出し、有機層を飽和食塩水で洗浄後、無水硫酸マグネシウムにて乾燥後、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、2-[(3-ニトロ-4-フェニルフェニル)メチル]-2,3-ジヒドロ-1H-イソインドール-1,3-ジオン(600.8mg)を得た。
[参考例60]
2-[4-(ヒドロキシメチル)フェノキシ]-N-[(3-ニトロ-4-フェニルフェニル)メチル]アセタミドの合成
参考例59で得られた(3-ニトロ-4-フェニルフェニル)メタンアミン(152.9mg、0.67mmol)をN,N-ジメチルホルムアミド(5mL)に溶解し、ブロモ酢酸無水物(346.5mg、1.5mmol)を加え、室温で1時間攪拌した。反応溶液に水を加えて反応を停止し、酢酸エチルで抽出した。有機層を飽和炭酸水素ナトリウム水溶液、及び飽和食塩水で洗浄後、無水硫酸ナトリウムにて乾燥後、減圧濃縮した。
残渣をN,N-ジメチルホルムアミド(5mL)に溶解させ、炭酸カリウム(207.0mg、1.5mmol)、及び4-(ヒドロキシメチル)フェノール(161.2mg、1.3mmol)を加えた。80℃で1時間攪拌した後、反応溶液を酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥し、減圧濃縮した。残渣をフラッシュカラムクロマトグラフィーにて精製し、2-[4-(ヒドロキシメチル)フェノキシ]-N-[(3-ニトロ-4-フェニルフェニル)メチル]アセタミド(212.8mg)を得た。
[参考例61]
1-メチルピペリジン-4-イル N-(5-{[(2-(4-{[(tert-ブチルジメチルシリル)オキシ]メチル}フェノキシ)アセタミド)メチル]-2-フェニルフェニル}カルバメートの合成
参考例53、11、12に従い、参考例60で得られた2-[4-(ヒドロキシメチル)フェノキシ]-N-[(3-ニトロ-4-フェニルフェニル)メチル]アセタミド(212.8mg、0.54mmol)から、1-メチルピペリジン-4-イル N-(5-{[(2-(4-{[(tert-ブチルジメチルシリル)オキシ]メチル}フェノキシ)アセタミド)メチル]-2-フェニルフェニル}カルバメート(254.4mg)を得た。
[実施例81]
4-({[5-({2-[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェノキシ]アセタミド}メチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテートの合成
実施例1に従い、参考例61で得られた1-メチルピペリジン-4-イル N-(5-{[(2-(4-{[(tert-ブチルジメチルシリル)オキシ]メチル}フェノキシ)アセタミド)メチル]-2-フェニルフェニル}カルバメート(123.6mg、0.20mmol)から、4-({[5-({2-[4-({[(2R)-2-ヒドロキシ-2-(8-ヒドロキシ-2-オキソ-1,2-ジヒドロキノリン-5-イル)エチル]アミノ}メチル)フェノキシ]アセタミド}メチル)-2-フェニルフェニル]カルバモイル}オキシ)-1,1-ジメチルピペリジン-1-イウムトリフルオロアセテート(13.5mg)を得た。
LC/MS:[M]+=720.3
[実施例82]ヒトM3ムスカリンレセプターへの競合的結合試験
ヒトM3ムスカリンレセプターの膜画分をPerkinElmer社から購入し、使用まで-80℃で保存した。アッセイ緩衝液としてリン酸緩衝生理食塩液(PBS(-)、Invitrogen社)を用い、ヒトM3ムスカリンレセプターの膜画分(10~15μgの膜タンパク質)及び1nM L-[N-メチル-3H]塩化メチルスコポラミン([3H]-NMS)(NET636、2.59TBq/mmol、PerkinElmer社)を添加し、最終容量を100μLとして室温で2時間インキュベートした(総結合量)。被験化合物の競合的阻害を調べるためには、異なる濃度(10pM-1μMの範囲)の被験化合物を添加した。なお非特異的結合量は5μMのアトロピン存在下で求めた。インキュベーション終了後、反応液をあらかじめ0.2%ポリエチレンイミンに浸漬したGF/Bガラス繊維濾過プレート上(PerkinElmer社)に急速濾過することにより反応を停止した。濾過プレートを洗浄液(50mM トリス塩酸 pH7.4、0.9%塩化ナトリウム)で3回洗浄し、非結合放射活性を除去した。次いでプレートを乾燥し、40μLのMicroScint-20液体トップカウントマイクロプレート用シンチレーションカクテル(PerkinElmer社)を加え、Packard Topcount液体シンチレーションカウンター(PerkinElmer社)で計測した。被験化合物の結合阻害率は、以下の式により算出した。
結合阻害率(%)=[(被験化合物添加サンプルの放射活性-非特異的結合量)/(総結合量-非特異的結合量)]x100
被験化合物の50%阻害濃度(IC50値)は異なる濃度の被験化合物の結合阻害率について、GraphPad Prism Softwareパッケージ(GraphPad Software社)を用い、ワンサイト競合結合の非線形回帰分析により解析した。
本アッセイにおいて試験された本発明の例証的な化合物は、ヒトM3ムスカリンレセプターに関して、約10nM未満のIC50値を有することが見出された。例えば、実施例1、48及び実施例51の化合物は、10nMより小さいIC50値を有することが見出された。
[実施例83]FLIPRアッセイを用いたメサコリン誘導性のカルシウム流入に対する阻害効果の評価
Gqタンパクに共役するムスカリンレセプターサブタイプ(M1、M3及びM5レセプター)は、アゴニストのレセプターへの結合によりホスホリパーゼC(PLC)経路を活性化する。結果として、活性化されたPLCは、ホスファチジルイノシトール二リン酸(PIP2)をジアシルグリセロール(DAG)及びホスファチジル-1,4,5-三リン酸(IP3)に加水分解し、次々に細胞内ストア(すなわち小胞体及び筋小胞体)からのカルシウム放出を生じる。FLIPR(Molecular devices社)アッセイは、遊離カルシウムが結合した場合、蛍光を発するカルシウム感受性の色素(Component A)を使用することにより細胞内カルシウムの増加を蛍光強度の変化により測定することが可能である。
被験化合物の阻害率(%)=[1-(FItest-FInegative)/(FIpositive-FInegative)]x100
被験化合物の50%阻害濃度(IC50値)は、異なる濃度の被験化合物の阻害率について、XLfit4(IDBS社)を使用し、4パラメータロジスティックモデルにより解析した。
Gsタンパクに共役するβ2アドレナリンレセプターは、アゴニストのレセプターへの結合によりアデニル酸サイクラーゼを活性化する。結果として、細胞内でcAMPが産生される。このcAMP量をcAMP-Screen System(Applied Biosystems社)を用いて測定することにより、β2アドレナリンレセプターの活性化能を測定することが可能である。
本試験ではリング状に切り出したモルモット摘出気管を、水浴中で一定の張力を負荷しながら固定し、アセチルコリン、ヒスタミン、あるいは電気刺激等により収縮反応を誘導する。なお張力の変化は多用途プリアンプ装置(日本光電株式会社)およびキャリア・アンプリファイヤ(日本光電株式会社)を通じてポータブルレコーダに出力し、記録する。この収縮反応に対する抑制作用を調べることにより、被験化合物の気管に対する拡張作用強度を評価することが可能である。
[実施例86]モルモットにおけるアセチルコリンあるいはヒスタミン誘導性の気管支収縮に対する効果
これらのin vivoアッセイは、被験化合物のM3ムスカリンレセプターアンタゴニスト活性及びβ2アドレナリンレセプターアゴニスト活性に基づく気管支保護効果を評価するために用いられる。体重が400g-500gのHartley系雄性モルモット(日本SLC株式会社)を用いた。動物をプラスティックボックス内でフローセン(武田薬品工業株式会社)を吸入させることにより麻酔を施した。被験化合物はDMSO含有生理食塩液に溶解し、0.04-25μg/kgの用量を0.4mL/kgの容量で鼻腔を通じて気管内に投与した。なおコントロール動物については被験化合物を含まない溶媒を投与した。通常、投与終了から数分後には動物は覚醒する。動物に33% ウレタン/0.8% α-クロラロースを3mL/kgの用量で腹腔内投与することにより麻酔を施した。アセチルコリンあるいはヒスタミンを静脈内投与するために、頚静脈にカテーテルを挿入した。また人工呼吸ならびに気道通気圧を測定するために、気管にカニューレを挿入した。動物はベンチレータ(Harvard Apparatus社)を用いて、10mL/kgの容量で60回/分の頻度で人工呼吸を施した。気道通気圧は総合呼吸機能測定装置(株式会社M・I・P・S)を用い、コンツェット-レスラー(Konzett-Roessler)法により測定した。アセチルコリンあるいはヒスタミン投与に先立って、気道通気圧を測定し、ベースライン値を記録した。続いて生理食塩液を0.4mL/kgの容量で頚静脈カテーテルから投与し、気道通気圧を測定した。被験化合物投与から1時間後にアセチルコリン(40μg/kg、0.4mL/kg)あるいはヒスタミン(15μg/kg、0.4mL/kg)を頚静脈カテーテルを通じて投与することにより、気道収縮反応を誘発し、最大収縮反応における気道通気圧を記録した。また被験化合物の作用の持続性を評価するために、被験化合物投与から1時間、6時間、12時間、18時間、24時間後に上記の用量のアセチルコリンあるいはヒスタミンを投与し、同様の方法で気道通気圧を測定した。気道収縮反応に対する被験化合物の抑制率は、下記式により算出した。
気道収縮抑制率(%)=(被験化合物投与動物におけるアセチルコリンあるいはヒスタミン投与動物の気道通気圧-ベースライン値)/(アセチルコリンあるいはヒスタミン投与動物の気道通気圧-ベースライン値)x100
被験化合物の50%阻害用量(ID50値)は異なる用量の被験化合物の気道収縮抑制率について、XLfit4(IDBS社)を使用し、シグモイダルロジスティックモデルにより解析した。
Claims (14)
- 一般式(I)
R1は、水素原子、又は無置換のC1~C8アルキル基を表し;
R2は、単結合、(無置換もしくは炭素原子が1~2個の酸素原子により置換された)C1~C8アルキレン、無置換のC2~C4アルケニレン、又は無置換の-O-C1~C4アルキレンを表し;
Xは、単結合、-O-、-CONR3-、-NR3CO-、又は-NR3CO-CH2-O-を表し(ここで、R3は、水素原子、又は無置換のC1~C8アルキル基を表す。);
A1は、単結合、無置換もしくは(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~4個の置換基で置換されたC6~C10アリーレン、無置換もしくは(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~4個の置換基で置換された5~10員のヘテロアリーレン、無置換のC1~C4アルキレン-置換もしくは無置換のC6~C10アリーレン(このC6~C10アリーレンの置換基としては、(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~3個の置換基である。)、無置換のC1~C4アルキレン-置換もしくは無置換の5~10員ヘテロアリーレン(この5~10員ヘテロアリーレンの置換基としては、(ハロゲン原子、水酸基、シアノ基、ニトロ基、カルボキシル基、トリフルオロメチル基、無置換のC1~C6アルキル基、無置換のC3~C8シクロアルキル基、無置換のC1~C6アルコキシ基、無置換のC3~C8シクロアルキルオキシ基、メルカプト基、無置換のC1~C6アルキルチオ基、無置換のC3~C8シクロアルキルチオ基、アミノ基、無置換のモノ(C1~C6アルキル)アミノ基、及び無置換のジ(C1~C6アルキル)アミノ基)からなる群から選ばれる1~3個の置換基である。)、又は無置換もしくは(ハロゲン及び無置換のC1~C6アルキル基)からなる群から選ばれる1~3個の置換基で置換されたC3~C8シクロアルキレンを表し;
R4は、無置換のC1~C10アルキレンを表し;
R8及びR9は、それぞれ独立して、ハロゲン原子、シアノ基、無置換のC1~C6アルキル基、ニトロ基、-NR10R11(ここで、R10及びR11は、それぞれ独立して、水素原子、又は無置換のC1~C6アルキル基を表す。)、無置換のC1~C6アルコキシ基、カルボキシル基、無置換のC1~C6アルコキシカルボニル基、水酸基、トリフルオロメチル基、メルカプト基又は無置換のC1~C6アルキルチオ基を表し;
a及びbは、それぞれ独立して、0~3の整数を表し;
Yは式(II)
Qは、式(III)
R5は、無置換もしくは(ハロゲン原子、水酸基、及び無置換のC1~C6アルコキシ基)からなる群から選ばれる1~4個の置換基で置換されたC1~C6アルキル基を表し、あるいは
R5、R6、及びR7は任意の2つが結合して環を形成してもよく、
nは0~2の整数を表し、
mは0~3の整数を表す。)を表し;
W-は陰イオンを表す。]
で表される四級アンモニウム塩化合物又はその薬学的に許容される塩。 - R2、X、及びA1が、下記の(i)~(iv)のいずれかである、請求項1に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(i)R2が、単結合、(炭素原子が1個の酸素原子により置換された)C1~C4アルキレン、無置換のC1~C8アルキレン、又は無置換の-O-C1~C4アルキレン;Xが-O-;A1が単結合又は無置換のフェニレンを表す。
(ii)R2が無置換のC1~C4アルキレン、無置換のC2~C4アルケニレン、又は無置換の-O-C1~C4のアルキレン;Xが-CONR3-;A1が単結合、無置換のフェニレン、無置換のC1~C4アルキレン-無置換のフェニレン、又は無置換のC6~C8のシクロアルキレンを表す。
(iii)R2が無置換のC1~C4アルキレン;Xが-NR3CO-又は-NR3CO-CH2-O-;A1が無置換のフェニレンを表す。
(iv)R2、X、A1が単結合を表す。 - R2、X、A1、及びR4が、下記の(v)~(xviii)のいずれかである、請求項1に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。
(v)R2が単結合;Xが-O-;A1が単結合:R4が無置換のC1~C10アルキレンを表す。
(vi)R2が(無置換もしくは炭素原子が1個の酸素原子により置換された)C1~C8アルキレン;Xが-O-;A1が単結合;R4が無置換のC1~C10アルキレンを表す。
(vii)R2が無置換のC1~C8アルキレン;Xが-O-;A1が無置換のフェニレン-;R4が無置換のC1~C4アルキレンを表す。
(viii)R2が-O-無置換のC1~C4アルキレン;Xが-O-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(ix)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が単結合;R4が無置換のC1~C8アルキレンを表す。
(x)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のC1~C4アルキレン-無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す
(xi)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のC6~C8シクロアルキレン;R4が無置換のC1~C4アルキレンを表す。
(xii)R2が無置換のC1~C4アルキレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xiii)R2が無置換の-O-C1~C4アルキレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xiv)R2が無置換のC2~C4アルケニレン;Xが-CONR3-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xv)R2が無置換のC2~C4アルケニレン;Xが-CONR3-;A1が無置換のC1~C4アルキレン-無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xvi)R2が無置換のC1~C4アルキレン;Xが-NR3CO-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xvii)R2が無置換のC1~C4アルキレン;Xが-NR3CO-CH2-O-;A1が無置換のフェニレン;R4が無置換のC1~C4アルキレンを表す。
(xviii)R2が単結合;Xが単結合;A1が単結合;R4が無置換のC1~C8アルキレンを表す。 - R2が、(無置換もしくは炭素原子が1個の酸素原子により置換された)C1~C6アルキレン、又は無置換の-O-C1~C4アルキレン;
Xが、-CONR3-、又は-NR3CO-CH2-O-;
A1が、無置換もしくは(ハロゲン原子、水酸基、無置換のC1~C4アルキル基、無置換のC1~C4アルコキシ基、及びトリフルオロメチル基)からなる群から選ばれる1~3個の置換基で置換された(C6~C10アリーレン又は5~10員のヘテロアリーレン);及び
R4が、無置換のC1~C6アルキレンである、
請求項1に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。 - R2が、無置換のC1~C6アルキレン;
Xが、-CONR3-;
A1が、無置換もしくは(ハロゲン原子、水酸基、無置換のC1~C4アルキル基、無置換のC1~C4アルコキシ基、及びトリハロメチル基)からなる群から選ばれる1~4個の置換基で置換された(フェニレン又はナフチレン);及び
R4が、無置換のC1~C6アルキレンである、
請求項1に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。 - R2が、無置換のC1~C6アルキレン;
Xが、-CONH-;
A1が、無置換もしくはハロゲン及びメトキシ基からなる群から選ばれる1~2個の置換基で置換されたフェニレン;及び
R4が、無置換のC1~C6アルキレンである、
請求項1に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。 - R1が、水素原子を表し、
aが0の整数を表す、
請求項1~6のいずれか1項に記載の四級アンモニウム塩化合物又はその薬学的に許容される塩。 - 請求項1~10のいずれか1項に記載の化合物又はその薬学的に許容される塩と、薬学的に許容される担体を含む医薬組成物。
- 請求項1~10のいずれか1項に記載の化合物又はその薬学的に許容される塩を有効成分として含有する、β2アドレナリンレセプターアゴニスト活性及びムスカリンレセプターアンタゴニスト活性を有する医薬組成物。
- 請求項1~10のいずれか1項に記載の化合物又はその薬学的に許容される塩を有効成分として含有する、肺疾患の予防剤又は治療剤。
- 前記肺疾患が、慢性閉塞性肺疾患又は喘息である、請求項13に記載の化合物もしくはその薬学的に許容される塩を有効成分として含有する予防剤又は治療剤。
Priority Applications (14)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SG2011097920A SG177468A1 (en) | 2009-04-30 | 2010-04-27 | Quaternary ammonium salt compound |
| KR1020117028059A KR20120061061A (ko) | 2009-04-30 | 2010-04-27 | 4 급 암모늄염 화합물 |
| BRPI1014390A BRPI1014390A2 (pt) | 2009-04-30 | 2010-04-27 | composto de sal de amônio quaternário, composição medicinal, e, agente preventivo ou terapêutico |
| MX2011011446A MX2011011446A (es) | 2009-04-30 | 2010-04-27 | Compuestos de sal de amonio cuaternario. |
| US13/266,651 US9072734B2 (en) | 2009-04-30 | 2010-04-27 | Quaternary ammonium salt compounds |
| NZ595810A NZ595810A (en) | 2009-04-30 | 2010-04-27 | Quaternary ammonium salt compound |
| AU2010242646A AU2010242646A1 (en) | 2009-04-30 | 2010-04-27 | Quaternary ammonium salt compound |
| JP2011511402A JP5379224B2 (ja) | 2009-04-30 | 2010-04-27 | 四級アンモニウム塩化合物 |
| CN201080029330.3A CN102459231B (zh) | 2009-04-30 | 2010-04-27 | 季铵盐化合物 |
| EP10769723A EP2426121A4 (en) | 2009-04-30 | 2010-04-27 | QUARTER AMMONIUM SALT CONNECTION |
| CA2760630A CA2760630A1 (en) | 2009-04-30 | 2010-04-27 | Quaternary ammonium salt compounds |
| IL216015A IL216015A0 (en) | 2009-04-30 | 2011-10-27 | Quaternary ammonium salt compounds |
| ZA2011/08372A ZA201108372B (en) | 2009-04-30 | 2011-11-15 | Quaternary ammonium salt compound |
| HK12107408.7A HK1166790A1 (en) | 2009-04-30 | 2012-07-27 | Quaternary ammonium salt compound |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009-110760 | 2009-04-30 | ||
| JP2009110760 | 2009-04-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2010126025A1 true WO2010126025A1 (ja) | 2010-11-04 |
Family
ID=43032170
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2010/057422 WO2010126025A1 (ja) | 2009-04-30 | 2010-04-27 | 四級アンモニウム塩化合物 |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US9072734B2 (ja) |
| EP (1) | EP2426121A4 (ja) |
| JP (1) | JP5379224B2 (ja) |
| KR (1) | KR20120061061A (ja) |
| CN (1) | CN102459231B (ja) |
| AR (1) | AR078121A1 (ja) |
| AU (1) | AU2010242646A1 (ja) |
| BR (1) | BRPI1014390A2 (ja) |
| CA (1) | CA2760630A1 (ja) |
| HK (1) | HK1166790A1 (ja) |
| IL (1) | IL216015A0 (ja) |
| MX (1) | MX2011011446A (ja) |
| MY (1) | MY155212A (ja) |
| NZ (1) | NZ595810A (ja) |
| SG (1) | SG177468A1 (ja) |
| TW (1) | TWI486343B (ja) |
| WO (1) | WO2010126025A1 (ja) |
| ZA (1) | ZA201108372B (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014519508A (ja) * | 2011-06-10 | 2014-08-14 | キエスィ ファルマチェウティチ エス.ピー.エー. | ムスカリン受容体拮抗薬及びβ2アドレナリン受容体作動薬活性を有する化合物 |
| JP2016502557A (ja) * | 2012-12-06 | 2016-01-28 | チエシ ファルマスティスィ エス.ピー.エー. | ムスカリン受容体アンタゴニストおよびβ2アドレナリン受容体アゴニスト活性を有する化合物 |
| JP2016505582A (ja) * | 2012-12-18 | 2016-02-25 | アルミラル・ソシエダッド・アノニマAlmirall, S.A. | β2アドレナリンアゴニスト活性およびM3ムスカリンアンタゴニスト活性を有する新規のシクロヘキシルおよびキヌクリジニルカルバメート誘導体 |
| WO2018108089A1 (zh) | 2016-12-14 | 2018-06-21 | 北京硕佰医药科技有限责任公司 | 一类具有季铵盐结构的双功能化合物 |
| US11841822B2 (en) | 2019-04-27 | 2023-12-12 | Cambricon Technologies Corporation Limited | Fractal calculating device and method, integrated circuit and board card |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITRM20110083U1 (it) | 2010-05-13 | 2011-11-14 | De La Cruz Jose Antonio Freire | Piastra per la costruzione di carrelli per aeroplani |
| EP2386555A1 (en) | 2010-05-13 | 2011-11-16 | Almirall, S.A. | New cyclohexylamine derivatives having beta2 adrenergic agonist and m3 muscarinic antagonist activities |
| EP2592078A1 (en) | 2011-11-11 | 2013-05-15 | Almirall, S.A. | New cyclohexylamine derivatives having beta2 adrenergic agonist and M3 muscarinic antagonist activities |
| TWI643853B (zh) | 2013-02-27 | 2018-12-11 | 阿爾米雷爾有限公司 | 同時具有β2腎上腺素受體促效劑和M3毒蕈鹼受體拮抗劑活性之2-氨基-1-羥乙基-8-羥基喹啉-2(1H)-酮衍生物之鹽類 |
| TWI641373B (zh) | 2013-07-25 | 2018-11-21 | 阿爾米雷爾有限公司 | 具有蕈毒鹼受體拮抗劑和β2腎上腺素受體促效劑二者之活性的2-胺基-1-羥乙基-8-羥基喹啉-2(1H)-酮衍生物之鹽 |
| TW201517906A (zh) | 2013-07-25 | 2015-05-16 | Almirall Sa | 含有maba化合物和皮質類固醇之組合 |
| JP6588924B2 (ja) * | 2014-04-25 | 2019-10-09 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | ルテニウムの触媒作用によってアニリド類からビフェニルアミン類を製造する方法 |
| TW201617343A (zh) | 2014-09-26 | 2016-05-16 | 阿爾米雷爾有限公司 | 具有β2腎上腺素促效劑及M3蕈毒拮抗劑活性之新穎雙環衍生物 |
| CN104557589A (zh) * | 2014-12-24 | 2015-04-29 | 天津大学 | N-(1,1’-二芳基)取代的酰胺类衍生物的制备方法 |
| CN107108502A (zh) * | 2015-05-14 | 2017-08-29 | 四川海思科制药有限公司 | 具有β2受体激动及M受体拮抗活性的联苯衍生物及其在医药上的用途 |
| CN107108562B (zh) * | 2015-05-14 | 2020-07-10 | 四川海思科制药有限公司 | 具有β2受体激动及M受体拮抗活性的含氮杂螺环衍生物及其在医药上的用途 |
| CN108854841B (zh) * | 2018-06-25 | 2020-09-29 | 长治学院 | 一种连接基含酯基的吡咯烷类手性Gemini表面活性剂及其制备方法 |
| CN111217746B (zh) * | 2020-03-10 | 2021-09-24 | 佛山市隆信医药科技有限公司 | 一种盐酸丙卡特罗的制备方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004007426A1 (en) | 2002-07-17 | 2004-01-22 | Chiang Long Y | Fullerene compounds |
| WO2004089892A2 (en) | 2003-04-01 | 2004-10-21 | Theravance, Inc. | Diarylmethyl and related compounds having beta2 andrenergic receptor agonist and muscarinic receptor antagonist activity |
| WO2004106333A1 (en) | 2003-05-28 | 2004-12-09 | Theravance, Inc. | Azabicycloalkane compounds as muscarinic receptor antagonists |
| JP2005509024A (ja) * | 2001-11-13 | 2005-04-07 | セラヴァンス インコーポレーテッド | アリールアニリンβ2アドレナリン作用性レセプタアゴニスト |
| JP2006517971A (ja) * | 2003-02-14 | 2006-08-03 | セラヴァンス インコーポレーテッド | β2アドレナリン作用性レセプターアゴニスト活性およびムスカリン性レセプターアンタゴニスト活性を有するビフェニル誘導体 |
| WO2007107828A2 (en) | 2006-03-20 | 2007-09-27 | Pfizer Limited | Amine derivatives |
| WO2008096127A2 (en) | 2007-02-07 | 2008-08-14 | Argenta Discovery Ltd | Bicyclo[2.2.1]hept-7-ylamine derivatives and their use as m3 muscarinic receptor modulators |
| WO2009098448A1 (en) | 2008-02-06 | 2009-08-13 | Astrazeneca Ab | Compounds |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3240784A (en) * | 1966-03-15 | Esters of quaternary z-hydroxy methyl piperidinium compounds | ||
| CN101239971B (zh) * | 2003-02-14 | 2011-07-20 | 施万制药 | 联苯衍生物 |
| JP4869066B2 (ja) | 2003-04-25 | 2012-02-01 | ケイオウエス ライフ サイエンスイズ,インコーポレイテッド | 丈夫な超多孔性ヒドロゲルの形成技術 |
| PT1656370E (pt) * | 2003-06-03 | 2012-11-29 | Rib X Pharmaceuticals Inc | Compostos biaril-heterocíclicos e métodos de os produzir e de os utilizar |
| PE20050231A1 (es) * | 2003-06-24 | 2005-05-20 | Novartis Ag | Derivados de piperidinium y pirrolidinium como antagonistas del receptor muscarinico m3 |
| TW200534855A (en) * | 2004-01-13 | 2005-11-01 | Glaxo Group Ltd | Muscarinic acetylcholine receptor antagonists |
-
2010
- 2010-04-27 KR KR1020117028059A patent/KR20120061061A/ko not_active Application Discontinuation
- 2010-04-27 MX MX2011011446A patent/MX2011011446A/es active IP Right Grant
- 2010-04-27 NZ NZ595810A patent/NZ595810A/xx not_active IP Right Cessation
- 2010-04-27 EP EP10769723A patent/EP2426121A4/en not_active Withdrawn
- 2010-04-27 CA CA2760630A patent/CA2760630A1/en active Pending
- 2010-04-27 BR BRPI1014390A patent/BRPI1014390A2/pt not_active IP Right Cessation
- 2010-04-27 WO PCT/JP2010/057422 patent/WO2010126025A1/ja active Application Filing
- 2010-04-27 US US13/266,651 patent/US9072734B2/en not_active Expired - Fee Related
- 2010-04-27 CN CN201080029330.3A patent/CN102459231B/zh not_active Expired - Fee Related
- 2010-04-27 AU AU2010242646A patent/AU2010242646A1/en not_active Abandoned
- 2010-04-27 MY MYPI2011005166A patent/MY155212A/en unknown
- 2010-04-27 SG SG2011097920A patent/SG177468A1/en unknown
- 2010-04-27 JP JP2011511402A patent/JP5379224B2/ja not_active Expired - Fee Related
- 2010-04-29 AR ARP100101446A patent/AR078121A1/es unknown
- 2010-04-30 TW TW099113895A patent/TWI486343B/zh not_active IP Right Cessation
-
2011
- 2011-10-27 IL IL216015A patent/IL216015A0/en unknown
- 2011-11-15 ZA ZA2011/08372A patent/ZA201108372B/en unknown
-
2012
- 2012-07-27 HK HK12107408.7A patent/HK1166790A1/xx not_active IP Right Cessation
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005509024A (ja) * | 2001-11-13 | 2005-04-07 | セラヴァンス インコーポレーテッド | アリールアニリンβ2アドレナリン作用性レセプタアゴニスト |
| WO2004007426A1 (en) | 2002-07-17 | 2004-01-22 | Chiang Long Y | Fullerene compounds |
| JP2006517971A (ja) * | 2003-02-14 | 2006-08-03 | セラヴァンス インコーポレーテッド | β2アドレナリン作用性レセプターアゴニスト活性およびムスカリン性レセプターアンタゴニスト活性を有するビフェニル誘導体 |
| WO2004089892A2 (en) | 2003-04-01 | 2004-10-21 | Theravance, Inc. | Diarylmethyl and related compounds having beta2 andrenergic receptor agonist and muscarinic receptor antagonist activity |
| WO2004106333A1 (en) | 2003-05-28 | 2004-12-09 | Theravance, Inc. | Azabicycloalkane compounds as muscarinic receptor antagonists |
| WO2007107828A2 (en) | 2006-03-20 | 2007-09-27 | Pfizer Limited | Amine derivatives |
| WO2008096127A2 (en) | 2007-02-07 | 2008-08-14 | Argenta Discovery Ltd | Bicyclo[2.2.1]hept-7-ylamine derivatives and their use as m3 muscarinic receptor modulators |
| WO2009098448A1 (en) | 2008-02-06 | 2009-08-13 | Astrazeneca Ab | Compounds |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP2426121A4 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014519508A (ja) * | 2011-06-10 | 2014-08-14 | キエスィ ファルマチェウティチ エス.ピー.エー. | ムスカリン受容体拮抗薬及びβ2アドレナリン受容体作動薬活性を有する化合物 |
| JP2016502557A (ja) * | 2012-12-06 | 2016-01-28 | チエシ ファルマスティスィ エス.ピー.エー. | ムスカリン受容体アンタゴニストおよびβ2アドレナリン受容体アゴニスト活性を有する化合物 |
| JP2016505582A (ja) * | 2012-12-18 | 2016-02-25 | アルミラル・ソシエダッド・アノニマAlmirall, S.A. | β2アドレナリンアゴニスト活性およびM3ムスカリンアンタゴニスト活性を有する新規のシクロヘキシルおよびキヌクリジニルカルバメート誘導体 |
| WO2018108089A1 (zh) | 2016-12-14 | 2018-06-21 | 北京硕佰医药科技有限责任公司 | 一类具有季铵盐结构的双功能化合物 |
| US11841822B2 (en) | 2019-04-27 | 2023-12-12 | Cambricon Technologies Corporation Limited | Fractal calculating device and method, integrated circuit and board card |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102459231A (zh) | 2012-05-16 |
| EP2426121A1 (en) | 2012-03-07 |
| TWI486343B (zh) | 2015-06-01 |
| BRPI1014390A2 (pt) | 2016-04-05 |
| JPWO2010126025A1 (ja) | 2012-11-01 |
| US20120046467A1 (en) | 2012-02-23 |
| EP2426121A4 (en) | 2012-10-31 |
| AR078121A1 (es) | 2011-10-19 |
| MX2011011446A (es) | 2011-11-18 |
| JP5379224B2 (ja) | 2013-12-25 |
| TW201103909A (en) | 2011-02-01 |
| US9072734B2 (en) | 2015-07-07 |
| SG177468A1 (en) | 2012-02-28 |
| AU2010242646A1 (en) | 2011-11-03 |
| CN102459231B (zh) | 2015-04-22 |
| HK1166790A1 (en) | 2012-11-09 |
| NZ595810A (en) | 2013-05-31 |
| IL216015A0 (en) | 2012-01-31 |
| KR20120061061A (ko) | 2012-06-12 |
| CA2760630A1 (en) | 2010-11-04 |
| ZA201108372B (en) | 2012-07-25 |
| MY155212A (en) | 2015-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5379224B2 (ja) | 四級アンモニウム塩化合物 | |
| JP6080051B2 (ja) | ムスカリン受容体拮抗薬及びβ2アドレナリン受容体作動薬活性を有する化合物 | |
| ES2329586T3 (es) | Compuestos que tienen actividad agonista del receptor beta2 adrenergico y antagonista del receptor muscarino. | |
| CN103936716B (zh) | 具蕈毒碱受体拮抗剂和β2肾上腺素受体激动剂活性的二酰胺化合物 | |
| KR101906630B1 (ko) | 무스카린 수용체 길항제 및 베타2 아드레날린 수용체 작용제 효능을 갖는 화합물 | |
| CA2971858A1 (en) | Compounds, compositions, and methods for increasing cftr activity | |
| BRPI0514413B1 (pt) | Sal cristalino de composto de bifenil, sua composição farmacêutica, seus processos de preparação, processo de purificação, usos do referido sal e medicamento. | |
| TW201945337A (zh) | 用於治療疾病之葡萄糖苷基腦醯胺(glucosylceramide)合成酶抑制劑 | |
| JP6905466B2 (ja) | ムスカリン受容体拮抗薬およびβ2アドレナリン受容体作動薬活性を有する化合物及び医薬品組成物 | |
| KR20150092126A (ko) | 무스카린성 수용체 길항제 및 베타2 아드레날린성 수용체 효능제 활성을 가지는 화합물 | |
| JP5807058B2 (ja) | 二機能キノリン誘導体 | |
| US8697724B2 (en) | Crystalline oxalate salts of a diamide compound | |
| EP1723111A1 (en) | Biphenyl compounds useful as muscarinic receptor antagonists | |
| ES2351392T3 (es) | Derivados bifenilo que tienen actividad agonista de receptores beta2-adrenérgicos y actividad antagonista de receptores muscarínicos. | |
| TW201625600A (zh) | 胺基酯衍生物 | |
| JP2020504724A (ja) | 4級アンモニウム塩構造を有する二官能性化合物 | |
| CA2911037A1 (en) | .alpha.-substituted glycinamide derivative | |
| JP2012107008A (ja) | 四級アンモニウム塩化合物 | |
| NZ618727B2 (en) | Compounds having muscarinic receptor antagonist and beta2 adrenergic receptor agonist activity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201080029330.3 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10769723 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011511402 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 595810 Country of ref document: NZ |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 216015 Country of ref document: IL Ref document number: 13266651 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: MX/A/2011/011446 Country of ref document: MX |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2760630 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2010242646 Country of ref document: AU Date of ref document: 20100427 Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 8616/DELNP/2011 Country of ref document: IN |
|
| ENP | Entry into the national phase |
Ref document number: 20117028059 Country of ref document: KR Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2011148582 Country of ref document: RU Kind code of ref document: A |
|
| REEP | Request for entry into the european phase |
Ref document number: 2010769723 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2010769723 Country of ref document: EP |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: PI1014390 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: PI1014390 Country of ref document: BR Kind code of ref document: A2 Effective date: 20111028 |