RU2247704C2 - Обработка композиции, включающей триметилолалкан бис-монолинейный формаль - Google Patents
Обработка композиции, включающей триметилолалкан бис-монолинейный формаль Download PDFInfo
- Publication number
- RU2247704C2 RU2247704C2 RU2001135811/04A RU2001135811A RU2247704C2 RU 2247704 C2 RU2247704 C2 RU 2247704C2 RU 2001135811/04 A RU2001135811/04 A RU 2001135811/04A RU 2001135811 A RU2001135811 A RU 2001135811A RU 2247704 C2 RU2247704 C2 RU 2247704C2
- Authority
- RU
- Russia
- Prior art keywords
- tmp
- tme
- mcp
- acid
- specified
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/09—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrolysis
- C07C29/10—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrolysis of ethers, including cyclic ethers, e.g. oxiranes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D319/00—Heterocyclic compounds containing six-membered rings having two oxygen atoms as the only ring hetero atoms
- C07D319/04—1,3-Dioxanes; Hydrogenated 1,3-dioxanes
- C07D319/06—1,3-Dioxanes; Hydrogenated 1,3-dioxanes not condensed with other rings
Abstract
Изобретение относится к усовершенствованному способу осуществления реакции трансалкоголиза триметилолпропан моноциклического формаля (ТМП-МЦФ) или триметилолэтан моноциклического формаля (ТМЭ-МЦФ) с избытком одноатомного или двухатомного спирта при повышенной температуре и в присутствии кислотного катализатора для получения триметилолпропана (ТМП) или триметилолэтана (ТМЭ), соответственно, которые используются в качестве промежуточных соединений для получения широкого круга продуктов, и побочного продукта – ацеталя, а также относится к способу осуществления взаимодействия композиции, содержащей, по меньшей мере, 10 мас.% триметилолпропан-бис-монолинейного формаля (ТМП-БМЛФ) или триметилолэтан-бис-монолинейного формаля (ТМЭ-БМЛФ), не более чем около 5 мас.% воды и одноатомный или двухатомный спирт в избытке от стехиометрического количества, с сильным кислотным катализатором при температуре 30-3000С и в течение промежутка времени, достаточного для превращения значительного количества указанного ТМП-БМЛФ или ТМЭ-БМЛФ в триметилолпропан или триметилолэтан, соответственно, и побочный продукт - ацеталь. Способ позволяет получить дополнительное количество целевых продуктов. 2 н. и 25 з.п. ф-лы, 11 табл.
Description
Перекрестная ссылка на родственную заявку
Данная заявка является частичным продолжением заявки №09/324435, поданной 1 июня 1999.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Область изобретения
Настоящее изобретение относится к новому способу обработки композиции, содержащей триметилолалкан бис-монолинейный формаль, такой, которую получают в виде остатков тяжелых фракций при очистке сырых триметилолалканов, с получением полезных соединений.
Описание известного уровня техники
Триметилолпропан (ТМП) и триметилолэтан (ТМЭ) являются хорошо известными химическими продуктами, которые используют в качестве промежуточных соединений при получении широкого круга продуктов, например лаков, алкидных и полиэфирных смол, синтетических сохнущих маcел, уретановых пен и покрытий, силиконовых смазочных маcел, лактоновых пластификаторов, средств для обработки текстиля, поверхностно-активных средств, продуктов эпоксидирования и т.д. ТМП и ТМЭ получают при взаимодействии одного моля н-бутиральдегида или пропиональдегида, соответственно, с избытком в 3 моля формальдегида в водной среде и в присутствии щелочного конденсирующего агента. Однако эти условия приводят к образованию не только ТМП или ТМЭ, но также и высококипящих примесей. Таким образом, возникает необходимость подвергнуть полученный в реакции сырой ТМП или ТМЭ продукт процессу очистки, который включает стадии перегонки и экстракции растворителем, не только для отделения относительно чистых ТМП или ТМЭ от избытка формальдегида, воды и основного конденсирующего агента, но также и от высококипящих примесей.
Критической стадией процесса очистки, для получения относительно чистых ТМП или ТМЭ, из сырого продукта реакции является вакуумная перегонка или “флешинг” массы ТМП или ТМЭ, полученных в реакции, которые таким образом удаляют в виде паров; при этом высококипящие примеси остаются в виде жидкого тяжелого остатка. Хотя такой остаток может все еще содержать ТМП или ТМЭ, процентное содержание этих желаемых соединений довольно мало, и с экономической точки зрения их трудно выделить. Кроме того, некоторые из высококипящих примесей, получаемых в реакции в достаточно больших количествах, имеют лишь ограниченную коммерческую ценность. Поэтому был бы очень желателен любой способ обработки остатка тяжелых фракций или любого из соединений, присутствующих в таких остатках в больших количествах, позволяющий преобразовать, по крайней мере, часть таких соединений в ТМП или ТМЭ и/или другие более ценные соединения.
В патенте США №3076854, выданном 5 февраля 1963 г. Клейну (Klein), описан способ очистки сырого ТМП - продукта с помощью процесса, включающего экстракцию реакционного раствора не смешивающимся с водой растворителем ТМП, например, н-бутанолом или амиловым спиртом, и последующую экстракцию полученного экстракта водой с получением вторичного экстракта, содержащего ТМП с примесью формиата металла и продуктов, содержащих несколько замещаемых атомов водорода; отделение водного вторичного экстракта очищенного от легких фракций растворителя, нагревание загрязненного ТМП с метанолом или другим низшим спиртом и минеральной кислотой для образования формиата металла в соль добавленной кислоты, и дальнейшую обработку водного вторичного экстракта, содержащего ТМП, с помощью кислотной катионообменной смолы для удаления из раствора ионов металла.
В патенте Великобритании №1290036 описан способ выделения триметилпропан-монометилформаля из сырого продукта ТМП путем обработки продукта сульфокислотной катионообменной смолой. Триметилолпропан-монометилформаль разлагается с образованием триметилолпропан-моноциклического формаля и метанола.
В патенте Германской Демократической Республики №142184 описан способ выделения ТМП из высококипящих остатков, включающий добавление воды и метанола к остаткам, так, чтобы они содержали, по крайней мере, 15 мас.% воды или 10-40 мас.% метанола, предварительную обработку остатков с помощью катионообменной смолы для удаления следов конденсирующего агента, содержащегося в остатках, обработку остатков в условиях перегонки сильно кислотной, высоко поперечно-сшитой катионообменной смолой на основе полистирола и выделение образовавшегося ТМП обычными способами выделения.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
Частью описанного здесь изобретения является обнаружение того, что основная часть остатка тяжелых фракций, полученного после удаления массы ТМП или ТМЭ, избытка формальдегида, воды и основного конденсирующего агента представляет собой триметилолалкан бис-монолинейный формаль следующей формулы:
где R представляет собой этил в случае триметилолпропан-бис-монолинейного формаля (ТМП-БМЛФ) СА Index Name: 1,3-пропандиол, 2,2’-[метиленбис(оксиметилен)]бис[2-этил-], CAS No. [93983-16-5], или метил в случае триметилолэтан-бис-монолинейного формаля (ТМЭ-БМЛФ), СА Index Name: 1,3-пропандиол, 2,2’-[метиленбис(оксиметилен)]бис[2-метил-], CAS No. [636073-72-5]. Таким образом, в соответствии с более широким аспектом, настоящее изобретение включает то, что композицию, содержащую значительное количество в процентах, например, по крайней мере, около 40 мас.% ТМП-БМЛФ или ТМЭ-БМЛФ, не более чем около 5 мас.% воды и не более чем около 0,5 мас.% метанола (все проценты даны в расчете на общую массу композиции), подвергают взаимодействию с сильным кислотным катализатором при повышенной температуре и в течение достаточного промежутка времени для преобразования значительного количества указанного ТМП-БМЛФ или ТМЭ-БМЛФ до ТМП или ТМЭ, и соответствующего триметилолалкан-бис-монолинейного формаля следующей формулы:
где R представляет собой этил в случае триметилолпропан моноциклического формаля (ТМП-МЦФ) СА Index Name 1,3-диоксан-5-метанол, 5-этил, САS №[5187-23-5]; или метил в случае триметилолэтан-моноциклического формаля (ТМЭ-МЦФ) СА Index Name: 1,3-диоксан-5-метанол, 5-метил, CAS №[1121-97-7]. Дополнительные количества ТМП и ТМП-МЦФ или ТМЭ и ТМЭ-МЦФ, полученные по этому способу, имеют гораздо большую ценность, чем израсходованные ТМП-БМЛФ или ТМЭ-БМЛФ. Во многих случаях обрабатываемые композиции представляют собой остатки тяжелых фракций, полученные из сырых ТМП или ТМЭ продуктов в процессе очистки после того, как были выделены массы воды, избыток формальдегида, основный конденсирующий агент и очищенные ТМП или ТМЭ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Композиция, которую подвергают кислотной обработке по способу настоящего изобретения, во многих случаях содержит, например, по крайней мере, 10 мас.%, предпочтительно, по крайней мере около 20-30 мас.% ТМП-БМЛФ или ТМЭ-БМЛФ, обычно без воды, или содержит не более чем около 5 мас.%, предпочтительно не более чем около 1,0 мас.% воды и не более чем около 0,5 мас.%, предпочтительно не более чем около 0,1 мас.% метанола. Кроме того, подлежащая обработке композиция обычно содержит не более чем около 5 мас.%, предпочтительно не более чем около 0,6 мас.%, любого соединения в свободной форме, имеющего температуру кипения при атмосферном давлении ниже температуры кипения воды, такого как формальдегид. Композицию подвергают воздействию при повышенной температуре, например, от около 30°С до около 300°С, предпочтительно от около 90°C до около 220°С, катализатора на основе сильной кислоты в течение промежутка времени, например, от около 2 до около 8 часов, предпочтительно от около 1 до около 6 часов, достаточного для преобразования значительного количества ТМП-БМЛФ или ТМЭ-БМЛФ в ТМП и ТМП-МЦФ или ТМЭ и ТМЭ-МЦФ, соответственно.
В качестве катализатора для способа настоящего изобретения можно использовать любую сильную кислоту. Хотя такой кислотой может быть неорганическая кислота, такая как серная или фосфорная, в большинстве случаев предпочтительно использовать алкансульфоновую кислоту, такую как метансульфоновая кислота, арилсульфоновую кислоту, такую как толуолсульфоновая кислота, или сульфированную катионообменную смолу в кислотной форме, например сульфированную катионообменную смолу на основе полистирола. Количество кислоты может меняться в очень широких пределах, но чаще она бывает в таком количестве, чтобы кислотность реакции преобразования была в интервале, например, эквивалентном кислотности, даваемой сильной кислотой, взятой в количестве менее чем около 15 мас.%, предпочтительно от около 0,3 до около 1,3 мас.%.
Обычно сильную кислоту добавляют в количестве, достаточном для достижения величины рН в интервале не менее чем около 4, предпочтительно в интервале от 2 до 3; было обнаружено, что очищенный БМЛФ оптимально преобразуется в ТМП примерно за 4 часа при около 102°С, рН около 2,35.
Как предполагалось ранее, в композиции может быть небольшое количество воды, менее 5 мас.%, которую подвергают кислотной обработке по способу настоящего изобретения. Кроме того, дополнительное количество воды образуется в результате преобразования ТМП-БМЛФ или ТМЭ-БМЛФ в ТМП-МЦФ или ТМЭ-МЦФ, соответственно. Хотя это и не необходимо для достижения преимуществ способа, в некоторых случаях может оказаться желательным поддерживать количество воды на более низком уровне, чем обычно используется. Для этой цели перед началом реакции можно добавить небольшое количество, например, менее чем около 15 мас.%, предпочтительно, менее чем около 10 мас.% в расчете на массу композиции соединения, которое образует низкокипящий азеотроп с водой и практически не смешивается ни с одним из компонентов композиции. Такое соединение предпочтительно является углеводородом, например циклогексаном, толуолом или бензолом.
Как указывалось, способ настоящего изобретения приводит к преобразованию значительного количества ТМП-БМЛФ или ТМЭ-БМЛФ в исходной композиции в ТМП и ТМП-МЦФ или ТМЭ и ТМЭ-МЦФ, соответственно. Например, в случае ТМП было обнаружено, что продукт, образующийся в результате кислотной обработки по способу настоящего изобретения, может содержать, по крайней мере, примерно на 5 мас.% больше ТМП-МЦФ, чем имеется в исходной композиции, подвергающейся такой кислотной обработке (в расчете на общую массу композиции).
Напротив, например, количество ТМП-БМЛФ в продукте оказалось сниженным на, по крайней мере, примерно 70 мас.%, по сравнению с исходной композицией (в расчете на вес ТМП-БМЛФ перед кислотной обработкой).
Как было указано ранее, композиция, подвергающаяся обработке по способу настоящего изобретения, во многих случаях получается как остаток тяжелых фракций процесса получения ТМП или ТМЭ в реакции н-бутиральдегида или пропиональдегида с формальдегидом в водной системе в присутствии основного конденсирующего агента, такого как гидроксид натрия. Такой остаток получают при очистке продукта реакции, включающей следующие стадии: 1) удаления избытка формальдегида; 2) удаления воды; 3) выделения ТМП или ТМЭ и высококипящих примесей из подлежащей очистке жидкости, и основного конденсирующего агента, и 4) нагревания сырого ТМП в вакууме, для мгновенного испарения и выделения ТМП или ТМЭ с высокой степенью чистоты. Полученный остаток представляет собой остаток тяжелых фракций, содержащий высококипящие примеси, предназначенные для обработки кислотой по способу настоящего изобретения.
Если подлежащая обработке композиция представляет собой остаток тяжелых фракций из ТМП процесса, такая композиция обычно содержит, кроме ТМП-БМЛФ, ТМП в количестве, менее чем около 60 мас.%, обычно от около 8 до около 20 мас.%, менее чем около 15 мас.%, обычно от около 7 до около 10 мас.% дитриметилпропана (Di-ТМП). Количество ТМП-МЦФ, присутствующего в указанном остатке тяжелых фракций, обычно меньше, чем количество последних соединений, обычно менее чем около 0,1 мас.%, и часто не определяется.
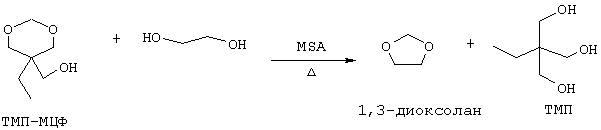
В соответствии с другим аспектом изобретения ТМП-МЦФ или ТМЭ-МЦФ в композиции, получаемой в процессе настоящего изобретения, подвергают реакции трансалкоголиза с избытком одноатомного или двухатомного спирта, например, содержащего от 1 до 6 атомов углерода, при повышенной температуре, например от около 30 до около 300°С, в присутствии кислотного катализатора, например любой из тех же кислот, которые были указаны ранее в связи с кислотной обработкой ТМП-БМЛФ или ТМЭ-БМЛФ, для получения дополнительного количества ТМП или ТМЭ и побочного продукта ацеталя, который часто представляет коммерческий интерес. Так, например, ТМП-МЦФ или ТМЭ-МЦФ в композиции, полученной в результате кислотной обработки по способу настоящего изобретения, можно подвергнуть взаимодействию с избытком метанола для получения дополнительного количества ТМП или ТМЭ и метилаля, который используют в качестве растворителя в органическом синтезе, в парфюмерии, в адгезивах и т.д., тогда как ТМП-МЦФ или ТМЭ-МЦФ можно подвергнуть взаимодействию с этиленгликолем для получения дополнительного количества ТМП или ТМЭ и 1,3-диоксолана, который можно использовать в качестве низкокипящего растворителя и в качестве экстрагирующего агента для масел, жиров, восков, красителей и производных целлюлозы.
В дополнении к их использованию в качестве промежуточных соединений в реакциях трансалкоголиза для получения дополнительных количеств ТМП или ТМЭ и других полезных соединений ТМП-МЦФ и ТМЭ-МЦФ можно использовать для получения полезных продуктов в других реакциях. Как раскрыто в патентах США №4076727; 4207155 и 4876368, можно получить сложный акрилатный и метакриловый эфиры ТМП-МЦФ и ТМЭ-МЦФ, которые можно использовать в качестве реакционноспособных мономеров при создании кроющих композиций, пластиковых пленок, волокон, пластиковых покрытий и в качестве растворителей в различных ненасыщенных системах, особенно в отверждаемых ультрафиолетом кроющих композициях.
Нижеследующие примеры иллюстрируют далее изобретение. Небольшие количества воды удаляют из системы, используя циклогексан в качестве агента для азеотропной перегонки.
Примеры 1 и 1А
В примере 1 в круглодонную колбу, снабженную верхней мешалкой, ловушкой Дина-Старка с конденсатором и системой обогрева, загружают при комнатной температуре 91,30 г предварительно проанализированного остатка тяжелых фракций, полученного в результате очистки сырого ТМП продукта, как было раскрыто выше, 12,53 г циклогексана, и 0,25 г метансульфоновой кислоты в качестве катализатора. Содержимое нагревают до 98°С в течение 90 минут и отбирают образец продукта для анализа.
В примере 1А повторяют процедуру примера 1, за исключением того, что содержимое нагревают до 110°С в течение 275 мин.
В таблице I представлены композиции исходного остатка тяжелых фракций и обработанных композиций примеров 1 и 1А в массовых процентах наиболее существенных компонент в расчете на полную массу композиции.
| Таблица I | |||
| Компонент | Исходное сырье | Обработанные композиции | |
| Пример 1 | Пример 1А | ||
| ТМП-МЦФ | 0,05% | 27,77% | 25,64 |
| ТМП | 22,67% | 36,31% | 34,13 |
| ТМП-ацетат | Не определено | Не определено | 0,15 |
| Ди-ТМП | 7,65% | 4,39% | 3,54 |
| ТМП-БМЛФ | 41,74% | 0,55% | Не определено |
| ДМБ | 0,11% | 8,86% | 7,66 |
| ММБ | 5,99% | 0,31% | 0,25 |
Пример 2
Повторяют процедуру примеров 1 и 1А, за исключением того, что исходная загрузка составляет 462,00 г остатка тяжелых фракций, 69,19 г циклогексана и, в качестве катализатора, 69,19 г катионообменной смолы на основе сульфированного акрил-полистирола в кислотной форме, поставляемого под торговой маркой “Amberlyst 36 (dry)” Rohm and Haas Co. При использовании катализатора из твердой смолы экспериментальный реактор модифицируют следующим образом: смолу взвешивают и выливают в “сетчатую корзину из нержавеющей стальной проволоки”, которая прикреплена к валу мешалки. Эта корзина выполнена в форме, похожей на “X”, и имеет четыре компонента, которые заполнены смолой. После заполнения корзину соединяют с мотором верхней мешалки. Каждая из сторон “корзины” имеет в длину примерно 7,5 см, ширину 4 см и глубину 1,5 см, и размер ячеек проволочной сетки составляет примерно 42 меш. Конструкция и использование корзины позволяют осуществлять тесный контакт остатка тяжелых фракций с твердой кислотной смолой, а также предотвратить разложение твердого катализатора в результате “растирания” перемешивающими лопастями мешалки.
Содержимое реактора нагревают с 25 до 99,6°С за 190 минут и выдерживают в интервале между 99,5 и 99,8°С в течение еще 180 минут (полное время нагревания 370 мин). Состав образцов, отобранных с различными временными интервалами, и соответствующие температуры представлены в таблице II. “N/D” означает “не определяется”.
| Таблица II | ||||||
| Время (мин) | Темп., °С | ТМП-МЦФ | ТМП | Ди-ТМП | ТМП-БМЛФ | Н2O |
| 0 | 25 | N/D | 10,04 | 7,11 | 58,56 | 0,10 |
| 40 | 83,4 | 0,42 | 10,85 | 7,00 | 52,90 | 0,25 |
| 105 | 95,5 | 23,28 | 26,87 | 4,23 | 5,60 | 0,79 |
| 190 | 99,6 | 32,77 | 28,58 | 4,46 | 0,61 | 0,56 |
| 250 | 99,8 | 32,89 | 28,43 | 4,18 | 0,56 | 0,53 |
| 320 | 99,6 | 32,84 | 28,46 | 4,06 | 0,56 | 0,53 |
| 370 | 99,5 | 31,36 | 27,19 | 3,88 | 0,53 | 0,53 |
Пример 3
Повторяют процедуру примера 2, за исключением того, что исходная загрузка составляет 709,43 г остатка тяжелых фракций, 96,00 г циклогексана и, в качестве катализатора, 67,35 г катионообменной смолы на основе сульфонированного акрил-полистирола в кислотной форме, поставляемого как “Amberlyst 35 (dry)” Rohm and Haas Co.
Содержимое реактора нагревают с 25 до 95,7°С за 295 минут; состав образцов, отобранных с различными интервалами времени, и температуры, представлен в таблице III.
| Таблица III | ||||||
| Время (мин) | Темп., °С | ТМП-МЦФ | ТМП | Ди-ТМП | ТМП-БМЛФ | H2O |
| 0 | 25 | N/D | 10,04 | 7,11 | 58,56 | 0,10 |
| 38 | 73,9 | N/D | 10,38 | 7,31 | 57,54 | 0,28 |
| 72 | 83,3 | 14,81 | 25,07 | 4,05 | 11,02 | 1,39 |
| 130 | 91,6 | 34,06 | 30,64 | 4,81 | 0,63 | 1,03 |
| 175 | 93 | 33,24 | 30,03 | 4,52 | 0,61 | 1,25 |
| 245 | 94,3 | 33,65 | 29,77 | 4,20 | 0,62 | 0,63 |
| 295 | 95,7 | 33,5 | 30,02 | 4,30 | 0,62 | 0,89 |
Пример 4
Повторяют процедуру примера 1, за исключением того, что исходная загрузка реактора составляет 157,85 г остатка тяжелых фракций, 24,58 г циклогексана, и, в качестве катализатора, 0,86 г модифицированной толуолсульфоновой кислоты, поставляемой как “Witco TX Acid” Witco Chemical Corp., содержащей 1,0 мас.% влаги и 2,0 мас.% серной кислоты, с температурой плавления ниже 15°С, удельной массой 1,30 при 254°С и с кислотным числом 330. Содержимое реактора нагревают с 25 до 200°С за 182 минуты; состав образцов, отобранных с различными временными интервалами, и температуры представлены в таблице IV.
| Таблица IV | ||||||
| Время (мин) | Темп., °С | ТМП-МЦФ | ТМП | Ди-ТМП | ТМП-БМЛФ | H2O |
| 0 | 25 | N/D | 10,04 | 7,11 | 58,56 | 0,10 |
| 60 | 100 | 31,39 | 29,62 | 5,07 | 0,78 | 0,20 |
| 75 | 112 | 32,65 | 30,80 | 5,14 | 0,65 | 0,10 |
| 80 | 127 | 32,37 | 31,31 | 5,06 | 0,71 | 0,14 |
| 85 | 143 | 32,28 | 32,22 | 4,55 | 0,62 | 0,11 |
| 98 | 160 | 33,00 | 32,13 | 4,51 | 0,80 | 0,27 |
| 108 | 175 | 34,06 | 31,72 | 4,38 | 0,80 | 0,38 |
| 120 | 185 | 36,61 | 27,89 | 3,76 | 0,82 | 0,45 |
| 151 | 190 | 41,66 | 20,45 | 2,58 | 0,75 | 0,37 |
| 182 | 200 | 46,13 | 57,43 | 2,36 | 0,84 | 0,34 |
Пример 5
Повторяют процедуру примера 4, за исключением того, что исходная загрузка реактора составляет 186,54 г остатка тяжелых фракций, 24,82 г циклогексана и 0,92 г модифицированной толуолсульфоновой кислоты в качестве катализатора. Содержимое реактора нагревают до 121°С за 138 минут и выдерживают при температуре от 121 до 133°С еще 265 минут, при этом полное время нагревания составляет 403 минуты. Состав образцов, отобранных с различными временными интервалами, и температуры представлены в таблице V.
| Таблица V | ||||||
| Время (мин) | Темп., °С | ТМП-МЦФ | ТМП | Ди-ТМП | ТМП-БМЛФ | H2O |
| 0 | 25 | N/D | 10,04 | 7,11 | 58,56 | 0,10 |
| --- | 40 | 2,09 | 17,66 | 6,23 | 39,4 | 0,81 |
| 11 | 50 | 11,91 | 25,97 | 4,13 | 11,61 | 0,62 |
| 17 | 60 | 12,56 | 25,53 | 4,21 | 11,02 | 0,72 |
| 24 | 74 | 16,36 | 26,77 | 4,36 | 8,46 | 0,85 |
| 28 | 80 | 12,76 | 25,91 | 4,23 | 11,62 | 0,79 |
| 59 | 90 | 29,88 | 28,81 | 5,04 | 0,85 | 0,52 |
| 88 | 100 | 31,66 | 29,92 | 4,99 | 0,62 | 0,19 |
| 126 | 112 | 31,80 | 31,71 | 4,51 | 0,73 | 0,12 |
| 138 | 121 | 32,38 | 32,22 | 4,39 | 0,72 | 0,12 |
| 151 | 125 | 32,67 | 32,01 | 4,43 | 0,78 | 0,19 |
| 223 | 125 | 34,8 | 28,71 | 4,04 | 0,78 | 0,36 |
| 283 | 133 | 34,56 | 28,26 | 3,92 | 0,72 | 0,15 |
| 343 | 121 | 34,22 | 27,6 | 3,76 | 0,65 | 0,17 |
| 403 | 126 | 35,39 | 28,11 | 4,06 | 0,76 | 0,11 |
Как видно из результатов, представленных выше в таблицах примеров 1-5, кислотная обработка остатка тяжелых фракций в условиях настоящего изобретения, полученного при очистке сырого ТМП продукта, содержащего значительный процент ТМП-БМЛФ, приводит к превращению основной массы ТМП-БМЛФ в ТМП и ТМП-МЦФ. Соответствующая кислотная обработка остатка тяжелых фракций, полученного при очистке сырого ТМЭ продукта, приводит к аналогичному превращению ТМЭ-БМЛФ в этом остатке в ТМЭ и ТМЭ-МЦФ.
Как указывалось выше, ТМП-МЦФ или ТМЭ-МЦФ в композиции, полученной в процессе настоящего изобретения, можно подвергнуть реакции трансалкоголиза с избытком одноатомного или двухатомного спирта в присутствии кислотного катализатора для получения дополнительного ТМП или ТМЭ и ценного побочного продукта - ацеталя. Реакцию можно вести при температуре от около 20°С до около 400°С, предпочтительно от около 25°С до около 300°С и более предпочтительно от около 35°С до около 110°С, и ее можно вести в течение промежутка времени, например от около 0 до около 300 минут, предпочтительно от около 60 до около 240 минут.
Одноатомный или двухатомный спирт, который реагирует с ТМП-МЦФ или ТМЭ-МЦФ, может содержать, например, от 1 до около 6 атомов углерода, как, например, метанол для получения метилаля, этиленгликоль для получения 1,3-диоксолана, 1-пропанол для получения ди-1-пропоксиметана, 2-пропанол для получения ди-2-пропоксиметана или 2-бромпропанол для получения ди-2-бромпропоксиметана, причем каждый в дополнении к ТМП или ТМЭ. Как было также указано ранее, кислотный катализатор для этой реакции может быть любым из сильных жидких или твердых кислотных катализаторов, раскрытых как подходящие для осуществления катализа реакции между ТМП-БМЛФ или ТМЭ-БМЛФ с образованием ТМП-МЦФ или ТМЭ-МЦФ и дополнительного ТМП или ТМЭ, соответственно. Например, реакция ТМП-МЦФ с этиленгликолем (ЭГ) для получения 1,3-диоксолана и дополнительного ТМП, протекает в соответствии со следующим уравнением:
Количество одноатомного или двухатомного спирта может быть в интервале, например, несколько больше стехиометрического количества, необходимого для взаимодействия с ТМП-МЦФ или ТМЭ-МЦФ для получения дополнительного количества ТМП или ТМЭ и побочного продукта - ацеталя, т.е. двух молей одноатомного спирта на моль ТМП-МЦФ или ТМЭ-МЦФ, или вплоть до около 5-20-кратного избытка над вышеуказанным стехиометрическим количеством. Реально используемое количество зависит от различных факторов, известных специалистам, например, используемого спирта, концентрации реагентов в обрабатываемом потоке, наряду с другими факторами.
ТМП-МЦФ или ТМЭ-МЦФ, которые реагируют с одноатомным или двухатомным спиртом, могут быть относительно чистым материалом, таким как материал, получаемый при дальнейшей перегонке содержащих ТМП-МЦФ или ТМЭ-МЦФ материалов, полученных в результате кислотной обработки способом настоящего изобретения, содержащего ТМП-БМЛФ или ТМЭ-БМЛФ остатка тяжелых фракций, оставшегося после удаления массы ТМП или ТМЭ, избытка формальдегида, воды и основного конденсирующего агента из продукта реакции н-бутиральдегида или пропиональдегида с формальдегидом. Такое превращение относительно чистого ТМП-МЦФ с помощью этиленгликоля (EG) проиллюстрировано в примере 6.
Пример 6
В реактор, описанный в примерах 1 и 1А, вначале загружают ЭГ (50,5 г, 0,82 моль), затем ТМП-МЦФ (30,25 г, 0,21 моль) и, наконец, метансульфоновую кислоту (MSA) в виде 70% по массе раствора (0,13 г, 0,001 моль). Затем реакционную смесь медленно нагревают до около 205°С.
По данным газовой хроматографии (ГХ) состав исходной загрузки при комнатной температуре (25,5°С) до добавления MSA составляет 1,39 мас.% Н2O, 63,59 мас.% ЭГ и 36,95 мас.% ТМП-МЦФ и неопределяемое количество 1,3-диоксолана, ТМП или ди-ТМП. Температура и состав отбираемых образцов после добавления MSA через различные интервалы времени, выраженный в мас.% наиболее значимых компонентов, определенной с помощью ГХ, представлены в таблице VI, где “ND” означает “не определяется”.
| Таблица VI | |||||||
| Время (мин) | Темп., °С | Н2О | 1,3-Диоксолан | ЭГ | ТМП-МЦФ | ТМП | ди-ТМП |
| 0 | 25,5 | 0,97 | ND | 56,15 | 37,44 | <0,1 | ND |
| 15 | 51,0 | 1,08 | ND | 61,89 | 36,9 | <0,1 | ND |
| 30 | 87,8 | 1,16 | ND | 62,52 | 36,64 | 0,1 | ND |
| 45 | 116,0 | 0,95 | 1,02 | 56,46 | 29,16 | 5,86 | ND |
| 60 | 134,6 | 0,82 | 1,57 | 54,94 | 27,83 | 7,38 | ND |
| 90 | 152,1 | 1,15 | 2,01 | 55,9 | 26,45 | 8,35 | ND |
| 120 | 159,7 | 1,00 | 2,07 | 52,18 | 26,45 | 8,07 | ND |
| 150 | 158,0 | 1,02 | 1,12 | 53,43 | 25,94 | 8,88 | ND |
| 180 | 162,7 | 1,13 | 1,52 | 51,11 | 25,97 | 9,06 | ND |
| 210 | 164,1 | 1,08 | 1,39 | 51,53 | 24,75 | 10,65 | ND |
| 240 | 165,5 | 1,20 | 1,24 | 50,25 | 24,61 | 11,61 | ND |
| 270 | 168,7 | 1,23 | 0,73 | 47,17 | 24,55 | 12,57 | ND |
| 300 | 171,1 | 1,15 | 0,94 | 50,43 | 21,01 | 15,52 | ND |
| 330 | 169,5 | 1,18 | 0,78 | 49,12 | 19,86 | 16,73 | ND |
| 360 | 170,9 | 1,14 | 0,77 | 47,82 | 18,53 | 18,41 | ND |
| 390 | 170,3 | 1,12 | 0,65 | 46,17 | 17,54 | 19,34 | ND |
| 420 | 170,6 | 1,27 | ND | 44,62 | 17,49 | 19,91 | ND |
| 450 | 184,2 | 1,11 | 0,28 | 43,59 | 13,10 | 23,84 | <0,4 |
| 480 | 189,1 | 1,27 | 0,40 | 38,98 | 8,52 | 24,65 | <0,4 |
| 510 | 190,2 | 1,1 | ND | 35,63 | 5,71 | 26,8 | 0,37 |
| 540 | 195,6 | 0,86 | ND | 29,53 | 3,73 | 25,46 | 0,89 |
| 570 | 196,8 | 1,09 | ND | 26,26 | 3,10 | 21,64 | 1,16 |
| 615 | 202,7 | 1,09 | ND | 16,26 | 3,67 | 15,9 | 0,99 |
| 662 | 204,4 | 0,89 | ND | 11,57 | 2,86 | 10,56 | 1,03 |
Реакционный раствор сразу после добавления MSA становится бесцветным. Через 150 минут протекания реакции цвет реакционного раствора становится бледно-желтым. Через 180 минут ловушка Дина-Старка начинает заполняться. Через 360 минут реакционный раствор становится коричневым.
Ловушку Дина-Старка (DST) опорожняют через 480 минут, и жидкость, накопившаяся в ловушке, образует две фазы через 510 минут. После завершения реакции по данным ГХ реакционный раствор содержит 0,92 мас.% H2O, 9,03 мас.% ЭГ, 3,34 мас.% ТМП-МЦФ, 10,59 мас.% ТМП и 0,97 мас.% ди-ТМП. В результате донная фаза в ловушке весит 6,72 г и содержит по данным ГХ 56,24 мас.% Н2О и 24,56 мас.% 1,3-диоксолана; и верхняя фаза в ловушке весит 4,28 г и содержит 3,97 мас.% Н2O и 27,2 мас.% 1,3-диоксолана, тогда как содержимое ловушки, извлеченное после 480 минут реакции, весит 10,55 г и содержит 13,16 мас.% Н2О и 78,75 мас.% 1,3-диоксолана.
На основании данных ГХ анализа оказывается, что полное количество собранного 1,3-диоксолана составляет 11,12 г (0,15 моль). Однако, на основании анализа воды, оказывается, что количество полученного 1,3-диоксолана составляет 16,21 г (0,21 моль). Такое расхождение можно приписать отчасти факторам, которые связаны с методом ГХ. Так как в методе газовой хроматографии не наблюдается других компонентов, результат, полученный на основании анализа воды, по-видимому, является более точным. Количество ТМП, оставшегося в реакционной смеси к концу эксперимента, определено как 2,46 г, (0,018 моль). Однако, как было найдено в процессе получения 1,3-диоксолана, количество ТМП составляет 7,42 г (0,53 моль). Высокую температуру реакции легко объяснить небольшим количеством образующегося ТМП.
Хотя ТМП-МЦФ или ТМЭ-МЦФ для указанной выше реакции трансалкоголиза с одноатомным или двухатомным спиртом для получения ТМП или ТМЭ и побочного продукта - ацеталя, были описаны как полученные в результате обработки ТМП-БМЛФ или ТМЭ-БМЛФ, полученных в реакции н-бутиральдегида или пропиональдегида с формальдегидом, для получения ТМП или ТМЭ, эти ТМП-МЦФ или ТМЭ-МЦФ для реакции трансалкоголиза фактически могут быть получены из любого источника.
При очистке содержащего ТМП или ТМЭ, ТМП-МЦФ или ТМЭ-МЦФ, соответственно, полученных в результате кислотной обработки осадка, содержащего ТМП-БМЛФ или ТМЭ-БМЛФ, легкие фракции верхнего погона получают в результате окончательной обработки перегонкой сырых ТМП или ТМЭ, причем такие легкие фракции содержат некоторое количество ТМП или ТМЭ, а также небольшие количества ТМП-МЦФ или ТМЭ-МЦФ, соответственно. Однако последние соединения, как было обнаружено, представляют при промывке кислотой образующие окраску агенты, т.е. они окрашивают ТМП или ТМЭ, когда последние подвергаются контактированию с кислотой в некоторых применениях. Хотя относительно легко отделить ТМП-МЦФ или ТМЭ-МЦФ от ТМП или ТМЭ в результате перегонки, это приводит к некоторым потерям ТМП или ТМЭ, рециклизуемых в систему. Так, в соответствии с другим аспектом настоящего изобретения, легкие фракции верхнего погона подвергают обработке избытком одноатомного или двухатомного спирта в присутствии кислотного катализатора для осуществления трансалкоголиза, по крайней мере, части ТМП-МЦФ или ТМЭ-МЦФ, присутствующих в потоке, получаемом при образовании дополнительного количества ТМП или ТМЭ и ценного побочного продукта - ацеталя.
Легкая фракция верхнего погона, которую подвергают обработке с помощью трансалкоголиза, обычно содержит некоторое количество ТМП или ТМЭ, например, около 70 мас.%, предпочтительно от около 50 до около 60 мас.%, и ТМП-МЦФ или ТМЭ-МЦФ в количестве, например, от около 1 до 15 мас.%, предпочтительно от около 2 до около 10 мас.%. Условия в отношении времени и температуры и примеры подходящих кислотных катализаторов те же самые, что и указанные выше для трансалкоголиза относительно чистых ТМП-МЦФ или ТМЭ-МЦФ. Трансалкоголиз ТМП-МЦФ в легких фракциях верхнего погона потока ТМП с использованием MSA в качестве катализатора и этиленгликоля в качестве реагирующего спирта проиллюстрирован в примерах 7 и 8.
Пример 7
В реактор, описанный в примерах 1 и 1А, загружают 121,9 г легкой фракции верхнего погона ТМП, содержащей 4,15 мас.% ТМП-МЦФ (5,06 г, 0,035 моль), 36,55 мас.% ТМП и 0,12 мас.% Н2O, по данным ГХ, затем ЭГ (8,31 г, 0,13 моль) и, наконец, MSA в виде 70% раствора (0,201 г, 0,0002 моль).
Затем реакционную смесь медленно нагревают примерно до 190°С. Температура и состав значимых компонентов (в мас.%) по данным ГХ в образцах, отбираемых через различные интервалы времени после добавления MSA, представлены в таблице VII, где “ND” означает “не определено”.
| Таблица VII | |||||
| Время (мин) | Темп., °С | Н2О | ЭГ | ТМП-МЦФ | ТМП |
| 0 | 26 | 0,28 | ND | 5,42 | 33,09 |
| 15 | 43,7 | 0,34 | <0,21 | 5,87 | 34,02 |
| 30 | 79,3 | 0,06 | 1,97 | 4,08 | 34,60 |
| 45 | 109,7 | 0,44 | <0,21 | 5,22 | 34,01 |
| 60 | 127,2 | 0,42 | <0,21 | 7,99 | 35,27 |
| 90 | 142,5 | 0,52 | 1,77 | 12,20 | 37,00 |
| 120 | 189,9 | 0,60 | <0,21 | 14,55 | 35,98 |
| 150 | 19,2 | 0,72 | 1,37 | 14,69 | 37,89 |
| 180 | 154,7 | 0,58 | ND | 14,19 | 37,50 |
| 210 | 158,5 | 0,66 | 0,26 | 15,07 | 37,70 |
| 240 | 161,7 | 0,86 | 1,39 | 14,43 | 37,22 |
| 270 | 163,9 | 0,90 | 0,63 | 15,16 | 38,13 |
| 300 | 170,1 | 0,78 | <0,21 | 16,14 | 35,93 |
| 330 | 174,9 | 0,75 | <0,21 | 15,25 | 36,66 |
| 360 | 177,4 | 0,77 | 0,21 | 14,87 | 37,23 |
| 390 | 179,2 | 0,83 | <0,21 | 15,99 | 36,98 |
| 423 | 179,2 | 0,08 | 1,40 | 14,38 | 37,38 |
| 450 | 179,7 | 0,83 | <0,21 | 15,75 | 36,98 |
| 480 | 180,4 | 0,73 | <0,21 | 15,3 | 36,23 |
| 510 | 181,2 | 0,75 | <0,21 | 14,72 | 36,38 |
| 540 | 188,2 | 0,46 | <0,21 | 14,64 | 38,57 |
Ни в одном из отобранных образцов практически не определяется 1,3-диоксолан. Ловушка Дина-Старка начинает заполняться жидкостью через 120 минут, и собранная после завершения реакции жидкость содержит, по данным ГХ, 2,55 мас.% Н2О, 5,74 мас.% 1,3-диоксолана, что представляет практически весь полученный в реакции 1,3-диоксолан, и менее, чем 0,21 мас.% ЭГ.
В конце реакции количество собранного в ловушке DS 1,3-диоксолана составляет 1,30 г (0,018 моль) на основе анализа воды. Как и в примере 6, расхождения в данных, полученных с помощью ГХ и при анализе воды, могут быть отчасти приписаны факторам, используемым в методе ГХ, и по аналогичным причинам результаты, полученные для анализа воды, рассматривают как более точные. Количество ТМП, которое остается в реакционной смеси в конце эксперимента, возрастает на 1,03 г.
Пример 8
Для того чтобы проверить и оптимизировать реакцию легких фракций верхнего погона ТМП, описанную в предыдущем примере, с ЭГ, верхний погон дополняют относительно чистым ТМП-МЦФ. В реактор, описанный в примерах 1 и 1А, загружают 250,0 г легких фракций верхнего погона ТМП, содержащих ТМП-МЦФ (10,38 г, 0,07 моль), а затем ЭГ (18,10 г, 0,29 моль), и наконец MSA в виде 70% раствора (0,59 г, 0,004 моль), и полученную смесь медленно нагревают. Когда температура достигает 150°С, добавляют дополнительно 10,91 г (0,18 моль) ЭГ, и полученную смесь нагревают затем примерно до 207°С. Результаты, полученные способами примеров 6 и 7, представлены в таблице VIII.
| Таблица VIII | |||||
| Время (мин) | Темп., °С | H2O | ЭГ | ТМП-МЦФ | ТМП |
| 0 | 26,6 | 1,30 | <0,44 | 9,21 | 31,07 |
| 15 | 51 | 0,58 | <0,44 | 9,50 | 32,12 |
| 30 | 83,1 | 0,55 | <0,44 | 10,37 | 32,85 |
| 45 | 112,5 | 0,65 | <0,44 | 16,88 | 34,14 |
| 60 | 136,6 | 0,63 | <0,44 | 18,76 | 36,17 |
| 90 | 153,3 | 0,78 | 0,80 | 17,08 | 36,37 |
| 92 | 150 | 0,73 | <0,44 | 18,54 | 34,11 |
| 105 | 156,6 | 0,88 | 7,51 | 15,44 | 34,41 |
| 120 | 162,2 | 0,93 | <0,44 | 19,95 | 31,51 |
| 135 | 166,3 | 0,99 | 3,83 | 16,67 | 33,25 |
| 150 | 172 | 1,18 | 7,26 | 15,56 | 33,98 |
| 173 | 176,7 | 1,13 | 1,73 | 17,90 | 33,42 |
| 195 | 178 | 1,37 | 0,44 | 18,02 | 32,28 |
| 210 | 179,5 | 1,33 | 5,50 | 15,84 | 33,84 |
| 240 | 189,9 | 1,27 | <0,44 | 19,99 | 33,29 |
| 270 | 203,5 | 1,18 | 0,46 | 16,63 | 32,15 |
| 300 | 205,8 | 1,49 | <0,44 | 17,22 | 28,79 |
| 330 | 204,9 | 1,09 | 3,72 | 15,01 | 31,65 |
| 360 | 204,9 | 1,62 | 2,88 | 13,86 | 27,83 |
| 390 | 204,3 | 0,93 | 2,38 | 13,54 | 28,46 |
| 420 | 205,6 | 0,92 | 3,01 | 12,53 | 27,11 |
| 450 | 206,5 | 0,79 | 0,82 | 12,97 | 25,59 |
Ловушка Дина-Старка начинает заполняться жидкостью примерно через 60 минут от начала реакции, и жидкость в ловушке разделяется на две фазы примерно через 270 минут. Примерно через 90 минут после начала реакции добавляют дополнительно ЭГ.
Жидкости в нижней и верхней фазах в ловушке Дина-Старка отбирают при различных температурах в интервале 203-207°С и с помощью ГХ определяют массу и массовый процент 1,3-диоксолана и Н2О. Полученные результаты представлены в таблице IX.
| Таблица IX | |||
| Н2О | 1,3-Диоксолан | г | |
| нижняя фаза в ловушке при 203°С | 22,78 | 4,63 | 15,29 |
| нижняя фаза в ловушке при 205,5°С | 82,12 | 4,98 | 5,88 |
| нижняя фаза в ловушке при 204,3°С | 85,68 | 5,73 | 2,01 |
| верхняя фаза в ловушке при 204,3°С | 2,29 | 8,35 | 16,62 |
| нижняя фаза в ловушке при 206,5°С | 85,19 | 6,24 | 2,51 |
| верхняя фаза в ловушке при 206,5°С | 2,85 | 8,56 | 4,84 |
По данным ГХ анализа в этом примере образовалось около 3,1 г (0,04 моль) 1,3-диоксолана. Результаты примеров 7 и 8 показывают, что способ настоящего изобретения для обработки легких фракций верхнего погона эффективен для получения побочного продукта 1,3-диоксолана и дополнительного количества ТМП, что приводит к уменьшению полного количества ТМП-МЦФ в системе.
В соответствии с еще одним вариантом изобретения описанную ранее кислотную обработку композиции, содержащей значительный процент ТМП-БМЛФ или ТМЭ-БМЛФ, например остатка тяжелых фракций, содержащего ТМП-БМЛФ или ТМЭ-БМЛФ, полученного в процессе получения и очистки ТМП или ТМЭ путем осуществления взаимодействия н-бутиральдегида или пропиональдегида с формальдегидом, осуществляют в присутствии одноатомного или двухатомного спирта для получения большего количества дополнительного ТМП или ТМЭ, нежели можно было бы получить путем кислотной обработки без одноатомного или двухатомного спирта, и, кроме того, побочного продукта - ацеталя. В некоторых случаях этот процесс может заменять описанную ранее и осуществляемую отдельно кислотную обработку остатка тяжелых фракций, содержащего ТМП-БМЛФ или ТМЭ-БМЛФ без одноатомного или двухатомного спирта, с последующей обработкой полученного потока, содержащего ТМП-МЦФ или ТМЭ-МЦФ, одноатомным или двухатомным спиртом, или же использоваться в сочетании с такой обработкой.
Остаток тяжелых фракций, содержащий ТМП-БМЛФ или ТМЭ-БМЛФ и условия кислотной обработки, т.е. время, температура и природа кислотного катализатора, являются теми же, что и описанные ранее для кислотной обработки в отсутствие одноатомного или двухатомного спирта, и природа и количество избыточного спирта, который добавляют к остатку тяжелых фракций, являются теми же, что и описанные ранее как пригодные для реакции с ТМП-МЦФ или ТМЭ-МЦФ: необходимо заметить, что стехиометрические количества спирта, необходимые для завершения реакции, составляют, по крайней мере, два моля одноатомного спирта, или один моль двухатомного спирта на моль ТМП-БМЛФ или ТМЭ-БМЛФ в остатке.
Примеры 9 и 10 иллюстрируют обработку этиленгликолем (ЭГ) остатка тяжелых фракций, содержащего ТМП-БМЛФ, состав которого представлен в таблице I как “исходное сырье”.
Пример 9
В реактор, описанный в примерах 1 и 1А, вначале загружают 404,28 г остатка тяжелых фракций, затем избыток ЭГ (48,0 г, 0,77 моль) и, наконец, MSA-катализатор в виде 70% раствора (1,48 г, 1,08×10-2 моль). Условия и результаты, полученные способом, аналогичным способам предшествующих примеров, включая определенные с помощью ГХ массовые проценты различных компонентов в отобранных образцах, представлены в таблице X, где “NR” означает “ГХ анализ не проводился”.
| Таблица Х | |||||
| Время(мин) | Темп., °С | ЭГ | ТМП-МЦФ | ТМП | Ди-ТМП |
| 0 | 63,5 | NR | NR | NR | NR |
| 40 | 97,8 | NR | NR | NR | NR |
| 70 | 110 | 5,71 | 29,39 | 32,90 | 3,04 |
| 95 | 118,1 | 4,82 | 30,006 | 33,50 | 2,35 |
| 115 | 123,1 | NR | NR | NR | NR |
| 140 | 127,4 | 3,83 | 29,29 | 32,94 | 2,39 |
| 170 | 131,2 | 2,03 | 29,98 | 33,94 | 2,02 |
| 220 | 139,9 | 4,28 | 29,87 | 33,43 | 2,42 |
| 237 | 143,1 | NR | NR | NR | NR |
| 294 | 153,4 | NR | NR | NR | NR |
Конденсация жидкости в ловушке Дина-Старка начинается через 237 минут, и все количество жидкости в ловушке к концу эксперимента разделяется на две фазы; ни в одном из отобранных образцов не наблюдается ни Н2O, ни 1,3-диоксолана, и все количество этих соединений, по-видимому, собирается в ловушке, причем нижняя фаза массой 12,41 г содержит по данным ГХ 73,59 мас.% Н2О, 9,28 мас.% 1,3-диоксолана и 2,93 мас.% ТМП-МЦФ, а верхняя фаза весит 8,69 г и содержит 2,37 мас.% Н2O, 19,64 мас.% 1,3-диоксолана и 4,41 мас.% ТМП-МЦФ.
Пример 10
В основном повторяют способ примера 9, за исключением того, что загружают 202,14 г остатка тяжелых фракций, затем добавляют избыток ЭГ (24 г, 0,39 моль) и, наконец, MSA-катализатор в виде 70% раствора (0,74 г, 5,38×10-3 моль). Перед добавлением MSA, при температуре 26,7 °С, реакционный раствор содержит (по данным ГХ) 22,93 мас.% ЭГ, 25,71 мас.% ТМП, 4,42 мас.% ди-ТМП и 17,75 мас.% ТМП-БМЛФ. ТМП-МЦФ не обнаружен. Условия и результаты реакции представлены далее в таблице XI, где “ND” означает “не определяется с помощью ГХ”.
| Таблица XI | ||||||
| Время(мин) | Темп., °С | ЭГ | ТМП-МЦФ | ТМП | ди-ТМП | ТМП-БМЛФ |
| 0 | 30 | ND | 6,05 | 29,61 | 3,83 | 15,214 |
| 5 | 44 | ND | 5,10 | 30,12 | 3,08 | 12,212 |
| 20 | 47,4 | 24,779 | 4,99 | 25,32 | 2,27 | 5,910 |
| 35 | 89,9 | 2,257 | 15,82 | 30,97 | 2,42 | 5,631 |
| 65 | 105,5 | 5,615 | 29,04 | 33,07 | 3,03 | ND |
| 95 | 120 | 4,113 | 29,58 | 33,52 | 2,53 | ND |
| 125 | 140 | 3,405 | 29,72 | 32,67 | 2,25 | ND |
| 185 | 150 | 4,120 | 30,57 | 30,62 | 2,32 | ND |
| 270 | 168,9 | 3,138 | 36,25 | 31,79 | 2,60 | ND |
Конденсация в ловушке Дина-Старка начинается через 65 минут, и жидкость собирается и разделяется на две фазы через 185 минут. В конце реакции нижняя фаза в ловушке весит 23,31 г и содержит 10,74 мас.% 1,3-диоксолана и 3,14 мас.% ТМП-МЦФ, тогда как верхняя фаза в ловушке весит 38,73 г и содержит 25,04 мас.% 1,3-диоксолана и 2,51 мас.% ТМП-МЦФ. Результаты примеров 9 и 10 показывают, что катализируемая кислотой обработка остатка тяжелых фракций ТМП, содержащего ТМП-БМЛФ, в присутствии этиленгликоля эффективно приводит к получению побочного продукта 1,3-диоксолана и дополнительного количества ТМП и снижает или исключает присутствие ТМП-БМЛФ в остатке.
Claims (27)
1. Способ, включающий осуществление реакции трансалкоголиза триметилолпропан моноциклического формаля (ТМП-МЦФ) или триметилолэтан моноциклического формаля (ТМЭ-МЦФ) с избытком одноатомного или двухатомного спирта при повышенной температуре и в присутствии кислотного катализатора для получения триметилолпропана (ТМП) или триметилолэтана (ТМЭ) соответственно и побочного продукта - ацеталя.
2. Способ по п.1, где указанный одноатомный или двухатомный спирт содержит от 1 до 6 атомов углерода.
3. Способ по п.1 или 2, где указанный одноатомный или двухатомный спирт выбирают из группы, состоящей из этиленгликоля, метанола, 1-пропанола, 2-пропанола и 2-бромпропанола, а указанный побочный продукт - ацеталь представляет 1,3-диоксолан, метилаль, ди-1-пропоксиметан, ди-2-пропоксиметан или ди-2-бромпропоксиметан соответственно.
4. Способ по любому из пп.1-3, где указанный одноатомный или двухатомный спирт является этиленгликолем, а указанный побочный продукт - ацеталь является 1,3-диоксоланом.
5. Способ по п.1, где указанный избыток одноатомного или двухатомного спирта превышает в 5-20 раз стехиометрическое количество указанного спирта, необходимое для взаимодействия с ТМП-МЦФ или ТМЭ-МЦФ.
6. Способ по п.1, где указанный кислотный катализатор выбирают из группы, состоящей из алкансульфоновой кислоты, арилсульфоновой кислоты, сульфированного катионообменного катализатора в кислотной форме, серной кислоты и фосфорной кислоты.
7. Способ по п.6, где указанным катализатором является метансульфоновая кислота.
8. Способ по любому из пп. 1-7, где указанный ТМП-МЦФ или ТМЭ-МЦФ получен в результате процесса, включающего осуществление контактирования композиции, содержащей не менее, 5 мас.% триметилолпропан бис-монолинейного формаля (ТМП-БМЛФ) или триметилолэтан бис-монолинейного формаля (ТМЭ-БМЛФ), не более чем около 5 мас.% воды и не более чем около 0,5 мас.% метанола, с сильным кислотным катализатором при повышенной температуре и в течение достаточного промежутка времени, необходимого для превращения, по меньшей мере, 70 мас.% указанного ТМП-БМЛФ или ТМЭ-БМЛФ в триметилолпропан (ТМП) и триметилолпропан моноциклический формаль (ТМП-МЦФ), или триметилолэтан (ТМЭ) и триметилолэтан моноциклический формаль (ТМЭ-МЦФ) соответственно.
9. Способ по любому из пп. 1-7, где указанный ТМП-МЦФ или ТМЭ-МЦФ получен из легких фракций верхнего погона, полученных в результате окончательной обработки сырого ТМП или ТМЭ.
10. Способ по п.9, где указанные легкие фракции содержат от около 1 до около 15 мас.% ТМП-МЦФ или ТМЭ-МЦФ.
11. Способ, включающий осуществление взаимодействия композиции, содержащей, по меньшей мере, 10 мас.% триметилолпропан-бис-монолинейного формаля (ТМП-БМЛФ) или триметилолэтан-бис-монолинейного формаля (ТМЭ-БМЛФ), не более чем около 5 мас.% воды и одноатомный или двухатомный спирт в избытке от стехиометрического количества, с сильным кислотным катализатором при температуре 30-3000С и в течение промежутка времени, достаточного для превращения значительного количества указанного ТМП-БМЛФ или ТМЭ-БМЛФ в триметилолпропан или триметилолэтан соответственно и побочный продукт - ацеталь.
12. Способ по п.11, где указанная композиция является остатком тяжелых фракций, полученных при удалении массы воды, избытка формальдегида, основного конденсирующего агента и очищенного ТМП или ТМЭ, полученного при очистке сырого ТМП- или ТМЭ-содержащего продукта, полученного при взаимодействии н-бутиральдегида или пропиональдегида соответственно с формальдегидом в водной среде и в присутствии щелочного конденсирующего агента.
13. Способ по п.12, где указанный остаток тяжелых фракций содержит ТМП-БМЛФ и получен в процессе очистки сырого ТМП-содержащего продукта.
14. Способ по п.13, где указанный остаток тяжелых фракций содержит, по крайней мере, около 20 мас.% ТМП-БМЛФ и не более чем около 1 мас.% воды.
15. Способ по любому из пп. 11-14, где указанный промежуток времени составляет от около 2 до около 8 ч.
16. Способ по п.15, где температура составляет от около 90 до около 220°С и указанный промежуток времени составляет от около 1 до около 6 ч.
17. Способ по любому из пп.11-16, где указанный кислотный катализатор является алкансульфоновой кислотой, арилсульфоновой кислотой, сульфированной катионообменной смолой в кислотной форме, серной кислотой или фосфорной кислотой.
18. Способ по п.17, где указанный кислотный катализатор выбирают из группы, состоящей из серной кислоты и фосфорной кислоты.
19. Способ по п.17, где указанным кислотным катализатором является метансульфоновая кислота.
20. Способ по п.17, где указанным кислотным катализатором является толуолсульфоновая кислота.
21. Способ по п.17, где указанным кислотным катализатором является катионообменная смола на основе сульфированного полистирола в кислотной форме.
22. Способ по п.11, где указанный кислотный катализатор присутствует в таком количестве, что кислотность композиции эквивалентна кислотности, которую вносит метансульфоновая кислота в количестве от около 0,1 до около 15 мас.%.
23. Способ по п.22, где указанный интервал составляет от около 0,3 до около 1,3 мас.%.
24. Способ по п.13, где указанный остаток тяжелых фракций, вводимый в процесс, содержит также менее чем около 60 мас.% ТМП.
25. Способ по п.11, где указанный одноатомный или двухатомный спирт содержит от 1 до около 6 атомов углерода.
26. Способ по п.25, где указанный одноатомный или двухатомный спирты выбирают из группы, состоящей из этиленгликоля, метанола, 1-пропанола, 2-пропанола и 2-бромпропанола, а указанный побочный продукт - ацеталь является 1,3-диоксоланом, метилалем, ди-1-пропоксиметаном, ди-2-пропоксиметаном или ди-2-бромпропоксиметаном, соответственно.
27. Способ по п.26, где указанный одноатомный или двухатомный спирт является этиленгликолем, а указанный побочный продукт - ацеталь является 1,3-диоксоланом.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/324,435 US6096905A (en) | 1999-06-01 | 1999-06-01 | Treatment of a composition comprising a trimethylolalkane bis-monolinear formal |
| US09/324,435 | 1999-06-01 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2001135811A RU2001135811A (ru) | 2003-08-20 |
| RU2247704C2 true RU2247704C2 (ru) | 2005-03-10 |
Family
ID=23263574
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2001135811/04A RU2247704C2 (ru) | 1999-06-01 | 2000-05-26 | Обработка композиции, включающей триметилолалкан бис-монолинейный формаль |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US6096905A (ru) |
| EP (1) | EP1181263B1 (ru) |
| JP (1) | JP5069388B2 (ru) |
| KR (1) | KR100748797B1 (ru) |
| CN (1) | CN1217896C (ru) |
| AT (1) | ATE276221T1 (ru) |
| AU (1) | AU762408B2 (ru) |
| BR (1) | BR0010837B1 (ru) |
| CA (1) | CA2373974C (ru) |
| CZ (1) | CZ20014303A3 (ru) |
| DE (1) | DE60013814T2 (ru) |
| ES (1) | ES2226849T3 (ru) |
| HU (1) | HUP0201517A3 (ru) |
| MX (1) | MXPA01012324A (ru) |
| NO (1) | NO321348B1 (ru) |
| NZ (1) | NZ515480A (ru) |
| RU (1) | RU2247704C2 (ru) |
| WO (1) | WO2000073250A1 (ru) |
| ZA (1) | ZA200109382B (ru) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6096905A (en) * | 1999-06-01 | 2000-08-01 | Celanese International Corporation | Treatment of a composition comprising a trimethylolalkane bis-monolinear formal |
| DE10223054A1 (de) * | 2002-05-24 | 2003-12-04 | Basf Ag | Verfahren zur Herstellung von Polyetherolen |
| DE10223055A1 (de) * | 2002-05-24 | 2003-12-11 | Basf Ag | Verfahren zur Herstellung von Polyesterpolyolen mehrwertiger Alkohole |
| DE10234016A1 (de) * | 2002-07-26 | 2004-02-05 | Basf Ag | Verfahren zur Ausbeuteerhöhung bei der Herstellung von mehrwertigen Alkoholen durch Spaltung acetalhaltiger Nebenprodukte |
| SE525080C2 (sv) * | 2003-03-21 | 2004-11-23 | Perstorp Specialty Chem Ab | Förfarande för framställning av en allyleter |
| CN101092410B (zh) * | 2007-05-21 | 2010-04-14 | 吉化集团公司 | 用三羟甲基丙烷重质残液制备环状三羟甲基丙烷缩甲醛的方法及设备 |
| CN100534967C (zh) * | 2007-06-12 | 2009-09-02 | 无锡百川化工股份有限公司 | 烷氧基化三羟甲基丙烷的生产方法 |
| CN101239320B (zh) * | 2008-01-17 | 2010-11-17 | 复旦大学 | 用于合成戊二醛的含钨超大介孔泡沫催化剂及其制造方法 |
| CN101671233B (zh) * | 2009-09-14 | 2012-12-12 | 无锡百川化工股份有限公司 | 一种生产甲酸钠的方法 |
| JP2012041310A (ja) * | 2010-08-20 | 2012-03-01 | Hitachi Chem Co Ltd | ヒドロキシアルキル(メタ)アクリル酸エステルの製造方法 |
| DE102011118993A1 (de) * | 2011-11-19 | 2013-05-23 | Oxea Gmbh | Verfahren zur Gewinnung von Di-Trimethylpropan und mit Trimethylpropan angereicherten Produktströmen aus den Nebenströmen der Trimethylolpropanherstellung |
| WO2014042768A1 (en) * | 2012-09-17 | 2014-03-20 | Oxea Bishop, Llc | Recovery of trimethylolpropane from purification residue |
| US8759593B2 (en) | 2012-09-17 | 2014-06-24 | Oxea Bishop Llc | Recovery of alcohols from purification residue |
| US8921618B2 (en) | 2012-09-17 | 2014-12-30 | Oxea Bishop Llc | Recovery of trimethylolpropane from purification residue |
| RU2616004C1 (ru) * | 2016-03-10 | 2017-04-12 | Открытое акционерное общество "Нефтяная компания "Роснефть" | Способ переработки высококипящих побочных продуктов процесса получения этриола |
| CN115850028A (zh) * | 2022-12-16 | 2023-03-28 | 赤峰瑞阳化工有限公司 | 一种三羟甲基丙烷多塔串联萃取精馏除杂精制的方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE142184C (ru) * | ||||
| US3076854A (en) * | 1955-12-05 | 1963-02-05 | Heyden Newport Chemical Corp | Recovery of trimethylolpropane |
| JPS509B1 (ru) * | 1969-11-28 | 1975-01-06 | ||
| JPS4924043B1 (ru) * | 1969-11-29 | 1974-06-20 | ||
| DD142184A1 (de) * | 1979-02-27 | 1980-06-11 | Helmut Dietze | Gewinnung von trimethylolpropan |
| DD287251A5 (de) * | 1989-08-21 | 1991-02-21 | Veb Leuna-Werke "Walter Ulbricht",De | Verfahren zur gewinnung von trimethylolpropan |
| DD287250A5 (de) * | 1989-08-21 | 1991-02-21 | Veb Leuna-Werke "Walter Ulbricht",De | Verfahren zur gewinnung von trimethylolpropan |
| SE9502355L (sv) * | 1995-06-29 | 1996-12-30 | Perstorp Ab | Spaltning av cykloalkyletrar |
| US6096905A (en) * | 1999-06-01 | 2000-08-01 | Celanese International Corporation | Treatment of a composition comprising a trimethylolalkane bis-monolinear formal |
-
1999
- 1999-06-01 US US09/324,435 patent/US6096905A/en not_active Expired - Lifetime
-
2000
- 2000-05-26 CN CN008083681A patent/CN1217896C/zh not_active Expired - Fee Related
- 2000-05-26 DE DE60013814T patent/DE60013814T2/de not_active Expired - Lifetime
- 2000-05-26 NZ NZ515480A patent/NZ515480A/en not_active IP Right Cessation
- 2000-05-26 WO PCT/US2000/014643 patent/WO2000073250A1/en active Application Filing
- 2000-05-26 HU HU0201517A patent/HUP0201517A3/hu unknown
- 2000-05-26 US US09/579,743 patent/US6316679B1/en not_active Expired - Lifetime
- 2000-05-26 ES ES00936359T patent/ES2226849T3/es not_active Expired - Lifetime
- 2000-05-26 BR BRPI0010837-5A patent/BR0010837B1/pt not_active IP Right Cessation
- 2000-05-26 JP JP2000621318A patent/JP5069388B2/ja not_active Expired - Fee Related
- 2000-05-26 RU RU2001135811/04A patent/RU2247704C2/ru not_active IP Right Cessation
- 2000-05-26 EP EP00936359A patent/EP1181263B1/en not_active Expired - Lifetime
- 2000-05-26 AT AT00936359T patent/ATE276221T1/de not_active IP Right Cessation
- 2000-05-26 MX MXPA01012324A patent/MXPA01012324A/es active IP Right Grant
- 2000-05-26 KR KR1020017015332A patent/KR100748797B1/ko not_active IP Right Cessation
- 2000-05-26 AU AU51683/00A patent/AU762408B2/en not_active Ceased
- 2000-05-26 CZ CZ20014303A patent/CZ20014303A3/cs unknown
- 2000-05-26 CA CA002373974A patent/CA2373974C/en not_active Expired - Fee Related
-
2001
- 2001-11-14 ZA ZA200109382A patent/ZA200109382B/en unknown
- 2001-11-30 NO NO20015861A patent/NO321348B1/no not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| NO20015861L (no) | 2001-11-30 |
| CZ20014303A3 (cs) | 2002-05-15 |
| EP1181263A1 (en) | 2002-02-27 |
| CA2373974C (en) | 2008-07-08 |
| NO20015861D0 (no) | 2001-11-30 |
| NO321348B1 (no) | 2006-05-02 |
| CA2373974A1 (en) | 2000-12-07 |
| BR0010837A (pt) | 2002-03-05 |
| EP1181263B1 (en) | 2004-09-15 |
| US6096905A (en) | 2000-08-01 |
| AU5168300A (en) | 2000-12-18 |
| ZA200109382B (en) | 2002-12-17 |
| MXPA01012324A (es) | 2002-07-22 |
| WO2000073250A1 (en) | 2000-12-07 |
| CN1217896C (zh) | 2005-09-07 |
| BR0010837B1 (pt) | 2010-11-03 |
| KR20020003400A (ko) | 2002-01-12 |
| ATE276221T1 (de) | 2004-10-15 |
| JP5069388B2 (ja) | 2012-11-07 |
| NZ515480A (en) | 2003-08-29 |
| AU762408B2 (en) | 2003-06-26 |
| HUP0201517A3 (en) | 2003-08-28 |
| US6316679B1 (en) | 2001-11-13 |
| CN1353682A (zh) | 2002-06-12 |
| HUP0201517A2 (en) | 2002-08-28 |
| KR100748797B1 (ko) | 2007-08-13 |
| DE60013814D1 (de) | 2004-10-21 |
| JP2003500463A (ja) | 2003-01-07 |
| DE60013814T2 (de) | 2005-09-29 |
| ES2226849T3 (es) | 2005-04-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2247704C2 (ru) | Обработка композиции, включающей триметилолалкан бис-монолинейный формаль | |
| KR100463360B1 (ko) | 폴리알코올의제조방법 | |
| FR2906807A1 (fr) | Procede de synthese d'acetals cycliques par extraction reactive d'un polyol en solution concentree | |
| CN1402701A (zh) | 甲酸的制备方法 | |
| KR20010031121A (ko) | 저반응 색채 트리메틸올프로판의 개선된 제조 방법 | |
| CA1268773A (en) | Process for the preparation of glyoxal monoacetals | |
| KR101543810B1 (ko) | 다이-n-부틸 테레프탈레이트로의 테레프탈산의 전환 | |
| JP2000191568A (ja) | 高純度トリメチロ―ルプロパンの製造法 | |
| RU2001135811A (ru) | Обработка композиции, включающей триметилолалкан бис-монолинейный формаль | |
| PL182127B1 (pl) | Sposób destylacyjnego oczyszczania alkoholi PL PL PL PL PL | |
| CZ200037A3 (cs) | Zpracování směsí obsahujících formaldehyd | |
| US3947504A (en) | Separation and recovery of 3-methyl-3-butene-1-ol | |
| NL8202030A (nl) | Werkwijze voor de bereiding van carbonzuuresters uit onverzadigde en meerwaardige alcoholen. | |
| AU2002301312B2 (en) | Treatment of a composition comprising a trimethylolalkane bis-monolinear formal | |
| JP2003267904A (ja) | ジトリメチロールプロパンの製造方法 | |
| WO2007143356A2 (en) | Alkoxylations in ketone solvents | |
| US5659073A (en) | Process for making glycol ether acetates | |
| EP0065774B1 (en) | Method for the recovery of pentaerythritol from the residual mixtures of the synthesis from acetaldehyde and formaldehyde | |
| EP0573763B1 (de) | Verfahren zur Herstellung von Hydroxypivalinsäureestern | |
| EP3466941B1 (en) | Process for producing cyclic acetal compound | |
| US4695410A (en) | Recovery of phenol from aqueous solution | |
| RU2028285C1 (ru) | Способ выделения изобутенилкарбинола из фракции возвратного 4,4-диметилдиоксана-1,3 | |
| CS230491B1 (cs) | Způsob odstraňování 4-fenyl-l,3-dioxanu ze směsi 3-fenyl-l-propanolu a 4-feny1-1,3- -dioxanu | |
| CZ279446B6 (cs) | Způsob zpracování produktu z hydroformylace propylénu | |
| JPH0631214B2 (ja) | イソクロマン類の製造法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20050527 |
|
| NF4A | Reinstatement of patent | ||
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20110527 |