JP5067522B2 - 二次電池用電解液および二次電池 - Google Patents
二次電池用電解液および二次電池 Download PDFInfo
- Publication number
- JP5067522B2 JP5067522B2 JP2006037698A JP2006037698A JP5067522B2 JP 5067522 B2 JP5067522 B2 JP 5067522B2 JP 2006037698 A JP2006037698 A JP 2006037698A JP 2006037698 A JP2006037698 A JP 2006037698A JP 5067522 B2 JP5067522 B2 JP 5067522B2
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- negative electrode
- secondary battery
- electrolyte
- positive electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/058—Construction or manufacture
- H01M10/0587—Construction or manufacture of accumulators having only wound construction elements, i.e. wound positive electrodes, wound negative electrodes and wound separators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/4235—Safety or regulating additives or arrangements in electrodes, separators or electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/386—Silicon or alloys based on silicon
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/387—Tin or alloys based on tin
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0037—Mixture of solvents
- H01M2300/004—Three solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
Description
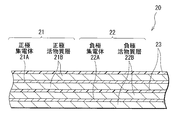
図1は、本実施の形態に係る電解液を用いた第1の二次電池の断面構成を表すものである。この二次電池は、負極の容量が、電極反応物質であるリチウムの吸蔵および放出による容量成分により表されるいわゆるリチウムイオン二次電池である。この二次電池は、いわゆる円筒型といわれるものであり、ほぼ中空円柱状の電池缶11の内部に、一対の正極21と負極22とがセパレータ23を介して巻回された巻回電極体20を有している。電池缶11は、例えばニッケル(Ni)のめっきがされた鉄(Fe)により構成されており、一端部が閉鎖され他端部が開放されている。電池缶11の内部には、巻回電極体20を挟むように巻回周面に対して垂直に一対の絶縁板12, 13がそれぞれ配置されている。
第2の二次電池は、負極の構成が異なることを除き、他は第1の二次電池と同様の構成・作用および効果を有しており、同様にして製造することができる。よって、図1および図2を参照し、対応する構成要素には同一の符号を付して同一部分の説明は省略する。
第3の二次電池は、負極22の容量がリチウムの析出および溶解による容量成分により表される、いわゆるリチウム金属二次電池である。この二次電池は、負極活物質層22Bをリチウム金属により構成したことを除き、他は第1の二次電池と同様の構成を有しており、同様にして製造することができる。従って、図1および図2を参照し、対応する構成要素には同一の符号を付して同一部分の説明は省略する。
第4の二次電池は、負極の容量が電極反応物質であるリチウムの吸蔵および放出による容量成分と、リチウムの析出および溶解による容量成分とを含み、かつその和により表されるものである。この二次電池は、負極活物質層22Bの構成が異なることを除き、他は第1の二次電池と同様の構成を有しており、同様にして製造することができる。従って、図1および図2を参照し、対応する構成要素には同一の符号を付して同一部分の説明は省略する。
図3は、第5の二次電池の構成を表すものである。この二次電池は、いわゆるラミネートフィルム型といわれるものであり、正極リード31および負極リード32が取り付けられた巻回電極体30をフィルム状の外装部材40の内部に収容したものである。
第6の二次電池は、正極活物質と負極活物質との量を調節することにより、一対の正極および負極当たりの完全充電時における開回路電圧(すなわち電池電圧)を4.25V以上6.00V以下の範囲内としたことを除き、他は第1から第5の二次電池と同様の構成を有しており、同様にして製造することができる。
図5に示したコイン型の二次電池を作製した。この二次電池は、正極51と、負極52とを電解液を含浸させたセパレータ53を介して積層し、外装缶54と外装カップ55との間に挟み、ガスケット56を介してかしめたものである。まず、正極活物質としてリチウムコバルト複合酸化物(LiCoO2 )94質量部と、導電材としてグラファイト3質量部と、結着材としてポリフッ化ビニリデン3質量部とを混合したのち、溶剤としてN−メチル−2−ピロリドンを添加し正極合剤スラリーを得た。次いで、得られた正極合剤スラリーを、厚み20μmのアルミニウム箔よりなる正極集電体51Aに均一に塗布し乾燥させて厚み70μmの正極活物質層51Bを形成した。そののち、正極活物質層51Bが形成された正極集電体51Aを直径15mmの円形に打ち抜き、正極51を作製した。
実験例2−1〜2−5として、負極活物質にスズを用い、厚み15μmの銅箔よりなる負極集電体52Aの上に蒸着法により厚み5μmのスズよりなる負極活物質層52Bを形成したことを除き、他は実験例1−1〜1−5と同様にしてコイン型の二次電池を作製した。その際、正極活物質と負極活物質との充填量を調節し、完全充電時における開回路電圧を4.20Vとなるようにすると共に、充電の途中で負極52にリチウム金属が析出しないようにして、負極52の容量がリチウムの吸蔵および放出による容量成分により表されるようにした。
負極活物質に黒鉛を用い、この黒鉛97質量部と、結着材としてポリフッ化ビニリデン3質量部とを混合し、N−メチル−2−ピロリドンを添加して、厚み15μmの銅箔よりなる負極集電体52Aに均一に塗布し乾燥させることにより厚み70μmの負極活物質層52Bを形成したことを除き、他は実験例1−1と同様にして、コイン型のリチウムイオン二次電池を作製した。その際、正極活物質はリチウム・マンガン・コバルト・ニッケル複合酸化物(LiMn0.3 Co0.2 Ni0.5 O2 )とした。更に、正極活物質と負極活物質との充填量を調節し、完全充電時における開回路電圧を、実験例4−1では4.60Vとなるように、実験例4−2では4.50Vとなるように、実験例4−3では4.35Vとなるように、実験例4−4では4.25Vとなるようにした。また、充電の途中で負極52にリチウム金属が析出しないようにして、負極の容量22がリチウムの吸蔵および放出による容量成分により表されるようにした。
負極活物質に黒鉛を用い、この黒鉛97質量部と、結着材としてポリフッ化ビニリデン3質量部とを混合し、N−メチル−2−ピロリドンを添加して、厚み15μmの銅箔よりなる負極集電体52Aに均一に塗布し乾燥させることにより厚み70μmの負極活物質層52Bを形成したことを除き、他は実験例1−2〜1−5と同様にして、コイン型のリチウムイオン二次電池を作製した。その際、正極活物質はリチウム・マンガン・コバルト・ニッケル複合酸化物(LiMn0.3 Co0.2 Ni0.5 O2 )とした。更に、正極活物質と負極活物質との充填量を調節し、完全充電時における開回路電圧を4.50Vとなるようにした。また、充電の途中で負極52にリチウム金属が析出しないようにして、負極の容量22がリチウムの吸蔵および放出による容量成分により表されるようにした。
電解液における1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウムの含有量を10質量%または0.1質量%になるようにしたことを除き、他は実験例1−3,2−3,3−3,4−2と同様にして二次電池を作製した。
実験例10−1〜10−4では、溶媒として炭酸エチレンおよび炭酸ジメチルに加え、化3(1)に示した1,3−ジオキソール−2−オン(VC),化3(2)に示した4−ビニル−1,3−ジオキソラン−2−オン(VEC),化4(1)に示した1,3−プロパンスルトン(PS)または化4(2)に示した1,3−プロペンスルトン(PRS)を用いたことを除き、他は実験例1−1と同様にして二次電池を作製した。具体的な溶媒の組成は、実験例10−1では、炭酸エチレン:炭酸ジメチル:1,3−ジオキソール−2−オン=40:42:2(質量比)とし、実験例10−2では、炭酸エチレン:炭酸ジメチル:4−ビニル−1,3−ジオキソラン−2−オン=40:42:2(質量比)とし、実験例10−3では、炭酸エチレン:炭酸ジメチル:1,3−プロパンスルトン=40:42:2(質量比)とし、実験例10−4では、炭酸エチレン:炭酸ジメチル:1,3−プロペンスルトン=40:42:2(質量比)とした。
図1,2に示した円筒型の二次電池を作製した。まず、炭酸リチウム(Li2 CO3 )と炭酸コバルト(CoCO3 )とを0.5:1のモル比で混合し、空気中において890℃で5時間焼成してリチウム・コバルト複合酸化物(LiCoO2 )を得た。得られたLiCoO2 についてX線回折を行ったところ、JCPDS(Joint Committee of Powder Diffraction Standard)ファイルに登録されたLiCoO2 のピークとよく一致していた。続いて、このリチウム・コバルト複合酸化物を粉砕して平均粒子径が10μmの粉末状とし、正極活物質とした。
SnCoC含有材料の組成を変化させたことを除き、他は実験例12−1−2と同様にして二次電池を作製した。作製した実験例13−1〜13−6のCoSnC含有材料についても、実験例5−1−2と同様にして組成の分析を行った。それらの結果を表18,19に示す。また、実験例12−1−2および実験例13−1〜13−6のCoSnC含有材料についてX線回折を行ったところ、回折角2θ=20°〜50°の間に、回折角2θが1.0°以上の広い半値幅を有する回折ピークが観察された。更に、これらのCoSnC含有材料についてXPSを行ったところ、図6に示したようにピークP1が得られた。ピークP1を解析すると、表面汚染炭素のピークP2と、ピークP2よりも低エネルギー側にSnCoC含有材料中におけるC1sのピークP3とが得られた。このピークP3は、284.5eVよりも低い領域に得られた。すなわち、SnCoC含有材料中の炭素が他の元素と結合していることが確認された。
電解液における1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウムの含有量を表20に示したように変化させたことを除き、他は12−1−2と同様にして二次電池を作製した。電解液の各組成は、表20に示したようにした。
溶媒として4−フルオロ−1,3−ジオキソラン−2−オン、炭酸エチレンおよび炭酸ジメチルに加え、化3(1)に示した1,3−ジオキソール−2−オン,化3(2)に示した4−ビニル−1,3−ジオキソラン−2−オン,化4(1)に示した1,3−プロパンスルトンまたは化4(2)に示した1,3−プロペンスルトンを用いたことを除き、他は実験例12−1−2〜12−27−2と同様にして二次電池を作製した。電解液の各組成は、表21〜表25に示したようにした。
実験例16−1−1〜16−1−8では、電解液における1,3−ジオキソール−2−オンの含有量を0.05質量%〜20質量%の範囲内で変化させたことを除き、他は実験例15−1−1と同様にして二次電池を作製した。実験例16−2−1〜16−2−8では、電解液における4−ビニル−1,3−ジオキソラン−2−オンの含有量を0.05質量%〜20質量%の範囲内で変化させたことを除き、他は実験例15−1−2と同様にして二次電池を作製した。実験例17−1−1〜17−1−8では、電解液における1,3−プロパンスルトンの含有量を0.01質量%〜5質量%の範囲内で変化させたことを除き、他は実験例15−1−3と同様にして二次電池を作製した。実験例17−2−1〜17−2−7では、電解液における1,3−プロペンスルトンの含有量を0.05質量%〜5質量%の範囲内で変化させたことを除き、他は実験例15−1−4と同様にして二次電池を作製した。電解液の各組成は、表26,27に示したようにした。
図3および図4に示した二次電池を作製した。まず、実験例12−1−1と同様にして正極33および負極34を作製し、正極リード31および負極リード32を取り付けた。なお、負極活物質は、実験例12−1−1と同様のSnCoC含有材料を用いた。
アルミニウムよりなる中空角柱状の電池缶を用いたことを除き、他は実験例12−1−1と同様にして二次電池を作製した。その際、電解液には、溶媒として4−フルオロ−1,3−ジオキソラン−2−オンと炭酸エチレンと炭酸ジメチルとを混合した溶媒に、電解質塩としてLiPF6 と環状のイミド塩である1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウムを混合したものを用いた。電解液の各組成は表29に示したようにした。なお、負極活物質は、実験例12−1−1と同様のSnCoC含有材料を用いた。
負極22の容量が、リチウムの析出および溶解による容量成分により表される電池、いわゆるリチウム金属二次電池を作製した。その際、電池は、図1に示したものとした。
溶媒における4−フルオロ−1, 3−ジオキソラン−2−オンの含有量を1体積%,5体積%,20体積%または50体積%としたことを除き、他は実験例20−3と同様にして二次電池を作製した。その際、溶媒は、実験例21−1では4−フルオロ−1, 3−ジオキソラン−2−オンと炭酸ジメチルとを、4−フルオロ−1, 3−ジオキソラン−2−オン:炭酸ジメチル=50:50の体積比で混合した。また、実験例21−2〜21−4では、4−フルオロ−1, 3−ジオキソラン−2−オンと炭酸エチレンと炭酸ジメチルとを、4−フルオロ−1, 3−ジオキソラン−2−オン:炭酸エチレン:炭酸ジメチル=20:10:70、5:25:70、または1:29:70の体積比で混合した。
電解質塩として更にLiBF4 またはLiB(OCOCF3 )4 を0.2mol/kgとなるように溶解した電解液を用いたことを除き、他は実験例20−2と同様にして二次電池を作製した。その際、ハロゲン原子を有する環式炭酸エステル誘導体は、実験例22−1,22−2では4−フルオロ−1,3−ジオキソラン−2−オンとし、実験例22−3,22−4では4−クロロ−1,3−ジオキソラン−2−オンとした。
溶媒として4−フルオロ−1,3−ジオキソラン−2−オンおよび炭酸ジメチルに加え、化3(1)に示した1,3−ジオキソール−2−オン,化3(2)に示した4−ビニル−1,3−ジオキソラン−2−オン,化4(1)に示した1,3−プロパンスルトンまたは化4(2)に示した1,3−プロペンスルトンを用いたことを除き、他は実験例20−3と同様にして二次電池を作製した。溶媒の組成は、表33に示したように変化させた。
リチウムの吸蔵および放出による容量成分と、リチウムの析出および溶解による容量成分とを含み、かつその和により表される二次電池を作製した。その際、負極材料に人造黒鉛を用い、比較例20−3〜20−6と同様にして負極22を作製したことを除き、他は実験例20−1〜20−9と同様にして二次電池を作製した。また、負極22の容量がリチウムの吸蔵および放出による容量成分と、リチウムの析出および溶解による容量成分とを含み、かつその和により表されるように、正極材料と負極材料との充填量を設計した。更に、電解液には、4−フルオロ−1,3−ジオキソラン−2−オンと、炭酸エチレンと、炭酸ジメチルとを表34に示した割合で混合した溶媒に、化6(1)に示した1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウムを0.2mol/kgとなるように、またLiPF6 を0.8mol/kgとなるように溶解したものを用いた。
溶媒として4−フルオロ−1,3−ジオキソラン−2−オンおよび炭酸ジメチルに加え、化3(1)に示した1,3−ジオキソール−2−オン,化3(2)に示した4−ビニル−1,3−ジオキソラン−2−オン,化4(1)に示した1,3−プロパンスルトンまたは化4(2)に示した1,3−プロペンスルトンを用いたことを除き、他は実験例24−2と同様にして二次電池を作製した。溶媒の組成は、表35に示したように変化させた。
負極22の容量が、リチウムの析出および溶解による容量成分により表される電池、すなわちリチウム金属二次電池を作製した。
溶媒における4−フルオロ−1, 3−ジオキソラン−2−オンの含有量を1体積%,5体積%,20体積%または50体積%としたことを除き、すなわち、実験例21−1〜21−4と同様の電解液を用いたことを除き、他は実験例26−3,27−3と同様にして二次電池を作製した。
電解質塩として更にLiBF4 またはLiB(OCOCF3 )4 を0.2mol/kgとなるように溶解した電解液を用いたことを除き、すなわち、実験例22−1〜22−4と同様の電解液を用いたことを除き、他は実験例26−1,27−1と同様にして二次電池を作製した。
Claims (12)
- 正極および負極と共に非水溶媒および電解質塩を含む電解液を備え、
前記負極は、電極反応物質を吸蔵および放出することが可能であり、構成元素としてスズ(Sn)およびケイ素(Si)のうちの少なくとも一方を含む負極材料を含有し、
前記電解液は、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドリチウム、オルト−スルホベンズイミドリチウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドナトリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドナトリウム、オルト−スルホベンズイミドナトリウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドカリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドカリウム、オルト−スルホベンズイミドカリウム、1,1,2,2−テトラフルオロエタン−1,3−ジスルホンイミドリチウム、1−トリフルオロメチル−1,2,2,3,3−ペンタフルオロプロパン−1,3−ジスルホンイミドリチウムおよび1,1,2,2,3,3,4,4−オクタフルオロブチル−1,3−ジスルホンイミドリチウムのうちの少なくとも1種の環状のイミド塩と、ハロゲン原子を有する環状の炭酸エステル誘導体とを含む
二次電池。 - 前記電解液は、更に、不飽和結合を有する環状の炭酸エステルおよびスルトンからなる群のうちの少なくとも1種を含む請求項1記載の二次電池。
- 正極および負極と共に非水溶媒および電解質塩を含む電解液を備え、
一対の正極および負極当たりの完全充電状態における開回路電圧が4.25V以上であり、
前記電解液は、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドリチウム、オルト−スルホベンズイミドリチウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドナトリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドナトリウム、オルト−スルホベンズイミドナトリウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドカリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドカリウム、オルト−スルホベンズイミドカリウム、1,1,2,2−テトラフルオロエタン−1,3−ジスルホンイミドリチウム、1−トリフルオロメチル−1,2,2,3,3−ペンタフルオロプロパン−1,3−ジスルホンイミドリチウムおよび1,1,2,2,3,3,4,4−オクタフルオロブチル−1,3−ジスルホンイミドリチウムのうちの少なくとも1種の環状のイミド塩と、ハロゲン原子を有する環状の炭酸エステル誘導体とを含む
二次電池。 - 前記電解液は、更に、不飽和結合を有する環状の炭酸エステルおよびスルトンからなる群のうちの少なくとも1種を含む請求項3記載の二次電池。
- 正極および負極と共に非水溶媒および電解質塩を含む電解液を備え、
負極活物質としてリチウム金属を用い、
前記電解液は、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドリチウム、オルト−スルホベンズイミドリチウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドナトリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドナトリウム、オルト−スルホベンズイミドナトリウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドカリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドカリウム、オルト−スルホベンズイミドカリウム、1,1,2,2−テトラフルオロエタン−1,3−ジスルホンイミドリチウム、1−トリフルオロメチル−1,2,2,3,3−ペンタフルオロプロパン−1,3−ジスルホンイミドリチウムおよび1,1,2,2,3,3,4,4−オクタフルオロブチル−1,3−ジスルホンイミドリチウムのうちの少なくとも1種の環状のイミド塩と、ハロゲン原子を有する環状の炭酸エステル誘導体とを含む
二次電池。 - 前記電解液は、更に、不飽和結合を有する環状の炭酸エステルおよびスルトンからなる群のうちの少なくとも1種を含む請求項5記載の二次電池。
- 1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドリチウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドリチウム、オルト−スルホベンズイミドリチウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドナトリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドナトリウム、オルト−スルホベンズイミドナトリウム、1,1,2,2,3,3−ヘキサフルオロプロパン−1,3−ジスルホンイミドカリウム、2,2,3,3,4,4−ヘキサフルオログルタルイミドカリウム、オルト−スルホベンズイミドカリウム、1,1,2,2−テトラフルオロエタン−1,3−ジスルホンイミドリチウム、1−トリフルオロメチル−1,2,2,3,3−ペンタフルオロプロパン−1,3−ジスルホンイミドリチウムおよび1,1,2,2,3,3,4,4−オクタフルオロブチル−1,3−ジスルホンイミドリチウムのうちの少なくとも1種の環状のイミド塩を含有する電解質塩と、ハロゲン原子を有する環状の炭酸エステル誘導体を含有する非水溶媒とを含む
二次電池用電解液。 - 前記イミド塩を0.1質量%以上31質量%以下の範囲内で含む請求項7記載の二次電池用電解液。
- 前記炭酸エステル誘導体として、4−フルオロ−1,3−ジオキソラン−2−オンおよび4−クロロ−1,3−ジオキソラン−2−オンのうちの少なくとも一方を含む請求項7記載の二次電池用電解液。
- 更に、不飽和結合を有する環状の炭酸エステルおよびスルトンからなる群のうちの少なくとも1種を含む請求項7記載の二次電池用電解液。
- 前記不飽和結合を有する環状の炭酸エステルの含有量は、0.05質量%以上20質量%以下の範囲内である請求項10記載の二次電池用電解液。
- 前記スルトンの含有量は、0.01質量%以上5質量%以下の範囲内である請求項10記載の二次電池用電解液。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006037698A JP5067522B2 (ja) | 2005-04-08 | 2006-02-15 | 二次電池用電解液および二次電池 |
| US11/278,977 US9583791B2 (en) | 2005-04-08 | 2006-04-07 | Electrolytic solution and battery |
| KR1020060031974A KR101315528B1 (ko) | 2005-04-08 | 2006-04-07 | 전해액 및 전지 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005112052 | 2005-04-08 | ||
| JP2005112052 | 2005-04-08 | ||
| JP2005116187 | 2005-04-13 | ||
| JP2005116187 | 2005-04-13 | ||
| JP2006037698A JP5067522B2 (ja) | 2005-04-08 | 2006-02-15 | 二次電池用電解液および二次電池 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2006318888A JP2006318888A (ja) | 2006-11-24 |
| JP2006318888A5 JP2006318888A5 (ja) | 2009-03-19 |
| JP5067522B2 true JP5067522B2 (ja) | 2012-11-07 |
Family
ID=37083520
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006037698A Expired - Fee Related JP5067522B2 (ja) | 2005-04-08 | 2006-02-15 | 二次電池用電解液および二次電池 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US9583791B2 (ja) |
| JP (1) | JP5067522B2 (ja) |
| KR (1) | KR101315528B1 (ja) |
Families Citing this family (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2584613C (en) * | 2004-10-28 | 2014-04-29 | University Of Stellenbosch | Impedance monitoring system and method |
| JP5070753B2 (ja) * | 2005-12-13 | 2012-11-14 | ソニー株式会社 | 電池 |
| JP4706528B2 (ja) * | 2006-03-22 | 2011-06-22 | ソニー株式会社 | リチウムイオン二次電池用電解液およびリチウムイオン二次電池 |
| KR101508788B1 (ko) * | 2006-06-02 | 2015-04-06 | 미쓰비시 가가꾸 가부시키가이샤 | 비수계 전해액 및 비수계 전해액 전지 |
| CN101517811B (zh) * | 2006-09-12 | 2012-01-11 | 株式会社杰士汤浅国际 | 非水电解质二次电池的制造方法 |
| JP5298419B2 (ja) * | 2006-10-16 | 2013-09-25 | ソニー株式会社 | 二次電池 |
| JP4241815B2 (ja) | 2006-12-07 | 2009-03-18 | ソニー株式会社 | 電解液および電池 |
| JP4836767B2 (ja) * | 2006-12-13 | 2011-12-14 | ソニー株式会社 | リチウムイオン二次電池 |
| KR20080067050A (ko) * | 2007-01-15 | 2008-07-18 | 제일모직주식회사 | 리튬 2차전지용 비수성 전해액 및 이를 포함하는 리튬2차전지 |
| KR100884439B1 (ko) * | 2007-03-12 | 2009-02-19 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 전해액 및 상기 전해액을 포함하는 리튬이차 전지 |
| JP4501963B2 (ja) * | 2007-05-28 | 2010-07-14 | ソニー株式会社 | リチウムイオン二次電池用負極およびリチウムイオン二次電池 |
| CN104393242B (zh) * | 2007-06-11 | 2018-02-02 | 株式会社Lg化学 | 非水电解质及包含该非水电解质的二次电池 |
| EP2162942B1 (en) * | 2007-06-29 | 2016-11-23 | Commonwealth Scientific and Industrial Research Organisation | Lithium energy storage device |
| US9509015B2 (en) | 2007-07-09 | 2016-11-29 | Sony Corporation | Battery |
| JP5167713B2 (ja) * | 2007-07-27 | 2013-03-21 | 株式会社Gsユアサ | 非水電解質二次電池 |
| KR100976958B1 (ko) * | 2008-01-08 | 2010-08-18 | 주식회사 엘지화학 | 리튬 이차전지용 비수 전해액 및 이를 구비한 리튬이차전지 |
| JP5217536B2 (ja) * | 2008-03-17 | 2013-06-19 | ソニー株式会社 | 二次電池および電子機器 |
| JP5827122B2 (ja) * | 2008-04-25 | 2015-12-02 | エルジー・ケム・リミテッド | リチウム二次電池用非水電解質及びそれを含むリチウム二次電池 |
| JP5605221B2 (ja) * | 2008-04-28 | 2014-10-15 | 旭硝子株式会社 | 二次電池用非水電解液および二次電池 |
| CN101640288B (zh) * | 2008-07-30 | 2012-03-07 | 比亚迪股份有限公司 | 一种锂离子电池电解液及含有该电解液的锂离子电池 |
| KR101056441B1 (ko) * | 2009-04-01 | 2011-08-11 | 삼성에스디아이 주식회사 | 첨가제를 포함하는 리튬 이차 전지용 전해질 및 이를 포함하는 리튬 이차 전지 |
| JP2010287431A (ja) * | 2009-06-11 | 2010-12-24 | Sony Corp | 電池 |
| KR101147240B1 (ko) * | 2009-11-10 | 2012-05-21 | 삼성에스디아이 주식회사 | 리튬 이차 전지 |
| KR101212203B1 (ko) * | 2010-03-16 | 2012-12-13 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 전해액 및 이를 포함하는 리튬 이차 전지 |
| JP5677779B2 (ja) * | 2010-07-26 | 2015-02-25 | 三星電子株式会社Samsung Electronics Co.,Ltd. | 固体リチウムイオン二次電池 |
| US20120021299A1 (en) * | 2010-07-26 | 2012-01-26 | Samsung Electronics Co., Ltd. | Solid lithium ion secondary battery and electrode therefor |
| EP2609646A1 (en) * | 2010-08-24 | 2013-07-03 | Basf Se | Electrolyte materials for use in electrochemical cells |
| US9166222B2 (en) | 2010-11-02 | 2015-10-20 | Envia Systems, Inc. | Lithium ion batteries with supplemental lithium |
| KR20120089211A (ko) | 2011-02-01 | 2012-08-09 | 고려대학교 산학협력단 | 회전하는 나노선 및 이를 이용한 세포 괴사 유도 방법 |
| JP2012243471A (ja) * | 2011-05-17 | 2012-12-10 | Sony Corp | 二次電池用電解液、二次電池、電子機器、電動工具、電動車両および電力貯蔵システム |
| JP2015018603A (ja) * | 2011-11-11 | 2015-01-29 | 旭硝子株式会社 | 非水電解液二次電池 |
| US20130157147A1 (en) * | 2011-12-14 | 2013-06-20 | Bing Li | Low Temperature Electrolyte for High Capacity Lithium Based Batteries |
| US9780358B2 (en) | 2012-05-04 | 2017-10-03 | Zenlabs Energy, Inc. | Battery designs with high capacity anode materials and cathode materials |
| US10553871B2 (en) | 2012-05-04 | 2020-02-04 | Zenlabs Energy, Inc. | Battery cell engineering and design to reach high energy |
| US9577289B2 (en) | 2012-12-17 | 2017-02-21 | Sion Power Corporation | Lithium-ion electrochemical cell, components thereof, and methods of making and using same |
| US10411299B2 (en) | 2013-08-02 | 2019-09-10 | Zenlabs Energy, Inc. | Electrolytes for stable cycling of high capacity lithium based batteries |
| JP6386406B2 (ja) * | 2015-03-30 | 2018-09-05 | マクセルホールディングス株式会社 | 非水電解液一次電池 |
| KR102093972B1 (ko) * | 2017-06-26 | 2020-03-26 | 주식회사 엘지화학 | 리튬 이차전지 |
| US11094925B2 (en) | 2017-12-22 | 2021-08-17 | Zenlabs Energy, Inc. | Electrodes with silicon oxide active materials for lithium ion cells achieving high capacity, high energy density and long cycle life performance |
| JP6965839B2 (ja) * | 2018-07-12 | 2021-11-10 | トヨタ自動車株式会社 | 二次電池の充電方法 |
| JPWO2021049178A1 (ja) * | 2019-09-11 | 2021-03-18 | ||
| AU2020386444A1 (en) * | 2019-11-18 | 2022-06-09 | Albemarle Corporation | Flame retardants for battery electrolytes |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2606217B1 (fr) | 1986-10-30 | 1990-12-14 | Elf Aquitaine | Nouveau materiau a conduction ionique constitue par un sel en solution dans un electrolyte liquide |
| JP3383454B2 (ja) * | 1995-03-03 | 2003-03-04 | 新神戸電機株式会社 | リチウム二次電池 |
| US5652072A (en) * | 1995-09-21 | 1997-07-29 | Minnesota Mining And Manufacturing Company | Battery containing bis(perfluoroalkylsulfonyl)imide and cyclic perfluoroalkylene disulfonylimide salts |
| US5691081A (en) * | 1995-09-21 | 1997-11-25 | Minnesota Mining And Manufacturing Company | Battery containing bis(perfluoroalkylsulfonyl)imide and cyclic perfluoroalkylene disulfonylimide salts |
| AU9095198A (en) * | 1997-09-19 | 1999-04-12 | Mitsubishi Chemical Corporation | Non-aqueous electrolyte cell |
| US6350545B2 (en) | 1998-08-25 | 2002-02-26 | 3M Innovative Properties Company | Sulfonylimide compounds |
| WO2001022519A1 (fr) | 1999-09-20 | 2001-03-29 | Sony Corporation | Cellule secondaire |
| JP2001093572A (ja) * | 1999-09-27 | 2001-04-06 | Hitachi Ltd | 非水電解液二次電池及びそれを用いた電気自動車、ハイブリット式自動車及び電力貯蔵システム |
| KR100520872B1 (ko) | 1999-10-22 | 2005-10-12 | 산요덴키가부시키가이샤 | 리튬 전지용 전극 및 리튬 2차전지 |
| CN1175512C (zh) * | 1999-11-29 | 2004-11-10 | 松下电器产业株式会社 | 非水电解质及非水电解质电池 |
| EP1403957A1 (en) * | 2001-05-10 | 2004-03-31 | Nisshinbo Industries, Inc. | Nonaqueous electrolytic solution, composition for polymer gel electrolyte, polymer gel electrolyte, secondary cell, and electric double-layer capacitor |
| CN100385727C (zh) * | 2002-03-08 | 2008-04-30 | 三菱化学株式会社 | 非水电解液及采用它的锂二次电池 |
| CN101853959A (zh) * | 2002-04-02 | 2010-10-06 | 株式会社日本触媒 | 电解质溶液用材料及其用途 |
| JP4248258B2 (ja) * | 2003-01-16 | 2009-04-02 | 三洋電機株式会社 | リチウム二次電池 |
| JP4352719B2 (ja) * | 2003-02-21 | 2009-10-28 | 日本電気株式会社 | リチウムイオン二次電池用電解液およびそれを用いたリチウムイオン二次電池 |
| US7083878B2 (en) * | 2003-02-27 | 2006-08-01 | Mitsubishi Chemical Corporation | Nonaqueous electrolytic solution and lithium secondary battery |
| KR100515298B1 (ko) * | 2003-03-24 | 2005-09-15 | 삼성에스디아이 주식회사 | 비수성 전해질 및 이를 포함하는 리튬 이차 전지 |
| JP4433833B2 (ja) * | 2003-05-13 | 2010-03-17 | 三菱化学株式会社 | 非水系電解液及び非水系電解液二次電池 |
| US7901810B2 (en) * | 2003-06-03 | 2011-03-08 | Valence Technology, Inc. | Battery active materials and methods for synthesis |
| JP2006077107A (ja) * | 2004-09-09 | 2006-03-23 | Japan Carlit Co Ltd:The | ゲル状電解質及びその製造方法 |
| JP4951933B2 (ja) * | 2005-02-18 | 2012-06-13 | ソニー株式会社 | リチウムイオン二次電池用電解質およびリチウムイオン二次電池 |
-
2006
- 2006-02-15 JP JP2006037698A patent/JP5067522B2/ja not_active Expired - Fee Related
- 2006-04-07 KR KR1020060031974A patent/KR101315528B1/ko active IP Right Grant
- 2006-04-07 US US11/278,977 patent/US9583791B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| KR101315528B1 (ko) | 2013-10-08 |
| US20060228626A1 (en) | 2006-10-12 |
| KR20060107410A (ko) | 2006-10-13 |
| JP2006318888A (ja) | 2006-11-24 |
| US9583791B2 (en) | 2017-02-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5067522B2 (ja) | 二次電池用電解液および二次電池 | |
| JP4940625B2 (ja) | 電解液および電池 | |
| JP4984022B2 (ja) | 二次電池 | |
| JP5055710B2 (ja) | 二次電池用電解液、二次電池および電子機器 | |
| JP4349321B2 (ja) | 電池 | |
| JP4706528B2 (ja) | リチウムイオン二次電池用電解液およびリチウムイオン二次電池 | |
| JP4968503B2 (ja) | リチウム二次電池 | |
| JP4329806B2 (ja) | 二次電池 | |
| KR20160097181A (ko) | 전해액 및 전지 | |
| JP4951933B2 (ja) | リチウムイオン二次電池用電解質およびリチウムイオン二次電池 | |
| JP4957944B2 (ja) | 二次電池 | |
| JP4792919B2 (ja) | 電池 | |
| JP5109359B2 (ja) | 非水電解質二次電池 | |
| JP2006134719A (ja) | 電解液および電池 | |
| JP2007042387A (ja) | 電解液,電極および電池 | |
| JP2006331866A (ja) | 電池 | |
| JP2006286532A (ja) | 電池 | |
| JP4359780B2 (ja) | リチウムイオン二次電池 | |
| JP2008053054A (ja) | 電池 | |
| JP2007242545A (ja) | 電解質および電池 | |
| JP2007273396A (ja) | 電解液および電池 | |
| JP2007250191A (ja) | 電解質および電池 | |
| JP2011154963A (ja) | 非水電解質電池 | |
| JP2010165549A (ja) | 二次電池 | |
| JP5598457B2 (ja) | 二次電池および電子機器 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090129 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090129 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110825 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110906 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111031 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120718 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120731 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150824 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150824 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |