JP4705986B2 - 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 - Google Patents
5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 Download PDFInfo
- Publication number
- JP4705986B2 JP4705986B2 JP2008539007A JP2008539007A JP4705986B2 JP 4705986 B2 JP4705986 B2 JP 4705986B2 JP 2008539007 A JP2008539007 A JP 2008539007A JP 2008539007 A JP2008539007 A JP 2008539007A JP 4705986 B2 JP4705986 B2 JP 4705986B2
- Authority
- JP
- Japan
- Prior art keywords
- formula
- compound
- substituted
- pyridin
- unsubstituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 108090000411 5-Lipoxygenase-Activating Proteins Proteins 0.000 title abstract description 28
- 102000004023 5-Lipoxygenase-Activating Proteins Human genes 0.000 title abstract description 28
- 239000003112 inhibitor Substances 0.000 title description 47
- 150000001875 compounds Chemical class 0.000 claims abstract description 558
- -1 5-methyl-pyridin-2-ylmethyl Chemical group 0.000 claims description 199
- 150000003839 salts Chemical class 0.000 claims description 35
- 239000012453 solvate Substances 0.000 claims description 12
- 159000000000 sodium salts Chemical class 0.000 claims description 5
- DFQGDHBGRSTTHX-UHFFFAOYSA-N fiboflapon Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC(C)=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DFQGDHBGRSTTHX-UHFFFAOYSA-N 0.000 claims 3
- NOJNFULGOQGBKB-UHFFFAOYSA-M sodium;3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoate Chemical compound [Na+].C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC(C)=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C([O-])=O NOJNFULGOQGBKB-UHFFFAOYSA-M 0.000 claims 1
- 150000002617 leukotrienes Chemical class 0.000 abstract description 211
- 238000000034 method Methods 0.000 abstract description 190
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 142
- 201000010099 disease Diseases 0.000 abstract description 109
- 239000008194 pharmaceutical composition Substances 0.000 abstract description 82
- 230000001419 dependent effect Effects 0.000 abstract description 48
- 230000001404 mediated effect Effects 0.000 abstract description 47
- 230000000694 effects Effects 0.000 abstract description 42
- 230000000241 respiratory effect Effects 0.000 abstract description 3
- 230000002526 effect on cardiovascular system Effects 0.000 abstract 1
- 239000003814 drug Substances 0.000 description 117
- 125000000217 alkyl group Chemical group 0.000 description 100
- 241000124008 Mammalia Species 0.000 description 93
- 238000011282 treatment Methods 0.000 description 93
- 208000006673 asthma Diseases 0.000 description 86
- 125000001072 heteroaryl group Chemical group 0.000 description 81
- 239000000203 mixture Substances 0.000 description 78
- 125000003118 aryl group Chemical group 0.000 description 74
- 108090000623 proteins and genes Proteins 0.000 description 61
- GWNVDXQDILPJIG-CCHJCNDSSA-N 11-trans-Leukotriene C4 Chemical compound CCCCC\C=C/C\C=C\C=C\C=C\[C@H]([C@@H](O)CCCC(O)=O)SC[C@@H](C(=O)NCC(O)=O)NC(=O)CC[C@H](N)C(O)=O GWNVDXQDILPJIG-CCHJCNDSSA-N 0.000 description 57
- 229940079593 drug Drugs 0.000 description 57
- 125000000623 heterocyclic group Chemical group 0.000 description 51
- 102000054766 genetic haplotypes Human genes 0.000 description 50
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 45
- 239000003795 chemical substances by application Substances 0.000 description 42
- 125000000753 cycloalkyl group Chemical group 0.000 description 42
- 230000002265 prevention Effects 0.000 description 41
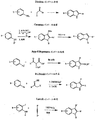
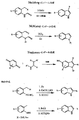
- 238000003786 synthesis reaction Methods 0.000 description 39
- 230000015572 biosynthetic process Effects 0.000 description 38
- 208000006011 Stroke Diseases 0.000 description 35
- 230000037361 pathway Effects 0.000 description 35
- 235000002639 sodium chloride Nutrition 0.000 description 34
- 208000035475 disorder Diseases 0.000 description 33
- 206010028980 Neoplasm Diseases 0.000 description 32
- 239000000651 prodrug Substances 0.000 description 32
- 229940002612 prodrug Drugs 0.000 description 32
- 239000002253 acid Substances 0.000 description 31
- 229910052717 sulfur Inorganic materials 0.000 description 30
- 108010093579 Arachidonate 5-lipoxygenase Proteins 0.000 description 26
- 102000001381 Arachidonate 5-Lipoxygenase Human genes 0.000 description 25
- 125000003342 alkenyl group Chemical group 0.000 description 25
- 229910052799 carbon Inorganic materials 0.000 description 24
- 210000001519 tissue Anatomy 0.000 description 24
- 201000011510 cancer Diseases 0.000 description 23
- 238000006243 chemical reaction Methods 0.000 description 23
- 238000009472 formulation Methods 0.000 description 23
- 210000000056 organ Anatomy 0.000 description 23
- 235000018102 proteins Nutrition 0.000 description 23
- 102000004169 proteins and genes Human genes 0.000 description 23
- 125000003831 tetrazolyl group Chemical group 0.000 description 23
- 210000004027 cell Anatomy 0.000 description 22
- 230000002757 inflammatory effect Effects 0.000 description 22
- 230000004054 inflammatory process Effects 0.000 description 22
- 239000002904 solvent Substances 0.000 description 22
- 208000024891 symptom Diseases 0.000 description 22
- 206010061218 Inflammation Diseases 0.000 description 21
- 238000001727 in vivo Methods 0.000 description 21
- 208000023504 respiratory system disease Diseases 0.000 description 21
- 125000001424 substituent group Chemical group 0.000 description 21
- 239000002585 base Substances 0.000 description 20
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 20
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 20
- 208000010125 myocardial infarction Diseases 0.000 description 20
- 102000005962 receptors Human genes 0.000 description 20
- 108020003175 receptors Proteins 0.000 description 20
- 108700028369 Alleles Proteins 0.000 description 19
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 19
- 239000005557 antagonist Substances 0.000 description 19
- 239000003199 leukotriene receptor blocking agent Substances 0.000 description 19
- 229910052757 nitrogen Inorganic materials 0.000 description 19
- 125000006239 protecting group Chemical group 0.000 description 19
- 239000000126 substance Substances 0.000 description 19
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 18
- 229910052760 oxygen Inorganic materials 0.000 description 18
- 229940044551 receptor antagonist Drugs 0.000 description 18
- 239000002464 receptor antagonist Substances 0.000 description 18
- 229940124597 therapeutic agent Drugs 0.000 description 18
- 230000001225 therapeutic effect Effects 0.000 description 18
- 238000002560 therapeutic procedure Methods 0.000 description 18
- 208000026935 allergic disease Diseases 0.000 description 17
- 208000010668 atopic eczema Diseases 0.000 description 17
- 230000008901 benefit Effects 0.000 description 17
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 17
- 206010020751 Hypersensitivity Diseases 0.000 description 16
- 239000000090 biomarker Substances 0.000 description 16
- 238000002648 combination therapy Methods 0.000 description 16
- 229910052736 halogen Inorganic materials 0.000 description 16
- 150000002367 halogens Chemical class 0.000 description 16
- 125000004404 heteroalkyl group Chemical group 0.000 description 16
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 16
- 206010040070 Septic Shock Diseases 0.000 description 15
- 125000004429 atom Chemical group 0.000 description 15
- 125000004093 cyano group Chemical group *C#N 0.000 description 15
- 125000004122 cyclic group Chemical group 0.000 description 15
- 230000004048 modification Effects 0.000 description 15
- 238000012986 modification Methods 0.000 description 15
- 210000003491 skin Anatomy 0.000 description 15
- 230000000172 allergic effect Effects 0.000 description 14
- 230000007815 allergy Effects 0.000 description 14
- 230000009977 dual effect Effects 0.000 description 14
- 239000002773 nucleotide Substances 0.000 description 14
- 125000003729 nucleotide group Chemical group 0.000 description 14
- 239000000546 pharmaceutical excipient Substances 0.000 description 14
- 230000004044 response Effects 0.000 description 14
- 208000024535 susceptibility to myocardial infarction Diseases 0.000 description 14
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 13
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 13
- 210000003979 eosinophil Anatomy 0.000 description 13
- 239000003550 marker Substances 0.000 description 13
- 230000002062 proliferating effect Effects 0.000 description 13
- 239000000243 solution Substances 0.000 description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 102000014962 Monocyte Chemoattractant Proteins Human genes 0.000 description 12
- 108010064136 Monocyte Chemoattractant Proteins Proteins 0.000 description 12
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 12
- 230000004071 biological effect Effects 0.000 description 12
- 210000004072 lung Anatomy 0.000 description 12
- 239000002207 metabolite Substances 0.000 description 12
- 210000000440 neutrophil Anatomy 0.000 description 12
- 108090000765 processed proteins & peptides Proteins 0.000 description 12
- 239000000725 suspension Substances 0.000 description 12
- 206010014824 Endotoxic shock Diseases 0.000 description 11
- 241000700159 Rattus Species 0.000 description 11
- 230000001154 acute effect Effects 0.000 description 11
- 229940121363 anti-inflammatory agent Drugs 0.000 description 11
- 239000002260 anti-inflammatory agent Substances 0.000 description 11
- 125000004432 carbon atom Chemical group C* 0.000 description 11
- 208000027866 inflammatory disease Diseases 0.000 description 11
- 229940065725 leukotriene receptor antagonists for obstructive airway diseases Drugs 0.000 description 11
- 238000012544 monitoring process Methods 0.000 description 11
- 201000001320 Atherosclerosis Diseases 0.000 description 10
- 108010074051 C-Reactive Protein Proteins 0.000 description 10
- 102100032752 C-reactive protein Human genes 0.000 description 10
- 102000004190 Enzymes Human genes 0.000 description 10
- 108090000790 Enzymes Proteins 0.000 description 10
- 108010092408 Eosinophil Peroxidase Proteins 0.000 description 10
- 102000044708 Eosinophil peroxidases Human genes 0.000 description 10
- 208000029523 Interstitial Lung disease Diseases 0.000 description 10
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical group CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 10
- 102000003896 Myeloperoxidases Human genes 0.000 description 10
- 108090000235 Myeloperoxidases Proteins 0.000 description 10
- 102000054727 Serum Amyloid A Human genes 0.000 description 10
- 101710190759 Serum amyloid A protein Proteins 0.000 description 10
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 10
- 239000004480 active ingredient Substances 0.000 description 10
- 230000027455 binding Effects 0.000 description 10
- 239000002775 capsule Substances 0.000 description 10
- 239000002552 dosage form Substances 0.000 description 10
- 229940088598 enzyme Drugs 0.000 description 10
- 230000002401 inhibitory effect Effects 0.000 description 10
- 210000001616 monocyte Anatomy 0.000 description 10
- 229960005127 montelukast Drugs 0.000 description 10
- 230000000704 physical effect Effects 0.000 description 10
- 239000003381 stabilizer Substances 0.000 description 10
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 9
- 102100038496 Cysteinyl leukotriene receptor 1 Human genes 0.000 description 9
- 102000003816 Interleukin-13 Human genes 0.000 description 9
- 108090000176 Interleukin-13 Proteins 0.000 description 9
- 102000004388 Interleukin-4 Human genes 0.000 description 9
- 108090000978 Interleukin-4 Proteins 0.000 description 9
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 9
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 9
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 9
- 239000000556 agonist Substances 0.000 description 9
- 125000000304 alkynyl group Chemical group 0.000 description 9
- 229940114079 arachidonic acid Drugs 0.000 description 9
- 235000021342 arachidonic acid Nutrition 0.000 description 9
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 230000014509 gene expression Effects 0.000 description 9
- 230000005764 inhibitory process Effects 0.000 description 9
- 229940028885 interleukin-4 Drugs 0.000 description 9
- 210000003734 kidney Anatomy 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 102000054765 polymorphisms of proteins Human genes 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 102000004196 processed proteins & peptides Human genes 0.000 description 9
- 208000002815 pulmonary hypertension Diseases 0.000 description 9
- 125000004076 pyridyl group Chemical group 0.000 description 9
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 description 9
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 8
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 8
- 208000020084 Bone disease Diseases 0.000 description 8
- 101000882759 Homo sapiens Cysteinyl leukotriene receptor 1 Proteins 0.000 description 8
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 8
- 150000001204 N-oxides Chemical class 0.000 description 8
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 8
- 206010047139 Vasoconstriction Diseases 0.000 description 8
- 150000001413 amino acids Chemical class 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 210000004204 blood vessel Anatomy 0.000 description 8
- 239000000872 buffer Substances 0.000 description 8
- 239000000969 carrier Substances 0.000 description 8
- 230000008859 change Effects 0.000 description 8
- 239000003085 diluting agent Substances 0.000 description 8
- 125000000524 functional group Chemical group 0.000 description 8
- 239000000499 gel Substances 0.000 description 8
- 229910052739 hydrogen Inorganic materials 0.000 description 8
- 239000007924 injection Substances 0.000 description 8
- 238000002347 injection Methods 0.000 description 8
- 239000000843 powder Substances 0.000 description 8
- 239000003755 preservative agent Substances 0.000 description 8
- 230000002829 reductive effect Effects 0.000 description 8
- 230000004043 responsiveness Effects 0.000 description 8
- 239000007787 solid Substances 0.000 description 8
- 230000025033 vasoconstriction Effects 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 102000010918 Cysteinyl leukotriene receptors Human genes 0.000 description 7
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 7
- 102000004889 Interleukin-6 Human genes 0.000 description 7
- 108090001005 Interleukin-6 Proteins 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- 230000009471 action Effects 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 210000003651 basophil Anatomy 0.000 description 7
- 125000000392 cycloalkenyl group Chemical group 0.000 description 7
- 230000036541 health Effects 0.000 description 7
- 238000001802 infusion Methods 0.000 description 7
- 230000000670 limiting effect Effects 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 230000002503 metabolic effect Effects 0.000 description 7
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 7
- 150000007523 nucleic acids Chemical class 0.000 description 7
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 7
- 238000006722 reduction reaction Methods 0.000 description 7
- 238000012216 screening Methods 0.000 description 7
- 150000003431 steroids Chemical class 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 7
- 239000003406 5-lipoxygenase-activating protein inhibitor Substances 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 208000004476 Acute Coronary Syndrome Diseases 0.000 description 6
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 201000006474 Brain Ischemia Diseases 0.000 description 6
- 206010008120 Cerebral ischaemia Diseases 0.000 description 6
- 201000004624 Dermatitis Diseases 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 208000005615 Interstitial Cystitis Diseases 0.000 description 6
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 6
- 208000019695 Migraine disease Diseases 0.000 description 6
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 6
- YEEZWCHGZNKEEK-UHFFFAOYSA-N Zafirlukast Chemical compound COC1=CC(C(=O)NS(=O)(=O)C=2C(=CC=CC=2)C)=CC=C1CC(C1=C2)=CN(C)C1=CC=C2NC(=O)OC1CCCC1 YEEZWCHGZNKEEK-UHFFFAOYSA-N 0.000 description 6
- 230000002159 abnormal effect Effects 0.000 description 6
- 239000000443 aerosol Substances 0.000 description 6
- 239000013566 allergen Substances 0.000 description 6
- 230000036772 blood pressure Effects 0.000 description 6
- 206010008118 cerebral infarction Diseases 0.000 description 6
- 150000002148 esters Chemical class 0.000 description 6
- 208000030533 eye disease Diseases 0.000 description 6
- 208000019622 heart disease Diseases 0.000 description 6
- 125000005842 heteroatom Chemical group 0.000 description 6
- 210000003630 histaminocyte Anatomy 0.000 description 6
- 150000002475 indoles Chemical class 0.000 description 6
- 125000001041 indolyl group Chemical group 0.000 description 6
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 210000002540 macrophage Anatomy 0.000 description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 6
- 206010027599 migraine Diseases 0.000 description 6
- 208000031225 myocardial ischemia Diseases 0.000 description 6
- 229920000642 polymer Polymers 0.000 description 6
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 6
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 206010039083 rhinitis Diseases 0.000 description 6
- 230000028327 secretion Effects 0.000 description 6
- 208000017520 skin disease Diseases 0.000 description 6
- 239000012730 sustained-release form Substances 0.000 description 6
- 239000003826 tablet Substances 0.000 description 6
- 125000001544 thienyl group Chemical group 0.000 description 6
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 6
- 238000011269 treatment regimen Methods 0.000 description 6
- 208000024827 Alzheimer disease Diseases 0.000 description 5
- 208000033309 Analgesic asthma syndrome Diseases 0.000 description 5
- 206010002329 Aneurysm Diseases 0.000 description 5
- 206010003557 Asthma exercise induced Diseases 0.000 description 5
- 206010011224 Cough Diseases 0.000 description 5
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 5
- 108010036949 Cyclosporine Proteins 0.000 description 5
- 208000004657 Exercise-Induced Asthma Diseases 0.000 description 5
- 102100033374 Leukotriene B4 receptor 1 Human genes 0.000 description 5
- 206010061296 Motor dysfunction Diseases 0.000 description 5
- 241000699670 Mus sp. Species 0.000 description 5
- 201000004681 Psoriasis Diseases 0.000 description 5
- 206010063837 Reperfusion injury Diseases 0.000 description 5
- 208000037883 airway inflammation Diseases 0.000 description 5
- 235000001014 amino acid Nutrition 0.000 description 5
- 206010003246 arthritis Diseases 0.000 description 5
- 208000024744 aspirin-induced respiratory disease Diseases 0.000 description 5
- 230000010072 bone remodeling Effects 0.000 description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 5
- 208000015114 central nervous system disease Diseases 0.000 description 5
- 208000029771 childhood onset asthma Diseases 0.000 description 5
- 208000023819 chronic asthma Diseases 0.000 description 5
- 230000001684 chronic effect Effects 0.000 description 5
- 229960001265 ciclosporin Drugs 0.000 description 5
- 239000013078 crystal Substances 0.000 description 5
- 229930182912 cyclosporin Natural products 0.000 description 5
- 230000002950 deficient Effects 0.000 description 5
- 230000000593 degrading effect Effects 0.000 description 5
- 210000004443 dendritic cell Anatomy 0.000 description 5
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 description 5
- 239000008298 dragée Substances 0.000 description 5
- 239000012039 electrophile Substances 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- NNYBQONXHNTVIJ-UHFFFAOYSA-N etodolac Chemical compound C1COC(CC)(CC(O)=O)C2=C1C(C=CC=C1CC)=C1N2 NNYBQONXHNTVIJ-UHFFFAOYSA-N 0.000 description 5
- 208000024695 exercise-induced bronchoconstriction Diseases 0.000 description 5
- 230000002496 gastric effect Effects 0.000 description 5
- 208000000122 hyperventilation Diseases 0.000 description 5
- 230000000870 hyperventilation Effects 0.000 description 5
- 230000004968 inflammatory condition Effects 0.000 description 5
- 239000000543 intermediate Substances 0.000 description 5
- 238000001990 intravenous administration Methods 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 239000002502 liposome Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 229950001413 metamfepramone Drugs 0.000 description 5
- 208000007892 occupational asthma Diseases 0.000 description 5
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 5
- 229960004583 pranlukast Drugs 0.000 description 5
- UAJUXJSXCLUTNU-UHFFFAOYSA-N pranlukast Chemical compound C=1C=C(OCCCCC=2C=CC=CC=2)C=CC=1C(=O)NC(C=1)=CC=C(C(C=2)=O)C=1OC=2C=1N=NNN=1 UAJUXJSXCLUTNU-UHFFFAOYSA-N 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 230000000069 prophylactic effect Effects 0.000 description 5
- 230000007115 recruitment Effects 0.000 description 5
- 230000001932 seasonal effect Effects 0.000 description 5
- 238000013268 sustained release Methods 0.000 description 5
- 125000000335 thiazolyl group Chemical group 0.000 description 5
- 230000002792 vascular Effects 0.000 description 5
- 229960004764 zafirlukast Drugs 0.000 description 5
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 4
- LBUJPTNKIBCYBY-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinoline Chemical compound C1=CC=C2CCCNC2=C1 LBUJPTNKIBCYBY-UHFFFAOYSA-N 0.000 description 4
- 125000005330 8 membered heterocyclic group Chemical group 0.000 description 4
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 4
- 206010048962 Brain oedema Diseases 0.000 description 4
- 206010006458 Bronchitis chronic Diseases 0.000 description 4
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 4
- 108020004414 DNA Proteins 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 4
- 206010014561 Emphysema Diseases 0.000 description 4
- 206010016654 Fibrosis Diseases 0.000 description 4
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 4
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 4
- 108010010803 Gelatin Proteins 0.000 description 4
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 4
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 4
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 4
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 4
- 239000000867 Lipoxygenase Inhibitor Substances 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- 208000010191 Osteitis Deformans Diseases 0.000 description 4
- 229930012538 Paclitaxel Natural products 0.000 description 4
- 208000027868 Paget disease Diseases 0.000 description 4
- 208000002193 Pain Diseases 0.000 description 4
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 4
- 208000018737 Parkinson disease Diseases 0.000 description 4
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 4
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N Propionic acid Substances CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 4
- 108020004459 Small interfering RNA Proteins 0.000 description 4
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 4
- 206010047115 Vasculitis Diseases 0.000 description 4
- 229960001138 acetylsalicylic acid Drugs 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- 208000024716 acute asthma Diseases 0.000 description 4
- 150000001336 alkenes Chemical class 0.000 description 4
- 208000002205 allergic conjunctivitis Diseases 0.000 description 4
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 4
- 125000003277 amino group Chemical group 0.000 description 4
- 239000003963 antioxidant agent Substances 0.000 description 4
- 235000006708 antioxidants Nutrition 0.000 description 4
- 208000007474 aortic aneurysm Diseases 0.000 description 4
- 239000007864 aqueous solution Substances 0.000 description 4
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 4
- 208000024998 atopic conjunctivitis Diseases 0.000 description 4
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 4
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 4
- 125000004601 benzofurazanyl group Chemical group N1=C2C(=NO1)C(=CC=C2)* 0.000 description 4
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 4
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 4
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 4
- 210000004556 brain Anatomy 0.000 description 4
- 208000006752 brain edema Diseases 0.000 description 4
- 206010006451 bronchitis Diseases 0.000 description 4
- 150000001735 carboxylic acids Chemical class 0.000 description 4
- 210000000170 cell membrane Anatomy 0.000 description 4
- 208000007451 chronic bronchitis Diseases 0.000 description 4
- 230000008602 contraction Effects 0.000 description 4
- 239000003246 corticosteroid Substances 0.000 description 4
- 229960001334 corticosteroids Drugs 0.000 description 4
- 108040002734 cysteinyl leukotriene receptor activity proteins Proteins 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 238000013461 design Methods 0.000 description 4
- 238000003745 diagnosis Methods 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 230000004064 dysfunction Effects 0.000 description 4
- 229960005293 etodolac Drugs 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- 230000003176 fibrotic effect Effects 0.000 description 4
- 125000003838 furazanyl group Chemical group 0.000 description 4
- 125000002541 furyl group Chemical group 0.000 description 4
- 239000008273 gelatin Substances 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 229940014259 gelatin Drugs 0.000 description 4
- 235000019322 gelatine Nutrition 0.000 description 4
- 235000011852 gelatine desserts Nutrition 0.000 description 4
- 230000002068 genetic effect Effects 0.000 description 4
- 125000005843 halogen group Chemical group 0.000 description 4
- 210000002216 heart Anatomy 0.000 description 4
- 239000005556 hormone Chemical class 0.000 description 4
- 229940088597 hormone Drugs 0.000 description 4
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 4
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 4
- 125000002883 imidazolyl group Chemical group 0.000 description 4
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 4
- 125000003406 indolizinyl group Chemical group C=1(C=CN2C=CC=CC12)* 0.000 description 4
- 208000014674 injury Diseases 0.000 description 4
- 229960004768 irinotecan Drugs 0.000 description 4
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 4
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 4
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 4
- 125000001786 isothiazolyl group Chemical group 0.000 description 4
- 125000000842 isoxazolyl group Chemical group 0.000 description 4
- 206010023332 keratitis Diseases 0.000 description 4
- 201000010666 keratoconjunctivitis Diseases 0.000 description 4
- 150000002576 ketones Chemical class 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- 230000003902 lesion Effects 0.000 description 4
- 210000000265 leukocyte Anatomy 0.000 description 4
- VNYSSYRCGWBHLG-AMOLWHMGSA-N leukotriene B4 Chemical compound CCCCC\C=C/C[C@@H](O)\C=C\C=C\C=C/[C@@H](O)CCCC(O)=O VNYSSYRCGWBHLG-AMOLWHMGSA-N 0.000 description 4
- 150000002632 lipids Chemical class 0.000 description 4
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 4
- 208000027202 mammary Paget disease Diseases 0.000 description 4
- 108020004999 messenger RNA Proteins 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 239000003607 modifier Substances 0.000 description 4
- 210000004877 mucosa Anatomy 0.000 description 4
- 201000006417 multiple sclerosis Diseases 0.000 description 4
- 208000024696 nocturnal asthma Diseases 0.000 description 4
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 4
- 102000039446 nucleic acids Human genes 0.000 description 4
- 108020004707 nucleic acids Proteins 0.000 description 4
- 150000007530 organic bases Chemical class 0.000 description 4
- 125000001715 oxadiazolyl group Chemical group 0.000 description 4
- 125000002971 oxazolyl group Chemical group 0.000 description 4
- 229960001592 paclitaxel Drugs 0.000 description 4
- 230000036407 pain Effects 0.000 description 4
- 201000002528 pancreatic cancer Diseases 0.000 description 4
- 208000008443 pancreatic carcinoma Diseases 0.000 description 4
- 208000033808 peripheral neuropathy Diseases 0.000 description 4
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 4
- 239000006187 pill Substances 0.000 description 4
- 229920000728 polyester Polymers 0.000 description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 4
- 150000003180 prostaglandins Chemical class 0.000 description 4
- 230000001185 psoriatic effect Effects 0.000 description 4
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 4
- 230000002685 pulmonary effect Effects 0.000 description 4
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 4
- 125000003373 pyrazinyl group Chemical group 0.000 description 4
- 125000003226 pyrazolyl group Chemical group 0.000 description 4
- 125000002098 pyridazinyl group Chemical group 0.000 description 4
- LXNHXLLTXMVWPM-UHFFFAOYSA-N pyridoxine Chemical compound CC1=NC=C(CO)C(CO)=C1O LXNHXLLTXMVWPM-UHFFFAOYSA-N 0.000 description 4
- 125000000714 pyrimidinyl group Chemical group 0.000 description 4
- 125000000168 pyrrolyl group Chemical group 0.000 description 4
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 4
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 4
- 206010039073 rheumatoid arthritis Diseases 0.000 description 4
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 4
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 4
- 210000002460 smooth muscle Anatomy 0.000 description 4
- 230000009870 specific binding Effects 0.000 description 4
- 208000020431 spinal cord injury Diseases 0.000 description 4
- 239000011593 sulfur Substances 0.000 description 4
- 239000000829 suppository Substances 0.000 description 4
- 239000000375 suspending agent Substances 0.000 description 4
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- 125000001113 thiadiazolyl group Chemical group 0.000 description 4
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 4
- 231100000331 toxic Toxicity 0.000 description 4
- 230000002588 toxic effect Effects 0.000 description 4
- 125000004306 triazinyl group Chemical group 0.000 description 4
- 125000001425 triazolyl group Chemical group 0.000 description 4
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 4
- LNPDTQAFDNKSHK-UHFFFAOYSA-N valdecoxib Chemical compound CC=1ON=C(C=2C=CC=CC=2)C=1C1=CC=C(S(N)(=O)=O)C=C1 LNPDTQAFDNKSHK-UHFFFAOYSA-N 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- 229940088594 vitamin Drugs 0.000 description 4
- 229930003231 vitamin Natural products 0.000 description 4
- 235000013343 vitamin Nutrition 0.000 description 4
- 239000011782 vitamin Substances 0.000 description 4
- MWLSOWXNZPKENC-SSDOTTSWSA-N zileuton Chemical compound C1=CC=C2SC([C@H](N(O)C(N)=O)C)=CC2=C1 MWLSOWXNZPKENC-SSDOTTSWSA-N 0.000 description 4
- 229960005332 zileuton Drugs 0.000 description 4
- MMRHLAWASYGFGE-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[(4-pyridin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 MMRHLAWASYGFGE-UHFFFAOYSA-N 0.000 description 3
- JHOYRZAAKYTOSC-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-methylpyridin-2-yl)methoxy]-1-[[4-[6-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=C(C=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 JHOYRZAAKYTOSC-UHFFFAOYSA-N 0.000 description 3
- 229940124125 5 Lipoxygenase inhibitor Drugs 0.000 description 3
- JNUUNUQHXIOFDA-XTDASVJISA-N 5-HPETE Chemical compound CCCCC\C=C/C\C=C/C\C=C/C=C/C(OO)CCCC(O)=O JNUUNUQHXIOFDA-XTDASVJISA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- 229940122361 Bisphosphonate Drugs 0.000 description 3
- 102000004506 Blood Proteins Human genes 0.000 description 3
- 108010017384 Blood Proteins Proteins 0.000 description 3
- 206010065687 Bone loss Diseases 0.000 description 3
- 206010006482 Bronchospasm Diseases 0.000 description 3
- 229940127291 Calcium channel antagonist Drugs 0.000 description 3
- 208000028698 Cognitive impairment Diseases 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 3
- 108050001116 Cysteinyl leukotriene receptors Proteins 0.000 description 3
- 201000003883 Cystic fibrosis Diseases 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 3
- 206010012442 Dermatitis contact Diseases 0.000 description 3
- CYQFCXCEBYINGO-DLBZAZTESA-N Dronabinol Natural products C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@H]21 CYQFCXCEBYINGO-DLBZAZTESA-N 0.000 description 3
- 206010016207 Familial Mediterranean fever Diseases 0.000 description 3
- 208000007882 Gastritis Diseases 0.000 description 3
- 206010018364 Glomerulonephritis Diseases 0.000 description 3
- 206010019196 Head injury Diseases 0.000 description 3
- 206010019233 Headaches Diseases 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101150101999 IL6 gene Proteins 0.000 description 3
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 3
- 102000004890 Interleukin-8 Human genes 0.000 description 3
- 108090001007 Interleukin-8 Proteins 0.000 description 3
- 231100000111 LD50 Toxicity 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 208000001145 Metabolic Syndrome Diseases 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 3
- 206010029155 Nephropathy toxic Diseases 0.000 description 3
- 206010030113 Oedema Diseases 0.000 description 3
- 208000001132 Osteoporosis Diseases 0.000 description 3
- 108010016731 PPAR gamma Proteins 0.000 description 3
- 102100038825 Peroxisome proliferator-activated receptor gamma Human genes 0.000 description 3
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 102100038277 Prostaglandin G/H synthase 1 Human genes 0.000 description 3
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 3
- 206010063897 Renal ischaemia Diseases 0.000 description 3
- 206010039085 Rhinitis allergic Diseases 0.000 description 3
- 241001303601 Rosacea Species 0.000 description 3
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- CYQFCXCEBYINGO-UHFFFAOYSA-N THC Natural products C1=C(C)CCC2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3C21 CYQFCXCEBYINGO-UHFFFAOYSA-N 0.000 description 3
- 208000024780 Urticaria Diseases 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 150000001345 alkine derivatives Chemical group 0.000 description 3
- 125000003545 alkoxy group Chemical group 0.000 description 3
- 201000010105 allergic rhinitis Diseases 0.000 description 3
- 150000001412 amines Chemical group 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- 230000002590 anti-leukotriene effect Effects 0.000 description 3
- 239000007900 aqueous suspension Substances 0.000 description 3
- 235000010323 ascorbic acid Nutrition 0.000 description 3
- 239000011668 ascorbic acid Substances 0.000 description 3
- 229960005070 ascorbic acid Drugs 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 229960002170 azathioprine Drugs 0.000 description 3
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 230000017531 blood circulation Effects 0.000 description 3
- 230000007885 bronchoconstriction Effects 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 239000000480 calcium channel blocker Substances 0.000 description 3
- 125000002837 carbocyclic group Chemical group 0.000 description 3
- 239000001768 carboxy methyl cellulose Substances 0.000 description 3
- 229960000590 celecoxib Drugs 0.000 description 3
- 210000000038 chest Anatomy 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- 208000037976 chronic inflammation Diseases 0.000 description 3
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 3
- 229960004106 citric acid Drugs 0.000 description 3
- 208000010877 cognitive disease Diseases 0.000 description 3
- 208000010247 contact dermatitis Diseases 0.000 description 3
- 229960004397 cyclophosphamide Drugs 0.000 description 3
- CYQFCXCEBYINGO-IAGOWNOFSA-N delta1-THC Chemical compound C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 CYQFCXCEBYINGO-IAGOWNOFSA-N 0.000 description 3
- 206010012601 diabetes mellitus Diseases 0.000 description 3
- 239000002270 dispersing agent Substances 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 229960004242 dronabinol Drugs 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 230000008406 drug-drug interaction Effects 0.000 description 3
- 230000002708 enhancing effect Effects 0.000 description 3
- 201000001564 eosinophilic gastroenteritis Diseases 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 230000004761 fibrosis Effects 0.000 description 3
- 230000037433 frameshift Effects 0.000 description 3
- 231100000869 headache Toxicity 0.000 description 3
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 3
- 230000000642 iatrogenic effect Effects 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 125000002632 imidazolidinyl group Chemical group 0.000 description 3
- 230000028709 inflammatory response Effects 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 230000002452 interceptive effect Effects 0.000 description 3
- 208000028867 ischemia Diseases 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 210000004698 lymphocyte Anatomy 0.000 description 3
- 238000002844 melting Methods 0.000 description 3
- 230000008018 melting Effects 0.000 description 3
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 210000003097 mucus Anatomy 0.000 description 3
- 230000007694 nephrotoxicity Effects 0.000 description 3
- 231100000417 nephrotoxicity Toxicity 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 239000012038 nucleophile Substances 0.000 description 3
- 230000009437 off-target effect Effects 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 239000003791 organic solvent mixture Substances 0.000 description 3
- 201000008482 osteoarthritis Diseases 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 3
- 201000005675 papillary conjunctivitis Diseases 0.000 description 3
- 229940043138 pentosan polysulfate Drugs 0.000 description 3
- 230000002974 pharmacogenomic effect Effects 0.000 description 3
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 231100000683 possible toxicity Toxicity 0.000 description 3
- 230000002980 postoperative effect Effects 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 229960004618 prednisone Drugs 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 230000001737 promoting effect Effects 0.000 description 3
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical class O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 208000032253 retinal ischemia Diseases 0.000 description 3
- 229960000371 rofecoxib Drugs 0.000 description 3
- 201000004700 rosacea Diseases 0.000 description 3
- 230000036303 septic shock Effects 0.000 description 3
- 229960002855 simvastatin Drugs 0.000 description 3
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 210000000278 spinal cord Anatomy 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 230000001988 toxicity Effects 0.000 description 3
- 231100000419 toxicity Toxicity 0.000 description 3
- 230000037317 transdermal delivery Effects 0.000 description 3
- 230000008733 trauma Effects 0.000 description 3
- 206010055031 vascular neoplasm Diseases 0.000 description 3
- 230000008728 vascular permeability Effects 0.000 description 3
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 2
- ZGGHKIMDNBDHJB-NRFPMOEYSA-M (3R,5S)-fluvastatin sodium Chemical compound [Na+].C12=CC=CC=C2N(C(C)C)C(\C=C\[C@@H](O)C[C@@H](O)CC([O-])=O)=C1C1=CC=C(F)C=C1 ZGGHKIMDNBDHJB-NRFPMOEYSA-M 0.000 description 2
- FELGMEQIXOGIFQ-CYBMUJFWSA-N (3r)-9-methyl-3-[(2-methylimidazol-1-yl)methyl]-2,3-dihydro-1h-carbazol-4-one Chemical compound CC1=NC=CN1C[C@@H]1C(=O)C(C=2C(=CC=CC=2)N2C)=C2CC1 FELGMEQIXOGIFQ-CYBMUJFWSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 2
- OGYGFUAIIOPWQD-UHFFFAOYSA-N 1,3-thiazolidine Chemical compound C1CSCN1 OGYGFUAIIOPWQD-UHFFFAOYSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- HJTAZXHBEBIQQX-UHFFFAOYSA-N 1,5-bis(chloromethyl)naphthalene Chemical compound C1=CC=C2C(CCl)=CC=CC2=C1CCl HJTAZXHBEBIQQX-UHFFFAOYSA-N 0.000 description 2
- 102100025573 1-alkyl-2-acetylglycerophosphocholine esterase Human genes 0.000 description 2
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 2
- DDAQTTBNRIQGGS-UHFFFAOYSA-N 2,2-dimethyl-3-[5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]propanoic acid Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3SC=CN=3)C(CC(C)(C)C(O)=O)=CC2=CC=1OCC1=CC=CC=N1 DDAQTTBNRIQGGS-UHFFFAOYSA-N 0.000 description 2
- NDWLLRIDKMHYRQ-UHFFFAOYSA-N 2,2-dimethyl-3-[5-[(2-methyl-1,3-thiazol-4-yl)methoxy]-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]propanoic acid Chemical compound S1C(C)=NC(COC=2C=C3C=C(CC(C)(C)C(O)=O)N(CC=4C=CC(=CC=4)C=4SC=CN=4)C3=CC=2)=C1 NDWLLRIDKMHYRQ-UHFFFAOYSA-N 0.000 description 2
- HGUFODBRKLSHSI-UHFFFAOYSA-N 2,3,7,8-tetrachloro-dibenzo-p-dioxin Chemical compound O1C2=CC(Cl)=C(Cl)C=C2OC2=C1C=C(Cl)C(Cl)=C2 HGUFODBRKLSHSI-UHFFFAOYSA-N 0.000 description 2
- ZABMHLDQFJHDSC-UHFFFAOYSA-N 2,3-dihydro-1,3-oxazole Chemical compound C1NC=CO1 ZABMHLDQFJHDSC-UHFFFAOYSA-N 0.000 description 2
- LWTIGYSPAXKMDG-UHFFFAOYSA-N 2,3-dihydro-1h-imidazole Chemical compound C1NC=CN1 LWTIGYSPAXKMDG-UHFFFAOYSA-N 0.000 description 2
- JECYNCQXXKQDJN-UHFFFAOYSA-N 2-(2-methylhexan-2-yloxymethyl)oxirane Chemical compound CCCCC(C)(C)OCC1CO1 JECYNCQXXKQDJN-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- VOXBZHOHGGBLCQ-UHFFFAOYSA-N 2-amino-3,7-dihydropurine-6-thione;hydrate Chemical class O.N1C(N)=NC(=S)C2=C1N=CN2.N1C(N)=NC(=S)C2=C1N=CN2 VOXBZHOHGGBLCQ-UHFFFAOYSA-N 0.000 description 2
- VSWICNJIUPRZIK-UHFFFAOYSA-N 2-piperideine Chemical compound C1CNC=CC1 VSWICNJIUPRZIK-UHFFFAOYSA-N 0.000 description 2
- RSEBUVRVKCANEP-UHFFFAOYSA-N 2-pyrroline Chemical compound C1CC=CN1 RSEBUVRVKCANEP-UHFFFAOYSA-N 0.000 description 2
- AGIJRRREJXSQJR-UHFFFAOYSA-N 2h-thiazine Chemical compound N1SC=CC=C1 AGIJRRREJXSQJR-UHFFFAOYSA-N 0.000 description 2
- XAUGTJPEBBCVJL-UHFFFAOYSA-N 3-[1-[[4-(5-aminopyrazin-2-yl)phenyl]methyl]-3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CN=C(N)C=N1 XAUGTJPEBBCVJL-UHFFFAOYSA-N 0.000 description 2
- XMAMQVDWPZFPLH-UHFFFAOYSA-N 3-[1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C=C1CC(C)(C)C(O)=O XMAMQVDWPZFPLH-UHFFFAOYSA-N 0.000 description 2
- WZJJTLXVHVPHKD-UHFFFAOYSA-N 3-[1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]-5-[(2-methyl-1,3-thiazol-4-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C(C)SC=3)C=C2C=C1CC(C)(C)C(O)=O WZJJTLXVHVPHKD-UHFFFAOYSA-N 0.000 description 2
- GIEUQZQVPKLKIC-UHFFFAOYSA-N 3-[1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-3-(2-methylpropyl)-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(CC(C)C)=C1CC(C)(C)C(O)=O GIEUQZQVPKLKIC-UHFFFAOYSA-N 0.000 description 2
- ZBKCEARSPLLLMD-UHFFFAOYSA-N 3-[3-(3,3-dimethylbutanoyl)-5-[(2-methyl-1,3-thiazol-4-yl)methoxy]-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(C)=NC(COC=2C=C3C(C(=O)CC(C)(C)C)=C(CC(C)(C)C(O)=O)N(CC=4C=CC(=CC=4)C=4SC=CN=4)C3=CC=2)=C1 ZBKCEARSPLLLMD-UHFFFAOYSA-N 0.000 description 2
- NAIONLJZLUSLDQ-UHFFFAOYSA-N 3-[3-(3,3-dimethylbutyl)-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(CCC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CS1 NAIONLJZLUSLDQ-UHFFFAOYSA-N 0.000 description 2
- FZRLGBRQWAMIGJ-UHFFFAOYSA-N 3-[3-(cyclobutylmethyl)-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC(C)=CC=3)C=C2C(CC2CCC2)=C1CC(C)(C)C(O)=O FZRLGBRQWAMIGJ-UHFFFAOYSA-N 0.000 description 2
- PMZKPUUOQIMMIO-UHFFFAOYSA-N 3-[3-(cyclobutylmethyl)-5-[(5-methylpyridin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2CC3CCC3)C2=C1 PMZKPUUOQIMMIO-UHFFFAOYSA-N 0.000 description 2
- HEZRQLOAHFADHG-UHFFFAOYSA-N 3-[3-acetyl-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(C(=O)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CS1 HEZRQLOAHFADHG-UHFFFAOYSA-N 0.000 description 2
- HURJSQOEOFOZQX-UHFFFAOYSA-N 3-[3-ethyl-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(CC)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CS1 HURJSQOEOFOZQX-UHFFFAOYSA-N 0.000 description 2
- NSQKHWNLVFRDMX-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[(4-pyridin-2-ylphenyl)methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=CC=N1 NSQKHWNLVFRDMX-UHFFFAOYSA-N 0.000 description 2
- RVVDMDKOMQAFFU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[(4-pyridin-3-ylphenyl)methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=CN=C1 RVVDMDKOMQAFFU-UHFFFAOYSA-N 0.000 description 2
- DIXCNSKJPHNYGR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[3-(4-methoxyoxan-4-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C=1C=CC(CN2C3=CC=C(OCC=4N=CC=CC=4)C=C3C(SC(C)(C)C)=C2CC(C)(C)C(O)=O)=CC=1C1(OC)CCOCC1 DIXCNSKJPHNYGR-UHFFFAOYSA-N 0.000 description 2
- KGMBHQHCFFDTJI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[3-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C1=CC=CC(CN2C3=CC=C(OCC=4N=CC=CC=4)C=C3C(SC(C)(C)C)=C2CC(C)(C)C(O)=O)=C1 KGMBHQHCFFDTJI-UHFFFAOYSA-N 0.000 description 2
- QEQVTLKTHATXEI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2,4-dimethyl-1,3-thiazol-5-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(C)=NC(C)=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O QEQVTLKTHATXEI-UHFFFAOYSA-N 0.000 description 2
- OLYQPJKKMMJCQZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-ethoxy-1,3-thiazol-4-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(OCC)=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 OLYQPJKKMMJCQZ-UHFFFAOYSA-N 0.000 description 2
- HLYKLGSFPZUSEQ-QHCPKHFHSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-ethoxy-1,3-thiazol-4-yl)phenyl]methyl]-5-[(1s)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(OCC)=NC(C=2C=CC(CN3C4=CC=C(O[C@@H](C)C=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 HLYKLGSFPZUSEQ-QHCPKHFHSA-N 0.000 description 2
- BFLOZKQSKFBIBG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-ethoxy-1,3-thiazol-4-yl)phenyl]methyl]-5-[(6-fluoroquinolin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(OCC)=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=C6C=CC(F)=CC6=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 BFLOZKQSKFBIBG-UHFFFAOYSA-N 0.000 description 2
- QHUZWPOFUKDTDC-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-methoxy-1,3-thiazol-4-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(OC)=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 QHUZWPOFUKDTDC-UHFFFAOYSA-N 0.000 description 2
- DTYPVUPXBYWEHM-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-methoxypyridin-3-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=NC=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DTYPVUPXBYWEHM-UHFFFAOYSA-N 0.000 description 2
- GNWZVDVADCUMKQ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-methoxypyridin-3-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=NC=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC(C)=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O GNWZVDVADCUMKQ-UHFFFAOYSA-N 0.000 description 2
- FAOCBEKUWYMXDP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(2-methoxypyrimidin-5-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=NC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O FAOCBEKUWYMXDP-UHFFFAOYSA-N 0.000 description 2
- DDHDOJLPFNPXDP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(4-methoxypyridin-2-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC(C)=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 DDHDOJLPFNPXDP-UHFFFAOYSA-N 0.000 description 2
- XHIQYLMECBBILN-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(4-methyl-1,3-thiazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CSC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 XHIQYLMECBBILN-UHFFFAOYSA-N 0.000 description 2
- NBEVWAJVRMIARR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoro-1,3-thiazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=C(F)S1 NBEVWAJVRMIARR-UHFFFAOYSA-N 0.000 description 2
- VUQHTDBGVQUJPQ-HSZRJFAPSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-2-yl)phenyl]methyl]-5-[(1r)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound O([C@H](C)C=1N=CC=CC=1)C(C=C1C(SC(C)(C)C)=C2CC(C)(C)C(O)=O)=CC=C1N2CC(C=C1)=CC=C1C1=CC=C(F)C=N1 VUQHTDBGVQUJPQ-HSZRJFAPSA-N 0.000 description 2
- RXIYTLYKWJVLSP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-2-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(F)=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 RXIYTLYKWJVLSP-UHFFFAOYSA-N 0.000 description 2
- XOGLXAWLCMCZPN-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-2-yl)phenyl]methyl]-5-[(6-fluoroquinolin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC(F)=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(F)C=N1 XOGLXAWLCMCZPN-UHFFFAOYSA-N 0.000 description 2
- DAJDTSXLOXVMIE-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-3-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CN=CC(F)=C1 DAJDTSXLOXVMIE-UHFFFAOYSA-N 0.000 description 2
- GKVLLUZKLDCBMI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-3-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C=C(F)C=NC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 GKVLLUZKLDCBMI-UHFFFAOYSA-N 0.000 description 2
- SCACKEQKPSOXPR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methoxy-1,3-thiazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(OC)=CN=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SCACKEQKPSOXPR-UHFFFAOYSA-N 0.000 description 2
- OVUZIHBRMGWZRW-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methoxypyridin-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O OVUZIHBRMGWZRW-UHFFFAOYSA-N 0.000 description 2
- JQSLFZOCHNOAGP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CN=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 JQSLFZOCHNOAGP-UHFFFAOYSA-N 0.000 description 2
- OUXUSVMGRBPPDJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methyl-1,3-thiazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(C)=CN=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O OUXUSVMGRBPPDJ-UHFFFAOYSA-N 0.000 description 2
- IOLHJZSGYWTNBR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methyl-1h-imidazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CNC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 IOLHJZSGYWTNBR-UHFFFAOYSA-N 0.000 description 2
- HSSVHWASBRHWGP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-cyanopyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C#N)N=C1 HSSVHWASBRHWGP-UHFFFAOYSA-N 0.000 description 2
- SBSYRHFGLSSUEP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridazin-3-yl)phenyl]methyl]-5-[(6-fluoroquinolin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC(F)=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SBSYRHFGLSSUEP-UHFFFAOYSA-N 0.000 description 2
- YVXFRURGRRBTTR-RUZDIDTESA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-2-yl)phenyl]methyl]-5-[(1r)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CCOC1=CC=CC(C=2C=CC(CN3C4=CC=C(O[C@H](C)C=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 YVXFRURGRRBTTR-RUZDIDTESA-N 0.000 description 2
- WOOSKEULIBABRR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-2-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CCOC1=CC=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC(C)=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 WOOSKEULIBABRR-UHFFFAOYSA-N 0.000 description 2
- KWYJEVMQYUZNBZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-2-yl)phenyl]methyl]-5-[(6-fluoroquinolin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CCOC1=CC=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=C6C=CC(F)=CC6=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 KWYJEVMQYUZNBZ-UHFFFAOYSA-N 0.000 description 2
- SCBTXSXSBUOMQA-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SCBTXSXSBUOMQA-UHFFFAOYSA-N 0.000 description 2
- SZWXLMAHVSNUHT-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SZWXLMAHVSNUHT-UHFFFAOYSA-N 0.000 description 2
- MFUNSOHSQHTOJF-RUZDIDTESA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(1r)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(O[C@H](C)C=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O MFUNSOHSQHTOJF-RUZDIDTESA-N 0.000 description 2
- CBLZAAPRXUGQPC-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(3-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3C(=CC=CN=3)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O CBLZAAPRXUGQPC-UHFFFAOYSA-N 0.000 description 2
- PCYFQFGACFIYKP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(5-ethylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC(CC)=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O PCYFQFGACFIYKP-UHFFFAOYSA-N 0.000 description 2
- AQBFUTJZRSPNCP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(5-methyl-1,2-oxazol-3-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC3=NOC(C)=C3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O AQBFUTJZRSPNCP-UHFFFAOYSA-N 0.000 description 2
- NKVCOXLBLBKEDS-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]-5-[(7-fluoroquinolin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=C(F)C=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O NKVCOXLBLBKEDS-UHFFFAOYSA-N 0.000 description 2
- BINQBOKNVFCCIG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 BINQBOKNVFCCIG-UHFFFAOYSA-N 0.000 description 2
- ZMJTXHLYRCCVEO-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-2-yl)phenyl]methyl]-5-[(5-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=CC(C)=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 ZMJTXHLYRCCVEO-UHFFFAOYSA-N 0.000 description 2
- DGCSBHYGDCRAOB-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DGCSBHYGDCRAOB-UHFFFAOYSA-N 0.000 description 2
- CFYSRLSRJHAWDX-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O CFYSRLSRJHAWDX-UHFFFAOYSA-N 0.000 description 2
- IESSVOFSRKTJJC-XMMPIXPASA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-[(1r)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(O[C@H](C)C=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O IESSVOFSRKTJJC-XMMPIXPASA-N 0.000 description 2
- COAQRGYDJFLOJB-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-[(3-methylpyridin-2-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3C(=CC=CN=3)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O COAQRGYDJFLOJB-UHFFFAOYSA-N 0.000 description 2
- KCQKANLXECDDTE-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-[(5-methyl-1,2-oxazol-3-yl)methoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC3=NOC(C)=C3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O KCQKANLXECDDTE-UHFFFAOYSA-N 0.000 description 2
- OTHIKAKKQMCVQF-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-propan-2-ylindol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(C(C)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O OTHIKAKKQMCVQF-UHFFFAOYSA-N 0.000 description 2
- SCLIQFQTAGFOLX-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methylpyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(C)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SCLIQFQTAGFOLX-UHFFFAOYSA-N 0.000 description 2
- LGUNQAAOEKDWLU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methylpyridazin-3-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(C)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O LGUNQAAOEKDWLU-UHFFFAOYSA-N 0.000 description 2
- PLHNFKKCQTYEQM-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methylpyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(C)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O PLHNFKKCQTYEQM-UHFFFAOYSA-N 0.000 description 2
- XXJOXCUONDZYRT-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-oxo-1h-pyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(O)N=N1 XXJOXCUONDZYRT-UHFFFAOYSA-N 0.000 description 2
- ZLRVCNRIPPMSGK-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-oxo-1h-pyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(O)N=C1 ZLRVCNRIPPMSGK-UHFFFAOYSA-N 0.000 description 2
- DVYOLEUFNIOPMJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[6-(4-methoxyphenyl)pyridin-3-yl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=CC(OC)=CC=C1C(N=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DVYOLEUFNIOPMJ-UHFFFAOYSA-N 0.000 description 2
- HHGIGPRKFSSYJH-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[6-(6-methoxypyridin-3-yl)pyridin-3-yl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(N=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O HHGIGPRKFSSYJH-UHFFFAOYSA-N 0.000 description 2
- HKMFVKRDAUAEAG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[(4-pyrimidin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CC=N1 HKMFVKRDAUAEAG-UHFFFAOYSA-N 0.000 description 2
- VVQHJQAFIKPKKZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[(4-pyrimidin-5-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CN=CN=C1 VVQHJQAFIKPKKZ-UHFFFAOYSA-N 0.000 description 2
- HJNPWYSJDKOZNC-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3,4-thiadiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NN=CS1 HJNPWYSJDKOZNC-UHFFFAOYSA-N 0.000 description 2
- GRQYMCJQVKMJAT-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CS1 GRQYMCJQVKMJAT-UHFFFAOYSA-N 0.000 description 2
- ZBNZUKZQBCEEOL-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)C=N1 ZBNZUKZQBCEEOL-UHFFFAOYSA-N 0.000 description 2
- DQOMTYJZTAXWHZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-[6-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=CC(C(F)(F)F)=N1 DQOMTYJZTAXWHZ-UHFFFAOYSA-N 0.000 description 2
- HETKNCQUFOVNFM-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-[6-(trifluoromethyl)pyridin-3-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)N=C1 HETKNCQUFOVNFM-UHFFFAOYSA-N 0.000 description 2
- DCKBRHLXZORIDG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[6-[4-(trifluoromethoxy)phenyl]pyridin-3-yl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=N1)=CC=C1C1=CC=C(OC(F)(F)F)C=C1 DCKBRHLXZORIDG-UHFFFAOYSA-N 0.000 description 2
- FDGOEAVGGZCTTK-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(quinolin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=NC=CS1 FDGOEAVGGZCTTK-UHFFFAOYSA-N 0.000 description 2
- BEVUNQGQFSTOEI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(quinolin-2-ylmethoxy)-1-[[4-[4-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC(C(F)(F)F)=CC=N1 BEVUNQGQFSTOEI-UHFFFAOYSA-N 0.000 description 2
- HONAJTCIOQGCJI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(quinolin-2-ylmethoxy)-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)C=N1 HONAJTCIOQGCJI-UHFFFAOYSA-N 0.000 description 2
- JXESCLFWHHZPSM-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(1,5-dimethylpyrazol-3-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC3=NN(C)C(C)=C3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O JXESCLFWHHZPSM-UHFFFAOYSA-N 0.000 description 2
- SHRAXZCSUMGPKU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(2,5-dimethylpyrazol-3-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N(N=C(C)C=3)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SHRAXZCSUMGPKU-UHFFFAOYSA-N 0.000 description 2
- YAOLVIQUVOFNJI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(2-methyl-1,3-thiazol-4-yl)methoxy]-1-[(4-pyrimidin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(C)=NC(COC=2C=C3C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N(CC=4C=CC(=CC=4)C=4N=CC=CN=4)C3=CC=2)=C1 YAOLVIQUVOFNJI-UHFFFAOYSA-N 0.000 description 2
- HEBUXUAXAZLCFY-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(2-methyl-1,3-thiazol-4-yl)methoxy]-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound S1C(C)=NC(COC=2C=C3C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N(CC=4C=CC(=CC=4)C=4SC=CN=4)C3=CC=2)=C1 HEBUXUAXAZLCFY-UHFFFAOYSA-N 0.000 description 2
- DQIRUBZXMHKNDZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(3,5-dimethylpyridin-2-yl)methoxy]-1-[[4-(6-ethoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OCC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3C(=CC(C)=CN=3)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DQIRUBZXMHKNDZ-UHFFFAOYSA-N 0.000 description 2
- RNIPYBIIQLYPFJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(3,5-dimethylpyridin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CC(C)=CN=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 RNIPYBIIQLYPFJ-UHFFFAOYSA-N 0.000 description 2
- ARQQEELCRJGVFY-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(3-methylpyridin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CC=CN=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 ARQQEELCRJGVFY-UHFFFAOYSA-N 0.000 description 2
- CNEDPZMMBRZFLR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(3-methylpyridin-2-yl)methoxy]-1-[[4-[6-(trifluoromethyl)pyridin-3-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CC=CN=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C=NC(=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 CNEDPZMMBRZFLR-UHFFFAOYSA-N 0.000 description 2
- QPRWHJWQYGQZIS-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(4-methylpyridin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound CC1=CC=NC(COC=2C=C3C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N(CC=4C=CC(=CC=4)C=4N=CC(=CC=4)C(F)(F)F)C3=CC=2)=C1 QPRWHJWQYGQZIS-UHFFFAOYSA-N 0.000 description 2
- QYWXUUUTBHRRKR-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5,6-dimethylpyridin-2-yl)methoxy]-1-[(4-pyridin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=C(C)C(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 QYWXUUUTBHRRKR-UHFFFAOYSA-N 0.000 description 2
- ZKTNNVKHLSCZOP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5,6-dimethylpyridin-2-yl)methoxy]-1-[[4-(3-fluoropyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=C(C)C(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C(=CC=CN=2)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 ZKTNNVKHLSCZOP-UHFFFAOYSA-N 0.000 description 2
- FYZGJYZHBJJDDT-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5,6-dimethylpyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C(C)C(C)=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O FYZGJYZHBJJDDT-UHFFFAOYSA-N 0.000 description 2
- QAACIEQXMVDJBG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5,6-dimethylpyridin-2-yl)methoxy]-1-[[4-[4-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=C(C)C(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC=C(C=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 QAACIEQXMVDJBG-UHFFFAOYSA-N 0.000 description 2
- FCYIYWYGFCOWLB-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[(4-pyridin-3-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C=NC=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 FCYIYWYGFCOWLB-UHFFFAOYSA-N 0.000 description 2
- VSNYDFRPXRRAJK-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(3-fluoropyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C(=CC=CN=2)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 VSNYDFRPXRRAJK-UHFFFAOYSA-N 0.000 description 2
- SVJHWAVUWUKDTG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(3-methoxypyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C(=CC=CN=2)OC)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 SVJHWAVUWUKDTG-UHFFFAOYSA-N 0.000 description 2
- XJFCUVLIRGQZLG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(4-methoxypyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC=C(OC)C=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 XJFCUVLIRGQZLG-UHFFFAOYSA-N 0.000 description 2
- DMKYXZWFXUTMIS-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=NC(OC)=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 DMKYXZWFXUTMIS-UHFFFAOYSA-N 0.000 description 2
- VLYGYKJKEWIQAN-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C=NC(OC)=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 VLYGYKJKEWIQAN-UHFFFAOYSA-N 0.000 description 2
- NOUDUNZGBPIGQQ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-methylpyridin-2-yl)methoxy]-1-[(4-pyridin-3-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C=NC=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 NOUDUNZGBPIGQQ-UHFFFAOYSA-N 0.000 description 2
- IRQIBOAVBGKTBW-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-methylpyridin-2-yl)methoxy]-1-[[4-(5-methylpyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(C)=CC=2)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 IRQIBOAVBGKTBW-UHFFFAOYSA-N 0.000 description 2
- DVNZJSKVLGJKSU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-methylpyridin-2-yl)methoxy]-1-[[4-[3-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C(=CC=CN=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 DVNZJSKVLGJKSU-UHFFFAOYSA-N 0.000 description 2
- NRQRGTDPLVJDKA-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-methylpyridin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2N=CC(=CC=2)C(F)(F)F)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 NRQRGTDPLVJDKA-UHFFFAOYSA-N 0.000 description 2
- ZYPXXZYVAQILDK-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-cyclopropylpyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C(C=CC=3)C3CC3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O ZYPXXZYVAQILDK-UHFFFAOYSA-N 0.000 description 2
- SETQMRSHZVXSSQ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoropyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C(F)C=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O SETQMRSHZVXSSQ-UHFFFAOYSA-N 0.000 description 2
- XZTXFIQYANLFCL-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoroquinolin-2-yl)methoxy]-1-[(4-pyridin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC(F)=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=CC=N1 XZTXFIQYANLFCL-UHFFFAOYSA-N 0.000 description 2
- CMXFNSXOVXOALU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoroquinolin-2-yl)methoxy]-1-[[4-(4-methoxypyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=C6C=CC(F)=CC6=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 CMXFNSXOVXOALU-UHFFFAOYSA-N 0.000 description 2
- OTGBPCPAOGOTMH-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoroquinolin-2-yl)methoxy]-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC(F)=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O OTGBPCPAOGOTMH-UHFFFAOYSA-N 0.000 description 2
- IUGZYOQUQGGJRV-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoroquinolin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=CC(C=2C=CC(CN3C4=CC=C(OCC=5N=C6C=CC(F)=CC6=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 IUGZYOQUQGGJRV-UHFFFAOYSA-N 0.000 description 2
- LEMCEGNLFMJGSK-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-fluoroquinolin-2-yl)methoxy]-1-[[4-(6-methylpyridazin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(C)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=CC(F)=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O LEMCEGNLFMJGSK-UHFFFAOYSA-N 0.000 description 2
- CXRLZVLRLCHPLL-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-methoxypyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C(OC)C=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O CXRLZVLRLCHPLL-UHFFFAOYSA-N 0.000 description 2
- FRUPVACQKFJPHA-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(6-methylquinolin-2-yl)methoxy]-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=CC2=CC(C)=CC=C2N=C1COC(C=C1C(SC(C)(C)C)=C2CC(C)(C)C(O)=O)=CC=C1N2CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)C=N1 FRUPVACQKFJPHA-UHFFFAOYSA-N 0.000 description 2
- NYMDWHNSBRZCCH-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(7-fluoroquinolin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=C4C=C(F)C=CC4=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O NYMDWHNSBRZCCH-UHFFFAOYSA-N 0.000 description 2
- IKTKMBJJSLOEEG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(7-fluoroquinolin-2-yl)methoxy]-1-[[4-[6-(trifluoromethyl)pyridin-3-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=C(F)C=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)N=C1 IKTKMBJJSLOEEG-UHFFFAOYSA-N 0.000 description 2
- SWWQOAMPMCAOIU-UHFFFAOYSA-N 3-[3-tert-butylsulfonyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(S(=O)(=O)C(C)(C)C)=C1CC(C)(C)C(O)=O SWWQOAMPMCAOIU-UHFFFAOYSA-N 0.000 description 2
- GLSWASHMXFKLMS-UHFFFAOYSA-N 3-[5-(1,3-benzothiazol-2-ylmethoxy)-3-(cyclobutanecarbonyl)-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3SC4=CC=CC=C4N=3)C=C2C(C(=O)C2CCC2)=C1CC(C)(C)C(O)=O GLSWASHMXFKLMS-UHFFFAOYSA-N 0.000 description 2
- DTQBFZXQYCMNDO-UHFFFAOYSA-N 3-[5-(1,3-benzothiazol-2-ylmethoxy)-3-(cyclobutylmethyl)-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3SC4=CC=CC=C4N=3)C=C2C(CC2CCC2)=C1CC(C)(C)C(O)=O DTQBFZXQYCMNDO-UHFFFAOYSA-N 0.000 description 2
- CXMZZZUGKJLFGL-UHFFFAOYSA-N 3-[5-(1,3-benzothiazol-2-ylmethoxy)-3-tert-butylsulfanyl-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3SC4=CC=CC=C4N=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O CXMZZZUGKJLFGL-UHFFFAOYSA-N 0.000 description 2
- DWXJRVNESNKSTB-UHFFFAOYSA-N 3-[5-(1,3-benzothiazol-2-ylmethoxy)-3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3SC4=CC=CC=C4N=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O DWXJRVNESNKSTB-UHFFFAOYSA-N 0.000 description 2
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 2
- XMIIGOLPHOKFCH-UHFFFAOYSA-N 3-phenylpropionic acid Chemical compound OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 2
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Chemical class N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 2
- CXLZKUZGWZDZPQ-UHFFFAOYSA-N 6-hydroxyhexyl 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoate Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(=O)OCCCCCCO CXLZKUZGWZDZPQ-UHFFFAOYSA-N 0.000 description 2
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 2
- RSWGJHLUYNHPMX-UHFFFAOYSA-N Abietic-Saeure Natural products C12CCC(C(C)C)=CC2=CCC2C1(C)CCCC2(C)C(O)=O RSWGJHLUYNHPMX-UHFFFAOYSA-N 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 208000009304 Acute Kidney Injury Diseases 0.000 description 2
- 229930024421 Adenine Natural products 0.000 description 2
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 2
- 108010024976 Asparaginase Proteins 0.000 description 2
- 206010003645 Atopy Diseases 0.000 description 2
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 2
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 2
- PKJINWOACFYDQN-RBVMPENBSA-N BAYu9773 Chemical compound CCCCC\C=C/C\C=C/C=C/C=C/[C@H]([C@@H](O)CCCC(O)=O)SC1=CC=C(C(O)=O)C=C1 PKJINWOACFYDQN-RBVMPENBSA-N 0.000 description 2
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 2
- 239000002083 C09CA01 - Losartan Substances 0.000 description 2
- 108700012434 CCL3 Proteins 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 229940122156 Cathepsin K inhibitor Drugs 0.000 description 2
- 108010067225 Cell Adhesion Molecules Proteins 0.000 description 2
- 102000016289 Cell Adhesion Molecules Human genes 0.000 description 2
- 102000000013 Chemokine CCL3 Human genes 0.000 description 2
- 108010061846 Cholesterol Ester Transfer Proteins Proteins 0.000 description 2
- 102000012336 Cholesterol Ester Transfer Proteins Human genes 0.000 description 2
- 208000017667 Chronic Disease Diseases 0.000 description 2
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 206010010741 Conjunctivitis Diseases 0.000 description 2
- 108010037464 Cyclooxygenase 1 Proteins 0.000 description 2
- 108010037462 Cyclooxygenase 2 Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- 108010061435 Enalapril Proteins 0.000 description 2
- 241000792859 Enema Species 0.000 description 2
- 241001125671 Eretmochelys imbricata Species 0.000 description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 2
- 108010029961 Filgrastim Proteins 0.000 description 2
- 238000006641 Fischer synthesis reaction Methods 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 2
- 101000764535 Homo sapiens Lymphotoxin-alpha Proteins 0.000 description 2
- 206010020772 Hypertension Diseases 0.000 description 2
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 description 2
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 108010050904 Interferons Proteins 0.000 description 2
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 2
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 2
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 2
- 239000002841 Lewis acid Substances 0.000 description 2
- 102000003820 Lipoxygenases Human genes 0.000 description 2
- 108090000128 Lipoxygenases Proteins 0.000 description 2
- 101001089108 Lotus tetragonolobus Anti-H(O) lectin Proteins 0.000 description 2
- 102100026238 Lymphotoxin-alpha Human genes 0.000 description 2
- PCZOHLXUXFIOCF-UHFFFAOYSA-N Monacolin X Natural products C12C(OC(=O)C(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 PCZOHLXUXFIOCF-UHFFFAOYSA-N 0.000 description 2
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- BLXXJMDCKKHMKV-UHFFFAOYSA-N Nabumetone Chemical compound C1=C(CCC(C)=O)C=CC2=CC(OC)=CC=C21 BLXXJMDCKKHMKV-UHFFFAOYSA-N 0.000 description 2
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 2
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 102000003982 Parathyroid hormone Human genes 0.000 description 2
- 108090000445 Parathyroid hormone Proteins 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- TUZYXOIXSAXUGO-UHFFFAOYSA-N Pravastatin Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(O)C=C21 TUZYXOIXSAXUGO-UHFFFAOYSA-N 0.000 description 2
- 206010037597 Pyelonephritis acute Diseases 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- 208000033626 Renal failure acute Diseases 0.000 description 2
- 208000002200 Respiratory Hypersensitivity Diseases 0.000 description 2
- 241000219061 Rheum Species 0.000 description 2
- 206010039094 Rhinitis perennial Diseases 0.000 description 2
- KHPCPRHQVVSZAH-HUOMCSJISA-N Rosin Natural products O(C/C=C/c1ccccc1)[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 KHPCPRHQVVSZAH-HUOMCSJISA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 102100021993 Sterol O-acyltransferase 1 Human genes 0.000 description 2
- 102100036673 Sterol O-acyltransferase 2 Human genes 0.000 description 2
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical compound O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 description 2
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 2
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical class O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 2
- 229940123464 Thiazolidinedione Drugs 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 208000025865 Ulcer Diseases 0.000 description 2
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 2
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 2
- 201000011040 acute kidney failure Diseases 0.000 description 2
- 201000001555 acute pyelonephritis Diseases 0.000 description 2
- 208000012998 acute renal failure Diseases 0.000 description 2
- 229960000643 adenine Drugs 0.000 description 2
- OIRDTQYFTABQOQ-KQYNXXCUSA-N adenosine Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 230000010085 airway hyperresponsiveness Effects 0.000 description 2
- 229960000548 alemtuzumab Drugs 0.000 description 2
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 2
- OFCNXPDARWKPPY-UHFFFAOYSA-N allopurinol Chemical compound OC1=NC=NC2=C1C=NN2 OFCNXPDARWKPPY-UHFFFAOYSA-N 0.000 description 2
- 229960003459 allopurinol Drugs 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 239000003263 anabolic agent Substances 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 230000002280 anti-androgenic effect Effects 0.000 description 2
- 229940046836 anti-estrogen Drugs 0.000 description 2
- 230000001833 anti-estrogenic effect Effects 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 239000000051 antiandrogen Substances 0.000 description 2
- 229940030495 antiandrogen sex hormone and modulator of the genital system Drugs 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 2
- GOLCXWYRSKYTSP-UHFFFAOYSA-N arsenic trioxide Inorganic materials O1[As]2O[As]1O2 GOLCXWYRSKYTSP-UHFFFAOYSA-N 0.000 description 2
- 229960002594 arsenic trioxide Drugs 0.000 description 2
- 229940072224 asacol Drugs 0.000 description 2
- 229960003272 asparaginase Drugs 0.000 description 2
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 2
- 229960005370 atorvastatin Drugs 0.000 description 2
- 125000002393 azetidinyl group Chemical group 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 239000002876 beta blocker Substances 0.000 description 2
- 229960000397 bevacizumab Drugs 0.000 description 2
- 150000004663 bisphosphonates Chemical class 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 2
- 239000004327 boric acid Substances 0.000 description 2
- 230000007883 bronchodilation Effects 0.000 description 2
- 229960002092 busulfan Drugs 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 159000000007 calcium salts Chemical class 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 230000000747 cardiac effect Effects 0.000 description 2
- 238000006555 catalytic reaction Methods 0.000 description 2
- 229940047495 celebrex Drugs 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 229960005395 cetuximab Drugs 0.000 description 2
- 125000003636 chemical group Chemical group 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 208000023652 chronic gastritis Diseases 0.000 description 2
- 230000006020 chronic inflammation Effects 0.000 description 2
- 208000020832 chronic kidney disease Diseases 0.000 description 2
- 208000022831 chronic renal failure syndrome Diseases 0.000 description 2
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 2
- 229960004316 cisplatin Drugs 0.000 description 2
- 229960002436 cladribine Drugs 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 229940110456 cocoa butter Drugs 0.000 description 2
- 235000019868 cocoa butter Nutrition 0.000 description 2
- 206010009887 colitis Diseases 0.000 description 2
- 229940125782 compound 2 Drugs 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- RMRCNWBMXRMIRW-BYFNXCQMSA-M cyanocobalamin Chemical compound N#C[Co+]N([C@]1([H])[C@H](CC(N)=O)[C@]\2(CCC(=O)NC[C@H](C)OP(O)(=O)OC3[C@H]([C@H](O[C@@H]3CO)N3C4=CC(C)=C(C)C=C4N=C3)O)C)C/2=C(C)\C([C@H](C/2(C)C)CCC(N)=O)=N\C\2=C\C([C@H]([C@@]/2(CC(N)=O)C)CCC(N)=O)=N\C\2=C(C)/C2=N[C@]1(C)[C@@](C)(CC(N)=O)[C@@H]2CCC(N)=O RMRCNWBMXRMIRW-BYFNXCQMSA-M 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 201000003146 cystitis Diseases 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 2
- 229960000975 daunorubicin Drugs 0.000 description 2
- 229940070230 daypro Drugs 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 229960002086 dextran Drugs 0.000 description 2
- 238000002405 diagnostic procedure Methods 0.000 description 2
- DCOPUUMXTXDBNB-UHFFFAOYSA-N diclofenac Chemical compound OC(=O)CC1=CC=CC=C1NC1=C(Cl)C=CC=C1Cl DCOPUUMXTXDBNB-UHFFFAOYSA-N 0.000 description 2
- 229960001259 diclofenac Drugs 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- 230000037213 diet Effects 0.000 description 2
- 125000004852 dihydrofuranyl group Chemical group O1C(CC=C1)* 0.000 description 2
- 125000005043 dihydropyranyl group Chemical group O1C(CCC=C1)* 0.000 description 2
- 229960001760 dimethyl sulfoxide Drugs 0.000 description 2
- OSVXSBDYLRYLIG-UHFFFAOYSA-N dioxidochlorine(.) Chemical compound O=Cl=O OSVXSBDYLRYLIG-UHFFFAOYSA-N 0.000 description 2
- 208000016097 disease of metabolism Diseases 0.000 description 2
- 208000037765 diseases and disorders Diseases 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 239000003534 dna topoisomerase inhibitor Substances 0.000 description 2
- 229960004679 doxorubicin Drugs 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 239000003596 drug target Substances 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- GBXSMTUPTTWBMN-XIRDDKMYSA-N enalapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(O)=O)CC1=CC=CC=C1 GBXSMTUPTTWBMN-XIRDDKMYSA-N 0.000 description 2
- 229960000873 enalapril Drugs 0.000 description 2
- 238000003821 enantio-separation Methods 0.000 description 2
- 210000002889 endothelial cell Anatomy 0.000 description 2
- 239000007920 enema Substances 0.000 description 2
- 229940079360 enema for constipation Drugs 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 239000002532 enzyme inhibitor Substances 0.000 description 2
- 229940125532 enzyme inhibitor Drugs 0.000 description 2
- 230000002327 eosinophilic effect Effects 0.000 description 2
- 230000003628 erosive effect Effects 0.000 description 2
- 239000000328 estrogen antagonist Substances 0.000 description 2
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 2
- 230000000763 evoking effect Effects 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 229960002297 fenofibrate Drugs 0.000 description 2
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 description 2
- 239000002319 fibrinogen receptor antagonist Substances 0.000 description 2
- 229960004177 filgrastim Drugs 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 229960000390 fludarabine Drugs 0.000 description 2
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- 229960003765 fluvastatin Drugs 0.000 description 2
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 125000004612 furopyridinyl group Chemical group O1C(=CC2=C1C=CC=N2)* 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 2
- 229960002584 gefitinib Drugs 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical class C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 description 2
- MFWNKCLOYSRHCJ-BTTYYORXSA-N granisetron Chemical compound C1=CC=C2C(C(=O)N[C@H]3C[C@H]4CCC[C@@H](C3)N4C)=NN(C)C2=C1 MFWNKCLOYSRHCJ-BTTYYORXSA-N 0.000 description 2
- 229960003727 granisetron Drugs 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 238000000227 grinding Methods 0.000 description 2
- 125000004438 haloalkoxy group Chemical group 0.000 description 2
- 125000001188 haloalkyl group Chemical group 0.000 description 2
- 201000011200 hepatorenal syndrome Diseases 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 238000007327 hydrogenolysis reaction Methods 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 2
- 206010020718 hyperplasia Diseases 0.000 description 2
- 230000009610 hypersensitivity Effects 0.000 description 2
- 229960000908 idarubicin Drugs 0.000 description 2
- KTUFNOKKBVMGRW-UHFFFAOYSA-N imatinib Chemical compound C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 KTUFNOKKBVMGRW-UHFFFAOYSA-N 0.000 description 2
- 229960002411 imatinib Drugs 0.000 description 2
- YAMHXTCMCPHKLN-UHFFFAOYSA-N imidazolidin-2-one Chemical compound O=C1NCCN1 YAMHXTCMCPHKLN-UHFFFAOYSA-N 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 229940089536 indocin Drugs 0.000 description 2
- 229960000905 indomethacin Drugs 0.000 description 2
- 210000004969 inflammatory cell Anatomy 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 230000008776 intercellular pathway Effects 0.000 description 2
- 229940047124 interferons Drugs 0.000 description 2
- 229940100601 interleukin-6 Drugs 0.000 description 2
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 description 2
- 229940096397 interleukin-8 Drugs 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 2
- 229960000991 ketoprofen Drugs 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 150000007517 lewis acids Chemical class 0.000 description 2
- 229960004773 losartan Drugs 0.000 description 2
- KJJZZJSZUJXYEA-UHFFFAOYSA-N losartan Chemical compound CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C=2[N]N=NN=2)C=C1 KJJZZJSZUJXYEA-UHFFFAOYSA-N 0.000 description 2
- 229960004844 lovastatin Drugs 0.000 description 2
- PCZOHLXUXFIOCF-BXMDZJJMSA-N lovastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 PCZOHLXUXFIOCF-BXMDZJJMSA-N 0.000 description 2
- QLJODMDSTUBWDW-UHFFFAOYSA-N lovastatin hydroxy acid Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(C)C=C21 QLJODMDSTUBWDW-UHFFFAOYSA-N 0.000 description 2
- 210000003563 lymphoid tissue Anatomy 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- HYYBABOKPJLUIN-UHFFFAOYSA-N mefenamic acid Chemical compound CC1=CC=CC(NC=2C(=CC=CC=2)C(O)=O)=C1C HYYBABOKPJLUIN-UHFFFAOYSA-N 0.000 description 2
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 2
- 229960001924 melphalan Drugs 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 208000030159 metabolic disease Diseases 0.000 description 2
- 230000037353 metabolic pathway Effects 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- 229960000485 methotrexate Drugs 0.000 description 2
- 239000000693 micelle Substances 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- TXXHDPDFNKHHGW-UHFFFAOYSA-N muconic acid Chemical compound OC(=O)C=CC=CC(O)=O TXXHDPDFNKHHGW-UHFFFAOYSA-N 0.000 description 2
- RTGDFNSFWBGLEC-SYZQJQIISA-N mycophenolate mofetil Chemical compound COC1=C(C)C=2COC(=O)C=2C(O)=C1C\C=C(/C)CCC(=O)OCCN1CCOCC1 RTGDFNSFWBGLEC-SYZQJQIISA-N 0.000 description 2
- 229960004866 mycophenolate mofetil Drugs 0.000 description 2
- 229960004270 nabumetone Drugs 0.000 description 2
- 229960002009 naproxen Drugs 0.000 description 2
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 2
- 229910017604 nitric acid Inorganic materials 0.000 description 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 2
- 239000002736 nonionic surfactant Substances 0.000 description 2
- 229960002748 norepinephrine Drugs 0.000 description 2
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 2
- 210000000633 nuclear envelope Anatomy 0.000 description 2
- 229960000470 omalizumab Drugs 0.000 description 2
- 229960005343 ondansetron Drugs 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 230000003204 osmotic effect Effects 0.000 description 2
- 238000012261 overproduction Methods 0.000 description 2
- OFPXSFXSNFPTHF-UHFFFAOYSA-N oxaprozin Chemical compound O1C(CCC(=O)O)=NC(C=2C=CC=CC=2)=C1C1=CC=CC=C1 OFPXSFXSNFPTHF-UHFFFAOYSA-N 0.000 description 2
- 229960002131 palonosetron Drugs 0.000 description 2
- CPZBLNMUGSZIPR-NVXWUHKLSA-N palonosetron Chemical compound C1N(CC2)CCC2[C@@H]1N1C(=O)C(C=CC=C2CCC3)=C2[C@H]3C1 CPZBLNMUGSZIPR-NVXWUHKLSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- 229960001319 parathyroid hormone Drugs 0.000 description 2
- 239000000199 parathyroid hormone Substances 0.000 description 2
- 239000003614 peroxisome proliferator Substances 0.000 description 2
- 239000000825 pharmaceutical preparation Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 description 2
- XUWHAWMETYGRKB-UHFFFAOYSA-N piperidin-2-one Chemical compound O=C1CCCCN1 XUWHAWMETYGRKB-UHFFFAOYSA-N 0.000 description 2
- 229960002702 piroxicam Drugs 0.000 description 2
- QYSPLQLAKJAUJT-UHFFFAOYSA-N piroxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 QYSPLQLAKJAUJT-UHFFFAOYSA-N 0.000 description 2
- RHGYHLPFVJEAOC-FFNUKLMVSA-L pitavastatin calcium Chemical compound [Ca+2].[O-]C(=O)C[C@H](O)C[C@H](O)\C=C\C1=C(C2CC2)N=C2C=CC=CC2=C1C1=CC=C(F)C=C1.[O-]C(=O)C[C@H](O)C[C@H](O)\C=C\C1=C(C2CC2)N=C2C=CC=CC2=C1C1=CC=C(F)C=C1 RHGYHLPFVJEAOC-FFNUKLMVSA-L 0.000 description 2
- 229940096701 plain lipid modifying drug hmg coa reductase inhibitors Drugs 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 2
- 229940068968 polysorbate 80 Drugs 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 229960002965 pravastatin Drugs 0.000 description 2
- TUZYXOIXSAXUGO-PZAWKZKUSA-N pravastatin Chemical compound C1=C[C@H](C)[C@H](CC[C@@H](O)C[C@@H](O)CC(O)=O)[C@H]2[C@@H](OC(=O)[C@@H](C)CC)C[C@H](O)C=C21 TUZYXOIXSAXUGO-PZAWKZKUSA-N 0.000 description 2
- 230000000770 proinflammatory effect Effects 0.000 description 2
- AQHHHDLHHXJYJD-UHFFFAOYSA-N propranolol Chemical compound C1=CC=C2C(OCC(O)CNC(C)C)=CC=CC2=C1 AQHHHDLHHXJYJD-UHFFFAOYSA-N 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000002599 prostaglandin synthase inhibitor Substances 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 201000001474 proteinuria Diseases 0.000 description 2
- 208000005069 pulmonary fibrosis Diseases 0.000 description 2
- USPWKWBDZOARPV-UHFFFAOYSA-N pyrazolidine Chemical compound C1CNNC1 USPWKWBDZOARPV-UHFFFAOYSA-N 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 230000010410 reperfusion Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 229940043266 rosin Drugs 0.000 description 2
- BPRHUIZQVSMCRT-VEUZHWNKSA-N rosuvastatin Chemical compound CC(C)C1=NC(N(C)S(C)(=O)=O)=NC(C=2C=CC(F)=CC=2)=C1\C=C\[C@@H](O)C[C@@H](O)CC(O)=O BPRHUIZQVSMCRT-VEUZHWNKSA-N 0.000 description 2
- 229960000672 rosuvastatin Drugs 0.000 description 2
- 229960004889 salicylic acid Drugs 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 230000037390 scarring Effects 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 2
- 229960002930 sirolimus Drugs 0.000 description 2
- 230000016160 smooth muscle contraction Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 235000010413 sodium alginate Nutrition 0.000 description 2
- 239000000661 sodium alginate Substances 0.000 description 2
- 229940005550 sodium alginate Drugs 0.000 description 2
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 2
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 229910000104 sodium hydride Inorganic materials 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 239000004059 squalene synthase inhibitor Substances 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 108010016093 sterol O-acyltransferase 1 Proteins 0.000 description 2
- 108010016092 sterol O-acyltransferase 2 Proteins 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 230000008961 swelling Effects 0.000 description 2
- 208000011580 syndromic disease Diseases 0.000 description 2
- 238000001308 synthesis method Methods 0.000 description 2
- 229960001967 tacrolimus Drugs 0.000 description 2
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- RMMXLENWKUUMAY-UHFFFAOYSA-N telmisartan Chemical compound CCCC1=NC2=C(C)C=C(C=3N(C4=CC=CC=C4N=3)C)C=C2N1CC(C=C1)=CC=C1C1=CC=CC=C1C(O)=O RMMXLENWKUUMAY-UHFFFAOYSA-N 0.000 description 2
- 229960004964 temozolomide Drugs 0.000 description 2
- XBXCNNQPRYLIDE-UHFFFAOYSA-N tert-butylcarbamic acid Chemical compound CC(C)(C)NC(O)=O XBXCNNQPRYLIDE-UHFFFAOYSA-N 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 238000011285 therapeutic regimen Methods 0.000 description 2
- 125000003396 thiol group Chemical class [H]S* 0.000 description 2
- 210000000115 thoracic cavity Anatomy 0.000 description 2
- 229940113082 thymine Drugs 0.000 description 2
- 229960003087 tioguanine Drugs 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 229940044693 topoisomerase inhibitor Drugs 0.000 description 2
- 239000003440 toxic substance Substances 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- KHPCPRHQVVSZAH-UHFFFAOYSA-N trans-cinnamyl beta-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OCC=CC1=CC=CC=C1 KHPCPRHQVVSZAH-UHFFFAOYSA-N 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- 230000000472 traumatic effect Effects 0.000 description 2
- 229960001727 tretinoin Drugs 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 2
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 2
- 229960002004 valdecoxib Drugs 0.000 description 2
- 201000011531 vascular cancer Diseases 0.000 description 2
- 210000003556 vascular endothelial cell Anatomy 0.000 description 2
- 230000024883 vasodilation Effects 0.000 description 2
- 235000019154 vitamin C Nutrition 0.000 description 2
- 239000011718 vitamin C Substances 0.000 description 2
- 229940011671 vitamin b6 Drugs 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- 230000029663 wound healing Effects 0.000 description 2
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- YCYMCMYLORLIJX-SNVBAGLBSA-N (2r)-2-propyloctanoic acid Chemical compound CCCCCC[C@H](C(O)=O)CCC YCYMCMYLORLIJX-SNVBAGLBSA-N 0.000 description 1
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 1
- METKIMKYRPQLGS-GFCCVEGCSA-N (R)-atenolol Chemical compound CC(C)NC[C@@H](O)COC1=CC=C(CC(N)=O)C=C1 METKIMKYRPQLGS-GFCCVEGCSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- TWBNMYSKRDRHAT-RCWTXCDDSA-N (S)-timolol hemihydrate Chemical compound O.CC(C)(C)NC[C@H](O)COC1=NSN=C1N1CCOCC1.CC(C)(C)NC[C@H](O)COC1=NSN=C1N1CCOCC1 TWBNMYSKRDRHAT-RCWTXCDDSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- DDMOUSALMHHKOS-UHFFFAOYSA-N 1,2-dichloro-1,1,2,2-tetrafluoroethane Chemical compound FC(F)(Cl)C(F)(F)Cl DDMOUSALMHHKOS-UHFFFAOYSA-N 0.000 description 1
- JPRPJUMQRZTTED-UHFFFAOYSA-N 1,3-dioxolanyl Chemical group [CH]1OCCO1 JPRPJUMQRZTTED-UHFFFAOYSA-N 0.000 description 1
- ZOBPZXTWZATXDG-UHFFFAOYSA-N 1,3-thiazolidine-2,4-dione Chemical compound O=C1CSC(=O)N1 ZOBPZXTWZATXDG-UHFFFAOYSA-N 0.000 description 1
- QEMSVZNTSXPFJA-HNAYVOBHSA-N 1-[(1s,2s)-1-hydroxy-1-(4-hydroxyphenyl)propan-2-yl]-4-phenylpiperidin-4-ol Chemical compound C1([C@H](O)[C@H](C)N2CCC(O)(CC2)C=2C=CC=CC=2)=CC=C(O)C=C1 QEMSVZNTSXPFJA-HNAYVOBHSA-N 0.000 description 1
- RXOGAWKVVDLQGZ-UHFFFAOYSA-N 1-[3-tert-butylsulfanyl-1-[[4-(1,3,4-oxadiazol-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2-methylpropan-2-ol Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3OC=NN=3)C(CC(C)(O)C)=C(SC(C)(C)C)C2=CC=1OCC1=CC=CC=N1 RXOGAWKVVDLQGZ-UHFFFAOYSA-N 0.000 description 1
- NZOYMVMWDFNFTH-UHFFFAOYSA-N 1-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[(4-pyridin-2-ylphenyl)methyl]indol-2-yl]-2-methylpropan-2-ol Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3N=CC=CC=3)C(CC(C)(O)C)=C(SC(C)(C)C)C2=CC=1OCC1=CC=CC=N1 NZOYMVMWDFNFTH-UHFFFAOYSA-N 0.000 description 1
- YSVGMFLFPFSFOJ-UHFFFAOYSA-N 1-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[4-(1,3-thiazol-2-yl)phenyl]methyl]indol-2-yl]-2-methylpropan-2-ol Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3SC=CN=3)C(CC(C)(O)C)=C(SC(C)(C)C)C2=CC=1OCC1=CC=CC=N1 YSVGMFLFPFSFOJ-UHFFFAOYSA-N 0.000 description 1
- MCTWTZJPVLRJOU-UHFFFAOYSA-N 1-methyl-1H-imidazole Chemical compound CN1C=CN=C1 MCTWTZJPVLRJOU-UHFFFAOYSA-N 0.000 description 1
- AMMPLVWPWSYRDR-UHFFFAOYSA-N 1-methylbicyclo[2.2.2]oct-2-ene-4-carboxylic acid Chemical compound C1CC2(C(O)=O)CCC1(C)C=C2 AMMPLVWPWSYRDR-UHFFFAOYSA-N 0.000 description 1
- 125000001462 1-pyrrolyl group Chemical group [*]N1C([H])=C([H])C([H])=C1[H] 0.000 description 1
- XDJWZONZDVNKDU-UHFFFAOYSA-N 1314-24-5 Chemical compound O=POP=O XDJWZONZDVNKDU-UHFFFAOYSA-N 0.000 description 1
- YTQQIHUQLOZOJI-UHFFFAOYSA-N 2,3-dihydro-1,2-thiazole Chemical compound C1NSC=C1 YTQQIHUQLOZOJI-UHFFFAOYSA-N 0.000 description 1
- ZIIUUSVHCHPIQD-UHFFFAOYSA-N 2,4,6-trimethyl-N-[3-(trifluoromethyl)phenyl]benzenesulfonamide Chemical compound CC1=CC(C)=CC(C)=C1S(=O)(=O)NC1=CC=CC(C(F)(F)F)=C1 ZIIUUSVHCHPIQD-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- UCHDWCPVSPXUMX-UHFFFAOYSA-N 2-[1-[[[1-[3-[2-(7-chloro-2-quinolinyl)ethenyl]phenyl]-3-[2-(2-hydroxypropan-2-yl)phenyl]propyl]thio]methyl]cyclopropyl]acetic acid Chemical compound CC(C)(O)C1=CC=CC=C1CCC(C=1C=C(C=CC=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- HNLXNOZHXNSSPN-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[4-(2,4,4-trimethylpentan-2-yl)phenoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CC(C)(C)CC(C)(C)C1=CC=C(OCCOCCOCCOCCOCCOCCOCCO)C=C1 HNLXNOZHXNSSPN-UHFFFAOYSA-N 0.000 description 1
- NDUWJHRKDYXRAD-UHFFFAOYSA-N 2-ethoxy-1,3-thiazole Chemical compound CCOC1=NC=CS1 NDUWJHRKDYXRAD-UHFFFAOYSA-N 0.000 description 1
- RSYDDJMZYDRCOF-ARJAWSKDSA-N 2-hydroxy-3-[(z)-16-(2-hydroxy-5-methoxy-3,6-dioxocyclohexa-1,4-dien-1-yl)hexadec-8-enyl]-5-methoxycyclohexa-2,5-diene-1,4-dione Chemical compound O=C1C(OC)=CC(=O)C(O)=C1CCCCCCC\C=C/CCCCCCCC1=C(O)C(=O)C=C(OC)C1=O RSYDDJMZYDRCOF-ARJAWSKDSA-N 0.000 description 1
- SGUAFYQXFOLMHL-UHFFFAOYSA-N 2-hydroxy-5-{1-hydroxy-2-[(4-phenylbutan-2-yl)amino]ethyl}benzamide Chemical compound C=1C=C(O)C(C(N)=O)=CC=1C(O)CNC(C)CCC1=CC=CC=C1 SGUAFYQXFOLMHL-UHFFFAOYSA-N 0.000 description 1
- UPHOPMSGKZNELG-UHFFFAOYSA-N 2-hydroxynaphthalene-1-carboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=C(O)C=CC2=C1 UPHOPMSGKZNELG-UHFFFAOYSA-N 0.000 description 1
- HZLCGUXUOFWCCN-UHFFFAOYSA-N 2-hydroxynonadecane-1,2,3-tricarboxylic acid Chemical compound CCCCCCCCCCCCCCCCC(C(O)=O)C(O)(C(O)=O)CC(O)=O HZLCGUXUOFWCCN-UHFFFAOYSA-N 0.000 description 1
- IWTFOFMTUOBLHG-UHFFFAOYSA-N 2-methoxypyridine Chemical compound COC1=CC=CC=N1 IWTFOFMTUOBLHG-UHFFFAOYSA-N 0.000 description 1
- YZQLWPMZQVHJED-UHFFFAOYSA-N 2-methylpropanethioic acid S-[2-[[[1-(2-ethylbutyl)cyclohexyl]-oxomethyl]amino]phenyl] ester Chemical compound C=1C=CC=C(SC(=O)C(C)C)C=1NC(=O)C1(CC(CC)CC)CCCCC1 YZQLWPMZQVHJED-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 1
- 125000001698 2H-pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- MLMQPDHYNJCQAO-UHFFFAOYSA-N 3,3-dimethylbutyric acid Chemical compound CC(C)(C)CC(O)=O MLMQPDHYNJCQAO-UHFFFAOYSA-N 0.000 description 1
- XLZYKTYMLBOINK-UHFFFAOYSA-N 3-(4-hydroxybenzoyl)benzoic acid Chemical compound OC(=O)C1=CC=CC(C(=O)C=2C=CC(O)=CC=2)=C1 XLZYKTYMLBOINK-UHFFFAOYSA-N 0.000 description 1
- MFEIKQPHQINPRI-UHFFFAOYSA-N 3-Ethylpyridine Chemical compound CCC1=CC=CN=C1 MFEIKQPHQINPRI-UHFFFAOYSA-N 0.000 description 1
- ZHQLGXXIQHLVOE-UHFFFAOYSA-N 3-[3-acetyl-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(C(C)=O)=C1CC(C)(C)C(O)=O ZHQLGXXIQHLVOE-UHFFFAOYSA-N 0.000 description 1
- RMPJSNYQJHTTBK-UHFFFAOYSA-N 3-[3-ethyl-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(CC)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(OC)N=N1 RMPJSNYQJHTTBK-UHFFFAOYSA-N 0.000 description 1
- NZOONKHCNQFYCI-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[(4-chlorophenyl)methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CC4=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC1=CC=C(Cl)C=C1 NZOONKHCNQFYCI-UHFFFAOYSA-N 0.000 description 1
- LVQDUPNLDGOFLJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(4-methoxypyridin-2-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=C6C=CC=CC6=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 LVQDUPNLDGOFLJ-UHFFFAOYSA-N 0.000 description 1
- PBWWKYNPRXMZHJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-fluoropyridin-2-yl)phenyl]methyl]-5-(quinolin-2-ylmethoxy)indol-2-yl]-N-carbamimidoyl-N-[2-(dimethylamino)ethyl]-2,2-dimethylpropanamide Chemical compound C(C)(C)(C)SC1=C(N(C2=CC=C(C=C12)OCC1=NC2=CC=CC=C2C=C1)CC1=CC=C(C=C1)C1=NC=C(C=C1)F)CC(C(=O)N(C(=N)N)CCN(C)C)(C)C PBWWKYNPRXMZHJ-UHFFFAOYSA-N 0.000 description 1
- PKSYDJNVHMPQCJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(5-methylpyridin-2-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(C)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O PKSYDJNVHMPQCJ-UHFFFAOYSA-N 0.000 description 1
- VSYWLXSRFUTNAH-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridazin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O VSYWLXSRFUTNAH-UHFFFAOYSA-N 0.000 description 1
- GNNHADUYIRCLSB-DEOSSOPVSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-2-yl)phenyl]methyl]-5-[(1s)-1-pyridin-2-ylethoxy]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=CC(C=2C=CC(CN3C4=CC=C(O[C@@H](C)C=5N=CC=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=N1 GNNHADUYIRCLSB-DEOSSOPVSA-N 0.000 description 1
- CJAWPOGTNPVLTJ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethyl-n-(1,3-thiazol-2-yl)propanamide Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(=O)NC1=NC=CS1 CJAWPOGTNPVLTJ-UHFFFAOYSA-N 0.000 description 1
- ZYQATABFPXDHCG-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethyl-n-pyrazin-2-ylpropanamide Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(=O)NC1=CN=CC=N1 ZYQATABFPXDHCG-UHFFFAOYSA-N 0.000 description 1
- GTCSYPCSOZJZDD-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethyl-n-pyridin-3-ylpropanamide Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(=O)NC1=CC=CN=C1 GTCSYPCSOZJZDD-UHFFFAOYSA-N 0.000 description 1
- OAIUOHKKKMEMAY-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-n-[2-(dimethylamino)ethyl]-2,2-dimethylpropanamide Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(=O)NCCN(C)C OAIUOHKKKMEMAY-UHFFFAOYSA-N 0.000 description 1
- ZEZBHCCKISKWIL-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(imidazo[1,2-a]pyridin-2-ylmethoxy)-1-[[4-[5-(trifluoromethyl)pyridin-2-yl]phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=C4C=CC=CN4C=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(C=C1)=CC=C1C1=CC=C(C(F)(F)F)C=N1 ZEZBHCCKISKWIL-UHFFFAOYSA-N 0.000 description 1
- RITLXXCGDGQBEU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[(4-pyridin-2-ylphenyl)methyl]indol-2-yl]-2,2-dimethylpropanamide Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(N)=O)N1CC(C=C1)=CC=C1C1=CC=CC=N1 RITLXXCGDGQBEU-UHFFFAOYSA-N 0.000 description 1
- BMPCKGSLYZNYFP-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-(pyridin-2-ylmethoxy)-1-[[5-[4-(trifluoromethoxy)phenyl]pyridin-2-yl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C12=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C(CC(C)(C)C(O)=O)N1CC(N=C1)=CC=C1C1=CC=C(OC(F)(F)F)C=C1 BMPCKGSLYZNYFP-UHFFFAOYSA-N 0.000 description 1
- ZVFGQEHAFRQOQZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(3,5-dimethylpyridin-2-yl)methoxy]-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3C(=CC(C)=CN=3)C)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O ZVFGQEHAFRQOQZ-UHFFFAOYSA-N 0.000 description 1
- JCQPMKIBHZXBRZ-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5,6-dimethylpyridin-2-yl)methoxy]-1-[[4-(4-methoxypyridin-2-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound COC1=CC=NC(C=2C=CC(CN3C4=CC=C(OCC=5N=C(C)C(C)=CC=5)C=C4C(SC(C)(C)C)=C3CC(C)(C)C(O)=O)=CC=2)=C1 JCQPMKIBHZXBRZ-UHFFFAOYSA-N 0.000 description 1
- SIHVXDBOTSAWRU-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-[(5-ethylpyridin-2-yl)methoxy]-1-[[4-(2-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound N1=CC(CC)=CC=C1COC1=CC=C(N(CC=2C=CC(=CC=2)C=2C(=NC=CC=2)OC)C(CC(C)(C)C(O)=O)=C2SC(C)(C)C)C2=C1 SIHVXDBOTSAWRU-UHFFFAOYSA-N 0.000 description 1
- WUSZIKHYERYCFY-UHFFFAOYSA-N 3-[3-tert-butylsulfanyl-5-hydroxy-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]indol-2-yl]-2,2-dimethylpropanoic acid Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(O)C=C2C(SC(C)(C)C)=C1CC(C)(C)C(O)=O WUSZIKHYERYCFY-UHFFFAOYSA-N 0.000 description 1
- WSNKEJIFARPOSQ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-(1-benzothiophen-2-ylmethyl)benzamide Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)NCC2=CC3=C(S2)C=CC=C3)C=CC=1 WSNKEJIFARPOSQ-UHFFFAOYSA-N 0.000 description 1
- VTNULXUEOJMRKZ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-(2H-tetrazol-5-ylmethyl)benzamide Chemical compound N=1NN=NC=1CNC(C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)=O VTNULXUEOJMRKZ-UHFFFAOYSA-N 0.000 description 1
- GDSLUYKCPYECNN-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[(4-fluorophenyl)methyl]benzamide Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)NCC2=CC=C(C=C2)F)C=CC=1 GDSLUYKCPYECNN-UHFFFAOYSA-N 0.000 description 1
- ZMCQQCBOZIGNRV-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[2-(1,2,4-triazol-1-yl)ethyl]benzamide Chemical compound NCC1=CC(OC2=CC=CC(=C2)C(=O)NCCN2C=NC=N2)=NC(=C1)C(F)(F)F ZMCQQCBOZIGNRV-UHFFFAOYSA-N 0.000 description 1
- AJZDHLHTTJRNQJ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[2-(tetrazol-1-yl)ethyl]benzamide Chemical compound N1(N=NN=C1)CCNC(C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)=O AJZDHLHTTJRNQJ-UHFFFAOYSA-N 0.000 description 1
- MZSAMHOCTRNOIZ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-phenylaniline Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(NC2=CC=CC=C2)C=CC=1 MZSAMHOCTRNOIZ-UHFFFAOYSA-N 0.000 description 1
- HAEQAUJYNHQVHV-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-phenylbenzamide Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)NC2=CC=CC=C2)C=CC=1 HAEQAUJYNHQVHV-UHFFFAOYSA-N 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical compound OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- 125000004364 3-pyrrolinyl group Chemical group [H]C1=C([H])C([H])([H])N(*)C1([H])[H] 0.000 description 1
- 125000001397 3-pyrrolyl group Chemical group [H]N1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000001963 4 membered heterocyclic group Chemical group 0.000 description 1
- CYDQOEWLBCCFJZ-UHFFFAOYSA-N 4-(4-fluorophenyl)oxane-4-carboxylic acid Chemical compound C=1C=C(F)C=CC=1C1(C(=O)O)CCOCC1 CYDQOEWLBCCFJZ-UHFFFAOYSA-N 0.000 description 1
- IIYVNMXPYWIJBL-UHFFFAOYSA-N 4-(trifluoromethyl)pyridine Chemical compound FC(F)(F)C1=CC=NC=C1 IIYVNMXPYWIJBL-UHFFFAOYSA-N 0.000 description 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 1
- 125000001826 4H-pyranyl group Chemical group O1C(=CCC=C1)* 0.000 description 1
- FBXGQDUVJBKEAJ-UHFFFAOYSA-N 4h-oxazin-3-one Chemical compound O=C1CC=CON1 FBXGQDUVJBKEAJ-UHFFFAOYSA-N 0.000 description 1
- 125000002373 5 membered heterocyclic group Chemical group 0.000 description 1
- RDEYORKJEDLLDB-DQVHGTJVSA-N 5-Hydroperoxyeicosatetraenoic acid Chemical compound CCCCCCCCCCC\C=C\C=C\C(\OO)=C\C=C\C(O)=O RDEYORKJEDLLDB-DQVHGTJVSA-N 0.000 description 1
- NFFXEUUOMTXWCX-UHFFFAOYSA-N 5-[(2,4-dioxo-1,3-thiazolidin-5-yl)methyl]-2-methoxy-n-[[4-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound C1=C(C(=O)NCC=2C=CC(=CC=2)C(F)(F)F)C(OC)=CC=C1CC1SC(=O)NC1=O NFFXEUUOMTXWCX-UHFFFAOYSA-N 0.000 description 1
- ACKQJGLSRFVPFA-UHFFFAOYSA-N 5-[1-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2-methylpropan-2-yl]-1,3,4-oxadiazol-2-amine Chemical compound C1=NC(OC)=CC=C1C(C=C1)=CC=C1CN1C2=CC=C(OCC=3N=CC=CC=3)C=C2C(SC(C)(C)C)=C1CC(C)(C)C1=NN=C(N)O1 ACKQJGLSRFVPFA-UHFFFAOYSA-N 0.000 description 1
- KKVKZXYVUYSAHA-UHFFFAOYSA-N 5-[4-[[3-tert-butylsulfanyl-2-(2,2-dimethylpropyl)-5-(pyridin-2-ylmethoxy)indol-1-yl]methyl]phenyl]-1,3,4-oxadiazol-2-amine Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3OC(N)=NN=3)C(CC(C)(C)C)=C(SC(C)(C)C)C2=CC=1OCC1=CC=CC=N1 KKVKZXYVUYSAHA-UHFFFAOYSA-N 0.000 description 1
- ODQJQEROUCVZNG-UHFFFAOYSA-N 5-fluoropyridine Chemical compound FC1=C=NC=C[CH]1 ODQJQEROUCVZNG-UHFFFAOYSA-N 0.000 description 1
- 102100022738 5-hydroxytryptamine receptor 1A Human genes 0.000 description 1
- 101710138638 5-hydroxytryptamine receptor 1A Proteins 0.000 description 1
- 125000004070 6 membered heterocyclic group Chemical group 0.000 description 1
- RMDCSDVIVXJELQ-UHFFFAOYSA-N 6-fluoroquinoline Chemical compound N1=CC=CC2=CC(F)=CC=C21 RMDCSDVIVXJELQ-UHFFFAOYSA-N 0.000 description 1
- 239000005541 ACE inhibitor Substances 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 208000036764 Adenocarcinoma of the esophagus Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 206010001889 Alveolitis Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 229940123413 Angiotensin II antagonist Drugs 0.000 description 1
- 102100029470 Apolipoprotein E Human genes 0.000 description 1
- 101710095339 Apolipoprotein E Proteins 0.000 description 1
- 200000000007 Arterial disease Diseases 0.000 description 1
- 206010003210 Arteriosclerosis Diseases 0.000 description 1
- 208000009657 Aspirin-Induced Asthma Diseases 0.000 description 1
- 208000037260 Atherosclerotic Plaque Diseases 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 238000006159 Bartoli reaction Methods 0.000 description 1
- 238000005679 Batcho-Leimgruber synthesis reaction Methods 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- 208000006386 Bone Resorption Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 1
- 239000002080 C09CA02 - Eprosartan Substances 0.000 description 1
- 239000004072 C09CA03 - Valsartan Substances 0.000 description 1
- 239000002947 C09CA04 - Irbesartan Substances 0.000 description 1
- 239000002053 C09CA06 - Candesartan Substances 0.000 description 1
- 239000005537 C09CA07 - Telmisartan Substances 0.000 description 1
- 101100289995 Caenorhabditis elegans mac-1 gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-N Caprylic acid Natural products CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 208000020446 Cardiac disease Diseases 0.000 description 1
- 208000010867 Carotid Artery injury Diseases 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- LZZYPRNAOMGNLH-UHFFFAOYSA-M Cetrimonium bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](C)(C)C LZZYPRNAOMGNLH-UHFFFAOYSA-M 0.000 description 1
- 241000819038 Chichester Species 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 239000004155 Chlorine dioxide Substances 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- OJLOPKGSLYJEMD-LNQMSSPSSA-N Cyotec Chemical group CCCCC(C)(O)CC=C[C@H]1[C@H](O)CC(=O)[C@@H]1CCCCCCC(=O)OC OJLOPKGSLYJEMD-LNQMSSPSSA-N 0.000 description 1
- 108050009460 Cysteinyl leukotriene receptor 1 Proteins 0.000 description 1
- 102100033539 Cysteinyl leukotriene receptor 2 Human genes 0.000 description 1
- 108090000655 Cysteinyl leukotriene receptor 2 Proteins 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- 102000003849 Cytochrome P450 Human genes 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- VVNCNSJFMMFHPL-VKHMYHEASA-N D-penicillamine Chemical group CC(C)(S)[C@@H](N)C(O)=O VVNCNSJFMMFHPL-VKHMYHEASA-N 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- PQUCIEFHOVEZAU-UHFFFAOYSA-N Diammonium sulfite Chemical compound [NH4+].[NH4+].[O-]S([O-])=O PQUCIEFHOVEZAU-UHFFFAOYSA-N 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 102000004860 Dipeptidases Human genes 0.000 description 1
- 108090001081 Dipeptidases Proteins 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 102000002045 Endothelin Human genes 0.000 description 1
- 108050009340 Endothelin Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 206010015866 Extravasation Diseases 0.000 description 1
- 206010015943 Eye inflammation Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 229940123457 Free radical scavenger Drugs 0.000 description 1
- 238000010650 Fukuyama indole synthesis reaction Methods 0.000 description 1
- 108091006027 G proteins Proteins 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 1
- 238000006355 Gassman indole synthesis reaction Methods 0.000 description 1
- HEMJJKBWTPKOJG-UHFFFAOYSA-N Gemfibrozil Chemical compound CC1=CC=C(C)C(OCCCC(C)(C)C(O)=O)=C1 HEMJJKBWTPKOJG-UHFFFAOYSA-N 0.000 description 1
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 1
- 208000007465 Giant cell arteritis Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000016354 Glucuronosyltransferase Human genes 0.000 description 1
- 108010092364 Glucuronosyltransferase Proteins 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 102000017011 Glycated Hemoglobin A Human genes 0.000 description 1
- 229940123856 Glycogen synthase kinase 3 inhibitor Drugs 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 238000006196 Hemetsberger Knittel synthesis reaction Methods 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 229920001499 Heparinoid Polymers 0.000 description 1
- 206010056328 Hepatic ischaemia Diseases 0.000 description 1
- 101000755875 Homo sapiens Arachidonate 5-lipoxygenase-activating protein Proteins 0.000 description 1
- 101001046686 Homo sapiens Integrin alpha-M Proteins 0.000 description 1
- 101000935040 Homo sapiens Integrin beta-2 Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 108010000775 Hydroxymethylglutaryl-CoA synthase Proteins 0.000 description 1
- 102100028889 Hydroxymethylglutaryl-CoA synthase, mitochondrial Human genes 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- 101150081923 IL4 gene Proteins 0.000 description 1
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 description 1
- HCUARRIEZVDMPT-UHFFFAOYSA-N Indole-2-carboxylic acid Chemical group C1=CC=C2NC(C(=O)O)=CC2=C1 HCUARRIEZVDMPT-UHFFFAOYSA-N 0.000 description 1
- 102100022338 Integrin alpha-M Human genes 0.000 description 1
- 102100025390 Integrin beta-2 Human genes 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 206010061246 Intervertebral disc degeneration Diseases 0.000 description 1
- 238000006147 Japp-Klingemann synthesis reaction Methods 0.000 description 1
- 208000011200 Kawasaki disease Diseases 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 238000007211 Larock indole synthesis reaction Methods 0.000 description 1
- 101710127901 Leukotriene B4 receptor 1 Proteins 0.000 description 1
- 102000011965 Lipoprotein Receptors Human genes 0.000 description 1
- 108010061306 Lipoprotein Receptors Proteins 0.000 description 1
- 239000012448 Lithium borohydride Substances 0.000 description 1
- 208000019693 Lung disease Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 102100037611 Lysophospholipase Human genes 0.000 description 1
- 229940122696 MAP kinase inhibitor Drugs 0.000 description 1
- 238000006861 Madelung synthesis reaction Methods 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 244000062730 Melissa officinalis Species 0.000 description 1
- 235000010654 Melissa officinalis Nutrition 0.000 description 1
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 description 1
- 208000029725 Metabolic bone disease Diseases 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-N Metaphosphoric acid Chemical compound OP(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-N 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- TXXHDPDFNKHHGW-CCAGOZQPSA-N Muconic acid Natural products OC(=O)\C=C/C=C\C(O)=O TXXHDPDFNKHHGW-CCAGOZQPSA-N 0.000 description 1
- KCWZGJVSDFYRIX-YFKPBYRVSA-N N(gamma)-nitro-L-arginine methyl ester Chemical compound COC(=O)[C@@H](N)CCCN=C(N)N[N+]([O-])=O KCWZGJVSDFYRIX-YFKPBYRVSA-N 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- OVBPIULPVIDEAO-UHFFFAOYSA-N N-Pteroyl-L-glutaminsaeure Natural products C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-UHFFFAOYSA-N 0.000 description 1
- RODUKNYOEVZQPR-UHFFFAOYSA-N N-[3-(aminomethyl)benzyl]acetamidine Chemical compound CC(=N)NCC1=CC=CC(CN)=C1 RODUKNYOEVZQPR-UHFFFAOYSA-N 0.000 description 1
- 229940127523 NMDA Receptor Antagonists Drugs 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 238000006789 Nenitzescu synthesis reaction Methods 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- 102400001111 Nociceptin Human genes 0.000 description 1
- 108090000622 Nociceptin Proteins 0.000 description 1
- 102000007399 Nuclear hormone receptor Human genes 0.000 description 1
- 108020005497 Nuclear hormone receptor Proteins 0.000 description 1
- 206010030111 Oedema mucosal Diseases 0.000 description 1
- 206010030137 Oesophageal adenocarcinoma Diseases 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010049088 Osteopenia Diseases 0.000 description 1
- 102100035593 POU domain, class 2, transcription factor 1 Human genes 0.000 description 1
- 101710084414 POU domain, class 2, transcription factor 1 Proteins 0.000 description 1
- 102000023984 PPAR alpha Human genes 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 108090000279 Peptidyltransferases Proteins 0.000 description 1
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 1
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 1
- 108010064785 Phospholipases Proteins 0.000 description 1
- 102000015439 Phospholipases Human genes 0.000 description 1
- 108010058864 Phospholipases A2 Proteins 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 229920000148 Polycarbophil calcium Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 208000026301 Postoperative Cognitive Complications Diseases 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 206010036790 Productive cough Diseases 0.000 description 1
- 108050003243 Prostaglandin G/H synthase 1 Proteins 0.000 description 1
- 108050003267 Prostaglandin G/H synthase 2 Proteins 0.000 description 1
- 102000004005 Prostaglandin-endoperoxide synthases Human genes 0.000 description 1
- 108090000459 Prostaglandin-endoperoxide synthases Proteins 0.000 description 1
- 206010037596 Pyelonephritis Diseases 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 238000010716 Reissert indole synthesis reaction Methods 0.000 description 1
- 208000033464 Reiter syndrome Diseases 0.000 description 1
- 206010038910 Retinitis Diseases 0.000 description 1
- 102000034527 Retinoid X Receptors Human genes 0.000 description 1
- 108010038912 Retinoid X Receptors Proteins 0.000 description 1
- 208000025747 Rheumatic disease Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 1
- 208000008765 Sciatica Diseases 0.000 description 1
- 206010039705 Scleritis Diseases 0.000 description 1
- 206010048908 Seasonal allergy Diseases 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- 102000005782 Squalene Monooxygenase Human genes 0.000 description 1
- 108020003891 Squalene monooxygenase Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 102000001494 Sterol O-Acyltransferase Human genes 0.000 description 1
- 108010054082 Sterol O-acyltransferase Proteins 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 101710137302 Surface antigen S Proteins 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- 229940122388 Thrombin inhibitor Drugs 0.000 description 1
- 102000009843 Thyroglobulin Human genes 0.000 description 1
- 108010034949 Thyroglobulin Proteins 0.000 description 1
- 206010044248 Toxic shock syndrome Diseases 0.000 description 1
- 231100000650 Toxic shock syndrome Toxicity 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 206010044541 Traumatic shock Diseases 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- GLEVLJDDWXEYCO-UHFFFAOYSA-N Trolox Chemical compound O1C(C)(C(O)=O)CCC2=C1C(C)=C(C)C(O)=C2C GLEVLJDDWXEYCO-UHFFFAOYSA-N 0.000 description 1
- XCCTYIAWTASOJW-XVFCMESISA-N Uridine-5'-Diphosphate Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(=O)OP(O)(O)=O)O[C@H]1N1C(=O)NC(=O)C=C1 XCCTYIAWTASOJW-XVFCMESISA-N 0.000 description 1
- 206010046851 Uveitis Diseases 0.000 description 1
- 208000035868 Vascular inflammations Diseases 0.000 description 1
- 229930003779 Vitamin B12 Natural products 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- ZEEBGORNQSEQBE-UHFFFAOYSA-N [2-(3-phenylphenoxy)-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound C1(=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)C1=CC=CC=C1 ZEEBGORNQSEQBE-UHFFFAOYSA-N 0.000 description 1
- REAYFGLASQTHKB-UHFFFAOYSA-N [2-[3-(1H-pyrazol-4-yl)phenoxy]-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound N1N=CC(=C1)C=1C=C(OC2=NC(=CC(=C2)CN)C(F)(F)F)C=CC=1 REAYFGLASQTHKB-UHFFFAOYSA-N 0.000 description 1
- SAHIZENKTPRYSN-UHFFFAOYSA-N [2-[3-(phenoxymethyl)phenoxy]-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound O(C1=CC=CC=C1)CC=1C=C(OC2=NC(=CC(=C2)CN)C(F)(F)F)C=CC=1 SAHIZENKTPRYSN-UHFFFAOYSA-N 0.000 description 1
- ABRVLXLNVJHDRQ-UHFFFAOYSA-N [2-pyridin-3-yl-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound FC(C1=CC(=CC(=N1)C=1C=NC=CC=1)CN)(F)F ABRVLXLNVJHDRQ-UHFFFAOYSA-N 0.000 description 1
- YQYBUJYBXOVWQW-UHFFFAOYSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-(3,4-dihydro-1H-isoquinolin-2-yl)methanone Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C=CC=1)C(=O)N1CC2=CC=CC=C2CC1 YQYBUJYBXOVWQW-UHFFFAOYSA-N 0.000 description 1
- YKKPYMXANSSQCA-UHFFFAOYSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-(3-pyrazol-1-ylazetidin-1-yl)methanone Chemical compound N1(N=CC=C1)C1CN(C1)C(=O)C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F YKKPYMXANSSQCA-UHFFFAOYSA-N 0.000 description 1
- 101150090313 abc1 gene Proteins 0.000 description 1
- 206010000059 abdominal discomfort Diseases 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- GPWHDDKQSYOYBF-UHFFFAOYSA-N ac1l2u0q Chemical compound Br[Br-]Br GPWHDDKQSYOYBF-UHFFFAOYSA-N 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 229940020697 accolate Drugs 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 229960002122 acebutolol Drugs 0.000 description 1
- GOEMGAFJFRBGGG-UHFFFAOYSA-N acebutolol Chemical compound CCCC(=O)NC1=CC=C(OCC(O)CNC(C)C)C(C(C)=O)=C1 GOEMGAFJFRBGGG-UHFFFAOYSA-N 0.000 description 1
- 239000003377 acid catalyst Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 230000006022 acute inflammation Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 229960005305 adenosine Drugs 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 229940040563 agaric acid Drugs 0.000 description 1
- 125000003158 alcohol group Chemical group 0.000 description 1
- IAJILQKETJEXLJ-QTBDOELSSA-N aldehydo-D-glucuronic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-QTBDOELSSA-N 0.000 description 1
- DCSBSVSZJRSITC-UHFFFAOYSA-M alendronate sodium trihydrate Chemical compound O.O.O.[Na+].NCCCC(O)(P(O)(O)=O)P(O)([O-])=O DCSBSVSZJRSITC-UHFFFAOYSA-M 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000005037 alkyl phenyl group Chemical group 0.000 description 1
- 125000005360 alkyl sulfoxide group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- OENHQHLEOONYIE-UKMVMLAPSA-N all-trans beta-carotene Natural products CC=1CCCC(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C OENHQHLEOONYIE-UKMVMLAPSA-N 0.000 description 1
- 230000009285 allergic inflammation Effects 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 239000003194 amino acid receptor blocking agent Substances 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 229940070021 anabolic steroids Drugs 0.000 description 1
- 230000002052 anaphylactic effect Effects 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000002333 angiotensin II receptor antagonist Substances 0.000 description 1
- 239000000400 angiotensin II type 1 receptor blocker Substances 0.000 description 1
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000002946 anti-pancreatic effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 229940027983 antiseptic and disinfectant quaternary ammonium compound Drugs 0.000 description 1
- 229960004676 antithrombotic agent Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- RSYDDJMZYDRCOF-UHFFFAOYSA-N ardisiaquinone A Natural products O=C1C(OC)=CC(=O)C(O)=C1CCCCCCCC=CCCCCCCCC1=C(O)C(=O)C=C(OC)C1=O RSYDDJMZYDRCOF-UHFFFAOYSA-N 0.000 description 1
- KXNPVXPOPUZYGB-XYVMCAHJSA-N argatroban Chemical compound OC(=O)[C@H]1C[C@H](C)CCN1C(=O)[C@H](CCCN=C(N)N)NS(=O)(=O)C1=CC=CC2=C1NC[C@H](C)C2 KXNPVXPOPUZYGB-XYVMCAHJSA-N 0.000 description 1
- 229960003856 argatroban Drugs 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 229940097776 arthrotec Drugs 0.000 description 1
- 125000005362 aryl sulfone group Chemical group 0.000 description 1
- 125000005361 aryl sulfoxide group Chemical group 0.000 description 1
- 125000005110 aryl thio group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 210000001130 astrocyte Anatomy 0.000 description 1
- 229960002274 atenolol Drugs 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical compound C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 description 1
- 229940064856 azulfidine Drugs 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- 125000000043 benzamido group Chemical group [H]N([*])C(=O)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- GONOPSZTUGRENK-UHFFFAOYSA-N benzyl(trichloro)silane Chemical compound Cl[Si](Cl)(Cl)CC1=CC=CC=C1 GONOPSZTUGRENK-UHFFFAOYSA-N 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 229940097320 beta blocking agent Drugs 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 235000013734 beta-carotene Nutrition 0.000 description 1
- 239000011648 beta-carotene Substances 0.000 description 1
- TUPZEYHYWIEDIH-WAIFQNFQSA-N beta-carotene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2=CCCCC2(C)C TUPZEYHYWIEDIH-WAIFQNFQSA-N 0.000 description 1
- 229960002747 betacarotene Drugs 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- 229940110331 bextra Drugs 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 208000002352 blister Diseases 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000002449 bone cell Anatomy 0.000 description 1
- 230000024279 bone resorption Effects 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- 229960002645 boric acid Drugs 0.000 description 1
- MOOAHMCRPCTRLV-UHFFFAOYSA-N boron sodium Chemical compound [B].[Na] MOOAHMCRPCTRLV-UHFFFAOYSA-N 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 210000000621 bronchi Anatomy 0.000 description 1
- 229940057344 bufferin Drugs 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 1
- 239000000920 calcium hydroxide Substances 0.000 description 1
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 1
- 239000003710 calcium ionophore Substances 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 229960000932 candesartan Drugs 0.000 description 1
- SGZAIDDFHDDFJU-UHFFFAOYSA-N candesartan Chemical compound CCOC1=NC2=CC=CC(C(O)=O)=C2N1CC(C=C1)=CC=C1C1=CC=CC=C1C1=NN=N[N]1 SGZAIDDFHDDFJU-UHFFFAOYSA-N 0.000 description 1
- FAKRSMQSSFJEIM-RQJHMYQMSA-N captopril Chemical compound SC[C@@H](C)C(=O)N1CCC[C@H]1C(O)=O FAKRSMQSSFJEIM-RQJHMYQMSA-N 0.000 description 1
- 229960000830 captopril Drugs 0.000 description 1
- 230000002252 carbamoylating effect Effects 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 229960001631 carbomer Drugs 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 229960004424 carbon dioxide Drugs 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 239000003183 carcinogenic agent Substances 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 229940087110 celestone Drugs 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 238000002659 cell therapy Methods 0.000 description 1
- 229960001927 cetylpyridinium chloride Drugs 0.000 description 1
- NFCRBQADEGXVDL-UHFFFAOYSA-M cetylpyridinium chloride monohydrate Chemical compound O.[Cl-].CCCCCCCCCCCCCCCC[N+]1=CC=CC=C1 NFCRBQADEGXVDL-UHFFFAOYSA-M 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 150000005829 chemical entities Chemical class 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 230000003399 chemotactic effect Effects 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 229940060038 chlorine Drugs 0.000 description 1
- 235000019398 chlorine dioxide Nutrition 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 230000001906 cholesterol absorption Effects 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 201000009151 chronic rhinitis Diseases 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 230000007882 cirrhosis Effects 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 229960001284 citicoline Drugs 0.000 description 1
- 229960001214 clofibrate Drugs 0.000 description 1
- KNHUKKLJHYUCFP-UHFFFAOYSA-N clofibrate Chemical compound CCOC(=O)C(C)(C)OC1=CC=C(Cl)C=C1 KNHUKKLJHYUCFP-UHFFFAOYSA-N 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- AGVAZMGAQJOSFJ-WZHZPDAFSA-M cobalt(2+);[(2r,3s,4r,5s)-5-(5,6-dimethylbenzimidazol-1-yl)-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl] [(2r)-1-[3-[(1r,2r,3r,4z,7s,9z,12s,13s,14z,17s,18s,19r)-2,13,18-tris(2-amino-2-oxoethyl)-7,12,17-tris(3-amino-3-oxopropyl)-3,5,8,8,13,15,18,19-octamethyl-2 Chemical compound [Co+2].N#[C-].[N-]([C@@H]1[C@H](CC(N)=O)[C@@]2(C)CCC(=O)NC[C@@H](C)OP(O)(=O)O[C@H]3[C@H]([C@H](O[C@@H]3CO)N3C4=CC(C)=C(C)C=C4N=C3)O)\C2=C(C)/C([C@H](C\2(C)C)CCC(N)=O)=N/C/2=C\C([C@H]([C@@]/2(CC(N)=O)C)CCC(N)=O)=N\C\2=C(C)/C2=N[C@]1(C)[C@@](C)(CC(N)=O)[C@@H]2CCC(N)=O AGVAZMGAQJOSFJ-WZHZPDAFSA-M 0.000 description 1
- RGJOEKWQDUBAIZ-UHFFFAOYSA-N coenzime A Natural products OC1C(OP(O)(O)=O)C(COP(O)(=O)OP(O)(=O)OCC(C)(C)C(O)C(=O)NCCC(=O)NCCS)OC1N1C2=NC=NC(N)=C2N=C1 RGJOEKWQDUBAIZ-UHFFFAOYSA-N 0.000 description 1
- 239000005516 coenzyme A Substances 0.000 description 1
- 229940093530 coenzyme a Drugs 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 238000006880 cross-coupling reaction Methods 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 235000000639 cyanocobalamin Nutrition 0.000 description 1
- 239000011666 cyanocobalamin Substances 0.000 description 1
- 229960002104 cyanocobalamin Drugs 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- JMFVWNKPLURQMI-UHFFFAOYSA-N cyclopentyl carbamate Chemical compound NC(=O)OC1CCCC1 JMFVWNKPLURQMI-UHFFFAOYSA-N 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 208000018180 degenerative disc disease Diseases 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 229940027008 deltasone Drugs 0.000 description 1
- KDTSHFARGAKYJN-UHFFFAOYSA-N dephosphocoenzyme A Natural products OC1C(O)C(COP(O)(=O)OP(O)(=O)OCC(C)(C)C(O)C(=O)NCCC(=O)NCCS)OC1N1C2=NC=NC(N)=C2N=C1 KDTSHFARGAKYJN-UHFFFAOYSA-N 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 125000002576 diazepinyl group Chemical group N1N=C(C=CC=C1)* 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- 229940042935 dichlorodifluoromethane Drugs 0.000 description 1
- 229940087091 dichlorotetrafluoroethane Drugs 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 125000005057 dihydrothienyl group Chemical group S1C(CC=C1)* 0.000 description 1
- 125000000532 dioxanyl group Chemical group 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- CEALXSHFPPCRNM-UHFFFAOYSA-L disodium;carboxylato carbonate Chemical compound [Na+].[Na+].[O-]C(=O)OC([O-])=O CEALXSHFPPCRNM-UHFFFAOYSA-L 0.000 description 1
- 125000005883 dithianyl group Chemical group 0.000 description 1
- 125000005411 dithiolanyl group Chemical group S1SC(CC1)* 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 230000035620 dolor Effects 0.000 description 1
- 230000002222 downregulating effect Effects 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 239000003118 drug derivative Substances 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 206010013990 dysuria Diseases 0.000 description 1
- 229950009041 edaravone Drugs 0.000 description 1
- QELUYTUMUWHWMC-UHFFFAOYSA-N edaravone Chemical compound O=C1CC(C)=NN1C1=CC=CC=C1 QELUYTUMUWHWMC-UHFFFAOYSA-N 0.000 description 1
- 150000002066 eicosanoids Chemical class 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 210000004696 endometrium Anatomy 0.000 description 1
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 231100000284 endotoxic Toxicity 0.000 description 1
- 230000002346 endotoxic effect Effects 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 239000003248 enzyme activator Substances 0.000 description 1
- 229960004563 eprosartan Drugs 0.000 description 1
- OROAFUQRIXKEMV-LDADJPATSA-N eprosartan Chemical compound C=1C=C(C(O)=O)C=CC=1CN1C(CCCC)=NC=C1\C=C(C(O)=O)/CC1=CC=CS1 OROAFUQRIXKEMV-LDADJPATSA-N 0.000 description 1
- 229960003745 esmolol Drugs 0.000 description 1
- AQNDDEOPVVGCPG-UHFFFAOYSA-N esmolol Chemical compound COC(=O)CCC1=CC=C(OCC(O)CNC(C)C)C=C1 AQNDDEOPVVGCPG-UHFFFAOYSA-N 0.000 description 1
- 208000028653 esophageal adenocarcinoma Diseases 0.000 description 1
- AFAXGSQYZLGZPG-UHFFFAOYSA-N ethanedisulfonic acid Chemical compound OS(=O)(=O)CCS(O)(=O)=O AFAXGSQYZLGZPG-UHFFFAOYSA-N 0.000 description 1
- CJAONIOAQZUHPN-KKLWWLSJSA-N ethyl 12-[[2-[(2r,3r)-3-[2-[(12-ethoxy-12-oxododecyl)-methylamino]-2-oxoethoxy]butan-2-yl]oxyacetyl]-methylamino]dodecanoate Chemical compound CCOC(=O)CCCCCCCCCCCN(C)C(=O)CO[C@H](C)[C@@H](C)OCC(=O)N(C)CCCCCCCCCCCC(=O)OCC CJAONIOAQZUHPN-KKLWWLSJSA-N 0.000 description 1
- IQRFPYJXRWLEJV-UHFFFAOYSA-N ethyl 3-[3-tert-butylsulfanyl-1-[[4-(6-methoxypyridin-3-yl)phenyl]methyl]-5-(pyridin-2-ylmethoxy)indol-2-yl]-2,2-dimethylpropanoate Chemical compound C=1C=C2N(CC=3C=CC(=CC=3)C=3C=NC(OC)=CC=3)C(CC(C)(C)C(=O)OCC)=C(SC(C)(C)C)C2=CC=1OCC1=CC=CC=N1 IQRFPYJXRWLEJV-UHFFFAOYSA-N 0.000 description 1
- SBVYURPQULDJTI-UHFFFAOYSA-N ethyl n-[amino-[4-[[3-[[4-[2-(4-hydroxyphenyl)propan-2-yl]phenoxy]methyl]phenyl]methoxy]phenyl]methylidene]carbamate Chemical compound C1=CC(C(=N)NC(=O)OCC)=CC=C1OCC1=CC=CC(COC=2C=CC(=CC=2)C(C)(C)C=2C=CC(O)=CC=2)=C1 SBVYURPQULDJTI-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- LYCAIKOWRPUZTN-UHFFFAOYSA-N ethylene glycol Natural products OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 1
- 230000036251 extravasation Effects 0.000 description 1
- 210000003414 extremity Anatomy 0.000 description 1
- 201000001155 extrinsic allergic alveolitis Diseases 0.000 description 1
- OLNTVTPDXPETLC-XPWALMASSA-N ezetimibe Chemical compound N1([C@@H]([C@H](C1=O)CC[C@H](O)C=1C=CC(F)=CC=1)C=1C=CC(O)=CC=1)C1=CC=C(F)C=C1 OLNTVTPDXPETLC-XPWALMASSA-N 0.000 description 1
- 229960000815 ezetimibe Drugs 0.000 description 1
- NGOGFTYYXHNFQH-UHFFFAOYSA-N fasudil Chemical compound C=1C=CC2=CN=CC=C2C=1S(=O)(=O)N1CCCNCC1 NGOGFTYYXHNFQH-UHFFFAOYSA-N 0.000 description 1
- 229960002435 fasudil Drugs 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 230000001723 fibrinogenic effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 125000004428 fluoroalkoxy group Chemical group 0.000 description 1
- 125000003709 fluoroalkyl group Chemical group 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 239000011724 folic acid Substances 0.000 description 1
- 229960000304 folic acid Drugs 0.000 description 1
- 235000019152 folic acid Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 229920001002 functional polymer Polymers 0.000 description 1
- 238000007306 functionalization reaction Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 230000002178 gastroprotective effect Effects 0.000 description 1
- 229960003627 gemfibrozil Drugs 0.000 description 1
- 229960000578 gemtuzumab Drugs 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 230000007614 genetic variation Effects 0.000 description 1
- 230000001434 glomerular Effects 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 229940097043 glucuronic acid Drugs 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 108091005995 glycated hemoglobin Proteins 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 239000003572 glycogen synthase kinase 3 inhibitor Substances 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 210000000224 granular leucocyte Anatomy 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 238000001631 haemodialysis Methods 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 125000000262 haloalkenyl group Chemical group 0.000 description 1
- 125000000232 haloalkynyl group Chemical group 0.000 description 1
- 230000009931 harmful effect Effects 0.000 description 1
- 208000018578 heart valve disease Diseases 0.000 description 1
- 230000000322 hemodialysis Effects 0.000 description 1
- 230000000004 hemodynamic effect Effects 0.000 description 1
- 230000002008 hemorrhagic effect Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 239000002554 heparinoid Substances 0.000 description 1
- 229940025770 heparinoids Drugs 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 102000043957 human ALOX5AP Human genes 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 229920001600 hydrophobic polymer Polymers 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000002390 hyperplastic effect Effects 0.000 description 1
- 208000022098 hypersensitivity pneumonitis Diseases 0.000 description 1
- 230000001969 hypertrophic effect Effects 0.000 description 1
- 230000007954 hypoxia Effects 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 125000002140 imidazol-4-yl group Chemical group [H]N1C([H])=NC([*])=C1[H] 0.000 description 1
- 125000000336 imidazol-5-yl group Chemical group [H]N1C([H])=NC([H])=C1[*] 0.000 description 1
- 125000002636 imidazolinyl group Chemical group 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 208000036971 interstitial lung disease 2 Diseases 0.000 description 1
- 208000021600 intervertebral disc degenerative disease Diseases 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000007914 intraventricular administration Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229960002198 irbesartan Drugs 0.000 description 1
- YCPOHTHPUREGFM-UHFFFAOYSA-N irbesartan Chemical compound O=C1N(CC=2C=CC(=CC=2)C=2C(=CC=CC=2)C=2[N]N=NN=2)C(CCCC)=NC21CCCC2 YCPOHTHPUREGFM-UHFFFAOYSA-N 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 125000001261 isocyanato group Chemical group *N=C=O 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- 125000001810 isothiocyanato group Chemical group *N=C=S 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 239000008274 jelly Substances 0.000 description 1
- 210000001503 joint Anatomy 0.000 description 1
- 208000017169 kidney disease Diseases 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 229960001632 labetalol Drugs 0.000 description 1
- 239000004922 lacquer Substances 0.000 description 1
- 210000000867 larynx Anatomy 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- UFPQIRYSPUYQHK-WAQVJNLQSA-N leukotriene A4 Chemical compound CCCCC\C=C/C\C=C/C=C/C=C/[C@@H]1O[C@H]1CCCC(O)=O UFPQIRYSPUYQHK-WAQVJNLQSA-N 0.000 description 1
- 239000003913 leukotriene B4 receptor antagonist Substances 0.000 description 1
- GWNVDXQDILPJIG-NXOLIXFESA-N leukotriene C4 Chemical compound CCCCC\C=C/C\C=C/C=C/C=C/[C@H]([C@@H](O)CCCC(O)=O)SC[C@@H](C(=O)NCC(O)=O)NC(=O)CC[C@H](N)C(O)=O GWNVDXQDILPJIG-NXOLIXFESA-N 0.000 description 1
- YEESKJGWJFYOOK-IJHYULJSSA-N leukotriene D4 Chemical compound CCCCC\C=C/C\C=C/C=C/C=C/[C@H]([C@@H](O)CCCC(O)=O)SC[C@H](N)C(=O)NCC(O)=O YEESKJGWJFYOOK-IJHYULJSSA-N 0.000 description 1
- 102000003835 leukotriene receptors Human genes 0.000 description 1
- 108090000146 leukotriene receptors Proteins 0.000 description 1
- 239000000865 liniment Substances 0.000 description 1
- 230000002248 lipoperoxidative effect Effects 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000008338 local blood flow Effects 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 229940063718 lodine Drugs 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical class ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 description 1
- 229960004961 mechlorethamine Drugs 0.000 description 1
- 229940064748 medrol Drugs 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- BUGYDGFZZOZRHP-UHFFFAOYSA-N memantine Chemical compound C1C(C2)CC3(C)CC1(C)CC2(N)C3 BUGYDGFZZOZRHP-UHFFFAOYSA-N 0.000 description 1
- 229960004640 memantine Drugs 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 238000006241 metabolic reaction Methods 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- IZXGZAJMDLJLMF-UHFFFAOYSA-N methylaminomethanol Chemical compound CNCO IZXGZAJMDLJLMF-UHFFFAOYSA-N 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 229960002237 metoprolol Drugs 0.000 description 1
- IUBSYMUCCVWXPE-UHFFFAOYSA-N metoprolol Chemical compound COCCC1=CC=C(OCC(O)CNC(C)C)C=C1 IUBSYMUCCVWXPE-UHFFFAOYSA-N 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 230000003228 microsomal effect Effects 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000003595 mist Substances 0.000 description 1
- 239000002829 mitogen activated protein kinase inhibitor Substances 0.000 description 1
- 229940112801 mobic Drugs 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 1
- 230000003232 mucoadhesive effect Effects 0.000 description 1
- 208000001725 mucocutaneous lymph node syndrome Diseases 0.000 description 1
- 230000009854 mucosal lesion Effects 0.000 description 1
- 108010066052 multidrug resistance-associated protein 1 Proteins 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N n-hexanoic acid Natural products CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- VWPOSFSPZNDTMJ-UCWKZMIHSA-N nadolol Chemical compound C1[C@@H](O)[C@@H](O)CC2=C1C=CC=C2OCC(O)CNC(C)(C)C VWPOSFSPZNDTMJ-UCWKZMIHSA-N 0.000 description 1
- 229960004255 nadolol Drugs 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 230000001338 necrotic effect Effects 0.000 description 1
- 230000001613 neoplastic effect Effects 0.000 description 1
- 230000007383 nerve stimulation Effects 0.000 description 1
- 208000004296 neuralgia Diseases 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 208000021722 neuropathic pain Diseases 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 239000004090 neuroprotective agent Substances 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 229960003512 nicotinic acid Drugs 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- HYIMSNHJOBLJNT-UHFFFAOYSA-N nifedipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1[N+]([O-])=O HYIMSNHJOBLJNT-UHFFFAOYSA-N 0.000 description 1
- 229960001597 nifedipine Drugs 0.000 description 1
- 210000002445 nipple Anatomy 0.000 description 1
- 239000000236 nitric oxide synthase inhibitor Substances 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- PULGYDLMFSFVBL-SMFNREODSA-N nociceptin Chemical compound C([C@@H](C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O)[C@@H](C)O)NC(=O)CNC(=O)CNC(=O)[C@@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 PULGYDLMFSFVBL-SMFNREODSA-N 0.000 description 1
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229920004905 octoxynol-10 Polymers 0.000 description 1
- 229920004914 octoxynol-40 Polymers 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 229920001542 oligosaccharide Polymers 0.000 description 1
- 150000002482 oligosaccharides Chemical class 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 1
- 230000001599 osteoclastic effect Effects 0.000 description 1
- 208000005368 osteomalacia Diseases 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- SXCHDDWMFBETRA-UHFFFAOYSA-N oxazinan-3-one Chemical compound O=C1CCCON1 SXCHDDWMFBETRA-UHFFFAOYSA-N 0.000 description 1
- 125000003551 oxepanyl group Chemical group 0.000 description 1
- 125000003566 oxetanyl group Chemical group 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 150000002924 oxiranes Chemical class 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- SHZKQBHERIJWAO-AATRIKPKSA-N ozagrel Chemical compound C1=CC(/C=C/C(=O)O)=CC=C1CN1C=NC=C1 SHZKQBHERIJWAO-AATRIKPKSA-N 0.000 description 1
- 229950003837 ozagrel Drugs 0.000 description 1
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 1
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 1
- 239000006179 pH buffering agent Substances 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000001991 pathophysiological effect Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 208000022719 perennial allergic rhinitis Diseases 0.000 description 1
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 208000030613 peripheral artery disease Diseases 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 210000001428 peripheral nervous system Anatomy 0.000 description 1
- 108091008725 peroxisome proliferator-activated receptors alpha Proteins 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 210000003800 pharynx Anatomy 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 229960004838 phosphoric acid Drugs 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- VSAISIQCTGDGPU-UHFFFAOYSA-N phosphorus trioxide Inorganic materials O1P(O2)OP3OP1OP2O3 VSAISIQCTGDGPU-UHFFFAOYSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- JZQKKSLKJUAGIC-UHFFFAOYSA-N pindolol Chemical compound CC(C)NCC(O)COC1=CC=CC2=C1C=CN2 JZQKKSLKJUAGIC-UHFFFAOYSA-N 0.000 description 1
- 229960002508 pindolol Drugs 0.000 description 1
- 229960005095 pioglitazone Drugs 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 229960002797 pitavastatin Drugs 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229950005134 polycarbophil Drugs 0.000 description 1
- 229940068918 polyethylene glycol 400 Drugs 0.000 description 1
- 229920000151 polyglycol Polymers 0.000 description 1
- 239000010695 polyglycol Substances 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 229940068977 polysorbate 20 Drugs 0.000 description 1
- 235000020777 polyunsaturated fatty acids Nutrition 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- WSHYKIAQCMIPTB-UHFFFAOYSA-M potassium;2-oxo-3-(3-oxo-1-phenylbutyl)chromen-4-olate Chemical compound [K+].[O-]C=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 WSHYKIAQCMIPTB-UHFFFAOYSA-M 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 229940116317 potato starch Drugs 0.000 description 1
- 229940069328 povidone Drugs 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- FYPMFJGVHOHGLL-UHFFFAOYSA-N probucol Chemical compound C=1C(C(C)(C)C)=C(O)C(C(C)(C)C)=CC=1SC(C)(C)SC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FYPMFJGVHOHGLL-UHFFFAOYSA-N 0.000 description 1
- 229960003912 probucol Drugs 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 229960003712 propranolol Drugs 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 235000004252 protein component Nutrition 0.000 description 1
- 230000029983 protein stabilization Effects 0.000 description 1
- 210000001147 pulmonary artery Anatomy 0.000 description 1
- 201000009732 pulmonary eosinophilia Diseases 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 1
- 125000002755 pyrazolinyl group Chemical group 0.000 description 1
- RADKZDMFGJYCBB-UHFFFAOYSA-N pyridoxal hydrochloride Natural products CC1=NC=C(CO)C(C=O)=C1O RADKZDMFGJYCBB-UHFFFAOYSA-N 0.000 description 1
- 235000008160 pyridoxine Nutrition 0.000 description 1
- 239000011677 pyridoxine Substances 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000006340 racemization Effects 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 208000002574 reactive arthritis Diseases 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 239000003087 receptor blocking agent Substances 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 238000007894 restriction fragment length polymorphism technique Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 230000000552 rheumatic effect Effects 0.000 description 1
- 239000003590 rho kinase inhibitor Substances 0.000 description 1
- 229940100486 rice starch Drugs 0.000 description 1
- GLLPUTYLZIKEGF-HAVVHWLPSA-N ridogrel Chemical compound C=1C=CC(C(F)(F)F)=CC=1C(=N/OCCCCC(=O)O)\C1=CC=CN=C1 GLLPUTYLZIKEGF-HAVVHWLPSA-N 0.000 description 1
- 229950006674 ridogrel Drugs 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 230000036185 rubor Effects 0.000 description 1
- CSYSULGPHGCBQD-UHFFFAOYSA-N s-ethylisothiouronium diethylphosphate Chemical compound CCSC(N)=N.CCOP(O)(=O)OCC CSYSULGPHGCBQD-UHFFFAOYSA-N 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 230000002784 sclerotic effect Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000000849 selective androgen receptor modulator Substances 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 208000012201 sexual and gender identity disease Diseases 0.000 description 1
- 208000015891 sexual disease Diseases 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- DRNXZGJGRSUXHW-UHFFFAOYSA-N silyl carbamate Chemical compound NC(=O)O[SiH3] DRNXZGJGRSUXHW-UHFFFAOYSA-N 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 229940125794 sodium channel blocker Drugs 0.000 description 1
- 239000003195 sodium channel blocking agent Substances 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 239000001540 sodium lactate Substances 0.000 description 1
- 235000011088 sodium lactate Nutrition 0.000 description 1
- 229940005581 sodium lactate Drugs 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- YWAFNFGRBBBSPD-OCMLZEEQSA-M sodium;[[(2r,3s,4r,5r)-5-(4-amino-2-oxopyrimidin-1-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-oxidophosphoryl] 2-(trimethylazaniumyl)ethyl phosphate Chemical compound [Na+].O[C@@H]1[C@H](O)[C@@H](COP([O-])(=O)OP([O-])(=O)OCC[N+](C)(C)C)O[C@H]1N1C(=O)N=C(N)C=C1 YWAFNFGRBBBSPD-OCMLZEEQSA-M 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 239000012439 solid excipient Substances 0.000 description 1
- 239000008137 solubility enhancer Substances 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 208000024794 sputum Diseases 0.000 description 1
- 210000003802 sputum Anatomy 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 1
- LZOZLBFZGFLFBV-UHFFFAOYSA-N sulfene Chemical compound C=S(=O)=O LZOZLBFZGFLFBV-UHFFFAOYSA-N 0.000 description 1
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- DHCDFWKWKRSZHF-UHFFFAOYSA-N sulfurothioic S-acid Chemical compound OS(O)(=O)=S DHCDFWKWKRSZHF-UHFFFAOYSA-N 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000002511 suppository base Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229960005187 telmisartan Drugs 0.000 description 1
- 206010043207 temporal arteritis Diseases 0.000 description 1
- ILMRJRBKQSSXGY-UHFFFAOYSA-N tert-butyl(dimethyl)silicon Chemical group C[Si](C)C(C)(C)C ILMRJRBKQSSXGY-UHFFFAOYSA-N 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000005958 tetrahydrothienyl group Chemical group 0.000 description 1
- 125000004632 tetrahydrothiopyranyl group Chemical group S1C(CCCC1)* 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 125000005308 thiazepinyl group Chemical group S1N=C(C=CC=C1)* 0.000 description 1
- 150000001467 thiazolidinediones Chemical class 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 125000001583 thiepanyl group Chemical group 0.000 description 1
- 125000002053 thietanyl group Chemical group 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 1
- 125000000858 thiocyanato group Chemical group *SC#N 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- 229960004906 thiomersal Drugs 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- IBBLKSWSCDAPIF-UHFFFAOYSA-N thiopyran Chemical compound S1C=CC=C=C1 IBBLKSWSCDAPIF-UHFFFAOYSA-N 0.000 description 1
- 239000003868 thrombin inhibitor Substances 0.000 description 1
- RZWIIPASKMUIAC-VQTJNVASSA-N thromboxane Chemical compound CCCCCCCC[C@H]1OCCC[C@@H]1CCCCCCC RZWIIPASKMUIAC-VQTJNVASSA-N 0.000 description 1
- 229940107955 thymoglobulin Drugs 0.000 description 1
- 229960002175 thyroglobulin Drugs 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 229960004605 timolol Drugs 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- 231100000167 toxic agent Toxicity 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 210000003437 trachea Anatomy 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 229950005135 traxoprodil Drugs 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 229940029284 trichlorofluoromethane Drugs 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- BSVBQGMMJUBVOD-UHFFFAOYSA-N trisodium borate Chemical compound [Na+].[Na+].[Na+].[O-]B([O-])[O-] BSVBQGMMJUBVOD-UHFFFAOYSA-N 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- GXPHKUHSUJUWKP-UHFFFAOYSA-N troglitazone Chemical compound C1CC=2C(C)=C(O)C(C)=C(C)C=2OC1(C)COC(C=C1)=CC=C1CC1SC(=O)NC1=O GXPHKUHSUJUWKP-UHFFFAOYSA-N 0.000 description 1
- 229960001641 troglitazone Drugs 0.000 description 1
- GXPHKUHSUJUWKP-NTKDMRAZSA-N troglitazone Natural products C([C@@]1(OC=2C(C)=C(C(=C(C)C=2CC1)O)C)C)OC(C=C1)=CC=C1C[C@H]1SC(=O)NC1=O GXPHKUHSUJUWKP-NTKDMRAZSA-N 0.000 description 1
- 229960000281 trometamol Drugs 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 125000004417 unsaturated alkyl group Chemical group 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 230000036325 urinary excretion Effects 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 229960004699 valsartan Drugs 0.000 description 1
- SJSNUMAYCRRIOM-QFIPXVFZSA-N valsartan Chemical compound C1=CC(CN(C(=O)CCCC)[C@@H](C(C)C)C(O)=O)=CC=C1C1=CC=CC=C1C1=NN=N[N]1 SJSNUMAYCRRIOM-QFIPXVFZSA-N 0.000 description 1
- 230000006496 vascular abnormality Effects 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
- 230000004218 vascular function Effects 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 239000005526 vasoconstrictor agent Substances 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 235000019163 vitamin B12 Nutrition 0.000 description 1
- 239000011715 vitamin B12 Substances 0.000 description 1
- 235000019158 vitamin B6 Nutrition 0.000 description 1
- 239000011726 vitamin B6 Substances 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
- 229920003176 water-insoluble polymer Polymers 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 229940100445 wheat starch Drugs 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- OENHQHLEOONYIE-JLTXGRSLSA-N β-Carotene Chemical compound CC=1CCCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OENHQHLEOONYIE-JLTXGRSLSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/10—Drugs for disorders of the urinary system of the bladder
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/02—Non-specific cardiovascular stimulants, e.g. drugs for syncope, antihypotensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/06—Antiarrhythmics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biomedical Technology (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Pulmonology (AREA)
- Dermatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Immunology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Vascular Medicine (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Oncology (AREA)
- Otolaryngology (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Ophthalmology & Optometry (AREA)
- Toxicology (AREA)
- Obesity (AREA)
- Psychology (AREA)
- Diabetes (AREA)
Description
Zは、[C(R1)2]m[C(R2)2]n、[C(R2)2]n[C(R1)2]mO、O[C(R1)2]m[C(R2)2]n、[C(R2)2]nO[C(R1)2]n、または[C(R1)2]nO[C(R2)2]nから選択され、各R1は、独立に、H、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR1が結合してカルボニル(=O)を形成してもよく、各R2は、独立に、H、OH、OMe、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR2が結合してカルボニル(=O)を形成してもよく、mは0、1、または2であり、各nは、独立に0、1、2、または3であり、
Yは、Hまたは-(置換もしくは非置換のアリール)または-(置換もしくは非置換のヘテロアリール)であり、YまたはZ上の各置換基は(LsRs)jであり、各Lsは、独立に、結合、-O-、-C(=O)-、-S-、-S(=O)-、-S(=O)2-、-NHC(O)-、-C(O)NH-、S(=O)2NH-、-NHS(=O)2、-OC(O)NH-、-NHC(O)O-、-OC(O)O-、-NHC(O)NH-、-C(O)O-、-OC(O)-、置換もしくは非置換のC1〜C6アルキル、C2〜C6アルケニル、-C1〜C6フルオロアルキル、置換もしくは非置換のヘテロアリール、置換もしくは非置換のアリール、または置換もしくは非置換の複素環から選択され、各Rsは、独立に、H、ハロゲン、-N(R4)2、-CN、-NO2、N3、-S(=O)2NH2、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、-C1〜C6フルオロアルキル、置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のヘテロアルキルから選択され、jは、0、1、2、3、または4であり、
R6は、H、L2-(置換もしくは非置換のアルキル)、L2-(置換もしくは非置換のシクロアルキル)、L2-(置換もしくは非置換のアルケニル)、L2-(置換もしくは非置換のシクロアルケニル)、L2-(置換もしくは非置換の複素環)、L2-(置換もしくは非置換のヘテロアリール)、またはL2-(置換もしくは非置換のアリール)であり、L2は、結合、O、S、-S(=O)、-S(=O)2、C(O)、-CH(OH)、-(置換もしくは非置換のC1〜C6アルキル)、または-(置換もしくは非置換のC2〜C6アルケニル)であり、
R7は、L3-X-L4-G1であり、
L3は置換もしくは非置換のアルキルであり、
Xは、結合、O、-C(=O)、-CR9(OR9)、S、-S(=O)、-S(=O)2、-NR9、-NR9C(O)、-C(O)NR9、-NR9C(O)NR9-であり、
L4は、結合、または置換もしくは非置換のアルキルであり、
G1は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、-OR9、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-OC(O)O-、-NHC(O)NH-、-NHC(O)O、-O(O)CNH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG1は、W-G5であり、Wは、置換もしくは非置換のアリール、置換もしくは非置換の複素環、または置換もしくは非置換のヘテロアリールであり、G5は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8であり、
各R8は、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニル、または置換もしくは非置換のベンジルから選択され、
各R9は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニル、または置換もしくは非置換のベンジルから選択され、あるいは2つのR9基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR8およびR9が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R10は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
R5は、H、ハロゲン、置換もしくは非置換のC1〜C6アルキル、置換もしくは非置換のO-C1〜C6アルキルであり、
R11は、L7-L10-G6であり、L7は、結合、-C(O)、-C(O)NH、-NHC(O)、または(置換もしくは非置換のC1〜C6アルキル)であり、L10は、結合、(置換もしくは非置換のアルキル)、(置換もしくは非置換のシクロアルキル)、(置換もしくは非置換のヘテロアリール)、(置換もしくは非置換のアリール)、または(置換もしくは非置換の複素環)であり、
G6は、OR9、-C(=O)R9、-C(=O)OR9、-SR8、-S(=O)R8、-S(=O)2R8、N(R9)2、テトラゾリル、-NHS(=O)2R8、-S(=O)2N(R9)2、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、-C(=O)N(R9)2、NR9C(O)R9、C(R9)2C(=O)N(R9)2-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいは、G6は、W-G7であり、Wは、(置換もしくは非置換の複素環)、(置換もしくは非置換のアリール)、または(置換もしくは非置換のヘテロアリール)であり、G7は、H、ハロゲン、CN、NO2、N3、CF3、OCF3、C1〜C6アルキル、C3〜C6シクロアルキル、-C1〜C6フルオロアルキル、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアルキル)、-L5-(置換もしくは非置換のヘテロアリール)、-L5-(置換もしくは非置換の複素環)、または-L5-(置換もしくは非置換のアリール)であり、L5は、結合、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、ただし、R11は、少なくとも1つの(非置換もしくは置換の)芳香族部分、および少なくとも1つの(非置換もしくは置換の)環状部分を含み、(非置換もしくは置換の)環状部分は、(非置換もしくは置換の)複素環基または(非置換もしくは置換の)ヘテロアリール基であり、R11は、チエニル-フェニル基ではなく、
R12は、H、(置換もしくは非置換のC1〜C6アルキル)、(置換もしくは非置換のC3〜C6シクロアルキル)である]、
あるいはその活性代謝物、または溶媒和物、または医薬として許容可能な塩、または医薬として許容可能なプロドラッグ。
]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-78);3-[3-tert-ブチルスルファニル-1-[4-(3-フルオロ-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-82);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(3-フルオロ-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-84);3-[3-tert-ブチルスルファニル-1-[4-(3-フルオロ-ピリジン-2-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-85);3-[3-tert-ブチルスルファニル-1-[4-(5-カルバモイル-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-87);3-[3-tert-ブチルスルファニル-1-[4-(5-シアノ-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-88);3-[3-tert-ブチルスルファニル-1-[4-(5-メトキシ-チアゾール-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-89);3-[3-tert-ブチルスルファニル-1-[4-(6-メチル-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-90);3-{3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-91);3-[3-tert-ブチルスルファニル-1-[4-(2-エトキシ-チアゾール-4-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-92);3-[3-tert-ブチルスルファニル-1-[4-(4-メチル-1H-イミダゾール-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-93);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-94);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-95);3-[3-tert-ブチルスルファニル-1-[4-(5-メトキシ-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-96);3-[3-tert-ブチルスルファニル-1-[4-(6-カルバモイル-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-97);3-[3-tert-ブチルスルファニル-1-[4-(5-メチル-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-98);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-99);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(6-メトキシ-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-100);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(6-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-101);3-{3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-102);3-{3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-103);3-{3-tert-ブチルスルファニル-5-(6-シクロプロピル-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-104);3-[3-tert-ブチルスルファニル-1-[4-(5-メチル-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-105);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-106);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-107);3-{3-tert-ブチルスルファニル-5-(5-クロロ-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-108);3-{3-tert-ブチルスルファニル-5-((S)-1-ピリジン-2-イル-エトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-109);3-{3-tert-ブチルスルファニル-5-((R)-1-ピリジン-2-イル-エトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-110);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-((S)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-111);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-112);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-5-((S)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-113);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-114);3-[3-tert-ブチルスルファニル-1-[4-(2-エトキシ-チアゾール-4-イル)-ベンジル]-5-((S)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-115);3-[3-tert-ブチルスルファニル-1-[4-(2-エトキシ-チアゾール-4-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-116);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(3-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-117);3-{3-tert-ブチルスルファニル-5-(3-メチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-118);3-{3-tert-ブチルスルファニル-5-(3,5-ジメチル-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-119);3-{3-tert-ブチルスルファニル-5-(3,5-ジメチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-120);3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-121);3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-tert-ブチルスルファニル-1-[4-(5-メトキシ-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-122);3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-シクロブタンカルボニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-123);3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-シクロブチルメチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-124);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-125);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-エチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-126);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-127);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-128);3-[3-tert-ブチルスルファニル-1-[4-(2-エトキシ-チアゾール-4-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-129);3-[3-tert-ブチルスルファニル-1-[4-(2-メトキシ-チアゾール-4-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-130);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-131);3-[3-シクロブチルメチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-132);3-[3-シクロブチルメチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-133);3-[3-イソブチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-134);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-135);3-{3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-136);3-{3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-137);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-138);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-139);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-140);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-141);3-[3-tert-ブチルスルファニル-1-[4-(2-エトキシ-チアゾール-4-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-142);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン
酸(化合物2-143);3-{3-tert-ブチルスルファニル-5-(7-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-144);3-{3-tert-ブチルスルファニル-5-(7-フルオロ-キノリン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-145);3-{3-tert-ブチルスルファニル-5-(7-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-146);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(7-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-147);3-[3-tert-ブチルスルファニル-1-[4-(3-フルオロ-ピリジン-2-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-148);3-{3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-[4-(3-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-149);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(3-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-150);3-{3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-[4-(3-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-151);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(3-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-156);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(3-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-157);3-{3-tert-ブチルスルファニル-5-(3-メチル-ピリジン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-158);3-{3-tert-ブチルスルファニル-5-(3,5-ジメチル-ピリジン-2-イルメトキシ)-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-159);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(4-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-160);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(4-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-161);3-{3-tert-ブチルスルファニル-5-(4-メチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-162);3-{3-シクロブチルメチル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-163);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-164);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-165);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(6-メチル-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-166);3-{3-tert-ブチルスルファニル-5-(6-メチル-キノリン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-167);3-[3-tert-ブチルスルファニル-1-[4-(6-メチル-ピリダジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-168);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリダジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-169);3-[3-イソブチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-170);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-171);3-[1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-3-(2-メチル-プロパン-2-スルホニル)-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-172);3-[1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-3-(2-メチル-プロパン-2-スルフィニル)-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-173);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(1-オキシ-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-174);3-{3-tert-ブチルスルファニル-5-(イミダゾ[1,2-a]ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-175);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(イミダゾ[1,2-a]ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-176);3-{3-tert-ブチルスルファニル-5-(イミダゾ[1,2-a]ピリジン-2-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-177);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-178);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メチル-ピリダジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-179);3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-イソオキサゾール-3-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-180);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-イソオキサゾール-3-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-181);3-{3-tert-ブチルスルファニル-5-(5-メチル-イソオキサゾール-3-イルメトキシ)-1-[4-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-182);3-{3-tert-ブチルスルファニル-5-(2,5-ジメチル-2H-ピラゾール-3-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-183);3-{3-tert-ブチルスルファニル-5-(1,5-ジメチル-1H-ピラゾール-3-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-184);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリダジン-3-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-185);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリダジン-3-イル)-ベンジル]-5-(5-エチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-186);3-{3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-187);3-[3-tert-ブチルスルファニル-1-[4-(5-フルオロ-ピリジン-2-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-188);3-[3-tert-ブチルスルファニル-1-[4-(5-フルオロ-ピリジン-2-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-189);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-2-イル)-ベンジル]-5-(6-フルオロ-キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-190);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-2-イル)-ベンジル]-5-((R)-1-ピリジン-2-イル-エトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-191);3-[3-tert-ブチルスルファニル-1-[4-(5-フルオロ-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-192);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-193);3-{5-(6-フルオロ-キノリン-2-イルメトキシ)-3-イソブチル-1-[4-(6-トリフルオロメチル-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-194);3-{3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1-[3-(5-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-195);3-[3-tert-ブチルスルファニル-1-[3-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-196);3-[3-tert-ブチルスルファニル-1-[4-(5-フルオロ-ピリジン-2-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-197);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-2-イル)-ベンジル]-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-198);3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-199);3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-200);3-[3-tert-ブチルスルファニル-1-[4-(5-フルオロ-ピリジン-2-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-201);3-{3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-202);3-{3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-203);3-{3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1-[4-(6-トリフルオロメチル-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-204);3-[3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-(4-チアゾール-2-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-205);3-[3-tert-ブチルスルファニル-1-[3-(4-メトキシ-テトラヒドロ-ピラン-4-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-206);3-[
3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-(4-ピリジン-2-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-207);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-ピリジン-3-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-208);3-[3-tert-ブチルスルファニル-1-(4-ピリジン-3-イル-ベンジル)-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-209);3-[3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-(4-ピリジン-3-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-210);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-ピリジン-2-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-211);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-ピリジン-2-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-212);3-[3-tert-ブチルスルファニル-1-(4-ピリジン-2-イル-ベンジル)-5-(キノリン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-213);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-ピリジン-3-イル-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-214);3-[3-tert-ブチルスルファニル-1-[4-(4-メトキシ-ピリジン-2-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-215);3-[3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-(4-(3-メトキシピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-216);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-(3-メトキシピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-217);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-(3-メトキシピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-218);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-(4-トリフルオロメチルピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-219);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-(4-トリフルオロメチルピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-220);3-[3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-(4-(4-トリフルオロメチルピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-221);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-(5-フルオロピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-222);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-(5-フルオロピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-223);3-[3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-(4-(5-フルオロピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-224);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(2-メトキシピリジン-5-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-225);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(3-トリフルオロメチルピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-226);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(4-トリフルオロメチルピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-227);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(3-フルオロピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-228);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(5-フルオロピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-229);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(4-メトキシピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-230);3-[3-tert-ブチルスルファニル-5-(2,3-ジメチル-ピリジン-6-イルメトキシ)-1-(4-(ピリジン-2-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-231);3-[3-tert-ブチルスルファニル-5-(5-メチル-ピリジン-2-イルメトキシ)-1-(4-(2-メトキシ-ピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-232);3-[3-tert-ブチルスルファニル-5-(5-エチル-ピリジン-2-イルメトキシ)-1-(4-(2-メトキシ-ピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-233);3-[3-tert-ブチルスルファニル-5-(キノリン-2-イルメトキシ)-1-(4-(2-メトキシ-ピリジン-3-イル)-ベンジル)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-234);3-[3-tert-ブチルスルファニル-1-(6'-メトキシ-[2,3']ビピリジニル-5-イルメチル)-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物3-1);3-[3-tert-ブチルスルファニル-1-[6-(4-メトキシ-フェニル)-ピリジン-3-イルメチル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物3-2);3-{3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1-[6-(4-トリフルオロメトキシ-フェニル)-ピリジン-3-イルメチル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物3-3);3-[3-tert-ブチルスルファニル-1-[5-(4-メトキシ-フェニル)-ピリジン-2-イルメチル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物3-4);3-{3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1-[5-(4-トリフルオロメトキシ-フェニル)-ピリジン-2-イルメチル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物3-5);3-{3-tert-ブチルスルファニル-5-イソプロピル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物4-1);および3-{3-tert-ブチルスルファニル-5-ヒドロキシ-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物4-2)。
i)少なくとも1種のロイコトリエン関連炎症バイオマーカー、または
ii)ロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答、または
iii)少なくとも1種のロイコトリエン関連炎症バイオマーカーおよびロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答
について患者をモニターすることによって患者を同定することを含む、さらなる実施形態が提供される。さらなるまたは代替の実施形態では、ロイコトリエン関連炎症バイオマーカーは、LTB4、システイニルロイコトリエン、CRP、SAA、MPO、EPO、MCP-1、MIP-α、sICAM、IL-6、IL-4、およびIL-13からなる群から選択され、別のさらなるまたは代替の実施形態では、機能的マーカーの応答は、著しく大きい肺容量である(FEV1)。
i)少なくとも1種のロイコトリエン遺伝子SNPおよび/またはイントロンまたはエキソン位置にSNPを含むハプロタイプについて患者をスクリーニングし、または
ii)少なくとも1種のロイコトリエン関連炎症バイオマーカーについて患者をモニターし、または
iii)ロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答について患者をモニターする
ことによって患者を同定することを含む、さらなる実施形態が提供される。さらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、ロイコトリエン経路遺伝子である。別のさらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、5-リポキシゲナーゼ活性化タンパク質(FLAP)SNPまたはハプロタイプである。さらなるまたは代替の実施形態では、ロイコトリエン関連炎症バイオマーカーは、LTB4、システイニルロイコトリエン、CRP、SAA、MPO、EPO、MCP-1、MIP-α、sICAM、IL-6、IL-4、およびIL-13からなる群から選択され、別のさらなるまたは代替の実施形態では、機能的マーカーの応答は、著しく大きい肺容量である(FEV1)。
i)少なくとも1種のロイコトリエン遺伝子SNPまたはハプロタイプについて患者をスクリーニングすること、
ii)少なくとも1種のロイコトリエン関連炎症バイオマーカーについて患者をモニターすること、
iii)ロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答について患者をモニターすること、
の少なくとも2つによって患者を同定することを含むさらなる実施形態が提供される。さらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、ロイコトリエン経路遺伝子である。別のさらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、5-リポキシゲナーゼ活性化タンパク質(FLAP)SNPまたはハプロタイプである。さらなるまたは代替の実施形態では、ロイコトリエン関連炎症バイオマーカーは、LTB4、システイニルロイコトリエン、CRP、SAA、MPO、EPO、MCP-1、MIP-α、sICAM、IL-6、IL-4、およびIL-13からなる群から選択され、別のさらなるまたは代替の実施形態では、機能的マーカーの応答は、著しく大きい肺容量である(FEV1)。
i)少なくとも1種のロイコトリエン遺伝子SNPまたはハプロタイプについて患者をスクリーニングすること、および
ii)少なくとも1種のロイコトリエン関連炎症バイオマーカーについて患者をモニターすること、および
iii)ロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答について患者をモニターすること、
によって患者を同定することを含むさらなる実施形態が提供される。さらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、ロイコトリエン経路遺伝子である。別のさらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、5-リポキシゲナーゼ活性化タンパク質(FLAP)SNPまたはハプロタイプである。さらなるまたは代替の実施形態では、ロイコトリエン関連炎症バイオマーカーは、LTB4、システイニルロイコトリエン、CRP、SAA、MPO、EPO、MCP-1、MIP-α、sICAM、IL-6、IL-4、およびIL-13からなる群から選択され、別のさらなるまたは代替の実施形態では、機能的マーカーの応答は、著しく大きい肺容量である(FEV1)。
i)少なくとも1種のロイコトリエン遺伝子SNPまたはハプロタイプについて患者をスクリーニングすること、および
ii)少なくとも1種のロイコトリエン関連炎症バイオマーカーについて患者をモニターすること、および
iii)ロイコトリエン修飾薬に対する少なくとも1種の機能的マーカーの応答について患者をモニターすること、
によって得られる情報を使用して同定された患者に、有効量のFLAPモジュレータを投与することを含む、ロイコトリエン依存性またはロイコトリエン媒介性の疾病または状態の防止または治療が提供される。さらなるまたは代替の実施形態では、FLAPモジュレータは、FLAP阻害剤である。さらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、ロイコトリエン経路遺伝子である。別のさらなるまたは代替の実施形態では、ロイコトリエン遺伝子SNPまたはハプロタイプは、5-リポキシゲナーゼ活性化タンパク質(FLAP)SNPまたはハプロタイプである。さらなるまたは代替の実施形態では、ロイコトリエン関連炎症バイオマーカーは、LTB4、システイニルロイコトリエン、CRP、SAA、MPO、EPO、MCP-1、MIP-α、sICAM、IL-6、IL-4、およびIL-13からなる群から選択され、別のさらなるまたは代替の実施形態では、機能的マーカーの応答は、著しく大きい肺容量である(FEV1)。さらなるまたは代替の実施形態では、3つの診断方法から得られた情報は、その情報を分析してFLAPモジュレータを用いた治療を必要とする患者、治療レジメン、および使用するFLAPモジュレータのタイプを同定するアルゴリズムにおいて使用することができる。
別段の記載がない限り、明細書および特許請求の範囲を含み、本出願で使用される以下の用語は、以下に示す意味を有する。本明細書および添付の特許請求の範囲に使用されるように、単数形「a」、「an」、および「the」には、その内容が明確に定められない限り、複数の指示対象が含まれることに留意する必要がある。標準の化学用語の定義は、Carey and Sundberg"ADVANCED ORGANIC CHEMISTRY 4THED."Vols.A(2000) and B(2001),Plenum Press,New Yorkを含む参考文献に見ることができる。別段の指定がない限り、当業者に周知の質量分析、NMR、HPLC、タンパク質化学、生化学、組換えDNA技術、および薬理学の通常の方法が使用される。本明細書では、「または」の使用は、別段指定されない限り「および/または」を意味する。さらに、「含む」ならびに「含めた」および「含まれる」などの他の形の使用は、限定的なものではない。
本明細書では、製剤、組成物、または成分に関する「許容可能な」という用語は、治療を受ける対象の全般的な健康に、持続的に有害な影響を及ぼさないことを意味する。
ロイコトリエン(LT)は、細胞膜からのアラキドン酸の放出、ならびに5-リポキシゲナーゼ、5-リポキシゲナーゼ活性化タンパク質、LTA4分解酵素、およびLTC4シンターゼの作用によるロイコトリエンへの変換によって生成される強力な収縮性および炎症性伝達物質である。ロイコトリエン合成経路、または5-リポキシゲナーゼ経路は、アラキドン酸がロイコトリエンLTB4、またはシステイニルロイコトリエン、LTC4、LTD4、およびLTE4に変換される一連の酵素反応を含む。その経路は主に核膜で生じるものであり、文献に記載されている。例えば、Wood,JW et al,J.Exp.Med.,178:1935-1946,1993;Peters-Golden,Am.J.Respir.Crit.Care Med.157:S227-S232,1998;Drazen,et al.,ed.Five-Lipoxygenase Products in Asthma,Lung Biology in Health and Disease Series,Vol.120,Chs.1,2,and 7,Marcel Dekker,Inc.NY,1998参照。ロイコトリエン合成経路に関与するタンパク質成分には、5-リポキシゲナーゼ(5-LO)、5-リポキシゲナーゼ活性化タンパク質、LTA4分解酵素、およびLTC4シンターゼが含まれる。ロイコトリエンの合成は、例えばSamuelsson等による文献、Science,220,568-575,1983;Peters-Golden,"Cell Biology of the 5-Lipoxygenase Pathway"Am J Respir Crit Care Med 157:S227-S232(1998)に記載されている。ロイコトリエンは、好酸球、好中球、好塩基球、リンパ球、マクロファージ、単球、およびマスト細胞を含む様々な細胞によって、アラキドン酸から直接合成される。例えば活性好中球からの過剰のLTA4は、細胞間経路によって細胞に入ることができる。体内の殆どの細胞は、LTA4分解酵素を有しており、したがってLTB4を生成することができる。血小板および内皮細胞はLTC4シンターゼを有しており、したがって細胞間経路によってLTA4が提供される場合、LTC4を生成することができる。
疾患へのロイコトリエンの関与は、文献に詳説されている。例えば、Busse,Clin.Exp.Allergy 26:868-79,1996;O'Byrne,Chest 111(Supp.2):27S-34S,1977;Sheftell,F.D.,et al.,Headache,40:158-163,2000;Klickstein et al.,J.Clin.Invest.,66:1166-1170,1950;Davidson et al.,Ann.Rheum.Dis.,42:677-679,1983参照。ロイコトリエンは、ヒトの皮膚に著しい炎症反応を生じる。ヒトの疾患へのロイコトリエンの関与についての証拠は、乾癬に見られ、ロイコトリエンは乾癬病巣内で検出されている(Kragballe et al.,Arch.Dermatol.,119:548-552,1983)。
ロイコトリエンは、喘息患者の気道の炎症に寄与することが知られている。モンテルカスト(シングレア(商標))などのCysLT1受容体拮抗薬は、喘息およびアレルギー性鼻炎に有効であることが示されている[Reiss et al.Arch Intern Med 158:1213-1220(1998);Phillip et al.Clin Exp Allergy 32:1020-1028(2002)]。CysLT1R拮抗薬プランルカスト(オノン(商標))およびザフィルルカスト(アコレート(商標))も、喘息に有効であることが示されている。
idonic acid metabolites",Spine.1999 Jan 15;24(2):128-32参照)、脳浮腫および頭部外傷、(xiv)それに限定されるものではないが、膵臓癌および他の固形腫瘍または血管腫瘍を含む癌(例えば、Poff and Balazy,Curr.Drug Targets Inflamm.Allergy,v3,19-33(2004)およびSteele et al,Cancer Epidemiology&Prevention,v8,467-483(1999)参照)、(xv)内毒素性ショックおよび敗血症性ショック(例えば、Leite MS,et al.,"Mechanisms of increased survival after lipopolysaccharide-induced endotoxic shock in mice consuming olive oil-enriched diet",Shock.2005 Feb;23(2):173-8参照)、(xvi)関節リウマチおよび変形性関節炎(例えば、Alten R,et al.,"Inhibition of leukotriene B4-induced CD11B/CD18(Mac-1)expression by BIIL 284,a new long acting LTB4 receptor antagonist,in patients with rheumatoid arthritis",Ann Rheum Dis.2004 Feb;63(2):170-6参照)、(xvii)ほんの一例として、慢性胃炎、好酸球性胃腸炎、および胃の運動機能障害を含むGI疾患の増大の防止(例えば、Gyomber et al,J Gastroenterol Hepatol.,v11,922-927(1996);Quack I et al BMC Gastroenterol v18,24(2005);Cuzzocrea S,et al.,"5-Lypoxygenase modulates colitis through the regulation of adhesion molecule expression and neutrophil migration",Lab Invest.2005 Jun;85(6):808-22参照)、(xviii)ほんの一例として、糸球体腎炎、シクロスポリンの腎毒性による腎虚血再かん流を含む腎疾患(例えば、Guasch et al Kidney Int.,v56,261-267;Butterly et al,v 57,2586-2593(2000);Guasch A et al."MK-591 acutely restores glomerular size selectivity and reduces proteinuria in human glomerulonephritis",Kidney Int.1999;56:261-7;Butterly DW et al."A role for leukotrienes in cyclosporine nephrotoxicity",Kidney Int.2000;57:2586-93参照)、(xix)急性または慢性腎不全の防止または治療(例えば、Maccarrone M,et al.,"Activation of 5-lypoxygenase and related cell membrane lipoperoxidation in hemodialysis patients",J Am Soc Nephrol.1999;10:1991-6参照)、(xx)II型糖尿病(例えば、Valdivielso et al,v16,85-94(2003)参照)、(xxi)腎臓の急性腎盂腎炎などの、1つまたは複数の固形臓器または組織内の急性感染症の炎症態様の低減(例えば、Tardif M,et al.,L-651,392,"A potent leukotriene inhibitor,controls inflammatory process in Escherichia coli pyelonephritis",Antimicrob Agents Chemother.1994 Jul;38(7):1555-60参照)、(xxii)好酸球の動員または活性化を伴う急性または慢性障害の防止または治療(例えば、Quack I,et al."Eosinophilic gastroenteritis in a young girl-long term remission under monteluka
st",BMC Gastroenterol.,2005;5:24参照)、(xxiii)非ステロイド系抗炎症薬(選択的または非選択的シクロオキシゲナーゼ-1または-2阻害剤を含む)によって生じる消化管の急性または慢性びらん性疾患または運動機能障害の防止または治療(例えば、Marusova IB,et al.,"Potential gastroprotective effect of a CysLT1 receptor blocker sodium montelukast in aspirin-induced lesions of the rat stomach mucosa",Eksp Klin Farmakol,2002;65:16-8およびGyomber E,et al.,"Effect of lypoxygenase inhibitors and leukotriene antagonists on acute and chronic gastric haemorrhagic mucosal lesions in ulcer models in the rat",J.Gastroenterol.Hepatol.,1996,11,922-7)およびMartin St et al.,"Gastric motor dysfunction: is eosinophilic mural gastritis a causative factor?",Eur J Gastroenterol.Hepatol.,2005,17:983-6参照)、(xxiv)II型糖尿病の治療(例えば、Valdivielso JM,et al.,"Inhibition of 5-lypoxygenase activating protein decreases proteinuria in diabetic rats",J Nephrol.2003 Jan-Feb;16(1):85-94;Parlapiano C,et al.,"The relationship between glycated hemoglobin and polymorphonuclear leukocyte leukotriene B4 release in people with diabetes mellitus",Diabetes Res Clin Pract.1999 Oct;46(1):43-5参照)、(xxv)ほんの一例として、家族性地中海熱を含む代謝性症候群の治療(例えば、Bentancur AG,et al.,"Urine leukotriene B4 in familial Mediterranean fever",Clin Exp Rheumatol.2004 Jul-Aug;22(4 Suppl 34):S56-8参照)、ならびに(xxvi)肝腎症候群の治療(例えば、Capella GL.,"Anti-leukotriene drugs in the prevention and treatment of hepatorenal syndrome",Prostaglandins Leukot Essent Fatty Acids.2003 Apr;68(4):263-5参照)。
単独でも他の薬剤との組合せでも有効であり、マイナスの副作用が最小限に抑えられた新規FLAP阻害剤の開発および試験は、ロイコトリエン依存性またはロイコトリエン媒介性の疾病または状態の治療にとって有益となるはずである。本明細書に記載のロイコトリエン合成経路の阻害剤は、ロイコトリエンの形成を防止または低減する経路のいずれかのステップを標的にすることができる。このようなロイコトリエン合成阻害剤は、例えば、FLAPまたは5-LOのレベルで阻害することができ、したがって、ロイコトリエン経路における様々な生成物の形成を最小限に抑え、それによって細胞内で利用可能なこのような化合物の量が低減される。ロイコトリエン合成阻害剤は、ロイコトリエン合成経路におけるそれらのタンパク質結合能に基づいて同定することができる。例えば、FLAP阻害剤は、FLAPへのそれらの結合性に基づいて同定することができる。
式(G)、式(G-I)、および式(G-II)の化合物
式(G)、式(G-I)、および式(G-II)の化合物、それらの医薬として許容可能な塩、医薬として許容可能なN-オキシド、医薬として活性な代謝物、医薬として許容可能なプロドラッグ、および医薬として許容可能な溶媒和物は、FLAPを拮抗または阻害し、それに限定されるものではないが、喘息、心筋梗塞、癌、および炎症状態を含むロイコトリエン依存性またはロイコトリエン媒介性の状態または疾患に罹患している患者を治療するために使用することができる。
Zは、N(R1)、S(O)m、CR1=CR1、-C≡C-、C(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2O、OC(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2S(O)m、S(O)mC(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2NR1、NR1C(R1)2[C(R2)2]n、[C(R2)2]nO[C(R1)2]n、[C(R1)2]nO[C(R2)2]n、-C(O)NR2-、-NR2C(O)-、-NR2C(O)O-、-OC(O)NR2-、-S(O)2NR2-、-CR1=N-N-、NR2C(O)NR2-、-OC(O)O-、S(O)2NR2、または-NR2S(O)2-から選択され、各R1は、独立に、H、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR1が結合してカルボニル(=O)を形成してもよく、各R2は、独立に、H、OH、OMe、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR2が結合してカルボニル(=O)を形成してもよく、mは0、1、または2であり、各nは、独立に0、1、2、または3であり、
Yは、-L1-(置換もしくは非置換のアリール)、-L1-(置換もしくは非置換のヘテロアリール)、-L1-(置換もしくは非置換の非芳香族複素環)であり、ただしヘテロ原子がZに直接結合する場合、非芳香族複素環は置換されており、L1は、結合、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換の複素環、置換もしくは非置換のヘテロアリール、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のアリール、-C(O)、C(R8)(OH)、C(R8)(OMe)、C(=NOH)、C(=NOR4b)、C(=O)NH、C(=O)NR4b、-NHC(=O)、NR4bC(=O)、S、S(=O)、S(=O)2、-NHC(=O)NH、またはNR4bC(=O)NR4bであり、
YまたはZ上の各置換基は、(LsRs)jであり、各Lsは、独立に、結合、-O-、-C(=O)-、-S-、-S(=O)-、-S(=O)2-、-NHC(O)-、-C(O)NH-、S(=O)2NH-、-NHS(=O)2、-OC(O)NH-、-NHC(O)O-、-OC(O)O-、-NHC(O)NH-、-C(O)O-、-OC(O)-、C1〜C6アルキル、C2〜C6アルケニル、-C1〜C6フルオロアルキル、ヘテロアリール、アリール、または複素環から選択され、各Rsは、独立に、H、ハロゲン、-N(R4)2、-CN、-NO2、N3、-S(=O)2NH2、低級アルキル、低級シクロアルキル、-C1〜C6フルオロアルキル、ヘテロアリール、またはヘテロアルキルから選択され、jは、0、1、2、3、または4であり、
各R3は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
各R3bは、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニルまたはベンジルから選択され、
各R4は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、またはベンジルから選択され、あるいは2つのR4基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR3bおよびR4が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R4bは、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のアリールまたは置換もしくは非置換のベンジル、置換もしくは非置換のヘテロアリール、置換もしくは非置換の複素環から選択され、
R6は、H、L2-(置換もしくは非置換のアルキル)、L2-(置換もしくは非置換のシクロアルキル)、L2-(置換もしくは非置換のアルケニル)、L2-(置換もしくは非置換のシクロアルケニル)、L2-(置換もしくは非置換の複素環)、L2-(置換もしくは非置換のヘテロアリール)、またはL2-(置換もしくは非置換のアリール)であり、L2は、結合、O、S、-S(=O)、-S(=O)2、C(O)、-CH(OH)、-(置換もしくは非置換のC1〜C6アルキル)、または-(置換もしくは非置換のC2〜C6アルケニル)であり、
R7は、L3-X-L4-G1であり、
L3は、結合、または置換もしくは非置換のアルキルであり、
Xは、結合、O、-C(=O)、-CR9(OR9)、S、-S(=O)、-S(=O)2、-NR9、-NR9C(O)、-C(O)NR9、-NR9C(O)NR9-、またはアリールであり、
L4は、結合、または置換もしくは非置換のアルキルであり、
G1は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、-OR9、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-OC(O)O-、-NHC(O)NH-、-NHC(O)O、-O(O)CNH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG1は、W-G5であり、Wは、置換もしくは非置換のアリール、置換もしくは非置換の複素環、または置換もしくは非置換のヘテロアリールであり、G5は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8であり、
各R8は、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、もしくはベンジルから選択され、
各R9は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、もしくはベンジルから選択され、あるいは2つのR9基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR8およびR9が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R10は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
R5は、H、ハロゲン、-N3、-CN、-ONO2、-L6-(置換もしくは非置換のC1〜C6アルキル)、-L6-(置換もしくは非置換のC2〜C6アルケニル)、-L6-(置換もしくは非置換のヘテロアリール)、または-L6-(置換もしくは非置換のアリール)であり、L6は、結合、O、S、-S(=O)、S(=O)2、NH、C(O)、-NHC(O)O、-OC(O)NH、-NHC(O)、-NHC(O)NH-、または-C(O)NHであり、
R11は、L7-L10-G6であり、L7は、結合、-O、-S、-S(=O)、-S(=O)2、-NH、-C(O)、-C(O)NH、-NHC(O)、(置換もしくは非置換のC1〜C6アルキル)、または(置換もしくは非置換のC2〜C6アルケニル)であり、
L10は、結合、(置換もしくは非置換のアルキル)、(置換もしくは非置換のシクロアルキル)、(置換もしくは非置換のシクロアルケニル)、(置換もしくは非置換のヘテロアリール)、(置換もしくは非置換のアリール)、または(置換もしくは非置換の複素環)であり、
G6は、H、CN、SCN、N3、NO2、ハロゲン、OR9、-C(=O)CF3、-C(=O)R9、-C(=O)OR9、-SR8、-S(=O)R8、-S(=O)2R8、N(R9)2、テトラゾリル、-NHS(=O)2R8、-S(=O)2N(R9)2、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、-C(=O)N(R9)2、N R9C(O)R9、C(R9)2C(=O)N(R9)2-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG6は、W-G7であり、Wは、(置換もしくは非置換の複素環)または(置換もしくは非置換のヘテロアリール)であり、G7は、H、ハロゲン、CN、NO2、N3、CF3、OCF3、C1〜C6アルキル、C3〜C6シクロアルキル、-C1〜C6フルオロアルキル、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアルキル)、-L5-(置換もしくは非置換のヘテロアリール)、-L5-(置換もしくは非置換の複素環)、または-L5-(置換もしくは非置換のアリール)であり、L5は、結合、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
ただし、L10が、フェニルまたはチオフェニルであり、Yが、-(置換もしくは非置換のヘテロアリール)、-(置換もしくは非置換のアリール)であり、Zが、[C(R2)2]nC(R1)2Oである場合、G6はW-G7であり、
R12は、H、(置換もしくは非置換のC1〜C6アルキル)、(置換もしくは非置換のC3〜C6シクロアルキル)である]。
Zは、N(R1)、S(O)m、CR1=CR1、-C≡C-、C(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2O、OC(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2S(O)m、S(O)mC(R1)2[C(R2)2]n、[C(R2)2]nC(R1)2NR1、NR1C(R1)2[C(R2)2]n、[C(R2)2]nO[C(R1)2]n、[C(R1)2]nO[C(R2)2]n、-C(O)NR2-、-NR2C(O)-、-NR2C(O)O-、-OC(O)NR2-、-S(O)2NR2-、-CR1=N-N-、NR2C(O)NR2-、-OC(O)O-、S(O)2NR2、または-NR2S(O)2-から選択され、各R1は、独立に、H、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR1が結合してカルボニル(=O)を形成してもよく、各R2は、独立に、H、OH、OMe、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR2が結合してカルボニル(=O)を形成してもよく、mは、0、1、または2であり、各nは、独立に、0、1、2、または3であり、
Yは、-L1-(置換もしくは非置換のアリール)、-L1-(置換もしくは非置換のヘテロアリール)、-L1-(置換もしくは非置換の非芳香族複素環)であり、ただしヘテロ原子がZと直接結合する場合、非芳香族複素環は置換されており、L1は、結合、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換の複素環、置換もしくは非置換のヘテロアリール、置換もしくは非置換のシクロアルキル、または置換もしくは非置換のアリール、-C(O)、C(R8)(OH)、C(R8)(OMe)、C(=NOH)、C(=NOR4b)、C(=O)NH、C(=O)NR4b、-NHC(=O)、NR4bC(=O)、S、S(=O)、S(=O)2、-NHC(=O)NH、またはNR4bC(=O)NR4bであり、
YまたはZ上の各置換基は、(LsRs)jであり、各Lsは、独立に、結合、-O-、-C(=O)-、-S-、-S(=O)-、-S(=O)2-、-NHC(O)-、-C(O)NH-、S(=O)2NH-、-NHS(=O)2、-OC(O)NH-、-NHC(O)O-、-OC(O)O-、-NHC(O)NH-、-C(O)O-、-OC(O)-、C1〜C6アルキル、C2〜C6アルケニル、-C1〜C6フルオロアルキル、ヘテロアリール、アリール、または複素環から選択され、各Rsは、独立に、H、ハロゲン、-N(R4)2、-CN、-NO2、N3、-S(=O)2NH2、低級アルキル、低級シクロアルキル、-C1〜C6フルオロアルキル、ヘテロアリール、またはヘテロアルキルから選択され、jは、0、1、2、3、または4であり、
各R3は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
各R3bは、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニルもしくはベンジルから選択され、
各R4は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、もしくはベンジルから選択され、あるいは2つのR4基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR3bおよびR4が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R4bは、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のアリールまたは置換もしくは非置換のベンジル、置換もしくは非置換のヘテロアリール、置換もしくは非置換の複素環から選択され、
R6は、H、L2-(置換もしくは非置換のアルキル)、L2-(置換もしくは非置換のシクロアルキル)、L2-(置換もしくは非置換のアルケニル)、L2-(置換もしくは非置換のシクロアルケニル)、L2-(置換もしくは非置換の複素環)、L2-(置換もしくは非置換のヘテロアリール)、またはL2-(置換もしくは非置換のアリール)であり、L2は、結合、O、S、-S(=O)、-S(=O)2、C(O)、-CH(OH)、-(置換もしくは非置換のC1〜C6アルキル)、または-(置換もしくは非置換のC2〜C6アルケニル)であり、
R7は、L3-X-L4-G1であり、
L3は、結合、または置換もしくは非置換のアルキルであり、
Xは、結合、O、-C(=O)、-CR9(OR9)、S、-S(=O)、-S(=O)2、-NR9、-NR9C(O)、-C(O)NR9、-NR9C(O)NR9-、またはアリールであり、
L4は、結合、または置換もしくは非置換のアルキルであり、
G1は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、-OR9、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-OC(O)O-、-NHC(O)NH-、-NHC(O)O、-O(O)CNH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG1は、W-G5であり、Wは、置換もしくは非置換のアリール、置換もしくは非置換の複素環、または置換もしくは非置換のヘテロアリールであり、G5は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8であり、
各R8は、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、もしくはベンジルから選択され、
各R9は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、フェニル、もしくはベンジルから選択され、あるいは2つのR9基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR8およびR9が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R10は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
R5は、H、ハロゲン、-N3、-CN、-ONO2、-L6-(置換もしくは非置換のC1〜C6アルキル)、-L6-(置換もしくは非置換のC2〜C6アルケニル)、-L6-(置換もしくは非置換のヘテロアリール)、または-L6-(置換もしくは非置換のアリール)であり、L6は、結合、O、S、-S(=O)、S(=O)2、NH、C(O)、-NHC(O)O、-OC(O)NH、-NHC(O)、-NHC(O)NH-、または-C(O)NHであり、
R11は、L7-L10-G6であり、L7は、結合、-O、-S、-S(=O)、-S(=O)2、-NH、-C(O)、-C(O)NH、-NHC(O)、(置換もしくは非置換のC1〜C6アルキル)、または(置換もしくは非置換のC2〜C6アルケニル)であり、
L10は、結合、(置換もしくは非置換のアルキル)、(置換もしくは非置換のシクロアルキル)、(置換もしくは非置換のシクロアルケニル)、(置換もしくは非置換のヘテロアリール)、(置換もしくは非置換のアリール)、または(置換もしくは非置換の複素環)であり、
G6は、H、CN、SCN、N3、NO2、ハロゲン、OR9、-C(=O)CF3、-C(=O)R9、-C(=O)OR9、-SR8、-S(=O)R8、-S(=O)2R8、N(R9)2、テトラゾリル、-NHS(=O)2R8、-S(=O)2N(R9)2、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、-C(=O)N(R9)2、NR9C(O)R9、C(R9)2C(=O)N(R9)2-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG6は、W-G7であり、Wは、(置換もしくは非置換の複素環)または(置換もしくは非置換のヘテロアリール)であり、G7は、H、ハロゲン、CN、NO2、N3、CF3、OCF3、C1〜C6アルキル、C3〜C6シクロアルキル、-C1〜C6フルオロアルキル、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアルキル)、-L5-(置換もしくは非置換のヘテロアリール)、-L5-(置換もしくは非置換の複素環)、または-L5-(置換もしくは非置換のアリール)であり、L5は、結合、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
ただし、L10がフェニルまたはチオフェニルであり、Yが、-(置換もしくは非置換のヘテロアリール)、-(置換もしくは非置換のアリール)であり、Zが、[C(R2)2]nC(R1)2Oである場合、G6は、W-G7であり、
R12は、H、(置換もしくは非置換のC1〜C6アルキル)、(置換もしくは非置換のC3〜C6シクロアルキル)である]。
Zは、[C(R1)2]m[C(R2)2]n、[C(R2)2]n[C(R1)2]mO、O[C(R1)2]m[C(R2)2]n、[C(R2)2]nO[C(R1)2]n、または[C(R1)2]nO[C(R2)2]nから選択され、各R1は、独立に、H、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR1が結合してカルボニル(=O)を形成してもよく、各R2は、独立に、H、OH、OMe、CF3、または任意選択で置換された低級アルキルであり、同じ炭素上の2つのR2が結合してカルボニル(=O)を形成してもよく、mは、0、1、または2であり、各nは、独立に、0、1、2、または3であり、
Yは、Hまたは-(置換もしくは非置換のアリール)、または-(置換もしくは非置換のヘテロアリール)であり、
YまたはZ上の各置換基は、(LsRs)jであり、各Lsは、独立に、結合、-O-、-C(=O)-、-S-、-S(=O)-、-S(=O)2-、-NHC(O)-、-C(O)NH-、S(=O)2NH-、-NHS(=O)2、-OC(O)NH-、-NHC(O)O-、-OC(O)O-、-NHC(O)NH-、-C(O)O-、-OC(O)-、置換もしくは非置換のC1〜C6アルキル、C2〜C6アルケニル、-C1〜C6フルオロアルキル、置換もしくは非置換のヘテロアリール、置換もしくは非置換のアリール、または置換もしくは非置換の複素環から選択され、各Rsは、独立に、H、ハロゲン、-N(R4)2、-CN、-NO2、N3、-S(=O)2NH2、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、-C1〜C6フルオロアルキル、置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、または置換もしくは非置換のヘテロアルキルから選択され、jは、0、1、2、3、または4であり、
R6は、H、L2-(置換もしくは非置換のアルキル)、L2-(置換もしくは非置換のシクロアルキル)、L2-(置換もしくは非置換のアルケニル)、L2-(置換もしくは非置換のシクロアルケニル)、L2-(置換もしくは非置換の複素環)、L2-(置換もしくは非置換のヘテロアリール)、またはL2-(置換もしくは非置換のアリール)であり、L2は、結合、O、S、-S(=O)、-S(=O)2、C(O)、-CH(OH)、-(置換もしくは非置換のC1〜C6アルキル)、または-(置換もしくは非置換のC2〜C6アルケニル)であり、
R7は、L3-X-L4-G1であり、
L3は、置換もしくは非置換のアルキルであり、
Xは、結合、O、-C(=O)、-CR9(OR9)、S、-S(=O)、-S(=O)2、-NR9、-NR9C(O)、-C(O)NR9、-NR9C(O)NR9-であり、
L4は、結合、または置換もしくは非置換のアルキルであり、
G1は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、-OR9、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-OC(O)O-、-NHC(O)NH-、-NHC(O)O、-O(O)CNH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいはG1は、W-G5であり、Wは、置換もしくは非置換のアリール、置換もしくは非置換の複素環、または置換もしくは非置換のヘテロアリールであり、G5は、H、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8であり、
各R8は、独立に、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニル、または置換もしくは非置換のベンジルから選択され、
各R9は、独立に、H、置換もしくは非置換の低級アルキル、置換もしくは非置換の低級シクロアルキル、置換もしくは非置換のフェニル、または置換もしくは非置換のベンジルから選択され、あるいは2つのR9基が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、あるいはR8およびR9が一緒になって、5-、6-、7-、または8員複素環を形成してもよく、
各R10は、独立に、H、-S(=O)2R8、-S(=O)2NH2-C(O)R8、-CN、-NO2、ヘテロアリール、またはヘテロアルキルから選択され、
R5は、H、ハロゲン、置換もしくは非置換のC1〜C6アルキル、置換もしくは非置換のO-C1〜C6アルキルであり、
R11は、L7-L10-G6であり、L7は、結合、-C(O)、-C(O)NH、-NHC(O)、または(置換もしくは非置換のC1〜C6アルキル)であり、L10は、結合、(置換もしくは非置換のアルキル)、(置換もしくは非置換のシクロアルキル)、(置換もしくは非置換のヘテロアリール)、(置換もしくは非置換のアリール)、または(置換もしくは非置換の複素環)であり、
G6は、OR9、-C(=O)R9、-C(=O)OR9、-SR8、-S(=O)R8、-S(=O)2R8、N(R9)2、テトラゾリル、-NHS(=O)2R8、-S(=O)2N(R9)2、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、-C(=O)N(R9)2、NR9C(O)R9、C(R9)2C(=O)N(R9)2-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアリール)、または-L5-(置換もしくは非置換のアリール)であり、L5は、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、
あるいは、G6は、W-G7であり、Wは、(置換もしくは非置換の複素環)、(置換もしくは非置換のアリール)、または(置換もしくは非置換のヘテロアリール)であり、G7は、H、ハロゲン、CN、NO2、N3、CF3、OCF3、C1〜C6アルキル、C3〜C6シクロアルキル、-C1〜C6フルオロアルキル、テトラゾリル、-NHS(=O)2R8、S(=O)2N(R9)2、OH、-OR8、-C(=O)CF3、-C(O)NHS(=O)2R8、-S(=O)2NHC(O)R9、CN、N(R9)2、-N(R9)C(O)R9、-C(=NR10)N(R9)2、-NR9C(=NR10)N(R9)2、-NR9C(=CR10)N(R9)2、-C(O)NR9C(=NR10)N(R9)2、-C(O)NR9C(=CR10)N(R9)2、-CO2R9、-C(O)R9、-CON(R9)2、-SR8、-S(=O)R8、または-S(=O)2R8、-L5-(置換もしくは非置換のアルキル)、-L5-(置換もしくは非置換のアルケニル)、-L5-(置換もしくは非置換のヘテロアルキル)、-L5-(置換もしくは非置換のヘテロアリール)、-L5-(置換もしくは非置換の複素環)、または-L5-(置換もしくは非置換のアリール)であり、L5は、結合、-O-、C(=O)、S、S(=O)、S(=O)2、-NH、-NHC(O)O、-NHC(O)NH-、-OC(O)O-、-OC(O)NH-、-NHC(O)、-C(O)NH、-C(O)O、または-OC(O)であり、ただし、R11は、少なくとも1つの(非置換もしくは置換の)芳香族部分、および少なくとも1つの(非置換もしくは置換の)環状部分を含み、(非置換もしくは置換の)環状部分は、(非置換もしくは置換の)複素環基または(非置換もしくは置換の)ヘテロアリール基であり、R11は、チエニル-フェニル基ではなく、
R12は、H、(置換もしくは非置換のC1〜C6アルキル)、(置換もしくは非置換のC3〜C6シクロアルキル)である]、
あるいはその活性代謝物、または溶媒和物、または医薬として許容可能な塩、または医薬として許容可能なプロドラッグ。
先の節に記載の式(G)、式(G-I)、および式(G-II)の化合物は、当業者に知られている標準の合成技術を使用して、または当技術分野で知られている方法を本明細書に記載の方法と併用して合成することができる。さらに、本明細書で提供される溶媒、温度、および他の反応条件は、当業者によって変えることができる。
本明細書に記載の化合物を、様々な求電子試薬または求核試薬を使用して改変して、新しい官能基または置換基を形成することができる。「共有結合の例およびその前駆体」と題する表5は、選択された共有結合の例および産出される前駆体官能基を列挙するものであり、様々な求電子試薬および求核試薬の利用可能な組合せに対する指針として使用できる。前駆体官能基は、求電子基および求核基として示されている。
記載の反応では、反応性官能基、例えばヒドロキシ、アミノ、イミノ、チオ、またはカルボキシ基を、それらが最終生成物において望ましい場合には保護して、反応における望ましくない沈殿を回避する必要があり得る。保護基を使用して、いくつかまたはすべての反応性部分を封鎖し、保護基が除去されるまで、このような基が化学反応において沈殿するのを防止する。各保護基が、様々な手段によって除去可能であることが好ましい。完全に異種の反応条件下で開裂する保護基は、様々な除去要件を満たす。保護基は、酸、塩基、および水素化分解によって除去することができる。トリチル、ジメトキシトリチル、アセチル、およびt-ブチルジメチルシリルなどの基は、酸に不安定であり、それらを使用して、水素化分解によって除去可能なCbz基および塩基に不安定であるFmoc基で保護されたアミノ基の存在下で、カルボキシおよびヒドロキシ反応性部分を保護することができる。カルボン酸およびヒドロキシ反応性部分は、それに限定されるものではないが、メチル、エチル、およびアセチルなどの塩基に不安定な基を用いて、t-ブチルカルバメートなどの酸に不安定な基または酸に安定でも塩基に安定でもあるが加水分解除去可能なカルバメートなどで封鎖されたアミンの存在下で封鎖することができる。
式(G)、式(G-I)、および式(G-II)の化合物のインドールまたはインドールに類似の骨格に対する合成戦略の追加の非限定的な例には、それに限定されるものではないが、Batcho-Leimgruberインドール合成、Reissertインドール合成、Hegedusインドール合成、福山インドール合成、Sugasawaインドール合成、Bischlerインドール合成、Gassmanインドール合成、フィッシャーインドール合成、Japp-Klingemannインドール合成、Buchwaldインドール合成、Larockインドール合成、Bartoliインドール合成、Castroインドール合成、Hemetsbergerインドール合成、Mori-Banインドール合成、Madelungインドール合成、Nenitzescuインドール合成、および他の無名の反応を含む、インドールの様々な合成の改変形態が含まれる。このような合成方法の非限定的な例を、図3〜7に示す。
式(G)、式(G-I)、および式(G-II)の化合物は、該化合物の遊離塩基形態と、それに限定されるものではないが、塩酸、臭化水素酸、硫酸、硝酸、リン酸、メタリン酸などの無機酸、ならびに酢酸、プロピオン酸、ヘキサン酸、シクロペンタンプロピオン酸、グリコール酸、ピルビン酸、乳酸、マロン酸、コハク酸、リンゴ酸、マレイン酸、フマル酸、p-トルエンスルホン酸、酒石酸、トリフルオロ酢酸、クエン酸、安息香酸、3-(4-ヒドロキシベンゾイル)安息香酸、桂皮酸、マンデル酸、アリールスルホン酸、メタンスルホン酸、エタンスルホン酸、1,2-エタンジスルホン酸、2-ヒドロキシエタンスルホン酸、ベンゼンスルホン酸、2-ナフタレンスルホン酸、4-メチルビシクロ-[2.2.2]オクト-2-エン-1-カルボン酸、グルコヘプトン酸、4,4'-メチレンビス-(3-ヒドロキシ-2-エン-1-カルボン酸)、3-フェニルプロピオン酸、トリメチル酢酸、第三ブチル酢酸、ラウリル硫酸、グルコン酸、グルタミン酸、ヒドロキシナフトエ酸、サリチル酸、ステアリン酸、およびムコン酸などの有機酸を含む、医薬として許容可能な無機または有機酸とを反応させることによって、医薬として許容可能な酸付加塩(あるタイプの医薬として許容可能な塩)として調製することができる。
適切な投与経路には、それに限定されるものではないが、静脈、経口、直腸、エアロゾル、非経口、経眼、経肺、経粘膜、経皮、膣内、点耳、経鼻、および局所投与が含まれる。さらにほんの一例として、非経口送達には、筋肉内、皮下、静脈、髄内注入、ならびに髄腔内、直接脳室内、腹腔内、リンパ管内、および鼻腔内注入が含まれる。
医薬組成物は、活性化合物を、医薬として使用できる調製物に処理するのを容易にする賦形剤および助剤を含む1種または複数種の生理学的に許容可能な担体を使用して、通常の方式で配合することができる。適切な製剤は、選択される投与経路に依存して変わる。周知の技術のいずれか、担体、および賦形剤を、適切に、当技術分野で理解されているように使用することができる。本明細書に記載の医薬組成物の概略は、その全体が参照によって本明細書に組み込まれる、例えば、Remington:The Science and Practice of Pharmacy,Nineteenth Ed(Easton,Pa.:Mack Publishing Company,1995);Hoover,John E.,Remington's Pharmaceutical Sciences,Mack Publishing Co.,Easton,Pennsylvania 1975;Liberman,H.A.and Lachman,L.,Eds.,Pharmaceutical Dosage Forms,Marcel Decker,New York,N.Y.,1980;およびPharmaceutical Dosage Forms and Drug Delivery Systems,Seventh Ed.(Lippincott Williams&Wilkins1999)に見ることができる。
式(G)、式(G-I)、および式(G-II)の化合物は、ロイコトリエン依存性またはロイコトリエン媒介性の疾病または状態の治療のための医薬品の調製に使用することができる。さらに、このような治療を必要とする対象における本明細書に記載の疾患または状態のいずれかを治療する方法は、前記対象に対して治療有効量の、式(G)、式(G-I)、または式(G-II)のいずれかの少なくとも1つの化合物、あるいはその医薬として許容可能な塩、医薬として許容可能なN-オキシド、医薬として活性な代謝物、医薬として許容可能なプロドラッグ、または医薬として許容可能な溶媒和物を含有する医薬組成物を投与することを含む。
ロイコトリエン依存性またはロイコトリエン媒介性の疾病または状態の療法は、FLAPの活性を変調するように設計される。このような変調には、ほんの一例として、FLAP活性を阻害または拮抗することが含まれ得る。例えば、個体内でのロイコトリエンの合成を低減するために、または場合により、FLAP mRNAまたはFLAP mRNAの特異的スプライシング変異体の発現またはアベイラビリティーを下方制御または低減するために、FLAP阻害剤を投与することができる。天然FLAP mRNAまたは特定のスプライシング変異体の発現またはアベイラビリティーを下方制御または低減することによって、欠陥性(defective)核酸または特定のスプライシング変異体の発現または活性を最小限に抑え、それによって欠陥性核酸または特定のスプライシング変異体の影響を最小限に抑えることができよう。
いくつかの場合、式(G)、式(G-I)、または式(G-II)のいずれかの少なくとも1つの化合物を、別の治療剤と共に投与することが適切となり得る。ほんの一例として、本明細書の化合物の1つを投与された患者が受ける副作用の1つが炎症である場合、最初の治療剤と共に抗炎症剤を投与することが適切となり得る。あるいは、ほんの一例として、本明細書に記載の化合物の1つの治療有効性を、助剤を投与することによって増大することができる(すなわち、助剤それ自体は、最小限の治療利益を有することができるが、別の治療剤と組み合わせると、患者にとっての全体の治療利益が増大する)。あるいは、ほんの一例として、本明細書に記載の化合物の1つを、やはり治療利益を有する別の治療剤(治療レジメンも含む)と共に投与することによって、患者が受ける利益を増大することができる。ほんの一例として、本明細書に記載の化合物の1つを投与することを含む喘息の治療では、やはり喘息用の他の治療剤または療法を患者に提供することによって、治療利益の増大が得られる。治療される疾患、障害、または状態に関わらず、いかなる場合も患者が受ける全体の利益は、単に2種の治療剤を添加することにあり、すなわち患者は相乗的な利益を受けることができる。
本明細書に記載の別の実施形態では、ロイコトリエン依存性またはロイコトリエン媒介性の状態または疾患の治療方法には、本発明に記載の化合物、医薬組成物、または医薬品を、それに限定されるものではないが、アースロテック、アサコール、アウラルガン、アザルフィジン、デイプロ、エトドラク、ポンスタン、サロファルク、およびソルメドロールを含む抗炎症剤、非ステロイド系抗炎症剤、例えば、アスピリン(バイエル(商標)、バファリン(商標))、インドメタシン(インドシン(商標))、ロフェコキシブ(バイオックス(商標))、セレコキシブ(セレブレックス(商標))、バルデコキシブ(ベクストラ(商標))、ジクロフェナク、エトドラク、ケトプロフェン、ロジン、モビック、ナブメトン、ナプロキセン、ピロキシカム、ならびにコルチコステロイド、例えば、セレストン、プレドニゾン、およびデルタソンと組み合わせて患者に投与することが含まれる。コルチコステロイドは、ロイコトリエン生成を直接的には阻害せず、したがってステロイドとの併用投与によって、さらなる抗炎症性の利益が付与されるであろう。
本明細書に記載の別の実施形態では、ロイコトリエン依存性またはロイコトリエン媒介性の状態または疾患の治療方法は、本明細書に記載の化合物、医薬組成物、または医薬品を、それに限定されるものではないが、CysLT1/CysLT2二重受容体拮抗薬およびCysLT1受容体拮抗薬を含むロイコトリエン受容体拮抗薬と組み合わせて患者に投与することを含む。本明細書に記載の別の実施形態では、ロイコトリエン依存性またはロイコトリエン媒介性の状態または疾患の治療方法は、本明細書に記載の化合物、医薬組成物、または医薬品を、CysLT1/CysLT2二重受容体拮抗薬と組み合わせて患者に投与することを含む。CysLT1/CysLT2二重受容体拮抗薬には、それに限定されるものではないが、BAY u9773(Cuthbert等の欧州特許第00791576号(1997年8月27日公開))、DUO-LT(American Thoracic Society,May 2002に提示されているGalczenski et al,D38,Poster F4)およびTsuji et al,Org.Biomol.Chem.,1,3139-3141,2003が含まれる。特定の患者について、最も適切な製剤またはこのような併用療法の使用方法は、ロイコトリエン依存性またはロイコトリエン媒介性の障害のタイプ、FLAP阻害剤が障害を治療するように作用する期間、およびCysLT1/CysLT2二重受容体拮抗薬がCysLT受容体活性を阻害するように作用する期間によって決まり得る。ほんの一例として、このような併用療法は、呼吸器障害に罹患している患者を治療するために使用できる。
本明細書に記載の別の実施形態では、癌を含む増殖性障害などのロイコトリエン依存性またはロイコトリエン媒介性の状態または疾患を治療する方法は、本明細書に記載の化合物、医薬組成物、または医薬品を、アレムツズマブ、三酸化ヒ素、アスパラギナーゼ(ペグまたは非ペグ)、ベバシツマブ、セツキシマブ、シスプラチンなどのプラチナベースの化合物、クラドリビン、ダウノルビシン/ドキソルビシン/イダルビシン、イリノテカン、フルダラビン、5-フルオロウラシル、ゲムツズマブ、メトトレキサート、パクリタキセル(商標)、タキソール、テモゾロミド、チオグアニン、あるいはホルモン(抗エストロゲン、抗アンドロゲン、またはゴナドトロピン放出ホルモン類似体を含む薬剤のクラス、αインターフェロンなどのインターフェロン、ブスルファンまたはメルファランまたはメクロレタミンなどのナイトロジェンマスタード、トレチノインなどのレチノイド、イリノテカンまたはトポテカンなどのトポイソメラーゼ阻害剤、ゲフィニチニブまたはイマチニブなどのチロシンキナーゼ阻害剤、あるいはアロプリノール、フィルグラスチム、グラニセトロン/オンダンセトロン/パロノセトロン、ドロナビノールを含む、このような療法によって誘発される徴候または症状を治療するための薬剤からなる群から選択される、少なくとも1種の追加の薬剤と組み合わせて患者に投与することを含む。
別の態様によれば、本明細書に記載の組成物および方法は、CysLT受容体活性を妨害するためのCysLT1/CysLT2二重受容体拮抗薬を送達するように設計される。「CysLT拮抗薬」または「CysLT受容体拮抗薬」または「ロイコトリエン受容体拮抗薬」という用語は、CysLT受容体を介してCysLTのシグナル伝達を低減する療法を指す。CysLTは、一般に、LTC4、LTD4、またはLTE4を指す。システイニルロイコトリエンは、特に、呼吸器系および循環系における強力な平滑筋収縮剤である。これらは、少なくとも2つの細胞受容体CysLT1およびCysLT2によって媒介される。CysLT1受容体およびCysLT2受容体は、7つの推定膜貫通領域およびG-タンパク質と相互作用する細胞内ドメインを含むG-タンパク質結合受容体である。Evans et al,Prostaglandins and Other Lipid Mediators,68-69,p587-597,(2002)。CysLT1/CysLT2二重受容体拮抗薬の例は、BAY u9773(Cuthbert等の欧州特許第00791576号(1997年8月27日公開))、DUO-LT(American Thoracic Society,May 2002に提示されているGalczenski et al,D38,Poster F4)およびTsuji et al,Org.Biomol.Chem.,1,3139-3141,2003。
式(G)、式(G-I)、または式(G-II)のいずれかの化合物、あるいは式(G)、式(G-I)、または式(G-II)のいずれかの化合物を含む本明細書に記載の医薬組成物または医薬品、あるいは他のFLAPモジュレータを用いる治療に対して選択され得る「ロイコトリエン反応性の患者」のスクリーニングは、本発明に記載の技術および方法を使用して達成することができる。このような技術および方法には、ロイコトリエン経路の知られているモジュレータに応答する患者を示唆する、例えば遺伝子ハプロタイプの評価(遺伝子型分析)、バイオマーカーのモニター/測定(表現型分析)、機能的マーカーのモニター/測定(表現型分析)、またはそれらの組合せが含まれる。
ヒトFLAPは、精製され、クローン化されており、ヒト好中球に最も高度に発現する18キロダルトンの膜結合型タンパク質である。FLAP遺伝子は13q12に位置し、この遺伝子は、いくつかの集団における心筋梗塞および卒中の両方の高いリスクと関連付けられている。FLAPをコードする遺伝子のいくつかの多形およびハプロタイプが、個体において同定されてきた(米国特許出願第2005113408号;Sayers,Clin.Exp.Allergy,33(8):1103-10,2003;Kedda,et al.,Clin.Exp.Allergy,35(3):332-8,2005)。特定のFLAPハプロタイプは、いくつかの集団における心筋梗塞および卒中と関連付けられている(Helgadottir A et al.Nature Genet.36:233-239(2004);Helgadottir A et al.Am J Hum Genet 76:505-509(2004);Lohmussaar E et al.Stroke 36:731-736(2005);Kajimoto K et al.Circ J 69:1029-1034(2005))。これまでに、いくつかの遺伝子の多形が、所与の療法に対する反応性、例えば特定の化学療法薬に対する癌の反応性に相関していることが示されている(Erichsen,et al.,Br.J.Cancer,90(4):747-51,2004;Sullivan,et al.,Oncogene,23(19):3328-37,2004)。したがって、本明細書に記載の新規FLAP阻害剤、またはこのような新規FLAP阻害剤を含む薬物の組合せを用いる治療の対象となる患者を、それらのFLAP多形またはハプロタイプをベースとする治療に対する潜在的な反応性についてスクリーニングすることができる。
式(G)、式(G-I)、または式(G-II)のいずれかの化合物、あるいは式(G)、式(G-I)、または式(G-II)のいずれかの化合物を含む本明細書に記載の薬物の組合せを用いた治療の対象となる患者を、ロイコトリエン誘発性炎症バイオマーカー表現型をベースとする治療に対する潜在的な反応性についてスクリーニングすることができる。
式(G)、式(G-I)、または式(G-II)のいずれかの化合物、あるいは式(G)、式(G-I)、または式(G-II)のいずれかの化合物を含む本明細書に記載の薬物の組合せを用いた治療の対象となる患者を、ロイコトリエン経路の知られているモジュレータに対する反応性についてスクリーニングすることができる。ロイコトリエン経路の知られているモジュレータに対する患者の応答の指標としての機能的マーカーを評価することによる患者のスクリーニングは、ロイコトリエン経路遺伝子ハプロタイプ検出(遺伝子型分析)および/またはロイコトリエン誘発性炎症バイオマーカー表現型のモニター/測定による患者のスクリーニングの代替として使用することができ、あるいはそれと相互補完することができる。機能的マーカーには、それに限定されるものではないが、ロイコトリエン依存性状態または疾患に関連する任意の物理的特徴、あるいは現行または過去の薬物治療レジメンの知識が含まれ得る。
かの化合物を含む医薬組成物または医薬品を、治療有効量の別の抗炎症剤と組み合わせて投与することを含む。さらに別の実施形態では、ロイコトリエン遺伝子ハプロタイプ、ほんの一例としてFLAPハプロタイプ、および表現型バイオマーカー、およびロイコトリエン修飾薬に対する表現型機能的マーカー応答について、患者のサンプルを分析する。次いで、様々な治療方法を使用して該患者を治療することができる。このような治療方法は、それに限定されるものではないが、治療有効量のFLAP阻害剤、あるいはFLAP阻害剤を含む医薬組成物または医薬品を投与すること、治療有効量のFLAP阻害剤、あるいはFLAP阻害剤を含む医薬組成物または医薬品を、治療有効量のロイコトリエン受容体拮抗薬(例えば、CysLT1/CysLT2拮抗薬またはCysLT1拮抗薬)と組み合わせて投与すること、あるいは治療有効量のFLAP阻害剤、あるいはFLAP阻害剤を含む医薬組成物または医薬品を、治療有効量の別の抗炎症剤と組み合わせて投与することを含む。
本明細書に記載の治療適用における使用については、キットおよび製品も本明細書に記載される。このようなキットは、バイアル、チューブ等の1つまたは複数の容器を入れるように区分されたキャリヤ、パッケージ、または容器を含むことができ、容器(複数)のそれぞれは、本明細書に記載の方法に使用される別々の要素の1つを含む。適切な容器には、例えば、ボトル、バイアル、注射器、および試験管が含まれる。容器は、ガラスまたはプラスチックなどの様々な材料から形成することができる。
これらの実施例は、単に例示目的で提供されるものであり、本明細書に示す特許請求の範囲を制限するものではない。
式(G)、式(G-I)、および式(G-II)の化合物の合成に使用する出発材料および中間体は、市販で入手可能であり、または当技術分野で知られている合成方法もしくは本明細書に記載の合成方法によって合成することができる。本明細書で使用されるが市販で入手できない、例えば表6に示されるようなものなどの中間体の調製を以下に示す。本明細書では特に言及されず、式(G)、式(G-I)、および式(G-II)の化合物の合成に使用される他の中間体は、本明細書に記載の方法または当技術分野で知られている方法を使用して調製することができる。
ステップ1:BOC保護(Int-10)
3-アゼチジンカルボン酸(Sigma Aldrich、0.25g、2.5mmol)を、tBuOH(5mL)および1NのNaOH(2.7mL、2.7mmol)に溶かした。二炭酸ジ-tert-ブチル(0.59g、2.7mmol)を添加し、反応物を終夜室温で攪拌した。該反応物を水で希釈し、1NのHClでゆっくりpH4に酸性化し、ニンヒドリン染色によってすべての生成物が水層から除去されるまで、その混合物をEtOAcで抽出した。混合有機層を乾燥し、濾過し、濃縮して所望の生成物を得た。
ステップ1からの酸(0.7g、3.5mmol)を、THFに溶かし、N2下で0℃に冷却した。ボラン-THF複合体をその溶液に添加し、反応物を終夜室温で攪拌した。反応物を0℃に冷却し、水でクエンチした。混合物をEtOAcで3回抽出し、混合有機層をMgSO4で乾燥し、濾過し、濃縮した。粗材料をシリカゲルのプラグを介して濾過し、EtOAcで溶出して、所望の化合物を得た。
トリフェニルホスフィン(1.7g、6.5mmol)をDMFに溶かし、0℃に冷却した。臭素(0.31mL、5.9mmol)をゆっくり添加し、その溶液を30分間攪拌した。ステップ2からのアルコール(0.32g、2.0mmol)を、DMF中で添加し、反応物を終夜室温で攪拌した。反応物を水で希釈し、EtOAcで3回抽出し、混合有機層をMgSO4で乾燥し、濾過し、濃縮した。粗材料をシリカゲルのプラグを介して濾過し、EtOAcで溶出して、所望の化合物を得た。
(6-ブロモ-ピリジン-3-イル)-メタノール(0.5g、2.7mmol)を、トルエン(20mL)に溶かした。トリフェニルホスフィン(0.9g、3.5mmol)およびイミダゾール(0.4g、6.0mmol)に次いで、ヨウ素溶液(0.88g、3.5mmol)を、トルエン中で滴加した。反応物を室温で15分間攪拌し、次いでNa2CO3飽和水溶液に注いだ。有機層を、チオ硫酸ナトリウム水溶液、水で洗浄し、次いでMgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(EtOAc:ヘキサン勾配)で精製して、所望の生成物を得た。
(S)-(-)-1-(tert-ブトキシカルボニル)-2-ピロリジンメタノール(1.0g、5.0mmol)を、ピリジン(3mL)に溶かし、塩化トルエンスルホニル(1.0g、5.5mmol)を添加した。反応物を室温で終夜攪拌し、水で希釈し、EtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣を、シリカゲル(ヘキサン中0〜10%のEtOAc)で精製して、所望の生成物を得た。
(R)-α-メチル-2-ピリジンメタノール(1.0g、8.1mmol)を、CH2Cl2(20mL)に溶かし、0℃に冷却した。トリエチルアミン(1.7mL、12.2mmol)に次いで、塩化メタンスルホニル(0.66mL、8.4mmol)を滴加した。反応物を30分間攪拌し、次いでCH2Cl2で希釈し、水で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物を得た。
ステップ1:アミドの形成(Int-19)
シクロプロピルアミン(0.35mL、5.0mmol)およびトリエチルアミン(0.7mL、5.1mmol)を、CH2Cl2(10mL)に溶かした。反応物を、-10℃に冷却し、塩化クロロアセチル(0.4mL、5.0mmol)を滴加した。反応物を-10℃で1時間攪拌し、次いで室温で2時間攪拌した後、水でクエンチした。水層をCH2Cl2で抽出し、有機層を乾燥し、濾過し、濃縮して、所望の生成物を得た。
ステップ1:イミンの形成(Int-20)
クロロアセトニトリル(0.5g、6.6mmol)を、Et2O(10mL)に溶かし、0℃に冷却した。EtOH(0.43mL、7.3mmol)に次いで、1,4-ジオキサン中4NのHCl(15mL、59.6mmol)を添加した。反応物を0℃で4日間攪拌し、次いで濃縮して、所望の生成物を白色固体として得た。
ステップ1からのイミン(0.3g、2.0mmol)を、EtOH(4mL)に溶かし、0℃に冷却した。1,3-ジアミノプロパン(0.17mL、2.0mmol)に次いで、iPr2NEt(0.35mL、2.0mmol)を添加した。反応物を、0℃で2時間攪拌し、次いで1,4-ジオキサン中4NのHCl(0.5mL、2mmol)を添加した。混合物を濾過し、濾液を濃縮して、所望の生成物を得た。
ステップ1:mCPBA酸化(Int-46)
2,5-ルチジン(5.0g、46.7mmol)をCHCl3(125mL)に溶かし、0℃に冷却した。m-クロロペルオキシ安息香酸(70%;13.9g、55.2mmol)を添加し、反応物を終夜室温で攪拌した。反応物を、Na2CO3飽和水溶液で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物を得た。
ステップ1からのN-オキシド(46.7mmol)を、無水酢酸(25mL)に溶かし、100℃で1時間加熱還流した。混合物を室温に冷却し、エタノール(46.7mmol)をゆっくり添加して反応をクエンチした。その溶液を乾燥するまで蒸発させ、シリカゲルで精製して、所望の生成物を得た。
ステップ2からの酢酸塩(46.7mmol)を、濃縮HCl(20mL)に溶かし、1時間還流した。反応物を冷却し、乾燥するまで蒸発させて、橙色の固体を得、それを次の反応で直接使用した。
ステップ3からのアルコール(1.0g、8.1mmol)を、塩化チオニル(3mL)に溶かし、N2下、室温で30分間攪拌した。混合物を乾燥するまで蒸発させて、所望の生成物を塩酸塩として得、それを次の反応で直接使用した。
ステップ1:濃縮(Int-60)
p-トルイジン(10g、60.0mmol)およびトリエチルアミン(8.4mL、60.3mmol)を、室温でCH2Cl2(200mL)に溶かした。塩化シンナモイル(6.5g、60.7mmol)を添加し、反応物を1時間攪拌した。反応物を水で洗浄し、乾燥し、濾過し、濃縮した。その残渣に塩化アルミニウム(5g、37.5mmol)を添加し、それを手際よく加熱した。45分後、氷を添加して、沈殿物を形成した。混合物を終夜室温で攪拌した。次いで、沈殿物を濾過し、CH2Cl2に溶かし、1NのHCl、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をエタノールから再結晶化して、所望のキノリノン生成物を得た。
ステップ1からのキノリノン(3.12g、19.6mmol)を、POCl3(10mL)中、90℃に加熱した。出発材料が残らなくなったら、反応物を冷却し、濃縮した。残渣をEtOAcおよびNaHCO3飽和水溶液で希釈し、水層をEtOAcで抽出した。混合有機物を乾燥し、濾過し、濃縮してクロロキノリン生成物を得た。
ステップ2からのキノリン(19.6mmol)を、ベンゼン(200mL)中、NBS(3.6g、20.2mmol)および触媒としての過酸化ベンゾイルと共に1時間80℃に加熱した。反応混合物を濃縮し、シリカゲルで精製して、所望の生成物を得た。
2-アミノピラジン(4g、42mmol)を、水(2mL)およびDMSO(70mL)に溶かし、NBS(7.5g、42mmol)を、1時間かけて0℃で冷却した。反応物を室温に温め、終夜攪拌した。混合物を氷に注ぎ、EtOAcで4回抽出した。混合有機層を、5%のNa2CO3、水、およびブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物を得た。
2-フルオロ-6-メチルピリジン(1.11g、10mmol)、NCS(2.0g、15mmol)、および触媒としての過酸化ベンゾイルを、ベンゼンに溶かし、終夜加熱還流した。反応物を濃縮し、水およびEtOAcで希釈した。有機層をNaHCO3飽和水溶液で洗浄し、乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物を得た。
ステップ1:鈴木カップリング(Int-71)
DME/H2O(16mL、2:1)中、(4-ヒドロキシメチルフェニル)ボロン酸(Combi-Blocks;1.0g、6.6mmol)に、2-ブロモチアゾール(1.2g、7.2mmol)およびK2CO3(2.7g、19.7mmol)を添加した。反応物を、N2で20分間脱ガスした。Pd(PPh3)4(0.76g、0.7mmol)を添加し、反応物をさらに10分間脱ガスした。次いで反応物を、終夜N2下で90℃に加熱した。LCMSによって、生成物の形成を確認した。反応物を、水およびEtOAcに分離し、水層を、EtOAcで2回抽出した。混合有機層を、MgSO4で乾燥し、濾過し、濃縮し、シリカゲル(EtOAc:ヘキサン勾配)で精製して、所望の生成物を得た。
ステップ1からのチアゾール(0.35g、1.8mmol)を、THF(15mL)に溶かし、N2下で-78℃に冷却した。n-ブチルリチウム(1.6M;4.6mL、7.3mmol)、次いでNFSi(1.2g、3.7mmol)を滴加した。NH4Cl飽和水溶液で-78℃にて反応をクエンチし、EtOAcおよび水で希釈した。水層を、EtOAcで2回抽出し、混合有機物を、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の化合物を得た。
ステップ1からのチアゾール(0.33g、1.7mmol)を、THF(15mL)に溶かし、N2下で-78℃に冷却した。n-ブチルリチウム(1.6M;4.3mL、6.7mmol)、次いでヨードメタン(0.16、2.6mmol)を滴加した。NH4Cl飽和水溶液で-78℃にて反応をクエンチし、EtOAcおよび水で希釈した。水層を、EtOAcで2回抽出し、混合有機物を、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の化合物を得た。
ステップ1:酸塩化物形成(Int135)
3-フェノキシ-安息香酸(0.50g、0.23mmol)を、CH2Cl2に溶かした。塩化オキサリル(0.32g、0.25mmol)に次いで、1〜2滴のDMFを添加した。反応物を室温で攪拌し、次いで濃縮して、所望の酸塩化物を得た。
ステップ1:アルキル化(Int-5)
CH2Cl2中、イミダゾール(0.41g、6.0mmol)に、ブロモアセトニトリル(0.21g、2.0mmol)を添加し、反応物を30分間還流した。混合物を室温に冷却し、濾過し、濾液を濃縮して所望の生成物を得た。
ステップ1:メチル化(Int-74)
THF(50mL)中、4-m-トリル-テトラヒドロ-ピラン-4-オル(2.5g、13.0mmol)に、室温で水素化ナトリウム(60%;0.8g、20.0mmol)を添加した。ヨードメタン(1.25mL、20mmol)を添加し、反応物を1時間攪拌した。混合物を水でクエンチし、水層をEtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の化合物を得た。
ステップ1:臭素化
0℃のMeOH(2.8mL)中の4,4-ジメチル-ペンタン-2-オン(3.7mL、26.3mmol)に、単一ストリームの臭素(1.34mL、26.3mmol)を添加した。反応物を10℃までゆっくり30分間温めて、反応を開始し、次いで室温でさらに15分間攪拌した。反応物を水およびジエチルエーテルで希釈し、水層をジエチルエーテルで3回抽出した。混合有機層を、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物を無色液体として得た。
ステップ1からの臭化物(26.3mmol)を、THF(50mL)に溶かし、混合物を0℃に冷却した。2-メチル-2-プロパンチオール(2.45mL、21.6mmol)に次いで、トリエチルアミン(7.9mL、56.8mmol)を添加した。反応物を、室温で18時間攪拌し、次いで水で希釈した。水層を、ジエチルエーテルで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物を得た。
化合物1-2、化合物2-19、化合物2-21、化合物2-35、化合物2-62、化合物2-89、化合物2-195、化合物2-196、化合物2-206、化合物3-1、化合物3-2、化合物3-3、化合物3-4、化合物3-5、および化合物4-1を、スキームAに概説のように調製した。スキームAに示す反応条件の詳細な例は、3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-19)の合成に記載されている。
DMF(1L)中、4-アセトアミドフェノール(Sigma Aldrich;73.6g)、塩酸2-クロロメチルピリジン(80g)、および炭酸セシウム(320g)の混合物を、70℃で2日間攪拌した。混合物を冷却し、水(2L)に注ぎ、EtOAC(×6)で抽出した。有機層を、ブラインで洗浄し、乾燥し(MgSO4)、濾過して褐色の固体(A-1、114g)を得、それを次のステップでそのまま使用した。
A-1(114g)をEtOH(1L)に溶かし、これに、水(200mL)中、KOH(50g)を添加した。溶液を、2日間110℃に加熱し、KOH(水100mL中20g)を添加し、さらに2日間加熱を続けた。溶液を冷却し、EtOHを減圧下で除去し、残渣をEtOAcおよび水に分離した。水とEtOAc(×3)の抽出後、有機層をブラインで洗浄し、乾燥し(MgSO4)、濾過した。この溶液に、EtOAc中、飽和HClを添加すると、直ちに沈殿物が形成された。濾過に次ぐ真空下の乾燥によって固体を回収し、標題化合物(A-2、95g)を桃色の固体として生成した。
A-2(95g)を、水(1L)に0℃で溶かし、これに、水(100mL)中、NaNO2(26g)を添加した。ジアゾニウム塩を、45分かけて形成させ、次いでそれを、急速に攪拌したNa2S2O4(350g)の水(1L)およびエーテル(1L)中混合液に、0℃で15分かけてゆっくり注いだ。40分間攪拌を続け、次いで濃KOHを使用して、混合物を塩基性にした。EtOAc(×2)を使用して抽出した後、水に次いでブラインで有機層を洗浄し、乾燥し(MgSO4)、濾過した。この溶液に、EtOAc中、飽和HClを添加すると、直ちに沈殿物が形成された。濾過に次ぐ真空下の乾燥によって固体を回収し、標題の化合物(A-3、75g)を褐色固体として生成した。
トルエン(800mL)およびHOAc(400mL)中、A-3(75g)、エチル5-(t-ブチルチオ)-2,2-ジメチル-4-オキソ-ペンタノアート(1994年2月22日発行の米国特許第5,288,743号に記載の手順に従って調製した;64g)、NaOAc(40g)を、室温で3日間攪拌した。混合物を水に注ぎ、固体のNa2CO3で塩基性にした。混合物をEtOAc(×3)で抽出し、次いで水(×2)、ブラインで洗浄し、乾燥し(MgSO4)、濾過し、濃縮して、濃い赤黒色の油を得た。母液のカラムクロマトグラフィー(ヘキサンに入れたシリカゲル、ヘキサンに次いで9:1のヘキサン-EtOAcを4:1に上げて溶出した)によって、標題化合物(A-4)68gを、黄色の固体として得た。
3-[3-tert-ブチルスルファニル-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸エチルエステル(A-4;20.0g、45.4mmol)を、DMF(150mL)に溶かし、N2下で-10℃に冷却した。水素化ナトリウム(鉱油中60%分散液;2.0g、50.0mmol)を滴加し、気泡が消えるまで、反応物を-10℃で45分間攪拌した。この濃い赤褐色溶液に、DMF中、メタンスルホン酸4-(6-メトキシ-ピリジン-3-イル)-ベンジルエステル(Int-72;16.0g、54.5mmol)を滴加した。次いで反応物を-10℃で1時間攪拌し、室温にゆっくり温めた。16時間後、LCMSによって生成物の形成を確認した。飽和NH4Clで反応をクエンチし、メチルtert-ブチルエーテル(MTBE)および水で希釈した。水相を、MTBEで2回抽出した。混合有機層を、MgSO4で乾燥し、濾過し、濃縮し、粗生成物をカラムクロマトグラフィーで精製して、所望の生成物(A-5)を得た。
A-5(21.5g、33.7mmol)を、THF(100mL)およびMeOH(100mL)に溶かし、それが透明な溶液になるまで攪拌した。3NのLiOH水溶液(56mL、168.5mmol)を添加し、反応物を80℃で2時間還流した。LCMSによって、生成物の形成を確認し、反応物を室温に冷却し、EtOAcおよび水に分離した。水溶液のpHを、10%のHClでpH1に調節し、水相をEtOAcで3回抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の遊離酸(A-6)を得た。
化合物1-2については、ステップ6は実施しなかった。
化合物1-4、化合物1-5、および化合物1-6を、スキームBに概説のように調製した。スキームBに示す反応条件の詳細な例は、1-[3-tert-ブチルスルファニル-1-(4-クロロ-ベンジル)-5-(ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2-メチル-プロパン-2-オルの合成に記載されている。
エチル4-クロロアセトアセテート(7.5mL、51.9mmol)、2-メチル-2-プロパンチオール(5.6mL、49.7mmol)、トリエチルアミン(10.8mL、77.4mmol)、および触媒としての臭化テトラブチルアンモニウムを、THF(250mL)に溶かし、終夜室温で攪拌した。シリカゲルを添加し、シリカゲルのプラグで混合物を濃縮し濾過して、所望の生成物(B-1)を得、それをさらなる精製なしで使用した。
塩酸4-メトキシフェニルヒドラジン(7.7g、44.1mmol)およびB-1(7.4g、33.9mmol)を、2-プロパノール(150mL)に溶かし、24時間加熱還流した。反応混合物を濃縮し、EtOAcおよびNaHCO3飽和水溶液に分離した。水層を、EtOAcで抽出し、混合有機層をブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲル(ヘキサン中0〜30%のEtOAc)で精製して、所望の生成物(B-2)を得た。
塩化アルミニウム(7.5g、56.0mmol)を、0℃でtert-ブチルチオール(21mL、186.7mmol)に懸濁した。B-2(6.0g、18.7mmol)をCH2Cl2(21mL)に添加し、反応物を室温に温めた。2時間後、TLC分析によって反応を完了し、溶液を氷に注ぎ、10%のHCl水溶液で酸性化した。水層を、EtOAcで3回抽出し、混合有機物を、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物(B-3)を得た。
B-3(2.2g、7.0mmol)をTHF(70mL)に溶かし、0℃に冷却した。塩化メチルマグネシウム(3M;14mL、42.0mmol)を滴加し、反応物を室温で1時間攪拌した。反応を、NH4Cl水溶液でクエンチし、EtOAcで抽出した。混合有機層を、MgSO4で乾燥し、濾過し、濃縮し、シリカゲルで精製して、所望の生成物(B-4)を得た。
DMF(6mL)中、B-4(0.18g、0.61mmol)に、炭酸セシウム(1.0g、3.1mmol)を添加した。反応物を室温で30分間攪拌し、次いで塩酸2-クロロメチルピリジン(0.11g、0.67mmol)およびヨウ化テトラブチルアンモニウム(0.05g、0.13mmol)を添加し、反応物を室温でさらに16時間攪拌した。反応物を、水およびジエチルエーテルに分離し、水層をジエチルエーテルで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物(B-5)を得た。
DMF(3mL)中、B-5(0.05g、0.13mmol)に、炭酸セシウム(0.21g、0.65mmol)を添加した。反応物を室温で30分間攪拌し、次いで1-クロロ-4-クロロメチルベンゼン(0.03g、0.20mmol)およびヨウ化テトラブチルアンモニウム(0.05g、0.13mmol)を添加し、反応物を終夜室温で攪拌した。反応物を、水およびEtOAcに分離し、水層をEtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮し、残渣をシリカゲル(EtOAc:ヘキサン勾配)で精製して、所望の生成物(B-6)を得た。
ステップ1:塩酸N-(4-クロロ-ベンジル)-N-(4-メトキシ-フェニル)-ヒドラジン
塩酸4-メトキシフェニルヒドラジン(10.0g、57.3mmol)、塩化4-クロロベンジル(9.2g、57.2mmol)、臭化テトラブチルアンモニウム(3.7g、11.5mmol)、およびジイソプロピルエチルアミン(20mL、115mmol)のCH2Cl2(250mL)中溶液を、室温で数日間攪拌した。反応混合物を水で希釈し、有機層を、MgSO4で乾燥し、濾過し、濃縮した。残渣をトルエン(200mL)およびジエチルエーテル(100mL)に溶かし、ジオキサン中1当量の4NのHClを、0℃で添加した。混合物を室温で2時間攪拌し、次いで乾燥するまで蒸発させて、所望の生成物(C-1;X=Cl)を紫色の固体として得た。
C-1(〜16g、57.3mmol)、エチル5-(t-ブチルチオ)-2,2-ジメチル-4-オキソ-ペンタノアート(1994年2月22日発行の米国特許第5,288,743号に記載の手順に従って調製した;14.8g、57.3mmol)、トルエン(120mL)およびHOAc(66mL)中、NaOAc(5.2g)を、室温にて暗室で5日間攪拌した。混合物を、EtOAcおよび水に分離し、有機層を、固体のNaHCO3と共に攪拌し、濾過し、蒸発させた。残渣をシリカゲル(ヘキサン中0〜55%のCH2Cl2)で精製し、単離生成物をヘキサンから再結晶化して、所望の生成物(C-2;X=Cl)を得た。
塩化アルミニウム(0.820g、6.15mmol)を、tert-ブチルチオール(1.8mL、16mmol)に懸濁し、0℃に冷却した。C-2(1.0g、2.0mmol)を、CH2Cl2(2.4mL)に添加し、反応物を室温に温めた。3時間後、TLC分析によって反応を完了し、溶液をCH2Cl2で希釈し、10%の氷冷HCl水溶液で洗浄した。水層を、CH2Cl2で3回抽出し、混合有機物を、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物(C-3;X=Cl)を無色の気泡として得た。
DMF(2.5mL)中、3-[1-(4-クロロ-ベンジル)-3-tert-ブチルスルファニル-5-ヒドロキシ-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸エチルエステル(C-3;0.5g、1.05mmol)に、N-BOC-(S)-2-(トルエン-4-スルホニルオキシメチル)ピロリジン(0.39g、1.10mmol)およびCs2CO3(0.69g、2.1mmol)を添加した。反応物を、45℃で2時間攪拌し、次いで触媒としてのヨウ化カリウムを添加し、反応物を終夜60℃に加熱した。反応混合物をEtOAcで希釈し、水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲル(ヘキサン中0〜15%のEtOAc)で精製して、所望の生成物(C-4;X=Cl)を得た。
ステップ4からのエステル(0.16g、0.26mmol)を、MeOH(1mL)、THF(1mL)、および水(1mL)に溶かした。水酸化リチウム(0.6g、1.43mmol)を添加し、TLC分析によって出発材料が見られなくなるまで、反応物を12時間加熱した。反応物を水で希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を、水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲル(ヘキサン中0〜40%のEtOAc)で精製して、所望の生成物(C-5;X=Cl)を得た。
化合物2-23、化合物2-24、化合物2-31、化合物2-32、化合物2-33、化合物2-76、化合物2-77、化合物2-78、化合物2-79、化合物2-80、化合物2-81、化合物2-82、化合物2-84、化合物2-85、化合物2-99、化合物2-100、化合物2-101、化合物2-104、化合物2-108、化合物2-122、化合物2-135、化合物2-141、化合物2-148、化合物2-149、化合物2-150、化合物2-151、化合物2-156、化合物2-183、化合物2-184、化合物2-188、化合物2-189、化合物2-190、化合物2-191、化合物2-192、化合物2-193、化合物2-197、化合物2-198、化合物2-199、化合物2-200、化合物2-201、化合物2-202、化合物2-203、化合物2-204、化合物2-205、化合物2-207、化合物2-208、化合物2-209、化合物2-210、化合物2-211、化合物2-212、化合物2-213、化合物2-214、化合物2-215、化合物2-216、化合物2-217、化合物2-218、化合物2-219、化合物2-220、化合物2-221、化合物2-222、化合物2-223、化合物2-224、化合物2-225、化合物2-226、化合物2-227、化合物2-228、化合物2-229、化合物2-230、化合物2-231、化合物2-232、化合物2-233、化合物2-234、および化合物4-2を、スキームDに示すように調製した。スキームDに示す反応条件の詳細な例は、3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-141)の合成に記載されている。
実施例3、ステップ3からのフェノール(C-3、X=Br;35.0g、67.5mmol)、ビス(ピナコラート)ジボロン(Combi-Blocks;25.0g、98.4mmol)、およびKOAc(19.9g、209.1mmol)を、1,4-ジオキサン(350mL)に溶かし、N2で30分間脱ガスした。PdCl2dppf(2.5g、3.1mmol)を添加し、反応混合物を、N2でさらに30分間脱ガスした。反応物を、終夜85℃に加熱した。反応混合物を、水およびEtOAcに分離し、水層をEtOAcで3回抽出し、混合有機層を水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中15%のEtOAc)で精製して、所望の生成物(D-1、33.5g)を得た。
D-1(25.34g、44.8mmol)、5-ブロモ-2-メトキシピリジン(Combi-blocks;10.9g、70.3mmol)、およびK2CO3(15.5g、112.1mmol)を、DME(300mL)および水(150mL)に溶かし、N2で30分間脱ガスした。Pd(PPh3)4(1.6g、1.4mmol)を添加し、反応混合物を、N2でさらに15分間脱ガスした。溶液を、終夜80℃に加熱し、次いで室温に冷却し、EtOAcおよび水で希釈した。水層をEtOAcで3回抽出し、混合有機層を、水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中0〜8%のEtOAc)で精製して、所望の生成物(D-2、23.7g)を得た。
MeCN(75mL)中、3-{3-tert-ブチルスルファニル-5-ヒドロキシ-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸エチルエステル(D-2;6.5g、11.9mmol)に、2-ブロモメチル-6-フルオロ-キノリン(3.14g、13.1mmol)およびCs2CO3(9.7g、29.8mmol)を添加した。反応物を、終夜室温で攪拌し、その後LCMSによって、反応が完了したことが示された。反応混合物を、EtOAcおよび水に分離し、水層をEtOAcで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮した。残渣を、シリカゲル(ヘキサン中0〜25%のEtOAc)で精製して、所望の生成物(D-3、7.6g)を得た。
D-3(6.58g、9.3mmol)を、MeOH(36mL)、THF(75mL)、および水(36mL)に溶かした。水酸化リチウム(2.42g、57.7mmol)を添加し、TLC分析によって出発材料が見られなくなるまで、反応物を60℃で6時間加熱した。反応物を、水で希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を、水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣を、ヘキサン:EtOAc(9:1)で終夜磨砕し、濾過して、所望の生成物(D-4、5.9g)を得た。
化合物2-33については、ステップ3の間、イミダゾールをやはりアルキル化して、最終生成物を得た。
化合物2-30、化合物2-64、化合物2-73、化合物2-87、化合物2-88、化合物2-97、化合物2-107、および化合物2-121を、スキームEに示すように調製した。スキームEに示す反応条件の詳細な例は、3-[3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(化合物2-73)の合成に記載されている。
DMF(2mL)中、3-[1-(4-ブロモ-ベンジル)-3-tert-ブチルスルファニル-5-ヒドロキシ-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸エチルエステル(C-3;0.25g、0.48mmol)に、塩酸2-クロロメチル-5-メチル-ピリジン(0.13g、0.72mmol)、Cs2CO3(0.39g、1.21mmol)、および触媒としてのヨウ化テトラブチルアンモニウムを添加した。反応物を、終夜室温で攪拌し、その後LCMSによって、反応が完了したことが示された。反応混合物を、EtOAcおよび水に分離し、水層をEtOAcで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中0〜15%のEtOAc)で精製して、追加の所望の生成物(E-1、0.30g)を得た。
E-1(0.06g、0.10mmol)、2-メトキシ-ピリジン-5-ボロン酸(0.02g、0.14mmol)、およびK2CO3(0.03g、0.24mmol)を、DME(1mL)および水(0.5mL)に溶かし、N2で10分間脱ガスした。Pd(PPh3)4(0.01g、0.01mmol)を添加し、反応混合物を、N2でさらに10分間脱ガスした。溶液を、4時間80℃に加熱し、次いで室温に冷却し、EtOAcおよび水で希釈した。水層をEtOAcで3回抽出し、混合有機層を、水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中0〜50%のEtOAc)で精製して、所望の生成物(E-2)を得た。
E-2(0.22g、0.31mmol)を、MeOH(0.1mL)、THF(0.1mL)、および水(0.1mL)に溶かした。水酸化リチウム1N水溶液(0.1mL)を添加し、LCMSによって出発材料が見られなくなるまで、反応物を60℃で4時間加熱した。反応物を、水およびEtOAcで希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物(F-4)を得た。
化合物2-64については、ステップ2および3を逆の順序で実施した。
化合物2-1、化合物2-2、化合物2-3、化合物2-4、化合物2-5、化合物2-6、化合物2-7、化合物2-17、化合物2-18、化合物2-20、化合物2-34、化合物2-39、化合物2-41、化合物2-43、化合物2-47、化合物2-55、化合物2-65、化合物2-67、化合物2-68、化合物2-90、化合物2-91、化合物2-92、化合物2-93、化合物2-94、化合物2-95、化合物2-96、化合物2-98、化合物2-102、化合物2-103、化合物2-105、化合物2-106、化合物2-109、化合物2-110、化合物2-111、化合物2-112、化合物2-113、化合物2-114、化合物2-115、化合物2-116、化合物2-117、化合物2-118、化合物2-119、化合物2-120、化合物2-125、化合物2-126、化合物2-127、化合物2-128、化合物2-129、化合物2-130、化合物2-131、化合物2-136、化合物2-137、化合物2-138、化合物2-139、化合物2-140、化合物2-142、化合物2-143、化合物2-144、化合物2-145、化合物2-146、化合物2-147、化合物2-157、化合物2-158、化合物2-159、化合物2-160、化合物2-161、化合物2-162、化合物2-164、化合物2-165、化合物2-166、化合物2-167、化合物2-168、化合物2-169、化合物2-171、化合物2-172、化合物2-173、化合物2-174、化合物2-175、化合物2-176、化合物2-177、化合物2-178、化合物2-179、化合物2-180、化合物2-181、化合物2-182、化合物2-185、化合物2-186、および化合物2-187を、スキームFに示すように調製した。スキームFに示す反応条件の詳細な例は、3-{3-tert-ブチルスルファニル-5-(6-フルオロ-キノリン-2-イルメトキシ)-1-[4-(6-メトキシ-ピリジン-2-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-140)の合成に記載されている。
MeCN(25mL)中、3-[1-(4-ブロモ-ベンジル)-3-tert-ブチルスルファニル-5-ヒドロキシ-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸エチルエステル(C-3;2.0g、3.9mmol)に、2-ブロモメチル-6-フルオロ-キノリン(1.0g、4.2mmol)およびCs2CO3(2.5g、7.7mmol)を添加した。反応物を、終夜室温で攪拌し、その後LCMSによって、反応が完了したことが示された。反応混合物を、EtOAcおよび水に分離し、水層をEtOAcで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮した。残渣を、EtOAc:ヘキサン中で再結晶化して、所望の生成物(F-1、1.9g)を得た。濾液を濃縮し、シリカゲル(ヘキサン中0〜15%のEtOAc)で精製して、さらに1gのF-1を得た。
F-1(1.0g、1.5mmol)、ビス(ピナコラート)ジボロン(Combi-Blocks;1.1g、4.3mmol)、およびKOAc(0.44g、4.5mmol)を、1,4-ジオキサン(15mL)に溶かし、密封容器中、N2で10分間脱ガスした。PdCl2dppf(0.13g、0.16mmol)を添加し、反応混合物を、N2でさらに10分間脱ガスした。容器を密封し、反応物を終夜95℃で加熱した。反応混合物を、水およびEtOAcに分離し、水層をEtOAcで3回抽出し、混合有機層を、水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中0〜20%EtOAc)で精製して、所望の生成物(F-2)を得た。
F-2(0.25g、0.35mmol)、2-ブロモ-6-メトキシピリジン(0.09g、0.48mmol)、およびK2CO3(0.15g、1.05mmol)を、DME(3.5mL)および水(1.8mL)に溶かし、N2で10分間脱ガスした。Pd(PPh3)4(0.06g、0.05mmol)を添加し、反応混合物を、N2でさらに10分間脱ガスした。溶液を、4時間85℃に加熱し、次いで室温に冷却し、EtOAcおよび水で希釈した。水層を、EtOAcで3回抽出し、混合有機層を、水、ブラインで洗浄し、MgSO4で乾燥し、濾過し、濃縮した。粗材料を、シリカゲル(ヘキサン中0〜25%のEtOAc)で精製して、所望の生成物(F-3)を得た。
F-3(0.22g、0.31mmol)を、MeOH(1.5mL)、THF(3mL)、および水(1.5mL)に溶かした。水酸化リチウム(0.08g、1.9mmol)を添加し、TLC分析によって出発材料が見られなくなるまで、反応物を60℃で3.5時間加熱した。反応物を、水で希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物(F-4)を得た。
化合物2-17については、ステップ4の間、前駆体中の6-メトキシピリダジニルをやはり加水分解して、6-ヒドロキシピリダジニルを最終生成物として得た。
ステップ1:3-{3-tert-ブチルスルファニル-5-[(S)-1-(2,3-ジヒドロ-1H-インドール-2-イル)メトキシ]-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸エチルエステル
(S)-2-{3-tert-ブチルスルファニル-2-(2-エトキシカルボニル-2-メチル-プロピル)-1-[4-(6-メトキシ-ピリダジン-3-イル)-ベンジル]-1H-インドール-5-イルオキシメチル}-2,3-ジヒドロ-インドール-1-カルボン酸tert-ブチルエステル(0.23g、0.30mmol)を、CH2Cl2(1.5mL)に溶かした。TFA(1.5mL)を添加し、TLC分析によって出発材料が見られなくなるまで、反応物を室温で10分間攪拌した。溶液を減圧濃縮し、粗生成物(G-1)をさらなる精製なしで使用した。
G-1(0.30mmol)を、CH2Cl2(1mL)に溶かした。ジイソプロピルエチルアミン(0.5mL)に次いで、無水酢酸(33uL、0.35mmol)を添加し、LCMSによって出発材料が見られなくなるまで、反応物を室温で攪拌した。反応物を、CH2Cl2およびMeOHで希釈し、濃縮し、CH2Cl2に再び溶かし、水で洗浄し、Na2SO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物(G-2)を得た。
G-2(0.05g、0.07mmol)を、MeOH(0.5mL)、THF(0.5mL)、および水(0.5mL)に溶かした。水酸化リチウム(0.03g、0.7mmol)を添加し、TLC分析によって出発材料が見られなくなるまで、反応物を60℃で6時間加熱した。反応物を、水で希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物(G-3)を得た。
化合物2-8、化合物2-9、化合物2-10、化合物2-11、化合物2-12、化合物2-13、化合物2-14、化合物2-15、化合物2-16、化合物2-22、化合物2-25、化合物2-26、化合物2-27、化合物2-28、化合物2-29、化合物2-123、化合物2-124、化合物2-132、化合物2-133、化合物2-134、化合物2-163、化合物2-170、および化合物2-194を、スキームHに示すように調製した。スキームHに示す反応条件の詳細な例は、3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-シクロブチルメチル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸(化合物2-124)の合成に記載されている。
塩化アルミニウム(0.18g、1.37mmol)をCH2Cl2(1mL)に懸濁し、水(19uL、1.0mmol)を、室温でゆっくり添加した。混合物を5分間攪拌し、次いで0℃に冷却した。3-{5-(ベンゾチアゾール-2-イルメトキシ)-3-tert-ブチルスルファニル-1-[4-(6-メトキシ-ピリジン-3-イル)-ベンジル]-1H-インドール-2-イル}-2,2-ジメチル-プロピオン酸エチルエステル(0.12g、0.17mmol)を、CH2Cl2(1mL)に添加し、反応物を室温で2時間攪拌した。tlcによって出発材料が観測されなくなったら、水を添加し、混合物をCH2Cl2で抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮した。残渣を精製して、所望の生成物(H-1)を得た。
ジクロロエタン(5mL)中、H-1(0.10g、0.17mmol)に、塩化シクロブタンカルボニル(57uL、0.50mmol)および塩化アルミニウム(0.09g、0.66mmol)を添加した。反応物を、N2下で1.5時間加熱し、次いで室温に冷却し、酒石酸カリウムナトリウム飽和水溶液でクエンチした。混合物をEtOAcで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮し、シリカゲルで精製して、所望の生成物(H-2)を得た。
H-2(0.05g、0.08mmol)を、CH2Cl2に懸濁し、水素化ホウ素ナトリウム(0.03g、0.8moml)を、TFA(1mL)およびCH2Cl2(1mL)に滴加した。混合物を、室温で4時間攪拌し、次いで水でクエンチし、NaOHの固体ペレットで塩基性化した。混合物を、CH2Cl2で抽出し、混合有機物を、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲルで精製して、所望の生成物(H-3)を得た。
H-3(0.03g、0.04mmol)を、MeOH(0.5mL)およびTHF(0.5mL)に溶かした。水酸化リチウム水溶液(1N、0.5mL)を添加し、LCMSによって出発材料が見られなくなるまで、反応物を60℃で4時間加熱した。反応物を、水で希釈し、クエン酸でpH5に酸性化し、EtOAcで抽出した。混合有機層を水で洗浄し、MgSO4で乾燥し、濾過し、濃縮して、所望の生成物(H-4)を得た。
化合物2-8については、ステップ1、2、および4のみ実施した。
化合物1-1、化合物1-3、化合物1-7、化合物1-8、化合物1-9、化合物1-10、化合物1-11、化合物1-12、化合物1-13、化合物1-14、および化合物1-15を、スキームIに概説のように調製した。スキームHに示す反応条件の詳細な例は、3-[3-tert-ブチルスルファニル-1-(4-クロロ-ベンジル)-5-イソプロピル-1H-インドール-2-イル]-N-(2-ヒドロキシ-エチル)-2,2-ジメチル-プロピオンアミドの合成に記載されている。
CH2Cl2(5mL)に懸濁した3-[3-tert-ブチルスルファニル-1-(4-クロロ-ベンジル)-5-イソプロピル-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸(1992年1月14日発行の米国特許第5,081,138号に記載の手順に従って調製した;0.25g、0.53mmol)に、塩化オキサリル(48uL、0.56mmol)および触媒としてのDMFを添加した。反応物を、室温で3時間攪拌し、次いで濃縮してI-1を得、それをさらなる精製なしに使用した。
CH2Cl2中、I-1(0.18mmol)に、トリエチルアミン(0.1mL、0.70mmol)および2-アミノエタノール(10uL、0.19mmol)を添加した。反応物を、室温で2日間攪拌し、次いで濃縮し、シリカゲル(EtOAc:ヘキサン勾配)で精製して、所望の生成物(I-2)を得た。
DMF(1mL)中、4-[3-tert-ブチルスルファニル-2-(2,2-ジメチル-プロピル)-5-(ピリジン-2-イルメトキシ)-インドール-1-イルメチル]-安息香酸ヒドラジド(0.05g、0.10mmol)に、C-(ジ-イミダゾール-1-イル)-メチレンアミン(0.08g、0.50mmol)を添加し、反応物を、85℃で3時間加熱した。混合物を室温に冷却し、水およびEtOAcに分離した。水層をEtOAcで抽出し、混合有機層を、MgSO4で乾燥し、濾過し、濃縮した。残渣をシリカゲル(EtOAc:ヘキサン勾配)で精製して、所望の生成物を得た。
化合物1-3については、1H NMR(CDCl3)δ8.6(d,1H)、8.31(d,1H)、7.70(m,2H)、7.57(d,1H)、7.38(d,2H)、7.32(d,1H)、7.20(m,1H)、7.08(d,1H)、6.80(m,4H)、5.41(s,2H)、5.27(s,2H)、3.96(t,5H)、3.57(t,2H)、3.27(s,2H)、1.57〜1.20(m,23H)。
このようなFLAP結合アッセイの非限定的な例は、以下の通りである。濃縮したヒト多形核白血球のペレット(1.8×109個の細胞)(Biological Speciality Corporation)を、再懸濁し、溶解し、100,000gの膜を記載のように調製した(Charleson et al.Mol.Pharmacol,41,873-879,1992)。100,000×gのペレット化膜を、Tris-Tweenアッセイ緩衝液(100mMのTrisHCl、pH7.4、140mMのNaCl、2mMのEDTA、0.5mMのDTT、5%のグリセロール、0.05%のTween20)に再懸濁して、50〜100ug/mLの濃度のタンパク質を産出した。膜懸濁液10uLを、96ウェルのMilliporeプレート、Tris-Tween緩衝剤78μL、約30,000cpmまでの3HのMK886または3Hの3-[5-(ピリド-2-イルメトキシ)-3-tert-ブチルチオ-1-ベンジル-インドール-2-イル]-2,2-ジメチルプロピオン酸(または、125IのMK591誘導体(Eggler et al、J.Labelled Compounds and Radiopharmaceuticals,1994,vXXXIV,1147))10μL、阻害剤2μLに添加し、室温で30分間インキュベートした。洗浄済みの氷冷緩衝剤100μLを、インキュベーション混合物に添加した。次いで、プレートを濾過し、氷冷Tris-Tween緩衝剤200μLで3回洗浄し、シンチレーション検出器の底部を封止し、シンチラント100μLを添加し、15分間振とうし、次いでTopCountで計数した。特異的結合は、10μMのMK886の存在下、全放射性結合から非特異的結合を引いたものとして定義して決定した。IC50は、薬物滴定曲線のGraphpad prism分析を使用して決定した。
このようなヒト血液LTB4阻害アッセイの非限定的な例は、以下の通りである。同意が得られたヒトボランティアから採血した血液をヘパリン管に入れ、一定分量125μLを、50%のDMSO(媒体)2.5μLまたは50%のDMSO中薬物2.5μLを入れた各ウェルに添加した。サンプルを、37℃で15分間インキュベートした。カルシウムイオノフォアA23817(ハンクス液(Invitrogen)でのアッセイの直前に1.25mMに希釈した50mMのDMSOストックから)2μLを添加し、溶液を混合し、37℃で30分間インキュベートした。サンプルを、4℃において1,000rpm(約200×g)で10分間遠心分離にかけ、血漿を除去し、ELISA(Assay Designs)を使用して、LTB4濃縮物について1:100希釈物をアッセイした。媒体LTB4の50%阻害(IC50)を実現する薬物濃度は、阻害%対ログ薬物濃度の非線形回帰(Graphpad Prism)によって決定した。
このようなラットの腹膜炎症および浮腫のアッセイの非限定的な例は、以下の通りである。ロイコトリエン生合成阻害剤のin vivo効果を、腹膜炎症のラットモデルを使用して評価した。雄性Sprague-Dawleyラット(体重200〜300グラム)に、ザイモサン(5mg/mL)を含有する生理食塩水3mLを、単回腹腔内(i.p.)注入し、その後直ちに、エバンスブルー染料(1.5%の溶液2mL)を静脈(i.v.)注入した。化合物(0.5%のメチルセルロース媒体中3mL/kg)を、ザイモサン注入の2〜4時間前に経口投与した。ザイモサン注入の1〜2時間後、ラットを安楽死させ、腹腔をリン酸緩衝生理食塩溶液(PBS)10mLでフラッシュした。得られた流体を、1,200rpmで10分間遠心分離にかけた。分光光度計(吸光度610nm)を使用して、上澄みのエバンスブルー染料の量を定量化することによって、血管性水腫を評価した。上澄みのLTB4およびシステイニルロイコトリエン濃度を、ELISAによって決定した。血漿漏出の50%阻害、ならびに腹膜のLTB4およびシステイニルロイコトリエンの50%阻害を達成する薬物濃度(エバンスブルー染料)は、阻害%対ログ薬物濃度の非線形回帰(Graphpad Prism)によって計算できよう。
ヒト白血球阻害アッセイの非限定的な例は、以下の通りである。同意が得られたヒトボランティアから採血した血液をヘパリン管に入れ、3%のデキストラン、0.9%の生理食塩水を等量添加した。赤血球の沈殿後、残存する赤血球の低張溶解を行い、白血球を1000rpmで沈殿させた。1mL当たり1.25×105個の細胞の該ペレットを再懸濁し、20%のDMSO(媒体)2.5μLまたは20%のDMSO中薬物2.5μLを入れた各ウェルに等分した。サンプルを37℃で5分間インキュベートし、カルシウムイオノフォアA23817(ハンクス液(Invitrogen)でのアッセイの直前に1.25mMに希釈した50mMのDMSOストックから)2μLを添加し、溶液を混合し、37℃で30分間インキュベートした。サンプルを、4℃において1,000rpm(約200×g)で10分間遠心分離にかけ、血漿を除去し、ELISA(Assay Designs)を使用して、LTB4濃縮物について1:4希釈物をアッセイした。媒体LTB4の50%阻害(IC50)を実現する薬物濃度は、阻害%対ログ薬物濃度の非線形回帰(Graphpad Prism)によって決定した。表1〜4に提示した化合物は、このアッセイに関して1nM〜5μMのアッセイ結果を有した。
実施例14a:非経口組成物
注入投与に適した非経口医薬組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物の水溶性の塩100mgをDMSOに溶かし、次いで0.9%の滅菌生理食塩水10mLと混合する。その混合物を、注入投与に適した単位剤形に組み込む。
経口送達用の医薬組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物100mgを、デンプン750mgと混合する。その混合物を、経口投与に適した硬質ゼラチンカプセル用などの経口単位剤形に組み込む。
硬質ロゼンジなどの口腔送達用の医薬組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物100mgを、混合砂糖粉末420mg、ライトコーンシロップ1.6mL、蒸留水2.4mL、およびミント抽出物0.42mLと混合する。その混合物を、穏やかにブレンドし、成形型に注いで、口腔投与に適したロゼンジを形成する。
吸入送達用の医薬組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物20mgを、無水クエン酸50mgおよび0.9%の塩化ナトリウム溶液100mLと混合する。その混合物を、吸入投与に適したネブライザーなどの吸入送達単位に組み込む。
直腸送達用の医薬組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物100mgを、メチルセルロース(1500mPa)2.5g、メチルパラペン100mg、グリセリン5g、および精製水100mLと混合する。次いで、得られたゲル混合物を、直腸投与に適した注射器などの直腸送達単位に組み込む。
医薬としての局所ゲル組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物100mgを、ヒドロキシプロピルセルロース1.75g、プロピレングリコール10mL、ミリスチン酸イソプロピル10mL、および精製アルコールUSP100mLと混合する。次いで、得られたゲル混合物を、局所投与に適したチューブなどの容器に組み込む。
医薬としての経眼溶液組成物を調製するために、式(G)、式(G-I)、または式(G-II)のいずれかの化合物100mgを、精製水100mL中0.9gのNaClと混合し、0.2ミクロンのフィルターを使用して濾過する。次いで、得られた等張溶液を、経眼投与に適した点眼容器などの経眼送達単位に組み込む。
Claims (8)
- 3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸である化合物、あるいはその医薬として許容可能な塩、または医薬として許容可能な溶媒和物。
- 3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸である化合物、またはその医薬として許容可能な塩。
- 3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸である化合物。
- 3-[3-tert-ブチルスルファニル-1-[4-(6-エトキシ-ピリジン-3-イル)-ベンジル]-5-(5-メチル-ピリジン-2-イルメトキシ)-1H-インドール-2-イル]-2,2-ジメチル-プロピオン酸のナトリウム塩。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US73403005P | 2005-11-04 | 2005-11-04 | |
| US60/734,030 | 2005-11-04 | ||
| US74717406P | 2006-05-12 | 2006-05-12 | |
| US60/747,174 | 2006-05-12 | ||
| US82334406P | 2006-08-23 | 2006-08-23 | |
| US60/823,344 | 2006-08-23 | ||
| US11/553,946 | 2006-10-27 | ||
| US11/553,946 US7977359B2 (en) | 2005-11-04 | 2006-10-27 | 5-lipdxygenase-activating protein (FLAP) inhibitors |
| PCT/US2006/042690 WO2007056021A2 (en) | 2005-11-04 | 2006-10-30 | 5-lipoxygenase-activating protein (flap) inhibitors |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009276800A Division JP5451347B2 (ja) | 2005-11-04 | 2009-12-04 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
| JP2011015870A Division JP5506707B2 (ja) | 2005-11-04 | 2011-01-28 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2009528975A JP2009528975A (ja) | 2009-08-13 |
| JP2009528975A5 JP2009528975A5 (ja) | 2010-09-09 |
| JP4705986B2 true JP4705986B2 (ja) | 2011-06-22 |
Family
ID=38004604
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008539007A Expired - Fee Related JP4705986B2 (ja) | 2005-11-04 | 2006-10-30 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
| JP2009276800A Expired - Fee Related JP5451347B2 (ja) | 2005-11-04 | 2009-12-04 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
| JP2011015870A Active JP5506707B2 (ja) | 2005-11-04 | 2011-01-28 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009276800A Expired - Fee Related JP5451347B2 (ja) | 2005-11-04 | 2009-12-04 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
| JP2011015870A Active JP5506707B2 (ja) | 2005-11-04 | 2011-01-28 | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
Country Status (27)
| Country | Link |
|---|---|
| US (3) | US7977359B2 (ja) |
| EP (2) | EP2404904A1 (ja) |
| JP (3) | JP4705986B2 (ja) |
| KR (1) | KR101031766B1 (ja) |
| CN (1) | CN102295637A (ja) |
| AT (1) | ATE530521T1 (ja) |
| AU (2) | AU2006311973B9 (ja) |
| BR (1) | BRPI0618046A2 (ja) |
| CA (1) | CA2628490C (ja) |
| CR (1) | CR9942A (ja) |
| CY (1) | CY1112383T1 (ja) |
| DK (1) | DK1943219T3 (ja) |
| EA (2) | EA018616B1 (ja) |
| ES (1) | ES2373977T3 (ja) |
| HK (1) | HK1114099A1 (ja) |
| HR (1) | HRP20120033T1 (ja) |
| IL (2) | IL190873A0 (ja) |
| MA (1) | MA29931B1 (ja) |
| MY (1) | MY151159A (ja) |
| NO (1) | NO342361B1 (ja) |
| NZ (2) | NZ567718A (ja) |
| PL (1) | PL1943219T3 (ja) |
| PT (1) | PT1943219E (ja) |
| RS (1) | RS52189B (ja) |
| SG (1) | SG166813A1 (ja) |
| SI (1) | SI1943219T1 (ja) |
| WO (1) | WO2007056021A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011520982A (ja) * | 2008-05-23 | 2011-07-21 | アミラ ファーマシューティカルス,インコーポレーテッド | 5−リポキシゲナーゼ活性化タンパク質阻害剤 |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070219206A1 (en) * | 2005-11-04 | 2007-09-20 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| US20070225285A1 (en) * | 2005-11-04 | 2007-09-27 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| GB2431927B (en) * | 2005-11-04 | 2010-03-17 | Amira Pharmaceuticals Inc | 5-Lipoxygenase-activating protein (FLAP) inhibitors |
| US7977359B2 (en) | 2005-11-04 | 2011-07-12 | Amira Pharmaceuticals, Inc. | 5-lipdxygenase-activating protein (FLAP) inhibitors |
| US20070244128A1 (en) * | 2005-11-04 | 2007-10-18 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| US8399666B2 (en) * | 2005-11-04 | 2013-03-19 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| WO2008067566A1 (en) | 2006-11-30 | 2008-06-05 | Amira Pharmaceuticals, Inc. | Compositions and treatments comprising 5-lipoxygenase-activating protein inhibitors and nitric oxide modulators |
| TW200920369A (en) * | 2007-10-26 | 2009-05-16 | Amira Pharmaceuticals Inc | 5-lipoxygenase activating protein (flap) inhibitor |
| EP2331541B1 (en) | 2008-09-04 | 2015-04-22 | Boehringer Ingelheim International GmbH | Indolizine inhibitors of leukotriene production |
| US8546431B2 (en) | 2008-10-01 | 2013-10-01 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| WO2010075314A2 (en) * | 2008-12-23 | 2010-07-01 | Amira Pharmaceuticals, Inc. | Topical formulations of flap inhibitors for the treatment of dermatological conditions |
| CN102264370A (zh) * | 2008-12-23 | 2011-11-30 | 艾米拉制药公司 | 投与眼的flap抑制剂的局部调配物 |
| MY198422A (en) | 2009-04-29 | 2023-08-29 | Amarin Pharmaceuticals Ie Ltd | Pharmaceutical compositions comprising epa and a cardiovascular agent and methods of using the same |
| US8592402B2 (en) | 2009-08-04 | 2013-11-26 | Amira Pharmaceuticals, Inc. | Compounds as lysophosphatidic acid receptor antagonists |
| JP2013515677A (ja) * | 2009-09-23 | 2013-05-09 | アミラ ファーマシューティカルズ,インク. | 5−リポキシゲナーゼのインドリジンインヒビター |
| US20120214840A1 (en) * | 2009-09-23 | 2012-08-23 | Panmira Pharmaceuticals, Llc | Indolizine inhibitors of 5-lipoxygenase |
| GB2474120B (en) | 2009-10-01 | 2011-12-21 | Amira Pharmaceuticals Inc | Compounds as Lysophosphatidic acid receptor antagonists |
| CN102822166A (zh) * | 2009-11-03 | 2012-12-12 | 葛兰素集团有限公司 | 制备5-脂氧合酶活化蛋白抑制剂及其中间体的方法 |
| PE20130751A1 (es) | 2010-08-16 | 2013-06-21 | Boehringer Ingelheim Int | Inhibidores de oxadiazol de la produccion de leucotrieno |
| JP5862669B2 (ja) * | 2010-08-26 | 2016-02-16 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | ロイコトリエン産生のオキサジアゾール阻害剤 |
| WO2012040137A1 (en) | 2010-09-23 | 2012-03-29 | Boehringer Ingelheim International Gmbh | Oxadiazole inhibitors of leukotriene production |
| US8575201B2 (en) * | 2010-09-23 | 2013-11-05 | Boehringer Ingelheim International Gmbh | Oxadiazole inhibitors of leukotriene production |
| AU2011338561A1 (en) | 2010-12-07 | 2013-07-25 | Amira Pharmaceuticals, Inc. | Lysophosphatidic acid receptor antagonists and their use in the treatment of fibrosis |
| LT2648726T (lt) | 2010-12-07 | 2018-06-25 | Amira Pharmaceuticals, Inc. | Policiklinis lap1 antagonistas ir jo panaudojimai |
| UA110816C2 (uk) | 2011-01-30 | 2016-02-25 | Мейдзі Сейка Фарма Ко., Лтд. | Місцевий протигрибковий засіб |
| JP2014513077A (ja) | 2011-04-05 | 2014-05-29 | アミラ ファーマシューティカルス,インコーポレーテッド | 線維症、疼痛、癌、ならびに呼吸器、アレルギー性、神経系または心血管疾患の治療に有用な3−または5−ビフェニル−4−イルイソキサゾールに基づく化合物 |
| WO2012166415A1 (en) | 2011-05-27 | 2012-12-06 | Amira Pharmaceuticals, Inc. | Heterocyclic autotaxin inhibitors and uses thereof |
| AR089853A1 (es) | 2012-02-01 | 2014-09-24 | Boehringer Ingelheim Int | Inhibidores de oxadiazol de la produccion de leucotrienos para terapia de combinacion, composicion farmaceutica, uso |
| US20150209301A1 (en) | 2012-07-30 | 2015-07-30 | Nichiban Company Limited | Patch for anti-dermatophytosis |
| AR092358A1 (es) | 2012-07-30 | 2015-04-15 | Meiji Seika Pharma Co Ltd | Agente liquido topico para el tratamiento de la dermatofitosis |
| WO2014031586A2 (en) * | 2012-08-20 | 2014-02-27 | Tallikut Pharmaceuticals, Inc. | Methods for treating cardiovascular diseases |
| EP3102209B1 (en) | 2014-02-04 | 2021-04-07 | Bioscience Pharma Partners, LLC | Use of flap inhibitors to reduce neuroinflammation mediated injury in the central nervous system |
| US9533951B2 (en) * | 2014-10-20 | 2017-01-03 | Eastman Chemical Company | Heterocyclic amphoteric compounds |
| MX2017011269A (es) | 2015-03-06 | 2018-01-12 | Pharmakea Inc | Inhibidores de lisil oxidasa tipo 2 fluorinados y usos de los mismos. |
| CN105085401B (zh) * | 2015-08-17 | 2018-02-13 | 北京大学 | 六氢吲唑类15‑脂氧合酶激活剂及应用 |
| JP7079772B2 (ja) | 2016-09-07 | 2022-06-02 | ファーマケア,インク. | リシルオキシダーゼ様2阻害剤の結晶形態および製造方法 |
| KR102615565B1 (ko) | 2016-09-07 | 2023-12-18 | 파마케아, 인크. | 리실 옥시다제 유사 2 억제제의 용도 |
| AU2017348598B2 (en) * | 2016-10-28 | 2020-02-20 | Astrazeneca Ab | Crystalline form of (1R,2R)-2-[4-(3-methyl-1H-pyrazol-5-yl)benzoyl]-N- (4-oxo-4,5,6,7-tetrahydropyrazolo[1,5-a]pyrazin-3- yl)cyclohexanecarboxamide |
| WO2018152405A1 (en) * | 2017-02-16 | 2018-08-23 | Autoimmune Pharma Llc | Reduction of pro-inflammatory hdl using a leukotriene inhibitor |
| EP3628669A1 (en) * | 2018-09-28 | 2020-04-01 | GenKyoTex Suisse SA | Novel compounds as nadph oxidase inhibitors |
| EP4377297A1 (en) * | 2021-07-30 | 2024-06-05 | The Regents of the University of California | Compounds for modulating epithelial 15-(s)-lipoxygenase-2 and methods of use for same |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5420282A (en) * | 1994-02-15 | 1995-05-30 | Abbott Laboratories | Thiopyrano(2,3,4-c,d) indolyloxime ether alkylcarboxylates |
Family Cites Families (206)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2431491A1 (fr) | 1978-07-18 | 1980-02-15 | Delalande Sa | Nouveaux derives aminoalkoxy-5 benzofurannes et indoles, leur procede de preparation et leur application en therapeutique |
| DK151884C (da) | 1979-03-07 | 1988-06-13 | Pfizer | Analogifremgangsmaade til fremstilling af 3-(1-imidazolylalkyl)indolderivater eller farmaceutisk acceptable syreadditionssalte deraf |
| JPS60123485A (ja) | 1983-12-08 | 1985-07-02 | Yoshitomi Pharmaceut Ind Ltd | インド−ル−3−カルボキサミド誘導体 |
| IE58870B1 (en) | 1985-03-08 | 1993-11-17 | Leo Pharm Prod Ltd | Pyridine derivatives |
| US5109009A (en) | 1985-03-08 | 1992-04-28 | Leo Pharmaceutical Products Ltd. | Quinoline and pyridine compounds and inhibition of 5-lipoxygenases therewith |
| DE3632411A1 (de) | 1986-09-24 | 1988-04-07 | Merck Patent Gmbh | Verfahren zur herstellung von ethanderivaten |
| US5225421A (en) | 1986-12-17 | 1993-07-06 | Merck Frosst Canada, Inc. | 3-hetero-substituted-N-benzyl-indoles and medical methods of use therefor |
| NZ222878A (en) | 1986-12-17 | 1991-02-26 | Merck Frosst Canada Inc | 3-hetero-substituted-n-benzyl-indole derivatives, and pharmaceutical compositions |
| US5081138A (en) | 1986-12-17 | 1992-01-14 | Merck Frosst Canada, Inc. | 3-hetero-substituted-n-benzyl-indoles and prevention of leucotriene synthesis therewith |
| MY103259A (en) | 1987-04-15 | 1993-05-29 | Ici America Inc | Aliphatic carboxamides |
| DE68904342T2 (de) | 1988-04-13 | 1993-05-06 | Ici America Inc | Cyclische amide. |
| US5232916A (en) | 1988-06-27 | 1993-08-03 | Merck Frosst Canada, Inc. | Quinoline ether alkanoic acids |
| NZ234883A (en) | 1989-08-22 | 1995-01-27 | Merck Frosst Canada Inc | Quinolin-2-ylmethoxy indole derivatives, preparation and pharmaceutical compositions thereof |
| US5204344A (en) | 1989-08-22 | 1993-04-20 | Merck Frosst Canada, Inc. | (Quinolin-2-ylmethoxy)indoles as inhibitors of the biosynthesis of leukotrienes |
| NZ248177A (en) | 1989-08-22 | 1995-01-27 | Merck Frosst Canada Inc | Benzyl phenyl hydrazine derivatives |
| US5252585A (en) | 1992-02-03 | 1993-10-12 | Merck Frosst Canada, Inc. | Fluorinated quinoline indoles as inhibitors of the biosynthesis of leukotrienes |
| CA1337427C (en) | 1989-08-22 | 1995-10-24 | Merck Frosst Canada Incorporated | (quinolin-2-ylmethoxy)indoles as inhibitors of the biosynthesis of leukotrienes |
| US5272145A (en) | 1989-08-22 | 1993-12-21 | Merck Frosst Canada, Inc. | (Quinolin-2-ylmethoxy)indoles as inhibitors of the biosynthesis of leukotrienes |
| US5420289A (en) | 1989-10-27 | 1995-05-30 | American Home Products Corporation | Substituted indole-, indene-, pyranoindole- and tetrahydrocarbazole-alkanoic acid derivatives as inhibitors of PLA2 and lipoxygenase |
| PT95692A (pt) | 1989-10-27 | 1991-09-13 | American Home Prod | Processo para a preparacao de derivados de acidos indole-,indeno-,piranoindole- e tetra-hidrocarbazole-alcanoicos, ou quais sao uteis como inibidores de pla2 e da lipoxigenase |
| US5229516A (en) | 1989-10-27 | 1993-07-20 | American Home Products Corporation | Substituted indole-, indene-, pyranoindole- and tetrahydrocarbazole-alkanoic acid derivatives as inhibitors of PLA2 and lipoxygenase |
| CA2032253C (en) | 1989-12-15 | 2000-11-28 | John W. Gillard | 5-lipoxygenase activating protein |
| US5093356A (en) | 1990-01-16 | 1992-03-03 | Merck Frosst Canada, Inc. | Indenyl hydroxamic acids and hydroxy ureas as inhibitors of 5-lipoxygenase |
| US5081145A (en) | 1990-02-01 | 1992-01-14 | Merck Frosst Canada, Inc. | Indole-2-alkanoic acids compositions of and anti allergic use thereof |
| US5095031A (en) | 1990-08-20 | 1992-03-10 | Abbott Laboratories | Indole derivatives which inhibit leukotriene biosynthesis |
| JPH0764841B2 (ja) | 1990-10-03 | 1995-07-12 | ファイザー製薬株式会社 | インドール誘導体およびその用途 |
| US5182367A (en) | 1990-11-30 | 1993-01-26 | Merck & Co., Inc. | 5-lipoxygenase activating protein |
| GB9108811D0 (en) | 1991-04-24 | 1991-06-12 | Erba Carlo Spa | N-imidazolyl derivatives of substituted indole |
| US5202321A (en) | 1991-06-13 | 1993-04-13 | Merck Frosst Canada, Inc. | Thiopyrano[2,3,4-c,d]indoles as inhibitors of leukotriene biosynthesis |
| JPH06100551A (ja) | 1991-09-06 | 1994-04-12 | Dainippon Ink & Chem Inc | 光学活性な2,5置換テトラヒドロフラン誘導体、その製造方法、その誘導体を含む液晶組成物及び液晶表示素子 |
| US5273980A (en) | 1991-09-30 | 1993-12-28 | Merck Frosst Canada Inc. | Bicyclic-azaarylmethoxy) indoles as inhibitors of leukotriene biosynthesis |
| US5389650A (en) | 1991-09-30 | 1995-02-14 | Merck Frosst Canada, Inc. | (Azaarylmethoxy)indoles as inhibitors of leukotriene biosynthesis |
| US5308850A (en) | 1991-09-30 | 1994-05-03 | Merck Frosst Canada, Inc. | (Bicyclic-hetero-arylmethoxy)indoles as inhibitors of leukotriene biosynthesis |
| US5290798A (en) | 1991-09-30 | 1994-03-01 | Merck Frosst Canada, Inc. | (hetero-arylmethoxy)indoles as inhibitors of leukotriene biosynthesis |
| CA2079374C (en) | 1991-09-30 | 2003-08-05 | Merck Frosst Canada Incorporated | (bicyclic-azaarylmethoxy)indoles as inhibitors of leukotriene biosynthesis |
| US5190968A (en) | 1991-09-30 | 1993-03-02 | Merck Frosst Canada, Inc. | (Polycyclic-arylmethoxy) indoles as inhibitors of leukotriene biosynthesis |
| ZA928276B (en) | 1991-10-31 | 1993-05-06 | Daiichi Seiyaku Co | Aromatic amidine derivates and salts thereof. |
| US5254567A (en) | 1991-11-15 | 1993-10-19 | Merck Frosst Canada, Inc. | Amorphous (quinolin-2-ylmethoxy)indole compounds which have useful pharmaceutical utility |
| CA2129429A1 (en) | 1992-02-13 | 1993-08-14 | Richard Frenette | (azaaromaticalkoxy) indoles as inhibitors of leukotriene biosynthesis |
| CH683522A5 (de) | 1992-03-13 | 1994-03-31 | Hoffmann La Roche | Verfahren zur Herstellung von Diarylen. |
| EP0597112A4 (en) | 1992-03-27 | 1994-06-22 | Kyoto Pharma Ind | Novel imidazole derivative, pharmaceutical use thereof, and intermediate therefor. |
| EP0640080B1 (en) | 1992-05-13 | 1997-10-22 | Syntex (U.S.A.) Inc. | Substituted indoles as angiotensin ii antagonists |
| JPH0658881A (ja) | 1992-06-12 | 1994-03-04 | Mitsubishi Rayon Co Ltd | 光学活性化合物の絶対配置判定法、絶対配置判定用試薬及び絶対配置判定装置 |
| US5334719A (en) | 1992-06-17 | 1994-08-02 | Merck Frosst Canada, Inc. | Bicyclic(azaaromatic)indoles as inhibitors of leukotriene bisynthesis |
| WO1994000446A1 (en) | 1992-06-22 | 1994-01-06 | Merck Frosst Canada Inc. | Fluorinated quinoline indoles as inhibitors of the biosynthesis of leukotrienes |
| US5314898A (en) | 1992-06-29 | 1994-05-24 | Merck & Co., Inc. | Aryl thiopyrano[4,3,2-cd]indoles as inhibitors of leukotriene biosynthesis |
| US5314900A (en) | 1992-11-19 | 1994-05-24 | Merck Frosst Canada, Inc. | Aryl thiopyrano[2,3,4-C,D]indoles as inhibitors of leukotriene biosynthesis |
| US5288743A (en) | 1992-11-20 | 1994-02-22 | Abbott Laboratories | Indole carboxylate derivatives which inhibit leukotriene biosynthesis |
| ZA939516B (en) | 1992-12-22 | 1994-06-06 | Smithkline Beecham Corp | Endothelin receptor antagonists |
| JP3457694B2 (ja) | 1993-02-04 | 2003-10-20 | 第一製薬株式会社 | インフルエンザ感染予防・治療薬 |
| US5374635A (en) | 1993-03-29 | 1994-12-20 | Merck Frosst Canada, Inc. | Furo[3,2-b]pyridines and thieno[3,2-b]pyridines as inhibitors of leukotriene biosynthesis |
| IL109309A (en) | 1993-04-16 | 2000-06-29 | Lilly Co Eli | 1-H-indole-3-acetic acid hydrazide SPLA2 inhibitors and pharmaceutical compositions containing them |
| PL312005A1 (en) | 1993-06-14 | 1996-04-01 | Pfizer | Binary amines as antidiabetic and antiobesitic agents |
| JPH075651A (ja) | 1993-06-14 | 1995-01-10 | Fuji Photo Film Co Ltd | ハロゲン化銀カラー写真感光材料の処理方法 |
| WO1995006637A1 (en) | 1993-09-03 | 1995-03-09 | Smithkline Beecham Plc | Indole and indoline derivatives as 5ht1d receptor antagonists |
| DE4338770A1 (de) | 1993-11-12 | 1995-05-18 | Matthias Dr Lehr | Indol-2-alkansäuren und ihre Derivate als Hemmstoffe der Phospholipase A¶2¶ |
| US5399699A (en) | 1994-01-24 | 1995-03-21 | Abbott Laboratories | Indole iminooxy derivatives which inhibit leukotriene biosynthesis |
| US5696076A (en) | 1994-06-22 | 1997-12-09 | Human Genome Sciences, Inc. | 5-lipoxygenase-activating protein II |
| FR2721610B1 (fr) | 1994-06-28 | 1996-08-23 | Adir | Nouveaux dérivés (thia)cycloalkyl [b] indoles, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent. |
| JPH0820532A (ja) | 1994-07-05 | 1996-01-23 | Dai Ichi Seiyaku Co Ltd | 抗膵炎剤 |
| CZ24197A3 (en) | 1994-07-27 | 1997-08-13 | Sankyo Co | Heterocyclic compounds, usable as allosteric efectors in muscarine receptors |
| TW396200B (en) | 1994-10-19 | 2000-07-01 | Sumitomo Chemical Co | Liquid crystal composition and liquid crystal element containing such composition |
| TW321649B (ja) | 1994-11-12 | 1997-12-01 | Zeneca Ltd | |
| WO1996018393A1 (en) | 1994-12-13 | 1996-06-20 | Smithkline Beecham Corporation | Novel compounds |
| JPH11503445A (ja) | 1995-04-10 | 1999-03-26 | 藤沢薬品工業株式会社 | cGMP−PDE阻害剤としてのインドール誘導体 |
| US5702637A (en) | 1995-04-19 | 1997-12-30 | Minnesota Mining And Manufacturing Company | Liquid crystal compounds having a chiral fluorinated terminal portion |
| EP0828712A1 (en) | 1995-05-10 | 1998-03-18 | Pfizer Inc. | Beta-adrenergic agonists |
| JPH092977A (ja) | 1995-06-21 | 1997-01-07 | Dai Ichi Seiyaku Co Ltd | 経口投与用医薬組成物 |
| GB9523946D0 (en) | 1995-11-23 | 1996-01-24 | Bayer Ag | Leukotriene antagonistic benzoic acid derivatives |
| ES2171878T3 (es) | 1996-01-22 | 2002-09-16 | Fujisawa Pharmaceutical Co | Derivados de tiazolilbenzofurano y composiciones farmaceuticas que los contienen. |
| EP0827943B1 (en) | 1996-01-29 | 2003-05-21 | Kaneka Corporation | Processes for the reduction of carbonyl compounds |
| US5756531A (en) | 1996-04-30 | 1998-05-26 | Abbott Laboratories | Iminoxy derivatives of indole and indene compounds as inhibitors of prostaglandin biosynthesis |
| US5750558A (en) | 1996-06-06 | 1998-05-12 | Abbott Laboratories | Oxime derivatives of indole and indene compounds as inhibitors of prostaglandin biosynthesis |
| EP0966973A1 (en) | 1996-07-23 | 1999-12-29 | Daiichi Pharmaceutical Co., Ltd. | Sorbefacients |
| US5877329A (en) | 1996-08-13 | 1999-03-02 | Merck & Co., Inc. | Palladium catalyzed indolization |
| AU4634697A (en) | 1996-11-14 | 1998-06-03 | Pfizer Inc. | Process for substituted pyridines |
| GB9710523D0 (en) | 1997-05-23 | 1997-07-16 | Smithkline Beecham Plc | Novel compounds |
| WO1998056757A1 (fr) | 1997-06-11 | 1998-12-17 | Sankyo Company, Limited | Derives de benzylamine |
| JPH1180032A (ja) | 1997-09-12 | 1999-03-23 | Dai Ichi Seiyaku Co Ltd | 複合体 |
| US6548490B1 (en) | 1997-10-28 | 2003-04-15 | Vivus, Inc. | Transmucosal administration of phosphodiesterase inhibitors for the treatment of erectile dysfunction |
| PT1042287E (pt) | 1997-12-24 | 2005-08-31 | Aventis Pharma Gmbh | Derivados de indole como inibidores do factor xa |
| WO1999033458A1 (fr) | 1997-12-25 | 1999-07-08 | Daiichi Pharmaceutical Co., Ltd. | Composition medicinale pour administration percutanee |
| JPH11189531A (ja) | 1997-12-26 | 1999-07-13 | Dai Ichi Seiyaku Co Ltd | 経粘膜投与用医薬組成物 |
| JPH11193265A (ja) | 1997-12-26 | 1999-07-21 | Dai Ichi Seiyaku Co Ltd | 3−(7−アミジノ−2−ナフチル)−2−フェニルプロピオン酸誘導体の塩 |
| CA2260499A1 (en) | 1998-01-29 | 1999-07-29 | Sumitomo Pharmaceuticals Company Limited | Pharmaceutical compositions for the treatment of ischemic brain damage |
| EP1062216A1 (en) | 1998-02-25 | 2000-12-27 | Genetics Institute, Inc. | Inhibitors of phospholipase a2 |
| US6500853B1 (en) | 1998-02-28 | 2002-12-31 | Genetics Institute, Llc | Inhibitors of phospholipase enzymes |
| EP1071710B2 (en) | 1998-04-15 | 2011-11-02 | Merck Serono Biodevelopment | Genomic sequence of the 5-lipoxygenase-activating protein (flap), polymorphic markers thereof and methods for detection of asthma |
| US6867209B1 (en) | 1998-05-22 | 2005-03-15 | Scios, Inc. | Indole-type derivatives as inhibitors of p38 kinase |
| DE69929689T2 (de) | 1998-05-22 | 2006-11-02 | Scios Inc., Fremont | Heterocyclische Verbindungen und Verfahren zur Behandlung von Herzversagen und anderer Erkrankungen |
| JP2000007590A (ja) | 1998-06-23 | 2000-01-11 | Daicel Chem Ind Ltd | 置換芳香族化合物の製造方法 |
| CA2350415A1 (en) | 1998-11-18 | 2000-05-25 | Incyte Pharmaceuticals, Inc. | Inflammation-associated genes |
| UA73492C2 (en) | 1999-01-19 | 2005-08-15 | Aromatic heterocyclic compounds as antiinflammatory agents | |
| JP2000302671A (ja) | 1999-04-27 | 2000-10-31 | Hitoshi Sezaki | 経口投与用医薬組成物 |
| WO2000071535A1 (en) | 1999-05-21 | 2000-11-30 | Scios Inc. | INDOLE-TYPE DERIVATIVES AS INHIBITORS OF p38 KINASE |
| SK3832002A3 (en) | 1999-09-21 | 2002-11-06 | Astrazeneca Ab | Quinazoline compounds and pharmaceutical compositions containing them |
| DE19948417A1 (de) | 1999-10-07 | 2001-04-19 | Morphochem Ag | Imidazol-Derivate und ihre Verwendung als Arzneimittel |
| WO2001032621A1 (fr) | 1999-10-29 | 2001-05-10 | Wakunaga Pharmaceutical Co., Ltd. | Nouveaux derives d'indole, et medicaments contenant lesdits derives comme principe actif |
| JP2001139462A (ja) | 1999-11-10 | 2001-05-22 | Dai Ichi Seiyaku Co Ltd | 新規製剤 |
| WO2001036403A1 (en) | 1999-11-16 | 2001-05-25 | Boehringer Ingelheim Pharmaceuticals, Inc. | Urea derivatives as anti-inflammatory agents |
| WO2001044184A1 (en) | 1999-12-16 | 2001-06-21 | Eli Lilly And Company | Synthesis of indole-containing spla2 inhibitors |
| US7345051B2 (en) | 2000-01-31 | 2008-03-18 | Genaera Corporation | Mucin synthesis inhibitors |
| GB0003079D0 (en) | 2000-02-10 | 2000-03-29 | Glaxo Group Ltd | Novel protein |
| US6653304B2 (en) | 2000-02-11 | 2003-11-25 | Bristol-Myers Squibb Co. | Cannabinoid receptor modulators, their processes of preparation, and use of cannabinoid receptor modulators for treating respiratory and non-respiratory diseases |
| US6436965B1 (en) | 2000-03-02 | 2002-08-20 | Merck Frosst Canada & Co. | PDE IV inhibiting amides, compositions and methods of treatment |
| MXPA02008801A (es) | 2000-03-09 | 2003-07-07 | Ono Pharmaceutical Co | Derivados de indol, proceso para la preparacion de los mismos y su uso. |
| US6476037B1 (en) | 2000-03-23 | 2002-11-05 | The Regents Of The University Of California | L-arginine and phosphodiesterase (PDE) inhibitor synergism |
| US20010039037A1 (en) | 2000-04-05 | 2001-11-08 | Lee Harland | Novel polypeptide |
| AU2001254790A1 (en) | 2000-04-07 | 2001-10-23 | Bayer Aktiengesellschaft | Regulation of human cyslt2-like gpcr protein |
| JP2004503553A (ja) | 2000-06-14 | 2004-02-05 | ワーナー−ランバート・カンパニー、リミテッド、ライアビリティ、カンパニー | 6,5−縮合二環式複素環 |
| AU2001267823A1 (en) | 2000-06-29 | 2002-01-08 | Shionogi And Co., Ltd. | Compounds exhibiting x-type spla2 inhibiting effect |
| DE10037310A1 (de) | 2000-07-28 | 2002-02-07 | Asta Medica Ag | Neue Indolderivate und deren Verwendung als Arzneimittel |
| PL362546A1 (en) | 2000-10-05 | 2004-11-02 | Fujisawa Pharmaceutical Co, Ltd. | Benzamide compounds as apo b secretion inhibitors |
| DK1355904T3 (da) | 2000-12-22 | 2007-10-15 | Wyeth Corp | Heterocyclindazol- og -azaindazolforbindelser som 5-hydroxytryptamin-6-ligander |
| CA2432713C (en) | 2000-12-22 | 2009-10-27 | Ishihara Sangyo Kaisha, Ltd. | Aniline derivatives or salts thereof and cytokine production inhibitors containing the same |
| US6855722B2 (en) | 2001-01-29 | 2005-02-15 | Dimensional Pharmaceuticals, Inc. | Substituted indoles and their use as integrin antagonists |
| JP2002226429A (ja) | 2001-02-06 | 2002-08-14 | Fuji Photo Film Co Ltd | アクリル酸エステル化合物の製造方法 |
| US6627646B2 (en) | 2001-07-17 | 2003-09-30 | Sepracor Inc. | Norastemizole polymorphs |
| EP1424325A4 (en) | 2001-09-07 | 2005-12-21 | Ono Pharmaceutical Co | INDOLE DERIVATIVES, METHOD FOR THE PRODUCTION THEREOF AND MEDICAMENTS CONTAINING THEM AS AN ACTIVE AGENT |
| KR20040044856A (ko) | 2001-09-07 | 2004-05-31 | 오노 야꾸힝 고교 가부시키가이샤 | 인돌 유도체 화합물 |
| EP1427707A1 (en) | 2001-09-19 | 2004-06-16 | Pharmacia Corporation | Substituted indazole compounds for the treatment of inflammation |
| DE10147672A1 (de) | 2001-09-27 | 2003-04-10 | Bayer Ag | Substituierte 2,5-Diamidoindole und ihre Verwendung |
| EP1314733A1 (en) | 2001-11-22 | 2003-05-28 | Aventis Pharma Deutschland GmbH | Indole-2-carboxamides as factor Xa inhibitors |
| WO2003050174A1 (en) | 2001-12-11 | 2003-06-19 | Rhodia Chimie | Catalytic pgm mixture for hydrosilylation |
| USH2153H1 (en) | 2002-04-24 | 2006-04-04 | Smithkline Beecham Corp. | Association of asthma with polymorphisms in the cysteinyl leukotriene 2 receptor |
| WO2003094889A1 (fr) | 2002-05-13 | 2003-11-20 | Daiichi Pharmaceutical Co., Ltd. | Produit de lyophilisation |
| AR037647A1 (es) | 2002-05-29 | 2004-12-01 | Novartis Ag | Derivados de diarilurea utiles para el tratamiento de enfermedades dependientes de la cinasa de proteina |
| CA2490715A1 (en) | 2002-06-20 | 2003-12-31 | Kyowa Hakko Kogyo Co., Ltd. | Process for producing vinyl perfluoroalkanesulfonate derivative |
| CN100497334C (zh) | 2002-06-24 | 2009-06-10 | 先灵公司 | 用作组胺h3拮抗剂的吲哚衍生物 |
| CA2495903A1 (en) | 2002-08-23 | 2004-03-04 | University Of Connecticut | Novel biphenyl and biphenyl-like cannabinoids |
| AU2003260025A1 (en) | 2002-08-26 | 2004-03-11 | Merck & Co., Inc. | Method for the prevention and/or treatment of atherosclerosis |
| DK1537078T3 (da) | 2002-08-29 | 2010-08-02 | Merck Sharp & Dohme | Indoler med anti-diabetisk aktivitet |
| US7851486B2 (en) | 2002-10-17 | 2010-12-14 | Decode Genetics Ehf. | Susceptibility gene for myocardial infarction, stroke, and PAOD; methods of treatment |
| WO2004048331A1 (en) | 2002-11-28 | 2004-06-10 | Suven Life Sciences Limited | N-arylalkyl-3-aminoalkoxyindoles and their use as 5-ht ligands |
| US7642277B2 (en) | 2002-12-04 | 2010-01-05 | Boehringer Ingelheim International Gmbh | Non-nucleoside reverse transcriptase inhibitors |
| US20040198800A1 (en) | 2002-12-19 | 2004-10-07 | Geoffrey Allan | Lipoxygenase inhibitors as hypolipidemic and anti-hypertensive agents |
| GB0301350D0 (en) | 2003-01-21 | 2003-02-19 | Merck Sharp & Dohme | Therapeutic agents |
| JP4513351B2 (ja) | 2003-02-12 | 2010-07-28 | チッソ株式会社 | 結合基にフッ素化されたアルキル基を有する液晶性化合物、液晶組成物および液晶表示素子 |
| WO2004078719A1 (ja) | 2003-03-06 | 2004-09-16 | Ono Pharmaceutical Co., Ltd. | インドール誘導体化合物およびその化合物を有効成分とする薬剤 |
| EP1479677A1 (en) | 2003-05-19 | 2004-11-24 | Aventis Pharma Deutschland GmbH | New indole derivatives as factor xa inhibitors |
| WO2004108671A1 (en) | 2003-06-06 | 2004-12-16 | Suven Life Sciences Limited | Substituted indoles with serotonin receptor affinity, process for their preparation and pharmaceutical compositions containing them |
| EP1651231A4 (en) | 2003-07-24 | 2009-04-01 | Merck & Co Inc | CYCLOALKANES DIPHENYL-SUBSTITUTES, COMPOSITIONS CONTAINING THESE COMPOUNDS, AND METHODS OF USE |
| DE602004012873T2 (de) | 2003-08-25 | 2009-08-20 | Merck Patent Gmbh | Flüssigkristallines medium |
| BRPI0414136A (pt) | 2003-09-04 | 2006-10-31 | Aventis Pharma Inc | indóis substituìdos como inibidores de poli(adp-ribose) polimerase (parp) |
| CA2537829A1 (en) | 2003-09-05 | 2005-03-17 | Neurogen Corporation | Heteroaryl fused pyridines, pyrazines and pyrimidines as crf1 receptor ligands |
| JP4363133B2 (ja) | 2003-09-09 | 2009-11-11 | 東洋インキ製造株式会社 | 有機エレクトロルミネッセンス用素子材料およびそれを用いた有機エレクトロルミネッセンス素子 |
| US7268159B2 (en) | 2003-09-25 | 2007-09-11 | Wyeth | Substituted indoles |
| AU2004285811B2 (en) | 2003-10-31 | 2008-06-12 | Otsuka Pharmaceutical Co., Ltd. | 2,3-dihydro-6-nitroimidazo (2,1-B) oxazole compounds for the treatment of tuberculosis |
| JP2005170939A (ja) | 2003-11-20 | 2005-06-30 | Takeda Chem Ind Ltd | 糖尿病の予防・治療剤 |
| ATE386715T1 (de) | 2003-11-25 | 2008-03-15 | Lilly Co Eli | Modulatoren des peroxisomproliferatoraktivierten rezeptors |
| JPWO2005054213A1 (ja) | 2003-12-02 | 2007-12-06 | 塩野義製薬株式会社 | ペルオキシソーム増殖活性化受容体アゴニスト活性を有するイソキサゾール誘導体 |
| ATE446285T1 (de) | 2003-12-03 | 2009-11-15 | Merck & Co Inc | Für die behandlung von alzheimer-krankheit und ähnlichen leiden geeignete 1-alkyl-3- thiosubstituierte indol-2-alkinsäuren |
| US20050137234A1 (en) | 2003-12-19 | 2005-06-23 | Syrrx, Inc. | Histone deacetylase inhibitors |
| JP5142450B2 (ja) | 2003-12-25 | 2013-02-13 | 徹也 西尾 | ジアミノ化合物、ビニル化合物、高分子化合物、配向膜、該配向膜を用いた有機半導体装置、導電性高分子、該導電性高分子を使用したエレクトロルミネッセンス素子、液晶配向膜、及び該液晶配向膜を用いた光学素子 |
| US7064203B2 (en) | 2003-12-29 | 2006-06-20 | Bristol Myers Squibb Company | Di-substituted pyrrolotriazine compounds |
| WO2005066157A1 (en) | 2004-01-02 | 2005-07-21 | Suven Life Sciences | 3-(pyrolidin-3-l) indoles as 5-ht6 receptor modulators |
| JP2005194250A (ja) | 2004-01-09 | 2005-07-21 | Sumitomo Chemical Takeda Agro Co Ltd | トリアゾール化合物、その製造法および用途 |
| US8158362B2 (en) | 2005-03-30 | 2012-04-17 | Decode Genetics Ehf. | Methods of diagnosing susceptibility to myocardial infarction and screening for an LTA4H haplotype |
| US20070197585A1 (en) | 2004-02-26 | 2007-08-23 | Jilly Evans | Use of cysteinyl leukotriene 2 receptor antagonists |
| WO2005097203A2 (en) | 2004-04-01 | 2005-10-20 | Cardiome Pharma Corp. | Serum protein conjugates of ion channel modulating compounds and uses thereof |
| US7491744B2 (en) | 2004-04-26 | 2009-02-17 | Vanderbilt University | Indoleacetic acid and indenacetic acid derivatives as therapeutic agents with reduced gastrointestinal toxicity |
| EP1756096B1 (en) | 2004-05-03 | 2009-08-12 | F.Hoffmann-La Roche Ag | Indolyl derivatives as liver-x-receptor modulators |
| JP2008502670A (ja) | 2004-06-18 | 2008-01-31 | バイオリポックス エービー | 炎症の治療に有用なインドール類 |
| CA2571789A1 (en) | 2004-07-02 | 2006-02-09 | Merck & Co., Inc. | Indoles having anti-diabetic activity |
| CA2577664A1 (en) | 2004-08-20 | 2006-03-02 | Bayer Pharmaceuticals Corporation | Novel heterocycles |
| GB0420719D0 (en) | 2004-09-17 | 2004-10-20 | Addex Pharmaceuticals Sa | Novel allosteric modulators |
| WO2006041961A1 (en) | 2004-10-05 | 2006-04-20 | GOVERNMENT OF THE UNITED STATES OF AMERICA, as represented by THE SECRETARY, DEPARTMENT OF HEALTHAND HUMAN SERVICES | Arylthioindole tubulin polymerization inhibitors and methods of treating or preventing cancer using same |
| JP2008516968A (ja) | 2004-10-18 | 2008-05-22 | メルク エンド カムパニー インコーポレーテッド | ジフェニル置換アルカン類 |
| JP5190270B2 (ja) | 2005-01-14 | 2013-04-24 | ジヤンセン・フアーマシユーチカ・ナームローゼ・フエンノートシヤツプ | 細胞周期キナーゼ阻害剤としてのピラゾロピリミジン |
| CA2594777A1 (en) | 2005-01-19 | 2006-07-27 | Biolipox Ab | Indoles useful in the treatment of inflamation |
| CA2594878A1 (en) | 2005-01-19 | 2006-07-27 | Biolipox Ab | Indoles useful in the treatment of inflammation |
| EP1838669A1 (en) | 2005-01-19 | 2007-10-03 | Biolipox AB | Indoles useful in the treatment of inflammation |
| AU2005325497A1 (en) | 2005-01-19 | 2006-07-27 | Biolipox Ab | Indoles useful in the treatment of inflammation |
| JP2008537930A (ja) | 2005-03-09 | 2008-10-02 | メルク エンド カムパニー インコーポレーテッド | ジフェニル置換シクロアルカン、前記化合物を含む組成物及び使用方法 |
| BRPI0610035A2 (pt) | 2005-04-21 | 2010-05-18 | Serono Lab | sulfonamidas de pirazina 2,3 substituìdas |
| PT1888033E (pt) | 2005-06-09 | 2014-05-15 | Meda Ab | Método e composição para tratamento de distúrbios inflamatórios |
| GB0516156D0 (en) | 2005-08-05 | 2005-09-14 | Eisai London Res Lab Ltd | JNK inhibitors |
| JP2009504776A (ja) | 2005-08-18 | 2009-02-05 | アクセラロクス, インコーポレイテッド | アラキドン酸代謝経路またはシグナル伝達経路を調節することによる骨を処置するための方法 |
| US7394658B2 (en) | 2005-09-01 | 2008-07-01 | Harman International Industries, Incorporated | Heat sink with twist lock mounting mechanism |
| ES2379987T3 (es) | 2005-10-11 | 2012-05-07 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Compuestos de benzofurano marcados isotópicamente como radiotrazadores para proteínas amiloidógenas |
| US7405302B2 (en) | 2005-10-11 | 2008-07-29 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| EP1947943A4 (en) | 2005-10-21 | 2009-11-25 | Univ Alabama | SMALL MOLECULAR INHIBITORS OF HIV-1 CAPSIDE FORMATION |
| UY29892A1 (es) | 2005-11-04 | 2007-06-29 | Astrazeneca Ab | Nuevos derivados de cromano, composiciones farmaceuticas conteniendolos, procesos de preparacion y aplicaciones |
| UY29896A1 (es) | 2005-11-04 | 2007-06-29 | Astrazeneca Ab | Nuevos derivados de cromano, composiciones farmacéuticas conteniéndolos, procesos de preparación y aplicaciones |
| US20070225285A1 (en) | 2005-11-04 | 2007-09-27 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| GB2431927B (en) | 2005-11-04 | 2010-03-17 | Amira Pharmaceuticals Inc | 5-Lipoxygenase-activating protein (FLAP) inhibitors |
| US20070219206A1 (en) | 2005-11-04 | 2007-09-20 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| US8399666B2 (en) | 2005-11-04 | 2013-03-19 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| US7977359B2 (en) | 2005-11-04 | 2011-07-12 | Amira Pharmaceuticals, Inc. | 5-lipdxygenase-activating protein (FLAP) inhibitors |
| US20070244128A1 (en) | 2005-11-04 | 2007-10-18 | Amira Pharmaceuticals, Inc. | 5-lipoxygenase-activating protein (flap) inhibitors |
| NL2000284C2 (nl) | 2005-11-04 | 2007-09-28 | Pfizer Ltd | Pyrazine-derivaten. |
| AR059901A1 (es) | 2006-03-20 | 2008-05-07 | Bayer Pharmaceuticals Corp | Compuestos de tetrahidropiridotienopirimidina utiles para tratar o prevenir trastornos proliferativos celulares. |
| TW200815377A (en) | 2006-04-24 | 2008-04-01 | Astellas Pharma Inc | Oxadiazolidinedione compound |
| EP2041071B1 (en) | 2006-06-29 | 2014-06-18 | Kinex Pharmaceuticals, LLC | Biaryl compositions and methods for modulating a kinase cascade |
| JP2009023986A (ja) | 2006-11-08 | 2009-02-05 | Pharma Ip | 抗癌剤としてのビアリール誘導体 |
| EP2848610B1 (en) | 2006-11-15 | 2017-10-11 | YM BioSciences Australia Pty Ltd | Inhibitors of kinase activity |
| WO2008067566A1 (en) | 2006-11-30 | 2008-06-05 | Amira Pharmaceuticals, Inc. | Compositions and treatments comprising 5-lipoxygenase-activating protein inhibitors and nitric oxide modulators |
| US20100204282A1 (en) | 2007-02-05 | 2010-08-12 | Hutchinson John H | Reverse indoles as 5-lipoxygenase-activating protein (FLAP) inhibitors |
| US8039505B2 (en) | 2007-04-11 | 2011-10-18 | University Of Utah Research Foundation | Compounds for modulating T-cells |
| WO2009002746A1 (en) | 2007-06-22 | 2008-12-31 | Decode Genetics Ehf. | Dosing schedules of leukotriene synthesis inhibitors for human therapy |
| WO2009009041A2 (en) | 2007-07-06 | 2009-01-15 | Kinex Pharmaceuticals, Llc | Compositions and methods for modulating a kinase cascade |
| JP2010540641A (ja) | 2007-10-05 | 2010-12-24 | アミラ ファーマシューティカルス,インコーポレーテッド | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 |
| TW200920369A (en) | 2007-10-26 | 2009-05-16 | Amira Pharmaceuticals Inc | 5-lipoxygenase activating protein (flap) inhibitor |
| US8685740B2 (en) | 2008-03-14 | 2014-04-01 | National Jewish Health | Methods to determine susceptibility to treatment with leukotriene modifiers |
| SG190667A1 (en) | 2008-05-23 | 2013-06-28 | Panmira Pharmaceuticals Llc | 5-lipoxygenase-activating protein inhibitor |
| US8546431B2 (en) | 2008-10-01 | 2013-10-01 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
-
2006
- 2006-10-27 US US11/553,946 patent/US7977359B2/en not_active Expired - Fee Related
- 2006-10-30 RS RS20120006A patent/RS52189B/en unknown
- 2006-10-30 DK DK06836773.9T patent/DK1943219T3/da active
- 2006-10-30 PT PT06836773T patent/PT1943219E/pt unknown
- 2006-10-30 BR BRPI0618046-9A patent/BRPI0618046A2/pt not_active Application Discontinuation
- 2006-10-30 CN CN201110179642A patent/CN102295637A/zh active Pending
- 2006-10-30 NZ NZ567718A patent/NZ567718A/en not_active IP Right Cessation
- 2006-10-30 KR KR1020087013547A patent/KR101031766B1/ko active IP Right Grant
- 2006-10-30 JP JP2008539007A patent/JP4705986B2/ja not_active Expired - Fee Related
- 2006-10-30 WO PCT/US2006/042690 patent/WO2007056021A2/en active Application Filing
- 2006-10-30 EP EP11171816A patent/EP2404904A1/en not_active Withdrawn
- 2006-10-30 NZ NZ592541A patent/NZ592541A/xx not_active IP Right Cessation
- 2006-10-30 CA CA2628490A patent/CA2628490C/en not_active Expired - Fee Related
- 2006-10-30 AU AU2006311973A patent/AU2006311973B9/en not_active Ceased
- 2006-10-30 SG SG201008041-4A patent/SG166813A1/en unknown
- 2006-10-30 EP EP06836773A patent/EP1943219B8/en active Active
- 2006-10-30 ES ES06836773T patent/ES2373977T3/es active Active
- 2006-10-30 MY MYPI20081429 patent/MY151159A/en unknown
- 2006-10-30 SI SI200631225T patent/SI1943219T1/sl unknown
- 2006-10-30 PL PL06836773T patent/PL1943219T3/pl unknown
- 2006-10-30 EA EA201000584A patent/EA018616B1/ru not_active IP Right Cessation
- 2006-10-30 AT AT06836773T patent/ATE530521T1/de active
- 2006-10-30 EA EA200801163A patent/EA015495B1/ru not_active IP Right Cessation
-
2008
- 2008-04-15 IL IL190873A patent/IL190873A0/en not_active IP Right Cessation
- 2008-04-16 NO NO20081838A patent/NO342361B1/no not_active IP Right Cessation
- 2008-04-28 CR CR9942A patent/CR9942A/es unknown
- 2008-05-05 MA MA30900A patent/MA29931B1/fr unknown
- 2008-08-25 HK HK08109452.4A patent/HK1114099A1/xx not_active IP Right Cessation
-
2009
- 2009-12-04 JP JP2009276800A patent/JP5451347B2/ja not_active Expired - Fee Related
-
2010
- 2010-11-10 AU AU2010241356A patent/AU2010241356B2/en not_active Ceased
-
2011
- 2011-01-24 US US13/012,045 patent/US20110118315A1/en not_active Abandoned
- 2011-01-28 JP JP2011015870A patent/JP5506707B2/ja active Active
- 2011-05-24 IL IL213107A patent/IL213107A0/en unknown
-
2012
- 2012-01-10 HR HR20120033T patent/HRP20120033T1/hr unknown
- 2012-01-11 CY CY20121100021T patent/CY1112383T1/el unknown
-
2013
- 2013-07-16 US US13/942,934 patent/US8710081B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5420282A (en) * | 1994-02-15 | 1995-05-30 | Abbott Laboratories | Thiopyrano(2,3,4-c,d) indolyloxime ether alkylcarboxylates |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011520982A (ja) * | 2008-05-23 | 2011-07-21 | アミラ ファーマシューティカルス,インコーポレーテッド | 5−リポキシゲナーゼ活性化タンパク質阻害剤 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4705986B2 (ja) | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 | |
| JP5320590B2 (ja) | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 | |
| AU2008247672B2 (en) | 5-lipoxygenase-activating protein (FLAP) inhibitors | |
| US8399666B2 (en) | 5-lipoxygenase-activating protein (FLAP) inhibitors | |
| US20070225285A1 (en) | 5-lipoxygenase-activating protein (flap) inhibitors | |
| JP2010526817A (ja) | 5−リポキシゲナーゼ活性化タンパク質(flap)阻害剤 | |
| US8546431B2 (en) | 5-lipoxygenase-activating protein (FLAP) inhibitors | |
| CN101331117A (zh) | 5-脂氧合酶活化蛋白(flap)抑制剂 | |
| MX2008005633A (en) | 5-lipoxygenase-activating protein (flap) inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091204 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20091204 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20091224 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100119 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100413 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100420 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100716 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20100716 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20101012 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110128 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110214 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110308 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110314 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4705986 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |