JP2017108752A - 抗αβTCR抗体 - Google Patents
抗αβTCR抗体 Download PDFInfo
- Publication number
- JP2017108752A JP2017108752A JP2017024560A JP2017024560A JP2017108752A JP 2017108752 A JP2017108752 A JP 2017108752A JP 2017024560 A JP2017024560 A JP 2017024560A JP 2017024560 A JP2017024560 A JP 2017024560A JP 2017108752 A JP2017108752 A JP 2017108752A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- seq
- humanized
- human
- set forth
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2893—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD52
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1138—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against receptors or cell surface proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/71—Decreased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Abstract
Description
重鎖可変領域を含み、フレームワークの38位、44位および/または48位のうち1つまたはそれ以上はドナー残基であり、その代わりの実施形態において、フレームワークの44位および48位はドナー残基である。
本発明は、ヒト化抗αβTCR抗体の抗原結合断片を包含する。上記抗体の断片は、αβTCR.CD3複合体と結合することができる。このような断片は、Fab、Fab’、F(ab’)2、およびF(v)断片、または個々の軽鎖または重鎖可変領域もしくはそれらの部分を包含する。断片としては、例えば、Fab、Fab’、F(ab’)2、FvおよびscFvが挙げられる。これらの断片は、無傷抗体のFc部分がなく、無傷抗体よりも迅速に循環系から排出され、無傷抗体よりも非特異的な組織結合を少なくすることができる。これらの断片は、周知の方法を用いて無傷抗体から生産することができ、例えばパパイン(Fab断片を生産する)またはペプシン(F(ab’)2断片を生産する)などの酵素でのタンパク質分解的切断によって生産することができる。
抗体の重鎖可変領域(VH)を含み、これらの重鎖可変領域および軽鎖可変領域は、一緒
にまたは個々に、αβTCRと結合する結合部位を形成する。scFvは、アミノ末端の端部にVH領域、およびカルボキシ末端の端部にVL領域を含んでいてもよい。あるいはscFvは、アミノ末端の端部にVL領域、およびカルボキシ末端の端部にVH領域を含んでいてもよい。さらに、Fv断片の2つのドメイン、VLおよびVHは別々の遺伝子によってコードされているが、組換え法を用いて、これらをVL領域とVH領域とが対になった単一のタンパク質鎖にすることができる合成リンカーによって連結して、1価の分子(単鎖Fv(scFv)として知られている)を形成することができる。scFvは、場合により、重鎖可変領域と軽鎖可変領域との間にポリペプチドリンカーをさらに含んでいてもよい。
本明細書に記載の抗体の可変ドメインのアミノ酸配列は、配列番号5〜7および12〜16に記載される。抗体産生は、当技術分野で周知のいかなる技術によっても行うことができ、例えば、ヤギ(Pollockら(1999)J.Immunol.Methods 231:147〜157を参照)、ニワトリ(Morrow,K.J.J.(2000)Genet.Eng.News 20:1〜55を参照)、マウス(上記のPollockらを参照)、または植物(Doran,P.M.(2000)Curr.Opinion Biotechnol.11:199〜204、Ma.J.K−C.(1998)Nat.Med.4:601〜606、Baez,J.ら(2000)BioPharm.13:50〜54、Stoger,E.ら(2000)Plant Mol.Biol.42:583〜590を参照)などのトランスジェニック生物において行うことができる。また抗体は、化学合成によって、または宿主細胞での抗体をコードする遺伝子の発現によっても生産することができる。
T細胞活性の抑制は、免疫抑制が認められる、および/または自己免疫性状態が発生する多数の状況において望ましい。従って、不適切な、または望ましくない免疫反応、例えば炎症、自己免疫、およびこのようなメカニズムが関与するその他の状態が関与する疾患の治療において、αβTCR.CD3複合体の標的化が必要である。一実施形態において、このような疾患または障害は、自己免疫および/または炎症性疾患である。このような自己免疫および/または炎症性疾患の例は、全身性エリテマトーデス(SLE)、リウマチ様関節炎(RA)および炎症性腸疾患(IBD)(例えば潰瘍性大腸炎(UC)およびクローン病(CD)など)、多発性硬化症(MS)、強皮症および1型糖尿病(T1D)、ならびにその他の疾患および障害、例えばPV(尋常性天疱瘡)、乾癬、アトピー性皮膚炎、セリアック病、慢性閉塞性肺疾患、橋本甲状腺炎、グレーブス病(甲状腺)、シェーグレン症候群、ギヤン−バレー症候群、グッドパスチャー症候群、アディソン病、ヴェグナー肉芽腫症、原発性胆管硬化症、硬化性胆管炎、自己免疫性肝炎、リウマチ性多発性筋痛、レイノー現象、側頭動脈炎、巨細胞性動脈炎、自己免疫性溶血性貧血、悪性貧血、結節性多発性動脈炎、ベーチェット病、原発性胆汁性肝硬変、ブドウ膜炎、心筋炎、リウマチ熱、強直性脊椎炎、糸球体腎炎、サルコイドーシス、皮膚筋炎、重症筋無力症、多発性筋炎、円形脱毛症、および白斑である。
好ましい実施形態において、本発明に係る抗体、または本発明の前述の態様で定義されたようなアッセイ方法によって同定可能なリガンドもしくは複数のリガンドを含む医薬組成物が提供される。リガンドは、本明細書で考察されたような、免疫グロブリン、ペプチド、核酸または低分子物質であってもよい。以下の考察において、これらは「化合物」と称される。
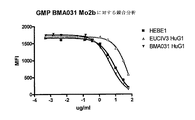
EuCIV3の結合および生物活性はBMA031と比較して低い
フローサイトメトリーを用いて、発明者等は、EuCIV3は、T細胞の結合に関してBMA031より劣っていることを示した(図1)。この競合アッセイでは、固定濃度の直接フィコエリトリンで標識したMoIgG2b−BMA031(マウスの競合剤)および濃度を増加させた抗αβTCR抗体の存在下で、T細胞を氷上でインキュベートした。20分インキュベートした後、細胞を洗浄し、表面に直接結合したフィコエリトリン標識MoIgG2b−BMA031をフローサイトメトリーによって検出した。BMA031 HuIgG1キメラ抗体は、EuCIV3よりもかなり効果的に競合した。
orp.、Van Nuys、CAから得た。フィコール(GE Healthcare、Piscataway、NJ)上で遠心分離することによってPBMCを単離した。磁気ビーズ(Invitrogen、Carlsbad、California)を製造元の説明書に従って用いてCD8+T細胞を単離した。自己由来の未成熟の樹状細胞を得るために、PBMCをRPMI1640/5%ヒトAB血清(Sigma)中に再懸濁し、三連フラスコ(Corning)で平板培養し、37℃/5%CO2で2時間より長くインキュベートした。続いて付着単球をPBSですすぎ、GM−CSF(Immunex、Seattle、WA)およびIL−4(PeproTech、RockyHill、NJ)が補足されたRPMI1640/5%ヒトAB血清中で6日間培養した。T細胞/DCの共培養を安定化させる前、DCに4時間にわたりペプチド(10μg/ml)をパルス投与し、次いで成熟させた。50ng/mlのTNF−アルファ、25ng/mlのIL−1β、10ng/mlのIL−6、500ng/mlのPGE−2(PeproTech、Rocky Hill、NJ)を添加し、樹状細胞をさらに24時間培養することにより成熟樹状細胞を作製した。続いてペプチドがパルス投与されたDCを前もって単離したCD8+T細胞に10:1のT:DC比で添加した。IL−2(100IU/ml)を培養物に即座に添加することによって培養物に与えた。4日目にIL−2(100IU/ml)を培養物に補足した。7日目に、クロム放出アッセイでバルクの培養物をペプチド反応性に関してアッセイした。
BMA031キメラ抗体のFc工学
in vitroのプロファイル
発明者等は、アッセイパネルでBMA031のin vitroのプロファイルを評価した。表1は、BMA031のin vitroのプロファイルを示す。これらのアッセイにおいて、BMA031をOKT3と比較した。
結合が改善されたヒト化抗体の構築
発明者等は、HEBE1シリーズ(IGH3−23)およびGL1BMシリーズ(IGHV1−3*01およびIGKV3−11*01;VBase、vbase.mrc−cpe.cam.ac.ukを参照)と称される2つのシリーズのBMA031のヒト化バージョンを作製した。最初にBMA031重鎖のCDR領域をIGH3−23フレームワーク領域(配列番号5および6を参照)にグラフトすることにより、競合アッセイで示した通り(図3)抗体のαβTCRへの結合が改善された;実施例2を参照されたい。しかしながら、この改善は、IVEアッセイで示した通り(図4)抗体の機能的な改善には反映されなかった。
ヒト化抗体の最適化
ヒト化抗体を最適化する方策は、変異誘発および機能的なスクリーニングに基づく。可変ドメインのそれぞれ4つのフレームワーク領域のうち1つにおいて、マウスからヒトへのアミノ酸残基のブロック変化を行うことで最適化を開始した。GL1BM HC、GL1BM LC、およびHEBE1 HCシリーズそれぞれにおいて主要なフレームワーク領域を同定した。この同定後、そのフレームワーク領域内の個々の残基を、元のマウス配列からヒト生殖細胞系の残基に突然変異させた。マウス配列と同一であることが抗体の結合特性を保持するのに重要であることが見出されたフレームワークの残基が、マウス残基として保持されていた。別の方法でフレームワーク残基を変更して、ヒト生殖細胞系のアミノ酸配列と一致させた。抗体の元の結合特性を保持するための最低限のマウス残基が同定されるまで、これを配列全体に対して続けた。図5を参照されたい。発明者等は、T細胞からの抗体オフレートによって決定したところ、これらのシリーズのうちいくつかの抗体が、BMA031と比較して改善された結合を示すことを実証した(図6、7、および8)。
発現された2μg/mLの抗体を含む100μLの完全増殖培地中で、室温で30〜60分インキュベートした。続いて細胞を洗浄し、50μLの完全増殖培地に再懸濁し、解離した候補抗体の再結合を防ぐために20μg/mLのHEBE1F(ab’)2を添加し
た。この時間経過アッセイの最後に、細胞を固定し、細胞表面に結合した残りのHuIgG1−Δab抗体のレベルをフローサイトメトリーでPE標識ヤギ抗HuIgG二次抗体によって測定した。
エフェクター機能を減少させるためのFc突然変異体の作製
天然に存在するAsn297部位の隣のアミノ酸Ser298位にグリコシル化部位が導入されるように改変されたFc変異体を設計して作製した。Asn297でのグリコシル化は、維持するか、または突然変異でノックアウトするかのいずれかとした。表2に突然変異およびグリコシル化の結果を示す。
改変されたH66 IgG1 Fc変異体を、20mMのDTTで37℃で30分、部分的に還元した。QSTAR qq TOFハイブリッドシステム(Applied Biosystem)を備えたアジレント1100(Agilent 1100)キャピラリーHPLCシステムでのキャピラリーLC/MSによってサンプルを解析した。アナリストQS1.1(Analyst QS1.1)(Applied Bisoystem)での基準の補正およびコンピューターモデリングによるベイズのタンパク質再構築をデータ解析に使用した。突然変異体S298N/T299A/Y300S H66リード抗体に関して、アミノ酸298位に1つのグリコシル化部位が観察され、主要な種として二分岐および三分岐の複合型グリカン、加えてG0F、G1F、およびG2Fが検出された。
Biacoreを用いて、組換えヒトFcγRIIIa(V158およびF158)およびFcγRIへの結合を評価した。CM5チップの4つ全てのフローセルを、Biacoreによって提供された標準的なアミンカップリング法で抗HPC4抗体で固定した。抗HPC4抗体をカップリング反応のためにpH5.0の10mMの酢酸ナトリウムで50μg/mLに希釈し、5μL/分で25分注入した。チップ表面におよそ12,000RUの抗体を固定した。組換えヒトFcγRIIIa−V158およびFcγRIIIa−F158を、結合緩衝液の1mMのCaCl2を含むHBS−Pで0.6μg/mLに希釈し、フローセル2および4それぞれに5μL/分で3分注入し、抗HPC4チップに300〜400RUの受容体を捕捉した。弱い結合物質を識別するために、このアッセイで通常用いられる量より3倍多くのrhFcγRIIIaを抗HPC4表面に捕捉させた。参照対照としてフローセル1および3を使用した。各抗体を結合緩衝液で200nMに希釈し、4つ全てのフローセルに4分注入し、続いて緩衝液中で5分解離させた。表面をHBS−EP緩衝液中の10mMのEDTAで20μL/分で3分再生した。
Far−UV CD熱融解実験によるS298N/T299A/Y300S抗体の突然変異体の安定性のモニターは、216nmおよび222nmにおけるCDシグナルを、最終的に抗体のアンフォールディングを引き起こすまで温度を上昇させながらモニターすることによりなされた。ジャスコ815(Jasco 815)分光光度計で、PBS緩衝液中およそ0.5mg/mLのタンパク質濃度で、パス長10mmの石英キュベット(Hellma,Inc)でCDスペクトルを回収した。熱電気でのペルチエ効果(ジャスコのモデルAWC100)によって温度を制御し、1℃/分の速度で25℃から89℃に温度を徐々に高めた。CDシグナルおよびHT電圧の両方のデータを取った。210〜260nmの範囲で、0.5nmのデータインターバル、1℃の温度インターバルでデータを得た。スキャン速度は50nm/分であり、データピッチは0.5nmであった。培地の感度設定で2.5nmの帯域幅を使用した。サンプルごとにスキャンを4回重複して行った。結果から、デルタAB H66およびS298N/T299A/Y300S H66突然変異体はいずれも、類似の熱挙動を示し、約63℃の同じ分解開始温度を有することが示唆される。言い換えれば、この突然変異体は、デルタAB様式と同等に安定である。
Fcで改変された突然変異体の機能的な解析
実施例2に記載されたようにしてPBMC増殖およびサイトカイン放出アッセイを行った。正常なドナーのPBMCを融解し、以下の条件下で処理した(全て補体を含む培地中で):
・未処理
・BMA031、moIgG2b 10μg/ml
・OKT3、moIgG2a 10μg/ml
・H66、huIgG1デルタAB 10μg/ml、1μg/ml、および0.1μg/ml
・H66、huIgG1 S298N/T299A/Y300S 10μg/ml、1μg/ml、および0.1μg/ml。
二重特異性抗体
一方のアームが腫瘍標的と結合でき、他方がαβTCRを介してT細胞と結合できるように短いアミノ酸リンカーを介して一緒に連結された2つの単鎖抗体(scFv)で構成される二重特異性分子を構築した。二重特異性分子は、本明細書では、TRACER(T cell Receptor Activated Cytotoxic EnableR)と称される。
GL1BMΔS×VK1
GL1BMΔS×VK27
GL1BMΔSVH11×VK1
GL1BMΔSVH15×VK1
GL1BMΔSVH28×VK43
GL1BMΔSVH31×VK43。
本明細書において記述されるFc突然変異の適応性に関する概説を試験するために、抗CD52抗体でグリコシル化突然変異体S298N/Y300Sも製造して(クローン2C3)、FcγRIII結合がないエフェクター機能のモジュレーションが異なる抗体主鎖にも当てはまるかどうかを調べた。クイックチェンジ変異誘発によってS298N/Y300S 2C3変異体のDNAを製造した。HEK293の一過性トランスフェクション後、タンパク質を調整培地から精製した。対照として抗CD52 2C3野生型抗体を平行して生産した。Biacoreを用いて、精製した抗体の抗原結合、FcγRIII、および結合特性を特徴付けた(図26を参照)。
Fcのエフェクター機能をアッセイするために、結合研究にFcγRIII受容体(Val158)を使用した。突然変異体および野生型対照抗体を200nMに希釈し、HPC4−タグで捕捉したFcγRIIIaに注入した。FcγRIII結合は、S298N/Y300S突然変異体ではほとんど検出できなかったが、これは、この変異体はエフェクター機能を喪失したことを示す(図26B)。またこの突然変異体は、野生型抗体対照と同じ親和性でFcRn受容体にも結合したことから、発明者等は、その循環半減期またはその他の薬物動態学的特性は変化しないと予想する。(図26Cを参照)。発明者等は、例えばヒトFcγ受容体のエンゲージメントにより望ましくないFcのエフェクター機能を減少させたりまたは除去したりするために、S298N/Y300S突然変異は一般的に抗体に適用が可能であると結論付けた。
Claims (28)
- 配列番号7、12または13に記載のCDRと、配列番号17に記載のヒトIGH3−23フレームワークとを含む重鎖可変領域を含み、フレームワークの6位はドナー残基である、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号7、12または13に記載のCDRと、配列番号17に記載のヒトIGH3−23フレームワークとを含む重鎖可変領域を含み、フレームワークの18位はドナー残基である、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- フレームワークの49位および/または69位はドナー残基である、請求項1または2に記載のヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号15または16に記載のCDRと、配列番号18に記載のヒトIGHV1−3*01フレームワークとを含む重鎖可変領域を含み、フレームワークの38位、44位および/または48位のうち1つまたはそれ以上はドナー残基である、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号15または16に記載のCDRと、配列番号18に記載のヒトIGHV1−3*01フレームワークとを含む重鎖可変領域を含み、フレームワークの44位および48位はドナー残基である、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号14に記載のCDRと、配列番号19に記載のヒトIGKV3−11*01フレームワークとを含む軽鎖可変領域を含み、フレームワークの70位および/または71位はドナー残基である、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- フレームワークの46位はドナー残基である、請求項6に記載のヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号7、配列番号12、および配列番号13に記載のアミノ酸配列を含む重鎖から選択される重鎖可変領域と、配列番号14に記載のアミノ酸配列を含む軽鎖可変領域の配列とを含む、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- 配列番号15および配列番号16に記載のアミノ酸配列を含む重鎖から選択される重鎖可変領域と、配列番号14に記載のアミノ酸配列を含む軽鎖可変領域とを含む、ヒトαβTCR/CD3複合体に特異的なヒト化モノクローナル抗体。
- ヒト由来の定常領域をさらに含む、請求項1〜9のいずれか1項に記載のヒト化抗体。
- Fcγ受容体結合を減少させるFc改変をさらに含む、請求項10に記載のヒト化抗体。
- 非グリコシル化Fc領域またはデルタab改変を含む、請求項11に記載のヒト化抗体。
- 改変されたグリコシル化パターンを含む、請求項11に記載のヒト化抗体。
- 突然変異S298N、T299A、およびY300Sのうち1つまたはそれ以上を含む、請求項13に記載のヒト化抗体。
- 突然変異N297Q、S298N、T299A、およびY300Sのうち2つまたはそれ以上を含む、請求項14に記載のヒト化抗体。
- 複数の突然変異N297Q/S298N/Y300S、S298N/T299A/Y300SまたはS298N/Y300Sを含む、請求項14に記載のヒト化抗体。
- 請求項1〜16のいずれか1項に記載のヒト化モノクローナル抗体の、少なくとも1つの重鎖可変領域をコードする核酸。
- 請求項17に記載の核酸を発現する細胞。
- 対象におけるT細胞媒介応答を抑制するのに使用するための、請求項1〜16のいずれか1項に記載のヒト化抗体。
- T細胞媒介応答が、固形臓器移植および複合組織移植を含めた組織移植、組織グラフト、多発性硬化症、ならびに1型糖尿病から選択される状態に関連する、請求項19に記載のヒト化抗体。
- 改変Fcを含む抗体であって、前記改変Fcは、Fcγ受容体結合を減少させる改変グリコシル化パターンを含み、突然変異S298N、T299A、およびY300Sのうち1つまたはそれ以上を含む、上記抗体。
- 突然変異N297Q、S298N、T299A、およびY300Sのうち2つまたはそれ以上を含む、請求項21に記載の抗体。
- 複数の突然変異N297Q/S298N/Y300S、S298N/T299A/Y300SまたはS298N/Y300Sを含む、請求項14に記載の抗体。
- 抗体は、請求項1〜10のいずれか1項に記載のヒト化抗体である、請求項21〜23のいずれか1項に記載の抗体。
- 請求項1〜9のいずれか1項に記載の第1の結合ドメインおよび腫瘍特異抗原に特異的な第2の結合ドメインの少なくとも1つの重鎖を含む、多重特異性を有する抗体。
- 請求項4、5または9のいずれか1項に記載の結合ドメインの、少なくとも1つの重鎖を含む、請求項25に記載の多重特異性を有する抗体。
- 抗αβTCR/CD3 scFvと、抗腫瘍scFvとを含む、請求項25または26に記載の多重特異性を有する抗体。
- 二重特異性を有する、請求項25〜27のいずれか1項に記載の多重特異性を有する抗体。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161533510P | 2011-09-12 | 2011-09-12 | |
| US61/533,510 | 2011-09-12 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014528901A Division JP6096196B2 (ja) | 2011-09-12 | 2012-09-12 | 抗αβTCR抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017108752A true JP2017108752A (ja) | 2017-06-22 |
| JP6599911B2 JP6599911B2 (ja) | 2019-10-30 |
Family
ID=46851393
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014528901A Active JP6096196B2 (ja) | 2011-09-12 | 2012-09-12 | 抗αβTCR抗体 |
| JP2017024560A Active JP6599911B2 (ja) | 2011-09-12 | 2017-02-14 | 抗αβTCR抗体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014528901A Active JP6096196B2 (ja) | 2011-09-12 | 2012-09-12 | 抗αβTCR抗体 |
Country Status (34)
| Country | Link |
|---|---|
| US (3) | US10017573B2 (ja) |
| EP (1) | EP2755999B1 (ja) |
| JP (2) | JP6096196B2 (ja) |
| KR (1) | KR20140072092A (ja) |
| CN (2) | CN110272492A (ja) |
| AU (2) | AU2012307816C1 (ja) |
| BR (2) | BR112014005644A2 (ja) |
| CA (1) | CA2847949C (ja) |
| CL (2) | CL2014000574A1 (ja) |
| CO (1) | CO6930307A2 (ja) |
| CR (1) | CR20140127A (ja) |
| DK (1) | DK2755999T3 (ja) |
| DO (1) | DOP2014000052A (ja) |
| EC (1) | ECSP14013307A (ja) |
| ES (1) | ES2667893T3 (ja) |
| GT (1) | GT201400045A (ja) |
| HK (1) | HK1199268A1 (ja) |
| HU (1) | HUE037470T2 (ja) |
| IL (2) | IL231304B (ja) |
| LT (1) | LT2755999T (ja) |
| MA (1) | MA35711B1 (ja) |
| MX (1) | MX355735B (ja) |
| MY (1) | MY173924A (ja) |
| NI (1) | NI201400019A (ja) |
| PE (1) | PE20141548A1 (ja) |
| PL (1) | PL2755999T3 (ja) |
| PT (1) | PT2755999T (ja) |
| RU (2) | RU2017129721A (ja) |
| SG (2) | SG10201601738UA (ja) |
| TN (1) | TN2014000107A1 (ja) |
| TW (1) | TWI593706B (ja) |
| UA (1) | UA115533C2 (ja) |
| UY (1) | UY34317A (ja) |
| WO (1) | WO2013037484A2 (ja) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UY34317A (es) | 2011-09-12 | 2013-02-28 | Genzyme Corp | Anticuerpo antireceptor de célula T (alfa)/ß |
| US9790268B2 (en) | 2012-09-12 | 2017-10-17 | Genzyme Corporation | Fc containing polypeptides with altered glycosylation and reduced effector function |
| PT3366705T (pt) * | 2012-09-12 | 2023-07-19 | Genzyme Corp | Polipéptidos contendo fc com glicosilação alterada e função efetora reduzida |
| IL275376B2 (en) | 2013-03-11 | 2024-01-01 | Genzyme Corp | Polypeptides with hyperglycosidic bonds |
| SG10201803473WA (en) * | 2013-10-30 | 2018-06-28 | Genzyme Corp | Methods for enhancing immunosuppressive therapy by multiple administration of alpha beta tcr-binding polypeptide |
| SG10201808158UA (en) | 2014-03-19 | 2018-10-30 | Genzyme Corp | Site-specific glycoengineering of targeting moieties |
| CA2964123C (en) | 2014-10-09 | 2023-09-05 | Genzyme Corporation | Glycoengineered antibody drug conjugates |
| WO2016059220A1 (en) | 2014-10-16 | 2016-04-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Tcr-activating agents for use in the treatment of t-all |
| KR20180020202A (ko) * | 2015-06-01 | 2018-02-27 | 메디진 이뮤노테라피스 게엠바하 | T 세포 수용체 특이적 항체 |
| CA3069842A1 (en) | 2017-07-14 | 2019-01-17 | Immatics Biotechnologies Gmbh | Improved dual specificity polypeptide molecule |
| RU2708558C1 (ru) * | 2018-12-13 | 2019-12-09 | Российская Федерация, от имени которой выступает ФОНД ПЕРСПЕКТИВНЫХ ИССЛЕДОВАНИЙ | Способ создания противоопухолевой иммунологической защиты к клеткам лимфомы EL-4 |
| MA55529A (fr) | 2019-04-03 | 2022-02-09 | Genzyme Corp | Polypeptides de liaison anti-alpha bêta tcr à fragmentation réduite |
| KR102503349B1 (ko) | 2019-05-14 | 2023-02-23 | 프로벤션 바이오, 인코포레이티드 | 제1형 당뇨병을 예방하기 위한 방법 및 조성물 |
| CN113122503B (zh) * | 2019-12-30 | 2022-10-11 | 博雅缉因(北京)生物科技有限公司 | 一种靶向t细胞淋巴瘤细胞的通用型car-t及其制备方法和应用 |
| WO2021136415A1 (zh) * | 2019-12-30 | 2021-07-08 | 博雅辑因(北京)生物科技有限公司 | 一种纯化ucart细胞的方法与应用 |
| CN113122504A (zh) * | 2019-12-30 | 2021-07-16 | 博雅辑因(北京)生物科技有限公司 | 一种纯化ucart细胞的方法与应用 |
| CN113088495A (zh) * | 2020-01-09 | 2021-07-09 | 苏州方德门达新药开发有限公司 | 工程改造的t细胞、其制备及应用 |
| WO2023227018A1 (zh) * | 2022-05-25 | 2023-11-30 | 羿尊生物医药(浙江)有限公司 | 靶向细胞膜受体蛋白的融合蛋白及其应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006197930A (ja) * | 2004-12-22 | 2006-08-03 | Hiroshima Pref Gov | ヒト抗体酵素およびその生産方法 |
| WO2010027797A1 (en) * | 2008-08-26 | 2010-03-11 | Macrogenics Inc. | T-cell receptor antibodies and methods of use thereof |
Family Cites Families (120)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| GB8422238D0 (en) | 1984-09-03 | 1984-10-10 | Neuberger M S | Chimeric proteins |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| EP0307434B2 (en) | 1987-03-18 | 1998-07-29 | Scotgen Biopharmaceuticals, Inc. | Altered antibodies |
| US5149782A (en) | 1988-08-19 | 1992-09-22 | Tanox Biosystems, Inc. | Molecular conjugates containing cell membrane-blending agents |
| EP0359096B1 (en) | 1988-09-15 | 1997-11-05 | The Trustees Of Columbia University In The City Of New York | Antibodies having modified carbohydrate content and methods of preparation and use |
| US6780613B1 (en) | 1988-10-28 | 2004-08-24 | Genentech, Inc. | Growth hormone variants |
| US5108921A (en) | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| CA2018248A1 (en) | 1989-06-07 | 1990-12-07 | Clyde W. Shearman | Monoclonal antibodies against the human alpha/beta t-cell receptor, their production and use |
| ES2246502T3 (es) | 1990-08-29 | 2006-02-16 | Genpharm International, Inc. | Animales no humanos transgenicos capaces de producir anticuerpos heterologos. |
| EP0519596B1 (en) | 1991-05-17 | 2005-02-23 | Merck & Co. Inc. | A method for reducing the immunogenicity of antibody variable domains |
| JPH07501451A (ja) | 1991-11-25 | 1995-02-16 | エンゾン・インコーポレイテッド | 多価抗原結合タンパク質 |
| US5622929A (en) | 1992-01-23 | 1997-04-22 | Bristol-Myers Squibb Company | Thioether conjugates |
| US5837821A (en) | 1992-11-04 | 1998-11-17 | City Of Hope | Antibody construct |
| WO1994026087A2 (en) | 1993-05-14 | 1994-11-24 | Connor Kim C O | Recombinant protein production and insect cell culture and process |
| US5429746A (en) | 1994-02-22 | 1995-07-04 | Smith Kline Beecham Corporation | Antibody purification |
| US5792456A (en) | 1994-08-04 | 1998-08-11 | Bristol-Myers Squibb Company | Mutant BR96 antibodies reactive with human carcinomas |
| ES2167391T3 (es) | 1994-09-16 | 2002-05-16 | Merck Patent Gmbh | Inmunoconjugados ii. |
| GB9422383D0 (en) | 1994-11-05 | 1995-01-04 | Wellcome Found | Antibodies |
| US6121022A (en) | 1995-04-14 | 2000-09-19 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US5739277A (en) | 1995-04-14 | 1998-04-14 | Genentech Inc. | Altered polypeptides with increased half-life |
| US6096871A (en) | 1995-04-14 | 2000-08-01 | Genentech, Inc. | Polypeptides altered to contain an epitope from the Fc region of an IgG molecule for increased half-life |
| WO1996040662A2 (en) | 1995-06-07 | 1996-12-19 | Cellpro, Incorporated | Aminooxy-containing linker compounds and their application in conjugates |
| WO1997014719A1 (en) | 1995-10-16 | 1997-04-24 | Unilever N.V. | A bifunctional or bivalent antibody fragment analogue |
| GB9524973D0 (en) | 1995-12-06 | 1996-02-07 | Lynxvale Ltd | Viral vectors |
| SE9601245D0 (sv) | 1996-03-29 | 1996-03-29 | Pharmacia Ab | Chimeric superantigens and their use |
| UA71889C2 (uk) | 1996-04-02 | 2005-01-17 | Йєда Рісерч Енд Дівелопмент Ко. Лтд. | Модулятори зв'язаного з рецептором tnf фактора (traf), їх одержання та застосування |
| AU3968897A (en) | 1996-08-02 | 1998-02-25 | Bristol-Myers Squibb Company | A method for inhibiting immunoglobulin-induced toxicity resulting from the use of immunoglobulins in therapy and in vivo diagnosis |
| WO1998023289A1 (en) | 1996-11-27 | 1998-06-04 | The General Hospital Corporation | MODULATION OF IgG BINDING TO FcRn |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| ATE419009T1 (de) | 1997-10-31 | 2009-01-15 | Genentech Inc | Methoden und zusammensetzungen bestehend aus glykoprotein-glykoformen |
| US6953675B2 (en) | 1997-11-06 | 2005-10-11 | Immunomedics, Inc. | Landscaped antibodies and antibody fragments for clinical use |
| US6242195B1 (en) | 1998-04-02 | 2001-06-05 | Genentech, Inc. | Methods for determining binding of an analyte to a receptor |
| US6194551B1 (en) | 1998-04-02 | 2001-02-27 | Genentech, Inc. | Polypeptide variants |
| ATE375365T1 (de) | 1998-04-02 | 2007-10-15 | Genentech Inc | Antikörper varianten und fragmente davon |
| US6528624B1 (en) | 1998-04-02 | 2003-03-04 | Genentech, Inc. | Polypeptide variants |
| GB9809951D0 (en) | 1998-05-08 | 1998-07-08 | Univ Cambridge Tech | Binding molecules |
| EP1105427A2 (en) | 1998-08-17 | 2001-06-13 | Abgenix, Inc. | Generation of modified molecules with increased serum half-lives |
| EP1115740A1 (en) | 1998-09-23 | 2001-07-18 | The Regents of the University of California | Synthetic peptides, conjugation reagents and methods |
| EP1006183A1 (en) | 1998-12-03 | 2000-06-07 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Recombinant soluble Fc receptors |
| US7183387B1 (en) | 1999-01-15 | 2007-02-27 | Genentech, Inc. | Polypeptide variants with altered effector function |
| HUP0104865A3 (en) | 1999-01-15 | 2004-07-28 | Genentech Inc | Polypeptide variants with altered effector function |
| US6737056B1 (en) | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| US20020102208A1 (en) | 1999-03-01 | 2002-08-01 | Paul Chinn | Radiolabeling kit and binding assay |
| CN1110322C (zh) | 1999-07-21 | 2003-06-04 | 中国医学科学院医药生物技术研究所 | 单克隆抗体Fab'-平阳霉素偶联物及其抗肿瘤作用 |
| AU2001270609A1 (en) | 2000-06-30 | 2002-01-14 | Vlaams Interuniversitair Instituut Voor Biotechnologie Vzw | Heterodimeric fusion proteins |
| GB0029407D0 (en) | 2000-12-01 | 2001-01-17 | Affitech As | Product |
| EP2341060B1 (en) | 2000-12-12 | 2019-02-20 | MedImmune, LLC | Molecules with extended half-lives, compositions and uses thereof |
| US7829084B2 (en) | 2001-01-17 | 2010-11-09 | Trubion Pharmaceuticals, Inc. | Binding constructs and methods for use thereof |
| US20050107595A1 (en) | 2001-06-20 | 2005-05-19 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| WO2004006955A1 (en) | 2001-07-12 | 2004-01-22 | Jefferson Foote | Super humanized antibodies |
| US6900292B2 (en) | 2001-08-17 | 2005-05-31 | Lee-Hwei K. Sun | Fc fusion proteins of human erythropoietin with increased biological activities |
| US20040002587A1 (en) | 2002-02-20 | 2004-01-01 | Watkins Jeffry D. | Fc region variants |
| US20040018557A1 (en) | 2002-03-01 | 2004-01-29 | Immunomedics, Inc. | Bispecific antibody point mutations for enhancing rate of clearance |
| US20040132101A1 (en) | 2002-09-27 | 2004-07-08 | Xencor | Optimized Fc variants and methods for their generation |
| US7317091B2 (en) | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| GB0216648D0 (en) | 2002-07-18 | 2002-08-28 | Lonza Biologics Plc | Method of expressing recombinant protein in CHO cells |
| EP1534335B9 (en) | 2002-08-14 | 2016-01-13 | Macrogenics, Inc. | Fcgammariib-specific antibodies and methods of use thereof |
| BRPI0314814C1 (pt) | 2002-09-27 | 2021-07-27 | Xencor Inc | anticorpo compreendendo uma variante de fc |
| PT1562972E (pt) | 2002-10-15 | 2010-11-10 | Facet Biotech Corp | Alteração de afinidades de ligação ao fcrn ou semi-vidas séricas de anticorpos por mutagénese |
| EP2368578A1 (en) | 2003-01-09 | 2011-09-28 | Macrogenics, Inc. | Identification and engineering of antibodies with variant Fc regions and methods of using same |
| BRPI0411132B8 (pt) | 2003-06-12 | 2021-05-25 | Lilly Co Eli | protéina de fusão heteróloga e seus usos |
| CN1871259A (zh) | 2003-08-22 | 2006-11-29 | 比奥根艾迪克Ma公司 | 具有改变的效应物功能的经改进的抗体和制备它的方法 |
| RU2392324C2 (ru) * | 2003-09-18 | 2010-06-20 | Симфоген А/С | Способ связывания интересующих последовательностей |
| GB0324368D0 (en) | 2003-10-17 | 2003-11-19 | Univ Cambridge Tech | Polypeptides including modified constant regions |
| KR101520209B1 (ko) | 2003-11-06 | 2015-05-13 | 시애틀 지네틱스, 인크. | 리간드에 접합될 수 있는 모노메틸발린 화합물 |
| CA2545603A1 (en) | 2003-11-12 | 2005-05-26 | Biogen Idec Ma Inc. | Neonatal fc receptor (fcrn)-binding polypeptide variants, dimeric fc binding proteins and methods related thereto |
| US7001978B2 (en) | 2003-11-19 | 2006-02-21 | Xerox Corporation | Unsaturated ester substituted polymers with reduced halogen content |
| EP2221315A1 (en) | 2003-12-04 | 2010-08-25 | Xencor, Inc. | Methods of generating variant proteins with increased host string content and compositions thereof |
| WO2005077981A2 (en) | 2003-12-22 | 2005-08-25 | Xencor, Inc. | Fc POLYPEPTIDES WITH NOVEL Fc LIGAND BINDING SITES |
| DE602005015542D1 (de) | 2004-01-12 | 2009-09-03 | Applied Molecular Evolution | Varianten der fc-region |
| EP2053062A1 (en) | 2004-03-24 | 2009-04-29 | Xencor, Inc. | Immunoglobin variants outside the Fc region |
| WO2005123780A2 (en) | 2004-04-09 | 2005-12-29 | Protein Design Labs, Inc. | Alteration of fcrn binding affinities or serum half-lives of antibodies by mutagenesis |
| ATE455861T1 (de) | 2004-05-04 | 2010-02-15 | Novo Nordisk Healthcare Ag | O-verknüpfte glykoformen von faktor vii und verfahren zu deren herstellung |
| WO2006085967A2 (en) | 2004-07-09 | 2006-08-17 | Xencor, Inc. | OPTIMIZED ANTI-CD20 MONOCONAL ANTIBODIES HAVING Fc VARIANTS |
| EP1919950A1 (en) | 2004-07-15 | 2008-05-14 | Xencor, Inc. | Optimized fc variants |
| EP1791565B1 (en) | 2004-09-23 | 2016-04-20 | Genentech, Inc. | Cysteine engineered antibodies and conjugates |
| EP1799700A4 (en) | 2004-09-27 | 2009-02-11 | Centocor Inc | SRAGE MIMETIC BODIES, COMPOSITIONS, PROCESSES AND USES |
| WO2006047350A2 (en) | 2004-10-21 | 2006-05-04 | Xencor, Inc. | IgG IMMUNOGLOBULIN VARIANTS WITH OPTIMIZED EFFECTOR FUNCTION |
| EP1866339B8 (en) | 2005-03-25 | 2021-12-01 | GITR, Inc. | Gitr binding molecules and uses therefor |
| JP2008537941A (ja) | 2005-03-31 | 2008-10-02 | ゼンコー・インコーポレイテッド | 最適化特性を有するFc変異体 |
| EP1871808A2 (en) | 2005-03-31 | 2008-01-02 | Xencor, Inc. | Fc VARIANTS WITH OPTIMIZED PROPERTIES |
| US8163881B2 (en) | 2005-05-31 | 2012-04-24 | The Board Of Regents Of The University Of Texas System | Immunoglobulin molecules with improved characteristics |
| EP2937360A1 (en) | 2005-06-17 | 2015-10-28 | Merck Sharp & Dohme Corp. | Ilt3 binding molecules and uses therefor |
| CN101506238B (zh) | 2005-06-30 | 2013-11-06 | 森托科尔公司 | 具有提高治疗活性的方法和成分 |
| US7612181B2 (en) | 2005-08-19 | 2009-11-03 | Abbott Laboratories | Dual variable domain immunoglobulin and uses thereof |
| CZ2005627A3 (cs) | 2005-10-03 | 2006-09-13 | Flek@Jaroslav | Zubní kartácek |
| US7846724B2 (en) | 2006-04-11 | 2010-12-07 | Hoffmann-La Roche Inc. | Method for selecting CHO cell for production of glycosylated antibodies |
| JP5597793B2 (ja) * | 2006-06-19 | 2014-10-01 | メルク・シャープ・アンド・ドーム・コーポレーション | Ilt3結合分子およびその使用 |
| FI20060946A0 (fi) | 2006-10-26 | 2006-10-26 | Glykos Finland Oy | Influenssaviruksen nukleiinihappoja ja peptidejä |
| JP2010512306A (ja) | 2006-10-27 | 2010-04-22 | ザ ロックフェラー ユニバーシティー | 抗炎症特性が増強され、細胞毒性特性が減少したポリペプチドおよび関連する方法 |
| CL2007003411A1 (es) | 2006-11-28 | 2008-07-04 | Centelion | Proteina fusion que consiste en una region fc de una inmunoglobulina con un fragmento o dominio soluble de un receptor para fgf; polinucleotido que la codifica y vector y celula que lo comprenden; composicion farmaceutica que comprende la proteina fu |
| DK2740744T3 (da) * | 2007-01-09 | 2018-04-23 | Biogen Ma Inc | Sp35-antistoffer og anvendelser deraf |
| WO2008091954A2 (en) | 2007-01-23 | 2008-07-31 | Xencor, Inc. | Optimized cd40 antibodies and methods of using the same |
| CA2683568A1 (en) | 2007-05-08 | 2008-11-20 | Genentech, Inc. | Cysteine engineered anti-muc16 antibodies and antibody drug conjugates |
| US20100260751A1 (en) | 2007-09-28 | 2010-10-14 | Raju T Shantha | Methods and Structural Conformations of Antibody Preparations with Increased Resistance to Proteases |
| EP2050764A1 (en) | 2007-10-15 | 2009-04-22 | sanofi-aventis | Novel polyvalent bispecific antibody format and uses thereof |
| AU2008312457B2 (en) | 2007-10-19 | 2014-04-17 | Genentech, Inc. | Cysteine engineered anti-TENB2 antibodies and antibody drug conjugates |
| JP5647899B2 (ja) | 2008-01-08 | 2015-01-07 | ラツィオファルム ゲーエムベーハーratiopharm GmbH | オリゴサッカリルトランスフェラーゼを使用するポリペプチドの複合糖質化 |
| SI2657253T1 (sl) | 2008-01-31 | 2017-10-30 | Genentech, Inc. | Protitelesa proti CD79b in imunokonjugati in postopki za uporabo |
| EP2268807A2 (en) | 2008-04-21 | 2011-01-05 | Novo Nordisk A/S | Hyperglycosylated human coagulation factor ix |
| UA40611U (ru) | 2008-05-26 | 2009-04-27 | Владимир Семенович Живченко | Способ десульфурации железоуглеродистого расплава в тигельной печи |
| EP2233499A1 (en) | 2009-03-26 | 2010-09-29 | CSL Behring AG | Antibody composition with altered Fab sialylation |
| US10087236B2 (en) | 2009-12-02 | 2018-10-02 | Academia Sinica | Methods for modifying human antibodies by glycan engineering |
| ME03447B (me) * | 2010-03-04 | 2020-01-20 | Macrogenics Inc | Anтitela reakтivna sa b7-нз, njihovi imunološki akтivni fragmenтi i upotreba |
| EP2603528B1 (en) | 2010-08-10 | 2016-10-12 | Glycotope GmbH | Fab-glycosylated antibodies |
| AR085302A1 (es) | 2011-02-24 | 2013-09-18 | Sanofi Sa | Metodo de produccion de anticuerpos sialilados |
| AU2012229330B2 (en) | 2011-03-11 | 2016-04-21 | Amicus Therapeutics, Inc. | Dosing regimens for the treatment of Fabry disease |
| TWI622597B (zh) | 2011-03-28 | 2018-05-01 | 賽諾菲公司 | 具有交叉結合區定向之雙重可變區類抗體結合蛋白 |
| UY34317A (es) | 2011-09-12 | 2013-02-28 | Genzyme Corp | Anticuerpo antireceptor de célula T (alfa)/ß |
| US9790268B2 (en) | 2012-09-12 | 2017-10-17 | Genzyme Corporation | Fc containing polypeptides with altered glycosylation and reduced effector function |
| PT3366705T (pt) | 2012-09-12 | 2023-07-19 | Genzyme Corp | Polipéptidos contendo fc com glicosilação alterada e função efetora reduzida |
| IL275376B2 (en) | 2013-03-11 | 2024-01-01 | Genzyme Corp | Polypeptides with hyperglycosidic bonds |
| SG10201808158UA (en) | 2014-03-19 | 2018-10-30 | Genzyme Corp | Site-specific glycoengineering of targeting moieties |
| WO2015157446A1 (en) | 2014-04-08 | 2015-10-15 | University Of Georgia Research Foundation Inc. | Site-specific antibody-drug glycoconjugates and methods |
| CA2964123C (en) | 2014-10-09 | 2023-09-05 | Genzyme Corporation | Glycoengineered antibody drug conjugates |
| WO2018071076A2 (en) | 2016-07-07 | 2018-04-19 | Northwestern University | Enhanced conductivity, adhesion and environmental stability of printed graphene inks with nitrocellulose |
-
2012
- 2012-09-10 UY UY0001034317A patent/UY34317A/es not_active Application Discontinuation
- 2012-09-12 BR BR112014005644A patent/BR112014005644A2/pt not_active Application Discontinuation
- 2012-09-12 RU RU2017129721A patent/RU2017129721A/ru not_active Application Discontinuation
- 2012-09-12 MX MX2014002963A patent/MX355735B/es active IP Right Grant
- 2012-09-12 KR KR1020147009515A patent/KR20140072092A/ko not_active Application Discontinuation
- 2012-09-12 BR BR122021001193-1A patent/BR122021001193B1/pt active IP Right Grant
- 2012-09-12 RU RU2014114527A patent/RU2630656C2/ru not_active IP Right Cessation
- 2012-09-12 TW TW101133389A patent/TWI593706B/zh not_active IP Right Cessation
- 2012-09-12 DK DK12759019.8T patent/DK2755999T3/en active
- 2012-09-12 US US14/241,099 patent/US10017573B2/en active Active
- 2012-09-12 EP EP12759019.8A patent/EP2755999B1/en active Active
- 2012-09-12 AU AU2012307816A patent/AU2012307816C1/en not_active Ceased
- 2012-09-12 CN CN201910265294.3A patent/CN110272492A/zh active Pending
- 2012-09-12 LT LTEP12759019.8T patent/LT2755999T/lt unknown
- 2012-09-12 HU HUE12759019A patent/HUE037470T2/hu unknown
- 2012-09-12 CA CA2847949A patent/CA2847949C/en active Active
- 2012-09-12 ES ES12759019.8T patent/ES2667893T3/es active Active
- 2012-09-12 SG SG10201601738UA patent/SG10201601738UA/en unknown
- 2012-09-12 WO PCT/EP2012/003819 patent/WO2013037484A2/en active Application Filing
- 2012-09-12 CN CN201280055556.XA patent/CN104684930B/zh active Active
- 2012-09-12 PT PT127590198T patent/PT2755999T/pt unknown
- 2012-09-12 MY MYPI2014000458A patent/MY173924A/en unknown
- 2012-09-12 SG SG11201400126PA patent/SG11201400126PA/en unknown
- 2012-09-12 PL PL12759019T patent/PL2755999T3/pl unknown
- 2012-09-12 JP JP2014528901A patent/JP6096196B2/ja active Active
- 2012-09-12 PE PE2014000338A patent/PE20141548A1/es active IP Right Grant
- 2012-12-09 UA UAA201403678A patent/UA115533C2/uk unknown
-
2014
- 2014-03-04 IL IL231304A patent/IL231304B/en active IP Right Grant
- 2014-03-10 CL CL2014000574A patent/CL2014000574A1/es unknown
- 2014-03-10 DO DO2014000052A patent/DOP2014000052A/es unknown
- 2014-03-11 GT GT201400045A patent/GT201400045A/es unknown
- 2014-03-11 TN TNP2014000107A patent/TN2014000107A1/en unknown
- 2014-03-11 NI NI201400019A patent/NI201400019A/es unknown
- 2014-03-17 CR CR20140127A patent/CR20140127A/es unknown
- 2014-04-08 CO CO14075370A patent/CO6930307A2/es unknown
- 2014-04-11 MA MA36913A patent/MA35711B1/fr unknown
- 2014-04-11 EC ECSP14013307 patent/ECSP14013307A/es unknown
- 2014-12-22 HK HK14112798.3A patent/HK1199268A1/xx not_active IP Right Cessation
-
2017
- 2017-02-14 JP JP2017024560A patent/JP6599911B2/ja active Active
- 2017-06-29 CL CL2017001730A patent/CL2017001730A1/es unknown
- 2017-11-16 AU AU2017261557A patent/AU2017261557B2/en not_active Ceased
-
2018
- 2018-01-10 US US15/867,364 patent/US11186638B2/en active Active
- 2018-06-05 IL IL259826A patent/IL259826A/en unknown
-
2021
- 2021-10-26 US US17/511,218 patent/US20220153841A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006197930A (ja) * | 2004-12-22 | 2006-08-03 | Hiroshima Pref Gov | ヒト抗体酵素およびその生産方法 |
| WO2010027797A1 (en) * | 2008-08-26 | 2010-03-11 | Macrogenics Inc. | T-cell receptor antibodies and methods of use thereof |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6599911B2 (ja) | 抗αβTCR抗体 | |
| KR102632202B1 (ko) | Cd40 및 cd137에 대한 다중특이적 항체 | |
| CN111406067B (zh) | 与pd-l1和cd137结合的结合剂及其用途 | |
| EP3464367B1 (en) | Bispecific binding proteins binding an immunomodulatory protein and a tumor antigen | |
| KR20100074220A (ko) | Cdr의 아미노산 치환에 의해 항체의 등전점을 개변하는 방법 | |
| JP7093794B2 (ja) | 免疫関連障害のための抗体-サイトカイングラフト化タンパク質及び使用方法 | |
| JP2014515598A (ja) | 二重特異性三鎖抗体様分子 | |
| JP2020525005A (ja) | 抗vista抗体および使用方法 | |
| EP3947458A1 (en) | Anti-alpha beta tcr binding polypeptides with reduced fragmentation | |
| US20230357343A1 (en) | Il-21 polypeptides and targeted constructs | |
| OA16754A (en) | Anti-alphabeta TCR antibody. | |
| NZ717726B2 (en) | Anti-??tcr antibody | |
| NZ623656B2 (en) | Anti-??tcr antibody |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170308 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170308 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180227 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180727 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190108 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190408 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190613 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190903 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20191003 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6599911 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |