JP2010517529A - ヘプシジン及びヘプシジン抗体 - Google Patents
ヘプシジン及びヘプシジン抗体 Download PDFInfo
- Publication number
- JP2010517529A JP2010517529A JP2009548312A JP2009548312A JP2010517529A JP 2010517529 A JP2010517529 A JP 2010517529A JP 2009548312 A JP2009548312 A JP 2009548312A JP 2009548312 A JP2009548312 A JP 2009548312A JP 2010517529 A JP2010517529 A JP 2010517529A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- antibody
- amino acid
- monoclonal antibody
- hepcidin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/26—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against hormones ; against hormone releasing or inhibiting factors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1816—Erythropoietin [EPO]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/12—Drugs for disorders of the metabolism for electrolyte homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1136—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against growth factors, growth regulators, cytokines, lymphokines or hormones
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/74—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving hormones or other non-cytokine intercellular protein regulatory factors such as growth factors, including receptors to hormones and growth factors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
- C12N2310/111—Antisense spanning the whole gene, or a large part of it
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
Abstract
Description
本願は、2007年2月2日に出願された米国仮出願60/888,059号及び2007年12月19日に出願された米国仮出願61/015,138号(これらは、参照により、本明細書に組み込まれる。)の利益を主張する。
本発明は、ヘプシジン、ヘプシジンアンタゴニスト(ヘプシジンを結合する抗体を含む。)及びヘプシジン活性を調節するこれらの能力に関する。
生物的に活性を有するためには、ヘプシジンポリペプチドは、「再折り畳みされ」、適切な三次構造へ酸化され、ジスルフィド結合を生成する必要があり得る。再折り畳みは、本明細書に記載されている手順及び本分野において周知のその他の手順を用いて達成することができる。このような方法は、例えば、カオトロピック剤の存在下で、通常、7を上回るpHへ、可溶化されたポリペプチド剤を曝露することを含む。カオトロピック剤は、塩酸グアニジン(塩酸グアニジニウム、GdnHCl)、硫酸グアニジン、尿素、チオシアン酸ナトリウム、サルコシル、ドデシル硫酸ナトリウム、オクチル硫酸ナトリウム及び/又はタンパク質内の非共有分子間結合を崩壊させ、ポリペプチド鎖が実質的にランダムな立体構造を採ることを可能にする他の化合物など(これらに限定されない。)の化合物である。
本発明の様々な実施形態は、(a)ヘプシジン活性アンタゴニスト又は(b)ヘプシジン発現阻害剤というヘプシジンアンタゴニストの2つの異なるカテゴリーの生産及び使用を提供する。
本発明の様々な実施形態は、ヒトヘプシジンを結合する抗体(モノクローナル抗体を含む。)、このような抗体を生産する方法、ヘプシジンを検出するためにこのような抗体を使用する方法、このような抗体を含む医薬製剤、医薬製剤を調製する方法及び以下に記載されているような赤血球新生刺激物質との組み合わせ療法を含む、医薬製剤を用いて患者を治療する方法を提供する。このような抗体をコードする核酸、ベクター及びこのような核酸を含む組み換え宿主細胞及びこのような抗体を生産する方法も提供される。
2)抗体Ab43、2.7、2.41、R9、1C9;1S1、1S2、1S3、1S4、1S5、3B3;4E1、7A3、9D12、12B9、15E1、18D8、19C1、19D12、19H6、23F11及び26F11のいずれかのCDRH1、CDRH2、CDRH3又は重鎖可変領域の全部を保持するモノクローナル抗体(このようなCDR中には、1つ又は2つの変異を場合によって含む。)、
3)抗体Ab43、2.7、2.41、R9、1C9;1S1、1S2、1S3、1S4、1S5、3B3;4E1、7A3、9D12、12B9、15E1、18D8、19C1、19D12、19H6、23F11及び26F11のいずれかのCDRL1、CDRL2、CDRL3又は軽鎖可変領域の全てを保持するモノクローナル抗体(このようなCDR中には、1つ又は2つの変異を場合によって含む。)、
4)例えば、X線結晶解析学を通じて測定された場合に、抗体Ab43、2.7、2.41、R9、1C9;1S1、1S2、1S3、1S4、1S5、3B3;4E1、7A3、9D12、12B9、15E1、18D8、19C1、19D12、19H6、23F11及び26F11と同じ成熟ヒトヘプシジンのエピトープに結合し、又は配列番号9のアミノ酸1から5内のアミノ酸及び/又は配列番号9のアミノ酸10から13によって形成されるループ内のアミノ酸及び/又は配列番号9のアミノ酸14から22によって形成されるループ内のアミノ酸を含む立体構造エピトープに結合するモノクローナル抗体;並びに
5)成熟ヒトヘプシジンへの結合に関して、約75%超、約80%超、又は約81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%若しくは95%超、抗体Ab43、2.7、2.41、R9、1C9;1S1、1S2、1S3、1S4、1S5、3B3;4E1、7A3、9D12、12B9、15E1、18D8、19C1、19D12、19H6、23F11及び26F11と競合するモノクローナル抗体。
宿主細胞によって認識される調節配列へ場合によって作用可能に連結された、本明細書に記載されているモノクローナル抗体をコードする単離された核酸、該核酸を含むベクター及び宿主細胞、並びに核酸が発現されるように宿主細胞を培養すること、及び宿主細胞培養又は培地から場合によって抗体を回収することを含み得る、抗体を生産するための組換え技術も提供される。
キメラ又はヒト化は、親げっ歯類モノクローナル抗体より、ヒトにおいてより低免疫原性であり、ずっと低いアナフィラキシーのリスクで、ヒトの治療のために使用することができる。従って、ヒトへのインビボ投与を含む治療的用途において、これらの抗体が想定される。
「Human EngineeredTM抗体」という用語は、非ヒト抗体、典型的には、げっ歯類モノクローナル抗体又は可能であればキメラ抗体に由来する抗体を表す。抗体可変ドメインのHuman EngineeringTMが、抗体分子の結合活性を維持しながら免疫原性を低下させるための方法として、Studnicka[例えば、Studnicka et al.米国特許第5,766,886号;Studnicka et al.Protein Engineering7:805−814(1994)参照]によって記載されている。この方法に従えば、各可変領域アミノ酸に、置換のリスクが割り当てられる。アミノ酸置換は、3つのリスクカテゴリーの1つによって区別される。(1)低リスク変化は、免疫原性を低下させる可能性が最も大きく、抗原結合を崩壊させる確率が最も低い変化であり、(2)中リスク変化は、免疫原性をさらに低下させるが、抗原結合又はタンパク質の折り畳みに影響を及ぼす確率がより大きい変化であり、(3)高リスク残基は、結合のために又は抗体構造を維持するために重要であり、抗原結合又はタンパク質の折り畳みが影響を受ける最も高いリスクを有する残基である。プロリンの三次元構造における役割のために、その位置が、典型的には低リスク位置である場合でさえ、プロリンの修飾は、少なくとも中リスク変化であると一般に考えられる。
ヘプシジンに対する抗体は、内在性免疫グロブリン産生を有さず、ヒト免疫グロブリン遺伝子座を含有するように操作されたトランスジェニック動物を用いて生産することも可能である。例えば、WO98/24893号は、内在性重鎖及び軽鎖遺伝子座の不活化のために、動物が機能的な内在性免疫グロブリンを産生しないヒトIg遺伝子座を有するトランスジェニック動物を開示する。WO91/741は、抗体が霊長類定常及び/又は可変領域を有し、並びに内在性免疫グロブリンをコードする遺伝子座が置換又は不活化されている、免疫原に対する免疫応答を引き起こすことができるトランスジェニック非霊長類哺乳動物宿主も開示している。WO96/30498号は、定常又は可変領域の全部又は一部を置換して修飾された抗体分子を形成するためなど、哺乳動物中免疫グロブリン遺伝子座を修飾するためにCre/Lox系を使用することを開示している。WO94/02602号は、不活化された内在性Ig遺伝子座及び機能的ヒトIg遺伝子座を有する非ヒト哺乳動物宿主を開示している。米国特許第5,939,598号は、マウスが内在性の重鎖を欠如し、及び1つ又はそれ以上の異種性定常領域を含む外来性免疫グロブリン遺伝子座を発現するトランスジェニックマウスを作製する方法を開示している。
組換えヒト抗体遺伝子のレパートリーを作製し、糸状バクテリオファージの表面上に、コードされている抗体断片をディスプレイするための技術の発達は、ヒト由来の抗体を作製するための別の手段を提供してきた。ファージディスプレイは、例えば、Dower et al.,WO91/17271、McCafferty et al.,WO92/01047、及び「Caton and Koprowski,Proc.Natl.Acad.Sci.USA,87:6450−6454(1990)」(これらの各々の全体が、参照により、本明細書中に組み込まれる。)に記載されている。ファージ技術によって作製される抗体は、通常、抗原結合断片(例えば、Fv又はFab断片)として、細菌中で生産され、従って、エフェクター機能を欠如する。エフェクター機能は、2つの戦略のうちの1つによって導入することができる。哺乳動物細胞中での発現のための完全な抗体へと、又はエフェクター機能の引き金を引くことができる第二の結合部位を有する二重特異的抗体断片へと断片を操作することができる。
上述されているように、抗体断片は、完全な状態の完全長抗体の一部、好ましくは、完全な状態の抗体の抗原結合又は可変領域を含み、抗体断片には、抗体断片から形成された直鎖抗体及び多重特異的抗体が含まれる。抗体断片の非限定的な例には、Fab、Fab’、F(ab’)2、Fv、Fd、ドメイン抗体(dAb)、相補性決定領域(CDR)断片、一本鎖抗体(scFv)、一本鎖抗体断片、ダイアボディ、トリアボディ、テトラボディ、ミニボディ、直鎖抗体、キレート化組換え抗体、トリボディ又はバイボディ、イントラボディ、ナノボディ、小モジュラー免疫医薬(SMIP)、抗原結合ドメイン免疫グロブリン融合タンパク質、ラクダ化された抗体、VHH含有抗体、又は変異タンパク質若しくはその誘導体、又は抗体が所望の生物活性を保持している限り、CDR配列など、ポリペプチドへの特異的抗原結合を付与するのに十分である免疫グロブリンの少なくとも一部を含有するポリペプチドが含まれる。このような抗原断片は、完全な抗体の修飾によって作製することができ、又は組換えDNA技術若しくはペプチド合成を用いて、新規に合成することができる。
幾つかの実施形態において、多価又は多重特異的(例えば、二重特異的、三重特異的など)モノクローナル抗体さえ作製することが望ましい場合があり得る。このような抗体は、標的抗原の少なくとも2つの異なるエピトープに対して結合特異性を有し得、あるいは、2つの異なる分子に、例えば、標的抗原に及び細胞表面タンパク質若しくは受容体に結合し得る。例えば、二重特異的抗体は、細胞の防御機構を標的発現細胞へ集中させるために、標的に結合するアーム並びにT細胞受容体分子(例えば、CD2又はCD3)などの白血球上のトリガリング分子又はFcγI(CD64)、FcγRII(CD32)及びFcγRIII(CD16)などのIgGに対するFc受容体(FcγR)に結合する別のアームを含み得る。別の例として、標的抗原を発現する細胞へ細胞毒性因子を局在化させるために、二重特異的抗体を使用し得る。これらの抗体は、標的結合アーム及び細胞毒性因子(例えば、サポニン、抗インターフェロン−60、ビンカアルカロイド、リシンA鎖、メトトレキサート又は放射性同位体ハプテン)を結合するアームを有する。多重特異的抗体は、完全長抗体又は抗体断片として調製することができる。
ヘプシジンを結合し、本明細書中の典型的な抗体を交叉遮断し、及び/又はヘプシジン活性を阻害する抗体を同定する方法も提供される。このような方法は、本明細書中に挙げられている(化学的に合成され、又は細菌若しくは非哺乳動物細胞中で産生された)高度に精製され、生物活性を有し、正しく折り畳まれた非尿性ヒトヘプシジンの組成物を使用し得る。
他のヘプシジン特異的結合剤は、例えば、抗体由来のCDRを基礎として、又はヒトヘプシジンに対する所望の結合特性を示すペプチド又は化合物に関して、多様なペプチド又は有機化学化合物のライブラリーをスクリーニングすることによって調製することができる。ヘプシジン特異的結合剤には、マウス抗体Ab43(配列番号16から21);マウス抗体2.7(配列番号28から33);マウス抗体2.41(配列番号40から45)、ラット抗体R9(配列番号52から57)又はヒト抗体1C9(配列番号111から116)、ヒト抗体3B3(配列番号121から126)、ヒト抗体4E1(配列番号131から136)、ヒト抗体7A3(配列番号141から46)、ヒト抗体9D12(配列番号151から156)、ヒト抗体12B9(配列番号161から166)、ヒト抗体15E1(配列番号171から176)、ヒト抗体18D8(配列番号314から319)、ヒト抗体19C1(配列番号324から329)、ヒト抗体19D12(配列番号294から299)、ヒト抗体19H6(配列番号304から309)、ヒト抗体23F11(配列番号181から186)、ヒト抗体26F11(配列番号191から196)又はヒト抗体1S1(配列番号203から205及び131から133)又はヒト抗体1S2(配列番号214から216及び144から146)又はヒト抗体1S3(配列番号225から227及び164から166)又はヒト抗体1S4(配列番号236から238及び174から176)又はヒト抗体1S5(配列番号247から249及び184から186)の1つ又はそれ以上のCDRと少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%又はそれ以上同一であるアミノ酸配列を含有するペプチドが含まれる。
ヘプシジンを結合し、及び/又は本明細書中に記載されている典型的な抗体を交叉遮断し、及び/又はヘプシジン活性を阻害する抗体又は特異的結合剤を同定する方法も提供される。このような方法は、本明細書中に挙げられている(化学的に合成され、又は細菌若しくは非哺乳動物細胞中で産生された)高度に精製され、生物活性を有し、正しく折り畳まれた非尿性ヒトヘプシジンの組成物を使用し得る。
本明細書中に記載されている方法に従って使用され得るヘプシジン発現阻害剤には、阻害剤オリゴヌクレオチド又はポリヌクレオチド(医薬として許容されるその塩、例えば、ナトリウム塩を含む。)が含まれる。非限定的な例には、アンチセンスオリゴヌクレオチド[Eckstein,Antisense Nucleic Acid Drug Dev.,10:117−121(2000);Crooke,Methods Enzymol,313:3−45(2000);Guvakova et al,J.Biol.Chem.,270:2620−2627(1995);Manoharan,Biochim.Biophys.Acta,1489:117−130(1999);Baker et al,J.Biol Chem.,272:11994−12000(1997);Kurreck,Eur.J.Biochem.,270:1628−1644(2003);Sierakowska et al,Proc.Natl.Acad.Sci.USA,93:12840−12844(1996);Marwick,J.Am.Med.Assoc.280:871(1998);Tomita and Morishita,Curr.Pharm.Des.,10:797−803(2004);Gleave and Monia,Nat.Rev.Cancer,5:468−479(2005)and Patil,AAPSJ.7:E61− E77(2005]、三重鎖オリゴヌクレオチド[Francois et al,Nucleic Acids Res.,16:11431−11440(1988)及びMoser and Dervan,Science,238:645−650(1987)]、リボザイム/デオキシリボザイム(DNAザイム)[Kruger et al,Tetrahymena.Cell,31:147−157(1982);Uhlenbeck,Nature,328:596−600(1987);Sigurdsson and Eckstein,Trends Biotechnol,13 286−289(1995);Kumar et al,Gene Ther.,12:1486−1493(2005);Breaker and Joyce,Chem.Biol,1:223−229(1994);Khachigian,Curr.Pharm.Biotechnol,5:337−339(2004);Khachigian,BioChem.Pharmacol,68:1023−1025(2004)and Trulzsch and Wood,J.Neurochem.,88:257−265(2004)]、低分子干渉RNA/RNAi[Fire et al,Nature,391:806−811(1998);Montgomery et al.,Proc.Natl.Acad.Sci.U.S.A.,95:15502−15507(1998);Cullen,Nat.Immunol,3:597−599(2002);Hannon,Nature,418:244−251(2002);Bernstein et al,Nature,409:363−366(2001);Nykanen et al,Cell,107:309−321(2001);Gilmore et al,J.Drug Target,12:315−340(2004);Reynolds et al,Nat.Biotechnol,22:326−330(2004);Soutschek et al,Nature,432173−178(2004);Ralph et al,Nat.Med.,11:429−433(2005);Xia et al,Nat.Med.,10816−820(2004)及びMiller et al,Nucleic Acids Res.,32:661−668(2004)]、アプタマー[Ellington and Szostak,Nature,346:818−822(1990);Doudna et al,Proc.Natl.Acad.Sci.U.S.A.,92:2355−2359(1995);Tuerk and Gold,Science,249:505−510(1990);White et al,Mol.Ther.,4:567−573(2001);Rusconi et al,Nature,419:90−94(2002);Nimjee et al,Mol.Ther.,14:408−415(2006);Gragoudas et al,N.Engl.J.Med.,351:3805−2816(2004);Vinores,Curr.Opin.Mol.Ther.,5673−679(2003)及びKourlas and Schiller et al,Clin.Ther.,28,36−44(2006)]又は囮(decoy)オリゴヌクレオチド[Morishita et al,Proc.Natl.Acad.Sci.U.S.A.,92:5855−5859(1995);Alexander et al,J.Am.Med.Assoc.,294:2446−2454(2005);Mann and Dzau,J.Clin.Invest.,106:1071−1075(2000)and Nimjee et al,Annu.Rev.Med.,56:555−583(2005)。先述の文献の全体が、参照により、本明細書中に組み込まれ、阻害性オリゴヌクレオチドを設計、製造及び使用する方法に関連する文献の節が特に強調される。
オリゴヌクレオチドの設計において使用される特異的配列は、標的の発現された遺伝子メッセージ内に含有されるヌクレオチドのあらゆる連続する配列であり得る。適切な標的配列を選択するために、本分野において公知のプログラム及びアルゴリズムを使用し得る。さらに、特定の一本鎖核酸配列の二次構造を予測するように設計され、折り畳まれたmRNAの露出された一本鎖領域中で、配列の選択が行われ得るようにするプログラムを用いて、最適な配列を選択し得る。適切なオリゴヌクレオチドを設計するための方法及び組成物は、例えば、米国特許第6,251,588号(その内容全体が、参照により、本明細書に組み込まれる。)中に見出され得る。
細胞中でのアンチセンスオリゴヌクレオチドの恒常的発現は、おそらく翻訳の遮断又はスプライシングの抑制を介して、遺伝子発現を阻害することが示されている。適切な阻害性オリゴヌクレオチドは、一本鎖であり得、mRNA又はDNA分子にハイブリッド形成し、転写、スプライシング又は翻訳を阻害するように、mRNA又はDNA分子に対して十分に相補的であり、及びmRNA又はDNA分子に対して十分に特異的である、例えば、少なくとも12、15又は18塩基長のセグメントを含有し得る。一般に、30塩基未満の長さにわたる相補性が十分すぎるほどである。
低分子干渉(si)RNA技術(RNAiとしても知られる。)は、ある配列に対して相同的である二本鎖RNA(dsRNA)によって誘導されるある配列のmRNAの分解を一般に含み、これにより、対応する遺伝子の発現を「妨害する」。選択された遺伝子に対するmRNAの全部又は大部分に対応するdsRNAを導入することによって、あらゆる選択された遺伝子を抑制し得る。長いdsRNAが発現されると、長いdsRNAは、まず、リボヌクレアーゼIIIによって、21から22塩基対の長さのより短いdsRNAオリゴヌクレオチドへと加工されるようである。従って、siRNAは、相対的に短い相同的dsRNAの導入又は発現によって実施され得る。典型的なsiRNAは、各3’末端に2つのヌクレオチドの突出を有する二本鎖RNAの約19ヌクレオチドを形成する約21ヌクレオチドのセンス及びアンチセンス鎖を有する。実際に、相対的に短い相同的dsRNAの使用は、ある種の利点を有し得る。
siRNAと比べて、shRNAは、発現停止の寿命及び送達の選択肢において利点を与える。例えば、概説のために、「Hannon et al.,Nature,431:371−378,2004」を参照されたい。shRNA(siRNA様特性を有する短い二重鎖RNAへ細胞内でプロセッシングされる。)を産生するベクターが報告されている(Brummelkamp et al.,Science296,550−553,2000;Paddison et al.,Genes Dev.16,948−958(2002))。このようなベクターは、宿主細胞ゲノム中へのベクターの安定な組み込み後に、持続的な遺伝子発現停止を媒介することができる遺伝子発現停止試薬の再生可能な源を与える。さらに、コア発現停止「ヘアピン」カセットは、レトロウイルス、レンチウイルス又はアデノウイルスベクター中へ容易に挿入することが可能であり、異所性mRNA発現を可能とするDNA構築物の送達のために考案されてきた多数の方法の何れかで、細胞種の幅広い範囲中へのshRNAの送達を促進する(Brummelkamp et al.,CancerCell2:243−247,2002;Dirac,et al.,J.Biol.Chem.278:11731−11734,2003;Michiels et al.,Nat.Biotechnol.20:1154−1157,2002;Stegmeie et al.,Proc.Natl.Acad.Sci.USA102:13212−13217,2005;Khvorova et al.,Cell,115:209−216(2003)。
リボザイムは、mRNAの特異的な切断を触媒することができ、従って翻訳を妨げることができる酵素的RNA分子である(概説として、Rossi,1994,Current Biology4:469−471を参照されたい。)。リボザイムの作用機序は、相補的な標的RNAへのリボザイム分子の配列特異的なハイブリッド形成、これに続く、核内溶解切断現象を含む。リボザイム分子は、好ましくは、(1)標的mRNAに対して相補的な1つ又はそれ以上の配列及び(2)mRNA切断のために必要とされる周知の触媒配列又は機能的に等価な配列を含む(例えば、米国特許第5,093,246号参照(その全体が、参照により、本明細書に組み込まれる。))。
あるいは、体内の標的細胞中での遺伝子の転写を妨げる三重らせん構造を形成させるために、遺伝子の制御領域(すなわち、プロモーター及び/又はエンハンサー)に相補的なデオキシリボヌクレオチド配列を標的誘導することによって、標的遺伝子の発現を低下させることができる(全般に、Helene,C,1991,Anticancer Drug Des.,6:569−84;Helene,C,et al.,1992,Ann.N.Y.Acad.Sci.,660:27−36;及びMaher,L.J.,1992,Bioassays14:807−15参照)。
あるいは、標的遺伝子の発現を阻害するために、DNA酵素を使用し得る。DNA酵素は、アンチセンスとリボザイム技術の両者の機構的な特徴の幾つかを取り込んでいる。DNA酵素は、アンチセンスオリゴヌクレオチドとほぼ同様に特定の標的核酸配列を認識するように設計される。しかしながら、DNA酵素は、触媒作用も有しており、標的核酸を特異的に切断する。
所望の細胞中で阻害性オリゴヌクレオチドの発現をもたらすために、適切な制御配列(プロモーターを含む。)とともに、阻害性オリゴヌクレオチドをコードするDNAがその中に配置されたベクター(ウイルスベクター又はプラスミドなど)を介した形質転換又は形質移入によって、阻害性オリゴヌクレオチドを細胞へ直接的に投与し、又は細胞に送達することができる。公知の方法には、レトロウイルスからアデノウイルスにわたるウイルスを使用する、標準的な一過性形質移入、安定な形質移入及び送達が含まれる。複製ベクター又は複製欠損ベクターによる核酸阻害剤の送達が想定される。発現は、恒常的又は誘導性プロモーター系の何れかによっても誘導され得る(Paddison et al.,MethodsMol.Biol.265:85−100,2004)。他の実施形態において、発現は、組織又は発達特異的なプロモーターの調節下にあり得る。
ヒトヘプシジンポリペプチドに関して、固有の成熟ヒトヘプシジン配列に比べて、1つ又はそれ以上の置換、挿入又は欠失を含むが、8つのシステイン全てを保持し及びヘプシジンの生物活性(例えば、抗微生物及び/又は鉄制御活性)を阻害するアンタゴニスト変形物が想定される。変形物は、C2−C4及び/又はC5−C7ジスルフィド結合を維持し、場合によって、C1−C8及びC3−C6ジスルフィド結合も維持し得る。フェロポーティン結合活性を保持するが、フェロポーティンの内部取り込み又は分解を引き起こさないヘプシジン変形物並びにヘプシジン受容体結合活性を保持するが、フェロポーティン受容体を活性化しないヘプシジン変形物も想定される。
固有の成熟ヒトヘプシジン配列に比べて、1つ又はそれ以上の置換、挿入又は欠失を含むが、8つのシステイン全てを保持し及びヘプシジンの生物活性(例えば、抗微生物及び/又は鉄制御活性)を保持するヒトヘプシジンポリペプチドのアゴニスト変形物も想定される。変形物は、C2−C4及び/又はC5−C7ジスルフィド結合を維持し、場合によって、C1−C8及びC3−C6ジスルフィド結合も維持し得る。フェロポーティン結合活性を保持する及び/又はヘプシジン受容体結合活性を保持するヘプシジン変形物も想定される。
本発明のヘプシジンポリペプチド(ヘプシジン変形物を含む。)又は本発明の抗ヘプシジン抗体は、当業者に周知の技術によって容易に修飾することができる。想定可能な変異には、1つ又はそれ以上の残基の挿入、欠失又は置換が含まれる。挿入又は欠失は、好ましくは、約1から5個のアミノ酸、より好ましくは1から3個、最も好ましくは1又は2個のアミノ酸の範囲である。
(1)疎水性:ノルロイシン、met、ala、val、leu、ile;
(2)中性親水性:cys、ser、thr;
(3)酸性:asp、glu;
(4)塩基性:asn、gln、his、lys、arg;
(5)鎖の方向性に影響を与える残基:gly、pro;及び
(6)芳香族:trp、tyr、phe
ある種の事例では、エピトープ結合に直接関与するアミノ酸残基を修飾することを意図して、抗体変形物が調製される。別の実施形態において、エピトープ結合に直接関与していない残基又はいかなる様式でもエピトープ結合に関与していない残基の修飾が、本明細書中に論述されている目的のために望ましい。CDR領域及び/又はフレームワーク領域の何れかの中での突然変異誘発が想定される。
例えば、特異的結合剤若しくは抗体へ結合された炭水化物部分の1つ若しくはそれ以上を付加若しくは欠失させて、及び/又は特異的結合剤若しくは抗体中の1つ若しくはそれ以上のグリコシル化部位を付加若しくは欠失させて、親抗体に比べて修飾されたグリコシル化パターンを有する抗体変形物も作製することができる。
抗体又はFc含有ポリペプチドのFc領域中において、システイン残基を除去し又は導入することにより、この領域中の鎖間ジスルフィド結合の形成を除去又は増加させ得る。このようにして作製されたホモ二量体の特異的結合剤又は抗体は、改善された内部取り込み能力及び/又は増大された補体媒介性細胞死滅及び抗体依存性細胞傷害(ADCC)を有し得る。「Caron et al.,J.Exp Med.176:1191−1195(1992)」及び「Shopes,B.J.Immunol.148:2918−2922(1992)」を参照されたい。ホモ二量体の特異的結合剤又は抗体は、「Wolff et al.,Cancer Research53:2560−2565(1993)」に記載されているように、ヘテロ二機能性架橋剤を用いても調製され得る。あるいは、二重のFc領域を有し、これにより増強された補体溶解及びADCC能を有し得る特異的結合剤又は抗体を改作することができる。「Stevenson et al.,Anti−CancerDrug Design 3:219−230(1989)」を参照されたい。
ポリペプチド又は抗体の共有結合的修飾も、本発明の範囲内に含められる。共有結合的修飾は、適宜、化学的合成によって、又はポリペプチド若しくは抗体の酵素的若しくは化学的切断によって作製され得る。選択された側鎖又はN若しくはC末端残基と反応することができる有機性誘導化剤と、標的とされるアミノ酸残基を反応させることによって、共有結合的修飾の他の種類を導入することができる。
適切な細胞へのヘプシジンアゴニスト又はアンタゴニストの送達は、本分野において公知のあらゆる適切なアプローチの使用によって、エキソビボ、インサイチュ又はインビボでの遺伝子治療を介して実施することができる。例えば、インビボ治療の場合、所望のヘプシジン活性アンタゴニスト又はヘプシジン発現阻害剤をコードする核酸は、単独で、又はベクター、リポソーム若しくは沈殿物と組み合わせて、対象中へ直接注射され得、幾つかの実施形態では、ヘプシジン活性アンタゴニスト又はヘプシジン発現阻害剤の発現が望まれる部位へ注射され得る。エキソビボ治療の場合、対象の細胞を取り出し、これらの細胞中に核酸を導入し、修飾された細胞を直接対象に戻し、又は、例えば、患者中に移植される多孔性膜内に封入されて対象に戻される。例えば、米国特許第4,892,538号及び米国特許第5,283,187号を参照されたい。
ヘプシジン関連貧血又はヘプシジン過剰又はヘプシジン欠乏の他の疾患などのヘプシジン関連疾患を診断するための方法及びヘプシジン活性アンタゴニスト又はヘプシジン発現阻害剤を用いた治療法を含むこのような疾病に対する治療の有効性を監視する方法も提供される。ヘプシジン関連貧血の存在又は不存在を決定するために、免疫複合体の形成が可能となるのに十分な条件下及び時間にわたって、患者から得られた生物試料を本明細書に開示されている抗ヘプシジン抗体の1つ又はそれ以上と接触させる。次いで、生物試料中の抗ヘプシジン抗体とヘプシジン間で形成された免疫複合体が検出される。試料中のヘプシジンの量は、抗体とヘプシジンの間で形成された免疫複合体の量を測定することによって定量される。ある種の方法の中で、生物試料は患者から単離され、本明細書中に開示されている抗ヘプシジン抗体の1つ又はそれ以上とともに温置され、ある閾値を上回る抗体−ヘプシジン複合体のレベルはヘプシジン関連貧血の存在と相関付けられ、前記閾値を下回るレベルは患者がヘプシジン関連貧血を有する可能性が少ないことを示唆する。例えば、正常な範囲内のレベルは、患者がヘプシジン関連貧血を有する可能性が少ないことを示唆する。血清ヘプシジンの正常な範囲は、ある種のアッセイ、すなわち、共有された米国特許出願11/880,313号及び国際特許出願PCT/US2007/016477号(これらの開示全体が、参照により、本明細書に組み込まれる。)に記載されている質量分析技術によって測定された場合、一般に10ng/mL未満であるが、アッセイに応じて、及び検査されている集団の亜集団に応じて変動する。
(a)抗体23F11と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体23F11と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(b)抗体15E1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体15E1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(c)抗体12B9と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体12B9と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;
(a)抗体18D8と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体18D8と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(b)抗体19C1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19C1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(c)抗体19D12と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19D12と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(d)抗体19H6と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19H6と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(e)抗体1S1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体1S1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(a)抗体18D8と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体18D8と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(b)抗体19C1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19C1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(c)抗体19D12と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19D12と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(d)抗体19H6と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体19H6と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(e)抗体1S1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体4E1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;又は
(f)抗体3B3と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体3B3と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体;
(a)抗体1S1と同一のエピトープに結合する抗体又は配列番号9の成熟ヒトヘプシジンへの結合に関して、抗体1S1と少なくとも約75%、80%、85%、90%若しくはそれ以上競合する抗体。
治療を必要としている対象を治療するために、ヒトヘプシジンを結合する本明細書中に記載されているモノクローナル抗体を含むヘプシジン活性アンタゴニストの使用も提供される。典型的な実施形態において、対象は、ヘプシジンの上昇したレベル、ヘプシジン関連疾患、鉄恒常性の障害又は貧血のリスクがあり、又はこれらに罹患し得る。
さらに改善された効力を与えるために、(同じ又は異なる標的抗原に結合する)2つ若しくはそれ以上の抗体を一緒に混合すること、又は本発明の抗体を第二の治療剤とともに同時投与することがさらに有利であり得る。薬剤が治療効果を発揮している期間に重複が存在する限り、2つの治療剤の同時投与は、薬剤が同時に又は同じ経路によって投与されることを要しない。異なる日又は週に投与されるような、同時又は逐次投与が想定される。
幾つかの実施形態において、本発明の方法の実施において使用されるヘプシジン活性アンタゴニスト又は抗体は、所望の送達方法に適した担体を含む医薬組成物中に調合され得る。適切な担体には、ヘプシジン活性アンタゴニスト又は抗体と組み合わされた場合に、ヘプシジンの高親和性結合を保持し、対象の免疫系と非反応性であるあらゆる材料が含まれる。例には、無菌のリン酸緩衝化された生理的食塩水溶液、静菌水などの多数の標準的な医薬担体の全てが含まれるが、これらに限定されない。様々な水性担体(例えば、水、緩衝化された水、0.4%生理的食塩水、0.3%グリシンなど)が使用され得、穏やかな化学的修飾などに供される、アルブミン、リポタンパク質、グロブリンなどの増強された安定性のための他のタンパク質を含み得る。
便宜のために、本明細書に開示されている抗体は、キット(すなわち、診断アッセイを実施するための指示書との、所定量の試薬の梱包された組み合わせ)中に提供することができる。抗体が酵素で標識されている場合、キットは、酵素によって必要とされる基質及び補因子(例えば、検出可能な色素団又は蛍光団を与える基質前駆体)を含む。さらに、安定化剤、緩衝液(例えば、ブロック緩衝液又は溶解緩衝液)などの他の添加物を含めることができる。様々な試薬の相対量は、アッセイの感度を実質的に最適化する試薬の溶液中における濃度を与えるために、幅広く変動され得る。特に、試薬は、溶解すると直ちに、適切な濃度を有する試薬溶液を与える賦形剤を含む乾燥した(通常、凍結乾燥された)粉末として提供され得る。
本明細書に開示されている抗体は、標的抗原に対するアフィニティー精製剤として、又は標的抗原に対する診断用アッセイ(例えば、特異的な細胞、組織又は血清中における標的抗原の発現を検出する。)において使用され得る。抗体は、インビボ診断用アッセイにおいても使用され得る。一般に、これらの目的のために、イムノシンチオグラフィーを用いて部位を局在化することができるように、抗体は、放射性核種(111In、99Tc、14C、131I、125I、3H、32P又は35Sなど)で標識される。
精製:敗血症患者の尿(S.オーレウス(S.aureus)及びS.ニューモニアエ(S.peumoniae)に感染、商業的に入手され、「Park et al.,Journal Biol.Chem.,276:7806−7810,2001)」によって記載されている方法を用いて精製された。)から、ヒトヘプシジンを単離した。要約すれば、凍結された尿約2Lを融解し、0.45及び0.22μのフィルターを通してろ過し、10mL床容積のCMmacroprep(BioRad)カラム上に搭載し、80mL/時間の流速で、PBSで平衡化した。溶出液のOD280が0.1未満になるまで、カラムをPBSで洗浄した。水中の5%酢酸を用いて、ヘプシジンを溶出した。溶出液は数個の他のペプチドを含有しているので、0.1%TFAを含有するアセトニトリル対0.1%水性TFAの勾配を用いて、RP−HPLC(C18)によってさらにこの材料を精製した。質量分析によって、ヘプシジンを含有するHPLC画分を分析した。
ヒトプロヘプシジン(配列番号102)をコードする配列番号101を含むDNAで、AM−1/サイクリンDチャイニーズハムスター卵巣(AM−1/DCHO)細胞(その全体が、参照により本明細書に組み込まれる米国特許第6,210,924号参照)を形質移入することによって、ヒトヘプシジンを安定に発現させた。製造業者の推奨に従って、LipofectamineTM2000(LF2000)試薬(Invitrogen Corporation,Carlsbad,CA)を用いて、形質移入を行った。要約すれば、5%ウシ胎児血清、1×ペニシリン−ストレプトマイシン及びグルタミン(Invitrogen)、非必須アミノ酸(Invitrogen)、ピルビン酸ナトリウム及びヒポキサンチンナトリウム/チミジン(HT)補充物(Invitrogen)が補充されたダルベッコ改変イーグル培地(D−MEM、Invitrogen)10mL中の100mm直径のプラスチックBD−FalconTMペトリ皿(BD Biosciences,Bedford,MA)中に形質移入する24時間前に、4×106個のAM−1/DCHO細胞を播種した。制限酵素PvuI(New England Biolabs,Inc.,Ipswich,MA)を用いて、ヒトプロヘプシジンプラスミドDNA約30μgを直鎖化し、OptiMEM(Invitrogen)の2mL中に希釈した。希釈されたDNAをOptiMEMの2mL中に希釈されたLF2000の75μLと混合し、室温で20分間、混合物を温置した。DNA−LF2000混合物を細胞に添加し、形質移入のために一晩温置した。翌日、新鮮な増殖培地を添加し、5%CO2とともに、37℃で48時間、細胞を培養し、次いで、1:20と1:50の希釈でHT選択培地中に播種した。
ヒトプロヘプシジン(配列番号102)をコードする配列番号101を含むDNAをイー・コリ中で発現させた。培養後、遠心によって細胞を採集し、微小流体装置によって溶解し、洗浄した。室温で1時間、6M塩酸グアニジン、50mMTris−HCl、6mMDTT、pH8.5中に、1:10の容量対重量比で、イー・コリのペーストから得た封入体を可溶化した。次いで、2M尿素、50mMTris−HCl、160mMアルギニン、3mMシステイン中に、pH8.5、4℃で、混合物を1:25希釈し、3から4日間撹拌した。0.45μMろ過によって、この溶液を清澄化し、濃HClを用いて、3.0までpHを低下させる前に、5mMシトラートに移した。3MWCO膜を用いて、10倍濃縮を行い、2M尿素、5mMクエン酸、pH3.0と緩衝液交換した。遠心によって、再度、混合物を清澄化し、S−HPカラムへの搭載の前に、NaOHを用いてpH4.5になるように調整した。20mM酢酸ナトリウム、250mMNaCl、2M尿素、pH4.5中で、カラムを走行した。RP−MSによって画分をアッセイしながら、750mMNaClまでの勾配を実行し、予想される質量及び保持時間に従ってプールした。Kexプロテアーゼとの温置によって、タンパク質のプロ領域を酵素的に切断し、3mUプロテアーゼ/mgプロヘプシンの添加によって実現した。30mMTRISpH7.0及び5mMCaCl2を含む緩衝液中において、室温で1.5時間、混合物を温置した。逆相HPLCを用いて、プールを再度精製した。
N−メチル−ピロリジン(NMP)中で1.0MN,N’−ジシクロヘキシルカルボジイミド(DCC)/1−ヒドロキシベンゾトリアゾール水和物(HOBT)(1:1)カップリング化学を用いるNα−Fmoc/側鎖tBuオルソゴナル保護戦略及び20%(v/v)ピペリジン/NMP脱保護化学(E.Atherton and R.C.Sheppard,Solid Phase Peptide Synthesis:A Practical Approach,IRL Press,Oxford,1989)を使用し、ABI433合成装置((Applied Biosystems,Foster City,CA)を用いて、ヒトヘプシジンペプチド配列:水素−DTHFPICIFCCGCCHRSKCGMCCKT−遊離の酸、配列番号9を化学的に合成した。合成のために、1mmolスケールでの単一のアミノ酸カップリングサイクルを使用し、このサイクルは、58分のカップリング時間と3+15分のFmoc脱保護時間からなった。合成のために、Fmoc−Thr(tBu)−Wang樹脂(0.12mmol当量の規模、Novabiochem)を使用した。Nα−Fmoc保護されたアミノ酸(Novabiochem):Asp(tBu)、Asn(Trt)、Gln(Trt)、Thr(tBu)、His(Trt)、Cys(Trt)、Arg(Pbf)、Ser(tBu)及びLys(Boc)とともに、以下の側鎖保護戦略を使用した。樹脂上での鎖の組み立て及びN末端Fmoc基の除去後、側鎖を保護し、ジクロロメタン(DCM)を用いて、樹脂に結合されたヒトヘプシジンペプチド誘導体を洗浄し、乾燥させた。典型的には2から3時間、ゆっくり撹拌しながら、20mLの総容量中のトリフルオロ酢酸(TFA)/H2O/トリイソプロピルシラン(TIS)/3,6−ジオキサ−1,8−オクタン−ジチオール(DODT)(92.5:2.5:2.5:2.5v/v)の調製直後の混合物で処理することによって、側鎖の脱保護及び固体支持体からの切断を達成した。ポリマー性の固体支持体を除去するために、溶液をろ過し、次いで、蒸発させた。氷冷したジエチルエーテル(50mL)で残留物を処理し、沈殿したペプチドを遠心(2000rpmで10分)によって集め、次いで、容器を傾けてエーテル溶液を除去し、真空中でペプチドを乾燥させた。
天然、組換え及び合成物質の同等性を示すために、実施例1に記載されているように尿から精製されたヒトヘプシジンを、CHO由来の組換え的に作製された物質(実施例2)、イー・コリに由来する組換え的に作製された物質(実施例3)及び化学的に合成された物質(実施例4)に対して比較した。IRMPD断片化スペクトルを比較した(図1)。観察された断片の全てに対して、直接的な配列帰属は不可能であるが、全ての試料のMS/MSフィンガープリントは同一であった。衝突活性化解離(CAD)によっても試料が解離され、ECD及びスペクトルは全ての調製物に対して一貫していた。生物分子イオンの構造の小さな変化でさえ、直列の質量スペクトルを大幅に変化させることができる。従って、これらの異なる解離技術によって4つのヘプシジン調製物全てが同一であることは、分析されたヘプシジンの4つの形態全てに対して、ジスルフィド結合性が同一であることを示唆する。
インビトロ細胞アッセイ中で、鉄制御生物活性に関して、実施例1、2、3及び4に従って精製又は作製されたヒトヘプシジンをアッセイした。293細胞中で誘導的に発現されたフェロポーティンは鉄の搬出を刺激し、細胞内の鉄を低下させ、従って、フェリチンレベルを低下させる(Nemeth et al.,Science,306:2090−2093,2004)。フェローポーティンの作用は、ヘプシジン処理によって、用量依存的な様式で低下させることができる。この作用は、ヘプシジンによって誘導されたフェロポーティンの内部取り込み及び分解のために、並びにこれによる鉄搬出の低下によるものであることが示されている。
2つの異なる技術、NEM部分的還元的アルキル化及びフーリエ変換質量分析(FT−MS)を用いて、尿から精製された内在性ヒトヘプシジンペプチドのジスルフィド結合性を調べた。
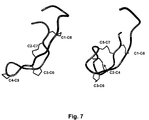
ヒトヘプシジンの構造は、NRM分光法によっても決定された。ジスルフィド結合を形成する全てのシステイン残基のプロトン間で、NOE(核オーバーハウザー効果)が直接観察されたこれらのデータによって、ジスルフィド結合性が以下のように明らかとなり(C7−C23(C1−C8)、C11−C19(C3−C6)、C10−C13(C2−C4)及びC14−C22(C5−C7))、前述した部分的アルキル化還元の結果と一致していた。これらの実験的観察は、以前に公表された構造(Hunter et al.2002)と著しく異なるヘプシジンの三次元構造の決定を可能にした。これらの実験中で使用された濃度及び温度条件下で、長期間にわたって、最も優れた安定性特性を示したので(高品質の溶液NMR研究にとって重要である。)、CHO由来の組換えヒトヘプシジンから結果を作製した。安定性を示唆するパラメータは、物質凝集のパーセント及び図2に示されているNRM1H線幅によって測定される、溶液中での分子の単分散の程度であった。
実施例4に記載されている一般的手順に従って、多数のヘプシジン変形物を化学的に合成した。N末端の5つのアミノ酸を欠如するヘプシジンの変形物(「ヘプシジン20」又は「hepc20」と表記される。)を合成した。8つのシステイン残基全てが2−アミノ酪酸で置換され、従って、ジスルフィド結合を形成する能力を完全に失った直鎖ヘプシジン変形物も合成した。2つのジスルフィド結合(C1−C8及びC3−C6)のみの形成も可能とするために、システイン2、4、5及び7が2−アミノ酪酸で置換されたC1−C8、C3−C6ヘプシジン変形物も合成した。
以下のようにして、ヒトヘプシジン特異的モノクローナル抗体(mAb)2.7及び2.41をマウス中で作製した。動物に投与する前に、標準的なEDC化学を用いて、組換え的に発現され及び再折り畳みされたヒトヘプシジンを担体タンパク質KLHに連結した。簡潔に述べると、ヒトヘプシジン及びKLHの等量を含有するMES緩衝化された溶液へ、EDC(Pierce)の4倍モル濃度過剰を直接添加した。室温で2時間、反応を進行させた。次いで、完全フロイントアジュバント(Pierce)又はRIBI(Sigma)及びPBS(Gibco)の1:1比中で、ヒトヘプシジンーKLH連結体を乳化した。BDF1マウス及びC57BL/6の首筋及び後肢に、ヘプシジン−KLH/アジュバント乳化の50μgで皮下に免疫を行った。14日後に、RIBIアジュバント中のヒトヘプシジン−KLH25μgの第二の免疫化を皮下及び腹腔内に送達した。この免疫化から10日後に、抗ヒトヘプシジン血清レベルを評価するために、採血を行った。
以下のウイルス免疫化法によって、ヒトヘプシジン特異的モノクローナル抗体Ab43をマウス中で作製した。ヒトヘプシジンを発現するアデノウイルスを作製するために、ViraPower Adenoviral Expression System(カタログ番号K4930−00,Invitrogen,Carlsbad,CA)を使用した。ヒトヘプシジンcDNA(rAd−hHepc)を担持する組換えアデノウイルスを以下のようにして構築した。簡潔に述べると、pENTR1A(Invitrogen)中にヒトヘプシジン遺伝子を挿入することによって、pENTR−hHepcを構築した。得られたヒトヘプシジン遺伝子は、attPDNA断片と隣接しており、pAd/CMV/V5−DEST中のattBDNA断片との組換えが可能である。LRクロナーゼを用いて、pENTR−hHepcとpAd/CMV/V5−DESTの間の組換え反応によって、PAd/CMV−hHepcを構築した。rAd−hHepcを作製するために、PacIによってpAd/CMV−hHepcを直鎖化し、Lipofectamine2000を用いて293T細胞中に形質移入した。約80%の細胞変性効果(CPE)が観察されるまで、形質移入された293T細胞を培養した。形質移入された細胞は、膨張した丸型の形態、溶解された細胞及び可視的なプラークを示す。RAd−hHepcを含有する細胞を採集し、rAd−hHepcの増幅のために使用した。塩化セシウム勾配法によって、RAd−hHepCを精製し、Adeno−Xrapid titer kit(BD Biosciences,Palo Alto,CA)を用いて滴定した。
修飾を施したRIMMS法を用いて、ラット中でヒトヘプシジン特異的モノクローナル抗体(mAb)を作製した。簡潔に述べると、2匹の8から10週齢の雌Lewisラット(Charles River Laboratory)のそれぞれに、11日の期間にわたって、ヒトヘプシジンーKLH連結されたタンパク質での免疫化を5巡行った。各免疫化の前に、酸素及びイソフルランの気体混合物を用いて、ラットに麻酔をかけた。第0日目の第一の免疫化のために、600μL容量のフロイント完全アジュバント(DIFCO)中に抗原10μgを乳化し、ラットの背中に沿って、50μL/部位で、流入領域リンパ節に対して近位の6つの部位(襟首の2箇所及び鼠径部及びふくらはぎに対して両側2箇所)に皮下投与した。腹部に沿って、6つの隣接部位(腋窩、太もも及びふくらはぎの両側2箇所)へ、さらに抗原混合物300μLを投与した。全体を通じてRIBI(Corixa CORP,cat# R700)アジュバントを使用したことを除き、類似の様式で、3日目、6日目、8日目及び11日目に、強化免疫を与えた。
標準的な方法を用いて、XenomouseTMIgG2κλ及びIgG4κλマウスを、KLH連結されたヒトヘプシジン(配列番号9)で免疫化した。プレートに固着された、ビオチン化されたヒトヘプシジンに対して、23,040のIgG2上清及び11,520IgG4上清を単一の濃度でスクリーニングした。このスクリーニングから、上清間の濃度差の影響を最小限に抑えるために、捕捉された抗体の量を制限した抗体捕捉ELISAを用いて、ヒト及びマウスのビオチン化されたヘプシジンの両方への結合に関して、617IgG2及び1013IgG4上清を検査した。抗体濃度のある範囲にわたって、溶液相ヘプシジン−抗体結合を測定する架橋ELISA中で、最上位ランクの試料(70のIgG2及び110のIgG4)をさらに性質決定した。このアッセイによって、抗体結合の相対的な親和の順位が得られた。
R9、Ab43、2.7及び2.41抗体の、組換えマウスヘプシジン(配列番号80)及びヒトヘプシジン(配列番号9)との相互作用を研究するために、BIAcoreを用いて、溶液平衡結合分析を行った。
以下の実施例は、組換えカニクイザルヘプシジン(rcyno)への様々な抗体に対するKinExA及びBIAcore結合分析を記載する。
4℃で一晩、0.1M酢酸ナトリウム(pH5.5)中において、100から1000ng/mLのビオチン連結された組換えヒト又はビオチン連結されたマウスヘプシジンで、96ウェルのE.I.A./R.I.A.平底プレート(Costar359)を被覆した。室温で1時間、2%BSA及び0.2%ヤギ血清を含有するPBS(GIBCO)でプレートをブロックした。プレートを洗浄した後、ハイブリドーマ馴化培地50μLを各ウェルに添加し、室温で2時間、振盪装置上で温置した。洗浄溶液(PBS中の0.05%Tween−20)でプレートを3回洗浄し、室温で30分間、西洋ワサビペルオキシダーゼが連結されたヤギ抗ラットIgG(Chemicon)の50μL/ウェルとともに温置した。プレートを3回洗浄した後、TMB基質(KPL)の50μL/ウェルを添加し、室温で5から10分間温置した。0.5NH2SO4の50μLを添加して反応を停止させ、マイクロプレート読取装置中において、450nmでプレートを読み取った。陽性対照抗体として、免疫されたラットの抗血清を使用し、バックグラウンド対照として、溶媒のみを使用した。
ヘプシジンはフェロポーティンを内部に取り込ませ、細胞表面から取り除いて、鉄の放出を阻害し、細胞内鉄濃度を上昇させる。ヘプシジンによって媒介されたこの鉄の隔離に対する抗ヒトヘプシジン抗体の効果をインビトロで評価した。ドキシサイクリン誘導性フェロポーティン(Fpn)発現構築物及び以下のヌクレオチド配列を有する、mRNAの翻訳を制御するフェリチン由来の5’鉄応答要素(IRE)の1コピーを含有するβ−ラクタマーゼ(BLA)発現構築物を含有する293細胞株を構築した(tcggccccgcctcctgccaccgcagattggccgctagccctccccgagcgccctgcctccgagggccggcgcaccataaaagaagccgccctagccacgtcccctcgcagttcggcggtcccgcgggtctgtctcttgcttcaacagtgtttggacggaacagatccggggactctcttccagcctccgaccgccctccgatttcctctccgcttgcaacctccgggaccatcttctcggccatctcctgcttctgggacctgccagcaccgtttttgtggttagctccttcttgccaacc)(配列番号103)。BioCoatポリD−リジン被覆されたプレート(Becton−Dickinsonカタログ番号35−6640)中に90μL/ウェル(25,000細胞/ウェル)で、DMEM(Invitrogenカタログ番号11965)、5%FBS(Invitrogenカタログ番号10099−141)、PSQ(Invitrogenカタログ番号10378−016)中に2.8×105細胞/mLで、70から80%の集密状態の培養物から採取されたこれらの293/Fpn/BLA細胞を播種し、5%CO2とともに37℃で温置した。同じ日の終わりに、100μg/mLドキシサイクリンを加えたアッセイ培地(DMEM5%FBSPSQ)の溶液を作製し、その10μL/ウェルをプレートに添加し、プレートを一晩又は少なくとも20時間温置した。翌日、ウェルから培地を除去し、DMEM5%FBSPSQ、2.5μg/mLクエン酸第二鉄、50ng/mL合成ヒトヘプシジン及び抗体の系列希釈(以下の実施例8及び9に記載されているように作製された2.7、2.41及びAb43)の予め作製された混合物と置き換えた(全て、アッセイプレートに添加する直前に、96ウェルポリプロピレンディープウェルブロックプレート中で調製した。)。100μL/ウェルで混合物を添加し、細胞培養温置装置中において、37℃、5%CO2で一晩温置した。次いで、温置装置からプレートを取り出し、調製されたInvitrogenGeneBlazerCCF4A/M 展開試薬(Invitrogen Kit#K1085)の20μL/ウェルを添加し、暗所で90分間温置する前に、室温で10分間平衡化した。アッセイ培地100μL(DMEM5%FBSPSQ)を含有する、細胞なしの対照アッセイプレートの16ウェルにも、展開試薬を添加し、同じ時間、温置した。次いで、409nmで励起し、447nm(青)及び520nm(緑)での発光を読み取ることによって、Envision Multilabel Reader(Perkin−Elmer Inc.)上で、青及び緑色の蛍光シグナルを読み取った。結果は、図8から10に図示されている。mAB43、2.7及び2.41は、それぞれ、1.380×10−8、1.700×10−8及び1.636×10−8のEC50で、鉄の細胞内濃度を減少させた。
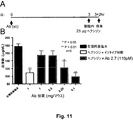
低鉄血症応答を生成するのに十分な量で、ヒトヘプシジンを投与されたマウス中で、抗ヒトヘプシジン抗体の活性をインビボにおいて評価した。0日目に、ヒトヘプシジンに対して誘導されたマウスモノクローナル(Ab2.7)を雌のC57BL/6マウスに皮下注射した。対照マウスには、イソタイプ対照としてマウスIgG1を与えた。3日目に、マウスに、イー・コリ由来の組換えヒトヘプシジン(rhHepc)25μgの単回腹腔内注射を与えた。2時間後に、血清鉄レベルを分析した。生理的食塩水で処理された対照動物は正常な血清鉄レベルを有していたのに対して、ヘプシジン及びイソタイプ対照抗体で処理された動物は低鉄血症を示した。結果は、図11に示されている。mAb2.7の1mg及び0.5mgは何れも、低鉄血症応答からの統計学的に有意な保護を与えた。Ab2.7の0.25mg用量で、低鉄血症の低下が観察されたが、より低い用量(0.25及び0.1mg)が非中和用量と定義された。統計は、生理的食塩水対照に対して全ての群を比較するダネットの後知恵検定を用いたANOVAを表す。
以下の実施例は、エリスロポエチン低応答性マウス中で、ヘプシジン及びヘプシジン活性アンタゴニストの役割を調べた。
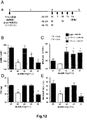
エリスロポエチン耐性表現型を有するマウスを抗ヘプシジン抗体で処理することによって、ダルベポエチンαでの処理に対する応答性が回復した。ヒトヘプシジン又は発現対照としてのGFPをコードする遺伝子を含有するAAV(5×1012粒子/マウス、静脈内)を、雄のC57BL/6マウスに注射した(n=5/群)。恒常的なタンパク質発現を2週間確立させた後、ベースラインヘモグロビン(Hb)レベルを測定するためにマウスを採血し、次いで、様々な投薬頻度で、Ab2.7(1mg/マウス)又はイソタイプ対照で処理した。第一の投薬の翌日、マウスをダルベポエチンα(100μg/kg、皮下)で処理した。投薬スケジュールの模式図が、図15A示されている。
マウスヘプシジン1siRNAのインビボでのスクリーニング:CHO−mヘプシジン安定細胞(HelenKim)を、30,000細胞/ウェルで、96ウェルプレート中に播種した。翌日、培地を除去し、形質移入複合体100μLを添加することによって、細胞を形質移入した。以下のようにして、形質移入複合体を作製した。チューブA中のOpti−MEM(Invitrogen#31985)125μLに、100μMsiRNAの1μLを添加した。チューブBには、TransIT−TKO形質移入試薬15μL(Mirus#MIR−2154)をOpti−MEM125μLに添加した。室温で12分間、両チューブを温置した。2つのチューブの内容を混合し、室温で15分間温置し、次いで、細胞に添加した。形質移入から18時間後に、培地を除去し、1×QuantiGene Lysis Mixture(Panomics #QG0502)の100μLを用いて、細胞を溶解した。分岐DNAアッセイ(QuantiGene Assay Kit,Panomics #QG0003)を用いて、mヘプシジン及びmシクロフィリンAのmRNAレベルに関して、可溶化液を分析した。CHO−mヘプシジン細胞中でのsiRNA配列及び%mRNAノックダウンに関して、表8を参照されたい。
マウス炎症性貧血モデルにおいて、ヘプシジン発現阻害剤及び赤血球新生刺激物質を用いた組み合わせ療法を以下のように評価した。
マウス炎症性貧血モデルにおいて、ヘプシジン活性アンタゴニスト及び赤血球新生刺激物質を用いた組み合わせ療法も以下のように評価した。
ヒト患者中のヘプシジンのレベルは、同時係属、共有の米国特許出願11/880,313号及び国際特許出願PCT/US2007/016477号(これらの開示全体が、参照により、本明細書中に組み込まれる。)に以前記載されたように測定された。この方法は、以下で再現される。
以下の実施例は、市販のプロヘプシジンELISAキット(DRGIntl.Inc.,ドイツ)は、試料中の成熟ヘプシジンを検出することができないことを示す。
ヘプシジンを炎症状態と相関付けるために、DRGプロヘプシジンELISAキットを使用する試みを行った(例えば、Hsu et al.,Blood Purification,24:311−16,2006;Kemna et al.,Blood,106:1864−66,2005;Ouz et al.,Anadolu Kardiyoloji Dergisi,6:239−42,2006; Taes et al.,Clinical Chemistry & Laboratory Medicine,42:387−89,2004;Theurl et al.,Blood,107:4142−48,2006を参照されたい。)。この実施例は、しかしながら、DRGプロヘプシジンELISAキットを用いて測定されたプロヘプシジンレベルは、患者の成熟ヘプシジンレベルと相関しないのみならず、プロヘプシジンレベルは患者の炎症状態とも相関しないことを示している。
ポリクローナル抗体は、免疫原に対する異なる抗体の複雑な複合体に相当するので、タンパク質中に存在する全ての可能性のあるエピトープを検出する1つの方法である。ヘプシジンに対するモノクローナル抗体サンドイッチELISAが可能であるかどうかを決定するために、KLH連結された成熟ヒトヘプシジンに対して産生されたポリクローナル抗体を用いて、予備的実験を行った。
以下の実施例は、試料中のヘプシジンレベルを測定するためのサンドイッチイムノアッセイを記載する。
実施例30で得られたBiacoreの結果に従い、ヘプシジンとの反応性を有することが以前に示された1100の抗体を、1S1と「対形成する」能力に関してスクリーニングした。適切である僅か11の抗体(すなわち約1%)が同定された。従って、ヘプシジンに対するサンドイッチアッセイを開発する上で使用可能な「対」を形成できることは稀なようである。1S1及び23F11をサンドイッチELISAフォーマットへ組み立てると、ヘプシジンレベルを検出するためのイムノアッセイの感度は50倍向上した。図29に示されているように、このアッセイは、50倍の前希釈工程後に、正常な血清中のヘプシジンのレベルを測定できることが明らかとなった。軸は、希釈前ヘプシジンレベルを表している。
以下の実施例は、ヘプシジンレベルを測定するための競合的結合アッセイを記載している。1つのプロトコールにおいて、血清中に存在する非標識ヘプシジンは、抗ヘプシジン抗体(例えば、抗体2.7)への結合に関して、ビオチン化されたヘプシジンと競合する。
質量分析法(実施例25)、競合的ELISA(実施例32)及びサンドイッチELISA(実施例30から31)を含む様々な技術によって得られたヘプシジンのレベルを比較した。結果は、図33に示されている。
Claims (268)
- ヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、前記ヒトヘプシジンが配列番号9に記載されているアミノ酸配列からなり、並びに配列番号9中に位置している残基7と23、10と13、11と19及び14から22の間で形成された4つのジスルフィド結合ループを含む立体構造を有する、単離されたモノクローナル抗体。
- 前記抗体が、BIAcore又はKinExAによって測定された場合に、約1×10−7M又はそれ以下のKDで前記ヒトヘプシジンへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、BIAcore又はKinExAによって測定された場合に、約1×10−8M又はそれ以下のKDで前記ヒトヘプシジンへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、BIAcore又はKinExAによって測定された場合に、約1×10−9M又はそれ以下のKDで前記ヒトヘプシジンへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体がさらにヒトヘプシジンの活性を拮抗する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、フェリチンアッセイによって測定された場合に、約1×10−8M又はそれ以下のEC50でフェリチン発現のレベルを減少させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が約1×10−8M又はそれ以下のEC50で対象中の細胞内鉄レベルを減少させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が対象中の循環鉄レベル又はTsatを増加させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体がヘモグロビン若しくはヘマトクリットの少なくとも1つ又は両方の、対象中におけるレベルを増加させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が少なくとも赤血球数、赤血球ヘモグロビン含量若しくは赤血球数の赤血球平均細胞容積の少なくとも1つ又はこれらの何れかの組み合わせを対象中において増加させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が網状赤血球数、網状赤血球ヘモグロビン含量又は網状赤血球数の網状赤血球平均細胞容積の少なくとも1つ又はこれらの何れかの組み合わせを対象中において増加させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が対象の血清中の遊離ヘプシジンのレベルを低下させる、請求項1に記載の単離されたモノクローナル抗体。
- 前記レベルが前記対象中において少なくとも約20%低下される、請求項12に記載の単離されたモノクローナル抗体。
- 前記対象が哺乳動物である、請求項7から13の何れか一項に記載の単離されたモノクローナル抗体。
- 前記哺乳動物がヒトである、請求項14に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置1から5の中に位置する少なくとも1つのアミノ酸を含む前記ヒトヘプシジンのエピトープへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置10から13の中に位置する少なくとも1つのアミノ酸を含む前記ヒトヘプシジンのエピトープへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置14から22の中に位置する少なくとも1つのアミノ酸を含む前記ヒトヘプシジンのエピトープへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置6から25の中に位置する少なくとも1つのアミノ酸を含む前記ヒトヘプシジンのエピトープへ結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置10及び13に位置するアミノ酸の間のジスルフィド結合によって形成されたループに結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が、配列番号9の位置14及び22に位置するアミノ酸の間のジスルフィド結合によって形成されたループに結合する、請求項1に記載の単離されたモノクローナル抗体。
- 抗体が少なくとも2つのループによって形成された前記ヒトヘプシジンのエピトープへ結合し、前記ループの第一が配列番号9の位置10と13に位置するアミノ酸の間のジスルフィド結合によって形成され、及び前記ループの第二が配列番号9の位置14と22に位置するアミノ酸の間のジスルフィド結合によって形成される、請求項1に記載の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ結合し、及びヘプシジンの鉄制御活性を阻害する単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ結合し、及び循環鉄濃度又はTsatを増加させる、単離されたモノクローナル抗体。
- ヘプシジン(配列番号9)への結合に関して、Ab43、1S1、1S2、1S3、1S4、1S5、2.7、2.41、R9、1C9、3B3、4E1、7A3、9D12、12B9、15E1、18D8、19C1、19D12、19H6、23F11及び26F11からなる群から選択される抗体と少なくとも約75%競合する、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号15又は配列番号13と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号16から21からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号16から21の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 抗体が配列番号16から21からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 抗体が配列番号16から21からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号27又は配列番号25と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号28から33からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号28から33の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号28から33からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号28から33からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号39又は配列番号37と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号40から45からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号40から45の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号40から45からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号40から45からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号74(XASNLES)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号75(XQSNEE)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1又は35の単離されたモノクローナル抗体。
- 配列番号76(QQXNEX)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1又は36の単離されたモノクローナル抗体。
- 配列番号16(RASESVDSYGNSFMH)のアミノ酸配列を含む、請求項1又は35から37の単離されたモノクローナル抗体。
- 配列番号77(WINTXSGVPTYADDFXG)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1又は38の単離されたモノクローナル抗体。
- 配列番号78(XXYYGX*A*Y)(Xは任意のアミノ酸であり、及び*は不存在であり、又は任意のアミノ酸であり得る。)のアミノ酸配列を含む、請求項1又は39の単離されたモノクローナル抗体。
- 配列番号43(TYGMS)のアミノ酸配列を含む、請求項1又は40の単離されたモノクローナル抗体。
- 配列番号283(VIXYXXSNKYYADSVKG)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号284(WIXAXNGXXXXAXXXQX)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号285(AQEGXAPDAFDI)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号286(QAWYSSTNVX)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号287(QAWDSSTAXX)(Xは、任意のアミノ酸である。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号288(QSDYSSXXX**)(Xは任意のアミノ酸であり、及び*は不存在であり、又は任意のアミノ酸であり得る。)のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号51又は配列番号49と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号52から57からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号52から57の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号52から57からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号52から57からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号110又は配列番号108と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号111から116からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号111から116の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号111から116からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号111から116からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号120又は配列番号118と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号121から126からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号121から126の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号121から126からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号121から126からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号130又は配列番号128と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号131から146からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号131から136の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号131から136からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号131から136からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号140又は配列番号138と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号141から146からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号141から146の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号141から146からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号141から146からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号150又は配列番号148と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号151から156からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号151から156の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号151から156からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号151から156からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号160又は配列番号158と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号161から166からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号161から166の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号161から166からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号161から166からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号170又は配列番号168と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号171から176からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号171から176の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号171から176からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号171から176からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号313(Ab18D8重可変)又は配列番号311(18D8軽可変)と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号314から319からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号314から319の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号314から319からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号314から319からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号323又は配列番号321と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号324から329からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号324から329の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号324から329からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号324から329からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号293又は配列番号291と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号294から299からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号294から299の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号294から299からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号294から299からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号303又は配列番号301と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号304から309からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号304から309の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号304から309からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号304から309からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号180又は配列番号178と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号181から186からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号181から186の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号181から186からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号181から186からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号190又は配列番号188と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号191から196からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号191から196の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号191から196からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号191から196からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号202又は配列番号128と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号131から133及び203から205からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号131から133及び203から205の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号131から133及び203から205からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号131から133及び203から205からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号140又は配列番号213と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号144から146及び214から216からなる群から選択される少なくとも1つのアミノ酸配列及び配列番号144から146及び214から216の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号144から146及び214から216からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号144から146及び214から216からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号160又は配列番号224と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号164から166及び225から227からなる群から選択される少なくとも1つのアミノ酸配列並びに配列番号164から166及び225から227の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号164から166及び225から227からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号164から166及び225から227からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号170又は配列番号235と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号174から176及び236から238からなる群から選択される少なくとも1つのアミノ酸配列並びに配列番号174から176及び236から238の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号174から176及び236から238からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号174から176及び236から238からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号9のヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、配列番号190又は配列番号246と少なくとも65%同一のアミノ酸配列を有するポリペプチドを含み、前記ポリペプチドが配列番号194から196及び247から249からなる群から選択される少なくとも1つのアミノ酸配列並びに配列番号194から196及び247から249の何れかに対して少なくとも1つのアミノ酸の変化を含む何れかの配列を含む、単離されたモノクローナル抗体。
- 配列番号194から146及び247から249からなる群から選択される少なくとも1つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 配列番号194から196及び247から249からなる群から選択される少なくとも3つのアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 抗体が配列番号16、28、40、52、111、121、131、141、151、161、171、181、191、214、225、236、247、294、304、314及び324からなる群から選択されるアミノ酸配列、配列番号17、29、41、53、112、122、132、142、152、162、172、182、192、215、226、237、248、295、305、315及び325からなる群から選択されるアミノ酸配列並びに配列番号18、30、42、54、113、123、133、143、153、163、173、183、193、216、227、238、249、296、306、316及び326からなる群から選択されるアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 抗体が配列番号19、31、43、55、114、124、134、144、154、164、174、184、194、203、297、307、317及び327からなる群から選択されるアミノ酸配列、配列番号20、32、44、56、115、125、135、145、155、165、175、185、195、204、298、308、318及び328からなる群から選択されるアミノ酸配列並びに配列番号21、33、45、57、116、126、136、146、156、166、176、186、196、205、299、309、319及び329からなる群から選択されるアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 抗体が配列番号15、配列番号13、配列番号27、配列番号25、配列番号39、配列番号37、配列番号51、配列番号49、配列番号110、配列番号108、配列番号120、配列番号118、配列番号130、配列番号128、配列番号140、配列番号138、配列番号150、配列番号148、配列番号160、配列番号158、配列番号170、配列番号168、配列番号180、配列番号178、配列番号190、配列番号188、配列番号202、配列番号212、配列番号218、配列番号224、配列番号235、配列番号246、配列番号293、配列番号291、配列番号303、配列番号301、配列番号313、配列番号311、配列番号323及び配列番号321からなる群から選択されるアミノ酸配列と少なくとも90%同一のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 重鎖及び軽鎖を含む単離されたモノクローナル抗体であって、重鎖が配列番号207のアミノ酸20から467を含み、及び軽鎖が配列番号220のアミノ酸21から234を含む、単離されたモノクローナル抗体。
- 重鎖及び軽鎖を含む単離されたモノクローナル抗体であって、重鎖が配列番号233のアミノ酸20から466を含み、及び軽鎖が配列番号218のアミノ酸23から234を含む、単離されたモノクローナル抗体。
- 重鎖及び軽鎖を含む単離されたモノクローナル抗体であって、重鎖が配列番号255のアミノ酸20から466を含み、及び軽鎖が配列番号229のアミノ酸23から234を含む、単離されたモノクローナル抗体。
- 重鎖及び軽鎖を含む単離されたモノクローナル抗体であって、重鎖が配列番号259のアミノ酸20から466を含み、及び軽鎖が配列番号240のアミノ酸23から234を含む、単離されたモノクローナル抗体。
- 重鎖及び軽鎖を含む単離されたモノクローナル抗体であって、重鎖が配列番号267のアミノ酸20から466を含み、及び軽鎖が配列番号251のアミノ酸23から234を含む、単離されたモノクローナル抗体。
- 前記抗体がキメラ、ヒト化又は完全なヒト抗体である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- 前記抗体がキメラ化されており、キメラ化がマウスとヒトの間であり、又はラクダとヒトの間である、請求項113の単離されたモノクローナル抗体。
- モノクローナル抗体がヒト化抗体である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- モノクローナル抗体が一本鎖Fv抗体断片である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- モノクローナル抗体がFab断片、F(ab’)2断片、Fd、ドメイン抗体(dAb)、ダイアボディ、マキシボディ又はナノボディである、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- 抗体がヒト抗体である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- ヒトコンセンサス抗体配列、ヒト生殖系列抗体配列又はヒト生殖系列コンセンサス抗体配列であるフレームワークアミノ酸配列を含む、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- 抗体がIgA、IgG、IgE、IgD又はIgMイソタイプの抗体である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- 抗体がIgG1、IgG2、IgG3又はIgG4イソタイプの抗体である、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- ヒトヘプシジン(配列番号9)及びカニクイザルヘプシジン(配列番号6)の両方を結合する、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- ヒトヘプシジン(配列番号9)及びマウスヘプシジン(配列番号80)の両方を結合する、請求項1から112の何れか一項の単離されたモノクローナル抗体。
- 配列番号9と少なくとも70%同一であり、及び8つのシステイン残基を有する25アミノ酸からなるポリペプチドへも結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記ポリペプチドが配列番号2の位置59から83に位置するアミノ酸からなる、請求項124に記載の単離されたモノクローナル抗体。
- 前記ポリペプチドが配列番号6に記載されているアミノ酸配列からなる、請求項125に記載の単離されたモノクローナル抗体。
- 検出可能な標識を含む、請求項1から126の何れか一項の単離されたモノクローナル抗体。
- 請求項1から127の何れか一項の抗体をコードするヌクレオチド配列を含む、単離された核酸分子。
- 制御調節配列へ作用可能に連結された、請求項128の核酸分子を含む発現ベクター。
- 請求項129のベクター又は請求項128の核酸分子を含む宿主細胞。
- 抗体を生産するために請求項130の宿主細胞を使用する方法であって、抗体を生産するために核酸が発現されるような適切な条件下で、請求項130の宿主細胞を培養することを含む、方法。
- 宿主細胞培養物から抗体を回収することをさらに含む、請求項131の方法。
- 請求項1から126の何れか一項の抗体及び医薬として許容される担体、希釈剤又は賦形剤を含む、組成物。
- 生物試料中のヒトヘプシジンの存在を検出する方法であって、配列番号9の成熟ヒトヘプシジンへのモノクローナル抗体の結合を可能とする条件下で、請求項1から127の何れか一項に記載されているモノクローナル抗体の少なくとも1つとともに生物試料を温置すること、及び結合されたモノクローナル抗体又は結合されたヘプシジンを検出することを含む、方法。
- モノクローナル抗体が抗体1S1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体1S1と約75%競合する、請求項134の方法。
- 配列番号9の成熟ヘプシジンを結合する第二のモノクローナル抗体とともに試料を温置することをさらに含む、請求項135の方法。
- 第二のモノクローナル抗体が抗体23F11と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体23F11と約75%競合する、請求項136の方法。
- 第二のモノクローナル抗体が抗体15E1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体15E1と約75%競合する、請求項136の方法。
- 第二のモノクローナル抗体が抗体12B9と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体12B9と約75%競合する、請求項136の方法。
- モノクローナル抗体が抗体12B9と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体12B9と約75%競合する、請求項134の方法。
- 配列番号9の成熟ヘプシジンを結合する第二のモノクローナル抗体とともに試料を温置することをさらに含む、請求項140の方法。
- 第二のモノクローナル抗体が抗体18D8と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体18D8と約75%競合する、請求項141の方法。
- 第二のモノクローナル抗体が抗体19C1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19C1と約75%競合する、請求項141の方法。
- 第二のモノクローナル抗体が抗体19D12と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19D12と約75%競合する、請求項141の方法。
- 第二のモノクローナル抗体が抗体19H6と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19H6と約75%競合する、請求項141の方法。
- 第二のモノクローナル抗体が抗体1S1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体1S1と約75%競合する、請求項141の方法。
- モノクローナル抗体が抗体23F11と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体23F11と約75%競合する、請求項134の方法。
- 配列番号9の成熟ヘプシジンを結合する第二のモノクローナル抗体とともに試料を温置することをさらに含む、請求項147の方法。
- 第二のモノクローナル抗体が抗体18D8と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体18D8と約75%競合する、請求項148の方法。
- 第二のモノクローナル抗体が抗体19C1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19C1と約75%競合する、請求項148の方法。
- 第二のモノクローナル抗体が抗体19D12と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19D12と約75%競合する、請求項148の方法。
- 第二のモノクローナル抗体が抗体19H6と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体19H6と約75%競合する、請求項148の方法。
- 第二のモノクローナル抗体が抗体15E1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体1S1と約75%競合する、請求項148の方法。
- 第二のモノクローナル抗体が抗体3B3と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体3B3と約75%競合する、請求項148の方法。
- モノクローナル抗体が抗体15E1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体15E1と約75%競合する、請求項134の方法。
- 配列番号9の成熟ヘプシジンを結合する第二のモノクローナル抗体とともに試料を温置することをさらに含む、請求項155の方法。
- 第二のモノクローナル抗体が抗体1S1と同じエピトープに結合し、又は配列番号9の成熟ヒトヘプシジンへの結合に関して抗体1S1と約75%競合する、請求項156の方法。
- 配列番号9の成熟ヘプシジンを結合するポリクローナル抗体とともに試料を温置することをさらに含む、請求項134の方法。
- モノクローナル抗体が固体支持体上に固定化されている、請求項158に記載の方法。
- ポリクローナル抗体が標識されている、請求項159の方法。
- ポリクローナル抗体が固体支持体上に固定化されている、請求項158の方法。
- モノクローナル抗体が標識されている、請求項161の方法。
- 抗体が固体支持体上に固定化されており、及び結合されたヘプシジンを検出するために、請求項1から127に記載の何れか一項に記載の第二の抗体とヘプシジンを接触させることをさらに含む、請求項134の方法。
- 前記生物試料がヒトから単離される、請求項134に記載の方法。
- 前記生物試料が、血漿、血清、尿及びこれらから得られる何れかの画分からなる群から選択される、請求項134に記載の方法。
- 第二の抗体が固体支持体上に固定化された抗体によって認識されるものと異なるエピトープを認識する、請求項163に記載の方法。
- 第二の抗体が標識されている、請求項163に記載の方法。
- 試料中のヘプシジンの量を定量することを含む、請求項164に記載の方法。
- 既知量の精製されたヘプシジン標準を前記抗体とともに温置することを含む、請求項134に記載の方法。
- 既知量の複数のヘプシジン標準を用いて標準曲線を決定することを含む、請求項169に記載の方法。
- 前記方法が競合的酵素連結免疫吸着検定法(ELISA)である、請求項134に記載の方法。
- 生物試料中のヒトヘプシジンを検出するためのイムノアッセイキットであって、請求項1から127の何れか一項の1つ又はそれ以上の抗体、及び任意選択で標準としての精製されたヘプシジンを含む、イムノアッセイキット。
- 生物試料中のヒトヘプシジンを検出するためのイムノアッセイキットであって、
(a)配列番号9に記載されているアミノ酸配列からなるヒトヘプシジンへ特異的に結合する抗体を含む捕捉剤、及び
(b)(a)における抗体によって認識されるものと異なるエピトープにおいて前記ヒトヘプシジンへ結合する請求項1から127の何れか一項の抗体を含む検出試薬、
を含む、イムノアッセイキット。 - 捕捉剤がポリクローナル抗体である、請求項173のキット。
- 生物試料中のヒトヘプシジンを検出するためのイムノアッセイキットであって、
(a)配列番号9に記載されているアミノ酸配列からなるヒトヘプシジンへ特異的に結合する抗体を含む検出試薬、及び
(b)(a)における抗体によって認識されるものと異なるエピトープにおいて前記ヒトヘプシジンへ結合する請求項1から127の何れか一項の抗体を含む捕捉試薬、
を含む、イムノアッセイキット。 - 検出試薬がポリクローナル抗体である、請求項175のキット。
- 精製されたヘプシジンを標準としてさらに含む、請求項173又は175に記載のイムノアッセイキット。
- 捕捉剤がAb43、1S1、1S2、1S3、1S4、1S5、2.7、2.41、R9、1C9、3B3、4El、7A3、9D12、12B9、18D8、19C1、19D12、19H6、15E1、23F11及び26F11からなる群から選択される抗体を含む、請求項173に記載のイムノアッセイキット。
- ヘプシジン関連疾患を診断する方法であって、
(a)ヒトヘプシジンへの抗体の結合を可能とする条件下で、請求項1から127の何れか一項に記載されている抗体の少なくとも1つと、ヘプシジン関連疾患を有することが疑われているヒトから得られた生物試料を接触させること、並びに
(b)前記抗体に結合されたヘプシジンを検出及び/又は定量すること
を含み、(b)において定量された、閾値レベルを上回る前記試料中のヘプシジンの量がヘプシジン関連疾患の存在を示唆し、閾値レベルを下回る前記試料中のヘプシジンの量がヘプシジン関連疾患の不存在を示唆する、方法。 - 抗体が固体支持体上に固定化されている、請求項179の方法。
- 前記疾患が、貧血、敗血症、炎症の貧血、癌の貧血、化学療法によって誘発される貧血、慢性炎症性貧血、うっ血性心不全、終末段階腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の障害、フェロポーティン病、ヘモクロマトーシス、糖尿病、炎症、関節リウマチ、アテローム性動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症及び赤血球病からなる群から選択される、請求項179に記載の方法。
- 炎症性疾患を非炎症性疾患から識別する方法であって、
(a)ヒトヘプシジンへの抗体の結合を可能とする条件下で、請求項1から127の何れか一項に記載されている抗体の少なくとも1つと、炎症性疾患を有することが疑われているヒトから得られた生物試料を接触させること、並びに
(b)抗体に結合されたヘプシジンへ検出及び又は定量すること、
を含み、
(b)において定量された、閾値レベルを上回るヘプシジンの量が炎症性疾患の存在を示唆し、及び閾値レベルを下回るヘプシジンの量が炎症性疾患の不存在を示唆する、方法。 - 抗体が固体支持体上に固定化されている、請求項182の方法。
- 炎症性疾患が、癌の貧血、慢性疾患の貧血、炎症の貧血、化学療法によって誘発された貧血、慢性腎臓病(段階I、II、III、IV又はV)、終末段階の腎臓病、慢性腎不全、うっ血性心不全、癌、関節リウマチ、全身性紅斑性狼瘡、クローン病、H.ピロリ感染又は他の細菌感染症、C型肝炎、HIV及び他のウイルス疾患、動脈硬化症、アテローム性動脈硬化症、肝硬変、肝炎、膵炎、敗血症、脈管炎、鉄欠乏症、貧血、低色素性小球性貧血及びヘプシジン過剰を伴う症状である、請求項182に記載の方法。
- ヘプシジンアンタゴニストが投与されている治療を監視する方法であって、
(a)ヒトヘプシジンへの抗体の結合を可能とする条件下で、請求項1から127の何れか一項に記載されている抗体の少なくとも1つと、ヘプシジンアンタゴニストを投与されたヒトから得られた生物試料を接触させること、並びに
(b)抗体に結合されたヘプシジンを検出及び/又は定量すること、
を含み、
(b)において定量された、閾値レベルを上回るヘプシジンの量が、ヘプシジンアンタゴニストの用量が治療的に有効でないことを示唆し、前記閾値レベルを下回るヘプシジンの量が、ヘプシジンアンタゴニストの用量が治療的に有効であることを示唆する、方法。 - 抗体が固体支持体上に固定化されている、請求項185の方法。
- 鉄恒常性の障害の治療を必要としている対象における鉄恒常性の障害を治療する方法であって、請求項1から126の何れか一項のモノクローナル抗体を前記対象へ投与することを含む、方法。
- 鉄恒常性の障害が、貧血、敗血症、炎症の貧血、癌の貧血、化学療法によって誘発された貧血、慢性炎症性貧血、うっ血性心不全、終末段階腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の障害、フェロポーティン病、ヘモクロマトーシス、糖尿病、炎症、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症及び赤血球病からなる群から選択される、請求項187に記載の方法。
- 請求項133の組成物を投与することを含む、ヘプシジンの上昇したレベルを有する哺乳動物を治療する方法。
- 請求項133の組成物を投与することを含む、貧血を有する哺乳動物を治療する方法。
- 哺乳動物が、貧血、敗血症、炎症の貧血、癌の貧血、慢性炎症性貧血、うっ血性心不全、終末段階腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の疾患、フェロポーティン病、ヘモクロマトーシス、糖尿病、炎症、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症、赤血球病に罹患しているヒトである、請求項190の方法。
- 請求項133の組成物を含むバイアル又は予め充填された注射器。
- 治療を必要としている哺乳動物を治療する方法であって、前記哺乳動物に、(a)約10−7M又はそれ以下のKDで、配列番号9からなるヒトヘプシジンを結合する抗体及び(b)エリスロポエチン、エリスロポエチン変形物及びエリスロポエチンを結合する抗体からなる群から選択される赤血球新生刺激物質を投与することを含む、方法。
- ヒトヘプシジンを結合する抗体と赤血球新生刺激物質が同じ組成物中に存在する、請求項193の方法。
- 前記患者に鉄を投与することをさらに含む、請求項193又は194の方法。
- 鉄が経口又は全身投与される、請求項195の方法。
- 約10−7M又はそれ以下のKDで、配列番号9からなるヒトヘプシジンを結合する抗体を投与することを含む、赤血球新生刺激物質での治療に対して低応答性である哺乳動物を治療する方法。
- 赤血球新生刺激物質を投与することをさらに含む、請求項197の方法。
- 哺乳動物が、敗血症、貧血、炎症の貧血、癌の貧血、化学療法によって誘発された貧血、うっ血性心不全、終末段階の腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の障害、フェロポーティン病、ヘモクロマトーシス、糖尿病、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症、赤血球病及び腎不全からなる群から選択される症状に罹患している、請求項193から198の何れか一項の方法。
- 哺乳動物が貧血に罹患している、請求項193から198の何れか一項の方法。
- 抗体がキメラ抗体、ヒト化抗体、ヒト抗体、抗体断片及び一本鎖抗体からなる群から選択される、請求項193から200の何れか一項の方法。
- 哺乳動物がヒトである、請求項193から201の何れか一項の方法。
- 赤血球新生刺激物質が配列番号72のヒトエリスロポエチンである、請求項193から196及び198から202の何れか一項の方法。
- 赤血球新生刺激物質が配列番号73のダルベポエチンαである、請求項193から196及び198から202の何れか一項の方法。
- 請求項1から126の何れか一項の抗体と赤血球新生刺激物質を含む、上昇したヘプシジンレベルに関連する障害又は鉄恒常性の障害を伴う疾患を治療するためのキット。
- 抗体及び赤血球新生刺激物質が1つのバイアル中に存在する、請求項205のキット。
- 経口投与又は全身投与のための鉄をさらに含む、請求項206のキット。
- 鉄及び抗体が1つのバイアル中に存在する、請求項207のキット。
- 赤血球新生刺激物質及び鉄が1つのバイアル中に存在する、請求項207のキット。
- 上昇したヘプシジンレベルに関連する疾患又は鉄恒常性の障害を伴う疾患を治療するためのキットであって、請求項1から126の何れか一項の抗体及び容器に付着され又は同封されたラベルを含み、ラベルが赤血球新生刺激物質と一緒の前記抗体の使用を記載している、キット。
- 上昇したヘプシジンレベルに関連する疾患を治療するためのキットであって、赤血球新生刺激物質及び容器に付着され又は同封されたラベルとを含み、ラベルが請求項1から126の何れか一項の抗体と一緒の赤血球新生刺激物質の使用を記載している、キット。
- 鉄治療と一緒の抗体及び赤血球新生刺激物質の使用を記載したラベルをさらに含む、請求項210又は211のキット。
- 赤血球新生刺激物質がエリスロポエチン又はダルベポエチンである、請求項205又は211のキット。
- 配列番号96に記載されているアミノ酸配列を含む、生物活性を有する、精製された、非尿性の、非哺乳動物のヒトヘプシジンの組成物であって、ヒトヘプシジンの少なくとも75%がC2−C4ジスルフィド結合、C5−C7ジスルフィド結合、C1−C8ジスルフィド結合及びC3−C6ジスルフィド結合を有する、組成物。
- ヒトヘプシジンへ結合する化合物を同定する方法であって、
請求項214の組成物と候補化合物を接触させること、及び
候補化合物と組成物中のヒトヘプシジンの間の複合体を検出すること
を含み、複合体の検出は、候補化合物がヒトヘプシジンへ結合することを示唆する、方法。 - ヒトヘプシジンへ結合する化合物を同定及び使用する方法であって、
請求項214の組成物と候補化合物を接触させること、及び
候補化合物と組成物中のヒトヘプシジンの間の複合体を検出すること(複合体の検出は、候補化合物がヒトヘプシジンへ結合することを示唆する。)、及び
候補化合物を哺乳動物へ投与すること、
を含む、方法。 - ヒトヘプシジンに対する抗体を作製する方法であって、
免疫グロブリン産生細胞を請求項214の組成物と接触させること、及び
前記細胞によって産生された免疫グロブリンを単離すること
を含む、方法。 - ヒトヘプシジンを結合する能力に関して抗体を含む組成物を検査する方法であって、
抗体を含む組成物を請求項214の組成物と接触させること、及び
抗体とヒトヘプシジンの間の複合体を検出することを含み、複合体の検出は、抗体がヒトヘプシジンへ結合することを示唆する、方法。 - 配列番号96に記載されているアミノ酸配列を含むヒトヘプシジンポリペプチドを、生物活性を有する形態へ再折り畳みする方法であって、
(a)変性を促進する条件下で、カオトロピック剤へヒトヘプシジンポリペプチドを曝露すること、
(b)適切に折り畳まれた及び生物活性を有する形態への再生を促進する条件下で、酸化剤へ(a)の生成物を曝露すること、並びに
(c)ヒトヘプシジンポリペプチドの少なくとも75%が少なくともC2−C4ジスルフィド結合とC5−C7ジスルフィド結合を有する、生物活性を有するヒトヘプシジンポリペプチドを含む溶液を回収すること、
を含む、方法。 - (b)がヒトヘプシジンポリペプチドを空気以外の酸化剤と接触させることを含む、請求項219の方法。
- 酸化剤がグルタチオンを含む、請求項219の方法。
- (a)が5未満のpHで行われる、請求項219の方法。
- (b)が0.1%未満の酢酸を含有する溶液中で行われる、請求項219の方法。
- (b)が8より大きなpHで行われる、請求項219の方法。
- カオトロピック剤がグアニジン又はその塩である、請求項219の方法。
- グアニジンが約4Mから約6Mの範囲の濃度で存在する、請求項225の方法。
- ヒトヘプシジンポリペプチドを精製することをさらに含む、請求項219から226の何れか一項の方法。
- 8つのシステイン全てを保持し、及びC2−C4ジスルフィド結合をさらに保持する配列番号96に記載されているアミノ酸配列と少なくとも70%同一であるアミノ酸配列を含む、ヘプシジンペプチド類縁体。
- 8つのシステイン全てを保持し、及びC5−C7ジスルフィド結合をさらに保持する配列番号96に記載されているアミノ酸配列と少なくとも70%同一であるアミノ酸配列を含む、ヘプシジンペプチド類縁体。
- C2−C4ジスルフィド結合をさらに保持する、請求項229のヘプシジン類縁体ペプチド。
- フェロポーティン結合活性を保持する請求項228から230の何れか一項のヘプシジン類縁体ペプチド。
- フェロポーティンを活性化する、請求項231のヘプシジン類縁体ペプチド。
- 循環鉄レベルをインビボで減少させる、請求項228から230の何れか一項のヘプシジン類縁体ペプチド。
- フェロポーティン鉄輸送を阻害する、請求項231のヘプシジン類縁体ペプチド。
- 配列番号9の成熟ヒトヘプシジンの鉄制御活性を阻害する、請求項228から230の何れか一項のヘプシジン類縁体ペプチド。
- 循環鉄レベルをインビボで増加させる、請求項228から230の何れか一項のヘプシジン類縁体ペプチド。
- ヒトヘプシジンへ特異的に結合する単離されたモノクローナル抗体であって、前記ヒトヘプシジンは、配列番号9に記載されたアミノ酸配列からなり、並びに配列番号9中に位置する残基10と13及び14から22の間に形成された少なくとも1つのジスルフィド結合ループを含む立体構造を有する、単離されたモノクローナル抗体。
- 抗体が配列番号15、配列番号13、配列番号27、配列番号25、配列番号39、配列番号37、配列番号51、配列番号49、配列番号110、配列番号108、配列番号120、配列番号118、配列番号130、配列番号128、配列番号140、配列番号138、配列番号150、配列番号148、配列番号160、配列番号158、配列番号170、配列番号168、配列番号180、配列番号178、配列番号190、配列番号188、配列番号202、配列番号212、配列番号218、配列番号224、配列番号235、配列番号246、配列番号293、配列番号291、配列番号303、配列番号301、配列番号313、配列番号311、配列番号323及び配列番号321からなる群から選択されるアミノ酸配列と少なくとも95%同一のアミノ酸配列を含む、請求項1の単離されたモノクローナル抗体。
- 1つ又は数個のアミノ酸置換、欠失又は付加によって、配列番号15、配列番号13、配列番号27、配列番号25、配列番号39、配列番号37、配列番号51、配列番号49、配列番号110、配列番号108、配列番号120、配列番号118、配列番号130、配列番号128、配列番号140、配列番号138、配列番号150、配列番号148、配列番号160、配列番号158、配列番号170、配列番号168、配列番号180、配列番号178、配列番号190、配列番号188、配列番号202、配列番号212、配列番号218、配列番号224、配列番号235、配列番号246、配列番号293、配列番号291、配列番号303、配列番号301、配列番号313、配列番号311、配列番号323及び配列番号321からなる群から選択されるアミノ酸配列から得られるアミノ酸配列を含み、並びに元のアミノ酸配列の生物活性を有する、請求項1の単離されたモノクローナル抗体。
- 前記抗体が、配列番号9と少なくとも80%同一であり、及び8つのシステイン残基を有する25アミノ酸からなるポリペプチドへも結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、配列番号9と少なくとも90%同一であり、及び8つのシステイン残基を有する25アミノ酸からなるポリペプチドへも結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、配列番号9と少なくとも95%同一であり、及び8つのシステイン残基を有する25アミノ酸からなるポリペプチドへも結合する、請求項1に記載の単離されたモノクローナル抗体。
- 前記抗体が、1つ又は数個のアミノ酸置換、欠失又は付加によって、配列番号9のアミノ酸配列から誘導され及び配列番号9の生物活性を有し、並びに8つのシステイン残基を有する、25のアミノ酸からなるポリペプチドにも結合する、請求項1に記載の単離されたモノクローナル抗体。
- アミノ酸配列が配列番号96に記載されているアミノ酸配列と少なくとも80%同一である、請求項228から236のヘプシジンペプチド類縁体。
- アミノ酸配列が配列番号96に記載されているアミノ酸配列と少なくとも90%同一である、請求項228から236のヘプシジンペプチド類縁体。
- アミノ酸配列が、1つ又は数個のアミノ酸置換、欠失又は付加によって、配列番号96に記載されているアミノ酸配列から誘導され、及び配列番号96の生物活性を有する、請求項228から236のヘプシジンペプチド類縁体。
- 請求項1から126の何れか一項のモノクローナル抗体を含む、鉄恒常性の障害の治療を必要としている対象における鉄恒常性の障害を治療するための組成物。
- 鉄恒常性の障害が、貧血、敗血症、炎症の貧血、癌の貧血、化学療法によって誘発された貧血、慢性炎症性貧血、うっ血性心不全、終末段階腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の障害、フェロポーティン病、ヘモクロマトーシス、糖尿病、炎症、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症及び赤血球病からなる群から選択される、請求項247に記載の組成物。
- ヘプシジンの上昇したレベルを有する哺乳動物を治療するための請求項133の組成物。
- 貧血を有する哺乳動物を治療するための、請求項133の組成物。
- 哺乳動物が、貧血、敗血症、炎症の貧血、癌の貧血、慢性炎症性貧血、うっ血性心不全、終末段階腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の疾患、フェロポーティン病、ヘモクロマトーシス、糖尿病、炎症、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症及び赤血球病に罹患しているヒトである、請求項250の組成物。
- 約10−7M又はそれ以下のKDで、配列番号9からなるヒトヘプシジンを結合する抗体並びにエリスロポエチン、エリスロポエチン変形物及びエリスロポエチンを結合する抗体からなる群から選択される赤血球新生刺激物質を含む、治療を必要としている哺乳動物を治療するための組成物。
- ヒトヘプシジンを結合する抗体と赤血球新生刺激物質が同じ組成物中に存在する、請求項252の組成物。
- 方法が鉄をさらに含み、前記鉄は前記患者へ投与されるように調合されている請求項252又は253の組成物。
- 鉄が経口又は全身投与されるように調合されている、請求項254の組成物。
- 約10−7M又はそれ以下のKDで、配列番号9からなるヒトヘプシジンを結合する抗体を含む、赤血球新生刺激物質での治療に対して低応答性である哺乳動物を治療するための組成物。
- 赤血球新生刺激物質をさらに含む、請求項256の組成物。
- 哺乳動物が、敗血症、貧血、炎症の貧血、癌の貧血、化学療法によって誘発された貧血、うっ血性心不全、終末段階の腎疾患、慢性腎臓病(段階I、II、III、IV又はV)、鉄欠乏性貧血、鉄恒常性の障害、フェロポーティン病、ヘモクロマトーシス、糖尿病、関節リウマチ、動脈硬化症、腫瘍、脈管炎、全身性紅斑性狼瘡、異常ヘモグロビン症、赤血球病及び腎不全からなる群から選択される症状に罹患している、請求項252から257の何れか一項の組成物。
- 哺乳動物が貧血に罹患している、請求項252から257の何れか一項の組成物。
- 抗体がキメラ抗体、ヒト化抗体、ヒト抗体、抗体断片及び一本鎖抗体からなる群から選択される、請求項252から259の何れか一項の組成物。
- 哺乳動物がヒトである、請求項252から260の何れか一項の組成物。
- 赤血球新生刺激物質が配列番号72のヒトエリスロポエチンである、請求項252から255及び257から261の何れか一項の組成物。
- 赤血球新生刺激物質が配列番号73のダルベポエチンαである、請求項252から255及び257から261の何れか一項の組成物。
- 前記抗体がAb43、241及び2.7から選択される抗体である、請求項247から263の何れか一項の組成物。
- 工程(c)で回収されたヘプシジンの生物活性形態が、C2−C4又はC5−C7ジスルフィド結合の形成に関して、NEM部分的還元的アルキル化又はフーリエ変換質量分析によって評価される、請求項219に記載の方法。
- 請求項219又は請求項265の方法によって取得可能な、生物活性を有する非尿性ヒトヘプシジン。
- 請求項266に記載のヒトヘプシジンへ特異的に結合するモノクローナル抗体。
- 請求項1から112の何れか一項の抗ヘプシジン抗体と同時投与するための医薬の製造における、赤血球新生刺激物質の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US88805907P | 2007-02-02 | 2007-02-02 | |
| US1513807P | 2007-12-19 | 2007-12-19 | |
| PCT/US2008/001325 WO2008097461A2 (en) | 2007-02-02 | 2008-01-30 | Hepcidin and hepcidin antibodies |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014119334A Division JP2014221763A (ja) | 2007-02-02 | 2014-06-10 | ヘプシジン及びヘプシジン抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010517529A true JP2010517529A (ja) | 2010-05-27 |
| JP2010517529A5 JP2010517529A5 (ja) | 2012-06-14 |
Family
ID=39682290
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009548312A Withdrawn JP2010517529A (ja) | 2007-02-02 | 2008-01-30 | ヘプシジン及びヘプシジン抗体 |
| JP2014119334A Withdrawn JP2014221763A (ja) | 2007-02-02 | 2014-06-10 | ヘプシジン及びヘプシジン抗体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014119334A Withdrawn JP2014221763A (ja) | 2007-02-02 | 2014-06-10 | ヘプシジン及びヘプシジン抗体 |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US8629250B2 (ja) |
| EP (1) | EP2111412A2 (ja) |
| JP (2) | JP2010517529A (ja) |
| AR (2) | AR065083A1 (ja) |
| AU (1) | AU2008214386B2 (ja) |
| CA (1) | CA2676036A1 (ja) |
| CL (1) | CL2008000278A1 (ja) |
| MX (1) | MX2009008104A (ja) |
| PE (2) | PE20090722A1 (ja) |
| TW (3) | TW201206954A (ja) |
| WO (1) | WO2008097461A2 (ja) |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015504859A (ja) * | 2011-12-09 | 2015-02-16 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 改変ミニヘプシジンペプチドおよびその使用方法 |
| JP2016513664A (ja) * | 2013-03-15 | 2016-05-16 | イントリンシック ライフサイエンシズ リミテッド ライアビリティ カンパニー | 抗ヘプシジン抗体およびその使用 |
| JP2016521257A (ja) * | 2013-03-15 | 2016-07-21 | プロタゴニスト セラピューティクス, インコーポレイテッド | ヘプシジン類似体及びその使用 |
| JP2017507328A (ja) * | 2014-01-30 | 2017-03-16 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 室温での全血の安定化 |
| US10323088B2 (en) | 2014-09-22 | 2019-06-18 | Intrinsic Lifesciences Llc | Humanized anti-hepcidin antibodies and uses thereof |
| WO2019235420A1 (ja) * | 2018-06-04 | 2019-12-12 | 中外製薬株式会社 | 複合体を検出する方法 |
| US10787490B2 (en) | 2015-07-15 | 2020-09-29 | Protaganist Therapeutics, Inc. | Peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory diseases |
| US10941183B2 (en) | 2014-07-17 | 2021-03-09 | Protagonist Therapeutics, Inc. | Oral peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory bowel diseases |
| US11041000B2 (en) | 2019-07-10 | 2021-06-22 | Protagonist Therapeutics, Inc. | Peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory diseases |
| US11111272B2 (en) | 2014-10-01 | 2021-09-07 | Protagonist Therapeutics, Inc. | α4α7 peptide monomer and dimer antagonists |
| WO2022154121A1 (ja) * | 2021-01-18 | 2022-07-21 | 富士フイルム和光純薬株式会社 | ヘプシジンの吸着抑制剤、吸着抑制方法、標準品、試薬、キットおよび測定方法 |
| US11472842B2 (en) | 2015-12-30 | 2022-10-18 | Protagonist Therapeutics, Inc. | Analogues of hepcidin mimetics with improved in vivo half lives |
| US11753443B2 (en) | 2018-02-08 | 2023-09-12 | Protagonist Therapeutics, Inc. | Conjugated hepcidin mimetics |
| US11840581B2 (en) | 2014-05-16 | 2023-12-12 | Protagonist Therapeutics, Inc. | α4β7 thioether peptide dimer antagonists |
Families Citing this family (57)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE60231804D1 (de) | 2001-05-25 | 2009-05-14 | Inst Nat Sante Rech Med | Verwendung von hepcidin zur herstellung eines arzneimittels zur behandlung von eisenhomöostase störungen |
| AU2007299629C1 (en) | 2006-09-21 | 2012-05-10 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of the HAMP gene |
| US8487081B2 (en) | 2007-10-02 | 2013-07-16 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies specific for human hepcidin |
| JO2828B1 (en) | 2007-11-02 | 2014-09-15 | ايلي ليلي اند كومباني | Anti-Hepsidine antibodies and their uses |
| AU2009206306B2 (en) * | 2008-01-25 | 2013-06-06 | Amgen Inc. | Ferroportin antibodies and methods of use |
| EP2816059A1 (en) * | 2008-05-01 | 2014-12-24 | Amgen, Inc | Anti-hepcidin antibodies and methods of use |
| MX2011001363A (es) * | 2008-08-06 | 2011-04-26 | Lilly Co Eli | Anticuerpos selectivos de anti-hepcidina-25 y usos de los mismos. |
| EP2157432A1 (en) * | 2008-08-15 | 2010-02-24 | Qiagen GmbH | Method for analysing a complex sample by mass spectrometry |
| US8183346B2 (en) * | 2008-12-05 | 2012-05-22 | Eli Lilly And Company | Anti-ferroportin 1 monoclonal antibodies and uses thereof |
| EP3208279B1 (en) | 2008-12-05 | 2021-04-21 | The Regents of The University of California | Mini-hepcidin peptides and methods of using thereof |
| US8999935B2 (en) * | 2009-02-11 | 2015-04-07 | New York University | Treatment of osteoporosis in peri- and post-menopausal women with hepcidin |
| TWI578992B (zh) * | 2009-04-30 | 2017-04-21 | 諾克森製藥股份有限公司 | 與鐵調節激素(hepcidin)結合之核酸類 |
| EP3660032A1 (en) | 2009-06-25 | 2020-06-03 | Amgen, Inc | Capture purification processes for proteins expressed in a non-mammalian system |
| WO2011005818A1 (en) * | 2009-07-08 | 2011-01-13 | Bio-Rad Laboratories, Inc. | Purification of monoclonal antibodies |
| DE102009034150A1 (de) | 2009-07-20 | 2011-01-27 | Fresenius Medical Care Deutschland Gmbh | Adsorbens zur Adsorption von Hepcidin |
| BR112012003701A2 (pt) | 2009-08-20 | 2019-09-24 | Vifor Int Ag | "novos antagonistas de quinolina-hepcidina" |
| AR077958A1 (es) | 2009-08-27 | 2011-10-05 | Vifor Int Ag | Quinoxalinonas antagonistas de la hepcidina |
| AR077999A1 (es) | 2009-09-02 | 2011-10-05 | Vifor Int Ag | Antagonistas de pirimidin y triazin-hepcidina |
| WO2011026959A1 (de) | 2009-09-07 | 2011-03-10 | Vifor (International) Ag | Neue ethandiamin-hepcidin-antagonisten |
| TW201111379A (en) | 2009-09-09 | 2011-04-01 | Vifor Int Ag | Novel thiazole-and oxazole-hepcidine-antagonists |
| WO2011057744A1 (en) | 2009-11-13 | 2011-05-19 | Roche Diagnostics Gmbh | Differential diagnosis of iron deficiencies based on hepcidin and mean hemoglobin content per reticulocyte |
| WO2011071368A1 (en) | 2009-12-11 | 2011-06-16 | Umc St. Radboud | Method for measuring hepcidin |
| CN101955525B (zh) * | 2010-07-13 | 2012-11-07 | 中国农业科学院兰州畜牧与兽药研究所 | 一种人工抗菌肽及其基因与制备方法 |
| CN103154023B (zh) | 2010-08-16 | 2017-04-05 | 皮里斯制药有限公司 | 铁调素的结合蛋白 |
| WO2012055573A1 (en) * | 2010-10-29 | 2012-05-03 | Noxxon Pharma Ag | Use of hepcidin binding nucleic acids for depletion of hepcidin from the body |
| US20120214803A1 (en) | 2011-02-18 | 2012-08-23 | Vifor (International) Ag | Novel Sulfonaminoquinoline Hepcidin Antagonists |
| WO2012122025A2 (en) | 2011-03-04 | 2012-09-13 | Intrexon Corporation | Vectors conditionally expressing protein |
| CA2839896A1 (en) * | 2011-06-21 | 2012-12-27 | Alnylam Pharmaceuticals, Inc. | Assays and methods for determining activity of a therapeutic agent in a subject |
| EP2723861A4 (en) * | 2011-06-21 | 2014-12-10 | Alnylam Pharmaceuticals Inc | COMPOSITIONS AND METHODS FOR INHIBITING HEPCIDINE ANTIMICROBIAL PEPTIDE (HAMP) OR THE ASSOCIATED GENE EXPRESSION |
| US20130012429A1 (en) * | 2011-07-06 | 2013-01-10 | Lucy Ann Eddowes | Anti-viral therapy |
| EP3309555A3 (en) * | 2011-12-12 | 2018-05-30 | Pieris Pharmaceuticals GmbH | Methods for preventing or treating disorders by increasing bioavailability of iron and related pharmaceutical formulation |
| WO2014022759A1 (en) * | 2012-08-03 | 2014-02-06 | Dana-Farber Cancer Institute, Inc. | Agents that modulate immune cell activation and methods of use thereof |
| CN104854130A (zh) * | 2012-11-01 | 2015-08-19 | 加利福尼亚大学董事会 | Erythroferrone和erfe多肽以及调控铁代谢的方法 |
| AU2014236867A1 (en) * | 2013-03-15 | 2015-09-24 | Amgen Inc. | Methods and compositions relating to anti-CCR7 antigen binding proteins |
| US9315545B2 (en) | 2014-04-07 | 2016-04-19 | Merganser Biotech, Inc. | Hepcidin mimetic peptides and uses thereof |
| SG11201610799WA (en) * | 2014-06-27 | 2017-01-27 | Protagonist Therapeutics Inc | Hepcidin and mini-hepcidin analogues and uses therof |
| US10301371B2 (en) | 2014-10-01 | 2019-05-28 | Protagonist Therapeutics, Inc. | Cyclic monomer and dimer peptides having integrin antagonist activity |
| WO2016146587A1 (en) | 2015-03-13 | 2016-09-22 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Hepcidin antagonists for use in the treatment of inflammation |
| EP3316159A4 (en) | 2015-06-25 | 2019-08-14 | Advanced Telecommunications Research Institute International | PREDICTIVE EQUIPMENT BASED ON A SYSTEM ASSOCIATED WITH SEVERAL INSTITUTIONS AND PREDICTION PROGRAM |
| KR20180042431A (ko) | 2015-09-04 | 2018-04-25 | 헬스 리서치 인코포레이티드 | 암 치료용 안티-서비빈 항체 |
| US10407468B2 (en) | 2016-03-23 | 2019-09-10 | Protagonist Therapeutics, Inc. | Methods for synthesizing α4β7 peptide antagonists |
| WO2017170803A1 (ja) | 2016-03-29 | 2017-10-05 | 株式会社国際電気通信基礎技術研究所 | 医薬組成物又は食品組成物、及び有効成分の体内での効果の評価方法 |
| EP3438282A4 (en) * | 2016-03-29 | 2020-05-06 | Advanced Telecommunications Research Institute International | METHOD FOR SCREENING CANDIDATE SUBSTANCES FOR AN ACTIVE COMPONENT TO PREVENT OR TREAT AT LEAST ONE SELECTED DISEASE IN THE KIDNEY HYPOFUNCTION GROUP, CHRONIC KIDNEY DISEASE AND KIDNEY DEFICIENCY |
| US10347656B2 (en) * | 2016-07-18 | 2019-07-09 | Semiconductor Components Industries, Llc | Semiconductor device and monolithic semiconductor device including a power semiconductor device and a control circuit |
| WO2018027184A1 (en) * | 2016-08-05 | 2018-02-08 | Silarus Therapeutics, Inc. | Erfe specific antibodies compositions and methods of use |
| WO2018053468A1 (en) * | 2016-09-19 | 2018-03-22 | The University Of Toledo | Monoclonal igm antibodies from entirely carbohydrate constructs |
| WO2018234538A1 (en) | 2017-06-23 | 2018-12-27 | INSERM (Institut National de la Santé et de la Recherche Médicale) | ANTAGONIST OR AGONIST OF HEPCIDINE FOR USE IN THE TREATMENT OF DYSREGULATION OF MO AND / OR MN METABOLISM |
| US10278957B2 (en) | 2017-09-11 | 2019-05-07 | Protagonist Therapeutics, Inc. | Opioid agonist peptides and uses thereof |
| GB2590642B (en) * | 2019-12-20 | 2024-02-14 | Kymab Ltd | Improved lambda antibodies |
| AU2020308463A1 (en) * | 2019-06-26 | 2022-02-17 | Ap Biosciences, Inc. | Antibodies for T-cell activation |
| KR20220088699A (ko) * | 2019-09-27 | 2022-06-28 | 디스크 메디슨, 인크. | 골수섬유증 및 관련 상태의 치료 방법 |
| WO2021062171A1 (en) * | 2019-09-27 | 2021-04-01 | Disc Medicine, Inc. | Methods for treating anemia of chronic disease |
| EP4090670A1 (en) | 2020-01-15 | 2022-11-23 | Janssen Biotech, Inc. | Peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory diseases |
| BR112022015876A2 (pt) * | 2020-02-11 | 2022-10-25 | Quest Diagnostics Invest Llc | Sistema para determinar uma causa subjacente de anemia |
| KR20230007368A (ko) | 2020-04-07 | 2023-01-12 | 맵웰 테라퓨틱스 인크. | 항-tmprss6 항체 및 이의 용도 |
| JP7397239B2 (ja) | 2020-11-20 | 2023-12-12 | ヤンセン ファーマシューティカ エヌ.ベー. | インターロイキン-23受容体のペプチド阻害剤の組成物 |
| CN115356414A (zh) * | 2022-08-19 | 2022-11-18 | 珠海市丽珠单抗生物技术有限公司 | 糖蛋白二硫键的鉴定方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1403154A (zh) * | 2002-10-21 | 2003-03-19 | 钱忠明 | Hepcidin(海魄喜定)在制药中的应用 |
| JP2006517198A (ja) * | 2002-11-19 | 2006-07-20 | ディーアールジー・インターナショナル,インコーポレイテッド | ヒトまたは動物の組織、血液もしくは体液中のヘプシジンをスクリーニングすることによる疾患の診断方法およびそのための治療的使用 |
Family Cites Families (133)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| NL154598B (nl) | 1970-11-10 | 1977-09-15 | Organon Nv | Werkwijze voor het aantonen en bepalen van laagmoleculire verbindingen en van eiwitten die deze verbindingen specifiek kunnen binden, alsmede testverpakking. |
| US3901654A (en) * | 1971-06-21 | 1975-08-26 | Biological Developments | Receptor assays of biologically active compounds employing biologically specific receptors |
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| US3935074A (en) * | 1973-12-17 | 1976-01-27 | Syva Company | Antibody steric hindrance immunoassay with two antibodies |
| US3996345A (en) | 1974-08-12 | 1976-12-07 | Syva Company | Fluorescence quenching with immunological pairs in immunoassays |
| US4034074A (en) * | 1974-09-19 | 1977-07-05 | The Board Of Trustees Of Leland Stanford Junior University | Universal reagent 2-site immunoradiometric assay using labelled anti (IgG) |
| US3984533A (en) | 1975-11-13 | 1976-10-05 | General Electric Company | Electrophoretic method of detecting antigen-antibody reaction |
| US4098876A (en) * | 1976-10-26 | 1978-07-04 | Corning Glass Works | Reverse sandwich immunoassay |
| USRE30985E (en) * | 1978-01-01 | 1982-06-29 | Serum-free cell culture media | |
| JPS6023084B2 (ja) | 1979-07-11 | 1985-06-05 | 味の素株式会社 | 代用血液 |
| US4452901A (en) * | 1980-03-20 | 1984-06-05 | Ciba-Geigy Corporation | Electrophoretically transferring electropherograms to nitrocellulose sheets for immuno-assays |
| US4376110A (en) * | 1980-08-04 | 1983-03-08 | Hybritech, Incorporated | Immunometric assays using monoclonal antibodies |
| JPS5896026A (ja) * | 1981-10-30 | 1983-06-07 | Nippon Chemiphar Co Ltd | 新規ウロキナ−ゼ誘導体およびその製造法ならびにそれを含有する血栓溶解剤 |
| US4640835A (en) * | 1981-10-30 | 1987-02-03 | Nippon Chemiphar Company, Ltd. | Plasminogen activator derivatives |
| DE3380726D1 (en) | 1982-06-24 | 1989-11-23 | Japan Chem Res | Long-acting composition |
| US4560655A (en) | 1982-12-16 | 1985-12-24 | Immunex Corporation | Serum-free cell culture medium and process for making same |
| US4657866A (en) * | 1982-12-21 | 1987-04-14 | Sudhir Kumar | Serum-free, synthetic, completely chemically defined tissue culture media |
| US4767704A (en) * | 1983-10-07 | 1988-08-30 | Columbia University In The City Of New York | Protein-free culture medium |
| US4703008A (en) | 1983-12-13 | 1987-10-27 | Kiren-Amgen, Inc. | DNA sequences encoding erythropoietin |
| KR850004274A (ko) | 1983-12-13 | 1985-07-11 | 원본미기재 | 에리트로포이에틴의 제조방법 |
| NZ210501A (en) * | 1983-12-13 | 1991-08-27 | Kirin Amgen Inc | Erythropoietin produced by procaryotic or eucaryotic expression of an exogenous dna sequence |
| US4496689A (en) * | 1983-12-27 | 1985-01-29 | Miles Laboratories, Inc. | Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer |
| DE3675588D1 (de) * | 1985-06-19 | 1990-12-20 | Ajinomoto Kk | Haemoglobin, das an ein poly(alkenylenoxid) gebunden ist. |
| US4667016A (en) * | 1985-06-20 | 1987-05-19 | Kirin-Amgen, Inc. | Erythropoietin purification |
| US4766106A (en) * | 1985-06-26 | 1988-08-23 | Cetus Corporation | Solubilization of proteins for pharmaceutical compositions using polymer conjugation |
| US4676980A (en) * | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| US4927762A (en) * | 1986-04-01 | 1990-05-22 | Cell Enterprises, Inc. | Cell culture medium with antioxidant |
| US4791192A (en) | 1986-06-26 | 1988-12-13 | Takeda Chemical Industries, Ltd. | Chemically modified protein with polyethyleneglycol |
| US5567610A (en) | 1986-09-04 | 1996-10-22 | Bioinvent International Ab | Method of producing human monoclonal antibodies and kit therefor |
| US4987071A (en) * | 1986-12-03 | 1991-01-22 | University Patents, Inc. | RNA ribozyme polymerases, dephosphorylases, restriction endoribonucleases and methods |
| US5283187A (en) * | 1987-11-17 | 1994-02-01 | Brown University Research Foundation | Cell culture-containing tubular capsule produced by co-extrusion |
| US4892538A (en) * | 1987-11-17 | 1990-01-09 | Brown University Research Foundation | In vivo delivery of neurotransmitters by implanted, encapsulated cells |
| US5223409A (en) * | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| GB8823869D0 (en) * | 1988-10-12 | 1988-11-16 | Medical Res Council | Production of antibodies |
| US5175384A (en) * | 1988-12-05 | 1992-12-29 | Genpharm International | Transgenic mice depleted in mature t-cells and methods for making transgenic mice |
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5244805A (en) | 1989-05-17 | 1993-09-14 | University Of Georgia Research Foundation, Inc. | Baculovirus expression vectors |
| DE3920358A1 (de) * | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| US5856298A (en) * | 1989-10-13 | 1999-01-05 | Amgen Inc. | Erythropoietin isoforms |
| US7217689B1 (en) * | 1989-10-13 | 2007-05-15 | Amgen Inc. | Glycosylation analogs of erythropoietin |
| DE69120146T2 (de) | 1990-01-12 | 1996-12-12 | Cell Genesys Inc | Erzeugung xenogener antikörper |
| US5229275A (en) * | 1990-04-26 | 1993-07-20 | Akzo N.V. | In-vitro method for producing antigen-specific human monoclonal antibodies |
| US5723286A (en) * | 1990-06-20 | 1998-03-03 | Affymax Technologies N.V. | Peptide library and screening systems |
| GB9014932D0 (en) * | 1990-07-05 | 1990-08-22 | Celltech Ltd | Recombinant dna product and method |
| US5122469A (en) * | 1990-10-03 | 1992-06-16 | Genentech, Inc. | Method for culturing Chinese hamster ovary cells to improve production of recombinant proteins |
| ES2136092T3 (es) | 1991-09-23 | 1999-11-16 | Medical Res Council | Procedimientos para la produccion de anticuerpos humanizados. |
| US5733731A (en) * | 1991-10-16 | 1998-03-31 | Affymax Technologies N.V. | Peptide library and screening method |
| US5270170A (en) * | 1991-10-16 | 1993-12-14 | Affymax Technologies N.V. | Peptide library and screening method |
| ATE244763T1 (de) | 1992-02-11 | 2003-07-15 | Cell Genesys Inc | Erzielen von homozygotem durch zielgerichtete genetische ereignisse |
| US5573905A (en) | 1992-03-30 | 1996-11-12 | The Scripps Research Institute | Encoded combinatorial chemical libraries |
| US5885527A (en) * | 1992-05-21 | 1999-03-23 | Biosite Diagnostics, Inc. | Diagnostic devices and apparatus for the controlled movement of reagents without membrances |
| US5359681A (en) | 1993-01-11 | 1994-10-25 | University Of Washington | Fiber optic sensor and methods and apparatus relating thereto |
| US5807549A (en) * | 1993-05-21 | 1998-09-15 | Research Corporation Technologies, Inc. | Lymphocyte chemoattractant factor and uses thereof |
| US5922545A (en) * | 1993-10-29 | 1999-07-13 | Affymax Technologies N.V. | In vitro peptide and antibody display libraries |
| US5773569A (en) * | 1993-11-19 | 1998-06-30 | Affymax Technologies N.V. | Compounds and peptides that bind to the erythropoietin receptor |
| US5830851A (en) | 1993-11-19 | 1998-11-03 | Affymax Technologies N.V. | Methods of administering peptides that bind to the erythropoietin receptor |
| US6054287A (en) * | 1994-05-27 | 2000-04-25 | Methodist Hospital Of Indiana, Inc. | Cell-type-specific methods and devices for the low temperature preservation of the cells of an animal species |
| US5885574A (en) | 1994-07-26 | 1999-03-23 | Amgen Inc. | Antibodies which activate an erythropoietin receptor |
| US5723750A (en) * | 1995-01-12 | 1998-03-03 | Vanderbilt University | Transgenic plants expressing disassembly deficient viral coat proteins |
| US5767078A (en) * | 1995-06-07 | 1998-06-16 | Johnson; Dana L. | Agonist peptide dimers |
| WO1997014719A1 (en) | 1995-10-16 | 1997-04-24 | Unilever N.V. | A bifunctional or bivalent antibody fragment analogue |
| GB9712818D0 (en) * | 1996-07-08 | 1997-08-20 | Cambridge Antibody Tech | Labelling and selection of specific binding molecules |
| US6306393B1 (en) | 1997-03-24 | 2001-10-23 | Immunomedics, Inc. | Immunotherapy of B-cell malignancies using anti-CD22 antibodies |
| US20020032315A1 (en) | 1997-08-06 | 2002-03-14 | Manuel Baca | Anti-vegf antibodies |
| US6278039B1 (en) | 1997-05-28 | 2001-08-21 | Axys Pharmaceuticals, Inc. | C. elegans deletion mutants |
| US6171586B1 (en) * | 1997-06-13 | 2001-01-09 | Genentech, Inc. | Antibody formulation |
| NZ502375A (en) * | 1997-07-14 | 2001-11-30 | Bolder Biotechnology Inc | The addition of non-natural cysteine derivatives to cause the protein to act as antagonists of the GH family |
| US6753165B1 (en) * | 1999-01-14 | 2004-06-22 | Bolder Biotechnology, Inc. | Methods for making proteins containing free cysteine residues |
| PT986644E (pt) * | 1997-07-23 | 2007-01-31 | Roche Diagnostics Gmbh | Preparação de eritropoietina por activação genética endógena com promotores virais |
| US20030044772A1 (en) * | 1997-08-04 | 2003-03-06 | Applied Molecular Evolution [Formerly Ixsys] | Methods for identifying ligand specific binding molecules |
| US6251588B1 (en) * | 1998-02-10 | 2001-06-26 | Agilent Technologies, Inc. | Method for evaluating oligonucleotide probe sequences |
| US20020029391A1 (en) * | 1998-04-15 | 2002-03-07 | Claude Geoffrey Davis | Epitope-driven human antibody production and gene expression profiling |
| US6310078B1 (en) | 1998-04-20 | 2001-10-30 | Ortho-Mcneil Pharmaceutical, Inc. | Substituted amino acids as erythropoietin mimetics |
| ES2273497T3 (es) | 1998-06-15 | 2007-05-01 | Gtc Biotherapeutics, Inc. | Proteina de fusion de la albumina serica humana de eritropoyetina analoga. |
| US20050181482A1 (en) | 2004-02-12 | 2005-08-18 | Meade Harry M. | Method for the production of an erythropoietin analog-human IgG fusion proteins in transgenic mammal milk |
| US6210924B1 (en) * | 1998-08-11 | 2001-04-03 | Amgen Inc. | Overexpressing cyclin D 1 in a eukaryotic cell line |
| MXPA01005515A (es) * | 1998-12-01 | 2003-07-14 | Protein Design Labs Inc | Anticuerpos humanizados para gamma-interferon. |
| US20030190669A1 (en) | 1998-12-30 | 2003-10-09 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| US6110462A (en) | 1999-03-03 | 2000-08-29 | The Scripps Research Institute | Enzymatic DNA molecules that contain modified nucleotides |
| WO2000061637A1 (en) | 1999-04-14 | 2000-10-19 | Smithkline Beecham Corporation | Erythropoietin receptor antibodies |
| US7297680B2 (en) | 1999-04-15 | 2007-11-20 | Crucell Holland B.V. | Compositions of erythropoietin isoforms comprising Lewis-X structures and high sialic acid content |
| CZ299516B6 (cs) * | 1999-07-02 | 2008-08-20 | F. Hoffmann-La Roche Ag | Konjugát erythropoetinového glykoproteinu, zpusobjeho výroby a použití a farmaceutická kompozice sjeho obsahem |
| US6262247B1 (en) * | 1999-08-30 | 2001-07-17 | Incyte Genomics, Inc. | Polycyclic aromatic hydrocarbon induced molecules |
| US20050202538A1 (en) | 1999-11-12 | 2005-09-15 | Merck Patent Gmbh | Fc-erythropoietin fusion protein with improved pharmacokinetics |
| US6586398B1 (en) * | 2000-04-07 | 2003-07-01 | Amgen, Inc. | Chemically modified novel erythropoietin stimulating protein compositions and methods |
| US7476383B2 (en) | 2000-05-02 | 2009-01-13 | The Uab Research Foundation | Antibody selective for DR4 and uses thereof |
| US7560534B2 (en) * | 2000-05-08 | 2009-07-14 | Celldex Research Corporation | Molecular conjugates comprising human monoclonal antibodies to dendritic cells |
| JP3523245B1 (ja) | 2000-11-30 | 2004-04-26 | メダレックス,インコーポレーテッド | ヒト抗体作製用トランスジェニック染色体導入齧歯動物 |
| US20030133939A1 (en) * | 2001-01-17 | 2003-07-17 | Genecraft, Inc. | Binding domain-immunoglobulin fusion proteins |
| US7829084B2 (en) * | 2001-01-17 | 2010-11-09 | Trubion Pharmaceuticals, Inc. | Binding constructs and methods for use thereof |
| US7754208B2 (en) * | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| US20030157561A1 (en) | 2001-11-19 | 2003-08-21 | Kolkman Joost A. | Combinatorial libraries of monomer domains |
| US20060223114A1 (en) | 2001-04-26 | 2006-10-05 | Avidia Research Institute | Protein scaffolds and uses thereof |
| DE60231804D1 (de) * | 2001-05-25 | 2009-05-14 | Inst Nat Sante Rech Med | Verwendung von hepcidin zur herstellung eines arzneimittels zur behandlung von eisenhomöostase störungen |
| MXPA04000747A (es) * | 2001-07-25 | 2004-07-08 | Protein Desing Labs Inc | Formulacion farmaceutica liofilizada estable de anticuerpos igg. |
| US6900292B2 (en) * | 2001-08-17 | 2005-05-31 | Lee-Hwei K. Sun | Fc fusion proteins of human erythropoietin with increased biological activities |
| WO2003025020A1 (fr) * | 2001-09-13 | 2003-03-27 | Institute For Antibodies Co., Ltd. | Procede pour creer une banque d'anticorps de chameaux |
| US6930086B2 (en) * | 2001-09-25 | 2005-08-16 | Hoffmann-La Roche Inc. | Diglycosylated erythropoietin |
| US7214660B2 (en) * | 2001-10-10 | 2007-05-08 | Neose Technologies, Inc. | Erythropoietin: remodeling and glycoconjugation of erythropoietin |
| WO2003064664A1 (en) * | 2002-01-31 | 2003-08-07 | Oxford Biomedica (Uk) Limited | Physiologically regulated erythropoietin- exprressing vector for the treatment of anaemia |
| GB0202252D0 (en) * | 2002-01-31 | 2002-03-20 | Oxford Biomedica Ltd | Anemia |
| ATE363541T1 (de) * | 2002-03-26 | 2007-06-15 | Lek Tovarna Farmacevtskih | Verfahren für die herstellung eines gewünschten profils von erythropoietin glyko-isoformen |
| ES2327830T3 (es) | 2002-03-29 | 2009-11-04 | Schering Corporation | Anticuerpos monoclonales humanos anti-interleuquina-5 y metodos y composiciones que los contienen. |
| WO2003094858A2 (en) * | 2002-05-13 | 2003-11-20 | Modigenetech Ltd. | Ctp-extended erythropoietin |
| TW200413406A (en) | 2002-08-26 | 2004-08-01 | Kirin Brewery | Peptides and drugs containing the same |
| US7396913B2 (en) | 2002-10-14 | 2008-07-08 | Abbott Laboratories | Erythropoietin receptor binding antibodies |
| US20040071694A1 (en) * | 2002-10-14 | 2004-04-15 | Devries Peter J. | Erythropoietin receptor binding antibodies |
| US20040091961A1 (en) * | 2002-11-08 | 2004-05-13 | Evans Glen A. | Enhanced variants of erythropoietin and methods of use |
| JP2006507841A (ja) | 2002-11-14 | 2006-03-09 | ダーマコン, インコーポレイテッド | 機能的siRNAおよび超機能的siRNA |
| US8017737B2 (en) * | 2002-11-19 | 2011-09-13 | Hasan Kulaksiz | Diagnostic methods for diseases by screening for hepcidin in human or animal tissues, blood or body fluids; monoclonal antibodies specific to human hepcidin and associated uses therefor |
| US7411048B2 (en) * | 2002-11-19 | 2008-08-12 | Drg International, Inc. | Diagnostic method for diseases by screening for hepcidin in human or animal tissues, blood or body fluids |
| CA2522680A1 (en) * | 2003-04-15 | 2004-10-28 | Xenon Pharmaceuticals Inc. | Juvenile hemochromatosis gene (hfe2a), expression products and uses thereof |
| ATE428727T1 (de) * | 2003-05-12 | 2009-05-15 | Affymax Inc | Neue, an den erythropoietinrezeptor bindende peptide |
| BRPI0411160A (pt) * | 2003-05-12 | 2006-07-11 | Affymax Inc | novos compostos modificados com poli(glicol etilênico) e usos dos mesmos |
| US7074755B2 (en) | 2003-05-17 | 2006-07-11 | Centocor, Inc. | Erythropoietin conjugate compounds with extended half-lives |
| KR20060032140A (ko) | 2003-05-30 | 2006-04-14 | 센토코 인코포레이티드 | 트랜스글루타미나아제를 이용한 신규 에리트로포이에틴접합체의 형성 |
| GB0312352D0 (en) * | 2003-05-30 | 2003-07-02 | Cellpep Sa | Oxidation of peptides |
| US8614204B2 (en) * | 2003-06-06 | 2013-12-24 | Fibrogen, Inc. | Enhanced erythropoiesis and iron metabolism |
| US20050019914A1 (en) * | 2003-07-24 | 2005-01-27 | Aventis Pharma Deutschland Gmbh | Perfusion process for producing erythropoietin |
| EP1654370B1 (en) * | 2003-08-01 | 2018-05-30 | GOVERNMENT OF THE UNITED STATES OF AMERICA, as represented by THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES | Accelerated ebola vaccination |
| DE10349124A1 (de) * | 2003-10-22 | 2005-05-19 | Roche Diagnostics Gmbh | Differenzialdiagnostik mit Hepcidin |
| EP1694347B1 (en) * | 2003-11-24 | 2013-11-20 | BioGeneriX AG | Glycopegylated erythropoietin |
| US8633157B2 (en) * | 2003-11-24 | 2014-01-21 | Novo Nordisk A/S | Glycopegylated erythropoietin |
| JP2008500275A (ja) | 2003-12-31 | 2008-01-10 | セントカー・インコーポレーテツド | N末端の遊離チオールを有する新規な組み換えタンパク質 |
| PT1699821E (pt) | 2003-12-31 | 2012-08-23 | Merck Patent Gmbh | Proteína de fusão fc-eritropoietina com farmacocinética melhorada |
| US7423139B2 (en) * | 2004-01-20 | 2008-09-09 | Insight Biopharmaceuticals Ltd. | High level expression of recombinant human erythropoietin having a modified 5′-UTR |
| KR101147147B1 (ko) | 2004-04-01 | 2012-05-25 | 머크 샤프 앤드 돔 코포레이션 | Rna 간섭의 오프 타겟 효과 감소를 위한 변형된폴리뉴클레오타이드 |
| US20050227289A1 (en) | 2004-04-09 | 2005-10-13 | Reilly Edward B | Antibodies to erythropoietin receptor and uses thereof |
| US7723063B2 (en) * | 2004-04-28 | 2010-05-25 | Intrinsic Lifesciences | Methods for measuring levels of bioactive human hepcidin |
| CN101189516A (zh) * | 2005-03-11 | 2008-05-28 | 赛弗吉生物系统公司 | 卵巢癌及子宫内膜癌的生物标记:抗菌蛋白(hepcidin) |
| ES2446266T3 (es) * | 2006-07-21 | 2014-03-06 | Amgen Inc. | Método de detección y/o de medición de hepcidina en una muestra |
| JO2828B1 (en) | 2007-11-02 | 2014-09-15 | ايلي ليلي اند كومباني | Anti-Hepsidine antibodies and their uses |
-
2008
- 2008-01-30 TW TW100141324A patent/TW201206954A/zh unknown
- 2008-01-30 TW TW101140904A patent/TW201307390A/zh unknown
- 2008-01-30 CL CL200800278A patent/CL2008000278A1/es unknown
- 2008-01-30 AU AU2008214386A patent/AU2008214386B2/en not_active Ceased
- 2008-01-30 AR ARP080100364A patent/AR065083A1/es unknown
- 2008-01-30 EP EP08725041A patent/EP2111412A2/en not_active Withdrawn
- 2008-01-30 WO PCT/US2008/001325 patent/WO2008097461A2/en active Application Filing
- 2008-01-30 PE PE2008000218A patent/PE20090722A1/es not_active Application Discontinuation
- 2008-01-30 PE PE2012001627A patent/PE20130588A1/es not_active Application Discontinuation
- 2008-01-30 MX MX2009008104A patent/MX2009008104A/es active IP Right Grant
- 2008-01-30 TW TW097103507A patent/TW200900420A/zh unknown
- 2008-01-30 CA CA002676036A patent/CA2676036A1/en not_active Abandoned
- 2008-01-30 US US12/022,515 patent/US8629250B2/en active Active
- 2008-01-30 JP JP2009548312A patent/JP2010517529A/ja not_active Withdrawn
-
2011
- 2011-07-15 AR ARP110102562A patent/AR082235A2/es not_active Application Discontinuation
-
2012
- 2012-09-14 US US13/620,007 patent/US20130018176A1/en not_active Abandoned
-
2013
- 2013-12-11 US US14/103,351 patent/US20140286953A1/en not_active Abandoned
-
2014
- 2014-06-10 JP JP2014119334A patent/JP2014221763A/ja not_active Withdrawn
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1403154A (zh) * | 2002-10-21 | 2003-03-19 | 钱忠明 | Hepcidin(海魄喜定)在制药中的应用 |
| JP2006517198A (ja) * | 2002-11-19 | 2006-07-20 | ディーアールジー・インターナショナル,インコーポレイテッド | ヒトまたは動物の組織、血液もしくは体液中のヘプシジンをスクリーニングすることによる疾患の診断方法およびそのための治療的使用 |
Non-Patent Citations (2)
| Title |
|---|
| JPN6010062349; Gene Vol.137, No.1, 19931227, p.109-118 * |
| JPN6014005183; Journal of Immunological Methods Vol.231, No.1-2, 19991210, p.11-23 * |
Cited By (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015504859A (ja) * | 2011-12-09 | 2015-02-16 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 改変ミニヘプシジンペプチドおよびその使用方法 |
| JP2018087215A (ja) * | 2011-12-09 | 2018-06-07 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 改変ミニヘプシジンペプチドおよびその使用方法 |
| JP2016513664A (ja) * | 2013-03-15 | 2016-05-16 | イントリンシック ライフサイエンシズ リミテッド ライアビリティ カンパニー | 抗ヘプシジン抗体およびその使用 |
| JP2016521257A (ja) * | 2013-03-15 | 2016-07-21 | プロタゴニスト セラピューティクス, インコーポレイテッド | ヘプシジン類似体及びその使用 |
| US11807674B2 (en) | 2013-03-15 | 2023-11-07 | Protagonist Therapeutics, Inc. | Hepcidin analogues and uses thereof |
| JP2018123169A (ja) * | 2013-03-15 | 2018-08-09 | プロタゴニスト セラピューティクス, インコーポレイテッド | ヘプシジン類似体及びその使用 |
| JP2019037236A (ja) * | 2013-03-15 | 2019-03-14 | イントリンシック ライフサイエンシズ リミテッド ライアビリティ カンパニー | 抗ヘプシジン抗体およびその使用 |
| US10239941B2 (en) | 2013-03-15 | 2019-03-26 | Intrinsic Lifesciences Llc | Anti-hepcidin antibodies and uses thereof |
| JP2017507328A (ja) * | 2014-01-30 | 2017-03-16 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 室温での全血の安定化 |
| US11840581B2 (en) | 2014-05-16 | 2023-12-12 | Protagonist Therapeutics, Inc. | α4β7 thioether peptide dimer antagonists |
| US11884748B2 (en) | 2014-07-17 | 2024-01-30 | Protagonist Therapeutics, Inc. | Oral peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory bowel diseases |
| US10941183B2 (en) | 2014-07-17 | 2021-03-09 | Protagonist Therapeutics, Inc. | Oral peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory bowel diseases |
| US10323088B2 (en) | 2014-09-22 | 2019-06-18 | Intrinsic Lifesciences Llc | Humanized anti-hepcidin antibodies and uses thereof |
| US11111272B2 (en) | 2014-10-01 | 2021-09-07 | Protagonist Therapeutics, Inc. | α4α7 peptide monomer and dimer antagonists |
| US10787490B2 (en) | 2015-07-15 | 2020-09-29 | Protaganist Therapeutics, Inc. | Peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory diseases |
| US11472842B2 (en) | 2015-12-30 | 2022-10-18 | Protagonist Therapeutics, Inc. | Analogues of hepcidin mimetics with improved in vivo half lives |
| US11753443B2 (en) | 2018-02-08 | 2023-09-12 | Protagonist Therapeutics, Inc. | Conjugated hepcidin mimetics |
| JP7370322B2 (ja) | 2018-06-04 | 2023-10-27 | 中外製薬株式会社 | 複合体を検出する方法 |
| JPWO2019235420A1 (ja) * | 2018-06-04 | 2021-06-17 | 中外製薬株式会社 | 複合体を検出する方法 |
| WO2019235420A1 (ja) * | 2018-06-04 | 2019-12-12 | 中外製薬株式会社 | 複合体を検出する方法 |
| US11041000B2 (en) | 2019-07-10 | 2021-06-22 | Protagonist Therapeutics, Inc. | Peptide inhibitors of interleukin-23 receptor and their use to treat inflammatory diseases |
| WO2022154121A1 (ja) * | 2021-01-18 | 2022-07-21 | 富士フイルム和光純薬株式会社 | ヘプシジンの吸着抑制剤、吸着抑制方法、標準品、試薬、キットおよび測定方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130018176A1 (en) | 2013-01-17 |
| EP2111412A2 (en) | 2009-10-28 |
| AR082235A2 (es) | 2012-11-21 |
| AU2008214386B2 (en) | 2013-09-19 |
| US20140286953A1 (en) | 2014-09-25 |
| AU2008214386A2 (en) | 2009-10-08 |
| AU2008214386A1 (en) | 2008-08-14 |
| AR065083A1 (es) | 2009-05-13 |
| MX2009008104A (es) | 2009-08-07 |
| TW200900420A (en) | 2009-01-01 |
| PE20130588A1 (es) | 2013-05-21 |
| TW201307390A (zh) | 2013-02-16 |
| WO2008097461A3 (en) | 2009-05-14 |
| TW201206954A (en) | 2012-02-16 |
| JP2014221763A (ja) | 2014-11-27 |
| US20080213277A1 (en) | 2008-09-04 |
| CL2008000278A1 (es) | 2008-09-26 |
| CA2676036A1 (en) | 2008-08-14 |
| PE20090722A1 (es) | 2009-07-13 |
| WO2008097461A2 (en) | 2008-08-14 |
| US8629250B2 (en) | 2014-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8629250B2 (en) | Hepcidin, hepcidin antagonists and methods of use | |
| AU2009246946B2 (en) | Anti-hepcidin antibodies and methods of use | |
| US9688759B2 (en) | Ferroportin antibodies and methods of use | |
| KR101368596B1 (ko) | Prlr 특이적 항체 및 그 용도 | |
| WO2017147742A1 (en) | Gfral receptor therapies | |
| AU2013221906A1 (en) | Hepcidin and Hepcidin Antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110128 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110128 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120127 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120425 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130122 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20130312 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130416 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130423 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130719 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140610 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20140611 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20140812 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20141006 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20141010 |