JP2004504295A - 安定化1α−ヒドロキシビタミンD - Google Patents
安定化1α−ヒドロキシビタミンD Download PDFInfo
- Publication number
- JP2004504295A JP2004504295A JP2002512124A JP2002512124A JP2004504295A JP 2004504295 A JP2004504295 A JP 2004504295A JP 2002512124 A JP2002512124 A JP 2002512124A JP 2002512124 A JP2002512124 A JP 2002512124A JP 2004504295 A JP2004504295 A JP 2004504295A
- Authority
- JP
- Japan
- Prior art keywords
- shvd
- hydroxyvitamin
- stabilized
- composition
- vitamin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- OFHCOWSQAMBJIW-AVJTYSNKSA-N alfacalcidol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C OFHCOWSQAMBJIW-AVJTYSNKSA-N 0.000 title claims abstract description 21
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 9
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims description 42
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 claims description 36
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 33
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 claims description 25
- 238000006243 chemical reaction Methods 0.000 claims description 25
- 239000000203 mixture Substances 0.000 claims description 22
- 229930003316 Vitamin D Natural products 0.000 claims description 18
- QYSXJUFSXHHAJI-XFEUOLMDSA-N Vitamin D3 Natural products C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C/C=C1\C[C@@H](O)CCC1=C QYSXJUFSXHHAJI-XFEUOLMDSA-N 0.000 claims description 18
- 235000019166 vitamin D Nutrition 0.000 claims description 18
- 239000011710 vitamin D Substances 0.000 claims description 18
- 229940046008 vitamin d Drugs 0.000 claims description 18
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical group COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 claims description 12
- 239000012535 impurity Substances 0.000 claims description 10
- 150000003710 vitamin D derivatives Chemical group 0.000 claims description 10
- 150000001875 compounds Chemical class 0.000 claims description 9
- -1 vitamin D compound Chemical class 0.000 claims description 9
- 238000004128 high performance liquid chromatography Methods 0.000 claims description 8
- 238000000034 method Methods 0.000 claims description 8
- 238000003860 storage Methods 0.000 claims description 8
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 claims description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 6
- 238000001953 recrystallisation Methods 0.000 claims description 6
- 239000007903 gelatin capsule Substances 0.000 claims description 5
- 239000007858 starting material Substances 0.000 claims description 5
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 claims description 4
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 claims description 4
- 239000004480 active ingredient Substances 0.000 claims description 4
- 239000002775 capsule Substances 0.000 claims description 4
- 239000003960 organic solvent Substances 0.000 claims description 4
- 239000007787 solid Substances 0.000 claims description 4
- 239000002904 solvent Substances 0.000 claims description 4
- 235000019864 coconut oil Nutrition 0.000 claims description 3
- 239000003240 coconut oil Substances 0.000 claims description 3
- 239000002552 dosage form Substances 0.000 claims description 3
- 230000000694 effects Effects 0.000 claims description 3
- 239000003921 oil Substances 0.000 claims description 3
- 235000019198 oils Nutrition 0.000 claims description 3
- 239000013557 residual solvent Substances 0.000 claims description 3
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 claims description 2
- FKCBLVCOSCZFHV-UHFFFAOYSA-N acetonitrile;ethanol Chemical compound CCO.CC#N FKCBLVCOSCZFHV-UHFFFAOYSA-N 0.000 claims description 2
- 239000003814 drug Substances 0.000 claims description 2
- WBJINCZRORDGAQ-UHFFFAOYSA-N formic acid ethyl ester Natural products CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 claims description 2
- QKGYJVXSKCDGOK-UHFFFAOYSA-N hexane;propan-2-ol Chemical compound CC(C)O.CCCCCC QKGYJVXSKCDGOK-UHFFFAOYSA-N 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 239000000843 powder Substances 0.000 claims description 2
- 239000003826 tablet Substances 0.000 claims description 2
- 229940088594 vitamin Drugs 0.000 claims description 2
- 229930003231 vitamin Natural products 0.000 claims description 2
- 235000013343 vitamin Nutrition 0.000 claims description 2
- 239000011782 vitamin Substances 0.000 claims description 2
- 150000003722 vitamin derivatives Chemical group 0.000 claims description 2
- 201000010099 disease Diseases 0.000 claims 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 claims 2
- 230000005856 abnormality Effects 0.000 claims 2
- 230000009102 absorption Effects 0.000 claims 2
- 238000010521 absorption reaction Methods 0.000 claims 2
- 229910052791 calcium Inorganic materials 0.000 claims 2
- 239000011575 calcium Substances 0.000 claims 2
- 230000003463 hyperproliferative effect Effects 0.000 claims 2
- 230000028993 immune response Effects 0.000 claims 2
- 230000028709 inflammatory response Effects 0.000 claims 2
- 230000004060 metabolic process Effects 0.000 claims 2
- 230000032258 transport Effects 0.000 claims 2
- NEETXMRNUNEBRH-GOTXBORWSA-N (1r,3s,5z)-5-[(2e)-2-[(1r,3as,7ar)-1-[(2r,5s)-5,6-dimethylheptan-2-yl]-7a-methyl-2,3,3a,5,6,7-hexahydro-1h-inden-4-ylidene]ethylidene]-4-methylidenecyclohexane-1,3-diol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CC[C@H](C)C(C)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C NEETXMRNUNEBRH-GOTXBORWSA-N 0.000 claims 1
- 201000004681 Psoriasis Diseases 0.000 claims 1
- 238000001035 drying Methods 0.000 claims 1
- 239000008187 granular material Substances 0.000 claims 1
- 230000000640 hydroxylating effect Effects 0.000 claims 1
- 230000001678 irradiating effect Effects 0.000 claims 1
- 230000006641 stabilisation Effects 0.000 claims 1
- 238000011105 stabilization Methods 0.000 claims 1
- 239000000243 solution Substances 0.000 description 30
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 20
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 12
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 12
- 239000011653 vitamin D2 Substances 0.000 description 12
- MECHNRXZTMCUDQ-RKHKHRCZSA-N vitamin D2 Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)/C=C/[C@H](C)C(C)C)=C\C=C1\C[C@@H](O)CCC1=C MECHNRXZTMCUDQ-RKHKHRCZSA-N 0.000 description 11
- 238000012360 testing method Methods 0.000 description 10
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 9
- MECHNRXZTMCUDQ-UHFFFAOYSA-N Vitamin D2 Natural products C1CCC2(C)C(C(C)C=CC(C)C(C)C)CCC2C1=CC=C1CC(O)CCC1=C MECHNRXZTMCUDQ-UHFFFAOYSA-N 0.000 description 9
- 229960002061 ergocalciferol Drugs 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 239000000741 silica gel Substances 0.000 description 9
- 229910002027 silica gel Inorganic materials 0.000 description 9
- 235000001892 vitamin D2 Nutrition 0.000 description 9
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 8
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 239000008186 active pharmaceutical agent Substances 0.000 description 7
- 229940088679 drug related substance Drugs 0.000 description 7
- 229960004756 ethanol Drugs 0.000 description 7
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 7
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- 239000013078 crystal Substances 0.000 description 6
- 239000012259 ether extract Substances 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 5
- 229960000935 dehydrated alcohol Drugs 0.000 description 5
- HKXBNHCUPKIYDM-CGMHZMFXSA-N doxercalciferol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)/C=C/[C@H](C)C(C)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C HKXBNHCUPKIYDM-CGMHZMFXSA-N 0.000 description 5
- 239000010410 layer Substances 0.000 description 5
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 5
- 235000019341 magnesium sulphate Nutrition 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 238000013112 stability test Methods 0.000 description 5
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 229910052786 argon Inorganic materials 0.000 description 4
- 238000010828 elution Methods 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 230000014759 maintenance of location Effects 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000012300 argon atmosphere Substances 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 0 CC(C)[C@@](C)C=C[C@@](C(CC1)C(C)(CCC2)C1C2=CC=C(C[C@@](C1)O)C(C)[C@]1O)*=C Chemical compound CC(C)[C@@](C)C=C[C@@](C(CC1)C(C)(CCC2)C1C2=CC=C(C[C@@](C1)O)C(C)[C@]1O)*=C 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- DTXXSJZBSTYZKE-ZDQKKZTESA-N Maxacalcitol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@@H](OCCC(C)(C)O)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C DTXXSJZBSTYZKE-ZDQKKZTESA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- ZVQOOHYFBIDMTQ-UHFFFAOYSA-N [methyl(oxido){1-[6-(trifluoromethyl)pyridin-3-yl]ethyl}-lambda(6)-sulfanylidene]cyanamide Chemical compound N#CN=S(C)(=O)C(C)C1=CC=C(C(F)(F)F)N=C1 ZVQOOHYFBIDMTQ-UHFFFAOYSA-N 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 239000011612 calcitriol Substances 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- DHRLEVQXOMLTIM-UHFFFAOYSA-N phosphoric acid;trioxomolybdenum Chemical compound O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.OP(O)(O)=O DHRLEVQXOMLTIM-UHFFFAOYSA-N 0.000 description 2
- 238000006303 photolysis reaction Methods 0.000 description 2
- 230000015843 photosynthesis, light reaction Effects 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- JPJALAQPGMAKDF-UHFFFAOYSA-N selenium dioxide Chemical compound O=[Se]=O JPJALAQPGMAKDF-UHFFFAOYSA-N 0.000 description 2
- 230000003595 spectral effect Effects 0.000 description 2
- 239000012258 stirred mixture Substances 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002211 ultraviolet spectrum Methods 0.000 description 2
- PKFBWEUIKKCWEW-WEZTXPJVSA-N (1r,3r)-5-[(2e)-2-[(1r,3as,7ar)-1-[(2r)-6-hydroxy-6-methylheptan-2-yl]-7a-methyl-2,3,3a,5,6,7-hexahydro-1h-inden-4-ylidene]ethylidene]cyclohexane-1,3-diol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@@H](CCCC(C)(C)O)C)=C\C=C1C[C@@H](O)C[C@H](O)C1 PKFBWEUIKKCWEW-WEZTXPJVSA-N 0.000 description 1
- DYLIWHYUXAJDOJ-OWOJBTEDSA-N (e)-4-(6-aminopurin-9-yl)but-2-en-1-ol Chemical compound NC1=NC=NC2=C1N=CN2C\C=C\CO DYLIWHYUXAJDOJ-OWOJBTEDSA-N 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- NXXNVJDXUHMAHU-UHFFFAOYSA-N 1-anthracen-9-ylethanone Chemical compound C1=CC=C2C(C(=O)C)=C(C=CC=C3)C3=CC2=C1 NXXNVJDXUHMAHU-UHFFFAOYSA-N 0.000 description 1
- JRMXMUCILWKNNW-UHFFFAOYSA-N 1-butoxy-2-methylbenzene Chemical compound CCCCOC1=CC=CC=C1C JRMXMUCILWKNNW-UHFFFAOYSA-N 0.000 description 1
- 102100027324 2-hydroxyacyl-CoA lyase 1 Human genes 0.000 description 1
- 101001009252 Homo sapiens 2-hydroxyacyl-CoA lyase 1 Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical class [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 238000007605 air drying Methods 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- LWQQLNNNIPYSNX-UROSTWAQSA-N calcipotriol Chemical compound C1([C@H](O)/C=C/[C@@H](C)[C@@H]2[C@]3(CCCC(/[C@@H]3CC2)=C\C=C\2C([C@@H](O)C[C@H](O)C/2)=C)C)CC1 LWQQLNNNIPYSNX-UROSTWAQSA-N 0.000 description 1
- 229960002882 calcipotriol Drugs 0.000 description 1
- GMRQFYUYWCNGIN-NKMMMXOESA-N calcitriol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@@H](CCCC(C)(C)O)C)=C\C=C1\C[C@@H](O)C[C@H](O)C1=C GMRQFYUYWCNGIN-NKMMMXOESA-N 0.000 description 1
- 239000012159 carrier gas Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 229960000413 doxercalciferol Drugs 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- LHGVFZTZFXWLCP-UHFFFAOYSA-N guaiacol Chemical compound COC1=CC=CC=C1O LHGVFZTZFXWLCP-UHFFFAOYSA-N 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 230000033444 hydroxylation Effects 0.000 description 1
- 238000005805 hydroxylation reaction Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 229960000987 paricalcitol Drugs 0.000 description 1
- BPKAHTKRCLCHEA-UBFJEZKGSA-N paricalcitol Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@@H](\C=C\[C@H](C)C(C)(C)O)C)=C\C=C1C[C@@H](O)C[C@H](O)C1 BPKAHTKRCLCHEA-UBFJEZKGSA-N 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- YUGCAAVRZWBXEQ-WHTXLNIXSA-N previtamin D3 Chemical compound C=1([C@@H]2CC[C@@H]([C@]2(CCC=1)C)[C@H](C)CCCC(C)C)\C=C/C1=C(C)CC[C@H](O)C1 YUGCAAVRZWBXEQ-WHTXLNIXSA-N 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 238000003797 solvolysis reaction Methods 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- CIHOLLKRGTVIJN-UHFFFAOYSA-N tert‐butyl hydroperoxide Chemical compound CC(C)(C)OO CIHOLLKRGTVIJN-UHFFFAOYSA-N 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 235000010215 titanium dioxide Nutrition 0.000 description 1
- 238000000870 ultraviolet spectroscopy Methods 0.000 description 1
- 239000011647 vitamin D3 Substances 0.000 description 1
- QYSXJUFSXHHAJI-YRZJJWOYSA-N vitamin D3 Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C\C=C1\C[C@@H](O)CCC1=C QYSXJUFSXHHAJI-YRZJJWOYSA-N 0.000 description 1
- DIPPFEXMRDPFBK-JPWDPSJFSA-N vitamin D4 Chemical compound C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CC[C@H](C)C(C)C)=C\C=C1\C[C@@H](O)CCC1=C DIPPFEXMRDPFBK-JPWDPSJFSA-N 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C401/00—Irradiation products of cholesterol or its derivatives; Vitamin D derivatives, 9,10-seco cyclopenta[a]phenanthrene or analogues obtained by chemical preparation without irradiation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/59—Compounds containing 9, 10- seco- cyclopenta[a]hydrophenanthrene ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/02—Nutrients, e.g. vitamins, minerals
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Engineering & Computer Science (AREA)
- Nutrition Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
【発明の属する技術分野】
本発明は、安定化1α−ヒドロキシビタミンD(SHVD)、特に医薬製剤に適しているものに関する。
【0002】
【従来の技術】
ヒドロキシ基を1α位に有するビタミンD化合物は、強いビタミンD活性のため、近年、かなり注目されてきた。しかしながら、これら活性化ビタミンD化合物は、また、特に光の曝露下及び酸素の存在下で化学的に不安定であるとして及びより高温で低い貯蔵安定性を有するとして知られている。活性化ビタミンDの医薬製剤への調剤は、これら安定性の問題を悪化させる。
この問題の種々の態様の認識及び研究、並びに活性化ビタミンDの医薬組成物を安定させる従来技術での試みにもかかわらず、先行技術は、医薬製剤に有用な安定化化合物を提供する特定の化学及び物理的性質を有する1α−ヒドロキシビタミンD形態についてほとんど示していない。これまで未知の技術的な特性を有する安定化1α−ヒドロキシビタミンDは、活性化ビタミンDの既知の形態と比較して意外にも安定していることがここで見出された。
【0003】
【発明の実施の形態】
本発明は、優れた技術的特性及び優れた安定性を有する安定する1α−ヒドロキシビタミンD形態(SHVD)に関連する。SHVDは、医薬組成物又は製剤における使用に特によく適応する。従って、本発明を、ここに詳細に、このような努力について記載する;しかしながら、発明のこのような説明は、例示目的のみを意味し、その全範囲に制限的に見られるべきでないことを当業者は認識するだろう。
【0004】
以下の、発明の方法の説明において、他に特定しない限り、生産工程は、室温及び大気圧で行われる。
ここで使用する「ビタミンD」の語は、ビタミンD2、D3及びD4並びに関連する類似体を含むことを意図する。「1α−ヒドロキシビタミンD」の語は、少なくとも化合物のA環の炭素−1α位に、置換されたヒドロキシ基を有するビタミンD化合物又は類似体について言及する。1α位だけがヒドロキシに置換した化合物、例えば、1α−ヒドロキシビタミンD2及び1α−ヒドロキシビタミンD3は、更にヒドロキシル化を受けて代謝的に活性なビタミンD化合物を形成するようなプロドラッグである。24又は25位並びに1α位がヒドロキシル化されたこれらの化合物は、典型的に代謝的に活性なビタミンD化合物、即ち、1α,24−ジヒドロキシビタミンD2及び1α,25−ジヒドロキシビタミンD3である。「活性(active)ビタミンD」又は「活性化(activated)ビタミンD」の語は、少なくとも、1α、24又は25の位においてヒドロキシル化されるビタミンD化合物をいう。ここで使用する、「安定化1α−ヒドロキシビタミンD」又は「SHVD」の語は、一定の市販のビタミンD化合物を含まないことを意味する、即ち、1α−ヒドロキシビタミンD3、1α,25−ジヒドロキシビタミンD3、1,24−ジヒドロキシビタミンD3、22−オキサ−1,25−ジヒドロキシビタミンD3(OCT)、パリカルシトール(paricalcitol)(19−nor−ビタミンD2)及びカルシポトリオール(calcipotriol)を除く。「非SHVD」の語は、純度プロフィール及びここでSHVDに対して記載された他の特性を満たさない1α−ヒドロキシビタミンD化合物をいう。
【0005】
本発明のSHVDは、結晶性であり、実質的に溶媒フリーであり、貯蔵安定性であり及び現代治療製剤に適している。研究は、本発明において見いだされる技術的な特性を有するSHVDは、意外にも安定しており、特に、熱攻撃(challenge)又は上昇した温度において、対応するプレビタミン形態への転換率が減少することを示した。本発明のSHVDは、実質的に6年間−70℃で貯蔵の後で分解しない。これは、医薬投与形態、例えばソフトゼラチンカプセルに処方される場合、優れた貯蔵安定性に対応する。本発明のSHVDは、いくらかの先行技術の安定化製剤によってすすめられていたような、貯蔵のための低酸素又は不活性雰囲気を必要としない。
本発明のSHVDは、さらに、モル吸光係数で約265nmでの紫外スペクトルピーク最大値(λmax)、17490のΣ265nm、及び、約227nmでの最小値(λmin)を有し、並びに特定の純度プロフィールを有する点で特徴付けられる。SHVDは、高速液体クロマトグラフィー(HPLC)によって質量ベースで98%以上の純度(すなわち少なくとも98%)、0.5%以下の残留溶媒、1.5%以下の合計不純物を有し、及び、HPLCによって0.5%より大きい単一の不純物を有しない。不純物は、シス−1α−OH−D4及びcis−1β−OH−D2を含む。いかなる特定の理論によって束縛されることを望まないが、SHVDの注目すべき安定性は、それが実質的に溶媒フリーであること及び実質的に不純物がないことに関連すると思われる。
【0006】
本発明のSHVDは、同じ非SHVDと比較した場合、熱攻撃における対応するプレビタミンへの転換率の実質的な減少によって更に特徴づけられる。対応するプレビタミンDへの転換に関するSHVDのこの安定性は、特に驚くべきである。1α−ヒドロキシビタミンD化合物は、そのプレビタミン形態と熱平衡にある、すなわち、これらは、お互いに熱異性体である。
例えば、1α−OH−D2に対する均衡を、以下に示す。
1α−ヒドロキシプレビタミンD2は、259nmにおいて特徴ある紫外スペクトルピーク最大値(λmax)を有する。溶液中で又は上昇した温度での1α−ヒドロキシビタミンD形態の貯蔵は、1α−ヒドロキシプレビタミンD形態を生じる。異性体は、室温であっても、お互いに平衡である。増大した温度は、この平衡をプレビタミンの形成にシフトする。
【0007】
本発明のSHVDは、同一条件、例えば熱攻撃下で、対応する非SHVDと比較して、1α−ヒドロキシプレビタミンDへの減少した転換率を示す。熱攻撃は、好ましくは、継続した期間、空中に保持される上昇した温度であり、その期間は、10日までであってもよい。上昇した温度は、好ましくは、約60℃である。このような熱攻撃において、本発明のSHVDは、同じ条件下の非SHVD化合物と比較して、より低い転換率を有する。
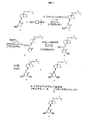
1α−ヒドロキシビタミンD化合物は、いかなる既知の合成方法によって調製されてもよい。一定の合成の経路は、精製において、本発明のSHVDの優れた技術的な特性を有し得る化合物を提供する事が見出された。例示的な合成のスキームを、1α−ヒドロキシビタミンD2(ドキセルカルシフェロール(doxercalciferol)として公知である)の合成を例示する図1に示す。一般的に、合成は、出発物質ビタミンD(すなわち1α位がヒドロキシル化された化合物)の、シクロビタミン形態への転換、シクロビタミンの1α位におけるヒドロキシル化、ヒドロキシル化したシクロビタミンの、ビタミンのシス及びトランス形態への再転換、及びトランス形態の、シス形への転換を含む。3位のヒドロキシ基は、好ましくは、合成の第1工程としてトシラートへ転換することによって保護される。
【0008】
例えば、図1に示すように、ビタミンD2(又はエルゴカルシフェロール)が出発物質である。ビタミンD2は、まず、3位においてトシル化されて、ビタミンD2 3−トシラートを形成する。その後、このトシラートは、シクロビタミンに転換されて、その後1α−ヒドロキシル化される。ヒドロキシル化シクロビタミンは、その後、シス及びトランス1α−ヒドロキシビタミンD2に転換される。トランス異性体は、紫外線に照射され、シス異性体、すなわち1α−ヒドロキシビタミンD2に転換する。
得られる製品は、カラムクロマトグラフィによって精製される。カラム精製された1α−ヒドロキシビタミンD2は、その後、有機溶剤、例えばギ酸メチルから再結晶される。再結晶された結晶は、その後、<0.5%の残留溶媒含量まで真空オーブン乾燥され、SHVDを与える。連続して(一般的に少なくとも2回)再結晶が行われる場合、本発明のSHVDは、特に良好である。好適な溶媒は、ギ酸メチルに加えて、ギ酸エチル、酢酸エチル、アセトン、メチルエチルケトン、ヘキサン、2−プロパノール−ヘキサン、ペンタン、ヘプタン、ジエチルエーテル、ジイソプロピルエーテル、メタノール、エタノールアセトニトリル及びその組み合わせを含む。
【0009】
本発明のSHVDは、経口使用のような医薬製剤、例えば、ソフトゼラチンカプセル、溶液、タブレットに好適に使用される。便利な単位投与形態の活性成分の濃度は、1μg〜100μg/週の週間用量で、0.5μg〜25μgである。ソフトゼラチン製剤において、カプセル充填材は、好適な医薬上許容できる油、例えば分画されたココナッツ油に溶解された本発明のSHVDを含み、及び、酸化防止剤を含み、これは、例えば、ブチルヒドロキシアニソール(BHA)、ブチルオキシトルエン(BHT)又はビタミンEであってもよい。カプセルシェルは、好ましくは、ゼラチン、グリセリン、二酸化チタン及び着色剤を含む。充填材は、典型的に全体のカプセルの質量の約58〜59%である。
【0010】
本発明は、更に以下の例によって説明されるが、本発明の範囲を制限するように解釈されるべきでない。
例において、UVスペクトルを島津(Shimadzu)UV 160Vで、IRスペクトルをAnalect DS−20で、及びNMRをSEOL NMRスペクトロメータで400MH3で操作して、又は公知技術の機器で取った。
【0011】
【実施例】
安定化1α−ヒドロキシビタミンD2(SHVD2)の調製
実施例1:1α−ヒドロキシビタミンD2粗製薬剤の調製
(1)エルゴカルシフェロールトシラート(2)の調製
エルゴカルシフェロール(ビタミンD2)100gに対し、4−ジメチルアミノピリジン3.1g、100mL無水ピリジン、及び340mL無水ジクロロメタンに加えた。フラスコの内容物を内部の反応温度が≦5℃になるまで撹拌した。その後、p−トルエンスルホニルクロライド122.6gを加え、すべての固体が溶解するまで混合物を撹拌した。反応をゆっくりと撹拌しながら、アルゴン下で進めた。32時間後、反応の完了を、TLC(シリカゲルプレート;ヘキサン中酢酸エチル;エタノール中20%ホスホモリブデン酸)によってモニターした。
約20分間にわたり、反応混合物を、飽和炭酸水素ナトリウムを含む冷却したビーカーに滴下した。反応混合物を分液ロートに入れて900mLイソプロピルエーテルですすいだ。混合物を振とうすることによってイソプロピルエーテルで抽出し、有機層及び水層を分離した。イソプロピルエーテル抽出物を希塩酸、飽和炭酸水素ナトリウム、及び飽和塩化ナトリウムで洗浄した。混合したイソプロピルエーテル抽出物を無水硫酸マグネシウム250gで乾燥し、濾過した。イソプロピルエーテル抽出物を混合し、真空中で濃縮した。粗製のトシラートは、以下の加溶媒分解に使用するのに好適であった。
【0012】
(2)6(R)−メトキシ−3,5−シクロビタミンD2(3)の調製
乾燥メチルアルコール1950mLと炭酸水素ナトリウム500gとの撹拌混合物に対し、250mLジクロロメタンに溶解しかつすすいだ工程1からのエルゴカルシフェロールトシラートを加えた。撹拌混合物を、アルゴン雰囲気下、18〜22時間、約56℃の内部温度で還流した。約20時間後、反応の程度をTLC(シリカゲル;溶媒 エタノール中20%ホスホモリブデン酸)によってモニターした。
反応混合物を25〜30℃に冷却し、炭酸水素ナトリウムを濾過によって除去した。反応フラスコ、濾過した炭酸水素ナトリウム及び濾過フラスコを1000mLのイソプロピルエーテルですすいだ。有機濾液を真空中で濃縮し、浴槽の温度を50℃に維持した。半固体残渣をイソプロピルエーテルで希釈した。このイソプロピルエーテル溶液を水で3回、飽和塩化ナトリウムで1回洗浄し、その後硫酸マグネシウムで乾燥した。硫酸マグネシウムを濾過して除去し、イソプロピルエーテルですすいだ。混合した有機濾液及び濾過フラスコのイソプロピルエーテルすすぎ液を真空中で4〜18時間濃縮し、6(R)−メトキシシクロビタミンを得た。
【0013】
(3)1αヒドロキシ−6(R)−メトキシ−3,5−シクロビタミンD2(4)の調製
1,2−ジクロロエタン1500mL中、挽きたての二酸化セレン12.3gの撹拌懸濁液に対し、81mLの無水t−ブチルヒドロペルオキシド(デカン中5−6M)を加えた。正のアルゴン雰囲気下、3〜4時間、周囲温度で撹拌した後、ピリジン18mLを加えた。1,2−ジクロロエタンに溶解した、工程2からの6(R)−メトキシ−3,5−シクロビタミンD2を冷却した反応フラスコ中に滴下して加え、その後1,2−ジクロロエタンですすいだ。反応を、撹拌しながら<5℃の内部温度で続け、反応の進行を15分おきにTLCによってモニターした。反応は、出発の6(R)−メトキシ−3,5−シクロビタミンD2がもはや見えなくなるか、又は2つの連続モニタリング薄層クロマトグラムの間に変化が現れなくなったときに完了したと考えた。
反応を、10%水酸化ナトリウムで停止した。水層及び有機層を分離し、水層をイソプロピルエーテルで抽出した。このイソプロピルエーテル抽出物を反応混合物からの有機層に加えた。混合した抽出物を無水硫酸マグネシウムで乾燥し、濾過した。フラスコ及び残りの硫酸マグネシウムをイソプロピルエーテルですすぎ、混合したイソプロピルエーテル抽出物及び濾過フラスコのイソプロピルエーテルすすぎ液を真空中で濃縮した。
生産物をヘキサン中5%酢酸エチル500mLに溶解し、カラム(75mmI.D.)に入ったシリカゲル(60/230〜400メッシュ)で精製し、ヘキサン中5%酢酸エチル約4000mL、次いで正のアルゴン圧力下、ヘキサン中20%酢酸エチル8000mLで溶出した。各約200mLの画分を溶出中に集めた。画分をシリカゲルTLCで分析した。1α−ヒドロキシ−6(R)−メトキシ−3,5−シクロビタミンD2を含む画分が確認され、混合され及び真空中で濃縮された。
【0014】
(4) シス−及びトランス−1α−ヒドロキシビタミンD2(5及び6)の調製
ジメチルスルホキシド120mL及び氷酢酸130mL中の工程3からの1α−ヒドロキシ−6(R)−メトキシ−3,5−シクロビタミンD2撹拌溶液を、約60℃に加熱し、この温度、アルゴン雰囲気下で60分間撹拌した。反応は、シリカゲルTLCで反応物1α−ヒドロキシ−6(R)−メトキシ−3,5−シクロビタミンD2の消費について周期的にモニターした。終了したら、反応を20〜25℃に冷却した。反応を、混合物とイソプロピルエーテルリンス液を飽和炭酸水素ナトリウム及び温度≦10℃に維持された水に注ぐことによって停止した。イソプロピルエーテルを加え、混合物を撹拌した。この混合物は、その後、950mLイソプロピルエーテルで別々に漏斗に通し、振とうして抽出した。水層及び有機層を分離した。水層をイソプロピルエーテルで抽出した。反応混合物からの有機層をこのイソプロピルエーテル抽出物と混合し、飽和塩化ナトリウムで3回、水で3回、及び飽和塩化ナトリウムで1回洗浄した。有機抽出物を、硫酸マグネシウムで乾燥し、濾過し、及びケーキ硫酸マグネシウム及び濾過フラスコをイソプロピルエーテルですすいだ。混合したイソプロピルエーテル濾液を真空中で濃縮し、浴槽の温度を35℃に維持した。残りの溶媒を残りの残渣から真空で除去した。
ジクロロメタン350mLに溶解した生産物を、カラム(75mmI.D.) に入ったシリカゲル(60/230〜400メッシュ)で精製し、アルゴン下のヘキサン中40%酢酸エチルで溶出した。約125mLの画分を集めた。画分を、ヘキサン中40%酢酸エチルで溶出したシリカゲルTLCで分析した。シス−及びトランス−1α−OH−D2を含む画分が確認され、混合され及び真空中で濃縮された。
【0015】
(5)シス−1α−ヒドロキシビタミンD2(5)の調製
工程4からのシス−及びトランス−1α−OH−D2及び9−アセチルアントラセン1.1gを2000mLメチルアルコールに溶解し、メチルアルコールすすぎ液全量2000mLとともに光分解チャンバーに移し、追加のメチルアルコールで13.7Lの全量まで溶解した。光分解を終了まで、約2〜6時間行った。生成溶液及び400mLメチルアルコールすすぎ液を真空中で濃縮し、浴槽の温度を35℃に維持した。
残りの溶液を高真空下で除去した。ジクロロメタンに溶解した生産物を、カラム(75mmI.D.) に入ったシリカゲル(60/230〜400メッシュ)で精製し、アルゴン下のヘキサン中40%酢酸エチル並びに酢酸エチルで溶出した。画分(125mL)の画分をヘキサン中40%酢酸エチル溶出で集め、その後、画分(200mL)を100%酢酸エチル溶出で集めた。画分をヘキサン中40%酢酸エチルで溶出したシリカゲルTLCで分析した。シス−1α−OH−D2を含む画分が確認され、混合され及び真空中で濃縮された。残りの溶液を高真空下で除去した。この工程の典型的な収量は、15〜30g(出発物質、エルゴカルシフェロールからの全体の収量の15〜30%)だった。
【0016】
実施例2:SHVD2を得るための粗製薬剤物質の精製
カラム精製シス−1α−ヒドロキシビタミンD2(粗製薬剤物質)をギ酸メチルから連続的に再結晶化した。
各再結晶に対し、カラム精製粗製薬剤物質(通常、15〜30g)を丸底フラスコ中の3500mLギ酸メチルに再懸濁した。このフラスコは、冷却コンデンサーを有するロータリーエバポレーターを備え、固体が溶解するまで40℃の水浴中をゆっくりと回転させた。溶液をロータリーエバポレーター中で濃縮し、結晶が形成し始めるまで、40℃に維持した。結晶が観察されたとき、フラスコを−20℃のフリーザーに置き、48〜72時間冷却した。
再結晶から得られた結晶を5〜10分間空気乾燥した後、結晶を粉末までひき、その後、結晶化皿に移した。結晶の入った皿を約55℃にセットした真空オーブンに72〜120時間置いた。得られた薬剤物質(SHVD2)の量は、通常5〜10gであり、これは、出発物質、エルゴカルシフェロールの5〜10%の収量を意味する。
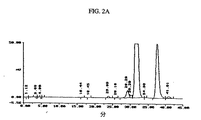
精製手順が粗製薬剤物質の精製を改善する証拠は、図2のHPLCクロマトグラムによって説明される。最初のクロマトグラム(A)は、カラム精製した粗製の薬剤物質で得られたものである。クロマトグラム(B)は、最終製品を示す。図2に示すように、約37.7及び41分の反応時間における不純物のレベルが、再結晶によって減少した。
【0017】
実施例3:SHVD2の残りの溶液の測定
残りの溶液をトルエンで定量化する方法を使用した。分析ターゲットは、メタノール、ギ酸メチル、塩化メチレン、ヘキサン、ジイソプロピルエーテル、1,1−ジクロロエタン及び酢酸エチルを含む。
ガスクロマトグラフ法を、ヘリウムをキャリアガスとし、スプリットインジェクション/ラン、及びシングルイオンモード(SIMモード)のランで使用した。これは、60m×0.25mmID、フィルム厚1.4μmを有するDB−624キャピラリーカラム、スプリット/スプリットレスインジェクター、50℃〜250℃の立ち上がりが可能なガスクロマトグラフ、及び質量選択性検出器を要求する。クロマトグラフは、31,32、43,45,49,60,61,62,84,86及び87のイオンをイオン当たり25msの滞留時間(dwell time)で検出するようにセットした。
外部較正を使用し、これは、ブランク、マトリックスブランク、及び4点曲線からなる。曲線は、1μg/g、10μg/g及び50μg/gの濃度で作成した。シス−1α−OH−D2の10mgサンプルをトルエン中で調製した。このサンプルからの結果を上記作成した線状曲線を使用して算出した。すべての分析物に対する下限は100μg/gである。この結果は、シス−1α−OH−D2(SHVD2)中の残りの溶液の量は、≦0.5%であることを示した。
【0018】
実施例4:SHVD2の貯蔵安定性試験
4ロットのSHVD2からのサンプルの安定性を、−70℃での長期間貯蔵の間に6月おきに実験した。すべてのロットは、薬剤物質用の包装として選択された容器密栓システム中に貯蔵した。安定性を(1)質量パーセント 1α−OH−D2含量、(2)パーセント 関連物質含量、及び(3)不純物プロフィールの変化につき、HPLCを使用してサンプルを試験することによって評価した。加えて、すべてのロットをUV分光法によってUVスペクトルの変化について試験した。
この研究の結果は、ベースラインと6分または12分との間に、1α−OH−D2含量の平均質量%について、大きな違いを示さなかった。実験したすべてのロットに対する1α−OH−D2含量の質量%は、すべての時点で、>98.0%であった。クロマトグラフィーの不純物プロフィールは、6ヵ月または12ヵ月でベースラインと比べて新しいピークは測定されなかった。関連物質のパーセントは、<2.0%残っていた。
【0019】
実施例5:SHVD2ソフトゼラチンカプセル充填材の調製
BHAを、分画されたココナッツ油(FCO)に加え、加熱し、及びBHAが完全に溶解するまで撹拌した。この溶液をその後冷却した。SHVD2を好適な容器に入れて正確に秤量し、脱水アルコールを加え、及び溶液を、SHVD2が溶解するまで撹拌した。FCOをステンレス混合タンクに入れて秤量した。BHA/FCO溶液を、撹拌しながらFCOに加えた。その後、SHVD2/脱水アルコール溶液を加え、及び溶液を均一になるまで撹拌した。SHVD2/脱水アルコール溶液を含む容器を脱水アルコールですすぎ、すすぎ液をFCO/SHVD2/脱水アルコールミックスに加えた。このミックスを含む混合タンクを塞ぎ、真空にし、内容物を混合(脱気)した。得られた溶液をフィルターを通して受け器に移動し、窒素でガスシールした。
【0020】
実施例6: 安定性試験:SHVD2対非SHVD2
約1mgのSHVD2または非安定化1α−ヒドロキシビタミンD2(非SHVD2)をそれぞれ9つの(12×75mm)試験チューブに置いた。試験チューブを約60℃のオーブンに置いた。各2つのビタミンD2製剤の1つの試験チューブを0,3,6,9,12,18,24,36及び48時間のインキュベーションで除去した。各試験チューブ中の内容物を、エタノールに溶解して1mg/mL溶液を生成した。各溶液(10μL)を以下のHPCL条件で分析した:アセトニトリル:メタノール:水(60:20:20)の移動相を有するYMCパックC8カラム(4.6×250mm、5μm)、流速1.0mL/分。1α−ヒドロキシビタミンD2ピークと比較して約0.9相対保持時間移動したピークの出現率は、SHVD2よりも非SHVD2で大きかった。
【0021】
実施例7:安定性試験:SHVD2対市販の1α−OH−D2
約1mgのSHVD2または市販の1α−ヒドロキシビタミンD2をそれぞれ2つの(12×75mm)試験チューブに置いた。各2つの製剤から1つの試験チューブを約60℃のオーブンに置いた。分析のため、各試験チューブ中の内容物を、エタノールに溶解して1mg/mL溶液を生成した。各溶液(10μL)を以下のHPLC条件で分析した:アセトニトリル:メタノール:水(60:20:20)の移動相を有するYMCパックC8カラム(4.6×250mm、5μm)、流速1.0mL/分。1α−ヒドロキシビタミンD2ピークと比較して約0.9相対保持時間移動したピークの出現率は、SHVD2よりも市販の1α−ヒドロキシビタミンD2で大きかった。
【0022】
実施例8:SHVD2対非SHVD2の安定性試験
約1mgの安定化1αヒドロキシビタミンD2(ドキセルカルシフェロール)(SHVD2)をそれぞれ2つの試験チューブ(12×75mm)に置いた。1つのサンプルをエタノール蒸気の雰囲気を含むデシケーターに置き、物質の残りの溶液を増加して、非安定化ドキセルカルシフェロール(非SHVD2)を得た。このデシケーター内の物質を60℃に48時間加熱した。他方のサンプルは、エタノール雰囲気にせず、安定化形態を保持したが、60℃に48時間加熱した。各試験チューブの内容物を、エタノールに溶解して1mg/mL溶液を生成した。各溶液(10μL)を以下のHPLC条件で分析した:アセトニトリル:メタノール:水(60:20:20)の移動相を有するYMCパックC8カラム(4.6×250mm、5μm)、流速1.0mL/分。ドキセルカルシフェロールピークと比較して約0.9相対保持時間移動したピークの出現率は、SHVD2よりも非SHVD2で大きかった。
【0023】
実施例9:安定性試験:>0.5%残渣溶液を含む1α,24(S)−ジヒドロキシビタミンD2(非SHVD2)
>0.5%残渣溶液を含む1α,24(S)−ジヒドロキシビタミンD2(非SHVD) 約1mgを、キャップしたバイアルに置き、約60℃で48時間加熱した。バイアルの内容物を、エタノールに溶解して1mg/mL溶液を生成した。溶液(10μL)を以下のHPLC条件で分析した:アセトニトリル:水(50:50)の移動相を有するYMCパックプロC18カラム(4.6×150mm、5μm)、流速1.0mL/分。非SHVDを加熱した後、標準1α,24(S)−ジヒドロキシビタミンD2と比較して約0.85相対保持時間を有する化合物を観察した。
【0024】
結果、本発明は、優れた技術的特性及び優れた安定性を有するSHVD、安定化1α−ヒドロキシビタミンD形態を提供する。本発明の新規形態は、結晶性、実質的に溶液フリー、安定、かつ現代の治療製剤に良好に適合するものである。
本発明は、いくらか特異性をもってここで開示され、かつ例示されているが、当業者であれば、記載されている事項からなされる変化、追加、及び省略を含む種々の改変を理解できるだろう。従って、これらの改変も、本発明に包含され、本発明の範囲は、請求の範囲と合法的に合致し得る最も広い解釈によってもっぱら限定されることを意図している。
【図面の簡単な説明】
【図1】1α−OH−D2の合成のための例示的な反応スキームである。
【図2】本発明のSHVDの製剤を示すHPLCクロマトグラムである。
Claims (22)
- 純度が質量ベースのHPLC分析によって98%以上であり、残留溶媒が0.5%以下であり、合計不純物が1.5%以下であり、及び、0.5%より大きい単一の不純物を有しないことを特徴とする、安定化1α−ヒドロキシビタミンD(SHVD)。
- 不純物が、1α−ヒドロキシビタミンD4である、請求項1に記載の安定化1α−ヒドロキシビタミンD。
- 熱攻撃におけるビタミンD形態からプレビタミン形態への転換率が、同一条件下での非安定化1α−ヒドロキシビタミンD(非SHVD2)より低い、請求項1に記載の安定化1α−ヒドロキシビタミンD。
- 請求項1のSHVDを含む医薬組成物。
- ソフトゼラチンカプセルである請求項4の組成物。
- 溶液である、請求項4の組成物。
- 単位投与形態であり、0.5μg〜25μgの活性成分を含む、請求項4の組成物。
- 油中、請求項1のSHVDの効果的量の溶液を含み、該溶液が、ソフトゼラチンカプセルに含まれている組成物。
- 油が分画されたココナッツ油である、請求項8に記載の組成物。
- 請求項1のSHVDの効果的な量の固体医薬製剤を含み、該固体医薬製剤が、タブレット、カプセル、粒剤、粉体の形態である組成物。
- 活性成分としての請求項1のSHVDの効果的量を含む、カルシウム吸収、輸送または代謝、高増殖細胞活性、免疫応答不均衡または炎症応答不均衡の異常性が原因の病気の治療用薬剤。
- 活性成分としての請求項1のSHVDの効果的量を、治療が必要な被検者に投与することを含む、カルシウム吸収、輸送または代謝、高増殖細胞活性、免疫応答不均衡または炎症応答不均衡の異常性が原因の病気の治療方法。
- 病気が乾癬である、請求項12に記載の方法。
- 熱攻撃のときの1α−ヒドロキシプレビタミンDへの転化率が、同一条件下での非SHVDと比較して減少することを特徴とする、安定化1α−ヒドロキシビタミンD(SHVD)。
- 熱攻撃が、約60℃の一定温度で起こる、請求項14に記載の安定化1α−ヒドロキシビタミンD。
- 実質的に純粋で、実質的に溶媒フリーで、かつ貯蔵安定性である、安定化1α−ヒドロキシビタミンD(SHVD)。
- 対応するプレビタミン形態と比較して実質的に減少した転換率によって特徴付けられる安定化1α−ヒドロキシプレビタミンDを含む、医薬化合物。
- (a)ビタミンD化合物である出発物質の3位のヒドロキシル基をトシル化してヒドロキシを1α位に加える工程;
(b)トシル化形態をシクロビタミンに転換する工程;
(c)1α位のシクロビタミンをヒドロキシル化する工程;
(d)シクロビタミンをシス及びトランスビタミン形態に転換する工程;
(e)トランスビタミン形態を照射してシス形態を生成する工程;
(f)シス形態を、有機溶媒中で再結晶化し、再結晶化形態を72〜120時間55℃で真空オーブン乾燥してSHVDを生成する工程、
を含む、安定化1α−ヒドロキシビタミンD(SHVD)の製造方法。 - 請求項18に記載の方法によって合成される、安定化1α−ヒドロキシビタミンD(SHVD)。
- 少なくとも3回、粗製のヒドロキシビタミンD製品を有機溶媒から連続的に再結晶化することを含む、安定化1α−ヒドロキシビタミンD(SHVD)の製造方法。
- 再結晶化方法が、2つの再結晶化を含む、請求項20に記載の方法。
- 有機溶媒が、ギ酸メチル、ギ酸エチル、酢酸エチル、アセトン、メチルエチルケトン、ヘキサン、2−プロパノール−ヘキサン、ペンタン、ヘプタン、ジエチルエーテル、ジイソプロピルエーテル、メタノール、エタノールアセトニトリル又はその組み合わせである、請求項21に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US21906800P | 2000-07-18 | 2000-07-18 | |
| PCT/US2001/022729 WO2002006218A2 (en) | 2000-07-18 | 2001-07-18 | STABILIZED 1α-HYDROXY VITAMIN D |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004504295A true JP2004504295A (ja) | 2004-02-12 |
| JP2004504295A5 JP2004504295A5 (ja) | 2008-09-04 |
Family
ID=22817719
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002512124A Pending JP2004504295A (ja) | 2000-07-18 | 2001-07-18 | 安定化1α−ヒドロキシビタミンD |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US6903083B2 (ja) |
| EP (2) | EP2070911A2 (ja) |
| JP (1) | JP2004504295A (ja) |
| AU (2) | AU2001278956B2 (ja) |
| CA (1) | CA2414407A1 (ja) |
| IL (2) | IL153378A0 (ja) |
| WO (1) | WO2002006218A2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005247803A (ja) * | 2004-03-08 | 2005-09-15 | Zeria Pharmaceut Co Ltd | 点眼剤及びその容器 |
| JP2014062131A (ja) * | 2008-03-12 | 2014-04-10 | Cytochroma Inc | 安定化1,25−ジヒドロキシビタミンd2及びその製造方法 |
| JP6186532B1 (ja) * | 2017-03-31 | 2017-08-23 | ナガセ医薬品株式会社 | マキサカルシトール含有水溶液製剤 |
Families Citing this family (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6087350A (en) * | 1997-08-29 | 2000-07-11 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Use of pretreatment chemicals to enhance efficacy of cytotoxic agents |
| IL153378A0 (en) * | 2000-07-18 | 2003-07-06 | Bone Care Internat Inc | STABILIZED 1alpha-HYDROXY VITAMIN D |
| US20030191093A1 (en) * | 2001-12-03 | 2003-10-09 | Novacea, Inc. | Pharmaceutical compositions comprising active vitamin D compounds |
| US7148211B2 (en) * | 2002-09-18 | 2006-12-12 | Genzyme Corporation | Formulation for lipophilic agents |
| US20050101576A1 (en) * | 2003-11-06 | 2005-05-12 | Novacea, Inc. | Methods of using vitamin D compounds in the treatment of myelodysplastic syndromes |
| US7351869B2 (en) * | 2002-11-18 | 2008-04-01 | Teva Pharmaceutical Industries Ltd | Crystallization method for purification of calcipotriene |
| US20050026877A1 (en) * | 2002-12-03 | 2005-02-03 | Novacea, Inc. | Pharmaceutical compositions comprising active vitamin D compounds |
| US20050020546A1 (en) * | 2003-06-11 | 2005-01-27 | Novacea, Inc. | Pharmaceutical compositions comprising active vitamin D compounds |
| ATE469127T1 (de) * | 2004-11-22 | 2010-06-15 | Wisconsin Alumni Res Found | 17,20(z)-dehydro-vitamin-d-analoge und deren verwendungen |
| ES2567595T3 (es) * | 2005-10-12 | 2016-04-25 | Opko Renal, Llc | Métodos y artículos para tratar la insuficiencia y la deficiencia de 25-hidroxivitamina D |
| DK1993559T3 (en) | 2006-02-03 | 2016-10-03 | Opko Renal Llc | Treatment of vitamin D deficiency and MALFUNCTION with 25-hydroxyvitamin D2 and 25-hydroxyvitamin D3 |
| BRPI0621471A2 (pt) | 2006-03-17 | 2012-09-11 | Leo Pharma As | métodos de isomerização de uma solução de um derivado de vitamina d, para produzir e preparar calcipotriol ou monoidrato de calcipotriol, e para a fabricação de uma formulação farmacêutica ou medicamento, e, uso de um reator foto-reator de fluxo direto ou foto-reator de fluxo contìnuo |
| SI2037936T1 (sl) * | 2006-06-21 | 2014-11-28 | Opko Renal, Llc | Postopek zdravljenja in prepreäśevanja sekundarnega hiperparatiroidizma |
| AU2007325387B2 (en) * | 2006-11-16 | 2014-04-03 | Kai Pharmaceuticals, Inc. | Polycationic calcium modulator peptides for the treatment of hyperparathyroidism and hypercalcemic disorders |
| WO2008134518A2 (en) * | 2007-04-25 | 2008-11-06 | Cytochroma Inc. | Methods and compounds for vitamin d therapy |
| US11752158B2 (en) * | 2007-04-25 | 2023-09-12 | Eirgen Pharma Ltd. | Method of treating vitamin D insufficiency and deficiency |
| KR20190141269A (ko) | 2007-04-25 | 2019-12-23 | 사이토크로마 인코포레이티드 | 비타민 d 화합물과 밀랍성 담체를 포함하는 경구 조절성 방출 조성물 |
| CA2683514C (en) * | 2007-04-25 | 2019-07-09 | Proventiv Therapeutics, Llc | Method of safely and effectively treating and preventing secondary hyperparathyroidism in chronic kidney disease |
| AU2008345083B2 (en) * | 2007-12-28 | 2014-05-08 | Wisconsin Alumni Research Foundation | (20R)-23,23-difluoro-2-methylene-19-nor-bishomopregnacalciferol-vitamin D analogs |
| EP2240439B1 (en) * | 2007-12-28 | 2015-03-18 | Wisconsin Alumni Research Foundation | (20s)-23,23-difluoro-2-methylene-19-nor-bishomopregnacalciferol-vitamin d analogs |
| CN106853250A (zh) | 2008-04-02 | 2017-06-16 | 赛特克罗公司 | 用于维生素d缺乏症和相关障碍的方法、组合物、用途和试剂盒 |
| US8013176B2 (en) * | 2008-09-11 | 2011-09-06 | Alphora Research Inc. | Paricalcitol purification |
| US20120130133A1 (en) * | 2008-11-26 | 2012-05-24 | Cytochroma Inc. | Method For Synthesizing Vitamin D Analogs |
| PT3192520T (pt) | 2009-07-29 | 2019-06-12 | Kai Pharmaceuticals Inc | Agentes terapêuticos para redução dos níveis da paratormona |
| RS60087B1 (sr) | 2010-03-29 | 2020-05-29 | Opko Ireland Global Holdings Ltd | Postupci i kompozicije za snižavanje nivoa paratireoidnog hormona |
| CA2698160C (en) * | 2010-03-30 | 2017-07-25 | Alphora Research Inc. | Stabilized doxercalciferol and process for manufacturing the same |
| US20120108554A1 (en) * | 2010-10-28 | 2012-05-03 | Formosa Laboratories, Inc. | PROCESS FOR PREPARING HIGH PURITY 1alpha-HYDROXY VITAMIN D2 |
| BR112013031539A2 (pt) | 2011-06-08 | 2019-07-30 | Kai Pharmaceuticals Inc | agentes terapêuticos para regular fósforo sérico |
| JP6204369B2 (ja) | 2011-11-10 | 2017-09-27 | カイ・ファーマシューティカルズ・インコーポレイテッドKai Pharmaceuticals,Inc. | カルシウム模倣薬およびその使用方法 |
| KR101847947B1 (ko) | 2013-03-15 | 2018-05-28 | 옵코 아이피 홀딩스 Ⅱ 인코포레이티드 | 안정화되고 변형된 비타민 d 방출 제형 |
| CN114681468A (zh) | 2014-08-07 | 2022-07-01 | 欧普科爱尔兰环球控股有限公司 | 利用25-羟基维生素d的辅助疗法 |
| CN105348164B (zh) * | 2015-10-29 | 2017-03-29 | 无锡福祈制药有限公司 | 一种1α‑羟基维生素D2的制备方法 |
| CN108883120A (zh) | 2016-03-28 | 2018-11-23 | 欧普科爱尔兰环球控股有限公司 | 维生素d治疗方法 |
| CN106748942B (zh) * | 2016-11-28 | 2018-06-29 | 无锡福祈制药有限公司 | 度骨化醇类似物wxfq-65及其合成方法 |
| CN106748642B (zh) * | 2016-11-28 | 2019-11-05 | 无锡福祈制药有限公司 | 一种度骨化醇类似物wxfq-65的合成方法 |
| CN113666858A (zh) * | 2021-08-20 | 2021-11-19 | 江苏四环生物制药有限公司 | 一种度骨化醇及其制备方法 |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58126862A (ja) * | 1981-11-02 | 1983-07-28 | リサ−チ・インステイチユ−ト・フオア・メデイスン・アンド・ケミストリ−・インコ−ポレ−テツド | 1−ヒドロキシル化ビタミンd化合物の製法 |
| JPS62298572A (ja) * | 1986-06-19 | 1987-12-25 | Chugai Pharmaceut Co Ltd | 1α−ヒドロキシビタミンD3の精製法 |
| JPS63126862A (ja) * | 1987-10-30 | 1988-05-30 | Nisshin Flour Milling Co Ltd | 1α−ヒドロキシビタミンD↓2の製造方法 |
| JPS63126891A (ja) * | 1986-11-14 | 1988-05-30 | Nisshin Flour Milling Co Ltd | ステロイド誘導体およびその製造方法 |
| JPH01246276A (ja) * | 1988-03-25 | 1989-10-02 | Teikoku Chem Ind Corp Ltd | 1α−ヒドロキシ―6―(1,3−ベンゾジチオール−2−イル)オキシー3,5−シクロビタミンD↓3 |
| JPH02270860A (ja) * | 1988-03-25 | 1990-11-05 | Teikoku Chem Ind Corp Ltd | 1α―ヒドロキシ―ビタミンD↓3の製造方法 |
| JPH05279260A (ja) * | 1991-04-09 | 1993-10-26 | Takeda Chem Ind Ltd | 安定化されたビタミンd類製剤 |
| JPH05320127A (ja) * | 1992-03-27 | 1993-12-03 | Nisshin Flour Milling Co Ltd | 活性型ビタミンd誘導体 |
| JPH05339230A (ja) * | 1992-03-12 | 1993-12-21 | Nisshin Flour Milling Co Ltd | 活性型ビタミンd2及びその誘導体の製造法 |
| JPH06256301A (ja) * | 1992-11-04 | 1994-09-13 | Wisconsin Alumni Res Found | 1α,24−ジヒドロキシビタミンD類似体の製造方法 |
| JP2002535307A (ja) * | 1999-01-20 | 2002-10-22 | ウィスコンシン・アルムニ・リサーチ・ファウンデーション | 結晶1α−ヒドロキシビタミンD2とその精製方法 |
Family Cites Families (112)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2383446A (en) | 1941-06-04 | 1945-08-28 | Du Pont | Antirachitic materials and processes for their production |
| US3697559A (en) | 1971-02-25 | 1972-10-10 | Wisconsin Alumni Res Found | 1,25-dihydroxycholecalciferol |
| US3741996A (en) | 1971-12-02 | 1973-06-26 | Wisconsin Alumni Res Found | 1{60 -hydroxycholecalciferol |
| US5472957A (en) * | 1973-01-10 | 1995-12-05 | Research Institute For Medicine And Chemistry | Chemical compounds and process |
| US3907843A (en) | 1974-06-14 | 1975-09-23 | Wisconsin Alumni Res Found | 1{60 -Hydroxyergocalciferol and processes for preparing same |
| JPS5452717A (en) | 1977-09-29 | 1979-04-25 | Chugai Pharmaceut Co Ltd | Stable oily pharmaceuticals containing 1alpha-hydroxyvitamin d |
| US4202829A (en) | 1978-01-05 | 1980-05-13 | Wisconsin Alumni Research Foundation | Process for preparing 1α-hydroxylated compounds |
| US4195027A (en) | 1978-01-16 | 1980-03-25 | Wisconsin Alumni Research Foundation | Process for preparing 1α-hydroxylated compounds |
| US4260549A (en) | 1979-05-21 | 1981-04-07 | Wisconsin Alumni Research Foundation | Process for preparing 1α-hydroxylated compounds |
| US4160803A (en) | 1978-03-23 | 1979-07-10 | Corning Glass Works | Self packaged test kit |
| US4225596A (en) | 1978-10-13 | 1980-09-30 | Wisconsin Alumni Research Foundation | Method for treating calcium imbalance and improving calcium absorption in mammals |
| US4234495A (en) | 1979-09-10 | 1980-11-18 | Wisconsin Alumni Research Foundation | Process for preparing 1α-hydroxyvitamin D compounds from 1α-hydroxy-3,5-cyclovitamin D compounds |
| US4362710A (en) | 1980-07-04 | 1982-12-07 | Nissan Gosei Kogyo Co., Ltd. | Feeds for baby pigs, process for preparing the same and method of breeding baby pigs |
| JPS57149224A (en) | 1981-03-13 | 1982-09-14 | Chugai Pharmaceut Co Ltd | Tumor-suppressing agent |
| US4508651A (en) | 1983-03-21 | 1985-04-02 | Hoffmann-La Roche Inc. | Synthesis of 1α,25-dihydroxyergocalciferol |
| US4689180A (en) | 1984-01-30 | 1987-08-25 | Wisconsin Alumni Research Foundation | 1α,25-dihydroxy-22Z-dehydroxyvitamin D compound |
| US4588716A (en) | 1984-05-04 | 1986-05-13 | Wisconsin Alumni Research Foundation | Method for treating metabolic bone disease in mammals |
| US4555364A (en) | 1984-11-01 | 1985-11-26 | Wisconsin Alumni Research Foundation | Method for preparing 1-hydroxyvitamin D compounds |
| US4554106A (en) * | 1984-11-01 | 1985-11-19 | Wisconsin Alumni Research Foundation | Method for preparing 1α-hydroxyvitamin D compounds |
| US4728643A (en) | 1984-11-02 | 1988-03-01 | The General Hospital Corporation | Method of treating psoriasis |
| US5037816A (en) | 1984-11-02 | 1991-08-06 | The General Hospital Corporation | Method of treating psoriasis |
| US4717721A (en) | 1985-05-30 | 1988-01-05 | Howard W. Bremer | Sidechain homo-vitamin D compounds with preferential anti-cancer activity |
| US4661294A (en) | 1985-03-18 | 1987-04-28 | The General Hospital Corporation | Biologically active 1-thio derivatives of vitamin D |
| IL78342A (en) | 1985-04-04 | 1991-06-10 | Gen Hospital Corp | Pharmaceutical composition for treatment of osteoporosis in humans comprising a parathyroid hormone or a fragment thereof |
| WO1987000834A1 (en) | 1985-08-02 | 1987-02-12 | Leo Pharmaceutical Products Ltd. A/S | Novel vitamin d analogues |
| US5554386A (en) | 1986-07-03 | 1996-09-10 | Advanced Magnetics, Inc. | Delivery of therapeutic agents to receptors using polysaccharides |
| US5527524A (en) | 1986-08-18 | 1996-06-18 | The Dow Chemical Company | Dense star polymer conjugates |
| US5338532A (en) | 1986-08-18 | 1994-08-16 | The Dow Chemical Company | Starburst conjugates |
| US4833125A (en) | 1986-12-05 | 1989-05-23 | The General Hospital Corporation | Method of increasing bone mass |
| US4902481A (en) | 1987-12-11 | 1990-02-20 | Millipore Corporation | Multi-well filtration test apparatus |
| US5145846A (en) | 1988-01-20 | 1992-09-08 | Hoffmann-La Roche Inc. | Vitamin D3 analogs |
| US5087619A (en) | 1988-01-20 | 1992-02-11 | Hoffman-La Roche Inc. | Vitamin D3 analogs |
| US5232836A (en) | 1988-05-04 | 1993-08-03 | Ire-Medgenix S.A. | Vitamin D derivatives: therapeutic applications and applications to assays of metabolites of vitamin D |
| US5602116A (en) | 1988-08-02 | 1997-02-11 | Bone Care International, Inc. | Method for treating and preventing secondary hyperparathyroidism |
| US5104864A (en) | 1988-08-02 | 1992-04-14 | Bone Care International, Inc. | Method for treating and preventing loss of bone mass |
| US5098899A (en) | 1989-03-06 | 1992-03-24 | Trustees Of Boston University | Method for therapeutically treating psoriatic arthritis using vitamin D analogues and metabolites |
| US5321018A (en) | 1989-03-09 | 1994-06-14 | Wisconsin Alumni Research Foundation | Use of 1α-hydroxylated-19-nor-vitamin D compounds to treat psoriasis |
| CA1333616C (en) | 1989-03-09 | 1994-12-20 | Hector F. Deluca | 19-nor-vitamin d compounds |
| US5372996A (en) | 1989-03-10 | 1994-12-13 | Endorecherche, Inc. | Method of treatment of androgen-related diseases |
| US4948789A (en) | 1989-03-28 | 1990-08-14 | Chugai Seiyaku Kabushiki Kaisha | Suppression of parathyroid hormone synthesis and secretion |
| JP2645130B2 (ja) | 1989-03-31 | 1997-08-25 | 日清製粉株式会社 | ステロイド誘導体 |
| GB2229921B (en) | 1989-04-05 | 1992-12-16 | Chugai Pharmaceutical Co Ltd | Treatment for hyperparathyroidism with use of vitamin d derivatives |
| US5219528A (en) | 1989-07-28 | 1993-06-15 | Pierce Chemical Company | Apparatus for rapid immunoassays |
| DE3933034A1 (de) | 1989-10-02 | 1991-04-11 | Schering Ag | 24-homo-vitamin-d-derivate, verfahren zu ihrer herstellung |
| US5260290A (en) | 1990-02-14 | 1993-11-09 | Wisconsin Alumni Research Foundation | Homologated vitamin D2 compounds and the corresponding 1α-hydroxylated derivatives |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| US5194248A (en) | 1990-06-21 | 1993-03-16 | Trustees Of Boston University | Compositions comprising vitamin D analog precursors and the use thereof |
| US5141719A (en) | 1990-07-18 | 1992-08-25 | Bio-Rad Laboratories, Inc. | Multi-sample filtration plate assembly |
| DK0503035T3 (da) | 1990-09-21 | 2002-04-15 | Bone Care Int Inc | Hidtil ukendt 1alfa-hydroxy-vitamin D4 og hidtil ukendte mellemprodukter og analoger |
| US5763428A (en) | 1990-09-21 | 1998-06-09 | Bone Care International, Inc. | Methods of treating skin disorders with novel 1a-hydroxy vitamin D4 compounds and derivatives thereof |
| US6251883B1 (en) | 1991-01-08 | 2001-06-26 | Bone Care International, Inc. | Methods for preparation and use of 1α,24(S)-dihydroxy vitamin D2 |
| ATE240736T1 (de) | 1991-01-08 | 2003-06-15 | Bone Care Int Inc | Verfahren zur herstellung von 1-alpha-24- dihydroxy-vitamin d2 |
| EP0503630B1 (en) | 1991-03-13 | 1995-12-27 | Kuraray Co., Ltd. | Cyclohexanetriol derivatives |
| US5264184A (en) | 1991-03-19 | 1993-11-23 | Minnesota Mining And Manufacturing Company | Device and a method for separating liquid samples |
| US5417923A (en) | 1991-04-24 | 1995-05-23 | Pfizer Inc. | Assay tray assembly |
| ES2093180T3 (es) | 1991-07-05 | 1996-12-16 | Duphar Int Res | Compuesto de vitamina d, metodo de preparar este compuesto y producto intermedio de dicho metodo. |
| US5205989A (en) | 1991-09-18 | 1993-04-27 | Minnesota Mining And Manufacturing Company | Multi-well filtration apparatus |
| US6113946A (en) | 1992-04-03 | 2000-09-05 | The Regents Of The University Of California | Self-assembling polynucleotide delivery system comprising dendrimer polycations |
| US5962731A (en) | 1992-04-22 | 1999-10-05 | Ligand Pharmaceuticals Incorporated | Compounds having selective activity for retinoid X receptors, and means for modulation of processes mediated by retinoid X receptors |
| CA2116238C (en) | 1992-06-22 | 2007-09-04 | Joyce C. Knutson | Oral 1 .alpha.-hydroxyprevitamin d |
| US5795882A (en) | 1992-06-22 | 1998-08-18 | Bone Care International, Inc. | Method of treating prostatic diseases using delayed and/or sustained release vitamin D formulations |
| DE4221961A1 (de) | 1992-06-30 | 1994-01-05 | Schering Ag | 22-En-25-oxa-Derivate in der Vitamin D-Reihe, Verfahren zu ihrer Herstellung, diese Derivate enthaltenen pharmazeutische Präparate sowie deren Verwendung als Arzneimittel |
| DK0614456T3 (da) | 1992-08-28 | 1999-12-06 | Bone Care Int Inc | 1alfa,24(S)-dihydroxy-vitamin D2, dets fremstilling og anvendelse |
| IL103224A (en) * | 1992-09-18 | 1998-08-16 | Teva Pharma | Stabilized pharmaceutical compositions containing derivatives of vitamins d2 and d3 |
| US5753638A (en) | 1992-10-07 | 1998-05-19 | Hoffmann-La Roche Inc. | Method of treating hyperproliferative skin disease with Vitamin D3 fluorinated analogs |
| CA2096105A1 (en) | 1992-10-07 | 1994-04-08 | Enrico Giuseppe Baggiolini (Deceased) | Vitamin d3 fluorinated analogs |
| US5366965A (en) | 1993-01-29 | 1994-11-22 | Boehringer Mannheim Gmbh | Regimen for treatment or prophylaxis of osteoporosis |
| US5478816A (en) | 1993-07-02 | 1995-12-26 | Bristol-Myers Squibb Company | Liquid vitamin formulations containing vitamin D esters |
| US5612327A (en) | 1993-09-01 | 1997-03-18 | Teijin Limited | 1α,24-(OH)2 -cholecalciferol emulsion composition and method for treating psoriasis |
| US5763429A (en) | 1993-09-10 | 1998-06-09 | Bone Care International, Inc. | Method of treating prostatic diseases using active vitamin D analogues |
| US6103709A (en) | 1993-12-23 | 2000-08-15 | The Regents Of The University Of California | Therapeutically effective 1α,25-dihydroxyvitamin D3 analogs and methods for treatment of vitamin D diseases |
| US5597575A (en) | 1994-06-06 | 1997-01-28 | Breitbarth; Richard | Composition for stimulating and inducing hair growth |
| WO1996002501A1 (en) * | 1994-07-18 | 1996-02-01 | Lunar Corporation | SYNTHESIS OF 1α-HYDROXY VITAMIN D |
| US6242434B1 (en) | 1997-08-08 | 2001-06-05 | Bone Care International, Inc. | 24-hydroxyvitamin D, analogs and uses thereof |
| US5739271A (en) | 1995-06-07 | 1998-04-14 | Gen-Probe Incorporated | Thiocationic lipids |
| US6221911B1 (en) | 1995-06-07 | 2001-04-24 | Karo Bio Ab | Uses for thyroid hormone compounds or thyroid hormone-like compounds |
| US5952317A (en) | 1995-09-21 | 1999-09-14 | Wisconsin Alumni Research Foundation | Calcitriol derivatives and their uses |
| JPH11514999A (ja) | 1995-10-10 | 1999-12-21 | ストルーブ,マリリン | ビタミンdおよびその誘導体による掻痒症治療 |
| EP0771789B1 (en) | 1995-10-30 | 2000-02-16 | F. Hoffmann-La Roche Ag | 1 alpha, 26-dihydroxy-D-homo-vitamin D3 |
| US5691328A (en) | 1996-02-02 | 1997-11-25 | Clarion Pharmaceuticals Inc. | Phosphoethanolamine conjugates of vitamin D compounds |
| AU710931B2 (en) | 1996-02-28 | 1999-09-30 | Sumitomo Pharmaceuticals Company, Limited | Crystalline vitamin D derivative |
| DK0892638T3 (da) | 1996-04-04 | 2003-03-03 | Cilag Ag | Liposombaseret, topisk vitamin D-præparat |
| DE19619036A1 (de) * | 1996-04-30 | 1997-11-13 | Schering Ag | Neue Vitamin D-Derivate mit carbo- oder heterocyclischen Substituenten an C-25, Verfahren zu ihrer Herstellung und die Verwendung zur Herstellung von Arzneimitteln |
| US5976784A (en) | 1996-09-20 | 1999-11-02 | Wisconsin Alumni Research Foundation | Calcitriol derivatives and their uses |
| US6372234B1 (en) * | 1997-05-27 | 2002-04-16 | Sembiosys Genetics Inc. | Products for topical applications comprising oil bodies |
| US6599513B2 (en) * | 1997-05-27 | 2003-07-29 | Sembiosys Genetics Inc. | Products for topical applications comprising oil bodies |
| US6359152B2 (en) * | 1997-07-21 | 2002-03-19 | Wisconsin Alumni Research Foundation | 18-substituted-19-nor-vitamin D compounds |
| US6087350A (en) * | 1997-08-29 | 2000-07-11 | University Of Pittsburgh Of The Commonwealth System Of Higher Education | Use of pretreatment chemicals to enhance efficacy of cytotoxic agents |
| AU762481C (en) | 1998-03-27 | 2004-08-19 | Oregon Health Sciences University | Vitamin D and its analogs in the treatment of tumors and other hyperproliferative disorders |
| US6114317A (en) | 1998-05-21 | 2000-09-05 | Wisconsin Alumni Research Foundation | Method of locking 1α-OH of vitamin D compounds in axial orientation |
| US5972917A (en) | 1998-05-29 | 1999-10-26 | Bone Care Int Inc | 1 α-hydroxy-25-ene-vitamin D, analogs and uses thereof |
| US6552009B2 (en) * | 1998-07-16 | 2003-04-22 | Gentrix Llc | Compositions and methods of treating abnormal cell proliferation |
| US20010002396A1 (en) * | 1998-07-16 | 2001-05-31 | Charles Achkar | Compositions and methods of treating skin conditions |
| US6218430B1 (en) | 1998-08-24 | 2001-04-17 | Ligand Pharmaceuticals Incorporated | Vitamin D3 mimics |
| US6531460B1 (en) | 1998-10-23 | 2003-03-11 | Teijin Limited | Vitamin D, derivatives and remedies for inflammatory respiratory diseases containing the same |
| US6548789B1 (en) * | 1999-04-22 | 2003-04-15 | Malden Mills Industries, Inc. | Electric resistance heating/warming fabric articles |
| US6524594B1 (en) | 1999-06-23 | 2003-02-25 | Johnson & Johnson Consumer Companies, Inc. | Foaming oil gel compositions |
| CN1181048C (zh) * | 1999-07-16 | 2004-12-22 | 里奥药物制品有限公司 | 作为IL-1β和TNF-α的抑制剂的氨基二苯酮 |
| PT1202957E (pt) * | 1999-07-16 | 2005-01-31 | Leo Pharma As | Aminobenzofenonas como inibidoras de il-1beta e tnf-alpha |
| DE19935771A1 (de) * | 1999-07-23 | 2001-02-01 | Schering Ag | Neue Vitamin D-Derivate mit cyclischen Substrukturen in den Seitenketten, Verfahren und Zwischenprodukte zu ihrer Herstellung und die Verwendung zur Herstellung von Arzneimitteln |
| FR2798855B1 (fr) | 1999-09-28 | 2003-04-25 | Oreal | Utilisation de complexes inorganiques-organiques dans une composition a usage topique |
| US6369098B1 (en) | 1999-10-05 | 2002-04-09 | Bethesda Pharmaceuticals, Inc. | Dithiolane derivatives |
| CA2393312C (en) * | 1999-12-06 | 2011-07-12 | Leo Pharma A/S | Aminobenzophenones as inhibitors of il-1.beta. and tnf-.alpha. |
| US6989377B2 (en) * | 1999-12-21 | 2006-01-24 | Wisconsin Alumni Research Foundation | Treating vitamin D responsive diseases |
| US6251608B1 (en) * | 2000-04-20 | 2001-06-26 | Technion Research & Development Foundation, Ltd. | Method of determining a potential of a hyperglycemic patients of developing vascular complications |
| RU2270194C2 (ru) | 2000-05-22 | 2006-02-20 | Лео Фарма А/С | Бензофеноны как ингибиторы il-1бета и tnf-альфа, фармацевтическая композиция и способ лечения |
| US6395784B1 (en) | 2000-06-07 | 2002-05-28 | Bristol-Myers Squibb Company | Benzamide ligands for the thyroid receptor |
| AU6428001A (en) * | 2000-06-15 | 2001-12-24 | Chugai Pharmaceutical Co Ltd | Vitamin d derivatives |
| IL153378A0 (en) * | 2000-07-18 | 2003-07-06 | Bone Care Internat Inc | STABILIZED 1alpha-HYDROXY VITAMIN D |
| JP2004529853A (ja) * | 2000-09-22 | 2004-09-30 | ブリストル−マイヤーズ スクイブ ファーマ カンパニー | 第Xa因子阻害剤の効率的な製造方法 |
| US20030149005A1 (en) * | 2001-08-22 | 2003-08-07 | Posner Gary H. | 24-sulfur-substituted analogs of 1alpha, 25-dihydroxy vitamin D3 |
| DE10156596A1 (de) * | 2001-11-13 | 2003-05-28 | Schering Ag | Vitamin D-Derivate mit Acyloxygruppen in der Seitenkette, Verfahren zu ihrer Herstellung und die Verwendung zur Herstellung von Arzneimitteln |
-
2001
- 2001-07-18 IL IL15337801A patent/IL153378A0/xx active IP Right Grant
- 2001-07-18 AU AU2001278956A patent/AU2001278956B2/en not_active Ceased
- 2001-07-18 JP JP2002512124A patent/JP2004504295A/ja active Pending
- 2001-07-18 WO PCT/US2001/022729 patent/WO2002006218A2/en active IP Right Grant
- 2001-07-18 EP EP09002505A patent/EP2070911A2/en not_active Withdrawn
- 2001-07-18 AU AU7895601A patent/AU7895601A/xx active Pending
- 2001-07-18 CA CA002414407A patent/CA2414407A1/en not_active Abandoned
- 2001-07-18 EP EP01957187A patent/EP1301479A2/en not_active Withdrawn
-
2002
- 2002-08-20 US US10/223,986 patent/US6903083B2/en not_active Expired - Lifetime
- 2002-12-11 IL IL153378A patent/IL153378A/en not_active IP Right Cessation
-
2005
- 2005-02-24 US US11/065,429 patent/US20050148558A1/en not_active Abandoned
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58126862A (ja) * | 1981-11-02 | 1983-07-28 | リサ−チ・インステイチユ−ト・フオア・メデイスン・アンド・ケミストリ−・インコ−ポレ−テツド | 1−ヒドロキシル化ビタミンd化合物の製法 |
| JPS62298572A (ja) * | 1986-06-19 | 1987-12-25 | Chugai Pharmaceut Co Ltd | 1α−ヒドロキシビタミンD3の精製法 |
| JPS63126891A (ja) * | 1986-11-14 | 1988-05-30 | Nisshin Flour Milling Co Ltd | ステロイド誘導体およびその製造方法 |
| JPS63126862A (ja) * | 1987-10-30 | 1988-05-30 | Nisshin Flour Milling Co Ltd | 1α−ヒドロキシビタミンD↓2の製造方法 |
| JPH01246276A (ja) * | 1988-03-25 | 1989-10-02 | Teikoku Chem Ind Corp Ltd | 1α−ヒドロキシ―6―(1,3−ベンゾジチオール−2−イル)オキシー3,5−シクロビタミンD↓3 |
| JPH02270860A (ja) * | 1988-03-25 | 1990-11-05 | Teikoku Chem Ind Corp Ltd | 1α―ヒドロキシ―ビタミンD↓3の製造方法 |
| JPH05279260A (ja) * | 1991-04-09 | 1993-10-26 | Takeda Chem Ind Ltd | 安定化されたビタミンd類製剤 |
| JPH05339230A (ja) * | 1992-03-12 | 1993-12-21 | Nisshin Flour Milling Co Ltd | 活性型ビタミンd2及びその誘導体の製造法 |
| JPH05320127A (ja) * | 1992-03-27 | 1993-12-03 | Nisshin Flour Milling Co Ltd | 活性型ビタミンd誘導体 |
| JPH06256301A (ja) * | 1992-11-04 | 1994-09-13 | Wisconsin Alumni Res Found | 1α,24−ジヒドロキシビタミンD類似体の製造方法 |
| JP2002535307A (ja) * | 1999-01-20 | 2002-10-22 | ウィスコンシン・アルムニ・リサーチ・ファウンデーション | 結晶1α−ヒドロキシビタミンD2とその精製方法 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005247803A (ja) * | 2004-03-08 | 2005-09-15 | Zeria Pharmaceut Co Ltd | 点眼剤及びその容器 |
| JP2014062131A (ja) * | 2008-03-12 | 2014-04-10 | Cytochroma Inc | 安定化1,25−ジヒドロキシビタミンd2及びその製造方法 |
| JP6186532B1 (ja) * | 2017-03-31 | 2017-08-23 | ナガセ医薬品株式会社 | マキサカルシトール含有水溶液製剤 |
| JP2018172299A (ja) * | 2017-03-31 | 2018-11-08 | ナガセ医薬品株式会社 | マキサカルシトール含有水溶液製剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| IL153378A (en) | 2007-02-11 |
| WO2002006218A3 (en) | 2002-07-18 |
| US6903083B2 (en) | 2005-06-07 |
| AU2001278956B2 (en) | 2007-04-05 |
| EP1301479A2 (en) | 2003-04-16 |
| AU7895601A (en) | 2002-01-30 |
| WO2002006218A2 (en) | 2002-01-24 |
| CA2414407A1 (en) | 2002-01-24 |
| US20050148558A1 (en) | 2005-07-07 |
| IL153378A0 (en) | 2003-07-06 |
| EP2070911A2 (en) | 2009-06-17 |
| US20030045509A1 (en) | 2003-03-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2004504295A (ja) | 安定化1α−ヒドロキシビタミンD | |
| AU2001278956A1 (en) | Stabilized 1alpha-hydroxy vitamin d | |
| US7235679B2 (en) | Crystals of a vitamin D derivative and a method for the preparation thereof | |
| JP2004504295A5 (ja) | ||
| FR2554444A1 (fr) | 1,25-dihydroxyvitamines d2 et procedes pour les preparer | |
| Yamada et al. | Stereoselective synthesis of (5E)-and (5Z)-vitamin D3 19-alkanoic acids via vitamin D3-sulfur dioxide adducts | |
| IE49753B1 (en) | 24,24-difluoro-cyclovitamin d3 derivatives | |
| McMorris et al. | Sesquiterpenes from Omphalotus illudens | |
| US11926583B2 (en) | Stabilized 1, 25-dihydroxyvitamin D2 and method of making same | |
| FR2630739A1 (fr) | Homologues a chaine laterale insaturee de vitamine d, compositions pharmaceutiques contenant ces composes, et leur utilisation | |
| JPS6346728B2 (ja) | ||
| KR100554560B1 (ko) | 비타민d유도체결정및그의제조방법 | |
| GB2051818A (en) | Derivative of 1 ,25-dihydroxy-cholecalciferol | |
| Brandl et al. | Chemical Reactivity of Ro-26-9228, 1α-Fluoro-25-hydroxy-16, 23E-diene-26, 27-bishomo-20-epi-cholecalciferol in Aqueous Solution | |
| JPH0495082A (ja) | 1α,25―ジヒドロキシビタミンD↓3―26,23―ラクトール | |
| Kallumkal | Solid-State Photochemistry of Provitamin D | |
| Cheng et al. | Preparation of 14C‐and 3H‐methoxyl‐labelled forms of ubiquinone by photochemical O‐demethylation and subsequent remethylation | |
| JP2000016987A (ja) | 活性型ビタミンd誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080715 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080715 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110519 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110518 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20111013 |