ES2806498T3 - Métodos para el análisis de una muestra de orina - Google Patents
Métodos para el análisis de una muestra de orina Download PDFInfo
- Publication number
- ES2806498T3 ES2806498T3 ES16727797T ES16727797T ES2806498T3 ES 2806498 T3 ES2806498 T3 ES 2806498T3 ES 16727797 T ES16727797 T ES 16727797T ES 16727797 T ES16727797 T ES 16727797T ES 2806498 T3 ES2806498 T3 ES 2806498T3
- Authority
- ES
- Spain
- Prior art keywords
- lysis buffer
- buffer
- urine sample
- sample
- urine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57555—Immunoassay; Biospecific binding assay; Materials therefor for cancer of the prostate
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/34—Purifying; Cleaning
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/40—Concentrating samples
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/40—Concentrating samples
- G01N1/4077—Concentrating samples by other techniques involving separation of suspended solids
- G01N2001/4088—Concentrating samples by other techniques involving separation of suspended solids filtration
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Hospice & Palliative Care (AREA)
- Oncology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
Un método para el análisis de una muestra de orina de un sujeto que comprende a. exponer la muestra de orina a un tampón de lisis que es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina, en donde el tampón de lisis comprende: (i) un detergente que comprende o consiste en tritón X-100; y (ii) un componente tampón que comprende o consiste en tampón Tris o Trizma; y b. realizar un ensayo para detectar la presencia de la proteína Mcm en la muestra de orina.
Description
DESCRIPCIÓN
Métodos para el análisis de una muestra de orina
Campo de la invención
La invención se refiere a métodos para el análisis de muestras de orina y a métodos para la preparación de células a partir de una muestra de orina. La invención también se refiere al uso de un tampón de lisis.
Antecedentes de la invención
Los cánceres urológicos (en ocasiones denominados 'cánceres del aparato urinario') son un problema epidemiológico importante y en aumento continuo. Dos de los cánceres urinarios de mayor importancia económica son el cáncer de vejiga y el cáncer de próstata.
El cáncer de próstata es el segundo cáncer más común en hombres después del cáncer de piel no melanoma, con más de 35.000 nuevos casos diagnosticados cada año en el RU; el cáncer de próstata provoca aproximadamente 10.200 muertes al año. Cada año se producen alrededor de 300.000 casos nuevos en Europa, 190.000 en los Estados Unidos y 670.000 en todo el mundo. Cancer Research UK informa que un cuarto de todos los casos nuevos de cáncer diagnosticados en hombres en el RU son cánceres de próstata y que el 60 % de los nuevos diagnósticos son en hombres de más de 70 años. La forma más común de la enfermedad es el adenocarcinoma. La tasa de supervivencia a 5 años es de casi el 80 % en el RU. No se conoce una causa ambiental, pero las personas con parientes cercanos con cáncer de próstata o de mama tienen más riesgo de desarrollar la enfermedad. Los hombres de África Occidental y afrocaribeños tienen un mayor riesgo de cáncer de próstata.
Los síntomas del cáncer de próstata son similares a los provocados por la hiperplasia benigna de la próstata e incluyen la necesidad imperiosa de orinar, dificultad o disuria, y rara vez, sangre en la orina o en el semen. Sin embargo, en muchos hombres, la enfermedad permanece asintomática hasta que se forman metástasis dolorosas, predominantemente en los huesos.
El tratamiento depende del estadio y del grado de malignidad del tumor, y de la salud general y edad del paciente. Las opciones incluyen vigilancia activa, prostatectomía parcial o radical, orquiectomía, el tratamiento hormonal y radioterapia, tal como la braquirradioterapia. La orquiectomía y el tratamiento hormonal reducen o eliminan la producción de testosterona, que es esencial para el crecimiento tumoral.
El diagnóstico definitivo de cáncer de próstata precisa un enfoque multifacético. La prueba de diagnóstico de referencia actual para el cáncer de próstata es el examen histológico del material de biopsia. La decisión de tomar una biopsia está basada en el nivel sérico del APS relacionado con la edad y/o en tacto rectal (TR) anómalo. El TR, en el cual se palpa la glándula por vía transrectal para examinar la morfología anómala, también es inespecífico. Los tumores que son demasiado pequeños para alterar la morfología de la glándula no se detectarán, y las afecciones benignas también provocan una morfología o agrandamiento anómalos. Este es un problema en la técnica. Habitualmente, las muestras de próstata se toman con biopsia de próstata por punción dirigida por ecografía transrectal TRUS (forma siglada del inglés transrectal ultrasound, ecografía transrectal). Se toman varias muestras con aguja gruesa, normalmente hasta 12, para maximizar el área de glándula de la que se toma una muestra. El procedimiento lo lleva a cabo un urólogo en el servicio de consultas externas, con anestesia local, con la ayuda de personal de enfermería o un auxiliar de clínica. Este procedimiento tiene inconvenientes, que incluyen ser algo doloroso para el paciente y exponer al paciente a un riesgo de sepsis y/o hemorragia. Las muestras de tejido con aguja gruesa se examinan al microscopio en el laboratorio en cuanto a la presencia de células malignas, lo que tiene el problema de ser laborioso y de precisar citólogos muy entrenados, además de ser susceptible de error humano. Se puede apreciar que las biopsias son invasivas y costosas. Existe una necesidad en la técnica de una herramienta más rentable, fiable y/o no invasiva para el diagnóstico y/o vigilancia del cáncer urinario, tal como el cáncer de próstata. Los procedimientos conocidos de diagnóstico alternativos y/o menos invasivos para el cáncer de próstata implican el análisis de marcadores biológicos específicos ('biomarcadores').
Un ejemplo de un biomarcador de ácido nucleico del cáncer de próstata es la prueba de PCA3 (gen de cáncer de próstata 3). Este ensayo urinario identifica el ARNm no codificante del gen PCA3, que se sobrexpresa en el cáncer de próstata (Hessels y Schalken, The use of PCA3 in the diagnosis of prostate cancer. Nat Rev Urol, 6, 255-61; 2009). La prueba PCA3 (Gen-Probe, Inc) se basa en el análisis de una muestra de ensayo de la primera micción producida después de una forma definida de masaje prostático, utilizado para expresar secreciones prostáticas, que contienen células epiteliales de la uretra. Como diagnóstico del cáncer de próstata PCA3 tiene un valor de curva ROC de 0,68 (Chun et al, Prostate Cancer Gene 3 (PCA3): development and internal validation of a novel biopsy nomogram. Eur Urol; 2009 vol. 56 pág. 659-668), que es similar al de la prueba de PSA analizada a continuación. Sin embargo, la prueba PCA3 es costosa y no es apta para el uso como análisis de diagnóstico inmediato, que son los problemas con esta técnica de la técnica anterior.
Un ejemplo de biomarcador proteico, que se usa con frecuencia para indicar la presencia de cáncer de próstata, es el PSA (antígeno prostático específico). A los pacientes sintomáticos que se presentan en atención primaria generalmente se les realiza una prueba de PSA sérica y un TR. Sin embargo, el PSA no es específico para el cáncer de próstata. El PSA es una enzima intracelular específica de tejido expresada constitutivamente. El PSA está presente a bajas concentraciones en el suero de hombres con una próstata sana. Un nivel elevado de PSA en suero se produce debido a la filtración procedente de la próstata y es una indicación del tamaño relativo de la glándula. El PSA elevado puede producirse en afecciones benignas, tales como la hiperplasia prostática benigna y la prostatitis, y también en el cáncer de próstata. A medida que los hombres se hacen mayores, el volumen de la glándula aumenta, lo que da como resultado un aumento de los niveles de PSA, en ausencia de neoplasia maligna. En un estudio reciente, se encontró que el 60-70 % de las pruebas de PSA 'positivas' (nivel sérico de PSA superior a 4 ng/ml) no estaban asociadas con cáncer (Kilpelainen et al., False-positive screening results in the Finnish prostate cancer screening trial, British Journal of Cancer. 102, 469-474; 2010). La alta tasa de resultados positivos falsos conduce a muchas operaciones de biopsia innecesarias y hace que la prueba sea inapropiada para el cribado poblacional. Además, la prueba de PSA no detecta un número significativo de casos de cáncer de próstata, particularmente en hombres más jóvenes. La precisión de la prueba de PSA medida en el análisis ROC (curva de eficacia diagnóstica) es de 0,678 (Thompson et al., Operating characteristics of a prostate-specific antigen in men with an initial PSA level of 3.0 ng/ml or lower. JAMA, 294, 66-70; 2005). En el RU, Habitualmente, las pruebas de PSA se llevan a cabo en laboratorios de hospitales, aunque están disponibles análisis de diagnóstico inmediato rápidos.
El cáncer de vejiga es el cuarto cáncer más común en los hombres y el noveno cáncer más común en las mujeres, y da como resultado una morbilidad y mortalidad significativas (Jemal et al. CA Cancer J Clin. 2007. 57:43-66.). La mayoría de los pacientes con cáncer de vejiga reciben el diagnóstico después de presentar hematuria macroscópica o microscópica, o con otros síntomas de micción irritativa, tal como la frecuencia y la disuria. En el diagnóstico inicial, aproximadamente el 70 % de los pacientes tienen cánceres de vejiga que están restringido al epitelio o al tejido conectivo subepitelial.
Estos cánceres se pueden tratar con resección endoscópica y terapia intravesical. La tasa de recidiva de estos tumores varía del 50 % al 70 %, y del 10 % al 15 % de los casos progresa a invasión muscular a lo largo de un período de 5 años (Shariat et al., 2008. Rev Urol. 10:120-135). La recidiva se puede ver de forma local y más raramente en las vías urinarias superiores, incluso después de varios años, necesitando una vigilancia de por vida. El 30 % restante de los pacientes tiene cáncer músculo invasivo en el momento del diagnóstico inicial. De esta población, el 50 % tiene metástasis a distancia dentro de los 2 años y el 60 % muere dentro de los 5 años, a pesar del tratamiento.
El diagnóstico definitivo de cáncer de vejiga requiere una combinación de procedimientos. Actualmente no existen métodos para identificar con precisión y facilidad la presencia de cáncer de vejiga temprano. El cribado de cáncer de vejiga en pacientes que se presentan en el consultorio de urología con los síntomas apropiados se realiza actualmente con análisis de orina, cistoscopia y un procedimiento de exploración tal como ecografía abdominal, urografía intravenosa, tomografía computarizada o resonancia magnética. La citología de orina, en que se examinan microscópicamente células de muestras de orina, se usa de forma ocasional. La cistoscopia, el pilar para la detección del cáncer de vejiga, es un procedimiento relativamente corto, mínimamente traumático, realizado con anestesia local de la uretra, que identifica casi todas las lesiones papilares y sésiles. No obstante, sigue siendo invasivo y una causa de malestar y angustia para el paciente. Además, en ocasiones la cistoscopia puede no ser concluyente debido a al aspecto anómalo macroscópico de la mucosa de la vejiga, especialmente en pacientes con una sonda permanente o inflamación activa, y es incapaz de detectar cánceres dentro de los uréteres. Aunque se considera se la considera el diagnóstico de referencia del cáncer de vejiga debido a que permite la visualización directa y la biopsia del urotelio de la vejiga, la cistoscopia tiene una tasa de negativos falsos considerable ya sea por error del técnico o por las áreas pequeñas de "carcinoma in situ", que puedes ser difíciles de detectar. (van der Poel y Debruyne. Curr Opin Urol. 2001; 11:503-509; Herr. BJU Int. 1999; 84:1102-1103.)
En la citología urinaria para el cáncer de vejiga, se pueden investigar células exfoliadas en cuanto a la presencia de antígenos específicos de la superficie celular, la morfología nuclear, expresión génica u otros marcadores biológicos. La citología urinaria tiene una alta sensibilidad y especificidad para la detección del cáncer de vejiga de gran malignidad, pero carece de sensibilidad para detectar tumores de baja malignidad (Wiener et al., Acta Cytol. 1993; 37:163-169). La precisión de la citología urinaria para predecir la recidiva del cáncer de vejiga puede variar ampliamente, en parte debido a que hay un elemento de subjetividad en la interpretación de los resultados. Por lo tanto, la citología no es ideal para cribar y vigilar el cáncer de vejiga.
Mcm5 es un biomarcador de cáncer (documento WO99021014). En un estudio no invasivo del cáncer de vejiga se demostró que los resultados de la detección inmunofluorométrica del componente 5 del complejo de mantenimiento de minicromosomas (Mcm5) en la orina combinados con los resultados de la detección por ELISA de NMP22 urinaria (proteína de matriz nuclear 22) permitían identificar una enfermedad potencialmente mortal para casi toda la vida del paciente (Kelly et al., Bladder Cancer Diagnosis and Identification of Clinically Significant Disease by Combined Urinary Detection of Mcm5 and Nuclear Matrix Protein 22 PlosONE. 7, e40305; 2012).
Un nivel aumentado de proteínas Mcm, tal como Mcm5, en el sedimento urinario está asociado con cambios malignos en la próstata. Por lo tanto, los niveles aumentados de estas proteínas Mcm podrían utilizarse para detectar el cáncer de próstata. Usando el DELFIA® (forma siglada de dissociation-enhanced lanthanide fluorometric immunoassay inmunoensayo fluorométrico de intensificación disociativa de la fluorescencia por lantánido) y anticuerpos monoclonales anti Mcm5 en un doble ensayo de anticuerpos, Dudderidge et al. (BJC, 103, 701 - 707; 2010) investigaron el uso de Mcm5 como un biomarcador urinario para la detección del cáncer de próstata y concluyeron que 'parece ser un método simple, preciso y no invasivo para la identificación de pacientes con cáncer de próstata'. En comparación con la prueba de PSA, que tiene una especificidad del 30 %, la especificidad de Mcm5 se estimó como de entre el 73 % y 93 %. Es importante destacar que, la hiperplasia prostática benigna no generó resultados positivos falsos, lo cual es una desventaja de la prueba de PSA. La evaluación de Mcm5 y otras proteínas Mcm actualmente precisa un laboratorio especializado con instrumentación sofisticada y operarios altamente cualificados, por lo tanto, el ensayo no es adecuado para el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato.
Esto se ve agravado por los métodos complicados que se utilizan para preparar muestras para el análisis mediante la detección de biomarcadores. Dado que las proteínas Mcm están presentes en las células, las proteínas Mcm deben liberarse de las células de una muestra, tal como una muestra de orina. Un método para la preparación de tales muestras se divulga en, Dudderidge et al. (BJC, 103, 701 - 707; 2010), el cual describe que las muestras deben procesarse utilizando una gran cantidad de etapas, que incluyen (1) centrifugación a 1500 g durante 5 minutos a 4 °C, (2) descarte del sobrenadante, (3) lavado del sedimento celular tres veces con 500 ml de PBS, (3) resuspensión de los sedimentos celulares en 250 ml o 500 ml de tampón de procesamiento (PBS, dodecilsulfato de sodio al 0,4 % y azida de sodio al 0,02 %), (4) incubación de las muestras resuspendidas a 95 °C durante 45 minutos, (5) rotura del ADN de la muestra haciendo pasar la lisis a través de una aguja de 0,813 mm de diámetro, (6) digestión de los ácidos nucleicos con ADNasa I y ARNasa A durante 2 h a 37 °C, y (7) centrifugación a 15000 g durante 10 min. Este método también se observa en otros documentos, tal como Stoeber et al 2002 (Journal of the National Cancer Institute, 94, 1071-1079; 2002). Este método de preparación de muestras de orina implica múltiples etapas utilizando múltiples reactivos y es extremadamente lento. Normalmente, estos métodos toman al menos dos horas. Por lo tanto, existe la necesidad de un método y/o aparato para la preparación de muestras de orina que sea considerablemente menos oneroso. Dicho método sería más adecuado para en el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato.
Los actuales ensayos para la detección de proteínas Mcm, particularmente de Mcm5, precisan el uso de la tecnología DELFIA, que es complicada de utilizar e implica equipos y reactivos caros. Por lo tanto, un ensayo basado en DELFIA no es adecuado para en el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato, y existe la necesidad de un ensayo que sea adecuado para tales aplicaciones.
Sumario de la invención
En el presente documento se describen métodos, composiciones y kits útiles para la detección temprana del cáncer urológico, tal como el cáncer de próstata, sin la necesidad de intervenciones quirúrgicas invasivas. Los métodos y composiciones son adecuados para su uso en el laboratorio clínico y/o para aplicaciones en análisis de diagnóstico inmediato.
Los presentes inventores han demostrado que los complicados métodos de preparación de muestras de orina descritos en la técnica anterior no son necesarios para la liberación de biomarcadores, tales como Mcm5, de las células de las muestras, tales como muestras de orina. En su lugar, todo lo que se precisa es exponer la muestra a un tampón de lisis que sea capaz de liberar el biomarcador de las células de la muestra. Esto es mucho más simple que los métodos de la técnica anterior. De acuerdo con la presente invención, en algunas realizaciones las células de una muestra (tal como una muestra de orina) pueden prepararse y lisarse mediante la adición de un único tampón de lisado. De manera similar, los inventores han diseñado un aparato que puede utilizarse para realizar fácilmente esta exposición al tampón de lisis.
Los presentes inventores también han demostrado que un ensayo de proteína Mcm que no utiliza inmunofluorescencia puede detectar con precisión si un sujeto tiene un cáncer urológico. Esto es beneficioso con respecto a las técnicas de la técnica anterior, que utilizan marcadores de Europio y detección DELFIA. Dichos métodos son caros y complicados y, por lo tanto, inadecuados para su uso en el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato.
Por consiguiente, la invención proporciona un método para el análisis de una muestra de orina de un sujeto que comprende
a. exponer la muestra de orina a un tampón de lisis que es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina, en donde el tampón de lisis comprende: (i) un detergente que comprende o consiste en tritón X-100; y (ii) un componente tampón que comprende o consiste en tampón Tris o Trizma; y b. realizar un ensayo para detectar la presencia de la proteína Mcm en la muestra de orina.
La invención también proporciona un método para la preparación de células a partir de una muestra de orina,
comprendiendo el método:
hacer pasar la muestra de orina a través de un filtro para la captura de células, de manera que las células se capturen en el filtro;
hacer pasar a través del filtro un tampón de lisis que es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina,
de manera que las células capturadas estén expuestas al tampón de lisis;
incubar el filtro durante un período de tiempo, de manera que el tampón de lisis provoque que las células liberen la proteína Mcm,
en donde el tampón de lisis comprende: (i) un detergente que comprende o consiste en tritón X-100; y (ii) un componente tampón que comprende o consiste en tampón Tris o Trizma.
La invención proporciona adicionalmente el uso de un tampón de lisis como se define anteriormente para la liberación de una proteína Mcm a partir de las células de una muestra de orina.
Además, en el presente documento se describe un método para el análisis de una muestra de orina de un sujeto que comprende
a. exponer la muestra de orina a un tampón de lisis, en donde el tampón de lisis es capaz de liberar al menos un biomarcador a partir de las células de la muestra de orina; y
b. realizar un ensayo para determinar la concentración del al menos un biomarcador en la muestra de orina. En el presente documento se describe un método para el análisis de una muestra de orina de un sujeto, que comprende una etapa de exposición de la muestra de orina a un tampón de lisis, en donde:
a. el tampón de lisis no es PBS que contiene desoxicolato de sodio al 0,4 % y azida de sodio al 0,02 %;
b. el método no comprende la incubación de la muestra de orina a una temperatura mayor que 90 °C durante alrededor de 45 minutos;
c. el método no comprende la rotura de los ácidos nucleicos haciendo pasar la muestra de orina a través de una aguja de 0,813 mm de diámetro;
d. el método no comprende la digestión de ácidos nucleicos mediante la exposición de la muestra de orina a ADNasa I o ARNasa A; y/o
e. el método no comprende la centrifugación de la muestra a 15.000 g durante diez minutos;
y donde el método comprende adicionalmente una etapa de realización de un ensayo para determinar la concentración de al menos un biomarcador en la muestra de orina.
En el presente documento se describe un método para el análisis de una muestra de orina que comprende células de un sujeto, en donde la muestra de orina se prepara utilizando un procedimiento que consiste en las siguientes etapas:
a. concentración de las células en la muestra de orina; y
b. exposición de las células concentradas a tampón de lisis;
y donde el método comprende adicionalmente una etapa de realización de un ensayo para determinar la concentración de al menos un biomarcador en la muestra de orina.
En el presente documento se describe un método para el análisis de una muestra de orina que comprende células de un sujeto, en donde la muestra de orina se prepara utilizando un procedimiento que consiste en las siguientes etapas:
a. centrifugación de la muestra para proporcionar un sedimento de muestra; y
b. resuspensión de las células sedimentadas de la muestra en un tampón de lisis;
y donde el método comprende adicionalmente una etapa de realización de un ensayo para determinar la concentración de al menos un biomarcador en la muestra de orina.
En el presente documento se describe un kit que comprende un tampón de lisis que es capaz de liberar al menos un biomarcador de las células en una muestra de orina, un anticuerpo de captura y un anticuerpo de detección, en donde el anticuerpo de captura y el anticuerpo de detección se unen a Mcm5.
En el presente documento se describe un aparato para la preparación de células de una muestra de orina, comprendiendo el aparato:
una entrada;
una primera disposición de válvula colocada aguas abajo de la entrada y en comunicación fluida con la entrada; un filtro para la captura de células de la orina, estando el filtro dispuesto aguas abajo de la primera disposición de válvula y en comunicación fluida con la primera disposición de válvula;
una segunda disposición de válvula colocada aguas abajo del filtro y en comunicación fluida con el filtro; una salida dispuesta aguas abajo de la segunda disposición de válvula y en comunicación fluida con la segunda disposición de válvula;
un primer depósito de tampón para contener un tampón de lisis, estando el primer depósito de tampón en comunicación fluida con la primera disposición de válvula;
un segundo depósito de tampón para contener un tampón de lisis, estando el segundo depósito de tampón en comunicación fluida con la segunda disposición de válvula;
en donde la primera y segunda disposiciones de válvula pueden configurarse de manera que:
en una primera configuración de la primera y la segunda disposiciones de válvulas, la comunicación fluida entre el primer depósito de tampón y el filtro está bloqueada, la comunicación fluida entre el segundo depósito de tampón y el filtro está bloqueada, y la comunicación fluida entre la entrada, el filtro y la salida está abierta, de manera que la orina pueda fluir desde la entrada a la salida a través del filtro; y
en una segunda configuración de la primera y la segunda disposiciones de válvulas, la comunicación fluida entre el primer depósito de tampón y el filtro está abierta, la comunicación fluida entre el segundo depósito de tampón y el filtro está abierta, y el flujo a través de la entrada y la salida está bloqueado, de manera que el tampón de lisis pueda fluir entre el primer depósito de tampón y el segundo depósito de tampón a través del filtro.
En el presente documento se describe un método para la preparación de células a partir de una muestra de orina, comprendiendo el método:
hacer pasar la muestra de orina a través de un filtro para la captura de células, de manera que las células se capturen en el filtro;
hacer pasar un tampón de lisis a través del filtro, de manera que las células capturadas estén expuestas al tampón de lisis;
incubar el filtro durante un período de tiempo, de manera que el tampón de lisis provoque que las células liberen al menos un biomarcador.
En el presente documento se describe un método para la detección de la presencia de un biomarcador indicativo de un cáncer urológico en un sujeto, comprendiendo el método:
a. realizar un ensayo en una muestra de un sujeto para determinar la concentración de una proteína Mcm; b. comparar la concentración de la proteína Mcm determinada en la etapa a. con valores de referencia;
en donde el ensayo no es un ensayo inmunofluorométrico.
En el presente documento se describe un kit adecuado para realizar los métodos de la invención.
En el presente documento se describe un kit para su uso en el diagnóstico de un cáncer urológico que comprende un anticuerpo de captura y un anticuerpo de detección, en donde (a) el anticuerpo de captura y el anticuerpo de detección se unen específicamente a Mcm5, (b) el anticuerpo de captura está unido a un soporte sólido, y (c) el anticuerpo de detección está conjugado con peroxidasa de rábano picante.
En el presente documento se describe un dispositivo para el análisis de una muestra de orina de un sujeto, comprendiendo el dispositivo:
un aparato descrito en el presente documento; y
un dispositivo de ensayo capaz de determinar la concentración de al menos un biomarcador en la muestra de orina.
En el presente documento se describe un uso del tampón de lisis como se describe en el presente documento para la liberación de al menos un biomarcador de las células en una muestra de orina.
Breve descripción de los dibujos
La Figura 1 es un listado de secuencias.
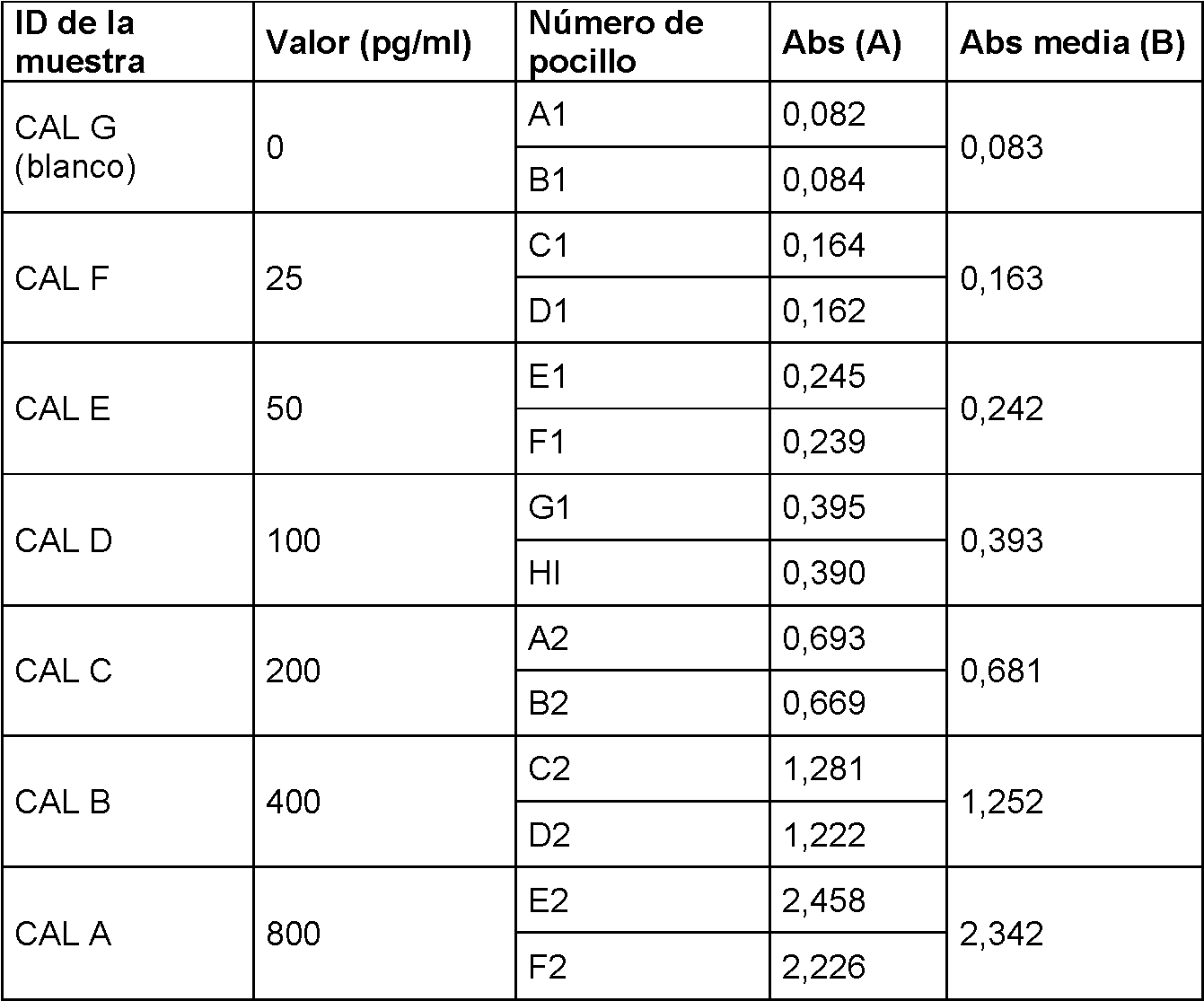
La Figura 2 muestra un gráfico que describe la absorbancia a 450 nm de distintas concentraciones de Mcm5. La Figura 3 muestra un diagrama que describe cómo diluir la solución de calibración madre.
La Figura 4 muestra un gráfico que compara la cantidad de Mcm5 liberada de células de carcinoma urotelial
después de la exposición a 4 tampones de lisis distintos (Uro LB "desoxicolato de sodio al 0,08 %, CHAPS al 0,08 %, EDTA 2 mM, Trizma 150 mM pH 7,6), Cytobuster TM, Glolysis TM y SDS al 0,1 % Trizma 50 mM pH 7,6, NaC 150 mM, EDTA 1 mM.
La Figura 5 muestra un gráfico que compara el CytoBuster, el tampón RIPA y el tampón TBS-T antes de la modificación.
La Figura 6 muestra un gráfico que compara tampones basados en tampón TBST y que comprenden elementos del tampón RIPA, antes y después de la congelación y descongelación del lisado.
La Figura 7 muestra un gráfico que compara tampones basados en tampón RIPA pero en los que se han eliminados algunos elementos del tampón RIPA, antes y después de la congelación y descongelación del lisado. La Figura 8 muestra un gráfico que compara tampones que tienen distintas concentraciones de Tris y de Tritón X-100, utilizando lisados frescos.
La Figura 9 muestra un gráfico que compara distintas formulaciones de base de tampón (TBS, PBS, bicarbonato, MOPS y HEPES), utilizando lisados frescos.
La Figura 10 muestra un gráfico que compara tampones que tienen distintas concentraciones de Tris (100 mM -350 mM), utilizando lisados frescos.
La Figura 11 muestra un gráfico que compara los tampones basados en los tampones TBS-T y RIPA pero que tienen una fuerza iónica modificada, utilizando lisados congelados y descongelados.
La Figura 12 muestra un gráfico que compara tampones TBS-T que tienen una fuerza de NaCl modificada, utilizando lisados congelados y descongelados.
Las Figuras 13A y 13B muestran gráficos que comparan tampones TBS-T que comprenden adicionalmente diversos agentes estabilizadores. La Figura 14 muestra un gráfico que compara tampones TBST que comprenden distintas concentraciones de agentes estabilizadores, después de 6 días de almacenamiento.
Las figuras 15A, 15B y 15C muestran gráficos que evalúan la eficacia del tampón TBST /- BSA al 2,5 % en diversas líneas celulares. La Figura 16 muestra un gráfico que compara tampones TBST BSA al 2,5 % con o sin ProClin950.
La Figura 17 muestra un gráfico que compara tampones TBST BSA al 2,5 % con o sin azida de sodio (NaN3). En la Figura 18 se representa un aparato para la preparación de células a partir de una muestra de orina.
Descripción detallada
Definiciones
Debe entenderse que el término 'comprende' (comprenden, que comprende/n) tiene su significado normal en la técnica, es decir, que se incluye la característica o grupo de características indicadas, pero que el término no excluye que ninguna otra característica establecida o grupo de características determinado esté también presente.
Debe entenderse también que el término "consiste en" tiene su significado normal en la técnica, es decir, que se incluye la característica o grupo de características indicadas, con exclusión de otras características. Por ejemplo, un tampón de lisis que consiste en un detergente contiene detergente y no otros componentes. Por otro lado, un tampón de lisis que comprende un detergente que consiste en polisorbato 80 puede comprender componentes distintos de detergentes, pero el único detergente en el tampón de lisis es polisorbato 80.
Para cada realización en la que se utiliza "comprende" o "que comprende", los inventores anticipan una realización adicional en la que se usa "consiste en" o "que consiste en". Por lo tanto, toda divulgación de "comprende" debe considerarse como una divulgación de "consiste en".
Métodos de preparación de muestras de orina
La presente invención se refiere a métodos para el análisis de muestras de orina que comprenden exponer la muestra de orina a un tampón de lisis. Estos métodos son considerablemente más simples y más rentables que los métodos de la técnica anterior.
Se puede considerar que la expresión 'exponer la muestra de orina a un tampón de lisis' se refiere a la manipulación de la muestra de orina de tal manera que las células dentro de la muestra de orina (o una parte sustancial de estas células) estén en contacto con el tampón de lisis. De manera adecuada, la muestra de orina se centrifuga para proporcionar un sedimento de muestra, el sobrenadante se descarta y el sedimento de muestra se resuspende en el tampón de lisis. Como alternativa, por ejemplo, los componentes tampón concentrados se añaden a una muestra de orina líquida para formar una solución que comprende la muestra de orina expuesta al tampón de lisis.
La muestra de orina puede prepararse utilizando un procedimiento que consiste en las siguientes etapas:
a. concentración de las células en la muestra de orina; y
b. exposición de las células concentradas a tampón de lisis.
De manera adecuada, la etapa a. de concentración de las células en la muestra de orina se realiza filtrando la muestra de orina para capturar las células. De manera adecuada, las etapas a. de concentración de las células en el
tampón de lisis y b. de exposición de las células concentradas al tampón de lisis se llevan a cabo utilizando un dispositivo o aparato descrito en el presente documento o utilizando el método para preparar células a partir de una muestra de orina de la invención.
En una realización preferente adicional, el método comprende una etapa de concentración de células en la muestra de orina antes de la etapa de exposición de la muestra de orina a un tampón de lisis, la exposición de las células concentradas a tampón de lisis o la resuspensión de las células sedimentadas de la muestra en tampón de lisis. La muestra de orina que comprende células puede prepararse utilizando un procedimiento que consiste en las siguientes etapas: a. centrifugación de la muestra para proporcionar un sedimento de muestra; y b. resuspensión de las células sedimentadas de la muestra en un tampón de lisis.
De manera adecuada, la muestra se centrifuga durante entre 1 minuto y 30 minutos a entre 500 g y 5000 g, durante entre 1 minuto y 20 minutos a entre 750 g y 2500 g, durante entre 3 minutos y 10 minutos a entre 750 g y 2000 g, o durante alrededor de 5 minutos a 1500 g.
De manera adecuada, el sedimento se resuspende utilizando una pipeta ajustable con una punta desechable.
En una realización, el método no comprende la incubación de la muestra de orina a una temperatura mayor que 90 °C durante alrededor de 45 minutos. Opcionalmente, el método no comprende la incubación de la muestra de orina a una temperatura alta. En una realización, la temperatura alta es una temperatura mayor que 50 °C, mayor que 60 °C, mayor que 70 °C, mayor que 80 °C, mayor que 90 °C, entre 50 °C y 120 °C, entre 60 °C y 110 °C, entre 70 °C y 100 °C, o entre 80 °C y 100 °C. Opcionalmente, el método no comprende la incubación de la muestra de orina a una temperatura alta durante más de 30 minutos, más de 35 minutos, más de 40 minutos, más de 45 minutos, entre 30 minutos y 2 horas, entre 35 minutos y 2 horas, o entre 40 minutos y 2 horas.
En una realización adicional, el método no comprende la rotura de los ácidos nucleicos haciendo pasar la muestra de orina a través de una aguja de 0,813 mm de diámetro. En otra realización, el método no comprende la exposición de la muestra de orina a rotura mecánica.
En un método adicional, el método no comprende la digestión de ácidos nucleicos mediante la exposición de la muestra de orina a ADNasa I o ARNasa A.
Opcionalmente, el método no comprende la incubación de la muestra de orina a una temperatura mayor que 90 °C durante más de 45 minutos, la rotura de los ácidos nucleicos en la muestra de orina haciendo pasar la muestra de orina a través de una aguja de 0,813 mm de diámetro, la digestión de ácidos nucleicos mediante la exposición de la muestra de orina a ADNasa I o ARNasa A, la centrifugación de la muestra a 15.000 g durante 10 minutos, en donde el tampón de lisis no es PBS que contiene desoxicolato de sodio al 0,4 % y azida de sodio al 0,02 %.
La frase 'no comprende la digestión de los ácidos nucleicos mediante la exposición de la muestra de orina a ADNasa I o ARNasa A' significa que la muestra no debe exponerse a una concentración de ADNasa I o ARNasa A que sea eficaz para provocar una digestión significativa de los ácidos nucleicos en la muestra. Preferentemente, la muestra no se expone a ADNasa I a más de 20 U/ml o a ARNasa A a más de 1 mg/ml. De manera adecuada, la muestra no se expone a ADNasa I a más de 1 U/ml, más de 5 U/ml, más de 10 U/ml, más de 15 U/ml, entre 1 U/ml y 500 U/ml, entre 5 U/ml y 250 U/ml, entre 10 U/ml y 100 U/ml o entre 15 U/ml y 100 U/ml. De manera adecuada, la muestra no se expone a ARNasa A a más de 0,1 mg/ml, más de 0,2/mg/ml, más de 0,5 mg/ml, más de 0,7 mg/ml, entre 0,1/mg/ml y 100 mg/ml, entre 0,5/mg/ml y 50 mg/ml o entre 0,5 mg/ml y 25/mg/ml.
En una realización adicional, el método no comprende la centrifugación de la muestra a 15.000 g durante diez minutos. En una realización adicional, el método no comprende la centrifugación de la muestra. En una realización adicional, el método no comprende la centrifugación de la muestra a más de 10.000 g, más de 12.000 g, más de 14.000 g o más de 14.500 g. En una realización adicional, el método no comprende la centrifugación de la muestra durante más de 2 minutos, más de 5 minutos, más de 7 minutos o más de 8 minutos.
El método puede ser un método para la liberación de al menos un biomarcador, tal como Mcm5, a partir de las células de la muestra de orina y la determinación de la concentración del al menos un biomarcador liberado de las células.
Los métodos para el análisis de una muestra de orina de la invención pueden ser parte de un método más amplio para ayudar al diagnóstico de un cáncer urológico en un sujeto.
Tampones de lisis de la invención
Los tampones de lisis son, generalmente, tampones que se utilizan con el fin de lisar células. Además de liberar uno o más biomarcadores de las células, el tampón de lisis debe ser compatible con el método utilizado para el análisis posterior. Por ejemplo, cuando el método de análisis es ELISA tipo sándwich de doble anticuerpo, el tampón de lisis
no debe degradar el anticuerpo de captura unido a la superficie de la placa de microtitulación. Los tampones de lisis en general, pero no exclusivamente, comprenden uno o más detergentes (también conocidos como tensioactivos), una o más sales y un agente tamponador. Las concentraciones de estos componentes afectan la eficacia del tampón de lisis.
El tampón de lisis es capaz de liberar un biomarcador, tal como Mcm5, de las células de la muestra. Se considerará que un tampón de lisis es "capaz de liberar un biomarcador, tal como Mcm5, de las células de la muestra" si la cantidad del biomarcador (tal como Mcm5) liberada es mayor al 40 %, 50 %, 60 %, 70 % u 80 % de la cantidad liberada cuando se utiliza un tampón que contiene desoxicolato de sodio al 0,08 %, CHAPS al 0,08 %, EDTA 2 mM, Trizma 150 mM pH 7,6. En una realización, se considerará que un tampón de lisis es "capaz de liberar un biomarcador, tal como Mcm5, de las células de la muestra" si la cantidad del biomarcador, tal como Mcm5, liberada es mayor al 40 %, 50 %, 60 %, 70 % u 80 % de la cantidad liberada cuando se utiliza un tampón que contiene Tris 10 mM (pH 7,6), NaCl 200 mM, BSA al 2,5 %, Tritón X100 al 0,1 % y azida de sodio al 0,09 %. La cantidad del biomarcador, tal como Mcm5, que se libera utilizando un tampón de lisis se puede determinar analizando la cantidad presente después de la exposición al tampón de lisis y comparándola con una muestra de referencia (preferentemente una muestra que sea sustancialmente la misma o idéntica a la primera muestra) que se ha expuesto a un tampón que contiene desoxicolato de sodio al 0,08 %, CHAPS al 0,08 %, EDTA 2 mM, Trizma 150 mM pH 7,6. En una realización, la cantidad de un biomarcador, tal como Mcm5, que se libera utilizando un tampón de lisis se puede determinar analizando la cantidad presente después de la exposición al tampón de lisis y comparándola con una muestra de referencia (preferentemente una muestra que sea sustancialmente la misma o idéntica a la primera muestra) que se ha expuesto a un tampón que contiene desoxicolato Tris 10 mM (pH 7,6), NaCl 200 mM, BSA al 2,5 %, Tritón X100 al 0,1 % y azida de sodio al 0,09 %. La cantidad de un biomarcador, tal como Mcm5, que se libera puede medirse utilizando un ensayo de ELISA de tipo sándwich tal como el ensayo descrito en el Ejemplo 1. Los anticuerpos utilizados en el ensayo tipo sándwich deben ser anticuerpos que se unan al biomarcador, tal como Mcm5, por ejemplo, un primer anticuerpo monoclonal o un segundo anticuerpo monoclonal descrito en el presente documento. Preferentemente, se utilizan los anticuerpos 12A7 y 4B4.
En una realización aún más preferente de la invención, el tampón de lisis es capaz de liberar Mcm5 a partir de las células de la muestra de orina y no degrada sustancialmente la proteína Mcm5. Se puede considerar que un tampón no degrada sustancialmente la proteína Mcm5 si la cantidad de Mcm5 intacta presente después de la exposición de la muestra al tampón de lisis es mayor al 40 %, 50 %, 60 %, 70 % u 80 % de la cantidad de Mcm5 intacta después de la exposición a un tampón que contiene desoxicolato de sodio al 0,08 %, CHAPS al 0,08 %, EDTA 2 mM, Trizma 150 mM pH 7,6. La proteína Mcm5 puede considerarse intacta, si los sitios de unión para los anticuerpos que se unen a la SEQ ID NO: 1 y la SEQ ID NO: 2 (tal como el primer anticuerpo monoclonal y el segundo anticuerpo monoclonal, o los anticuerpos 12A7 y 4B4) están presentes. Está dentro de las capacidades del experto en la materia determinar cuánta Mcm5 se degrada dentro de una muestra. La muestra debe analizarse para observar si la Mcm5 dentro de la muestra puede unirse al primer anticuerpo monoclonal y al segundo anticuerpo monoclonal descritos en el presente documento. Esto puede medirse utilizando un ensayo de ELISA de tipo sándwich, tal como el descrito en el Ejemplo 1. Los anticuerpos utilizados en el ensayo tipo sándwich deben ser anticuerpos que se unan a Mcm5, por ejemplo, un primer anticuerpo monoclonal o un segundo anticuerpo monoclonal de la invención. Preferentemente, se utilizan los anticuerpos 12A7 y 4B4.
Se puede considerar que un tampón de lisis no desnaturaliza un anticuerpo si la actividad del anticuerpo después de la exposición al tampón de lisis es del 40 %, 50 %, 60 %, 70 % u 80 % de la actividad del anticuerpo antes de la exposición al tampón de lisis. La actividad del anticuerpo se puede analizar utilizando un ensayo de ELISA como el descrito en el Ejemplo 1.
En una realización, el tampón de lisis es capaz de liberar Mcm5 a partir de las células de una muestra fresca. La expresión "muestra fresca" se refiere a una muestra que no se ha congelado. Preferentemente, la "muestra fresca" se ha obtenido de un paciente de menos de 10 días, menos de 5 días, menos de 2 días o menos de 1 día antes de su uso en los métodos de la invención. En una realización, las células se exponen al tampón de lisis y después se congelan antes del tratamiento adicional. Por ejemplo, la muestra de orina se puede concentrar por centrifugación seguido del descarte del sobrenadante y a continuación se puede añadir el tampón de lisis a las células concentradas. Preferentemente, la muestra congelada se descongela antes de una etapa de realización de un ensayo para determinar la concentración del al menos un biomarcador en la muestra de orina. Preferentemente, la muestra se congela durante al menos 1 hora, al menos 1 día, al menos 5 días o al menos 10 días antes de una etapa de realización de un ensayo para determinar la concentración del al menos un biomarcador en la muestra de orina. Preferentemente, la muestra se congela durante entre 1 hora y 1 año, entre 1 hora y 6 meses, entre 1 día y 3 meses o alrededor de una semana antes de una etapa de realización de un ensayo para determinar la concentración del al menos un biomarcador en la muestra de orina.
El tampón de lisis descrito en el presente documento puede ser el reactivo de extracción de proteínas Cytobuster™.
En una realización, el tampón de lisis no es PBS que contiene desoxicolato de sodio al 0,4 % y azida de sodio al 0,02 %.
El tampón de lisis utilizado en la presente invención comprende un detergente (también denominado tensioactivo). El tampón de lisis utilizado en la presente invención comprende un detergente que comprende o consiste en Tritón X-100. En general, los detergentes son compuestos que se sabe que rompen las paredes celulares. Los detergentes son anfifílicos que tienen regiones hidrófobas e hidrófilas. Los detergentes adecuados son bien conocidos por el experto en la materia.
De manera adecuada, el detergente es un detergente aniónico, un detergente catiónico, un detergente no iónico o un detergente zwitteriónico. De manera adecuada, el detergente se selecciona del grupo que consiste en desoxicolato de sodio, 3-[(3-Colamidopropil)dimetilamonio]-1-propanosulfonato (CHAPS), alquilbencenosulfonatos, dodecilbencenosulfonato de sodio, un detergente Tween (tal como monooleato de polioxietilen (2b) sorbitano o Tween-20), y un detergente Tritón (tal como polietilenglicol p-(1,1,3, 3,-tetrametilbutil)-fenil éter o Tritón X-100). De manera adecuada, el detergente comprende desoxicolato de sodio. De manera adecuada, el detergente comprende CHAPS. De manera adecuada, el detergente comprende desoxicolato de sodio y CHAPS. De manera adecuada, el tampón de lisis comprende desoxicolato de sodio a una concentración de entre el 0,01 % y el 0,15 %, entre el 0,03 % y el 0,10 %, entre el 0,05 % y el 0,09 %, o aproximadamente el 0,08 %. De manera adecuada, el tampón de lisis comprende CHAPS a una concentración de entre el 0,01 % y el 0,15 %, entre el 0,03 % y el 0,10 %, entre el 0,05 % y el 0,09 %, o aproximadamente el 0,08 %. De manera adecuada, el detergente comprende X-100. Preferentemente, el detergente comprende tritón X-100 a una concentración de entre el 0,01 % y el 25 %, entre el 0,01 % y el 10 %, entre el 0,05 % y el 5 %, entre el 0,05 % y el 1 %, entre el 0,05 % y el 0,5 %, entre 0,075 % y el 0,125 % o alrededor del 0,1 %. De manera adecuada, el detergente consiste en tritón X-100. Preferentemente, el detergente consiste en tritón X-100 a una concentración de entre el 0,01 % y el 25 %, entre el 0,01 % y el 10 %, entre el 0,05 % y el 5 %, entre el 0,05 % y el 1 %, entre el 0,05 % y el 0,5 %, entre 0,075 % y el 0,125 % o alrededor del 0,1 %. De manera adecuada, el detergente comprende polisorbato, preferentemente polisorbato 20 (también conocido como Tween 20). De manera adecuada, el detergente comprende polisorbato a una concentración de entre el 0,01 % y el 5 %, entre el 0,02 % y el 1 %, entre 0,03 % y el 0,07 % o alrededor del 0,05 %. De manera adecuada, el detergente comprende desoxicolato de sodio o dodecilsulfato de sodio. Por ejemplo, el detergente puede comprender desoxicolato de sodio o dodecilsulfato de sodio a una concentración de entre el 0,1 % y el 20 %, entre el 0,5 % y el 10 %, entre el 0,5 % y el 5 %, entre 0,75 % y el 1,25 % o alrededor del 1 %.
En una realización adicional, el tampón de lisis comprende un agente quelante. En una realización adicional, el tampón de lisis no comprende un agente quelante. Los agentes quelantes son ligandos multidentados que pueden coordinar iones metálicos. De manera adecuada, el agente quelante es EDTA (ácido etilendiaminotetraacético). Opcionalmente, el tampón de lisis comprende EDTA a una concentración de entre 0,5 mM y 10 mM, entre 1 mM y 5 mM, entre 1,5 mM y 3 mM, o aproximadamente 2 mM.
El tampón de lisis utilizado en la presente invención comprende un componente tampón que comprende o consiste en tampón Tris o Trizma. Se puede considerar que un componente tampón es cualquier componente que mantiene el pH del tampón de lisis a un pH que varía en menos de 2,0 unidades de pH, 1,5 unidades de pH o 1,0 unidades de pH. Los expertos en la materia conocen bien ejemplos de tampones que son adecuados para este fin. El componentes tampón puede ser un tampón seleccionado del grupo que consiste en TAPS (ácido 3-{[tris(hidroximetil)metil]amino} propanosulfónico), Bicina (N,N-bis(2-hidroxietil)glicina), Tris (tris(hidroximetil)metilamina), Tricina (N-tris(hidroximetil(metilglicina), TAPSO (3-[ácido N-Tris(ácido hidroximetil)metilamino]-2-hidroxipropanosulfónico, HEPES (ácido 4-2-hidroxietil-1-piperazinetanosulfónico) y MOPS (ácido 3-(N-morfolino)propanosulfónico. De manera adecuada, el componente tampón comprende tampón Tris, solución salina tamponada con fosfato (PBS), MOPS, bicarbonato o HEPES. De manera adecuada, el componente tampón comprende Tris, tampón PBS, MOPS o de bicarbonato. De manera adecuada, el componente tampón comprende Tris, tampón PBS o de bicarbonato. El componente tampón puede ser tampón Tris o Trizma. En la presente invención el componente tampón comprende o consiste en tampón Tris o Trizma. Trizma puede referirse a cristales de Trizma® preajustados a pH 7,6' (Sigma-Aldrich N.° de Cat. T7943). En una realización adicional, el componente tampón mantiene el pH del tampón a un pH entre pH 4 y pH 9, entre pH 5 y pH 8, entre pH 6 y pH 8, o a alrededor de pH 7,6. Opcionalmente, el componente tampón es el tampón Tris o Trizma, y el componente tampón mantiene el pH del tampón de lisis entre pH 4 y pH 9, entre pH 5 y pH 8, entre pH 6 y pH 8, o a alrededor de pH 7,6. Opcionalmente, el componente tampón comprende o consiste en tampón Tris o Trizma, y el componente tampón mantiene el pH del tampón de lisis entre pH 4 y pH 9, entre pH 5 y pH 8, entre pH 6 y pH 8, o a alrededor de pH 7,6.
Preferentemente, el componente tampón comprende tampón tris, por ejemplo, a una concentración mayor de 5 mM, entre 5 mM y 350 mM, entre 200 mM y 300 mM, entre 225 mM y 275 mM, entre 10 mM y 25 mM, entre 8 mM y 12 mM, alrededor de 10 mM o alrededor de 250 mM. Preferentemente, el componente tampón consiste en tampón tris, por ejemplo, a una concentración mayor de 5 mM, entre 5 mM y 350 mM, entre 200 mM y 300 mM, entre 225 mM y 275 mM, entre 10 mM y 25 mM, entre 8 mM y 12 mM, alrededor de 10 mM o alrededor de 250 mM. De manera adecuada, el componente tampón comprende solución salina tamponada con fosfato, por ejemplo, a una concentración de entre 5 mM y 250 mM, entre 50 mM y 250 mM, o alrededor de 100 mM.
En una realización, el tampón de lisis comprende desoxicolato de sodio a una concentración de entre el 0,01 % y el 0,15 %, CHAPS a una concentración de entre el 0,01 % y el 0,15 %, EDTA a una concentración de entre 0,5 mM y 10 mM, y tampón Tris o Trizma, en donde el tampón Tris o Trizma mantiene el pH del tampón de lisis entre pH 4 y
pH 9. En una realización adicional, el tampón de lisis comprende desoxicolato de sodio a una concentración de entre el 0,05 % y el 0,09 %, CHAPS a una concentración de entre el 0,05 % y el 0,09 %, EDTA a una concentración de entre 1,5 mM y 3 mM, y tampón Tris o Trizma, en donde el tampón Tris o Trizma mantiene el pH del tampón de lisis entre pH 6 y pH 8. En una realización adicional, el tampón de lisis comprende desoxicolato de sodio a una concentración de aproximadamente el 0,08 %, CHAPS a una concentración de aproximadamente el 0,08 %, EDTA a una concentración de aproximadamente 2 mM, y tampón Tris o Trizma, en donde el tampón Tris o Trizma mantiene el pH del tampón de lisis en alrededor de un pH 7,6.
En una realización, el tampón de lisis comprende una sal seleccionada del grupo que consiste en cloruro de sodio, cloruro de potasio, cloruro de magnesio, sulfato de sodio, sulfato de potasio, sulfato de magnesio, acetato de sodio, acetato de potasio, acetato de magnesio, fosfato de sodio, fosfato de potasio o fosfato de magnesio. Preferentemente, la sal es una sal de sodio o una sal de potasio. De manera adecuada, la sal es cloruro de sodio o cloruro de potasio. De manera adecuada, la sal está a una concentración de entre 20 mM y 300 mM, entre 150 mM y 300 mM, entre 100 mM y 200 mM, entre 150 mM y 250 mM, entre 175 mM y 275 mM, o alrededor de 200 mM. De manera adecuada, la sal comprende o consiste en cloruro de sodio o cloruro de potasio. De manera adecuada, la sal está a una concentración de entre 20 mM y 300 mM, entre 150 mM y 300 mM, entre 100 mM y 200 mM, entre 150 mM y 250 mM, entre 175 mM y 275 mM, o alrededor de 200 mM. Preferentemente la sal es cloruro de sodio, por ejemplo, a una concentración entre 20 mM y 300 mM, entre 150 mM y 300 mM, entre 100 mM y 200 mM, o alrededor de 200 mM. Preferentemente, la sal comprende o consiste en cloruro de sodio, por ejemplo, a una concentración entre 20 mM y 300 mM, entre 150 mM y 300 mM, entre 100 mM y 200 mM, o alrededor de 200 mM.
En una realización, el tampón de lisis tiene una fuerza iónica de entre 1 mM y 500 mM, entre 50 mM y 450 mM, entre 100 mM y 250 mM, entre 100 mM y 175 mM, o entre 125 mM y 175 mM. Diversos componentes tampón pueden contribuir a esta fuerza iónica. Por ejemplo, el tampón de lisis puede comprender un componente tampón (tal como Tris) y un componente de sal adicional (tal como cloruro de sodio), y ambos componentes pueden contribuir a la fuerza iónica del tampón de lisis.
En una realización, el tampón de lisis comprende un estabilizador. Un "estabilizador" es un componente que reduce la degradación de las proteínas. Por ejemplo, un estabilizador reduce la degradación de Mcm5. Se puede analizar si un componente tampón estabiliza Mcm5 utilizando un ensayo de ELISA de tipo sándwich, tal como el ensayo descrito en el Ejemplo 1. Por ejemplo, una muestra puede exponerse a un tampón de lisis que comprenda el posible estabilizador y una muestra de control puede exponerse a un tampón de lisis que carezca del posible estabilizador. El nivel de Mcm5 que se puede detectar después de la exposición se mide utilizando ELISA de tipo sándwich. Si el nivel de Mcm5 en la muestra que tiene el tampón que comprende el posible estabilizador es mayor que el nivel de Mcm5 en la muestra que tiene el tampón que no comprende el posible estabilizador, entonces el posible estabilizador es un estabilizador. Un estabilizador puede impedir la degradación de Mcm5, de modo que el 1 %, 2 %, 5 %, 10 %, 20% o 25% más de Mcm5 esté presente después del almacenamiento en un tampón que comprenda un estabilizador durante 1 día, 3 días, 5 días, 1 semana o 2 semanas (en comparación con un tampón que no comprende el estabilizador).
El estabilizador puede ser un estabilizador seleccionado del grupo que consiste en seroalbúmina bovina (BSA), suero bovino fetal (SFB) y un inhibidor de proteasas. Por ejemplo, los inhibidores de proteasas incluyen clorhidrato de fluoruro de 4-(2-aminoetil)bencensulfonilo (Petrabloc s C o AEBSF), un cóctel de inhibidores de proteasas (tal como Sigma P8340) que comprende AEBSF, aprotinina, clorhidrato de bestatina, N-(trans-epoxisuccinil)-L-leucina 4-guanidinobutilamida (E-64), sal de hemisulfato de leupeptina y pepstatina A, e inhibidor de proteasas complete de Roche. Preferentemente, el estabilizador es BSA, por ejemplo, a una concentración de entre el 0,1 % y el 20 %, entre el 0,1 % y el 10 %, entre el 0,1 % y el 5 %, entre el 1 % y el 3 %, entre 2,2 % y el 2,7 % o alrededor del 2,5 %. Preferentemente, el estabilizador comprende o consiste en BSA, por ejemplo, a una concentración de entre el 0,1 % y el 20 %, entre el 0,1 % y el 10 %, entre el 0,1 % y el 5 %, entre el 1 % y el 3 %, entre 2,2 % y el 2,7 % o alrededor del 2,5 %.
El tampón de lisis puede comprender un agente antimicrobiano. Un componente es un "agente antimicrobiano" si reduce la replicación de microbios, por ejemplo bacterias, virus u hongos. El agente antimicrobiano puede ser azida de sodio o una isotiazolona. El agente antimicrobiano puede comprender o consistir en azida de sodio o una isotiazolona. La isotiazolona puede ser 2-metil-4-isotiazolin-3-ona y/o 5-cloro-2-metil-4-isotiazolin-3-ona. Preferentemente, el agente antimicrobiano comprende azida de sodio, por ejemplo, a una concentración de entre el 0,01 % y el 5 %, entre el 0,02 % y el 1,5 %, entre 0,07 % y el 0,12 % o alrededor del 0,09 %. Preferentemente, el agente antimicrobiano consiste en azida de sodio, por ejemplo, a una concentración de entre el 0,01 % y el 5 %, entre el 0,02 % y el 1,5 %, entre 0,07 % y el 0,12 % o alrededor del 0,09 %.
El tampón de lisis puede comprender:
(i) Tris entre 1 mM y 500 mM;
(ii) cloruro de sodio entre 5 mM y 500 mM;
(iii) BSA entre el 0,1 % y el 20 %;
(iv) Tritón X-100 entre el 0,001 % y el 10 %; y
(v) azida de sodio entre el 0,001 % y el 1 %.
El tampón de lisis puede consistir en:
(i) Tris entre 1 mM y 500 mM;
(ii) cloruro de sodio entre 5 mM y 500 mM;
(iii) BSA entre el 0,1 % y el 20 %;
(iv) Tritón X-100 entre el 0,001 % y el 10 %; y
(v) azida de sodio entre el 0,001 % y el 1 %.
Como alternativa, el tampón de lisis puede comprender:
(i) Tris entre 1 mM y 150 mM;
(ii) cloruro de sodio entre 50 mM y 400 mM;
(iii) BSA entre el 0,5 % y el 10 %;
(iv) Tritón X-100 entre el 0,01 % y el 5 %; y
(v) azida de sodio entre el 0,01 % y el 0,5 %.
Como alternativa, el tampón de lisis puede consistir en:
(i) Tris entre 1 mM y 150 mM;
(ii) cloruro de sodio entre 50 mM y 400 mM;
(iii) BSA entre el 0,5 % y el 10 %;
(iv) Tritón X-100 entre el 0,01 % y el 5 %; y
(v) azida de sodio entre el 0,01 % y el 0,5 %.
Como alternativa, el tampón de lisis puede comprender:
(i) Tris entre 1 mM y 100 mM;
(ii) cloruro de sodio entre 100 mM y 300 mM;
(iii) BSA entre el 1 % y el 5 %;
(iv) Tritón X-100 entre el 0,01 % y el 1 %; y
(v) azida de sodio entre el 0,01 % y el 0,1 %.
Como alternativa, el tampón de lisis puede consistir en:
(i) Tris entre 1 mM y 100 mM;
(ii) cloruro de sodio entre 100 mM y 300 mM;
(iii) BSA entre el 1 % y el 5 %;
(iv) Tritón X-100 entre el 0,01 % y el 1 %; y
(v) azida de sodio entre el 0,01 % y el 0,1 %.
El tampón de lisis puede comprender:
(i) Tris a alrededor de 10 mM;
(ii) cloruro de sodio a alrededor de 200 mM;
(iii) BSA a alrededor del 2,5 %;
(iv) T ritón X-100 a alrededor del 0,1 %; y
(v) azida de sodio a alrededor del 0,09 %.
El tampón de lisis puede consistir en:
(i) Tris a alrededor de 10 mM;
(ii) cloruro de sodio a alrededor de 200 mM;
(iii) BSA a alrededor del 2,5 %;
(iv) T ritón X-100 a alrededor del 0,1 %; y
(v) azida de sodio a alrededor del 0,09 %.
El tampón de lisis puede ser tampón RIPA.
En una realización, el tampón de lisis de la invención se utiliza para liberar al menos un biomarcador de las células en una muestra de orina, en donde el al menos un biomarcador es una proteína Mcm, preferentemente Mcm5. Kits
En el presente documento se describe un kit que comprende un tampón de lisis, un anticuerpo de captura y un
anticuerpo de detección, en donde el anticuerpo de captura y el anticuerpo de detección se unen a Mcm5. El kit se puede utilizar como parte de un ensayo (por ejemplo, un ensayo de ELISA) para determinar la concentración de Mcm5 en una muestra. El tampón de lisis puede liberar Mcm5 de las células de la muestra. El anticuerpo de captura y el anticuerpo de detección pueden utilizarse para cuantificar la concentración de Mcm5 en la muestra.
Anticuerpo de captura y anticuerpo de detección
Un "anticuerpo de captura" es un anticuerpo unido a la superficie de un soporte sólido, por ejemplo, una placa de ELISA, también conocida como placa de microtitulación. El "anticuerpo de captura" es capaz de unirse a Mcm5, uniendo así a la Mcm5 al soporte sólido. En una realización, se inmoviliza un "anticuerpo de captura" en una placa de ELISA.
Un "anticuerpo de detección" es un anticuerpo que se une a una diana, tal como Mcm5, y que puede utilizarse para detectar la concentración de la diana. Por ejemplo, el anticuerpo puede marcarse directa o indirectamente mediante un marcador detectable. Alternativamente, el "anticuerpo de detección" puede marcarse poniendo en contacto el anticuerpo de detección con un tercer anticuerpo específico para la región Fc del "anticuerpo de detección", en cuyo caso el tercer anticuerpo debe llevar un marcador. Los ejemplos de etiquetas adecuadas incluyen enzimas (tales como peroxidasa de rábano picante, fosfatasa alcalina o glucosa oxidasa), isotipos radiactivos (tales como Europio2+), indicadores de ADN, indicadores fluorogénicos o etiquetas electroquimioluminiscentes. En una realización preferente, el "anticuerpo de detección" está marcado mediante conjugación con peroxidasa de rábano picante.
Anticuerpos
El término "anticuerpo" puede referirse a formas de origen natural o a anticuerpos recombinantes, tales como los anticuerpos monocatenarios, los anticuerpos quiméricos o los anticuerpos humanizados. Puede considerarse que los términos "anticuerpo" y "anticuerpos" también abarcan fragmentos de anticuerpos que pueden unirse a una proteína diana, tal como una proteína Mcm como Mcm5. Dichos fragmentos pueden incluir un Fab'2, un F'(ab)2, Fv, anticuerpos monocatenarios o diacuerpos. Los anticuerpos descritos en el presente documento pueden ser de origen natural, anticuerpos de longitud completa (en lugar de fragmentos). Los anticuerpos preferentes adicionales no son anticuerpos humanizados.
En general, los anticuerpos están formados por dos cadenas pesadas y dos cadenas ligeras. Cada cadena pesada está compuesta por una región constante de la cadena pesada (CH) y una región variable de la cadena pesada (VH). De forma similar, cada cadena ligera está compuesta por una región constante de la cadena ligera (CL) y una región variable de la cadena ligera (VL). Las regiones VH y VL comprenden regiones que definen la complementariedad (las CDR). Las CDR principalmente son responsables de la unión específica a la proteína diana. Adicionalmente, un anticuerpo descrito en el presente documento se unirá a un epítopo (fragmento) de Mcm5. Por lo tanto, la expresión "anticuerpo que se une a Mcm5" se refiere a un anticuerpo que se une a un único epítopo de Mcm5. Opcionalmente, un anticuerpo que se une a Mcm5 es un anticuerpo que "se une específicamente" a Mcm5. La expresión "se une específicamente" se refiere a un anticuerpo que se une a una diana, tal como Mcm5, con una afinidad de unión que es al menos 2 veces, 10 veces, 50 veces o 100 veces superior que su afinidad de unión por una molécula no diana.
Un anticuerpo de detección puede conjugarse con un marcador (por ejemplo, Europio2* o peroxidasa de rábano picante). El marcador puede unirse directamente o puede unirse a través de un enlazador (tal como ácido adípico dihidrazida o ADH).
El marcador se puede unir por conjugación química. Se conocen en la técnica métodos de conjugación de marcadores con anticuerpos. Por ejemplo, carbodiimida conjugada (Bauminger y Wilchek (1980) Methods Enzymol.
70, 151-159) se pueden usar para conjugar marcadores a anticuerpos. Además, se pueden usar otros métodos para conjugar un marcador con un anticuerpo. Por ejemplo, se puede usar la oxidación con peryodato de sodio seguida de alquilación reductora o de amidación de reducción de reactivos apropiados, al igual que la reticulación con glutaraldehído. Sin embargo, se reconoce que, independientemente de qué método de producción de un conjugado de la invención se seleccione, debe hacerse una determinación de que el anticuerpo conjugado mantiene su capacidad de direccionamiento y de que el marcador conjugado mantiene su función.
El anticuerpo de detección puede marcarse por conjugación con Europio. Esto se puede lograr utilizando un kit de marcaje con Eu DELFIA(R) de EG&G Wallac y siguiendo el protocolo del fabricante.
Está dentro de las competencias del experto en la materia desarrollar un anticuerpo que se una a Mcm5. Esto se puede realizar inmunizando a un mamífero, tal como un ratón, conejo o cobaya, con Mcm5. Puede ser beneficioso incluir un adyuvante, tal como el adyuvante completo de Freund. Las células del bazo del mamífero inmunizado se retiran y se fusionan con células de mieloma para formar líneas de hibridoma que son inmortales dadas las condiciones apropiadas y que secretan anticuerpos. Los hibridomas se separan en clones individuales y los
anticuerpos secretados por cada clon se evalúan en cuanto a su capacidad de unión a la proteína Mcm5.
Componentes adicionales del kit
El kit puede comprender un calibrador. El "calibrador" es una preparación de una o más concentraciones conocidas de Mcm5.
El kit puede comprender un reactivo de sustrato. Se puede utilizar un reactivo de sustrato para detectar el anticuerpo de detección. Por ejemplo, cuando el "anticuerpo de detección" está conjugado con peroxidasa de rábano picante, el reactivo de sustrato puede comprender TMB (3, 3', 5,5'-tetrametilbencidina), DAB (3,3'-diaminobencidina) o ABTS (ácido 2,2'-azino-bis(3-etilbenzotiazolin-6-sulfónico). El reactivo de sustrato puede comprender TMB. El reactivo de sustrato puede ser peróxido y TMB. El kit puede comprender además una solución de lavado y/o una solución de parada. El kit puede ser adecuado para realizar un ELISA de tipo sándwich.
Métodos para la detección de la presencia de un cáncer urológico en un sujeto
La presente divulgación también proporciona métodos para la detección de la presencia de un cáncer urológico en un sujeto. Dichos métodos son, preferentemente, métodos in vitro. Dichos métodos incluyen una etapa de "realización de un ensayo para determinar la concentración" de al menos un biomarcador.
Realización de un ensayo para determinar la concentración de un biomarcador (tal como una proteína Mcm) En una realización de la invención, la expresión "detectar la presencia de un biomarcador" puede considerarse como sustituible por la expresión "realizar un ensayo para determinar la concentración" de un biomarcador. En tales realizaciones, la presencia de un biomarcador puede considerarse detectada, cuando su concentración es más alta que un valor de corte definido.
Los marcadores biológicos, o biomarcadores, son moléculas que se encuentran en la sangre u otros líquidos o tejidos corporales que ayudan a indicar un estado, proceso, suceso biológico, afección o enfermedad. Los expertos en la materia tendrán claro que los biomarcadores podrían consistir en, pero sin limitación, ADN, ARN, anomalías cromosómicas, proteínas y sus derivados, o metabolitos. En términos generales, un biomarcador puede considerarse como un indicador distintivo, biológico u obtenido biológicamente, de un proceso, suceso o afección. En otras palabras, un biomarcador es indicativo de determinado estado biológico, tal como la presencia de tejido canceroso. En algunos casos, distintas formas de biomarcadores pueden ser indicativas de determinadas patologías. Alternativamente, la mera presencia de niveles elevados (o reducidos) del biomarcador (o biomarcadores) en los líquidos corporales tales como la sangre y/o la orina son indicativos de cáncer urológico. Los biomarcadores pueden ser proteínas o péptidos específicos cuya presencia, sobreexpresión o subexpresión en líquidos biológicos tales como la orina (incluido el sedimento urinario), sangre, saliva o semen, puede reflejar la existencia, progresión, respuesta al tratamiento o gravedad de un cáncer urológico, tal como el cáncer de próstata. Por lo tanto, el término "biomarcador' incluye todas las formas biológicamente importantes de la proteína o ácido nucleico identificado, incluyendo polipéptidos modificados postraduccionalmente. Por ejemplo, cuando el biomarcador es un polipéptido, la proteína marcadora puede estar presente en la muestra en una forma glucosilada, fosforilada, multimérica o precursora.
No existe un requisito particular de que se califique la concentración de, por ejemplo, el polipéptido de longitud completa (o ácido nucleico). De hecho, es posible que la detección pueda tener lugar sometiendo a ensayo fragmentos particulares de un polipéptido de interés presentes, que se toman así para indicar la presencia del polipéptido biomarcador global en la muestra. Esto es especialmente cierto si las muestras se analizan, por ejemplo, mediante espectrometría de masas. Por lo tanto, la invención abarca la detección de fragmentos de los biomarcadores polipeptídicos (o de ácido nucleico). Además, los kits y péptidos pueden comprender fragmentos de los polipéptidos y no necesitan comprender las secuencias de longitud completa ejemplificadas en el presente documento. De manera adecuada, el fragmento es lo suficientemente largo como para permitir su identificación exclusiva mediante métodos de espectrometría de masas o inmunológicos.
Por lo tanto, para polipéptidos, un fragmento es, de manera adecuada, de al menos 6 aminoácidos de longitud, de manera adecuada, de al menos 7 aminoácidos de longitud, de manera adecuada, de al menos 8 aminoácidos de longitud, de manera adecuada, de al menos 9 aminoácidos de longitud, de manera adecuada, de al menos 10 aminoácidos de longitud, de manera adecuada, de al menos 15 aminoácidos, de manera adecuada, de al menos 25 aminoácidos, de manera adecuada, de al menos 50 aminoácidos, de manera adecuada, de al menos 100 aminoácidos, o de manera adecuada, la mayoría del polipéptido biomarcador de interés. De manera adecuada, un fragmento comprende un pequeño fragmento del polipéptido biomarcador de interés, mientras que lo suficientemente largo como para conservar una secuencia o masa de aminoácidos identificable.
Las mismas consideraciones se aplican a las secuencias de nucleótidos de ácido nucleico. Para secuencias de ácido nucleico, un fragmento es, de manera adecuada, de al menos 15 nucleótidos de longitud, de manera
adecuada, de al menos 30 nucleótidos de longitud, de manera adecuada, de al menos 50 nucleótidos de longitud, de manera adecuada, de al menos 80 nucleótidos de longitud, de manera adecuada, de al menos 100 nucleótidos de longitud, de manera adecuada, de al menos 200 nucleótidos de longitud o, de manera adecuada, la mayoría de la secuencia de interés.
Homología/identidad de secuencia
Aunque la homología de secuencia también puede considerarse en términos de similitud funcional (es decir, restos de aminoácido que tienen propiedades/funciones químicas similares), en el contexto del presente documento, se prefiere expresar la homología en términos de identidad de secuencia. Las comparaciones de secuencias se pueden realizar a simple vista o, más habitualmente, con la ayuda de programas de comparación de secuencias fácilmente disponibles. Estos programas informáticos disponibles pública y comercialmente pueden calcular el porcentaje de homología (tal como el porcentaje de identidad) entre dos o más secuencias.
El porcentaje de identidad se puede calcular sobre secuencias contiguas, es decir, una secuencia se alinea con la otra secuencia y cada aminoácido en una secuencia se compara directamente con el correspondiente aminoácido en la otra secuencia, un resto cada vez. Esto se llama un alineamiento "sin huecos". Normalmente, tales alineamientos sin huecos se realizan solo en un número relativamente corto de restos (por ejemplo, menos de 50 aminoácidos contiguos). Para comparar sobre secuencias más largas, la puntuación de huecos se utiliza para producir un alineamiento óptimo para reflejar con precisión los niveles de identidad en secuencias relacionadas que tienen una inserción (o inserciones) o una eliminación (o eliminaciones) una con respecto a la otra. Un programa informático adecuado para llevar a cabo tal alineamiento es el paquete GCG Wisconsin Bestfit (University of Wisconsin, EE. UU.; Devereux et al., 1984, Nucleic Acids Research 12:387). Los ejemplos de otros programas informáticos que pueden realizar comparaciones de secuencias incluyen, pero sin limitación, el paquete BLAST, FASTA (Altschul et al., 1990, J. Mol. Biol. 215:403-410) y el paquete de herramientas de comparación Ge NEWORKS.
En el contexto del presente documento, se considera que una secuencia de aminoácidos homóloga incluye una secuencia de aminoácidos que es al menos el 40, 50, 60, 70, 80 o 90 % idéntica. De forma muy adecuada, un polipéptido que tiene al menos el 90 % de identidad de secuencia con el biomarcador de interés se tomará como indicativo de la presencia de ese biomarcador; de manera más adecuada, se tomará que un polipéptido que es el 95 % o de forma más adecuada el 98 % idéntico al nivel de aminoácidos indica la presencia de ese biomarcador. De manera adecuada, dicha comparación se realiza sobre al menos la longitud del polipéptido o fragmento que se está sometiendo a ensayo para determinar la presencia o ausencia del biomarcador de interés. De forma muy adecuada, la comparación se realiza a lo largo de la longitud completa del polipéptido de interés.
Los biomarcadores específicos pueden detectarse y/o cuantificarse por interacción con un ligando o ligandos, sistemas de análisis basados en geles bidimensionales o unidimensionales, cromatografía líquida, cromatografía líquida combinada y cualquier técnica de espectrometría de masas, incluido MSMS, ICAT(R) o iTRAQ(R), ensayos de aglutinación, cromatografía de capa fina, espectroscopia de RMN, inmunoensayos de tipo sándwich, ensayos inmunoabsorbentes ligados a enzima (los ELISA), radioinmunoensayos (RAI), inmunoensayos enzimáticos (IEE), pruebas en tiras de flujo lateral/inmunocromatográficas, transferencia de Western, inmunoprecipitación, inmunoensayos basados en partículas que incluyen el uso de partículas de oro, plata o látex y partículas magnéticas, o puntos cuánticos, o cualquier otra técnica adecuada conocida en la técnica.
La concentración de un biomarcador tal como Mcm5 puede detectarse y/o cuantificarse mediante la interacción con un ligando o ligandos, sistemas de análisis basados en geles bidimensionales o unidimensionales, cromatografía líquida, cromatografía líquida combinada y cualquier técnica de espectrometría de masas, incluido MSMS, ICAT(R) o iTRAQ(R), ensayos de aglutinación, cromatografía de capa fina, espectroscopia de RMN, inmunoensayos de tipo sándwich, ensayos inmunoabsorbentes ligados a enzima (los ELISA), radioinmunoensayos (RAI), inmunoensayos enzimáticos (IEE), pruebas en tiras de flujo lateral/inmunocromatográficas, transferencia de Western, inmunoprecipitación, inmunoensayos basados en partículas que incluyen el uso de partículas de oro, plata o látex y partículas magnéticas, o puntos cuánticos, o cualquier otra técnica adecuada conocida en la técnica.
En determinados aspectos o realizaciones de la invención, el ensayo para determinar la concentración de un biomarcador no es un ensayo inmunofluorométrico. En tales realizaciones, el ensayo es preferentemente un ensayo de ELISA. En una realización adicional, el ensayo de ELISA es un ensayo de ELISA de tipo sándwich. Un ensayo de ELISA de tipo sándwich comprende las etapas de captura del biomarcador a analizar (tal como una proteína Mcm) utilizando un "anticuerpo de captura" ya unido a la placa y de detección de cuánto antígeno se ha capturado utilizando un "anticuerpo de detección". El anticuerpo de detección se ha preconjugado a un marcador tal como la enzima HRP (peroxidasa de rábano picante). Después, la placa de ELISA con el anticuerpo de detección marcado se lava para eliminar cualquier exceso de anticuerpo de detección no unido. Después, la placa lavada se expone a un agente cuyas propiedades son cambiadas por la etiqueta de manera medible. La concentración del anticuerpo de detección puede entonces determinarse. Por ejemplo, si el anticuerpo de detección está conjugado con (marcado con) peroxidasa de rábano picante, la placa de ELISA puede exponerse al sustrato TMB. La concentración del anticuerpo de detección y, por lo tanto, la concentración de Mcm5 en la muestra original, puede determinarse entonces cuantificando el cambio de color correspondiente a la conversión del TMB en un producto coloreado.
La presente invención comprende las etapas de realización de un ensayo para determinar la concentración de al menos un biomarcador en la muestra de orina. En una realización preferente, el al menos un biomarcador comprende una proteína Mcm, opcionalmente Mcm5. En una realización adicional, un valor anómalo para la concentración de Mcm5 indica una probabilidad aumentada de un cáncer urológico en el sujeto.
Cánceres urológicos
La divulgación también proporciona métodos para la detección de un cáncer urológico. Dichos métodos ofrecen una ventaja significativa ya que detectarán cualquier tumor que esté en contacto íntimo con el flujo o la orina en el aparato urinario (es decir, riñones, uréteres, vejiga y uretra) del paciente que se analiza.
El cáncer urológico incluye todos los tipos de carcinoma de células de transición que pueden surgir en el aparato urinario. Un ejemplo de carcinoma de células de transición es el cáncer de vejiga. Sin embargo, las células de transición están presentes en todo el aparato urinario, incluido el revestimiento de la pelvis renal, los uréteres que conducen la orina desde los riñones hasta la vejiga y la uretra, así como la pared de la vejiga misma. El carcinoma de células de transición puede surgir en cualquiera de estos lugares. Cabe señalar que existe una variedad de distintos subtipos de cáncer de vejiga, es decir, hay otros tipos de cáncer de vejiga además del carcinoma de células de transición, aunque este (carcinoma de células de transición) es el tipo más común de cáncer de vejiga.
Una ventaja de los métodos de la invención es que también se pueden detectar otros cánceres primarios tales como el cáncer de pene, por ejemplo, si afectan al tracto uretral a medida que pasa a través del pene.
Además, determinados tumores urológicos pueden detectarse aunque no estén en contacto directo con el flujo de orina. Un ejemplo es un tumor de próstata que normalmente no está en contacto con el flujo de orina, pero del que se desprenden y exudan células hacia la uretra.
Los métodos de la invención también ofrecen la ventaja de ser capaces de detectar cánceres metastásicos, por ejemplo, metástasis de un cáncer primario distinto cuya metástasis se ha establecido en el aparato urinario. Los métodos de la invención son capaces de detectar cualquier cáncer que crezca en el aparato urinario (por ejemplo, un cáncer de colon que puede haber invadido localmente) o cualquier cáncer que haya invadido a través de una metástasis (por ejemplo, un cáncer primario distante, que ha dado lugar a uno o más tumores metastásicos dentro del aparato urinario del sujeto).
Los métodos de la invención también se pueden aplicar ventajosamente a la detección del cáncer de próstata. En una realización, la invención se aplica ventajosamente a la detección del cáncer de vejiga.
En una realización, la invención se aplica a la detección del cáncer de próstata y de vejiga.
Proteínas de mantenimiento de minicromosomas (las Mcm)
Las proteínas de mantenimiento de minicromosomas (MCM; forma siglada de minichromosome maintenance) se han utilizado anteriormente como biomarcadores de diagnóstico para el cáncer de cuello de uterino. El biomarcador de acuerdo con la presente invención es una proteína Mcm. De forma muy adecuada, la proteína Mcm es Mcm5.
Los niveles elevados de una proteína de la familia del complejo de mantenimiento de minicromosomas (MCM), tal como la proteína nuclear Mcm5, se pueden utilizar para detectar células del cáncer de vejiga en sedimentos de orina así como cáncer de próstata. La evaluación de Mcm5 a menudo se lleva a cabo en un laboratorio especializado con instrumentación sofisticada y operarios altamente cualificados (Stoeber et al. JNCI. 2002: 94: 1071-1079) y este estilo de análisis puede ser costoso o poco práctico de llevar a cabo en las en el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato. Sin embargo, es una ventaja que los inventores de la presente solicitud hayan logrado desarrollar un formato de ELISA tipo sándwich de doble de anticuerpo modificado utilizando una pareja de anticuerpos monoclonales específicos que son adecuados para el laboratorio de anatomía patológica o en aplicaciones en análisis de diagnóstico inmediato, para medir con precisión los niveles de Mcm5 en sedimentos urinarios. Sin embargo, este tipo de ensayo preferente no limita el análisis de Mcm5 a este modo de acuerdo con la invención, Mcm5 puede someterse a ensayo de acuerdo con cualquier método adecuado conocido en la técnica.
Las proteínas MCM 2 - 7 comprenden parte de los complejos de prerreplicación que se forman en la cromatina y que son prerrequisitos esenciales o factores permisivos, para la posterior replicación del ADN. Los complejos de proteínas MCM actúan como helicasas replicativas y, por lo tanto, son componentes centrales de la maquinaria de replicación del ADN. Las MCM están reguladas al alza en la transición de la fase G0 a G1/S del ciclo celular y participan activamente en la regulación del ciclo celular. Las proteínas MCM forman una estructura anular alrededor de la cromatina.
El gen de Mcm5 humana mapea en 22q 13.1 y la proteína Mcm5 madura consiste en 734 aminoácidos (SEQ ID NO: 1; Figura 1: UNIPROT P33992: factor permisivo de replicación de ADN HUMANO MCM5). El término "Mcm5" se refiere a un polipéptido de la SEQ ID nO: 1, un polipéptido con el 85 %, 90 %, 95 %, 98 % o 100 % de identidad con la SEQ ID NO: 1.
La presente invención proporciona de manera útil nuevos métodos de ensayo para Mcm5, que son adecuados para el uso general en el laboratorio clínico y en aplicaciones en análisis de diagnóstico inmediato.
Mcm5 se registra como una concentración en orina. Cuando la concentración supera un punto de corte, hay una mayor probabilidad de cáncer urológico. El punto de corte se puede establecer de varias maneras distintas. Por ejemplo, se puede establecer en la media de los valores de la orina de pacientes sanos más un múltiplo de la desviación típica de los valores en la población sana, por lo general, un múltiplo de dos o tres veces. Alternativamente, el punto de corte puede establecerse como el valor generado por una concentración conocida de células en división que expresan Mcm5, ejemplificado por Stoeber et al (2002), quienes adoptaron como punto de corte el número de recuentos en DELFIA generados a partir de muestras que contenían 1500 células en replicación por pocillo de una placa.
Por lo tanto, una presencia de Mcm5 superior que la media más dos desviaciones típicas de la concentración en la orina de pacientes sanos, o la presencia de Mcm5 en recuentos mayores que el número de recuentos en DELFIA generados a partir de muestras que contienen 1500 células en replicación por pocillo de una placa, indica una probabilidad aumentada de cáncer urológico.
En una realización, un valor anómalo para la presencia de la proteína Mcm indica una probabilidad aumentada de un cáncer urológico en un sujeto. Un método descrito en el presente documento puede comprender una etapa para diagnosticar que un paciente tiene un cáncer urológico, cuando la concentración de la proteína Mcm determinada mediante la realización de un ensayo es superior que el valor medio de pacientes sanos más un múltiplo de la desviación típica mostrada por los valores obtenidos de sujetos sanos.
Anticuerpos
Se encuentran disponibles en el mercado varios anticuerpos anti Mcm5 adecuados para su uso en la invención. Los ejemplos se muestran a continuación:
Muestra
Los métodos descritos en el presente documento pueden comprender una etapa de "proporcionar una muestra de un sujeto". Preferentemente, esta etapa es no invasiva (no quirúrgica), por ejemplo, recolección de orina. La muestra puede comprender cualquier líquido biológico tal como sangre, suero, saliva, semen, orina o sedimento de orina, o un extracto preparado a partir de uno de tales líquidos. La muestra es, de manera adecuada, orina.
Mcm5 se encuentra normalmente en los núcleos de las células presentes en la orina. Por lo tanto, de manera adecuada, la muestra comprende células dentro de la orina. De manera más adecuada, esas células pueden concentrarse mediante cualquier técnica conocida común en la técnica, tal como la filtración o de forma más adecuada la recolección centrífuga de las células de la orina. Enriquecer las células de la orina puede aumentar la señal y puede facilitar la detección.
Cuando se analiza el cáncer de próstata, de forma muy adecuada la muestra es orina del primer chorro, como se puede obtener después del masaje de la próstata (cuando el sujeto es hombre). De manera aún más adecuada, la muestra puede comprender los primeros pocos mililitros de orina del primer chorro. En otras palabras, de manera adecuada, la muestra puede comprender la primera parte del chorro de orina, de manera adecuada, la primera parte del chorro de orina producida después del masaje de la próstata. De manera aún más adecuada, la muestra puede comprender sedimento de orina, tal como células sedimentadas recogidas de la orina (tal como de la orina total, o la orina del primer chorro, como se explicó anteriormente).
Formatos de ensayo
En el presente documento se describe un sistema de ensayo para determinar la presencia y/o concentración de
biomarcadores mediante la detección de la unión entre biomarcadores y anticuerpos específicos en un ELISA de tipo sándwich o un ELISA de dos sitios. Los biomarcadores pueden determinarse por separado (por ejemplo, en ensayos físicamente separados, realizados de manera adecuada en fracciones de la misma muestra). En cada ensayo, la muestra puede ponerse en contacto con un solo ligando, tal como un anticuerpo específico para el biomarcador a analizar. Por ejemplo, la muestra se puede añadir a distintos pocillos de una placa de microtitulación, en donde cada pocillo contiene un anticuerpo distinto.
De manera adecuada, la determinación se lleva a cabo en una solución acuosa. La muestra y/o el ligando (por ejemplo, el anticuerpo) pueden estar presentes en solución. En algunas realizaciones, el anticuerpo o la muestra puede inmovilizarse sobre un soporte sólido. Normalmente, tal soporte puede comprender la superficie del recipiente en el que se realiza la determinación, tal como la superficie de un pocillo de una placa de microtitulación. El soporte puede ser una membrana (por ejemplo, una membrana de nitrocelulosa o nylon) o una perla (por ejemplo, de látex u oro), o la superficie de una matriz.
La determinación de si el anticuerpo se une (detecta) un biomarcador en la muestra puede realizarse mediante cualquier método conocido en la técnica para detección de la unión entre dos fracciones. La unión puede determinarse midiendo una característica en el anticuerpo o biomarcador (tal como la proteína) que cambia cuando se produce la unión, tal como un cambio espectroscópico.
La determinación puede llevarse a cabo utilizando un anticuerpo como ligando, anticuerpo que está inmovilizado en un soporte sólido. Cuando la muestra se pone en contacto con el anticuerpo, las moléculas de biomarcadores (tales como las moléculas de proteínas) de la muestra se unen al anticuerpo.
Opcionalmente, la superficie del soporte sólido se lava a continuación, para eliminar cualquier biomarcador (tal como proteína) de la muestra que no esté unido al anticuerpo. A continuación se puede determinar la presencia del biomarcador unido al soporte sólido (a través de la unión con el anticuerpo), lo que indica que la proteína está unida al anticuerpo. Esto se puede hacer, por ejemplo, poniendo en contacto el soporte sólido (que puede o no tener un biomarcador unido a él) con un agente que se une específicamente a la proteína. Este agente puede estar marcado, ya sea directa o indirectamente, mediante un marcador detectable. Normalmente, el agente es un segundo anticuerpo, que es capaz de unirse al biomarcador de una manera específica mientras el biomarcador se encuentra unido al primer anticuerpo inmovilizado. Este segundo anticuerpo puede marcarse indirectamente poniéndolo en contacto con un tercer anticuerpo específico para la región Fc del segundo anticuerpo, en donde el tercer anticuerpo porta un marcador detectable.
Otro sistema que puede utilizarse para determinar la unión entre la proteína biomarcadora y el anticuerpo es un sistema de unión competitiva. Dicho sistema puede determinar si el biomarcador en la muestra es capaz de inhibir la unión del anticuerpo a un compuesto de referencia que es capaz de unirse al anticuerpo. Si la proteína biomarcadora en la muestra puede inhibir la unión entre el anticuerpo y el compuesto de referencia, entonces esto indica que tal muestra contiene el biomarcador reconocido por el anticuerpo.
Patrón de referencia
Patrón de referencia normalmente se refiere a una muestra de un individuo sano, es decir, uno que no ha padecido un cáncer urológico.
El patrón de referencia puede ser una muestra real analizada en paralelo. Alternativamente, el patrón de referencia puede ser uno o más valores obtenidos previamente de una muestra comparativa, por ejemplo, una muestra de un sujeto sano. En tales realizaciones, se puede hacer una mera comparación numérica comparando el valor determinado para la muestra del sujeto con el valor numérico de una muestra de referencia analizada previamente. La ventaja de esto es no tener que duplicar el análisis al determinar las concentraciones en muestras de referencia individuales en paralelo cada vez que se analiza una muestra de un sujeto.
De manera adecuada, el patrón de referencia coincide con el sujeto analizada, por ejemplo, en género, por ejemplo, en edad, por ejemplo, en origen étnico u otros criterios de este tipo que son bien conocidos en la técnica. El patrón de referencia puede ser un número tal como una concentración absoluta determinada por uno o más estudios anteriores.
Los patrones de referencia pueden coincidir de manera adecuada a subgrupos específicos de pacientes, por ejemplo, ancianos, o los que tienen antecedentes importantes anteriores, tales como una predisposición al cáncer urológico.
De manera adecuada, el patrón de referencia coincide con el tipo de muestra analizada. Por ejemplo, la concentración del polipéptido biomarcador (o polipéptidos biomarcadores) analizado puede variar del tipo o la naturaleza de la muestra (por ejemplo, muestra de orina convencional frente a una muestra del primer chorro después de un masaje prostático). Será inmediatamente obvio para el experto en la materia que el valor de concentración (o valores de concentración) para el patrón de referencia deben ser para la misma muestra o una
muestra comparable a la analizada en el método (o métodos) de la invención. Por ejemplo, si la muestra sometida a ensayo es orina del primer chorro, entonces el valor del patrón de referencia debe ser para la orina del primer chorro, para asegurar que se pueda realizar una comparación cruzada significativa. En particular, se debe tener extremo cuidado si se intentan inferencias por la comparación entre las concentraciones determinadas para un sujeto de interés y las concentraciones determinadas para los patrones de referencia, en que la naturaleza de la muestra no es idéntica para los dos casos. De manera adecuada, el tipo de muestra para el patrón de referencia y el tipo de muestra para el sujeto de interés son los mismos.
Cabe señalar que las concentraciones de proteína determinadas pueden compararse con una muestra anterior del mismo sujeto. Esto puede ser beneficioso para controlar la posibilidad de recaída en un sujeto. Esto puede ser beneficioso para controlar el curso y/o eficacia de un tratamiento de un sujeto. El método puede comprender una etapa (o etapas) adicional de comparación del valor (o valores) determinado para la muestra de interés con uno o más valores determinados para el mismo biomarcador (o biomarcadores) de distintas muestras, tales como muestras tomadas en distintos puntos de tiempo para el mismo sujeto. Al hacer tal comparación, se puede recopilar información sobre si un marcador en particular está aumentando o disminuyendo en un sujeto en particular. Esta información puede ser útil para diagnosticar o predecir cambios a lo largo del tiempo, o los cambios inhibidos o estimulados por un tratamiento particular o un régimen de terapia, o cualquier otra variable de interés.
De esta manera, los métodos se pueden utilizar para determinar si, por ejemplo, después del tratamiento del paciente con un fármaco o fármaco candidato, o mediante resección de un tumor, la enfermedad ha progresado o no, o que la tasa de progresión de la enfermedad se ha modificado. El resultado puede informar sobre el curso del tratamiento adicional.
Ligandos/Anticuerpos
Los modos preferidos para determinar la presencia y/o concentración de los biomarcadores que se analizan en el presente documento hacen uso de moléculas o ligandos de unión a antígeno adecuados, que se unen específicamente a los biomarcadores seleccionados. De manera adecuada, el ligando puede ser un anticuerpo, o un derivado de anticuerpo tal como un scFv o Fab.
Método para la preparación de células a partir de una muestra de orina
La invención proporciona un método para la preparación de células a partir de una muestra de orina.
En dicho método se hace pasar una muestra de orina a través de un filtro para la captura de las células, de manera que se capturen las células de la muestra orina en el filtro. El volumen de orina que pasa a través del filtro es preferentemente de entre 1 ml y 100 ml, más preferentemente de entre 30 ml y 70 ml, y aún más preferentemente de aproximadamente 50 ml.
Después, se hace pasar un tampón de lisis de la invención a través del filtro, de manera que las células estén expuestas al tampón de lisis. El tampón de lisis es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina. El tampón de lisis se hace pasar al menos una vez a través del filtro para exponer las células al tampón de lisis, de modo que la proteína Mcm se libere de las células. Puede ser necesario hacer pasar el tampón de lisis a través del filtro una pluralidad de veces, por ejemplo, al menos dos veces, al menos tres veces o al menos cuatro veces. Esto ayuda a saturar completamente el filtro con el tampón de lisis, para que el al menos un biomarcador se libere de forma más eficaz de las células capturadas. En el caso en que el tampón de lisis se pase una pluralidad de veces a través del filtro, preferentemente el tampón de lisis se hace pasar a través del filtro alternativamente aguas arriba y aguas abajo (es decir, en direcciones opuestas) para ayudar a saturar completamente el filtro con tampón de lisis. El volumen de tampón de lisis (es decir, el volumen de tampón de lisis que fluye a través del filtro en un pase) es preferentemente de entre 250 ml y 1000 ml, más preferentemente de entre 300 ml y 500 ml, y aún más preferentemente de aproximadamente 500 ml.
Después de la exposición de las células capturadas al tampón de lisis, el filtro se incuba a continuación durante un período de tiempo de forma que el tampón de lisis libera la proteína Mcm de las células, dando como resultado un tampón de lisis que comprende la proteína Mcm liberada de las células (lisado). El tiempo de incubación del filtro es preferentemente de entre 5 minutos y 1 hora, más preferentemente de entre 20 minutos y 30 minutos, e incluso más preferentemente de aproximadamente 10 minutos. De manera adecuada, "incubar el filtro" comprende mantener el tampón de lisis en contacto con el filtro durante un período de tiempo. De manera adecuada, se incuba un filtro a una temperatura bastante constante (que varíe en menos de 5 °C durante el período de incubación). Opcionalmente, la temperatura está entre 15 °C y 30 °C, preferentemente a alrededor de la temperatura ambiente. Opcionalmente, después de incubar el filtro, el tampón de lisis se hace pasar nuevamente a través del filtro al menos una vez.
Aparato para la preparación de células a partir de una muestra de orina
En el presente documento se describe un aparato para la preparación de células de una muestra de orina. En la descripción del aparato a continuación, las expresiones "aguas arriba" y "aguas abajo" se definen con respecto a la
dirección del flujo de orina a través del aparato, es decir, el flujo desde la entrada hasta la salida es flujo en una dirección aguas abajo. Que los componentes del aparato se describan como en "comunicación fluida" entre sí significa que un líquido puede fluir entre estos componentes, aunque es posible que no pueda seguir fluyendo (por ejemplo, en el caso de una válvula cerrada). Dichos componentes podrían conectarse a través de medios conocidos en la técnica, por ejemplo, un tubo o una tubería. Cada componente del aparato puede estar conectado de forma desmontable a otros componentes. Algunos o todos los componentes del aparato pueden estar formados de manera integrada.
La Figura 18 muestra una realización del aparato 100. El aparato 100 comprende una entrada 101 a través de la cual la orina de una muestra de orina puede pasar al aparato (desde la izquierda, como se representa) cuando está en uso. La entrada 101 comprende, opcionalmente, una válvula unidireccional (no mostrada) para impedir que el líquido vuelva a salir del aparato (es decir, aguas arriba de la entrada).
Una primera válvula 102 está dispuesta aguas abajo de la entrada 101 y está en comunicación fluida con la entrada 101. La primera válvula 102 no está limitada a un tipo de válvula particular, siempre que pueda configurarse para abrir o bloquear la comunicación fluida entre distintas partes del aparato según sea necesario. Dichas configuraciones se explicarán con más detalle a continuación. La primera válvula 102 es, opcionalmente, una válvula luer. La primera válvula 102 es, opcionalmente, una válvula de 3 vías o de 4 vías.
Un filtro 103 está dispuesto aguas abajo de la primera válvula 102 y está en comunicación fluida con la primera válvula 102. El filtro 103 es adecuado para la captura de células de la orina a medida que la orina fluye a través del filtro. El filtro 103 impide, preferentemente, que pasen partículas esféricas que tienen un diámetro mayor que 15 mm, 10 mm o 5 mm, mientras permite que pasen partículas más pequeñas. Para partículas no esféricas, el filtro 103 impide, preferentemente, que pasen partículas esféricas equivalentes que tengan un diámetro mayor que 15 mm, 10 mm o 5 mm, teniendo las partículas esféricas equivalentes el mismo volumen que las partículas no esféricas. El diámetro dv de tal partícula esférica equivalente viene dado por la ecuación dv = en que V es el volumen de la partícula no esférica. El filtro 103 tiene, opcionalmente, una estructura de poro con un tamaño de poro (diámetro de poro) de aproximadamente 15 mm, aproximadamente 10 mm o aproximadamente 5 mm. El filtro 103 tiene, preferentemente, una estructura de poro con un tamaño de poro (diámetro de poro) de entre 1 y 6 mm, más preferentemente de entre 4 y 6 mm, e incluso más preferentemente de aproximadamente 5 mm. Sin embargo, El tipo de filtro no está limitado, siempre que sea adecuado para la captura de células de la orina a medida que la orina fluye a través del filtro. El filtro 103 podría tener, opcionalmente, una estructura de malla en lugar de una estructura de poros, por ejemplo.
Una segunda válvula 104 está dispuesta aguas abajo del filtro 103 y está en comunicación fluida con el filtro 103. La segunda válvula 104 no está limitada a un tipo de válvula particular, siempre que pueda configurarse para abrir o bloquear la comunicación fluida entre distintas partes del aparato según sea necesario. Dichas configuraciones se explicarán con más detalle a continuación. La segunda válvula 104 es, opcionalmente, una válvula luer. La segunda válvula 104 es, opcionalmente, una válvula de 3 vías o de 4 vías.
Una salida 105 a través de la cual la orina puede fluir hacia afuera mientras el aparato está en uso está dispuesta aguas abajo de la segunda válvula 104 y está en comunicación fluida con la segunda válvula 104. La salida 105 comprende, opcionalmente, una válvula (no mostrada) para bloquear el paso hacia afuera del líquido a través de la salida 105 cuando sea necesario.
Se proporciona un primer depósito de tampón 106 para contener un tampón de lisis. El primer depósito de tampón 106 está en comunicación fluida con la primera válvula 102. El primer depósito de tampón 106 está dimensionado preferentemente para contener al menos 500 ml de tampón de lisis, más preferentemente al menos 1 ml de tampón de lisis, e incluso más preferentemente al menos 5 ml de tampón de lisis. El primer depósito de tampón 106 está opcionalmente dimensionado para contener un máximo de 50 ml de tampón de lisis, más preferentemente un máximo de 25 ml de tampón de lisis, e incluso más preferentemente un máximo de 10 ml de tampón de lisis. El primer depósito de tampón 106 es, opcionalmente, una jeringa, pero podría utilizarse cualquier recipiente adecuado para contener un tampón de lisis.
También se proporciona un segundo depósito de tampón 107 para contener un tampón de lisis. El segundo depósito de tampón 107 está en comunicación fluida con la segunda válvula 104. El segundo depósito de tampón 107 está dimensionado preferentemente para contener al menos 500 ml de tampón de lisis, más preferentemente al menos 1 ml de tampón de lisis, e incluso más preferentemente al menos 5 ml de tampón de lisis. El segundo depósito de tampón 107 está opcionalmente dimensionado para contener un máximo de 50 ml de tampón de lisis, más preferentemente un máximo de 25 ml de tampón de lisis, e incluso más preferentemente un máximo de 10 ml de tampón de lisis. El segundo depósito de tampón 107 es, opcionalmente, una jeringa, pero podría utilizarse cualquier recipiente adecuado para contener un tampón de lisis.
A continuación se describirán las configuraciones de las primera y segunda válvulas 102, 104.
En una primera configuración de las primera y segunda válvulas 102, 104, la comunicación fluida entre el primer depósito de tampón 106 y el filtro 103 está bloqueada, la comunicación fluida entre el segundo depósito de tampón 107 y el filtro 103 está bloqueada, y la comunicación fluida entre la entrada 101, el filtro 103 y la salida 105 está abierta. En esta primera configuración, la orina puede fluir desde la entrada 101 a la salida 105 a través del filtro 103 mientras el aparato está en uso. En la primera configuración, preferentemente, la orina no puede fluir desde la entrada 101 o la salida 105 al primer y/o segundo depósitos de tampón 106, 107. En la primera configuración, preferentemente, el tampón de lisis no puede fluir desde el primer depósito de tampón 106 a la entrada 101 o a la salida 105. En la primera configuración, preferentemente, el tampón de lisis no puede fluir desde el segundo depósito de tampón 107 a la entrada 101 o a la salida 105.
En una segunda configuración de las primera y segunda válvulas 102, 104, la comunicación fluida entre el primer depósito de tampón 106 y el filtro 103 está abierta, la comunicación fluida entre el segundo depósito de tampón 107 y el filtro 103 está abierta, y el flujo a través de la entrada 101 y la salida 105 está bloqueado. En esta segunda configuración, el tampón de lisis puede fluir entre el primer depósito de tampón 106 y el segundo depósito de tampón 107 a través del filtro 103 mientras el aparato está en uso. En la segunda configuración, preferentemente, el tampón de lisis no puede fluir desde el primer depósito de tampón 106 a la entrada 101 o a la salida 105. En la segunda configuración, preferentemente, el tampón de lisis no puede fluir desde el segundo depósito de tampón 107 a la salida 105 o a la entrada 101. En la segunda configuración, preferentemente, la orina no puede fluir entre la entrada 101 y la salida 105.
En la segunda configuración, se forma preferentemente un sistema cerrado entre el primer depósito de tampón 106, el filtro 103 y el segundo depósito de tampón 107. Por lo tanto, cuando un volumen de tampón de lisis fluye hacia afuera del primer depósito de tampón 106, un volumen igual de tampón de lisis fluye preferentemente hacia el segundo depósito de tampón 107, y viceversa. Por lo tanto, en un momento dado cuando el aparato está en uso, el tampón de lisis se proporciona en uno o ambos de los primero y segundo depósitos de tampón 106, 107. En otras palabras, en un momento dado cuando el aparato está en uso, (i) el tampón de lisis está presente en el primer depósito de tampón 106 pero no en el segundo depósito de tampón 107; (ii) el tampón de lisis está presente en el segundo depósito de tampón 107 pero no en el primer depósito de tampón 106; o (iii) el tampón de lisis está presente tanto en el primero como en el segundo depósitos de tampón 106, 107.
El aparato 100 comprende, opcionalmente, un depósito de orina 108 para contener orina. El depósito de orina 108 está dispuesto aguas abajo de la salida 105 y está en comunicación fluida con la salida 105. El depósito de orina 108 está dimensionado preferentemente para contener al menos 10 ml de orina, más preferentemente al menos 25 ml de orina, e incluso más preferentemente al menos 50 ml de orina. El depósito de orina 108 está dimensionado, opcionalmente, para contener un máximo de 1000 ml de orina, más preferentemente un máximo de 500 ml de orina, e incluso más preferentemente un máximo de 250 ml de orina. En la primera configuración de las primera y segunda válvulas 102, 104, la orina puede fluir desde la entrada 101 a través del depósito de orina 108 a través del filtro 103 y la salida 105. El depósito de orina 108 está configurado, por lo tanto, para retener la orina que se ha filtrado a través del filtro 103 mientras el aparato está en uso. La salida 105 puede bloquearse de forma reversible utilizando una válvula o medios de sellado (no mostrados) para impedir que la orina fluya desde el depósito de orina 108 de regreso a través de la salida 105 (es decir, en una dirección aguas arriba). El depósito de orina puede estar conectado de forma desmontable a la salida 105.
El aparato 100 comprende, opcionalmente, medios 110 para proporcionar un flujo de orina. Dichos medios pueden ser, por ejemplo, una bomba o parte de una jeringa. Cuando use una jeringa, la jeringa puede proporcionar tanto el depósito de orina 108 como los medios 110 para proporcionar un flujo de orina. En ese caso, se puede proporcionar un flujo de orina extrayendo la jeringa del depósito de orina 108, haciendo que la orina fluya desde la entrada 101 hacia el depósito de orina 108. Se puede proporcionar un flujo de orina "empujando" una muestra de orina a través del aparato desde la entrada 101, por ejemplo, utilizando una jeringa en comunicación fluida con la entrada 101.
El aparato 100 comprende, opcionalmente, medios 109 para proporcionar un flujo de tampón de lisis. Dichos medios pueden ser, por ejemplo, una bomba o parte de una jeringa. Cuando use una jeringa, la jeringa puede proporcionar tanto el depósito de tampón de lisis como los medios 109 para proporcionar un flujo de tampón de lisis. De manera similar, si el segundo depósito de tampón 107 es parte de una jeringa, el segundo depósito de tampón puede actuar como medio 109 para proporcionar un flujo de tampón de lisis. Si tanto el primero como el segundo depósito de tampón 106, 107 se proporcionan mediante jeringas, entonces ambos pueden actuar puede actuar como medios 109 para proporcionar un flujo de tampón de lisis.
En el presente documento también se describe un dispositivo para el análisis de una muestra de orina de un sujeto. El dispositivo comprende el aparato 100 descrito anteriormente y un dispositivo de ensayo capaz de determinar la concentración de al menos un biomarcador en la muestra de orina. El dispositivo de ensayo comprende preferentemente un primer anticuerpo que está inmovilizado y un segundo anticuerpo de detección. El dispositivo está dispuesto preferentemente de modo que el lisado pueda fluir por el anticuerpo inmovilizado (por ejemplo, por flujo lateral) y que el biomarcador pueda unirse al anticuerpo inmovilizado. La cantidad de biomarcador unido puede detectarse utilizando el anticuerpo de detección. El dispositivo de ensayo puede proporcionarse como un componente separado, no conectado al aparato 100, o puede formar parte integral o ser conectable al aparato 100,
para estar en comunicación fluida con el aparato 100. El dispositivo de ensayo está configurado preferentemente para recibir el lisado desde el aparato 100. En el caso de que el dispositivo de ensayo esté en comunicación fluida con el aparato 100, la primera y segunda válvulas pueden configurarse en una tercera configuración, de modo que el lisado pueda fluir desde el primer depósito de tampón 106 o desde el segundo depósito de tampón 107 al dispositivo de ensayo.
Por ejemplo, la primera válvula 102 está configurada para permitir el flujo desde el primer depósito de tampón 106 al dispositivo de ensayo. En este caso, preferentemente, la comunicación fluida entre el primer depósito de tampón 106 y segundo depósito de tampón 107 está bloqueada. La segunda válvula 104 puede configurarse para permitir el flujo desde el segundo depósito de tampón 107 al dispositivo de ensayo. En este caso, preferentemente, la comunicación fluida entre el primer depósito de tampón 106 y segundo depósito de tampón 107 está bloqueada.
La primera válvula 102 es un ejemplo de una primera disposición de válvula y la segunda válvula 104 es un ejemplo de una segunda disposición de válvula, que permiten controlar la trayectoria de los líquidos a través del aparato de acuerdo con las primera y segunda (y opcionalmente la tercera) configuraciones descritas anteriormente. Sin embargo, la primera disposición de válvula no se limita a una válvula. La primera disposición de válvula puede comprender una pluralidad de válvulas. Por ejemplo, en el caso de que la primera disposición de válvulas comprenda dos válvulas, una válvula podría estar dispuesta para abrir y bloquear la comunicación fluida entre la entrada 101 y el filtro 103, y la otra válvula podría estar dispuesta para abrir y bloquear la comunicación fluida entre el primer depósito de tampón 106 y el filtro 103. De manera similar, la segunda disposición de válvula no se limita a una válvula. La segunda disposición de válvula puede comprender una pluralidad de válvulas. Por ejemplo, en el caso de que la segunda disposición de válvulas comprenda dos válvulas, una válvula podría estar dispuesta para abrir y bloquear la comunicación fluida entre el filtro 103 y la salida 105, y la otra válvula podría estar dispuesta para abrir y bloquear la comunicación fluida entre el segundo depósito de tampón 107 y el filtro 103.
Método de uso del aparato
Además se describe en el presente documento un método de uso del aparato 100. Como anteriormente, las expresiones "aguas arriba" y "aguas abajo" se definen con respecto a la dirección del flujo de orina a través del aparato, es decir, el flujo desde la entrada hasta la salida es flujo en una dirección aguas abajo.
La orina de una muestra de orina fluye a través de la entrada 101 a la salida 105 a través del filtro 103, con la primera disposición de válvula (por ejemplo, la primera válvula 102) y la segunda disposición de válvula (por ejemplo, la segunda válvula 104) configuradas en la primera configuración. Esto ocasiona que se capturen en el filtro 103 las células de la orina, mientras que la orina filtrada pasa hacia afuera de la salida 105 y, opcionalmente, al depósito de orina 108. El flujo de orina se proporciona, opcionalmente, mediante medios 110 para proporcionar un flujo de orina. Después, un gas inerte (por ejemplo, aire) fluye preferentemente a través de la entrada 101 a la salida 105 para eliminar cualquier volumen residual de orina en el aparato. Esto se puede lograr utilizando los medios 108 para proporcionar un flujo de orina, por ejemplo, haciendo fluir un gas inerte desde la entrada a la salida. Como alternativa, se puede proporcionar un medio separado para proporcionar un flujo de gas inerte.
Después, preferentemente la salida 105 se bloquea o se sella para impedir que la orina pase de regreso a través de la salida en una dirección aguas arriba.
Las primera y segunda válvulas 102, 104 se configuran después en la segunda configuración, formando de este modo un sistema cerrado entre el primer depósito de tampón 106, el filtro 103 (que contiene las células) y el segundo depósito de tampón 107. El tampón de lisis contenido en el primer depósito de tampón 106 pasa después al segundo depósito de tampón 107 a través del filtro 103, o viceversa. El tampón de lisis se hace pasar al menos una vez a través del filtro 103 para exponer las células al tampón de lisis, de modo que el al menos un biomarcador se libere de las células. Puede ser necesario hacer pasar el tampón de lisis a través del filtro 103 una pluralidad de veces, por ejemplo, al menos dos veces, al menos tres veces o al menos cuatro veces. Esto ayuda a saturar completamente el filtro con el tampón de lisis, para que el al menos un biomarcador se libere de forma más eficaz de las células capturadas. En el caso en que el tampón de lisis se pase una pluralidad de veces a través del filtro, preferentemente el tampón de lisis se hace pasar a través del filtro alternativamente aguas arriba y aguas abajo (es decir, en direcciones opuestas) para ayudar a saturar completamente el filtro con tampón de lisis.
El filtro 103 se incuba después durante un período de tiempo de forma que el tampón de lisis ocasione que al menos un biomarcador se libere de las células. La incubación se lleva a cabo preferentemente durante un período de entre 10 segundos y 5 horas, más preferentemente de entre 30 segundos y 1 hora, e incluso más preferentemente de aproximadamente 10 minutos. De manera adecuada, "incubar el filtro" comprende mantener el tampón de lisis en contacto con el filtro durante un período de tiempo. De manera adecuada, se incuba un filtro a una temperatura bastante constante (que varíe en menos de 5 °C). Opcionalmente, la temperatura está entre 15 °C y 30 °C, preferentemente a alrededor de la temperatura ambiente. El tampón de lisis que contiene al menos un biomarcador liberado de las células (el lisado) se vuelve a hacer pasar después, opcionalmente, de regreso hacia uno de los primero y segundo depósitos de tampón 106, 107.
En el caso del dispositivo para analizar una muestra de orina de un sujeto que comprende el aparato 100 y el dispositivo de ensayo, el tampón de lisis que contiene al menos un biomarcador se puede hacer pasar al dispositivo de ensayo. En el caso de que el dispositivo de ensayo esté en comunicación fluida con el aparato 100, esto se puede lograr configurando las primera y segunda válvulas 102, 104 en la tercera configuración y después haciendo pasar el lisado que contiene el al menos un biomarcador hacia el dispositivo de ensayo. En el caso de que el dispositivo de ensayo no esté en comunicación fluida con el aparato 100, el lisado se puede hacer pasar de forma externa desde el aparato 100 al dispositivo de ensayo.
La invención se describe ahora a modo de ejemplos, que pretenden ser de carácter ilustrativo más que restrictivo.
Ejemplos
Todos los productos químicos se adquirieron en Sigma-Aldrich, a menos que se indique otra cosa.
Ejemplo 1
Materiales
Se obtuvieron muestras de ensayo de orina de una única micción de pacientes que asistían a una consulta de hematuria en el Hospital Heatherwood (Heatherwood and Wexham Park Hospitals n Hs Foundation Trust), habiendo obtenido la aprobación ética del Comité de ética de investigación local. Se llevó a cabo un análisis de orina utilizando tiras reactivas Multistix 10 SG (Siemens) en muestras frescas y la orina restante se dispensó en tubos Falcon de 1 ml o de 15 ml, que se colocaron en hielo seco para su transporte al laboratorio.
Mcm5
Una realización de la invención es una prueba de ELISA simple para Mcm5, que reemplaza de manera útil la prueba especializada y compleja DELFIA® para Mcm5 (véase Stoeber et al 2002 (Journal of the National Cancer Institute, 94, 1071-1079; 2002), así, lo que la prueba podría llevarse a cabo en un laboratorio de bioquímica clínica atípico. La prueba es un inmunoensayo ligado a enzimas de tipo sándwich de doble anticuerpo monoclonal directo. Ambos anticuerpos tienen alta afinidad y especificidad por el antígeno Mcm5. Cualquier Mcm5 en la muestra bajo prueba es capturado por un anticuerpo monoclonal específico unido a la superficie de la placa de microtitulación. A continuación, se añade el anticuerpo detector, que se une a un sitio distinto en el antígeno y que está unido a la enzima peroxidasa de rábano picante (HRP). La presencia y la cantidad de HRP retenida en los pocillos de la placa se evalúa midiendo la intensidad del color que se desarrolla después de la adición de tetrametilbencidina (TMB), que es un sustrato cromogénico de la HRP. La densidad óptica es proporcional a la concentración de Mcm5 en la muestra, dentro de los límites definidos. Analizando un intervalo de concentraciones de Mcm5, se puede generar una curva respuesta a la dosis a partir de la cual se puede determinar la concentración de antígeno de un desconocido (véanse las Figuras 2 y 3).
En el ensayo se utilizan dos anticuerpos monoclonales (los mAb), 12A7 y 4B4. Los anticuerpos se obtuvieron de Cancer Research Technology Ltd (c Rt ) en virtud de un acuerdo de licencia no exclusivo con el solicitante. Para pruebas de ELISA, se utilizó el mAb 12A7 para el recubrimiento de la placa y el mAb 4B4 para la detección.
Recogida y preparación de las muestras de ensayo: La prueba se puede realizar en orina humana. Las muestras deben recogerse en, por ejemplo, frascos de plástico de 150 ml con tapón de rosca, que deben estar limpios pero no necesariamente estériles. El frasco de recolección no debe contener ningún conservante e, idealmente, debe tener un volumen mayor que 100 ml. Las muestras pueden almacenarse hasta 4 horas a 2 - 8 °C antes de su uso. Para preparar las muestras de ensayo de orina para el ensayo, se transfieren 30 ml de la muestra a un tubo de centrífuga de plástico de 50 ml con tapón de rosca Después de la centrifugación durante 5 min a 1.500 g, el sobrenadante se decanta cuidadosamente y se trata como desecho de acuerdo con las directrices locales sobre Salud y seguridad. Los tubos se colocan invertidos sobre papel absorbente y se deja que drene el exceso de líquido. Se añaden 250 ml de tampón de lisis/muestra al sedimento; el sedimento se resuspende utilizando una pipeta ajustable con punta desechable.
Reactivos: Los componentes de prueba se describen en la presente en forma de un kit (véase la Tabla 1). Cada kit contiene materiales suficientes para una sola microplaca de 96 pocillos, u 80 determinaciones en pocillos duplicados si se utiliza toda la placa.
Tabla 1:
Además de los componentes enumerados en la Tabla 1, los siguientes materiales adicionales son útiles y pueden proporcionarse opcionalmente en un kit de la invención. Estos materiales deben considerarse como divulgados por separado y, por lo tanto, pueden añadirse de forma individual al kit de la invención. Un pipeta (o pipetas) capaces de suministrar volúmenes de 50 ml y 100 ml con una precisión mejor del 1,5 %; un dosificador (o dosificadores) para suministros repetitivos de volúmenes de 100 ml y 300 ml con una precisión mejor del 1,5 %; un lavador de microplacas o una botella exprimible (opcional); un lector de microplacas con capacidades de absorbancia de longitud de onda de 450 nm y 620 nm, papel absorbente para secar los pocillos de la microplaca y envolturas de plástico o cubiertas de microplacas para las etapas de incubación más un temporizador.
Procedimiento de ensayo: Antes de proceder con el ensayo, todos los reactivos deben llevarse a temperatura ambiente (20 - 27 °C) durante 30 minutos. Los reactivos no utilizados se almacenan a 2-8 °C después del uso. Se retiran suficientes tiras de microplacas para cada muestra a analizar, incluyendo una serie de diluciones de calibradores y de muestras de control de calidad, a someter a ensayo por duplicado. Se pipetean 100 ml del calibrador o muestra apropiada en el pocillo asignado, lo que se incuba a temperatura ambiente (20-27 °C) durante treinta (30) minutos en un agitador rotativo de placas de microtitulación a 700 rpm. Los contenidos se descartan y los pocillos se lavan con seis cambios de 300 ml de tampón de lavado. A continuación, se añaden 100 ml del reactivo/conjugado de anticuerpo anti Mcm5 HRP a cada pocillo. Después de mezclar, los pocillos se incuban inmóviles durante 30 minutos a temperatura ambiente (20-27 °C). A continuación, los contenidos de la microplaca se descartan por decantación o aspiración. Si se decantan, se golpear y seca la placa con papel absorbente y a continuación se lavan los pocillos como se describe anteriormente. A continuación, se añaden 100 ul de reactivo de sustrato a todos los pocillos y se incuba a temperatura ambiente (20-27 °C) durante treinta 30 minutos. La reacción se detiene mediante la adición de 100 ul de solución de parada a cada pocillo. Se lee a 450 nm la absorbancia en cada pocillo (utilizando una longitud de onda de referencia de 620-630 nm para minimizar las imperfecciones del pocillo) en un lector de microplacas. Los resultados deben leerse dentro de los 30 minutos posteriores a la adición de la solución de parada.
Se proporcionan muestras de calibrador. Estas se preparan utilizando una dilución en serie en el momento del ensayo y se descartan después de su uso (véase la Figura 3).
Para interpretar los resultados, se utiliza una curva de respuesta a la dosis para determinar la concentración de Mcm5 en las muestras de ensayo desconocidas. Esto se puede construir manual o automáticamente utilizando un programa informático. Para el cálculo manual, se registra la absorbancia obtenida de la impresión del lector de microplacas. Se representa la absorbancia para cada dilución por duplicado frente a la concentración de Mcm5 correspondiente en ng/ml en papel para gráfico lineal y después se dibuja la curva de mejor ajuste a través de los puntos representados. Para determinar la concentración de Mcm5 para un desconocido, se sitúa la absorbancia promedio de los duplicados para cada desconocido en el eje vertical del gráfico, se encuentra el punto de intersección en la curva y se lee la concentración (en ng/ml) en el eje horizontal del gráfico.
La Tabla 2 ilustra los resultados de un experimento típico.
Tabla 2.
El procedimiento para Mcm5 tiene un límite de detección analítica de < 7 pg/ml.
Ejemplo 2 - Estudio clínico de Mcm5 en 116 sujetos investigados en cuanto a cáncer de vejiga.
Se obtuvieron muestras de ensayo de orina de 116 pacientes, la mayoría de los cuales se examinaron posteriormente por cistoscopia flexible y exploración por TAC o ecografía. Si se obtenían resultados anómalos, los pacientes derivaban para la realización de una biopsia. Cuando estuvieron disponible, los resultados de estas investigaciones se recopilaron y añadieron al conjunto de datos. Los niveles de Mcm5 se midieron en cada sujeto utilizando la técnica de ELISA descrita anteriormente (Ejemplo 1). Se confirmaron clínicamente ocho casos de cáncer de vejiga, de los cuales cinco se calificaron como positivos en el ensayo de Mcm5.
Tabla: En la tabla, "+" indica que el resultado del ensayo de Mcm5 superó la media de los negativos conocidos 3 DT (DO media negativa 0,05, Dt 0,0593). Por lo tanto, el punto de corte se estableció arbitrariamente en una DO de
023
continuación
Además, hubo cuatro casos en los que se produjo un resultado de ELISA positivo en ausencia de un diagnóstico confirmado de malignidad: el Paciente 13 (se observaron lesiones papilares en la vejiga; el resultado de la biopsia no se registró. Próstata oclusiva); el Paciente 30 (ninguna otra patología registrada); el Paciente 65 (nefrectomía registrada); el Paciente 101 (próstata agrandada con calcificación). Se sabe que la presencia de cálculos puede provocar resultados positivos falsos debido al efecto abrasivo del material sobre la membrana basal de la epidermis, lo que conduce a la liberación de células MCM+, pero la tasa de tales casos es demasiado pequeña para afectar el presente ensayo.
Estadísticas del ensayo
Se calcularon las estadísticas convencionales del ensayo para los datos de ensayo de Mcm5. Aunque el verdadero criterio clínico no estaba disponible para todos los pacientes del estudio, el experto apreciará que este modesto panel ha arrojado resultados convincentes. En particular, el estudio ha proporcionado una estimación realista de especificidad del 96 % (104/108).
Ejemplo 3 - comparación de diversos tampones
Se lisaron en cada tampón cantidades conocidas de células de carcinoma urotelial T24, y los lisados se analizaron en ELISA para Mcm5. Los resultados demuestran una notable diferencia en la eficacia de lisis en este ensayo. El tampón que contiene SDS es típico de los descritos en la bibliografía, pero es significativamente menos eficaz que Cytobuster o 'Urosens LB' (desoxicolato de sodio al 0,08 %, CHAPS al 0,08 %, EDTA 2 mM, Trizma 150 mM pH 7,6). Los resultados se presentan en la Figura 4.
Ejemplo 4
La lisis de las células en CytoBuster se comparó con las células en tampón TBS Tritón (TBST) y tampón RIPA, con un control de sedimentos celulares reconstituidos en DMEM (medio de cultivo celular). Los resultados se describen en la Figura 5.
Se analizó la potencia de Mcm5 en las muestras lisadas después de la aplicación de tampón a las células. Algunas muestras se congelaron después de la exposición al tampón y antes del análisis. De manera ideal, sería útil un búfer universal que se utilizaría en ambas situaciones.
Los resultados del control demostraron que, cuando se analizaron muestras frescas, las células permanecían intactas cuando no se añadía agente de lisis, pero después de congelar-descongelar (CD), las células estallan por destrucción mecánica de la membrana celular, liberando así Mcm5. Este experimento mostró que, cuando se utilizan lisados frescos, el tampón TBST es aproximadamente equivalente al CytoBuster. Sin embargo, después de haber congelado las muestras, los lisados de CytoBuster experimentan una pérdida drástica de potencia, mientras que el TBST no se ve tan fuertemente afectado. El tampón de lisados con RIPA, aunque menor cuando se obtienen de una muestra fresca, conservan toda la potencia posterior a la CD.
Ejemplo 5
Se añadieron componentes adicionales al TBT para tratar de mejorar la estabilidad de los lisados de TBST. Se analizó la potencia de Mcm5 en las muestras lisadas después de la aplicación de tampón a las células tanto frescas como congeladas. Los resultados de este experimento se presentan en la Figura 6.
Estos datos (descritos en la Figura 6) demostraron que los componentes estabilizadores del tampón RIPA son el desoxicolato de sodio (SDC) y el dodecilsulfato de sodio (SDS), pero desafortunadamente la incorporación de estos elementos en el tampón TBST más simple provoca una pérdida dramática de la señal. Se realizó una prueba complementaria para eliminar elementos del tampón RIPA uno por uno, para observar si la eliminación de algún elemento podría mejorar la señal del RIPA al mismo nivel que el TBST, mientras se conserva la estabilidad. Los resultados se describen en la Figura 7.
Ejemplo 6
Se compararon diversos tampones que comprendían concentraciones de Tris y Tritón x-100 que diferían. Se analizó la potencia de Mcm5 en las muestras lisadas después de la aplicación de tampón a las células tanto frescas como congeladas. Los resultados se presentan en la Figura 8.
Los datos mostraron que el aumento de la concentración de Tris provocó una mejora de los niveles de Mcm5 del lisado celular, aunque el aumento de la concentración de Tritón X-100 no tuvo efecto.
Para garantizar que se utilice la base óptima para el tampón de lisis antes de continuar, se analizaron varios compuestos en diversos intervalos de pH y tipos de tampón. Varios de estos tampones dieron buenos resultados, pero se demostró que el TBS tenía la señal más alta. Estos resultados se describen en la Figura 9.
Ejemplo 7
Se realizó una titulación adicional de Tris para observar si la señal aún aumentaría si se usara una concentración de tampón más alta, y para observar dónde se estabilizaba la mejora. Los resultados se presentan en la Figura 10. El nivel de Mcm5 comienza a estabilizarse a Tris 225 mM, solo siendo más alta con Tris 250 mM y después la señal es estable hasta 325 mM, después de lo cual observa una disminución. Para evitar posibles problemas con la fabricación y la variación, una concentración en una zona estable de la meseta sería la opción óptima, tal como 300 mM.
Ejemplo 8
Se planteó la hipótesis de que la modificación de la concentración de Tris podía ser eficaz debido al aumento de la fuerza iónica. Dado que esto se puede lograr igualmente añadiendo NaCI, se analizaron composiciones que tenían distintas concentraciones de NaCl. Los resultados se presentan en la Figura 11.
Los datos muestran que el aumento de la concentración de NaCI en los tampones TBST (TBS Tween 20) con niveles más bajos de Tris mejora la señal, pero el mismo efecto no se observa en el tampón RIPA, independientemente de la concentración de Tris. El aumento de la concentración de Tris no parece tener ninguna mejora sustancial en la señal del tampón RIPA convencional (Tris 25 mM y NaCI 150 mM), incluso si el nivel de NaCI se reduce en compensación. El TBST con Tris 10 mM, NaCI 150 mM tiene la señal más alta obtenida en el conjunto de datos (aproximadamente el doble que la de CytoBuster), por lo que este tampón se optimizó en términos de concentración de NaCl y se evaluó por separado para los componentes estabilizadores.
Ejemplo 9
Los datos presentados en el Ejemplo 8 sugieren que los tampones que tienen alrededor de tris 10 mM son los más eficaces, por lo que se investigaron tampones que tenían tris 10 mM y distintas concentraciones de NaCl. Los resultados se presentan en la Figura 12.
La titulación de NaCI muestra que el mejor candidato es el Tris 10 mM con NaCI 200 mM. Los datos también parecen mostrar que cuando la fuerza iónica alcanza cierto punto, la precisión está comprometida. La formulación elegida del tampón a partir de este punto fue Tris 10 mM, NaCI 200 mM y Tritón X-100 0,1 %, a lo que luego se añadieron compuestos estabilizadores para encontrar una formulación final adecuada.
Ejemplo 10
Se analizaron diversos estabilizadores para probar su eficacia en la estabilización de las muestras de Mcm5 cuando se combinaron con TBS-T.
En términos de posibles candidatos, el SFB (suero bovino fetal) al 1 %, la BSA (seroalbúmina bovina) al 2,5 %, Pefabloc SC 0,25 mM, Pefabloc SC 0,1 mM, el cóctel de inhibidor de proteasas Sigma P8340 al 0,5 % y el cóctel de inhibidores de proteasas complete de Roche 0,25x tuvieron datos alentadores sin comprometer el fondo o la señal de las muestras positivas en comparación con el tampón sin aditivos de estabilidad. Estos resultados se presentan en las Figuras 13A y 13B.
Estos compuestos se analizaron con diversas temperaturas de almacenamiento después de 6 días para observar cómo se comparaban con el TBST sin aditivos y el CytoBuster. Estos resultados se presentan en la Figura 14. Todos los estabilizadores fueron eficaces para estabilizar las composiciones. Los cócteles inhibidores de proteasas producidos comercialmente (Pefabloc, Sigma P3840 y complete de Roche) fueron estables, pero redujeron la señal de Mcm5. La BSA al 2,5 % funcionó mejor que el SFB al 1 % a -20 °C. El desempeño a 4 °C y fresco fue equivalente para SFB al 1 % y BSA al 2,5 %, y ambos parecen aumentar la comparación de la señal con el tampón TBST convencional. Como hubo una pérdida a -20 °C para la BSA, se realizó un experimento repetido utilizando líneas celulares adicionales para confirmar la mejora de la estabilidad.
Ejemplo 11
Claims (13)
1. Un método para el análisis de una muestra de orina de un sujeto que comprende
a. exponer la muestra de orina a un tampón de lisis que es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina, en donde el tampón de lisis comprende: (i) un detergente que comprende o consiste en tritón X-100; y (ii) un componente tampón que comprende o consiste en tampón Tris o Trizma; y b. realizar un ensayo para detectar la presencia de la proteína Mcm en la muestra de orina.
2. El método de la reivindicación 1, en donde
a. el tampón de lisis no es PBS que contiene desoxicolato de sodio al 0,4 % y azida de sodio al 0,02 %;
b. el método no comprende la incubación de la muestra de orina a una temperatura mayor que 90 °C durante más de 45 minutos;
c. el método no comprende la rotura de los ácidos nucleicos en la muestra de orina haciendo pasar la muestra de orina a través de una aguja de 0,813 mm de diámetro;
d. el método no comprende la digestión de los ácidos nucleicos mediante la exposición de la muestra de orina a ADNasa I o ARNasa A; y/o
e. el método no comprende la centrifugación de la muestra a 15.000 g durante 10 minutos.
3. El método de la reivindicación 1 o 2, en donde:
(i) el método es un método para la liberación de una proteína Mcm a partir de las células de la muestra de orina y la detección de la presencia de la proteína Mcm liberada a partir de las células; y/o
(ii) el método comprende una etapa de concentración de células en la muestra de orina antes de la etapa de exposición de la muestra de orina a un tampón de lisis, la exposición de las células concentradas a tampón de lisis o la resuspensión de las células sedimentadas de la muestra en un tampón de lisis.
4. Un método para la preparación de células a partir de una muestra de orina, comprendiendo el método:
hacer pasar la muestra de orina a través de un filtro para la captura de células, de manera que las células se capturen en el filtro;
hacer pasar a través del filtro un tampón de lisis que es capaz de liberar una proteína Mcm a partir de las células de la muestra de orina, de manera que las células capturadas estén expuestas al tampón de lisis;
incubar el filtro durante un período de tiempo, de manera que el tampón de lisis provoque que las células liberen la proteína Mcm, en donde el tampón de lisis comprende: (i) un detergente que comprende o consiste en tritón X-100; y (ii) un componente tampón que comprende o consiste en tampón Tris o Trizma.
5. El método de una cualquiera de las reivindicaciones precedentes, en donde:
(i) la proteína Mcm es una proteína Mcm5;
(ii) el tampón de lisis es capaz de liberar Mcm5 a partir de las células de la muestra de orina y no desnaturaliza sustancialmente la proteína Mcm5;
(iii) el tampón de lisis no desnaturaliza un anticuerpo;
(iv) el detergente comprende tritón X-100 a una concentración de entre el 0,01 % y el 25 %, entre el 0,01 % y el 10 %, entre el 0,05 % y el 5 %, entre el 0,05 % y el 1 %, entre 0,05 % y el 0,5 % o alrededor del 0,1 %;
(v) el detergente comprende desoxicolato de sodio o dodecilsulfato de sodio;
(vi) el detergente comprende desoxicolato de sodio o dodecilsulfato de sodio a una concentración de entre el 0,1 % y el 20 %, entre el 0,5 % y el 10 %, entre 0,5 % y el 5 % o alrededor del 1 %;
(vii) el tampón de lisis comprende desoxicolato de sodio a una concentración de entre el 0,01 % y el 0,15 %, entre el 0,03 % y el 0,10 %, entre el 0,05 % y el 0,09 %, o aproximadamente el 0,08 %;
(viii) el componente tampón comprende o consiste en tampón Tris a una concentración mayor que 5 mM, entre 5 mM y 350 mM, entre 200 mM y 300 mM, entre 10 mM y 25 mM, alrededor de 10 mM o alrededor de 250 mM; (ix) el componente tampón mantiene el pH del tampón de lisis entre pH 4 y pH 9, entre pH 5 y pH 8, entre pH 6 y pH 8, o a alrededor de pH 7,6;
(x) el tampón de lisis comprende una sal seleccionada del grupo que consiste en cloruro de sodio, cloruro de potasio, cloruro de magnesio, sulfato de sodio, sulfato de potasio, sulfato de magnesio, acetato de sodio, acetato de potasio, acetato de magnesio, fosfato de sodio, fosfato de potasio y fosfato de magnesio;
(xi) el tampón de lisis comprende una sal que está a una concentración de entre 20 mM y 300 mM, entre 150 mM y 300 mM, entre 100 mM y 200 mM, o alrededor de 200 mM;
(xii) el tampón de lisis tiene una fuerza iónica de entre 1 mM y 500 mM, entre 50 mM y 450 mM, entre 100 mM y 250 mM, o entre 100 mM y 175 mM;
(xiii) el tampón de lisis comprende tampón RIPA;
(xiv) el método no comprende la incubación de la muestra de orina a una temperatura alta;
(xv) el método no comprende la incubación de la muestra de orina a una temperatura alta y la temperatura alta es una temperatura mayor que 50 °C, mayor que 60 °C, mayor que 70 °C, mayor que 80 °C, entre 50 °C y
120 °C, entre 60 °C y 110 °C, entre 70 °C y 100 °C, o entre 80 °C y 100 °C;
(xvi) el método no comprende la incubación de la muestra de orina a una temperatura alta durante más de 30 minutos, más de 35 minutos, más de 40 minutos, más de 45 minutos, entre 30 minutos y 2 horas, entre 35 minutos y 2 horas, o entre 40 minutos y 2 horas;
(xvii) el método no comprende la rotura de ácidos nucleicos en la muestra de orina mediante rotura mecánica; (xviii) el método no comprende la exposición de la muestra de orina a enzimas que digieren ácidos nucleicos; (xix) el método no comprende la centrifugación de la muestra a 15.000 g durante 10 minutos;
(xx) la proteína Mcm es Mcm5 y un valor anómalo para la concentración de Mcm5 indica una probabilidad aumentada de cáncer urológico en el sujeto;
(xxi) el método es un método para la detección de la presencia de un cáncer urológico en un sujeto;
(xxii) el método es un método para la detección de la presencia de un cáncer urológico en un sujeto y el cáncer urológico es cáncer de próstata y/o de vejiga;
(xxiii) el ensayo para detectar la presencia de la proteína Mcm es un ensayo de ELISA;
(xxiv) el ensayo para detectar la presencia de la proteína Mcm es un ensayo de ELISA de tipo sándwich; y/o (xxv) el ensayo para detectar la presencia de la proteína Mcm es un ensayo de ELISA de tipo sándwich que comprende la captura del al menos un biomarcador o de la proteína Mcm en la muestra utilizando un anticuerpo de captura y la detección de la concentración de la proteína Mcm utilizando un anticuerpo de detección, en donde el anticuerpo de captura y el anticuerpo de detección se unen específicamente a el al menos un biomarcador o la proteína Mcm, opcionalmente en donde el anticuerpo de captura está inmovilizado en una placa de ELISA y/o el anticuerpo de detección está conjugado con peroxidasa de rábano picante.
6. El método de una cualquiera de las reivindicaciones precedentes, en donde el tampón de lisis comprende cloruro de sodio a una concentración de entre 20 mM y 300 mM, entre 150 mM y 300 mM, o entre 100 mM y 200 mM.
7. El método de una cualquiera de las reivindicaciones precedentes, en donde:
el componente tampón comprende o consiste en Tris a una concentración mayor que 5 mM, entre 5 mM y 350 mM, o entre 10 mM y 25 mM;
el componente tampón mantiene el pH del tampón de lisis entre pH 4 y pH 9, entre pH 5 y pH 8, entre pH 6 y pH 8, o a alrededor de pH 7,6;
el detergente comprende Tritón X-100 a una concentración de entre el 0,01 % y el 25 %, entre el 0,01 % y el 10 %, entre el 0,05 % y el 5 %, o entre el 0,05 % y el 1 %;
el detergente comprende desoxicolato de sodio o dodecilsulfato de sodio a una concentración de entre el 0,1 % y el 20 %, entre el 0,5 % y el 10 %, entre 0,5 % y el 5 % o alrededor del 1 %; y
el tampón de lisis comprende cloruro de sodio a una concentración de entre 20 mM y 300 mM, entre 150 mM y 300 mM, o entre 100 mM y 200 mM.
8. El método de una cualquiera de las reivindicaciones precedentes, en donde:
el componente tampón comprende o consiste en Tris a una concentración de entre 10 mM y 25 mM;
el componente tampón mantiene el pH del tampón de lisis a alrededor de pH 7,6;
el detergente comprende Tritón X-100 a una concentración de entre el 0,05 % y el 1 %;
el detergente comprende desoxicolato de sodio a una concentración de alrededor del 1 %; y
el tampón de lisis comprende cloruro de sodio a una concentración de entre 100 mM y 200 mM.
9. El método de una cualquiera de las reivindicaciones precedentes, en donde la muestra de orina:
(i) comprende sedimento de orina; y/o
(ii) comprende sedimento de orina obtenido de la orina del primer chorro recogida después de masaje prostático.
10. El método de la reivindicación 4, en donde:
(i) la etapa de hacer pasar un tampón de lisis a través del filtro comprende hacer pasar el tampón de lisis a través del filtro en una dirección aguas arriba, con respecto al flujo de orina a través del filtro, al menos una vez, y hacer pasar el tampón de lisis a través del filtro en una dirección aguas abajo al menos una vez, opcionalmente en donde el tampón de lisis se hace pasar alternativamente a través del filtro aguas arriba y aguas abajo;
(ii) el volumen de la muestra de orina es de entre 1 y 100 ml, preferentemente de aproximadamente 50 ml;
(iii) el volumen del tampón de lisis es de entre 250 ml y 1000 ml, preferentemente de aproximadamente 500 ml; (iv) la muestra de orina se hace pasar a través del filtro utilizando una jeringa;
(v) el tampón de lisis se hace pasar a través del filtro utilizando una jeringa;
(vi) el tampón de lisis se hace pasar entre dos jeringas a través del filtro, formando las dos jeringas y el filtro un sistema cerrado para la etapa de hacer pasar el tampón de lisis;
(vii) el tiempo de incubación es de entre 30 segundos y 1 hora, preferentemente de aproximadamente 10 minutos; y/o
(viii) el al menos un biomarcador es Mcm5.
11. El método de una cualquiera de las reivindicaciones 1-3 o 5-9, en donde la exposición de la muestra de orina a un tampón de lisis se lleva a cabo utilizando el método de la reivindicación 4 o 10.
12. Uso de un tampón de lisis como se define en una cualquiera de las reivindicaciones precedentes para la liberación de una proteína Mcm a partir de las células de una muestra de orina.
13. El uso de la reivindicación 12, en donde la proteína Mcm es Mcm5.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1509909.6A GB201509909D0 (en) | 2015-06-08 | 2015-06-08 | Methods |
| GBGB1603559.4A GB201603559D0 (en) | 2016-03-01 | 2016-03-01 | Methods |
| PCT/GB2016/051608 WO2016198833A2 (en) | 2015-06-08 | 2016-06-01 | Methods |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2806498T3 true ES2806498T3 (es) | 2021-02-17 |
Family
ID=56113001
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16727797T Active ES2806498T3 (es) | 2015-06-08 | 2016-06-01 | Métodos para el análisis de una muestra de orina |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US11519916B2 (es) |
| EP (1) | EP3304082B1 (es) |
| JP (1) | JP6854246B2 (es) |
| CN (1) | CN107771285A (es) |
| ES (1) | ES2806498T3 (es) |
| WO (1) | WO2016198833A2 (es) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6854246B2 (ja) * | 2015-06-08 | 2021-04-07 | アーケア ダイアグノスティクス リミテッド | 尿サンプルの分析方法 |
| KR101923199B1 (ko) * | 2018-04-25 | 2018-11-28 | 주식회사 무진메디 | 펩스타틴 a를 함유하는 소변 내 en2 진단용 조성물 |
| WO2019239514A1 (ja) * | 2018-06-13 | 2019-12-19 | 日立化成株式会社 | 細胞溶解装置および細胞溶解方法 |
| GB201820867D0 (en) * | 2018-12-20 | 2019-02-06 | Arquer Diagnostics Ltd | Detection method |
| GB201912605D0 (en) * | 2019-09-02 | 2019-10-16 | Arquer Diagnostics Ltd | Cancer assay |
| CN114929242A (zh) * | 2019-09-05 | 2022-08-19 | 小利兰·斯坦福大学托管委员会 | 修饰线粒体功能的方法和化合物 |
| CN111323585A (zh) * | 2020-02-27 | 2020-06-23 | 北京健平金星生物科技有限公司 | 一种核基质蛋白22酶联免疫检测试剂盒制备方法及试剂盒 |
| CN112229995B (zh) * | 2020-09-30 | 2024-07-05 | 北京安图生物工程有限公司 | 胃蛋白酶原pgi/ii复合校准品的稀释液及其应用 |
| CN114878804A (zh) * | 2022-05-23 | 2022-08-09 | 山东博科快速检测技术有限公司 | 一种用于胶体金法新冠病毒抗原检测卡的样本稀释液 |
| CN115389291A (zh) * | 2022-10-26 | 2022-11-25 | 北京肿瘤医院(北京大学肿瘤医院) | 一种尿液微量蛋白的富集、纯化和保护方法 |
| CN119178710B (zh) * | 2024-11-19 | 2025-03-25 | 浙江博真生物科技有限公司 | 一种基于流式细胞术检测dna倍体的方法 |
Family Cites Families (144)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4022576A (en) | 1975-06-09 | 1977-05-10 | I. C. L. Scientific | Method and apparatus for preparation of liquids containing suspended material for examination |
| US4794076A (en) | 1985-09-23 | 1988-12-27 | Vxr, Inc. | Simultaneous extraction of a ligand from a sample and capture by anti-ligands therefor in ligand/anti-ligand assays |
| GB8526741D0 (en) | 1985-10-30 | 1985-12-04 | Boots Celltech Diagnostics | Binding assay device |
| US4868108A (en) | 1985-12-12 | 1989-09-19 | Hygeia Sciences, Incorporated | Multiple-antibody detection of antigen |
| US5016644A (en) | 1989-01-10 | 1991-05-21 | La Mina Ltd. | Urine testing module and method of collecting urine antigen |
| US5087556A (en) | 1989-05-17 | 1992-02-11 | Actimed Laboratories, Inc. | Method for quantitative analysis of body fluid constituents |
| CA2040088A1 (en) | 1991-04-09 | 1992-10-10 | Raouf A. Guirguis | Method for testing urine antigen |
| EP0509158A1 (en) | 1991-04-10 | 1992-10-21 | La Mina Ltd. | Method of testing for urine antigen |
| US5314804A (en) * | 1992-03-24 | 1994-05-24 | Serim Research Corporation | Test for Helicobacter pylori |
| EP0763738A1 (en) | 1995-09-14 | 1997-03-19 | Unipath Limited | Assays for Chlamydia in diluted urine samples |
| US6361954B1 (en) | 1996-05-02 | 2002-03-26 | Cold Spring Harbor Laboratory | Methods of immunoassay for human CDC6 |
| EP1025444B1 (en) | 1997-10-21 | 2005-03-02 | Cancer Research Technology Limited | Determination of cellular growth abnormality |
| US6008003A (en) | 1997-10-28 | 1999-12-28 | Promega Corporation | Non-invasive diagnostic method for interstitial cystitis and bladder cancer |
| AUPP713498A0 (en) | 1998-11-17 | 1998-12-10 | Chandler, Howard Milne | A method of detecting blood |
| WO2000039586A2 (en) | 1998-12-30 | 2000-07-06 | Sedum Laboratories | Tetramethylbenzidine formulation for horseradish peroxidase enzyme assays |
| DE19915057A1 (de) | 1999-04-01 | 2000-10-19 | Forschungszentrum Borstel | Monoklonale Antikörper gegen das humane Mcm3 Protein, Verfahren zu ihrer Herstellung und ihre Verwendung |
| WO2001002599A2 (en) | 1999-07-06 | 2001-01-11 | Cancer Research Ventures Limited | Assay method to identify s-phase cells on cell sections or permeabilised cells and uses thereof |
| DE19936618A1 (de) | 1999-08-04 | 2001-03-15 | Monotec Gmbh | Diagnostisches Kit und dessen Verwendung |
| US20050208558A1 (en) | 1999-10-19 | 2005-09-22 | Applera Corporation | Detection kits, such as nucleic acid arrays, for detecting the expression or 10,000 or more Drosophila genes and uses thereof |
| AU2001245945A1 (en) | 2000-03-23 | 2001-10-03 | Pe Corporation (Ny) | Detection kits, such as nucleic acid arrays, for detecting the expression of 10,000 or more drosophila genes and uses thereof |
| US6812339B1 (en) | 2000-09-08 | 2004-11-02 | Applera Corporation | Polymorphisms in known genes associated with human disease, methods of detection and uses thereof |
| US20070037165A1 (en) | 2000-09-08 | 2007-02-15 | Applera Corporation | Polymorphisms in known genes associated with human disease, methods of detection and uses thereof |
| DE10054632B4 (de) | 2000-11-03 | 2007-07-26 | Michael Prof. Dr.med. Giesing | Verfahren zur Isolierung von disseminierten Krebszellen aus einer zellhaltigen Körperflüssigkeit und Verwendung einer Filtervorrichtung in einem solchen Verfahren |
| US20040241876A1 (en) | 2000-12-22 | 2004-12-02 | France Fannes | Flow through assay device, diagnostic kit comprising said assay device and use of said assay device in the detection of an analyte present in a sample |
| KR100420400B1 (ko) | 2001-04-30 | 2004-03-04 | (주)이인 | 액상의 다기능성 원적외선 방사체 및 그의 용도 |
| WO2002101075A2 (en) | 2001-06-13 | 2002-12-19 | Millennium Pharmaceuticals, Inc. | Novel genes, compositions, kits, and methods for identification, assessment, prevention, and therapy of cervical cancer |
| ATE443259T1 (de) | 2001-09-20 | 2009-10-15 | Univ Texas | Bestimmung der zirkulierenden therapeutischen antikörper, antigene sowie antigen-antikörper- komplexe mit elisa-tests |
| US20070237770A1 (en) | 2001-11-30 | 2007-10-11 | Albert Lai | Novel compositions and methods in cancer |
| WO2003072035A2 (en) | 2002-02-22 | 2003-09-04 | Genentech, Inc. | Compositions and methods for the treatment of immune related diseases |
| DK1388734T3 (da) | 2002-08-01 | 2004-05-03 | Mtm Lab Ag | Metode til opløsningsbaseret diagnose |
| EP1507148B1 (en) | 2003-08-25 | 2005-02-23 | MTM Laboratories AG | Method for detecting carcinomas in a solubilized cervical body sample |
| DE10238046A1 (de) | 2002-08-20 | 2004-03-04 | Giesing, Michael, Prof. Dr.med. | Verfahren zum Untersuchen von Körperflüssigkeiten auf Krebszellen, dessen Verwendung, entsprechende Analysekits und Verwendung bestimmter Wirkstoffe zur Behandlung von Krebs |
| WO2004023973A2 (en) | 2002-09-12 | 2004-03-25 | Incyte Corporation | Molecules for diagnostics and therapeutics |
| AU2003298261A1 (en) | 2002-09-26 | 2004-05-04 | Cellzome Ag | Protein complexes of the tumor-necrosis-factor-alpha (tnf-alpha) signalling pathway |
| EP1594447A2 (en) | 2002-10-02 | 2005-11-16 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| EP1422526A1 (en) | 2002-10-28 | 2004-05-26 | MTM Laboratories AG | Method for improved diagnosis of dysplasias |
| EP2322203A3 (en) | 2002-10-29 | 2011-07-27 | Genentech, Inc. | Compositions and methods for the treatment of immune related diseases |
| EP2364716A3 (en) | 2002-11-08 | 2012-01-11 | Genentech, Inc. | Compositions and methods for the treatment of natural killer cell related diseases |
| CA2515075C (en) | 2003-02-05 | 2012-10-02 | Iquum, Inc. | Sample processing |
| DE10316701A1 (de) | 2003-04-09 | 2004-11-04 | Hinzmann, Bernd, Dr. | Humane Nukleinsäuresequenzen aus Bronchialkarzinomen |
| US7361460B2 (en) | 2003-04-11 | 2008-04-22 | Digene Corporation | Approach to molecular diagnosis of human papillomavirus-related diseases |
| EP1510820B1 (en) | 2003-08-25 | 2010-03-17 | MTM Laboratories AG | Method for detecting medically relevant conditions in a solubilized LBC sample |
| TW200510721A (en) | 2003-08-29 | 2005-03-16 | Toshiba Kk | Color reagent, concentration measuring kit, concentration measuring method and sensor chip for use therein |
| JP2005080524A (ja) | 2003-09-05 | 2005-03-31 | Japan Science & Technology Agency | 前立腺癌マーカポリペプチド、該ポリペプチドに対する抗体、及び該ポリペプチドを利用した前立腺癌の診断方法 |
| WO2005026211A2 (en) | 2003-09-05 | 2005-03-24 | Eli Lilly And Company | Anti-ghrelin antibodies |
| US20050069900A1 (en) | 2003-09-25 | 2005-03-31 | Cytyc Corporation | Analyte sample detection |
| US8344211B2 (en) | 2008-08-13 | 2013-01-01 | Ceres, Inc. | Plant nucleotide sequences and corresponding polypeptides |
| JP4848355B2 (ja) | 2004-02-27 | 2011-12-28 | アンスティテュ・キュリ | 臨床診療における新規増殖マーカーおよび癌の予後または診断のためのそれらの用途 |
| US7604956B2 (en) | 2004-03-01 | 2009-10-20 | Biotraces, Inc. | Supersensitive immunoassays |
| CN1957256B (zh) | 2004-03-24 | 2013-01-02 | 三路影像公司 | 用于子宫颈疾病检测的方法和组合物 |
| US8193332B2 (en) | 2004-04-09 | 2012-06-05 | Genecare Research Institute Co., Ltd. | Cancer cell-specific apoptosis-inducing agents that target chromosome stabilization-associated genes |
| JP4685369B2 (ja) | 2004-04-30 | 2011-05-18 | 独立行政法人科学技術振興機構 | 関節リウマチ診断用試薬 |
| AU2011236061B2 (en) | 2004-07-23 | 2015-02-19 | Pacific Edge Limited | Urine markers for detection of bladder cancer |
| EP2436779B1 (en) | 2004-07-23 | 2015-03-25 | Pacific Edge Limited | Urine markers for detection of bladder cancer |
| EP1628135A1 (en) | 2004-08-20 | 2006-02-22 | MTM Laboratories AG | Method for detecting medically relevant conditions in a solubilized LBC sample |
| US20090163406A1 (en) | 2004-09-30 | 2009-06-25 | The Regents Of The University Of California | Compositions and methods for diagnosing and treating brain cancer and identifying neural stem cells |
| US8951746B2 (en) * | 2004-11-05 | 2015-02-10 | Southwest Research Institute | Method and devices for screening cervical cancer |
| US20070259336A1 (en) | 2004-12-23 | 2007-11-08 | Georgetown University | Methods for the detection of analytes in a sample |
| WO2006086573A2 (en) | 2005-02-09 | 2006-08-17 | The United States Of America As Represented By The Secretary Of The Navy | Diagnostic assay for orientia tsutsugamushi by detection of responsive gene expression |
| FR2883488B1 (fr) | 2005-03-24 | 2010-12-10 | Inst Nat Sante Rech Med | Procede et dispositif pour separer par filtration verticale des particules biologiques contenues dans un liquide |
| US7595380B2 (en) | 2005-04-27 | 2009-09-29 | Tripath Imaging, Inc. | Monoclonal antibodies and methods for their use in the detection of cervical disease |
| US7842467B1 (en) | 2005-05-12 | 2010-11-30 | Celera Corporation | Breast disease targets and uses thereof |
| US8497101B2 (en) | 2005-05-13 | 2013-07-30 | Centre National De La Recherche Scientifique (Cnrs) | Use of a new gene coding for a new member of the MCM2-8 family in pharmaceutical compositions |
| KR101068612B1 (ko) | 2005-05-24 | 2011-09-30 | 휴마시스 주식회사 | 유사구조 단백질 비율 측정을 이용한 진단장치 |
| WO2007018309A1 (ja) | 2005-08-11 | 2007-02-15 | Banyu Pharmaceutical Co., Ltd. | Rbパスウェイ上の分子を指標とする化合物の評価方法及び分子診断方法 |
| GB0518877D0 (en) | 2005-09-15 | 2005-10-26 | Medical Res Council | Markers and methods |
| EP1775590A1 (en) | 2005-10-11 | 2007-04-18 | Laboratorios S.A.L.V.A.T., S.A. | Non-invasive in vitro method to detect transitional cell carcinoma of the bladder |
| GB0521521D0 (en) | 2005-10-21 | 2005-11-30 | Medical Res Council | Diagnostic methods and kits |
| CA2630597A1 (en) | 2005-12-08 | 2007-06-14 | Novartis Ag | Effects of inhibitors of fgfr3 on gene transcription |
| EP1816460B1 (en) | 2006-02-03 | 2009-07-22 | MTM Laboratories AG | Method of performing a denaturing immunassay |
| US20070184460A1 (en) | 2006-02-09 | 2007-08-09 | Wei-Mei Ching | Diagnostic assay for Orientia tsutsugamushi by detection of responsive gene expression |
| MX2008012252A (es) | 2006-03-24 | 2009-01-14 | Basf Plant Science Gmbh | Proteinas que se relacionan con la respuesta al estres abiotico y homologos. |
| EP1852186A1 (en) * | 2006-05-03 | 2007-11-07 | Eppendorf Array Technologies | Method and means for multiparametric assays being compartmentalized |
| WO2008021290A2 (en) | 2006-08-09 | 2008-02-21 | Homestead Clinical Corporation | Organ-specific proteins and methods of their use |
| US20100094560A1 (en) | 2006-08-15 | 2010-04-15 | Prometheus Laboratories Inc. | Methods for diagnosing irritable bowel syndrome |
| DK2074230T3 (da) | 2006-10-11 | 2013-02-25 | Janssen Pharmaceutica Nv | Sammensætninger og fremgangsmåder til behandling og diagnosticering af colon irritabile |
| KR100886670B1 (ko) | 2007-01-11 | 2009-03-04 | 김현기 | 유두갑상선암의 새로운 진단마커 및 진단방법 |
| ES2304306B1 (es) | 2007-03-20 | 2009-07-07 | Indas Biotech, S.L.U. | Metodo de diagnostico y/o pronostico de cancer vesical. |
| US20080254455A1 (en) | 2007-04-12 | 2008-10-16 | Haiying Wang | Detecting prostate cancer |
| GB0708002D0 (en) | 2007-04-25 | 2007-06-06 | Univ Sheffield | Antibodies |
| CN101801431B (zh) | 2007-06-22 | 2014-11-19 | 循环生物制品有限责任公司 | 流体浓缩器和自体浓缩体液及其使用方法 |
| JP5196890B2 (ja) | 2007-06-29 | 2013-05-15 | オリンパス株式会社 | 有核細胞回収装置および有核細胞の回収方法 |
| US20110236953A1 (en) | 2007-08-03 | 2011-09-29 | Beth Israel Deaconness Medical Center | EMBRYONIC CEREBROSPINAL FLUID (e-CSF), PROTEINS FROM e-CSF, AND RELATED METHODS AND COMPOSITIONS |
| EP2196803B1 (en) | 2007-09-27 | 2015-07-29 | Niigata University | Urine pretreatment agent for urinary protein determination, urine pretreatment method, and urinary protein determination method |
| CA3170924A1 (en) | 2007-10-02 | 2009-04-09 | Labrador Diagnostics Llc | Modular point-of-care devices and uses thereof |
| GB0720113D0 (en) | 2007-10-15 | 2007-11-28 | Cambridge Cancer Diagnostics L | Diagnostic, prognostic and predictive testing for cancer |
| WO2009145815A2 (en) | 2008-04-01 | 2009-12-03 | The Brigham And Women's Hospital, Inc. | Biomarkers of ovarian cancer |
| CN101358976A (zh) | 2008-04-28 | 2009-02-04 | 北京华大吉比爱生物技术有限公司 | 检测六项肿瘤标志物的微阵列-酶联免疫检测试剂盒 |
| US20110065605A1 (en) | 2008-05-14 | 2011-03-17 | Eth Zurich | Method for biomarker and drug-target discovery for prostate cancer diagnosis and treatment as well as biomarker assays determined therewith |
| GB0811567D0 (en) | 2008-06-24 | 2008-07-30 | Cytosystems Ltd | Assay |
| US8071815B2 (en) | 2008-07-17 | 2011-12-06 | Arup Kumar Indra | CTIP2 expression in squamous cell carcinoma |
| US8728745B2 (en) | 2008-09-04 | 2014-05-20 | Ventana Medical Sysems, Inc. | Method for prediction of the progression risk of tumors |
| JP2010088376A (ja) | 2008-10-09 | 2010-04-22 | Olympus Corp | 細胞回収装置および脂肪由来細胞含有液 |
| WO2010042228A2 (en) | 2008-10-10 | 2010-04-15 | Cornell University | Methods for predicting disease outcome in patients with colon cancer |
| EP2350317A4 (en) | 2008-10-20 | 2012-06-27 | Univ Colorado Regents | BIOLOGICAL MARKERS FOR PREDICTING THE ANTICIPATE RESPONSE TO INSULINARY GROWTH FACTOR 1 RECEPTOR KINASE INHIBITORS |
| CN101738469A (zh) | 2008-11-19 | 2010-06-16 | 中国海洋大学 | 一种基于可视化蛋白芯片的食物过敏原检测方法 |
| KR101343035B1 (ko) | 2008-12-22 | 2013-12-18 | 삼성전자 주식회사 | 제1수용체, 차단물질 및 제2수용체가 고정화된 고체 기판을포함하는 표적물질을 분석하기 위한 물품 및 그 용도 |
| WO2010107654A2 (en) | 2009-03-16 | 2010-09-23 | Abaxis, Inc. | Split flow device for analyses of specific-binding partners |
| US20100240546A1 (en) | 2009-03-20 | 2010-09-23 | Samuel Chun Lap Lo | Use of biomarkers for the diagnosis and prognosis of lung cancer |
| US8741581B2 (en) * | 2009-04-27 | 2014-06-03 | Technion Research And Development Foundation Ltd. | Markers for cancer detection |
| CN101993926A (zh) | 2009-08-10 | 2011-03-30 | 芮屈生物技术(上海)有限公司 | 一种mcm2基因的原位杂交检测试剂盒及其检测方法和应用 |
| GB0921873D0 (en) | 2009-12-15 | 2010-01-27 | Cytosystems Ltd | Assay |
| WO2011082345A2 (en) | 2009-12-30 | 2011-07-07 | Brigham Young University | Compositions and methods for cancer management using antibodies binding to nucleotide salvage pathway enzymes and complexes thereof |
| WO2011097412A1 (en) | 2010-02-03 | 2011-08-11 | President And Fellows Of Harvard College | Devices and methods for multiplexed assays |
| WO2011109705A2 (en) | 2010-03-04 | 2011-09-09 | Purdue Research Foundation | Integrated assay that combines flow-cytometry and multiplexed hpv genotype identification |
| WO2011126482A1 (en) | 2010-04-07 | 2011-10-13 | Egenix, Inc. | Immunoassay for the diagnosis of prostate cancer |
| SE535084C2 (sv) | 2010-04-16 | 2012-04-10 | Prostasom Handelsbolag | Förfarande för cancerdiagnos |
| US20110262921A1 (en) | 2010-04-23 | 2011-10-27 | Sabichi Anita L | Test for the Detection of Bladder Cancer |
| US8900813B2 (en) * | 2010-08-17 | 2014-12-02 | Medical Diagnostic Laboratories, Llc | CIP2A as a biomarker in detection of cervical cancer |
| CA2814067A1 (en) | 2010-10-08 | 2012-04-12 | Ashok C. Chander | Systems, methods, and devices for measuring growth/oncogenic potential and migration/metastatic potential |
| US8658376B2 (en) * | 2010-10-20 | 2014-02-25 | Medical Diagnostic Laboratories, Llc | DEK as a urine based biomarker for bladder cancer |
| WO2012065117A2 (en) | 2010-11-12 | 2012-05-18 | William Marsh Rice University | Oral cancer point of care diagnostics |
| WO2012090479A1 (en) | 2010-12-28 | 2012-07-05 | Oncotherapy Science, Inc. | Mcm7 as a target gene for cancer therapy and diagnosis |
| GB201100223D0 (en) | 2011-01-07 | 2011-02-23 | Cytosystems Ltd | Diagnostic method |
| US20130136786A1 (en) | 2011-02-10 | 2013-05-30 | Sanford-Burnham Medical Research Institute | Long non-coding rna spry4-it1 as a diagnostic and therapeutic agent |
| RU2470301C2 (ru) | 2011-03-16 | 2012-12-20 | Учреждение Российской академии наук Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН | Способ диагностики рака мочевого пузыря с помощью онкомаркера kifc1 (варианты) и набор для его осуществления |
| RU2463354C1 (ru) | 2011-03-16 | 2012-10-10 | Учреждение Российской академии наук Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН | Способ диагностики рака мочевого пузыря с помощью онкомаркера tfdp1 (варианты) и набор для его осуществления |
| CN102707063A (zh) | 2011-03-28 | 2012-10-03 | 侯亚义 | 微小染色体维持蛋白在系统性红斑狼疮疾病诊断和防治中的作用 |
| RU2456607C1 (ru) | 2011-04-27 | 2012-07-20 | ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ "РОССИЙСКИЙ НАУЧНЫЙ ЦЕНТР РАДИОЛОГИИ И ХИРУРГИЧЕСКИХ ТЕХНОЛОГИЙ" МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ (ФГУ "РНЦРХТ" Минздравсоцразвития России) | Способ диагностики переходноклеточного рака мочевого пузыря |
| EP2705366B1 (en) | 2011-05-04 | 2017-07-12 | Pop Test LLC | Diagnostic device |
| CN102375061B (zh) | 2011-09-20 | 2014-07-30 | 国家人口计生委科学技术研究所 | 一种检测前列腺癌的elisa试剂盒 |
| US20130115599A1 (en) | 2011-11-08 | 2013-05-09 | Medical Diagnostic Laboratories, Llc | Increased cip2a expression and bladder cancer in humans |
| US9670549B2 (en) | 2011-11-10 | 2017-06-06 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Gene expression signatures of neoplasm responsiveness to therapy |
| GB201200178D0 (en) | 2012-01-06 | 2012-02-22 | Cytosystems Ltd | Diagnostic method and system |
| CN102998455B (zh) | 2012-02-14 | 2016-01-13 | 昂科生物医学技术(苏州)有限公司 | 一种检测或诊断前列腺癌的试剂盒 |
| US9638696B2 (en) | 2012-02-15 | 2017-05-02 | Biocon Limited | Process for detection and optional quantification of an analyte |
| EP2834259A4 (en) | 2012-04-02 | 2016-08-24 | Moderna Therapeutics Inc | MODIFIED POLYNUCLEOTIDES |
| JP2012196211A (ja) | 2012-04-10 | 2012-10-18 | Japan Science & Technology Agency | 前立腺癌マーカポリペプチド、該ポリペプチドに対する抗体、及び該ポリペプチドを利用した前立腺癌の診断方法 |
| WO2013181418A2 (en) | 2012-05-30 | 2013-12-05 | Clarient Diagnostic Services, Inc. | Multiplexed diagnosis method for classical hodgkin lymphoma |
| US20150147761A1 (en) | 2012-06-20 | 2015-05-28 | Helmut E. Meyer | Specific biomarkers for hepatocellular carcinoma (hcc) |
| US20150218646A1 (en) | 2012-07-20 | 2015-08-06 | Diagnocure Inc | Methods, kits and compositions for providing a clinical assessment of prostate cancer |
| US10613087B2 (en) | 2012-08-10 | 2020-04-07 | Analiza, Inc. | Methods and devices for analyzing species to determine diseases |
| WO2014032899A1 (en) | 2012-08-31 | 2014-03-06 | Novo Nordisk A/S | Diagnosis and treatment of lupus nephritis |
| US20150226743A1 (en) | 2012-10-28 | 2015-08-13 | Clarient Diagnostics Services, Inc. | Multiplexed method for diagnosing classical hodgkin lymphoma |
| WO2014071029A1 (en) | 2012-10-31 | 2014-05-08 | The General Hospital Corporation | Methods and assays for treatment of bladder cancer |
| RU2522231C1 (ru) | 2012-11-14 | 2014-07-10 | Евгений Иосифович Гоуфман | Способ диагностики онкологических заболеваний и иммуноферментный набор для его осуществления |
| MY176888A (en) | 2012-11-26 | 2020-08-25 | Univ Sains Malaysia | Method for detection of target analyte(s) |
| US8945827B2 (en) * | 2013-03-13 | 2015-02-03 | Awareness Technology, Inc. | Serological methods and diagnostic tests for syphilis antibodies |
| GB201316347D0 (en) * | 2013-09-13 | 2013-10-30 | Cancer Rec Tech Ltd | Biological fluid filtration assembly |
| CN103558384A (zh) | 2013-11-08 | 2014-02-05 | 点亮生物科技无锡有限公司 | 一种同时检测四种肿瘤标志物的化学发光试剂盒及其制备方法 |
| CN103725599B (zh) | 2014-01-14 | 2015-05-27 | 刘韬 | 一种流体膜过滤细胞分离装置 |
| KR101627408B1 (ko) | 2014-03-06 | 2016-06-03 | 김홍 | 고농축 혈장 추출장치 및 방법 |
| JP6854246B2 (ja) * | 2015-06-08 | 2021-04-07 | アーケア ダイアグノスティクス リミテッド | 尿サンプルの分析方法 |
| EP4060344A1 (en) * | 2015-06-08 | 2022-09-21 | Arquer Diagnostics Limited | Methods and kits |
-
2016
- 2016-06-01 JP JP2017564356A patent/JP6854246B2/ja not_active Expired - Fee Related
- 2016-06-01 US US15/580,657 patent/US11519916B2/en active Active
- 2016-06-01 EP EP16727797.9A patent/EP3304082B1/en active Active
- 2016-06-01 CN CN201680033479.6A patent/CN107771285A/zh active Pending
- 2016-06-01 WO PCT/GB2016/051608 patent/WO2016198833A2/en not_active Ceased
- 2016-06-01 ES ES16727797T patent/ES2806498T3/es active Active
-
2022
- 2022-10-21 US US17/970,775 patent/US20230184773A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN107771285A (zh) | 2018-03-06 |
| JP2018523110A (ja) | 2018-08-16 |
| US20230184773A1 (en) | 2023-06-15 |
| WO2016198833A3 (en) | 2017-03-16 |
| EP3304082B1 (en) | 2020-05-13 |
| US20180203012A1 (en) | 2018-07-19 |
| EP3304082A2 (en) | 2018-04-11 |
| JP6854246B2 (ja) | 2021-04-07 |
| US11519916B2 (en) | 2022-12-06 |
| WO2016198833A2 (en) | 2016-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2806498T3 (es) | Métodos para el análisis de una muestra de orina | |
| ES2347485T3 (es) | Uso de la proteina s100a12, como marcador para el cancer colorrectal. | |
| ES2911415T3 (es) | Métodos y kits | |
| CN103547923B (zh) | 乳腺癌的生物标记 | |
| NZ577548A (en) | Cancer biomarkers | |
| Varma et al. | Polyclonal anti-PSA is more sensitive but less specific than monoclonal anti-PSA: implications for diagnostic prostatic pathology | |
| ES2394925T3 (es) | Uso de N-miristoiltransferasa en tejido no tumoral para el diagnóstico de cáncer | |
| CN101680898A (zh) | Timp-1作为结肠直肠癌标志的用途 | |
| US8211659B2 (en) | Methods and kits for detection of cancer metastasis | |
| ES2316997T3 (es) | Uso de la proteina proteinasa 3 (prn3) y del inhibidor de la elastasa leucocitaria (ileu) como un marcador para el cancer colorrectal. | |
| ES2938313T3 (es) | Uso de MCM5 como marcador para los cánceres ginecológicos | |
| Santinelli et al. | α-Methylacyl coenzyme A racemase, Ki-67, and topoisomerase IIα in cystoprostatectomies with incidental prostate cancer | |
| ES2818089T3 (es) | Procedimiento de detección del cáncer | |
| JP2012519290A (ja) | 肺の扁平上皮癌のためのマーカーとしてのセルピンb13 | |
| Obaitan et al. | Management of Idiopathic Acute Pancreatitis and Recurrent Acute Pancreatitis | |
| HK1142130A (en) | Use of timp-1 as a marker for colorectal cancer | |
| Sachdev et al. | Characterization of a Cancer Biomarker Sas1b for the Early Detection of Cervical Cancer | |
| ES2455745A1 (es) | Empleo del receptor de cannabinoides CB1 como marcador de carcinoma renal de células cromófobas (CRCCh) y oncocitoma renal (OR) |