ES2768330T3 - Membranas de intercambio aniónico y proceso para su producción - Google Patents
Membranas de intercambio aniónico y proceso para su producción Download PDFInfo
- Publication number
- ES2768330T3 ES2768330T3 ES11833543T ES11833543T ES2768330T3 ES 2768330 T3 ES2768330 T3 ES 2768330T3 ES 11833543 T ES11833543 T ES 11833543T ES 11833543 T ES11833543 T ES 11833543T ES 2768330 T3 ES2768330 T3 ES 2768330T3
- Authority
- ES
- Spain
- Prior art keywords
- membrane
- substrate
- solution
- resistance
- monomer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 35
- 230000008569 process Effects 0.000 title claims abstract description 18
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 10
- 239000003011 anion exchange membrane Substances 0.000 title description 14
- 239000000758 substrate Substances 0.000 claims abstract description 44
- 239000000178 monomer Substances 0.000 claims abstract description 26
- 239000003014 ion exchange membrane Substances 0.000 claims abstract description 19
- 238000000909 electrodialysis Methods 0.000 claims abstract description 18
- 239000011148 porous material Substances 0.000 claims abstract description 17
- 238000006116 polymerization reaction Methods 0.000 claims abstract description 11
- 239000003505 polymerization initiator Substances 0.000 claims abstract description 7
- 229920000642 polymer Polymers 0.000 claims abstract description 6
- 229920006395 saturated elastomer Polymers 0.000 claims abstract description 6
- 238000004132 cross linking Methods 0.000 claims abstract description 5
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 4
- 238000005349 anion exchange Methods 0.000 claims abstract description 3
- 238000009738 saturating Methods 0.000 claims abstract description 3
- KKFHAJHLJHVUDM-UHFFFAOYSA-N n-vinylcarbazole Chemical compound C1=CC=C2N(C=C)C3=CC=CC=C3C2=C1 KKFHAJHLJHVUDM-UHFFFAOYSA-N 0.000 claims abstract 2
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 claims description 10
- SLBOQBILGNEPEB-UHFFFAOYSA-N 1-chloroprop-2-enylbenzene Chemical compound C=CC(Cl)C1=CC=CC=C1 SLBOQBILGNEPEB-UHFFFAOYSA-N 0.000 claims description 8
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical group ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 claims description 6
- 229940073608 benzyl chloride Drugs 0.000 claims description 6
- -1 polypropylene Polymers 0.000 claims description 5
- 239000004342 Benzoyl peroxide Substances 0.000 claims description 3
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical group C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 claims description 3
- 235000019400 benzoyl peroxide Nutrition 0.000 claims description 3
- LWMFAFLIWMPZSX-UHFFFAOYSA-N bis[2-(4,5-dihydro-1h-imidazol-2-yl)propan-2-yl]diazene Chemical compound N=1CCNC=1C(C)(C)N=NC(C)(C)C1=NCCN1 LWMFAFLIWMPZSX-UHFFFAOYSA-N 0.000 claims description 3
- DBCAQXHNJOFNGC-UHFFFAOYSA-N 4-bromo-1,1,1-trifluorobutane Chemical compound FC(F)(F)CCCBr DBCAQXHNJOFNGC-UHFFFAOYSA-N 0.000 claims description 2
- 239000002033 PVDF binder Substances 0.000 claims description 2
- LXEKPEMOWBOYRF-UHFFFAOYSA-N [2-[(1-azaniumyl-1-imino-2-methylpropan-2-yl)diazenyl]-2-methylpropanimidoyl]azanium;dichloride Chemical compound Cl.Cl.NC(=N)C(C)(C)N=NC(C)(C)C(N)=N LXEKPEMOWBOYRF-UHFFFAOYSA-N 0.000 claims description 2
- STVZJERGLQHEKB-UHFFFAOYSA-N ethylene glycol dimethacrylate Substances CC(=C)C(=O)OCCOC(=O)C(C)=C STVZJERGLQHEKB-UHFFFAOYSA-N 0.000 claims description 2
- QYZFTMMPKCOTAN-UHFFFAOYSA-N n-[2-(2-hydroxyethylamino)ethyl]-2-[[1-[2-(2-hydroxyethylamino)ethylamino]-2-methyl-1-oxopropan-2-yl]diazenyl]-2-methylpropanamide Chemical compound OCCNCCNC(=O)C(C)(C)N=NC(C)(C)C(=O)NCCNCCO QYZFTMMPKCOTAN-UHFFFAOYSA-N 0.000 claims description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 claims description 2
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 claims 2
- 239000003112 inhibitor Substances 0.000 claims 2
- 150000001451 organic peroxides Chemical group 0.000 claims 2
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical group COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 claims 2
- VUAXHMVRKOTJKP-UHFFFAOYSA-N 2,2-dimethylbutyric acid Chemical compound CCC(C)(C)C(O)=O VUAXHMVRKOTJKP-UHFFFAOYSA-N 0.000 claims 1
- XESZUVZBAMCAEJ-UHFFFAOYSA-N 4-tert-butylcatechol Chemical compound CC(C)(C)C1=CC=C(O)C(O)=C1 XESZUVZBAMCAEJ-UHFFFAOYSA-N 0.000 claims 1
- 239000004705 High-molecular-weight polyethylene Substances 0.000 claims 1
- 239000004743 Polypropylene Substances 0.000 claims 1
- 239000004699 Ultra-high molecular weight polyethylene Substances 0.000 claims 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 claims 1
- 229920001155 polypropylene Polymers 0.000 claims 1
- 229920000785 ultra high molecular weight polyethylene Polymers 0.000 claims 1
- 230000000977 initiatory effect Effects 0.000 abstract description 2
- 239000012528 membrane Substances 0.000 description 90
- 210000004027 cell Anatomy 0.000 description 37
- 239000000243 solution Substances 0.000 description 37
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 30
- 239000011780 sodium chloride Substances 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 229920002799 BoPET Polymers 0.000 description 12
- 239000005041 Mylar™ Substances 0.000 description 12
- 238000005259 measurement Methods 0.000 description 10
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 9
- 229910052782 aluminium Inorganic materials 0.000 description 9
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 9
- 150000001450 anions Chemical class 0.000 description 9
- 150000002500 ions Chemical class 0.000 description 9
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 238000005341 cation exchange Methods 0.000 description 8
- 239000010410 layer Substances 0.000 description 8
- 229920006267 polyester film Polymers 0.000 description 7
- 238000005303 weighing Methods 0.000 description 7
- OSSNTDFYBPYIEC-UHFFFAOYSA-N 1-ethenylimidazole Chemical compound C=CN1C=CN=C1 OSSNTDFYBPYIEC-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 230000003750 conditioning effect Effects 0.000 description 6
- 229910001873 dinitrogen Inorganic materials 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 239000004033 plastic Substances 0.000 description 6
- 229920003023 plastic Polymers 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- 238000011161 development Methods 0.000 description 5
- 238000010790 dilution Methods 0.000 description 5
- 239000012895 dilution Substances 0.000 description 5
- 239000013535 sea water Substances 0.000 description 5
- 229920006037 cross link polymer Polymers 0.000 description 4
- 238000010612 desalination reaction Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000009296 electrodeionization Methods 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- 229920000728 polyester Polymers 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 150000003512 tertiary amines Chemical class 0.000 description 4
- 230000032258 transport Effects 0.000 description 4
- MSBLMBWXUVQCDY-UHFFFAOYSA-N 1-(4,4-dimethyl-1-piperazin-4-iumyl)ethanone Chemical compound CC(=O)N1CC[N+](C)(C)CC1 MSBLMBWXUVQCDY-UHFFFAOYSA-N 0.000 description 3
- 101000988793 Homo sapiens Host cell factor C1 regulator 1 Proteins 0.000 description 3
- 101000613207 Homo sapiens Pre-B-cell leukemia transcription factor-interacting protein 1 Proteins 0.000 description 3
- 102100029105 Host cell factor C1 regulator 1 Human genes 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 150000001768 cations Chemical class 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 239000003792 electrolyte Substances 0.000 description 3
- 239000000446 fuel Substances 0.000 description 3
- 238000005342 ion exchange Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 229920000098 polyolefin Polymers 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 2
- KGIGUEBEKRSTEW-UHFFFAOYSA-N 2-vinylpyridine Chemical compound C=CC1=CC=CC=N1 KGIGUEBEKRSTEW-UHFFFAOYSA-N 0.000 description 2
- VVJKKWFAADXIJK-UHFFFAOYSA-N Allylamine Chemical compound NCC=C VVJKKWFAADXIJK-UHFFFAOYSA-N 0.000 description 2
- 239000004971 Cross linker Substances 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- 229910021607 Silver chloride Inorganic materials 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- ROOXNKNUYICQNP-UHFFFAOYSA-N ammonium persulfate Chemical compound [NH4+].[NH4+].[O-]S(=O)(=O)OOS([O-])(=O)=O ROOXNKNUYICQNP-UHFFFAOYSA-N 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000012141 concentrate Substances 0.000 description 2
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 2
- 230000005684 electric field Effects 0.000 description 2
- 238000002848 electrochemical method Methods 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000009499 grossing Methods 0.000 description 2
- 239000003999 initiator Substances 0.000 description 2
- 239000003456 ion exchange resin Substances 0.000 description 2
- 229920003303 ion-exchange polymer Polymers 0.000 description 2
- 125000003010 ionic group Chemical group 0.000 description 2
- 238000011005 laboratory method Methods 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000012982 microporous membrane Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 238000001223 reverse osmosis Methods 0.000 description 2
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229920002818 (Hydroxyethyl)methacrylate Polymers 0.000 description 1
- VANWFJFIBPQSIT-UHFFFAOYSA-N 1,1-difluoroethene hydrochloride Chemical compound Cl.FC(F)=C VANWFJFIBPQSIT-UHFFFAOYSA-N 0.000 description 1
- QTKPMCIBUROOGY-UHFFFAOYSA-N 2,2,2-trifluoroethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC(F)(F)F QTKPMCIBUROOGY-UHFFFAOYSA-N 0.000 description 1
- JJBFVQSGPLGDNX-UHFFFAOYSA-N 2-(2-methylprop-2-enoyloxy)propyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC(C)COC(=O)C(C)=C JJBFVQSGPLGDNX-UHFFFAOYSA-N 0.000 description 1
- BTVWZWFKMIUSGS-UHFFFAOYSA-N 2-methylpropane-1,2-diol Chemical compound CC(C)(O)CO BTVWZWFKMIUSGS-UHFFFAOYSA-N 0.000 description 1
- DXIJHCSGLOHNES-UHFFFAOYSA-N 3,3-dimethylbut-1-enylbenzene Chemical compound CC(C)(C)C=CC1=CC=CC=C1 DXIJHCSGLOHNES-UHFFFAOYSA-N 0.000 description 1
- JLBJTVDPSNHSKJ-UHFFFAOYSA-N 4-Methylstyrene Chemical compound CC1=CC=C(C=C)C=C1 JLBJTVDPSNHSKJ-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- UYTJTHAIXYEYKS-UHFFFAOYSA-N CCC=C(C)C(Cl)=O.CN(C)C Chemical compound CCC=C(C)C(Cl)=O.CN(C)C UYTJTHAIXYEYKS-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 229920010741 Ultra High Molecular Weight Polyethylene (UHMWPE) Polymers 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 1
- 229910001870 ammonium persulfate Inorganic materials 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- XFOZBWSTIQRFQW-UHFFFAOYSA-M benzyl-dimethyl-prop-2-enylazanium;chloride Chemical compound [Cl-].C=CC[N+](C)(C)CC1=CC=CC=C1 XFOZBWSTIQRFQW-UHFFFAOYSA-M 0.000 description 1
- 235000013361 beverage Nutrition 0.000 description 1
- 229940075397 calomel Drugs 0.000 description 1
- 239000003518 caustics Substances 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000010924 continuous production Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- ZOMNIUBKTOKEHS-UHFFFAOYSA-L dimercury dichloride Chemical compound Cl[Hg][Hg]Cl ZOMNIUBKTOKEHS-UHFFFAOYSA-L 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000000840 electrochemical analysis Methods 0.000 description 1
- 238000004070 electrodeposition Methods 0.000 description 1
- 239000008151 electrolyte solution Substances 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 238000009713 electroplating Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- AINBZKYUNWUTRE-UHFFFAOYSA-N ethanol;propan-2-ol Chemical compound CCO.CC(C)O AINBZKYUNWUTRE-UHFFFAOYSA-N 0.000 description 1
- FWDBOZPQNFPOLF-UHFFFAOYSA-N ethenyl(triethoxy)silane Chemical compound CCO[Si](OCC)(OCC)C=C FWDBOZPQNFPOLF-UHFFFAOYSA-N 0.000 description 1
- NKSJNEHGWDZZQF-UHFFFAOYSA-N ethenyl(trimethoxy)silane Chemical compound CO[Si](OC)(OC)C=C NKSJNEHGWDZZQF-UHFFFAOYSA-N 0.000 description 1
- ZLNAFSPCNATQPQ-UHFFFAOYSA-N ethenyl-dimethoxy-methylsilane Chemical compound CO[Si](C)(OC)C=C ZLNAFSPCNATQPQ-UHFFFAOYSA-N 0.000 description 1
- WOXXJEVNDJOOLV-UHFFFAOYSA-N ethenyl-tris(2-methoxyethoxy)silane Chemical compound COCCO[Si](OCCOC)(OCCOC)C=C WOXXJEVNDJOOLV-UHFFFAOYSA-N 0.000 description 1
- SUPCQIBBMFXVTL-UHFFFAOYSA-N ethyl 2-methylprop-2-enoate Chemical compound CCOC(=O)C(C)=C SUPCQIBBMFXVTL-UHFFFAOYSA-N 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000013505 freshwater Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- VOZRXNHHFUQHIL-UHFFFAOYSA-N glycidyl methacrylate Chemical compound CC(=C)C(=O)OCC1CO1 VOZRXNHHFUQHIL-UHFFFAOYSA-N 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000037427 ion transport Effects 0.000 description 1
- 230000005865 ionizing radiation Effects 0.000 description 1
- 230000009191 jumping Effects 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- DCUFMVPCXCSVNP-UHFFFAOYSA-N methacrylic anhydride Chemical compound CC(=C)C(=O)OC(=O)C(C)=C DCUFMVPCXCSVNP-UHFFFAOYSA-N 0.000 description 1
- ZQMHJBXHRFJKOT-UHFFFAOYSA-N methyl 2-[(1-methoxy-2-methyl-1-oxopropan-2-yl)diazenyl]-2-methylpropanoate Chemical compound COC(=O)C(C)(C)N=NC(C)(C)C(=O)OC ZQMHJBXHRFJKOT-UHFFFAOYSA-N 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 239000005518 polymer electrolyte Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- HJWLCRVIBGQPNF-UHFFFAOYSA-N prop-2-enylbenzene Chemical compound C=CCC1=CC=CC=C1 HJWLCRVIBGQPNF-UHFFFAOYSA-N 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000004575 stone Substances 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 229920001187 thermosetting polymer Polymers 0.000 description 1
- UZNHKBFIBYXPDV-UHFFFAOYSA-N trimethyl-[3-(2-methylprop-2-enoylamino)propyl]azanium;chloride Chemical compound [Cl-].CC(=C)C(=O)NCCC[N+](C)(C)C UZNHKBFIBYXPDV-UHFFFAOYSA-N 0.000 description 1
- OEIXGLMQZVLOQX-UHFFFAOYSA-N trimethyl-[3-(prop-2-enoylamino)propyl]azanium;chloride Chemical compound [Cl-].C[N+](C)(C)CCCNC(=O)C=C OEIXGLMQZVLOQX-UHFFFAOYSA-N 0.000 description 1
- 238000009489 vacuum treatment Methods 0.000 description 1
- 239000002351 wastewater Substances 0.000 description 1
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D69/00—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor
- B01D69/02—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor characterised by their properties
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F212/02—Monomers containing only one unsaturated aliphatic radical
- C08F212/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F212/14—Monomers containing only one unsaturated aliphatic radical containing one ring substituted by heteroatoms or groups containing heteroatoms
- C08F212/16—Halogens
- C08F212/18—Chlorine
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D67/00—Processes specially adapted for manufacturing semi-permeable membranes for separation processes or apparatus
- B01D67/0002—Organic membrane manufacture
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D69/00—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor
- B01D69/10—Supported membranes; Membrane supports
- B01D69/107—Organic support material
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/46—Treatment of water, waste water, or sewage by electrochemical methods
- C02F1/469—Treatment of water, waste water, or sewage by electrochemical methods by electrochemical separation, e.g. by electro-osmosis, electrodialysis, electrophoresis
- C02F1/4693—Treatment of water, waste water, or sewage by electrochemical methods by electrochemical separation, e.g. by electro-osmosis, electrodialysis, electrophoresis electrodialysis
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/46—Treatment of water, waste water, or sewage by electrochemical methods
- C02F1/469—Treatment of water, waste water, or sewage by electrochemical methods by electrochemical separation, e.g. by electro-osmosis, electrodialysis, electrophoresis
- C02F1/4693—Treatment of water, waste water, or sewage by electrochemical methods by electrochemical separation, e.g. by electro-osmosis, electrodialysis, electrophoresis electrodialysis
- C02F1/4695—Treatment of water, waste water, or sewage by electrochemical methods by electrochemical separation, e.g. by electro-osmosis, electrodialysis, electrophoresis electrodialysis electrodeionisation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F12/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F12/02—Monomers containing only one unsaturated aliphatic radical
- C08F12/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F12/14—Monomers containing only one unsaturated aliphatic radical containing one ring substituted by hetero atoms or groups containing heteroatoms
- C08F12/16—Halogens
- C08F12/18—Chlorine
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F212/02—Monomers containing only one unsaturated aliphatic radical
- C08F212/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F212/14—Monomers containing only one unsaturated aliphatic radical containing one ring substituted by heteroatoms or groups containing heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F226/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen
- C08F226/06—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen by a heterocyclic ring containing nitrogen
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/22—Fuel cells in which the fuel is based on materials comprising carbon or oxygen or hydrogen and other elements; Fuel cells in which the fuel is based on materials comprising only elements other than carbon, oxygen or hydrogen
- H01M8/227—Dialytic cells or batteries; Reverse electrodialysis cells or batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01Q—ANTENNAS, i.e. RADIO AERIALS
- H01Q3/00—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system
- H01Q3/26—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture
- H01Q3/30—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01Q—ANTENNAS, i.e. RADIO AERIALS
- H01Q3/00—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system
- H01Q3/26—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture
- H01Q3/30—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array
- H01Q3/34—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01Q—ANTENNAS, i.e. RADIO AERIALS
- H01Q3/00—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system
- H01Q3/26—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture
- H01Q3/30—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array
- H01Q3/34—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means
- H01Q3/36—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means with variable phase-shifters
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01Q—ANTENNAS, i.e. RADIO AERIALS
- H01Q3/00—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system
- H01Q3/26—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture
- H01Q3/30—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array
- H01Q3/34—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means
- H01Q3/36—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means with variable phase-shifters
- H01Q3/38—Arrangements for changing or varying the orientation or the shape of the directional pattern of the waves radiated from an antenna or antenna system varying the relative phase or relative amplitude of energisation between two or more active radiating elements; varying the distribution of energy across a radiating aperture varying the relative phase between the radiating elements of an array by electrical means with variable phase-shifters the phase-shifters being digital
-
- H—ELECTRICITY
- H03—ELECTRONIC CIRCUITRY
- H03K—PULSE TECHNIQUE
- H03K5/00—Manipulating of pulses not covered by one of the other main groups of this subclass
- H03K5/01—Shaping pulses
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2323/00—Details relating to membrane preparation
- B01D2323/30—Cross-linking
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2323/00—Details relating to membrane preparation
- B01D2323/40—Details relating to membrane preparation in-situ membrane formation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2325/00—Details relating to properties of membranes
- B01D2325/16—Membrane materials having positively charged functional groups
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2325/00—Details relating to properties of membranes
- B01D2325/42—Ion-exchange membranes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/42—Electrodialysis; Electro-osmosis ; Electro-ultrafiltration; Membrane capacitive deionization
- B01D61/44—Ion-selective electrodialysis
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F2103/00—Nature of the water, waste water, sewage or sludge to be treated
- C02F2103/08—Seawater, e.g. for desalination
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F2201/00—Apparatus for treatment of water, waste water or sewage
- C02F2201/46—Apparatus for electrochemical processes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2327/00—Characterised by the use of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Derivatives of such polymers
- C08J2327/02—Characterised by the use of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Derivatives of such polymers not modified by chemical after-treatment
- C08J2327/04—Characterised by the use of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a halogen; Derivatives of such polymers not modified by chemical after-treatment containing chlorine atoms
- C08J2327/06—Homopolymers or copolymers of vinyl chloride
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2379/00—Characterised by the use of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen with or without oxygen, or carbon only, not provided for in groups C08J2361/00 - C08J2377/00
- C08J2379/04—Polycondensates having nitrogen-containing heterocyclic rings in the main chain; Polyhydrazides; Polyamide acids or similar polyimide precursors
- C08J2379/06—Polyhydrazides; Polytriazoles; Polyamino-triazoles; Polyoxadiazoles
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/20—Manufacture of shaped structures of ion-exchange resins
- C08J5/22—Films, membranes or diaphragms
- C08J5/2206—Films, membranes or diaphragms based on organic and/or inorganic macromolecular compounds
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M2008/1095—Fuel cells with polymeric electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0082—Organic polymers
-
- H—ELECTRICITY
- H03—ELECTRONIC CIRCUITRY
- H03K—PULSE TECHNIQUE
- H03K5/00—Manipulating of pulses not covered by one of the other main groups of this subclass
- H03K2005/00286—Phase shifter, i.e. the delay between the output and input pulse is dependent on the frequency, and such that a phase difference is obtained independent of the frequency
Abstract
Un proceso para la producción de una membrana de intercambio iónico capaz de usarse para la electrodiálisis, que comprende: elegir un sustrato poroso adecuado; saturar las regiones porosas del sustrato con una solución monomérica que comprende al menos un monómero funcional seleccionado del grupo que consiste en vinilmidazol y vinilcarbazol, al menos un monómero de reticulación, al menos un agente de cuaternización, y al menos un iniciador de la polimerización; retirar la solución en exceso de las superficies del sustrato mientras se deja el volumen poroso saturado con la solución; e iniciar la polimerización para formar un polímero de intercambio aniónico reticulado básicamente rellenando completamente los poros del sustrato.
Description
DESCRIPCIÓN
Membranas de intercambio aniónico y proceso para su producción
Campo
Las realizaciones de la presente invención proporcionan procesos para la fabricación de membranas de intercambio iónico.
Antecedentes
Las membranas de intercambio aniónico transportan aniones bajo un potencial eléctrico o químico. Las membranas de intercambio aniónico tendrán cargas positivas fijas y aniones cargados negativamente móviles. Las propiedades de la membrana de intercambio iónico están controladas por la cantidad, el tipo y la distribución de los grupos iónicos fijos.
Las aminas cuaternarias y terciarias producen respectivamente los grupos cargados positivos fijos en membranas de intercambio aniónico de base fuerte y débil.
Entre las aplicaciones más importantes de las membranas de intercambio iónico están la desalinización del agua por electrodiálisis (ED), como una fuente generadora de energía en electrodiálisis inversa y como separadores en celdas de combustibles. Otras aplicaciones incluyen la recuperación de iones metálicos en las industrias de galvanoplastía y acabado de metales y diversas aplicaciones en la industria alimentaria y de bebidas.
La electrodiálisis desaliniza el agua transfiriendo iones y algunos compuestos orgánicos cargados a través de membranas selectivas de catión y anión emparejadas bajo la fuerza motriz de un voltaje de corriente. Un aparato de ED consiste en membranas selectivas de catión y selectivas de anión eléctricamente conductivas y básicamente impermeables al agua dispuestas como paredes opuestas de una celda. Las celdas adyacentes forman un par de celda. Las pilas de membrana consisten en muchos, algunos cientos de pares de celda, y un sistema de ED puede consistir en muchas pilas. Cada pila de membrana tiene un ánodo de CD (corriente directa) en un extremo de la pila y un cátodo de CD en el otro extremo. Bajo un voltaje de CD, los iones se mueven al electrodo de la carga opuesta. Un par de celda consiste en dos tipos de celdas, una celda de dilución y una celda de concentración. Como ejemplo ilustrativo, considerar un par de celda con una pared de membrana de intercambio catiónico común y dos paredes de membrana de intercambio aniónico que forman las dos celdas. Es decir, una primera membrana de intercambio aniónico y la membrana de intercambio catiónico forman la celda diluida y la membrana de intercambio catiónico y una segunda membrana aniónica forman la celda de concentración. En la celda de dilución, los cationes pasarán a través de la membrana de intercambio catiónico enfrentada al ánodo, pero será parada por la membrana de intercambio aniónico emparejada de la celda de concentración en esa dirección enfrentada al cátodo. Igualmente, los aniones pasan a través de la membrana de intercambio aniónico de la celda de dilución enfrentada al cátodo, pero será parada por la membrana de intercambio catiónico del par adyacente enfrentado al ánodo. De esta manera, se retirará la sal en una celda de dilución y se meterá en las celdas de concentración adyacentes desde una dirección y los aniones desde la dirección opuesta. El flujo en la pila se dispone de manera que los flujos diluido y concentrado se mantienen separados y se produce una corriente de agua desalinizada desde el flujo diluido.
En el proceso de ED, el material comúnmente se desarrolla en la superficie de la membrana en la dirección del campo eléctrico, el cual puede, y normalmente reduce la eficiencia del proceso. Para combatir este efecto, se desarrolló la inversión de electrodiálisis (EDR, del inglés “Electrodialysis Reversal”) y es el método principal de uso actualmente. En la EDR, los electrodos se invierten en polaridad sobre una base regular, por ejemplo, cada quince a sesenta minutos. Los flujos diluido y concentrado también se intercambian simultáneamente, llegando a ser el concentrado el flujo diluido y viceversa. De este modo los depósitos contaminantes se retiran y se limpian.
Una vez que la concentración en las celdas de dilución baja a menos de 2.000 miligramos/litro (mg/l), la resistencia eléctrica está a un nivel en el que la demanda de energía llega a ser cada vez más cara. Para superar esto, y ser capaz de producir agua de alta calidad, se desarrolló la electrodesionización (EDI), algunas veces denominada electrodesionización continua (CEDI, del inglés “Continuos Electrodeionization”). En este método las celdas se rellenan con medio de intercambio iónico, normalmente perlas de resina de intercambio iónico. El medio de intercambio iónico está en órdenes de magnitud más conductivos que la solución. Los iones se transportan por las perlas a la superficie de la membrana para transferirse a las celdas de concentrado. La EDI es capaz de producir agua más pura que la ED a menos energía cuando la concentración suministrada se reduce suficientemente.
Los procesos de ED para la desalinización de agua tienen ventajas sobre la RO. Requieren menos pretratamiento lo cual reducirá los costes de funcionamiento. Tendrán mayor recuperación de agua de producto y una mayor concentración de solución salina, es decir, se dispone de menos solución salina.
Las membranas selectivas univalentes o selectivas monovalentes principalmente transfieren iones monovalentes. Las membranas de intercambio catiónico selectivas monovalentes principalmente transfieren sodio o potasio. Asimismo, las membranas aniónicas selectivas monovalentes transfieren iones tales como cloruro, bromuro, y
nitrato.
La osmosis inversa (RO, del inglés “Reverse Osmosis”) domina la producción de agua fresca a partir de agua de mar por procesos de membrana. Mientras que la electrodiálisis (ED) se usa para la desalinización de agua salobre y aguas residuales, generalmente se considera demasiado cara para su uso para agua de mar. Para ser competitiva con la RO, la ED y EDR requerirán resistencia de membrana de menos de 1 Ohm cm2, preferiblemente menos de 0,8 Ohm cm2, y lo más preferiblemente menos de 0,5 Ohm cm2. Se desea permselectividad iónica de más del 90 %, más preferiblemente más del 95 %, y lo más preferiblemente más del 98 %. La membrana debe tener larga vida útil, y ser físicamente fuerte y químicamente durable y ser de bajo coste.
La electrodiálisis inversa (RED, del inglés “Reverse electrodialysis”) convierte la energía libre generada al mezclar las dos soluciones acuosas de diferentes salinidades en energía eléctrica. A mayor diferencia de salinidad, mayor potencial de generación de energía. Por ejemplo, los investigadores han estudiado la RED usando agua del Mar Muerto y fresca o agua de mar.
Investigadores en Holanda han mezclado el agua de río que entra en el mar y el agua de mar. Las membranas de RED preferiblemente tendrán una resistencia eléctrica baja y una alta selectividad coiónica y largo tiempo de vida útil, resistencia aceptable y estabilidad dimensional y, de manera importante, bajo coste.
La membrana de electrolito polimérico (PEM, del inglés “Polymer Electrolyte Membrane”) es un tipo de membrana de intercambio iónico que sirve tanto de electrolito como de separador para prevenir la mezcla física directa del hidrógeno del ánodo y el oxígeno suministrado al cátodo. Una PEM contiene grupos positivamente cargados, normalmente grupos de ácido sulfónico, unidos o como parte del polímero que compone la PEM. Los protones migran a través de la membrana saltando de una carga positiva fija a otra para penetrar la membrana.
Los requerimientos de la PEM incluyen estabilidad química, térmica y electroquímica, y adecuada estabilidad mecánica y resistencia cuando se hincha y bajo estrés mecánico. Otros requerimientos incluyen baja resistencia, bajo o preferiblemente no transporte de metanol en celdas de combustible de metanol directo (DMFC, del inglés “Direct Methanol Fuel Cell”), y bajo coste.
Las membranas bipolares están hechas de una membrana de intercambio catiónico y una de intercambio aniónico en extractos o unidas, algunas con una fina capa neutra entremedias. Bajo un campo eléctrico el agua se divide en iones H+ y OH-. Los iones de hidroxilo se transportan a través de la membrana de intercambio aniónico y los iones H+ a través de la capa de intercambio aniónico y formarán la base y el ácido en las respectivas celdas. Los ácidos orgánicos también se producen usando membranas bipolares.
El desarrollo de las membranas de intercambio iónico requiere una optimización de las propiedades para superar los efectos competentes. Tradicionalmente se ha tenido que encontrar en las membranas de intercambio iónico para la desalinización de agua cuatro características principales para ser consideradas con éxito. Estas son:
Baja resistencia eléctrica para reducir la caída potencial durante el funcionamiento e incrementar la eficiencia energética.
Alta permselectividad - es decir, alta permeabilidad a contraiones pero aproximadamente impermeable a coiones. Alta estabilidad química - capacidad de resistir pH de 0 a 14 y compuestos químicos oxidantes.
Resistencia mecánica - La membrana debe ser capaz de resistir las tensiones de ser manejada cuando se está fabricando en un módulo u otro dispositivo de procesamiento. La membrana también debe tener buena estabilidad dimensional en el funcionamiento y no hincharse o encogerse excesivamente cuando el fluido que se pone en contacto con la misma cambia la concentración o la temperatura.
Los desarrolladores de membrana han reconocido que para un compuesto químico dado usado para producir una membrana de intercambio iónico, una membrana más fina debería dar una resistencia inferior y también dejar más área de membrana por unidad de volumen del dispositivo. Sin embargo, las membranas más finas son más susceptibles a cambio dimensional a partir de los efectos ambientales, tales como los cambios en la concentración iónica de los fluidos que se ponen en contacto con las mismas o que intervienen en los cambios de temperatura. Además, desarrollar y producir membranas libres de defecto es más difícil para el caso de membranas más finas debido a que hay menos margen de error durante la producción de membrana que el que hay para membranas más espesas donde el espesor de la membrana cubre los defectos que se pueden dar en la formación de la membrana. Los siguientes documentos pueden ser útiles en el entendimiento de la presente descripción: el documento JP 2010 92660 A (también el documento EP 2333887 A1) describe la producción de una membrana de intercambio aniónico para una celda de combustible de tipo electrolito polimérico sólido; el documento WO 03/008078 A2 describe membranas microporosas rellenadas con gel asimétricas que tienen un gradiente de densidad de gel en la dimensión del espesor de la membrana; el documento US 6 117297 A describe un aparato de electrodiálisis que incluye un marco que define la cavidad, conteniendo la cavidad un cuerpo permeable a fluido de resina de intercambio iónico encerrada en una lámina de intercambio iónico.
Descripción detallada
La solicitud internacional PCT/US 10/46777 describe un método para fabricar membranas de intercambio iónico producidas por polimerización de uno o más monómeros ionogénicos monofuncionales con al menos un monómero multifuncional en los poros de un sustrato poroso. En la presente memoria se describe un proceso según la reivindicación 1 para producir una membrana de intercambio aniónico de electrodiálisis. Como se describe en la presente memoria el inventor ha encontrado que usando monómeros funcionales que tienen un grupo amina terciaria con un compuesto químico de cuaternización, se pueden producir membranas de intercambio aniónico de alta permeabilidad baja resistencia y buena resistencia química. Los grupos funcionales de amonio cuaternario son fuertemente básicos y se ionizan para actuar durante el intervalo de pH de 0 a 13 permitiendo un amplio intervalo operativo.
La amina terciaria que contiene monómero se polimeriza con al menos un monómero de reticulación y al menos un agente de cuaternización y uno o más iniciadores de polimerización para formar el polímero ionogénico en los poros del sustrato poroso.
La amina terciaria que contiene monómero se puede someter a copolimerización con al menos un monómero funcional secundario tal como, pero sin limitación; cloruro de vinilbenciltrimetilamonio, trimetilamonio etilmetacrílico cloruro, cloruro de metacrilamido-propiltrimetilamonio, cloruro de (3-acrilamidopropil)trimetilamonio, 2-vinilpiridina, y 4-vinilpiridina, al menos un monómero de reticulación y al menos un agente de cuaternización, y uno o más iniciadores de polimerización.
Además, cualquiera de estos métodos se puede hacer con al menos un monómero secundario no funcional añadido tal como, pero sin limitación; estireno, vinil tolueno, 4-metilestireno, t-butilestireno, alfa-metilestireno, anhídrido metacrílico, ácido metacrílico, n-vinil-2-pirrolidona, viniltrimetoxisilano, viniltrietoxisilano, vinil-tris-(2-metoxietoxi)silano, cloruro de vinilideno, fluoruro de vinilideno, vinilmetildimetoxisilano, 2,2,2-trifluoroetil metacrilato alilamina, vinilpiridina, anhídrido maleico, metacrilato de glicidilo, hidroxietilmetacrilato, metilmetacrilato o etilmetacrilato.
El al menos un reticulante es preferiblemente divinilbenceno o dimetacrilato de etilenglicol.
Opcionalmente, se puede elegir al menos un reticulante entre dimetacrilato de propilenglicol, y dimetacrilato de isobutilenglicol).
Los disolventes encontrados útiles son N-propanol y dipropilenglicol. En algunos casos pueden ser útiles disolventes que contienen hidroxi similares, tales como alcoholes, por ejemplo, isopropanol, butanol; dioles tales como diversos glicoles, o polioles, tales como glicerina.
Se pueden usar además disolventes apróticos tales como N-metilpirrolidona y dimetilacetamida. Estos se dan como ejemplos, no para ser limitantes para un profesional.
El dipropilenglicol es un disolvente preferido.
Los iniciadores radicales libres útiles para la presente invención incluyen, pero sin limitación; peróxido de benzoilo (BPO, del inglés “Benzoyl Peroxide”), persulfato de amonio, 2,2'-azobisisobutironitrilo (AIBN), dihidrocloruro de 2,2'-azobis(2-metilpropionamidina), dihidrocloruro de 2,2'-azobis[2-(2-imidazolin-2-il)propano], 2,2'-azobis[2-(2-imidazolin-2-il)propano] y 2,2'-azobis(2-metilpropionato) de dimetilo.
Un experto en la técnica de desarrollo y fabricación de membrana se dará cuenta que este método de laboratorio conveniente se puede adaptar a otros métodos escalado de laboratorio y se pueden ampliar para la producción continua.
Por ejemplo, el relleno de poro de sustrato o saturación se puede hacer a una temperatura ligeramente elevada (>40 °C) para reducir la solubilidad del aire, o esta etapa se podría hacer después de un tratamiento con vacío suave de la muestra de sustrato sumergida en la solución de formulación. Las muestras de sustrato se pueden poner en remojo previamente y, a continuación, colocarse sobre el poliéster o lámina similar y ser cubiertas con una lámina de cubrimiento y alisadas para eliminar las burbujas de aire. Diversas piezas puestas en remojo previamente se pueden poner en capas y, a continuación, colorarse sobre el poliéster o lámina similar y ser cubiertas con una lámina de cubrimiento y alisadas para eliminar las burbujas de aire.
En lugar de calentar en una estufa, el sándwich de sustrato saturado se puede colocar sobre una superficie calentada a una temperatura suficiente y durante un tiempo necesario para iniciar y completar la polimerización. Se pueden usar métodos alternativos para la iniciación de la reacción de polimerización. Se puede usar luz ultravioleta o radiación ionizante, tal como la radiación gama o la radiación de haz de electrones para iniciar la reacción de polimerización.
La baja resistencia reduce la energía eléctrica requerida para desalinizar y baja el coste de funcionamiento. La resistencia de membrana específica se mide en Ohmcentímetros (Q cm). Una medida de ingeniería más
conveniente es la resistencia del área. Ohm cm2 (Q cm2).
La resistencia del área se puede medir usando una celda que tiene dos electrodos de área conocida, generalmente se usan platino o grafito negro, con la muestra de membrana de área conocida entre ellos en una solución de electrolito. Los electrodos no tocan la membrana. La resistencia de membrana se estima restando la resistencia del electrolito sin la membrana del resultado del ensayo con la membrana en el lugar. La resistencia también se puede medir determinando un voltaje frente a la curva de corriente en una celda que tiene dos cámaras bien mezcladas separadas por la membrana. Un electrodo de calomel mide la caída potencial a través de la membrana. La pendiente de la caída potencial frente a las curvas de corriente, las cuales se pueden obtener variando el voltaje y midiendo la corriente. También se puede usar la impedancia electroquímica. En este método, la corriente alterna se aplica a través de la membrana. La medida a una frecuencia única da datos relacionados con las propiedades electroquímicas de la membrana. Usando las variaciones de frecuencia y amplitud, se puede obtener información estructural detallada. En la presente memoria, la resistencia se definirá por los métodos descritos en la sección Experimental.
La permselectividad se refiere al transporte relativo de contraiones a coiones durante la electrodiálisis. Para una membrana de intercambio catiónico ideal pasarían la membrana únicamente iones cargados positivamente, dando una permselectividad de 1,0. La permselectividad se encuentra midiendo el potencial a través de la membrana mientras que separa las soluciones de sal monovalente de diferentes concentraciones. El método y los cálculos usados en la presente memoria se describen en la sección Experimental.
Para encontrar estos objetivos iniciales los inventores desarrollaron un tipo de membrana de intercambio iónico compuesta en la que el polímero reticulado que tiene grupos iónicos cargados unidos está contenido en los poros de un sustrato de membrana microporosa. El sustrato de membrana porosa preferiblemente es menos de aproximadamente 155 micras de espesor, más preferiblemente menos de aproximadamente 55 micras de espesor. Se prefieren las membranas de sustrato que tienen porosidad mayor del 45 %, siendo más preferidas aquellas que tienen porosidades mayores del 60 %. En las realizaciones más preferidas, las membranas de sustrato tienen porosidades mayores del 70 %. Membranas de sustrato preferidas tienen un tamaño de poro tasado de desde aproximadamente 0,05 micras a aproximadamente 10 micras, con un intervalo más preferido de desde aproximadamente 0,1 micras a aproximadamente 1,0 micras. Los sustratos porosos más preferidos tienen un tamaño de poro tasado de desde aproximadamente 0,1 micras a aproximadamente 0,2 micras.
Los soportes de membrana microporosa pueden estar fabricados de poliolefinas, mezclas de poliolefina, fluoruro de polivinilideno, u otros polímeros. Una clase de sustratos preferidos comprende membranas de poliolefina finas fabricadas principalmente para su uso como separadores de batería. Una clase de sustrato más preferida son los separadores de batería finos fabricados de polietileno de peso molecular ultra alto (UHMWPE, del inglés “Ultrahigh Molecular Weight Polyetylene”).
Para producir las membranas de intercambio iónico deseadas, los inventores desarrollaron un método de colocación del polímero cargado reticulado en los poros del sustrato mediante polimerización del polímero reticulado en estos poros. El método implicaba saturar el sustrato poroso con una solución de monómero cargado, monómero multifuncional, (por ejemplo, un agente de reticulación) e iniciador de polimerización. En la presente memoria los inventores usan el término monómero ionogénico para querer decir una especie de monómero que tiene al menos un grupo cargado covalentemente unido. El grupo cargado puede estar cargado positivamente o cargado negativamente. En una realización, el polímero reticulado se produjo mediante polimerización de un monómero cargado multifuncional. La polimerización se inició por calor o por luz UV, preferiblemente con un iniciador de polimerización tal como un iniciador radical libre. Los monómeros monofuncionales son monómeros que tienen un sitio único para llevar a cabo la reacción de polimerización. Los monómeros multifuncionales tienen más de un sitio de reacción de polimerización y por tanto pueden formar polímeros en red o reticulados.
El siguiente método de laboratorio se usó para investigar los efectos de la formulación y el proceso produciendo cupones pequeños para el ensayo de la resistividad y la permselectividad.
Los cupones de 43 mm de diámetro de sustrato de membrana porosa se troquelaron. De alguna forma los discos mayores (50 mm o 100 mm de diámetro) de las láminas de poliéster transparentes también se troquelaron. Generalmente se usó un platillo de pesar de aluminio de 105 mm para sostener un conjunto de cupones. Los cupones se intercalaron entre dos discos de película de poliéster. En primer lugar, los cupones de sustrato se humedecieron a conciencia con una solución de monómero para preparar una muestra de ensayo. Esto se hizo añadiendo la solución formulada al platillo de aluminio, y sumergiendo un disco de película de poliéster con un cupón de sustrato en capas sobre la misma dentro de la solución de manera que se satura el soporte poroso. A continuación, el soporte saturado se retiró de la solución de monómero y se colocó sobre una pieza de película de poliéster.
Las burbujas de aire se eliminaron del cupón, por ejemplo, alisando o apretando el cupón con una herramienta conveniente, tal como un rodillo de vidrio pequeño, o con la mano. A continuación, se puso en capas un segundo disco de poliéster por encima del primer cupón y se alisó para tener contacto superficial completo entre el cupón y
las capas de película de poliéster inferior y superior. A continuación, se puso en capas un segundo sustrato poroso sobre la película de poliéster superior y la saturación, el alisado y la adición de una capa por encima de la película de poliéster se repitieron para dar un sándwich multicapa de dos cupones y tres capas de película de poliéster protectoras. Un desarrollo experimental típico tendría un sándwich multicapa de 10 o más capas de cupón de sustrato saturado. El borde del platillo de aluminio se puede ondular hacia abajo para sujetar el montaje de disco/cupón si se requiere.
El platillo y el montaje, a continuación, se colocaron en una bolsa sellable, generalmente un bolsa de polietileno con cierre tipo zip y se añadió una baja presión positiva de gas inerte, normalmente nitrógeno, antes de sellar la bolsa. La bolsa que contenía el montaje de platillo y cupón se coloca en una estufa a 80 °C durante hasta 60 minutos. A continuación, la bolsa se retira y se enfría, y los cupones de membrana de intercambio iónico ya reaccionados se colocan en solución de NaCl 0,S N a 40 °Ca 50 °C durante al menos 30 minutos, encontrándose satisfactorio con un remojo en solución de NaCl de hasta 18 horas.
Ejemplos experimentales
Los siguientes ejemplos son para ilustrar el alcance del esfuerzo gastado en el desarrollo de las membranas objeto. El descubrimiento dio como resultado la demostración de que se podían producir membranas de intercambio iónico que tienen las propiedades deseadas y que las mejoras son posibles con experimentación adicional. Estos resultados son ilustrativos e indican las direcciones de desarrollo para los expertos en la técnica del desarrollo de membrana y las técnicas asociadas y no son limitantes para el alcance del asunto descrito en la presente memoria. Las propiedades y los proveedores de los soportes usados se dan en la Tabla 1 de a continuación.
Tabla 1: Sustratos usados
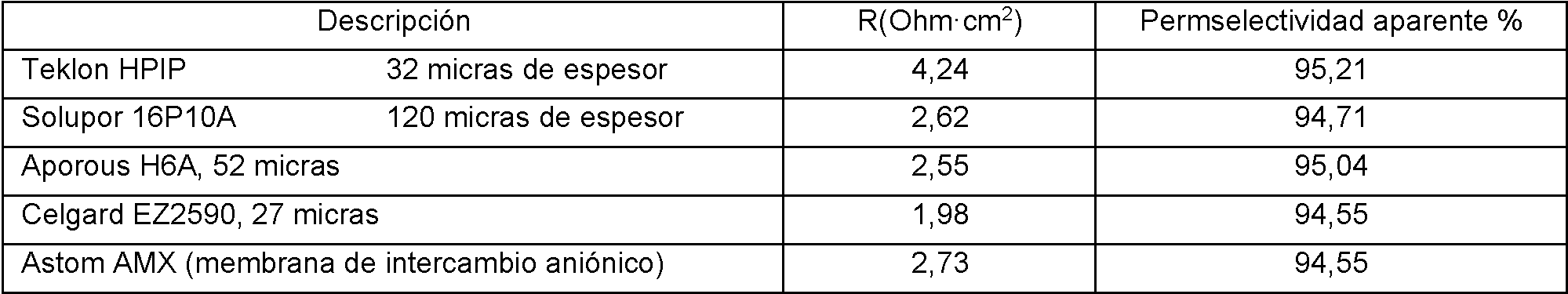
Se ensayaron sustratos porosos representativos para la permselectividad y la resistencia de referencia. Se lavaron previamente usando isopropanol-etanol y agua DI cada uno durante 5 minutos, a continuación, se enjuagaron con NaCl 0,5 N (acuoso) 3 veces para ensayo. La Tabla 2 de a continuación muestra los resultados de la resistencia del área en Ohmcm2 de la MIA producida así y su permselectividad aparente %:
Tabla 2
Ejemplo 1. En un tarro de 118,29 ml (4 oz) con 17,08 g de 1-vinilimidazol, se combinaron con agitación 9,14 g de cloruro de vinilbencilo, 5,39 g de divinilbenceno (80 %), 16,61 g de cloruro de bencilo, 20,65 g de dipropilglicol (DPG) y 0,40 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los sustratos Solupor 16P10A, 16P05A, Teklon, Aporous S14, Celgard EZ2090, EZ2590, Novatexx 2431ND, Delstar 6SLG, Ahlstrom 3329, Delpore DP3924-80PNAT, Delpore 6002-20PNAT se pusieron en remojo en la solución durante 1 hora para asegurar el completo relleno de poro. A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc®, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 80 °C durante 1 hora. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 3 de a continuación muestra los resultados de la resistencia del área en Ohmcm2 de la MIA producida así y su permselectividad aparente %:
Tabla 3
Ejemplo 2
En un tarro de 118,29 ml (4 oz) con 15,71 g de 1-vinilimidazol, se combinaron con agitación 25,47 g de cloruro de vinilbencilo, 13,25 g de DPG y 0,42 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los sustratos Solupor 16P10A, 16P05A y Teklon HPIP se pusieron en remojo en la solución durante 1 hora para asegurar el completo relleno de poro.
A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 80 °C durante 1 hora. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 4 de a continuación muestra los resultados de la resistencia del área en Ohm cm2 de la MIA producida así y su permselectividad aparente %.
También se muestran membranas de intercambio iónico comercialmente disponibles AMX y CMX de Astom-Japón. Ambas son de 125 micras de espesor.
Tabla 4
Los resultados en las Tablas 3 y 4 muestran que las membranas producidas por el método inventivo tienen propiedades aproximadamente equivalentes a membranas mucho más espesas. Las membranas más finas permiten un número incrementado de membranas por volumen de módulo o caja y, por lo tanto, más productividad por unidad de volumen.
Ejemplo 3
En un tarro de 118,29 ml (4 oz) con 17,12 g de 1-vinilimidazol, se combinaron con agitación 20,00 g de cloruro de vinilbencilo, 16,00 g de cloruro de bencilo, 11,02 g de DPG y 0,51 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los sustratos Solupor 16P10A, y Teklon (HPIP, 32 micras, capa única) se pusieron en remojo en la solución durante 1,5 hora para asegurar el completo relleno de poro.
A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc®, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 80 °C durante 40 minutos. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 5 de a continuación muestra los resultados de la resistencia del área en Ohm cm2 de la MIA producida así y su permselectividad aparente %.
También se muestra una membrana de intercambio iónico comercialmente disponible AMX de Astom-Japón. Su espesor es de 125 micras.
Tabla 5
Ejemplo 4
En un tarro de 118,29 ml (4 oz) con 8,55 g de 1-vinilimidazol, se combinaron con agitación 10,01 g de cloruro de vinilbencilo, 1,02 g de divinilbenceno (80 %), 12,01 g de cloruro de bencilo, 5,61 g de DPG y 0,31 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los sustratos Solupor 16P10A, y Teklon HPIP (capa única), Aporous H6A y Celgard EZ 2590 se pusieron en remojo en la solución durante 75 minutos para asegurar el completo relleno de poro.
A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc®, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 80 °C durante 47 minutos. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 6 de a continuación muestra los resultados de la resistencia del área en Qcm2 de la MIA producida así y su permselectividad aparente %.
También se muestra una membrana de intercambio iónico comercialmente disponible AMX de Astom-Japón. Su espesor es de 125 micras.
Tabla 6
Ejemplo 5
En un tarro de 236,58 ml (8 oz) con 30,7 g de 1-vinilimidazol, se combinaron con agitación 17,2 g de cloruro de vinilbencilo, 42,5 g de cloruro de bencilo, 11,8 g de divinilbenceno (80 %), 27,0 g de DPG y 0,41 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los cupones de sustratos Solupor 16P05A se pusieron en remojo en la solución durante 2 horas para asegurar el completo relleno de poro.
A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc®, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 80 °C durante 1 hora. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 7 de a
continuación muestra los resultados de la resistencia del área en Qcm2 de la MIA producida así y su permselectividad aparente %.
También se muestra una membrana de intercambio iónico comercialmente disponible AMX de Astom-Japón. Su espesor es de 125 micras.
Tabla 7
Ejemplo 6
En un vial de 20 ml con 3,43 g de 1-vinilimidazol, se combinaron con agitación 3,0 de cloruro de vinilbencilo, 1,0 g de EP0409 (Hybrid Plastics, mezcla glicidil-POSS® cage CAS N.° 68611-45-0), 3,2 g de cloruro de bencilo, 2,20 g de DPG y 0,10 g de Vazo-64. Inmediatamente se formó una solución marrón claro. Los cupones de sustrato Solupor 16P10A se pusieron en remojo en la solución durante 0,5 hora para asegurar el completo relleno de poro.
A continuación, se intercalaron entre discos de Mylar, las burbujas de aire entre los discos de Mylar se eliminaron por presión y los sustratos estratificados se colocaron en un disco de pesar de aluminio. El disco se cargó en una bolsa Ziploc®, la bolsa se presurizó con gas de nitrógeno y se colocó en una estufa a 90 °C durante 1 hora. El cupón de membrana producida así se colocó en NaCl 0,5 N (acuoso) para acondicionamiento. La Tabla 8 de a continuación muestra el resultado de la resistencia del área en Ohm cm2 de la MIA producida así y su permselectividad aparente %.
También se muestra una membrana de intercambio iónico comercialmente disponible AMX de Astom-Japón que tiene un espesor de 125 micras.
Tabla 8
Procedimientos experimentales para la caracterización de la resistividad del área de membrana y la permselectividad aparente
La resistencia de membrana y el número de transporte de contraiones (permselectividad) se puede medir usando una celda electroquímica. Este experimento sobre el banco nos proporciona un experimento muy eficaz y rápido que usa una pequeña pieza de muestra. El equipo y el procedimiento se describen en la presente memoria.
Preparación del experimento
(1) Unidad de medida electroquímica Solartron 1280
La unidad de medida electroquímica Solartron 1280 nos permite aplicar una corriente entre los dos electrodos de platino sobre los dos lados de la celda y medir la caída de voltaje a través de la membrana. Tiene 4 conectores: electrodo de trabajo (ET), contra electrodo (CE), electrodos de referencia (ER1 y ER2). El CE y el ET se usan para aplicar corriente y el ER1 y el ER2 miden la caída de voltaje.
(2) Electrodos de referencia
Los electrodos de referencia (véase el inserto en la Figura 1) usados para la caracterización de la membrana están producidos en R&D Lab. Se ablanda un tubo de vidrio de 0,635 cm (%”), a continuación, se dobla y se moldea a la forma mostrada. Se inserta un tapón poroso en la punta para controlar el flujo de la solución a un bajo caudal. El alambre de plata/cloruro de plata se produce recién para el ensayo de cada día. Se suministró una corriente de 2-3 mA y se controló por un distribuidor de energía y un medidor de amperio para un cátodo del alambre de platino y el ánodo del alambre de plata sumergido en una solución de HCl 0,1 N. Después de varios minutos, el alambre de plata comienza a volverse negro, indicativo de la formación de capa de AgCl sobre la superficie. La solución usada dentro del tubo de electrodo de referencia es una solución de KCl 1,0 M. Puesto que la solución goteará a través de la punta porosa, es necesaria la adición constante de KCl (aproximadamente cada 20 min) durante el experimento.
(3) Celda de ensayo de membrana
La Figura 1 muestra la construcción de la celda de ensayo electroquímica detallada usada para el experimento para medir la resistencia y la permselectividad de contraión de la membrana. Las membranas se cortan en disco usando una troqueladora. Los electrodos de referencia se usan para hacer un seguimiento de la caída del voltaje a través de la membrana de ensayo y los 2 discos de platino se usan para proporcionar una corriente a través de la membrana. El paso cilíndrico de la celda tiene un área de sección transversal de 7,0 cm2
(4) Soluciones
Todas las soluciones necesitan ser preparadas con el nivel cuantitativo indicado por sus figuras significativas. Estas incluyen NaCl 0,500 N, HCl 1,0 N y NaOH 1,0 N (caustico, usando recipiente de plástico o matraces volumétricos). El Na2SO40,S N se usa para alimentar los compartimentos del electrodo sin evolución de gas de cloro.
3-111. Procedimientos de medida
(1) Medida de la resistencia
En la presente memoria resistencia se refiere a la resistencia del área Qcm2 La medida contiene 3 etapas.
(a) Establecer las posiciones del electrodo: antes de una medida, se establecen las posiciones horizontales del electrodo de referencia. Para establecer la posición del electrodo de referencia, se usa un disco de plástico rígido como un sustituto para la membrana. Cada electrodo de referencia se ajusta para tocar justo el disco de plástico y su posición se fija por dos tornillos de ajuste.
(b) Medida de la conductividad de la solución: a continuación, se retiró el disco de plástico y los dos electrodos de referencia se alejaron 1,0 cm al retirar los dos bloques de plástico de 0,50 mm. La caída de voltaje entre los dos electrodos de referencia se registra en una corriente aplicada (aproximadamente 10-50 mA) por el Solartron 1280. La distancia de los 2 electrodos de referencia (1,00 cm en la presente), la densidad de corriente (10,00 mA) y el voltaje (a 0,1 mV de precisión) se usan para obtener la conductividad de la solución (NaCl 0,50 N generalmente). (c) Medida de la resistencia de membrana: a continuación, la muestra de membrana se coloca por el deslizador de muestra y se mide de nuevo el voltaje y la corriente. La resistencia de membrana es la resistencia total menos la resistencia de la solución medida en el procedimiento (b).
(2) Permselectividad del contraión (número de transporte)
Los procedimientos de medida son:
(a) La posición del electrodo de referencia se establece como se describe en la parte (a) de la medida de la resistencia. La posición de los electrodos de referencia puede ser aproximada puesto que el voltaje medido en este ensayo es teóricamente independiente de la distancia, pero se recomienda que la posición se coloque tan reproduciblemente como sea posible.
(b) Soluciones: después de emplazar la membrana de muestra con el deslizador, se vierte solución de NaCl 0,500 N en la parte derecha de la celda separada por la membrana de ensayo y NaCl 0,250 N sobre el lado izquierdo de la celda.
(c) Medición del voltaje: el voltaje se midió (sin aplicar corriente) usando un medidor de voltaje unido a los electrodos de platino y los datos se introdujeron en la hoja de cálculo para obtener la permselectividad de contraión.
3-IV. Cálculos de la muestra:
C=conductividad (siemens/cm) p=resistencia (Ohm/cm)
R=resistividad (Ohmcm2 o Q cm2) A=área (cm2)
U, V= voltaje medido (mV)
I=corriente medida (mA)
L=distancia entre los electrodos de referencia
(1) Conductividad de la NaCl 0,500 M a corriente de 10,00 mA y 33,1 mV medida para una distancia de electrodo de referencia de 1,00 cm, la conductividad de la solución:
La resistencia del área del cálculo de la membrana necesita restar la resistencia de la solución. Para una membrana CMX con un potencial medido de 38,0 mV, la resistencia del área es:
(2) Permselectividad (número de transporte) membrana de anión (+) o anión(-) T± se obtiene por:
que se reorganiza a;
En donde V es el voltaje medido por los electrodos de referencia, R es la constante de gas (8,314 JulioK'1 mol'1) T es la temperatura en Kelvin de la solución, F es la constante de Faraday (96.480 culombios/mol) y aR y aL son la concentración (formato de actividad) de la solución sobre los dos lados de la membrana en la celda.
Claims (8)
1. Un proceso para la producción de una membrana de intercambio iónico capaz de usarse para la electrodiálisis, que comprende:
elegir un sustrato poroso adecuado;
saturar las regiones porosas del sustrato con una solución monomérica que comprende al menos un monómero funcional seleccionado del grupo que consiste en vinilmidazol y vinilcarbazol, al menos un monómero de reticulación, al menos un agente de cuaternización, y al menos un iniciador de la polimerización;
retirar la solución en exceso de las superficies del sustrato mientras se deja el volumen poroso saturado con la solución; e
iniciar la polimerización para formar un polímero de intercambio aniónico reticulado básicamente rellenando completamente los poros del sustrato.
2. El proceso de la reivindicación 1, en donde el al menos un monómero de reticulación se selecciona de: divinilbenceno, cloruro de vinilbencilo, dicloroetano, un silsesquioxano oligomérico de polihédrico de octaglicidil, y dimetacrilato de etilenglicol.
3. El proceso de la reivindicación 1, en donde el al menos un agente de cuaternización se selecciona de cloruro de bencilo, cloruro de vinilbencilo, dicloroetano, o yoduro de metilo.
4. El proceso de la reivindicación 1, en donde el al menos un iniciador de polimerización se selecciona entre peróxidos orgánicos, dihidrocloruro de 2,2'-azobis[2-[2-imidazolin-2-il)-propano], a ,a '-azoisobutironitrilo, dihidrocloruro de 2,2'-azobis(2-metilpropionamidina), 2,2'-azobis[2-(2-imidazolin-2-il)-propano], y 2,2'-azobis(2-metilpropionato) de dimetilo.
5. El proceso de la reivindicación 4, en donde el peróxido orgánico es peróxido de benzoílo.
6. El proceso de la reivindicación 1, en donde la solución monomérica comprende además al menos un inhibidor de la polimerización.
7. El proceso de la reivindicación 6, en donde el al menos un inhibidor de la polimerización se selecciona entre 4-metoxifenol y 4-terc-butil catecol.
8. El proceso de la reivindicación 1, en donde el sustrato poroso comprende polipropileno, polietileno de alto peso molecular, polietileno de peso molecular ultra alto o fluoruro de polivinilideno.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US39371510P | 2010-10-15 | 2010-10-15 | |
| PCT/US2011/056501 WO2012051608A1 (en) | 2010-10-15 | 2011-10-17 | Anion exchange membranes and process for making |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2768330T3 true ES2768330T3 (es) | 2020-06-22 |
Family
ID=45938742
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19197132T Active ES2886889T3 (es) | 2010-10-15 | 2011-10-17 | Membranas de intercambio aniónico y proceso para su producción |
| ES11833543T Active ES2768330T3 (es) | 2010-10-15 | 2011-10-17 | Membranas de intercambio aniónico y proceso para su producción |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19197132T Active ES2886889T3 (es) | 2010-10-15 | 2011-10-17 | Membranas de intercambio aniónico y proceso para su producción |
Country Status (13)
| Country | Link |
|---|---|
| US (3) | US8969424B2 (es) |
| EP (2) | EP2627447B1 (es) |
| JP (2) | JP2013545595A (es) |
| CN (2) | CN106110898B (es) |
| AU (1) | AU2011315852B2 (es) |
| CA (1) | CA2814699C (es) |
| CL (1) | CL2013001033A1 (es) |
| EA (1) | EA024707B1 (es) |
| ES (2) | ES2886889T3 (es) |
| IL (1) | IL225696B (es) |
| SG (1) | SG189895A1 (es) |
| WO (1) | WO2012051608A1 (es) |
| ZA (1) | ZA201302674B (es) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3670561B1 (en) | 2009-01-12 | 2023-12-06 | University Of Massachusetts Lowell | Polyisobutylene-based polyurethanes |
| KR101741243B1 (ko) | 2009-08-26 | 2017-06-15 | 에보쿠아 워터 테크놀로지스 피티이. 리미티드 | 이온 교환막 |
| EP2627447B1 (en) | 2010-10-15 | 2019-12-11 | Evoqua Water Technologies LLC | Anion exchange membranes and process for making |
| JP5889907B2 (ja) | 2010-10-15 | 2016-03-22 | エヴォクア ウォーター テクノロジーズ エルエルシーEvoqua Water Technologiesllc | カチオン交換膜を製造するためのモノマー溶液の製造方法 |
| US8470896B2 (en) * | 2010-12-23 | 2013-06-25 | General Electric Company | Acid block anion membrane |
| CA2884791C (en) * | 2012-10-04 | 2021-09-07 | Evoqua Water Technologies Llc | High-performance anion exchange membranes and methods of making same |
| SG11201502696UA (en) * | 2012-10-11 | 2015-05-28 | Evoqua Water Technologies Llc | Ion exchange membranes and methods of making the same |
| EP2906330B1 (en) | 2012-10-11 | 2020-06-17 | Evoqua Water Technologies LLC | Coated ion exchange membranes |
| WO2017180264A2 (en) * | 2016-03-08 | 2017-10-19 | Giner, Inc. | Separator for use in electrochemical cells and method of fabrication thereof |
| CN106008862B (zh) * | 2016-05-26 | 2018-03-27 | 常州大学 | 一种碱性阴离子交换膜的制备方法 |
| CN106925357B (zh) * | 2017-03-02 | 2019-05-31 | 浙江工业大学 | 一种单价选择性阴离子交换膜的制备方法 |
| EP3592786B1 (en) | 2017-03-07 | 2023-05-10 | Cardiac Pacemakers, Inc. | Hydroboration/oxidation of allyl-terminated polyisobutylene |
| WO2019118662A1 (en) * | 2017-12-13 | 2019-06-20 | Evoqua Water Technologies Llc | Anion exchange membranes for redox flow batteries |
| KR101873260B1 (ko) | 2018-01-04 | 2018-07-02 | 상명대학교 천안산학협력단 | 음이온 교환막 제조방법 및 이로부터 제조된 음이온 교환막 |
| CN111479596B (zh) | 2018-01-17 | 2023-04-07 | 心脏起搏器股份公司 | 封端聚异丁烯聚氨酯 |
| CN110292957B (zh) * | 2018-03-22 | 2022-12-09 | 戴安公司 | 基于交联的羟基烷基胺层和缩水甘油的阴离子交换固定相 |
| JP7022200B2 (ja) | 2018-09-13 | 2022-02-17 | 株式会社東芝 | グラフェン含有膜の陰イオン透過性評価方法および光電変換素子 |
| CN110078961B (zh) * | 2019-05-05 | 2021-07-06 | 大连理工大学 | 一种多羟基功能化聚苯并咪唑离子交换膜及制备方法 |
| CN110813387B (zh) * | 2019-09-11 | 2022-05-24 | 浙江工业大学 | 一种单价阴离子交换膜的制备方法 |
| WO2021150742A1 (en) * | 2020-01-21 | 2021-07-29 | 1S1 Energy, Inc. | Alkaline anion exchange membrane and methods of use thereof |
| JP2023530938A (ja) * | 2020-06-17 | 2023-07-20 | インテグリス・インコーポレーテッド | イオン交換膜、フィルタ及び方法 |
Family Cites Families (132)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2780604A (en) | 1953-01-22 | 1957-02-05 | Ionics | Mono (chloromethyl) styrene, its derivatives, and ion-exchange resins from polymers of aminated compound |
| US3009895A (en) | 1956-12-31 | 1961-11-21 | Monsanto Chemicals | Compatible blends of two or more interpolymers that follow the slocombewesp rule of azeotropic line clarity and solutions thereof |
| NL134681C (es) | 1966-04-26 | |||
| JPS501707B1 (es) | 1969-12-20 | 1975-01-21 | ||
| US3926864A (en) | 1971-06-21 | 1975-12-16 | Ionics | Ion exchange membranes having a macroporous surface area |
| US4297431A (en) | 1978-09-15 | 1981-10-27 | Polaroid Corporation | Diffusion control layers in diffusion transfer photographic products |
| US4231855A (en) | 1979-03-02 | 1980-11-04 | Ionics, Incorporated | Electrodialysis membranes of high interstitial molality based upon methacrylate ester derivatives |
| US4585833A (en) | 1983-05-26 | 1986-04-29 | Union Carbide Corporation | Low shrinkling curable poly(acrylate) molding compositions |
| US4828772A (en) | 1984-10-09 | 1989-05-09 | Millipore Corporation | Microporous membranes of ultrahigh molecular weight polyethylene |
| US4778601A (en) | 1984-10-09 | 1988-10-18 | Millipore Corporation | Microporous membranes of ultrahigh molecular weight polyethylene |
| US4704324A (en) | 1985-04-03 | 1987-11-03 | The Dow Chemical Company | Semi-permeable membranes prepared via reaction of cationic groups with nucleophilic groups |
| GB8608430D0 (en) | 1986-04-07 | 1986-05-14 | Raychem Ltd | Porous polymer article |
| US4933405A (en) | 1986-06-10 | 1990-06-12 | The Dow Chemical Company | Homogeneous copolymerization of non-polar monomers with ionic amphiphilic monomers |
| US4874567A (en) | 1987-04-24 | 1989-10-17 | Millipore Corporation | Microporous membranes from polypropylene |
| US5032274A (en) | 1988-05-04 | 1991-07-16 | Millipore Corporation | Process for producing fluorocarbon membranes and membrane product |
| US5194189A (en) | 1989-09-08 | 1993-03-16 | Ionics, Incorporated | Process for manufacturing continuous, supported polymeric sheet from polymerizable liquid starting materials |
| US5145618A (en) | 1989-09-08 | 1992-09-08 | Ionics, Incorporated | Process for manufacturing continuous supported ion selective membranes using non-polymerizable high boiling point solvents |
| US5264125A (en) | 1989-09-08 | 1993-11-23 | Ionics' Incorporated | Process for manufacturing continuous supported ion selective membranes using non-polymerizable high boiling point solvents |
| US5118717A (en) | 1990-02-13 | 1992-06-02 | Ionics, Incorporated | High ion exchange capacity polyelectrolytes having high crosslink densities and caustic stability |
| US5039420A (en) | 1990-08-16 | 1991-08-13 | Elias Klein | Hydrophilic semipermeable membranes based on copolymers of acrylonitrile and hydroxyalkyl esters of (meth) acrylic acid |
| US5120632A (en) | 1990-12-28 | 1992-06-09 | Xerox Corporation | Pigment passivation via polymer encapsulation |
| US5510394A (en) | 1991-02-19 | 1996-04-23 | Ionics Incorporated | High ionic conductance ion exchange membranes and their preparation |
| EP0600470A3 (en) | 1992-12-04 | 1995-01-04 | Asahi Glass Co Ltd | Bipolar membrane. |
| BE1006940A6 (fr) | 1993-04-08 | 1995-01-31 | Solvay | Procede de fabrication d'une membrane bipolaire et procede de fabrication d'une solution aqueuse d'hydroxyde de metal alcalin. |
| US5447636A (en) | 1993-12-14 | 1995-09-05 | E. I. Du Pont De Nemours And Company | Method for making reinforced ion exchange membranes |
| IL109240A (en) | 1994-04-07 | 1998-02-22 | Yeda Res & Dev | Ion exchange membranes |
| US5503729A (en) | 1994-04-25 | 1996-04-02 | Ionics Incorporated | Electrodialysis including filled cell electrodialysis (electrodeionization) |
| CN1038562C (zh) | 1994-06-20 | 1998-06-03 | 中国科学院化学研究所 | 聚丙烯微孔膜为基膜的离子交换膜及其制法 |
| BE1008471A3 (fr) | 1994-07-05 | 1996-05-07 | Solvay | Membrane bipolaire et procede de fabrication d'une membrane bipolaire. |
| IT1269982B (it) | 1994-09-20 | 1997-04-16 | Solvay | Procedimento di fabbricazione di una membrana bipolare e procedimento di preparazione di una soluzione acquosa di un idrossido di un metalloalcalino mediante elettrodialisi |
| CA2215977A1 (en) * | 1995-03-23 | 1996-09-26 | Arthur L. Goldstein | Improvements in membrane processes including electrodialysis |
| US6258276B1 (en) | 1996-10-18 | 2001-07-10 | Mcmaster University | Microporous membranes and uses thereof |
| KR19980079940A (ko) | 1997-03-05 | 1998-11-25 | 후지이 히로시 | 빗물오염방지성 도막, 도료 조성물, 도막 형성방법 및 도장물 |
| US5868976A (en) | 1997-03-14 | 1999-02-09 | Koch Membrane Systems, Inc. | Process of making a dialysis membrane |
| US5961796A (en) | 1997-06-03 | 1999-10-05 | Lynntech, Inc. | Bipolar membranes with fluid distribution passages |
| US6248469B1 (en) | 1997-08-29 | 2001-06-19 | Foster-Miller, Inc. | Composite solid polymer electrolyte membranes |
| US6635384B2 (en) | 1998-03-06 | 2003-10-21 | Gore Enterprise Holdings, Inc. | Solid electrolyte composite for electrochemical reaction apparatus |
| US6723758B2 (en) | 1997-11-12 | 2004-04-20 | Ballard Power Systems Inc. | Graft polymeric membranes and ion-exchange membranes formed therefrom |
| US6221248B1 (en) | 1998-03-23 | 2001-04-24 | Ionics Incorporated | Styrene sulfonate cation exchange membrane |
| ATE413365T1 (de) | 1998-03-24 | 2008-11-15 | Ebara Corp | Elektrische entionisierungsvorrichtung |
| US6780327B1 (en) | 1999-02-25 | 2004-08-24 | Pall Corporation | Positively charged membrane |
| DE19919881A1 (de) | 1999-04-30 | 2000-11-02 | Univ Stuttgart | Organisch-Anorganische Komposites und Kompositmembranen aus Ionomeren oder Ionomerblends und aus Schicht- oder Gerätsilicaten |
| US6277512B1 (en) | 1999-06-18 | 2001-08-21 | 3M Innovative Properties Company | Polymer electrolyte membranes from mixed dispersions |
| US6410672B1 (en) | 1999-07-28 | 2002-06-25 | Ionics, Incorporated | Ion exchange and electrochemical methods and devices employing one-step quaternized and polymerized anion selective polymers |
| JP4398031B2 (ja) | 1999-12-03 | 2010-01-13 | 株式会社トクヤマ | イオン交換膜及びその製造方法 |
| US6596137B2 (en) | 2000-02-25 | 2003-07-22 | Tokoyama Corporation | Bipolar membrane |
| US6368486B1 (en) | 2000-03-28 | 2002-04-09 | E. I. Du Pont De Nemours And Company | Low temperature alkali metal electrolysis |
| FR2807950B1 (fr) | 2000-04-19 | 2002-07-19 | Solvay | Procede de fabrication d'une membrane bipolaire et utilisation de la membrane bipolaire ainsi obtenue |
| US20040028977A1 (en) | 2000-05-30 | 2004-02-12 | Peter Pickup | Fuel cell incorporating a modified ion exchange membrane |
| US7081484B2 (en) | 2000-07-24 | 2006-07-25 | Asahi Glass Company, Limited | Anion exchange membrane, process for its production and solution treating apparatus |
| US20020156207A1 (en) | 2000-09-07 | 2002-10-24 | Junichi Imuta | Polar group-containing olefin copolymer, process for preparing the same, thermoplastic resin composition containing the copolymer, and uses thereof |
| US7361729B2 (en) | 2000-09-20 | 2008-04-22 | Virginia Tech Intellectual Properties, Inc. | Ion-conducting sulfonated polymeric materials |
| KR20030016291A (ko) | 2001-04-13 | 2003-02-26 | 오르가노 가부시키가이샤 | 이온교환체 |
| US6830671B2 (en) | 2001-06-29 | 2004-12-14 | Tokuyama Corporation | Ion-exchange membrane |
| EP1409119B1 (en) | 2001-07-20 | 2006-06-21 | McMaster University | Asymmetric gel-filled microporous membranes |
| ATE339466T1 (de) | 2001-07-30 | 2006-10-15 | Asahi Glass Engineering Co Ltd | Anionenaustauscher und verfahren zur herstellung einer anionenaustauschmembran |
| US7318972B2 (en) | 2001-09-07 | 2008-01-15 | Itm Power Ltd. | Hydrophilic polymers and their use in electrochemical cells |
| DE60228303D1 (de) | 2001-10-15 | 2008-09-25 | Du Pont | Festpolymermembran für eine brennstoffzelle mit darin eingebettetem polyvinylamin für verringerte methanoldurchlässigkeit |
| US6814865B1 (en) | 2001-12-05 | 2004-11-09 | Seventy-Seventh Meridian Corporation Llc | Ion exchange membranes, methods and processes for production thereof and uses in specific applications |
| US20030153708A1 (en) | 2002-01-11 | 2003-08-14 | Caneba Gerald Tablada | Free radical retrograde precipitation copolymers and process for making same |
| US6849688B2 (en) | 2002-03-26 | 2005-02-01 | Sachem, Inc. | Polymer grafted support polymers |
| US20070261962A1 (en) | 2002-04-02 | 2007-11-15 | Ryszard Gajek | Separation Systems with Charge Mosaic Membrane |
| JP3773190B2 (ja) | 2002-05-15 | 2006-05-10 | オルガノ株式会社 | 電気式脱イオン水製造装置 |
| US7740967B2 (en) | 2002-07-04 | 2010-06-22 | Ben Gurion University Of The Negev Research And Development Authority | Highly conductive ordered ion exchange membranes |
| FR2843399B1 (fr) | 2002-08-06 | 2004-09-03 | Commissariat Energie Atomique | Polymeres de type polyphenylenes, leur procede de preparation, membranes et dispositif de pile a combustible comprenant ces membranes |
| US6828386B2 (en) | 2002-09-20 | 2004-12-07 | Ballard Power Systems Inc. | Process for preparing graft copolymers and membranes formed therefrom |
| AU2003273034A1 (en) | 2002-10-17 | 2004-05-04 | Toyo Boseki Kabushiki Kaisha | Composite ion-exchange membrane |
| EP2143481A1 (en) | 2003-02-19 | 2010-01-13 | Natrix Separations Inc. | Composite materials comprising supported porous gels |
| US20040175625A1 (en) | 2003-03-06 | 2004-09-09 | Lotfi Hedhli | Non-perfluorinated resins containing ionic or ionizable groups and products containing the same |
| US7449111B2 (en) | 2003-07-30 | 2008-11-11 | Arkema Inc. | Resins containing ionic or ionizable groups with small domain sizes and improved conductivity |
| US7179847B2 (en) | 2003-11-13 | 2007-02-20 | 3M Innovative Properties Company | Polymer electrolytes crosslinked by e-beam |
| US7632406B2 (en) | 2004-04-20 | 2009-12-15 | Lawrence Livermore National Security, Llc | Smart membranes for nitrate removal, water purification, and selective ion transportation |
| US7604746B2 (en) | 2004-04-27 | 2009-10-20 | Mcmaster University | Pervaporation composite membranes |
| JP2005334263A (ja) | 2004-05-26 | 2005-12-08 | Tokuyama Corp | イオントフォレーシス装置及びイオン交換膜 |
| US20080023334A1 (en) | 2004-06-18 | 2008-01-31 | Ebara Corporation | Liquid Treatment Apparatus |
| JP4613528B2 (ja) | 2004-06-24 | 2011-01-19 | コニカミノルタホールディングス株式会社 | プロトン伝導性電解質膜とその製造方法、及び該プロトン伝導性電解質膜を用いた固体高分子型燃料電池 |
| US7959780B2 (en) | 2004-07-26 | 2011-06-14 | Emporia Capital Funding Llc | Textured ion exchange membranes |
| KR100723389B1 (ko) | 2005-12-21 | 2007-05-30 | 삼성에스디아이 주식회사 | 폴리머 전해질막 및 이를 채용한 연료전지 |
| US20060045985A1 (en) | 2004-09-02 | 2006-03-02 | Kozak Paul D | Method and apparatus for electrostatically coating an ion-exchange membrane or fluid diffusion layer with a catalyst layer |
| US20060062982A1 (en) | 2004-09-17 | 2006-03-23 | Massachusetts Institute Of Technology | Carbon-polymer electrochemical systems and methods of fabricating them using layer-by-layer technology |
| FR2876299B1 (fr) | 2004-10-12 | 2007-01-12 | Solvay | Membranes echangeuses d'ions structurees dans l'epaisseur et procede pour la fabrication de ces membranes |
| CN101048434B (zh) | 2004-10-27 | 2011-04-13 | 旭硝子株式会社 | 电解质材料、电解质膜及固体高分子型燃料电池用膜电极接合体 |
| WO2006082653A1 (ja) | 2005-02-04 | 2006-08-10 | Jsr Corporation | ポリアリーレンおよびその製造方法、ならびに高分子固体電解質およびプロトン伝導膜 |
| US7833644B2 (en) | 2005-03-17 | 2010-11-16 | Teijin Limited | Electrolytic membrane |
| KR100668339B1 (ko) | 2005-06-18 | 2007-01-12 | 삼성전자주식회사 | 이온 교환성 혼합물 및 그의 제조방법 |
| EP1901379A4 (en) | 2005-07-01 | 2012-06-06 | Tokuyama Corp | Disconnect membrane for a fuel cell |
| US20070031716A1 (en) | 2005-08-05 | 2007-02-08 | Rajendran Raj G | Process for making cation exchange membranes with reduced methanol permeability |
| NZ565662A (en) | 2005-08-09 | 2010-10-29 | Univ Sunderland | Fingerprint analysis using mass spectrometry |
| JP4708133B2 (ja) | 2005-09-14 | 2011-06-22 | 旭化成ケミカルズ株式会社 | 電解用フッ素系陽イオン交換膜及びその製造方法 |
| GB2446077B (en) * | 2005-09-30 | 2010-10-13 | Ilypsa Inc | Methods and compositions for selectively removing potassium ion from the gastrointestinal tract of a mammal |
| US8367267B2 (en) | 2005-10-28 | 2013-02-05 | 3M Innovative Properties Company | High durability fuel cell components with cerium oxide additives |
| US7977392B2 (en) | 2005-12-22 | 2011-07-12 | Daimler Ag | Water insoluble additive for improving conductivity of an ion exchange membrane |
| US7368200B2 (en) | 2005-12-30 | 2008-05-06 | Tekion, Inc. | Composite polymer electrolyte membranes and electrode assemblies for reducing fuel crossover in direct liquid feed fuel cells |
| US7829218B2 (en) | 2006-03-09 | 2010-11-09 | Samsung Sdi Co., Ltd | Proton conductive electrolyte and fuel cell comprising the same |
| EP2002451B1 (en) | 2006-03-30 | 2014-03-26 | Fujifilm Corporation | Method and apparatus for producing solid electrolyte membrane |
| JP5066865B2 (ja) | 2006-08-09 | 2012-11-07 | トヨタ自動車株式会社 | 燃料電池用補強型電解質膜、その製造方法、燃料電池用膜−電極接合体、及びそれを備えた固体高分子型燃料電池 |
| GB0701449D0 (en) | 2007-01-26 | 2007-03-07 | Secr Defence | Anion Exchange Membranes |
| US20080223785A1 (en) | 2007-03-13 | 2008-09-18 | Miller Jeffrey T | Ionic Polymer Membranes |
| JP5050285B2 (ja) | 2007-03-14 | 2012-10-17 | 財団法人塩事業センター | 製塩用陰イオン交換膜及びその製造方法 |
| GB0706634D0 (en) | 2007-04-04 | 2007-05-16 | Itm Fuel Cells Ltd | Membrane production |
| EP1982757A1 (de) | 2007-04-10 | 2008-10-22 | Stichting Voor De Technische Wetenschappen | Ionendurchlässige Membran und ihre Herstellung |
| US7806275B2 (en) | 2007-05-09 | 2010-10-05 | The United States Of America As Represented By The Secretary Of The Interior, The Bureau Of Reclamation | Chlorine resistant polyamides and membranes made from the same |
| JP2008288065A (ja) | 2007-05-18 | 2008-11-27 | Keio Gijuku | 電解質膜、膜−電極接合体、燃料電池及び電解質膜の製造方法 |
| JP5579365B2 (ja) * | 2007-12-13 | 2014-08-27 | 公益財団法人 塩事業センター | 陰イオン交換膜およびその製造方法 |
| US7968663B2 (en) | 2007-12-18 | 2011-06-28 | General Electric Company | Anion exchange polymers, methods for making and materials prepared therefrom |
| JP5196234B2 (ja) | 2008-01-25 | 2013-05-15 | 財団法人塩事業センター | 陰イオン交換膜及びその製造方法 |
| JP5196236B2 (ja) | 2008-01-28 | 2013-05-15 | 財団法人塩事業センター | 陽イオン交換膜及びその製造方法 |
| JP5196242B2 (ja) | 2008-03-12 | 2013-05-15 | 財団法人塩事業センター | 陰イオン交換膜及びその製造方法 |
| JP5196241B2 (ja) | 2008-03-12 | 2013-05-15 | 財団法人塩事業センター | 陽イオン交換膜及びその製造方法 |
| EP2264087B1 (en) | 2008-03-26 | 2014-08-13 | Teijin Limited | Film for reinforcing electrolyte membrane of solid polymer fuel cell |
| US7888397B1 (en) | 2008-04-30 | 2011-02-15 | Sandia Corporation | Poly(phenylene)-based anion exchange membrane |
| KR101000214B1 (ko) | 2008-05-28 | 2010-12-10 | 주식회사 엘지화학 | 이온전도성 수지 파이버, 이온전도성 복합막, 막-전극 접합체 및 연료전지 |
| GB0813227D0 (en) | 2008-07-18 | 2008-08-27 | Fuji Film Mfg Europ B V | Process for preparing membranes |
| KR100999048B1 (ko) | 2008-08-01 | 2010-12-09 | 한국화학연구원 | 스티렌계-비닐벤질계 공중합체가 함유된 음이온교환 복합막의 제조방법 |
| JP4606487B2 (ja) * | 2008-10-06 | 2011-01-05 | 株式会社トクヤマ | 固体高分子電解質型燃料電池用陰イオン交換膜の製造方法 |
| WO2010055889A1 (ja) | 2008-11-14 | 2010-05-20 | 株式会社トクヤマ | 陰イオン交換膜及びその製造方法 |
| WO2010082069A1 (en) | 2009-01-19 | 2010-07-22 | Fujifilm Manufacturing Europe Bv | Process for preparing membranes |
| WO2010095740A1 (ja) | 2009-02-23 | 2010-08-26 | 旭硝子株式会社 | 陽イオン交換膜およびその製造方法、並びにこれを用いた電解槽 |
| GB0904560D0 (en) | 2009-03-17 | 2009-04-29 | Fujifilm Mfg Europe Bv | Process for preparing composite membranes |
| GB0904558D0 (en) | 2009-03-17 | 2009-04-29 | Fujifilm Mfg Europe Bv | Membranes |
| WO2010110333A1 (ja) | 2009-03-25 | 2010-09-30 | 株式会社クラレ | 陰イオン交換膜及びその製造方法 |
| JP5531267B2 (ja) | 2009-04-13 | 2014-06-25 | 国立大学法人山口大学 | イオン交換膜およびその製造方法 |
| KR101741243B1 (ko) | 2009-08-26 | 2017-06-15 | 에보쿠아 워터 테크놀로지스 피티이. 리미티드 | 이온 교환막 |
| US8696882B2 (en) | 2009-12-03 | 2014-04-15 | Lawrence Livermore National Security, Llc. | Nanoengineered field induced charge separation membranes and methods of manufacture thereof |
| GB0921951D0 (en) | 2009-12-16 | 2010-02-03 | Fujifilm Mfg Europe Bv | Curable compositions and membranes |
| GB0921949D0 (en) | 2009-12-16 | 2010-02-03 | Fujifilm Mfg Europe Bv | Curable compositions and membranes |
| WO2011079062A1 (en) | 2009-12-21 | 2011-06-30 | Siemens Industry, Inc. | Charged porous polymeric membranes and their preparation |
| JP5889907B2 (ja) | 2010-10-15 | 2016-03-22 | エヴォクア ウォーター テクノロジーズ エルエルシーEvoqua Water Technologiesllc | カチオン交換膜を製造するためのモノマー溶液の製造方法 |
| EP2627447B1 (en) | 2010-10-15 | 2019-12-11 | Evoqua Water Technologies LLC | Anion exchange membranes and process for making |
| JP6008870B2 (ja) | 2010-12-12 | 2016-10-19 | ベン‐グリオン ユニバーシティ オブ ザ ネゲヴ リサーチ アンド デベロップメント オーソリティ | 陰イオン交換膜、その調製方法および用途 |
| ES2705000T3 (es) | 2011-07-25 | 2019-03-21 | Fujifilm Mfg Europe Bv | Método para producir membranas compuestas con poros llenos de polímero |
| US9073050B2 (en) | 2011-10-05 | 2015-07-07 | General Electric Company | Ion exchange compositions, methods for making and materials prepared therefrom |
-
2011
- 2011-10-17 EP EP11833543.9A patent/EP2627447B1/en active Active
- 2011-10-17 SG SG2013028048A patent/SG189895A1/en unknown
- 2011-10-17 AU AU2011315852A patent/AU2011315852B2/en active Active
- 2011-10-17 CN CN201610543273.XA patent/CN106110898B/zh active Active
- 2011-10-17 WO PCT/US2011/056501 patent/WO2012051608A1/en active Application Filing
- 2011-10-17 EA EA201390560A patent/EA024707B1/ru not_active IP Right Cessation
- 2011-10-17 CA CA2814699A patent/CA2814699C/en active Active
- 2011-10-17 ES ES19197132T patent/ES2886889T3/es active Active
- 2011-10-17 JP JP2013534060A patent/JP2013545595A/ja active Pending
- 2011-10-17 CN CN201180060490.9A patent/CN103237600B/zh active Active
- 2011-10-17 ES ES11833543T patent/ES2768330T3/es active Active
- 2011-10-17 EP EP19197132.4A patent/EP3626341B1/en active Active
- 2011-10-17 US US13/879,519 patent/US8969424B2/en active Active
-
2013
- 2013-04-11 IL IL225696A patent/IL225696B/en active IP Right Grant
- 2013-04-12 ZA ZA2013/02674A patent/ZA201302674B/en unknown
- 2013-04-15 CL CL2013001033A patent/CL2013001033A1/es unknown
-
2015
- 2015-01-22 US US14/603,098 patent/US9944546B2/en active Active
-
2016
- 2016-06-29 JP JP2016128452A patent/JP6293822B2/ja active Active
- 2016-08-01 US US15/225,352 patent/US9768502B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP2627447B1 (en) | 2019-12-11 |
| CN106110898B (zh) | 2019-03-22 |
| CN103237600A (zh) | 2013-08-07 |
| US20130313118A1 (en) | 2013-11-28 |
| JP6293822B2 (ja) | 2018-03-14 |
| SG189895A1 (en) | 2013-06-28 |
| US9768502B2 (en) | 2017-09-19 |
| CA2814699A1 (en) | 2012-04-19 |
| US8969424B2 (en) | 2015-03-03 |
| CN106110898A (zh) | 2016-11-16 |
| CN103237600B (zh) | 2016-07-13 |
| IL225696A0 (en) | 2013-06-27 |
| JP2017018947A (ja) | 2017-01-26 |
| JP2013545595A (ja) | 2013-12-26 |
| EP3626341B1 (en) | 2021-06-09 |
| WO2012051608A1 (en) | 2012-04-19 |
| ES2886889T3 (es) | 2021-12-21 |
| EA024707B1 (ru) | 2016-10-31 |
| CA2814699C (en) | 2019-08-06 |
| EA201390560A1 (ru) | 2014-01-30 |
| AU2011315852A1 (en) | 2013-04-04 |
| EP3626341A1 (en) | 2020-03-25 |
| IL225696B (en) | 2019-02-28 |
| US20160346741A1 (en) | 2016-12-01 |
| CL2013001033A1 (es) | 2013-10-04 |
| AU2011315852B2 (en) | 2014-12-18 |
| EP2627447A1 (en) | 2013-08-21 |
| US9944546B2 (en) | 2018-04-17 |
| EP2627447A4 (en) | 2017-03-08 |
| US20150299001A1 (en) | 2015-10-22 |
| ZA201302674B (en) | 2014-09-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2768330T3 (es) | Membranas de intercambio aniónico y proceso para su producción | |
| ES2882803T3 (es) | Membranas de intercambio iónico | |
| EP2627436B1 (en) | Process for making a monomer solution for making cation exchange membranes | |
| ES2922731T3 (es) | Membranas de intercambio aniónico de alto rendimiento y métodos para producir las mismas |