-
Hintergrund der Erfindung
-
Gebiet der Erfindung
-
Die
vorliegende Erfindung betrifft einen Katalysator zur Reinigung eines
Abgases, das von einer Brennkraftmaschine eines Kraftfahrzeugs oder
dergleichen ausgestoßen
wird, und ein Abgasreinigungsverfahren, bei dem der Katalysator
verwendet wird. Sie betrifft insbesondere einen Katalysator und
ein Reinigungsverfahren, mit denen sich im Abgas enthaltene Stickstoffoxide
(NOx) auf effiziente Weise vermindern und reinigen lassen. Das Abgas
enthält
einen Überschuss
an Sauerstoff in einer höheren
Menge, als für
die vollständige
Oxidation von Reduktionsverbindungen wie Kohlenmonoxid (CO), Wasserstoff
(H2) oder Kohlenwasserstoff (HC) erforderlich
ist.
-
Beschreibung
des Standes der Technik
-
Als
Katalysator zur Reinigung des Abgases des Kraftfahrzeugs oder dergleichen
wurde üblicherweise ein
Drei-Wege-Katalysator verwendet, der das Abgas reinigt, indem er
im Abgas in einem theoretischen Luft-Kraftstoff-Verhältnis (stöchiometrisch) gleichzeitig
CO und HC oxidiert und NOx reduziert. Ein gut bekanntes Beispiel
des Drei-Wege-Katalysators setzt sich aus einem hitzebeständigen Substrat
aus Cordierit oder dergleichen und einer porösen Trägerschicht aus γ-Aluminiumoxid,
die darauf ausgebildet ist, zusammen. Die poröse Trägerschicht wird mit bei Katalysatoren
verwendeten Edelmetallen wie Platin (Pt), Rhodium (Rh) oder dergleichen
beladen.
-
Zum
Schutze der Umwelt wurde demgegenüber in letzter Zeit gefordert,
das im Abgas der Brennkraftmaschine des Kraftfahrzeugs oder dergleichen
enthaltene Kohlendioxid (CO2) zu reduzieren.
Das System, das dieses Erfordernis erfüllen kann, ist das System mit „magerer
Verbrennung", das
große
Aufmerksamkeit erregte und bei welchem der Kraftstoff in einer Atmosphäre, die
einen Überschuss
an Sauerstoff enthält,
mager verbrannt wird. Beim System mit magerer Verbrennung kann der
verminderte Kraftstoffverbrauch die Emission von CO2,
das bei der Verbrennung des Kraftstoffs erzeugt wird, einschränken.
-
Um
das Abgas zu reinigen, wenn das Luft-Kraftstoffverhältnis innerhalb
des theoretischen Luft-Kraftstoff-Verhältnisses
(stöchiometrisch)
liegt, oxidiert oder reduziert der herkömmliche Drei-Wege-Katalysator im Gegenteil
dazu gleichzeitig CO, HC oder NOx, er zeigt jedoch keine ausreichende
Reinigungsleistung dafür, NOx
durch eine Reduktion in der Atmosphäre des Abgases bei dem System
mit magerer Verbrennung, das einen Überschuss an Sauerstoff enthält, zu entfernen.
Unter diesen Umständen
wird gefordert, sowohl den Katalysator, als auch das Reinigungssystem,
die NOx sogar in einer einen Überschuss
an Sauerstoff enthaltenen Atmosphäre in effizienter Weise reinigen
können,
zu entwickeln.
-
Die
vorliegenden Anmelder schlugen Katalysatoren zur Abgasreinigung
vor, bei denen ein poröser Träger aus
Aluminiumoxid oder dergleichen mit Pt und Erdalkalimetallen, beispielsweise
Barium (Ba), beladen wird (Japanische Patentveröffentlichung 5-317625).
-
Wenn
das Luft-Kraftstoffverhältnis
impulsartig von der mageren Seite zur stöchiometrischen oder fetten
Seite hin gesteuert wird (Anfettungsimpuls), wird NOx bei diesem
Katalysator bei einem mageren Luft-Kraftstoffverhältnis im Erdalkalimetall okkludiert
(NOx-okkludierendes Material) und reagiert bei einem stöchiometrischen
oder fetten Luft-Kraftstoffverhältnis
mit den im zu reinigen Abgas enthaltenen Reduktionsverbindungen
wie HC oder CO. So kann NOx sogar im System mit magerer Verbrennung
auf effiziente Weise gereinigt werden.
-
Es
ist bekannt, dass die Reaktion der NOx-Reinigung durch den obigen
Katalysator zur Abgasreinigung aus einem ersten Schritt des Oxidierens
von im Abgas enthaltenem NO zu NOx, einem zweiten Schritt des Okkludierens
von NOx i. NOx-okkludierenden Material und einem dritten Schritt
des Reduzierens von aus dem NOx-okkludierenden Material emittierten
NOx durch im Abgas enthaltenes HC und CO auf dem Katalysator besteht.
-
Der
herkömmliche
Katalysator zur Abgasreinigung wies jedoch Nachteil auf dass in
der mageren Atmosphäre
bei Pt Partikelwachstum auftrat, so dass sich die Anzahl aktiver
Stellen auf dem Katalysator und somit der Reaktionsumsatz im obigen
ersten und dritten Schritt verminderte.
-
Andererseits
ist Rh als Edelmetall für
Katalysatoren bekannt, bei dem in der mageren Atmosphäre kaum
Partikelwachstum auftritt, obwohl das Oxidationsvermögen von
Rh demjenigen von Pt unterlegen ist. Aus diesem Grund wurde sowohl
der Einsatz von Pt als auch der von Rh als Katalysator untersucht.
-
Wenn
jedoch sowohl Pt als auch Rh verwendet werden, zeigt sich deutlich
der negative Effekt, dass Rh das Oxidationsvermögen von Pt behindert. Dass
heißt,
dass, wenn die Menge an zugegebenem Rh steigt, Rh den Reaktionsumsatz
von Pt, NO zu NOx in einem ersten Schritt zu oxidieren und somit
die Fähigkeit
des NOx-okkludierenden
Materials, NOx in einem zweiten Schritt zu okkludieren, vermindert.
Da sich Rh und das NOx-okkludierende
Material gegenseitig behindern, verhindert ein Nebeneinandervorliegen
von Rh und dem NOx-okkludierenden
Material, dass deren Eigenschaften zur Geltung kommen.
-
Daneben
kann das NOx-okkludierende Material, wenn es mit Schwefeloxiden
(SOx) wie Schwefeloxid (SO2), die im Abgas
enthalten sind, unter Erzeugung eines Salzes reagiert, keine Funktion
zur NOx-Okklusion mehr ausüben.
Da das gebildete Sulfat oder Sulfit nicht leicht löslich sind,
kann das NOx-okkludierende Material zudem seine natürliche NOx-okkludierende
Fähigkeit
kaum zeigen. Dies wird „Schwefelvergiftung" genannt und bezeichnet
die Vergiftung des NOx-okkludierenden Materials durch Schwefel.
-
Die
Japanische Patentveröffentlichung
10-356 offenbart einen Katalysator zur Abgasreinigung, der durch
Mischen von ersten Pulvern, bei denen Rh auf Aluminiumoxid oder
Zirkonoxid aufgetragen wird, mit zweiten Pulvern, bei denen Pt und
das NOx-okkludierende Material auf Aluminiumoxid aufgetragen werden, hergestellt
wird. Bei diesem Katalysator zur Abgasreinigung wird aufgrund der
getrennten Auftragung von Pt und Rh eine Abnahme des Oxidationsvermögens von
Pt durch Rh verhindert. Da auch Rh und das NOx-okkludierende Material getrennt aufgetragen
werden, behindern diese sich nicht gegenseitig und können so
ihre Eigenschaften ausreichend zur Geltung bringen.
-
Das
getrennt aufgebrachte Rh wirkt ferner dabei mit, dass das im Abgas
enthaltene HC und H2O Wasserstoff mit hohem
Reduktionsvermögen
erzeugt (Dampfreformierungsreaktion), der zur Reduktion der NOx und
Abtrennung der SOx vom Sulfat oder Sulfit im NOx-okkludierenden
Material beiträgt.
Auf diese Weise nimmt die Menge an reduziertem NOx im Anfettungsimpuls
zu und die Schwefelvergiftung des NOx-okkludierenden Materials deutlich ab.
-
Für eine Beladung
mit Rh wird als Träger übrigens
Zirconiumdioxid bevorzugt, das die Aktivität der Dampfreformierungsreaktion
von Rh erhöhen
kann. Zirconiumdioxid besitzt jedoch eine geringere Hitzebeständigkeit
als das oft für
Edelmetalle als Träger
verwendete Aluminiumoxid und deshalb nimmt die spezifische Oberfläche des
Trägers
bei Hitze ab, wenn der Katalysator zur Abgasreinigung verwendet
wird. Infolgedessen nimmt das Dispersionsvermögen des aufgetragenen Rh und
damit dessen Reinigungsleistung ab.
-
Da
Zirconiumdioxid unzureichend die Aktivität der Dampfreformierungsreaktion
von Rh erhöht,
wurde zudem die Entwicklung eines Trägers erwartet, der die Aktivität der Dampfreformierungsreaktion
von Rh weiter steigern kann.
-
US-A-5063192
offenbart einen Katalysator, der bei Abgasen verwendet wird, die
unter der Bedingung dass L/K (Luft/Kraftstoff) = 14,7 ist, verbrannt
wurden. Der Katalysator ist somit ein Drei-Wege-Katalysator zur Reinigung
von Abgasen in einer stöchiometrischen
Atmosphäre.
-
Die
vorliegende Erfindung wurde ausgehend von der obigen Situation gemacht
und es ist eine erste Aufgabe, das hohe Oxidationsvermögen von
Pt aufrechtzuerhalten, indem man eine Senkung des Oxidationsvermögens von
Pt durch Rh einschränkt.
-
Eine
zweite Aufgabe der vorliegenden Erfindung ist es, zu bewirken, dass
Rh eine ausreichende Aktivität
der Dampfreformierungsreaktion bei Verwendung von Zirconiumdioxid
als Träger
aufzeigt.
-
Eine
weitere Aufgabe der vorliegenden Erfindung ist es, die Vergiftung
des NOx-okkludierenden Materials durch Schwefel einzuschränken.
-
Ein
Katalysator zur Reinigung von Abgas, das von einer Brennkraftmaschine
ausgestoßen
wird, in der Kraftstoff in einem Zustand verbrannt wird, bei dem
ein Mischgas einer fetten Atmosphäre, das einen Überschuss
an Kraftstoff enthält,
impulsartig zu einem Mischgas einer mageren Atmosphäre, das
einen Überschuss an
Sauerstoff enthält,
zugeführt
wird, wie er in Anspruch 1 zur Lösung
der obigen Aufgabe angegeben ist, wird durch Mischen von ersten
Pulvern, bei denen wenigstens Platin (Pt) auf einen ersten Träger aus
porösen
Teilchen aufgetragen wird, mit zweiten Pulvern, bei denen wenigstens
Rhodium (Rh) auf einen zweiten Träger aufgetragen wird, und Auftragen
von NOx-okkludierendem Material auf wenigstens den ersten Träger hergestellt. Der
Katalysator zur Abgasreinigung ist dadurch gekennzeichnet, dass
der zweite Träger
aus Erdalkalimetall enthaltendem Zirconiumdioxid besteht, wobei
das Erdalkalimetall in einer Menge von nicht mehr als 11,35 Mol-%
enthalten ist.
-
Der
in Anspruch 3 angegebene Katalysator zur Abgasreinigung ist dadurch
gekennzeichnet, dass bei dem in Anspruch 1 angegebenen Katalysator
zur Abgasreinigung der zweite Träger
aus Zirconiumdioxid besteht, das wenigstens eines der aus Barium
und Calcium ausgewählten
Elemente enthält.
-
Ein
in Anspruch 4 angegebenes Abgasreinigungsverfahren ist dadurch gekennzeichnet,
dass das Abgas, das von einer Brennkraftmaschine ausgestoßen wird,
in der Kraftstoff in einem Zustand verbrannt wird, bei dem ein Mischgas
einer fetten Atmosphäre,
das einen Überschuss
an Kraftstoff enthält,
impulsartig zu einem Mischgas einer mageren Atmosphäre, das
einen Überschuss
an Sauerstoff enthält,
zugeführt
wird, mit einem Katalysator zur Abgasreinigung gereinigt wird. Der
Katalysator zur Abgasreinigung wird hierbei durch Mischen von ersten
Pulvern, bei denen wenigstens Pt auf einen ersten Träger aus
porösen
Teilchen aufgetragen wird, mit zweiten Pulvern, bei denen wenigstens
Rh auf einen zweiten Träger
aus Erdalkalimetall enthaltendem Zirconiumdioxid, wobei das Erdalkalimetall
in einer Menge von nicht mehr als 11,35 Mol-% enthalten ist, aufgetragen
wird, und Auftragen von NOx-okkludierendem Material auf wenigstens
den ersten Träger
hergestellt.
-
Das
in Anspruch 6 angegebene Abgasreinigungsverfahren ist dadurch gekennzeichnet,
dass bei dem in Anspruch 4 angegebenen Abgasreinigungsverfahren
der zweite Träger
aus Zirconiumdioxid besteht, das wenigstens eines der aus Barium
und Calcium ausgewählten
Elemente enthält.
-
Der
Katalysator zur Reinigung von Abgas, das von einer Brennkraftmaschine
ausgestoßen
wird, in der Kraftstoff in einem Zustand verbrannt wird, bei dem
ein Mischgas einer fetten Atmosphäre, das einen Überschuss
an Kraftstoff enthält,
impulsartig zu einem Mischgas einer mageren Atmosphären, das
einen Überschuss
an Sauerstoff enthält,
zugeführt
wird, wie in Anspruch 7 angegeben, wird durch Mischen von ersten Pulvern,
bei denen wenigstens Platin (Pt) auf einen ersten Träger aus
porösen
Teilchen aufgetragen wird, mit zweiten Pulvern, bei denen wenigstens
Rhodium (Rh) auf einen zweiten Träger aufgetragen wird, und Auftragen
von NOx-okkludierendem Material auf wenigstens den ersten Träger hergestellt.
Der Katalysator ist dadurch gekennzeichnet, dass der zweite Träger aus
Seltenerdelement enthaltendem Zirconiumdioxid besteht, wobei das
Seltenerdelement in einer Menge von nicht mehr als 11,0 Mol-% enthalten
ist.
-
Der
in Anspruch 8 angegebene Katalysator zur Abgasreinigung ist dadurch
gekennzeichnet, dass bei dem in Anspruch 7 angegebenen Katalysator
zur Abgasreinigung der zweite Träger
aus Lanthan enthaltendem Zirconiumdioxid besteht.
-
In
Anspruch 9 ist ein Abgasreinigungsverfahren zur Reinigung von Abgas,
das von einer Brennkraftmaschine ausgestoßen wird, in der Kraftstoff
in einem Zustand verbrannt wird, bei dem ein Mischgas einer fetten
Atmosphäre,
das einen Überschuss
an Kraftstoff enthält,
impulsartig zu einem Mischgas einer mageren Atmosphäre, das
einen Überschuss
an Sauerstoff enthält,
zugeführt
wird, mit einem Katalysator zur Abgasreinigung, der durch Mischen
von ersten Pulvern, bei denen wenigstens Pt auf einen ersten Träger aus
porösen Teilchen
aufgetragen wird, mit zweiten Pulvern, bei denen wenigstens Rh auf
einen zweiten Träger
aus Seltenerdmetall enthaltendem Zirconiumdioxid, wobei das Seltenerdelement
in einer Menge von nicht mehr als 11,0 Mol-% enthalten ist, aufgetragen
wird, und Aufragen von NOx-okkludierendem Material auf wenigstens den
ersten Träger
hergestellt wird, angegeben.
-
Das
in Anspruch 10 angegebene Abgasreinigungsverfahren ist dadurch gekennzeichnet,
dass bei dem in Anspruch 9 angegebenen Abgasreinigungsverfahren
der zweite Träger
aus Lanthan enthaltendem Zirconiumdioxid besteht.
-
Kurze Beschreibung
der Zeichnungen
-
1 ist
ein Graph, der die Beziehung zwischen der Menge an zugegebenem Ca
und der spezifischen Oberfläche
des Ca enthaltenden Zirconiumdioxids zeigt.
-
2 ist
ein Graph, der die Beziehung zwischen der Menge an zugegebenem Ba
und der spezifischen Oberfläche
des Ba enthaltenden Zirconiumdioxids zeigt.
-
3 ist
ein Graph, der die Beziehung zwischen der Menge an zugegebenem Ca
und der Menge an absorbiertem CO des Ca enthaltenden Zirconiumdioxids
zeigt.
-
4 ist
ein Graph, der die Beziehung zwischen der Menge an zugegebenem Ba
und der Menge an absorbiertem CO des Ba enthaltenden Zirconiumdioxids
zeigt.
-
5 ist
ein Graph, der die Beziehung zwischen der Temperatur des eingespeisten
Gases und der Menge an erzeugtem Wasserstoff des Ca enthaltenden,
mit Rh beladenen Zirconiumdioxids zeigt.
-
6 ist
ein Graph, der die Beziehung zwischen der Temperatur des eingespeisten
Gases und der Menge an erzeugtem Wasserstoff des Ba enthaltenden,
mit Rh beladenen Zirconiumdioxids zeigt.
-
7 ist
ein Diagramm, das das Infrarotabsorptionsspektrum des Ba enthaltenden
Zirconiumdioxids zeigt.
-
8 ist
eine schematische Darstellung zur Erläuterung des Katalysators zur
Abgasreinigung gemäß einer
Ausführungsform
der Erfindung.
-
9 ist
eine Darstellung zur Erläuterung
des Aufbaus, die das Innere der Beschichtungsschicht 2 aus 8 zeigt.
-
10 ist
ein Aufriss des Katalysators zur Abgasreinigung gemäß der neunten
Ausführungsform
der Erfindung.
-
11 ist
der Graphen einer Infrarotspektralanalyse der Zirconiumdioxidpulver,
die in den Ausführungsformen
und Vergleichsproben verwendet werden.
-
12 ist
ein Graph, der die spezifische Oberfläche der Zirconiumdioxidpulver,
die in den Ausführungsformen
und den Vergleichsproben verwendet werden, zeigt.
-
13 ist
ein Graphen, der die Menge an absorbiertem CO der zweiten Pulver,
die in den Ausführungsformen
und den Vergleichsproben verwendet werden, zeigt.
-
14 ist
ein Graph, der die Menge an erzeugtem Wasserstoff der zweiten Pulver,
die in den Ausführungsformen
und den Vergleichsproben verwendet werden, zeigt.
-
Bevorzugte
Ausführungsform
der Erfindung
-
Bei
dem erfindungsgemäßen Katalysator
zur Abgasreinigung wird Pt auf den ersten Träger aufgetragen, während Rh
auf den zweiten Träger
aufgetragen wird. Dass heißt,
dass aufgrund der getrennten Auftragung von Rh und Pt der negative
Effekt, dass das Oxidationsvermögen
von Pt durch benachbartes Rh behindert wird, behoben werden kann.
Zudem ist das Partikelwachstum von Rh bei magerer Atmosphäre sehr
viel kleiner als das von Pt. Die Gegenwart von Rh verlängert somit
die Lebensdauer des Katalysators zur Abgasreinigung.
-
Ferner
erzeugt das im Abgas enthaltene HC und H2O
unter Mitwirkung von Rh Wasserstoff mit hohem Reduktionsvermögen (Dampfreformierungsreaktion),
der, zusammen mit im Abgas enthaltenem HC und CO, zur Reduktion
der NOx und zur Abtrennung von SOx vom Sulfat oder Sulfit im NOx-okkludierenden
Material beiträgt.
Die Menge an reduziertem NOx im Anfettungsimpuls somit somit zu
und die Schwefelvergiftung des NOx-okkludierenden Materials nimmt
deutlich ab.
-
Für eine Beladung
mit Rh bevorzugt man als zweiten Träger übrigens Zirconiumdioxid, das
die Aktivität
der Dampfreformierungsreaktion von Rh extrem erhöhen kann. Wie oben erwähnt besitzt
Zirconiumdioxid jedoch eine geringere Hitzebeständigkeit als das oft für Edelmetalle
als Träger
verwendete Aluminiumoxid und deshalb nimmt die spezifische Oberfläche des
zweiten Trägers
bei Hitze ab, wenn der Katalysator zur Abgasreinigung verwendet
wird. Infolgedessen nimmt das Dispersionsvermögen des aufgetragenen Rh und
damit dessen Reinigungsleistung ab.
-
In
der vorliegenden Erfindung wird darum für eine Beladung mit Rh als
zweiter Träger
hitzebeständiges
Zirconiumdioxid verwendet, das hitzebeständig gemacht worden ist. Eine
Abnahme der spezifischen Oberfläche
des zweiten Trägers
bei ihrem Einsatz bei Hitze wird somit beschränkt und das hohe Dispersionsvermögen von
Rh aufrechterhalten, so dass der Katalysator sogar nach dem Dauerversuch
eine hohe Reinigungsleistung zeigt.
-
Als
hitzebeständiges
Zirconiumdioxid wird vorzugsweise Zirconiumdioxid verwendet, das
mit einem der Erdalkalimetalle und Seltenerdmetalle stabilisiert
worden ist. Der zweite Träger,
bei dem ein solches hitzebeständiges
Zirconiumdioxid verwendet wird und der durch das Erdalkalimetall
oder das Seltenerdmetall alkalisch wurde, zeigt ein ausgezeichnetes
Absorptionsvermögen
von Dampf (H2O). Die Dampfreformierungsreaktion
von Rh fördert
somit in ausreichender Weise die Erzeugung von Wasserstoff, der
die Reduktion der NOx und die Abtrennung der SOx vom Sulfat oder
Sulfit im NOx-okkludierenden Material vorantreibt.
-
Zudem
behält
der zweite Träger
mit der deutlich erhöhten
Hitzebeständigkeit
den hoch dispergierten Zustand von Rh bei und beschleunigt deshalb
gleichmäßiger die
Dampfreformierungsreaktion von Rh, so dass die Schwefelvergiftung
des NOx-okkludierenden Materials weiter eingeschränkt wird.
Gemäß dem erfindungsgemäßen Katalysator
zur Abgasreinigung hat sich die Leistungsfähigkeit zur Reinigung von NOx
mit diesen Funktionen deutlich verbessert und die hohe Reinigungsleistung
wurde sogar nach dem Dauerversuch beibehalten.
-
Die
den ersten Träger
bildenden porösen
Teilchen können
ausgewählt
sein aus Materialien wie Aluminiumoxid, Siliciumdioxid, Titandioxid,
Zirconiumdioxid, Siliciumdioxid-Aluminiumoxid und Zeolith. Für den ersten
Träger
können
eines dieser Materialien oder mehrere dieser Materialien, zusammengesetzt
oder miteinander vermischt, verwendet werden.
-
Um
die ersten Pulver zu bilden, wird wenigstens Pt auf den ersten Träger aufgetragen.
Die Menge an aufgetragenem Pt, bezogen auf 120 g ersten Träger, beträgt vorzugsweise
0,1 g bis 10 g. Die Menge an aufgetragenem Pt, bezogen auf den ersten
Träger,
von weniger als 0,1 g/120 g, vermindert die Reinigungsgeschwindigkeit
von HC, CO und NOx, wohingegen, wenn sie größer als 10 g/120 g ist, nicht
nur der Reinigungseffekt gesättigt
sondern auch die Kosten erhöht
sind. Neben Pt kann hier auch Pd auf den ersten Träger aufgetragen
werden; oder neben Pt kann auch Rh auf den ersten Träger aufgetragen
werden, wobei das Gewichtsverhältnis
bezogen auf Pt nicht mehr als 10 % beträgt.
-
Der
zweite Träger,
der aus mit wenigstens einem der Erdalkalimetalle und Seltenerdelemente
stabilisierten Zirconiumdioxid gebildet wird, kann mit dem Verfahren
der Copräzipitation
oder dem Sol-Gel-Verfahren hergestellt
werden. Beim Verfahren der Copräzipitation
kann der zweite Träger,
der aus mit wenigstens einem der Erdalkalimetalle und Seltenerdelemente
stabilisierten Zirconiumdioxid gebildet wird, durch Waschen, Trocknen
und Sintern (Verbacken) des Präzipitats,
das aus der Lösung,
in der die Zirconiumdioxidverbindung und eine der Erdalkalimetallverbindungen
und Seltenerdverbindungen gelöst
sind, copräzipitiert
wird, erhalten werden.
-
Im
Sol-Gel-Verfahren kann der zweite Träger, der aus mit wenigstens
einem der Erdalkalimetalle und Seltenerdelemente stabilisierten
Zirconiumdioxid gebildet wird, durch Trocknen und Sinter der, nach
Zugabe von Wasser, durch Hydrolysieren der Mischlösung aus
Alkoxid des Zirconiumdioxids und Alkoxid eines der Erdalkalimetalle
und Seltenerdenelemente erhaltenen Sole hergestellt werden.
-
Wenn
der auf diese Weise erhaltene zweite Träger einer Röntgenbeugung unterzogen wird,
lässt sich nur
ein Peak beim Zirconiumdioxid, aber kein Peak beim Erdalkalimetall
oder Seltenerdenmetall beobachten Ausgehend von dieser Tatsache
nimmt man an, dass sich das Erdalkalimetall oder das Seltenerdmetall
in dem Zirconiumdioxid gelöst
haben. Neben den oben angegebenen Herstellungsverfahren kann der
zweite Träger hier
mit anderen Verfahren, beispielsweise dem Mischen und Sintern von
Pulvern und so weiter hergestellt werden, und das Alkalimetall oder
Seltenerdmetall hat sich nicht zwingenderweise in Zirconiumdioxid
gelöst Die
bevorzugten Erdalkalimetalle, die im dem hitzebeständigen,
den zweiten Träger
bildenden Zirconiumdioxid enthalten sind, umfassen Magnesium (Mg),
Calcium (Ca), Strontium (Sr) und Barium (Ba). Die besten Ergebnisse
erhält
man mit Ba und Ca.
-
Die
bevorzugten Seltenerdmetalle, die in dem zweiten Träger enthalten
sind, umfassen Lanthan (La), Scandium (Sc), Yttrium (Y), Cer (Ce),
Praseodymium (Pr), Neodym (Nd), Samarium (Sm) und Ytterbium (Yb). Das
beste Ergebnis erhält
man mit La.
-
Mit
der im zweiten Träger
enthaltenen Menge an einem der Erdalkalimetalle und Seltenerdmetalle kann
unabhängig
davon, wie klein ihre Mengen sind, ein positiver Effekt erreicht
werden. Das Erdalkalimetall oder Seltenerdmetall ist jedoch als
Obergrenze in einer Menge von nicht mehr als 11,35 Mol-% bzw. 11,0 Mol-%
enthalten. Ein Überschuss
an Erdalkalimetall oder Seltenerdmetall über der Obergrenze wird nicht
bevorzugt, da dies die Leistungsfähigkeit zur Reinigung von NOx
vermindert.
-
Um
die zweiten Pulver aufzubauen wird wenigstens Rh auf den zweiten
Träger
aufgetragen. Die Menge an aufgetragenem Rh in den zweiten Pulvern,
bezogen auf 120 g an zweitem Träger,
beträgt
vorzugsweise 0,1 g bis 10 g. Eine Menge an aufgetragenem Rh von
kleiner als 0,1 g/120 g vermindert die Lebensdauer des zweiten Trägers, wohingegen,
wenn sie größer als
10 g/120 g ist, nicht nur der Reinigungseffekt gesättigt sondern
auch die Kosten erhöht
sind. Neben Rh kann hier auch Pd auf den zweiten Träger aufgetragen
werden oder neben Rh kann auch Pt auf den zweiten Träger aufgetragen
werden, wobei das Gewichtsverhältnis
bezogen auf Rh nicht mehr als 10 % beträgt.
-
Die
ersten Pulver und die zweiten Pulver werden in einem Mischungsverhältnis vermischt,
so dass das Gewichtsverhältnis
zwischen erstem Träger
und zweitem Träger
vorzugsweise zwischen 1:10 und 20:1 und besonders bevorzugt zwischen
1:2 und 5:1 liegt. Wenn das Gewichtsverhältnis größer oder kleiner als dieser Bereich
ist, können
die gleichen negativen Effekte entstehen, die von einem Mangel oder Überschuss
an Rh und Pt verursacht werden.
-
Die
Teilchendurchmesser der ersten und zweiten Pulver betragen zudem
vorzugsweise 1 μm
bis 100 μm.
Wenn die Teilchendurchmesser der Pulver kleiner als 1 μm sind, kann
der durch die getrennte Auftragung von Rh und Pt entstehende positive
Effekt kaum erhalten werden, während
die Wirkung zwischen den ersten und den zweiten Pulvern, wenn die
Teilchen größer als
100 μm sind,
klein wird und deshalb die Reinigungsleistung sinkt.
-
Wenigstens
eine der aus Alkalimetallen, Erdalkalimetallen und Seltenerdelementen
ausgewählten Elementsorten
kann als NOx-okkludierendes Material verwendet werden. Die Alkalimetalle
können
Lithium (Li), Natrium (Na), Kalium (K) und Caesium (Cs) umfassen.
Die Erdalkalimetalle, die den Elementen der Gruppe 2A des Periodensystems
entsprechen, umfassen Magnesium (Mg), Calcium (Ca), Strontium (Sr)
und Barium (Ba). Die Seltenerdmetalle umfassen Lanthan (La), Cer
(Ce) und Praseodym (Pr).
-
Diese
NOx-okkludierenden Elemente können
auf einen oder beide, den ersten und den zweiten Träger, aufgetragen
werden. Da sich Rh und das NOx-okkludierende Material gegenseitig
behindern stellt sich, wenn sie nebeneinander vorliegen, jedoch
das Problem, dass sich die Eigenschaften von Rh und dem NOx-okkludierenden Material
nicht ausreichend zeigen. Die Dampfreformierungsreaktion von Rh
wird zudem vom NOx-okkludierenden Material behindert. Aus diesem
Grund wird das NOx-okkludierende Material vorzugsweise nur auf den
ersten Träger
aufgetragen. Bei einem solchen Aufbau können sich die Eigenschaften
des NOx-okkludierenden Materials ausreichend zeigen und die Aktivität der Dampfreformierungsreaktion
von Rh maximal zeigen.
-
Die
Menge an aufgetragenem NOx-okkludierendem Material beträgt vorzugsweise
0,01 mol bis 5 mol pro 120 g Gesamtmenge des Trägers und besonders bevorzugt
0,1 mol bis 0,5 mol. Eine Menge an aufgetragenem NOx-okkludierendem
Material von kleiner als 0,01 mol/120 g senkt die Reinigungsgeschwindigkeit
von NOx, wohingegen, wenn sie größer als
5 mol/120 g ist, der Reinigungseffekt gesättigt ist.
-
Der
erfindungsgemäße Katalysator
zur Abgasreinigung kann durch Mischen der ersten, mit wenigstens
Pt beladenen Pulver und der zweiten, wenigstens mit Rh beladenen
Pulver und Auftragen des NOx-okkludierenden
Materials auf die vermischten Pulver hergestellt werden. Der Katalysator
kann auch durch Mischen der ersten, wenigstens mit Pt und NOx-okkludierendem
Material beladenen Pulver und der zweiten, wenigstens mit Rh beladenen
Pulver hergestellt werden. Der Katalysator kann ferner durch Auftragen
des NOx-okkludierenden
Materials zwischen den ersten, wenigstens mit Pt beladenen Pulvern
und den zweiten, wenigstens mit Rh beladenen Pulvern, auf wenigstens
die ersten Pulver oder sowohl auf die ersten als auch die zweiten
Pulver und Vermischen der ersten und der zweiten Pulver hergestellt
werden.
-
Der
erfindungsgemäße Katalysator
zur Abgasreinigung kann ein Pelletkatalysator, der aus im obigen Herstellungsverfahren
erhaltenen Katalysatorpulvern aufgebaut wird, oder ein Monolithkatalysator
sein, der aufgebaut wird, indem die Beschichtungsschicht der Katalysatorpulver
auf dem wabenförmigen
Trägersubstrat mit
Hitzebeständigkeit
gebildet wird.
-
Wenn
die Beschichtungsschicht der Katalysatorpulver auf dem Trägersubstrat
gebildet wird, ist die Beladungsdichte von Pt an der Oberfläche der
Beschichtungsschicht vorzugsweise höher als im Inneren der Schicht.
Bei dieser Beladungsdichte von Pt nehmen die Kontaktmöglichkeiten
zwischen der Abgasverbindung und Pt zu, so dass die Reaktionseffizienz
zwischen den beiden verbessert und auf diese Weise die Reinigungsleistung
des Katalysators weiter erhöht
wird.
-
Dass
heißt,
dass in magerer Atmosphäre
sich an die Katalysatoroberfläche
der Beschichtungsschicht annäherndes
NO durch Pt an der Oberflächenschicht
zu NOx oxidiert wird und in das Innere vordringt, wo es vom NOx-okkludierenden
Material okkludiert wird. Im Zustand des Anfettungsimpulses reagiert
das aus dem NOx-okkludierenden Material emittierte NOx mit dem in
der Dampfreformierungsreaktion von Rh aus HC und H2O
erzeugten Wasserstoff unter der Katalysatorwirkung von Pt, das in
hoher Dichte auf die Oberflächenschicht
geladen ist, indem es durch die Oberflächenschicht wandert. Somit
wird NOx vom Wasserstoff zu N2 reduziert
und anschließend
ausgestoßen.
Durch die Beladung der Oberflächenschicht
mit Pt in hoher Dichte erhöht
sich somit nicht nur weiter der Nutzwirkungsgrad von HC, sondern
auch die Leistungsfähigkeit
zur Reinigung von NOx im Zustand des Anfettungsimpulses. Zudem wird
die Reduktion von stark mit dem NOx-okkludierenden Material verbundenen
SOx mit Wasserstoff weiter aktiviert. Das NOx-okkludierende Material
erhält
somit wieder seine ursprüngliche
NOx-okkludierende Funktion zurück,
so dass sich die Leistungsfähigkeit zur
Reinigung von NOx weiter erhöht.
-
Die
auf die Oberflächenschicht
der Beschichtungsschicht aufgetragene Menge an Pt beträgt vorzugsweise
0,1 g bis 10 g pro 120 g poröse
Teilchen im gesamten Katalysator und besonders bevorzugt 0,1 g bis
2 g. Wenn die Menge an aufgetragenem Pt kleiner als 0,1 g ist, kann
der oben angegebene Effekt von Pt, der aus der Beladung mit hoher
Dichte der Oberflächenschicht
resultiert, nicht erfolgen, wohingegen die Reinigungsleistung, wenn
sie größer als
2 g ist, gesättigt
ist und die Kosten vermehrt werden.
-
Die
Menge an Pt, die derjenigen bei einem herkömmlichen Katalysator entspricht,
wird in ausreichender Weise auf den gesamten Katalysator aufgetragen,
so dass ein Kostenanstieg vermieden wird. Beispielsweise beträgt die Gesamtmenge
an Pt, die auf die ersten Pulver und die Oberflächenschicht aufgetragen wird, 0,1
g bis 10 g, was bedeutet, dass die Menge bei ersteren zwischen 0
g und 10 g und bei letzteren zwischen 10 g und 0 g variieren kann.
-
Daneben
kann Rh außer
auf die zweiten Pulver auch auf die Oberflächenschicht der Beschichtungsschicht
aufgetragen werden. In diesem Fall beträgt die Menge an auf die Oberflächenschicht
aufgetragenem Rh, bezogen auf die Menge an auf die Oberflächenschicht
aufgetragenem Pt, vorzugsweise nicht mehr als 10 %. Wenn dieser
Anteil größer als
10% ist, nimmt das Oxidationsvermögen des auf die Oberflächenschicht
aufgetragenen Pt ab und senkt dadurch die Leistungsfähigkeit
des Katalysators zur Reinigung von NOx.
-
Das
NOx-okkludierende Material kann zudem in konzentrierter Form auf
die Oberflächenschicht
der Beschichtungsschicht aufgetragen werden. In diesem Fall werden
vorzugsweise Alkalimetalle mit hohem Vermögen zur Okklusion bei kleiner
Menge als NOx-okkludierendes Material verwendet. Die Menge an NOx-okkludierendem Material
in der Oberflächenschicht
pro 120 g poröse
Teilchen des gesamten Katalysators beträgt 0 mol bis 5 mol und besonders
bevorzugt 0,1 mol bis 0,5 mol. Das im Überschuss aufgetragene NOx-okkludierende Material
kann die Reinigungsleistung der Edelmetalle deutlich beschränken.
-
Bei
dem erfindungsgemäßen Katalysator
zur Abgasreinigung und dem erfindungsgemäßen Abgasreinigungsverfahren
und unter Verwendung der zweiten Pulver, bei denen Rh auf das hitzebeständige Zirconiumdioxid
aufgetragen wird, hat sich so die Aktivität der Dampfreformierungsreaktion
von Rh deutlich erhöht. Durch
die getrennte Beladung mit Pt und Rh, durch welche sich das Oxidationsvermögen von
Pt nicht vermindert hat, hat sich auch die Hitzebeständigkeit
des Katalysators erhöht.
Durch diese Funktionen zeigt der Katalysator sogar nach dem Dauerversuch
eine höhere
Aktivität
zur Reinigung von NOx.
-
Der
deutliche Anstieg der Aktivität
der Dampfreformierungsreaktion von Rh beschränkt zudem die Schwefelvergiftung
des NOx-okkludierenden Materials durch Schwefel, so dass die hohe
Aktivität
des Katalysators zur Reinigung von NOx sogar nach dem Dauerversuch
beibehalten wird und somit die Lebensdauer weiter verlängert.
-
Ausführungsformen
-
Im
Folgenden wird die vorliegende Erfindung unter Bezugnahme von Testproben,
Ausführungsformen und
Vergleichsproben in konkreter Weise beschrieben.
-
Testproben
-
Durch
Testproben wurden zunächst
die Eigenschaften des mit dem Erdalkalimetall stabilisierten Zirconiumdioxids
getestet.
-
Herstellung
von mit Ca stabilisiertem Zirconiumdioxid
-
Sechs
Sorten mit Ca stabilisiertem Zirconiumdioxid, die jeweils 0,66 Mol-%
Ca, 1,09 Mol-% Ca, 1,74 Mol-% Ca, 2,39 Mol-% Ca, 4,6 Mol-% Ca, 3
Mol-% Ca und 11,35 Mol-% Ca enthielten, wurden mit dem Verfahren
der Copräzipitation
hergestellt, bei dem Ammoniakwasser zu der Mischlösung aus
Zirconiumverbindung und Calciumverbindung gegeben wurde.
-
Herstellung
von Ba enthaltendem Zirconiumdioxid
-
Fünf Sorten
Ba enthaltendes Zirconiumdioxid, die jeweils 0,48 Mol-% Ba, 0,94
Mol-% Ba, 1,83 Mol-% Ba, 2,94 Mol-% Ba und 5,37 Mol-% Ba enthielten,
wurden mit dem Verfahren der Copräzipitation hergestellt, bei
dem Ammoniakwasser zu der Mischlösung
aus Zirconiumverbindung und Bariumverbindung gegeben wurde.
-
Testprobe 1
-
Die
spezifische Oberfläche
des Ca enthaltenden Zirconiumdioxids (Ca enthaltendes Zirconiumdioxid) und
des Ba enthaltenden Zirconiumdioxids (Ba enthaltendes Zirconiumdioxid)
wurden gemessen und sind als Anfangswerte (frisch) in 1 bzw. 2 angegeben.
Die spezifischen Oberflächen
des Ca enthaltenden Zirconiumdioxids und des Ba enthaltenden Zirconiumdioxids,
die jeweils einer Behandlung bei hoher Temperatur an Luft unter
zwei Bedingungen, 5 Stunden bei 600 °C und 10 Stunden bei 800 °C, ausgesetzt
wurden, sind in 1 bzw. 2 gezeigt.
Das reine Zirconiumdioxid, das kein Erdalkalimetall enthält, wird
auf ähnliche
Weise getestet.
-
Wie
aus den 1 und 2 zu sehen
ist, erhöht
die Zugabe von Ca und Ba die spezifischen Oberflächen der stabilisierten Zirconiumdioxide
nach Behandlung bei hoher Temperatur im Vergleich zu derjenigen von
reinem Zirconiumdioxid. Wenn die Menge an zugegebenem Ca ansteigt,
erhöht
sich auch die spezifische Oberfläche
des stabilisierten Zirconiumdioxids nach Behandlung bei hoher Temperatur,
während
sich bestätigt, dass
eine Zugabe von Ba von 2 bis 3 % die spezifische Oberfläche des
mit Ba stabilisierten Zirconiumdioxids gesättigt.
-
Testprobe 2
-
Ca
enthaltendes Zirconiumdioxid, Ba enthaltendes Zirconiumdioxid und
reines Zirconiumdioxid wurden mit einer wässrigen Rhodiumnitratlösung imprägniert,
diese jeweils abgedampft und getrocknet, um so mit Rh beladen zu
werden. 0,5 g Rh wird auf jeweils 120 g an Ca enthaltendem Zirconiumdioxid,
Ba enthaltendem Zirconiumdioxid und reinem Zirconiumdioxid aufgetragen.
-
Jedes
der drei mit Rh beladenen Zirconiumdioxide absorbierte CO im chemischen
Absorptionsverfahren von CO, so dass die absorbierte Menge an CO
gemessen werden konnte. Jedes der drei mit Rh beladenen Zirconiumdioxide
wurde auch 5 Stunden lang einer Behandlung bei hoher Temperatur
an Luft bei 600 °C
unterzogen und anschließend
wurde die von ihnen absorbierte Menge an CO in ähnlicher Weise gemessen. Die Messergebnisse
des Ca enthaltenden Zirconiumdioxids und des Ba enthaltenden Zirconiumdioxids
sind in 3 bzw. 4 gezeigt.
-
Wie
aus den 3 und 4 zu sehen
ist, erhöhte
sich die Menge an absorbiertem CO nach Behandlung bei hoher Temperatur
durch das zum Zirconiumdioxid zugegebene Erdalkalimetall. Ausgehend
von dieser Tatsache nimmt man an, dass das hohe Dispersionsvermögen von
Rh und die große
Oberfläche
von Rh nach Behandlung bei hoher Temperatur viele Aktivierungsstellen
für Rh
ermöglichen.
Somit bestätigt
sich, dass die Verschlechterung des aufgetragenen Rh zum größten Teil
durch die Zugabe von Erdalkalimetall zum Zirconiumdioxid eingeschränkt wird.
-
Testprobe 3
-
Ca
enthaltendes Zirconiumdioxid, Ba enthaltendes Zirconiumdioxid und
reines Zirconiumdioxid wurden mit einer wässrigen Rhodiumnitratlösung imprägniert,
diese jeweils abgedampft und getrocknet, um so mit Rh beladen zu
werden. 0,5 g Rh wurden auf jeweils 120 g eines einen Zusatz enthaltenden
Zirconiumdioxids und reinen Zirconiumdioxids aufgetragen.
-
Jedes
der drei mit Rh beladenen Zirconiumdioxide wurde 10 Stunden lang
einer Behandlung bei hoher Temperatur bei 600 °C und anschließend der
Dampfreformierungsreaktion unter Verwendung des Gases mit der in
der folgenden Tabelle 1 gezeigten Zusammensetzung in einem Temperaturbereich
von 300 °C
bis 600 °C
unterzogen. Die Menge an erzeugtem Wasserstoff wurde mit einem Gaschromatographen
gemessen und die Messergebnisse davon sind in den 5 und 6 gezeigt.
-
-
Wie
aus den 4 und 5 zu sehen
ist, erhöht
die Menge an zugegebenem Erdalkalimetall die Menge an erzeugtem
Wasserstoff nach Behandlung bei hoher Temperatur, was zeigt, dass
das zugegebene Erdalkalimetall die Aktivität der Dampfreformierungsreaktion
verbessert.
-
Testprobe 4
-
Das
mit Ca stabilisierte Zirconiumdioxid wurde einer Infrarotspektralanalyse
unterworfen und das resultierende IR-Spektrum davon ist in 7 gezeigt.
Wie aus 7 zu sehen ist, erhöht die Menge
an zugegebenem Ca den Intensitätspeak,
da sich die Hydroxylgruppe zu einer höheren Wellenzahl hin verschoben
hat und stärkere
alkalische Funktionen zeigt. Ausgehend von dieser Tatsache nimmt
man an, dass sich das Absorptionsvermögen von Zirconiumdioxid für Wasser
mit Zunahme der Menge an zugegebenem Ca erhöht hat, was die Aktivität der Dampfreformierungsreaktion
verbessert, wie oben in Testprobe 3 beschrieben ist.
-
Mit
den Ergebnissen der obigen Testproben 1 bis 4 wurden die folgenden
Punkte verdeutlicht. Die Zirconiumdioxide, die mit den Erdalkalimetallen
stabilisiert worden waren, zeigten nach Behandlung bei hoher Temperatur
eine große
spezifische Oberfläche,
welche die Beständigkeit
des Dispersionsvermögens
von Rh erhöht,
so dass die Verschlechterung des Katalysators eingeschränkt wird.
Daneben wird aufgrund der erhöhten
alkalischen Funktion der Hydroxylgruppe die Aktivität der Dampfreformierungsreaktion
von Rh sogar nach Behandlung bei hoher Temperatur in hohem Maße aufrechterhalten,
so dass sich die Aktivität
zur Erzeugung von Wasserstoff stark erhöht, wenn Erdalkalimetalle enthaltende
Zirconiumdioxide verwendet werden. Aus diesem Grund erwartet man,
dass man durch eine Verwendung der Erdalkalimetalle enthaltenden
Zirconiumdioxide die Aktivität
zur Reinigung von NOx nach dem Dauerversuch erhöhen und die Schwefelvergiftung
des NOx-okkludierenden Materials vermindern kann.
-
Ausführungsform 1
-
Die 8 und 9 zeigen
den Katalysator zur Abgasreinigung gemäß der ersten Ausführungsform der
vorliegenden Erfindung. Dieser Katalysator ist aus einem wabenförmigen Substrat 1 aus
Cordierit und einer Beschichtungsschicht 2, die auf einer
Oberfläche
des wabenförmigen
Substrats 1 ausgebildet wird und aus Aluminiumoxid, Titandioxid
und Ca enthaltendem Zirconiumdioxid besteht, aufgebaut.
-
Die
Beschichtungsschicht 2 wird, wie in 9 gezeigt,
durch Mischen von ersten Pulvern 3, bei denen Ba 31 und
Pt 32 auf einem ersten Träger 30 aus Aluminiumoxid
und Titandioxid aufgetragen sind, mit zweiten Pulvern 4,
bei denen Rh 41 auf einem zweiten Träger 40 aus Ca enthaltendem
Zirconiumdioxid aufgetragen ist, gebildet. Auf die Oberflächenschicht
der Beschichtungsschicht 2 werden Pt, Rh, K und Li (nicht
gezeigt) aufgetragen.
-
Um
den Aufbau zu verdeutlichen, soll im Folgenden ein Herstellungsverfahren
für diesen
Katalysator beschrieben werden.
-
Herstellung von ersten
Pulvern
-
Die
ersten Trägerpulver,
die durch Mischen von 480 g γ-Aluminiumoxidpulvern
und 120 g Titandioxidpulvern hergestellt wurden, wurden mit einer
vorher festgelegten Menge einer wässrigen Bariumacetatlösung mit
vorher festgelegter Dichte imprägniert
und anschließend
wurde die Mischung aus Pulvern und wässriger Lösung 3 Stunden lang unter Rühren bei
110 °C getrocknet,
um den Wasseranteil zu verdampfen. Die getrockneten Pulver werden,
nachdem sie zerstoßen
wurden, bei 500 °C
3 Stunden lang gesintert, so dass Ba aufgetragen werden kann. Die
Menge an aufgetragenem Ba beträgt
1,6 mol pro 600 g des ersten Trägerpulvers.
-
Anschließend werden
die so erhaltenen Pulver in 6 l wässrige Ammoniumhydrogencarbonatlösung mit einer
Dichte von 0,3 mol/l getaucht und die wässrige Lösung wird nach 15-minütigem Rühren filtriert.
Die abfiltrierten Pulver werden 3 Stunden lang bei 110 °C getrocknet
und anschließend
zerstoßen.
Bei dieser Behandlung wandelt sich das Ba in Bariumcarbonat um und
wird gleichmäßig auf
die ersten Trägerpulver
geladen.
-
Die
mit Ba beladenen ersten Trägerpulver
werden in eine wässrige
Dinitrodiaminplatinnitratlösung
mit vorher bestimmter Dichte getaucht und die wässrige Lösung wird anschließend filtriert.
Die abfiltrierten Pulver werden 3 Stunden lang bei 110 °C getrocknet,
zerstoßen
und 1 Sunde lang bei 400 °C
getrocknet, um Pt darauf zu laden. Anschließend werden die mit Pt beladenen
Pulver in eine wässrige
Rhodiumnitratlösung
mit vorher festgelegter Dichte getaucht und dann wird die wässrige Lösung filtriert.
Die abfiltrierten Pulver werden 3 Stunden lang bei 110 °C getrocknet,
zerstoßen
und 2 Stunden lang bei 400 °C
getrocknet, um Rh darauf zu laden. Die Menge an aufgetragenem Pt
beträgt
4,0 g und die von Rh 0,2 g pro 600 g des ersten Trägerpulvers.
Die ersten Pulver wurden auf diese Weise hergestellt.
-
Herstellung
von zweiten Pulvern
-
Durch
Zugabe von Ammoniakwasser zur wässrigen
Mischlösung
aus der Zirconiumverbindung und der Calciumverbindung wurden die
Ca enthaltenden Zirconiumdioxidpulver, die 0,66 Mol-% Ca enthalten,
mit dem Verfahren der Copräzipitation
hergestellt.
-
384
g Ca enthaltendes Zirconiumdioxidpulver werden in eine wässrige Rhodiumnitratlösung mit
vorher festgelegter Dichte getaucht und anschließend wird die wässrige Lösung filtriert.
Die abfiltrierten Pulver werden 3 Stunden lang bei 110 °C getrocknet,
zerstoßen
und 1 Stunde lang bei 400 °C
gesintert, um Rh darauf zu laden. Die Menge an aufgetragenem Rh
beträgt
2,0 g pro 384 g des Ca enthaltenden Zirconiumdioxidpulvers. Die
zweiten Pulver wurden auf diese Weise hergestellt.
-
Ausbildung
der Beschichtungsschicht
-
Mit
der gleichförmigen
Mischung der gesamten ersten Pulver und der gesamten zweiten Pulver
wurden 340 g alkalisches Zirconiumdioxidsol, 1000 g reines Wasser
und 10 g 28% Ammoniakwasser gemischt. Die Mischung wird nach ausreichend
langem Rühren
mit einer Reibe zu einer Aufschlämmung
vermahlen. Die Aufschlämmung
hat einen pH von 9.
-
Das
wabenförmige
Substrat mit einem Volumen von 1,3 l, das aus Cordierit besteht,
wird in die Aufschlämmung
getaucht und anschließend
herausgezogen, so dass die überschüssige Aufschlämmung abgeblasen
werden kann. Das wabenförmige
Substrat wird anschließend
getrocknet und gesintert, so dass die Beschichtungsschicht darauf
ausgebildet werden kann. 320,5 g Beschichtungsschicht wurden pro
1 l wabenförmiges
Substrat im gesinterten Gewicht ausgebildet.
-
Beladung der Oberflächenschicht
mit Pt, Rh, K und Li
-
Das
wabenförmige
Substrat, auf welchem die Beschichtungsschicht ausgebildet wurde,
wird in eine wässrige
Dinitrodiaminplatinnitratlösung
mit vorher festgelegter Dichte getaucht, herausgezogen, so dass
die nicht erforderlichen Tröpfchen
abgeblasen werden können
und 3 Stunden lang bei 110 °C
getrocknet. Dann wurde das wabenförmige Substrat in eine wässrige Rhodiumnitratlösung mit
vorher festgelegter Dichte getaucht, herausgezogen, so dass die
nicht erforderlichen Tröpfchen
abgeblasen werden können
und 3 Stunden lang bei 250 °C
getrocknet. Anschließend
wurde das wabenförmige
Substrat 1 Stunde lang bei 400 °C
gesintert. Auf die Oberflächenschicht
der Beschichtungsschicht wurden zusätzlich 1 g Pt bzw. 0,05 g Rh
pro 1 l Substrat aufgetragen.
-
Das
wabenförmige
Substrat wird zudem in eine wässrige
Kaliumnitratlösung
mit vorher festgelegter Dichte und eine wässrige Lithiumnitratlösung mit
vorher festgelegter Dichte getaucht, herausgezogen, so dass die
nicht erforderlichen Tröpfchen
abgeblasen werden können,
bei 250 °C
getrocknet und 1 Stunde lang bei 500 °C gesintert. Auf diese Weise
wurde der Katalysator der Ausführungsform
1 erhalten. Auf die Oberflächenschicht
der Beschichtungsschicht wurden zusätzlich 0,1 mol K bzw. 0,1 mol
Li pro 1 l Substrat aufgetragen.
-
Bewertungstest
-
Jeder
der erhaltenen wabenförmigen
Katalysatoren, der in der Abgasanlage einer 1,8 1-Maschine mit magerer
Verbrennung eingebaut wurde, wurde einem Dauerversuch unterzogen,
der einer effektiven Laufleistung von 50.000 km entspricht, unterzogen.
Danach wurden in der gleichen Abgasanlage (Temperatur des eingespeisten
Gases: 400 °C)
die Menge an okkludiertem NOx im mageren Zustand, die Menge an reduziertem NOx
im Anfettungsimpuls (0,3 Sekunden) und die NOx-Emission unter den
Fhrtbedingungen des 10–15
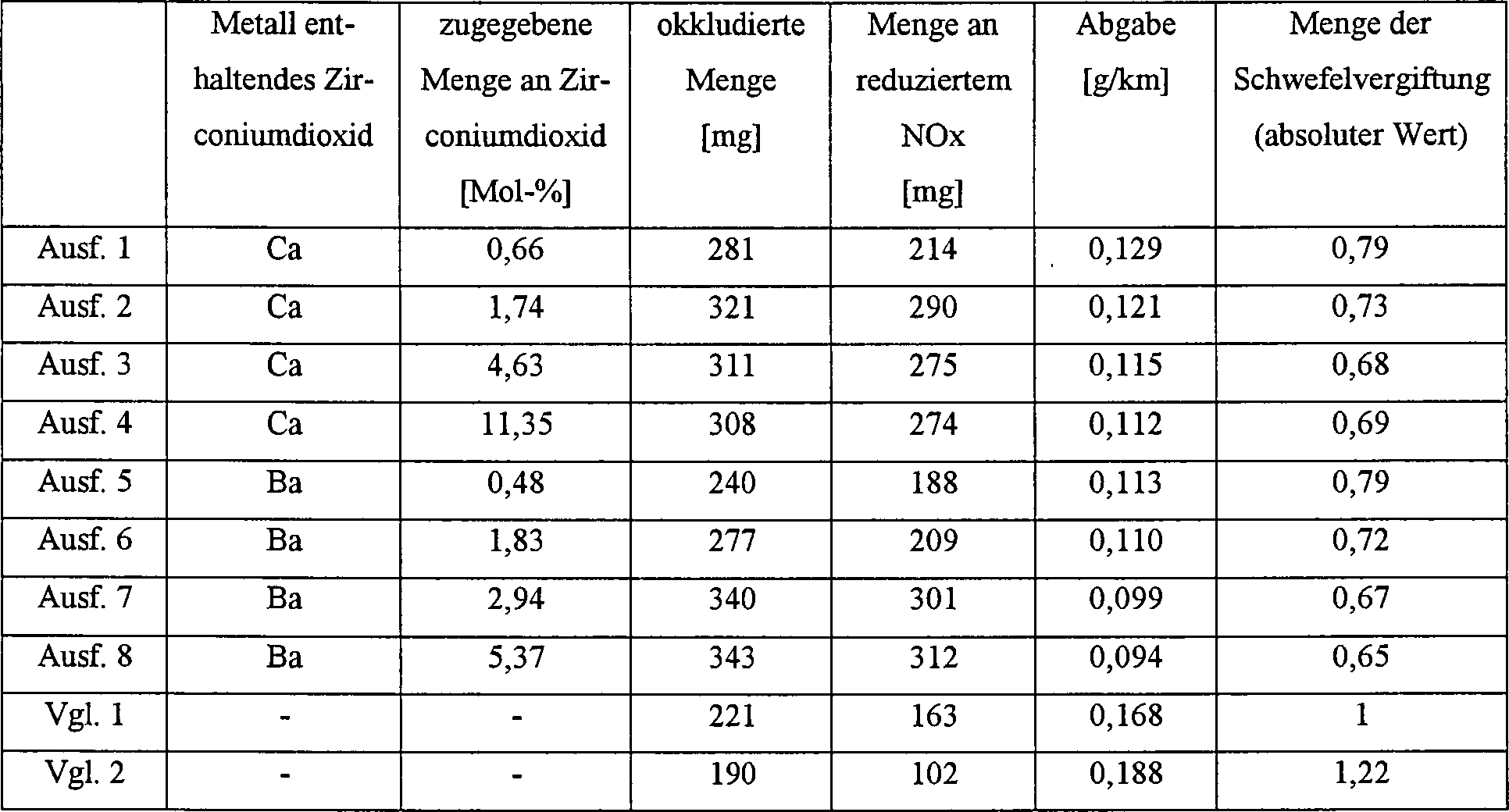
Modus gemessen. Die Messergebnisse sind in Tabelle 2 gezeigt.
-
Der
Grad der Schwefelvergiftung des NOx-okkludierenden Materials im
Dauerversuch wurde aus der Differenz der Reinigungsgeschwindigkeiten
von NOx vor und nach dem Dauerversuch gemessen und ist als absoluter
Wert bezogen auf das Ergebnis mit dem Katalysators der Vergleichsprobe
1, das später
erklärt
werden soll, in Tabelle 2 gezeigt,
-
Ausführungsform 2
-
Bei
den mit Ca stabilisierten Zirconiumdioxidpulvern, die so hergestellt
wurden, dass sie 1,74 mol Ca enthielten, wurde Rh auf die gleiche
Weise wie bei der Ausführungsform
1 oben aufgetragen, wodurch die zweiten Pulver hergestellt wurden.
Die zweiten Pulver werden genauso so wie in der Ausführungsform
1 oben mit den ersten Pulvern vermischt, so dass sie die Beschichtungsschicht
bilden, und anschließend
werden zusätzlich
Pt, Rh, K und Li auf die Beschichtungsschicht aufgetragen. Der Katalysator
der Ausführungsform
2 wurde auf diese Weise hergestellt. Dieser Katalysator der Ausführungsform
2 wurde einem Bewertungstest unterzogen, der demjenigen des Katalysators
der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 3
-
Bei
den mit Ca stabilisierten Zirconiumdioxidpulvern, die so hergestellt
wurden, dass sie 4,63 mol Ca enthielten, wurde Rh auf die gleiche
Weise wie bei der Ausführungsform
1 oben aufgetragen, wodurch die zweiten Pulver hergestellt wurden.
Die zweiten Pulver werden genauso so wie in der Ausführungsform
1 oben mit den ersten Pulvern vermischt, so dass sie die Beschichtungsschicht
bilden, und anschließend
werden zusätzlich
Pt, Rh, K und Li auf die Beschichtungsschicht aufgetragen. Der Katalysator
der Ausführungsform
3 wurde auf diese Weise hergestellt. Dieser Katalysator der Ausführungsform
3 wurde einem Bewertungstest unterzogen, der demjenigen des Katalysators
der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 4
-
Bei
den mit Ca stabilisierten Zirconiumdioxidpulvern, die so hergestellt
wurden, dass sie 11,35 mol Ca enthielten, wurde Rh auf die gleiche
Weise wie bei der Ausführungsform
1 oben aufgetragen, wodurch die zweiten Pulver hergestellt wurden.
Die zweiten Pulver werden genauso so wie in der Ausführungsform
1 oben mit den ersten Pulvern vermischt, so dass sie die Beschichtungsschicht
bilden, und anschließend
werden zusätzlich
Pt, Rh, K und Li auf die Beschichtungsschicht aufgetragen. Der Katalysator
der Ausführungsform
4 wurde auf diese Weise hergestellt. Dieser Katalysator der Ausführungsform
4 wurde einem Bewertungstest unterzogen, der demjenigen des Katalysators
der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 5
-
Aus
einer wässrigen
Lösung
der Bariumverbindung wie Bariumacetat usw. wurden die mit Ba stabilisierten
Zirconiumdioxidpulver, die 0,48 mol Ba enthielten, auf die gleiche
Weise hergestellt, wie die mit
-
Ba
stabilisierten Zirconiumdioxidpulver der Ausführungsform 1 oben. Anschließend wird
Rh auf die gleiche Weise wie bei der Ausführungsform 1 oben auf die Ba
enthaltenden Zirconiumdioxidpulver aufgetragen, wodurch die zweiten
Pulver hergestellt wurden. Dann werden die zweiten Pulver mit den
ersten Pulvern auf die gleiche Weise wie in der Ausführungsform
1 vermischt, so dass sie die Beschichtungsschicht ausbilden, und
Pt, Rh, K und Li werden zusätzlich
auf die gleiche Weise wie bei der Ausführungsform 1 auf die Beschichtungsschicht
aufgetragen. Der Katalysator der Ausführungsform 5 wurde auf diese
Weise hergestellt. Der Katalysator der Ausführungsform 5 wurde einem Bewertungstest
unterzogen, der demjenigen des Katalysators der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 6
-
Aus
einer wässrigen
Lösung
der Bariumverbindung wie Bariumacetat usw. wurden die mit Ba stabilisierten
Zirconiumdioxidpulver, die 1,38 mol Ba enthielten, auf die gleiche
Weise hergestellt, wie die mit Ba stabilisierten Zirconiumdioxidpulver
der Ausführungsform
1 oben. Anschließend
wird Rh auf die gleiche Weise wie bei der Ausführungsform 1 oben auf die Ba
enthaltenden Zirconiumdioxidpulver aufgetragen, wodurch die zweiten
Pulver hergestellt wurden. Dann werden die zweiten Pulver mit den
ersten Pulvern auf die gleiche Weise wie in der Ausführungsform
1 vermischt, so dass sie die Beschichtungsschicht ausbilden, und
Pt, Rh, K und Li werden zusätzlich
auf die gleiche Weise wie bei der Ausführungsform 1 auf die Beschichtungsschicht
aufgetragen. Der Katalysator der Ausführungsform 6 wurde auf diese
Weise hergestellt. Der Katalysator der Ausführungsform 6 wurde einem Bewertungstest
unterzogen, der demjenigen des Katalysators der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 7
-
Aus
einer wässrigen
Lösung
der Bariumverbindung wie Bariumacetat usw. wurden die mit Ba stabilisierten
Zirconiumdioxidpulver, die 2,94 mol Ba enthielten, auf die gleiche
Weise hergestellt, wie die mit Ba stabilisierten Zirconiumdioxidpulver
der Ausführungsform
1 oben. Anschließend
wird Rh auf die gleiche Weise wie bei der Ausführungsform 1 oben auf die Ba
enthaltenden Zirconiumdioxidpulver aufgetragen, wodurch die zweiten
Pulver hergestellt wurden. Dann werden die zweiten Pulver mit den
ersten Pulvern auf die gleiche Weise wie in der Ausführungsform
1 vermischt, so dass sie die Beschichtungsschicht ausbilden, und
Pt, Rh, K und Li werden zusätzlich
auf die gleiche Weise wie bei der Ausführungsform 1 auf die Beschichtungsschicht
aufgetragen. Der Katalysator der Ausführungsform 7 wurde auf diese
Weise hergestellt. Der Katalysator der Ausführungsform 7 wurde einem Bewertungstest
unterzogen, der demjenigen des Katalysators der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Ausführungsform 8
-
Aus
einer wässrigen
Lösung
der Bariumverbindung wie Bariumacetat usw. wurden die mit Ba stabilisierten
Zirconiumdioxidpulver, die 5,37 mol Ba enthielten, auf die gleiche
Weise hergestellt, wie die mit Ba stabilisierten Zirconiumdioxidpulver
der Ausführungsform
1 oben. Anschließend
wird Rh auf die gleiche Weise wie bei der Ausführungsform 1 oben auf die Ba
enthaltenden Zirconiumdioxidpulver aufgetragen, wodurch die zweiten
Pulver hergestellt wurden. Dann werden die zweiten Pulver mit den
ersten Pulvern auf die gleiche Weise wie in der Ausführungsform
1 vermischt, so dass sie die Beschichtungsschicht ausbilden, und
Pt, Rh, K und Li werden zusätzlich
auf die gleiche Weise wie bei der Ausführungsform 1 auf die Beschichtungsschicht
aufgetragen. Der Katalysator der Ausführungsform 8 wurde auf diese
Weise hergestellt. Der Katalysator der Ausführungsform 8 wurde einem Bewertungstest
unterzogen, der demjenigen des Katalysators der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Vergleichsprobe 1
-
Rh
wird auf die Zirconiumdioxidpulver mit einer Reinheit von 99,5 %
(einschließlich
HfO2) statt auf die mit Ca stabilisierten
Zirconiumdioxidpulver aufgetragen, so dass die zweiten Pulver auf
die gleiche Weise wie bei der Ausführungsform 1 oben hergestellt
werden können.
Die zweiten Pulver werden mit den ersten Pulvern auf die gleiche
Weise wie bei der Ausführungsform
1 vermischt, so dass sie die Beschichtungsschicht ausbilden und
Pt, Rh, K und Li werden zusätzlich
auf die gleiche Weise wie bei der Ausführungsform 1 auf die Beschichtungsschicht
aufgetragen, um den Katalysator der Vergleichsprobe 1 herzustellen.
Der Katalysator dieser Vergleichsprobe 1 wurde einem Bewertungstest
unterzogen, der demjenigen des Katalysators der Ausführungsform
1 ähnelt
und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
Vergleichsprobe 2
-
Die
Aufschlämmung
wurde hergestellt, indem die gemischten Pulver, einschließlich 480
g γ-Aluminiumoxidpulver,
120 g Titandioxidpulver und 384 g Zirconiumdioxidpulver, mit 340
g alkalischem Zirconiumdioxidsol, 1000 g reinem Wasser und 10 g
28% Ammoniakwasser ausreichend vermischt wurden und die Mischung
anschließend
mit einer Reibe vermahlen wurde. Diese Aufschlämmung wird dazu verwendet,
die Beschichtungsschicht auf die gleiche Weise wie bei der Ausführungsform
1 oben auszubilden.
-
Danach
wird das wabenförmige
Substrat mit einer wässrigen
Bariumacetatlösung
mit vorher festgelegter Dichte beschichtet, um die Beschichtungsschicht
in vorher bestimmter Menge zu bekommen, und dann wird das wabenförmige Substrat
bei 110 °C
getrocknet und 3 Stunden lang bei 500 °C gesintert, damit es mit Ba
beladen werden kann. Die Menge an aufgetragenem Ba pro 1 l wabenförmiges Substrat
entspricht derjenigen des Katalysators der Ausführungsform 1. Da mit Ba beladene
wabenförmige
Substrat wird in die wässrige
Ammoniumcarbonatlösung
getaucht und herausgezogen, so dass es bei 110 °C getrocknet werden kann.
-
Anschließend wird
das wabenförmige
Substrat in eine wässrige
Dinitrodiaminplatinnitratlösung
mit vorher festgelegter Dichte getaucht, herausgezogen, so dass
sie nicht erforderlichen Tröpfchen
abgeblasen werden können
und 3 Stunden lang bei 110 °C
getrocknet. Danach wird das wabenförmige Substrat in eine wässrige Rhodiumnitratlösung mit
vorher festgelegter Dichte getaucht, herausgezogen, um die nicht
erforderlichen Tröpfchen
wegzublasen, 3 Stunden lang bei 110 °C getrocknet und 2 Stunden lang
bei 400 °C
gesintert. Auf diese Weise wurden Pt und Rh auf die Beschichtungsschicht
aufgetragen. Die jeweiligen Mengen an Pt und Rh entsprechenden denjenigen
der Ausführungsform
1.
-
Anschließend wurden
auf die gleiche Weise wie in der Ausführungsform 1 oben Pt, Rh, K
und Li auf die Oberflächenschicht
der Beschichtungsschicht aufgetragen, wodurch der Katalysator der
Vergleichsprobe 2 hergestellt wurde. Der Katalysator der Vergleichsprobe
2 wurde in gleicher Weise wie bei der Ausführungsform 1 einem Bewertungstest
unterzogen und das Ergebnis davon ist in Tabelle 2 gezeigt.
-
-
Wie
aus Tabelle 2 zu sehen ist haben sich die bei den Katalysatoren
der Ausführungsformen
1 bis 8 sowohl die Fähigkeit
zur NOx-Okklusion als auch die Menge an reduzierten NOx nach dem
Dauerversuch im Vergleich zu denjenigen der Vergleichsproben 1 und
2 stark erhöht,
so dass die NOx-Emission im 10–15-Modus
größtenteils
reduziert wurde. Diese positiven Effekte ergaben sich klar aus der
Verwendung von Ca enthaltendem Zirconiumdioxid oder Ba enthaltendem
Zirconiumdioxid.
-
Daneben
zeigen die Katalysatoren der Ausführungsformen 1 bis 8 geringere
Mengen einer Schwefelvergiftung als die Vergleichsproben 1 und 2,
was sich klar aus der Verwendung von Ca enthaltendem Zirconiumdioxid
oder Ba enthaltendem Zirconiumdioxid ergibt. Die Beziehung kann
zudem zwischen der steigenden Tendenz der Menge an okkludierten
NOx, der Menge an reduzierten NOx und der abnehmenden Tendenz der NOx-Emission
und der Menge an Schwefelvergiftung beobachtet werden.
-
Ausführungsform
9
-
10 zeigt
den Katalysator zur Abgasreinigung gemäß der neunten Ausführungsform
der vorliegenden Erfindung. Dieser Katalysator wird aus einem wabenförmigen Substrat 1 aus
Cordierit und einer Beschichtungsschicht 2', die auf einer Oberfläche des
wabenförmigen
Substrats 1 ausgebildet ist und aus Aluminiumoxid, Titandioxid
und La enthaltendem Zirconiumdioxid besteht, aufgebaut.
-
Die
Beschichtungsschicht 2' wird
durch Mischen der Pulver, bei denen Ba und Pt auf Aluminiumoxidpulver 5 mit
Ba und Pt aufgetragen wurden, mit Pulvern, bei denen Ba und Pt auf
Titandioxidpulver 6 aufgetragen wurden, und Pulvern, bei
denen Rh und Ba auf den zweiten Träger 7 aus La enthaltenden
Zirconiumdioxidpulvern aufgetragen wurden, aufgebaut. Die Pulver,
bei denen Ba und Pt auf die Aluminiumoxidpulver 5 und Ba
und Pt auf die Titandioxidpulver 6 aufgetragen wurden,
bildeten die ersten Pulver und die Pulver, bei denen Rh und Ba auf
den zweiten Träger 7 aufgetragen
wurden, bildeten die zweiten Pulver. Auf die Oberflächenschicht
der Beschichtungsschicht 2' werden
zusätzlich
K und Li aufgetragen.
-
Um
den Aufbau des Katalysators zu erklären, soll im Folgenden das
Herstellungsverfahren beschrieben werden.
-
100
g Aluminiumoxidpulver und 100 g Titandioxidpulver werden gemischt,
um die ersten Trägerpulver herzustellen.
-
Durch
Zugabe von Ammoniakwasser zu der Mischlösung aus der Zirconiumdioxidverbindung
und der Lanthanverbindung wurden die La enthaltenden Zirconiumdioxidpulver,
die 1,1 Mol-% La enthielten, mit dem Verfahren der Copräzipitation
hergestellt. 50 g La enthaltende Zirconiumdioxidpulver werden in
eine wässrige Rhodiumnitratlösung mit
vorher festgelegter Dichte getaucht und anschließend wird die wässrige Lösung filtriert.
Die abfiltrierten Pulver werden 3 Stunden lang bei 110 °C getrocknet,
zerstoßen
und 1 Stunde lang bei 400 °C
gesintert. Die mit Rh beladenen zweiten Pulver wurden so hergestellt.
Bei den zweiten Pulvern beträgt die
Menge an aufgetragenem Rh 0,5 g pro 50 g La enthaltende Zirconiumdioxidpulver.
-
Die
gesamten ersten Pulver, die gesamten zweiten Pulver, 140 g Aluminiumoxidsole
und 250 g reines Wasser wurden gemischt und die Mischlösung wird
nach ausreichend langem Rühren
mit einer Reibe zu einer Aufschlämmung
vermahlen.
-
Das
wabenförmige
Substrat mit einem Volumen von 1,3 l, das aus Cordierit besteht,
wird in diese Aufschlämmung
getaucht und anschließend
herausgezogen, so dass die überschüssige Aufschlämmung abgeblasen
werden kann. Das wabenförmige
Substrat wird anschließend
getrocknet und gesintert, so dass die Beschichtungsschicht darauf
ausgebildet werden kann. 260 g Beschichtungsschicht wurden pro 1
l wabenförmiges
Substrat im gesinterten Gewicht ausgebildet.
-
Danach
wird das wabenförmige
Substrat mit der Beschichtungsschicht mit einer vorher festgelegten Menge
an wässriger
Bariumacetatlösung
mit vorher festgelegter Dichte beschichtet und der Wasseranteil
wird unter Rühren
der wässrigen
Lösung
abgedampft. Anschließend
wird das wabenförmige
Substrat 3 Stunden lang bei 500 °C
gesintert, so dass die Beschichtungsschicht mit Ba beladen werden
kann. Pro 1 l wabenförmiges
Substrat werden 0,2 mol Ba aufgetragen. Das mit Ba beladene wabenförmige Substrat
wird in eine wässrige
Ammoniumhydrogencarbonatlösung
mit einer Dichte von 0,3 mol/l getaucht und die wässrige Lösung wird nach
15-minütigem
Rühren
filtriert. Dann wird das wabenförmige
Substrat 3 Stunden lang bei 110 °C
getrocknet. Dadurch wandelt sich Ba in Bariumcarbonat um und wird
gleichmäßig auf
die Beschichtungsschicht aufgetragen.
-
Als
nächstes
wird das wabenförmige
Substrat mit der Beschichtungsschicht, die mit dem obigen Rh und
Ba beladen ist, in eine wässrige
Dinitrodiaminplatinnitratlösung
getaucht, herausgezogen, bei 250 °C
getrocknet und 1 Stunde lang bei 400 °C gesintert. 2,0 g Pt wurden
auf diese Weise auf 1 l wabenförmiges
Substrat aufgetragen. Das Aluminiumoxid der ersten Trägerpulver
zeigt hier viel höhere
Pt absorbierende Eigenschaften als das mit La stabilisierte Zirconiumdioxid
der zweiten Pulver, so dass Pt hauptsächlich auf das Aluminiumoxid
der ersten Pulver aufgetragen wird.
-
Zudem
wird das mit Rh, Ba und Pt beladene wabenförmige Substrat in die wässrige Kaliumnitratlösung und
die wässrige
Lithiumnitratlösung
mit jeweils vorher festgelegter Dichte getaucht, herausgezogen und
bei 250 °C
getrocknet und 1 Stunde lang bei 500 °C gesintert. Pro 1 l wabenförmiges Substrat
werden jeweils 0,1 mol K und Li aufgetragen und K und Li werden
gleichmäßig auf
die Oberflächenschicht
der Beschichtungsschicht aufgetragen.
-
Ausführungsform 10
-
Der
Katalysator der Ausführungsform
10 wurde auf die gleiche Weise wie bei der Ausführungsform 9 oben hergestellt,
außer
dass die mit La stabilisierten Zirconiumdioxidpulver, die 3,3 Mol-%
La enthielten, anstelle der mit La stabilisierten Zirconiumdioxidpulver
oben, die 1,1 Mol-% La enthielten, verwendet wurden.
-
Ausführungsform 11
-
Der
Katalysator der Ausführungsform
11 wurde auf die gleiche Weise wie bei der Ausführungsform 9 oben hergestellt,
außer
dass die mit La stabilisierten Zirconiumdioxidpulver, die 5,6 Mol-%
La enthielten, anstelle der mit La stabilisierten Zirconiumdioxidpulver
oben, die 1,1 Mol-% La enthielten, verwendet wurden.
-
Ausführungsform 12
-
Der
Katalysator der Ausführungsform
10 wurde auf die gleiche Weise wie bei der Ausführungsform 9 oben hergestellt,
außer
dass die mit La stabilisierten Zirconiumdioxidpulver, die 11,0 Mol-%
La enthielten, anstelle der mit La stabilisierten Zirconiumdioxidpulver
oben, die 1,1 Mol-% La enthielten, verwendet wurden.
-
Vergleichsprobe 3
-
Der
Katalysator der Vergleichsprobe 3 wurde auf die gleiche Weise wie
bei der Ausführungsform
9 hergestellt, außer
dass 99,5%-iges Zirconiumdioxidpulver, die kein La enthielten, anstelle
der mit La stabilisierten Zirconiumdioxidpulver, die 1,1 Mol-% La
enthielten, verwendet wurden.
-
Test, Bewertung
-
Die
mit La stabilisierten Zirconiumdioxidpulver jeder der Ausführungsformen
9 bis 12 und die Zirconiumdioxidpulver mit einer Reinheit von 99,5
% der Vergleichsprobe 3 wurden einer Infrarotspektralanalyse (IR) unterzogen
und die Ergebnisse davon sind in Tabelle 3 angegeben.
-
Wie
aus 11 zu sehen ist, hat sich die Wellenzahl der Absorptionen
durch die Hydroxylgruppe mit dem Anstieg der Menge an enthaltenem
La zu größeren Wellenzahlen
hin verschoben. Es wird bestätigt,
dass sich die alkalische Funktion der Hydroxylgruppe an der Oberfläche mit
einem Anstieg der Menge an enthaltenem La erhöht. Das Absorptionsvermögen für Dampf
(H2O) im Abgas nimmt somit zu, wenn sich
die Menge an La enthaltenden Zirconiumdioxidpulvern erhöht.
-
Bei
den in jeder der Ausführungsformen
9 bis 12 verwendeten, mit La stabilisierten Zirconiumdioxidpulver
und den Zirconiumdioxidpulver mit einer Reinheit von 99,5 %, die
in der Vergleichsprobe 3 verwendet werden, wird die spezifische
Oberfläche
gemessen. Ihre spezifische Oberfläche wurde auch nach einem Versuch
zur Hitzebeständigkeit
gemessen, bei dem die Zirconiumdioxidpulver 10 Stunden lang auf
800 °C erwärmt werden.
Die spezifische Oberfläche
wird mit dem BET-Verfahren gemessen. Die Messergebnisse sind in 12 gezeigt.
-
Wie
aus 12 zu sehen ist, hat sich die spezifische Oberfläche nach
dem Versuch zur Hitzebeständigkeit
mit dem Anstieg der in den Zirconiumdioxidpulvern enthaltenen Menge
an La deutlich erhöht
und die sinkende Abmessung der spezifischen Oberfläche nach
dem Versuch zur Hitzebeständigkeit
wurde durch den Zusatz von La deutlich eingeschränkt. Ausgehend von diesen Tatsachen
wird der Anstieg der Abmessung der Oberfläche und die Abnahme der spezifischen
Oberfläche
des Zirconiumdioxids, die durch eine Stabilisierung mit La und durch
die große
Menge an enthaltenem La groß wird,
bestätigt.
-
Auch
bei den zweiten Pulvern, die in jeder der Ausführungsformen 9 bis 12 und i
der Vergleichsprobe 3 verwendet wurden, wurde die absorbierte Menge
an CO gemessen. Die von ihnen absorbierte Menge an CO vor und nach
dem Versuch zur Hitzebeständigkeit,
der 10 Stunden lang bei 600 °C
durchgeführt
wurde, wurde in ähnlicher
Weise gemessen. Die Messergebnisse sind in 13 gezeigt.
Die absorbierte Menge an CO wurde hierbei mit einem Apparat zur
Gasabsorption gemessen.
-
Wie
aus 13 zu sehen ist, bestätigt sich, dass das enthaltene
La die Menge an absorbiertem CO nach dem Versuch zur Hitzebeständigkeit
erhöht
und die Verschlechterung an Rh eingeschränkt hat.
-
Die
Menge an erzeugtem Wasserstoff der zweiten Pulver, die bei jeder
der Ausführungsformen
9 bis 12 und bei der Vergleichsprobe 3 verwendet wurden, wurde gemessen.
Die Messergebnisse sind in 14 gezeigt.
Die Menge an erzeugtem Wasserstoff wird hier mit Gaschromatographie
gemessen.
-
Wie
aus 14 zu sehen ist, wird bestätigt, dass das enthaltene La
die Menge an erzeugtem Wasserstoff erhöht und die Aktivität der Wasserstofferzeugung
durch die Dampfreformierungsreaktion von Rh stark verbessert hat.
-
Insgesamt
haben die obigen Versuche klar gezeigt, dass La das Zirconiumdioxid
stabilisiert hat und dass die Beladung des mit La stabilisierten
Zirconiumdioxids mit Rh die Aktivität der Dampfreformierungsreaktion
von Rh stark verbessert hat. Daher erwartet man, dass die Verwendung
von solchen zweiten Pulvern als erfindungsgemäßer Katalysator zur Abgasreinigung
nicht nur die Leistungsfähigkeit
zur Reinigung von NOx verbessern, sondern auch die Beständigkeit
der Leistungsfähigkeit
zur Reinigung von NOx verlängern
wird.
-
Die
Katalysatoren in jeder der Ausführungsformen
9 bis 12 und in der Vergleichsprobe 3 wurden in der Abgasanlage
einer 1,8 1-Maschine mit magerer Verbrennung eingebaut und einem
Dauerversuch unterzogen, der einer effektiven Laufleistung von 50.000
km entspricht. Danach wurden in der gleichen Abgasanlage (Temperatur
des eingespeisten Gases: 400 °C)
die Menge an abgesättigt
okkludiertem NOx, die okkludierte Menge bei RS (RS = Anfettungsimpuls
(Spitze) 0,5 Sekunden) und die NOx-Emission unter den Bedingungen
der 10–15
Antriebsarten gemessen. Die Messergebnisse sind in Tabelle 3 gezeigt.
-
Der
Grad der Schwefelvergiftung im Dauerversuch wurde aus der Differenz
der Reinigungsgeschwindigkeiten von NOx vor und nach dem Dauerversuch
gemessen und ist als absoluter Wert bezogen auf das Ergebnis des
Katalysators des vergleichenden Beispiels 3 oben in der Tabelle
3 gezeigt.
-
-
Wie
aus Tabelle 3 zu sehen ist, haben sich bei den Katalysatoren der
Ausführungsformen
9 bis 12 sowohl die Menge an okkludiertem NOx, als auch die okkludierte
Menge bei RS und die Menge der Schwefelvergiftung nach dem Versuch
zur Hitzebeständigkeit
im Vergleich zu denjenigen der Vergleichsprobe 3 stark erhöht. Infolgedessen
sank die NOx-Emission beim 10–15-Modus
stark ab.
-
Daneben ähnelt die
Beziehung zwischen der Fähigkeit
zur NOx-Okklusion und der Fähigkeit
zur RS-Okklusion
jeder der Ausführungsformen
9 bis 12 und der Vergleichsprobe 3 nach dem Versuch zur Hitzebeständigkeit
und der Menge an enthaltenem La der Beziehung zwischen der Menge
an absorbiertem CO und der Menge an enthaltenem La, die in 13 gezeigt
ist, und der Beziehung zwischen der Menge an erzeugtem Wasserstoff
und der Menge an enthaltenem La, die in 14 gezeigt
ist. Somit wird bestätigt,
dass das La enthaltende Zirconiumdioxid die Aktivität der Dampfreformierungsreaktion
von Rh stark verbessert.