DE60019086T2 - Zusammensetzungen zur behandlung von hautkrankheiten - Google Patents
Zusammensetzungen zur behandlung von hautkrankheiten Download PDFInfo
- Publication number
- DE60019086T2 DE60019086T2 DE60019086T DE60019086T DE60019086T2 DE 60019086 T2 DE60019086 T2 DE 60019086T2 DE 60019086 T DE60019086 T DE 60019086T DE 60019086 T DE60019086 T DE 60019086T DE 60019086 T2 DE60019086 T2 DE 60019086T2
- Authority
- DE
- Germany
- Prior art keywords
- formula
- compound
- group
- chloride
- methylnicotinamide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 208000017520 skin disease Diseases 0.000 title claims abstract description 25
- 239000000203 mixture Substances 0.000 title claims description 27
- 150000001875 compounds Chemical class 0.000 claims abstract description 60
- 239000001257 hydrogen Substances 0.000 claims abstract description 22
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 22
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims abstract description 12
- 150000002431 hydrogen Chemical class 0.000 claims abstract description 10
- 230000000699 topical effect Effects 0.000 claims abstract description 10
- 206010042496 Sunburn Diseases 0.000 claims abstract description 5
- 230000029663 wound healing Effects 0.000 claims abstract description 4
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims abstract 6
- 206010053615 Thermal burn Diseases 0.000 claims abstract 2
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract 2
- -1 alkyl radical Chemical class 0.000 claims description 15
- 239000002674 ointment Substances 0.000 claims description 14
- 239000003085 diluting agent Substances 0.000 claims description 12
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 11
- 239000002537 cosmetic Substances 0.000 claims description 8
- BWVDQVQUNNBTLK-UHFFFAOYSA-N 1-methylpyridin-1-ium-3-carboximidate;hydrochloride Chemical compound [Cl-].C[N+]1=CC=CC(C(N)=O)=C1 BWVDQVQUNNBTLK-UHFFFAOYSA-N 0.000 claims description 7
- 150000003839 salts Chemical class 0.000 claims description 7
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 6
- 238000000034 method Methods 0.000 claims description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 5
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 5
- HVLXRXOKGPRDGL-UHFFFAOYSA-N 2-hydroxypropanoic acid;1-methyl-2h-pyridine-3-carboxamide Chemical compound CC(O)C(O)=O.CN1CC(C(N)=O)=CC=C1 HVLXRXOKGPRDGL-UHFFFAOYSA-N 0.000 claims description 4
- 241001465754 Metazoa Species 0.000 claims description 4
- 238000002560 therapeutic procedure Methods 0.000 claims description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 claims description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 claims description 3
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 claims description 3
- 125000000217 alkyl group Chemical group 0.000 claims description 3
- 150000001450 anions Chemical class 0.000 claims description 3
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 claims description 3
- 239000003814 drug Substances 0.000 claims description 3
- 238000004519 manufacturing process Methods 0.000 claims description 3
- 229960001860 salicylate Drugs 0.000 claims description 3
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 claims description 3
- DPJGLVDIPLXNIB-UHFFFAOYSA-N 1-methyl-2h-pyridine-3-carbonyl chloride Chemical compound CN1CC(C(Cl)=O)=CC=C1 DPJGLVDIPLXNIB-UHFFFAOYSA-N 0.000 claims description 2
- LDHMAVIPBRSVRG-UHFFFAOYSA-O 1-methylnicotinamide Chemical compound C[N+]1=CC=CC(C(N)=O)=C1 LDHMAVIPBRSVRG-UHFFFAOYSA-O 0.000 claims description 2
- WWNNZCOKKKDOPX-UHFFFAOYSA-O N-methylnicotinic acid Chemical compound C[N+]1=CC=CC(C(O)=O)=C1 WWNNZCOKKKDOPX-UHFFFAOYSA-O 0.000 claims description 2
- WCYWZMWISLQXQU-UHFFFAOYSA-N methyl Chemical compound [CH3] WCYWZMWISLQXQU-UHFFFAOYSA-N 0.000 claims description 2
- 230000008569 process Effects 0.000 claims description 2
- GNVQERVFKXFTJZ-UHFFFAOYSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;1-methyl-2h-pyridine-3-carboxamide Chemical compound CN1CC(C(N)=O)=CC=C1.OC(=O)CC(O)(C(O)=O)CC(O)=O GNVQERVFKXFTJZ-UHFFFAOYSA-N 0.000 claims 3
- IAMZQBQPEHEFTL-UHFFFAOYSA-N Cl.CCCOC(=O)C1=CC=CN(C)C1 Chemical compound Cl.CCCOC(=O)C1=CC=CN(C)C1 IAMZQBQPEHEFTL-UHFFFAOYSA-N 0.000 claims 3
- SYSKBRBSPQAWBR-UHFFFAOYSA-N Cl.CCOC(=O)C1=CC=CN(C)C1 Chemical compound Cl.CCOC(=O)C1=CC=CN(C)C1 SYSKBRBSPQAWBR-UHFFFAOYSA-N 0.000 claims 3
- 150000001805 chlorine compounds Chemical group 0.000 claims 1
- JEHRNGFVVJBPPC-UHFFFAOYSA-N ethyl 1-methyl-2h-pyridine-3-carboxylate Chemical compound CCOC(=O)C1=CC=CN(C)C1 JEHRNGFVVJBPPC-UHFFFAOYSA-N 0.000 claims 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims 1
- 229950005422 hydroxymethylnicotinamide Drugs 0.000 claims 1
- FFPMCRYJIUFLDG-UHFFFAOYSA-N propyl 1-methyl-2h-pyridine-3-carboxylate Chemical compound CCCOC(=O)C1=CC=CN(C)C1 FFPMCRYJIUFLDG-UHFFFAOYSA-N 0.000 claims 1
- 201000004384 Alopecia Diseases 0.000 abstract description 13
- 208000024963 hair loss Diseases 0.000 abstract description 13
- 230000003676 hair loss Effects 0.000 abstract description 13
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical compound O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 abstract 1
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 15
- 239000000499 gel Substances 0.000 description 15
- 239000000243 solution Substances 0.000 description 14
- 238000009472 formulation Methods 0.000 description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 11
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- 230000000694 effects Effects 0.000 description 10
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 9
- 208000002874 Acne Vulgaris Diseases 0.000 description 7
- 206010000496 acne Diseases 0.000 description 7
- 239000003974 emollient agent Substances 0.000 description 7
- 235000019441 ethanol Nutrition 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical class OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 5
- 201000004681 Psoriasis Diseases 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 239000006210 lotion Substances 0.000 description 5
- 235000005152 nicotinamide Nutrition 0.000 description 5
- 239000011570 nicotinamide Substances 0.000 description 5
- 229960003966 nicotinamide Drugs 0.000 description 5
- 239000012049 topical pharmaceutical composition Substances 0.000 description 5
- 206010030113 Oedema Diseases 0.000 description 4
- 239000004902 Softening Agent Substances 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- POJWUDADGALRAB-UHFFFAOYSA-N allantoin Chemical compound NC(=O)NC1NC(=O)NC1=O POJWUDADGALRAB-UHFFFAOYSA-N 0.000 description 4
- 239000006071 cream Substances 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 4
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 4
- 239000002453 shampoo Substances 0.000 description 4
- 206010015150 Erythema Diseases 0.000 description 3
- 208000025865 Ulcer Diseases 0.000 description 3
- 239000000443 aerosol Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000003659 hair regrowth Effects 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000001575 pathological effect Effects 0.000 description 3
- 239000003380 propellant Substances 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- ARXKVVRQIIOZGF-UHFFFAOYSA-N 1,2,4-butanetriol Chemical compound OCCC(O)CO ARXKVVRQIIOZGF-UHFFFAOYSA-N 0.000 description 2
- POJWUDADGALRAB-PVQJCKRUSA-N Allantoin Natural products NC(=O)N[C@@H]1NC(=O)NC1=O POJWUDADGALRAB-PVQJCKRUSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 206010006797 Burns first degree Diseases 0.000 description 2
- 206010006802 Burns second degree Diseases 0.000 description 2
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 208000005230 Leg Ulcer Diseases 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 208000003251 Pruritus Diseases 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 2
- 206010052428 Wound Diseases 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- DFPAKSUCGFBDDF-ZQBYOMGUSA-N [14c]-nicotinamide Chemical compound N[14C](=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-ZQBYOMGUSA-N 0.000 description 2
- 229960000458 allantoin Drugs 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 231100000321 erythema Toxicity 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 230000003203 everyday effect Effects 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- 230000007803 itching Effects 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- 235000001968 nicotinic acid Nutrition 0.000 description 2
- 229960003512 nicotinic acid Drugs 0.000 description 2
- 239000011664 nicotinic acid Substances 0.000 description 2
- 239000004584 polyacrylic acid Substances 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 230000003449 preventive effect Effects 0.000 description 2
- 229960004889 salicylic acid Drugs 0.000 description 2
- 239000000344 soap Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 239000000600 sorbitol Substances 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- 231100000397 ulcer Toxicity 0.000 description 2
- NOOLISFMXDJSKH-UTLUCORTSA-N (+)-Neomenthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@@H]1O NOOLISFMXDJSKH-UTLUCORTSA-N 0.000 description 1
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 1
- DSSYKIVIOFKYAU-XCBNKYQSSA-N (R)-camphor Chemical compound C1C[C@@]2(C)C(=O)C[C@@H]1C2(C)C DSSYKIVIOFKYAU-XCBNKYQSSA-N 0.000 description 1
- ZWVMLYRJXORSEP-UHFFFAOYSA-N 1,2,6-Hexanetriol Chemical compound OCCCCC(O)CO ZWVMLYRJXORSEP-UHFFFAOYSA-N 0.000 description 1
- CRJFOPZHQMBHNQ-UHFFFAOYSA-N 1-methyl-2h-pyridine-3-carboxamide Chemical class CN1CC(C(N)=O)=CC=C1 CRJFOPZHQMBHNQ-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 241000195940 Bryophyta Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- SNPLKNRPJHDVJA-ZETCQYMHSA-N D-panthenol Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCCO SNPLKNRPJHDVJA-ZETCQYMHSA-N 0.000 description 1
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- AEMRFAOFKBGASW-UHFFFAOYSA-M Glycolate Chemical compound OCC([O-])=O AEMRFAOFKBGASW-UHFFFAOYSA-M 0.000 description 1
- 206010027982 Morphoea Diseases 0.000 description 1
- 206010067482 No adverse event Diseases 0.000 description 1
- 206010039792 Seborrhoea Diseases 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 1
- FPIPGXGPPPQFEQ-BOOMUCAASA-N Vitamin A Natural products OC/C=C(/C)\C=C\C=C(\C)/C=C/C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-BOOMUCAASA-N 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- UFUVLHLTWXBHGZ-MGZQPHGTSA-N [(2r,3r,4s,5r,6r)-6-[(1s,2s)-2-chloro-1-[[(2s,4r)-1-methyl-4-propylpyrrolidine-2-carbonyl]amino]propyl]-4,5-dihydroxy-2-methylsulfanyloxan-3-yl] dihydrogen phosphate Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@H](C)Cl)[C@@H]1[C@H](O)[C@H](O)[C@@H](OP(O)(O)=O)[C@@H](SC)O1 UFUVLHLTWXBHGZ-MGZQPHGTSA-N 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 1
- 230000001548 androgenic effect Effects 0.000 description 1
- 239000010775 animal oil Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000001139 anti-pruritic effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- CDQSJQSWAWPGKG-UHFFFAOYSA-N butane-1,1-diol Chemical compound CCCC(O)O CDQSJQSWAWPGKG-UHFFFAOYSA-N 0.000 description 1
- 229940025250 camphora Drugs 0.000 description 1
- 239000010238 camphora Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 150000001734 carboxylic acid salts Chemical class 0.000 description 1
- XMEVHPAGJVLHIG-FMZCEJRJSA-N chembl454950 Chemical compound [Cl-].C1=CC=C2[C@](O)(C)[C@H]3C[C@H]4[C@H]([NH+](C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O XMEVHPAGJVLHIG-FMZCEJRJSA-N 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 150000003841 chloride salts Chemical class 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229960002291 clindamycin phosphate Drugs 0.000 description 1
- 235000017471 coenzyme Q10 Nutrition 0.000 description 1
- ACTIUHUUMQJHFO-UPTCCGCDSA-N coenzyme Q10 Chemical compound COC1=C(OC)C(=O)C(C\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CCC=C(C)C)=C(C)C1=O ACTIUHUUMQJHFO-UPTCCGCDSA-N 0.000 description 1
- 238000002485 combustion reaction Methods 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000010339 dilation Effects 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 125000005909 ethyl alcohol group Chemical group 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 238000009499 grossing Methods 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000000366 juvenile effect Effects 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 229940041616 menthol Drugs 0.000 description 1
- 235000011929 mousse Nutrition 0.000 description 1
- 150000005480 nicotinamides Chemical class 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 229940101267 panthenol Drugs 0.000 description 1
- 235000020957 pantothenol Nutrition 0.000 description 1
- 239000011619 pantothenol Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 201000004700 rosacea Diseases 0.000 description 1
- 210000004761 scalp Anatomy 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 230000009759 skin aging Effects 0.000 description 1
- 231100000075 skin burn Toxicity 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229960004989 tetracycline hydrochloride Drugs 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 230000036269 ulceration Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 235000019155 vitamin A Nutrition 0.000 description 1
- 239000011719 vitamin A Substances 0.000 description 1
- 235000019160 vitamin B3 Nutrition 0.000 description 1
- 239000011708 vitamin B3 Substances 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940045997 vitamin a Drugs 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/79—Acids; Esters
- C07D213/80—Acids; Esters in position 3
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/81—Amides; Imides
- C07D213/82—Amides; Imides in position 3
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
- Die vorliegende Erfindung bezieht sich auf Verfahren und Zusammensetzungen zur Behandlung von Hautkrankheiten und Hautstörungen. Insbesondere bezieht sie sich auf Verfahren und Zusammensetzungen zur Behandlung von Hautkrankheiten und Hautstörungen, in denen Ödem, Erythem, Hautausschlag, Erweiterung von Oberflächenblutgefäßen und Hornhautabschuppung manifestiert sind (einschließlich, wenn sie von Hautjucken und Brennen begleitet werden), sowie in den Fällen von verstärkter Seborrhoe.
- Es gibt mehrere topische therapeutische Produkte in Verwendung, die meistens Corticosteroide enthalten, welche entzündungshemmende, Ödem-reduzierende, antiseborrhoische und antipruritische Wirkungen ausüben. Nicotinamid, d. h. Vitamin PP wird ebenso bei der begleitenden medizinischen Behandlung von Hautkrankheiten verabreicht. Es gibt ebenso eine Salbe in Verwendung, bekannt als "Dernilan", die Nicotinamid, Allantoin, Salicylsäure und Camphora enthält, die entzündungshemmende und abschuppende Wirkungen auf die Haut ausübt. Die Verwendung von Nicotinamid zur Behandlung von gewöhnlicher Akne wird ebenso in EP-A-0052705 offenbart; die Verwendung von Nicotinamidderivaten zur Behandlung von Schuppenflechte wird in US-A-4,067,975 offenbart; und die Verwendung von bestimmten Nicotinamid- und Nicotinsäurederivaten zur Behandlung von verschiedenen Hautzuständen wird in WO-A-98/52927 offenbart.
- Es ist nun überraschenderweise herausgefunden worden, daß 1-Alkylnicotinamidsalze and 1-Alkylnicotinsäureestersalze verwendet werden können, um eine breite Vielzahl von Hautkrankheiten und Hautstörungen zu behandeln, und daß die Verwendung von diesen Verbindungen bestimmte Vorteile gegenüber der Verwendung von Nicotinamid bereitstellt, insbesondere eine erhöhte Wirksamkeit bei einer speziellen Dosierung und/oder eine Verringerung der unerwünschten Nebenwirkungen. Insbesondere ist gezeigt worden, daß die topische Behandlung von Hautkrankheiten wie Akne durch Verabreichung einer Lösung aus 1-Methylnicotinamidsalzen und 1-Methylnicotinsäureestersalzen der vorliegenden Erfindung zumindest eine ähnliche therapeutische Wirkung bei einer Konzentration von ungefähr dem 100fachen niedriger als die entsprechende Behandlung mit Nicotinamid bzw. Nicotinsäure, aber ohne spürbare Nebenwirkungen bereitstellt.
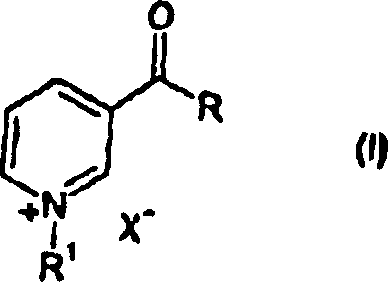
- Daher wird gemäß einem Aspekt der vorliegenden Erfindung die Verwendung einer Verbindung von Formel (I): worin R die Gruppe NR2R3 oder die Gruppe OR4 bedeutet;
R1 einen C1-4-Alkylrest bedeutet;
R2 und R4 unabhängig voneinander jeweils Wasserstoff oder einen C1-4-Alkylrest bedeuten;
R3 Wasserstoff, einen C1-4-Alkylrest oder CH2OH bedeutet;
und X– ein physiologisch geeignetes Gegenanion bedeutet;
für die Herstellung eines Medikaments zur Behandlung von Hautkrankheiten oder Hautstörungen, insbesondere Haarausfall, Sonnenbrand, Verbrennungen, Brandwunden und zur Wundheilung, bereitgestellt. - Gemäß einem weiteren Aspekt der vorliegenden Erfindung wird ein Verfahren zur kosmetischen Behandlung der Haut eines Menschen oder eines Tiers bereitgestellt, umfassend die Verabreichung einer effektiven Menge einer Verbindung von Formel (I), wie oben definiert, an einen Patienten.
- Gemäß einem weiteren Aspekt der vorliegenden Erfindung wird eine Verbindung von Formel (I), wie oben definiert, zur Verwendung in der Kosmetologie bereitgestellt.
- In den Verbindungen von Formel (I) bedeutet R2 vorzugsweise Ethyl, Methyl oder Wasserstoff, stärker bevorzugt Methyl oder Wasserstoff, am stärksten bevorzugt Wasserstoff. Vorzugsweise bedeutet R3 CH2OH, Methyl oder Wasserstoff, stärker bevorzugt CH2OH oder Wasserstoff, am stärksten bevorzugt Wasserstoff. In einer weiteren Bevorzugung bedeutet R4 C1-4-Alkyl. In einer weiteren Bevorzugung bedeutet R4 Propyl, Ethyl, Methyl oder Wasserstoff, stärker bevorzugt Propyl, Ethyl oder Methyl, am stärksten bevorzugt Propyl oder Ethyl. Vorzugsweise bedeutet R die Gruppe NR2R3.
- In einer besonders bevorzugten Ausführungsform der vorliegenden Erfindung ist die Verbindung von Formel (I) ein 1-Methylnicotinamidsalz, d. h. R1 bedeutet Methyl und R2 und R3 bedeuteten jeweils Wasserstoff.
- In einer weiteren besonders bevorzugten Ausführungsform der vorliegenden Erfindung ist die Verbindung von Formel (I) ein 1-Methyl-N'-hydroxymethylnicotinamidsalz, d. h. R1 bedeutet Methyl, R2 bedeutet Wasserstoff und R3 bedeutet CH2OH.
- In einer weiteren besonders bevorzugten Ausführungsform der vorliegenden Erfindung ist die Verbindung von Formel (I) ein 1-Methylnicotinsäuresalz, d. h. R1 bedeutet Methyl und R4 bedeutet Wasserstoff.
- In einer weiteren besonders bevorzugten Ausführungsform der vorliegenden Erfindung ist die Verbindung von Formel (I) ein 1-Methylnicotinsäureethylester oder 1-Methylnicotinsäurepropylestersalz, d. h. R1 bedeutet Methyl und R4 bedeutet Propyl oder Ethyl.
- Wie oben angegeben, ist X– irgendein physiologisch geeignetes Gegenanion. Das 1-Alkylnicotinamid, 1-Alkylnicotinsäure und 1-Alkylnicotinsäureestersalze der vorliegenden Erfindung können daher von irgendeiner physiologisch akzeptablen Säure, ob organisch oder anorganisch im Ursprung, abgeleitet werden. Geeignete anorganische Säuresalze umfassen beispielsweise Chlorid, Bromid, Iodid und Carbonat; geeignete organische Säuresalze umfassen Mono-, Di- und Tri-C1-18-Carbonsäuresalze, beispielsweise Acetat, Benzoat, Salicylat, Glycolat, Lactat, Maleat und Citrat. Bevorzugte Salze umfassen Chlorid, Benzoat, Salicylat, Acetat, Citrat und Lactat. Besonders bevorzugt sind Chloridsalze.
- Einige der Verbindungen von Formel (I) sind kommerziell erhältlich, beispielsweise 1-Methylnicotinamidchlorid (Sigma) und 1-Methylnicotinsäurechlorid (Sigma). Alternativ können die Verbindungen ohne weiteres aus kommerziell erhältlichen Verbindungen (einschließlich Nicotinamid und Nicotinsäure) durch Syntheseverfahren, die dem Fachmann allgemeine bekannt sind, hergestellt werden. Diese Verfahren würden die Synthese von geeignet substituierten Pyridinverbindungen umfassen.
- Gemäß einem weiteren Aspekt der vorliegenden Erfindung wird eine pharmazeutische Formulierung bereitgestellt, umfassend eine Verbindung von Formel (I) in Verbindung mit ein oder mehreren pharmazeutisch akzeptablen Trägern, Verdünnungsmitteln oder Hilfsmitteln.
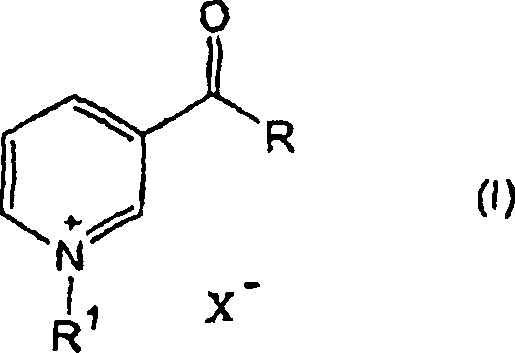
- Gemäß einem weiteren Aspekt der vorliegenden Erfindung wird eine Verbindung von Formel (I): worin R die Gruppe NR2R3 oder die Gruppe OR4 bedeutet;
R1 einen Methylrest bedeutet;
R2 Wasserstoff oder einen C1-4-Alkylrest bedeutet;
R3 Wasserstoff, einen C1-4-Alkylrest oder CH2OH bedeutet; R4 einen C1-4-Alkylrest bedeutet;
und X– ein physiologisch geeignetes Gegenanion bedeutet;
zur Verwendung zur Therapie bereitgestellt. - Bei der Behandlung von Hautzuständen ist es möglich, die Verbindung von Formel (I) oral in geeigneten Formulierungen, vorzugsweise Tabletten oder Kapseln, zu verabreichen. Jedoch sind topische Formulierungen einer Verbindung von Formel (I) von besonderer Nützlichkeit. Der Trägertyp, der in der vorliegenden Erfindung verwendet wird, hängt von dem Typ der Produktform ab, die für die Zusammensetzung gewünscht ist. Die topischen Zusammensetzungen, die in der vorliegenden Erfindung nützlich sind, können zu einer breiten Vielzahl von Produktformen, wie sie in der Technik bekannt sind, hergestellt werden. Diese umfassen Lotionen, Cremes, Gele, Stifte, Shampoos, Seifen, Sprays, Salben, Pasten und Mousse, sind aber nicht darauf beschränkt. Diese Produktformen können mehrere Typen von Trägern umfassen, einschließlich Lösungen, Aerosole, Emulsionen, Gele, Feststoffe und Liposomen, sind aber nicht darauf beschränkt. Topische Formulierungen sind in der Form von Salben, Gel, Creme, Shampoo, Seife, Spray, Lotion oder einer Lösung am meisten geeignet.
- Die Verbindung von Formel (I) kann topisch auf die Haut (einschließlich Kopfhaut) oder auf die Schleimhautoberflächen beispielsweise durch intranasale, orale, intravaginale oder intrarektale Verabreichung verabreicht werden. Bevorzugt ist die topische Verabreichung auf die Haut an der Stelle der Hauptmanifestation der Hautkrankheit oder Hautstörung, der Verbrennung oder Wunde.
- Die topischen Formulierungen der vorliegenden Erfindung umfassen eine sichere und effektive Menge eines dermatologisch akzeptablen Trägers, in den die Verbindung von Formel (I) und andere optionale Komponenten aufgenommen werden, damit die Verbindung von Formel (I) und andere optionale Komponenten der Haut oder anderen relevanten Stellen bei einer geeigneten Konzentration zugeführt werden. Der Träger kann daher als ein Verdünnungsmittel, Dispergiermittel, Lösungsmittel oder dergleichen fungieren, was sicherstellt, daß die Formulierung auf dem ausgewählten Zielorgan aufgetragen und gleichmäßig darüber verteilt werden kann, um eine geeignete Konzentration der Verbindung von Formel (I) bereitzustellen.
- Bevorzugte topische Formulierungen gemäß der vorliegenden Erfindung umfassen etwa 90 bis 99,95% eines pharmazeutischen Grundträgers und etwa 0,005 bis etwa 10 Gew.-% einer Verbindung von Formel (I), wie oben definiert. Stärker bevorzugt enthält die topische Formulierung etwa 0,01 bis etwa 10 Gew.-% einer Verbindung von Formel (I). Bevorzugte pharmazeutische Grundträger sind eine Salbe, ein Gel oder eine wässerige Lösung. Bei einer Salbe liegt die Verbindung von Formel (I) vorzugsweise bei einer Konzentration von 0,1 bis 10 Gew.-%, stärker bevorzugt 0,5 bis 10 Gew.-% vor. Bei einem Gel liegt die Verbindung von Formel (I) vorzugsweise in einer Konzentration von 0,05 bis 2 Gew.-%, stärker bevorzugt 0,05 bis 1 Gew.-%, am stärksten bevorzugt 0,1 bis 0,5 Gew.-% vor. Bei einer Lösung liegt die Verbindung von Formel (I) vorzugsweise in einer Konzentration von 0,005 bis 0,1 Gew.-%, stärker bevorzugt 0,005 bis 0,05 Gew.-%, am stärksten bevorzugt 0,01 Gew.-% vor.
- Der Träger kann ein oder mehrere dermatologisch akzeptable feste, halbfeste oder flüssige Füllstoffe, Verdünnungsmittel, Lösungsmittel, Streckmittel und dergleichen enthalten. Der Träger kann fest, halbfest oder flüssig sein. Bevorzugte Träger sind im wesentlichen flüssig. Der Träger kann selbst inert sein oder er kann dermatologische Vorteile besitzen. Die Konzentrationen des Trägers können mit dem ausgewählten Träger und den beabsichtigten Konzentrationen der Verbindung von Formel (I) und anderen optionalen Komponenten variieren.
- Geeignete Träger umfassen konventionelle oder anderweitig bekannte Träger, die dermatologisch akzeptabel sind. Der Träger sollte ebenso mit der Verbindung von Formel (I) physikalisch und chemisch verträglich sein, und sollte nicht übermäßig die Stabilität, Wirksamkeit oder andere Vorteile, die mit den erfindungsgemäßen Formulierungen verbunden sind, beeinträchtigen. Bevorzugte Komponenten der erfindungsgemäßen Formulierungen sollten fähig sein, sich in einer Weise zu vermischen, so daß es keine Wechselwirkung gibt, die im wesentlichen die Wirksamkeit der Formulierung unter üblichen Verwendungssituationen verringern würden.
- Bevorzugte Träger enthalten ein dermatologisch akzeptables, hydrophiles Verdünnungsmittel. Wie hierin verwendet, umfaßt „Verdünnungsmittel" Materialien, in die die Verbindung von Formel (1) dispergiert, gelöst oder anderweitig aufgenommen werden kann. Nicht einschränkende Beispiele von hydrophilen Verdünnungsmitteln sind Wasser, organische hydrophile Verdünnungsmittel, wie einwertige Niederalkohole (beispielsweise C1-C4) und Glykole und Polyole mit niedrigem Molekulargewicht, einschließlich Propylenglykol, Polyethylenglykol (beispielsweise Molekulargewicht 200 bis 600 g/Mol), Polypropylenglykol (beispielsweise Molekulargewicht 425 bis 2025 g/Mol), Glycerol, Butylenglykol, 1,2,4-Butantriol, Sorbitolester, 1,2,6-Hexantriol, Ethanol, Isopropanol, Sorbitolester, Butandiol, Etherpropanol, ethoxylierte Ether, propoxylierte Ether und Kombinationen davon. Wasser ist ein bevorzugtes Verdünnungsmittel. Die Zusammensetzung umfaßt vorzugsweise etwa 60 bis etwa 99,99% des hydrophilen Verdünnungsmittels.
- Die Lösungen gemäß der vorliegenden Erfindung umfassen typischerweise ein dermatologisch akzeptables hydrophiles Verdünnungsmittel. Die Lösungen, die in der vorliegenden Erfindung nützlich sind, enthalten vorzugsweise etwa 60 bis etwa 99,99% des hydrophilen Verdünnungsmittels.
- Aerosole gemäß der vorliegenden Erfindung können durch Zugeben eines Treibmittels zu einer Lösung, wie oben beschrieben, gebildet werden. Beispielhafte Treibmittel umfassen Chlor-fluorierte Kohlenwasserstoffe mit niedrigem Molekulargewicht. Zusätzliche Treibmittel, die hierin nützlich sind, werden in Sagarin, Cosmetics Science and Technology, 2. Auflage, Bd. 2, S. 443 bis 465 (1972) beschrieben, was hierin als Verweis aufgenommen wird. Aerosole werden typischerweise als ein Sprühprodukt auf die Haut aufgetragen.
- Die topischen erfindungsgemäßen Zusammensetzungen, einschließlich Lotionen und Cremes, aber nicht darauf beschränkt, können ein dermatologisch akzeptables Aufweichungsmittel umfassen. Solche Zusammensetzungen enthalten vorzugsweise etwa 2% bis etwa 50% des Aufweichungsmittels. Aufweichungsmittel schmieren gewöhnlich die Haut, erhöhen die Glätte und Geschmeidigkeit der Haut, verhindern oder mildern die Trockenheit der Haut und/oder schützen die Haut. Aufweichungsmittel sind typischerweise nicht mit Wasser mischbare, ölige oder wachsartige Materialien. Eine breite Vielzahl an geeigneten Aufweichungsmitteln ist bekannt und kann hierin verwendet werden. Sagarin, Cosmetics Science and Technology, 2. Auflage, Bd. 1, S. 32 bis 43 (1972), hierin als Verweis aufgenommen, enthält zahlreiche Beispiele von Materialien, die als ein Aufweichungsmittel geeignet sind.
- Lotionen und Cremes gemäß der vorliegenden Erfindung umfassen im allgemeinen ein Lösung-Träger-System und ein oder mehrere Aufweichungsmittel. Lotionen umfassen typischerweise etwa 1% bis etwa 20%, vorzugsweise etwa 5% bis etwa 10% Aufweichungsmittel; etwa 50% bis etwa 90%, vorzugsweise etwa 60% bis etwa 80% Wasser. Eine Creme umfaßt typischerweise etwa 5% bis etwa 50%, vorzugsweise etwa 10% bis etwa 20% Aufweichungsmittel; und etwa 45% bis etwa 85%, vorzugsweise etwa 50% bis etwa 75% Wasser.
- Salben der vorliegenden Erfindung können eine einfache Trägergrundlage von tierischen oder pflanzlichen Ölen oder halbfesten Kohlenwasserstoffen (ölig); Absorptionssalbengrundlage, die Wasser absorbiert, um Emulsionen zu bilden, oder wasserlösliche Träger, beispielsweise einen wasserlöslichen Lösungsträger, umfassen. Salben können außerdem ein Verdickungsmittel, wie in Sagarin, Cosmetics, Science and Technology, 2. Auflage, Bd. 1, S. 72 bis 73 (1972) beschrieben, hierin als Verweis aufgenommen, und/oder ein Aufweichungsmittel umfassen. Beispielsweise kann eine Salbe etwa 2% bis etwa 10% eines Aufweichungsmittels und etwa 0,1% bis etwa 2% eines Verdickungsmittels umfassen.
- Bevorzugte Salben umfassen Eucerine und Glycerol; bevorzugte Gele umfassen Methylcellulose, Glycerol und Wasser oder umfassen Polyacrylsäure, Polyethylenglykol, Ethanol, Triethanolamin, Paraben und Wasser; bevorzugte Lösungen umfassen wässerige Lösungen oder Lösungen aus Ethylalkohole oder Propylenglykol.
- Gemäß der Erfindung sind die Verbindungen von Formel (I) zur Behandlung von Hautstörungen oder Hautkrankheiten, einschließlich Schenkelgeschwürbildung, Jugendakne, Akne-Rosazea, Schuppenflechte, atopische Dermatitis und Weißfleckenkrankheit, nützlich.
- Außerdem ist gezeigt worden, daß die Verbindungen von Formel (I) bei der Behandlung von Haarausfall, insbesondere Haarschwund, androgener Haarschwund und Haarschwund, verursacht als eine Nebenwirkung der Chemotherapie oder Strahlentherapie, nützlich sind.
- Außerdem ist gezeigt worden, daß die Verbindungen von Formel (I) bei der Behandlung von Verbrennungen und Brandwunden (insbesondere ersten und ersten/zweiten Verbrennungsgrades und Brandwunden) und bei der Wundheilung sowie bei der Behandlung von Sonnenbränden nützlich sind.
- Eine prophylaktische oder präventive Fähigkeit der Verbindungen von Formel (I) ist ebenso für chronische und wiederkehrende Krankheiten, wie beispielsweise Schuppenflechte, Beingeschwüre oder Akne, gezeigt worden. Die präventive Wirkung besteht darin, die Verbesserung eines vorher geheilten Status für einen verlängerten Zeitraum nach dem Aufhören der aktiven pathologischen Symptome zu halten.
- Die Verbindungen von Formel (I) zeigen ebenso Nützlichkeit in der Kosmetologie, insbesondere bei der Bereitstellung der Regeneration und Glättung der Haut; daher wird die Behandlung von hautalternden Wirkungen, wie Falten usw., ebenso von der vorliegenden Erfindung berücksichtigt.
- Zusätzliche Hilfsmittel, die in der Technik bekannt sind, können ebenso in den Formulierungen der vorliegenden Erfindung einbezogen werden; insbesondere können allgemein verwendete Stabilisatoren vorteilhaft einbezogen werden, was es ermöglicht, daß die Formulierungen für einen geeigneten Zeitraum, beispielsweise für bis zu 2 Jahre stabil bleiben.
- Gemäß einem weiteren Aspekt der vorliegenden Erfindung wird ebenso die Verwendung von Verbindungen von Formel (I), wie oben definiert, in Verbindung mit anderen therapeutisch wirksamen Verbindungen, die bei der Behandlung von Hautstörungen und Hautkrankheiten und anderen Zuständen, auf die man sich oben bezieht, verwendet werden, bereitgestellt. Ebenso werden Formulierungen bereitgestellt, die eine Verbindung von Formel (I) in Verbindung mit ein oder mehreren dieser anderen therapeutisch wirksamen Verbindungen umfassen. Geeignete andere thera peutisch wirksame Verbindungen umfassen beispielsweise Vitamin A, Vitamin C, Vitamin E, Coenzym Q, Harnstoff (insbesondere 1 bis 30%), Allantoin (insbesondere 0,1 bis 1%), Benzoylperoxid (5 bis 10%), Menthol, Lecithin, Salicylsäure (insbesondere 0,5 bis 10%), Panthenol (insbesondere 0,5 bis 5%) und Antibiotika, insbesondere Erythromycinbase (1 bis 5%), Clindamycinphosphat (1 bis 5%) und Tetracyclinhydrochlorid (1 bis 5%), wobei die Mengen, die in den Klammern spezifiziert werden, besonders geeignete, aber nicht-einschränkende Mengen sind, die sich für diese Formulierungen auf das Gewicht beziehen.
- Die folgenden nicht-einschränkenden Beispiele dienen dazu, die vorliegende Erfindung weiter darzustellen. Die prozentualen Mengen beziehen sich auf das Gewicht.
- Die Salbe wurde folgendermaßen hergestellt. Die Verbindung von Formel (I) wurde pulverisiert und mit einer kleinen Menge an Eucerine gemischt, bis sie homogen war, dann wurden das restliche Eucerine und Glycerol zugegeben und das gesamte Gemisch, bis es homogen war, gerührt.
- Eine Salbe von Beispiel 1, die 1-Methylnicotinamidchlorid enthält, wurde topisch zur Behandlung von Schuppenflechte in einer Gruppe von 7 Patienten aufgetragen. Nach zehn Tagen Behandlung mit der Salbe zeigten sechs von den Patienten eine beträchtliche Verbesserung, die aus der Verminderung der Knötchen und Aufhören der Rötungen bestand. Keiner der Patienten zeigte irgendwelche negativen Wirkungen bei der Behandlung mit der Salbe.
- Das Gel wurde folgendermaßen hergestellt. Pulverisierte Methylcellulose wurde zu heißem Wasser während intensiven Rührens zugegeben. Die resultierende Dispersion wurde auf etwa 6°C abgekühlt und mit Glycerol gemischt. Die Verbindung von Formel (I) wurde dann zugegeben und das gesamte Gemisch, bis es homogen war, gerührt.
- Ein Gel von Beispiel 2, das 1-Methylnicotinamidcitrat enthält, wurde zur topischen Behandlung von Beingeschwüren in einer Gruppe von 5 Patienten aufgetragen. Nach zehn Tagen Behandlung zeigten alle Patienten eine signifikante Verbesserung, die in der Beschleunigung der Granulation und Epithelisation bestand. Keiner der Patienten zeigte irgendwelche negativen Wirkungen bei der Behandlung mit dem Gel.
- Das Gel wurde analog zu Beispiel 3 hergestellt.
- Ein Gel von Beispiel 3, das 1-Methylnicotinamidchlorid enthält, wurde zur topischen Behandlung von Jugendakne in einer Gruppe von 6 Patienten aufgetragen. Nach der Behandlung hörten die aktiven pathologischen Symptome bei allen Patienten auf.
- Es ist ebenso gezeigt worden, daß eine analoge Gelformulierung der Beispiele 2 und 3, umfassend Polyacrylsäure, Propylenglykol, Ethanol, Triethanolamin, Paraben und vollentsalztes Wasser zusätzlich zu einer Verbindung von Formel (I), klinisch wirksam ist.
- Die Lösung wurde folgendermaßen hergestellt. Die Verbindung von Formel (I) wurde in Wasser gelöst, dann wurde Ethylalkohol zugegeben und die resultierende Lösung auf Umgebungstemperatur abgekühlt.
- Eine Lösung von Beispiel 4, die 1-Methylnicotinamidlactat enthält, wurde aufgetragen, um ein Wiederauftreten der Jugendakne in der Gruppe von Patienten aus Beispiel 3 zu verhindern. Alle Patienten zeigten über einen längeren Zeitraum die Verbesserung nach dem Aufhören der aktiven pathologischen Symptome. Keiner der Patienten zeigte irgendwelche negativen Wirkungen bei der Behandlung mit der Lösung.
- Beispiel 5
- Der Einfluß der topischen Auftragung von 1-Methylnicotinamidsalzen auf Haarausfall wurde bei 10 Patienten mit Haarschwund und bei 24 Patienten mit Haarausfall ohne besonders bekannte Ursache untersucht.
- Die Patienten mit Haarschwund nutzten ein Shampoo, das 0,5 Gew.-% 1-Methylnicotinamidchlorid enthält, entweder jeden Tag oder jeden zweiten Tag, und trugen das Gel von Beispiel 3 zweimal täglich auf. Der Haarnachwuchs wurde bei 8 der Patienten während des ersten Monats der Behandlung beobachtet. Bei den übrigen Patienten ist, obwohl kein Haarnachwuchs nach einen Monat Behandlung beobachtet wurde, das Fortschreiten der Krankheit gestoppt worden.
- Die anderen Patienten mit Haarausfall nutzten das Shampoo, das 0,5 Gew.-% 1-Methylnicotinamidchlorid enthält, täglich. Bei allen Patienten ist das Fortschreiten des Haarausfalls gestoppt worden; bei einigen Patienten ist Haarnachwuchs beobachtet worden.
- Keiner der Patienten berichtete nachteilige Wirkungen bei der Behandlung, wie Jucken und Hautirritationen.
- Außerdem ist eine überraschende Wirkung, die in Verbindung mit der Behandlung von Haarausfall beobachtet wurde, daß in einigen Fällen graues Haar zu seiner früheren natürlichen Farbe zurückkehrte; außerdem ist diese Behandlung dafür gedacht, das Grauwerden der Haare zu verhindern. Diese Verwendung der Verbindungen von Formel (I), wie oben definiert, stellt einen weiteren Aspekt der vorliegenden Erfindung dar.
- Beispiel 6
- Der Einfluß der topischen Auftragung von 1-Methylnicotinamidsalzen auf Hautverbrennungen wurde bei 19 Patienten untersucht.
- Das Gel von Beispiel 3 wurde mehrmals am Tag direkt auf die betroffene Stelle bei den Patienten mit Verbrennungen von UV-Strahlung und hohen Temperaturen sowie Brandwunden von heißen Flüssigkeiten topisch aufgetragen. Es waren 15 Patienten mit Verbrennungen ersten Grades und 4 Patienten mit Verbrennungen zweiten Grades.
- Bei den Patienten mit Verbrennungen ersten Grades verminderten sich der Schmerz und das Ödem innerhalb der ersten 24 Stunden, löste sich das Erythem innerhalb 2 bis 3 Tagen bei 11 der Patienten wieder auf und bei den übrigen 4 Patienten wurde es nach 6 Tagen wieder aufgelöst.
- Bei den Patienten mit Verbrennungen zweiten Grades verminderte sich der Schmerz ebenso innerhalb der ersten 2 Tage, wurden die Blasen in 1 bis 3 Tagen absorbiert, das Ödem in 2 bis 3 Tagen. Der Epithelisationsprozess von Abschürfungen und Oberflächengeschwüren war sehr schnell und trat innerhalb 7 bis 14 Tage in Abhängigkeit der Fläche auf.
- Die übrigen Narben, die das Ergebnis der Geschwürheilung waren, wurden als rein kosmetisch betrachtet und wurden als solche sowohl vom Patienten als auch vom Arzt akzeptiert. Es wurden keine nachteiligen Wirkungen der Behandlung bemerkt.
- Außerdem führte die ähnliche Auftragung des Gels von Beispiel 3 bei zehn Patienten mit ernsten Sonnenbränden zur effektiven Verbesserung ihres Zustandes.
- Weitere Beispiele
- Ebenso ist gezeigt worden, daß Formulierungen, die die folgenden Verbindungen enthalten, bei der Behandlung von Hautkrankheiten und Hautstörungen, auf die man sich oben bezieht, speziell Akne und Schuppenflechte, klinisch wirksam sind:
1-Methylnicotinsäure;
1-Methylnicotinsäureethylestersalze;
1-Methylnicotinsäurepropylestersalze. - Es ist ebenso gezeigt worden, daß Formulierungen, die 1-Methyl-N'-hydroxymethylnicotinamidsalze enthalten, bei der Behandlung von Hautkrankheiten und Hautstörungen, auf die man sich oben bezieht, klinisch wirksam sind.
Claims (23)
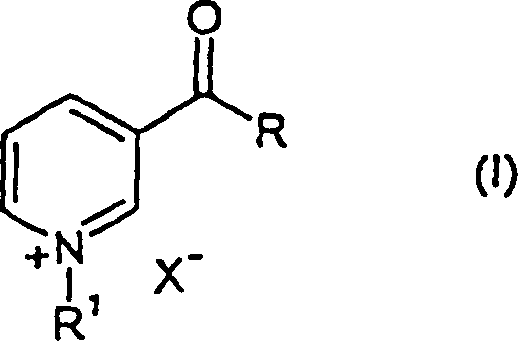
- Verwendung einer Verbindung der Formel (I): worin R die Gruppe NR2R3 oder die Gruppe OR4 bedeutet; R1 einen Methylrest bedeutet; R2 und R4 unabhängig voneinander jeweils Wasserstoff oder einen C1-4-Alkylrest bedeuten; R3 Wasserstoff, einen C1-4-Alkylrest oder CH2OH bedeutet und X– ein physiologisch geeignetes Gegenanion bedeutet; für die Herstellung eines Medikaments zur Behandlung von Hautkrankheiten oder Hautstörungen.
- Verwendung einer Verbindung der Formel (I) gemäß Anspruch 1 zur Herstellung eines Medikaments für die Behandlung von Sonnenbrand, Verbrennungen oder Verbrühungen sowie zur Wundheilung.
- Verwendung gemäß Anspruch 1 oder 2, wobei R die Gruppe NR2R3 bedeutet.
- Verwendung gemäß einem der Ansprüche 1 bis 3, wobei R2 eine Methylgruppe oder Wasserstoff bedeutet.
- Verwendung gemäß einem der Ansprüche 1 bis 4, wobei R3 CH2OH oder Wasserstoff bedeutet.
- Verwendung gemäß Anspruch 1 oder 2, wobei R die Gruppe OR4 und R4 einen C1-4-Alkylrest bedeuten.
- Verwendung gemäß einem der Ansprüche 1, 2 oder 6, wobei R4 eine Propyl- oder Ethylgruppe bedeutet.
- Verwendung gemäß einem der Ansprüche 1 bis 7, wobei die Verbindung der Formel (I) ein Satz von 1-Methylnicotinamid oder ein Salz von 1-Methyl-N'-hydroxymethylnicotinamid ist.
- Verwendung gemäß einem der Ansprüche 1 bis 7, wobei die Verbindung der Formel (I) ein Salz von 1-Methylnicotinsäureethylester oder ein Salz von 1-Methylnicotinsäurepropylester ist.
- Verwendung gemäß einem der Ansprüche 1 bis 7, wobei die Verbindung der Formel (I) ein Salz der 1-Methylnicotinsäure ist.
- Verwendung gemäß einem der Ansprüche 1 bis 10, wobei das Salz ein Chlorid, Benzoat, Salicylat, Acetat, Citrat oder Lactat ist.
- Verwendung gemäß Anspruch 1 oder 2, wobei die Verbindung der Formel (I) 1-Methylnicotinamid-chlorid; 1-Methylnicotinamid-citrat; 1-Methylnicotinamid-lactat; 1-Methyl-N'-hydroxymethylnicotinamid-chlorid; 1-Methylnicotinsäure-chlorid; 1-Methylnicotinsäure-ethylester-chlorid oder 1-Methylnicotinsäure-propylester-chlorid ist.
- Verbindung der Formel (I) worin R eine NR2R3-Gruppe oder eine OR4-Gruppe bedeutet; R1 eine Methylgruppe bedeutet; R2 Wasserstoff oder eine C1-4-Alkylgruppe bedeutet; R3 Wasserstoff, eine C1-4-Alkylgruppe oder eine CH2OH-Gruppe bedeutet; R4 eine C1-4-Alkylgruppe bedeutet und X– ein physiologisch geeignetes Gegenanion bedeutet; zur Verwendung zur Therapie.
- Verbindung der Formel (I) gemäß einem der Ansprüche 3 bis 9 und 11 zur Verwendung zur Therapie.
- Verbindung der Formel (I) gemäß Anspruch 13, wobei die Verbindung 1-Methylnicotinamid-chlorid; 1-Methylnicotinamid-citrat; 1-Methylnicotinamid-lactat; 1-Methyl-N'-hydroxymethylnicotinamid-chlorid; 1-Methylnicotinsäure-ethylester-chlorid oder 1-Methylnicotinsäure-propylester-chlorid ist, zur Verwendung zur Therapie.
- Pharmazeutische Zusammensetzung, enthaltend eine Verbindung der Formel (I) gemäß einem der Ansprüche 13 bis 15 in Verbindung mit einem oder mehreren pharmazeutisch annehmbaren Trägern, Verdünnungsmitteln oder Hilfsmitteln.
- Zusammensetzung gemäß Anspruch 16, zur topischen Anwendung und enthaltend etwa 90 bis 99.95% eines pharmazeutischen Grundträgers und etwa 0,005 bis etwa 10 Gewichts-% an der Verbindung gemäß Formel (I).
- Zusammensetzung gemäß Anspruch 17, enthaltend etwa 0,01 bis etwa 10 Gewichts-% der Verbindung gemäß Formel (I).
- Zusammensetzung gemäß Anspruch 17 oder 18 in Form einer Salbe oder eines Gels.
- Zusammensetzung gemäß Anspruch 17 oder 18 in Form einer wässerigen Lösung.
- Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 12 zur Verwendung als Kosmetikum.
- Verbindung der Formel (I) gemäß Anspruch 21 aus der Gruppe, bestehend aus 1-Methylnicotinamid-chlorid; 1-Methylnicotinamid-citrat; 1-Methylnicotinamid-lactat; 1-Methyl-N'-hydroxymethylnicotinamid-chlorid; 1-Methylnicotinsäure-ethylester-chlorid oder 1-Methylnicotinsäure-propylester-chlorid, zur Verwendung als Kosmetikum.
- Verfahren zur kosmetischen Behandlung der Haut eines Menschen oder Tieres, wobei man den Menschen oder das Tier mit einer wirksamen Menge einer Verbindung der Formel (I) gemäß einem der Ansprüche 1 bis 12 behandelt.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PL33076899 | 1999-01-07 | ||
| PL330768A PL190755B1 (pl) | 1999-01-07 | 1999-01-07 | Preparat do leczenia i profilaktyki chorób skóry |
| PCT/IB2000/000019 WO2000040559A1 (en) | 1999-01-07 | 2000-01-07 | Compositions for the treatment of skin diseases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60019086D1 DE60019086D1 (de) | 2005-05-04 |
| DE60019086T2 true DE60019086T2 (de) | 2006-02-02 |
Family
ID=20073560
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60019086T Expired - Lifetime DE60019086T2 (de) | 1999-01-07 | 2000-01-07 | Zusammensetzungen zur behandlung von hautkrankheiten |
Country Status (12)
| Country | Link |
|---|---|
| EP (1) | EP1147086B9 (de) |
| AT (1) | ATE292117T1 (de) |
| AU (1) | AU1792700A (de) |
| CZ (1) | CZ299662B6 (de) |
| DE (1) | DE60019086T2 (de) |
| ES (1) | ES2238985T3 (de) |
| HU (1) | HU225475B1 (de) |
| PL (2) | PL190755B1 (de) |
| RU (1) | RU2199319C1 (de) |
| SK (1) | SK285869B6 (de) |
| UA (1) | UA73491C2 (de) |
| WO (1) | WO2000040559A1 (de) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CZ303214B6 (cs) * | 2001-03-21 | 2012-05-30 | Torrent Pharmaceuticals Ltd | Pyridiniová sloucenina, zpusob její výroby, její použití, farmaceutický prostredek ji obsahující, zpusob jeho výroby a jeho použití |
| SE0102380D0 (sv) * | 2001-07-02 | 2001-07-02 | Macronova Ab | Kräm för behandling av åldersförändringar i huden hos människa |
| RU2336867C2 (ru) * | 2003-05-30 | 2008-10-27 | ПАОЛИ АМБРОЗИ Джанфранко ДЕ | Композиция для дермального применения, обладающая фотозащитным и антиэритемным действием, содержащая солнечный фильтр и диметилсульфон |
| RU2266538C2 (ru) * | 2003-08-27 | 2005-12-20 | Ванчакова Нина Павловна | Способ идентификации противозудного эффекта антидепрессанта |
| PL364348A1 (en) | 2004-01-12 | 2005-07-25 | PHARMENA Sp.z o.o. | Application of quaternary pyridine salts as vessel protection agent |
| DE102004013798A1 (de) * | 2004-03-20 | 2005-10-06 | Wella Aktiengesellschaft | Verwendung von Mitteln zur kosmetischen Behandlung von Keratin enthaltenden Material |
| PL1919466T3 (pl) | 2005-07-11 | 2012-05-31 | Cortria Corp | Formulacje do leczenia nieprawidłowości lipoproteinowych obejmujące statynę i pochodną metylonikotynoamidu |
| DE602006008349D1 (de) * | 2005-12-09 | 2009-09-17 | Cerecon Ag | Quaternäre 3-amido, n-methylpyridiniumsalze als entzündungshemmende mittel |
| CA2657606A1 (en) * | 2006-03-08 | 2007-09-13 | Cortria Corporation | Combination therapy with non-selective cox inhibitors to prevent cox-related gastric injuries |
| WO2008062324A2 (en) * | 2006-10-11 | 2008-05-29 | Dermena | Compositions comprising nicotinamide and wakame extract having skin anti-aging properties |
| JP2010506900A (ja) * | 2006-10-18 | 2010-03-04 | デルメナ | リポ蛋白質異常症並びに皮膚疾病および皮膚障害の処置のためのn−メチルニコチンアミドを含有する食品抽出物 |
| RU2470645C2 (ru) * | 2007-09-10 | 2012-12-27 | Гленмарк Фармасьютикалс Лимитед | Фармацевтическая композиция для местного применения, содержащая комбинацию фузидовой кислоты и кортикостероида |
| EP2211858B1 (de) | 2007-10-12 | 2015-03-25 | Politechnika Lodzka | Verwendung von quarternären pyridiniumsalzen zur inhibition von tumor metastasen |
| TWI432188B (zh) * | 2008-12-19 | 2014-04-01 | Merz Pharma Gmbh & Co Kgaa | 供治療發炎性皮膚疾病之1-胺基-烷基環己烷衍生物類 |
| WO2018015862A1 (en) | 2016-07-18 | 2018-01-25 | Pharmena S.A. | 1-methylnicotinamide salts for use in raising the blood levels of adiponectin |
| JP7608422B2 (ja) | 2019-07-12 | 2025-01-06 | ユニリーバー・アイピー・ホールディングス・ベスローテン・ヴェンノーツハップ | 生体エネルギー組み合わせ及びそれの使用方法 |
| WO2021205341A1 (en) | 2020-04-07 | 2021-10-14 | Pharmena S.A. | 1-methylnicotinamide for the prevention/treatment of inflammatory airway diseases |
| PL246761B1 (pl) * | 2023-05-10 | 2025-03-03 | Politechnika Poznanska | Sposób otrzymywania czwartorzędowych soli amoniowych z kationem 3-karbamoilo-1-alkilopirydyniowym i anionem salicylanowym |
| PL248942B1 (pl) * | 2024-01-31 | 2026-02-16 | Politechnika Poznanska | Czwartorzędowe sole amoniowe zawierające anion 2-furanokarboksylanowy i kation będący alkilową pochodną nikotynamidu, sposób ich otrzymywania i zastosowanie jako środki myjąco-dezynfekujące |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3823076A (en) * | 1972-05-23 | 1974-07-09 | Du Pont | Zinc electroplating additive |
| US4067975A (en) * | 1975-08-04 | 1978-01-10 | Yu Ruey J | Treatment of psoriasis with 6-aminonicotinamide and thionicotinamide |
| US4505896A (en) * | 1979-04-19 | 1985-03-19 | Elorac, Ltd. | Method of treating acne vulgaris and composition |
| US4578394A (en) * | 1984-12-10 | 1986-03-25 | Hoechst-Roussel Pharmaceuticals Incorporated | Cholinergic function increasing 3-[N-(pyridyl) carbamoyl]-1,4-dihydropyridines |
| DE3603601C3 (de) * | 1986-02-06 | 1999-12-23 | Jutta Mai | Verwendung eines Bockshornkleesamenextraktes |
| US4786647A (en) * | 1986-06-30 | 1988-11-22 | University Of Florida | Method for eliciting anxiolysis |
| ZA892928B (en) * | 1988-04-25 | 1991-01-30 | Pro Neuron Inc | Pharmaceutical compositions containing deoxyribonucleosides for wound healing |
| US5372911A (en) * | 1991-06-13 | 1994-12-13 | Dainippon Ink And Chemicals, Inc. | Process of forming super high-contrast negative images and silver halide photographic material and developer being used therefor |
| US6238678B1 (en) * | 1995-11-06 | 2001-05-29 | The Procter & Gamble Company | Methods of regulating skin appearance with vitamin B3 compound |
| RU2085187C1 (ru) * | 1995-11-22 | 1997-07-27 | Исследовательская корпорация МДТ | Гель для ухода за кожей и лечения ее заболеваний и композиция для его получения |
| US6028111A (en) * | 1996-03-08 | 2000-02-22 | Oxigene, Inc. | Compositions and use of benzamides and nicotinamides as anti-inflammatory agents |
| US20040102358A1 (en) * | 1997-05-19 | 2004-05-27 | Scivoletto Rosemarie | Composition for treating skin conditions |
| AU3082699A (en) * | 1998-03-16 | 1999-10-11 | Procter & Gamble Company, The | Method of treating skin irritation |
-
1999
- 1999-01-07 PL PL330768A patent/PL190755B1/pl unknown
-
2000
- 2000-01-07 CZ CZ20012450A patent/CZ299662B6/cs not_active IP Right Cessation
- 2000-01-07 AU AU17927/00A patent/AU1792700A/en not_active Abandoned
- 2000-01-07 DE DE60019086T patent/DE60019086T2/de not_active Expired - Lifetime
- 2000-01-07 SK SK951-2001A patent/SK285869B6/sk not_active IP Right Cessation
- 2000-01-07 HU HU0104963A patent/HU225475B1/hu unknown
- 2000-01-07 AT AT00900030T patent/ATE292117T1/de active
- 2000-01-07 EP EP00900030A patent/EP1147086B9/de not_active Expired - Lifetime
- 2000-01-07 ES ES00900030T patent/ES2238985T3/es not_active Expired - Lifetime
- 2000-01-07 WO PCT/IB2000/000019 patent/WO2000040559A1/en not_active Ceased
- 2000-01-07 RU RU2001121650/14A patent/RU2199319C1/ru active
- 2000-01-07 PL PL396696A patent/PL396696A1/pl unknown
- 2000-07-01 UA UA2001075379A patent/UA73491C2/uk unknown
Also Published As
| Publication number | Publication date |
|---|---|
| RU2001121650A (ru) | 2004-02-27 |
| SK9512001A3 (en) | 2001-12-03 |
| HUP0104963A2 (hu) | 2002-04-29 |
| ATE292117T1 (de) | 2005-04-15 |
| PL190755B1 (pl) | 2006-01-31 |
| CZ20012450A3 (cs) | 2002-10-16 |
| UA73491C2 (uk) | 2005-08-15 |
| PL396696A1 (pl) | 2012-01-16 |
| EP1147086B1 (de) | 2005-03-30 |
| ES2238985T3 (es) | 2005-09-16 |
| WO2000040559A1 (en) | 2000-07-13 |
| DE60019086D1 (de) | 2005-05-04 |
| CZ299662B6 (cs) | 2008-10-08 |
| AU1792700A (en) | 2000-07-24 |
| HUP0104963A3 (en) | 2002-11-28 |
| RU2199319C1 (ru) | 2003-02-27 |
| SK285869B6 (sk) | 2007-10-04 |
| ES2238985T9 (es) | 2011-03-24 |
| HU225475B1 (en) | 2006-12-28 |
| EP1147086A1 (de) | 2001-10-24 |
| EP1147086B9 (de) | 2010-09-22 |
| PL330768A1 (en) | 2000-07-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60019086T2 (de) | Zusammensetzungen zur behandlung von hautkrankheiten | |
| DE3650068T2 (de) | Pharmazeutische träger zum reduzieren des transdermalen flusses. | |
| DE3690187C2 (de) | Naphthalinderivate mit retinoider Wirkung, Verfahren zu deren Herstellung und diese enthaltende pharmazeutische und kosmetische Mittel | |
| DE69526103T2 (de) | Dermatologische zusammensetzungen, welche benzylneroxid und ein mittel zur verminderung von hautreizungen enthalten | |
| EP0188749B1 (de) | Fumarsäurederivate, Verfahren zu ihrer Herstellung und sie enthaltende pharmazeutische Zubereitungen | |
| DE69814146T2 (de) | Topische zusammensetzungen zur kontrolle von öligem/glänzenden aussehen der haut | |
| DE3889287T2 (de) | Tocopherolsorbat und entzündungshemmende Wirkstoffe enthaltende Lichtschutzmittel. | |
| EP0859592B1 (de) | Hautpflegemittel für gealterte haut | |
| DE69231647T2 (de) | Verwendungvon salicylsäure zur kontrolle der hautatrophie | |
| DE69326292T2 (de) | Retinsäuren und Tocopherol enthaltende Zusammensetzungen | |
| EP0751763B1 (de) | Gegen hautalterung wirksame stoffe oder wirkstoffkombinationen und zubereitungen | |
| DE69811263T2 (de) | Konjugierte linolsäure enthaltendes verteilungssystem in kosmetika | |
| DE3443230C2 (de) | 2,6-disubstituierte Naphthalin-Derivate, Verfahren zu ihrer Herstellung und ihre Verwendung auf dem pharmazeutischen und kosmetischen Gebiet | |
| DE3750934T2 (de) | Behandlung von nicht-Akne-entzündlichen und -infektiösen Hautkrankheiten. | |
| DE19531893A1 (de) | Juckreizmildernde, kosmetische und/oder pharmazeutische Zusammensetzungen | |
| DE68928756T2 (de) | Topische Zubereitungen enthaltend aliphatische Amine zur Behandlung von Hautkrankheiten | |
| DE3707245C2 (de) | 2,3,4,4a-Tetrahydro-4a,10,10-trimethyl - 1H-3, 9b - methandibenzofuranderivate, Verfahren zur Herstellung dieser Verbindungen und pharmazeutische und kosmetische Mittel, die diese Verbindungen enthalten | |
| EP0369263A2 (de) | Präparate zur topischen Behandlung von Hautkrankheiten | |
| DE102005026380A1 (de) | Mittel zur Unterdrückung von Entzündungen, umfassend Zinkpyrrolidoncarboxylat | |
| CH654287A5 (de) | Verbindungen und kompositionen zur reduktion der sebumsekretion. | |
| DE3544267C2 (de) | ||
| US6485714B1 (en) | Use of salicylic acid for regulating hyperpigmented spots | |
| WO2002069927A1 (de) | Melatonin-vitamin-a-präparate | |
| DE2514878B2 (de) | Allantoin-ascorbinsaeure-komplexe | |
| DE3529032C2 (de) | In 1-Stellung substituierte 4-Methoxy-2,3,6-trimethylbenzolderivate, Verfahren zu deren Herstellung und diese Verbindungen enthaltende pharmazeutische und kosmetische Mittel |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8327 | Change in the person/name/address of the patent owner |
Owner name: PHARMENA SP.Z.O.O., LODZ, PL |
|
| 8364 | No opposition during term of opposition |