CN103038364A - 诊断和治疗具有或发展对于第一种癌症治疗的抗性的患者中的癌症的方法 - Google Patents
诊断和治疗具有或发展对于第一种癌症治疗的抗性的患者中的癌症的方法 Download PDFInfo
- Publication number
- CN103038364A CN103038364A CN2011800231091A CN201180023109A CN103038364A CN 103038364 A CN103038364 A CN 103038364A CN 2011800231091 A CN2011800231091 A CN 2011800231091A CN 201180023109 A CN201180023109 A CN 201180023109A CN 103038364 A CN103038364 A CN 103038364A
- Authority
- CN
- China
- Prior art keywords
- kinase
- protein kinase
- inhibitor
- raf
- kinases
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/12—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/12—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
- C12N9/1205—Phosphotransferases with an alcohol group as acceptor (2.7.1), e.g. protein kinases
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y207/00—Transferases transferring phosphorus-containing groups (2.7)
- C12Y207/11—Protein-serine/threonine kinases (2.7.11)
- C12Y207/11024—Mitogen-activated protein kinase (2.7.11.24), i.e. MAPK or MAPK2 or c-Jun N-terminal kinase
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Abstract
提供了鉴定具有可能获益于用组合疗法的治疗的癌症的受试者的方法,所述组合疗法利用RAF抑制剂和第二种抑制剂。还提供了治疗在有此需要的受试者中的癌症的方法,并且包括给受试者施用有效量的RAF抑制剂和有效量的第二种抑制剂,其中所述第二种抑制剂是MEK抑制剂、CRAF抑制剂、CrkL抑制剂或TPL2/COT抑制剂。还提供了鉴定赋予对于第一种抑制剂的抗性的激酶靶的方法。
Description
相关申请
本申请根据35 U.S.C. §119(e)要求下述临时美国专利申请序列号的提交日期的利益:于2010年3月9日提交的61/312,193;于2010年3月10日提交的61/312,519;于2010年4月20日提交的61/326,021;和于2010年11月19日提交的61/415,569,所有这些在此整体引入作为参考。
联邦赞助的研究或开发
本发明在由美国国立卫生研究院(National Institutes of Health)授予的联邦授权号K08 CA115927和1DP20D002750下由政府支持进行。政府在本发明中拥有一定权利。
背景
丝氨酸/苏氨酸激酶B-RAF(也称为BRAF)中的致癌突变在50–70%的恶性黑素瘤中发现。(Davies,H.等人,Nature 417,949–954(2002)。)临床前研究已证实B-RAF(V600E)突变预测对黑素瘤中的丝裂原活化蛋白激酶(MAPK)信号传导级联的依赖性(Hoeflich,K. P.等人,Cancer Res. 69,3042–3051(2009);McDermott,U.等人,Proc. Natl Acad. Sci. USA 104,19936–19941(2007);Solit,D. B.等人BRAF mutation predicts sensitivity to MEK inhibition. Nature 439,358–362(2006);Wan,P. T.等人,Cell 116,855–867(2004);Wellbrock,C.等人,Cancer Res. 64,2338–2342(2004))—已通过RAF或MEK抑制剂在临床试验中的成功得到验证的观察(Flaherty,K. T.等人,N. Engl. J. Med. 363,809–819(2010);Infante,J. R.等人,J. Clin. Oncol.28(suppl.),2503(2010);Schwartz,G. K.等人,J. Clin. Oncol.27(suppl.),3513(2009)。)然而,对靶向抗癌治疗的临床应答频繁地被从新或获得的抗性挫败。(Engelman,J. A.等人,Science 316,1039–1043(2007);Gorre,M. E.等人,Science 293,876–880(2001);Heinrich,M. C.等人,J. Clin. Oncol. 24,4764–4774(2006);Daub,H.,Specht,K. & Ullrich,A. Nature Rev. Drug Discov. 3,1001–1010(2004)。)相应地,存在用于以阐明用于有效长期治疗策略的“可用药物控制的(druggable)”靶的方式鉴定抗性机制的新方法,鉴定可能获益于治疗策略的患者的新方法,和用有效的长期治疗策略治疗患者的方法的需要。
概述
本发明涉及在癌症治疗中对治疗剂的抗性的发展和赋予对癌症治疗的抗性的靶的鉴定。本发明还涉及用于促进有效的长期治疗策略的平行药物靶的鉴定且鉴定将获益于此类治疗的患者。
相应地,在一个方面,提供了鉴定具有可能获益于用组合疗法的治疗的癌症的受试者的方法,所述组合疗法利用RAF抑制剂和第二种抑制剂。该方法包括测定得自受试者的癌细胞中选自下述的一种或多种激酶靶的基因拷贝数、mRNA或蛋白质水平或磷酸化:MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)。该方法进一步包括比较基因拷贝数、mRNA或蛋白质水平或磷酸化与得自不含癌症的受试者的细胞中靶激酶的基因拷贝数、mRNA或蛋白质水平或磷酸化,并且将相对于不含癌症的受试者的细胞,在癌细胞中靶激酶的增加的基因拷贝数或mRNA表达中的改变或蛋白质过表达或磷酸化与具有可能获益于用组合疗法的治疗的癌症的受试者关联。
在另一个方面,提供了治疗在有此需要的受试者中的癌症的方法。该方法包括给受试者施用有效量的RAF抑制剂和有效量的第二种抑制剂,其中所述第二种抑制剂是MEK抑制剂或TPL2/COT抑制剂。
在另一个方面,提供了鉴定赋予对于第一种抑制剂的抗性的激酶靶的方法。该方法包括培养对于第一种抑制剂具有敏感性的细胞且在细胞培养物中表达多个激酶ORF克隆,每种细胞培养物表达不同的激酶ORF克隆。该方法进一步包括使每种细胞培养物暴露于抑制剂,且鉴定在暴露于抑制剂后具有大于对照细胞培养物的生存的细胞培养物,以鉴定赋予对于第一种抑制剂的抗性的激酶ORF克隆。
附图简述
图1举例说明基于ORF的功能筛选,其鉴定COT和C‐RAF激酶作为对于B‐RAF抑制的抗性的驱动物。(a)CCSB/Broad Institute激酶ORF集合的示意性概述。指出了激酶分类和每个分类的激酶数目;(b)表达CCSB/Broad Institute激酶ORF集合的A375细胞就在1μM PLX4720中的相对生存测定,且针对组成性活化的MEK1(MEK1DD)标准化。九个ORFs(圆圈)评分距所有ORFs平均值(虚线,44.26%)的2个标准差(虚线,58.64%);(c)所示ORFs在5个B‐RAFV600E细胞系中表达,且用DMSO或1 μM PLX4720处理。在4天后定量生存(相对于DMSO)。误差条代表在重复(n=6)之间的标准差;(d)在A375和SKMEL28中的二次筛选对跨越多点PLX4720浓度标度的前9个候选ORFs区分优先次序。
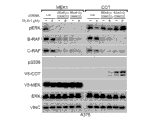
图2举例说明经由MAPK途径活化对于B‐RAF抑制的抗性。(a)所示ORFs在A375中表达。磷酸化MEK和ERK的水平在用DMSO(‐)或PLX4720(所示浓度)18小时处理后进行测定;(b)表达所示ORFs的A375的增殖。误差条代表在重复(n=6)之间的标准差。(c)在来自表达所示ORFs的A375的裂解产物中的C‐RAF(S338)和ERK磷酸化。(d)在来自表达BRAFV600E或空载体的永生化原代黑素细胞的裂解产物中的COT表达。COT mRNA具有内部起始密码子(30M),导致不同长度的两种蛋白质产物;由箭头指出的氨基酸1‐467或30‐467。(e)相对于对照shRNA(shLuc),在shRNA介导的B‐RAF缺失(shBRAF)后,在来自表达所示ORFs的A375的裂解产物中的COT和ERK磷酸化。(f)在用DMSO(‐)或1 μM PLX4720(+)18小时处理后,在来自在shRNA介导的C‐RAF缺失(shCRAF)后表达所示ORFs的A375的裂解产物或对照shRNA(shLuc)中的ERK磷酸化。
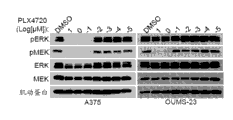
图3举例说明COT表达预测在癌细胞系中对于B‐RAF抑制的抗性。(a)MAP3K8/COT拷贝数;红色条:COT扩增,蓝色条:非扩增的COT;(b)在B‐RAFV600E细胞系中的COT表达和(c)短期培养物;(d)在B‐RAFV600E细胞系中的PLX4720 GI50。颜色与(a)中一样;(e)在用DMSO或PLX4720(所示浓度)处理后的MEK和ERK磷酸化;(f)在用DMSO或1 μM PLX4720(PLX)或CI‐1040(CI)处理的M307 裂解产物(AZD‐R;AZD6244‐抗性的)中的ERK磷酸化;(g)在患者/损伤匹配的PLX4032处理的转移性黑素瘤组织样品中的COT mRNA表达(QRT/PCR)。患者1和3具有来自相同损伤的多个活组织检查。误差条代表SEM(n=3)U;未确定的/无法检测的;(h)在与对照(shLuc)比较shRNA介导的COT缺失(shCOT)和用DMSO(‐)或1 μM PLX4720(+)处理后,RPMI‐7951中的ERK和MEK磷酸化。定量ERK和MEK磷酸化;(i)在用小分子COT激酶抑制剂1小时处理后,在RPMI‐7951中的ERK和MEK磷酸化。定量ERK和MEK磷酸化。(j)在BRAFV600E细胞系的实验对象组中的PLX4720灵敏度曲线。OUMS-23和M307代表具有COT表达/扩增的细胞系,并且所有其他代表具有无法检测/未改变的COT的细胞系;(k)在对于PLX4032具有获得抗性的转移性皮下恶性黑素瘤中COT的选择性表达和相应MAPK途径活化(*指示本底带,MET-MM(PLX-R);转移性黑素瘤,PLX4032-抗性的)。
图4举例说明表达COT的B‐RAFV600E细胞系显示出对于变构MEK抑制剂的抗性。(a)在B‐RAFV600E细胞系的实验对象组中的CI‐1040 GI50;(b)在来自用DMSO或CI‐1040(所示浓度)处理的所示细胞系的裂解产物中的 MEK和ERK磷酸化;(c)对于PLX4720、RAF265、CI‐1040和AZD6244,异位表达所示ORFs的A375的GI50倍数变化(相对于MEK1);(d)在用DMSO或1 μM PLX4720、RAF265、CI‐1040或AZD6244处理后,在表达所示ORFs的A375中的ERK磷酸化;(e)在表达所示ORFs且用DMSO、PLX4720(所示浓度)和与CI‐1040或AZD6244(都是1 μM)组合的PLX4720处理的A375的生存。误差条代表标准差(n=6);(f)在用DMSO、PLX4720(1μM)或与CI‐1040或AZD6244(都是1 μM)组合的PLX4720处理后,在表达所示ORFs的A375中的ERK磷酸化;(g)具有异常MAP3K8/COT拷贝数/表达的细胞系对于变构MEK抑制剂CI-1040是不敏感的或(h)AZD6244;(i)在B-RAFV600E-突变细胞系中响应B-RAF抑制的MAP3K复合物形成的示意性略图。PLX4720定位在信号传导组分复合物(右上图)中的C-RAF,其通过C-RAF上游的致癌事件活化(右下图),随后驱动抗性。在COT表达的背景中,含COT/RAF复合物足以活化MAPK途径且介导抗性(左下图)。
图5举例说明关于激酶的基于ORF的功能筛选的示意性略图,所述激酶驱动对于B-RAF抑制的抗性。B-RAFV600E细胞系A375用在CCSB/Broad Institute激酶ORF集合中的597激酶慢病毒转导。鉴定对在对照处理的A375中的增殖具有正面或负面效应的ORFs,且从最后分析中去除。通过生成在B-RAF抑制(PLX4720处理的)和对照处理的细胞之间的差异生存比鉴定促进抗性的ORFs。差异生存针对组成性活化的MEK1等位基因MEK1DD;测定特异性阳性对照进行标准化。
图6举例说明CCSB/Broad Institute激酶ORF集合经由高滴度慢病毒良好表达。(a),用于所有ORF筛选和后续验证的pLX-BLAST-V5慢病毒表达载体的示意图。(b)代表宽尺寸范围的加上GFP标签的ORFs在Jurkat细胞中慢病毒表达,并且定量表达GFP的细胞/ORF(例如受感染细胞)百分比,证实跨越一系列ORF大小的高病毒滴度。(c),相对于细胞DNA,经由LiCor用针对V5附加表位的抗体检测的96个随机ORFs的表达。表达在83%的孔中是可检测的。
图7举例说明候选抗性ORFs的表达。用pLX-BLAST-V5-ORF(所示的)瞬时转染293T,并且使用抗V5-HRP抗体检测表达。AXL克隆是‘闭合的’,并且具有在V5标签前的终止密码子。关于表达的验证,参见图12;在暗曝光上的(*)指示在更亮曝光上不可见的三个ORFs的表达。
图8举例说明二次筛选对前9个候选B-RAF抑制剂抗性ORFs区分优先次序。在初次筛选中评分的前九个ORFs在A375或SKMEL28中表达和来自8点PLX4720浓度范围的GI50。
图9举例说明ORF表达对B-RAFV600E细胞系中的增殖的作用。相对于MEK1,在生长7天后表达所示ORFs的(a)A375或(b)SKMEL28中的增殖。
图10举例说明组成性活化的MEK1(MEK1DD)和COT的异位表达导致在A375中增加的pMEK/pERK,而C-RAF减少pMEK/pERK水平。来自异位表达GFP、MEK1、MEKDD、COT或C-RAF的A375的裂解产物经由免疫印迹分析pERK和pMEK水平。将GFP和MEK1(泳道1-3)与COT/C-RAF(泳道4-5)分离,以防止残留V5-MEK1信号压倒以低得多的水平表达的COT和C-RAF的那种。
图11举例说明COT和C-RAF的激酶活性是在PLX4720处理的背景中的持续ERK磷酸化所需的。表达异位的(a)MEK1、野生型COT或激酶活性COT(COTK167R)或(b)MEK1、野生型C-RAF或激酶失活的C-RAF(C-RAFK375M),用1 μM PLX4720处理18小时的A375的免疫印迹分析。
图12举例说明在B-RAF抑制剂PLX4720的背景中ORF表达对MAPK信号传导的作用。在PLX4720(18小时,所示浓度)的存在下表达所示ORFs的A375中,通过pERK和pMEK的免疫印迹分析评估MAPK途径活化。(*)指示针对表达的ORF而不是V5表位的抗体的使用。克隆不含V5表位的AXL。
图13举例说明在用1μM PLX4720(+)或DMSO(-)18小时处理后,在A375中B-RAF与免疫沉淀的C-RAF结合,(a). WCE;全细胞提取物对照。异位表达的C-RAF与B-RAF组成性结合,并且在S338处是磷酸化的,与膜定位和活化一致。表达MEK1,MEKDD和COT的A375未显示C-RAF活化的证据,(b)。
图14举例说明野生型C-RAF的逆转录病毒表达或C-RAF(C-RAF(22W))的高活性平截突变型致使A375对于B抑制剂PLX4720有抵抗力(a),并且导致在PLX4720(1μM,18小时)处理背景中的持续pERK水平,(b)。用逆转录病毒实现的C-RAF表达水平显著低于基于慢病毒的系统,导致比用慢病毒C-RAF实现的那种更低的GI50。
图15举例说明B-RAFV600E对COT mRNA的作用(a)。相对于在表达野生型B-RAF(载体)或B-RAFV600E的经转化的原代黑素细胞中的GAPDH mRNA表达,COT mRNA表达的定量RT/PCR。COT表达针对表达载体的原代黑素细胞的那种进行标准化。(**)显著的,p 0.05(斯氏双尾、配对T检验)。内源COT mRNA在PLX4720敏感的A375中是无法检测的,并且异位表达的COT mRNA水平不受1 μM PLX4720处理影响。表达GFP或COT的A375用1 μM PLX4720处理18小时。相对于表达GFP、DMSO处理的A375,就GAPDH标准化的COT表达分析逆转录的mRNA。(*)不显著的,p > 0.05(斯氏双尾、配对T检验)。误差条代表SEM。
图16举例说明B-和C-RAF蛋白质水平不是COT介导的ERK磷酸化所需的。表达异位MEK1(对照)或COT的A375用表达靶向B-RAF、C-RAF的shRNAs或对照shRNA(shLuc)的慢病毒序贯感染,并且在1 μM PLX4720,18小时的存在(+)或不存在(-)下测定所示蛋白质的表达。
图17举例说明752个细胞系的SNP分析揭示在MAP3K8/COT中的拷贝数改变。在已经历拷贝数分析的752个细胞系中,534个还已经历突变概况分析。三十八(7.1%)个突变概况分析的细胞具有B-RAFV600E突变。两种细胞系(所示的OUMS-23,RPMI-7951)具有B-RAFV600E突变连同在MAP3K8/COT中的拷贝数增益。
图18举例说明在癌细胞系OUMS-23中的MAP3K8/COT改变。(a)来自mRNA微阵列分析的MAP3K8 /COT探针(指出的)的RMA信号。OUMS-23是表达COT mRNA的前2%(在765个细胞系中)之一。(b)在B-RAFV600E突变细胞系的实验对象组中的COT mRNA表达。(c)如经由所示细胞的免疫印迹分析测定的,相对于在A375和SKMEL28细胞系中异位表达的COT,在OUMS-23中的内源COT蛋白质表达。
图19举例说明COT mRNA和蛋白质在B RAF-抑制剂抗性细胞系和组织中表达。(a)在细胞系、短期培养物和来自复发的、PLX4032处理的、恶性黑素瘤(MM-R)的组织的实验对象组中,GAPDH 标准化的COT mRNA表达的RT/PCR分析。来自细胞系和短期培养物的相应蛋白质表达分别显示于图3b和3c中。(b)来自原代黑素细胞(1o Mel(B-RAF WT))、患者匹配的正常皮肤(皮肤)和转移性恶性黑素瘤(MM-R;小图a中所示的COT mRNA)、表达B-RAFV600E的A375细胞和原代黑素细胞(1o Mel(B-RAFV600E))的裂解产物的蛋白质印迹分析。
图20举例说明COT的缺失影响在COT扩增的细胞系RPMI-7951中的生存。(a)相对于对照shRNA(shLuc),在慢病毒shRNA介导的COT缺失(shCOT)后,RPMI-7951生存的定量。误差条代表在重复之间的标准差。(b)免疫印迹分析显示在表达shLuc和shCOT的RPMI-7951中的相对COT蛋白质表达。
图21举例说明ORF表达对MAPK途径抑制剂的实验对象组在SKMEL28中的GI50的作用。对于RAF抑制剂PLX4720和RAF265以及MEK1/2抑制剂CI-1040和AZD6244测定异位表达MEK1、MEK1DD或COT的SKMEL28的半最大生长抑制浓度(GI50)。对于每种化合物测定对于MEK1DD和COT(相对于MEK1)在GI50中的变化。
图22举例说明COT可以经由MEK不依赖性和MEK依赖性机制活化ERK。(a)相对于对照shRNA(shLuc),在GFP或COT表达以及后续慢病毒shRNA介导的MEK1、MEK2或MEK1和MEK2(MEK1+2)缺失后,在来自A375的裂解产物中的ERK磷酸化的免疫印迹分析。左和右图代表两对不同的MEK1和MEK2 shRNA构建体。(b)在体外激酶测定中通过重组COT的重组、失活的ERK磷酸化(Thr202/Tyr204)的免疫印迹分析。
图23举例说明组合的MAPK途径抑制有效压制SKMEL28中的增殖。异位表达MEK1、MEK1DD或COT且用DMSO、PLX4720(所示浓度)、PLX4720(1 μM)和CI-1040(1 μM)或PLX4720(1 μM)和AZD6244(1 μM)处理的SKMEL28的生存(相对于DMSO)。误差条代表在重复之间的标准差。
图24举例说明COT过表达足以致使具有B-RAFV600E突变的黑素瘤癌细胞对于B-RAF抑制有抵抗力。
图25举例说明在初次筛选中评分的前九个ORFs在(b)A375 的(a)SKEL28中表达,并且显示了对于4种MAPK途径抑制剂(PLX4720、RAF265、CI-1040、AZD-6244)的aGI50。
图26举例说明在B-RAFv600E细胞系的实验对象组中,CRKL表达修饰对选择性B-RAF抑制剂PLX4720的敏感性。
图27举例说明MAP3K8/COT扩增的/B-RAFV600E突变癌细胞系OUMS-23显示跨越PLX4720的剂量范围的ERK/MEK的组成性磷酸化。
图28举例说明对于MAPK途径抑制的不敏感性对应于皮肤癌细胞系子集中的MAP3K8/COT拷贝数增益。显示了B-RAFV600E突变细胞系的实验对象组及其对(a)B-RAF抑制剂PLX4720和(b)MEK抑制剂AZD6244的敏感性。
发明详述
本发明涉及在癌症治疗中对治疗剂的抗性发展和赋予对癌症治疗的抗性的靶鉴定。本发明还涉及用于促进有效的长期治疗策略的平行药物靶鉴定且鉴定将获益于此类治疗的患者。在一些实施方案中,本发明涉及激酶且特别是MAP激酶途径组分。
除非另有说明,本发明的实践将采用在领域技术内的分子生物学、免疫学、微生物学、细胞生物学和重组DNA的常规技术。参见例如,Sambrook,Fritsch和Maniatis,MOLECULAR CLONING:A LABORATORY MANUAL,(目前版本);CURRENT PROTOCOLS IN MOLECULAR BIOLOGY(F. M. Ausubel等人编辑,(目前版本));系列METHODS IN ENZYMOLOGY(Academic Press,Inc.):PCR 2:A PRACTICAL APPROACH(目前版本)ANTIBODIES,A LABORATORY MANUAL and ANIMAL CELL CULTURE(R. I. Freshney,编辑(1987)). DNA Cloning:A Practical Approach,第I & II卷(D. Glover,编辑);Oligonucleotide Synthesis(N. Gait,编辑,目前版本);Nucleic Acid Hybridization(B. Hames & S. Higgins,编辑,目前版本);Transcription and Translation(B. Hames & S. Higgins,编辑,目前版本);Fundamental Virology,第2版,第I & II卷(B. N. Fields和D. M. Knipe,编辑)。
丝裂原活化蛋白激酶(MAPK)级联是关键细胞内信号传导途径,其调节响应不同细胞外刺激的信号转导,所述细胞外刺激包括生长因子、细胞因子和原癌基因。这个途径的活化导致转录因子活化和基因表达中的改变,其最终导致细胞功能中的变化,所述细胞功能包括细胞增殖、细胞周期调节、细胞存活、血管生成和细胞迁移。经典MAPK信号传导通过在细胞表面上的受体酪氨酸激酶起始,然而,许多其他细胞表面分子能够活化MAPK级联,包括整联蛋白、异源三聚体G蛋白和细胞因子受体。
与细胞表面受体例如受体赖氨酸激酶的配体结合一般导致受体的磷酸化。衔接蛋白Grb2与活化受体的磷酸化细胞内结构域结合,并且这种结合召募鸟嘌呤核苷酸交换因子包括SOS-I和CDC25至细胞膜。这些鸟嘌呤核苷酸交换因子与GTP酶Ras相互作用且活化GTP酶Ras。常见Ras同种型包括K-Ras、N-Ras、H-Ras及其他。在Ras活化后,丝氨酸/苏氨酸激酶Raf(例如A-Raf、B-Raf或Raf-1)通过与Ras相互作用召募至细胞膜。Raf随后磷酸化。Raf通过在位置217和221上的两个丝氨酸残基的磷酸化直接活化MEKl和MEK2。在活化后,MEKl和MEK2磷酸化在丝氨酸/苏氨酸激酶Erkl和Erk2中的酪氨酸(Tyr-185)和苏氨酸(Thr-183)残基,导致Erk活化。活化的Erk调节细胞溶质中的许多靶并且还易位至核,在其中它磷酸化调节基因表达的许多转录因子。Erk激酶具有众多靶,包括EIk-I、c-Etsl、c-Ets2、p90RSKl、MNKl、MNK2、MSKl、MSK2和TOB。虽然前述途径是MAPK信号传导的经典表示,但在MAPK途径及其他信号传导级联之间存在相当大的串扰。
MAPK信号传导中的异常在癌症生物学中具有显著作用。Ras的改变表达在许多癌症中是常见的,并且Ras中的活化突变也已得到鉴定。此类突变在高达30%的所有癌症中发现,并且在胰腺(90%)和结肠(50%)癌中特别常见。此外,活化Raf突变已在黑素瘤和卵巢癌中鉴定。最常见突变BRAFV600E导致下游MAP激酶途径的组成性活化,且是黑素瘤细胞增殖、软琼脂生长和肿瘤异种移植物形成所需的。基于MAPK过度活化在人癌症中的确定作用,用特异性抑制剂靶向MAPK途径的组分是对于癌症疗法的有希望的方法。然而,患者可以对于这些有希望的疗法具有先天抗性或获得抗性。靶激酶、诊断和/或预后标记和用于具有先天或获得抗性的这些患者的治疗疗法的鉴定在下文描述。
高流通量功能筛选测定
在一些方面,本发明涉及使用高流通量筛选测定鉴定能够驱动对于临床有效疗法的抗性的靶的方法。在一些实施方案中,该方法可以包括关于激酶的基于开放读码框(ORF)的功能筛选,所述激酶驱动对于治疗剂的抗性。该方法可以包括给细胞系提供已知具有致癌突变的激酶。激酶ORFs的文库可以在细胞系上个别表达,从而使得可以进一步估计各自表达来自文库的不同ORF的多个克隆。每个克隆可以是(i)暴露于细胞系中已知激酶的抑制剂,和(2)基于不含抑制剂的细胞系中的ORF表达监控生长变化。消除具有来自单独的ORF表达的生长效应的任何克隆,正或负生长。随后就在对照和处理克隆之间的生存比较各自表达不同激酶的剩余克隆,并且针对阳性对照进行标准化。在用抑制剂处理后增加的细胞生存鉴定赋予抗性的ORFs,并且因此鉴定关于用另一种抑制剂处理的激酶靶。在一些实施方案中,评分超过距标准化平均值的两个标准差的克隆可以是指示用另外抑制剂的处理对于受试者是有利的靶激酶。
作为非限制性例子,关于驱动对于B-RAF抑制的抗性的激酶的高流通量功能筛选测定的简图显示于图5中。装配~600个克隆且序列验证的ORFs的集合,占所有注释的激酶的~75%(Center for Cancer Systems Biology(CCSB)/Broad Institute激酶ORF Collection,图1a,1b,表3)。这个可公开获得的集合可以快速转移到多种表达载体用于多种最终应用。本领域技术人员已知的任何类型的表达载体可以用于表达激酶ORF集合。作为非限制性例子,可以制备能够在哺乳动物细胞中产生高滴度病毒和强ORF表达的,可选择、已附加表位的慢病毒表达载体,以表达激酶集合(pLX-BLAST-V5,图6a)。
为了鉴定能够防止RAF抑制的激酶,形成阵列的(arrayed)激酶ORF集合可以在A375中稳定表达,所述A375是对RAF激酶抑制剂PLX4720敏感的B-RAFV600E恶性黑素瘤细胞系(图1a,1b和6c,表3)。用1 μM PLX4720处理的ORF表达细胞的克隆就相对于未处理细胞的生存进行筛选,并且针对测定特异性阳性对照MEK1S218/222D(MEK1DD)进行标准化(表4)。从分析中去除影响基线生存或增殖的ORFs。可以进一步估计评分超过距标准化平均值的两个标准差的克隆,以鉴定对于第二种抑制剂的抗性赋予靶激酶。在一些实施方案中,编码靶激酶的基因可以是MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)。在一些实施方案中,编码靶激酶的基因可以是MAPK途径活化剂。在一些实施方案中,编码靶激酶的基因可以是直接磷酸化且活化MEK的MAP3激酶。在一些实施方案中,编码靶激酶的基因可以编码在黑素瘤中扩增且磷酸化的衔接蛋白。
在其他实施方案中,ORF集合可以是在B-RAF中具有不同突变的细胞系中稳定表达的,例如在约氨基酸位置600上的另一个突变,例如V600K、V600D和V600R。另外的B-RAF突变包括在Davies等人Nature,417,949-954,2002,表1中所述的突变。可以使用对其他RAF激酶抑制剂敏感的细胞系,包括但不限于PLX4032;GDC-0879;RAF265;索拉非尼;SB590855和/或ZM 336372。在一些实施方案中,ORF集合可以在对于MEK抑制剂具有敏感性的细胞系中稳定表达。MEK抑制剂的非限制性例子包括AZD6244;CI-1040;PD184352;PD318088、PD98059、PD334581、RDEA119、6-甲氧基-7-(3-吗啉-4-基-丙氧基)-4-(4-苯氧基-苯氨基)-喹啉-3-甲腈和4-[3-氯-4-(1-甲基-1H-咪唑-2-基硫烷基)-苯氨基]-6-甲氧基-7-(3-吗啉-4-基-苯氧基)-喹啉-3-甲腈。另外的RAF和MEK抑制剂在下文描述。作为非限制性例子,示例性RAF抑制剂显示于表1中,并且示例性MEK抑制剂显示于表2中。
表1:示例性RAF抑制剂
| 名称 | CAS No. | 结构 | |
| 1 | RAF265 | 927880-90- | |
| 2 | 甲磺酸索拉非尼Nexavar Bay 43-9006 | 475207-59-1 | |
| 索拉非尼4-[4-[[4-氯-3-(三氟甲基)苯基] 氨甲酰氨基]苯氧基]-N-甲基-吡啶-2-甲酰胺 | 284461-73-0 | ||
| 3 | SB590885 | ||
| 4 | PLX4720 | 918505-84-7 | |
| 5 | PLX4032 | 1029872-54-5 | |
| 6 | GDC-0879 | 905281-76-7 | |
| 7 | ZM 336372 | 208260-29-1 |
表2:示例性MEK抑制剂
| 名称 | CAS No. | 结构 | |
| 1 | CI-1040/PD184352 | 212631-79-3 | |
| 2 | AZD6244 | 606143-52-6 | |
| 3 | PD318088 | 391210-00-7 | |
| 4 | PD98059 | 167869-21-8 | |
| 5 | PD334581 | ||
| 6 | RDEA119N-[3,4-二氟-2-[(2-氟-4-碘苯基)氨基]-6-甲氧基苯基]-1-[(2R)-2,3-二羟丙基]- 环丙磺酰胺 | 923032-38-6 | |
| 7 | 6-甲氧基-7-(3-吗啉-4-基-丙氧基)-4-(4-苯氧基-苯氨基)-喹啉-3-甲腈 | ||
| 8 | 4-[3-氯-4-(1-甲基-1H-咪唑-2-基硫烷基)-苯氨基]-6-甲氧基-7-(3-吗啉-4-基-丙氧基)-喹啉-3-甲腈 |
用于针对靶向疗法的先天和获得抗性的诊断/预后标记
在一些方面,本发明涉及检测样品(例如来自癌症患者的生物学样品)中的一种或多种诊断或预后标记的存在的方法。本领域技术人员已知的多种筛选方法可以用于检测样品中的标记的存在,包括DNA、RNA和蛋白质检测。下文描述的技术可以用于测定在得自患者的样品中激酶靶的存在或不存在。在一些实施方案中,患者可以具有对于激酶靶向疗法,包括B-RAF抑制剂或MEK抑制剂的先天或获得抗性。例如,患者可以具有对于B-RAF抑制剂PLX4720和/或PLX4032的先天或获得抗性。在一些实施方案中,患者可以具有对于MEK抑制剂AZD6244的先天或获得抗性。在患者中一种或多种激酶靶标记的鉴定帮助医生决定用于患者的治疗方案。例如,在具有一种或多种激酶靶标记的患者中,医生可以用如下文更详细地描述的组合疗法治疗患者。
在一些实施方案中,激酶靶可以包括但不限于MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)。标记可以是关于激酶靶的基因拷贝数中的增加、蛋白质表达中的增加、一种或多种MAP激酶途径成员的磷酸化、mRNA表达中的变化等。
作为非限制性例子,在具有B-RAF中的致癌突变的患者中,活化靶激酶的鉴定可以用于表征用于患者的治疗方案。例如,在具有B-RAFV600E突变的患者中,用RAF抑制剂单独的治疗可以指示患者在一段时间后处于获得对于治疗的抗性的相对高危险中。在具有致癌突变的患者中,在那个患者中的活化激酶靶的鉴定可以指示在治疗方案中第二种抑制剂的包括。
活化激酶靶的鉴定可以包括基因拷贝数的分析和靶激酶的拷贝数中的增加的鉴定。例如,MAP3K8中的拷贝数增益指示患者具有先天抗性或发展获得抗性,特别是如果患者还具有B-RAFV600E突变。
在一些实施方案中,活化激酶靶的鉴定可以包括激酶靶和/或MAP激酶途径的成员的磷酸化分析。例如,C-RAF在S338上的磷酸化指示患者具有先天抗性或发展获得抗性,特别是如果患者还具有B-RAFV600E突变。在一些实施方案中,MEK/ERK磷酸化中的增加的鉴定可以指示患者具有先天抗性或发展获得抗性。在具有B-RAFV600E突变的患者中增加的COT蛋白质表达可以预测对于RAF抑制和MEK抑制的抗性。
活化激酶靶的鉴定可以包括激酶靶的mRNA表达分析。例如,在用第一种激酶抑制剂的最初治疗后COT mRNA表达中的增加指示患者具有或发展抗性。在一些实施方案中,第一种激酶抑制剂可以是RAF抑制剂或MEK抑制剂。
治疗方法
在多种实施方案中,本发明提供了用于治疗具有癌症的患者的方法。该方法一般包括第一种抑制剂和第二种抑制剂的施用。一种抑制剂可以是RAF抑制剂。RAF抑制剂可以是泛RAF抑制剂或选择性RAF抑制剂。泛RAF抑制剂包括但不限于RAF265、索拉非尼或SB590885。在一些实施方案中,RAF抑制剂是B-RAF抑制剂。在一些实施方案中,选择性RAF抑制剂是PLX4720、PLX4032或GDC-0879-A。一种抑制剂可以是MEK抑制剂(参见表2举例说明示例性MEK抑制剂)。一种抑制剂可以是COT抑制剂。作为非限制性例子,COT抑制剂可以是如下所述的shRNA抑制剂,或小分子COT抑制剂,4-(3-氯-4-氟苯氨基)-6-(嘧啶-3-基-甲氨基)-3-氰基-[1,7]- 二氮杂萘(EMD;TPL2抑制剂I;目录号616373,PubChem ID:9549300) 。本发明的抑制剂抑制一种或多种激酶靶,包括MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)或其他MAP激酶途径靶。
在一些实施方案中,提供了用于癌症的组合疗法,其包含有效量的RAF抑制剂和有效量的MAP3K8(TPL2/COT)抑制剂。本文还提供的是用于癌症的组合疗法,其包含有效量的RAF抑制剂和有效量的MEK抑制剂。其他组合疗法包括有效量的RAF抑制剂和有效量的靶向下述中的一种或多种的基因、mRNA或编码的蛋白质的第二种抑制剂:MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)。组合疗法适合于治疗其中癌症含有B-RAF突变细胞且特别是B-RAFV600E突变细胞的患者。本发明进一步提供了用于癌症的组合疗法,其包括有效量的RAF抑制剂和有效量的MEK抑制剂,其中所述具有癌症的受试者含有具有改变的MAP3K8(TPL2/COT)表达或基因拷贝数的细胞。在一些实施方案中,MEK抑制剂是CI-1040/PD184352或AZD6244。
作为非限制性例子,本文提供的MEK抑制剂可以是CI-1040、AZD6244、PD318088、PD98059、PD334581、RDEA119、6-甲氧基-7-(3-吗啉-4-基-丙氧基)-4-(4-苯氧基-苯氨基)-喹啉-3-甲腈或4-[3-氯-4-(1-甲基-1H-咪唑-2-基硫烷基)-苯氨基]-6-甲氧基-7-(3-吗啉-4-基-苯氧基)-喹啉-3-甲腈、Roche化合物RG7420或其组合。还可以使用本领域已知的另外的MEK抑制剂。
在前述方面的示例性实施方案中,本文提供的RAF抑制剂是PLX4720、PLX4032、BAY 43-9006(索拉非尼)、ZM 336372、RAF 265、AAL-881、LBT-613或CJS352(NVP-AAL881-NX(下文称为AAL881)和NVP-LBT613-AG-8(LBT613)是异喹啉化合物(Novartis、Cambridge、MA)。对于组合疗法有用的另外的示例性RAF抑制剂包括泛RAF抑制剂、B-RAF的抑制剂、A-RAF的抑制剂、和RAF-1的抑制剂。在示例性实施方案中,对于组合疗法有用的RAF抑制剂包括PLX4720、PLX4032、BAY 43-9006(Sorafenib)、ZM 336372、RAF 265、AAL-881、LBT-613和CJS352。示例性RAF抑制剂进一步包括PCT公开号WO/2008/028141中所示的化合物,所述申请的整个内容引入本文作为参考。示例性RAF抑制剂另外包括PCT公开号WO/2006/024836中所述的喹唑啉酮衍生物和PCT公开号WO/2008/020203中所述的吡啶基喹唑啉胺衍生物,所述申请的整个内容引入本文作为参考。
组合的施用包括以单一制剂或单位剂型的组合的施用,组合的个别试剂同时但分离的施用,或组合的个别试剂通过任何合适途径序贯施用。组合的个别试剂的剂量可以要求与组合中的其他试剂相比较,试剂之一的更频繁施用。因此,为了允许合适给药,包装的药物产品可以包含含有试剂的组合的一种或多种剂型,和含有试剂组合之一的一种或多种剂型,而不是组合的一种或多种其他试剂。
试剂可以含有一个或多个不对称元件,例如产立体(stereogenic)中心或产立体轴,例如不对称碳原子,从而使得化合物可以以不同立体异构形式存在。这些化合物可以是例如外消旋物或光学活性形式。对于具有两个或更多个不对称元件的化合物,这些化合物可以另外是非对映体的混合物。对于具有不对称中心的化合物,应当理解包含所有光学异构体及其混合物。另外,具有碳-碳双键的化合物可以以Z-和E-形式出现;化合物的所有异构形式包括在本发明中。在这些情况下,单一对映体(光学活性形式)可以通过不对称合成、来自光学纯的前体的合成或通过外消旋物的拆分获得。外消旋物的拆分还可以例如通过常规方法完成,例如在拆分剂的存在下结晶,或使用例如手性HPLC柱的层析。
除非上下文另有说明或明确指示,提及在本发明的组合疗法中有用的化合物包括化合物的游离碱和化合物的所有药学可接受的盐。优选的盐是盐酸盐。
术语“药学可接受的盐”包括公开化合物的衍生物,其中母体化合物通过制备其无毒酸或碱加成盐进行修饰,并且进一步指此类化合物和此类盐的药学可接受的溶剂化物,包括水合物。药学可接受的盐的例子包括但不限于碱性残基例如胺的无机或有机酸加成盐;酸性残基例如羧酸的碱性或有机加成盐;等,和包含前述盐中的一种或多种的组合。药学可接受的盐包括例如由无毒无机或有机酸形成的母体化合物的无毒盐和季铵盐。例如,无毒酸盐包括衍生自无机酸例如盐酸、氢溴酸、硫酸、磺酸、磷酸和硝酸的那些;其他可接受的无机盐包括金属盐例如钠盐、钾盐和铯盐;和碱土金属盐例如钙盐和镁盐;和包含前述盐中的一种或多种的组合。
药学可接受的有机盐包括由有机酸制备的盐,例如乙酸、三氟乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、扑酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、甲磺酸、乙磺酸、苯磺酸、磺胺酸、2-乙氧基苯甲酸、延胡索酸、甲苯磺酸、甲磺酸、乙烷二磺酸、草酸、羟乙磺酸、其中n是0-4的HOOC(CH2)nCOOH;有机胺盐例如三乙胺盐、吡啶盐、甲基吡啶盐、乙醇胺盐、三乙醇胺盐、二环己胺盐、N,N'-二苄乙烯二胺盐;和氨基酸盐例如精氨酸盐、天冬氨酸盐和谷氨酸盐,和包含前述盐中的一种或多种的组合。
试剂组合的“有效量”(例如MEK和RAF抑制剂、或RAF和COT抑制剂、或RAF和靶向MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)的抑制剂)是足以提供超过用组合治疗的病症的基线临床可观察的体征和症状的可观察改善的量。
药物产品可以通过口服或其他形式例如经直肠或通过肠胃外注射施用。“口服剂型”意欲包括开处方或预期用于口服施用的单位剂型。口服剂型可以包含或不包含包装用于在单次剂量中施用的多个亚单位,例如微胶囊或微片剂。
药物产品可以以多种形式释放。“可释放形式”意欲包括瞬间释放、立即释放、控制释放和持续释放形式。
“瞬间释放”意欲包括通过修饰活性剂的正常晶型以获得更快速的溶解,设计为确保活性剂的快速溶解的剂型。
“立即释放”意欲包括常规或非修饰的释放形式,其中大于或等于约50%或更优选约75%的活性剂在施用的两小时内,优选在施用的一小时内释放。
“持续释放”或“延长释放”包括活性剂以这样的速率释放,从而使得在施用后至少约8小时、优选至少约12小时、更优选约24小时,血液(例如血浆)水平以稳态维持在治疗范围内,但低于毒性水平。术语“稳态”意指已达到关于给定活性剂或活性剂的组合的血浆水平,并且用一种或多种活性剂的后续剂量维持在处于或超过最低限度有效治疗水平的水平,且低于关于一种或多种给定活性剂的最低限度毒性血浆水平。
术语“治疗”在本文中用于意指减轻、减少或缓和受试者中疾病的至少一种症状。例如,治疗可以是病症的一种或几种症状的减小,或病症例如癌症的完全根除。在本发明的意义内,术语“治疗”还指示停止、延迟疾病的发作(即在疾病的临床表现前的时期)和/或减少发展或恶化疾病的危险。术语“保护”在本文中用于意指预防、延迟或治疗(或合适时,所有)受试者中疾病的发展或持续或加重。在本发明的意义内,疾病与癌症相关联。
术语“受试者”或“患者”预期包括能够患有癌症或任何病症或者受癌症或任何病症折磨的动物,所述病症直接或间接涉及癌症。受试者的例子包括哺乳动物,例如人、犬、牛、马、猪、绵羊、山羊、猫、小鼠、兔、大鼠和转基因非人动物。在特定实施方案中,受试者是人,例如患有癌症、处于患有癌症的危险中或潜在地能够患有癌症的人。
术语“约”或“大约”通常意指在给定值或范围的20%内,更优选在10%内,且最优选仍在5%内。可替代地,尤其在生物学系统中,术语“约”意指在约对数(即数量级)内,优选在给定值的两倍内。
在描述本发明的背景中(尤其是在下述权利要求的背景中),术语“a”和“an”和“the”及相似指示物的使用应理解为涵盖单数和复数,除非本文另有说明或上下文明确指出相反。除非另有说明,术语“包含”、“具有”、“包括”和“含有”应解释为开放式术语(即,意指“包括但不限于”)。在本文中值范围的叙述仅仅预期充当个别涉及属于该范围的每个分开值的速记方法,除非本文另有说明,并且每个分开值引入说明书内,如同它在本文中个别叙述一样。
如上所述,在一个方面,本发明提供了对于下述有用的药物组合:治疗、预防、停止、延迟受试者中的癌症发作和/或减少发展受试者中的癌症的至少一种症状的危险,或逆转受试者中的癌症的至少一种症状,其包括给受试者施用组合疗法,其包含有效量的RAF抑制剂和有效量的MAP3K8(TPL2/COT)抑制剂,或有效量的RAF抑制剂和有效量的MEK抑制剂,或有效量的RAF抑制剂和有效量的靶向MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、 ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3)的第二种抑制剂。优选地,这些抑制剂以治疗有效剂量施用,当组合时,其提供有利效应。施用可以是同时或序贯的。
术语“癌症”在本文中用于意指广谱肿瘤,包括所有实体瘤和血液学恶性肿瘤。此类肿瘤的例子包括但不限于白血病、淋巴瘤、骨髓瘤、癌、转移癌、肉瘤、腺瘤、神经系统癌症和泌尿生殖道(geritourinary)癌症。在示例性实施方案中,前述方法在治疗下述中有用:成人和儿科急性成淋巴细胞性白血病、急性髓样白血病、肾上腺皮质癌、AIDS相关癌症、肛门癌、盲肠癌、星形细胞瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、骨肉瘤、纤维组织细胞瘤、脑癌、脑干神经胶质瘤、小脑星形细胞瘤、恶性神经胶质瘤、室管膜瘤、成髓细胞瘤、幕上原始神经外胚瘤、下丘脑神经胶质瘤、乳腺癌、男性乳腺癌、支气管腺瘤、伯基特淋巴瘤、类癌瘤、原因不明癌、中枢神经系统淋巴瘤、小脑星形细胞瘤、恶性神经胶质瘤、宫颈癌、儿童期癌、慢性淋巴细胞性白血病、慢性髓性白血病、慢性骨髓增殖性病症、结肠直肠癌、皮肤T细胞淋巴瘤、子宫内膜癌、室管膜瘤、食管癌、Ewing家族肿瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、肝外胆管癌、眼内黑素瘤、成视网膜细胞瘤、胆囊癌、胃癌、胃肠道间质瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、卵巢生殖细胞肿瘤、妊娠滋养细胞肿瘤、神经胶质瘤、多毛细胞白血病、头与颈癌、肝细胞癌、何杰金淋巴瘤、非何杰金淋巴瘤、下咽癌、下丘脑和视通路神经胶质瘤、眼内黑素瘤、胰岛细胞肿瘤、卡波济肉瘤、肾癌、肾细胞癌、喉癌、唇和口腔癌、小细胞肺癌、非小细胞肺癌、原发性中枢神经系统淋巴瘤、Waldenstrom巨球蛋白血症(macroglobulinema)、恶性纤维组织细胞瘤、成髓细胞瘤、黑素瘤、Merkel细胞癌、恶性间皮瘤、鳞状颈癌、多发性内分泌肿瘤综合征、多发性骨髓瘤、蕈状真菌病、骨髓增生异常综合征、骨髓增殖性病症、慢性骨髓增殖性病症、鼻腔和鼻旁窦癌、鼻咽癌、成神经细胞瘤、口咽癌、卵巢癌、胰腺癌、甲状旁腺癌、阴茎癌、喉癌、嗜铬细胞瘤、成松果体细胞瘤和幕上原始神经外胚瘤、垂体癌、浆细胞瘤、胸膜肺母细胞瘤、前列腺癌、直肠癌、横纹肌肉瘤、唾液腺癌、软组织肉瘤、子宫肉瘤、Sezary综合征、非黑素瘤皮肤癌、小肠癌、鳞状细胞癌、鳞状颈癌、幕上原始神经外胚瘤、睾丸癌、喉癌、胸腺瘤和胸腺癌、甲状腺癌、移行细胞癌、滋养细胞肿瘤、尿道癌、子宫癌、子宫肉瘤、阴道癌、外阴癌和Wilms肿瘤。
特别地,癌症可以与B-RAF基因中的突变相关联。这些癌症包括黑素瘤、乳腺癌、结肠直肠癌、神经胶质瘤、肺癌、卵巢癌、肉瘤和甲状腺癌。
在特定实施方案中,本文提供的治疗组合对于治疗受试者中的中至重度癌症是有效的。
剂量
用于癌症治疗的试剂组合的最佳剂量可以使用已知方法对于每个受试者凭经验决定,并且将取决于多种因素,包括试剂的活性;受试者的年龄、体重、一般健康、性别和饮食;施用时间和途径;和受试者服用的其他药物。最佳剂量可以使用本领域众所周知的常规测试和程序进行确定。
可以与载体材料组合以产生单一剂型的试剂组合的量将取决于治疗的个体和具体施用方式而改变。在一些实施方案中,含有如本文描述的试剂组合的单位剂型将含有组合的每种试剂的量,所述量一般在试剂单独施用时施用。
具有本领域普通技术的医生或兽医可以容易地决定且开出所需药物组合物的有效量。例如,医生或兽医可以起始在药物组合物中采用的本发明的化合物的剂量,其水平低于为了实现所需疗效需要的那种,且逐步增加剂量直至实现所需效应。
一般而言,本发明的化合物的合适日剂量将是有效产生疗效的最低剂量的化合物量。此类有效剂量一般将取决于上述因素,并且由具有本领域技术的人员容易地决定。
一般地,当用于所示镇痛作用时,本发明的化合物对于患者的治疗有效剂量范围为约0.0001 - 约1000 mg/千克体重/天,更优选约0.01 - 约50 mg/kg/天。
需要时,活性化合物的有效日剂量可以作为在全天以合适间隔分开施用的两个、三个、四个、五个、六个或更多个亚剂量施用,任选地,以单位剂型。
药物剂型和施用途径
本文提供的是包含用于治疗癌症例如黑素瘤的试剂组合的药物制剂。药物制剂可以另外包含载体或赋形剂、稳定剂、调味剂和/或着色剂。
本文提供的是包含试剂组合的药物制剂,所述试剂组合可以是例如两类试剂的组合:(1)RAF抑制剂和/或该抑制剂的药理学活性代谢产物、盐、溶剂化物和外消旋物,和(2)MAP3K8(TPL2/COT)抑制剂和/或COT抑制剂的药理学活性代谢产物、盐、溶剂化物和外消旋物。在另一个实施方案中,可以提供试剂组合用于包含BRAF突变细胞或包含过表达MAP3K8(TPL2/COT)的细胞的受试者,并且包括:(1)RAF抑制剂和/或该抑制剂的药理学活性代谢产物、盐、溶剂化物和外消旋物,和(2)MEK抑制剂和/或MEK抑制剂的药理学活性代谢产物、盐、溶剂化物和外消旋物。
试剂的组合可以使用本领域技术人员已知的多种施用途径进行施用。试剂的组合可以在根据需要含有常规无毒药学可接受的载体、佐剂和媒介物的剂量单位制剂中,口服、肠胃外、舌下、通过气溶胶化或吸入喷雾、经直肠、脑池内、阴道内、腹膜内、经颊或局部施用于人及其他动物。局部施用还可以涉及经皮施用例如经皮贴剂或离子电泳装置的使用。如本文使用的术语肠胃外的包括皮下注射、静脉内、肌内、胸骨内注射或输注技术。
配制方法是本领域众所周知的,并且例如公开于Remington:The Science and Practice of Pharmacy,Mack Publishing Company,Easton,Pa.,第19版(1995)中。用于在本发明中使用的药物组合物可以是无菌、无热原液体溶液或悬液、包被胶囊、栓剂、冻干粉末、经皮贴剂的形式或本领域已知的其他形式。
可注射制备物例如无菌可注射的水性或油性悬液可以使用合适的分散或湿润剂和悬浮剂根据已知技术进行配制。无菌可注射的制备物还可以是在无毒的肠胃外可接受的稀释剂或溶剂中的无菌可注射溶液、悬液或乳状液,例如作为溶于1,3丙二醇或1,3丁二醇的溶液。在可以采用的可接受的媒介物和溶剂中的是水、林格氏溶液、U.S.P.和等渗氯化钠溶液。另外,无菌不挥发性油照常规用作溶剂或悬浮介质。为了这个目的,可以采用任何温和的不挥发性油,包括合成甘油单酯或甘油二酯。另外,脂肪酸例如油酸在可注射物的制备中有用。可注射制剂可以是例如通过经由细菌保留滤器过滤,或通过以无菌固体组合物的形式掺入灭菌剂进行灭菌,所述无菌固体组合物可以在使用前溶解于或分散于无菌水或其他无菌可注射介质中。
为了延长药物的效应,通常希望减慢来自皮下或肌内注射的药物吸收。这可以通过使用具有弱水溶性的结晶或无定形材料的液体悬液完成。药物的吸收速率随后取决于其溶解速率,溶解速率又可以取决于晶体大小和晶型。可替代地,肠胃外施用的药物形式的延迟吸收可以通过将药物溶解于或悬浮于油媒介物中完成。可注射贮库形式通过在生物可降解的聚合物例如聚交酯聚乙醇酸交酯中形成药物的微胶囊基质进行制备。取决于药物与聚合物的比和采用的具体聚合物的性质,可以控制药物释放的速率。其他生物可降解聚合物的例子包括聚(原酸酯)和聚(酐)。贮库可注射制剂还可以通过将药物诱陷入与身体组织相容的脂质体或微乳液中进行制备。
用于直肠或阴道施用的组合物优选是栓剂,其可以通过将本发明的化合物与合适的非刺激性赋形剂或载体例如可可脂、聚乙二醇或栓剂蜡混合进行制备,其在环境温度是固体的但在体温是液体的,并且因此在直肠或阴道腔中融化且释放活性化合物。
用于口服施用的固体剂型包括胶囊、片剂、丸剂、粉末和颗粒剂。在此类固体剂型中,将活性化合物与至少一种惰性、药学可接受的赋形剂或载体混合,例如柠檬酸钠或磷酸二钙和/或a)填充剂或增量剂,例如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸,b)粘合剂例如羧甲基纤维素、海藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和阿拉伯胶,c)保湿剂例如甘油,d)崩解剂例如琼脂-琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、特定硅酸盐和碳酸钠,e)溶解阻滞剂例如石蜡,f)吸收加速剂例如季铵化合物,g)湿润剂例如乙酰基醇和单硬脂酸甘油酯,h)吸收剂例如高岭土和膨润土,和i)润滑剂例如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠及其混合物。在胶囊、片剂和丸剂的情况下,剂型还可以包含缓冲剂。
相似类型的固体组合物还可以用作软和硬填充明胶胶囊中的填充剂,使用此类赋形剂如乳糖(lactose)或乳糖(milk sugar)以及高分子量聚乙二醇等。
片剂、锭剂、胶囊、丸剂和颗粒剂的固体剂型可以用包衣和壳例如肠包衣和药物配制领域中众所周知的其他包衣进行制备。它们可以任选含有遮光剂,并且还可以是仅或优先在肠道的特定部分中任选以延迟方式释放一种或多种活性成分的组合物。可以使用的包埋组合物的例子包括聚合物质和蜡。
活性化合物还可以是具有如上所述的一种或多种赋形剂的微胶囊化形式。片剂、锭剂、胶囊、丸剂和颗粒剂的固体剂型可以用包衣和壳例如肠包衣、释放控制包衣和药物配制领域中众所周知的其他包衣进行制备。在此类固体剂型中,活性化合物可以与至少一种惰性稀释剂例如蔗糖、乳糖或淀粉混合。如通常实践一样,此类剂型还可以包含除惰性稀释剂外的另外物质,例如压片润滑剂及其他压片助剂例如硬脂酸镁和微晶纤维素。在胶囊、片剂和丸剂的情况下,剂型还可以包含缓冲剂。它们可以任选含有遮光剂,并且还可以是仅或优先在肠道的特定部分中任选以延迟方式释放一种或多种活性成分的组合物。可以使用的包埋组合物的例子包括聚合物质和蜡。
用于口服施用的液体剂型包括药学可接受的乳状液、微乳液、溶液、悬液、糖浆剂和酏剂。除了活性化合物外,液体剂型可以含有本领域中常用的惰性稀释剂,例如水或其他溶剂、增溶剂和乳化剂,例如乙醇、异丙醇、碳酸乙酯、EtOAc、苯甲醇、苯甲酸苄酯、丙二醇、1,3丁二醇、二甲基甲酰胺、油(特别是棉籽、花生、玉米、胚、橄榄、蓖麻和芝麻油)、甘油、四氢糠醇、聚乙二醇和脱水山梨糖醇的脂肪酸酯、及其混合物。除了惰性稀释剂外,口服组合物还可以包括佐剂例如湿润剂、乳化剂和悬浮剂、增甜剂、调味剂和芳香剂。
用于本发明的化合物的局部或经皮施用的剂型包括软膏、糊剂、乳膏剂、洗剂、凝胶、粉末、溶液、喷雾剂、吸入剂或贴片。活性组分在无菌条件下与药学可接受的载体混合,并且可能需要任何所需的防腐剂或缓冲剂。眼制剂、滴耳剂等也考虑在本发明的范围内。
除了本发明的活性化合物外,软膏、糊剂、乳膏剂和凝胶还可以含有赋形剂例如动物和植物脂肪、油、蜡、石蜡、淀粉、西黄蓍胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、硅酸、滑石和氧化锌、或其混合物。
本发明的组合物还可以配制用于作为液体气溶胶或可吸入干粉递送。液体气溶胶制剂可以占优势地喷雾成粒子大小,其可以递送至末端和呼吸细支气管。
本发明的气溶胶化制剂可以使用气溶胶形成装置例如喷嘴、振动多孔板或超声波喷雾器进行递送,优选选择为允许形成具有占优势地在1 - 5 μm之间的质量介质平均直径的气溶胶粒子。进一步地,制剂优选具有平衡的摩尔渗透压浓度离子强度和氯化物浓度,并且能够将本发明的化合物的有效剂量递送至感染部位的最小可气溶胶化体积。另外,气溶胶化制剂优选不负面损害气道的功能性,并且不引起不希望的副作用。
适合于本发明的气溶胶制剂施用的气溶胶化装置包括例如喷嘴、振动多孔板、超声波喷雾器和供能干粉吸入器,其能够将本发明的制剂喷雾成占优势地在1 5 m的大小范围中的气溶胶粒子大小。在本申请中占优势地意指所有生成的气溶胶粒子的至少70%但优选超过90%在1 5 m范围中。喷射喷雾器通过气压起作用,以将液体溶液破坏成气溶胶小滴。振动多孔板喷雾器通过使用由快速振动多孔板产生的声波真空起作用,以通过多孔板挤出溶剂小滴。超声波喷雾器通过将液体剪切成小气溶胶小滴的压电晶体起作用。多种合适的装置是可获得的,包括例如AERONEB和AERODOSE振动多孔板喷雾器(AeroGen,Inc.,Sunnyvale,California)、SIDESTREAM喷雾器(Medic Aid Ltd.,West Sussex,England)、PARI LC和PARI LC STAR喷射喷雾器(Pari Respiratory Equipment,Inc.,Richmond,Virginia)、以及AEROSONIC(DeVilbiss Medizinische Produkte(Deutschland)GmbH,Heiden,Germany)和ULTRAAIRE(Omron Healthcare,Inc.,Vernon Hills,Illinois)超声波喷雾器。
本发明的化合物还可以配制用于用作局部粉末和喷雾剂,除了本发明的化合物外,其还可以含有赋形剂例如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末,或这些物质的混合物。喷雾剂可以另外含有惯常推进剂例如氯氟烃。
经皮贴剂具有提供化合物对于身体的控制递送的附加优点。此类剂型可以通过将化合物溶解于或分散于合适介质中进行制备。吸收增强剂还可以用于增加化合物跨越皮肤的流量。可以通过提供速率控制膜或通过在聚合物基质或凝胶中分散化合物来控制速率。本发明的化合物还可以以脂质体的形式施用。如本领域已知的,脂质体一般由磷脂或其他脂质物质递送。脂质体通过分散于水性介质中的单或多层水合液晶形成。可以使用能够形成脂质体的任何无毒、生理学可接受和可代谢脂质。除了本发明的化合物外,以脂质体形式的呈现的组合物还可以含有稳定剂、防腐剂、赋形剂等。优选脂质是天然和合成的磷脂和磷脂酰胆碱(卵磷脂)。形成脂质体的方法是本领域已知的。参见例如,Prescott(编辑),"Methods in Cell Biology," 第XIV卷,Academic Press,New York,1976,第33页以及下列等等。
实施例
实施例1:基于ORF的功能筛选鉴定特异性激酶作为对于B-RAF抑制的抗性的驱动器
为了鉴定能够防止RAF抑制的激酶,装配597个序列验证的激酶ORFs克隆,代表注释的激酶的~75%(Center for Cancer Systems Biology(CCSB)/Broad Institute激酶ORF Collection),并且可以在A375中稳定表达,所述A375是对RAF激酶抑制剂PLX4720敏感的B-RAFV600E恶性黑素瘤细胞系(Tsai,J.等人Proc. Natl Acad. Sci. USA 105,3041–3046(2008))(图1a,1b,表3,图6c)。用1 μM PLX4720处理的ORF表达细胞就相对于未处理细胞的生存进行筛选,并且针对测定特异性阳性对照MEK1S218/222D(MEK1DD)进行标准化(Emery,C. M.等人Proc. Natl Acad. Sci. USA 106,20411–20416(2009)。)(表4且概括于图5中)。九个ORFs赋予在超过距平均值的两个标准差水平的抗性(图1b和表4),并且选择用于后续分析(图7)。九个候选ORFs中的三个是受体酪氨酸激酶,强调这类激酶衔接抗性途径的潜力。验证抗性效应且在B‐RAFV600E细胞系A375和SKMEL28中跨越多点PLX4720药物浓度标度区分优先次序。Ser/Thr MAP激酶激酶激酶(MAP3Ks)MAP3K8(COT/Tpl2)和RAF1(C‐RAF)作为在前(top)候选物自两个细胞系出现;这些ORFs将PLX4720 GI50转变10‐600倍,而不影响生存(表5以及图8和9)。CRKL,将PLX4720 GI50转变至更少程度的ORF(在SKMEL28细胞中9.7倍;图8),编码由酪氨酸激酶例如BCR-ABL磷酸化的衔接蛋白(Birge,R.B.等人,Cell Commun Signal 7,13(2009)),但缺乏固有的激酶活性。COT和C‐RAF减少多重B‐RAFV600E细胞系中对于PLX4720的敏感性(图1c),赋予这些激酶介导对于RAF抑制的抗性的能力。A375和SKMEL28中的二次筛选对跨越多点PLX4720浓度标度的前9个候选ORFs区分优先次序(图1d)。
有利的是,在前两种验证的激酶都是已知在几个背景中活化MEK/ERK信号传导的Ser/Thr MAP激酶激酶激酶(MAP3Ks)。如同B-RAF,C-RAF是规范MAPK级联中的MAP3K(McKay,M.M.和Morrison,D.K. Oncogene 26,3113‐3121(2007)),其先前牵涉与使用泛RAF抑制剂的体外逐步选择结合的抗性(Montagut,C.等人Cancer Res 68,4853-4861(2008))。COT(人MAP3K8基因的蛋白质产物)最佳表征为炎症细胞(Banerjee,A.等人,Proc Natl Acad Sci U.S.A. 103,3274‐3279(2006))中的NFKB信号传导下游的MAP3K(Salmeron,A.等人EMBO J 15,817‐826(1996));然而,先前仍未阐明它在人癌症中的功能重要性。
实施例2:经由MAPK途径活化对于B-RAF抑制的抗性。
还测试了这些基因的过表达是否足以活化MAPK途径。在基线时,COT表达以与MEK1DD类似的方式增加ERK磷酸化,与MAP激酶途径活化一致(图2a和10)。野生型COT或C‐RAF的过表达导致在PLX4720的存在下ERK和MEK的组成性磷酸化,而激酶死亡的衍生物没有作用(图2a和11)。因此,COT和C‐RAF占优势地通过MAPK信号传导的再活化来驱动对于RAF抑制的抗性。值得注意的是,在来自最初筛选的九个候选物ORFs中,子集(3)未显示在RAF抑制后的持续ERK/MEK磷酸化,暗示药物敏感性的MAPK途径不依赖性改变(图12)。
实施例3:C-RAF活化和与B-RAF的异源二聚化。
C-RAF活化和与B-RAF的异源二聚化构成对于B‐RAF抑制的细胞应答的关键组分。在A375细胞中,内源C‐RAF:B‐RAF异源二聚体在用PLX4720处理后是可测量和可诱导的(图13)。然而,在S338处的内源C‐RAF磷酸化—C‐RAF活化所需的事件—保持为低的(图13)。相比之下,异位表达的C‐RAF在S338上是磷酸化的(图13),并且它的PLX4720抗性表型与持续MEK/ERK活化结合(图2a和13)。此外,高活性C‐RAF平截突变体(C‐RAF(W22)的异位表达在介导PLX4720抗性和ERK活化中比野生型C‐RAF更有效(图14),进一步指示升高的C‐RAF活性指导对于这种试剂的抗性。与这种模型一致,NRAS和KRAS的致癌等位基因赋予在A375细胞中的PLX4720抗性(图2b),并且在药物治疗的背景中获得持续的C‐RAF(S338)和ERK磷酸化(图2c)。因此,尽管引起C‐RAF活化的遗传改变(例如致癌RAS突变)趋于显示与B‐RAFV600E突变的相互排斥性,但此类共同出现的事件在对于B‐RAF抑制的获得活性背景中是有利的。
实施例4:在黑素瘤中COT表达的研究
虽然C-RAF先前已与黑素瘤和MAPK途径依赖性联系(Montagut,C.等人2008;Karreth,F.A.,DeNicola,G.M.等人,2009;Dumaz,N.等人Cancer Res 66,9483‐9491(2006); Hatzivassiliou,G.等人Nature(2010);Heidorn,S.J.等人,Cell 140,209-221(2010);Poulikakos,P.I.等人,Nature(2010)),但COT也已描述为黑素瘤相关激酶。
研究COT在黑素瘤中的作用,并且检查其在人黑素细胞中的表达。原代永生化黑素细胞(B‐RAF野生型)表达COT(图2d),尽管异位B-RAFV600E表达减少COT mRNA水平(图15),并且致使COT蛋白质无法检测(图2d)。相反地,虽然异位表达的COT在A375细胞中仅是弱可检测的(图2a,2e),但shRNA介导的内源B‐RAFV600E的缺失引起COT蛋白质水平中的增加,其与B‐RAF敲除的程度相关(图2e)。此外,用PLX4720处理表达COT的A375细胞导致COT蛋白质中的剂量依赖性增加(图2a),而不影响异位COT mRNA水平(图15)。致癌B‐RAF在很大程度上通过改变的蛋白质稳定性来拮抗COT表达(图2a,d,e和15),并且B‐RAF抑制加强在治疗过程期间COT表达细胞的长出。值得注意的是,即使在PLX4720的存在下,单独或组合的C‐RAF和B‐RAF也是COT表达背景中的ERK磷酸化所需的(图2e,2f和图16)。如所示的,COT表达足以以RAF不依赖性方式诱导MAP激酶途径活化。
实施例5:COT表达预测在癌细胞系中对于B-RAF抑制的抗性
测试在B‐RAFV600E背景中表达升高COT的细胞系是否显示出对于PLX4720治疗的从新抗性。为了鉴定此类抗性,在细胞系的实验对象组中筛选与B‐RAFV600E突变一致的MAP3K8/COT拷贝数增益的证据。在已经历拷贝数分析和突变概况分析的534个细胞系中,38个细胞系(7.1%)含有B‐RAFV600E突变。在这个亚组内,两个细胞系—OUMS‐23(结肠癌)和RPMI‐7951(黑素瘤)—还显示跨越MAP3K8/COT基因座的染色体拷贝增益(图3a和17)和强COT蛋白质表达(图3b和18)的证据。还在黑素瘤短期培养物的实验对象组中筛选COT蛋白质表达。这些系之一表达COT:M307,衍生自B-RAFV600E肿瘤的短期培养物,其在最初疾病稳定化后发展对于变构MEK抑制的抗性(图3c)。所有三个细胞系对于PLX4720治疗都是难治性的,显示出在8‐10 μM范围中的GI50值(图3d),并且在B‐RAF抑制的背景中显示持续的ERK磷酸化(图3e,3f)。OUMS‐23和RPMI‐7951是MAPK途径抑制剂首次用于实验的细胞系;因此,这些结果证实COT赋予对于RAF抑制的从头(de novo)抗性(在~10%的B‐RAFV600E黑素瘤中观察到的现象)。
实施例6:在用RAF抑制剂治疗的患者中的COT表达。
通过获得来自具有转移性、B‐RAFV600E黑素瘤的3个患者的活组织检查材料,检查在对于临床RAF抑制剂PLX4032的抗性背景中的COT表达。每个病例由在治疗前和在治疗过程中获得的冻干的、损伤匹配的活组织检查材料组成(“治疗前”和“治疗时”;图3g,表6);另外,一个样品含有来自相同复发肿瘤部位的两个独立活组织检查样品(“复发后”;图3g)。与上文呈现的实验模型一致,定量实时RT‐PCR(qRT/PCR)分析揭示在3个病例的2个中与PLX4032治疗一致的增加的COT mRNA表达。相对于其治疗前和治疗时配对物,COT mRNA水平在复发样品中进一步增加(图3g,患者#1)。另外的、不匹配的复发的恶性黑素瘤活组织检查显示与在RAF抑制剂抗性、COT扩增的细胞系中观察到的水平类似的升高的COT mRNA表达(图19)。这个样品还显示出强MAPK途径活化,以及相对于匹配的正常皮肤或B‐RAFV600E细胞系,B‐RAF、C‐RAF和COT的升高表达(图19)。这个肿瘤的测序研究未揭示在BRAF、NRAS或KRAS中的另外突变(数据未显示)。这些分析提供COT依赖性机制在PLX4032抗性恶性黑素瘤中操作的临床证据。
实施例7:MEK/ERK磷酸化的COT调节
通过将靶向COT的shRNA构建体引入RPMI‐7951细胞内,测试COT是否主动调节具有天然升高COT表达的B‐RAFV600E细胞中的MEK/ERK磷酸化。COT的缺失抑制RPMI‐7951生存(图20)和减少ERK磷酸化(图3h);因此,靶向COT激酶活性压制在具有COT过表达或扩增的癌细胞中的MEK/ERK磷酸化。另外,在B-RAF抑制剂(PLX4720)的存在下的靶向COT激酶活性压制MEK/IRK磷酸化(图3h)。用小分子COT激酶抑制剂处理RPMI‐7951细胞(Wyeth,Abbot compound ID 9549300)(George,D.等人,Bioorg. Med. Chem. Lett. 18,4952–4955(2008);Hirata,K.等人,Biol. Pharm. Bull. 33,133–137(2010);Lee,K. M.等人,Cancer Res. 69,8043–8049(2009))导致MEK和ERK磷酸化的剂量依赖性压制,提供COT促成这些细胞中的MEK/ERK活化的另外证据(图3i)。
实施例8:表达COT的B-RAFV600E细胞系显示出对于变构MEK抑制剂的抗性。
分析表达COT的癌细胞是否仍对在COT或RAF下游的靶的MAPK途径抑制敏感。就对于MEK1/2抑制剂CI‐1040的敏感性查询OUMS‐23和RPMI‐7951细胞系。两个细胞系都是对于MEK抑制难治性的(图4a),并且即使在1 μM CI‐1040也展示持续的ERK磷酸化(图4b)。在A375和SKMEL28细胞中的异位COT表达还赋予对于MEK抑制剂CI‐1040和AZD6244的减少敏感性,暗示单独的COT表达足以诱导这种表型(图4c,4d和21)。类似于用药理学MEK抑制剂观察到的结果,MEK1/2敲除在A375细胞中仅适当地压制COT介导的ERK磷酸化(图22)。这些数据证实COT通过MEK不依赖性和MEK依赖性机制活化ERK。此外,执行使用重组COT和ERK1的体外激酶测定,并且证实重组COT诱导在体外的ERK1的pThr202/Tyr204磷酸化(图22)。因此,COT表达以MEK依赖性方式加强ERK活化。
实施例9:组合的MAPK途径抑制以压制细胞增殖。
如图23中所示,RAF和MEK抑制剂以组合的使用可以克服对于单一试剂的抗性。测试组合的RAF/MEK抑制是否可能防止COT驱动的抗性。在异位COT表达的设置中,即使在10 μM的浓度下,暴露于与PLX470组合的AZD6244或CI‐1040(各1 μM)也比单一试剂PLX4720更有效地减少细胞生长和pERK表达(图4e,4f和23)。这些数据强调这个途径在B‐RAFV600E肿瘤细胞中的重要性,并且证实双重B‐RAF/MEK抑制帮助防止对于RAF抑制剂的抗性。
方法
Center for Cancer Systems Biology(CCSB)/Broad Institute激酶开放读码框集合
装配pDONR-223 Entry载体(Invitrogen)中597个激酶ORFs的文库。在两个方向使用载体特异性引物末端测序个别克隆。弃去与报道序列具有大量偏差的克隆。条目(Entry)克隆和序列经由Addgene(http://www.addgene.org/human_kinases)可获得。激酶ORFs由多个来源装配;337种激酶从ORFeome 5.1集合(http://horfdb.dfci.harvard.edu)中作为单个克隆分离,183种激酶通过逆转录和后续PCR扩增从正常人组织RNA(Ambion)中克隆,以增加Gateway序列(Invitrogen),64种激酶从由Harvard Institute of Proteomics(HIP)提供的模板中克隆,并且将13种激酶从得自协作实验室的模板克隆到Gateway系统内。Gateway相容的慢病毒载体pLX-Blast-V5由pLKO.1主链制备。根据制造商的方案(Invitrogen),执行LR Clonase酶促重组反应,以将597种激酶引入pLX-Blast-V5内。
高流通量ORF筛选
将A375黑素瘤细胞在384孔微量滴定板中铺平板(500个细胞/孔)。第二天,细胞在8 ug/ml聚凝胺的存在下用慢病毒包装的激酶ORF文库旋转感染。感染后48小时,将培养基替换为标准生长培养基(2个重复),含有1 μM PLX4720的培养基(2个重复,2个时间点)或含有10 ug/ml杀稻瘟菌素的培养基(2个重复)。在四天和6天后,根据制造商说明书,使用Cell Titer‐Glo(Promega)测定细胞生长。将整个实验执行两次。
候选物抗性ORFs的鉴定
将原始发光值输入Microsoft Excel内。相对于未选择的细胞,通过在杀稻瘟菌素选择的细胞中一式两份求平均值原始发光的百分比测定感染效率。从进一步分析中排除具有小于0.70的感染效率的ORFs,连同在一式两份之间具有>15,000原始发光单位的标准差的任何ORF。为了鉴定其表达影响增殖的ORFs,我们经由下文的z-得分和标准分数针对所有对照处理的细胞的平均值和标准差比较个别ORFs的一式两份求平均值的原始发光。
其中x = 给定ORF的平均原始发光,μ= 所有ORFs的平均原始发光,和σ= 所有孔的原始发光的标准差。具有z-得分>+2或<‐2的任何个别ORF注释为影响增殖且从最后分析中去除。相对于未处理的细胞,通过在PLX4720(1 μM)处理的细胞中一式两份求平均值的原始发光值的百分比测定差异增殖。随后,差异增殖针对用于PLX4720抗性的阳性对照MEK1S218/222D(MEK1DD)进行标准化,其中MEK1DD差异增殖 = 1.0。对于每个个别ORF,MEK1DD标准化的差异增殖跨越两次一式两份实验求平均值,其中每个实验具有两个时间点(第4天和第6天)。随后如上所述对于平均MEK1DD标准化的差异增殖生成z-得分。具有z得分>2的ORFs视为命中,并且在二次筛选中继续。
ORF和shRNA表达
由pLX‐Blast‐V5(慢病毒)或pWZL‐Blast、pBABE‐Puro或pBABE‐博莱霉素(zeocin)(逆转录病毒)表达质粒表达ORFs。对于慢病毒转导,使用6 μl Fugene6转染试剂(Roche),用1 μg pLX‐Blast‐V5‐ORF或pLKO.1‐shRNA、900 ng Δ8.9(gag、pol)和100 ng VSV‐G转染293T细胞。转染后72小时收获病毒上清液。在5 μg/ml聚凝胺的存在下,在6孔板中以1:10‐1:20的病毒稀释度感染哺乳动物细胞,并且以2250 RPM在37℃离心1小时。在感染后二十四小时,加入杀稻瘟菌素(pLX‐Blast‐V5,10 μg/ml)或puro(pLKO.1,0.75 μg/ml),并且将细胞选择48小时。对于逆转录病毒生产,如上所述,用1 μg逆转录病毒质粒-ORF、1 μg pCL‐AMPHO和100 ng VSV‐G转染293T。用含逆转录病毒的上清液以1:2稀释度在5 μg/ml聚凝胺中感染细胞过夜,随后将培养基更换为生长培养基。将感染再一次重复(总共两次),随后为上文的选择。
二次筛选
将A375(1.5 x 103)和SKMEL28细胞(3 x 103)种植到96孔板中18小时。在8 μg/ml聚凝胺的存在下,将表达ORF的慢病毒以1:10稀释度加入,并且在2250 RPM和37℃离心1小时。在离心后,将含病毒培养基更换为正常生长培养基,并且允许温育18小时。在感染后二十四小时,加入DMSO(1:1000)或10x PLX4720(溶于DMSO中)至100、10、1、0.1、0.01、0.001、0.0001或0.00001 μM的终浓度。根据制造商建议,在PLX4720加入后4天,使用WST‐1(Roche)测定细胞生存。
细胞系和试剂
A375、SKMEL28、SKMEL30、COLO‐679、WM451lu、SKMEL5、Malme 3M、SKMEL30、WM3627、WM1976、WM3163、WM3130、WM3629、WM3453、WM3682和WM3702都在RPMI(Cellgro)、10% FBS和1%青霉素/链霉素中生长。M307在补充有1 mM丙酮酸钠的RPMI(Cellgro)、10% FBS和1%青霉素/链霉素中生长。293T和OUMS‐23在DMEM(Cellgro)、10% FBS和1%青霉素/链霉素中生长。RPMI‐7951细胞(ATCC)在MEM(Cellgro)、10% FBS和1%青霉素/链霉素中生长。野生型原代黑素细胞在HAM’s F10(Cellgro)、10% FBS和1%青霉素/链霉素中生长。表达B‐RAFV600E的原代黑素细胞在TIVA培养基[Ham’s F‐10(Cellgro)、7% FBS、1%青霉素/链霉素、2mM 谷氨酰胺(Cellgro)、100 uM IBMX、50 ng/ml TPA、1mM dbcAMP(Sigma)和1 μM钒酸钠]中生长。CI‐1040(PubChem ID:6918454)购自Shanghai Lechen International Trading Co.,AZD6244(PubChem ID:10127622)购自Selleck Chemicals,并且PLX4720(PubChem ID:24180719)购自Symansis。RAF265(PubChem ID:11656518)是来自Novartis Pharma AG的慷慨赠予。除非另有说明,所有药物处理都是共16小时。NRAS和KRAS的活化等位基因先前已描述。(Boehm,J. S.等人Cell 129,1065–1079(2007);Lundberg,A. S.等人Oncogene 21,4577–4586(2002))。
药理学生长抑制测定
对于所有黑素瘤细胞系,将培养细胞种植到96孔板(3,000个细胞/孔)内;对于A375种植1,500个细胞。在种植后二十四小时,将在DMSO中制备的有关化合物的系列稀释物加入细胞中,获得范围为100 μM - 1 x 105 μM的最终药物浓度,其中DMSO的最终体积不超过1%。在药物加入后将细胞温育96小时。使用WST1生存测定(Roche)测量细胞生存。将生存计算为在本底扣除后对照(未处理细胞)的百分比。对于每个细胞系和药物组合执行最低限度六次重复。使用与S形剂量应答的非线性回归曲线拟合,建模来自生长抑制测定的数据。使用用于Windows的GraphPad Prism 5(GraphPad),展示这些曲线并且生成GI50。跨越在或超过10 μM的50%抑制点的S形应答曲线具有注释为>10 μM的GI50值。对于单次剂量研究,遵循等同方案,使用所示药物的单次剂量(1 μM,除非另有说明)。
免疫印迹和免疫沉淀
将细胞用冰冷的PBS洗涤两次,并且用含有2x蛋白酶抑制剂(Roche)以及1x磷酸酶抑制剂混合物(Cocktails)I和II(CalBioChem)的1% NP‐40缓冲液[150 mM NaCl、50 mM Tris pH 7.5、2 mM EDTA pH 8、25 mM NaF和1% NP‐40]裂解。将裂解产物定量(Bradford测定),标准化,还原,变性(95℃)并且通过在10% Tris/甘氨酸凝胶(Invitrogen)上的SDS凝胶电泳解析。将蛋白质转移至PVDF膜,并且用识别下述的初次抗体探测:pERK1/2(T202/Y204)、pMEK1/2(S217/221)、MEK1/2、MEK1、MEK2、C‐RAF(兔宿主)、pC‐RAF(pS338)(Cell Signaling Technology;1:1,000)、V5‐HRP(Invitrogen;(1:5,000)、COT(1:500)、B‐RAF(1:2,000)、肌动蛋白(1:1,000)、肌动蛋白‐HRP(1:1,000;Santa Cruz))、C‐RAF(小鼠宿主;1:1,000;BD Transduction Labs)、纽蛋白(Sigma;1:20,000)、AXL(1:500;R&D Systems)。在与合适的二次抗体(抗兔、抗小鼠IgG,HRP连接的;1:1,000稀释度,Cell Signaling Technology,或抗山羊IgG、HRP连接的;1:1,000稀释度;Santa Cruz)温育后,使用化学发光(Pierce)检测蛋白质。如上所述,免疫沉淀在4℃在1% NP‐40裂解缓冲液中以1 μg/μl总蛋白的浓度执行过夜,使用识别C‐RAF的抗体(1:50;Cell Signaling Technology)。抗体:抗原复合物与蛋白A琼脂糖(25 μL、50%浆;Pierce)在4℃结合2小时。将珠离心,并且在裂解缓冲液中洗涤三次,并且在2x还原样品缓冲液(Invitrogen)中洗脱且变性(95℃)。如上执行免疫印迹。使用NIH Image J执行磷蛋白定量。
如上通过在含有蛋白酶和磷酸酶抑制剂的RIPA [50 mM Tris(pH 7.4)、150 mM NaCl、1mM EDTA、0.1% SDS、1.0% NaDOC、1.0% Triton X‐100、25 mM NaF、1mM NA3VO4]中的组织机械匀浆化,生成来自肿瘤和匹配的正常皮肤的裂解产物。如上执行后续标准化和免疫印迹。
活组织检查的黑素瘤肿瘤材料
活组织检查的肿瘤材料由弃去和去鉴定的(de‐identified)组织组成,其伴随知情同意书获得并且在方案02‐017(配对样品,Massachusetts General Hospital)和07‐087(未配对样品,Dana‐Farber Cancer Institute)下表征。对于配对样品,在PLX4032治疗开始后10‐14天收集‘治疗时’样品(表6)。
COT激酶活性的抑制
将贴壁RPMI‐7951细胞用1x PBS洗涤两次,并且在无血清生长培养基中温育过夜。随后将以所示浓度悬浮于DMSO中的4-(3-氯-4-氟苯氨基)-6-(嘧啶-3-基-甲氨基)-3-氰基-[1,7]- 二氮杂萘(EMD;TPL2抑制剂I;目录#:616373,PubChem ID:9549300)加入细胞中1小时,这之后如上所述进行蛋白质提取。
定量RT-PCR
使用RNeasy试剂盒(Qiagen)从细胞系和新鲜冷冻的肿瘤中提取mRNA。对于细胞系和未配对的肿瘤样品,使用SuperScript III First‐Strand Synthesis SuperMix(Invitrogen),并且对于配对的冷冻肿瘤样品,使用SuperScript VILO cDNA合成试剂盒(Invitrogen),将总mRNA用于后续逆转录。5 μl RT反应用于定量PCR,使用SYBR Green PCR Master Mix和基因特异性引物,一式三份,使用ABI 7300 Real Time PCR System。用于检测的引物如下:
| 引物 | 序列 | SEQ.ID. NO. |
| COT正向 | CAAGTGAAGAGCCAGCAGTTT | SEQ. ID.NO:1 |
| COT反向 | GCAAGCAAATCCTCCACAGTTC | SEQ. ID.NO:2 |
| TBP正向 | CCCGAAACGCCGAATATAATCC | SEQ. ID.NO:3 |
| TBP反向 | GACTGTTCTTCACTCTTGGCTC | SEQ. ID.NO:4 |
| GAPDH正向 | CATCATCTCTGCCCCCTCT | SEQ. ID.NO:5 |
| GAPDH反向 | GGTGCTAAGCAGTTGGTGGT | SEQ. ID.NO:6 |
体外激酶测定
使用各1 μg COT(氨基酸30‐ 397,R&D Systems)和失活的ERK1(Millipore),如前所述执行体外激酶测定。
细胞生存测定
如上所述用表达针对COT或萤光素酶的shRNAs的病毒感染贴壁RPMI‐7951细胞。在选择后,将细胞一式四份地铺平板(1.5x105细胞/孔)到24孔板上。根据制造商的说明书,使用VI‐CELL Cell Viability Analyzer,经由台盼蓝排除计数活细胞。将一式四份的细胞计数求平均值,并且相对于对照shRNA的那种标准化。
癌细胞系百科全书(Cancer Cell Line Encyclopedia)(CCLE)
癌细胞系百科全书(CCLE)计划是在Broad Institute,the Novartis Institutes for Biomedical Research(NIBR)和Genomics Institute of the Novartis Research Foundation(GNF)之间的协作,以进行人癌症模型的大实验对象组的详细遗传和药理学表征,以开发整合的计算分析,其将不同的药理学弱点与基因组模式联系,并且将细胞系整合基因组学转变为癌症患者分层。用于这个研究的染色体拷贝数和基因表达数据是可在http://www.broadinstitute.org/cgi-bin/cancer/datasets.cgi处在线获得的。
癌细胞系的表达概况分析
使用GeneChip Human Genome U133 Plus 2.0 Affymetrix表达阵列(Affymetrix)进行寡核苷酸微阵列分析。根据Affymetrix方案,将样品转换为标记的、断裂的cDNA用于在表达微阵列上使用。
使用的shRNA构建体(pLKO.1)
用于制备所使用的shRNA构建体的DNA序列如下:
本文提供的定义和公开内容支配且接替引入作为参考的所有其他。尽管本发明已在本文中与其优选实施方案结合描述,但对于本领域技术人员应当理解,可以进行未具体描述的添加、修饰、取代和缺失,而不背离如附加权利要求中定义的本发明的精神和范围。因此预期前述详述应视为举例说明性而不是限制性的,并且应当理解下述权利要求包括所有等价物预期定义本发明的精神和范围。
表3: CCSB/Broad Institute激酶ORF文库描述和ORF分类
缩写: RS/TK(受体丝氨酸/苏氨酸激酶);RTK(受体酪氨酸激酶);NRS/TK(非受体丝氨酸/苏氨酸激酶);NRTK(非受体酪氨酸激酶)
| hGENE | GENE ID | 描述 | 激酶类别 |
| AAK1 | 22848 | AP2结合的激酶1 | 蛋白激酶(NRS/TK) |
| ABL1 | 25 | v-abl Abelson鼠白血病病毒癌基因同系物1 | 蛋白激酶(NRTK) |
| ABL2 | 27 | v-abl Abelson鼠白血病病毒癌基因同系物2(arg,Abelson-相关基因) | 蛋白激酶(NRTK) |
| ACVR1 | 90 | 活化素A受体,I型 | 蛋白激酶(RS/TK) |
| ACVR1B | 91 | 活化素A受体,IB型 | 蛋白激酶(RS/TK) |
| ACVR1C | 130399 | 活化素A受体,IC型 | 蛋白激酶(RS/TK) |
| ACVR2A | 92 | 活化素A受体,II型 | 蛋白激酶(RS/TK) |
| ACVR2B | 93 | 活化素A受体,IIB型 | 蛋白激酶(RS/TK) |
| ACVRL1 | 94 | 活化素A受体II型-样1 | 蛋白激酶(RS/TK) |
| ADCK1 | 57143 | 含aarF结构域激酶1 | 蛋白激酶 |
| ADCK2 | 90956 | 含aarF结构域激酶2 | 蛋白激酶 |
| ADCK4 | 79934 | 含aarF结构域激酶4 | 蛋白激酶 |
| ADPGK | 83440 | ADP依赖性葡糖激酶 | 激酶相关的 |
| ADRBK1 | 156 | 肾上腺素能,β,受体激酶1 | 蛋白激酶(NRS/TK) |
| ADRBK2 | 157 | 肾上腺素能,β,受体激酶2 | 蛋白激酶(NRS/TK) |
| AGK | 55750 | 多底物脂质激酶;MULK | 激酶相关的 |
| AK1 | 203 | 腺苷酸激酶1 | 核苷酸激酶 |
| AK2 | 204 | 腺苷酸激酶2 | 核苷酸激酶 |
| AK3 | 205 | 腺苷酸激酶3 | 核苷酸激酶 |
| AK3L1 | 50808 | 腺苷酸激酶3样1 | 核苷酸激酶 |
| AK7 | 122481 | 腺苷酸激酶7 | 核苷酸激酶 |
| AKT1 | 207 | v-akt鼠胸腺瘤病毒癌基因同系物1 | 蛋白激酶(NRS/TK) |
| AKT3 | 10000 | v-akt鼠胸腺瘤病毒癌基因同系物3(蛋白激酶B,γ) | 蛋白激酶(NRS/TK) |
| ALDH18A1 | 5832 | 醛脱氢酶18家族,成员A1;ALDH18A1 | 激酶相关的 |
| ALK | 238 | 间变性淋巴瘤激酶(Ki-1) | 蛋白激酶(RTK) |
| ALPK1 | 80216 | α-激酶1 | 蛋白激酶(NRS/TK) |
| ALPK2 | 115701 | α-激酶2 | 蛋白激酶(NRS/TK) |
| ALS2CR7 | 65061 | 肌萎缩侧索硬化2(青少年)染色体区,候选物7 | 蛋白激酶(NRS/TK) |
| AMHR2 | 269 | 抗苗勒管激素受体,II型 | 蛋白激酶(RS/TK) |
| ARAF | 369 | v-raf鼠肉瘤3611病毒癌基因同系物1 | 蛋白激酶(NRS/TK) |
| ARSG | 22901 | 芳基硫酸酯酶G;ARSG | 激酶相关的 |
| ASCIZ | 23300 | ATM/ATR-底物Chk2-相互作用Zn2+-指蛋白;ASCIZ | 蛋白激酶(NRS/TK) |
| AURKA | 6790 | 丝氨酸/苏氨酸激酶6 | 蛋白激酶(NRS/TK) |
| AURKB | 9212 | 极光激酶B | 蛋白激酶(NRS/TK) |
| AURKC | 6795 | 极光激酶C | 蛋白激酶(NRS/TK) |
| AXL | 558 | AXL受体酪氨酸激酶 | 蛋白激酶(RTK) |
| BCKDK | 10295 | 支链α-酮酸脱氢酶激酶 | 蛋白激酶 |
| BLK | 640 | B淋巴样酪氨酸激酶 | 蛋白激酶(NRTK) |
| BMP2K | 55589 | BMP2诱导型激酶 | 蛋白激酶(NRS/TK) |
| BMP2KL | 347359 | BMP2诱导型激酶-样 | 蛋白激酶(NRS/TK) |
| BMPR1A | 657 | 骨形态发生蛋白受体,IA型 | 蛋白激酶(RS/TK) |
| BMPR1B | 658 | 骨形态发生蛋白受体,IB型 | 蛋白激酶(RS/TK) |
| BMPR2 | 659 | 骨形态发生蛋白受体,II型(丝氨酸/苏氨酸激酶) | 蛋白激酶(RS/TK) |
| BMX | 660 | BMX非受体酪氨酸激酶 | 蛋白激酶(NRTK) |
| BRAF | 673 | v-raf鼠肉瘤病毒癌基因同系物B1 | 蛋白激酶(NRS/TK) |
| BRD3 | 8019 | 含溴结构域3 | 蛋白激酶(NRS/TK) |
| BRD4 | 23476 | 含溴结构域4 | 蛋白激酶(NRS/TK) |
| BRSK1 | 84446 | KIAA1811蛋白质 | 蛋白激酶(NRS/TK) |
| BRSK2 | 9024 | 丝氨酸/苏氨酸激酶29 | 蛋白激酶(NRS/TK) |
| BTK | 695 | Bruton无丙种球蛋白血症酪氨酸激酶 | 蛋白激酶(NRTK) |
| BUB1 | 699 | 不被苯并咪唑1同系物抑制的BUB1芽殖(酵母) | 蛋白激酶(NRS/TK) |
| BUB1B | 701 | 不被苯并咪唑1同系物β抑制的BUB1芽殖(酵母) | 蛋白激酶(NRS/TK) |
| C1orf57 | 84284 | 染色体1开放读码框57;C1orf57 | 激酶相关的 |
| C9orf95 | 54981 | 染色体9开放读码框95;C9orf95 | 激酶相关的 |
| C9orf98 | 158067 | 染色体9开放读码框98;C9orf98 | 核苷酸激酶 |
| CABC1 | 56997 | 伴侣蛋白,bc1复合物样的ABC1活性(栗酒裂殖酵母(S. pombe)) | 蛋白激酶 |
| CALM1 | 801 | 钙调蛋白1(磷酸化酶激酶,δ) | 激酶相关的 |
| CALM2 | 805 | 钙调蛋白2(磷酸化酶激酶,δ) | 激酶相关的 |
| CALM3 | 808 | 钙调蛋白3(磷酸化酶激酶,δ) | 激酶相关的 |
| CAMK1 | 8536 | 钙/钙调蛋白依赖性蛋白激酶I | 蛋白激酶(NRS/TK) |
| CAMK1D | 57118 | 钙/钙调蛋白依赖性蛋白激酶ID | 蛋白激酶(NRS/TK) |
| CAMK1G | 57172 | 钙/钙调蛋白依赖性蛋白激酶IG | 蛋白激酶(NRS/TK) |
| CAMK2A | 815 | 钙/钙调蛋白依赖性蛋白激酶(CaM激酶)IIα | 蛋白激酶(NRS/TK) |
| CAMK2B | 816 | 钙/钙调蛋白依赖性蛋白激酶(CaM激酶)IIβ | 蛋白激酶(NRS/TK) |
| CAMK2D | 817 | 钙/钙调蛋白依赖性蛋白激酶(CaM激酶)II δ | 蛋白激酶(NRS/TK) |
| CAMK2G | 818 | 钙/钙调蛋白依赖性蛋白激酶(CaM激酶)IIγ | 蛋白激酶(NRS/TK) |
| CAMK4 | 814 | 钙/钙调蛋白依赖性蛋白激酶IV | 蛋白激酶(NRS/TK) |
| CAMKK1 | 84254 | 钙/钙调蛋白依赖性蛋白激酶激酶1,α | 蛋白激酶(NRS/TK) |
| CAMKK2 | 10645 | 钙/钙调蛋白依赖性蛋白激酶激酶2,β | 蛋白激酶(NRS/TK) |
| CAMKV | 79012 | 假定蛋白质MGC8407 | 蛋白激酶(NRS/TK) |
| CARD11 | 84433 | 半胱天冬酶召募结构域家族,成员11;CARD11 | 核苷酸激酶 |
| CARKL | 23729 | 碳水化合物激酶-样 | 碳水化合物激酶 |
| CASK | 8573 | 钙/钙调蛋白依赖性丝氨酸蛋白激酶(MAGUK家族) | 核苷酸激酶 |
| CCL2 | 6347 | 趋化因子(C-C基序)配体2;CCL2 | 蛋白激酶 |
| CCL4 | 6351 | 趋化因子(C-C基序)配体4;CCL4 | 蛋白激酶(RTK) |
| CCRK | 23552 | 细胞周期相关激酶 | 蛋白激酶(NRS/TK) |
| CD2 | 914 | CD2抗原(p50),绵羊红细胞受体;CD2 | 蛋白激酶 |
| CDC2 | 983 | 细胞分裂周期2,G1至S和G2至M | 蛋白激酶(NRS/TK) |
| CDC2L1 | 984 | 细胞分裂周期2-样1(PITSLRE蛋白质) | 蛋白激酶(NRS/TK) |
| CDC2L2 | 985 | 细胞分裂周期2-样2(PITSLRE蛋白质) | 蛋白激酶(NRS/TK) |
| CDC2L6 | 23097 | 细胞分裂周期2-样6(CDK8-样) | 蛋白激酶(NRS/TK) |
| CDC42BPG | 55561 | CDC42结合蛋白激酶γ(DMPK-样) | 蛋白激酶(NRS/TK) |
| CDC7 | 8317 | CDC7 细胞分裂周期7(酿酒酵母(S. cerevisiae)) | 蛋白激酶(NRS/TK) |
| CDK10 | 8558 | 细胞周期蛋白依赖性激酶(CDC2-样)10 | 蛋白激酶(NRS/TK) |
| CDK2 | 1017 | 细胞周期蛋白依赖性激酶2 | 蛋白激酶(NRS/TK) |
| CDK3 | 1018 | 细胞周期蛋白依赖性激酶3 | 蛋白激酶(NRS/TK) |
| CDK4 | 1019 | 细胞周期蛋白依赖性激酶4 | 蛋白激酶(NRS/TK) |
| CDK5 | 1020 | 细胞周期蛋白依赖性激酶5 | 蛋白激酶(NRS/TK) |
| CDK5R1 | 8851 | 细胞周期蛋白依赖性激酶5,调节亚单位1(p35) | 蛋白激酶(NRS/TK) |
| CDK6 | 1021 | 细胞周期蛋白依赖性激酶6 | 蛋白激酶(NRS/TK) |
| CDK7 | 1022 | 细胞周期蛋白依赖性激酶7(MO15同系物,光滑爪蟾(Xenopus laevis),cdk活化激酶) | 蛋白激酶(NRS/TK) |
| CDK8 | 1024 | 细胞周期蛋白依赖性激酶8 | 蛋白激酶(NRS/TK) |
| CDK9 | 1025 | 细胞周期蛋白依赖性激酶9(CDC2相关激酶) | 蛋白激酶(NRS/TK) |
| CDKL1 | 8814 | 细胞周期蛋白依赖性激酶-样1(CDC2相关激酶) | 蛋白激酶(NRS/TK) |
| CDKL2 | 8999 | 细胞周期蛋白依赖性激酶-样2(CDC2相关激酶) | 蛋白激酶(NRS/TK) |
| CDKL3 | 51265 | 细胞周期蛋白依赖性激酶-样3 | 蛋白激酶(NRS/TK) |
| CDKL4 | 344387 | 细胞周期蛋白依赖性激酶-样4 | 蛋白激酶(NRS/TK) |
| CDKL5 | 6792 | 细胞周期蛋白依赖性激酶-样5 | 蛋白激酶(NRS/TK) |
| CHEK1 | 1111 | CHK1检查点同系物(栗酒裂殖酵母) | 蛋白激酶(NRS/TK) |
| CHEK2 | 11200 | CHK2检查点同系物(栗酒裂殖酵母) | 蛋白激酶(NRS/TK) |
| CHKA | 1119 | 胆碱激酶α | 激酶相关的 |
| CIB1 | 10519 | 钙和整联蛋白结合1(calmyrin);CIB1 | 激酶相关的 |
| CIB4 | 130106 | 钙和整联蛋白结合家族成员4;CIB4 | 激酶相关的 |
| CKB | 1152 | 肌酸激酶,脑 | 激酶相关的 |
| CKM | 1158 | 肌酸激酶,肌肉 | 激酶相关的 |
| CKMT1A | 548596 | 肌酸激酶,线粒体1A;CKMT1A | 激酶相关的 |
| CKMT2 | 1160 | 肌酸激酶,线粒体2(肌节(sarcomeric)) | 激酶相关的 |
| CKS1B | 1163 | CDC28蛋白激酶调节亚单位1B | 蛋白激酶 |
| CKS2 | 1164 | CDC28蛋白激酶调节亚单位2 | 蛋白激酶 |
| CLK1 | 1195 | CDC-样激酶1 | 蛋白激酶(NRS/TK) |
| CLK2 | 1196 | CDC-样激酶2 | 蛋白激酶(NRS/TK) |
| CLK3 | 1198 | CDC-样激酶3 | 蛋白激酶(NRS/TK) |
| COASY | 80347 | 辅酶A合酶;COASY | 激酶相关的 |
| COL4A3BP | 10087 | 胶原,IV型,α3(Goodpasture抗原)结合蛋白;COL4A3BP | 蛋白激酶 |
| CRKL | 1399 | v-crk肉瘤病毒CT10癌基因同系物(禽类)-样;CRKL | 激酶相关的 |
| CSF1R | 1436 | 集落刺激因子1受体,以前的McDonough猫肉瘤病毒(v-fms)癌基因同系物 | 蛋白激酶(RTK) |
| CSK | 1445 | c-src酪氨酸激酶 | 蛋白激酶(NRTK) |
| CSNK1A1 | 1452 | 酪蛋白激酶1,α1 | 蛋白激酶(NRS/TK) |
| CSNK1A1L | 122011 | 酪蛋白激酶1,α1-样 | 蛋白激酶(NRS/TK) |
| CSNK1D | 1453 | 酪蛋白激酶1,δ | 蛋白激酶(NRS/TK) |
| CSNK1E | 1454 | 酪蛋白激酶1,ε | 蛋白激酶(NRS/TK) |
| CSNK1G1 | 53944 | 酪蛋白激酶1,γ1 | 蛋白激酶(NRS/TK) |
| CSNK1G2 | 1455 | 酪蛋白激酶1,γ2 | 蛋白激酶(NRS/TK) |
| CSNK1G3 | 1456 | 酪蛋白激酶1,γ3 | 蛋白激酶(NRS/TK) |
| CSNK2A1 | 1457 | 酪蛋白激酶2,α1多肽 | 蛋白激酶(NRS/TK) |
| CSNK2B | 1460 | 酪蛋白激酶2,β多肽 | 蛋白激酶(NRS/TK) |
| DAK | 26007 | 二羟丙酮激酶2同系物(酿酒酵母);DAK | 激酶相关的 |
| DAPK1 | 1612 | 死亡结合的蛋白激酶1 | 蛋白激酶(NRS/TK) |
| DAPK2 | 23604 | 死亡结合的蛋白激酶2 | 蛋白激酶(NRS/TK) |
| DAPK3 | 1613 | 死亡结合的蛋白激酶3 | 蛋白激酶(NRS/TK) |
| DCAKD | 79877 | 含脱磷-CoA激酶结构域;DCAKD | 激酶相关的 |
| DCAMKL2 | 166614 | 假定蛋白质MGC45428 | 蛋白激酶(NRS/TK) |
| DCK | 1633 | 脱磷脱氧胞苷激酶 | 核苷酸激酶 |
| DDR1 | 780 | 盘状结构域受体家族,成员1 | 蛋白激酶(RTK) |
| DDR2 | 4921 | 盘状结构域受体家族,成员2 | 蛋白激酶(RTK) |
| DGKA | 1606 | 二酰甘油激酶,α80kDa | 激酶相关的 |
| DGKB | 1607 | 二酰甘油激酶,β90kDa | 激酶相关的 |
| DGKG | 1608 | 二酰甘油激酶,γ90kDa | 激酶相关的 |
| DGKK | 139189 | 二酰甘油激酶,κ;DGKK | 激酶相关的 |
| DGKZ | 8525 | 二酰甘油激酶,ζ104kDa | 激酶相关的 |
| DGUOK | 1716 | 脱氧鸟苷激酶 | 核苷酸激酶 |
| DKFZp434B1231 | 91156 | eEF1A2结合蛋白;DKFZp434B1231 | 蛋白激酶(NRS/TK) |
| DKFZp761P0423 | 157285 | 假定蛋白质DKFZp761P0423 | 蛋白激酶(RS/TK) |
| DLG1 | 1739 | 盘,大同系物1(果蝇);DLG1 | 核苷酸激酶 |
| DLG3 | 1741 | 盘,大同系物3(神经内分泌-dlg,果蝇);DLG3 | 核苷酸激酶 |
| DTYMK | 1841 | 脱氧胸苷酸激酶(胸苷酸激酶) | 核苷酸激酶 |
| DYRK1A | 1859 | 双重特异性酪氨酸-(Y)-磷酸化调节的激酶1A | 蛋白激酶(NRS/TK) |
| DYRK1B | 9149 | 双重特异性酪氨酸-(Y)-磷酸化调节的激酶1B | 蛋白激酶(NRS/TK) |
| DYRK2 | 8445 | 双重特异性酪氨酸-(Y)-磷酸化调节的激酶2 | 蛋白激酶(NRS/TK) |
| DYRK3 | 8444 | 双重特异性酪氨酸-(Y)-磷酸化调节的激酶3 | 蛋白激酶(NRS/TK) |
| DYRK4 | 8798 | 双重特异性酪氨酸-(Y)-磷酸化调节的激酶4 | 蛋白激酶(NRS/TK) |
| EEF2K | 29904 | 真核生物延伸因子-2激酶 | 蛋白激酶(NRS/TK) |
| EGFR | 1956 | 表皮生长因子受体(成红细胞白血病病毒(v-erb-b)癌基因同系物,禽类) | 蛋白激酶(RTK) |
| EIF2AK1 | 27102 | 血红素调节的起始因子2-α激酶 | 蛋白激酶(NRS/TK) |
| EIF2AK4 | 415116 | 丝氨酸/苏氨酸-蛋白激酶pim-3 | 蛋白激酶(RS/TK) |
| EPHA1 | 2041 | EPH受体A1 | 蛋白激酶(RTK) |
| EPHA2 | 1969 | EPH受体A2 | 蛋白激酶(RTK) |
| EPHA3 | 2042 | EPH受体A3 | 蛋白激酶(RTK) |
| EPHA4 | 2043 | EPH受体A4 | 蛋白激酶(RTK) |
| EPHA6 | 285220 | EPH受体A6 | 蛋白激酶(RTK) |
| EPHB1 | 2047 | EPH受体B1 | 蛋白激酶(RTK) |
| EPHB4 | 2050 | EPH受体B4 | 蛋白激酶(RTK) |
| EPHB6 | 2051 | EPH受体B6 | 蛋白激酶(RTK) |
| ERBB2 | 2064 | v-erb-b2成红细胞白血病病毒癌基因同系物2,神经/成胶质细胞瘤衍生的癌基因同系物(禽类) | 蛋白激酶(RTK) |
| ERBB3 | 2065 | v-erb-b2成红细胞白血病病毒癌基因同系物3(禽类) | 蛋白激酶(RTK) |
| ERBB4 | 2066 | v-erb-a成红细胞白血病病毒癌基因同系物4(禽类) | 蛋白激酶(RTK) |
| ERN1 | 2081 | 内质网至核信号传导1 | 蛋白激酶 |
| ETNK1 | 55500 | 乙醇胺激酶1 | 激酶相关的 |
| ETNK2 | 55224 | 乙醇胺激酶2 | 激酶相关的 |
| EXOSC10 | 5394 | 外来体组分10;EXOSC10 | 蛋白激酶(NRS/TK) |
| FASTK | 10922 | FAST激酶 | 蛋白激酶(NRS/TK) |
| FASTKD1 | 79675 | FAST激酶结构域1;FASTKD1 | 蛋白激酶 |
| FASTKD2 | 22868 | FAST激酶结构域2;FASTKD2 | 蛋白激酶 |
| FASTKD3 | 79072 | FAST激酶结构域3;FASTKD3 | 蛋白激酶 |
| FASTKD5 | 60493 | FAST激酶结构域5;FASTKD5 | 蛋白激酶 |
| FER | 2241 | fer(fps/fes相关的)酪氨酸激酶(磷蛋白NCP94) | 蛋白激酶(NRTK) |
| FES | 2242 | 猫肉瘤癌基因 | 蛋白激酶(NRTK) |
| FGFR1 | 2260 | 成纤维细胞生长因子受体1(fms相关酪氨酸激酶2,Pfeiffer综合征) | 蛋白激酶(RTK) |
| FGFR2 | 2263 | 成纤维细胞生长因子受体2(颅面骨发育不全1,Crouzon、Pfeiffer和Jackson-Weiss综合征) | 蛋白激酶(RTK) |
| FGFR3 | 2261 | 成纤维细胞生长因子受体3(软骨发育不全,致死性侏儒症) | 蛋白激酶(RTK) |
| FGFRL1 | 53834 | 成纤维细胞生长因子 receptor-样1;FGFRL1 | 蛋白激酶(RTK) |
| FGR | 2268 | Gardner-Rasheed猫肉瘤病毒(v-fgr)癌基因同系物 | 蛋白激酶(NRTK) |
| FLJ10986 | 55277 | 假定蛋白质FLJ10986;FLJ10986 | 碳水化合物激酶 |
| FLJ23356 | 84197 | 假定蛋白质FLJ23356 | 蛋白激酶 |
| FLJ25006 | 124923 | 假定蛋白质FLJ25006 | 蛋白激酶(NRS/TK) |
| FLJ40852 | 285962 | 假定蛋白质FLJ40852 | 蛋白激酶 |
| FLT1 | 2321 | fms相关酪氨酸激酶1(血管内皮生长因子/血管通透性因子受体) | 蛋白激酶(RTK) |
| FLT3 | 2322 | fms相关酪氨酸激酶3 | 蛋白激酶(RTK) |
| FLT4 | 2324 | fms相关酪氨酸激酶4 | 蛋白激酶(RTK) |
| FN3K | 64122 | 果糖胺3激酶 | 激酶相关的 |
| FN3KRP | 79672 | 果糖胺-3-激酶相关蛋白质 | 激酶相关的 |
| FRK | 2444 | fyn相关激酶 | 蛋白激酶(NRTK) |
| FUK | 197258 | 岩藻糖激酶 | 激酶相关的 |
| FXN | 2395 | frataxin;FXN | 激酶相关的 |
| FYN | 2534 | 与SRC、FGR、YES有关的FYN癌基因 | 蛋白激酶(NRTK) |
| GALK1 | 2584 | 半乳糖激酶1 | 碳水化合物激酶 |
| GALK2 | 2585 | 半乳糖激酶2 | 碳水化合物激酶 |
| GCK | 2645 | 葡糖激酶(己糖激酶4,年轻起病的成年发病型糖尿病2) | 碳水化合物激酶 |
| GK | 2710 | 甘油激酶 | 碳水化合物激酶 |
| GK2 | 2712 | 甘油激酶2 | 碳水化合物激酶 |
| GK5 | 256356 | 假定蛋白质MGC40579;MGC40579 | 碳水化合物激酶 |
| GLYCTK | 132158 | 甘油酸激酶 | 碳水化合物激酶 |
| GNE | 10020 | 葡糖胺(UDP-N-乙酰基)-2-表异构酶/N-乙酰甘露糖胺激酶 | 碳水化合物激酶 |
| GRK6 | 2870 | G蛋白偶联受体激酶6 | 蛋白激酶(NRS/TK) |
| GRK7 | 131890 | G蛋白偶联受体激酶7 | 蛋白激酶(NRS/TK) |
| GSG2 | 83903 | haspin | 蛋白激酶(RS/TK) |
| GSK3A | 2931 | 糖原合酶激酶3α | 蛋白激酶(NRS/TK) |
| GTF2H1 | 2965 | 通用转录因子IIH,多肽1,62kDa;GTF2H1 | 蛋白激酶(NRS/TK) |
| GUK1 | 2987 | 鸟苷酸激酶1 | 核苷酸激酶 |
| HCK | 3055 | 造血细胞激酶 | 蛋白激酶(NRTK) |
| HIPK1 | 204851 | 同源结构域相互作用蛋白激酶1 | 蛋白激酶(NRS/TK) |
| HIPK2 | 28996 | 同源结构域相互作用蛋白激酶2 | 蛋白激酶(NRS/TK) |
| HIPK3 | 10114 | 同源结构域相互作用蛋白激酶3 | 蛋白激酶(NRS/TK) |
| HIPK4 | 147746 | 同源结构域相互作用蛋白激酶4 | 蛋白激酶(NRS/TK) |
| HK1 | 3098 | 己糖激酶1 | 碳水化合物激酶 |
| HK2 | 3099 | 己糖激酶2 | 碳水化合物激酶 |
| HK3 | 3101 | 己糖激酶3(白细胞) | 碳水化合物激酶 |
| HKDC1 | 80201 | 含己糖激酶结构域1;HKDC1 | 碳水化合物激酶 |
| HSPB8 | 26353 | 热休克22kDa蛋白质8 | 蛋白激酶(NRS/TK) |
| IGF1R | 3480 | 胰岛素-样生长因子1受体 | 蛋白激酶(RTK) |
| IHPK1 | 9807 | 肌醇六磷酸激酶1 | 激酶相关的 |
| IHPK2 | 51447 | 肌醇六磷酸激酶2 | 脂质激酶 |
| IHPK3 | 117283 | 肌醇六磷酸激酶3 | 脂质激酶 |
| IKBKE | 9641 | 在B细胞中的κ轻多肽基因增强子抑制剂,激酶ε | 蛋白激酶(NRS/TK) |
| ILK | 3611 | 整联蛋白连接的激酶 | 蛋白激酶(NRS/TK) |
| INSRR | 3645 | 胰岛素受体相关受体 | 蛋白激酶(RTK) |
| IPMK | 253430 | 肌醇多磷酸多激酶 | 脂质激酶 |
| IPPK | 64768 | 肌醇1,3,4,5,6-戊基磷酸2-激酶;IPPK | 脂质激酶 |
| IRAK2 | 3656 | 白细胞介素-1受体结合激酶2 | 蛋白激酶(RS/TK) |
| IRAK3 | 11213 | 白细胞介素-1受体结合激酶3 | 蛋白激酶(RS/TK) |
| IRAK4 | 51135 | 白细胞介素-1受体结合激酶4 | 蛋白激酶(RS/TK) |
| ITGB1BP3 | 27231 | 整联蛋白β1结合蛋白3;ITGB1BP3 | 激酶相关的 |
| ITK | 3702 | IL2-诱导型T细胞激酶 | 蛋白激酶(NRTK) |
| ITPKB | 3707 | 肌醇1,4,5-三磷酸3-激酶B | 激酶相关的 |
| JAK1 | 3716 | Janus激酶1(蛋白质酪氨酸激酶) | 蛋白激酶(NRTK) |
| JAK2 | 3717 | Janus激酶2(蛋白质酪氨酸激酶) | 蛋白激酶(NRTK) |
| JAK3 | 3718 | Janus激酶3(蛋白质酪氨酸激酶,白细胞) | 蛋白激酶(NRTK) |
| KDR | 3791 | 激酶插入结构域受体(III型受体酪氨酸激酶) | 蛋白激酶(RTK) |
| KHK | 3795 | 己酮糖激酶(果糖激酶) | 碳水化合物激酶 |
| KIAA0999 | 23387 | KIAA0999蛋白质 | 蛋白激酶(RS/TK) |
| KIAA2002 | 79834 | KIAA2002蛋白质 | 蛋白激酶(RS/TK) |
| KSR | 8844 | ras的激酶抑制基因 | 蛋白激酶(NRS/TK) |
| KSR2 | 283455 | Ras-2的激酶抑制基因 | 蛋白激酶(NRS/TK) |
| LATS1 | 9113 | LATS,大肿瘤抑制基因,同系物1(果蝇) | 蛋白激酶(NRS/TK) |
| LATS2 | 26524 | LATS,大肿瘤抑制基因,同系物2(果蝇) | 蛋白激酶(NRS/TK) |
| LCK | 3932 | 淋巴细胞特异性蛋白质酪氨酸激酶 | 蛋白激酶(NRTK) |
| LIMK1 | 3984 | LIM结构域激酶1 | 蛋白激酶(NRS/TK) |
| LIMK2 | 3985 | LIM结构域激酶2 | 蛋白激酶(NRS/TK) |
| LMTK2 | 22853 | 狐猴酪氨酸激酶2 | 蛋白激酶(RTK) |
| LOC220686 | 220686 | 假定蛋白质LOC220686;LOC220686 | 激酶相关的 |
| LOC340156 | 340156 | 假定蛋白质LOC340156 | 蛋白激酶(NRS/TK) |
| LOC340371 | 340371 | 假定蛋白质LOC340371 | 蛋白激酶(NRS/TK) |
| LOC375133 | 375133 | 类似于磷脂酰肌醇4-激酶α | 脂质激酶 |
| LOC388957 | 388957 | 类似于BMP2诱导型激酶 | 蛋白激酶(NRS/TK) |
| LOC389599 | 389599 | 类似于肌萎缩侧索硬化2(青少年)chr.区,候选物2;ILP-相互作用蛋白质ILPIPA | 蛋白激酶 |
| LOC390877 | 390877 | 类似于腺苷酸激酶(EC 2.7.4.3),细胞溶质 – 鲤鱼 | 核苷酸激酶 |
| LOC442075 | 442075 | 类似于丝氨酸/苏氨酸激酶,确定胚胎极性 | 蛋白激酶(NRS/TK) |
| LOC54103 | 54103 | 假定蛋白质LOC54103;LOC54103 | 蛋白激酶(RTK) |
| LOC646505 | 646505 | 类似于双重特异性蛋白激酶CLK3(CDC-样激酶3);未指定的 | 蛋白激酶(NRS/TK) |
| LOC647279 | 647279 | 类似于MAP/微管亲和力调节激酶3;未指定的 | 蛋白激酶(NRS/TK) |
| LOC648152 | 648152 | 类似于共济失调毛细血管扩张症和Rad3相关蛋白质;未指定的 | 蛋白激酶(NRS/TK) |
| LOC649288 | 649288 | 类似于腺苷酸激酶同工酶4,线粒体(腺苷酸激酶3-样1) | 核苷酸激酶 |
| LOC650122 | 650122 | 类似于胆碱激酶α同种型a;未指定的 | 激酶相关的 |
| LOC652722 | 652722 | 类似于PTK2蛋白质酪氨酸激酶2 同种型a;未指定的 | 蛋白激酶(NRTK) |
| LOC652799 | 652799 | 类似于Mast/干细胞生长因子受体前体(SCFR)(c-kit)(CD117抗原);未指定的 | 蛋白激酶(RTK) |
| LOC653052 | 653052 | 类似于同源结构域-相互作用蛋白激酶2(hHIPk2);未指定的 | 蛋白激酶(NRS/TK) |
| LOC653155 | 653155 | 类似于PRP4 mRNA前体加工因子4同系物B;未指定的 | 蛋白激酶(NRS/TK) |
| LOC727761 | 727761 | 类似于脱氧胸苷酸激酶(胸苷酸激酶);未指定的 | 核苷酸激酶 |
| LOC730000 | 730000 | 类似于睾丸特异性丝氨酸激酶6;未指定的 | 蛋白激酶(NRS/TK) |
| LOC732306 | 732306 | 类似于牛痘相关激酶2;未指定的 | 蛋白激酶(NRS/TK) |
| LOC91461 | 91461 | 假定蛋白质BC007901 | 蛋白激酶(NRTK) |
| LOC91807 | 91807 | 肌球蛋白轻链激酶(MLCK) | 蛋白激酶(NRS/TK) |
| LRGUK | 136332 | 含富含亮氨酸的重复单位和鸟苷酸激酶结构域;LRGUK | 核苷酸激酶 |
| LRPPRC | 10128 | 含富含亮氨酸的PPR基序;LRPPRC | 蛋白激酶(RS/TK) |
| LRRK2 | 120892 | 富含亮氨酸的重复单位激酶2 | 蛋白激酶(NRS/TK) |
| LYK5 | 92335 | 蛋白激酶LYK5 | 蛋白激酶 |
| LYN | 4067 | v-yes-1 Yamaguchi肉瘤病毒相关癌基因同系物 | 蛋白激酶(NRTK) |
| MAGI1 | 9223 | 膜结合的鸟苷酸激酶,含WW和PDZ结构域1;MAGI1 | 核苷酸激酶 |
| MAK | 4117 | 男性生殖细胞结合的激酶 | 蛋白激酶(NRS/TK) |
| MAP2K1 | 5604 | 丝裂原活化蛋白激酶激酶1 | 蛋白激酶 |
| MAP2K1IP1 | 8649 | 丝裂原活化蛋白激酶激酶1相互作用蛋白质1 | 蛋白激酶 |
| MAP2K2 | 5605 | 丝裂原活化蛋白激酶激酶2 | 蛋白激酶 |
| MAP2K5 | 5607 | 丝裂原活化蛋白激酶激酶5 | 蛋白激酶 |
| MAP2K6 | 5608 | 丝裂原活化蛋白激酶激酶6 | 蛋白激酶 |
| MAP2K7 | 5609 | 丝裂原活化蛋白激酶激酶7 | 蛋白激酶 |
| MAP3K11 | 4296 | 丝裂原活化蛋白激酶激酶激酶11 | 蛋白激酶(NRS/TK) |
| MAP3K12 | 7786 | 丝裂原活化蛋白激酶激酶激酶12 | 蛋白激酶(NRS/TK) |
| MAP3K14 | 9020 | 丝裂原活化蛋白激酶激酶激酶14 | 蛋白激酶 |
| MAP3K15 | 389840 | FLJ16518蛋白质 | 蛋白激酶 |
| MAP3K2 | 10746 | 丝裂原活化蛋白激酶激酶激酶2 | 蛋白激酶 |
| MAP3K5 | 4217 | 丝裂原活化蛋白激酶激酶激酶5 | 蛋白激酶 |
| MAP3K6 | 9064 | 丝裂原活化蛋白激酶激酶激酶6 | 蛋白激酶 |
| MAP3K7 | 6885 | 丝裂原活化蛋白激酶激酶激酶7 | 蛋白激酶(NRS/TK) |
| MAP3K8 | 1326 | 丝裂原活化蛋白激酶激酶激酶8 | 蛋白激酶 |
| MAP4K1 | 11184 | 丝裂原活化蛋白激酶激酶激酶激酶1 | 蛋白激酶 |
| MAP4K2 | 5871 | 丝裂原活化蛋白激酶激酶激酶激酶2 | 蛋白激酶 |
| MAP4K3 | 8491 | 丝裂原活化蛋白激酶激酶激酶激酶3 | 蛋白激酶 |
| MAP4K4 | 9448 | 丝裂原活化蛋白激酶激酶激酶激酶4 | 蛋白激酶 |
| MAP4K5 | 11183 | 丝裂原活化蛋白激酶激酶激酶激酶5 | 蛋白激酶 |
| MAPK1 | 5594 | 丝裂原活化蛋白激酶1 | 蛋白激酶(NRS/TK) |
| MAPK10 | 5602 | 丝裂原活化蛋白激酶10 | 蛋白激酶(NRS/TK) |
| MAPK12 | 6300 | 丝裂原活化蛋白激酶12 | 蛋白激酶(NRS/TK) |
| MAPK13 | 5603 | 丝裂原活化蛋白激酶13 | 蛋白激酶(NRS/TK) |
| MAPK14 | 1432 | 丝裂原活化蛋白激酶14 | 蛋白激酶(NRS/TK) |
| MAPK15 | 225689 | 细胞外信号调节的激酶8 | 蛋白激酶(NRS/TK) |
| MAPK3 | 5595 | 丝裂原活化蛋白激酶3 | 蛋白激酶(NRS/TK) |
| MAPK4 | 5596 | 丝裂原活化蛋白激酶4 | 蛋白激酶(NRS/TK) |
| MAPK6 | 5597 | 丝裂原活化蛋白激酶6 | 蛋白激酶(NRS/TK) |
| MAPK8 | 5599 | 丝裂原活化蛋白激酶8 | 蛋白激酶(NRS/TK) |
| MAPK9 | 5601 | 丝裂原活化蛋白激酶9 | 蛋白激酶(NRS/TK) |
| MAPKAPK2 | 9261 | 丝裂原活化蛋白激酶活化蛋白激酶2 | 蛋白激酶(NRS/TK) |
| MAPKAPK3 | 7867 | 丝裂原活化蛋白激酶活化蛋白激酶3 | 蛋白激酶(NRS/TK) |
| MAPKAPK5 | 8550 | 丝裂原活化蛋白激酶活化蛋白激酶5 | 蛋白激酶(NRS/TK) |
| MARK2 | 2011 | MAP/微管亲和力调节激酶2 | 蛋白激酶(NRS/TK) |
| MARK3 | 4140 | MAP/微管亲和力调节激酶3 | 蛋白激酶(NRS/TK) |
| MAST1 | 22983 | 微管结合的丝氨酸/苏氨酸激酶1 | 蛋白激酶(NRS/TK) |
| MAST2 | 23139 | 微管结合的丝氨酸/苏氨酸激酶2 | 蛋白激酶(NRS/TK) |
| MASTL | 84930 | 微管结合的丝氨酸/苏氨酸激酶-样 | 蛋白激酶(NRS/TK) |
| MATK | 4145 | 巨核细胞结合的酪氨酸激酶 | 蛋白激酶(NRTK) |
| MERTK | 10461 | c-mer原癌基因酪氨酸激酶 | 蛋白激酶(RTK) |
| MET | 4233 | met原癌基因(肝细胞生长因子受体) | 蛋白激酶(RTK) |
| MGC16169 | 93627 | 假定蛋白质MGC16169 | 蛋白激酶 |
| MGC42105 | 167359 | 假定蛋白质MGC42105 | 蛋白激酶(NRS/TK) |
| MINK1 | 50488 | 畸形/NIK相关激酶 | 蛋白激酶 |
| MKNK1 | 8569 | MAP激酶相互作用丝氨酸/苏氨酸激酶1 | 蛋白激酶(NRS/TK) |
| MKNK2 | 2872 | MAP激酶相互作用丝氨酸/苏氨酸激酶2 | 蛋白激酶(NRS/TK) |
| MORN2 | 378464 | 含MORN重复单位2;MORN2 | 激酶相关的 |
| MOS | 4342 | v-mos莫洛尼鼠肉瘤病毒癌基因同系物 | 蛋白激酶(NRS/TK) |
| MPP1 | 4354 | 膜蛋白,棕榈酰化的1,55kDa;MPP1 | 蛋白激酶 |
| MPP2 | 4355 | 膜蛋白,棕榈酰化的2(MAGUK p55亚家族成员2);MPP2 | 核苷酸激酶 |
| MPP3 | 4356 | 膜蛋白,棕榈酰化的3(MAGUK p55亚家族成员3);MPP3 | 核苷酸激酶 |
| MPP4 | 58538 | 膜蛋白,棕榈酰化的4(MAGUK p55亚家族成员4);MPP4 | 核苷酸激酶 |
| MPP5 | 64398 | 膜蛋白,棕榈酰化的5(MAGUK p55亚家族成员5);MPP5 | 核苷酸激酶 |
| MPP6 | 51678 | 膜蛋白,棕榈酰化的6(MAGUK p55亚家族成员6);MPP6 | 核苷酸激酶 |
| MPP7 | 143098 | 膜蛋白,棕榈酰化的7(MAGUK p55亚家族成员7);MPP7 | 核苷酸激酶 |
| MST1R | 4486 | 巨噬细胞刺激1受体(c-met相关酪氨酸激酶) | 蛋白激酶(RTK) |
| MUSK | 4593 | 肌肉,骨骼肌,受体酪氨酸激酶 | 蛋白激酶(RTK) |
| MVK | 4598 | 甲羟戊酸激酶(甲羟戊酸尿症) | 激酶相关的 |
| MYLK2 | 85366 | 肌球蛋白轻链激酶2,骨骼肌肌肉 | 蛋白激酶(NRS/TK) |
| MYO3B | 140469 | 肌球蛋白IIIB | 蛋白激酶(NRS/TK) |
| NADK | 65220 | NAD激酶 | 激酶相关的 |
| NAGK | 55577 | N-乙酰葡糖胺激酶 | 激酶相关的 |
| NEK10 | 152110 | NIMA(永离有丝分裂基因a)相关激酶10 | 蛋白激酶 |
| NEK11 | 79858 | NIMA(永离有丝分裂基因a)相关激酶11 | 蛋白激酶 |
| NEK2 | 4751 | NIMA(永离有丝分裂基因a)相关激酶2 | 蛋白激酶 |
| NEK3 | 4752 | NIMA(永离有丝分裂基因a)相关激酶3 | 蛋白激酶 |
| NEK4 | 6787 | NIMA(永离有丝分裂基因a)相关激酶4 | 蛋白激酶 |
| NEK5 | 341676 | NIMA(永离有丝分裂基因a)相关激酶5 | 蛋白激酶 |
| NEK6 | 10783 | NIMA(永离有丝分裂基因a)相关激酶6 | 蛋白激酶 |
| NEK7 | 140609 | NIMA(永离有丝分裂基因a)相关激酶7 | 蛋白激酶 |
| NEK8 | 284086 | NIMA(永离有丝分裂基因a)相关激酶8 | 蛋白激酶 |
| NEK9 | 91754 | NIMA(永离有丝分裂基因a)相关激酶9 | 蛋白激酶 |
| NJMU-R1 | 64149 | 蛋白激酶Njmu-R1 | 蛋白激酶 |
| NLK | 51701 | nemo样激酶 | 蛋白激酶(NRS/TK) |
| NME1 | 4830 | 二磷酸核苷激酶1 | 核苷酸激酶 |
| NME1-NME2 | 654364 | NME1-NME2蛋白质;NME1-NME2 | 核苷酸激酶 |
| NME2 | 4831 | 二磷酸核苷激酶2 | 核苷酸激酶 |
| NME3 | 4832 | 二磷酸核苷激酶3 | 核苷酸激酶 |
| NME4 | 4833 | 二磷酸核苷激酶4 | 核苷酸激酶 |
| NME5 | 8382 | 非转移性细胞5,其中表达的蛋白质(二磷酸核苷激酶) | 核苷酸激酶 |
| NME6 | 10201 | 非转移性细胞6,其中表达的蛋白质(二磷酸核苷激酶) | 核苷酸激酶 |
| NME7 | 29922 | 非转移性细胞7,其中表达的蛋白质(二磷酸核苷激酶) | 核苷酸激酶 |
| NPR2 | 4882 | 利钠肽受体B/鸟苷酸环化酶B(心房利钠肽受体B) | 蛋白激酶 |
| NRBP | 29959 | 核受体结合蛋白 | 蛋白激酶(NRS/TK) |
| NTRK1 | 4914 | 神经营养性酪氨酸激酶,受体,1型 | 蛋白激酶(RTK) |
| NTRK2 | 4915 | 神经营养性酪氨酸激酶,受体,2型 | 蛋白激酶(RTK) |
| NTRK3 | 4916 | 神经营养性酪氨酸激酶,受体,3型 | 蛋白激酶(RTK) |
| NUAK2 | 81788 | 大鼠SNF1/AMP活化蛋白激酶的可能直向同源物 | 蛋白激酶(NRS/TK) |
| NUP62 | 23636 | 核孔蛋白62kDa;NUP62 | 蛋白激酶(NRS/TK) |
| NYD-SP25 | 89882 | 蛋白激酶NYD-SP25 | 蛋白激酶 |
| OXSR1 | 9943 | 氧化性应激应答的1 | 蛋白激酶 |
| PAK1 | 5058 | p21/Cdc42/Rac1活化激酶1(STE20同系物,酵母) | 蛋白激酶 |
| PAK2 | 5062 | p21(CDKN1A)活化激酶2 | 蛋白激酶 |
| PAK3 | 5063 | p21(CDKN1A)活化激酶3 | 蛋白激酶 |
| PAK4 | 10298 | p21(CDKN1A)活化激酶4 | 蛋白激酶 |
| PAK6 | 56924 | p21(CDKN1A)活化激酶6 | 蛋白激酶 |
| PAK7 | 57144 | p21(CDKN1A)活化激酶7 | 蛋白激酶 |
| PANK2 | 80025 | 泛酸激酶2(Hallervorden-Spatz综合征) | 激酶相关的 |
| PANK3 | 79646 | 泛酸激酶3 | 激酶相关的 |
| PANK4 | 55229 | 泛酸激酶4 | 激酶相关的 |
| PAPSS1 | 9061 | 3'-磷酸腺苷5'-磷酸硫酸合酶1;PAPSS1 | 激酶相关的 |
| PAPSS2 | 9060 | 3'-磷酸腺苷5'-磷酸硫酸合酶2;PAPSS2 | 激酶相关的 |
| PBK | 55872 | T-LAK细胞起源的蛋白激酶 | 蛋白激酶 |
| PCK2 | 5106 | 磷酸烯醇丙酮酸羧基激酶2(线粒体) | 激酶相关的 |
| PCTK1 | 5127 | PCTAIRE蛋白激酶1 | 蛋白激酶(NRS/TK) |
| PCTK2 | 5128 | PCTAIRE蛋白激酶2 | 蛋白激酶(NRS/TK) |
| PCTK3 | 5129 | PCTAIRE蛋白激酶3 | 蛋白激酶(NRS/TK) |
| PDGFRA | 5156 | 血小板衍生的生长因子受体,α多肽 | 蛋白激酶(RTK) |
| PDGFRB | 5159 | 血小板衍生的生长因子受体,β多肽 | 蛋白激酶(RTK) |
| PDGFRL | 5157 | 血小板衍生的生长因子受体-样;PDGFRL | 蛋白激酶(RTK) |
| PDIK1L | 149420 | PDLIM1相互作用激酶1样 | 蛋白激酶(NRS/TK) |
| PDK1 | 5163 | 丙酮酸脱氢酶激酶,同工酶1 | 蛋白激酶 |
| PDK2 | 5164 | 丙酮酸脱氢酶激酶,同工酶2 | 蛋白激酶 |
| PDK3 | 5165 | 丙酮酸脱氢酶激酶,同工酶3 | 蛋白激酶 |
| PDK4 | 5166 | 丙酮酸脱氢酶激酶,同工酶4 | 蛋白激酶 |
| PDPK1 | 5170 | 3-磷酸肌醇依赖性蛋白激酶-1 | 蛋白激酶 |
| PDXK | 8566 | 吡哆醛(吡哆醇,维生素B6)激酶 | 激酶相关的 |
| PFKFB1 | 5207 | 6-磷酸果糖-2-激酶/果糖-2,6-二磷酸1 | 碳水化合物激酶 |
| PFKFB2 | 5208 | 6-磷酸果糖-2-激酶/果糖-2,6-二磷酸2 | 碳水化合物激酶 |
| PFKFB3 | 5209 | 6-磷酸果糖-2-激酶/果糖-2,6-二磷酸3 | 碳水化合物激酶 |
| PFKL | 5211 | 磷酸果糖激酶,肝 | 碳水化合物激酶 |
| PFKM | 5213 | 磷酸果糖激酶,肌肉 | 碳水化合物激酶 |
| PFKP | 5214 | 磷酸果糖激酶,血小板 | 碳水化合物激酶 |
| PFTK1 | 5218 | PFTAIRE蛋白激酶1 | 蛋白激酶(NRS/TK) |
| PGK1 | 5230 | 磷酸甘油酸激酶1 | 碳水化合物激酶 |
| PGK2 | 5232 | 磷酸甘油酸激酶2 | 碳水化合物激酶 |
| PHKA1 | 5255 | 磷酸化酶激酶,α1(肌肉) | 蛋白激酶(NRS/TK) |
| PHKA2 | 5256 | 磷酸化酶激酶,α2(肝) | 蛋白激酶(NRS/TK) |
| PHKB | 5257 | 磷酸化酶激酶,β | 蛋白激酶(NRS/TK) |
| PHKG1 | 5260 | 磷酸化酶激酶,γ1(肌肉) | 蛋白激酶(NRS/TK) |
| PHKG2 | 5261 | 磷酸化酶激酶,γ2(睾丸) | 蛋白激酶(NRS/TK) |
| PI4K2B | 55300 | 磷脂酰肌醇4-激酶IIβ型 | 脂质激酶 |
| PI4KII | 55361 | 磷脂酰肌醇4-激酶II型 | 脂质激酶 |
| PIK3C2G | 5288 | 磷酸肌醇-3-激酶,2类,γ多肽 | 脂质激酶 |
| PIK3C3 | 5289 | 磷酸肌醇-3-激酶,3类 | 脂质激酶 |
| PIK3CA | 5290 | 磷酸肌醇-3-激酶,催化的,α多肽 | 脂质激酶 |
| PIK3CBP | 5291 | 磷酸肌醇-3-激酶,催化的,β多肽 | 脂质激酶 |
| PIK3CG | 5294 | 磷酸肌醇-3-激酶,催化的,γ多肽 | 脂质激酶 |
| PIK3R1 | 5295 | 磷酸肌醇-3-激酶,调节亚单位1(p85α) | 脂质激酶 |
| PIK3R3 | 8503 | 磷酸肌醇-3-激酶,调节亚单位3(p55,γ) | 脂质激酶 |
| PIK3R4 | 30849 | 磷酸肌醇-3-激酶,调节亚单位4,p150 | 脂质激酶 |
| PIK3R5 | 23533 | 磷酸肌醇-3-激酶,调节亚单位5,p101 | 脂质激酶 |
| PIK4CA | 5297 | 磷脂酰肌醇4-激酶,催化的,α多肽 | 脂质激酶 |
| PIK4CB | 5298 | 磷脂酰肌醇4-激酶,催化的,β多肽 | 脂质激酶 |
| PIM1 | 5292 | pim-1癌基因 | 蛋白激酶(RS/TK) |
| PIM2 | 11040 | pim-2癌基因 | 蛋白激酶(RS/TK) |
| PINK1 | 65018 | PTEN诱导的假定激酶1 | 蛋白激酶(RS/TK) |
| PIP5K1A | 8394 | 磷脂酰肌醇-4-磷酸5-激酶,I型,α | 脂质激酶 |
| PIP5K1B | 8395 | 磷脂酰肌醇-4-磷酸5-激酶,I型,β | 脂质激酶 |
| PIP5K2A | 5305 | 磷脂酰肌醇-4-磷酸5-激酶,II型,α | 脂质激酶 |
| PIP5K2C | 79837 | 磷脂酰肌醇-4-磷酸5-激酶,II型,γ | 激酶相关的 |
| PIP5K3 | 200576 | 磷脂酰肌醇-3-磷酸/磷脂酰肌醇5-激酶,III型 | 脂质激酶 |
| PIP5KL1 | 138429 | 磷脂酰肌醇-4-磷酸5-激酶-样1 | 脂质激酶 |
| PKLR | 5313 | 丙酮酸激酶,肝和RBC | 碳水化合物激酶 |
| PKM2 | 5315 | 丙酮酸激酶,肌肉 | 碳水化合物激酶 |
| PKMYT1 | 9088 | 膜结合的酪氨酸和苏氨酸特异性cdc2-抑制性激酶 | 蛋白激酶(NRS/TK) |
| PLAU | 5328 | 纤溶酶原激活物,尿激酶 | 激酶相关的 |
| PLK1 | 5347 | polo-样激酶1(果蝇) | 蛋白激酶(NRS/TK) |
| PLK2 | 10769 | polo-样激酶2(果蝇) | 蛋白激酶(NRS/TK) |
| PLK4 | 10733 | polo-样激酶4(果蝇) | 蛋白激酶(NRS/TK) |
| PLXNA3 | 55558 | plexin A3;PLXNA3 | 蛋白激酶(RTK) |
| PLXNA4B | 91584 | plexin A4,B;PLXNA4B | 蛋白激酶(RTK) |
| PLXNB2 | 23654 | plexin B2;PLXNB2 | 蛋白激酶(RTK) |
| PMVK | 10654 | 磷酸甲羟戊酸激酶 | 激酶相关的 |
| PNCK | 139728 | 妊娠上调的非遍在表达的CaM激酶 | 蛋白激酶(NRS/TK) |
| PNKP | 11284 | 多核苷酸激酶3'-磷酸酶 | 核苷酸激酶 |
| PRKAA1 | 5562 | 蛋白激酶,AMP活化,α1催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAA2 | 5563 | 蛋白激酶,AMP活化,α2催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAB1 | 5564 | 蛋白激酶,AMP活化,β1非催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAB2 | 5565 | 蛋白激酶,AMP活化,β2非催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKACA | 5566 | 蛋白激酶,cAMP-依赖性,催化的,α | 蛋白激酶(NRS/TK) |
| PRKACB | 5567 | 蛋白激酶,cAMP-依赖性,催化的,β | 蛋白激酶(NRS/TK) |
| PRKACG | 5568 | 蛋白激酶,cAMP-依赖性,催化的,γ | 蛋白激酶(NRS/TK) |
| PRKAG1 | 5571 | 蛋白激酶,AMP活化,γ1非催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAG2 | 51422 | 蛋白激酶,AMP活化,γ2非催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAG3 | 53632 | 蛋白激酶,AMP活化,γ3非催化亚单位 | 蛋白激酶(NRS/TK) |
| PRKAR1A | 5573 | 蛋白激酶,cAMP-依赖性,调节的,I型,α(组织特异性消失基因1) | 蛋白激酶(NRS/TK) |
| PRKAR1B | 5575 | 蛋白激酶,cAMP-依赖性,调节的,I型,β | 蛋白激酶(NRS/TK) |
| PRKAR2A | 5576 | 蛋白激酶,cAMP-依赖性,调节的,II型,α | 蛋白激酶(NRS/TK) |
| PRKAR2B | 5577 | 蛋白激酶,cAMP-依赖性,调节的,II型,β | 蛋白激酶(NRS/TK) |
| PRKCA | 5578 | 蛋白激酶C,α | 蛋白激酶(NRS/TK) |
| PRKCB1 | 5579 | 蛋白激酶C,β1 | 蛋白激酶(NRS/TK) |
| PRKCE | 5581 | 蛋白激酶C,ε | 蛋白激酶(NRS/TK) |
| PRKCG | 5582 | 蛋白激酶C,γ | 蛋白激酶(NRS/TK) |
| PRKCH | 5583 | 蛋白激酶C,η | 蛋白激酶(NRS/TK) |
| PRKCI | 5584 | 蛋白激酶C,ι | 蛋白激酶(NRS/TK) |
| PRKCQ | 5588 | 蛋白激酶C,θ | 蛋白激酶(NRS/TK) |
| PRKCZ | 5590 | 蛋白激酶C,ζ | 蛋白激酶(NRS/TK) |
| PRKD1 | 5587 | 蛋白激酶D1 | 蛋白激酶(NRS/TK) |
| PRKD2 | 25865 | 蛋白激酶D2 | 蛋白激酶(NRS/TK) |
| PRKD3 | 23683 | 蛋白激酶D3 | 蛋白激酶(NRS/TK) |
| PRKG1 | 5592 | 蛋白激酶,cGMP-依赖性,I型 | 蛋白激酶(NRS/TK) |
| PRKG2 | 5593 | 蛋白激酶,cGMP-依赖性,II型 | 蛋白激酶(NRS/TK) |
| PRKR | 5610 | 蛋白激酶,干扰素诱导型双链RNA依赖性 | 蛋白激酶(NRS/TK) |
| PRKX | 5613 | 蛋白激酶,X连锁的 | 蛋白激酶(NRS/TK) |
| PRKY | 5616 | 蛋白激酶,Y连锁的 | 蛋白激酶(NRS/TK) |
| PRPF4B | 8899 | PRP4 mRNA前体加工因子4同系物B(酵母) | 蛋白激酶(NRS/TK) |
| PRPS1 | 5631 | 磷酸核糖焦磷酸合成酶1;PRPS1 | 激酶相关的 |
| PRPS1L1 | 221823 | 磷酸核糖焦磷酸合成酶1-样1;PRPS1L1 | 激酶相关的 |
| PRPS2 | 5634 | 磷酸核糖焦磷酸合成酶2;PRPS2 | 激酶相关的 |
| PSKH1 | 5681 | 蛋白质丝氨酸激酶H1 | 蛋白激酶(NRS/TK) |
| PTK2 | 5747 | PTK2蛋白质酪氨酸激酶2 | 蛋白激酶(NRTK) |
| PTK2B | 2185 | PTK2B蛋白质酪氨酸激酶2β | 蛋白激酶(NRTK) |
| PTK6 | 5753 | PTK6蛋白质酪氨酸激酶6 | 蛋白激酶(NRTK) |
| PTK7 | 5754 | PTK7蛋白质酪氨酸激酶7 | 蛋白激酶(RTK) |
| PTK9 | 5756 | PTK9蛋白质酪氨酸激酶9 | 蛋白激酶(NRTK) |
| PXK | 54899 | 含PX结构域的丝氨酸/苏氨酸激酶 | 激酶相关的 |
| RAF1 | 5894 | v-raf-1鼠白血病病毒癌基因同系物1 | 蛋白激酶(NRS/TK) |
| RAGE | 5891 | 肾肿瘤抗原 | 蛋白激酶(NRS/TK) |
| RBKS | 64080 | 核糖激酶 | 核苷酸激酶 |
| RET | 5979 | ret原癌基因(多内分泌腺腺瘤形成和甲状腺髓样癌1,Hirschsprung病) | 蛋白激酶(RTK) |
| RFK | 55312 | 核黄素激酶 | 激酶相关的 |
| RIOK1 | 83732 | RIO激酶1(酵母) | 蛋白激酶(NRS/TK) |
| RIOK2 | 55781 | RIO激酶2(酵母) | 蛋白激酶(NRS/TK) |
| RIOK3 | 8780 | RIO激酶3(酵母) | 蛋白激酶(NRS/TK) |
| RIPK1 | 8737 | 受体(TNFRSF)-相互作用丝氨酸-苏氨酸激酶1 | 蛋白激酶(NRS/TK) |
| RIPK2 | 8767 | 受体-相互作用丝氨酸-苏氨酸激酶2 | 蛋白激酶(NRS/TK) |
| RIPK5 | 25778 | 受体相互作用蛋白激酶5 | 蛋白激酶(NRS/TK) |
| RKHD3 | 84206 | 含环指和KH结构域3;RKHD3 | 蛋白激酶 |
| ROR2 | 4920 | 受体酪氨酸激酶-样孤儿受体2 | 蛋白激酶(RTK) |
| RP2 | 6102 | 色素性视网膜炎2(X连锁隐性);RP2 | 核苷酸激酶 |
| RP6-213H19.1 | 51765 | Mst3和SOK1相关激酶 | 蛋白激酶 |
| RPS6KA1 | 6195 | 核糖体蛋白质S6激酶,90kDa,多肽1 | 蛋白激酶(NRS/TK) |
| RPS6KA2 | 6196 | 核糖体蛋白质S6激酶,90kDa,多肽2 | 蛋白激酶(NRS/TK) |
| RPS6KA3 | 6197 | 核糖体蛋白质S6激酶,90kDa,多肽3 | 蛋白激酶(NRS/TK) |
| RPS6KA4 | 8986 | 核糖体蛋白质S6激酶,90kDa,多肽4 | 蛋白激酶(NRS/TK) |
| RPS6KA5 | 9252 | 核糖体蛋白质S6激酶,90kDa,多肽5 | 蛋白激酶(NRS/TK) |
| RPS6KA6 | 27330 | 核糖体蛋白质S6激酶,90kDa,多肽6 | 蛋白激酶(NRS/TK) |
| RPS6KB1 | 6198 | 核糖体蛋白质S6激酶,70kDa,多肽1 | 蛋白激酶(NRS/TK) |
| RPS6KB2 | 6199 | 核糖体蛋白质S6激酶,70kDa,多肽2 | 蛋白激酶(NRS/TK) |
| RPS6KC1 | 26750 | 核糖体蛋白质S6激酶,52kDa,多肽1 | 蛋白激酶(NRS/TK) |
| RPS6KL1 | 83694 | 核糖体蛋白质S6激酶-样1 | 蛋白激酶(NRS/TK) |
| SCYL1 | 57410 | SCY1-样1(酿酒酵母) | 蛋白激酶(NRTK) |
| SCYL2 | 55681 | 假定蛋白质FLJ10074 | 蛋白激酶(NRTK) |
| SCYL3 | 57147 | ezrin-结合配偶体PACE-1 | 蛋白激酶(NRTK) |
| SEPHS2 | 22928 | 硒代磷酸合成酶2;SEPHS2 | 激酶相关的 |
| SGK | 6446 | 血清/糖皮质激素调节的激酶 | 蛋白激酶(NRS/TK) |
| SGK2 | 10110 | 血清/糖皮质激素调节的激酶2 | 蛋白激酶(NRS/TK) |
| SGK3 | 23678 | 血清/糖皮质激素调节的激酶-样 | 蛋白激酶(NRS/TK) |
| SH3BP4 | 23677 | SH3结构域结合蛋白4;SH3BP4 | 蛋白激酶(NRTK) |
| SH3BP5 | 9467 | SH3结构域结合蛋白5(BTK结合的);SH3BP5 | 激酶相关的 |
| SH3BP5L | 80851 | SH3结合结构域蛋白质5-样;SH3BP5L | 激酶相关的 |
| SLAMF6 | 114836 | SLAM家族成员6;SLAMF6 | 蛋白激酶(RTK) |
| SNF1LK | 150094 | SNF1-样激酶 | 蛋白激酶(NRS/TK) |
| SNRK | 54861 | SNF-1相关激酶 | 蛋白激酶(NRS/TK) |
| SNX16 | 64089 | 排序连接蛋白16;SNX16 | 激酶相关的 |
| SPHK1 | 8877 | 鞘氨醇激酶1 | 碳水化合物激酶 |
| SPHK2 | 56848 | 鞘氨醇激酶2 | 碳水化合物激酶 |
| SRC | 6714 | v-src肉瘤(Schmidt-Ruppin A-2)病毒癌基因同系物(禽类) | 蛋白激酶(NRTK) |
| SRPK1 | 6732 | SFRS蛋白激酶1 | 蛋白激酶(NRS/TK) |
| SRPK2 | 6733 | SFRS蛋白激酶2 | 蛋白激酶(NRS/TK) |
| SRPK3 | 26576 | 丝氨酸/苏氨酸激酶23 | 蛋白激酶(NRS/TK) |
| STK11 | 6794 | 丝氨酸/苏氨酸激酶11(Peutz-Jeghers综合征) | 蛋白激酶(NRS/TK) |
| STK16 | 8576 | 丝氨酸/苏氨酸激酶16 | 蛋白激酶(NRS/TK) |
| STK17B | 9262 | 丝氨酸/苏氨酸激酶17b(细胞凋亡诱导性) | 蛋白激酶(NRS/TK) |
| STK19 | 8859 | 丝氨酸/苏氨酸激酶19 | 蛋白激酶(NRS/TK) |
| STK24 | 8428 | 丝氨酸/苏氨酸激酶24(STE20同系物,酵母) | 蛋白激酶 |
| STK25 | 10494 | 丝氨酸/苏氨酸激酶25(STE20同系物,酵母) | 蛋白激酶 |
| STK3 | 6788 | 丝氨酸/苏氨酸激酶3(STE20同系物,酵母) | 蛋白激酶 |
| STK32A | 202374 | 丝氨酸/苏氨酸激酶32A | 蛋白激酶(NRS/TK) |
| STK32B | 55351 | 丝氨酸/苏氨酸激酶32B | 蛋白激酶(NRS/TK) |
| STK32C | 282974 | 丝氨酸/苏氨酸激酶32C | 蛋白激酶(NRS/TK) |
| STK33 | 65975 | 丝氨酸/苏氨酸激酶33 | 蛋白激酶(NRS/TK) |
| STK36 | 27148 | 丝氨酸/苏氨酸激酶36(融合的同系物,果蝇) | 蛋白激酶(RS/TK) |
| STK38 | 11329 | 丝氨酸/苏氨酸激酶38 | 蛋白激酶(NRS/TK) |
| STK38L | 23012 | 丝氨酸/苏氨酸激酶38样 | 蛋白激酶(NRS/TK) |
| STK40 | 83931 | Ser/Thr-样激酶 | 蛋白激酶 |
| STYK1 | 55359 | 蛋白激酶STYK1 | 蛋白激酶(RTK) |
| SYK | 6850 | 脾酪氨酸激酶 | 蛋白激酶(NRTK) |
| TAOK3 | 51347 | TAO激酶3 | 蛋白激酶 |
| TBK1 | 29110 | TANK结合激酶1 | 蛋白激酶(NRS/TK) |
| TEC | 7006 | tec蛋白质酪氨酸激酶 | 蛋白激酶(NRTK) |
| TESK1 | 7016 | 睾丸特异性激酶1 | 蛋白激酶(NRS/TK) |
| TESK2 | 10420 | 睾丸特异性激酶2 | 蛋白激酶(NRS/TK) |
| TGFBR1 | 7046 | 转化生长因子,β受体 I(活化素A受体II型-样激酶,53kDa) | 蛋白激酶(RS/TK) |
| TGFBR2 | 7048 | 转化生长因子,β受体 II(70/80kDa) | 蛋白激酶(RS/TK) |
| TGFBR3 | 7049 | 转化生长因子,β受体 III(β聚糖,300kDa);TGFBR3 | 蛋白激酶(RS/TK) |
| TIE1 | 7075 | 具有免疫球蛋白-样和EGF-样结构域的酪氨酸激酶1 | 蛋白激酶(RTK) |
| TK1 | 7083 | 胸苷激酶1,可溶的 | 核苷酸激酶 |
| TLK1 | 9874 | tousled-样激酶1 | 蛋白激酶(NRS/TK) |
| TLK2 | 11011 | tousled-样激酶2 | 蛋白激酶(NRS/TK) |
| TNK1 | 8711 | 酪氨酸激酶,非受体,1 | 蛋白激酶(NRTK) |
| TNNI3K | 51086 | TNNI3相互作用激酶 | 蛋白激酶 |
| TP53RK | 112858 | TP53调节激酶 | 蛋白激酶(NRS/TK) |
| TPK1 | 27010 | 硫胺素焦磷酸激酶1 | 激酶相关的 |
| TPR | 7175 | 易位的启动子区(至活化的MET癌基因);TPR | 蛋白激酶(RTK) |
| TRIB1 | 10221 | tribbles同系物1(果蝇) | 蛋白激酶 |
| TRIB2 | 28951 | tribbles同系物2(果蝇) | 蛋白激酶 |
| TRIB3 | 57761 | tribbles同系物3(果蝇) | 蛋白激酶 |
| TRIM27 | 5987 | 含三分基序27;TRIM27 | 蛋白激酶(RTK) |
| TRPM7 | 54822 | 瞬时受体潜在的阳离子通道,亚家族 M,成员7 | 蛋白激酶(NRS/TK) |
| TSSK1 | 83942 | 丝氨酸/苏氨酸激酶22D(精子形成结合的) | 蛋白激酶(NRS/TK) |
| TSSK2 | 23617 | 丝氨酸/苏氨酸激酶22B(精子形成结合的) | 蛋白激酶(NRS/TK) |
| TSSK3 | 81629 | 丝氨酸/苏氨酸激酶22C(精子形成结合的) | 蛋白激酶(NRS/TK) |
| TSSK6 | 83983 | 丝氨酸/苏氨酸蛋白激酶SSTK | 蛋白激酶(NRS/TK) |
| TTK | 7272 | TTK蛋白激酶 | 蛋白激酶 |
| TWF2 | 11344 | PTK9L蛋白质酪氨酸激酶9-样(A6相关蛋白质) | 蛋白激酶(NRTK) |
| TXK | 7294 | TXK酪氨酸激酶 | 蛋白激酶(NRTK) |
| TXNDC3 | 51314 | 含硫氧还蛋白结构域3(精子);TXNDC3 | 核苷酸激酶 |
| TYK2 | 7297 | 酪氨酸激酶2 | 蛋白激酶(NRTK) |
| TYRO3 | 7301 | TYRO3蛋白质酪氨酸激酶 | 蛋白激酶(RTK) |
| UCK2 | 7371 | 尿苷-胞苷激酶2 | 核苷酸激酶 |
| UHMK1 | 127933 | U2AF同系物y基序(UHM)激酶1 | 蛋白激酶(NRS/TK) |
| ULK2 | 9706 | unc-51-样激酶2(秀丽隐杆线虫(C. elegans)) | 蛋白激酶(NRS/TK) |
| ULK3 | 25989 | DKFZP434C131蛋白质 | 蛋白激酶(NRS/TK) |
| ULK4 | 54986 | 假定蛋白质FLJ20574 | 蛋白激酶 |
| VRK1 | 7443 | 牛痘相关激酶1 | 蛋白激酶(NRS/TK) |
| VRK2 | 7444 | 牛痘相关激酶2 | 蛋白激酶(NRS/TK) |
| VRK3 | 51231 | 牛痘相关激酶3 | 蛋白激酶(NRS/TK) |
| WNK1 | 65125 | 蛋白激酶,赖氨酸缺陷型1 | 蛋白激酶(NRS/TK) |
| WNK4 | 65266 | 蛋白激酶,赖氨酸缺陷型4 | 蛋白激酶(NRS/TK) |
| XRCC6BP1 | 91419 | XRCC6结合蛋白1;XRCC6BP1 | 蛋白激酶 |
| XYLB | 9942 | 木酮糖激酶同系物(流感嗜血杆菌(H. influenzae)) | 碳水化合物激酶 |
| YES1 | 7525 | v-yes-1 Yamaguchi肉瘤病毒癌基因同系物1 | 蛋白激酶(NRTK) |
| YSK4 | 80122 | 假定蛋白质FLJ23074 | 蛋白激酶 |
| ZAK | 51776 | 含不育α基序和亮氨酸拉链激酶AZK | 蛋白激酶(NRS/TK) |
| ZAP70 | 7535 | ζ-链(TCR)结合的蛋白激酶70kDa | 蛋白激酶(NRTK) |
表4:相对于MEK DD,对于597个激酶相关ORFs的平均差异增殖(1 μM PLX4720/对照)的排序
表5:定量通过前9个候选ORFs诱导的在PLX4720 Gl50中的变化的二次筛选结果
序列表
<110> Garraway,Levi A.
Johannessen,Cory M.
<120> 诊断和治疗具有或发展对于第一种癌症治疗的抗性的患者中的癌症的方法
<130> 14293/79
<150> US 61/312,193
<151> 2010-03-09
<150> US 61/312,519
<151> 2010-03-10
<150> US 61/326,021
<151> 2010-04-20
<150> US 61/415,569
<151> 2010-11-19
<160> 17
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 合成正向COT引物
<400> 1
caagtgaaga gccagcagtt t 21
<210> 2
<211> 22
<212> DNA
<213> 人工序列
<220>
<223> 合成反向COT引物
<400> 2
gcaagcaaat cctccacagt tc 22
<210> 3
<211> 22
<212> DNA
<213> 人工序列
<220>
<223> 合成正向TBP引物
<400> 3
cccgaaacgc cgaatataat cc 22
<210> 4
<211> 22
<212> DNA
<213> 人工序列
<220>
<223> 合成反向TBP引物
<400> 4
gactgttctt cactcttggc tc 22
<210> 5
<211> 19
<212> DNA
<213> 人工序列
<220>
<223> 合成正向GAPDH引物
<400> 5
catcatctct gccccctct 19
<210> 6
<211> 20
<212> DNA
<213> 人工序列
<220>
<223> 合成反向GAPDH引物
<400> 6
ggtgctaagc agttggtggt 20
<210> 7
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shLuc shRNA的合成DNA构建体
<400> 7
cttcgaaatg tccgttcggt t 21
<210> 8
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shBRAF(1)shRNA的合成DNA构建体
<400> 8
cttcgaaatg tccgttcggt t 21
<210> 9
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shBRAF(2)shRNA的合成DNA构建体
<400> 9
gctggtttcc aaacagagga t 21
<210> 10
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shCRAF(1)shRNA的合成DNA构建体
<400> 10
cggagatgtt gcagtaaaga t 21
<210> 11
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shCRAF(2)shRNA的合成DNA构建体
<400> 11
gagacatgaa atccaacaat a 21
<210> 12
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shMEK1(1)shRNA的合成DNA构建体
<400> 12
gattacatag tcaacgagcc t 21
<210> 13
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shMEK1(2)shRNA的合成DNA构建体
<400> 13
gcttctatgg tgcgttctac a 21
<210> 14
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shMEK2(1)shRNA的合成DNA构建体
<400> 14
tggactatat tgtgaacgag c 21
<210> 15
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shMEK2(2)shRNA的合成DNA构建体
<400> 15
ccaacatcct cgtgaactct a 21
<210> 16
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于hCOT(1)shRNA的合成DNA构建体
<400> 16
caagagccgc agacctacta a 21
<210> 17
<211> 21
<212> DNA
<213> 人工序列
<220>
<223> 用于shCOT(2)shRNA的合成DNA构建体
<400> 17
gatgagaatg tgacctttaa g 21
Claims (29)
1.一种鉴定具有可能获益于用组合疗法的治疗的癌症的受试者的方法,所述组合疗法利用RAF抑制剂和第二种抑制剂,所述方法包括:
(a)测定得自受试者的癌细胞中选自下述的一种或多种激酶靶的基因拷贝数、mRNA或蛋白质水平或磷酸化:MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3),并且比较所述基因拷贝数、mRNA或蛋白质水平或磷酸化与得自不含癌症的受试者的细胞中靶激酶的基因拷贝数、mRNA或蛋白质水平或磷酸化;和
(b)将相对于来自不含癌症的受试者的细胞在癌细胞中增加的靶激酶的基因拷贝数或mRNA表达中的改变或蛋白质过表达或磷酸化与具有可能获益于用组合疗法的治疗的癌症的受试者关联。
2.权利要求1的方法,其进一步包括(c)就核酸分子中的突变的存在测定得自所述癌细胞的核酸样品,所述核酸分子编码在约氨基酸位置600处具有突变的B-RAF多肽,和(d)将编码B-RAF多肽的核酸分子中的突变的存在与可能获益于用所述组合疗法的治疗的受试者关联。
3.权利要求1的方法,其包括将编码B-RAF的核酸分子中在约氨基酸位置600处的缬氨酸至谷氨酸突变(V600E)的存在与可能获益于用所述组合疗法的治疗的受试者关联。
4.权利要求1的方法,其包括测定MAP3K8(TPL/COT)的基因拷贝数、mRNA或蛋白质水平。
5.权利要求1的方法,其包括测定在氨基酸S338处C-RAF的磷酸化。
6.权利要求1的方法,其中所述第二种抑制剂是MEK抑制剂、CRAF抑制剂、CrkL抑制剂或TPL2/COT抑制剂。
7.权利要求1的方法,其中所述RAF抑制剂是B-RAF抑制剂或泛RAF抑制剂。
8.权利要求1的方法,其中所述RAF抑制剂选自RAF265、索拉非尼、SB590885、PLX 4720、PLX4032、GDC-0879和ZM 336372。
9.权利要求1的方法,其中所述受试者具有对于所述RAF抑制剂的先天抗性或可能发展对于所述RAF抑制剂的抗性。
10.权利要求1的方法,其中所述癌症选自黑素瘤、乳腺癌、结肠直肠癌、神经胶质瘤、肺癌、卵巢癌、肉瘤和甲状腺癌。
11.权利要求10的方法,其中所述癌症是黑素瘤。
12.一种治疗在有此需要的受试者中的癌症的方法,其包括给所述受试者施用有效量的RAF抑制剂和有效量的第二种抑制剂,其中所述第二种抑制剂是MEK抑制剂或MAP3K8(TPL2/COT)抑制剂。
13.权利要求12的方法,其中所述受试者具有包含在B-RAF中的突变的癌细胞。
14.权利要求12的方法,其中所述受试者具有包含B-RAFV600E突变的癌细胞。
15.权利要求12的方法,其进一步包括测定得自受试者的癌细胞中选自下述的一种或多种激酶靶的基因拷贝数、mRNA或蛋白质水平或磷酸化:MAP3K8(TPL2/COT)、RAF1(CRAF)、CRKL(CrkL)、FGR(Fgr)、PRKCE(Prkce)、PRKCH(Prkch)、ERBB2(ErbB2)、AXL(Axl)或PAK3(Pak3),并且比较所述基因拷贝数、mRNA或蛋白质水平或磷酸化与得自不含癌症的受试者的细胞中靶激酶的基因拷贝数、mRNA或蛋白质水平或磷酸化;和
在具有所述癌细胞中增加的靶激酶的基因拷贝数或mRNA表达中的改变或蛋白质过表达或磷酸化的受试者中,给所述受试者施用有效量的RAF抑制剂和有效量的第二种抑制剂。
16.权利要求12的方法,其中所述RAF抑制剂选自RAF265、索拉非尼、SB590885、PLX 4720、PLX4032、GDC-0879和ZM 336372。
17.权利要求12的方法,其中所述MEK抑制剂选自CI-1040/PD184352、AZD6244、PD318088、PD98059、PD334581、RDEA119、6-甲氧基-7-(3-吗啉-4-基-丙氧基)-4-(4-苯氧基-苯氨基)-喹啉-3-甲腈和4-[3-氯-4-(1-甲基-1H-咪唑-2-基硫烷基)-苯氨基]-6-甲氧基-7-(3-吗啉-4-基-苯氧基)-喹啉-3-甲腈。
18.权利要求12的方法,其中所述受试者具有对于所述RAF抑制剂的先天抗性或可能发展对于所述RAF抑制剂的抗性。
19.权利要求12的方法,其中所述癌症选自黑素瘤、乳腺癌、结肠直肠癌、神经胶质瘤、肺癌、卵巢癌、肉瘤和甲状腺癌。
20.权利要求12的方法,其中所述癌症是黑素瘤。
21.权利要求12的方法,其中所述受试者具有对于所述MEK抑制剂的先天抗性或可能发展对于所述MEK抑制剂的抗性。
22.权利要求12的方法,其中所述第二种抑制剂是MAP3K8(TPL2/COT)抑制剂。
23.一种鉴定赋予对于第一种抑制剂的抗性的激酶靶的方法,所述方法包括:
培养对于所述第一种抑制剂具有敏感性的细胞;
在所述细胞培养物中表达多个激酶ORF克隆,每种细胞培养物表达不同的激酶ORF克隆;
使每种细胞培养物暴露于所述抑制剂;
鉴定在暴露于所述抑制剂后具有大于对照细胞培养物的生存的细胞培养物,以鉴定赋予对于所述第一种抑制剂的抗性的一个或多个激酶ORF克隆。
24.权利要求23的方法,其中所述培养细胞具有对于RAF抑制剂的敏感性。
25.权利要求23的方法,其中所述培养细胞具有对于MEK抑制剂的敏感性。
26.权利要求23的方法,其中所述培养细胞包含B-RAF突变。
27.权利要求26的方法,其中所述培养细胞包含B-RAFV600E突变。
28.权利要求23的方法,其中所述培养细胞包含黑素瘤细胞系。
29.权利要求23的方法,其包括提供在慢病毒载体或逆转录病毒载体中的多个激酶ORF克隆。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US31219310P | 2010-03-09 | 2010-03-09 | |
| US61/312193 | 2010-03-09 | ||
| US31251910P | 2010-03-10 | 2010-03-10 | |
| US61/312519 | 2010-03-10 | ||
| US32602110P | 2010-04-20 | 2010-04-20 | |
| US61/326021 | 2010-04-20 | ||
| US41556910P | 2010-11-19 | 2010-11-19 | |
| US61/415569 | 2010-11-19 | ||
| PCT/US2011/027689 WO2011112678A1 (en) | 2010-03-09 | 2011-03-09 | Methods of diagnosing and treating cancer in patients having or developing resistance to a first cancer therapy |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103038364A true CN103038364A (zh) | 2013-04-10 |
Family
ID=43837946
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2011800231091A Pending CN103038364A (zh) | 2010-03-09 | 2011-03-09 | 诊断和治疗具有或发展对于第一种癌症治疗的抗性的患者中的癌症的方法 |
Country Status (12)
| Country | Link |
|---|---|
| US (3) | US20130059851A1 (zh) |
| EP (1) | EP2545187B1 (zh) |
| JP (1) | JP5985401B2 (zh) |
| KR (1) | KR20120139767A (zh) |
| CN (1) | CN103038364A (zh) |
| AU (1) | AU2011224410B2 (zh) |
| BR (1) | BR112012022801B8 (zh) |
| CA (1) | CA2791247C (zh) |
| EA (1) | EA030276B1 (zh) |
| ES (1) | ES2714875T3 (zh) |
| MX (1) | MX343368B (zh) |
| WO (1) | WO2011112678A1 (zh) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105695616A (zh) * | 2016-04-22 | 2016-06-22 | 王冬国 | 诊断甲状腺癌的分析标志物及其应用 |
| CN108872438A (zh) * | 2018-08-06 | 2018-11-23 | 杭州迪相实业有限公司 | 一种外泌体中肺癌标志物gk5快速检测试剂盒 |
| CN110862968A (zh) * | 2019-10-30 | 2020-03-06 | 中国农业科学院兰州兽医研究所 | Map3k8基因敲除pk-15细胞系的构建方法及其应用 |
| CN111601615A (zh) * | 2017-11-02 | 2020-08-28 | 乔治亚大学研究基金公司 | 与轮状病毒产量增加有关的方法和组合物 |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7723477B2 (en) | 2005-10-31 | 2010-05-25 | Oncomed Pharmaceuticals, Inc. | Compositions and methods for inhibiting Wnt-dependent solid tumor cell growth |
| MX2011003183A (es) | 2008-09-26 | 2011-04-21 | Oncomed Pharm Inc | Agentes que se unen a receptor encrespado y usos de los mismos. |
| TWI535445B (zh) | 2010-01-12 | 2016-06-01 | 安可美德藥物股份有限公司 | Wnt拮抗劑及治療和篩選方法 |
| MX347515B (es) | 2010-04-01 | 2017-04-28 | Oncomed Pharmaceuticals Inc * | Agentes que se unen al receptor encrespado y usos de los mismos. |
| WO2012138783A2 (en) * | 2011-04-04 | 2012-10-11 | Netherlands Cancer Institute | Methods and compositions for predicting resistance to anticancer treatment |
| US10202643B2 (en) | 2011-10-31 | 2019-02-12 | University Of Utah Research Foundation | Genetic alterations in glioma |
| WO2013086260A2 (en) * | 2011-12-09 | 2013-06-13 | Oncomed Pharmaceuticals, Inc. | Combination therapy for treatment of cancer |
| EP3693741B1 (en) | 2012-03-28 | 2022-01-05 | Dana-Farber Cancer Institute, Inc. | Medical uses involving c-raf mutants that confer resistance to raf inhibitors |
| MX367970B (es) | 2012-08-17 | 2019-09-11 | Hoffmann La Roche | Tratamientos de combinación para melanoma que comprenden la administración de cobimetinib y vemurafinib. |
| JP2015536933A (ja) | 2012-10-23 | 2015-12-24 | オンコメッド ファーマシューティカルズ インコーポレイテッド | Wnt経路結合剤を用いて神経内分泌腫瘍を処置する方法 |
| WO2014121196A1 (en) | 2013-02-04 | 2014-08-07 | Oncomed Pharmaceuticals, Inc. | Methods and monitoring of treatment with a wnt pathway inhibitor |
| US9168300B2 (en) | 2013-03-14 | 2015-10-27 | Oncomed Pharmaceuticals, Inc. | MET-binding agents and uses thereof |
| US10968484B2 (en) | 2013-03-15 | 2021-04-06 | The Broad Institute, Inc. | Methods of identifying responses to map kinase inhibition therapy |
| WO2014204261A1 (ko) * | 2013-06-21 | 2014-12-24 | 사회복지법인 삼성생명공익재단 | Tpl2의 발현억제제 또는 활성억제제를 유효성분으로 포함하는 신세포암의 예방 또는 치료용 약학적 조성물 |
| US20170242015A1 (en) * | 2014-09-17 | 2017-08-24 | Institut Curie | Map3k8 as a marker for selecting a patient affected with an ovarian cancer for a treatment with a mek inhibitor |
| KR20160129609A (ko) | 2015-04-30 | 2016-11-09 | 삼성전자주식회사 | Braf 저해제를 포함하는 세포 또는 개체의 노화를 감소시키기 위한 조성물 및 그의 용도 |
| SI3319955T1 (sl) | 2015-07-06 | 2021-01-29 | Gilead Sciences, Inc. | 6-amino-kinolin-3-karbonitrili kot modulatorji COT |
| KR20240008398A (ko) | 2015-07-06 | 2024-01-18 | 길리애드 사이언시즈, 인코포레이티드 | Cot 조정제 및 그의 사용 방법 |
| GB201520178D0 (en) * | 2015-11-16 | 2015-12-30 | Univ London Queen Mary | Method |
| WO2018005435A1 (en) | 2016-06-30 | 2018-01-04 | Gilead Sciences, Inc. | 4,6-diaminoquinazolines as cot modulators and methods of use thereof |
| WO2018027223A1 (en) * | 2016-08-05 | 2018-02-08 | Duke University | Camkk2 inhibitor compositions and methods of using the same |
| CA3045744A1 (en) * | 2016-12-20 | 2018-06-28 | Eth Zurich | Identification of drugs targeting non-genetic drug tolerance programs in cancer |
| US10793901B2 (en) * | 2016-12-28 | 2020-10-06 | Roche Molecular Systems, Inc. | Reversibly protected nucleotide reagents with high thermal stability |
| AU2018209164B2 (en) | 2017-01-17 | 2021-11-04 | Heparegenix Gmbh | Protein kinase inhibitors for promoting liver regeneration or reducing or preventing hepatocyte death |
| WO2020097396A1 (en) * | 2018-11-07 | 2020-05-14 | Dana-Farber Cancer Institute, Inc. | Benzimidazole derivatives and aza-benzimidazole derivatives as janus kinase 2 inhibitors and uses thereof |
| EP3931564A4 (en) * | 2019-02-26 | 2023-04-26 | Cell Response, Inc. | METHODS OF TREATMENT OF MAP3K8 POSITIVE TUMORS |
| TWI770527B (zh) | 2019-06-14 | 2022-07-11 | 美商基利科學股份有限公司 | Cot 調節劑及其使用方法 |
| CA3175541A1 (en) | 2020-03-30 | 2021-10-07 | Gilead Sciences, Inc. | Solid forms of (s)-6-(((1-(bicyclo[1.1.1]pentan-1-yl)-1h-1,2,3-triazol-4-yl)2-methyl-1-oxo-1,2- dihydroisoquinolin-5-yl)methyl)))amino)8-chloro-(neopentylamino)quinoline-3-carb onitrile a cot inhibitor compound |
| TWI778562B (zh) | 2020-04-02 | 2022-09-21 | 美商基利科學股份有限公司 | 製備cot抑制劑化合物的方法 |
| US11691963B2 (en) | 2020-05-06 | 2023-07-04 | Ajax Therapeutics, Inc. | 6-heteroaryloxy benzimidazoles and azabenzimidazoles as JAK2 inhibitors |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1758910A (zh) * | 2003-03-11 | 2006-04-12 | 诺瓦提斯公司 | 异喹啉衍生物治疗癌症和map激酶相关疾病的用途 |
| CN1889951A (zh) * | 2003-10-16 | 2007-01-03 | 希龙公司 | 取代的苯并唑及其用作raf激酶抑制剂的应用 |
| CN101415689A (zh) * | 2006-04-05 | 2009-04-22 | 阿斯利康(瑞典)有限公司 | 具有抗癌活性的经取代的喹唑啉 |
Family Cites Families (93)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR8108820A (pt) | 1980-09-24 | 1982-08-24 | Cetus Corp | Processo e sonda de diagnostico |
| DE3381518D1 (de) | 1982-01-22 | 1990-06-07 | Cetus Corp | Verfahren zur charakterisierung von hla und die darin benutzten cdns-testmittel. |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| CA1284931C (en) | 1986-03-13 | 1991-06-18 | Henry A. Erlich | Process for detecting specific nucleotide variations and genetic polymorphisms present in nucleic acids |
| CA1338457C (en) | 1986-08-22 | 1996-07-16 | Henry A. Erlich | Purified thermostable enzyme |
| EP0266032A1 (en) | 1986-08-29 | 1988-05-04 | Beecham Group Plc | Modified fibrinolytic enzyme |
| US7705215B1 (en) | 1990-04-17 | 2010-04-27 | Dekalb Genetics Corporation | Methods and compositions for the production of stably transformed, fertile monocot plants and cells thereof |
| FR2650840B1 (fr) | 1989-08-11 | 1991-11-29 | Bertin & Cie | Procede rapide de detection et/ou d'identification d'une seule base sur une sequence d'acide nucleique, et ses applications |
| US6004744A (en) | 1991-03-05 | 1999-12-21 | Molecular Tool, Inc. | Method for determining nucleotide identity through extension of immobilized primer |
| GB9222888D0 (en) | 1992-10-30 | 1992-12-16 | British Tech Group | Tomography |
| AT404556B (de) | 1995-11-23 | 1998-12-28 | Pharma Consult Gmbh | Einrichtung zum dichten verschliessen eines glas- oder kunststoffbehälters zur aufnahme flüssiger pharmazeutischer produkte |
| GB2323845A (en) | 1997-03-31 | 1998-10-07 | Merck & Co Inc | MEK inhibiting lactones |
| NZ501277A (en) | 1997-07-01 | 2002-12-20 | Warner Lambert Co | -2(4-bromo or 4-iodo phenylamino) benzoic acid derivatives and their use as MEK inhibitors |
| US6310060B1 (en) | 1998-06-24 | 2001-10-30 | Warner-Lambert Company | 2-(4-bromo or 4-iodo phenylamino) benzoic acid derivatives and their use as MEK inhibitors |
| US6821963B2 (en) | 1997-07-01 | 2004-11-23 | Warner-Lambert Company | 4-Bromo or 4-iodo phenylamino benzhydroxamic acid derivatives and their use as MEK inhibitors |
| US6506798B1 (en) | 1997-07-01 | 2003-01-14 | Warner-Lambert Company | 4-Arylamino, 4-aryloxy, and 4-arylthio diarylamines and derivatives thereof as selective MEK inhibitors |
| PT993439E (pt) | 1997-07-01 | 2004-12-31 | Warner Lambert Co | Derivados de acido 4-bromo ou 4-iodofenilaminobenzidroxamico e sua utilizacao como inibidores de mek |
| ATE310567T1 (de) | 1998-12-22 | 2005-12-15 | Warner Lambert Co | Chemotheriapie mit einem antimitotischen mittel und einem mek inhibitor |
| US20040171632A1 (en) | 1998-12-22 | 2004-09-02 | Gowan Richard Carleton | Combination chemotherapy |
| CA2349467A1 (en) | 1999-01-13 | 2000-07-20 | Warner-Lambert Company | Sulphohydroxamic acids and sulphohydroxamates and their use as mek inhibitors |
| CA2348236A1 (en) | 1999-01-13 | 2000-07-20 | Stephen Douglas Barrett | 4-arylamino, 4-aryloxy, and 4-arylthio diarylamines and derivatives thereof as selective mek inhibitors |
| EP1144371B1 (en) | 1999-01-13 | 2005-11-09 | Warner-Lambert Company Llc | Benzenesulphonamide derivatives and their use as mek inhibitors |
| JP2000204079A (ja) | 1999-01-13 | 2000-07-25 | Warner Lambert Co | ジアリ―ルアミン |
| JP2000212157A (ja) | 1999-01-13 | 2000-08-02 | Warner Lambert Co | ジアリ―ルアミン |
| JP2000204077A (ja) | 1999-01-13 | 2000-07-25 | Warner Lambert Co | ジアリ―ルアミン |
| JP2000204075A (ja) | 1999-01-13 | 2000-07-25 | Warner Lambert Co | ジアリ―ルアミン |
| OA11819A (en) | 1999-01-13 | 2005-08-17 | Warner Lambert Co | 1-Heterocycle substituted diarylamines. |
| EP1144385B1 (en) | 1999-01-13 | 2005-08-17 | Warner-Lambert Company Llc | Benzoheterocycles and their use as mek inhibitors |
| EE05450B1 (et) | 2000-07-19 | 2011-08-15 | Warner-Lambert Company | 4-jodofenlaminobenshdroksaamhapete oksgeenitud estrid, nende kristallvormid ja farmatseutilised kompositsioonid ning kasutamine |
| EP1438295B1 (en) | 2001-10-23 | 2012-08-15 | Merck Serono SA | Azole derivatives and pharmaceutical compositions containing them |
| US7307071B2 (en) | 2001-12-04 | 2007-12-11 | Onyx Pharmaceuticals, Inc | RAF-MEK-ERK pathway inhibitors to treat cancer |
| AU2002365665A1 (en) | 2001-12-05 | 2003-06-17 | Astrazeneca Ab | Pharmaceutical compositions comprising benzofuranyl substituted 3-cyanoquinoline derivatives and their use for the treatment of solid tumours |
| WO2003047585A1 (en) | 2001-12-05 | 2003-06-12 | Astrazeneca Ab | Pharmaceutical compositions comprising benzofuranyl substituted 3-cyanoquinoline derivatives and their use for the treatment of solid tumours |
| DOP2003000556A (es) | 2002-01-23 | 2003-10-31 | Warner Lambert Co | Esteres hidroxamato de acido n-(4-fenil-sustituido)-antranilico. |
| BR0307060A (pt) | 2002-01-23 | 2004-10-26 | Warner Lambert Co | ésteres hidroxamato do ácido n-(fenil 4-substituìdo)-antranìlico |
| MXPA04008894A (es) | 2002-03-13 | 2005-06-20 | Array Biopharma Inc | Derivados de bencimidazol n3 alquilados como inhibidores de mek. |
| US6989451B2 (en) | 2002-06-04 | 2006-01-24 | Valeant Research & Development | Heterocyclic compounds and uses thereof |
| EP1837025A3 (en) * | 2002-06-05 | 2007-12-19 | Cedars-Sinai Medical Center | Method of treating cancer using kinase inhibitors |
| EP1545529A4 (en) | 2002-09-30 | 2010-03-03 | Bristol Myers Squibb Co | NEW TYROSINE KINASE HEMMER |
| AU2003287366A1 (en) | 2002-10-31 | 2004-06-07 | University Of Rochester | Hyfroxyflutamide induced pathways related to androgen receptor negative prostate cancer cells |
| GB0225579D0 (en) | 2002-11-02 | 2002-12-11 | Astrazeneca Ab | Chemical compounds |
| WO2004044219A2 (en) | 2002-11-12 | 2004-05-27 | Mercury Therapeutics, Inc. | Xanthene compounds for cancer chemotherapy |
| US20050004186A1 (en) | 2002-12-20 | 2005-01-06 | Pfizer Inc | MEK inhibiting compounds |
| WO2005000818A1 (en) | 2003-06-27 | 2005-01-06 | Warner-Lambert Company Llc | 5-substituted-4-`(substituted phenyl)!amino!-2-pyridone deviatives for use as mek inhibitors |
| WO2005007616A1 (en) | 2003-07-23 | 2005-01-27 | Warner-Lambert Company Llc | Diphenylamino ketone derivatives as mek inhibitors |
| US20050049276A1 (en) | 2003-07-23 | 2005-03-03 | Warner-Lambert Company, Llc | Imidazopyridines and triazolopyridines |
| CA2532067C (en) | 2003-07-24 | 2010-12-21 | Stephen Douglas Barrett | N-methyle-substituted benzamidazoles |
| US7538120B2 (en) | 2003-09-03 | 2009-05-26 | Array Biopharma Inc. | Method of treating inflammatory diseases |
| US7144907B2 (en) | 2003-09-03 | 2006-12-05 | Array Biopharma Inc. | Heterocyclic inhibitors of MEK and methods of use thereof |
| TW200520745A (en) | 2003-09-19 | 2005-07-01 | Chugai Pharmaceutical Co Ltd | Novel 4-phenylamino-benzaldoxime derivatives and uses thereof as mitogen-activated protein kinase kinase (MEK) inhibitors |
| WO2005051302A2 (en) | 2003-11-19 | 2005-06-09 | Array Biopharma Inc. | Bicyclic inhibitors of mek and methods of use thereof |
| US7517994B2 (en) | 2003-11-19 | 2009-04-14 | Array Biopharma Inc. | Heterocyclic inhibitors of MEK and methods of use thereof |
| US7732616B2 (en) | 2003-11-19 | 2010-06-08 | Array Biopharma Inc. | Dihydropyridine and dihydropyridazine derivatives as inhibitors of MEK and methods of use thereof |
| TW200529846A (en) | 2004-02-20 | 2005-09-16 | Wyeth Corp | 3-quinolinecarbonitrile protein kinase inhibitors |
| ME01480B (me) | 2004-06-11 | 2014-04-20 | Japan Tobacco Inc | DERIVATI 5-AMIN0-2,4,7-TRIOKS0-3,4,7,8-TETRAHIDR0-2H-PIRID0[2,3-d]PIRIMIDINA I SRODNI SPOJEVI, NAMIJENJENI LIJEČENJU RAKA |
| US7378423B2 (en) | 2004-06-11 | 2008-05-27 | Japan Tobacco Inc. | Pyrimidine compound and medical use thereof |
| MY144232A (en) | 2004-07-26 | 2011-08-15 | Chugai Pharmaceutical Co Ltd | 5-substituted-2-phenylamino benzamides as mek inhibitors |
| CA2576599A1 (en) | 2004-08-17 | 2006-02-23 | F. Hoffmann-La Roche Ag | Substituted hydantoins |
| CN101006085A (zh) | 2004-08-17 | 2007-07-25 | 霍夫曼-拉罗奇有限公司 | 取代的乙内酰脲类 |
| EP2532653A1 (en) | 2004-08-25 | 2012-12-12 | Targegen, Inc. | Benzo[1,2,4]triazines as protein kinase modulators |
| CN101654452A (zh) | 2004-08-25 | 2010-02-24 | 塔尔基公司 | 杂环化合物和应用方法 |
| CN101010303A (zh) | 2004-09-01 | 2007-08-01 | 阿斯利康(瑞典)有限公司 | 喹唑啉酮衍生物和它们作为b-raf抑制剂的用途 |
| JP2006083133A (ja) | 2004-09-17 | 2006-03-30 | Sankyo Co Ltd | スルファミド誘導体医薬組成物 |
| TW200621766A (en) | 2004-09-17 | 2006-07-01 | Hoffmann La Roche | Substituted hydantoins |
| DK1802579T3 (da) | 2004-10-20 | 2014-01-20 | Merck Serono Sa | Derivater af 3-arylaminopyridin |
| CA2587178A1 (en) | 2004-11-24 | 2006-06-01 | Laboratoires Serono S.A. | Novel 4-arylamino pyridone derivatives as mek inhibitors for the treatment of hyperproliferative disorders |
| ATE443063T1 (de) | 2004-12-01 | 2009-10-15 | Merck Serono Sa | Ä1,2,4ütriazoloä4,3-aüpyridin-derivative zur behandlung hyperproliferativer erkrankungen |
| US7429667B2 (en) | 2005-01-20 | 2008-09-30 | Ardea Biosciences, Inc. | Phenylamino isothiazole carboxamidines as MEK inhibitors |
| KR20080019236A (ko) | 2005-05-18 | 2008-03-03 | 어레이 바이오파마 인크. | Mek의 헤테로시클릭 억제제 및 그의 사용 방법 |
| WO2006133417A1 (en) | 2005-06-07 | 2006-12-14 | Valeant Pharmaceuticals International | Phenylamino isothiazole carboxamidines as mek inhibitors |
| US8101799B2 (en) | 2005-07-21 | 2012-01-24 | Ardea Biosciences | Derivatives of N-(arylamino) sulfonamides as inhibitors of MEK |
| CA2618218C (en) | 2005-07-21 | 2015-06-30 | Ardea Biosciences, Inc. | N-(arylamino)-sulfonamide inhibitors of mek |
| WO2007025090A2 (en) | 2005-08-25 | 2007-03-01 | Kalypsys, Inc. | Heterobicyclic and - tricyclic inhibitors of mapk/erk kinase |
| NZ567140A (en) | 2005-10-07 | 2011-09-30 | Exelixis Inc | Azetidines as MEK inhibitors for the treatment of proliferative diseases |
| WO2007071951A1 (en) | 2005-12-21 | 2007-06-28 | Astrazeneca Ab | Tosylate salt of 6- (4-br0m0-2-chl0r0phenylamin0) -7-fluoro-n- (2-hydroxyethoxy) -3-methyl-3h-benzimi dazole- 5 - carboxamide , mek inhibitor useful in the treatment of cancer |
| US7612212B2 (en) | 2006-02-22 | 2009-11-03 | Hoffmann-La Roche Inc. | Substituted hydantoins |
| WO2007121269A2 (en) | 2006-04-11 | 2007-10-25 | Ardea Biosciences, Inc. | N-aryl-n'alkyl sulfamides as mek inhibitors |
| ATE483463T1 (de) | 2006-04-18 | 2010-10-15 | Ardea Biosciences Inc | Pyridonsulfonamide und pyridonsulfamide als mek- hemmer |
| EP2013180A1 (en) | 2006-04-19 | 2009-01-14 | Laboratoires Serono SA | Novel heteroaryl-substituted arylaminopyridine derivatives as mek inhibitors |
| WO2007123939A2 (en) | 2006-04-19 | 2007-11-01 | Laboratoires Serono S.A. | Novel arylamino n-heteraryls as mek inhibitors |
| CN101528231A (zh) | 2006-08-16 | 2009-09-09 | 埃克塞利希斯股份有限公司 | 在癌症的治疗中使用pi3k和mek调控剂 |
| WO2008020203A1 (en) | 2006-08-17 | 2008-02-21 | Astrazeneca Ab | Pyridinylquinaz0linamine derivatives and their use as b-raf inhibitors |
| BRPI0714635A2 (pt) | 2006-08-21 | 2013-06-18 | Genentech Inc | compostos, composiÇço farmacÊutica, mÉtodo para inibir, o crescimento celular anormal ou tratar uma disfunÇço hiperproliferativa, mÉtodo para tratar uma doenÇa inflamatària e mÉtodo para tratar uma doenÇa autoimune |
| BRPI0714629A2 (pt) | 2006-08-21 | 2013-05-07 | Genentech Inc | composto, composiÇço farmacÊutica, mÉtodo para inibir o crescimento celular, mÉtodo para tratar uma doenÇa inflamatària e mÉtodo para trataruma doenÇa auto-imune, lesço àsseo destrutiva, distérbios proliferativos, doenÇas infecciosas, doenÇas virais, doenÇas fibràticas ou doenÇas neurodegenerativas |
| BRPI0716224A2 (pt) | 2006-08-31 | 2013-10-15 | Array Biopharma Inc | Compostos inibidores de raf e métodos de uso dos mesmos. |
| JP2010508307A (ja) | 2006-10-31 | 2010-03-18 | 武田薬品工業株式会社 | Mapk/erkキナーゼ阻害剤 |
| EP2099796B1 (en) | 2006-11-30 | 2011-06-01 | Genentech, Inc. | Aza-indolyl compounds and methods of use |
| US7999006B2 (en) | 2006-12-14 | 2011-08-16 | Exelixis, Inc. | Methods of using MEK inhibitors |
| WO2008120004A1 (en) | 2007-04-02 | 2008-10-09 | Astrazeneca Ab | Combination of a mek- inhibitor and a b-raf inhibitor for the treatment of cancer |
| US8178317B2 (en) * | 2007-05-01 | 2012-05-15 | Dana-Farber Cancer Institute, Inc. | Compositions and methods for identifying transforming and tumor suppressor genes |
| CA2694646C (en) * | 2007-07-30 | 2017-09-05 | Ardea Biosciences, Inc. | Combinations of mek inhibitors and raf kinase inhibitors and uses thereof |
| US9084781B2 (en) * | 2008-12-10 | 2015-07-21 | Novartis Ag | MEK mutations conferring resistance to MEK inhibitors |
| RS59181B1 (sr) | 2009-10-16 | 2019-10-31 | Novartis Ag | Kombinacija koja sadrži inhibitor mek i inhibitor b-raf |
-
2011
- 2011-03-09 AU AU2011224410A patent/AU2011224410B2/en not_active Ceased
- 2011-03-09 ES ES11709278T patent/ES2714875T3/es active Active
- 2011-03-09 MX MX2012010420A patent/MX343368B/es active IP Right Grant
- 2011-03-09 JP JP2012557201A patent/JP5985401B2/ja active Active
- 2011-03-09 EA EA201290883A patent/EA030276B1/ru not_active IP Right Cessation
- 2011-03-09 WO PCT/US2011/027689 patent/WO2011112678A1/en active Application Filing
- 2011-03-09 EP EP11709278.3A patent/EP2545187B1/en active Active
- 2011-03-09 BR BR112012022801A patent/BR112012022801B8/pt not_active IP Right Cessation
- 2011-03-09 CN CN2011800231091A patent/CN103038364A/zh active Pending
- 2011-03-09 KR KR1020127025801A patent/KR20120139767A/ko active IP Right Grant
- 2011-03-09 US US13/583,056 patent/US20130059851A1/en not_active Abandoned
- 2011-03-09 CA CA2791247A patent/CA2791247C/en not_active Expired - Fee Related
-
2017
- 2017-04-05 US US15/480,126 patent/US11078540B2/en active Active
-
2021
- 2021-06-24 US US17/357,642 patent/US20210404014A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1758910A (zh) * | 2003-03-11 | 2006-04-12 | 诺瓦提斯公司 | 异喹啉衍生物治疗癌症和map激酶相关疾病的用途 |
| CN1889951A (zh) * | 2003-10-16 | 2007-01-03 | 希龙公司 | 取代的苯并唑及其用作raf激酶抑制剂的应用 |
| CN101415689A (zh) * | 2006-04-05 | 2009-04-22 | 阿斯利康(瑞典)有限公司 | 具有抗癌活性的经取代的喹唑啉 |
Non-Patent Citations (2)
| Title |
|---|
| CAROLINE M. EMERYA等: "MEK1 mutations confer resistance to MEK and B-RAF inhibition", 《PNAS》 * |
| CLARA MONTAGUT等: "Elevated CRAF as a Potential Mechanism of Acquired Resistance to BRAF Inhibition in Melanoma", 《CANCER RESARCH》 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105695616A (zh) * | 2016-04-22 | 2016-06-22 | 王冬国 | 诊断甲状腺癌的分析标志物及其应用 |
| CN111601615A (zh) * | 2017-11-02 | 2020-08-28 | 乔治亚大学研究基金公司 | 与轮状病毒产量增加有关的方法和组合物 |
| CN108872438A (zh) * | 2018-08-06 | 2018-11-23 | 杭州迪相实业有限公司 | 一种外泌体中肺癌标志物gk5快速检测试剂盒 |
| CN110862968A (zh) * | 2019-10-30 | 2020-03-06 | 中国农业科学院兰州兽医研究所 | Map3k8基因敲除pk-15细胞系的构建方法及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2791247A1 (en) | 2011-09-15 |
| BR112012022801B1 (pt) | 2019-10-15 |
| EP2545187A1 (en) | 2013-01-16 |
| US20210404014A1 (en) | 2021-12-30 |
| AU2011224410A1 (en) | 2012-09-20 |
| US11078540B2 (en) | 2021-08-03 |
| US20170268069A1 (en) | 2017-09-21 |
| BR112012022801A2 (pt) | 2017-01-10 |
| CA2791247C (en) | 2019-05-14 |
| EA201290883A1 (ru) | 2013-04-30 |
| EP2545187B1 (en) | 2018-09-05 |
| US20130059851A1 (en) | 2013-03-07 |
| WO2011112678A1 (en) | 2011-09-15 |
| EA030276B1 (ru) | 2018-07-31 |
| KR20120139767A (ko) | 2012-12-27 |
| JP2013526843A (ja) | 2013-06-27 |
| JP5985401B2 (ja) | 2016-09-06 |
| ES2714875T3 (es) | 2019-05-30 |
| MX2012010420A (es) | 2012-11-30 |
| BR112012022801B8 (pt) | 2019-10-29 |
| AU2011224410B2 (en) | 2015-05-28 |
| MX343368B (es) | 2016-11-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210404014A1 (en) | Methods of diagnosing and treating cancer in patients having or developing resistance to a first cancer therapy | |
| US11564947B2 (en) | Methods and compositions for cellular immunotherapy | |
| Annesley et al. | Dictyostelium discoideum—a model for many reasons | |
| Boison | Adenosine kinase: exploitation for therapeutic gain | |
| Sasaki et al. | Stimulation of nicotinamide adenine dinucleotide biosynthetic pathways delays axonal degeneration after axotomy | |
| CN101595219B (zh) | 作为编码抗原和蛋白毒素的核苷酸序列的载体的微生物,其制备方法和用途 | |
| Satyanarayana et al. | Mammalian cell-cycle regulation: several Cdks, numerous cyclins and diverse compensatory mechanisms | |
| US11685954B2 (en) | Biomarkers predictive of endocrine resistance in breast cancer | |
| Chen et al. | A chemical-genetic approach reveals the distinct roles of GSK3α and GSK3β in regulating embryonic stem cell fate | |
| CN111133315A (zh) | 用于治疗癌症转移的靶向激酶 | |
| WO2020257730A1 (en) | Compositions comprising circular polyribonucleotides for protein modulation and uses thereof | |
| US20130040853A1 (en) | Context Specific Genetic Screen Platform to Aid in Gene Discovery and Target Validation | |
| US20220125814A1 (en) | Cancer combination therapies utilizing a nicotinamide phosphoribosyltransferase inhibitor in combination with a nicotinamide adenine dinucleotide salvage pathway precursor | |
| US11639508B2 (en) | Engineered TSC2 | |
| US20220118017A1 (en) | Engineered tuberous sclerosis complex 2 polypeptides | |
| WO2020140927A1 (en) | Cancer treatment using multi-targeted kinase inhibitor in combination of protein kinase biomarkers | |
| Sherman Jr | A Metabolic Checkpoint in G2 Regulates Mitotic Entry in Response to Metabolic Stress | |
| Gunnewiek et al. | Sonlicromanol improves neuronal network dysfunction and transcriptome changes linked to m. 3243A> G heteroplasmy | |
| Sousa | The Role of P38α Stress Response Kinase in Aneuploidy Suppression | |
| Duffy | Targeting CTNNB1-Mutant Hepatocellular Carcinoma with a Novel Kinase Inhibitor | |
| CN107091930B (zh) | 快速预测和提高非小细胞肺癌细胞对表皮细胞生长因子受体抑制剂敏感性的方法 | |
| Prahallad et al. | The final version is available at | |
| Al-Mahdi | Identification of novel roles and new modes of regulation for the atypical MAP kinases ERK3 and ERK4 | |
| Puga | Identification of the Saccharomyces Cerevisiae Identification of the SaccharomycesCerevisiae Target of Cetuximab-Erbitux, the Anti-EGFR Antibody Used in the Treatment of Colorectal Cancer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C12 | Rejection of a patent application after its publication | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20130410 |