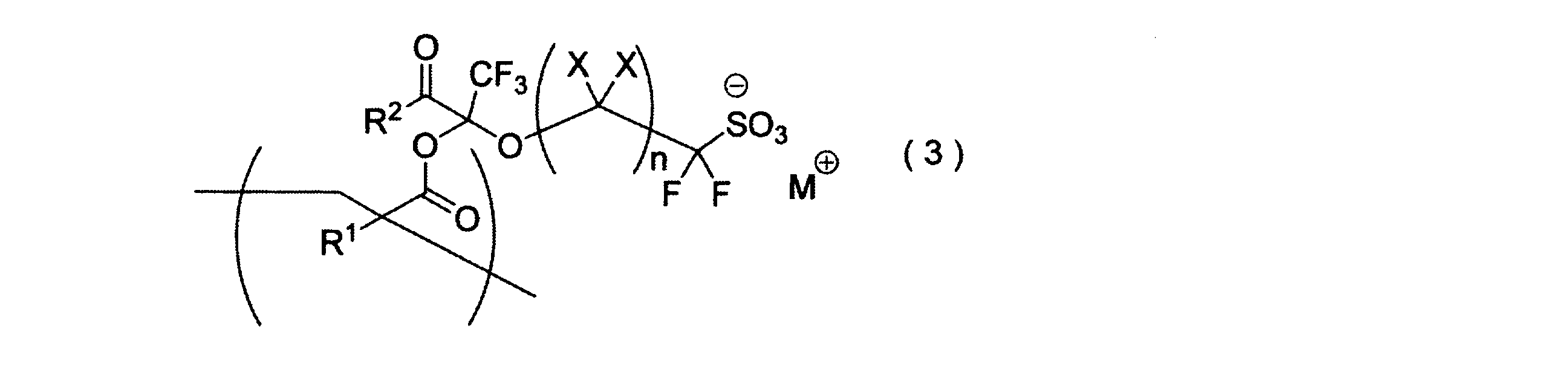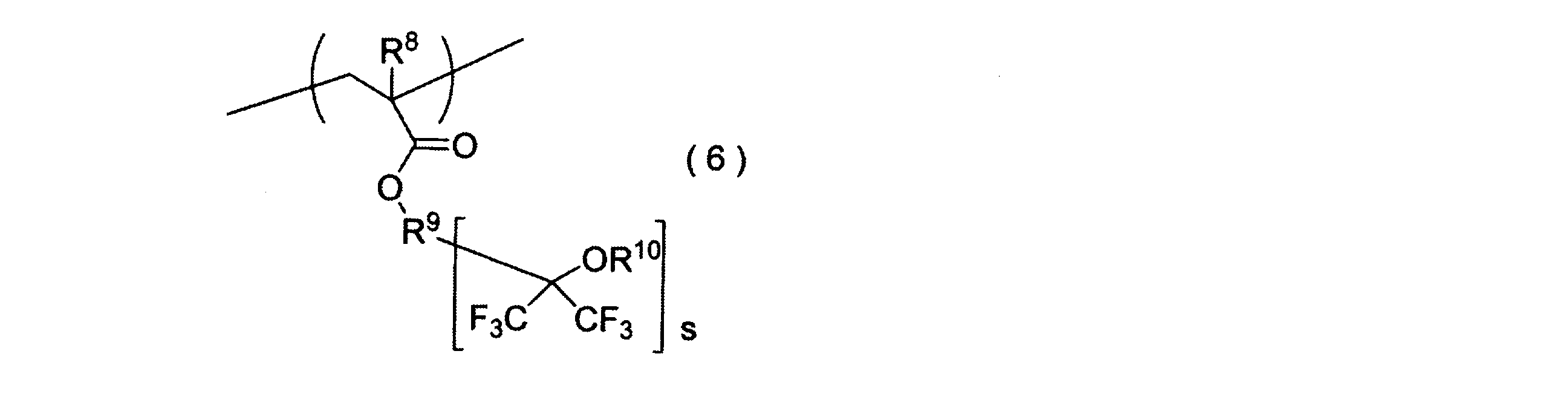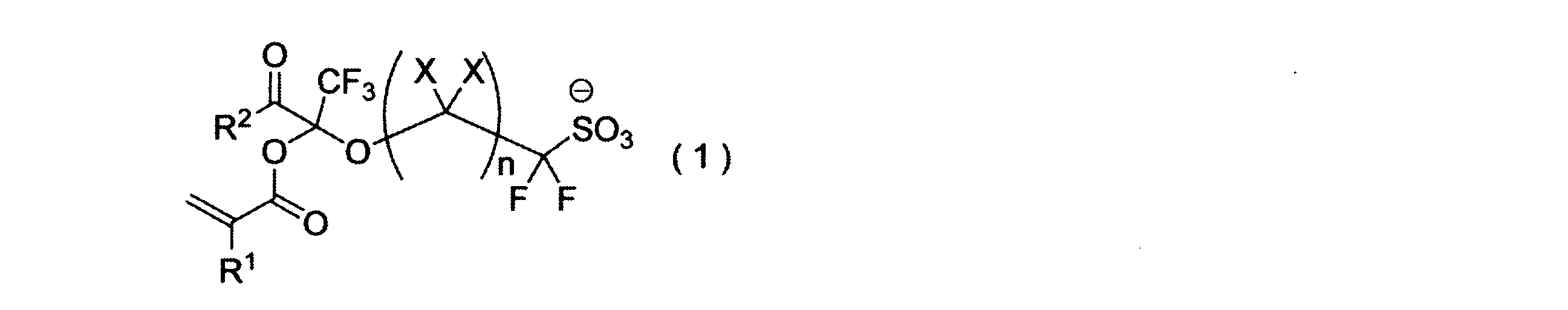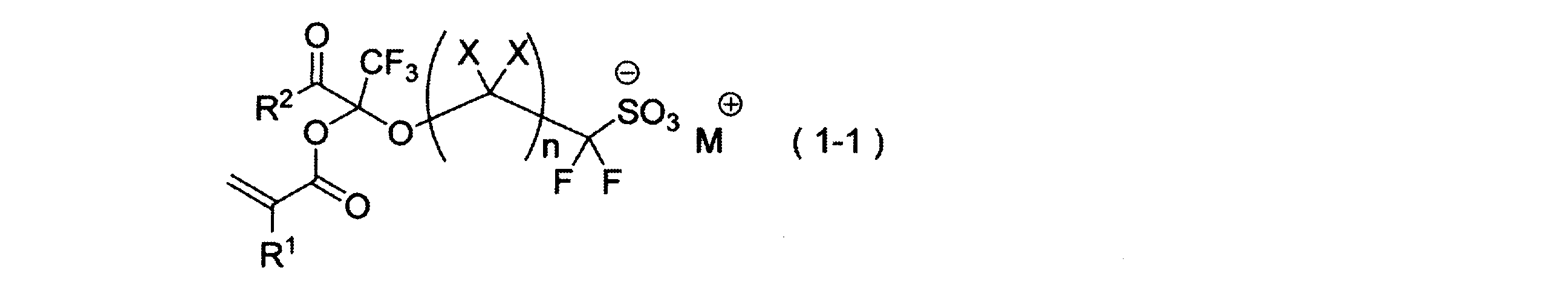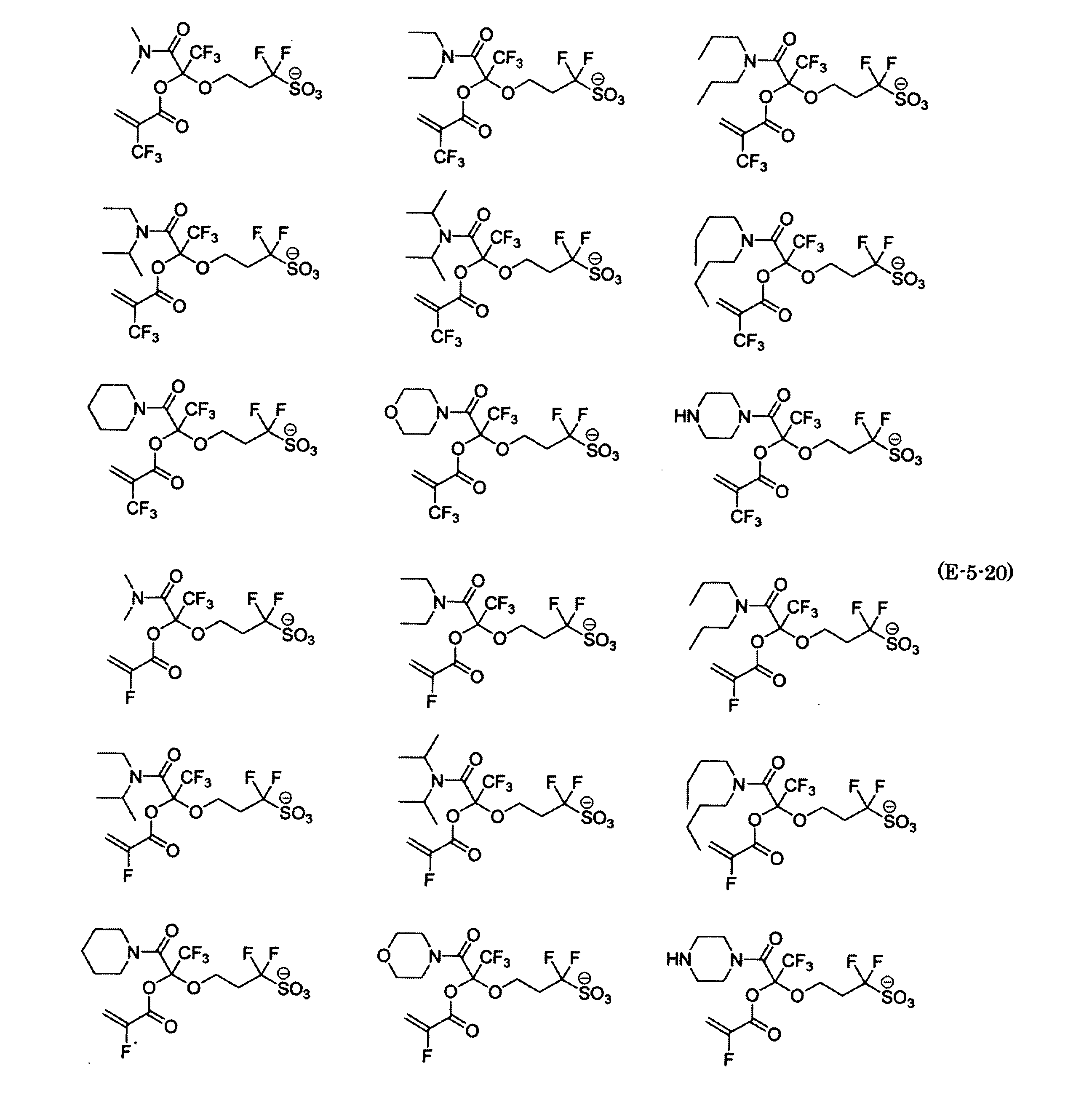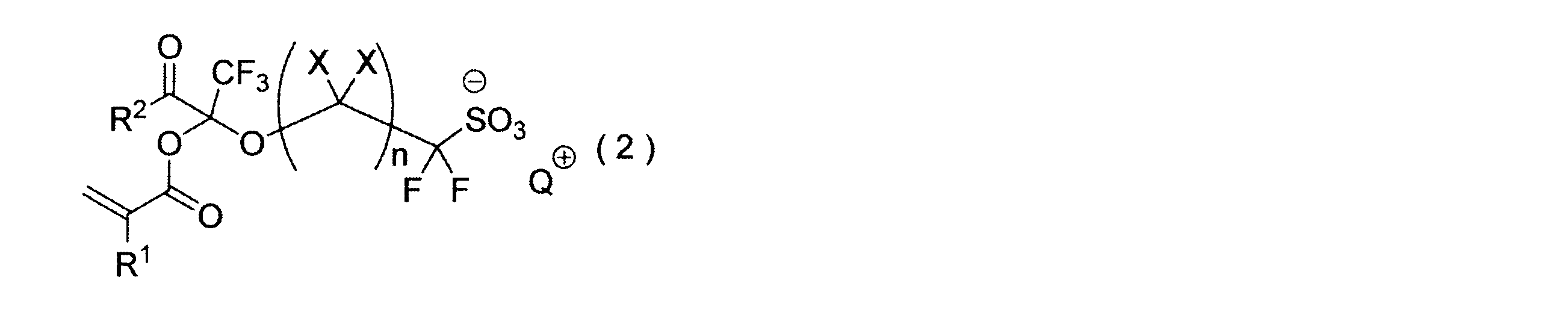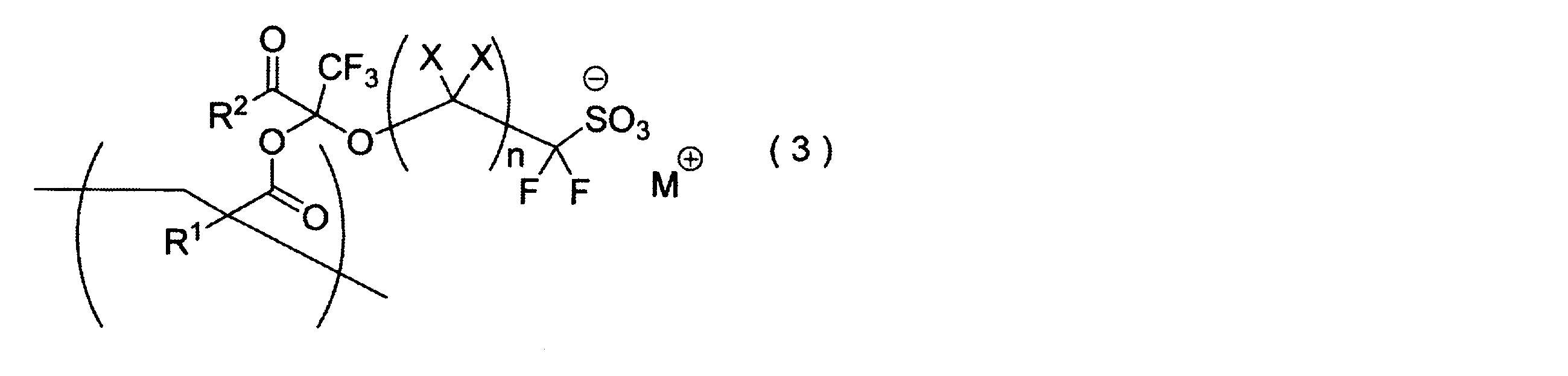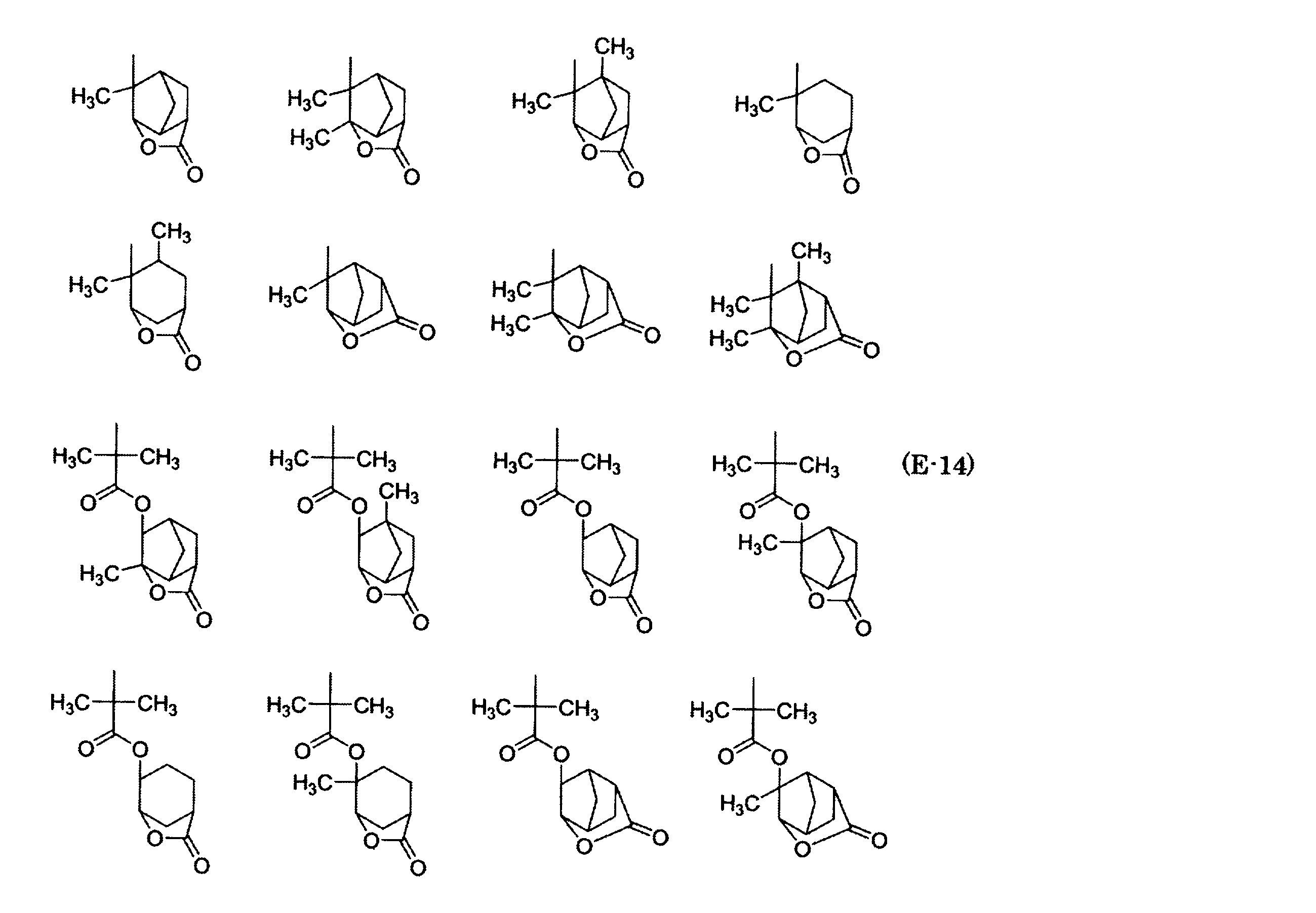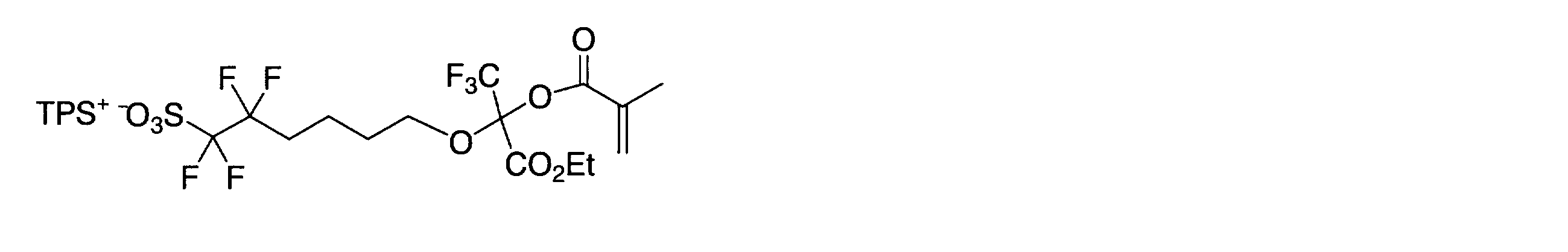WO2012050015A1 - 重合性含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 - Google Patents
重合性含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 Download PDFInfo
- Publication number
- WO2012050015A1 WO2012050015A1 PCT/JP2011/072931 JP2011072931W WO2012050015A1 WO 2012050015 A1 WO2012050015 A1 WO 2012050015A1 JP 2011072931 W JP2011072931 W JP 2011072931W WO 2012050015 A1 WO2012050015 A1 WO 2012050015A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- carbon atoms
- fluorine
- atom
- general formula
- Prior art date
Links
- 0 CCC(CC(C(F)(F)F)(C(F)(F)F)O)OC(C(*)(CC(C)C)*C)=O Chemical compound CCC(CC(C(F)(F)F)(C(F)(F)F)O)OC(C(*)(CC(C)C)*C)=O 0.000 description 17
- WLOQLWBIJZDHET-UHFFFAOYSA-N c(cc1)ccc1[S+](c1ccccc1)c1ccccc1 Chemical compound c(cc1)ccc1[S+](c1ccccc1)c1ccccc1 WLOQLWBIJZDHET-UHFFFAOYSA-N 0.000 description 3
- PYVVEKAUYKIDAH-UHFFFAOYSA-N CCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O Chemical compound CCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O PYVVEKAUYKIDAH-UHFFFAOYSA-N 0.000 description 2
- VBIVMBWRYIKJHM-UHFFFAOYSA-N C=CC(O)OC(C(F)(F)F)(C(Nc1ccc(C(F)(F)F)cc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F Chemical compound C=CC(O)OC(C(F)(F)F)(C(Nc1ccc(C(F)(F)F)cc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F VBIVMBWRYIKJHM-UHFFFAOYSA-N 0.000 description 1
- FEQKBVZINYYDNJ-UHFFFAOYSA-N C=CC(O)OC(C(F)(F)F)(C(Nc1ccccc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F Chemical compound C=CC(O)OC(C(F)(F)F)(C(Nc1ccccc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F FEQKBVZINYYDNJ-UHFFFAOYSA-N 0.000 description 1
- LFJFXZKRUYWUBL-UHFFFAOYSA-N C=CC(OC(C(F)(F)F)(C(NC(C(F)(F)F)C(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O Chemical compound C=CC(OC(C(F)(F)F)(C(NC(C(F)(F)F)C(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O LFJFXZKRUYWUBL-UHFFFAOYSA-N 0.000 description 1
- KYZKWTDHHKOORV-UHFFFAOYSA-N C=CC(OC(C(F)(F)F)(C(NCC(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O Chemical compound C=CC(OC(C(F)(F)F)(C(NCC(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O KYZKWTDHHKOORV-UHFFFAOYSA-N 0.000 description 1
- HLQRCWPXFUFTHT-UHFFFAOYSA-N C=CC(OC(C(F)(F)F)(C(NCCC(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O Chemical compound C=CC(OC(C(F)(F)F)(C(NCCC(F)(F)F)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O HLQRCWPXFUFTHT-UHFFFAOYSA-N 0.000 description 1
- IXZSEIZOXBZPGB-UHFFFAOYSA-N C=CC(OC(C(F)(F)F)(C(NCc1ccccc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O Chemical compound C=CC(OC(C(F)(F)F)(C(NCc1ccccc1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O IXZSEIZOXBZPGB-UHFFFAOYSA-N 0.000 description 1
- JLKZWITVQJLPOG-UHFFFAOYSA-N C=CCNC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C=C)=O)=O Chemical compound C=CCNC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C=C)=O)=O JLKZWITVQJLPOG-UHFFFAOYSA-N 0.000 description 1
- RPXWICBYBMNAGD-UHFFFAOYSA-N CC(C(C1CC2)OC1=O)C2OC(C(C)(C)C)=O Chemical compound CC(C(C1CC2)OC1=O)C2OC(C(C)(C)C)=O RPXWICBYBMNAGD-UHFFFAOYSA-N 0.000 description 1
- XGASNPYAQAFKTQ-UHFFFAOYSA-N CC(C(OC(C(F)(F)F)(C(O)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C Chemical compound CC(C(OC(C(F)(F)F)(C(O)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C XGASNPYAQAFKTQ-UHFFFAOYSA-N 0.000 description 1
- ZSSUMPVOZXPPLO-UHFFFAOYSA-N CC(C(OC(C(F)(F)F)(C(OC)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C Chemical compound CC(C(OC(C(F)(F)F)(C(OC)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C ZSSUMPVOZXPPLO-UHFFFAOYSA-N 0.000 description 1
- JOWFGYOADJPZHU-UHFFFAOYSA-N CC(C(OC(C(F)(F)F)(C(OC1CCCCC1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C Chemical compound CC(C(OC(C(F)(F)F)(C(OC1CCCCC1)=O)OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)=O)=C JOWFGYOADJPZHU-UHFFFAOYSA-N 0.000 description 1
- QDEQKWJUTULMCS-UHFFFAOYSA-N CC(C(OCC(F)(F)[S](C)(O)(=O)=O)=O)=C Chemical compound CC(C(OCC(F)(F)[S](C)(O)(=O)=O)=O)=C QDEQKWJUTULMCS-UHFFFAOYSA-N 0.000 description 1
- LFYHJTAZTYYZQP-UHFFFAOYSA-N CC(C(OCC(OCC(F)(F)[S](C)(O)(=O)=O)=O)=O)=C Chemical compound CC(C(OCC(OCC(F)(F)[S](C)(O)(=O)=O)=O)=O)=C LFYHJTAZTYYZQP-UHFFFAOYSA-N 0.000 description 1
- UEHLSSPEUVUNOJ-QMDOVSTPSA-N CC(C)(C(C)(C[C@H]1C2)C2C=O)C1(C)OC Chemical compound CC(C)(C(C)(C[C@H]1C2)C2C=O)C1(C)OC UEHLSSPEUVUNOJ-QMDOVSTPSA-N 0.000 description 1
- WBJAFQBFCJOVSL-UHFFFAOYSA-N CC(C)(C(CC1)CC23)C1(C)[O]2C3=O Chemical compound CC(C)(C(CC1)CC23)C1(C)[O]2C3=O WBJAFQBFCJOVSL-UHFFFAOYSA-N 0.000 description 1
- NKCUWVKVKWRLEH-UHFFFAOYSA-N CC(C)(C)C(COC(C(C1C2)O3)C2(C)CC1C3=O)=O Chemical compound CC(C)(C)C(COC(C(C1C2)O3)C2(C)CC1C3=O)=O NKCUWVKVKWRLEH-UHFFFAOYSA-N 0.000 description 1
- VJSAZARMYCBGDD-UHFFFAOYSA-N CC(C)(C)C(O)OC(C)(CCC1C2)C2OC1=O Chemical compound CC(C)(C)C(O)OC(C)(CCC1C2)C2OC1=O VJSAZARMYCBGDD-UHFFFAOYSA-N 0.000 description 1
- XMRWETRALXTWDF-UHFFFAOYSA-N CC(C)(C)C(OC(C)(C(C1C2C3)C13C=O)C2O)=O Chemical compound CC(C)(C)C(OC(C)(C(C1C2C3)C13C=O)C2O)=O XMRWETRALXTWDF-UHFFFAOYSA-N 0.000 description 1
- JTFKXFKZCJIPJJ-UHFFFAOYSA-N CC(C)(C)C(OC(C1[O]2C1(C1)C3)C1CC3C2=O)=O Chemical compound CC(C)(C)C(OC(C1[O]2C1(C1)C3)C1CC3C2=O)=O JTFKXFKZCJIPJJ-UHFFFAOYSA-N 0.000 description 1
- RCIWRWVEVGSSSL-UHFFFAOYSA-N CC(C)(C)OC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)O)=O Chemical compound CC(C)(C)OC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)O)=O RCIWRWVEVGSSSL-UHFFFAOYSA-N 0.000 description 1
- WCJHFKYIRISSNV-UHFFFAOYSA-N CC(C)(C12)C(CC34)CC13[O]2C4=O Chemical compound CC(C)(C12)C(CC34)CC13[O]2C4=O WCJHFKYIRISSNV-UHFFFAOYSA-N 0.000 description 1
- OWCVADAHTHKQCI-UHFFFAOYSA-N CC(C)(C1C2CC3C1)C3(C)OC2=O Chemical compound CC(C)(C1C2CC3C1)C3(C)OC2=O OWCVADAHTHKQCI-UHFFFAOYSA-N 0.000 description 1
- JIDUYKVRIBICNS-UHFFFAOYSA-N CC(C)(C1C2CC3C1)C3OC2=O Chemical compound CC(C)(C1C2CC3C1)C3OC2=O JIDUYKVRIBICNS-UHFFFAOYSA-N 0.000 description 1
- DCZKEYQDFAKVHA-UHFFFAOYSA-N CC(C)(C1CC2)C2(C)CC2[O]1C2=O Chemical compound CC(C)(C1CC2)C2(C)CC2[O]1C2=O DCZKEYQDFAKVHA-UHFFFAOYSA-N 0.000 description 1
- DRTQJBJJOIPIIE-UHFFFAOYSA-N CC(C)(CCC1C2)C2OC1=O Chemical compound CC(C)(CCC1C2)C2OC1=O DRTQJBJJOIPIIE-UHFFFAOYSA-N 0.000 description 1
- UOHGSASLIWKBFF-UHFFFAOYSA-N CC(C)COC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O Chemical compound CC(C)COC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O UOHGSASLIWKBFF-UHFFFAOYSA-N 0.000 description 1
- KHYRJDWXXYTMEO-UHFFFAOYSA-N CC(C)OC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O Chemical compound CC(C)OC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O KHYRJDWXXYTMEO-UHFFFAOYSA-N 0.000 description 1
- SXCPEDAWXQTVGY-HPGAGZEXSA-N CC(C1)(CC(C2)CC(C3)O4)[C@@]23C1C4=O Chemical compound CC(C1)(CC(C2)CC(C3)O4)[C@@]23C1C4=O SXCPEDAWXQTVGY-HPGAGZEXSA-N 0.000 description 1
- IJYSIKPQVCCQMN-UHFFFAOYSA-N CC(CC1C2)(CC(C3)OC1=O)CC23O Chemical compound CC(CC1C2)(CC(C3)OC1=O)CC23O IJYSIKPQVCCQMN-UHFFFAOYSA-N 0.000 description 1
- VHWIQHFAHMMBMR-GIROJAGPSA-N CC(CC1C2)([C@@]1(C1)C2CC1O1)C1=O Chemical compound CC(CC1C2)([C@@]1(C1)C2CC1O1)C1=O VHWIQHFAHMMBMR-GIROJAGPSA-N 0.000 description 1
- RBVYJVWTFIKORT-UHFFFAOYSA-N CC(CNC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C=C)=O)=O)=O Chemical compound CC(CNC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C=C)=O)=O)=O RBVYJVWTFIKORT-UHFFFAOYSA-N 0.000 description 1
- JKNDVLIYSJWLIB-UHFFFAOYSA-N CC1(C=CC=CC1)S(c1ccccc1)c1ccccc1 Chemical compound CC1(C=CC=CC1)S(c1ccccc1)c1ccccc1 JKNDVLIYSJWLIB-UHFFFAOYSA-N 0.000 description 1
- AWIAYVVIPVYJMI-UHFFFAOYSA-N CC1(CC(C2)C3)C(O)OC3CC2C1 Chemical compound CC1(CC(C2)C3)C(O)OC3CC2C1 AWIAYVVIPVYJMI-UHFFFAOYSA-N 0.000 description 1
- HFWILJLAXOZDFK-UHFFFAOYSA-N CC1(CC2CC(C3)C1)CC3OC2=O Chemical compound CC1(CC2CC(C3)C1)CC3OC2=O HFWILJLAXOZDFK-UHFFFAOYSA-N 0.000 description 1
- QUBREXKQBMNJJQ-UHFFFAOYSA-N CC1C([S+](c2ccccc2)c2ccccc2)=CC=CC1 Chemical compound CC1C([S+](c2ccccc2)c2ccccc2)=CC=CC1 QUBREXKQBMNJJQ-UHFFFAOYSA-N 0.000 description 1
- JVOFPHOOCKKVER-UHFFFAOYSA-N CCCCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OCOCC(C)=C)=O Chemical compound CCCCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OCOCC(C)=C)=O JVOFPHOOCKKVER-UHFFFAOYSA-N 0.000 description 1
- KYTULBHLTSGKBZ-UHFFFAOYSA-N CCCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O Chemical compound CCCOC(C(C(F)(F)F)(OCCCCC(C(F)(F)S(O)(=O)=O)(F)F)OC(C(C)=C)=O)=O KYTULBHLTSGKBZ-UHFFFAOYSA-N 0.000 description 1
- DQCPNLDURFHLSU-UHFFFAOYSA-N CCOC(C(C(F)(F)F)(OCC(F)(F)[S](C)(O)(=O)=O)OC(C(C)=C)=O)=O Chemical compound CCOC(C(C(F)(F)F)(OCC(F)(F)[S](C)(O)(=O)=O)OC(C(C)=C)=O)=O DQCPNLDURFHLSU-UHFFFAOYSA-N 0.000 description 1
- XICUHAYRFUYFMX-UHFFFAOYSA-N CCOC(C(C(F)(F)F)(OCCC(C)(C(F)(F)[S](C)(O)(=O)=O)F)[O](C)C(C(C)=C)=O)=O Chemical compound CCOC(C(C(F)(F)F)(OCCC(C)(C(F)(F)[S](C)(O)(=O)=O)F)[O](C)C(C(C)=C)=O)=O XICUHAYRFUYFMX-UHFFFAOYSA-N 0.000 description 1
- JGTNAGYHADQMCM-UHFFFAOYSA-N OS(C(C(C(C(F)(F)F)(F)F)(F)F)(F)F)(=O)=O Chemical compound OS(C(C(C(C(F)(F)F)(F)F)(F)F)(F)F)(=O)=O JGTNAGYHADQMCM-UHFFFAOYSA-N 0.000 description 1
- GBGBCPSGWNTKEK-UHFFFAOYSA-N c(cc1)ccc1S(c1ccccc1)c1ccccc1 Chemical compound c(cc1)ccc1S(c1ccccc1)c1ccccc1 GBGBCPSGWNTKEK-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F28/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a bond to sulfur or by a heterocyclic ring containing sulfur
- C08F28/02—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a bond to sulfur or by a heterocyclic ring containing sulfur by a bond to sulfur
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F20/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride, ester, amide, imide or nitrile thereof
- C08F20/02—Monocarboxylic acids having less than ten carbon atoms, Derivatives thereof
- C08F20/10—Esters
- C08F20/38—Esters containing sulfur
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/03—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton
- C07C309/07—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton
- C07C309/09—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton containing etherified hydroxy groups bound to the carbon skeleton
- C07C309/10—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton containing etherified hydroxy groups bound to the carbon skeleton with the oxygen atom of at least one of the etherified hydroxy groups further bound to an acyclic carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C381/00—Compounds containing carbon and sulfur and having functional groups not covered by groups C07C301/00 - C07C337/00
- C07C381/12—Sulfonium compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/26—Esters containing oxygen in addition to the carboxy oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F232/00—Copolymers of cyclic compounds containing no unsaturated aliphatic radicals in a side chain, and having one or more carbon-to-carbon double bonds in a carbocyclic ring system
- C08F232/02—Copolymers of cyclic compounds containing no unsaturated aliphatic radicals in a side chain, and having one or more carbon-to-carbon double bonds in a carbocyclic ring system having no condensed rings
- C08F232/04—Copolymers of cyclic compounds containing no unsaturated aliphatic radicals in a side chain, and having one or more carbon-to-carbon double bonds in a carbocyclic ring system having no condensed rings having one carbon-to-carbon double bond
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0046—Photosensitive materials with perfluoro compounds, e.g. for dry lithography
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/038—Macromolecular compounds which are rendered insoluble or differentially wettable
- G03F7/0382—Macromolecular compounds which are rendered insoluble or differentially wettable the macromolecular compound being present in a chemically amplified negative photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0397—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having an alicyclic moiety in a side chain
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
- G03F7/2037—Exposure with X-ray radiation or corpuscular radiation, through a mask with a pattern opaque to that radiation
- G03F7/2039—X-ray radiation
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
- G03F7/2041—Exposure; Apparatus therefor in the presence of a fluid, e.g. immersion; using fluid cooling means
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/26—Processing photosensitive materials; Apparatus therefor
- G03F7/42—Stripping or agents therefor
- G03F7/422—Stripping or agents therefor using liquids only
- G03F7/426—Stripping or agents therefor using liquids only containing organic halogen compounds; containing organic sulfonic acids or salts thereof; containing sulfoxides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
Definitions
- the present invention relates to novel polymerizable fluorine-containing sulfonates having an anion structure, fluorine-containing sulfonate resins, resist compositions, and a pattern forming method using the same.
- a resist composition suitable as a chemically amplified resist useful for microfabrication using high energy rays a novel fluorine-containing sulfonate resin used in the composition, and used for the synthesis of this fluorine-containing sulfonate resin
- the present invention relates to novel fluorine-containing sulfonates.
- the exposure becomes shorter in wavelength, the focus depth margin (hereinafter referred to as “DOF”) is wide, and the pattern line edge roughness (hereinafter referred to as “LER”). ) Is low, the resolution is excellent, and further, there is a demand for a resist composition that is excellent in sensitivity, substrate adhesion, and etching resistance.
- DOE focus depth margin
- LER pattern line edge roughness
- Measures for shortening the exposure wavelength were obtained by introducing fluorine atoms or introducing an alicyclic structure into the resist resin.
- fluorine-containing sulfonic acid having a high acid strength as an anion
- an acid generator is used in order to improve these resist characteristics.
- Attempts have been made to incorporate the function into the resist resin (Patent Documents 1 to 7), and a resin having an onium sulfonate salt in the side chain in which the anion side of the acid generator is incorporated into the resist resin has been proposed.
- Patent Documents 6 and 7 disclose resist compositions using a resin obtained by polymerizing or copolymerizing a methacrylic acid ester having a triphenylsulfonium salt structure of a sulfonic acid having a fluorine atom at the ⁇ -position in the side chain. ing.
- a sulfonate onium salt is incorporated in a side chain as an anion with an excellent resolution, a wide DOF, a low LER, a high sensitivity, and a resist pattern capable of forming an excellent pattern shape.
- Resist resins fixed on the resin side have been proposed, but such resins have low solubility in commonly used resist solvents (eg, propylene glycol monomethyl ether acetate) and generate a sufficient amount of acid.
- resist solvents eg, propylene glycol monomethyl ether acetate
- a resist solvent for example, propylene glycol monomethyl
- a polymerizable fluorine-containing sulfonic acid onium salt having a specific fluorine-containing sulfonate structure is generally used.
- a positive or negative resist composition prepared therefrom has excellent resolution, wide DOF, L It found that to form a R is small pattern, and completed the present invention.
- the present invention is as follows.
- each X independently represents a hydrogen atom or a fluorine atom.
- N represents an integer of 1 to 10.
- R 1 represents a hydrogen atom, a halogen atom having 1 to 3 carbon atoms or a C 1 to 3 carbon atom.
- R 2 represents R A O or R B R C N, where R A , R B and R C are each independently a hydrogen atom, having 1 to 20 carbon atoms An alkyl group, an alkenyl group having 2 to 20 carbon atoms, an oxoalkyl group having 2 to 20 carbon atoms, an aryl group having 6 to 18 carbon atoms, an aralkyl group having 6 to 18 carbon atoms, or a lactone group having 3 to 30 carbon atoms.
- R B and R C may be bonded to each other to form a heterocyclic ring having 3 to 18 ring members together with the nitrogen atom (N) of R B R C N.
- R A , R B and R C a hydrogen atom on the carbon contained is to optionally .M + is substituted by a substituent, a monovalent Representing the thione.
- R 6 and R 7 are each independently a substituted or unsubstituted alkyl group having 1 to 20 carbon atoms, an alkenyl group or an oxoalkyl group, or a substituted or unsubstituted aryl group having 6 to 18 carbon atoms, It represents an aralkyl group or an aryloxoalkyl group, or R 6 and R 7 may be bonded to each other to form a ring together with the iodine atom in the formula.
- invention 3 The sulfonate resin of invention 1 having a repeating unit represented by the following general formula (5). (Wherein, X, n, R 1 and R 2 are each X, n, R 1 and R 2 synonymous in the general formula (3).)
- invention 4 Further, olefins, fluorine-containing olefins, acrylic esters, methacrylic esters, fluorine-containing acrylic esters, fluorine-containing methacrylate esters, norbornene compounds, fluorine-containing norbornene compounds, styrene compounds, fluorine-containing styrene compounds, vinyl ethers, and fluorine-containing compounds
- the sulfonate resin of inventions 1 to 3 having one or more repeating units selected from the group consisting of repeating units formed by cleavage of a polymerizable double bond contained in vinyl ether.
- the sulfonate resin of inventions 1 to 4 having a repeating unit represented by the following general formula (6).
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 9 represents a substituted or unsubstituted aliphatic hydrocarbon group, a substituted or unsubstituted aromatic group.
- R 10 is a group or an organic group in which a plurality of them are connected, and any number of hydrogen atoms may be substituted with a fluorine atom, and R 10 is a hydrogen atom, a substituted or unsubstituted C 1-25, An aliphatic hydrocarbon group or a substituted or unsubstituted aromatic hydrocarbon group having 1 to 25 carbon atoms in which any number of hydrogen atoms may be substituted with a fluorine atom, including an ether bond and a carbonyl group And s represents an integer of 1 to 2.
- the sulfonate resin of inventions 1 to 5 having a repeating unit represented by the following general formula (7).
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 11 , R 12 and R 13 is CF 3 C (CF 3 ) (OH) CH 2 — group, the remaining two being hydrogen atoms.
- the sulfonate resin of inventions 1 to 6 having a repeating unit represented by the following general formula (8).
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 14 represents a hydrogen atom, an alkyl group having 1 to 4 carbon atoms or a fluorine-containing alkyl group.
- the sulfonate resin of inventions 1 to 7 having a repeating unit represented by the following general formula (9).
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group
- R 15 represents a methyl group or a trifluoromethyl group
- R 16 represents a hydrogen atom, substituted or A group containing an unsubstituted aliphatic hydrocarbon group having 1 to 25 carbon atoms or a substituted or unsubstituted aromatic hydrocarbon group having 1 to 25 carbon atoms, a part of which is a fluorine atom, an ether bond, or a carbonyl group
- U represents an integer of 0 to 2
- t and v each represents an integer of 1 to 8, and satisfies v ⁇ t + 2.
- R 15 and R 16 may be the same. May be different.
- invention 9 Furthermore, the sulfonate resin of inventions 1 to 8 having a repeating unit represented by the following general formula (10). (In the formula, Y represents —CH 2 —, —O—, or —S—. W represents an integer of 2 to 6)
- the sulfonate resin of inventions 1 to 9 having a repeating unit represented by the following general formula (11) or general formula (11-1).
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 18 represents a hydrogen atom, a fluorine atom or a fluorine-containing alkyl group, and J represents a divalent linking group.
- R 17 represents a hydrogen atom, a substituted or unsubstituted aliphatic hydrocarbon group having 1 to 25 carbon atoms, or a substituted or unsubstituted aromatic hydrocarbon group having 1 to 25 carbon atoms, a part of which May contain a fluorine atom, an ether bond or a carbonyl group, and R 17-1 represents an acid labile group.
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 19 and R 20 each independently represents a hydrogen atom, a substituted or unsubstituted carbon atom having 1 carbon atom.
- invention 12 An invention having a repeating unit in which — (CX 2 ) — is represented by — (CH 2 ) p — (CF 2 ) q —, p is an integer of 0 to 10 and q is an integer of 0 to 8. 1 to 11 sulfonate resins.
- a resist composition comprising at least the sulfonate resin of inventions 1 to 13 and a solvent.
- invention 15 The chemically amplified positive resist composition according to invention 14, wherein the sulfonate resin is a sulfonate resin having an acid labile group.
- invention 16 The chemically amplified positive resist composition of Invention 14 or Invention 15, further comprising a resin having an acid labile group.
- invention 17 The chemically amplified negative resist composition of invention 14, wherein the sulfonate resin is a sulfonate resin having an alcoholic hydroxyl group or a carboxyl group.
- invention 18 The chemically amplified negative resist composition of Invention 12 or Invention 17, further comprising a resin having an alcoholic hydroxyl group or a carboxyl group.
- invention 19 A step of applying the resist composition of the invention 14 to 18 on a substrate, a step of exposing with a high energy ray having a wavelength of 300 nm or less through a photomask after the heat treatment, and a heat treatment if necessary; And a developing process using the pattern forming method.
- invention 20 In the exposure process, immersion lithography is performed in which an ArF excimer laser having a wavelength of 193 nm is used and water or a liquid other than water having a refractive index higher than that of air is inserted between the substrate coated with the resist composition and the projection lens.
- the pattern formation method of the invention 19 characterized by the above-mentioned.
- invention 21 The pattern forming method according to invention 19, wherein the exposure step uses soft X-rays (EUV light) having a wavelength of 10 to 14 nm.
- EUV light soft X-rays
- each X independently represents a hydrogen atom or a fluorine atom.
- N represents an integer of 1 to 10.
- R 1 represents a hydrogen atom, a halogen atom having 1 to 3 carbon atoms or an alkyl group having 1 to 3 carbon atoms.
- R 2 represents R A O or R B R C N, where R A , R B and R C are each independently a hydrogen atom, having 1 to 20 carbon atoms An alkyl group, an alkenyl group having 2 to 20 carbon atoms, an oxoalkyl group having 2 to 20 carbon atoms, an aryl group having 6 to 18 carbon atoms, an aralkyl group having 6 to 18 carbon atoms, or a lactone group having 3 to 30 carbon atoms.
- R B and R C may be bonded to each other to form a heterocyclic ring having 3 to 18 ring members together with the nitrogen atom (N) of R B R C N.
- N nitrogen atom
- R B , R B and R C The hydrogen atom on the contained carbon may be substituted with a substituent.
- each X independently represents a hydrogen atom or a fluorine atom.
- N represents an integer of 1 to 10.
- R 1 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms, or 1 to 3 carbon atoms.
- R 2 represents one of R A O and R B R C N, where R A , R B and R C are each independently a hydrogen atom, having 1 to 20 carbon atoms An alkyl group having 2 to 20 carbon atoms, an oxoalkyl group having 2 to 20 carbon atoms, an aryl group having 6 to 18 carbon atoms, an aralkyl group having 6 to 18 carbon atoms, or a lactone group having 3 to 30 carbon atoms.
- R B and R C may be bonded to each other to form a heterocyclic ring having 3 to 18 ring members together with the nitrogen atom (N) of R B R C N.
- R A , R B and a hydrogen atom on the carbon contained in the R C is optionally substituted by a substituent .
- Q + is Serial formula (a) represented by the sulfonium cation, or an iodonium cation represented by the following formula (b).)
- R 3 , R 4 and R 5 are each independently a substituted or unsubstituted alkyl group, alkenyl group or oxoalkyl group having 1 to 20 carbon atoms, or a substituted or unsubstituted carbon group having 6 to 18 carbon atoms.
- R 6 and R 7 are each independently a substituted or unsubstituted alkyl group having 1 to 20 carbon atoms, an alkenyl group or an oxoalkyl group, or a substituted or unsubstituted aryl group having 6 to 18 carbon atoms, It represents an aralkyl group or an aryloxoalkyl group, or R 6 and R 7 may be bonded to each other to form a ring together with the iodine atom in the formula.
- the resin having the fluorine-containing sulfonate structure of the present invention as a repeating unit has high solubility in propylene glycol monomethyl ether acetate, and a positive or negative resist prepared therefrom has excellent resolution, wide DOF, and low LER. Furthermore, there is an effect that an excellent pattern shape with high sensitivity can be formed. Also.
- the polymerizable fluorine-containing sulfonate of the present invention can be copolymerized with a wide range of monomers used for introducing a repeating unit contained in a resin used in a resist, and has an effect that the design of the resin is easy. Play.
- the high energy ray means an electromagnetic wave or a particle beam that acts on the resist composition to generate an acid, and is generally near ultraviolet (wavelength 380 to 200 nm) or vacuum ultraviolet (far ultraviolet, VUV, wavelength).
- EUV extreme ultraviolet rays
- soft X-rays electromagnetic waves classified as X-rays or ⁇ rays, or particle beams such as electron beams.
- the names of these electromagnetic waves are for convenience, and for example, a wavelength of 10 to 14 nm may be called EUV light or soft X-ray.
- salt includes the case where the cation is “H + ” unless otherwise noted.
- the polymerizable fluorine-containing sulfonic acid or polymerizable fluorine-containing sulfonate having an anion represented by the general formula (1) is a polymerizable fluorine-containing sulfonic acid or polymerizable fluorine-containing salt represented by the general formula (1-1). It can be a sulfonate.
- M represents a proton or a monovalent cation.
- M + represents a metal cation such as lithium ion, sodium ion or potassium ion, or an onium ion such as ammonium ion, sulfonium ion, iodonium ion or phosphonium ion.
- each X independently represents a hydrogen atom or a fluorine atom.
- n represents an integer of 1 to 10 and is preferably an integer of 1 to 6.
- the structure represented by — (CX 2 ) n — is a linear alkylene group having 1 to 10 carbon atoms, and an arbitrary hydrogen atom is Of these, an alkylene group substituted with a fluorine atom, and a structure represented by — (CH 2 ) p — (CF 2 ) q — is preferred.
- p is an integer of 0 to 10
- q is an integer of 0 to 8
- p is an integer of 1 to 6
- q is preferably an integer of 0 to 5
- p is an integer of 1 to 4
- q is 0 Or it is more preferable that it is 1.
- the resin having an onium sulfonic acid salt fixed to the side chain of the polymer has a site that functions as a chemically amplified photoacid generator fixed to the side chain of the polymer chain.
- it is easy to diffuse by specifying the chemical structure of the linking group separating the acid site from the main chain and the length of the side chain in this way. The diffusion distance can be adjusted.
- R 1 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 1 includes a fluorine atom, a chlorine atom, a bromine atom, and an iodine atom as the halogen atom.
- alkyl group having 1 to 3 carbon atoms include a methyl group, an ethyl group, an n-propyl group, and an i-propyl group.
- fluorine-containing alkyl group having 1 to 3 carbon atoms examples include fluoromethyl group, difluoromethyl group, trifluoromethyl group, 2-fluoroethyl group, 2,2-difluoroethyl group, 2,2,2-trifluoroethyl group Pentafluoroethyl group, 1-methyl-2,2,2-trifluoroethyl group, 1- (trifluoromethyl) -2,2,2-trifluoroethyl group, 1- (trifluoromethyl) -1, Examples include 2,2,2-tetrafluoroethyl group.
- preferred as R 1 are a hydrogen atom, a fluorine atom, a methyl group, and a trifluoromethyl group.
- R 2 represents any group of R A O and R B R C N.
- R A , R B and R C are each independently a hydrogen atom, an alkyl group having 1 to 20 carbon atoms, an alkenyl group having 2 to 20 carbon atoms or an oxoalkyl group having 2 to 20 carbon atoms, or 6 to 6 carbon atoms.
- 18 represents an aryl group, an aralkyl group having 6 to 18 carbon atoms, or a lactone group having 3 to 30 carbon atoms.
- the alkyl group having 1 to 20 carbon atoms is a linear alkyl group having 1 to 20 carbon atoms, a branched alkyl group having 3 to 20 carbon atoms, or a cyclic alkyl group having 3 to 20 carbon atoms.
- the lactone group having 3 to 30 carbon atoms is a monocyclic or polycyclic lactone group having 3 to 30 carbon atoms.
- R B and R C may be bonded to each other to form a heterocyclic ring having 3 to 18 ring members together with the nitrogen atom (N) of R B R C N.
- the hydrogen atoms on carbon contained in R A, R B and R C may be substituted by a substituent.
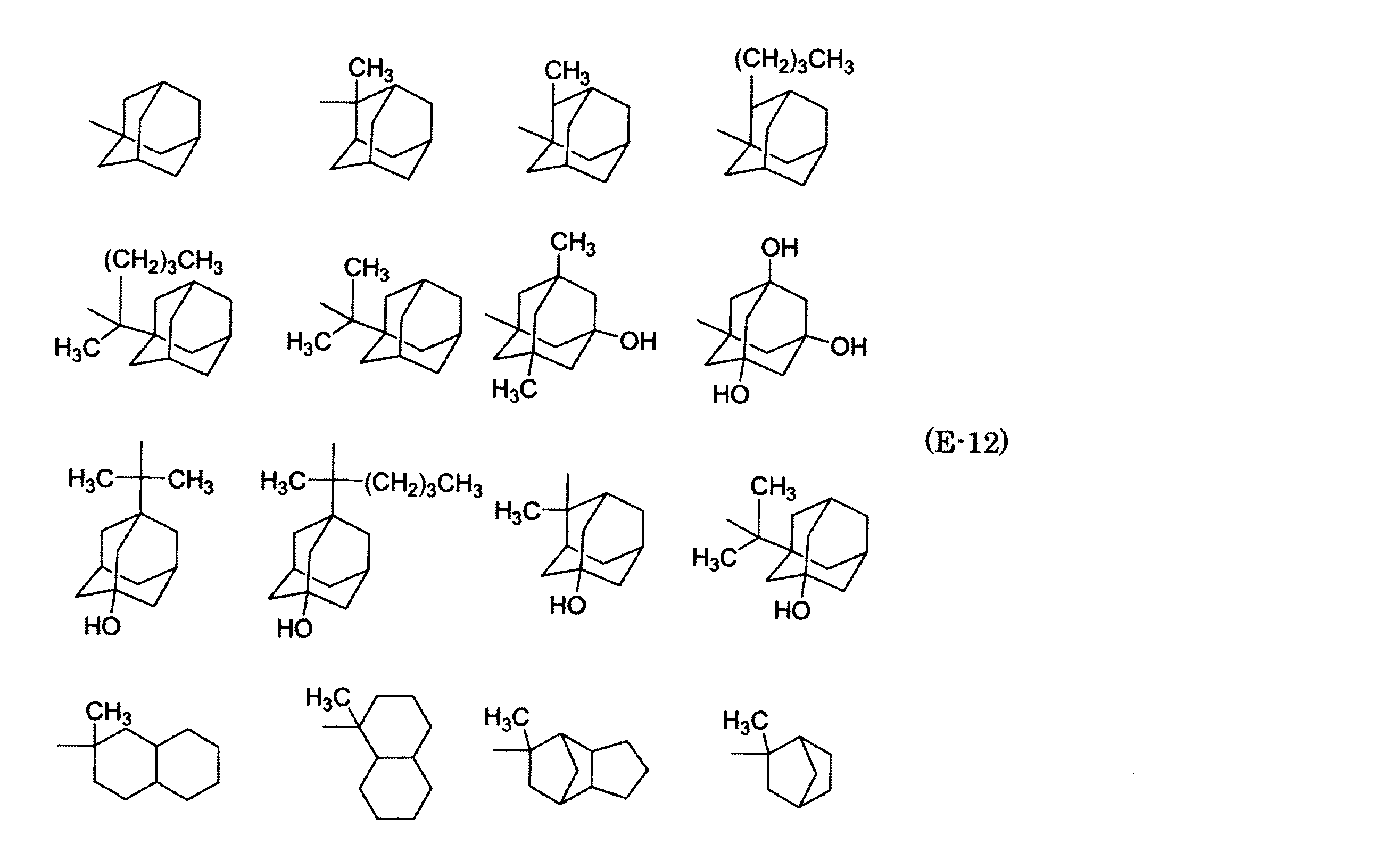
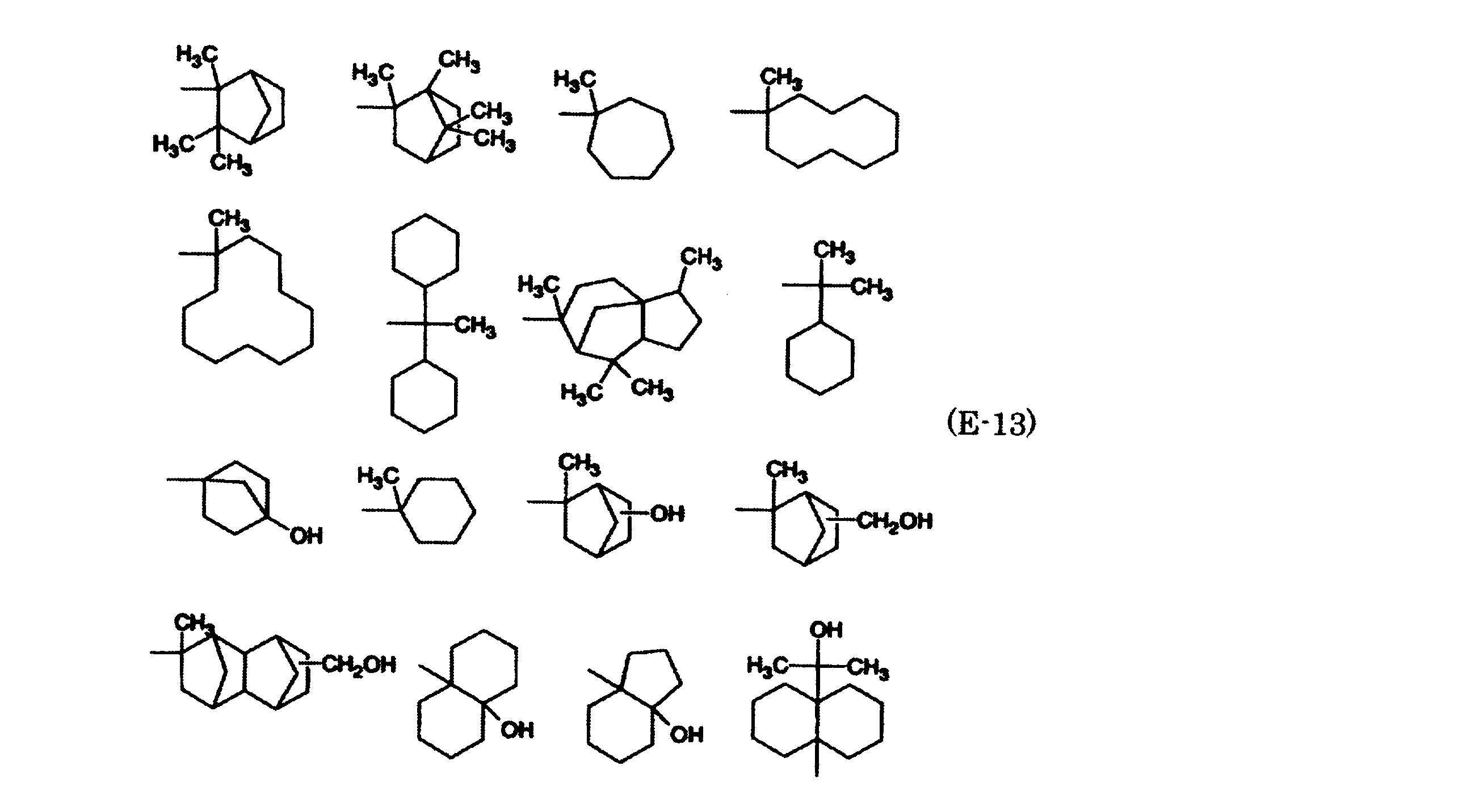
- examples of the linear alkyl group having 1 to 20 carbon atoms include, for example, methyl group, ethyl group, n-propyl group, n-butyl group, n- Pentyl group, n-hexyl group, n-heptyl group, n-octyl group, n-nonyl group, n-decyl group, etc., and those having substituents such as cyclopentylmethyl group, cyclopentylethyl group, cyclohexylmethyl group, cyclohexyl Mention may be made of linear alkyl groups having cyclic alkyl groups such as ethyl group, adamantylmethyl group, adamantylethyl group, norbornylmethyl group, norbornylethyl group, camphoroylmethyl group, camphoroylethyl group, etc. it can.
- Examples of the branched alkyl group having 3 to 20 carbon atoms include i-propyl group, sec-butyl group, i-butyl group, t-butyl group and the like.
- Examples of the cyclic alkyl group having 3 to 20 carbon atoms include a cyclopentyl group, a cyclohexyl group, an adamantyl group, a methylcyclopentyl group, a methylcyclohexyl group, a methyladamantyl group, an ethylcyclopentyl group, an ethylcyclohexyl group, an ethyladamantyl group, and a norbornyl group. , Canholoyl groups and the like.
- alkenyl group having 2 to 20 carbon atoms examples include vinyl group, 1-methylethenyl group, allyl group, 3-butenyl group, 1-methylallyl group, 2-methylallyl group, 4-pentenyl group, and 5-hexenyl group. Can be mentioned.
- Examples of the oxoalkyl group having 2 to 20 carbon atoms include 2-oxo-propyl group, 2-oxo-butyl group, 2-oxo-3-methyl-butyl group, 2-oxo-pentyl group, 2-oxo- 3-methyl-pentyl group, 2-oxo-4-methyl-pentyl group, 2-oxo-3-ethyl-pentyl group, 2-oxo-hexyl group, 2-oxo-3-methyl-hexyl group, 2-oxo -4-methyl-hexyl group, 2-oxo-5-methyl-hexyl group, 2-oxo-3-ethyl-hexyl group, 2-oxo-4-ethyl-hexyl group, 2-oxo-heptyl group, 2- Oxo-3-methyl-heptyl group, 2-oxo-4-methyl-heptyl group, 2-oxo-5-methyl-heptyl group, 2-oxo-6
- Examples of the aryl group having 6 to 18 carbon atoms include phenyl group, o-tolyl group, m-tolyl group, p-tolyl group, p-hydroxyphenyl group, p-trifluoromethylphenyl group, 1-naphthyl group, Examples thereof include a 1-anthracenyl group.
- Examples of the aralkyl group having 6 to 18 carbon atoms include benzyl group, 1-phenylethyl group, 2-phenylethyl group, 1-phenylpropyl group, 2-phenylpropyl group, 3-phenylpropyl group, and 1-naphthylmethyl. Group, 2-naphthylmethyl group and the like.
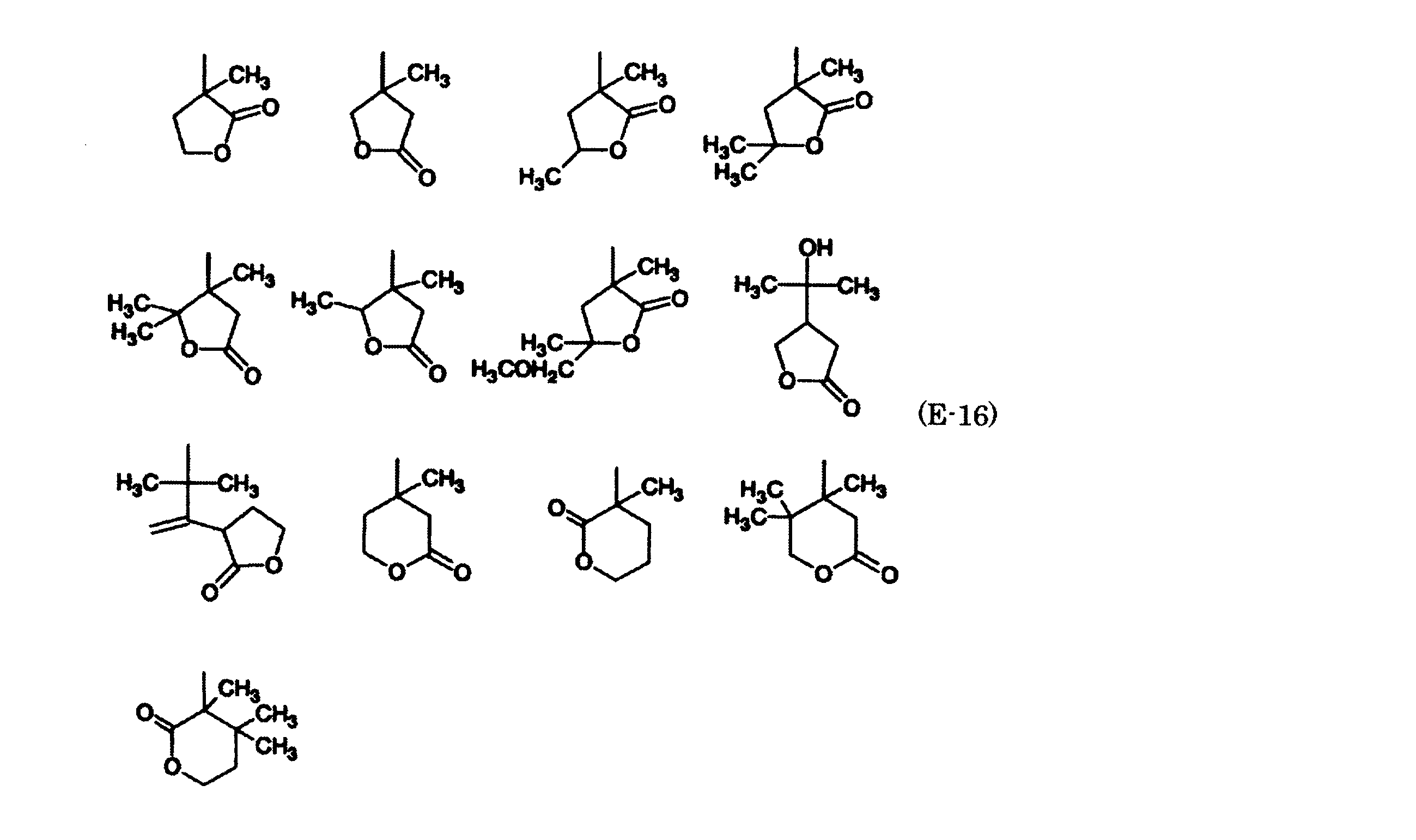
- Examples of monocyclic or polycyclic lactone groups having 3 to 30 carbon atoms include ⁇ -butyrolaclone, ⁇ -valerolactone, angelica lactone, ⁇ -hexalactone, ⁇ -heptalactone, ⁇ -octalactone, ⁇ -nonalactone, 3- Methyl-4-octanolide (whiskey lactone), ⁇ -decalactone, ⁇ -undecalactone, ⁇ -dodecalactone, ⁇ -jasmolactone (7-decenolactone), ⁇ -hexalactone, 4,6,6 (4,4 , 6) -trimethyltetrahydropyran-2-one, ⁇ -octalactone, ⁇ -nonalactone, ⁇ -decalactone, ⁇ -2-decenolactone, ⁇ -undecalactone, ⁇ -dodecalactone, ⁇ -tridecalactone, ⁇ - Tetradecalactone, lacto
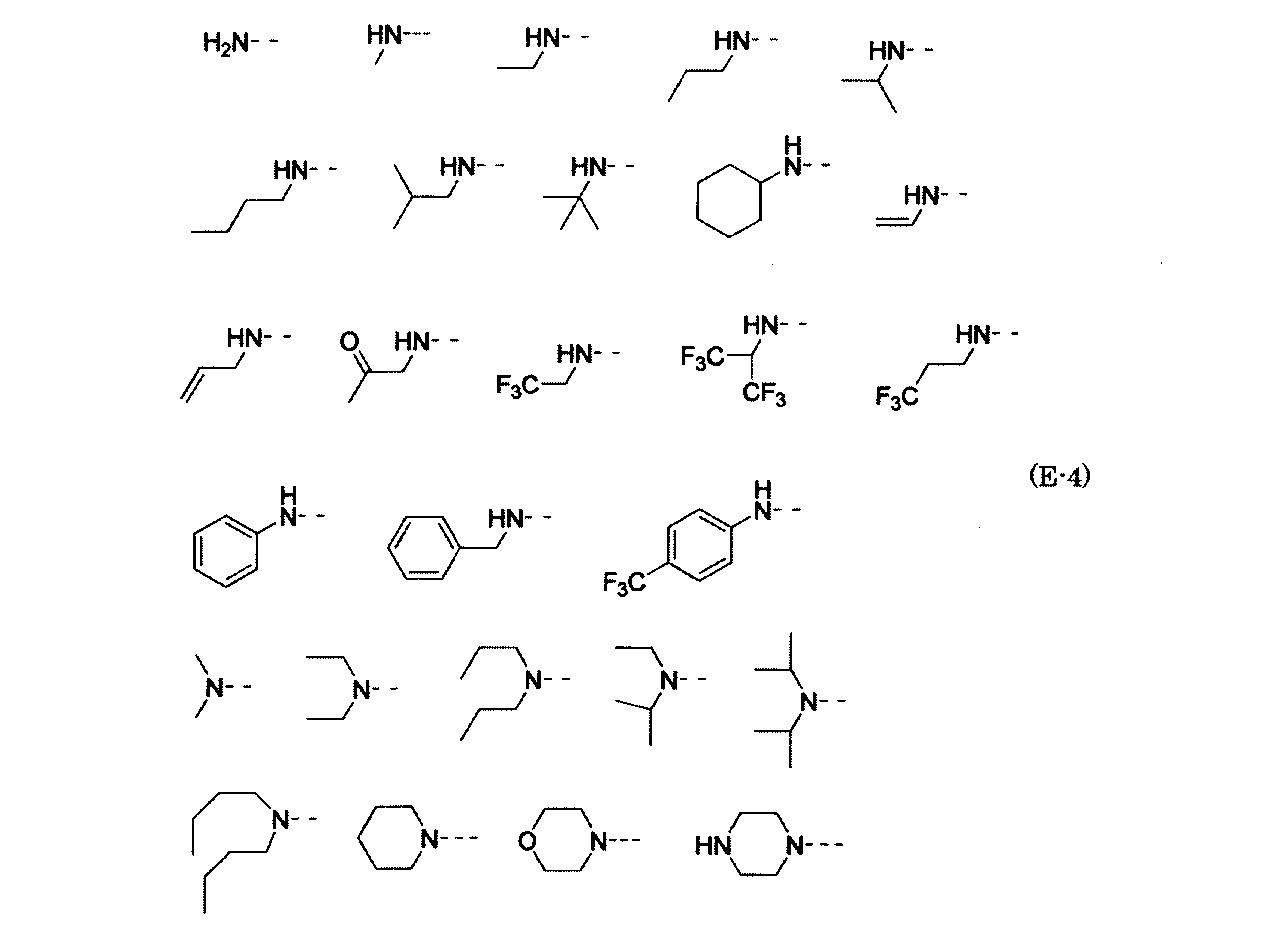
- Examples of the heterocyclic ring having 3 to 18 ring members formed by R B and R C include the following.
- a dotted line represents a coupling position.
- the hydrogen atom on carbon contained in R A , R B and R C described above may be substituted with a substituent.
- substituents include halogen atoms such as fluorine atom, chlorine atom, bromine atom and iodine atom, hydroxyl group, thiol group, aryl group and the like, or halogen atom, oxygen atom, nitrogen atom, sulfur atom, phosphorus atom and silicon atom.
- An organic group containing a hetero atom such as Furthermore, a ketone group in which two hydrogen atoms on the same carbon of R A , R B and R C described above are substituted with one oxygen atom can be exemplified. Any number of these substituents may be present as long as structurally possible.
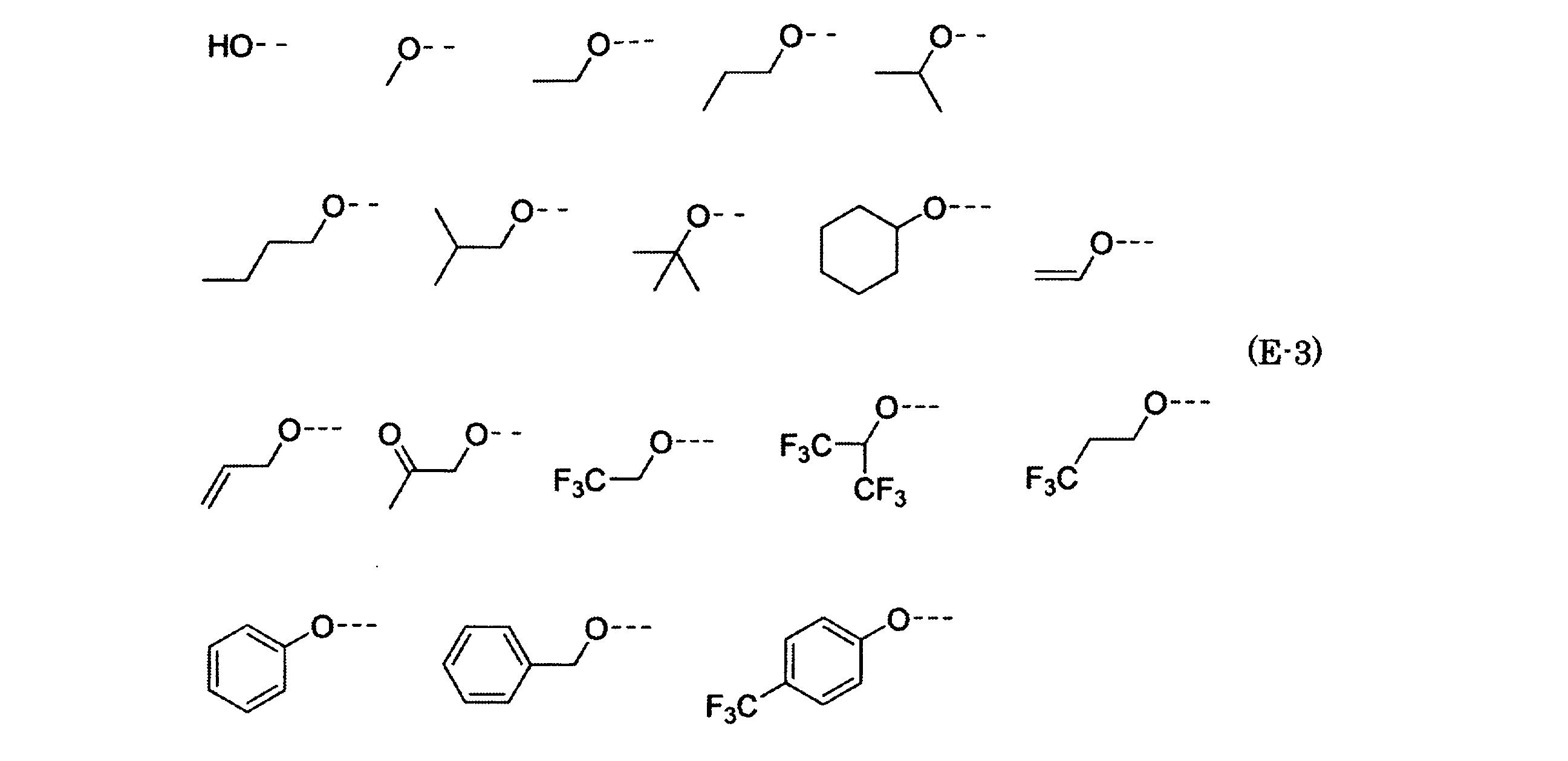
- R 2 the following groups can be mentioned as preferred groups.
- a dotted line represents a coupling position.
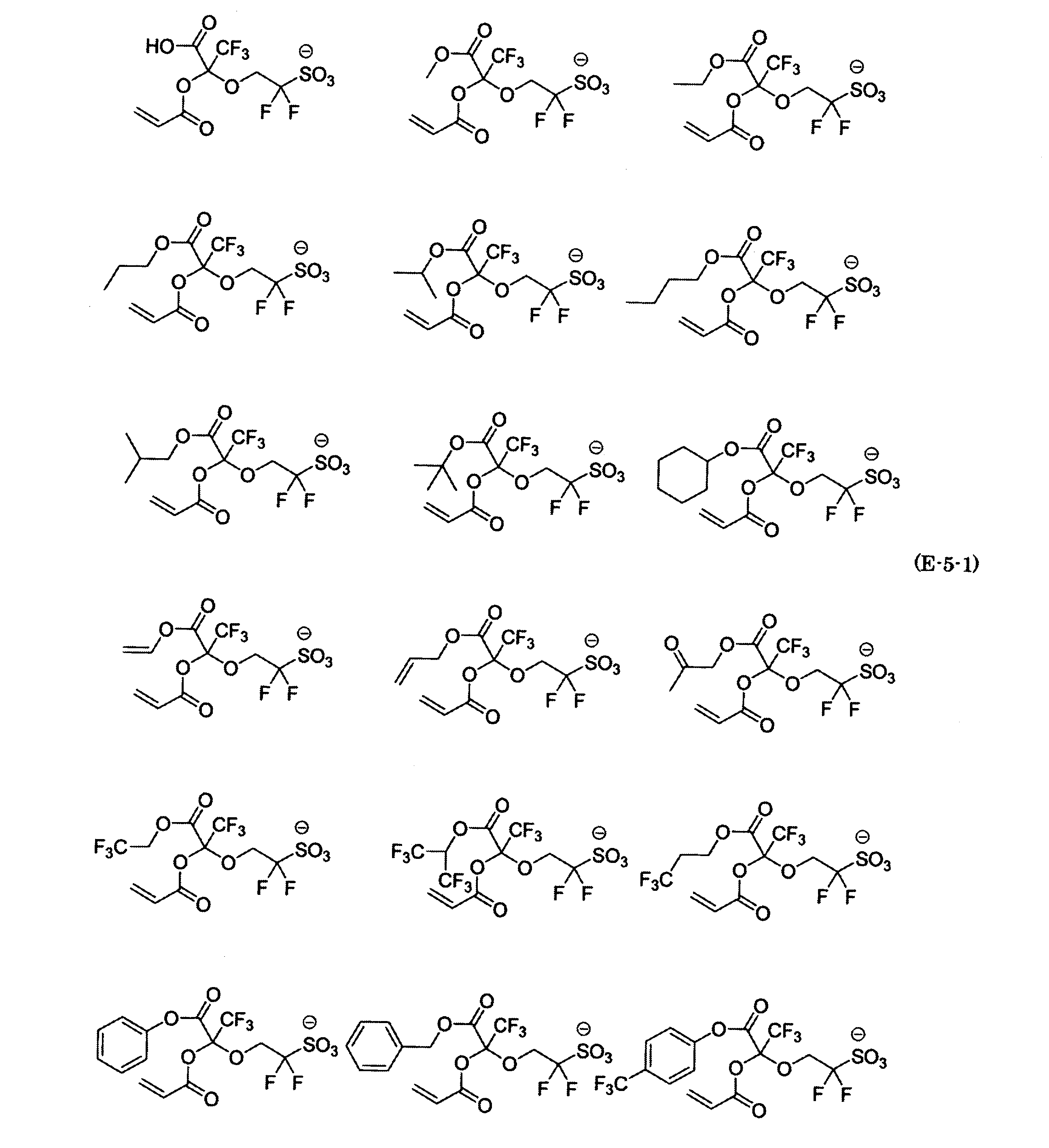
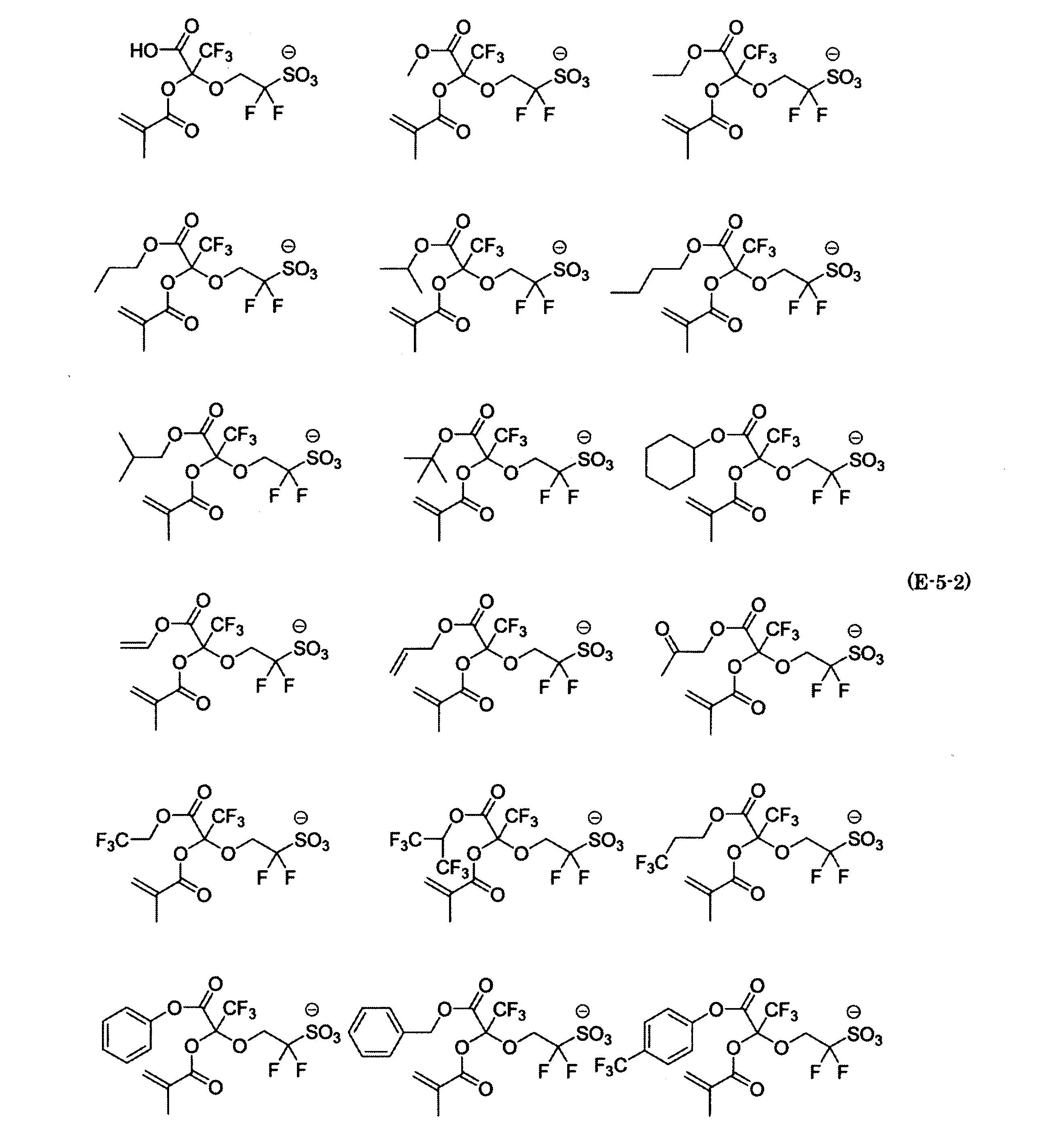
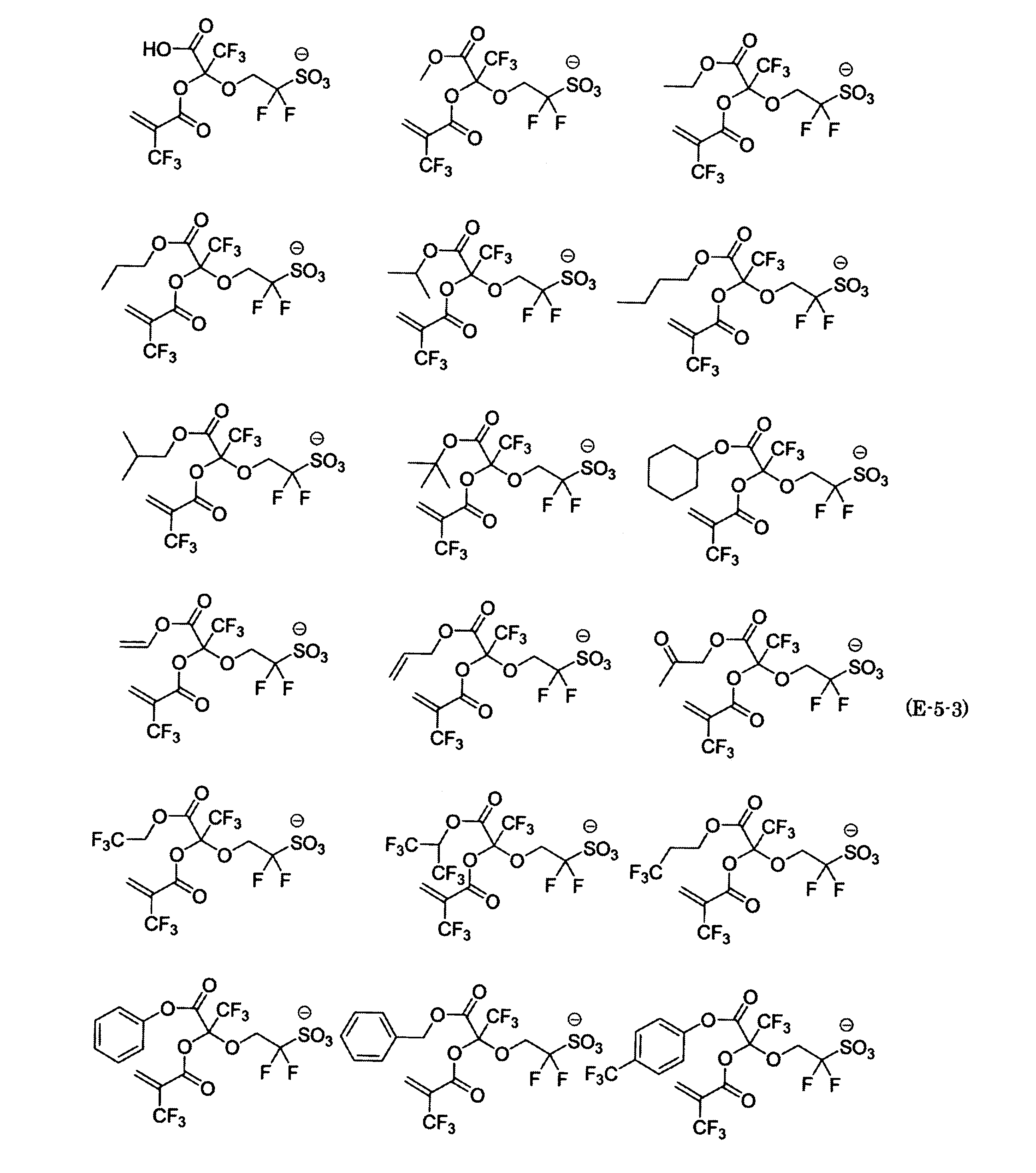
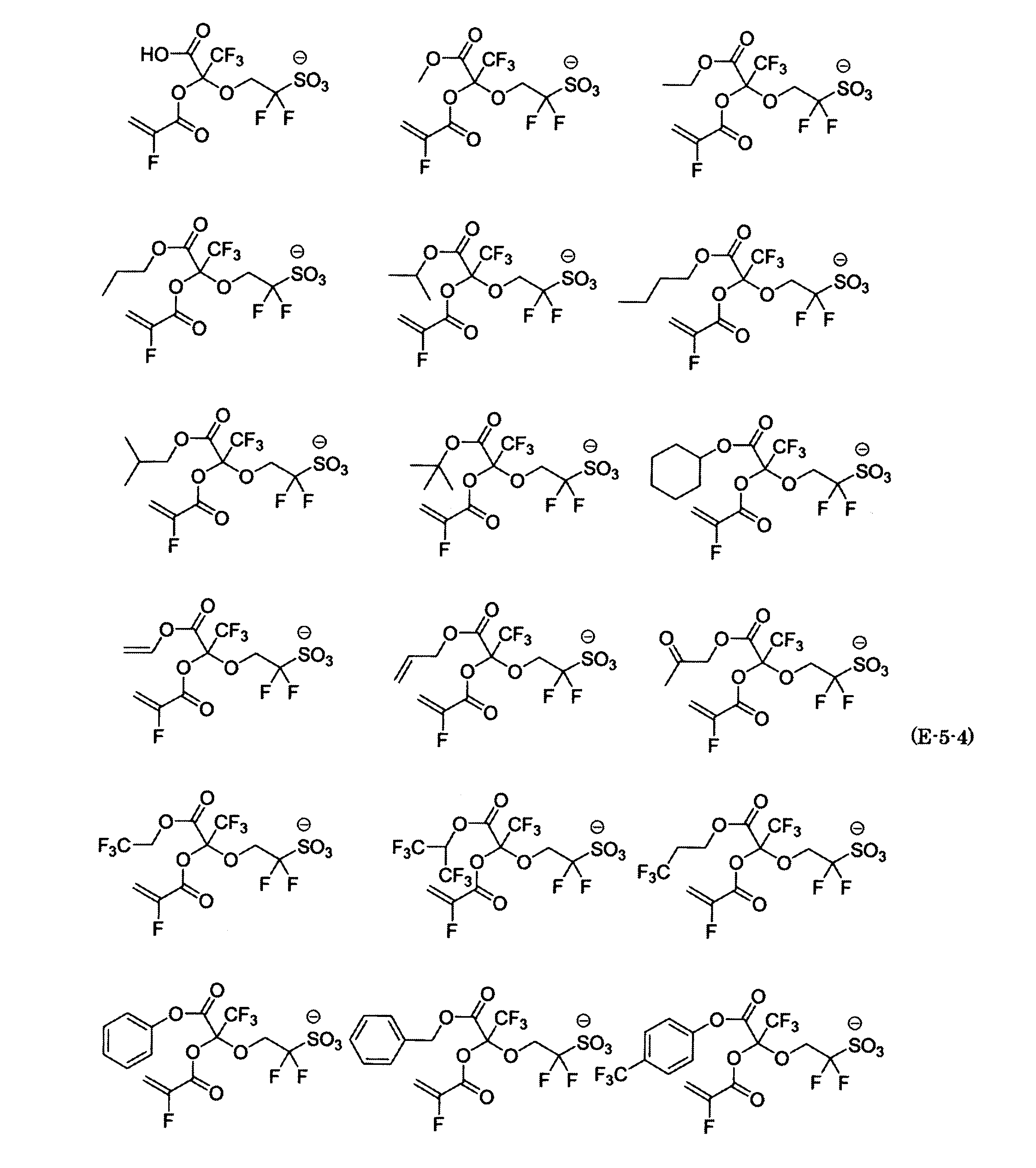
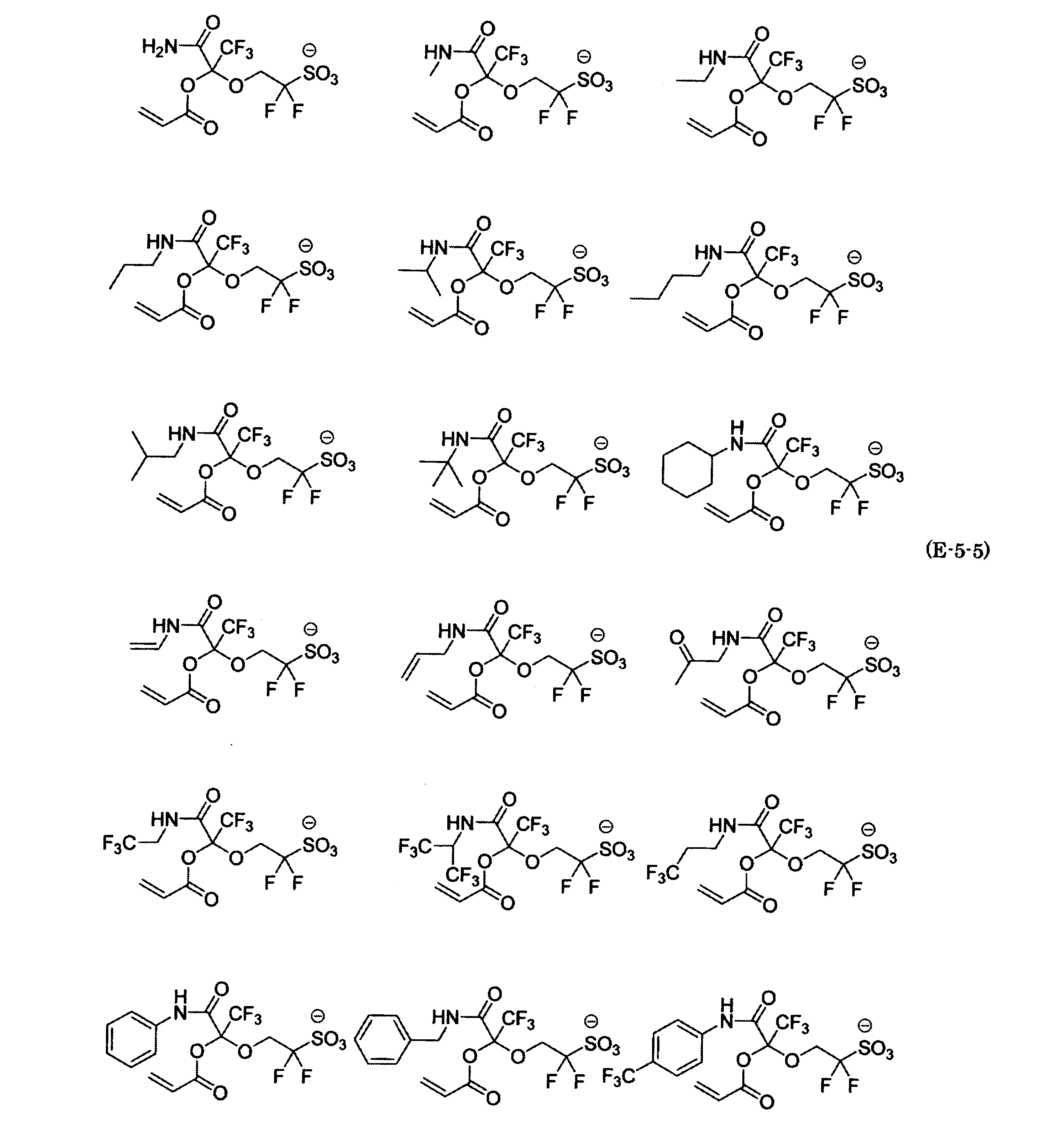
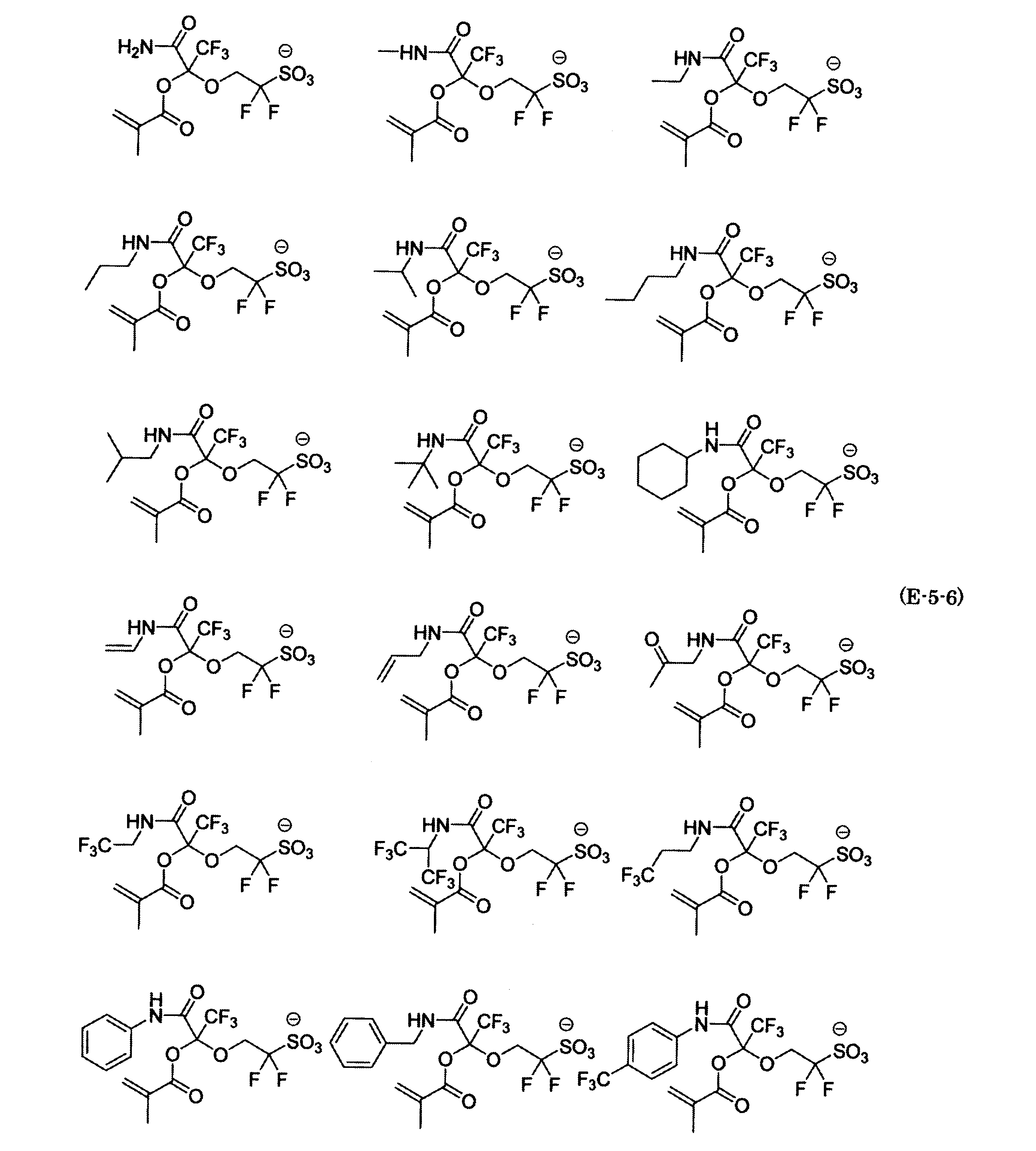
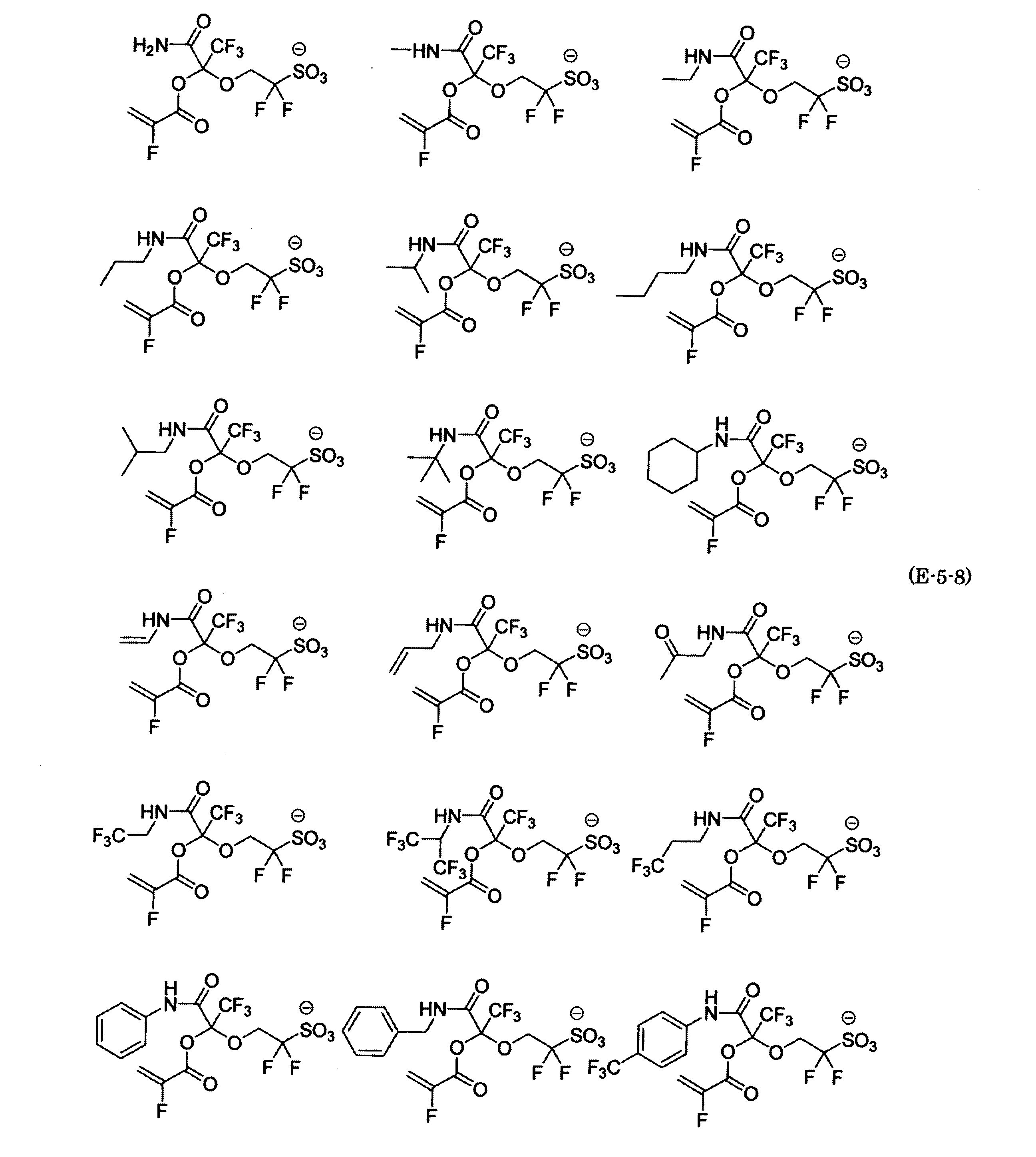
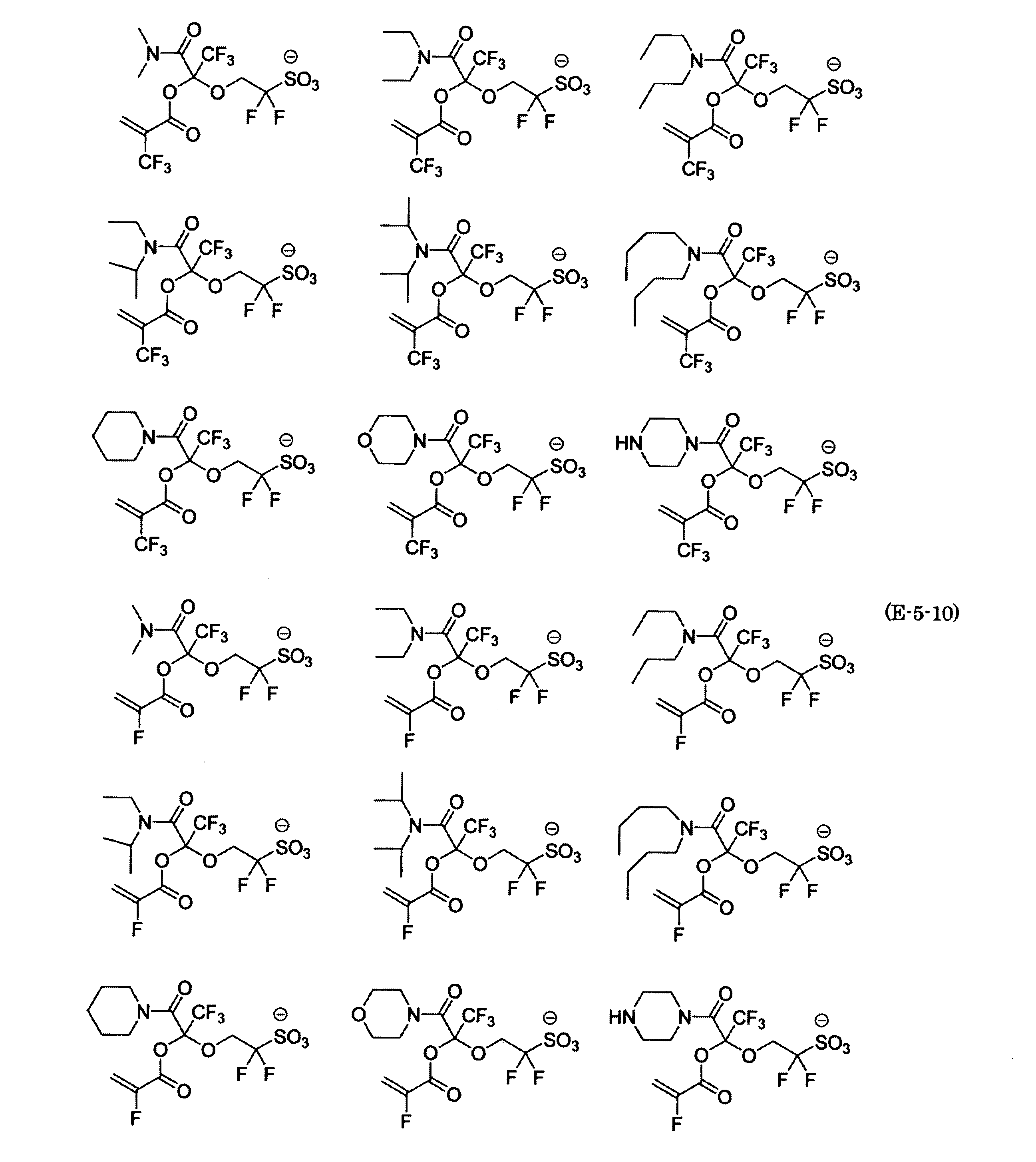
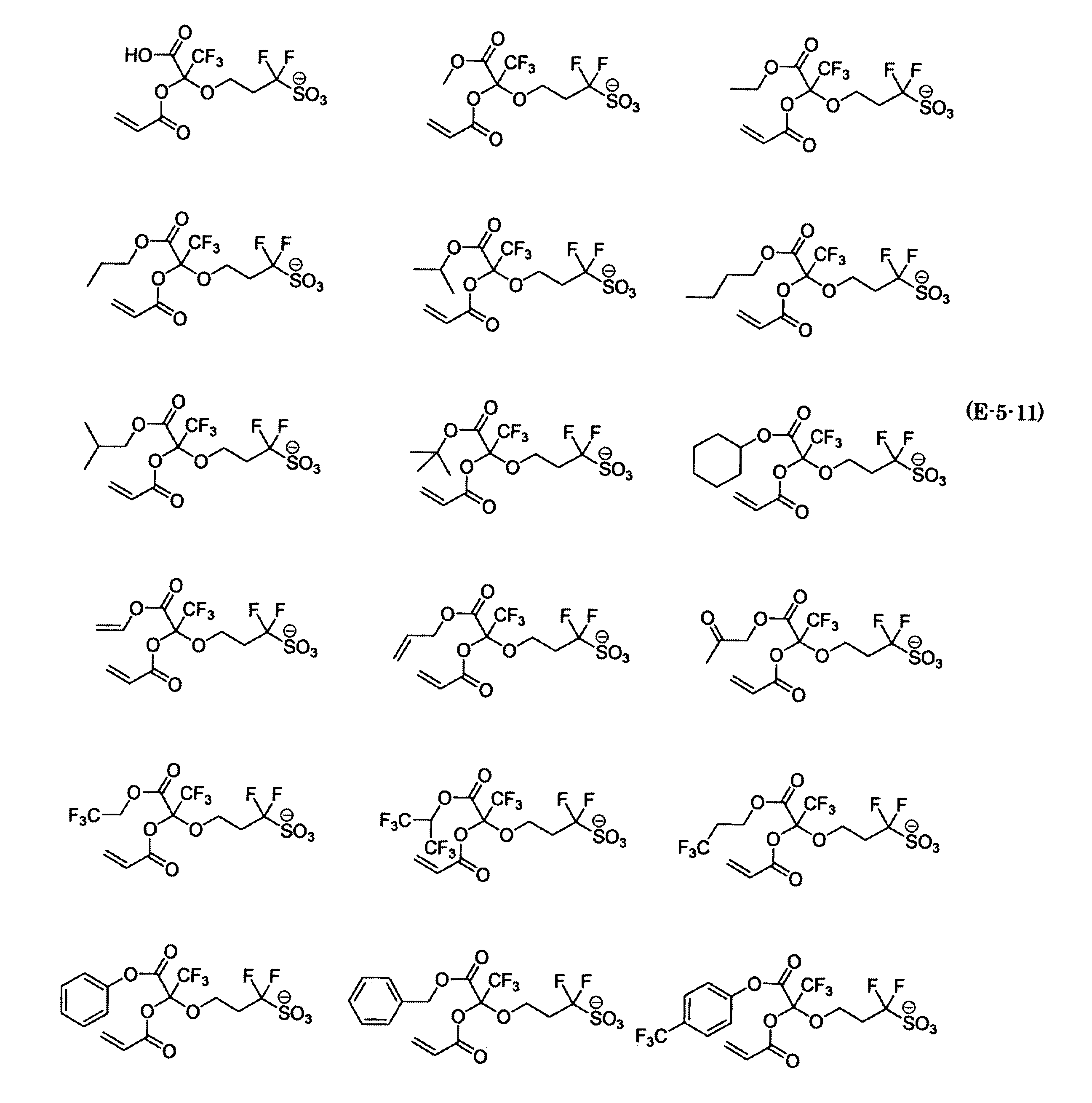
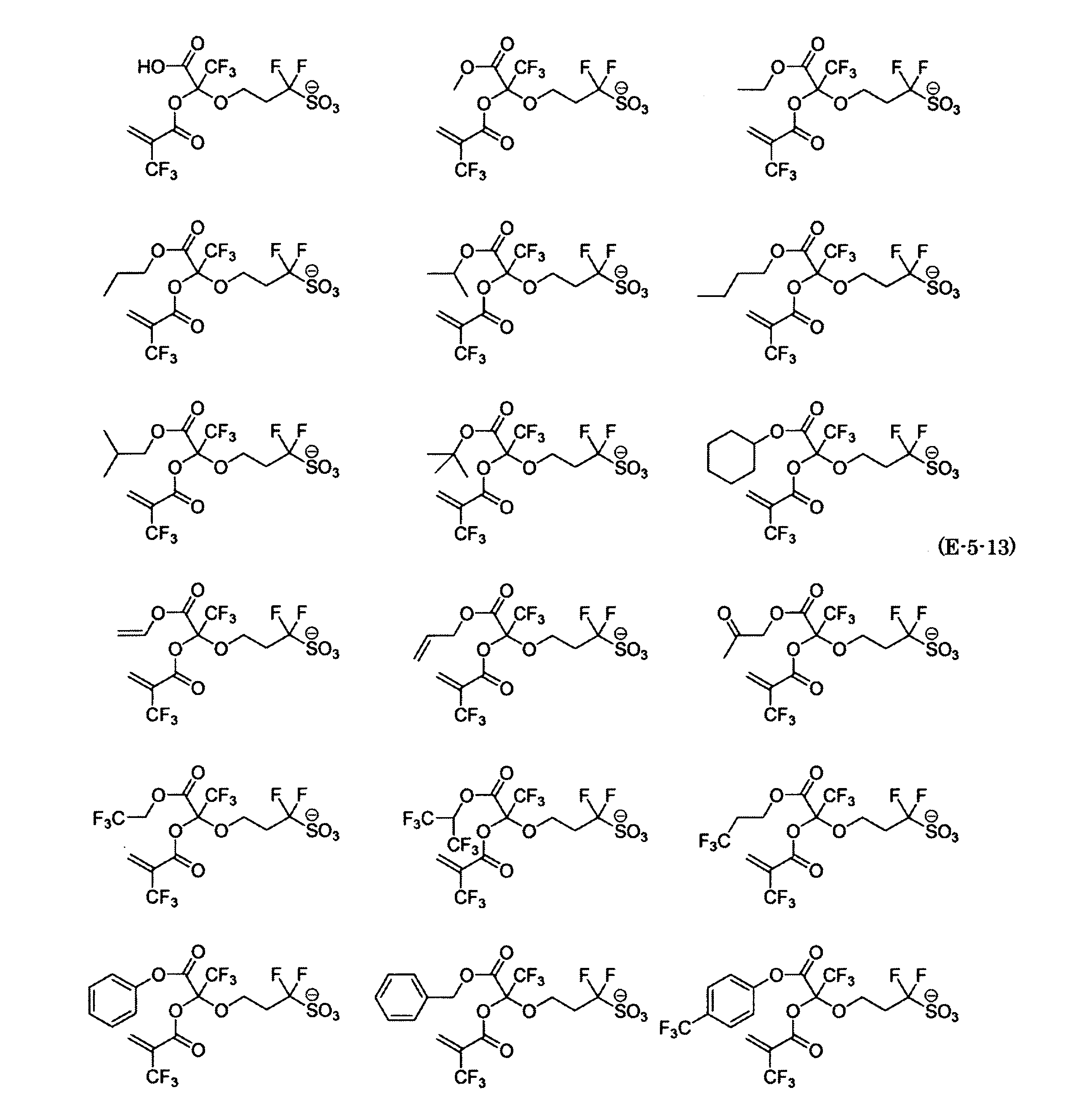
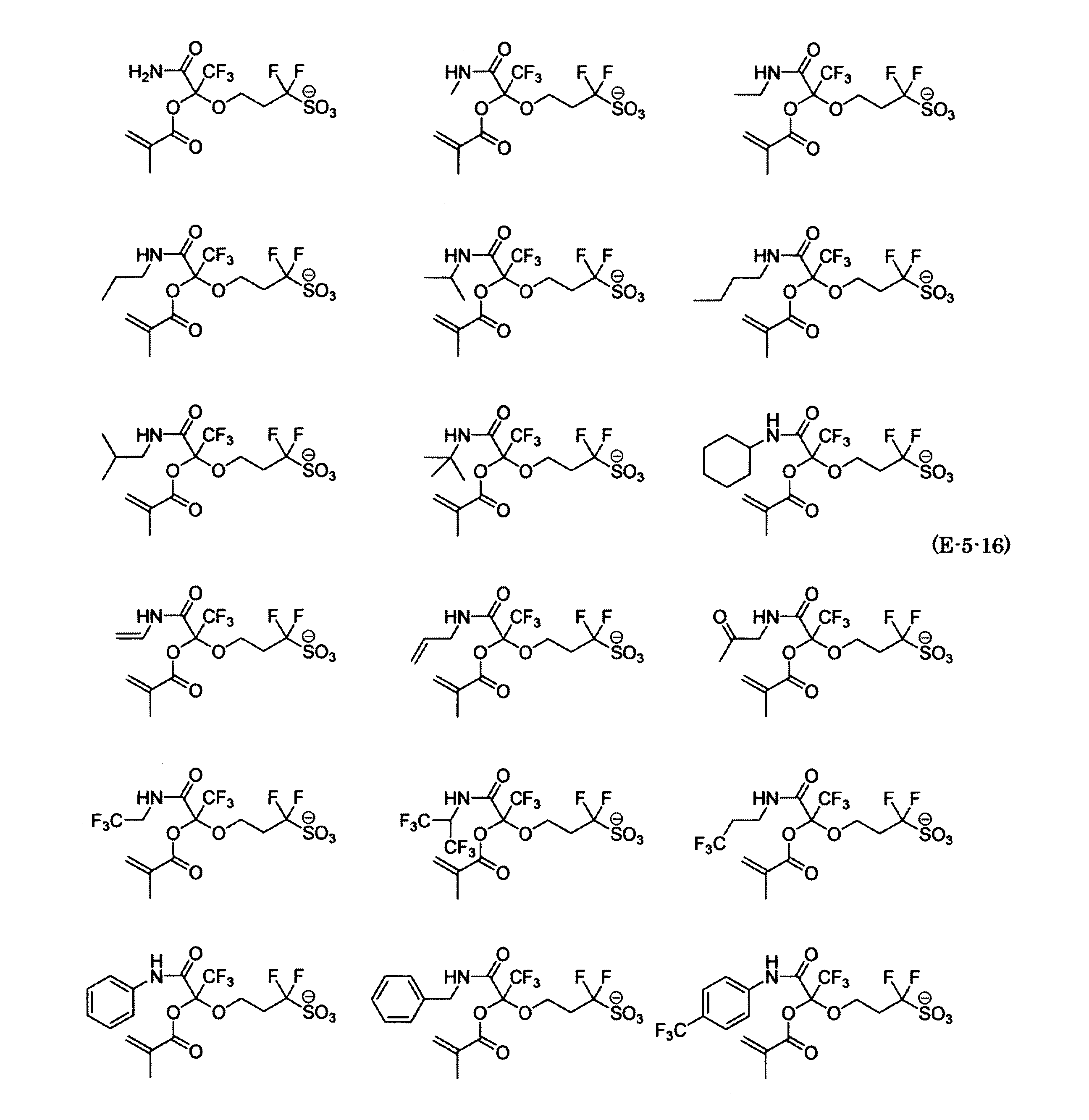
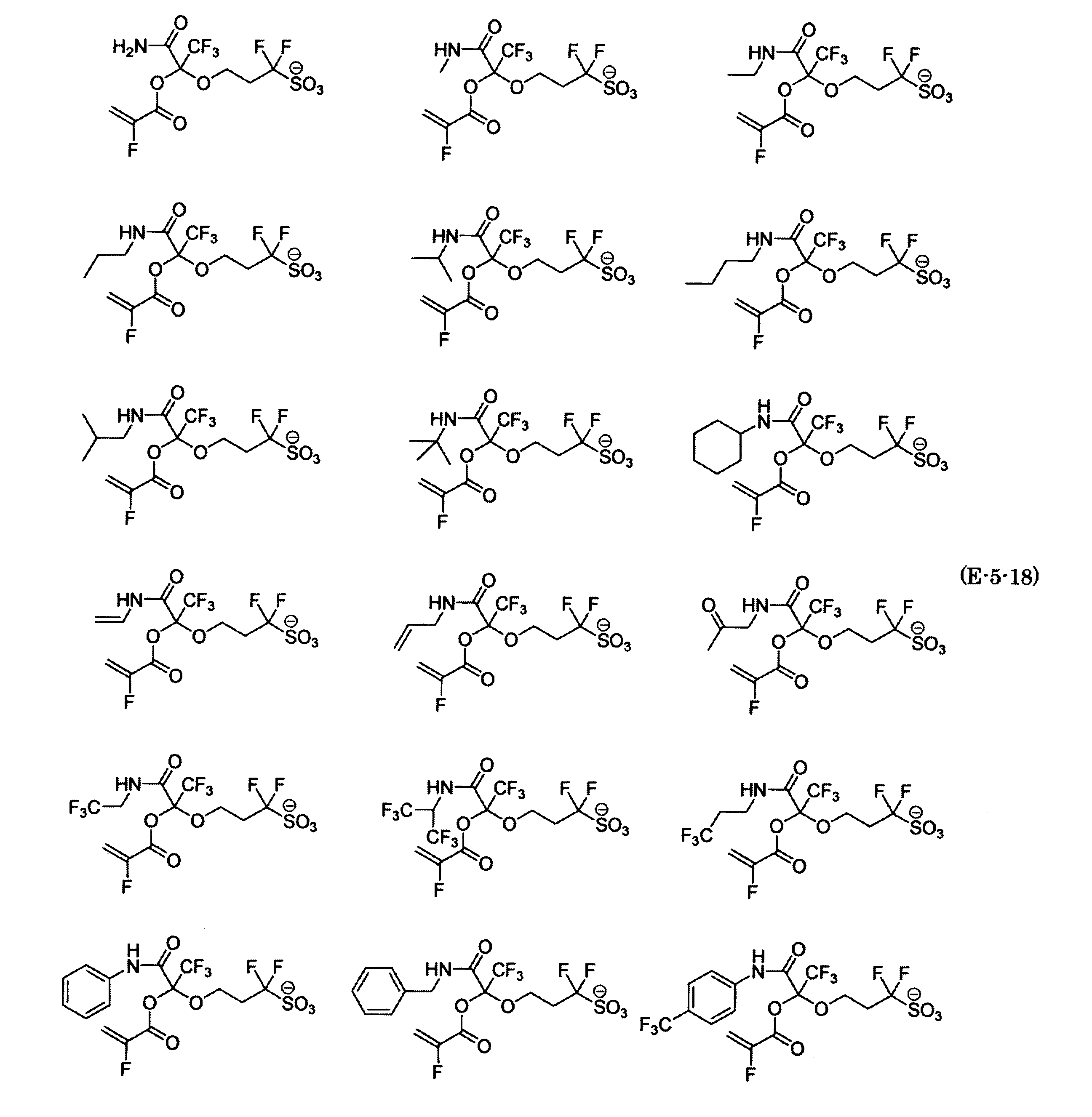
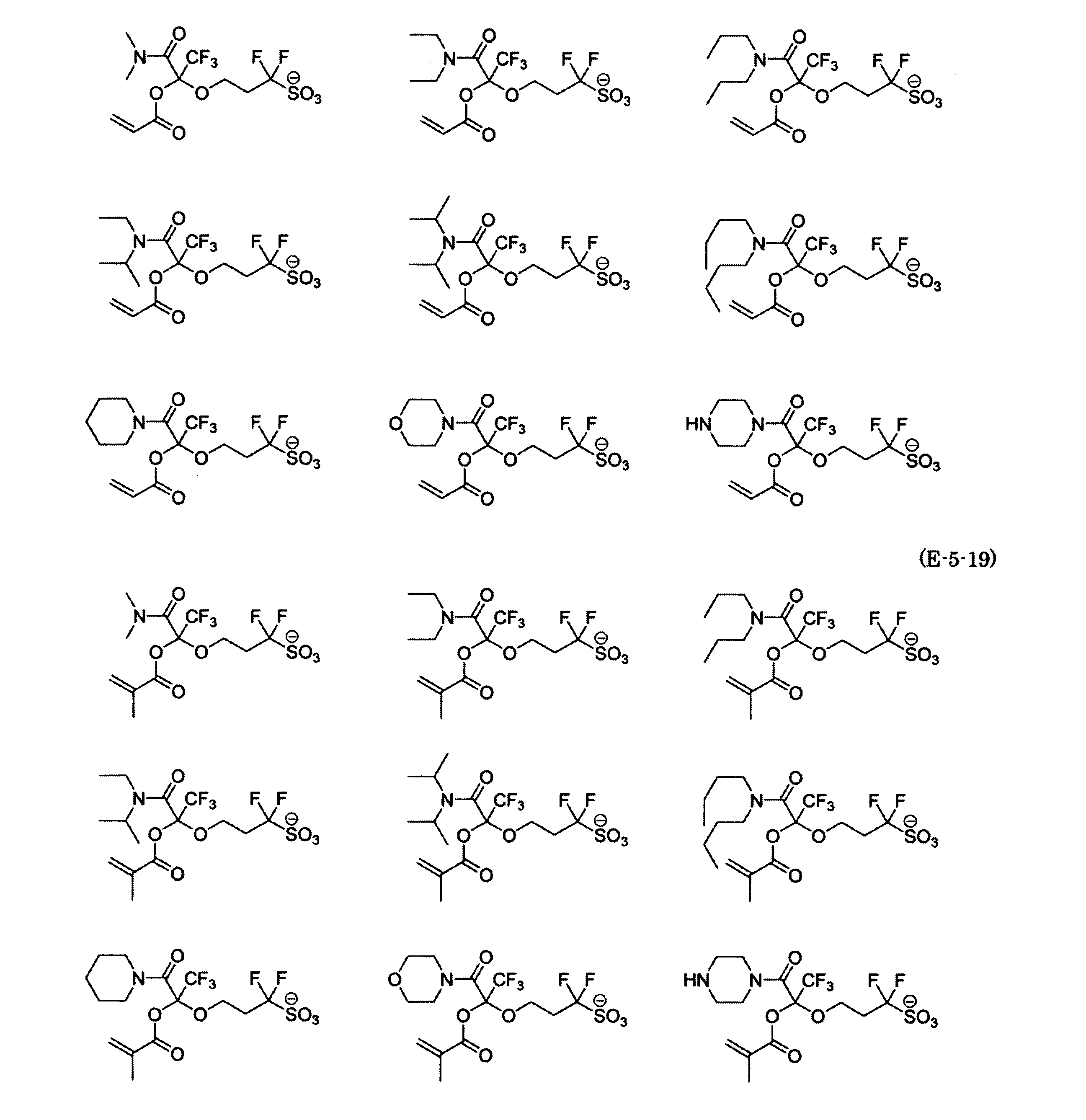
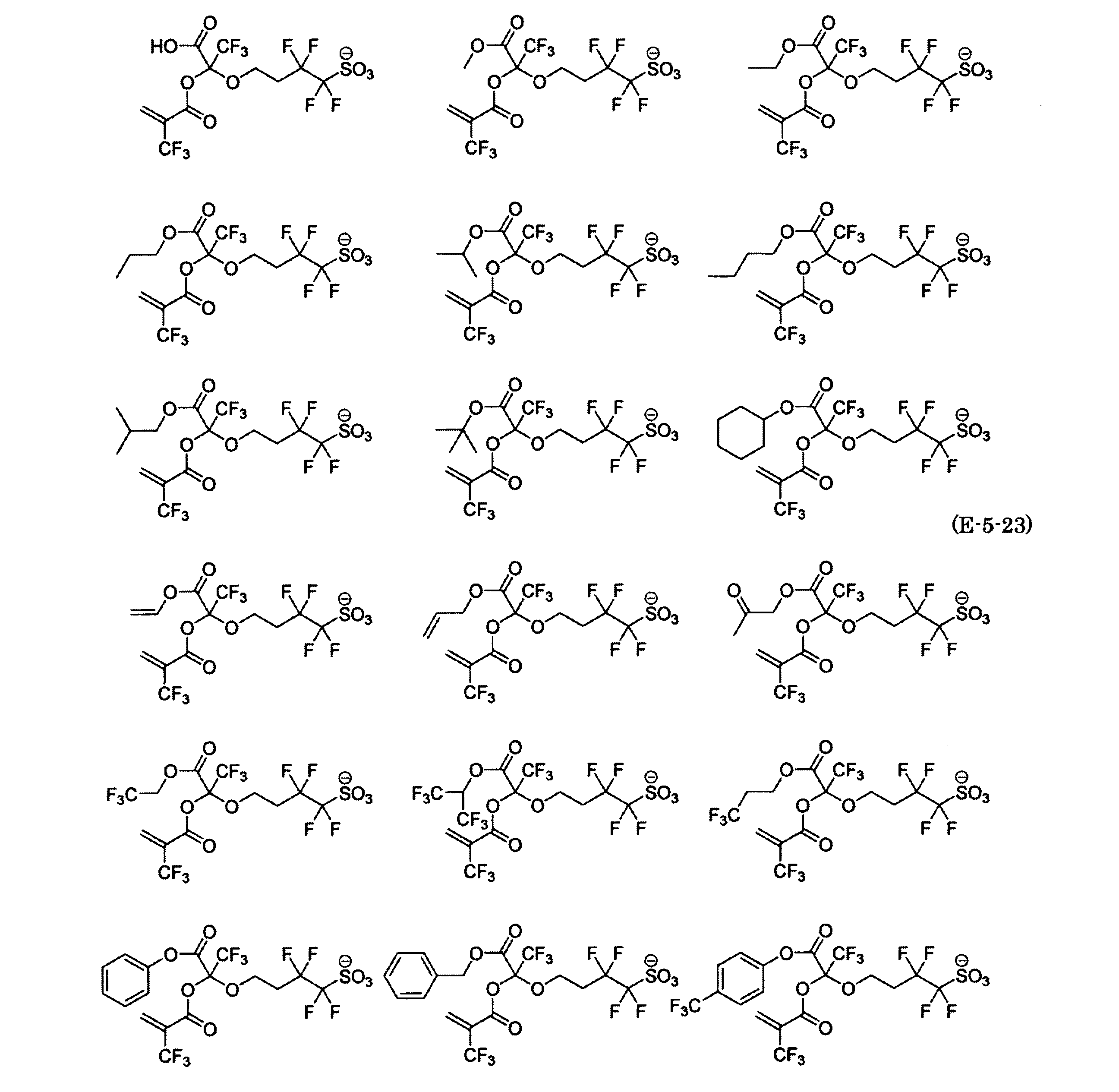
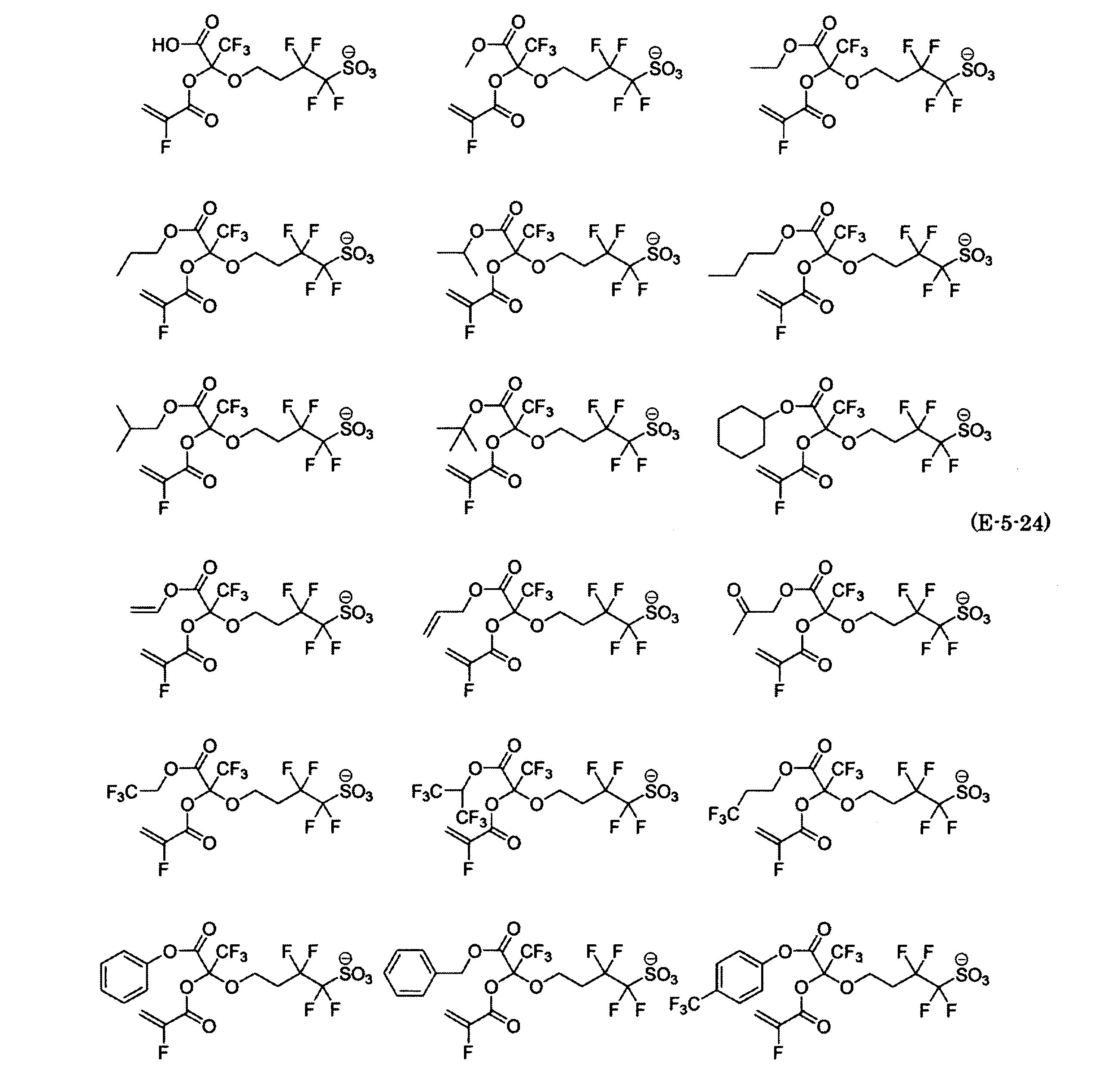
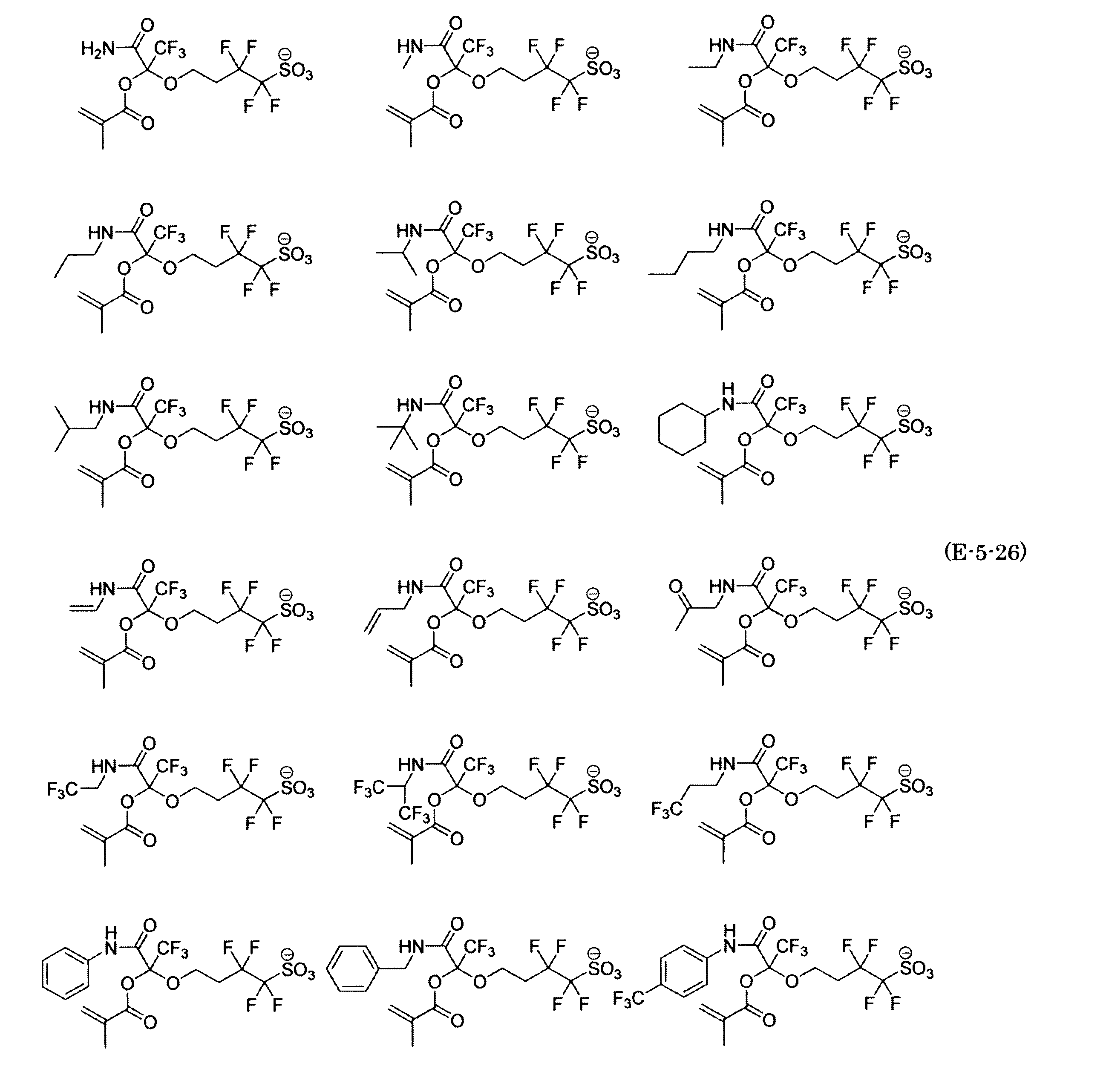
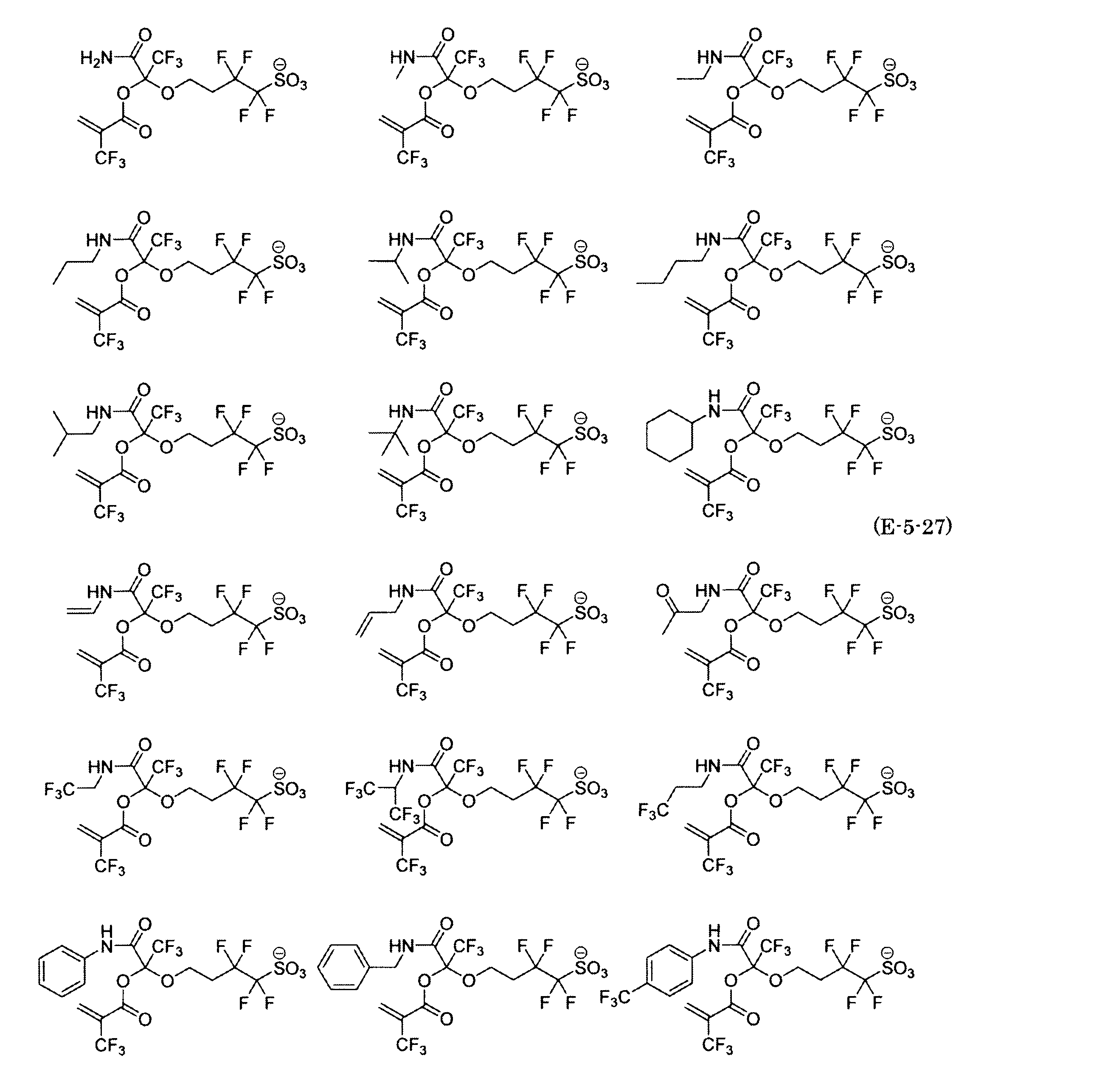
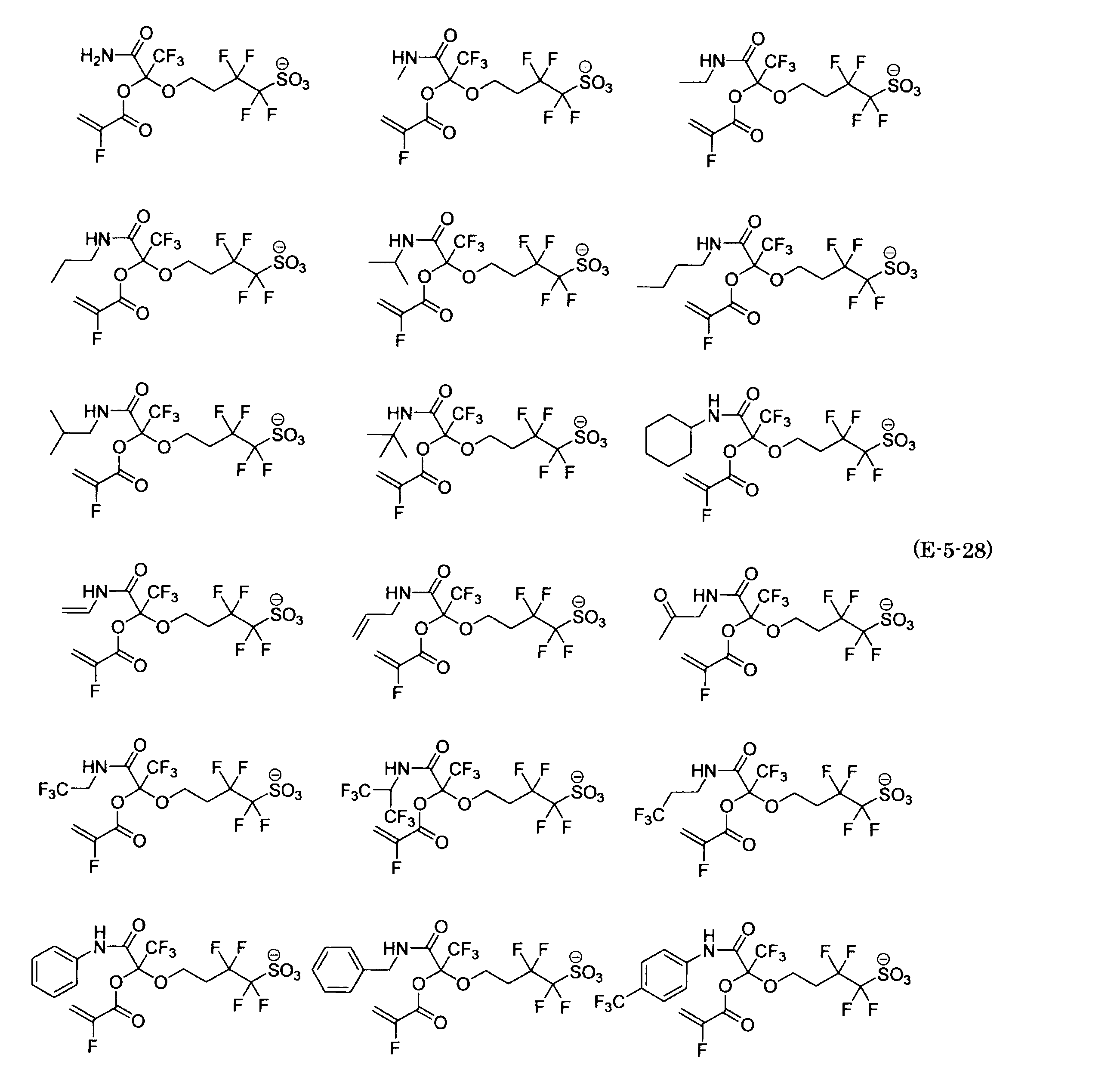
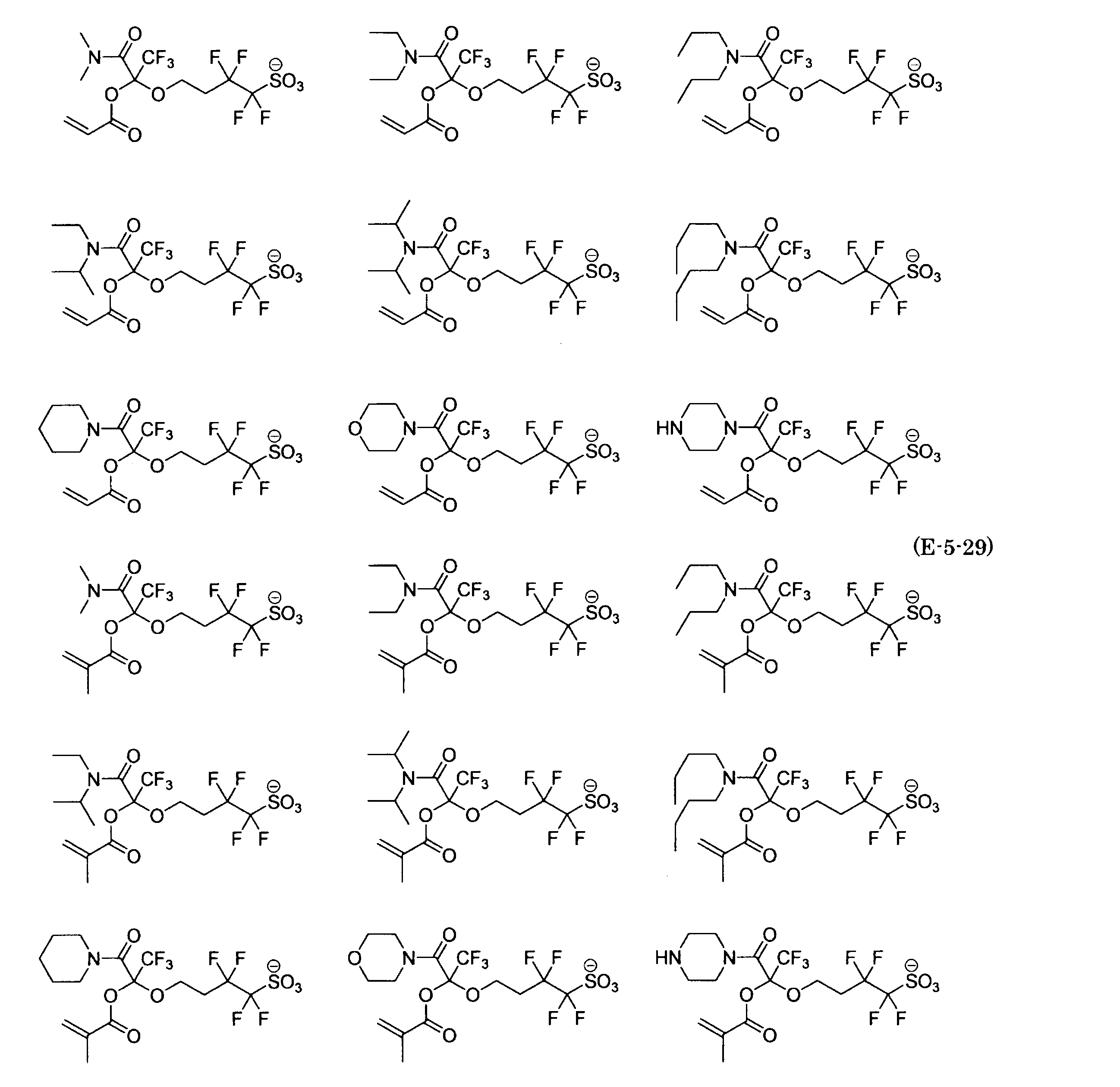
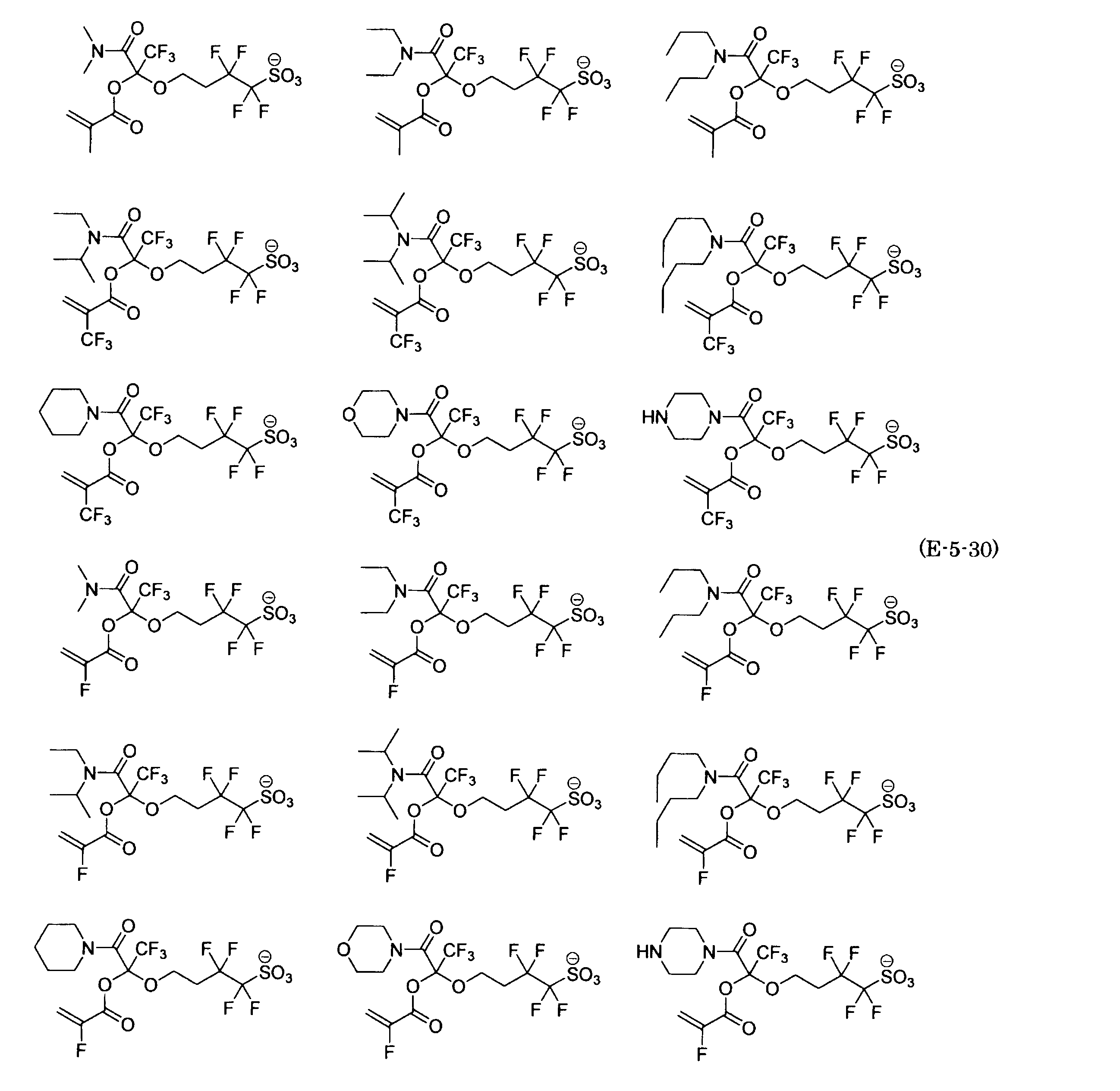
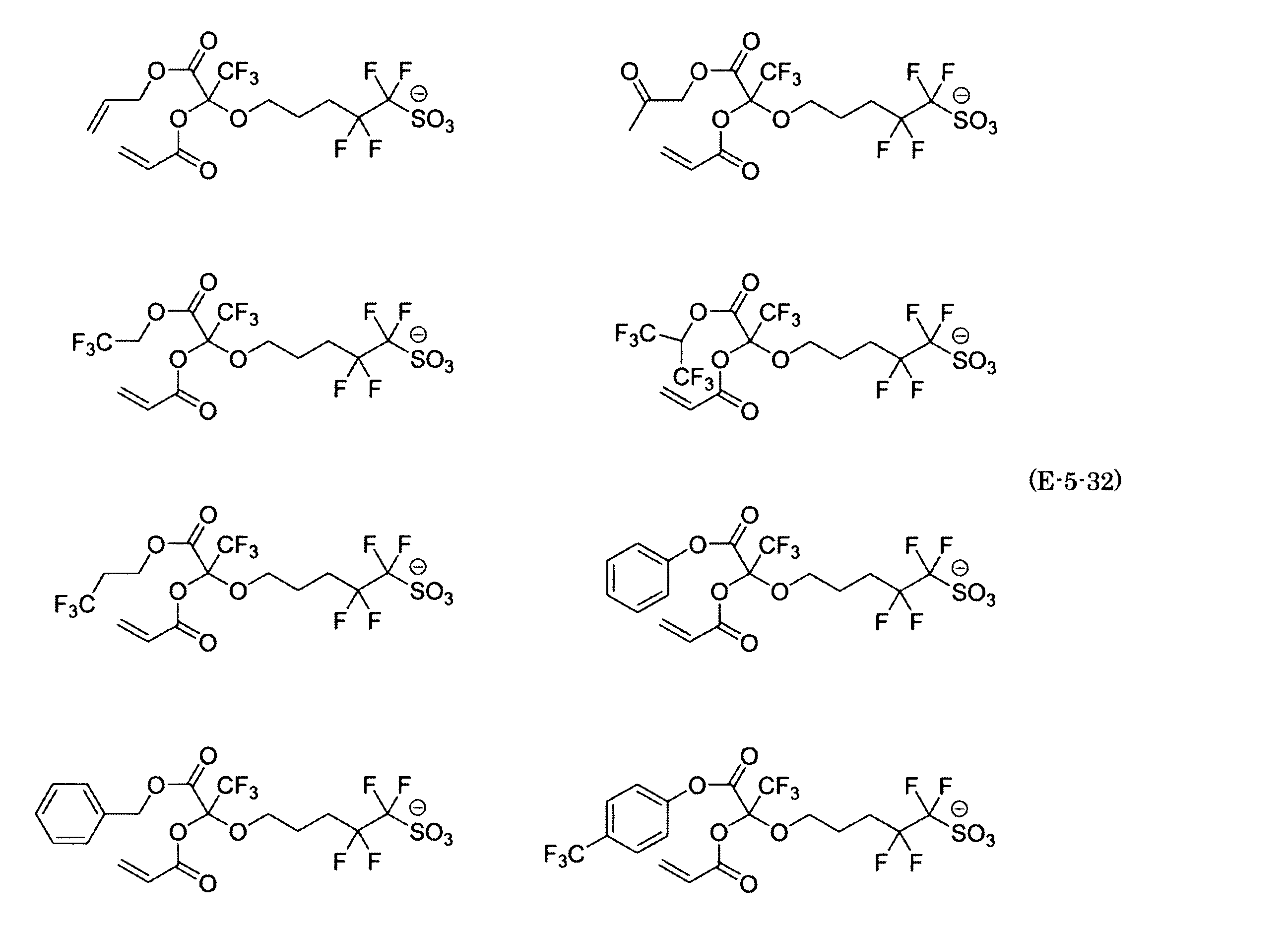
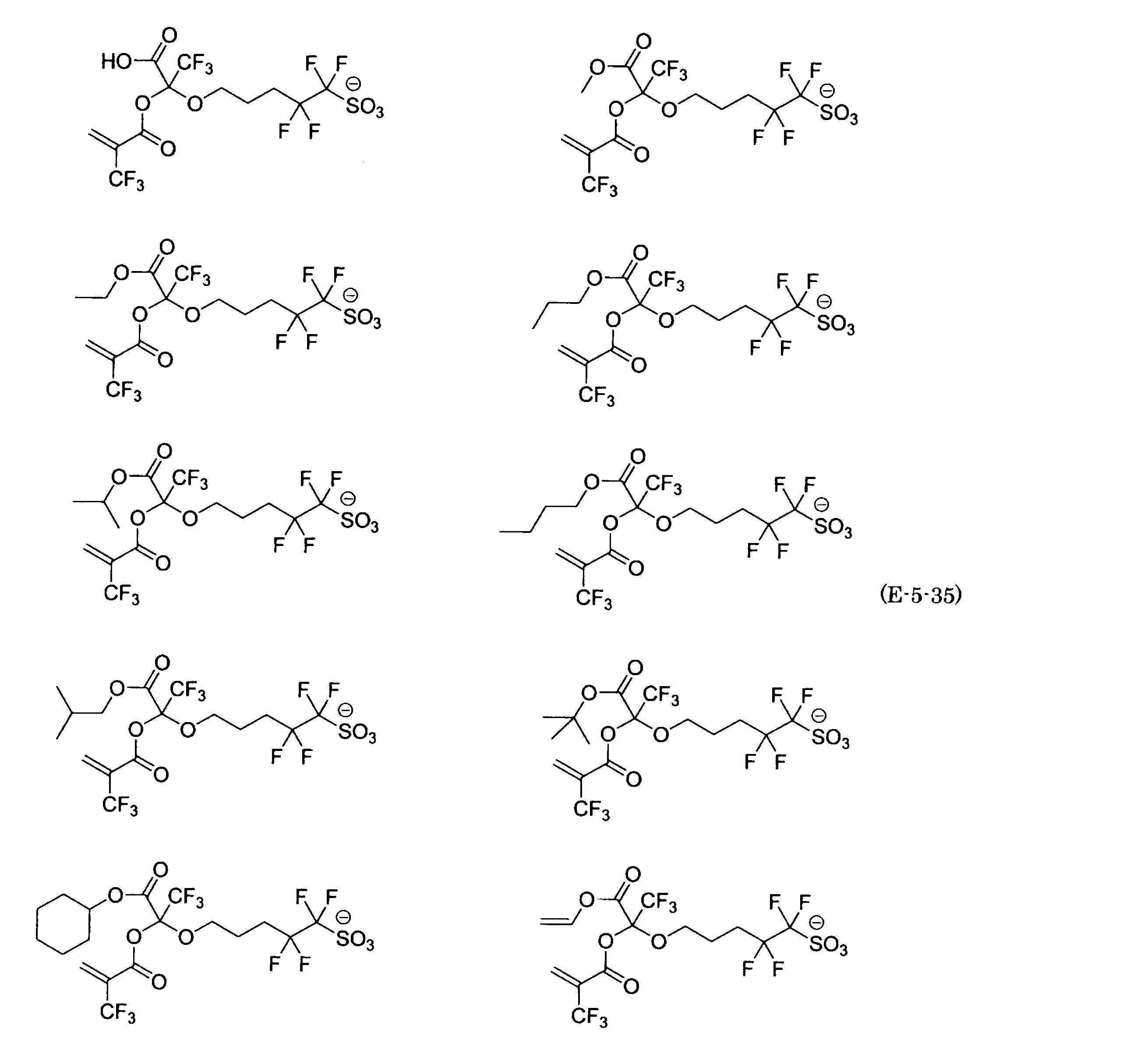
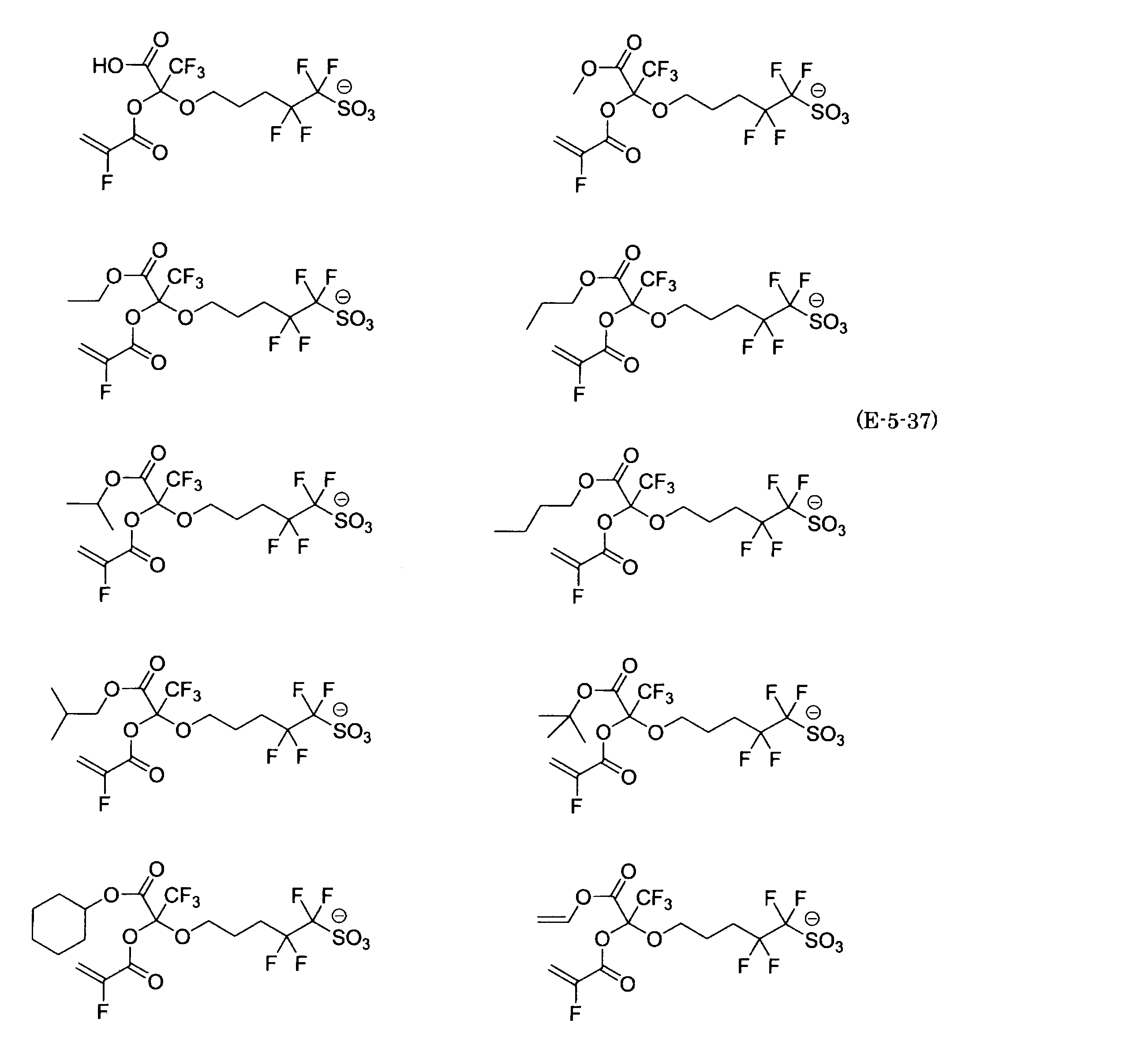
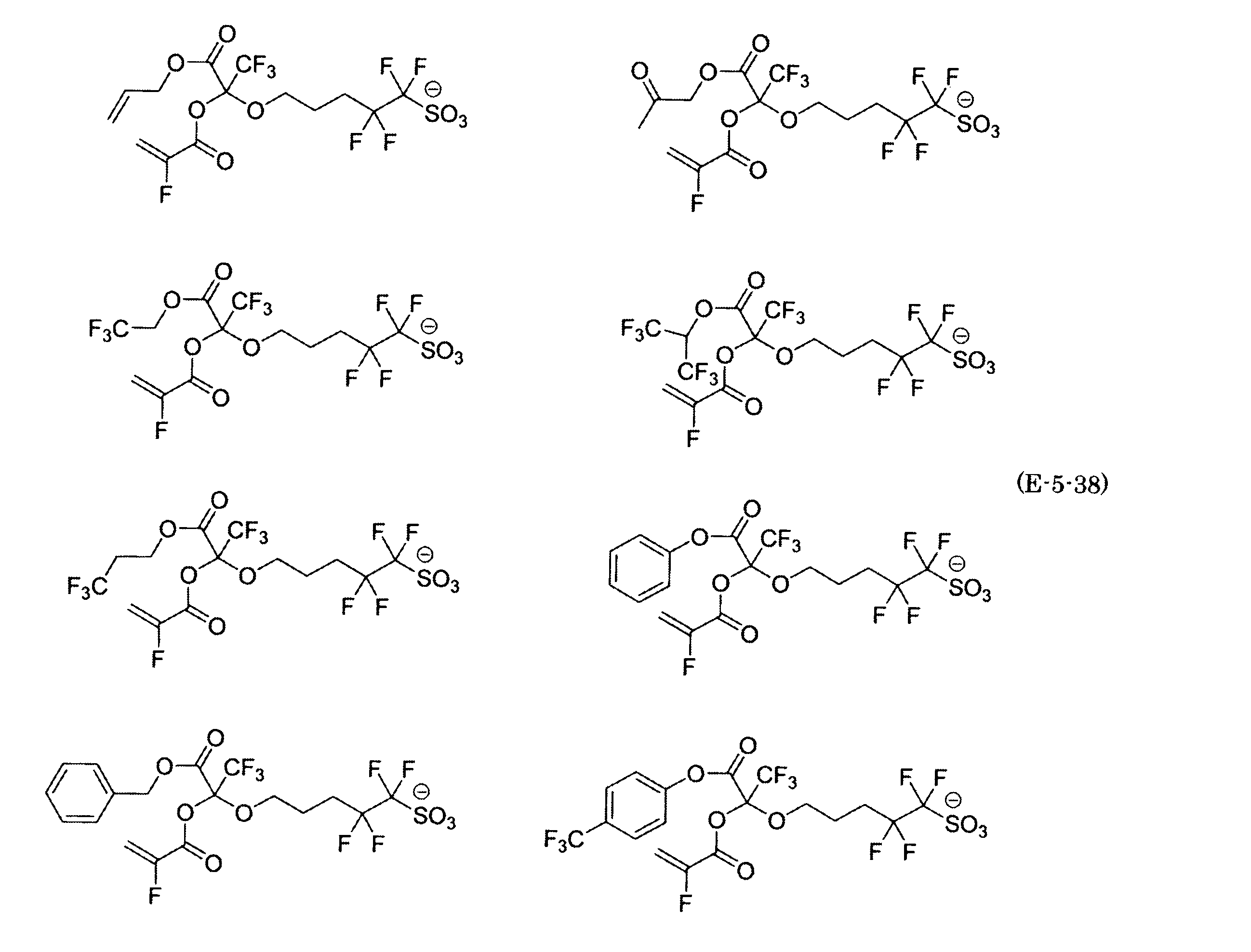
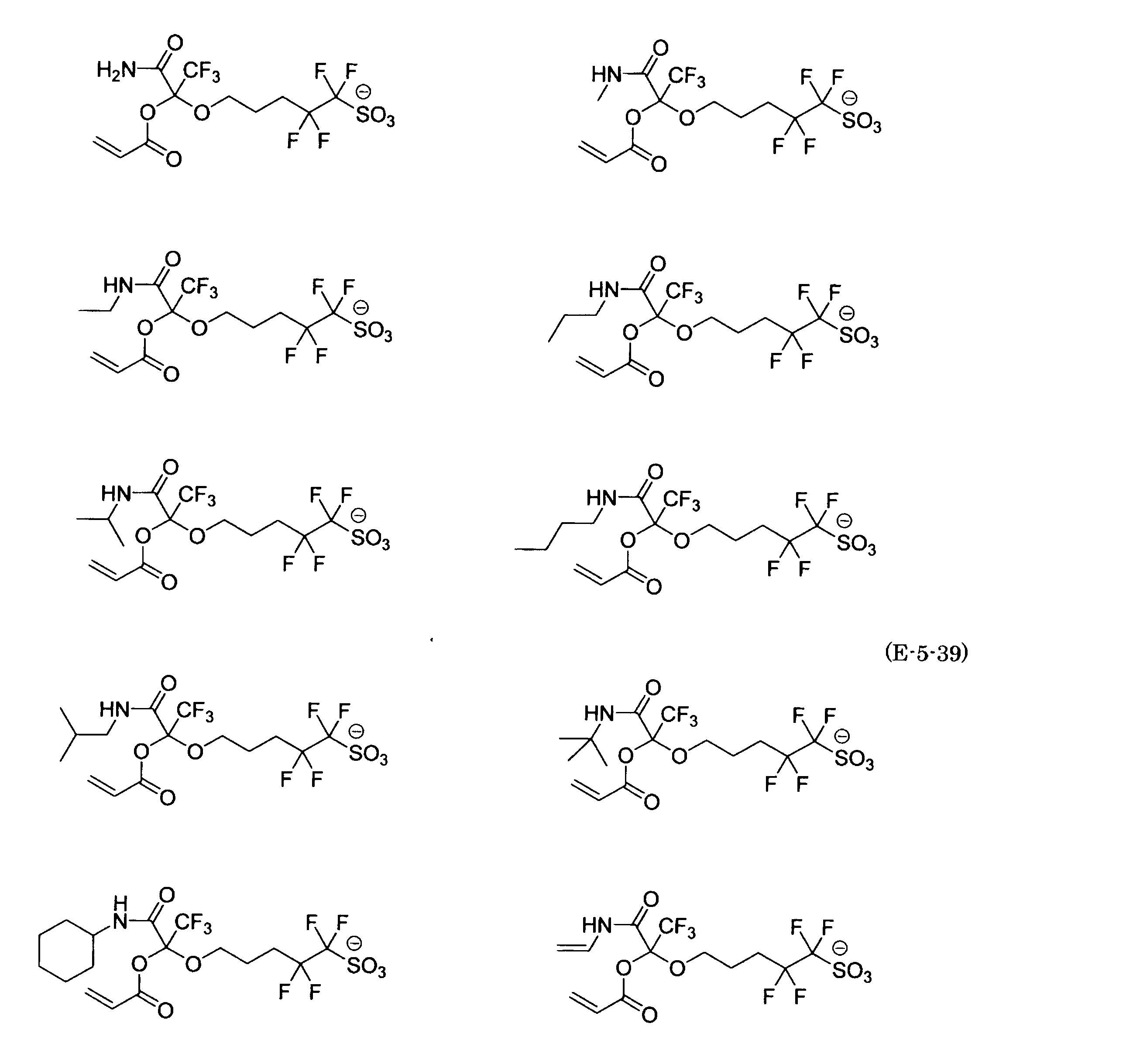
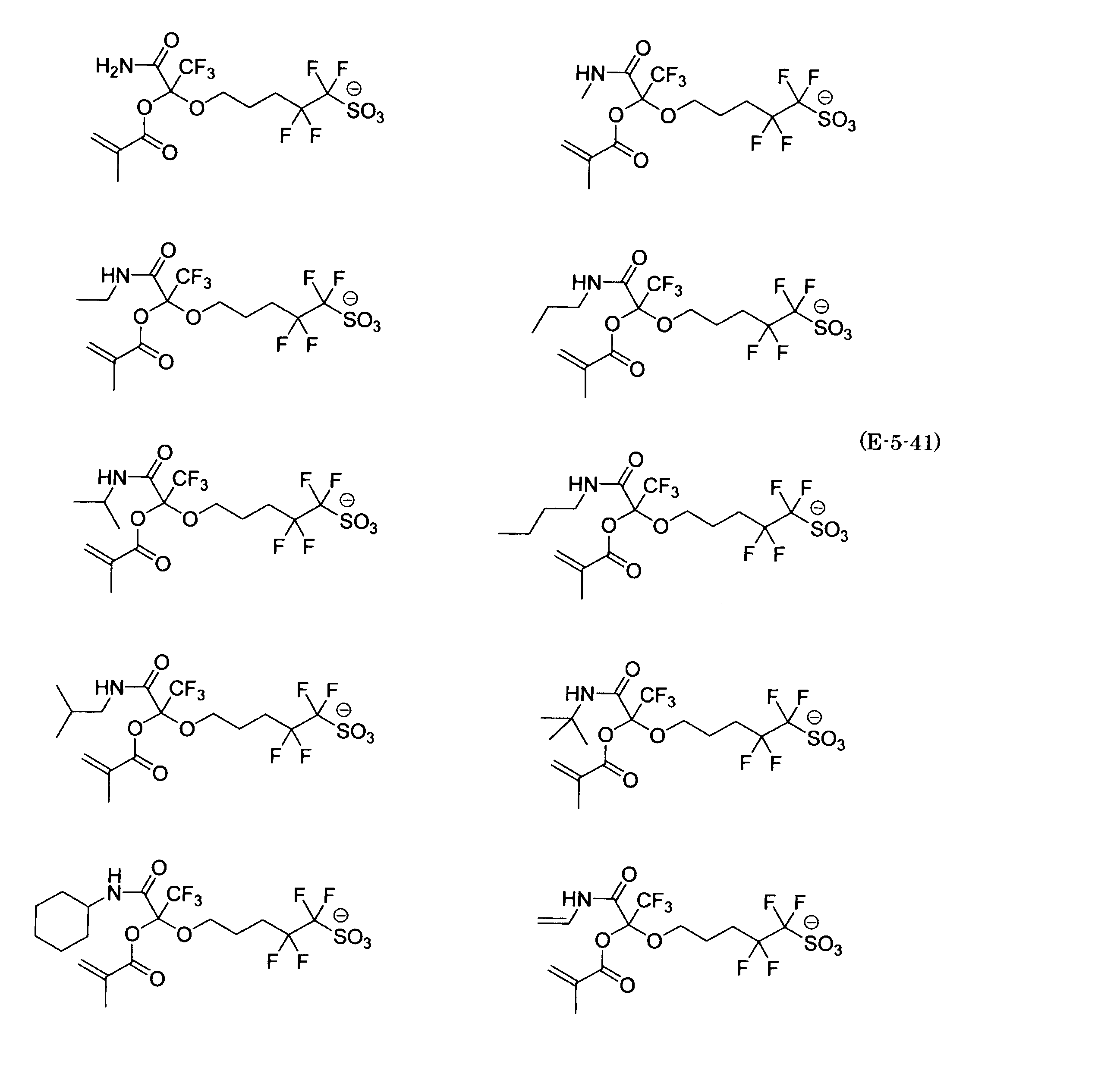
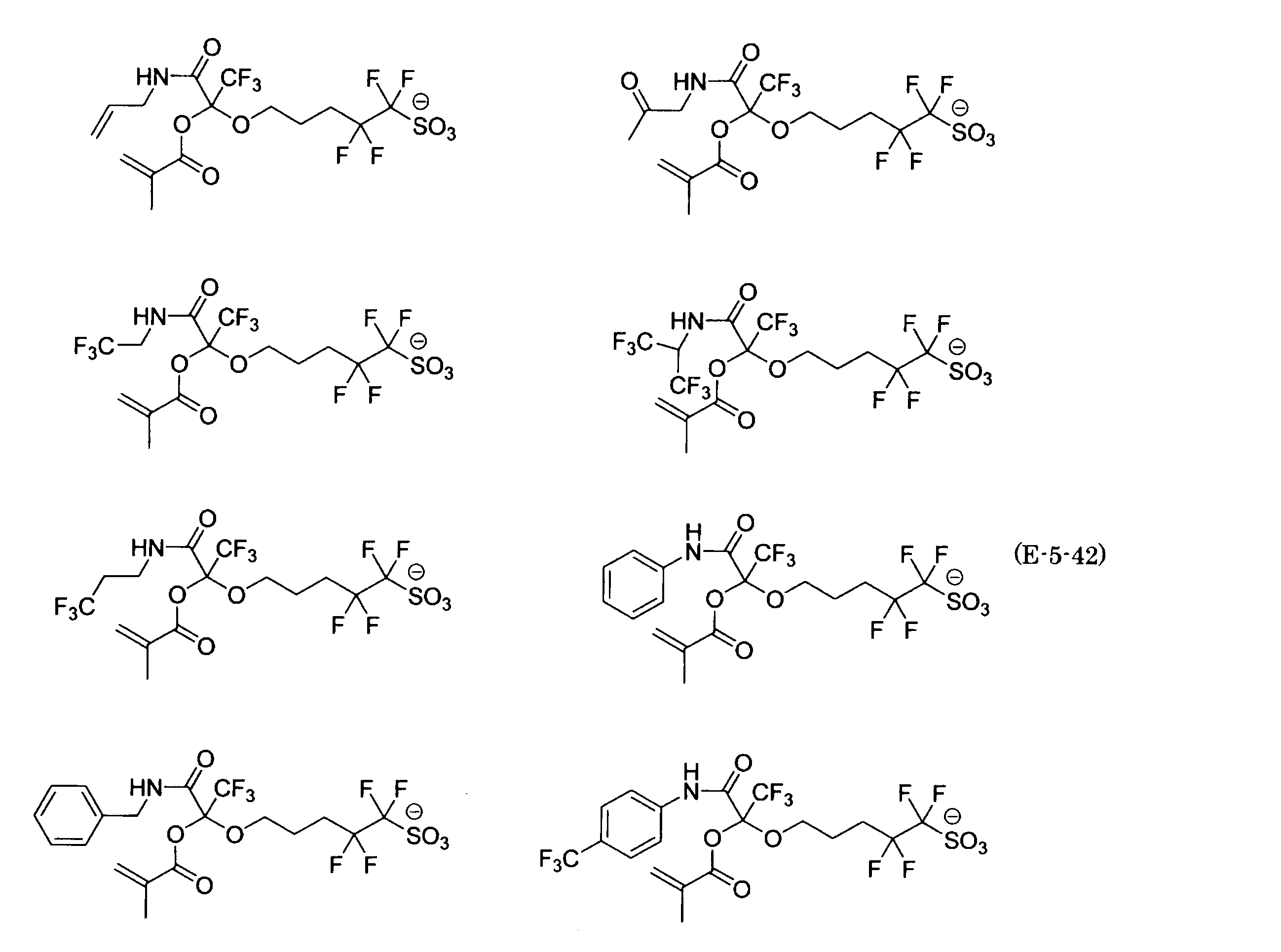
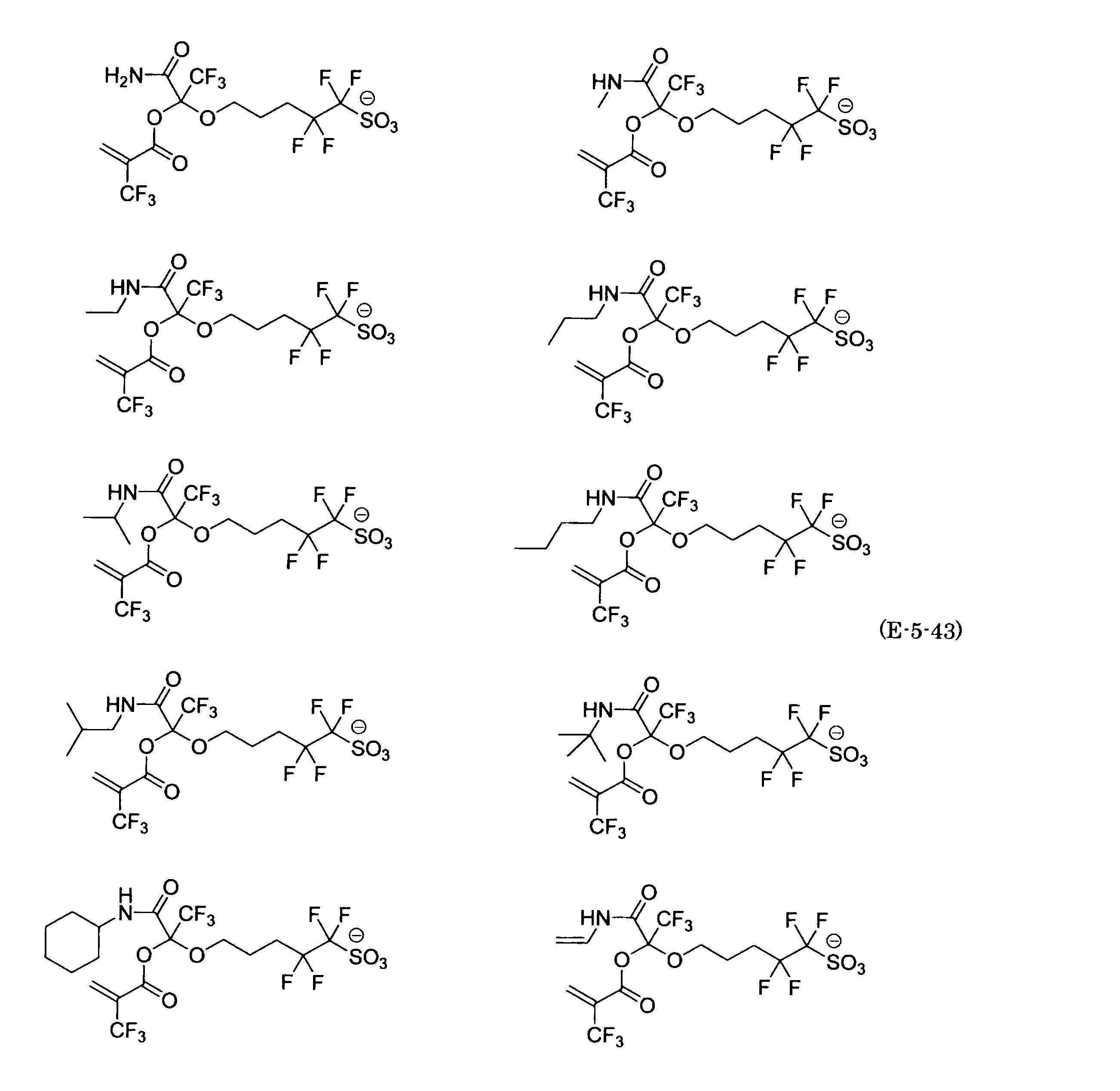
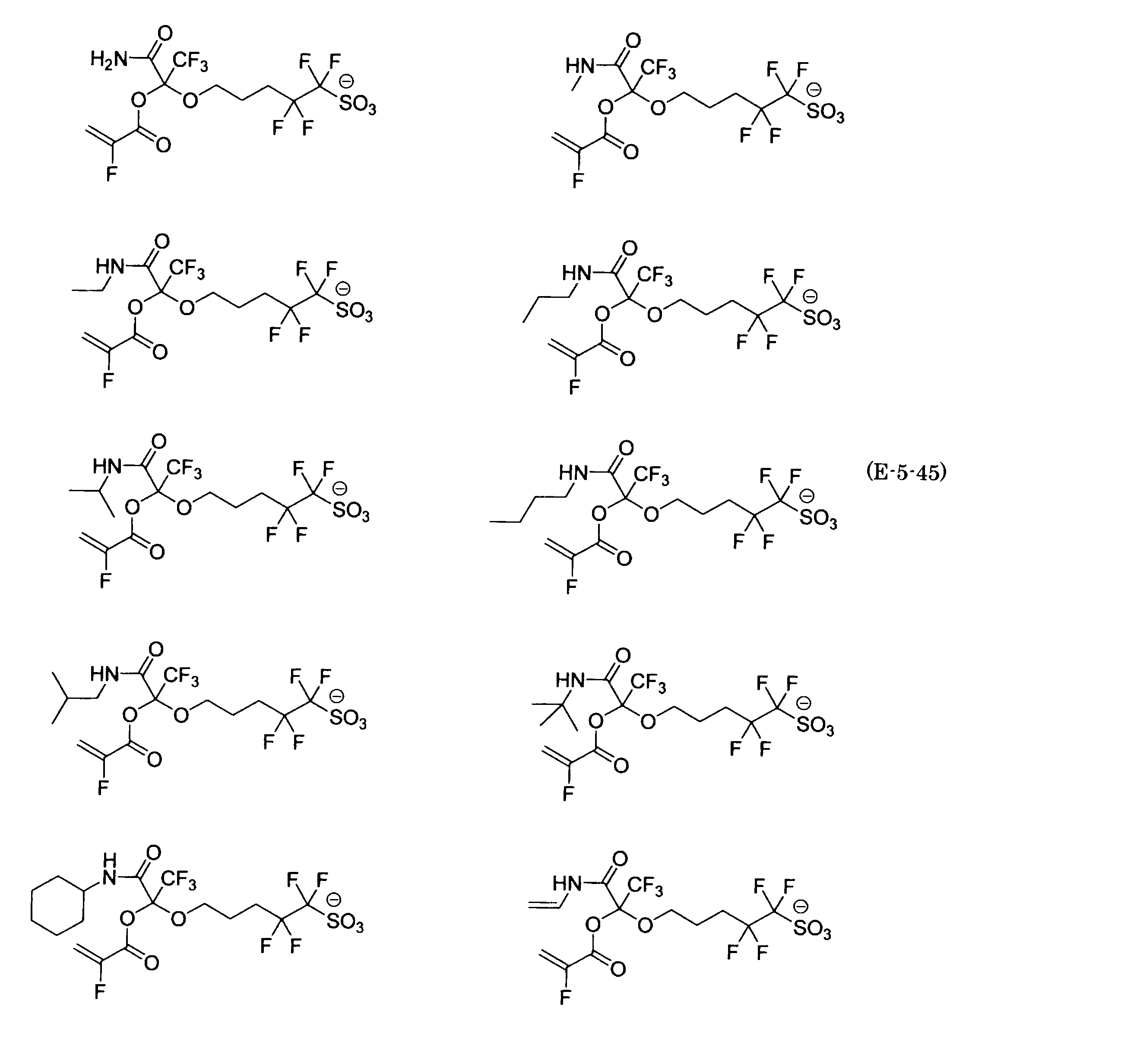
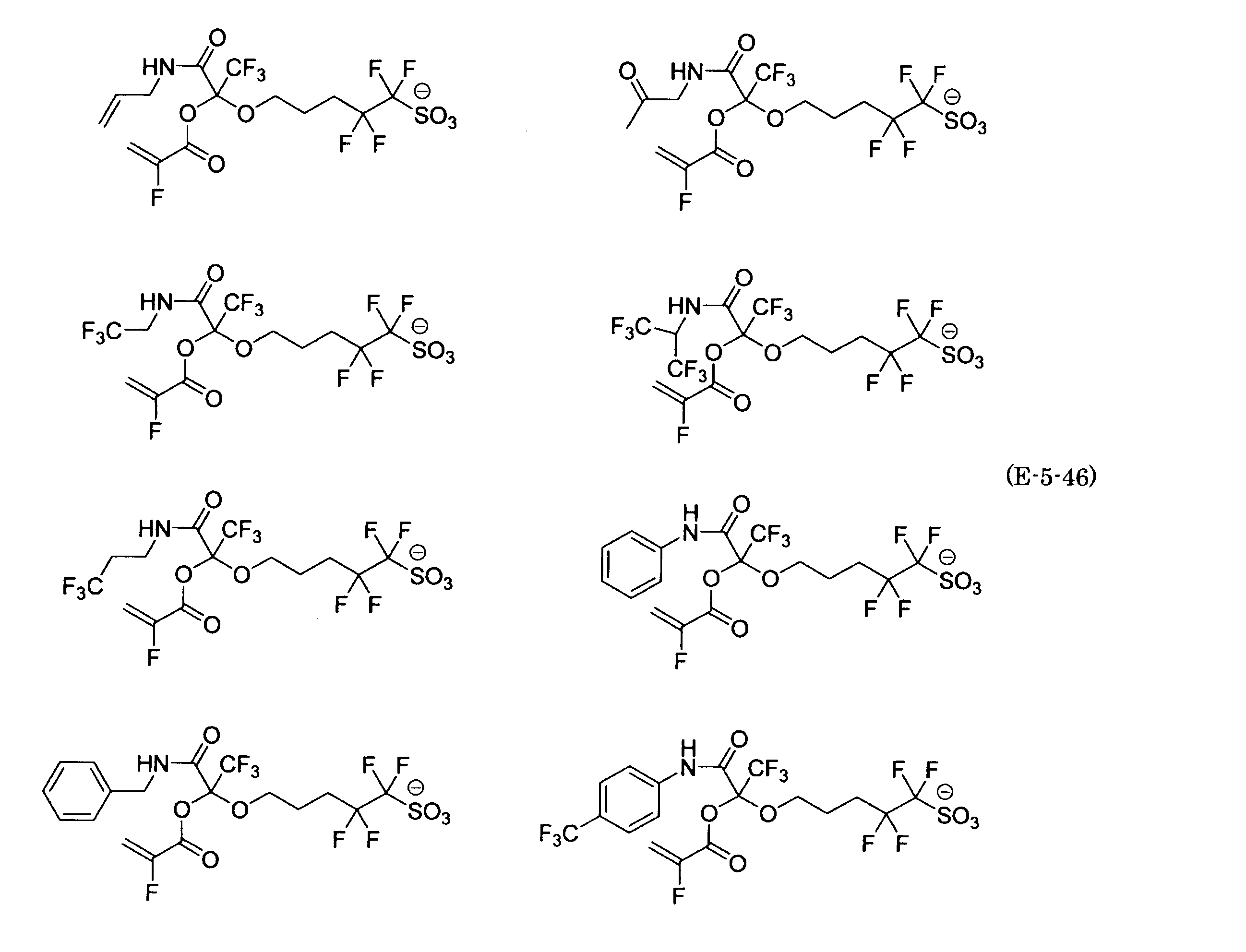
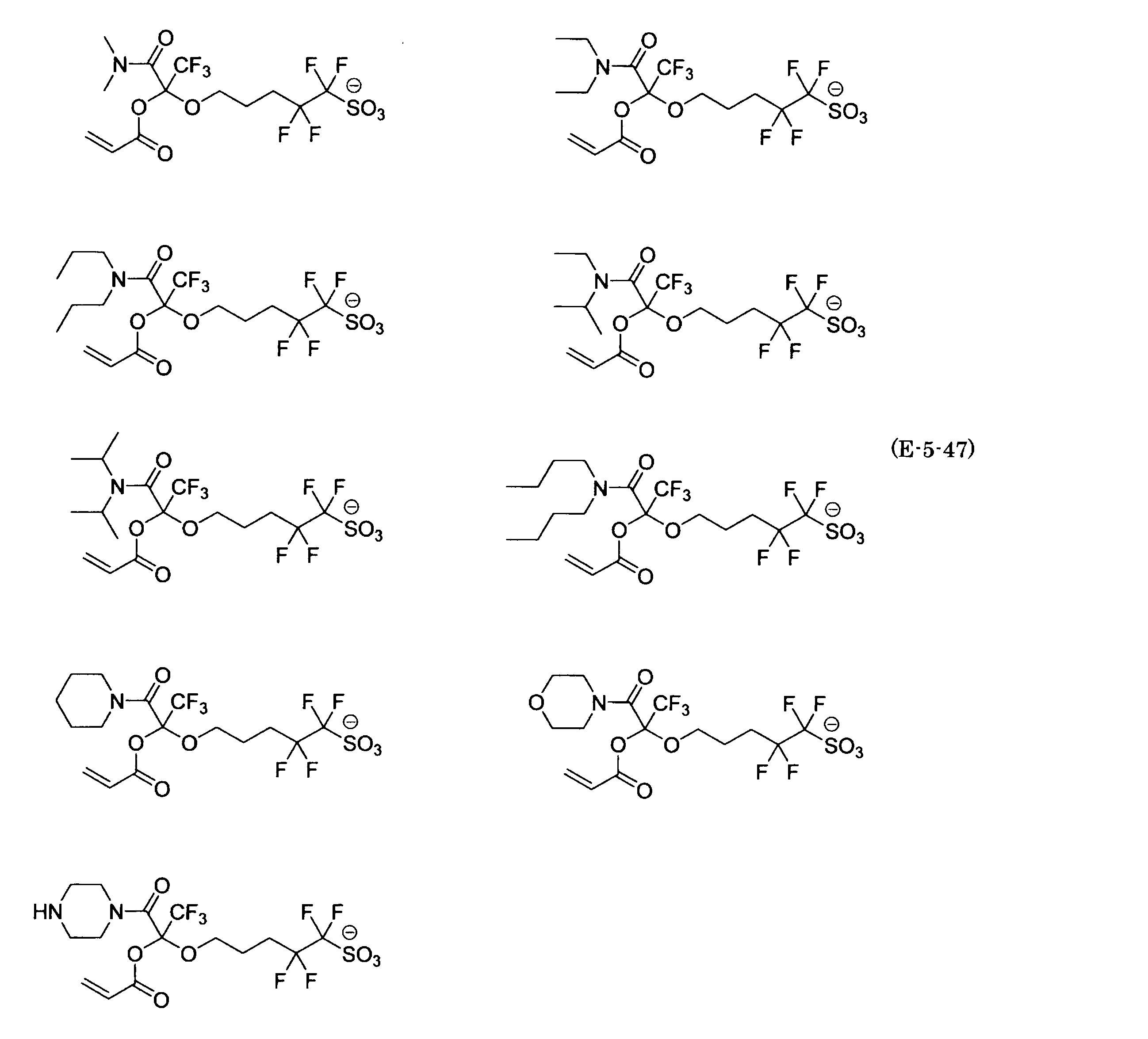
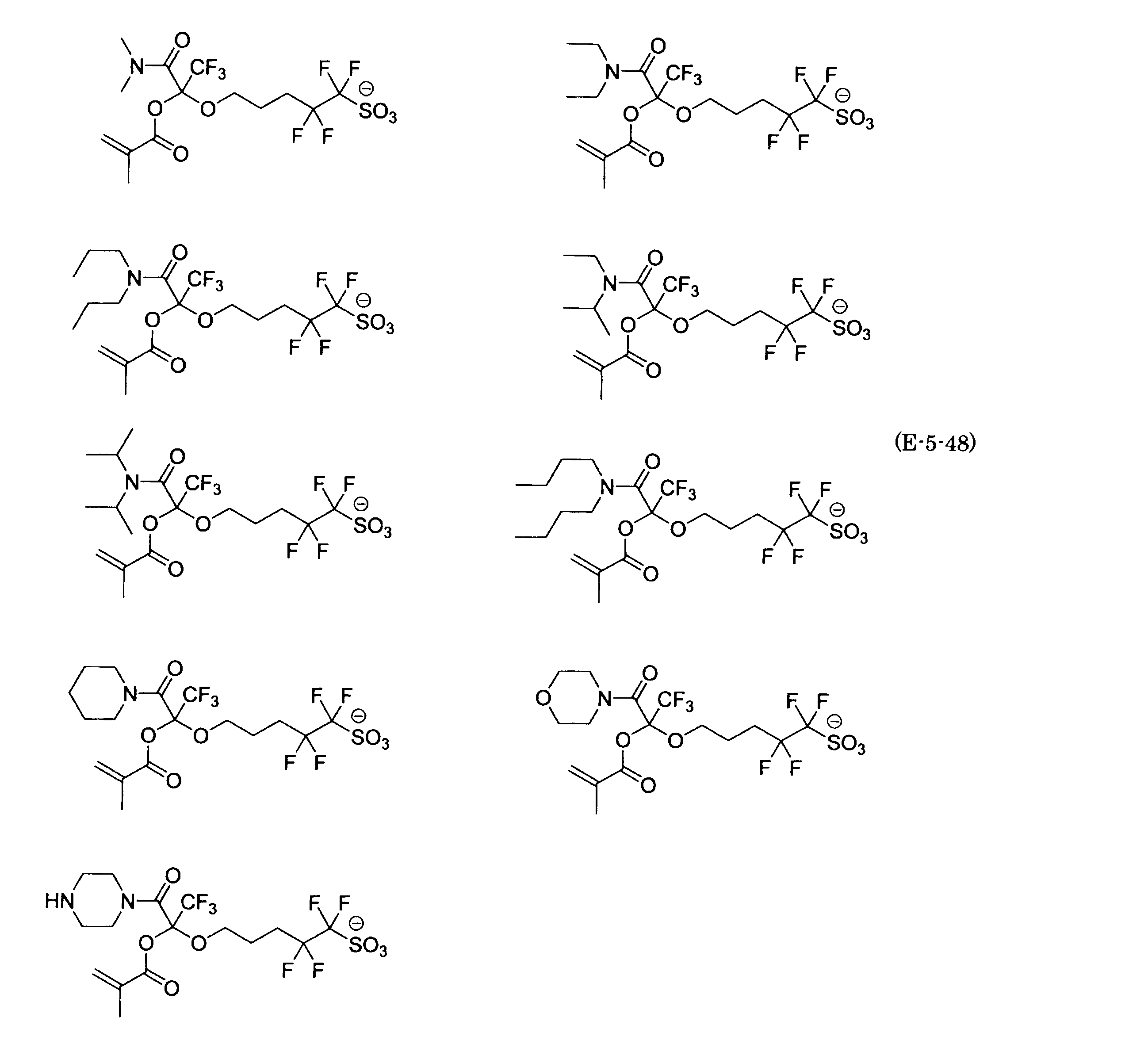
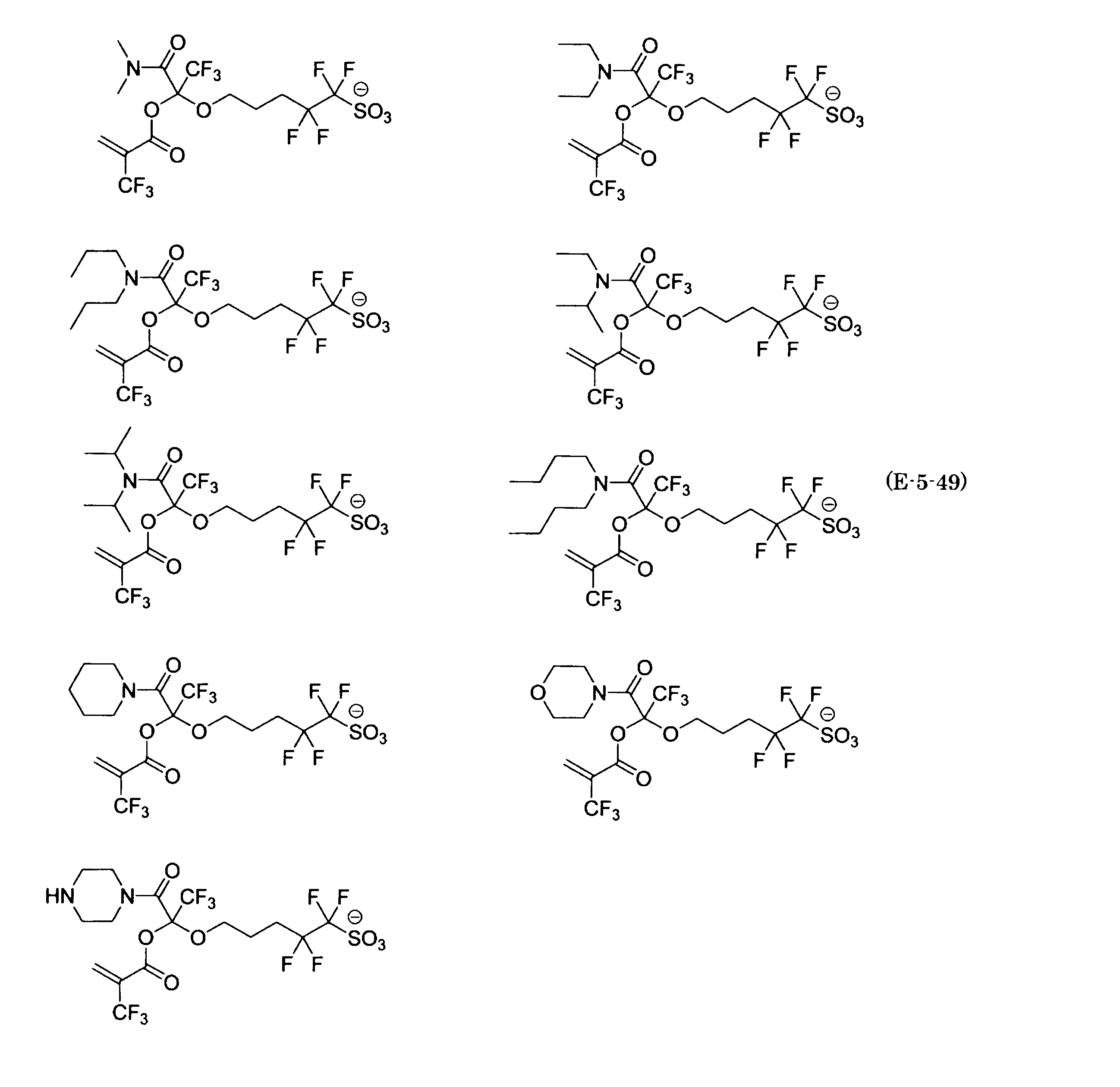
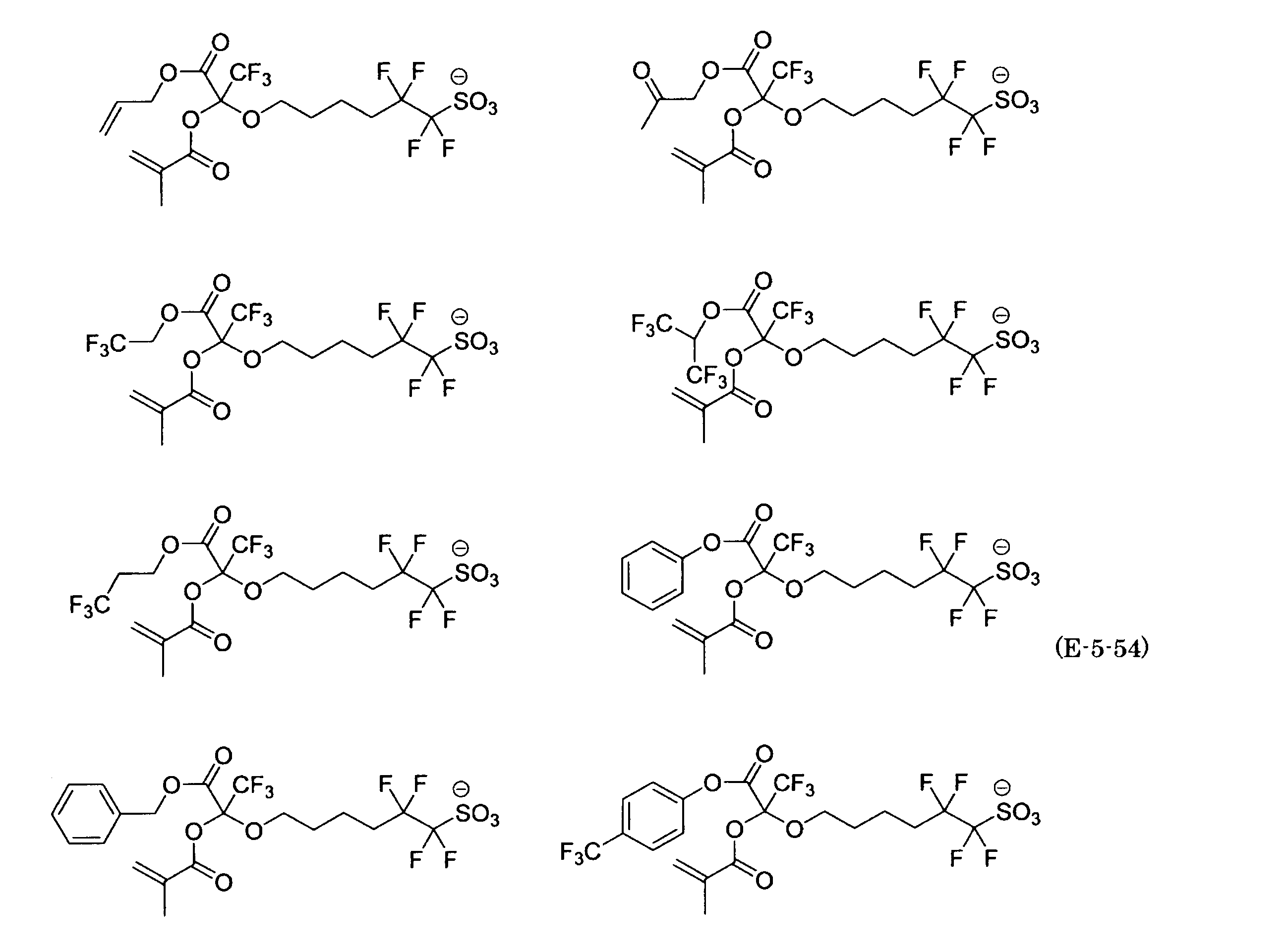
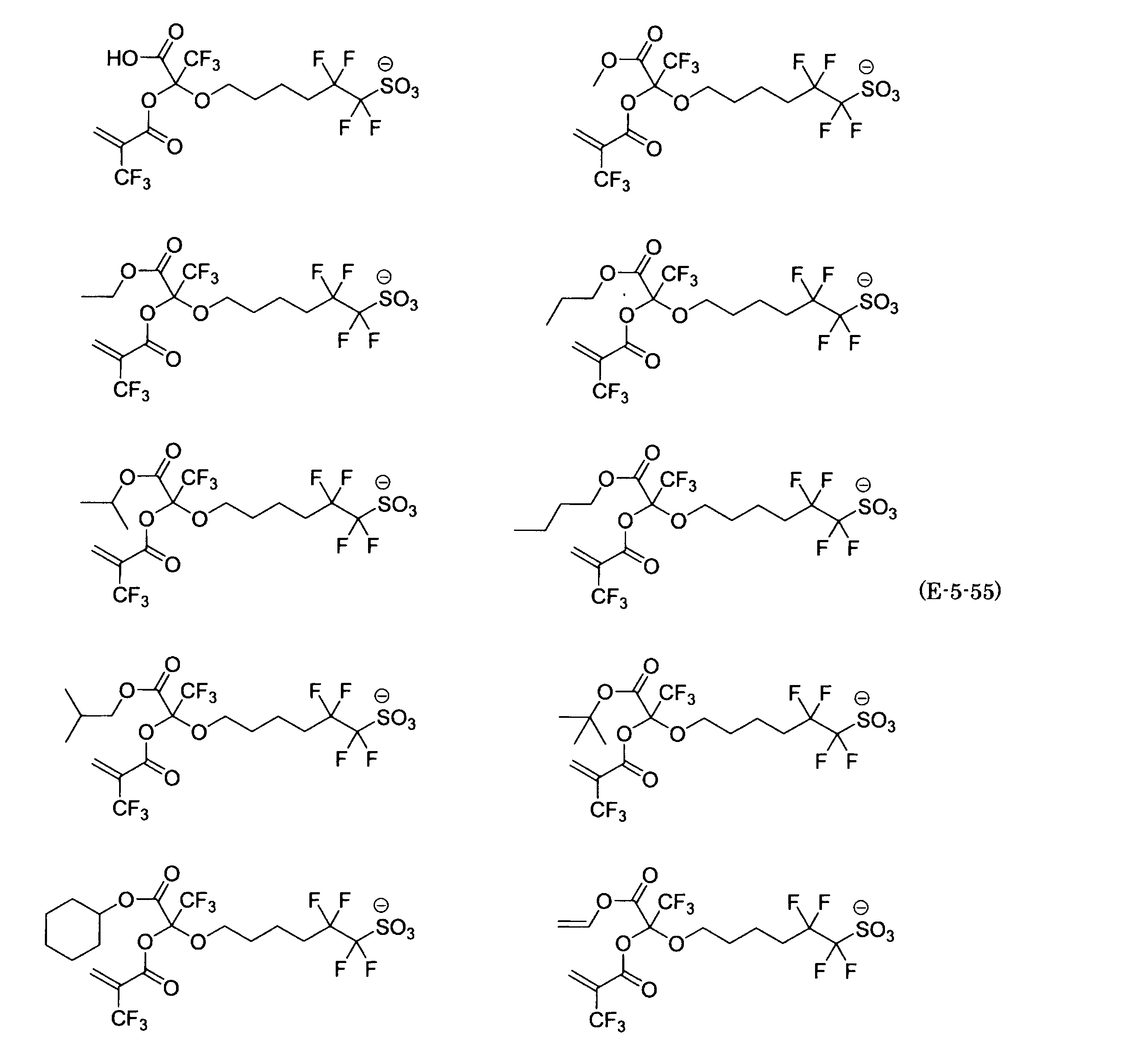
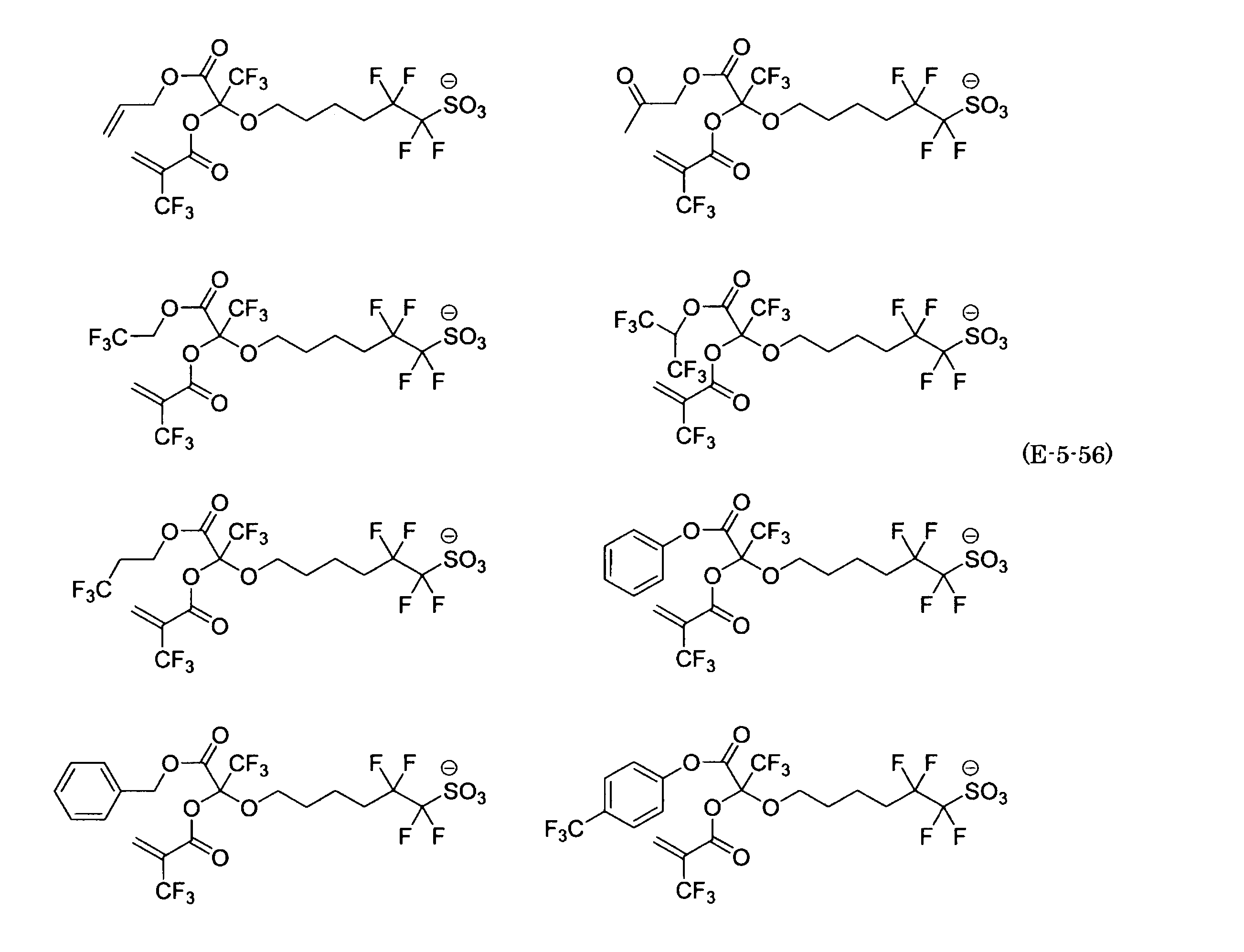
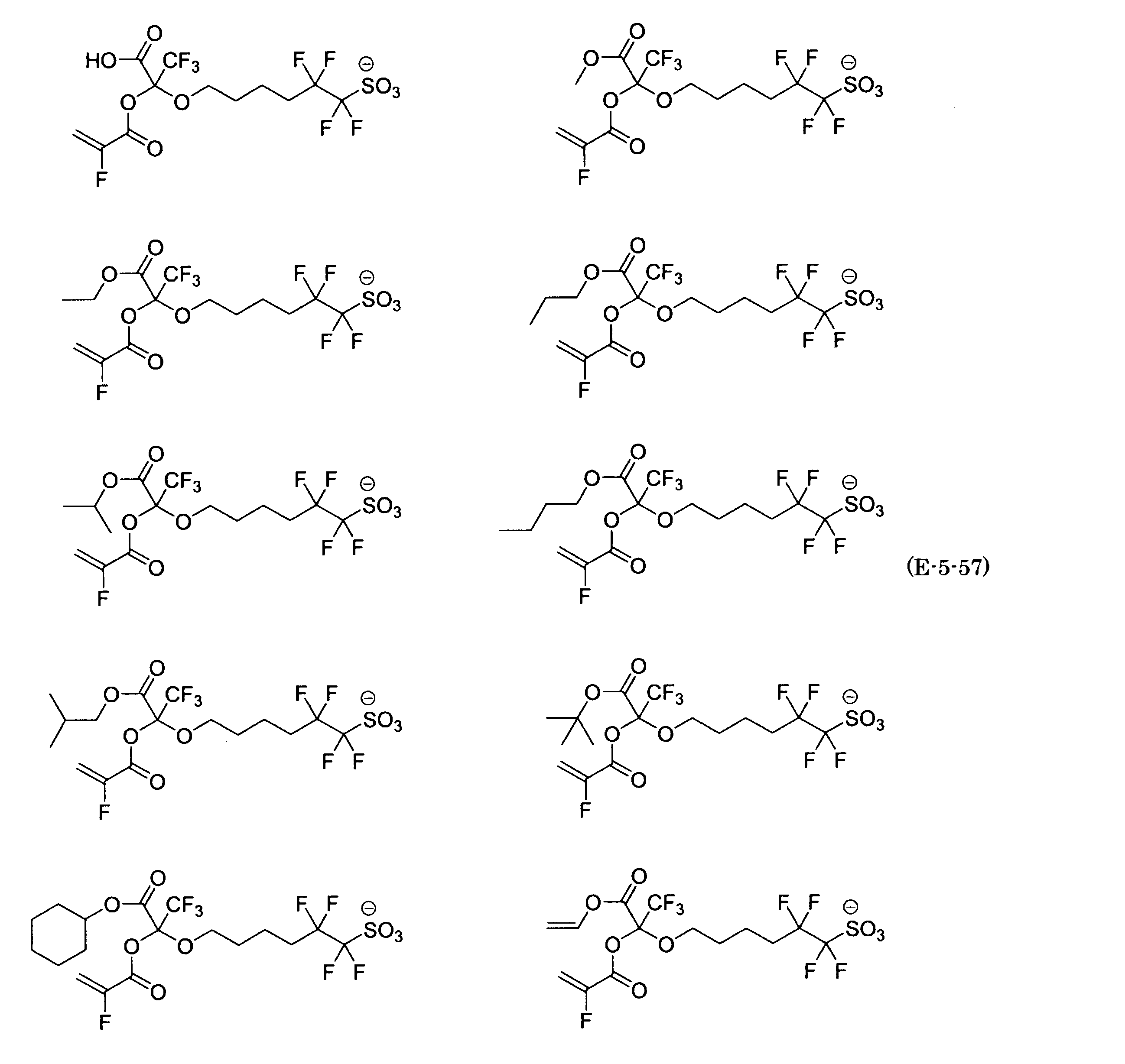
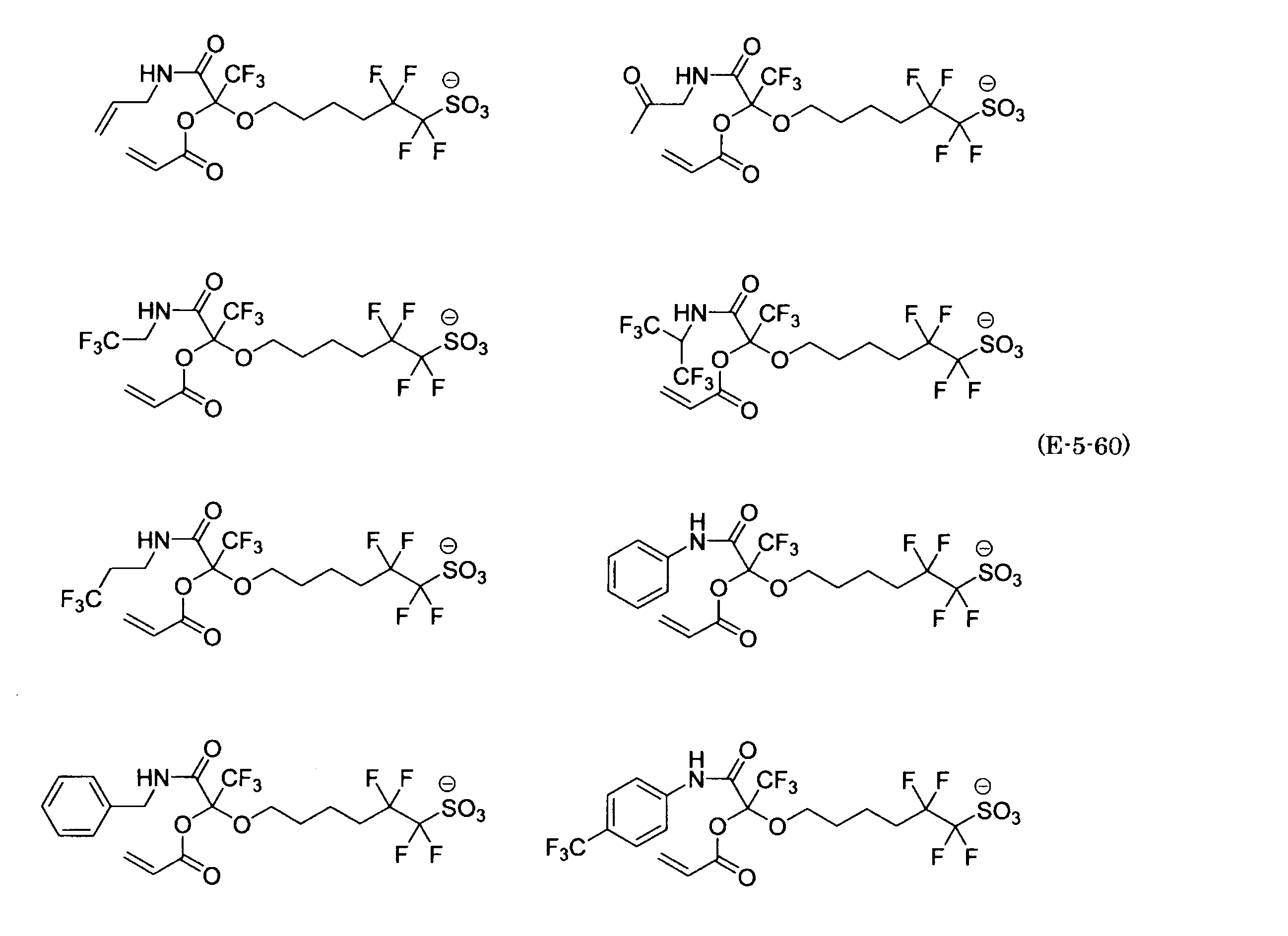
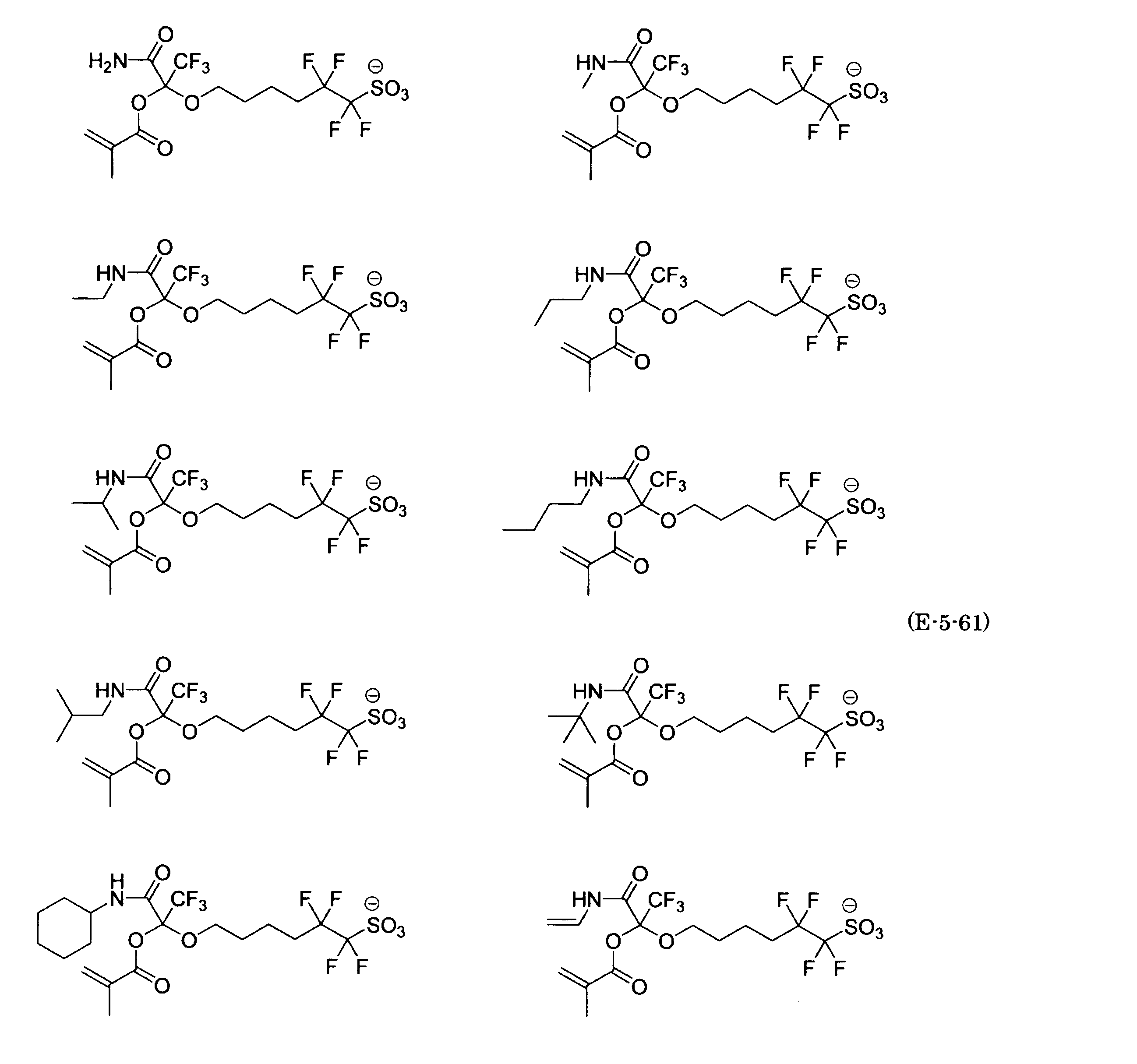
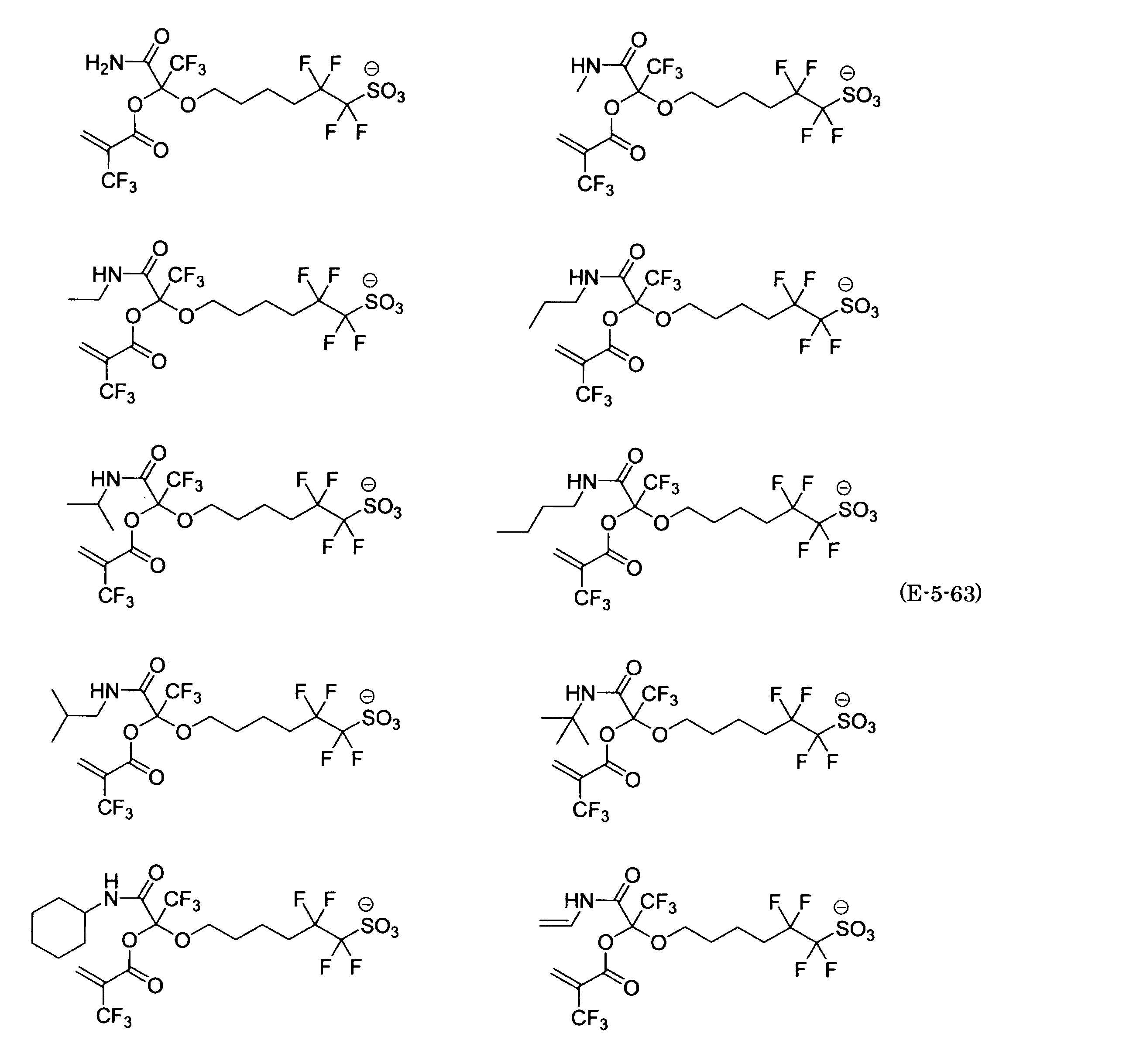
- the fluorinated sulfonate represented by the general formula (1-1) is a cation M + bonded to each of the following anion structures.
- the fluorinated sulfonate onium salt represented by the general formula (2) is A salt in which a cation Q + is bonded to each of the following anion structures.
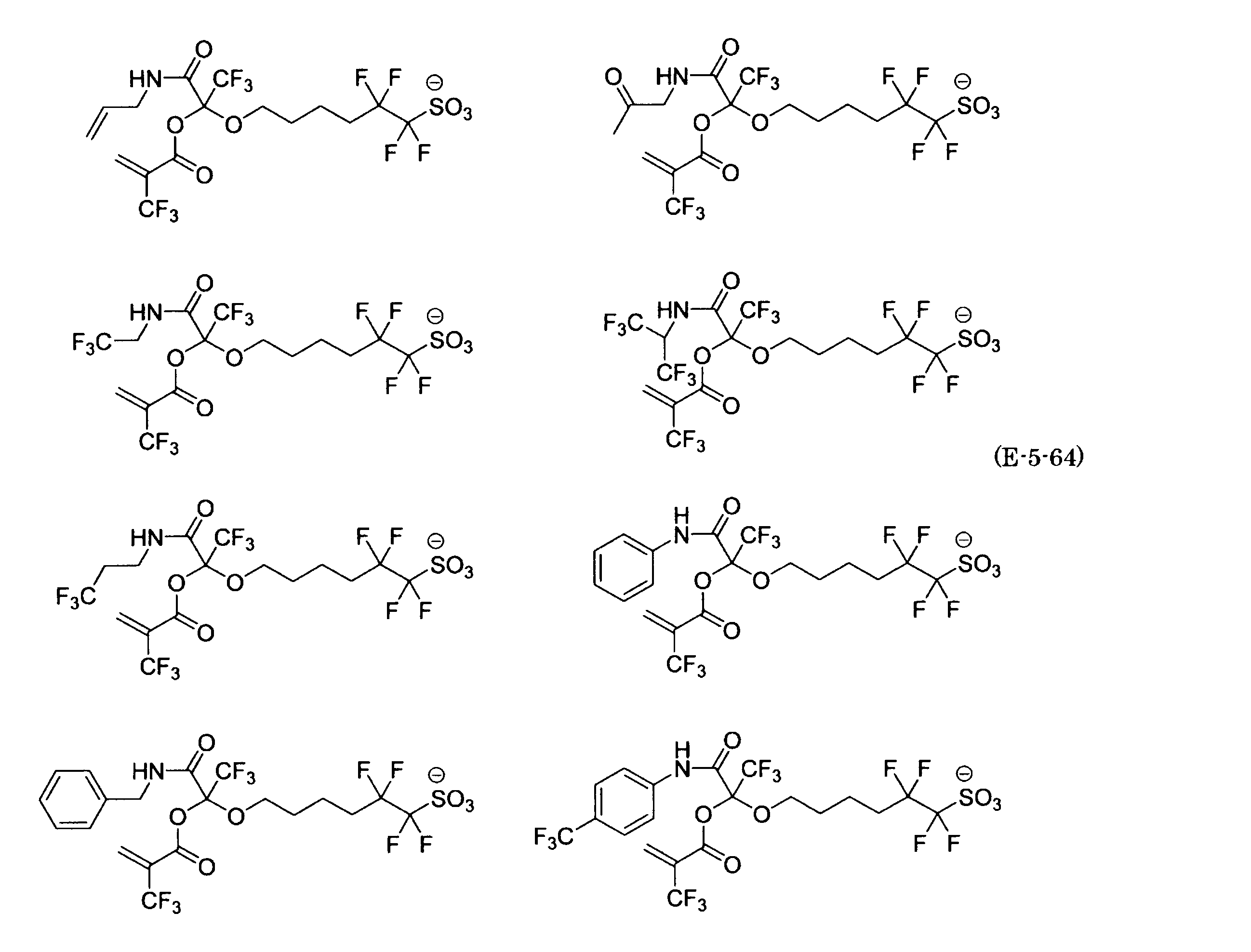
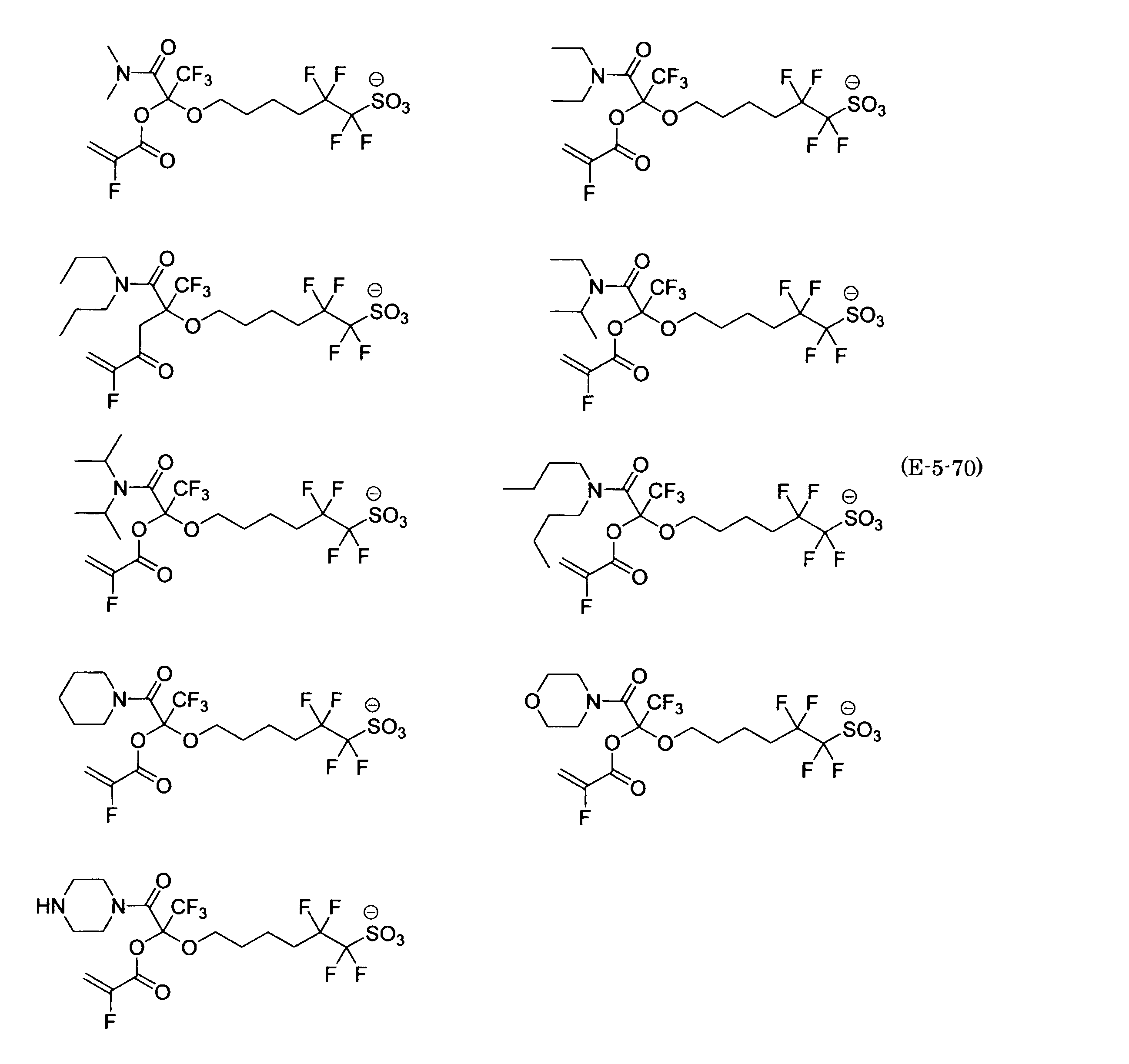
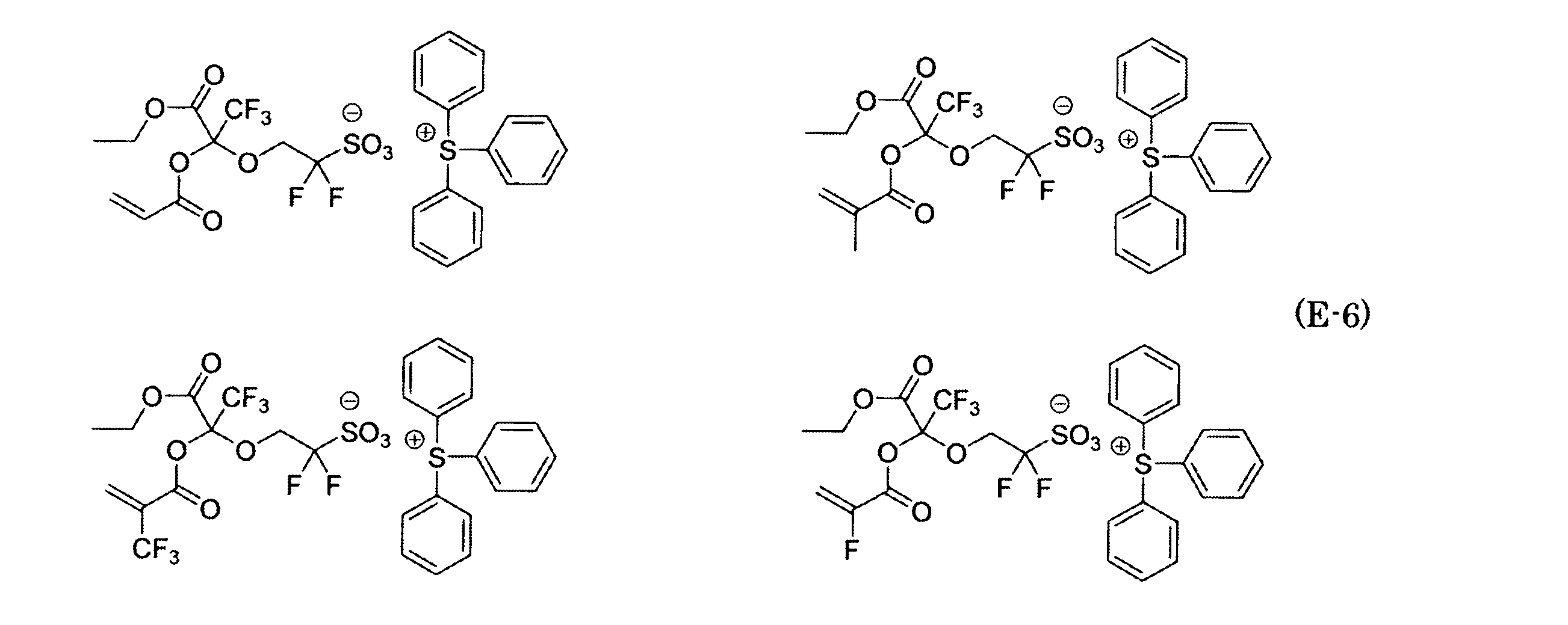
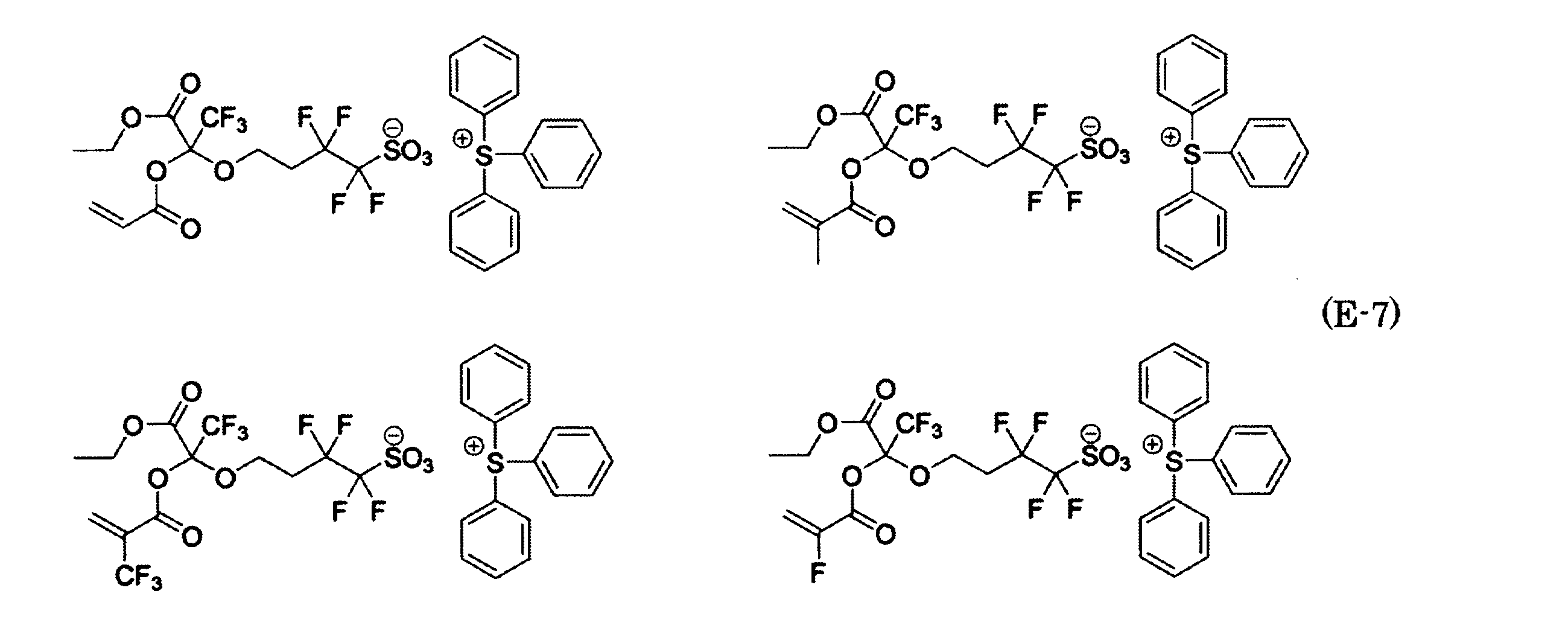
- Polymerizable fluorine-containing sulfonic acid onium salt A preferred example of the polymerizable fluorine-containing sulfonate having an anion structure represented by the general formula (1) of the present invention is a polymerizable fluorine-containing sulfonic acid onium salt represented by the following general formula (2).
- This polymerizable fluorine-containing sulfonic acid onium salt is a monomer, and the resin obtained by homopolymerizing or copolymerizing it is a fluorine-containing fluorine salt with very high acid strength in response to high energy rays.
- the polymerizable fluorine-containing sulfonic acid onium salt or a resin obtained therefrom can function as a photoacid generator.
- the polymerizable fluorine-containing sulfonic acid onium salt can be copolymerized with a monomer having an acid labile group or a crosslinking site, and is used for producing a base resin of a resist composition for high energy rays. It is also useful as a monomer.
- Q + is represented by the following general formula (a) (It represents a sulfonium cation or an iodonium cation represented by the following general formula (b).) Wherein R 3 , R 4 and R 5 are each independently a substituted or unsubstituted alkyl group, alkenyl group or oxoalkyl group having 1 to 20 carbon atoms, or substituted or unsubstituted 6 to 18 carbon atoms.
- R 6 and R 7 are each independently a substituted or unsubstituted alkyl group having 1 to 20 carbon atoms, an alkenyl group or an oxoalkyl group, or a substituted or unsubstituted aryl group having 6 to 18 carbon atoms, It represents an aralkyl group or an aryloxoalkyl group, or R 6 and R 7 may be bonded to each other to form a ring together with an iodine atom in the formula.
- Q + a specific structure of Q + is exemplified.
- the sulfonium cation represented by the general formula (a) and the iodonium cation represented by the general formula (b) will be described in
- R 3 , R 4 and R 5 in the general formula (a) include the following.
- the substituted or unsubstituted alkyl group having 1 to 20 carbon atoms may be a linear, branched or cyclic alkyl group, and may have a substituent.
- the substituted or unsubstituted alkenyl group having 1 to 20 carbon atoms may be a linear, branched or cyclic alkenyl group, and may have a substituent.
- vinyl group, allyl group, propenyl group, butenyl group, hexenyl group, cyclohexenyl group and the like can be mentioned.
- the substituted or unsubstituted oxoalkyl group having 1 to 20 carbon atoms may be a linear, branched or cyclic oxoalkyl group, and may have a substituent.
- 2-oxocyclopentyl group 2-oxocyclohexyl group, 2-oxopropyl group, 2-oxoethyl group, 2-cyclopentyl-2-oxoethyl group, 2-cyclohexyl-2-oxoethyl group, 2- (4-methylcyclohexyl) ) -2-oxoethyl group and the like.
- Examples of the substituted or unsubstituted aryl group having 6 to 18 carbon atoms include phenyl group, naphthyl group, thienyl group, p-methoxyphenyl group, m-methoxyphenyl group, o-methoxyphenyl group, p-ethoxyphenyl group, Alkoxyphenyl groups such as p-tert-butoxyphenyl group and m-tert-butoxyphenyl group, alkylphenyl groups such as 2-methylphenyl group, 3-methylphenyl group, 4-methylphenyl group and ethylphenyl group, methylnaphthyl Group, alkyl naphthyl group such as ethyl naphthyl group, dialkyl naphthyl group such as diethyl naphthyl group, dialkoxy naphthyl group such as dimethoxy naphthyl group, diethoxy naphthyl group and the like
- Examples of the substituted or unsubstituted aralkyl group having 6 to 18 carbon atoms include benzyl group, 1-phenylethyl group, 2-phenylethyl group and the like.
- Examples of the substituted or unsubstituted aryloxoalkyl group having 6 to 18 carbon atoms include 2-phenyl-2-oxoethyl group, 2- (1-naphthyl) -2-oxoethyl group, 2- (2-naphthyl) -2- And 2-aryl-2-oxoethyl group such as oxoethyl group.
- R 3 , R 4 and R 5 are bonded to each other to form a cyclic structure via a sulfur atom, 1,4-butylene, 3 -Oxa-1,5-pentylene and the like.
- substituents include aryl groups having a polymerizable substituent such as acryloyloxy group and methacryloyloxy group.
- 4- (acryloyloxy) phenyl group, 4- (methacryloyloxy) phenyl group, 4 -Vinyloxyphenyl group, 4-vinylphenyl group and the like can be mentioned.
- the sulfonium cation represented by the general formula (a) is represented by triphenylsulfonium, (4-tert-butylphenyl) diphenylsulfonium, bis (4-tert-butylphenyl) phenylsulfonium, tris (4- tert-butylphenyl) sulfonium, (3-tert-butylphenyl) diphenylsulfonium, bis (3-tert-butylphenyl) phenylsulfonium, tris (3-tert-butylphenyl) sulfonium, (3,4-ditert-butyl Phenyl) diphenylsulfonium, bis (3,4-ditert-butylphenyl) phenylsulfonium, tris (3,4-ditert-butylphenyl) sulfonium, (4-tert-butoxyphenyl) di
- triphenylsulfonium (4-tert-butylphenyl) diphenylsulfonium, (4-tert-butoxyphenyl) diphenylsulfonium, tris (4-tert-butylphenyl) sulfonium, (4-tert-butoxycarbonylmethyloxyphenyl) ) Diphenylsulfonium and the like.
- Specific iodonium cations include bis (4-methylphenyl) iodonium, bis (4-ethylphenyl) iodonium, bis (4-tert-butylphenyl) iodonium, bis (4- (1,1-dimethylpropyl) phenyl. ) Iodonium, (4-methoxyphenyl) phenyliodonium, (4-tert-butoxyphenyl) phenyliodonium, 4- (acryloyloxy) phenylphenyliodonium, 4- (methacryloyloxy) phenylphenyliodonium, and the like. (4-tert-butylphenyl) iodonium is preferably used.
- polymerizable fluorine-containing sulfonic acid onium salt represented by the general formula (2) include a polymerizable fluorine-containing sulfone having a structure represented by the general formula (1) specifically exemplified above.
- a combination of the acid salt and the sulfonium cation represented by the general formula (a) or the iodonium cation represented by the general formula (b) exemplified here can be exemplified.
- the polymerizable fluorine-containing sulfonic acid onium salt represented by the general formula (2) includes the first step and the second step from the compound represented by the general formula (13) as shown in the following scheme (2). It can be manufactured in a process.
- X, n, R 1, R 2 and Q + are X, n, R 1, R 2 and Q + and respectively the same in the general formula (1-1).
- Z represents a hydroxyl group, a halogen atom or —O (C ⁇ O) C (R 1 ) ⁇ CH 2 group.
- General formula (13) represents hydroxyfluoroalkanesulfonic acid onium salt.
- X represents a hydrogen atom or a fluorine atom, n represents an integer of 1 to 10, and Q + represents a sulfonium cation or an iodonium cation.
- the cation illustrated by description of General formula (2) can be illustrated again.
- the production methods of these compounds are described in Japanese Patent Application Laid-Open No. 2009-91351, International Publication No. 2008/56795, International Publication No. 2006/121096, and Japanese Patent Application Laid-Open No. 2010-18573.
- General formula (14) represents a trifluoropyruvic acid derivative.
- R 2 represents R A O or R B R C N.
- R A , R B and R C are each independently a hydrogen atom, an alkyl group having 1 to 20 carbon atoms, an alkenyl group having 2 to 20 carbon atoms or an oxoalkyl group having 2 to 20 carbon atoms, or 6 to 6 carbon atoms.
- 18 represents an aryl group, an aralkyl group having 6 to 18 carbon atoms, or a lactone group having 3 to 30 carbon atoms.
- R B and R C may form a heterocyclic ring having 3 to 18 ring members.
- the hydrogen atoms on carbon contained in R A, R B and R C may be substituted by a substituent.
- Specific examples of R 2 include the cations exemplified in the description of the general formula (1-1).
- the commercially available trifluoropyruvic acid derivative represented by the general formula (14) can be used as it is, or can be prepared by a known method.
- General formula (16) represents a carboxylic acid derivative.
- Z is a hydroxyl group, it is a carboxylic acid, and when Z is any halogen atom of fluorine, chlorine, bromine and iodine, it is an acid halide.
- Z is —O (C ⁇ O) C (R 1 ) ⁇ CH 2 group, it represents an acid anhydride.
- R 1 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- carboxylic acid derivative represented by the general formula (16) a commercially available product can be used as it is, or it can be prepared by a known method.
- the first step is a step of adding the trifluoromethylpyruvic acid derivative represented by the general formula (14) to the hydroxyfluoroalkanesulfonic acid onium salt represented by the general formula (13).
- the trifluoromethylpyruvic acid derivative represented by the general formula (14) is added to the hydroxyfluoroalkanesulfonic acid onium salt represented by the general formula (13) in the presence of an acid catalyst or without catalyst. The method of making it react on conditions can be illustrated.
- the amount of the trifluoromethylpyruvic acid derivative used to act on the hydroxyfluoroalkanesulfonic acid onium salt represented by the general formula (13) Is not particularly limited, but is usually 0.1 to 5 mol, preferably 0.2 to 3 mol, more preferably, to 1 mol of hydroxyfluoroalkanesulfonic acid onium salt. 0.5 to 2 moles.
- the amount of the trifluoromethylpyruvic acid derivative used is particularly preferably 0.8 to 1.5 mol.
- This addition reaction can be performed in the presence or absence of a solvent, but it is usually preferable to use an aprotic solvent.
- an aprotic solvent diisopropyl ether, dichloroethane, chloroform, toluene, ethylbenzene, monochlorobenzene, acetonitrile, N, N-dimethylformamide and the like are used. These solvents may be used alone or in combination of two or more.
- the reaction temperature is not particularly limited and is usually in the range of 0 to 100 ° C, preferably 10 to 80 ° C.
- the reaction is preferably carried out with stirring.
- reaction time depends on the reaction temperature, it is usually several minutes to 100 hours, preferably 30 minutes to 50 hours, and more preferably 1 to 20 hours. It is preferable to use the analytical instrument such as) as the end point of the reaction when the raw material hydroxyfluoroalkanesulfonic acid onium salt is consumed.
- This reaction is usually performed under non-catalytic conditions, but the reaction proceeds in the same manner even when an acid catalyst is used.
- an acid catalyst an organic acid such as p-toluenesulfonic acid and / or an inorganic acid such as sulfuric acid is used.
- the target fluorine-containing sulfonic acid onium salt represented by the general formula (15) can be obtained by removing the solvent under reduced pressure.
- the fluorine-containing sulfonic acid onium salt represented by the general formula (15) can be purified by ordinary means such as extraction and recrystallization.
- esterification method examples include a method of dehydrating and condensing the carboxylic acid (Z is a hydroxyl group) represented by the general formula (16) and a fluorine-containing sulfonic acid onium salt in the presence of an acid catalyst (Fischer ester synthesis reaction), Carboxylic acid halides represented by general formula (16) (Z is a halogen atom) or carboxylic acid anhydride (Z is —O (C ⁇ O) C (R 1 ) ⁇ CH 2 group), and general formula (15 And the like, and the like.
- the amount of the carboxylic acid to be used for the fluorine-containing sulfonic acid onium salt is not particularly limited.
- the amount is from 0.1 to 5 mol, preferably from 0.2 to 3 mol, more preferably from 0.5 to 2 mol, per mol of the fluorine-containing sulfonic acid onium salt.
- the amount of carboxylic acid used is particularly preferably 0.8 to 1.5 mol.
- This esterification reaction can be performed in the presence or absence of a solvent, but it is usually preferable to use an aprotic solvent.
- an aprotic solvent dichloroethane, toluene, ethylbenzene, monochlorobenzene, acetonitrile, N, N-dimethylformamide and the like are used. These solvents may be used alone or in combination of two or more.
- Fluorine-containing sulfonic acid onium salt is hardly dissolved in aromatic hydrocarbons such as toluene, ethylbenzene, and monochlorobenzene and becomes a slurry, but the reaction proceeds even in such a state.
- the reaction temperature is not particularly limited, and is usually in the range of 0 to 200 ° C., preferably 20 to 180 ° C., more preferably 50 to 150 ° C.
- the reaction is preferably carried out with stirring.
- reaction time depends on the reaction temperature, it is usually from several minutes to 100 hours, preferably from 30 minutes to 50 hours, more preferably from 1 to 20 hours, but gas chromatography (GC) And the end point of the reaction is preferably the time when the fluorine-containing sulfonic acid onium salt represented by the general formula (15) is consumed.
- GC gas chromatography
- a catalyst is usually used, and an acid catalyst is preferable.
- the acid catalyst may be selected from known catalysts in the esterification reaction, and an organic acid such as p-toluenesulfonic acid and / or an inorganic acid such as sulfuric acid is used.
- a dehydrating agent may be added to the reaction system, and 1,1′-carbonyldiimidazole, N, N′-dicyclohexylcarbodiimide or the like can be used as the dehydrating agent.
- the amount of the acid catalyst to be used is not particularly limited, but is 0.0001 to 10 mol, preferably 0.001 to 5 mol, more preferably 1 mol with respect to 1 mol of the fluorine-containing sulfonic acid onium salt. Is from 0.01 to 1.5 mol.
- the esterification reaction using an acid catalyst is preferably carried out while dehydrating using a Dean Stark apparatus or the like because the reaction time tends to be shortened.
- the polymerizable fluorine-containing sulfonic acid onium salt represented by the general formula (2) can be obtained by ordinary means such as extraction, reprecipitation, recrystallization and the like. Moreover, it can also refine
- the amount of the carboxylic acid halide or carboxylic acid anhydride represented by the general formula (16) that acts on the fluorinated sulfonic acid onium salt is not particularly limited, but is usually fluorinated sulfonic acid onium.
- the amount is 0.1 to 5 mol, preferably 0.2 to 3 mol, and more preferably 0.5 to 2 mol with respect to 1 mol of the salt.
- the amount of carboxylic acid halides or carboxylic acid anhydrides used is particularly preferably 0.8 to 1.5 mol.
- the reaction may be performed without a solvent or may be performed in a solvent inert to the reaction.
- a solvent is not particularly limited as long as it is a reaction-inert solvent, and for example, water, an organic solvent, or a mixed system thereof may be used.
- organic solvent examples include ketone solvents such as acetone, methyl ethyl ketone and methyl isobutyl ketone, ester solvents such as ethyl acetate and butyl acetate, ether solvents such as diethyl ether, diethylene glycol dimethyl ether, tetrahydrofuran and dioxane, dichloromethane, chloroform, Halogen solvents such as carbon chloride, 1,2-dichloroethane, tetrachloroethylene, chlorobenzene, orthochlorobenzene, polar solvents such as acetonitrile, N, N-dimethylformamide, N, N-dimethylimidazolidinone, dimethyl sulfoxide, sulfolane, etc. An example is represented. These solvents may be used alone or in combination of two or more.
- the reaction temperature is not particularly limited and is usually in the range of ⁇ 78 to 150 ° C., preferably ⁇ 20 to 120 ° C., and more preferably 0 to 100 ° C.
- reaction time depends on the reaction temperature, it is usually from several minutes to 100 hours, preferably from 30 minutes to 50 hours, more preferably from 1 to 20 hours, but gas chromatography (GC) It is preferable to use an analytical instrument such as NMR or a nuclear magnetic resonance apparatus (NMR) as the end point of the reaction when the raw material fluorine-containing sulfonic acid onium salt is consumed.
- GC gas chromatography
- NMR nuclear magnetic resonance apparatus
- Examples of the acid acceptor include triethylamine, pyridine, picoline, dimethylaniline, diethylaniline, 1,4-diazabicyclo [2.2.2] octane (DABCO), 1,8-diazabicyclo [5.4.0].
- Examples include organic bases such as undec-7-ene (DBU) or inorganic bases such as sodium bicarbonate, sodium carbonate, potassium carbonate, lithium carbonate, sodium hydroxide, potassium hydroxide, calcium hydroxide, magnesium oxide, etc. Is done.
- the amount of the acid acceptor used is not particularly limited, but is 0.05 to 10 mol, preferably 0.1 to 5 mol, based on 1 mol of the fluorine-containing sulfonic acid onium salt, and more Preferably, it is 0.5 to 3 mol.
- the polymerizable fluorine-containing sulfonate represented by the general formula (2) can be obtained by ordinary means such as extraction, distillation, recrystallization and the like. Moreover, it can also refine
- [Sulfonate resin] A resin containing a repeating unit represented by the following general formula (3) (sometimes referred to as “sulfonate resin” in the present specification) is a polymerizable fluorine-containing compound represented by the general formula (1-1). The polymerizable double bond of the sulfonate is formed by cleavage. In the polymerization reaction, the structure other than the polymerizable double bond does not change, and the original structure is maintained. (Wherein, X, n, R 1 and R 2 X in the general formula (1-1), n, respectively R 1 and R 2 have the same meanings .M + represents a monovalent cation.)
- the cation (M + ) is an onium ion (Q + ), which is formed by cleavage of the polymerizable double bond of the polymerizable fluorine-containing sulfonic acid onium salt represented by the general formula (2).
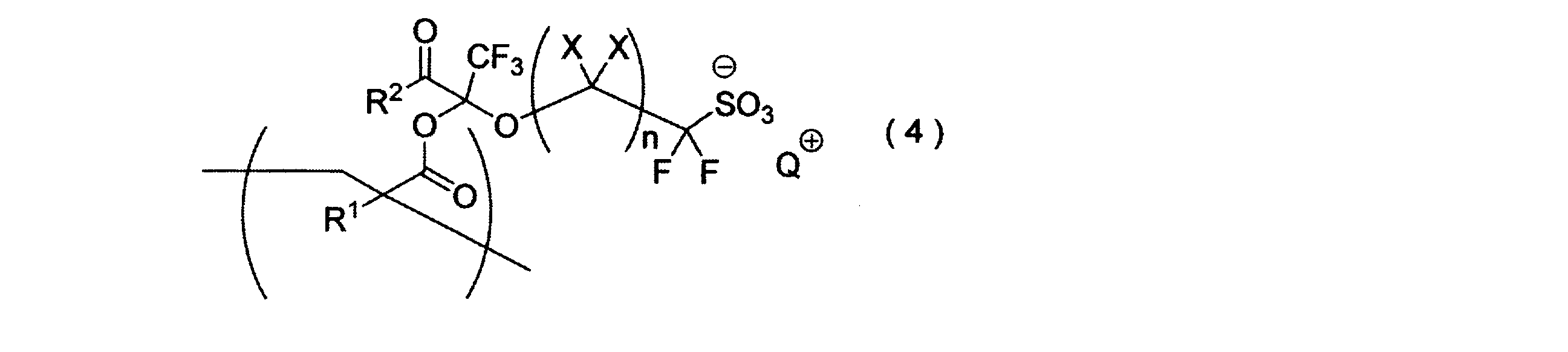
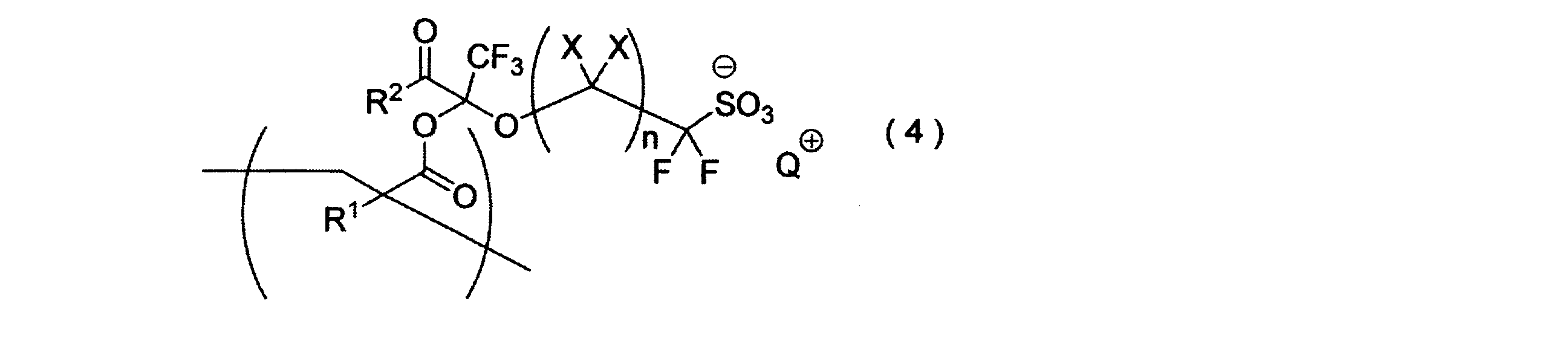
- the resin having a repeating unit include a resin having a repeating unit represented by the following general formula (4). (Wherein, X, n, R 1 and R 2 X in the general formula (1-1), n, respectively R 1 and R 2 have the same meanings .Q + and Q + in the general formula (2) Each is synonymous.)
- the resin having a repeating unit represented by the general formula (4) is converted into a resin having a repeating unit represented by the following general formula (5) by exposing the resin with a high energy ray.
- X, n, R 1 and R 2 are X in the general formula (1-1), n, R 1 and R 2 respectively the same.
- High energy rays are not particularly limited, and include excimer lasers such as KrF excimer lasers, ArF excimer lasers, and F 2 excimer lasers, electromagnetic waves (light) generated by synchrotron radiation, and charged particle beams such as electron beams.
- excimer lasers such as KrF excimer lasers, ArF excimer lasers, and F 2 excimer lasers
- electromagnetic waves (light) generated by synchrotron radiation and charged particle beams such as electron beams.
- charged particle beams such as electron beams.
- an excimer laser such as a KrF excimer laser, an ArF excimer laser, or an F 2 excimer laser, or a high energy beam having a wavelength of 300 nm or less generated by synchrotron radiation is effective.
- the terminal of the repeating unit after the elimination of Q + is difluorosulfonic acid, exhibits very strong acidity, and functions as a photoacid generator for a chemically amplified resist composition.
- the resin having at least the repeating unit represented by the general formula (4) functions as a photoacid generator, and the composition containing at least a resin having a positive or negative photosensitive solubility change function and a solvent is used as a resist. It can be used as a composition.
- the sulfonate resin may be selected from [I] a repeating unit represented by the general formula (4) formed from a polymerizable fluorine-containing sulfonic acid onium salt having a structure represented by the general formula (2). And [II] a sulfonate resin comprising a repeating unit having an acid labile group or a crosslinking site and a repeating unit represented by the general formula (4). Repeating units (referred to herein as secondary repeating units) can be included.
- the secondary repeating unit refers to a repeating unit that does not correspond to any of the repeating unit represented by the general formula (4), the acid labile group, or the repeating unit having a crosslinking site.
- the secondary monomer is a monomer in which a double bond is cleaved to form a secondary repeating unit.
- the sulfonate resin has a single weight consisting only of a repeating unit represented by the general formula (4) obtained by homopolymerizing a polymerizable fluorine-containing sulfonic acid onium salt having a structure represented by the general formula (2). It may be a coalescence or may contain secondary repeating units. Although these cannot be used as positive or negative resists themselves, they can constitute a resist composition as a photoacid generator together with a base resin.
- the sulfonate resin is 0.1 to 100 mol% of a polymerizable fluorine-containing sulfonic acid onium salt having a structure represented by the general formula (2).
- % Preferably 2 to 100 mol%, and more preferably the remainder is a secondary repeating unit in each composition ratio. If it is 0.1 mol% or less, when a resist composition is prepared using this as an acid generator, it is necessary to use a large amount in order to develop sufficient photosensitivity to high energy rays, such being undesirable.
- the sulfonate resin is a sulfonate resin consisting only of a repeating unit having an acid labile group or a crosslinking site and a repeating unit represented by the general formula (4)
- the sulfonate resin is represented by the general formula (4).
- the repeating unit is 0.1 to 90 mol%, preferably 0.5 to 50 mol%, more preferably 1 to 30 mol%, and the remainder in each composition ratio has an acid labile group or a crosslinking site. It is.
- the repeating unit represented by the general formula (4) is less than 0.1 mol%, the photoacid generator does not have sufficient photosensitivity, and a separate photoacid generator is used in combination.
- the sulfonate resin is a sulfonate resin containing a repeating unit having an acid labile group or a crosslinking site and a repeating unit represented by the general formula (4), 0.1 to 70 mol%, preferably 1 to 60 mol%, more preferably 10 to 50 mol%, and in each composition ratio, the remainder is a repeating unit having an acid labile group or a crosslinking site and the general formula (4) It is preferable that the composition is proportional to the composition ratio of the repeating unit represented by
- the repeating unit is less than 0.1 mol%, it is difficult to adjust the adhesion of the resist resin to the substrate and the etching resistance, and if it exceeds 70 mol%, the sulfonate resin of the present invention is not preferred. Is not preferable because it is difficult to sufficiently exert the function as an acid generator to be possessed or the function of a positive or negative resist.
- the sulfonate resin having both the photoacid generator function and the positive or negative resist function include a repeating unit represented by the general formula (4) / an acid labile group or a crosslinking site.
- the repeating unit having 1 to 60 mol% / 10 to 85 mol%, preferably 2 to 40 mol / 10 to 70 mol%, more preferably 4 to 30 mol% / 15 to 60 mol%, in each composition ratio Although the remainder is a secondary repeating unit, it is as above-mentioned that it is not restricted to this composition range.
- the molecular weight of the sulfonate resin of the present invention is 1,000 to 1,000,000, preferably 2,000 to 500,000 in terms of mass average molecular weight (MW) measured by gel permeation chromatography (GPC).
- MW mass average molecular weight
- GPC gel permeation chromatography
- the mass average molecular weight is 1,000 to 100,000, preferably 2,000 to 50,000.
- the generated acid may diffuse and move in the resist film during the heat treatment after pattern exposure, and may be diffused to the unexposed area, resulting in degraded resolution.
- the effect as a sulfonate resin is low, and if it exceeds 1,000,000, the solubility in a solvent is lowered, and it becomes difficult to obtain a smooth coating film of a resist.
- the dispersity (Mw / Mn) is preferably 1.01 to 5.00, more preferably 1.01 to 4.00, particularly preferably 1.01 to 3.00, and most preferably 1.10 to 2.50. preferable.
- the sulfonate resin of the present invention may be a homopolymer or a copolymer with other monomers.
- a monomer having an acid labile group is used as another monomer, a sulfonate resin having a function of changing the photo-solubility that can be used in a positive resist composition is obtained, and a monomer having a crosslinking site Can be used to obtain a sulfonate resin having a function of changing the photo-solubility that can be used for a negative resist composition.
- the monomer used for copolymerization is not limited to monomers having such acid labile groups and cross-linked sites, and the sulfonate resin is suitable for dry etching resistance and standard developer suitability.
- Various secondary monomers can be copolymerized for the purpose of adjusting the substrate adhesion, the resist profile, and the general required properties of the resist, such as resolution, heat resistance, and sensitivity.
- the sulfonate resin having a repeating unit having a positive or negative photosensitive solubility-changing function is a polymerization represented by the general formula (2) of a monomer having a positive or negative photosensitive solubility-changing function. It can be obtained by copolymerizing with a fluorinated sulfonic acid onium salt.
- the sulfonate resin using the photosensitive solubility changing function as a positive resist is a resin having a leaving group such as a carboxyl group or a hydroxyl group protected by an acid labile group in the side chain, and the main chain is a vinyl group.
- a repeating unit formed by cleavage of a polymerizable double bond such as 1-methylvinyl group, 1-fluorovinyl group, 1-trifluoromethylvinyl group, 1-cyanovinyl group, norbornenyl group, etc. And the elimination site are bonded via a linking group W.
- the acid labile group is a group that is released by the action of an acid generated from a photoacid generator or the like to become an acid, and causes a function of increasing the dissolution rate of the resin containing the acid labile group in an alkaline developer.
- Partial structures containing acid labile groups having such functions such as ester structures (— (C ⁇ O) OR ′, alkoxycarbonyl groups), ether structures (—O—R ′, alkoxy groups, R ′) Represents a qualitative group) is sometimes referred to as an acid-decomposable group or a leaving site.
- the sulfonate resin using the photosensitive solubility changing function as a negative resist is a resin having a crosslinking site such as a hydroxyl group or a carboxyl group in the side chain, and the main chain is a vinyl group, 1-methylvinyl group, It is composed of repeating units formed by cleavage of a polymerizable double bond such as 1-fluorovinyl group, 1-trifluoromethylvinyl group, 1-cyanovinyl group, norbornenyl group, etc. Are connected through.
- This hydroxyl group is an alcoholic hydroxyl group.
- the alcoholic hydroxyl group is an almost neutral hydroxyl group, and usually has an ester bond, an ether bond, a ureido bond, etc. with a cross-linking agent described later, regardless of the solubility characteristics of the resin in an alkaline solution. It refers to a hydroxyl group having a function of making an alkali-soluble resin component insoluble in an alkaline solution by crosslinking by a reaction involving a hydroxyl group.
- the linking group W ′ will be described.
- the linking group W ′ linking the elimination site in the positive type or the crosslinking site in the negative type and the main chain is a single bond, — (CR 21 R 22 ) n— (n represents an integer of 1 to 10), —O. —, —C ( ⁇ O) —, —C ( ⁇ O) O— or —O—C ( ⁇ O) —, a divalent alicyclic hydrocarbon group, a divalent aromatic hydrocarbon group, a thioether group. , An ester group, an amide group, a sulfonamide group, a urethane group, or a urea group, or a divalent linking group consisting of a single group or a combination thereof.
- B is a cyclic group composed of a divalent alicyclic hydrocarbon group or a divalent aromatic hydrocarbon group, and further includes an aryl group or alicyclic hydrocarbon group described later for R 21 and R 22.
- 1 represents a group from which one hydrogen atom has been removed, l, m, and n represent an integer of 0 to 10, m is preferably 0, and n is preferably 0 or 1.
- monovalent organic groups represented by R 21 and R 22 of each substituted methylene group are not particularly limited, but include a hydrogen atom, a hydroxyl group, or an alkyl group, an alicyclic hydrocarbon group, and a substituted alkyl group.
- R 21 and R 22 may be the same or different from each other. When a plurality of R 21 or R 22 are contained, they may be the same or different.
- R 21 and R 22 may be combined to form a ring, and this ring is preferably an alicyclic hydrocarbon group.
- the alkyl group has 1 to 30 carbon atoms, preferably 1 to 12 carbon atoms.
- one or more of hydrogen atoms of the alkyl group is an alkoxy group having 1 to 4 carbon atoms, halogen atom, acyl group, acyloxy group, cyano group, hydroxyl group, carboxy group, alkoxycarbonyl
- a fluoroalkyl group substituted with a fluorine atom is preferred, and specific examples include a trifluoromethyl group, a pentafluoroethyl group, 2,2,2-trifluoroethyl, and the like.
- lower fluoroalkyl groups such as n-heptafluoropropyl group, 2,2,3,3,3-pentafluoropropyl group, 3,3,3-trifluoropropyl group and hexafluoroisopropyl group.
- alkoxy group examples include those having 1 to 4 carbon atoms such as a methoxy group, an ethoxy group, a propoxy group, and a butoxy group.
- the aryl group has 1 to 30 carbon atoms.
- the monocyclic group those having 3 to 12 ring carbon atoms are preferable, and those having 3 to 6 ring carbon atoms are more preferable.
- Examples of the condensed polycyclic aromatic group having 1 to 30 carbon atoms include pentalene, indene, naphthalene, azulene, heptalene, biphenylene, indacene, acenaphthylene, fluorene, phenalene, phenanthrene, anthracene, fluoranthene, acephenanthrylene, and acanthrylene.
- Organic groups in which one or more of these hydrogen atoms are substituted with a fluorine atom, an alkyl group having 1 to 4 carbon atoms or a fluorine-containing alkyl group are preferred. It can be mentioned as.
- Examples of the monocyclic or polycyclic heterocyclic group having 3 to 25 ring atoms include pyridyl group, furyl group, thienyl group, pyranyl group, pyrrolyl group, thiantenyl group, pyrazolyl group, isothiazolyl group, isoxazolyl group, Pyrazinyl group, pyrimidinyl group, pyridazinyl group, tetrahydropyranyl group, tetrahydrofuranyl group, tetrahydrothiopyranyl group, tetrahydrothiofuranyl group, 3-tetrahydrothiophene-1,1-dioxide group, etc.
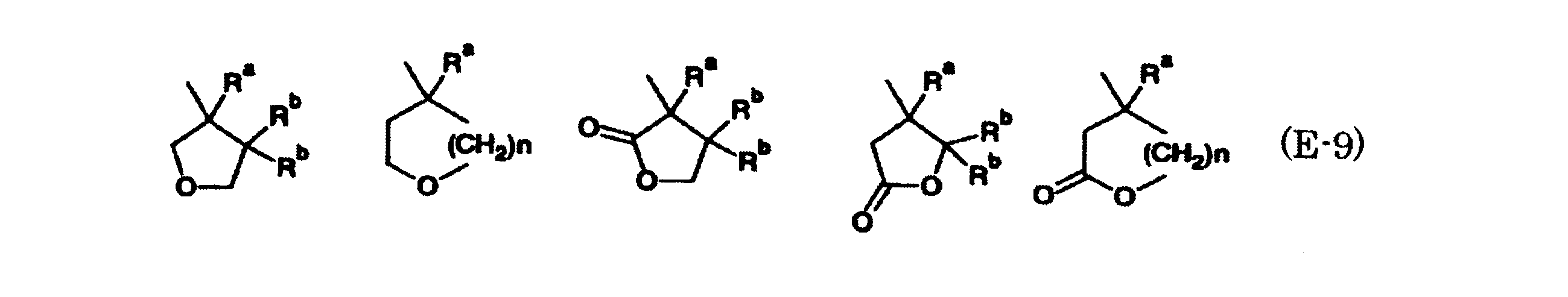
- R a and R b each independently represents a hydrogen atom or an alkyl group having 1 to 4 carbon atoms.
- n represents an integer of 2 to 4.
- the alicyclic hydrocarbon group in R 21 and R 22 constituting the linking group W ′ or the alicyclic hydrocarbon group formed including the carbon atom to which they are bonded may be monocyclic or polycyclic. . Specific examples include groups having a monocyclo, bicyclo, tricyclo, tetracyclo structure or the like having 3 or more carbon atoms. The number of carbon atoms is preferably 3 to 30, and particularly preferably 3 to 25 carbon atoms. These alicyclic hydrocarbon groups may have a substituent.
- the monocyclic group those having 3 to 12 ring carbon atoms are preferable, and those having 3 to 7 ring carbon atoms are more preferable.
- preferred are cyclopropyl group, cyclobutyl group, cyclopentyl group, cyclohexyl group, cycloheptyl group, cyclooctyl group, cyclodecanyl group, cyclododecanyl group and 4-tert-butylcyclohexyl group.
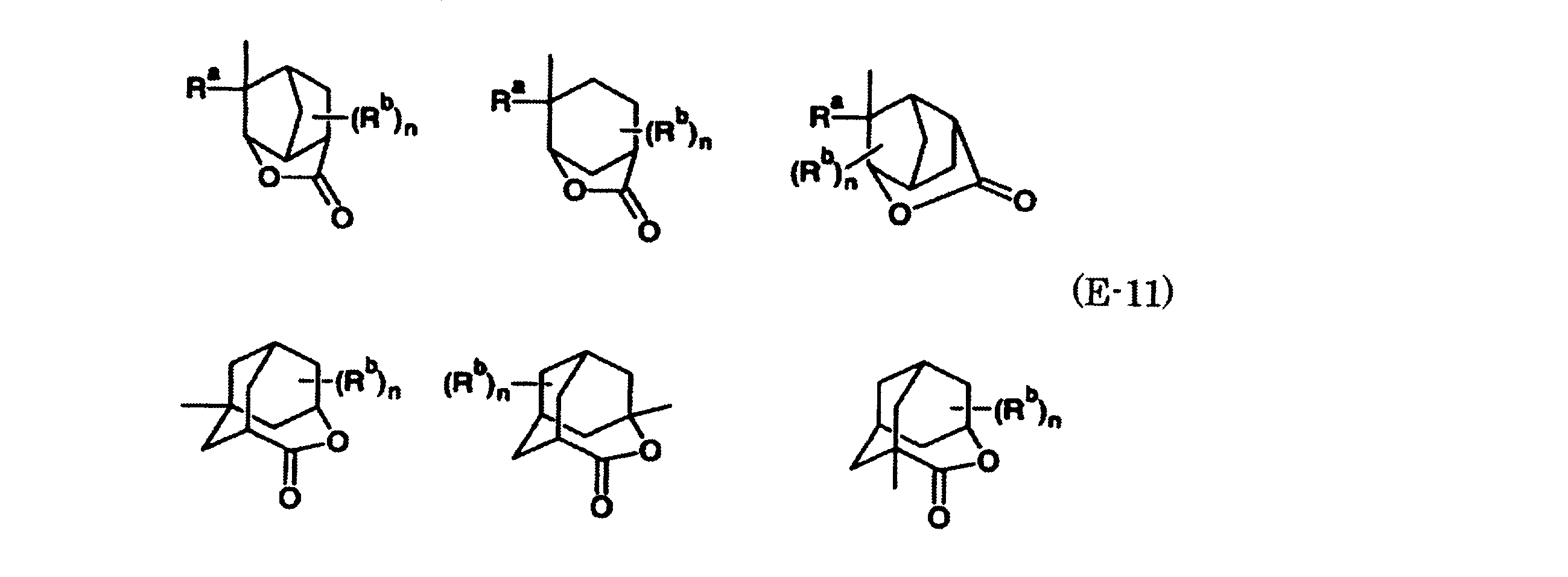
- polycyclic group examples include adamantyl group having 7 to 15 ring carbon atoms, noradamantyl group, decalin residue, tricyclodecanyl group, tetracyclododecanyl group, norbornyl group, cedrol group and the like.
- the alicyclic hydrocarbon group may be a spiro ring, and preferably a spiro ring having 3 to 6 carbon atoms.
- An adamantyl group, a decalin residue, a norbornyl group, a cedrol group, a cyclohexyl group, a cycloheptyl group, a cyclooctyl group, a cyclodecanyl group, a cyclododecanyl group, a tricyclodecanyl group and the like are preferable.
- One or more of the ring carbons of these organic groups or the hydrogen atoms of the linking group are each independently the above alkyl group or substituted alkyl group having 1 to 25 carbon atoms, hydroxyl group, alkoxy group, carboxyl group, alkoxycarbonyl. And groups in which one or more hydrogen atoms thereof are substituted with a fluorine atom or a trifluoromethyl group.
- a lower alkyl group is preferable, and an alkyl group selected from the group consisting of a methyl group, an ethyl group, a propyl group, and an isopropyl group is more preferable.
- substituent of the substituted alkyl group include a hydroxyl group, a halogen atom, and an alkoxy group.
- alkoxy group include those having 1 to 4 carbon atoms such as a methoxy group, an ethoxy group, a propoxy group, and a butoxy group.
- the alkoxycarbonyl group include a methoxycarbonyl group, an ethoxycarbonyl group, and an isopropoxycarbonyl group.
- the linking group W ′ is -(Single bond) -CH 2- —CH 2 —CH 2 — —CH 2 —B—
- B represents a cyclic group composed of a divalent alicyclic hydrocarbon group or a divalent aromatic hydrocarbon group
- R 21 and R 22 are each independently a hydrogen atom, a fluorine atom, an alkyl group, a substituted alkyl group, or an alicyclic hydrocarbon group. These may have one or more hydrogen atoms substituted with fluorine atoms. Of these, —C ( ⁇ O) —O—, —C ( ⁇ O) —O—CH 2 —, —C 6 H 4 — and —C ( ⁇ O) —O— (CR 21 R 22 ) 2 Among them, more preferred are those in which R 21 and R 22 are each independently a hydrogen atom, a fluorine atom, an alkyl group or a fluorine-containing alkyl group.
- the repeating unit represented by the following general formula (11-1) can be specifically exemplified by assuming that the acid labile group is R 17 and the main chain is — (CH 2 —C (R 8 )) —.
- R 8 has the same meaning as R 8 in the general formula (6) to be described later.
- R 18 represents a hydrogen atom, a fluorine atom or a fluorine-containing alkyl group.
- R 17-1 is an acid labile group, and an acid labile group represented by any one of the following general formulas (d) to (h) is preferable.
- J is a divalent linking group, and —J—CF (R 18 ) — corresponds to the linking group W ′, and the description of W ′ is applicable.
- the acid labile group in the sulfonate resin having the function of changing the photo-solubility of the present invention is an acid labile group represented by any one of the following general formulas (d) to (h).
- R X1 represents an alkyl group, an alicyclic hydrocarbon group or an aryl group.
- R X2 represents a hydrogen atom, an alkyl group, an alicyclic hydrocarbon group, an alkenyl group, an aralkyl group, an alkoxy group or an aryl group.
- R X3 , R X4 and R X5 may be the same or different and each represents an alkyl group, an alicyclic hydrocarbon group, an alkenyl group, an aralkyl group or an aryl group. Two groups out of R X3 to R X5 may be bonded to form a ring.
- the alkyl group is preferably an alkyl group having 1 to 4 carbon atoms such as methyl group, ethyl group, propyl group, isopropyl group, n-butyl group, sec-butyl group and tert-butyl group.
- the hydrocarbon group include those having 3 to 30 carbon atoms, specifically, cyclopropyl group, cyclopentyl group, cyclohexyl group, adamantyl group, norbornyl group, bornyl group, tricyclodecanyl group, dicyclohexane.
- Pentenyl group nobornane epoxy group, menthyl group, isomenthyl group, neomenthyl group, tetracyclododecanyl group, and those having 3 to 30 carbon atoms such as steroid residues are preferable.
- alkenyl group vinyl group, propenyl group, Preferred are those having 2 to 4 carbon atoms such as allyl group and butenyl group.
- the aryl group phenyl group, xylyl group, toluyl group are preferable.
- Cumenyl group, naphthyl group preferably having from 6 to 14 carbon atoms, such as anthracenyl group, which may have a substituent.
- the aralkyl group include those having 7 to 20 carbon atoms, which may have a substituent. Examples include a benzyl group, a phenethyl group, and a cumyl group.
- examples of the substituent further possessed by the organic group include a hydroxyl group, a halogen atom (fluorine, chlorine, bromine, iodine), a nitro group, a cyano group, the alkyl group or alicyclic hydrocarbon group, a methoxy group, Ethoxy group, hydroxyethoxy group, propoxy group, hydroxypropoxy group, n-butoxy group, isobutoxy group, sec-butoxy group, alkoxy group such as tert-butoxy group, alkoxycarbonyl group such as methoxycarbonyl group, ethoxycarbonyl group, benzyl Group, phenethyl group, aralkyl group such as cumyl group, aralkyloxy group, formyl group, acetyl group, butyryl group, benzoyl group, cyanyl group, acyl group such as valeryl group, acyloxy group such as butyryloxy group, the alkenyl group,
- R a represents an alkyl group having 1 to 4 carbon atoms or a perfluoroalkyl group.
- Each R b independently represents a hydrogen atom, an alkyl or perfluoroalkyl group having 1 to 4 carbon atoms, a hydroxy group, a carboxylic acid group, an alkyloxycarbonyl group, an alkoxy group, or the like.
- n represents an integer of 1 to 4.
- (d), (e), and (f) function as a chemical amplification type, they are used as a resist composition applied to a pattern forming method that is exposed with a laser beam or a high energy beam of an electron beam. Particularly preferred.
- alkoxycarbonyl group represented by the general formula (d) R X1 —O—C ( ⁇ O) — examples include a tert-butoxycarbonyl group, a tert-amyloxycarbonyl group, a methoxycarbonyl group, an ethoxycarbonyl group, i -Propoxycarbonyl group, cyclohexyloxycarbonyl group, isobornyloxycarbonyl group, adamantaneoxycarbonyl group and the like can be exemplified.
- Examples of the acetal group represented by the general formula (e) R X1 —O—CHR X2 — include a methoxymethyl group, an ethoxymethyl group, a 1-ethoxyethyl group, a 1-butoxyethyl group, and a 1-isobutoxyethyl group.
- the acetal group obtained by adding vinyl ethers with respect to a hydroxyl group can be mentioned.
- Examples of the tertiary hydrocarbon group represented by the general formula (f) CR X3 R X4 R X5 — include tert-butyl, tert-amyl, 1,1-dimethylpropyl, 1-ethyl-1- Methylpropyl group, 1,1-dimethylbutyl group, 1-ethyl-1-methylbutyl group, 1,1-diethylpropyl group, 1,1-dimethyl-1-phenylmethyl group, 1-methyl-1-ethyl-1 -Phenylmethyl group, 1,1-diethyl-1-phenylmethyl group, 1-methylcyclohexyl group, 1-ethylcyclohexyl group, 1-methylcyclopentyl group, 1-ethylcyclopentyl group, 1-isobornyl group, 1-methyladamantyl Group, 1-ethyladamantyl group, 1-isopropyladamantyl group, 1-isopropylnorborny
- alicyclic hydrocarbon group or the acid labile group containing the alicyclic hydrocarbon group are shown in Formula (E-12) and Formula (E-13).
- the methyl group (CH 3 ) may independently be an ethyl group.
- one or more of the ring carbons may have a substituent.
- Examples of the silyl group represented by the general formula (g) SiR X3 R X4 R X5 — include trimethylsilyl group, ethyldimethylsilyl group, methyldiethylsilyl group, triethylsilyl group, i-propyldimethylsilyl group, methyldi -I-propylsilyl group, tri-i-propylsilyl group, tert-butyldimethylsilyl group, methyldi-tert-butylsilyl group, tri-tert-butylsilyl group, phenyldimethylsilyl group, methyldiphenylsilyl group, triphenylsilyl group Etc.
- acyl group represented by the general formula (h) R X1 —C ( ⁇ O) — examples include acetyl group, propionyl group, butyryl group, heptanoyl group, hexanoyl group, valeryl group, pivaloyl group, isovaleryl group, laurylyl.
- acid labile groups containing a lactone group as a substituent are exemplified by the following formulas (E-14), (E-15) and (E-16).
- the methyl group (CH 3 ) may independently be an ethyl group.
- examples of the acid labile group include tertiary alkyl groups such as tert-butyl group and tert-amyl group, 1-ethoxyethyl group, 1-butoxyethyl group, Alkoxyethyl groups such as 1-isobutoxyethyl group and 1-cyclohexyloxyethyl group, alkoxymethyl groups such as methoxymethyl group and ethoxymethyl group, and alicyclic hydrocarbon groups such as adamantyl group and isobornyl group described above Alternatively, an acid labile group containing an alicyclic hydrocarbon group, an acid labile group containing a lactone group, and the like can be mentioned as preferable examples.
- the sulfonate resin of the present invention can use a secondary monomer as a copolymerization component, and the secondary monomer can use one or more monomers selected from the group consisting of monomers described below. Repeating units can be introduced into the sulfonate resin of the present invention.
- Other copolymer components are not particularly limited, but olefins, fluorine-containing olefins, acrylic esters, methacrylic esters, fluorine-containing acrylic esters, fluorine-containing methacrylate esters, norbornene compounds, fluorine-containing norbornene compounds, and styrene compounds.
- Fluorine-containing styrene compounds vinyl ethers, fluorine-containing vinyl ethers, and the like.
- acrylic ester, methacrylic ester, fluorine-containing acrylic ester, fluorine-containing methacrylate ester, norbornene compound, fluorine-containing norbornene compound, styrene-based compound, vinyl ether, and fluorine-containing vinyl ether are preferable.
- Examples of the olefin include ethylene and propylene, and examples of the fluoroolefin include vinyl fluoride, vinylidene fluoride, trifluoroethylene, chlorotrifluoroethylene, tetrafluoroethylene, hexafluoropropylene, and hexafluoroisobutene.
- acrylic ester or methacrylic ester it can be used without particular limitation for the ester side chain.
- a known compound is exemplified, methyl acrylate or methacrylate, ethyl acrylate or methacrylate, n-propyl acrylate or methacrylate, Isopropyl acrylate or methacrylate, n-butyl acrylate or methacrylate, isobutyl acrylate or methacrylate, n-hexyl acrylate or methacrylate, n-octyl acrylate or methacrylate, 2-ethylhexyl acrylate or methacrylate, lauryl acrylate or methacrylate, 2-hydroxyethyl acrylate or methacrylate 2-hydroxypropyl acrylate or methacrylate Alkyl ester of acrylic acid or methacrylic acid such as ethylene glycol, propylene glycol, acrylate or methacrylate containing
- unsaturated amides such as acrylamide, methacrylamide, N-methylol acrylamide, N-methylol methacrylamide and diacetone acrylamide, and acryloyl group-containing compounds such as acrylonitrile and methacrylonitrile can also be used.
- maleic acid, fumaric acid, maleic anhydride and the like can also be used.
- the fluorinated acrylate ester and the fluorinated methacrylate ester are an acrylate ester or a methacrylic ester having a fluorine atom-containing group at the ⁇ -position or the ester site of the acryloyl group.
- a monomer having a fluorine-containing alkyl group introduced at the ⁇ -position in the above-mentioned non-fluorinated acrylic acid ester or methacrylic acid ester, a trifluoromethyl group, a trifluoroethyl group, a nonafluoro-n at the ⁇ -position
- a monomer substituted with a butyl group or the like is preferably used.
- the fluorine-containing group is a perfluoroalkyl group or a fluoroalkyl group
- the ring carbon is a fluorine atom or a trifluoromethyl group.
- a fluorine-containing cyclic group such as a fluorine-containing benzene ring, a fluorine-containing cyclopentane ring, a fluorine-containing cyclohexane ring, or a fluorine-containing cycloheptane ring.
- fluorine-containing allylic acid ester or fluorine-containing methacrylate unit are 2,2,2-trifluoroethyl acrylate, 2,2,3,3-tetrafluoropropyl.
- Acrylate 1,1,1,3,3,3-hexafluoroisopropyl acrylate, heptafluoroisopropyl acrylate, 1,1-dihydroheptafluoro-n-butyl acrylate, 1,1,5-trihydrooctafluoro-n- Pentyl acrylate, 1,1,2,2-tetrahydrotridecafluoro-n-octyl acrylate, 1,1,2,2-tetrahydroheptadecafluoro-n-decyl acrylate, 2,2,2-trifluoroethyl methacrylate, 2,2,3,3-tetrafluoropropylmeta Relate, 1,1,1,3,3,3-hexafluoroisopropyl
- an acrylic ester or a fluorine-containing acrylic ester having a cyano group introduced at the ⁇ -position can also be used.
- the norbornene compound and the fluorine-containing norbornene compound are norbornene monomers having a mononuclear structure or a plurality of nuclear structures, and these can be used without any particular limitation.
- a norbornene compound obtained by a Diels Alder addition reaction using a saturated compound and cyclopentadiene or cyclohexadiene can be preferably used.
- styrene compounds fluorine-containing styrene compounds, vinyl ethers, fluorine-containing vinyl ethers, allyl ethers, vinyl esters, vinyl silanes, and the like can also be used.
- styrene compounds and fluorine-containing styrene compounds include styrene, fluorinated styrene, hydroxystyrene, styrene compounds in which hexafluoroacetone is added to the benzene ring, and hydrogen atoms in the benzene ring are replaced by trifluoromethyl groups.
- Styrene or hydroxystyrene and the above styrene compound or fluorine-containing styrene compound in which a halogen atom, an alkyl group, or a fluorine-containing alkyl group is bonded to the ⁇ -position can be used.
- vinyl ether, fluorine-containing vinyl ether and the like can also be used.
- it may have an alkyl group that may contain a hydroxy group such as a methyl group, an ethyl group, a hydroxyethyl group, or a hydroxybutyl group. It is an alkyl vinyl ether, and some or all of the hydrogen atoms may be substituted with fluorine.
- cyclic vinyl ethers having an oxygen atom or a carbonyl bond in the cyclic structure and monomers in which some or all of the hydrogen atoms of the cyclic vinyl ether are substituted with fluorine atoms, such as cyclohexyl vinyl ether, can also be used.
- Allyl ether, vinyl ester, and vinyl silane can be used without particular limitation as long as they are known compounds.
- R 8 represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 3 carbon atoms or a fluorine-containing alkyl group.
- R 9 is a substituted or unsubstituted aliphatic hydrocarbon group, a substituted or unsubstituted aromatic group, or an organic group in which a plurality of them are linked, and an arbitrary number of hydrogen atoms are substituted with fluorine atoms. May be.
- R 10 is a hydrogen atom, a substituted or unsubstituted aliphatic hydrocarbon group having 1 to 25 carbon atoms, or a substituted or unsubstituted aromatic hydrocarbon group having 1 to 25 carbon atoms, wherein any number of hydrogen atoms is It may be substituted with a fluorine atom and may contain an ether bond or a carbonyl group.
- S represents an integer of 1 to 2.
- R 8 in the general formula (6) is fluorine, chlorine, bromine or the like as a halogen atom, methyl group, ethyl group, propyl group, isopropyl group or the like as an alkyl group having 1 to 3 carbon atoms, or 1 to 3 carbon atoms.
- fluorine-containing alkyl group include those in which part or all of the hydrogen atoms of the alkyl group are substituted with fluorine atoms.
- the fluorine-containing alkyl group includes —CF 3 trifluoromethyl group, —CH 2 CF 3 trifluoroethyl group, 1,1,1,3,3,3-hexafluoroisopropyl group, heptafluoroisopropyl group, etc.
- a hydrogen atom, a fluorine atom, a methyl group, and a trifluoromethyl group are particularly preferable.
- R 9 in the general formula (6) is a substituted or unsubstituted aliphatic hydrocarbon group, a substituted or unsubstituted divalent aromatic group, or an organic group in which a plurality of them are linked, Any number of hydrogen atoms may be substituted with fluorine atoms.
- the unsubstituted aliphatic hydrocarbon group may be linear, branched or cyclic.
- Examples of the divalent aliphatic hydrocarbon group include a linear or branched alkylene group such as methylene, ethylene, isopropylene, and t-butylene, cyclobutylene, cyclohexylene, a divalent norbornane group, and a divalent adamantane.
- a cyclic alkylene group such as a group, and as an unsubstituted aromatic group, for example, a trivalent group such as a divalent aromatic group such as a phenylene group or a naphthylene group, A group in which one hydrogen atom is eliminated can be mentioned.
- These unsubstituted groups can be aliphatic hydrocarbon groups or aromatic groups in which any hydrogen atom contained therein is substituted with any substituent.
- particularly preferred structures include repeating units represented by the following general formulas (7) to (9).
- R 8 has the same meaning as R 8 in the general formula (6). Any one of R 11 , R 12 and R 13 is a CF 3 C (CF 3 ) (OH) CH 2 — group, and the remaining two are hydrogen atoms.
- R 8 has the same meaning as R 8 in the general formula (6).
- R 14 is a hydrogen atom, an alkyl group having 1 to 4 carbon atoms, or a fluorine-containing alkyl group.
- alkyl group having 1 to 4 carbon atoms or the fluorine-containing alkyl group examples include a methyl group, an ethyl group, an n-propyl group, an isopropyl group, an n-butyl group, a sec-butyl group, a tert-butyl group, Examples thereof include a fluoromethyl group, a difluoromethyl group, a trifluoromethyl group, and a perfluoroethyl group.
- R 8 has the same meaning as R 8 in the general formula (6).
- R 15 represents a methyl group or a trifluoromethyl group
- R 16 represents a hydrogen atom, a substituted or unsubstituted aliphatic hydrocarbon group having 1 to 25 carbon atoms, or a substituted or unsubstituted aromatic carbon group having 1 to 25 carbon atoms.
- u represents an arbitrary integer of 0 to 2
- t represents an arbitrary integer of 1 to 8, and satisfies v ⁇ t + 2.
- R 15 ⁇ R 16 is plural, respectively, it may be different in each of R 15 ⁇ R 16 same.
- Examples of the substituted or unsubstituted aliphatic hydrocarbon group having 1 to 25 carbon atoms or the substituted or unsubstituted aromatic hydrocarbon group having 1 to 25 carbon atoms that can be used for R 16 in the general formula (9) include a methyl group, Ethyl, propyl, isopropyl, cyclopropyl, n-propyl, sec-butyl, tert-butyl, n-pentyl, cyclopentyl, sec-pentyl, neopentyl, hexyl, cyclohexyl Group, ethylhexyl group, norbornel group, adamantyl group, vinyl group, allyl group, butenyl group, pentenyl group, ethynyl group, phenyl group, benzyl group, 4-methoxybenzyl group and the like.
- Some or all of them may be substituted with fluorine atoms.
- those containing an oxygen atom include an alkoxycarbonyl group, an acetal group, and an acyl group.
- the alkoxycarbonyl group include a tert-butoxycarbonyl group, a tert-amyloxycarbonyl group, a methoxycarbonyl group, an ethoxycarbonyl group, Examples thereof include i-propoxycarbonyl group.
- methoxymethyl group methoxyethoxymethyl group, ethoxyethyl group, butoxyethyl group, cyclohexyloxyethyl group, benzyloxyethyl group, phenethyloxyethyl group, ethoxypropyl group, benzyloxypropyl group, phenethyloxypropyl group
- cyclic ethers such as chain ether of ethoxybutyl group and ethoxyisobutyl group, tetrahydrofuranyl group and tetrahydropyranyl group.
- acyl group acetyl group, propionyl group, butyryl group, heptanoyl group, hexanoyl group, valeryl group, pivaloyl group, isovaleryl group, lauryl group, myristoyl group, palmitoyl group, stearoyl group, oxalyl group, malonyl group, succinyl group, Glutaryl group, adipoyl group, piperoyl group, suberoyl group, azelaoil group, sebacoyl group, acryloyl group, propioroyl group, methacryloyl group, crotonoyl group, oleoyl group, maleoyl group, fumaroyl group, mesaconoyl group, canholoyl group, benzoyl group, phthaloyl group Group, isophthaloyl group, terephthaloyl group, naphthoyl group, toluo
- repeating unit represented by the following general formula (10) is also suitably used as a combination partner of the repeating unit represented by the general formula (4).
- Y represents —CH 2 —, —O—, or —S—.
- w represents an integer of 2 to 6.
- R 8 has the same meaning as R 8 in the general formula (6).
- R 18 represents a hydrogen atom, a fluorine atom or a fluorine-containing alkyl group.
- R 17 corresponds to the description of R 16 in the general formula (9).
- J is a divalent linking group, and —J—CF (R 18 ) — corresponds to the linking group W ′, and the description of W ′ is applicable.
- R 18 is a hydrogen atom, a fluorine atom or a fluorine-containing alkyl group.
- a fluorine-containing alkyl group is not particularly limited, but has 1 to 12 carbon atoms, preferably 1 to 3 carbon atoms, trifluoromethyl group, pentafluoroethyl group, 2,2,2 -Trifluoroethyl group, n-heptafluoropropyl group, 2,2,3,3,3-pentafluoropropyl group, 3,3,3-trifluoropropyl group, hexafluoroisopropyl group and the like.
- R 18 is more preferably a fluorine atom or a trifluoromethyl group.
- R 8 has the same meaning as R 8 in the general formula (6).
- R 19 and R 20 each independently represent a hydrogen atom, a substituted or unsubstituted linear, branched or cyclic aliphatic hydrocarbon group having 1 to 25 carbon atoms, or a substituted or unsubstituted carbon group having 1 to 25 carbon atoms. It is an aromatic hydrocarbon group, and an arbitrary number of hydrogen atoms may be substituted with a fluorine atom, and may include an ether bond or a carbonyl group.
- the substituents exemplified as R 16 in the general formula (9) can be exemplified again.
- the polymerization method of the resin having a repeating unit represented by the general formula (4) according to the present invention is not particularly limited as long as it is a generally used method, but radical polymerization, ionic polymerization, etc. are preferable. Coordination anion polymerization, living anion polymerization, cationic polymerization, ring-opening metathesis polymerization, vinylene polymerization, vinyl addition, and the like can also be used. As each polymerization method, a known method can be applied.
- Radical polymerization is carried out in the presence of a radical polymerization initiator or a radical initiator by a known polymerization method such as bulk polymerization, solution polymerization, suspension polymerization or emulsion polymerization, and is either batch-wise, semi-continuous or continuous. This can be done by operation.
- a radical polymerization initiator or a radical initiator by a known polymerization method such as bulk polymerization, solution polymerization, suspension polymerization or emulsion polymerization, and is either batch-wise, semi-continuous or continuous. This can be done by operation.
- the radical polymerization initiator is not particularly limited, but examples include azo compounds, peroxide compounds, and redox compounds. Particularly, azobisisobutyronitrile, tert-butyl peroxypivalate, Di-tert-butyl peroxide, i-butyryl peroxide, lauroyl peroxide, succinic acid peroxide, dicinnamyl peroxide, di-n-propyl peroxydicarbonate, tert-butyl peroxyallyl monocarbonate, benzoyl peroxide, Hydrogen peroxide, ammonium persulfate and the like are preferable.
- the reaction vessel used for the polymerization reaction is not particularly limited.
- a polymerization solvent may be used.
- the polymerization solvent those which do not inhibit radical polymerization are preferable, and typical ones are ester systems such as ethyl acetate and n-butyl acetate, ketone systems such as acetone and methyl isobutyl ketone, and hydrocarbons such as toluene and cyclohexane.
- alcohol solvents such as methanol, isopropyl alcohol, and ethylene glycol monomethyl ether. It is also possible to use a solvent such as water, ether, cyclic ether, chlorofluorocarbon, and aromatic.
- the reaction temperature of the copolymerization reaction is appropriately changed depending on the radical polymerization initiator or radical polymerization initiator, and is usually preferably 20 to 200 ° C, particularly preferably 30 to 140 ° C.
- resist composition The resist composition will be described.
- the resin having a repeating unit represented by the general formula (4) of the present invention is used as a resist composition comprising a solution to which other components are added.
- This sulfonate resin functions as a photoacid generator.
- a sulfonate resin having a repeating unit having an acid labile group or a crosslinking site is a resin having a repeating unit having an acid labile group or a crosslinking site. It can be used as a chemically amplified resist alone without adding (base resin).
- a resist composition is prepared containing a base resin as an essential component. Is done.
- various additives commonly used in resist compositions such as additional resins, quenchers, dissolution inhibitors, plasticizers, stabilizers, colorants, surfactants, thickeners, leveling agents.
- a negative resist composition such as an antifoaming agent, a compatibilizing agent, an adhesion agent, and an antioxidant
- additives such as a crosslinking agent and a basic compound can be further contained. These additives can be appropriately used as well as those described below.
- the base resin refers to a resin having an acid labile group or a crosslinking site and having a positive or negative resist function.
- the sulfonate resin having the function of changing the photo-solubility is also one form of the base resin.
- the base resin used in the positive resist composition is a resin having a leaving site such as a carboxyl group or a hydroxyl group protected with an acid labile group in the side chain, and the main chain is acrylic acid, methacrylic acid, ⁇ -trimethyl. It is composed of repeating units formed by cleavage of polymerizable double bonds such as fluoromethylacrylic acid, vinyl group, allyl group, norbornene group.
- the base resin used in the negative resist composition is a resin having a crosslinking site such as hydroxyl group or carboxyl group in the side chain, and the main chain is acrylic acid, methacrylic acid, ⁇ -trifluoromethylacrylic acid, vinyl group. , Allyl groups, norbornene groups, and the like, and a repeating unit formed by cleavage of a polymerizable double bond.
- the base resin is often a copolymer in order to adjust the resist properties, and various resins are known.
- the copolymer component, acid labile group, crosslinking site, and linking group (W or W ′) are described in this book. Each description in the specification can be applied as it is.
- a particularly preferred copolymer component is a monomer having a lactone ring, which is useful for enhancing the adhesion of the resist to the substrate.
- These base resins can contain a repeating unit represented by the general formula (4).
- This base resin also has a function as a photoacid generator possessed by the sulfonate resin, and a positive resist composition can be prepared only from a base resin having an acid labile group and a solvent.
- a negative resist composition can be prepared only from a base resin having a crosslinking site, a crosslinking agent, and a solvent.
- the molecular weight of the base resin is 1,000 to 1,000,000, preferably 2,000 to 500,000, as a weight average molecular weight measured by gel permeation chromatography (GPC). If the weight average molecular weight is less than 1,000, the strength of the coating film is insufficient, and if it exceeds 1,000,000, the solubility in a solvent is lowered, and it becomes difficult to obtain a smooth coating film, which is not preferable.
- the dispersity (Mw / Mn) is preferably 1.01 to 5.00, more preferably 1.01 to 4.00, particularly preferably 1.01 to 3.00, and most preferably 1.10 to 2.50. preferable.
- a negative resist composition it can be arbitrarily selected from known crosslinking agents used in chemically amplified negative resist compositions.
- amino group-containing compounds such as melamine, acetoguanamine, benzoguanamine, urea, ethylene urea, propylene urea, glycoluril are reacted with formaldehyde or formaldehyde and a lower alcohol, and the hydrogen atom of the amino group is converted into a hydroxymethyl group or Examples include compounds substituted with a lower alkoxymethyl group.
- melamine are melamine-based crosslinking agents
- those using urea are urea-based crosslinking agents
- those using alkylene ureas such as ethylene urea and propylene urea are alkylene urea-based crosslinking agents
- glycoluril is used. This was called a glycoluril-based crosslinking agent.
- the component (C) is preferably at least one selected from the group consisting of melamine-based crosslinking agents, urea-based crosslinking agents, alkylene urea-based crosslinking agents, and glycoluril-based crosslinking agents, and glycoluril-based crosslinking agents are particularly preferred. preferable.
- melamine-based crosslinking agent examples include hexamethoxymethyl melamine, hexaethoxymethyl melamine, hexapropoxymethyl melamine, hexabutoxybutyl melamine and the like, and among them, hexamethoxymethyl melamine is preferable.
- urea-based crosslinking agent examples include bismethoxymethylurea, bisethoxymethylurea, bispropoxymethylurea, bisbutoxymethylurea, etc. Among them, bismethoxymethylurea is preferable.
- alkylene urea crosslinking agent examples include mono and / or dihydroxymethylated ethylene urea, mono and / or dimethoxymethylated ethylene urea, mono and / or diethoxymethylated ethylene urea, mono and / or dipropoxymethylated ethylene Ethylene urea crosslinking agents such as urea, mono and / or dibutoxymethylated ethylene urea; mono and / or dihydroxymethylated propylene urea, mono and / or dimethoxymethylated propylene urea, mono and / or diethoxymethylated propylene urea Propylene urea-based crosslinking agents such as mono- and / or dipropoxymethylated propylene urea, mono and / or dibutoxymethylated propylene urea; 1,3-di (methoxymethyl) 4,5-dihydroxy-2-imidazolidinone 1,3-di (methoxymethyl) ) -4,5-like and dimethoxy-2
- glycoluril-based crosslinking agent examples include mono, di, tri and / or tetrahydroxymethylated glycoluril, mono, di, tri and / or tetramethoxymethylated glycoluril, mono, di, tri and / or tetraethoxymethyl.
- Glycoluril mono, di, tri and / or tetrapropoxymethylated glycoluril, mono, di, tri and / or tetrabutoxymethylated glycoluril.
- the crosslinking agent component one kind may be used alone, or two or more kinds may be used in combination.
- the content of the entire crosslinking agent component in the negative resist composition of the present invention is preferably 3 to 30 parts by mass, more preferably 3 to 25 parts by mass, and most preferably 5 to 20 parts by mass with respect to 100 parts by mass of the base resin. preferable.
- the content of the crosslinking agent component is at least the lower limit value, the crosslinking formation proceeds sufficiently and a good resist pattern can be obtained.
- it is below this upper limit the storage stability of the resist coating solution is good, and the deterioration of sensitivity with time is suppressed.
- a basic compound as an optional component to the resist composition of the present invention as a quencher or in order to improve the resist pattern shape, retention time stability, and the like.
- This basic compound component may be a known one, for example, primary, secondary, tertiary aliphatic amines, aromatic amines, heterocyclic amines, nitrogen-containing compounds having a hydroxyphenyl group, alcohols Nitrogenous compounds, amide derivatives and the like can be used, among which secondary aliphatic amines, tertiary aliphatic amines, aromatic amines and heterocyclic amines are preferred.
- Examples of the aliphatic amine include alkyl amines or alkyl alcohol amines in which at least one hydrogen atom of ammonia NH 3 is substituted with an alkyl group or hydroxyalkyl group having 12 or less carbon atoms.
- monoalkylamines such as n-hexylamine, n-heptylamine, n-octylamine, n-nonylamine, n-decylamine; diethylamine, di-n-propylamine, di-n-heptylamine, Dialkylamines such as di-n-octylamine and dicyclohexylamine; trimethylamine, triethylamine, tri-n-propylamine, tri-n-butylamine, tri-n-hexylamine, tri-n-pentylamine, tri-n-heptyl Trialkylamines such as amine, tri-n-octylamine, tri-n-nonylamine, tri-n-decanylamine, tri-n-dodecylamine; diethanolamine, triethanolamine, diisopropanolamine, triisopropanolamine, di-n -Ok Nor
- examples of other basic compounds include the following compounds.
- aromatic amines and heterocyclic amines include aniline, N-methylaniline, N-ethylaniline, N-propylaniline, N, N-dimethylaniline, 2-methylaniline, 3-methylaniline, 4-methyl.
- the basic compound component is usually used in the range of 0.01 to 5 parts by mass with respect to 100 parts by mass of the base resin.
- an organic carboxylic acid is further added as an optional component for the purpose of preventing sensitivity deterioration due to the blending of the basic compound component and improving the resist pattern shape, stability with time, etc.
- an oxo acid of phosphorus or a derivative thereof can be contained.
- these can also be used together with a basic compound component, and any one can also be used.
- organic carboxylic acid for example, malonic acid, citric acid, malic acid, succinic acid, benzoic acid, salicylic acid and the like are suitable.
- Phosphorus oxoacids or derivatives thereof include phosphoric acid, phosphoric acid di-n-butyl ester, phosphoric acid diphenyl ester and other phosphoric acid or derivatives thereof such as phosphonic acid, phosphonic acid dimethyl ester, phosphonic acid- Like phosphonic acids such as di-n-butyl ester, phenylphosphonic acid, phosphonic acid diphenyl ester, phosphonic acid dibenzyl ester and their esters, phosphinic acids such as phosphinic acid, phenylphosphinic acid and their esters Among these, phosphonic acid is particularly preferable.
- solvent As a method of forming the fluorine-containing polymer compound according to the present invention into a thin film, for example, a method of forming a film by dissolving in an organic solvent and applying and drying can be used.
- the organic solvent to be used is not particularly limited as long as the fluorine-containing polymer compound is soluble, but ketones such as acetone, methyl ethyl ketone, cyclohexanone, methyl isoamyl ketone, 2-heptanone, ethylene glycol, ethylene glycol monoacetate, diethylene glycol , Diethylene glycol monoacetate, propylene glycol, propylene glycol monoacetate, propylene glycol monomethyl ether, propylene glycol monomethyl ether acetate (PGMEA), dipropylene glycol, or monomethyl ether of dipropylene glycol monoacetate, monoethyl ether, monopropyl ether, mono Polyhydric alcohols such as butyl ether or monophenyl
- Fluorine solvents such as aromatic solvents, chlorofluorocarbons, alternative chlorofluorocarbons, perfluoro compounds, hexafluoroisopropyl alcohol, and terpene petroleum naphtha solvents and paraffin solvents that are high boiling point weak solvents for the purpose of improving coatability. Is possible. These may be used alone or in combination of two or more.
- the resist composition of the present invention is a surfactant, preferably a fluorine-based and / or silicon-based surfactant (a fluorine-containing surfactant and a silicon-based surfactant, a surfactant containing both fluorine atoms and silicon atoms). It is preferable to contain any one of 2) or 2 types or more.
- the resist composition of the present invention contains the surfactant, it is particularly effective when using an exposure light source of 250 nm or less, particularly 220 nm or less, and when the pattern line width is narrower, and has good sensitivity and resolution. Thus, it is possible to provide a resist pattern with less adhesion and development defects.
- a known photoacid generator can be used in combination with the sulfonate resin.
- the photoacid generator an arbitrary one can be selected from those used as the acid generator of the chemically amplified resist.
- acid generators include bissulfonyldiazomethanes, nitrobenzyl derivatives, onium salts, halogen-containing triazine compounds, cyano group-containing oxime sulfonate compounds, and other oxime sulfonate compounds.
- These photoacid generators may be used alone or in combination of two or more, and the content thereof is 100 parts by mass of the resist composition together with the sulfonate resin of the present invention.
- the sulfonate resin of the present invention is 1 to 100 parts by mass of the total mass of the photoacid generator of 100 parts by mass, preferably 10 to 100 parts by mass, more preferably 30 to 100 parts by mass. preferable.
- the additional resin is not particularly limited as long as it is a resin that dissolves in the solvent used and is compatible with the components constituting the other resist composition. Acts as a solubilizer and adhesive.
- a resist pattern forming method of a conventional photoresist technique can be used. That is, first, a resist composition solution is applied to a substrate such as a silicon wafer using a spinner or the like, and dried to form a photosensitive layer. Then, a high energy beam or an electron beam is applied to the substrate by using an exposure apparatus or the like. Irradiate and heat through mask pattern. Next, this is developed using a developer, for example, an alkaline aqueous solution such as an aqueous solution of 0.1 to 10% by mass of tetramethylammonium hydroxide. With this forming method, a pattern faithful to the mask pattern can be obtained.
- a developer for example, an alkaline aqueous solution such as an aqueous solution of 0.1 to 10% by mass of tetramethylammonium hydroxide.
- additives that are miscible with the resist composition as desired such as additional resins, quenchers, plasticizers, stabilizers, colorants, surfactants, thickeners, leveling agents, antifoaming agents, compatibilizing agents.
- additives such as an adhesive and an antioxidant can be contained.
- the high energy beam used in the present invention is not particularly limited, but particularly in the case of performing fine processing, near ultraviolet rays (wavelength 380 to 200 nm) such as F 2 excimer laser, ArF excimer laser, KrF excimer laser, or vacuum ultraviolet rays (far ultraviolet rays, VUV, wavelength 200 to 10 nm), extreme ultraviolet rays such as synchrotron radiation (EUV, wavelength 10 nm or less), soft X-rays, X-rays or ⁇ -rays and the like and electron beams are effective.
- near ultraviolet rays such as F 2 excimer laser, ArF excimer laser, KrF excimer laser, or vacuum ultraviolet rays (far ultraviolet rays, VUV, wavelength 200 to 10 nm), extreme ultraviolet rays such as synchrotron radiation (EUV, wavelength 10 nm or less), soft X-rays, X-rays or ⁇ -rays and the like and electron beams are effective.
- EUV synchrotron radiation
- the pattern forming method of the present invention it is effective to use an exposure apparatus provided with such a high-energy ray or electron beam source having a short wavelength of 300 nm or less.
- a high-energy ray or electron beam source having a short wavelength of 300 nm or less.
- vacuum ultraviolet rays having a wavelength of 10 to 14 nm (in the lithography field, sometimes referred to as EUV or soft X-rays).
- EUV or soft X-rays in part of the optical path
- an immersion exposure system that enables more efficient microfabrication at the numerical aperture and effective wavelength
- This resist composition is also suitable for use in such an apparatus.
- an exposure process uses an ArF excimer laser with a wavelength of 193 nm, and water or air is used between a substrate coated with a resist composition and a projection lens.
- Chloroform 35 g was added to a white solid 5.0 g (purity 62.2%; equivalent to 7.3 mmol) of triphenylsulfonium 2-hydroxy-1,1-difluoroethanesulfonate, and dissolved by stirring. Thereto was added 1.46 g (8.55 mmol) of ethyl trifluoromethyl pyruvate, and the mixture was reacted at room temperature for 3 hours. Next, the reaction solution was concentrated under reduced pressure, and then 26.5 g of acetonitrile was added and stirred to dissolve the reaction intermediate.
- Table 1 shows a comparison of the solubility of the polymerizable fluorine-containing sulfonic acid onium salt (polymerizable monomer) in propylene glycol monomethyl ether acetate (PGMEA).
- PAG-1, PAG-2, and PAG-3 are polymerizable fluorine-containing sulfonic acid onium salts according to the present invention.
- the filtered white powder was washed twice with 400 g of methanol in the form of a slurry and then filtered and dried at 50 ° C. for 17 hours to obtain a white powder polymer (74.1 g).
- This polymer has a weight average molecular weight (MW) of 7,700, and as a result of 13 C-NMR analysis, the repeating unit derived from the compound (PAG-1): the repeating unit derived from the compound (B-1): the compound (C It was a copolymer having a content ratio of the repeating unit derived from -1) of 14.4: 45.5: 40.1 (mol%).
- This copolymer was designated as resin (P-1).
- the filtered white powder was washed twice with 400 g of methanol in the form of a slurry and then filtered and dried at 50 ° C. for 17 hours to obtain a white powder polymer (67.0 g).
- This polymer has a MW of 8,200, and as a result of 13 C-NMR analysis, the repeating unit derived from compound (PAG-2): the repeating unit derived from compound (B-1): derived from compound (C-1) The content ratio of the repeating unit was 15.2: 44.3: 40.5 (mol%).
- This copolymer was designated as resin (P-2).
- a resist composition was prepared by blending each of the produced resins, solvents, other additives, and nonafluorobutanesulfonic acid triphenylsulfonium salt (PAG-C3), which is an existing photoacid generator (PAG).
- PAG-C3 nonafluorobutanesulfonic acid triphenylsulfonium salt
- each component in the prepared resist composition is shown in Table 4 and Table 5. Further, each resist composition was filtered through a 0.2 ⁇ m membrane filter to prepare a resist composition.
- solvents, basic compounds, and crosslinking agents used are as follows.
- S-1 Propylene glycol monomethyl ether acetate (PGMEA)
- S-2 ⁇ -butyrolactone
- S-3 Ethyl lactate
- S-4 Cyclohexanone (basic compound)
- O-1 N, N-dibutylaniline
- O-2 2,6-diisopropylaniline
- O-3 diazabicyclo [4.3.0] nonene
- O-4 2,4,5-triphenylimidazole
- O-5 Trioctylamine
- Cross-linking agent Nicalak MX-270 (glycoluril-based cross-linking agent, Sanwa Chemical Products)
- PAG Nonafluorobutanesulfonic acid triphenylsulfonium salt (PAG-C3)
- each resist composition was spin-coated on a silicon wafer to obtain a resist film having a thickness of 250 nanometers. After pre-baking at 110 ° C., exposure with 248 nm ultraviolet light was performed through a photomask, and then post-exposure baking was performed at 120 ° C. Then, it developed for 1 minute at 23 degreeC using 2.38 mass% tetramethylammonium hydroxide aqueous solution. A high resolution pattern shape was obtained from any of the resist compositions, and defects due to poor adhesion to the substrate, defective film formation, development defects, and poor etching resistance were not observed. Tables 4 and 5 show the compositions and evaluation results of the resist compositions.
- Examples 49 and 51 A resist composition was prepared in the same manner as in Example 1 using the resin P′-1 obtained in Reference Polymerization Example 1 as a base resin and the polymerizable fluorine-containing sulfonic acid onium salt according to the present invention as an acid generator. A pattern was formed in the same manner as other resist compositions, and the pattern shape was observed. A high resolution pattern shape was obtained from any of the resist compositions, and defects due to poor adhesion to the substrate, defective film formation, development defects, and poor etching resistance were not observed. Table 9 shows the composition and evaluation results of each resist composition.
- the resin according to the present invention can be used as a photoacid generator for photoresists and as a positive type or negative type resist resin. Moreover, the monomer for synthesizing these resins can be used as an acid generator and is also useful as a raw material for synthesizing other compounds.
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Organic Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Materials For Photolithography (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
下記一般式(3)で表される繰り返し単位を有するスルホン酸塩樹脂。
下記一般式(4)で表される繰り返し単位を有する発明1のスルホン酸塩樹脂。
さらにオレフィン、含フッ素オレフィン、アクリル酸エステル、メタクリル酸エステル、含フッ素アクリル酸エステル、含フッ素メタクリル酸エステル、ノルボルネン化合物、含フッ素ノルボルネン化合物、スチレン系化合物、含フッ素スチレン系化合物、ビニルエーテル、および含フッ素ビニルエーテルに含まれる重合性二重結合が開裂して形成された繰り返し単位からなる群より選ばれた一種以上の繰り返し単位を有する発明1~3のスルホン酸塩樹脂。
さらに下記一般式(6)で表される繰り返し単位を有する発明1~4のスルホン酸塩樹脂。
さらに下記一般式(7)で表される繰り返し単位を有する発明1~5のスルホン酸塩樹脂。
さらに下記一般式(8)で表される繰り返し単位を有する発明1~6のスルホン酸塩樹脂。
さらに下記一般式(9)で表される繰り返し単位を有する発明1~7のスルホン酸塩樹脂。
さらに下記の一般式(11)または一般式(11-1)で表される繰り返し単位を有する発明1~9のスルホン酸塩樹脂。
さらに下記一般式(12)で表される繰り返し単位を有する発明1~10記載のスルホン酸塩樹脂。
式中、-(CX2)-が、-(CH2)p-(CF2)q-で表され、pが0~10の整数かつqが0~8の整数である繰り返し単位を有する発明1~11のスルホン酸塩樹脂。
式中、-(CX2)-が、-(CH2)p-(CF2)q-で表され、pが0~4の整数かつqが0または1である繰り返し単位を有する発明1~11のスルホン酸塩樹脂。
発明1~13のスルホン酸塩樹脂と溶剤を少なくとも含むレジスト組成物。
スルホン酸塩樹脂が酸不安定性基を有するスルホン酸塩樹脂である発明14の化学増幅ポジ型レジスト組成物。
さらに酸不安定性基を有する樹脂を含む発明14または発明15の化学増幅ポジ型レジスト組成物。
スルホン酸塩樹脂がアルコール性ヒドロキシル基またはカルボキシル基を有するスルホン酸塩樹脂である発明14の化学増幅ネガ型レジスト組成物。
さらにアルコール性ヒドロキシル基またはカルボキシル基を有する樹脂を含む発明12または発明17の化学増幅ネガ型レジスト組成物。
発明14~18のレジスト組成物を基板上に塗布する工程と、加熱処理後フォトマスクを介して波長300nm以下の高エネルギー線で露光する工程と、必要に応じて加熱処理した後、現像液を用いて現像する工程とを含むことを特徴とするパターン形成方法。
露光する工程が、波長193nmのArFエキシマレーザーを用い、レジスト組成物を塗布した基板と投影レンズの間に水、もしくは空気の屈折率より高い屈折率を有する水以外の液体を挿入する液浸リソグラフィー法であることを特徴とする発明19のパターン形成方法。
露光する工程が、波長10~14nmの軟X線(EUV光)を用いることを特徴とする発明19のパターン形成方法。
下記一般式(1)で表されるアニオンを有する重合性含フッ素スルホン酸または重合性含フッ素スルホン酸塩。
下記一般式(2)で表される重合性含フッ素スルホン酸オニウム塩。
本発明の一般式(1)で表されるアニオン構造を有する重合性含フッ素スルホン酸塩として、下記一般式(2)で表される重合性含フッ素スルホン酸オニウム塩が好ましい例として挙げられる。この重合性含フッ素スルホン酸オニウム塩は、単量体のままで、また、それを単独重合もしくは共重合して得られた樹脂が、高エネルギー線に感応して非常に酸強度の大きい含フッ素スルホン酸を発生する能力を有することから、重合性含フッ素スルホン酸オニウム塩またはそれから得られた樹脂は光酸発生剤として機能することができる。のみならず、この重合性含フッ素スルホン酸オニウム塩は、酸不安定性基または架橋部位を有する単量体と共重合することができ、高エネルギー線用レジスト組成物のベース樹脂を製造するための単量体としても有用である。
一般式(a)におけるR3、R4およびR5としては具体的に以下のものが挙げられる。置換もしくは非置換の炭素数1~20のアルキル基としては、直鎖状、分岐状または環状のアルキル基であってよく、置換基を有してもよい。例えば、メチル基、エチル基、n-プロピル基、イソプロピル基、シクロプロピル基、n-ブチル基、sec-ブチル基、イソブチル基、tert-ブチル基、n-ペンチル基、シクロペンチル基、n-ヘキシル基、n-ヘプチル基、2-エチルヘキシル基、シクロヘキシル基、シクロヘプチル基、4-メチルシクロヘキシル基、シクロヘキシルメチル基、n-オクチル基、n-デシル基、1-アダマンチル基、2-アダマンチル基、ビシクロ[2.2.1]ヘプテン-2-イル基、1-アダマンタンメチル基、2-アダマンタンメチル基等が挙げられる。置換もしくは非置換の炭素数1~20のアルケニル基としては、直鎖状、分岐状または環状のアルケニル基であってよく、置換基を有してもよい。例えば、ビニル基、アリル基、プロペニル基、ブテニル基、ヘキセニル基、シクロヘキセニル基等が挙げられる。置換もしくは非置換の炭素数1~20のオキソアルキル基としては、直鎖状、分岐状または環状のオキソアルキル基であってよく、置換基を有してもよい。例えば、2-オキソシクロペンチル基、2-オキソシクロヘキシル基、2-オキソプロピル基、2-オキソエチル基、2-シクロペンチル-2-オキソエチル基、2-シクロヘキシル-2-オキソエチル基、2-(4-メチルシクロヘキシル)-2-オキソエチル基等を挙げることができる。置換もしくは非置換の炭素数6~18のアリール基としては、フェニル基、ナフチル基、チエニル基等やp-メトキシフェニル基、m-メトキシフェニル基、o-メトキシフェニル基、p-エトキシフェニル基、p-tert-ブトキシフェニル基、m-tert-ブトキシフェニル基等のアルコキシフェニル基、2-メチルフェニル基、3-メチルフェニル基、4-メチルフェニル基、エチルフェニル基等のアルキルフェニル基、メチルナフチル基、エチルナフチル基等のアルキルナフチル基、ジエチルナフチル基等のジアルキルナフチル基、ジメトキシナフチル基、ジエトキシナフチル基等のジアルコキシナフチル基等が挙げられる。置換もしくは非置換の炭素数6~18のアラルキル基としては、ベンジル基、1-フェニルエチル基、2-フェニルエチル基等が挙げられる。置換もしくは非置換の炭素数6~18のアリールオキソアルキル基としては、2-フェニル-2-オキソエチル基、2-(1-ナフチル)-2-オキソエチル基、2-(2-ナフチル)-2-オキソエチル基等の2-アリール-2-オキソエチル基等が挙げられる。また、R3、R4およびR5のうちのいずれか2つ以上が相互に結合して硫黄原子を介して環状構造を形成する場合には、二価の基として1,4-ブチレン、3-オキサ-1,5-ペンチレン等が挙げられる。さらには置換基としてアクリロイルオキシ基、メタクリロイルオキシ基等の重合可能な置換基を有するアリール基が挙げられ、具体的には4-(アクリロイルオキシ)フェニル基、4-(メタクリロイルオキシ)フェニル基、4-ビニルオキシフェニル基、4-ビニルフェニル基等が挙げられる。
R6ならびにR7の具体例は上述した一般式(a)におけるR3、R4及びR5と同じものを再び挙げることができる。
次いで上述した、一般式(1-1)で表される重合性含フッ素スルホン酸塩の製造方法について述べる。一般式(1-1)で表される重合性含フッ素スルホン酸塩は、一般式(2)で表される重合性含フッ素スルホン酸オニウム塩と同様に製造することができる。以下の説明においてQ+をM+と読み替えることができる。
第1工程について説明する。第1工程は、一般式(13)で表されるヒドロキシフルオロアルカンスルホン酸オニウム塩に一般式(14)で表されるトリフルオロメチルピルビン酸誘導体を付加させる工程である。この付加反応の方法としては、一般式(13)で表されるヒドロキシフルオロアルカンスルホン酸オニウム塩に一般式(14)で表されるトリフルオロメチルピルビン酸誘導体を、酸触媒存在下、あるいは無触媒条件下で反応させる方法が例示できる。
次いで第2工程について説明する。第2工程は、一般式(15)で表される含フッ素スルホン酸オニウム塩と一般式(16)で表されるカルボン酸誘導体とをエステル化反応させ、一般式(2)で表される重合性含フッ素スルホン酸オニウム塩を合成する工程である。具体的な方法としては、これまで公知となっているエステル化法のいずれも採用することができる。
下記一般式(3)で表される繰り返し単位を含む樹脂(本明細書において、「スルホン酸塩樹脂」ということがある。)は、一般式(1-1)で表される重合性含フッ素スルホン酸塩の重合性二重結合が開裂して形成される。重合反応においては、重合性二重結合以外の構造に変化は起こらず、元の構造が維持される。
-(CR21R22)m-C(=O)-O-(CR21R22)n-
-(CR21R22)m-C(=O)-O-(CR21R22)n-B-(CR21R22)l-
-(CR21R22)m-O-(CR21R22)n-
-(CR21R22)m-O-(CR21R22)n-B-(CR21R22)l-
-(CR21R22)n-B-(CR21R22)l-C(=O)-O-(CR21R22)m-
-(CR21R22)n-B-(CR21R22)l-O-(CR21R22)m-などが挙げられる。ここで、Bは二価の脂環式炭化水素基または二価の芳香族炭化水素基からなる環式基であり、R21、R22 について後記するアリール基または脂環式炭化水素基からさらに1個の水素原子が除かれた基を表し、l、m、nは0~10の整数を表し、mは0が好ましく、1、nは0または1が好ましい。
-(単結合)
-CH2-
-CH2-CH2-
-CH2-B-(Bは二価の脂環式炭化水素基または二価の芳香族炭化水素基からなる環式基を表す)
-B-CH2-
-C6H4-
-O-C6H4-
-C(=O)-O-CH2-
-C(=O)-O-CH2-CH2-
-CH2-C(=O)-O-CH2-
-O-CH2-
-O-CH2-CH2-
-CH2-O-CH2-および、
-C(=O)-O-(CR21R22)2-または
-C6H4-O-(CR21R22)2-などとして挙げられる。
RX1-O-C(=O)- (d)
RX1-O-CHRX2- (e)
CRX3RX4RX5- (f)
SiRX3RX4RX5- (g)
RX1-C(=O)- (h)
レジスト組成物について説明する。
本明細書において、ベース樹脂とは、酸不安定性基または架橋部位を有しポジ型またはネガ型のレジスト機能を有する樹脂をいう。前記感光溶解性変化機能を有するスルホン酸塩樹脂もベース樹脂の一形態である。
ネガ型レジスト組成物の場合、化学増幅型のネガ型レジスト組成物に用いられている架橋剤として公知のものの中から任意に選択して用いることができる。
本発明による含フッ素高分子化合物を薄膜に成膜する方法としては、例えば有機溶媒に溶解させて塗布、乾燥によって成膜する方法を用いることが可能である。使用する有機溶媒としては、含フッ素高分子化合物が可溶であれば特に制限されないが、アセトン、メチルエチルケトン、シクロヘキサノン、メチルイソアミルケトン、2‐ヘプタノンなどのケトン類やエチレングリコール、エチレングリコールモノアセテート、ジエチレングリコール、ジエチレングリコールモノアセテート、プロピレングリコール、プロピレングリコールモノアセテート、プロピレングリコールモノメチルエーテル、プロピレングリコールモノメチルエーテルアセテート(PGMEA)、ジプロピレングリコール、又はジプロピレングリコールモノアセテートのモノメチルエーテル、モノエチルエーテル、モノプロピルエーテル、モノブチルエーテル又はモノフェニルエーテルなどの多価アルコール類及びその誘導体や、ジオキサンのような環式エーテル類や乳酸メチル、乳酸エチル、酢酸メチル、酢酸エチル、酢酸ブチル、ピルビン酸メチル、ピルビン酸エチル、メトキシプロピオン酸メチル、エトキシプロピオン酸エチルなどのエステル類、キシレン、トルエンなどの芳香族系溶媒、フロン、代替フロン、パーフルオロ化合物、ヘキサフルオロイソプロピルアルコールなどのフッ素系溶剤、塗布性を高める目的で高沸点弱溶剤であるターペン系の石油ナフサ溶媒やパラフィン系溶媒などが使用可能である。これらは単独で用いてもよいし、2種以上混合して用いてもよい。
本発明のレジスト組成物は、界面活性剤、好ましくはフッ素系及び/又はシリコン系界面活性剤(フッ素系界面活性剤及びシリコン系界面活性剤、フッ素原子と珪素原子の両方を含有する界面活性剤)のいずれか、あるいは2種以上を含有することが好ましい。
本発明のレジスト組成物には、スルホン酸塩樹脂と併せて公知の光酸発生剤を使用することができる。光酸発生剤としては、化学増幅型レジストの酸発生剤として用いられるものの中から、任意のものを選択して使用することができる。このような酸発生剤の例としては、ビススルホニルジアゾメタン類、ニトロベンジル誘導体類、オニウム塩類、ハロゲン含有トリアジン化合物類、シアノ基含有オキシムスルホネート化合物類、その他のオキシムスルホネート化合物などが挙げられる。これらの光酸発生剤は単独で用いてもよいし、2種以上を組み合わせて用いてもよく、また、その含有量は本発明のスルホン酸塩樹脂と合わせてレジスト組成物100質量部に対して、通常0.5~20質量部の範囲で選ばれる。この量が0.5質量部未満では像形成性が不十分であるし、20質量部を超えると均一な溶液が形成されにくく、保存安定性が低下する傾向がみられ好ましくない。また、光酸発生剤合計質量100質量部のうち本発明のスルホン酸塩樹脂は1~100質量部であり、10~100質量部とするのが好ましく、30~100質量部とするのがより好ましい。
付加的樹脂は、使用溶剤に溶解し他のレジスト組成物を構成する成分と相溶する樹脂であれば特に限定されず、可塑剤、安定剤、増粘剤、レベリング剤、消泡剤、相溶化剤、密着剤などとして作用する。
パターン形成方法について説明する。
1H NMR(測定溶媒:重クロロホルム,基準物質:テトラメチルシラン);δ=7.73-7.67(m,15H;Ph3S+)6.28(s,1H;=CH2),5.77(s,1H;=CH2),4.34(q,J=8.0 Hz,2H),4.05(m,2H),2.23(m,2H),2.00(s,3H),1.58(m,2H),1.50(m,2H),1.30(t,J=8.0 Hz,3H).19F NMR(測定溶媒:重クロロホルム,基準物質:トリクロロフルオロメタン);δ=-79.4(s,3F),-112.0(s,2F),-117.5(s,2F)。
重合性含フッ素スルホン酸オニウム塩(重合性単量体)のプロピレングリコールモノメチルエーテルアセテート(PGMEA)に対する溶解度の比較を表1に示す。本実施例で使用した重合性単量体の構造と略号を以下に示す。このうち、PAG-1、PAG-2、PAG-3は本発明にかかる重合性含フッ素スルホン酸オニウム塩である。
製造した各樹脂、溶剤、その他の添加剤、並びに既存の光酸発生剤(PAG)であるノナフルオロブタンスルホン酸トリフェニルスルホニウム塩(PAG-C3)を配合してレジスト組成物を調合した。
(溶剤)
S-1:プロピレングリコールモノメチルエーテルアセテート(PGMEA)
S-2:γ-ブチロラクトン
S-3:乳酸エチル
S-4:シクロヘキサノン
(塩基性化合物)
O-1:N,N-ジブチルアニリン
O-2:2,6-ジイソプロピルアニリン
O-3:ジアザビシクロ[4.3.0]ノネン
O-4:2,4,5-トリフェニルイミダゾール
O-5:トリオクチルアミン
架橋剤:ニカラックMX-270(グリコールウリル系架橋剤、三和ケミカル製品
次いで、各レジスト組成物をシリコンウェハー上にスピンコートし膜厚250ナノメータのレジスト膜を得た。110℃でプリベークを行った後、フォトマスクを介して248nm紫外線での露光を行ったのち、120℃でポストエクスポーザーベークを行った。その後、2.38質量%テトラメチルアンモニウムヒドロキシド水溶液を用い、23℃で1分間現像した。いずれのレジスト組成物からも高解像のパターン形状が得られ、基板への密着不良欠陥、成膜不良欠陥、現像欠陥、エッチング耐性不良による欠陥は見られなかった。各レジスト組成物の組成及び評価結果を表4および表5に示す。
表6に示すように、各種の単量体を用いて重合例P-1またはP-2と同様の手段でスルホン酸塩を含まない樹脂(P-1’~P-5’)を合成した。得られた樹脂の繰り返し単位のモル比と質量平均分子量(MW)を表6に示した。
参考重合例2で製造した従来型のオニウム塩重合性単量体を用いた樹脂(P-C1~P-C4)、溶剤、並びにその他の添加剤を配合して実施例1~48と同様にレジスト組成物を調合することを試みた。しかし、多くの樹脂はプロピレングリコールモノメチルエーテルアセテート(PGMEA)に難溶であり、PGMEAの量を倍にしても完全に溶解することは無かった。溶剤にシクロヘキサノンを使用した場合、溶解した樹脂があったが、これらは実施例1~48と同様にパターン形成を実施した。結果を表8に示した。
Claims (23)
- 下記一般式(3)で表される繰り返し単位を有するスルホン酸塩樹脂。
- 下記一般式(4)で表される繰り返し単位を有する請求項1に記載のスルホン酸塩樹脂。
- さらにオレフィン、含フッ素オレフィン、アクリル酸エステル、メタクリル酸エステル、含フッ素アクリル酸エステル、含フッ素メタクリル酸エステル、ノルボルネン化合物、含フッ素ノルボルネン化合物、スチレン系化合物、含フッ素スチレン系化合物、ビニルエーテル、および含フッ素ビニルエーテルに含まれる重合性二重結合が開裂して形成された繰り返し単位からなる群より選ばれた一種以上の繰り返し単位を有する請求項1~3のいずれか1項に記載のスルホン酸塩樹脂。
- さらに下記一般式(6)で表される繰り返し単位を有する請求項1~4のいずれか1項に記載のスルホン酸塩樹脂。
- さらに下記一般式(9)で表される繰り返し単位を有する請求項1~7のいずれか1項に記載のスルホン酸塩樹脂。
- 式中、-(CX2)-が、-(CH2)p-(CF2)q-で表され、pが0~10の整数かつqが0~8の整数である繰り返し単位を有する請求項1~11の何れか1項に記載のスルホン酸塩樹脂。
- 式中、-(CX2)-が、-(CH2)p-(CF2)q-で表され、pが0~4の整数かつqが0または1である繰り返し単位を有する請求項1~11の何れか1項に記載のスルホン酸塩樹脂。
- 請求項1~13のいずれか1項に記載のスルホン酸塩樹脂と溶剤を少なくとも含むレジスト組成物。
- スルホン酸塩樹脂が酸不安定性基を有するスルホン酸塩樹脂である請求項14に記載の化学増幅ポジ型レジスト組成物。
- さらに酸不安定性基を有する樹脂を含む請求項14または15に記載の化学増幅ポジ型レジスト組成物。
- スルホン酸塩樹脂がアルコール性ヒドロキシル基またはカルボキシル基を有するスルホン酸塩樹脂である請求項14に記載の化学増幅ネガ型レジスト組成物。
- さらにアルコール性ヒドロキシル基またはカルボキシル基を有する樹脂を含む請求項12または請求項17に記載の化学増幅ネガ型レジスト組成物。
- 請求項14~18のいずれか1項に記載のレジスト組成物を基板上に塗布する工程と、加熱処理後フォトマスクを介して波長300nm以下の高エネルギー線で露光する工程と、必要に応じて加熱処理した後、現像液を用いて現像する工程とを含むことを特徴とするパターン形成方法。
- 露光する工程が、波長193nmのArFエキシマレーザーを用い、レジスト組成物を塗布した基板と投影レンズの間に水、もしくは空気の屈折率より高い屈折率を有する水以外の液体を挿入する液浸リソグラフィー法であることを特徴とする請求項19に記載のパターン形成方法。
- 露光する工程が、波長10~14nmの軟X線(EUV光)を用いることを特徴とする請求項19に記載のパターン形成方法。
- 下記一般式(1)で表されるアニオンを有する重合性含フッ素スルホン酸または重合性含フッ素スルホン酸塩。
- 下記一般式(2)で表される重合性含フッ素スルホン酸オニウム塩。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020137012134A KR101535197B1 (ko) | 2010-10-13 | 2011-10-05 | 중합성 함불소 술폰산염류, 함불소 술폰산염 수지, 레지스트 조성물 및 그것을 사용한 패턴 형성 방법 |
| US13/878,597 US9182664B2 (en) | 2010-10-13 | 2011-10-05 | Polymerizable fluorine-containing sulfonate, fluorine-containing sulfonate resin, resist composition and pattern-forming method using same |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010-230238 | 2010-10-13 | ||
| JP2010230238 | 2010-10-13 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012050015A1 true WO2012050015A1 (ja) | 2012-04-19 |
Family
ID=45938244
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/072931 WO2012050015A1 (ja) | 2010-10-13 | 2011-10-05 | 重合性含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9182664B2 (ja) |
| JP (1) | JP5704046B2 (ja) |
| KR (1) | KR101535197B1 (ja) |
| TW (1) | TWI444391B (ja) |
| WO (1) | WO2012050015A1 (ja) |
Cited By (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014196396A1 (ja) * | 2013-06-05 | 2014-12-11 | Jsr株式会社 | 着色組成物、着色硬化膜及び表示素子 |
| WO2018110430A1 (ja) | 2016-12-14 | 2018-06-21 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
| WO2018110429A1 (ja) | 2016-12-14 | 2018-06-21 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
| WO2018147094A1 (ja) | 2017-02-08 | 2018-08-16 | 住友化学株式会社 | 化合物、樹脂、レジスト組成物及びレジストパターンの製造方法 |
| BE1025923A1 (fr) | 2017-11-09 | 2019-08-08 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026157A1 (fr) | 2018-04-12 | 2019-10-22 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026164A1 (fr) | 2018-04-12 | 2019-10-22 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026363A1 (fr) | 2018-05-29 | 2020-01-14 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026526A1 (fr) | 2018-08-27 | 2020-03-04 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| BE1026584A1 (fr) | 2019-01-18 | 2020-03-25 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| BE1026621A1 (fr) | 2019-01-18 | 2020-04-08 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| TWI691786B (zh) * | 2015-03-24 | 2020-04-21 | 日商東京應化工業股份有限公司 | 阻劑組成物、阻劑圖型之形成方法、酸產生劑、光反應性抑制劑及化合物 |
| BE1026753A1 (fr) | 2018-11-20 | 2020-05-28 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de photoresist |
| BE1027107A1 (fr) | 2019-03-25 | 2020-10-05 | Sumitomo Chemical Co | Compose, resine, composition de photoresist et procede de production de motif de photoresist |
| BE1027246A1 (fr) | 2019-05-17 | 2020-11-25 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de photoresist |
| BE1027311A1 (fr) | 2019-06-04 | 2020-12-18 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist, et un procede de production de sel |
| BE1027310A1 (fr) | 2019-06-04 | 2020-12-18 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027509A1 (fr) | 2019-08-29 | 2021-03-10 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027510A1 (fr) | 2019-08-29 | 2021-03-10 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027801A1 (fr) | 2019-12-18 | 2021-06-22 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist et compose |
| BE1028011A1 (fr) | 2020-02-06 | 2021-08-18 | Sumitomo Chemical Co | Carboxylate, generateur d'acide carboxylique, composition de resist et procede de production de motif de resist |
| BE1028013A1 (fr) | 2020-02-06 | 2021-08-18 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028077A1 (fr) | 2020-03-05 | 2021-09-14 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028078A1 (fr) | 2020-03-05 | 2021-09-14 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028139A1 (fr) | 2020-03-23 | 2021-10-05 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028199A1 (fr) | 2020-04-22 | 2021-11-03 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028239A1 (fr) | 2020-05-15 | 2021-11-25 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028240A1 (fr) | 2020-05-15 | 2021-11-25 | Sumitomo Chemical Co | Carboxylate, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1028249A1 (fr) | 2020-05-21 | 2021-11-29 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028305A1 (fr) | 2020-06-01 | 2021-12-09 | Sumitomo Chemical Co | Compose, resine, composition de resist et procede de production de motif de resist |
| BE1028306A1 (fr) | 2020-06-01 | 2021-12-09 | Sumitomo Chemical Co | Compose, resine, composition de resist et procede de production de motif de resist |
| BE1028387A1 (fr) | 2020-06-25 | 2022-01-13 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028388A1 (fr) | 2020-07-01 | 2022-01-13 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028733A1 (fr) | 2020-11-06 | 2022-05-18 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1028753A1 (fr) | 2020-11-12 | 2022-05-23 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1028751A1 (fr) | 2020-11-11 | 2022-05-23 | Sumitomo Chemical Co | Carboxylate, composition de resist et procede de production de motif de resist |
| BE1029044A1 (fr) | 2021-02-12 | 2022-08-19 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1029265A1 (fr) | 2021-04-15 | 2022-10-25 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029259A1 (fr) | 2021-04-15 | 2022-10-25 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029393A1 (fr) | 2021-05-28 | 2022-12-05 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029391A1 (fr) | 2021-05-28 | 2022-12-05 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029606A1 (fr) | 2021-08-06 | 2023-02-13 | Sumitomo Chemical Co | Composition de resist et procede de production de motif de resist |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012056901A1 (ja) * | 2010-10-27 | 2012-05-03 | セントラル硝子株式会社 | 含フッ素スルホン酸塩類、光酸発生剤、レジスト組成物及びそれを用いたパターン形成方法 |
| KR20130076598A (ko) * | 2011-12-28 | 2013-07-08 | 금호석유화학 주식회사 | 친수성 광산발생제 및 이를 포함하는 레지스트 조성물 |
| US9488914B2 (en) | 2012-01-23 | 2016-11-08 | Central Glass Company, Limited | Fluorine-containing sulfonic acid salt, fluorine-containing sulfonic acid salt resin, resist composition, and pattern forming method using same |
| JP6024496B2 (ja) * | 2012-02-07 | 2016-11-16 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
| JP6119283B2 (ja) * | 2012-02-16 | 2017-04-26 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP5836201B2 (ja) * | 2012-06-05 | 2015-12-24 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、及びそれを用いたパターン形成方法 |
| JP6274760B2 (ja) * | 2012-07-03 | 2018-02-07 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6261890B2 (ja) * | 2012-07-03 | 2018-01-17 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6274762B2 (ja) * | 2012-07-03 | 2018-02-07 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6159592B2 (ja) * | 2012-07-03 | 2017-07-05 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6274761B2 (ja) * | 2012-07-03 | 2018-02-07 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6295067B2 (ja) * | 2012-11-26 | 2018-03-14 | 住友化学株式会社 | レジスト組成物及びレジストパターンの製造方法 |
| JP6287369B2 (ja) * | 2013-03-08 | 2018-03-07 | Jsr株式会社 | フォトレジスト組成物、レジストパターン形成方法、化合物及び重合体 |
| US9551930B2 (en) * | 2014-10-10 | 2017-01-24 | Rohm And Haas Electronic Materials Llc | Photoresist composition and associated method of forming an electronic device |
| US9606434B2 (en) | 2014-10-10 | 2017-03-28 | Rohm And Haas Electronic Materials, Llc | Polymer comprising repeat units with photoacid-generating functionality and base-solubility-enhancing functionality, and associated photoresist composition and electronic device forming method |
| US9557642B2 (en) | 2014-10-10 | 2017-01-31 | Rohm And Haas Electronic Materials Llc | Photoresist composition and associated method of forming an electronic device |
| JP6501481B2 (ja) * | 2014-10-14 | 2019-04-17 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006121096A1 (ja) * | 2005-05-11 | 2006-11-16 | Jsr Corporation | 新規化合物および重合体、ならびに感放射線性樹脂組成物 |
| JP2008133448A (ja) * | 2006-10-27 | 2008-06-12 | Shin Etsu Chem Co Ltd | 重合性アニオンを有するスルホニウム塩及び高分子化合物、レジスト材料及びパターン形成方法 |
| JP2009007327A (ja) * | 2007-02-15 | 2009-01-15 | Central Glass Co Ltd | 光酸発生剤用化合物及びそれを用いたレジスト組成物、パターン形成方法 |
| JP2009275155A (ja) * | 2008-05-15 | 2009-11-26 | Jsr Corp | 上層膜用組成物及びレジストパターン形成方法 |
| JP2010095643A (ja) * | 2008-10-17 | 2010-04-30 | Central Glass Co Ltd | 重合性アニオンを有する含フッ素スルホン塩類とその製造方法、含フッ素樹脂、レジスト組成物及びそれを用いたパターン形成方法 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0473547A1 (de) | 1990-08-27 | 1992-03-04 | Ciba-Geigy Ag | Olefinisch ungesättigte Oniumsalze |
| US6007963A (en) * | 1995-09-21 | 1999-12-28 | Sandia Corporation | Method for extreme ultraviolet lithography |
| JP3613491B2 (ja) | 1996-06-04 | 2005-01-26 | 富士写真フイルム株式会社 | 感光性組成物 |
| JP4244755B2 (ja) | 2003-09-09 | 2009-03-25 | Jsr株式会社 | 感放射線性樹脂組成物 |
| JP3993549B2 (ja) * | 2003-09-30 | 2007-10-17 | 株式会社東芝 | レジストパターン形成方法 |
| US7063931B2 (en) * | 2004-01-08 | 2006-06-20 | International Business Machines Corporation | Positive photoresist composition with a polymer including a fluorosulfonamide group and process for its use |
| JP4425776B2 (ja) * | 2004-12-24 | 2010-03-03 | 信越化学工業株式会社 | レジスト材料及びこれを用いたパターン形成方法 |
| US7799883B2 (en) * | 2005-02-22 | 2010-09-21 | Promerus Llc | Norbornene-type polymers, compositions thereof and lithographic process using such compositions |
| EP2031007B1 (en) * | 2005-02-22 | 2011-07-20 | Tokyo Ohka Kogyo Co., Ltd. | Top-coat compositions with norbornene-type polymers and immersion lithographic processes using such compositions |
| JP5061612B2 (ja) | 2005-12-27 | 2012-10-31 | 住友化学株式会社 | 化学増幅型ポジ型レジスト組成物用酸発生樹脂 |
| US7569326B2 (en) | 2006-10-27 | 2009-08-04 | Shin-Etsu Chemical Co., Ltd. | Sulfonium salt having polymerizable anion, polymer, resist composition, and patterning process |
| US7956142B2 (en) | 2006-11-10 | 2011-06-07 | Jsr Corporation | Polymerizable sulfonic acid onium salt and resin |
| KR100985929B1 (ko) * | 2007-06-12 | 2010-10-06 | 샌트랄 글래스 컴퍼니 리미티드 | 불소 함유 화합물, 불소 함유 고분자 화합물, 포지티브형레지스트 조성물 및 이것을 사용한 패턴 형성방법 |
| JP5347349B2 (ja) | 2007-09-18 | 2013-11-20 | セントラル硝子株式会社 | 2−ブロモ−2,2−ジフルオロエタノール及び2−(アルキルカルボニルオキシ)−1,1−ジフルオロエタンスルホン酸塩類の製造方法 |
| JP4998746B2 (ja) * | 2008-04-24 | 2012-08-15 | 信越化学工業株式会社 | スルホニウム塩を含む高分子化合物、レジスト材料及びパターン形成方法 |
| JP5407203B2 (ja) | 2008-07-14 | 2014-02-05 | セントラル硝子株式会社 | 新規スルホン酸塩及びその誘導体、光酸発生剤並びにスルホン酸塩の製造方法 |
| JP5841707B2 (ja) * | 2008-09-05 | 2016-01-13 | 富士フイルム株式会社 | ポジ型レジスト組成物、該組成物を用いたパターン形成方法及び該組成物に用いられる樹脂 |
| WO2012056901A1 (ja) * | 2010-10-27 | 2012-05-03 | セントラル硝子株式会社 | 含フッ素スルホン酸塩類、光酸発生剤、レジスト組成物及びそれを用いたパターン形成方法 |
-
2011
- 2011-10-05 KR KR1020137012134A patent/KR101535197B1/ko active IP Right Grant
- 2011-10-05 WO PCT/JP2011/072931 patent/WO2012050015A1/ja active Application Filing
- 2011-10-05 US US13/878,597 patent/US9182664B2/en not_active Expired - Fee Related
- 2011-10-12 JP JP2011224454A patent/JP5704046B2/ja not_active Expired - Fee Related
- 2011-10-13 TW TW100137177A patent/TWI444391B/zh not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006121096A1 (ja) * | 2005-05-11 | 2006-11-16 | Jsr Corporation | 新規化合物および重合体、ならびに感放射線性樹脂組成物 |
| JP2008133448A (ja) * | 2006-10-27 | 2008-06-12 | Shin Etsu Chem Co Ltd | 重合性アニオンを有するスルホニウム塩及び高分子化合物、レジスト材料及びパターン形成方法 |
| JP2009007327A (ja) * | 2007-02-15 | 2009-01-15 | Central Glass Co Ltd | 光酸発生剤用化合物及びそれを用いたレジスト組成物、パターン形成方法 |
| JP2009275155A (ja) * | 2008-05-15 | 2009-11-26 | Jsr Corp | 上層膜用組成物及びレジストパターン形成方法 |
| JP2010095643A (ja) * | 2008-10-17 | 2010-04-30 | Central Glass Co Ltd | 重合性アニオンを有する含フッ素スルホン塩類とその製造方法、含フッ素樹脂、レジスト組成物及びそれを用いたパターン形成方法 |
Cited By (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014196396A1 (ja) * | 2013-06-05 | 2014-12-11 | Jsr株式会社 | 着色組成物、着色硬化膜及び表示素子 |
| CN105246978A (zh) * | 2013-06-05 | 2016-01-13 | Jsr株式会社 | 着色组合物、着色固化膜及显示元件 |
| JPWO2014196396A1 (ja) * | 2013-06-05 | 2017-02-23 | Jsr株式会社 | 着色組成物、着色硬化膜及び表示素子 |
| TWI691786B (zh) * | 2015-03-24 | 2020-04-21 | 日商東京應化工業股份有限公司 | 阻劑組成物、阻劑圖型之形成方法、酸產生劑、光反應性抑制劑及化合物 |
| WO2018110430A1 (ja) | 2016-12-14 | 2018-06-21 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
| WO2018110429A1 (ja) | 2016-12-14 | 2018-06-21 | 住友化学株式会社 | 樹脂、レジスト組成物及びレジストパターンの製造方法 |
| WO2018147094A1 (ja) | 2017-02-08 | 2018-08-16 | 住友化学株式会社 | 化合物、樹脂、レジスト組成物及びレジストパターンの製造方法 |
| BE1025923A1 (fr) | 2017-11-09 | 2019-08-08 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026164A1 (fr) | 2018-04-12 | 2019-10-22 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| US11378883B2 (en) | 2018-04-12 | 2022-07-05 | Sumitomo Chemical Company, Limited | Salt, acid generator, resist composition and method for producing resist pattern |
| BE1026157A1 (fr) | 2018-04-12 | 2019-10-22 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| US11820735B2 (en) | 2018-04-12 | 2023-11-21 | Sumitomo Chemical Company, Limited | Salt, acid generator, resist composition and method for producing resist pattern |
| BE1026363A1 (fr) | 2018-05-29 | 2020-01-14 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede pour produire un motif de resist |
| BE1026526A1 (fr) | 2018-08-27 | 2020-03-04 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| US11681224B2 (en) | 2018-08-27 | 2023-06-20 | Sumitomo Chemical Company, Limited | Resin, resist composition and method for producing resist pattern |
| BE1026753A1 (fr) | 2018-11-20 | 2020-05-28 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de photoresist |
| BE1026621A1 (fr) | 2019-01-18 | 2020-04-08 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| BE1026584A1 (fr) | 2019-01-18 | 2020-03-25 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist |
| BE1027107A1 (fr) | 2019-03-25 | 2020-10-05 | Sumitomo Chemical Co | Compose, resine, composition de photoresist et procede de production de motif de photoresist |
| BE1027246A1 (fr) | 2019-05-17 | 2020-11-25 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de photoresist |
| BE1027311A1 (fr) | 2019-06-04 | 2020-12-18 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist, et un procede de production de sel |
| BE1027310A1 (fr) | 2019-06-04 | 2020-12-18 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027509A1 (fr) | 2019-08-29 | 2021-03-10 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027510A1 (fr) | 2019-08-29 | 2021-03-10 | Sumitomo Chemical Co | Sel, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1027801A1 (fr) | 2019-12-18 | 2021-06-22 | Sumitomo Chemical Co | Resine, composition de photoresist et procede de production de motif de photoresist et compose |
| BE1028011A1 (fr) | 2020-02-06 | 2021-08-18 | Sumitomo Chemical Co | Carboxylate, generateur d'acide carboxylique, composition de resist et procede de production de motif de resist |
| BE1028013A1 (fr) | 2020-02-06 | 2021-08-18 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028077A1 (fr) | 2020-03-05 | 2021-09-14 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028078A1 (fr) | 2020-03-05 | 2021-09-14 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028139A1 (fr) | 2020-03-23 | 2021-10-05 | Sumitomo Chemical Co | Composition de résist et procédé de production de motif de résist |
| BE1028199A1 (fr) | 2020-04-22 | 2021-11-03 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028239A1 (fr) | 2020-05-15 | 2021-11-25 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028240A1 (fr) | 2020-05-15 | 2021-11-25 | Sumitomo Chemical Co | Carboxylate, agent de desactivation, composition de resist et procede de production de motif de resist |
| BE1028249A1 (fr) | 2020-05-21 | 2021-11-29 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028306A1 (fr) | 2020-06-01 | 2021-12-09 | Sumitomo Chemical Co | Compose, resine, composition de resist et procede de production de motif de resist |
| BE1028305A1 (fr) | 2020-06-01 | 2021-12-09 | Sumitomo Chemical Co | Compose, resine, composition de resist et procede de production de motif de resist |
| BE1028387A1 (fr) | 2020-06-25 | 2022-01-13 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028388A1 (fr) | 2020-07-01 | 2022-01-13 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1028733A1 (fr) | 2020-11-06 | 2022-05-18 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1028751A1 (fr) | 2020-11-11 | 2022-05-23 | Sumitomo Chemical Co | Carboxylate, composition de resist et procede de production de motif de resist |
| BE1028753A1 (fr) | 2020-11-12 | 2022-05-23 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029044A1 (fr) | 2021-02-12 | 2022-08-19 | Sumitomo Chemical Co | Sel, generateur d'acide, composition de resist et procede de production de motif de resist |
| BE1029259A1 (fr) | 2021-04-15 | 2022-10-25 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029265A1 (fr) | 2021-04-15 | 2022-10-25 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029393A1 (fr) | 2021-05-28 | 2022-12-05 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029391A1 (fr) | 2021-05-28 | 2022-12-05 | Sumitomo Chemical Co | Sel, generateur d’acide, composition de resist et procede de production de motif de resist |
| BE1029606A1 (fr) | 2021-08-06 | 2023-02-13 | Sumitomo Chemical Co | Composition de resist et procede de production de motif de resist |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130209937A1 (en) | 2013-08-15 |
| JP2012102323A (ja) | 2012-05-31 |
| KR20130084666A (ko) | 2013-07-25 |
| JP5704046B2 (ja) | 2015-04-22 |
| KR101535197B1 (ko) | 2015-07-08 |
| TW201221527A (en) | 2012-06-01 |
| US9182664B2 (en) | 2015-11-10 |
| TWI444391B (zh) | 2014-07-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5704046B2 (ja) | 重合性含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP5742662B2 (ja) | 含フッ素スルホン酸塩類、光酸発生剤、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP5401910B2 (ja) | 重合性アニオンを有する含フッ素スルホン塩類とその製造方法、含フッ素樹脂、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP6019849B2 (ja) | 含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP6112018B2 (ja) | 含フッ素スルホン酸塩類、含フッ素スルホン酸塩樹脂、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP5402113B2 (ja) | 新規含フッ素カルバニオン構造を有する塩及びその誘導体、光酸発生剤並びにこれを用いたレジスト材料及びパターン形成方法 | |
| JP5589281B2 (ja) | 含フッ素化合物、含フッ素高分子化合物、レジスト組成物及びそれを用いたパターン形成方法 | |
| JP2010132560A (ja) | 新規スルホン酸塩及びその誘導体、光酸発生剤並びにこれを用いたレジスト材料及びパターン形成方法 | |
| US20120322006A1 (en) | Fluorine-Containing Sulfonate Resin, Resist Composition and Pattern Formation Method | |
| US9221928B2 (en) | Fluorine-containing sulfonate resin, fluorine-containing N-sulfonyloxyimide resin, resist composition and pattern formation method | |
| JP2013227466A (ja) | 含フッ素スルホン酸塩樹脂、含フッ素n−スルホニルオキシイミド樹脂、レジスト組成物及びそれを用いたパターン形成方法 | |
| KR20120140216A (ko) | 함불소 술폰산염 수지, 함불소 n-술포닐옥시이미드 수지, 레지스트 조성물 및 그것을 이용한 패턴 형성 방법, 중합성 함불소 술폰산염, 중합성 함불소 n-술포닐옥시이미드 화합물, 함불소 술폰산 에스테르 수지 및 중합성 함불소 술폰산 에스테르 화합물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11832450 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13878597 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20137012134 Country of ref document: KR Kind code of ref document: A |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 11832450 Country of ref document: EP Kind code of ref document: A1 |