RU2443683C2 - Новые материалы для покрытий офсетных печатных форм, офсетные печатные формы и покрытия, содержащие эти материалы, способы получения и применение - Google Patents
Новые материалы для покрытий офсетных печатных форм, офсетные печатные формы и покрытия, содержащие эти материалы, способы получения и применение Download PDFInfo
- Publication number
- RU2443683C2 RU2443683C2 RU2008131537/05A RU2008131537A RU2443683C2 RU 2443683 C2 RU2443683 C2 RU 2443683C2 RU 2008131537/05 A RU2008131537/05 A RU 2008131537/05A RU 2008131537 A RU2008131537 A RU 2008131537A RU 2443683 C2 RU2443683 C2 RU 2443683C2
- Authority
- RU
- Russia
- Prior art keywords
- functional group
- offset printing
- alkyl
- polyvinyl alcohol
- attached
- Prior art date
Links
- 238000000576 coating method Methods 0.000 title claims abstract description 70
- 239000011248 coating agent Substances 0.000 title claims abstract description 56
- 238000007645 offset printing Methods 0.000 title claims abstract description 33
- 239000000463 material Substances 0.000 title description 8
- 238000004519 manufacturing process Methods 0.000 title description 7
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical class I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 claims abstract description 60
- 229920002451 polyvinyl alcohol Polymers 0.000 claims abstract description 54
- 239000004372 Polyvinyl alcohol Substances 0.000 claims abstract description 53
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 claims abstract description 42
- 125000000524 functional group Chemical group 0.000 claims abstract description 42
- 229920001577 copolymer Polymers 0.000 claims abstract description 35
- 239000002491 polymer binding agent Substances 0.000 claims abstract description 32
- 229920005596 polymer binder Polymers 0.000 claims abstract description 24
- 239000011230 binding agent Substances 0.000 claims abstract description 14
- 125000002091 cationic group Chemical group 0.000 claims abstract description 13
- 125000003118 aryl group Chemical group 0.000 claims abstract description 12
- 239000000126 substance Substances 0.000 claims abstract description 12
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical compound C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 claims abstract description 10
- 229920003086 cellulose ether Polymers 0.000 claims abstract description 7
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 claims abstract description 6
- 239000000178 monomer Substances 0.000 claims abstract description 6
- XSQUKJJJFZCRTK-UHFFFAOYSA-N urea group Chemical group NC(=O)N XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 claims abstract description 4
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims abstract description 3
- 229910052740 iodine Inorganic materials 0.000 claims abstract description 3
- 239000000203 mixture Substances 0.000 claims description 44
- -1 hexafluoroantimonate Chemical compound 0.000 claims description 40
- 125000000217 alkyl group Chemical group 0.000 claims description 26
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 25
- 239000001257 hydrogen Substances 0.000 claims description 23
- 229910052739 hydrogen Inorganic materials 0.000 claims description 23
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 20
- 238000010538 cationic polymerization reaction Methods 0.000 claims description 15
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 15
- 238000010526 radical polymerization reaction Methods 0.000 claims description 14
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical group OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 13
- 150000001241 acetals Chemical class 0.000 claims description 13
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 13
- 238000010521 absorption reaction Methods 0.000 claims description 12
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 claims description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical group [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 9
- 150000001875 compounds Chemical class 0.000 claims description 9
- 150000003839 salts Chemical class 0.000 claims description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 8
- 239000002904 solvent Substances 0.000 claims description 7
- 125000003545 alkoxy group Chemical group 0.000 claims description 6
- 125000001424 substituent group Chemical group 0.000 claims description 6
- 229920003171 Poly (ethylene oxide) Polymers 0.000 claims description 5
- 230000005855 radiation Effects 0.000 claims description 5
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 5
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 claims description 5
- 239000004202 carbamide Substances 0.000 claims description 4
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims description 4
- 150000002431 hydrogen Chemical class 0.000 claims description 4
- MGFYSGNNHQQTJW-UHFFFAOYSA-N iodonium Chemical compound [IH2+] MGFYSGNNHQQTJW-UHFFFAOYSA-N 0.000 claims description 4
- YOZHLACIXDCHPV-UHFFFAOYSA-N n-(methoxymethyl)-2-methylprop-2-enamide Chemical compound COCNC(=O)C(C)=C YOZHLACIXDCHPV-UHFFFAOYSA-N 0.000 claims description 4
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 claims description 3
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical group C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 claims description 3
- 125000004663 dialkyl amino group Chemical group 0.000 claims description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 3
- 229920001451 polypropylene glycol Polymers 0.000 claims description 3
- 125000005208 trialkylammonium group Chemical group 0.000 claims description 3
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 claims description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 2
- LZDLRJOUWKXNIG-UHFFFAOYSA-N carbonic acid;fluoroform Chemical compound OC(O)=O.FC(F)F LZDLRJOUWKXNIG-UHFFFAOYSA-N 0.000 claims description 2
- 229920002678 cellulose Polymers 0.000 claims description 2
- 239000001913 cellulose Substances 0.000 claims description 2
- YRIUSKIDOIARQF-UHFFFAOYSA-N dodecyl benzenesulfonate Chemical compound CCCCCCCCCCCCOS(=O)(=O)C1=CC=CC=C1 YRIUSKIDOIARQF-UHFFFAOYSA-N 0.000 claims description 2
- 229940071161 dodecylbenzenesulfonate Drugs 0.000 claims description 2
- ULYOZOPEFCQZHH-UHFFFAOYSA-N n-(methoxymethyl)prop-2-enamide Chemical compound COCNC(=O)C=C ULYOZOPEFCQZHH-UHFFFAOYSA-N 0.000 claims description 2
- 125000001624 naphthyl group Chemical group 0.000 claims description 2
- 229910052708 sodium Chemical group 0.000 claims description 2
- 125000004964 sulfoalkyl group Chemical group 0.000 claims description 2
- 150000005621 tetraalkylammonium salts Chemical class 0.000 claims description 2
- JBVRYPIKNHCBMG-UHFFFAOYSA-N C(N)(OS(=O)(=O)C(C1=CC=CC=C1)C)=O.C1C(C)O1 Chemical group C(N)(OS(=O)(=O)C(C1=CC=CC=C1)C)=O.C1C(C)O1 JBVRYPIKNHCBMG-UHFFFAOYSA-N 0.000 claims 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 claims 1
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 claims 1
- 125000002777 acetyl group Chemical class [H]C([H])([H])C(*)=O 0.000 abstract 1
- 238000006243 chemical reaction Methods 0.000 description 50
- 239000000243 solution Substances 0.000 description 37
- 239000000975 dye Substances 0.000 description 33
- 239000011541 reaction mixture Substances 0.000 description 23
- 238000003756 stirring Methods 0.000 description 19
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 17
- 150000003254 radicals Chemical class 0.000 description 17
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 16
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 15
- 0 CC*C(C(C1C*(CC(CC2CCC2)(CC2C(CC(*=CC)=C)CC2)C*=CC[C@@](C)C(C(*(C)=CC)=C)=C2C(C3)CC3C2)C1)=C1CCC1)=C Chemical compound CC*C(C(C1C*(CC(CC2CCC2)(CC2C(CC(*=CC)=C)CC2)C*=CC[C@@](C)C(C(*(C)=CC)=C)=C2C(C3)CC3C2)C1)=C1CCC1)=C 0.000 description 12
- HVVWZTWDBSEWIH-UHFFFAOYSA-N [2-(hydroxymethyl)-3-prop-2-enoyloxy-2-(prop-2-enoyloxymethyl)propyl] prop-2-enoate Chemical compound C=CC(=O)OCC(CO)(COC(=O)C=C)COC(=O)C=C HVVWZTWDBSEWIH-UHFFFAOYSA-N 0.000 description 12
- 238000001228 spectrum Methods 0.000 description 12
- 239000008367 deionised water Substances 0.000 description 11
- 229910021641 deionized water Inorganic materials 0.000 description 11
- 238000010438 heat treatment Methods 0.000 description 11
- 229920001223 polyethylene glycol Polymers 0.000 description 11
- 239000007787 solid Substances 0.000 description 11
- RGHHSNMVTDWUBI-UHFFFAOYSA-N 4-hydroxybenzaldehyde Chemical compound OC1=CC=C(C=O)C=C1 RGHHSNMVTDWUBI-UHFFFAOYSA-N 0.000 description 10
- 239000000047 product Substances 0.000 description 9
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 8
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 8
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 8
- 229910052782 aluminium Inorganic materials 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 8
- 229910052757 nitrogen Inorganic materials 0.000 description 8
- 229920000642 polymer Polymers 0.000 description 8
- 239000000758 substrate Substances 0.000 description 8
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 7
- 239000002253 acid Substances 0.000 description 7
- 239000012298 atmosphere Substances 0.000 description 7
- 239000003054 catalyst Substances 0.000 description 7
- 239000012975 dibutyltin dilaurate Substances 0.000 description 7
- 238000004090 dissolution Methods 0.000 description 7
- 239000010410 layer Substances 0.000 description 7
- 238000006116 polymerization reaction Methods 0.000 description 7
- 229920013730 reactive polymer Polymers 0.000 description 7
- MACMNSLOLFMQKL-UHFFFAOYSA-N 1-sulfanyltriazole Chemical compound SN1C=CN=N1 MACMNSLOLFMQKL-UHFFFAOYSA-N 0.000 description 6
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 239000002250 absorbent Substances 0.000 description 6
- 230000002745 absorbent Effects 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 229920002689 polyvinyl acetate Polymers 0.000 description 6
- 239000011118 polyvinyl acetate Substances 0.000 description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 6
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 5
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 5
- 238000003384 imaging method Methods 0.000 description 5
- 239000002480 mineral oil Substances 0.000 description 5
- 235000010446 mineral oil Nutrition 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 229910000104 sodium hydride Inorganic materials 0.000 description 5
- 239000012312 sodium hydride Substances 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical group N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 4
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 4
- 239000007795 chemical reaction product Substances 0.000 description 4
- 238000000034 method Methods 0.000 description 4
- 230000001737 promoting effect Effects 0.000 description 4
- 125000003003 spiro group Chemical group 0.000 description 4
- 239000003381 stabilizer Substances 0.000 description 4
- 238000000584 ultraviolet--visible--near infrared spectrum Methods 0.000 description 4
- FDSUVTROAWLVJA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol;prop-2-enoic acid Chemical compound OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OCC(CO)(CO)COCC(CO)(CO)CO FDSUVTROAWLVJA-UHFFFAOYSA-N 0.000 description 3
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 3
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 3
- 238000007639 printing Methods 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- WNZQDUSMALZDQF-UHFFFAOYSA-N 2-benzofuran-1(3H)-one Chemical compound C1=CC=C2C(=O)OCC2=C1 WNZQDUSMALZDQF-UHFFFAOYSA-N 0.000 description 2
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N Butyraldehyde Chemical compound CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 2
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000000412 dendrimer Substances 0.000 description 2
- 229920000736 dendritic polymer Polymers 0.000 description 2
- 125000005442 diisocyanate group Chemical group 0.000 description 2
- 239000004815 dispersion polymer Substances 0.000 description 2
- 150000002148 esters Chemical group 0.000 description 2
- 239000003999 initiator Substances 0.000 description 2
- 239000000976 ink Substances 0.000 description 2
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 2
- RBQRWNWVPQDTJJ-UHFFFAOYSA-N methacryloyloxyethyl isocyanate Chemical compound CC(=C)C(=O)OCCN=C=O RBQRWNWVPQDTJJ-UHFFFAOYSA-N 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920001228 polyisocyanate Polymers 0.000 description 2
- 239000005056 polyisocyanate Substances 0.000 description 2
- 238000001542 size-exclusion chromatography Methods 0.000 description 2
- 239000006104 solid solution Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 229920001567 vinyl ester resin Chemical group 0.000 description 2
- QGKMIGUHVLGJBR-UHFFFAOYSA-M (4z)-1-(3-methylbutyl)-4-[[1-(3-methylbutyl)quinolin-1-ium-4-yl]methylidene]quinoline;iodide Chemical compound [I-].C12=CC=CC=C2N(CCC(C)C)C=CC1=CC1=CC=[N+](CCC(C)C)C2=CC=CC=C12 QGKMIGUHVLGJBR-UHFFFAOYSA-M 0.000 description 1
- FYADHXFMURLYQI-UHFFFAOYSA-N 1,2,4-triazine Chemical compound C1=CN=NC=N1 FYADHXFMURLYQI-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- ZNRLMGFXSPUZNR-UHFFFAOYSA-N 2,2,4-trimethyl-1h-quinoline Chemical compound C1=CC=C2C(C)=CC(C)(C)NC2=C1 ZNRLMGFXSPUZNR-UHFFFAOYSA-N 0.000 description 1
- JSRDFBJEJMXYCJ-UHFFFAOYSA-N 2-[2-[2-chloro-3-[2-(1,3,3-trimethyl-1,2-dihydroindol-1-ium-2-yl)ethenyl]cyclohex-2-en-1-ylidene]ethylidene]-1,3,3-trimethylindole 4-methylbenzenesulfonate Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1.CC1(C)C2=CC=CC=C2N(C)C1=CC=C1C(Cl)=C(C=CC2C(C3=CC=CC=C3[NH+]2C)(C)C)CCC1 JSRDFBJEJMXYCJ-UHFFFAOYSA-N 0.000 description 1
- BQMKNHKNQCKQBF-UHFFFAOYSA-N 2-[2-[2-chloro-3-[2-(1,3,3-trimethyl-1,2-dihydroindol-1-ium-2-yl)ethenyl]cyclohex-2-en-1-ylidene]ethylidene]-1,3,3-trimethylindole chloride Chemical compound [Cl-].CC1(C)C2=CC=CC=C2N(C)C1=CC=C1C(Cl)=C(C=CC2C(C3=CC=CC=C3[NH+]2C)(C)C)CCC1 BQMKNHKNQCKQBF-UHFFFAOYSA-N 0.000 description 1
- KXRMREPJUITWDU-UHFFFAOYSA-N 2-amino-4,6-dimethyl-3-oxophenoxazine-1,9-dicarboxylic acid Chemical compound N1=C2C(C(O)=O)=C(N)C(=O)C(C)=C2OC2=C1C(C(O)=O)=CC=C2C KXRMREPJUITWDU-UHFFFAOYSA-N 0.000 description 1
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 description 1
- YMZVFFIXEPBLJX-UHFFFAOYSA-N 3-(4-butyl-2-methyl-1h-indol-3-yl)-3-(2-methyl-1-octylindol-3-yl)-2-benzofuran-1-one Chemical compound C1=CC(CCCC)=C2C(C3(C4=CC=CC=C4C(=O)O3)C3=C(C)N(C4=CC=CC=C43)CCCCCCCC)=C(C)NC2=C1 YMZVFFIXEPBLJX-UHFFFAOYSA-N 0.000 description 1
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical group [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 description 1
- SQFMIHCARVMICF-UHFFFAOYSA-N 3-phenyl-3h-2-benzofuran-1-one Chemical compound C12=CC=CC=C2C(=O)OC1C1=CC=CC=C1 SQFMIHCARVMICF-UHFFFAOYSA-N 0.000 description 1
- SALNRVMKIQAKAN-UHFFFAOYSA-N 3-prop-2-enoyl-2-propoxybenzaldehyde Chemical compound CCCOC1=C(C=O)C=CC=C1C(=O)C=C SALNRVMKIQAKAN-UHFFFAOYSA-N 0.000 description 1
- YKXAYLPDMSGWEV-UHFFFAOYSA-N 4-hydroxybutyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCO YKXAYLPDMSGWEV-UHFFFAOYSA-N 0.000 description 1
- NDWUBGAGUCISDV-UHFFFAOYSA-N 4-hydroxybutyl prop-2-enoate Chemical compound OCCCCOC(=O)C=C NDWUBGAGUCISDV-UHFFFAOYSA-N 0.000 description 1
- XFOFBPRPOAWWPA-UHFFFAOYSA-N 6-hydroxyhexyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCO XFOFBPRPOAWWPA-UHFFFAOYSA-N 0.000 description 1
- OCIFJWVZZUDMRL-UHFFFAOYSA-N 6-hydroxyhexyl prop-2-enoate Chemical compound OCCCCCCOC(=O)C=C OCIFJWVZZUDMRL-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- SWMNLAODZIXEBO-UHFFFAOYSA-N C(C=C)(=O)O.C(C(=C)C)(=O)O.C=CC Chemical compound C(C=C)(=O)O.C(C(=C)C)(=O)O.C=CC SWMNLAODZIXEBO-UHFFFAOYSA-N 0.000 description 1
- BUQTZIARCXCBNA-UHFFFAOYSA-N C(N)(OS(=O)(=O)C(C1=CC=CC=C1)C)=O Chemical compound C(N)(OS(=O)(=O)C(C1=CC=CC=C1)C)=O BUQTZIARCXCBNA-UHFFFAOYSA-N 0.000 description 1
- MLLIQTYOEMRMQK-UHFFFAOYSA-N CC(CC(C)O1)OC1[Mn] Chemical compound CC(CC(C)O1)OC1[Mn] MLLIQTYOEMRMQK-UHFFFAOYSA-N 0.000 description 1
- OQGOSNRNRKMTEX-UHFFFAOYSA-N CC1OC(C)OC(C)C1 Chemical compound CC1OC(C)OC(C)C1 OQGOSNRNRKMTEX-UHFFFAOYSA-N 0.000 description 1
- NRDAHVBNELEBMG-UHFFFAOYSA-N CCC1(CC2)CC2CC1 Chemical compound CCC1(CC2)CC2CC1 NRDAHVBNELEBMG-UHFFFAOYSA-N 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- GXGJIOMUZAGVEH-UHFFFAOYSA-N Chamazulene Chemical group CCC1=CC=C(C)C2=CC=C(C)C2=C1 GXGJIOMUZAGVEH-UHFFFAOYSA-N 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- WKVQVRXDNSOOSK-UHFFFAOYSA-N [2-(3-bromopropyl)-4-methyl-3-oxopent-4-enyl] carbamate Chemical compound BrCCCC(C(=O)C(=C)C)COC(N)=O WKVQVRXDNSOOSK-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 239000011358 absorbing material Substances 0.000 description 1
- 239000003929 acidic solution Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- HFBMWMNUJJDEQZ-UHFFFAOYSA-N acryloyl chloride Chemical compound ClC(=O)C=C HFBMWMNUJJDEQZ-UHFFFAOYSA-N 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000004103 aminoalkyl group Chemical group 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000004181 carboxyalkyl group Chemical group 0.000 description 1
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 1
- CEZCCHQBSQPRMU-UHFFFAOYSA-L chembl174821 Chemical compound [Na+].[Na+].COC1=CC(S([O-])(=O)=O)=C(C)C=C1N=NC1=C(O)C=CC2=CC(S([O-])(=O)=O)=CC=C12 CEZCCHQBSQPRMU-UHFFFAOYSA-L 0.000 description 1
- 239000008199 coating composition Substances 0.000 description 1
- 239000011247 coating layer Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000007334 copolymerization reaction Methods 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- LHGVFZTZFXWLCP-UHFFFAOYSA-N guaiacol Chemical compound COC1=CC=CC=C1O LHGVFZTZFXWLCP-UHFFFAOYSA-N 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- GOCLJAKNIYYTMF-UHFFFAOYSA-N n,n-dimethyl-4-[2-(2-octoxyphenyl)-6-phenylpyridin-4-yl]aniline Chemical compound CCCCCCCCOC1=CC=CC=C1C1=CC(C=2C=CC(=CC=2)N(C)C)=CC(C=2C=CC=CC=2)=N1 GOCLJAKNIYYTMF-UHFFFAOYSA-N 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical compound COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 229920001568 phenolic resin Polymers 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229920005606 polypropylene copolymer Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000006748 scratching Methods 0.000 description 1
- 230000002393 scratching effect Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 238000004381 surface treatment Methods 0.000 description 1
- 229920001169 thermoplastic Polymers 0.000 description 1
- 239000004416 thermosoftening plastic Substances 0.000 description 1
- 150000003673 urethanes Chemical class 0.000 description 1
- HGBOYTHUEUWSSQ-UHFFFAOYSA-N valeric aldehyde Natural products CCCCC=O HGBOYTHUEUWSSQ-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C275/00—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C275/46—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups containing any of the groups, X being a hetero atom, Y being any atom, e.g. acylureas
- C07C275/58—Y being a hetero atom
- C07C275/62—Y being a nitrogen atom, e.g. biuret
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D159/00—Coating compositions based on polyacetals; Coating compositions based on derivatives of polyacetals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C1/00—Forme preparation
- B41C1/10—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C1/00—Forme preparation
- B41C1/10—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme
- B41C1/1008—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme by removal or destruction of lithographic material on the lithographic support, e.g. by laser or spark ablation; by the use of materials rendered soluble or insoluble by heat exposure, e.g. by heat produced from a light to heat transforming system; by on-the-press exposure or on-the-press development, e.g. by the fountain of photolithographic materials
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C1/00—Forme preparation
- B41C1/10—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme
- B41C1/1008—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme by removal or destruction of lithographic material on the lithographic support, e.g. by laser or spark ablation; by the use of materials rendered soluble or insoluble by heat exposure, e.g. by heat produced from a light to heat transforming system; by on-the-press exposure or on-the-press development, e.g. by the fountain of photolithographic materials
- B41C1/1016—Forme preparation for lithographic printing; Master sheets for transferring a lithographic image to the forme by removal or destruction of lithographic material on the lithographic support, e.g. by laser or spark ablation; by the use of materials rendered soluble or insoluble by heat exposure, e.g. by heat produced from a light to heat transforming system; by on-the-press exposure or on-the-press development, e.g. by the fountain of photolithographic materials characterised by structural details, e.g. protective layers, backcoat layers or several imaging layers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/06—Esters of carbamic acids
- C07C271/08—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/06—Esters of carbamic acids
- C07C271/08—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms
- C07C271/10—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C271/16—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms to carbon atoms of hydrocarbon radicals substituted by singly-bound oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/027—Organoboranes and organoborohydrides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B11/00—Preparation of cellulose ethers
- C08B11/193—Mixed ethers, i.e. ethers with two or more different etherifying groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/22—Esters containing halogen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/62—Polymers of compounds having carbon-to-carbon double bonds
- C08G18/6216—Polymers of alpha-beta ethylenically unsaturated carboxylic acids or of derivatives thereof
- C08G18/622—Polymers of esters of alpha-beta ethylenically unsaturated carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/77—Polyisocyanates or polyisothiocyanates having heteroatoms in addition to the isocyanate or isothiocyanate nitrogen and oxygen or sulfur
- C08G18/78—Nitrogen
- C08G18/785—Nitrogen containing tertiary amino groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D101/00—Coating compositions based on cellulose, modified cellulose, or cellulose derivatives
- C09D101/08—Cellulose derivatives
- C09D101/26—Cellulose ethers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D175/00—Coating compositions based on polyureas or polyurethanes; Coating compositions based on derivatives of such polymers
- C09D175/04—Polyurethanes
- C09D175/14—Polyurethanes having carbon-to-carbon unsaturated bonds
- C09D175/16—Polyurethanes having carbon-to-carbon unsaturated bonds having terminal carbon-to-carbon unsaturated bonds
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/028—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with photosensitivity-increasing substances, e.g. photoinitiators
- G03F7/029—Inorganic compounds; Onium compounds; Organic compounds having hetero atoms other than oxygen, nitrogen or sulfur
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/032—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with binders
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/032—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with binders
- G03F7/0325—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with binders the binders being polysaccharides, e.g. cellulose
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/032—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with binders
- G03F7/033—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with binders the binders being polymers obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. vinyl polymers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C2210/00—Preparation or type or constituents of the imaging layers, in relation to lithographic printing forme preparation
- B41C2210/04—Negative working, i.e. the non-exposed (non-imaged) areas are removed
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C2210/00—Preparation or type or constituents of the imaging layers, in relation to lithographic printing forme preparation
- B41C2210/22—Preparation or type or constituents of the imaging layers, in relation to lithographic printing forme preparation characterised by organic non-macromolecular additives, e.g. dyes, UV-absorbers, plasticisers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41C—PROCESSES FOR THE MANUFACTURE OR REPRODUCTION OF PRINTING SURFACES
- B41C2210/00—Preparation or type or constituents of the imaging layers, in relation to lithographic printing forme preparation
- B41C2210/24—Preparation or type or constituents of the imaging layers, in relation to lithographic printing forme preparation characterised by a macromolecular compound or binder obtained by reactions involving carbon-to-carbon unsaturated bonds, e.g. acrylics, vinyl polymers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2603/00—Systems containing at least three condensed rings
- C07C2603/02—Ortho- or ortho- and peri-condensed systems
- C07C2603/04—Ortho- or ortho- and peri-condensed systems containing three rings
- C07C2603/06—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members
- C07C2603/10—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings
- C07C2603/12—Ortho- or ortho- and peri-condensed systems containing three rings containing at least one ring with less than six ring members containing five-membered rings only one five-membered ring
- C07C2603/18—Fluorenes; Hydrogenated fluorenes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- General Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Health & Medical Sciences (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Wood Science & Technology (AREA)
- Manufacturing & Machinery (AREA)
- Thermal Sciences (AREA)
- Optics & Photonics (AREA)
- Biochemistry (AREA)
- Inorganic Chemistry (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Paints Or Removers (AREA)
- Macromonomer-Based Addition Polymer (AREA)
- Polyurethanes Or Polyureas (AREA)
- Detergent Compositions (AREA)
- Printing Plates And Materials Therefor (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Изобретение относится к новым веществам для покрытий офсетных печатных форм и к покрывающему раствору офсетной печатной формы, содержащему указанные вещества. Описывается полимеризуемая соль иодония, включающая положительно заряженный атом иода, к которому присоединены два арильных кольца и отрицательно заряженный противоион, и по меньшей мере один заместитель, содержащий группу уретана и/или мочевины, присоединенную по меньшей мере к одному из указанных арильных колец, причем указанный заместитель содержит по меньшей мере одну функциональную группу, способную к катионной или радикальной полимеризации. Описывается также сополимер ацеталя поливинилового спирта, содержащий по меньшей мере одну функциональную группу, способную к катионной или радикальной полимеризации, предпочтительно, виниловый эфир, алкокси-метилакриламид или алкоксиметакриламид. Описывается также полимерное связующее для покрытий офсетной печатной формы ряда ацеталя поливинилового спирта, ряда эфира целлюлозы и связующее на основе мономеров, каждое из которых содержит по меньшей мере одну функциональную группу, способную к катионной или радикальной полимеризации. Описывается также покрывающий раствор офсетной печатной формы, включающий указанную полимеризуемую соль иодония, указанный сополимер ацеталя поливинилового спирта и связующее из указанного ряда. Изобретение обеспечивает повышение качества изображения высокого разрешения при многократном использовании печатной формы. 6 н. и 11 з.п. ф-лы, 25 ил., 21 пр.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым материалам, пригодным для покрытий офсетных печатных форм, и к формам, покрытиям и покрывающим растворам, содержащим эти материалы. Более конкретно, эти новые материалы и покрывающие растворы пригодны при получении покрытий для литографических офсетных печатных форм для прямого цифрового формирования изображений с помощью лазера с излучением в ближней инфракрасной области спектра.
Уровень техники
Непрерывно проявляемые негативные литографические офсетные печатные формы известны из уровня техники. Например, из патента США №5569573 известны офсетные печатные формы, включающие слой лазерного формирования изображения, содержащий микроинкапсулированные олеофильные материалы в гидрофильных полимерных связующих веществ. Из EP 0770495 A1 известны офсетные печатные формы, включающие поглощающие материалы в ближней инфракрасной области, полимерные связующие и термопластичные частицы, способные к соединению при нагревании. Из патента США 6983694 известны непрерывно проявляемые негативные офсетные печатные формы, покрытые соединениями покрытия, чувствительными к ближней инфракрасной области, включающие термопластичные полимерные частицы, такие как полистирольные или поли(акрилонитрил-ко-стирольные) частицы, не реакционноспособное гидрофильное полимерное связующее вещество и красители, поглощающие в ближней инфракрасной области излучения.
Кроме того, из патента США №6261740 известны негативные офсетные печатные формы, покрытые соединениями покрытия, чувствительными в ближней инфракрасной области, включающие метоксиметакриламидные сополимеры, фенольные смолы, соли иодония и красители, поглощающие в ближней инфракрасной области. Из патента США №6124425 и 6177182 известны непрерывно проявляемые негативные офсетные печатные формы, покрытые термически поглощающими в ближней инфракрасной области полимерами, которые подвергаются реакциям поперечного сшивания через катионную полимеризацию после подвергания излучению ближнего инфракрасного диапазона. Ближние инфракрасные хромофорные части являются функционализированными к полимерному скелету через эфирные и аммониевые связи. Из патента США 6960422 известны негативные офсетные печатные формы, которые содержат чувствительные поглощающие в ближней инфракрасной области покрытые основанием композиции, включающие молекулярные красители, поглощающие в ближней инфракрасной области, радикальные генераторы, радикальные полимеризующиеся соединения уретана, реакционноспособные полимерные связующие вещества и другие добавки.
Кроме того, из патента США №6969575 и 7001704 известны непрерывно проявляемые негативные офсетные печатные формы, имеющие формирующий изображение слой, который включает микрокапсулы, поглощающие в ближней инфракрасной области, и соединение генератора кислоты. Из патента США №6582882 и совместно рассматриваемой заявки на патент США 2003/0157433; патента США 6899994 и заявки на патент США 2005/0123853 известны непрерывно проявляемые негативные офсетные печатные формы, которые покрыты термически проявляемыми композициями, содержащими полимерные связующие вещества, системы инициатора и полимеризующиеся компоненты. Описанные полимерные связующие вещества представляют собой сополимеры, имеющие нереакционноспособные полиэтиленоксид и блок-полипропилен, или графт-сополимеры, имеющие нереакционноспособные боковые цепи полиэтиленоксида, со-полимеризующиеся с акрилонитрилом, стиролом и другими мономерами. Полимеризующиеся компоненты представляют собой вязкие жидкие олигомеры, содержащие многочисленные акриловые функциональные группы. Система инициатора содержит красители, поглощающие в ближней инфракрасной области, и соединения, производящие радикалы, такие как триазин и соли иодония.
Все из этих покрывающих композиций и печатных форм показывают некоторые недостатки, такие как наличие липкой поверхности, которая приводит к трудностям при обработке и хранении, проявление разделения фаз и/или поверхностной кристаллизации, сложность получения, требование высокой мощности лазера для достижения отображения, наличие низкой адгезии основания и, следовательно, недостаточное обеспечение достаточной величины тиража на прессе, не являются непрерывно проявляемыми, показывают низкое сопротивление образованию царапин, требуют дополнительного покрывающего слоя и/или специальной обработки поверхности основания и являются дорогими при изготовлении.
Таким образом, остается необходимость в новых материалах и новых покрытиях для офсетных печатных форм, которые преодолели бы некоторые или все недостатки предшествующего уровня техники.
Сущность изобретения
Настоящее изобретение относится к солям иодония, сополимерам ацеталя поливинилового спирта и полимерным связующим веществом, каждое из которых содержит по меньшей мере одну функциональную группу, способную к катионной или радикальной полимеризации.
Настоящее изобретение далее относится к способу получения солей иодония, сополимеров ацеталя поливинилового спирта и полимерных связующих веществ по изобретению. Более конкретно, один такой способ получения соли иодония по изобретению включает присоединение боковой группы к соли иодония, где боковая группа получена реакцией моноизоцианата, диизоцианата или полиизоцианата с амином или спиртом, который имеет на конце одну или более групп, каждая из которых независимо выбрана из акрилата, метакрилата и винилового эфира.
Настоящее изобретение далее относится к применению солей иодония, сополимеров ацеталя поливинилового спирта и полимерных связующих веществ по изобретению или их смеси при получении покрывающих растворов и к покрытиям, полученным, используя эти растворы.
Изобретение также относится к покрывающим растворам и к негативной офсетной печатной форме, включающей покрытия и/или соли иодония, сополимеры ацеталя поливинилового спирта и полимерные связующие вещества по изобретению.
Термически реакционноспособные соли иодония
Настоящее изобретение относится к соли иодония, включающей положительно заряженный атом иода, к которому присоединены два арильных кольца, и отрицательно заряженный противоион. При облучении ближней инфракрасной области или нагревании эти соли представляют собой генераторы радикалов и кислот.
Соли иодония настоящего изобретения включают одну или более функциональных групп, которые могут подвергаться радикальной и/или катионной полимеризации. После нагревания соль иодония генерирует радикалы и кислоту, которые инициируют радикальную или катионную полимеризацию этих функциональных групп. Это способствует образованию сетчатой структуры в пределах облученной области покрытия.
В частности, соли иодония изобретения могут содержать радикальные полимеризующиеся группы, такие как акрилат, метакрилат и виниловый эфир. Эти радикальные полимеризующиеся группы могут представлять собой боковые цепи арильных колец указанной соли через связи уретана и/или мочевины. Эти соли могут иметь следующие общие структуры:
где
A1 представляет собой анионный противоион, выбранный из тозилата, трифлата, гексафторантимоната, тетрафторбората, тетрафенилбората и трифенил-н-алкилбората;
w представляет собой число повторений единицы и может изменяться между 0 и 18;
R8 и R9 независимо представляют собой водород, линейный или разветвленный C1-C18алкил, алкилокси, поли(этиленоксид), поли (пропиленоксид) и могут включать акрилат, метакрилат и виниловый эфир концевых групп (в случае Иодония IV и V, или R8, R9, или как R8, так и R9 действительно включают такой акрилат, метакрилат и виниловый эфир концевых групп); и
Y1 и Y2 независимо представляют собой уретан и/или мочевину, содержащую соединения, которые включают одну или более полимеризующихся функциональных групп, таких как акрилат, метакрилат или виниловый эфир.
В более определенном варианте осуществления Y1 и/или Y2 могут быть получены реакцией моноизоцианата, диизоцианата и/или полиизоцианата с амином или спиртом, включающим один или более акрилатов, метакрилатов и/или виниловых эфиров концевых групп. Эти соединения изоцианата могут быть Desmodur™ N100, Desmodur™ N3300, Desmodur™ CB 75N, Desmodur™ I, Desmodur™ W, Desmodur™ M, Desmodur™ H и Desmodur™ TD 80, которые предоставлены Bayer, Канада.
В определенном варианте осуществления спирт включает многочисленный акрилат концевых групп. Такой спирт может быть получен от Sartomer. Этот спирт может представлять собой пентаэритритолтриакрилат (Торговая марка SR 444) и дипентаэритритолпентаакрилат (Торговая марка SR399).
В другом определенном варианте осуществления спирт включает единичный акрилат и соединения метакрилата и может быть получен от Sigma-Aldrich, Канада. Спирт может представлять собой 2-гидроксиэтилакрилат, 2-гидроксиэтилметакрилат, 4-гидроксибутилакрилат, 4-гидроксибутилметакрилат, 6-гидроксигексилакрилат, 6-гидроксигексилметакрилат, поли(этиленгликоль)акрилат, поли(этиленгликоль)метакрилат, поли(пропиленгликоль)акрилат и поли(пропиленгликоль)метакрилат.
Y1 и Y2 могут иметь следующие химические структуры:
где
m варьируется между 1 и 18,
R представляет собой водород или метил
R10 представляет собой водород или линейную или разветвленную C1-C18алкильную цепь;
Q1 и Q2 независимо представляют собой конечное соединение, включающее одну или более полимеризующихся функциональных групп; и
Более конкретно, Q1 и Q2 могут независимо иметь любую из следующих структур:
где R представляет собой водород или метил, и m определен выше и находится предпочтительно между 0 и 7.
Синтез уретана, содержащего соли иодония, не имеющего никаких реакционноспособных (полимеризирующихся) функциональных групп, может быть отмечен в патенте США №6380277, который включен в настоящее описание путем ссылки.
Соль иодония настоящего изобретения можно использовать для получения покрывающих растворов и покрытий. Такое покрытие может включать от около 5 до около 60 вес.% твердого вещества иодония. Покрытия обычно получают, осаждая покрывающий раствор, включающий соли иодония, на основание. Эти растворы включают растворитель или смесь растворителей, позволяющие образование покрытия. С этой целью можно использовать любой соответствующий растворитель, известный специалисту в данной области техники. Примеры таких растворителей включают н-пропанол, воду и другие подобные растворители.
В конкретном варианте осуществления покрытие/покрывающий раствор настоящего изобретения включает смесь солей иодония, которые могут облегчить производственный процесс.
Красители, поглощающие в ближней инфракрасной области
Покрытие/покрывающий раствор настоящего изобретения может также включать краситель, поглощающий в ближней инфракрасной области, который получают нагреванием при облучении ближней инфракрасной области. В частности, этот краситель, поглощающий в ближней инфракрасной области, может быть молекулярным красителем, димерным красителем, дендримерным красителем или полимерным красителем. В определенном варианте осуществления этот краситель представляет собой сополимер ацеталя поливинилового спирта.
Этот молекулярный краситель и, в частности, этот сополимер ацеталя поливинилового спирта может иметь присоединенную к нему функциональную группу, способную к катионной или радикальной полимеризации. Поэтому, когда соль иодония способствует получению кислоты/радикалов, эта функциональная группа будет реагировать с другой такой функциональной группой, присутствующей в покрытии, например, группой из соли иодония для получения химической связи, и способствует образованию сетчатой структуры в пределах облученной области покрытия.
В частности, сополимеры ацеталя поливинилового спирта, поглощающие в ближней инфракрасной области, могут иметь молекулярную массу больше, чем около 2000 г/моль, и могу быть растворимыми или в органических растворителях, или в водных растворах. Кроме того, они могут иметь следующую общую структуру:
где
G1 представляет собой необязательно обрабатываемый сегмент, который обеспечивает растворимость в органических растворителях, таких как спирт, кетон и эфир;
G2 представляет собой необязательно термический реакционноспособный сегмент;
G3 представляет собой поглощающий излучение сегмент, который показывает одну или более высоких полос поглощения между 700 и 1100 нм. Необязательно, этот сегмент может также показывать высокие полосы поглощения между 400 и 700 нм;
a, b, c, d и e представляют собой молярные соотношения, которые могут изменяться от 0,01 до 0,99; и
когда, необязательно, сегменты G1 и/или G2 не присутствуют, и/или , соответственно замещены с помощью
В частности, обрабатываемый сегмент G1 по настоящему изобретению может быть линейным или разветвленным алкильным или арильным соединением, содержащим циано, гидрокси, диалкиламино, соли триалкиламмония, этиленоксид, пропиленоксид, метилбензилсульфонил-карбамат или функциональные группы карбоновой кислоты и фосфорной кислоты.
Термический реакционноспособный сегмент G2 по настоящему изобретению может быть линейным или разветвленным алкильным или арильным соединением и может содержать функциональную группу, способную к радикальной и/или катионной полимеризации, такую как акрилат, метакрилат, алкокси-метилакриламид, алкоксиметакриламид и виниловый эфир.
Термический реакционноспособный сегмент G2 может иметь следующие структуры:
где
R представляет собой водород или метил;
R2 представляет собой C1-C8алкил или алкокси;
m и w представляют собой число повторений и могут изменяться между 0 и 50;
y представляет собой 1 или 2.
В другом конкретном варианте осуществления сегменты G2 могут иметь боковые группы по отношению к иллюстрированным в формулах 2-7, но завершенные виниловым эфиром, алкоксиметилакриламидом или алкоксиметакриламидом функциональными группами.
В определенных вариантах осуществления G2 может быть:
сегмент G3 может быть подобным сегменту, описанному в заявке США 2006/0275698, которая включена в настоящее описание путем ссылки. В частности, сегмент G3 может иметь следующие структуры:
где NIR представляет собой хромофор, поглощающий в ближней инфракрасной области спектра, который показывает один или более высоких абсорбционных пиков между 700 и 1100 нм и может необязательно показывать один или более высоких абсорбционных пиков между 400 и 700 нм.
Полимер ацеталя поливинилового спирта по изобретению может также включать различные сегменты G3, включающие различные хромофоры, поглощающие в ближней инфракрасной области.
Хромофоры, поглощающие в ближней инфракрасной области спектра (хромофоры NIR), могут быть органическими соединениями, поглощающими в ближней инфракрасной области, содержащими функциональные группы цианина и/или арилимина. Эти хромофоры могут иметь следующие структуры:
NIR Хромофор I
NIR Хромофор II
NIR Хромофор III
NIR Хромофор IV
NIR Хромофор V
где
D1 и D2 являются одинаковыми или различными и представляют собой -O-, -S-, -Se-, -CH=CH- и -C(CH3)2;
Z1 и Z2 являются одинаковыми или различными и представляют одно или более конденсированных замещенных или незамещенных ароматических колец, таких как фенил и нафтил;
h представляет собой целое число от 2 до 8;
n представляет собой 0 или 1;
М представляет собой водород или катионный противоион, выбранный из Na, K и солей тетраалкиламмония.
A1 представляет анионный противоион, выбранный из бромида, хлорида, иодида, тозилата, трифлата, трифторметанкарбоната, додецилбензосульфоната и тетрафторбората, тетрафенилбората и трифенил-н-бутилбората.
R3 и R7 представляют собой водород или алкил; и
R4, R5 и R6 являются одинаковыми или различными и представляют собой алкил, арилалкил, гидроксиалкил, аминоалкил, карбоксиалкил, сульфоалкил.
В конкретном варианте осуществления R4, R5 и R6 могут представлять собой полимеризующиеся заместители, имеющие следующую структуру:
где
m представляет собой число -CH2- в алкильной цепи и может изменяться между 0 и 50; и
R представляет собой водород или метил.
Сополимеры ацеталя поливинилового спирта, поглощающие в ближней инфракрасной области, можно использовать в покрытии настоящего изобретения в количествах в диапазоне от около 5 до 50 вес.% твердого вещества.
Полимерные связующие вещества
Покрытие/покрывающий раствор настоящего изобретения может также включать полимерное связующее вещество. Это полимерное связующее вещество можно использовать в покрытии в количествах в диапазоне от около 1 до около 50 вес.% твердого вещества.
В частности, полимерные связующие вещества по настоящему изобретения могут быть полимерами, сополимерами или дендримерами, которые могут включать функциональную группу(ы), которая может подвергаться радикальной и/или катионной полимеризации. Поэтому, когда соль иодония производит кислоту/радикалы, эти функциональные группы будут реагировать с другими такими функциональным группами, присутствующими в покрытии, например, группами из соли иодония и красителя (если присутствует) для получения химических связей, и способствуют образованию сетчатой структуры в пределах покрытия.
В частности, эти функциональные группы могут быть акрилатом, метакрилатом и виниловым эфиром. Более конкретно, эти функциональные группы могут быть катионными реакционноспособными функциональными группами, такими как гидрокси, алкокси-метилакриламид, алкоксиметакриламид, N-метоксиметилакриламид и N-метоксиметилметакриламид.
Полимерные связующие вещества по изобретению могут быть эфирами целлюлозы, растворимыми в растворителе и/или воде, включающими функциональную группу, которая может подвергаться радикальной и/или катионной полимеризации. Этот эфир целлюлозы может быть получен реакцией 2-изоцианат-этилметакрилата с гидроксиметильной, гидроксиэтильной и гидроксипропильной группой на структуре целлюлозы. Эфир целлюлозы по изобретению может иметь следующую структуру:
где
G4 представляет собой гидрокси, гидроксиэтил и гидроксипропил.
G5 представляет собой функциональную группу, которая может подвергаться радикальной и/или катионной полимеризации.
где m представляет собой 0 или 1, и R представляет собой водород или метил.
Полимерное связующее вещество по изобретению может также быть сополимером ацеталя поливинилового спирта, который не поглощает ближнее инфракрасное излучение. Более точно, сополимеры ацеталя поливинилового спирта по изобретению могут иметь следующую общую структуру:
где G1, G2, a, b, d и e подобны определенным в Формуле 1 выше и где когда, необязательно, сегменты G1 и/или G2 не присутствуют,
Полимерные связующие вещества по изобретению могут также быть сополимерами, включающими функциональную группу, которая может подвергнуться радикальной и/или катионной полимеризации. Такие сополимеры могут быть получены из акрилонитрила, стирола, поли(этиленгликоль)акрилата, мономеров поли(этиленгликоль)метакрилата и метоксиметилметакриламида.
Кроме того, сополимеры изобретения могут быть получены сополимеризацией по меньшей мере одного мономера, выбранного из:
где
m и w представляют собой число повторений единицы и могут изменяться между 0 и 50;
R представляет собой водород или метил;
R11 представляет собой линейную и разветвленную алкильную цепь; и
R12 представляет собой алкил, гидроксил и карбоновую кислоту.
Сополимер ацеталя поливинилового спирта по настоящему изобретению может использоваться при получении покрытия/покрывающего раствора. Покрытие/покрывающий раствор может также включать соль иодония по настоящему изобретению и полимерное связующее вещество в вышеупомянутых количествах.
Полимерное связующее вещество по настоящему изобретению можно использовать при получении покрытия/покрывающего раствора. Покрытие/покрывающий раствор может также включать соль иодония по настоящему изобретению и группу, поглощающую в ближней инфракрасной области спектра в вышеупомянутых количествах.
Красители и стабилизаторы
Покрытия/покрывающие растворы изобретения могут также включать красители для обеспечения хорошей распечатки изображения после лазерного отображения. Данные красители по настоящему изобретению могут быть производными триарилпиридина, ксантена и изобензофуранона. Данные производящие цвет соединения могут быть бесцветными и затем стать окрашенными в присутствии свободного радикала или кислоты. В частности, данные соединения могут представлять собой:
3',6'-бис[N-[2-хлорфенил]-N-метиламино]спиро[2-бутил-1,1-диоксо[1,2-бензизотиазол-3(3H),9'-(9H)ксантен]] (полученный способом патента США №4345017);
3',6'-бис[N-[2-[метансульфонил]фенил]-N-метиламино]спиро[2-бутил-1,1-диоксо[1,2-бензизотиазол-3(3H),9'-(9H)ксантен]] (полученный способом патента США №4345017);
9-диэтиламино[спиро[12Н-бензо(a)ксантен-12,1'(3'H)-изобензофуран)-3'-он] (доступный от BF Goodrich, Канада);
2'-ди(фенилметил)амино-6'-[диэтиламино]спиро[изобензофуран-1(3H),9'-(9H)-ксантен]-3-он (доступный от BF Goodrich, Канада);
3-[бутил-2-метилиндол-3-ил]-3-[1-октил-2-метилиндол-3-ил]-1-(3H)-изобензофуранон (доступный от BF Goodrich, Канада);
6-[диметиламино]-3,3-бис[4-диметиламино]-фенил-(3H)-изобензофуранон (доступный от BF Goodrich, Канада);
2-[2-октилоксифенил]4-[4-диметиламинофенил]-6-фенилпиридин (доступный от BF Goodrich, Канада); или
лактонные лейкокрасители, такие как Синий-63, GN-169 и Красный-40 (доступный от Yamamoto Chemicals Inc., Япония).
Красители можно использовать в покрытиях настоящего изобретения в количествах в диапазоне от 0,5 до 5 вес.% твердого вещества.
Покрытия/покрывающие растворы изобретения могут также включать стабилизаторы для продления срока годности печатных форм в течение хранения. Эти стабилизаторы могут представлять собой метоксифенол, гидроксифенол, фенотиазин, 3-меркаптотриазол или монометиловый эфир гидрохинона. Данные стабилизаторы можно использовать в покрытиях настоящего изобретения в количествах в диапазоне от 0,5 до 5 вес.% твердого вещества.
Негативные офсетные печатные формы
Покрывающие растворы настоящего изобретения можно использовать при получении негативных офсетных печатных форм.
Настоящее изобретение поэтому также относится к печатным формам, содержащим соли иодония, сополимеры ацеталя поливинилового спирта и/или полимерные связующие вещества по настоящему изобретению. Данные негативные офсетные печатные формы могут быть непосредственно изображены лазерными устройствами отображения ближней инфракрасной области в системе компьютер - форма и цифровыми офсетными печатными технологиями.
Более конкретно, такие покрывающие растворы можно использовать при получении непрерывно проявляемых негативных офсетных печатных форм, которые включают однослойные или многослойные покрытия, нанесенные на подложку, такую как анодированный алюминий, пластическая пленка или бумага.
Алюминиевая подложка может быть гранулирована щеткой или гранулирована с помощью электричества, затем анодирована кислотными растворами.
Анодированная алюминиевая подложка может быть покрыта полимерным способствующим адгезии слоем. Способствующий адгезии и теплоизоляционный слой может быть получен из водных растворов, содержащих поли(акриловую кислоту), поли(акриловую кислоту-co-винилфосфорную кислоту) или поливинилфосфорную кислоту, которые затем высушивают, используя горячий воздух при около 110°C. Вес покрытия способствующего адгезии слоя может составлять от около 0,1 до около 1,0 г/м2.
Термически реакционноспособные покрывающие растворы могут быть осаждены на слое, способствующем адгезии, и могут иметь вес покрытия между около 0,5 и около 2,5 г/м2.
Другие варианты осуществления и дальнейшие возможности применимости настоящего изобретения станут очевидными из детального описания, приведенного далее. Следует понимать, однако, что это детальное описание, указывая предпочтительные варианты осуществления изобретения, дается посредством только иллюстрации, так как различные изменения и модификации в пределах сущности и объема изобретения станут очевидными специалистам в данной области техники.
Краткое описание чертежей
На прилагаемых чертежах:
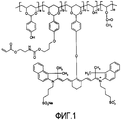
Фигура 1 представляет собой идеальную структуру сополимера ацеталя поливинилового спирта PVA 01;
Фигура 2 представляет собой идеальную структуру сополимера ацеталя поливинилового спирта PVA 02;
Фигура 3 представляет собой идеальную структуру сополимера ацеталя поливинилового спирта PVA 03;
Фигура 4 представляет собой идеальную структуру сополимера ацеталя поливинилового спирта PVA 04;
Фигура 5 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 6 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 7 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 8 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 9 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 10 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 11 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 12 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 13 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 14 представляет собой идеальную структуру конкретного варианта осуществления соли иодония, синтезируемой из соединения флуорена;
Фигура 15 представляет собой идеальную структуру полимерного связующего вещества RPB-01;
Фигура 16 представляет собой идеальную структуру полимерного связующего вещества RPB-03;
Фигура 17 представляет собой идеальную структуру полимерного связующего вещества RPB-04;
Фигура 18 представляет собой идеальную структуру полимерного связующего вещества RPB-05;
Фигура 19 представляет собой идеальную структуру полимерного связующего вещества RPB-06;
Фигура 20 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 21 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
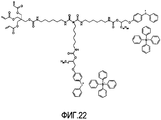
Фигура 22 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 23 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения;
Фигура 24 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения; и
Фигура 25 представляет собой возможную структуру конкретного варианта осуществления соли иодония настоящего изобретения.
Подробное описание предпочтительного варианта осуществления
Настоящее изобретение иллюстрировано в дальнейших деталях следующими неограничивающими примерами.
В этих примерах эти синтезы выполняли в 4-горловом стеклянном реакторе, оборудованном водным конденсатором, механической мешалкой, капельной воронкой и входным отверстием азота или воздуха. Молекулярные структуры полученных материалов были определены протонным ЯМР и ИК-Фурье-спектроскопией. Средняя молекулярная масса полученных сополимеров была определена эксклюзионной хроматографией (SEC), используя растворы N,N-диметилформамида (ДМФ), и калибрована со стандартами полистирола. УФ-видимые спектры ближней инфракрасной области синтезируемых полимеров измеряли в растворах метанола или на твердых пленках, используя спектрофотометр UF-VIS (PerkinElmer, Model Lambda 35™).
Кроме того, покрытые формы были изображены, используя Creo Trendsetter 3244™, оборудованный 830 нм лазерами. Изображенную форму устанавливали на копировальную машину AB Dick™, используя черную краску (доступную от Pacific Inks, Вьетнам) и увлажняющий раствор, содержащий 3,0 части MYLAN-FS100™ в 97,0 частях воды (доступный от MyLan Chemicals Inc, Вьетнам).
Синтез реакционноспособных чувствительных в ближней инфракрасной области спектра сополимеров ацеталя поливинилового спирта (красители):
Пример 1
Термически реакционноспособный, чувствительный в ближней инфракрасной области спектра сополимер PVA-01 ацеталя поливинилового спирта синтезировали, добавляя частями 90 граммов поливинилового спирта (Celvol™ 103, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 грамм диметилсульфоксида (ДМСО) при 60°C, в атмосфере азота и при постоянном перемешивании. После полного растворения добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 12,2 грамма 4-гидроксибензальдегида (100 ммоль, доступный от Sigma-Aldrich, Канада) медленно добавляли в колбу и смесь перемешивали при 60°C в течение 4 часов. Затем 1 грамм гидрида натрия (60% в минеральном масле, доступный от Sigma-Aldrich, Канада) медленно добавляли в реакцию. После того как газообразный водород больше не получали из реакции, 3,0 грамма 3-бромпропил-метакрилоил-этилкарбамата (см. структуру ниже, доступный от American Dye Source Inc., Канада) добавляли в реакционную смесь.
3-бромпропил-метакрилоил-этилкарбамат
Реакцию продолжали в течение 30 минут, затем 20 граммов 2-[2-[2-хлор-3-[[1,3-дигидро-1,1-диметил-3-(4-сульфонилбутил)-2H-бензо[e]индол-2-илиден]-этилиден]-1-циклогексен-1-ил]этенил]-1,1-диметил-3-(4-сульфонилбутил)-1H-бензо[e]индолия гидрокси внутренней соли, соль натрия (13 ммоль, доступный от American Dye Source, Inc) медленно добавляли в колбу. Результирующую смесь перемешивали при 60°C в течение еще 5 часов. Продукт реакции осаждали в ацетоне, отфильтровали и промывали обильно ацетоном. Его затем высушивали на воздухе до постоянного веса.
Спектр UV-Vis-NIR полученного термически реакционноспособного поглощающего в ближней инфракрасной области сополимера PVA-01 ацеталя поливинилового спирта регистрировали в метаноле, и была показана высокая полоса поглощения при 803 нм. Идеальная структура PVA-01, поглощающего в ближней инфракрасной области сополимера ацеталя поливинилового спирта, показана на Фигуре 1, где а = 6,65%, b = 1,00%, c = 2,35%, d = 88,00% и e = 2,00%.
Пример 2
Термически реакционноспособный, поглощающий в ближней инфракрасной области спектра сополимер PVA-01 ацеталя поливинилового спирта синтезировали, добавляя частями 90 граммов поливинилового спирта (Celvol™ 103, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 граммов диметилсульфоксида (ДМСО) при 60°C в атмосфере азота и при постоянном перемешивании. После полного растворения добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 12,2 грамма 4-гидроксибензальдегида (100 ммоль, доступный от Sigma-Aldrich, Канада) медленно добавляли в колбу и смесь перемешивали при 60°C в течение 4 часов. Затем 1 грамм гидрида натрия (60% в минеральном масле, доступный от Sigma-Aldrich, Канада) медленно добавляли в реакцию. После того как газообразный водород больше не получали из реакции, 3,0 грамма 3-бромпропил-метакрилоил-этилкарбамата добавляли в реакционную смесь. Реакцию продолжали в течение 30 минут, затем 20 граммов 2-[2-[2-хлор-3-[2-(1,3-дигидро-1,3,3-триметил-2H-индол-2-илиден)-этилиден]-1-циклогексен-1-ил]этенил]-1,3,3-триметил-1H-индолия хлорида (доступный от American Dye Source, Inc) медленно добавляли в колбу. Результирующую смесь перемешивали при 60°C в течение еще 3 часов. Затем 5 граммов тетрафенилбората натрия добавляли в реакционную колбу и продолжали перемешивать в течение дополнительных 2 часов. Продукт реакции осаждали в деионизированной воде, отфильтровывали и обильно промывали водой. Затем высушивали на воздухе до постоянного веса.
Спектр UV-Vis-NIR полученного термически реакционноспособного поглощающего в ближней инфракрасной области сополимера PVA-02 ацеталя поливинилового спирта регистрировали на тонкой пленке, и была показана высокая полоса поглощения при 800 нм. Идеальная структура поглощающего в ближней инфракрасной области сополимера PVA-02 ацеталя поливинилового спирта показана на Фигуре 2, где а = 5,15%, b = 1,00%, c = 3,85%, d = 88,00% и e = 2,00%.
Пример 3
Термически реакционноспособный поглощающий в ближней инфракрасной области спектра сополимер PVA-01 ацеталя поливинилового спирта синтезировали, добавляя частями 90 граммов поливинилового спирта (Celvol™, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 граммов диметилсульфоксида (ДМСО) при 60°C, в атмосфере азота и при постоянном перемешивании. После полного растворения добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 6,1 грамма 4-гидроксибензальдегида (доступный от Sigma-Aldrich, Канада) медленно добавляли в колбу и смесь перемешивали при 60°C в течение 4 часов. Затем 0,5 грамма гидрида натрия (60% в минеральном масле, доступный от Sigma-Aldrich, Канада) медленно добавляли в реакцию. После того как газообразный водород больше не получали из реакции, 10,0 граммов соединения, поглощающего в ближней инфракрасной области, содержащего реакционноспособные функциональные группы, имеющего структуру, показанную ниже (доступный от American Dye Source, Inc.), медленно добавляли в колбу.
Результирующую смесь перемешивали при 50°C в течение еще 5 часов. Продукт реакции осаждали в 10 литрах деионизированной воды, отфильтровывали и обильно промывали водой. Затем высушивали на воздухе до постоянного веса.
Спектр UV-Vis-NIR полученного термически реакционноспособного поглощающего в ближней инфракрасной области сополимера PVA-03 ацеталя поливинилового спирта регистрировали на тонкой пленке, и была показана высокая полоса поглощения при 830 нм. Идеальная структура поглощающего в ближней инфракрасной области сополимера PVA 03 ацеталя поливинилового спирта показана на Фигуре 3, где а = 3,42%, c = 1,58%, d = 93,00% и e = 2,00%.
Пример 4
Термически реакционноспособный поглощающий в ближней инфракрасной области спектра сополимер PVA-01 ацеталя поливинилового спирта синтезировали, добавляя частями 90 граммов поливинилового спирта (Celvol™ 103, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 граммов диметилсульфоксида (ДМСО) при 60°C в атмосфере азота и при постоянном перемешивании. После полного растворения добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 12,2 грамма 4-гидроксибензальдегида (доступный от Sigma-Aldrich, Канада) медленно добавляли в колбу, и смесь перемешивали при 60°C в течение 4 часов. Затем 1 грамм гидрида натрия (60% в минеральном масле, доступный от Sigma-Aldrich, Канада) медленно добавляли в реакцию. После того как газообразный водород больше не получали из реакции, 11,0 граммов из 10 граммов бром-концевого поли(этиленгликоля)акрилата (см. ниже структуру, доступный от American Dye Source Inc.) добавляли в реакционную смесь.
Бром-концевой поли(этиленгликоль)акрилат
Реакцию продолжали в течение 30 минут, затем 20 граммов 2-[2-[2-хлор-3-[2-(1,3-дигидро-1,3,3-триметил-2H-индол-2-илиден)-этилиден]-1-циклогексен-1-ил]этенил]-1,3,3-триметил-1H-индолия 4-метилбензолсульфоната (доступный от American Dye Source, Inc) медленно добавляли в колбу. Результирующую смесь перемешивали при 60°C в течение еще 3 часов. Затем 5 граммов тетрафенилбората натрия добавляли в реакционную колбу и продолжали перемешивать в течение дополнительных 2 часов. Продукт реакции осаждали в деионизированной воде, отфильтровывали и обильно промывали водой. Затем высушивали на воздухе до постоянного веса.
Спектр UV-Vis-NIR полученного термически реакционноспособного поглощающего в ближней инфракрасной области сополимера PVA-04 ацеталя поливинилового спирта регистрировали на тонкой пленке, и была показана высокая полоса поглощения при 800 нм. Идеальная структура поглощающего в ближней инфракрасной области сополимера PVA 04 ацеталя поливинилового спирта показана на Фигуре 4, где а = 5,15%, b = 1,00%, c = 3,85%, d = 88,00% и e = 2,00%.
Синтез реакционноспособных солей иодония:
Для простоты производства и экономической эффективности соли иодония, содержащие реакционноспособные функциональные группы, можно синтезировать и использовать как смесь различных солей. Далее эту смесь можно использовать непосредственно без дальнейшей очистки.
Пример 5
Смесь реакционноспособного иодония тетрафенилбората, имеющего возможные структуры, как на Фигурах 5, 6, 7, 8, 9 и 10, получали, нагревая 320 граммов раствора 1,3-диоксолана, содержащего 573 грамма Desmodur™ N100 (доступный от Bayer Канада), 60 граммов 2-гидроксиэтилакрилата (доступный от Sigma-Aldrich, Канада), 245 граммов поли(этиленгликоль)акрилата (Mn ~ 375, доступный от Sigma-Aldrich, Канада), 500 граммов пентаэритритолтриакрилата (SR-444, доступный от Sartomer, США), 1 грамм гидрохинона (доступный от Sigma-Aldrich, Канада) и 1 грамм дилаурата дибутилолова (доступный от Sigma-Aldrich, Канада) до 60°C в атмосфере кислорода и при постоянном перемешивании в течение 10 часов. Образец реакционной смеси брали из реакционной колбы, и его ИК-Фурье-спектр, записанный на таблетке KBr, показал пик -N=C=O при 2274 см-1. Затем 150 граммов [4-(2-гидрокси-1-тетрадецилокси)фенил]фенилиодоний тетрафенилбората (доступный от American Dye Source Inc., Канада) медленно добавляли в реакционную смесь, которую перемешивали при 60°C в течение дополнительных 6 часов. ИК-Фурье-спектр тогда показал, что пик -N=C=O при 2274 см-1 исчез, что являлось показателем для завершения реакции. Чистый вязкий полученный продукт был готов к применению.
Пример 6
Смесь реакционноспособного иодония тетрафенилбората, имеющего возможные структуры, как на Фигурах 6, 7 и 8, получали, нагревая 320 граммов безводного раствора метилэтилкетона, содержащего 573 грамма Desmodur™ N100 (доступный от Lanxess, Канада), 138 граммов гидроксиэтилакрилата (доступный от Sigma-Aldrich, Канада) и 500 граммов пентаэритритолтриакрилата (SR-444, доступный от Sartomer, США), 1 грамм гидрохинона (доступный от Sigma-Aldrich, Канада) и 1 грамм дилаурата дибутилолова (доступный от Sigma-Aldrich, Канада) до 60°C в атмосфере кислорода и при постоянном перемешивании в течение 10 часов. Образец реакционной смеси брали из реакционной колбы, и его ИК-Фурье-спектр, записанный на таблетке KBr, показал пик -N=C=O при 2274 см-1. Затем 150 граммов [4-(2-гидрокси-1-тетрадецилокси)фенил]фенилиодония тетрафенилбората (доступный от American Dye Source Inc, Канада) медленно добавляли в реакционную смесь, которую перемешивали при 60°C в течение дополнительных 6 часов. ИК-Фурье-спектр тогда показал, что пик -N=C=O при 2274 см-1 исчез, что являлось показателем для завершения реакции. Чистый вязкий полученный продукт был готов к применению.
Пример 7
Смесь реакционноспособного иодония тетрафенилбората, имеющего возможные структуры, как на Фигурах 8, 9 и 10, получали, нагревая 320 граммов раствора метилэтилкетона, содержащего 573 грамма Desmodur™ N100 (доступный от Lanxess, Канада), 430 граммов поли(этиленгликоль)акрилата (Mn ~ 375, доступный от Sigma-Aldrich, Канада), 500 граммов пентаэритритолтриакрилата (SR-444, доступный от Sartomer, США) и 1 грамм гидрохинона (доступный от Sigma-Aldrich, Канада) и 1 грамм дилаурата дибутилолова (доступный от Sigma-Aldrich, Канада) до 60°C в атмосфере кислорода и при постоянном перемешивании в течение 10 часов. Образец реакционной смеси брали из реакционной колбы, и его ИК-Фурье-спектр, записанный на таблетке KBr, показал пик -N=C=O при 2274 см-1. Затем 150 граммов [4-(2-гидрокси-1-тетрадецилокси)фенил]фенилиодония тетрафенилбората (доступный от American Dye Source Inc., Канада) медленно добавляли в реакционную смесь, которую перемешивали при 60°C в течение дополнительных 6 часов. ИК-Фурье-спектр тогда показал, что пик-N=C=O при 2274 см-1 исчез, что являлось показателем для завершения реакции. Чистый вязкий полученный продукт был готов к применению.
Пример 8
Смесь реакционноспособного иодония тетрафенилбората, имеющего возможные структуры, как на Фигурах 6, 7, 11, 12 и 13, получали, нагревая 320 граммов раствора 1,3-диоксолана, содержащего 573 граммов Desmodur™ N100 (доступный от Bayer, Канада), 50 грамм 2-гидроксиэтилметакрилата (доступный от Sigma-Aldrich, Канада), 275 граммов пентаэритритолтриакрилата (SR-444, доступный от Sartomer, США), 780 граммов дипентаэритритолпентаакрилата (SR-399, доступный от Sartomer, США), 1 грамм гидрохинона (доступный от Sigma-Aldrich, Канада) и 1 грамм дилаурата дибутилолова (доступный от Sigma-Aldrich, Канада) до 60°C в атмосфере кислорода и при постоянном перемешивании в течение 10 часов. Образец реакционной смеси брали из реакционной колбы, и его ИК-Фурье-спектр, записанный на таблетке KBr, показал пик -N=C=O при 2274 см-1. Затем 150 граммов [4-(2-гидрокси-1-тетрадецилокси)фенил]фенилиодония тетрафенилбората (доступный от American Dye Source Inc., Канада) медленно добавляли в реакционную смесь, которую перемешивали при 60°C в течение дополнительных 6 часов. ИК-Фурье-спектр тогда показал, что пик -N=C=O при 2274 см-1 исчез, что являлось показателем для завершения реакции. Чистый вязкий полученный продукт был готов к применению.
Пример 9
Смесь реакционноспособного иодония тетрафенилбората, имеющего возможные структуры, как на Фигурах 7, 9, 10, 11 и 12, получали, нагревая 137 граммов раствора 1,3-диоксолана, содержащего 245 граммов Desmodur™ N100 (доступный от Bayer, Канада), 310 граммов поли(этиленгликоль)акрилата (Mn ~ 375, доступный от Sigma-Aldrich, Канада), 244 грамма пентаэритритолтриакрилата (SR-444, доступный от Sartomer, США), 100 граммов дипентаэритритолпентаакрилата (SR 399 доступный от Sartomer, США), 1 грамм гидрохинона (доступный от Sigma-Aldrich, Канада) и 1 грамм дилаурата дибутилолова (доступный от Sigma-Aldrich, Канада) до 60°C в атмосфере кислорода и при постоянном перемешивании в течение 10 часов. Образец реакционной смеси брали из реакционной колбы, и его ИК-Фурье-спектр, записанный на таблетке KBr, показал пик -N=C=O при 2274 см-1. Затем 75 граммов [4-(2-гидрокси-1-тетрадецилокси)фенил]фенилиодония тетрафенилбората (доступный от American Dye Source Inc., Канада) медленно добавляли в реакционную смесь, которую перемешивали при 60°C в течение дополнительных 6 часов. ИК-Фурье-спектр тогда показал, что пик -N=C=O при 2274 см-1 исчез, что являлось показателем для завершения реакции. Чистый вязкий полученный продукт был готов к применению.
Пример 10
Реакционноспособную соль иодония, имеющую структуру, как показано на Фигуре 14, синтезировали, медленно добавляя 31,5 граммов 2-изоцианат-этилметакрилата в 300 мл раствора 1,3-диоксолана, растворяющего 80 граммов [2-[9,9-(3-гидроксипропил)флуоренил]4-метилфенилиодония трифенил-н-бутилбората и 0,1 грамма дилаурата дибутилолова при 60°C при постоянном перемешивании и в атмосфере кислорода. Реакцию контролировали ИК-Фурье-спектром, который указал, что реакция была завершена в течение 5 часов. Продукт осаждали в деионизированной воде, отфильтровывали и обильно промывали деионизированной водой. Затем промывали эфиром и сушили на воздухе до постоянного веса.
Также синтезировали соли иодония Фигур 20-25.
Синтез термически реакционноспособных полимерных связующих:
Пример 11
Термически реакционноспособное полимерное связующее вещество RPB-01 синтезировали, добавляя частями 25 граммов гидроксипропилцеллюлозы (Klucel® E, доступный от Hercules, США) в реакционную колбу, содержащую 500 граммов 1,3-диоксолана при 60°C в атмосфере воздуха и при постоянном перемешивании. После полного растворения добавляли в колбу 3 капли дилаурата дибутилолова, который действует в качестве катализатора для этой реакции. Затем 5,0 граммов 2-изоцианатоэтилметакрилата (доступный от American Dye Source, Канада) медленно добавляли в реакционную колбу и смесь перемешивали при 60°C в течение 7 часов. ИК-Фурье-спектр полимера на таблетке KBr указал, что реакция была завершена с исчезновением пика -N=C=O при 2274 см-1. Идеальная структура RPB-01 показана на Фигуре 15. Н-Пропанол добавляли в реакцию для обеспечения 5,0% твердого содержания раствора.
Пример 12
Реакционноспособное полимерное связующее вещество RPB-02 синтезировали способом, подобным способу из Примера 11, за исключением того, что использовали в реакции 10 граммов 2-изоцианатоэтилметакрилата. Идеальная структура RPB-02 подобна структуре RPB-01 с более реакционноспособными функциональными группами в полимере. Н-Пропанол добавляли в реакцию для обеспечения 5,0% твердого содержания раствора.
Пример 13
Реакционноспособное полимерное связующее вещество RPB-03 синтезировали добавлением частями 90 граммов поливинилового спирта (Celvol™ 103, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 граммов диметилсульфоксида (ДМСО), при 60°C, в атмосфере азота и при постоянном перемешивании. После полного растворения, добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 12,2 граммов 4-гидроксибензальдегида (100 ммоль, доступный от Sigma-Aldrich, Канада) медленно добавляли в колбу и смесь перемешивали при 60°C в течение 4 часов. Затем 0,5 граммов гидрида натрия (60% в минеральном масле, доступный от Sigma-Aldrich, Канада) медленно добавляли в реакцию. После того как газообразный водород больше не получали из реакции, 3,0 грамма 3-бромпропил-метакрилоил-этил карбамата добавляли в реакционную смесь. Реакцию продолжали в течение 5 часов при 60°C. Продукт осаждали в деионизированной воде, отфильтровывали и обильно промывали деионизированной водой. Затем высушивали на воздухе до постоянного веса. Идеальная структура RPB-03 показана на Фигуре 16, где а = 9,00%, b = 1,00%, d = 88,00% и e = 2,00%.
Пример 14
Реакционноспособное полимерное связующее вещество RPB-04 синтезировали добавлением частями 90 граммов поливинилового спирта (Celvol™ 103, 98% гидролизованный поливинилацетат, имеющий среднюю молекулярную массу около 18000) в реакционную колбу, содержащую 500 грамм диметилсульфоксида (ДМСО), при 60°C, в атмосфере азота и при постоянном перемешивании. После полного растворения добавляли в колбу 3 мл концентрированной серной кислоты, которая действует в качестве катализатора для этой реакции. После тридцати минут 6,5 граммов бутиральдегида и 2,35 граммов акрилоил-пропилоксибензальдегида (доступный от American Dye Source Inc., Канада) добавляли в реакционную смесь. Реакцию продолжали в течение 5 часов при 60°C. Продукт осаждали в деионизированной воде, отфильтровывали и обильно промывали деионизированной водой. Затем высушивали на воздухе до постоянного веса. Идеальная структура RPB-04 показана на Фигуре 17, где а = 9,00%, b = 1,00%, d = 88,00% и e = 2,00%.
Пример 15
Реакционноспособное полимерное связующее вещество RPB-05 синтезировали, нагревая смесь из 200 граммов безводного 1,3-диоксолана, растворяющего 15,0 г поли(этиленгликоль)акрилата (Mn ~ 2010, доступный от American Dye Source Inc., Канада), 15,0 граммов стирола, 50,0 граммов акрилонитрила и в 1 л 4-горловой колбе при 75°C в атмосфере азота и при постоянном перемешивании. После нагревания в течение 30 минут 0,5 г Vazo™ 64 добавляли в реакционную смесь. После 10 часов полимеризации при 75°C добавляли в реакционную смесь другие 0,5 г Vazo™ 64 и полимеризацию продолжали в течение еще 14 часов. Вводили в реакционную смесь воздух, и перемешивание продолжали при 75°C в течение дополнительных 2 часов до окончания полимеризации. Температуру реакции понижали до 5°C, и в реакционную смесь добавляли 4 грамма триэтиламина. Затем раствор, содержащий 10 граммов 1,3-диоксолана и 2 грамма акрилоилхлорида, медленно вводили в реакцию. Реакционную смесь перемешивали при комнатной температуре в течение 5 часов. Продукт осаждали в воде и высушивали до постоянного веса. Молекулярная масса RPB-03 была определена около 28000 с полимерной дисперсностью 1,4. Идеальная структура RPB-05 показана на Фигуре 18, где a = 86,16%, b = 13,16% и c = 0,68%.
Эмульсию RPB-05 готовили, медленно добавляя 50 граммов деионизированной воды в 200 граммов раствора н-пропанола, в котором растворяли 80 граммов RPB-03, используя мешалку с большими сдвиговыми усилиями при 7500 оборотов в минуту.
Пример 16
Реакционноспособное полимерное связующее вещество RPB-06 синтезировали, нагревая смесь из 200 граммов н-пропанола и 50 граммов деионизированной воды, в которой 15,0 г поли(этиленгликоль)акрилата (Mn ~ 2000, доступный от American Dye Source Inc., Канада) растворяли, 5,0 граммов N-метоксиметилметакриламида (доступный от American Dye Source Inc., Канада), 15,0 граммов стирола и 50,0 граммов акрилонитрила, в 1-литровой 4-горловой колбе при 75oC в атмосфере азота и при постоянном перемешивании. После нагревания в течение 30 минут добавляли в реакционную смесь 0,5 г Vazo™ 64. Раствор становился мутным в течение 30 минут после полимеризации. После полимеризации в течение 10 часов при 75oC в реакционную смесь добавляли другие 0,5 г Vazo™ 64, и полимеризацию продолжали в течение еще 14 часов. В реакционную смесь вводили воздух и продолжали перемешивание при 75oC в течение дополнительных 2 часов для окончания полимеризации. Молекулярная масса RPB-06 была определена около 29000 с полимерной дисперсностью 1,7. Идеальная структура RPB-06 показана на Фигуре 19, где a = 82,88%, b = 12,66%, c = 3,81% и d = 0,65%.
Непрерывно проявляемая негативная офсетная печатная форма
Пример 17
Покрывающий раствор со следующей композицией наносили на гранулированную щеткой алюминиевую подложку, анодированную фосфорной кислотой, используя проволочный прут, и высушивали при 80°C горячим воздухом. Полученный вес покрытия был около 1,0 г/м2.
| Композиция | Из примера | вес.% твердого вещества |
| PVA-01 | 1 | 2,00 |
| Смесь соли иодония | 9 | 5,00 |
| RPB-01 | 10 | 0,50 |
| RPB-05 | 14 | 2,15 |
| 3-Меркаптотриазол | 0,25 | |
| Синий компонент-цветообразователь (*) | 0,10 | |
| н-Пропанол | 90,0 | |
| Вода | 10,0 | |
| BYK 336 | 0,10 | |
| (*)Синий компонент-цветообразователь представляет собой Синий-63 (доступный от Yamamoto Chemicals Inc., Япония) | ||
Форму отображали между 100 и 250 мДж/см2 и устанавливали на прессе AB Dick. Высококачественное изображение печати получали на бумаге после 10 печатаний. Форму можно использовать, чтобы напечатать более чем 20000 копий высокого разрешения.
Пример 18
Покрывающий раствор со следующей композицией наносили на гранулированную щеткой фосфорной кислотой анодированную алюминиевую подложку, используя проволочный прут, и высушивали при 80°C горячим воздухом. Полученный вес покрытия был около 1,0 г/м2.
| Композиция | Из примера | вес.% твердого вещества |
| PVA-02 | 2 | 2,00 |
| Смесь соли иодония | 9 | 5,00 |
| RPB-01 | 10 | 0,50 |
| RPB-05 | 14 | 2,15 |
| 3-Меркаптотриазол | 0,25 | |
| Синий компонент-цветообразователь (*) | 0,10 | |
| н-Пропанол | 90,0 | |
| Вода | 10,0 | |
| BYK 336 | 0,10 | |
| (*)Синий компонент-цветообразователь представляет собой Синий-63 (доступный от Yamamoto Chemicals Inc., Япония) | ||
Форму отображали между 100 и 250 мДж/см2 и устанавливали на прессе AB Dick. Высококачественное изображение печати получали на бумаге после 10 печатаний. Форму можно использовать, чтобы напечатать более чем 20000 копий высокого разрешения.
Пример 19
Покрывающий раствор со следующей композицией наносили на гранулированную щеткой алюминиевую подложку, анодированную фосфорной кислотой, используя проволочный прут, и высушивали при 80°C горячим воздухом. Полученный вес покрытия был около 1,0 г/м2.
| Композиция | Из примера | вес.% твердого вещества |
| PVA-01 | 1 | 2,00 |
| Смесь соли иодония | 9 | 5,00 |
| RPB-01 | 10 | 0,50 |
| RPB-06 | 15 | 2,15 |
| 3-Меркаптотриазол | 0,25 | |
| Синий компонент-цветообразователь (*) | 0,10 | |
| н-Пропанол | 90,0 | |
| Вода | 10,0 | |
| BYK 336 | 0,10 | |
| (*)Синий компонент-цветообразователь представляет собой Синий-63 (доступный от Yamamoto Chemicals Inc., Япония) | ||
Форму отображали между 100 и 250 мДж/см2 и устанавливали на прессе AB Dick. Высококачественное изображение печати получали на бумаге после 10 печатаний. Форму можно использовать, чтобы напечатать более чем 20000 копий высокого разрешения.
Пример 20
Покрывающий раствор со следующей композицией наносили на гранулированную щеткой алюминиевую подложку, анодированную фосфорной кислотой, используя проволочный прут, и высушивали при 80°C горячим воздухом. Полученный вес покрытия был около 1,0 г/м2.
| Композиция | Из примера | вес.% твердого вещества |
| PVA-01 | 1 | 2,00 |
| Смесь соли иодония | 9 | 5,00 |
| RPB-01 | 10 | 1,00 |
| RPB-03 | 15 | 1,65 |
| 3-Меркаптотриазол | 0,25 | |
| Синий компонент-цветообразователь (*) | 0,10 | |
| н-Пропанол | 90,0 | |
| Вода | 10,0 | |
| BYK 336 | 0,10 | |
| (*)Синий компонент-цветообразователь представляет собой Синий-63 (доступный от Yamamoto Chemicals Inc., Япония) | ||
Форму отображали между 100 и 250 мДж/см2 и устанавливали на прессе AB Dick. Высококачественное изображение печати получали на бумаге после 10 печатаний. Форму можно использовать, чтобы напечатать более чем 20000 копий высокого разрешения.
Пример 21
Покрывающий раствор со следующей композицией наносили на гранулированную щеткой алюминиевую подложку, анодированную фосфорной кислотой, используя проволочный прут, и высушивали при 80°C горячим воздухом. Полученный вес покрытия был около 1,0 г/м2.
| Композиция | Из примера | вес.% твердого вещества |
| PVA-01 | 1 | 2,00 |
| Смесь соли иодония | 9 | 5,00 |
| RPB-01 | 10 | 1,00 |
| RPB-04 | 15 | 1,65 |
| 3-Меркаптотриазол | 0,25 | |
| Синий компонент-цветообразователь (*) | 0,10 | |
| н-Пропанол | 90,0 | |
| Вода | 10,0 | |
| BYK 336 | 0,10 | |
| (*)Синий компонент-цветообразователь представляет собой Синий-63 (доступный от Yamamoto Chemicals Inc., Япония) | ||
Форму отображали между 100 и 250 мДж/см2 и устанавливали на прессе AB Dick. Высококачественное изображение печати получали на бумаге после 10 печатаний. Форму можно использовать, чтобы напечатать более чем 20000 копий высокого разрешения.
Несмотря на то что настоящее изобретение было описано выше посредством определенных вариантов осуществления, оно может быть изменено, не отступая от сущности и основного свойства объекта изобретения, как определено в прилагаемой формуле изобретения.
Claims (17)
1. Полимеризуемая соль иодония, включающая положительно заряженный атом иода, к которому присоединены два арильных кольца, и отрицательно заряженный противоион, причем указанная соль иодония включает по меньшей мере один заместитель, содержащий уретан и/или мочевину, присоединенный по меньшей мере к одному из указанных арильных колец, где к указанному заместителю присоединена по меньшей мере одна функциональная группа, способная к катионной или радикальной полимеризации,
причем соль иодония имеет общую формулу:
или
где А1 представляет собой тозилатный, трифлатный, гексафторантимонатный, тетрафторборатный, тетрафенилборатный или трифенил-н-алкилборатный анионный противоион;
w может изменяться между 1 и 18;
R8 и R9 представляют собой независимо водород, линейный C1-С18алкил, разветвленный С1-С18алкил, алкилокси, поли(этиленоксид) или поли(пропиленоксид); и
Y1 и Y2 каждый независимо представляет собой
или
где R представляет собой водород или метил,
m изменяется между 1 и 18,
R10 представляет собой водород, линейную или разветвленную С1-С18алкильную цепь;
Q1 и Q2 каждый независимо представляет концевое соединение, к которому присоединена указанная функциональная группа, представляющая собой, предпочтительно
или
где R представляет собой водород или метил, и m определен выше, и находится предпочтительно между 0 и 7; и
Z представляет собой заместитель, включающий
где А1 определен выше.
причем соль иодония имеет общую формулу:
или
где А1 представляет собой тозилатный, трифлатный, гексафторантимонатный, тетрафторборатный, тетрафенилборатный или трифенил-н-алкилборатный анионный противоион;
w может изменяться между 1 и 18;
R8 и R9 представляют собой независимо водород, линейный C1-С18алкил, разветвленный С1-С18алкил, алкилокси, поли(этиленоксид) или поли(пропиленоксид); и
Y1 и Y2 каждый независимо представляет собой
или
где R представляет собой водород или метил,
m изменяется между 1 и 18,
R10 представляет собой водород, линейную или разветвленную С1-С18алкильную цепь;
Q1 и Q2 каждый независимо представляет концевое соединение, к которому присоединена указанная функциональная группа, представляющая собой, предпочтительно
или
где R представляет собой водород или метил, и m определен выше, и находится предпочтительно между 0 и 7; и
Z представляет собой заместитель, включающий
где А1 определен выше.
2. Соль иодония по п.1, в которой функциональная группа представляет собой акрилат, метакрилат, акриламид, метакриламид или виниловый эфир.
3. Соль иодония по п.1, в которой к R8 или по меньшей мере одному из R9 присоединена указанная функциональная группа.
4. Соль иодония по п.1, имеющая общую структуру:
или
где А1 представляет собой тозилатный, трифлатный, гексафторантимонатный, тетрафторборатный, тетрафенилборатный или трифенил-н-алкилборатный анионный противоион; и
R8 и R9 представляют собой независимо водород, линейный C1-С18алкил, разветвленный С1-С18алкил, алкилокси, поли (этиленоксид) или поли(пропиленоксид),
и где по меньшей мере один из R8 или R9 не является водородом и представляет собой указанный заместитель, содержащий уретан и/или мочевину, к которому присоединена указанная функциональная группа.
или
где А1 представляет собой тозилатный, трифлатный, гексафторантимонатный, тетрафторборатный, тетрафенилборатный или трифенил-н-алкилборатный анионный противоион; и
R8 и R9 представляют собой независимо водород, линейный C1-С18алкил, разветвленный С1-С18алкил, алкилокси, поли (этиленоксид) или поли(пропиленоксид),
и где по меньшей мере один из R8 или R9 не является водородом и представляет собой указанный заместитель, содержащий уретан и/или мочевину, к которому присоединена указанная функциональная группа.
5. Соль иодония по любому из пп.1-4 или смесь этих солей, включенная в состав покрывающего раствора офсетной печатной формы.
6. Соль иодония по любому из пп.1-4 или смесь этих солей, включенная в состав негативной офсетной печатной формы.
7. Сополимер ацеталя поливинилового спирта, к которому присоединена по меньшей мере одна функциональная группа, способная к катионной или радикальной полимеризации, причем указанная функциональная группа предпочтительно представляет собой виниловый эфир, алкокси-метилакриламид или алкоксиметакриламид, причем указанный сополимер ацеталя поливинилового спирта представляет собой:
где G1 представляет собой линейный алкил, разветвленный алкил или арил, в котором указанный линейный алкил, разветвленный алкил или арил замещен циано, гидрокси, диалкиламино, солями триалкиламмония, этиленоксидом, пропиленоксидметилбензилсульфонил-карбаматом, функциональной группой карбоновой кислоты или фосфорной кислоты;
G2 представляет собой:
или
где R представляет собой водород или метил;
R2 представляет собой C1-С6алкил или алкокси;
m и w могут изменяться между 0 и 50; и
у представляет собой 1 или 2,
или или
G3 представляет собой или , где NIR представляет собой
или
где D1 и D2 представляют собой независимо -СН=СН- или -С(СН3)2;
Z1 и Z2 каждый независимо представляет собой одно или более конденсированных замещенных или незамещенных ароматических колец, предпочтительно Z1 и Z2 каждый независимо представляют собой фенил или нафтил;
h может изменяться от 2 до 8;
n представляет собой 0 или 1;
М представляет водород или Na, K, или катионный противоион солей тетраалкиламмония;
А1 представляет собой бромид, хлорид, иодид, тозилат, трифлат, карбонат трифторметана, додецилбензосульфонатный и тетрафторборатный, тетрафенилборатный или трифенил-н-бутилборатный анионный противоион;
R3 и R7 каждый независимо представляет собой водород или алкил;
R4, R5 и R6 каждый независимо представляет собой алкил, сульфоалкил или полимеризующийся заместитель, причем указанный заместитель включает указанную функциональную группу и представляет собой формулу:
или
где m может изменяться между 0 и 50, и R представляет собой водород или метил,
поглощающий излучение, показывающий одну или более интенсивных полос поглощения между 700 и 1100 нм;
а, b, с, d и е представляют собой молярные соотношения и могут изменяться от 0,01 до 0,99;
любой из и может независимо быть заменен на и
указанная функциональная группа присоединена к G2, G3 или обеим.
где G1 представляет собой линейный алкил, разветвленный алкил или арил, в котором указанный линейный алкил, разветвленный алкил или арил замещен циано, гидрокси, диалкиламино, солями триалкиламмония, этиленоксидом, пропиленоксидметилбензилсульфонил-карбаматом, функциональной группой карбоновой кислоты или фосфорной кислоты;
G2 представляет собой:
или
где R представляет собой водород или метил;
R2 представляет собой C1-С6алкил или алкокси;
m и w могут изменяться между 0 и 50; и
у представляет собой 1 или 2,
или или
G3 представляет собой или , где NIR представляет собой
или
где D1 и D2 представляют собой независимо -СН=СН- или -С(СН3)2;
Z1 и Z2 каждый независимо представляет собой одно или более конденсированных замещенных или незамещенных ароматических колец, предпочтительно Z1 и Z2 каждый независимо представляют собой фенил или нафтил;
h может изменяться от 2 до 8;
n представляет собой 0 или 1;
М представляет водород или Na, K, или катионный противоион солей тетраалкиламмония;
А1 представляет собой бромид, хлорид, иодид, тозилат, трифлат, карбонат трифторметана, додецилбензосульфонатный и тетрафторборатный, тетрафенилборатный или трифенил-н-бутилборатный анионный противоион;
R3 и R7 каждый независимо представляет собой водород или алкил;
R4, R5 и R6 каждый независимо представляет собой алкил, сульфоалкил или полимеризующийся заместитель, причем указанный заместитель включает указанную функциональную группу и представляет собой формулу:
или
где m может изменяться между 0 и 50, и R представляет собой водород или метил,
поглощающий излучение, показывающий одну или более интенсивных полос поглощения между 700 и 1100 нм;
а, b, с, d и е представляют собой молярные соотношения и могут изменяться от 0,01 до 0,99;
любой из и может независимо быть заменен на и
указанная функциональная группа присоединена к G2, G3 или обеим.
8. Сополимер ацеталя поливинилового спирта по п.7, в котором G3 далее показывает одну или более интенсивных полос поглощения между 400 и 700 нм.
9. Сополимер ацеталя поливинилового спирта по п.7, в котором сополимер ацеталя поливинилового спирта включает более одного сегмента G3, которые являются различными.
10. Сополимер ацеталя поливинилового спирта по любому из пп.7-9, включенный в состав покрывающего раствора офсетной печатной формы.
11. Сополимер ацеталя поливинилового спирта по любому из пп.7-9, включенный в состав негативной офсетной печатной формы.
12. Полимерное связующее вещество для покрытий офсетной печатной формы, к которому присоединена по меньшей мере одна функциональная группа, способная к катионной или радикальной полимеризации, причем полимерное связующее вещество имеет следующую структуру:
где G1 представляет собой С3Н7, линейный алкил, разветвленный алкил или арил, в котором указанный линейный алкил, разветвленный алкил или арил замещен циано, гидрокси, диалкиламино, солями триалкиламмония, этиленоксидом, пропиленоксидметилбензилсульфонил-карбаматом, функциональной группой карбоновой кислоты или фосфорной кислоты;
G2 представляет собой термически реакционноспособный сегмент, к которому присоединена указанная функциональная группа:
или
где R представляет собой водород или метил;
R2 представляет собой C1-С8алкил или алкокси;
m и w могут изменяться между 0 и 50; и
y представляет собой 1 или 2,
или
a, b, d и e представляют собой молярные соотношения и могут изменяться от 0,01 до 0,99; и
может быть заменен на
где G1 представляет собой С3Н7, линейный алкил, разветвленный алкил или арил, в котором указанный линейный алкил, разветвленный алкил или арил замещен циано, гидрокси, диалкиламино, солями триалкиламмония, этиленоксидом, пропиленоксидметилбензилсульфонил-карбаматом, функциональной группой карбоновой кислоты или фосфорной кислоты;
G2 представляет собой термически реакционноспособный сегмент, к которому присоединена указанная функциональная группа:
или
где R представляет собой водород или метил;
R2 представляет собой C1-С8алкил или алкокси;
m и w могут изменяться между 0 и 50; и
y представляет собой 1 или 2,
или
a, b, d и e представляют собой молярные соотношения и могут изменяться от 0,01 до 0,99; и
может быть заменен на
13. Полимерное связующее вещество для покрытий офсетной печатной формы, к которому присоединена по меньшей мере одна функциональная группа, способная к катионной или радикальной полимеризации, причем полимерное связующее вещество является растворимым в растворителе эфиром целлюлозы, растворимым в воде эфиром целлюлозы или их смесью, причем к указанным эфирам целлюлозы присоединена указанная функциональная группа,
причем указанное полимерное связующее вещество имеет формулу
где а и b представляют собой молярные соотношения и могут
изменяться между около 0,01 и около 0,99,
G4 представляет собой гидрокси, гидроксиэтил или гидроксипропил; и
G5 представляет собой
где m представляет собой 0 или 1, и R представляет собой водород или метил,
где указанная функциональная группа, способная к катионной или радикальной полимеризации, представляет собой акрилат, метакрилат, виниловый эфир, алкоксиметилакриламид, алкоксиметакриламид, N-метоксиметилакриламид или N-метоксиметилметакриламид.
причем указанное полимерное связующее вещество имеет формулу
где а и b представляют собой молярные соотношения и могут
изменяться между около 0,01 и около 0,99,
G4 представляет собой гидрокси, гидроксиэтил или гидроксипропил; и
G5 представляет собой
где m представляет собой 0 или 1, и R представляет собой водород или метил,
где указанная функциональная группа, способная к катионной или радикальной полимеризации, представляет собой акрилат, метакрилат, виниловый эфир, алкоксиметилакриламид, алкоксиметакриламид, N-метоксиметилакриламид или N-метоксиметилметакриламид.
15. Полимерное связующее вещество по любому из пп.12-14, включенное в состав покрывающего раствора офсетной печатной формы.
16. Полимерное связующее вещество по любому из пп.12-14 или смесь этих веществ, включенные в состав негативной офсетной печатной формы.
17. Покрывающий раствор офсетной печатной формы, включающий полимеризуемую соль иодония по пп.1-6, сополимер ацеталя поливинилового спирта по пп.7-11, полимерное связующее, выбранное из группы, состоящей из связующего ацеталя поливинилового спирта по п.12, связующего эфира целлюлозы по п.13, связующего на основе мономеров по пп.14-16.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US74747406P | 2006-05-17 | 2006-05-17 | |
| US60/747,474 | 2006-05-17 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2008131537A RU2008131537A (ru) | 2010-02-10 |
| RU2443683C2 true RU2443683C2 (ru) | 2012-02-27 |
Family
ID=38693485
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2008131537/05A RU2443683C2 (ru) | 2006-05-17 | 2007-05-09 | Новые материалы для покрытий офсетных печатных форм, офсетные печатные формы и покрытия, содержащие эти материалы, способы получения и применение |
Country Status (12)
| Country | Link |
|---|---|
| US (4) | US7910768B2 (ru) |
| EP (1) | EP2018365B1 (ru) |
| JP (1) | JP5254958B2 (ru) |
| KR (1) | KR101174949B1 (ru) |
| CN (1) | CN101454277B (ru) |
| BR (1) | BRPI0707574B1 (ru) |
| CA (1) | CA2652294C (ru) |
| ES (1) | ES2530792T3 (ru) |
| HK (1) | HK1121132A1 (ru) |
| RU (1) | RU2443683C2 (ru) |
| UA (1) | UA98450C2 (ru) |
| WO (1) | WO2007131336A1 (ru) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5254958B2 (ja) * | 2006-05-17 | 2013-08-07 | アメリカン・ダイ・ソース・インコーポレーテッド | 平版印刷版コーティング用新規材料、それを含有する平版印刷版およびコーティング、調製方法ならびに使用 |
| CN101484484B (zh) * | 2006-08-24 | 2012-10-10 | 美洲染料资源公司 | 反应性近红外吸收聚合物粒子、其制备方法和用途 |
| US7723013B2 (en) * | 2007-01-11 | 2010-05-25 | Southern Lithoplate, Inc. | Negative-acting photolithographic printing plate with improved pre-burn performance |
| EP2098367A1 (en) * | 2008-03-05 | 2009-09-09 | Eastman Kodak Company | Sensitizer/Initiator Combination for Negative-Working Thermal-Sensitive Compositions Usable for Lithographic Plates |
| US8354216B2 (en) * | 2008-07-15 | 2013-01-15 | Eastman Kodak Company | Negative-working imaging elements and methods of use |
| US8137896B2 (en) * | 2008-07-29 | 2012-03-20 | Eastman Kodak Company | Method of preparing lithographic printing plates |
| JP5622484B2 (ja) * | 2009-08-20 | 2014-11-12 | 富士フイルム株式会社 | 発色感光性組成物、平版印刷版原版及び新規シアニン色素 |
| KR101390985B1 (ko) | 2009-09-15 | 2014-05-02 | 밀란 그룹 | 코폴리머, 상기 코폴리머를 포함하는 폴리머성 입자 및 네거티브형 감방사선성 평판 인쇄판용 감방사선성 코팅 조성물의 코폴리머성 결합제 |
| EP2451821B1 (en) | 2009-10-29 | 2016-07-20 | Mylan Group | Gallotannic compounds for lithographic printing plate coating compositions |
| CN102844196B (zh) | 2010-04-20 | 2015-06-10 | 米兰集团 | 用于平版印刷板的基材、其制备方法及其回收处理方法 |
| MX336236B (es) | 2010-09-14 | 2016-01-11 | Mylan Group | Copolimeros para composiciones de revestimiento sensibles a radiacion casi-infrarroja para placas de impresion litografica termica de trabajo positivo. |
| JP5955584B2 (ja) * | 2012-02-24 | 2016-07-20 | 株式会社Adeka | 新規化合物及び着色アルカリ現像性感光性組成物 |
| CA2895913A1 (en) | 2013-04-10 | 2014-10-16 | Mylan Group | Lithographic printing plate comprising a laminated substrate |
| CN106463061B (zh) * | 2014-05-27 | 2019-10-18 | 本田技研工业株式会社 | 碰撞可能性判定装置 |
| US20160259243A1 (en) * | 2015-03-03 | 2016-09-08 | Eastman Kodak Company | Negative-working lithographic printing plate precursor |
| CN111560094A (zh) * | 2015-05-29 | 2020-08-21 | 富士胶片株式会社 | 近红外线吸收性色素多聚物、组合物、膜、滤光片、图案形成方法及装置 |
| CN105778041B (zh) * | 2016-05-06 | 2019-01-15 | 南昌航空大学 | 一种耐磨耐指纹树脂的制备方法 |
| CN105778040B (zh) * | 2016-05-06 | 2018-08-24 | 南昌航空大学 | 一种环保耐指纹树脂的制备方法 |
| CN105732943B (zh) * | 2016-05-06 | 2019-01-22 | 南昌航空大学 | 一种聚甲基丙烯酸甲酯用高透明防指纹树脂的制备方法 |
| CN105859631B (zh) * | 2016-05-06 | 2019-04-02 | 南昌航空大学 | 一种镀锌钢板用高透明防指纹树脂的制备方法 |
| CN105859632B (zh) * | 2016-05-06 | 2019-04-02 | 南昌航空大学 | 一种电子束固化高透明防指纹树脂的制备方法 |
| CN105778042B (zh) * | 2016-05-06 | 2018-09-07 | 南昌航空大学 | 一种电子束固化耐指纹聚氨酯丙烯酸酯的制备方法 |
| WO2019013139A1 (ja) * | 2017-07-13 | 2019-01-17 | 富士フイルム株式会社 | 平版印刷版原版、平版印刷版の製版方法、発色組成物、硬化性組成物、及び、画像形成材料 |
| KR102435745B1 (ko) * | 2018-03-05 | 2022-08-24 | 후지필름 가부시키가이샤 | 감광성 조성물 |
| CN112512825B (zh) * | 2018-07-30 | 2022-10-25 | 富士胶片株式会社 | 机上显影型平版印刷版原版、平版印刷版的制作方法及平版印刷方法 |
| WO2021039252A1 (ja) * | 2019-08-28 | 2021-03-04 | 富士フイルム株式会社 | 感活性光線性又は感放射線性樹脂組成物、レジスト膜、パターン形成方法、電子デバイスの製造方法、化合物、樹脂 |
| US20210078350A1 (en) | 2019-09-17 | 2021-03-18 | Eastman Kodak Company | Lithographic printing plate precursor and method of use |
| US11714354B2 (en) | 2020-03-25 | 2023-08-01 | Eastman Kodak Company | Lithographic printing plate precursor and method of use |
| CN111691219B (zh) * | 2020-05-28 | 2022-02-08 | 仙鹤股份有限公司 | 一种高撕裂度ctp版衬纸及其制备方法 |
| WO2022212032A1 (en) | 2021-04-01 | 2022-10-06 | Eastman Kodak Company | Lithographic printing plate precursor and method of use |
| US20230314935A1 (en) | 2022-03-03 | 2023-10-05 | Eastman Kodak Company | Lithographic printing plate precursor and method of use |
| US20240069439A1 (en) | 2022-08-12 | 2024-02-29 | Eastman Kodak Company | Lithographic printing plate precursor and method of use |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1204000A1 (en) * | 2000-11-06 | 2002-05-08 | Fuji Photo Film Co., Ltd. | Photosensitive lithographic printing plate |
| US6566035B1 (en) * | 1999-10-29 | 2003-05-20 | Fuji Photo Film Co., Ltd. | Negative-type image recording material and precursor for negative-type lithographic printing plate |
| RU2210798C2 (ru) * | 1997-08-22 | 2003-08-20 | Циба Спешиалти Кемикалз Холдинг Инк. | Композиция и способ ее отверждения |
| RU2253573C2 (ru) * | 1999-03-30 | 2005-06-10 | Миннесота Майнинг Энд Мэнюфекчуринг Компани | Маркировочное изделие (варианты) и способ его изготовления (варианты) |
| US20060032390A1 (en) * | 2004-07-30 | 2006-02-16 | Fuji Photo Film Co., Ltd. | Lithographic printing plate precursor and lithographic printing method |
| EP1627732A1 (en) * | 2004-08-18 | 2006-02-22 | Fuji Photo Film Co., Ltd. | Planographic printing plate precursor |
Family Cites Families (58)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2929710A (en) * | 1954-10-08 | 1960-03-22 | Du Pont | Polyvinyl acetal with terminal vinylidene groups |
| US3043805A (en) * | 1958-08-05 | 1962-07-10 | Du Pont | Polymeric amides and their preparation |
| US3418295A (en) * | 1965-04-27 | 1968-12-24 | Du Pont | Polymers and their preparation |
| US3448089A (en) * | 1966-03-14 | 1969-06-03 | Du Pont | Photopolymerizable polymers containing free acid or acid anhydride groups reacted with glycidyl acrylate or glycidyl methacrylate |
| US3885964A (en) * | 1974-05-31 | 1975-05-27 | Du Pont | Photoimaging process using nitroso dimer |
| LU76471A1 (ru) * | 1976-12-24 | 1978-07-10 | ||
| US4345017A (en) | 1980-10-06 | 1982-08-17 | Polaroid Corporation | Photographic products and processes with a pH sensitive xanthene light screening dye |
| DE3144905A1 (de) * | 1981-11-12 | 1983-05-19 | Basf Ag, 6700 Ludwigshafen | Zur herstellung von druck- und reliefformen geeignetes lichtempfindliches auszeichnungsmaterial und verfahren zur herstellung von druck- und reliefformen mittels dieses aufzeichnungsmaterials |
| US4701402A (en) * | 1984-02-13 | 1987-10-20 | Minnesota Mining And Manufacturing Company | Oxidative imaging |
| US4656229A (en) | 1985-12-02 | 1987-04-07 | National Starch And Chemical Corporation | Anaerobic adhesive compositions |
| DE69411242T2 (de) * | 1993-04-20 | 1999-03-25 | Asahi Chemical Ind | Lithographische druckplatte sowie verfahren zu ihrer herstellung |
| WO1996018133A1 (en) | 1994-12-06 | 1996-06-13 | Napp Systems, Inc. | High-resolution letterpress printing plates and water-soluble photopolymerizable compositions comprising a polyvinylalcohol derivative useful therefor |
| ATE177583T1 (de) | 1995-09-02 | 1999-03-15 | New Transducers Ltd | Schwingungswandler |
| EP0770495B1 (en) | 1995-10-24 | 2002-06-19 | Agfa-Gevaert | A method for making a lithographic printing plate involving on press development |
| CA2187046A1 (fr) * | 1996-10-03 | 1998-04-03 | Alain Vallee | Sulfonylimidures et sulfonylmethylures, leur utilisation comme photoinitiateur |
| US6008813A (en) | 1997-08-01 | 1999-12-28 | Mitsubishi Electric Information Technology Center America, Inc. (Ita) | Real-time PC based volume rendering system |
| US6261740B1 (en) * | 1997-09-02 | 2001-07-17 | Kodak Polychrome Graphics, Llc | Processless, laser imageable lithographic printing plate |
| JP3770436B2 (ja) * | 1997-12-15 | 2006-04-26 | 富士写真フイルム株式会社 | 光重合性組成物 |
| DE69936995T2 (de) * | 1998-03-20 | 2008-05-21 | Nippon Soda Co. Ltd. | Photohärtbare zusammensetzung welche ein iodoniumsalz enthält |
| JP2000119306A (ja) | 1998-03-20 | 2000-04-25 | Nippon Soda Co Ltd | ヨ―ドニウム塩化合物を含有する光硬化性組成物 |
| DE19824546A1 (de) * | 1998-06-03 | 1999-12-09 | Basf Drucksysteme Gmbh | Herstellung vernetzbarer wasserlöslicher oder wasserdispergierbarer Zusammensetzungen und daraus erhältlicher strahlungsempfindlicher Gemische |
| US6884562B1 (en) * | 1998-10-27 | 2005-04-26 | E. I. Du Pont De Nemours And Company | Photoresists and processes for microlithography |
| US6687402B1 (en) | 1998-12-18 | 2004-02-03 | Cognex Corporation | Machine vision methods and systems for boundary feature comparison of patterns and images |
| EP1035105A1 (de) * | 1999-03-11 | 2000-09-13 | Goldschmidt AG | Estergruppen enthaltende Iodoniumsalze und ihre Verwendung zur Strahlenhärtung kationisch härtender Massen |
| US6124425A (en) | 1999-03-18 | 2000-09-26 | American Dye Source, Inc. | Thermally reactive near infrared absorption polymer coatings, method of preparing and methods of use |
| US6255033B1 (en) | 1999-07-30 | 2001-07-03 | Creo, Ltd. | Positive acting photoresist compositions and imageable element |
| AU5649400A (en) * | 1999-09-21 | 2001-10-11 | Goldschmidt Ag | Photoinitiators containing urethane groups for cationic curing |
| US20020015826A1 (en) * | 2000-04-11 | 2002-02-07 | Darryl Desmarteau | Zwitterionic iodonium compounds and methods of application |
| JP2002069110A (ja) * | 2000-09-01 | 2002-03-08 | Fuji Photo Film Co Ltd | 光重合性組成物 |
| US6548222B2 (en) * | 2000-09-06 | 2003-04-15 | Gary Ganghui Teng | On-press developable thermosensitive lithographic printing plates |
| US6777155B2 (en) | 2000-10-03 | 2004-08-17 | Fuji Photo Film Co., Ltd. | Photosensitive lithographic printing plate |
| JP4102014B2 (ja) | 2000-10-03 | 2008-06-18 | 富士フイルム株式会社 | 感光性平版印刷版 |
| JP4253432B2 (ja) * | 2000-11-01 | 2009-04-15 | 富士フイルム株式会社 | 平版印刷版用原版 |
| JP2002207293A (ja) * | 2001-01-12 | 2002-07-26 | Fuji Photo Film Co Ltd | 平版印刷版原版 |
| US7049046B2 (en) * | 2004-03-30 | 2006-05-23 | Eastman Kodak Company | Infrared absorbing compounds and their use in imageable elements |
| US6899994B2 (en) * | 2001-04-04 | 2005-05-31 | Kodak Polychrome Graphics Llc | On-press developable IR sensitive printing plates using binder resins having polyethylene oxide segments |
| US6582882B2 (en) | 2001-04-04 | 2003-06-24 | Kodak Polychrome Graphics Llc | Imageable element comprising graft polymer |
| US6846614B2 (en) * | 2002-02-04 | 2005-01-25 | Kodak Polychrome Graphics Llc | On-press developable IR sensitive printing plates |
| JP2003248285A (ja) * | 2001-08-07 | 2003-09-05 | Konica Corp | 熱現像銀塩写真感光材料 |
| EP1336630A3 (en) * | 2002-02-15 | 2003-12-10 | Shipley Co. L.L.C. | Functionalized polymer |
| US7659046B2 (en) | 2002-04-10 | 2010-02-09 | Eastman Kodak Company | Water-developable infrared-sensitive printing plate |
| US6983694B2 (en) * | 2002-04-26 | 2006-01-10 | Agfa Gevaert | Negative-working thermal lithographic printing plate precursor comprising a smooth aluminum support |
| JP2004012706A (ja) * | 2002-06-05 | 2004-01-15 | Fuji Photo Film Co Ltd | 平版印刷版原版 |
| US6969575B2 (en) | 2002-08-29 | 2005-11-29 | Fuji Photo Film Co., Ltd. | On-press developable lithographic printing plate precursor |
| EP1442877B1 (en) * | 2003-01-29 | 2007-04-18 | FUJIFILM Corporation | Presensitized lithographic plate comprising microcapsules |
| JP4070637B2 (ja) * | 2003-03-05 | 2008-04-02 | 富士フイルム株式会社 | 重合性組成物、それに用いる化合物、それに用いた画像形成材料および感光性平版印刷版 |
| WO2004081662A2 (en) | 2003-03-14 | 2004-09-23 | Creo Inc. | Development enhancement of radiation-sensitive elements |
| US7368215B2 (en) * | 2003-05-12 | 2008-05-06 | Eastman Kodak Company | On-press developable IR sensitive printing plates containing an onium salt initiator system |
| DE102004029501A1 (de) * | 2004-06-18 | 2006-01-12 | Kodak Polychrome Graphics Gmbh | Modifizierte Polymere und ihre Verwendung bei der Herstellung von Lithographie-Druckplattenvorläufern |
| US7279263B2 (en) * | 2004-06-24 | 2007-10-09 | Kodak Graphic Communications Canada Company | Dual-wavelength positive-working radiation-sensitive elements |
| JP2006335826A (ja) | 2005-05-31 | 2006-12-14 | Fujifilm Holdings Corp | インクジェット記録用インク組成物およびこれを用いた平版印刷版の作製方法 |
| BRPI0611018B1 (pt) * | 2005-06-03 | 2017-03-07 | American Dye Source Inc | copolímeros de acetal de absorção próxima do infravermelho termicamente reativos, métodos de preparo e métodos de uso |
| JP5204371B2 (ja) | 2005-06-06 | 2013-06-05 | 富士フイルム株式会社 | インクジェット記録用インク組成物およびこれを用いた平版印刷版の作製方法 |
| JP5170960B2 (ja) | 2005-08-29 | 2013-03-27 | 富士フイルム株式会社 | 平版印刷版原版、及び平版印刷方法 |
| US7169518B1 (en) * | 2006-04-17 | 2007-01-30 | Eastman Kodak Company | Multilayer imageable element with improved chemical resistance |
| JP5254958B2 (ja) * | 2006-05-17 | 2013-08-07 | アメリカン・ダイ・ソース・インコーポレーテッド | 平版印刷版コーティング用新規材料、それを含有する平版印刷版およびコーティング、調製方法ならびに使用 |
| CN101269564B (zh) * | 2007-03-19 | 2012-02-15 | 成都新图印刷技术有限公司 | 热敏阴图平版印刷版的制备方法 |
| WO2021062463A1 (en) | 2019-09-30 | 2021-04-08 | Robert Bosch (Australia) Pty Ltd | Method and system for relay attack prevention incorporating channel coherence |
-
2007
- 2007-05-09 JP JP2009510242A patent/JP5254958B2/ja not_active Expired - Fee Related
- 2007-05-09 KR KR1020087030720A patent/KR101174949B1/ko active IP Right Grant
- 2007-05-09 ES ES07719744T patent/ES2530792T3/es active Active
- 2007-05-09 US US11/746,252 patent/US7910768B2/en not_active Expired - Fee Related
- 2007-05-09 CN CN200780005807.2A patent/CN101454277B/zh not_active Expired - Fee Related
- 2007-05-09 CA CA2652294A patent/CA2652294C/en not_active Expired - Fee Related
- 2007-05-09 WO PCT/CA2007/000820 patent/WO2007131336A1/en active Application Filing
- 2007-05-09 RU RU2008131537/05A patent/RU2443683C2/ru not_active IP Right Cessation
- 2007-05-09 BR BRPI0707574A patent/BRPI0707574B1/pt not_active IP Right Cessation
- 2007-05-09 EP EP07719744.0A patent/EP2018365B1/en not_active Not-in-force
- 2007-09-05 UA UAA200810363A patent/UA98450C2/ru unknown
-
2009
- 2009-01-30 HK HK09100896.6A patent/HK1121132A1/xx not_active IP Right Cessation
- 2009-10-15 US US12/579,881 patent/US8323867B2/en not_active Expired - Fee Related
- 2009-10-15 US US12/579,844 patent/US8021827B2/en not_active Expired - Fee Related
-
2011
- 2011-07-25 US US13/189,908 patent/US20120003584A1/en not_active Abandoned
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2210798C2 (ru) * | 1997-08-22 | 2003-08-20 | Циба Спешиалти Кемикалз Холдинг Инк. | Композиция и способ ее отверждения |
| RU2253573C2 (ru) * | 1999-03-30 | 2005-06-10 | Миннесота Майнинг Энд Мэнюфекчуринг Компани | Маркировочное изделие (варианты) и способ его изготовления (варианты) |
| US6566035B1 (en) * | 1999-10-29 | 2003-05-20 | Fuji Photo Film Co., Ltd. | Negative-type image recording material and precursor for negative-type lithographic printing plate |
| EP1204000A1 (en) * | 2000-11-06 | 2002-05-08 | Fuji Photo Film Co., Ltd. | Photosensitive lithographic printing plate |
| US20060032390A1 (en) * | 2004-07-30 | 2006-02-16 | Fuji Photo Film Co., Ltd. | Lithographic printing plate precursor and lithographic printing method |
| EP1627732A1 (en) * | 2004-08-18 | 2006-02-22 | Fuji Photo Film Co., Ltd. | Planographic printing plate precursor |
Also Published As
| Publication number | Publication date |
|---|---|
| US8323867B2 (en) | 2012-12-04 |
| US8021827B2 (en) | 2011-09-20 |
| EP2018365B1 (en) | 2014-11-19 |
| US20070269739A1 (en) | 2007-11-22 |
| UA98450C2 (ru) | 2012-05-25 |
| CN101454277B (zh) | 2014-02-19 |
| ES2530792T3 (es) | 2015-03-05 |
| BRPI0707574A2 (pt) | 2011-05-10 |
| RU2008131537A (ru) | 2010-02-10 |
| CA2652294A1 (en) | 2007-11-22 |
| EP2018365A1 (en) | 2009-01-28 |
| HK1121132A1 (en) | 2009-04-17 |
| US20100062370A1 (en) | 2010-03-11 |
| EP2018365A4 (en) | 2010-07-07 |
| WO2007131336A1 (en) | 2007-11-22 |
| US20100035183A1 (en) | 2010-02-11 |
| JP5254958B2 (ja) | 2013-08-07 |
| KR101174949B1 (ko) | 2012-08-17 |
| JP2009537458A (ja) | 2009-10-29 |
| US7910768B2 (en) | 2011-03-22 |
| CN101454277A (zh) | 2009-06-10 |
| CA2652294C (en) | 2012-07-10 |
| US20120003584A1 (en) | 2012-01-05 |
| BRPI0707574B1 (pt) | 2017-06-06 |
| KR20090016588A (ko) | 2009-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2443683C2 (ru) | Новые материалы для покрытий офсетных печатных форм, офсетные печатные формы и покрытия, содержащие эти материалы, способы получения и применение | |
| EP2054454B1 (en) | Reactive near infrared absorbing polymeric particles, methods of preparation and uses thereof | |
| EP2173827B1 (en) | Polymeric dyes, overcoat compositions and thermal lithographic printing plates | |
| KR101430576B1 (ko) | 평판 인쇄판 코팅 조성물용 갈로탄닉 화합물 | |
| CN104684735B (zh) | 平版印刷版原版以及平版印刷版的制版方法 | |
| JP5749269B2 (ja) | ネガ型輻射線感応性リソグラフィック印刷プレートのための輻射線感応性コーティング組成物用のコポリマー、前記コポリマーを含むポリマー粒子、及びコポリマーバインダー | |
| EP2566900B1 (en) | Copolymers for near-infrared radiation-sensitive coating compositions for positive-working thermal lithographic printing plates | |
| TWI401238B (zh) | 用於微影板塗覆物之新穎材料、包含其之微影板及塗覆物、製備及使用的方法 | |
| JP2011073215A (ja) | 平版印刷版原版及び平版印刷方法 | |
| WO2023136334A1 (ja) | 式(i)で表される化合物の製造方法 | |
| TWI447129B (zh) | 用於正片及熱感印刷版之近紅外線輻射敏感的塗料成分之共聚物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20190510 |