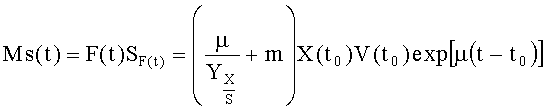RU2012105621A - Ферментация и очистка гепаросана к5 - Google Patents
Ферментация и очистка гепаросана к5 Download PDFInfo
- Publication number
- RU2012105621A RU2012105621A RU2012105621/10A RU2012105621A RU2012105621A RU 2012105621 A RU2012105621 A RU 2012105621A RU 2012105621/10 A RU2012105621/10 A RU 2012105621/10A RU 2012105621 A RU2012105621 A RU 2012105621A RU 2012105621 A RU2012105621 A RU 2012105621A
- Authority
- RU
- Russia
- Prior art keywords
- heparosan
- maintained
- cultivation
- feed
- elution
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/04—Polysaccharides, i.e. compounds containing more than five saccharide radicals attached to each other by glycosidic bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/006—Heteroglycans, i.e. polysaccharides having more than one sugar residue in the main chain in either alternating or less regular sequence; Gellans; Succinoglycans; Arabinogalactans; Tragacanth or gum tragacanth or traganth from Astragalus; Gum Karaya from Sterculia urens; Gum Ghatti from Anogeissus latifolia; Derivatives thereof
- C08B37/0063—Glycosaminoglycans or mucopolysaccharides, e.g. keratan sulfate; Derivatives thereof, e.g. fucoidan
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/0003—General processes for their isolation or fractionation, e.g. purification or extraction from biomass
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Sustainable Development (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
1. Способ получения по существу чистого гепаросана из E.coli К5, включающий:(а) культивирование клеток E.coli K5 в заданной среде, содержащей глюкозу в качестве основного источника углерода,(б) осуществление связывания гепаросана с твердофазным носителем с последующим элюированием и(в) осаждение гепаросана из элюата;при этом указанный по существу чистый гепаросан является по меньшей мере на 90% чистым.2. Способ по п.1, отличающийся тем, что культивирование включает фазу периодического культивирования и фазу периодического культивирования с подпиткой, при этом(а) среда, применяемая на стадии периодического культивирования, содержит (на литр) примерно 20 г глюкозы, 10-300 мг тиамина, примерно 13,5 г КНРО, примерно 4,0 г (NH)HPOпримерно 1,4 г MgSO·7HO, примерно 1,7 г лимонной кислоты, и примерно 10,0 мл раствора микроэлементов, при этом раствор микроэлементов по существу состоит из (на 1 л 5М HCl) 10,0 г FeSO·7HO, 2,0 г CaCl, 2,2 г ZnSO·7HO, 0,5 г MnSO·4HO, 1,0 г CuSO·5HO, 0,1 г (NH)MoO·4HO и 0,02 г NaBO·10HO и при этом;(б) среда для подпитки, применяемая на стадии периодического культивирования с подпиткой, содержит (на литр): 250-1000 г глюкозы, 20 г MgSO, 0,15-0,5 г тиамина, и возможно 47 г KHPOи(в) при этом снабжение кислородом осуществляют путем барботирования воздуха с дополнительной подачей или без дополнительной подачи кислорода.3. Способ по п.2, отличающийся тем, что содержание растворенного кислорода поддерживают на уровне примерно 20%.4. Способ по п.2, отличающийся тем, что температуру поддерживают на уровне примерно 37°С, а рН поддерживают на уровне примерно 7.5. Способ по п.4, отличающийся тем, что рН поддерживают путем добавления 29%-ным раствора аммиака.6. Способ по п.2, отличающийся тем, что среду, применяе�
Claims (18)
1. Способ получения по существу чистого гепаросана из E.coli К5, включающий:
(а) культивирование клеток E.coli K5 в заданной среде, содержащей глюкозу в качестве основного источника углерода,
(б) осуществление связывания гепаросана с твердофазным носителем с последующим элюированием и
(в) осаждение гепаросана из элюата;
при этом указанный по существу чистый гепаросан является по меньшей мере на 90% чистым.
2. Способ по п.1, отличающийся тем, что культивирование включает фазу периодического культивирования и фазу периодического культивирования с подпиткой, при этом
(а) среда, применяемая на стадии периодического культивирования, содержит (на литр) примерно 20 г глюкозы, 10-300 мг тиамина, примерно 13,5 г КН2РО4, примерно 4,0 г (NH4)2HPO4 примерно 1,4 г MgSO4·7H2O, примерно 1,7 г лимонной кислоты, и примерно 10,0 мл раствора микроэлементов, при этом раствор микроэлементов по существу состоит из (на 1 л 5М HCl) 10,0 г FeSO4·7H2O, 2,0 г CaCl2, 2,2 г ZnSO4·7H2O, 0,5 г MnSO4·4H2O, 1,0 г CuSO4·5H2O, 0,1 г (NH4)6Mo7O24·4H2O и 0,02 г Na2B4O7·10H2O и при этом;
(б) среда для подпитки, применяемая на стадии периодического культивирования с подпиткой, содержит (на литр): 250-1000 г глюкозы, 20 г MgSO4, 0,15-0,5 г тиамина, и возможно 47 г KH2PO4 и
(в) при этом снабжение кислородом осуществляют путем барботирования воздуха с дополнительной подачей или без дополнительной подачи кислорода.
3. Способ по п.2, отличающийся тем, что содержание растворенного кислорода поддерживают на уровне примерно 20%.
4. Способ по п.2, отличающийся тем, что температуру поддерживают на уровне примерно 37°С, а рН поддерживают на уровне примерно 7.
5. Способ по п.4, отличающийся тем, что рН поддерживают путем добавления 29%-ным раствора аммиака.
6. Способ по п.2, отличающийся тем, что среду, применяемую на стадии периодического культивирования с подпиткой, подают со скоростью, определяемой по формуле:
где MS представляет собой скорость потока источника углерода (г/ч), F - скорость подачи раствора для подпитки (л/ч); SF представляет собой концентрацию источника углерода в подпитке (г/л); Х - концентрация клеток (г/л с.м.к.), m - удельный коэффициент поддержания (г/г DCW/ч), V - объем культуры (л); t0 - время начала подпитки; t - время процесса; µ - удельная скорость роста (ч-1) и Yx/s - выход клеток па количество источника углерода (г/г).
7. Способ по п.2, отличающийся тем, что выход гепаросана составляет более 12 г/л супернатанта культуры.
8. Способ по п.7, отличающийся тем, что ферментацию проводят в течение менее 48 ч, без учета роста стартовой культуры.
9. Способ по п.1, отличающийся тем, что стадия осуществления связывания и элюирования включает (I) удаление клеток, (II) смешивание анионной смолы с супернатантом культуры и удаление супернатанта, (III) промывку смолы с помощью 50 мМ хлорида натрия в натрий-ацетатном буфере при рН 4, (IV) элюирование 1 М хлорида натрия в натрий-ацетатном буфере при рН 4.
10. Способ по п.1, отличающийся тем, что стадия осуществления связывания и элюирования включает (I) удаление клеток, (II) смешивание раствора хитозана с супернатантом культуры, (III) осаждение хитозана и выделение осадка; (III) промывку хитозана. (IV) элюирование гепаросаиа с помощью примерно 1 М раствора NaOH.
11. Способ по п.1, отличающийся тем, что осаждение гепаросана из элюата включает осаждение с помощью этанола.
12. Способ по п.1, дополнительно включающий депирогенизацию с помощью перекиси водорода.
13. Способ по п.1, отличающийся тем, что указанный гепаросан содержит менее 1% ДНК и менее 2% белка.
14. Способ по п.1, отличающийся тем, что указанный гепаросан имеет среднечисленный молекулярный вес примерно 58000 Да, средневесовой молекулярный вес 84000 Да и индекс полидисперсности (ИПД) примерно 1,4.
15. Способ по п.1, отличающийся тем, что указанный гепаросан является по меньшей мере на 95% чистым.
16. Гепаросан, полученный с помощью способа по любому из пп.1-15.
17. Гепарин, изготовленный из гепаросана по п.16.
18. Применение гепаросана, полученного с помощью способа по любому из пп.1-15.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US27567509P | 2009-09-01 | 2009-09-01 | |
| US61/275,675 | 2009-09-01 | ||
| PCT/US2010/047183 WO2011028668A2 (en) | 2009-09-01 | 2010-08-30 | K5 heparosan fermentation and purification |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2012105621A true RU2012105621A (ru) | 2013-10-10 |
| RU2564566C2 RU2564566C2 (ru) | 2015-10-10 |
Family
ID=43649920
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012105621/10A RU2564566C2 (ru) | 2009-09-01 | 2010-08-30 | Ферментация и очистка гепаросана к5 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US8883452B2 (ru) |
| EP (1) | EP2473614A4 (ru) |
| JP (1) | JP5830464B2 (ru) |
| KR (1) | KR101515892B1 (ru) |
| CN (1) | CN102712942B (ru) |
| BR (1) | BR112012008053B8 (ru) |
| MY (1) | MY163367A (ru) |
| RU (1) | RU2564566C2 (ru) |
| SG (1) | SG178349A1 (ru) |
| TW (1) | TWI485251B (ru) |
| WO (1) | WO2011028668A2 (ru) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2898515C (en) * | 2013-01-25 | 2022-01-04 | Marinova Pty Ltd | Methods for depyrogentating a seaweed extract |
| CN103149198B (zh) * | 2013-02-08 | 2015-04-22 | 浙江工业大学 | 一种酶法快速定量检测heparosan的方法 |
| EP3620525A1 (en) | 2013-10-02 | 2020-03-11 | Ajinomoto Co., Inc. | Heparosan-producing bacterium and heparosan manufacturing method |
| CN105602980B (zh) * | 2016-01-25 | 2019-02-01 | 浙江工业大学 | 一种waaR基因缺陷型细菌合成低分子量肝素前体的方法 |
| CN108624516B (zh) * | 2017-03-20 | 2022-08-26 | 华东理工大学 | 一种提高发酵细胞中的代谢产物量及制备idms标准品的方法 |
| WO2021199444A1 (en) * | 2020-04-03 | 2021-10-07 | Rensselaer Polytechnic Institute | Method for producing heparosan and bacterium of genus escherichia having heparosan-producing ability |
| EP4067500A1 (en) * | 2021-04-01 | 2022-10-05 | Givaudan SA | Heparosan-producing recombinant cells |
| CN112791186A (zh) * | 2021-04-14 | 2021-05-14 | 江苏艾洛特医药研究院有限公司 | 一种多糖纳米复合材料及其制备与应用 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2669932B1 (fr) * | 1990-12-03 | 1994-07-01 | Sanofi Sa | Nouvel heparosane-n,o-sulfate, son procede de preparation et les compositions pharmaceutiques qui le contiennent. |
| FR2684385B1 (fr) * | 1991-11-28 | 1997-08-01 | Sanofi Elf | Heparosanes-n,o-sulfates de haute masse moleculaire, leur procede de preparation et les compositions pharmaceutiques qui les contiennent. |
| US20060188966A1 (en) * | 1998-04-02 | 2006-08-24 | Deangelis Paul L | Natural, chimeric and hybrid glycosaminoglycan polymers and methods of making and using same |
| ITMI991465A1 (it) * | 1999-07-02 | 2001-01-02 | Inalco Spa | Processo per la preparazione dei polisaccaridi k4 e k5 da escherichiacoli |
| JP4084099B2 (ja) * | 2002-06-20 | 2008-04-30 | 生化学工業株式会社 | N−アセチルヘパロサン画分の製造方法 |
| AU2003293122A1 (en) * | 2002-11-27 | 2004-06-23 | Massachusetts Institute Of Technology | Methods for synthesizing polysaccharides |
| ITMI20031618A1 (it) * | 2003-08-06 | 2005-02-07 | Inalco Spa | Derivati polisaccaridici dotati di alta attivita' |
| JP4505631B2 (ja) * | 2004-03-31 | 2010-07-21 | 独立行政法人産業技術総合研究所 | ヘパラン硫酸糖鎖を付加したヘパリン結合性タンパク質、その製造方法及びそれを含有する医薬組成物 |
| JP2005290383A (ja) * | 2004-04-05 | 2005-10-20 | Seikagaku Kogyo Co Ltd | 6−o−硫酸化n−アセチルヘパロサン及び造血幹細胞増殖助剤 |
| FR2874931B1 (fr) * | 2004-09-08 | 2006-11-24 | Aventis Pharma Sa | Procede de production de polysaccharide k5 |
| JP2007252396A (ja) * | 2006-03-20 | 2007-10-04 | Kitasato Gakuen | 医療用透析液の製造装置および製造方法 |
| EP2173360B1 (en) | 2007-03-30 | 2014-11-19 | The Board of Regents for the University of Oklahoma | Heparosan-based biomaterials and coatings and methods of production and use thereof |
| DE102007016707A1 (de) * | 2007-04-04 | 2008-10-09 | Qiagen Gmbh | Verfahren zur Aufreinigung von Biomolekülen |
-
2010
- 2010-08-30 US US13/261,193 patent/US8883452B2/en active Active
- 2010-08-30 JP JP2012527074A patent/JP5830464B2/ja active Active
- 2010-08-30 KR KR1020127004862A patent/KR101515892B1/ko active IP Right Review Request
- 2010-08-30 EP EP10814338.9A patent/EP2473614A4/en not_active Withdrawn
- 2010-08-30 SG SG2012009262A patent/SG178349A1/en unknown
- 2010-08-30 WO PCT/US2010/047183 patent/WO2011028668A2/en active Application Filing
- 2010-08-30 BR BR112012008053A patent/BR112012008053B8/pt active IP Right Grant
- 2010-08-30 CN CN201080038931.0A patent/CN102712942B/zh active Active
- 2010-08-30 RU RU2012105621/10A patent/RU2564566C2/ru active
- 2010-08-30 MY MYPI2012000910A patent/MY163367A/en unknown
- 2010-08-31 TW TW099129401A patent/TWI485251B/zh active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2013503606A (ja) | 2013-02-04 |
| RU2564566C2 (ru) | 2015-10-10 |
| EP2473614A4 (en) | 2013-04-24 |
| EP2473614A2 (en) | 2012-07-11 |
| BR112012008053B1 (pt) | 2021-04-20 |
| BR112012008053A2 (pt) | 2017-06-13 |
| US20120157669A1 (en) | 2012-06-21 |
| KR20120090948A (ko) | 2012-08-17 |
| WO2011028668A4 (en) | 2011-09-09 |
| CN102712942A (zh) | 2012-10-03 |
| BR112012008053B8 (pt) | 2022-02-15 |
| JP5830464B2 (ja) | 2015-12-09 |
| WO2011028668A2 (en) | 2011-03-10 |
| TWI485251B (zh) | 2015-05-21 |
| TW201114900A (en) | 2011-05-01 |
| US8883452B2 (en) | 2014-11-11 |
| CN102712942B (zh) | 2014-05-14 |
| WO2011028668A3 (en) | 2011-07-28 |
| KR101515892B1 (ko) | 2015-05-04 |
| MY163367A (en) | 2017-09-15 |
| SG178349A1 (en) | 2012-03-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2012105621A (ru) | Ферментация и очистка гепаросана к5 | |
| US7432091B2 (en) | Highly efficient hydrogen production method using microorganism | |
| Chen et al. | Heterotrophic growth of Chlamydomonas reinhardtii on acetate in chemostat culture | |
| KR102015829B1 (ko) | 온라인 산소 소비율과 전도율의 통합 제어를 기반으로 한 코엔자임 q10 발효 생산 공정 | |
| EP0077014A2 (en) | Process for producing hydrogen by alga in alternating light/dark cycle | |
| CN1298861C (zh) | 用氢代谢甲烷细菌生产维生素b12的方法 | |
| CN105385713A (zh) | 一种菌体循环利用的葡萄糖酸钠发酵方法 | |
| CN114231450A (zh) | 一种粘着箭菌及其制备方法和在生产维生素b12中的应用 | |
| CN102268402A (zh) | 无血清培养基及cho细胞中高效表达促红素的培养方法 | |
| JPH08508875A (ja) | 蛋白分泌細胞の流加回分培養法 | |
| CN102181502A (zh) | 一种提高发酵生产l-苏氨酸产率的方法 | |
| NZ512962A (en) | Production of exopolysaccharides unattached to the surface of bacterial cells from Sphingomonas bacteria | |
| CN116179356B (zh) | 高密度异养培养莱茵衣藻的方法及其应用 | |
| CN102653775A (zh) | 一种尿液资源化和能源化的处理方法 | |
| AU775301B2 (en) | Method for increasing the yield of recombinant proteins in microbial fermentation processes | |
| CN100355898C (zh) | 一种海洋绿藻两步法生物光解水制氢方法 | |
| JP3224992B2 (ja) | 水素生産光合成微生物及びこれを用いた水素の生産方法 | |
| JPS5860992A (ja) | 緑藻による明暗サイクル利用水素生産方法 | |
| JP2677602B2 (ja) | 継代シード培養によるl−ソルボースの製造法およびそれに用いる装置 | |
| JPS6262156B2 (ru) | ||
| KR900007000B1 (ko) | 칸디다 유틸리스의 변이주 sh 8636 및 이를 이용한 단세포단백질의 제조방법 | |
| CN101555504B (zh) | 一种利用短小芽孢杆菌转酮醇酶变异株发酵生产d-核糖的方法 | |
| SU1017733A1 (ru) | Способ производства лимонной кислоты | |
| CN117757878A (zh) | 雨生红球藻发酵产虾青素方法 | |
| KR960004038B1 (ko) | 고정화균체 및 이의 제조방법 |