KR20140136488A - 뇌 유래 신경영양 인자(bdnf)에 대한 천연 안티센스 전사체의 저해에 의한 뇌 유래 신경영양 인자(bdnf)관련 질환의 치료 - Google Patents
뇌 유래 신경영양 인자(bdnf)에 대한 천연 안티센스 전사체의 저해에 의한 뇌 유래 신경영양 인자(bdnf)관련 질환의 치료 Download PDFInfo
- Publication number
- KR20140136488A KR20140136488A KR1020147028058A KR20147028058A KR20140136488A KR 20140136488 A KR20140136488 A KR 20140136488A KR 1020147028058 A KR1020147028058 A KR 1020147028058A KR 20147028058 A KR20147028058 A KR 20147028058A KR 20140136488 A KR20140136488 A KR 20140136488A
- Authority
- KR
- South Korea
- Prior art keywords
- bdnf
- seq
- oligonucleotide
- antisense
- oligonucleotides
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/02—Muscle relaxants, e.g. for tetanus or cramps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/32—Alcohol-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1136—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against growth factors, growth regulators, cytokines, lymphokines or hormones
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
- C12N2310/113—Antisense targeting other non-coding nucleic acids, e.g. antagomirs
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/321—2'-O-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3231—Chemical structure of the sugar modified ring structure having an additional ring, e.g. LNA, ENA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/341—Gapmers, i.e. of the type ===---===
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/352—Nature of the modification linked to the nucleic acid via a carbon atom
- C12N2310/3521—Methyl
Abstract
본 발명은 특히, 뇌 유래 신경영양 인자(BDNF)의 천연 안티센스 폴리뉴클레오티드를 표적으로 함으로써, 뇌 유래 신경영양 인자(BDNF)의 발현 및/또는 기능을 조정하는 안티센스 올리고뉴클레오티드에 관한 것이다. 본 발명은 또한 이들 안티센스 올리고뉴클레오티드의 확인 및 BDNF의 발현과 관련된 질환 및 장애를 치료하는데 있어서 이들의 용도에 관한 것이다.
Description
교차 참조
본 출원은 2012년 3월 15일자로 출원된 미국 가특허 출원 제61/611,225호; 및 2012년 3월 23일자로 출원된 미국 가특허 출원 제61/614,664호에 대한 우선권을 주장하고, 상기 출원은 그 전문이 본원에 참고로 포함된다.
기술분야
본 발명의 양태는 뇌 유래 신경영양 인자(BDNF: brain derived neurotrophic factor) 및 연관된 분자의 발현 및/또는 기능을 조정하는 올리고뉴클레오티드를 포함한다.
DNA-RNA 및 RNA-RNA 하이브리드화는 DNA 복제, 전사 및 번역을 포함한 핵산 기능의 많은 측면에 중요하다. 하이브리드화는 또한 특정한 핵산을 검출하거나 이의 발현을 변경시키는 다양한 기술에 중심적이다. 안티센스 뉴클레오티드는, 예를 들면, 표적 RNA에 하이브리드화되어 RNA 스플라이싱, 전사, 번역, 및 복제를 간섭함으로써 유전자 발현을 교란시킨다. 안티센스 DNA는 DNA-RNA 하이브리드가 대부분의 세포 유형에서 존재하는 활성인 리보뉴클라제 H에 의한 절단을 위한 기질로서 역할을 하는 부가된 특징을 갖는다. 안티센스 분자는 올리고데옥시뉴클레오티드(ODN: oligodeoxynucleotide)의 경우에서처럼 세포 내로 전달될 수 있거나, 이들은 내생성 유전자로부터 RNA 분자로서 발현될 수 있다. FDA는 최근에 안티센스 약물, VITRAVENE™(거대세포바이러스 망막염의 치료용)를 승인하였는데, 이는 안티센스가 치료적 유용성을 갖는다는 것을 반영한다.
WO 제2010/093904호 및 이의 미국 대응출원 제US/2011/0319475호에는 그 안에 기재된 올리고뉴클레오티드를 사용하여 조정하기 위한 표적으로서 BDNF가 기재되어 있다. 천연 안티센스 표적 및 이러한 표적을 보완하고 BDNF 단백질 발현을 조정하여 잠재적으로 BDNF 관련 질환 및 질병을 치료하거나 이와 관련된 연구에서 사용되는 신규하게 개발된 올리고뉴클레오티드에 대한 계속적인 개발에 대한 필요성이 존재한다.
개요
본 요약은 본 발명의 특성 및 요점을 간략하게 나타내는 본 발명의 개요를 제시하기 위하여 제공된다. 이는 특허청구범위의 범위 또는 의미를 해석하거나 제한하는데 사용되지 않는 것으로 이해될 것이다.
하나의 양태에서, 본 발명은 포유동물 유기체에서 상응하는 BDNF 센스 유전자의 상향-조절을 유발하는 천연 안티센스 전사체의 임의의 영역에 표적화된 안티센스 올리고뉴클레오티드(들)를 사용함으로써 천연 안티센스 전사체의 작용을 저해하는 방법을 제공한다. 또한, 본원에 기재된 천연 안티센스 전사체의 저해는 siRNA, 리보자임 및 소분자에 의해 달성될 수 있을 것으로 본원에서 기대되고, 이는 본 발명의 범위 내에 있는 것으로 간주된다.
하나의 양태는 생체내에서 또는 시험관내에서 환자 세포 또는 조직을 포함하지만 이에 한정되지 않는 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법을 제공하고, 상기 방법은 상기 생물학적 시스템 또는 상기 세포 또는 조직을 약 5 내지 약 30개 뉴클레오티드 길이의 안티센스 올리고뉴클레오티드와 접촉시키고, 여기서 상기 올리고뉴클레오티드는 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에 5 내지 30개의 연속 뉴클레오티드를 포함하는 폴리뉴클레오티드의 역 상보체에 50% 이상의 서열 동일성을 갖고; 이로써 생체내에서 또는 시험관내에서 상기 환자 세포 또는 조직을 포함하는 상기 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하고, 단 서열 번호 50-55을 갖는 올리고뉴클레오티드는 제외된다.
하나의 양태에서, 상기 기재된 올리고뉴클레오티드는 생물학적 시스템에 존재하는 BDNF 폴리뉴클레오티드의 천연 안티센스 서열, 예를 들면, 서열 번호 3 내지 11에 기재된 뉴클레오티드, 및 이들의 임의의 변이체, 대립유전자, 동족체, 돌연변이체, 유도체, 단편 및 상보성 서열을 표적으로 한다. 이러한 안티센스 올리고뉴클레오티드의 예는 서열 번호 12 내지 49에 제시된다.
또 다른 양태에서, 본 발명은 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 또는 발현을 조정하는 방법을 포함하고, 상기 방법은 상기 생물학적 시스템을 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개의 연속 뉴클레오티드를 포함하는 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체를 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시키고, 이로써 상기 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함한다.
또 다른 양태에서, 본 발명은 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 또는 발현을 조정하는 방법을 포함하고, 상기 방법은 상기 생물학적 시스템을 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개의 연속 뉴클레오티드를 포함하는 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체의 영역을 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시키고, 이로써 상기 생물학적 시스템에서 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함한다.
하나의 양태에서, 본 발명은 생물학적 시스템에서 서열 번호 1 및 2를 갖는 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 증가시키는 방법을 포함하고, 상기 방법은 상기 생물학적 시스템을 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개의 연속 뉴클레오티드를 포함하는 상기 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체를 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시키고, 이로써 BDNF 폴리뉴클레오티드의 기능 및/또는 발현 또는 이의 발현 산물을 증가시키는 것을 포함한다.
또 다른 양태에서, 본 발명은 생물학적 시스템에서 서열 번호 1 및 2를 갖는 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 증가시키는 방법을 포함하고, 상기 방법은 상기 생물학적 시스템을 상기 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체를 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시키고, 이로써 상기 BDNF 폴리뉴클레오티드의 기능 및/또는 발현 또는 이의 발현 산물의 증가시키는 것을 포함하고, 여기서 천연 안티센스 전사체는 서열 번호 3 내지 11로부터 선택된다.
또 다른 양태에서, 본 발명은 생물학적 시스템에서 서열 번호 1 및 2를 갖는 BDNF 폴리뉴클레오티드의 기능 및/또는 발현을 증가시키는 방법을 포함하고, 상기 방법은 상기 생물학적 시스템을 상기 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체를 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시키고, 이로써 상기 BDNF 폴리뉴클레오티드의 기능 및/또는 발현 또는 이의 발현 산물을 증가시키는 것을 포함하고, 여기서 천연 안티센스 전사체는 서열 번호 3 내지 11로부터 선택되고, 안티센스 올리고뉴클레오티드는 서열 번호 12 내지 49 중 하나 이상으로부터 선택된다.
하나의 양태에서, 조성물을 센스 및/또는 안티센스 BDNF 폴리뉴클레오티드에 결합하는 하나 이상의 안티센스 올리고뉴클레오티드를 포함한다.
하나의 양태에서, 올리고뉴클레오티드는 하나 이상의 변형된 또는 치환된 뉴클레오티드를 포함한다.
하나의 양태에서, 올리고뉴클레오티드는 하나 이상의 변형된 결합을 포함한다.
또 다른 양태에서, 변형된 뉴클레오티드는 포스포로티오에이트, 메틸포스포네이트, 펩티드 핵산, 2'-O-메틸, 플루오로- 또는 탄소, 메틸렌 또는 다른 잠금 핵산(LNA: locked nucleic acid) 분자를 포함하는 변형된 염기를 포함한다. 바람직하게는, 변형된 뉴클레오티드는 α-L-LNA을 포함하는 잠금 핵산 분자이다.
하나의 양태에서, 올리고뉴클레오티드는 환자에게 피하, 근육내, 정맥내 또는 복강내 투여된다.
하나의 양태에서, 올리고뉴클레오티드는 약제학적 조성물로 투여된다. 치료 요법은 안티센스 화합물을 환자에게 1회 이상 투여하는 것을 포함하고; 하지만, 이러한 치료는 일정한 기간 동안 복수 투약을 포함하도록 변형될 수 있다. 치료는 한 가지 이상의 다른 유형의 치료법과 조합될 수 있다.
하나의 양태에서, 올리고뉴클레오티드는 리포좀 내에 캡슐화되거나, 담체 분자(예를 들면, 콜레스테롤, TAT 펩티드)에 부착된다.
하나의 양태에서, 본 발명은 BDNF 폴리뉴클레오티드의 발현을 조정하는 천연 안티센스 전사체(NAT: natural antisense transcript)를 표적으로 하는 올리고뉴클레오티드로서 서열 번호 50-55의 용도를 포함하고, 여기서 상기 NAT는 서열 번호 3 내지 11로 이루어진 군으로부터 선택된다. 또 다른 양태에서, 본 발명은 BDNF 폴리뉴클레오티드의 발현을 조정하는 천연 안티센스 전사체(NAT)를 표적으로 하는 올리고뉴클레오티드로서 서열 번호 50-55의 용도를 포함하고, 여기서 상기 NAT는 서열 번호 3, 4, 5, 7, 8, 9, 10 및 11로 이루어진 군으로부터 선택된다.
다른 측면은 하기 기술된다.
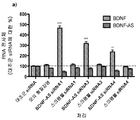
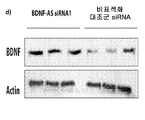
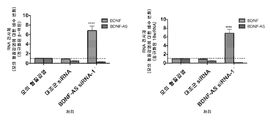
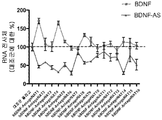
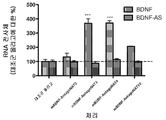
도 1a-e은 센스 mRNA 및 단백질의 안티센스-매개된 조절을 도시한다. 도 1a는 BDNF-AS 전사체의 비-중복 영역을 표적으로 하는 3개의 siRNA 올리고뉴클레오티드로 몇몇 인간 및 마우스 세포주의 형질감염 후, BDNF 전사체의 녹다운(knockdown) 및 상향조절이 발생함을 보여주는 것이다. 도 1b는 BDNF 및 BDNF-AS 전사체 둘 다의 내생성 발현에서 BDNF-AS-표적화된 siRNA의 투여 후, 시간 경과 연구 데이타를 보여주는 것이다. 데이타는 시간이 경과함에 따라 BDNF-AS가 하향조절되고, 그 후 BDNF 발현이 상향조절되고 가역적임을 보여주는 것이다. 도 1c는 ELISA에 의해 측정된 BDNF 단백질이 BDNF-AS 전사체에 표적화된 2개의 siRNA에 의해서는 뚜렷하게 증가하지만, 스크램블된 siRNA 또는 대조군 비표적화 siRNA에 의해서는 그렇지 않음을 보여주는 것이다. 도 1d는 다양한 siRNA의 투여 후, ELISA 및/또는 웨스턴 블롯(Western blot)을 사용한 BDNF의 단백질 수준을 보여주는 것이다. 도 1e는 모의 대조군에 대한 BDNF의 배수적 변화 백분율 대 올리고뉴클레오티드의 증가하는 농도(10-12 내지 10-6 M)를 보여주는 것이다.
도 2는 Bdnf 상향조절이 뉴런의 성장을 증가시킴을 보여주는 것이다.
도 3은 Bdnf-AS가 생체내에서 Bdnf mRNA 및 단백질을 조절함을 보여주는 것이다.
도 4는 생체내에서 Bdnf-AS의 차단이 뉴런 생존 및 증식의 증가를 유발함을 보여주는 것이다.
도 5는 BDNF-AS 녹다운이 BDNF mRNA 상향조절을 야기함을 보여주는 것이다.
도 6은 Bdnf 발현의 전사후 조절을 보여주는 것이다.
도 7은 hBDNFAntagoNAT에 의한 인간 BDNF-AS 전사체의 저해를 보여주는 것이다.
도 8은 AntagoNAT에 의한 N2a 세포에서 마우스 Bdnf-AS 전사체의 저해를 보여주는 것이다.
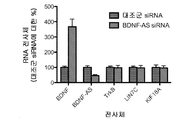
도 9는 BDNF-AS 녹다운이 TrkB 또는 BDNF 이웃 유전자(Let7C 및 KIF18A)의 수준을 두 방향 어느 쪽으로도 변화시키기 않음을 보여주는 것이다: LIN7C 및 KIF18A는 각각 BDNF의 3' 하류(downstream) 및 5' 상류(upstream)에 위치한 유전자이다.
서열 목록 설명: 서열 번호 1: 호모 사피엔스(Homo sapiens) 뇌 유래 신경영양 인자(BDNF), 전사체 변이체 3, mRNA(NCBI 수탁 번호: NM_170735); 서열 번호 2: 무스 무스쿨루스(Mus musculus) 뇌 유래 신경영양 인자(Bdnf), 전사체 변이체 1, mRNA(NCBI 수탁 번호: NM_007540); 서열 번호 3: 천연 BDNF 안티센스 서열(전사체 변이체 BT1A; NR_033313.1); 서열 번호 4: 천연 BDNF 안티센스 서열(전사체 변이체 BT2A; NR_033314.1); 서열 번호 5: 천연 BDNF 안티센스 서열(전사체 변이체 BT1B; NR_033315.1); 서열 번호 6: 천연 BDNF 안티센스 서열(전사체 변이체 BT2B; NR_002832.2); 서열 번호 7: 천연 BDNF 안티센스 서열(전사체 변이체 BT1C; NR_033312.1); 서열 번호 8: 천연 BDNF 안티센스 서열(BDNF-AS 변이체); 서열 번호 9: 천연 BDNF 안티센스 서열; 서열 번호 10: 마우스 천연 BDNF 안티센스 서열(마우스 BDNF-AS 변이체 1); 서열 번호 11: 마우스 천연 BDNF 안티센스 서열(마우스 BDNF-AS 변이체 2); 서열 번호 12 내지 55: 안티센스 올리고뉴클레오티드; 서열 번호 56 내지 59: 각각 안티센스 올리고뉴클레오티드 12 내지 15의 역 상보체; 서열 번호 60 내지 64: 각각 안티센스 올리고뉴클레오티드 42 내지 46의 역 상보체; 서열 번호 65 및 66: 분석 서열. LNA(2'-O, 4'-C 메틸렌 잠금 핵산): +A* 또는 +T* 또는 +C* 또는 +G*; 2'OM(2'-O-메틸): mU* 또는 mA* 또는 mC* 또는 mG*; PS(포스포티오에이트): T* 또는 A* 또는 G* 또는 c*; RNA: rU 또는 rA 또는 rG 또는 rC.
도 2는 Bdnf 상향조절이 뉴런의 성장을 증가시킴을 보여주는 것이다.
도 3은 Bdnf-AS가 생체내에서 Bdnf mRNA 및 단백질을 조절함을 보여주는 것이다.
도 4는 생체내에서 Bdnf-AS의 차단이 뉴런 생존 및 증식의 증가를 유발함을 보여주는 것이다.
도 5는 BDNF-AS 녹다운이 BDNF mRNA 상향조절을 야기함을 보여주는 것이다.
도 6은 Bdnf 발현의 전사후 조절을 보여주는 것이다.
도 7은 hBDNFAntagoNAT에 의한 인간 BDNF-AS 전사체의 저해를 보여주는 것이다.
도 8은 AntagoNAT에 의한 N2a 세포에서 마우스 Bdnf-AS 전사체의 저해를 보여주는 것이다.
도 9는 BDNF-AS 녹다운이 TrkB 또는 BDNF 이웃 유전자(Let7C 및 KIF18A)의 수준을 두 방향 어느 쪽으로도 변화시키기 않음을 보여주는 것이다: LIN7C 및 KIF18A는 각각 BDNF의 3' 하류(downstream) 및 5' 상류(upstream)에 위치한 유전자이다.
서열 목록 설명: 서열 번호 1: 호모 사피엔스(Homo sapiens) 뇌 유래 신경영양 인자(BDNF), 전사체 변이체 3, mRNA(NCBI 수탁 번호: NM_170735); 서열 번호 2: 무스 무스쿨루스(Mus musculus) 뇌 유래 신경영양 인자(Bdnf), 전사체 변이체 1, mRNA(NCBI 수탁 번호: NM_007540); 서열 번호 3: 천연 BDNF 안티센스 서열(전사체 변이체 BT1A; NR_033313.1); 서열 번호 4: 천연 BDNF 안티센스 서열(전사체 변이체 BT2A; NR_033314.1); 서열 번호 5: 천연 BDNF 안티센스 서열(전사체 변이체 BT1B; NR_033315.1); 서열 번호 6: 천연 BDNF 안티센스 서열(전사체 변이체 BT2B; NR_002832.2); 서열 번호 7: 천연 BDNF 안티센스 서열(전사체 변이체 BT1C; NR_033312.1); 서열 번호 8: 천연 BDNF 안티센스 서열(BDNF-AS 변이체); 서열 번호 9: 천연 BDNF 안티센스 서열; 서열 번호 10: 마우스 천연 BDNF 안티센스 서열(마우스 BDNF-AS 변이체 1); 서열 번호 11: 마우스 천연 BDNF 안티센스 서열(마우스 BDNF-AS 변이체 2); 서열 번호 12 내지 55: 안티센스 올리고뉴클레오티드; 서열 번호 56 내지 59: 각각 안티센스 올리고뉴클레오티드 12 내지 15의 역 상보체; 서열 번호 60 내지 64: 각각 안티센스 올리고뉴클레오티드 42 내지 46의 역 상보체; 서열 번호 65 및 66: 분석 서열. LNA(2'-O, 4'-C 메틸렌 잠금 핵산): +A* 또는 +T* 또는 +C* 또는 +G*; 2'OM(2'-O-메틸): mU* 또는 mA* 또는 mC* 또는 mG*; PS(포스포티오에이트): T* 또는 A* 또는 G* 또는 c*; RNA: rU 또는 rA 또는 rG 또는 rC.
상세한 설명
본 발명의 일부 측면은 예시를 위한 실례 적용과 관련하여 하기에 기재된다. 다수의 특정한 세부사항, 상관관계 및 방법은 본 발명의 완전한 이해를 제공하기 위하여 기술되는 것으로 이해되어야 한다. 그러나, 당업자는 본 발명이 하나 이상의 특정한 세부사항 없이 또는 다른 방법으로 실시될 수 있음을 용이하게 인지할 것이다. 일부 행위가 상이한 순서로 및/또는 다른 행위 또는 현상과 동시에 발생할 수 있기 때문에, 본 발명은 행위 또는 현상의 순서에 의해 한정되지 않는다. 게다가, 본 발명에 따른 방법을 실행하는데 모든 예시된 행위 또는 현상이 요구되는 것은 아니다.
본원에 기재된 모든 유전자, 유전자 명칭 및 유전자 산물은 본원에 기재된 조성물 및 방법이 적용될 수 있는 임의의 종으로부터 동족체에 상응하는 것으로 의도된다. 따라서 용어는 인간 및 마우스로부터 유전자와 유전자 산물을 포함하지만 이에 한정되지 않는다. 특정 종으로부터 유전자 또는 유전자 산물이 기재될 때, 이러한 기재는 단지 예로서만 의도되고, 해당 문맥에서 달리 명시되지 않으면 한정으로서 해석되지 않는 것으로 이해된다. 따라서, 예를 들면, 본원에 기재된 유전자의 경우에, 이들은 일부 양태에서, 포유동물 핵산에 관한 것이고, 아미노산 서열은 다른 포유동물, 어류, 양서류, 파충류 및 조류가 포함되지만 이에 한정되지 않는 다른 동물로부터 상동(homologous) 및/또는 병렬상동(orthologous) 유전자 및 유전자 산물을 포함하는 것으로 의도된다. 하나의 양태에서, 유전자 또는 핵산 서열은 인간이다.
정의
본원에서 사용되는 용어는 단지 특정한 양태를 설명하는 것을 목적으로 하고, 본 발명을 한정하는 것으로 의도되지 않는다. 본원에서, 단수형("a", "an" 및 "the")은 해당 문맥에서 달리 명시되지 않으면, 복수형 역시 포함하는 것으로 의도된다. 게다가, 용어 "포함하는", "포함한다", "갖는", "갖는다", "와 함께", 또는 이들의 변이체는 상세한 설명 및/또는 특허청구범위에서 사용되는 한, 이러한 용어들은 용어 "포함하는"과 유사한 방식으로 포괄적인 것으로 의도된다.
용어 "약" 또는 "대략"은 당업자에 의해 결정되는, 특정한 값에 대하여 허용되는 오차 범위 내를 의미하고, 이는 값이 측정되거나 결정되는 방법, 다시 말하면, 측정 체계의 한계에 따라 부분적으로 좌우될 것이다. 예를 들면, "약"은 당해 분야에서 실시에 대해 1 또는 1 이상의 표준 편차 내를 의미할 수 있다. 대안적으로, "약"은 주어진 값의 20% 이하, 바람직하게는 10% 이하, 보다 바람직하게는 5% 이하, 매우 보다 바람직하게는 1% 이하의 범위를 의미할 수 있다. 대안적으로, 특히 생물학적 시스템 또는 공정에 관하여, 용어는 값의 자릿수 이내, 바람직하게는 5배 이내, 보다 바람직하게는 2배 이내를 의미할 수 있다. 특정 값이 명세서 및 특허청구범위에 기재되는 경우, 달리 명시되지 않으면, 특정 값에 대하여 허용되는 오차 범위 이내를 의미하는 용어 "약"이 가정되어야 한다.
본원에서, 용어 "mRNA"는 표적화된 유전자의 현재 공지된 mRNA 전사체(들) 및 설명될 수 있는 임의의 추가의 전사체를 의미한다.
"안티센스 올리고뉴클레오티드" 또는 "안티센스 화합물"은 또 다른 RNA 또는 DNA(표적 RNA, DNA)에 결합하는 RNA 또는 DNA 분자를 의미한다. 예를 들면, RNA 올리고뉴클레오티드의 경우, 이는 RNA-RNA 상호작용에 의해 또 다른 RNA 표적에 결합하고 표적 RNA의 활성을 변경시킨다. 안티센스 올리고뉴클레오티드는 특정한 폴리뉴클레오티드의 발현 및/또는 기능을 상향조절하거나 하향조절할 수 있다. 이러한 정의에는 치료적 관점, 진단적 관점, 또는 다른 관점에서 유용한 임의의 외래 RNA 또는 DNA 분자가 포함되는 것으로 의도된다. 이러한 분자는, 예를 들면, 안티센스 RNA 또는 DNA 분자, 간섭 RNA(RNAi), 마이크로 RNA, 데코이 RNA 분자, siRNA, 효소 RNA, 치료 편집 RNA 및 효능제 및 길항제 RNA, 안티센스 올리고머 화합물, 안티센스 올리고뉴클레오티드, 외부 가이드 서열(EGS: external guide sequence) 올리고뉴클레오티드, 교대 스플라이서(alternate splicer), 프라이머, 프로브, 그리고 표적 핵산의 최소한 일부분에 하이브리드화되는 다른 올리고머 화합물을 포함한다. 따라서 이들 화합물은 단일-가닥, 이중-가닥, 부분적으로 단일-가닥, 또는 원형 올리고머 화합물의 형태로 도입될 수 있다.
본 발명의 맥락에서, 용어 "올리고뉴클레오티드"는 리보핵산(RNA: ribonucleic acid) 또는 데옥시리보핵산(DNA: deoxyribonucleic acid)의 올리고머 또는 중합체, 또는 이의 모방체를 지칭한다. 용어 "올리고뉴클레오티드"에는 또한, 데옥시리보뉴클레오시드, 리보뉴클레오시드, 이들의 치환된 및 알파-아노머 형태(alpha-anomeric form), 펩티드 핵산(PNA: peptide nucleic acid), 잠금 핵산(LNA), 포스포로티오에이트, 메틸포스포네이트 등을 포함한 천연 및/또는 변형된 단량체 또는 연결기(linkage)의 선형 또는 원형 올리고머가 포함된다. 올리고뉴클레오티드는 단량체-단량체 상호작용의 규칙적인 패턴, 예를 들면, 왓슨-크릭(Watson-Crick) 유형의 염기 대합(pairing), 후그스틴(Hoogsteen) 또는 역 후그스틴 유형의 염기 대합 등에 의해, 표적 폴리뉴클레오티드에 특이적으로 결합할 수 있다.
올리고뉴클레오티드는 "키메라"일 수 있고, 다시 말하면, 서로 다른 영역으로 구성될 수 있다. 본 발명의 맥락에서, "키메라" 화합물은 2개 이상의 화학적 영역, 예를 들면, DNA 영역(들), RNA 영역(들), PNA 영역(들) 등을 함유하는 올리고뉴클레오티드이다. 각각의 화학적 영역은 하나 이상의 단량체 단위, 다시 말하면, 올리고뉴클레오티드 화합물의 경우에 뉴클레오티드로 구성된다. 이들 올리고뉴클레오티드는 전형적으로, 하나 이상의 영역을 포함하고, 여기서 올리고뉴클레오티드는 하나 이상의 목적되는 특성을 나타내기 위하여 변형된다. 올리고뉴클레오티드의 목적되는 특성은, 예를 들면, 뉴클레아제 분해에 증가된 내성, 증가된 세포 흡수, 및/또는 표적 핵산에 대한 증가된 결합 친화성(binding affinity)을 포함하지만 이에 한정되지 않는다. 따라서, 올리고뉴클레오티드의 서로 다른 영역은 상이한 특성을 가질 수 있다. 본 발명의 키메라 올리고뉴클레오티드는 둘 이상의 올리고뉴클레오티드, 변형된 올리고뉴클레오티드, 올리고뉴클레오시드 및/또는 상기 기재된 바와 같은 올리고뉴클레오티드 유사체의 혼합된 구조로서 형성될 수 있다.
올리고뉴클레오티드는 "레지스터(register)"에서, 다시 말하면, 단량체가 고유 DNA에서처럼 연속적으로 연결되거나, 또는 스페이서(spacer)를 통해 연결될 때, 연결될 수 있는 영역으로 구성될 수 있다. 스페이서는 영역간에 공유 "브릿지(bridge)"를 구성하고, 바람직한 경우에 약 100개의 탄소 원자를 초과하지 않는 길이를 갖도록 의도된다. 스페이서는, 예를 들면, 양 또는 음 전하를 갖고, 특정한 핵산 결합 특성(삽입물, 그루브 접합제(groove binder), 독소, 형광단 등)을 보유하고, 친유성이고, 예를 들면, 알파-나선을 유도하는 알라닌-함유 펩티드와 같은 특수한 이차 구조를 유도하는 상이한 관능기(functionality)를 보유할 수 있다.
본원에서 "BDNF" 및 "뇌 유래 신경영양 인자"는 모든 집단 구성원, 돌연변이체, 대립유전자, 단편, 종, 코딩 및 비-코딩 서열, 센스 및 안티센스 폴리뉴클레오티드 가닥 등을 포함한다.
본원에서, 단어 '뇌 유래 신경영양 인자', '뇌-유래된 신경영양성 인자' 및 BDNF는 본 출원에서 동의어로 간주되고 상호교환적으로 사용된다.
본원에서, 용어 "특이적인 올리고뉴클레오티드" 또는 "표적으로 하는 올리고뉴클레오티드"는 (i) 표적화된 유전자의 일부와 안정된 복합체를 형성할 수 있거나, (ii) 표적화된 유전자의 mRNA 전사체의 일부와 안정된 이중나선을 형성할 수 있는 서열을 갖는 올리고뉴클레오티드를 지칭한다. 복합체 및 이중나선의 안정성은 이론적 계산 및/또는 시험관내 분석에 의해 결정될 수 있다. 하이브리드화 복합체 및 이중나선의 안정성을 결정하는 대표적인 분석법은 하기 실시예에서 기술된다.
본원에서, 용어 "표적 핵산"은 DNA, 이러한 DNA로부터 전사된 RNA(premRNA 및 mRNA 포함), 및 또한 이러한 RNA, 코딩, 비-코딩 서열, 센스 또는 안티센스 폴리뉴클레오티드로부터 유래된 cDNA를 포괄한다. 올리고머 화합물의 표적 핵산과의 특이적인 하이브리드화는 핵산의 정상적인 기능을 간섭한다. 표적 핵산에 특이적으로 하이브리드화되는 화합물에 의한 상기 표적 핵산의 기능의 이러한 조정은 일반적으로, "안티센스"로 지칭된다. 간섭되는 DNA의 기능은, 예를 들면, 복제 및 전사를 포함한다. 간섭되는 RNA의 기능은, 예를 들면, RNA의 단백질 번역 부위로의 전좌, RNA로부터 단백질의 번역, 하나 이상의 mRNA 종을 산출하기 위한 RNA의 스플라이싱, 및 RNA에 관련되거나 RNA에 의해 촉진될 수 있는 촉매 활성과 같은 생명 유지에 필요한 모든 기능을 포함한다. 표적 핵산 기능에 의한 이러한 간섭의 전반적인 효과는 코딩된 산물 또는 올리고뉴클레오티드의 발현의 조정이다.
RNA 간섭 "RNAi"는 "표적" 핵산 서열에 서열-특이적 상동성(homology)을 갖는 이중 가닥 RNA(dsRNA) 분자에 의해 매개된다. 본 발명의 특정한 양태에서, 매개체는 5 내지 25개 뉴클레오티드 "작은 간섭" RNA 이중나선(siRNA)이다. 이들 siRNA는 다이서(Dicer)로 알려져 있는 RNase 효소에 의한 dsRNA의 가공으로부터 유래된다. siRNA 이중나선 산물은 RISC(RNA Induced Silencing Complex)로 명명된 다중-단백질 siRNA 복합체 내로 동원된다. 특정 이론에 한정됨 없이, RISC는 이후, 표적 핵산(적합하게는 mRNA)로 안내되는 것으로 생각되고, 여기서 siRNA 이중나선은 서열-특이적 방식으로 상호작용하여 촉매 방식으로 절단을 매개한다. 본 발명에 따라 사용될 수 있는 작은 간섭 RNA는 당해 분야에 널리 공지되고 당업자에게 익숙한 절차에 따라서 합성되고 이용될 수 있다. 본 발명의 방법에 이용되는 작은 간섭 RNA는 적절하게는, 약 1 내지 약 50개 뉴클레오티드(nt)를 포함한다. 비제한적인 양태의 예에서, siRNA는 약 5 내지 약 40개 nt, 약 5 내지 약 30개 nt, 약 10 내지 약 30개 nt, 약 15 내지 약 25개 nt, 또는 약 20 내지 25개 뉴클레오티드를 포함할 수 있다.
적절한 올리고뉴클레오티드의 선별은 핵산 서열을 자동적으로 정렬하고 동일성 또는 상동성의 영역을 표시하는 컴퓨터 프로그램을 이용함으로써 가능하게 된다. 이러한 프로그램은, 예를 들면, GenBank와 같은 데이터베이스를 검색하거나, PCR 산물을 서열화함으로써, 수득된 핵산 서열을 비교하는데 사용된다. 일정한 범위의 종으로부터 핵산 서열의 비교는 종 간에 적절한 정도의 동일성을 보이는 핵산 서열의 선별을 가능하게 한다. 서열화되지 않은 유전자의 경우에, 표적 종 및 다른 종에서 유전자 간에 동일성 정도를 결정하기 위하여 서던 블롯(Southern blot)이 수행된다. 당해 분야에 널리 공지된 바와 같이, 다양한 정도의 엄격함(stringency)에서 서던 블롯을 수행함으로써, 동일성의 근사 측정(approximate measure)을 달성하는 것이 가능하다. 이들 절차는 통제되는 개체에서 표적 핵산 서열에 높은 정도의 상보성 및 다른 종에서 상응하는 핵산 서열에 더욱 낮은 정도의 상보성을 나타내는 올리고뉴클레오티드의 선별을 가능하게 한다. 당업자는 본 발명에서 사용을 위한 유전자의 적절한 영역을 선별하는데 상당한 허용 범위(latitude)가 존재한다는 것을 인지할 것이다.
"효소 RNA"은 효소 활성을 갖는 RNA 분자를 의미한다(문헌 [Cech, (1988) J. American. Med. Assoc. 260, 3030-3035]). 효소 핵산(리보자임)은 먼저, 표적 RNA에 결합함으로써 작용한다. 이러한 결합은 표적 RNA를 절단하는 작용을 하는 분자의 효소 부분에 매우 가깝게 유지되는 효소 핵산의 표적 결합 부분을 통하여 발생한다. 따라서, 효소 핵산은 먼저, 표적 RNA를 인식하고, 이후 염기 대합을 통하여 표적 RNA에 결합하고, 일단 정확한 부위에 결합되면, 표적 RNA을 절단하는데 효소적으로 작용한다.
"데코이(decoy) RNA"는 리간드에 대한 천연 결합 도메인을 모방하는 RNA 분자를 의미한다. 따라서, 데코이 RNA는 특정 리간드의 결합에 대하여 천연 결합 표적과 경쟁한다. 예를 들면, HIV 전사활성화 반응(TAR: trans-activation response) RNA의 과다-발현은 "유인자"로서 작용할 수 있고 HIV tat 단백질에 효율적으로 결합하고, 따라서 상기 단백질이 HIV RNA에 코딩된 TAR 서열에 결합하는 것을 예방하는 것으로 밝혀졌다. 이는 특정한 예인 것으로 의도된다. 당업자는 이것이 단지 하나의 예이고, 당해 분야에 일반적으로 공지된 기술을 사용하여 다른 양태가 발생할 수 있다는 것을 인지할 것이다.
본원에서, 용어 "단량체"는 전형적으로, 포스포디에스테르 결합 또는 이의 유사체에 의해 연결되어 수개의 단량체 단위, 예를 들면, 약 3-4개 내지 약 수백 개의 단량체 단위 범위의 크기를 갖는 올리고뉴클레오티드를 형성하는 단량체를 지시한다. 포스포디에스테르 연결기의 유사체는, 하기 보다 상세하게 기술된 바와 같이, 포스포로티오에이트, 포스포로디티오에이트, 메틸포스포네이트, 포스포로셀레노에이트, 포스포라미데이트 등을 포함한다.
용어 "뉴클레오티드"는 천연 발생 뉴클레오티드 뿐만 아니라 비-천연 발생 뉴클레오티드를 포함한다. 이전에 "비-천연 발생" 인 것으로 간주되었던 다양한 뉴클레오티드가 차후에, 천연에서 발견되고 있음은 당업자에게 명백할 것이다. 따라서, "뉴클레오티드"는 공지된 퓨린과 피리미딘 헤테로사이클-함유 분자 뿐만 아니라 이들의 헤테로사이클 유사체 및 호변체(tautomer) 역시 포함한다. 다른 유형의 뉴클레오티드의 예시적인 예는 아데닌, 구아닌, 티민, 시토신, 우라실, 퓨린, 크산틴, 디아미노퓨린, 8-옥소-N6-메틸아데닌, 7-데아자크산틴, 7-데아자구아닌, N4,N4-에타노시토신, N6,N6-에타노-2,6-디아미노퓨린, 5-메틸시토신, 5-(C3-C6)-알키닐시토신, 5-플루오르우라실, 5-브로모우라실, 슈도이소시토신, 2-하이드록시-5-메틸-4-트리아졸로피리딘, 이소시토신, 이소구아닌, 이노신 및 미국 특허 제5,432,272호(Benner et al.,)에 기술된 "비-천연 발생" 뉴클레오티드를 함유하는 분자이다. 용어 "뉴클레오티드"는 이들 예 모두 뿐만 아니라 이의 유사체 및 호변체를 포함하는 것으로 의도된다. 특히 흥미로운 뉴클레오티드는 아데닌, 구아닌, 티민, 시토신, 및 우라실을 함유하는 것들이고, 이들은 인간에서 치료적 및 진단적 적용에 관하여 천연 발생 뉴클레오티드로서 간주된다. 뉴클레오티드는, 예를 들면, 문헌 [Kornberg and Baker, DNA Replication, 2nd Ed.(Freeman, San Francisco, 1992)]에 기술된 바와 같은 천연 2'-데옥시 및 2'-히드록실 당 뿐만 아니라 이의 유사체를 포함한다.
뉴클레오티드와 관련하여 "유사체"는 변형된 염기 모이어티 및/또는 변형된 당 모이어티를 갖는 합성 뉴클레오티드(예를 들면, 문헌 [Scheit, Nucleotide Analogs, John Wiley, New York, 1980]; [Freier & Altmann, (1997) Nucl. Acid. Res., 25(22), 4429-4443, Toulme J.J., (2001) Nature Biotechnology 19:17-18]; [Manoharan M., (1999) Biochemica et Biophysica Acta 1489:117-139]; [Freier S. M., (1997) Nucleic Acid Research, 25:4429-4443, Uhlman, E., (2000) Drug Discovery & Development, 3: 203-213, Herdewin P., (2000) Antisense & Nucleic Acid Drug Dev., 10:297-310]에서 전반적으로 기술됨); 2'-O, 3`-C-연결된 [3.2.0] 비시클로아라비노뉴클레오시드를 포함한다. 이러한 유사체는 결합 특성, 예를 들면, 이중나선 또는 삼중나선 안정성, 특이성 등을 증강시키도록 설계된 합성 뉴클레오티드를 포함한다.
본원에서, "하이브리드화"는 올리고머 화합물의 실질적으로 상보성 가닥의 대합을 의미한다. 하나의 대합 기전은 수소 결합을 수반하고, 이는 올리고머 화합물의 가닥의 상보성 뉴클레오시드 또는 뉴클레오티드 염기(뉴클레오티드) 간에 왓슨-크릭, 후그스틴 또는 역 후그스틴 수소 결합일 수 있다. 예를 들면, 아데닌 및 티민은 수소 결합의 형성을 통하여 대합하는 상보성 뉴클레오티드이다. 하이브리드화는 다양한 상황하에서 발생할 수 있다.
안티센스 화합물은 표적 핵산에 화합물의 결합이 표적 핵산의 정상적인 기능을 간섭하여 기능 및/또는 활성의 조정을 유발하고, 특정한 결합이 목적되는 조건 하에, 다시 말하면, 생체내 분석 또는 치료적 처리의 경우에 생리학적 조건 하에, 및 시험관내 분석의 경우에 이들 분석이 수행되는 조건 하에 비-표적 핵산 서열에 안티센스 화합물의 비-특이적 결합을 회피할 수 있을 만큼 충분한 정도의 상보성이 존재할 때, "특이적으로 하이브리드화가능"하다.
본원에서, 문구 "엄격한 하이브리드화 조건" 또는 "엄격한 조건"은 본 발명의 화합물이 표적 서열에 하이브리드화되지만, 최소 숫자의 다른 서열에 하이브리드화되는 조건을 지칭한다. 엄격한 조건은 서열-의존성이고 서로 다른 환경에서 상이할 것이고, 본 발명의 맥락에서, 올리고머 화합물이 표적 서열에 하이브리드화되는 "엄격한 조건"은 이들 올리고머 화합물의 본성과 조성 및 이들이 조사되는 분석법에 의해 결정된다. 일반적으로, 엄격한 하이브리드화 조건은 무기 양이온, 예를 들면, Na+ 또는 K+를 갖는 낮은 농도(<0.15M)의 염(다시 말하면, 낮은 이온 강도), 올리고머 화합물:표적 서열 복합체의 Tm 미만에서 20℃ 내지 25℃보다 높은 온도, 및 변성제, 예를 들면, 포름아미드, 디메틸포름아미드, 디메틸 설폭시드, 또는 세정제 나트륨 도데실 설페이트(SDS)의 존재를 포함한다. 예를 들면, 하이브리드화 속도는 각 1% 포름아미드에 대하여 1.1% 감소한다. 높은 엄격한 하이브리드화 조건의 예는 60℃에서 30분 동안 0.1X 염화나트륨-시트르산나트륨 완충액(SSC)/0.1%(w/v) SDS이다.
본원에서, "상보성"은 1개 또는 2개의 올리고머 가닥에서 2개의 뉴클레오티드 간에 정확한 대합 능력을 지칭한다. 예를 들면, 안티센스 화합물의 일정한 위치에서 핵염기(nucleobase)가 표적 핵산의 일정한 위치에서 핵염기와 수소 결합을 형성할 수 있고, 상기 표적 핵산이 DNA, RNA, 또는 올리고뉴클레오티드 분자이면, 상기 올리고뉴클레오티드 및 표적 핵산 사이에 수소 결합의 위치는 상보성 위치인 것으로 간주된다. 올리고머 화합물 및 추가의 DNA, RNA, 또는 올리고뉴클레오티드 분자는 각 분자 내에서 충분한 숫자의 상보성 위치가 서로에 수소 결합될 수 있는 뉴클레오티드에 의해 점유될 때, 서로에 상보성이다. 따라서, "특이적으로 하이브리드화가능" 및 "상보성"은 올리고머 화합물 및 표적 핵산 사이에 안정되고 특정한 결합이 발생할 만큼 충분한 숫자의 뉴클레오티드에 걸쳐 충분한 정도의 정확한 대합 또는 상보성을 지시하는데 사용되는 용어이다.
당해 분야에서, 올리고머 화합물의 서열은 특이적으로 하이브리드화되기 위하여, 표적 핵산의 서열에 100% 상보성일 필요가 없는 것으로 이해된다. 게다가, 올리고뉴클레오티드는 개재성 또는 인접 분절(segment)이 하이브리드화 현상에 관련되지 않도록 하나 이상의 분절에 걸쳐 하이브리드화될 수 있다(예를 들면, 루프 구조, 미스매치 또는 헤어핀 구조). 본 발명의 올리고머 화합물은 그들이 표적화되는 표적 핵산 서열 내에 표적 영역에 약 70% 이상, 또는 약 75% 이상, 또는 약 80% 이상, 약 85% 이상, 또는 약 90% 이상, 또는 약 95% 이상, 또는 약 99% 이상의 서열 상보성을 포함한다. 예를 들면, 안티센스 화합물의 20개 뉴클레오티드 중에서 18개가 표적 영역에 상보성이고, 따라서 특이적으로 하이브리드화되는 안티센스 화합물은 90% 상보성을 나타낼 것이다. 이러한 예에서, 나머지 비-상보성 뉴클레오티드는 상보성 뉴클레오티드와 함께 군집되거나 산재될 수 있고, 서로에 또는 상보성 뉴클레오티드에 인접할 필요가 없다. 이와 같이, 표적 핵산과 완전 상보성의 두 영역이 측면에서 접하는 4개의 비-상보성 뉴클레오티드를 보유하는 18개 뉴클레오티드 길이를 갖는 안티센스 화합물은 표적 핵산과 77.8% 전체 상보성을 가질 것이고, 따라서 본 발명의 범위 내에 속할 것이다. 안티센스 화합물의 표적 핵산의 영역과의 상보성 비율은 당해 분야에 공지된 BLAST 프로그램(basic local alignment search tools) 및 PowerBLAST 프로그램을 이용하여 일과적으로 결정될 수 있다. 상동성, 서열 동일성 또는 상보성 비율은, 예를 들면, 디폴트 설정을 이용한 Gap 프로그램(Wisconsin Sequence Analysis Package, Version 8 for Unix, Genetics Computer Group, University Research Park, Madison Wis.)에 의해 결정될 수 있고, 문헌 [Smith and Waterman(Adv. Appl. Math., (1981) 2, 482-489)]의 알고리즘을 사용한다.
본원에서, 용어 "열 융점 (Tm)"은 표적 서열에 상보성인 올리고뉴클레오티드 중에서 50%가 평형에서 표적 서열에 하이브리드화되는 규정된 이온 강도, pH, 및 핵산 농도 하에 온도를 지칭한다. 전형적으로, 엄격한 조건은 염 농도가 pH 7.0 내지 8.3에서 최소한 대략 0.01 내지 1.0 M Na 이온 농도(또는 다른 염)이고, 짧은 올리고뉴클레오티드(예를 들면, 10 내지 50개 뉴클레오티드)의 경우에 온도가 약 30℃ 이상인 조건일 것이다. 엄격한 조건은 또한, 불안정화제, 예를 들면, 포름아미드의 첨가로 달성될 수도 있다.
본원에서, "조정(modulation)"은 유전자의 발현에서 증가(촉진) 또는 감소(저해)를 의미한다.
폴리뉴클레오티드 서열의 맥락에서 이용될 때, 용어 "변이체"는 야생형 유전자에 관련된 폴리뉴클레오티드 서열을 포함할 수 있다. 이러한 정의는 또한, 예를 들면, "대립유전자", "스플라이스", "종", 또는 "다형성" 변이체를 포함할 수 있다. 스플라이스 변이체는 참조 분자에 현저한 동일성을 가질 수도 있지만, 일반적으로 mRNA 가공 동안 엑손의 교대성 스플라이싱(alternate splicing)으로 인하여 더욱 많은 또는 더욱 적은 숫자의 폴리뉴클레오티드를 보유할 것이다. 상응하는 폴리펩티드는 추가의 기능적 도메인을 보유하거나, 도메인이 부재할 수 있다. 종 변이체는 종에 따라 달라지는 폴리뉴클레오티드 서열이다. 야생형 유전자 산물의 변이체가 본 발명에 특히 유용하다. 변이체는 핵산 서열 내에서 하나 이상의 돌연변이로부터 유래할 수 있고, 변경된 mRNA, 또는 구조 또는 기능이 변경되거나 변경되지 않은 폴리펩티드를 야기할 수 있다. 임의의 주어진 천연 또는 재조합 유전자는 대립유전자 형태를 보유하지 않거나, 1개 또는 다수의 대립유전자 형태를 보유할 수 있다. 변이체를 발생시키는 공통의 돌연변이 변화는 일반적으로, 뉴클레오티드의 자연적인 결실, 부가, 또는 치환에 기인하는 것으로 생각된다. 이들 유형의 변화는 각각, 주어진 서열 내에서 단독으로, 또는 다른 것들과 조합으로, 1회 이상 발생할 수 있다
수득된 폴리펩티드는 일반적으로 서로에 대하여 현저한 아미노산 동일성을 가질 것이다. 다형성 변이체는 주어진 종의 개체 간에 특정 유전자의 폴리뉴클레오티드 서열에서 변형물이다. 다형성 변이체는 또한 "단일 뉴클레오티드 다형성(SNP: single nucleotide polymorphism)" 또는 폴리뉴클레오티드 서열이 1개 염기에 의해 달라지는 단일 염기 돌연변이를 포함할 수 있다. SNP의 존재는, 예를 들면, 질환 상태에 대한 경향, 다시 말하면, 감수성 대 내성을 갖는 일정한 개체군을 지시할 수 있다.
유도체 폴리뉴클레오티드는 화학적 변형, 예를 들면, 알킬, 아실, 또는 아미노 기에 의한 수소의 대체의 대상이 되는 핵산을 포함한다. 유도체, 예를 들면, 유도체 올리고뉴클레오티드는 비-천연-발생 부분, 예를 들면, 변경된 당 모이어티 또는 당-내 연결기를 포함할 수 있다. 포스포로티오에이트 및 해당 분야에 공지되어 있는 다른 황-보유 종이 이들 중에서 대표적이다. 유도체 핵산은 또한, 방사성뉴클레오티드, 효소, 형광제, 화학발광제, 발색제(chromogenic agent), 기질, 보조인자, 저해제, 자기 입자 등을 포함하는 라벨을 함유할 수 있다.
"유도체" 폴리펩티드 또는 펩티드는, 예를 들면, 글리코실화, 페길화, 인산화, 황산화, 환원/알킬화, 아실화, 화학적 커플링, 또는 순한 포르말린 처리에 의해 변형된 것이다. 유도체는 또한 방사성동위원소, 형광, 그리고 효소 라벨을 포함하지만 이에 한정되지 않는 검출가능한 라벨을 직접적으로 또는 간접적으로 함유하도록 변형될 수 있다.
본원에서, 용어 "동물" 또는 "환자"는, 예는 들면, 인간, 양, 엘크, 사슴, 뮬 사슴, 밍크, 포유동물, 원숭이, 말, 소, 돼지, 염소, 개, 고양이, 랫트, 마우스, 조류, 닭, 파충류, 어류, 곤충 및 거미류 동물을 포함하는 것으로 의도된다.
"포유동물"은 전형적으로 건강 관리를 받고 있는 온혈 포유동물(예를 들면, 인간 및 가축)을 포함한다. 예는 단지 인간 뿐만 아니라 고양이, 개, 말, 소, 및 인간을 포함한다.
"치료하는" 또는 "치료"는 포유동물에서 질환-상태의 치료를 커버하고, (a) 포유동물에서, 특히 이러한 포유동물이 질환-상태의 성향이 있지만 아직 발병된 것으로 진단되지 않았을 때 질환-상태가 발생하는 것을 예방하는 것; (b) 질환-상태를 저해하고, 예를 들면, 이의 발생을 중지시키는 것; 및/또는 (c) 질환-상태를 완화하는, 예를 들면, 원하는 종점에 도달될 때까지 질환 상태의 퇴보를 유발하는 것을 포함한다. 치료는 또한, 질환의 증상의 개선(예를 들면, 통증 또는 불쾌감 경감)을 포함하고, 여기서 이러한 개선은 질환(예를 들면, 원인, 전염, 발현 등)에 직접적으로 영향을 주거나 주지 않을 수 있다.
본원에서, "암"은 백혈병, 림프종, 흑색종, 암종 및 육종을 포함하지만 이에 한정되지 않는 포유동물에서 발견되는 모든 유형의 암 또는 신생물 또는 악성 종양을 지칭한다. 암은 "종양" 또는 암의 악성 세포를 포함하는 조직으로서 그 자신을 드러낸다. 종양의 예는 육종 및 암종, 예를 들면, 섬유육종, 점액육종, 지방육종, 연골육종, 골원성 육종, 척삭종, 혈관육종, 내피육종, 림프관육종, 림프관내피육종, 윤활막종, 중피종, 유잉 종양, 평활근육종, 횡문근육종, 결장 암종, 췌장암, 유방암, 난소암, 전립선암, 편평 세포 암종, 기저 세포 암종, 선암종, 한선 암종, 피지선 암종, 유두 암종, 유두 선암종, 낭선종, 속질 암종, 기관지원성 암종, 신장 세포 암종, 간암, 담관 암종, 융모막 암종, 정상피종, 배아 암종, 윌름 종양, 자궁경부암, 고환 종양, 폐 암종, 소세포 폐 암종, 방광 암종, 상피 암종, 신경교종, 별아교세포종, 속질모세포종, 두개인두종, 뇌실막세포종, 송과체종, 혈관모세포종, 청신경초종, 희소돌기아교세포종, 수막종, 흑색종, 신경아세포종, 및 망막모세포종을 포함하지만 이에 한정되지 않는다. 본 발명에 따라 기술된 조성물에 의해 치료될 수 있는 추가의 암은, 예를 들면, 호지킨병, 비-호지킨 림프종, 다발성 골수종, 신경아세포종, 유방암, 난소암, 폐암, 횡문근육종, 원발성 혈소판증가증, 원발성 마크로글로블린혈증, 소세포 폐 종양, 원발성 뇌 종양, 위암(stomach cancer), 결장암, 악성 췌장 인슐린종, 악성 암양종, 방광암, 위장암(gastric cancer), 전암성 피부 병변, 고환암, 림프종, 갑상선암, 신경아세포종, 식도암, 비뇨생식관암, 악성 고칼슘혈증, 자궁경부암, 자궁내막암, 부신피질암, 및 전립선암을 포함하지만 이에 한정되지 않는다.
본원에서, "신경학적 질환 또는 장애"는 신경계 및/또는 시각계의 임의의 질환 또는 장애를 지칭한다. "신경학적 질환 또는 장애"는 중추 신경계(뇌, 뇌간 및 소뇌), 말초 신경계(뇌신경 포함), 및 자율 신경계(중추 및 말초 신경계 둘 다에 위치한 부분)를 수반하는 질환 또는 장애를 포함한다. 신경학적 질환 또는 장애는 후천성 간질성 실어증; 급성 파종성 뇌척수염; 부신피질이영양증; 연령 관련된 황반 변성; 뇌량의 무발생증; 실인증; 에이카르디 증후군; 알렉산더병; 알퍼스병; 교대성 편마비; 알츠하이머병; 혈관성 치매; 근위축성 측삭경화증; 무뇌증; 엔젤맨 증후군; 혈관종증; 산소결핍; 실어증; 운동불능; 거미막 낭종; 거미막염; 아놀드-키아리 기형; 동정맥 기형; 아스퍼거 증후군; 모세혈관확장; 주의력결핍 과잉행동장애; 자폐증; 자율신경 실조증; 요통; 바텐병; 베체트병; 벨 마비; 양성 본태성 안검경련증; 양성 국소 근위축증; 특발성 두개강내고압증; 빈스완거병; 안검 경련증; 색소 실조증; 상완 신경총 손상; 뇌 농량; 뇌 손상; 뇌종양(다형성아교모세포종을 포함함); 척추 종양; 브라운 세카르 증후군; 카나반병; 수근관 증후군; 작열통; 중추성 통증 증후군; 중심부 뇌교수초 용해증; 뇌질환; 뇌동맥류; 뇌동맥 경화증; 뇌 수축; 뇌 거대증; 뇌성 마비; 샤르코-마린-투스병; 화학요법-유도 신경 장애 및 신경병적 통증; 키아리 증후군; 무도병; 만성 염증성 탈수초화 다발성 신경병증; 만성 통증; 만성 부위 통증 증후군; 코핀-로리 증후군; 식물 인간을 포함한 혼수 상태; 선천성 얼굴 양측마비 증후군; 피질기저핵 변성; 관자 동맥염; 조기유합증; 크로이츠펠트-야콥병; 누적 외상성 질환; 쿠싱 증후군; 거대 세포 봉입체 질환; 사이토메갈로바이러스 감염; 춤추는 눈-춤추는 발 증후군; 댄디-워커 증후군; 다우슨 질병; 데 모지르 증후군; 데제린-클룸프케 마비; 치매; 피부 근염; 당뇨병적 신경 장애; 미만성 경화증; 자율 신경 장애; 서자 장애; 난독증; 실조; 초기 유아성 간질성 뇌병증; 공터기안 증후군; 뇌염; 뇌류; 뇌상차 신경성 혈관종증; 간질; 어브 마비; 본태성 진전; 파브리병; 파흐르 증후군(Fahr's syndrome); 실신; 유전성 강직성 대마비; 발열 뇌졸증; 피셔 증후군; 프리드라이히 실조증; 전두 관자 치매 및 다른 "타우병증"; 고셰병; 거스트만 증후군; 거대세포 동맥염; 거대세포 함유 질병; 구형 세포 대뇌피질 위축증; 갈렝 바레 증후군; HTLV-1-관련 골수 장애; 할러포르덴-슈파츠병; 두뇌 손상; 두통; 반측성 안면 경련증; 유전성 강직성 대마비; 유전성 다발신경염성 실조; 이성 대상 포진; 대상포진; 히라야마 증후군; HIV 관련 치매 및 신경 장애(또한 AIDS의 신경학적 징후); 전전뇌증; 헌팅턴병 및 다른 폴리글루타민 반복 질병; 물무뇌증; 뇌수종; 고코티솔혈증; 저산소증; 면역-매개 뇌척수염; 봉입체 근염; 색소 실조증; 유아성 피탄산 저장 질병; 영아형 레프숨병; 영아 연축; 염증성 근병증; 대뇌 낭종; 대뇌 고혈압; 주버트 증후군; 컨스-세이어 증후군; 케네디병 킹스본 증후군; 클리펠-파일 증후군; 크라베병; 쿠겔베르그-웰란더병; 쿠루병; 라포라병; 람베르트-이튼 근무력 증후군; 란다우-클레프너 증후군; 외측연수(발렌버그) 증후군; 학습 장애; 리씨 증후군; 레녹스-가스토 증후군; 레시-니한 증후군; 대뇌백질 위축증; 루이소체 치매; 활택뇌증; 고정 증후군; 루게릭병(다시 말하면, 운동 신경 질환 또는 근위축성 측색 경화증); 요추 디스크 질환; 라임병-신경학적 후유증; 마카도 조셉병; 대뇌증; 거대뇌증; 멜커슨 로젠탈 증후군; 메니에르병; 수막염; 멘케스병; 이염성 백질 이영양증; 소두증; 편두통; 밀러 피셔 증후군; 소중풍; 사립체 근병증; 뫼비우스 증후군; 단일사지 근육위축증; 운동 뉴런 장애; 모야모야병; 뮤코다당증; 다발경색 치매; 다병소성 운동신경병증; 다발성 경화증 및 다른 탈수초 질환; 자세성 저혈압이 있는 다계통 위축증; 근이영양증; 중증 근무력증; 수초탈락성 미만성 경화증; 영아 중 근간대성 뇌증; 간대성 근경련증; 근병증; 선천적 근경직증; 수면 발작; 신경 섬유종증; 신경 이완성 악성 증후군; AIDS의 신경학적 징후; 낭창의 신경학적 후유증; 신경근긴장증; 신경세로이드 리포푸스신증; 신경 이주 이상; 니만-픽병; 오설리번-맥레오드 증후군(O'Sullivan-McLeod syndrome); 후두 신경통; 잠혈 척추후만증 연쇄; 오타하라 증후군; 올리브교 소뇌 위축증; 안구간대경련-근간대경련증; 시신경염; 기립성 저혈압; 과사용 증후군; 이상 감각; 신경퇴행성 질환 또는 장애(파킨슨병, 헌팅턴병, 알츠하이머병, 근위축성 측삭경화증(ALS), 치매, 다발성 경화증 및 다른 신경 세포 사멸과 관련된 질환 및 장애); 선천성 이상근긴장증; 방종양성 질환; 발작 공격; 패리-롬버그병; 펠리제우스-메르츠바흐병; 주기 마비; 말초신경병증; 통증성 신경병증 및 신경병성 통증; 식물 인간; 전반적 발달장애; 광반사 재채기; 피탄산 저장 질병; 픽병; 신경 압박; 뇌하수체 종양; 다발성근염; 공뇌증; 회색질 척수염 후증후군; 대상포진후 신경통; 감염성후의 뇌염; 자세성 저혈압; 프라더-윌리 증후군; 원발성 측삭 경화증; 프리온병; 진행성 반얼굴 위축; 진행 다초점 백질 뇌증; 진행성 경화 폴리오디스트로피; 진행성 핵상 마비; 가뇌종양; 람세이-헌트 증후군(타입 I 및 II); 라스무센 뇌염; 반사성 교감신경 이영양증 증후군; 레프숨병; 반복적 움직임에 따른 병; 반복사용 긴장성 손상 증후군; 하지 불안 증후군; 레트로바이러스-관련 골수 장애; 레트 증후군; 라이 증후군; 세인트 바이터스 춤; 샌드호프병; 쉴더병; 뇌갈림증; 중격-시신경 형성장애; 흔들린 아이 증후군; 대상 포진; 샤이-드래거 증후군; 쇼그렌 증후군; 수면 무호흡; 소토스 증후군; 경련; 척추 파열; 척수 손상; 척추 종양; 척추 근육 위축; 강직인간 증후군; 발작; 스터지 웨버 증후군; 아급성 경화성 범뇌염; 피질하 동맥경화성 뇌증; 시덴함 무도병; 실신; 척수 공동증; 지발성 안면 마비; 테이-삭스병; 일시적 동맥염; 구속성 척수 증후군; 톰슨병; 흉곽출구 증후군; 동통성 틱; 토트 마비; 뚜렛 증후군; 일과성 뇌허혈 발작; 전염성 해면 상뇌증; 횡단 척수염; 외상성 뇌손상; 진전; 삼차 신경통; 열대 경직 하반신 마비; 결절 경화; 혈관성 치매(다발경색 치매); 일시적 동맥염을 포함하는 혈관염; 폰 힙펠-린도우병; 발렌버그 증후군; 베르드니히-호프만병; 웨스트 증후군; 목뼈의 골절; 윌리엄스 증후군; 윌슨병; 및 젤웨거 증후군을 포함하지만 이에 한정되지 않는다.
"증식성 질환 또는 장애"는 골수성, 림프구성 또는 적혈구성 계통, 또는 이들의 전구 세포로부터 발생하는 조혈 기원의 과형성/신생물성 세포와 관련된 조혈 신생물성 장애를 포함하지만 이에 한정되지 않는다. 이들은 적혈모구성 백혈병; 급성 전골수구성 백혈병(APML); 만성 골수성 백혈병(CML); B-계통 ALL과 T-계통 ALL을 포함하는 급성 림프성모구성 백혈병(ALL), 만성 림프구성 백혈병(CLL), 전림프구성 백혈병(PLL), 모발상 세포 백혈병(HLL) 및 발덴스트롬 마크로글로불린혈증(WM)을 포함한 악성 림프종을 포함하지만 이에 한정되지 않는다. 추가 형태의 악성 림프종은 비-호지킨 림프종과 이의 변이체, 말초 T 세포 림프종, 성체 T 세포 백혈병/림프종(ATL), 피부 T-세포 림프종(CTCL), 거대 과립 림프구성 백혈병(LGF), 호지킨병 및 리드-스턴버그(Reed-Sternberg) 질환을 포함하지만 이에 한정되지 않는다.
"염증"은 전신 염증성 이상 및 단핵세포, 백혈구 및/또는 호중구의 이동 및 견인과 국소적으로 관련된 이상을 지칭한다. 염증의 예는 병원성 유기체(그람-양성 세균, 그람-음성 세포, 바이러스, 곰팡이, 및 원생동물문 및 연충류와 같은 기생충을 포함)에 의한 감염, 이식 거부(신장, 간, 심장, 폐, 또는 각막과 같은 고형 장기의 거부 뿐만 아니라 이식편대 숙주병(GVHD)을 포함한 골수 이식의 거부를 포함), 또는 국소화된 만성 또는 급성 자가면역 또는 알레르기 반응으로 인한 염증을 포함하지만 이에 한정되지 않는다. 자가면역 질환은 급성 사구체신염; 류마티즘성 또는 반응성 관절염; 만성 사구체신염; 염증성 장 질환, 예를 들면, 크론병, 궤양성 결장염 및 괴사성 전장염; 간염; 폐혈증; 알코올성 간 질환; 비-알코올성 지방증; 과립구 주입 관련 증후군; 염증성 피부질환, 예를 들면, 접촉성 피부염, 아토피성 피부염, 건선; 전신 홍반성 루프스(SLE), 자가면역 갑상선염, 다발성 경화증, 및 일부 형태의 당뇨병, 또는 환자의 자기 면역계의 공격에 의해 병인성 조직 파괴를 야기하는 임의의 기타 자가면역상태를 포함하지만 이에 한정되지 않는다. 알레르기성 반응은 알레르기성 천식, 만성 기관지염, 급성 및 지연된 과민성을 포함한다. 전신 염증성 질환 상태는 외상, 화상, 허혈후에 따른 재관류와 관련된 염증(예를 들면, 심장, 뇌, 내장 또는 말초 맥관에서 심근경색 및 발작을 포함하는 혈전증), 폐혈증, ARDS 또는 다발성 장기부전 증후군을 포함한다. 염증성 세포 모집은 또한 죽상경화성 플라크에서도 발생한다. 염증은 비-호지킨 림프종, 베게너 육아종증, 하시모토 갑상선염, 간세포 암종, 흉선 위축, 만성 췌장염, 류마티즘성 관절염, 반응성 림프 비후증, 골관절염, 궤양성 결장염, 유두상 암종, 크론병, 궤양성 결장염, 급성 담낭염, 만성 담낭염, 간경변, 만성 타액선염, 복막염, 급성 췌장염, 만성 췌장염, 만성 위염, 자궁선근종, 자궁내막증, 급성 자궁경관염, 만성 자궁경관염, 림프 비후, 다발성 경화증, 특발성 혈소판 감소 자색반병에 후속되는 비대, 일차성 IgA 신증, 전신 홍반성 루프스, 건선, 폐기종, 만성 신우신염, 및 만성 방광염을 포함하지만 이에 한정되지 않는다.
폴리뉴클레오티드 및 올리고뉴클레오티드 조성물 및 분자
표적: 하나의 양태에서, 표적은 제한 없이 BDNF와 연관된 센스 및/또는 안티센스 비-코딩 및/또는 코딩 서열을 포함하는, 뇌 유래 신경영양 인자(BDNF)의 핵산 서열을 포함한다. 둘 다 제목이 "BDNF에 대한 천연 안티센스 전사체의 저해에 의한 뇌 유래 신경영양 인자(BDNF) 관련 질환의 치료(Treatment of Brain Derived Neurotrophic Factor(BDNF) Related Diseases by Inhibition of Natural Antisense Transcript to BDNF)"인 PCT 공개 번호 제WO 2010/093904호 및 미국 특허 출원 공개 번호 제2011/0319475호에는 그 안에 기재된 올리고뉴클레오티드를 사용하는 조정을 위한 표적으로서 BDNF가 기재되고, 상기 출원의 개시내용은 그 전문이 본원에 참고로 포함된다.
뉴로트로핀(neurotrophin)은 신경 생존과 분화를 증진하는 일군의 구조적으로 관련된 성장 인자이다. 이들은 신경돌기 성장(neurite outgrowth)을 촉진하는데, 이는 이들이 손상된 뉴런의 재생을 증진하고, 뉴로트로핀을 생산하는 표적 조직에서 측부 발아(collateral sprouting)를 촉진하는 표적-유래된 신경영양성 인자로서 기능한다는 것을 암시한다. 뇌-유래된 신경영양성 인자(BDNF)는 초기에, 뇌 추출물 내에 존재하고 뒤뿌리 신경절(dorsal root ganglia)의 생존을 증가시킬 수 있는 염기성 단백질로서 특징되었다. 세포체와 축색 소통(axonal communication)이 손상에 의해 중단될 때, 슈반(Schwann) 세포는 신경영양성 인자, 예를 들면, 신경 성장 인자(NGF: nerve growth factor) 및 BDNF를 생산한다. 뉴로트로핀은 슈반 세포로부터 방출되고, 재생 축삭 주변에 기울기 방식으로 확산 분산되고, 이들은 이후, 뉴로트로핀의 밀도 기울기를 따라 원위로 연장된다. 신생아 쥐에서 가로로 절개된 신경에 BDNF의 국소 적용은 축색절단(axotomy) 이후에 운동 뉴런의 대규모 사멸을 예방하는 것으로 밝혀졌다. BDNF의 mRNA 역가는 축삭절단후 4일 시점에 정상 수준의 수배로 증가하고 4주 시점에 최대에 도달한다. 게다가, BDNF는 배양 동안 콜린성 뉴런의 생존을 증강시키는 것으로 보고되었다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 BDNF와 연관된 질환 또는 장애를 예방하거나 치료하는데 사용된다. 본 발명의 안티센스 올리고뉴클레오티드로 치료될 수 있고/있거나, 안티센스 화합물을 사용하고/사용하거나 보유함으로써 수득된 줄기 세포로부터 재생된 세포/조직으로 치료될 수 있는 대표적인 뇌 유래 신경영양 인자(BDNF) 매개된 질환 및 장애는 BDNF의 비정상적인 기능 및/또는 발현과 연관된 질환 또는 장애, 신경병성 질환 또는 장애, 결함성 신경발생(defective neurogenesis)과 연관된 질환 또는 장애; 신경퇴행성 질환 또는 장애(예를 들면, 알츠하이머병, 파키슨병, 헌팅턴병, 근위축성 축삭 경화증 등); 신경정신병적 장애(우울증, 정신분열증, 정신분열형 장애, 분열정동 장애, 및 망상 장애; 불안 장애, 예를 들면, 공황 장애, 공포증(광장공포증 포함), 강박 장애, 외상후 스트레스 장애, 양극성 장애, 신경성 식욕부진증, 신경성 폭식증), 중추신경계의 자가면역 질환(예를 들면, 다발성 경화증), 기억 상실, 장기 또는 단기 기억 장애, 건망증, 소아 학습 장애, 폐쇄성 뇌 손상, 주의력 결핍 장애, 바이러스 감염에 대한 뉴런 반응, 뇌 손상, 기면 발작, 수면 장애(예를 들면, 일주기성 리듬 장애, 불면증 및 기면 발작); 신경의 단절 또는 신경 손상, 뇌척수 신경삭(CNS)의 단절 및 뇌 또는 신경 세포의 손상, AIDS와 연관된 신경학적 결함, 운동 및/또는 음성 틱으로 특징되는 운동 틱 장애(예를 들면, 뚜렛 장애, 만성 운동 또는 음성 틱 장애, 일시적 틱 장애, 및 상동적 운동장애), 약물 남용 장애(예를 들면, 약물 의존, 약물 남용 및 약물 남용/의존의 후유증, 예를 들면, 약물-유도된 심리학적 장애, 약물 금단 증상 및 약물-유도된 치매 또는 건망증 장애), 외상성 뇌 손상, 이명, 신경통(예를 들면, 삼차 신경통), 통증(예를 들면, 만성 통증, 만성 염증성 통증, 관절염과 연관된 통증, 섬유근육통, 요통, 암-연관된 통증, 소화성 질환과 연관된 통증, 크론병과 연관된 통증, 자가면역 질환과 연관된 통증, 내분비 질환과 연관된 통증, 당뇨성 신경병증과 연관된 통증, 환지통, 자발통, 수술후 만성 통증, 만성 측두하악 통증, 작열통, 대상포진후 신경통, AIDS-관련된 통증, 복합 부위 통증 증후군 타입 I과 II, 삼차 신경통, 만성적인 요통, 척수 손상과 연관된 통증, 약물 복용과 연관된 통증 및 재발성 급성 통증, 신경병증성 통증), 당뇨병과 같은 질환에서 신경이감각증(neurodysthesias)을 유발하는 부적절한 뉴런 활성, MS 및 운동 뉴런 질환, 운동실조, 근육 강직(경직), 턱관절 기능장애, 보상 결핍 증후군(RDS), 알코올 또는 약물 남용(예를 들면, 엑스터시, 메스암페타민 등)에 의해 유발된 신경독성, 정신 지체 또는 인지 장애(예를 들면, 비증후군성 X-염색체 연관 정신 지체, 취약 X 증후군, 다운 증후군, 자폐증), 실어증, 벨 마비, 크로이츠펠트-야곱병, 뇌염, 연령 관련된 황반 변성, 온다인 증후군, WAGR 증후군, 청력 상실, 레트 증후군, 간질, 척수 손상, 뇌졸중, 저산소증, 허혈, 뇌 손상, 시신경 손상, 당뇨성 신경병증, 말초 신경병증, 신경 이식 합병증, 운동 뉴런 질환, 말초 신경 손상, 비만, 대사 증후군, 암, 천식, 아토피 질환, 염증, 알레르기, 습진, 신경-종양학적 질환 또는 장애, 신경-면역학적 질환 또는 장애 및 신경-이과학적 질환 또는 장애; 및 가령 및 노화와 연관된 질환 또는 장애를 포함한다.
본 발명은 내생성 NAT가 이의 센스 유전자 대응물(counterpart)의 전사를 억제하는 기전을 제공한다. 본 발명은 대부분의 전사 단위로부터 전사되는 NAT의 제거 또는 저해에 의하여, 내생성 유전자 발현이 자위(locus) 특이적 방식으로 상향조절될 수 있음을 제공한다.
본 발명의 하나의 양태는 단백질 생산량을 조절하는 기능적 ncRNA의 예를 제공하고, 이러한 현상은 다수의 다른 게놈 자위에 적용할 수 있다.
뇌 유래 신경영양 인자(BDNF)는 신경 성장, 성숙 분화 및 유지에 필수적인 성장 인자의 "뉴로트로핀" 군의 구성원이다. BDNF는 또한 신경 가소성에 필수적이고, 학습, 및 기억 과정과 관련이 있는 것으로 보인다. BDNF 자위는 염색체 11 상에 있고, 두 가닥 모두로부터 활성 전사를 보이고, 이는 비코딩 NAT의 전사를 야기한다.
본 발명은 이러한 안티센스 RNA 분자의 조절 역할, 시험관내에서 및 생체내에서 센스 BDNF mRNA 및 단백질의 발현에 대하여 강력한 상호간 및 동력학적 조절을 행사하는 BDNF-AS를 특징짓는다.
본 발명의 하나의 양태는 AntagoNAT로 지칭되는 안티센스 RNA 전사체 저해성 분자를 사용하는 mRNA 발현의 상향조절을 위한 전략을 제공한다. AntagoNAT는, 예를 들면, PCT 공개 번호 제WO 2012/068340호에 기술되고, 상기 출원은 그 전문이 본원에 참고로 포함된다.
진핵생물 게놈에서 ncRNA의 수는 발달 복합성에 따라 증가함을 보여주었고, 예를 들면, 신경계에서 발현된 ncRNA의 다량의 다양성이 존재한다. 지난 몇 년간, 기능적 NAT에 대해 보고되었고, 이들의 알츠하이머병, 파킨슨병 및 취약 X 증후군을 포함하는 인간 장애에서 잠재적인 관련이 보여져 왔다. 게다가, CD97 센스 유전자의 상향조절은 이의 안티센스 RNA 전사체의 녹다운에 의해 획득될 수 있음이 보고되었다. 프로게스테론 수용체(PR: progesterone receptor)의 상향조절, 및 다른 내생성 전사체가 프로모터-유도된 비코딩 RNA의 표적화 후 보고되었다. p21 유전자의 전사활성 및 Oct4 프로모터가 NAT 감손 후 보고되었다. 안티센스 RNA-유도된 염색질 재형성은 많은 저 복사 수(low copy number) NAT에 대한 실현가능하고 동력학적인 방식으로 보인다. 만약 그렇다면, 안티센스 RNA는 주로 염색질 구조를 유지하거나 변형하는, 궁극적으로 센스 유전자 발현을 활성화시키거나 억제하는 국소적 효과를 미칠 수 있다.
PCR2는 4개의 코어 아단위로 이루어진 단백질 복합체이다: Eed, Suz12, RbAp48 및 촉매적 Ezh2, 이는 히스톤 H3-리신의 트리메틸화를 촉매한다(H3K27met3). 최근 연구는 Ezh2와 많은 ncRNA 전사체 사이의 직접적인 RNA-단백질 상호작용에 대한 증거를 제공한다. X 불활성화 및 HOX 유전자 클러스터의 다른 연구는 억제성 염색질 마크인 H3K27met3의 PRC2-매개된 유도에 관련된 RNA 전사체를 보여준다. PRC2 전사체 프로파일링은 배아 줄기 세포에서 9,000개의 PRC2-상호작용 RNA에 대해 확인되었고, 이들 중 다수는 안티센스 RNA 전사체로서 분류되었다. p15 및 DM1 유전자의 후생적 침묵은 이의 안티센스 RNA에 의해 이질염색질 형성을 수반하는 것으로 보고되었다. 최근 연구가 원래 생각하던 것 보다 동적이고 유연한 5개의 주된 염색질 유형이 존재함을 보여주기 때문에, 이질- 또는 진정-염색질 범주로의 염색질의 전통적인 이분은 완전하지 않을 수 있다. 다수의 유전자 자위에 적용할 수 있듯이, NAT는 염색질 변형에서 자위-특이적 변경을 수득하기 위하여 조작될 수 있다. 예로서, BDNF 유전자의 안티센스 전사체의 절단(siRNA에 의함) 또는 저해(AntagoNAT에 의함)는 상응하는 mRNA의 상향조절을 야기함을 보여준다.
뉴로트로핀은 뉴런의 생존, 발달, 분화 및 기능을 개선시키는 분비된 일종의 성장 인자에 속하고, BDNF는 시냅스 가소성의 중요한 분자 매개체이다. BDNF는 뉴런 및 신경교 성숙을 동시에 발생시키고, 축색 및 수지상 분화에 참여하고, 뉴런 세포 생존을 개선시키는 것으로 제시된다. 뉴로트로핀 발현 수준은 신경퇴행성 및 정신병성 및 신경발달 장애에서 손상된다. 뉴로트로핀의 상향조절은 여러 신경학적 장애에 대한 이로운 효과를 갖는 것으로 여겨진다. AntagoNAT는 BDNF-AS를 저해하고, 그 결과 다양한 질병 상태에서 뉴런 증식 및 생존을 개선시키는 치료적 전략으로서 사용될 수 있다. 자연적인 변형을 보유하고 모든 공지된 스플라이스 형태를 나타내는 것으로 추정되는, 내생성 BDNF 분자의 합성을 상향조절하는 본원에 기재된 접근법은 합성 BDNF 분자를 투여하는데 분명하고, 어쩌면 우수할 것임이 제외될 수 없다.
하나의 양태에서, 하나 이상의 안티센스 올리고뉴클레오티드에 의한 BDNF의 조정은 이의 필요가 있는 환자에게 투여되어 정상적인 대조군에 비해 BDNF 비정상적인 발현, 기능, 활성과 관련된 임의의 질환 또는 장애를 예방하거나 치료한다.
하나의 양태에서, 올리고뉴클레오티드는 본원에 기재된 BDNF의 천연 안티센스 전사체에 특이적이고, 이는 제한 없이 비-코딩 영역을 포함한다. BDNF 표적은 BDNF의 변이체; SNP를 포함한 BDNF의 돌연변이체; BDNF의 비-코딩 서열; 대립유전자, 단편 등을 포함한다. 바람직하게는, 올리고뉴클레오티드는 안티센스 RNA 분자이다.
본 발명의 양태에 따라, 표적 핵산 분자는 BDNF 폴리뉴클레오티드 단독에 한정되지 않고 BDNF의 임의의 동종형, 수용체, 동족체, 비-코딩 영역 등으로 확장된다.
하나의 양태에서, 올리고뉴클레오티드는 제한 없이 BDNF 표적의 변이체, 대립유전자, 동족체, 돌연변이체, 유도체, 단편 및 상보성 서열을 포함하는, 이들 표적의 천연 안티센스 서열(코딩과 비-코딩 영역에 대한 천연 안티센스)을 표적으로 한다. 바람직하게는, 올리고뉴클레오티드는 안티센스 RNA 또는 DNA 분자이다.
하나의 양태에서, 본 발명의 올리고머 화합물은 또한 화합물 내에서 하나 이상의 뉴클레오티드 위치에 상이한 염기가 존재하는 변이체를 포함한다. 예를 들면, 첫 번째 뉴클레오티드가 아데닌이면, 상기 위치에서 티미딘, 구아노신, 시티딘 또는 다른 천연 또는 비-천연 뉴클레오티드를 보유하는 변이체가 생성될 수 있다. 이는 안티센스 화합물의 임의의 위치에서 수행될 수 있다. 이들 화합물은 이후, 표적 핵산의 발현을 저해하는 그들의 능력을 결정하기 위하여 본 명세서에서 기술된 방법을 사용하여 시험된다.
일부 양태에서, 안티센스 화합물 및 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 50% 내지 약 60%이다. 일부 양태에서, 상동성, 서열 동일성 또는 상보성은 약 60% 내지 약 70%이다. 일부 양태에서, 상동성, 서열 동일성 또는 상보성은 약 70% 내지 약 80%이다. 일부 양태에서, 상동성, 서열 동일성 또는 상보성은 약 80% 내지 약 90%이다. 일부 양태에서, 상동성, 서열 동일성 또는 상보성은 약 90%, 약 92%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99% 또는 약 100%이다.
안티센스 화합물은 표적 핵산에 화합물의 결합이 표적 핵산의 정상적인 기능을 간섭하여 활성의 상실을 유발하고, 특정한 결합이 목적되는 조건 하에, 비-표적 핵산 서열에 안티센스 화합물의 비-특이적 결합을 회피할 수 있을 만큼 충분한 정도의 상보성이 존재할 때, 특이적으로 하이브리드화가능하다. 이러한 조건은, 다시 말하면, 생체내 분석 또는 치료적 처리의 경우에 생리학적 조건, 및 시험관내 분석의 경우에 이들 분석이 수행되는 조건을 포함한다.
안티센스 화합물은 DNA, RNA, 키메라, 치환된 것 등인 지에 상관없이, 표적 DNA 또는 RNA 분자에 화합물의 결합이 표적 DNA 또는 RNA의 정상적인 기능을 간섭하여 유용성의 상실을 유발하고, 특정한 결합이 목적되는 조건, 다시 말하면, 생체내 분석 또는 치료적 처리의 경우에 생리학적 조건, 및 시험관내 분석의 경우에 이들 분석이 수행되는 조건 하에, 비-표적 서열에 안티센스 화합물의 비-특이적 결합을 회피할 수 있을 만큼 충분한 정도의 상보성이 존재할 때, 특이적으로 하이브리드화가능하다.
하나의 양태에서, 제한 없이, 예를 들면, PCR, 하이브리드화 등을 이용하여 확인되고 확장되는 안티센스 서열, 서열 번호 3 내지 11에 제시된 하나 이상의 서열 등을 포함하는 BDNF의 표적화는 BDNF의 발현 또는 기능을 조정한다. 하나의 양태에서, 발현 또는 기능은 대조군에 비해 상향조절된다. 하나의 양태에서, 발현 또는 기능은 대조군에 비해 하향조절된다.
하나의 양태에서, 올리고뉴클레오티드는, 예를 들면, PCR, 하이브리드화 등을 사용하여 확인되고 확장되는 안티센스 서열을 포함하는 서열 번호 12 내지 49에 제시된 핵산 서열을 포함한다. 이들 올리고뉴클레오티드는 하나 이상의 변형된 뉴클레오티드, 더욱 짧은 또는 더욱 긴 단편, 변형된 결합 등을 포함할 수 있다. 변형된 결합 또는 뉴클레오티드간 연결기의 예는 포스포로티오에이트, 포스포로디티오에이트 등을 포함한다. 하나의 양태에서, 뉴클레오티드는 인 유도체를 포함한다. 본 발명의 변형된 올리고뉴클레오티드 내에서 당 또는 당 유사체 모이어티에 부착될 수 있는 인 유도체(또는 변형된 포스페이트 기)는 모노포스페이트, 디포스페이트, 트리포스페이트, 알킬포스페이트, 알칸포스페이트, 포스포로티오에이트 등일 수 있다. 상기 언급된 포스페이트 유사체의 제조, 및 뉴클레오티드, 변형된 뉴클레오티드 및 올리고뉴클레오티드 내로 그들의 통합은, 그 자체로, 공지되어 있고 본원에 기술될 필요가 없다.
안티센스의 특이성 및 민감성은 또한 치료 용도를 위하여 당업자에 의해 이용된다. 안티센스 올리고뉴클레오티드는 동물 및 인간에서 질환 상태의 치료에서 치료적 모이어티로서 사용되어 왔다. 안티센스 올리고뉴클레오티드는 인간에 안전하고 효과적으로 투여되어 왔고, 다수의 임상 시험이 현재 진행 중에 있다. 따라서 올리고뉴클레오티드는 세포, 조직 및 동물, 특히 인간의 치료를 위한 치료 섭생에서 유용하도록 형성될 수 있는 유용한 치료 양식일 수 있는 것으로 확립된다.
본 발명의 양태에서, 올리고머 안티센스 화합물, 특히 올리고뉴클레오티드는 표적 핵산 분자에 결합하고 표적 유전자에 의해 코딩된 분자의 발현 및/또는 기능을 조정한다. 간섭되는 DNA의 기능은, 예를 들면, 복제 및 전사를 포함한다. 간섭되는 RNA의 기능은, 예를 들면, RNA의 단백질 번역 부위로의 전좌, RNA로부터 단백질의 번역, 하나 이상의 mRNA 종을 수득하기 위한 RNA의 스플라이싱, 및 RNA에 관련되거나 RNA에 의해 촉진될 수 있는 촉매 활성과 같은 생명 유지에 필요한 모든 기능을 포함한다. 이들 기능은 목적되는 기능에 따라서, 상향조절되거나 저해될 수 있다.
안티센스 화합물은 안티센스 올리고머 화합물, 안티센스 올리고뉴클레오티드, 외부 가이드 서열(EGS) 올리고뉴클레오티드, 교대 스플라이서, 프라이머, 프로브, 및 표적 핵산의 일부분 이상에 하이브리드화되는 다른 올리고머 화합물을 포함한다. 이와 같이, 이들 화합물은 단일-가닥, 이중-가닥, 부분적으로 단일-가닥, 또는 원형 올리고머 화합물의 형태로 도입될 수 있다.
본 발명의 맥락에서, 특정 핵산 분자에 안티센스 화합물의 표적화는 다단계 과정일 수 있다. 이러한 과정은 통상적으로, 기능이 조정되어야 하는 표적 핵산의 확인으로 시작된다. 표적 핵산은, 예를 들면, 발현이 특정 장애 또는 질환 상태, 또는 감염성 병원체로부터 핵산 분자와 연관되는 세포 유전자(또는 유전자로부터 전사된 mRNA)일 수 있다. 본 발명에서, 표적 핵산은 뇌 유래 신경영양 인자(BDNF)를 코딩한다.
표적화 과정은 통상적으로 또한 목적되는 효과, 예를 들면, 발현의 조정이 야기될 수 있도록 안티센스 상호작용이 발생하는 표적 핵산 내에서 최소한 하나의 표적 영역, 분절, 또는 부위의 결정을 포함한다. 본 발명의 맥락에서, 용어 "영역"은 하나 이상의 확인가능한 구조, 기능, 또는 특징을 갖는 표적 핵산의 부분으로서 정의된다. 분절은 표적 핵산의 영역 내에 있다. "분절"은 표적 핵산 내에 영역의 더욱 작은 또는 하위-부분으로서 정의된다. 본 발명에서, "부위"는 표적 핵산 내에 위치로서 정의된다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF)의 천연 안티센스 서열에 결합하고 뇌 유래 신경영양 인자(BDNF)의 발현 및/또는 기능을 조정한다(서열 번호 1 및 2). 안티센스 서열의 예는 서열 번호 3 내지 55를 포함한다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 하나 이상의 분절에 결합하고 뇌 유래 신경영양 인자(BDNF)의 발현 및/또는 기능을 조정한다. 분절은 뇌 유래 신경영양 인자(BDNF) 센스 또는 안티센스 폴리뉴클레오티드의 5개 이상의 연속 뉴클레오티드를 포함한다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF)의 천연 안티센스 서열에 특이적이고, 여기서 뇌 유래 신경영양 인자(BDNF)의 천연 안티센스 서열에 올리고뉴클레오티드의 결합은 뇌 유래 신경영양 인자(BDNF)의 발현 및/또는 기능을 조정한다.
하나의 양태에서, 올리고뉴클레오티드 화합물은, 예를 들면, PCR, 하이브리드화 등을 사용하여 확인되고 확장되는 안티센스 서열, 서열 번호 12 내지 49에 제시된 서열을 포함한다. 이들 올리고뉴클레오티드는 하나 이상의 변형된 뉴클레오티드, 더욱 짧은 또는 더욱 긴 단편, 변형된 결합 등을 포함할 수 있다. 변형된 결합 또는 뉴클레오티드간 연결기의 예는 포스포로티오에이트, 포스포로디티오에이트 등을 포함한다. 하나의 양태에서, 뉴클레오티드는 인 유도체를 포함한다. 본 발명의 변형된 올리고뉴클레오티드 내에서 당 또는 당 유사체 모이어티에 부착될 수 있는 인 유도체(또는 변형된 포스페이트 기)는 모노포스페이트, 디포스페이트, 트리포스페이트, 알킬포스페이트, 알칸포스페이트, 포스포로티오에이트 등일 수 있다. 상기 언급된 포스페이트 유사체의 제조, 및 뉴클레오티드, 변형된 뉴클레오티드 및 올리고뉴클레오티드 내로 그들의 통합은, 그 자체로, 공지되어 있고 본원에 기술될 필요가 없다.
당해 분야에 공지된 바와 같이, 번역 개시 코돈이 전형적으로 5'-AUG(전사된 mRNA 분자에서; 상응하는 DNA 분자에서 5'-ATG)이기 때문에, 상기 번역 개시 코돈은 "AUG 코돈", "시작 코돈", 또는 "AUG 시작 코돈"으로도 지칭된다. 소수의 유전자는 RNA 서열 5'-GUG, 5'-UUG 또는 5'-CUG를 갖는 번역 개시 코돈을 갖고; 5'-AUA, 5'-ACG 및 5'-CUG는 생체내에서 기능하는 것으로 밝혀졌다. 따라서, 용어 "번역 개시 코돈" 및 "시작 코돈"은 각 경우에 개시자 아미노산이 전형적으로 메티오닌(진핵생물에서) 또는 포르밀메티오닌(원핵생물에서)이긴 하지만, 많은 코돈 서열을 포함할 수 있다. 진핵 및 원핵 유전자는 2개 이상의 대안적 시작 코돈을 갖을 수도 있고, 이들 중에서 임의의 하나가 특정 세포 유형 또는 조직에서, 또는 특정한 일단의 조건하에 번역 개시에 우선적으로 이용될 수 있다. 본 발명의 맥락에서, "시작 코돈" 및 "번역 개시 코돈"은 이러한 코돈의 서열(들)에 상관없이, 뇌 유래 신경영양 인자(BDNF)를 코딩하는 유전자로부터 전사된 mRNA의 번역을 개시하기 위하여 생체내에서 이용되는 코돈(들)을 지칭한다. 유전자의 번역 종결 코돈(또는 "종결 코돈")은 3가지 서열, 다시 말하면, 5'-UAA, 5'-UAG 및 5'-UGA(상응하는 DNA 서열은 각각 5'-TAA, 5'-TAG 및 5'-TGA이다) 중에서 하나를 가질 수 있다.
용어 "시작 코돈 영역" 및 "번역 개시 코돈 영역"은 번역 개시 코돈으로부터 어느 한쪽 방향(다시 말하면, 5' 또는 3')으로 약 25 내지 약 50개 연속 뉴클레오티드를 포함하는 이러한 mRNA 또는 유전자의 일부분을 지칭한다. 유사하게, 용어 "종결 코돈 영역" 및 "번역 종결 코돈 영역"은 번역 종결 코돈으로부터 어느 한쪽 방향(다시 말하면, 5'또는 3')으로 약 25 내지 대략 50개 연속 뉴클레오티드를 포함하는 이러한 mRNA 또는 유전자의 일부분을 지칭한다. 결과적으로, "시작 코돈 영역"(또는 "번역 개시 코돈 영역") 및 "종결 코돈 영역"(또는 "번역 종결 코돈 영역")은 본 발명의 안티센스 화합물로 효과적으로 표적화될 수 있는 최대 영역이다.
당해 분야에서 번역 개시 코돈 및 번역 종결 코돈 사이에 영역을 지칭하는 것으로 알려져 있는 오픈 리딩 프레임(open reading frame, ORF) 또는 "코딩 영역"은 또한 효과적으로 표적화될 수 있는 영역이다. 본 발명의 맥락에서, 표적화된 영역은 유전자의 오픈 리딩 프레임(ORF)의 번역 개시 또는 종결 코돈을 포함하는 유전자내(intragenic) 영역이다.
다른 표적 영역에는 당분야에서 번역 개시 코돈으로부터 5' 방향으로 mRNA의 일부분을 지칭하는 것으로 알려져 있고, 따라서 mRNA(또는 유전자 상에서 상응하는 뉴클레오티드)의 5' 캡 부위 및 번역 개시 코돈 사이에 뉴클레오티드를 포함하는 5' 비번역 영역(5'UTR)이 포함된다. 또 다른 표적 영역은 당분야에서 번역 종결 코돈으로부터 3' 방향으로 mRNA의 일부분을 지칭하는 것으로 알려져 있고, 따라서 mRNA(또는 유전자 상에서 상응하는 뉴클레오티드)의 번역 종결 코돈 및 3' 말단 사이에 뉴클레오티드를 포함하는 3' 비번역 영역(3'UTR)을 포함한다. mRNA의 5' 캡 부위는 5'-5' 트리포스페이트 연결기를 통하여 상기 mRNA의 5'-최말단 잔기에 결합된 N7-메틸화된 구아노신 잔기를 포함한다. mRNA의 5' 캡 영역은 캡 부위에 인접한 첫 50개 뉴클레오티드 뿐만 아니라 5' 캡 구조 자체를 포함하는 것으로 간주된다. 본 발명을 위한 다른 표적 영역은 5' 캡 영역이다.
일부 진핵 mRNA 전사체는 직접적으로 번역되지만, 대부분은 "인트론"으로 알려져 있는 하나 이상의 영역을 보유하고, 이들은 번역되기 전에 전사체로부터 잘려나간다. 나머지(및 따라서 번역된) 영역은 "엑손"으로 알려져 있으며, 함께 스플라이스되어 연속 mRNA를 형성한다. 하나의 양태에서, 스플라이스 부위, 다시 말하면, 인트론-엑손 접합 또는 엑손-인트론 접합 부위를 표적화하는 것은 이상 스플라이싱이 질환에 연관되거나, 특정 스플라이스 산물의 과다 생산이 질환과 연관되는 상황에서 특히 유용하다. 재배열 또는 결실로 인한 이상 융합 접합은 표적 부위의 다른 양태이다. 상이한 유전자 소스로부터 2개(또는 이상)의 mRNA의 스플라이싱 과정을 통하여 생산된 mRNA 전사체는 "융합 전사체"로 알려져 있다. 인트론은, 예를 들면, DNA 또는 pre-mRNA를 표적으로 하는 안티센스 화합물을 이용하여 효과적으로 표적화될 수 있다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 표적 폴리뉴클레오티드의 코딩 및/또는 비-코딩 영역에 결합하고 표적 분자의 발현 및/또는 기능을 조정한다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 천연 안티센스 폴리뉴클레오티드에 결합하고 표적 분자의 발현 및/또는 기능을 조정한다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 센스 폴리뉴클레오티드에 결합하고 표적 분자의 발현 및/또는 기능을 조정한다.
대안적 RNA 전사체는 DNA의 동일한 게놈 영역으로부터 만들어질 수 있다. 이들 대안적 전사체는 일반적으로 "변이체"로 알려져 있다. 더욱 특이적으로, "pre-mRNA 변이체"는 그들의 시작 또는 종결 위치에서 동일한 게놈 DNA로부터 만들어진 다른 전사체와 상이하며 인트론 및 엑손 서열을 모두 보유하는 동일한 게놈 DNA로부터 생산된 전사체이다.
스플라이싱 동안 하나 이상의 엑손 또는 인트론 영역, 또는 이들의 일부분을 잘라낼 때, pre-mRNA 변이체는 더욱 작은 "mRNA 변이체"를 만든다. 결과적으로, mRNA 변이체는 가공된 pre-mRNA 변이체이고, 각 독특한 pre-mRNA 변이체는 스플라이스의 결과로 독특한 mRNA 변이체를 항상 만들어낸다. 이들 mRNA 변이체는 또한 "대안적 스플라이싱 변이체"로 알려져 있다. pre-mRNA 변이체의 스플라이싱이 발생되지 않으면, pre-mRNA 변이체는 mRNA 변이체와 동일하게 된다.
변이체는 전사의 시작 또는 종결에 대한 대안적 신호를 이용하여 만들어질 수 있다. Pre-mRNA 및 mRNA는 하나 이상의 시작 코돈 또는 종결 코돈을 보유할 수 있다. 대안적 시작 코돈을 이용하는 pre-mRNA 또는 mRNA으로부터 기원하는 변이체는 pre-mRNA 또는 mRNA의 "대안적 시작 변이체"로 알려져 있다. 대안적 종결 코돈을 이용하는 이들 전사체는 pre-mRNA 또는 mRNA의 "대안적 종결 변이체"로 알려져 있다. 대안적 종결 변이체 중 한 가지 특정 유형은 "polyA 변이체"이며, 여기서 만들어진 다중 전사체는 전사 기전에 의해 "polyA 종결 신호" 중 하나의 대안적 선별에 기인하고, 따라서 독특한 polyA 부위에서 종결되는 전사체가 만들어진다. 본 발명의 맥락에서, 본원에 기술된 변이체의 유형은 또한 표적 핵산의 양태이다.
안티센스 화합물이 하이브리드화되는 표적 핵산 상의 위치는 활성 안티센스 화합물이 표적화되는 표적 영역의 5개 이상 뉴클레오티드 길이 부분으로 정의된다.
일정한 예시적인 표적 분절의 특정한 서열이 본원에서 기술되긴 하지만, 당업자는 이들이 본 발명의 범위 내에서 특정 양태를 예시하고 기술한다는 것을 인지할 것이다. 추가적인 표적 단편은 본 내용을 근거하여 당업자에 의해 용이하게 인지될 수 있다.
예시된 바람직한 표적 분절로부터 선택된 5개 이상의 연속 뉴클레오티드 스트레치(stretch)를 포함하는 5 내지 100개 뉴클레오티드 길이의 표적 분절은 표적화에도 적합한 것으로 간주된다.
표적 분절은 예시된 바람직한 표적 분절 중에서 하나의 5'-말단으로부터 5개 이상의 연속 뉴클레오티드(나머지 뉴클레오티드는 표적 분절의 5' 말단의 바로 상류에서 시작하고, DNA 또는 RNA가 약 5 내지 약 100개 뉴클레오티드를 포함할 때까지 연속되는 동일한 DNA 또는 RNA의 연속 스트레치이다)를 포함하는 DNA 또는 RNA 서열을 포함할 수 있다. 유사하게, 바람직한 표적 분절은 예시된 바람직한 표적 분절 중에서 하나의 3'-말단으로부터 5개 이상의 연속 뉴클레오티드(나머지 뉴클레오티드는 표적 분절의 3' 말단의 바로 하류에서 시작하고, DNA 또는 RNA가 약 5 내지 약 100개 뉴클레오티드를 포함할 때까지 연속되는 동일한 DNA 또는 RNA의 연속 스트레치이다)를 포함하는 DNA 또는 RNA 서열로 대표된다. 본원에 예시된 표적 분절을 갖춘 당업자는, 과도한 실험 없이, 더욱 바람직한 표적 분절을 확인할 수 있을 것이다.
일단 하나 이상의 표적 영역, 분절 또는 부위가 확인되면, 표적에 충분한 상보성을 가진, 다시 말하면, 원하는 효과를 제공할 만큼 충분히 잘 하이브리드화되고 충분한 특이성을 갖는 안티센스 화합물이 선택된다.
본 발명의 양태에서, 올리고뉴클레오티드는 특정 표적의 안티센스 가닥에 결합한다. 올리고뉴클레오티드는 5개 이상 길이의 뉴클레오티드이고, 전체 길이의 표적 뉴클레오티드를 수용하는 올리고뉴클레오티드가 합성되도록 위하여, 각 올리고뉴클레오티드가 중복 서열을 표적으로 하도록 합성될 수 있다. 표적은 또한 코딩 뿐만 아니라 비-코딩 영역을 포함한다.
하나의 양태에서, 안티센스 올리고뉴클레오티드에 의해 특정 핵산을 표적으로 하는 것이 바람직하다. 특정 핵산에 안티센스 화합물의 표적화는 다단계 과정이다. 과정은 통상적으로 기능이 조정되는 핵산 서열의 확인으로 시작된다. 이는, 예를 들면, 발현이 특정 질환 또는 질환 상태와 연관되는 세포 유전자(또는 상기 유전자로부터 전사된 mRNA), 또는, 예를 들면, 비-코딩 RNA(ncRNA)와 같은 비-코딩 폴리뉴클레오티드일 수 있다.
RNA는 (1) 단백질로 번역되는, 메신저 RNA(mRNA), 및 (2) 비-단백질-코딩 RNA(ncRNA)로 분류될 수 있다. ncRNA는 마이크로 RNA, 안티센스 전사체 및 고밀도의 종결 코돈을 포함하고 임의의 광범위한 "오픈 리딩 프레임"이 부족한 다른 전사 단위(TU)를 포함한다. 많은 ncRNA는 단백질-코딩 좌위의 3' 비번역 영역(3'UTR)에서 개시 부위로부터 시작되는 것으로 보인다. ncRNA는 아주 드물고, FANTOM 협회에 의해 서열화된 ncRNA의 최소한 절반은 폴리아데닐화되지 않는 것으로 보인다. 대부분의 조사자들은 분명한 이유로, 가공되고 세포질로 배출되는 폴리아데닐화된 mRNA에 초점을 맞추었다. 최근에, 비-폴리아데닐화된 핵 RNA 세트는 매우 크고, 이와 같은 많은 전사체가 소위 유전자내 영역에서 생성되는 것으로 밝혀졌다. ncRNA가 유전자 발현을 조정할 수 있는 기전은 표적 전사체와의 염기 대합에 의한 것이다. 염기 대합에 의해 기능하는 RNA는 (1) 동일한 유전적 위치에서, 그러나 그들이 작용하는 RNA에 반대 가닥 상에 코딩되고, 따라서 그들의 표적에 대해 완벽한 상보성을 나타내는 cis-코딩된 RNA, 및 (2) 그들이 작용하는 RNA와는 별개의 염색체 위치에서 코딩되며, 일반적으로 그들의 표적과 완벽한 염기-대합 잠재력을 나타내지 않는 trans-코딩된 RNA로 분류될 수 있다.
이론에 한정됨 없이, 본원에 기술된 안티센스 올리고뉴클레오티드에 의한 안티센스 폴리뉴클레오티드의 교란은 상응하는 센스 메신저 RNA의 발현을 변경시킬 수 있다. 하지만, 이와 같은 조절은 부조화적(discordant)(안티센스 녹다운은 메신저 RNA 상승을 야기한다) 또는 조화적(concordant)(안티센스 녹다운은 수반되는 메신저 RNA 감소를 야기한다)일 수 있다. 이들 경우에, 안티센스 올리고뉴클레오티드는 안티센스 전사체의 중복 또는 비-중복 부위로 표적화되어, 이의 녹다운 또는 제거를 초래할 수 있다. 코딩 뿐만 아니라 비-코딩 안티센스는 동일한 방식으로 표적화될 수 있고, 어느 종류든 조화적 또는 부조화적 방식으로 상응하는 센스 전사체를 조절할 수 있다. 표적에 대항하여 사용되는 신규한 올리고뉴클레오티드를 확인하는데 사용되는 전략은 안티센스 올리고뉴클레오티드에 의한 안티센스 RNA 전사체의 녹다운 또는 원하는 표적을 조정하는 임의의 다른 수단에 기초될 수 있다.
전략 1: 부조화적 조절의 경우, 안티센스 전사체의 녹다운은 통상적(센스) 유전자의 발현을 상승시킨다. 후자 유전자가 공지의 또는 가상 약물 표적을 코딩하면, 이의 안티센스 대응물의 녹다운은 수용체 효능제 또는 효소 자극물질의 작용을 의식적으로 모방할 수 있다.
전략 2: 조화적 조절의 경우, 안티센스 및 센스 전사체 둘 모두를 동시에 녹다운 시킬 수 있고, 따라서 통상의(센스) 유전자 발현의 상승적 감소를 얻을 수 있다. 예를 들면, 안티센스 올리고뉴클레오티드가 녹다운을 달성하는데 이용되면, 이러한 전략은 센스 전사체를 표적으로 하는 하나의 안티센스 올리고뉴클레오티드 및 상응하는 안티센스 전사체를 표적으로 하는 다른 안티센스 올리고뉴클레오티드, 또는 중복 센스 및 안티센스를 동시에 표적으로 하는 단일 대칭적 안티센스 올리고뉴클레오티드에 적용하는데 이용될 수 있다.
본 발명에 따르면, 안티센스 화합물은 안티센스 올리고뉴클레오티드, 리보자임, 외부 가이드 서열(EGS) 올리고뉴클레오티드, siRNA 화합물, 단일 또는 이중-가닥 RNA 간섭(RNAi) 화합물, 예를 들면, siRNA 화합물, 및 표적 핵산의 최소한 일부분에 하이브리드화되고 이의 기능을 조정하는 기타 올리고머 화합물을 포함한다. 이와 같이, 안티센스 화합물들은 DNA, RNA, DNA-유사, RNA-유사, 또는 이들의 혼합물이거나, 이들 중에서 하나 이상의 모방체일 수 있다. 이들 화합물은 단일-가닥, 이중-가닥, 원형 또는 헤어핀 올리고머 화합물일 수 있고, 내부 또는 말단 중배(bulge), 미스매치 또는 루프와 같은 구조적 요소를 포함할 수 있다. 안티센스 화합물은 일과적으로 선형으로 제조되지만, 결합되거나, 원형 및/또는 분지형으로 제조될 수 있다. 안티센스 화합물은, 예를 들면, 하이브리드화되면 전체적으로 또는 부분적으로 이중-가닥 화합물을 형성하는 2개의 가닥, 또는 하이브리드화 및 전체적으로 또는 부분적으로 이중-가닥 화합물의 형성을 가능하게 할 만큼 충분한 자가-상보성을 갖는 단일 가닥과 같은 구조체를 포함할 수 있다. 2개 가닥은 내부에서 연결되어 3' 또는 5' 말단이 자유로운 상태로 남아 있거나, 또는 연결되어 연속적인 헤어핀 구조 또는 루프를 형성할 수 있다. 헤어핀 구조는 단일 가닥 특성의 연장부를 발생시키는 5' 또는 3' 말단 상에 오버행(overhang)을 함유할 수 있다. 이중 가닥 화합물은 선택적으로 이들 말단에 오버행을 포함할 수 있다. 추가 변형은 말단 중의 한쪽, 선택된 뉴클레오티드 위치, 당 위치, 또는 뉴클레오티드간 연결기 중의 하나에 부착된 접합체(conjugate) 기를 포함할 수 있다. 대안적으로, 2개 가닥은 비-핵산 모이어티 또는 링커 기를 통하여 연결될 수 있다. 한 개 가닥으로부터만 형성될 때, dsRNA는 이중나선을 형성하기 위하여 자체적으로 둘로 접히는 자가-상보성 헤어핀 유형 분자의 형태를 취할 수 있다. 따라서, dsRNA는 완전히 또는 부분적으로 이중 가닥이 될 수 있다. 유전자 발현의 특이적 조정은 유전자도입 세포주에서 dsRNA 헤어핀의 안정된 발현에 의해 달성될 수 있지만, 일부 양태에서, 유전자 발현 또는 기능은 상향조절된다. 2개 가닥, 또는 이중나선을 형성하기 위하여 자체적으로 둘로 접히는 자가-상보성 헤어핀 유형 분자의 형태를 취하는 단일 가닥으로부터 형성될 때, 이들 2개 가닥(또는 단일 가닥의 이중나선 형성 영역)은 왓슨-크릭 방식으로 염기 쌍을 이루는 상보성 RNA 가닥이다.
일단 시스템내로 도입되면, 본 발명의 화합물은 표적 핵산의 절단 또는 다른 변형을 달성하기 위하여 하나 이상의 효소 또는 구조적 단백질의 작용을 유도하거나, 점유-기반 기전(occupancy-based mechanisms)을 통하여 작용할 수 있다. 일반적으로, 핵산(올리고뉴클레오티드 포함)은 "DNA-유사"(즉, 일반적으로 하나 이상의 2'-데옥시 당을 보유하고, 일반적으로 U 염기 대신 T를 보유함) 또는 "RNA-유사"(즉, 일반적으로 하나 이상의 2'-히드록실 또는 2'-변형된 당을 보유하고, 일반적으로 T 염기 대신 U 염기를 보유함)로 기술될 수 있다. 핵산 나선은 한 가지 이상의 구조 유형을 채택할 수 있지만, 가장 일반적으로 A- 및 B-형이다. 일반적으로, B-형-유사 구조를 가지는 올리고뉴클레오티드는 "DNA-유사"이며, A-형-유사 구조를 가지는 올리고뉴클레오티드는 "RNA-유사"이다. 일부(키메라) 양태에서, 안티센스 화합물은 A- 및 B-형 영역을 모두 함유할 수 있다.
하나의 양태에서, 목적되는 올리고뉴클레오티드 또는 안티센스 화합물은 안티센스 RNA, 안티센스 DNA, 키메라 안티센스 올리고뉴클레오티드, 변형된 연결기를 포함하는 안티센스 올리고뉴클레오티드, 간섭 RNA(RNAi), 짧은 간섭 RNA(siRNA); 마이크로 간섭 RNA(miRNA); 작은, 일시적 RNA(stRNA); 또는 짧은 헤어핀 RNA(shRNA); 작은 RNA-유도된 유전자 활성화(RNAa); 작은 활성화 RNA(saRNA), 또는 이들의 조합 중 하나 이상을 포함한다.
dsRNA는 또한 "작은 RNA-유도된 유전자 활성화" 또는 RNAa로 명명된 기전인 유전자 발현을 활성화시킬 수 있다. dsRNA 표적화 유전자 프로모터는 관련 유전자의 강력한 전사 활성화를 유도한다. RNAa는 "작은 활성화 RNA(saRNA)"로 불리는 합성 dsRNA를 이용하여 인간 세포에서 설명되었다. 현재까지 RNAa가 다른 유기체에서 보존되는 지는 밝혀지지 않았다.
작은 이중-가닥 RNA(dsRNA), 예를 들면, 작은 간섭 RNA(siRNA) 및 마이크로RNA(miRNA)는 RNA 간섭(RNAi)으로 알려져 있는 진화론적으로 보존된 기전의 촉발자인 것으로 밝혀졌다. RNAi는 재형성 크로마틴을 통하여 유전자 침묵을 일관되게 유도하여, 전사 억제, 상보성 mRNA 분해 또는 단백질 번역 차단을 유발한다. 하지만, 하기 실시예 부분에서 상세하게 설명된 경우에서, 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드 및 이들의 코딩된 산물의 발현 및/또는 기능을 증가시키는 것으로 보인다. dsRNA는 또한, 작은 활성화 RNA(saRNA)로 작용할 수 있다. 이론에 한정됨 없이, 유전자 프로모터 내에 서열을 표적으로 함으로써, saRNA는 dsRNA-유도된 전사 활성화(RNAa)로 지칭되는 현상에서 표적 유전자 발현을 유도할 것이다.
추가의 양태에서, 본 발명에서 확인된 "바람직한 표적 분절"은 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 발현을 조정하는 추가 화합물을 스크리닝하는데 이용될 수 있다. "조정물질(modulator)"은 뇌 유래 신경영양 인자(BDNF)를 코딩하는 핵산 분자의 발현을 감소 또는 증가시키는 화합물이며, 바람직한 표적 분절에 상보성인 5개 이상의 뉴클레오티드 부분을 포함한다. 스크리닝 방법은 뇌 유래 신경영양 인자(BDNF)의 센스 또는 천연 안티센스 폴리뉴클레오티드를 코딩하는 핵산 분자의 바람직한 표적 분절을 하나 이상의 후보 조정물질과 접촉시키는 단계, 및 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드, 예를 들면, 서열 번호 12 내지 49를 코딩하는 핵산 분자의 발현을 감소 또는 증가시키는 하나 이상의 후보 조정물질을 선별하는 단계를 포함한다. 일단 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드를 코딩하는 핵산 분자의 발현을 조정(예를 들면, 감소 또는 증가)시킬 수 있는 것으로 확인되면, 조정물질은 이후, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능의 추가 연구, 또는 본 발명에 따른 연구, 진단 또는 치료 물질로서 용도에 이용될 수 있다.
천연 안티센스 서열의 표적화는 바람직하게는 표적 유전자, 예를 들면, BDNF 유전자(예를 들면, NM_170735 및 NM_007540)의 기능을 조정한다. 하나의 양태에서, 표적은 BDNF 유전자의 안티센스 폴리뉴클레오티드이다. 하나의 양태에서, 안티센스 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드(예를 들면, 수탁 번호 NM_170735 및 NM_007540)의 센스 및/또는 천연 안티센스 서열, 변이체, 대립유전자, 동종형, 동족체, 돌연변이체, 유도체, 단편 및 이들의 상보성 서열이다. 바람직하게는, 올리고뉴클레오티드는 안티센스 분자이고, 표적은 안티센스 및/또는 센스 BDNF 폴리뉴클레오티드의 코딩 및 비-코딩 영역을 포함한다.
본 발명의 바람직한 표적 분절은 본 발명의 개별 상보성 안티센스 화합물과 복합되어 안정화된 이중-가닥(duplexed) 올리고뉴클레오티드를 형성할 수도 있다.
이러한 이중 가닥 올리고뉴클레오티드 모이어티는 당해 분야에서 표적 발현을 조정하고, 안티센스 기전을 통하여 번역 뿐만 아니라 RNA 가공을 조절하는 것으로 알려져 있다. 게다가, 이들 이중-가닥 모이어티는 화학적 변형을 받을 수도 있다. 예를 들면, 이러한 이중-가닥 모이어티는 표적에 대한 이중나선의 안티센스 가닥의 고전적인 하이브리드화에 의해 표적을 저해하여, 표적의 효소적 분해를 촉발시키는 것으로 밝혀졌다.
하나의 양태에서, 안티센스 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드(예를 들면, 수탁 번호 NM_170735 및 NM_007540), 변이체, 대립유전자, 동종형, 동족체, 돌연변이체, 유도체, 단편 및 이들의 상보성 서열을 표적으로 한다. 바람직하게는 올리고뉴클레오티드는 안티센스 분자이다.
본 발명의 양태에 따르면, 표적 핵산 분자는 BDNF에만 한정되지 않고, 이의 임의의 폴리뉴클레오티드 변이체 및, BDNF 발현 산물 및/또는 이의 임의의 동종형을 생산하거나, 이에 영향을 주거나, 이에 충격을 주거나, 이를 야기하거나, 이와 관련된 임의의 폴리뉴클레오티드까지 확장된다.
하나의 양태에서, 올리고뉴클레오티드는 BDNF 폴리뉴클레오티드의 천연 안티센스 서열, 예를 들면, 서열 번호 3 내지 11로서 기술된 폴리뉴클레오티드 및 임의의 변이체, 대립유전자, 동족체, 돌연변이체, 유도체, 단편 및 이들의 상보성 서열을 표적으로 한다. 안티센스 올리고뉴클레오티드의 예는 서열 번호 12 내지 49로서 기술된다.
하나의 양태에서, 올리고뉴클레오티드는, 예를 들면, BDNF 폴리뉴클레오티드와 연관된 비-코딩 센스 및/또는 안티센스 서열을 포함하지만 이에 한정되지 않는 BDNF 안티센스의 핵산 서열에 상보성이거나 또는 이들에 결합하고, BDNF 분자의 발현 및/또는 기능을 조정한다.
하나의 양태에서, 올리고뉴클레오티드는 서열 번호 3 내지 11로서 기술된 BDNF 천연 안티센스의 핵산 서열에 상보성이거나 이들에 결합하고, BDNF 분자의 발현 및/또는 기능을 조정한다.
하나의 양태에서, 올리고뉴클레오티드는 서열 번호 12 내지 49의 5개 이상의 연속 뉴클레오티드 서열을 포함하고, BDNF 분자의 발현 및/또는 기능을 조정한다.
폴리뉴클레오티드 표적은 BDNF의 일족 구성원, BDNF의 변이체; SNP를 포함하는 BDNF의 돌연변이체; BDNF의 비-코딩 서열; BDNF의 대립유전자; 종 변이체, 단편 등을 포함한 BDNF를 포함한다. 바람직하게는, 올리고뉴클레오티드는 안티센스 분자이다.
하나의 양태에서, BDNF 폴리뉴클레오티드를 표적으로 하는 올리고뉴클레오티드는 안티센스 RNA, 간섭 RNA(RNAi), 짧은 간섭 RNA(siRNA); 마이크로 간섭 RNA(miRNA); 작은, 일시적 RNA(stRNA); 또는 짧은, 헤어핀 RNA(shRNA); 작은 RNA-유도된 유전자 활성화(RNAa); 또는 작은 활성화 RNA(saRNA)를 포함한다.
하나의 양태에서, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드, 예를 들면, 서열 번호 3 내지 55의 표적화는 이들 표적의 발현 또는 기능을 조정한다. 하나의 양태에서, 발현 또는 기능은 대조군과 비교하여 상향조절된다. 하나의 양태에서, 발현 또는 기능은 대조군과 비교하여 하향조절된다.
하나의 양태에서, 안티센스 화합물은 서열 번호 12 내지 49로서 기술된 서열을 포함한다. 이들 올리고뉴클레오티드는 하나 이상의 변형된 뉴클레오티드, 더욱 짧은 또는 더욱 긴 단편, 변형된 결합 등을 포함할 수 있다.
하나의 양태에서, 서열 번호 12 내지 49는 하나 이상의 LNA 뉴클레오티드를 포함한다. 표 1에서는 본 발명의 방법에 유용한 대표적인 안티센스 올리고뉴클레오티드를 도시한다.
목적되는 표적 핵산의 조정은 당해 분야에 공지된 몇 가지 방식으로 수행될 수 있다. 예를 들면, 안티센스 올리고뉴클레오티드, siRNA 등. 효소적 핵산 분자(예를 들면, 리보자임)는 뉴클레오티드 염기 서열-특이적 방식으로 다른 별도의 핵산 분자를 반복적으로 절단하는 능력을 포함하여, 다양한 반응 중에서 하나 이상을 촉매할 수 있는 핵산 분자이다. 이러한 효소적 핵산 분자는, 예를 들면, 실질적으로 임의의 RNA 전사체를 표적으로 하는데 사용될 수 있다
이들의 서열-특이성 때문에, trans-절단 효소적 핵산 분자는 인간 질환에 대한 치료 물질로서 가능성을 보여준다. 효소적 핵산 분자는 세포성 RNA의 배경 내에 특이적 RNA 표적을 절단하도록 설계될 수 있다. 이러한 절단 현상은 mRNA를 비-기능성으로 만들고, 상기 RNA로부터 단백질 발현을 폐기시킨다. 이러한 방식에서, 질환 상태와 연관된 단백질의 합성이 선택적으로 억제될 수 있다.
일반적으로, RNA 절단 활성을 가진 효소적 핵산은 먼저, 표적 RNA에 결합함으로써 작용한다. 이러한 결합은 표적 RNA를 절단하는 작용을 하는 분자의 효소적 부분에 근접하게 유지되는 효소적 핵산의 표적 결합 부분을 통하여 일어난다. 따라서, 효소적 핵산은 먼저 표적 RNA를 인지하고, 그 다음 상보성 염기 대합을 통하여 표적 RNA에 결합하고, 정확한 부위에 일단 결합되면, 효소적으로 작용하여 표적 RNA를 절단한다. 이러한 표적 RNA의 전략적 절단은 코딩된 단백질의 합성을 지시하는 능력을 파괴시킬 것이다. 효소적 핵산은 RNA 표적에 결합하여 이를 절단시킨 후, 다른 표적을 찾기 위하여 RNA로부터 방출되고, 새로운 표적에 반복적으로 결합하여 이들을 절단할 수 있다.
시험관내 선별(진전) 전략(문헌 [Orgel, (1979) Proc. R. Soc. London, B 205, 435])과 같은 여러 전략이 포스포디에스테르 연결기와 아미드 연결기의 절단 및 결찰과 같은 다양한 반응을 촉매할 수 있는 새로운 핵산 촉매를 개발하는데 사용되고 있다.
촉매 활성에 최적인 리보자임의 개발은 유전자 발현을 조절하기 위한 목적으로 RNA-절단 리보자임을 사용하는 임의의 전략에 상당히 기여할 것이다. 예를 들면, 해머헤드(hammerhead) 리보자임은 Mg2+ 보조인자의 포화 농도(10mM)의 존재에서 대략 1분의 촉매 속도(kcat)로 기능한다. 인공 "RNA 리가아제" 리보자임은 대략 100분-1의 속도로 상응하는 자가-변형 반응을 촉매하는 것으로 나타났다. 또한, DNA로 구성된 기질 결합 팔(arm)을 가지고 있는 일정한 변형된 해머헤드 리보자임은 100분-1에 근접하는 다중 턴-오버 속도로 RNA 절단을 촉매한다. 최종적으로, 일정한 뉴클레오티드 유사체로 해머헤드의 촉매 코어 내에 특이적 잔기의 대체는 촉매 속도에서 많게는 10배 향상을 보이는 변형된 리보자임을 제공한다. 이들 발견은 리보자임이 대부분의 천연 자가-절단 리보자임에 의해 시험관내에서 나타나는 것보다 훨씬 큰 촉매 속도로 화학적 변형을 촉진할 수 있다는 것을 설명한다. 그 다음, 최대 촉매 활성을 제공하기 위하여 일정한 자가-절단 리보자임의 구조를 최적화하거나, RNA 포스포디에스테르 절단에 대해 훨씬 빠른 속도를 보여주는 완전히 신규한 RNA 모티프를 만드는 것이 가능하다.
"해머헤드" 모델에 적합한 RNA 촉매에 의한 RNA 기질의 분자내 절단은 1987년에 처음 밝혀졌다(문헌 [Uhlenbeck, O. C. (1987) Nature, 328: 596-600]). RNA 촉매가 회수되고 다중 RNA 분자와 반응되었는데, 이는 상기 촉매가 진정한 촉매성임을 증명하였다.
"해머헤드" 모티프에 기초하여 설계된 촉매 RNA은 표적 서열과의 필수적인 염기 대합을 유지하기 위하여 촉매 RNA 내에 적절한 염기 변화를 만듦으로써 특이적 표적 서열을 절단하는데 사용되고 있다. 이것은 특이적 표적 서열을 절단하기 위하여 촉매 RNA의 사용을 가능하게 하고, "해머헤드" 모델에 따라 설계된 촉매 RNA가 생체내에서 특이적 기질 RNA를 절단하는 것이 가능하다는 것을 나타낸다.
RNA 간섭(RNAi)은 포유동물 및 포유동물 세포에서 유전자 발현을 조정하는 강력한 도구가 되고 있다. 이러한 접근은 발현 플라스미드 또는 바이러스, 및 siRNA로 가공되는 작은 헤어핀 RNA에 대한 코딩 서열을 이용하여 RNA 자체로 또는 DNA로서 작은 간섭 RNA(siRNA) 운반을 요구한다. 이러한 시스템은 pre-siRNA를 세포질로 효과적으로 운반할 수 있는데, 세포질에서 이들 RNA는 활동적이고 유전자 발현을 위한 조절된 조직 특이적인 프로모터의 사용을 허용한다.
하나의 양태에서, 올리고뉴클레오티드 또는 안티센스 화합물은 리보핵산(RNA) 및/또는 데옥시리보핵산(DNA)의 올리고머 또는 중합체, 또는 이의 모방체, 키메라, 유사체 또는 동족체를 포함한다. 상기 용어는 천연 발생 뉴클레오티드, 당 및 공유적 뉴클레오시드간(골격) 연결기로 구성된 올리고뉴클레오티드 뿐만 아니라 유사하게 기능하는 비-천연 발생 부분을 보유하는 올리고뉴클레오티드를 포함한다. 이와 같은 변형된 또는 치환된 올리고뉴클레오티드는, 예를 들면, 증강된 세포 취입, 표적 핵산에 대한 증강된 친화력 및 뉴클레아제의 존재에서 증가된 안정성과 같은 바람직한 성질로 인하여, 고유 형태 비하여 종종 바람직하다.
본 발명에 따르면, 올리고뉴클레오티드 또는 "안티센스 화합물"은 안티센스 올리고뉴클레오티드(예를 들면, RNA, DNA, 이의 모방체, 키메라, 유사체 또는 동족체), 리보자임, 외부 가이드 서열(EGS) 올리고뉴클레오티드, siRNA 화합물, 단일- 또는 이중-가닥 RNA 간섭(RNAi) 화합물, 예를 들면, siRNA 화합물, saRNA, aRNA, 및 표적 핵산의 최소한 일부분에 하이브리드화되어 이의 기능을 조정하는 기타 올리고머 화합물을 포함한다. 이와 같이, 이들은 DNA, RNA, DNA-유사, RNA-유사, 또는 이들의 혼합물이거나, 또는 이들 중에서 하나 이상의 모방체일 수 있다. 이들 화합물은 단일-가닥, 이중-가닥, 원형 또는 헤어핀 올리고머 화합물일 수 있고, 내부 또는 말단 중배, 미스매치 또는 루프와 같은 구조적 요소를 포함할 수 있다. 안티센스 화합물은 일과적으로 선형으로 제조되지만, 결합되거나, 원형 및/또는 분지형으로 제조될 수 있다. 안티센스 화합물은, 예를 들면, 하이브리드화되어 전체적으로 또는 부분적으로 이중-가닥 화합물을 형성하는 2개의 가닥, 또는 하이브리드화 및 전체적으로 또는 부분적으로 이중-가닥 화합물의 형성을 가능하게 할 만큼 충분한 자가-상보성을 갖는 단일 가닥과 같은 구조체를 포함할 수 있다. 2개 가닥은 내부에서 연결되어 3' 또는 5' 말단이 자유로운 상태로 남아 있거나, 또는 연결되어 연속적인 헤어핀 구조 또는 루프를 형성할 수 있다. 헤어핀 구조는 단일 가닥 특성의 연장부를 발생시키는 5' 또는 3' 말단 상에 오버행을 포함할 수 있다. 이중 가닥 화합물은 선택적으로 이들 말단에 오버행을 포함할 수 있다. 추가 변형에는 말단 중의 한쪽, 선택된 뉴클레오티드 위치, 당 위치, 또는 뉴클레오티드간 연결기 중의 하나에 부착된 접합체 군을 포함할 수 있다. 대안적으로, 2개 가닥은 비-핵산 모이어티 또는 링커 기를 통하여 연결될 수 있다. 한 개 가닥으로부터만 형성될 때, dsRNA는 이중나선을 형성하기 위하여 자체적으로 둘로 접히는 자가-상보성 헤어핀 유형 분자의 형태를 취할 수 있다. 따라서, 이들 dsRNA는 완전히 또는 부분적으로 이중 가닥이 될 수 있다. 유전자 발현의 특이적 조정은 유전자도입 세포주에서 dsRNA 헤어핀의 안정된 발현에 의해 달성될 수 있다. 2개 가닥, 또는 이중나선을 형성하기 위하여 자체적으로 둘로 접히는 자가-상보성 헤어핀 유형 분자의 형태를 취하는 단일 가닥으로부터 형성될 때, 이들 2개 가닥(또는 단일 가닥의 이중나선 형성 영역)은 왓슨-크릭 방식으로 염기 쌍을 이루는 상보성 RNA 가닥이다.
일단 시스템내로 도입되면, 본 발명의 화합물은 표적 핵산의 절단 또는 다른 변형을 달성하기 위하여 하나 이상의 효소 또는 구조적 단백질의 작용을 유도하거나, 또는 점유-기반 기전을 통하여 작용할 수 있다. 일반적으로, 핵산(올리고뉴클레오티드 포함)은 "DNA-유사"(즉, 일반적으로 하나 이상의 2'-데옥시 당을 보유하고, 일반적으로 U 염기 대신 T를 보유함) 또는 "RNA-유사"(즉, 일반적으로 하나 이상의 2'-히드록실 또는 2'-변형된 당을 보유하고, 일반적으로 T 염기 대신 U 염기를 보유함)로 기술될 수 있다. 핵산 나선은 한 가지 이상의 구조 유형을 채택할 수 있지만, 가장 일반적으로 A- 및 B-형이다. 일반적으로, B-형-유사 구조를 가지는 올리고뉴클레오티드는 "DNA-유사"이며, A-형-유사 구조를 가지는 올리고뉴클레오티드는 "RNA-유사"이다. 일부(키메라) 양태에서, 안티센스 화합물은 A- 및 B-형 영역을 모두 포함할 수 있다.
본 발명에 따른 안티센스 화합물은 길이가 약 5 내지 약 80개 뉴클레오티드(즉, 약 5 내지 약 80개의 연결된 뉴클레오시드)의 안티센스 부분을 포함할 수 있다. 이는 안티센스 화합물의 안티센스 가닥 또는 부분의 길이를 지칭한다. 다시 말해서, 본 발명의 단일-가닥 안티센스 화합물은 5 내지 약 80개 뉴클레오티드를 포함하고, 본 발명의 이중-가닥 안티센스 화합물(예를 들면, dsRNA)은 길이가 5 내지 약 80개 뉴클레오티드인 센스 및 안티센스 가닥 또는 부분을 포함한다. 이것은 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 26개, 27개, 28개, 29개, 30개, 31개, 32개, 33개, 34개, 35개, 36개, 37개, 38개, 39개, 40개, 41개, 42개, 43개, 44개, 45개, 46개, 47개, 48개, 49개, 50개, 51개, 52개, 53개, 54개, 55개, 56개, 57개, 58개, 59개, 60개, 61개, 62개, 63개, 64개, 65개, 66개, 67개, 68개, 69개, 70개, 71개, 72개, 73개, 74개, 75개, 76개, 77개, 78개, 79개, 또는 80개 뉴클레오티드 길이, 또는 그 내에 임의의 범위의 안티센스 부분을 포함한다는 것을 당업자는 이해할 것이다.
하나의 양태에서, 본 발명의 안티센스 화합물은 10 내지 50개 뉴클레오티드 길이의 안티센스 부분을 갖는다. 이것은 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 26개, 27개, 28개, 29개, 30개, 31개, 32개, 33개, 34개, 35개, 36개, 37개, 38개, 39개, 40개, 41개, 42개, 43개, 44개, 45개, 46개, 47개, 48개, 49개, 또는 50개 뉴클레오티드 길이, 또는 그 내에 임의의 범위의 안티센스 부분을 갖는 올리고뉴클레오티드를 구현한다는 것을 당업자는 이해할 것이다.
하나의 양태에서, 본 발명의 안티센스 또는 올리고뉴클레오티드 화합물은 12개 또는 13개 내지 30개 뉴클레오티드 길이의 안티센스 부분을 갖는다. 이것은 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 26개, 27개, 28개, 29개, 또는 30개 뉴클레오티드 길이, 또는 그 내에 임의의 범위의 안티센스 부분을 갖는 안티센스 화합물을 구현한다는 것을 당업자는 이해할 것이다.
하나의 양태에서, 본 발명의 올리고머 화합물은 화합물 내에 하나 이상의 뉴클레오티드 위치에 상이한 염기가 존재하는 변이체를 포함한다. 예를 들면, 첫 번째 뉴클레오티드가 아데노신이면, 이 위치에 티미딘, 구아노신 또는 시티딘을 포함하는 변이체가 만들어질 수 있다. 이것은 안티센스 또는 dsRNA 화합물의 임의의 위치에서 일어날 수 있다. 이들 화합물은 표적 핵산의 발현을 저해하는 능력을 측정하기 위하여 본 명세서에서 기술된 방법을 이용하여 시험된다.
일부 양태에서, 안티센스 화합물과 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 40% 내지 약 60%이다. 일부 양태에서, 안티센스 화합물과 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 60% 내지 약 70%이다. 일부 양태에서, 안티센스 화합물과 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 70% 내지 약 80%이다. 일부 양태에서, 안티센스 화합물과 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 80% 내지 약 90%이다. 일부 양태에서, 안티센스 화합물과 표적 사이에 상동성, 서열 동일성 또는 상보성은 약 90%, 약 92%, 약 94%, 약 95%, 약 96%, 약 97%, 약 98%, 약 99% 또는 약 100%이다.
하나의 양태에서, 서열 번호 12 내지 49에서 기술된 핵산 분자와 같은 안티센스 올리고뉴클레오티드는 하나 이상의 치환 또는 변형을 포함한다. 하나의 양태에서, 뉴클레오티드는 잠금 핵산(LNA)으로 치환된다.
하나의 양태에서, 올리고뉴클레오티드는 BDNF 및 서열 번호 1 내지 11로서 기술된 서열과 연관된 코딩 및/또는 비-코딩 서열의 핵산 분자 센스 및/또는 안티센스의 하나 이상의 영역을 표적으로 한다. 올리고뉴클레오티드는 또한, 서열 번호 1 내지 11의 중복 영역을 표적으로 한다.
본 발명의 일정한 바람직한 올리고뉴클레오티드는 키메라 올리고뉴클레오티드이다. 본 발명의 맥락에서, "키메라 올리고뉴클레오티드" 또는 "키메라"는 2개 이상의 화학적으로 별개의 영역을 포함하는 올리고뉴클레오티드이며, 각 영역은 1개 이상의 뉴클레오티드로 구성된다. 이들 올리고뉴클레오티드는 전형적으로 하나 이상의 유익한 성질(예를 들면, 증가된 뉴클레아제 내성, 세포내로의 증가된 취입, 표적에 대한 증가된 결합 친화성)을 부여하는 변형된 뉴클레오티드의 하나 이상의 영역 및 RNA:DNA 또는 RNA:RNA 하이브리드를 절단할 수 있는 효소에 대한 기질이 되는 영역을 포함한다. 예를 들면, RNase H는 RNA:DNA 이중나선의 RNA 가닥을 절단하는 세포성 엔도뉴클레아제이다. 따라서, RNase H의 활성화는 RNA 표적의 절단을 유발하여, 유전자 발현의 안티센스 조정의 효과를 강화시킨다. 결과적으로, 동일한 표적 영역에 하이브리드화되는 포스포로티오에이트 데옥시올리고뉴클레오티드와 비교하여, 키메라 올리고뉴클레오티드가 사용될 때 더욱 짧은 올리고뉴클레오티드로 필적하는 결과가 종종 획득될 수 있다. RNA 표적의 절단은 겔 전기영동에 의해, 필요한 경우, 당해 분야에 공지된 핵산 하이브리드화 기술과 연합하여 일과적으로 검출될 수 있다. 하나의 양태에서, 키메라 올리고뉴클레오티드는 표적 결합 친화력을 증가시키도록 변형된 하나의 이상의 영역, 및 통상적으로, RNAse H에 대한 기질로서 기능하는 영역을 포함한다. 표적(본 발명의 경우에, ras를 코딩하는 핵산)에 대한 올리고뉴클레오티드 친화성은 올리고뉴클레오티드/표적 쌍의 Tm을 측정함으로써 일과적으로 결정되는데, 이는 상기 올리고뉴클레오티드와 표적이 해리되는 온도이고; 해리는 분광광도법으로 검출된다. Tm이 높을수록, 표적에 대한 올리고뉴클레오티드의 친화성이 커진다.
본 발명의 키메라 안티센스 화합물은 상기에서 설명된 것과 같이 2개 이상의 올리고뉴클레오티드, 변형된 올리고뉴클레오티드, 올리고뉴클레오시드 및/또는 올리고뉴클레오티드 모방체의 혼성 구조로 형성될 수 있다. 이러한 화합물은 또한 당해 분야에서 하이브리드 또는 갭머(gapmer)로 지칭된다. 이러한 하이브리드 구조의 제조에 대해 교시하는 대표적인 미국 특허는 미국 특허 제5,013,830호; 제5,149,797호; 제5,220,007호; 제5,256,775호; 제5,366,878호; 제5,403,711호; 제5,491,133호; 제5,565,350호; 제5,623,065호; 제5,652,355호; 제5,652,356호; 및 제5,700,922호를 포함하지만 이에 한정되지 않고, 상기 출원은 그 전문이 본원에 참고로 포함된다.
하나의 양태에서, 변형된 올리고뉴클레오티드의 영역은 당의 2' 위치에서 변형된 하나 이상의 뉴클레오티드, 바람직하게는 2'-O알킬, 2'-O-알킬-O-알킬 또는 2'-플루오르-변형된 뉴클레오티드를 포함한다. 다른 양태에서, RNA 변형은 피리미딘의 리보즈, 염기소실 잔기 또는 RNA의 3' 말단에서 역전된 염기 상에 2'-플루오르, 2'-아미노 및 2' O-메틸 변형을 포함한다. 이와 같은 변형은 올리고뉴클레오티드에 일과적으로 통합되고, 이들 올리고뉴클레오티드는 소정의 표적에 대해 2'-데옥시올리고뉴클레오티드보다 높은 Tm(즉, 더욱 높은 표적 결합 친화성)을 가지는 것으로 밝혀졌다. 증가된 친화성의 효과는 유전자 발현의 RNAi 올리고뉴클레오티드 저해를 상당히 증강시키는 것이다. RNAse H는 RNA:DNA 이중나선의 RNA 가닥을 절단하는 세포성 엔도뉴클레아제이고; 따라서 상기 효소의 활성화는 RNA 표적의 절단을 유발하여, RNAi 저해의 효과를 상당히 증강시킬 수 있다. RNA 표적의 절단은 겔 전기영동에 의해 일과적으로 증명될 수 있다. 하나의 양태에서, 키메라 올리고뉴클레오티드는 또한 뉴클레아제 내성을 증강시키기 위하여 변형된다. 세포는 핵산을 분해시킬 수 있는 다양한 엑소- 및 엔도-뉴클레아제를 포함한다. 다수의 뉴클레오티드 및 뉴클레오시드 변형은 그들이 통합된 올리고뉴클레오티드가 고유한 올리고데옥시뉴클레오티드보다 뉴클레아제 절단에 더욱 강한 내성을 갖도록 만드는 것으로 밝혀졌다. 뉴클레아제 내성은 올리고뉴클레오티드를 세포 추출물 또는 분리된 뉴클레아제 용액과 함께 항온처리하고, 통상적으로 겔 전기영동에 의해 시간의 흐름 동안 남아있는 본래 올리고뉴클레오티드의 수준을 측정함으로써 일과적으로 결정된다. 뉴클레아제 내성을 증강시키도록 변형된 올리고뉴클레오티드는 변형되지 않은 올리고뉴클레오티드보다 더욱 긴 시간 동안 본래 상태로 존재한다. 다양한 올리고뉴클레오티드 변형이 뉴클레아제 내성을 증강시키거나 부여하는 것으로 증명되었다. 최소한 하나의 포스포로티오에이트 변형을 포함하는 올리고뉴클레오티드가 더욱 바람직하다. 일부 경우, 표적 결합 친화성이 증강된 올리고뉴클레오티드 변형은 독립적으로 뉴클레아제 내성을 증강시킬 수 있다.
본 발명에서 구상된 일부 바람직한 올리고뉴클레오티드의 특정한 예는 변형된 골격을 포함하는 것들, 예를 들면, 포스포로티오에이트, 포스포트리에스테르, 메틸 포스포네이트, 짧은 사슬 알킬 또는 사이클로알킬 당간(intersugar) 연결기 또는 짧은 사슬 헤테로원자 또는 헤테로사이클릭 당간 연결기를 포함한다. 가장 바람직한 것은 포스포로티오에이트 골격을 가진 올리고뉴클레오티드 및 헤테로원자 골격, 특히, CH2--NH--O--CH2, CH, --N(CH3)--O--CH2[메틸렌(메틸이미노) 또는 MMI 골격으로 공지됨], CH2--O--N (CH3)--CH2, CH2--N(CH3)--N(CH3)--CH2 및 O--N (CH3)--CH2--CH2 골격을 가진 올리고뉴클레오티드이고, 이때 고유 포스포디에스테르 골격은 O--P--O--CH로 표시된다). 문헌 [De Mesmaeker et al. (1995) Acc. Chem. Res. 28:366-374]에서 설명된 아미드 골격이 또한 바람직하다. 모르폴리노 골격 구조를 가진 올리고뉴클레오티드 역시 바람직하다(Summerton and Weller, 미국 특허 제5,034,506호). 다른 양태에서, 예를 들면, 펩티드 핵산(PNA) 골격에서, 올리고뉴클레오티드의 포스포디에스테르 골격은 폴리아미드 골격으로 대체되며, 뉴클레오티드는 폴리아미드 골격의 아자 질소 원자에 직간접적으로 결합된다. 올리고뉴클레오티드는 하나 이상의 치환된 당 모이어티를 또한 포함할 수 있다. 바람직한 올리고뉴클레오티드는 2' 위치에 다음 중 하나를 포함한다: OH, SH, SCH3, F, OCN, OCH3, O(CH2)n CH3, O(CH2)n NH2 또는 O(CH2)n CH3, 여기서 n은 1 내지 약 10이다; C1 내지 C10 저급 알킬, 알콕시알콕시, 치환된 저급 알킬, 알크아릴 또는 아르알킬; Cl; Br; CN; CF3; OCF3; O--, S--, 또는 N-알킬; O--, S--, 또는 N-알케닐; SOCH3; SO2 CH3; ONO2; NO2; N3; NH2; 헤테로사이클로알킬; 헤테로사이클로알크아릴; 아미노알킬아미노; 폴리알킬아미노; 치환된 실릴; RNA 절단 기; 리포터 기; 삽입제(intercalator); 올리고뉴클레오티드의 약역학적 성질을 개선하는 기; 또는 올리고뉴클레오티드 및 유사한 성질을 가진 다른 치환기의 약동학적 성질을 개선하는 기. 바람직한 변형은 2'-메톡시에톡시[2'-O-CH2 CH2 OCH3, 또한 2'-O-(2-메톡시에틸)로 공지됨]을 포함한다. 다른 바람직한 변형은 2'-메톡시 (2'-O--CH3), 2'-프로폭시(2'-OCH2 CH2CH3) 및 2'-플루오르(2'-F)를 포함한다. 올리고뉴클레오티드 상에서 다른 위치, 특히 3' 말단 뉴클레오티드 상에서 당의 3' 위치 및 5' 말단 뉴클레오티드의 5' 위치에서 유사한 변형이 만들어 질 수 있다. 올리고뉴클레오티드는 또한 펜토푸라노실 기 대신에 사이클로부틸과 같은 당 모방체를 보유할 수 있다.
올리고뉴클레오티드는 또한 추가적으로 또는 대안적으로, 핵염기(당분야에서 종종 간단히 "염기"로 지칭됨) 변형 또는 치환을 포함할 수 있다. 본원에서, "변형되지 않은" 또는 "천연" 뉴클레오티드는 아데닌(A), 구아닌(G), 티민(T), 시토신(C) 및 우라실(U)을 포함한다. 변형된 뉴클레오티드는 천연 핵산에 드물게 또는 일시적으로 발견되는 뉴클레오티드, 예를 들면, 하이포산틴, 6-메틸아데닌, 5-Me 피리미딘, 특히 5-메틸시토신(또한, 5-메틸-2'데옥시시토신, 종종 당해 분야에서 5-Me-C로 지칭됨), 5-하이드록시메틸시토신(HMC), 글리코실 HMC 및 겐토바이오실 HMC, 뿐만 아니라 합성 뉴클레오티드, 예를 들면, 2-아미노아데닌, 2-(메틸아미노)아데닌, 2-(이미다졸일알킬)아데닌, 2-(아미노알킬아미노)아데닌 또는 다른 헤테로치환된 알킬아데닌, 2-티오우라실, 2-티오티민, 5-브로모우라실, 5-하이드록시메틸우라실, 8-아자구아닌, 7-데아자구아닌, N6(6-아미노헥실)아데닌 및 2,6-디아미노퓨린을 포함한다. 당분야에 공지된 "범용(universal)" 염기, 예를 들면, 이노신이 포함될 수 있다. 5-Me-C 치환은 핵산 이중나선 안정성을 0.6-1.2℃ 증가시키는 것으로 밝혀졌고, 현재 바람직한 염기 치환이다.
본 발명의 올리고뉴클레오티드의 다른 변형은 올리고뉴클레오티드의 활성 또는 세포 취입을 증강시키는 하나 이상의 모이어티 또는 접합체를 올리고뉴클레오티드에 화학적으로 연결하는 것을 수반한다. 이러한 모이어티는 지질 모이어티, 예를 들면, 콜레스테롤 모이어티, 콜레스테릴 모이어티, 지방족 사슬, 예를 들면, 도데칸디올 또는 운데실 잔기, 폴리아민 또는 폴리에틸렌 글리콜 사슬, 또는 아다만탄 아세트산을 포함하지만 이에 한정되지 않는다. 친유성 모이어티를 포함하는 올리고뉴클레오티드, 및 이러한 올리고뉴클레오티드를 제조하는 방법은 당해 분야에 공지되어 있고, 예를 들면, 미국 특허 제5,138,045호, 제5,218,105호 및 제5,459,255호에 공지되어 있다.
주어진 올리고뉴클레오티드 내에 모든 위치가 균일하게 변형될 필요는 없고, 실제로, 전술한 변형 중 하나 이상이 단일 올리고뉴클레오티드에 통합되거나, 또는 심지어 올리고뉴클레오티드내 단일 뉴클레오시드에 통합될 수 있다. 본 발명은 또한, 상기에서 정의된 바와 같은 키메라 올리고뉴클레오티드인 올리고뉴클레오티드를 포함한다.
또 다른 양태에서, 본 발명의 핵산 분자는 염기소실 뉴클레오티드, 폴리에테르, 폴리아민, 폴리아미드, 펩티드, 탄수화물, 지질 또는 폴리하이드로카본 화합물을 포함하지만 이에 한정되지 않는 다른 모이어티와 접합된다. 이들 분자가 당, 염기 또는 포스페이트 기 상에서 여러 위치에서 핵산 분자를 포함하는 하나 이상의 임의의 뉴클레오티드에 연결될 수 있다는 것을 당업자는 인지할 것이다.
본 발명에 따라 사용되는 올리고뉴클레오티드는 널리 공지된 고형상 합성 기술을 통하여 통상적으로 및 일과적으로 만들어질 수 있다. 이와 같은 합성을 위한 장비는 Applied Biosystems를 비롯한 여러 업체에 의해 판매된다. 이러한 합성을 위하여 임의의 다른 수단 역시 이용될 수 있고; 올리고뉴클레오티드의 실제 합성은 당업자의 능력 범위 내에 있다. 포스포로티오에이트 및 알킬화된 유도체와 같은 다른 올리고뉴클레오티드를 제조하기 위하여 유사한 기술을 이용하는 것 역시 공지되어 있다. 형광 표지된, 비오틴화된 또는 기타 변형된 올리고뉴클레오티드, 예를 들면, 콜레스테롤-변형된 올리고뉴클레오티드를 합성하기 위하여 유사한 기술 및 상업적으로 이용가능한 변형된 아미디트(amidite) 및 제어된 공극 유리(CPG: controlled-pore glass) 제품, 예를 들면, 비오틴, 플루오레세인, 아크리딘 또는 소랄렌(psoralen)-변형된 아미디트 및/또는 CPG(Glen Research(Sterling VA)로부터 구입가능)를 이용하는 것이 또한 공지되어 있다.
본 발명에 따르면, 올리고뉴클레오티드의 효능, 특이성 및 작용 기간을 증강시키고 투여 경로를 확장시키기 위한 LNA 단량체와 같은 변형의 사용은 MOE, ANA, FANA, PS 등과 같은 현재 화학물질로 구성되었다. 이것은 현재 올리고뉴클레오티드에서 일부 단량체를 LNA 단량체로 치환함으로써 달성될 수 있다. LNA 변형된 올리고뉴클레오티드는 부모 화합물과 유사한 크기를 갖거나, 더욱 큰, 또는 바람직하게는 더욱 작은 크기를 가질 수 있다. 이러한 LNA-변형된 올리고뉴클레오티드는 약 70% 미만, 더욱 바람직하게는 약 60% 미만, 가장 바람직하게는 약 50% 미만의 LNA 단량체를 포함하고, 그들의 크기는 약 5 내지 25개 뉴클레오티드, 더욱 바람직하게는 약 12 내지 20개 뉴클레오티드 사이이다.
바람직한 변형된 올리고뉴클레오티드 골격은 포스포로티오에이트, 키랄 포스포로티오에이트, 포스포로디티오에이트, 포스포트리에스테르, 아미노알킬포스포트리에스테르, 메틸 및 3' 알킬렌 포스포네이트와 키랄 포스포네이트를 포함하는 기타 알킬 포스포네이트, 포스피네이트, 3'-아미노 포스포르아미데이트와 아미노알킬포스포르아미데이트를 포함하는 포스포르아미데이트, 티오노포스포르아미데이트, 티오노알킬포스포네이트, 티오노알킬포스포트리에스테르, 및 정상적인 3'-5' 연결기를 가진 보라노포스페이트, 이들의 2'-5' 연결된 유사체, 및 역전된 극성을 가진 것들을 포함하지만 이에 한정되지 않고, 여기서 뉴클레오시드 단위의 인접 쌍은 3'-5'에서 5'-3'로, 또는 2'-5'에서 5'-2'로 연결된다. 다양한 염, 혼합된 염 및 유리 산 형태 역시 포함된다.
상기 인-함유 연결기의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제3,687,808호; 제4,469,863호; 제4,476,301호; 제5,023,243호; 제5,177,196호; 제5,188,897호; 제5,264,423호; 제5,276,019호; 제5,278,302호; 제5,286,717호; 제5,321,131호; 제5,399,676호; 제5,405,939호; 제5,453,496호; 제5,455,233호; 제5,466,677호; 제5,476,925호; 제5,519,126호; 제5,536,821호; 제5,541,306호; 제5,550,111호; 제5,563,253호; 제5,571,799호; 제5,587,361호; 및 제5,625,050호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
인 원자를 포함하지 않는 바람직한 변형된 올리고뉴클레오티드 골격은 짧은 사슬 알킬 또는 사이클로알킬 뉴클레오시드간 연결기, 혼성 헤테로원자 및 알킬 또는 사이클로알킬 뉴클레오시드간 연결기, 또는 하나 이상의 짧은 사슬 헤테로원자 또는 헤테로환상 뉴클레오시드간 연결기에 의해 형성된 골격을 갖는다. 이들은 모르폴리노 연결기(뉴클레오시드의 당 부분으로부터 부분적으로 형성됨); 실록산 골격; 설파이드, 설폭시드 및 설폰 골격; 포름아세틸 및 티오포름아세틸 골격; 메틸렌 포름아세틸 및 티오포름아세틸 골격; 알켄 함유 골격; 설파메이트 골격; 메틸렌이미노 및 메틸렌히드라지노 골격; 설포네이트 및 설폰아미드 골격; 아미드 골격; 및 N, O, S 및 CH2 성분 부분이 혼합된 것을 갖는 것을 포함한다.
상기 올리고뉴클레오시드의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제5,034,506호; 제5,166,315호; 제5,185,444호; 제5,214,134호; 제5,216,141호; 제5,235,033호; 제5,264,562호; 제5,264,564호; 제5,405,938호; 제5,434,257호; 제5,466,677호; 제5,470,967호; 제5,489,677호; 제5,541,307호; 제5,561,225호; 제5,596,086호; 제5,602,240호; 제5,610,289호; 제5,602,240호; 제5,608,046호; 제5,610,289호; 제5,618,704호; 제5,623,070호; 제5,663,312호; 제5,633,360호; 제5,677,437호; 및 제5,677,439호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
다른 바람직한 올리고뉴클레오티드 모방체에서, 당 및 뉴클레오시드간 연결기, 다시 말하면, 뉴클레오티드 단위의 골격은 신규한 기로 대체된다. 염기 단위는 적합한 핵산 표적 화합물과의 하이브리드화를 위해 유지된다. 이와 같은 올리고머 화합물 중 하나인, 우수한 하이브리드화 성질을 가진 것으로 확인된 올리고뉴클레오티드 모방체는 펩티드 핵산(PNA)으로 지칭된다. PNA 화합물에서, 올리고뉴클레오티드의 당-골격은 아미드 포함 골격, 특히 아미도에틸글리신 골격으로 치환된다. 핵염기는 보유되며, 골격의 아미드 부분의 아자 질소 원자에 직간접적으로 결합된다. PNA 화합물의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제5,539,082호; 제5,714,331호; 및 제5,719,262호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다. PNA 화합물의 추가 교시는 문헌 [Nielsen et al., (1991) Science, 254, 1497-1500]에서 확인할 수 있다.
본 발명의 양태에서, 포스포로티오에이트 골격을 가진 올리고뉴클레오티드, 및 헤테로원자 골격, 특히, CH2-NH-O-CH2-, -CH2-N(CH3)-O-CH2-(메틸렌(메틸이미노) 또는 MMI 골격으로 공지됨), -CH2-O-N(CH3)-CH2-, -CH2N(CH3)-N(CH3) CH2- 및 -O-N(CH3)-CH2-CH2-를 가진 올리고뉴클레오시드이고, 여기서 고유 포스포디에스테르 골격은 상기 언급된 미국 특허 제5,489,677호의 -O-P-O-CH2-, 및 상기 언급된 US 특허 제5,602,240호의 아미드 골격으로서 표시된다. 또한, 상기 언급된 미국 특허 제5,034,506호의 모르폴리노 골격 구조를 가진 올리고뉴클레오티드가 바람직하다.
변형된 올리고뉴클레오티드는 또한 하나 이상의 치환된 당 모이어티를 함유할 수 있다. 바람직한 올리고뉴클레오티드는 2' 위치에서 다음 중 하나를 포함한다: OH; F; O-, S-, 또는 N-알킬; O-, S-, 또는 N-알케닐; O-, S- 또는 N-알키닐; 또는 O 알킬-O-알킬, 여기서 알킬, 알케닐 및 알키닐은 치환되거나 치환되지 않은 C 내지 CO 알킬 또는 C2 내지 C10 알케닐 및 알키닐일 수 있다. O(CH2)nOmCH3, O(CH2)n, OCH3, O(CH2)nNH2, O(CH2)nCH3, O(CH2)nONH2, 및 O(CH2)nON(CH3)2이 특히 바람직하고, 여기서 n 및 m은 1 내지 약 10일 수 있다. 다른 바람직한 올리고뉴클레오티드는 2' 위치에 다음 중 하나를 포함한다: C 내지 CO, (저급 알킬, 치환된 저급 알킬, 알크아릴, 아르알킬, O-알크아릴 또는 O-아르알킬, SH, SCH3, OCN, Cl, Br, CN, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, 헤테로사이클로알킬, 헤테로사이클로알크아릴, 아미노알킬아미노, 폴리알킬아미노, 치환된 실릴, RNA 절단 기, 리포터 기, 삽입제, 올리고뉴클레오티드의 약역학적 성질을 개선하는 기, 또는 올리고뉴클레오티드의 약동학적 성질을 개선하는 기, 및 유사한 성질을 가진 다른 치환체. 바람직한 변형은 2'-메톡시에톡시(2'-O-CH2CH2OCH3, 또한 2'-O-(2-메톡시에틸) 또는 2'-MOE로 공지됨), 다시 말하면, 알콕시알콕시 기를 포함한다. 다른 바람직한 변형은 하기 실시예에서 설명된 바와 같은 2'-디메틸아미노옥시에톡시, 다시 말하면, O(CH2)2ON(CH3)2 기, 일명 2'-DMAOE, 및 2'-디메틸아미노에톡시에톡시(당해 분야에서 2'-O-디메틸아미노에톡시에틸 또는 2'-DMAEOE로 공지됨), 다시 말하면, 2'-O-CH2-O-CH2-N(CH2)2을 포함한다.
다른 바람직한 변형은 2'-메톡시(2'-OCH3), 2'-아미노프로폭시(2'-O CH2CH2CH2NH2) 및 2'-플루오르 (2'-F)을 포함한다. 또한, 올리고뉴클레오티드 상에서 다른 위치, 특히 3' 말단 뉴클레오티드 상에서 또는 2'-5' 연결된 올리고뉴클레오티드에서 당의 3' 위치, 그리고 5' 말단 뉴클레오티드의 5' 위치에서 유사한 변형이 만들어질 수 있다. 올리고뉴클레오티드는 또한 펜토푸라노실 당 대신에 사이클로부틸 모이어티와 같은 당 모방체를 갖을 수 있다. 이와 같은 변형된 당 구조의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제4,981,957호; 제5,118,800호; 제5,319,080호; 제5,359,044호; 제5,393,878호; 제5,446,137호; 제5,466,786호; 제5,514,785호; 제5,519,134호; 제5,567,811호; 제5,576,427호; 제5,591,722호; 제5,597,909호; 제5,610,300호; 제5,627,053호; 제5,639,873호; 제5,646,265호; 제5,658,873호; 제5,670,633호; 및 제5,700,920호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
올리고뉴클레오티드는 또한 핵염기(당해 분야에서 종종 간단히 "염기"로 지칭됨) 변형 또는 치환을 포함할 수 있다. 본원에서, "변형되지 않은" 또는 "천연" 뉴클레오티드는 퓨린 염기 아데닌(A) 및 구아닌(G), 및 피리미딘 염기 티민(T), 시토신(C) 및 우라실(U)을 포함한다. 변형된 뉴클레오티드는 다른 합성 및 천연 뉴클레오티드, 예를 들면, 5-메틸시토신(5-me-C), 5-하이드록시메틸 시토신, 크산틴, 하이포산틴, 2-아미노아데닌, 아데닌과 구아닌의 6-메틸 및 다른 알킬 유도체, 아데닌과 구아닌의 2-프로필 및 다른 알킬 유도체, 2-티오우라실, 2-티오티민 및 2-티오시토신, 5-할로우라실 및 시토신, 5-프로피닐 우라실 및 시토신, 6-아조 우라실, 시토신 및 티민, 5-우라실(슈도-우라실), 4-티오우라실, 8-할로, 8-아미노, 8-티올, 8-티오알킬, 8-히드록실 및 다른 8-치환된 아데닌 및 구아닌, 5-할로, 특히 5-브로모, 5-트리플루오르메틸 및 다른 5-치환된 우라실 및 시토신, 7-메틸구아닌 및 7-메틸아데닌, 8-아자구아닌 및 8-아자아데닌, 7-데아자구아닌 및 7-데아자아데닌, 및 3-데아자구아닌 및 3-데아자아데닌을 포함한다.
추가로, 뉴클레오티드는 미국 특허 제3,687,808호, 문헌 ['The Concise Encyclopedia of Polymer Science And Engineering', pages 858-859, Kroschwitz, J.I., ed. John Wiley & Sons, 1990]에 기재된 것들, 문헌 [Englisch et al., 'Angewandle Chemie, International Edition', 1991, 30, page 613]에 기재된 것들, 및 문헌 [Sanghvi, Y.S., Chapter 15, 'Antisence Research and Applications', pages 289-302, Crooke, S.T. and Lebleu, B. ea., CRC Press, 1993]에 기재된 것들을 포함한다. 이들 일정한 뉴클레오티드는 본 발명의 올리고머 화합물의 결합 친화성을 증가시키는데 특히 유용하다. 이들은 2-아미노프로필아데닌, 5-프로피닐우라실 및 5-프로피닐시토신을 포함하는 5-치환된 피리미딘, 6-아자피리미딘 및 N-2, N-6과 0-6 치환된 퓨린을 포함한다. 5-메틸시토신 치환은 핵산 이중나선 안정도를 0.6 내지 1.2℃ 증가시키는 것으로 밝혀졌고(문헌 [Sanghvi, Y.S., Crooke, S.T. and Lebleu, B., eds, 'Antisence Research and Applications', CRC Press, Boca Raton, 1993, pp. 276-278]), 2'-O메톡시에틸 당 변형과 복합될 때 특히 바람직한 염기 치환이다.
상기 변형된 뉴클레오티드 및 기타 변형된 뉴클레오티드의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제3,687,808호, 뿐만 아니라 제4,845,205호; 제5,130,302호; 제5,134,066호; 제5,175,273호; 제5,367,066호; 제5,432,272호; 제5,457,187호; 제5,459,255호; 제5,484,908호; 제5,502,177호; 제5,525,711호; 제5,552,540호; 제5,587,469호; 제5,596,091호; 제5,614,617호; 제5,750,692호, 및 제5,681,941호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
본 발명의 올리고뉴클레오티드의 또 다른 변형은 하나 이상의 모이어티 또는 접합체를 올리고뉴클레오티드에 화학적으로 연결하는 것을 수반하는데, 이는 활성, 세포 분포 또는 올리고뉴클레오티드의 세포 취입을 증강시킨다.
이러한 모이어티는 지질 모이어티, 예를 들면, 콜레스테롤 모이어티, 담즙산, 티오에테르, 예를 들면, 헥실-S-트리릴티올, 티오콜레스테롤, 지방족 사슬, 예를 들면, 도데칸디올 또는 운데실 잔기, 인지질, 예를 들면, 디-헥사데실-rac-글리세롤 또는 트리에틸암모늄 1,2-디-O-헥사데실-rac-글리세로-3-H-포스포네이트, 폴리아민 또는 폴리에틸렌 글리콜 사슬, 또는 아다만탄 아세트산, 팔미틸 모이어티, 또는 옥타데실아민 또는 헥실아미노-카르보닐-t 옥시콜레스테롤 모이어티를 포함하지만 이에 한정되지 않는다.
이러한 올리고뉴클레오티드 접합체의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제4,828,979호; 제4,948,882호; 제5,218,105호; 제5,525,465호; 제5,541,313호; 제5,545,730호; 제5,552,538호; 제5,578,717호; 5,580,731호; 제5,580,731호; 제5,591,584호; 제5,109,124호; 제5,118,802호; 제5,138,045호; 제5,414,077호; 제5,486,603호; 제5,512,439호; 제5,578,718호; 제5,608,046호; 제4,587,044호; 제4,605,735호; 제4,667,025호; 제4,762,779호; 제4,789,737호; 제4,824,941호; 제4,835,263호; 제4,876,335호; 제4,904,582호; 제4,958,013호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5, 245,022호; 제5,254,469호; 제5,258,506호; 제5,262,536호; 제5,272,250호; 제5,292,873호; 제5,317,098호; 제5,371,241호; 제5,391,723호; 제5,416,203호; 제5,451,463호; 제5,510,475호; 제5,512,667호; 제5,514,785호; 제5,565,552호; 제5,567,810호; 제5,574,142호; 제5,585,481호; 제5,587,371호; 제5,595,726호; 제5,597,696호; 제5,599,923호; 제5,599,928호 및 제5,688,941호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
약물 발견: 본 발명의 화합물은 약물 발견 및 표적 검증 분야에도 적용될 수 있다. 본 발명은 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드 및 질환 상태, 표현형 또는 장애 사이에 존재하는 상관관계를 설명하기 위한 약물 발견 노력에서, 본 발명에서 확인된 화합물 및 바람직한 표적 분절의 사용을 포함한다. 이들 방법은 BDNF 폴리뉴클레오티드를 검출 또는 조정하는 것을 포함하며, 샘플, 조직, 세포 또는 유기체를 본 발명의 화합물과 접촉시키는 단계, BDNF 폴리뉴클레오티드의 핵산 또는 단백질 수준 및/또는 처치후 일정 시점에 관련된 표현형 또는 화학적 종점을 측정하는 단계, 및 임의로, 측정된 값을 처리되지 않은 샘플 또는 본 발명의 다른 화합물로 처리된 샘플에 비교하는 단계를 포함한다. 이들 방법은 표적 검증 과정을 위한 미지의 유전자 기능을 결정하기 위하여, 또는 특정 질환, 상태 또는 표현형의 치료 또는 예방을 위한 표적으로서 특정 유전자 산물의 유효성을 결정하기 위하여 다른 실험과 병행하여 또는 조합으로 실행될 수 있다.
유전자 발현의 상향조절 또는 저해의 평가:
외인성 핵산의 숙주 세포 또는 유기체 내로의 전달은 세포내 또는 유기체내 핵산이 존재하는 것을 직접적으로 검출함으로써 평가될 수 있다. 이와 같은 검출은 당해 분야에 공지된 여러 방법에 의해 달성될 수 있다. 예를 들면, 외인성 핵산의 존재는 서던 블롯에 의해, 또는 핵산과 연관된 뉴클레오티드 서열을 특이적으로 증폭시키는 프라이머를 이용한 중합효소 연쇄 반응(PCR: polymerase chain reaction) 기술에 의해 검출될 수 있다. 외인성 핵산의 발현은 또한 유전자 발현 분석을 포함한 통상적인 방법을 이용하여 측정될 수 있다. 예를 들면, 외인성 핵산으로부터 생성된 mRNA는 노던 블롯(Northern blot) 및 역전사 PCR(RT-PCR)을 이용하여 검출되고 정량화될 수 있다.
외인성 핵산으로부터의 RNA 발현 역시 효소적 활성 또는 리포터 단백질 활성을 측정함으로써 검출될 수 있다. 예를 들면, 안티센스 조정 활성은 외인성 핵산이 효과물질 RNA를 생산하고 있다는 표시로서 표적 핵산 발현에서 증가 또는 감소로서 간접적으로 측정될 수 있다. 서열 보존에 근거하여, 프라이머가 설계되고 표적 유전자의 코딩 영역을 증폭하는데 이용될 수 있다. 초기에, 각 유전자로부터 가장 많이 발현된 코딩 영역은 비록 임의의 코딩 또는 비-코딩 영역이 이용될 수 있긴 하지만, 모델 기준 유전자를 구축하는데 이용될 수 있다. 각 기준 유전자(control gene)는 리포터 코딩 영역 및 이의 폴리(A) 신호 사이에 각 코딩 영역을 삽입함으로써 어셈블리된다. 이와 같은 플라스미드는 유전자의 상류 부분에 리포터 유전자, 및 3' 비-코딩 영역에 잠재적인 RNAi 표적을 보유하는 mRNA를 생산할 것이다. 개별 안티센스 올리고뉴클레오티드의 효능은 리포터 유전자를 조정함으로써 평가될 것이다. 본 발명의 방법에 유용한 리포터 유전자는 아세토하이드록시산 합성효소(AHAS), 알칼리 포스파타제(AP), 베타 갈락토시다아제(LacZ), 베타 글루코로니다제(GUS), 클로람페니콜 아세틸전이효소(CAT), 녹색 형광 단백질(GFP), 적색 형광 단백질(RFP), 황색 형광 단백질(YFP), 청록색 형광 단백질(CFP), 서양고추냉이 과산화효소(HRP), 루시페라제(Luc), 노팔린 합성효소(NOS), 옥토파인 합성효소(OCS), 및 이들의 유도체를 포함한다. 암피실린, 블레오마이신, 클로람페니콜, 젠타마이신, 하이그로마이신, 카나마이신, 린코마이신, 메토트렉세이트, 포스피노트리친, 퓨로마이신, 및 테트라사이클린에 내성을 부여하는 다중 선택성 마커가 이용될 수 있다. 리포터 유전자의 조정을 결정하는 방법은 당해 분야에 공지되어 있으며, 이들 방법은 형광 측정법(예를 들면, 형광 분광학, 형광 활성화된 세포 분류(FACS: Fluorescence Activated Cell Sorting), 형광 현미경), 항생제 내성 결정을 포함하지만 이에 한정되지 않는다.
BDNF 단백질 및 mRNA 발현은 당업자에게 공지되고 본원에서 설명된 방법을 이용하여 평가될 수 있다. 예를 들면, 면역분석법, 예를 들면, ELISA가 단백질 수준을 측정하는데 이용될 수 있다. BDNF ELISA 분석 키트는, 예를 들면, R&D Systems(Minneapolis, MN)로부터 상업적으로 이용할 수 있다.
양태에서, 본 발명의 안티센스 올리고뉴클레오티드를 이용하여 처리된 샘플(예를 들면, 생체내에서 또는 시험관내에서 세포 또는 조직)에서 BDNF 발현(예를 들면, mRNA 또는 단백질)은 대조 샘플에서 BDNF 발현과의 비교에 의해 평가된다. 예를 들면, 단백질 또는 핵산의 발현은 당업자에게 공지된 방법을 이용하여, 모의-처리된 또는 처리되지 않은 샘플에서 발현과 비교될 수 있다. 대안적으로, 대조 안티센스 올리고뉴클레오티드(예를 들면, 변경된 또는 상이한 서열을 보유하는 것)로 처리된 샘플과의 비교는 목적되는 정보에 따라 수행될 수 있다. 또 다른 양태에서, 처리된 샘플 대 처리되지 않은 샘플에서 BDNF 단백질 또는 핵산의 발현에서 차이는 처리된 샘플 대 처리되지 않은 샘플에서 상이한 핵산(연구자에 의해 적절한 것으로 간주되는 임의의 표준, 예를 들면, 항존 유전자(housekeeping gene) 포함)의 발현에서 차이와 비교될 수 있다.
관찰된 차이는 대조군과의 비교에서 사용을 위하여, 목적하는 대로, 예를 들면, 비율(ratio) 또는 분율(fraction)의 형태로 표시될 수 있다. 양태에서, 본 발명의 안티센스 올리고뉴클레오티드로 처리된 샘플에서 BDNF mRNA 또는 단백질의 수준은 처리되지 않은 샘플, 또는 대조군 핵산으로 처리된 샘플과 비교하여, 약 1.25배 내지 약 10배 또는 그 이상 증가되거나 감소된다. 양태에서, BDNF mRNA 또는 단백질의 수준은 약 1.25배 이상, 약 1.3배 이상, 약 1.4배 이상, 약 1.5배 이상, 약 1.6배 이상, 약 1.7배 이상, 약 1.8배 이상, 약 2배 이상, 약 2.5배 이상, 약 3배 이상, 약 3.5배 이상, 약 4배 이상, 약 4.5배 이상, 약 5배 이상, 약 5.5배 이상, 약 6배 이상, 약 6.5배 이상, 약 7배 이상, 약 7.5배 이상, 약 8배 이상, 약 8.5배 이상, 약 9배 이상, 약 9.5배 이상, 또는 약 10배 이상 증가되거나 감소된다.
키트, 연구 시약, 진단제, 및 치료제
본 발명의 화합물은 진단용, 치료용 및 예방용으로 이용되거나, 또는 연구 시약 및 키트 성분으로 이용될 수 있다. 게다가, 정교한 특이성으로 유전자 발현을 저해할 수 있는 안티센스 올리고뉴클레오티드는 특정 유전자의 기능을 밝히거나, 또는 생물학적 경로의 다양한 구성원의 기능을 구별하기 위하여 당업자에 의해 종종 이용된다.
키트 및 진단제에서 및 다양한 생물학적 시스템에서 사용을 위하여, 본 발명의 화합물은 단독으로 또는 다른 화합물 또는 치료제와 조합으로, 세포 및 조직 내에서 발현되는 유전자의 일부 또는 전체 보체의 발현 패턴을 밝히기 위한 차등적 및/또는 복합적 분석에서 도구로서 유용하다.
본원에서, 용어 "생물학적 시스템" 또는 "시스템"은 뇌 유래 신경영양 인자(BDNF) 유전자의 산물을 발현하는, 또는 이들을 발현하는데 적격인 임의의 유기체, 세포, 세포 배양액 또는 조직으로 정의된다. 이들은 인간, 유전자도입 동물, 세포, 세포 배양액, 조직, 이형이식편, 이식물 및 이들의 조합을 포함하지만 이에 한정되지 않는다.
비제한적인 예로서, 하나 이상의 안티센스 화합물로 처리된 세포 또는 조직 내에서 발현 패턴은 안티센스 화합물로 처리되지 않은 대조군 세포 또는 조직과 비교되고, 생성된 패턴은 검사되는 유전자의 질환 연관성, 신호전달 경로, 세포 국부화, 발현 수준, 크기, 구조 또는 기능에 관련되기 때문에 차등적인 유전자 발현 수준에 대해 분석된다. 이들 분석은 자극된 또는 자극되지 않은 세포 상에서 및 발현 패턴에 영향을 주는 다른 화합물의 존부하에 실행될 수 있다.
당해 분야에 공지된 유전자 발현 분석 방법의 예는 DNA 어레이 또는 마이크로어레이, SAGE(유전자 발현의 일련의 분석), READS(절단된 cDNA의 제한 효소 증폭), TOGA(전체 유전자 발현 분석), 단백질 어레이 및 단백체학(proteomics), 발현된 서열 tag(EST) 염기서열분석, 차감성 RNA 핑거프린팅(SuRF), 차감성 클로닝, 차등적 디스플레이(DD), 비교 게놈 하이브리드화, FISH(형광 원위치 하이브리드화) 기술 및 질량 분석법 방법을 포함한다.
본 발명의 화합물은 이들 화합물이 뇌 유래 신경영양 인자(BDNF)를 코딩하는 핵산에 하이브리드화되기 때문에, 연구 및 진단에 유용하다. 예를 들면, 효과적인 뇌 유래 신경영양 인자(BDNF) 조정물질이 될 수 있을 만큼, 본원에 기술된 조건 하에 충분한 효율로 하이브리드화되는 올리고뉴클레오티드는 각각, 유전자 증폭 또는 검출에 유리한 조건하에 효과적인 프라이머 또는 프로브이다. 이들 프라이머 및 프로브는 뇌 유래 신경영양 인자(BDNF)를 코딩하는 핵산 분자의 특이적 검출을 요구하는 방법에서 및 뇌 유래 신경영양 인자 (BDNF)의 검출 또는 추가 연구에 이용을 위한 이들 핵산 분자의 증폭에서 유용하다. 본 발명의 안티센스 올리고뉴클레오티드, 특히, 프라이머 및 프로브와 뇌 유래 신경영양 인자(BDNF)를 코딩하는 핵산의 하이브리드화는 당해 분야에 공지된 방법에 의해 검출될 수 있다. 이러한 수단은 올리고뉴클레오티드에 효소의 접합(conjugation), 올리고뉴클레오티드의 방사성라벨링, 또는 임의의 다른 적합한 검출 수단을 포함할 수 있다. 샘플에서 뇌 유래 신경영양 인자(BDNF)의 수준을 검출하기 위하여 이와 같은 검출 수단을 이용하는 키트가 또한 제조될 수 있다.
안티센스의 특이성 및 민감성 역시 치료적 용도를 위하여 당업자에 의해 이용된다. 인간을 비롯한 동물의 질환 상태의 치료에서 치료적 모이어티로서 안티센스 화합물이 이용되고 있다. 안티센스 올리고뉴클레오티드 약물은 인간에게 안전하고 효과적으로 투여되고 있고, 다수의 임상 시험이 현재 진행중이다. 따라서 안티센스 화합물은 세포, 조직 및 동물, 특히 인간의 치료를 위한 치료 섭생에서 유용하도록 설정되는 유용한 치료 양식이 될 수 있는 것으로 확립된다.
치료를 위하여, BDNF 폴리뉴클레오티드의 발현을 조정함으로써 치료될 수 있는 질환 또는 장애를 앓는 것으로 의심되는 동물, 바람직하게는 인간은 본 발명에 따른 안티센스 화합물을 투여함으로써 치료된다. 예를 들면, 하나의 비제한적인 양태에서, 이들 방법은 치료를 요하는 동물에 BDNF 조정물질의 치료적 유효량을 투여하는 단계를 포함한다. 본 발명의 BDNF 조정물질은 BDNF의 활성을 효과적으로 조정하거나, BDNF 단백질의 발현을 효과적으로 조정한다. 하나의 양태에서, 동물에서 BDNF의 활성 또는 발현은 대조군과 비교하여 약 10% 저해된다. 바람직하게는, 동물에서 BDNF의 활성 또는 발현은 약 30% 저해된다. 더욱 바람직하게는, 동물에서 BDNF의 활성 또는 발현은 약 50% 이상 저해된다. 따라서, 이들 올리고머 화합물은 뇌 유래 신경영양 인자(BDNF) mRNA의 발현을 대조군과 비교하여, 10% 이상, 최50% 이상, 25% 이상, 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 75% 이상, 80% 이상, 85% 이상, 90% 이상, 95% 이상, 98% 이상, 99% 이상, 또는 100% 조정한다.
하나의 양태에서, 동물에서 뇌 유래 신경영양 인자(BDNF)의 활성 또는 발현은 대조군과 비교하여 약 10% 증가된다. 동물에서 BDNF의 활성 또는 발현은 대조군과 비교하여 약 30% 증가된다. 더욱 바람직하게는, 동물에서 BDNF의 활성 또는 발현은 대조군과 비교하여 50% 이상 증가된다. 따라서, 올리고머 화합물은 BDNF mRNA의 발현을 대조군과 비교하여, 10% 이상, 50% 이상, 25% 이상, 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 75% 이상, 80% 이상, 85% 이상, 90% 이상, 95% 이상, 98% 이상, 99% 이상, 또는 100% 조정한다.
예를 들면, 뇌 유래 신경영양 인자(BDNF)의 발현 감소는 동물의 혈청, 혈액, 지방 조직, 간 또는 임의의 기타 체액, 조직 또는 기관에서 측정될 수 있다. 바람직하게는, 분석되는 체액, 조직 또는 기관 내에 함유된 세포는 BDNF 펩티드를 코딩하는 핵산 분자 및/또는 BDNF 단백질 자체를 함유한다.
본 발명의 화합물은 적절한 약제학적으로 허용되는 희석제 또는 담체에 유효량의 화합물을 첨가함으로써 약제학적 조성물에 이용될 수 있다. 본 발명의 화합물 및 방법의 사용은 또한 예방학적으로 유용할 수 있다.
접합체
본 발명의 올리고뉴클레오티드의 다른 변형은 올리고뉴클레오티드의 활성, 세포 분포 또는 세포 취입을 증강시키는 하나 이상의 모이어티 또는 접합체를 올리고뉴클레오티드에 화학적으로 연결시키는 것을 수반한다. 이들 모이어티 또는 접합체는 1차 또는 2차 하이드록실 기와 같은 기능기에 공유 결합된 접합체 기를 포함할 수 있다. 본 발명의 접합체 기에는 삽입제, 리포터 분자, 폴리아민, 폴리아미드, 폴리에틸렌 글리콜, 폴리에테르, 올리고머의 약력학적 성질을 강화시키는 기, 및 올리고머의 약동학적 성질을 강화시키는 기가 포함된다. 전형적인 접합체 기는 콜레스테롤, 지질, 인지질, 비오틴, 페나진, 폴레이트, 페난트리딘, 안트라퀴논, 아크리딘, 플루오레세인, 로다민, 쿠마린 및 염료를 포함한다. 본 발명의 맥락에서, 약력학적 성질을 강화시키는 기에는 취입을 개선하고, 분해에 대한 내성을 강화시키고, 및/또는 표적 핵산과의 서열 특이적 하이브리드화를 강화시키는 기가 포함된다. 본 발명의 맥락에서, 약동학적 성질을 강화시키는 기에는 본 발명의 화합물의 취입, 분포, 대사 또는 배출을 개선하는 기가 포함된다. 대표적인 접합체 기는 국제 특허 출원 제PCT/US92/09196호(1992년 10월 23일 출원) 및 미국 특허 제6,287,860호에서 설명되고, 상기 출원은 본원에 참고로 포함된다. 접합체 모이어티는 지질 모이어티, 예를 들면, 콜레스테롤 모이어티, 콜린산, 티오에테르, 예를 들면, 헥실-5-트리틸티올, 티오콜레스테롤, 지방족 사슬, 예를 들면, 도데칸디올 또는 운데실 잔기, 인지질, 예를 들면, 디-헥사데실-rac-글리세롤 또는 트리에틸암모늄 1,2-디-O-헥사데실-rac-글리세로-3-H포스포네이트, 폴리아민 또는 폴리에틸렌 글리콜 사슬, 또는 마다만탄 아세트산, 팔미틸 모이어티, 또는 옥타데실아민 또는 헥실아미노-카르보닐-옥시콜레스테롤 모이어티를 포함하지만 이에 한정되지 않는다. 본 발명의 올리고뉴클레오티드는 활성 약물 물질, 예를 들면, 아스피린, 와파린, 페닐부타존, 이부프로펜, 수프로펜, 펜부펜, 케토프로펜, (S)-(+)-프라노프로펜, 카르프로펜, 단실사르코신, 2,3,5-트리요오드벤조산, 풀루페남산, 폴린산, 벤조티아디아지드, 클로로티아지드, 디아제핀, 인도메티신, 바르비투레이트, 세팔로스포린, 설파제, 당뇨병치료제, 항균제 또는 항생제에 접합될 수도 있다.
이러한 올리고뉴클레오티드 접합제의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제4,828,979호; 제4,948,882호; 제5,218,105호; 제5,525,465호; 제5,541,313호; 제5,545,730호; 제5,552,538호; 제5,578,717호; 제5,580,731호; 제5,580,731호; 제5,591,584호; 제5,109,124호; 제5,118,802호; 제5,138,045호; 제5,414,077호; 제5,486,603호; 제5,512,439호; 제5,578,718호; 제5,608,046호; 제4,587,044호; 제4,605,735호; 제4,667,025호; 제4,762,779호; 제4,789,737호; 제4,824,941호; 제4,835,263호; 제4,876,335호; 제4,904,582호; 제4,958,013호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5,082,830호; 제5,112,963호; 제5,214,136호; 제5,245,022호; 제5,254,469호; 제5,258,506호; 제5,262,536호; 제5,272,250호; 제5,292,873호; 제5,317,098호; 제5,371,241호; 제5,391,723호; 제5,416,203호; 제5,451,463호; 제5,510,475호; 제5,512,667호; 제5,514,785호; 제5,565,552호; 제5,567,810호; 제5,574,142호; 제5,585,481호; 제5,587,371호; 제5,595,726호; 제5,597,696호; 제5,599,923호; 제5,599,928호 및 제5,688,941호를 포함하지만 이에 한정되지 않는다.
제형
본 발명의 화합물은 취입, 분포 및/또는 흡수를 지원하기 위한 화합물의 다른 분자, 분자 구조 또는 혼합물, 예를 들면, 리포좀, 수용체-표적화된 분자, 경구, 직장, 국소 또는 기타 제제와 혼합되거나, 캡슐화되거나, 접합되거나 또는 연합될 수 있다. 이와 같은 취입, 분포 및/또는 흡수-지원 제제의 제조를 교시하는 대표적인 미국 특허는 미국 특허 제5,108,921호; 제5,354,844호; 제5,416,016호; 제5,459,127호; 제5,521,291호; 제5,543,165호; 제5,547,932호; 제5,583,020호; 제5,591,721호; 제4,426,330호; 제4,534,899호; 제5,013,556호; 제5,108,921호; 제5,213,804호; 제5,227,170호; 제5,264,221호; 제5,356,633호; 제5,395,619호; 제5,416,016호; 제5,417,978호; 제5,462,854호; 제5,469,854호; 제5,512,295호; 제5,527,528호; 제5,534,259호; 제5,543,152호; 제5,556,948호; 제5,580,575호 및 제5,595,756호를 포함하지만 이에 한정되지 않고, 상기 출원은 본원에 참고로 포함된다.
비록 안티센스 올리고뉴클레오티드가 표적 발현 및/또는 기능을 조정하기 위하여 벡터로 투여될 필요는 없지만, 본 발명의 양태는 안티센스 올리고뉴클레오티드의 발현을 위한 발현 벡터 구조체에 관한 것이고, 이들 벡터 구조체는 프로모터, 하이브리드 프로모터 유전자 서열을 포함하고, 강한 구조성 프로모터 활성, 또는 목적하는 경우 유도될 수 있는 프로모터 활성을 갖는다.
하나의 양태에서, 본 발명의 실시는 적절한 핵산 운반 시스템으로 전술한 안티센스 올리고뉴클레오티드 중에서 하나 이상을 투여하는 것을 수반한다. 하나의 양태에서, 상기 시스템은 폴리뉴클레오티드에 작동가능하게 연결된 비-바이러스 벡터를 포함한다. 이러한 비-바이러스 벡터의 예는 단독으로, 또는 적합한 단백질, 폴리사카라이드 또는 지질 제제와 조합으로 올리고뉴클레오티드(예를 들면, 서열 번호 12 내지 49 중에서 임의의 하나 이상)를 포함한다.
추가로 적합한 핵산 운반 시스템은 바이러스 벡터, 전형적으로 아데노바이러스, 아데노바이러스-연합된 바이러스(AAV), 헬퍼-의존성 아데노바이러스, 레트로바이러스 또는 Japan-리포좀의 헤마글루티닌 바이러스(HVJ) 복합체 중의 하나 이상으로부터의 서열을 포함한다. 바람직하게는, 바이러스 벡터는 폴리뉴클레오티드에 작동가능하게 연결된 강한 진핵 프로모터, 예를 들면, 사이토메갈로바이러스(CMV) 프로모터를 포함한다.
추가적으로 바람직한 벡터는 바이러스 벡터, 융합 단백질 및 화학적 접합체를 포함한다. 레트로바이러스 벡터는 몰로니(Moloney) 뮤린 백혈병 바이러스 및 HIV-계 바이러스를 포함한다. 한 가지 바람직한 HIV-계 바이러스 벡터는 최소한 2개 벡터를 포함하고, 여기서 gag 및 pol 유전자는 HIV 게놈으로부터 유래되고, env 유전자는 다른 바이러스로부터 유래된다. DNA 바이러스 벡터가 바람직하다. 이들 벡터는 폭스 벡터, 예를 들면, 오르토폭스(orthopox) 또는 아비폭스(avipox) 벡터, 헤르페스바이러스 벡터, 예를 들면, 헤르페스 심플렉스 I 바이러스(HSV) 벡터 및 아데노-연합된 바이러스 벡터를 포함한다.
본 발명의 안티센스 화합물은 임의의 약제학적으로 허용되는 염, 에스테르 또는 이러한 에스테르의 염, 또는 인간을 비롯한 동물에 투여시 생물학적 활성 대사물질 또는 이의 잔기를 직간접적으로 제공할 수 있는 임의의 다른 화합물을 포함한다.
용어 "약제학적으로 허용되는 염"은 본 발명의 화합물의 생리학적으로 및 약제학적으로 허용되는 염, 다시 말하면, 부모 화합물의 바람직한 생물학적 활성을 보유하지만 여기에 바람직하지 않은 독성 효과를 부여하지 않는 염을 지칭한다. 올리고뉴클레오티드의 경우, 약제학적으로 허용되는 염의 바람직한 예 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명되고, 상기 출원은 본원에 참고로 포함된다.
본 발명은 또한 본 발명의 안티센스 화합물을 포함하는 약제학적 조성물 및 제형을 포함한다. 본 발명의 약제학적 조성물은 국소 또는 전신 치료가 바람직한지 여부 및 치료되는 부위에 따라 여러 방법으로 투여될 수 있다. 투여는 국소(눈, 및 질 및 직장 운반을 비롯한 점막 포함), 예를 들면, 분무기를 비롯하여 분말 또는 에어로졸의 흡입 또는 통기에 의해 폐; 기관내, 비내, 상피 또는 경피, 구강 또는 비경구일 수 있다. 비경구 투여는 정맥내, 동맥내, 피하, 복강내 또는 근육내 주사 또는 주입; 또는 두개내, 예를 들면, 수막강내 또는 뇌실내 투여를 포함한다.
중추신경계 내에 조직을 치료하기 위하여, 투여는, 예를 들면, 뇌척수액 내로 주사 또는 주입에 의해 수행될 수 있다. 뇌척수액 내로 안티센스 RNA의 투여는, 예를 들면, 미국 특허 출원 공개 번호 제2007/0117772호("Methods for slowing familial ALS disease progression")에서 설명되고, 상기 출원은 본원에 참고로 포함된다.
본 발명의 안티센스 올리고뉴클레오티드가 중추신경계 내에 세포에 투여되는 것으로 의도될 때, 투여는 뇌-혈관 장벽을 교차하여 본 발명의 안티센스 올리고뉴클레오티드의 침투를 촉진할 수 있는 하나 이상의 작용제로 수행될 수 있다. 주사는, 예를 들면, 내후각뇌피질 또는 해마에서 수행될 수 있다. 근육 조직 내에 운동 뉴런에 아데노바이러스 벡터의 투여에 의한 신경영양성 인자의 운반은, 예를 들면, 미국 특허 제6,632,427호("Adenoviral-vector-mediated gene transfer into medullary motor neurons")에서 설명되고, 상기 출원은 본원에 참고로 포함된다. 뇌, 예를 들면, 선조체, 시상, 해마, 또는 흑색질에 직접적으로 벡터의 전달은 당해 분야에 공지되어 있고, 예를 들면, 본원에 참고로 포함되는 미국 특허 제6,756,523호("Adenovirus vectors for the transfer of foreign genes into cells of the central nervous system particularly in brain")에서 설명된다. 투여는 주사와 같이 신속하게 수행되거나, 서방성 제형(slow release formulation)의 느린 주입 또는 투여와 같이 장기간 동안 수행될 수 있다.
본 발명의 안티센스 올리고뉴클레오티드는 또한 바람직한 약제학적 또는 약력학적 성질을 제공하는 작용제와 연결되거나 접합될 수 있다. 예를 들면, 안티센스 올리고뉴클레오티드는 뇌-혈관 장벽을 교차하여 침투 또는 운반을 증진하는 당분야에 공지된 임의의 물질, 예를 들면, 트랜스페린 수용체에 대한 항체에 결합되고, 정맥내 주사에 의해 투여될 수 있다. 안티센스 화합물은 바이러스 벡터, 예를 들면, 안티센스 화합물을 더욱 효과적으로 만들고/만들거나 뇌-혈관 장벽을 교차하여 안티센스 화합물의 운반을 증가시키기 위하여 바이러스 벡터와 연결될 수 있다. 삼투성 뇌-혈관 장벽 파괴는 또한, 예를 들면, 메소 에리트리톨, 자일리톨, D(+) 갈락토오스, D(+) 락토오스, D(+) 자일로오스, 둘시톨, 미오-이노시톨, L(-) 프럭토오스, D(-) 만니톨, D(+) 글루코오스, D(+) 아라비노스, D(-) 아라비노스, 셀로비오스, D(+) 말토오스, D(+) 라피노오스, L(+) 람노스, D(+) 멜리비오스, D(-) 리보오스, 아도니톨, D(+) 아라비톨, L(-) 아라비톨, D(+) 푸코오스, L(-) 푸코오스, D(-) 릭소스, L(+) 릭소스, 및 L(-) 릭소스를 포함하지만 이에 한정되지 않는 당, 또는 글루타민, 리신, 아르기닌, 아스파라긴, 아스파르트산, 시스테인, 글루타민산, 글리신, 히스티딘, 류신, 메티오닌, 페닐알라닌, 프롤린, 세린, 트레오닌, 티로신, 발린, 및 타우린을 포함하지만 이에 한정되지 않는 아미노산의 주입에 의해 달성될 수 있다. 뇌-혈관 장벽 침투를 증강시키기 위한 방법과 물질은, 예를 들면, 미국 특허 제4,866,042호("Method for the delivery of genetic material across the blood brain barrier"), 제6,294,520호("Material for passage through the blood-brain barrier") 및 제6,936,589호("Parenteral delivery systems")에서 설명되고, 상기 출원은 그 전문이 본원에 참고로 포함된다.
본 발명의 안티센스 화합물은 취입, 분포 및/또는 흡수를 지원하기 위한 화합물의 다른 분자, 분자 구조 또는 혼합물, 예를 들면, 리포좀, 수용체-표적화된 분자, 경구, 직장, 국소 또는 기타 제형과 혼합되거나, 캡슐화되거나, 접합되거나 또는 연합될 수 있다. 예를 들면, 양이온성 지질이 올리고뉴클레오티드 취입을 용이하게 하기 위하여 제형 내에 포함될 수 있다. 취입을 용이하게 하는 것으로 밝혀진 이와 같은 한 가지 조성물은 LIPOFECTIN(GIBCO-BRL(Bethesda, MD)로부터 이용가능)이다.
하나 이상의 2'-O-메톡시에틸 변형을 가진 올리고뉴클레오티드는 경구 투여용으로 특히 유용한 것으로 생각된다. 국소 투여를 위한 약제학적 조성물 및 제형은 경피 패치, 연고, 로션, 크림, 겔, 드롭, 좌약, 스프레이, 액상 및 분말을 포함할 수 있다. 통상적인 약제학적 담체, 수성, 분말 또는 오일 베이스, 증점제 등이 필수적이거나 바람직할 수 있다. 피복된 콘돔, 장갑 등이 또한 유용할 수 있다.
본 발명의 약제학적 제형은 통상적으로 단위 약형(unit dosage form)으로 제공될 수 있고, 제약 산업에서 공지된 전통적인 기술에 따라 제조될 수 있다. 이와 같은 기술은 활성 성분을 약제학적 담체 또는 부형제와 연합시키는 단계를 포함한다. 일반적으로, 제형은 활성 성분을 액상 담체 또는 미세하게 분할된 고형 담체 또는 둘 모두와 균일하게 및 친밀하게 연합시키고, 이후 필요에 따라 제품의 형태를 만듦으로써 제조된다.
본 발명의 조성물은 정제, 캡슐, 겔 캡슐, 액체 시럽, 연성 겔, 좌약 및 관장제를 포함하지만 이에 한정되지 않는 많은 가능한 약형으로 제형화될 수 있다. 본 발명의 조성물은 또한 수성, 비-수성 또는 혼성 매질에서 현탁액으로 제형화될 수 있다. 수성 현탁액은 나트륨 카르복시메틸셀룰로오스, 소르비톨 및/또는 덱스트란을 포함하는 현탁액의 점성을 증가시키는 성분을 추가로 포함할 수 있다. 현탁액은 또한 안정화제를 함유할 수 있다.
본 발명의 약제학적 조성물은 용액, 에멀젼, 폼 및 리포좀-함유 제형을 포함하지만 이에 한정되지 않는다. 본 발명의 약제학적 조성물 및 제형은 하나 이상의 침투 강화제, 담체, 부형제 또는 기타 활성 또는 비활성 성분을 포함할 수 있다.
에멀젼은 전형적으로, 0.1㎛ 직경을 초과하는 액적의 형태로 서로 분산된 하나의 액체의 불균일계이다. 에멀젼은 분산된 상 이외에, 추가 성분, 및 수성 상, 오일상 또는 별도의 상으로서 그 자체 내에 용액으로서 존재하는 활성 성분을 포함할 수 있다. 본 발명의 양태로서 마이크로에멀젼이 포함된다. 에멀젼 및 이들의 용도는 당해 분야에 공지되어 있으며, 미국 특허 제6,287,860호에서 추가로 설명된다.
본 발명의 제형은 리포좀 제형을 포함한다. 본 발명에서, 용어 "리포좀"은 구형 이중층 또는 이중층에 배열된 양쪽성 지질로 구성된 소포(vesicle)를 의미한다. 리포좀은 단층라멜라 또는 다층라멜라 소포이고, 이들은 친유성 물질로부터 형성된 막 및 운반되는 조성물을 포함하는 수성 내부를 가진다. 양이온성 리포좀은 안정된 복합체를 형성하기 위하여 음전하를 띈 DNA 분자와 상호작용하는 것으로 생각되는 양전하를 띈 리포좀이다. pH-민감성 또는 음전하를 띈 리포좀은 DNA와 복합체를 형성하기 보다는 DNA를 포집하는 것으로 생각된다. 양이온성 및 비-양이온성 리포좀은 DNA를 세포로 운반하는데 이용된다.
리포좀은 또한 "입체구조적으로 안정화된" 리포좀을 포함하는데, 본원에서 상기 용어는 하나 이상의 특화된 지질을 포함하는 리포좀을 지칭한다. 리포좀에 통합될 때, 이와 같은 특화된 지질은 이들 특화된 지질이 없는 리포좀과 비교하여 순환 반감기가 강화된 리포좀을 발생시킨다. 입체구조적으로 안정화된 리포좀의 예는 리포좀의 소포-형성 지질 부분의 일부가 하나 이상의 글리코리피드를 포함하거나, 하나 이상의 친수성 폴리머, 예를 들면, 폴리에틸렌 글리콜(PEG) 모이어티로 유도화된 것들이다. 리포좀 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명된다.
본 발명의 약제학적 제형 및 조성물은 또한 계면활성제를 포함할 수 있다. 약물 제품, 제형 및 에멀젼에서 계면활성제의 사용은 당해 분야에 잘 공지되어 있다. 계면활성제 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명되고, 상기 출원은 본원에 참고로 포함된다.
하나의 양태에서, 본 발명은 핵산, 특히 올리고뉴클레오티드의 효과적인 운반을 달성하기 위하여 다양한 침투 강화제를 이용한다. 세포 막을 교차하여 비-친유성 약물의 확산을 지원하는 것 이외에, 침투 강화제는 또한 친유성 약물의 침투성을 강화시킨다. 침투 강화제는 5가지 넓은 범주, 다시 말하면, 계면활성제, 지방산, 담즙산 염, 킬레이트화제, 및 비-킬레이트화 비-계면활성제 중의 하나에 속하는 것으로 분류될 수 있다. 침투 강화제 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명되고, 상기 출원은 본원에 참고로 포함된다.
당업자는 제형이 그들의 의도된 용도, 다시 말하면, 투여 경로에 따라 일과적으로 설계된다는 것을 인지할 것이다.
국소 투여에 바람직한 제형은 그 안에서 본 발명의 올리고뉴클레오티드가 국소 운반제, 예를 들면, 지질, 리포좀, 지방산, 지방산 에스테르, 스테로이드, 킬레이트화제 및 계면활성제와 혼합되는 것들을 포함한다. 바람직한 지질 및 리포좀은 중성(예를 들면, 디올레일-포스파티딜 DOPE 에탄올아민, 디미리스토일포스파티딜 콜린 DMPC, 디스테아로일포스파티딜 콜린), 음성(예를 들면, 디미리스토일포스파티딜 글리세롤 DMPG) 및 양이온(예를 들면, 디올레일테트라메틸아미노프로필 DOTAP 및 디올레일-포스파티딜 에탄올아민 DOTMA)을 포함한다.
국소 또는 기타 투여를 위하여, 본 발명의 올리고뉴클레오티드는 리포좀 내에 캡슐화되거나, 리포좀에, 특히 양이온 리포좀에 복합체를 형성할 수 있다. 대안적으로, 올리고뉴클레오티드는 지질, 특히 양이온 지질에 복합될 수 있다. 바람직한 지방산 및 에스테르, 이들의 약제학적으로 허용되는 염, 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명된다.
경구 투여용 조성물 및 제형은 분말 또는 과립, 미립자, 나노입자, 물 또는 비-수성 매질 중의 현탁액 또는 용액, 캡슐, 겔 캡슐, 향낭, 정제 또는 미니정제를 포함한다. 증점제, 향료, 희석제, 유화제, 분산 보조제 또는 결합제가 바람직할 수 있다. 바람직한 경구 제형은 본 발명의 올리고뉴클레오티드가 하나 이상의 침투 강화제, 계면활성제 및 킬레이터와 함께 투여되는 것들이다. 바람직한 계면활성제는 지방산 및/또는 이들의 에스테르 또는 염, 담즙산 및/또는 이들의 염을 포함한다. 바람직한 담즙산/염 및 지방산 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명되고, 상기 출원은 본원에 참고로 포함된다. 침투 강화제의 조합, 예를 들면, 담즙산/염과 공동으로 지방산/염이 또한 바람직하다. 특히 바람직한 조합은 라우르산, 카프르산 및 UDCA의 나트륨 염이다. 추가의 침투 강화제는 폴리옥시에틸렌-9-라우릴 에테르, 폴리옥시에틸렌-20-세틸 에테르를 포함한다. 본 발명의 올리고뉴클레오티드는 분무된 건조 입자를 비롯한 과립형으로 경구 운반되거나, 미립자 또는 나노입자를 형성하기 위하여 복합될 수 있다. 올리고뉴클레오티드 착화제 및 이들의 용도는 미국 특허 제6,287,860호에서 추가로 설명되고, 상기 출원은 본원에 참고로 포함된다.
비경구, 기관내 또는 심실내 투여를 위한 조성물 및 제형은 완충액, 희석액, 및 침투 강화제, 담체 화합물 및 기타 약제학적으로 허용되는 담체 또는 부형제를 포함하지만 이에 한정되지 않는 기타 적합한 첨가제를 또한 함유할 수 있는 무균 수용액을 포함할 수 있다.
본 발명의 일정한 양태는 하나 이상의 올리고머 화합물 및 비-안티센스 기전에 의해 기능하는 하나 이상의 다른 화학요법제를 포함하는 약제학적 조성물을 제공한다. 이러한 화학요법제의 예는 암 화학요법 약물, 예를 들면, 다우노루비신, 다우노마이신, 닥티노마이신, 독소루비신, 에피루비신, 이다루비신, 에소루비신, 블레오마이신, 마포스파미드, 이포스파미드, 시토신 아라비노시드, 비스클로로에틸-니트로소우레아, 부설판, 미토마이신 C, 악티노마이신 D, 미트라마이신, 프레드니손, 히드록시프로게스테론, 테스토스테론, 타목시펜, 다카르바진, 프로카르바진, 헥사메틸멜라민, 펜타메틸멜라민, 미톡산트론, 암사크린, 클로람부실, 메틸사이클로헥실니트로소우레아, 질소 머스터드, 멜파란, 사이클로포스파미드, 6-머캅토퓨린, 6-티오구아닌, 시타라빈, 5-아자시티딘, 히드록시우레아, 데옥시코포르마이신, 4-히드록시퍼옥시사이클로-포스포라미드, 5-플루오르우라실(5-FU), 5-플루오르데옥시우리딘(5-FUdR), 메토트렉세이트(MTX), 콜히친, 탁솔, 빈크리스틴, 빈블라스틴, 에토포시드(VP-16), 트리메트렉세이트, 이리노테칸, 토포테칸, 젬시타빈, 테니포시드, 시스플라틴 및 디에틸스틸베스트롤(DES)을 포함하지만 이에 한정되지 않는다. 본 발명의 화합물과 함께 사용될 때, 이러한 화학요법제는 개별적으로(예를 들면, 5-FU 및 올리고뉴클레오티드), 순차적으로(예를 들면, 일정 기간 동안 5-FU 및 올리고뉴클레오티드, 그 이후에 MTX 및 올리고뉴클레오티드), 또는 하나 이상의 다른 화학요법제(예를 들면, 5-FU, MTX 및 올리고뉴클레오티드, 또는 5-FU, 방사능요법 및 올리고뉴클레오티드)와 조합되어 이용될 수 있다. 비-스테로이드성 소염제 약물 및 코르티코스테로이드를 포함하지만 이에 한정되지 않는 소염제 약물, 및 리비비린, 비다라빈, 아시클로비르 및 강시클로비르를 포함하지만 이에 한정되지 않는 항바이러스 약물이 또한 본 발명의 조성물에 조합될 수 있다. 안티센스 화합물 및 다른 비-안티센스 약물의 조합은 또한 본 발명의 범위 내에 있다. 2개 이상의 조합된 화합물이 함께 또는 순차적으로 이용될 수 있다.
또 다른 관련 양태에서, 본 발명의 조성물은 제1 핵산을 표적으로 하는 하나 이상의 안티센스 화합물, 특히 올리고뉴클레오티드 및 제2 핵산 표적을 표적으로 하는 하나 이상의 추가 안티센스 화합물을 함유할 수 있다. 예를 들면, 제1 표적은 뇌 유래 신경영양 인자(BDNF)의 특정 안티센스 서열일 수 있고, 제2 표적은 다른 뉴클레오티드 서열로부터 영역일 수 있다. 대안적으로, 본 발명의 조성물은 동일한 뇌 유래 신경영양 인자(BDNF) 핵산 표적의 상이한 영역을 표적으로 하는 2개 이상의 안티센스 화합물을 함유할 수 있다. 안티센스 화합물의 다양한 예가 본원에서 예시되고, 다른 예는 당해 분야에 공지된 적합한 화합물 중에서 선택될 수 있다. 2개 이상의 복합 화합물이 함께 또는 순차적으로 이용될 수 있다.
투약(dosing):
치료 조성물의 제형 및 이들의 후속 투여(투약)는 당해 분야의 기술에 속한다고 여겨진다. 투약은 수 일 내지 수개월 간, 또는 치료 효과 또는 질환 상태의 감소가 달성될 때까지 지속되는 치료 과정과 함께, 치료되는 질환 상태의 중증도와 반응성에 따라 좌우된다. 최적의 투약 일정은 환자의 신체에 약물 축적의 측량으로부터 계산될 수 있다. 당업자는 최적 용량, 투약 방법 및 반복률을 용이하게 결정할 수 있다. 최적 용량은 개별 올리고뉴클레오티드의 상대적 효능에 따라 달라질 수 있고, 일반적으로, 시험관내 및 생체내 동물 모델에서 효과적인 것으로 밝혀진 EC50에 근거하여 예측된다. 일반적으로, 용량은 체중 ㎏당 0.01㎍ 내지 10㎎이고, 매일, 매주, 매월 또는 매년 1회 이상, 또는 심지어 2 내지 20년 마다 1회로 제공될 수 있다. 당업자는 측정된 잔류 시간 및 체액 또는 조직 내에 약물의 농도에 근거하여 투약을 위한 반복률을 용이하게 예측할 수 있다. 성공적인 치료 후, 질환 상태의 재발을 방지하기 위하여 환자가 유지요법을 받도록 하는 것이 바람직하며, 이때 올리고뉴클레오티드는 체중 ㎏당 0.01㎍ 내지 10㎎ 범위의 유지 용량으로, 매일 1회 이상 내지 매 20년마다 1회로 투여된다.
양태에서, 환자는 체중 ㎏당 약 1㎎ 이상, 약 2㎎ 이상, 약 3㎎ 이상, 약 4㎎ 이상, 약 5㎎ 이상, 약 6㎎ 이상, 약 7㎎ 이상, 약 8㎎ 이상, 약 9㎎ 이상, 약 10㎎ 이상, 약 15㎎ 이상, 약 20㎎ 이상, 약 25㎎ 이상, 약 30㎎ 이상, 약 35㎎ 이상, 약 40㎎ 이상, 약 45㎎ 이상, 약 50㎎ 이상, 약 60㎎ 이상, 약 70㎎ 이상, 약 80㎎ 이상, 약 90㎎ 이상, 또는 약 10㎎ 이상인 약물의 용량으로 치료된다. 안티센스 올리고뉴클레오티드의 일정한 주사 용량은, 예를 들면, 미국 특허 제7,563,884호("Antisense modulation of PTP1B expression")에서 설명되고, 상기 출원은 본원에 참고로 포함된다.
본 발명의 다양한 양태가 상기에서 설명되긴 했지만, 이들은 단지 예시로써 제공되고 제한으로서 간주되지 않는 것으로 이해되어야 한다. 본 발명의 취지 또는 범위를 벗어나지 않으면서, 본 발명의 개시에 따라서 이들 설명된 양태에 대해 다양한 변화가 만들어질 수 있다. 따라서, 본 발명의 너비 및 범위는 상기 설명된 임의의 양태에 의해 한정되지 않는다.
본원에서 언급된 모든 문헌은 본원에 참고로 포함된다. 본 출원에서 인용된 모든 간행물 및 특허 문헌은 각 간행물 또는 특허 문헌이 개별적으로 그렇게 언급된 것처럼, 순전히 참고로서 포함된다. 본 문서에서 다양한 참고문헌의 인용에 의해, 출원인은 임의의 특정한 참고문헌이 본 발명에 대한 "선행 기술"임을 인정하지 않는다. 본 발명의 조성물 및 방법의 양태는 하기 실시예에서 예시된다.
실시예
하기 비제한적 실시예는 본 발명의 선택된 양태를 예시하기 위한 것이다. 제시된 성분의 비율 변화 및 구성요소의 대안예는 당업자에 자명할 것이고 본 발명의 양태의 범위 내에 있다.
실시예 1: 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 센스 가닥 및/또는 BDNF에 대한 핵산 분자 안티센스에 특이적인 안티센스 올리고뉴클레오티드의 설계
상기 지시된 바와 같이, 용어 "특이적인 올리고뉴클레오티드" 또는 "표적으로 하는 올리고뉴클레오티드"는 (i) 표적화된 유전자의 일부와 안정된 복합체를 형성할 수 있거나, (ii) 표적화된 유전자의 mRNA 전사체의 일부와 안정된 이중나선을 형성할 수 있는 서열을 갖는 올리고뉴클레오티드를 지칭한다.
적절한 올리고뉴클레오티드의 선별은 목적되는 용융 온도(일반적으로 50-60℃)로 표적 폴리뉴클레오티드 서열과 함께 하이브리드를 형성하지만 셀프-다이머(self-dimer) 또는 다른 복합체 이차 구조를 형성하지 않을 것인 19 내지 25개 뉴클레오티드의 하위서열을 각각의 주어진 서열 내에서 자동적으로 확인하는 컴퓨터 프로그램(예를 들면, IDT AntiSense Design, IDT OligoAnalyzer)를 사용하여 가능할 수 있다.
적절한 올리고뉴클레오티드의 선별은 핵산 서열을 자동적으로 정렬하고 동일성 또는 상동성의 영역을 표시하는 컴퓨터 프로그램을 사용하여 추가로 가능할 수 있다. 이러한 프로그램은, 예를 들면, GenBank와 같은 데이터베이스를 검색하거나 PCR 산물을 서열화함으로써, 획득된 핵산 서열을 비교하는데 사용된다. 주어진 게놈의 유전자 및 유전자간 영역 범위에서 핵산 서열의 비교는 흥미있는 유전자에 적절한 정도의 특이성을 나타내는 핵산 서열의 선별을 가능하게 한다. 이들 절차는 주어진 게놈에서 표적 핵산 서열에 높은 정도의 상보성을 나타내고 다른 핵산 서열에 낮은 정도의 상보성을 나타내는 올리고뉴클레오티드의 선별을 가능하게 한다. 당업자는 본 발명에서 사용을 위한 유전자의 적절한 영역을 선별하는데 상당한 허용 범위가 존재한다는 것을 인지할 것이다.
안티센스 화합물은 표적 핵산에 화합물의 결합이 표적 핵산의 정상적인 기능을 간섭하여 기능 및/또는 활성의 조정을 유발하고, 특정한 결합이 요망되는 조건 하에, 다시 말하면, 생체내 분석 또는 치료적 처리의 경우에 생리학적 조건 하에, 및 시험관내 분석의 경우에 이들 분석이 수행되는 조건 하에, 비-표적 핵산 서열에 안티센스 화합물의 비-특이적 결합을 회피할 수 있을 만큼 충분한 정도의 상보성이 존재할 때, "특이적으로 하이브리드화가능"하다
본원에 기술된 올리고뉴클레오티드의 하이브리드화 성질은 당해 분야에 공지된 하나 이상의 시험관내 분석에 의해 결정될 수 있다. 예를 들면, 본원에 기술된 올리고뉴클레오티드의 성질은 용융 곡선 분석(melting curve assay)을 이용하여 표적 천연 안티센스와 잠재적인 약물 분자 사이에 결합 강도를 측정함으로써 획득될 수 있다.
표적 천연 안티센스와 잠재적인 약물 분자(Molecule) 사이에 결합 강도는 용융 곡선 분석과 같은 분자간 상호 작용의 강도를 측정하는 임의의 확립된 방법을 이용하여 예측될 수 있다.
용융 곡선 분석은 천연 안티센스/Molecule 복합체에서 이중 가닥으로부터 단일 가닥 형태로 신속한 전이가 일어나는 온도를 결정한다. 이러한 온도는 2개 분자 사이에 상호작용 강도의 신뢰성 있는 척도로서 폭넓게 인정된다.
용융 곡선 분석은 실제 천연 안티센스 RNA 분자 또는 Molecule의 결합 부위에 상응하는 합성 DNA 또는 RNA 뉴클레오티드의 cDNA 사본을 사용하여 수행될 수 있다. 이러한 분석을 실행하기 위하여 모든 필수 시약을 함유하는 다중 키트가 사용가능하다(예를 들면, Applied Biosystems Inc. MeltDoctor kit). 이들 키트는 이중 가닥 DNA(dsDNA) 결합 염료(예를 들면, ABI HRM 염료, SYBR Green, SYTO 등) 중에서 하나를 포함하는 적절한 완충액을 포함한다. dsDNA 염료의 성질은 그들이 자유 형태에서는 형광을 거의 방출하지 않지만, dsDNA에 결합될 때 상당한 형광성이다.
분석을 수행하기 위하여, cDNA 또는 대응하는 올리고뉴클레오티드는 특정 제조업체의 프로토콜에 규정된 농도에서 Molecule와 혼합된다. 혼합물은 95℃로 가열되어 모든 미리-형성된 dsDNA 복합체가 해리된 다음, 실온 또는 키트 제조업체에 의해 규정된 더욱 낮은 온도로 서서히 냉각되어 DNA 분자가 어닐링(annealing)되도록 한다. 그 다음, 새로 형성된 복합체는 95℃로 천천히 가열되고, 반응에 의해 생성된 형광물질의 양에 대한 데이터가 동시에 연속적으로 수집된다. 형광 강도는 반응에 존재하는 dsDNA의 양에 반비례한다. 데이터는 키트에 적합한 실시간 PCR 장비(예를 들면, ABI의 StepOne Plus Real Time PCR System 또는 lightTyper 장치, Roche Diagnostics, Lewes, UK)를 이용하여 수집될 수 있다.
용융 피크는 적합한 소프트웨어(예를 들면, lightTyper(Roche) 또는 SDS Dissociation Curve, ABI)를 이용하여 온도(x-축)에 대하여 온도에 관련된 형광의 네거티브 도함수(negative derivative)(y축에서 -d(형광)/dT)를 플롯팅(plotting)함으로써 구성된다. 데이터는 dsDNA 복합체에서 단일 가닥 분자로의 신속한 전이 온도를 확인하기 위하여 분석된다. 이러한 온도는 Tm으로 불리고, 두 분자간의 상호작용 강도에 직접적으로 비례한다. 전형적으로, Tm은 40℃를 초과할 것이다.
변형된 AntagoNAT 분자의 설계:
다수의 DNA 기반의 안티센스 올리고뉴클레오티드가 설계되고, 시험되고, 비코딩 Bdnf-AS 및 다른 안티센스 전사체를 표적으로 하는 AntagoNAT로 지칭되었다. 다양한 AntagoNAT는 완전한 포스포로티오에이트 변형이 있거나 없는 12 내지 20개 뉴클레오티드 길이 ± 2-O'-메틸 RNA 또는 LNA 변형된 뉴클레오티드 범위로 설계되었다. 가장 높은 효능이 각 말단의 3개의 LNA-변형된 뉴클레오티드(XXXnnnnnnnnnnXXX)가 있는 16-뉴클레오티드 포스포로티오에이트 갭머에 의한 Bdnf mRNA 수준에서 관찰되었다. 인간 BDNF 센스-안티센스 전사체 사이에 상호작용을 차단하기 위하여, LNA 및 2-O'-메틸 RNA 분자를 둘 다 함유하는 14-뉴클레오티드 믹스머(mixmer)가 사용되었다. 이들 2-O'-메틸 RNA-변형된 올리고뉴클레오티드가 단지 RNA를 차단하기 위하여 제안됨에도 불구하고, 표적화된 RNA의 근소한 하향조절이 이 실험에서 관찰되었다(도 11). 이들 연구에서 사용된 다양한 AntagoNAT의 서열, 뿐만 아니라 다른 siRNA, 프라이머 및 프로브는 표 1에 열거된다.
실시예 2:
BDNF 폴리뉴클레오티드의 조정
실시예 2에서 사용된 모든 안티센스 올리고뉴클레오티드는 실시예 1에서 기술된 바와 같이 설계되었다. 제조업체(Coralville, IA의 IDT Inc.)는 설계된 포스포티오에이트 결합 올리고뉴클레오티드를 제조하도록 지시를 받고 표 1에 도시된 설계된 포스포티오에이트 유사체를 제공하였다. 뉴클레오티드 사이에 별표 지정은 포스포티오에이트 결합의 존재를 지시한다. 실시예 2에서 실험에 요구되는 올리고뉴클레오티드는 임의의 적절한 최신 방법, 예를 들면, IDT에 의해 사용된 방법을 이용하여 합성될 수 있다: 고형 서포트, 예를 들면, 5 마이크론 제어된 구멍 유리 비드(CPG) 상에서, 포스포라미디트 단량체(모든 활성 기가 보호 기, 예를 들면, 당에서 트리틸 기, A와 C에서 벤조일 및 G에서 N-2-이소부티릴로 보호되는 정상적인 뉴클레오티드)를 이용하여. 보호 기는 올리고뉴클레오티드 합성 동안 바람직하지 않은 반응을 예방한다. 보호 기는 합성 과정의 종결 시점에서 제거된다. 최초 뉴클레오티드는 3' 탄소를 통해 고형 서포트에 연결되고, 합성은 3'에서 5' 방향으로 진행된다. 성장하는 올리고뉴클레오티드 사슬에 새로운 염기의 추가는 4단계로 진행된다: 1) 보호 기가 트리클로로아세트산을 이용하여 고정된 뉴클레오티드의 5' 산소로부터 제거되고; 2) 고정된 뉴클레오티드 및 차순 뉴클레오티드는 테트라졸을 이용하여 서로 결합되고; 이러한 반응은 테트라졸릴 포스포라미디트 중간물질을 통하여 진행되고; 3) 반응되지 않은 유리 뉴클레오티드 및 반응 부산물은 세척되고, 반응되지 않은 고정된 올리고뉴클레오티드는 다음 라운드의 합성에 그들의 참여를 예방하기 위해 캡핑(capping)되고; 캡핑은 아세트산 무수물 및 N-메틸 이미다졸을 이용하여 유리 5' 하이드록실을 아세틸화시킴으로써 달성되고; 4) 뉴클레오티드 간에 결합을 안정화시키기 위해, 포스포디에스테르 결합이 발생해야 하는 경우에 요오드와 물, 또는 포스포티오에이트 결합이 요구되는 경우에 Beaucage 시약(3H-1,2-벤조디티올-3-온-1,1-디옥시드)을 이용하여 인이 산화된다. 이들 2가지 산화제를 교대시킴으로써, 키메라 골격이 작제될 수 있다. 앞서 기술된 4 단계 사이클은 서열 내에 모든 뉴클레오티드에 대해 반복된다. 완전한 서열이 합성될 때, 올리고뉴클레오티드는 고형 서포트로부터 절단되고, 높은 온도에서 수산화암모늄을 이용하여 탈보호된다. 보호 기는 탈염(desalting)에 의해 세척되고, 나머지 올리고뉴클레오티드는 동결건조된다.
BDNF mRNA의 양을 정량하기 위한 상이한 siRNA에 의한 Hek293 세포 처리
1. ATCC(cat# CRL-1573)로부터의 Hek293 세포를 37℃ 및 5% CO2에서 MEM/EBSS(Hyclone cat# SH30024) + 10% FBS + 페니실린 + 스트렙토마이신 중에서 성장시켰다. 실험 1일 전, 세포를 5x105/웰의 밀도로 6개의 웰 플레이트에 재플레이팅하고, 37℃ 및 5% CO2에서 배양시켰다.
2. 실험일에, 6개의 웰 플레이트의 배지를 신선한 MEM/EBSS +10% FBS로 교체하였다.
3. 모든 BDNF-AntagoNAT(BDNF-AS의 올리고뉴클레오티드 안티센스)를 20uM 농도로 희석하고, BDNF-AS siRNA(BDNF-AS의 siRNA 상보성)를 10uM로 희석하고; 두 올리고뉴클레오티드 화합물은 모두 IDT에 의해 제조되었다. 하나의 웰에 투약하기 위하여, 이러한 용액 2㎕를 실온에서 20분 동안 Opti-MEM 배지(Gibco cat#31985-070) 400㎕ 및 Lipofectamine 2000(Invitrogen cat# 11668019) 4ul와 함께 배양하고, 6개의 웰 플레이트 중 하나의 웰에 HepG2 세포를 적가 방식으로 적용하였다. 올리고뉴클레오티드 용액 대신 물 2㎕를 포함하는 유사한 혼합물을 모의-형질감염된 대조군을 위해 사용하였다.
4. 37℃ 및 5% CO2에서 배양 3 내지 18시간 후, 배지를 신선한 MEM/EBSS + 10% FBS + 페니실린 + 스트렙토마이신으로 교체하였다.
5. 48시간 후 안티센스 올리고뉴클레오티드의 첨가를 수행하였다. 그 다음, 배지를 제거하고, Promega로부터의 SV Total RNA Isolation System(cat# Z3105)을 사용하여 제조업체의 지시에 따라 세포로부터 RNA를 추출하였다.
6. 추출된 RNA 200-400ng을 무작위 육량체, dNTP의 2.5mM 혼합물, MgCl2 및 적절한 버퍼를 사용하여 수행된 역전사 반응에 가한다. 이러한 역전사 반응으로부터의 cDNA(20-40ng)를 사용하여 ABI Taqman Gene Expression Mix(cat#4369510), 포워드 및 리버스 프라이버 300nM, 15㎕의 최종 반응 용적 중의 200nM 프로브를 사용하는 실시간 PCR에 의한 유전자 발현을 모니터링하였다. 프라이머/프로브는 FileBuilder 소프트웨어(Applied Biosystem)를 사용하여 설계되었다. 프라이머는 센스-안티센스 쌍에 특이적인 가닥이고, 프로브는 게놈 DNA 증폭의 기회를 제거하는 엑손 범주를 포함하였다. 인간 BDNF를 위한 ABI 분석은 Applied Biosystems Taqman Gene Expression Assay이었다: Applied Biosystems Inc.(Foster City CA)에 의한 Hs00542425_s1(BDNF). 하기 PCR 사이클을 사용하였다: 2분 동안 50℃, 10분 동안 95℃, GeneAmp 7900 Machine(Applied Biosystems)을 사용하여 40 사이클(15초 동안 95℃, 1분 동안 60℃). 안티센스 올리고뉴클레오티드로 처리된 후 유전자 발현에서 배수 변화는 처리된 및 모의-형질감염된 샘플 사이의 18S-정규화된 dCt 값에서 차이를 기반으로 계산하였다.
7. BDNF-AS에 대한 올리고 검출:
ABI 분석 ID Hs00417345_m1
컨텍스트 서열(Context sequence) GCACACCTGGAGATACTCTATTATA(서열 번호 65)
8. BDNF에 대한 올리고 검출:
ABI 분석 ID Hs00542425_s1
CCTGCAGAATGGCCTGGAATTACAA(서열 번호 66)
BDNF-AS에 대한 올리고 검출: ABI 분석 ID Hs00417345_m1
컨텍스트 서열 GCACACCTGGAGATACTCTATTATA(서열 번호 65)
BDNF에 대한 올리고 검출: ABI 분석 ID Hs00542425_s1
CCTGCAGAATGGCCTGGAATTACAA(서열 번호 66)
9. 결과는 사이클 임계값(cycle threshold, Ct)을 기반으로 한다. ddCt로서 실험 및 참조 유전자(18S RNA)를 위한 Ct 값 사이의 계산된 차이를 각각의 RNA의 백분율로서 교정기 샘플에 그래프로 그린다.
결과: BDNF-AS 전사체의 비-중복 영역을 표적으로 하는 상이한 siRNA를 갖는 HEK293T 세포를 포함하는 몇몇 인간 및 마우스 세포주의 형질감염은 48시간에서 BDNF 전사체의 2 내지 6배 상향조절을 나타낸다(도 1a 및 도 6). BDNF의 상향조절은 내생성 대조군의 선택과 관련되지 않는다(도 5a-b). 상향조절은 다른 BDNF 이웃자리 유전자의 조절에 영향을 미치지 않는다(도 9).
도 5는 BDNF-AS 녹다운이 BDNF mRNA 상향조절을 야기함을 보여준다. BDNF-AS 전사체의 비-중복 영역을 표적으로 하는 siRNA-1(10nM)를 사용하는 BDNF-AS의 녹다운은 BDNF(센스) mRNA의 6배 상향조절을 야기하였다(**** = P < 0.0001). 본원에 기재된 결과는 내생성 대조군으로서 베타 액틴(좌측 패널) 또는 18S rRNA(우측 패널)를 사용하고 참조 샘플로서 모의 형질감염을 사용하여, HEK293T 세포에서 실험으로부터 수득되었다. 이러한 실험은 내생성 대조군 또는 참조 교정기 샘플의 선택이 BDNF mRNA의 관찰된 상향조절을 변경시키지 않음을 나타내는 것을 의도한다.
도 6은 Bdnf 발현의 전사후 조절을 나타낸다. 마우스 Bdnf-AS 전사체를 표적으로 하는 mBdnf-AntagoNAT9와 Drosha 단백질을 표적으로 하는 Drosha siRNA의 조합에 의해 형질감염된 N2a 세포는 마이크로RNA(miRNA) 과정에 관여된다. Bdnf mRNA 상향조절은 mBdnf-ANtagoNAT9에 의한 세포 처리 후 관찰되었다(*** = p 값 < 0.0001). Drosha siRNA의 첨가는 mBdnf-AntagoNAT9 처리에 비해 Bdnf 전사체를 증가시켰다(* = p 값 < 0.05). 이러한 실험은 다른 전사후 기전, 예를 들면, Bdnf 전사체의 조절에서 miRNA와 같은 다른 전사후 기전의 관여를 제시할 수 있다.
도 9는 BDNF-AS 녹다운이 양 방향 어느 쪽으로든 TrkB 또는 BDNF 이웃자리 유전자(Let7C 및 KIF18A)의 수준을 변경하지 않음을 나타낸다: LIN7C 및 KIF18A는 각각 BDNF의 3' 하류 및 5' 상류에 위치한 유전자이다. 신경영양성 티로신 키나아제, 수용체, 유형 2(TrkB)는 BDNF를 위한 막-결합된 수용체를 코딩하고, DNF로서 상이한 염색체(Chr-9) 상에 위치한다. 이들 유전자가 BDNF-AS 전사체의 소모에 따라 변경되었는지 여부가 결정되었다. HEK293T 세포는 대조군 siRNA 또는 BDNF-AS siRNA에 의해 형질감염되고, 몇몇 전사체 수준에 대해 측정되었다. 본원에서 다른 곳에서 지시된 바와 같이 BDNF-AS 전사체는 하향조절되고 BDNF mRNA는 상향조절되었음이 관찰되었다. BDNFAS의 녹다운은 TrkB 발현 또는 이웃자리 유전자 Let7C 및 KIF18A에 영향을 주지 않음이 확인되었다. 이들 데이타는 BDNF-AS 소모에 따라 BDNF 발현의 자위-특이적 변경이 존재함을 제시한다.
BDNF 및 BDNF-AS의 양을 정량하기 위한 0-96h의 시간 경로에서 하나의 siRNA에 의한 Hek293 세포 처리
하기 방법론은 siRNA에 의한 Hek293 세포 처리와 동일하지만, 이번에는 세포가 올리고 첨가 0 내지 96h 후에 수확되었다.
결과: BDNF 및 BDNF-AS 발현의 시간 경로는 BDNF-AS의 최적 하향조절과 동시에, 48h에서 siRNA로 인한 BDNF의 최적 상향조절을 나타낸다(도 1b).
BDNF 및 BDNF-AS의 양을 정량하기 위한 상이한 hBDNF-AntagoNAT에 의한 Hek293 세포 처리
하기 방법론은 siRNA에 의한 Hek293 세포 처리와 동일하지만, 이번에는 세포가 AntagoNAT로 처리되었다.
결과: BDNF-AS 전사체는 BDNF mRNA에 대한 완전한 상보성을 갖는 225개 뉴클레오티드 중복 영역을 함유한다. RNA-RNA 상호작용은 이의 안티센스 전사체에 의한 BDNF의 부조화 조절에 원인이 될 수 있다. BDNF mRNA에 대한 BDNF-AS의 조절 역할을 결정하기 위하여, LNA 및 2'OMe RNA 변형을 둘 다 함유하는 갭머(AntagoNAT)를 센스 및 안티센스 전사체 사이에 상호작용을 차단하는데 사용하였다. 중복 영역은 hBDNF-AatagoNAT을 타일링(tiling)함으로써 커버된다. hBDNF-AntagoNAT의 사용은 BDNF mRNA를 상향조절하는 것으로 확인되었다. BDNF-AS 전사체의 근소한 하향조절이 관찰되었고, 이는 차단 올리고를 함유하는 2'OMe-RNA에 있어서 예상되지 않았던 것이다. 16 hBDNF-AntagoNAT를 시험하였고, BDNF-AS 중복 영역의 전반(first half)의 차단이 BDNF mRNA의 상향조절에 더욱 큰 효과를 갖는 것으로 확인되었다. 특히, hBDNF-AntagoNAT1 및 hBDNFAntagoNAT4는 BDNF mRNA의 뚜렷한 상향조절을 유발하였다. 합성 siRNA와 달리, 안티센스 올리고뉴클레오티드는 단일 가닥이고, 길이가 더 짧을 수 있고; 따라서, 비특이적(표적을 벗어난) 결합 효과를 감소시킨다. 단일-가닥 잠금 핵산(LNA)-변형된 올리고뉴클레오티드가 변형되지 않은 siRNA와 비교하여, 생체내에서, 일반적으로 더 효과적이다(도 7).
BDNF 및 BDNF-AS의 양을 정량하기 위한 상이한 mBDNF-AntagoNAT에 의한 마우스 N2a 세포 처리
하기 방법론은 BDNF 및 BDNF-AS의 양을 정량하기 위한 상이한 hBDNF-AntagoNAT에 의한 Hek293 처리와 동일하지만, 이번에는 세포가 N2a 세포이다. 게다가, 하기 PCR 사이클이 사용되었다: 2분 동안 50℃, 10분 동안 95℃, GeneAmp 7900 Machine(Applied Biosystems)을 사용하는 50 사이클(15초 동안 95℃, 1분 동안 60℃).
결과 도 8은 N2a 세포에서, AntagoNAT에 의한 마우스 Bdnf-AS 전사체의 저해를 나타낸다: 인간 BDNF 센스 및 안티센스 전사체 사이에 중복 영역의 차단은 BDNF mRNA 수준을 상향조절한다. 그 다음, 유사한 조절 기전이 마우스 세포주에 존재하는지 여부가 결정되고, 마우스 Bdnf-AS 전사체를 표적으로 하는 11개의 mBdnf-AntagoNAT를 시험하였다. mBdnf-AntagoNAT는 포스포로티오에이트 골격 및 양 3' 및 5' 말단에 3개의 LNA-변형된 뉴클레오티드를 함유한다, 대조군 올리고뉴클레오티드는 유사한 골격 및 변형을 갖지만, 포유동물 게놈에서 어떠한 서열도 표적으로 하지 않는다. 2개의 mBdnf-AntagoNAT(mBdnf-AntagoNA3 및 mBdnf-AntagoNAT-9)는 N2a 세포에서 Bdnf mRNA 수준을 증가시킬 수 있었다. 요컨대, 단일-가닥 AntagoNAT(16-mer)에 의한 마우스 Bdnf-AS 전사체 차단은 마우스 N2a 세포에서 Bdnf mRNA 수준의 상향조절을 야기하였다. 이들 데이타는 Bdnf의 안티센스 전사체가 Bdnf mRNA에 억제 효과를 행사함을 제시한다.
BDNF 단백질을 정량하기 위한 상이한 siRNA에 의한 Hek293 세포 처리
하기 방법론은, siRNA 첨가 48h 후 수행되는 단계 5를 제외하고, BDNF mRNA의 양을 정량하기 위한 상이한 siRNA에 의한 Hek293 세포 처리와 동일하였다. 그 다음, 배지를 제거하고, 세포를 분쇄하고, 이들의 BDNF 단백질 수준을 ELISA(도 1c) 및 웨스턴 블롯(도 1d)으로 정량하였다.
웨스턴 블롯: HEK293T 세포를 10nM BDNF-AS, 또는 대조군 siRNA로 형질감염시켰다. 형질감염 48h 후, 350mM DTT를 함유하는 Laemmli 샘플 완충액(Biorad) 200㎕와 함께 세포를 분쇄하였다. 용해물 20㎕를 10% SDS PAGE 상에서 분리하고, 밤새 이를 니트로셀룰로스 막에 이동시켰다. 그 다음, MecP2(Abcam)를 위한 일차 항체, BDNF(Promega, catalog number G164B) 및 HRP에 접합된 이차 항체와 함께 막을 배양시켰다. HRP 기질 첨가 후, 화학발광 신호가 X선 필름에 의해 검출되었다. 하중 대조군으로서 β-액틴의 검출을 위해 동일한 막을 벗겨내고 재사용하였다.
ELISA: 세포를 20nM BDNF-AS siRNA 또는 대조군 siRNA로 형질감염시켰다. 세포 상청액을 ELISA 실험을 위해 수집하였다. 대안적으로, 프로테아제 억제제(BCA kit, Fisher)를 더한 단백질 추출 완충액에 삽입된 마우스 뇌 조직으로부터 총 단백질을 추출하고, 바이오럽터(bioruptor) 및 금속 비드로 균질화시켰다. 총 단백질을 BCA 단백질 분석 키트(Pierce catalog number 23227)를 사용하여 측정하고, 샘플 하중을 총 단백질 농도로 정규화시켰다. ELISA 키트는 Promega로부터 인간 BDNF(catalog number G7611) 또는 Millipore로부터의 마우스 Bdnf(catalog number CYT306)를 위하여 구입하였고, ELISA는 제조업체의 프로토콜에 따라 수행하였다. 평균 흡광도는 배경으로부터 450nm에서 3회 반복을 차감하였다.
BDNF mRNA를 정량하기 위한 상이한 농도의 mBDNF-AntagoNAT9에 의한 Hek293 세포(확실하지 않음) 처리
하기 방법론은 Opti-MEM 배지(Gibco cat# 31985-070)의 동일한 용적을 사용하는, BDNF mRNA의 양을 정량하기 위한 상이한 siRNA에 의한 Hek293 세포 처리에서와 같이 Lipofectamine 2000(Invitrogen cat# 11668019)의 동일한 비례하는 양을 사용하여, 모든 mBDNF-AntagoNAT9가 상이한 농도로 희석되는, 예를 들면, 11개의 상이한 최종 농도가 세포에 적용되는(300nM 내지 5pM 범위의 1:3 계열 희석) 단계 3을 제외하고, BDNF mRNA 양을 정량하기 위한 상이한 siRNA에 의한 Hek293 세포 처리와 동일하였다. 이는 실온에서 20분 동안 수행되었고, HepG2 세포가 있는 6개의 웰 플레이트의 하나의 웰에 적가로 적용되었다. 올리고뉴클레오티드 용액 대신에 물을 포함하는 유사한 혼합물을 모의-형질감염된 대조군으로 사용하였다.
결과: 본원에서 도 1e에 도시된 바와 같이, BDNF-AS가 mBDNF-AntagoNAT9에 의해 표적화될 때, BDNF의 용량-의존적 상향조절이 존재한다.
도 1은 센스 mRNA 및 단백질의 안티센스-매개된 조절을 도시한다. (A) BDNF-AS 전사체의 비-중복 영역을 표적으로 하는 3개의 특유한 siRNA(10nM)의 각각에 의한 HEK293T 세포(처리 당 n=12)에서 뇌 유래 신경영양 인자(BDNF) 천연 안티센스 전사체, BDNF-AS의 녹다운은 BDNF(센스) mRNA의 2 내지 6배 상향조절을 야기하였다(각각의 데이타 점/처리에 있어서 n=6, *** = P < 0.001, ** = P < 0.01). 인간 대뇌피질 뉴런(HCN: Human cortical neuron), 교아세포종(MK059) 세포, 마우스 N2a 세포 및 신경구를 사용하는 실험으로부터 유사한 결과 "데이타가 보이지 않음"이 수득되었다. 스크램블된 서열, 모의 형질감염 및 대조군 siRNA를 대조군으로서 사용하였다. 이러한 및 다른 실험을 위한 대조군 siRNA는 포유동물 게놈에서 어떠한 공지된 서열도 표적으로 하지 않는 비활성 siRNA(CCUCUCCACGCGCAGUACATT)이다. 모든 측정은 18S rRNA에 정규화되고, 네가티브 siRNA 대조군 샘플에 대해 각각의 mRNA의 백분율로서 그래프화된다.
(B) BDNF-AS 녹다운 후, BDNF 및 BDNF-AS 전사체에서 변화는 일정 시간의 기간 동안 평가되었다(각각의 데이타 점/처리에 있어서 n=6). 인간 BDNF-AS의 siRNA 녹다운은 6h에서 출발하고 72h에 계속되는 BDNF-AS의 효율적이고 일관된 하향조절을 야기하였다. BDNF mRNA 수준은 18h에서 상승하였고, 72h 이상 동안 높게 남아 있었고, 96h에서 전-처리 수준으로 역전되었다. 48h에서 피크가 일관되고 재생가능함을 주의한다. BDNF-AS 녹다운이 6h 후 시작됨에도 불구하고, BDNF의 상향조절은 18h 후-처리에서 시작되었다. BDNF-AS의 소모와 BDNF mRNA의 증가 사이에 이러한 시간 지연은 세포가 BDNF 상향조절 전 안티센스 전사체의 제거에 적합화된 시간이 필요함을 지시하는 현상의 순차적인 순서를 보여준다.
(C) BDNF-AS 전사체의 siRNA-매개된 녹다운은 ELISA에 의해 측정된 BDNF 단백질 수준에서 증가를 야기시켰다. 세포를 48시간 동안 BDNF-AS를 위한 10nM 2개의 활성 siRNA, 스크램블된 siRNA 또는 대조군 siRNA에 의해 형질감염시켰다. 상업적으로 사용가능한 키트를 사용하여, 이들 세포의 상청액을 농축시키고 ELISA로 BDNF 단백질에 대해 분석하였다. BDNF-AS 전사체를 표적으로 하는 siRNA에 따라 BDNF 단백질이 뚜렷하게 증가하였다(처리 당 n=6, *** = P < 0.0001, ** = P < 0.001).
(D) 웨스턴 블롯은, 대조군 비-표적 siRNA 전사체가 아닌, BDNF-AS siRNA1에 의한 비-단백질-코딩 BDNF-AS의 녹다운은 베타-액틴의 수준을 변화시키지 않고 BDNF 단백질 수준을 증가시켰음을 확인해주었다. 집합적으로, 이들 데이타는, BDNF-AS가 BDNF mRNA 및 단백질의 발현을 억제하는, 센스 및 안티센스 BDNF 전사체 사이의 부조화적 관계가 존재함을 제시한다. BDNF-AS 녹다운에 의한 이러한 네가티브 조절 효과의 제거는 BDNF mRNA 및 단백질 수준의 상향조절을 야기한다.
(E) Bdnf-AS 소모 후 Bdnf에서 용량-의존적 증가: 용량 반응 실험은 mBdnf-AntagoNAT9(데이타 점/처리 당 n=6)의 11개의 상이한 농도(300nM 내지 5pM 범위의 1:3 계열 희석)를 사용하여 수행하였고, 용량-의존적 증가는 6.6nM EC50와 함께 1 내지 300nM 농도에서 Bdnf mRNA 수준에서 관찰되었다.
siRNA에 의한 해마 신경구 처리
신경구에서 마우스 해마 신경 줄기 세포 해부: 신경 줄기 세포를 마우스 새끼, P0-P1의 해마로부터 분리하였다. 해마를 단일 세포로 기게적으로 분리하고, 짧은 스핀으로 수집하고, 글루타민, 항생제, B27 용액 및 둘 다 0.001mM 농도인 EGF 및 FGF를 함유하는 DMEM 및 F12의 혼합물에서 성장시켰다. 3 내지 4일 후, 떠오른 신경구들이 형성되었다. 100,000개의 세포를 폴리-L-리신(PLL)으로 피복된 24-웰 플레이트에 플레이팅하였다. PLL 상에 신경구 세포의 플레이팅은 분화 과정을 시작할 것이다. 플레이팅 후 3일에서, 성장 인자를 배지로부터 제거하고, 세포가 4일 더(플레이팅 후 7일) 성장하도록 하였다. 이때까지, 세포 배양은 성상세포, 뉴런, 올리고덴드로사이트 및 이를 성숙한 뇌 조직에 보다 유사하게 만드는 이들의 전구체로 이루어진 신경 세포 계통의 혼합을 가졌다. Bdnf 및 Bdnf-AS의 발현은 떠오른 신경구 뿐만 아니라 플레이팅-후 3 및 7일에 배양에서 측정하였다. 플레이팅-후 3 또는 7일에 Bdnf-AS 전사체를 표적으로 하는 50nM siRNA 또는 20nM 안티센스 올리고뉴클레오티드를 사용하여 녹다운 실험을 수행하였다. 신경 줄기 세포를 또한 총 용적 80㎕로 면역세포화학 챔버에서 접종한다(웰 당 18,000개 세포). 그 다음, 동일한 프로토콜을 사용하여 신경구를 형질감염시켜 뮤린 일차 세포에 대한 Bdnf-AS 녹다운의 기능적 효과를 평가하였다. 48h 내지 72h 후, 세포를 20분 동안 파라포름알데히드(4%)로 고정시키고, 1X PBS로 수 회 세척하였다. FBS로 차단 후, 신경구를 일차 항체(Monoclonal Rabbit β tubulin III, TUJ1)와 함께 1:2000 농도로 밤새 배양하였다. 고정된 세포를 이차 항체와 함께 배양하고, Alexafluor 568(goat anti-rabbit IgG, 2㎎/㎖, 1:5000 농도)로 라벨링하였다. 핵을 회흐스트(Hoechst) 염색제로 염색하였다. 면역형광 항원 검출 현미경으로 이미지를 수득하였다.
AntagoNAT에 의한 BDNF-AS의 표적화:
용어 AntagoNAT는 본원에서 (상이한 변형과 함께, 상보성 방법 참조) 센스-안티센스 상호작용을 저해하는 단일-가닥 올리고뉴클레오티드 분자를 기술하는데 사용된다. 단일-가닥 갭머는 2'O-메틸 RNA 및/또는 잠금 핵산(LNA) 변형을 갖는 길이가 14개 뉴클레오티드인 올리고뉴클레오티드로 설계되었다. 이러한 전략을 사용하여, 인간 BDNF-AS 및 BDNF 전사체 사이에 전체 중복 영역을 타일링하고, 가장 큰 반응을 생성하는, 중복 영역의 제1 부분을 표적으로 하는, BDNF mRNA. hBDNF-AntagoNAT1 및 hBDNF-AntagoNAT4의 상향조절을 가능하게 하는 몇몇 효과적인 AntagoNAT을 확인하였다. 데이타는 단일-가닥 AntagoNAT에 의한 BDNF 안티센스 RNA의 차단이 BDNF mRNA에서 증가를 야기하는데 충분함을 제시한다.
그 다음, 단일-가닥 갭머는 포스포로티오에이트 골격을 갖고, 마우스 Bdnf-AS에 상보성인, 길이가 16-뉴클레오티드인 LNA-변형된, 15 DNA 올리고뉴클레오티드(AntagoNAT)로 설계되었다. 2개의 AntagoNAT(mBdnf-AntagoNAT3 및 mBdnf-AntagoNAT9)는 마우스 N2a 세포에서 Bdnf mRNA 수준의 통계학적으로 유의미한 증가를 일관되게 보여주었다(도 7).
도 7은 hBDNFAntagoNAT에 의한 인간 BDNF-AS 전사체의 저해를 도시한다: BDNF-AS 전사체는 BDNF mRNA에 완전한 상보성을 갖는 225-뉴클레오티드 중복 영역을 함유한다. RNA-RNA 상호작용은 이의 안티센스 전사체에 의한 BDNF의 부조화 조절의 원인이 될 수 있다. BDNF mRNA 상에 BDNF-AS의 조절 역할을 결정하기 위하여, LNA 및 2'OMe RNA 변형 둘 다를 함유하는 갭머(AntagoNAT)를 이용하여 센스 및 안티센스 전사체 사이에 상호작용을 차단하였다. 중복 영역은 hBDNF-AatagoNAT의 타일링에 의해 커버되었다. hBDNF-AntagoNAT의 사용이 BDNF mRNA를 상향조절함이 확인되었다. BDNF-AS 전사체의 근소한 하향조절이 관찰되었고, 이는 차단 올리고를 함유하는 2'OMe-RNA에 있어서 예상되지 않은 것이었다. 16 hBDNF-AntagoNAT(하기 제공된 서열에 의해 각각 14-mers)를 시험하였고, BDNF-AS 중복 영역의 전반의 차단이 BDNF mRNA의 상향조절에 대해 보다 큰 효과를 갖는 것으로 확인되었다. 특히, hBDNF-AntagoNAT1 및 hBDNFAntagoNAT4는 BDNF mRNA의 뚜렷한 상향조절을 야기하였다. 합성 siRNA와 달리, 안티센스 올리고뉴클레오티드는 단일-가닥이고, 길이가 더 짧을 수 있고; 따라서, 비특이적(표적을 벗어난) 결합 효과를 감소시킨다. 단일-가닥 잠금 핵산(LNA)-변형된 올리고뉴클레오티드가 변형되지 않은 siRNA와 비교하여, 생체내에서, 일반적으로 더 효과적이다. Bdnf 상향조절은 뉴런 성장을 증가시킨다.
Bdnf 상향조절은 뉴런 성장을 증가시킨다:
뉴런 성장 및 성체 신경발생 16-17에 대한 Bdnf의 자극 효과를 지시하는 많은 이전 보고와 일치하게, Bdnf-AS 전사체의 녹다운으로 인한 내생성 Bdnf 수준에서 증가는 신경구에서 플레이팅-후 3 및 7일에 증가된 뉴런 세포수 및 신경돌기 성장 및 성숙을 야기함이 확인되었다(도 5a-d). 이들 데이타는 안티센스 RNA의 저해로 인한 내생성 Bdnf의 상향조절이 뉴런 전구 세포에서 뉴런 분화를 유도하고 초기 뉴런에서 성숙한 표현형을 야기할 수 있음을 제시한다.
결과: 도 2는 Bdnf 상향조절이 뉴런 성장을 증가시킴을 보여주었다. 플레이팅-후 3일에 대조군 siRNA(A) 또는 Bdnf-AS siRNA(B)으로 처리된 해마 신경구의 면역세포화학 이미지(A-B). 플레이팅-후 7일에 대조군 siRNA(C) 또는 Bdnf-AS siRNA(D)으로 처리된 해마 신경구에서 뉴런 성숙 및 신경돌기 성장의 면역세포화학 이미지(C-D). Bdnf-AS 전사체를 표적으로 하는 siRNA에 의한 세포 처리는 증가된 뉴런 세포수 뿐만 아니라 플레이팅 후 3일 또는 7일 둘 다에서 신경구에서 신경돌기 성장 및 성숙의 증가를 야기하였다. B-튜블린 III은 적색으로 염색되고, GFAP는 녹색으로 염색되고, DAPI는 청색으로 염색되었다.
삼투 미니펌프를 사용하는 mBDNF-AntagoNAT9의 측뇌실내(ICV: intracerebroventicular) 전달에 의한 BDNF-AS 녹다운 및 BDNF 상향조절
마우스 연구: 8주 연령의 숫컷 C57BL/6 마우스 10 마리를 생체내 실험에 사용하였다. 마우스는 4주 동안 1.5㎎/㎏/d 용량으로 Bdnf-AS에 직접 대항하는 합성 안티센스 올리고뉴클레오티드(mBdnf-AntagoNAT9) 또는 대조군 올리고뉴클레오티드(인간 또는 마우스에 존재하지 않는 비활성 서열)의 연속 주입(0.11 마이크로리터/h)이 전달되는 삼투 미니펌프와 함께, 경피적으로 이식된 등쪽 제3 뇌실에서 만성 유치 캐뉼라와 함께 준비되었다. 처리가 뇌 내로 직접적으로 전달되도록, 관은 삼투 미니펌프의 출구 포트에 연결되고 유치 캐뉼라에 피하적으로 관통된다. 이식-후 5일에, 모든 동물에게 연속 5일 동안 매일 BrdU(80㎎/㎏)의 복강내(IP: intra-peritoneal) 주사를 제공하였다. 수술-후 28일 째 되는 날에, 동물을 희생시키고, 정량적 RNA 측정을 위하여 각각의 마우스 뇌로부터 3개의 조직을 잘라냈다(해마, 전두 피질 및 소뇌).
Bdnf-AS의 녹다운은 생체내에서 Bdnf를 증가시킨다:
C57BL/6 마우스에 mBdnf-AntagoNAT9의 측뇌실내(ICV) 전달을 위하여 삼투 미니펌프를 이용하였다. 그 다음, mBdnf-AntagoNAT9를 선택하고, 이는 시험관내에서 Bdnf mRNA를 증가시키는 이의 높은 효능을 기반으로 하여, 다른 활성 AntagoNAT에 비해, 마우스 Bdnf-AS의 비-중복 영역을 표적으로 한다. 연속적인 AntagoNAT 주입 28일 후, Bdnf mRNA 수준은 비활성 대조군 올리고뉴클레오티드에 의해 변경되지 않은 수준과 비교하여, mBdnf-AntagoNAT9로 처리된 마우스에서 제3 뇌실에 인접한 전뇌 영역을 교차하여 증가되었다(도 3a, b). Bdnf 및 Bdnf-AS 전사체는 제3 뇌실에 바로 인접하지 않은 구조인 해마에서는 변경되지 않았다(도 3c). 게다가, Bdnf-AS의 AntagoNAT-매개된 봉쇄(blockade)는 증가된 Bdnf 단백질 수준을 야기함이 확인되었다(도 3d, e). 이들 발견은 상기 기술된 시험관내 데이타와 상응하고, Bdnf-AS의 봉쇄는 생체내에서 Bdnf mRNA 및 단백질 발현의 증가를 야기함을 지시한다.
마우스 뇌 샘플의 RNA 추출 및 RT-PCR: 마우스를 28일 후 안락사시키고, 뇌를 잘라냈다. 각각의 마우스로부터 하나의 반뇌(hemibrain)를 조직학적 연구를 위하여 밤새 4% 포름알데히드 중에서 고정시켰다. 또 다른 반뇌를 해마, 전두 피질 및 소뇌로부터의 RNA 정량 측정을 위하여 절개하였다. 제조업체의 프로토콜에 따라 Trizol 시약(Invitrogen, 15596-026) 중에서 균질화 후 RNA를 추출하였다. 수성 상을 분리하고, Qiagen RNeasy 컬럼(QIAGEN, 74106)을 통해 샘플을 통과시키기 전, 동일한 용적의 70% 에탄올을 가하고, DNA 오염을 제거하기 위하여 이들 RNA 샘플을 컬럼-상(on-column) DNAse로 처리하였다. 각각의 샘플 400ng을 제1 가닥 cDNA 합성에 사용하고, RT-PCR 측정을 수행하였다. 백분위 변화를 각각의 그래프에서 대조군 마우스와 비교하여 개별적인 조직에 대한 RNA 수준에서 플롯팅하였다.
결과: 도 3은 Bdnf-AS가 생체내에서 Bdnf mRNA 및 단백질을 조절함을 보여주고; (A-C) 삼투 미니펌프를 사용하여, mBdnf-AntagoNAT9(CAACATATCAGGAGCC) 또는 대조군 올리고뉴클레오티드(CCACGCGCAGTACATG)를 마우스 뇌의 제3 뇌실로 28일의 기간 동안 일정하게 주입하였다(처리 그룹 당 n = 5, * = P < 0.05, ** = P < 0.01, *** = P < 0.001). Bdnf-AS에 직접적으로 대항하는 mBdnf-AntagoNAT9는 해마(A) 및 전두 피질(B)에서 Bdnf 수준에서 증가를 야기하였지만, 대조군 올리고뉴클레오티드는 그렇지 않았다. 해마(C)에서, 두 전사체는 뇌의 제3 뇌실에 직접적으로 연결되지 않은 조직에서 예상된 바와 같이 둘 다 변경되었다. (D-E) BDNF 단백질 수준을 ELISA로 평가하였고, mBdnf-AntagoNAT9 처리는 대조군 올리고뉴클레오티드 처리된 마우스와 비교하여, 해마(D) 및 전두 피질(E) 둘 다에서, BDNF 단백질에서 증가를 야기하는 것으로 확인되었다.
삼투 미니펌프를 사용하는 mBDNF-AntagoNAT9의 측뇌실내(ICV) 전달, BDNF-AS 녹다운 및 BDNF 상향조절
BrdU를 5일 동안 연구의 제1 주에 mBdnf-AntagoNAT9로 처리된 마우스에 주사하였다. 연속 AntagoNAT 주입 28일 후, 뇌 조직의 조직학적 검사를 수행하고, 각각 Ki67 및 BrdU 마커를 사용하여 뉴런 증식 및 생존을 정량하였다. mBdnf-AntagoNAT9로 처리된 마우스에서, 대조군 마우스와 비교하여 Ki67 양성(증식)에서 증가가 관찰되었다(도 4a, b). Ki67 양성 세포의 수를 정량하였고, 세포 증식에서 뚜렷한 증가는 대조군 올리고뉴클레오티드와 비교하여 mBdnf-AntagoNAT9로 처리된 마우스에서 확인되었다(도 4c). mBdnf-AntagoNAT9로 처리된 마우스에서, 대조군 올리고뉴클레오티드-처리된 마우스와 비교하여 BrdU 혼입(생존 세포)에서 뚜렷한 증가가 존재하였다(도 4d). 대조군 및 mBdnf-AntagoNAT9 처리된 마우스 사이에서 해마 용적에는 차이가 존재하지 않았다(도 4e). 이들 발견은 생체내에서 Bdnf-AS가 Bdnf 수준을 조절함을 입증한다.
결과: 도 4는 생체내에서 Bdnf-AS의 차단이 뉴런의 생존 및 증식에서 증가를 야기함을 나타내고; (A-B) 마우스는 mBdnf-AntagoNAT9 또는 대조군 올리고로 처리하였다. 연속 mBdnf-AntagoNAT9 주입 28일 후, Ki67를 사용하여 뇌 조직의 조직학적 실험을 수행하였다. Ki67는 해마에서 증식 세포의 마커이고, 대조군 올리고를 제공받은 마우스와 비교하여 Bdnf-AntagoNAT 처리된 마우스에서 증식 세포 수의 증가가 관찰되었다. mBdnf-AntagoNAT9(B)로 처리된 마우스에서, 대조군 처리된 마우스와 비교하여 Ki67 양성 세포(증식 세포)에서 증가가 존재하였다(A). (C) mBdnf-AntagoNAT9로 처리된 마우스는 대조군 처리된 마우스와 비교하여 Ki67 양성 세포의 수에서 뚜렷한 증가를 가졌다. (D) mBdnf-AntagoNAT9 처리된 마우스에서, 대조군 올리고뉴클레오티드 처리된 마우스와 비교하여 생존 세포(BrdU 양성)의 수에서 뚜렷한 증가가 존재하였다. (E) 대조군 및 mBdnf-AntagoNAT9 처리된 마우스 사이에 해마 용적에는 차이가 존재하지 않았다. 함께 이들 데이타(처리 그룹 당 n=5, * = P < 0.05, *** = P < 0.001)는 Bdnf-AS가 생체내에서 Bdnf 수준을 조절하고, Bdnf 센스-안티센스 상호작용이 뉴런 계통, 증식 및 생존에서 증가를 야기함을 입증한다.
본 발명이 하나 이상의 실행에 관하여 예시되고 설명되었지만, 본 명세서 및 첨부된 도면을 읽고 이해하는 당업자에게 동등한 변경 및 변형이 발생할 것이다. 이에 더하여, 본 발명의 특정한 특징이 여러 실행 중에서 단지 하나에 관하여 개시되고 있긴 하지만, 이러한 특징은 임의의 주어진 또는 특정한 적용을 위하여 바람직하고 유리한 경우에, 다른 실행의 하나 이상의 다른 특징과 조합될 수 있다.
내용의 요약은 독자가 기술 내용의 성격을 신속하게 확인할 수 있도록 도와줄 것이다. 이는 아래의 특허청구범위의 범위 또는 의미를 해석하거나 제한하는데 이용되지 않는 것으로 이해되어야 한다.
SEQUENCE LISTING
<110> CURNA, INC.
<110> THE SCRIPPS RESEARCH INSTITUTE
<120> TREATMENT OF BRAIN DERIVED NEUROTROPHIC FACTOR (BDNF) RELATED
DISEASES BY INHIBITION OF NATURAL ANTISENSE TRANSCRIPT TO BDNF
<130> US61/614,664
<150> US61/614,664
<151> 2012-03-23
<160> 66
<170> PatentIn version 3.5
<210> 1
<211> 4755
<212> DNA
<213> Homo sapiens
<400> 1
cacacacaca cacacacaca gagagaacat ctctagtaaa aagaaaagtt gagctttctt 60
agctagatgt gtgtattagc cagaaaaagc caaggagtga agggttttag agaactggag 120
gagataaagt ggagtctgca tatgggaggc atttgaaatg gacttaaatg tctttttaat 180
gctgactttt tcagttttct ccttaccaga cacattgttt tcatgacatt agccccaggc 240
atagacacat cattaaaatg aacatgtcaa aaaatgattt ctgtttagaa ataagcaaaa 300
cattttcagt tgtgaccacc caggtgtaga ataaagaaca gtggaattgg gagccctgag 360
ttctaacata aactttcttc atgacataag gcaagtcttc tatggccttt ggtttcctta 420
cctgtaaaac aggatggctc aatgaaatta tctttcttct ttgctataat agagtatctc 480
tgtgggaaga ggaaaaaaaa agtcaattta aaggctcctt atagttcccc aactgctgtt 540
ttattgtgct attcatgcct agacatcaca tagctagaaa ggcccatcag acccctcagg 600
ccactgctgt tcctgtcaca cattcctgca aaggaccatg ttgctaactt gaaaaaaatt 660
actattaatt acacttgcag ttgttgctta gtaacattta tgattttgtg tttctcgtga 720
cagcatgagc agagatcatt aaaaattaaa cttacaaagc tgctaaagtg ggaagaagga 780
gaacttgaag ccacaatttt tgcacttgct tagaagccat ctaatctcag gttatatgct 840
agatcttggg ggcaaacact gcatgtctct ggtttatatt aaaccacata cagcacacta 900
ctgacactga tttgtgtctg gtgcagctgg agtttatcac caagacataa aaaaaccttg 960
accctgcaga atggcctgga attacaatca gatgggccac atggcatccc ggtgaaagaa 1020
agccctaacc agttttctgt cttgtttctg ctttctccct acagttccac caggtgagaa 1080
gagtgatgac catccttttc cttactatgg ttatttcata ctttggttgc atgaaggctg 1140
cccccatgaa agaagcaaac atccgaggac aaggtggctt ggcctaccca ggtgtgcgga 1200
cccatgggac tctggagagc gtgaatgggc ccaaggcagg ttcaagaggc ttgacatcat 1260
tggctgacac tttcgaacac gtgatagaag agctgttgga tgaggaccag aaagttcggc 1320
ccaatgaaga aaacaataag gacgcagact tgtacacgtc cagggtgatg ctcagtagtc 1380
aagtgccttt ggagcctcct cttctctttc tgctggagga atacaaaaat tacctagatg 1440
ctgcaaacat gtccatgagg gtccggcgcc actctgaccc tgcccgccga ggggagctga 1500
gcgtgtgtga cagtattagt gagtgggtaa cggcggcaga caaaaagact gcagtggaca 1560
tgtcgggcgg gacggtcaca gtccttgaaa aggtccctgt atcaaaaggc caactgaagc 1620
aatacttcta cgagaccaag tgcaatccca tgggttacac aaaagaaggc tgcaggggca 1680
tagacaaaag gcattggaac tcccagtgcc gaactaccca gtcgtacgtg cgggccctta 1740
ccatggatag caaaaagaga attggctggc gattcataag gatagacact tcttgtgtat 1800
gtacattgac cattaaaagg ggaagatagt ggatttatgt tgtatagatt agattatatt 1860
gagacaaaaa ttatctattt gtatatatac ataacagggt aaattattca gttaagaaaa 1920
aaataatttt atgaactgca tgtataaatg aagtttatac agtacagtgg ttctacaatc 1980
tatttattgg acatgtccat gaccagaagg gaaacagtca tttgcgcaca acttaaaaag 2040
tctgcattac attccttgat aatgttgtgg tttgttgccg ttgccaagaa ctgaaaacat 2100
aaaaagttaa aaaaaataat aaattgcatg ctgctttaat tgtgaattga taataaactg 2160
tcctctttca gaaaacagaa aaaaacacac acacacacaa caaaaatttg aaccaaaaca 2220
ttccgtttac attttagaca gtaagtatct tcgttcttgt tagtactata tctgttttac 2280
tgcttttaac ttctgatagc gttggaatta aaacaatgtc aaggtgctgt tgtcattgct 2340
ttactggctt aggggatggg ggatgggggg tatatttttg tttgttttgt gttttttttt 2400
cgtttgtttg ttttgttttt tagttcccac agggagtaga gatggggaaa gaattcctac 2460
aatatatatt ctggctgata aaagatacat ttgtatgttg tgaagatgtt tgcaatatcg 2520
atcagatgac tagaaagtga ataaaaatta aggcaactga acaaaaaaat gctcacactc 2580
cacatcccgt gatgcacctc ccaggccccg ctcattcttt gggcgttggt cagagtaagc 2640
tgcttttgac ggaaggacct atgtttgctc agaacacatt ctttcccccc ctccccctct 2700
ggtctcctct ttgttttgtt ttaaggaaga aaaatcagtt gcgcgttctg aaatatttta 2760
ccactgctgt gaacaagtga acacattgtg tcacatcatg acactcgtat aagcatggag 2820
aacagtgatt tttttttaga acagaaaaca acaaaaaata accccaaaat gaagattatt 2880
ttttatgagg agtgaacatt tgggtaaatc atggctaagc ttaaaaaaaa ctcatggtga 2940
ggcttaacaa tgtcttgtaa gcaaaaggta gagccctgta tcaacccaga aacacctaga 3000
tcagaacagg aatccacatt gccagtgaca tgagactgaa cagccaaatg gaggctatgt 3060
ggagttggca ttgcatttac cggcagtgcg ggaggaattt ctgagtggcc atcccaaggt 3120
ctaggtggag gtggggcatg gtatttgaga cattccaaaa cgaaggcctc tgaaggaccc 3180
ttcagaggtg gctctggaat gacatgtgtc aagctgcttg gacctcgtgc tttaagtgcc 3240
tacattatct aactgtgctc aagaggttct cgactggagg accacactca agccgactta 3300
tgcccaccat cccacctctg gataattttg cataaaattg gattagcctg gagcaggttg 3360
ggagccaaat gtggcatttg tgatcatgag attgatgcaa tgagatagaa gatgtttgct 3420
acctgaacac ttattgcttt gaaactagac ttgaggaaac cagggtttat cttttgagaa 3480
cttttggtaa gggaaaaggg aacaggaaaa gaaaccccaa actcaggccg aatgatcaag 3540
gggacccata ggaaatcttg tccagagaca agacttcggg aaggtgtctg gacattcaga 3600
acaccaagac ttgaaggtgc cttgctcaat ggaagaggcc aggacagagc tgacaaaatt 3660
ttgctcccca gtgaaggcca cagcaacctt ctgcccatcc tgtctgttca tggagagggt 3720
ccctgcctca cctctgccat tttgggttag gagaagtcaa gttgggagcc tgaaatagtg 3780
gttcttggaa aaatggatcc ccagtgaaaa ctagagctct aagcccattc agcccatttc 3840
acacctgaaa atgttagtga tcaccacttg gaccagcatc cttaagtatc agaaagcccc 3900
aagcaattgc tgcatcttag tagggtgagg gataagcaaa agaggatgtt caccataacc 3960
caggaatgaa gataccatca gcaaagaatt tcaatttgtt cagtctttca tttagagcta 4020
gtctttcaca gtaccatctg aatacctctt tgaaagaagg aagactttac gtagtgtaga 4080
tttgttttgt gttgtttgaa aatattatct ttgtaattat ttttaatatg taaggaatgc 4140
ttggaatatc tgctatatgt caactttatg cagcttcctt ttgagggaca aatttaaaac 4200
aaacaacccc ccatcacaaa cttaaaggat tgcaagggcc agatctgtta agtggtttca 4260
taggagacac atccagcaat tgtgtggtca gtggctcttt tacccaataa gatacatcac 4320
agtcacatgc ttgatggttt atgttgacct aagatttatt ttgttaaaat ctctctctgt 4380
tgtgttcgtt cttgttctgt tttgttttgt tttttaaagt cttgctgtgg tctctttgtg 4440
gcagaagtgt ttcatgcatg gcagcaggcc tgttgctttt ttatggcgat tcccattgaa 4500
aatgtaagta aatgtctgtg gccttgttct ctctatggta aagatattat tcaccatgta 4560
aaacaaaaaa caatatttat tgtattttag tatatttata taattatgtt attgaaaaaa 4620
attggcatta aaacttaacc gcatcagaac ctattgtaaa tacaagttct atttaagtgt 4680
actaattaac atataatata tgttttaaat atagaatttt taatgttttt aaatatattt 4740
tcaaagtaca taaaa 4755
<210> 2
<211> 4302
<212> DNA
<213> Mus musculus
<400> 2
taaagcagta gccggctggt gcagaaaagc aacaagttcc ccagcggtct tcccgcccta 60
gcttgacaag gcgaagggtt tcttacctgg cgacagggaa atctcctgag ccgagctcat 120
ctttgccaga gccccaggtg tgacctgagc agtgggcaaa ggatcggcgt gcaaattgga 180
ttatttttat gggggtactc tgaaactccc tcactttctc tgggaacttt ttgtgctagg 240
gctcagtgac aggcgttgag aaagctgctt caggaaacgc ccgctatata gcagggcaat 300
tggacagtca ttggtaacct cgctcattca ttagaatcac gtaagaactc aaagggaaac 360
gtgtctctca gaatgagggc gtttgcgtaa atctataggt ttttcaacat cgatgccagt 420
tgctttgtct tctgtagtcg ccaaggtgga tgagagttga agctttgcgg atattgcgaa 480
gggttattag attcataagt cacaccaagt ggtgggcgat ccactgagca aagccgaact 540
tctcacatga tgacttcaaa caagacacat taccttcctg catctgttgg ggagacaaga 600
ttttaagaca ctgagtctcc aggacagcaa agccacaatg ttccaccagg tgagaagagt 660
gatgaccatc cttttcctta ctatggttat ttcatacttc ggttgcatga aggcggcgcc 720
catgaaagaa gtaaacgtcc acggacaagg caacttggcc tacccaggtg tgcggaccca 780
tgggactctg gagagcgtga atgggcccag ggcaggttcg agaggtctga cgacgacatc 840
actggctgac acttttgagc acgtcatcga agagctgctg gatgaggacc agaaggttcg 900
gcccaacgaa gaaaaccata aggacgcgga cttgtacact tcccgggtga tgctcagcag 960
tcaagtgcct ttggagcctc ctctactctt tctgctggag gaatacaaaa attacctgga 1020
tgccgcaaac atgtctatga gggttcggcg ccactccgac cctgcccgcc gtggggagct 1080
gagcgtgtgt gacagtatta gcgagtgggt cacagcggca gataaaaaga ctgcagtgga 1140
catgtctggc gggacggtca cagtcctaga gaaagtcccg gtatccaaag gccaactgaa 1200
gcagtatttc tacgagacca agtgtaatcc catgggttac accaaggaag gctgcagggg 1260
catagacaaa aggcactgga actcgcaatg ccgaactacc caatcgtatg ttcgggccct 1320
tactatggat agcaaaaaga gaattggctg gcgattcata aggatagaca cttcctgtgt 1380
atgtacactg accattaaaa ggggaagata gtggatttat gttgtataga ttatattgag 1440
acaaaattat ctatttgtat atatacataa cagggtaaat tattcagtta agaaaaaata 1500
attttatgaa ctgcatgtat aaatgaagtt tatacagtac agtggttcta caatctattt 1560
attggacata tccatgacct gaaaggaaac agtcatttgc gcacaacttt aaaagtctgc 1620
attacattcc tcgataatgt tgtggtttgt tgccgttgcc aagaattgaa aacaaaaagt 1680
ttaaaaaaaa taataataaa ttgcatgctg ctttaattgt gaattgataa taaactgtcc 1740
ctctttcaga aaacagatta aaaaaacaaa aaacaaaaaa aaaaaaacaa aaaacaaaaa 1800
caaaaattgg aaccaaaaca ttccgtttac attttagaca ctaagtatct tcgttcttgt 1860
tagtactctg ttttactgct ttcgacttct gatagcgttg gaattaaaac aatgtcaagg 1920
tgctgttgtc attgctttac tggcgtaagg gacggggaat gggaggggta gatttctgtt 1980
tgttttgtgt tttattttgt ttgtttgttt gttttgtttt ttagttccac ccggagtagg 2040
gatggagaaa atttcttcac tatccattct ggttgataaa gcgttacatt tgtatgttgt 2100
aaagatgttt gcaaaatcca atcagatgac tggaaaacaa ataaaaatta aggcaactga 2160
ataaaatgct cacactccac tgcccatgat gtatctccct ggtccccctc agctcactct 2220
tctggcatgg gtcagggaaa attgctttta ttggaaagac cagcatttgt tcaaagcata 2280
ctctttccct ccctcctccc attttggtcc cttctttttg ttttgtttta agaaagaaaa 2340
ttaagttgcg cgctttaaaa tattttacta ctgctacaaa cagatgaaca atgtgtgtca 2400
ttttatgaca ctcatggaaa acagtgattt ttttttaccc taaagaaaaa caaataaaaa 2460
taacccaaaa tattcttttt ttaaaaggca taaatattgg gtaaattgta atatggccta 2520
acagtgtttg cagataaaag ttattgtata cacccagata cttagataag agcagggatc 2580
cacactgcca ttgaaatagg actgaatggc cctgcggagg ctaagtggag ctgacatact 2640
atttcctggc agtgcaggag gaatttctga gtggccatcc taaggtctag gatggaggtg 2700
gggaatggta cttgagacat tcctaaagga aggctcggaa gcacccttca gagcaggctc 2760
tggaatgatg tgtcaagttg cttaggcctt ctgctttaag tgcctacatt acctaacagt 2820
gctcaagagg ttctcgattg gagaaccaca ctcaaatcca tttatagcct ccatcccatt 2880
tctaaataat tgtgtataaa gttggattaa cctggagcaa ctttggatcc aaatatggca 2940
cagcaataat gatattaatg cagcatgatg ggaaatgttt gctgtgaaga gaattgattt 3000
gctttgagct tagacttcag gaagcctagg ttttttattt ttttattttt gagacatttt 3060
ggtaaaagga aaaaaagaaa acaaacaaac aaacaaacaa aaccagaaaa agcatcaaaa 3120
ctcaggcaga atgagcaatg tctgaaaggg ctagaaaaac aagacatagc aaggtgcttt 3180
cactgtgaaa gagacaagaa cacaggagga aatattgctt cagtgaagag cacagacggc 3240
tcctgccaat ttattacaag agtcccgtct gtactttacc ctttggggtt agaagtcaag 3300
ttggaagcct gaatgaatgg acccaatgag aactagtgtt aagcccattt ccctagtcag 3360
gtttttttca agcgtgaatg tgttagtggt tactctcctg ggttcctgag catcagaaaa 3420
aaaaaaaaaa agaggcaaac aatcgcttca tcttaggagt ggaaaggaaa cagaagtgga 3480
cgtccgctgt gactcaggga gtgaagatac catcagcaaa tagtttcttt tttgttcatt 3540
cgttcctttc gagttagcct gtcttttgga ataccactga atatgctgtt tttgaaagac 3600
ttcatgtagc atagattgtt ttgtgccgtt taccaaatta acctttgtca tcgtttttta 3660
acctattcag gaatgcttgg aatatctgct ctatgttaac tttttgcagc ttcattctga 3720
gagacattag tcaaacaaac aaaaggatcc ccatcacaat cttacagtac tgcaagggcc 3780
aggtctgtta atcggcttca caggagacat cagcaattgt gtggtcagtg gctggctctc 3840
ttacccacta agatacatca tagctacatg ttggtggttt atgttgacct gagatttatt 3900
tgttaaaatc tcttcttcgt ttctgttcgt tctggttctg ttctgttctg ttctgttctg 3960
ttttggtttt aaagtcttgc tgtggtctct tgttggcaga aatgttttat gcatggcagc 4020
aggcctgttg cttttttata gtgattccca ttgaaactgt aagtaaatgt ctgtggcctt 4080
gttctctcta tggtaaagat attattcacc atgtaaaaca agaaaaaata tttattgtat 4140
tttagtatat ttatataatt atgttattga aaaaattggc attaaaactt aaccacatca 4200
gaagcctatt gtaaatacag gttctattta agtgtaccaa ttaacatata atatatgttt 4260
taaatataga atttttaatg tttttaaata tattttcaaa gt 4302
<210> 3
<211> 1279
<212> DNA
<213> Homo sapiens
<400> 3
atcgcgagat caggaaggtg gccgagtgtg tcgccgcggc catcaggcac ttctccttcc 60
tgcccttgta tgaagaagga tgtgtttgct tccccttgtg ccatgattgt aaatttcctg 120
aggcctcctc agccctgcag aactggctag agcaatgtat cttaggctca cttaaggaag 180
ctgtagagat gagcccaagg agggaaacca gaagagcccc ccaggctcac cagttgtttg 240
ttggctccct acaaacatgt cattcaagtg gctaatctta caacagcaca aattcatcta 300
accagaaaga gaagaggagg ctccaaaggc acttgactac tgagcatcac cctggacgtg 360
tacaagtctg cgtccttatt gttttcttca ttgggccgaa ctttctggtc ctcatccaac 420
agctcttcta tcacgtgttc gaaagtgtca gccaatgatg tcaagcctct tgaacctgcc 480
ttgggcccat tcacgctctc cagagtccca tgggtccgca cacctggaga tactctatta 540
tagcaaagaa gaaagataat ttcattgagc catcctgttt tacaggattt tccctcctgg 600
tgagtcaaaa tgaacaagaa ataccccagg acctcccttc cctccttggc cattaatgag 660
atgaaggcaa ttaactcaca tagtataaat gaatcatttg aggtgatgac tgcattttag 720
gcaaatgatg actttcttgg ttccattggt ttgcaagtaa aagttacaca cattgaaaag 780
acactgaaac agatttccta aatgcttcat tttctggatg caccaatgtt gacctactat 840
acatgttaaa tggttttaaa atatcacctt aaaataaagg aaacttccag ctactaactc 900
agctctgaat gggctatgaa aggctccaaa ggtatgtgaa aaattactgt tattttgctt 960
taaaaaatgt gatgtctaag agtgtctgca atgttctaat gcttcaaaac atgtacgtaa 1020
gccttgttta tctggaaatc atttctttct gcttatatca tttataaata gaaaatgttc 1080
tgtaataact taaaatagtt ccacatacat aatgctttta gtgtcataat acttactact 1140
ggtctatatt taccaacatt tatcacattt tacaaaatga agtagaagaa aaaaaagaca 1200
acgactttat ggccctggaa ttccagtaat ggtgaccaac atgttttaaa ttccagtaaa 1260
ggttatggtt acatttcaa 1279
<210> 4
<211> 1478
<212> DNA
<213> Homo sapiens
<400> 4
atcgcgagat caggaaggtg gccgagtgtg tcgccgcggc catcaggcac ttctccttcc 60
tgcccttgta tgaagaagga tgtgtttgct tccccttgtg ccatgattgt aaatttcctg 120
aggcctcctc agccctgcag aactggggtt atagccatgt gactgatctt cgtccaagaa 180
tatgtaaaga aaaagtgttg agttggcttt tagggctaga gcaatgtatc ttaggctcac 240
ttaaggaagc tgtagagatg agcccaagga gggaaaccag aagagccccc caggctcacc 300
agttgtttgt tggctcccta caaacatgtc attcaagtgg ctaatcttac aacagcacaa 360
attcatctaa ccagaaagag aagaggaggc tccaaaggca cttgactact gagcatcacc 420
ctggacgtgt acaagtctgc gtccttattg ttttcttcat tgggccgaac tttctggtcc 480
tcatccaaca gctcttctat cacgtgttcg aaagtgtcag ccaatgatgt caagcctctt 540
gaacctgcct tgggcccatt cacgctctcc agagtcccat gggtccgcac acctggagat 600
actctattat agcaaagaag aaagataatt tcattgagcc atcctgtttt acaggaaatt 660
ctgcaagtgg caacgtgggt ccattccgtg tgtgtcacta gagctggcgc aagcccatgg 720
ccatggtgag gcagcgtttc cactggaact aatctgatac ctgcaccagc tcttgcaact 780
gtgcagtgtt cccactgcaa actacggatg gggtaaaaga ctgctcacct cctatttctc 840
atctaatctc acacactctg tttgatgagg ctatggagaa acaggtcttc tcatacacta 900
aaggtgggag tacaaacaat tcaagccctg tgcaggacaa ttaggcaata cctatcaaaa 960
ttatacatga tttttcctgc tgacccagca attccacttc tgggaataat tgacagatat 1020
aggtgcatat gtacaaaatg atggaaagct ctctggtata tattagtaag tgataaaaca 1080
aggtgtaaaa tagtgtatat atggctacta ccttttgttt taaaaatggg ggaaaatggt 1140
ggagcttgcg gtgagccgag atcgtgccac tgcactccag cctgggcgac agagcgagac 1200
tccgtctcaa aaaaaaaaca gggtggggtg ggggggaaat aatagtacat actcatattt 1260
acctgtatct atataaaaca cactatcaag gattcacaag aaactaatac aaatgatcac 1320
cttatagatg gtatgtattg ggggatactg aggtgagcag ggtataagtg gggcaagact 1380
tttcagtgta aacttctttt aaattttatt ttgatttttg aataatgtaa attaactgtc 1440
aaataattaa attaaaaata accaatttat taacaaaa 1478
<210> 5
<211> 1437
<212> DNA
<213> Homo sapiens
<400> 5
atcgcgagat caggaaggtg gccgagtgtg tcgccgcggc catcaggcac ttctccttcc 60
tgcccttgta tgaagaagga tgtgtttgct tccccttgtg ccatgattgt aaatttcctg 120
aggcctcctc agccctgcag aactggctag agcaatgtat cttaggctca cttaaggaag 180
ctgtagagat gagcccaagg agggaaacca gaagagcccc ccaggctcac cagttgtttg 240
ttggctccct acaaacatgt cattcaagtg gctaatctta caacagcaca aattcatcta 300
accagaaaga gaagaggagg ctccaaaggc acttgactac tgagcatcac cctggacgtg 360
tacaagtctg cgtccttatt gttttcttca ttgggccgaa ctttctggtc ctcatccaac 420
agctcttcta tcacgtgttc gaaagtgtca gccaatgatg tcaagcctct tgaacctgcc 480
ttgggcccat tcacgctctc cagagtccca tgggtccgca cacctggaga tactctatta 540
tagcaaagaa gaaagataat ttcattgagc catcctgttt tacaggaaat tctgcaagtg 600
gcaacgtggg tccattccgt gtgtgtcact agagctggcg caagcccatg gccatggtga 660
ggcagcgttt ccactggaac taatctgata cctgcaccag ctcttgcaac tgtgcagtgt 720
tcccactgca aactacggat ggggattttc cctcctggtg agtcaaaatg aacaagaaat 780
accccaggac ctcccttccc tccttggcca ttaatgagat gaaggcaatt aactcacata 840
gtataaatga atcatttgag gtgatgactg cattttaggc aaatgatgac tttcttggtt 900
ccattggttt gcaagtaaaa gttacacaca ttgaaaagac actgaaacag atttcctaaa 960
tgcttcattt tctggatgca ccaatgttga cctactatac atgttaaatg gttttaaaat 1020
atcaccttaa aataaaggaa acttccagct actaactcag ctctgaatgg gctatgaaag 1080
gctccaaagg tatgtgaaaa attactgtta ttttgcttta aaaaatgtga tgtctaagag 1140
tgtctgcaat gttctaatgc ttcaaaacat gtacgtaagc cttgtttatc tggaaatcat 1200
ttctttctgc ttatatcatt tataaataga aaatgttctg taataactta aaatagttcc 1260
acatacataa tgcttttagt gtcataatac ttactactgg tctatattta ccaacattta 1320
tcacatttta caaaatgaag tagaagaaaa aaaagacaac gactttatgg ccctggaatt 1380
ccagtaatgg tgaccaacat gttttaaatt ccagtaaagg ttatggttac atttcaa 1437
<210> 6
<211> 2322
<212> DNA
<213> Homo sapiens
<400> 6
atcgcgagat caggaaggtg gccgagtgtg tcgccgcggc catcaggcac ttctccttcc 60
tgcccttgta tgaagaagga tgtgtttgct tccccttgtg ccatgattgt aaatttcctg 120
aggcctcctc agccctgcag aactggggtt atagccatgt gactgatctt cgtccaagaa 180
tatgtaaaga aaaagtgttg agttggcttt tagggctaga gcaatgtatc ttaggctcac 240
ttaaggaagc tgtagagatg agcccaagga gggaaaccag aagagccccc caggctcacc 300
agttgtttgt tggctcccta caaacatgtc attcaagtgg ctaatcttac aacagcacaa 360
attcatctaa ccagaaagag aagaggaggc tccaaaggca cttgactact gagcatcacc 420
ctggacgtgt acaagtctgc gtccttattg ttttcttcat tgggccgaac tttctggtcc 480
tcatccaaca gctcttctat cacgtgttcg aaagtgtcag ccaatgatgt caagcctctt 540
gaacctgcct tgggcccatt cacgctctcc agagtcccat gggtccgcac acctggagat 600
actctattat agcaaagaag aaagataatt tcattgagcc atcctgtttt acagtattga 660
attattacca caaggtacca accatatatg catacttaat agggtatttt gtcaaaacta 720
tgcatgaagg tcatttgttt gagatgtcag aacattttcc cgtgagaaga tctcattggg 780
cattgaaaca gaaccacatg ctcttcagac cagcaaccgc gactaccaaa tactcctctg 840
tcaactctac ttgagtaaga acgctttcaa ttaaggccta agtgtcaaca tgcctttaaa 900
aaaaatcgtg gtgacacaaa atctttcttt ttagcaccca acagaatccc ttcaaagcct 960
cgtggtctga caccctatgc tacgtgactt gtgacccatc catttgtcat gttcttcggg 1020
aatgtggcta aggggctaag atgtgacttg aaaagaaagg tagaacaaga tcatctcaaa 1080
tttattatca aggaatagtt cagaaaacga cttcagacca cagagacagc agaacagatg 1140
gtccggcatg gatagagcat cagacactca cagactgtgc caacaagagc catcgagtca 1200
aaacagccaa aggaaggagg gtcatggaat gggttctctc acaccaaact gatgcccaga 1260
ggccctcagc atgaataaca aaggcaacca gacccacaag ccatactgag tggatacaaa 1320
acctatacct aggctgacat cccaaatgtg tgtggcaagt tagatgatga tggcacaaaa 1380
gacagaacac cttgcttctg gccattgtca gctcttggaa gagagcacac ttttagagga 1440
gcagctgcaa ggagcctgag aacaaaactg gaaatgtctg ttatgaaagc cttcacagga 1500
aattctgcaa gtggcaacgt gggtccattc cgtgtgtgtc actagagctg gcgcaagccc 1560
atggccatgg tgaggcagcg tttccactgg aactaatctg atacctgcac cagctcttgc 1620
aactgtgcag tgttcccact gcaaactacg gatggggtaa aagactgctc acctcctatt 1680
tctcatctaa tctcacacac tctgtttgat gaggctatgg agaaacaggt cttctcatac 1740
actaaaggtg ggagtacaaa caattcaagc cctgtgcagg acaattaggc aatacctatc 1800
aaaattatac atgatttttc ctgctgaccc agcaattcca cttctgggaa taattgacag 1860
atataggtgc atatgtacaa aatgatggaa agctctctgg tatatattag taagtgataa 1920
aacaaggtgt aaaatagtgt atatatggct actacctttt gttttaaaaa tgggggaaaa 1980
tggtggagct tgcggtgagc cgagatcgtg ccactgcact ccagcctggg cgacagagcg 2040
agactccgtc tcaaaaaaaa aacagggtgg ggtggggggg aaataatagt acatactcat 2100
atttacctgt atctatataa aacacactat caaggattca caagaaacta atacaaatga 2160
tcaccttata gatggtatgt attgggggat actgaggtga gcagggtata agtggggcaa 2220
gacttttcag tgtaaacttc ttttaaattt tattttgatt tttgaataat gtaaattaac 2280
tgtcaaataa ttaaattaaa aataaccaat ttattaacaa aa 2322
<210> 7
<211> 2036
<212> DNA
<213> Homo sapiens
<400> 7
atcgcgagat caggaaggtg gccgagtgtg tcgccgcggc catcaggcac ttctccttcc 60
tgcccttgta tgaagaagga tgtgtttgct tccccttgtg ccatgattgt aaatttcctg 120
aggcctcctc agccctgcag aactggctag agcaatgtat cttaggctca cttaaggaag 180
ctgtagagat gagcccaagg agggaaacca gaagagcccc ccaggctcac cagttgtttg 240
ttggctccct acaaacatgt cattcaagtg gctaatctta caacagcaca aattcatcta 300
accagaaaga gaagaggagg ctccaaaggc acttgactac tgagcatcac cctggacgtg 360
tacaagtctg cgtccttatt gttttcttca ttgggccgaa ctttctggtc ctcatccaac 420
agctcttcta tcacgtgttc gaaagtgtca gccaatgatg tcaagcctct tgaacctgcc 480
ttgggcccat tcacgctctc cagagtccca tgggtccgca cacctggaga tactctatta 540
tagcaaagaa gaaagataat ttcattgagc catcctgttt tacagcaccc aacagaatcc 600
cttcaaagcc tcgtggtctg acaccctatg ctacgtgact tgtgacccat ccatttgtca 660
tgttcttcgg gaatgtggct aaggggctaa gatgtgactt gaaaagaaag gtagaacaag 720
atcatctcaa atttattatc aaggaatagt tcagaaaacg acttcagacc acagagacag 780
cagaacagat ggtccggcat ggatagagca tcagacactc acagactgtg ccaacaagag 840
ccatcgagtc aaaacagcca aaggaaggag ggtcatggaa tgggttctct cacaccaaac 900
tgatgcccag aggccctcag catgaataac aaaggcaacc agacccacaa gccatactga 960
gtggatacaa aacctatacc taggctgaca tcccaaatgt gtgtggcaag ttagatgatg 1020
atggcacaaa agacagaaca ccttgcttct ggccattgtc agctcttgga agagagcaca 1080
cttttagagg agcagctgca aggagcctga gaacaaaact ggaaatgtct gttatgaaag 1140
ccttcacagg aaattctgca agtggcaacg tgggtccatt ccgtgtgtgt cactagagct 1200
ggcgcaagcc catggccatg gtgaggcagc gtttccactg gaactaatct gatacctgca 1260
ccagctcttg caactgtgca gtgttcccac tgcaaactac ggatgggaga ggataaagaa 1320
cttcaatctt taaaaaagag aggattttcc ctcctggtga gtcaaaatga acaagaaata 1380
ccccaggacc tcccttccct ccttggccat taatgagatg aaggcaatta actcacatag 1440
tataaatgaa tcatttgagg tgatgactgc attttaggca aatgatgact ttcttggttc 1500
cattggtttg caagtaaaag ttacacacat tgaaaagaca ctgaaacaga tttcctaaat 1560
gcttcatttt ctggatgcac caatgttgac ctactataca tgttaaatgg ttttaaaata 1620
tcaccttaaa ataaaggaaa cttccagcta ctaactcagc tctgaatggg ctatgaaagg 1680
ctccaaaggt atgtgaaaaa ttactgttat tttgctttaa aaaatgtgat gtctaagagt 1740
gtctgcaatg ttctaatgct tcaaaacatg tacgtaagcc ttgtttatct ggaaatcatt 1800
tctttctgct tatatcattt ataaatagaa aatgttctgt aataacttaa aatagttcca 1860
catacataat gcttttagtg tcataatact tactactggt ctatatttac caacatttat 1920
cacattttac aaaatgaagt agaagaaaaa aaagacaacg actttatggc cctggaattc 1980
cagtaatggt gaccaacatg ttttaaattc cagtaaaggt tatggttaca tttcaa 2036
<210> 8
<211> 2364
<212> DNA
<213> Homo sapiens
<400> 8
gtcatcgctg tctggaacag cgatgactcg atcgcgagat caggaaggtg gccgagtgtg 60
tcgccgcggc catcaggcac ttctccttcc tgcccttgta tgaagaagga tgtgtttgct 120
tccccttgtg ccatgattgt aaatttcctg aggcctcctc agccctgcag aactggggtt 180
atagccatgt gactgatctt cgtccaagaa tatgtaaaga aaaagtgttg agttggcttt 240
tagggctaga gcaatgtatc ttaggctcac ttaaggaagc tgtagagatg agcccaagga 300
gggaaaccag aagagccccc caggctcacc agttgtttgt tggctcccta caaacatgtc 360
attcaagtgg ctaatcttac aacagcacaa attcatctaa ccagaaagag aagaggaggc 420
tccaaaggca cttgactact gagcatcacc ctggacgtgt acaagtctgc gtccttattg 480
ttttcttcat tgggccgaac tttctggtcc tcatccaaca gctcttctat cacgtgttcg 540
aaagtgtcag ccaatgatgt caagcctctt gaacctgcct tgggcccatt cacgctctcc 600
agagtcccat gggtccgcac acctggagat actctattat agcaaagaag aaagataatt 660
tcattgagcc atcctgtttt acagtattga attattacca caaggtacca accatatatg 720
catacttaat agggtatttt gtcaaaacta tgcatgaagg tcatttgttt gagatgtcag 780
aacattttcc cgtgagaaga tctcattggg cattgaaaca gaaccacatg ctcttcagac 840
cagcaaccgc gactaccaaa tactcctctg tcaactctac ttgagtaaga acgctttcaa 900
ttaaggccta agtgtcaaca tgcctttaaa aaaaatcgtg gtgacacaaa atctttcttt 960
ttagcaccca acagaatccc ttcaaagcct cgtggtctga caccctatgc tacgtgactt 1020
gtgacccatc catttgtcat gttcttcggg aatgtggcta aggggctaag atgtgacttg 1080
aaaagaaagg tagaacaaga tcatctcaaa tttattatca aggaatagtt cagaaaacga 1140
cttcagacca cagagacagc agaacagatg gtccggcatg gatagagcat cagacactca 1200
cagactgtgc caacaagagc catcgagtca aaacagccaa aggaaggagg gtcatggaat 1260
gggttctctc acaccaaact gatgcccaga ggccctcagc atgaataaca aaggcaacca 1320
gacccacaag ccatactgag tggatacaaa acctatacct aggctgacat cccaaatgtg 1380
tgtggcaagt tagatgatga tggcacaaaa gacagaacac cttgcttctg gccattgtca 1440
gctcttggaa gagagcacac ttttagagga gcagctgcaa ggagcctgag aacaaaactg 1500
gaaatgtctg ttatgaaagc cttcacagga aattctgcaa gtggcaacgt gggtccattc 1560
cgtgtgtgtc actagagctg gcgcaagccc atggccatgg tgaggcagcg tttccactgg 1620
aactaatctg atacctgcac cagctcttgc aactgtgcag tgttcccact gcaaactacg 1680
gatggggtaa aagactgctc acctcctatt tctcatctaa tctcacacac tctgtttgat 1740
gaggctatgg agaaacaggt cttctcatac actaaaggtg ggagtacaaa caattcaagc 1800
cctgtgcagg acaattaggc aatacctatc aaaattatac atgatttttc ctgctgaccc 1860
agcaattcca cttctgggaa taattgacag atataggtgc atatgtacaa aatgatggaa 1920
agctctctgg tatatattag taagtgataa aacaaggtgt aaaatagtgt atatatggct 1980
actacctttt gttttaaaaa tgggggaaaa tggtggagct tgcggtgagc cgagatcgtg 2040
ccactgcact ccagcctggg cgacagagcg agactccgtc tcaaaaaaaa aacagggtgg 2100
ggtggggggg aaataatagt acatactcat atttacctgt atctatataa aacacactat 2160
caaggattca caagaaacta atacaaatga tcaccttata gatggtatgt attgggggat 2220
actgaggtga gcagggtata agtggggcaa gacttttcag tgtaaacttc ttttaaattt 2280
tattttgatt tttgaataat gtaaattaac tgtcaaataa ttaaattaaa aataaccaat 2340
ttattaacaa aaaaaaaaaa aaaa 2364
<210> 9
<211> 3136
<212> DNA
<213> Homo sapiens
<400> 9
ctgcataaag atttcttcac agggtccttt aaaactgtct atttctaaga ggtcccttcc 60
actacaggta aaaggaaatt ccctctaccc tagggcccct caggatccct tcctctctca 120
cacgtttctt cgactgctcc tgatttaagc attcagctgg ccacgcaacg caagaagcaa 180
taagaacaca aaaaccctac cctgttcctc ctctatccgt ggcctttgcc accacctcca 240
caacctagtt cagattcctc ttcttttctc aagggaacgt ctaaagctct caagtccgtt 300
ttggcagggc gattttgtaa gtctgaaaca tttcagtgtg tctctcgatc tcaggcagct 360
caaaagaaaa gatctgctgg ctgcgtgaag gtgcattaga aacctgctgc taccttgcag 420
cctgggctga gcatatgctc cggaacttgc ttctcttcca acatcctgca cctcagggtt 480
gcacgctctg gttcccaaac ccccggccgc tggcttatgc aaatcactta ggtacatgca 540
aaagtatccc ttctcccgga gcgccattgg cccggggagg tctcgagctc attactatgc 600
agagaggaga gccgccattg gccaagagga ggaccagagg ggcgtgtttc tcgggcaaat 660
tggatctcct aaattggatg acctgggctg aaagacaact taaagacccc cagaaaactc 720
tggttttata gataagaaat ctgaggctcg agagagagtg tgttctgccc aacatcatca 780
cggaacagct cctgggctcc tggctcctaa tctgatcgcg agatcaggaa ggtggccgag 840
tgtgtcgccg cggccatcag gcacttctcc ttcctgccct tgtatgaaga aggatgtgtt 900
tgcttcccct tgtgccatga ttgtaaattt cctgaggcct cctcagccct gcagaactgg 960
ggttatagcc atgtgactga tcttcgtcca agaatatgta aagaaaaagt gttgagttgg 1020
cttttagggc tagagcaatg tatcttaggc tcacttaagg aagctgtaga gatgagccca 1080
aggagggaaa ccagaagagc cccccaggct caccagttgt ttgttggctc cctacaaaca 1140
tgtcattcaa gtggctaatc ttacaacagc acaaattcat ctaaccagaa agagaagagg 1200
aggctccaaa ggcacttgac tactgagcat caccctggac gtgtacaagt ctgcgtcctt 1260
attgttttct tcattgggcc gaactttctg gtcctcatcc aacagctctt ctatcacgtg 1320
ttcgaaagtg tcagccaatg atgtcaagcc tcttgaacct gccttgggcc cattcacgct 1380
ctccagagtc ccatgggtcc gcacacctgg agatactcta ttatagcaaa gaagaaagat 1440
aatttcattg agccatcctg ttttacagta ttgaattatt accacaaggt accaaccata 1500
tatgcatact taatagggta ttttgtcaaa actatgcatg aaggtcattt gtttgagatg 1560
tcagaacatt ttcccgtgag aagatctcat tgggcattga aacagaacca catgctcttc 1620
agaccagcaa ccgcgactac caaatactcc tctgtcaact ctacttgagt aagaacgctt 1680
tcaattaagg cctaagtgtc aacatgcctt taaaaaaaat cgtggtgaca caaaatcttt 1740
ctttttagca cccaacagaa tcccttcaaa gcctcgtggt ctgacaccct atgctacgtg 1800
acttgtgacc catccatttg tcatgttctt cgggaatgtg gctaaggggc taagatgtga 1860
cttgaaaaga aaggtagaac aagatcatct caaatttatt atcaaggaat agttcagaaa 1920
acgacttcag accacagaga cagcagaaca gatggtccgg catggataga gcatcagaca 1980
ctcacagact gtgccaacaa gagccatcga gtcaaaacag ccaaaggaag gagggtcatg 2040
gaatgggttc tctcacacca aactgatgcc cagaggccct cagcatgaat aacaaaggca 2100
accagaccca caagccatac tgagtggata caaaacctat acctaggctg acatcccaaa 2160
tgtgtgtggc aagttagatg atgatggcac aaaagacaga acaccttgct tctggccatt 2220
gtcagctctt ggaagagagc acacttttag aggagcagct gcaaggagcc tgagaacaaa 2280
actggaaatg tctgttatga aagccttcac aggaaattct gcaagtggca acgtgggtcc 2340
attccgtgtg tgtcactaga gctggcgcaa gcccatggcc atggtgaggc agcgtttcca 2400
ctggaactaa tctgatacct gcaccagctc ttgcaactgt gcagtgttcc cactgcaaac 2460
tacggatggg gtaaaagact gctcacctcc tatttctcat ctaatctcac acactctgtt 2520
tgatgaggct atggagaaac aggtcttctc atacactaaa ggtgggagta caaacaattc 2580
aagccctgtg caggacaatt aggcaatacc tatcaaaatt atacatgatt tttcctgctg 2640
acccagcaat tccacttctg ggaataattg acagatatag gtgcatatgt acaaaatgat 2700
ggaaagctct ctggtatata ttagtaagtg ataaaacaag gtgtaaaata gtgtatatat 2760
ggctactacc ttttgtttta aaaatggggg aaaatggtgg agcttgcggt gagccgagat 2820
cgtgccactg cactccagcc tgggcgacag agcgagactc cgtctcaaaa aaaaaacagg 2880
gtggggtggg ggggaaataa tagtacatac tcatatttac ctgtatctat ataaaacaca 2940
ctatcaagga ttcacaagaa actaatacaa atgatcacct tatagatggt atgtattggg 3000
ggatactgag gtgagcaggg tataagtggg gcaagacttt tcagtgtaaa cttcttttaa 3060
attttatttt gatttttgaa taatgtaaat taactgtcaa ataattaaat taaaaataac 3120
caatttatta acaaaa 3136
<210> 10
<211> 906
<212> DNA
<213> Mus musculus
<400> 10
cgctgtctca atataatcta tacaacataa atccactatc ttcccctttt aatggtcagt 60
gtacatacac aggaagtgtc tatccttatg aatcgccagc caattctctt tttgctatcc 120
atagtaaggg cccgaacata cgattgggta gttcggcatt gcgagttcca gtgccttttg 180
tctatgcccc tgcagccttc cttggtgtaa cccatgggat tacacttggt ctcgtagaaa 240
tactgcttca gttggccttt ggataccggg actttctcta ggactgtgac cgtcccgcca 300
gacatgtcca ctgcagtctt tttatctgcc gctgtgaccc actcgctaat actgtcacac 360
acgctcagct ccccacggcg ggcagggtcg gagtggcgcc gaaccctcat agacatgttt 420
gcggcatcca ggtaattttt gtattcctcc agcagaaaga gtagaggagg ctccaaaggc 480
acttgactgc tgagcatcac ccgggaagtg tacaagtccg cgtccttatg gttttcttcg 540
ttgggccgaa ccttctggtc ctcatccagc agctcttcga tgacgtgctc aaaagtgtca 600
gccagtgatg tcgtcgtcag acctctcgaa cctgccctgg gcccattcac gctctccaga 660
gtcccatggg tccgcacacc tgggtaggcc aagttgcctt gtccgtggac gtttacttct 720
ttcatgggcg ccgccttcat gcaaccgaag tatgaaataa ccatagtaag gaaaaggatg 780
gtcatcactc ttctcacctg gtggaactgt gggaaggaag cagagacaga cacagaacag 840
gttagaactt ctttctcggg gacagcatgt ggcccatctg cttcaataat ttaatttaaa 900
aaaaaa 906
<210> 11
<211> 992
<212> DNA
<213> Mus musculus
<400> 11
cgctgtctca atataatcta tacaacataa atccactatc ttcccctttt aatggtcagt 60
gtacatacac aggaagtgtc tatccttatg aatcgccagc caattctctt tttgctatcc 120
atagtaaggg cccgaacata cgattgggta gttcggcatt gcgagttcca gtgccttttg 180
tctatgcccc tgcagccttc cttggtgtaa cccatgggat tacacttggt ctcgtagaaa 240
tactgcttca gttggccttt ggataccggg actttctcta ggactgtgac cgtcccgcca 300
gacatgtcca ctgcagtctt tttatctgcc gctgtgaccc actcgctaat actgtcacac 360
acgctcagct ccccacggcg ggcagggtcg gagtggcgcc gaaccctcat agacatgttt 420
gcggcatcca ggtaattttt gtattcctcc agcagaaaga gtagaggagg ctccaaaggc 480
acttgactgc tgagcatcac ccgggaagtg tacaagtccg cgtccttatg gttttcttcg 540
ttgggccgaa ccttctggtc ctcatccagc agctcttcga tgacgtgctc aaaagtgtca 600
gccagtgatg tcgtcgtcag acctctcgaa cctgccctgg gcccattcac gctctccaga 660
gtcccatggg tccgcacacc tgggtaggcc aagttgcctt gtccgtggac gtttacttct 720
ttcatgggcg ccgccttcat gcaaccgaag tatgaaataa ccatagtaag gaaaaggatg 780
gtcatcactc ttctcacctg gtggaactgt gggaaggaag cagagacaga cacagaacag 840
gatggttggc tccagcctca ttccttctgt cccagcttct gaagttctgg gaatacaaca 900
tgtaccatca tgccaagctc tactttttga aatcatggct cctgatatgt tgggcagccc 960
tgttgtgctt tgaagataaa atgctccaca aa 992
<210> 12
<211> 43
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 12
ararcrarar arcrararcr urgrgrurgr argrcrcrur grg 43
<210> 13
<211> 44
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 13
rurgrargrc rcrurararg rarurarcra rururgrcru rcru 44
<210> 14
<211> 44
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 14
rgrurgrcru rgrururgru rarargraru rurargrcrc rarc 44
<210> 15
<211> 44
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 15
rararurgra rcrarurgru rururgrura rgrgrgrarg rcrc 44
<210> 16
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 16
cmcmagmgmu gmumgmcgmg mac 23
<210> 17
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 17
cmcmaumgmg gmamcmucmu mgg 23
<210> 18
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 18
amgmagmcmg umgmamaumg mgg 23
<210> 19
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 19
cmcmcamamg gmcmamggmu muc 23
<210> 20
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 20
amamgamumg cmumumgamc mau 23
<210> 21
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 21
cmamuumgmg cmumgmacma mcu 23
<210> 22
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 22
umumcgmama cmamcmgumg mau 23
<210> 23
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 23
amgmaamgma gmcmumgumu mgg 23
<210> 24
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 24
amumgamgmg amcmcmagma maa 23
<210> 25
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 25
gmumucmgmg cmcmcmaamu mga 23
<210> 26
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 26
amgmaamama cmamamuama mgg 23
<210> 27
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 27
amcmgcmamg amcmumugmu mac 23
<210> 28
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 28
amcmgumcmc amgmgmgumg mau 23
<210> 29
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 29
gmcmucmamg umamgmucma mag 23
<210> 30
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 30
umgmccmumu umgmgmagmc mcu 23
<210> 31
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 31
cmcmucmumu cmumcmuumu mcu 23
<210> 32
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 32
cccggtatcc aaaggc 16
<210> 33
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 33
gtattagcga gtgggt 16
<210> 34
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 34
gtctatgagg gttcgg 16
<210> 35
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 35
cctcctctac tctttc 16
<210> 36
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 36
ggcaggttcg agaggt 16
<210> 37
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 37
ttccttccca cagttc 16
<210> 38
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 38
cggttgcatg aaggcg 16
<210> 39
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 39
tggctggcga ttcata 16
<210> 40
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 40
caacatatca ggagcc 16
<210> 41
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 41
tgtattccca gaactt 16
<210> 42
<211> 56
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 42
rurarurgrg rururaruru rurcrarura rcrururcrg rgrururgrc rarurg 56
<210> 43
<211> 56
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 43
rargrararg rurarararc rgrurcrcra rcrgrgrarc rarargrgrc rararc 56
<210> 44
<211> 56
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 44
rarurururc rurarcrgra rgrarcrcra rargrurgru rararurcrc rcraru 56
<210> 45
<211> 56
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 45
rurarargrg rarcrgrcrg rgrarcruru rgrurarcra rcrururcrc rgrgrg 56
<210> 46
<211> 56
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 46
rargrarara rgrarararg rururcrura rarcrcrurg rururcrurg rurgru 56
<210> 47
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 47
gatttcagag ccgcag 16
<210> 48
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 48
gacacatcca tcccag 16
<210> 49
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 49
cctcgtcatg tctgtg 16
<210> 50
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 50
cttgaattgt ttgta 15
<210> 51
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 51
agttgcaaga gttgg 15
<210> 52
<211> 15
<212> DNA
<213> Artificial sequence
<220>
<223> Antisense oligonucleotide
<400> 52
atctgttctg ctgtc 15
<210> 53
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 53
catattcttg gacga 15
<210> 54
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 54
tgtgctgttg taaga 15
<210> 55
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Antisense oligonucleotide
<400> 55
tgacagagga gtatt 15
<210> 56
<211> 38
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 11
<400> 56
rgrgrcrurc rarcrcrarg rururgruru rurgruru 38
<210> 57
<211> 38
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 12
<400> 57
rgrcrararu rgrurarurc rururargrg rcrurcra 38
<210> 58
<211> 38
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 13
<400> 58
rgrcrurara rurcrurura rcrararcra rgrcrarc 38
<210> 59
<211> 38
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 14
<400> 59
rurcrcrcru rarcrarara rcrarurgru rcraruru 38
<210> 60
<211> 50
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 41
<400> 60
rgrcrararc rcrgrararg rurarurgra rararurara rcrcrarura 50
<210> 61
<211> 50
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 42
<400> 61
rgrcrcruru rgrurcrcrg rurgrgrarc rgrururura rcrururcru 50
<210> 62
<211> 50
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 43
<400> 62
rgrgraruru rarcrarcru rurgrgrurc rurcrgrura rgrarararu 50
<210> 63
<211> 50
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 44
<400> 63
rgrgrararg rurgrurarc rarargrurc rcrgrcrgru rcrcrurura 50
<210> 64
<211> 50
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse complement of the antisense oligonucleotide SEQ ID NO: 45
<400> 64
rcrargrara rcrargrgru rurargrara rcrurururc rurururcru 50
<210> 65
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> Assay Sequence
<400> 65
gcacacctgg agatactcta ttata 25
<210> 66
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> Assay Sequence
<400> 66
cctgcagaat ggcctggaat tacaa 25
Claims (39)
- 생물학적 시스템에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법으로서,
상기 시스템을 5 내지 30개 뉴클레오티드 길이의 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시킴으로써, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하고,
상기 하나 이상의 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 천연 안티센스의 역 상보체에 대해 50% 이상의 서열 동일성을 갖고, 단 서열 번호 50-55의 올리고뉴클레오티드는 제외되는 것인 방법. - 제1항의 생물학적 시스템에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법으로서,
상기 생물학적 시스템을 5 내지 30개 뉴클레오티드 길이의 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시킴으로써, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하며,
상기 하나 이상의 올리고뉴클레오티드는 천연 안티센스 전사체 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개 연속 뉴클레오티드를 포함하는 폴리뉴클레오티드의 역 상보체에 대해 50% 이상의 서열 동일성을 갖고, 단 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되는 것인 방법. - 생체내에서 또는 시험관내에서 환자 세포 또는 조직에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법으로서,
상기 세포 또는 조직을 5 내지 30개 뉴클레오티드 길이의 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시킴으로써, 생체내에서 또는 시험관내에서 환자 세포 또는 조직에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하고,
상기 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드에 대한 안티센스 올리고뉴클레오티드에 대해 50% 이상의 서열 동일성을 갖고, 단, 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되는 것인 방법. - 제3항에 따른 환자 세포 또는 조직에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법으로서,
상기 생물학적 시스템을 5 내지 30개 뉴클레오티드 길이의 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시킴으로써, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하고,
상기 하나 이상의 올리고뉴클레오티드는 천연 안티센스 전사체 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개 연속 뉴클레오티드를 포함하는 폴리뉴클레오티드의 역 상보체에 대해 50% 이상의 서열 동일성을 갖고, 단 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되는 것인 방법. - 생물학적 시스템에서 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 방법으로서,
상기 시스템을 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 천연 안티센스 올리고뉴클레오티드의 영역을 표적으로 하는 하나 이상의 안티센스 올리고뉴클레오티드와 접촉시킴으로써, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 기능 및/또는 발현을 조정하는 것을 포함하고, 단 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되는 것인 방법. - 제5항에 있어서, 뇌 유래 신경영양 인자(BDNF)의 기능 및/또는 발현이 대조군에 대하여 생체내에서 또는 시험관내에서 증가되는 것인 방법.
- 제5항에 있어서, 하나 이상의 안티센스 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 천연 안티센스 서열을 표적으로 하는 것인 방법.
- 제5항에 있어서, 하나 이상의 안티센스 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 코딩 및/또는 비코딩 핵산 서열을 포함하는 핵산 서열을 표적으로 하는 것인 방법.
- 제5항에 있어서, 하나 이상의 안티센스 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 중복 및/또는 비-중복 서열을 표적으로 하는 것인 방법.
- 제5항에 있어서, 하나 이상의 안티센스 올리고뉴클레오티드가 하나 이상의 변형된 당 모이어티, 하나 이상의 변형된 뉴클레오시드간 연결기, 하나 이상의 변형된 뉴클레오티드, 및 이의 조합으로부터 선택된 하나 이상의 변형을 포함하는 것인 방법.
- 제10항에 있어서, 하나 이상의 변형이 2'-O-메톡시에틸 변형된 당 모이어티, 2'-메톡시 변형된 당 모이어티, 2'-O-알킬 변형된 당 모이어티, 이환식 당 모이어티, 및 이의 조합으로부터 선택된 하나 이상의 변형된 당 모이어티를 포함하는 것인 방법.
- 제10항에 있어서, 하나 이상의 변형이 포스포로티오에이트, 2'-O메톡시에틸(MOE), 2'-플루오로, 알킬포스포네이트, 포스포로디티오에이트, 알킬포스포노티오에이트, 포스포라미데이트, 카바메이트, 카보네이트, 포스페이트 트리에스테르, 아세트아미데이트, 카복시메틸 에스테르, 및 이의 조합으로부터 선택된 하나 이상의 변형된 뉴클레오시드간 연결기를 포함하는 것인 방법.
- 제10항에 있어서, 하나 이상의 변형이 펩티드 핵산(PNA), 잠금 핵산(LNA), 아라비노-핵산(FANA), 유사체, 유도체, 및 이의 조합으로부터 선택된 하나 이상의 변형된 뉴클레오티드를 포함하는 것인 방법.
- 제1항에 있어서, 하나 이상의 올리고뉴클레오티드가 서열 번호 12 내지 49에 제시된 하나 이상의 올리고뉴클레오티드 서열을 포함하는 것인 방법.
- 생체내에서 또는 시험관내에서 포유동물 세포 또는 조직에서 뇌 유래 신경영양 인자(BDNF) 유전자의 기능 및/또는 발현을 조정하는 방법으로서,
상기 세포 또는 조직을 5 내지 30개 뉴클레오티드 길이의 하나 이상의 짧은 간섭 RNA(siRNA) 올리고뉴클레오티드와 접촉시키고, 생체내에서 또는 시험관내에서 포유동물 세포 또는 조직에서 뇌 유래 신경영양 인자(BDNF)의 기능 및/또는 발현을 조정하는 것을 포함하고,
상기 하나 이상의 siRNA 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 폴리뉴클레오티드에 특이적이고, 상기 하나 이상의 siRNA 올리고뉴클레오티드는 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 및/또는 센스 핵산 분자의 약 5개 이상의 연속 핵산의 상보성 서열에 대해 50% 이상의 서열 동일성을 갖는 것인 방법. - 제15항에 있어서, 상기 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 및/또는 센스 핵산 분자에 상보성인 약 5개 이상의 연속 핵산의 서열에 대해 80% 이상의 서열 동일성을 갖는 것인 방법.
- 5 내지 30개 뉴클레오티드 길이의 올리고뉴클레오티드로서,
상기 올리고뉴클레오티드가 천연 안티센스 전사체 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개 연속 뉴클레오티드를 포함하는 폴리뉴클레오티드의 역 상보체에 대해 50% 이상의 서열 동일성을 갖고, 단 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되고, 임의로 하나 이상의 변형을 추가로 포함하고, 여기서 하나 이상의 변형은 하나 이상의 변형된 당 모이어티; 하나 이상의 변형된 뉴클레오티드간 연결기; 하나 이상의 변형된 뉴클레오티드, 및 이의 조합으로부터 선택되고, 상기 올리고뉴클레오티드가 정상 대조군과 비교하여 생체내에서 또는 시험관내에서 뇌 유래 신경영양 인자(BDNF) 유전자에 하이드리드화하여 기능 및/또는 발현을 조정하는 안티센스 화합물인 올리고뉴클레오티드. - 제17항에 있어서, 상기 올리고뉴클레오티드가 5 내지 30개 뉴클레오티드 길이이고 BDNF 유전자의 천연 안티센스 전사체 내에서 5 내지 30개 연속 뉴클레오티드의 역 상보체에 대해 50% 이상의 서열 동일성을 갖는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 하나 이상의 변형이 포스포로티오에이트, 알킬포스포네이트, 포스포로디티오에이트, 알킬포스포노티오에이트, 포스포라미데이트, 카바메이트, 카보네이트, 포스페이트 트리에스테르, 아세트아미데이트, 카복시메틸 에스테르, 및 이의 조합으로 이루어진 군으로부터 선택된 뉴클레오티드간 연결기를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 상기 올리고뉴클레오티드가 하나 이상의 포스포로티오에이트 뉴클레오티드간 연결기를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 상기 올리고뉴클레오티드가 포스포로티오에이트 뉴클레오티드간 연결기의 골격을 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 상기 올리고뉴클레오티드가 하나 이상의 변형된 뉴클레오티드를 포함하고, 상기 변형된 뉴클레오티드가 펩티드 핵산, 잠금 핵산(LNA), 유사체, 유도체, 및 이의 조합으로부터 선택되는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 복수의 변형을 포함하고, 상기 변형이 포스포로티오에이트, 알킬포스포네이트, 포스포로디티오에이트, 알킬포스포노티오에이트, 포스포라미데이트, 카바메이트, 카보네이트, 포스페이트 트리에스테르, 아세트아미데이트, 카복시메틸 에스테르, 및 이의 조합으로부터 선택된 변형된 뉴클레오티드를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 복수의 변형을 포함하고, 상기 변형이 펩티드 핵산, 잠금 핵산(LNA), 유사체, 유도체, 및 이의 조합으로부터 선택된 변형된 뉴클레오티드를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 2'-O-메톡시에틸 변형된 당 모이어티, 2'-메톡시 변형된 당 모이어티, 2'-O-알킬 변형된 당 모이어티, 이환식 당 모이어티, 및 이의 조합으로부터 선택된 하나 이상의 변형된 당 모이어티를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 복수의 변형을 포함하고, 상기 변형이 2'-O-메톡시에틸 변형된 당 모이어티, 2'-메톡시 변형된 당 모이어티, 2'-O-알킬 변형된 당 모이어티, 이환식 당 모이어티, 및 이의 조합으로부터 선택된 변형된 당 모이어티를 포함하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 적어도 약 5 내지 30개 길이의 뉴클레오티드의 것이고, 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 및/또는 센스 가닥에 하이브리드화하고, 상기 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 및/또는 센스 코딩 및/또는 비코딩 핵산 서열의 약 5개 이상의 연속 핵산의 상보성 서열에 대해 약 60% 이상의 서열 동일성을 갖는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 안티센스 및/또는 센스 코딩 및/또는 비코딩 핵산 서열의 약 5개 이상의 연속 핵산의 상보성 서열에 대해 약 80% 이상의 서열 동일성을 갖는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 상기 올리고뉴클레오티드가 정상 대조군과 비교하여 생체내에서 또는 시험관내에서 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드에 하이브리드화하여 이의 발현 및/또는 기능을 조정하는 것인 올리고뉴클레오티드.
- 제18항에 있어서, 올리고뉴클레오티드가 서열 번호 12 내지 49에 제시된 서열을 포함하는 것인 올리고뉴클레오티드.
- 제17항에 따른 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드에 특이적인 하나 이상의 올리고뉴클레오티드 및 약제학적으로 허용되는 부형제를 포함하는 약제학적 조성물.
- 제31항에 있어서, 올리고뉴클레오티드가 서열 번호 12 내지 49에 제시된 뉴클레오티드 서열 중 어느 하나와 비교하여 약 40% 이상의 서열 동일성을 갖는 것인 조성물.
- 제31항에 있어서, 올리고뉴클레오티드가 서열 번호 12 내지 49에 제시된 뉴클레오티드 서열을 포함하는 것인 조성물.
- 제33항에 있어서, 서열 번호 12 내지 49에 제시된 올리고뉴클레오티드가 하나 이상의 변형 또는 치환을 포함하는 것인 조성물.
- 제34항에 있어서, 하나 이상의 변형이 포스포로티오에이트, 메틸포스포네이트, 펩티드 핵산, 잠금 핵산(LNA) 분자, 및 이의 조합으로부터 선택되는 것인 조성물.
- 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드 및/또는 하나 이상의 이의 코딩된 산물과 연관된 질환을 예방 또는 치료하는 방법으로서,
환자에게 5 내지 30개 뉴클레오티드 길이의 하나 이상의 안티센스 올리고뉴클레오티드의 치료적 유효량을 투여함으로써, 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드 및/또는 하나 이상의 이의 코딩된 산물과 관련된 질환을 예방 또는 치료하는 것을 포함하고,
상기 하나 이상의 올리고뉴클레오티드는 천연 안티센스 전사체 뉴클레오티드 서열 번호 3의 1 내지 1279, 또는 서열 번호 4의 1 내지 1478, 또는 서열 번호 5의 1 내지 1437, 또는 서열 번호 6의 1 내지 2322, 또는 서열 번호 7의 1 내지 2036, 또는 서열 번호 8의 1 내지 2364, 또는 서열 번호 9의 1 내지 3136, 또는 서열 번호 10의 1 내지 906, 또는 서열 번호 11의 1 내지 992 내에서 5 내지 30개 연속 뉴클레오티드를 포함하는 폴리뉴클레오티드의 역 상보체에 대해 50% 이상의 서열 동일성을 갖고, 단 서열 번호 50-55를 갖는 올리고뉴클레오티드는 제외되고, 상기 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 천연 안티센스 서열에 결합하고 상기 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드의 발현을 조정하는 것인 방법. - 제36항에 있어서, 하나 이상의 뇌 유래 신경영양 인자(BDNF) 폴리뉴클레오티드와 연관된 질환이 BDNF의 비정상적인 기능 및/또는 발현과 연관된 질환 또는 장애, 신경병성 질환 또는 장애, 결함성 신경발생(defective neurogenesis)과 연관된 질환 또는 장애; 신경퇴행성 질환 또는 장애(예를 들면, 알츠하이머병, 파키슨병, 헌팅턴병, 근위축성 축삭 경화증 등); 신경정신병적 장애(우울증, 정신분열증, 정신분열형 장애, 분열정동 장애, 및 망상 장애; 불안 장애, 예를 들면, 공황 장애, 공포증(광장공포증 포함), 강박 장애, 외상후 스트레스 장애, 양극성 장애, 신경성 식욕부진증, 신경성 폭식증), 중추신경계의 자가면역 장애(예를 들면, 다발성 경화증), 기억 상실, 장기 또는 단기 기억 장애, 건망증, 소아 학습 장애, 폐쇄성 뇌 손상, 주의력 결핍 장애, 바이러스 감염에 대한 뉴런 반응, 뇌 손상, 기면 발작, 수면 장애(예를 들면, 일주기성 리듬 장애, 불면증 및 기면 발작); 신경의 단절 또는 신경 손상, 뇌척수 신경삭(CNS)의 단절 및 뇌 또는 신경 세포의 손상, AIDS와 연관된 신경학적 결함, 운동 및/또는 음성 틱으로 특징되는 운동 틱 장애(예를 들면, 뚜렛 장애, 만성 운동 또는 음성 틱 장애, 일시적 틱 장애, 및 상동적 운동장애), 약물 남용 장애(예를 들면, 약물 의존, 약물 남용 및 약물 남용/의존의 후유증, 예를 들면, 약물-유도된 심리학적 장애, 약물 금단 증상 및 약물-유도된 치매 또는 건망증 장애), 외상성 뇌 손상, 이명, 신경통(예를 들면, 삼차 신경통), 통증(예를 들면, 만성 통증, 만성 염증성 통증, 관절염과 연관된 통증, 섬유근육통, 요통, 암-연관된 통증, 소화성 질환과 연관된 통증, 크론병과 연관된 통증, 자가면역 질환과 연관된 통증, 내분비 질환과 연관된 통증, 당뇨성 신경병증과 연관된 통증, 환지통, 자발통, 수술후 만성 통증, 만성 측두하악 통증, 작열통, 대상포진후 신경통, AIDS-관련된 통증, 복합 부위 통증 증후군 타입 I과 II, 삼차 신경통, 만성적인 요통, 척수 손상과 연관된 통증, 약물 복용과 연관된 통증 및 재발성 급성 통증, 신경병증성 통증), 당뇨병과 같은 질환에서 신경이감각증(neurodysthesias)을 유발하는 부적절한 뉴런 활성, MS 및 운동 뉴런 질환, 운동실조, 근육 강직(경직), 턱관절 기능장애, 보상 결핍 증후군(RDS), 알코올 또는 약물 남용(예를 들면, 엑스터시, 메스암페타민 등)에 의해 유발된 신경독성, 정신 지체 또는 인지 장애(예를 들면, 비증후군성 X-염색체 연관 정신 지체, 취약 X 증후군, 다운 증후군, 자폐증), 실어증, 벨 마비(Bell's palsy), 크로이츠펠트-야곱병, 뇌염, 연령 관련된 황반 변성, 온다인(Ondine) 증후군, WAGR 증후군, 청력 상실, 레트(Rett) 증후군, 간질, 척수 손상, 뇌졸중, 저산소증, 허혈, 뇌 손상, 당뇨성 신경병증, 말초 신경병증, 신경 이식 합병증, 운동 뉴런 질환, 말초 신경 손상, 비만, 대사 증후군, 암, 천식, 아토피 질환, 염증, 알레르기, 습진, 신경-종양학적 질환 또는 장애, 신경-면역학적 질환 또는 장애 및 신경-이과학적 질환 또는 장애; 및 가령(aging) 및 노화와 연관된 질환 또는 장애로부터 선택되는 것인 방법.
- BDNF 폴리뉴클레오티드의 발현을 조정하기 위한 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체("NAT")를 표적으로 하는 서열 번호 50-55로 이루어진 군으로부터 선택된 올리고뉴클레오티드의 용도로서, 상기 NAT가 서열 번호 3 내지 11로 이루어진 군으로부터 선택되는 용도.
- BDNF 폴리뉴클레오티드의 발현을 조정하기 위한 BDNF 폴리뉴클레오티드의 천연 안티센스 전사체(NAT)를 표적으로 하는 서열 번호 50-55로 이루어진 군으로부터 선택된 올리고뉴클레오티드의 용도로서, 상기 NAT가 서열 번호 3, 4, 5, 7, 8, 9, 10 및 11로 이루어진 군으로부터 선택되는 용도.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261611225P | 2012-03-15 | 2012-03-15 | |
| US61/611,225 | 2012-03-15 | ||
| US201261614664P | 2012-03-23 | 2012-03-23 | |
| US61/614,664 | 2012-03-23 | ||
| PCT/US2013/030589 WO2013138374A2 (en) | 2012-03-15 | 2013-03-12 | Treatment of brain derived neurotrophic factor (bdnf) related diseases by inhibition of natural antisense transcript to bdnf |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140136488A true KR20140136488A (ko) | 2014-11-28 |
Family
ID=47998530
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147028058A KR20140136488A (ko) | 2012-03-15 | 2013-03-12 | 뇌 유래 신경영양 인자(bdnf)에 대한 천연 안티센스 전사체의 저해에 의한 뇌 유래 신경영양 인자(bdnf)관련 질환의 치료 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US20150031750A1 (ko) |
| EP (1) | EP2825648B1 (ko) |
| JP (2) | JP2015511494A (ko) |
| KR (1) | KR20140136488A (ko) |
| CN (2) | CN110438125A (ko) |
| CA (1) | CA2867262C (ko) |
| DK (1) | DK2825648T3 (ko) |
| ES (1) | ES2694592T3 (ko) |
| HK (1) | HK1210211A1 (ko) |
| HU (1) | HUE040179T2 (ko) |
| PL (1) | PL2825648T3 (ko) |
| PT (1) | PT2825648T (ko) |
| RU (1) | RU2661104C2 (ko) |
| TR (1) | TR201815503T4 (ko) |
| WO (1) | WO2013138374A2 (ko) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101437933B (zh) | 2005-12-28 | 2013-11-06 | 斯克里普斯研究所 | 作为药物靶标的天然反义和非编码的rna转录物 |
| US9920317B2 (en) | 2010-11-12 | 2018-03-20 | The General Hospital Corporation | Polycomb-associated non-coding RNAs |
| EP2638163B1 (en) | 2010-11-12 | 2017-05-17 | The General Hospital Corporation | Polycomb-associated non-coding rnas |
| US20150031750A1 (en) | 2012-03-15 | 2015-01-29 | The Scripps Research Institute | Treatment of brain derived neurotrophic factor (bdnf) related diseases by inhibition of natural antisense transcript to bdnf |
| AU2013262656A1 (en) | 2012-05-16 | 2015-01-22 | Rana Therapeutics, Inc. | Compositions and methods for modulating UTRN expression |
| JP2015518712A (ja) | 2012-05-16 | 2015-07-06 | ラナ セラピューティクス インコーポレイテッド | Mecp2発現を調節するための組成物及び方法 |
| AP2014008100A0 (en) | 2012-05-16 | 2014-12-31 | Gen Hospital Corp | Compositions and methods for modulating hemoglobingene family expression |
| US10059941B2 (en) | 2012-05-16 | 2018-08-28 | Translate Bio Ma, Inc. | Compositions and methods for modulating SMN gene family expression |
| US10837014B2 (en) | 2012-05-16 | 2020-11-17 | Translate Bio Ma, Inc. | Compositions and methods for modulating SMN gene family expression |
| CN104602714A (zh) * | 2012-05-16 | 2015-05-06 | Rana医疗有限公司 | 用于调节bdnf表达的组合物和方法 |
| EA201492120A1 (ru) | 2012-05-16 | 2015-10-30 | Рана Терапьютикс, Инк. | Композиции и способы для модулирования экспрессии atp2a2 |
| CA2966044A1 (en) | 2014-10-30 | 2016-05-06 | The General Hospital Corporation | Methods for modulating atrx-dependent gene repression |
| US10900036B2 (en) | 2015-03-17 | 2021-01-26 | The General Hospital Corporation | RNA interactome of polycomb repressive complex 1 (PRC1) |
| CN106466479A (zh) * | 2015-08-18 | 2017-03-01 | 周意 | 脑源性神经营养因子前体蛋白用作治疗情感障碍的靶点 |
| AU2016315268B2 (en) * | 2015-08-31 | 2022-12-22 | Société des Produits Nestlé S.A. | Methods and compositions using Bifidobacterium longum to modulate emotional reactivity and treat or prevent sub-clinical mood disturbances |
| MX2019005101A (es) | 2016-11-01 | 2019-08-22 | Univ New York State Res Found | Microarns modificados con 5-halouracilo y su uso en el tratamiento del cancer. |
| GB201705484D0 (en) * | 2017-04-05 | 2017-05-17 | Quethera Ltd | Genetic construct |
| CN110184338B (zh) * | 2019-05-31 | 2023-04-07 | 南方医科大学第三附属医院(广东省骨科研究院) | 脑脊液外泌体miRNA在MMD诊断和治疗中的应用 |
| CN113201534A (zh) * | 2020-05-29 | 2021-08-03 | 中山大学孙逸仙纪念医院 | 一种长非编码rna bdnf-as及其作为标志物和治疗靶点的应用 |
| CN112359107B (zh) * | 2020-11-15 | 2021-09-14 | 安徽中医药大学第一附属医院(安徽省中医院) | Linc02085基因的应用及其检测方法 |
| WO2023140658A1 (ko) * | 2022-01-24 | 2023-07-27 | 고려대학교 산학협력단 | 뇌유래신경성장인자를 이용한 패혈증 진단, 예방 또는 치료용 약학적 조성물 |
Family Cites Families (384)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| US4469863A (en) | 1980-11-12 | 1984-09-04 | Ts O Paul O P | Nonionic nucleic acid alkyl and aryl phosphonates and processes for manufacture and use thereof |
| US4534899A (en) | 1981-07-20 | 1985-08-13 | Lipid Specialties, Inc. | Synthetic phospholipid compounds |
| US4426330A (en) | 1981-07-20 | 1984-01-17 | Lipid Specialties, Inc. | Synthetic phospholipid compounds |
| US5023243A (en) | 1981-10-23 | 1991-06-11 | Molecular Biosystems, Inc. | Oligonucleotide therapeutic agent and method of making same |
| US4476301A (en) | 1982-04-29 | 1984-10-09 | Centre National De La Recherche Scientifique | Oligonucleotides, a process for preparing the same and their application as mediators of the action of interferon |
| JPS5927900A (ja) | 1982-08-09 | 1984-02-14 | Wakunaga Seiyaku Kk | 固定化オリゴヌクレオチド |
| FR2540122B1 (fr) | 1983-01-27 | 1985-11-29 | Centre Nat Rech Scient | Nouveaux composes comportant une sequence d'oligonucleotide liee a un agent d'intercalation, leur procede de synthese et leur application |
| US4605735A (en) | 1983-02-14 | 1986-08-12 | Wakunaga Seiyaku Kabushiki Kaisha | Oligonucleotide derivatives |
| US4948882A (en) | 1983-02-22 | 1990-08-14 | Syngene, Inc. | Single-stranded labelled oligonucleotides, reactive monomers and methods of synthesis |
| NZ207394A (en) | 1983-03-08 | 1987-03-06 | Commw Serum Lab Commission | Detecting or determining sequence of amino acids |
| US4824941A (en) | 1983-03-10 | 1989-04-25 | Julian Gordon | Specific antibody to the native form of 2'5'-oligonucleotides, the method of preparation and the use as reagents in immunoassays or for binding 2'5'-oligonucleotides in biological systems |
| US4587044A (en) | 1983-09-01 | 1986-05-06 | The Johns Hopkins University | Linkage of proteins to nucleic acids |
| US5118800A (en) | 1983-12-20 | 1992-06-02 | California Institute Of Technology | Oligonucleotides possessing a primary amino group in the terminal nucleotide |
| US5118802A (en) | 1983-12-20 | 1992-06-02 | California Institute Of Technology | DNA-reporter conjugates linked via the 2' or 5'-primary amino group of the 5'-terminal nucleoside |
| US5550111A (en) | 1984-07-11 | 1996-08-27 | Temple University-Of The Commonwealth System Of Higher Education | Dual action 2',5'-oligoadenylate antiviral derivatives and uses thereof |
| FR2567892B1 (fr) | 1984-07-19 | 1989-02-17 | Centre Nat Rech Scient | Nouveaux oligonucleotides, leur procede de preparation et leurs applications comme mediateurs dans le developpement des effets des interferons |
| US5367066A (en) | 1984-10-16 | 1994-11-22 | Chiron Corporation | Oligonucleotides with selectably cleavable and/or abasic sites |
| US5258506A (en) | 1984-10-16 | 1993-11-02 | Chiron Corporation | Photolabile reagents for incorporation into oligonucleotide chains |
| US5430136A (en) | 1984-10-16 | 1995-07-04 | Chiron Corporation | Oligonucleotides having selectably cleavable and/or abasic sites |
| US4828979A (en) | 1984-11-08 | 1989-05-09 | Life Technologies, Inc. | Nucleotide analogs for nucleic acid labeling and detection |
| US4754065A (en) | 1984-12-18 | 1988-06-28 | Cetus Corporation | Precursor to nucleic acid probe |
| FR2575751B1 (fr) | 1985-01-08 | 1987-04-03 | Pasteur Institut | Nouveaux nucleosides de derives de l'adenosine, leur preparation et leurs applications biologiques |
| US5166315A (en) | 1989-12-20 | 1992-11-24 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| US5235033A (en) | 1985-03-15 | 1993-08-10 | Anti-Gene Development Group | Alpha-morpholino ribonucleoside derivatives and polymers thereof |
| US5405938A (en) | 1989-12-20 | 1995-04-11 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5506337A (en) | 1985-03-15 | 1996-04-09 | Antivirals Inc. | Morpholino-subunit combinatorial library and method |
| US5185444A (en) | 1985-03-15 | 1993-02-09 | Anti-Gene Deveopment Group | Uncharged morpolino-based polymers having phosphorous containing chiral intersubunit linkages |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US4762779A (en) | 1985-06-13 | 1988-08-09 | Amgen Inc. | Compositions and methods for functionalizing nucleic acids |
| US4800159A (en) | 1986-02-07 | 1989-01-24 | Cetus Corporation | Process for amplifying, detecting, and/or cloning nucleic acid sequences |
| US5317098A (en) | 1986-03-17 | 1994-05-31 | Hiroaki Shizuya | Non-radioisotope tagging of fragments |
| JPS638396A (ja) | 1986-06-30 | 1988-01-14 | Wakunaga Pharmaceut Co Ltd | ポリ標識化オリゴヌクレオチド誘導体 |
| DE3788914T2 (de) | 1986-09-08 | 1994-08-25 | Ajinomoto Kk | Verbindungen zur Spaltung von RNS an eine spezifische Position, Oligomere, verwendet bei der Herstellung dieser Verbindungen und Ausgangsprodukte für die Synthese dieser Oligomere. |
| US5276019A (en) | 1987-03-25 | 1994-01-04 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| US5264423A (en) | 1987-03-25 | 1993-11-23 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| US4904582A (en) | 1987-06-11 | 1990-02-27 | Synthetic Genetics | Novel amphiphilic nucleic acid conjugates |
| DE3851889T2 (de) | 1987-06-24 | 1995-04-13 | Florey Howard Inst | Nukleosid-derivate. |
| US5585481A (en) | 1987-09-21 | 1996-12-17 | Gen-Probe Incorporated | Linking reagents for nucleotide probes |
| US5188897A (en) | 1987-10-22 | 1993-02-23 | Temple University Of The Commonwealth System Of Higher Education | Encapsulated 2',5'-phosphorothioate oligoadenylates |
| US4924624A (en) | 1987-10-22 | 1990-05-15 | Temple University-Of The Commonwealth System Of Higher Education | 2,',5'-phosphorothioate oligoadenylates and plant antiviral uses thereof |
| US5525465A (en) | 1987-10-28 | 1996-06-11 | Howard Florey Institute Of Experimental Physiology And Medicine | Oligonucleotide-polyamide conjugates and methods of production and applications of the same |
| DE3738460A1 (de) | 1987-11-12 | 1989-05-24 | Max Planck Gesellschaft | Modifizierte oligonukleotide |
| US4866042A (en) | 1987-11-18 | 1989-09-12 | Neuwelt Edward A | Method for the delivery of genetic material across the blood brain barrier |
| ATE151467T1 (de) | 1987-11-30 | 1997-04-15 | Univ Iowa Res Found | Durch modifikationen an der 3'-terminalen phosphodiesterbindung stabilisierte dna moleküle, ihre verwendung als nukleinsäuresonden sowie als therapeutische mittel zur hemmung der expression spezifischer zielgene |
| US5403711A (en) | 1987-11-30 | 1995-04-04 | University Of Iowa Research Foundation | Nucleic acid hybridization and amplification method for detection of specific sequences in which a complementary labeled nucleic acid probe is cleaved |
| US5288512A (en) | 1987-12-15 | 1994-02-22 | The Procter & Gamble Company | Reduced calorie fats made from triglycerides containing medium and long chain fatty acids |
| US5082830A (en) | 1988-02-26 | 1992-01-21 | Enzo Biochem, Inc. | End labeled nucleotide probe |
| EP0406309A4 (en) | 1988-03-25 | 1992-08-19 | The University Of Virginia Alumni Patents Foundation | Oligonucleotide n-alkylphosphoramidates |
| NL8800756A (nl) | 1988-03-25 | 1989-10-16 | Vereniging Voor Christelijk Wetenschappelijk Onderwijs | Genetisch gemanipuleerde plantecellen en planten, alsmede daarvoor bruikbaar recombinant dna. |
| US5278302A (en) | 1988-05-26 | 1994-01-11 | University Patents, Inc. | Polynucleotide phosphorodithioates |
| US5109124A (en) | 1988-06-01 | 1992-04-28 | Biogen, Inc. | Nucleic acid probe linked to a label having a terminal cysteine |
| US5216141A (en) | 1988-06-06 | 1993-06-01 | Benner Steven A | Oligonucleotide analogs containing sulfur linkages |
| US5175273A (en) | 1988-07-01 | 1992-12-29 | Genentech, Inc. | Nucleic acid intercalating agents |
| US5262536A (en) | 1988-09-15 | 1993-11-16 | E. I. Du Pont De Nemours And Company | Reagents for the preparation of 5'-tagged oligonucleotides |
| US5512439A (en) | 1988-11-21 | 1996-04-30 | Dynal As | Oligonucleotide-linked magnetic particles and uses thereof |
| US5599923A (en) | 1989-03-06 | 1997-02-04 | Board Of Regents, University Of Tx | Texaphyrin metal complexes having improved functionalization |
| US5457183A (en) | 1989-03-06 | 1995-10-10 | Board Of Regents, The University Of Texas System | Hydroxylated texaphyrins |
| US5354844A (en) | 1989-03-16 | 1994-10-11 | Boehringer Ingelheim International Gmbh | Protein-polycation conjugates |
| US6294520B1 (en) | 1989-03-27 | 2001-09-25 | Albert T. Naito | Material for passage through the blood-brain barrier |
| US5108921A (en) | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| US5391723A (en) | 1989-05-31 | 1995-02-21 | Neorx Corporation | Oligonucleotide conjugates |
| US5256775A (en) | 1989-06-05 | 1993-10-26 | Gilead Sciences, Inc. | Exonuclease-resistant oligonucleotides |
| US4958013A (en) | 1989-06-06 | 1990-09-18 | Northwestern University | Cholesteryl modified oligonucleotides |
| US5227170A (en) | 1989-06-22 | 1993-07-13 | Vestar, Inc. | Encapsulation process |
| US5451463A (en) | 1989-08-28 | 1995-09-19 | Clontech Laboratories, Inc. | Non-nucleoside 1,3-diol reagents for labeling synthetic oligonucleotides |
| US5134066A (en) | 1989-08-29 | 1992-07-28 | Monsanto Company | Improved probes using nucleosides containing 3-dezauracil analogs |
| US5180820A (en) * | 1989-08-30 | 1993-01-19 | Barde Yves Alain | Brain-derived neurotrophic factor |
| US5254469A (en) | 1989-09-12 | 1993-10-19 | Eastman Kodak Company | Oligonucleotide-enzyme conjugate that can be used as a probe in hybridization assays and polymerase chain reaction procedures |
| US5591722A (en) | 1989-09-15 | 1997-01-07 | Southern Research Institute | 2'-deoxy-4'-thioribonucleosides and their antiviral activity |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| US5356633A (en) | 1989-10-20 | 1994-10-18 | Liposome Technology, Inc. | Method of treatment of inflamed tissues |
| US5527528A (en) | 1989-10-20 | 1996-06-18 | Sequus Pharmaceuticals, Inc. | Solid-tumor treatment method |
| US5399676A (en) | 1989-10-23 | 1995-03-21 | Gilead Sciences | Oligonucleotides with inverted polarity |
| US5264562A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences, Inc. | Oligonucleotide analogs with novel linkages |
| US5264564A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences | Oligonucleotide analogs with novel linkages |
| EP0942000B1 (en) | 1989-10-24 | 2004-06-23 | Isis Pharmaceuticals, Inc. | 2'-Modified oligonucleotides |
| US5292873A (en) | 1989-11-29 | 1994-03-08 | The Research Foundation Of State University Of New York | Nucleic acids labeled with naphthoquinone probe |
| US5177198A (en) | 1989-11-30 | 1993-01-05 | University Of N.C. At Chapel Hill | Process for preparing oligoribonucleoside and oligodeoxyribonucleoside boranophosphates |
| US5130302A (en) | 1989-12-20 | 1992-07-14 | Boron Bilogicals, Inc. | Boronated nucleoside, nucleotide and oligonucleotide compounds, compositions and methods for using same |
| US5469854A (en) | 1989-12-22 | 1995-11-28 | Imarx Pharmaceutical Corp. | Methods of preparing gas-filled liposomes |
| US5580575A (en) | 1989-12-22 | 1996-12-03 | Imarx Pharmaceutical Corp. | Therapeutic drug delivery systems |
| US5486603A (en) | 1990-01-08 | 1996-01-23 | Gilead Sciences, Inc. | Oligonucleotide having enhanced binding affinity |
| US5623065A (en) | 1990-08-13 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Gapped 2' modified oligonucleotides |
| US5578718A (en) | 1990-01-11 | 1996-11-26 | Isis Pharmaceuticals, Inc. | Thiol-derivatized nucleosides |
| US5587361A (en) | 1991-10-15 | 1996-12-24 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5852188A (en) | 1990-01-11 | 1998-12-22 | Isis Pharmaceuticals, Inc. | Oligonucleotides having chiral phosphorus linkages |
| US5587470A (en) | 1990-01-11 | 1996-12-24 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5459255A (en) | 1990-01-11 | 1995-10-17 | Isis Pharmaceuticals, Inc. | N-2 substituted purines |
| US5681941A (en) | 1990-01-11 | 1997-10-28 | Isis Pharmaceuticals, Inc. | Substituted purines and oligonucleotide cross-linking |
| US5670633A (en) | 1990-01-11 | 1997-09-23 | Isis Pharmaceuticals, Inc. | Sugar modified oligonucleotides that detect and modulate gene expression |
| US5646265A (en) | 1990-01-11 | 1997-07-08 | Isis Pharmceuticals, Inc. | Process for the preparation of 2'-O-alkyl purine phosphoramidites |
| US5149797A (en) | 1990-02-15 | 1992-09-22 | The Worcester Foundation For Experimental Biology | Method of site-specific alteration of rna and production of encoded polypeptides |
| US5220007A (en) | 1990-02-15 | 1993-06-15 | The Worcester Foundation For Experimental Biology | Method of site-specific alteration of RNA and production of encoded polypeptides |
| US5214136A (en) | 1990-02-20 | 1993-05-25 | Gilead Sciences, Inc. | Anthraquinone-derivatives oligonucleotides |
| WO1991013080A1 (en) | 1990-02-20 | 1991-09-05 | Gilead Sciences, Inc. | Pseudonucleosides and pseudonucleotides and their polymers |
| US5321131A (en) | 1990-03-08 | 1994-06-14 | Hybridon, Inc. | Site-specific functionalization of oligodeoxynucleotides for non-radioactive labelling |
| US5470967A (en) | 1990-04-10 | 1995-11-28 | The Dupont Merck Pharmaceutical Company | Oligonucleotide analogs with sulfamate linkages |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| GB9009980D0 (en) | 1990-05-03 | 1990-06-27 | Amersham Int Plc | Phosphoramidite derivatives,their preparation and the use thereof in the incorporation of reporter groups on synthetic oligonucleotides |
| DK0455905T3 (da) | 1990-05-11 | 1998-12-07 | Microprobe Corp | Dipsticks til nukleinsyrehybridiseringsassays og fremgangsmåde til kovalent immobilisering af oligonukleotider |
| IE66205B1 (en) | 1990-06-14 | 1995-12-13 | Paul A Bartlett | Polypeptide analogs |
| US5650489A (en) | 1990-07-02 | 1997-07-22 | The Arizona Board Of Regents | Random bio-oligomer library, a method of synthesis thereof, and a method of use thereof |
| US5218105A (en) | 1990-07-27 | 1993-06-08 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5489677A (en) | 1990-07-27 | 1996-02-06 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent oxygen and nitrogen atoms |
| US5677437A (en) | 1990-07-27 | 1997-10-14 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5138045A (en) | 1990-07-27 | 1992-08-11 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US5602240A (en) | 1990-07-27 | 1997-02-11 | Ciba Geigy Ag. | Backbone modified oligonucleotide analogs |
| US5618704A (en) | 1990-07-27 | 1997-04-08 | Isis Pharmacueticals, Inc. | Backbone-modified oligonucleotide analogs and preparation thereof through radical coupling |
| US5688941A (en) | 1990-07-27 | 1997-11-18 | Isis Pharmaceuticals, Inc. | Methods of making conjugated 4' desmethyl nucleoside analog compounds |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| US5610289A (en) | 1990-07-27 | 1997-03-11 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogues |
| US5623070A (en) | 1990-07-27 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| ATE154246T1 (de) | 1990-07-27 | 1997-06-15 | Isis Pharmaceuticals Inc | Nuklease resistente, pyrimidin modifizierte oligonukleotide, die die gen-expression detektieren und modulieren |
| US5541307A (en) | 1990-07-27 | 1996-07-30 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs and solid phase synthesis thereof |
| US5245022A (en) | 1990-08-03 | 1993-09-14 | Sterling Drug, Inc. | Exonuclease resistant terminally substituted oligonucleotides |
| WO1992002534A2 (en) | 1990-08-03 | 1992-02-20 | Sterling Drug, Inc. | Compounds and methods for inhibiting gene expression |
| US5177196A (en) | 1990-08-16 | 1993-01-05 | Microprobe Corporation | Oligo (α-arabinofuranosyl nucleotides) and α-arabinofuranosyl precursors thereof |
| US5512667A (en) | 1990-08-28 | 1996-04-30 | Reed; Michael W. | Trifunctional intermediates for preparing 3'-tailed oligonucleotides |
| US5214134A (en) | 1990-09-12 | 1993-05-25 | Sterling Winthrop Inc. | Process of linking nucleosides with a siloxane bridge |
| US5561225A (en) | 1990-09-19 | 1996-10-01 | Southern Research Institute | Polynucleotide analogs containing sulfonate and sulfonamide internucleoside linkages |
| WO1992005186A1 (en) | 1990-09-20 | 1992-04-02 | Gilead Sciences | Modified internucleoside linkages |
| US5432272A (en) | 1990-10-09 | 1995-07-11 | Benner; Steven A. | Method for incorporating into a DNA or RNA oligonucleotide using nucleotides bearing heterocyclic bases |
| KR930702373A (ko) | 1990-11-08 | 1993-09-08 | 안토니 제이. 페이네 | 합성 올리고누클레오티드에 대한 다중 리포터(Reporter)그룹의 첨합 |
| WO1992008796A1 (en) | 1990-11-13 | 1992-05-29 | Immunex Corporation | Bifunctional selectable fusion genes |
| JP3220180B2 (ja) | 1991-05-23 | 2001-10-22 | 三菱化学株式会社 | 薬剤含有タンパク質結合リポソーム |
| US5539082A (en) | 1993-04-26 | 1996-07-23 | Nielsen; Peter E. | Peptide nucleic acids |
| US5714331A (en) | 1991-05-24 | 1998-02-03 | Buchardt, Deceased; Ole | Peptide nucleic acids having enhanced binding affinity, sequence specificity and solubility |
| US5719262A (en) | 1993-11-22 | 1998-02-17 | Buchardt, Deceased; Ole | Peptide nucleic acids having amino acid side chains |
| IL101683A0 (en) * | 1991-07-03 | 1992-12-30 | Regeneron Pharma | Method and assay system for neurotrophin activity |
| US5371241A (en) | 1991-07-19 | 1994-12-06 | Pharmacia P-L Biochemicals Inc. | Fluorescein labelled phosphoramidites |
| US6307040B1 (en) | 1992-03-05 | 2001-10-23 | Isis Pharmaceuticals, Inc. | Sugar modified oligonucleotides that detect and modulate gene expression |
| US5571799A (en) | 1991-08-12 | 1996-11-05 | Basco, Ltd. | (2'-5') oligoadenylate analogues useful as inhibitors of host-v5.-graft response |
| US5474796A (en) | 1991-09-04 | 1995-12-12 | Protogene Laboratories, Inc. | Method and apparatus for conducting an array of chemical reactions on a support surface |
| US5521291A (en) | 1991-09-30 | 1996-05-28 | Boehringer Ingelheim International, Gmbh | Conjugates for introducing nucleic acid into higher eucaryotic cells |
| NZ244306A (en) | 1991-09-30 | 1995-07-26 | Boehringer Ingelheim Int | Composition for introducing nucleic acid complexes into eucaryotic cells, complex containing nucleic acid and endosomolytic agent, peptide with endosomolytic domain and nucleic acid binding domain and preparation |
| EP0538194B1 (de) | 1991-10-17 | 1997-06-04 | Novartis AG | Bicyclische Nukleoside, Oligonukleotide, Verfahren zu deren Herstellung und Zwischenprodukte |
| US6335434B1 (en) | 1998-06-16 | 2002-01-01 | Isis Pharmaceuticals, Inc., | Nucleosidic and non-nucleosidic folate conjugates |
| US5605662A (en) | 1993-11-01 | 1997-02-25 | Nanogen, Inc. | Active programmable electronic devices for molecular biological analysis and diagnostics |
| US5484908A (en) | 1991-11-26 | 1996-01-16 | Gilead Sciences, Inc. | Oligonucleotides containing 5-propynyl pyrimidines |
| US5359044A (en) | 1991-12-13 | 1994-10-25 | Isis Pharmaceuticals | Cyclobutyl oligonucleotide surrogates |
| US5700922A (en) | 1991-12-24 | 1997-12-23 | Isis Pharmaceuticals, Inc. | PNA-DNA-PNA chimeric macromolecules |
| US5565552A (en) | 1992-01-21 | 1996-10-15 | Pharmacyclics, Inc. | Method of expanded porphyrin-oligonucleotide conjugate synthesis |
| US5595726A (en) | 1992-01-21 | 1997-01-21 | Pharmacyclics, Inc. | Chromophore probe for detection of nucleic acid |
| FR2687679B1 (fr) | 1992-02-05 | 1994-10-28 | Centre Nat Rech Scient | Oligothionucleotides. |
| US5573905A (en) | 1992-03-30 | 1996-11-12 | The Scripps Research Institute | Encoded combinatorial chemical libraries |
| US5633360A (en) | 1992-04-14 | 1997-05-27 | Gilead Sciences, Inc. | Oligonucleotide analogs capable of passive cell membrane permeation |
| US5434257A (en) | 1992-06-01 | 1995-07-18 | Gilead Sciences, Inc. | Binding compentent oligomers containing unsaturated 3',5' and 2',5' linkages |
| EP0577558A2 (de) | 1992-07-01 | 1994-01-05 | Ciba-Geigy Ag | Carbocyclische Nukleoside mit bicyclischen Ringen, Oligonukleotide daraus, Verfahren zu deren Herstellung, deren Verwendung und Zwischenproduckte |
| US5272250A (en) | 1992-07-10 | 1993-12-21 | Spielvogel Bernard F | Boronated phosphoramidate compounds |
| US5652355A (en) | 1992-07-23 | 1997-07-29 | Worcester Foundation For Experimental Biology | Hybrid oligonucleotide phosphorothioates |
| US5288514A (en) | 1992-09-14 | 1994-02-22 | The Regents Of The University Of California | Solid phase and combinatorial synthesis of benzodiazepine compounds on a solid support |
| EP0669987B1 (en) | 1992-09-25 | 2008-08-13 | Aventis Pharma S.A. | Adenovirus vectors for the transfer of foreign genes into cells of the central nervous system, particularly in brain |
| US6710174B2 (en) | 2001-09-13 | 2004-03-23 | Isis Pharmaceuticals, Inc. | Antisense inhibition of vascular endothelial growth factor receptor-1 expression |
| WO1994009148A1 (en) | 1992-10-15 | 1994-04-28 | Toray Industries, Inc. | Process for producing major histocompatibility antigen class ii protein and material having the same immobilized thereon |
| US5583020A (en) | 1992-11-24 | 1996-12-10 | Ribozyme Pharmaceuticals, Inc. | Permeability enhancers for negatively charged polynucleotides |
| US5574142A (en) | 1992-12-15 | 1996-11-12 | Microprobe Corporation | Peptide linkers for improved oligonucleotide delivery |
| JP3351476B2 (ja) | 1993-01-22 | 2002-11-25 | 三菱化学株式会社 | リン脂質誘導体及びそれを含有するリポソーム |
| US5476925A (en) | 1993-02-01 | 1995-12-19 | Northwestern University | Oligodeoxyribonucleotides including 3'-aminonucleoside-phosphoramidate linkages and terminal 3'-amino groups |
| US5395619A (en) | 1993-03-03 | 1995-03-07 | Liposome Technology, Inc. | Lipid-polymer conjugates and liposomes |
| GB9304618D0 (en) | 1993-03-06 | 1993-04-21 | Ciba Geigy Ag | Chemical compounds |
| EP0691968B1 (en) | 1993-03-30 | 1997-07-16 | Sanofi | Acyclic nucleoside analogs and oligonucleotide sequences containing them |
| EP0691977B1 (en) | 1993-03-31 | 1997-11-26 | Sanofi | Oligonucleotides with amide linkages replacing phosphodiester linkages |
| DE4311944A1 (de) | 1993-04-10 | 1994-10-13 | Degussa | Umhüllte Natriumpercarbonatpartikel, Verfahren zu deren Herstellung und sie enthaltende Wasch-, Reinigungs- und Bleichmittelzusammensetzungen |
| US5462854A (en) | 1993-04-19 | 1995-10-31 | Beckman Instruments, Inc. | Inverse linkage oligonucleotides for chemical and enzymatic processes |
| EP1897942A1 (en) | 1993-05-11 | 2008-03-12 | The University Of North Carolina At Chapel Hill | Antisense oligonucleotides which combat aberrant splicing and methods of using the same |
| CA2163427A1 (en) | 1993-05-21 | 1994-12-08 | Stephen D. Lupton | Bifunctional selectable fusion genes based on the cytosine deaminase (cd) gene |
| US5534259A (en) | 1993-07-08 | 1996-07-09 | Liposome Technology, Inc. | Polymer compound and coated particle composition |
| US5417978A (en) | 1993-07-29 | 1995-05-23 | Board Of Regents, The University Of Texas System | Liposomal antisense methyl phosphonate oligonucleotides and methods for their preparation and use |
| ATE247128T1 (de) | 1993-09-03 | 2003-08-15 | Isis Pharmaceuticals Inc | Aminoderivatisierte nukleoside und oligonukleoside |
| US5491084A (en) | 1993-09-10 | 1996-02-13 | The Trustees Of Columbia University In The City Of New York | Uses of green-fluorescent protein |
| US5502177A (en) | 1993-09-17 | 1996-03-26 | Gilead Sciences, Inc. | Pyrimidine derivatives for labeled binding partners |
| US6184211B1 (en) | 1993-11-30 | 2001-02-06 | Methylgene Inc. | Inhibition of DNA methyltransferase |
| US5457187A (en) | 1993-12-08 | 1995-10-10 | Board Of Regents University Of Nebraska | Oligonucleotides containing 5-fluorouracil |
| DE69425903T2 (de) | 1993-12-09 | 2001-02-15 | Thomas Jefferson University Ph | Verbindungen und verfahren zur ortsspezifischen mutation in eukaryotischen zellen |
| US5446137B1 (en) | 1993-12-09 | 1998-10-06 | Behringwerke Ag | Oligonucleotides containing 4'-substituted nucleotides |
| US5595756A (en) | 1993-12-22 | 1997-01-21 | Inex Pharmaceuticals Corporation | Liposomal compositions for enhanced retention of bioactive agents |
| US5519134A (en) | 1994-01-11 | 1996-05-21 | Isis Pharmaceuticals, Inc. | Pyrrolidine-containing monomers and oligomers |
| US5593853A (en) | 1994-02-09 | 1997-01-14 | Martek Corporation | Generation and screening of synthetic drug libraries |
| JPH10501681A (ja) | 1994-02-22 | 1998-02-17 | ダナ−ファーバー キャンサー インスティチュート | 核酸送達システムならびにその合成および使用方法 |
| US5539083A (en) | 1994-02-23 | 1996-07-23 | Isis Pharmaceuticals, Inc. | Peptide nucleic acid combinatorial libraries and improved methods of synthesis |
| US6015880A (en) | 1994-03-16 | 2000-01-18 | California Institute Of Technology | Method and substrate for performing multiple sequential reactions on a matrix |
| US5596091A (en) | 1994-03-18 | 1997-01-21 | The Regents Of The University Of California | Antisense oligonucleotides comprising 5-aminoalkyl pyrimidine nucleotides |
| US5627053A (en) | 1994-03-29 | 1997-05-06 | Ribozyme Pharmaceuticals, Inc. | 2'deoxy-2'-alkylnucleotide containing nucleic acid |
| US5625050A (en) | 1994-03-31 | 1997-04-29 | Amgen Inc. | Modified oligonucleotides and intermediates useful in nucleic acid therapeutics |
| US5525711A (en) | 1994-05-18 | 1996-06-11 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Pteridine nucleotide analogs as fluorescent DNA probes |
| US5807522A (en) | 1994-06-17 | 1998-09-15 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for fabricating microarrays of biological samples |
| US5543152A (en) | 1994-06-20 | 1996-08-06 | Inex Pharmaceuticals Corporation | Sphingosomes for enhanced drug delivery |
| US5525735A (en) | 1994-06-22 | 1996-06-11 | Affymax Technologies Nv | Methods for synthesizing diverse collections of pyrrolidine compounds |
| US5549974A (en) | 1994-06-23 | 1996-08-27 | Affymax Technologies Nv | Methods for the solid phase synthesis of thiazolidinones, metathiazanones, and derivatives thereof |
| US5597696A (en) | 1994-07-18 | 1997-01-28 | Becton Dickinson And Company | Covalent cyanine dye oligonucleotide conjugates |
| US5597909A (en) | 1994-08-25 | 1997-01-28 | Chiron Corporation | Polynucleotide reagents containing modified deoxyribose moieties, and associated methods of synthesis and use |
| US5580731A (en) | 1994-08-25 | 1996-12-03 | Chiron Corporation | N-4 modified pyrimidine deoxynucleotides and oligonucleotide probes synthesized therewith |
| US5591721A (en) | 1994-10-25 | 1997-01-07 | Hybridon, Inc. | Method of down-regulating gene expression |
| US6645943B1 (en) | 1994-10-25 | 2003-11-11 | Hybridon, Inc. | Method of down-regulating gene expression |
| US5512295A (en) | 1994-11-10 | 1996-04-30 | The Board Of Trustees Of The Leland Stanford Junior University | Synthetic liposomes for enhanced uptake and delivery |
| FR2727867B1 (fr) | 1994-12-13 | 1997-01-31 | Rhone Poulenc Rorer Sa | Transfert de genes dans les motoneurones medullaires au moyen de vecteurs adenoviraux |
| DE19502912A1 (de) | 1995-01-31 | 1996-08-01 | Hoechst Ag | G-Cap Stabilisierte Oligonucleotide |
| IT1275862B1 (it) | 1995-03-03 | 1997-10-24 | Consiglio Nazionale Ricerche | Trascritto antisenso associato ad alcuni tipi di cellule tumorali ed oligodeossinucleotidi sintetici utili nella diagnosi e nel trattamento |
| US5543165A (en) | 1995-06-06 | 1996-08-06 | Hill; Julie B. | Process of making a soluble tea product with champagne-like properties |
| US5569588A (en) | 1995-08-09 | 1996-10-29 | The Regents Of The University Of California | Methods for drug screening |
| US5652356A (en) | 1995-08-17 | 1997-07-29 | Hybridon, Inc. | Inverted chimeric and hybrid oligonucleotides |
| JP4293636B2 (ja) | 1996-02-14 | 2009-07-08 | アイシス・ファーマシューティカルス・インコーポレーテッド | 糖修飾ギャップ付オリゴヌクレオチド |
| IL125839A0 (en) | 1996-03-14 | 1999-04-11 | Genentech Inc | Uses of gdnf and gdnf receptor |
| CA2251945A1 (en) | 1996-04-17 | 1997-10-23 | Aronex Pharmaceuticals, Inc. | Antisense inhibitors of vascular endothelial growth factor (vefg/vpf) expression |
| JPH10212241A (ja) | 1996-05-27 | 1998-08-11 | Sumitomo Pharmaceut Co Ltd | Bdnfを安定に含有する製剤 |
| US5898031A (en) | 1996-06-06 | 1999-04-27 | Isis Pharmaceuticals, Inc. | Oligoribonucleotides for cleaving RNA |
| US7008776B1 (en) | 1996-12-06 | 2006-03-07 | Aventis Pharmaceuticals Inc. | Compositions and methods for effecting the levels of high density lipoprotein (HDL) cholesterol and apolipoprotein AI very low density lipoprotein (VLDL) cholesterol and low density lipoprotein (LDL) cholesterol |
| US7235653B2 (en) | 1996-12-31 | 2007-06-26 | Isis Pharmaceuticals, Inc. | Oligonucleotide compositions and methods for the modulation of the expression of B7 protein |
| JP3756313B2 (ja) | 1997-03-07 | 2006-03-15 | 武 今西 | 新規ビシクロヌクレオシド及びオリゴヌクレオチド類縁体 |
| US6221586B1 (en) * | 1997-04-09 | 2001-04-24 | California Institute Of Technology | Electrochemical sensor using intercalative, redox-active moieties |
| CA2303299C (en) | 1997-09-12 | 2016-02-23 | Exiqon A/S | Oligonucleotide analogues |
| US7572582B2 (en) | 1997-09-12 | 2009-08-11 | Exiqon A/S | Oligonucleotide analogues |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| US7285288B1 (en) | 1997-10-03 | 2007-10-23 | Board Of Regents, The University Of Texas System | Inhibition of Bcl-2 protein expression by liposomal antisense oligodeoxynucleotides |
| US6034883A (en) | 1998-01-29 | 2000-03-07 | Tinney; Charles E. | Solid state director for beams |
| US6175409B1 (en) | 1999-04-02 | 2001-01-16 | Symyx Technologies, Inc. | Flow-injection analysis and variable-flow light-scattering methods and apparatus for characterizing polymers |
| US7321828B2 (en) | 1998-04-13 | 2008-01-22 | Isis Pharmaceuticals, Inc. | System of components for preparing oligonucleotides |
| US20040186071A1 (en) | 1998-04-13 | 2004-09-23 | Bennett C. Frank | Antisense modulation of CD40 expression |
| US6221587B1 (en) | 1998-05-12 | 2001-04-24 | Isis Pharmceuticals, Inc. | Identification of molecular interaction sites in RNA for novel drug discovery |
| US6833361B2 (en) | 1998-05-26 | 2004-12-21 | Ribapharm, Inc. | Nucleosides having bicyclic sugar moiety |
| NZ507913A (en) | 1998-05-26 | 2003-02-28 | Icn Pharmaceuticals | Novel nucleosides having bicyclic sugar moiety |
| US20030139359A1 (en) | 2001-12-04 | 2003-07-24 | Isis Pharmaceuticals Inc. | Antisense modulation of phospholipid scramblase 3 expression |
| US6242589B1 (en) | 1998-07-14 | 2001-06-05 | Isis Pharmaceuticals, Inc. | Phosphorothioate oligonucleotides having modified internucleoside linkages |
| US6867294B1 (en) | 1998-07-14 | 2005-03-15 | Isis Pharmaceuticals, Inc. | Gapped oligomers having site specific chiral phosphorothioate internucleoside linkages |
| US6214986B1 (en) | 1998-10-07 | 2001-04-10 | Isis Pharmaceuticals, Inc. | Antisense modulation of bcl-x expression |
| WO2000027424A2 (en) | 1998-11-06 | 2000-05-18 | Alcon Laboratories, Inc. | Upregulation of endogenous prostaglandins to lower intraocular pressure |
| ATE300959T1 (de) | 1999-01-27 | 2005-08-15 | Becker David Dr | Formulierungen enthaltend antisense nukleotide spezifisch für connexine |
| EP1152009B2 (en) | 1999-02-12 | 2017-09-06 | Daiichi Sankyo Company, Limited | Novel nucleosides and oligonucleotide analogues |
| ATE385237T1 (de) | 1999-02-26 | 2008-02-15 | Univ British Columbia | Antisense-therapie für trpm-2 |
| JP4726302B2 (ja) | 1999-03-15 | 2011-07-20 | ユニバーシティ オブ ブリティッシュ コロンビア | Abc1ポリペプチドおよびコレステロール水準を調節する方法と試薬 |
| US20040137423A1 (en) | 1999-03-15 | 2004-07-15 | Hayden Michael R. | Compositions and methods for modulating HDL cholesterol and triglyceride levels |
| US7084125B2 (en) | 1999-03-18 | 2006-08-01 | Exiqon A/S | Xylo-LNA analogues |
| ATE501269T1 (de) | 1999-03-18 | 2011-03-15 | Exiqon As | Detektion von genmutationen mittels lna primer |
| ATE332909T1 (de) | 1999-03-24 | 2006-08-15 | Exiqon As | Verbesserte synthese für 2.2.1.öbicyclo- nukleoside |
| US6734291B2 (en) | 1999-03-24 | 2004-05-11 | Exiqon A/S | Synthesis of [2.2.1]bicyclo nucleosides |
| AU776684B2 (en) | 1999-03-26 | 2004-09-16 | Aventis Pharmaceuticals Inc. | Compositions and methods for effecting the levels of high density lipoprotein (HDL) cholesterol and apolipoprotein AI, very low density lipoprotein (VLDL) cholesterol and low density lipoprotein (LDL) cholesterol |
| US5998148A (en) | 1999-04-08 | 1999-12-07 | Isis Pharmaceuticals Inc. | Antisense modulation of microtubule-associated protein 4 expression |
| AU4077100A (en) | 1999-04-08 | 2000-11-14 | Chiron Corporation | Enhancement of the immune response for vaccine and gene therapy applications |
| WO2000063365A1 (en) | 1999-04-21 | 2000-10-26 | Pangene Corporation | Locked nucleic acid hybrids and methods of use |
| ATE356824T1 (de) | 1999-05-04 | 2007-04-15 | Santaris Pharma As | L-ribo-lna analoge |
| US6525191B1 (en) | 1999-05-11 | 2003-02-25 | Kanda S. Ramasamy | Conformationally constrained L-nucleosides |
| DE19925073C2 (de) | 1999-06-01 | 2001-07-19 | Stefan Weiss | Nucleinsäuremoleküle mit spezifischer Erkennung von nativem PrP·S··c·, Herstellung und Verwendung |
| US6656730B1 (en) | 1999-06-15 | 2003-12-02 | Isis Pharmaceuticals, Inc. | Oligonucleotides conjugated to protein-binding drugs |
| EP1189940A2 (en) | 1999-06-25 | 2002-03-27 | Genset | A bap28 gene and protein |
| US20040006031A1 (en) | 2002-07-02 | 2004-01-08 | Isis Pharmaceuticals Inc. | Antisense modulation of HMG-CoA reductase expression |
| EP1218411A4 (en) | 1999-09-20 | 2004-09-01 | Millennium Pharm Inc | SECRETED PROTEINS AND THEIR USES |
| US6617442B1 (en) | 1999-09-30 | 2003-09-09 | Isis Pharmaceuticals, Inc. | Human Rnase H1 and oligonucleotide compositions thereof |
| AU7863200A (en) | 1999-10-06 | 2001-05-10 | Quark Biotech, Inc. | Method for enrichment of natural antisense messenger rna |
| US6986988B2 (en) | 1999-10-06 | 2006-01-17 | Quark Biotech, Inc. | Method for enrichment of natural antisense messenger RNA |
| WO2001051630A1 (en) | 2000-01-07 | 2001-07-19 | Baylor University | Antisense compositions and methods |
| ATE336492T1 (de) | 2000-01-14 | 2006-09-15 | Us Gov Health & Human Serv | Methonocarbacycloalkylanaloga von nucleosiden |
| US6303374B1 (en) | 2000-01-18 | 2001-10-16 | Isis Pharmaceuticals Inc. | Antisense modulation of caspase 3 expression |
| US20020055479A1 (en) | 2000-01-18 | 2002-05-09 | Cowsert Lex M. | Antisense modulation of PTP1B expression |
| US6287860B1 (en) | 2000-01-20 | 2001-09-11 | Isis Pharmaceuticals, Inc. | Antisense inhibition of MEKK2 expression |
| JP2001247459A (ja) | 2000-03-03 | 2001-09-11 | Oakland Uniservices Ltd | 癌の組み合わせ療法 |
| MXPA02009627A (es) | 2000-03-27 | 2004-05-14 | Univ Delaware | Modificaciones genomicas cromosomicas selectivas con oligonucleotidos modificados de un solo filamento.. |
| US6936467B2 (en) | 2000-03-27 | 2005-08-30 | University Of Delaware | Targeted chromosomal genomic alterations with modified single stranded oligonucleotides |
| US7402434B2 (en) | 2000-05-08 | 2008-07-22 | Newman Stuart A | Splice choice antagonists as therapeutic agents |
| US6713276B2 (en) | 2000-06-28 | 2004-03-30 | Scios, Inc. | Modulation of Aβ levels by β-secretase BACE2 |
| JP2004530420A (ja) | 2000-06-29 | 2004-10-07 | ファーマ パシフィック プロプライエタリー リミテッド | インターフェロン−α誘導性遺伝子 |
| AU2001282717A1 (en) | 2000-07-28 | 2002-02-13 | Cancer Research Technology Limited | Cancer treatment by combination therapy |
| EP1314734A1 (en) | 2000-08-29 | 2003-05-28 | Takeshi Imanishi | Novel nucleoside analogs and oligonucleotide derivatives containing these analogs |
| US20030190635A1 (en) | 2002-02-20 | 2003-10-09 | Mcswiggen James A. | RNA interference mediated treatment of Alzheimer's disease using short interfering RNA |
| US20050209179A1 (en) | 2000-08-30 | 2005-09-22 | Sirna Therapeutics, Inc. | RNA interference mediated treatment of Alzheimer's disease using short interfering nucleic acid (siNA) |
| HUP0301805A3 (en) | 2000-09-02 | 2005-12-28 | Gruenenthal Gmbh | Antisense oligonucleotides against vanilloid receptor 1 |
| US6444464B1 (en) | 2000-09-08 | 2002-09-03 | Isis Pharmaceuticals, Inc. | Antisense modulation of E2F transcription factor 2 expression |
| AU2001289085A1 (en) | 2000-09-20 | 2002-04-02 | Isis Pharmaceuticals, Inc. | Antisense modulation of flip-c expression |
| EP1325121A2 (en) | 2000-10-13 | 2003-07-09 | Institut de Cardiologie de Montreal | Antisense oligonucleotide directed toward mammalian vegf receptor genes and uses thereof |
| US20020157122A1 (en) | 2000-10-27 | 2002-10-24 | Wong Philip C. | Beta-secretase transgenic organisms, anti-beta-secretase antibodies, and methods of use thereof |
| US20030228618A1 (en) | 2000-11-24 | 2003-12-11 | Erez Levanon | Methods and systems for identifying naturally occurring antisense transcripts and methods, kits and arrays utilizing same |
| CZ308053B6 (cs) | 2000-12-01 | 2019-11-27 | Max Planck Gesellschaft | Izolovaná molekula dvouřetězcové RNA, způsob její výroby a její použití |
| US20050222029A1 (en) | 2001-01-04 | 2005-10-06 | Myriad Genetics, Incorporated | Compositions and methods for treating diseases |
| US7423142B2 (en) | 2001-01-09 | 2008-09-09 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of anti-apoptotic genes |
| US20040175803A1 (en) | 2001-02-20 | 2004-09-09 | Jean-Francois Meritet | Interferon-alpha induced gene |
| US20020147165A1 (en) | 2001-02-22 | 2002-10-10 | Isis Pharmaceuticals, Inc. | Antisense modulation of calreticulin expression |
| US20070021360A1 (en) | 2001-04-24 | 2007-01-25 | Nyce Jonathan W | Compositions, formulations and kit with anti-sense oligonucleotide and anti-inflammatory steroid and/or obiquinone for treatment of respiratory and lung disesase |
| AUPR497101A0 (en) | 2001-05-14 | 2001-06-07 | Queensland University Of Technology | Polynucleotides and polypeptides linked to cancer and/or tumorigenesi |
| IL143379A (en) | 2001-05-24 | 2013-11-28 | Yissum Res Dev Co | Oligonucleotide against human ache isoform r and its uses |
| US7053195B1 (en) | 2001-06-12 | 2006-05-30 | Syngenta Participatious Ag | Locked nucleic acid containing heteropolymers and related methods |
| US20050019915A1 (en) | 2001-06-21 | 2005-01-27 | Bennett C. Frank | Antisense modulation of superoxide dismutase 1, soluble expression |
| US7153954B2 (en) | 2001-07-12 | 2006-12-26 | Santaris Pharma A/S | Method for preparation of LNA phosphoramidites |
| EP2345720A3 (en) | 2001-07-12 | 2012-01-25 | University of Massachusetts | In vivo production of small interfering RNAs that mediate gene silencing |
| US7425545B2 (en) | 2001-07-25 | 2008-09-16 | Isis Pharmaceuticals, Inc. | Modulation of C-reactive protein expression |
| US20030096772A1 (en) | 2001-07-30 | 2003-05-22 | Crooke Rosanne M. | Antisense modulation of acyl CoA cholesterol acyltransferase-2 expression |
| US7259150B2 (en) | 2001-08-07 | 2007-08-21 | Isis Pharmaceuticals, Inc. | Modulation of apolipoprotein (a) expression |
| EP1446412B1 (en) | 2001-09-04 | 2012-03-07 | Exiqon A/S | Novel lna compositions and uses thereof |
| US6936589B2 (en) | 2001-09-28 | 2005-08-30 | Albert T. Naito | Parenteral delivery systems |
| US20040214766A1 (en) | 2001-10-01 | 2004-10-28 | Kari Alitalo | VEGF-C or VEGF-D materials and methods for treatment of neuropathologies |
| AU2002333434B2 (en) | 2001-10-10 | 2007-12-13 | Societe Des Produits Nestle S.A. | Coffee plant with reduced alpha-D-galactosidase activity |
| AR037699A1 (es) | 2001-12-04 | 2004-12-01 | Monsanto Technology Llc | Maiz transgenico con fenotipo mejorado |
| US7125982B1 (en) | 2001-12-05 | 2006-10-24 | Frayne Consultants | Microbial production of nuclease resistant DNA, RNA, and oligo mixtures |
| US6965025B2 (en) | 2001-12-10 | 2005-11-15 | Isis Pharmaceuticals, Inc. | Antisense modulation of connective tissue growth factor expression |
| CA2365811A1 (en) | 2001-12-21 | 2003-06-21 | Institut De Cardiologie | A new gene therapy using antisense strategy to estrogen receptors (er .alpha. and/or er .beta.) to optimize vascular healing and cardioprotection after vascular injury |
| KR20030056538A (ko) | 2001-12-28 | 2003-07-04 | 주식회사 웰진 | 리본형 안티센스 올리고뉴클레오티드에 의한 형질전이성장 인자-β1의 효과적 저해제 개발 |
| US20030191075A1 (en) | 2002-02-22 | 2003-10-09 | Cook Phillip Dan | Method of using modified oligonucleotides for hepatic delivery |
| AU2003212729A1 (en) | 2002-02-25 | 2003-09-09 | Gunnar Norstedt | Vitamin d upregulated protein 1 (vdup-1) methods and uses thereof |
| US20040138156A1 (en) | 2002-02-26 | 2004-07-15 | Schneider Michael C | Therapeutic regulation of deoxyribonuclease-1-like-3 activity |
| WO2003077215A2 (en) | 2002-03-08 | 2003-09-18 | Glen Research Corporation | Fluorescent nitrogenous base and nucleosides incorporating same |
| GB2386836B (en) | 2002-03-22 | 2006-07-26 | Cancer Res Ventures Ltd | Anti-cancer combinations |
| US7169916B2 (en) | 2002-04-01 | 2007-01-30 | Isis Pharmaceuticals, Inc. | Chloral-free DCA in oligonucleotide synthesis |
| US20050215504A1 (en) | 2002-04-02 | 2005-09-29 | Bennett C F | Antisense modulation of sterol regulatory element-binding protein-1 expression |
| WO2003085110A2 (en) | 2002-04-05 | 2003-10-16 | Santaris Pharma A/S | Oligomeric compounds for the modulation hif-1alpha expression |
| US6808906B2 (en) | 2002-05-08 | 2004-10-26 | Rigel Pharmaceuticals, Inc. | Directionally cloned random cDNA expression vector libraries, compositions and methods of use |
| US7569575B2 (en) | 2002-05-08 | 2009-08-04 | Santaris Pharma A/S | Synthesis of locked nucleic acid derivatives |
| US7199107B2 (en) | 2002-05-23 | 2007-04-03 | Isis Pharmaceuticals, Inc. | Antisense modulation of kinesin-like 1 expression |
| US7148342B2 (en) | 2002-07-24 | 2006-12-12 | The Trustees Of The University Of Pennyslvania | Compositions and methods for sirna inhibition of angiogenesis |
| US20040033480A1 (en) | 2002-08-15 | 2004-02-19 | Wong Norman C.W. | Use of resveratrol to regulate expression of apolipoprotein A1 |
| WO2004024079A2 (en) | 2002-09-10 | 2004-03-25 | The Samuel Roberts Noble Foundation, Inc. | Methods and compositions for production of flavonoid and isoflavonoid nutraceuticals |
| EP1549387A1 (en) | 2002-09-25 | 2005-07-06 | Pharmacia Corporation | Antisense modulation of farnesoid x receptor expression |
| EP1549767A4 (en) | 2002-09-26 | 2006-06-07 | Amgen Inc | MODULATION OF FORKHEAD BOX O1A GENE EXPRESSION |
| AU2003291678B2 (en) | 2002-11-01 | 2009-01-15 | The Trustees Of The University Of Pennsylvania | Compositions and methods for siRNA inhibition of HIF-1 alpha |
| GB2394658A (en) | 2002-11-01 | 2004-05-05 | Cancer Rec Tech Ltd | Oral anti-cancer composition |
| AU2003261405A1 (en) | 2002-11-01 | 2004-06-07 | University Of Massachusetts | Regulation of transcription elongation factors |
| AU2003291753B2 (en) | 2002-11-05 | 2010-07-08 | Isis Pharmaceuticals, Inc. | Polycyclic sugar surrogate-containing oligomeric compounds and compositions for use in gene modulation |
| EP1578765A4 (en) | 2002-11-05 | 2008-04-23 | Isis Pharmaceuticals Inc | OLIGOMERIC COMPOUNDS CONTAINING SUGAR SUBSTITUTE AND COMPOSITIONS FOR USE IN GENE MODULATION |
| US20060009410A1 (en) | 2002-11-13 | 2006-01-12 | Crooke Rosanne M | Effects of apolipoprotein B inhibition on gene expression profiles in animals |
| DK2752488T3 (da) | 2002-11-18 | 2020-04-20 | Roche Innovation Ct Copenhagen As | Antisense-design |
| US7144999B2 (en) | 2002-11-23 | 2006-12-05 | Isis Pharmaceuticals, Inc. | Modulation of hypoxia-inducible factor 1 alpha expression |
| US20050048641A1 (en) | 2002-11-26 | 2005-03-03 | Medtronic, Inc. | System and method for delivering polynucleotides to the central nervous system |
| EP1589988A2 (en) | 2002-12-20 | 2005-11-02 | Neuronicon ApS | Modulation of activity of neurotrophins |
| US7713738B2 (en) | 2003-02-10 | 2010-05-11 | Enzon Pharmaceuticals, Inc. | Oligomeric compounds for the modulation of survivin expression |
| US7598227B2 (en) | 2003-04-16 | 2009-10-06 | Isis Pharmaceuticals Inc. | Modulation of apolipoprotein C-III expression |
| US7339051B2 (en) | 2003-04-28 | 2008-03-04 | Isis Pharmaceuticals, Inc. | Compositions and methods for the treatment of severe acute respiratory syndrome (SARS) |
| WO2004108081A2 (en) | 2003-06-02 | 2004-12-16 | Isis Pharmaceuticals, Inc. | Oligonucleotide synthesis with alternative solvents |
| WO2005002507A2 (en) | 2003-06-03 | 2005-01-13 | Isis Pharmaceuticals, Inc. | Modulation of survivin expression |
| US7825235B2 (en) | 2003-08-18 | 2010-11-02 | Isis Pharmaceuticals, Inc. | Modulation of diacylglycerol acyltransferase 2 expression |
| EP2182063A3 (en) | 2003-09-18 | 2012-07-18 | Isis Pharmaceuticals, Inc. | Modulation of EIF4E expression |
| EP1687410A4 (en) | 2003-10-07 | 2008-04-09 | Isis Pharmaceuticals Inc | ANTISENSE OLIGONUCLEOTIDES OPTIMIZED TO TARGET THE KIDNEY |
| WO2005045034A2 (en) | 2003-10-23 | 2005-05-19 | Sirna Therapeutics, Inc. | RNA INTERFERENCE MEDIATED TREATMENT OF PARKINSON DISEASE USING SHORT INTERERING NUCLEIC ACID (siNA) |
| US7622453B2 (en) | 2003-12-23 | 2009-11-24 | Santaris Pharma A/S | Oligomeric compounds for the modulation of Bcl-2 |
| EP1716228A4 (en) | 2004-01-12 | 2009-06-17 | Univ Pennsylvania | A SYSTEM AND METHOD FOR HIGH-REGULATING BMP (BONE MORPHOGENETIC PROTEIN) GENE EXPRESSION IN BONE CELLS THROUGH THE APPLICATION OF FIELDS PRODUCED BY SPECIFIC AND SELECTIVE ELECTRICAL AND ELECTROMAGNETIC SIGNALS |
| US7468431B2 (en) | 2004-01-22 | 2008-12-23 | Isis Pharmaceuticals, Inc. | Modulation of eIF4E-BP2 expression |
| GB0403041D0 (en) | 2004-02-11 | 2004-03-17 | Milner Anne J | Induction of apoptosis |
| EP1566202A1 (en) | 2004-02-23 | 2005-08-24 | Sahltech I Göteborg AB | Use of resistin antagonists in the treatment of rheumatoid arthritis |
| US7402574B2 (en) | 2004-03-12 | 2008-07-22 | Avi Biopharma, Inc. | Antisense composition and method for treating cancer |
| US8394947B2 (en) | 2004-06-03 | 2013-03-12 | Isis Pharmaceuticals, Inc. | Positionally modified siRNA constructs |
| WO2006085987A2 (en) | 2004-07-09 | 2006-08-17 | University Of Iowa Research Foundation | Rna interference in respiratory epitheial cells |
| WO2006023880A2 (en) | 2004-08-23 | 2006-03-02 | Isis Pharmaceuticals, Inc. | Compounds and methods for the characterization of oligonucleotides |
| EP1802350A4 (en) * | 2004-10-22 | 2009-02-18 | Univ Laval | MODULATION OF NEUROTROPHIC BRAIN DERIVED FACTOR (BDNF) FROM NEVERROGIA IN THE TREATMENT AND PREVENTION OF PAIN |
| MX2007005558A (es) | 2004-11-09 | 2008-01-31 | Santaris Pharma As | Oligonucleotidos de lna potentes para la inhibicion dela expresion de hif-1a. |
| US7220549B2 (en) | 2004-12-30 | 2007-05-22 | Helicos Biosciences Corporation | Stabilizing a nucleic acid for nucleic acid sequencing |
| AU2006261732B2 (en) | 2005-06-27 | 2011-09-15 | Alnylam Pharmaceuticals, Inc. | RNAi modulation of HIF-1 and theraputic uses thereof |
| US20070213292A1 (en) | 2005-08-10 | 2007-09-13 | The Rockefeller University | Chemically modified oligonucleotides for use in modulating micro RNA and uses thereof |
| EP1937312B1 (en) | 2005-08-30 | 2016-06-29 | Ionis Pharmaceuticals, Inc. | Chimeric oligomeric compounds for modulation of splicing |
| AU2006305886C1 (en) | 2005-10-28 | 2011-03-17 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of huntingtin gene |
| RU2448974C2 (ru) * | 2005-11-01 | 2012-04-27 | Элнилэм Фармасьютикалз, Инк. | РНКи-ИНГИБИРОВАНИЕ РЕПЛИКАЦИИ ВИРУСА ГРИППА |
| EP1942948A4 (en) | 2005-11-04 | 2010-03-03 | Alnylam Pharmaceuticals Inc | COMPOSITIONS AND METHODS FOR INHIBITING THE EXPRESSION OF THE NAV1.8 GENE |
| US7709456B2 (en) | 2005-11-17 | 2010-05-04 | Board Of Regents, The University Of Texas System | Modulation of gene expression by oligomers targeted to chromosomal DNA |
| WO2007102861A2 (en) | 2005-12-02 | 2007-09-13 | Sirtris Pharmaceuticals, Inc. | Modulators of cdc2-like kinases (clks) and methods of use thereof |
| US20070213274A1 (en) | 2005-12-20 | 2007-09-13 | Oy Jurilab Ltd | Novel genes and markers associated with high-density lipoprotein-cholesterol (HDL-C) |
| CN100356377C (zh) | 2005-12-20 | 2007-12-19 | 无锡永中科技有限公司 | 文档显示方法 |
| CN101437933B (zh) | 2005-12-28 | 2013-11-06 | 斯克里普斯研究所 | 作为药物靶标的天然反义和非编码的rna转录物 |
| EP2314594B1 (en) | 2006-01-27 | 2014-07-23 | Isis Pharmaceuticals, Inc. | 6-modified bicyclic nucleic acid analogs |
| US7569686B1 (en) | 2006-01-27 | 2009-08-04 | Isis Pharmaceuticals, Inc. | Compounds and methods for synthesis of bicyclic nucleic acid analogs |
| KR101547579B1 (ko) | 2006-03-31 | 2015-08-27 | 알닐람 파마슈티칼스 인코포레이티드 | Eg5 유전자의 발현을 억제하는 이본쇄 리보핵산 |
| US20090326041A1 (en) | 2006-05-05 | 2009-12-31 | Isis Pharmaceuticals, Inc. | Compounds and methods for modulating expression of sglt2 |
| DK2066684T3 (da) | 2006-05-11 | 2012-10-22 | Isis Pharmaceuticals Inc | 5´-Modificerede bicycliske nukleinsyreanaloge |
| US7666854B2 (en) | 2006-05-11 | 2010-02-23 | Isis Pharmaceuticals, Inc. | Bis-modified bicyclic nucleic acid analogs |
| WO2007134161A2 (en) | 2006-05-11 | 2007-11-22 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of the pcsk9 gene |
| EP1867338A1 (en) | 2006-05-30 | 2007-12-19 | Université Libre De Bruxelles | Pharmaceutical composition comprising apolipoproteins for the treatment of human diseases |
| WO2008066672A2 (en) | 2006-11-06 | 2008-06-05 | Beth Israel Deaconess Medical Center | Identification and use of small molecules to modulate transcription factor function and to treat transcription factor associated diseases |
| WO2008057556A2 (en) | 2006-11-06 | 2008-05-15 | Beth Israel Deaconess Medical Center | Identification and use of small molecules to modulate ese-1 transcription factor function and to treat ese-1 transcription factor associated diseases |
| US8093222B2 (en) | 2006-11-27 | 2012-01-10 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| EP2121939B1 (en) | 2007-01-19 | 2013-12-04 | Plant Bioscience Limited | Methods for modulating the sirna and rna-directed-dna methylation pathways |
| US20080234197A1 (en) | 2007-03-19 | 2008-09-25 | Undurti N Das | Method(s) of stabilizing and potentiating the actions and administration of brain-derived neurotrophic factor (BDNF) |
| CA2686933A1 (en) | 2007-04-06 | 2008-10-16 | The Johns Hopkins University | Methods and compositions for the treatment of cancer |
| US20080293142A1 (en) | 2007-04-19 | 2008-11-27 | The Board Of Regents For Oklahoma State University | Multiple shRNA Expression Vectors and Methods of Construction |
| US20090214637A1 (en) | 2007-10-30 | 2009-08-27 | Neurologix, Inc. | Novel Gene Therapy Approach For Treating The Metabolic Disorder Obesity |
| CA2704418A1 (en) | 2007-10-30 | 2009-05-07 | Neurologix, Inc. | A novel gene therapy approach for treating the metabolic disorder obesity |
| WO2009120978A2 (en) | 2008-03-27 | 2009-10-01 | The Ohio State University | Treatment of metabolic-related disorders using hypothalamic gene transfer of bdnf and compositions therfor |
| EP2924118A1 (en) | 2008-07-01 | 2015-09-30 | Monsanto Technology LLC | Recombinant DNA constructs and methods for modulating expression of a target gene |
| JP6128732B2 (ja) | 2008-10-03 | 2017-05-17 | クルナ・インコーポレーテッド | アポリポタンパク質−a1に対する天然アンチセンス転写物の抑制によるアポリポタンパク質−a1関連疾患の治療 |
| EP2177615A1 (en) | 2008-10-10 | 2010-04-21 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Method for a genome wide identification of expression regulatory sequences and use of genes and molecules derived thereof for the diagnosis and therapy of metabolic and/or tumorous diseases |
| US20110274718A1 (en) | 2008-10-29 | 2011-11-10 | The Ohio State University | System for Modulating Expression of Hypothalmic Brain-Derived Neurotrophic Factor (BDNF) |
| US8606289B2 (en) | 2008-11-10 | 2013-12-10 | Qualcomm Incorporated | Power headroom-sensitive scheduling |
| EP2358382A2 (en) | 2008-11-22 | 2011-08-24 | The University of Bristol | NOVEL USES OF VEGFxxxB |
| PL2396038T3 (pl) | 2009-02-12 | 2016-05-31 | Curna Inc | Leczenie chorób związanych z neurotropowym czynnikiem pochodzenia mózgowego (bdnf) poprzez zahamowanie naturalnego antysensownego transkryptu bdnf |
| KR101138048B1 (ko) | 2009-11-06 | 2012-04-23 | 성균관대학교산학협력단 | Bdnf의 발현을 증가시키는 신규 펩타이드 및 이를 포함하는 알츠하이머병 또는 파킨슨병의 예방 및 치료용 약학 조성물 |
| US10000752B2 (en) | 2010-11-18 | 2018-06-19 | Curna, Inc. | Antagonat compositions and methods of use |
| US9209196B2 (en) | 2011-11-30 | 2015-12-08 | Sharp Kabushiki Kaisha | Memory circuit, method of driving the same, nonvolatile storage device using the same, and liquid crystal display device |
| US20150031750A1 (en) | 2012-03-15 | 2015-01-29 | The Scripps Research Institute | Treatment of brain derived neurotrophic factor (bdnf) related diseases by inhibition of natural antisense transcript to bdnf |
-
2013
- 2013-03-12 US US14/384,659 patent/US20150031750A1/en not_active Abandoned
- 2013-03-12 PT PT13712635T patent/PT2825648T/pt unknown
- 2013-03-12 PL PL13712635T patent/PL2825648T3/pl unknown
- 2013-03-12 RU RU2014140112A patent/RU2661104C2/ru active
- 2013-03-12 JP JP2015500527A patent/JP2015511494A/ja active Pending
- 2013-03-12 EP EP13712635.5A patent/EP2825648B1/en active Active
- 2013-03-12 DK DK13712635.5T patent/DK2825648T3/en active
- 2013-03-12 WO PCT/US2013/030589 patent/WO2013138374A2/en active Application Filing
- 2013-03-12 CA CA2867262A patent/CA2867262C/en active Active
- 2013-03-12 CN CN201910388967.4A patent/CN110438125A/zh active Pending
- 2013-03-12 TR TR2018/15503T patent/TR201815503T4/tr unknown
- 2013-03-12 CN CN201380024874.4A patent/CN104583405A/zh not_active Withdrawn
- 2013-03-12 KR KR1020147028058A patent/KR20140136488A/ko not_active Application Discontinuation
- 2013-03-12 ES ES13712635.5T patent/ES2694592T3/es active Active
- 2013-03-12 HU HUE13712635A patent/HUE040179T2/hu unknown
-
2015
- 2015-10-29 HK HK15110742.3A patent/HK1210211A1/xx unknown
-
2017
- 2017-01-04 US US15/398,630 patent/US10214745B2/en active Active
-
2018
- 2018-01-31 JP JP2018016012A patent/JP6738841B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2015511494A (ja) | 2015-04-20 |
| PL2825648T3 (pl) | 2019-01-31 |
| HK1210211A1 (en) | 2016-04-15 |
| US10214745B2 (en) | 2019-02-26 |
| RU2661104C2 (ru) | 2018-07-11 |
| RU2014140112A (ru) | 2016-05-10 |
| WO2013138374A3 (en) | 2013-12-12 |
| PT2825648T (pt) | 2018-11-09 |
| CA2867262A1 (en) | 2013-09-19 |
| US20170211071A1 (en) | 2017-07-27 |
| JP2018110582A (ja) | 2018-07-19 |
| EP2825648A2 (en) | 2015-01-21 |
| ES2694592T3 (es) | 2018-12-21 |
| HUE040179T2 (hu) | 2019-02-28 |
| CA2867262C (en) | 2021-03-16 |
| WO2013138374A2 (en) | 2013-09-19 |
| US20150031750A1 (en) | 2015-01-29 |
| CN104583405A (zh) | 2015-04-29 |
| DK2825648T3 (en) | 2018-10-15 |
| JP6738841B2 (ja) | 2020-08-12 |
| TR201815503T4 (tr) | 2018-11-21 |
| CN110438125A (zh) | 2019-11-12 |
| EP2825648B1 (en) | 2018-09-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6738841B2 (ja) | 脳由来神経栄養因子(bdnf)に対する天然アンチセンス転写物の阻害によるbdnf関連の疾患の処置 | |
| JP6073133B2 (ja) | 腫瘍壊死因子受容体2(tnfr2)に対する天然アンチセンス転写物の抑制によるtnfr2関連疾患の治療 | |
| JP6072842B2 (ja) | 脳由来神経栄養因子(bdnf)関連疾病の、bdnfに対する天然アンチセンス転写物の抑制による治療 | |
| KR101857090B1 (ko) | 무조(無調)의 동소체 1 (atoh1)에 대한 자연 안티센스 전사체의 저해에 의한 atoh1 관련된 질환의 치료 | |
| KR102043422B1 (ko) | 프라탁신 (fxn)에 대한 자연 안티센스 전사체의 저해에 의한 프라탁신 (fxn) 관련된 질환의 치료 | |
| JP5943836B2 (ja) | ‘hsp70相互作用タンパク質c末端’(chip)に対する天然アンチセンス転写産物の阻害によるchip関連疾患の治療 | |
| JP5993744B2 (ja) | 核呼吸因子1(nrf1)に対する天然アンチセンス転写物の阻害による核呼吸因子1関連疾患の治療 | |
| KR101854926B1 (ko) | 성 호르몬 결합 글로불린 (shbg)에 대한 자연 안티센스 전사체의 저해에 의한 성 호르몬 결합 글로불린 (shbg) 관련된 질환의 치료 | |
| JP6031356B2 (ja) | Ucp2に対する天然アンチセンス転写産物の阻害による脱共役タンパク質2(ucp2)関連疾患の治療 | |
| JP5964232B2 (ja) | ‘iqモチーフ含有gtpアーゼ活性化タンパク質’(iqgap)に対する天然アンチセンス転写産物の阻害によるiqgap関連疾患の治療 | |
| KR101886452B1 (ko) | 디스크 라지 호모로그(dlg)에 대한 천연 안티센스 전사체의 저해에 의한 dlg 관련된 질환의 치료 | |
| JP5934106B2 (ja) | 肝細胞増殖因子(hgf)に対する天然アンチセンス転写物の阻害によるhgf関連性疾患の治療 | |
| JP6083735B2 (ja) | インスリン受容体基質2(irs2)および転写因子3(tfe3)に対する天然アンチセンス転写物の阻害によるインスリン受容体基質2(irs2)関連疾患の治療 | |
| JP5982362B2 (ja) | Par4への天然アンチセンス転写物の阻害によるpar4関連疾患の治療 | |
| JP6128848B2 (ja) | インスリン遺伝子(ins)に対する天然アンチセンス転写物の抑制によるインスリン遺伝子(ins)関連疾患の治療 | |
| JP2012531427A (ja) | ダウン症候群遺伝子に対する天然アンチセンス転写物の抑制によるダウン症候群遺伝子関連疾患の治療 | |
| KR20130126605A (ko) | 인터페론-관련된 발달성 조절물질 1 (ifrd1)에 대한 자연 안티센스 전사체의 저해에 의한 ifrd1 관련된 질환의 치료 | |
| KR20120114288A (ko) | 인터페론 조절 인자 8 (irf8)에 대한 자연 안티센스 전사체의 저해에 의한 인터페론 조절 인자 8 (irf8) 관련된 질환의 치료 | |
| KR20130138233A (ko) | 시알리다아제 4 (neu4)에 대한 자연 안티센스 전사체의 저해에 의한 neu4 관련된 질환의 치료 | |
| KR20140001225A (ko) | Nanog에 대한 자연 안티센스 전사체의 저해에 의한 nanog 관련된 질환의 치료 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |