KR102055772B1 - 약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 - Google Patents
약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 Download PDFInfo
- Publication number
- KR102055772B1 KR102055772B1 KR1020147018695A KR20147018695A KR102055772B1 KR 102055772 B1 KR102055772 B1 KR 102055772B1 KR 1020147018695 A KR1020147018695 A KR 1020147018695A KR 20147018695 A KR20147018695 A KR 20147018695A KR 102055772 B1 KR102055772 B1 KR 102055772B1
- Authority
- KR
- South Korea
- Prior art keywords
- titania
- nanotubes
- nanotube membrane
- titanium substrate
- titania nanotubes
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M31/00—Devices for introducing or retaining media, e.g. remedies, in cavities of the body
- A61M31/002—Devices for releasing a drug at a continuous and controlled rate for a prolonged period of time
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/21—Interferons [IFN]
- A61K38/212—IFN-alpha
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
- A61K9/0092—Hollow drug-filled fibres, tubes of the core-shell type, coated fibres, coated rods, microtubules or nanotubes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25D—PROCESSES FOR THE ELECTROLYTIC OR ELECTROPHORETIC PRODUCTION OF COATINGS; ELECTROFORMING; APPARATUS THEREFOR
- C25D11/00—Electrolytic coating by surface reaction, i.e. forming conversion layers
- C25D11/02—Anodisation
- C25D11/26—Anodisation of refractory metals or alloys based thereon
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25D—PROCESSES FOR THE ELECTROLYTIC OR ELECTROPHORETIC PRODUCTION OF COATINGS; ELECTROFORMING; APPARATUS THEREFOR
- C25D11/00—Electrolytic coating by surface reaction, i.e. forming conversion layers
- C25D11/02—Anodisation
- C25D11/34—Anodisation of metals or alloys not provided for in groups C25D11/04 - C25D11/32
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25D—PROCESSES FOR THE ELECTROLYTIC OR ELECTROPHORETIC PRODUCTION OF COATINGS; ELECTROFORMING; APPARATUS THEREFOR
- C25D5/00—Electroplating characterised by the process; Pretreatment or after-treatment of workpieces
- C25D5/48—After-treatment of electroplated surfaces
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25D—PROCESSES FOR THE ELECTROLYTIC OR ELECTROPHORETIC PRODUCTION OF COATINGS; ELECTROFORMING; APPARATUS THEREFOR
- C25D5/00—Electroplating characterised by the process; Pretreatment or after-treatment of workpieces
- C25D5/48—After-treatment of electroplated surfaces
- C25D5/50—After-treatment of electroplated surfaces by heat-treatment
-
- F—MECHANICAL ENGINEERING; LIGHTING; HEATING; WEAPONS; BLASTING
- F04—POSITIVE - DISPLACEMENT MACHINES FOR LIQUIDS; PUMPS FOR LIQUIDS OR ELASTIC FLUIDS
- F04C—ROTARY-PISTON, OR OSCILLATING-PISTON, POSITIVE-DISPLACEMENT MACHINES FOR LIQUIDS; ROTARY-PISTON, OR OSCILLATING-PISTON, POSITIVE-DISPLACEMENT PUMPS
- F04C2270/00—Control; Monitoring or safety arrangements
- F04C2270/04—Force
- F04C2270/041—Controlled or regulated
Abstract
본 발명은 티탄 기재 상에 복수의 티타니아 나노튜브들을 갖는 티타니아 나노튜브 멤브레인을 포함하는 디바이스로서, 티타니아 나노튜브들의 양 단부가 개방되어 있고, 멤브레인의 한 측면에서 다른 측면으로 티타니아 나노튜브들을 통해 액체 또는 고체의 확산을 가능하게 할 수 있는 디바이스를 제공한다. 티타니아 나노튜브 멤브레인을 제조하는 방법이 또한 제공된다.
Description
관련 출원에 대한 상호 참조
본 출원은 2011년 12월 5일에 출원된 미국가출원번호 제61/566,810호를 우선권으로 주장하며, 이러한 문헌은 모든 목적을 위하여 이의 전문이 본원에 포함된다.
현재의 주사가능한 약물 전달 요법들은 환자들의 삶의 질을 크게 떨어뜨리는 약화 부작용(debilitating side effect)들을 갖는다. 일 예로서, C형 간염(HCV)에 대해 인터페론-알파(IFN-a) 치료를 받은 환자들은, 이러한 치료의 부작용들이 너무 심각하여 이러한 환자들이 종종 일을 할 수 없다고 보고되어 있다. IFN-a를 포함하는 여러 주사 요법들의 약화 효과들의 결과로서, HCV에 걸린 사람들에 대해 급성 간 염증과 같은 질환의 손상 효과들이 심각하게 될 때까지 환자들에게 종종 치료법이 처방되지 못한다. 환자들은 몇 일 동안 매우 나쁜 느낌을 가지게 하는 것으로 알려진 물질을 주사하는 것이 요구된다. 그 결과, 환자들은 처방된 바와 같이 이러한 치료법들을 받아들이는데 마음이 내키지 않으며, 일부 환자들은 이러한 치료법을 조기 중단하여, 이들의 요법에 악영향을 미친다. 인터페론 요법으로부터의 여러 부작용들은 주사 직후 약물 농도의 급등(spike)와 관련된다. 이상적으로, IFN-α는 환자에게 일정 속도로 들어갈 것이며, 이에 의해 부작용을 감소시킬 것이다. 이식가능한 티타니아 나노기공성 멤브레인에서의 최근 발전은 주사와 관련한 농도 급등을 제거하는, 거대 분자의 방출을 조절하는 신규한 방법을 형성시켰다. 또한, 피하로 이식되는 디바이스는 환자 순응성을 증가시킬 수 있고, 이에 의해 치료 효능을 증가시키면서 동시에 부작용을 감소시킨다. 놀랍게도, 본 발명의 이러한 요구 및 다른 요구를 충족시킨다.
일 구체예에서, 본 발명은 이식을 위해 적합한 캡슐을 갖는 디바이스를 제공한다. 이러한 디바이스는 또한 캡슐에 의해 캡슐화된 저장소를 포함하며, 여기서 저장소는 치료제를 함유하기에 적합하다. 이러한 디바이스는 또한 티탄 기재 상에 티타니아 나노튜브 멤브레인을 포함하며, 여기서 티탄 기재가 저장소와 접촉하도록 티탄 기재가 캡슐에 부착되며, 티타니아 나노튜브 멤브레인은 저장소와 유체 접촉하는 복수의 티타니아 나노튜브들을 포함한다. 이러한 디바이스는 복수의 티타니아 나노튜브들이 치료제를 위한 저장소로부터의 유일한 확산 경로인 것이다.
다른 구체예에서, 본 발명은 각 나노튜브의 제 1 단부가 닫혀져 있고 티탄 기재에 부착되며 각 나노튜브의 제 2 단부가 개방되어 있도록, 양극산화 조건들 하에서 티탄 기재의 제 1 측면 상에 복수의 티타니아 나노튜브들을 성장시키는 것을 포함하는, 티타니아 나노튜브 멤브레인을 제조하는 방법을 제공한다. 이러한 방법은 또한 티타니아 나노튜브들의 제 1 그룹의 제 1 단부를 개방시키기에 충분한 조건들 하에서, 제 1 측면에 마주하는 측면 상의 티탄 기재를 에칭시켜, 티타니아 나노튜브 멤브레인을 제조하는 것을 포함한다.
다른 구체예에서, 본 발명은 상기 공정에 의해 제조된 티타니아 나노튜브 멤브레인을 제공한다.
다른 구체예에서, 본 발명은 티탄 기재 상에 복수의 티타니아 나노튜브들을 갖는 티타니아 나노튜브 멤브레인으로서, 각 나노튜브는, 티타니아 나노튜브들의 제 1 그룹의 제 1 단부 및 제 2 단부 둘 모두가 개방되도록 제 1 단부 및 제 2 단부를 갖는, 티타니아 나노튜브 멤브레인을 제공한다.
도 1은 캡슐(100), 캡슐에 의해 캡슐화된 저장소(110), 저장소와 접촉되어 있는 티타니아 나노튜브 멤브레인(120)을 갖는 본 발명의 디바이스의 일 구체예들을 도시한 것으로서, 여기서 티타니아 나노튜브 멤브레인은 티탄 기재(130) 상에 존재하며, 티타니아 나노튜브 멤브레인은 복수의 티타니아 나노튜브들(121)을 포함한다.
도 2는 고정부 베이스(fixture base) 상에서 나노튜브 제작을 위해 사용되는 챔버를 도시한 것이다.
도 3은 챔버에서의 그루브에 캐소드가 삽입된 챔버를 도시한 것이다.
도 4는 애노드의 개스킷 측면이 챔버에 존재하면서, 챔버의 베이스에서의 홀에 애노드가 삽입되어 있는 챔버를 도시한 것이다.
도 5는 챔버 내측의 실린더 정렬 피쳐들과 함께 배치된 뚜껑(lid)을 지닌 챔버를 도시한 것이다.
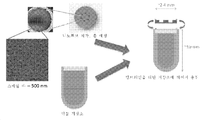
도 6은 티타니아 나노튜브들을 성장시켜 티탄 기재(CP 등급 1 또는 2)를 제조하고, 이후에 티탄 기재를 에칭시켜 티타니아 나노튜브 멤브레인을 나타내는 것을 포함하는, 본 발명의 방법에 대핸 개략도를 도시한 것이다.
도 7은 저장소 함유물의 방출을 위한 유일한 방안(avenue)이 티타니아 나노튜브 멤브레인을 통하는 것이도록, 티탄 기재 상의 티타니아 나노튜브 멤브레인, 및 저장소에 대한 티탄 기재의 레이저 용접을 포함하는, 본 발명의 디바이스의 추가 세부사항을 도시한 것이다.
도 8은 나노튜브의 하부(A), ~60 마이크론 길이의 나노튜브를 나타내는 측면(B), 및 나노튜브 상부(C)를 포함하는 본 발명의 방법에서 제작된 티타니아 나노튜브를 도시한 것이다.
도 2는 고정부 베이스(fixture base) 상에서 나노튜브 제작을 위해 사용되는 챔버를 도시한 것이다.
도 3은 챔버에서의 그루브에 캐소드가 삽입된 챔버를 도시한 것이다.
도 4는 애노드의 개스킷 측면이 챔버에 존재하면서, 챔버의 베이스에서의 홀에 애노드가 삽입되어 있는 챔버를 도시한 것이다.
도 5는 챔버 내측의 실린더 정렬 피쳐들과 함께 배치된 뚜껑(lid)을 지닌 챔버를 도시한 것이다.
도 6은 티타니아 나노튜브들을 성장시켜 티탄 기재(CP 등급 1 또는 2)를 제조하고, 이후에 티탄 기재를 에칭시켜 티타니아 나노튜브 멤브레인을 나타내는 것을 포함하는, 본 발명의 방법에 대핸 개략도를 도시한 것이다.
도 7은 저장소 함유물의 방출을 위한 유일한 방안(avenue)이 티타니아 나노튜브 멤브레인을 통하는 것이도록, 티탄 기재 상의 티타니아 나노튜브 멤브레인, 및 저장소에 대한 티탄 기재의 레이저 용접을 포함하는, 본 발명의 디바이스의 추가 세부사항을 도시한 것이다.
도 8은 나노튜브의 하부(A), ~60 마이크론 길이의 나노튜브를 나타내는 측면(B), 및 나노튜브 상부(C)를 포함하는 본 발명의 방법에서 제작된 티타니아 나노튜브를 도시한 것이다.
I. 일반
본 발명은 치료제의 전달을 위한 티탄 기재 상에 티타니아 나노튜브 멤브레인을 형성시키는 복수의 티타니아 나노튜브들을 갖는 약물 전달 디바이스를 제공한다. 티타니아 나노튜브 멤브레인은 먼저 티탄 기재 상에 티타니아 나노튜브들을 성장시키고 이후에 나노튜브들의 내부 부분이 티타니아 나노튜브들의 제 1 그룹에 노출될 때까지 나노튜브들이 존재하지 않는 티탄 기재의 후측면을 에칭시킴으로써 제조된다. 티타니아 나노튜브 멤브레인은 또한, 티타니아 나노튜브들의 제 2 그룹을 포함할 수 있으며, 여기서 티타니아 나노튜브들의 제 1 단부는 닫혀져 있다. 티타니아 나노튜브들의 좁은 직경은, 티타니아 나노튜브들이 디바이스로부터의 확산을 위한 유일한 경로이기 때문에, 약물 전달 디바이스에서 치료제의 방출을 조절한다. 치료제의 방출속도는 영차일 수 있다.
II
. 정의
"치료제"는 치료학적 반응을 제공할 수 있는 임의의 제제, 예를 들어 약물 또는 생물제제(biologic)를 지칭한다.
"티타니아 나노튜브 멤브레인"은 티탄 기재 상의 티타니아 나노튜브들의 어레이를 지칭하는 것으로서, 여기서 티타니아 나노튜브들의 적어도 일부는 양 단부가 개방되고, 멤브레인의 한 측면에서 다른 한 측면으로 티타니아 나노튜브들을 통해 액체 또는 고체의 확산을 가능하게 할 수 있다.
"유체 접촉"은 저장소에서 티타니아 나노튜브들로 확산할 수 있는 저장소의 내용물들을 지칭한다. 저장소의 내용물들은 액체 형태일 수 있지만, 또한 분말 또는 고체 형태일 수 있다.
"종횡비"는 내부 직경 및 외부 직경을 포함하는, 티타니아 나노튜브들의 작경에 대한 길이의 비율을 지칭한다.
"영차 방출 속도"는 저장소에서의 치료제의 농도에 독립적인 방출 속도를 지칭한다.
"접촉하는"은 적어도 두 개의 별도의 종들이 반응할 수 있도록 적어도 두 개의 별도의 종들을 접촉시키는 공정을 지칭한다. 그러나, 얻어진 반응 생성물이 첨가된 시약들 간의 반응으로부터 직접적으로, 또는 반응 혼합물에서 형성될 수 있는 하나 이상의 첨가된 시약들로부터의 중간체로부터 형성될 수 있는 것으로 인식되어야 한다.
"할로겐 이온"은 플루오라이드, 클로라이드, 브로마이드, 및 요오다이드 이온을 지칭한다. 할로겐 이온은 암모늄과 같은 적합한 반대이온과 쌍을 이룰 수 있다.
"수혼화성 용매"는 물과 적어도 일부 혼화 가능하거나 물과 완전히 혼화 가능할 수 있는 용매를 지칭한다.
III
.
디바이스
본 발명은 디바이스로부터 임의의 치료제에 대한 유일한 확산 경로를 제공하는 티탄 기재 상의 티타니아 나노튜브 멤브레인을 갖는 약물 전달 디바이스를 제공한다.
일부 구체예들에서, 본 발명은 이식을 위해 적합한 캡슐을 갖는 디바이스를 제공한다. 이러한 디바이스는 또한 캡슐에 의해 캡슐화된 저장소를 포함하며, 여기서 저장소는 치료제를 함유하기에 적합하다. 이러한 디바이스는 또한 티탄 기재 상에 티타니아 나노튜브 멤브레인을 포함하며, 여기서 티탄 기재가 저장소와 접촉하도록, 티탄 기재는 캡슐에 부착되며, 여기서 티타니아 나노튜브 멤브레인은 저장소와 유체 접촉하는 복수의 티타니아 나노튜브를 포함한다. 이러한 디바이스는 복수의 티타니아 나노튜브들이 치료제를 위한 저장소로부터의 유일한 확산 경로이게 한다.
도 1의 캡슐(100)은 신체와 생체적합성이 있는 임의의 캡슐일 수 있다. 캡슐은 임의의 적합한 물질, 예를 들어 금속들, 폴리머들, 및 이들의 조합들로부터 제조될 수 있다. 유용한 금속들은 순수 금속들 또는 합금들일 수 있고, 티탄 및 스틸을 포함하지만, 이로 제한되지 않는다. 본 발명에서 유용한 폴리머들은 신체와 생체적합성이 있는 임의의 천연 또는 합성 폴리머를 포함한다. 일부 구체예들에서, 캡슐은 티탄을 포함한다.
캡슐은 임의의 적합한 형상 또는 크기를 가질 수 있다. 캡슐은 그 중에서도, 구형, 타원형, 긴타원형, 원형, 또는 실린더형일 수 있다.
디바이스는 또한 치료제를 함유하는 도 1의 저장소(110)를 포함한다. 임의의 치료제는 본 발명의 디바이스에서 유용하다. 유용한 치료제들은 약물들 및 생물제제들을 포함한다. 적합한 치료제들은 생물학적 활성 거대분자들, 예를 들어 펩티드들, 단백질 약물들, 또는 다중 핵산들을 포함한다. 적합한 펩티드들 또는 단백질 생물약제는 호르몬, 호르몬 작용제, 호르몬 길항제, 성장 인자, 예를 들어 CSF, EPO, 및 성장 호르몬, 시토카인, 예를 들어 인터루킨, 면역 조절제, 예를 들어 인터페론 감마 및 인터페론 베타, 항감염제, 예를 들어 인터페론 알파 2b, 항염증제, 면역 억제제/항-거부 약물, 항체, 항-관절염 약물, 및 항종양제를 포함한다. 적합한 다중 핵산들은 DNA, RNA, 플라스미드 분자, 안티센스 DNA, 및 리보자임을 포함한다. 작은 분자량의 분자들은 또한 본 발명과 양립가능하다. 적합한 작은 분자량의 분자들은 진통제 또는 항정신병제를 포함하지만, 이로 제한되지 않는다.
바람직하게, 저장소 내에 함유된 치료제와 동시에 제형화되는 안정화제들은 수혼화성 용매, 또는 폴리머를 포함한다. 적합한 안정화제들은 탄수화물, 당, 덱스트란, 폴리비닐 피롤리돈, 아라비검, 폴리에틸렌 글리콜, 알부민, 수지상 폴리머, 가교된 폴리머 매트릭스, 및 계면활성제를 포함하지만, 이로 제한되지 않는다. 예시적인 당은 트레할로즈, 글루코즈 및 수크로즈를 포함한다.
일부 구체예들에서, 치료제는 베타-글루코세로브로시다제, 인터페론 알파, 인터페론 베타, 아가시다제 알파, 아가시다제 베타, 엑세나타이드, 누트로핀/소마트로핀, VIII 인자, 폰다파리눅스, 알데스루키난드, 리스페리돈, 포리게리모드, NP 융합 단백질들, IL-12, 멜라닌 세포 자극 호르몬, 또는 바피뉴주마브일 수 있다. 이러한 치료제들의 유사체들이 또한 고려된다. 일부 구체예들에서, 치료제는 인터페론 알파이다.
치료제는 저장소에 임의의 적합한 형태, 예를 들어 액체, 고체 또는 현탁액으로 존재할 수 있다. 고체 형태는 분말 및 미소화된 입자들(micronized particle)을 포함하지만, 이로 제한되지 않는다. 예를 들어, 분말은 동결건조될 수 있다.
도 1의 티탄 기재(130)는 당해 분야에서의 임의의 적합한 방법들에 의해 캡슐에 부착될 수 있다. 예를 들어, 티탄 기재는 캡슐에 레이저 용접될 수 있다.
도 1의 티타니아 나노튜브들(121)은 내부 직경, 길이 및 종횡비를 포함하는 임의의 적합한 치수들을 가질 수 있다. 내부 직경은 약 1 ㎚ 내지 약 1000 ㎚일 수 있고, 티타니아 나노튜브의 길이를 따라 동일하거나 가변적일 수 있다. 내부 직경이 가변적일 때, 내부 직경은 티타니아 나노튜브의 한 단부에서 다른 단부쪽으로 증가할 수 있다. 예를 들어, 저장소와 접촉하는 단부에서의 티타니아 나노튜브의 내부 직경은 저장소와 마주하는 단부에서의 내부 직경 보다 더욱 작을 수 있으며, 여기서 내부 직경은 티타니아 나노튜브의 길이를 따라 점진적으로 증가한다. 내부 직경은 약 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 50, 75, 100, 200, 300, 400, 500 또는 1000 ㎚일 수 있다. 내부 직경은 약 1 내지 1000 ㎚, 또는 약 1 내지 약 100 ㎚, 또는 약 1 내지 약 50 ㎚, 또는 약 1 내지 약 20 ㎚일 수 있다. 일부 구체예들에서, 내부 직경은 약 10 ㎚ 내지 약 1000 ㎚일 수 있다.
티타니아 나노튜브들은 임의의 적합한 길이를 가질 수 있다. 예를 들어, 티타니아 나노튜브들은 약 100 ㎚ 내지 약 100 ㎛, 또는 약 500 ㎚, 1 ㎛, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90 또는 100 ㎛일 수 있다. 일부 구체예들에서, 티타니아 나노튜브들은 약 1 ㎛ 내지 약 100 ㎛의 길이를 갖는다.
티타니아 나노튜브들은 또한, 티타니아 나노튜브의 길이를 내부 또는 외부 직경으로 나눔으로써 규정되는 임의의 적합한 종횡비를 가질 수 있다. 종횡비는 약 10 내지 약 10,000, 또는 약 10 내지 약 1,000일 수 있다. 다른 종횡비는 약 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000, 또는 10,000을 포함하지만, 이로 제한되지 않는다.
티타니아 나노튜브들은, 치료제가 액체, 고체 또는 현탁액 형태이든 간에 저장소로부터 티탄 기재에서의 티타니아 나노튜브들로 확산한 후에 마주하는 단부에서 티타니아 나노튜브들로부터 배출되고 신체로 진입할 수 있도록, 저장소와 유체 접촉한다. 치료제의 방출 속도는 임의의 적합한 방출 속도, 예를 들어 영차 방출 속도일 수 있다. 일부 구체예들에서, 저장소로부터 티타니아 나노튜브 멤브레인을 통한 치료제의 방출은 영차 방출 속도이다.
티타니아 나노튜브 멤브레인은 임의의 적합한 방법에 의해 제조될 수 있다. 일부 구체예들에서, 티타니아 나노튜브 멤브레인은 본 발명의 방법에 의해 제조된다.
IV
.
티타니아
나노튜브
멤브레인의
제조
본 발명의 디바이스의 티타니아 나노튜브 멤브레인은 임의의 적합한 방법에 의해, 즉 티탄 기재 상에서 티타니아 나노튜브들을 성장시킨 후에, 나노튜브들의 서브세트의 내측 부분이 노출될 때까지 티타니아 나노튜브들을 마주하는 측면인 티탄 기재의 후측면을 에칭시킴으로써 제조될 수 있다. 일부 구체예들에서, 본 발명은 각 나노튜브의 제 1 단부가 닫혀져 있고 티탄 기재에 부착되며 각 나노튜브의 제 2 단부가 개방되어 있도록, 양극산화 조건들 하에서 티탄 기재의 제 1 측면 상에 복수의 티타니아 나노튜브들을 성장시키는 것을 포함하는, 티타니아 나노튜브 멤브레인을 제조하는 방법을 제공한다. 이러한 방법은 또한, 티타니아 나노튜브들의 제 1 그룹의 제 1 단부를 개방시키기에 충분한 조건들 하에서, 제 1 측면에 마주하는 측면 상에 티탄 기재를 에칭시켜, 티타니아 나노튜브 멤브레인을 제조하는 것을 포함한다.
티타니아 나노튜브 멤브레인은 티타니아 나노튜브들의 연속 멤브레인일 수 있거나, 패턴화될 수 있다. 패턴화된 티타니아 나노튜브 멤브레인은 티타니아 나노튜브들의 영역들 및 티탄의 영역들을 갖는다. 패턴화된 티타니아 나노튜브 멤브레인은 임의의 타입의 패턴, 예를 들어 라인, 체커판 등을 가질 수 있다.
본 발명의 방법에 의해 제조된 티타니아 나노튜브 멤브레인은 모두가 양 단부가 개방되어 있는 티타니아 나노튜브들을 가질 수 있거나, 단지 일부가 양 단부가 개방되어 있는 티타니아 나노튜브들을 가질 수 있다. 예를 들어, 티타니아 나노튜브 멤브레인은 티타니아 나노튜브들의 제 1 단부 및 제 2 단부가 개방되어 있는 티타니아 나노튜브들의 제 1 그룹을 가질 수 있다. 나노튜브들의 제 1 그룹은 티타니아 나노튜브 멤브레인에서의 모든 나노튜브들, 또는 멤브레인에서 티타니아 나노튜브들의 서브세트일 수 있다. 티타니아 나노튜브들의 제 1 그룹이 멤브레인에서 티타니아 나노튜브들 전부가 아닐 때, 티타니아 나노튜브 멤브레인은 또한, 제 1 단부가 닫혀져 있는 티타니아 나노튜브들의 제 2 그룹을 포함한다. 일부 구체예들에서, 티타니아 나노튜브들의 제 2 그룹의 제 1 단부는 닫혀져 있다. 티타니아 나노튜브 멤브레인은 티타니아 나노튜브들의 다른 그룹들을 포함할 수 있다.
양극산화 조건들은 티타니아 나노튜브들을 성장시킬 수 있는 임의의 조건들을 포함한다. 일부 구체예들에서, 티타니아 나노튜브들을 성장시키는 것은 티탄 기재의 제 1 측면을 할로겐 이온, 물 및 수혼화성 용매를 갖는 양극산화 용액과 접촉시키는 것을 포함한다.
티탄 기재는 임의의 적합한 두께, 티타니아 나노튜브 멤브레인을 제조하거나 상술된 디바이스에서 티타니아 나노튜브 멤브레인을 지지하기 위해 추가 기재 또는 지지체가 필요치 않는 두께일 수 있다.
할로겐 이온은 플루오라이드, 클로라이드, 브로마이드, 또는 요오다이드일 수 있다. 일부 구체예들에서, 할로겐 이온은 플루오라이드일 수 있다. 일부 구체예들에서, 양극산화 용액은 암모늄 플루오라이드를 포함한다.
수혼화성 용매는 수중에서 혼화 가능한 임의의 용매일 수 있다. 일부 구체예들에서, 수혼화성 용매는 에탄올, 에틸렌 글리콜, 프로필렌 글리콜 또는 1,3-프로판디올일 수 있다. 일부 구체예들에서, 수혼화성 용매는 에틸렌 글리콜일 수 있다. 양극산화 용액에 존재하는 수혼화성 용매는 임의의 적합한 양으로 존재할 수 있다. 예를 들어, 수혼화성 용매는 50, 55, 60, 65, 70, 75, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 또는 99 중량%와 같은 양으로 존재할 수 있다. 일부 구체예들에서, 수혼화성 용매는 약 50 내지 약 99 중량%의 양으로 존재할 수 있다. 일부 구체예들에서, 수혼화성 용매는 약 95 내지 약 99 중량%의 양으로 존재할 수 있다.
양극산화 용액은 임의의 적합한 양의 할로겐 이온, 물 및 수혼화성 용매를 포함한다. 예를 들어, 할로겐 이온으로서 암모늄 플루오라이드는 약 0.01 내지 약 10 중량%, 또는 약 0.1, 0.2, 0.3, 0.4, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0, 2.0, 3.0, 4.0, 5.0, 6.0, 7.0, 8.0, 9.0 또는 10.0 중량%의 양으로 존재할 수 있다. 일부 구체예들에서, 암모늄 플루오라이드는 약 0.01 내지 약 5 중량%의 양으로 존재할 수 있다. 일부 구체예들에서, 암모늄 플루오라이드는 약 0.1 내지 약 1 중량%의 양으로 존재할 수 있다. 일부 구체예들에서, 암모늄 플루오라이드는 약 0.3 중량%의 양으로 존재할 수 있다.
양극산화 용액에 존재하는 물은 임의의 적합한 양으로 존재할 수 있다. 예를 들어, 물은 0.1, 0.5 1, 2, 3, 4, 5, 10, 20, 30, 40 또는 50 중량%와 같은 양으로 존재할 수 있다. 일부 구체예들에서, 물은 약 0.1 내지 약 50 중량%의 양으로 존재한다. 일부 구체예들에서, 물은 약 0.1 내지 약 5 중량%의 양으로 존재한다.
일부 구체예들에서, 양극산화 용매는 약 0.1 내지 약 1 중량% 양의 암모늄 플루오라이드, 약 1 내지 약 5 중량% 양의 물, 및 약 95 내지 약 99 중량% 양의 수혼화성 용매를 포함한다.
일부 구체예들에서, 티타니아 나노튜브 멤브레인을 제조하는 방법은 또한 티탄 기재 상의 티타니아 나노튜브들을 어닐링하는 것을 포함한다. 어닐링은 임의의 적합한 온도에서 임의의 적합한 기간 동안 수행될 수 있다. 일부 구체예들에서, 어닐링 단계는 티탄 기재 상의 복수의 티타니아 나노튜브들을 약 200℃ 내지 약 1000℃의 온도에서 가열하는 것을 포함한다. 어닐링 단계에서 유용한 다른 온도는 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900, 또는 1000℃를 포함하지만, 이로 제한되지 않는다. 일부 구체예들에서, 온도는 약 300℃ 내지 약 600℃, 또는 약 400℃ 내지 약 500℃일 수 있다. 일부 구체예들에서, 온도는 약 450℃일 수 있다.
에칭은 임의의 적합한 에칭 방법에 의해 수행될 수 있다. 예를 들어, 에칭은 플라즈마 에치, 또는 반응성-이온 에치, 예를 들어 염소 심도 반응성-이온 에치(chlorine deep reactive-ion etch)일 수 있다.
다른 구체예에서, 본 발명은 상기 방법에 의해 제조된 티타니아 나노튜브 멤브레인을 제공한다.
다른 구체예에서, 본 발명은 티탄 기재 상에 복수의 티타니아 나노튜브들을 갖는 티타니아 나노튜브 멤브레인으로서, 각 나노튜브가 티타니아 나노튜브들의 제 1 그룹의 제 1 단부 및 제 2 단부 둘 모두가 개방되어 있는 제 1 단부 및 제 2 단부를 갖는 티타니아 나노튜브 멤브레인을 제공한다. 일부 구체예들에서, 티타니아 나노튜브 멤브레인은 단지 제 1 단부가 개방되어 있는 티타니아 나노튜브들의 제 2 그룹을 추가로 포함한다. 일부 구체예들에서, 티타니아 나노튜브 멤브레인은 상술된 방법에 의해 제조될 수 있다.
V.
실시예
실시예
1: 패턴화된 디스크 상에 나노튜브 제작
일반
시약들 및 패턴화된 디스크들을 사용 전에 검사하였다. 암모늄 플루오라이드(NH4F) 및 온화한(mild) 불화수소산의 물질 안전 데이타 시트(MSDS)를 검토하고, 노출을 막기 위해 불소 및 불소-오염된 물질들의 조작 동안에 적절한 안전 장치를 사용하였다. 절차들에서 사용되는 플루오라이드-함유 염을 물에 용해시켜 수성 불소를 형성시켰으며, 이는 섭취, 흡입 및 피부 접촉에 의해 독성을 나타낸다. 18.2 MΩ 탈이온수(하기에서 "DI수"로서 지칭됨)를 모든 시약 제조 및 장비 세정을 위해 사용하였다. 시약 용액들을 각 제작 실행(fabrication run)의 마지막에 중화시켰다.
나노튜브 제작 어셈블리
셋업
고정부(fixture)를 수직으로 세워진 위치(upright position)로 배치시켰다(도 2). 캐소드를 고정부의 챔버에서의 그루브에 올려놓여질 때까지 슬라이딩시켜 캐소드를 삽입하였다(도 3). 챔버의 베이스에서의 홀을 통해 와이어를 밀어넣음으로써 애노드를 삽입하였으며, 애노드의 개스킷 측면은 챔버에 잔류해야 한다(도 4). 필요한 경우에, 뚜껑을 챔버 내측에 실린더 정렬 피쳐(cylinder alignment feature)들과 함께 배치시켰다(도 5). 고정부를 사용하는 동안에 잠재적으로 독성인 수성 불소 이온들에 노출시켰다. 이에 따라, 고정부는 적절하게 세정되어야 하며, 글로브(glove) 및 안전 고글이 어셈블리 및 조작 동안에 사용되어야 한다.
양극산화
용액 제조
1-리터 HDPE 병에서 20 +/- 0.25 mL의 H2O 중에 3 +/- 0.1 g의 NH4F를 용해시켜 수성 98%(v/v) 에틸렌 글리콜(EG) 중 0.3 중량% 암모늄 플루오라이드의 용액을 제조하였다. NH4F를 완전히 용해시킨 후에, 980 +/- 5 mL의 EG를 용액에 첨가하였다.
세정
패턴화된 디스크를 수성 10% (v/v) Micro-90 용액(Aldrich)에서 초음파처리를 이용하여 6분 동안 세정하였다. 디스크를 초음파처리욕에서 빼내고, H2O로 린싱한 후에 에탄올로 린싱하고, 질소 스트림 하에서 건조시켰다. 제작 고정부 및 백금 와이어를 필요한 경우 유사한 방식으로 세정할 수 있다. 편의를 위하여, 나노튜브 제작 어셈블리의 셋업이 완료될 때까지 초음파처리욕에 패턴화된 디스크를 잔류시킬 수 있다.
실행 셋업(
Run
Set
-
Up
)
나노튜브 제작 어셈블리를 위한 전력 공급원을 조정하여 60 V +/- 0.1 V로 설정하였다. 실행 파라미터들을 사용자에 의해 소프트웨어 인터페이스를 이용하여 설정하였다:
1. 화살표 키를 눌러 프로그램을 시작한다.
2. 실행 시간(예를 들어, 18 시간)을 각 실행에 대한 "시간" 텍스트 박스에 입력한다.
3. 파일 브라우저에서 적절한 폴더를 열고 가장 최근 실행을 선택하여 제 1 실행에 대한 파일명을 부여한다. 파일명을 복사하고, 각 실행에 대한 파일 경로에 복사하고, 이후에 파일명들을 수정하여 정확한 실행 번호를 반영한다.
4. 실행 파라미터들을 엑셀의 튜브 테이블에 입력한다.
나노튜브 제작 고정부를 제 2 격납용기(containment)에 배치시키고, 패턴화된 디스크를 놓여질 때까지 기계처리된 윈도우가 아래쪽을 향하게 하면서 Viton 개스킷에 견고하게 가압한다. 디스크는 작업 표면과 평평해야 한다. 전기 전도도를 옴미터(ohmmeter)를 이용하여 확인하였다. 애노드 및 캐소드를 상응하는 급속-단절 전력 리드에 연결하였다. 고정부 챔버를 상술된 바와 같이 제조된, 30 mL의 양극산화 용액으로 채웠다. 고정부를 뚜껑으로 덮어서, 챔버 내측에 실린더 정렬 피쳐들이 있도록 한다. 서미스터를 에탄올-액침된 와이프(wipe)로 세정하고, 뚜껑을 통해 용액에 삽입하였다.
실행(
Run
)
소프트웨어 인터페이스에서 "실행 개시(Begin Run)" 버튼을 눌러서 각 실행의 기록을 개시하였다. 튜브 성장의 개시는 전류 급등 및 쇠퇴에 의해 지시된다. 실행 셋업 동안 입력된 바와 같은 실행 시간의 전체 기간 후에, 실행 기록은 실행 동안 전력이 끊어지지 않았음을 보장하기 위해 검토되어야 한다. 온도 및 전류 변동을 기록하였다. 큰 전류 변동은 실행 동안 물리적 장애를 지시할 수 있다. "정지(Stop)" 버튼을 눌러서 프로그램을 종료하고, 어셈블리의 세정을 즉시 수행하였다.
청소(
Cleanup
)
전력 공급원을 끄고, 계전기(relay)를 개방시킨 후 제작 고정부로의 리드를 분리하고, 전류의 강하를 기재하였다. 남은 양극산화 용액을 어셈블리에서 대략 1 내지 1.5 그램의 칼슘 카보네이트를 함유한 비이커에 부었다. 양극산화 용액을 제거하면서, 에탄올 스프레이 병으로 적어도 8회 분무시킴으로써 제작 고정부를 에탄올로 철저히 린싱하였다. 모든 에탄올 린스를 폐비이커에 모으고, 에탄올 린스를 반복하였다. 추가 에탄올을 어셈블리에 분무하여, 디스크 및 수 밀리미터의 챔버를 덮도록 하였으며, 고정부를 다시 뚜껑으로 덮었다. 고정부를 필요한 경우에 최대 24시간 이하 동안 이러한 상태로 있게 할 수 있다.
디스크로부터 양극산화 용액을 제거하는 시간을 기록하였다. 디스크 및 용액을 칼라, 패턴, 또는 다른 마킹의 측면에서 검사하였다. 고정부 뚜껑을 에탄올을 함유한 스테인레스 스틸 팬에 배치시켰다. 고정부 자체를 팬에서 옆으로 배치시켜, 디스크가 에탄올에 잠겨 있도록 하였다. 에탄올에 디스크를 잠긴 상태로 유지시키면서 Viton 개스킷/와이어 어셈블리를 제작 고정부의 바닥에서 벗어나게 하였다. 디스크가 튀어나오도록 개스킷의 베이스를 가압하고/거나 개스킷 측면을 후퇴하게 하여 디스크를 조심스럽게 제거하였다. 디스크를 에탄올로 세정하고, 공기 중에서 건조시키고, 겔 팩에 배치시키고, 라벨링하였다. 겔 팩의 양 측면을 스캐닝하였다. 각 제작 고정부 및 캐소드 인서트를 별도로 질소로 건조시키고, 세정된 스크류-톱 용기에 배치시켰다. 핀셋 및 제 2 격납 용기를 물로 린싱하고, 질소로 건조시키거나 공기 건조되게 하였다. 중화된 양극산화 용액을 싱크(sink)에서 수 리터의 물(수도꼭지는 ~2 내지 3분 동안 작동시킴)로 플러싱하였다.
실시예
2: 나노튜브
어닐링
일반
어닐링 절차는 고온로의 사용을 포함한다. 이러한 로는 부품들을 제거하거나 그밖에 기기를 제조하기 전에 (예를 들어, 실온)으로 작업하기에 충분히 냉각되어야 한다. 적절한 안전 장치는 핀셋 또는 부젓가락, 밀폐된 토우 슈즈, 및 내열성 글로브를 포함한다. 어닐링 후에, 나노튜브를 갖는 패턴화된 디스크를 수중에서 사용하기 위해 안정화시키고, 튜브 파편을 세정하였다.
어닐링을
위한 디스크의 제조
디스크가 중앙에 놓이게, 패턴화된 디스크를 적절한 로(예를 들어, Ney Vulcan 3-550)에 삽입하였다. 로를 사용자에 의해 하기 파리미터들로 프로그래밍하였다.
a. 시간: 1시간
b. 상승속도: 10℃/min
c. 온도: 450℃
d. 제2 및 제 3 상승이 450℃까지이고 0분 동안임을 확인한다.
e. 사이클은 1시간 42분 길이이어야 한다.
로 도어를 닫고, 출발 버튼을 눌러서 어닐링을 개시한다.
어닐링
로로부터
디스크의 제거
어닐링을 완료하고 15분 내에, 로 도어를 열고, 계속하기 전에 280℃ 또는 그 미만으로 냉각시켰다. 디스크를 핀셋을 이용하여 알루미늄 냉각 블록으로 옮겼다. 디스크에서 알루미늄 호일을 제거하여 냉각을 완료하였다. 이후에, 냉각된 디스크를 라벨링된 겔 팩에 배치시키고, 각 겔 팩의 전면 및 후면을 스캐닝하였다.
후가공
각 디스크를 에탄올로 세정하고, 공기 중에서 건조시키고, 겔 팩으로 보내었다. 각 겔 팩의 전면 및 후면을 스캐닝하였다. 나노튜브 어닐링 이후에 통상적으로 나노튜브 에칭을 수행하였다.
실시예
3: 나노튜브 에칭
티탄
에치
지그
어셈블리 셋업
티탄 에치 지그(titanium etch jig)를 Micro-90 용액에서 초음파 처리하였다. 에치 지그를 탈이온수로 린싱한 후에 에탄올로 린싱하고, 질소 스트림 하에서 건조하였다. 에치 지그를 필요한 경우에 끝말림을 제거하였다(deburr). 지그를 세정된 한 쌍의 니들-노즈 플라이어(needle-nose plier)를 이용하여 갭을 유연하게 줄이기 위해 방사상으로 스퀴징하였다. 지그를 분무기 툴로 분무하고, 나노구조를 갖는 패턴화된 디스크를 삽입하였다. 지그의 바닥에 실행 번호를 라벨링하고, 겔 팩에 배치시켰다.
디스크 에칭
디스크 에칭을 변압기-결합된 플라즈마(TCP) 에칭기(예를 들어, Lam Research TCP 9600SE II)로 수행하였다. 에치 지그를 0.005" 접착제-후면처리된 Kapton을 사용하여 6" 산화규소 웨이퍼에 부착시켰다. 웨이퍼를 TCP 에칭기의 진입 웨이퍼 카세트에 배치시키기 전에 웨이퍼의 바닥에 질소 스트림을 불어넣어 웨이퍼의 바닥을 세정하였다. 아르곤을 불활성 가스 라인에서 사용하고, 냉각기 온도를 15℃로 설정하였다. 하기 파라미터를 갖는 적절한 에칭 프로그램을 사용자에 의해 프로그래밍하였다: 400W 소스 전력(Source Power), 100W 바이어스(Bias), 18.75 mT 챔버 압력, 120 sccm Cl2, 및 15 sccm Ar.
총 60분의 에치를 5분 온-사이클(RF 없는 5분 오프-사이클, 60 mT의 챔버 압력, 500 sccm Ar)에서 수행하였다. 로에서 연장된 기간 동안 성장된 옥사이드 층을 갖는 실리콘 웨이퍼 상에서 Kapton 테이프를 이용하여 에치 지그를 마운팅하였다. 에칭 공정을 사용자에 의해 소프트웨어 제어를 통해 개시하고, 에칭기로의 적절한 웨이퍼 공급을 확인하였다. 에칭 공정을 통상적으로 120분에 걸쳐 수행하고, 기기에 의해 자동적으로 제어하였다. 에칭 후에 기기가 공회전할 때 웨이퍼를 배출 카셋트로부터 제거하고, 패턴화된 디스크를 갖는 지그를 웨이퍼로부터 제거하였다.
실시예
4: 패턴화된 디스크 상에 나노튜브 제작
일반
시약들 및 패턴화된 디스크들을 사용 전에 검사하였다. 암모늄 플루오라이드(NH4F) 및 온화한 불화수소산의 물질 안전 데이타 시트(MSDS)를 검토하고, 노출을 막기 위해 불소 및 불소-오염된 물질들의 조작 동안에 적절한 안전 장치를 사용하였다. 절차들에서 사용되는 플루오라이드-함유 염을 물에 용해시켜 수성 불소를 형성시켰으며, 이는 섭취, 흡입 및 피부 접촉에 의해 독성을 나타낸다. 18.2 MΩ 탈이온수(하기에서 "DI수"로서 지칭됨)를 모든 시약 제조 및 장비 세정을 위해 사용하였다. 시약 용액들을 각 제작 실행(fabrication run)의 마지막에 중화시켰다.
나노튜브 제작 어셈블리
셋업
고정부를 수직으로 세워진 위치로 배치시켰다(도 2). 캐소드를 고정부의 챔버에서의 그루브에 올려놓여질 때까지 슬라이딩시켜 캐소드를 삽입하였다(도 3). 챔버의 베이스에서의 홀을 통해 와이어를 밀어넣음으로써 애노드를 삽입하였으며, 애노드의 개스킷 측면은 챔버에 잔류해야 한다(도 4). 필요한 경우에, 뚜껑을 챔버 내측에 실린더 정렬 피쳐들과 함께 배치시켰다(도 5). 고정부를 사용하는 동안에 잠재적으로 독성인 수성 불소 이온들에 노출시켰다. 이에 따라, 고정부는 적절하게 세정되어야 하며, 글로브 및 안전 고글이 어셈블리 및 조작 동안에 사용되어야 한다.
양극산화
용액 제조
1-리터 HDPE 병에서 10 +/- 0.25 mL의 DI H2O 중에 1.5 +/- 0.1 g의 NH4F를 용해시켜 2% DI수/98% 에틸렌 글리콜(EG)(v/v) 중의 0.3 중량% 암모늄 플루오라이드의 500 mL 용액을 제조하였다. NH4F를 완전히 용해시킨 후에, 490 +/- 5 mL의 EG를 용액에 첨가하였다.
세정
패턴화된 디스크 및 스테인레스 스틸 와이어를 10% Micro-90/90% 물(v/v)의 용액에서 초음파처리를 이용하여 10분 동안 세정하였다. 디스크 및 와이어를 초음파처리욕에서 빼내고, DI로 린싱하였다. 디스크를 공기 건조시키고, 제작 고정부 및 스테인레스 스틸 와이어를 질소로 건조시켰다. 편의를 위하여, 나노튜브 제작 어셈블리의 셋업이 완료될 때까지 초음파처리욕에 패턴화된 디스크를 잔류시킬 수 있다.
실행 셋업(
Run
Set
-
Up
)
나노튜브 제작 어셈블리를 위한 전력 공급원을 조정하여 60 V +/- 0.1 V로 설정하였다. 실행 파라미터들을 사용자에 의해 소프트웨어 인터페이스를 이용하여 설정하였다:
1. 화살표 키를 눌러 프로그램을 시작한다.
2. 실행 시간(예를 들어, 18 시간)을 각 실행에 대한 "시간" 텍스트 박스에 입력한다.
3. 파일 브라우저에서 적절한 폴더를 열고 가장 최근 실행을 선택하여 제 1 실행에 대한 파일명을 부여한다. 파일명을 복사하고, 각 실행에 대한 파일 경로에 복사하고, 이후에 파일명들을 수정하여 정확한 실행 번호를 반영한다.
4. 실행 파라미터들을 엑셀의 튜브 테이블에 입력한다.
나노튜브 제작 고정부를 제 2 격납용기에 배치시켰다. 애노드 및 캐소드를 상응하는 급속-단절 전력 리드에 연결하였다. 패턴화된 디스크를 놓여질 때까지 기계처리된 윈도우가 아래쪽을 향하게 하면서 Viton 개스킷에 견고하게 가압하였다. 디스크는 작업 표면과 평평해야 한다. 전기 전도도를 옴미터를 이용하여 확인하였다. 디스크를 에탄올(< 100 ㎕)로 습윤화시켰다. 제작 고정부 챔버를 상술된 바와 같이 제조된, 30 +/- 0.25 mL의 양극산화 용액으로 채웠다. 고정부를 뚜껑으로 덮어서, 챔버 내측에 실린더 정렬 피쳐들이 있도록 하였다.
실행(
Run
)
소프트웨어 인터페이스에서 "실행 개시(Begin Run)" 버튼을 눌러서 각 실행의 기록을 개시하였다. 성장의 개시는 전류 급등 및 쇠퇴에 의해 지시된다. 실행 셋업 동안 입력된 바와 같은 실행 시간의 전체 기간 후에, 실행 기록은 실행 동안 전력이 끊어지지 않았음을 보장하기 위해 검토되어야 한다. 온도 및 전류 변동을 기록하였다. 큰 전류 변동은 실행 동안 물리적 장애를 지시할 수 있다. "정지(Stop)" 버튼을 눌러서 프로그램을 종료하고, 어셈블리의 세정을 즉시 수행하였다.
청소
5 mL 튜브를 에탄올(병으로부터 대략 2회 스프레이)로 일부 채웠다. 전력 공급원을 끄고, 계전기를 개방시킨 후 제작 고정부로의 리드를 분리하고, 전류의 강하를 기재하였다. 남은 에틸렌 글리콜 용액을 어셈블리에서 대략 1 내지 1.5 그램의 칼슘 카보네이트를 함유한 비이커로 부었다. 에틸렌 글리콜 용액을 제거하면서, 에탄올 스프레이 병으로 적어도 8회 분무시킴으로써 제작 고정부를 에탄올로 철저히 린싱하였다. 모든 에탄올 린스를 폐비이커에 모으고, 에탄올 린스를 반복하였다. 추가 에탄올을 어셈블리에 분무하여, 디스크 및 수 밀리미터의 챔버를 덮도록 하였으며, 고정부를 다시 뚜껑으로 덮었다. 고정부를 필요한 경우에 최대 24시간 이하 동안 이러한 상태로 있게 할 수 있다.
디스크로부터 양극산화 용액을 제거하는 시간을 기록하였다. 디스크 및 용액을 칼라, 패턴, 또는 다른 마킹의 측면에서 검사하였다. 고정부 뚜껑을 에탄올을 함유한 튜브에 배치시켰다. 고정부 자체를 팬에서 옆으로 배치시켜, 디스크가 에탄올에 잠겨 있도록 하였다. 에탄올에 디스크를 잠긴 상태로 유지시키면서 Viton 개스킷/와이어 어셈블리를 제작 고정부의 바닥에서 벗어나게 하였다. 디스크가 튀어나오도록 개스킷의 베이스를 가압하고/거나 개스킷 측면을 후퇴하게 하여 디스크를 조심스럽게 제거하였다. 디스크를 에탄올로 일부 채워진 5 ml 튜브에 나노튜브 측면이 아래를 향하도록 배치하고 15분 동안 초음파처리하였다. 디스크를 튜브에서 빼내고, 여기에 에탄올을 수차례 분무하였다. 디스크를 건조시키기 위해 100℃의 핫플레이트로 바로 옮겼다. 건조되었을 때(대개, 핫플레이트 상에서 30 내지 60초 후) 디스크를 제거하였다. 디스크를 냉각시키고, 겔 팩에 배치시키고, 라벨링하였다. 겔 팩의 양 측면을 스캐닝하였다. 각 제작 고정부 및 캐소드 인서트를 별도로 질소로 건조시키고, 세정된 스크류-톱 용기에 배치시켰다. 핀셋 및 제 2 격납 용기를 물로 린싱하고, 질소로 건조시키거나 공기 건조되게 하였다. 중화된 양극산화 용액을 싱크(sink)에서 수 리터의 물(수도꼭지는 ~2 내지 3분 동안 작동시킴)로 플러싱하였다.
실시예
5: 패턴화된 디스크 상에 나노튜브 제작
일반
시약들 및 패턴화된 디스크들을 사용 전에 검사하였다. 암모늄 플루오라이드(NH4F) 및 온화한 불화수소산의 물질 안전 데이타 시트(MSDS)를 검토하고, 노출을 막기 위해 불소 및 불소-오염된 물질들의 조작 동안에 적절한 안전 장치를 사용하였다. 절차들에서 사용되는 플루오라이드-함유 염을 물에 용해시켜 수성 불소를 형성시켰으며, 이는 섭취, 흡입 및 피부 접촉에 의해 독성을 나타낸다. 18.2 MΩ 탈이온수(하기에서 "DI수"로서 지칭됨)를 모든 시약 제조 및 장비 세정을 위해 사용하였다. 시약 용액들을 각 제작 실행의 마지막에 중화시켰다.
나노튜브 제작 어셈블리
셋업
고정부를 수직으로 세워진 위치로 배치시켰다(도 2). 캐소드를 고정부의 챔버에서의 그루브에 올려놓여질 때까지 슬라이딩시켜 캐소드를 삽입하였다(도 3). 챔버의 베이스에서의 홀을 통해 와이어를 밀어넣음으로써 애노드를 삽입하였으며, 애노드의 개스킷 측면은 챔버에 잔류해야 한다(도 4). 필요한 경우에, 뚜껑을 챔버 내측에 실린더 정렬 피쳐들과 함께 배치시켰다(도 5). 고정부를 사용하는 동안에 잠재적으로 독성인 수성 불소 이온들에 노출시켰다. 이에 따라, 고정부는 적절하게 세정되어야 하며, 글로브 및 안전 고글이 어셈블리 및 조작 동안에 사용되어야 한다.
양극산화
용액 제조
1-리터 HDPE 병에서 15 +/- 0.1 mL의 H2O 중에 7.5 +/- 0.005 g의 NH4F를 용해시켜 수성 98%(v/v) 에틸렌 글리콜(EG) 중 1.0 중량% 암모늄 플루오라이드의 용액을 제조하였다. NH4F를 완전히 용해시킨 후에, 980 +/- 5 mL의 EG를 용액에 첨가하였다.
세정
패턴화된 디스크를 수성 10% (v/v) Micro-90 용액(Aldrich)에서 초음파처리를 이용하여 6분 동안 세정하였다. 디스크를 초음파처리욕에서 빼내고, H2O로 린싱한 후에 에탄올로 린싱하고, 질소 스트림 하에서 건조시켰다. 제작 고정부 및 백금 와이어를 필요한 경우 유사한 방식으로 세정할 수 있다. 편의를 위하여, 나노튜브 제작 어셈블리의 셋업이 완료될 때까지 초음파처리욕에 패턴화된 디스크를 잔류시킬 수 있다.
실행
셋업
나노튜브 제작 어셈블리를 위한 전력 공급원을 조정하여 50 V +/- 0.1 V로 설정하였다. 실행 파라미터들을 사용자에 의해 소프트웨어 인터페이스를 이용하여 설정하였다:
1. 화살표 키를 눌러 프로그램을 시작한다.
2. 실행 시간(예를 들어, 18 시간)을 각 실행에 대한 "시간" 텍스트 박스에 입력한다.
3. 파일 브라우저에서 적절한 폴더를 열고 가장 최근 실행을 선택하여 제 1 실행에 대한 파일명을 부여한다. 파일명을 복사하고, 각 실행에 대한 파일 경로에 복사하고, 이후에 파일명들을 수정하여 정확한 실행 번호를 반영한다.
4. 실행 파라미터들을 엑셀의 튜브 테이블에 입력한다.
나노튜브 제작 고정부를 제 2 격납용기에 배치시키고, 패턴화된 디스크를 놓여질 때까지 기계처리된 윈도우가 아래쪽을 향하게 하면서 Viton 개스킷에 견고하게 가압한다. 디스크는 작업 표면과 평평해야 한다. 전기 전도도를 옴미터를 이용하여 확인하였다. 애노드 및 캐소드를 상응하는 급속-단절 전력 리드에 연결하였다. 고정부 챔버를 상술된 바와 같이 제조된, 30 mL의 양극산화 용액으로 채웠다. 고정부를 뚜껑으로 덮어서, 챔버 내측에 실린더 정렬 피쳐들이 있도록 한다. 서미스터를 에탄올-액침된 와이프로 세정하고, 뚜껑을 통해 용액에 삽입하였다.
실행
소프트웨어 인터페이스에서 "실행 개시(Begin Run)" 버튼을 눌러서 각 실행의 기록을 개시하였다. 튜브 성장의 개시는 전류 급등 및 쇠퇴에 의해 지시된다. 실행 셋업 동안 입력된 바와 같은 실행 시간의 전체 기간 후에, 실행 기록은 실행 동안 전력이 끊어지지 않았음을 보장하기 위해 검토되어야 한다. 온도 및 전류 변동을 기록하였다. 큰 전류 변동은 실행 동안 물리적 장애를 지시할 수 있다. "정지(Stop)" 버튼을 눌러서 프로그램을 종료하고, 어셈블리의 세정을 즉시 수행하였다.
청소
전력 공급원을 끄고, 계전기(relay)를 개방시킨 후 제작 고정부로의 리드를 분리하고, 전류의 강하를 기재하였다. 남은 양극산화 용액을 어셈블리에서 대략 1 내지 1.5 그램의 칼슘 카보네이트를 함유한 비이커에 부었다. 양극산화 용액을 제거하면서, 에탄올 스프레이 병으로 적어도 8회 분무시킴으로써 제작 고정부를 에탄올로 철저히 린싱하였다. 모든 에탄올 린스를 폐비이커에 모으고, 에탄올 린스를 반복하였다. 추가 에탄올을 어셈블리에 분무하여, 디스크 및 수 밀리미터의 챔버를 덮도록 하였으며, 고정부를 다시 뚜껑으로 덮었다. 고정부를 필요한 경우에 최대 24시간 이하 동안 이러한 상태로 있게 할 수 있다.
디스크로부터 양극산화 용액을 제거하는 시간을 기록하였다. 디스크 및 용액을 칼라, 패턴, 또는 다른 마킹의 측면에서 검사하였다. 에탄올로 디스크를 습윤화시키면서 Viton 개스킷/와이어 어셈블리를 제작 고정부의 바닥에서 벗어나게 하였다. 디스크가 튀어나오도록 개스킷의 베이스를 가압하고/거나 개스킷 측면을 후퇴하게 하여 디스크를 조심스럽게 제거하였다. 디스크를 이소프로판올로 세정하고, 이소프로판올 중에서 초음파처리하고(10분, 이후 새로운 이소프로판올 중에서 다른 5분), 공기 중에서 건조시키고, 겔 팩에 배치시키고, 라벨링하였다. 겔 팩의 양 측면을 스캐닝하였다. 각 제작 고정부 및 캐소드 인서트를 별도로 질소로 건조시키고, 세정된 스크류-톱 용기에 배치시켰다. 핀셋 및 제 2 격납 용기를 물로 린싱하고, 질소로 건조시키거나 공기 건조되게 하였다. 중화된 양극산화 용액을 싱크에서 수 리터의 물(수도꼭지는 ~2 내지 3분 동안 작동시킴)로 플러싱하였다.
실시예
6: 나노튜브 에칭
실시예 3에 기술된 동일한 티탄 에치 지그 어셈블리를 사용하여, 디스크 에칭을 변환기-결합된 플라즈마(TCP) 에칭기(예를 들어, Lam Research TCP 9600SE II)로 수행하였다. 에치 지그를 열 커플링 유체를 사용하여 6" 실리콘 웨이퍼에 부착시켰다. 웨이퍼를 TCP 에칭기의 진입 웨이퍼 카세트에 배치시키기 전에 질소 스트림을 불어넣어 웨이퍼의 바닥을 세정하였다. 냉각기 온도를 15℃로 설정하였다.
티탄을 에칭하기 전에, 기재의 양극산화처리되지 않은 측면을 CF4 에치를 이용하여 제거하였다. 총 75분의 에칭을 수행하여 티탄을 제거하고, 하기 파라미터를 이용하여 티타니아 나노튜브를 노출시켰다: 400W 소스 전력, 100W 바이어스, 18.75 mT 챔버 압력, 100 sccm Cl2. 이후에 산소 플라즈마를 이용하여 임의의 잔류 염소를 제거하였다.
상기 발명이 이해를 명확하게 할 목적으로 예시 및 실시예를 이용하여 어느 정도 상세하게 기술하였지만, 당업자는, 특정 변형 및 개질이 첨부된 특허청구범위 내에서 실행될 수 있는 것으로 인식할 것이다. 또한, 본원에 제공된 각 참조문헌은 각 참조문헌이 개별적으로 참조로 포함되는 것과 같이 동일한 정도로 이의 전문이 참조로 포함된다. 본 출원과 본원에 제공된 참조문헌 간에 충돌이 존재하는 경우에, 본 출원이 우세할 것이다.
Claims (26)
- 각 나노튜브의 제 1 단부가 닫혀져 있고 티탄 기재에 부착되어 있으며 각 나노튜브의 제 2 단부가 개방되도록, 양극산화 조건들 하에서 티탄 기재의 제 1 측면 상에 복수의 티타니아 나노튜브들을 성장시키는 단계, 및
티타니아 나노튜브들의 제 1 그룹의 제 1 단부를 개방시키기에 충분한 조건들 하에서, 제 1 측면에 마주하는 측면 상에 티탄 기재를 에칭시켜, 티타니아 나노튜브 멤브레인을 제조하는 단계를 포함하고,
제 1 단부 및 제 2 단부에서 개방된 티타니아 나노튜브들이 티타니아 멤브레인의 한 측면에서 다른 측면으로의 유일한 확산 경로인, 티타니아 나노튜브 멤브레인을 제조하는 방법. - 제 1항에 있어서, 티타니아 나노튜브들의 제 2 그룹의 제 1 단부가 닫혀져 있는 방법.
- 제 1항에 있어서, 성장시키는 단계가 티탄 기재의 제 1 측면을 할로겐 이온, 물 및 수혼화성 용매를 포함하는 양극산화 용액과 접촉시키는 것을 포함하는 방법.
- 제 3항에 있어서, 양극산화 용액이 암모늄 플루오라이드를 포함하는 방법.
- 제 3항에 있어서, 수혼화성 용매가 에탄올, 에틸렌 글리콜, 프로필렌 글리콜, 및 1,3-프로판디올로 이루어진 군으로부터 선택되는 방법.
- 제 3항에 있어서, 양극산화 용매가 0.01 내지 5 중량% 양의 암모늄 플루오라이드를 포함하는 방법.
- 제 3항에 있어서, 양극산화 용매가 0.1 내지 50 중량% 양의 물을 포함하는 방법.
- 제 3항에 있어서, 양극산화 용매가 50 내지 99 중량% 양의 수혼화성 용매를 포함하는 방법.
- 제 3항에 있어서, 양극산화 용매가 0.1 내지 1 중량% 양의 암모늄 플루오라이드, 1 내지 4 중량% 양의 물, 및 95 내지 98 중량% 양의 수혼화성 용매를 포함하는 방법.
- 제 1항에 있어서, 티탄 기재 상의 복수의 티타니아 나노튜브들을 어닐링하는 단계를 추가로 포함하는 방법.
- 제 10항에 있어서, 어닐링하는 단계가 티탄 기재 상의 복수의 티타니아 나노튜브들을 200 내지 1000℃의 온도에서 가열하는 것을 포함하는 방법.
- 제 11항에 있어서, 가열이 450℃의 온도에서 수행되는 방법.
- 제 1항에 있어서, 에칭이 심도 반응성-이온 에치(deep reactive-ion etch)를 이용하여 수행되는 방법.
- 제 1항의 방법에 의해 제조된 티타니아 나노튜브 멤브레인.
- 티탄 기재 상에 복수의 티타니아 나노튜브들을 포함하는 티타니아 나노튜브 멤브레인으로서, 각 나노튜브가, 티타니아 나노튜브들의 제 1 그룹의 제 1 단부 및 제 2 단부 둘 모두가 개방되어 있는, 제 1 단부 및 제 2 단부를 가지고, 제 1 단부 및 제 2 단부에서 개방된 티타니아 나노튜브들이 티타니아 멤브레인의 한 측면에서 다른 측면으로의 유일한 확산 경로인, 티타니아 나노튜브 멤브레인.
- 제 15항에 있어서, 티타니아 나노튜브 멤브레인이 단지 제 1 단부들만이 개방되어 있는 티타니아 나노튜브들의 제 2 그룹을 추가로 포함하는 티타니아 나노튜브 멤브레인.
- 삭제
- 이식을 위해 적합한 캡슐;
캡슐에 의해 캡슐화되고, 치료제를 함유하기에 적합한 저장소; 및
티탄 기재가 저장소와 접촉하도록, 캡슐에 부착되어 있는 티탄 기재 상의 티타니아 나노튜브 멤브레인으로서, 저장소와 유체 접촉하는 복수의 티타니아 나노튜브들을 포함하며, 제 1항의 방법에 의해 제조된 티타니아 나노튜브 멤브레인을 포함하며,
복수의 티타니아 나노튜브들이 치료제를 위한 저장소로부터의 유일한 확산 경로인 디바이스. - 제 18항에 있어서, 캡슐이 티탄을 포함하는 디바이스.
- 제 18항에 있어서, 티타니아 나노튜브가 10 ㎚ 내지 1000 ㎚의 내부 직경을 갖는 디바이스.
- 제 18항에 있어서, 티타니아 나노튜브가 1 ㎛ 내지 100 ㎛의 길이를 갖는 디바이스.
- 제 18항에 있어서, 티타니아 나노튜브가 10 내지 10,000의 종횡비를 갖는 디바이스.
- 제 18항에 있어서, 치료제가 베타-글루코세로브로시다제, 인터페론 알파, 인터페론 베타, 아가시다제 알파, 아가시다제 베타, 엑세나타이드, 누트로핀/소마트로핀, VIII 인자, 폰다파리눅스, 알데스루키난드, 리스페리돈, 포리게리모드, NP 융합 단백질들, IL-12, 멜라닌 세포 자극 호르몬, 및 바피뉴주마브로 이루어진 군으로부터 선택되는 디바이스.
- 제 18항에 있어서, 치료제가 인터페론 알파인 디바이스.
- 제 18항에 있어서, 저장소로부터 티타니아 나노튜브 멤브레인을 통한 치료제의 방출이 영차(zero-order) 방출 속도인 디바이스.
- 삭제
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161566810P | 2011-12-05 | 2011-12-05 | |
| US61/566,810 | 2011-12-05 | ||
| PCT/US2012/067868 WO2013085951A1 (en) | 2011-12-05 | 2012-12-05 | Device having titania nanotube membrane for drug delivery |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140106660A KR20140106660A (ko) | 2014-09-03 |
| KR102055772B1 true KR102055772B1 (ko) | 2019-12-13 |
Family
ID=48574812
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147018695A KR102055772B1 (ko) | 2011-12-05 | 2012-12-05 | 약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9814867B2 (ko) |
| EP (1) | EP2788439A4 (ko) |
| JP (2) | JP6564187B2 (ko) |
| KR (1) | KR102055772B1 (ko) |
| CN (1) | CN103998536B (ko) |
| WO (1) | WO2013085951A1 (ko) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3578205A1 (en) | 2010-08-06 | 2019-12-11 | ModernaTX, Inc. | A pharmaceutical formulation comprising engineered nucleic acids and medical use thereof |
| US20120237975A1 (en) | 2010-10-01 | 2012-09-20 | Jason Schrum | Engineered nucleic acids and methods of use thereof |
| EP2691101A2 (en) | 2011-03-31 | 2014-02-05 | Moderna Therapeutics, Inc. | Delivery and formulation of engineered nucleic acids |
| US9464124B2 (en) | 2011-09-12 | 2016-10-11 | Moderna Therapeutics, Inc. | Engineered nucleic acids and methods of use thereof |
| CA2850624A1 (en) | 2011-10-03 | 2013-04-11 | Moderna Therapeutics, Inc. | Modified nucleosides, nucleotides, and nucleic acids, and uses thereof |
| KR102055772B1 (ko) * | 2011-12-05 | 2019-12-13 | 나노 프리시전 메디컬, 인코포레이티드 | 약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 |
| KR20140102759A (ko) | 2011-12-16 | 2014-08-22 | 모더나 세라퓨틱스, 인코포레이티드 | 변형된 뉴클레오사이드, 뉴클레오타이드 및 핵산 조성물 |
| US9283287B2 (en) | 2012-04-02 | 2016-03-15 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of nuclear proteins |
| CA2868398A1 (en) | 2012-04-02 | 2013-10-10 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of cosmetic proteins and peptides |
| US9572897B2 (en) | 2012-04-02 | 2017-02-21 | Modernatx, Inc. | Modified polynucleotides for the production of cytoplasmic and cytoskeletal proteins |
| US9878056B2 (en) | 2012-04-02 | 2018-01-30 | Modernatx, Inc. | Modified polynucleotides for the production of cosmetic proteins and peptides |
| JP6144355B2 (ja) | 2012-11-26 | 2017-06-07 | モデルナティエックス インコーポレイテッドModernaTX,Inc. | 化学修飾mRNA |
| US8980864B2 (en) | 2013-03-15 | 2015-03-17 | Moderna Therapeutics, Inc. | Compositions and methods of altering cholesterol levels |
| JP2016538829A (ja) | 2013-10-03 | 2016-12-15 | モデルナ セラピューティクス インコーポレイテッドModerna Therapeutics,Inc. | 低密度リポタンパク質受容体をコードするポリヌクレオチド |
| US9770412B2 (en) | 2014-01-23 | 2017-09-26 | Nano Precision Medical, Inc. | Implant device for drug delivery |
| KR101458486B1 (ko) * | 2014-02-26 | 2014-11-07 | 재단법인대구경북과학기술원 | 다공성 한방침 및 이의 제조방법 |
| US20210246271A1 (en) * | 2014-09-04 | 2021-08-12 | Nano Precision Medical, Inc. | Polymeric stabilizing formulations |
| WO2016037128A1 (en) * | 2014-09-04 | 2016-03-10 | Nano Precision Medical, Inc. | Polymeric stabilizing formulations |
| WO2021173770A1 (en) | 2020-02-28 | 2021-09-02 | Nano Precision Medical, Inc. | Polymeric stabilizing agents for implantable drug delivery devices |
| CN107106499B (zh) | 2014-11-02 | 2021-09-17 | 纳诺精密医疗有限公司 | 用于延长释放治疗剂的可植入医药装置 |
| WO2016123027A1 (en) * | 2015-01-26 | 2016-08-04 | Nano Precision Medical, Inc. | Apparatus and method for promoting fluid uptake into an implant |
| US20160367677A1 (en) * | 2015-06-19 | 2016-12-22 | Board Of Regents, The University Of Texas System | Lipid nanodiscs and nanorods as modulators of clotting factor function in vivo |
| WO2017218354A1 (en) * | 2016-06-13 | 2017-12-21 | Nano Precision Medical, Inc. | Drug delivery device |
| WO2018067535A1 (en) | 2016-10-04 | 2018-04-12 | Nano Precision Medical, Inc. | Implant delivery system with hydration promotor capability |
| KR101946703B1 (ko) * | 2017-03-10 | 2019-04-29 | 성균관대학교산학협력단 | 친수성의 나노 필름 구조물을 이용한 무동력 액츄에이터 및 상기 무동력 액츄에이터를 제작하는 방법 |
| CN109692695B (zh) * | 2018-12-27 | 2022-02-01 | 东北大学 | 一种近红外光响应型纳米二氧化钛复合材料及其制备方法 |
| CN109686594B (zh) * | 2019-01-18 | 2020-11-24 | 三峡大学 | 钴基双金属硫化物负极材料的制备方法及其应用 |
| WO2022010846A1 (en) | 2020-07-08 | 2022-01-13 | Nano Precision Medical, Inc. | Methods to control the rate of release of therapeutic agents from implantable devices |
| WO2023107950A1 (en) * | 2021-12-06 | 2023-06-15 | Case Western Reserve University | Implant medical devices |
| WO2023235298A1 (en) | 2022-06-01 | 2023-12-07 | Nano Precision Medical, Inc. | Methods and devices to control release of therapeutic agents from implantable devices |
| WO2023235302A1 (en) | 2022-06-01 | 2023-12-07 | Nano Precision Medical, Inc. | Devices, methods and formulations to control release of therapeutic agents from implantable devices |
| WO2023235292A1 (en) * | 2022-06-03 | 2023-12-07 | Nano Precision Medical, Inc. | Devices and methods to improve bioavailability of therapeutic agents |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100937167B1 (ko) | 2007-06-05 | 2010-01-15 | 재단법인서울대학교산학협력재단 | 나노 포어 어레이를 이용한 나노 구조체의 제조방법 |
| US20100187172A1 (en) * | 2007-07-26 | 2010-07-29 | The Penn State Research Foundation | Highly-ordered titania nanotube arrays |
| US20100213046A1 (en) * | 2009-01-06 | 2010-08-26 | The Penn State Research Foundation | Titania nanotube arrays, methods of manufacture, and photocatalytic conversion of carbon dioxide using same |
| KR101063761B1 (ko) | 2008-11-19 | 2011-09-08 | 경원대학교 산학협력단 | 마개가 형성된 나노튜브를 제조하는 방법 및 이에 의해 제조된 나노튜브 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0883788A (ja) * | 1994-09-14 | 1996-03-26 | Oki Electric Ind Co Ltd | ドライエッチング方法 |
| DK0973499T3 (da) | 1997-03-31 | 2003-11-17 | Alza Corp | Implanterbart diffusionsafgivelsessystem |
| CN1585627A (zh) * | 2001-09-14 | 2005-02-23 | 弗朗西斯J·马丁 | 用于持续释放治疗剂的显微制作的纳米微孔装置 |
| CN101191248B (zh) * | 2006-12-01 | 2011-08-10 | 西南交通大学 | 在钛基底材料表面制备二氧化钛纳米管阵列层的方法 |
| US20090232870A1 (en) | 2008-03-13 | 2009-09-17 | Richmond Chemical Corporation | Apparatus and method of retaining and releasing molecules from nanostructures by an external stimulus |
| KR101043584B1 (ko) * | 2008-08-20 | 2011-06-22 | 한국과학기술원 | 질소 원자가 선택적으로 도핑된 TiO2-xNx 나노튜브 및 그의 제조방법 |
| CN101550581B (zh) | 2009-04-03 | 2011-05-11 | 西北有色金属研究院 | 一种双通大面积TiO2纳米管阵列膜的制备方法 |
| US20100269894A1 (en) * | 2009-04-28 | 2010-10-28 | Board Of Regents Of The Nevada System Of Higher Education, On Behalf Of The University Of Nevada | Titanium dioxide nanotubes and their use in photovoltaic devices |
| NL2003250C2 (en) * | 2009-07-20 | 2011-01-24 | Metal Membranes Com B V | Method for producing a membrane and such membrane. |
| CN101717984A (zh) * | 2009-11-05 | 2010-06-02 | 兰州大学 | 一种二氧化钛纳米管薄膜的制备方法 |
| JP2011111660A (ja) * | 2009-11-27 | 2011-06-09 | National Institute Of Advanced Industrial Science & Technology | チタニアナノチューブアレイ及びその形成方法 |
| CN102220616B (zh) * | 2011-05-26 | 2013-02-27 | 东南大学 | 二氧化钛纳米管阵列的制备方法 |
| KR102055772B1 (ko) * | 2011-12-05 | 2019-12-13 | 나노 프리시전 메디컬, 인코포레이티드 | 약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 |
-
2012
- 2012-12-05 KR KR1020147018695A patent/KR102055772B1/ko active IP Right Grant
- 2012-12-05 WO PCT/US2012/067868 patent/WO2013085951A1/en active Application Filing
- 2012-12-05 EP EP12854742.9A patent/EP2788439A4/en active Pending
- 2012-12-05 JP JP2014546010A patent/JP6564187B2/ja active Active
- 2012-12-05 US US14/362,554 patent/US9814867B2/en active Active
- 2012-12-05 CN CN201280059539.3A patent/CN103998536B/zh active Active
-
2018
- 2018-01-26 JP JP2018011874A patent/JP2018109236A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100937167B1 (ko) | 2007-06-05 | 2010-01-15 | 재단법인서울대학교산학협력재단 | 나노 포어 어레이를 이용한 나노 구조체의 제조방법 |
| US20100187172A1 (en) * | 2007-07-26 | 2010-07-29 | The Penn State Research Foundation | Highly-ordered titania nanotube arrays |
| KR101063761B1 (ko) | 2008-11-19 | 2011-09-08 | 경원대학교 산학협력단 | 마개가 형성된 나노튜브를 제조하는 방법 및 이에 의해 제조된 나노튜브 |
| US20100213046A1 (en) * | 2009-01-06 | 2010-08-26 | The Penn State Research Foundation | Titania nanotube arrays, methods of manufacture, and photocatalytic conversion of carbon dioxide using same |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20140106660A (ko) | 2014-09-03 |
| JP2018109236A (ja) | 2018-07-12 |
| EP2788439A4 (en) | 2015-09-02 |
| CN103998536A (zh) | 2014-08-20 |
| EP2788439A1 (en) | 2014-10-15 |
| US9814867B2 (en) | 2017-11-14 |
| CN103998536B (zh) | 2017-09-15 |
| WO2013085951A1 (en) | 2013-06-13 |
| US20140371687A1 (en) | 2014-12-18 |
| JP6564187B2 (ja) | 2019-08-21 |
| JP2015500288A (ja) | 2015-01-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102055772B1 (ko) | 약물 전달을 위한 티타니아 나노튜브 멤브레인을 갖는 디바이스 | |
| Jung et al. | Microneedle for transdermal drug delivery: current trends and fabrication | |
| JP5923007B2 (ja) | 物質投与用インプラント及びインプラントの製造方法 | |
| US6875208B2 (en) | Microchip devices with improved reservoir opening | |
| WO2013057819A1 (ja) | マイクロニードル溶着法 | |
| US6123861A (en) | Fabrication of microchip drug delivery devices | |
| US7465661B2 (en) | High aspect ratio microelectrode arrays | |
| US20030114366A1 (en) | Microfabricated particles and method for treating solid tumors | |
| TW201220386A (en) | Substrate treatment method and substrate treatment apparatus | |
| JP2004337616A5 (ko) | ||
| JP2006509534A5 (ko) | ||
| TW200908117A (en) | Cleaning method and method for manufacturing electronic device | |
| KR101271952B1 (ko) | 탄소 캡슐화된 방사성 입자의 주사가능한 방사성 조성물의제조 방법 | |
| KR101495686B1 (ko) | 방사성 에어로졸의 개선된 제조 방법 | |
| KR101847984B1 (ko) | 약물 전달 장치 | |
| JP7093356B2 (ja) | スカフォールド用のx線マーカー | |
| JP6198373B2 (ja) | マイクロニードル | |
| US7029986B2 (en) | Bonded products and methods of fabrication therefor | |
| TW200901360A (en) | Methods of and apparatus for aligning electrodes in a process chamber to protect an exclusion area within an edge environ of a wafer | |
| WO2018208222A1 (en) | Pyramidal microneedles with enhanced drug loading capacity and method for manufacturing | |
| US20220226639A1 (en) | Graphene cochlear implant electrode and manufacturing method thereof | |
| EP2633840A2 (en) | Punctal plug with energized containment array | |
| CN112670440B (zh) | 一种利用射流注射法制备微电极的方法 | |
| JP3824681B2 (ja) | 陽極接合装置 | |
| JP3360616B2 (ja) | 結晶成長方法および結晶成長用装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| X091 | Application refused [patent] | ||
| AMND | Amendment | ||
| X701 | Decision to grant (after re-examination) | ||
| GRNT | Written decision to grant |