JP7635657B2 - ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 - Google Patents
ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 Download PDFInfo
- Publication number
- JP7635657B2 JP7635657B2 JP2021109635A JP2021109635A JP7635657B2 JP 7635657 B2 JP7635657 B2 JP 7635657B2 JP 2021109635 A JP2021109635 A JP 2021109635A JP 2021109635 A JP2021109635 A JP 2021109635A JP 7635657 B2 JP7635657 B2 JP 7635657B2
- Authority
- JP
- Japan
- Prior art keywords
- bisphenol
- solution
- group
- ketone
- producing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Polyesters Or Polycarbonates (AREA)
Description
また、ポリカーボネート樹脂については、設計通りの分子量を有し、かつ色調が良好なポリカーボネート樹脂が求められている。このため、このようなポリカーボネート樹脂を製造するために、原料であるビスフェノールについては、溶融色に優れたビスフェノールが求められている。
[1] ビスフェノールの製造方法であって、
ビスフェノール溶液に酸化剤を添加した後、還元剤を添加する酸化還元工程を有する、ビスフェノールの製造方法。
[2] 前記ビスフェノール溶液が、
酸性触媒の存在下、ケトン又はアルデヒドと、芳香族アルコールとを縮合反応させて生成させて得られた反応工程の後、反応工程により得られた反応液の有機層を中和処理する中和工程によって得られた溶液である、[1]に記載のビスフェノールの製造方法。
[3] 前記ビスフェノール溶液が、
ビスフェノール組成物を有機溶媒に溶解させて得られた溶液である、[1]に記載のビスフェノールの製造方法。
[4] 前記ケトン又はアルデヒドが、アセトン又はアセトアルデヒドである、[2]に記載のビスフェノールの製造方法
[5] 前記ケトン又はアルデヒドが、ケトンである、[2]に記載のビスフェノールの製造方法。
[6] 前記ビスフェノールが、2,2-ビス(4-ヒドロキシ-3-メチルフェニル)プロパンである、[1]~[5]のいずれかに記載のビスフェノールの製造方法。
[7] [1]~[6]のいずれかに記載のビスフェノールの製造方法により製造したビスフェノールを原料に用いてポリカーボネート樹脂を重合する工程を有する、ポリカーボネート樹脂の製造方法。
本発明の一実施形態に係るビスフェノールの製造方法(以下、単に「ビスフェノールの製造方法」とも称する。)は、ビスフェノール溶液に酸化剤を添加した後、還元剤を添加する酸化還元工程を有する、ビスフェノールの製造方法である。
本実施形態に係るビスフェノールの製造方法は、上記の酸化還元工程以外の工程を有していてもよい。
本実施形態に係るビスフェノールの製造方法により、上記の効果が得られる理由を本発明者らは以下のように考察する。本発明者らによる鋭意研究の結果、酸化剤で酸化された後、還元剤で還元されて生成された成分であり、かつ、有機相と水相とに分離させたときに水相に含まれる成分(色調悪化原因成分)が、色調悪化の原因であることが判明した。そして本発明者らは、ビスフェノール溶液に対して、酸化剤を添加した後、還元剤を添加することにより、溶液中の色調悪化原因成分の量を低減させることができる、すなわち色調が良好なビスフェノールを製造することができることを見出した。
ビスフェノール溶液が、第1のビスフェノール溶液である場合、つまり、酸性触媒の存在下、ケトン又はアルデヒドと、芳香族アルコールとを縮合反応させて生成させて得られた反応工程の後、反応工程により得られた反応液の有機層を中和処理する中和工程によって得られる溶液である場合について以下に説明する。
第1のビスフェノール溶液の製造方法(以下、本項において「本実施形態に係るビスフェノールの製造方法」とも称する。)は、酸性触媒の存在下、アセトン又はアルデヒドと、芳香族アルコールとを縮合反応させてビスフェノールを生成させてビスフェノール溶液を得る反応工程を有する。
芳香族アルコールは、1種を単独で用いても、2種以上を任意の組み合わせ及び比率で用いてもよい。
本発明者らは、色調悪化原因成分が、酸化剤の添加及び還元剤の添加によって水相に分離されるアルデヒド由来の一部の成分であることを見出した。したがって、本実施形態に係るビスフェノールの製造方法に用いるケトン又はアルデヒドとしては、色調悪化原因成分を生成し得るアルデヒドの含有量が低いことが好ましいことから、ケトンであることが好ましく、具体的には、上記のR5とR6は水素原子以外の基であることが好ましい。なお、色調悪化成分は、アルデヒドから生成された全ての化合物が相当するわけではなく、アルデヒドから生成され得る一部の化合物である。
R5とR6とが隣接する炭素原子と一緒に結合し形成されるシクロアルキリデン基としては、例えば、シクロプロピリデン、シクロブチリデン、シクロペンチリデン、シクロヘキシリデン、3,3,5-トリメチルシクロヘキシリデン、シクロヘプチリデン、シクロオクチリデン、シクロノニリデン、シクロデシリデン、シクロウンデシリデン、シクロドデシリデン、フルオレニリデン、キサントニリデン、チオキサントニリデンなどが挙げられる。
ルデヒド、プロピオンアルデヒド、ブチルアルデヒド、ペンタンアルデヒド、ヘキサンアルデヒド、ヘプタンアルデヒド、オクタンアルデヒド、ノナンアルデヒド、デカンアルデヒド、ウンデカンアルデヒド、ドデカンアルデヒドなどのアルデヒド類、アセトン、ブタノン、ペンタノン、ヘキサノン、ヘプタノン、オクタノン、ノナノン、デカノン、ウンデカノン、ドデカノンなどのケトン類、ベンズアルデヒド、フェニルメチルケトン、フェニルエチルケトン、フェニルプロピルケトン、クレジルメチルケトン、クレジルエチルケトン、クレジルプロピルケトン、キシリルメチルケトン、キシリルエチルケトン、キシリルプロピルケトンなどのアリールアルキルケトン、シクロプロパノン、シクロブタノン、シクロペンタノン、シクロヘキサノン、シクロヘプタノン、シクロオクタノン、シクロノナノン、シクロデカノン、シクロウンデカノン、シクロドデカノンなどの環状アルカンケトン類等が挙げられる。アルデヒドとしては、アセトアルデヒドであることが好ましく、ケトンとしては、アセトンであることが好ましく、特に、アセトンを用いることが好ましい。
ケトン又はアルデヒドは、1種を単独で用いても、2種以上を任意の組み合わせ及び比率で用いてもよい。
本明細書における「質量」は、特段の断りがない限り、対象の要素が単一種から構成される場合には、その単一種の質量を示し、対象の要素が複数種から構成される場合には、その複数種の合計の質量を示す。
本実施形態に係るビスフェノールの製造方法で用いられる酸性触媒の種類は特段制限されず、硫酸、塩酸、塩化水素ガス、リン酸、p-トルエンスルホン酸等の芳香族スルホン酸、又はメタンスルホン酸等の脂肪族スルホン酸等を用いることができるが、反応性及び経済性の観点から、硫酸又は塩酸であることが好ましい。
多量化が進行する場合ある。これらのことから、縮合に用いるケトン又はアルデヒドに対する酸触媒のモル比は、好ましくは0.01以上、より好ましくは0.05以上、更に好ましくは0.1以上であり、また、好ましくは10以下、より好ましくは8以下、更に好ましくは5以下である。
また、本実施形態に係るビスフェノールの製造方法では、ケトン又はアルデヒドと、芳香族アルコールとを縮合させる反応において、助触媒としてチオール助触媒を用いることができる。助触媒として用いるチオール助触媒としては、例えば、メルカプト酢酸、チオグリコール酸、2-メルカプトプロピオン酸、3-メルカプトプロピオン酸、4-メルカプト酪酸などのメルカプトカルボン酸や、メチルメルカプタン、エチルメルカプタン、プロピルメルカプタン、ブチルメルカプタン、ペンチルメルカプタン、へキシルメルカプタン、へプチルメルカプタン、オクチルメルカプタン、ノニルメルカプタン、デシルメルカプタン(デカンチオール)、ウンデシルメルカプタン(ウンデカンチオール)、ドデシルメルカプタン(ドデカンチオール)、トリデシルメルカプタン、テトラデシルメルカプタン、ペンタデシルメルカプタン、メルカプトフェノールなどのアルキルチオールなどが挙げられるが、メルカプトカルボン酸は親水性が高いためにビスフェノール原料と混合し難いため、アルキルチオールが好ましく、アルキルチオールとしては、アルキル基が小さいと沸点が低く、取り扱いが難しい(臭気)ため、炭素数が6以上のものであることが好ましく、特に、手に入りやすく、親油性であり、沸点が高くハンドリングが容易である観点から、ドデシルメルカプタン(ドデカンチオール)が好ましい。
また、縮合に用いるケトン又はアルデヒドに対するチオール助触媒のモル比は、多い場合、ビスフェノールに混入して品質が悪化する場合がある。これらのことから、ケトン又はアルデヒドに対するチオール助触媒のモル比は、好ましくは0.001以上、より好ましくは0.005以上、更に好ましくは0.01以上であり、また、好ましくは1以下、より好ましくは0.5以下、更に好ましくは0.1以下である。
本実施形態に係るビスフェノールの製造方法では、芳香族アルコールとケトン又はアルデヒドとの縮合反応を、溶媒の存在下で行ってもよい。溶媒としては、ビスフェノールの生成反応を阻害しない範囲で特に限定されず、芳香族炭化水素、脂肪族アルコール、脂肪族炭化水素などが挙げられ、これらの溶媒を単独で用いても、2種以上を併用して用いて
もよい。
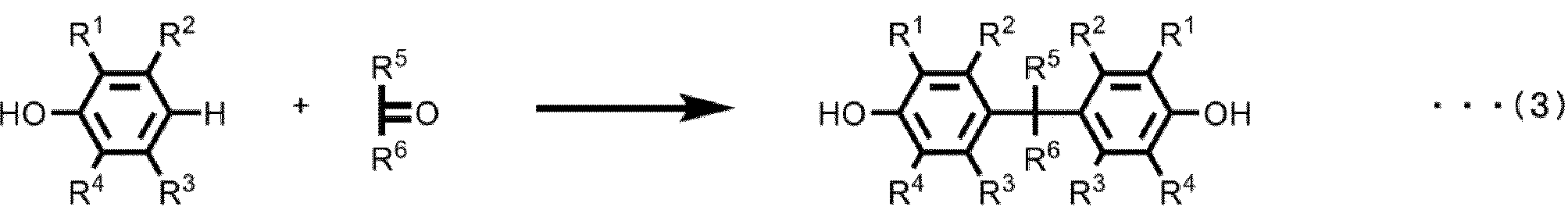
本実施形態に係るビスフェノールの製造方法では、以下に示す反応式(3)に従って、ケトン又はアルデヒドと、芳香族アルコールとの縮合により、以下の一般式(4)で表さ
れるビスフェノールが製造される。
ビスフェノールの生成反応が発熱反応であることから、ケトン又はアルデヒドを含有する溶液の供給は、少しずつ滴下して供給するなど分割して供給することが好ましい。
ケトン又はアルデヒドを含有する溶液の供給時間(滴下時間)は、反応槽の冷却能力や製造スケール、製造されるビスフェノールの種類等に応じて適宜調整され、反応槽の冷却能力等によるが、例えば、0.3時間以上又は0.5時間以上とすることができ、また、例えば、5時間以下、3時間以下、又は1時間以下とすることができる。このようにすることで、反応熱の発生を抑えながら、ビスフェノール溶液を調製することができる。
前記反応工程の後、さらに、反応工程により得られた反応液の有機層を中和処理する中和工程を有する。
中和処理では、縮合反応によって得られたビスフェノールにおいて、酸触媒を中和し、除去することができ、具体的には、ビスフェノールを含有する有機相と、脱塩水又は塩基性水溶液とを混合した後、有機相と水相とに相分離させ、水相を除去し、有機相を得る。
この除去される水相のpHが7.5以上、13.0以下、又は8.0以上、12.5以下、又は8.5以上、12.0以下の塩基性になるまで、脱塩水及び/又は塩基性水溶液を用いて、有機相の洗浄を繰り返し行う。塩基性水溶液としては、水酸化ナトリウム又は炭酸水素ナトリウム等の塩基物質が溶解した水溶液が挙げられる。複数回洗浄を行う場合は、同一の塩基性水溶液を用いても、異なる塩基性水溶液を用いてもよい。
水相のpHの測定温度は、室温(20~30℃)が好ましく、例えば25℃が好ましい。
水相の電気伝導度の測定温度は、室温(20~30℃)が好ましく、例えば25℃が好ましい。
本実施形態に係るビスフェノールの製造方法は、上述の反応工程と後述の酸化還元工程との間に、さらに、反応工程により得られたビスフェノール溶液を精製する工程、具体的には、晶析やカラムクロマトグラフィー等の手段により精製する工程を有していてよい。精製手段としては、作業容易性及び経済性の観点から、晶析が好ましく、この場合、本実施形態に係るビスフェノールの製造方法は、反応により得られたビスフェノール溶液を晶析してビスフェノール組成物を得た後、該ビスフェノール組成物を有機溶媒に溶解させてビスフェノール溶液を得る精製工程を有する。
晶析を行う場合、ビスフェノール溶液の有機相を冷却し晶析させてよく、芳香族アルコールを多量に用いる場合は、該晶析前に蒸留による余剰の芳香族アルコールを留去してから晶析させてよい。
晶析は複数回行ってもよい。例えば、本実施形態に係るビスフェノールの製造方法が第2の精製工程が有する場合、第1の精製工程と後述する酸化還元工程との間に、さらに、ビスフェノール溶液を晶析してビスフェノール組成物を得た後、該ビスフェノール組成物を有機溶媒に溶解させてビスフェノール溶媒を得る第2の精製工程を有していてよい。第2の精製工程の条件は、上述の精製工程の条件を同様に適用することができる。このように、精製工程を繰り返すことにより、第3の精製工程を有していてもよく、第4の精製工程を有していてもよいが、晶析の際にビスフェノールが一部母液に溶解し損失となるため、好ましくは5回以下であり、より好ましくは3回以下である。
晶析のための冷却温度は、特段制限されないが、冷却温度は高すぎると結晶が十分に析出しないため、通常30℃以下であり、25℃以下であることが好ましく、20℃以下であることがより好ましく、15℃以下であることがさらに好ましく、また、通常-30℃以上であり、-20℃以上であることが好ましく、-15℃以上であることがより好まし
く、-10℃以上であることがさらに好ましい。
晶析のための冷却時間は、特段制限されず、所望の量が入手できるまで行うことが好ましい。
晶析したビスフェノールを有機溶媒に溶解させることによって得られるビスフェノール溶液中の有機溶媒の含有量は、特段制限されないが、晶析時のビスフェノール濃度が高すぎると、結晶の成長を阻害し、また、流動性の悪化により抜出の際に配管の閉塞等のトラブルが生じるため、通常1質量%以上であり、5質量%以上であることが好ましく、10質量%以上であることがより好ましく、15質量%以上であることがさらに好ましく、また、経済的観点から、通常95質量%以下であり、85質量%以下であることが好ましく、80質量%以下であることがより好ましく、75質量%以下であることがさらに好ましい。
ビスフェノール溶液が、第2のビスフェノール溶液である場合、つまり、ビスフェノール組成物を有機溶媒に溶解させて得られたビスフェノール溶液である場合について、以下に説明する。
ビスフェノール組成物を有機溶媒に溶解させてビスフェノール溶液を得る方法は、特段制限されないが、例えば、上記の精製工程における、ビスフェノール組成物を有機溶媒に
溶解させてビスフェノール溶液を得る方法を同様に適用することができる。
ビスフェノール組成物は、ビスフェノールが含まれていれば特段制限されず、ビスフェノール以外の成分が含まれていてよく、例えば、上述した「1-2.精製工程」で説明したビスフェノール組成物を用いてもよく、具体的には、上述の反応工程、中和工程、及び精製工程を経て調製されたビスフェノール組成物であってよい。また、ビスフェノール組成物の形態は特段制限されないが、通常、固体である。
ビスフェノール組成物中に含まれるビスフェノールの種類は特段制限されず、上述の第1のビスフェノール溶液で説明したビスフェノールであってよい。ビスフェノール組成物中のビスフェノールの含有量は、特段制限されないが、少ないと経済的でなく、多すぎると均一溶液となり得ない観点から、通常0.1質量%以上であって、0.5質量%以上であることが好ましく、1質量%以上であることがより好ましく、5質量%以上であることがさらに好ましく、また、通常90質量%以下であって、85質量%以下であることが好ましく、80質量%以下であることがより好ましく、75質量%以下であることがさらに好ましい。
ビスフェノール組成物は、ビスフェノール以外の成分を含んでいてよく、例えば、クレゾール、フェノール、キシレノール、が挙げられる。
また、ビスフェノール組成物を溶解させるための有機溶媒の種類は特段制限されず、上述の第1のビスフェノール溶液で説明した有機溶媒であってよい。
また、第2のビスフェノール溶液は、ビスフェノール組成物及び有機溶媒以外の成分を含有していてもよい。
ビスフェノール溶液中の有機溶媒の含有量は、特段制限されないが、少ないと経済的でなく、多すぎると均一溶液となり得ない観点から、通常0.1質量%以上であって、0.5質量%以上であることが好ましく、1質量%以上であることがより好ましく、5質量%以上であることがさらに好ましく、また、通常90質量%以下であって、85質量%以下であることが好ましく、80質量%以下であることがより好ましく、75質量%以下であることがさらに好ましい。
本実施形態に係るビスフェノールの製造方法は、ビスフェノール溶液に、酸化剤を添加した後、還元剤を添加する酸化還元工程を有する。上述したように、酸化剤で酸化された後、還元剤で還元されて生成された成分であり、かつ、有機相と水相とに分離させたときに水相に含まれる成分(色調悪化原因成分)が、色調悪化の原因であることを本発明者らは見出した。よって、この色調悪化原因成分を酸化還元済み溶液から排水として除去することにより、該溶液中の色調悪化原因成分の量を低減させることができる、すなわち色調が良好なビスフェノールを製造することができる。
ビスフェノール溶液へ酸化剤を添加する方法、及び還元剤を添加する方法は、特段制限されず、公知の方法により行うことができ、適宜攪拌しながら行うことができる。
なお、酸化還元の処理は、1回のみ実施してもよく、複数回実施してもよい。
また、酸化処理と還元処理との間に別の処理を行ってもよいが、連続で行うことが好ましい。
、又は過マンガン酸カリウム水等を用いることができ、酸化剤が無色である方が好ましい観点から、過酸化水素水、塩素酸水、又は次亜塩素酸塩水が好ましく、過酸化水素水が特に好ましい。有機溶媒は、1種を単独で用いても、2種以上を任意の組み合わせ及び比率で用いてもよい。
ビスフェノール溶液において、ビスフェノールに対する還元剤の質量比は、特段制限されないが、少ないと効果が得られず、多いと廃水処理の負荷が増加する観点から、通常0.00001以上であり、0.0005以上であることが好ましく、0.001以上であることがより好ましく、0.005以上であることがさらに好ましく、また、通常10以下であり、5以下であることが好ましく、1以下であることがより好ましく、0.5以下であることがさらに好ましい。
本実施形態に係るビスフェノールの製造方法は、上述の酸化還元工程により得られた酸化還元処理済み溶液を濃縮することにより、該溶液中のビスフェノールを回収する濃縮工程を有していてよい。
濃縮する手段は特段制限されず、公知の方法を適用することができ、例えば、晶析処理を適用する場合、固体のビスフェノールを得ることができ、上述の精製工程で説明した晶
析処理の条件を適用することができる。また、晶析処理以外の手段としては、遠心分離法等の固液分離法を利用するこができ、この方法によれば固体のビスフェノールを得ることができる。
上述したビスフェノールの製造方法において得られるビスフェノールは、光学材料、記録材料、絶縁材料、透明材料、電子材料、接着材料、耐熱材料など種々の用途に用いられるポリエーテル樹脂、ポリエステル樹脂、ポリアリレ-ト樹脂、ポリカーボネート樹脂、ポリウレタン樹脂、アクリル樹脂など種々の熱可塑性樹脂や、エポキシ樹脂、不飽和ポリエステル樹脂、フェノール樹脂、ポリベンゾオキサジン樹脂、又はシアネート樹脂など種々の熱硬化性樹脂などの樹脂の原料として用いることができる。また、硬化剤、添加剤、又はこれらの前駆体などとして用いることができる。さらに、感熱記録材料等の顕色剤、退色防止剤、殺菌剤、又は防菌防カビ剤等の添加剤としても有用である。
本発明の別の実施形態は、上記の製造方法により得られたビスフェノールを原料に用いてポリカーボネート樹脂を重合する工程を有する、ポリカーボネート樹脂の製造方法(以下、単に「ポリカーボネート樹脂の製造方法」とも称する。)である。
ポリカーボネート樹脂の製造方法は、上記のビスフェノールと、炭酸ジフェニル等の炭酸ジエステルとを、例えば、アルカリ金属化合物及び/又はアルカリ土類金属化合物の存在下でエステル交換反応させる方法などにより製造する方法である。上記エステル交換反応は、公知の方法を適宜選択して行うことができるが、以下にビスフェノール及び炭酸ジフェニルを原料に用いた製造方法の一例を説明する。
エステル交換法によるポリカーボネート樹脂の製造においては、通常、原料混合槽に供給された両原料は、均一に攪拌された後、エステル交換触媒が添加される重合槽に供給され、ポリマーが生産される。
以下の実施例および比較例において、オルトクレゾール、トルエン、水酸化ナトリウム、98質量%硫酸、ドデカンチオール、アセトン、アセトアルデヒド、炭酸水素ナトリウム、炭酸セシウム、アセトニトリル、酢酸、酢酸アンモニウム、及び富士フィルム和光純薬株式会社製の試薬を使用した。
炭酸ジフェニルは、三菱ケミカル株式会社製の製品を使用した。
<ビスフェノールCの分析>
ビスフェノールの組成分析は、高速液体クロマトグラフィーにより、以下の手順と条件で行った。以下の各実施例で得られたビスフェノールはビスフェノールCであり、その純度は通常99質量%以上であることから、この分析では、得られた固体がビスフェノール
Cであることを確認するために用いた。
・装置:島津製作所社製「LC-2010A」
Imtakt ScherzoSM-C18 3μm 250mm×3.0mmID・低圧グラジェント法
・分析温度:40℃
・溶離液組成:
A液 酢酸アンモニウム:酢酸:脱塩水=3.000g:1mL:1Lの溶液
B液 酢酸アンモニウム:酢酸:アセトニトリル:脱塩水=1.500g:1mL:900mL:150mLの溶液
・分析時間0分では、溶離液組成はA液:B液=60:40(体積比、以下同様。)
分析時間0~41.67分はA液:B液=10:90へ徐々に変化させ、
分析時間41.67~50分はA液:B液=10:90に維持、
流速0.34mL/分にて分析した。
pHの測定は、株式会社堀場製作所製pH計「pH METER ES-73」を用いて、フラスコから取り出した25℃の水相に対して実施した。
電気伝導度の測定は、株式会社堀場製作所製電気伝導度計「COND METER D-71」を用いて、フラスコから取り出した25℃の水相に対して実施した。
ビスフェノールの溶融色は、日電理化硝子社製試験管「P-24」(24mmφ×200mm)にビスフェノールCを20g入れて、190℃で30分間溶融させ、日本電色工業社製「SE6000」を用い、そのハーゼン色数を測定した。
(1-1)ビスフェノールCの製造
温度計、滴下ロート、ジャケット及びイカリ型撹拌翼を備えたセパラブルフラスコに、窒素雰囲気下でトルエン320g、オルトクレゾール230g、及びメタノール15gを入れ、内温を10℃以下に維持しつつ、撹拌しながら98質量%硫酸95gを入れ、混合液A1とした。
次に、三角フラスコにアセトン65g、ドデカンチオール5g、及びトルエン50gを入れて攪拌して混合液B1を得て、滴下ロートに入れた。
混合液A1を10℃以下に維持した状態で、該滴下ロート内の混合液B1を撹拌しながら1時間分かけて混合液A1へ滴下し、10℃に維持した状態で更に2時間撹拌し、ビスフェノールCのビスフェノール溶液C1を得た。
ビスフェノール溶液C1に25%水酸化ナトリウム溶液190gを加えて撹拌し75℃まで昇温した後、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相D1を得た。
75℃で得られた有機相D1に、脱塩水100gを加え、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相E1を得た。
得られた有機相E1に、3重量%炭酸水素ナトリウム溶液100gを加えて撹拌して中和し、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相F1を得た。
得られた有機相F1に、脱塩水100gを加え、1時間攪拌して、静置させて油水分離した。油水分離後、水相1をセパラブルフラスコの底から除去し、有機相G1を得た。得られた水相1は525μS/cmであったが、水相が10μS/cm以下になるまで、脱塩水100gで有機相の水洗を繰り返し、有機相H1を得た。
有機相H1を75℃から5℃まで徐々に冷却し、ビスフェノールC含有結晶を析出させた。得られたビスフェノールC含有結晶を含むスラリー液を、遠心分離機により固液分離を行い、ビスフェノールC含有ケーキ180gを得た。
オイルバスを備えたエバポレータを用いて、減圧下オイルバス温度90℃で軽沸分を留去することで、白色固体152gを得た。得られた白色固体の一部を、高速液体クロマトグラフィーを用いて、ビスフェノールCであることを確認した。
(1-2)ビスフェノールCの色調
上記の(1-1)で得られたビスフェノールCの溶融色を測定したところ、ハーゼン色数は15であった。
(2-1)ビスフェノールCの製造
温度計、滴下ロート、ジャケット及びイカリ型撹拌翼を備えたセパラブルフラスコに、窒素雰囲気下でトルエン320g、オルトクレゾール230g、及びメタノール15gを入れ、内温を10℃以下に維持しつつ、撹拌しながら98質量%硫酸95gを入れ、混合液A1とした。
次に、三角フラスコにアセトン65g、ドデカンチオール5g、及びトルエン50gを入れて攪拌して混合液B1を得て、滴下ロートに入れた。
混合液A1を10℃以下に維持した状態で、該滴下ロート内の混合液B1を撹拌しながら1時間分かけて混合液A1へ滴下し、ビスフェノールCのビスフェノール溶液C1’を得た。
更に、アセトアルデヒド4gを該滴下ロートに入れ、滴下ロートを用いてビスフェノールの反応液C1’に10℃に維持した状態でアセトアルデヒドを供給した後に、更に2時間撹拌し、ビスフェノールCのビスフェノール溶液C2を得た。
ビスフェノール溶液C2に25%水酸化ナトリウム溶液190gを加えて撹拌し75℃まで昇温した後、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相D1を得た。
75℃で得られた有機相D1に、脱塩水100gを加え、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相E1を得た。
得られた有機相E1に、3重量%炭酸水素ナトリウム溶液100gを加えて撹拌して中和し、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相F1を得た。
得られた有機相F1に、脱塩水100gを加え、1時間攪拌して、静置させて油水分離した。油水分離後、水相1をセパラブルフラスコの底から除去し、有機相G1を得た。得られた水相1は625μS/cmであったが、水相が10μS/cm以下になるまで、脱塩水100gで有機相の水洗を繰り返し、有機相H1を得た。
有機相H1を75℃から5℃まで徐々に冷却し、ビスフェノールC含有結晶を析出させた。得られたビスフェノールC含有結晶を含むスラリー液を、遠心分離機により固液分離を行い、ビスフェノールC含有ケーキ160gを得た。
オイルバスを備えたエバポレータを用いて、減圧下オイルバス温度90℃で軽沸分を留去することで、白色固体140gを得た。得られた白色固体の一部を、高速液体クロマトグラフィーを用いて、ビスフェノールCであることを確認した。
(1-2)ビスフェノールCの色調
(1-1)で得られたビスフェノールCの溶融色を測定したところ、ハーゼン色数は87であった。
参考例1で得られたハーゼン色数(APHA)15のビスフェノールC 67gと参考例2で得られたハーゼン色数(APHA)87のビスフェノールC 100gを500リットルのポリ容器に入れ、十分に混合して、ビスフェノールC混合物を得た。得られたビスフェノールC混合物の溶融色を測定したところ、ハーゼン色数(APHA)が58であった。
温度計、滴下ロート、ジャケット及びイカリ型撹拌翼を備えたセパラブルフラスコに、窒素雰囲気下で、参考例3で得られたビスフェノールC混合物50g、トルエン100g、5質量%過酸化水素水100gを入れた後、75℃まで昇温した。その後、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相1を得た。
得られた有機相1に5質量%クエン酸ナトリウム水溶液100gを加え、1時間攪拌した。その後、静置させて油水分離した。油水分離後、水相をセパラブルフラスコの底から除去し、有機相2を得た。
得られた有機相2に、脱塩水100gを加え、1時間攪拌した。その後、静置させて油水分離した。油水分離後、水相1をセパラブルフラスコの底から除去し、有機相3を得た。得られた水相1の電気伝導度は734μS/cmであったが、水相が10μS/cm以下になるまで、脱塩水100gで有機相の水洗を繰り返し、有機相4を得た。
有機相4を75℃から5℃まで徐々に冷却し、ビスフェノールC含有結晶を析出させた。得られたビスフェノールC含有結晶を含むスラリー液を、遠心分離機により固液分離を行い、ビスフェノールC含有ケーキ40gを得た。
オイルバスを備えたエバポレータを用いて、減圧下オイルバス温度90℃で軽沸分を留去することで、白色固体25gを得た。得られた白色固体の一部を、高速液体クロマトグラフィーを用いて、ビスフェノールCであることを確認した。得られたビスフェノールCの色調を測定したところ、ハーゼン色数(APHA)が30であった。
5質量%過酸化水素水100gも、5質量%クエン酸ナトリウム水溶液100gを加えなかったこと以外は実施例1と同様に実施してビスフェノールCを得た。得られたビスフェノールCの色調を測定したところ、ハーゼン色数(APHA)が38であった。
5質量%過酸化水素水100gを加えなかったこと以外は実施例1と同様に実施してビスフェノールCを得た。得られたビスフェノールCの色調を測定したところ、ハーゼン色数(APHA)が38であった。
5質量%クエン酸ナトリウム水溶液100gを加えなかったこと以外は実施例1と同様に実施してビスフェノールCを得た。得られたビスフェノールCは、ビスフェノールC混合物よりも色調が悪化し、着色が激しいものであった。
下記表1より、ビスフェノールC混合物について、酸化剤を添加した後、還元剤を添加することで、ビスフェノールCの色調が大きく改善することが分かる。
Claims (6)
- ビスフェノールの製造方法であって、
ビスフェノール溶液に酸化剤を添加した後、還元剤を添加する酸化還元工程を有し、
前記ビスフェノール溶液が、
酸性触媒及びチオール助触媒の存在下、ケトン又はアルデヒドと、芳香族アルコールとを縮合反応させて生成させて得られた反応工程の後、反応工程により得られた反応液の有機層を中和処理する中和工程によって得られた溶液である、ビスフェノールの製造方法。 - 前記ビスフェノール溶液が、
前記中和工程によって得られた溶液を精製してビスフェノール組成物を得る精製工程、及び前記精製工程で得られたビスフェノール組成物を有機溶媒に溶解させる工程、により得られた溶液である、請求項1に記載のビスフェノールの製造方法。 - 前記ケトン又はアルデヒドが、アセトン又はアセトアルデヒドである、請求項1又は2に記載のビスフェノールの製造方法。
- 前記ケトン又はアルデヒドが、ケトンである、請求項1又は2に記載のビスフェノールの製造方法。
- 前記ビスフェノールが、2,2-ビス(4-ヒドロキシ-3-メチルフェニル)プロパンである、請求項1~4のいずれか1項に記載のビスフェノールの製造方法。
- 請求項1~5のいずれか1項に記載のビスフェノールの製造方法により製造したビスフェノールを原料に用いてポリカーボネート樹脂を重合する工程を有する、ポリカーボネート樹脂の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021109635A JP7635657B2 (ja) | 2021-06-30 | 2021-06-30 | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021109635A JP7635657B2 (ja) | 2021-06-30 | 2021-06-30 | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023006817A JP2023006817A (ja) | 2023-01-18 |
| JP7635657B2 true JP7635657B2 (ja) | 2025-02-26 |
Family
ID=85107028
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021109635A Active JP7635657B2 (ja) | 2021-06-30 | 2021-06-30 | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7635657B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116874355B (zh) * | 2023-06-25 | 2024-11-22 | 浙江工业大学 | 一种降低苯酚/双酚a产品色度的方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002037872A (ja) | 2000-07-27 | 2002-02-06 | Idemitsu Petrochem Co Ltd | ポリカーボネート樹脂原料およびポリカーボネート樹脂の製造法 |
| JP2004010566A (ja) | 2002-06-10 | 2004-01-15 | Idemitsu Petrochem Co Ltd | ビスフェノールaの製造方法 |
| JP2009500395A (ja) | 2005-07-07 | 2009-01-08 | ブロマイン コンパウンズ リミテッド | テトラブロモビスフェノールaの作製方法 |
-
2021
- 2021-06-30 JP JP2021109635A patent/JP7635657B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002037872A (ja) | 2000-07-27 | 2002-02-06 | Idemitsu Petrochem Co Ltd | ポリカーボネート樹脂原料およびポリカーボネート樹脂の製造法 |
| JP2004010566A (ja) | 2002-06-10 | 2004-01-15 | Idemitsu Petrochem Co Ltd | ビスフェノールaの製造方法 |
| JP2009500395A (ja) | 2005-07-07 | 2009-01-08 | ブロマイン コンパウンズ リミテッド | テトラブロモビスフェノールaの作製方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023006817A (ja) | 2023-01-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7087848B2 (ja) | ビスフェノールの製造方法、及びポリカーボネート樹脂の製造方法 | |
| JP7196438B2 (ja) | ビスフェノールの製造法およびポリカーボネート樹脂の製造法 | |
| JP7172308B2 (ja) | ビスフェノールの製造方法、及びポリカーボネート樹脂の製造方法 | |
| JP7167536B2 (ja) | ビスフェノール製造法、及びポリカーボネート樹脂の製造法 | |
| JP7635657B2 (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP7180344B2 (ja) | ビスフェノールの製造方法、及び、ポリカーボネート樹脂の製造方法 | |
| JP7255109B2 (ja) | ビスフェノールの製造法、及びポリカーボネート樹脂の製造法 | |
| JP7287018B2 (ja) | ビスフェノール組成物及びポリカーボネート樹脂の製造方法 | |
| JP7167537B2 (ja) | ビスフェノール製造方法、及びポリカーボネート樹脂の製造方法 | |
| JP7135610B2 (ja) | ビスフェノールの製造方法、及びポリカーボネート樹脂の製造方法 | |
| JP7615916B2 (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP7615920B2 (ja) | ビスフェノールの製造方法並びにポリカーボネート樹脂の製造方法 | |
| JP7615921B2 (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP7803356B2 (ja) | ビスフェノール組成物及びポリカーボネート樹脂 | |
| JP7631795B2 (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP2023006818A (ja) | ビスフェノールの製造方法並びにポリカーボネート樹脂の製造方法 | |
| JP7287019B2 (ja) | ビスフェノール組成物及びポリカーボネート樹脂の製造方法 | |
| JP7107044B2 (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP2020152650A (ja) | ビスフェノールの製造方法、及びポリカーボネート樹脂の製造方法 | |
| JP2023005689A (ja) | ビスフェノール組成物及びポリカーボネート樹脂の製造方法 | |
| JP2022114119A (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP2022152461A (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP2021123543A (ja) | ビスフェノールの製造方法及びポリカーボネート樹脂の製造方法 | |
| JP2024130529A (ja) | ビスフェノールの製造方法およびポリカーボネート樹脂の製造方法 | |
| JP2021123544A (ja) | ビスフェノールの製造法及びポリカーボネート樹脂の製造法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240312 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241030 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241223 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250114 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250127 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7635657 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |