JP6923549B2 - 灌注式焼灼のための改良されたシステム - Google Patents
灌注式焼灼のための改良されたシステム Download PDFInfo
- Publication number
- JP6923549B2 JP6923549B2 JP2018548898A JP2018548898A JP6923549B2 JP 6923549 B2 JP6923549 B2 JP 6923549B2 JP 2018548898 A JP2018548898 A JP 2018548898A JP 2018548898 A JP2018548898 A JP 2018548898A JP 6923549 B2 JP6923549 B2 JP 6923549B2
- Authority
- JP
- Japan
- Prior art keywords
- electrode
- temperature
- impedance
- orientation
- tissue
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/04—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating
- A61B18/12—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating by passing a current through the tissue to be heated, e.g. high-frequency current
- A61B18/14—Probes or electrodes therefor
- A61B18/1492—Probes or electrodes therefor having a flexible, catheter-like structure, e.g. for heart ablation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/02—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by cooling, e.g. cryogenic techniques
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/04—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/04—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating
- A61B18/12—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating by passing a current through the tissue to be heated, e.g. high-frequency current
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B34/00—Computer-aided surgery; Manipulators or robots specially adapted for use in surgery
- A61B34/20—Surgical navigation systems; Devices for tracking or guiding surgical instruments, e.g. for frameless stereotaxis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B34/00—Computer-aided surgery; Manipulators or robots specially adapted for use in surgery
- A61B34/25—User interfaces for surgical systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/01—Measuring temperature of body parts ; Diagnostic temperature sensing, e.g. for malignant or inflamed tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/01—Measuring temperature of body parts ; Diagnostic temperature sensing, e.g. for malignant or inflamed tissue
- A61B5/015—By temperature mapping of body part
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/05—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves
- A61B5/053—Measuring electrical impedance or conductance of a portion of the body
- A61B5/0538—Measuring electrical impedance or conductance of a portion of the body invasively, e.g. using a catheter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/06—Devices, other than using radiation, for detecting or locating foreign bodies ; determining position of probes within or on the body of the patient
- A61B5/061—Determining position of a probe within the body employing means separate from the probe, e.g. sensing internal probe position employing impedance electrodes on the surface of the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/06—Devices, other than using radiation, for detecting or locating foreign bodies ; determining position of probes within or on the body of the patient
- A61B5/065—Determining position of the probe employing exclusively positioning means located on or in the probe, e.g. using position sensors arranged on the probe
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/25—Bioelectric electrodes therefor
- A61B5/279—Bioelectric electrodes therefor specially adapted for particular uses
- A61B5/28—Bioelectric electrodes therefor specially adapted for particular uses for electrocardiography [ECG]
- A61B5/283—Invasive
- A61B5/287—Holders for multiple electrodes, e.g. electrode catheters for electrophysiological study [EPS]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/04—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating
- A61B18/08—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating by means of electrically-heated probes
- A61B18/082—Probes or electrodes therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B18/04—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating
- A61B18/12—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body by heating by passing a current through the tissue to be heated, e.g. high-frequency current
- A61B18/1206—Generators therefor
- A61B18/1233—Generators therefor with circuits for assuring patient safety
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B2017/00017—Electrical control of surgical instruments
- A61B2017/00022—Sensing or detecting at the treatment site
- A61B2017/00039—Electric or electromagnetic phenomena other than conductivity, e.g. capacity, inductivity, Hall effect
- A61B2017/00044—Sensing electrocardiography, i.e. ECG
- A61B2017/00048—Spectral analysis
- A61B2017/00053—Mapping
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B2017/00017—Electrical control of surgical instruments
- A61B2017/00022—Sensing or detecting at the treatment site
- A61B2017/00084—Temperature
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B2017/00017—Electrical control of surgical instruments
- A61B2017/00115—Electrical control of surgical instruments with audible or visual output
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00005—Cooling or heating of the probe or tissue immediately surrounding the probe
- A61B2018/00011—Cooling or heating of the probe or tissue immediately surrounding the probe with fluids
- A61B2018/00023—Cooling or heating of the probe or tissue immediately surrounding the probe with fluids closed, i.e. without wound contact by the fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00005—Cooling or heating of the probe or tissue immediately surrounding the probe
- A61B2018/00011—Cooling or heating of the probe or tissue immediately surrounding the probe with fluids
- A61B2018/00029—Cooling or heating of the probe or tissue immediately surrounding the probe with fluids open
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00053—Mechanical features of the instrument of device
- A61B2018/00059—Material properties
- A61B2018/00071—Electrical conductivity
- A61B2018/00083—Electrical conductivity low, i.e. electrically insulating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00053—Mechanical features of the instrument of device
- A61B2018/00107—Coatings on the energy applicator
- A61B2018/00136—Coatings on the energy applicator with polymer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00053—Mechanical features of the instrument of device
- A61B2018/00172—Connectors and adapters therefor
- A61B2018/00178—Electrical connectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00053—Mechanical features of the instrument of device
- A61B2018/00297—Means for providing haptic feedback
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00571—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body for achieving a particular surgical effect
- A61B2018/00577—Ablation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00642—Sensing and controlling the application of energy with feedback, i.e. closed loop control
- A61B2018/00648—Sensing and controlling the application of energy with feedback, i.e. closed loop control using more than one sensed parameter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/0066—Sensing and controlling the application of energy without feedback, i.e. open loop control
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00666—Sensing and controlling the application of energy using a threshold value
- A61B2018/00678—Sensing and controlling the application of energy using a threshold value upper
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00696—Controlled or regulated parameters
- A61B2018/00702—Power or energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00696—Controlled or regulated parameters
- A61B2018/00714—Temperature
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00696—Controlled or regulated parameters
- A61B2018/00755—Resistance or impedance
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00773—Sensed parameters
- A61B2018/00791—Temperature
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00773—Sensed parameters
- A61B2018/00791—Temperature
- A61B2018/00797—Temperature measured by multiple temperature sensors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00773—Sensed parameters
- A61B2018/00791—Temperature
- A61B2018/00821—Temperature measured by a thermocouple
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00773—Sensed parameters
- A61B2018/00839—Bioelectrical parameters, e.g. ECG, EEG
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00773—Sensed parameters
- A61B2018/00875—Resistance or impedance
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00898—Alarms or notifications created in response to an abnormal condition
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00636—Sensing and controlling the application of energy
- A61B2018/00904—Automatic detection of target tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B18/00—Surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2018/00988—Means for storing information, e.g. calibration constants, or for preventing excessive use, e.g. usage, service life counter
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B34/00—Computer-aided surgery; Manipulators or robots specially adapted for use in surgery
- A61B34/10—Computer-aided planning, simulation or modelling of surgical operations
- A61B2034/101—Computer-aided simulation of surgical operations
- A61B2034/102—Modelling of surgical devices, implants or prosthesis
- A61B2034/104—Modelling the effect of the tool, e.g. the effect of an implanted prosthesis or for predicting the effect of ablation or burring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2217/00—General characteristics of surgical instruments
- A61B2217/002—Auxiliary appliance
- A61B2217/007—Auxiliary appliance with irrigation system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2218/00—Details of surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body
- A61B2218/001—Details of surgical instruments, devices or methods for transferring non-mechanical forms of energy to or from the body having means for irrigation and/or aspiration of substances to and/or from the surgical site
- A61B2218/002—Irrigation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/68—Arrangements of detecting, measuring or recording means, e.g. sensors, in relation to patient
- A61B5/6846—Arrangements of detecting, measuring or recording means, e.g. sensors, in relation to patient specially adapted to be brought in contact with an internal body part, i.e. invasive
- A61B5/6847—Arrangements of detecting, measuring or recording means, e.g. sensors, in relation to patient specially adapted to be brought in contact with an internal body part, i.e. invasive mounted on an invasive device
- A61B5/6852—Catheters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B8/00—Diagnosis using ultrasonic, sonic or infrasonic waves
- A61B8/12—Diagnosis using ultrasonic, sonic or infrasonic waves in body cavities or body tracts, e.g. by using catheters
Description
本出願は、2016年3月15日に出願された米国仮特許出願第62/308,461号明細書、2016年3月30日に出願された米国仮特許出願第62/315,661号明細書、2016年4月15日に出願された米国仮特許出願第62/323,502号明細書、および2016年11月4日に出願された米国仮特許出願第62/418,057号明細書に対する優先権を主張し、それらの各々の全内容が全体として参照により本明細書に援用される。
去するように、電極を流体源と流体連通させて配置するように構成される、少なくとも1つの流体導管とを含む。
。いくつかの実施形態では、少なくとも1つの層またはコーティングは、100μm未満の厚さを含む。いくつかの構成では、少なくとも1つの層またはコーティングは、単一の層またはコーティングを含む。他の実施形態では、少なくとも1つの層またはコーティングは、2つ以上の層またはコーティングを含む。いくつかの実施形態では、少なくとも1つの層またはコーティングは、少なくとも1つのシャント部材の表面に沿って直接配置される。いくつかの実施形態では、少なくとも1つの層またはコーティングは、少なくとも1つのシャント部材の表面に沿って直接配置されていない。いくつかの実施形態では、少なくとも1つの中間部材または構造は、少なくとも1つのシャント部材と少なくとも1つの層またはコーティングとの間に配置される。いくつかの実施形態では、少なくとも1つの層またはコーティングは、接着剤を用いて少なくとも1つのシャント部材に固定される。いくつかの実施形態では、少なくとも1つの層またはコーティングは、押込み嵌め接続、ディップ成形または他の成形技術を用いて少なくとも1つの熱シャント部材に固定される。
ように構成され、少なくとも1つのプロセッサは、標的解剖学的位置の3次元モデルをユーザに表示する少なくとも1つの出力デバイスに動作可能に結合されるように構成され、プロセッサは、別個の焼灼システムの少なくとも1つの構成要素に動作可能に結合されるように構成され、別個の焼灼システムは、標的解剖学的位置の少なくとも一部を選択的に焼灼するように構成され、別個の焼灼システムは、カテーテルの遠位端に沿って配置された少なくとも1つの電極を含み、少なくとも1つのプロセッサは、別個の焼灼システムから焼灼データを受信するように構成され、焼灼データは、標的解剖学的位置の組織に沿って行われる少なくとも1つの焼灼に関し、マッピングシステムは、標的解剖学的位置の3次元モデルに対する少なくとも1つの電極のリアルタイムの位置を求めて、ユーザが標的解剖学的位置の組織を焼灼することを支援するように構成され、少なくとも1つのプロセッサは、少なくとも1つの出力デバイスにおける表現を生成するように構成され、表現は、標的解剖学的位置の3次元モデル、少なくとも1つの電極のリアルタイムの位置、および別個の焼灼システムから受信される焼灼データの少なくとも一部を含む。
位端を含む細長い本体(例えば、カテーテル、他の医療器具等)と、細長い本体の遠位端に沿って配置された電極アセンブリであって、第1の電極部分と、第1の電極部分に隣接して配置された第2の電極部分であって、前記第1の電極部分および前記第2の電極部分は、対象の組織と接触し、かつ組織を少なくとも部分的に焼灼するのに十分な高周波エネルギーを送達するように構成されている、少なくとも1つの第2の電極部分と、第1の電極部分と第2の電極部分との間に配置された少なくとも1つの電気絶縁ギャップであって、第1の電極部分と第2の電極部分とを分離するギャップ幅を有する、少なくとも1つの電気絶縁ギャップと、少なくとも1つの電気絶縁ギャップ内に配置された少なくとも1つのセパレータであって、第1の電極部分の近位端および第2の電極部分の遠位端と接触する少なくとも1つのセパレータとを含む、電極アセンブリとを含む。デバイスは、エネルギー送達モジュールを第1の電極部分および第2の電極部分のうちの少なくとも1つに電気的に結合するように構成された少なくとも1つの導体であって、エネルギー送達モジュールに電気的に結合され、第1の電極部分および第2の電極部分に提供されるエネルギーの周波数は高周波範囲内にある少なくとも1つの導体をさらに含む。
取得し、異なる周波数で取得されたインピーダンス測定値を処理し、およびインピーダンス測定値の前記処理に基づき、電極アセンブリが組織と接触しているか否かを判断するように構成された処理デバイスとをさらに含み、細長い本体は、少なくとも1つの灌注通路を含み、前記少なくとも1つの灌注通路は、第1の電極部分まで延在する。
部分もしくはセクション)と第3の電極(または電極部分もしくはセクション)との間にギャップが含まれる。いくつかの実施形態では、比は、0.2〜0.8(例えば、0.2〜0.3、0.3〜0.4、0.4〜0.5、0.5〜0.6、0.6〜0.7、0.7〜0.8、上記範囲間の比等)である。いくつかの実施形態では、デバイスは、第2の電極(または電極部分もしくはセクション)と第3の電極(または電極部分もしくはセクション)との間のギャップ内に配置されたセパレータをさらに含む。
にわたって導入される。
通電する間または通電した後に発生する。
の実施形態では、熱的対流流体の流量は、焼灼処置中に電極に沿って所望の温度を維持するためにおよそ5ml/minより小さい。いくつかの実施形態では、焼灼処置中の電極に沿った所望の温度は、60℃である。いくつかの実施形態では、熱的対流流体は、血液および/または別の体液を含む。
いくつかの実施形態では、内部部材は、電極によって生成される熱を放散させかつ/または伝達するように構成された少なくとも1つの熱伝導性材料を含む。
少なくとも一部と直接物理的に接触させる。いくつかの実施形態では、少なくとも1つの開口部は、少なくとも1つの導管または通路の穿孔部分に沿って配置され、少なくとも1つの導管または通路の穿孔部分は、電極の遠位側に配置される。
部材は、炭素系材料(例えば、グラフェン、シリカ等)を含む。いくつかの実施形態では、高周波(RF)電極は、複合電極(例えば、スプリットチップRF電極または他の高分解能電極)を含む。いくつかの実施形態では、本方法は、焼灼部材に隣接する対象の標的解剖学的位置の少なくとも1つの高解像度画像を取得するステップをさらに含む。
解能マッピングが容易になる。カテーテルは、電極から熱的に絶縁され、かつある深さで組織温度を検出するように構成された複数の温度センサ(例えば、熱電対)をさらに含むことができる。カテーテルはまた、電極および/または治療されている組織から離れるように熱を伝達する1つもしくは複数の熱シャント部材および/または構成要素も含むことができる。いくつかの実施形態では、こうした熱シャント部材および/または構成要素は、ダイヤモンド(例えば、工業用ダイヤモンド)および/または好ましい熱拡散率特徴を有する他の材料を含む。さらに、電極と標的組織との間で接触が達成されたか否かおよびどの程度達成されたかを検出するようにシステムを構成することができる。
、デバイスは、第1の電極および第2の電極の少なくとも1つにエネルギー送達モジュール(例えば、RF発生器または他の発生器)を電気的に結合するように構成された少なくとも1つの導体(例えば、ワイヤ、ケーブル等)をさらに含む。いくつかの実施形態では、デバイスは、前記電極によってピックアップされる信号(例えば、心臓信号)を電気生理学(EP)レコーダに分配する、第1の電極および第2の電極の各々に結合された1つまたは複数のさらなる導体をさらに含む。
て分離される複合電極(例えば、スプリットチップ電極またはスプリットセクション電極等)に通電するステップであって、第2の電極は、第1の電極の近位側に配置され、第1の電極および第2の電極は、対象の組織と接触して、かつ組織を少なくとも部分的に焼灼するのに十分なエネルギーを送達するように、および高分解能マッピングデータを受信するように構成され、高分解能マッピングは、第1の電極および第2の電極に隣接する対象の組織に関する、ステップを含む。いくつかの実施形態では、電気絶縁ギャップは、第1の電極と第2の電極との間に配置され、電気絶縁ギャップは、第1の電極と第2の電極とを分離するギャップ幅を有する。いくつかの実施形態では、フィルタリング素子は、動作RF周波数範囲でのみ第1の電極を第2の電極に電気的に結合する。一実施形態では、第1の電極および第2の電極を電気的に分離することにより、標的解剖学的領域に沿った高分解能マッピングが容易になる。
流流体の流量は、焼灼処置中に電極に沿って所望の温度を維持するために略10ml/minより小さい。いくつかの実施形態では、熱的対流流体の流量は、焼灼処置中に電極に沿って所望の温度を維持するために略5ml/minより小さい。いくつかの実施形態によれば、焼灼処置中の電極に沿った所望の温度は、60℃である。
生成される熱を除去しかつ放散させるのに役立つように、少なくとも部分的に焼灼部材の内部を通って延在する。いくつかの実施形態では、少なくとも1つの熱シャント部材は、少なくとも部分的に細長い本体の内部を通って延在する少なくとも1つの流体導管または通路と熱連通し、少なくとも1つの流体導管または通路は、焼灼部材を流体源と流体連通させて、焼灼部材および/または焼灼部材に隣接して配置された対象の組織から選択的に熱を除去する。
i)デバイスに選択的に通電する発生器および(ii)電気生理学レコーダの少なくとも1つをさらに含む。
例えば、RF電極、複合電極等)と、カテーテルの内部を通って焼灼部材までまたはその近くまで延在する灌注導管と、焼灼部材を選択的に活性化する少なくとも1つの導体(例えば、ワイヤ、ケーブル等)と、焼灼部材の少なくとも一部(例えば、焼灼部材の近位部分)を灌注導管と熱連通させる少なくとも1つの伝熱部材とからなる。
的位置まで前進される。いくつかの実施形態では、対象の体内腔は、血管、気道の気管もしくは別の管腔、消化管の管腔、尿管、または別の体内腔を含む。
から熱的に絶縁されている。第2の複数の温度測定デバイスは、少なくとも1つのエネルギー送達部材の近位端のすぐ近位にまたはすぐ遠位に配置することができる。医療器具が2つ以上のエネルギー送達部材を含む場合、第2の複数の温度測定デバイスは、最近位のエネルギー送達部材の近位縁に隣接して配置することができ、第1の複数の温度測定デバイスは、最遠位のエネルギー送達部材内に配置することができる。いくつかの実施形態では、第2の複数の温度測定デバイスは、少なくとも1つのエネルギー送達部材の近位側の熱シャント部材(例えば、伝熱部材)に沿って配置される。いくつかの実施形態では、第2の複数の温度測定デバイスは、細長い本体の遠位端の長手方向軸に対して垂直または実質的に垂直である平面に沿って配置され、第1の複数の温度測定デバイスに対して近位側に離間される。
在する。
と流体連通する複数の灌注出口ポートを含み、それにより、流体源によって供給される冷却流体が灌注出口ポートから放出され、それによって複合電極アセンブリ(例えば、スプリットチップ電極アセンブリ)に冷却を提供する。いくつかの実施形態では、熱交換チャンバの少なくとも内面または層は、ステンレス鋼等の生体適合性材料を含む。
に絶縁されている。一実施形態では、第2の複数の温度測定デバイスは、細長い本体の外面にわたって離間される。システムの実施形態のエネルギー源は、エネルギー源からエネルギー送達部材まで延在する1つまたは複数の導体(例えば、ワイヤ、ケーブル等)を通してエネルギー送達部材にエネルギーを提供するように構成することができる。
成される。いくつかの実施形態では、プロセッサは、計算されたピーク温度に基づき、治療の持続時間、エネルギーの出力、目標温度および最大温度を含む1つまたは複数の治療パラメータを調整するように構成される。
す信号を受信するステップを含む。一実施形態では、第1の複数の温度センサの各々は、焼灼カテーテルの遠位端の周囲に離間される。本方法は、第1の複数の温度センサの近位側に離間された第2の複数の温度センサから、温度を示す信号を受信するステップを含む。本方法は、第1の複数の温度センサおよび第2の複数の温度センサから受信された信号から、温度測定値を求めるステップと、求められた温度測定値を比較するステップとをさらに含む。本方法は、少なくとも部分的に上記比較に基づき、熱的損傷部のピーク温度ゾーンの位置を求めるステップを含むことができる。一実施形態では、本方法は、求められたピーク位置をディスプレイにテキストで視覚的にかつ/またはグラフィカルに出力するステップを含む。一実施形態では、第2の複数の温度センサの各々は、焼灼カテーテルの円周に離間される。
について、他の頻度(例えば、100ms毎、500ms毎、1500ms毎、2秒毎、3秒毎、4秒毎、5秒毎)が可能である。いくつかの実施形態では、第2の期間にわたる時点の頻度は、第1の期間にわたる時点の頻度より長い。
開始温度値であるが、5秒以外の時間(例えば、10秒以内、8秒以内、6秒以内、4秒以内、3秒以内、2秒以内、1秒または1秒以内)を使用することができる。開始温度値は、ある期間にわたって取得された温度値の平均(例えば、エネルギー送達後の0〜1秒で100ms毎に取得された温度値の平均)であり得る。
された複数の温度センサから温度を示す信号を受信するステップと、複数の温度センサの各々について、複数の時点の各々において温度測定値を求めるステップと、複数の時点の各々における求められた温度値と複数の温度センサの各々に関する開始温度値との間の変化率を計算するステップと、複数の時点の各時点において、複数の温度センサの少なくとも2つの計算された変化率の比較に基づき、標的表面に対する焼灼カテーテルの遠位端の向きを求めるステップとを含む。
求められた温度測定値に適用された第2の向き基準の組に基づき、標的表面に対する焼灼カテーテルの遠位端の向きを求めるステップとを含む。いくつかの実施形態では、第2の向き基準の組は、第1の向き基準の組と異なる。例えば、第1の向き基準の組は、複数の温度センサの少なくとも2つの温度応答の時間ベースの特徴の比較を含むことができ、第2の向き基準の組は、複数の温度センサの少なくとも2つの温度測定値の比較を含む。第1の期間は、温度上昇段階に対応することができ、第2の期間は、定常状態段階に対応することができる。第1の向き基準の組および第2の向き基準の組は、経験的に決定することができる。
波数範囲外であり得る。例として、1つの限定しない実施形態では、システムは、組織焼灼または他の治療に対して構成された周波数を有するエネルギーを送達するように少なくとも電極部材の対に対して(かつ接地パッドまたは参照電極に対して)信号を生成、送達または印加するように適合されたエネルギー源と、接触検知および/または組織タイプ判断(例えば、組織が焼灼されたかまたは依然として生存しているか)に対して適合された周波数を有する信号を電極部材の対に対して生成、送達または印加する(接地パッドまたは参照電極に対して生成、送達、印加されない)ように構成された信号源とを含む。信号源によって生成される信号は、定電流AC励起信号またはAC電圧励起信号を含むことができる。励起信号は、有利には、焼灼周波数および/または電位図マッピング周波数の周波数範囲外であり得る。エネルギー源および信号源を両方ともエネルギー送達モジュール(例えば、RF発生器)内に組み込むことができ、または供給源の一方(例えば、信号源)を医療器具(例えば、焼灼カテーテル)の細長い本体またはハンドル内に組み込むことができる。いくつかの実施形態では、信号源は、エネルギー送達モジュールおよび医療器具とは別個の分離した構成要素であり得る接触検知サブシステム内にあるか、またはエネルギー送達モジュールもしくは医療器具内に組み込まれている。いくつかの実施形態では、焼灼または他の治療に適合された周波数を有する信号を印加するように構成され、かつ接触検知または組織タイプ判断機能に適合された周波数を有する信号を印加するように構成された単一の供給源が使用される。治療周波数(例えば、心臓組織の焼灼に適合された周波数)を有する信号も接地パッドまたは基準電極に送達することができる。
2つの別個の周波数からなり、または他の実施形態では、2つ以上の別個の周波数を含むことができる。処理デバイスは、電極の対に周波数の範囲(例えば、5kHz〜1000kHz)の最小周波数から最大周波数までの周波数の完全なスイープが適用される間、インピーダンス測定値を取得するように構成することができる。いくつかの実施形態では、インピーダンス測定値の1つの成分(例えば、インピーダンスの大きさ)は、第1の周波数で取得され、異なるインピーダンス測定値の第2の成分(例えば、位相角)は、第2の周波数で取得される。2つ以上の異なる周波数での電極の対間のインピーダンスの大きさの測定値の比較(例えば、インピーダンスの微分値対周波数、インピーダンスのデルタまたは勾配対周波数)も取得することができる。処理デバイスにより、2つ以上の異なる周波数でのさまざまなインピーダンス測定値の重み付き組合せを計算し、処理デバイスにより、全体的な接触レベルまたは状態を決定するために使用することができる。インピーダンス測定値は、直接取得することができ、または電圧および/もしくは電流測定値等、電気パラメータ測定値に基づいて計算することができる。いくつかの実施形態によれば、インピーダンス測定値は、双極インピーダンス測定値を含む。
が標的領域(例えば、組織)と接触しているか否かを判断する方法は、医療機器の電極または電極部分の対に第1の周波数および第2の周波数を有する信号を印加するステップと、結果としての波形を処理して第1の周波数および第2の周波数でのインピーダンス測定値を取得するステップと、第2の周波数および第1の周波数でのインピーダンスの大きさの間の比を求めるステップとを含むことができる。求められた比が接触を示す所定の閾値未満である場合、本方法は、接触を示す第1の出力を生成するステップを含む。求められた比が所定の閾値を超える場合、本方法は、非接触を示す第2の出力を生成するステップを含む。本方法は、電極または電極部分の対により、標的領域(例えば、心臓組織または他の体内組織)を焼灼するのに十分な焼灼エネルギーが送達されるようにするように適合された信号を印加するステップをさらに含むことができる。
臓組織または他の体内組織を焼灼するかまたは他の方法で治療するのに十分な焼灼エネルギーが送達されるようにするように適合された信号を印加するステップをさらに含むことができる。
の体内組織を焼灼するかまたは他の方法で治療するのに十分な焼灼エネルギーが送達されるようにするように適合された信号を印加するステップをさらに含むことができる。
わたるインピーダンス測定値の変動が所定の閾値未満である場合、本方法は、非接触を示す第2の出力を生成するステップを含む。インピーダンス測定値は、電圧および/または電流測定値に基づいて計算することができ、または直接測定されたインピーダンス測定値とすることができる。本方法は、電極または電極部分の対により、心臓組織または他の体内組織を焼灼するかまたは他の方法で治療するのに十分な焼灼エネルギーが送達されるようにするように適合された信号を印加するステップをさらに含むことができる。
5kHz〜1000kHzである。一実施形態では、第1の周波数は、10kHz〜100kHz(例えば、10〜30kHZ、15〜40kHz、20〜50kHz、30〜60kHz、40〜80kHz、50〜90kHz、60〜100kHz、それらの部分的に重なる範囲、20kHz、または10〜1000kHzの任意の値)であり、第2の周波数は、400kHz〜1000kHz(例えば、400〜600kHz、450〜750kHz、500〜800kHz、600〜850kHz、700〜900kHz、800〜1000kHz、それらの部分的に重なる範囲、800kHz、または400〜1000kHzの任意の値)であるが、要求および/または必要に応じて他の周波数を使用することができる。いくつかの実施形態では、インピーダンス測定値が取得される周波数は、治療(例えば、焼灼)周波数範囲外である。いくつかの実施形態では、フィルタ(バンドパスフィルタ等)を使用して、インピーダンス測定値周波数範囲から治療周波数範囲が隔離される。
号を生成するように構成された信号源からなるかまたはそれを含む。本システムはまた、本質的に、(a)信号源に対して、少なくとも1つの信号を生成して電極部材の対に印加させ、(b)電極の対にわたって定式化する結果としての波形を処理して、第1の周波数で第1の電気測定値を取得し、(c)電極の対にわたって定式化する結果としての波形を処理して、複数の周波数の第2の周波数で第2のインピーダンス測定値を取得し、(d)第1の電気測定値に基づいてインピーダンスの大きさを求め、(e)第2の電気測定値に基づいてインピーダンスの大きさおよび位相を求め、(f)第1の電気測定値に基づくインピーダンスの大きさと、第1の電気測定値および第2の電気測定値に基づくインピーダンスの大きさの比と、第2の電気測定値に基づく位相とを組み合わせる基準に基づき、医療器具の遠位端部分と標的領域との間の接触の状態を示す接触表示値を計算するように構成された処理デバイスからなるかまたはそれを含む。電気測定値は、電圧、電流および/または他の電気パラメータ測定値を含むことができ、そこから、インピーダンス測定値(インピーダンスの大きさまたは位相等)を計算することができ、または電気測定値は、直接取得されたインピーダンス測定値を含むことができる。基準は、第1の電気測定値と、第1の電気測定値および第2の電気測定値に基づくインピーダンス測定値の比と、第2の電気測定値に基づく位相との重み付きの組合せを含むことができ、または基準は、if−then case条件付き基準を含むことができる。
なる。4つの領域に対して、赤色、オレンジ色、黄色および緑色で着色することができる。複数の領域の各々は、現接触状態を示す数値の異なる範囲に対応することができる。ゲージは、接触関数のリアルタイムな数値に対応するゲージにおけるレベルを示すポインタを含むことができる。リアルタイム数値は、0〜1、または0〜1.25、または0〜1.5の範囲とすることができる。1を超える値は、組織の穿孔をもたらす可能性がある過剰な接触を防止する、臨床医に対する「接触警告」を生成することができる。例として、ゲージは、双極インピーダンスの大きさ、双極インピーダンス−周波数勾配および双極インピーダンス位相に基づいて計算された組織−電極接触の質の接触指標を含むことができる。
インピーダンス値を含むことができる。インピーダンス値は、インピーダンスの大きさの値およびインピーダンスの位相の値を含むことができる。インピーダンスの大きさの値は、2つ以上の周波数で取得することができ、異なる周波数での大きさの値間で勾配を求めることができる。インピーダンスの位相の値は、1つまたは複数の周波数で取得することができる。
、標的領域を焼灼するように電力を発生させ、かつそれを組合せ電極アセンブリに印加するように構成された焼灼エネルギー源も含むことができる。処理デバイスは、組合せ電極アセンブリが組織と接触しているか否かの判断に基づき、焼灼エネルギーの1つまたは複数のエネルギー送達パラメータを調整するように、かつ/または組合せ電極アセンブリが組織と接触しているか否かの判断に基づき、エネルギー送達を終了するように構成する(例えば、具体的にプログラムする)ことができる。いくつかの実施形態では、焼灼エネルギー源および信号源は、単一の供給源を構成する。いくつかの実施形態では、信号源は第1の供給源を構成し、および焼灼エネルギー源は、第1の供給源から分離されておりかつ別個である第2の供給源を構成する。いくつかの実施形態では、接触検知サブシステムは、エネルギー送達デバイス内に配置される。信号源および焼灼エネルギー源が別個の供給源であるいくつかの実施形態では、接触検知サブシステムは、ハウジング内に配置され、ハウジングは、焼灼エネルギー源も収容する。
構成される。いくつかの実施形態では、第3の周波数は、第1の周波数より高く、第2の周波数より低い。さまざまな実施形態において、第3の周波数は、20kHz〜120kHzである。ネットワークパラメータは、散乱パラメータまたはインピーダンスパラメータであり得る。ネットワークパラメータ値は、双極インピーダンスの大きさの値、双極インピーダンス位相値、および/または異なる周波数でのインピーダンスの大きさの値間の双極勾配値からなるインピーダンス値であり得る。
。
を用いて接触指標値を計算するようにも構成することができる。
た基準インピーダンス値に基づいて接触インピーダンス値を調整し、それにより、経時的に血液のインピーダンスおよび/または抵抗率の変化によってもたらされる接触インピーダンス値のドリフトを補償する調整された接触インピーダンス値をもたらすステップとを含むかまたは本質的にそれらからなる。基準インピーダンス値を求めるステップは、電極部材の対が組織と接触していないと判断することを含むことができる。いくつかの実施形態では、接触インピーダンス値を調整するステップは、求められた基準インピーダンス値と接触インピーダンス値との比例または他の関係を求めることと、求められた比例または他の関係に基づいて補正係数を適用することとを含む。
基質に関する精密な知識が必要である。加えて、焼灼処置を行った後の短期間内に焼灼処置の転帰を評価する(例えば、所望の臨床転帰が達成されたことを確認する)ことが望ましい場合がある。通常、焼灼カテーテルには、標準的なマッピング電極(例えば、ECG電極)のみが含まれる。しかしながら、いくつかの実施形態では、こうしたカテーテルが高分解能マッピング能力を組み込むことが望ましい場合がある。いくつかの実施形態では、高分解能マッピング電極は、解剖学的基質および焼灼処置の転帰に関するより正確かつより詳細な情報を提供することができる。例えば、こうした高分解能マッピング電極により、電気生理学(EP)専門家は、電位図の形態、それらの振幅および幅を評価し、かつ/またはペーシング閾値の変化を求めることができる。いくつかの構成によれば、形態、振幅および/またはペーシング閾値は、焼灼の転帰に関する有用な情報を提供する信頼性の高いEPマーカとして受け入れられる。したがって、高分解能電極は、組織に対して、こうした組織に/組織から熱を伝達することができる焼灼エネルギーまたは他のエネルギーを送達することができる一方、隣接する組織の正確なマッピングデータを取得することができる任意の電極として定義され、限定なしに、複合(例えば、スプリットチップ)RF電極、他の近接して向けられた電極または電極部分等を含む。
いくつかの実施形態によれば、本明細書では、高分解能マッピングに使用することができる電極(例えば、高周波すなわちRF電極)のさまざまな実施形態について開示する。例えば、本明細書においてより詳細に考察するように、焼灼または他のエネルギー送達システムは、高分解能チップ設計を含むことができ、エネルギー送達部材(例えば、高周波電極)は、2つ以上の別個の電極または電極部分を含む。本明細書において同様に考察するように、いくつかの実施形態では、こうした別個の電極または電極部分を、有利には、(例えば、標的組織の所望の加熱または焼灼をまとめてもたらすように)互いに電気的に結合することができる。
開示するいくつかの実施形態は、焼灼システムおよび方法に関して記載するが、システムおよび方法の任意のものを用いて、要求または必要に応じて、部分的または完全な焼灼があってもなくても、組織を刺激し、調整し、加熱し、かつ/または他の方法で組織に影響を与えることができる。図示するように、システム10は、医療器具20(例えば、カテーテル)を含むことができ、それは、その医療器具20の遠位端に沿って1つまたは複数のエネルギー送達部材30(例えば、高周波電極)を含む。医療器具は、治療されている対象を通して管腔内に(例えば、血管内に)通されるようなサイズとし、形状とし、かつ/またはそのように他の方法で構成することができる。さまざまな実施形態では、医療器具20は、カテーテル、シャフト、ワイヤおよび/または他の細長い器具を含む。他の実施形態では、医療器具は、血管内に配置されず、腹腔鏡または開腹処置を介して血管外に配置される。さまざまな実施形態では、医療器具20は、カテーテル、シャフト、ワイヤおよび/または他の細長い器具を含む。いくつかの実施形態では、医療器具20の遠位端に、またはその細長いシャフトに沿ってもしくはそのハンドル内に、1つまたは複数の温度検知デバイスまたはシステム60(例えば、熱電対、サーミスタ、放射計等)を含めることができる。「遠位端」という用語は、必ずしも遠位先端または遠位端を意味するとは限らない。遠位端は、遠位先端、または遠位先端から離間されているが、概して医療器具20の遠位端部分における位置を意味することができる。医療器具20は、任意選択的に、マッピング電極(例えば、近位側リング電極)を含むことができる。
1つまたは複数の態様を調節するように構成されるプロセッサ46(例えば、処理または制御ユニット)を含む。送達モジュール40はまた、システム10の動作に関連する動作パラメータおよび/または他のデータを格納するために使用することができる、メモリユニットまたは他の記憶デバイス48(例えば、非一時的コンピュータ可読媒体)も含むことができる。いくつかの実施形態では、プロセッサ46は、接触検知および/または組織タイプ検出モジュールもしくはサブシステムを含むかまたはそれと通信する。接触検知サブシステムまたはモジュールは、医療器具20のエネルギー送達部材30が組織と接触している(例えば、有効なエネルギー送達を提供するのに十分接触している)か否かを判断するように適合され得る。いくつかの実施形態では、プロセッサ46は、1つまたは複数のエネルギー送達部材30と接触している組織が焼灼されたまたは他の方法で治療されたか否かを判断するように構成される。いくつかの実施形態では、システム10は、接触検知サブシステム50を含む。接触検知サブシステム50は、プロセッサ46に通信可能に結合することができ、かつ/または別個のコントローラもしくはプロセッサおよびメモリもしくは他の記憶媒体を含む。接触検知サブシステム50は、接触検知機能および組織タイプ決定機能の両方を実行することができる。接触検知サブシステム50は、(図1に概略的に示すように)システムの別個の独立型サブコンポーネントであり得るか、またはエネルギー送達モジュール40もしくは医療器具20に組み込むことができる。接触検知サブシステムに関するさらなる詳細については後述する。組織タイプ検出モジュールまたはサブシステムは、組織が生存しているか焼灼されているかを判断するように適合され得る。いくつかの実施形態では、プロセッサ46は、1つまたは複数の動作方式に基づき、エネルギー発生デバイス42から医療器具20のエネルギー送達部材30へのエネルギーの送達を自動的に調節するように構成される。例えば、特に治療されている組織の検出された温度、組織が焼灼されたと判断されるか否か、またはエネルギー送達部材30が、治療される組織と「十分に」接触しているかまたは閾値レベルを超えて接触していると判断されるか否かに基づき、エネルギー送達部材30に提供されるエネルギー(したがって、標的組織に伝達されるかまたは標的組織から伝達される熱の量)を調節することができる。
は他の流体移送デバイスを含むことができる。こうした流体を用いて、使用中にエネルギー送達部材30を選択的に冷却する(例えば、エネルギー送達部材30から離れるように熱を伝達する)ことができる。他の実施形態では、システム10は、灌注流体システム70を含まない。
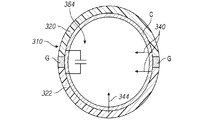
ことができる。いくつかの実施形態では、2つの電極または電極部分30A、30Bを含む高分解能チップ設計を用いて、高分解能双極電位図を記録することができる。こうした目的で、2つの電極または電極部分30A、30BをEPレコーダの入力に接続することができる。いくつかの実施形態では、電極または電極部分30A、30B間の相対的に小さい離隔距離(例えば、ギャップG)により、高分解能マッピングが可能になる。
回路を提示し、それにより、マッピング(例えば、EGMマッピングまたは記録)の目的で電気的に分離した別個の電極として挙動するようにする値を有することができる。図示するように、電極部分の一方(例えば、遠位側電極)30Aをエネルギー送達モジュール40(例えば、RF発生器)に電気的に結合することができる。本明細書で考察するように、モジュール40は、例えば、エネルギー部材(例えば、RF電極)、1つもしくは複数の入出力デバイスまたは構成要素、治療システムの1つまたは複数の態様を調節するように構成されるプロセッサ(例えば、処理または制御デバイス)、メモリ等を選択的に通電しかつ/または他の方法で作動させるように構成されるエネルギー発生デバイス等、1つまたは複数の構成要素または特徴を含むことができる。
極または電極部分110、114と同一かまたは同様の直径および構成を有することができる。したがって、いくつかの実施形態では、電極または電極部分110、114およびセパレータ118によって形成される外面は、概して均一または平滑であり得る。しかしながら、他の実施形態では、セパレータ118の形状、サイズ(例えば直径)および/または他の特徴は、特定の用途または使用に対する要求または必要に応じて、隣接する電極または電極部分110、114の1つまたは複数と異なる可能性がある。
チップ電極設計を含むことができる。図5に、1つまたは複数の電極310A、310Bを含むシステム300の一実施形態を示す。図示するように、2つ以上の電極が含まれる構成では、電極310A、310Bを互いに長手方向にまたは軸方向にずらすことができる。例えば、いくつかの実施形態では、電極310A、310Bは、カテーテルの遠位端に沿ってまたはその近くに配置される。いくつかの実施形態では、電極310A、310Bは、カテーテルまたは他の医療器具の外側部分に沿って配置される。しかしながら、他の構成では、要求または必要に応じて、カテーテルまたは他の医療器具の異なる部分に沿って(例えば、少なくともカテーテルの内側部分に沿って)、電極の1つまたは複数を配置することができる。
させるために使用することができる構成の一実施形態を概略的に示す。図示するように、電極の1つ(例えば、遠位側電極)30Aをエネルギー送達モジュール40(例えば、RF発生器)に電気的に結合することができる。本明細書において考察するように、モジュール40は、例えば、エネルギー部材(例えば、RF電極)を選択的に通電しかつ/または他の方法で活性化するように構成されたエネルギー発生デバイス、1つまたは複数の入出力デバイスまたはコンポーネント、治療システムの1つまたは複数の態様を調節するように構成されるプロセッサ(例えば、処理または制御ユニット)、メモリ等、1つまたは複数の構成要素または特徴を有することができる。さらに、こうしたモジュールは、要求または必要に応じて、手動でまたは自動的に操作されるように構成することができる。
は、電極または電極部分の直列インピーダンスは、電極にRFエネルギーを供給する導体のインピーダンスより低いように選択される。例えば、いくつかの実施形態では、フィルタリング素子の挿入インピーダンスは、導体82のインピーダンスの50%もしくはそれより低く、または均等な組織インピーダンスの10%もしくはそれより低い。
、高分解能チップ電極を用いて取得される電位図は、図8に示すように、電位図データ(例えば、グラフ式出力)400a、400bを提供することができる。図8に示すように、本明細書に開示する高分解能チップ電極実施形態を用いて生成される局所電位図400a、400bは、振幅A1、A2を含む。
図9は、カテーテル1120の遠位端にまたはその近くに配置された電極1130(例えば、単体のRF電極、2つ、3つまたは4つ以上の部分を有する複合(例えば、スプリットチップ)電極、他のタイプの電極等)を含むシステム1100の一実施形態を示す。さらに、本明細書に開示する他の任意の実施形態と同様に、システムは、治療処置(例えば、治療部位に隣接する組織のマッピング、対象のモニタリング等)の実施に役立つ複数のリング電極1170をさらに含むことができる。本明細書に開示するさまざまなシステムおよび関連方法の実施形態について、高周波(RF)ベース焼灼に関連して記載するが、例えば、対象の標的組織に対してマイクロ波エミッタ、超音波変換器、クライオ焼灼部材等を使用するシステム等、他のタイプの焼灼システムにおいて、伝熱概念(熱分流実施形態を含む)を、単独でまたは本明細書に記載する他の実施形態(例えば、複合電極概念、温度検知概念等)とともに実施することができる。
よび/または比較的好適な伝熱特性を有する他の材料等)を含む灌注導管を含むことができる。さらに他の実施形態では、焼灼システムのカテーテルまたは他の医療器具は、要求または必要に応じて、いかなる能動的な流体冷却システム(例えば、その中を延在する開放または閉鎖灌注通路または他の構成要素)も含まない。本明細書においてより詳細に考察するように、カテーテルを通る流体通路を用いる能動的冷却を含まないこうした実施形態は、電極および/または治療されている組織から熱を有利に放散させかつ/または分散させるように、改善された伝熱構成要素および/または設計を利用することができる。
大きい等)。熱拡散率は、熱エネルギーを蓄積する材料の能力に対する、熱エネルギーを伝導する材料の能力を測定する。したがって、材料が熱を伝達するものとして効率的であり得る(例えば、比較的高い熱伝導率を有することができる)としても、それは、その蓄熱特性のために、好ましい熱拡散率特性を有していない可能性がある。伝熱と異なり、熱分流には、(例えば、質量または容積を通して熱を迅速に伝達するための)高い熱コンダクタンス特性と(例えば、熱を蓄積しないための)低い熱容量とを有する材料を使用する必要がある。好ましい熱拡散率、したがって好ましい熱分流特性を有するあり得る材料として、限定されないが、工業用ダイヤモンド(例えば、化学気相成長のための工業用ダイヤモンド)、グラフェン、シリカ、他の炭素系材料等が挙げられる。
エネルギーは、カテーテルの近位端に戻るように伝達することができ、そこで除去することができる。第2に、カテーテルまたは他の医療器具の外側に沿った露出したシャント面は、電極および/または治療されている組織からの熱の放散にさらに役立つことができる。例えば、こうした放熱は、電極の表面にわたって流れる血液の固有の対流冷却態様を介して達成することができる。
遠位端に沿って含まれる電極の近位端に対して近位側に延在することができる。例えば、図10に示すように、伝熱部材1150(例えば、熱シャント部材)は、電極1130の近位端まで、近位端の近くに、またはそれを越えて延在することができる。いくつかの実施形態では、伝熱部材1150は、電極1130の近位端1132でまたはその近くで終端する。しかしながら、他の構成では、限定なしに熱シャント部材を含む伝熱部材1150は、電極1130の近位端1132を越えて延在し、いくつかの実施形態では、要求または必要に応じて、熱シャント部材を含む、遠位側に配置された伝熱部材(例えば、電極1130の長さに沿ってまたはその近くに配置された伝熱ディスクまたは他の伝熱部材)と接触し、かつ/または他の方法で直接または間接的に熱連通する。さらに他の実施形態では、近位側伝熱部材(例えば、熱シャント部材)は、電極または他の焼灼部材の近位端1132に対して近位側で終端する。
部材に、その中にかつ/またはその近くに配置された他の任意の伝熱部材に加えてまたはその代わりであり得る。例えば、図示する実施形態では、電極1230の付近で、システム1200は、内部伝熱部材1250B、および1つまたは複数のディスク状もしくは円筒状伝熱部材1240(例えば、熱分流部材)の両方を含む。
(例えば、電極からの)熱の放散または除去をより容易にかつ/または迅速に具現化することができる。
ml/min、上記範囲間の流量等)であるか、または15ml/minより大きい(例えば、15〜16ml/min、16〜17ml/min、17〜18ml/min、18〜19ml/min、19〜20ml/min、上記流量間の流量等)場合がある。いくつかの実施形態では、こうした灌注流量は、電極および/または治療されている組織から離れるように熱を伝達するために、非熱分流部材(例えば、金属、合金、熱伝導性ポリマー、他の従来の伝熱部材等)が使用されていた場合に必要なものより大幅に低い。例えば、本明細書に開示するさまざまな実施形態またはその変形形態による熱分流部材を有するカテーテルの内部を通過する灌注流体の必要な流量は、従来の伝熱部材を使用するかまたは伝熱部材をまったく使用しないシステムと比較して(例えば、電極で同じ量の熱が生成され、同じ解剖学的位置が治療され、他のパラメータが同じであると想定すると)、20〜90%(例えば、20〜25%、25〜30%、30〜35%、35〜40%、40〜45%、45〜50%、50〜55%、55〜60%、60〜65%、65〜70%、70〜75%、75〜80%、80〜85%、85〜90%、上記範囲間のパーセンテージ等)低減させることができる。例えば、いくつかの市販のRF焼灼システムでは、電極から離れる所望のレベルの伝熱を達成するために、通常、約30ml/min(例えば、25〜35ml/min)の灌注流量が必要である。上述したように、いくつかの構成では、熱分流網を利用する本明細書に開示するシステムは、電極から離れるように熱を有効に分流させるために、約10ml/min以下の灌注流量を利用することができる。したがって、こうした実施形態では、従来のシステムおよび他の市販のシステムに対して少なくとも60〜70%だけ灌注流量を低減させることができる。
層流(および/または相対的に高い流量系に対して流体の流量が著しく低いこととともに)、電極、治療されている組織、および/またはカテーテルもしくは他の医療器具の遠位端に沿った他の任意の位置の近くに配置されたセンサによる温度測定の精度に役立つことができる。
極を加えた、カテーテルまたは他の医療器具の内部に沿って延在する熱分流部材の(例えば、長手方向に沿った)全長は、1〜30mm(例えば、1〜2mm、2〜3mm、3〜4mm、4〜5mm、5〜6mm、6〜7mm、7〜8mm、8〜9mm、9〜10mm、10〜11mm、11〜12mm、12〜13mm、13〜14mm、14〜15mm、15〜20mm、20〜25mm、25〜30mm、上記値間の長さ等)であり得る。上述したように、こうした比較的短い全長にも関わらず、熱分流部材は、電極および/または焼灼されている組織から、カテーテルまたは他の医療器具の灌注チャネルを通過する流体に熱を保持することなく有効に伝達することができる。
ー送達部材1930の内部内に延在する冷却チャンバまたは領域1920と流体連通している。図示する構成では、流体送達導管または通路1904の出口1905は、流体戻り導管または通路1906の遠位端または入口1907の近位側の位置に配置される。したがって、図示する実施形態では、冷却チャンバまたは領域1920は、概して、流体送達導管または通路1904の出口1905と、流体戻り導管または通路1906の入口1907との間に延在する。しかしながら、他の実施形態では、冷却チャンバまたは部分1920の長さ、向き、位置および/または他の細部は、要求または必要に応じて変更することができる。さらに、いくつかの実施形態では、カテーテルまたは他の医療器具は、別個の冷却チャンバまたは部分を含むことなく、閉鎖流体冷却システム(例えば、冷却流体がカテーテルまたは医療器具を通って循環する)を含むことができる。閉ループ流体冷却システムにおけるカテーテルまたは医療器具のさまざまな流体送達ラインおよび/または戻りライン(例えば、通路、導管等)の正確な向きに関わらず、流体は、単に、(例えば、通電されている電極またはエネルギー送達部材に隣接するかつ/またはその付近の)カテーテルまたは他の医療器具の少なくとも一部を通って循環して、電極またはエネルギー送達部材から離れるように選択的かつ有利に熱を伝達する。したがって、こうした実施形態では、さまざまな流体導管または通路は、電極または他のエネルギー送達部材と熱連通している。
ダイヤモンドまたはグラフェン等、熱シャント部材2050と同一または同様の熱拡散率特徴または特性を有する。いくつかの実施形態では、内部部材2070に含まれる材料および/または(例えば、単体部材または構造として見た場合)熱シャント網またはアセンブリ全体の熱拡散率は、1.5cm2/secより大きい(例えば、1.5〜2cm2/sec、2〜2.5cm2/sec、2.5〜3cm2/sec、3〜4cm2/sec、4〜5cm2/sec、5〜6cm2/sec、6〜7cm2/sec、7〜8cm2/sec、8〜9cm2/sec、9〜10cm2/sec、10〜11cm2/sec、11〜12cm2/sec、12〜13cm2/sec、13〜14cm2/sec、14〜15cm2/sec、15〜20cm2/sec、上記範囲間の値、20cm2/secより大きい等)。しかしながら、他の実施形態では、内部部材は、高熱分流材料および/または部材を含まない。しかしながら、他の実施形態では、内部部材2070は、熱シャント部材2050と同様の材料または部材を含まない。例えば、いくつかの構成では、内部部材2070は、熱拡散率が1cm2/secより小さい材料を含む1つまたは複数の構成要素または部材を含むことができる。
ましい熱拡散率特徴を有する熱シャント材料を使用することにより、こうした材料内に熱が保持されないことが確実になり、それにより、より安全な焼灼システムおよび治療処置がもたらされる。
のに役立つ。図示する実施形態では、穿孔部分2122に沿った開口部2123は、概して、形状が円形であり、互いに対して均一に分散配置される(例えば、互いに対して概して均一な分散または間隔を含む)。しかしながら、他の構成では、要求または必要に応じて、チャネル2120の穿孔または直接接触領域2122に沿った開口部2123のサイズ、形状、間隔および/または他の特徴は変更することができる。例えば、いくつかの実施形態では、開口部2123は、楕円形、多角形(例えば、正方形または矩形、三角形、五角形、六角形、八角形等)、不規則等であり得る。いくつかの実施形態では、開口部は、溝状であるかまたは細長い。
する熱を、電極および/または組織から離れるようにより迅速にかつ効率的に伝達することができるだけでなく、ダイヤモンドまたは他の絶縁熱分流部材または網2250が、金属(例えば、ステンレス鋼)灌注チャネル2220と近位側電極またはスラグ2230との間に必要な絶縁を提供する。本明細書で述べるように、こうした絶縁は、複合(例えば、スプリットチップ)設計に有用である。
ールドシステムから始まる流体導管2320の数は、要求または必要に応じて、4つ以上(例えば、4、5、6、7、8つ以上等)か、または2つ以下(例えば、2、3つ)であり得る。
たは凝血塊の形成の可能性を低減させるのに役立つように、それらの領域において血液を希釈するのにも役立つことができる。
いくつかの実施形態によれば、医療器具(例えば、焼灼カテーテル)は、医療器具の遠位部分に沿った異なる位置に軸方向に離間された複数の温度測定デバイス(例えば、熱電対、サーミスタ、他の温度センサ)を含むことができる。軸方向に間隔を空けることにより、有利には、重要な空間温度勾配の測定が容易になる。温度測定デバイスの各々を他の温度測定デバイスの各々から隔離して、独立した温度測定値を提供することができる。エネルギー送達部材の温度を直接測定しないように、温度測定デバイスを1つまたは複数のエネルギー送達部材(例えば、高周波電極)から熱的および/または電気的に絶縁することができ、それにより、エネルギー送達部材の熱的影響から隔離される温度測定が容易になる。医療器具は、医療器具の遠位チップまたは先端にまたはそれに隣接して(例えば、高分解能組合せ電極アセンブリまたは複合電極アセンブリの遠位電極部分内に)配置された第1の複数(例えば、組、アレイ、群)の温度測定デバイス(例えば、温度センサ)を含むことができる。第1の複数の温度測定デバイスは、医療器具の第1の断面に沿って医療器具の周囲で、等距離でまたは不等距離で(例えば、円周方向に、半径方向に)離間することができる。一実施形態では、第1の複数の温度測定デバイスは、医療器具の遠位端の長手方向軸を中心に対称的に配置される。医療器具はまた、第1の断面の近位側である医療器具の第2の断面に沿った第1の複数の温度測定デバイスから近位側に離間された第2の複数の温度測定デバイス(例えば、センサ)も含むことができ、それにより、複数の離間された位置で温度測定値を取得することができる。いくつかの実施形態では、第2の複数の温度測定デバイスは、(医療器具(例えば、焼灼カテーテル)が単一の電極または他のエネルギー送達部材を含む場合)電極または他のエネルギー送達部材の、または(医療器具が複数の電極部材または他のエネルギー送達部材を含む場合)最近位側電極または他のエネルギー送達部材の近位端(例えば縁)に隣接して配置される。
臨床的な課題に直面する。したがって、本明細書に開示するさまざまな実施形態を、標的組織を冷却するかまたは加熱する技術とともに用いることができる。
る範囲)突出することができる。いくつかの実施形態によれば、遠位チップ電極部材3130、および/または温度測定デバイス3125の外向き突出部または拡張部のドーム形状により、有利には、温度測定デバイスを、組織内により深くかつ灌注ポート3140によって提供される開放灌注の影響から離れるように埋め込むことができる。温度測定デバイスの近位側の群と温度測定デバイスの遠位側の群とは、(群としてかつ/または各群内で個別に)同じ量または異なる量を突出することができる。他の実施形態では、温度測定デバイス3125は、医療器具の細長い本体の他の面と同一平面であるかまたは他の面内に埋め込まれる(例えば、外面から0.0mm、−0.1mm、−0.2mm、−0.3mm、−0.4mm、−0.5mm)。いくつかの実施形態では、遠位側温度測定デバイス3125Aは、遠位側電極部材の遠位外面から遠位側に突出または延在し、近位側温度測定デバイス3125Bは、焼灼カテーテル3120Aの細長い本体の横方向外面内で同一平面にある。
ル3120Aの遠位部分の中心長手方向軸と平行であるかまたは実質的に平行である軸方向に遠位側電極部材の遠位外面から延在し、近位側温度測定デバイス3125Bは、焼灼カテーテル3120Aの外面から半径方向外向きに延在する。他の実施形態では、遠位側温度測定デバイス3125Aは、遠位先端の遠位外面内または外面上に配置されない場合があり、(図示する近位側温度測定デバイス3125Bと同様に)半径方向外向きに延在するように側面に配置することができる。いくつかの実施形態では、温度測定デバイス3125は、各群内で同一平面上の温度測定デバイスの2つの分離した群において離間されていないが、他の方法で空間的に分散されている。
伝熱部材3145は、近位側電極部材3135の近位端においてまたはその近くで終端する。しかしながら、(図18Cに示すような)他の構成では、伝熱部材3145は、近位側電極部材3135の近位端を越えて延在する。さらに他の実施形態では、伝熱部材3145は、近位側電極部材3135の近位端(例えば、縁)の遠位側で終端する。伝熱部材3145は、チップ電極部材3130の近位側面から近位側電極部材3135の近位端を越えた位置まで延在することができる。伝熱部材3145が近位側電極部材3135の近位端を越えて延在する実施形態は、伝導性冷却を通して近位縁における熱を低減させることにより、近位縁における電流濃度の量の増大によってもたらされる近位縁加熱効果の分流を増大させることができる。いくつかの実施形態では、伝熱部材3145の少なくとも一部は、(例えば、絶縁ギャップ3131内で)組織と直接接触し、加熱されている標的組織から直接熱を除去するかまたは放散させることができる。
に配置することができる。こうした層は、電極部材(または別のタイプの焼灼部材)と隣接する伝熱部材との間に連続的にまたは断続的に適用することができる。さらに、こうした層は、例えば、スパッタリング、他のめっき技法等、1つもしくは複数の方法または手順を用いて適用することができる。こうした層は、本明細書に開示する実施形態の任意のものまたはその変形形態において使用することができる。さらに、熱分流網を使用することは、特に電極部材によって治療されている組織から離れるように、それ自体が熱を吸収することなく、熱を伝達するのに役立つことができる。
。エポキシ樹脂は、熱伝導率を増大させる(例えば、酸化アルミニウムを含む)金属ペーストを含むことができる。いくつかの実施形態では、遠位チップ3165またはキャップは、温度測定デバイス3125の周囲に、温度測定デバイスと接触する組織の実際の温度に近い等温状態をもたらす。各温度測定デバイス3125の遠位チップ3165は、電極部材との熱伝導性接触から隔離されているため、この等温状態を保持し、それにより、電極部材の熱質量による放散の可能性を阻止するかまたは低減させる。図18Eおよび図18Fは、一実施形態による、焼灼カテーテルの遠位部分のそれぞれ斜視図および断面図を示し、電極チップからの遠位温度測定デバイスの隔離を示す。図示するように、空隙もしくはポケット3162および/または断熱材によって遠位側温度測定デバイス3125Aを包囲することができる。外側の管3160は、遠位側電極部材3130の全長またはその長さの少なくとも一部に沿って延在する断熱スリーブを含むことができる。スリーブは、遠位側電極部材3130を超えて、またはさらには近位側電極部材3135までもしくはそれを越えて延在することができる。
〜4mm、上記範囲間の長さ等)である。しかしながら、他の実施形態では、要求または必要に応じて、近位側電極部材3135は、4mmより大きい(例えば、4〜5mm、5〜6mm、6〜7mm、7〜8mm、8〜9mm、9〜10mm、10mmより大きい等)か、または1mmより小さい(例えば、0.1〜0.5mm、0.5〜1mm、1〜1.5mm、1.5〜2mm、上記範囲間の長さ等)である。スプリット電極がカテーテルシャフトに配置される実施形態では、電極部材の長さは1〜5mm(例えば、1〜2mm、2〜3mm、3〜4mm、4〜5mm、上記範囲間の長さ等)であり得る。しかしながら、他の実施形態では、要求または必要に応じて、電極部材は、5mmより長い(例えば、5〜6mm、6〜7mm、7〜8mm、8〜9mm、9〜10mm、10〜15mm、15〜20mm、上記範囲間の長さ、20mmより大きい長さ等)場合がある。
ギャップすなわち離隔距離は、要求または必要に応じて、例えば、0.1〜1mm等(例えば、0.1〜0.2mm、0.2〜0.3mm、0.3〜0.4mm、0.4〜0.5mm、0.5〜0.6mm、0.6〜0.7mm、0.7〜0.8mm、0.8〜0.9mm、0.9〜1.0mm、上記範囲間の値、0.1mmより小さい、1mmより大きい等)、0.5mmより大きいかまたは0.5mmより小さい。
の乱流、渦流、または他の循環流体運動もしくは経路が引き起こされ、それにより、流体を循環させて流体を伝熱部材3245および/または電極部材と接触するように常に流体をリフレッシュするかまたは交換することにより、改善された冷却を促進する。
を含む実施形態は、結果としてのデバイスおよびシステムとともに、結果としての使用および治療方法に対して、いくつかの利益および利点を提供することができる。例えば、コーティングまたは層は、(i)灌注流体の伝導冷却効果を改善し(それにより、灌注流量と患者の体内に注入される結果としての流体の容量とを著しく低減させることができ、いくつかの実施形態では、灌注流量の低下により、温度センサが灌注流体であふれる可能性が低くなるため、より優れた温度測定精度がもたらされる)、(ii)カテーテルまたは他の医療器具の製造および動作態様を改善し(例えば、熱シャント部分の表層が切断プロセスの結果として導電性となる影響を保障することができ、それにより、カテーテルまたは他の医療器具に対して一貫した外面を依然として維持しながら、熱シャント部分の製造に対してより柔軟性を提供することができる)、(iii)使用等の間に近位側電極の近位端にまたはその近くにおけるホットスポットまたは局所加熱の形成に対して追加の保護を提供することができる。
性能がもたらされる可能性がある。したがって、いくつかの実施形態では、カテーテルまたは他の医療器具に含まれる熱分流部材または部分のすべてまたは大部分がカテーテルまたは医療器具の外部に露出しない。いくつかの構成では、ダイヤモンドまたは他の熱分流網のいずれもカテーテルまたは他の医療器具の外部に露出する。他の実施形態では、熱分流の外面領域の70〜100%(例えば、70〜75%、75〜80%、80〜85%、85〜90%、90〜95%、95〜100%、上記範囲間のパーセンテージ等)、50〜70%、または50%未満が層またはコーティングで覆われるかまたはコーティングされる。
部材または部分の隣接する表面に直接接触し、それに直接固定される。しかしながら、他の実施形態では、コーティングまたは層6070は、熱シャント部材または部分の隣接する表面に接触せず、または直接固定されない。こうした構成では、例えば、熱シャント部材または部分とコーティングまたは層6070との間に1つまたは複数の中間層、コーティング、構造(例えば、エアギャップ)または他の部材を配置することができる。
スから受信される温度測定値が第2の近位側温度測定デバイスからの温度測定値よりかなり大きい場合、かつ第2の近位側温度測定デバイスから受信される温度測定値が第3の近位側温度測定デバイスからの温度測定値よりかなり大きい場合、処理デバイスは、向きが平行でも垂直でもなく、ある角度で傾いている(例えば、斜めの向き)と判断することができる。向きの判断に関するさらなる詳細は、図23C〜図23Eの考察に関連して後述する。いくつかの実施形態では、蛍光透視撮像、ICE撮像または他の撮像方法もしくは技法を用いて、向きを確認することができる。3次元心臓マッピングシステム等、組織マッピングシステムを用いても向きを確認することができる。
Tcomp(t)=k(t)*f(TC1(t),TC2(t),...,TCn(t));
式中、Tcompは複合温度であり、kはk関数または補正もしくは調整関数であり、fは、熱電対測定値TCi、i=1〜nの関数である。k関数は、経時的な関数または定数値を含むことができる。例えば、k関数は以下のように定義することができる。
式中、τは、組織時定数を表す時定数であり、kfinalは、後に図22Aに関連して記載するような補正係数または関数による、kの最終値である。
始するように構成することができる。さまざまな実施形態では、設定値または最大温度は、50℃〜90℃(例えば、50℃、55℃、60℃、65℃、70℃、75℃、80℃、85℃)である。いくつかの実施形態では、アルゴリズムは、いずれの温度測定デバイス(例えば、熱電対)が目下最高温度を記録しているかを特定し、その熱電対を選択して、設定値温度または他の目標温度に達しかつ維持するために必要な電力送達を制御する。チップ電極が組織に対して移動し、異なる温度測定デバイスが組織とより接触するか接触しなくなるに従い、プロセッサまたは処理デバイスは、自動的にいずれの温度測定デバイスが最高温度を示しているかを選択して、電力送達を制御することができる。
ΔT/Δd=(Tdistal−Tproximal)/TC_分離距離
換言すれば、温度空間勾配は、遠位側温度測定デバイスと近位側温度測定デバイスとの間の温度の差を遠位側温度測定デバイスと近位側温度測定デバイスとの間の距離で割った値として推定される。したがって、ピーク組織温度(ピークは山または谷であり得る)は以下のように推定することができる。
Tpeak=ΔT/Δd*Tpeak_dist+Tdistal
式中、iは温度測定デバイスの測定範囲に及び、max(TCi(t))は、時点tにおける温度測定デバイスの最大温度測定値を表す。例えば、図22Bは、上記式の実施形態を示す。トレース1は、1.8の定数k値および1のτ値における推定ピーク組織温度(Tpeak)を示し、トレース2、3および4は、組織に埋め込まれた赤外線プローブを用いて組織表面からそれぞれ1mm、3mmおよび5mmで測定された実際の組織温度を示す。図示するように、トレース1の推定ピーク組織温度(Tpeak)は、1mm深さで測定された実際のピーク組織温度(トレース2)を明確にたどる。
式中、Tnは現在の時点の温度であり、Tn−1は、以前の温度であり、tは時間であり、ρは組織密度であり、Cは組織の比熱であり、Taは中心動脈温度であり、Weは有効灌流速度であり、P・Nは、組織に蓄積した容積出力の推定値を与える。上記式は、温度測定デバイス位置とともにピーク温度の位置(例えば、ホットスポット)を含むさまざまな空間位置において定式化することができる。モデルパラメータを求める校正とともに、異なる位置でこのモデルを利用することにより、マッピング技法を利用して、1つの空間位置において他の空間位置からの測定データを用いて温度を予測することができる。
るように設定することができ、そこでは、一定出力レベルの高周波エネルギーが送出され、超えることができない最大温度が特定される。温度測定デバイスの各々は、周期的にまたは連続的に(同時にまたはトグルされるクエリを介して)モニタリングすることができる。本明細書に記載する焼灼カテーテルの温度測定デバイスの任意のものから受信される温度測定値によって求められるように、最大温度に達するかまたはそれを超える場合、制御信号をエネルギー送達モジュールに送出して、温度が最大温度未満に低下するまで、温度を低下させるかまたは(一時的にもしくは他の方法で)エネルギー送達を終了するように焼灼パラメータを調整する(例えば、電力レベルの低下)することができる。調整は、例えば、エネルギー送達モジュール40の比例−積分−微分コントローラ(PIDコントローラ)によって行うことができる。別の実施形態では、エネルギー送達モジュール40は、電力制御モジュールで実行するように設定することができ、そこでは、一定レベルの電力が連続的に印加され、温度測定デバイスの各々から受信される温度パラメータがモニタリングされて、最大温度を超えないことを確実にする。いくつかの実施形態では、温度制御モードは、設定値温度(例えば、70℃、75℃、80℃)を指定することと、その後、温度測定デバイスの各々から受信される温度測定値から求められるように、温度を設定値温度で、設定値温度未満でまたはその近くで維持するように、電力または他のパラメータを調整することとを含む。チップ電極が組織に対して移動し、異なる温度測定デバイスが組織とより接触するかまたは接触しなくなるに従い、エネルギー送達モジュールのプロセッサまたは処理デバイスは、自動的にいずれの温度測定デバイスが最高温度を示しているかを選択して、電力送達を制御することができる。
きは、組織に対して平行であると推定されるかまたは示され得る。同様に、遠位側温度が支配的である場合、電極の向きは、組織に対して垂直であると推断され、推定されかつ/または示され得る。近位側の支配的な温度および遠位側の支配的な温度の組合せにより、斜めの電極の向きを示すことができる。図23Aは、垂直の向きを示す、複数の温度測定デバイス(例えば、熱電対)からの温度データのプロットを示し、図23Bは、斜めの向きを示す、複数の温度測定デバイス(例えば、熱電対)からの温度データのプロットを示す。
中に向きの判断が行われる場合、特定の損傷部の輪郭またはパターン(例えば、体積、形状またはゾーン)がエネルギー送達によって形成されたという信頼性の向上を提供するように、エネルギー送達プロセスにおいて(例えば、エネルギー送達の開始後の数秒未満で)あらかじめ向きを求めることが特に有利である可能性がある。例えば、平行の向きは、相対的に浅いが長いかまたは幅の広い損傷部の輪郭を形成する可能性があり、垂直な向きは、相対的に深いが幅の狭い損傷部の輪郭を形成する可能性があり、斜めの向きは、平行の向きと垂直な向きとの間のいずれかに損傷部輪郭を形成する可能性がある。いくつかの実施形態では、臨床専門家により特定の向きを標的とすることができ、向きの判断は、臨床専門家に対して、標的向きが達成されたことを明らかにすることができる。場合により、臨床専門家は、標的向きが達成されない場合にエネルギー送達を終了して、求められた向きに基づいてエネルギー送達のパラメータを調整するか、または現治療部位に近い治療部位において追加の治療を行って、ギャップのない連続した損傷部形成の可能性を向上させるように決定することができる。
または100ms毎)取得し記録することができる。ブロック23010において、第1の期間中に取得された温度測定値に基づき、各温度測定デバイス(例えば、熱電対またはサーミスタ)に対して開始温度が求められる。各温度測定デバイスを、追跡しプロットすることができるチャネルと関連付ける(かつ表示するためにディスプレイに出力する)ことができる。いくつかの実施形態では、第1の期間中に取得された温度測定値を平均することにより、開始温度が求められる。本明細書に記載する温度測定デバイスの構成または配置の任意のものを使用することができる。例えば、温度測定デバイスは、本明細書で考察するように、遠位側の複数の温度測定デバイスと、遠位側の複数の温度測定デバイスに対して近位側に離間された近位側の複数の温度測定デバイスとを含むことができる。
えば、患者もしくは術者の動きまたは他の変動の結果として)向きが変化するか否かを有利に示すことができる。向きの判断は、温度測定デバイスの2つ以上間の温度応答の特徴(例えば、温度上昇値または変化率)間の種々の比較を行うことを含むことができる。例えば、比較は、複数の時点の各々または測定時点において、近位側温度測定デバイスの特徴と遠位側温度測定デバイスの特徴との間で行うことができる(遠位側温度測定デバイスの温度上昇値もしくは変化率の平均と比較した近位側温度測定デバイスの温度上昇値もしくは変化率の平均、または近位側温度測定デバイスの温度上昇値もしくは変化率の最大値と比較した遠位側温度測定デバイスの温度上昇値もしくは変化率の最小値、または近位側温度測定デバイスの温度上昇値もしくは変化率の最小値と比較した遠位側温度測定デバイスの温度上昇値もしくは変化率の最大値等)。一例として、平均近位側温度上昇または変化率が、平均遠位側温度上昇または変化率よりある係数N(Nは任意の実数であり得る)だけ大きい場合、1つまたは複数の処理デバイスは、向きが斜めであると判断することができる。いくつかの実施形態によれば、定常状態に達したときの温度測定値自体または温度測定値の広がりの比較の代わりに、温度応答の特徴の比較(例えば、変化率または上昇値または上昇時間の比較)に基づいて向きを求めることにより、エネルギー送達の開始後にはるかに迅速に向きの正確な判断を行うことができる。
の回転は完全に垂直であると想定して)平行の向きは、0〜20度(または160〜180度)であるとみなすことができ、斜めの向きは、20度〜80度(または120〜160度)であるとみなすことができ、垂直な向きは、80〜120度であるとみなすことができる。3つの向きオプションを含む実施形態では、向きの判断は、最初に、第1の向きの1つまたは複数の向き基準が満足されたか否かを判断することで開始する。第1の向きに対する1つまたは複数の向き基準が満足されると、ブロック23030において、1つまたは複数の処理デバイスは、任意選択的に、第1の向きを示す出力を生成する。第1の向きの1つまたは複数の向き基準が満足されない場合、1つまたは複数の処理デバイスは、第2の向きの1つまたは複数の向き基準が満足されたか否かを判断する。第2の向きに対する1つまたは複数の向き基準が満足された場合、ブロック23030において、1つまたは複数の処理デバイスは、任意選択的に、第2の向きを示す出力を生成する。第2の向きの1つまたは複数の向き基準が満足されない場合、ブロック23030において、1つまたは複数の処理デバイスは、3つの向きオプションのみがあるため、向きがデフォルトとして第3の向きでなければならないと判断し、任意選択的に、第3の向きを示す出力を生成する。2つの向きオプションのみが利用可能である場合、第1の向きに関連する基準が満足されない場合、デフォルトとして第2の向きが選択される。向きオプションが試験される順序に応じて、向き基準を変更することができる。試験されている特定の向きに複数の基準が関連付けられている場合、向き判断プロセス23000の速度を上げるために、別個のプロセッサによって試験を並列に行うことができる。
組を用いて行われる。温度測定値は名目上著しく変化していないが、定常状態段階における向きの判断は、例えば、患者もしくは術者の動きまたは他の変動により、温度のずれおよび変化に反応するように設計することができる。この場合にも、定常状態段階に対する向き基準は、各向きオプションに対して異なり、向きオプションが試験される順序に応じて変更することができる。
とに進む。第2の向きに対して基準が満足されない場合、プロセスは、向きが第3の向きであると判断することができる。ブロック23045において、1つまたは複数の処理デバイスは、任意選択的に、求められた向きを示す出力を生成する。定常状態段階は、エネルギーの印加が終了するまで続く。他の実施形態では、定常状態段階で取得される温度測定値は、周期的間隔で取得されない場合もある。いくつかの実施形態では、プロセス23000は、定常状態段階を含まず、ブロック23035の前で終了する。
場合、平行の向きと判断される。そうでない場合、プロセス23000は、向きが斜めであると判断することができる。
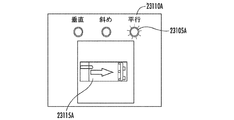
向きに対応するラジオボタンにマークし、または他のラジオボタンから識別する(例えば、図23Fにおけるラジオボタンの1つから放射する光線によって図示するように点灯した外観を有する)ことができる。マーキングは、それぞれのラジオボタンの充填、それぞれのラジオボタンの強調表示、またはそれぞれのラジオボタンの色の変化を含むことができる。一実施形態では、ラジオボタンはLEDとして現れることができ、求められた向きを知らせるために、求められた向きに対応するLEDを、緑色に変更するか、または他の方法で「点灯する」ことができる。出力はまた、求められた向きでの電極アイコンまたは医療器具の遠位端のグラフィカルイメージ23115も含むことができる。図示するように、出力はまた、求められた向きに従って向けられた矢印のグラフィカルイメージも含むことができる。図23F−1は、平行の向きと判断されたときの出力例を示す。図23F−2は、斜めの向きと判断されたときの出力例を示し、図23F−3は、垂直な向きと判断されたときの出力例を示す。ラジオボタンを、チェックボックスまたは他の視覚的指標に置き換えることができる。
いくつかの実施形態によれば、高分解能マッピングおよび高周波焼灼に使用することができる電極(例えば、高周波電極すなわちRF電極)のさまざまな実施形態について、本明細書に開示する。例えば、本明細書においてより詳細に考察するように、焼灼または他のエネルギー送達システムは、高分解能、または複合電極設計を含むことができ、そこでは、エネルギー送達部材(例えば、高周波電極、レーザ電極、マイクロ波伝送電極)が2つ以上の別個の電極または電極部材もしくは部分を含む。本明細書に同様に考察するように、いくつかの実施形態では、こうした別個の電極または電極部分を、有利には、(例えば、標的組織の所望の加熱または焼灼をまとめてもたらすように)互いに電気的に結合することができる。さまざまな実施形態において、組合せ電極または複合(例えば、スプリットチップ)設計を活用して、電極または他のエネルギー送達部材の1つまたは複数の部分が組織(例えば、心内膜組織)と接触しているか否か、および/または接触した組織が焼灼されたか否かを判断する(例えば、組織が生存可能であるか否かを判断する)ことができる。
プロセッサ46に通信可能に結合することができ、かつ/または別個のコントローラもしくはプロセッサおよびメモリもしくは他の記憶媒体を含む。接触検知サブシステム50は、接触検知機能および組織タイプ判断機能の両方を行うことができる。接触検知サブシステム50は、(図1に概略的に示すように)システムの分離した独立型サブコンポーネントである場合があり、またはエネルギー送達モジュール40または医療器具20に組み込まれる場合がある。接触検知サブシステムに関するさらなる詳細については後述する。
ダンスの大きさの値によって割ることによって正規化されている。図示するように、血液(または血液/生理食塩水の組合せ)の正規化されたインピーダンスは、周波数の範囲全体にわたって著しく変化しない。しかしながら、心臓組織の正規化されたインピーダンスは、周波数のその範囲にわたって著しく変化し、概して「s字型」の曲線を形成する。
とにより、異なる周波数(例えば、2つ、3つ、4つまたは5つ以上の異なる周波数)で周期的にまたは連続的に取得される。マルチトーン信号または波形は、時間領域でサンプリングし、その後、図25Cに示すように、周波数領域に変換して、対象周波数で抵抗またはインピーダンスを抽出することができる。いくつかの実施形態では、接触を示す測定値または判断は、周波数領域の代わりに時間領域で取得することができる。周波数の異なる信号または波形を使用することができる。いくつかの実施形態によれば、接触検知動作の実行は、組合せまたは複合(例えば、スプリットチップ)電極アセンブリの電位図(EGM)機能にほとんどまたはまったく影響を与えないように設計される。例えば、図25Dに示すようなインピーダンス測定回路の経路において、コモンモードチョークおよびDCブロック回路を利用することができる。この回路はまた、患者への最大電流を制限する基準抵抗器Rとともに、インピーダンス測定値の精度を向上させるように二重電圧サンプリング点V1およびV2も含むことができる。さらに、図25Dに示すように、EGM記録システムの経路において、(例えば、カットオフ周波数が7kHzである)ローパスフィルタ回路を利用することができる。いくつかの実施形態では、図25Dに示す回路のすべてまたは一部は、図1の接触検知サブシステム50または図27の接触検知サブシステム4650等、接触検知サブシステムで使用される。接触検知に使用される周波数は、EGM記録またはマッピング周波数の少なくとも5倍を超え、少なくとも6倍を超え、少なくとも7倍を超え、少なくとも8倍を超え、少なくとも9倍を超え、少なくとも10倍を超える可能性がある。接触検知サブシステムは、例えば、アナログ−デジタル変換器(ADC)およびマイクロコントローラ(MCU)を含む処理デバイスによって制御することができる。処理デバイスは、図1の処理デバイス46と一体的であり得るか、または別個の独立型処理デバイスであり得る。別個の処理デバイスが使用される場合、その別個の処理デバイスを図1の処理デバイス46に通信可能に結合することができる。
r(f)=a・f3+b・f2+c・f+d
式中、a、b、cおよびdは、r(f)の応答を測定データに整合させる多項式関数に対する項である。したがって、多項式の項に閾値を設定して、電極が組織と接触しているか否かを判断することができる。例えば、大きいd項は、組織接触を示す可能性がある。同
様に、大きいc項は、同じく組織接触を示す、インピーダンスの大きい勾配を示す可能性がある。高次の項を利用するほど、組織接触を示すインピーダンス応答の他のわずかな差を示すことができる。
送達している間に焼灼範囲(例えば、高周波エネルギー200kHz〜800kHz、名目上460kHz)で信号を生成し、送達し、かつ/または印加するように、エネルギー送達モジュール(図示せず、図1のエネルギー送達モジュール40等)または他の信号源4605を構成することができる。低出力信号4607は、周波数の異なるマルチトーン信号もしくは波形または別個の信号を含むことができる。接触検知サブシステム4650は、図25Dに示す素子とともに、焼灼周波数を遮断するノッチフィルタ回路(例えば、460kHz焼灼周波数が使用される場合、460kHzノッチフィルタ)を含むことができる。この構成では、フィルタ4684を利用して、接触検知周波数および焼灼周波数が分離される。
に低下する。血液の抵抗は、それより低い抵抗(125Ω)で開始し、同様に実質的に平坦または安定したままであり、その周波数範囲にわたってわずかに低下する。しかしながら、生存組織の抵抗は、高抵抗値(250Ω)で開始し、その周波数範囲にわたって著しく低下し、概して「s字型」曲線を形成する。焼灼された組織と生存組織との間で抵抗応答が異なる理由は、少なくとも部分的に、生存細胞(例えば、心臓細胞)が、低周波数信号を遮断し高周波信号の通過を可能にするハイパスコンデンサとして作用する膜によって包囲され、焼灼された組織の細胞は、焼灼されている結果としてこうした膜を有していないという事実による。血液抵抗に対する応答が実質的に平坦である理由は、血液の大部分が、事実上、単なるインピーダンスの低い電解質である血漿から構成されるためである。赤血球は、幾分かの変動を与え、それは、生存心臓細胞と同様の、コンデンサとして作用する膜を有するためである。しかしながら、赤血球は、血液組成のそうしたわずかな割合を構成するため、赤血球の影響はわずかである。
態および組織タイプが判断される。
− ラグタイムが0.07μsより小さい場合、組織非接触、
− ラグタイムが0.07μs〜0.13μsである場合、焼灼された組織との接触、
− ラグタイムが0.13μsを超える場合、生存すなわち焼灼されていない組織との接触
と判定することができる。判定閾値または基準は、信号4402の波長によって決まる。他のタイプの波形に対する閾値または判定基準も導出するかまたは確定することができる。
ムによって複数の入力を結合して、接触対非接触の表示、接触の量の表示(例えば、接触のレベル、接触状態または接触力の定性的または定量的表示)、および/または組織タイプ(例えば、焼灼された組織対生存(焼灼されていない)組織)の表示を提供するために使用することができる接触関数を生成することができる。例えば、(i)第1の周波数f1でのインピーダンスの大きさ、(ii)2つの周波数f2およびf1でのインピーダンスの大きさの比(勾配として定義される)、または2つの周波数でのインピーダンスの大きさのデルタもしくは変化、および/または(iii)第2の周波数f2での複素インピーダンスの位相の組合せを合わせて利用して、接触状態(例えば、組織接触対血液中)を示す接触関数が生成される。代替的に、勾配の代わりに、周波数に対するインピーダンスの導関数を使用することができる。いくつかの実施形態によれば、インピーダンス測定値または値は、電極部材の対間の双極インピーダンス測定値を含む。
式中、|Z|f1は、上述したように|Z|minの最小値および|Z|maxの最大値にクリップされた、第1の周波数f1での測定されたインピーダンスの大きさであり、Sは、上述したようにSminの最小値およびSmaxの最大値にクリップされた、f1でのインピーダンスの大きさに関する第2の周波数f2でのインピーダンスの大きさの比であり、Pf2は、上述したようにPminの最小値およびPmaxの最大値にクリップされた、周波数f2でのインピーダンスの位相である。大きさ、勾配および位相の測定値に、重み付け係数WF1、WF2およびWF3をそれぞれ適用することができる。上述したように、接触関数の出力が常に0〜1の範囲の値を与えるように、重み付け係数WF1+WF2+WF3は合計して1とすることができる。代替的に、1を超える値に対して、患
者に対してそれ以上の組織−電極の接触が危険となる可能性がある状況に関して、ユーザに対する警告の生成を促進するのを可能にすることができる。こうした警告は、危険なレベルの接触力が加わるのを防止するのに役立つことができる。例えば、1〜1.25の範囲のCF値に対して、「接触警告」としてフラグをたてることができ、それにより、接触検知サブシステムは、ユーザに表示するかまたは他の方法で出力するために警告を生成することができる。警告は、視覚、触覚および/または可聴であり得る。重み付け係数は、カテーテル設計、接続ケーブル、身体的な患者パラメータ等によって変更することができる。重み付け係数をメモリに格納し、さまざまなパラメータに応じて調整または変更する(例えば相殺する)ことができる。いくつかの実施形態では、初期インピーダンス測定値および/または患者パラメータ測定値に基づき、重み付け係数を調整することができる。
インピーダンスの大きさ|Z|成分、勾配S成分および/または位相P成分)は、治療処置の前にまたは治療処置中に患者の体内に液体が注入される際に経時的に「ドリフトする」可能性がある。治療処置の準備中にまたは処置中に導入される液体の例としては、例えば、生理食塩水、プロポフォール等の麻酔薬、ヘパリン等の血液希釈薬、または他の生理学的液体が挙げられる。液体は、治療デバイス(例えば、焼灼カテーテル)自体を通して導入することができ(例えば、灌注ポートを通しての生理食塩水)、かつ/またはIV注射(IV流体バッグ、管およびシリンジ)または他の送達機構を通して導入することができる。経時的な液体の導入は、経時的に血液の抵抗率および/またはインピーダンスに影響を与える可能性があり、それがさらに、経時的に接触検知電極の対間(例えば、本明細書に記載するような複合チップ(例えば、高分解能または組合せ電極)アセンブリの電極部材または部分の対間)の電気測定値(例えば、電圧および電流測定値または直接インピーダンス測定値)に基づき、接触検知サブシステムまたはモジュールによって求められる接触インピーダンス測定値または計算に影響を与える可能性がある。この血液の抵抗率および/またはインピーダンスの変化による経時的なドリフトは、考慮されずまたは補償されない場合、経時的に接触関数または接触指数(例えば、接触の質の指標、接触のレベルまたは接触状態)の精度または信頼性に影響を与える可能性がある。例えば、電気生理学的食塩水は、導電性があり、そのため、さらなる生理食塩水が血管系に導入されるに従い、患者の血液が希釈され、血液の抵抗率が低下し、経時的に接触インピーダンス測定値または計算値のドリフトをもたらす。その結果、ドリフトを考慮するかまたは補償し、それにより、接触関数または接触指数の決定またはアルゴリズムの精度を向上させるために、接触関数またはアルゴリズムに対する補正が望ましい場合がある。例えば、補償がなければ、ドリフトにより、(静的閾値に基づいて求めることができる)接触指標決定が、接触のレベル(例えば、接触力)が不変のままであっても実質的に変化する可能性があり、それにより、不正確なまたは信頼性の低い接触レベル指標または評価出力が提供され、実際の接触レベルに関して臨床医を誤解させることになる可能性がある。
±20%以内(例えば、20%以内、15%以内、10%以内、5%以内)である。いくつかの実施形態では、基準電極の対は、標的治療部位(例えば、焼灼部位)に隣接するかまたは近接するが、組織と接触しないように配置され得る。他の実施形態では、基準電極の対は、標的組織部位に隣接して配置されない。いくつかの実施形態では、基準電極の対は、患者の体外に配置されず、血液に露出することができないように医療器具内にはない。
ができる。図41Bに示すように、回路は、基準測定値のためのリング電極R1、R2と電極部材D1、D2との間で接触検知システムまたはモジュールへの接続を切り替えるかまたはトグルするスイッチSW1、SW2を含むことができる。要求および/または必要に応じて、他の代替的な接続実装形態を使用することができる。
|Z|max_adj=|Z|max *(1−A*(ZR1R2_initial−ZR1R2_current))
式中、|Z|maxは、生理食塩水または他の液体の注入がないときに有効であるベースライン閾値であり、ZR1R2_initialは、リング電極R1およびR2間の1つまたは複数の電気測定値から求められる初期ベースラインインピーダンス値であり、ZR1R2_currentは、リング電極R1およびR2間の1つまたは複数の電気測定値から求められる電流インピーダンス値であり、Aはスケーリング係数である。
|Z|min_adj=|Z|min *(1−B*(ZR1R2_initial−ZR1R2_current))
式中、Zminは、生理食塩水の注入がないときに有効であるベースライン閾値であり、ZR1R2_initialおよびZR1R2_currentは、上述したものと同じであり、Bはスケーリング係数である。
ことができるかを示す。
ることができる。
CC=IF(|ZMAG|>ZTHR1,Best,IF(AND(ZTHRI>|ZMAG|,|ZMAG|≧ZTHR2),Good,IF(AND(ZTHR2>|ZMAG|,|ZMAG|≧ZTHR3),Medium,IF(AND(ZTHR3>|ZMAG|,|ZMAG|≧ZTHR4),LOW,No_Contact))))+IF(|ZMAG|>ZTHR1,0,IF(AND(SLOPE≦STHR1|),Good,IF(AND(STHR1<SLOPE,SLOPE≦STHR2),Medium,IF(AND(STHR2<SLOPE,SLOPE≦STHR3),LOW,No_Contact))))+IF(|ZMAG|>ZTHR1,0,IF(AND(PHASE≦PTHR1),Good,IF(AND(PTHR1<PHASE,PHASE≦PTHR2),Medium,IF(AND(PTHR2<PHASE,PHASE≦PTHR3),LOW,No_Contact))))
る。判定ブロック5105において、(例えば、直接インピーダンス測定値に基づく、または2つの電極部分を含む複合電極アセンブリによって取得される電圧および/または電流測定値に基づく)測定されたまたは計算されたインピーダンスの大きさの値が、所定の閾値インピーダンスと比較される。測定されたまたは計算されたインピーダンスの大きさの値|ZMAG|が第1の閾値ZTHR1(例えば、350Ω)を超える場合、接触基準(CC)に対して、「最良」または最高値が割り当てられる。しかしながら、測定されたまたは計算されたインピーダンスの大きさの値|ZMAG|が第1の閾値ZTHR1より小さい場合、プロセス5100はブロック5110に進み、そこで、インピーダンスの大きさ、勾配および位相に対する個々のサブ値が求められる。ブロック5115において、個々のサブ値が結合されて(例えば、合計されて)、接触状態を示す全体値になる。いくつかの実施形態では、上述したように、組合せは重み付けされた組合せの和である。
測定された電圧と測定された電流との間の位相の差を含むことができ、または実際のインピーダンス位相測定値であり得る。
る。一実施形態では、定性的指標5260は、現接触関数値に対応する色をゲージ5250に表示する。ユーザに接触の質を伝えるために、接触関数とともに、水平または垂直バー、他のメータ、ビーコン、色変化インジケータまたは他のタイプのインジケータ等、他のタイプのインジケータを利用することも可能である。インジケータは、接触(または十分なレベルの接触)時または接触がなくなった時に駆動されるように適合された1つまたは複数の発光ダイオード(LED)を含むことができる。LEDは異なる色とすることができ、各色は、異なるレベルの接触を表す(例えば、非接触に対する赤色、不十分な接触に対するオレンジ色、中間の接触に対する黄色、および良好な接触に対する緑色)。LEDは、カテーテルハンドルに、ディスプレイもしくは患者モニタに、またはシステムに通信可能に結合された他の任意の別個のデバイスに配置することができる。
ΔTi/Δt<−闘値1(条件1)
または
ΔTcomp/ΔP<闘値2(条件2)
式中、ΔTiは、カテーテルまたは他の医療器具に沿って配置された複数の温度測定デバイス(例えば、センサ、熱電対、サーミスタ)の任意のものの温度の変化であり、Δtは、温度変化が測定される時間の間隔であり、ΔTcompは、温度測定デバイスの温度の最大値の変化であり、ΔPは、印加される電力の変化である。
電極アセンブリの電極または電極部分D1、D2との間のネットワークパラメータ回路に沿ったいずれかの点において接続することができる(またはそれらの間の電気経路に存在することができる)。カテーテルインタフェースユニットは、さまざまな周波数を有する信号をフィルタリングするように適合されたフィルタ(例えば、ハードウェアまたはソフトウェアで実装される、ローパスフィルタ、バンドパスフィルタ、ハイパスフィルタ)を含む場合もあれば含まない場合もある。一例として、カテーテルインタフェースユニットは、高周波発生器および電気解剖学的マッピングシステムの両方の、複数の電極部分または部材を有する高分解能マッピングおよびエネルギー送達カテーテル(デバイス(本明細書に記載する焼灼カテーテルまたは他のエネルギー送達デバイスおよび温度測定デバイス等))への接続を容易にするように適合されたハードウェアモジュールまたはユニットを含むことができ、それは、ネットワークパラメータ回路(例えば、インピーダンス測定回路)に沿ったいずれかの点で接続されるか、または他の方法で、分離された電極部材の電気経路に存在する。カテーテルインタフェースユニットまたは他のハードウェアモジュールもしくはユニットの存在もしくは不在、または使用されるケーブル、発生器もしくはワイヤのネットワークパラメータの相違により、ネットワークパラメータ(例えば、電圧および電流測定値によるまたはそれらからのインピーダンス測定値等の散乱パラメータまたは電気パラメータ)に変動がもたらされる可能性があり、またはネットワークパラメータ(例えば、インピーダンス測定値または値等、電気測定値または値)が、高分解能電極アセンブリの2つの電極間の実際のネットワークパラメータ値(例えば、インピーダンス)を正確に反映しない結果となり、それにより、より不正確かつ/または一貫しない接触指標値がもたらされる可能性がある。したがって、精度または一貫性がないことは、治療の転帰またはパラメータに悪影響を与える可能性があり、安全性および/または効力に関する有害な結果となる可能性がある。したがって、本明細書では、組合せ電極アセンブリ(例えば、離間された電極部材または部分の高分解能またはスプリットチップ電極配置)を含む焼灼システムによって取得されるネットワークパラメータ値(例えば、インピーダンスの大きさ、勾配、もしくは位相値、または電圧もしくは電流測定値等の電気測定値)の精度および一貫性を向上させるいくつかの実施形態について開示する。
しくは関数の他の接触表示もしくはレベルに対する入力として使用される。例えば、補正されたインピーダンス値を用いて、上述した重み付けされた接触関数(CF)におけるZ、SおよびPの値を求めることができる。
)は、ネットワークパラメータ回路を用いて直接測定され、ネットワークパラメータからSパラメータ行列が生成される。Sパラメータ行列における要素の各々は、複素数であり、周波数に依存する。Sパラメータは、複数の異なる周波数(例えば、5kHz〜20kHzの第1の周波数、25kHz〜100kHzの第2の周波数および500kHz〜1000kHzの第3の周波数等、kHz範囲の3つの異なる周波数)で測定することができる。一実施形態では、抵抗器Rcalが接続されコンデンサCcalが切断された状態で、コンデンサCcalが接続され抵抗器Rcalが切断された状態、抵抗器RcalおよびコンデンサCcalの両方が並列に接続された状態で、複素インピーダンスが測定される。測定された複素インピーダンス、ネットワーク1のSパラメータおよび既知の負荷間の関係は、3つの式として表すことができ、それを用いて、ネットワーク1のSパラメータを解くことができる。Sパラメータが特徴付けられると、それらを(例えば、伝送行列手法を用いて)発生器ケーブル5430およびカテーテルワイヤ5435の既知のネットワークパラメータと結合して、カテーテルの遠位端部分において(例えば、複合電極アセンブリの2つの離間された電極部分にわたって)補正された(実際の)インピーダンス測定値を提供することができる。
式中、1および2は回路のポート番号を示し、V1、I1、V2およびI2は、それぞれのポートの各々における電圧および電流を表す。R、LおよびCに対する値はまた、測定ツール(例えば、マルチメータ)を利用して測定することも可能である。上述した等価回路モデル手法は、この概念の一例である。他の実施形態では、より複雑な回路モデルを利用して、システムのさまざまな要素を表すことができる。
の構成では、比(すなわちA1/A2)が一定の最小閾値を超える場合、ユーザに対して、A2振幅が取得された組織が適切に焼灼されたことを通知することができる。例えば、いくつかの実施形態では、A1/A2比が1.5より大きい(例えば、1.5〜1.6、1.6〜1.7、1.7〜1.8、1.8〜1.9、1.9〜2.0、2.0〜2.5、2.5〜3.0、上記範囲間の値、3より大きい等)とき、適切な焼灼および治療を確認することができる。しかしながら、他の実施形態では、A1/A2の比が1.5より小さい(例えば、1〜1.1、1.1〜1.2、1.2〜1.3、1.3〜1.4、1.4〜1.5、上記範囲間の値等)とき、焼灼の確認を取得することができる。
ョンシステム)は、要求または必要に応じて、2つ以上の異なる焼灼デバイスまたはシステムとともに機能するように構成することができる。
法として、出力デバイスは、焼灼システムとは別個である(例えば、独立型デバイス)か、または別個のマッピングシステム(例えば、3D電気解剖学的ナビゲーションシステム、他のマッピングデバイスまたはシステム等)、別のタイプの撮像もしくは案内システム等の一部であり得る。こうした構成では、出力デバイスは、焼灼システム(例えば、発生器または他のエネルギー送達モジュール、プロセッサまたはコントローラ等)に動作可能に結合するように有利に構成することができる。
ステム)を、こうした選択された焼灼に関する特定のデータおよび/または他の情報を提供するように構成することができる。例えば、図37Aに図示するように、ユーザが特定の焼灼8202の上で「ホバーする」かまたは他の方法で特定の焼灼8202を選択すると、モニタまたは他の出力8000に別個のウィンドウ8300(例えば、ポップアップまたはサイドウィンドウ)を表示することができる。さらに、いくつかの構成によれば、ユーザが自らのカーソル、指および/または他の選択デバイスもしくは機能を特定の焼灼から離れる方向に移動させると、別個のウィンドウ8300はつぶれるかまたは他の方法で消えることができる。いくつかの実施形態では、ポップアップまたは別個のウィンドウは、要求または必要に応じて、選択または作動に続く特定の期間(例えば、0.5〜5秒間、5〜10秒間、10秒間より長く、上記範囲間の期間等)、作動または他の方法で可視のままであるように構成される。有利には、こうした構成により、ユーザは、焼灼システムを用いて行われる処置に関するデータおよび他の情報を迅速に、容易にかつ好都合に見ることができる。
まれるデータおよび情報を選択することができる。
とができる。さらに、ポップアップウィンドウに関するさまざまな他の特徴および特性を変更することができる。例えば、システムのホバー感度(例えば、ポップアップウィンドウを起動するためにカーソル、触れる動き、または他の選択方法もしくは技法がどの程度焼灼に対して近い必要があるか)、ポップアップウィンドウを起動するために、ユーザがコントローラ(例えば、マウスボタン、タッチスクリーンの押下等)をクリックするかまたは他の方法で操作する必要があるか否か、ポップアップウィンドウが、モニタまたは他の出力デバイスから消える前にどの程度起動したままであるか、ポップアップディスプレイに提供されるグラフィカル情報および/またはテキスト情報のサイズ、色および/または他の全体的な表示特徴(例えば、テキストフォントおよびサイズ、色等)等である。
部の深さ、幅または体積プロファイルを描きかつ推定するために、こうしたデータを組み込むように構成することができる。例えば、いくつかの実施形態では、焼灼経路は、対象の左心房内の肺静脈の対の周囲に(例えば、こうした静脈の口の周囲に)概して円周方向の経路を含むことができる。いくつかの構成では、本技術分野において既知であるように、こうした焼灼処置は、心房細動または他の心臓不整脈の対象において異常な伝導パターンを中断させるのに役立つことができる。したがって、(図38に図示するような)焼灼エリア近似と組み合わせてまたはその代わりに、システムは、治療されている組織に沿った有効な焼灼または標的加熱深さ、幅および/または体積を決定する(例えば、本明細書に開示するさまざまな実施形態に従って推定する)ように構成することができる。図39においてグラフィカル表現9600で示すように、システムは、治療経路に沿った距離の関数として焼灼深さ9650を示すことができる。こうした情報は、図37Aまたは図37Bまたは図38に示すように、全体的な焼灼表現とともに(例えば、連続して、間欠的に(例えば、ポップアップウィンドウの一部として)等)表示することができる。したがって、医師に対して、焼灼処置に関連する3次元評価を有効に提供することができ、そこでは、組織の焼灼(または所望の加熱)の面積の/空間的広がりおよび深さの両方が、処置中に医師にグラフィカルに表現される。他の実施形態では、面積の広がりおよび深さを単一の統合画像にグラフィカルに結合する焼灼組織の3次元容積表現を、ユーザに提供することができる。
まな病気を治療するために必要な焼灼の回数を低減させることができる。
システムは、本質的に、カテーテル、焼灼部材(例えば、RF電極、複合(例えば、スプリットチップ)電極、別のタイプの高分解能電極等)、カテーテルの内部を通って焼灼部材までまたはその近くまで延在する灌注導管、焼灼部材を選択的に活性化する少なくとも1つの導体(例えば、ワイヤ、ケーブル等)、および焼灼部材の少なくとも一部(例えば、焼灼部材の近位部分)を灌注導管と熱連通させる少なくとも1つの伝熱部材、電極および/または治療されている組織から離れるように有効に熱を伝達するように構成された少なくとも1つの熱シャント部材、カテーテルの2つの異なる長手方向位置に沿って配置された複数の温度センサ(例えば、熱電対)であって、電極から熱的に絶縁され、かつある深さで組織の温度を検出するように構成された温度センサ、電極と隣接する組織とが接触しているか否かおよびどの程度接触しているかを(例えば、組織を焼灼するようにも構成される高分解能電極から取得されるインピーダンス測定値を用いて)判断する接触検出サブシステム等からなる。
ュータプロセッサ(例えば、プログラマブルマイクロプロセッサもしくはマイクロコントローラまたは特定用途向け集積回路)によってアクセス可能なメモリにロードされる。したがって、少なくとも1つのコンピュータプロセッサはそれらの命令を実行し、コンピュータハードウェアに対して、コンピュータ実行可能命令によって定義された特定の関数を実行させる。当業者には理解されるように、コンピュータ実行可能命令のコンピュータによる実行は、特定の機能を実行するように配線されるハードウェア回路を含む電子ハードウェアによる同じ機能の実行と均等である。したがって、本明細書に例示する実施形態は、典型的には、コンピュータハードウェアおよびコンピュータ実行可能命令の何らかの組合せとして実施されるが、本明細書に例示する実施形態は、本明細書に例示する特定の関数を実行するように配線された1つまたは複数の電子回路として実施することも可能である。
。本明細書に開示した方法は、専門家によって行われるいくつかの行為を含むが、それらは、明示的にまたは暗示的に、それらの行為の任意の第3者の命令も含むことができる。例えば、「カテーテルを前進させること」または「焼灼部材にエネルギーを送達すること」等の行為は、それぞれ「カテーテルを前進させるように命令すること」または「焼灼部材にエネルギーを送達するように命令すること」を含む。本明細書に開示する範囲はまた、そのあらゆる部分的重なり、部分的範囲およびその組合せも包含する。「最大」、「少なくとも」、「〜を超える」、「より小さい」、「間」等の用語は、列挙される数字を含む。「約」または「およそ」等の用語に続く数字は、列挙される数字を含む。例えば、「約10mm」は「10mm」を含む。「実質的に」等の用語に続く用語または句は、列挙される用語または句を含む。例えば、「実質的に平行」は「平行」を含む。
Claims (24)
- 標的領域に対する焼灼カテーテルの向きを求めるシステムであって、
焼灼カテーテルであって、細長い本体を含み、前記細長い本体は、前記細長い本体の遠位端に配置された第1の複数の温度測定デバイスおよび前記第1の複数の温度測定デバイスに対して近位側に離間された第2の複数の温度測定デバイスと、前記細長い本体の前記遠位端に配置された少なくとも1つの電極部材とを有する、焼灼カテーテルと、
標的組織を焼灼するのに十分な焼灼エネルギーを前記焼灼カテーテルの前記少なくとも1つの電極部材に印加するように構成されたエネルギー源と、
少なくとも1つの処理デバイスであって、コンピュータ可読媒体に格納された特定の命令の実行時、
複数の時点で前記第1の複数の温度測定デバイスの各々および前記第2の複数の温度測定デバイスの各々から温度測定値を取得することと、
各時点において、前記取得された温度測定値から、前記第1の複数の温度測定デバイスの各々および前記第2の複数の温度測定デバイスの各々について以前の時点から現在の時点までの温度測定値の変化率を求めることと、
各時点において、前記温度測定デバイスの少なくとも2つに関する前記温度測定値の変化率の比較に少なくとも部分的に基づき、前記温度測定値が定常状態に達する前に3つの向きオプションの1つから前記細長い本体の前記遠位端の向きを求めることと
を行うように構成された少なくとも1つの処理デバイスと
を含むシステム。 - 前記複数の時点は、規則的な時間間隔で離間されている、請求項1に記載のシステム。
- 前記現在の時点における前記温度測定値は、移動平均値である、請求項1または2に記載のシステム。
- 前記以前の時点における前記温度測定値は、前記焼灼エネルギーが最初に前記エネルギー源によって印加された後の5秒以内に取得された開始温度値である、請求項1〜3のいずれか一項に記載のシステム。
- 前記以前の時点における前記温度測定値は、前記焼灼エネルギーが最初に前記エネルギー源によって印加された後の1秒以内に取得された開始温度値である、請求項1〜4のいずれか一項に記載のシステム。
- 前記定常状態は、各温度測定デバイスに関する前記温度測定値の移動平均が20%を超えて逸脱しない期間である、請求項1〜5のいずれか一項に記載のシステム。
- 前記第1の複数の温度測定デバイスは、3つの熱電対からなり、前記第2の複数の温度測定デバイスは、3つの熱電対からなる、請求項1〜6のいずれか一項に記載のシステム。
- 前記第1の複数の温度測定デバイスは、第1の平面に沿って配置され、前記第2の複数の温度測定デバイスは、前記第1の平面に対して近位側に離間された第2の平面に沿って配置される、請求項1〜7のいずれか一項に記載のシステム。
- 初期向きは、前記エネルギー源による焼灼エネルギーの印加後の15秒未満で求められる、請求項1〜8のいずれか一項に記載のシステム。
- 初期向きは、前記エネルギー源による焼灼エネルギーの印加後の10秒未満で求められる、請求項1〜8のいずれか一項に記載のシステム。
- 初期向きは、前記エネルギー源による焼灼エネルギーの印加後の5秒未満で求められる、請求項1〜8のいずれか一項に記載のシステム。
- 前記向きオプションは、平行の向き、垂直の向きおよび斜めの向きを含む、請求項1〜11のいずれか一項に記載のシステム。
- 前記少なくとも1つの処理デバイスは、前記斜めの向きについて定義された斜め向き基準に基づいて前記向きが斜めの向きであるか否かを最初に判断するように構成され、および前記斜め向き基準が満足されない場合、前記少なくとも1つの処理デバイスは、前記平行の向きについて定義された平行向き基準に基づいて前記向きが平行の向きであるか否かを判断するように構成され、および前記平行向き基準が満足されない場合、前記少なくとも1つの処理デバイスは、前記向きが垂直であると判断するように構成される、請求項12に記載のシステム。
- 前記少なくとも1つの処理デバイスは、前記求められた向きを示す出力を生成するように構成される、請求項1〜13のいずれか一項に記載のシステム。
- 前記出力は、前記求められた向きでの電極のグラフィカルアイコンを含む、請求項14に記載のシステム。
- 前記出力は、前記3つの向きオプションから前記求められた向きを識別する視覚的指標を含む、請求項14または15に記載のシステム。
- 前記出力は、各々に前記3つの向きオプションのそれぞれの1つのテキストラベルが付随する3つのラジオボタンを含むグラフィカルユーザインタフェースを含み、前記視覚的指標は、前記求められた向きに対応する前記ラジオボタンを示すことを含む、請求項16に記載のシステム。
- 前記少なくとも2つの温度測定デバイスの前記温度測定値の変化率の前記比較は、前記
第1の複数の温度測定デバイスの温度測定値の平均変化率と前記第2の複数の温度測定デバイスの温度測定値の平均変化率との間の関係を比較することを含む、請求項1〜17のいずれか一項に記載のシステム。 - 前記少なくとも2つの温度測定デバイスの前記温度測定値の変化率の前記比較は、前記第1の複数の温度測定デバイスの温度測定値の最大変化率と前記第2の複数の温度測定デバイスの温度測定値の最大変化率との間の関係を比較することを含む、請求項1〜18のいずれか一項に記載のシステム。
- 前記少なくとも2つの温度測定デバイスの温度応答の時間ベースの特徴の前記比較は、前記第1の複数の温度測定デバイスの温度測定値の最大変化率と前記第2の複数の温度測定デバイスの温度測定値の最小変化率との間の関係を比較することを含む、請求項1〜19のいずれか一項に記載のシステム。
- 前記少なくとも2つの温度測定デバイスの温度応答の時間ベースの特徴の前記比較は、前記第1の複数の温度測定デバイスの温度測定値の最小変化率と前記第2の複数の温度測定デバイスの温度測定値の最大変化率との間の関係を比較することを含む、請求項1〜20のいずれか一項に記載のシステム。
- 前記少なくとも2つの温度測定デバイスの温度応答の時間ベースの特徴の前記比較は、前記第1の複数の温度測定デバイスの少なくとも2つの間の、以前の時点から前記現在の時点までの温度測定値の変化率を比較することを含む、請求項1〜21のいずれか一項に記載のシステム。
- 前記少なくとも2つの温度測定デバイスの温度応答の時間ベースの特徴の前記比較は、前記第2の複数の温度測定デバイスの少なくとも2つの間の、以前の時点から前記現在の時点までの温度測定値の変化率を比較することを含む、請求項1〜22のいずれか一項に記載のシステム。
- 前記少なくとも1つの電極部材は、高分解能マッピングおよび高周波エネルギー送達のために構成された組合せ電極アセンブリの遠位側電極部材であり、前記組合せ電極アセンブリは、電気絶縁ギャップによって分離された前記遠位側電極部材と近位側電極部材とを含む、請求項1〜23のいずれか一項に記載のシステム。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662308461P | 2016-03-15 | 2016-03-15 | |
| US62/308,461 | 2016-03-15 | ||
| US201662315661P | 2016-03-30 | 2016-03-30 | |
| US62/315,661 | 2016-03-30 | ||
| US201662323502P | 2016-04-15 | 2016-04-15 | |
| US62/323,502 | 2016-04-15 | ||
| US201662418057P | 2016-11-04 | 2016-11-04 | |
| US62/418,057 | 2016-11-04 | ||
| PCT/US2017/022264 WO2017160808A1 (en) | 2016-03-15 | 2017-03-14 | Improved devices, systems and methods for irrigated ablation |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019517832A JP2019517832A (ja) | 2019-06-27 |
| JP2019517832A5 JP2019517832A5 (ja) | 2020-04-09 |
| JP6923549B2 true JP6923549B2 (ja) | 2021-08-18 |
Family
ID=59852401
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018548898A Active JP6923549B2 (ja) | 2016-03-15 | 2017-03-14 | 灌注式焼灼のための改良されたシステム |
Country Status (10)
| Country | Link |
|---|---|
| US (4) | US9993178B2 (ja) |
| EP (1) | EP3429462B1 (ja) |
| JP (1) | JP6923549B2 (ja) |
| KR (1) | KR20180124070A (ja) |
| CN (1) | CN109069006B (ja) |
| AU (1) | AU2017235224A1 (ja) |
| CA (1) | CA3017269A1 (ja) |
| IL (1) | IL261613A (ja) |
| SG (1) | SG11201807618QA (ja) |
| WO (1) | WO2017160808A1 (ja) |
Families Citing this family (146)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100298832A1 (en) | 2009-05-20 | 2010-11-25 | Osseon Therapeutics, Inc. | Steerable curvable vertebroplasty drill |
| US11871901B2 (en) | 2012-05-20 | 2024-01-16 | Cilag Gmbh International | Method for situational awareness for surgical network or surgical network connected device capable of adjusting function based on a sensed situation or usage |
| US11504192B2 (en) | 2014-10-30 | 2022-11-22 | Cilag Gmbh International | Method of hub communication with surgical instrument systems |
| WO2016081611A1 (en) | 2014-11-19 | 2016-05-26 | Advanced Cardiac Therapeutics, Inc. | High-resolution mapping of tissue with pacing |
| KR20170107428A (ko) | 2014-11-19 | 2017-09-25 | 어드밴스드 카디악 테라퓨틱스, 인크. | 고분해능 전극 어셈블리를 이용한 절제 장치, 시스템 및 방법 |
| US11209954B2 (en) * | 2015-12-10 | 2021-12-28 | Cmr Surgical Limited | Surgical robotic system using dynamically generated icons to represent orientations of instruments |
| SG11201807618QA (en) * | 2016-03-15 | 2018-10-30 | Epix Therapeutics Inc | Improved devices, systems and methods for irrigated ablation |
| JP2019534130A (ja) | 2016-10-27 | 2019-11-28 | ディーファイン,インコーポレイティド | セメント送達チャネルを有する関節接合型骨刀 |
| US11026744B2 (en) | 2016-11-28 | 2021-06-08 | Dfine, Inc. | Tumor ablation devices and related methods |
| US10463380B2 (en) | 2016-12-09 | 2019-11-05 | Dfine, Inc. | Medical devices for treating hard tissues and related methods |
| WO2018129180A1 (en) | 2017-01-06 | 2018-07-12 | Dfine, Inc. | Osteotome with a distal portion for simultaneous advancement and articulation |
| EP3614946B1 (en) | 2017-04-27 | 2024-03-20 | EPiX Therapeutics, Inc. | Determining nature of contact between catheter tip and tissue |
| US10856771B2 (en) * | 2017-09-29 | 2020-12-08 | Biosense Webster (Israel) Ltd. | Ablation size estimation and visual representation |
| US11564756B2 (en) | 2017-10-30 | 2023-01-31 | Cilag Gmbh International | Method of hub communication with surgical instrument systems |
| US11109878B2 (en) | 2017-10-30 | 2021-09-07 | Cilag Gmbh International | Surgical clip applier comprising an automatic clip feeding system |
| US11510741B2 (en) | 2017-10-30 | 2022-11-29 | Cilag Gmbh International | Method for producing a surgical instrument comprising a smart electrical system |
| US11291510B2 (en) | 2017-10-30 | 2022-04-05 | Cilag Gmbh International | Method of hub communication with surgical instrument systems |
| US11229436B2 (en) | 2017-10-30 | 2022-01-25 | Cilag Gmbh International | Surgical system comprising a surgical tool and a surgical hub |
| US11311342B2 (en) | 2017-10-30 | 2022-04-26 | Cilag Gmbh International | Method for communicating with surgical instrument systems |
| US11801098B2 (en) | 2017-10-30 | 2023-10-31 | Cilag Gmbh International | Method of hub communication with surgical instrument systems |
| US11413042B2 (en) | 2017-10-30 | 2022-08-16 | Cilag Gmbh International | Clip applier comprising a reciprocating clip advancing member |
| US11317919B2 (en) | 2017-10-30 | 2022-05-03 | Cilag Gmbh International | Clip applier comprising a clip crimping system |
| US11911045B2 (en) | 2017-10-30 | 2024-02-27 | Cllag GmbH International | Method for operating a powered articulating multi-clip applier |
| JP6941030B2 (ja) * | 2017-11-08 | 2021-09-29 | 日本光電工業株式会社 | 電極カテーテル |
| WO2019126260A1 (en) | 2017-12-19 | 2019-06-27 | St. Jude Medical, Cardiology Division, Inc. | Methods of assessing contact between an electrode and tissue using complex impedance measurements |
| US11744604B2 (en) | 2017-12-28 | 2023-09-05 | Cilag Gmbh International | Surgical instrument with a hardware-only control circuit |
| US11304720B2 (en) | 2017-12-28 | 2022-04-19 | Cilag Gmbh International | Activation of energy devices |
| US11633237B2 (en) | 2017-12-28 | 2023-04-25 | Cilag Gmbh International | Usage and technique analysis of surgeon / staff performance against a baseline to optimize device utilization and performance for both current and future procedures |
| US11589888B2 (en) | 2017-12-28 | 2023-02-28 | Cilag Gmbh International | Method for controlling smart energy devices |
| US11304745B2 (en) | 2017-12-28 | 2022-04-19 | Cilag Gmbh International | Surgical evacuation sensing and display |
| US11666331B2 (en) | 2017-12-28 | 2023-06-06 | Cilag Gmbh International | Systems for detecting proximity of surgical end effector to cancerous tissue |
| US20190200981A1 (en) | 2017-12-28 | 2019-07-04 | Ethicon Llc | Method of compressing tissue within a stapling device and simultaneously displaying the location of the tissue within the jaws |
| US11446052B2 (en) | 2017-12-28 | 2022-09-20 | Cilag Gmbh International | Variation of radio frequency and ultrasonic power level in cooperation with varying clamp arm pressure to achieve predefined heat flux or power applied to tissue |
| US11166772B2 (en) | 2017-12-28 | 2021-11-09 | Cilag Gmbh International | Surgical hub coordination of control and communication of operating room devices |
| US11389164B2 (en) | 2017-12-28 | 2022-07-19 | Cilag Gmbh International | Method of using reinforced flexible circuits with multiple sensors to optimize performance of radio frequency devices |
| US11253315B2 (en) | 2017-12-28 | 2022-02-22 | Cilag Gmbh International | Increasing radio frequency to create pad-less monopolar loop |
| US11284936B2 (en) | 2017-12-28 | 2022-03-29 | Cilag Gmbh International | Surgical instrument having a flexible electrode |
| US11273001B2 (en) | 2017-12-28 | 2022-03-15 | Cilag Gmbh International | Surgical hub and modular device response adjustment based on situational awareness |
| US11304699B2 (en) | 2017-12-28 | 2022-04-19 | Cilag Gmbh International | Method for adaptive control schemes for surgical network control and interaction |
| US11529187B2 (en) | 2017-12-28 | 2022-12-20 | Cilag Gmbh International | Surgical evacuation sensor arrangements |
| US11903601B2 (en) | 2017-12-28 | 2024-02-20 | Cilag Gmbh International | Surgical instrument comprising a plurality of drive systems |
| US11678881B2 (en) | 2017-12-28 | 2023-06-20 | Cilag Gmbh International | Spatial awareness of surgical hubs in operating rooms |
| US11179175B2 (en) | 2017-12-28 | 2021-11-23 | Cilag Gmbh International | Controlling an ultrasonic surgical instrument according to tissue location |
| US11317937B2 (en) | 2018-03-08 | 2022-05-03 | Cilag Gmbh International | Determining the state of an ultrasonic end effector |
| US11423007B2 (en) | 2017-12-28 | 2022-08-23 | Cilag Gmbh International | Adjustment of device control programs based on stratified contextual data in addition to the data |
| US11132462B2 (en) | 2017-12-28 | 2021-09-28 | Cilag Gmbh International | Data stripping method to interrogate patient records and create anonymized record |
| US11464559B2 (en) | 2017-12-28 | 2022-10-11 | Cilag Gmbh International | Estimating state of ultrasonic end effector and control system therefor |
| US11832899B2 (en) | 2017-12-28 | 2023-12-05 | Cilag Gmbh International | Surgical systems with autonomously adjustable control programs |
| US11571234B2 (en) | 2017-12-28 | 2023-02-07 | Cilag Gmbh International | Temperature control of ultrasonic end effector and control system therefor |
| US11540855B2 (en) * | 2017-12-28 | 2023-01-03 | Cilag Gmbh International | Controlling activation of an ultrasonic surgical instrument according to the presence of tissue |
| US11160605B2 (en) | 2017-12-28 | 2021-11-02 | Cilag Gmbh International | Surgical evacuation sensing and motor control |
| US11937769B2 (en) | 2017-12-28 | 2024-03-26 | Cilag Gmbh International | Method of hub communication, processing, storage and display |
| US11266468B2 (en) | 2017-12-28 | 2022-03-08 | Cilag Gmbh International | Cooperative utilization of data derived from secondary sources by intelligent surgical hubs |
| US11464535B2 (en) | 2017-12-28 | 2022-10-11 | Cilag Gmbh International | Detection of end effector emersion in liquid |
| US11424027B2 (en) | 2017-12-28 | 2022-08-23 | Cilag Gmbh International | Method for operating surgical instrument systems |
| US11419630B2 (en) | 2017-12-28 | 2022-08-23 | Cilag Gmbh International | Surgical system distributed processing |
| US10758310B2 (en) | 2017-12-28 | 2020-09-01 | Ethicon Llc | Wireless pairing of a surgical device with another device within a sterile surgical field based on the usage and situational awareness of devices |
| US11026751B2 (en) | 2017-12-28 | 2021-06-08 | Cilag Gmbh International | Display of alignment of staple cartridge to prior linear staple line |
| US11202570B2 (en) | 2017-12-28 | 2021-12-21 | Cilag Gmbh International | Communication hub and storage device for storing parameters and status of a surgical device to be shared with cloud based analytics systems |
| US20190201146A1 (en) | 2017-12-28 | 2019-07-04 | Ethicon Llc | Safety systems for smart powered surgical stapling |
| US11864728B2 (en) | 2017-12-28 | 2024-01-09 | Cilag Gmbh International | Characterization of tissue irregularities through the use of mono-chromatic light refractivity |
| US11832840B2 (en) | 2017-12-28 | 2023-12-05 | Cilag Gmbh International | Surgical instrument having a flexible circuit |
| US11576677B2 (en) | 2017-12-28 | 2023-02-14 | Cilag Gmbh International | Method of hub communication, processing, display, and cloud analytics |
| US11364075B2 (en) | 2017-12-28 | 2022-06-21 | Cilag Gmbh International | Radio frequency energy device for delivering combined electrical signals |
| US20190201039A1 (en) | 2017-12-28 | 2019-07-04 | Ethicon Llc | Situational awareness of electrosurgical systems |
| US11818052B2 (en) | 2017-12-28 | 2023-11-14 | Cilag Gmbh International | Surgical network determination of prioritization of communication, interaction, or processing based on system or device needs |
| US11324557B2 (en) | 2017-12-28 | 2022-05-10 | Cilag Gmbh International | Surgical instrument with a sensing array |
| US10892995B2 (en) | 2017-12-28 | 2021-01-12 | Ethicon Llc | Surgical network determination of prioritization of communication, interaction, or processing based on system or device needs |
| US11257589B2 (en) | 2017-12-28 | 2022-02-22 | Cilag Gmbh International | Real-time analysis of comprehensive cost of all instrumentation used in surgery utilizing data fluidity to track instruments through stocking and in-house processes |
| US11304763B2 (en) | 2017-12-28 | 2022-04-19 | Cilag Gmbh International | Image capturing of the areas outside the abdomen to improve placement and control of a surgical device in use |
| US11419667B2 (en) | 2017-12-28 | 2022-08-23 | Cilag Gmbh International | Ultrasonic energy device which varies pressure applied by clamp arm to provide threshold control pressure at a cut progression location |
| US11559307B2 (en) | 2017-12-28 | 2023-01-24 | Cilag Gmbh International | Method of robotic hub communication, detection, and control |
| US11896443B2 (en) | 2017-12-28 | 2024-02-13 | Cilag Gmbh International | Control of a surgical system through a surgical barrier |
| US11311306B2 (en) | 2017-12-28 | 2022-04-26 | Cilag Gmbh International | Surgical systems for detecting end effector tissue distribution irregularities |
| US11786251B2 (en) | 2017-12-28 | 2023-10-17 | Cilag Gmbh International | Method for adaptive control schemes for surgical network control and interaction |
| US11559308B2 (en) | 2017-12-28 | 2023-01-24 | Cilag Gmbh International | Method for smart energy device infrastructure |
| US11179208B2 (en) | 2017-12-28 | 2021-11-23 | Cilag Gmbh International | Cloud-based medical analytics for security and authentication trends and reactive measures |
| US11234756B2 (en) | 2017-12-28 | 2022-02-01 | Cilag Gmbh International | Powered surgical tool with predefined adjustable control algorithm for controlling end effector parameter |
| US11291495B2 (en) | 2017-12-28 | 2022-04-05 | Cilag Gmbh International | Interruption of energy due to inadvertent capacitive coupling |
| US11602393B2 (en) | 2017-12-28 | 2023-03-14 | Cilag Gmbh International | Surgical evacuation sensing and generator control |
| US11896322B2 (en) | 2017-12-28 | 2024-02-13 | Cilag Gmbh International | Sensing the patient position and contact utilizing the mono-polar return pad electrode to provide situational awareness to the hub |
| US11612444B2 (en) | 2017-12-28 | 2023-03-28 | Cilag Gmbh International | Adjustment of a surgical device function based on situational awareness |
| US11432885B2 (en) | 2017-12-28 | 2022-09-06 | Cilag Gmbh International | Sensing arrangements for robot-assisted surgical platforms |
| US11786245B2 (en) | 2017-12-28 | 2023-10-17 | Cilag Gmbh International | Surgical systems with prioritized data transmission capabilities |
| US11058498B2 (en) | 2017-12-28 | 2021-07-13 | Cilag Gmbh International | Cooperative surgical actions for robot-assisted surgical platforms |
| US11109866B2 (en) | 2017-12-28 | 2021-09-07 | Cilag Gmbh International | Method for circular stapler control algorithm adjustment based on situational awareness |
| US11278281B2 (en) | 2017-12-28 | 2022-03-22 | Cilag Gmbh International | Interactive surgical system |
| US11376002B2 (en) | 2017-12-28 | 2022-07-05 | Cilag Gmbh International | Surgical instrument cartridge sensor assemblies |
| US11308075B2 (en) | 2017-12-28 | 2022-04-19 | Cilag Gmbh International | Surgical network, instrument, and cloud responses based on validation of received dataset and authentication of its source and integrity |
| US11410259B2 (en) | 2017-12-28 | 2022-08-09 | Cilag Gmbh International | Adaptive control program updates for surgical devices |
| US11857152B2 (en) | 2017-12-28 | 2024-01-02 | Cilag Gmbh International | Surgical hub spatial awareness to determine devices in operating theater |
| US11013563B2 (en) | 2017-12-28 | 2021-05-25 | Ethicon Llc | Drive arrangements for robot-assisted surgical platforms |
| US11659023B2 (en) | 2017-12-28 | 2023-05-23 | Cilag Gmbh International | Method of hub communication |
| US11678927B2 (en) | 2018-03-08 | 2023-06-20 | Cilag Gmbh International | Detection of large vessels during parenchymal dissection using a smart blade |
| US11457944B2 (en) | 2018-03-08 | 2022-10-04 | Cilag Gmbh International | Adaptive advanced tissue treatment pad saver mode |
| US11259830B2 (en) | 2018-03-08 | 2022-03-01 | Cilag Gmbh International | Methods for controlling temperature in ultrasonic device |
| US11166716B2 (en) | 2018-03-28 | 2021-11-09 | Cilag Gmbh International | Stapling instrument comprising a deactivatable lockout |
| US11278280B2 (en) | 2018-03-28 | 2022-03-22 | Cilag Gmbh International | Surgical instrument comprising a jaw closure lockout |
| US11259806B2 (en) | 2018-03-28 | 2022-03-01 | Cilag Gmbh International | Surgical stapling devices with features for blocking advancement of a camming assembly of an incompatible cartridge installed therein |
| US11219453B2 (en) | 2018-03-28 | 2022-01-11 | Cilag Gmbh International | Surgical stapling devices with cartridge compatible closure and firing lockout arrangements |
| US11090047B2 (en) | 2018-03-28 | 2021-08-17 | Cilag Gmbh International | Surgical instrument comprising an adaptive control system |
| US11471156B2 (en) | 2018-03-28 | 2022-10-18 | Cilag Gmbh International | Surgical stapling devices with improved rotary driven closure systems |
| US11207067B2 (en) | 2018-03-28 | 2021-12-28 | Cilag Gmbh International | Surgical stapling device with separate rotary driven closure and firing systems and firing member that engages both jaws while firing |
| US11666232B2 (en) * | 2018-04-18 | 2023-06-06 | Boston Scientific Scimed, Inc. | Methods for assessing a vessel with sequential physiological measurements |
| WO2019217317A1 (en) | 2018-05-07 | 2019-11-14 | Farapulse, Inc. | Systems, apparatuses, and methods for filtering high voltage noise induced by pulsed electric field ablation |
| CN112087980B (zh) | 2018-05-07 | 2023-01-10 | 波士顿科学医学有限公司 | 用于将消融能量递送到组织的系统、设备和方法 |
| JP2021525559A (ja) * | 2018-05-30 | 2021-09-27 | アヴェント インコーポレイテッド | 冷却型高周波プローブの使用中にポンプアセンブリによってインピーダンス上昇を緩和するためのシステム及び方法 |
| US11241281B2 (en) * | 2018-08-13 | 2022-02-08 | Biosense Webster (Israel) Ltd. | Estimation of electrode-tissue contact using oscillator at common ground of electrocardiogram (ECG) system |
| CN112804955A (zh) * | 2018-10-05 | 2021-05-14 | Epix疗法公司 | 损伤形成评估和显示 |
| US11246505B2 (en) * | 2018-11-01 | 2022-02-15 | Biosense Webster (Israel) Ltd. | Using radiofrequency (RF) transmission system to find opening in tissue wall |
| US11937864B2 (en) * | 2018-11-08 | 2024-03-26 | Dfine, Inc. | Ablation systems with parameter-based modulation and related devices and methods |
| US11647980B2 (en) | 2018-12-27 | 2023-05-16 | Avent, Inc. | Methods for needle identification on an ultrasound display screen by determining a meta-frame rate of the data signals |
| US11464485B2 (en) | 2018-12-27 | 2022-10-11 | Avent, Inc. | Transducer-mounted needle assembly with improved electrical connection to power source |
| US11369377B2 (en) | 2019-02-19 | 2022-06-28 | Cilag Gmbh International | Surgical stapling assembly with cartridge based retainer configured to unlock a firing lockout |
| US11317915B2 (en) | 2019-02-19 | 2022-05-03 | Cilag Gmbh International | Universal cartridge based key feature that unlocks multiple lockout arrangements in different surgical staplers |
| US11357503B2 (en) | 2019-02-19 | 2022-06-14 | Cilag Gmbh International | Staple cartridge retainers with frangible retention features and methods of using same |
| US11291444B2 (en) | 2019-02-19 | 2022-04-05 | Cilag Gmbh International | Surgical stapling assembly with cartridge based retainer configured to unlock a closure lockout |
| US11464511B2 (en) | 2019-02-19 | 2022-10-11 | Cilag Gmbh International | Surgical staple cartridges with movable authentication key arrangements |
| CN113645915A (zh) * | 2019-04-02 | 2021-11-12 | 悉尼大学 | 用于通过受约束的阻抗测量监测组织消融的方法和系统 |
| US11045652B2 (en) * | 2019-04-26 | 2021-06-29 | Medtronic, Inc. | Determination of therapy electrode locations relative to oscillatory sources within patient |
| USD950728S1 (en) | 2019-06-25 | 2022-05-03 | Cilag Gmbh International | Surgical staple cartridge |
| USD964564S1 (en) | 2019-06-25 | 2022-09-20 | Cilag Gmbh International | Surgical staple cartridge retainer with a closure system authentication key |
| USD952144S1 (en) | 2019-06-25 | 2022-05-17 | Cilag Gmbh International | Surgical staple cartridge retainer with firing system authentication key |
| US10625080B1 (en) | 2019-09-17 | 2020-04-21 | Farapulse, Inc. | Systems, apparatuses, and methods for detecting ectopic electrocardiogram signals during pulsed electric field ablation |
| US11771488B2 (en) * | 2019-10-21 | 2023-10-03 | Biosense Webster (Israel) Ltd. | Ablation of lesions of low-medium depths using ultrahigh radiofrequency (RF) power for ultrashort durations |
| US11065047B2 (en) | 2019-11-20 | 2021-07-20 | Farapulse, Inc. | Systems, apparatuses, and methods for protecting electronic components from high power noise induced by high voltage pulses |
| US11497541B2 (en) | 2019-11-20 | 2022-11-15 | Boston Scientific Scimed, Inc. | Systems, apparatuses, and methods for protecting electronic components from high power noise induced by high voltage pulses |
| US10842572B1 (en) * | 2019-11-25 | 2020-11-24 | Farapulse, Inc. | Methods, systems, and apparatuses for tracking ablation devices and generating lesion lines |
| CN111374645A (zh) * | 2020-03-24 | 2020-07-07 | 聚融医疗科技(杭州)有限公司 | 一种热消融实时监控的呼吸伪像校正方法及系统 |
| US11559280B2 (en) * | 2020-05-08 | 2023-01-24 | GE Precision Healthcare LLC | Ultrasound imaging system and method for determining acoustic contact |
| US11635334B2 (en) * | 2020-06-30 | 2023-04-25 | Apple Inc. | Miniature external temperature sensing device for estimating subsurface tissue temperatures |
| US11408778B2 (en) | 2020-07-21 | 2022-08-09 | Apple Inc. | Temperature gradient sensing in portable electronic devices |
| US11771329B2 (en) | 2020-09-24 | 2023-10-03 | Apple Inc. | Flexible temperature sensing devices for body temperature sensing |
| JPWO2022113919A1 (ja) * | 2020-11-30 | 2022-06-02 | ||
| WO2022120127A1 (en) | 2020-12-03 | 2022-06-09 | Medtronic, Inc. | Lesion characterization processes |
| US20220175302A1 (en) * | 2020-12-04 | 2022-06-09 | Biosense Webster (Israel) Ltd. | Generating electrocardiograms from multiple references |
| US20220192748A1 (en) * | 2020-12-22 | 2022-06-23 | Biosense Webster (Israel) Ltd. | Displaying annotations on design line formed on anatomical map |
| US20220202474A1 (en) * | 2020-12-29 | 2022-06-30 | Ethicon Llc | Filter for monopolar surgical instrument energy path |
| IL307390A (en) | 2021-04-07 | 2023-11-01 | Btl Medical Dev A S | Apparatus and method for ablation (burning) by electric pulse field |
| EP4079243A1 (en) | 2021-04-23 | 2022-10-26 | Koninklijke Philips N.V. | Sensing for a catheter |
| IL309432A (en) | 2021-07-06 | 2024-02-01 | Btl Medical Dev A S | Apparatus and method for ablation (burning) by electric pulse field |
| GB2609232A (en) * | 2021-07-26 | 2023-02-01 | Gyrus Medical Ltd | Electrosurgical instrument |
| EP4190265A1 (de) * | 2021-12-01 | 2023-06-07 | Erbe Elektromedizin GmbH | Vorrichtung und verfahren zur bildgestützten unterstützung eines anwenders |
| KR20230082918A (ko) | 2021-12-02 | 2023-06-09 | 주식회사 스타메드 | 천공용 의료 장치 |
| EP4349288A1 (de) * | 2022-10-07 | 2024-04-10 | Erbe Elektromedizin GmbH | Ablationssonde mit innerer kühlung |
| CN117159128B (zh) * | 2023-11-03 | 2024-01-30 | 浙江伽奈维医疗科技有限公司 | 可用于陡脉冲消融和/或射频消融的消融装置及消融电极 |
Family Cites Families (771)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6014590A (en) | 1974-03-04 | 2000-01-11 | Ep Technologies, Inc. | Systems and methods employing structures having asymmetric mechanical properties to support diagnostic or therapeutic elements in contact with tissue in interior body regions |
| US5904680A (en) | 1992-09-25 | 1999-05-18 | Ep Technologies, Inc. | Multiple electrode support structures having optimal bio-mechanical characteristics |
| US4190053A (en) | 1977-06-20 | 1980-02-26 | Rca Corporation | Apparatus and method for hyperthermia treatment |
| US4197860A (en) | 1977-11-21 | 1980-04-15 | Rca Corporation | Hyperthermia applicator |
| US4346716A (en) | 1980-03-31 | 1982-08-31 | M/A Com, Inc. | Microwave detection system |
| US4557272A (en) | 1980-03-31 | 1985-12-10 | Microwave Associates, Inc. | Microwave endoscope detection and treatment system |
| US5385544A (en) | 1992-08-12 | 1995-01-31 | Vidamed, Inc. | BPH ablation method and apparatus |
| US5370675A (en) | 1992-08-12 | 1994-12-06 | Vidamed, Inc. | Medical probe device and method |
| US5421819A (en) | 1992-08-12 | 1995-06-06 | Vidamed, Inc. | Medical probe device |
| US5542915A (en) | 1992-08-12 | 1996-08-06 | Vidamed, Inc. | Thermal mapping catheter with ultrasound probe |
| US4614514A (en) | 1983-02-16 | 1986-09-30 | M/A Com, Inc. | Microwave sterilizer |
| US4955382A (en) | 1984-03-06 | 1990-09-11 | Ep Technologies | Apparatus and method for recording monophasic action potentials from an in vivo heart |
| US4979510A (en) | 1984-03-06 | 1990-12-25 | Ep Technologies, Inc. | Apparatus and method for recording monophasic action potentials from an in vivo heart |
| US4715727A (en) | 1984-07-05 | 1987-12-29 | M/A-Com, Inc. | Non-invasive temperature monitor |
| USRE33791E (en) | 1984-07-05 | 1992-01-07 | M/A-Com, Inc. | Non-invasive temperature monitor |
| US4727874A (en) | 1984-09-10 | 1988-03-01 | C. R. Bard, Inc. | Electrosurgical generator with high-frequency pulse width modulated feedback power control |
| US4647281A (en) | 1985-02-20 | 1987-03-03 | M/A-Com, Inc. | Infiltration detection apparatus |
| US4686498A (en) | 1985-04-15 | 1987-08-11 | M/A-Com, Inc. | Coaxial connector |
| US4632127A (en) | 1985-06-17 | 1986-12-30 | Rca Corporation | Scanning microwave hyperthermia with feedback temperature control |
| US4774961A (en) | 1985-11-07 | 1988-10-04 | M/A Com, Inc. | Multiple antennae breast screening system |
| US4815479A (en) | 1986-08-13 | 1989-03-28 | M/A Com, Inc. | Hyperthermia treatment method and apparatus |
| US5073167A (en) | 1987-06-26 | 1991-12-17 | M/A-Com, Inc. | In-line microwave warming apparatus |
| US5782897A (en) | 1987-06-26 | 1998-07-21 | Microwave Medical Systems, Inc. | Microwave heating apparatus for rapid tissue fixation |
| US6587732B1 (en) | 1987-06-26 | 2003-07-01 | Kenneth L. Carr | Heat treatment for viral inactivation |
| US5919218A (en) | 1987-06-26 | 1999-07-06 | Microwave Medical Systems | Cartridge for in-line microwave warming apparatus |
| US4922912A (en) | 1987-10-21 | 1990-05-08 | Hideto Watanabe | MAP catheter |
| US5588432A (en) * | 1988-03-21 | 1996-12-31 | Boston Scientific Corporation | Catheters for imaging, sensing electrical potentials, and ablating tissue |
| US5344435A (en) | 1988-07-28 | 1994-09-06 | Bsd Medical Corporation | Urethral inserted applicator prostate hyperthermia |
| US4949718B1 (en) | 1988-09-09 | 1998-11-10 | Gynelab Products | Intrauterine cauterizing apparatus |
| US5230349A (en) | 1988-11-25 | 1993-07-27 | Sensor Electronics, Inc. | Electrical heating catheter |
| US4945912A (en) | 1988-11-25 | 1990-08-07 | Sensor Electronics, Inc. | Catheter with radiofrequency heating applicator |
| FR2650390B1 (fr) | 1989-07-27 | 1992-10-30 | Inst Nat Sante Rech Med | Procede pour la mesure des temperatures par radiometrie microonde, avec calibration automatique de la mesure, et dispositif pour la mise en oeuvre de ce procede |
| US5624392A (en) | 1990-05-11 | 1997-04-29 | Saab; Mark A. | Heat transfer catheters and methods of making and using same |
| WO1992010932A1 (en) | 1990-12-17 | 1992-07-09 | Microwave Medical Systems, Inc. | Therapeutic probe for radiating microwave and nuclear radiation |
| US5531662A (en) | 1990-12-17 | 1996-07-02 | Microwave Medical Systems, Inc. | Dual mode microwave/ionizing probe |
| US5149198A (en) | 1991-05-02 | 1992-09-22 | Mmtc, Inc. | Temperature-measuring microwave radiometer apparatus |
| WO1992021285A1 (en) | 1991-05-24 | 1992-12-10 | Ep Technologies, Inc. | Combination monophasic action potential/ablation catheter and high-performance filter system |
| US5198776A (en) | 1991-06-26 | 1993-03-30 | Microwave Medical Systems, Inc. | Microwave system for detecting gaseous emboli |
| US20010051803A1 (en) | 1991-07-05 | 2001-12-13 | Desai Jawahar M. | Device and method for multi-phase radio-frequency ablation |
| FR2679455B1 (fr) | 1991-07-26 | 1998-08-28 | Inst Nat Sante Rech Med | Systeme pour le traitement thermique interne d'un corps certain et son utilisation. |
| GB9118670D0 (en) | 1991-08-30 | 1991-10-16 | Mcnicholas Thomas A | Surgical devices and uses thereof |
| WO1993008755A1 (en) | 1991-11-08 | 1993-05-13 | Ep Technologies, Inc. | Ablation electrode with insulated temperature sensing elements |
| US5906614A (en) | 1991-11-08 | 1999-05-25 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using predicted temperature for monitoring and control |
| US5383874A (en) | 1991-11-08 | 1995-01-24 | Ep Technologies, Inc. | Systems for identifying catheters and monitoring their use |
| US5282840A (en) | 1992-03-26 | 1994-02-01 | Medtronic, Inc. | Multiple frequency impedance measurement system |
| FR2689768B1 (fr) | 1992-04-08 | 1997-06-27 | Inst Nat Sante Rech Med | Dispositif applicateur d'hyperthermie par micro-ondes dans un corps certain. |
| US5334141A (en) | 1992-06-26 | 1994-08-02 | Medrad, Inc. | Extravasation detection system and apparatus |
| US5720718A (en) | 1992-08-12 | 1998-02-24 | Vidamed, Inc. | Medical probe apparatus with enhanced RF, resistance heating, and microwave ablation capabilities |
| US5667488A (en) | 1992-08-12 | 1997-09-16 | Vidamed, Inc. | Transurethral needle ablation device and method for the treatment of the prostate |
| US5334193A (en) | 1992-11-13 | 1994-08-02 | American Cardiac Ablation Co., Inc. | Fluid cooled ablation catheter |
| WO1994010922A1 (en) | 1992-11-13 | 1994-05-26 | Ep Technologies, Inc. | Cardial ablation systems using temperature monitoring |
| US5348554A (en) | 1992-12-01 | 1994-09-20 | Cardiac Pathways Corporation | Catheter for RF ablation with cooled electrode |
| US5385146A (en) | 1993-01-08 | 1995-01-31 | Goldreyer; Bruce N. | Orthogonal sensing for use in clinical electrophysiology |
| AU685086B2 (en) | 1993-02-02 | 1998-01-15 | Vidamed, Inc. | Transurethral needle ablation device |
| WO1994021170A1 (en) | 1993-03-16 | 1994-09-29 | Ep Technologies, Inc. | Flexible circuit assemblies employing ribbon cable |
| WO1994021166A1 (en) | 1993-03-16 | 1994-09-29 | Ep Technologies, Inc. | Multiple electrode support structures |
| US5336222A (en) | 1993-03-29 | 1994-08-09 | Boston Scientific Corporation | Integrated catheter for diverse in situ tissue therapy |
| US20020115941A1 (en) | 1993-04-15 | 2002-08-22 | Scimed Life Systems, Inc. | Systems and methods using annotated images for controlling the use of diagnostic or therapeutic instruments in interior body regions |
| DE69434185T2 (de) | 1993-06-10 | 2005-06-02 | Imran, Mir A., Los Altos Hills | Urethrales gerät zur ablation mittels hochfrequenz |
| WO1995005212A2 (en) | 1993-08-11 | 1995-02-23 | Electro-Catheter Corporation | Improved ablation electrode |
| US5562619A (en) | 1993-08-19 | 1996-10-08 | Boston Scientific Corporation | Deflectable catheter |
| US5807395A (en) | 1993-08-27 | 1998-09-15 | Medtronic, Inc. | Method and apparatus for RF ablation and hyperthermia |
| US6129724A (en) | 1993-10-14 | 2000-10-10 | Ep Technologies, Inc. | Systems and methods for forming elongated lesion patterns in body tissue using straight or curvilinear electrode elements |
| US5582609A (en) | 1993-10-14 | 1996-12-10 | Ep Technologies, Inc. | Systems and methods for forming large lesions in body tissue using curvilinear electrode elements |
| DE69434664T2 (de) | 1993-10-14 | 2006-11-09 | Boston Scientific Ltd., Barbados | Elektroden zur erzeugung bestimmter muster von pathologisch verändertem gewebe |
| US5797903A (en) | 1996-04-12 | 1998-08-25 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using porous electrode structures with electrically conductive surfaces |
| US5840076A (en) | 1996-04-12 | 1998-11-24 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using electrode structures with distally oriented porous regions |
| US6032061A (en) | 1997-02-20 | 2000-02-29 | Boston Scientifc Corporation | Catheter carrying an electrode and methods of assembly |
| US5991650A (en) | 1993-10-15 | 1999-11-23 | Ep Technologies, Inc. | Surface coatings for catheters, direct contacting diagnostic and therapeutic devices |
| US5536267A (en) | 1993-11-08 | 1996-07-16 | Zomed International | Multiple electrode ablation apparatus |
| US5683384A (en) | 1993-11-08 | 1997-11-04 | Zomed | Multiple antenna ablation apparatus |
| US5928229A (en) | 1993-11-08 | 1999-07-27 | Rita Medical Systems, Inc. | Tumor ablation apparatus |
| US6641580B1 (en) | 1993-11-08 | 2003-11-04 | Rita Medical Systems, Inc. | Infusion array ablation apparatus |
| US6632221B1 (en) | 1993-11-08 | 2003-10-14 | Rita Medical Systems, Inc. | Method of creating a lesion in tissue with infusion |
| US5462521A (en) | 1993-12-21 | 1995-10-31 | Angeion Corporation | Fluid cooled and perfused tip for a catheter |
| WO1995020344A1 (en) | 1994-01-28 | 1995-08-03 | Ep Technologies, Inc. | System for examining cardiac tissue electrical characteristics |
| WO1995020345A1 (en) | 1994-01-28 | 1995-08-03 | Ep Technologies, Inc. | Minimizing blood contact in cardiac tissue measurements |
| US5485849A (en) | 1994-01-31 | 1996-01-23 | Ep Technologies, Inc. | System and methods for matching electrical characteristics and propagation velocities in cardiac tissue |
| WO1995020348A1 (en) | 1994-01-28 | 1995-08-03 | Ep Technologies, Inc. | Matching electrical characteristics and propagation velocities to locate ablation sites |
| US5577509A (en) | 1994-01-28 | 1996-11-26 | Ep Technologies, Inc. | Systems and methods for examining the electrical characteristics and timing of electrical events in cardiac tissue |
| US5494042A (en) | 1994-01-28 | 1996-02-27 | Ep Technologies, Inc. | Systems and methods for deriving electrical characteristics of cardiac tissue for output in iso-characteristic displays |
| US5487391A (en) | 1994-01-28 | 1996-01-30 | Ep Technologies, Inc. | Systems and methods for deriving and displaying the propagation velocities of electrical events in the heart |
| US5447529A (en) | 1994-01-28 | 1995-09-05 | Philadelphia Heart Institute | Method of using endocardial impedance for determining electrode-tissue contact, appropriate sites for arrhythmia ablation and tissue heating during ablation |
| JP3347457B2 (ja) | 1994-02-24 | 2002-11-20 | 日本電解株式会社 | 非シアン系銅−亜鉛電気めっき浴、これを用いたプリント配線板用銅箔の表面処理方法及びプリント配線板用銅箔 |
| US6216043B1 (en) | 1994-03-04 | 2001-04-10 | Ep Technologies, Inc. | Asymmetric multiple electrode support structures |
| US6165169A (en) | 1994-03-04 | 2000-12-26 | Ep Technologies, Inc. | Systems and methods for identifying the physical, mechanical, and functional attributes of multiple electrode arrays |
| US5911739A (en) | 1994-03-04 | 1999-06-15 | Ep Technologies, Inc. | Structures for supporting diagnostic or therapeutic elements in internal body regions |
| US5968040A (en) | 1994-03-04 | 1999-10-19 | Ep Technologies, Inc. | Systems and methods using asymmetric multiple electrode arrays |
| US5584830A (en) | 1994-03-30 | 1996-12-17 | Medtronic Cardiorhythm | Method and system for radiofrequency ablation of cardiac tissue |
| US5598848A (en) | 1994-03-31 | 1997-02-04 | Ep Technologies, Inc. | Systems and methods for positioning multiple electrode structures in electrical contact with the myocardium |
| US5674191A (en) | 1994-05-09 | 1997-10-07 | Somnus Medical Technologies, Inc. | Ablation apparatus and system for removal of soft palate tissue |
| US5681308A (en) | 1994-06-24 | 1997-10-28 | Stuart D. Edwards | Ablation apparatus for cardiac chambers |
| US5827277A (en) | 1994-06-24 | 1998-10-27 | Somnus Medical Technologies, Inc. | Minimally invasive apparatus for internal ablation of turbinates |
| US6056744A (en) | 1994-06-24 | 2000-05-02 | Conway Stuart Medical, Inc. | Sphincter treatment apparatus |
| US5853409A (en) | 1994-06-27 | 1998-12-29 | E.P. Technologies, Inc. | Systems and apparatus for sensing temperature in body tissue |
| CA2194071C (en) | 1994-06-27 | 2005-12-13 | Roger A. Stern | Non-linear control systems and methods for heating and ablating body tissue |
| US6113591A (en) | 1994-06-27 | 2000-09-05 | Ep Technologies, Inc. | Systems and methods for sensing sub-surface temperatures in body tissue |
| US5735846A (en) | 1994-06-27 | 1998-04-07 | Ep Technologies, Inc. | Systems and methods for ablating body tissue using predicted maximum tissue temperature |
| JP3578460B2 (ja) | 1994-06-27 | 2004-10-20 | ボストン サイエンティフィック リミテッド | 体内の温度を感知するためのシステム及び方法 |
| WO1996000036A1 (en) | 1994-06-27 | 1996-01-04 | Ep Technologies, Inc. | System for controlling tissue ablation using temperature sensors |
| US5616268A (en) | 1994-07-07 | 1997-04-01 | Microwave Medical Systems | Microwave blood thawing with feedback control |
| US5810802A (en) * | 1994-08-08 | 1998-09-22 | E.P. Technologies, Inc. | Systems and methods for controlling tissue ablation using multiple temperature sensing elements |
| US6030382A (en) | 1994-08-08 | 2000-02-29 | Ep Technologies, Inc. | Flexible tissue ablatin elements for making long lesions |
| US5797905A (en) | 1994-08-08 | 1998-08-25 | E. P. Technologies Inc. | Flexible tissue ablation elements for making long lesions |
| US5967976A (en) | 1994-08-19 | 1999-10-19 | Novoste Corporation | Apparatus and methods for procedures related to the electrophysiology of the heart |
| US5549639A (en) | 1994-09-16 | 1996-08-27 | Sandia Corporation | Non-invasive hyperthermia apparatus including coaxial applicator having a non-invasive radiometric receiving antenna incorporated therein and method of use thereof |
| US6464700B1 (en) | 1994-10-07 | 2002-10-15 | Scimed Life Systems, Inc. | Loop structures for positioning a diagnostic or therapeutic element on the epicardium or other organ surface |
| US6142994A (en) | 1994-10-07 | 2000-11-07 | Ep Technologies, Inc. | Surgical method and apparatus for positioning a diagnostic a therapeutic element within the body |
| US5836947A (en) | 1994-10-07 | 1998-11-17 | Ep Technologies, Inc. | Flexible structures having movable splines for supporting electrode elements |
| US7175619B2 (en) | 1994-10-07 | 2007-02-13 | Boston Scientific Scimed, Inc. | Loop structures for positioning a diagnostic or therapeutic element on the epicardium or other organ surface |
| US5740808A (en) | 1996-10-28 | 1998-04-21 | Ep Technologies, Inc | Systems and methods for guilding diagnostic or therapeutic devices in interior tissue regions |
| US5722402A (en) | 1994-10-11 | 1998-03-03 | Ep Technologies, Inc. | Systems and methods for guiding movable electrode elements within multiple-electrode structures |
| US5514130A (en) | 1994-10-11 | 1996-05-07 | Dorsal Med International | RF apparatus for controlled depth ablation of soft tissue |
| US5876336A (en) | 1994-10-11 | 1999-03-02 | Ep Technologies, Inc. | Systems and methods for guiding movable electrode elements within multiple-electrode structure |
| US5941251A (en) | 1994-10-11 | 1999-08-24 | Ep Technologies, Inc. | Systems for locating and guiding operative elements within interior body regions |
| US5595183A (en) | 1995-02-17 | 1997-01-21 | Ep Technologies, Inc. | Systems and methods for examining heart tissue employing multiple electrode structures and roving electrodes |
| JP3681126B2 (ja) | 1995-02-17 | 2005-08-10 | ボストン サイエンティフィック リミテッド | 生物学的事象の時系列計測を行うためのシステム |
| US5609157A (en) | 1995-02-17 | 1997-03-11 | Ep Technologies, Inc. | Systems and methods for analyzing biopotential morphologies in body tissue using iterative techniques |
| US5630425A (en) | 1995-02-17 | 1997-05-20 | Ep Technologies, Inc. | Systems and methods for adaptive filtering artifacts from composite signals |
| US6101409A (en) | 1995-02-17 | 2000-08-08 | Ep Technologies, Inc. | Systems and methods for analyzing biopotential morphologies in body tissue |
| US5722416A (en) | 1995-02-17 | 1998-03-03 | Ep Technologies, Inc. | Systems and methods for analyzing biopotential morphologies in heart tissue to locate potential ablation sites |
| US5792064A (en) | 1995-02-17 | 1998-08-11 | Panescu; Dorin | Systems and methods for analyzing cardiac biopotential morphologies by cross-correlation |
| US5601088A (en) | 1995-02-17 | 1997-02-11 | Ep Technologies, Inc. | Systems and methods for filtering artifacts from composite signals |
| US5711305A (en) | 1995-02-17 | 1998-01-27 | Ep Technologies, Inc. | Systems and methods for acquiring endocardially or epicardially paced electrocardiograms |
| US5605157A (en) | 1995-02-17 | 1997-02-25 | Ep Technologies, Inc. | Systems and methods for filtering signals derived from biological events |
| US6409722B1 (en) | 1998-07-07 | 2002-06-25 | Medtronic, Inc. | Apparatus and method for creating, maintaining, and controlling a virtual electrode used for the ablation of tissue |
| US5897553A (en) | 1995-11-02 | 1999-04-27 | Medtronic, Inc. | Ball point fluid-assisted electrocautery device |
| US5715832A (en) | 1995-02-28 | 1998-02-10 | Boston Scientific Corporation | Deflectable biopsy catheter |
| WO1996026675A1 (en) | 1995-02-28 | 1996-09-06 | Boston Scientific Corporation | Deflectable catheter for ablating cardiac tissue |
| US5688050A (en) | 1995-04-03 | 1997-11-18 | Mmtc, Inc. | Temperature-measuring microwave radiometer apparatus |
| DE19514570A1 (de) | 1995-04-20 | 1996-10-24 | Rittershaus & Blecher Gmbh | Plattenfilterpresse |
| US5707369A (en) | 1995-04-24 | 1998-01-13 | Ethicon Endo-Surgery, Inc. | Temperature feedback monitor for hemostatic surgical instrument |
| WO1996034570A1 (en) | 1995-05-01 | 1996-11-07 | Ep Technologies, Inc. | Systems and methods for obtaining desired lesion characteristics while ablating body tissue |
| US6053912A (en) | 1995-05-01 | 2000-04-25 | Ep Techonologies, Inc. | Systems and methods for sensing sub-surface temperatures in body tissue during ablation with actively cooled electrodes |
| US6030379A (en) | 1995-05-01 | 2000-02-29 | Ep Technologies, Inc. | Systems and methods for seeking sub-surface temperature conditions during tissue ablation |
| US5800432A (en) | 1995-05-01 | 1998-09-01 | Ep Technologies, Inc. | Systems and methods for actively cooling ablation electrodes using diodes |
| US5688267A (en) | 1995-05-01 | 1997-11-18 | Ep Technologies, Inc. | Systems and methods for sensing multiple temperature conditions during tissue ablation |
| WO1996034567A1 (en) | 1995-05-02 | 1996-11-07 | Heart Rhythm Technologies, Inc. | System for controlling the energy delivered to a patient for ablation |
| US5683382A (en) | 1995-05-15 | 1997-11-04 | Arrow International Investment Corp. | Microwave antenna catheter |
| US5656030A (en) | 1995-05-22 | 1997-08-12 | Boston Scientific Corporation | Bidirectional steerable catheter with deflectable distal tip |
| US6022346A (en) | 1995-06-07 | 2000-02-08 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using self-heated electrodes |
| US6293943B1 (en) | 1995-06-07 | 2001-09-25 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods which predict maximum tissue temperature |
| US6080150A (en) | 1995-08-15 | 2000-06-27 | Rita Medical Systems, Inc. | Cell necrosis apparatus |
| US5980517A (en) | 1995-08-15 | 1999-11-09 | Rita Medical Systems, Inc. | Cell necrosis apparatus |
| US5863290A (en) | 1995-08-15 | 1999-01-26 | Rita Medical Systems | Multiple antenna ablation apparatus and method |
| US5672174A (en) | 1995-08-15 | 1997-09-30 | Rita Medical Systems, Inc. | Multiple antenna ablation apparatus and method |
| US6090105A (en) | 1995-08-15 | 2000-07-18 | Rita Medical Systems, Inc. | Multiple electrode ablation apparatus and method |
| US5810804A (en) | 1995-08-15 | 1998-09-22 | Rita Medical Systems | Multiple antenna ablation apparatus and method with cooling element |
| US5735847A (en) | 1995-08-15 | 1998-04-07 | Zomed International, Inc. | Multiple antenna ablation apparatus and method with cooling element |
| US6235023B1 (en) | 1995-08-15 | 2001-05-22 | Rita Medical Systems, Inc. | Cell necrosis apparatus |
| US6059780A (en) | 1995-08-15 | 2000-05-09 | Rita Medical Systems, Inc. | Multiple antenna ablation apparatus and method with cooling element |
| US5782827A (en) | 1995-08-15 | 1998-07-21 | Rita Medical Systems, Inc. | Multiple antenna ablation apparatus and method with multiple sensor feedback |
| US6132425A (en) | 1995-08-15 | 2000-10-17 | Gough; Edward J. | Cell necrosis apparatus |
| US6689127B1 (en) | 1995-08-15 | 2004-02-10 | Rita Medical Systems | Multiple antenna ablation apparatus and method with multiple sensor feedback |
| US5690614A (en) | 1995-09-06 | 1997-11-25 | Microwave Medical Systems, Inc. | Microwave apparatus for warming low flow rate infusates |
| US6496738B2 (en) | 1995-09-06 | 2002-12-17 | Kenneth L. Carr | Dual frequency microwave heating apparatus |
| US6210367B1 (en) | 1995-09-06 | 2001-04-03 | Microwave Medical Systems, Inc. | Intracorporeal microwave warming method and apparatus |
| US6424869B1 (en) | 1995-09-06 | 2002-07-23 | Meridian Medical Systems, Llc | Dual mode transurethral microwave warming apparatus |
| US6146359A (en) | 1995-09-06 | 2000-11-14 | Microwave Medical Systems, Inc. | Apparatus for controlledly warming low flow rate infusates |
| US5685878A (en) | 1995-11-13 | 1997-11-11 | C.R. Bard, Inc. | Snap fit distal assembly for an ablation catheter |
| US5823955A (en) | 1995-11-20 | 1998-10-20 | Medtronic Cardiorhythm | Atrioventricular valve tissue ablation catheter and method |
| US5837001A (en) | 1995-12-08 | 1998-11-17 | C. R. Bard | Radio frequency energy delivery system for multipolar electrode catheters |
| US5868743A (en) | 1995-12-13 | 1999-02-09 | Children's Medical Center Corporation | Cardiac ablation system with low temperature target site identification |
| FR2743498B1 (fr) | 1996-01-12 | 1998-03-06 | Sadis Bruker Spectrospin | Sonde, notamment sonde uretrale, pour le chauffage de tissus par micro-ondes et pour la mesure de temperature par radiometrie |
| US5853411A (en) | 1996-01-19 | 1998-12-29 | Ep Technologies, Inc. | Enhanced electrical connections for electrode structures |
| US5868736A (en) | 1996-04-12 | 1999-02-09 | Ep Technologies, Inc. | Systems and methods to control tissue heating or ablation with porous electrode structures |
| US5925038A (en) | 1996-01-19 | 1999-07-20 | Ep Technologies, Inc. | Expandable-collapsible electrode structures for capacitive coupling to tissue |
| US5879348A (en) | 1996-04-12 | 1999-03-09 | Ep Technologies, Inc. | Electrode structures formed from flexible, porous, or woven materials |
| US5830213A (en) | 1996-04-12 | 1998-11-03 | Ep Technologies, Inc. | Systems for heating and ablating tissue using multifunctional electrode structures |
| US5961513A (en) | 1996-01-19 | 1999-10-05 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using porous electrode structures |
| US5846239A (en) | 1996-04-12 | 1998-12-08 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using segmented porous electrode structures |
| US5891136A (en) | 1996-01-19 | 1999-04-06 | Ep Technologies, Inc. | Expandable-collapsible mesh electrode structures |
| US6071278A (en) | 1996-02-28 | 2000-06-06 | Ep Technologies, Inc. | Tissue heating and ablation systems and methods using porous electrode structures with specified electrical resistivities |
| US5836874A (en) | 1996-04-08 | 1998-11-17 | Ep Technologies, Inc. | Multi-function electrode structures for electrically analyzing and heating body tissue |
| US5871483A (en) | 1996-01-19 | 1999-02-16 | Ep Technologies, Inc. | Folding electrode structures |
| US5846238A (en) | 1996-01-19 | 1998-12-08 | Ep Technologies, Inc. | Expandable-collapsible electrode structures with distal end steering or manipulation |
| US5879349A (en) | 1996-02-23 | 1999-03-09 | Somnus Medical Technologies, Inc. | Apparatus for treatment of air way obstructions |
| US5755760A (en) | 1996-03-11 | 1998-05-26 | Medtronic, Inc. | Deflectable catheter |
| US5662110A (en) | 1996-04-03 | 1997-09-02 | Microwave Medical Systems, Inc. | Microwave detection apparatus for locating cancerous tumors particularly breast tumors |
| US5983124A (en) | 1996-04-03 | 1999-11-09 | Microwave Medical Systems, Inc. | Microwave detection of tumors, particularly breast tumors |
| US6302880B1 (en) | 1996-04-08 | 2001-10-16 | Cardima, Inc. | Linear ablation assembly |
| US5904709A (en) | 1996-04-17 | 1999-05-18 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Microwave treatment for cardiac arrhythmias |
| AUPN957296A0 (en) | 1996-04-30 | 1996-05-23 | Cardiac Crc Nominees Pty Limited | A system for simultaneous unipolar multi-electrode ablation |
| US6743197B1 (en) | 1996-07-10 | 2004-06-01 | Novasys Medical, Inc. | Treatment of discrete tissues in respiratory, urinary, circulatory, reproductive and digestive systems |
| US6311692B1 (en) | 1996-10-22 | 2001-11-06 | Epicor, Inc. | Apparatus and method for diagnosis and therapy of electrophysiological disease |
| US20040260278A1 (en) | 1996-10-22 | 2004-12-23 | Anderson Scott C. | Apparatus and method for ablating tissue |
| US6840936B2 (en) | 1996-10-22 | 2005-01-11 | Epicor Medical, Inc. | Methods and devices for ablation |
| US5904651A (en) | 1996-10-28 | 1999-05-18 | Ep Technologies, Inc. | Systems and methods for visualizing tissue during diagnostic or therapeutic procedures |
| US5722403A (en) | 1996-10-28 | 1998-03-03 | Ep Technologies, Inc. | Systems and methods using a porous electrode for ablating and visualizing interior tissue regions |
| US5848969A (en) | 1996-10-28 | 1998-12-15 | Ep Technologies, Inc. | Systems and methods for visualizing interior tissue regions using expandable imaging structures |
| US5752518A (en) | 1996-10-28 | 1998-05-19 | Ep Technologies, Inc. | Systems and methods for visualizing interior regions of the body |
| US5908445A (en) | 1996-10-28 | 1999-06-01 | Ep Technologies, Inc. | Systems for visualizing interior tissue regions including an actuator to move imaging element |
| US5893885A (en) | 1996-11-01 | 1999-04-13 | Cordis Webster, Inc. | Multi-electrode ablation catheter |
| US5782828A (en) | 1996-12-11 | 1998-07-21 | Irvine Biomedical, Inc. | Ablation catheter with multiple flexible curves |
| US5954719A (en) | 1996-12-11 | 1999-09-21 | Irvine Biomedical, Inc. | System for operating a RF ablation generator |
| US6076012A (en) | 1996-12-19 | 2000-06-13 | Ep Technologies, Inc. | Structures for supporting porous electrode elements |
| US5910129A (en) | 1996-12-19 | 1999-06-08 | Ep Technologies, Inc. | Catheter distal assembly with pull wires |
| US6048329A (en) | 1996-12-19 | 2000-04-11 | Ep Technologies, Inc. | Catheter distal assembly with pull wires |
| US6235022B1 (en) | 1996-12-20 | 2001-05-22 | Cardiac Pathways, Inc | RF generator and pump apparatus and system and method for cooled ablation |
| AU5722198A (en) | 1996-12-20 | 1998-07-17 | Ep Technologies Inc | Unified switching system for electrophysiological stimulation and signal recording and analysis |
| US5833688A (en) | 1997-02-24 | 1998-11-10 | Boston Scientific Corporation | Sensing temperature with plurality of catheter sensors |
| US5916163A (en) | 1997-03-07 | 1999-06-29 | Ep Technologies, Inc. | Graphical user interface for use with multiple electrode catheters |
| US6625482B1 (en) | 1998-03-06 | 2003-09-23 | Ep Technologies, Inc. | Graphical user interface for use with multiple electrode catheters |
| US6063078A (en) | 1997-03-12 | 2000-05-16 | Medtronic, Inc. | Method and apparatus for tissue ablation |
| US5954661A (en) | 1997-03-31 | 1999-09-21 | Thomas Jefferson University | Tissue characterization and treatment using pacing |
| ES2353846T3 (es) | 1997-04-11 | 2011-03-07 | United States Surgical Corporation | Aparato para ablación con rf y controlador del mismo. |
| US5876340A (en) | 1997-04-17 | 1999-03-02 | Irvine Biomedical, Inc. | Ablation apparatus with ultrasonic imaging capabilities |
| US5792140A (en) | 1997-05-15 | 1998-08-11 | Irvine Biomedical, Inc. | Catheter having cooled multiple-needle electrode |
| US5849028A (en) | 1997-05-16 | 1998-12-15 | Irvine Biomedical, Inc. | Catheter and method for radiofrequency ablation of cardiac tissue |
| US5913856A (en) | 1997-05-19 | 1999-06-22 | Irvine Biomedical, Inc. | Catheter system having a porous shaft and fluid irrigation capabilities |
| US6217576B1 (en) | 1997-05-19 | 2001-04-17 | Irvine Biomedical Inc. | Catheter probe for treating focal atrial fibrillation in pulmonary veins |
| US6251109B1 (en) | 1997-06-27 | 2001-06-26 | Daig Corporation | Process and device for the treatment of atrial arrhythmia |
| US6547788B1 (en) | 1997-07-08 | 2003-04-15 | Atrionx, Inc. | Medical device with sensor cooperating with expandable member |
| US6514249B1 (en) | 1997-07-08 | 2003-02-04 | Atrionix, Inc. | Positioning system and method for orienting an ablation element within a pulmonary vein ostium |
| US6009351A (en) | 1997-07-14 | 1999-12-28 | Urologix, Inc. | System and method for transurethral heating with rectal cooling |
| US6080151A (en) | 1997-07-21 | 2000-06-27 | Daig Corporation | Ablation catheter |
| JP2001514921A (ja) | 1997-08-13 | 2001-09-18 | サークス, インコーポレイテッド | 組織収縮のための非侵襲性デバイス、方法、およびシステム |
| US5836990A (en) | 1997-09-19 | 1998-11-17 | Medtronic, Inc. | Method and apparatus for determining electrode/tissue contact |
| US6086532A (en) | 1997-09-26 | 2000-07-11 | Ep Technologies, Inc. | Systems for recording use of structures deployed in association with heart tissue |
| US6238389B1 (en) | 1997-09-30 | 2001-05-29 | Boston Scientific Corporation | Deflectable interstitial ablation device |
| SE519310C2 (sv) | 1997-10-02 | 2003-02-11 | Prostalund Operations Ab | Anordning för värmetillförsel |
| US6579288B1 (en) | 1997-10-10 | 2003-06-17 | Scimed Life Systems, Inc. | Fluid cooled apparatus for supporting diagnostic and therapeutic elements in contact with tissue |
| US6645200B1 (en) | 1997-10-10 | 2003-11-11 | Scimed Life Systems, Inc. | Method and apparatus for positioning a diagnostic or therapeutic element within the body and tip electrode for use with same |
| US6610055B1 (en) | 1997-10-10 | 2003-08-26 | Scimed Life Systems, Inc. | Surgical method for positioning a diagnostic or therapeutic element on the epicardium or other organ surface |
| US6468272B1 (en) | 1997-10-10 | 2002-10-22 | Scimed Life Systems, Inc. | Surgical probe for supporting diagnostic and therapeutic elements in contact with tissue in or around body orifices |
| US6259941B1 (en) | 1997-10-20 | 2001-07-10 | Irvine Biomedical, Inc. | Intravascular ultrasound locating system |
| US6176857B1 (en) | 1997-10-22 | 2001-01-23 | Oratec Interventions, Inc. | Method and apparatus for applying thermal energy to tissue asymmetrically |
| US5935063A (en) | 1997-10-29 | 1999-08-10 | Irvine Biomedical, Inc. | Electrode catheter system and methods thereof |
| US6416490B1 (en) | 1997-11-04 | 2002-07-09 | Scimed Life Systems, Inc. | PMR device and method |
| US6049732A (en) | 1997-11-17 | 2000-04-11 | Ep Technologies, Inc. | Electrophysiological interface system for use with multiple electrode catheters |
| US6120476A (en) | 1997-12-01 | 2000-09-19 | Cordis Webster, Inc. | Irrigated tip catheter |
| US5935124A (en) | 1997-12-02 | 1999-08-10 | Cordis Webster, Inc. | Tip electrode with multiple temperature sensors |
| US5938658A (en) | 1997-12-02 | 1999-08-17 | Tu; Hosheng | Device and methods for treating canker sores by RF ablation |
| US6917834B2 (en) | 1997-12-03 | 2005-07-12 | Boston Scientific Scimed, Inc. | Devices and methods for creating lesions in endocardial and surrounding tissue to isolate focal arrhythmia substrates |
| DE19757720A1 (de) | 1997-12-23 | 1999-06-24 | Sulzer Osypka Gmbh | Verfahren zum Betrieb einer Hochfrequenz-Ablationsvorrichtung und Vorrichtung für die Hochfrequenz-Gewebe-Ablation |
| US6251130B1 (en) | 1998-03-24 | 2001-06-26 | Innercool Therapies, Inc. | Device for applications of selective organ cooling |
| US20100114087A1 (en) | 1998-02-19 | 2010-05-06 | Edwards Stuart D | Methods and devices for treating urinary incontinence |
| US6358245B1 (en) | 1998-02-19 | 2002-03-19 | Curon Medical, Inc. | Graphical user interface for association with an electrode structure deployed in contact with a tissue region |
| US8906010B2 (en) | 1998-02-19 | 2014-12-09 | Mederi Therapeutics, Inc. | Graphical user interface for association with an electrode structure deployed in contact with a tissue region |
| US6097976A (en) | 1998-02-27 | 2000-08-01 | Ep Technologies, Inc. | Catheter distal end assemblies with bonded surface coatings |
| US5933672A (en) | 1998-03-02 | 1999-08-03 | Sinpo Optical Co., Ltd. | Locking mechanism for a film compartment door |
| US5948009A (en) | 1998-03-06 | 1999-09-07 | Tu; Hosheng | Apparatus and methods for medical ablation use |
| US20070244534A1 (en) | 1998-03-17 | 2007-10-18 | Kochamba Gary S | Tissue stabilization and ablation methods |
| US20070244476A1 (en) | 1998-03-17 | 2007-10-18 | Kochamba Gary S | Tissue stabilization and ablation device |
| US6014581A (en) * | 1998-03-26 | 2000-01-11 | Ep Technologies, Inc. | Interface for performing a diagnostic or therapeutic procedure on heart tissue with an electrode structure |
| US6106460A (en) | 1998-03-26 | 2000-08-22 | Scimed Life Systems, Inc. | Interface for controlling the display of images of diagnostic or therapeutic instruments in interior body regions and related data |
| US6192266B1 (en) | 1998-03-26 | 2001-02-20 | Boston Scientific Corporation | Systems and methods for controlling the use of diagnostic or therapeutic instruments in interior body regions using real and idealized images |
| US6115626A (en) | 1998-03-26 | 2000-09-05 | Scimed Life Systems, Inc. | Systems and methods using annotated images for controlling the use of diagnostic or therapeutic instruments in instruments in interior body regions |
| US6045550A (en) | 1998-05-05 | 2000-04-04 | Cardiac Peacemakers, Inc. | Electrode having non-joined thermocouple for providing multiple temperature-sensitive junctions |
| US6312425B1 (en) | 1998-05-05 | 2001-11-06 | Cardiac Pacemakers, Inc. | RF ablation catheter tip electrode with multiple thermal sensors |
| US6042580A (en) | 1998-05-05 | 2000-03-28 | Cardiac Pacemakers, Inc. | Electrode having composition-matched, common-lead thermocouple wire for providing multiple temperature-sensitive junctions |
| US6522930B1 (en) | 1998-05-06 | 2003-02-18 | Atrionix, Inc. | Irrigated ablation device assembly |
| US6216703B1 (en) | 1998-05-08 | 2001-04-17 | Thermatrx, Inc. | Therapeutic prostatic thermotherapy |
| US6508815B1 (en) | 1998-05-08 | 2003-01-21 | Novacept | Radio-frequency generator for powering an ablation device |
| US6837885B2 (en) | 1998-05-22 | 2005-01-04 | Scimed Life Systems, Inc. | Surgical probe for supporting inflatable therapeutic devices in contact with tissue in or around body orifices and within tumors |
| US6035226A (en) | 1998-05-22 | 2000-03-07 | Scimed Life Systems, Inc. | Systems and methods for assessing stability of an operative instrument inside a body region |
| US6129669A (en) | 1998-05-22 | 2000-10-10 | Scimed Life Systems, Inc. | Systems and methods for assessing stability of an ablation electrode in contact with heart tissue |
| US6283962B1 (en) | 1998-06-08 | 2001-09-04 | Quantum Therapeutics Corp. | Device for valvular annulus treatment and methods thereof |
| US5997534A (en) | 1998-06-08 | 1999-12-07 | Tu; Hosheng | Medical ablation device and methods thereof |
| US6251107B1 (en) | 1998-06-25 | 2001-06-26 | Cardima, Inc. | Ep catheter |
| US6537272B2 (en) | 1998-07-07 | 2003-03-25 | Medtronic, Inc. | Apparatus and method for creating, maintaining, and controlling a virtual electrode used for the ablation of tissue |
| US5992419A (en) | 1998-08-20 | 1999-11-30 | Mmtc, Inc. | Method employing a tissue-heating balloon catheter to produce a "biological stent" in an orifice or vessel of a patient's body |
| US6183468B1 (en) | 1998-09-10 | 2001-02-06 | Scimed Life Systems, Inc. | Systems and methods for controlling power in an electrosurgical probe |
| US6123702A (en) | 1998-09-10 | 2000-09-26 | Scimed Life Systems, Inc. | Systems and methods for controlling power in an electrosurgical probe |
| US6245065B1 (en) | 1998-09-10 | 2001-06-12 | Scimed Life Systems, Inc. | Systems and methods for controlling power in an electrosurgical probe |
| US6123703A (en) | 1998-09-19 | 2000-09-26 | Tu; Lily Chen | Ablation catheter and methods for treating tissues |
| US8308719B2 (en) | 1998-09-21 | 2012-11-13 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Apparatus and method for ablating tissue |
| US6245062B1 (en) | 1998-10-23 | 2001-06-12 | Afx, Inc. | Directional reflector shield assembly for a microwave ablation instrument |
| US7137980B2 (en) | 1998-10-23 | 2006-11-21 | Sherwood Services Ag | Method and system for controlling output of RF medical generator |
| US7844319B2 (en) | 1998-11-04 | 2010-11-30 | Susil Robert C | Systems and methods for magnetic-resonance-guided interventional procedures |
| US6210406B1 (en) | 1998-12-03 | 2001-04-03 | Cordis Webster, Inc. | Split tip electrode catheter and signal processing RF ablation system |
| US6171275B1 (en) | 1998-12-03 | 2001-01-09 | Cordis Webster, Inc. | Irrigated split tip electrode catheter |
| US6402739B1 (en) | 1998-12-08 | 2002-06-11 | Y-Beam Technologies, Inc. | Energy application with cooling |
| US6122551A (en) | 1998-12-11 | 2000-09-19 | Urologix, Inc. | Method of controlling thermal therapy |
| US20070066972A1 (en) | 2001-11-29 | 2007-03-22 | Medwaves, Inc. | Ablation catheter apparatus with one or more electrodes |
| WO2000036987A1 (en) | 1998-12-23 | 2000-06-29 | Daig Corporation | Dual sensor ablation catheter |
| US7194294B2 (en) * | 1999-01-06 | 2007-03-20 | Scimed Life Systems, Inc. | Multi-functional medical catheter and methods of use |
| US6206831B1 (en) | 1999-01-06 | 2001-03-27 | Scimed Life Systems, Inc. | Ultrasound-guided ablation catheter and methods of use |
| US6423057B1 (en) | 1999-01-25 | 2002-07-23 | The Arizona Board Of Regents On Behalf Of The University Of Arizona | Method and apparatus for monitoring and controlling tissue temperature and lesion formation in radio-frequency ablation procedures |
| US6113593A (en) | 1999-02-01 | 2000-09-05 | Tu; Lily Chen | Ablation apparatus having temperature and force sensing capabilities |
| US6309384B1 (en) | 1999-02-01 | 2001-10-30 | Adiana, Inc. | Method and apparatus for tubal occlusion |
| US6217528B1 (en) | 1999-02-11 | 2001-04-17 | Scimed Life Systems, Inc. | Loop structure having improved tissue contact capability |
| US6325797B1 (en) | 1999-04-05 | 2001-12-04 | Medtronic, Inc. | Ablation catheter and method for isolating a pulmonary vein |
| US6577902B1 (en) | 1999-04-16 | 2003-06-10 | Tony R. Brown | Device for shaping infarcted heart tissue and method of using the device |
| US6463331B1 (en) | 1999-04-19 | 2002-10-08 | Novasys Medical, Inc. | Application of energy and substances in the treatment of uro-genital disorders |
| US6692490B1 (en) | 1999-05-18 | 2004-02-17 | Novasys Medical, Inc. | Treatment of urinary incontinence and other disorders by application of energy and drugs |
| US6277113B1 (en) | 1999-05-28 | 2001-08-21 | Afx, Inc. | Monopole tip for ablation catheter and methods for using same |
| US6391024B1 (en) | 1999-06-17 | 2002-05-21 | Cardiac Pacemakers, Inc. | RF ablation apparatus and method having electrode/tissue contact assessment scheme and electrocardiogram filtering |
| US7935108B2 (en) | 1999-07-14 | 2011-05-03 | Cardiofocus, Inc. | Deflectable sheath catheters |
| WO2001005306A1 (en) | 1999-07-19 | 2001-01-25 | Epicor, Inc. | Apparatus and method for ablating tissue |
| US6852120B1 (en) | 1999-08-10 | 2005-02-08 | Biosense Webster, Inc | Irrigation probe for ablation during open heart surgery |
| US6371955B1 (en) | 1999-08-10 | 2002-04-16 | Biosense Webster, Inc. | Atrial branding iron catheter and a method for treating atrial fibrillation |
| US6471693B1 (en) * | 1999-09-10 | 2002-10-29 | Cryocath Technologies Inc. | Catheter and system for monitoring tissue contact |
| FR2798296B1 (fr) | 1999-09-13 | 2002-05-31 | Centre Nat Rech Scient | Ensemble de traitement thermique de tissus biologiques et procede de mise en oeuvre de cet ensemble |
| US6264653B1 (en) | 1999-09-24 | 2001-07-24 | C. R. Band, Inc. | System and method for gauging the amount of electrode-tissue contact using pulsed radio frequency energy |
| EP1244392A1 (en) | 1999-09-28 | 2002-10-02 | Novasys Medical, Inc. | Treatment of tissue by application of energy and drugs |
| US6230060B1 (en) | 1999-10-22 | 2001-05-08 | Daniel D. Mawhinney | Single integrated structural unit for catheter incorporating a microwave antenna |
| US20060095032A1 (en) | 1999-11-16 | 2006-05-04 | Jerome Jackson | Methods and systems for determining physiologic characteristics for treatment of the esophagus |
| US6711444B2 (en) | 1999-11-22 | 2004-03-23 | Scimed Life Systems, Inc. | Methods of deploying helical diagnostic and therapeutic element supporting structures within the body |
| US6745080B2 (en) | 1999-11-22 | 2004-06-01 | Scimed Life Systems, Inc. | Helical and pre-oriented loop structures for supporting diagnostic and therapeutic elements in contact with body tissue |
| US6613046B1 (en) | 1999-11-22 | 2003-09-02 | Scimed Life Systems, Inc. | Loop structures for supporting diagnostic and therapeutic elements in contact with body tissue |
| US6529756B1 (en) | 1999-11-22 | 2003-03-04 | Scimed Life Systems, Inc. | Apparatus for mapping and coagulating soft tissue in or around body orifices |
| US6542781B1 (en) | 1999-11-22 | 2003-04-01 | Scimed Life Systems, Inc. | Loop structures for supporting diagnostic and therapeutic elements in contact with body tissue |
| US8083736B2 (en) | 2000-03-06 | 2011-12-27 | Salient Surgical Technologies, Inc. | Fluid-assisted medical devices, systems and methods |
| US8048070B2 (en) | 2000-03-06 | 2011-11-01 | Salient Surgical Technologies, Inc. | Fluid-assisted medical devices, systems and methods |
| US6770070B1 (en) | 2000-03-17 | 2004-08-03 | Rita Medical Systems, Inc. | Lung treatment apparatus and method |
| US6458123B1 (en) | 2000-04-27 | 2002-10-01 | Biosense Webster, Inc. | Ablation catheter with positional sensor |
| AU2001249874A1 (en) | 2000-04-27 | 2001-11-12 | Medtronic, Inc. | System and method for assessing transmurality of ablation lesions |
| US6558382B2 (en) | 2000-04-27 | 2003-05-06 | Medtronic, Inc. | Suction stabilized epicardial ablation devices |
| US6514250B1 (en) | 2000-04-27 | 2003-02-04 | Medtronic, Inc. | Suction stabilized epicardial ablation devices |
| EP2095784B1 (en) | 2000-05-03 | 2016-01-06 | Boston Scientific Scimed, Inc. | Apparatus for mapping and ablation in electrophysiology procedures |
| JP2003533267A (ja) | 2000-05-12 | 2003-11-11 | カーディマ・インコーポレイテッド | 凝塊を低減できるマルチチャネルrfエネルギーの伝達システム |
| US7252664B2 (en) | 2000-05-12 | 2007-08-07 | Cardima, Inc. | System and method for multi-channel RF energy delivery with coagulum reduction |
| US8486065B2 (en) | 2000-06-07 | 2013-07-16 | Wisconsin Alumni Research Foundation | Radio-frequency ablation system and method using multiple electrodes |
| CA2411938C (en) | 2000-06-13 | 2009-08-04 | Atrionix, Inc. | Surgical ablation probe for forming a circumferential lesion |
| US6477426B1 (en) | 2000-06-20 | 2002-11-05 | Celsion Corporation | System and method for heating the prostate gland to treat and prevent the growth and spread of prostate tumors |
| CN1437494A (zh) | 2000-06-20 | 2003-08-20 | 效思因公司 | 加热前列腺以治疗和防止前列腺肿瘤的生长和扩散的系统和方法 |
| US6958075B2 (en) | 2001-09-18 | 2005-10-25 | Celsion Corporation | Device and method for treatment of tissue adjacent a bodily conduit by thermocompression |
| US7837720B2 (en) | 2000-06-20 | 2010-11-23 | Boston Scientific Corporation | Apparatus for treatment of tissue adjacent a bodily conduit with a gene or drug-coated compression balloon |
| US6511478B1 (en) | 2000-06-30 | 2003-01-28 | Scimed Life Systems, Inc. | Medical probe with reduced number of temperature sensor wires |
| US6544257B2 (en) | 2000-07-03 | 2003-04-08 | Olympus Optical Co., Ltd. | Thermal treatment apparatus |
| US6477396B1 (en) | 2000-07-07 | 2002-11-05 | Biosense Webster, Inc. | Mapping and ablation catheter |
| US6405067B1 (en) | 2000-07-07 | 2002-06-11 | Biosense Webster, Inc. | Catheter with tip electrode having a recessed ring electrode mounted thereon |
| US6699241B2 (en) | 2000-08-11 | 2004-03-02 | Northeastern University | Wide-aperture catheter-based microwave cardiac ablation antenna |
| US6669692B1 (en) | 2000-08-21 | 2003-12-30 | Biosense Webster, Inc. | Ablation catheter with cooled linear electrode |
| US6942661B2 (en) | 2000-08-30 | 2005-09-13 | Boston Scientific Scimed, Inc. | Fluid cooled apparatus for supporting diagnostic and therapeutic elements in contact with tissue |
| US20030120171A1 (en) | 2000-09-08 | 2003-06-26 | Leonidas Diamantopoulos | Vasular temperature measuring device and process for measuring vascular temperature |
| US6635067B2 (en) | 2000-09-24 | 2003-10-21 | Medtronic, Inc. | Liquid cooled, powered surgical handpiece |
| US6470219B1 (en) | 2000-10-02 | 2002-10-22 | Novasys Medical, Inc. | Apparatus and method for treating female urinary incontinence |
| US6752804B2 (en) * | 2000-12-28 | 2004-06-22 | Cardiac Pacemakers, Inc. | Ablation system and method having multiple-sensor electrodes to assist in assessment of electrode and sensor position and adjustment of energy levels |
| US20020087151A1 (en) | 2000-12-29 | 2002-07-04 | Afx, Inc. | Tissue ablation apparatus with a sliding ablation instrument and method |
| US6740040B1 (en) | 2001-01-30 | 2004-05-25 | Advanced Cardiovascular Systems, Inc. | Ultrasound energy driven intraventricular catheter to treat ischemia |
| US6743225B2 (en) | 2001-03-27 | 2004-06-01 | Uab Research Foundation | Electrophysiologic measure of endpoints for ablation lesions created in fibrillating substrates |
| US20020165529A1 (en) | 2001-04-05 | 2002-11-07 | Danek Christopher James | Method and apparatus for non-invasive energy delivery |
| US7751903B2 (en) | 2002-04-15 | 2010-07-06 | Greatbatch Ltd. | Frequency selective passive component networks for implantable leads of active implantable medical devices utilizing an energy dissipating surface |
| US8977355B2 (en) | 2001-04-13 | 2015-03-10 | Greatbatch Ltd. | EMI filter employing a capacitor and an inductor tank circuit having optimum component values |
| US6648883B2 (en) | 2001-04-26 | 2003-11-18 | Medtronic, Inc. | Ablation system and method of use |
| US6663627B2 (en) | 2001-04-26 | 2003-12-16 | Medtronic, Inc. | Ablation system and method of use |
| US7959626B2 (en) | 2001-04-26 | 2011-06-14 | Medtronic, Inc. | Transmural ablation systems and methods |
| US7175734B2 (en) | 2001-05-03 | 2007-02-13 | Medtronic, Inc. | Porous medical catheter and methods of manufacture |
| US20020169444A1 (en) | 2001-05-08 | 2002-11-14 | Mest Robert A. | Catheter having continuous braided electrode |
| JP4252316B2 (ja) | 2001-05-10 | 2009-04-08 | リタ メディカル システムズ インコーポレイテッド | Rf組織切除装置および方法 |
| US20030130713A1 (en) | 2001-05-21 | 2003-07-10 | Stewart Mark T. | Trans-septal catheter with retention mechanism |
| US20020198520A1 (en) | 2001-06-20 | 2002-12-26 | Scimed Life Systems, Inc. | Irrigation sheath |
| US6611699B2 (en) | 2001-06-28 | 2003-08-26 | Scimed Life Systems, Inc. | Catheter with an irrigated composite tip electrode |
| US6685702B2 (en) | 2001-07-06 | 2004-02-03 | Rodolfo C. Quijano | Device for treating tissue and methods thereof |
| US6740083B2 (en) | 2001-07-09 | 2004-05-25 | Scimed Life Systems, Inc. | Distal catheter assembly with proximal mounting member |
| JP2003052736A (ja) | 2001-08-09 | 2003-02-25 | Olympus Optical Co Ltd | 加温治療装置 |
| US7615049B2 (en) | 2001-09-19 | 2009-11-10 | Mederi Therapeutics, Inc. | Devices, systems and methods for treating tissue regions of the body |
| EP1429678B1 (en) | 2001-09-28 | 2006-03-22 | Rita Medical Systems, Inc. | Impedance controlled tissue ablation apparatus |
| JP2003111848A (ja) | 2001-10-05 | 2003-04-15 | Nihon Medix | 加熱式バルーンカテーテル装置およびその加熱方法 |
| US6814730B2 (en) | 2001-10-09 | 2004-11-09 | Hong Li | Balloon catheters for non-continuous lesions |
| US6635056B2 (en) | 2001-10-09 | 2003-10-21 | Cardiac Pacemakers, Inc. | RF ablation apparatus and method using amplitude control |
| US7285116B2 (en) | 2004-05-15 | 2007-10-23 | Irvine Biomedical Inc. | Non-contact tissue ablation device and methods thereof |
| US20030078573A1 (en) | 2001-10-18 | 2003-04-24 | Csaba Truckai | Electrosurgical working end for controlled energy delivery |
| US6735465B2 (en) | 2001-10-24 | 2004-05-11 | Scimed Life Systems, Inc. | Systems and processes for refining a registered map of a body cavity |
| US6895267B2 (en) | 2001-10-24 | 2005-05-17 | Scimed Life Systems, Inc. | Systems and methods for guiding and locating functional elements on medical devices positioned in a body |
| US8175680B2 (en) | 2001-11-09 | 2012-05-08 | Boston Scientific Scimed, Inc. | Systems and methods for guiding catheters using registered images |
| US20030093067A1 (en) | 2001-11-09 | 2003-05-15 | Scimed Life Systems, Inc. | Systems and methods for guiding catheters using registered images |
| US20040092806A1 (en) | 2001-12-11 | 2004-05-13 | Sagon Stephen W | Microelectrode catheter for mapping and ablation |
| US6827715B2 (en) | 2002-01-25 | 2004-12-07 | Medtronic, Inc. | System and method of performing an electrosurgical procedure |
| US6790206B2 (en) | 2002-01-31 | 2004-09-14 | Scimed Life Systems, Inc. | Compensation for power variation along patient cables |
| EP1489983A4 (en) | 2002-02-15 | 2010-11-10 | Boston Scient Corp | METHOD AND DEVICE FOR TREATING TISSUE IN ADDITION TO A BODY THROUGH THERMOCOMPRESSION AND MEDICAMENTS |
| US8882755B2 (en) | 2002-03-05 | 2014-11-11 | Kimberly-Clark Inc. | Electrosurgical device for treatment of tissue |
| US7166075B2 (en) | 2002-03-08 | 2007-01-23 | Wisconsin Alumni Research Foundation | Elastographic imaging of in vivo soft tissue |
| US8150519B2 (en) | 2002-04-08 | 2012-04-03 | Ardian, Inc. | Methods and apparatus for bilateral renal neuromodulation |
| US8347891B2 (en) | 2002-04-08 | 2013-01-08 | Medtronic Ardian Luxembourg S.A.R.L. | Methods and apparatus for performing a non-continuous circumferential treatment of a body lumen |
| US8145316B2 (en) | 2002-04-08 | 2012-03-27 | Ardian, Inc. | Methods and apparatus for renal neuromodulation |
| US7617005B2 (en) | 2002-04-08 | 2009-11-10 | Ardian, Inc. | Methods and apparatus for thermally-induced renal neuromodulation |
| US6974455B2 (en) | 2002-04-10 | 2005-12-13 | Boston Scientific Scimed, Inc. | Auto advancing radio frequency array |
| US7008417B2 (en) | 2002-04-22 | 2006-03-07 | Medtronics, Inc. | Detecting coagulum formation |
| US6932813B2 (en) | 2002-05-03 | 2005-08-23 | Scimed Life Systems, Inc. | Ablation systems including insulated energy transmitting elements |
| US6746401B2 (en) | 2002-05-06 | 2004-06-08 | Scimed Life Systems, Inc. | Tissue ablation visualization |
| AUPS226502A0 (en) | 2002-05-13 | 2002-06-13 | Advanced Metal Coatings Pty Limited | A multi-electrode lead |
| US10130415B2 (en) | 2002-06-10 | 2018-11-20 | Wisconsin Alumni Research Foundation | Circumferential electrode array for tissue ablation |
| US7588568B2 (en) | 2002-07-19 | 2009-09-15 | Biosense Webster, Inc. | Atrial ablation catheter and method for treating atrial fibrillation |
| US20060167445A1 (en) | 2002-08-27 | 2006-07-27 | Gal Shafirstein | Selective conductive interstitial thermal therapy device |
| US7306593B2 (en) | 2002-10-21 | 2007-12-11 | Biosense, Inc. | Prediction and assessment of ablation of cardiac tissue |
| US7001383B2 (en) | 2002-10-21 | 2006-02-21 | Biosense, Inc. | Real-time monitoring and mapping of ablation lesion formation in the heart |
| US20040097803A1 (en) | 2002-11-20 | 2004-05-20 | Dorin Panescu | 3-D catheter localization using permanent magnets with asymmetrical properties about their longitudinal axis |
| US6888141B2 (en) | 2002-12-02 | 2005-05-03 | Multispectral Imaging, Inc. | Radiation sensor with photo-thermal gain |
| US6847848B2 (en) | 2003-01-07 | 2005-01-25 | Mmtc, Inc | Inflatable balloon catheter structural designs and methods for treating diseased tissue of a patient |
| US6984232B2 (en) | 2003-01-17 | 2006-01-10 | St. Jude Medical, Daig Division, Inc. | Ablation catheter assembly having a virtual electrode comprising portholes |
| US7819866B2 (en) | 2003-01-21 | 2010-10-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter and electrode |
| US6960207B2 (en) | 2003-01-21 | 2005-11-01 | St Jude Medical, Daig Division, Inc. | Ablation catheter having a virtual electrode comprising portholes and a porous conductor |
| CN1764419A (zh) | 2003-02-20 | 2006-04-26 | 普罗里森姆股份有限公司 | 心脏消融装置 |
| US8256428B2 (en) | 2003-03-12 | 2012-09-04 | Biosense Webster, Inc. | Method for treating tissue |
| AU2003901390A0 (en) | 2003-03-26 | 2003-04-10 | University Of Technology, Sydney | Microwave antenna for cardiac ablation |
| US7938828B2 (en) | 2003-03-28 | 2011-05-10 | Boston Scientific Scimed, Inc. | Cooled ablation catheter |
| US7101387B2 (en) | 2003-04-30 | 2006-09-05 | Scimed Life Systems, Inc. | Radio frequency ablation cooling shield |
| CA2524289C (en) | 2003-05-01 | 2016-01-19 | Sherwood Services Ag | Method and system for programming and controlling an electrosurgical generator system |
| US6932776B2 (en) | 2003-06-02 | 2005-08-23 | Meridian Medicalssystems, Llc | Method and apparatus for detecting and treating vulnerable plaques |
| US7163537B2 (en) | 2003-06-02 | 2007-01-16 | Biosense Webster, Inc. | Enhanced ablation and mapping catheter and method for treating atrial fibrillation |
| US7263398B2 (en) | 2003-06-25 | 2007-08-28 | Meridian Medical Systems, Llc | Apparatus for measuring intravascular blood flow |
| US7678104B2 (en) | 2003-07-17 | 2010-03-16 | Biosense Webster, Inc. | Ultrasound ablation catheter and method for its use |
| US10182734B2 (en) | 2003-07-18 | 2019-01-22 | Biosense Webster, Inc. | Enhanced ablation and mapping catheter and method for treating atrial fibrillation |
| US7588658B2 (en) | 2003-08-27 | 2009-09-15 | Orient Chemical Industries, Ltd. | Laser-transmissible resin composition and method for laser welding using it |
| US20050059963A1 (en) | 2003-09-12 | 2005-03-17 | Scimed Life Systems, Inc. | Systems and method for creating transmural lesions |
| US7229437B2 (en) | 2003-09-22 | 2007-06-12 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Medical device having integral traces and formed electrodes |
| US7234225B2 (en) | 2003-09-22 | 2007-06-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Method for manufacturing medical device having embedded traces and formed electrodes |
| US7435248B2 (en) | 2003-09-26 | 2008-10-14 | Boston Scientific Scimed, Inc. | Medical probes for creating and diagnosing circumferential lesions within or around the ostium of a vessel |
| WO2005050151A1 (en) | 2003-10-23 | 2005-06-02 | Sherwood Services Ag | Thermocouple measurement circuit |
| US7207989B2 (en) | 2003-10-27 | 2007-04-24 | Biosense Webster, Inc. | Method for ablating with needle electrode |
| NL1024658C2 (nl) | 2003-10-29 | 2005-05-02 | Univ Medisch Centrum Utrecht | Katheter en werkwijze, in het bijzonder voor ablatie en dergelijke techniek. |
| US7131860B2 (en) | 2003-11-20 | 2006-11-07 | Sherwood Services Ag | Connector systems for electrosurgical generator |
| US8002770B2 (en) | 2003-12-02 | 2011-08-23 | Endoscopic Technologies, Inc. (Estech) | Clamp based methods and apparatus for forming lesions in tissue and confirming whether a therapeutic lesion has been formed |
| JPWO2005065559A1 (ja) | 2004-01-06 | 2007-12-20 | 東レ株式会社 | バルーンカテーテル |
| US7371233B2 (en) | 2004-02-19 | 2008-05-13 | Boston Scientific Scimed, Inc. | Cooled probes and apparatus for maintaining contact between cooled probes and tissue |
| US20050197657A1 (en) | 2004-03-02 | 2005-09-08 | Goth Paul R. | Thermokeratoplasty system with a regulated power generator |
| WO2005089663A1 (en) | 2004-03-05 | 2005-09-29 | Medelec-Minimeca S.A. | Saline-enhanced catheter for radiofrequency tumor ablation |
| US7238184B2 (en) | 2004-03-15 | 2007-07-03 | Boston Scientific Scimed, Inc. | Ablation probe with peltier effect thermal control |
| US7565208B2 (en) | 2004-03-25 | 2009-07-21 | Boston Scientific Scimed, Inc. | Catheter with sensor tips, tool and device and methods of use of same |
| US7699829B2 (en) | 2004-03-25 | 2010-04-20 | Boston Scientific Scimed, Inc. | Catheter with sensor tip and method of use of same |
| US7582050B2 (en) | 2004-03-31 | 2009-09-01 | The Regents Of The University Of California | Apparatus for hyperthermia and brachytherapy delivery |
| US8262653B2 (en) | 2004-04-02 | 2012-09-11 | Biosense Webster, Inc. | Irrigated catheter having a porous tip electrode |
| US20050228370A1 (en) | 2004-04-12 | 2005-10-13 | Fred Sterzer | Balloon catheter designs which incorporate an antenna cooperatively situated with respect to an external balloon surface for use in treating diseased tissue of a patient |
| EP1737371B1 (en) | 2004-04-19 | 2011-06-08 | ProRhythm, Inc. | Ablation devices with sensor structures |
| US7715926B2 (en) | 2004-04-23 | 2010-05-11 | Medtronic, Inc. | Medical device conductor junctions |
| US20050245949A1 (en) | 2004-04-28 | 2005-11-03 | Goth Paul R | Thermokeratoplasty system with a guided probe tip |
| EP2368512A1 (en) | 2004-05-17 | 2011-09-28 | C.R. Bard, Inc. | Irrigated catheter |
| US7632265B2 (en) | 2004-05-28 | 2009-12-15 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Radio frequency ablation servo catheter and method |
| US20060064083A1 (en) | 2004-09-17 | 2006-03-23 | Steve Khalaj | Multi-tip probe used for an ocular procedure |
| US20070016272A1 (en) | 2004-09-27 | 2007-01-18 | Thompson Russell B | Systems and methods for treating a hollow anatomical structure |
| US20060089688A1 (en) | 2004-10-25 | 2006-04-27 | Dorin Panescu | Method and apparatus to reduce wrinkles through application of radio frequency energy to nerves |
| US8409191B2 (en) | 2004-11-04 | 2013-04-02 | Boston Scientific Scimed, Inc. | Preshaped ablation catheter for ablating pulmonary vein ostia within the heart |
| WO2006055658A1 (en) | 2004-11-15 | 2006-05-26 | Biosense Webster Inc. | Catheter with multiple microfabricated temperature sensors |
| EP1827278B1 (en) | 2004-11-15 | 2012-06-06 | Biosense Webster, Inc. | Catheter with microfabricated temperature sensing |
| US20060135957A1 (en) | 2004-12-21 | 2006-06-22 | Dorin Panescu | Method and apparatus to align a probe with a cornea |
| EP1681015A1 (en) | 2005-01-17 | 2006-07-19 | Imasys SA | Temperature mapping on structural data |
| US20060167529A1 (en) | 2005-01-26 | 2006-07-27 | Schecter Stuart O | Method and algorithm for defining the pathologic state from a plurality of intrinsically and extrinsically derived signals |
| US20090030332A1 (en) | 2005-01-26 | 2009-01-29 | Schecter Stuart O | microfabricated cardiac sensor with tactile feedback and method and apparatus for calibrating the same using a plurality of signals |
| US20100312129A1 (en) | 2005-01-26 | 2010-12-09 | Schecter Stuart O | Cardiovascular haptic handle system |
| US7918851B2 (en) | 2005-02-14 | 2011-04-05 | Biosense Webster, Inc. | Irrigated tip catheter and method for manufacturing therefor |
| US20060184166A1 (en) | 2005-02-16 | 2006-08-17 | Moises Valle | Method and apparatus to automatically insert a probe into a cornea |
| US7862563B1 (en) | 2005-02-18 | 2011-01-04 | Cosman Eric R | Integral high frequency electrode |
| US8075498B2 (en) | 2005-03-04 | 2011-12-13 | Endosense Sa | Medical apparatus system having optical fiber load sensing capability |
| US7771418B2 (en) | 2005-03-09 | 2010-08-10 | Sunnybrook Health Sciences Centre | Treatment of diseased tissue using controlled ultrasonic heating |
| US7670336B2 (en) | 2005-03-25 | 2010-03-02 | Boston Scientific Scimed, Inc. | Ablation probe with heat sink |
| US20060247615A1 (en) | 2005-04-28 | 2006-11-02 | Boston Scientific Scimed, Inc. | Multi-element bi-polar ablation electrode |
| WO2006121883A1 (en) | 2005-05-05 | 2006-11-16 | Boston Scientific Scimed, Inc. | Steerable catheter for performing medical procedure adjacent pulmonary vein ostia |
| US8128621B2 (en) | 2005-05-16 | 2012-03-06 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated ablation electrode assembly and method for control of temperature |
| US7857810B2 (en) | 2006-05-16 | 2010-12-28 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation electrode assembly and methods for improved control of temperature and minimization of coagulation and tissue damage |
| US7776034B2 (en) | 2005-06-15 | 2010-08-17 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter with adjustable virtual electrode |
| US20060293731A1 (en) | 2005-06-24 | 2006-12-28 | Boris Rubinsky | Methods and systems for treating tumors using electroporation |
| WO2007008954A2 (en) | 2005-07-11 | 2007-01-18 | Ablation Frontiers | Low power tissue ablation system |
| US20070055326A1 (en) | 2005-07-21 | 2007-03-08 | Farley Brian E | Method of treating a hollow anatomical structure with a thermal catheter |
| ITBO20050495A1 (it) | 2005-07-22 | 2007-01-23 | Fiab Spa | Elettrocatetere esogageo |
| EP2319444B1 (en) | 2005-08-02 | 2013-11-06 | Neurotherm, Inc. | Apparatus for diagnosing and treating neural dysfunction |
| US7819862B2 (en) | 2005-08-11 | 2010-10-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Method for arrhythmias treatment based on spectral mapping during sinus rhythm |
| JP2009504284A (ja) | 2005-08-19 | 2009-02-05 | ネーヴ,ヴェルナー,フランソワ デ | 心臓の熱切除治療を援助するための装置ならびに方法 |
| US8657814B2 (en) | 2005-08-22 | 2014-02-25 | Medtronic Ablation Frontiers Llc | User interface for tissue ablation system |
| US20070049915A1 (en) | 2005-08-26 | 2007-03-01 | Dieter Haemmerich | Method and Devices for Cardiac Radiofrequency Catheter Ablation |
| US20070055328A1 (en) | 2005-09-02 | 2007-03-08 | Mayse Martin L | Device and method for esophageal cooling |
| US20070055227A1 (en) | 2005-09-08 | 2007-03-08 | Refractec, Inc. | Probe used for an ocular procedure |
| US7623899B2 (en) | 2005-09-16 | 2009-11-24 | Biosense Webster, Inc. | Catheter with flexible pre-shaped tip section |
| US7819817B2 (en) | 2005-09-21 | 2010-10-26 | Siemens Aktiengesellschaft | Temperature probe for insertion into the esophagus |
| US20070073286A1 (en) | 2005-09-29 | 2007-03-29 | Dorin Panescu | Method and apparatus for an ocular procedure |
| US8672936B2 (en) | 2005-10-13 | 2014-03-18 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Systems and methods for assessing tissue contact |
| US8679109B2 (en) | 2005-10-13 | 2014-03-25 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Dynamic contact assessment for electrode catheters |
| WO2007067940A2 (en) | 2005-12-06 | 2007-06-14 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Assessment of electrode coupling for tissue ablation |
| US9254163B2 (en) | 2005-12-06 | 2016-02-09 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Assessment of electrode coupling for tissue ablation |
| US8406866B2 (en) | 2005-12-06 | 2013-03-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing coupling between an electrode and tissue |
| US8403925B2 (en) | 2006-12-06 | 2013-03-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing lesions in tissue |
| US8998890B2 (en) | 2005-12-06 | 2015-04-07 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Assessment of electrode coupling for tissue ablation |
| US10362959B2 (en) | 2005-12-06 | 2019-07-30 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing the proximity of an electrode to tissue in a body |
| US8449535B2 (en) | 2005-12-06 | 2013-05-28 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing coupling between an electrode and tissue |
| AU2006321918B2 (en) | 2005-12-06 | 2011-08-25 | St. Jude Medical, Atrial Fibrillation Division Inc. | Assessment of electrode coupling for tissue ablation |
| US20090177111A1 (en) | 2006-12-06 | 2009-07-09 | Miller Stephan P | System and method for displaying contact between a catheter and tissue |
| US8603084B2 (en) | 2005-12-06 | 2013-12-10 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing the formation of a lesion in tissue |
| US9492226B2 (en) | 2005-12-06 | 2016-11-15 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Graphical user interface for real-time RF lesion depth display |
| US20070156114A1 (en) | 2005-12-29 | 2007-07-05 | Worley Seth J | Deflectable catheter with a flexibly attached tip section |
| US7879029B2 (en) | 2005-12-30 | 2011-02-01 | Biosense Webster, Inc. | System and method for selectively energizing catheter electrodes |
| US7857809B2 (en) | 2005-12-30 | 2010-12-28 | Biosense Webster, Inc. | Injection molded irrigated tip electrode and catheter having the same |
| US7628788B2 (en) | 2005-12-30 | 2009-12-08 | Biosense Webster, Inc. | Ablation catheter with improved tip cooling |
| DE102006001849A1 (de) | 2006-01-13 | 2007-07-19 | Siemens Ag | Mapping-Katheter sowie Mapping-Katheter-Vorrichtung und zugehöriges Verfahren |
| CA2574934C (en) | 2006-01-24 | 2015-12-29 | Sherwood Services Ag | System and method for closed loop monitoring of monopolar electrosurgical apparatus |
| US7826904B2 (en) | 2006-02-07 | 2010-11-02 | Angiodynamics, Inc. | Interstitial microwave system and method for thermal treatment of diseases |
| US20070185478A1 (en) | 2006-02-08 | 2007-08-09 | Plasiatherm, Inc. | Device for local ablation of tissue |
| US7918850B2 (en) | 2006-02-17 | 2011-04-05 | Biosense Wabster, Inc. | Lesion assessment by pacing |
| US7699841B2 (en) | 2006-03-16 | 2010-04-20 | Meridian Medical Systems, Llc | Microwave apparatus for controlled tissue ablation |
| US20070225697A1 (en) | 2006-03-23 | 2007-09-27 | Ketan Shroff | Apparatus and methods for cardiac ablation |
| US8600497B1 (en) | 2006-03-31 | 2013-12-03 | Pacesetter, Inc. | Systems and methods to monitor and treat heart failure conditions |
| US8712519B1 (en) | 2006-03-31 | 2014-04-29 | Pacesetter, Inc. | Closed-loop adaptive adjustment of pacing therapy based on cardiogenic impedance signals detected by an implantable medical device |
| US7794404B1 (en) | 2006-03-31 | 2010-09-14 | Pacesetter, Inc | System and method for estimating cardiac pressure using parameters derived from impedance signals detected by an implantable medical device |
| US8628520B2 (en) | 2006-05-02 | 2014-01-14 | Biosense Webster, Inc. | Catheter with omni-directional optical lesion evaluation |
| US7846158B2 (en) | 2006-05-05 | 2010-12-07 | Covidien Ag | Apparatus and method for electrode thermosurgery |
| US8103356B2 (en) | 2006-05-23 | 2012-01-24 | Vertech, Inc. | High frequency epidural neuromodulation catheter without needle for effectuating RF treatment |
| US20140025056A1 (en) | 2006-05-24 | 2014-01-23 | Kambiz Dowlatshahi | Image-guided removal and thermal therapy of breast cancer |
| US8011055B2 (en) | 2006-06-01 | 2011-09-06 | Carl Freudenberg Kg | Cleaning implement |
| US7662152B2 (en) | 2006-06-13 | 2010-02-16 | Biosense Webster, Inc. | Catheter with multi port tip for optical lesion evaluation |
| US7769469B2 (en) | 2006-06-26 | 2010-08-03 | Meridian Medical Systems, Llc | Integrated heating/sensing catheter apparatus for minimally invasive applications |
| US8515554B2 (en) | 2006-06-26 | 2013-08-20 | Meridian Medical Systems, Llc | Radiometric heating/sensing probe |
| ATE494040T1 (de) | 2006-06-28 | 2011-01-15 | Ardian Inc | Systeme für wärmeinduzierte renale neuromodulation |
| US20080033300A1 (en) | 2006-08-04 | 2008-02-07 | Anh Hoang | Systems and methods for monitoring temperature during electrosurgery or laser therapy |
| JP5437068B2 (ja) | 2006-08-11 | 2014-03-12 | コーニンクレッカ フィリップス エヌ ヴェ | 無線周波数組織切除の最適な超音波撮像に対する画像ベースのパワーフィードバック |
| WO2008024714A1 (en) | 2006-08-21 | 2008-02-28 | Mayo Foundation For Medical Education And Research | Coagulum formation controlling apparatus |
| US7774039B2 (en) | 2006-09-05 | 2010-08-10 | Boston Scientific Scimed, Inc. | Multi-bend steerable mapping catheter |
| US20080082091A1 (en) | 2006-09-10 | 2008-04-03 | Vladimir Rubtsov | Fiber optic tissue ablation |
| US20080077126A1 (en) | 2006-09-22 | 2008-03-27 | Rassoll Rashidi | Ablation for atrial fibrillation |
| WO2008045877A2 (en) | 2006-10-10 | 2008-04-17 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Electrode tip and ablation system |
| EP2066251B1 (en) | 2006-10-10 | 2017-05-03 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation electrode assembly with insulated distal outlet |
| US7946995B1 (en) | 2006-11-09 | 2011-05-24 | Pacesetter, Inc. | Analyzing circadian variations of a hemodynamic parameter to determine an adverse cardiac condition |
| US8202224B2 (en) | 2006-11-13 | 2012-06-19 | Pacesetter, Inc. | System and method for calibrating cardiac pressure measurements derived from signals detected by an implantable medical device |
| AU2007231704B2 (en) | 2006-11-29 | 2011-02-24 | Cathrx Ltd | Heat treating a biological site in a patient's body |
| EP2101668B1 (en) | 2006-12-06 | 2012-09-05 | Boston Scientific Limited | Tissue ablation using pulse modulated radio frequency energy |
| US8690870B2 (en) | 2006-12-28 | 2014-04-08 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated ablation catheter system with pulsatile flow to prevent thrombus |
| US7766907B2 (en) | 2006-12-28 | 2010-08-03 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter with sensor array and discrimination circuit to minimize variation in power density |
| US8444637B2 (en) | 2006-12-29 | 2013-05-21 | St. Jude Medical, Atrial Filbrillation Division, Inc. | Steerable ablation device |
| US8460285B2 (en) * | 2006-12-29 | 2013-06-11 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter electrode having multiple thermal sensors and method of use |
| US8265745B2 (en) | 2006-12-29 | 2012-09-11 | St. Jude Medical, Atrial Fibillation Division, Inc. | Contact sensor and sheath exit sensor |
| US8449537B2 (en) | 2006-12-29 | 2013-05-28 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter with thermally mediated catheter body for mitigating blood coagulation and creating larger lesion |
| US7914528B2 (en) | 2006-12-29 | 2011-03-29 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter tip for generating an angled flow |
| GB2452103B (en) | 2007-01-05 | 2011-08-31 | Arthrocare Corp | Electrosurgical system with suction control apparatus and system |
| US9924998B2 (en) | 2007-01-12 | 2018-03-27 | Atricure, Inc. | Ablation system, clamp and method of use |
| US8211099B2 (en) | 2007-01-31 | 2012-07-03 | Tyco Healthcare Group Lp | Thermal feedback systems and methods of using the same |
| US7867227B2 (en) | 2007-02-22 | 2011-01-11 | A David Slater | Bipolar cardiac ablation system and method |
| US7679336B2 (en) | 2007-02-27 | 2010-03-16 | Ford Global Technologies, Llc | Interactive battery charger for electric vehicle |
| US20090187183A1 (en) | 2007-03-13 | 2009-07-23 | Gordon Epstein | Temperature responsive ablation rf driving for moderating return electrode temperature |
| KR101490374B1 (ko) | 2007-03-26 | 2015-02-05 | 보스톤 싸이엔티픽 리미티드 | 고해상도 전기 생리학 카테터 |
| US8208999B2 (en) | 2007-04-04 | 2012-06-26 | Pacesetter, Inc. | System and method for estimating electrical conduction delays from immittance values measured using an implantable medical device |
| US8764742B2 (en) | 2007-04-04 | 2014-07-01 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated catheter |
| US8517999B2 (en) | 2007-04-04 | 2013-08-27 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated catheter with improved fluid flow |
| US9089339B2 (en) | 2007-04-04 | 2015-07-28 | Biosense Webster, Inc. | Electrophysiology catheter with improved tip electrode |
| US8504153B2 (en) | 2007-04-04 | 2013-08-06 | Pacesetter, Inc. | System and method for estimating cardiac pressure based on cardiac electrical conduction delays using an implantable medical device |
| US7676264B1 (en) | 2007-04-13 | 2010-03-09 | Pacesetter, Inc. | Systems and methods for use by an implantable medical device for evaluating ventricular dyssynchrony based on T-wave morphology |
| US20080275440A1 (en) | 2007-05-03 | 2008-11-06 | Medtronic, Inc. | Post-ablation verification of lesion size |
| US7957813B1 (en) | 2007-05-08 | 2011-06-07 | Pacesetter, Inc. | Adaptive staged wake-up for implantable medical device communication |
| US7989741B2 (en) | 2007-05-08 | 2011-08-02 | Meridian Medical Systems, Llc | In-line microwave warming apparatus |
| US11395694B2 (en) | 2009-05-07 | 2022-07-26 | St. Jude Medical, Llc | Irrigated ablation catheter with multiple segmented ablation electrodes |
| US8974454B2 (en) | 2009-12-31 | 2015-03-10 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Kit for non-invasive electrophysiology procedures and method of its use |
| ITBA20070049A1 (it) | 2007-06-14 | 2008-12-15 | Massimo Grimaldi | Cateteri per ablazione transcatetere per via percutanea di aritmie cardiache mediante radiofrequenza bipolare |
| US20080312521A1 (en) | 2007-06-14 | 2008-12-18 | Solomon Edward G | System and method for determining electrode-tissue contact using phase difference |
| US7976537B2 (en) | 2007-06-28 | 2011-07-12 | Biosense Webster, Inc. | Optical pyrometric catheter for tissue temperature monitoring during cardiac ablation |
| US8123745B2 (en) | 2007-06-29 | 2012-02-28 | Biosense Webster, Inc. | Ablation catheter with optically transparent, electrically conductive tip |
| US8062228B2 (en) | 2007-07-03 | 2011-11-22 | Meridian Medical Systems, Llc | Dual mode intracranial temperature detector |
| WO2009009398A1 (en) | 2007-07-06 | 2009-01-15 | Tsunami Medtech, Llc | Medical system and method of use |
| US8019419B1 (en) | 2007-09-25 | 2011-09-13 | Dorin Panescu | Methods and apparatus for leadless, battery-less, wireless stimulation of tissue |
| US8868165B1 (en) | 2007-09-28 | 2014-10-21 | Pacesetter, Inc. | Use of cardiogenic impedance waveform morphology to analyze cardiac conditions and to adjust treatment therapy |
| WO2009048943A1 (en) | 2007-10-09 | 2009-04-16 | Boston Scientific Scimed, Inc. | Cooled ablation catheter devices and methods of use |
| JP5400784B2 (ja) | 2007-10-09 | 2014-01-29 | ボストン サイエンティフィック リミテッド | 電気生理学電極および電気生理学電極を含む装置 |
| US9474571B2 (en) | 2007-10-15 | 2016-10-25 | Boston Scientific Scimed, Inc. | Percutaneous tissue ablation probe with occlusive bodies |
| US9622813B2 (en) | 2007-11-01 | 2017-04-18 | Covidien Lp | Method for volume determination and geometric reconstruction |
| US8906011B2 (en) | 2007-11-16 | 2014-12-09 | Kardium Inc. | Medical device for use in bodily lumens, for example an atrium |
| EP2197377B1 (en) | 2007-11-16 | 2017-11-01 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Device for real-time lesion estimation during ablation |
| US8359092B2 (en) | 2007-11-29 | 2013-01-22 | Biosense Webster, Inc. | Determining locations of ganglia and plexi in the heart using complex fractionated atrial electrogram |
| US8052684B2 (en) | 2007-11-30 | 2011-11-08 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated ablation catheter having parallel external flow and proximally tapered electrode |
| US8475449B2 (en) | 2007-12-10 | 2013-07-02 | Medtronic Ablation Frontiers Llc | RF energy delivery system and method |
| US8162934B2 (en) * | 2007-12-21 | 2012-04-24 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Medical catheter assembly with deflection pull ring and distal tip interlock |
| US8273082B2 (en) | 2007-12-21 | 2012-09-25 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated ablation catheter assembly having a flow member to create parallel external flow |
| US8118809B2 (en) | 2007-12-21 | 2012-02-21 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Flexible conductive polymer electrode and method for ablation |
| US8562600B2 (en) | 2007-12-27 | 2013-10-22 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Integration of control software with a medical device and system |
| US8333762B2 (en) | 2007-12-28 | 2012-12-18 | Biosense Webster, Inc. | Irrigated catheter with improved irrigation flow |
| US9204927B2 (en) | 2009-05-13 | 2015-12-08 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for presenting information representative of lesion formation in tissue during an ablation procedure |
| US20110264000A1 (en) | 2007-12-28 | 2011-10-27 | Saurav Paul | System and method for determining tissue type and mapping tissue morphology |
| US8290578B2 (en) | 2007-12-28 | 2012-10-16 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Method and apparatus for complex impedance compensation |
| US7996078B2 (en) | 2007-12-31 | 2011-08-09 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Systems and methods of photodynamic-based cardiac ablation via the esophagus |
| US20090306643A1 (en) | 2008-02-25 | 2009-12-10 | Carlo Pappone | Method and apparatus for delivery and detection of transmural cardiac ablation lesions |
| US20090221999A1 (en) | 2008-02-29 | 2009-09-03 | Ramin Shahidi | Thermal Ablation Design and Planning Methods |
| US20090254083A1 (en) | 2008-03-10 | 2009-10-08 | Hansen Medical, Inc. | Robotic ablation catheter |
| US9198723B2 (en) | 2008-03-31 | 2015-12-01 | Covidien Lp | Re-hydration antenna for ablation |
| US8298227B2 (en) | 2008-05-14 | 2012-10-30 | Endosense Sa | Temperature compensated strain sensing catheter |
| WO2009140067A1 (en) | 2008-05-15 | 2009-11-19 | Boston Scientific Scimed, Inc. | Apparatus for cryogenically ablating tissue and adjusting cryogenic ablation regions |
| US9050069B2 (en) | 2008-05-16 | 2015-06-09 | Medtronic Cryocath Lp | Thermocouple-controlled catheter cooling system |
| US8128617B2 (en) | 2008-05-27 | 2012-03-06 | Boston Scientific Scimed, Inc. | Electrical mapping and cryo ablating with a balloon catheter |
| US8357149B2 (en) | 2008-06-05 | 2013-01-22 | Biosense Webster, Inc. | Filter for simultaneous pacing and ablation |
| US8206385B2 (en) | 2008-06-09 | 2012-06-26 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Catheter assembly with front-loaded tip and multi-contact connector |
| US8206380B2 (en) | 2008-06-13 | 2012-06-26 | Advanced Caridiac Therapeutics Inc. | Method and apparatus for measuring catheter contact force during a medical procedure |
| WO2010005727A2 (en) | 2008-06-16 | 2010-01-14 | Paul Zei | Devices and methods for exercise monitoring |
| US20090312756A1 (en) | 2008-06-17 | 2009-12-17 | Hansen Medical, Inc. | Irrigated ablation catheters |
| US8280511B2 (en) | 2008-07-07 | 2012-10-02 | Pacesetter, Inc. | Systems and methods for use by an implantable medical device for detecting heart failure based on the independent information content of immittance vectors |
| US9675411B2 (en) | 2008-07-15 | 2017-06-13 | Biosense Webster, Inc. | Catheter with perforated tip |
| US8882761B2 (en) | 2008-07-15 | 2014-11-11 | Catheffects, Inc. | Catheter and method for improved ablation |
| EP2317952A1 (en) | 2008-07-17 | 2011-05-11 | Maestroheart SA | Medical device for tissue ablation |
| US8554333B2 (en) | 2008-07-24 | 2013-10-08 | Pacesetter, Inc. | Adaptable communication sensitivity for an implantable medical device |
| US8032218B2 (en) | 2008-07-31 | 2011-10-04 | Pacesetter, Inc. | Implantable cardiac device with satellite refresh |
| WO2010024738A1 (en) | 2008-08-29 | 2010-03-04 | St. Jude Medical Ab | Implantable medical device and method for such a device for predicting hf status of a patient |
| EP2334248A2 (en) | 2008-09-02 | 2011-06-22 | Medtronic Ablation Frontiers LLC | Irrigated ablation catheter system |
| JP5827124B2 (ja) | 2008-10-04 | 2015-12-02 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 組織と接触する診断および/または治療要素を支持するループ構造 |
| US8852179B2 (en) | 2008-10-10 | 2014-10-07 | Covidien Lp | Apparatus, system and method for monitoring tissue during an electrosurgical procedure |
| EP2349045B1 (en) | 2008-10-21 | 2014-07-16 | Microcube, LLC | Devices for applying energy to bodily tissues |
| US20100114227A1 (en) | 2008-10-30 | 2010-05-06 | Pacesetter, Inc. | Systems and Methds for Use by an Implantable Medical Device for Controlling Vagus Nerve Stimulation Based on Heart Rate Reduction Curves and Thresholds to Mitigate Heart Failure |
| US9757189B2 (en) | 2008-12-03 | 2017-09-12 | Biosense Webster, Inc. | Prevention of kinks in catheter irrigation tubes |
| US8355799B2 (en) | 2008-12-12 | 2013-01-15 | Arthrocare Corporation | Systems and methods for limiting joint temperature |
| US8600472B2 (en) | 2008-12-30 | 2013-12-03 | Biosense Webster (Israel), Ltd. | Dual-purpose lasso catheter with irrigation using circumferentially arranged ring bump electrodes |
| US8475450B2 (en) | 2008-12-30 | 2013-07-02 | Biosense Webster, Inc. | Dual-purpose lasso catheter with irrigation |
| US20100168557A1 (en) * | 2008-12-30 | 2010-07-01 | Deno D Curtis | Multi-electrode ablation sensing catheter and system |
| US8652129B2 (en) | 2008-12-31 | 2014-02-18 | Medtronic Ardian Luxembourg S.A.R.L. | Apparatus, systems, and methods for achieving intravascular, thermally-induced renal neuromodulation |
| US8348937B2 (en) | 2008-12-31 | 2013-01-08 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigated ablation catheter |
| US8864757B2 (en) | 2008-12-31 | 2014-10-21 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for measuring force and torque applied to a catheter electrode tip |
| US9833217B2 (en) | 2008-12-31 | 2017-12-05 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Methods and apparatus for utilizing impeller-based rotationally-scanning catheters |
| US8333759B2 (en) | 2009-01-12 | 2012-12-18 | Covidien Lp | Energy delivery algorithm for medical devices |
| US8262652B2 (en) | 2009-01-12 | 2012-09-11 | Tyco Healthcare Group Lp | Imaginary impedance process monitoring and intelligent shut-off |
| US8731684B2 (en) | 2009-01-20 | 2014-05-20 | Meridian Medical Systems, Llc | Method and apparatus for aligning an ablation catheter and a temperature probe during an ablation procedure |
| WO2010090701A1 (en) | 2009-01-20 | 2010-08-12 | Advanced Cardiac Therapeutics Inc. | Method and apparatus for minimizing thermal trauma to an organ during tissue ablation of a different organ |
| JP5693471B2 (ja) | 2009-02-11 | 2015-04-01 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 絶縁された切除カテーテルデバイスおよびその使用法 |
| US8702693B2 (en) | 2009-02-17 | 2014-04-22 | Boston Scientific Scimed, Inc. | Apparatus and methods for supplying fluid to an electrophysiology apparatus |
| WO2010096579A1 (en) | 2009-02-20 | 2010-08-26 | Boston Scientific Scimed, Inc. | Steerable catheter having intermediate stiffness transition zone |
| EP2398416B1 (en) | 2009-02-23 | 2015-10-28 | Medtronic Advanced Energy LLC | Fluid-assisted electrosurgical device |
| US8287532B2 (en) | 2009-04-13 | 2012-10-16 | Biosense Webster, Inc. | Epicardial mapping and ablation catheter |
| US8523850B2 (en) | 2009-04-17 | 2013-09-03 | Domain Surgical, Inc. | Method for heating a surgical implement |
| CA2703347C (en) | 2009-05-08 | 2016-10-04 | Endosense Sa | Method and apparatus for controlling lesion size in catheter-based ablation treatment |
| JP5444840B2 (ja) | 2009-05-21 | 2014-03-19 | 東レ株式会社 | バルーン付きアブレーションカテーテル及びバルーン付きアブレーションカテーテルシステム |
| US8954161B2 (en) | 2012-06-01 | 2015-02-10 | Advanced Cardiac Therapeutics, Inc. | Systems and methods for radiometrically measuring temperature and detecting tissue contact prior to and during tissue ablation |
| US9226791B2 (en) | 2012-03-12 | 2016-01-05 | Advanced Cardiac Therapeutics, Inc. | Systems for temperature-controlled ablation using radiometric feedback |
| US8926605B2 (en) | 2012-02-07 | 2015-01-06 | Advanced Cardiac Therapeutics, Inc. | Systems and methods for radiometrically measuring temperature during tissue ablation |
| US9277961B2 (en) | 2009-06-12 | 2016-03-08 | Advanced Cardiac Therapeutics, Inc. | Systems and methods of radiometrically determining a hot-spot temperature of tissue being treated |
| US20100331838A1 (en) | 2009-06-25 | 2010-12-30 | Estech, Inc. (Endoscopic Technologies, Inc.) | Transmurality clamp systems and methods |
| EP2449544B1 (en) | 2009-06-29 | 2018-04-18 | Koninklijke Philips N.V. | Tumor ablation training system |
| US8414579B2 (en) | 2009-06-30 | 2013-04-09 | Boston Scientific Scimed, Inc. | Map and ablate open irrigated hybrid catheter |
| DE102009048312B4 (de) | 2009-07-07 | 2017-05-11 | Erbe Elektromedizin Gmbh | Elektrochirurgisches Instrument und Verfahren zur Herstellung eines elektrochirurgischen Instruments |
| EP2453821A1 (en) | 2009-07-13 | 2012-05-23 | Boston Scientific Scimed, Inc. | Open-irrigated ablation catheter with turbulent flow |
| US20110022041A1 (en) | 2009-07-24 | 2011-01-27 | Frank Ingle | Systems and methods for titrating rf ablation |
| US8442613B2 (en) | 2009-07-29 | 2013-05-14 | Boston Scientific Scimed, Inc | Mapping probe assembly with skived tube body frame |
| US20110028821A1 (en) | 2009-07-31 | 2011-02-03 | Newcardio, Inc. | Electrocardiographic Monitoring System and Method Using Orthogonal Electrode Pattern |
| JP5542937B2 (ja) | 2009-08-14 | 2014-07-09 | ボストン サイエンティフィック サイムド,インコーポレイテッド | 改善されたアンカ性能を備えたマッピングカテーテルを有する医療アブレーションシステムを製造および使用するためのシステムおよび方法 |
| GB2485924B (en) | 2009-09-15 | 2015-11-04 | Boston Scient Scimed Inc | System for predicting lesion size shortly after onset of RF energy delivery |
| US9474565B2 (en) | 2009-09-22 | 2016-10-25 | Mederi Therapeutics, Inc. | Systems and methods for treating tissue with radiofrequency energy |
| US8377054B2 (en) | 2009-09-24 | 2013-02-19 | Covidien Lp | Automatic control circuit for use in an electrosurgical generator |
| US9101733B2 (en) | 2009-09-29 | 2015-08-11 | Biosense Webster, Inc. | Catheter with biased planar deflection |
| GB2474233A (en) | 2009-10-06 | 2011-04-13 | Uk Investments Associates Llc | Cooling pump comprising a detachable head portion |
| US20110105928A1 (en) | 2009-11-05 | 2011-05-05 | Newcardio, Inc. | ECG Reconstruction For Atrial Activity Monitoring And Detection |
| US20110213356A1 (en) | 2009-11-05 | 2011-09-01 | Wright Robert E | Methods and systems for spinal radio frequency neurotomy |
| US20110112414A1 (en) | 2009-11-06 | 2011-05-12 | Newcardio, Inc | System for automated ekg analysis |
| US20110112413A1 (en) | 2009-11-06 | 2011-05-12 | Newcardio, Inc | Method for automated ekg analysis |
| US20110112415A1 (en) | 2009-11-06 | 2011-05-12 | Newcardio, Inc | System and method for automated ekg analysis |
| JP6013186B2 (ja) | 2009-11-13 | 2016-10-25 | セント ジュード メディカル インコーポレイテッド | 千鳥配置された焼灼素子のアセンブリ |
| US8414570B2 (en) | 2009-11-17 | 2013-04-09 | Bsd Medical Corporation | Microwave coagulation applicator and system |
| US8454589B2 (en) | 2009-11-20 | 2013-06-04 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for assessing effective delivery of ablation therapy |
| EP2445434B1 (en) | 2009-12-11 | 2018-08-22 | St. Jude Medical Atrial Fibrillation Division, Inc. | System for determining the likelihood of endocardial barotrauma in tissue during ablation |
| US9179827B2 (en) | 2009-12-15 | 2015-11-10 | Boston Scientific Scimed, Inc. | Systems and methods for determining the position and orientation of medical devices inserted into a patient |
| US8920415B2 (en) | 2009-12-16 | 2014-12-30 | Biosense Webster (Israel) Ltd. | Catheter with helical electrode |
| US8882759B2 (en) | 2009-12-18 | 2014-11-11 | Covidien Lp | Microwave ablation system with dielectric temperature probe |
| US8668686B2 (en) * | 2009-12-23 | 2014-03-11 | Biosense Webster (Israel) Ltd. | Sensing contact of ablation catheter using differential temperature measurements |
| US8641708B2 (en) | 2009-12-29 | 2014-02-04 | Biosense Webster (Israel), Ltd. | Measuring weak signals over ablation lines |
| US20110160726A1 (en) | 2009-12-30 | 2011-06-30 | Frank Ingle | Apparatus and methods for fluid cooled electrophysiology procedures |
| US20110184313A1 (en) | 2010-01-22 | 2011-07-28 | The Regents Of The University Of Michigan | Cauterization Device and Method of Cauterizing |
| US8374670B2 (en) | 2010-01-22 | 2013-02-12 | Biosense Webster, Inc. | Catheter having a force sensing distal tip |
| US20110184300A1 (en) | 2010-01-26 | 2011-07-28 | Newcardio, Inc. | Atrial fibrillation detection based on absence of consistent p-loops in averaged vectorcardiogram |
| JP6472940B2 (ja) | 2010-02-05 | 2019-02-20 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 組み合わされた切除及び超音波撮像 |
| US9265574B2 (en) | 2010-03-10 | 2016-02-23 | Biosense Webster (Israel) Ltd. | Monitoring tissue temperature while using an irrigated catheter |
| US9980772B2 (en) | 2010-03-10 | 2018-05-29 | Biosense Webster (Israel) Ltd. | Monitoring tissue temperature while using an irrigated catheter |
| EP2547276B1 (en) | 2010-03-15 | 2016-08-31 | Boston Scientific Scimed, Inc. | Ablation catheter with isolated temperature sensing tip |
| CA2796269A1 (en) | 2010-04-13 | 2011-10-20 | Sentreheart, Inc. | Methods and devices for accessing and delivering devices to a heart |
| US9949791B2 (en) | 2010-04-26 | 2018-04-24 | Biosense Webster, Inc. | Irrigated catheter with internal position sensor |
| US8870863B2 (en) | 2010-04-26 | 2014-10-28 | Medtronic Ardian Luxembourg S.A.R.L. | Catheter apparatuses, systems, and methods for renal neuromodulation |
| US9510894B2 (en) | 2010-04-28 | 2016-12-06 | Biosense Webster (Israel) Ltd. | Irrigated ablation catheter having irrigation ports with reduced hydraulic resistance |
| US8845631B2 (en) | 2010-04-28 | 2014-09-30 | Medtronic Ablation Frontiers Llc | Systems and methods of performing medical procedures |
| US9943363B2 (en) | 2010-04-28 | 2018-04-17 | Biosense Webster, Inc. | Irrigated ablation catheter with improved fluid flow |
| US9943362B2 (en) | 2010-04-28 | 2018-04-17 | Biosense Webster, Inc. | Irrigated ablation catheter with improved fluid flow |
| US8834388B2 (en) * | 2010-04-30 | 2014-09-16 | Medtronic Ablation Frontiers Llc | Method and apparatus to regulate a tissue temperature |
| US8696659B2 (en) | 2010-04-30 | 2014-04-15 | Arthrocare Corporation | Electrosurgical system and method having enhanced temperature measurement |
| US9179968B2 (en) | 2010-05-10 | 2015-11-10 | St. Jude Medical Luxembourg Holding S.À.R.L. | Irrigated finned ablation head |
| CN103118620B (zh) | 2010-05-12 | 2015-09-23 | 施菲姆德控股有限责任公司 | 小轮廓的电极组件 |
| US20110295267A1 (en) | 2010-05-28 | 2011-12-01 | Hansen Medical, Inc. | System and method for automated tissue structure traversal |
| ITRM20100314A1 (it) | 2010-06-09 | 2011-12-10 | Luca Viviana De | Catetere ad adesività reversibile, per la stabilizzazione durante l'ablazione transcatetere mediante radiofrequenza. |
| US10271889B2 (en) | 2010-06-27 | 2019-04-30 | Sunnybrook Health Sciences Centre | Apparatus and method for cooling a tissue volume during thermal therapy treatment |
| US9402560B2 (en) | 2010-07-21 | 2016-08-02 | Diros Technology Inc. | Advanced multi-purpose catheter probes for diagnostic and therapeutic procedures |
| US20120029512A1 (en) | 2010-07-30 | 2012-02-02 | Willard Martin R | Balloon with surface electrodes and integral cooling for renal nerve ablation |
| US9463062B2 (en) | 2010-07-30 | 2016-10-11 | Boston Scientific Scimed, Inc. | Cooled conductive balloon RF catheter for renal nerve ablation |
| US9023033B2 (en) | 2010-08-04 | 2015-05-05 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Magnetically guided catheters |
| US8380276B2 (en) * | 2010-08-16 | 2013-02-19 | Biosense Webster, Inc. | Catheter with thin film pressure sensing distal tip |
| US8690866B2 (en) | 2010-08-23 | 2014-04-08 | Covidien Lp | Ablation devices utilizing exothermic chemical reactions, system including same, and methods of ablating tissue using same |
| US9289606B2 (en) | 2010-09-02 | 2016-03-22 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System for electroporation therapy |
| WO2012061153A1 (en) | 2010-10-25 | 2012-05-10 | Medtronic Ardian Luxembourg S.A.R.L. | Devices, systems and methods for evaluation and feedback of neuromodulation treatment |
| RU2013118108A (ru) * | 2010-10-25 | 2014-12-10 | Медтроник Ардиан Люксембург С.А.Р.Л. | Катетерные устройства, содержащие группы из нескольких электродов, для почечной нейромодуляции и соответствующие системы и способы |
| US9220558B2 (en) | 2010-10-27 | 2015-12-29 | Boston Scientific Scimed, Inc. | RF renal denervation catheter with multiple independent electrodes |
| WO2012065177A2 (en) | 2010-11-12 | 2012-05-18 | Estech, Inc (Endoscopic Technologies, Inc) | Stabilized ablation systems and methods |
| US8992519B2 (en) | 2010-11-23 | 2015-03-31 | Boston Scientific Scime, Inc. | Inverted balloon RF ablation catheter and method |
| US9532828B2 (en) | 2010-11-29 | 2017-01-03 | Medtronic Ablation Frontiers Llc | System and method for adaptive RF ablation |
| US8560086B2 (en) | 2010-12-02 | 2013-10-15 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Catheter electrode assemblies and methods of construction therefor |
| US10016233B2 (en) | 2010-12-06 | 2018-07-10 | Biosense Webster (Israel) Ltd. | Treatment of atrial fibrillation using high-frequency pacing and ablation of renal nerves |
| US9737353B2 (en) | 2010-12-16 | 2017-08-22 | Biosense Webster (Israel) Ltd. | System for controlling tissue ablation using temperature sensors |
| US9788891B2 (en) | 2010-12-28 | 2017-10-17 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation electrode assemblies and methods for using same |
| US8814857B2 (en) | 2010-12-17 | 2014-08-26 | St. Jude Medical, Atrial Filbrillation Division, Inc. | Irrigated ablation electrode assemblies |
| US9089340B2 (en) | 2010-12-30 | 2015-07-28 | Boston Scientific Scimed, Inc. | Ultrasound guided tissue ablation |
| EP2627243B1 (en) | 2010-12-30 | 2020-01-22 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System for diagnosing arrhythmias and directing catheter therapies |
| US9044245B2 (en) | 2011-01-05 | 2015-06-02 | Medtronic Ablation Frontiers Llc | Multipolarity epicardial radiofrequency ablation |
| US9265557B2 (en) | 2011-01-31 | 2016-02-23 | Medtronic Ablation Frontiers Llc | Multi frequency and multi polarity complex impedance measurements to assess ablation lesions |
| WO2012120498A1 (en) | 2011-03-04 | 2012-09-13 | Technion Research & Development | Non-invasive thermal treatment monitoring |
| US8858548B2 (en) | 2011-03-15 | 2014-10-14 | Medtronic Ablation Frontiers Llc | Independent passive cooling design for ablation catheters |
| WO2012134911A1 (en) | 2011-03-25 | 2012-10-04 | Medtronic Ablation Frontiers Llc | Cooling systems for electrode arrays |
| WO2012130337A1 (en) * | 2011-04-01 | 2012-10-04 | Flux Medical N.V. | System, device and method for ablation of a vessel's wall from the inside |
| CN106420040B (zh) | 2011-04-12 | 2020-08-28 | 热医学公司 | 用于在流体增强型消融治疗中对流体进行加热的方法和装置 |
| US10039502B2 (en) * | 2011-04-12 | 2018-08-07 | Medtronic Ablation Frontiers Llc | Electrophysiological signal processing and utilization |
| AU2012242590B2 (en) | 2011-04-13 | 2016-08-04 | Auris Health, Inc. | Integrated ablation and mapping system |
| US8942828B1 (en) | 2011-04-13 | 2015-01-27 | Stuart Schecter, LLC | Minimally invasive cardiovascular support system with true haptic coupling |
| US8545409B2 (en) | 2011-04-14 | 2013-10-01 | St. Jude Medical, Inc. | Arrangement and interface for RF ablation system with acoustic feedback |
| US20120283722A1 (en) | 2011-05-02 | 2012-11-08 | Medtronic Ablation Frontiers Llc | Adiabatic cooling system for medical devices |
| US8934953B2 (en) | 2011-05-04 | 2015-01-13 | Meridian Medical Systems, Llc | Dual mode temperature transducer with oxygen saturation sensor |
| AU2012202857B2 (en) * | 2011-05-23 | 2014-10-30 | Biosense Webster (Israel), Ltd. | Monitoring tissue temperature while using an irrigated catheter |
| US9220433B2 (en) | 2011-06-30 | 2015-12-29 | Biosense Webster (Israel), Ltd. | Catheter with variable arcuate distal section |
| US9131853B2 (en) | 2011-07-01 | 2015-09-15 | Joseph Tiano | Medical probe and method of using same |
| WO2013009977A1 (en) | 2011-07-12 | 2013-01-17 | David Lambert | Device for reducing renal sympathetic nerve activity |
| US10743932B2 (en) | 2011-07-28 | 2020-08-18 | Biosense Webster (Israel) Ltd. | Integrated ablation system using catheter with multiple irrigation lumens |
| US9801683B2 (en) | 2011-07-29 | 2017-10-31 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Universal shaft for magnetic manipulation of catheters |
| US9662169B2 (en) | 2011-07-30 | 2017-05-30 | Biosense Webster (Israel) Ltd. | Catheter with flow balancing valve |
| US10201385B2 (en) | 2011-09-01 | 2019-02-12 | Biosense Webster (Israel) Ltd. | Catheter adapted for direct tissue contact |
| US8900228B2 (en) | 2011-09-01 | 2014-12-02 | Biosense Webster (Israel) Ltd. | Catheter adapted for direct tissue contact and pressure sensing |
| DE102011082307A1 (de) | 2011-09-07 | 2013-03-07 | Celon Ag Medical Instruments | Elektrochirurgisches Instrument, Elektrochirurgieanordnung und zugehörige Verfahren |
| US9125668B2 (en) | 2011-09-14 | 2015-09-08 | Boston Scientific Scimed Inc. | Ablation device with multiple ablation modes |
| WO2013040297A1 (en) | 2011-09-14 | 2013-03-21 | Boston Scientific Scimed, Inc. | Ablation device with ionically conductive balloon |
| US20130096447A1 (en) | 2011-09-27 | 2013-04-18 | Akshay Dhawan | System and methods for serial analysis of electrocardiograms |
| JP6277130B2 (ja) | 2011-10-05 | 2018-02-14 | エムシーテン、インコーポレイテッド | 医療用の装置およびそれの製造方法 |
| US10064678B2 (en) | 2011-10-26 | 2018-09-04 | Medtronic Ablation Frontiers Llc | Semi-circular pulmonary vein ablation catheter |
| US9131980B2 (en) | 2011-12-19 | 2015-09-15 | Medtronic Advanced Energy Llc | Electrosurgical devices |
| JP2015506209A (ja) | 2011-12-28 | 2015-03-02 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | アブレーションプローブならびにアブレーションおよび超音波撮像システム |
| US20130172879A1 (en) | 2011-12-29 | 2013-07-04 | Boston Scientific Scimed, Inc. | Renal nerve modulation medical devices |
| US8956353B2 (en) | 2011-12-29 | 2015-02-17 | Biosense Webster (Israel) Ltd. | Electrode irrigation using micro-jets |
| US9687289B2 (en) | 2012-01-04 | 2017-06-27 | Biosense Webster (Israel) Ltd. | Contact assessment based on phase measurement |
| JP2015506234A (ja) | 2012-01-10 | 2015-03-02 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 電気生理学システム |
| JP5830614B2 (ja) | 2012-01-31 | 2015-12-09 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 超音波組織撮像のための流体に基づいた音響結合を有するアブレーションプローブ、および、アブレーションおよび超音波撮像システム |
| US9636040B2 (en) | 2012-02-03 | 2017-05-02 | Intuitive Surgical Operations, Inc. | Steerable flexible needle with embedded shape sensing |
| WO2013123020A1 (en) | 2012-02-14 | 2013-08-22 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Ablation catheter with optic energy delivery system for photoacoustic tissue response |
| US9314299B2 (en) | 2012-03-21 | 2016-04-19 | Biosense Webster (Israel) Ltd. | Flower catheter for mapping and ablating veinous and other tubular locations |
| US9717554B2 (en) | 2012-03-26 | 2017-08-01 | Biosense Webster (Israel) Ltd. | Catheter with composite construction |
| WO2013158232A1 (en) | 2012-04-17 | 2013-10-24 | The Penn State Research Foundation | System and method for combined microwave heating and radiometry for characterizing biological tissues |
| US20130281851A1 (en) | 2012-04-19 | 2013-10-24 | Kenneth L. Carr | Heating/sensing catheter apparatus for minimally invasive applications |
| US20130296840A1 (en) | 2012-05-01 | 2013-11-07 | Medtronic Ablation Frontiers Llc | Systems and methods for detecting tissue contact during ablation |
| WO2013165584A1 (en) | 2012-05-04 | 2013-11-07 | St. Jude Medical, Atrial Fibrillation Division, Inc. | System and method for controlling delivery of ablation energy to tissue |
| US8900225B2 (en) | 2012-05-07 | 2014-12-02 | Biosense Webster (Israel) Ltd. | Automatic ablation tracking |
| US20130303945A1 (en) | 2012-05-14 | 2013-11-14 | Intuitive Surgical Operations, Inc. | Electromagnetic tip sensor |
| US10039473B2 (en) | 2012-05-14 | 2018-08-07 | Intuitive Surgical Operations, Inc. | Systems and methods for navigation based on ordered sensor records |
| CN104487013B (zh) | 2012-06-22 | 2017-06-20 | 柯惠有限合伙公司 | 微波消融系统和测量微波消融系统中温度的方法 |
| US20140018793A1 (en) | 2012-07-12 | 2014-01-16 | Covidien Lp | Heat-distribution indicators, thermal zone indicators, electrosurgical systems including same and methods of directing energy to tissue using same |
| US9757190B2 (en) | 2012-08-17 | 2017-09-12 | Medtronic Ablation Frontiers Llc | Methods of manufacturing monophasic action potential mapping catheters |
| US9168004B2 (en) | 2012-08-20 | 2015-10-27 | Biosense Webster (Israel) Ltd. | Machine learning in determining catheter electrode contact |
| US20140058244A1 (en) | 2012-08-21 | 2014-02-27 | Regents Of The University Of Minnesota | Photoacoustic monitoring |
| US20140058375A1 (en) | 2012-08-22 | 2014-02-27 | Boston Scientific Scimed, Inc. | High resolution map and ablate catheter |
| US9370329B2 (en) | 2012-09-18 | 2016-06-21 | Boston Scientific Scimed, Inc. | Map and ablate closed-loop cooled ablation catheter |
| WO2014047071A1 (en) | 2012-09-18 | 2014-03-27 | Boston Scientific Scimed, Inc. | Map and ablate closed-loop cooled ablation catheter with flat tip |
| WO2014047281A1 (en) | 2012-09-20 | 2014-03-27 | Boston Scientific Scimed Inc. | Nearfield ultrasound echography mapping |
| US9649146B2 (en) | 2012-10-02 | 2017-05-16 | Covidien Lp | Electro-thermal device |
| JP6175511B2 (ja) | 2012-11-14 | 2017-08-02 | アベヌ メディカル インコーポレイテッドAvenu Medical,Inc. | 動静脈ろうを作成するデバイス |
| US9066725B2 (en) | 2012-12-06 | 2015-06-30 | St. Jude Medical, Atrial Fibrillation Division, Inc. | Irrigant distribution system for electrodes |
| US9445725B2 (en) | 2012-12-17 | 2016-09-20 | Biosense Webster (Israel) Ltd. | Irrigated catheter tip with temperature sensor array |
| US20140171936A1 (en) | 2012-12-17 | 2014-06-19 | Biosense Webster (Israel) Ltd. | Irrigated catheter tip with temperature sensor and optic fiber arrays |
| WO2014100631A1 (en) | 2012-12-20 | 2014-06-26 | Boston Scientific Scimed, Inc. | Real-time feedback for electrode contact during mapping |
| EP2934357B1 (en) | 2012-12-20 | 2017-11-15 | Renal Dynamics Ltd. | Multi point treatment probes |
| US20140180077A1 (en) | 2012-12-21 | 2014-06-26 | Volcano Corporation | Tissue ablation catheter and methods of ablating tissue |
| US9044156B2 (en) | 2012-12-28 | 2015-06-02 | Biosense Webster (Israel) Ltd. | Catheter with improved safety line for distal tip and related method |
| US10588597B2 (en) | 2012-12-31 | 2020-03-17 | Intuitive Surgical Operations, Inc. | Systems and methods for interventional procedure planning |
| US9144460B2 (en) | 2012-12-31 | 2015-09-29 | Biosense Webster (Israel) Ltd. | Catheter with direct cooling on nonablating element |
| US9414879B2 (en) | 2013-03-12 | 2016-08-16 | Cook Medical Technologies Llc | Catalyzed exothermic ablation device |
| JP6122206B2 (ja) | 2013-03-12 | 2017-04-26 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 神経調節システム |
| US9486280B2 (en) | 2013-03-13 | 2016-11-08 | Boston Scientific Scimed, Inc. | Steerable ablation device with linear ionically conductive balloon |
| JP6117422B2 (ja) | 2013-03-15 | 2017-04-19 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 開放灌注式アブレーションカテーテル |
| EP2945558B1 (en) * | 2013-03-15 | 2018-01-31 | St. Jude Medical Atrial Fibrillation Division Inc. | Force-sensing ablation catheter |
| US9592095B2 (en) | 2013-05-16 | 2017-03-14 | Intuitive Surgical Operations, Inc. | Systems and methods for robotic medical system integration with external imaging |
| US10052495B2 (en) | 2013-09-08 | 2018-08-21 | Tylerton International Inc. | Detection of reduced-control cardiac zones |
| WO2015042173A1 (en) | 2013-09-20 | 2015-03-26 | Advanced Cardiac Therapeutics, Inc. | Temperature sensing and tissue ablation using a plurality of electrodes |
| EP3057488B1 (en) | 2013-10-14 | 2018-05-16 | Boston Scientific Scimed, Inc. | High resolution cardiac mapping electrode array catheter |
| US10682175B2 (en) * | 2013-11-06 | 2020-06-16 | Biosense Webster (Israel) Ltd. | Using catheter position and temperature measurement to detect movement from ablation point |
| WO2015077348A1 (en) | 2013-11-20 | 2015-05-28 | Boston Scientific Scimed, Inc. | Ablation medical devices and methods for making and using ablation medical devices |
| CN106102583A (zh) | 2014-01-10 | 2016-11-09 | 泰勒顿国际公司 | 瘢痕和纤维心脏区的检测 |
| US20150265348A1 (en) | 2014-03-18 | 2015-09-24 | Boston Scientific Scimed, Inc. | Electrophysiology system |
| JP2017508528A (ja) | 2014-03-18 | 2017-03-30 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 電気生理学システム |
| US9956035B2 (en) | 2014-03-27 | 2018-05-01 | Biosense Webster (Israel) Ltd. | Temperature measurement in catheter |
| US10639098B2 (en) * | 2014-05-06 | 2020-05-05 | Cosman Instruments, Llc | Electrosurgical generator |
| EP3160359B1 (en) | 2014-06-24 | 2021-05-19 | Apama Medical, Inc. | Tissue ablation and monitoring thereof |
| WO2016081611A1 (en) | 2014-11-19 | 2016-05-26 | Advanced Cardiac Therapeutics, Inc. | High-resolution mapping of tissue with pacing |
| WO2016081598A1 (en) | 2014-11-19 | 2016-05-26 | Advanced Cardiac Therapeutics, Inc. | Systems and methods for facilitating consistent radiometric tissue contact detection independent of orientation |
| US11357568B2 (en) | 2014-11-19 | 2022-06-14 | Epix Therapeutics, Inc. | Radiometric tissue contact and tissue type detection |
| CA2967829A1 (en) | 2014-11-19 | 2016-05-26 | Advanced Cardiac Therapeutics, Inc. | Systems and methods for high-resolution mapping of tissue |
| KR20170107428A (ko) | 2014-11-19 | 2017-09-25 | 어드밴스드 카디악 테라퓨틱스, 인크. | 고분해능 전극 어셈블리를 이용한 절제 장치, 시스템 및 방법 |
| US9636164B2 (en) | 2015-03-25 | 2017-05-02 | Advanced Cardiac Therapeutics, Inc. | Contact sensing systems and methods |
| US10182742B2 (en) | 2015-04-02 | 2019-01-22 | Medtronic Ablation Frontiers Llc | Tissue contact sensing with a multi electrode ablation catheter |
| US10143399B2 (en) | 2015-04-02 | 2018-12-04 | Medtronic Ablation Frontiers Llc | Tissue contact sensing with a multi electrode ablation catheter |
| WO2017048965A1 (en) | 2015-09-18 | 2017-03-23 | Adagio Medical Inc. | Tissue contact verification system |
| WO2017070559A1 (en) | 2015-10-21 | 2017-04-27 | St. Jude, Cardiology Division, Inc. | High density electrode mapping catheter |
| JP2018538041A (ja) | 2015-11-20 | 2018-12-27 | ボストン サイエンティフィック サイムド,インコーポレイテッドBoston Scientific Scimed,Inc. | 組織接触感知ベクトル |
| SG11201807618QA (en) * | 2016-03-15 | 2018-10-30 | Epix Therapeutics Inc | Improved devices, systems and methods for irrigated ablation |
-
2017
- 2017-03-14 SG SG11201807618QA patent/SG11201807618QA/en unknown
- 2017-03-14 CN CN201780027973.6A patent/CN109069006B/zh active Active
- 2017-03-14 CA CA3017269A patent/CA3017269A1/en not_active Abandoned
- 2017-03-14 JP JP2018548898A patent/JP6923549B2/ja active Active
- 2017-03-14 WO PCT/US2017/022264 patent/WO2017160808A1/en active Application Filing
- 2017-03-14 EP EP17767316.7A patent/EP3429462B1/en active Active
- 2017-03-14 AU AU2017235224A patent/AU2017235224A1/en not_active Abandoned
- 2017-03-14 KR KR1020187029420A patent/KR20180124070A/ko unknown
- 2017-10-12 US US15/782,714 patent/US9993178B2/en active Active
- 2017-10-12 US US15/782,703 patent/US11389230B2/en active Active
-
2018
- 2018-06-08 US US16/003,576 patent/US11179197B2/en active Active
- 2018-09-05 IL IL261613A patent/IL261613A/en unknown
-
2021
- 2021-11-22 US US17/532,124 patent/US20220079669A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20180289284A1 (en) | 2018-10-11 |
| EP3429462B1 (en) | 2022-08-03 |
| US20180078170A1 (en) | 2018-03-22 |
| US11179197B2 (en) | 2021-11-23 |
| SG11201807618QA (en) | 2018-10-30 |
| CA3017269A1 (en) | 2017-09-21 |
| WO2017160808A1 (en) | 2017-09-21 |
| JP2019517832A (ja) | 2019-06-27 |
| CN109069006B (zh) | 2022-08-23 |
| WO2017160808A9 (en) | 2018-07-05 |
| CN109069006A (zh) | 2018-12-21 |
| US20190038346A1 (en) | 2019-02-07 |
| AU2017235224A1 (en) | 2018-11-08 |
| EP3429462A4 (en) | 2019-11-20 |
| EP3429462A1 (en) | 2019-01-23 |
| US20220079669A1 (en) | 2022-03-17 |
| WO2017160808A8 (en) | 2018-09-27 |
| KR20180124070A (ko) | 2018-11-20 |
| IL261613A (en) | 2018-10-31 |
| US9993178B2 (en) | 2018-06-12 |
| US11389230B2 (en) | 2022-07-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6923549B2 (ja) | 灌注式焼灼のための改良されたシステム | |
| US11617618B2 (en) | Contact assessment between an ablation catheter and tissue | |
| JP6725178B2 (ja) | 高分解能電極アセンブリを使用するアブレーション装置、システムおよび方法 | |
| US11642166B2 (en) | Lesion formation assessment and display |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200225 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200225 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20210222 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210302 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210518 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210629 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210729 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6923549 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |