JP6232070B2 - 非水電解質二次電池及びその製造方法 - Google Patents
非水電解質二次電池及びその製造方法 Download PDFInfo
- Publication number
- JP6232070B2 JP6232070B2 JP2015535342A JP2015535342A JP6232070B2 JP 6232070 B2 JP6232070 B2 JP 6232070B2 JP 2015535342 A JP2015535342 A JP 2015535342A JP 2015535342 A JP2015535342 A JP 2015535342A JP 6232070 B2 JP6232070 B2 JP 6232070B2
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- secondary battery
- carbonate
- negative electrode
- electrolyte secondary
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000011255 nonaqueous electrolyte Substances 0.000 title claims description 136
- 238000004519 manufacturing process Methods 0.000 title claims description 25
- -1 cyclic carboxylic acid ester Chemical class 0.000 claims description 91
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 claims description 51
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 claims description 51
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 claims description 49
- 239000007789 gas Substances 0.000 claims description 49
- 229910052744 lithium Inorganic materials 0.000 claims description 44
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims description 41
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 39
- 229910001416 lithium ion Inorganic materials 0.000 claims description 38
- 229910001496 lithium tetrafluoroborate Inorganic materials 0.000 claims description 38
- 239000008151 electrolyte solution Substances 0.000 claims description 37
- 238000003860 storage Methods 0.000 claims description 37
- 238000007600 charging Methods 0.000 claims description 33
- 229910003002 lithium salt Inorganic materials 0.000 claims description 32
- 159000000002 lithium salts Chemical class 0.000 claims description 32
- 239000003125 aqueous solvent Substances 0.000 claims description 31
- 238000007789 sealing Methods 0.000 claims description 27
- 239000011149 active material Substances 0.000 claims description 26
- 239000010936 titanium Substances 0.000 claims description 24
- 239000002131 composite material Substances 0.000 claims description 21
- 150000005676 cyclic carbonates Chemical class 0.000 claims description 20
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 claims description 19
- 150000005678 chain carbonates Chemical class 0.000 claims description 17
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 claims description 13
- 125000004432 carbon atom Chemical group C* 0.000 claims description 12
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 claims description 11
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims description 11
- 150000001875 compounds Chemical class 0.000 claims description 10
- FSSPGSAQUIYDCN-UHFFFAOYSA-N 1,3-Propane sultone Chemical compound O=S1(=O)CCCO1 FSSPGSAQUIYDCN-UHFFFAOYSA-N 0.000 claims description 9
- 239000012298 atmosphere Substances 0.000 claims description 9
- 238000002844 melting Methods 0.000 claims description 9
- 230000008018 melting Effects 0.000 claims description 9
- WDXYVJKNSMILOQ-UHFFFAOYSA-N 1,3,2-dioxathiolane 2-oxide Chemical compound O=S1OCCO1 WDXYVJKNSMILOQ-UHFFFAOYSA-N 0.000 claims description 8
- GELKBWJHTRAYNV-UHFFFAOYSA-K lithium iron phosphate Chemical compound [Li+].[Fe+2].[O-]P([O-])([O-])=O GELKBWJHTRAYNV-UHFFFAOYSA-K 0.000 claims description 8
- 229910052596 spinel Inorganic materials 0.000 claims description 8
- 239000011029 spinel Substances 0.000 claims description 8
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 claims description 6
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 claims description 6
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 6
- 239000001257 hydrogen Substances 0.000 claims description 6
- 229910052739 hydrogen Inorganic materials 0.000 claims description 6
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 claims description 4
- PPMCFKAXXHZLMX-UHFFFAOYSA-N 1,3-dioxocan-2-one Chemical compound O=C1OCCCCCO1 PPMCFKAXXHZLMX-UHFFFAOYSA-N 0.000 claims description 4
- GAEKPEKOJKCEMS-UHFFFAOYSA-N gamma-valerolactone Chemical compound CC1CCC(=O)O1 GAEKPEKOJKCEMS-UHFFFAOYSA-N 0.000 claims description 4
- 229910000906 Bronze Inorganic materials 0.000 claims description 3
- 239000010974 bronze Substances 0.000 claims description 3
- KUNSUQLRTQLHQQ-UHFFFAOYSA-N copper tin Chemical compound [Cu].[Sn] KUNSUQLRTQLHQQ-UHFFFAOYSA-N 0.000 claims description 3
- 229910052719 titanium Inorganic materials 0.000 claims description 2
- 239000002904 solvent Substances 0.000 description 48
- 238000000034 method Methods 0.000 description 28
- 239000000203 mixture Substances 0.000 description 28
- 239000007773 negative electrode material Substances 0.000 description 26
- 239000007774 positive electrode material Substances 0.000 description 25
- 230000002829 reductive effect Effects 0.000 description 25
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 24
- 230000000052 comparative effect Effects 0.000 description 24
- 239000003792 electrolyte Substances 0.000 description 19
- 239000002033 PVDF binder Substances 0.000 description 16
- 239000011572 manganese Substances 0.000 description 16
- 238000005259 measurement Methods 0.000 description 16
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 16
- 239000002002 slurry Substances 0.000 description 16
- 239000000654 additive Substances 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 229910052751 metal Inorganic materials 0.000 description 13
- 239000002184 metal Substances 0.000 description 13
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 12
- 238000007599 discharging Methods 0.000 description 12
- 238000011156 evaluation Methods 0.000 description 12
- 239000011888 foil Substances 0.000 description 12
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 11
- 229910052782 aluminium Inorganic materials 0.000 description 11
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 11
- 239000006258 conductive agent Substances 0.000 description 11
- 239000005001 laminate film Substances 0.000 description 11
- 239000006230 acetylene black Substances 0.000 description 10
- 239000011230 binding agent Substances 0.000 description 10
- 238000001035 drying Methods 0.000 description 10
- 238000002156 mixing Methods 0.000 description 10
- 230000008569 process Effects 0.000 description 10
- 230000009467 reduction Effects 0.000 description 10
- 230000003750 conditioning effect Effects 0.000 description 9
- 238000002474 experimental method Methods 0.000 description 9
- 230000014759 maintenance of location Effects 0.000 description 9
- 239000000463 material Substances 0.000 description 9
- 229910052759 nickel Inorganic materials 0.000 description 9
- 238000012360 testing method Methods 0.000 description 8
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 7
- 230000007423 decrease Effects 0.000 description 7
- 229910052748 manganese Inorganic materials 0.000 description 7
- 239000011164 primary particle Substances 0.000 description 7
- IAHFWCOBPZCAEA-UHFFFAOYSA-N succinonitrile Chemical compound N#CCCC#N IAHFWCOBPZCAEA-UHFFFAOYSA-N 0.000 description 7
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 239000004743 Polypropylene Substances 0.000 description 6
- 230000000996 additive effect Effects 0.000 description 6
- 239000011248 coating agent Substances 0.000 description 6
- 238000000576 coating method Methods 0.000 description 6
- 229910017052 cobalt Inorganic materials 0.000 description 6
- 239000010941 cobalt Substances 0.000 description 6
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 6
- 125000004093 cyano group Chemical group *C#N 0.000 description 6
- 229920001155 polypropylene Polymers 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 229910013063 LiBF 4 Inorganic materials 0.000 description 5
- 238000012423 maintenance Methods 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 238000003825 pressing Methods 0.000 description 5
- 239000011163 secondary particle Substances 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 4
- 239000004698 Polyethylene Substances 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 239000003575 carbonaceous material Substances 0.000 description 4
- 229920000573 polyethylene Polymers 0.000 description 4
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 4
- 239000004810 polytetrafluoroethylene Substances 0.000 description 4
- 238000001179 sorption measurement Methods 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- SBLRHMKNNHXPHG-UHFFFAOYSA-N 4-fluoro-1,3-dioxolan-2-one Chemical compound FC1COC(=O)O1 SBLRHMKNNHXPHG-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 229910010707 LiFePO 4 Inorganic materials 0.000 description 3
- SOXUFMZTHZXOGC-UHFFFAOYSA-N [Li].[Mn].[Co].[Ni] Chemical compound [Li].[Mn].[Co].[Ni] SOXUFMZTHZXOGC-UHFFFAOYSA-N 0.000 description 3
- 239000001569 carbon dioxide Substances 0.000 description 3
- 229910002092 carbon dioxide Inorganic materials 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 238000005520 cutting process Methods 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 230000006866 deterioration Effects 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 229920005992 thermoplastic resin Polymers 0.000 description 3
- OZJPLYNZGCXSJM-UHFFFAOYSA-N 5-valerolactone Chemical compound O=C1CCCCO1 OZJPLYNZGCXSJM-UHFFFAOYSA-N 0.000 description 2
- 229910000838 Al alloy Inorganic materials 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 229910018871 CoO 2 Inorganic materials 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- 229910014422 LiNi1/3Mn1/3Co1/3O2 Inorganic materials 0.000 description 2
- 229910013870 LiPF 6 Inorganic materials 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 229910010413 TiO 2 Inorganic materials 0.000 description 2
- BTGRAWJCKBQKAO-UHFFFAOYSA-N adiponitrile Chemical compound N#CCCCCC#N BTGRAWJCKBQKAO-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000000010 aprotic solvent Substances 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- CKFRRHLHAJZIIN-UHFFFAOYSA-N cobalt lithium Chemical compound [Li].[Co] CKFRRHLHAJZIIN-UHFFFAOYSA-N 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- 230000005611 electricity Effects 0.000 description 2
- 239000007772 electrode material Substances 0.000 description 2
- 238000003411 electrode reaction Methods 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical compound CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- ZTOMUSMDRMJOTH-UHFFFAOYSA-N glutaronitrile Chemical compound N#CCCCC#N ZTOMUSMDRMJOTH-UHFFFAOYSA-N 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- 238000010030 laminating Methods 0.000 description 2
- 238000007561 laser diffraction method Methods 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- CUONGYYJJVDODC-UHFFFAOYSA-N malononitrile Chemical compound N#CCC#N CUONGYYJJVDODC-UHFFFAOYSA-N 0.000 description 2
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 description 2
- 239000002905 metal composite material Substances 0.000 description 2
- 239000012046 mixed solvent Substances 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 239000011356 non-aqueous organic solvent Substances 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 239000005020 polyethylene terephthalate Substances 0.000 description 2
- 239000002861 polymer material Substances 0.000 description 2
- YKYONYBAUNKHLG-UHFFFAOYSA-N propyl acetate Chemical compound CCCOC(C)=O YKYONYBAUNKHLG-UHFFFAOYSA-N 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 239000005060 rubber Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 238000001291 vacuum drying Methods 0.000 description 2
- 238000004804 winding Methods 0.000 description 2
- JYVXNLLUYHCIIH-UHFFFAOYSA-N (+/-)-mevalonolactone Natural products CC1(O)CCOC(=O)C1 JYVXNLLUYHCIIH-UHFFFAOYSA-N 0.000 description 1
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 1
- GEWWCWZGHNIUBW-UHFFFAOYSA-N 1-(4-nitrophenyl)propan-2-one Chemical compound CC(=O)CC1=CC=C([N+]([O-])=O)C=C1 GEWWCWZGHNIUBW-UHFFFAOYSA-N 0.000 description 1
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- 229920000049 Carbon (fiber) Polymers 0.000 description 1
- 229920008712 Copo Polymers 0.000 description 1
- QPLDLSVMHZLSFG-UHFFFAOYSA-N Copper oxide Chemical compound [Cu]=O QPLDLSVMHZLSFG-UHFFFAOYSA-N 0.000 description 1
- 239000005751 Copper oxide Substances 0.000 description 1
- 229910000881 Cu alloy Inorganic materials 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 1
- VXCUURYYWGCLIH-UHFFFAOYSA-N Dodecanenitrile Chemical compound CCCCCCCCCCCC#N VXCUURYYWGCLIH-UHFFFAOYSA-N 0.000 description 1
- 239000002000 Electrolyte additive Substances 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical compound CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 229920000265 Polyparaphenylene Polymers 0.000 description 1
- 241000156302 Porcine hemagglutinating encephalomyelitis virus Species 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- JYVXNLLUYHCIIH-ZCFIWIBFSA-N R-mevalonolactone, (-)- Chemical compound C[C@@]1(O)CCOC(=O)C1 JYVXNLLUYHCIIH-ZCFIWIBFSA-N 0.000 description 1
- 229920000297 Rayon Polymers 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- NXPZICSHDHGMGT-UHFFFAOYSA-N [Co].[Mn].[Li] Chemical compound [Co].[Mn].[Li] NXPZICSHDHGMGT-UHFFFAOYSA-N 0.000 description 1
- FKQOMXQAEKRXDM-UHFFFAOYSA-N [Li].[As] Chemical compound [Li].[As] FKQOMXQAEKRXDM-UHFFFAOYSA-N 0.000 description 1
- KLARSDUHONHPRF-UHFFFAOYSA-N [Li].[Mn] Chemical compound [Li].[Mn] KLARSDUHONHPRF-UHFFFAOYSA-N 0.000 description 1
- OHOIHSTWKIMQNC-UHFFFAOYSA-N [Li].[P]=O Chemical compound [Li].[P]=O OHOIHSTWKIMQNC-UHFFFAOYSA-N 0.000 description 1
- JBDIVCUIIIVNHR-UHFFFAOYSA-M [Li]F.OP(O)(O)=O Chemical compound [Li]F.OP(O)(O)=O JBDIVCUIIIVNHR-UHFFFAOYSA-M 0.000 description 1
- ZYXUQEDFWHDILZ-UHFFFAOYSA-N [Ni].[Mn].[Li] Chemical compound [Ni].[Mn].[Li] ZYXUQEDFWHDILZ-UHFFFAOYSA-N 0.000 description 1
- XHCLAFWTIXFWPH-UHFFFAOYSA-N [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] XHCLAFWTIXFWPH-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 239000002390 adhesive tape Substances 0.000 description 1
- 239000005456 alcohol based solvent Substances 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 229910021383 artificial graphite Inorganic materials 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 239000004917 carbon fiber Substances 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 239000002388 carbon-based active material Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 238000010277 constant-current charging Methods 0.000 description 1
- 229910000431 copper oxide Inorganic materials 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 230000006837 decompression Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000007872 degassing Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- QHGJSLXSVXVKHZ-UHFFFAOYSA-N dilithium;dioxido(dioxo)manganese Chemical class [Li+].[Li+].[O-][Mn]([O-])(=O)=O QHGJSLXSVXVKHZ-UHFFFAOYSA-N 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 150000004862 dioxolanes Chemical class 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 238000004146 energy storage Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003759 ester based solvent Substances 0.000 description 1
- 239000004210 ether based solvent Substances 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 238000005470 impregnation Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 239000011810 insulating material Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 1
- RUTXIHLAWFEWGM-UHFFFAOYSA-H iron(3+) sulfate Chemical compound [Fe+3].[Fe+3].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O RUTXIHLAWFEWGM-UHFFFAOYSA-H 0.000 description 1
- KQNPFQTWMSNSAP-UHFFFAOYSA-N isobutyric acid Chemical compound CC(C)C(O)=O KQNPFQTWMSNSAP-UHFFFAOYSA-N 0.000 description 1
- YWXYYJSYQOXTPL-SLPGGIOYSA-N isosorbide mononitrate Chemical compound [O-][N+](=O)O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 YWXYYJSYQOXTPL-SLPGGIOYSA-N 0.000 description 1
- 239000003273 ketjen black Substances 0.000 description 1
- 239000005453 ketone based solvent Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- PAZHGORSDKKUPI-UHFFFAOYSA-N lithium metasilicate Chemical compound [Li+].[Li+].[O-][Si]([O-])=O PAZHGORSDKKUPI-UHFFFAOYSA-N 0.000 description 1
- RSNHXDVSISOZOB-UHFFFAOYSA-N lithium nickel Chemical compound [Li].[Ni] RSNHXDVSISOZOB-UHFFFAOYSA-N 0.000 description 1
- 229910021441 lithium nickel cobalt complex oxide Inorganic materials 0.000 description 1
- MHCFAGZWMAWTNR-UHFFFAOYSA-M lithium perchlorate Chemical compound [Li+].[O-]Cl(=O)(=O)=O MHCFAGZWMAWTNR-UHFFFAOYSA-M 0.000 description 1
- 229910052912 lithium silicate Inorganic materials 0.000 description 1
- SWAIALBIBWIKKQ-UHFFFAOYSA-N lithium titanium Chemical compound [Li].[Ti] SWAIALBIBWIKKQ-UHFFFAOYSA-N 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 239000007769 metal material Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 1
- 229940017219 methyl propionate Drugs 0.000 description 1
- 229940057061 mevalonolactone Drugs 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229910021382 natural graphite Inorganic materials 0.000 description 1
- 229910000480 nickel oxide Inorganic materials 0.000 description 1
- 125000002560 nitrile group Chemical group 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- BTNXBLUGMAMSSH-UHFFFAOYSA-N octanedinitrile Chemical compound N#CCCCCCCC#N BTNXBLUGMAMSSH-UHFFFAOYSA-N 0.000 description 1
- 239000010450 olivine Substances 0.000 description 1
- 229910052609 olivine Inorganic materials 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- GHZRKQCHJFHJPX-UHFFFAOYSA-N oxacycloundecan-2-one Chemical compound O=C1CCCCCCCCCO1 GHZRKQCHJFHJPX-UHFFFAOYSA-N 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 238000006864 oxidative decomposition reaction Methods 0.000 description 1
- GNRSAWUEBMWBQH-UHFFFAOYSA-N oxonickel Chemical compound [Ni]=O GNRSAWUEBMWBQH-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Chemical group 0.000 description 1
- 229910052760 oxygen Chemical group 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000002964 rayon Substances 0.000 description 1
- 230000027756 respiratory electron transport chain Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 238000000790 scattering method Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 239000006104 solid solution Substances 0.000 description 1
- 239000002195 soluble material Substances 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical class O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 150000008053 sultones Chemical class 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- TXEYQDLBPFQVAA-UHFFFAOYSA-N tetrafluoromethane Chemical compound FC(F)(F)F TXEYQDLBPFQVAA-UHFFFAOYSA-N 0.000 description 1
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- VOVUARRWDCVURC-UHFFFAOYSA-N thiirane Chemical compound C1CS1 VOVUARRWDCVURC-UHFFFAOYSA-N 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- LLZRNZOLAXHGLL-UHFFFAOYSA-J titanic acid Chemical class O[Ti](O)(O)O LLZRNZOLAXHGLL-UHFFFAOYSA-J 0.000 description 1
- SZKKNEOUHLFYNA-UHFFFAOYSA-N undecanenitrile Chemical compound CCCCCCCCCCC#N SZKKNEOUHLFYNA-UHFFFAOYSA-N 0.000 description 1
- 229910001935 vanadium oxide Inorganic materials 0.000 description 1
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical compound O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/485—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of mixed oxides or hydroxides for inserting or intercalating light metals, e.g. LiTi2O4 or LiTi2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/5825—Oxygenated metallic salts or polyanionic structures, e.g. borates, phosphates, silicates, olivines
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/027—Negative electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0037—Mixture of solvents
- H01M2300/004—Three solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/483—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides for non-aqueous cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
Landscapes
- Chemical & Material Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- General Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Description
(a)エチレンカーボネート
(b)環状カルボン酸エステル又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
前記エチレンカーボネートが非水溶媒全体の5〜20体積%であり、
前記四フッ化硼酸リチウム濃度が非水電解液に対し0.05〜0.5モル/リットルである、非水電解質二次電池である。
(a)エチレンカーボネート
(b)環状カルボン酸エステル、又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、前記エチレンカーボネートが非水溶媒全体の5〜20体積%であり、前記四フッ化硼酸リチウム濃度が非水電解液に対し0.05〜0.5モル/リットルである、非水電解質二次電池の製造方法である。
前記仮封止二次電池の負極電位を0.8Vより高く1.4V以下の電位(対Li/Li+)に調整し、50℃以上80℃未満の雰囲気中で貯蔵する工程と、
前記仮封止二次電池を開封して内部の気体を排出し、次いで、前記外装部材を本封止する工程と
を含む、非水電解質二次電池の製造方法であって、
前記非水溶媒が、下記(a)、(b)及び(c)の3種を少なくとも含み、
(a)エチレンカーボネート
(b)環状カルボン酸エステル、又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
前記エチレンカーボネートが非水溶媒全体の5〜20体積%であり、
前記四フッ化硼酸リチウム濃度が非水電解液に対し0.05〜0.5モル/リットルである、
非水電解質二次電池の製造方法である。
(a)エチレンカーボネート
(b)環状カルボン酸エステル、又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
(a)エチレンカーボネートが非水溶媒全体の5〜20体積%であり、
四フッ化硼酸リチウム濃度が非水電解液に対し0.05〜0.5モル/リットルである。このようにして本発明の非水電解質二次電池を製造することができる。詳細は後述のコンディショニング工程を含む非水電解質二次電池の製造方法の項で合わせて説明する。
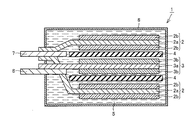
第1の工程において、仮封止二次電池を作製する。まず、外装部材内に電極群を収容する。電極群は正極、負極、及びセパレータから構成される。具体的には、例えば、正極、セパレータ、負極、及びセパレータを順に積層し、この積層体を扁平形状に捲回することにより扁平型の電極群が形成される。別の方法として、例えば、正極と負極とを、セパレータを介して一組又は複数組積層して電極群を形成してもよい。必要に応じて、該電極群を絶縁テープで捲回して固定してもよい。電極群の形成後及び/又は形成前に電極群や各構成部材を加熱及び/又は真空乾燥して吸着水分を低減させる工程を追加してもよい。
次いで、第2の工程を行う。仮封止二次電池の正極端子と負極端子の間に電流を流し、負極電位が0.8Vより高く1.4V以下の電位(対Li/Li+)の範囲になるように初充電する。負極活物質のリチウムイオン吸蔵電位よりも負極電位が350mV以上低くなるように初充電するとより好ましい。
次に、外装部材の一部を切断するか、又は穴を開け、第2の工程において外装部材の中に滞留した気体を外部に排出する。例えば、仮封止部の内側であってヒートシールされていない部分である開封部の何れかの位置においてラミネートフィルムを切断することにより、外装部材を開封することができる。開封は減圧下で行うことが好ましく、また、不活性雰囲気下又は乾燥空気中で行うことが好ましい。
(実施例1)
<正極の作製>
正極活物質としてリン酸鉄リチウム(LiFePO4)粉末、アセチレンブラック、及びポリフッ化ビニリデン(PVdF)のN−メチルピロリドン(NMP)溶液を、質量比がLiFePO4:アセチレンブラック:PVdF=83:10:7となるように混合し、NMPを加えて正極合剤スラリーを調製した。この正極合剤スラリーを厚さ20μmのアルミニウム箔からなる集電体に片面あたりの活物質量が9.5mg/cm2となるように両面に塗布した。塗布後に、乾燥、プレスして合剤密度が1.9g/cm3になるように正極を作製した。その後130℃で8時間減圧乾燥を行った。
負極活物質としてスピネル構造を有するチタン酸リチウム(Li4Ti5O12、リチウム吸蔵電位=1.55V対Li/Li+、比表面積=10.9m2/g、平均二次粒子径=7.4μm、平均一次粒径=0.8μm)の粉末、アセチレンブラック、及びポリフッ化ビニリデン(PVdF)のN−メチルピロリドン(NMP)溶液を、質量比がLi4Ti5O12:アセチレンブラック:PVdF=87.0:4.3:8.7となるように混合し、NMPを加えて負極合剤スラリーを調製した。このスラリーを厚さが20μmのアルミ箔からなる集電体に片面あたりの活物質量が8.0mg/cm2となるように両面に塗布した。塗布後、乾燥、プレスして合剤密度が1.8〜2.0g/cm3になるように負極を作製した。その後130℃で8時間減圧乾燥を行った。活物質の平均二次粒子径はレーザー回折法(堀場製作所製 レーザー回折/散乱式粒子径分布測定装置LA‐950)にて測定し、 一次粒子は電子顕微鏡法(日立ハイテクノロジーズ製走査電子顕微鏡 S‐4800、100個の平均)で求めた。比表面積については、比表面積測定装置(モノソーブ:Quantachrome Instruments社製)を用いて、窒素吸着によるBET一点法にて測定した。
シート状正電極と、厚さ50μmのレーヨンからなるセパレータと、上記で作製したシート状負電極と、セパレータとを、この順序で交互に積層して絶縁テープで固定した。固定後に正極、及び負極の集電体に厚さ20μmのアルミニウム箔からなるリードタブを溶接した。得られた電極群は幅が36mmで、厚さが3.9mmの偏平状電極群だった。
溶媒(a)エチレンカーボネート(EC)と溶媒(b)プロピレンカーボネート(PC)と溶媒(c)メチルエチルカーボネート(MEC)の混合溶媒(混合体積比5:35:60)に、リチウム塩として六フッ化リン酸リチウム(LiPF6)を0.5モル/リットル、四フッ化硼酸リチウム(LiBF4)を0.2モル/リットルとなるように溶解した溶液を調製した。これを電解液Aとした。
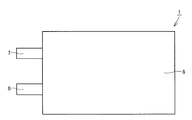
第1の工程として、ラミネートフィルムからなる外装部材に、上記で作製した電極群を、その正負極端子が一辺から延出した状態で収容し、80℃で8時間真空乾燥した。該外装部材中に非水電解液Aを注入し、電極群に含浸させた。次いで、ラミネートフィルムの開口部をヒートシールにより仮封止して密封し、仮封止二次電池を得た。
第2の工程として、仮封止二次電池を2枚の押し板で挟みクリップで固定することで加圧をして3時間放置後、その負極端子と正極端子の間に電流を流し0.25C(115mA)で負極電位が1.0Vになるまで、常温下(25℃)で充電を行った。このときのセル電圧は2.5Vであった。
非水電解質として、表1、2に記載の非水電解液B〜AA、AB〜ASを用いた以外は、実施例1と同様な方法にて実施例2〜27、比較例1〜18の非水電解質二次電池を製造した。表1中、六フッ化リン酸リチウム(LiPF6)の電解液中の濃度をxモル/リットル、四フッ化硼酸リチウム(LiBF4)の濃度をyモル/リットル、溶媒(a)エチレンカーボネート(EC)の溶媒に占める濃度をa体積%、溶媒(b)プロピレンカーボネート(PC)の溶媒に占める濃度をb体積%、溶媒(c)メチルエチルカーボネート(MEC)の溶媒に占める濃度をc体積%で表す。a+b+c=100体積%となるようにした。実施例12では、溶媒(b)としてプロピレンカーボネートに代えてγ−ブチロラクトンをb体積%用い、実施例13では、溶媒(c)としてメチルエチルカーボネートに代えてジエチルカーボネートをc体積%用いた。なお、添加剤として、実施例21にはビニレンカーボネート(VC)、実施例22にはスクシノニトリル(SCN)、実施例23にはエチレンサルファイド(ES)、実施例24には1,3−プロパンスルトン(PS)をそれぞれ電解液に対して2質量%添加した。
上記のようにして作製した実施例1〜27及び比較例1〜18の非水電解質二次電池について、以下の測定を行った。
非水電解質二次電池を、温度25℃の恒温槽に保存して温度を安定化させた後、一度SOC0%まで放電する(1C、終止電圧1.0V)。30分休止させた後、1Cで2.5Vまで定電流充電し、30分休止させた後、1Cで1.0Vまで放電したときの容量を放電容量とする。この条件で、コンディショニング工程後に放電容量測定を行ったものを初期容量とした。
非水電解質二次電池を、温度55℃の恒温槽に投入し、前記容量測定と同じ充放電条件(充電:1C−終止電圧2.5V、休止:30分、放電:1C−終止電圧1.0V、休止:30分)で500サイクルの充放電を行った。500サイクル後に再度前記放電容量測定を行ってサイクル後容量を求め、放電容量維持率(=サイクル後容量/初期容量)を算出した。結果を表3、4に示す。
非水電解質二次電池を500ミリリットルの水の入ったメスシリンダー内にいれて、電池の体積を測定した。前記初期容量測定後と前記高温サイクル試験500サイクル後に電池体積を測定し、その体積変化量をガス発生量とした。その結果も合わせて表3、4に示す。
(実施例28)
<正極の作製>
正極活物質としてリチウム・ニッケル・マンガン・コバルト複合酸化物(LiNi1/3Mn1/3Co1/3O2)粉末、アセチレンブラック、及びポリフッ化ビニリデン(PVdF)のN−メチルピロリドン(NMP)溶液を、質量比がLiNi1/3Mn1/3Co1/3O2:アセチレンブラック:PVdF=92:4:4となるように混合し、NMPを加えて正極合剤スラリーを調製した。この正極合剤スラリーを厚さ20μmのアルミニウム箔からなる集電体に片面あたりの活物質量が9.8mg/cm2となるように両面に塗布した。塗布後に、乾燥、プレスして合剤密度が2.5g/cm3になるように正極を作製した。その後130℃で8時間減圧乾燥を行った。
電解液AOを使用したこと以外は、実施例28と同様の方法にて比較例19の非水電解質二次電池を作製した。
電解液APを使用したこと以外は、実施例28と同様の方法にて比較例20の非水電解質二次電池を作製した。
上記のようにして作製した実施例28、比較例19,20の非水電解質二次電池について、以下の測定を行った。
非水電解質二次電池を、温度25℃の恒温槽に保存して温度を安定化させた後、一度SOC0%まで放電する(1C、終止電圧1.4V)。30分休止させた後、1Cで3.1Vまで定電流充電し、30分休止させた後、1Cで1.4Vまで放電したときの容量を放電容量とする。この条件でコンディショニング後に放電容量測定を行ったものを初期容量とした。
非水電解質二次電池を、温度55℃の恒温槽に投入し、前記容量測定と同じ充放電条件(充電:1C−終止電圧3.1V、休止:30分、放電:1C−終止電圧1.4V、休止:30分)で500サイクルの充放電を行った。500サイクル後に再度前記放電容量測定を行ってサイクル後容量を求め、放電容量維持率(=サイクル後容量/初期容量)を算出した。結果を表5に示す。
実験1と同様の方法で測定を行った。結果を表5に合わせて示す。
(実施例29)
<作用極の作製>
活物質として、実験1で用いたものと同じスピネル構造を有するチタン酸リチウムの粉末、導電剤としてのアセチレンブラックを混合した後に、ポリフッ化ビニリデン(PVdF)のN−メチルピロリドン(NMP)溶液を加えて混合し、NMPを加えたのち、撹拌・脱泡装置(あわとり練太郎:(株)シンキー社製)で、2000rpmで3分間撹拌し、2200rpmで30秒間脱泡を2回行った。その後、2000rpmで5分間撹拌し、2200rpmで30秒間脱泡を1回行い、合剤スラリーを調製した。質量比はLi4Ti5O12:アセチレンブラック:PVdF=89.3:4.5:6.2である。次に、得られた合剤スラリーを、厚さが20μmのアルミ箔からなる集電体に、片面当りの活物質量が3.0mg/cm2となるように片面に塗布した。乾燥後、合剤密度が1.8〜2.0g/cm3になるようにプレスし、電極材料を直径12mmの円形に切り出して作用極を作製した。その後130℃で8時間減圧乾燥を行った。
表1の電解液Aを使用した。
この作用極を露点−70℃以下のグローブボックス中で、密閉可能なコイン型評価用セルに組み込んだ。評価用セルには、材質がステンレス製(SUS316)で外径20mm、高さ3.2mmのものを用いた。対極(兼参照極)には厚み0.5mmの金属リチウム箔を直径12mmの円形に成形したものを用いた。上記で作製した作用極は評価用セルの下部缶に置き、その上に、厚さ20μmのポリプロピレン製の微多孔膜と、前記金属リチウム箔とを、この順序で、作用極の合剤層がセパレータを介して金属リチウム箔に向き合うように積層した後、その上から非水電解液を滴下し、電極群に非水電解質を含浸させた。さらにその上に厚み調整用の0.5mm厚スペーサー及びスプリング(いずれもSUS316製)をのせ、ポリプロピレン製ガスケットのついた上部缶を被せて外周縁部をかしめて密封し、評価セルを組み立てた。設計容量は、0.497mAhだった。
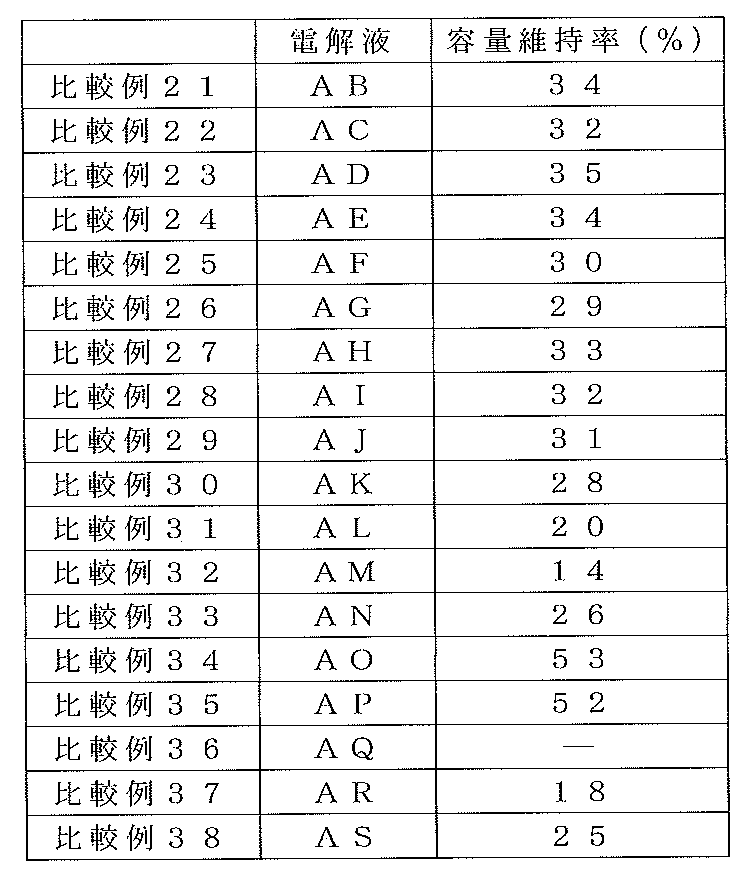
非水電解質として、電解液Aに代えて表1、2に記載の非水電解液B〜AA、AB〜ASを用いた以外は、実施例29と同様な方法にて実施例30〜55、比較例21〜38の評価セルを製造した。
上記手順で作製した実施例29〜55及び比較例21〜38の評価セルに対し、まず、25℃での放電容量を求める。具体的には、電流値0.5C(0.248mA)で1Vまで定電流充電し、30分休止後、0.5C(0.248mA)で3Vまで定電流放電した。この時の放電容量を25℃容量とした。次に、測定温度−40℃での放電容量を求める。評価セルを−40℃の恒温槽に投入し6時間保持したあとに、0.5C(0.248mA)で1Vまで定電流充電し、30分休止後、0.5Cで3Vまで定電流放電した。この時の放電容量を−40℃容量とした。そして、容量維持率=−40℃容量/25℃容量を算出した。結果を表6、7に示す。
Claims (13)
- 正極と、
リチウムイオン吸蔵電位が1.2V(対Li/Li+)以上のチタン酸化物を含有する活物質を含む負極と、
リチウム塩とこれを溶解する非水溶媒を含有してなる非水電解液と、
を備えた非水電解質二次電池であって、
前記非水溶媒が、下記(a)、(b)及び(c)の3種を少なくとも含み、
(a)エチレンカーボネート
(b)環状カルボン酸エステル又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
前記エチレンカーボネートが前記非水溶媒全体の5〜20体積%であり、前記四フッ化硼酸リチウムの濃度が前記非水電解液に対し0.05〜0.5モル/リットルであり、正極実電気容量をP、負極実電気容量をNとしたとき、正負極容量比R=N/Pが0.7≦R<1.0である、非水電解質二次電池。 - 前記非水溶媒中の前記(a)の割合をa(体積%)、前記(b)の割合をb(体積%)とした際、前記a及び前記bがb≧aを満たす請求項1に記載の非水電解質二次電池。
- 前記非水溶媒中の前記(c)の割合をc(体積%)とした際、前記a、前記b及び前記cが(a+b)≦cを満たす請求項1又は2に記載の非水電解質二次電池。
- 前記非水電解液中の六フッ化リン酸リチウムのモル濃度が、0.5〜1.4モル/リットルである請求項1〜3のいずれかに記載の非水電解質二次電池。
- 前記(b)は、融点が−30℃以下で比誘電率が30以上の環状カーボネート又は環状カルボン酸エステルを含み、前 記(c)は、融点が−40℃以下の鎖状カーボネートを含む請求項1〜4のいずれかに記載 の非水電解質二次電池。
- 前記(b)は、プロピレンカーボネート、ブチレンカーボネート、ペンチレンカーボネート、γ−ブチロラクトン及びγ−バレロラクトンから選ばれる少なくとも1種を含み、前記(c)は、エチルメチルカーボネート及びジエチルカーボネートから選ばれる少なくとも1種を含む請求項1〜5のいずれかに記載の非水電解質二次電池。
- 前記チタン酸化物は、スピネル構造のチタン酸リチウム、ラムスデライト構造のチタン酸リチウム、単斜晶系チタン酸化合物、単斜晶系チタン酸化物及びチタン酸水素リチウムから選ばれる少なくとも1種である請求項1〜6のいずれかに記載の非水電解質二次電池。
- 前記チタン酸化物は、Li4+xTi5O12、Li2+xTi3O7、一般式H2TinO2n+1で表されるチタン酸化合物、ブロンズ型酸化チタンから選ばれる少なくとも1種である請求項1〜7のいずれかに記載の非水電解質二次電池。(xは0≦x≦3を満たす実数であり、nは4以上の偶数である。)
- 前記非水電解液が、ジニトリル化合物、ビニレンカーボネート、エチレンサルファイト及び1,3−プロパンスルトンから選択される少なくとも1種をさらに含む請求項1〜8のいずれかに記載の非水電解質二次電池。
- 前記正極の活物質がリン酸鉄リチウムである請求項1〜9のいずれかに記載の非水電解質二次電池。
- 正極と、
リチウムイオン吸蔵電位が1.2V(対Li/Li+)以上のチタン酸化物を含有する活物質を含む負極と、
リチウム塩とこれを溶解する非水溶媒を含有してなる非水電解液と、
を外装部材に収容し、外装部材の開口部を封止して封止二次電池を得る工程と、
前記封止二次電池を充電する工程と、
を含む、非水電解質二次電池の製造方法であって、
前記非水溶媒が、下記(a)、(b)及び(c)の3種を少なくとも含み、
(a)エチレンカーボネート
(b)環状カルボン酸エステル、又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
前記エチレンカーボネートが前記非水溶媒全体の5〜20体積%であり、
前記四フッ化硼酸リチウム濃度が前記非水電解液に対し0.05〜0.5モル/リットルであり、正極実電気容量をP、負極実電気容量をNとしたとき、正負極容量比R=N/Pが0.7≦R<1.0である、
非水電解質二次電池の製造方法。 - 正極と、
リチウムイオン吸蔵電位が1.2V(対Li/Li+)以上のチタン酸化物を含有する活物質を含む負極と、
リチウム塩とこれを溶解する非水溶媒を含有してなる非水電解液と、
を外装部材に収容し、外装部材の開口部を仮封止して仮封止二次電池を得る工程と、
前記仮封止二次電池の負極電位を0.8Vより高く1.4V以下の電位(対Li/Li+)で、かつ、チタン複合酸化物のリチウムイオン吸蔵電位よりも350mV以上低い電位に調整し、50℃以上80℃未満の雰囲気中で貯蔵する工程と、
前記仮封止二次電池を開封して内部の気体を排出し、次いで、前記外装部材を本封止する工程と
を含み、正極実電気容量をP、負極実電気容量をNとしたとき、正負極容量比R=N/P
が0.7≦R<1.0とする、非水電解質二次電池の製造方法であって、
前記非水溶媒が、下記(a)、(b)及び(c)の3種を少なくとも含み、
(a)エチレンカーボネート
(b)環状カルボン酸エステル、又は炭素数が4以上の環状カーボネート
(c)鎖状カーボネート
前記リチウム塩が、六フッ化リン酸リチウム及び四フッ化硼酸リチウムを少なくとも含み、
前記エチレンカーボネートが前記非水溶媒全体の5〜20体積%であり、
前記四フッ化硼酸リチウム濃度が前記非水電解液に対し0.05〜0.5モル/リットルである、
非水電解質二次電池の製造方法。 - 前記貯蔵を開回路で行う請求項12に記載の非水電解質二次電池の製造方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013183742 | 2013-09-05 | ||
| JP2013183742 | 2013-09-05 | ||
| PCT/JP2014/063485 WO2015033620A1 (ja) | 2013-09-05 | 2014-05-21 | 非水電解質二次電池及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2015033620A1 JPWO2015033620A1 (ja) | 2017-03-02 |
| JP6232070B2 true JP6232070B2 (ja) | 2017-11-15 |
Family
ID=52628111
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015535342A Expired - Fee Related JP6232070B2 (ja) | 2013-09-05 | 2014-05-21 | 非水電解質二次電池及びその製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20160204432A1 (ja) |
| JP (1) | JP6232070B2 (ja) |
| KR (1) | KR20160054472A (ja) |
| CN (1) | CN105493332A (ja) |
| TW (1) | TWI616012B (ja) |
| WO (1) | WO2015033620A1 (ja) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20160181603A1 (en) * | 2014-09-12 | 2016-06-23 | Johnson Controls Technology Company | Systems and methods for lithium titanate oxide (lto) anode electrodes for lithium ion battery cells |
| EP3231024A4 (en) * | 2014-12-12 | 2018-08-08 | Pellion Technologies Inc. | Electrochemical cell and method of making the same |
| JPWO2016136212A1 (ja) * | 2015-02-27 | 2017-12-07 | 三洋電機株式会社 | 非水電解質二次電池 |
| WO2016188884A1 (en) * | 2015-05-27 | 2016-12-01 | Basf Se | Electrochemical cells using combinations of nitrile compounds as additives |
| KR102335587B1 (ko) * | 2016-03-29 | 2021-12-06 | 도레이 카부시키가이샤 | 이차전지용 세퍼레이터 및 이차전지 |
| MX2019001629A (es) | 2016-08-12 | 2019-09-16 | Pellion Tech Inc | Aditivo que contiene electrolitos para baterías recargables de ánodo de metal de alta eficiencia energética. |
| JP6776439B2 (ja) * | 2017-03-23 | 2020-10-28 | 株式会社東芝 | 非水電解質電池、電池パック及び電池システム |
| US11171362B2 (en) * | 2017-09-12 | 2021-11-09 | Sila Nanotechnologies, Inc. | Electrolyte for a metal-ion battery cell with high-capacity, micron-scale, volume-changing anode particles |
| CA3114636A1 (en) | 2018-09-27 | 2020-04-02 | Murata Manufacturing Co., Ltd. | Lithium-ion secondary battery |
| DE112020006663T5 (de) | 2020-03-31 | 2022-11-24 | Murata Manufacturing Co., Ltd. | Sekundärbatterie |
| KR20220100308A (ko) * | 2021-01-08 | 2022-07-15 | 삼성전자주식회사 | 유기전해액 및 이를 포함하는 이차전지 |
| JP7434209B2 (ja) * | 2021-04-27 | 2024-02-20 | 株式会社東芝 | 二次電池の製造方法、及び二次電池 |
| JP7504832B2 (ja) * | 2021-04-27 | 2024-06-24 | 株式会社東芝 | 二次電池の製造方法、及び二次電池 |
| CN114361446A (zh) * | 2021-12-29 | 2022-04-15 | 常州锂源新能源科技有限公司 | 一种磷酸铁锂正极材料低温性能的测试方法 |
| TWI904577B (zh) * | 2023-02-22 | 2025-11-11 | 中央研究院 | 鋰金屬電池用電解液、其製備方法以及包含其的鋰金屬電池 |
| CN117083745B (zh) * | 2023-06-01 | 2026-01-27 | 宁德时代新能源科技股份有限公司 | 锂二次电池用电解液、二次电池和用电设备 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH09213329A (ja) * | 1996-01-30 | 1997-08-15 | Fuji Photo Film Co Ltd | 非水二次電池 |
| KR100444410B1 (ko) * | 2001-01-29 | 2004-08-16 | 마쯔시다덴기산교 가부시키가이샤 | 비수전해액이차전지 |
| JP4184335B2 (ja) * | 2001-01-29 | 2008-11-19 | 松下電器産業株式会社 | 非水電解液 |
| JP2007172986A (ja) * | 2005-12-21 | 2007-07-05 | Toyota Central Res & Dev Lab Inc | 水系リチウム二次電池 |
| TWI430304B (zh) * | 2007-01-19 | 2014-03-11 | Stella Chemifa Corp | Storage element |
| CN101657416B (zh) * | 2007-04-20 | 2014-03-12 | 宇部兴产株式会社 | 锂二次电池用非水电解液及使用其的锂二次电池 |
| WO2008157363A1 (en) * | 2007-06-13 | 2008-12-24 | Altairnano, Inc. | Charging a lithium ion battery |
| JP5232631B2 (ja) * | 2008-12-25 | 2013-07-10 | 株式会社東芝 | 非水電解質電池 |
| JP5763889B2 (ja) * | 2010-03-16 | 2015-08-12 | パナソニック株式会社 | 非水電解質二次電池の充放電方法 |
| CN101867064A (zh) * | 2010-06-11 | 2010-10-20 | 西安瑟福能源科技有限公司 | 兼顾高温性能的低温型锂离子电池电解液及锂离子电池 |
| CN101958428B (zh) * | 2010-09-15 | 2013-11-13 | 东莞新能源科技有限公司 | 一种锂离子二次电池 |
| CN103069620A (zh) * | 2010-10-01 | 2013-04-24 | 株式会社东芝 | 非水电解质二次电池及其制造方法 |
| JP2012256502A (ja) * | 2011-06-08 | 2012-12-27 | Sony Corp | 非水電解質および非水電解質電池、ならびに非水電解質電池を用いた電池パック、電子機器、電動車両、蓄電装置および電力システム |
| JP5917049B2 (ja) * | 2011-08-26 | 2016-05-11 | 株式会社東芝 | 非水電解質二次電池及びその製造方法 |
| CN103208654A (zh) * | 2013-03-28 | 2013-07-17 | 东莞新能源科技有限公司 | 软包装锂离子二次电池用电解液及包含该电解液的电池 |
-
2014
- 2014-05-21 CN CN201480047147.4A patent/CN105493332A/zh active Pending
- 2014-05-21 JP JP2015535342A patent/JP6232070B2/ja not_active Expired - Fee Related
- 2014-05-21 WO PCT/JP2014/063485 patent/WO2015033620A1/ja not_active Ceased
- 2014-05-21 KR KR1020167005807A patent/KR20160054472A/ko not_active Withdrawn
- 2014-05-21 US US14/912,806 patent/US20160204432A1/en not_active Abandoned
- 2014-05-21 TW TW103117739A patent/TWI616012B/zh not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| US20160204432A1 (en) | 2016-07-14 |
| CN105493332A (zh) | 2016-04-13 |
| TW201511388A (zh) | 2015-03-16 |
| JPWO2015033620A1 (ja) | 2017-03-02 |
| KR20160054472A (ko) | 2016-05-16 |
| TWI616012B (zh) | 2018-02-21 |
| WO2015033620A1 (ja) | 2015-03-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6232070B2 (ja) | 非水電解質二次電池及びその製造方法 | |
| JP6447502B2 (ja) | 非水電解質二次電池及びその製造方法 | |
| JP6215318B2 (ja) | 非水電解質二次電池の製造方法 | |
| CN107431247B (zh) | 非水系电解液和非水系二次电池 | |
| EP2840639B1 (en) | Electrolyte solution for lithium secondary battery and lithium secondary battery using the same | |
| JP2004342607A (ja) | リチウム電池用非水電解液およびその製造方法ならびにリチウムイオン二次電池 | |
| JP2015015087A (ja) | 非水電解質二次電池の製造方法 | |
| CN105051966A (zh) | 非水电解质二次电池 | |
| JP2015018713A (ja) | 非水電解液、及び該非水電解液を用いたリチウムイオン二次電池 | |
| CN104868168A (zh) | 非水电解质二次电池 | |
| WO2015146024A1 (ja) | 非水電解質二次電池 | |
| WO2011117992A1 (ja) | 電池用活物質および電池 | |
| WO2013183769A1 (ja) | リチウムイオン二次電池 | |
| JP2016103325A (ja) | チタン酸化物及びそれを活物質として用いた負極並びに非水電解質二次電池 | |
| JP2016103326A (ja) | 非水電解液二次電池及びその製造方法 | |
| KR20170084894A (ko) | 리튬이차전지용 음극활물질, 그의 제조방법 및 그를 포함하는 리튬이차전지 | |
| CN105849951B (zh) | 非水电解质二次电池 | |
| JP2016103324A (ja) | 非水電解質二次電池 | |
| WO2022203048A1 (ja) | 非水系電解液及びそれを用いた非水系電解液電池 | |
| WO2022196375A1 (ja) | 非水系二次電池、及び非水系二次電池の製造方法 | |
| JP2014029782A (ja) | 非水電解質二次電池用正極活物質、その正極活物質を用いた非水電解質二次電池用正極、及びその正極を用いた非水電解質二次電池 | |
| JP2023130894A (ja) | 非水系電解液二次電池 | |
| JP2012018916A (ja) | 非水電解質および非水電解質電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161213 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20161213 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170829 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171017 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171020 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6232070 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |