JP6013328B2 - 標的粒子の定量方法 - Google Patents
標的粒子の定量方法 Download PDFInfo
- Publication number
- JP6013328B2 JP6013328B2 JP2013511024A JP2013511024A JP6013328B2 JP 6013328 B2 JP6013328 B2 JP 6013328B2 JP 2013511024 A JP2013511024 A JP 2013511024A JP 2013511024 A JP2013511024 A JP 2013511024A JP 6013328 B2 JP6013328 B2 JP 6013328B2
- Authority
- JP
- Japan
- Prior art keywords
- sample solution
- light
- probe
- target
- particles
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/76—Chemiluminescence; Bioluminescence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
- C12Q1/6818—Hybridisation assays characterised by the detection means involving interaction of two or more labels, e.g. resonant energy transfer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6456—Spatial resolved fluorescence measurements; Imaging
- G01N21/6458—Fluorescence microscopy
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N2021/6417—Spectrofluorimetric devices
- G01N2021/6419—Excitation at two or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N2021/6417—Spectrofluorimetric devices
- G01N2021/6421—Measuring at two or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6432—Quenching
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
- G01N2021/6441—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks with two or more labels
Description
本願は、2011年04月18日に、日本に出願された特願2011−092168号に基づき優先権を主張し、その内容をここに援用する。
ここで、走査分子計数法は、特願2010−044714に於いて、本願出願人により提案されている新規な光分析技術である。
本発明の第2の態様によれば、前記第1の態様において、前記移動工程に於いて、前記光検出領域の前記位置を所定の速度にて移動することが好ましい。
本発明の第4の態様によれば、前記第1の態様から前記第3の態様のいずれか1態様において、前記検出工程に於いて、検出された時系列の前記光信号の形状に基づいて、前記発光プローブ、又は発光プローブと結合した前記標的粒子が前記光検出領域に入ったことを検出することが好ましい。
本発明の第5の態様によれば、前記第1の態様から前記第4の態様のいずれか1態様において、前記標的粒子が核酸であり;前記発光プローブが、前記標的粒子と特異的にハイブリダイズし、且つ蛍光エネルギー移動現象におけるエネルギー・ドナーと成る蛍光物質及びエネルギー・アクセプターと成る物質の少なくとも一つが結合している1本鎖核酸であることが好ましい。
本発明の第7の態様によれば、前記第6の態様の態様において、(e)前記工程(d)において回収された前記複合体から前記発光プローブを解離させた後、遊離の発光プローブと前記標的粒子とを、互いに分離して回収する工程を有することが好ましい。
上記の標的粒子の定量方法において、蛍光強度のゆらぎを算出するといった統計的処理が実行されない。したがって、上記の標的粒子の定量方法により、解析対象である標的粒子が試料中に極微量にしか存在していない場合であっても、試料中の標的粒子の濃度を求めることができる。さらに、上記の標的粒子の定量方法では、標的粒子の濃度既知の標準試料から作成された検量線を用いることにより、計数された標的粒子の数から、試料溶液中の標的粒子の濃度をより簡便に求めることができる。
実施の形態において、典型的には、所定の閾値より大きい強度を有する光信号が検出されたときに、発光プローブが光検出領域に入ったと検出されるようになっていてよい。ここで、所定の閾値とは、予め設定された光強度の値であり、実験的に又は分析の目的に適合するよう設定された値である。
例えば、レーザ走査型光学顕微鏡において採用されているガルバノミラーを用いて光路を変更して光検出領域の位置が変更されるようになっていてよい。光検出領域の位置の移動軌跡は、任意に設定されてよく、例えば、円形、楕円形、矩形、直線及び曲線のうちから選択可能であってよい。
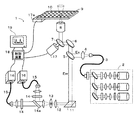
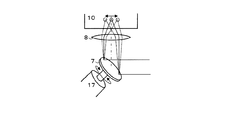
走査分子計数法は、基本的な構成に於いて、図1Aに模式的に例示されているように、FCS、FIDA等が実行可能な共焦点顕微鏡の光学系と光検出器とを組み合わせてなる光分析装置により実現可能である。図1Aに示すように、光分析装置1は、光学系2〜17と、光学系の各部の作動を制御すると共にデータを取得し解析するためのコンピュータ18とを備えている。光分析装置1の光学系は、通常の共焦点顕微鏡の光学系と同様であってよい。光源2から放射されシングルモードファイバー3内を伝播したレーザ光(Ex)が、ファイバーの出射端に於いて固有のNAにて決まった角度にて発散する光となって放射される。放射された光は、コリメーター4によって平行光となり、ダイクロイックミラー5、反射ミラー6、7にて反射され、対物レンズ8へ入射される。対物レンズ8の上方には、典型的には、1〜数十μLの試料溶液が分注される試料容器又はウェル10が配列されたマイクロプレート9が配置されている。対物レンズ8から出射したレーザ光は、試料容器又はウェル10内の試料溶液中で焦点を結び、光強度の強い領域(励起領域)が形成される。試料溶液中には、観測対象物である粒子と、この粒子と結合する発光プローブ、典型的には、蛍光色素等の発光標識が付加された分子が分散又は溶解されている。発光プローブと結合又は会合した粒子(実施の態様によっては、粒子と一旦結合した後に粒子から解離した発光プローブ)が励起領域に進入すると、その間、発光プローブが励起され光が放出される。放出された光(Em)は、対物レンズ8、ダイクロイックミラー5を通過し、ミラー11にて反射してコンデンサーレンズ12にて集光される。集光された光は、ピンホール13を通過し、バリアフィルター14を透過して(ここで、特定の波長帯域の光成分のみが選択される)、マルチモードファイバー15に導入されて、光検出器(光検出部)16に到達する。そして、光検出器16において、時系列の電気信号に変換された後、コンピュータ18へ入力され、後述する光分析のための処理が為される。当業者に於いて知られているように、上記の構成に於いて、ピンホール13は、対物レンズ8の焦点位置と共役の位置に配置されている。これにより、図1Bに模式的に示されているように、レーザ光の焦点領域、即ち、励起領域内から発せられた光のみがピンホール13を通過し、励起領域以外からの光は遮断される。図1Bに例示されたレーザ光の焦点領域は、通常、1〜10fL程度の実効体積を有する本光分析装置に於ける光検出領域であり(典型的には、光強度が領域の中心を頂点とするガウス型分布又はローレンツ型分布となる。実効体積は、光強度が1/e2 となる面を境界とする略楕円球体の体積である)、コンフォーカル・ボリュームと称される。また、走査分子計数法では、1つの粒子及び発光プローブの結合体又は発光プローブからの光、例えば、一個又は数個の蛍光色素分子からの微弱光が検出される。このため、光検出器16としては、好適には、フォトンカウンティングに使用可能な超高感度の光検出器が用いられる。また、顕微鏡のステージ(図示せず)には、観察するべきウェル10を変更するべく、マイクロプレート9の水平方向位置を移動するためのステージ位置変更装置17aが設けられていてよい。ステージ位置変更装置17aの作動は、コンピュータ18により制御されてよい。この構成により、検体が複数在る場合にも、迅速な計測が達成可能となる。
FIDA等の分光分析技術は、従前の生化学的な分析技術に比して、必要な試料量が極めて少なく、且つ、迅速に検査が実行できる点で優れている。しかしながら、FIDA等の分光分析技術では、原理的に、観測対象粒子の濃度や特性は、蛍光強度のゆらぎに基づいて算定される。したがって、精度のよい測定結果を得るためには、試料溶液中の観測対象粒子の濃度又は数密度が、蛍光強度の計測中に常に一個程度の観測対象粒子が光検出領域CV内に存在するレベルであり、計測時間中に常に有意な光強度(フォトンカウント)が検出されることが要求される。もし観測対象粒子の濃度又は数密度がそれよりも低い場合、例えば、観測対象粒子がたまにしか光検出領域CV内へ進入しないレベルである場合には、有意な光強度(フォトンカウント)が、計測時間の一部にしか現れないこととなり、精度のよい光強度のゆらぎの算定が困難となる。また、観測対象粒子の濃度が計測中に常に一個程度の観測対象粒子が光検出領域内に存在するレベルよりも大幅に低い場合には、光強度のゆらぎの演算において、バックグラウンドの影響を受けやすい。さらには、演算に十分な量の有意な光強度データを得るために計測時間が長くなる。これに対して、走査分子計数法では、観測対象粒子の濃度がFIDA等の分光分析技術にて要求されるレベルよりも低い場合でも、観測対象粒子の数密度又は濃度等の特性の検出が可能である。
検出された粒子の数をカウントすることにより、計測された領域内に存在する粒子の数、或いは、濃度若しくは数密度に関する情報が取得できる。この走査分子計数法の光分析技術の原理においては、蛍光強度のゆらぎの算出の如き、統計的な演算処理は行われず、粒子が一つずつ検出される。これにより、FIDA等では十分な精度にて分析ができないほど、観測されるべき粒子の濃度が低い試料溶液でも、粒子の濃度若しくは数密度に関する情報を取得することが可能となる。
走査分子計数法の光分析における光強度の測定は、測定中にミラー偏向器17を駆動して、試料溶液内での光検出領域の位置の移動(試料溶液内の走査)を行う他は、FCS又はFIDAにおける光強度の測定工程と同様の態様にて実行されてよい。操作処理において、典型的には、マイクロプレート9のウェル10に試料溶液を注入して顕微鏡のステージ上に載置した後、使用者がコンピュータ18に対して、測定の開始の指示を入力する。コンピュータ18は、記憶装置(図示せず)に記憶されたプログラムに従って、試料溶液内の光検出領域における励起光の照射及び光強度の計測が開始される。このプログラムには、試料溶液内において光検出領域の位置を移動するべく光路を変更する手順(変更手順)と、光検出領域の位置の移動中に光検出領域からの光を検出する手順(光検出手順)とが含まれている。この計測中、コンピュータ18のプログラムに従った処理動作の制御下、ミラー偏向器17は、ミラー7(ガルバノミラー)を駆動して、ウェル10内において光検出領域の位置の移動を実行する。これと同時に光検出器16は、逐次的に検出された光を電気信号に変換してコンピュータ18へ送信する。コンピュータ18では、任意の態様にて、送信された光信号から時系列の光強度データを生成して保存する。典型的には、光検出器16は、一光子の到来を検出できる超高感度光検出器であるので、光の検出は、所定時間に亘って、逐次的に、所定の単位時間毎(BINTIME)に、例えば、10μ秒毎に光検出器に到来するフォトンの数を計測する態様にて実行されるフォトンカウンティングである。時系列の光強度のデータは、時系列のフォトンカウントデータであってよい。
(2Wo)2 =6D・Δt …(1)
から、
Δt=(2Wo)2 /6D …(2)
となるので、観測対象粒子がブラウン運動により移動する速度(拡散移動速度)Vdifは、概ね、
Vdif=2Wo/Δt=3D/Wo …(3)
となる。そこで、光検出領域の位置の移動速度は、拡散移動速度Vdifを参照して、それよりも十分に早い値に設定されてよい。例えば、観測対象粒子の拡散係数が、D=2.0×10−10m2/s程度であると予想される場合には、Woが、0.62μm程度だとすると、Vdifは、1.0×10−3m/sとなるので、光検出領域の位置の移動速度は、その略10倍の15mm/sと設定されてよい。観測対象粒子の拡散係数が未知の場合には、光検出領域の位置の移動速度を種々設定して光強度の変化のプロファイルが、予想されるプロファイル(典型的には、励起光強度分布と略同様)となる条件を見つけるための予備実験を繰り返し実行して、好適な光検出領域の位置の移動速度が決定されてよい。
上記の処理により試料溶液の時系列の光強度データが得られると、コンピュータ18において、記憶装置に記憶されたプログラムに従った処理(検出された光から個々の発光粒子からの光信号を個別に検出する手順(光信号検出手順))により、下記に示すように光強度の分析が実行されてよい。
時系列の光強度データにおいて、一つの観測対象粒子の光検出領域を通過する際の軌跡が、図4Aに示されているように、略直線状である場合、その粒子に対応する光強度の変化は、図6Aに模式的に描かれているように、(光学系により決定される)光検出領域の光強度分布を反映したプロファイル(通常、略釣鐘状)を有する。そこで、観測対象粒子の検出の一つの手法において、光強度に対して閾値Ioが設定され、その閾値を超える光強度が継続する時間幅Δτが所定の範囲にあるとき、その光強度のプロファイルが一つの粒子が光検出領域を通過したことに対応すると判定され、一つの観測対象粒子の検出が為されるようになっていてよい。光強度に対する閾値Io及び時間幅Δτに対する所定の範囲は、光検出領域に対して所定の速度にて相対的に移動する観測対象粒子と発光プローブとの結合体(又は粒子との結合後分解され遊離した発光プローブ)から発せられる光の強度として想定されるプロファイルに基づいて定められる。具体的な値は、実験的に任意に設定されてよく、また、観測対象粒子と発光プローブとの結合体(又は粒子との結合後分解され遊離した発光プローブ)の特性によって選択的に決定されてよい。
ガウス分布:
I=A・exp(−2t2 /a2 ) …(4)
であると仮定でき、有意な光強度のプロファイル(バックグラウンドでないと明らかに判断できるプロファイル)に対して式(4)をフィッティングして算出された強度A及び幅aが所定の範囲内にあるとき、その光強度のプロファイルが一つの観測対象粒子が光検出領域を通過したことに対応すると判定され、一つの観測対象粒子の検出が為されてよい。一方、強度A及び幅aが所定の範囲外にあるときには、ノイズ又は異物として分析において無視されてよい。
観測対象粒子のカウンティングは、上記の観測対象粒子の検出の手法により検出された粒子の数を、任意の手法により、計数する(発光粒子数計数手順)ことにより為されてよい。しかしながら、粒子の数が大きい場合には、例えば、図5及び図6Bに例示された処理により為されてよい。
観測対象粒子のカウンティングが為されると、時系列光信号データの取得の間に光検出領域の通過した領域の総体積を用いて、観測対象粒子の数密度又は濃度が決定される。しかしながら、光検出領域の実効体積は、励起光又は検出光の波長、レンズの開口数、光学系の調整状態に依存して変動するため、設計値から算定することは、一般に困難である。従って、光検出領域の通過した領域の総体積を算定することも簡単ではない。そこで、典型的には、粒子の濃度が既知の溶液(参照溶液)について、検査されるべき試料溶液の測定と同様の条件にて、上記に説明した光強度の測定、粒子の検出及びカウンティングを行う。検出された粒子の数と参照溶液の粒子の濃度とから、光検出領域の通過した領域の総体積、即ち、観測対象粒子の検出数と濃度との関係が決定されてもよい。
参照溶液の粒子としては、好ましくは、観測対象粒子が形成する粒子及び発光プローブ結合体(又は観測対象粒子に結合後遊離した発光プローブ)と同様の発光特性を有する発光標識(蛍光色素等)であってよい。具体的には、例えば、粒子の濃度Cの参照溶液について、その粒子の検出数がNであったとすると、光検出領域の通過した領域の総体積Vtは、
Vt=N/C …(5)
により与えられる。また、参照溶液として、複数の異なる濃度の溶液が準備され、それぞれについて測定が実行されて、算出されたVtの平均値が光検出領域の通過した領域の総体積Vtとして採用されてもよい。そして、Vtが与えられると、粒子のカウンティング結果がnの試料溶液の粒子の数密度cは、
c=n/Vt …(6)
により与えられる。光検出領域の体積、光検出領域の通過した領域の総体積は、上記の方法によらず、任意の方法にて、例えば、FCS、FIDAを利用するなどして与えられてもよい。また、本実施形態の光分析装置においては、想定される光検出領域の移動パターンについて、種々の標準的な粒子についての濃度Cと粒子の数Nとの関係(式(5))の情報をコンピュータ18の記憶装置に予め記憶しておき、装置の使用者が光分析を実施する際に適宜記憶された関係の情報を利用できる構成であってもよい。
本発明の一実施形態に係る標的粒子の定量方法は、試料溶液中にて分散しランダムに運動する標的粒子を定量する方法であって、試料溶液中の標的粒子を発光プローブで結合させて標識させる。その後、走査分子計数法によって計数した発光プローブと結合した標的粒子の数から、標的粒子の濃度が既知の標準試料を用いて作成された検量線に基づいて、この試料溶液中の標的粒子の濃度を算出する(濃度算出手順)ことを特徴とする。走査分子計数法は、分子が離散的な状況において、発光粒子を一粒子毎に測定することができる測定方法であることから、pMオーダー以下の比較的低濃度の発光粒子に対しても測定が可能である。このため、本発明の一実施形態に係る標的粒子の定量方法により、試料溶液中の解析対象の標的粒子の濃度が非常に低い場合であっても、標的粒子を高感度に計数することができる。さらに、本発明の一実施形態に係る標的粒子の定量方法は、標的粒子を、発光プローブとの結合を介して検出しているが、検量線を用いるため、より簡便かつ容易に、試料溶液中の標的粒子の濃度を求めることができる。
また、標的粒子の定量方法は、検出された発光粒子の数に基づいて、試料溶液中の前記発光粒子の数密度又は濃度を決定する手順を含んでいても良い。
(a)前記標的粒子と、前記標的粒子に結合する発光プローブとを含む試料溶液を調製し、前記試料溶液中で、前記標的粒子と前記発光プローブとを結合させる工程
(b)前記工程(a)において調製された溶液中に存在する、前記標的粒子の数を計数する工程(c)前記試料溶液中の前記標的粒子の濃度又は量と前記標的粒子の前記数との相関関係を近似する検量線に基づいて、前記工程(b)において計数された前記標的粒子の前記数から、前記試料溶液中の前記標的粒子の濃度を算出する工程。
さらに、前記工程(b)が、共焦点顕微鏡又は多光子顕微鏡の光学系を用いて、前記試料溶液内において前記光学系の光検出領域の位置を移動する移動工程と、前記試料溶液内において前記光学系の前記光検出領域の前記位置を移動させながら、前記光検出領域中の前記発光プローブから放出される光信号を検出して、前記標的粒子を個別に検出する検出工程と、を有する。 以下、工程ごとに説明する。
核酸類似物質としては、DNAやRNAのような天然型ヌクレオチド(天然に存在するヌクレオチド)の側鎖等がアミノ基等の官能基により修飾された物質や、タンパク質や低分子化合物等で標識された物質等が挙げられる。より具体的には、例えば、Bridged nucleic acid(BNA)や、天然型ヌクレオチドの4’位酸素原子が硫黄原子に置換されているヌクレオチド、天然型リボヌクレオチドの2’位水酸基がメトキシ基に置換されているヌクレオチドやHexitol Nucleic Acid(HNA)、ペプチド核酸(PNA)等が挙げられる。
例えば、標的粒子が核酸分子又は核酸類似物質からなるオリゴヌクレオチドであり、発光プローブ中の標的粒子と結合する部位が、核酸分子又は核酸類似物質からなり標的粒子とハイブリダイズするオリゴヌクレオチドである場合、前記複合体を含む試料溶液の温度を、標的粒子と発光プローブの特異的会合条件よりも充分に高くしたり、前記複合体を含む試料溶液の塩濃度を、標的粒子と発光プローブの特異的会合条件よりも充分に低くする。これにより、発光プローブと標的粒子の結合を解消させ、前記複合体から発光プローブを解離させることができる。
走査分子計数法のための光分析装置及びこの装置のためのプログラムに、さらに工程(c)を行うための構成及び手順を追加した装置等を用いることにより、工程(b)〜(c)を上記の装置で行うことができる。
例えば、コンピュータ18が、上記信号処理部、記憶部、濃度計算器を備えていても良い。
濃度が異なる蛍光色素を用いて、走査分子計数法の計測値に基づく検量線作成が可能であることを示す実験を行った。
計測に於いては、光分析装置として、共焦点蛍光顕微鏡の光学系とフォトンカウンティングシステムとを備えた1分子蛍光測定装置MF20(オリンパス株式会社)を用いた。
まず、ATTO(登録商標)633(ATTO−TEC社製)を、リン酸緩衝液(0.1% Pluronic F−127を含む)を用いて100pM、10pM、1pM、100fM、又は10fMとなるようにそれぞれ調製した。次に、光分析装置の光学調整を行った後、上記の各試料溶液について計測を行い、時系列のフォトンカウントデータを取得した。その際、励起光は、633nmのレーザ光を用いて1mWで照射し、検出光波長は、バンドパスフィルターを用いて660〜710nmとした。試料溶液中に於ける光検出領域の位置の移動速度は、15mm/秒とし、BIN TIMEを10μ秒とし、測定時間は、100pM、10pM、及び1pMの試料については2秒間、100fM及び10fMの試料については20秒間(グラフ中のピーク数は2秒間換算)とした。また、測定は各試料について5回行い、その平均を算出した。光強度の測定後、各試料溶液について取得された時系列のフォトンカウントデータから、時系列データ中にて検出された光信号を計数した。データの移動平均法によるスムージングに於いては、一度に平均するデータ点は9個とし、移動平均処理を5回繰り返した。また、フィッティングに於いては、時系列データに対してガウス関数を最小二乗法によりフィッティングし、(ガウス関数に於ける)ピーク強度、ピーク幅(半値全幅)、相関係数を決定した。更に、ピークの判定処理では、下記の条件:
20μ秒<ピーク幅<400μ秒、
ピーク強度>1(フォトン/10μ秒)、
相関係数>0.95、
を満たすピーク信号のみを観測対象分子に対応する光信号であると判定した。一方、上記の条件を満たさないピーク信号はノイズとして無視し、観測対象分子に対応する光信号であると判定された信号の数を「ピーク数」として計数した。
また、図13は、図12のグラフを通常目盛表示としたグラフである。この結果、溶液中の蛍光物質ATTO633の濃度と計数されるピーク数とは強い正の相関があり、各測定値から求められた検量線(図13内に示す。)を用いることにより、濃度未知の試料の濃度を容易に決定できることがわかった。例えば、濃度未知の試料を測定した際のピーク数が100だった場合には、この試料のATTO633の濃度は2.5pMと算出することができる。
標的粒子として、配列番号1で表される塩基配列からなる核酸を用いた。以下、本実施例においては、この核酸を標的核酸という。また、この標的核酸と結合する発光プローブとして、配列番号2で表される塩基配列からなるオリゴヌクレオチドの5’末端にAlexa Fluor 488が付加され、3’末端にBHQ−1が付加された分子ビーコンプローブを用いた。これらのオリゴヌクレオチドは、シグマジェノシス株式会社に依頼して合成した。標的核酸及び分子ビーコンプローブの塩基配列を表1に示す。表1において、分子ビーコンプローブ中の下線が付された塩基は、分子内構造体を形成する際に互いにハイブリダイズする領域である。
各標準試料溶液を、95℃で5分間加熱することにより変性させた後、20℃まで徐々に液温を低下させて、標的核酸と分子ビーコンプローブが結合した会合体を形成させた。具体的には、降温速度を0.1℃/秒とし、90℃で5分間、80℃で10分間、70℃で10分間、60℃で10分間、50℃で10分間、40℃で10分間、30℃で10分間の降温処理を行った。
20μ秒<ピーク幅<400μ秒、
ピーク強度>1(フォトン/10μ秒)、
相関係数>0.95、
を満たすピーク信号のみを観測対象核酸に対応する光信号であると判定する一方、上記の条件を満たさないピーク信号はノイズとして無視し、観測対象核酸に対応する光信号であると判定された信号の数を「ピーク数」として計数した。
標的粒子として、配列番号3で表される塩基配列からなる核酸を用いた。以下、本実施例においては、前記核酸を標的核酸2という。また、発光プローブとして、蛍光プローブを用い、分離用プローブとして、ビオチンプローブを用い、固相担体として、ストレプトアビジンでコートした磁気ビーズを用いた。
また、前記標的核酸2と結合する発光プローブとして、配列番号4で表される塩基配列からなるオリゴヌクレオチドの5’末端にATTO 647Nが付加された蛍光プローブを用いた。さらに、前記標的核酸2と結合する、配列番号5で表される塩基配列からなるオリゴヌクレオチドの3’末端にビオチンが付加されたビオチンプローブを用いた。これらのオリゴヌクレオチドは、シグマジェノシス株式会社に依頼して合成した。標的核酸2及び蛍光プローブ、ビオチンプローブの塩基配列を表2に示す。
計測に於いては、光分析装置として、共焦点蛍光顕微鏡の光学系とフォトンカウンティングシステムを備えた1分子蛍光測定装置MF20(オリンパス株式会社)を用い、上記の上清について、時系列のフォトンカウントデータを取得した。その際、励起光は、642nmのレーザ光を用いて1mWで照射し、検出光波長は、バンドパスフィルターを用いて660〜710nmとした。試料溶液中に於ける光検出領域の位置の移動速度は、67.5mm/秒とし、BIN TIMEを10μ秒とし、測定時間は、600秒間とした。また測定は各5回行い、その平均と標準偏差を算出した。光強度の測定後、各上清について取得された時系列のフォトンカウントデータから時系列データ中にて検出された光信号を計数した。データの移動平均法によるスムージングに於いては、一度に平均するデータ点は11個とし、移動平均処理を5回繰り返した。また、フィッティングに於いては、時系列データに対してガウス関数を最小二乗法によりフィッティングし、(ガウス関数に於ける)ピーク強度、ピーク幅(半値全幅)、相関係数を決定した。更に、ピークの判定処理では、
下記の条件:
20μ秒<ピーク幅<400μ秒
ピーク強度>1(フォトン/10μ秒)
相関係数>0.90
を満たすピーク信号のみを蛍光プローブに対応する光信号であると判定する一方、上記の条件を満たさないピーク信号はノイズとして無視し、蛍光プローブに対応する光信号であると判定された信号の数を「ピーク数」として計数した。
図14は、横軸を標準試料溶液中の標的核酸2の濃度、縦軸をピーク数とし、各標準試料溶液から得られた計数値をプロットしたグラフである。この結果、標的核酸2の濃度依存的にピーク数が変化していることが確認された。
各プロットの近似曲線を検量線とし、濃度未知の試料溶液の標的核酸濃度を求めた。具体的には、濃度未知試料溶液に対して、上記標準試料溶液と同様にして測定用試料を作製し、光分析装置を用いて測定し、ピーク数を算出した。この結果、前記濃度未知試料溶液から計数されたピーク数は724であった。図14に示す検量線を参照し、前記濃度未知試料溶液の標的核酸濃度は、4.6fMであると算出することができた。
T…対象粒子(標的粒子)
1…光分析装置(共焦点顕微鏡)
2…光源
3…シングルモードオプティカルファイバー
4…コリメータレンズ
5…ダイクロイックミラー
6、7、11…反射ミラー
8…対物レンズ
9…マイクロプレート
10…ウェル(試料溶液容器)
12…コンデンサーレンズ
13…ピンホール
14…バリアフィルター
15…マルチモードオプティカルファイバー
16…光検出器
17…ミラー偏向器(光検出領域移動部)
17a…ステージ位置変更装置
18…コンピュータ
19…ディスプレイ(表示部)
Claims (7)
- 試料溶液中にて分散しランダムに運動する標的粒子を定量する方法であって、
(a)前記標的粒子と、前記標的粒子に結合する発光プローブとを含む試料溶液を調製し、前記試料溶液中で、前記標的粒子と前記発光プローブとを結合させる工程と;
(b)共焦点顕微鏡又は多光子顕微鏡の光学系を用いて、前記試料溶液内において前記光学系の光検出領域の位置を移動する移動工程と、前記試料溶液内において前記光学系の前記光検出領域の前記位置を移動させながら、前記光検出領域中の前記発光プローブから放出される光信号を検出して、直接的または間接的に前記標的粒子を個別に検出する検出工程と、
(c)前記検出工程において検出された、前記標的粒子の数を計数する計数工程及び前記試料溶液中の前記標的粒子の濃度又は量と前記標的粒子の前記数との相関関係を近似する検量線に基づいて、前記工程(b)において計数された前記標的粒子の前記数から、前記試料溶液中の前記標的粒子の濃度を算出する算出工程と;
を備え、
前記工程(b)において、前記光検出領域中の前記発光プローブから放出される光信号の検出及び前記標的粒子の検出を、
検出された光の時系列の光強度データを生成し、生成された時系列光信号データに対してスムージング処理をした後に時間についての一次微分値を演算してピーク存在領域を特定し、前記特定されたピーク存在領域におけるスムージングされた時系列光信号データに対して釣鐘型関数のフィッティングを行い、算出された釣鐘型関数のパラメータが一つの発光プローブに対応する光信号において想定される範囲内にあると判定された信号を、一つの標的粒子に対応する信号であると判定することによって、一つの標的粒子を検出することにより行い、
前記発光プローブが、互いに近接しているときに蛍光エネルギー移動現象を発生するエネルギー・ドナー部位とエネルギー・アクセプター部位とを有し;
前記発光プローブが前記標的粒子に結合した結合状態と前記標的粒子に結合していない非結合状態との間で前記エネルギー・ドナー部位と前記エネルギー・アクセプター部位との距離が異なり;
前記結合状態と、前記非結合状態との、前記発光プローブから放出される光の発光特性が異なる;
標的粒子の定量方法。 - 前記移動工程に於いて、前記光検出領域の前記位置を所定の速度にて移動する
請求項1に記載の標的粒子の定量方法。 - 前記移動工程に於いて、前記光検出領域の前記位置を、前記発光プローブ、又は前記発光プローブと結合した標的粒子のいずれか速い方の拡散移動速度よりも速い速度にて移動する
請求項1又は2に記載の標的粒子の定量方法。 - 前記検出工程に於いて、検出された時系列の前記光信号の形状に基づいて、前記発光プローブ、又は発光プローブと結合した前記標的粒子が前記光検出領域に入ったことを検出する
請求項1から請求項3のいずれか1項に記載の標的粒子の定量方法。 - 前記標的粒子が核酸であり;
前記発光プローブが、前記標的粒子と特異的にハイブリダイズし、且つ蛍光エネルギー移動現象におけるエネルギー・ドナーと成る蛍光物質及びエネルギー・アクセプターと成る物質の少なくとも一つが結合している1本鎖核酸である;
請求項1から請求項4のいずれか1項に記載の標的粒子の定量方法。 - (d)前記工程(a)の後、前記試料溶液から、前記標的粒子と結合していない発光プローブと分離して、前記標的粒子と前記発光プローブとを含む複合体を回収する工程を有する
請求項1から請求項5のいずれか1項に記載の標的粒子の定量方法。 - (e)前記工程(d)において回収された前記複合体から前記発光プローブを解離させた後、遊離の発光プローブと前記標的粒子とを、互いに分離して回収する工程を有する
請求項6に記載の標的粒子の定量方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011092168 | 2011-04-18 | ||
| JP2011092168 | 2011-04-18 | ||
| PCT/JP2012/060487 WO2012144528A1 (ja) | 2011-04-18 | 2012-04-18 | 標的粒子の定量方法、光分析装置及び光分析用コンピュータプログラム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2012144528A1 JPWO2012144528A1 (ja) | 2014-07-28 |
| JP6013328B2 true JP6013328B2 (ja) | 2016-10-25 |
Family
ID=47041634
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013511024A Active JP6013328B2 (ja) | 2011-04-18 | 2012-04-18 | 標的粒子の定量方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9116127B2 (ja) |
| EP (1) | EP2700935A4 (ja) |
| JP (1) | JP6013328B2 (ja) |
| CN (1) | CN103620389B (ja) |
| WO (1) | WO2012144528A1 (ja) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5856983B2 (ja) | 2011-01-20 | 2016-02-10 | オリンパス株式会社 | 単一発光粒子からの光の検出を用いた光分析方法及び光分析装置 |
| WO2013021687A1 (ja) | 2011-08-11 | 2013-02-14 | オリンパス株式会社 | 標的粒子の検出方法 |
| WO2013024650A1 (ja) | 2011-08-15 | 2013-02-21 | オリンパス株式会社 | 単一発光粒子検出を用いた光分析装置、光分析方法及び光分析用コンピュータプログラム |
| CN103765196B (zh) | 2011-08-26 | 2016-03-02 | 奥林巴斯株式会社 | 利用单个发光粒子检测的光分析装置及光分析方法 |
| EP2752655A4 (en) * | 2011-08-30 | 2015-06-17 | Olympus Corp | PROCEDURE FOR DETECTING TARGET PARTICLES |
| WO2013125124A1 (ja) | 2012-02-22 | 2013-08-29 | オリンパス株式会社 | 標的粒子の検出方法 |
| JP6095645B2 (ja) | 2012-03-21 | 2017-03-15 | オリンパス株式会社 | 標的核酸分子の検出方法 |
| WO2017098597A1 (ja) * | 2015-12-09 | 2017-06-15 | オリンパス株式会社 | 単一発光粒子検出を用いた光分析方法及び光分析装置 |
| EP3438649B1 (en) * | 2017-07-31 | 2020-03-11 | Vestel Elektronik Sanayi ve Ticaret A.S. | Identification tag and method of identifying an object |
| JP7209550B2 (ja) * | 2019-01-25 | 2023-01-20 | 浜松ホトニクス株式会社 | 標的物質に対する応答性の高い細胞を選択する方法、及び、試料中の未知濃度の標的物質の濃度を決定する方法 |
| CN111289425B (zh) * | 2020-03-12 | 2021-03-30 | 中国计量科学研究院 | 基于荧光标记流式单分子计数的蛋白质含量计量基准方法 |
| CN113340894B (zh) * | 2021-05-28 | 2023-04-07 | 上海睿钰生物科技有限公司 | 一种非透明微粒的检测方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008536093A (ja) * | 2005-01-31 | 2008-09-04 | ザ ボード オブ トラスティーズ オブ ザ ユニヴァーシティー オブ イリノイ | 透明媒質及び懸濁媒質内の粒子を特性評価する方法及びデバイス |
| JP2011508219A (ja) * | 2007-12-19 | 2011-03-10 | シンギュレックス・インコーポレイテッド | 単一分子検出走査分析器およびその使用方法 |
| JP5687684B2 (ja) * | 2010-03-01 | 2015-03-18 | オリンパス株式会社 | 光分析装置、光分析方法並びに光分析用コンピュータプログラム |
| JP5877155B2 (ja) * | 2010-07-26 | 2016-03-02 | オリンパス株式会社 | 発光プローブを用いて溶液中の希薄粒子を検出する方法 |
Family Cites Families (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4251733A (en) | 1978-06-29 | 1981-02-17 | Hirleman Jr Edwin D | Technique for simultaneous particle size and velocity measurement |
| JPH04337446A (ja) | 1991-05-15 | 1992-11-25 | Hitachi Ltd | 微粒子計測方法、定量方法および微粒子計測装置 |
| US5866336A (en) | 1996-07-16 | 1999-02-02 | Oncor, Inc. | Nucleic acid amplification oligonucleotides with molecular energy transfer labels and methods based thereon |
| EP0836090A1 (en) | 1996-10-12 | 1998-04-15 | Evotec BioSystems GmbH | Method of analysis of samples by determination of the distribution of specific brightnesses of particles |
| US6235471B1 (en) | 1997-04-04 | 2001-05-22 | Caliper Technologies Corp. | Closed-loop biochemical analyzers |
| US6710871B1 (en) | 1997-06-09 | 2004-03-23 | Guava Technologies, Inc. | Method and apparatus for detecting microparticles in fluid samples |
| GB2326229A (en) | 1997-06-13 | 1998-12-16 | Robert Jeffrey Geddes Carr | Detecting and analysing submicron particles |
| SE9800360D0 (sv) | 1998-02-06 | 1998-02-06 | Goeteborg University Science I | Method, apparatus and flow cell for high sensitivity detection of fluorescent molecules |
| US6388788B1 (en) | 1998-03-16 | 2002-05-14 | Praelux, Inc. | Method and apparatus for screening chemical compounds |
| US20030036855A1 (en) | 1998-03-16 | 2003-02-20 | Praelux Incorporated, A Corporation Of New Jersey | Method and apparatus for screening chemical compounds |
| IL138496A0 (en) | 1998-03-16 | 2001-10-31 | Praelux Inc | Confocal microscopy imaging system |
| WO2000066985A1 (en) | 1999-04-29 | 2000-11-09 | Evotec Biosystems Ag | A method of characterizing fluorescent molecules or other particles using generating functions |
| US6376843B1 (en) | 1999-06-23 | 2002-04-23 | Evotec Oai Ag | Method of characterizing fluorescent molecules or other particles using generating functions |
| US8264680B2 (en) | 1999-05-28 | 2012-09-11 | Yokogawa Electric Corporation | Biochip reader and electrophoresis system |
| US6965113B2 (en) | 2000-02-10 | 2005-11-15 | Evotec Ag | Fluorescence intensity multiple distributions analysis: concurrent determination of diffusion times and molecular brightness |
| US20010035954A1 (en) | 2000-03-10 | 2001-11-01 | Rahn John Richard | Method and apparatus for measuring particle size distributions using light scattering |
| DE10035190C5 (de) | 2000-07-20 | 2009-07-16 | MAX-PLANCK-Gesellschaft zur Förderung der Wissenschaften e.V. | Verfahren und Vorrichtung zur Fluoreszenzmessung |
| US6947133B2 (en) | 2000-08-08 | 2005-09-20 | Carl Zeiss Jena Gmbh | Method for increasing the spectral and spatial resolution of detectors |
| DE10038528A1 (de) | 2000-08-08 | 2002-02-21 | Zeiss Carl Jena Gmbh | Verfahren und Anordnung zur Erhöhung der spektralen und räumlichen Detektorauflösung |
| HU226937B1 (en) | 2000-11-17 | 2010-03-29 | Mta Szegedi Biolog Koezpont | Method and apparatus for determining polarization amount of material by a laser scanning microscope |
| EP1351048A4 (en) | 2000-12-14 | 2007-02-28 | Olympus Corp | FLUOROMETRIC ANALYZER AND FLUOROMETRIC ANALYSIS |
| US6782297B2 (en) | 2001-05-24 | 2004-08-24 | Eric Paul Tabor | Methods and apparatus for data smoothing |
| US6750963B2 (en) | 2002-05-21 | 2004-06-15 | Agilent Technologies, Inc. | Imaging systems for signals on a surface |
| EP1561114B1 (en) | 2002-11-07 | 2008-05-07 | Erasmus Universiteit Rotterdam | Fret probes and methods for detecting interacting molecules |
| US7038848B2 (en) | 2002-12-27 | 2006-05-02 | Olympus Corporation | Confocal microscope |
| JP4315794B2 (ja) | 2002-12-27 | 2009-08-19 | オリンパス株式会社 | 共焦点顕微鏡 |
| JP2005098876A (ja) | 2003-09-25 | 2005-04-14 | Institute Of Physical & Chemical Research | 2成分相互作用分析方法 |
| EP1805500A4 (en) | 2004-09-28 | 2008-05-07 | Singulex Inc | SYSTEM AND METHOD FOR THE SPECTROSCOPIC ANALYSIS OF INDIVIDUAL PARTICLES |
| JP2006333739A (ja) | 2005-05-31 | 2006-12-14 | Hitachi High-Technologies Corp | 単分子計測による核酸分析方法 |
| JP4757103B2 (ja) | 2005-06-13 | 2011-08-24 | 学校法人関西文理総合学園 | 試料中のウイルスを検出する方法およびシステム |
| US7919242B2 (en) * | 2005-06-30 | 2011-04-05 | Roche Molecular Systems, Inc. | Light emission modifiers and their uses in nucleic acid detection, amplification and analysis |
| EP1906172A4 (en) | 2005-07-15 | 2014-01-08 | Olympus Corp | LIGHT METER |
| WO2007118209A2 (en) * | 2006-04-07 | 2007-10-18 | Kim Laboratories | Apparatus and method for rapid detection of analytes |
| US8445655B2 (en) | 2006-06-16 | 2013-05-21 | Cornell Research Foundation, Inc. | Functional nucleic acid ligands to fluorescent proteins |
| WO2008007580A1 (fr) | 2006-07-13 | 2008-01-17 | Olympus Corporation | Procédé d'analyse de particules fines |
| US20080052009A1 (en) | 2006-08-23 | 2008-02-28 | Washington, University Of | Method for deconvolving single-molecule intensity distributions for quantitative biological measurements |
| GB0618057D0 (en) | 2006-09-14 | 2006-10-25 | Perkinelmer Ltd | Improvements in and relating to scanning confocal microscopy |
| JP5473202B2 (ja) | 2006-10-13 | 2014-04-16 | 滋賀県 | 試料中の蛍光性物質を検出する方法およびシステム |
| WO2008080417A1 (en) | 2006-12-28 | 2008-07-10 | Flult Biosystems Gmbh | A method of determining characteristic properties of a sample containing particles |
| JPWO2008099778A1 (ja) | 2007-02-14 | 2010-05-27 | 株式会社ニコン | スリット走査共焦点顕微鏡 |
| JP2008292371A (ja) | 2007-05-25 | 2008-12-04 | Institute Of Physical & Chemical Research | 蛍光相関分光による複数成分相互作用の分析方法及び相互作用制御化合物のスクリーニング方法 |
| JP2009145242A (ja) | 2007-12-14 | 2009-07-02 | Olympus Corp | 光測定装置 |
| JP5139885B2 (ja) | 2008-05-21 | 2013-02-06 | 浜松ホトニクス株式会社 | 蛍光解析装置及び解析方法 |
| JP2009288161A (ja) | 2008-05-30 | 2009-12-10 | Olympus Corp | 光測定装置及び光測定方法 |
| JP2010044714A (ja) | 2008-08-18 | 2010-02-25 | Hataguchi Masahiro | 業務管理システム及び業務管理方法 |
| US20100177190A1 (en) | 2008-12-16 | 2010-07-15 | Ann-Shyn Chiang | Microscopy system with revolvable stage |
| JP5265408B2 (ja) * | 2009-02-18 | 2013-08-14 | オリンパス株式会社 | 相関分光分析方法及び相関分光分析装置 |
| JP2011002415A (ja) * | 2009-06-22 | 2011-01-06 | Olympus Corp | 蛍光相関分光装置 |
| JP2011036150A (ja) * | 2009-08-07 | 2011-02-24 | Olympus Corp | 標的核酸分子の定量方法及び標的核酸分子定量キット |
| EP2602612A4 (en) * | 2010-09-10 | 2018-05-16 | Olympus Corporation | Optical analysis method using optical measurement in multiple wavelength bands |
| WO2012102260A1 (ja) * | 2011-01-26 | 2012-08-02 | オリンパス株式会社 | 核酸分子の多型識別方法 |
| CN103339256B (zh) * | 2011-01-26 | 2016-03-16 | 奥林巴斯株式会社 | 鉴别核酸分子多态性的方法 |
| WO2013024637A1 (ja) * | 2011-08-12 | 2013-02-21 | オリンパス株式会社 | 蛍光粒子の検出方法 |
| EP2752654A4 (en) * | 2011-08-30 | 2015-04-15 | Olympus Corp | OPTICAL ANALYZER WITH SINGLE DETECTION OF LIGHT-EMITTING PARTICLES, OPTICAL ANALYSIS PROCEDURE AND COMPUTER PROGRAM FOR OPTICAL ANALYZES |
| WO2013125124A1 (ja) * | 2012-02-22 | 2013-08-29 | オリンパス株式会社 | 標的粒子の検出方法 |
-
2012
- 2012-04-18 WO PCT/JP2012/060487 patent/WO2012144528A1/ja active Application Filing
- 2012-04-18 EP EP12774419.1A patent/EP2700935A4/en not_active Ceased
- 2012-04-18 CN CN201280029689.XA patent/CN103620389B/zh not_active Expired - Fee Related
- 2012-04-18 JP JP2013511024A patent/JP6013328B2/ja active Active
-
2013
- 2013-10-03 US US14/045,002 patent/US9116127B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008536093A (ja) * | 2005-01-31 | 2008-09-04 | ザ ボード オブ トラスティーズ オブ ザ ユニヴァーシティー オブ イリノイ | 透明媒質及び懸濁媒質内の粒子を特性評価する方法及びデバイス |
| JP2011508219A (ja) * | 2007-12-19 | 2011-03-10 | シンギュレックス・インコーポレイテッド | 単一分子検出走査分析器およびその使用方法 |
| JP5687684B2 (ja) * | 2010-03-01 | 2015-03-18 | オリンパス株式会社 | 光分析装置、光分析方法並びに光分析用コンピュータプログラム |
| JP5877155B2 (ja) * | 2010-07-26 | 2016-03-02 | オリンパス株式会社 | 発光プローブを用いて溶液中の希薄粒子を検出する方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2012144528A1 (ja) | 2012-10-26 |
| EP2700935A1 (en) | 2014-02-26 |
| JPWO2012144528A1 (ja) | 2014-07-28 |
| US9116127B2 (en) | 2015-08-25 |
| CN103620389B (zh) | 2016-08-17 |
| EP2700935A4 (en) | 2014-10-22 |
| US20140099630A1 (en) | 2014-04-10 |
| CN103620389A (zh) | 2014-03-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6013328B2 (ja) | 標的粒子の定量方法 | |
| JP5877155B2 (ja) | 発光プローブを用いて溶液中の希薄粒子を検出する方法 | |
| JP6010034B2 (ja) | 標的粒子の検出方法 | |
| JP5940651B2 (ja) | 標的粒子の検出方法 | |
| JP6104267B2 (ja) | 標的粒子の検出方法 | |
| JP6013332B2 (ja) | 標的粒子の計数方法 | |
| US9354176B2 (en) | Method for detecting a target particle | |
| JP6010029B2 (ja) | 蛍光粒子の検出方法 | |
| JP6013339B2 (ja) | 膵液を含む生体試料中の標的粒子の検出方法 | |
| JP6157326B2 (ja) | 光検出を用いた単一発光粒子検出方法 | |
| JP6013327B2 (ja) | 生体試料中の核酸分子の検出方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150306 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160315 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160513 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20160516 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160906 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160921 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6013328 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |