JP5872016B2 - 抗腫瘍活性があるクロメノン誘導体 - Google Patents
抗腫瘍活性があるクロメノン誘導体 Download PDFInfo
- Publication number
- JP5872016B2 JP5872016B2 JP2014235289A JP2014235289A JP5872016B2 JP 5872016 B2 JP5872016 B2 JP 5872016B2 JP 2014235289 A JP2014235289 A JP 2014235289A JP 2014235289 A JP2014235289 A JP 2014235289A JP 5872016 B2 JP5872016 B2 JP 5872016B2
- Authority
- JP
- Japan
- Prior art keywords
- ethyl
- morpholino
- oxo
- chromene
- carboxamide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C*(C1)COCCN1C(Oc(c1cc(C(O*)=O)c2)c2Br)=CC1=O Chemical compound C*(C1)COCCN1C(Oc(c1cc(C(O*)=O)c2)c2Br)=CC1=O 0.000 description 3
- RUCFCAIVBNFCSY-UHFFFAOYSA-N CC(c(cc(cc1Br)C(OC)=O)c1O)=O Chemical compound CC(c(cc(cc1Br)C(OC)=O)c1O)=O RUCFCAIVBNFCSY-UHFFFAOYSA-N 0.000 description 2
- SPCGMPXFIWKZFZ-UHFFFAOYSA-N CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Br Chemical compound CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Br SPCGMPXFIWKZFZ-UHFFFAOYSA-N 0.000 description 2
- PIJPVEDSEVINJH-UHFFFAOYSA-N CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)=O Chemical compound CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)=O PIJPVEDSEVINJH-UHFFFAOYSA-N 0.000 description 2
- MIIUCQQOKMDLDH-UHFFFAOYSA-N CC(c1cc(C(O)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F Chemical compound CC(c1cc(C(O)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F MIIUCQQOKMDLDH-UHFFFAOYSA-N 0.000 description 2
- NZBPEJWNZBACRV-UHFFFAOYSA-N CC(c1cc(C(OC)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F Chemical compound CC(c1cc(C(OC)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F NZBPEJWNZBACRV-UHFFFAOYSA-N 0.000 description 2
- JIFFIZXXTNYAPJ-UHFFFAOYSA-N CC(c(cc(cc12)C(N(C)C)=O)c1OC(N1CCOCC1)=CC2=O)Nc1cc(C#N)ccc1OC Chemical compound CC(c(cc(cc12)C(N(C)C)=O)c1OC(N1CCOCC1)=CC2=O)Nc1cc(C#N)ccc1OC JIFFIZXXTNYAPJ-UHFFFAOYSA-N 0.000 description 1
- RJCWTZOIDCLTCK-UHFFFAOYSA-N CC(c(cc(cc12)C(N(C)C)=O)c1OC(N1CCOCC1)=CC2=O)O Chemical compound CC(c(cc(cc12)C(N(C)C)=O)c1OC(N1CCOCC1)=CC2=O)O RJCWTZOIDCLTCK-UHFFFAOYSA-N 0.000 description 1
- HZZFCCFTMKIMMQ-UHFFFAOYSA-N CC(c(cc(cc12)C(OC)=O)c1OC(N1CCOCC1)=CC2=O)Br Chemical compound CC(c(cc(cc12)C(OC)=O)c1OC(N1CCOCC1)=CC2=O)Br HZZFCCFTMKIMMQ-UHFFFAOYSA-N 0.000 description 1
- ZIOAECFKGUUWGJ-UHFFFAOYSA-N CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(c(F)ccc1Cl)c1F Chemical compound CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(c(F)ccc1Cl)c1F ZIOAECFKGUUWGJ-UHFFFAOYSA-N 0.000 description 1
- UHDLRSYRMVRGIY-UHFFFAOYSA-N CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cc1F)ccc1F Chemical compound CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cc1F)ccc1F UHDLRSYRMVRGIY-UHFFFAOYSA-N 0.000 description 1
- PKOQQRKDYMICGM-UHFFFAOYSA-N CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(OC)c1 Chemical compound CC(c1cc(C(N(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(OC)c1 PKOQQRKDYMICGM-UHFFFAOYSA-N 0.000 description 1
- GMWIXYJWVBNHHV-VYRBHSGPSA-N CC(c1cc(C(N(C)C)=O)cc2c1OC(N1C[C@H](C)OCC1)=CC2=O)Nc(cc1)ccc1F Chemical compound CC(c1cc(C(N(C)C)=O)cc2c1OC(N1C[C@H](C)OCC1)=CC2=O)Nc(cc1)ccc1F GMWIXYJWVBNHHV-VYRBHSGPSA-N 0.000 description 1
- HANNCOPSXXARJM-UHFFFAOYSA-N CC(c1cc(C(N2CCOCC2)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(F)c1 Chemical compound CC(c1cc(C(N2CCOCC2)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(F)c1 HANNCOPSXXARJM-UHFFFAOYSA-N 0.000 description 1
- BVDGERTYPWXPSJ-UHFFFAOYSA-N CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F Chemical compound CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc(cccc1Cl)c1F BVDGERTYPWXPSJ-UHFFFAOYSA-N 0.000 description 1
- XUGMSUMJKZTWAC-UHFFFAOYSA-N CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)ccc1 Chemical compound CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)ccc1 XUGMSUMJKZTWAC-UHFFFAOYSA-N 0.000 description 1
- IGUXKRRCBYGCRH-UHFFFAOYSA-N CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1ccccc1 Chemical compound CC(c1cc(C(NCCN(C)C)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1ccccc1 IGUXKRRCBYGCRH-UHFFFAOYSA-N 0.000 description 1
- PSKDKFPIGKMDGE-UHFFFAOYSA-N CC(c1cc(C(O)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(F)c1 Chemical compound CC(c1cc(C(O)=O)cc2c1OC(N1CCOCC1)=CC2=O)Nc1cc(F)cc(F)c1 PSKDKFPIGKMDGE-UHFFFAOYSA-N 0.000 description 1
- FPYAQSSSRQZXMS-UHFFFAOYSA-N CC(c1cc(C(OC)=O)ccc1O)=O Chemical compound CC(c1cc(C(OC)=O)ccc1O)=O FPYAQSSSRQZXMS-UHFFFAOYSA-N 0.000 description 1
- XPOSPWHQDYLFFQ-UHFFFAOYSA-N CCS(C(Oc(c1cc(C(OC)=O)c2)c2Br)=CC1=O)(=O)=O Chemical compound CCS(C(Oc(c1cc(C(OC)=O)c2)c2Br)=CC1=O)(=O)=O XPOSPWHQDYLFFQ-UHFFFAOYSA-N 0.000 description 1
- UQRQNBIDRBDUHM-UHFFFAOYSA-N CCSC(Oc(c(Br)c1)c2cc1C(OC)=O)=CC2=O Chemical compound CCSC(Oc(c(Br)c1)c2cc1C(OC)=O)=CC2=O UQRQNBIDRBDUHM-UHFFFAOYSA-N 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N COC(c(cc1)ccc1O)=O Chemical compound COC(c(cc1)ccc1O)=O LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- SLWHOGGAFBNDFM-UHFFFAOYSA-N COC(c(cc12)cc(Br)c1OC(N1CCOCC1)=CC2=O)=O Chemical compound COC(c(cc12)cc(Br)c1OC(N1CCOCC1)=CC2=O)=O SLWHOGGAFBNDFM-UHFFFAOYSA-N 0.000 description 1
- RQLBGIYYRXGZFG-UHFFFAOYSA-N COC(c(cc1Br)cc(C(CC(N2CCOCC2)=O)=O)c1O)=O Chemical compound COC(c(cc1Br)cc(C(CC(N2CCOCC2)=O)=O)c1O)=O RQLBGIYYRXGZFG-UHFFFAOYSA-N 0.000 description 1
- QUJJJDXVKXXGLB-UHFFFAOYSA-N COC(c(cc1Br)cc(C(O)=C2)c1OC2=S)=O Chemical compound COC(c(cc1Br)cc(C(O)=C2)c1OC2=S)=O QUJJJDXVKXXGLB-UHFFFAOYSA-N 0.000 description 1
- RKUNSPWAQIUGEZ-UHFFFAOYSA-N COC(c(cc1Br)ccc1O)=O Chemical compound COC(c(cc1Br)ccc1O)=O RKUNSPWAQIUGEZ-UHFFFAOYSA-N 0.000 description 1
- SCCJAABLYRGCNN-SECBINFHSA-N C[C@H](C1)OCCN1C(Oc(c1cc(C(OC)=O)c2)c2Br)=CC1=O Chemical compound C[C@H](C1)OCCN1C(Oc(c1cc(C(OC)=O)c2)c2Br)=CC1=O SCCJAABLYRGCNN-SECBINFHSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/74—Benzo[b]pyrans, hydrogenated in the carbocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/22—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/275—Nitriles; Isonitriles
- A61K31/277—Nitriles; Isonitriles having a ring, e.g. verapamil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pyrane Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
ようなウイルスの腫瘍遺伝子、例えばpp60v−Srcチロシンキナーゼ(あるいは、v−Srcとして知られる)と正常細胞中の対応するチロシンキナーゼ、例えばpp60c−Srcチロシンキナーゼ(あるいは、c−Srcとして知られる)より現れた。
。この分類には、EGF、TGFα、Neu、及びerbB受容体のような受容体チロシンキナーゼのEGFファミリーを含んでなるクラスI受容体チロシンキナーゼが含まれる。
RのようなPI3−キナーゼの下流にあるものが含まれる(Blume-Jensen and Hunter, Nature, 2001, 411, 355)。
Vivanco and Sawyers, Nature Reviews Cancer, 2002, 2, 489-501)。例えば、p110αサブユニットは、卵巣(Shayesteh et al., Nature Genetics, 1999, 21: 99-102)及
び頚部(Ma et al., Oncogene, 2000, 19: 2739-2744)の腫瘍のようなある種の腫瘍において増幅されている。p110αの触媒部位内の活性化突然変異が結直腸領域と乳房及び肺の腫瘍のような他の様々な腫瘍と関連づけられてきた(Samuels et al., Science, 2004, 304, 554)。卵巣及び結腸の癌のような癌でも、腫瘍に関連した突然変異がp85α
に確認された(Philp et al., Cancer Research, 2001, 61, 7426-7429)。直接効果だけでなく、クラスIa PI3−キナーゼの活性化は、例えば、受容体チロシンキナーゼ、GPCR系、又はインテグリンのリガンド依存型又はリガンド非依存型の活性化により、シグナル伝達経路の上流で起こる腫瘍形成イベントへ寄与すると考えられている(Vara et al., Cancer Treatment Reviews, 2004, 30, 193-204)。そのような上流のシグナル伝達経路の例には、多様な腫瘍においてPI3−キナーゼ媒介経路の活性化をもたらす受容体チロシンキナーゼErb2の過剰発現(Harari et al., Oncogene, 2000, 19, 6102-6114)と腫瘍遺伝子Rasの過剰発現(Kauffmann-Zeh et al., Nature, 1997, 385, 544-548)が含まれる。さらに、クラスIa PI3−キナーゼは、様々な下流のシグナル伝達イベントによって引き起こされる腫瘍形成へ間接的に寄与する可能性がある。例えば、PI(3,4,5)P3のPI(4,5)P2への戻り変換を触媒するPTEN腫瘍抑制ホスファターゼの効果の消失は、PI3−キナーゼ媒介性のPI(3,4,5)P3の産生の脱調節を介して、きわめて広い範囲の腫瘍と関連づけられている(Simpson and Parsons, Exp. Cell Res., 2001, 264, 29-41)。さらに、他のPI3−キナーゼ媒介性シグナ
ル伝達イベントの効果の増強は、例えばAktの活性化によって、多様な癌へ寄与すると考えられている(Nicholson and Anderson, Cellular Signalling, 2002, 14, 381-395)。
いる(Sawyer, Expert Opinion Investig. Drugs, 2004, 13, 1-19)ので、PI3−キナーゼ阻害剤は、腫瘍細胞の浸潤及び転移の阻害を介して治療利益を提供するはずである。
るわけではないので、このファミリーメンバーの個別の役割の解析を可能にしない。この理由から、より強力で選択的な医薬品のPI3−キナーゼ阻害剤があれば、PI3−キナーゼ機能のより完全な理解を可能にして、有用な療法剤を提供するのに有用であろう。
、免疫系の細胞において重要な役割を有している(Koyasu, Nature Immunology, 2003, 4, 313-319)ので、それらは、炎症及びアレルギーの適応症の療法ターゲットとなる。P
I3−キナーゼの阻害はまた、先に記載のように、抗炎症効果を介して、又は心筋細胞に直接影響を及ぼすことによって直接的に、心臓血管系疾患を治療するのに有用である(Prasad et al., Trends in Cardiovascular Medicine, 2003, 13, 206-212)。PI3−キ
ナーゼの阻害は、血栓症を治療するのにも有用である。WO2004016607は、高剪断条件の下で生じる血小板の凝集及び癒着を破壊する方法と、剪断によって誘発される血小板活性化を阻害するための方法を提供し、ここではいずれの方法も、選択的PI3−キナーゼβ阻害剤の投与を含む。WO2004016607はまた、有効量の選択的PI3−キナーゼβ阻害剤を投与することを含んでなる、抗血栓の方法を提供する。この方法によれば、剪断誘発性の血小板活性化に重要であるPI3−キナーゼβに標的指向することによって、正常な止血作用に影響を及ぼすことなく、血栓症の特異的な阻害を得ることができる。故に、前記抗血栓の方法は、正常な止血作用の破壊によって引き起こされる、出血時間の延長のような副作用を伴わない。このように、クラスI PI3−キナーゼ酵素の阻害剤は、PI3−キナーゼβの阻害剤を含めて、癌に加えて、多種多様な疾患の予防及び治療に有用であることが期待されている。
c非受容体チロシンキナーゼに対してもほとんど活性を示さない一方で、クラスI PI3−キナーゼ酵素を阻害する、特にクラスIa PI3−キナーゼ酵素(PI3−キナーゼβが含まれる)を阻害するのに十分な量で使用することができる。
R1は、Hであるか、又はハロゲノ、ヒドロキシ、又は(1−3C)アルコキシより独立して選択される1、2又は3の置換基によって置換されていてもよい(1−4C)アルキルであり;
R2は、(1−4C)アルキル又は(1−4C)アルコキシであり、そのいずれも、ハロゲノ、ヒドロキシ、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノより独立して選択される1、2又は3の置換基によって置換されていてもよい;又は
R1とR2は、一緒に、酸素、窒素、及びイオウより選択される1又は2のさらなるヘテロ原子を含有してもよい、3〜8員の窒素含有ヘテロシクリル環系を形成し、ここで環イオウ原子は、酸化されてS−オキシド(複数)を生成してもよく、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、オキソ、ヒドロキシ−(1−3C)アルキル、ハロゲノ−(1−3C)アルキル、及び(1−3C)アルコキシ−(1−3C)アルキルより独立して選択される1、2又は3の置換基によって置換されていてもよい;
R3は、H又は(1−3C)アルキルであり;
R4とR5は、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択される;又は
R4とR5は、一緒に、フェニル環、又は5若しくは6員ヘテロシクリル環、又は5若しくは6員ヘテロアリール環を形成し、ここで該ヘテロシクリル又はヘテロアリール環は、酸素及び窒素より選択される1、2又は3のヘテロ原子を含有し、前記フェニル、ヘテロシクリル、又はヘテロアリール環は、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択される1、2又は3の置換基によって置換されていてもよい;
R6、R7、及びR8は、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択され;
nは、0、1、2、3又は4であり;
それぞれのR9基は、(1−3C)アルキルである]のクロメノン誘導体;又はその医薬的に許容される塩を提供する。
形成するとき、前記環には、R4基とR5基が付くコアフェニル基の炭素原子が含まれる。例えば、R4基とR5基が一緒にフェニル環を形成するとき、このときN(R3)基へ直接付く環系は、ナフチル環:
る。本発明のこの側面の1つの態様において、メチル基と−N(R3)フェニル(R4)(R5)(R6)(R7)(R8)基が付くキラル中心は、(R)−立体化学配置にある。本発明のこの側面のさらなる態様において、メチル基と−N(R3)フェニル(R4)(R5)(R6)(R7)(R8)基が付くキラル中心は、(S)−立体化学配置にある。
従って、本発明のさらなる側面は、(−)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミドのA型であり、ここで化学名の(−)−は、実施例3.06bに記載の条件を使用して測定される旋光性を表す。
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミドの結晶型、A型を提供する。
晶型、B型を提供し、ここで前記数値は、プラス又はマイナス0.5°2θであってよい。
従って、本発明のさらなる側面は、(−)−N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミドのA型であり、ここで化学名の(−)−は、実施例3.13bに記載の条件を使用して測定される旋光性を表す。
18.0°にあるX線粉末回折パターンを有する、(−)−N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミドの結晶型、A型を提供する。
リノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミドの結晶型、A型を提供する。
回折パターンの実質的な同一性を判定することが可能である。
本発明のさらなる側面により、本明細書に開示するような実施例のいずれにも従うことによって入手可能である、式Iのクロメノン誘導体を提供する。
上記に定義される式Iのある種の化合物は、互変異性の現象を明示する場合があると理解されたい。本発明には、その定義において、ホスホイノシチド(PI)3−キナーゼ阻害活性を保有するそのようなどの互変異性型又はその混合物も含まれ、式図内で利用されるか又は実施例で命名されるどの1つの互変異性型にも限定されないことを理解されたい。一般に、以下に続く実施例では、そして以下に続く関連の式図では、そのような互変異性型の唯1つが命名されるか又は提示される。
式IのR1基及びR2基によって形成される3〜8員の窒素含有ヘテロシクリル環系に適したものは、例えば、酸素、窒素、及びイオウより選択される1又は2のさらなるヘテロ原子を含有してもよい、窒素含有非芳香族の飽和又は部分飽和3〜8員環であって、ここで環イオウ原子は、酸化されてS−オキシド(複数)を形成してもよい。好適な例には、アゼパニル、オキサゼパニル、アジリジニル、アゼチジニル、ピロリニル、ピロリジニル、イミダゾリニル、イミダゾリジニル、ピラゾリニル、ピラゾリジニル、モルホリニル、チオモルホリニル、テトラヒドロ−1,4−チアジニル、1,1−ジオキソテトラヒドロ−1,4−チアジニル、ピペリジニル、ホモピペリジニル、ピペラジニル、ホモピペラジニル、ジヒドロピリジニル、テトラヒドロピリジニル、ジヒドロピリミジニル、又はテトラヒドロピリミジニルが含まれる。特別な化合物の群において、ヘテロシクリル環の特別な例には、アゼパニル、オキサゼパニル、アゼチジニル、ピロリジニル、モルホリニル、チオモルホリニル、ピペリジニル、ピペラジニル、そして特に、アゼパン−1−イル、1,4−オキサゼパン−4−イル、アゼチジン−1−イル、ピロリジン−1−イル、モルホリン−4−イル、チオモルホリン−4−イル、ピペリジン−1−イル、及びピペラジン−1−イルが含まれる。
ものは、例えば、酸素及び窒素より選択される1、2又は3のヘテロ原子を含有する、非芳香族の飽和又は部分飽和5若しくは6員環である。好適な例には、テトラヒドロフラニル、テトラヒドロピラニル、ピロリニル、ピロリジニル、イミダゾリニル、イミダゾリジニル、ピラゾリニル、ピラゾリジニル、モルホリニル、ピペリジニル、ホモピペリジニル、ピペラジニル、ホモピペラジニル、ジヒドロピリジニル、テトラヒドロピリジニル、ジヒドロピリミジニル、又はテトラヒドロピリミジニルが含まれる。
・ハロゲノ:フルオロ、クロロ、ブロモ、及びヨード;
・(1−8C)アルキル:メチル、エチル、プロピル、イソプロピル、tert−ブチル、シクロブチル、シクロヘキシル、シクロヘキシルメチル、及び2−シクロプロピルエチル;
・(2−8C)アルケニル:ビニル、イソプロペニル、アリル、及びブト−2−エニル;・(2−8C)アルキニル:エチニル、2−プロピニル、及びブト−2−イニル;
・(1−6C)アルコキシ:メトキシ、エトキシ、プロポキシ、イソプロポキシ、及びブトキシ;
・(1−6C)アルキルアミノ:メチルアミノ、エチルアミノ、プロピルアミノ、イソプロピルアミノ、及びブチルアミノ;
・ジ[(1−6C)アルキル]アミノ:ジメチルアミノ、ジエチルアミノ、N−エチル−N−メチルアミノ、及びジイソプロピルアミノ;
・ハロゲノ−(1−6C)アルキル:クロロメチル、2−フルオロエチル、2−クロロエチル、1−クロロエチル、2,2−ジフルオロエチル、2,2,2−トリフルオロエチル、3−フルオロプロピル、3−クロロプロピル、3,3−ジフルオロプロピル、及び3,3,3−トリフルオロプロピル;
・ヒドロキシ−(1−6C)アルキル:ヒドロキシメチル、2−ヒドロキシエチル、1−ヒドロキシエチル、及び3−ヒドロキシプロピル;並びに
・(1−6C)アルコキシ−(1−6C)アルキル:メトキシメチル、エトキシメチル、1−メトキシエチル、2−メトキシエチル、2−エトキシエチル、及び3−メトキシプロピル
式Iの化合物の好適な医薬的に許容される塩は、例えば、式Iの化合物の酸付加塩、例えば、塩酸、臭化水素酸、硫酸、トリフルオロ酢酸、又はクエン酸のような無機又は有機酸との酸付加塩;又は、例えば、十分に酸性である式Iの化合物の塩、例えば、カルシウム又はマグネシウム塩のようなアルカリ又はアルカリ土類金属の塩、又はアンモニウム塩、又はメチルアミン、ジメチルアミン、トリメチルアミン、ピペリジン、モルホリン、又はトリス−(2−ヒドロキシエチル)アミンのような有機塩基との塩である。式Iの化合物のさらに好適な医薬的に許容される塩は、例えば、式Iの化合物の投与後にヒト又は動物の体内で形成される塩である。
さらに理解されたい。従って、本発明の化合物は、ヒト又は動物の体内で分解されて本発明の化合物を放出する化合物であるプロドラッグの形態で投与してよい。プロドラッグは、本発明の化合物の物理特性及び/又は薬物動態特性を改変するために使用してよい。プロドラッグは、特性修飾基を付けることができる好適な基又は置換基を本発明の化合物が含有するときに生成することができる。プロドラッグの例には、式Iの化合物中のカルボキシ基又はヒドロキシ基で形成し得る in vivo 切断可能エステル誘導体と、式Iの化合
物中のカルボキシ基又はアミノ基で形成し得る in vivo 切断可能アミド誘導体が含まれ
る。
a)「Methods in Enzymology(酵素学の方法)」42巻、309-396頁、K. Widder et al.
監修(アカデミックプレス、1985)
b)「Design of Pro-drugs(プロドラッグの設計)」H. Bundgaard 監修(エルセヴィエ、1985);
c)「A Textbook of Drug Design and Development(医薬品の設計及び開発教程)」Krogsgaard-Larsen 及び H. Bundgaard 監修、第5章「Design and Application of Pro-drugs(プロドラッグの設計及び応用)」H. Bundgaard 著、p. 113-191(1991);
d)H. Bundgaard, Advanced Drug Delivery Reviews, 8, 1-38 (1992);
e)H. Bundgaard, et al., Journal of Pharmaceutical Sciences, 77, 285 (1988);
f)N. Kakeya, et al., Chem Pharm Bull, 32, 692 (1984);
g)T. Higuchi and V. Stella,「Pro-Drugs as Novel Delivery Systems(新規送達系としてのプロドラッグ)」A.C.S.シンポジウムシリーズ、14巻;及び
h)E. Roche(監修者)、「Bioreversible Carriers in Drug Design(ドラッグデザ
インにおける生可逆性担体)」ペルガモンプレス、1987。
Iの化合物の in vivo 切断可能エステル又はエーテルは、例えば、ヒト又は動物の体内
で切断されて元のヒドロキシ化合物を産生する医薬的に許容されるエステル又はエーテルである。ヒドロキシに適した医薬的に許容されるエステル形成基には、リン酸エステル(ホスホロアミド環式エステルを含めて)のような無機エステルが含まれる。ヒドロキシ基に適したさらなる医薬的に許容されるエステル形成基には、アセチル、ベンゾイル、フェニルアセチル、及び置換ベンゾイル及びフェニルアセチル基のような(1−10C)アルカノイル基、エトキシカルボニルのような(1−10C)アルコキシカルボニル基、N,N−[ジ(1−4C)アルキル]カルバモイル、2−ジアルキルアミノアセチル、及び2−カルボキシアセチル基が含まれる。フェニルアセチル及びベンゾイル基上の環置換基の例には、アミノメチル、N−アルキルアミノメチル、N,N−ジアルキルアミノメチル、モルホリノメチル、ピペラジン−1−イルメチル、及び4−(1−4C)アルキルピペラジン−1−イルメチルが含まれる。ヒドロキシ基に適した医薬的に許容されるエーテル形成基には、アセトキシメチル及びピバロイルオキシメチル基のようなα−アシルオキシアルキル基が含まれる。
ンのような(1−4C)アルキルアミン、ジメチルアミン、N−エチル−N−メチルアミン、又はジエチルアミンのようなジ(1−4C)アルキルアミン、2−メトキシエチルアミンのような(1−4C)アルコキシ−(2−4C)アルキルアミン、ベンジルアミンのようなフェニル−(1−4C)アルキルアミン、及びグリシンのようなアミノ酸と形成されるアミド、又はそのエステルである。
るアミドには、例えば、アセチル、ベンゾイル、フェニルアセチル及び置換ベンゾイル、及びフェニルアセチル基のような(1−10C)アルカノイル基と形成されるアミドが含まれる。フェニルアセチル及びベンゾイル基上の環置換基の例には、アミノメチル、N−アルキルアミノメチル、N,N−ジアルキルアミノメチル、モルホリノメチル、ピペラジン−1−イルメチル、及び4−(1−4C)アルキルピペラジン−1−イルメチルが含まれる。
される1以上の代謝産物により一部発揮される可能性がある。上記に述べたように、式Iの化合物の in vivo 効果は、前駆体化合物(プロドラッグ)の代謝により発揮されても
よい。
(a) R1は、H又は(1−4C)アルキルである;
(b) R1は、Hである;
(c) R1は、(1−4C)アルキルである;
(d) R1は、メチル、又はエチルである;
(e) R1は、H、メチル、又はエチルである;
(f) R1は、メチルである;
(g) R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい、(1−4C)アルキルである;
(h) R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい、(1−3C)アルキルである;
(i) R2は、ハロゲノ、ヒドロキシ、メトキシ、又はN,N−ジメチルアミノによって置換されていてもよい、(1−3C)アルキルである;
(j) R2は、メチル、エチル、プロピル、2−フルオロエチル、2−ヒドロキシエチル、2−メトキシエチル、3−メトキシプロピル、シクロプロピルメチル、又は1−(N,N−ジメチルアミノ)エチルである;
(k) R2は、メチルである;
(l) R1とR2は、ともにメチルである;
(m) R1とR2は、一緒に、酸素、窒素、及びイオウより選択される、1のさらなるヘテロ原子を含有してもよい4〜7員の窒素含有ヘテロシクリル環系を形成し、ここで環イオウ原子は、酸化されてS−オキシド(複数)を形成してもよく、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
(n) R1とR2は、一緒に、アゼパニル、オキサゼパニル、アゼチジニル、ピロリジニル、モルホリニル、チオモルホリニル、ピペリジニル、及びピペラジニルより選択される窒素含有ヘテロシクリル環系を形成し、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
(o) R1とR2は、一緒に、アゼパン−1−イル、1,4−オキサゼパン−4−イル、アゼチジン−1−イル、ピロリジン−1−イル、モルホリン−4−イル、チオモルホリン−4−イル、ピペリジン−1−イル、及びピペラジン−1−イルより選択される窒素含有ヘテロシクリル環系を形成し、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
(p) R3は、H又はメチルである;
(q) R3は、Hである;
(r) R3は、メチルである;
(s) R4とR5は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択される;
(t) R4とR5は、独立して、H、フルオロ、クロロ、メチル、エチニル、メトキシ、及びシアノより選択される;
(u) R4とR5は、独立して、H又はハロゲノより選択される;
(v) R4とR5は、独立して、H、フルオロ、又はクロロより選択される;
(w) R6、R7、及びR8は、独立して、H、フルオロ、クロロ、メチル、エチニル、メトキシ、及びシアノより選択される;
(x) R6、R7、及びR8は、独立して、H又はハロゲノより選択される;
(y) R6がHであって、R7とR8は、独立して、H、フルオロ、又はクロロより選択される;
(z) R6とR8がHであって、R4、R5、及びR7は、ハロゲノである;
(aa) R6とR8がHであって、R4、R5、及びR7は、フルオロである;
(bb) R4、R6、及びR8がHであって、R5とR7は、ハロゲノである;
(cc) R4、R6、及びR8がHであって、R5とR7は、フルオロである;
(dd) nは、0である;
(ee) nは、0又は1である;
(ff) nは、1である;
(gg) R9は、メチル又はエチルである;
(hh) R9は、メチルである;又は
(ii) nが1であって、R9は、モルホリン環の2位に位置するメチル基である。
R1がH又は(1−4C)アルキルであり;
R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい(1−4C)アルキルである;又は
R1とR2は、一緒に、酸素、窒素、及びイオウより選択される1のさらなるヘテロ原子を含有してもよい4〜7員の窒素含有ヘテロシクリル環系を形成し、ここで環イオウ原子は、酸化されてS−オキシド(複数)を形成してもよく、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
R3は、H又はメチルであり;
R4とR5は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
R6、R7、及びR8は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
nは、0である。
R1が、H、メチル、又はエチルであり;
R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい(1−4C)アルキルである;又は
R1とR2は、一緒に、アゼパニル、オキサゼパニル、アゼチジニル、ピロリジニル、モルホリニル、チオモルホリニル、ピペリジニル、及びピペラジニルより選択される窒素含有ヘテロシクリル環系を形成し、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
R3は、Hであり;
R4とR5は、独立して、H、フルオロ、又はクロロより選択され;
R6、R7、及びR8は、独立して、H又はハロゲノより選択され;
nは、0である。
R1とR2が、好適にも、上記のパラグラフ(a)〜(g)と(m)〜(o)のいずれにも定義される通りであり;
R3は、好適にも、上記のパラグラフ(p)〜(q)のいずれの1つにも定義される通りであり;
R4とR5は、好適にも、上記のパラグラフ(s)、(u)〜(v)のいずれの1つに
も定義される通りであり、そして特に上記のパラグラフ(u)〜(v)のいずれの1つにも定義される通りであり;
R6、R7、及びR8は、好適にも、上記のパラグラフ(x)〜(y)のいずれかの1つにも定義される通りであり;そして
nは、好適にも、上記のパラグラフ(dd)に定義される通りである。
R1とR2が、好適にも、上記のパラグラフ(a)〜(o)のいずれにも定義される通りであり、特に上記のパラグラフ(l)に定義される通りであり;
R3は、好適にも、上記のパラグラフ(p)〜(r)のいずれの1つにも定義される通りであり;
R4とR5は、好適にも、上記のパラグラフ(s)〜(v)のいずれの1つにも定義される通りであり、特に上記のパラグラフ(v)に定義される通りであり;
R6、R7、及びR8は、好適にも、上記のパラグラフ(w)〜(cc)のいずれの1つにも定義される通りであり、そして特に上記のパラグラフ(z)〜(cc)のいずれの1つにも定義される通りであり;そして
nとR9は、好適にも、上記のパラグラフ(dd)〜(ii)のいずれの1つにも定義される通りである。
R1が、H、メチル、又はエチルであり;
R2は、メチル、エチル、シクロプロピルメチル、2−フルオロエチル、2−ヒドロキシエチル、2−メトキシエチル、3−メトキシプロピル、又は2−(ジメチルアミノ)エチルである;又は
R1とR2は、一緒に、アゼパン−1−イル、1,4−オキサゼパン−4−イル、アゼチジン−1−イル、3−フルオロアゼチジン−1−イル、3−ヒドロキシアゼチジン−1−イル、ピロリジン−1−イル、(2R)−2−(ヒドロキシメチル)ピロリジン−1−イル、(2S)−2−(ヒドロキシメチル)ピロリジン−1−イル、モルホリン−4−イル、チオモルホリン−4−イル、ピペリジン−1−イル、4−ヒドロキシピペリジン−1−イル、4−メトキシピペリジン−1−イル、ピペラジン−1−イル、又は4−メチルピペラジン−1−イルより選択される、置換されていてもよい窒素含有ヘテロシクリル環系を形成し;
R3は、H又はメチルであり;
R4とR5は、独立して、H、フルオロ、又はクロロより選択され;
R6、R7、及びR8は、独立して、H、フルオロ、又はクロロより選択され;
nは、0である。
R1がメチルであり;
R2は、メチルである;又は
R1とR2は、一緒に、ピロリジン−1−イル環を形成する;
R3は、Hであり;
R4とR5は、独立して、H又はフルオロより選択され;
R6は、Hであり;
R7とR8は、独立して、H、フルオロ、又はクロロより選択され;
nは、0である。
R1が、H又は(1−4C)アルキルであり;
R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい(1−4C)アルキルである;又は
R1とR2は、一緒に、酸素、窒素、及びイオウより選択される1のさらなるヘテロ原子を含有してもよい4〜7員の窒素含有ヘテロシクリル環系を形成し、ここで環イオウ原子は、酸化されて、S−オキシド(複数)を形成してもよく、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
R3は、H又はメチルであり;
R4とR5は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
R6、R7、及びR8は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
nは、0又は1であり;
それぞれのR9基は、メチルである。
R1がメチルであり;
R2は、メチル又は(2−ヒドロキシ)エチルである;又は
R1とR2は、一緒に、6員の窒素含有ヘテロシクリル環系を形成し、前記環系は、ヒドロキシによって置換されていてもよい;
R3は、H又はメチルであり;
R4とR5は、独立して、H又はハロゲノより選択され;
R6、R7、及びR8は、独立して、H又はハロゲノより選択され;
nは、1であり;
R9は、モルホリン環の2位に位置するメチル基である。
R1が、H、メチル、又はエチルであり;
R2は、ハロゲノ、ヒドロキシ、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノによって置換されていてもよい(1−3C)アルキルである;又は
R1とR2は、一緒に、アゼパニル、オキサゼパニル、アゼチジニル、ピロリジニル、モルホリニル、チオモルホリニル、ピペリジニル、及びピペラジニルより選択される窒素含有ヘテロシクリル環系を形成し、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(1−3C)アルコキシ、又はヒドロキシ−(1−3C)アルキルによって置換されていてもよい;
R3は、Hであり;
R4とR5は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
R6、R7、及びR8は、独立して、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより選択され;
nは、0又は1であり;
それぞれのR9基は、(1−3C)アルキルである。
R1が、H、メチル、又はエチルであり;
R2は、メチル、エチル、シクロプロピルメチル、2−フルオロエチル、2−ヒドロキシエチル、2−メトキシエチル、3−メトキシプロピル、又は2−(ジメチルアミノ)エチルである;又は
R1とR2は、一緒に、アゼパン−1−イル、1,4−オキサゼパン−4−イル、アゼチジン−1−イル、3−フルオロアゼチジン−1−イル、3−ヒドロキシアゼチジン−1−イル、ピロリジン−1−イル、(2R)−2−(ヒドロキシメチル)ピロリジン−1−イル、(2S)−2−(ヒドロキシメチル)ピロリジン−1−イル、モルホリン−4−イル、チオモルホリン−4−イル、ピペリジン−1−イル、4−ヒドロキシピペリジン−1−イル、4−メトキシピペリジン−1−イル、ピペラジン−1−イル、又は4−メチルピペラジン−1−イルより選択される、置換されていてもよい窒素含有ヘテロシクリル環系を形成し;
R3は、H又はメチルであり;
R4とR5は、独立して、H、フルオロ、クロロ、メチル、エチニル、メトキシ、及びシアノより選択され;
R6、R7、及びR8は、独立して、H、フルオロ、クロロ、メチル、エチニル、メトキシ、及びシアノより選択され;
nは、0又は1であり;
R9は、メチルである。
R1がメチルであり;
R2は、メチルであり;
R3は、H又はメチルであり;
R4とR5は、独立して、H又はフルオロより選択され;
R6は、Hであり;
R7とR8は、独立して、H又はフルオロより選択され;
nは、0である。
例えば、本発明の特別な化合物は、以下のいずれの1つからも選択される式Iのクロメノン誘導体又はその医薬的に許容される塩である:
N−(2−(ジメチルアミノ)エチル)−8−(1−(4−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N−(2−(ジメチルアミノ)エチル)−8−(1−(3−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−8−(1−(フェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N−(2−(ジメチルアミノ)エチル)−8−(1−(4−フルオロフェニルアミノ)
エチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(モルホリン−4−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
N−(2−(ジメチルアミノ)エチル)−8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,4−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N−(2−(ジメチルアミノ)エチル)−8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3−クロロ−4−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(2,3−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(3,4,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−(1−(3−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジエチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−6−(ピロリジン−1−カルボニル)−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(4−メチルピペラ
ジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−6−(ピペラジン−1−カルボニル)−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−6−(チオモルホリン−4−カルボニル)−4H−クロメン−4−オン;
6−(アゼパン−1−カルボニル)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
6−(アゼチジン−1−カルボニル)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−6−(ピペリジン−1−カルボニル)−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−エチル−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(3−ヒドロキシアゼチジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(3−フルオロアゼチジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(2−メトキシエチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−N−プロピル−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−エチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(2−フルオロエチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(3−メトキシプロピル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−((R)−2−(ヒドロキシメチル)ピロリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−((S)−2−(ヒドロキシメチル)ピロリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N−(シクロプロピルメチル)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N−(2−メトキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−6−(1,4−オキサゼパン−4−カルボニル)−4H−クロメン−4−オン;及び
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(4−メトキシピペ
リジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン。
8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−((1R)−1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−((1S)−1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−(1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメ
ン−4−オン;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)
−N−(2−ヒドロキシエチル)−N−メチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−((R)−2−メチルモルホリノ)−4H−クロメン−4−オン;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−((R)−2−メチルモルホリノ)−4H−クロメン−4−オン;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−((R)−2−メチルモルホリノ)−4H−クロメン−4−オン;
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;及び
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド。
8−((1R)−1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−((1R)−1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−((1R)−1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カル
ボキサミド;
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1R)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−((R)−2−メチルモルホリノ)−4H−クロメン−4−オン;及び
8−((1R)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド。
8−((1S)−1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
N,N−ジメチル−2−モルホリノ−4−オキソ−8−((1S)−1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド;
8−((1S)−1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−((R)−2−メチルモルホリノ)−4H−クロメン−4−オン;及び
8−((1S)−1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド。
本発明のさらなる側面によれば、本発明の特別な化合物は、(−)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド又はその医薬的に許容される塩であり、ここで化学名の(−)−は、実施例3.06bに記載の条件を使用して測定される旋光性を表す。
本発明のさらなる側面によれば、本発明の特別な化合物は、(−)−N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド;又はその医薬的に許容される塩であり、ここで化学名の(−)−は、実施例3.13bに記載の条件を使用して測定される旋光性を表す。
、有機化学者の通常の技量内にある、例示のものに類似した手順によって入手可能である。
(a)簡便には、好適な活性化試薬の存在下での、式II:
この反応に適した活性化試薬には、例えば、四塩化スズ(IV)、三塩化アルミニウム(III)、又は四塩化チタン(IV)のようなルイス酸が含まれる。簡便には、好適な触媒は、四塩化チタン(IV)である。
又はN−メチルモルホリンといった有機塩基のような好適な塩基の存在下で実施する。簡便には、好適な塩基は、トリエチルアミンである。
らなる詳細については、例えば:「金属触媒化クロスカップリング反応(Metal-Catalyzed Cross-Coupling Reactions)」第2版、Armin Meijere, Francois Diederich(監修)
ウィリー・VCH(2004)第1巻、125 頁を参照のこと)下での反応(その後、存在するどの保護基も外す)によって製造することができる。
成してもよい。
式VIIIの化合物の式IXの化合物との反応は、簡便には、例えば、N,N−ジメチルホルムアミド、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン、ベンゼン、トルエン、キシレン、ジクロロメタン、クロロホルム、又は四塩化炭素のようなハロゲン化溶媒といった好適な溶媒又は希釈剤の存在下に、例えば20℃〜150℃の範囲、好ましくは60℃〜120℃の範囲の温度で行う。
式VIIIの化合物の式IXaの化合物との反応は、簡便には、例えば、テトラヒドロフラン、1,4−ジオキサン、1,2−ジメトキシエタン、ベンゼン、トルエン、又はキシレンのような好適な溶媒又は希釈剤の存在下に、例えば−100℃〜周囲温度の範囲、好ましくは−80℃〜20℃の範囲の温度で行う。
その後、存在するどの保護基も外す)によって製造することができる。
生成してもよい。
生成してもよい。簡便には、この触媒は、ビス(1,3−ジフェニルホスフィノ)プロパンの存在下での酢酸パラジウム(II)である。
例えば、式XIの化合物は、式XII:
範囲の温度で行う。
好適な置換可能基Lは、例えば、クロロ、ブロモ、ヨード基のようなハロゲノ基、メタンスルホニル、又はトリフルオロメタンスルホニル基である。簡便には、置換可能基Lは、ブロモである。
鹸化反応は、例えば、例えば0℃〜100℃の範囲、好ましくは20℃〜40℃の範囲の温度での、例えば、メタノール、又はエタノール及び水の混合物、又は水混和性溶媒(例えば、テトラヒドロフラン又はジオキサンのような)といった好適な溶媒中での水酸化リチウム、カリウム、又はナトリウムのようなアルカリ又はアルカリ土類金属水酸化物での式XIIの化合物の処理によって実施することができる。
基も外す)。
)ウィリー・VCH(2004)第1巻、699 頁において、パラジウム型カップリングブッフバルト(Buchwald)反応として記載されている。
例えばDCM中の酢酸銅(II)のような銅供給源によって触媒されて、大気酸素への曝露により周囲温度で行う(Tetrahedron Letters, 1998, 2933)。
ば、式Iの別の化合物へ変換し得ることを理解されたい。例えば、R3がHである式Iの化合物は、アルキル化剤でのアルキル化によって、R3が(1−3C)アルキルである式Iの化合物へ変換することができる。例えば、R3がメチルである場合、硫酸ジメチル又はヨウ化メチルのような好適なアルキル化剤を使用することができよう。この反応は、例えばナトリウムビス(トリメチルシリル)アミドのような強塩基の存在下に、好適なクラウン−エーテル(例えば、1,4,7,10,13−ペンタオキサシクロペンタデカン、ナトリウム用の15−クラウン−5としても知られている)の存在下であってもよく、低い温度(−78℃〜0℃)で、例えばTHFのような不活性溶媒において実施することができる。
式Iのクロメノン誘導体の医薬的に許容されるプロドラッグが求められるとき、それは、慣用の手順を使用して入手し得る。例えば、式Iのクロメノン誘導体の in vivo 切断
可能エステルは、例えば、カルボキシ基を含有する式Iの化合物の医薬的に許容されるアルコールとの反応によるか、又はヒドロキシ基を含有する式Iの化合物の医薬的に許容されるカルボン酸との反応によって入手し得る。例えば、式Iのクロメノン誘導体の in vivo 切断可能アミドは、例えば、カルボキシ基を含有する式Iの化合物の医薬的に許容さ
れるアミンとの反応によるか、又はアミノ基を含有する式Iの化合物の医薬的に許容されるカルボン酸との反応により入手し得る。
酸化物、例えば水酸化リチウム又はナトリウムのような好適な塩基での加水分解によって外してよい。あるいは、t−ブトキシカルボニル基のようなアシル基は、例えば、塩酸、硫酸、又はリン酸、又はトリフルオロ酢酸のような好適な酸での処理によって外してよく、ベンジルオキシカルボニル基のようなアリールメトキシカルボニル基は、例えば、パラジウム担持カーボンのような触媒上での水素化によって、又はルイス酸、例えばトリス(トリフルオロ酢酸)ホウ素での処理によって外してよい。一級アミノ基に適した代わりの保護基は、例えばフタロイル基であり、これは、アルキルアミン、例えばジメチルアミノプロピルアミンでの、又はヒドラジンでの処理によって外してよい。
本明細書で明確化される中間体のあるもの(例えば、式II、IV、V、VII、VIIIa、VIIIb、X、Xa、XI、XII、XIII、XIV、XV、XVa、XVI、XVIIの化合物)は新規であり、これらは、本発明のさらなる特徴として提供される。例えば、式VIIIa(式中、n、R9、及びR10は、上記に定義される意味のいずれも有する)の化合物は、本発明の特別な化合物の製造における中間体として有用であり得る:
以下のアッセイを使用して、PI3−キナーゼ酵素の阻害剤として、MAD−MB−468細胞におけるホスホAKT(ser473)の in vitro 阻害剤として、スイス無胸腺nu/nuマウスにおけるホスホAKT(ser473)の in vivo 阻害剤として、
及びヒト前立腺癌細胞系、PC3を移植したスイス無胸腺nu/nuマウスにおける腫瘍増殖の in vivo 阻害剤としての本発明の化合物の効果を測定することができる。
ヒト組換え酵素を使用する、Kinase Gloベースの酵素活性アッセイにおいて、PI3Kβ、PI3Kα、PI3Kγ、及びPI3Kδの阻害を評価した。このアッセイでは、酵素、PIP2、及びATP、+化合物とのインキュベーション後のATPの枯渇を測定する。この反応の終了時に、Kinase Glo試薬の添加によってATPを検出するが、ここでは、Ultra GloTMルシフェラーゼ(プロメガ)がATPを基質として使用して、ルシフェリンの一酸素添加と光の産生を触媒する。Kinase Glo Plus試薬で測定される発光と完了したキナーゼ反応物に残存するATPの量の間には正の相関性が存在して、発光は、キナーゼ活性に逆相関する。12種の異なる化合物濃度について試験して、PI3Kβ、PI3Kα、PI3Kγ、及びPI3Kδの阻害からの生データを阻害剤濃度に対してプロットした。
100% DMSO中の化合物を音響分配によってアッセイプレートへ加えた。PI3Kβをトリス緩衝液(50mM トリス(pH7.4)、0.05% CHAPS、2.1mM DTT、及び10mM MgCl2)に加えて、そのまま化合物とともに20分間プレインキュベートした後で、PIP2及びATPを含有する基質溶液を加えた。80分後に、Kinase Glo検出溶液の添加によってこの酵素反応を止めた。プレートをそのまま室温で30分放置してから、感度を最大ウェルに設定した Pherastar 機器(
発光ATP384プログラム)で読み取った。アッセイ液中のDMSO、ATP、及びPIP2の最終濃度は、それぞれ、1%、8μM、及び80μMであった。
生データを阻害剤濃度へ適合させる、非線形回帰パッケージへ適合した対数曲線を使用して、IC50値を計算した。IC50値は、酵素活性の50%を阻害した試験化合物の濃度である。
MDA−MB−468細胞(ヒト乳腺癌:ATCC HTB 132)を Greiner 3
84ウェル黒色平底プレートの中へ自動化細胞培養ロボット(Selec T)によって播く。細胞は、手動で維持して、マルチドロップ又は Wellmate を使用してプレート中へ播いてもよい。10% FCS及び1%グルタミンを含有する40μlのDMEN中に1500細胞/ウェルで細胞を播く。細胞プレートを37℃インキュベーターにおいて18
時間インキュベートする。
する通風室において、10μlの3.7%ホルムアルデヒド溶液の添加によって細胞を固定する。固定を可能にする30分後に固定液と培地を除去して、通風室において Tecan PW384 プレート洗浄器を使用して、プレートを Proclin PBS/Aで洗浄する。Wellmate
を使用して、0.5% Tween20及び1% marvelを含有する40μlの
PBSの添加でウェルをブロックして透過処理して、室温で60分間インキュベートする。
ギ抗ホスホAKT Ser473(Cell signaling technologies,カタログ番号378
7)を1%marvel(乾燥ミルク粉末)を含有するPBS/Tで500倍希釈したものであり、4℃で一晩インキュベートする。
キュベートする。二次抗体溶液は、Alexa Fluor 488 抗ウサギ(Molecular Probes,カタログ番号A11008)を、1% marvel を含有するリン酸緩衝化生理食塩水+0.05%(v/v)Polysorbate 20 で1000倍希釈したものである。プレートを先述のよう
に3回洗浄してから、各ウェルへ20μl PBSを加えて、プレートを黒色のプレートシーラーで密封する。
スイス無胸腺nu/nuマウスにヒト前立腺癌細胞系PC3(ATCC CRL1435)を皮下移植して、PI3−キナーゼ阻害剤の抗腫瘍活性を決定することができる。0日目、その動物の左脇腹に50% MatrigelTM(BD Biosciences #354234)中1X106個の細胞を皮下注射する。腫瘍が約400〜600mm3の体積に達したときに動物を必要とされる群サイズ(典型的には、各処置群につき5匹)へ無作為化して、処置を開始する。終了時に腫瘍を取って、液体窒素で瞬間凍結させて、分析まで−80℃で保存する。
P2850、Sigma #P5726(100倍希釈)とプロテアーゼ阻害剤、Sigma #P8340(200倍希釈)を加える。この腫瘍を、Fastprep マシーン上で1分間ホモジェ
ナイズしてから、氷上に10分間放置する。冷却した遠心分離機において、試料を13,000rpmで10分間スピンさせる。次いで、澄明化したライゼートを新鮮な試験管へ入れて、5μlをタンパク定量アッセイに使用する。すべての腫瘍試料を同じ濃度へ希釈して、4〜15% NuPAGEビス−トリスゲル(Invitrogen)上のレーンにつき15
μgを140ボルトで90分間泳動させる。試料は、ゲル効果が最小になるように無作為化する。ニトロセルロース膜へのブロッティングの後で、それらを1時間ブロックして、全AKT(CST #9272)又はホスホAKT−ser473(CST #9271)のいずれか一方に対する抗体の500倍希釈液とともに一晩インキュベートする。ブロットをPBS/T中で3回洗浄した後で、抗ウサギ二次HRP結合抗体(CST #7074)の2,000倍希釈液とともに室温で1時間インキュベートする。ブロック及び抗体インキュベーションの緩衝液は、0.05% Polysorbate 含有PBS中の5%乾燥ミ
ルク粉末である。ブロットをPBS/Tにおいて3回洗浄してから、Pierce West Dura ECL キットと ChemiGenius を使用して可視化する。各試料についてバンドを定量化して、ホスホのシグナル全体に対する比を入手する。対照値を平均して、それぞれの処置試料を平均化した対照値に対して正規化する。
スイス無胸腺nu/nuマウスにヒト前立腺癌細胞系PC3(ATCC CRL1435)を皮下移植して、PI3−キナーゼ阻害剤の抗腫瘍活性を決定することができる。0日目、その動物の左脇腹に50% Matrigel(BDM)中1X106個の細胞を皮下注射する。腫瘍が約200〜300mm3の体積に達したときに動物を10〜15匹の群へ無作為化して、処置を開始する。動物に、好適な担体中の化合物(及び、任意選択的に、1−アミノベンゾトリアゾールのようなcyp阻害剤)を一定の用量で経口、静脈内、又は腹腔内の経路によって2〜4週間投薬する。通常、週2回、腫瘍をノギスによって測定して、楕円の式(π/6x幅x幅x長さ)を使用して、腫瘍の体積を計算する。
試験(b):MAD−MB−468細胞中の細胞性ホスホAKT(ser473)に対して、例えば、1nM〜25μMの範囲のIC50
簡便には、本発明の特別な化合物は、上記の試験(a)及び(b)の1以上において、以下の濃度又は用量で活性を保有する。
試験(b):MAD−MB−468細胞中の細胞性ホスホAKT(ser473)に対して、例えば、1nM〜20μMの範囲のIC50
簡便には、本発明の特別な化合物は、上記の試験(a)、(b)、(c)及び(d)の1以上において、以下の濃度又は用量で活性を保有する。
試験(b):MAD−MB−468細胞中の細胞性ホスホAKT(ser473)に対して、例えば、1nM〜20μMの範囲のIC50
試験(c):例えば、1〜200mg/kg/日の範囲での、in vivo ホスホAKT(ser473)の>50%阻害
試験(d):例えば、1〜200mg/kg/日の範囲での、異種移植片活性
例えば、実施例1.00として開示されるクロメノン化合物は、試験(a)では、PI3Kβに対してほぼ2nMのIC50で活性を保有し;そして試験(b)では、MAD−MB−468細胞中の細胞性ホスホAKT(ser473)に対してほぼ9nMのIC50で活性を保有する。
表A
は油性の懸濁液剤、乳剤、分散性の散剤又は顆粒剤、シロップ剤又はエリキシル剤として)、局所使用に(例えば、クリーム剤、軟膏剤、ゲル剤、又は水性又は油性の溶液剤又は懸濁液剤として)、吸入による投与に(例えば、微細化散剤又は液体エアゾール剤として)、通気による投与に(例えば、微細化散剤として)、非経口投与に(例えば、静脈内、皮下、腹腔内、又は筋肉内投薬用の無菌の水性又は油性溶液剤として)、又は直腸投薬用に(坐剤として)適した形態であってよい。
薬品の製造における使用を提供する。
に対するか、又はEGF受容体チロシンキナーゼ、VEGF受容体チロシンキナーゼ、又はSrc非受容体チロシンキナーゼ酵素に対するよりも、クラスIa PI3−キナーゼ酵素に対して、実質的に優る効力を保有する。そのような化合物は、クラスIa PI3−キナーゼ酵素に対して十分な効力を保有するので、クラスIb PI3−キナーゼ酵素に対して、又はEGF受容体チロシンキナーゼ、VEGF受容体チロシンキナーゼ、又はSrc非受容体チロシンキナーゼ酵素に対してほとんど活性を示さない一方で、クラスIa PI3−キナーゼ酵素を阻害するには十分な量で使用し得る。そのような化合物は、クラスIa PI3−キナーゼ酵素の選択的な阻害に有用である可能性があり、例えば、クラスIa PI3−キナーゼ酵素推進性の腫瘍の有効な治療に有用である可能性がある。
(ALL及びCMLが含まれる)、多発性骨髄腫及びリンパ腫の治療に使用の医薬品の製造における使用を提供する。
又は動物の体内で生成される1以上の代謝産物によって一部発揮されてよい。
本発明の特別な化合物は、α、γ、及びδのような他のクラスI PI3−キナーゼアイソフォームに対してより、PI3−キナーゼβに対してより優れた効力を保有する。
PI3−キナーゼ脂質産物、PI(3,4,5)P3及びPI(3,4)P2の無制御の調節は、いくつかの悪性腫瘍のヒトにおける進展において重要な役割を担う(Leevers et
al., 1999, Current Opinion in Cell Biology 11:219-225)。これらの種類の癌では、ホスホイノシチド3−キナーゼβ(PI3Kβ)アイソフォームの特殊な役割が記載されている(Jia S et al., 2008, Nature 454(7205):776-9; Wee et al., 2008, PNAS 105(35):13057-62)。故に、PI3−キナーゼの阻害剤である、式(I)の化合物又はその医
薬的に許容される塩は、ヒトにおいて新生物を治療するために使用し得る。
(43):28025-31)とリンパ球の機能(Vicente-Manzanares et al., 1999, The Journal of
Immunology 163(7):4001-4012)にも重要な役割を担っている。例えば、炎症した内皮への白血球の付着には、PI3−キナーゼ依存性のシグナル伝達プロセスによる、内因性白血球インテグリンの活性化が関与する。さらに、PI3−キナーゼシグナル伝達には、好中球における酸化バースト(Nishioka et al., 1998, FEBS Letters 441(1):63-66 and Condliffe, A.M., et al., Blood, 2005. 106(4):1432-40)と細胞骨格の再組織化(Kirsch et al., 1999, Proceedings National Academy of Sciences USA 96(11):6211-6216)
が関与するらしい。好中球の遊走と指向性運動も、PI3−キナーゼ活性に依存している(Camps, M., et al., Nat Med, 2005. 11(9): p. 936-43 and Sadhu, C., et al., J Immunol, 2003. 170(5): 2647-54)。従って、PI3−キナーゼの阻害剤は、炎症の部位での白血球の付着及び活性化を抑制するのに有用であり得て、故に、急性及び/又は慢性の炎症障害を治療するのに使用し得る。PI3−キナーゼは、リンパ球の増殖及び活性化にも重要な役割を担っている(Fruman et al., 1999, Science 283 (5400): 393-397)。自己免疫疾患におけるリンパ球の重要な役割に照らせば、PI3−キナーゼ活性の阻害剤は、このような障害の治療に使用し得る。
(ii)抗エストロゲン(例えば、タモキシフェン、フルベストラント、トレミフェン、ラロキシフェン、ドロロキシフェン、及びヨードキシフェン)、抗アンドロゲン(例えば、ビカルタミド、フルタミド、ニルタミド、及び酢酸シプロテロン)、LHRLアンタゴニスト又はLHRHアゴニスト(例えば、ゴセレリン、リュープロレリン、及びブセレリン)、プロゲストゲン(例えば、酢酸メゲストロール)、アロマターゼ阻害剤(例えば、アナストロゾール、レトロゾール、ボラゾール、及びエキセメスタン)、並びにフィナステリドのような5α−レダクターゼの阻害剤といった、細胞増殖抑止剤;
(iii)抗浸潤剤[例えば、4−(6−クロロ−2,3−メチレンジオキシアニリノ)−7−[2−(4−メチルピペラジン−1−イル)エトキシ]−5−テトラヒドロピラン−4−イルオキシキナゾリン(AZD0530;国際特許出願WO01/94341)、N−(2−クロロ−6−メチルフェニル)−2−{6−[4−(2−ヒドロキシエチル)ピペラジン−1−イル]−2−メチルピリミジン−4−イルアミノ}チアゾール−5−カルボキサミド(ダサチニブ、BMS−354825;J. Med. Chem., 2004, 47, 6658-6661)、及びボスチニブ(SKI−606)のようなc−Srcキナーゼファミリー阻害剤、及びマリマスタトのようなメタロプロテイナーゼ阻害剤、ウロキナーゼプラスミノゲンアクチベータ受容体機能の阻害剤、又はヘパラナーゼへの抗体];
(iv)増殖因子機能の阻害剤:例えば、そのような阻害剤には、増殖因子抗体と増殖
因子受容体抗体(例えば、抗erbB2抗体のトラスツズマブ[HerceptinTM]、抗EGFR抗体のパニツムマブ、抗erbB1抗体のセツキシマブ[Erbitux,C225]、及び、Stern et al.Critical reviews in oncology/haematology, 2005, Vol. 54, pp11-29 によって開示されるあらゆる増殖因子又は増殖因子受容体の抗体が含
まれる;そのような阻害剤にはまた、例えば、チロシンキナーゼ阻害剤、例えば、表皮増殖因子ファミリーの阻害剤(例えば、N−(3−クロロ−4−フルオロフェニル)−7−メトキシ−6−(3−モルホリノプロポキシ)キナゾリン−4−アミン(ゲフィチニブ、ZD1839)、N−(3−エチルフェニル)−6,7−ビス(2−メトキシエトキシ)キナゾリン−4−アミン(エルロチニブ、OSI−774)、及び6−アクリルアミドーN−(3−クロロ−4−フルオロフェニル)−7−(3−モルホリノプロポキシ)−キナゾリン−4−アミン、CI 1033)のようなEGFRファミリーチロシンキナーゼ阻害剤、ラパチニブのようなerbB2チロシンキナーゼ阻害剤);肝細胞増殖因子ファミリーの阻害剤;インスリン増殖因子受容体の阻害剤;イマチニブ及び/又はニロチニブ(AMN107)のような血小板由来増殖因子ファミリーの阻害剤;セリン/スレオニンキナーゼの阻害剤(例えば、ファルネシルトランスフェラーゼ阻害剤のようなRas/Rafシグナル伝達阻害剤、例えば、ソラフェニブ(BAY43−9006)、チピファルニブ(R115777)及びロナファルニブ(SCH66336));MEK及び/又はAKTキナーゼを介した細胞シグナル伝達の阻害剤、c−kit阻害剤、ablキナーゼ阻害剤、PI3−キナーゼ阻害剤、Plt3キナーゼ阻害剤、CSF−1Rキナーゼ阻害剤、IGF受容体(インスリン様増殖因子)キナーゼ阻害剤;auroraキナーゼ阻害剤(例えば、AZD1152、PH739358、VX−680、MLN8054、R763、MP235、MP529、VX−528、及びAX39459)、並びに、CDK2及び/又はCDK4阻害剤のようなサイクリン依存型キナーゼ阻害剤が含まれる;
(v)血管内皮増殖因子の効果を阻害するような抗血管新生剤[例えば、抗血管内皮細胞増殖因子抗体のベバシズマブ(AvastinTM)、及び、例えば、バンデタニブ(ZD6474)、バタラニブ(PTK787)、スニチニブ(SU11248)、アキシチニブ(AG−013736)、パゾパニブ(GW786034)、及び4−(4−フルオロ−2−メチルインドール−5−イルオキシ)−6−メトキシ−7−(3−ピロリジン−1−イルプロポキシ)キナゾリン(AZD2171;WO00/47212内の実施例240)のようなVEGF受容体チロシンキナーゼ阻害剤、国際特許出願WO97/22596、WO97/30035、WO97/32856andWO98/13354に開示されるような化合物、並びに他の機序によって作用する化合物(例えば、リノマイド、インテグリンαvβ3機能の阻害剤、及びアンジオスタチン)];
(vi)コンブレタスタチンA4のような血管傷害剤と、国際特許出願WO99/02166、WO00/40529、WO00/41669、WO01/92224、WO02/04434、及びWO02/08213に開示される化合物;
(vii)エンドセリン受容体アンタゴニスト、例えば、ジボテンタン(ZD4054)又はアトラセンタン;
(viii)アンチセンス療法、例えば、ISIS2503、抗rasアンチセンスのような、上記に列挙される標的へ指向されるもの;
(ix)例えば、異常p53又は異常BRCA1若しくはBRCA2のような異常遺伝子を置換するアプローチ、シトシンデアミナーゼ、チミジンキナーゼ、又は細菌の窒素レダクターゼ酵素を使用するようなGDEPT(遺伝子指向型酵素プロドラッグ療法)アプローチ、及び、多剤耐性遺伝子治療のような、化学療法又は放射線療法への患者耐性を高めるアプローチが含まれる、遺伝子治療アプローチ;並びに
(x)インターロイキン2、インターロイキン4、又は顆粒球マクロファージコロニー刺激因子のようなサイトカインでのトランスフェクションのような、患者腫瘍細胞の免疫原性を高めるための ex-vivo 及び in-vivo アプローチ、T細胞アネルギーを減少させるアプローチ、サイトカインにトランスフェクトされた樹状細胞のようなトランスフェクトされた免疫細胞を使用するアプローチ、サイトカインにトランスフェクトされた腫瘍細胞
系を使用するアプローチ、及び抗イディオタイプ抗体を使用するアプローチが含まれる、免疫療法アプローチ。
a)第一の単位剤形における、式(I)の化合物又はその医薬的に許容される塩;
b)第二の単位剤形における、上記の(i)〜(ix)の下に列挙した1つより選択される抗腫瘍剤;及び
c)前記第一及び第二の剤形を含有するための容器手段;
を含んでなるキットが提供される。
(i)他に述べなければ、各種操作は、周囲温度で、即ち17〜25℃の範囲で、そして窒素のような不活性気体の雰囲気下で行った。
で利用することによって行って、後処理手順は、残留固形物の濾過による除去の後で行った。
又は40〜63μm)を使用する、自動化 Armen Glider Flash:Spot II Ultimate(Armen Instrument,サンアベ、フランス)で実施した。
(vi)全般に、式Iの最終生成物の構造は、核磁気共鳴(NMR)分光法によって確定した;NMR化学シフト値は、δスケールで測定した[Bruker Avance 500(500M
Hz)機器を使用して、プロトン磁気共鳴スペクトルを決定した];他に特定しなければ、測定値は、周囲温度で記録した;以下の略語を使用した:s,一重項;d,二重項;t,三重項;q,四重項;m,多重項;dd,二重項の二重項;ddd,二重項の二重項の二重項;dt,三重項の二重項;bs,ブロードシグナル。
分析計と X-Bridge 5μm C−18カラム(2.1x50mm)を装着した Waters Alliance HT(2790及び2795)を使用して、95% A+5% C〜95% B+
5% Cの溶媒系を2.4mL/分の流速で4分にわたって使用して行った[ここでA=水、B=メタノール、C=1:1 メタノール:水(0.2%炭酸アンモニウムを含有する)である]。
(ix)X線粉末回折スペクトルは、結晶性の材料の試料を Bruker 単シリコン結晶(
SSC)ウェファマウント上に載せて、顕微鏡スライドを利用してその試料を薄層へ広げることによって決定した。試料は、1分につき30回転でスピンさせて(計数統計を向上させるために)、1.5418オングストロームの波長、40kV及び40mAで操作する、銅ロングファインフォーカス管によって発生されるX線を照射した。視準化したX線源をV20に設定した自動可変発散スリットに通過させて、反射した放射線を5.89mm抗分散スリットと9.55mm検出器スリットに通して向けた。試料は、θ−θ形式で2°〜40°(2θ)の範囲にわたって、0.00570°(2θ)増分につき0.03秒間(連続スキャン形式)曝露した。操作時間は、3分と36秒であった。この機器には、位置有感検出器(Lynxeye)を取り付けた。対照及びデータの捕捉は、Diffrac+ソフトウェアで操作する、Dell Optiplex 686 NT 4.0 Workstation を利用した。X線粉末回折
の技術分野の当業者であれば、ピークの相対強度が、例えば、30ミクロンより大きいサイズの粒子と非ユニタリアスペクト比によって影響を受ける可能性があり、これが試料の分析に影響を及ぼす場合があることも理解されよう。当業者はまた、回折計において試料が載る正確な高さと回折計のゼロ較正によって反射の位置が影響を受ける可能性があることも理解されよう。試料の表面の平面性もわずかな影響を及ぼす場合がある。従って、提示される回折パターンデータを絶対的な数値とみなしてはならない。
典型的には、蓋付きの標準アルミニウム鍋に封じ込めた5mg未満の材料を10℃/分の一定した加熱速度で25℃〜300℃の温度範囲にわたって加熱した。窒素を使用するパージガスを50mL/分の流速で使用した。
aq. 水性
CDCl3 重クロロホルム
CHCl3 クロロホルム
DCM ジクロロメタン
DEA ジエチルアミン
DIPEA N−エチル−N−イソプロピルプロパン−2−アミン
DMF N,N−ジメチルホルムアミド
DMSO ジメチルスルホキシド
DSC 示差走査熱量測定法
DTAD ジアゼン−1,2−ジカルボン酸(E)−ジtert−ブチル
EDCI 1−(3−ジメチルアミノプロピル)−3−エチルカルボジイミド塩酸塩
Ether ジエチルエーテル
%ee エナンチオマー過剰率
HOPO 2−ヒドロキシ−ピリジンn−オキシド
IPA イソプロピルアルコール
MeCN アセトニトリル
MeOH メタノール
MTBE メチルtert−ブチルエーテル
NMP 1−メチル−2−ピロリジン
sat. 飽和
sol. 溶液
THF テトラヒドロフラン
TEA トリエチルアミン
TBTU テトラフルオロホウ酸2−(1H−ベンゾ[d][1,2,3]トリアゾール−1−イル)−1,1,3,3−テトラメチルイソウロニウム
TSTU テトラフルオロホウ酸2−(2,5−ジオキソピロリジン−1−イル)−1,1,3,3−テトラメチルイソウロニウム
N−(2−(ジメチルアミノ)エチル)−8−(1−(4−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
0mm、40mL/分の流速)と極性が減少する水(0.2%炭酸アンモニウムを含有する)及びアセトニトリルの混合物を溶出液として使用する分取用HPLCで第二の精製を行った。所望の化合物を含有する画分を蒸発乾固させて白色の固形物を得て、これをMTBEで摩砕してから真空下に乾燥させて、N−(2−(ジメチルアミノ)エチル)−8−(1−(4−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(73.0mg,58.6%)を得た。質量スペクトル: M+H+ 483。NMR スペクトル: (CDCl3) 1.60 (d, 3H), 2.25 (s, 6H), 2.50 (t, 2H), 3.45-3.58 (m, 6H), 3.79-3.89 (m, 4H), 4.02 (bs, 1H), 4.88-4.98 (m, 1H), 5.56 (s, 1H), 6.40 (dd, 2H), 6.81 (dd, 2H), 6.91 (bs, 1H), 8.27 (d, 1H), 8.34 (d, 1H)。
4−ヒドロキシ安息香酸メチル(180g,1183ミリモル)のDCM(3L)中の撹拌懸濁液へ臭素(64mL,1242ミリモル)を窒素下に0℃で滴下して、この反応混合物をそのまま室温で36時間撹拌した。次いで、温度を15℃付近に保ちながらチオ硫酸ナトリウムの溶液(10%溶液の500mL)を加えて、MeOH(250mL)の添加を続けた。有機層を水、次いで塩水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して濃縮乾固させて、3−ブロモ−4−ヒドロキシ安息香酸メチル(290g)を白色の固形物として得た。質量スペクトル: [M-H]- 229。
3−ブロモ−4−ヒドロキシ安息香酸メチル(270g,1168ミリモル)のDCM(1.5L)中の撹拌懸濁液へピリジン(150mL)を加えた。次いで、塩化アセチル(87mL,1227ミリモル)を室温で窒素下に滴下した。この混合物をそのまま室温で2時間撹拌した。次いで、水(1L)に続いて、HCl(2N)をpH1まで加えた。次いで、有機層を水、塩水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して蒸発乾固させて、4−アセトキシ−3−ブロモ安息香酸メチル(300g,94%)を白色の粉末として得た。NMR スペクトル: (DMSOd6) 2.34 (s, 3H), 3.87 (s, 3H), 7.47 (d, 1H), 8.01 (dd, 1H), 8.20 (d, 1H)。
4−アセトキシ−3−ブロモ安息香酸メチル(150g,549.3ミリモル)へ三塩化アルミニウム(220g,1647.9ミリモル)を加えて、この混合物を溶媒の非存在下に140℃で3時間加熱した。室温へ冷却後すぐにこの固形物を砕いて、撹拌しながら水(1.5L)へ慎重に加えた。次いで、HCl(12Nの250mL)を加えて、撹拌を30分間維持した。入手した固形物を濾過によって採取し、水(2x2L)で洗浄して一晩乾燥させて、3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸(120g,84%)を黄色の粉末として得た。質量スペクトル: [M-H]- 258。
3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸(240g,926ミリモル)のMeOH(2L)中の撹拌懸濁液へ二塩化イオウ(68mL,926.5ミリモル)を窒素下に滴下して、この混合物を80℃で3時間加熱した。この反応混合物を室温へ冷やし、濃縮し、DCMで希釈した。有機層を塩水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して濃縮して粗製の化合物を得て、これを石油エーテル中70%のDCMで溶出させるシリカで精製した。溶媒を蒸発乾固させて、3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸メチル(108g,42.7%)を白色の粉末として得た。質量スペクトル: [M-H]- 229。
モルホリン(201mL,2295ミリモル)の水(2L)中の撹拌溶液へ二硫化炭素(0.138L,2295.67ミリモル)を窒素下に加えた。次いで、水酸化ナトリウム(96g,1Lの水溶液中2410ミリモル)を滴下した。生じる混合物を室温で1時間撹拌してから、氷浴で5℃へ冷やして、硫酸ジメチル(217mL,2295ミリモル)を滴下した。この混合物を室温で1時間撹拌し、得られる固形物を濾過によって採取し、水(2x1L)で洗浄して真空下に五酸化リン上50℃で乾燥させて、モルホリン−4−カルボジチオ酸メチル(360g,88%)を得た。NMR スペクトル: (CDCl3): 2.68 (s, 3H), 3.71-3.84 (m, 4H), 4.02 (bs, 2H), 4.30 (bs, 2H)。
温度を10〜15℃付近に維持しながら、モルホリン−4−カルボジチオ酸メチル(170g,959ミリモル)のDCM(1.5L)溶液に塩素ガス(455g,6417ミリモル)を2時間の時間にわたって泡立てて通した。この塩素添加を完了してすぐに、撹拌をさらに1.5時間維持すると、その間に沈殿が生じた。次いで、窒素をこの混合物に30分間通した。この固形物を窒素下に濾過によって採取し、DCMで洗浄して、窒素下に冷蔵庫で保存した。このようにして、塩化4−(ジクロロメチレン)モルホリン−4−イウム(180g,92%)を白色の吸湿性固形物として入手した。
3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸メチル(106g,388ミリモル)のトルエン(1L)中の撹拌溶液へ(ジエチルオキソニオ)トリフルオロホウ酸塩(0.201L,1630ミリモル)を窒素下に滴下した。生じる溶液をそのまま室温で一晩撹拌してから、塩化4−(ジクロロメチレン)モルホリン−4−イウム(143g,698ミリモル)を加えて、この混合物を90℃で12時間加熱した。室温へ冷却後すぐにジエチルエーテル(1.5L)を加えて、固形物を濾過によって採取した。次いで、この固形物をMeOH(1L)に懸濁させて、この混合物を50℃で2時間加熱した。
MeOH(30mL)に溶かした8−ブロモ−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸メチル(1.6g,4.35ミリモル)の撹拌懸濁液へ水酸化ナトリウム(4.35mL,8.69ミリモル)を加えた。生じる懸濁液を23℃で16時間撹拌した。この混合物を水で希釈して、pHをHCl(2N)で3へ調整した。沈殿を濾過によって採取し、水で洗浄して五酸化リン上で一晩乾燥させて、8−ブロモ−2−モ
ルホリノ−4−オキソ−4H−クロメン−6−カルボン酸(1.30g,84%)をベージュ色の固形物として得た。質量スペクトル: M+H+ 356。
8−ブロモ−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸(215mg,0.61ミリモル)及びトリブチル(1−エトキシビニル)スタンナン(0.226mL,0.67ミリモル)の1,4−ジオキサン(5mL)中の撹拌混合物へ塩化ビス(トリフェニルホスフィン)パラジウム(II)(12.78mg,0.02ミリモル)を加えて、この混合物を窒素でパージした。生じる混合物を100℃で3時間撹拌した。HCl(2N)(0.5mL)を加えて、この反応混合物を50℃で25分間撹拌してから、そのまま室温へ冷やして、真空下に濃縮した。生成物をジエチルエーテルとペンタンで希釈しして固形物を得て、これを濾過によって採取してエーテル/ペンタンで洗浄して、8−アセチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸(200mg,104%)をベージュ色の固形物として得た。質量スペクトル: M+H+ 318。
8−アセチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸(470mg,1.48ミリモル)のDCM(10mL)懸濁液へ室温でDIPEA(0.284mL,1.63ミリモル)とTSTU(491mg,1.63ミリモル)を加えた。この混合物を15分間撹拌し、N1,N1−ジメチルエタン−1,2−ジアミン(0.171mL,1.56ミリモル)を加えて、撹拌をさらに1時間維持した。この混合物をシリカゲル上に吸着させて、DCM中5〜10%メタノールに次いでDCM中10%メタノール性アンモニア(7N)で溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させて、8−アセチル−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(352mg,61.3%)をベージュ色の固形物として得た。質量スペクトル: M+H+ 388。
4−ヒドロキシ安息香酸メチル(500g,3286ミリモル)のDCM(4L)中の撹拌懸濁液へ二臭素(0.185L,3614.92ミリモル)をN2下に0℃で滴下した。この混合物をそのままN2下に室温で24時間撹拌した(HBrを捕捉する必要がある)。次いで、温度を15℃付近に保ちながら、メタ重亜硫酸ナトリウム(62.5g,329ミリモル)の2Lの水溶液に続いて500mLのMeOHを加えた。有機層を水、塩水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して濃縮乾固させて、3−ブロモ−4−ヒドロキシ安息香酸メチル(710g,94%)を白色の固形物として得た。NMR スペ
クトル (CDCl3): 3.89 (s, 3H), 5.95 (s, 1H), 7.05 (d, 1H), 7.92 (dd, 1H), 8.19 (d, 1H)。
3−ブロモ−4−ヒドロキシ安息香酸メチル(350g,1514.87ミリモル)のエタノール(3L)中の脱気溶液へトリエチルアミン(0.528L,3787.17ミリモル)、1−(ビニルオキシ)ブタン(0.588L,4544.60ミリモル)、1,1’−ビス(ジフェニルホスフィノ)フェロセン(33.1g,60.6ミリモル)、及びジアセトキシパラジウム(8.50g,37.9ミリモル)を窒素下に加えた。この混合物を70℃で一晩加熱した。この反応物を冷却し、濾過して、濾液を濃縮した。生じる固形物をDCM(2L)で可溶化して、HCl(4N)(1.14L,4544ミリモル)を撹拌下に加えた。撹拌を2時間維持し、有機相を分離させ、硫酸マグネシウムで乾燥させ、濾過して濃縮して固形物を得て、これをジエチルエーテル(5L)中で2時間撹拌した。この固形物を濾過して除き、濾液を濃縮乾固させて、3−アセチル−4−ヒドロキシ安息香酸メチル(240g,82%)をベージュ色の粉末として得た。質量スペクトル: [M-H]- 193。
3−アセチル−4−ヒドロキシ安息香酸メチル(240g,1236ミリモル)のDCM(2L)中の撹拌溶液へピリジン(0.400L,4944ミリモル)を0℃で加えて、二臭素(0.070L,1360ミリモル)の滴下を続けた。この反応混合物を室温で2時間撹拌してから、5℃へ冷やして、HCl(4N)(0.927L,3708ミリモル)を滴下した。有機相を分離させ、硫酸マグネシウムで乾燥させ、濾過して濃縮して茶褐色の固形物を得て、これをエーテル/石油エーテル(1:1,1L)中で1時間撹拌した。この固形物を濾過によって採取して乾燥させて、3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸メチル(270g,80%)をベージュ色の粉末として得た。
リチウムビス(トリメチルシリル)アミドの溶液(1.41L,1406ミリモル)へ窒素下に−65℃でTHF(1.2L)中の3−アセチル−5−ブロモ−4−ヒドロキシ安息香酸メチル(120g,439ミリモル)を滴下した。この溶液をそのまま0℃へ温めて、この温度で1時間維持した。この溶液を再び−65℃へ冷やして、塩化モルホリン−4−カルボニル(0.055L,483ミリモル)を加えた。この混合物を室温で2時間撹拌してから−30℃へ冷やし、DCM(1.5L)と水(1L)を加えて、HCl(6N)(500mL)に次ぐHCl(2N)(300mL)の滴下をpH7まで続けて、この水溶液をDCM(3X)で抽出した。合わせた抽出物を硫酸マグネシウムで乾燥させて、蒸発させた。この粗生成物をMTBEで摩砕して、3−ブロモ−4−ヒドロキシ−5−(3−モルホリノ−3−オキソプロパノイル)安息香酸メチル(153g,90%)をベージュ色の固形物として得た。質量スペクトル: M+H+ 388。
1,2−ジクロロエタン(1L)に溶かした3−ブロモ−4−ヒドロキシ−5−(3−モルホリノ−3−オキソプロパノイル)安息香酸メチル(433g,1122ミリモル、いくつかのバッチよりプールした材料)の撹拌溶液へトリフルオロメタンスルホン酸無水物(0.755L,4487ミリモル)を窒素下に室温で加えた(発熱)。生じる溶液を50℃で一晩撹拌した。この混合物を一部蒸発させて、残渣をMeOH(1.6L)で、0℃で希釈して(発熱)、室温で1時間撹拌した。溶媒を再び蒸発させて、残渣をDCMに希釈し、炭酸ナトリウムの飽和水溶液で冷まして、DCMで抽出した。合わせた有機相を塩水で洗浄し、硫酸マグネシウムで乾燥させて濃縮して、粗生成物を得た。この粗生成物をMTBE(2x)、酢酸エチル(1x)、及びMTBE(1x)下で摩砕した。この
固形物を乾燥させて、8−ブロモ−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸メチル(208g,50%)をベージュ色の固形物として得た。質量スペクトル: M+H+ 370。
N−(2−(ジメチルアミノ)エチル)−8−(1−(3−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
(t, 2H), 3.44-3.58 (m, 6H), 3.78-3.89 (m, 4H), 4.55 (bs, 1H), 4.92-5.02 (m, 1H), 5.56 (s, 1H), 6.14 (ddd, 1H), 7.27 (dd, 1H), 7.36 (ddd, 1H), 6.95 (bs, 1H), 7.03 (dd, 1H), 8.28 (d, 1H), 8.35 (d, 1H)。
N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−8−(1−(フェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
mm、40mL/分の流速)と極性が減少する水(0.2%炭酸アンモニウムを含有する)及びアセトニトリルの混合物を溶出液として使用する分取用HPLCによって精製した。所望の化合物を含有する画分を蒸発させ、ジエチルエーテルで摩砕して乾燥させて、8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(59.2mg,60.2%)を白色の固形物として得た。質量スペクトル: M+H+ 517。NMR スペクトル: (DMSOd6) 1.57 (d, 3H), 2.15 (s, 6H), 2.37 (t, 2H), 3.26-3.34 (m,
H2Oによって一部隠れている, 2H), 3.50-3.62 (m, 4H), 3.70-3.79 (m, 4H), 5.03-5.12
(m, 1H), 5.61 (s, 1H), 6.34 (dd, 1H), 6.49 (d, 1H), 6.64 (ddd, 1H), 6.82 (d, 1H), 8.10 (d, 1H), 8.32 (d, 1H), 8.61 (t, 1H)。
水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して濃縮して粗製の化合物を得て、これをジエチルエーテルで摩砕し、濾過して乾燥させて、8−アセチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸メチル(25.0g,69.5%)を灰白色の固形物として得た。質量スペクトル: M+H+ 332。
−4H−クロメン−6−カルボン酸メチル(215mg,0.54ミリモル)の撹拌懸濁液へ3−クロロ−2−フルオロアニリン(0.239mL,2.17ミリモル)を室温で加えた。生じる懸濁液を16時間撹拌してから、温度を50℃へ16時間高めた。この粗生成物を、DCM中5%メタノールで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させて、8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸メチル(206mg,82%)を白色の固形物として得た。質量スペクトル: M+H+ 461。
8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
m, 4H), 3.70-3.81 (m, 4H), 4.92-5.02 (m, 1H), 5.60 (s, 1H), 6.27 (d, 1H), 6.46 (dd, 2H), 6.84 (dd, 2H), 7.56 (d, 1H), 7.77 (d, 1H)。
N−(2−(ジメチルアミノ)エチル)−8−(1−(4−フルオロフェニルアミノ)エチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
3.05 (bs, 1.5H), 3.47 (bs, 1H), 3.50-3.64 (m, 4H), 3.71-3.79 (m, 4H), 4.93-5.01
(m, 1H), 5.59 (s, 1H), 6.29 (bs, 1H), 6.46 (dd, 2H), 6.84 (dd, 2H), 6.54 (d, 1H), 6.73 (d, 1H)。
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
酸(125mg,0.28ミリモル)をピペリジン−4−オール(34.0mg,0.34ミリモル)と反応させて、8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン(110mg,74.2%)を白色の固形物として得た。質量スペクトル: M+H+ 530。NMR スペクトル: (DMSOd6) at 323 °K: 1.24 (bs, 2H), 1.51 (d, 3H), 2.99 (bs, 2H), 3.30 (bs, 2H), 3.37 (bs, 2H), 3.49-3.63 (m, 4H), 3.63-3.72 (m, 1H), 3.72-3.82 (m, 4H), 4.62 (d, 1H), 4.92-5.02 (m, 1H), 5.56 (s, 1H), 6.36-6.46
(m, 2H), 6.59 (dd, 1H), 7.01 (dd, 1H), 7.51 (d, 1H), 7.76 (d, 1H)。
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
2.76 (s, 1.5H), 2.94 (s, 1.5H), 3.07 (bs, 1H), 3.27 (bs, 1H), 3.45 (bs, 1H), 3.51-3.64 (m, 5H), 3.70-3.78 (m, 4H), 4.69 (bs, 0.5H), 4.78 (ns, 0.5H), 5.08 (bs, 1H), 5.60 (s, 1H), 6.33-6.47 (bs, 2H), 6.65 (ddd, 1H), 6.83 (dd, 1H), 7.60 (bs, 0.5H), 7.61 (bs, 0.5H), 7.79 (bs, 0.5H), 7.81 (bs, 0.5H)。
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−(モルホリン−4−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−6−((S)−3−ヒドロキシピロリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン(エナンチオマー2)
N−(2−(ジメチルアミノ)エチル)−8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
リカ、直径19mm、長さ100mm、40mL/分の流速)と極性が減少する水(0.2%炭酸アンモニウムを含有する)及びアセトニトリルの混合物を溶出液として使用する分取用HPLCによって精製した。所望の化合物を含有する画分を蒸発乾固させた。残渣をジエチルエーテルに摩砕し、濾過によって採取して乾燥させて、N−(2−(ジメチルアミノ)エチル)−8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(42.0mg,53.1%)を白色の固形物として得た。質量スペクトル: M+H+ 497。NMR スペクトル: (CDCl3) 1.66 (d, 3H), 2.33 (s, 6H), 2.33 (bs, 2H), 2.60 (bs, 2H), 2.61 (s, 3H), 3.09-3.24 (m, 4H), 3.44-3.57 (m, 4H), 3.57-3.66 (m, 2H), 5.36 (q, 1H), 5.48 (s, 1H), 6.75 (dd, 2H), 6.77 (dd, 2H), 7.14 (bs, 1H), 8.33 (s, 1H), 8.44 (s, 1H)。
NaOH水溶液(0.408mL,0.82ミリモル)で冷まして、そのまま室温へ1時間温めた。さらなるNaOH(0.408mL,0.82ミリモル)を加えて、撹拌をさらに15分間維持した。HCl(0.917mL,1.83ミリモル)を加えて、pHを2〜3へ調整した。生じる沈殿を約1mLの水で希釈し、濾過によって採取し、酢酸エチル、ジエチルエーテルで洗浄して一定の重量まで乾燥させて、8−(1−ヒドロキシエチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸(122mg,94%)を橙色の固形物として得て、これをさらに精製せずに使用した。質量スペクトル: M+H+ 320。
砕し、濾過によって採取して乾燥させて、N−(2−(ジメチルアミノ)エチル)−8−(1−ヒドロキシエチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(80mg,0.205ミリモル,59.6%)を灰白色の固形物として得た。質量スペクトル: M+H+ 390。
8−(1−((3,4−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−(ジメチルアミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
N−(2−(ジメチルアミノ)エチル)−8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−
6−カルボキサミド
8−(1−(3,4−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
458。NMR スペクトル: (DMSOd6) 1.50 (d, 3H), 2.70 (s, 3H), 2.94 (s, 3H), 3.50-3.
63 (m, 4H), 3.71-3.79 (m, 4H), 4.92-5.01 (m, 1H), 5.60 (s, 1H), 6.25 (d, 1H), 6.46 (ddd, 1H), 6.54 (d, 1H), 7.05 (dd, 1H), 7.54 (d, 1H), 7.78 (d, 1H)。
第一溶出エナンチオマー 1100mg(実施例3.03a)[α]D 20°:+119°(99.1% ee)、MeCN中、
第二溶出エナンチオマー 1090mg(実施例3.03b)[α]D 20°:−120°(99.3% ee)、MeCN中、を得た。
8−(1−(3−クロロ−2−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
第一溶出エナンチオマー 741mg(実施例3.04a)[α]D 20°:+159°(>98% ee)、MeCN中、
第二溶出エナンチオマー 622mg(実施例3.04b)[α]D 20°:−159°(>98% ee)、MeCN中、を得た。
8−(1−(3−クロロ−4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
474。NMR スペクトル: (DMSOd6) 1.51 (d, 3H), 2.70 (s, 3H), 2.94 (s, 3H), 3.50-3.64 (m, 4H), 3.69-3.81 (m, 4H), 4.94-5.05 (m, 1H), 5.60 (m, 1H), 6.47 (ddd, 1H), 6.52 (d, 1H), 6.67 (dd, 1H), 7.05 (dd, 1H), 7.55 (d, 1H), 7.79 (d, 1H)。
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
1H), 7.54 (d, 1H), 7.81 (d, 1H)。
第二溶出エナンチオマー(保持時間:15.4分)0.923g(実施例3.06b)[α]D 20=−122.6°、EtOH中。
N/MeOH/DEA 90/10/0.5)後の分析用HPLCからのものである。
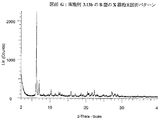
第二溶出エナンチオマー(実施例3.06b)をエタノール中で結晶化させた後に周囲条件の下で乾燥させて、A型の材料を得た。この型は、XRPD(図面Aを参照のこと)によって結晶性であると決定されて、以下の特徴的なX線粉末回折ピークを有した:
示した。
実施例3.07
8−(1−((4−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
。
8−(1−((3−クロロ−4−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
実施例3.09〜3.13の化合物(表Iに示す)の製造のために、適正なアニリン(1.20ミリモル)と8−(1−ブロモエチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド臭化水素酸塩(0.123g,0.3ミリモル)をNMP(1.0mL)に懸濁させて、試験管へ密封した。この反応物をアルゴンでパージして、75℃で15時間の時間にわたって加熱した。この反応混合物を Waters X-Bridge 逆相カラム(C−18,5ミクロンシリカ、直径19mm、長さ100m
m、40mL/分の流速)と極性が減少する水(0.2%炭酸アンモニウムを含有する)及びアセトニトリルの混合物を溶出液として使用する分取用HPLCによって精製した。所望の化合物を含有する画分を蒸発乾固させた。
NMR スペクトル: (CDCl3) 1.62 (d, 3H), 2.85 (s, 3H), 3.06 (s, 3H), 3.42-3.55 (m, 4H), 3.76-3.77 (m, 4H), 4.14 (d, 1H), 4.90-5.00 (m, 1H), 5.54 (s, 1H), 6.34 (dd, 1H), 6.45 (dd, 1H), 6.64 (dd, 1H), 7.01 (dd, 1H), 7.71 (d, 1H), 8.12 (d, 1H)
。
NMR スペクトル: (CDCl3) 1.67 (d, 3H), 2.86 (s, 3H), 3.07 (s, 3H), 3.44-3.57 (m, 4H), 3.79-3.88 (m, 4H), 4.38 (bs, 1H), 4.94-5.02 (m, 1H), 5.55 (s, 1H), 6.08 (dd, 1H), 6.48 (dd, 1H), 6.74 (dd, 1H), 7.71 (d, 1H), 8.12 (d, 1H)。
NMR スペクトル: (CDCl3) 1.56 (d, 3H), 2.91 (s, 3H), 3.07 (s, 3H), 3.45-3.59 (m, 4H), 3.78-3.92 (m, 4H), 4.39 (d, 1H), 4.77-4.88(m, 1H), 5.55 (s, 1H), 6.01 (dd, 2H), 7.70 (d, 1H), 8.12 (d, 1H)。
NMR スペクトル: (CDCl3) 1.60(d, 3H), 2.85 (s, 3H), 3.06 (s, 3H), 3.45-3.55 (m,
4H), 3.76-3.87 (m, 4H), 4.22 (d, 1H), 4.89-4.99 (m, 1H), 5.55 (s, 1H), 6.13 (ddd, 1H), 6.26 (dd, 1H), 6.36 (ddd, 1H), 7.04 (dd, 1H), 7.73 (d, 1H), 8.11 (d, 1H)。
NMR スペクトル: (CDCl3): 1.67 (d, 3H), 2.92 (s, 3H), 3.09 (s, 3H), 3.46-3.58 (m, 4H), 3.81-3.90 (m, 4H), 4.53 (bs, 1H), 4.88-4.96 (m, 1H), 5.56 (s, 1H), 5.80-5.88 (m, 1H), 6.17-6.27 (m, 1H), 7.71 (d, 1H), 8.13 (d, 1H)。
第二溶出エナンチオマー:1.9g単離、[α]D 20°:−50°、DCM中(エナンチオマー2)実施例3.13b。
A型材料を水/メタノール混合物中でスラリー化させることによって、B型材料を生成した。ほぼ20mgの元の材料を磁気撹拌子と一緒にバイアルに入れて、ほぼ100mLのメタノールと2mLの水を加えてから、このバイアルをキャップでしっかり密封して、そのまま磁気撹拌プレート上で撹拌させた。3日後、試料をプレートより外し、キャップを取り去って、スラリーを周囲条件の下でそのまま乾燥させた後で、これをXRPDとDSCによって分析した。この型(B型)は、XRPD(図面G)によって結晶性であることが決定されて、A型とは異なることがわかった。この型は、以下の特徴的なX線粉末回折ピークを有した:
を示した(図面I)。
8−(1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(2,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
458。NMR スペクトル (DMSOd6): 1.57 (d, 3H), 2.72 (bs, 3H), 2.94 (bs, 3H), 3.51-3.64 (m, 4H), 3.71-3.78 (m, 4H), 5.02-5.11 (m, 1H), 5.61 (s, 1H), 6.19-1.33 (m,
2H), 6.43 (d, 1H), 7.01-7.09 (m, 1H), 7.60 (d, 1H), 7.79 (d, 1H)。
8−(1−(3−フルオロ−5−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8.12 (d, 1H)。
8−(1−(3−シアノ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(3−シアノフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(2,3−ジクロロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(3−エチニルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(5−シアノ−2−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(5−フルオロ−2−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
(d, 1H)。
8−(1−(3−シアノ−5−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(5−フルオロ−2−メトキシフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(5−シアノ−2−メトキシフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(2−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(2,3,6−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド
8−(1−(5−クロロ−2−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(3−シアノ−2−メチルフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
1H), 5.81 (d, 1H), 6.46 (d, 1H), 6.92 (d, 1H), 7.02 (dd, 1H), 7.56 (d, 1H), 7.78 (d, 1H)。
8−(1−(3−フルオロ−5−メトキシフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
7.79 (d, 1H)。
8−(1−(3−フルオロ−2−メトキシフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
7.78 (d, 1H)。
8−(1−(3−クロロ−2,6−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
(bs, 3H), 3.50-3.58 (m, 4H), 3.70-3.80 (m, 4H), 5.37-5.46 (m, 1H), 5.57 (s, 1H), 5.99 (d, 1H), 6.81 (ddd, 1H), 6.94 (ddd, 1H), 7.72 (d, 1H), 7.76 (d, 1H)。
8−(1−(3,5−ジクロロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(3−エチニル−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−(2−シアノ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
(dd, 1H), 6.52 (ddd, 1H), 6.88 (d, 1H), 7.61 (dd, 1H), 7.68 (d, 1H), 7.82 (d, 1H)。
8−(1−(2−シアノ−3−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
1H), 5.61 (s, 1H), 6.33 (d, 1H), 6.56 (dd, 1H), 6.99 (d, 1H), 7.32 (dd, 1H), 7.69 (d, 1H), 7.81 (d, 1H)。
8−(1−((3−クロロ−5−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
って一部隠れている, 2H), 3.42-3.48 (m, 2H), 3.49-3.55 (m, 2H), 5.55 (s, 1H), 5.61 (q, 1H), 6.61 (d, 1H), 6.66 (d, 1H), 6.75 (s, 1H), 7.71 (d, 1H), 7.89 (d, 1H)
。
N,N−ジメチル−8−(1−(メチル(3,4,5−トリフルオロフェニル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
N,N−ジメチル−8−(1−(メチル(2,3,5−トリフルオロフェニル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
部隠れている, 2H), 3.49-3.56 (m, 2H), 3.56-3.63 (m, 2H), 5.38 (q, 1H), 5.53 (s, 1H), 6.68-6.75 (m, 1H), 6.88-6.96 (m, 1H), 7.78 (d, 1H), 7.86 (d, 1H)。
N,N−ジメチル−8−(1−(メチル(フェニル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−((3−エチニル−5−フルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
2H), 4.21 (s, 1H), 5.54 (q, 1H), 5.62 (s, 1H), 6.52 (d, 1H), 6.73 (d, 1H), 6.80
(s, 1H), 7.72 (d, 1H), 7.89 (d, 1H)。
1H), 6.11-6.22 (m, 3H), 6.72 (d, 1H), 7.54 (d, 1H), 7.78 (d, 1H)。
1H), 3.72-3.80 (ms, 4H), 4.98-5.06 (m, 1H), 5.62 (s, 1H), 6.15 (dd, 2H), 6.25 (ddd, 1H), 6.98 (d, 1H), 7.46 (d, 1H), 7.78 (d, 1H)。
1H), 6.98 (d, 1H), 7.47 (d, 1H), 7.78 (d, 1H)。
粗製溶液をクエン酸の10%溶液(pH〜4)、水で洗浄し、硫酸マグネシウムで乾燥させて、濃縮した。HCl(ジオキサン中4N;1066μl,4.27ミリモル)を加えて、この混合物を室温で30分間撹拌した。揮発物質を真空下に除去して、残渣をDCM中10%メタノール性アンモニア(5mL)に溶かした。不溶物を濾過によって除去し、濾液を濃縮して、粗生成物を上記に記載のような分取用HPLCによって精製した。
, 2H), 3.45 (bs, H2Oによって一部隠れている, 1H), 3.50-3.64 (m, 5H), 3.68 (bs, 1H), 3.70-3.81 (m, 4H), 3.96 (bs, 1H), 4.96-5.06 (m, 1H), 5.61 (s, 1H), 6.14 (dd, 2H), 6.25 (ddd, 1H), 6.96 (d, 1H), 7.51 (d, 1H), 7.80 (d, 1H)。
1.32-1.43 (m, 2H), 1.44-1.55 (m, 2H), 1.52 (d, 3H), 1.62-1.73 (m, 2H), 3.03-3.12 (m, 2H), 3.37-3.45 (m, H2Oによって一部隠れている, 1H), 3.51-3.70 (m, 5H), 3.71-3.79 (m, 4H), 4.97-5.06 (m, 1H), 5.61 (s, 1H), 6.14 (dd, 2H), 6.23 (ddd, 1H), 6.98 (d, 1H), 7.45 (d, 1H), 7.73 (d, 1H)。
3.20 (bs, H2Oによって一部隠れている, 2H), 3.47 (bs, 2H), 3.51-3.64 (m, 4H), 3.71-3.79 (m, 4H), 4.61 (bs, 1H), 4.97-5.05 (m, 1H), 5.58 (s, 1H), 6.15 (dd, 2H), 6.20 (ddd, 1H), 6.83 (d, 1H), 7.58 (d, 1H), 7.84 (d, 1H)。
1.64 (bs, 2H), 3.04 (bs, 2H), 3.49 (bs, 1H), 3.52-3.62 (m, 4H), 3.63 (bs, 1H), 3.66-3.74 (bs, 1H), 3.72-3.80 (m, 4H), 4.66 (d, 1H), 4.97-5.05 (m, 1H), 5.58 (s,
1H), 6.15 (dd, 2H), 6.20 (ddd, 1H), 6.86 (d, 1H), 7.53 (d, 1H), 7.80 (d, 1H)。
1.54-4.64 (m, 2H), 3.31 (bs, H2Oによって一部隠れている, 4H), 3.49-3.66 (m, 4H),
3.68-3.84 (m, 4H), 4.96-5.07 (m, 1H), 5.58 (s, 1H), 6.14 (dd, 2H), 6.20 (ddd, 1H), 6.86 (d, 1H), 7.52(d, 1H), 7.79 (d, 1H)。
6.86 (d, 1H), 7.54 (s, 1H), 7.79 (d, 1H)。
5.39 (ddddd, 1H), 5.59 (s, 1H), 6.17 (dd, 2H), 6.20 (ddd, 1H), 6.91 (d, 1H), 7.81(s, 1H), 8.06 (d, 1H)。
1H), 5.62 (s, 1H), 6.15 (dd, 2H), 6.22 (ddd, 1H), 7.03 (d, 1H), 8.08 (s, 1H), 8.38 (d, 1H), 8.69 (t, 1H)。
(m, H2Oによって一部隠れている, 2H), 3.42-3.48 (m, 2H), 3.50-3.64 (m, 4H), 3.70-3.79 (m, 4H), 4.96-5.05 (m, 1H), 5.62 (s, 1H), 6.14 (dd, 2H), 6.22 (ddd, 1H), 7.03 (d, 1H), 8.07 (s, 1H), 8.37 (d, 1H), 8.78 (t, 1H)。
(d, 3H), 3.13-3.24 (m, 2H), 3.50-3.64 (m, 4H), 3.70-3.79 (m, 4H), 4.96-5.05 (m,
1H), 5.62 (s, 1H), 6.14 (dd, 2H), 6.22 (ddd, 1H), 7.03 (d, 1H), 8.07 (s, 1H), 8.36 (d, 1H), 8.73 (t, 1H)。
(m, 2H), 3.50-3.64 (m, 4H), 3.69-3.80 (m, 4H), 4.96-5.04 (m, 1H), 5.62 (s, 1H),
6.14 (dd, 2H), 6.22 (ddd, 1H), 7.03 (d, 1H), 8.07 (s, 1H), 8.35 (d, 1H), 8.74 (t, 1H)。
(s, 3H), 3.24-3.30 (m, 2H), 3.36-3.42 (m, H2Oによって一部隠れている, 2H), 3.50-3.63 (m, 4H), 3.71-3.78 (m, 4H), 4.96-5.04 (m, 1H), 5.62 (s, 1H), 6.14 (dd, 2H),
6.22 (ddd, 1H), 7.03 (d, 1H), 8.06 (d, 1H), 8.35 (d, 1H), 8.73 (t, 1H)。
(m, 1H) 7.64 (s, 0.5H), 7.68 (s, 0.5H), 7.95 (s, 1H)。
(m, 1H) 7.64 (s, 0.5H), 7.68 (s, 0.5H), 7.95 (s, 1H)。
(m, 4H), 3.71-3.78 (m, 4H), 4.96-5.04 (m, 1H), 5.61 (s, 1H), 6.14 (dd, 2H), 6.22 (ddd, 1H), 7.03 (d, 1H), 8.07 (d, 1H), 8.33 (d, 1H), 8.67 (q, 1H)。
0.98-1.08 (m, 1H), 1.51 (d, 3H), 3.08-3.16 (m, 2H), 3.51-3.64 (m, 4H), 3.71-3.80 (m, 4H), 4.97-5.06 (m, 1H), 5.63 (s, 1H), 6.15 (dd, 2H), 6.23 (ddd, 1H), 7.05 (d, 1H), 8.09(d, 1H), 8.38 (d, 1H), 8.86 (t, 1H)。
1.87 (bs, 1H), 3.27-3.89 (m, 15H), 4.97-5.06 (m, 1H), 5.59(s, 1H), 6.15 (dd, 2H
), 6.21 (ddd, 1H), 6.87 (d, 1H), 7.54(d, 1H), 7.80 (d, 1H)。
1.72 (bs, 2H), 3.08 (bs, 2H), 3.25 (s, 3H), 3.36-3.44 (m, 1H), (m, 4H), 3.67 (bs, 2H), 3.69-3.82 (m, 4H), 4.97-5.07 (m, 1H), 5.58 (s, 1H), 6.15 (dd, 2H), 6.21 (ddd, 1H), 6.86 (d, 1H), 7.52(d, 1H), 7.80 (d, 1H)。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
で30分間撹拌した。水とDCMを加え、有機相を塩水で洗浄し、硫酸マグネシウムで乾燥させて、濃縮した。この粗生成物を、DCM/MeCN(1:1)に次いでDCM中0〜10% MeOHで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させてフォームを得て、これを酢酸エチル(10mL)より結晶化させた。エーテル(10mL)を加えて結晶化を完了させて、白色の固形物を濾過によって採取して乾燥させて、8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(1.65g,74%)を得た。質量スペクトル: M+H+ 472. NMR スペ
クトル (DMSOd6): 1.55 (d, 3H), 2.63 (s, 3H), 2.92 (bs, 3H), 3.01 (bs, 3H), 3.21-3.29 (m, 2H), 3.31-3.39 (m, H2Oによって一部隠れている, 2H), 3.41-3.49 (m, 2H), 3.49-3.57 (m, 2H), 5.55 (s, 1H), 5.58 (q, 1H), 6.40 (t, 1H), 6.53 (d, 2H), 7.70 (d, 1H), 7.89 (d, 1H)。
第一溶出エナンチオマー、0.7g(ee>98%)(実施例5.0a)[α]D 20°:+5°、MeCN中
第二溶出エナンチオマー、0.7g(ee>98%)(実施例5.0b)[α]D 20°:−5°、MeCN中、を得た。
ボン酸メチル(3.3g,8.33ミリモル、実施例2.00に記載のように製造)及び3,5−ジフルオロ−N−メチルアニリン(3.58g,24.99ミリモル)のCHCl3(16mL)及びMeOH(4mL)中の懸濁液へヨウ化カリウム(1.521g,9.16ミリモル)を加えた。この混合物を室温で週末にわたって撹拌した。この反応混合物を濃縮乾固させて、生じる暗色のオイルをジエチルエーテルで摩砕して固形物を得て、これを濾過によって採取した。この固形物を水に懸濁させて、pHを2N NaOHで6〜7へ調整した。この粗生成物を濾過してエーテルで洗浄し、乾燥させて、DCM中0〜10% MeOHで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させて、8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボン酸メチル(3.1g,81%)を白色の固形物として得た。質量スペクトル: M+H+ 459。
無水THF(60mL)に溶かした8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(6g,13.12ミリモル、実施例3.06bに記載のように製造;[α]D 20=−122.6°、EtOH中)の撹拌溶液へリチウムビス(トリメチルシリル)アミド(THF中1N)(26.2mL,26.23ミリモル)をアルゴン下に−60℃で加えた。この淡赤色の溶液をそのまま15分の時間にわたって−10℃へ温めてから−60℃へ冷却した後で、硫酸ジメチル(2.482mL,26.23ミリモル)を加えた。生じる淡黄色の溶液をそのまま0℃へ温めて、15分間撹拌した。この反応混合物を再び−10℃へ冷やした後で、NH4Clの飽和水溶液(30mL)の添加にDCMでの抽出を続けた。この粗生成物(7g)を、DCM/酢酸エチル中0〜15% EtOH(1/1)に次いでDCM中15% EtOHで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させて、(4.2g,8.91ミリモル、67.9%)の灰白色のフォームを得た。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
ステムを使用する分取用HPLCによって精製した。所望の化合物を含有する画分を蒸発させ、エーテルで摩砕して乾燥させて、8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン(90mg,58%)を白色の固形物として得た。質量スペクトル: M+H+ 528。NMR スペクトル (DMSOd6, 323°K): 1.38 (bs, 2H), 1.57
(d, 3H), 1.75 (bs, 2H), 2.66 (s, 3H), 3.23-3.30 (m, 2H), 3.30-3.38 (m, 2H), 3.61 (m, 4H), 3.65 (bs, 4H), 3.71-3.79 (m, 1H), 4.66 (d, 1H), 5.52 (s, 1H), 5.54 (q, 1H), 6.36 (t, 1H), 6.50 (d, 2H), 7.62 (d, 1H), 7.87 (d, 1H)。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(3−ヒドロキシピロリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
0.5H), 4.86 (bs, 0.5H), 4.92 (bs, 0.5H), 5.51 (s, 1H), 5.56 (q, 1H), 6.36 (t, 1H), 6.51 (d, 2H), 7.76 (d, 0.5H), 7.78 (bs, 0.5H), 8.02 (bs, 1H)。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−((R)−2−(ヒドロキシメチル)ピロリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−2−モルホリノ−6−(ピロリジン−1−カルボニル)−4H−クロメン−4−オン
3H), 3.23-3.29 (m, 2H), 3.35-3.56 (m, 10H), 5.55 (s, 1H), 5.59 (q, 1H), 6.40 (t, 1H), 6.53 (d, 2H), 7.79 (d, 1H), 8.01 (d, 1H)。
2H), 3.57-3.70 (m, 4H), 3.73-3.80 (m, 4H), 5.66 (s, 1H), 5.92 (q, 1H), 7.99-8.03 (m, 2H)。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(エナンチオマー1)
−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド・エナンチオマー1(79mg,56%)を白色の固形物として得た。質量スペクトル: M+H+ 502。[α]D 20°:−9°、MeCN中。
第一溶出エナンチオマー、24g(濃度76%)[α]D 20°:+115°、MeCN中(エナンチオマー1)
第二溶出エナンチオマー、24.1g(濃度81%)[α]D 20°:−102°、MeCN中(エナンチオマー2)を得た。
・エナンチオマー1(210mg,90%)を白色の固形物として得た。質量スペクトル: M+H+ 740。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−N−(2−ヒドロキシエチル)−N−メチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(エナンチオマー2)
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン(エナンチオマー2)
リモル、実施例7.0aのエナンチオマー2、[α]D 20°:−102°)の撹拌溶液へフッ化テトラブチルアンモニウム(THF中1N)(7.83mL,7.83ミリモル)を窒素下に室温で滴下して、2時間撹拌した。この混合物を蒸発乾固させ、DCMで希釈し、水で洗浄した。有機相を塩水で洗浄し、硫酸マグネシウムで乾燥させ、濾過して濃縮した。この粗生成物をDCM中3〜7% MeOHで溶出させるシリカゲル(80g)のフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させてフォームを得て、これをエーテル(2〜5mL)で摩砕した。生じる白色の固形物を濾過によって採取して乾燥させて、8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン・エナンチオマー2(1.7g,82%)を白色の固形物として得た。質量スペクトル: M+H+ 528。[α]D 20°:+7°、MeCN中。
8−(1−((3,5−ジフルオロフェニル)(メチル)アミノ)エチル)−6−(4−ヒドロキシピペリジン−1−カルボニル)−2−モルホリノ−4H−クロメン−4−オン(エナンチオマー1)
6−(アゼチジン−1−カルボニル)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4H−クロメン−4−オン(エナンチオマー2)
を蒸発乾固させて、白色の固形物、6−(アゼチジン−1−カルボニル)−8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−2−モルホリノ−4H−クロメン−4−オン(300mg,61%)を得た。質量スペクトル: M+H+ 470。[α]D 20°:−
113°,MeCN中。NMR スペクトル (DMSOd6): 1.50 (d, 3H), 2.18-2.28 (m, 2H), 3.50-3.63 (m, 4H), 3.69-3.78 (m, 4H), 3.98-4.07 (m, 2H), 4.09-4.19 (m, 2H), 4.97-5.05 (m, 1H), 5.61 (s, 1H), 6.15 (d, 2H), 6.21 (t, 1H), 7.03 (d, 1H), 7.79 (d, 1H), 8.02 (d, 1H)。
8−(1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(単一エナンチオマー)
の反応混合物をダイカライト(dicalite)の短いパッドに通して濾過して、減圧下に濃縮した。この粗生成物をDCM中0〜8%イソプロパノールで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させ、生成物をジエチルエーテル−DCM(9:1)で摩砕し、濾過によって採取して乾燥させて、8−(1−(3−クロロ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(320mg;67%)を澄明な黄色の固形物として得た。質量スペクトル: M+H+ 474。[α]D 20°:−138°。NMR
スペクトル (DMSOd6): 1.52 (d, 3H), 2.75 (bs, 3H), 2.95 (bs, 3H), 3.49-3.63 (m, 4H), 3.70-3.79 (m, 4H), 4.98-5.07 (m, 1H), 5.60 (s, 1H), 6.23 (d, 1H), 6.42 (d, 1H), 6.43 (ddd, 1H), 6.94 (d, 1H), 7.54 (d, 1H), 7.80 (d, 1H)。
所望の生成物を得た。この水相よりDCM抽出によってさらなる生成物(2.8g)を回収した。この2バッチを合わせて、8−(1−(tert−ブチルスルフィニルイミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(4.5g,87%)を黄色のフォームとして得て、これをさらに精製せずに次の工程に使用した。質量スペクトル: M+H+ 448。
Merck)のフラッシュクロマトグラフィーによって精製した。不純な生成物を含有する画分を濃縮して、同じシステムを使用して再精製した。純粋な8−(1−((R)−1,1−ジメチルエチルスルフィンアミド)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミドを含有する画分を合わせて、溶媒を蒸発乾固させて、2.48g(5.52ミリモル,54.9%)を白色のフォームとして得た。ジアステレオ異性体の混合物を含有する画分を合わせ、濃縮して、Waters X-Bridge システムでの分取用HPLCによって精製した。所望の化合物を含有する画分を蒸発乾固させて、さらなる収穫物の8−(1−((R)−1,1−ジメチルエチルスルフィンアミド)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(0.25g,0.556ミリモル、5.53%)を白色のフォームとして得た。これらの2バッチ、(2.48g)と(0.25g)を合わせて、8−(1−((R)−1,1−ジメチルエチルスルフィンアミド)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(2.73g,60%,ジアステレオマー過剰率>95%)を得た。質量スペクトル: M+H+ 450。
メン−6−カルボキサミド(2.7g,6.0ミリモル)へジオキサン中4M塩化水素(15mL,60.1ミリモル)を加えた。生じる白色の懸濁液を室温で1時間撹拌し、濾過によって採取し、ジエチルエーテルで洗浄して、乾燥させた。これをDCM中5%メタノール性アンモニア(7N)溶液(200mL)に溶かして、5分間撹拌した。沈殿(NH4Cl)を濾過によって除去して濾液を濃縮乾固させて、8−(1−アミノエチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(単一エナンチオマー、1.85g,89%)を灰白色の固形物として得た。質量スペクトル: M+H+ 346。[α]D 20°:+35°、アセトニトリル中。
8−(1−(3−シアノ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(単一エナンチオマー)
する画分を蒸発乾固させて、8−(1−(3−シアノ−5−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−モルホリノ−4−オキソ−4H−クロメン−6−カルボキサミド(330mg,82%)を澄明な白色の固形物として得た。質量スペクトル: M+H+ 465。[α]D 20°:−128°、MeCN中。NMR スペクトル (CDCl3): 1.51 (d, 3H), 2.91 (s, 3H), 3.09 (s, 3H), 3.44-3.60 (m, 4H), 3.78-3.93 (m, 4H), 4.85-4.94 (m, 1H), 5.17 (d, 1H), 5.56 (s, 1H), 6.38 (ddd, 1H), 6.51 (s, 1H), 6.61 (d, 1H), 7.70 (d, 1H), 8.12 (d, 1H)。
N,N−ジメチル−2−モルホリノ−4−オキソ−8−(1−(3,4,5−トリフルオロフェニルアミノ)エチル)−4H−クロメン−6−カルボキサミド(単一エナンチオマー)
スペクトル (CDCl3): 1.56 (d, 3H), 2.91 (s, 3H), 3.09 (s, 3H), 3.47-3.56 (m, 4H),
3.82-3.90 (m, 4H), 4.35 (d, 1H), 4.79-4.88 (m, 1H), 5.56 (s, 1H), 6.03 (dd, 2H), 7.70 (d, 1H), 8.12 (d, 1H)。
8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド
出液として使用する分取用HPLCによって精製した。DCM中0〜10% MeOHで溶出させるシリカゲルのフラッシュクロマトグラフィーによってさらなる精製を行った。溶媒を蒸発乾固させてオイルを得て、これをペンタンで摩砕して、8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド(80mg,59%)を白色の固形物として得た。NMR スペクトル (DMSOd6): 1.16 (d, 3H), 1.50 (d, 3H), 2.66 (bs,
3H), 2.81 (ddd, 1H), 2.93 (bs, 3H), 3.14 (ddd, 1H), 3.57-3.70 (m, 2H), 3.87-4.03 (m, 3H), 4.93-5.01 (m, 1H), 5.62 (s, 1H), 6.24-6.29 (m, 1H), 6.43-6.50 (m, 2H), 6.85 (t, 2H), 7.55 (d, 0.5H), 7.56 (d, 0.5H), 7.77 (d, 1H)。
CM中0〜10%酢酸エチルで溶出させるシリカゲルのフラッシュクロマトグラフィーによって精製した。溶媒を蒸発乾固させて、8−ブロモ−2−(エチルチオ)−4−オキソ−4H−クロメン−6−カルボン酸メチル(1.8g,72%)を橙色の固形物として得た。質量スペクトル: M+H+ 343。
ールで繰り返した後で、次の工程へ進めた。
348。
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((R)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド
第二溶出ジアステレオ異性体、240mg(実施例9.01b)[α]D 20°:−99°、MeCN中。
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド
第二溶出ジアステレオマー、105mg(実施例9.02b)[α]D 20°:−163°、MeCN中。
8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S
)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド
物を含有する画分を濃縮した。入手したゴムをジエチルエーテルと石油エーテルで摩砕し、生じる固形物を濾過によって採取して乾燥させて、8−(1−(4−フルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−2−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド(45mg,51%)を白色の固形物として得た。質量スペクトル: M+H+ 545。NMR スペクトル (CDCl3): 1.25 (d, 1.5H), 1.26 (d, 1.5H), 1.61 (d, 3H), 2.77-2.88 (m, 1H), 2.83 (bs, 3H), 3.06 (bs, 3H), 3.13-3.22 (m, 1H), 3.64-3.82 (m, 4H), 3.97 (bs, 1H), 3.98-4.06 (m, 1H), 4.91 (q, 1H), 5.56 (s, 1H), 6.37-6.43 (m, 2H), 6.82 (t, 2H), 7.73 (d, 1H), 8.11 (d, 1H)。
(bs, 6H), 3.31-3.55 (m, 2H), 3.61-3.81 (m, 4H), 5.56 (s, 1H), 5.59 (q, 1H), 6.3
7 (t, 1H), 6.57 (d, 2H), 7.70 (s, 1H), 7.92 (s, 1H)。
1H), 5.55 (s, 1H), 5.59 (q, 1H), 6.37 (t, 1H), 6.55 (d, 2H), 7.74 (bs, 1H), 7.93 (s, 1H)。
8−(1−(3,5−ジフルオロフェニルアミノ)エチル)−N,N−ジメチル−2−((S)−3−メチルモルホリノ)−4−オキソ−4H−クロメン−6−カルボキサミド
Claims (7)
- R10は(1−6C)アルキルであり;
nは、0、1、2、3又は4であり;そして
それぞれのR9基は、(1−3C)アルキルである、請求項1に記載の式VIIIaの化合物。 - R10がメチル又はエチルである、請求項1又は請求項2に記載の式VIIIaの化合物。
- nが0である、請求項1〜3のいずれか1項に記載の式VIIIaの化合物。
- 以下の式Iの化合物:
R1は、Hであるか、又はハロゲノ、ヒドロキシ、又は(1−3C)アルコキシより独立して選択される1、2又は3の置換基によって置換されていてもよい(1−4C)アルキルであり;
R2は、(1−4C)アルキル又は(1−4C)アルコキシであり、そのいずれも、ハロゲノ、ヒドロキシ、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、シアノ、(1−3C)アルキルアミノ、又はジ[(1−3C)アルキル]アミノより独立して選択される1、2又は3の置換基によって置換されていてもよい;又は
R1とR2は、一緒に、酸素、窒素、及びイオウより選択される1又は2のさらなるヘテロ原子を含有してもよい、3〜8員の窒素含有ヘテロシクリル環系を形成し、ここで環イオウ原子は、酸化されてS−オキシド(複数)を生成してもよく、前記環は、ハロゲノ、ヒドロキシ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、オキソ、ヒドロキシ−(1−3C)アルキル、ハロゲノ−(1−3C)アルキル、及び(1−3C)アルコキシ−(1−3C)アルキルより独立して選択される1、2又は3の置換基によって置換されていてもよい;
R3は、H又は(1−3C)アルキルであり;
R4とR5は、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択される;又は
R4とR5は、一緒に、フェニル環、又は5若しくは6員ヘテロシクリル環、又は5若しくは6員ヘテロアリール環を形成し、ここで該ヘテロシクリル又はヘテロアリール環は、酸素及び窒素より選択される1、2又は3のヘテロ原子を含有し、前記フェニル、ヘテロシクリル、又はヘテロアリール環は、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択される1、2又は3の置換基によって置換されていてもよい;
R6、R7、及びR8は、H、ハロゲノ、(1−3C)アルキル、(2−3C)アルケニル、(2−3C)アルキニル、(1−3C)アルコキシ、及びシアノより独立して選択され;
nは、0、1、2、3又は4であり;
それぞれのR9基は、(1−3C)アルキルである]
又はその医薬的に許容される塩を製造するための、請求項1に記載の式VIIIaの化合物の使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP09306017.6 | 2009-10-27 | ||
| EP09306017 | 2009-10-27 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012535931A Division JP5657010B2 (ja) | 2009-10-27 | 2010-10-25 | 抗腫瘍活性があるクロメノン誘導体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015078202A JP2015078202A (ja) | 2015-04-23 |
| JP5872016B2 true JP5872016B2 (ja) | 2016-03-01 |
Family
ID=43085922
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012535931A Expired - Fee Related JP5657010B2 (ja) | 2009-10-27 | 2010-10-25 | 抗腫瘍活性があるクロメノン誘導体 |
| JP2014235289A Expired - Fee Related JP5872016B2 (ja) | 2009-10-27 | 2014-11-20 | 抗腫瘍活性があるクロメノン誘導体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012535931A Expired - Fee Related JP5657010B2 (ja) | 2009-10-27 | 2010-10-25 | 抗腫瘍活性があるクロメノン誘導体 |
Country Status (41)
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5599783B2 (ja) | 2008-05-30 | 2014-10-01 | アムジエン・インコーポレーテツド | Pi3キナーゼの阻害薬 |
| US8399460B2 (en) * | 2009-10-27 | 2013-03-19 | Astrazeneca Ab | Chromenone derivatives |
| UY34013A (es) * | 2011-04-13 | 2012-11-30 | Astrazeneca Ab | ?compuestos de cromenona con actividad anti-tumoral?. |
| MA38287B1 (fr) | 2013-01-23 | 2018-08-31 | Astrazeneca Ab | Nouveaux dérivés aminopyrazine pour le traitement ou la prévention du cancer |
| AU2014224445C1 (en) * | 2013-03-04 | 2017-07-27 | Astrazeneca Ab | Combination treatment |
| WO2015191745A1 (en) | 2014-06-13 | 2015-12-17 | Gilead Sciences, Inc. | Phosphatidylinositol 3-kinase inhibitors |
| EP3154960A1 (en) | 2014-06-13 | 2017-04-19 | Gilead Sciences, Inc. | Phosphatidylinositol 3-kinase inhibitors |
| HK1231477A1 (zh) | 2014-06-13 | 2017-12-22 | 吉利德科学公司 | 磷脂酰肌醇3-激酶抑制剂 |
| CA2952018A1 (en) | 2014-06-13 | 2015-12-17 | Gilead Sciences, Inc. | Quinazolinone derivatives as phosphatidylinositol 3-kinase inhibitors |
| KR20170012558A (ko) | 2014-06-13 | 2017-02-02 | 길리애드 사이언시즈, 인코포레이티드 | 포스파티딜이노시톨 3-키나제 억제제 |
| CN104803921A (zh) * | 2015-03-14 | 2015-07-29 | 长沙深橙生物科技有限公司 | 一种苯取代嘧啶衍生物的制备方法 |
| CN104744376A (zh) * | 2015-03-14 | 2015-07-01 | 长沙深橙生物科技有限公司 | 一种2-异丙基嘧啶衍生物的制备方法 |
| KR101766731B1 (ko) | 2015-06-23 | 2017-08-10 | 충남대학교산학협력단 | 강심 활성을 갖는 크로메논 유도체 및 이를 포함하는 심부전의 예방 또는 치료용 약학 조성물 |
| US10526316B2 (en) * | 2015-10-09 | 2020-01-07 | Janssen Pharmaceutica Nv | Quinoxaline and pyridopyrazine derivatives as PI3Kβ inhibitors |
| WO2018057808A1 (en) | 2016-09-23 | 2018-03-29 | Gilead Sciences, Inc. | Benzimidazole derivatives and their use as phosphatidylinositol 3-kinase inhibitors |
| TW201813963A (zh) | 2016-09-23 | 2018-04-16 | 美商基利科學股份有限公司 | 磷脂醯肌醇3-激酶抑制劑 |
| TW201825465A (zh) | 2016-09-23 | 2018-07-16 | 美商基利科學股份有限公司 | 磷脂醯肌醇3-激酶抑制劑 |
| TW201815787A (zh) | 2016-09-23 | 2018-05-01 | 美商基利科學股份有限公司 | 磷脂醯肌醇3-激酶抑制劑 |
| AR121719A1 (es) * | 2020-04-03 | 2022-06-29 | Petra Pharma Corp | Inhibidores alostéricos de cromenona del fosfoinosítido 3-quinasa (pi3k) para el tratamiento de enfermedades |
| KR20210141214A (ko) * | 2020-05-15 | 2021-11-23 | 제이투에이치바이오텍 (주) | 3원환 화합물 및 이의 의약 용도 |
| US20240166617A1 (en) * | 2021-02-01 | 2024-05-23 | Geode Therapeutics Inc. | Phosphoinositide 3 kinase beta inhibitors and compositions and methods thereof |
| US20230014445A1 (en) * | 2021-05-03 | 2023-01-19 | Petra Pharma Corporation | Allosteric chromenone inhibitors of phosphoinositide 3-kinase (pi3k) for the treatment of disease |
| IL307950A (en) * | 2021-05-03 | 2023-12-01 | Petra Pharma Corp | Allosteric chromanone inhibitors of PHOSPHOINOSITIDE 3-KINASE (PI3K) for the treatment of diseases |
| CN117597343A (zh) * | 2021-05-03 | 2024-02-23 | 佩特拉制药公司 | 用于治疗疾病的磷酸肌醇3-激酶(pi3k)的变构色烯酮抑制剂 |
| MX2023013987A (es) * | 2021-05-27 | 2024-02-12 | Petra Pharma Corp | Inhibidores alostéricos de cromenona de la fosfoinosítido 3-quinasa (pi3k) para el tratamiento contra el cáncer. |
| CN117769546A (zh) * | 2021-05-27 | 2024-03-26 | 佩特拉制药公司 | 用于治疗疾病的磷酸肌醇3-激酶(pi3k)的变构色烯酮抑制剂 |
| TW202329930A (zh) * | 2021-09-30 | 2023-08-01 | 美商佩特拉製藥公司 | 用於治療疾病之磷酸肌醇3-激酶(pi3k)之異位色烯酮抑制劑 |
| US20250084048A1 (en) * | 2021-10-07 | 2025-03-13 | Relay Therapeutics, Inc. | Pi3k-alpha inhibitors and methods of use thereof |
| US20250136568A1 (en) * | 2021-12-08 | 2025-05-01 | Nanjing Zenshine Pharmaceuticals Co., Ltd. | Fused heterocyclic compounds as pi3kalpha inhibitors |
| WO2024003241A1 (en) | 2022-06-30 | 2024-01-04 | Astrazeneca Ab | Treatment for immuno-oncology resistant subjects with an anti pd-l1 antibody an antisense targeted to stat3 and an inhibitor of ctla-4 |
| WO2024081904A1 (en) * | 2022-10-14 | 2024-04-18 | Genesis Therapeutics, Inc. | Methods for treating cancer |
| TWI910755B (zh) * | 2023-08-02 | 2026-01-01 | 大陸商鄭州同源康醫藥有限公司 | 稠環類化合物及其用途 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6027A (en) * | 1849-01-09 | Rotary blacksmith s twyer | ||
| WO1990006921A1 (en) | 1988-12-21 | 1990-06-28 | The Upjohn Company | Antiatherosclerotic and antithrombotic 1-benzopyran-4-ones and 2-amino-1,3-benzoxazine-4-ones |
| JPH05509302A (ja) | 1990-06-20 | 1993-12-22 | ジ・アップジョン・カンパニー | 抗アテローム性動脈硬化性および抗血栓性1―ベンゾピラン―4―オン類および2―アミノ―1,3―ベンゾオキサジン―4―オン類 |
| DE4318756A1 (de) | 1993-06-05 | 1994-12-08 | Hoechst Ag | Substituierte Benzoylguanidine, Verfahren zu ihrer Herstellung, ihre Verwendung als Medikament oder Diagnostikum sowie sie enthaltendes Medikament |
| GB9624482D0 (en) | 1995-12-18 | 1997-01-15 | Zeneca Phaema S A | Chemical compounds |
| BR9707495A (pt) | 1996-02-13 | 1999-07-27 | Zeneca Ltd | Derivado de quinazolina processo para a preparação do mesmo composição farmacêutica e processo para a produç o de um efeito antiangiogênico e/ou de redução de permeabilidade vascular em um animal de sangue quente |
| US6291455B1 (en) | 1996-03-05 | 2001-09-18 | Zeneca Limited | 4-anilinoquinazoline derivatives |
| GB9718972D0 (en) | 1996-09-25 | 1997-11-12 | Zeneca Ltd | Chemical compounds |
| GB9714249D0 (en) | 1997-07-08 | 1997-09-10 | Angiogene Pharm Ltd | Vascular damaging agents |
| GB9900334D0 (en) | 1999-01-07 | 1999-02-24 | Angiogene Pharm Ltd | Tricylic vascular damaging agents |
| GB9900752D0 (en) | 1999-01-15 | 1999-03-03 | Angiogene Pharm Ltd | Benzimidazole vascular damaging agents |
| SK288365B6 (sk) | 1999-02-10 | 2016-07-01 | Astrazeneca Ab | Medziprodukty pre chinazolínové deriváty ako inhibítory angiogenézy |
| EP1857443B1 (en) | 2000-01-24 | 2012-03-28 | AstraZeneca AB | Therapeutic morpholino-substituted compounds |
| NZ522074A (en) | 2000-05-31 | 2004-06-25 | Astrazeneca Ab | Indole derivatives with vascular damaging activity |
| UA73993C2 (uk) | 2000-06-06 | 2005-10-17 | Астразенека Аб | Хіназолінові похідні для лікування пухлин та фармацевтична композиція |
| IL153484A0 (en) | 2000-07-07 | 2003-07-06 | Angiogene Pharm Ltd | Colchinol derivatives as angiogenesis inhibitors |
| CN1255392C (zh) | 2000-07-07 | 2006-05-10 | 安吉奥金尼药品有限公司 | 作为血管生成抑制剂的秋水仙醇衍生物 |
| JP4646626B2 (ja) * | 2002-08-16 | 2011-03-09 | アストラゼネカ アクチボラグ | ホスホイノシチド3−キナーゼβの阻害 |
| AR054438A1 (es) * | 2005-04-15 | 2007-06-27 | Kudos Pharm Ltd | Inhibidores de adn -pk |
| AU2006303037A1 (en) | 2005-10-21 | 2007-04-26 | Merz Pharma Gmbh & Co Kgaa | Chromenones and their use as modulators of metabotropic glutamate receptors |
| SI2004654T1 (sl) * | 2006-04-04 | 2013-11-29 | The Regents Of The University Of California | Pirazolopirimidinski derivati za uporabo kot kinazni antagonisti |
| WO2008064244A2 (en) | 2006-11-20 | 2008-05-29 | The Trustees Of Columbia University In The City Of New York | Phosphoinositide modulation for the treatment of neurodegenerative diseases |
| EP2112145A1 (en) | 2008-04-24 | 2009-10-28 | AxoGlia Therapeutics S.A. | Chromenone derivatives useful for the treatment of neurodegenerative diseases |
| WO2010134082A1 (en) | 2009-05-21 | 2010-11-25 | Proteologics Ltd | Chromenone derivatives for treatment of cancer |
| US8399460B2 (en) * | 2009-10-27 | 2013-03-19 | Astrazeneca Ab | Chromenone derivatives |
-
2010
- 2010-10-22 US US12/909,968 patent/US8399460B2/en active Active
- 2010-10-25 PE PE2012000578A patent/PE20130149A1/es active IP Right Grant
- 2010-10-25 PL PL10769052T patent/PL2493870T3/pl unknown
- 2010-10-25 MX MX2012005027A patent/MX2012005027A/es active IP Right Grant
- 2010-10-25 RS RS20150090A patent/RS53813B1/sr unknown
- 2010-10-25 SI SI201030875T patent/SI2493870T1/sl unknown
- 2010-10-25 EP EP10769052.1A patent/EP2493870B1/en active Active
- 2010-10-25 UA UAA201206000A patent/UA107474C2/uk unknown
- 2010-10-25 PT PT10769052T patent/PT2493870E/pt unknown
- 2010-10-25 EA EA201200618A patent/EA020523B9/ru not_active IP Right Cessation
- 2010-10-25 IN IN3328DEN2012 patent/IN2012DN03328A/en unknown
- 2010-10-25 ME MEP-2015-21A patent/ME02050B/me unknown
- 2010-10-25 MY MYPI2012001831A patent/MY179833A/en unknown
- 2010-10-25 PH PH1/2012/500804A patent/PH12012500804A1/en unknown
- 2010-10-25 BR BR112012010124A patent/BR112012010124B8/pt not_active IP Right Cessation
- 2010-10-25 KR KR1020127012933A patent/KR101738195B1/ko not_active Expired - Fee Related
- 2010-10-25 HR HRP20150146TT patent/HRP20150146T1/hr unknown
- 2010-10-25 CN CN201410654983.0A patent/CN104447657B/zh not_active Expired - Fee Related
- 2010-10-25 NZ NZ599457A patent/NZ599457A/en not_active IP Right Cessation
- 2010-10-25 ES ES10769052T patent/ES2530943T3/es active Active
- 2010-10-25 CA CA2776994A patent/CA2776994C/en active Active
- 2010-10-25 DK DK10769052.1T patent/DK2493870T3/en active
- 2010-10-25 JP JP2012535931A patent/JP5657010B2/ja not_active Expired - Fee Related
- 2010-10-25 WO PCT/GB2010/051788 patent/WO2011051704A1/en not_active Ceased
- 2010-10-25 AU AU2010311107A patent/AU2010311107B9/en not_active Ceased
- 2010-10-25 CN CN201080060262.7A patent/CN102712615B/zh not_active Expired - Fee Related
- 2010-10-26 AR ARP100103937 patent/AR078786A1/es active IP Right Grant
- 2010-10-27 UY UY32978A patent/UY32978A/es not_active Application Discontinuation
- 2010-10-27 SA SA110310808A patent/SA110310808B1/ar unknown
- 2010-10-27 TW TW099136762A patent/TWI483939B/zh not_active IP Right Cessation
-
2012
- 2012-04-15 IL IL219191A patent/IL219191A0/en not_active IP Right Cessation
- 2012-04-25 CL CL2012001056A patent/CL2012001056A1/es unknown
- 2012-04-26 CO CO12068977A patent/CO6541528A2/es active IP Right Grant
- 2012-04-27 NI NI201200081A patent/NI201200081A/es unknown
- 2012-04-27 HN HN2012000889A patent/HN2012000889A/es unknown
- 2012-04-27 CR CR20120217A patent/CR20120217A/es unknown
- 2012-04-27 EC ECSP12011838 patent/ECSP12011838A/es unknown
- 2012-04-27 GT GT201200126A patent/GT201200126A/es unknown
- 2012-04-27 DO DO2012000124A patent/DOP2012000124A/es unknown
- 2012-04-27 CU CU2012000069A patent/CU20120069A7/es unknown
-
2013
- 2013-02-13 US US13/765,850 patent/US8673906B2/en not_active Expired - Fee Related
-
2014
- 2014-01-24 US US14/163,105 patent/US9029374B2/en active Active
- 2014-11-20 JP JP2014235289A patent/JP5872016B2/ja not_active Expired - Fee Related
-
2015
- 2015-02-12 SM SM201500036T patent/SMT201500036B/xx unknown
- 2015-02-13 CY CY20151100157T patent/CY1116143T1/el unknown
- 2015-04-08 US US14/681,244 patent/US20160060240A1/en not_active Abandoned
-
2016
- 2016-03-24 US US15/079,633 patent/US9718800B2/en not_active Expired - Fee Related
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5872016B2 (ja) | 抗腫瘍活性があるクロメノン誘導体 | |
| JP5937674B2 (ja) | 癌の治療用のpi3−キナーゼ阻害剤としてのクロメノン化合物 | |
| HK1174027B (en) | Chromenone derivatives with anti-tumour activity | |
| HK1206335B (en) | Chromenone derivatives with anti-tumour activity | |
| HK1193823B (en) | Chromenone compounds as pi 3 -kinase inhibitors for the treatment of cancer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20151126 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20151214 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160112 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5872016 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |