JP5219084B2 - 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 - Google Patents
光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 Download PDFInfo
- Publication number
- JP5219084B2 JP5219084B2 JP2009034748A JP2009034748A JP5219084B2 JP 5219084 B2 JP5219084 B2 JP 5219084B2 JP 2009034748 A JP2009034748 A JP 2009034748A JP 2009034748 A JP2009034748 A JP 2009034748A JP 5219084 B2 JP5219084 B2 JP 5219084B2
- Authority
- JP
- Japan
- Prior art keywords
- meth
- acrylate
- resin composition
- phenylphenol
- reaction
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000011342 resin composition Substances 0.000 title claims description 58
- 230000003287 optical effect Effects 0.000 title claims description 19
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 98
- -1 acrylate compound Chemical class 0.000 claims description 47
- LLEMOWNGBBNAJR-UHFFFAOYSA-N biphenyl-2-ol Chemical compound OC1=CC=CC=C1C1=CC=CC=C1 LLEMOWNGBBNAJR-UHFFFAOYSA-N 0.000 claims description 34
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical group C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 claims description 30
- 239000000178 monomer Substances 0.000 claims description 24
- 150000001875 compounds Chemical class 0.000 claims description 21
- 239000004593 Epoxy Substances 0.000 claims description 14
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 claims description 11
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical group C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 claims description 10
- 235000010292 orthophenyl phenol Nutrition 0.000 claims description 7
- YXVFYQXJAXKLAK-UHFFFAOYSA-N biphenyl-4-ol Chemical compound C1=CC(O)=CC=C1C1=CC=CC=C1 YXVFYQXJAXKLAK-UHFFFAOYSA-N 0.000 claims description 6
- 125000004432 carbon atom Chemical group C* 0.000 claims description 6
- 239000003999 initiator Substances 0.000 claims description 5
- 239000000463 material Substances 0.000 claims description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 2
- 125000001183 hydrocarbyl group Chemical group 0.000 claims 2
- 238000006243 chemical reaction Methods 0.000 description 32
- 239000000047 product Substances 0.000 description 22
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 18
- 239000007795 chemical reaction product Substances 0.000 description 18
- DVWQNBIUTWDZMW-UHFFFAOYSA-N 1-naphthalen-1-ylnaphthalen-2-ol Chemical compound C1=CC=C2C(C3=C4C=CC=CC4=CC=C3O)=CC=CC2=C1 DVWQNBIUTWDZMW-UHFFFAOYSA-N 0.000 description 15
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 15
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 15
- 239000000203 mixture Substances 0.000 description 14
- 239000003822 epoxy resin Substances 0.000 description 13
- 229920000647 polyepoxide Polymers 0.000 description 13
- 239000002904 solvent Substances 0.000 description 13
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 11
- 125000002947 alkylene group Chemical group 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- 239000003054 catalyst Substances 0.000 description 10
- LYCAIKOWRPUZTN-UHFFFAOYSA-N ethylene glycol Natural products OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 10
- 229920005989 resin Polymers 0.000 description 10
- 239000011347 resin Substances 0.000 description 10
- 239000000758 substrate Substances 0.000 description 9
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 8
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 8
- 230000009477 glass transition Effects 0.000 description 8
- 238000000034 method Methods 0.000 description 8
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 7
- 230000000052 comparative effect Effects 0.000 description 7
- 239000003112 inhibitor Substances 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- TXBCBTDQIULDIA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)CO TXBCBTDQIULDIA-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical class C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 6
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 6
- 238000011156 evaluation Methods 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 229920000728 polyester Polymers 0.000 description 6
- 238000006116 polymerization reaction Methods 0.000 description 6
- XLPJNCYCZORXHG-UHFFFAOYSA-N 1-morpholin-4-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCOCC1 XLPJNCYCZORXHG-UHFFFAOYSA-N 0.000 description 5
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 5
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 5
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 5
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 5
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 5
- 238000006482 condensation reaction Methods 0.000 description 5
- 230000018044 dehydration Effects 0.000 description 5
- 238000006297 dehydration reaction Methods 0.000 description 5
- VFHVQBAGLAREND-UHFFFAOYSA-N diphenylphosphoryl-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 VFHVQBAGLAREND-UHFFFAOYSA-N 0.000 description 5
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 5
- 238000012545 processing Methods 0.000 description 5
- 230000035484 reaction time Effects 0.000 description 5
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 5
- PPTXVXKCQZKFBN-UHFFFAOYSA-N (S)-(-)-1,1'-Bi-2-naphthol Chemical compound C1=CC=C2C(C3=C4C=CC=CC4=CC=C3O)=C(O)C=CC2=C1 PPTXVXKCQZKFBN-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 4
- 150000008064 anhydrides Chemical class 0.000 description 4
- MQDJYUACMFCOFT-UHFFFAOYSA-N bis[2-(1-hydroxycyclohexyl)phenyl]methanone Chemical compound C=1C=CC=C(C(=O)C=2C(=CC=CC=2)C2(O)CCCCC2)C=1C1(O)CCCCC1 MQDJYUACMFCOFT-UHFFFAOYSA-N 0.000 description 4
- PXKLMJQFEQBVLD-UHFFFAOYSA-N bisphenol F Chemical compound C1=CC(O)=CC=C1CC1=CC=C(O)C=C1 PXKLMJQFEQBVLD-UHFFFAOYSA-N 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 4
- 229910052753 mercury Inorganic materials 0.000 description 4
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 4
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 4
- 239000003208 petroleum Substances 0.000 description 4
- 239000005056 polyisocyanate Substances 0.000 description 4
- 229920001228 polyisocyanate Polymers 0.000 description 4
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical class CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- 239000012956 1-hydroxycyclohexylphenyl-ketone Substances 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical class CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 3
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 230000001588 bifunctional effect Effects 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 150000002009 diols Chemical class 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 3
- 230000001678 irradiating effect Effects 0.000 description 3
- 239000012948 isocyanate Substances 0.000 description 3
- 150000002513 isocyanates Chemical class 0.000 description 3
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical compound COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 238000012719 thermal polymerization Methods 0.000 description 3
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical compound O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 3
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical group C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 2
- XTBMLAUOYNOIMZ-UHFFFAOYSA-N (2-phenylphenyl) 2-ethoxyprop-2-enoate Chemical compound C(C)OC(C(=O)OC1=C(C=CC=C1)C1=CC=CC=C1)=C XTBMLAUOYNOIMZ-UHFFFAOYSA-N 0.000 description 2
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 2
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 2
- ALVZNPYWJMLXKV-UHFFFAOYSA-N 1,9-Nonanediol Chemical compound OCCCCCCCCCO ALVZNPYWJMLXKV-UHFFFAOYSA-N 0.000 description 2
- ILBBNQMSDGAAPF-UHFFFAOYSA-N 1-(6-hydroxy-6-methylcyclohexa-2,4-dien-1-yl)propan-1-one Chemical compound CCC(=O)C1C=CC=CC1(C)O ILBBNQMSDGAAPF-UHFFFAOYSA-N 0.000 description 2
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- GIMQKKFOOYOQGB-UHFFFAOYSA-N 2,2-diethoxy-1,2-diphenylethanone Chemical compound C=1C=CC=CC=1C(OCC)(OCC)C(=O)C1=CC=CC=C1 GIMQKKFOOYOQGB-UHFFFAOYSA-N 0.000 description 2
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 2
- YIJYFLXQHDOQGW-UHFFFAOYSA-N 2-[2,4,6-trioxo-3,5-bis(2-prop-2-enoyloxyethyl)-1,3,5-triazinan-1-yl]ethyl prop-2-enoate Chemical compound C=CC(=O)OCCN1C(=O)N(CCOC(=O)C=C)C(=O)N(CCOC(=O)C=C)C1=O YIJYFLXQHDOQGW-UHFFFAOYSA-N 0.000 description 2
- LCZVSXRMYJUNFX-UHFFFAOYSA-N 2-[2-(2-hydroxypropoxy)propoxy]propan-1-ol Chemical compound CC(O)COC(C)COC(C)CO LCZVSXRMYJUNFX-UHFFFAOYSA-N 0.000 description 2
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 2
- XLLIQLLCWZCATF-UHFFFAOYSA-N 2-methoxyethyl acetate Chemical class COCCOC(C)=O XLLIQLLCWZCATF-UHFFFAOYSA-N 0.000 description 2
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical class COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 235000000126 Styrax benzoin Nutrition 0.000 description 2
- 244000028419 Styrax benzoin Species 0.000 description 2
- 235000008411 Sumatra benzointree Nutrition 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- HTMMMSIQFWMMIJ-UHFFFAOYSA-N [3-[2,2-dimethyl-3-(6-prop-2-enoyloxyhexanoyloxy)propanoyl]oxy-2,2-dimethylpropyl] 6-prop-2-enoyloxyhexanoate Chemical compound C=CC(=O)OCCCCCC(=O)OCC(C)(C)COC(=O)C(C)(C)COC(=O)CCCCCOC(=O)C=C HTMMMSIQFWMMIJ-UHFFFAOYSA-N 0.000 description 2
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 2
- GUCYFKSBFREPBC-UHFFFAOYSA-N [phenyl-(2,4,6-trimethylbenzoyl)phosphoryl]-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)P(=O)(C=1C=CC=CC=1)C(=O)C1=C(C)C=C(C)C=C1C GUCYFKSBFREPBC-UHFFFAOYSA-N 0.000 description 2
- 239000003377 acid catalyst Substances 0.000 description 2
- 239000001361 adipic acid Substances 0.000 description 2
- 235000011037 adipic acid Nutrition 0.000 description 2
- ISAOCJYIOMOJEB-UHFFFAOYSA-N benzoin Chemical compound C=1C=CC=CC=1C(O)C(=O)C1=CC=CC=C1 ISAOCJYIOMOJEB-UHFFFAOYSA-N 0.000 description 2
- 239000012965 benzophenone Substances 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 238000005266 casting Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- GYZLOYUZLJXAJU-UHFFFAOYSA-N diglycidyl ether Chemical group C1OC1COCC1CO1 GYZLOYUZLJXAJU-UHFFFAOYSA-N 0.000 description 2
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 2
- 230000032050 esterification Effects 0.000 description 2
- 238000005886 esterification reaction Methods 0.000 description 2
- UHESRSKEBRADOO-UHFFFAOYSA-N ethyl carbamate;prop-2-enoic acid Chemical compound OC(=O)C=C.CCOC(N)=O UHESRSKEBRADOO-UHFFFAOYSA-N 0.000 description 2
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 2
- 235000019382 gum benzoic Nutrition 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical compound OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 2
- QQVIHTHCMHWDBS-UHFFFAOYSA-N isophthalic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000004973 liquid crystal related substance Substances 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- BDJRBEYXGGNYIS-UHFFFAOYSA-N nonanedioic acid Chemical compound OC(=O)CCCCCCCC(O)=O BDJRBEYXGGNYIS-UHFFFAOYSA-N 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 239000002798 polar solvent Substances 0.000 description 2
- 229920000193 polymethacrylate Polymers 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 229930195734 saturated hydrocarbon Natural products 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- HHVIBTZHLRERCL-UHFFFAOYSA-N sulfonyldimethane Chemical compound CS(C)(=O)=O HHVIBTZHLRERCL-UHFFFAOYSA-N 0.000 description 2
- MUTNCGKQJGXKEM-UHFFFAOYSA-N tamibarotene Chemical compound C=1C=C2C(C)(C)CCC(C)(C)C2=CC=1NC(=O)C1=CC=C(C(O)=O)C=C1 MUTNCGKQJGXKEM-UHFFFAOYSA-N 0.000 description 2
- CNHDIAIOKMXOLK-UHFFFAOYSA-N toluquinol Chemical compound CC1=CC(O)=CC=C1O CNHDIAIOKMXOLK-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- QNODIIQQMGDSEF-UHFFFAOYSA-N (1-hydroxycyclohexyl)-phenylmethanone Chemical compound C=1C=CC=CC=1C(=O)C1(O)CCCCC1 QNODIIQQMGDSEF-UHFFFAOYSA-N 0.000 description 1
- BUPRYTFTHBNSBD-UHFFFAOYSA-N (2,3,4-tribromophenyl) prop-2-enoate Chemical compound BrC1=CC=C(OC(=O)C=C)C(Br)=C1Br BUPRYTFTHBNSBD-UHFFFAOYSA-N 0.000 description 1
- TVJREYNJXLOIJW-UHFFFAOYSA-N (2-methylphenyl)-diphenylstibane Chemical compound CC1=CC=CC=C1[Sb](C=1C=CC=CC=1)C1=CC=CC=C1 TVJREYNJXLOIJW-UHFFFAOYSA-N 0.000 description 1
- AWIZTCXVPWZTIX-UHFFFAOYSA-N (2-phenylphenyl) 3,3-diethoxyprop-2-enoate Chemical compound C(C)OC(=CC(=O)OC1=C(C=CC=C1)C1=CC=CC=C1)OCC AWIZTCXVPWZTIX-UHFFFAOYSA-N 0.000 description 1
- XKSUVRWJZCEYQQ-UHFFFAOYSA-N 1,1-dimethoxyethylbenzene Chemical compound COC(C)(OC)C1=CC=CC=C1 XKSUVRWJZCEYQQ-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical class CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- QWQFVUQPHUKAMY-UHFFFAOYSA-N 1,2-diphenyl-2-propoxyethanone Chemical compound C=1C=CC=CC=1C(OCCC)C(=O)C1=CC=CC=C1 QWQFVUQPHUKAMY-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- ALQLPWJFHRMHIU-UHFFFAOYSA-N 1,4-diisocyanatobenzene Chemical compound O=C=NC1=CC=C(N=C=O)C=C1 ALQLPWJFHRMHIU-UHFFFAOYSA-N 0.000 description 1
- OVBFMUAFNIIQAL-UHFFFAOYSA-N 1,4-diisocyanatobutane Chemical compound O=C=NCCCCN=C=O OVBFMUAFNIIQAL-UHFFFAOYSA-N 0.000 description 1
- SBJCUZQNHOLYMD-UHFFFAOYSA-N 1,5-Naphthalene diisocyanate Chemical compound C1=CC=C2C(N=C=O)=CC=CC2=C1N=C=O SBJCUZQNHOLYMD-UHFFFAOYSA-N 0.000 description 1
- FWWWRCRHNMOYQY-UHFFFAOYSA-N 1,5-diisocyanato-2,4-dimethylbenzene Chemical compound CC1=CC(C)=C(N=C=O)C=C1N=C=O FWWWRCRHNMOYQY-UHFFFAOYSA-N 0.000 description 1
- ATOUXIOKEJWULN-UHFFFAOYSA-N 1,6-diisocyanato-2,2,4-trimethylhexane Chemical compound O=C=NCCC(C)CC(C)(C)CN=C=O ATOUXIOKEJWULN-UHFFFAOYSA-N 0.000 description 1
- QGLRLXLDMZCFBP-UHFFFAOYSA-N 1,6-diisocyanato-2,4,4-trimethylhexane Chemical compound O=C=NCC(C)CC(C)(C)CCN=C=O QGLRLXLDMZCFBP-UHFFFAOYSA-N 0.000 description 1
- DKEGCUDAFWNSSO-UHFFFAOYSA-N 1,8-dibromooctane Chemical compound BrCCCCCCCCBr DKEGCUDAFWNSSO-UHFFFAOYSA-N 0.000 description 1
- ZIKLJUUTSQYGQI-UHFFFAOYSA-N 1-ethoxy-2-(2-ethoxypropoxy)propane Chemical class CCOCC(C)OCC(C)OCC ZIKLJUUTSQYGQI-UHFFFAOYSA-N 0.000 description 1
- KIAMPLQEZAMORJ-UHFFFAOYSA-N 1-ethoxy-2-[2-(2-ethoxyethoxy)ethoxy]ethane Chemical class CCOCCOCCOCCOCC KIAMPLQEZAMORJ-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- CERJZAHSUZVMCH-UHFFFAOYSA-N 2,2-dichloro-1-phenylethanone Chemical compound ClC(Cl)C(=O)C1=CC=CC=C1 CERJZAHSUZVMCH-UHFFFAOYSA-N 0.000 description 1
- PIZHFBODNLEQBL-UHFFFAOYSA-N 2,2-diethoxy-1-phenylethanone Chemical compound CCOC(OCC)C(=O)C1=CC=CC=C1 PIZHFBODNLEQBL-UHFFFAOYSA-N 0.000 description 1
- OJRJDENLRJHEJO-UHFFFAOYSA-N 2,4-diethylpentane-1,5-diol Chemical compound CCC(CO)CC(CC)CO OJRJDENLRJHEJO-UHFFFAOYSA-N 0.000 description 1
- BTJPUDCSZVCXFQ-UHFFFAOYSA-N 2,4-diethylthioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC(CC)=CC(CC)=C3SC2=C1 BTJPUDCSZVCXFQ-UHFFFAOYSA-N 0.000 description 1
- OPLCSTZDXXUYDU-UHFFFAOYSA-N 2,4-dimethyl-6-tert-butylphenol Chemical compound CC1=CC(C)=C(O)C(C(C)(C)C)=C1 OPLCSTZDXXUYDU-UHFFFAOYSA-N 0.000 description 1
- QFSYADJLNBHAKO-UHFFFAOYSA-N 2,5-dihydroxy-1,4-benzoquinone Chemical compound OC1=CC(=O)C(O)=CC1=O QFSYADJLNBHAKO-UHFFFAOYSA-N 0.000 description 1
- FPZWZCWUIYYYBU-UHFFFAOYSA-N 2-(2-ethoxyethoxy)ethyl acetate Chemical class CCOCCOCCOC(C)=O FPZWZCWUIYYYBU-UHFFFAOYSA-N 0.000 description 1
- WMYINDVYGQKYMI-UHFFFAOYSA-N 2-[2,2-bis(hydroxymethyl)butoxymethyl]-2-ethylpropane-1,3-diol Chemical compound CCC(CO)(CO)COCC(CC)(CO)CO WMYINDVYGQKYMI-UHFFFAOYSA-N 0.000 description 1
- PTJWCLYPVFJWMP-UHFFFAOYSA-N 2-[[3-hydroxy-2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)COCC(CO)(CO)CO PTJWCLYPVFJWMP-UHFFFAOYSA-N 0.000 description 1
- NQBXSWAWVZHKBZ-UHFFFAOYSA-N 2-butoxyethyl acetate Chemical class CCCCOCCOC(C)=O NQBXSWAWVZHKBZ-UHFFFAOYSA-N 0.000 description 1
- DSKYSDCYIODJPC-UHFFFAOYSA-N 2-butyl-2-ethylpropane-1,3-diol Chemical compound CCCCC(CC)(CO)CO DSKYSDCYIODJPC-UHFFFAOYSA-N 0.000 description 1
- FPKCTSIVDAWGFA-UHFFFAOYSA-N 2-chloroanthracene-9,10-dione Chemical compound C1=CC=C2C(=O)C3=CC(Cl)=CC=C3C(=O)C2=C1 FPKCTSIVDAWGFA-UHFFFAOYSA-N 0.000 description 1
- ZCDADJXRUCOCJE-UHFFFAOYSA-N 2-chlorothioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC(Cl)=CC=C3SC2=C1 ZCDADJXRUCOCJE-UHFFFAOYSA-N 0.000 description 1
- KMNCBSZOIQAUFX-UHFFFAOYSA-N 2-ethoxy-1,2-diphenylethanone Chemical compound C=1C=CC=CC=1C(OCC)C(=O)C1=CC=CC=C1 KMNCBSZOIQAUFX-UHFFFAOYSA-N 0.000 description 1
- SVONRAPFKPVNKG-UHFFFAOYSA-N 2-ethoxyethyl acetate Chemical class CCOCCOC(C)=O SVONRAPFKPVNKG-UHFFFAOYSA-N 0.000 description 1
- XMLYCEVDHLAQEL-UHFFFAOYSA-N 2-hydroxy-2-methyl-1-phenylpropan-1-one Chemical compound CC(C)(O)C(=O)C1=CC=CC=C1 XMLYCEVDHLAQEL-UHFFFAOYSA-N 0.000 description 1
- BQZJOQXSCSZQPS-UHFFFAOYSA-N 2-methoxy-1,2-diphenylethanone Chemical compound C=1C=CC=CC=1C(OC)C(=O)C1=CC=CC=C1 BQZJOQXSCSZQPS-UHFFFAOYSA-N 0.000 description 1
- LWRBVKNFOYUCNP-UHFFFAOYSA-N 2-methyl-1-(4-methylsulfanylphenyl)-2-morpholin-4-ylpropan-1-one Chemical compound C1=CC(SC)=CC=C1C(=O)C(C)(C)N1CCOCC1 LWRBVKNFOYUCNP-UHFFFAOYSA-N 0.000 description 1
- SDQROPCSKIYYAV-UHFFFAOYSA-N 2-methyloctane-1,8-diol Chemical compound OCC(C)CCCCCCO SDQROPCSKIYYAV-UHFFFAOYSA-N 0.000 description 1
- UMWZLYTVXQBTTE-UHFFFAOYSA-N 2-pentylanthracene-9,10-dione Chemical compound C1=CC=C2C(=O)C3=CC(CCCCC)=CC=C3C(=O)C2=C1 UMWZLYTVXQBTTE-UHFFFAOYSA-N 0.000 description 1
- KTALPKYXQZGAEG-UHFFFAOYSA-N 2-propan-2-ylthioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC(C(C)C)=CC=C3SC2=C1 KTALPKYXQZGAEG-UHFFFAOYSA-N 0.000 description 1
- YTPSFXZMJKMUJE-UHFFFAOYSA-N 2-tert-butylanthracene-9,10-dione Chemical compound C1=CC=C2C(=O)C3=CC(C(C)(C)C)=CC=C3C(=O)C2=C1 YTPSFXZMJKMUJE-UHFFFAOYSA-N 0.000 description 1
- SXFJDZNJHVPHPH-UHFFFAOYSA-N 3-methylpentane-1,5-diol Chemical compound OCCC(C)CCO SXFJDZNJHVPHPH-UHFFFAOYSA-N 0.000 description 1
- VATRWWPJWVCZTA-UHFFFAOYSA-N 3-oxo-n-[2-(trifluoromethyl)phenyl]butanamide Chemical class CC(=O)CC(=O)NC1=CC=CC=C1C(F)(F)F VATRWWPJWVCZTA-UHFFFAOYSA-N 0.000 description 1
- DOFIAZGYBIBEGI-UHFFFAOYSA-N 3-sulfanylphenol Chemical compound OC1=CC=CC(S)=C1 DOFIAZGYBIBEGI-UHFFFAOYSA-N 0.000 description 1
- VNGLVZLEUDIDQH-UHFFFAOYSA-N 4-[2-(4-hydroxyphenyl)propan-2-yl]phenol;2-methyloxirane Chemical compound CC1CO1.C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 VNGLVZLEUDIDQH-UHFFFAOYSA-N 0.000 description 1
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 1
- 229930185605 Bisphenol Natural products 0.000 description 1
- 229920002799 BoPET Polymers 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Chemical class CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- PUCBEDPNBBWYLB-UHFFFAOYSA-N C=CC(OCCOc(ccc1c2cccc1)c2-c(c(cccc1)c1cc1)c1OCCOC(C=C)=O)=O Chemical compound C=CC(OCCOc(ccc1c2cccc1)c2-c(c(cccc1)c1cc1)c1OCCOC(C=C)=O)=O PUCBEDPNBBWYLB-UHFFFAOYSA-N 0.000 description 1
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 1
- 239000005057 Hexamethylene diisocyanate Substances 0.000 description 1
- 239000005058 Isophorone diisocyanate Substances 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- OKIZCWYLBDKLSU-UHFFFAOYSA-M N,N,N-Trimethylmethanaminium chloride Chemical compound [Cl-].C[N+](C)(C)C OKIZCWYLBDKLSU-UHFFFAOYSA-M 0.000 description 1
- 229920000459 Nitrile rubber Polymers 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical class CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- VNQABZCSYCTZMS-UHFFFAOYSA-N Orthoform Chemical compound COC(=O)C1=CC=C(O)C(N)=C1 VNQABZCSYCTZMS-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- VZTQQYMRXDUHDO-UHFFFAOYSA-N [2-hydroxy-3-[4-[2-[4-(2-hydroxy-3-prop-2-enoyloxypropoxy)phenyl]propan-2-yl]phenoxy]propyl] prop-2-enoate Chemical compound C=1C=C(OCC(O)COC(=O)C=C)C=CC=1C(C)(C)C1=CC=C(OCC(O)COC(=O)C=C)C=C1 VZTQQYMRXDUHDO-UHFFFAOYSA-N 0.000 description 1
- DBHQYYNDKZDVTN-UHFFFAOYSA-N [4-(4-methylphenyl)sulfanylphenyl]-phenylmethanone Chemical compound C1=CC(C)=CC=C1SC1=CC=C(C(=O)C=2C=CC=CC=2)C=C1 DBHQYYNDKZDVTN-UHFFFAOYSA-N 0.000 description 1
- KXBFLNPZHXDQLV-UHFFFAOYSA-N [cyclohexyl(diisocyanato)methyl]cyclohexane Chemical compound C1CCCCC1C(N=C=O)(N=C=O)C1CCCCC1 KXBFLNPZHXDQLV-UHFFFAOYSA-N 0.000 description 1
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 1
- 150000008062 acetophenones Chemical class 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000002216 antistatic agent Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 229960002130 benzoin Drugs 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- 150000008366 benzophenones Chemical class 0.000 description 1
- UUZYBYIOAZTMGC-UHFFFAOYSA-M benzyl(trimethyl)azanium;bromide Chemical compound [Br-].C[N+](C)(C)CC1=CC=CC=C1 UUZYBYIOAZTMGC-UHFFFAOYSA-M 0.000 description 1
- KXHPPCXNWTUNSB-UHFFFAOYSA-M benzyl(trimethyl)azanium;chloride Chemical compound [Cl-].C[N+](C)(C)CC1=CC=CC=C1 KXHPPCXNWTUNSB-UHFFFAOYSA-M 0.000 description 1
- LRRJQNMXIDXNIM-UHFFFAOYSA-M benzyl(trimethyl)azanium;iodide Chemical compound [I-].C[N+](C)(C)CC1=CC=CC=C1 LRRJQNMXIDXNIM-UHFFFAOYSA-M 0.000 description 1
- HIFVAOIJYDXIJG-UHFFFAOYSA-N benzylbenzene;isocyanic acid Chemical class N=C=O.N=C=O.C=1C=CC=CC=1CC1=CC=CC=C1 HIFVAOIJYDXIJG-UHFFFAOYSA-N 0.000 description 1
- JGCWKVKYRNXTMD-UHFFFAOYSA-N bicyclo[2.2.1]heptane;isocyanic acid Chemical compound N=C=O.N=C=O.C1CC2CCC1C2 JGCWKVKYRNXTMD-UHFFFAOYSA-N 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- HXTBYXIZCDULQI-UHFFFAOYSA-N bis[4-(methylamino)phenyl]methanone Chemical compound C1=CC(NC)=CC=C1C(=O)C1=CC=C(NC)C=C1 HXTBYXIZCDULQI-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- RPBPCPJJHKASGQ-UHFFFAOYSA-K chromium(3+);octanoate Chemical compound [Cr+3].CCCCCCCC([O-])=O.CCCCCCCC([O-])=O.CCCCCCCC([O-])=O RPBPCPJJHKASGQ-UHFFFAOYSA-K 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000010924 continuous production Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- KORSJDCBLAPZEQ-UHFFFAOYSA-N dicyclohexylmethane-4,4'-diisocyanate Chemical compound C1CC(N=C=O)CCC1CC1CCC(N=C=O)CC1 KORSJDCBLAPZEQ-UHFFFAOYSA-N 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- XXBDWLFCJWSEKW-UHFFFAOYSA-N dimethylbenzylamine Chemical compound CN(C)CC1=CC=CC=C1 XXBDWLFCJWSEKW-UHFFFAOYSA-N 0.000 description 1
- SZXQTJUDPRGNJN-UHFFFAOYSA-N dipropylene glycol Chemical compound OCCCOCCCO SZXQTJUDPRGNJN-UHFFFAOYSA-N 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- GKIPXFAANLTWBM-UHFFFAOYSA-N epibromohydrin Chemical compound BrCC1CO1 GKIPXFAANLTWBM-UHFFFAOYSA-N 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000003292 glue Chemical class 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 1
- 230000020169 heat generation Effects 0.000 description 1
- RRAMGCGOFNQTLD-UHFFFAOYSA-N hexamethylene diisocyanate Chemical compound O=C=NCCCCCCN=C=O RRAMGCGOFNQTLD-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical class CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- NIMLQBUJDJZYEJ-UHFFFAOYSA-N isophorone diisocyanate Chemical compound CC1(C)CC(N=C=O)CC(C)(CN=C=O)C1 NIMLQBUJDJZYEJ-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000004611 light stabiliser Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000006082 mold release agent Substances 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229920003986 novolac Polymers 0.000 description 1
- OEIJHBUUFURJLI-UHFFFAOYSA-N octane-1,8-diol Chemical compound OCCCCCCCCO OEIJHBUUFURJLI-UHFFFAOYSA-N 0.000 description 1
- BTTPFGPVCJCQAZ-UHFFFAOYSA-N oxirane;2-phenylphenol Chemical compound C1CO1.OC1=CC=CC=C1C1=CC=CC=C1 BTTPFGPVCJCQAZ-UHFFFAOYSA-N 0.000 description 1
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920005668 polycarbonate resin Polymers 0.000 description 1
- 239000004431 polycarbonate resin Substances 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920005990 polystyrene resin Polymers 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- KCTAWXVAICEBSD-UHFFFAOYSA-N prop-2-enoyloxy prop-2-eneperoxoate Chemical compound C=CC(=O)OOOC(=O)C=C KCTAWXVAICEBSD-UHFFFAOYSA-N 0.000 description 1
- LLHKCFNBLRBOGN-UHFFFAOYSA-N propylene glycol methyl ether acetate Chemical class COCC(C)OC(C)=O LLHKCFNBLRBOGN-UHFFFAOYSA-N 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- DDFYFBUWEBINLX-UHFFFAOYSA-M tetramethylammonium bromide Chemical compound [Br-].C[N+](C)(C)C DDFYFBUWEBINLX-UHFFFAOYSA-M 0.000 description 1
- UOHMMEJUHBCKEE-UHFFFAOYSA-N tetramethylbenzene Natural products CC1=CC=C(C)C(C)=C1C UOHMMEJUHBCKEE-UHFFFAOYSA-N 0.000 description 1
- ILWRPSCZWQJDMK-UHFFFAOYSA-N triethylazanium;chloride Chemical compound Cl.CCN(CC)CC ILWRPSCZWQJDMK-UHFFFAOYSA-N 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical class COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 1
- HVYVMSPIJIWUNA-UHFFFAOYSA-N triphenylstibine Chemical compound C1=CC=CC=C1[Sb](C=1C=CC=CC=1)C1=CC=CC=C1 HVYVMSPIJIWUNA-UHFFFAOYSA-N 0.000 description 1
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 1
- 239000008096 xylene Chemical class 0.000 description 1
- 229910052726 zirconium Inorganic materials 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L33/00—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides or nitriles thereof; Compositions of derivatives of such polymers
- C08L33/04—Homopolymers or copolymers of esters
- C08L33/06—Homopolymers or copolymers of esters of esters containing only carbon, hydrogen and oxygen, which oxygen atoms are present only as part of the carboxyl radical
- C08L33/08—Homopolymers or copolymers of acrylic acid esters
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F290/00—Macromolecular compounds obtained by polymerising monomers on to polymers modified by introduction of aliphatic unsaturated end or side groups
- C08F290/02—Macromolecular compounds obtained by polymerising monomers on to polymers modified by introduction of aliphatic unsaturated end or side groups on to polymers modified by introduction of unsaturated end groups
- C08F290/06—Polymers provided for in subclass C08G
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/02—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds
- C08G63/12—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds derived from polycarboxylic acids and polyhydroxy compounds
- C08G63/16—Dicarboxylic acids and dihydroxy compounds
- C08G63/18—Dicarboxylic acids and dihydroxy compounds the acids or hydroxy compounds containing carbocyclic rings
- C08G63/181—Acids containing aromatic rings
- C08G63/185—Acids containing aromatic rings containing two or more aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B1/00—Optical elements characterised by the material of which they are made; Optical coatings for optical elements
- G02B1/04—Optical elements characterised by the material of which they are made; Optical coatings for optical elements made of organic materials, e.g. plastics
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Macromonomer-Based Addition Polymer (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
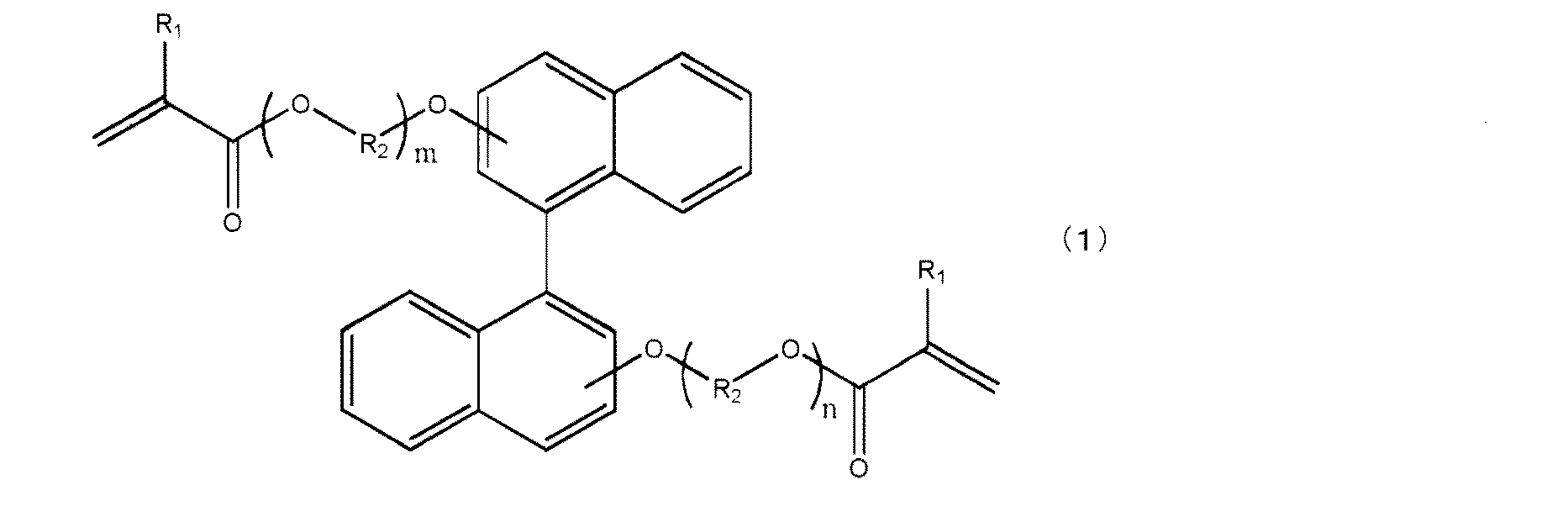
(1)フェニルエーテル基を有するモノアクリレートモノマー(A)、一般式(1)
で表される化合物(B)
及び光重合開始剤(C)を含む光学レンズシート用エネルギー線硬化型樹脂組成物、
(2)フェニルエーテル基を有するモノアクリレートモノマー(A)がo−フェニルフェノール(ポリ)エトキシ(メタ)アクリレート、p−フェニルフェノール(ポリ)エトキシ(メタ)アクリレート、o−フェニルフェノールエポキシ(メタ)アクリレート、p−フェニルフェノールエポキシ(メタ)アクリレートである前記(1)に記載の樹脂組成物、
(3)更に、フェニルエーテル基を有するモノアクリレートモノマー(A)および一般式(1)で表される化合物(B)以外の(メタ)アクリレート化合物(D)を含む前記(1)又は(2)に記載の樹脂組成物、
(4)(メタ)アクリレート化合物(D)がビスフェノールA骨格を含む構造の化合物である前記(1)ないし(3)のいずれか一項に記載の樹脂組成物、
(5)E型粘度計で測定した25℃での粘度が3000mPa・s以下である前記(1)ないし(4)のいずれか一項に記載の樹脂組成物、
(6)前記(1)ないし(5)のいずれか一項に記載の樹脂組成物を硬化して得られる25℃での屈折率が1.55以上である硬化物、
(7)前記(6)に記載の硬化物を用いる光学レンズシート、
に関する。
エピハロヒドリンの使用量はフェニルフェノール1モルに対し通常2〜20モル、好ましくは3〜15モルである。
合成例1
攪拌装置、還流管、温度計をつけたフラスコ中に、(RS)−1,1’−ビ−2−ナフトールを286.3g(1.0mol)、炭酸エチレンを264.2g(3.0mol)、炭酸カリウムを41.5g(0.3mol)、トルエン2000mlを仕込み、110℃で12時間反応させた。
反応後、得られた反応液を水洗、1%NaOH水溶液で洗浄し、次いで洗浄水が中性になるまで水洗を行った。水洗後の溶液をロータリーエバポレーターを用いて減圧下に溶媒を留去し、(RS)−1,1’−ビ−2−ナフトールのエチレンオキサイド2mol反応物300.0gを得た。
続いて、攪拌装置、還流管、温度計、及び水分離機をつけたフラスコ中に、(RS)−1,1’−ビ−2−ナフトールのエチレンオキサイド2mol反応物187.2g(0.5mol)、アクリル酸86.5g(2.4mol)、パラトルエンスルホン酸0.95g、ハイドロキノン0.87g、トルエン917.4g、シクロヘキサン393.2g仕込み、反応温度95〜105℃で生成水を溶媒と共沸留去しながら反応させた。反応後、25%NaOH水溶液で中和した後、15質量%食塩水200gで3回洗浄した。溶媒を減圧留去して淡黄色固体の下記構造式の生成物337.8gを得た。
液屈折率(D線、25℃) 1.62
1H−NMR(CDCl3、300MHz)、ppm:
4.00−4.30ppm=8H、5.60−5.90ppm=4H、6.05−6.15ppm=2H、7.05−7.50ppm=8H、7.80−8.00ppm=4H
合成例2
乾燥容器中に2,4−トリレンジイソシアネート139.3部、ジラウリン酸ジ−n−ブチルスズ0.05部、メトキノン0.16部を入れ40℃まで昇温、撹拌した。これに2−ヒドロキシエチルアクリレート185.6部を、発熱を確認しながら1時間かけて滴下し、80℃で1〜2時間反応させた。反応後のイソシアネート値は0.1以下であり、反応がほぼ定量的に終了したことを示した。
(2)離型性:硬化した樹脂を金型より離型させるときの難易度を表す。
○・・・・金型からの離型が良好である
△・・・・離型がやや困難あるいは離型時に剥離音がある
×・・・・離型が困難あるいは型残りがある
(3)型再現性:硬化した紫外線硬化性樹脂層の表面形状と金型の表面形状を観察した。
○・・・・再現性良好である
×・・・・再現性が不良である
評価結果は0〜2を○とし、3〜5を×とした。
(6)ガラス転移温度(Tg):硬化した紫外線硬化性樹脂層のTg点を粘弾性測定システム(DMS−6000:セイコー電子工業(株)製)において、引っ張りモード、周波数1Hzにて測定した。
成分(A)としてo−フェニルフェノールモノエトキシアクリレート31部、成分(B)として合成例1で得た化合物20部、成分(C)として1−ヒドロキシ−シクロヘキシルフェニルケトン3部、ジフェニル−(2,4,6−トリメチルベンゾイル)フォスフィンオキシド0.1部、成分(D)としてKAYARAD R−551(日本化薬製:ビスフェノールAポリエトキシジアクリレート)20部、KAYARAD R−115(日本化薬製:ビスフェノールAエポキシアクリレート)4部、トリス(2−アクリロイルオキシエチル)イソシアヌレート18部、アクリロイルモルホリン7部を60℃に加温、混合し、本発明の樹脂組成物を得た。この樹脂組成物の粘度は904mPa・sであった。又、この樹脂組成物を高圧水銀灯(80w/cm、オゾンレス)にて600mJ/cm2の照射を行って硬化した、膜厚200μmの紫外線硬化型樹脂層の屈折率(25℃)は1.587であり、ガラス転移温度(Tg)は94℃だった。
さらに、この樹脂組成物をプリズムレンズ金型の上に膜厚が50μmになるように塗布し、その上に基材として易接着PETフィルム(東洋紡コスモシャインA4300、100μm厚)を接着させ、更にその上から高圧水銀ランプで1000mJ/cm2の照射量の紫外線を照射して硬化させた後剥離して、本発明のプリズムレンズシートを得た。
評価結果
離型性:○、型再現性:○、密着性:○であった。
実施例1において、成分(A)としてo−フェニルフェノールモノエトキシアクリレート52部、成分(C)として2−ヒドロキシ−2−メチルー1−フェニルプロパン−1−オン3部、成分(D)として合成例2で得た化合物10部、アクリロイルモルホリン13部、テトラヒドロフルフリルアクリレート5部を用いた以外は実施例1と同様に本発明の樹脂組成物を得た。この樹脂組成物の粘度は195mPa・sであった。又、実施例1と同様にして得た樹脂層の屈折率(25℃)は1.597であり、ガラス転移温度(Tg)は69℃だった。
得られた樹脂組成物を用いて実施例1と同様にして本発明のプリズムレンズシートを得た。
評価結果
離型性:○、型再現性:○、密着性:○であった。
特許文献1(特開昭63−167301)の実施例1に従い、アロニックスM−315(トリス(2−アクリロイルオキシエチル)イソシアヌレート)を70部、テトラヒドロフルフリルアクリレート30部、光重合開始剤として1−(4−イソプロピルフェニル)−2−ヒドロキシ−2−メチルプロパン−1−オン3部を60℃に加温、混合し、比較用の樹脂組成物を得た。この樹脂組成物の粘度は134mPa・sであった。又、実施例1と同様にして得た樹脂層の屈折率(25℃)は1.52であった。
この結果から比較例1の組成物は本発明の組成物に比べて屈折率が低く、本発明のレンズ類の製造に不向きである。
特許文献3(特許第3209554号)の実施例1に従い、該文献の合成例1のウレタンアクリレート(ネオペンチルグリコールとアジピン酸のポリエステルジオール、エチレングリコール、トリレンジイソシアネート及び2−ヒドロキシエチルアクリレートの反応物)及び該文献合成例3の化合物(o−フェニルフェノールジエトキシアクリレート)を合成し、上記のウレタンアクリレートを30部、上記のo−フェニルフェノールジエトキシアクリレートを15部、KAYARAD R−551を45部、トリブロモフェニルアクリレートを10部、イルガキュアー184(1−ヒドロキシシクロヘキシルフェニルケトン)3部を60℃に加温、混合し、比較用の樹脂組成物を得た。この樹脂組成物の粘度は4420mPa・sであった。又、実施例1と同様にして得た樹脂層の屈折率(25℃)は1.574であった。
この結果から比較例2の組成物は本発明の組成物に比べて粘度が高く、微細な加工やロール状のシートやフィルムの連続加工に不向きである。
Claims (7)
- フェニルエーテル基を有するモノアクリレートモノマー(A)がo−フェニルフェノール(ポリ)エトキシ(メタ)アクリレート、p−フェニルフェノール(ポリ)エトキシ(メタ)アクリレート、o−フェニルフェノールエポキシ(メタ)アクリレート、p−フェニルフェノールエポキシ(メタ)アクリレートである請求項1に記載の樹脂組成物。
- 更に、フェニルエーテル基を有するモノアクリレートモノマー(A)および一般式(1)で表される化合物(B)以外の(メタ)アクリレート化合物(D)を含む請求項1又は2に記載の樹脂組成物。
- (メタ)アクリレート化合物(D)がビスフェノールA骨格を含む構造の化合物である請
求項3に記載の樹脂組成物。 - E型粘度計で測定した25℃での粘度が3000mPa・s以下である請求項1ないし4のいずれか一項に記載の樹脂組成物。
- 請求項1ないし5のいずれか一項に記載の樹脂組成物を硬化して得られる25℃での屈折率が1.55以上である硬化物。
- 請求項6に記載の硬化物を用いる光学レンズシート。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009034748A JP5219084B2 (ja) | 2009-02-18 | 2009-02-18 | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
| TW099103903A TWI454492B (zh) | 2009-02-18 | 2010-02-09 | 光學透鏡膜片用能量線硬化型樹脂組成物及其硬化物 |
| KR1020100013026A KR101558338B1 (ko) | 2009-02-18 | 2010-02-11 | 에너지선 경화형 수지 조성물 및, 그의 경화물 및 광학 렌즈 시트 |
| CN2010101192246A CN101805422B (zh) | 2009-02-18 | 2010-02-12 | 光学透镜片用能量射线固化型树脂组合物及其固化物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009034748A JP5219084B2 (ja) | 2009-02-18 | 2009-02-18 | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010189534A JP2010189534A (ja) | 2010-09-02 |
| JP5219084B2 true JP5219084B2 (ja) | 2013-06-26 |
Family
ID=42607385
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009034748A Expired - Fee Related JP5219084B2 (ja) | 2009-02-18 | 2009-02-18 | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
Country Status (4)
| Country | Link |
|---|---|
| JP (1) | JP5219084B2 (ja) |
| KR (1) | KR101558338B1 (ja) |
| CN (1) | CN101805422B (ja) |
| TW (1) | TWI454492B (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013028662A (ja) * | 2011-07-27 | 2013-02-07 | Nippon Kayaku Co Ltd | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
| JP2013166900A (ja) * | 2012-02-17 | 2013-08-29 | Nippon Kayaku Co Ltd | ハードコートフィルム用エネルギー線硬化型樹脂組成物及びハードコートフィルム(1) |
| JP2013167837A (ja) * | 2012-02-17 | 2013-08-29 | Nippon Kayaku Co Ltd | ハードコートフィルム用エネルギー線硬化型樹脂組成物及びハードコートフィルム(2) |
| WO2013151001A1 (ja) * | 2012-04-03 | 2013-10-10 | 東亞合成株式会社 | 活性エネルギー線硬化型組成物、並びに、硬化膜を有する金属基材及びその製造方法 |
| JP6057409B2 (ja) * | 2012-04-25 | 2017-01-11 | 日本化薬株式会社 | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物(1) |
| JP5974784B2 (ja) * | 2012-09-28 | 2016-08-23 | Jnc株式会社 | インクジェットインク |
| JP6083901B2 (ja) * | 2013-05-24 | 2017-02-22 | 田岡化学工業株式会社 | ビナフタレン化合物の製造方法 |
| JP6083900B2 (ja) * | 2013-05-24 | 2017-02-22 | 田岡化学工業株式会社 | ビナフタレン化合物の製造方法 |
| KR102048610B1 (ko) * | 2013-09-26 | 2019-11-25 | 타오카 케미컬 컴퍼니 리미티드 | 바이나프탈렌 골격을 가지는 에폭시 수지 |
| CN103553971A (zh) * | 2013-10-25 | 2014-02-05 | 张家港威迪森化学有限公司 | 聚氨酯丙烯酸酯的制备方法 |
| JP6535002B2 (ja) * | 2014-07-17 | 2019-06-26 | 日本化薬株式会社 | 液晶シール剤及びそれを用いた液晶表示セル |
| TWI558541B (zh) * | 2015-04-02 | 2016-11-21 | 長興材料工業股份有限公司 | 光固化型鏡片及其製造方法 |
| WO2018051713A1 (ja) * | 2016-09-15 | 2018-03-22 | 富士フイルム株式会社 | 硬化性組成物、硬化物、光学部材、レンズ及び化合物 |
| JP6881179B2 (ja) * | 2017-09-19 | 2021-06-02 | 三菱ケミカル株式会社 | 硬化性組成物 |
| JP6635999B2 (ja) * | 2017-10-13 | 2020-01-29 | 株式会社ダイセル | カリウム塩の製造方法、及びカリウム塩 |
| EP4105250A4 (en) * | 2020-02-10 | 2024-02-28 | Kuraray Noritake Dental Inc. | RESIN COMPOSITION FOR STEREOLITHOGRAPHY |
| JP2026503055A (ja) * | 2023-09-13 | 2026-01-27 | エルジー・ケム・リミテッド | 樹脂組成物、およびこれを含む物品 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5986615A (ja) * | 1982-11-11 | 1984-05-18 | Showa Denko Kk | 重合性組成物 |
| JP2807315B2 (ja) * | 1990-06-28 | 1998-10-08 | 日本化薬株式会社 | (メタ)アクリル酸エステル、これを含む樹脂組成物及びその硬化物 |
| JP3209554B2 (ja) * | 1991-12-19 | 2001-09-17 | 日本化薬株式会社 | 樹脂組成物、透過型スクリーン用紫外線硬化型樹脂組成物及びその硬化物 |
| JPH09272707A (ja) * | 1996-04-04 | 1997-10-21 | Toagosei Co Ltd | 活性エネルギー線硬化型(メタ)アクリレート組成物 |
| EP1331494A4 (en) * | 2000-10-13 | 2005-01-05 | Nof Corp | COMPOSITION FOR OPTICAL MATERIAL, OPTICAL MATERIAL, AND PLASTIC LENSES |
| JP4659288B2 (ja) * | 2001-07-19 | 2011-03-30 | 独立行政法人産業技術総合研究所 | ホログラム記録材料用組成物、ホログラム記録媒体およびその製造法 |
| CN1454933A (zh) * | 2003-04-01 | 2003-11-12 | 四川大学 | 一种光固化树脂组合物 |
| JP4802479B2 (ja) * | 2004-02-18 | 2011-10-26 | Jnc株式会社 | 重合性ビナフタレン誘導体 |
| JP2005283632A (ja) * | 2004-03-26 | 2005-10-13 | Fuji Photo Film Co Ltd | 重合性組成物およびネガ型画像記録材料 |
| JP4433300B2 (ja) * | 2005-01-05 | 2010-03-17 | 日本化薬株式会社 | 感光性樹脂組成物及びその硬化皮膜を有するフィルム |
| JP5017938B2 (ja) * | 2006-06-22 | 2012-09-05 | 川崎化成工業株式会社 | ビス(2−(メタ)アクリルオキシアルコキシ)ナフタレン化合物を有効成分とする光重合増感剤、およびその用途 |
| JP2008201972A (ja) * | 2007-02-22 | 2008-09-04 | Kyocera Chemical Corp | 高屈折材料及びそれを用いた光伝送体 |
| JP2010106046A (ja) * | 2007-02-28 | 2010-05-13 | Nippon Kayaku Co Ltd | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
| JPWO2008136262A1 (ja) | 2007-04-27 | 2010-07-29 | 日本化薬株式会社 | (メタ)アクリレート化合物、それを含有する樹脂組成物及びその硬化物並びに光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
-
2009
- 2009-02-18 JP JP2009034748A patent/JP5219084B2/ja not_active Expired - Fee Related
-
2010
- 2010-02-09 TW TW099103903A patent/TWI454492B/zh not_active IP Right Cessation
- 2010-02-11 KR KR1020100013026A patent/KR101558338B1/ko not_active Expired - Fee Related
- 2010-02-12 CN CN2010101192246A patent/CN101805422B/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| TW201035129A (en) | 2010-10-01 |
| TWI454492B (zh) | 2014-10-01 |
| CN101805422A (zh) | 2010-08-18 |
| CN101805422B (zh) | 2013-10-23 |
| JP2010189534A (ja) | 2010-09-02 |
| KR20100094369A (ko) | 2010-08-26 |
| KR101558338B1 (ko) | 2015-10-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5219084B2 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP5241023B2 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| KR101456513B1 (ko) | 광학 렌즈 시트용 에너지선 경화형 수지 조성물 및 그의 경화물 | |
| JPWO2008136262A1 (ja) | (メタ)アクリレート化合物、それを含有する樹脂組成物及びその硬化物並びに光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP2010138393A (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP5057367B2 (ja) | 活性エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP6381318B2 (ja) | 光学レンズ用活性エネルギー線硬化性樹脂組成物 | |
| JPWO2010137501A1 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP5083830B2 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及び光学レンズシート | |
| JP5744847B2 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| US20090239968A1 (en) | Resin composition, resin composition for lens, and cured product thereof | |
| JP2011033875A (ja) | 光学レンズ用エネルギー線硬化型樹脂組成物及び光学レンズ | |
| JP4678726B2 (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JP5328003B2 (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JPWO2010004959A1 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP4812069B2 (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JP5207388B2 (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 | |
| JP5429832B2 (ja) | ウレタン(メタ)アクリレート化合物 | |
| JP2005042034A (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JP2006008933A (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JP4678724B2 (ja) | 樹脂組成物、レンズ用樹脂組成物及びその硬化物 | |
| JP2009031779A (ja) | 光学レンズシート用エネルギー線硬化型樹脂組成物及び光学レンズシート |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110809 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130121 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130128 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130129 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130227 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130227 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160315 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5219084 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |